JP6273326B2 - 移動相の調整によって、ポリペプチド単量体、凝集物およびフラグメントを分離するための選択性を向上させた、イオン交換クロマトグラフィー - Google Patents
移動相の調整によって、ポリペプチド単量体、凝集物およびフラグメントを分離するための選択性を向上させた、イオン交換クロマトグラフィー Download PDFInfo
- Publication number
- JP6273326B2 JP6273326B2 JP2016151624A JP2016151624A JP6273326B2 JP 6273326 B2 JP6273326 B2 JP 6273326B2 JP 2016151624 A JP2016151624 A JP 2016151624A JP 2016151624 A JP2016151624 A JP 2016151624A JP 6273326 B2 JP6273326 B2 JP 6273326B2
- Authority
- JP
- Japan
- Prior art keywords
- antibody
- poly
- ethylene glycol
- solution
- polypeptide
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K1/00—General methods for the preparation of peptides, i.e. processes for the organic chemical preparation of peptides or proteins of any length
- C07K1/14—Extraction; Separation; Purification
- C07K1/16—Extraction; Separation; Purification by chromatography
- C07K1/18—Ion-exchange chromatography
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/39591—Stabilisation, fragmentation
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D15/00—Separating processes involving the treatment of liquids with solid sorbents; Apparatus therefor
- B01D15/08—Selective adsorption, e.g. chromatography
- B01D15/26—Selective adsorption, e.g. chromatography characterised by the separation mechanism
- B01D15/36—Selective adsorption, e.g. chromatography characterised by the separation mechanism involving ionic interaction, e.g. ion-exchange, ion-pair, ion-suppression or ion-exclusion
- B01D15/361—Ion-exchange
- B01D15/362—Cation-exchange
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/22—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against growth factors ; against growth regulators
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/24—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against cytokines, lymphokines or interferons
- C07K16/244—Interleukins [IL]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/26—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against hormones ; against hormone releasing or inhibiting factors
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2863—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against receptors for growth factors, growth regulators
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2866—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against receptors for cytokines, lymphokines, interferons
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/31—Immunoglobulins specific features characterized by aspects of specificity or valency multispecific
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- Immunology (AREA)
- General Health & Medical Sciences (AREA)
- Genetics & Genomics (AREA)
- Biophysics (AREA)
- Molecular Biology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biochemistry (AREA)
- Analytical Chemistry (AREA)
- Microbiology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Mycology (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Endocrinology (AREA)
- Peptides Or Proteins (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
Description
タンパク質、特に免疫グロブリンは、今日の医療ポートフォリオにおいて重要な役割を果たしている。医薬用途で使用するためのポリペプチドは主に、CHO細胞、NS0細胞、Sp2/0細胞、COS細胞、HEK細胞、BHK細胞、PER.C6(登録商標)細胞などの哺乳動物細胞において産生されている。
- 非イオン性ポリマーと添加剤とを含む溶液を、抗体が吸着されたクロマトグラフィー材料にアプライする工程であって、単量体形態の抗体がイオン交換クロマトグラフィー材料に吸着されたままである、工程、ならびに、
- 非イオン性ポリマーと添加剤と溶出化合物とを含む溶液をアプライすることによって、イオン交換クロマトグラフィー材料から単量体形態の抗体を回収し、それによって単量体形態の抗体を産生する工程
を含む、単量体形態の抗体を産生するための方法である。
- 非イオン性ポリマーと添加剤とを含む溶液を、ポリペプチドが吸着されたクロマトグラフィー材料にアプライする工程であって、単量体形態のポリペプチドがイオン交換クロマトグラフィー材料に吸着されたままである、工程、および
- 非イオン性ポリマーと添加剤と溶出化合物とを含む溶液をアプライすることによって、イオン交換クロマトグラフィー材料から単量体形態のポリペプチドを回収し、それによって宿主細胞タンパク質含量を低減させたポリペプチド調製物を産生する工程
を含む、宿主細胞タンパク質含量を低減させたポリペプチド調製物を産生するための方法であって、
該調製物は、哺乳動物細胞の培養上清、特にCHO細胞の培養上清から得られるものである。
- 添加剤が存在しない溶液中で、ポリペプチドの50%未満が溶液中に溶解して残存する非イオン性ポリマーの濃度を決定する工程、および
- 前工程で決定された濃度の非イオン性ポリマーが存在する溶液中で、ポリペプチドの95%超が溶液中に溶解して残存する添加剤の濃度を決定する工程
を含む、ポリペプチドのイオン交換クロマトグラフィーで使用するための非イオン性ポリマーおよび添加剤の濃度を決定するための方法であって、
それによって非イオン性ポリマーおよび添加剤の濃度を決定する。
- 非イオン性ポリマーと添加剤と溶出化合物とを含む溶液をアプライすることによって、イオン交換クロマトグラフィー材料から単量体形態の抗体を回収し、それによって単量体形態の抗体を産生する工程
を含む、単量体形態の抗体を産生するための方法であって、
ここで、クロマトグラフィーの分離効率(分離度)は、非イオン性ポリマーの非存在下でのクロマトグラフィーに比べて向上し、かつ
非イオン性ポリマーの採用された濃度により、添加剤の非存在下において、抗体の部分的または完全な沈殿がもたらされる。
- 非イオン性ポリマーと添加剤とを任意で含む第1の溶液をイオン交換クロマトグラフィー材料にアプライし、それによってイオン交換クロマトグラフィー材料を平衡化する工程、
- 平衡化したクロマトグラフィー材料にポリペプチドを含む緩衝溶液をアプライし、それによってポリペプチドをクロマトグラフィー材料に吸着させる工程であって、該溶液が非イオン性ポリマーおよび添加剤を本質的に含まない、工程、
- 非イオン性ポリマーと添加剤とを含む緩衝溶液をクロマトグラフィー材料にアプライする工程であって、単量体形態のポリペプチドがイオン交換クロマトグラフィー材料に吸着されたままである、工程、および
- 非イオン性ポリマーと添加剤と溶出化合物とを含む溶液をアプライすることによって、イオン交換クロマトグラフィー材料から単量体形態のポリペプチドを回収する工程
を含む。
[本発明1001]
- ポリ(エチレングリコール)と、ソルビトール、キシリトール、グリセロール、グリシン、ベタイン、プロリン、フルクトース、グルコース、およびスクロースを含む群より選択される1種またはそれ以上の添加剤とを含む溶液を、IgGクラスの抗体が吸着されたカチオン交換クロマトグラフィー材料にアプライする工程であって、単量体形態のIgGクラスの抗体がカチオン交換クロマトグラフィー材料に吸着されたままである、工程、ならびに
- ポリ(エチレングリコール)と前記1種またはそれ以上の添加剤とを含む溶液をアプライすることによって、カチオン交換クロマトグラフィー材料から単量体形態のIgGクラスの抗体を回収する工程
を含む、単量体形態のIgGクラスの抗体を産生するための方法であって、
ポリ(エチレングリコール)ポリマーが、約5〜15重量%の濃度を有し、かつ/または前記添加剤が、3〜25重量%の濃度を有する、方法。
[本発明1002]
- ポリ(エチレングリコール)と、ソルビトール、キシリトール、グリセロール、グリシン、ベタイン、プロリン、フルクトース、グルコース、およびスクロースを含む群より選択される1種またはそれ以上の添加剤とを含む溶液を、IgGクラスの抗体が吸着されたカチオン交換クロマトグラフィー材料にアプライする工程であって、単量体形態のIgGクラスの抗体がカチオン交換クロマトグラフィー材料に吸着されたままである、工程、ならびに
- ポリ(エチレングリコール)と、ソルビトール、キシリトール、グリセロール、グリシン、ベタイン、プロリン、フルクトース、グルコース、およびスクロースを含む群より選択される1種またはそれ以上の添加剤と、溶出化合物とを含む溶液をアプライすることによって、カチオン交換クロマトグラフィー材料から単量体形態のIgGクラスの抗体を回収し、それによって、宿主細胞タンパク質含量を低減させたIgGクラスの抗体調製物を産生する工程
を含む、宿主細胞タンパク質含量を低減させたIgGクラスの抗体調製物を産生するための方法であって、
ポリ(エチレングリコール)が、約5〜15重量%の濃度を有し、かつ/または前記添加剤が、3〜25重量%の濃度を有する、方法。
[本発明1003]
ポリ(エチレングリコール)が約7〜13重量%の濃度を有し、かつ/または前記添加剤が3〜25重量%の濃度を有することを特徴とする、前記本発明のいずれかの方法。
[本発明1004]
ポリ(エチレングリコール)が約7〜13重量%の濃度を有し、かつ/または前記添加剤が12〜25重量%の濃度を有することを特徴とする、前記本発明のいずれかの方法。
[本発明1005]
ポリ(エチレングリコール)が約7〜13重量%の濃度を有し、かつ/または前記添加剤が12〜20重量%の濃度を有することを特徴とする、前記本発明のいずれかの方法。
[本発明1006]
ポリ(エチレングリコール)が約3,500 Da±20%の分子量を有することを特徴とする、前記本発明のいずれかの方法。
[本発明1007]
前記添加剤がソルビトールであることを特徴とする、前記本発明のいずれかの方法。
[本発明1008]
単量体形態の抗体が100 kDa〜200 kDaの分子量を有することを特徴とする、前記本発明のいずれかの方法。
[本発明1009]
- ポリ(エチレングリコール)と、ソルビトール、キシリトール、グリセロール、グリシン、ベタイン、プロリン、フルクトース、グルコース、およびスクロースを含む群より選択される1種またはそれ以上の添加剤とを任意で含む第1の溶液を、カチオン交換クロマトグラフィー材料にアプライし、それによって該材料を平衡化する工程、
- 平衡化した該クロマトグラフィー材料にIgGクラスの抗体を含む溶液をアプライし、それによって該クロマトグラフィー材料にロードする工程、
- ポリ(エチレングリコール)と、ソルビトール、キシリトール、グリセロール、グリシン、ベタイン、プロリン、フルクトース、グルコース、およびスクロースを含む群より選択される1種またはそれ以上の添加剤とを含む溶液を、該クロマトグラフィー材料にアプライし、それによって、単量体形態のIgGクラスの抗体を該クロマトグラフィー材料から脱着/溶出することにより、単量体形態のIgGクラスの抗体を産生する工程
をさらに含むことを特徴とする、前記本発明のいずれかの方法。
本明細書には、単量体形態の関心対象ポリペプチドを、凝集形態の関心対象ポリペプチドなどの他の成分から分離することによって、単量体形態の関心対象ポリペプチドを産生するための、少なくとも1つのクロマトグラフィー工程を含む方法が報告される。一態様において、方法は、関心対象のポリペプチドを含む溶液とカチオン交換クロマトグラフィー材料とを接触させる工程を含み、その際、クロマトグラフィー材料との接触工程は非イオン性ポリマーおよび添加剤の非存在下で行われ、かつ回収工程は非イオン性ポリマーおよび添加剤の存在下で行われる。
(1) 疎水性:ノルロイシン, Met, Ala, Val, Leu, Ile;
(2) 中性親水性:Cys, Ser, Thr, Asn, Gln;
(3) 酸性:Asp, Glu;
(4) 塩基性:His, Lys, Arg;
(5) 鎖配向に影響を及ぼす残基:Gly, Pro;
(6) 芳香族:Trp, Tyr, Phe。
- 添加剤が存在しない溶液中で、ポリペプチドの50%未満が溶液中に残存する非イオン性ポリマーの濃度を決定する工程、
- 前工程で決定された濃度の非イオン性ポリマーが存在する溶液中で、ポリペプチドの95%超が溶液中に残存する添加剤の濃度を決定する工程、
を含み、それによって、非イオン性ポリマーおよび添加剤の濃度を決定する。
- 非イオン性ポリマーと添加剤とを含む溶液を、抗体が吸着されたクロマトグラフィー材料にアプライする工程であって、単量体形態の抗体がイオン交換クロマトグラフィー材料に吸着されたままである、工程、および
- 非イオン性ポリマーと添加剤と溶出化合物とを含む溶液をアプライすることによって、イオン交換クロマトグラフィー材料から単量体形態の抗体を回収し、それによって宿主細胞タンパク質含量を低減させた抗体調製物を産生する工程
を含む。
a)抗体をコードする核酸を含む哺乳動物細胞を培養し、該細胞または培養培地から抗体を回収する工程、
b)以下の工程:
- 非イオン性ポリマーと添加剤とを含む溶液を、抗体が吸着されたクロマトグラフィー材料にアプライする工程であって、単量体形態の抗体がイオン交換クロマトグラフィー材料に吸着されたままである、工程、および
- 非イオン性ポリマーと添加剤と溶出化合物とを含む溶液をアプライすることによって、イオン交換クロマトグラフィー材料から単量体形態の抗体を回収し、それによって抗体を産生する工程
を含むカチオン交換クロマトグラフィー法で抗体を精製する工程
を含む。
- クロマトグラフィーカラムに充填されたクロマトグラフィー材料を平衡化するサブ工程、
- 平衡化したクロマトグラフィー材料に、関心対象のポリペプチドを含む溶液を、クロマトグラフィー材料への該ポリペプチドの吸着/結合に適した条件下でアプライし、それによってクロマトグラフィーカラムにロードするサブ工程、
- 必要に応じて、クロマトグラフィー材料から該ポリペプチドを脱着/溶出することなく、クロマトグラフィー材料を洗浄するサブ工程、
- 回収溶液をクロマトグラフィー材料にアプライし、それによってクロマトグラフィー材料から該ポリペプチドを脱着/溶出することによって、関心対象のポリペプチドを回収するサブ工程。
a)該抗体をコードする核酸を含む哺乳動物細胞を培養し、該細胞または培養培地から該抗体を回収する工程、
b)以下の工程:
- 非イオン性ポリマーと添加剤とを含む溶液を、該抗体が吸着されたクロマトグラフィー材料にアプライする工程であって、単量体形態の4本鎖完全長抗体がイオン交換クロマトグラフィー材料に吸着されたままである、工程、および
- 非イオン性ポリマーと添加剤と溶出化合物とを含む溶液をアプライすることによって、イオン交換クロマトグラフィー材料から単量体形態の4本鎖完全長抗体を回収し、それによって該抗体を産生する工程
を含むカチオン交換クロマトグラフィー法で該抗体を精製する工程
を含む。
- 非イオン性ポリマーと添加剤とを任意で含む第1の溶液をイオン交換クロマトグラフィー材料にアプライし、それによってイオン交換クロマトグラフィー材料を平衡化する工程、
- 平衡化したクロマトグラフィー材料にポリペプチドを含む緩衝溶液をアプライし、それによってポリペプチドをクロマトグラフィー材料に吸着させる工程であって、該溶液が非イオン性ポリマーおよび添加剤を本質的に含まない、工程、
- 非イオン性ポリマーと添加剤とを含む緩衝溶液をクロマトグラフィー材料にアプライする工程であって、単量体形態のポリペプチドがイオン交換クロマトグラフィー材料に吸着されたままである、工程、ならびに
- 非イオン性ポリマーと添加剤と溶出化合物とを含む溶液をアプライすることによって、イオン交換クロマトグラフィー材料から単量体形態のポリペプチドを回収する工程
を含む。一態様では、回収する工程は勾配溶出により行う。
各抗体(抗IL17抗体:配列についてはWO 2010/034443参照;抗CSF-1R抗体:配列についてはPCT/EP2010/069090参照;抗Ang2/VEGF抗体:配列についてはWO 2010/040508参照)は第1段階においてプロテインAアフィニティクロマトグラフィーにより精製した。プロテインAカラムからの溶出は酸性条件下で実施した。その後サンプルを1Mクエン酸で約pH3.5に調整し、約1時間インキュベートした。続いて、1M TRIS/HCl, pH8〜9または1M TRIS溶液(TRIS:トリス-ヒドロキシメチル-アミノ-メタン)を加えることによってpHを5.0または5.5に調整した。4℃で12〜18時間インキュベートした後、サンプルを深層濾過した。このサンプルは5mg/ml〜20 mg/mlのタンパク質濃度を有する溶液である。この物質は以下では調整済みプロテインA溶出液と呼ばれ、カチオン交換クロマトグラフィー材料にロードするために調製された溶出液である。
クロマトグラフィー条件
ポリペプチド: 抗IL17抗体
交換材料: Poros 50HS
カラム: 内径8mm、長さ100mm、体積5.03ml
流速: 90cm/h(=0.75ml/分)
平衡化溶液: 10mMクエン酸ナトリウム緩衝液、pH5.0に調整、4カラム体積
ローディング: クロマトグラフィー材料1リットルあたり20gのタンパク質
洗浄液1: 10mMクエン酸ナトリウム緩衝液、pH5.0に調整、1カラム体積
洗浄液2: 10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、15%(w/w) D-ソルビトール、pH5.0に調整
溶出液: 750mM塩化ナトリウムを含有する、10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、15%(w/w) D-ソルビトール、pH5.0に調整
溶出法: 0%(v/v)から100%(v/v)溶出液までの線形勾配、22.5カラム体積
クロマトグラフィー条件
ポリペプチド: 抗CSF-1R抗体
クロマトグラフィー条件
ポリペプチド: 抗IL17抗体
平衡化溶液: 35mM酢酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、15%(w/w) D-ソルビトール、pH5.0に調整、4カラム体積
ローディング: クロマトグラフィー材料1リットルあたり20gのタンパク質
洗浄液: 35mM酢酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、15%(w/w) D-ソルビトール、pH5.0に調整、1カラム体積
溶出液: 750mM塩化ナトリウムを含有する、35mM酢酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、15%(w/w) D-ソルビトール、pH5.0に調整、
溶出法: 0%(v/v)から100%(v/v)溶出液までの線形勾配、22.5カラム体積
クロマトグラフィー条件
ポリペプチド: 抗IL17抗体
平衡化溶液: 25mM MES緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、15%(w/w) D-ソルビトール、pH5.5に調整、4カラム体積
ローディング: クロマトグラフィー材料1リットルあたり20gのタンパク質
洗浄液: 35mM MES緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、15%(w/w) D-ソルビトール、pH5.5に調整、4カラム体積
溶出液: 750mM塩化ナトリウムを含有する、35mM MES緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、15%(w/w) D-ソルビトール、pH5.5に調整、
溶出法: 0%(v/v)から100%(v/v)溶出液までの線形勾配、22.5カラム体積
クロマトグラフィー条件
ポリペプチド: 抗IL17抗体
交換材料: SP Sepharose FF
平衡化溶液: 30mMクエン酸ナトリウム緩衝液、pH5.0に調整、4カラム体積
ローディング: クロマトグラフィー材料1リットルあたり20gのタンパク質
洗浄液1: 30mMクエン酸ナトリウム緩衝液、pH5.0に調整、1カラム体積
洗浄液2: 30mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、15%(w/w) D-ソルビトール、pH5.0に調整
溶出液: 750mM塩化ナトリウムを含有する、30mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、15%(w/w) D-ソルビトール、pH5.0に調整
溶出法: 0%(v/v)から100%(v/v)溶出液までの線形勾配、22.5カラム体積
クロマトグラフィー条件
ポリペプチド: 抗IL17抗体
交換材料: Toyopearl CM-650 M
平衡化溶液: 30mMクエン酸ナトリウム緩衝液、pH5.0に調整、4カラム体積
ローディング: クロマトグラフィー材料1リットルあたり20gのタンパク質
洗浄液1: 30mMクエン酸ナトリウム緩衝液、pH5.0に調整、1カラム体積
洗浄液2: 30mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、15%(w/w) D-ソルビトール、pH5.0に調整
溶出液: 750mM塩化ナトリウムを含有する、30mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、15%(w/w) D-ソルビトール、pH5.0に調整
溶出法: 0%(v/v)から100%(v/v)溶出液までの線形勾配、22.5カラム体積
クロマトグラフィー条件
ポリペプチド: 抗IL17抗体
交換材料: CM Sepharose FF
平衡化溶液: 30mMクエン酸ナトリウム緩衝液、pH5.0に調整、4カラム体積
ローディング: クロマトグラフィー材料1リットルあたり20gのタンパク質
洗浄液1: 30mMクエン酸ナトリウム緩衝液、pH5.0に調整、1カラム体積
洗浄液2: 30mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、15%(w/w) D-ソルビトール、pH5.0に調整
溶出液: 750mM塩化ナトリウムを含有する、30mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、15%(w/w) D-ソルビトール、pH5.0に調整
溶出法: 0%(v/v)から100%(v/v)溶出液までの線形勾配、22.5カラム体積
クロマトグラフィー条件
ポリペプチド: 抗IL17抗体
平衡化溶液: 10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、20%(w/w)キシリトール、pH5.0に調整、2カラム体積
ローディング: クロマトグラフィー材料1リットルあたり20gのタンパク質
洗浄液: 10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、20%(w/w)キシリトール、pH5.0に調整、4カラム体積
溶出液: 750mM塩化ナトリウムを含有する、10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、20%(w/w)キシリトール、pH5.0に調整
溶出法: 0%(v/v)から100%(v/v)溶出液までの線形勾配、22.5カラム体積
クロマトグラフィー条件
ポリペプチド: 抗CSF-1R抗体
平衡化溶液: 10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、20%(w/w)キシリトール、pH5.0に調整、2カラム体積
ローディング: クロマトグラフィー材料1リットルあたり20gのタンパク質
洗浄液: 10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、20%(w/w)キシリトール、pH5.0に調整、4カラム体積
溶出液: 750mM塩化ナトリウムを含有する、10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、20%(w/w)キシリトール、pH5.0に調整
溶出法: 0%(v/v)から100%(v/v)溶出液までの線形勾配、22.5カラム体積
クロマトグラフィー条件
ポリペプチド: 抗IL17抗体
平衡化溶液: 10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、30%(w/w)グリセロール、pH5.0に調整、2カラム体積
ローディング: クロマトグラフィー材料1リットルあたり20gのタンパク質
洗浄液: 10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、30%(w/w)グリセロール、pH5.0に調整、4カラム体積
溶出液: 750mM塩化ナトリウムを含有する、10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、30%(w/w)グリセロール、pH5.0に調整
溶出法: 0%(v/v)から100%(v/v)溶出液までの線形勾配、22.5カラム体積
クロマトグラフィー条件
ポリペプチド: 抗CSF-1R抗体
平衡化溶液: 10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、30%(w/w)グリセロール、pH5.0に調整、2カラム体積
ローディング: クロマトグラフィー材料1リットルあたり20gのタンパク質
洗浄液: 10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、30%(w/w)グリセロール、pH5.0に調整、4カラム体積
溶出液: 750mM塩化ナトリウムを含有する、10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、30%(w/w)グリセロール、pH5.0に調整
溶出法: 0%(v/v)から100%(v/v)溶出液までの線形勾配、22.5カラム体積
クロマトグラフィー条件
ポリペプチド: 抗IL17抗体
平衡化溶液: 10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、25%(w/w)サッカロース、pH5.0に調整、2カラム体積
ローディング: クロマトグラフィー材料1リットルあたり20gのタンパク質
洗浄液: 10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、25%(w/w)サッカロース、pH5.0に調整、4カラム体積
溶出液: 750mM塩化ナトリウムを含有する、10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、25%(w/w)サッカロース、pH5.0に調整
溶出法: 0%(v/v)から100%(v/v)溶出液までの線形勾配、22.5カラム体積
クロマトグラフィー条件
ポリペプチド: 抗CSF-1R抗体
平衡化溶液: 10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、25%(w/w)サッカロース、pH5.0に調整、2カラム体積
ローディング: クロマトグラフィー材料1リットルあたり20gのタンパク質
洗浄液: 10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、25%(w/w)サッカロース、pH5.0に調整、4カラム体積
溶出液: 750mM塩化ナトリウムを含有する、10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、25%(w/w)サッカロース、pH5.0に調整
溶出法: 0%(v/v)から100%(v/v)溶出液までの線形勾配、22.5カラム体積
クロマトグラフィー条件
ポリペプチド: 抗IL17抗体
平衡化溶液: 10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、25%(w/w) D-フルクトース、pH5.0に調整、2カラム体積
ローディング: クロマトグラフィー材料1リットルあたり20gのタンパク質
洗浄液: 10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、25%(w/w) D-フルクトース、pH5.0に調整、4カラム体積
溶出液: 750mM塩化ナトリウムを含有する、10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、25%(w/w) D-フルクトース、pH5.0に調整
溶出法: 0%(v/v)から100%(v/v)溶出液までの線形勾配、22.5カラム体積
クロマトグラフィー条件
ポリペプチド: 抗CSF-1R抗体
平衡化溶液: 10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、25%(w/w) D-フルクトース、pH5.0に調整、2カラム体積
ローディング: クロマトグラフィー材料1リットルあたり20gのタンパク質
洗浄液: 10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、25%(w/w) D-フルクトース、pH5.0に調整、4カラム体積
溶出液: 750mM塩化ナトリウムを含有する、10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、25%(w/w) D-フルクトース、pH5.0に調整
溶出法: 0%(v/v)から100%(v/v)溶出液までの線形勾配、22.5カラム体積
クロマトグラフィー条件
ポリペプチド: 抗IL17抗体
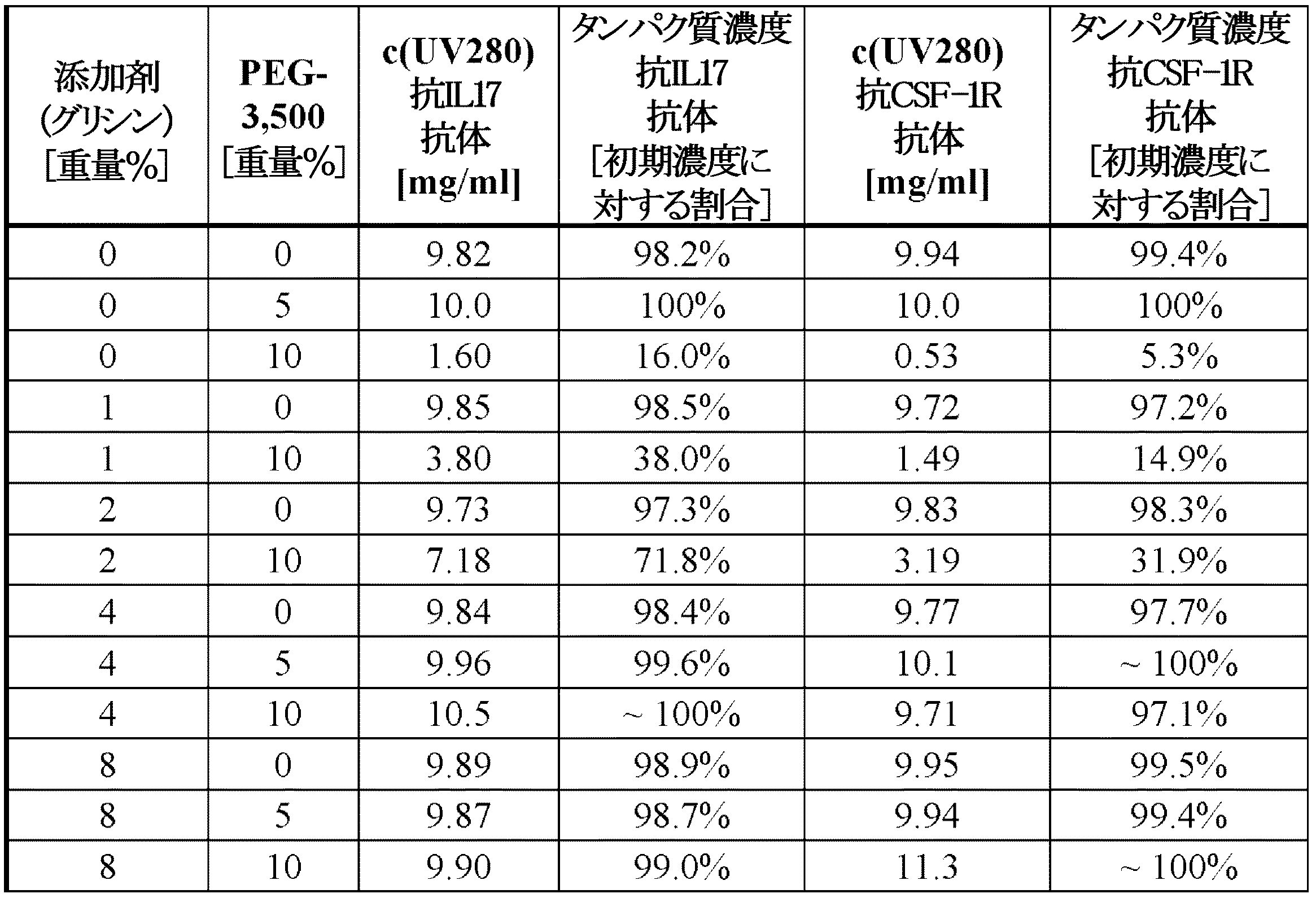
平衡化溶液: 10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、8%(w/w)グリシン、pH5.0に調整、2カラム体積
ローディング: クロマトグラフィー材料1リットルあたり20gのタンパク質
洗浄液: 10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、8%(w/w)グリシン、pH5.0に調整、4カラム体積
溶出液: 750mM塩化ナトリウムを含有する、10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、8%(w/w)グリシン、pH5.0に調整
溶出法: 0%(v/v)から100%(v/v)溶出液までの線形勾配、22.5カラム体積
クロマトグラフィー条件
ポリペプチド: 抗CSF-1R抗体
平衡化溶液: 10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、8%(w/w)グリシン、pH5.0に調整、2カラム体積
ローディング: クロマトグラフィー材料1リットルあたり20gのタンパク質
洗浄液: 10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、8%(w/w)グリシン、pH5.0に調整、4カラム体積
溶出液: 750mM塩化ナトリウムを含有する、10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、8%(w/w)グリシン、pH5.0に調整
溶出法: 0%(v/v)から100%(v/v)溶出液までの線形勾配、22.5カラム体積
クロマトグラフィー条件
ポリペプチド: 抗IL17抗体
平衡化溶液: 10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、8%(w/w) L-プロリン、pH5.0に調整、2カラム体積
ローディング: クロマトグラフィー材料1リットルあたり20gのタンパク質
洗浄液: 10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、8%(w/w) L-プロリン、pH5.0に調整、4カラム体積
溶出液: 750mM塩化ナトリウムを含有する、10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、8%(w/w) L-プロリン、pH5.0に調整
溶出法: 0%(v/v)から100%(v/v)溶出液までの線形勾配、22.5カラム体積
クロマトグラフィー条件
ポリペプチド: 抗CSF-1R抗体
平衡化溶液: 10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、8%(w/w) L-プロリン、pH5.0に調整、2カラム体積
ローディング: クロマトグラフィー材料1リットルあたり20gのタンパク質
洗浄液: 10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、8%(w/w) L-プロリン、pH5.0に調整、4カラム体積
溶出液: 750mM塩化ナトリウムを含有する、10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、8%(w/w) L-プロリン、pH5.0に調整
溶出法: 0%(v/v)から100%(v/v)溶出液までの線形勾配、22.5カラム体積
クロマトグラフィー条件
ポリペプチド: 抗IL17抗体
平衡化溶液: 10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、8%(w/w)ベタイン、pH5.0に調整、2カラム体積
ローディング: クロマトグラフィー材料1リットルあたり20gのタンパク質
洗浄液: 10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、8%(w/w)ベタイン、pH5.0に調整、4カラム体積
溶出液: 750mM塩化ナトリウムを含有する、10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、8%(w/w)ベタイン、pH5.0に調整
溶出法: 0%(v/v)から100%(v/v)溶出液までの線形勾配、22.5カラム体積
クロマトグラフィー条件
ポリペプチド: 抗CSF-1R抗体
平衡化溶液: 10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、8%(w/w)ベタイン、pH5.0に調整、2カラム体積
ローディング: クロマトグラフィー材料1リットルあたり20gのタンパク質
洗浄液: 10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、8%(w/w)ベタイン、pH5.0に調整、4カラム体積
溶出液: 750mM塩化ナトリウムを含有する、10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 3,500 Da)、8%(w/w)ベタイン、pH5.0に調整
溶出法: 0%(v/v)から100%(v/v)溶出液までの線形勾配、22.5カラム体積
クロマトグラフィー条件
ポリペプチド: 抗IL17抗体
平衡化溶液: 10mMクエン酸ナトリウム緩衝液、pH5.0に調整、2カラム体積
ローディング: クロマトグラフィー材料1リットルあたり20gのタンパク質
洗浄液: 10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 400 Da)、15%(w/w)ソルビトール、pH5.0に調整、4カラム体積
溶出液: 750mM塩化ナトリウムを含有する、10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 400 Da)、15%(w/w)ソルビトール、pH5.0に調整
溶出法: 0%(v/v)から100%(v/v)溶出液までの線形勾配、22.5カラム体積
クロマトグラフィー条件
ポリペプチド: 抗IL17抗体
平衡化溶液: 10mMクエン酸ナトリウム緩衝液、pH5.0に調整、2カラム体積
ローディング: クロマトグラフィー材料1リットルあたり20gのタンパク質
洗浄液: 10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 10,000 Da)、15%(w/w)ソルビトール、pH5.0に調整、4カラム体積
溶出液: 750mM塩化ナトリウムを含有する、10mMクエン酸ナトリウム緩衝液、10%(w/w)ポリ(エチレングリコール)(MW 10,000 Da)、15%(w/w)ソルビトール、pH5.0に調整
溶出法: 0%(v/v)から100%(v/v)溶出液までの線形勾配、30カラム体積
クロマトグラフィー条件
ポリペプチド: 抗Ang2/VEGF抗体
交換材料: Poros 50HS
カラム: 内径11mm、長さ250mm、体積23ml
流速: 90cm/h
平衡化溶液: 40mMリン酸ナトリウム緩衝液、pH5.0に調整、3カラム体積
ローディング: クロマトグラフィー材料1リットルあたり20gのタンパク質
洗浄液: 40mMリン酸ナトリウム緩衝液、pH5.0に調整、3カラム体積
溶出液: 40mMリン酸ナトリウム緩衝液、pH7.5に調整
溶出法: 0%(v/v)から100%(v/v)溶出液までの線形勾配、12カラム体積
クロマトグラフィー条件
ポリペプチド: 抗Ang2/VEGF抗体
交換材料: Poros 50HS
カラム: 内径11mm、長さ250mm、体積23ml
流速: 90cm/h
平衡化溶液: 40mMリン酸ナトリウム緩衝液、5%PEG 4000、pH5.0に調整、3カラム体積
ローディング: クロマトグラフィー材料1リットルあたり20gのタンパク質
洗浄液: 40mMリン酸ナトリウム緩衝液、5%PEG 4000、pH5.0に調整、3カラム体積
溶出液: 40mMリン酸ナトリウム緩衝液、5%PEG 4000、pH7.5に調整
溶出法: 0%(v/v)から100%(v/v)溶出液までの線形勾配、12カラム体積
クロマトグラフィー条件
ポリペプチド: 抗Ang2/VEGF抗体
交換材料: Poros 50HS
カラム: 内径11mm、長さ250mm、体積23ml
流速: 90cm/h
平衡化溶液: 40mMリン酸ナトリウム緩衝液、pH5.0に調整、3カラム体積
ローディング: クロマトグラフィー材料1リットルあたり20gのタンパク質
洗浄液: 40mMリン酸ナトリウム緩衝液、10%PEG 4000、8%グリシン、pH5.0に調整、3カラム体積
溶出液: 40mMリン酸ナトリウム緩衝液、10%PEG 4000、8%グリシン、pH7.5に調整
溶出法: 0%(v/v)から100%(v/v)溶出液までの線形勾配、12カラム体積
Claims (5)
- - ポリ(エチレングリコール)とグリシンとを任意で含む第1の溶液を、カチオン交換クロマトグラフィー材料にアプライし、それによって該材料を平衡化する工程、
- 平衡化した該クロマトグラフィー材料にIgGクラスの抗体を含む溶液をアプライし、それによって該クロマトグラフィー材料にロードする工程、および
- ポリ(エチレングリコール)とグリシンとを含む溶液を、該クロマトグラフィー材料にアプライし、それによって、単量体形態のIgGクラスの抗体を該クロマトグラフィー材料から脱着/溶出することにより、単量体形態のIgGクラスの抗体を産生する工程
を含む、単量体形態のIgGクラスの抗体を産生するための方法であって、
ポリ(エチレングリコール)が、5〜15重量%の濃度を有し、かつグリシンが、4〜8重量%の濃度を有する、前記方法。 - - ポリ(エチレングリコール)とグリシンとを任意で含む第1の溶液を、カチオン交換クロマトグラフィー材料にアプライし、それによって該材料を平衡化する工程、
- 平衡化した該クロマトグラフィー材料にIgGクラスの抗体を含む溶液をアプライし、それによって該クロマトグラフィー材料にロードする工程、および
- ポリ(エチレングリコール)とグリシンとを含む溶液を、該クロマトグラフィー材料にアプライし、それによって、単量体形態のIgGクラスの抗体を該クロマトグラフィー材料から脱着/溶出することにより、単量体形態のIgGクラスの抗体を産生する工程
を含む、宿主細胞タンパク質含量を低減させたIgGクラスの抗体調製物を産生するための方法であって、
ポリ(エチレングリコール)が、5〜15重量%の濃度を有し、かつグリシンが、4〜8重量%の濃度を有する、前記方法。 - ポリ(エチレングリコール)が、7〜13重量%の濃度を有する、請求項1から2のいずれか一項記載の方法。
- ポリ(エチレングリコール)が3,500 Da±20%の分子量を有することを特徴とする、請求項1から3のいずれか一項記載の方法。
- 単量体形態の抗体が100 kDa〜200 kDaの分子量を有することを特徴とする、請求項1から4のいずれか一項記載の方法。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP11158523 | 2011-03-16 | ||
| EP11158523.8 | 2011-03-16 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013558420A Division JP5984854B2 (ja) | 2011-03-16 | 2012-03-14 | 移動相の調整によって、ポリペプチド単量体、凝集物およびフラグメントを分離するための選択性を向上させた、イオン交換クロマトグラフィー |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018000397A Division JP6523491B2 (ja) | 2011-03-16 | 2018-01-05 | 移動相の調整によって、ポリペプチド単量体、凝集物およびフラグメントを分離するための選択性を向上させた、イオン交換クロマトグラフィー |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2017019805A JP2017019805A (ja) | 2017-01-26 |
| JP6273326B2 true JP6273326B2 (ja) | 2018-01-31 |
Family
ID=45819216
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013558420A Active JP5984854B2 (ja) | 2011-03-16 | 2012-03-14 | 移動相の調整によって、ポリペプチド単量体、凝集物およびフラグメントを分離するための選択性を向上させた、イオン交換クロマトグラフィー |
| JP2016151624A Active JP6273326B2 (ja) | 2011-03-16 | 2016-08-02 | 移動相の調整によって、ポリペプチド単量体、凝集物およびフラグメントを分離するための選択性を向上させた、イオン交換クロマトグラフィー |
| JP2018000397A Active JP6523491B2 (ja) | 2011-03-16 | 2018-01-05 | 移動相の調整によって、ポリペプチド単量体、凝集物およびフラグメントを分離するための選択性を向上させた、イオン交換クロマトグラフィー |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013558420A Active JP5984854B2 (ja) | 2011-03-16 | 2012-03-14 | 移動相の調整によって、ポリペプチド単量体、凝集物およびフラグメントを分離するための選択性を向上させた、イオン交換クロマトグラフィー |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018000397A Active JP6523491B2 (ja) | 2011-03-16 | 2018-01-05 | 移動相の調整によって、ポリペプチド単量体、凝集物およびフラグメントを分離するための選択性を向上させた、イオン交換クロマトグラフィー |
Country Status (9)
| Country | Link |
|---|---|
| US (3) | US9394337B2 (ja) |
| EP (2) | EP3318571B1 (ja) |
| JP (3) | JP5984854B2 (ja) |
| ES (2) | ES2865449T3 (ja) |
| HR (2) | HRP20180028T4 (ja) |
| PL (2) | PL3318571T3 (ja) |
| SG (1) | SG193378A1 (ja) |
| SI (2) | SI3318571T1 (ja) |
| WO (1) | WO2012123488A1 (ja) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SI3318571T1 (sl) | 2011-03-16 | 2021-08-31 | F. Hoffmann-La Roche Ag | Ionska izmenjevalna kromatografija z izboljšano selektivnostjo za ločevanje polipeptidnih monomerov, agregatov in fragmentov s spremembo mobilne faze |
| WO2014018420A1 (en) * | 2012-07-21 | 2014-01-30 | K-Technologies, Inc. | Processes for the removal and recovery of minor elements in wet-process phosphoric acid |
| EP2970379B1 (en) | 2013-03-14 | 2019-05-01 | EMD Millipore Corporation | Methods of increasing protein purity using protein a based chromatography |
| GB2516808A (en) * | 2013-05-31 | 2015-02-11 | Innova Biosciences Ltd | Antibody composition and buffer system therefor |
| CA2919174A1 (en) * | 2013-08-19 | 2015-02-26 | F. Hoffmann-La Roche Ag | Separation of bispecific antibodies and bispecific antibody production side products using hydroxyapatite chromatography |
| CA3156648A1 (en) * | 2019-10-04 | 2021-04-08 | Merck Patent Gmbh | Elution of monoclonal antibodies in protein a affinity chromatography |
| KR20230123498A (ko) * | 2020-12-20 | 2023-08-23 | 리제너론 파아마슈티컬스, 인크. | 생체분자에서 스크램블된 디설파이드의 식별 방법 |
| CN113388026B (zh) * | 2021-08-03 | 2022-09-27 | 江西理工大学 | 一种螺旋藻藻蓝蛋白和藻油的同步提取方法 |
Family Cites Families (24)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5204244A (en) | 1987-10-27 | 1993-04-20 | Oncogen | Production of chimeric antibodies by homologous recombination |
| US5202238A (en) | 1987-10-27 | 1993-04-13 | Oncogen | Production of chimeric antibodies by homologous recombination |
| US5429746A (en) | 1994-02-22 | 1995-07-04 | Smith Kline Beecham Corporation | Antibody purification |
| DK1084136T3 (da) | 1998-06-01 | 2005-01-03 | Genentech Inc | Adskillelse af monomere af et antistof fra dets multimere ved anvendelse af ionbytterchromatografi |
| ES2421736T3 (es) * | 1998-06-09 | 2013-09-05 | Csl Behring Ag | Procedimiento para la preparación de inmunoglobulinas para administración intravenosa y otros productos inmunoglobulínicos |
| KR100501263B1 (ko) | 1998-06-09 | 2005-07-18 | 스태튼스 세룸 인스티튜트 | 정맥 주사용 면역글로불린의 제조 방법 및 그 외의 면역글로불린 제품 |
| DE19836213A1 (de) * | 1998-08-11 | 2000-02-24 | Gerhard Harry Scholz | Verfahren zur Elution von Biomolekülen von Chromatographie-Materialien |
| WO2004013162A2 (en) | 2002-08-06 | 2004-02-12 | Akzo Nobel Nv. | Increased dynamic binding capacity in ion exchange chromatography by addition of polyethylene glycol |
| CN1208346C (zh) | 2003-04-09 | 2005-06-29 | 中国科学院过程工程研究所 | 血红蛋白-人血清白蛋白偶联物制备血液代用品及其制备方法 |
| SE0400886D0 (sv) | 2004-04-02 | 2004-04-02 | Amersham Biosciences Ab | Process of purification |
| KR100554481B1 (ko) * | 2004-06-30 | 2006-03-03 | 씨제이 주식회사 | 반코마이신 염산염의 정제방법 |
| TWI320788B (en) | 2005-05-25 | 2010-02-21 | Hoffmann La Roche | Method for the purification of antibodies |
| US8124743B2 (en) * | 2006-06-01 | 2012-02-28 | President And Fellows Of Harvard College | Purification of a bivalently active antibody using a non-chromatographic method |
| US7691980B2 (en) | 2007-01-09 | 2010-04-06 | Bio-Rad Laboratories, Inc. | Enhanced capacity and purification of antibodies by mixed mode chromatography in the presence of aqueous-soluble nonionic organic polymers |
| EP2182943B1 (en) * | 2007-07-23 | 2016-10-26 | Janssen Biotech, Inc. | Methods and compositions for treating fibrosis related disorders using il-17 antagonists |
| CA2709354C (en) * | 2007-12-21 | 2014-06-17 | Amgen Inc. | Anti-amyloid antibodies and uses thereof |
| EP2242762B1 (en) | 2008-01-18 | 2015-12-16 | Bio-Rad Laboratories, Inc. | Enhanced purification of antibodies and antibody fragments by apatite chromatography |
| CA2726823A1 (en) | 2008-06-03 | 2009-12-10 | Patrys Limited | Process for purification of antibodies |
| NZ591484A (en) | 2008-09-29 | 2012-09-28 | Roche Glycart Ag | Antibodies against human il 17 and uses thereof |
| US8268314B2 (en) | 2008-10-08 | 2012-09-18 | Hoffmann-La Roche Inc. | Bispecific anti-VEGF/anti-ANG-2 antibodies |
| HUE028341T2 (en) | 2009-06-16 | 2016-12-28 | Genzyme Corp | Improved methods for purification of recombinant aav vectors |
| US8394922B2 (en) * | 2009-08-03 | 2013-03-12 | Medarex, Inc. | Antiproliferative compounds, conjugates thereof, methods therefor, and uses thereof |
| AR080793A1 (es) * | 2010-03-26 | 2012-05-09 | Roche Glycart Ag | Anticuerpos biespecificos |
| SI3318571T1 (sl) | 2011-03-16 | 2021-08-31 | F. Hoffmann-La Roche Ag | Ionska izmenjevalna kromatografija z izboljšano selektivnostjo za ločevanje polipeptidnih monomerov, agregatov in fragmentov s spremembo mobilne faze |
-
2012
- 2012-03-14 SI SI201231907T patent/SI3318571T1/sl unknown
- 2012-03-14 ES ES17201391T patent/ES2865449T3/es active Active
- 2012-03-14 EP EP17201391.4A patent/EP3318571B1/en active Active
- 2012-03-14 PL PL17201391T patent/PL3318571T3/pl unknown
- 2012-03-14 EP EP12708546.2A patent/EP2686334B2/en active Active
- 2012-03-14 JP JP2013558420A patent/JP5984854B2/ja active Active
- 2012-03-14 ES ES12708546T patent/ES2656167T5/es active Active
- 2012-03-14 SG SG2013067947A patent/SG193378A1/en unknown
- 2012-03-14 SI SI201231179T patent/SI2686334T2/sl unknown
- 2012-03-14 WO PCT/EP2012/054449 patent/WO2012123488A1/en not_active Ceased
- 2012-03-14 PL PL12708546T patent/PL2686334T5/pl unknown
- 2012-03-14 HR HRP20180028TT patent/HRP20180028T4/hr unknown
-
2013
- 2013-09-12 US US14/025,622 patent/US9394337B2/en active Active
-
2016
- 2016-06-16 US US15/184,883 patent/US10377793B2/en active Active
- 2016-08-02 JP JP2016151624A patent/JP6273326B2/ja active Active
-
2018
- 2018-01-05 JP JP2018000397A patent/JP6523491B2/ja active Active
-
2019
- 2019-06-24 US US16/450,827 patent/US20200148719A1/en not_active Abandoned
-
2021
- 2021-04-13 HR HRP20210588TT patent/HRP20210588T1/hr unknown
Also Published As
| Publication number | Publication date |
|---|---|
| SI2686334T2 (sl) | 2020-10-30 |
| SG193378A1 (en) | 2013-10-30 |
| EP2686334B2 (en) | 2020-07-01 |
| EP3318571B1 (en) | 2021-02-17 |
| EP3318571A1 (en) | 2018-05-09 |
| EP2686334B1 (en) | 2017-11-15 |
| ES2656167T3 (es) | 2018-02-23 |
| ES2865449T3 (es) | 2021-10-15 |
| WO2012123488A1 (en) | 2012-09-20 |
| EP2686334A1 (en) | 2014-01-22 |
| PL2686334T5 (pl) | 2020-10-19 |
| US10377793B2 (en) | 2019-08-13 |
| JP2018058900A (ja) | 2018-04-12 |
| ES2656167T5 (es) | 2021-03-26 |
| US9394337B2 (en) | 2016-07-19 |
| HRP20210588T1 (hr) | 2021-05-28 |
| JP5984854B2 (ja) | 2016-09-06 |
| US20200148719A1 (en) | 2020-05-14 |
| JP6523491B2 (ja) | 2019-06-05 |
| PL3318571T3 (pl) | 2021-07-05 |
| PL2686334T3 (pl) | 2018-03-30 |
| JP2017019805A (ja) | 2017-01-26 |
| HRP20180028T1 (hr) | 2018-02-09 |
| US20140081000A1 (en) | 2014-03-20 |
| HRP20180028T4 (hr) | 2020-10-02 |
| JP2014511829A (ja) | 2014-05-19 |
| SI3318571T1 (sl) | 2021-08-31 |
| US20170107249A1 (en) | 2017-04-20 |
| SI2686334T1 (en) | 2018-03-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6273326B2 (ja) | 移動相の調整によって、ポリペプチド単量体、凝集物およびフラグメントを分離するための選択性を向上させた、イオン交換クロマトグラフィー | |
| KR101921767B1 (ko) | 단백질 정제 | |
| JP5448825B2 (ja) | 非凝集抗体Fcドメインの製造方法 | |
| TWI625335B (zh) | 純化抗體的方法 | |
| US10246484B2 (en) | Method for purifying recombinant protein | |
| RU2586515C2 (ru) | Препарат антитела, обогащенного изоформами и способ его получения | |
| US20140371427A1 (en) | IgG2 DISULFIDE ISOFORM SEPARATION | |
| JP2016519144A (ja) | 最小限の単量体の分離を伴う組換えポリクローナル多量体の分離 | |
| TWI754898B (zh) | 眼用蛋白質藥物的精制方法 | |
| JP2016504337A (ja) | イオン交換クロマトグラフィーを使用して高マンノースグリコフォームのレベルを制御する方法 | |
| CN110724204B (zh) | Fc融合蛋白的纯化方法 | |
| KR20220101168A (ko) | 이온 교환 크로마토그래피 동안 항체의 수율을 증가시키는 방법 | |
| HK1186484B (en) | Isoform enriched antibody preparation and method for obtaining it |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20170626 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20170925 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20171207 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20180105 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6273326 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |