JP5964729B2 - リチウム電池用正極活物質、及び当該リチウム電池用正極活物質を含有するリチウム電池 - Google Patents
リチウム電池用正極活物質、及び当該リチウム電池用正極活物質を含有するリチウム電池 Download PDFInfo
- Publication number
- JP5964729B2 JP5964729B2 JP2012248749A JP2012248749A JP5964729B2 JP 5964729 B2 JP5964729 B2 JP 5964729B2 JP 2012248749 A JP2012248749 A JP 2012248749A JP 2012248749 A JP2012248749 A JP 2012248749A JP 5964729 B2 JP5964729 B2 JP 5964729B2
- Authority
- JP
- Japan
- Prior art keywords
- positive electrode
- active material
- electrode active
- lithium battery
- lithium
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 229910052744 lithium Inorganic materials 0.000 title claims description 102
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 title claims description 98
- 239000007774 positive electrode material Substances 0.000 title claims description 83
- 239000000203 mixture Substances 0.000 claims description 33
- 239000003792 electrolyte Substances 0.000 claims description 17
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical class [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 claims description 14
- 235000002639 sodium chloride Nutrition 0.000 claims description 14
- 239000011780 sodium chloride Substances 0.000 claims description 14
- 239000013078 crystal Substances 0.000 claims description 12
- 230000001788 irregular Effects 0.000 claims description 7
- 229910017698 Ni 1-x-y Co Inorganic materials 0.000 claims description 3
- PXHVJJICTQNCMI-UHFFFAOYSA-N nickel Substances [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 21
- 230000000052 comparative effect Effects 0.000 description 20
- 239000007773 negative electrode material Substances 0.000 description 20
- HBBGRARXTFLTSG-UHFFFAOYSA-N Lithium ion Chemical compound [Li+] HBBGRARXTFLTSG-UHFFFAOYSA-N 0.000 description 19
- 229910001416 lithium ion Inorganic materials 0.000 description 14
- 229910003002 lithium salt Inorganic materials 0.000 description 13
- 159000000002 lithium salts Chemical class 0.000 description 13
- 239000011230 binding agent Substances 0.000 description 11
- 239000011572 manganese Substances 0.000 description 11
- OGIDPMRJRNCKJF-UHFFFAOYSA-N titanium oxide Inorganic materials [Ti]=O OGIDPMRJRNCKJF-UHFFFAOYSA-N 0.000 description 11
- 238000006243 chemical reaction Methods 0.000 description 10
- 229910052751 metal Inorganic materials 0.000 description 9
- 239000004020 conductor Substances 0.000 description 8
- 239000000463 material Substances 0.000 description 8
- 239000002184 metal Substances 0.000 description 8
- 229910052759 nickel Inorganic materials 0.000 description 8
- 239000007784 solid electrolyte Substances 0.000 description 8
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 7
- 239000008151 electrolyte solution Substances 0.000 description 7
- 238000004519 manufacturing process Methods 0.000 description 7
- 239000002245 particle Substances 0.000 description 7
- 239000002994 raw material Substances 0.000 description 7
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 6
- 241000627951 Osteobrama cotio Species 0.000 description 6
- 229910017052 cobalt Inorganic materials 0.000 description 6
- 239000010941 cobalt Substances 0.000 description 6
- GUTLYIVDDKVIGB-UHFFFAOYSA-N cobalt atom Chemical compound [Co] GUTLYIVDDKVIGB-UHFFFAOYSA-N 0.000 description 6
- 239000000126 substance Substances 0.000 description 6
- 239000010936 titanium Substances 0.000 description 6
- 238000002441 X-ray diffraction Methods 0.000 description 5
- 239000011888 foil Substances 0.000 description 5
- 239000011245 gel electrolyte Substances 0.000 description 5
- 150000004677 hydrates Chemical class 0.000 description 5
- 238000005259 measurement Methods 0.000 description 5
- 229920000642 polymer Polymers 0.000 description 5
- -1 polytetrafluoroethylene Polymers 0.000 description 5
- 150000003624 transition metals Chemical class 0.000 description 5
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 4
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 4
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 4
- 238000009792 diffusion process Methods 0.000 description 4
- 238000010304 firing Methods 0.000 description 4
- 239000010439 graphite Substances 0.000 description 4
- 229910002804 graphite Inorganic materials 0.000 description 4
- AMWRITDGCCNYAT-UHFFFAOYSA-L hydroxy(oxo)manganese;manganese Chemical compound [Mn].O[Mn]=O.O[Mn]=O AMWRITDGCCNYAT-UHFFFAOYSA-L 0.000 description 4
- 229910052748 manganese Inorganic materials 0.000 description 4
- 238000000034 method Methods 0.000 description 4
- 239000011255 nonaqueous electrolyte Substances 0.000 description 4
- ZUHZGEOKBKGPSW-UHFFFAOYSA-N tetraglyme Chemical compound COCCOCCOCCOCCOC ZUHZGEOKBKGPSW-UHFFFAOYSA-N 0.000 description 4
- 229910052723 transition metal Inorganic materials 0.000 description 4
- 229910018871 CoO 2 Inorganic materials 0.000 description 3
- 229910021503 Cobalt(II) hydroxide Inorganic materials 0.000 description 3
- OIFBSDVPJOWBCH-UHFFFAOYSA-N Diethyl carbonate Chemical compound CCOC(=O)OCC OIFBSDVPJOWBCH-UHFFFAOYSA-N 0.000 description 3
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 3
- XTHFKEDIFFGKHM-UHFFFAOYSA-N Dimethoxyethane Chemical compound COCCOC XTHFKEDIFFGKHM-UHFFFAOYSA-N 0.000 description 3
- KMTRUDSVKNLOMY-UHFFFAOYSA-N Ethylene carbonate Chemical compound O=C1OCCO1 KMTRUDSVKNLOMY-UHFFFAOYSA-N 0.000 description 3
- 229910008699 Li2Ni1/3Co1/3Mn1/3TiO4 Inorganic materials 0.000 description 3
- PWHULOQIROXLJO-UHFFFAOYSA-N Manganese Chemical compound [Mn] PWHULOQIROXLJO-UHFFFAOYSA-N 0.000 description 3
- 239000002033 PVDF binder Substances 0.000 description 3
- UCKMPCXJQFINFW-UHFFFAOYSA-N Sulphide Chemical compound [S-2] UCKMPCXJQFINFW-UHFFFAOYSA-N 0.000 description 3
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 description 3
- 150000001869 cobalt compounds Chemical class 0.000 description 3
- ASKVAEGIVYSGNY-UHFFFAOYSA-L cobalt(ii) hydroxide Chemical compound [OH-].[OH-].[Co+2] ASKVAEGIVYSGNY-UHFFFAOYSA-L 0.000 description 3
- 150000001875 compounds Chemical class 0.000 description 3
- 239000007772 electrode material Substances 0.000 description 3
- XEEYBQQBJWHFJM-UHFFFAOYSA-N iron Substances [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 3
- XGZVUEUWXADBQD-UHFFFAOYSA-L lithium carbonate Chemical compound [Li+].[Li+].[O-]C([O-])=O XGZVUEUWXADBQD-UHFFFAOYSA-L 0.000 description 3
- 150000002642 lithium compounds Chemical class 0.000 description 3
- 239000004745 nonwoven fabric Substances 0.000 description 3
- 229920002981 polyvinylidene fluoride Polymers 0.000 description 3
- 239000000843 powder Substances 0.000 description 3
- 239000007787 solid Substances 0.000 description 3
- 238000012360 testing method Methods 0.000 description 3
- YEJRWHAVMIAJKC-UHFFFAOYSA-N 4-Butyrolactone Chemical compound O=C1CCCO1 YEJRWHAVMIAJKC-UHFFFAOYSA-N 0.000 description 2
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 2
- 229910000733 Li alloy Inorganic materials 0.000 description 2
- 229910012851 LiCoO 2 Inorganic materials 0.000 description 2
- 229910013553 LiNO Inorganic materials 0.000 description 2
- 229910013870 LiPF 6 Inorganic materials 0.000 description 2
- WMFOQBRAJBCJND-UHFFFAOYSA-M Lithium hydroxide Chemical compound [Li+].[OH-] WMFOQBRAJBCJND-UHFFFAOYSA-M 0.000 description 2
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 2
- MCMNRKCIXSYSNV-UHFFFAOYSA-N Zirconium dioxide Chemical compound O=[Zr]=O MCMNRKCIXSYSNV-UHFFFAOYSA-N 0.000 description 2
- 239000006230 acetylene black Substances 0.000 description 2
- 229910052782 aluminium Inorganic materials 0.000 description 2
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 2
- 239000003125 aqueous solvent Substances 0.000 description 2
- 239000012300 argon atmosphere Substances 0.000 description 2
- FPCJKVGGYOAWIZ-UHFFFAOYSA-N butan-1-ol;titanium Chemical compound [Ti].CCCCO.CCCCO.CCCCO.CCCCO FPCJKVGGYOAWIZ-UHFFFAOYSA-N 0.000 description 2
- 239000006182 cathode active material Substances 0.000 description 2
- 238000010586 diagram Methods 0.000 description 2
- IEJIGPNLZYLLBP-UHFFFAOYSA-N dimethyl carbonate Chemical compound COC(=O)OC IEJIGPNLZYLLBP-UHFFFAOYSA-N 0.000 description 2
- 239000002612 dispersion medium Substances 0.000 description 2
- JBTWLSYIZRCDFO-UHFFFAOYSA-N ethyl methyl carbonate Chemical compound CCOC(=O)OC JBTWLSYIZRCDFO-UHFFFAOYSA-N 0.000 description 2
- 239000010408 film Substances 0.000 description 2
- 238000000227 grinding Methods 0.000 description 2
- 238000010438 heat treatment Methods 0.000 description 2
- 239000002608 ionic liquid Substances 0.000 description 2
- 229910052742 iron Inorganic materials 0.000 description 2
- 239000001989 lithium alloy Substances 0.000 description 2
- KWGKDLIKAYFUFQ-UHFFFAOYSA-M lithium chloride Chemical compound [Li+].[Cl-] KWGKDLIKAYFUFQ-UHFFFAOYSA-M 0.000 description 2
- IIPYXGDZVMZOAP-UHFFFAOYSA-N lithium nitrate Chemical compound [Li+].[O-][N+]([O-])=O IIPYXGDZVMZOAP-UHFFFAOYSA-N 0.000 description 2
- 150000002697 manganese compounds Chemical class 0.000 description 2
- 238000003701 mechanical milling Methods 0.000 description 2
- 229910044991 metal oxide Inorganic materials 0.000 description 2
- 150000004706 metal oxides Chemical class 0.000 description 2
- 150000002816 nickel compounds Chemical class 0.000 description 2
- AIBQNUOBCRIENU-UHFFFAOYSA-N nickel;dihydrate Chemical compound O.O.[Ni] AIBQNUOBCRIENU-UHFFFAOYSA-N 0.000 description 2
- 150000004767 nitrides Chemical class 0.000 description 2
- 239000012299 nitrogen atmosphere Substances 0.000 description 2
- 229920003229 poly(methyl methacrylate) Polymers 0.000 description 2
- 229920002239 polyacrylonitrile Polymers 0.000 description 2
- 239000005518 polymer electrolyte Substances 0.000 description 2
- 239000004926 polymethyl methacrylate Substances 0.000 description 2
- 229920001343 polytetrafluoroethylene Polymers 0.000 description 2
- 239000004810 polytetrafluoroethylene Substances 0.000 description 2
- 239000002243 precursor Substances 0.000 description 2
- RUOJZAUFBMNUDX-UHFFFAOYSA-N propylene carbonate Chemical compound CC1COC(=O)O1 RUOJZAUFBMNUDX-UHFFFAOYSA-N 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- 238000001228 spectrum Methods 0.000 description 2
- 150000003609 titanium compounds Chemical class 0.000 description 2
- ZZXUZKXVROWEIF-UHFFFAOYSA-N 1,2-butylene carbonate Chemical compound CCC1COC(=O)O1 ZZXUZKXVROWEIF-UHFFFAOYSA-N 0.000 description 1
- UUAMLBIYJDPGFU-UHFFFAOYSA-N 1,3-dimethoxypropane Chemical compound COCCCOC UUAMLBIYJDPGFU-UHFFFAOYSA-N 0.000 description 1
- JWUJQDFVADABEY-UHFFFAOYSA-N 2-methyltetrahydrofuran Chemical compound CC1CCCO1 JWUJQDFVADABEY-UHFFFAOYSA-N 0.000 description 1
- 229910000838 Al alloy Inorganic materials 0.000 description 1
- 238000012935 Averaging Methods 0.000 description 1
- 229910018111 Li 2 S-B 2 S 3 Inorganic materials 0.000 description 1
- 229910018127 Li 2 S-GeS 2 Inorganic materials 0.000 description 1
- 229910018130 Li 2 S-P 2 S 5 Inorganic materials 0.000 description 1
- 229910018119 Li 3 PO 4 Inorganic materials 0.000 description 1
- 229910009147 Li1.3Al0.3Ti0.7(PO4)3 Inorganic materials 0.000 description 1
- 229910009296 Li2S-P2S3-P2S5 Inorganic materials 0.000 description 1
- 229910009324 Li2S-SiS2-Li3PO4 Inorganic materials 0.000 description 1
- 229910009326 Li2S-SiS2-Li4SiO4 Inorganic materials 0.000 description 1
- 229910009328 Li2S-SiS2—Li3PO4 Inorganic materials 0.000 description 1
- 229910009185 Li2S—P2S3—P2S5 Inorganic materials 0.000 description 1
- 229910007295 Li2S—SiS2—Li3PO4 Inorganic materials 0.000 description 1
- 229910007290 Li2S—SiS2—Li4SiO4 Inorganic materials 0.000 description 1
- 229910013950 Li3.25P0.25Ge0.76S4 Inorganic materials 0.000 description 1
- 229910012266 Li3.4P0.6Si0.4S4 Inorganic materials 0.000 description 1
- 229910012425 Li3Fe2 (PO4)3 Inorganic materials 0.000 description 1
- 229910012847 Li3PS4-Li4GeS4 Inorganic materials 0.000 description 1
- 229910012840 Li3PS4—Li4GeS4 Inorganic materials 0.000 description 1
- 229910015015 LiAsF 6 Inorganic materials 0.000 description 1
- 229910013063 LiBF 4 Inorganic materials 0.000 description 1
- 229910013684 LiClO 4 Inorganic materials 0.000 description 1
- 229910010835 LiI-Li2S-P2S5 Inorganic materials 0.000 description 1
- 229910010840 LiI—Li2S—P2S5 Inorganic materials 0.000 description 1
- 229910010853 LiI—Li2S—SiS2—P2S5 Inorganic materials 0.000 description 1
- 229910015643 LiMn 2 O 4 Inorganic materials 0.000 description 1
- 229910013528 LiN(SO2 CF3)2 Inorganic materials 0.000 description 1
- 229910013641 LiNbO 3 Inorganic materials 0.000 description 1
- 229910014422 LiNi1/3Mn1/3Co1/3O2 Inorganic materials 0.000 description 1
- 229910013290 LiNiO 2 Inorganic materials 0.000 description 1
- 229910013086 LiNiPO Inorganic materials 0.000 description 1
- 229910021380 Manganese Chloride Inorganic materials 0.000 description 1
- GLFNIEUTAYBVOC-UHFFFAOYSA-L Manganese chloride Chemical compound Cl[Mn]Cl GLFNIEUTAYBVOC-UHFFFAOYSA-L 0.000 description 1
- 229910003289 NiMn Inorganic materials 0.000 description 1
- 229910021586 Nickel(II) chloride Inorganic materials 0.000 description 1
- 241000080590 Niso Species 0.000 description 1
- 229910000978 Pb alloy Inorganic materials 0.000 description 1
- 239000004698 Polyethylene Substances 0.000 description 1
- 239000004743 Polypropylene Substances 0.000 description 1
- 229910000676 Si alloy Inorganic materials 0.000 description 1
- 229910004298 SiO 2 Inorganic materials 0.000 description 1
- 229910004283 SiO 4 Inorganic materials 0.000 description 1
- 229910001128 Sn alloy Inorganic materials 0.000 description 1
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 description 1
- JFBZPFYRPYOZCQ-UHFFFAOYSA-N [Li].[Al] Chemical compound [Li].[Al] JFBZPFYRPYOZCQ-UHFFFAOYSA-N 0.000 description 1
- QSNQXZYQEIKDPU-UHFFFAOYSA-N [Li].[Fe] Chemical compound [Li].[Fe] QSNQXZYQEIKDPU-UHFFFAOYSA-N 0.000 description 1
- KLARSDUHONHPRF-UHFFFAOYSA-N [Li].[Mn] Chemical compound [Li].[Mn] KLARSDUHONHPRF-UHFFFAOYSA-N 0.000 description 1
- ZVLDJSZFKQJMKD-UHFFFAOYSA-N [Li].[Si] Chemical compound [Li].[Si] ZVLDJSZFKQJMKD-UHFFFAOYSA-N 0.000 description 1
- FDLZQPXZHIFURF-UHFFFAOYSA-N [O-2].[Ti+4].[Li+] Chemical compound [O-2].[Ti+4].[Li+] FDLZQPXZHIFURF-UHFFFAOYSA-N 0.000 description 1
- MQRWBMAEBQOWAF-UHFFFAOYSA-N acetic acid;nickel Chemical compound [Ni].CC(O)=O.CC(O)=O MQRWBMAEBQOWAF-UHFFFAOYSA-N 0.000 description 1
- 239000011149 active material Substances 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 239000012298 atmosphere Substances 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- HSLXOARVFIWOQF-UHFFFAOYSA-N bis(trifluoromethylsulfonyl)azanide;1-butyl-1-methylpyrrolidin-1-ium Chemical compound CCCC[N+]1(C)CCCC1.FC(F)(F)S(=O)(=O)[N-]S(=O)(=O)C(F)(F)F HSLXOARVFIWOQF-UHFFFAOYSA-N 0.000 description 1
- IEFUHGXOQSVRDQ-UHFFFAOYSA-N bis(trifluoromethylsulfonyl)azanide;1-methyl-1-propylpiperidin-1-ium Chemical compound CCC[N+]1(C)CCCCC1.FC(F)(F)S(=O)(=O)[N-]S(=O)(=O)C(F)(F)F IEFUHGXOQSVRDQ-UHFFFAOYSA-N 0.000 description 1
- DKNRELLLVOYIIB-UHFFFAOYSA-N bis(trifluoromethylsulfonyl)azanide;1-methyl-1-propylpyrrolidin-1-ium Chemical compound CCC[N+]1(C)CCCC1.FC(F)(F)S(=O)(=O)[N-]S(=O)(=O)C(F)(F)F DKNRELLLVOYIIB-UHFFFAOYSA-N 0.000 description 1
- WUFQNPMBKMKEHN-UHFFFAOYSA-N bis(trifluoromethylsulfonyl)azanide;diethyl-(2-methoxyethyl)-methylazanium Chemical compound CC[N+](C)(CC)CCOC.FC(F)(F)S(=O)(=O)[N-]S(=O)(=O)C(F)(F)F WUFQNPMBKMKEHN-UHFFFAOYSA-N 0.000 description 1
- NFLGAVZONHCOQE-UHFFFAOYSA-N bis(trifluoromethylsulfonyl)azanide;trimethyl(propyl)azanium Chemical compound CCC[N+](C)(C)C.FC(F)(F)S(=O)(=O)[N-]S(=O)(=O)C(F)(F)F NFLGAVZONHCOQE-UHFFFAOYSA-N 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 239000006229 carbon black Substances 0.000 description 1
- 239000003575 carbonaceous material Substances 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 229940011182 cobalt acetate Drugs 0.000 description 1
- GVPFVAHMJGGAJG-UHFFFAOYSA-L cobalt dichloride Chemical compound [Cl-].[Cl-].[Co+2] GVPFVAHMJGGAJG-UHFFFAOYSA-L 0.000 description 1
- UFMZWBIQTDUYBN-UHFFFAOYSA-N cobalt dinitrate Chemical compound [Co+2].[O-][N+]([O-])=O.[O-][N+]([O-])=O UFMZWBIQTDUYBN-UHFFFAOYSA-N 0.000 description 1
- 229910001981 cobalt nitrate Inorganic materials 0.000 description 1
- 229910000361 cobalt sulfate Inorganic materials 0.000 description 1
- 229940044175 cobalt sulfate Drugs 0.000 description 1
- KTVIXTQDYHMGHF-UHFFFAOYSA-L cobalt(2+) sulfate Chemical compound [Co+2].[O-]S([O-])(=O)=O KTVIXTQDYHMGHF-UHFFFAOYSA-L 0.000 description 1
- MULYSYXKGICWJF-UHFFFAOYSA-L cobalt(2+);oxalate Chemical compound [Co+2].[O-]C(=O)C([O-])=O MULYSYXKGICWJF-UHFFFAOYSA-L 0.000 description 1
- QAHREYKOYSIQPH-UHFFFAOYSA-L cobalt(II) acetate Chemical compound [Co+2].CC([O-])=O.CC([O-])=O QAHREYKOYSIQPH-UHFFFAOYSA-L 0.000 description 1
- NKDDWNXOKDWJAK-UHFFFAOYSA-N dimethoxymethane Chemical compound COCOC NKDDWNXOKDWJAK-UHFFFAOYSA-N 0.000 description 1
- 238000003411 electrode reaction Methods 0.000 description 1
- 238000005370 electroosmosis Methods 0.000 description 1
- 239000010419 fine particle Substances 0.000 description 1
- 239000003365 glass fiber Substances 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 239000011261 inert gas Substances 0.000 description 1
- 238000009830 intercalation Methods 0.000 description 1
- 230000002687 intercalation Effects 0.000 description 1
- 229910001337 iron nitride Inorganic materials 0.000 description 1
- 239000003273 ketjen black Substances 0.000 description 1
- 238000003475 lamination Methods 0.000 description 1
- JWZCKIBZGMIRSW-UHFFFAOYSA-N lead lithium Chemical compound [Li].[Pb] JWZCKIBZGMIRSW-UHFFFAOYSA-N 0.000 description 1
- XIXADJRWDQXREU-UHFFFAOYSA-M lithium acetate Chemical compound [Li+].CC([O-])=O XIXADJRWDQXREU-UHFFFAOYSA-M 0.000 description 1
- 229910001386 lithium phosphate Inorganic materials 0.000 description 1
- UIDWHMKSOZZDAV-UHFFFAOYSA-N lithium tin Chemical compound [Li].[Sn] UIDWHMKSOZZDAV-UHFFFAOYSA-N 0.000 description 1
- 235000002867 manganese chloride Nutrition 0.000 description 1
- 239000011565 manganese chloride Substances 0.000 description 1
- 229940099607 manganese chloride Drugs 0.000 description 1
- 229940099596 manganese sulfate Drugs 0.000 description 1
- 235000007079 manganese sulphate Nutrition 0.000 description 1
- 239000011702 manganese sulphate Substances 0.000 description 1
- UOGMEBQRZBEZQT-UHFFFAOYSA-L manganese(2+);diacetate Chemical compound [Mn+2].CC([O-])=O.CC([O-])=O UOGMEBQRZBEZQT-UHFFFAOYSA-L 0.000 description 1
- MIVBAHRSNUNMPP-UHFFFAOYSA-N manganese(2+);dinitrate Chemical compound [Mn+2].[O-][N+]([O-])=O.[O-][N+]([O-])=O MIVBAHRSNUNMPP-UHFFFAOYSA-N 0.000 description 1
- WPBNNNQJVZRUHP-UHFFFAOYSA-L manganese(2+);methyl n-[[2-(methoxycarbonylcarbamothioylamino)phenyl]carbamothioyl]carbamate;n-[2-(sulfidocarbothioylamino)ethyl]carbamodithioate Chemical compound [Mn+2].[S-]C(=S)NCCNC([S-])=S.COC(=O)NC(=S)NC1=CC=CC=C1NC(=S)NC(=O)OC WPBNNNQJVZRUHP-UHFFFAOYSA-L 0.000 description 1
- RGVLTEMOWXGQOS-UHFFFAOYSA-L manganese(2+);oxalate Chemical compound [Mn+2].[O-]C(=O)C([O-])=O RGVLTEMOWXGQOS-UHFFFAOYSA-L 0.000 description 1
- SQQMAOCOWKFBNP-UHFFFAOYSA-L manganese(II) sulfate Chemical compound [Mn+2].[O-]S([O-])(=O)=O SQQMAOCOWKFBNP-UHFFFAOYSA-L 0.000 description 1
- 229910052976 metal sulfide Inorganic materials 0.000 description 1
- 229940078494 nickel acetate Drugs 0.000 description 1
- QMMRZOWCJAIUJA-UHFFFAOYSA-L nickel dichloride Chemical compound Cl[Ni]Cl QMMRZOWCJAIUJA-UHFFFAOYSA-L 0.000 description 1
- LGQLOGILCSXPEA-UHFFFAOYSA-L nickel sulfate Chemical compound [Ni+2].[O-]S([O-])(=O)=O LGQLOGILCSXPEA-UHFFFAOYSA-L 0.000 description 1
- DOLZKNFSRCEOFV-UHFFFAOYSA-L nickel(2+);oxalate Chemical compound [Ni+2].[O-]C(=O)C([O-])=O DOLZKNFSRCEOFV-UHFFFAOYSA-L 0.000 description 1
- 229910000363 nickel(II) sulfate Inorganic materials 0.000 description 1
- KBJMLQFLOWQJNF-UHFFFAOYSA-N nickel(ii) nitrate Chemical compound [Ni+2].[O-][N+]([O-])=O.[O-][N+]([O-])=O KBJMLQFLOWQJNF-UHFFFAOYSA-N 0.000 description 1
- 229920000058 polyacrylate Polymers 0.000 description 1
- 229920000573 polyethylene Polymers 0.000 description 1
- 229920001155 polypropylene Polymers 0.000 description 1
- 229920002635 polyurethane Polymers 0.000 description 1
- 239000004814 polyurethane Substances 0.000 description 1
- 239000011164 primary particle Substances 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 229920005989 resin Polymers 0.000 description 1
- 239000011347 resin Substances 0.000 description 1
- HXJUTPCZVOIRIF-UHFFFAOYSA-N sulfolane Chemical compound O=S1(=O)CCCC1 HXJUTPCZVOIRIF-UHFFFAOYSA-N 0.000 description 1
- 229910052717 sulfur Inorganic materials 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- 239000010409 thin film Substances 0.000 description 1
- 229910052719 titanium Inorganic materials 0.000 description 1
- GQUJEMVIKWQAEH-UHFFFAOYSA-N titanium(III) oxide Chemical compound O=[Ti]O[Ti]=O GQUJEMVIKWQAEH-UHFFFAOYSA-N 0.000 description 1
- VXUYXOFXAQZZMF-UHFFFAOYSA-N titanium(IV) isopropoxide Chemical compound CC(C)O[Ti](OC(C)C)(OC(C)C)OC(C)C VXUYXOFXAQZZMF-UHFFFAOYSA-N 0.000 description 1
- TWQULNDIKKJZPH-UHFFFAOYSA-K trilithium;phosphate Chemical compound [Li+].[Li+].[Li+].[O-]P([O-])([O-])=O TWQULNDIKKJZPH-UHFFFAOYSA-K 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/48—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides
- H01M4/50—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of manganese
- H01M4/505—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of manganese of mixed oxides or hydroxides containing manganese for inserting or intercalating light metals, e.g. LiMn2O4 or LiMn2OxFy
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01G—COMPOUNDS CONTAINING METALS NOT COVERED BY SUBCLASSES C01D OR C01F
- C01G53/00—Compounds of nickel
- C01G53/40—Nickelates
- C01G53/42—Nickelates containing alkali metals, e.g. LiNiO2
- C01G53/44—Nickelates containing alkali metals, e.g. LiNiO2 containing manganese
- C01G53/54—Nickelates containing alkali metals, e.g. LiNiO2 containing manganese of the type [Mn2O4]-, e.g. Li(NixMn2-x)O4, Li(MyNixMn2-x-y)O4
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/052—Li-accumulators
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/48—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides
- H01M4/52—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of nickel, cobalt or iron
- H01M4/525—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of nickel, cobalt or iron of mixed oxides or hydroxides containing iron, cobalt or nickel for inserting or intercalating light metals, e.g. LiNiO2, LiCoO2 or LiCoOxFy
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2002/00—Crystal-structural characteristics
- C01P2002/70—Crystal-structural characteristics defined by measured X-ray, neutron or electron diffraction data
- C01P2002/72—Crystal-structural characteristics defined by measured X-ray, neutron or electron diffraction data by d-values or two theta-values, e.g. as X-ray diagram
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2002/00—Crystal-structural characteristics
- C01P2002/70—Crystal-structural characteristics defined by measured X-ray, neutron or electron diffraction data
- C01P2002/76—Crystal-structural characteristics defined by measured X-ray, neutron or electron diffraction data by a space-group or by other symmetry indications
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2004/00—Particle morphology
- C01P2004/60—Particles characterised by their size
- C01P2004/61—Micrometer sized, i.e. from 1-100 micrometer
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2006/00—Physical properties of inorganic compounds
- C01P2006/40—Electric properties
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2220/00—Batteries for particular applications
- H01M2220/30—Batteries in portable systems, e.g. mobile phone, laptop
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Landscapes
- Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Electrochemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Inorganic Chemistry (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Manufacturing & Machinery (AREA)
- Battery Electrode And Active Subsutance (AREA)
- Inorganic Compounds Of Heavy Metals (AREA)
Description
LixC6→6C+xLi++xe− (I)
(上記式(I)中、0<x<1である。)
上記式(I)の反応で生じる電子は、外部回路を経由し、外部の負荷で仕事をした後、正極に到達する。そして、上記式(I)の反応で生じたリチウムイオン(Li+)は、負極と正極に挟持された電解質内を、負極側から正極側に電気浸透により移動する。
Li1−xCoO2+xLi++xe−→LiCoO2 (II)
(上記式(II)中、0<x<1である。)
充電時においては、負極及び正極において、それぞれ上記式(I)及び式(II)の逆反応が進行し、負極においてはグラファイトインターカレーションによりリチウムが入り込んだグラファイト(LixC6)が、正極においてはコバルト酸リチウム(Li1−xCoO2)が再生するため、再放電が可能となる。
本発明は、上記実状を鑑みて成し遂げられたものであり、リチウム電池に使用されることにより従来のリチウム電池よりも放電容量を高くできる正極活物質、及び当該正極活物質を含有するリチウム電池を提供することを目的とする。
Li2Ni1−x−yCoxMnyTiO4 組成式(1)
(上記組成式(1)中、x及びyは、x>0、y>0、且つx+y<1を満たす実数である。)
本発明のリチウム電池用正極活物質は、下記組成式(1)で表され、且つ、結晶構造が岩塩型であることを特徴とする。
Li2Ni1−x−yCoxMnyTiO4 組成式(1)
(上記組成式(1)中、x及びyは、x>0、y>0、且つx+y<1を満たす実数である。)
また、理論上は、Li2MTiO4 1モルに対し、リチウムイオンは2モル拡散するはずである。しかし、従来のLi2MTiO4系の正極活物質材料においては、リチウムイオンが2モル拡散する例は知られていない。ここで、リチウムイオンが2モル拡散する例とは、すなわち、下記式(III)に示すような2電子が関与する充電反応の例、及び、下記式(III)の逆反応である2電子が関与する放電反応の例のことを指す。
Li2MTiO4→MTiO4+2Li++2e− (III)
x及びyのいずれか1つの値が上記好ましい範囲の上限よりも大きすぎ、他の1つの値が上記好ましい範囲の下限よりも小さすぎる場合には、遷移金属サイトMに1つの金属元素しか含まない従来の正極活物質と実質的に組成が変わらないため、十分な放電容量が得られない。
上記組成式(1)中、x及びyは、0.15<x<0.7、0.15<y<0.7、且つx+y<1を満たす実数であることがより好ましい。また、上記組成式(1)中、x、y、及びzは、x=y=z=1/3であることがさらに好ましい。
まず、原料として、リチウム化合物、ニッケル化合物、コバルト化合物、マンガン化合物、及びチタン化合物を準備する。なお、原料としてこれら5種類の化合物を全て準備する必要は必ずしもなく、例えば、リチウム化合物がコバルト元素を含む場合等には、コバルト化合物を他に準備する必要は必ずしもない。
リチウム化合物としては、例えば、炭酸リチウム(Li2CO3)、酢酸リチウム(CH3CO2Li)、及び硝酸リチウム(LiNO3)、並びにこれらの水和物等が挙げられる。
ニッケル化合物としては、例えば、水酸化ニッケル(II)(Ni(OH)2)、酢酸ニッケル(II)(Ni(CH3CO2)2)、硝酸ニッケル(II)(Ni(NO3)2)、硫酸ニッケル(II)(NiSO4)、シュウ酸ニッケル(II)(NiC2O4)、及び塩化ニッケル(II)(NiCl2)、並びにこれらの水和物等が挙げられる。
コバルト化合物としては、例えば、水酸化コバルト(II)(Co(OH)2)、酢酸コバルト(II)(Co(CH3CO2)2)、硝酸コバルト(II)(Co(NO3)2)、硫酸コバルト(II)(CoSO4)、シュウ酸コバルト(II)(CoC2O4)、及び塩化コバルト(II)(CoCl2)、並びにこれらの水和物等が挙げられる。
マンガン化合物としては、例えば、酸化マンガン(II)(MnO)、酢酸マンガン(II)(Mn(CH3CO2)2)、硝酸マンガン(II)(Mn(NO3)2)、硫酸マンガン(II)(MnSO4)、シュウ酸マンガン(II)(MnC2O4)、及び塩化マンガン(II)(MnCl2)、並びにこれらの水和物等が挙げられる。
チタン化合物としては、例えば、酸化チタン(II)(TiO)、オルトチタン酸テトライソプロピル(Ti(OCH(CH3)2)4)、テトラブトキシチタン(IV)(Ti(OC4H9)4)、及び三酸化二チタン(III)(Ti2O3)、並びにこれらの水和物等が挙げられる。
メカニカルミリングは、原料の混合物を、機械的エネルギーを付与しながら混合する方法であれば特に限定されるものではないが、例えばボールミル、ターボミル、メカノフュージョン、ディスクミル等を挙げることができ、中でもボールミルが好ましく、上記組成式(1)に示すような所望の組成のリチウム電池用正極活物質が得られるという観点から、遊星型ボールミルが好ましい。
遊星型ボールミルを行う際の台盤回転数としては、例えば100〜300rpm、中でも150〜250rpmであることが好ましい。また、遊星型ボールミルを行う際の処理時間は、例えば30分間〜24時間の範囲内、中でも1〜5時間の範囲内であることが好ましい。
最後に、メッシュ等にポットの中身を空け、ボールを分離することにより、本発明に係るリチウム電池用正極活物質の前駆体が得られる。
加熱方法は特に限定されないが、アルゴン雰囲気や窒素雰囲気などの不活性ガス雰囲気下において焼成することが好ましい。焼成温度は、500〜1100℃であることが好ましく、700〜1000℃であることがより好ましい。また、焼成時間は、5〜48時間であることが好ましく、10〜24時間であることがより好ましい。
本発明のリチウム電池は、正極、負極、並びに、当該正極及び当該負極の間に介在する電解質層を備えるリチウム電池であって、前記正極は、少なくとも上記リチウム電池用正極活物質を含有することを特徴とする。
上記リチウム電池用正極活物質が高い充放電容量を有することにより、当該リチウム電池用正極活物質を含むリチウム電池は、良好な充放電特性を発揮できる。
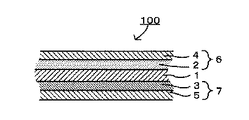
リチウム電池100は、正極活物質層2及び正極集電体4を備える正極6と、負極活物質層3及び負極集電体5を備える負極7と、正極6及び負極7に挟持される電解質層1を備える。
以下、本発明に係るリチウム電池に使用される、正極、負極、及び電解質層、並びに本発明に係るリチウム電池に好適に使用されるセパレータ及び電池ケースについて、詳細に説明する。
他の正極活物質としては、具体的には、LiCoO2、LiNi1/3Mn1/3Co1/3O2、LiNiPO4、LiMnPO4、LiNiO2、LiMn2O4、LiCoMnO4、Li2NiMn3O8、Li3Fe2(PO4)3及びLi3V2(PO4)3等を挙げることができる。正極活物質からなる微粒子の表面にLiNbO3等を被覆してもよい。
正極活物質層における正極活物質の総含有割合は、通常、50〜90質量%の範囲内である。
本発明に使用される導電性材料としては、正極活物質層の導電性を向上させることができれば特に限定されるものではないが、例えばアセチレンブラック、ケッチェンブラック等のカーボンブラック等を挙げることができる。また、正極活物質層における導電性材料の含有割合は、導電性材料の種類によって異なるものであるが、通常1〜30質量%の範囲内である。
また、正極活物質の調製には、N−メチル−2−ピロリドンやアセトン等の分散媒を用いてもよい。
リチウム合金としては、例えばリチウムアルミニウム合金、リチウムスズ合金、リチウム鉛合金、リチウムケイ素合金等を挙げることができる。また、リチウム元素を含有する金属酸化物としては、例えばリチウムチタン酸化物等を挙げることができる。また、リチウム元素を含有する金属窒化物としては、例えばリチウムコバルト窒化物、リチウム鉄窒化物、リチウムマンガン窒化物等を挙げることができる。また、負極活物質としては、固体電解質をコートしたリチウムを用いることもできる。
負極活物質層の膜厚としては、特に限定されるものではないが、例えば10〜100μmの範囲内、中でも10〜50μmの範囲内であることが好ましい。
電解質層には、電解液、ゲル電解質、及び固体電解質等を用いることができる。これらは、1種類のみを単独で用いてもよいし、2種類以上を組み合わせて用いてもよい。
非水系電解液としては、通常、リチウム塩及び非水溶媒を含有したものを用いる。上記リチウム塩としては、例えばLiPF6、LiBF4、LiClO4及びLiAsF6等の無機リチウム塩;LiCF3SO3、LiN(SO2CF3)2(Li−TFSA)、LiN(SO2C2F5)2及びLiC(SO2CF3)3等の有機リチウム塩等を挙げることができる。上記非水溶媒としては、例えばエチレンカーボネート(EC)、プロピレンカーボネート(PC)、ジメチルカーボネート(DMC)、ジエチルカーボネート(DEC)、エチルメチルカーボネート(EMC)、エチルカーボネート、ブチレンカーボネート、γ−ブチロラクトン、スルホラン、アセトニトリル(AcN)、ジメトキシメタン、1,2−ジメトキシエタン(DME)、1,3−ジメトキシプロパン、ジエチルエーテル、テトラエチレングリコールジメチルエーテル(TEGDME)、テトラヒドロフラン、2−メチルテトラヒドロフラン、ジメチルスルホキシド(DMSO)及びこれらの混合物等を挙げることができる。非水系電解液におけるリチウム塩の濃度は、例えば0.5〜3mol/kgである。
硫化物系固体電解質としては、具体的には、Li2S−P2S5、Li2S−P2S3、Li2S−P2S3−P2S5、Li2S−SiS2、Li2S−Si2S、Li2S−B2S3、Li2S−GeS2、LiI−Li2S−P2S5、LiI−Li2S−SiS2−P2S5、Li2S−SiS2−Li4SiO4、Li2S−SiS2−Li3PO4、Li3PS4−Li4GeS4、Li3.4P0.6Si0.4S4、Li3.25P0.25Ge0.76S4、Li4−xGe1−xPxS4等を例示することができる。
酸化物系固体電解質としては、具体的には、LiPON(リン酸リチウムオキシナイトライド)、Li1.3Al0.3Ti0.7(PO4)3、La0.51Li0.34TiO0.74、Li3PO4、Li2SiO2、Li2SiO4等を例示することができる。
ポリマー電解質は、通常、リチウム塩及びポリマーを含有する。リチウム塩としては、上述した無機リチウム塩及び有機リチウム塩の少なくともいずれか1つを使用できる。ポリマーとしては、リチウム塩と錯体を形成するものであれば特に限定されるものではなく、例えば、ポリエチレンオキシド等が挙げられる。
[実施例1]
炭酸リチウム(Li2CO3)、水酸化ニッケル(II)(Ni(OH)2)、水酸化コバルト(II)(Co(OH)2)、酸化マンガン(II)(MnO)、及び酸化チタン(II)(TiO)を、モル比がLi2CO3:Ni(OH)2:Co(OH)2:MnO:TiO=3:1:1:1:3となるように混合した。得られた粉体を、アルゴン雰囲気下、900℃にて24時間焼成することにより、実施例1のリチウム電池用正極活物質(Li2Ni1/3Co1/3Mn1/3TiO4)を製造した。
炭酸リチウム(Li2CO3)、水酸化コバルト(II)(Co(OH)2)、及び酸化チタン(II)(TiO)を、モル比がLi2CO3:Co(OH)2:TiO=1:1:1となるように混合した。あとは、実施例1と同様の条件下で焼成することにより、比較例1のリチウム電池用正極活物質(Li2CoTiO4)を製造した。
実施例1及び比較例1のリチウム電池用正極活物質について、X線回折測定を行った。詳細な測定条件は以下の通りである。
X線回折測定装置 RINT−2500(リガク製)
測定範囲 2θ=10〜80°
測定間隔 0.02°
走査速度 2°/min
測定電圧 50kV
測定電流 300mA
図2の下のスペクトルから分かるように、比較例1のXRDパターンにおいては、2θ=38°、43°、63°、76°、及び80°に鋭いピークがそれぞれ観察される。これらのピークは、比較例1のリチウム電池用正極活物質の結晶構造が不規則岩塩型であることを示す。また、2θ=38°のピークは(111)面の回折に、2θ=43°のピークは(200)面の回折に、2θ=63°のピークは(220)面の回折に、2θ=76°のピークは(311)面の回折に、2θ=80°のピークは(222)面の回折に、それぞれ帰属される。
一方、図2の上のスペクトルから分かるように、実施例1のXRDパターンにおいても、比較例1と同様に、2θ=38°、43°、63°、76°、及び80°に鋭いピークがそれぞれ観察される。したがって、図2より、実施例1のリチウム電池用正極活物質の結晶構造も不規則岩塩型であることが分かる。
以上より、実施例1においては、不純物を含まないLi2Ni1/3Co1/3Mn1/3TiO4が合成できたことが確認できた。また、実施例1のように、ニッケル、コバルト、及びマンガンを等しいモル比で加えても、比較例1と同様の不規則岩塩型の結晶構造をとることが確認できた。
[実施例2]
まず、正極活物質として上記実施例1のリチウム電池用正極活物質を、導電性材料としてアセチレンブラック(電気化学工業社製、商品名:HS−100)を、結着剤としてPVdF(株式会社クレハ製、KRポリマー#7305)を、それぞれ用意した。これら正極活物質、導電性材料及び結着剤を、正極活物質:導電性材料:結着剤=70質量%:25質量%:5質量%となるように混合し、正極合剤を調製した。また、正極合剤には、分散媒として、N−メチル−2−ピロリドン(ナカライテスク社製)を適宜加えた。
正極集電体として、ニッケルメッシュを準備した。
負極として、リチウム金属箔(本城金属製)を準備した。
電解液として、1mol/L LiPF6(溶媒 EC:DMC=1:1、キシダ化学社製)を準備した。
電池ケースとして、コインセル(SUS2032型)を準備した。上記正極集電体、正極合剤、上記電解質層、及び上記負極を、ニッケルメッシュ、正極合剤層、電解質層、リチウム金属箔の順となるように電池ケースに収納して、実施例2のリチウム電池を製造した。
以上の工程は、全て窒素雰囲気下のグローブボックス内で行った。
実施例2において、正極活物質として、上記実施例1のリチウム電池用正極活物質の替わりに、上記比較例1のリチウム電池用正極活物質を用いたこと以外は、実施例2と同様の材料を用いて、比較例2のリチウム電池を作製した。
実施例2及び比較例2のリチウム電池について、充放電試験を行った。具体的には、まず、以下の電流密度の条件下、4.8Vを上限として、定電流モードで充電を行った。次に、2Vまで放電を行い、得られた容量を放電容量とした。各電池についてそれぞれ2回ずつ充放電を行った。
実施例2の電流密度:0.011mA/cm2
比較例2の電流密度:0.0017mA/cm2
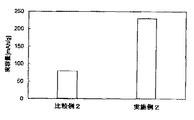
図5中の1回目の充電曲線から分かるように、比較例2のリチウム電池においては、Li2CoTiO4中のリチウムイオンは約1.8モル分しか電極反応に関与していない。その結果、比較例2のリチウム電池の放電容量は144mAh/gに留まる。
一方、図4に示すように、実施例2のリチウム電池の放電容量は230mAh/gである。
このように、実施例2のリチウム電池において高い放電容量が得られた理由は、以下の通りであると推測される。ニッケル、コバルト、及びマンガンの3種類の遷移金属を含む正極活物質においては、コバルトのみを含む従来の正極活物質と比較して、含まれる遷移金属原子のイオン半径や価数が多種多様であるため、従来の正極活物質とは異なる態様により、リチウム伝導パスが形成される。したがって、従来の正極活物質では不可能であった、正極活物質1モルに対するリチウムイオン2モルの拡散が可能となり、その結果、放電容量を向上させることができる。
また、図3から分かるように、実施例2のリチウム電池の充電時の電位は4V以上である。したがって、本発明に係る正極活物質を含むリチウム電池用正極は、いわゆる高電位の正極の中でも、非常に高い充放電容量を有することが分かる。
まず、Li2MnTiO4については、単相合成に成功した例が知られていない(参考:M.Kuzma,et al.,J.of Power Sources,189(2009)81−88)。そのため、Mnは、Fm−3m群の結晶構造中に入りにくいと考えられる。
一方、Li2NiTiO4は、所定の容量が得られるものの、酸化還元電位の観点から2電子反応が起こりにくいため、200mAh/gを超える容量が得にくいと考えられる(参考:S.R.S.Prabaharan,et al.,Solid State Ionics,172(2004)39−45)。
Li2CoTiO4は、上述したように実用量が150mAh/gに満たない。おそらく、Li2CoTiO4の結晶構造の観点から、リチウムイオンの拡散性が優れていないと考えられる(参考:M.Yang,et al.,J.Mater.Chem.,22(2012)6200)。
実施例1のLi2Ni1/3Co1/3Mn1/3TiO4は、Li2MnTiO4、Li2NiTiO4、及びLi2CoTiO4の上記各課題を克服でき、且つ、合成可能である点で、従来のLi2MTiO4系正極活物質よりも優れると考えられる。
2 正極活物質層
3 負極活物質層
4 正極集電体
5 負極集電体
6 正極
7 負極
100 リチウム電池
Claims (3)
- 下記組成式(1)で表され、且つ、結晶構造が岩塩型であることを特徴とする、リチウム電池用正極活物質。
Li2Ni1−x−yCoxMnyTiO4 組成式(1)
(上記組成式(1)中、x及びyは、0.1<x<0.8、0.1<y<0.8、且つx+y<1を満たす実数である。) - 前記岩塩型は不規則岩塩型である、請求項1に記載のリチウム電池用正極活物質。
- 正極、負極、並びに、当該正極及び当該負極の間に介在する電解質層を備えるリチウム電池であって、
前記正極は、少なくとも前記請求項1又は2に記載のリチウム電池用正極活物質を含有することを特徴とする、リチウム電池。
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2012248749A JP5964729B2 (ja) | 2012-11-12 | 2012-11-12 | リチウム電池用正極活物質、及び当該リチウム電池用正極活物質を含有するリチウム電池 |
| CN201380058911.3A CN104781963B (zh) | 2012-11-12 | 2013-11-12 | 锂电池用正极活性物质以及含有该锂电池用正极活性物质的锂电池 |
| US14/441,991 US9780369B2 (en) | 2012-11-12 | 2013-11-12 | Cathode active material for lithium batteries, and lithium battery comprising the cathode active material for lithium batteries |
| PCT/JP2013/080561 WO2014073700A1 (ja) | 2012-11-12 | 2013-11-12 | リチウム電池用正極活物質、及び当該リチウム電池用正極活物質を含有するリチウム電池 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2012248749A JP5964729B2 (ja) | 2012-11-12 | 2012-11-12 | リチウム電池用正極活物質、及び当該リチウム電池用正極活物質を含有するリチウム電池 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2014096333A JP2014096333A (ja) | 2014-05-22 |
| JP2014096333A5 JP2014096333A5 (ja) | 2015-06-18 |
| JP5964729B2 true JP5964729B2 (ja) | 2016-08-03 |
Family
ID=50684788
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2012248749A Active JP5964729B2 (ja) | 2012-11-12 | 2012-11-12 | リチウム電池用正極活物質、及び当該リチウム電池用正極活物質を含有するリチウム電池 |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US9780369B2 (ja) |
| JP (1) | JP5964729B2 (ja) |
| CN (1) | CN104781963B (ja) |
| WO (1) | WO2014073700A1 (ja) |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR3045211B1 (fr) | 2015-12-09 | 2020-06-05 | Commissariat A L'energie Atomique Et Aux Energies Alternatives | Materiau de cathode pour batteries li-ion |
| EP3255707A1 (en) * | 2016-06-07 | 2017-12-13 | Université de Liège | Process to prepare an electrode for an electrochemical storage device |
| WO2018012015A1 (ja) * | 2016-07-14 | 2018-01-18 | 三井金属鉱業株式会社 | 全固体型リチウム二次電池用正極活物質 |
| WO2024162139A1 (ja) * | 2023-01-30 | 2024-08-08 | パナソニックIpマネジメント株式会社 | 二次電池用正極活物質および二次電池 |
| WO2024162140A1 (ja) * | 2023-01-30 | 2024-08-08 | パナソニックIpマネジメント株式会社 | 二次電池用正極活物質および二次電池 |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH10251020A (ja) * | 1997-03-11 | 1998-09-22 | Ishihara Sangyo Kaisha Ltd | 金属置換チタン酸リチウムおよびその製造方法ならびにそれを用いてなるリチウム電池 |
| SI22771A (sl) * | 2008-03-27 | 2009-10-31 | Kemijski inštitut | Titanati prehodnih kovin kot materiali za katodo v litijevih akumulatorjih |
| JP5365126B2 (ja) | 2008-09-30 | 2013-12-11 | Tdk株式会社 | リチウムイオン二次電池の正極用活物質及びリチウムイオン二次電池の正極用活物質の製造方法 |
| JP5365125B2 (ja) * | 2008-09-30 | 2013-12-11 | Tdk株式会社 | リチウムイオン二次電池の正極用活物質 |
| US8821763B2 (en) | 2008-09-30 | 2014-09-02 | Tdk Corporation | Active material and method of manufacturing active material |
| JP5152246B2 (ja) | 2010-04-23 | 2013-02-27 | 株式会社豊田自動織機 | リチウムイオン二次電池用正極活物質およびリチウムイオン二次電池 |
| KR101531776B1 (ko) | 2010-11-16 | 2015-06-25 | 도요타지도샤가부시키가이샤 | 정극 활물질 및 그 제조 방법, 및 이것을 사용한 리튬 이차 전지 |
-
2012
- 2012-11-12 JP JP2012248749A patent/JP5964729B2/ja active Active
-
2013
- 2013-11-12 WO PCT/JP2013/080561 patent/WO2014073700A1/ja active Application Filing
- 2013-11-12 CN CN201380058911.3A patent/CN104781963B/zh active Active
- 2013-11-12 US US14/441,991 patent/US9780369B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| US20150295237A1 (en) | 2015-10-15 |
| US9780369B2 (en) | 2017-10-03 |
| JP2014096333A (ja) | 2014-05-22 |
| CN104781963B (zh) | 2017-05-03 |
| CN104781963A (zh) | 2015-07-15 |
| WO2014073700A1 (ja) | 2014-05-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6549565B2 (ja) | リチウム二次電池用正極活物質、リチウム二次電池用正極及びリチウム二次電池 | |
| KR102228109B1 (ko) | 리튬 이차 전지용 정극 활물질, 리튬 이차 전지용 정극, 및 리튬 이차 전지 | |
| JP6462250B2 (ja) | リチウム二次電池用正極活物質、その製造方法、そしてこれを含むリチウム二次電池用正極およびリチウム二次電池 | |
| JP4595987B2 (ja) | 正極活物質 | |
| JP6836369B2 (ja) | リチウム二次電池用正極活物質前駆体、リチウム二次電池用正極活物質の製造方法 | |
| KR101045416B1 (ko) | 리튬티탄산화물 분말, 그 제조방법, 이를 포함하는 전극,및 이차전지 | |
| JP2015022958A (ja) | 正極活物質、及び当該正極活物質を含むリチウム電池 | |
| WO2014073400A1 (ja) | 正極活物質およびハイブリッドイオン電池 | |
| JP2011165404A (ja) | 電池用電極の製造方法、当該製造方法により得られた電極、及び、当該電極を備える電池 | |
| KR20140048456A (ko) | 양극 활물질, 그 제조방법, 및 이를 포함하는 리튬 전지 | |
| US10170762B2 (en) | Lithium metal oxides with multiple phases and stable high energy electrochemical cycling | |
| KR102228750B1 (ko) | 리튬 이차 전지용 양극 활물질, 이의 제조 방법 및 이를 포함하는 리튬 이차 전지 | |
| WO2011118302A1 (ja) | 電池用活物質および電池 | |
| WO2015001957A1 (ja) | リチウムイオン二次電池用正極活物質、リチウムイオン二次電池用正極、リチウムイオン二次電池及びこれらの製造方法 | |
| CN114477310B (zh) | 正极活性物质的制造方法、正极活性物质和锂离子电池的制造方法 | |
| JP2015088266A (ja) | リチウム電池 | |
| JP5964729B2 (ja) | リチウム電池用正極活物質、及び当該リチウム電池用正極活物質を含有するリチウム電池 | |
| KR20210036869A (ko) | Li 및 Mn 기반의 플루오르화 산화물 | |
| WO2015045254A1 (ja) | リチウムチタン複合酸化物 | |
| WO2014073701A1 (ja) | 正極活物質、リチウム電池および正極活物質の製造方法 | |
| JP5565391B2 (ja) | 電極活物質、当該電極活物質の製造方法、及び当該電極活物質を含むリチウム二次電池 | |
| JP2013161597A (ja) | 非水電解質二次電池およびその製造方法ならびに非水電解質二次電池を備えた車両 | |
| JP6669345B2 (ja) | リチウム二次電池用正極活物質、その製造方法およびこれを含むリチウム二次電池 | |
| KR102626621B1 (ko) | 리튬금속전지 및 이의 제조 방법 | |
| JP5967101B2 (ja) | リチウムイオン二次電池用正極材料、リチウムイオン二次電池用正極部材、及びリチウムイオン二次電池 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150424 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20150424 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20160607 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20160630 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5964729 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| S531 | Written request for registration of change of domicile |
Free format text: JAPANESE INTERMEDIATE CODE: R313531 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |