JP5661031B2 - インドリノン誘導体の懸濁液製剤を含むカプセル医薬投薬形態 - Google Patents
インドリノン誘導体の懸濁液製剤を含むカプセル医薬投薬形態 Download PDFInfo
- Publication number
- JP5661031B2 JP5661031B2 JP2011512128A JP2011512128A JP5661031B2 JP 5661031 B2 JP5661031 B2 JP 5661031B2 JP 2011512128 A JP2011512128 A JP 2011512128A JP 2011512128 A JP2011512128 A JP 2011512128A JP 5661031 B2 JP5661031 B2 JP 5661031B2
- Authority
- JP
- Japan
- Prior art keywords
- capsule
- capsules
- formulation
- active substance
- methyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/4816—Wall or shell material
- A61K9/4825—Proteins, e.g. gelatin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61J—CONTAINERS SPECIALLY ADAPTED FOR MEDICAL OR PHARMACEUTICAL PURPOSES; DEVICES OR METHODS SPECIALLY ADAPTED FOR BRINGING PHARMACEUTICAL PRODUCTS INTO PARTICULAR PHYSICAL OR ADMINISTERING FORMS; DEVICES FOR ADMINISTERING FOOD OR MEDICINES ORALLY; BABY COMFORTERS; DEVICES FOR RECEIVING SPITTLE
- A61J1/00—Containers specially adapted for medical or pharmaceutical purposes
- A61J1/03—Containers specially adapted for medical or pharmaceutical purposes for pills or tablets
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
- A61K31/403—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil condensed with carbocyclic rings, e.g. carbazole
- A61K31/404—Indoles, e.g. pindolol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/496—Non-condensed piperazines containing further heterocyclic rings, e.g. rifampin, thiothixene or sparfloxacin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/14—Esters of carboxylic acids, e.g. fatty acid monoglycerides, medium-chain triglycerides, parabens or PEG fatty acid esters
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/4808—Preparations in capsules, e.g. of gelatin, of chocolate characterised by the form of the capsule or the structure of the filling; Capsules containing small tablets; Capsules with outer layer for immediate drug release
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/4816—Wall or shell material
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/4841—Filling excipients; Inactive ingredients
- A61K9/4858—Organic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/4841—Filling excipients; Inactive ingredients
- A61K9/4866—Organic macromolecular compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/5005—Wall or coating material
- A61K9/5021—Organic macromolecular compounds
- A61K9/5052—Proteins, e.g. albumin
- A61K9/5057—Gelatin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/04—Antineoplastic agents specific for metastasis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A50/00—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE in human health protection, e.g. against extreme weather
- Y02A50/30—Against vector-borne diseases, e.g. mosquito-borne, fly-borne, tick-borne or waterborne diseases whose impact is exacerbated by climate change
Landscapes
- Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Immunology (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Oncology (AREA)
- Transplantation (AREA)
- Medicinal Preparation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Description
溶液をベースとする系を製剤化するために、担体は活性物質を溶解する必要がある。低吸収性の薬物の改良された胃腸(GI)吸収は胆汁酸の存在下で薬物の溶解速度を増すことにより達成され得る。胃腸道内で、胆汁塩は、生物学的洗剤(これらはリン脂質と混合された場合に熱力学的に安定な混合ミセルを生成する)として挙動する。多くの場合、製剤化の選択は溶媒能により制限され、その他の場合には薬物が脂質製剤に充分に可溶性ではないであろう。
担体媒体は胃中でエマルション又はミクロエマルションを自然に生成するように設計されてもよく、それにより薬理学上活性な物質の吸収を促進する。これらの系は自己(ミクロ)乳化薬物送出系(SEDDS又はSMEDDS)として普通知られている。それらは正確に調製される必要があり、組成におけるわずかな変化でさえもがその系を不可逆的に乱さずに、またその有益な性質を損なわずに許容され得ない。例えば、活性物質がカプセル製剤の可溶化特性の変化の結果として沈殿し得る。この沈殿プロセスは不可逆的であり、患者の投薬不足をもたらし得る。カプセル製剤の乳化特性がまた変化され、投与後に、エマルションが胃中に生成されないかもしれない。結果として、薬理学上活性な物質が正確に、又は再現性良く吸収されないかもしれない。
懸濁液は熱力学的に不安定な多相系を呈するため、種々の特性がこれらの系の発生中に考慮される必要がある。懸濁液製剤の物理的安定性が粒子成長の予想からだけでなく、潜在的な多形(これは異なる溶解性を有し得る)の再結晶の予想又は沈降物のケーキングにより関連される沈降の予想から確実にされる必要がある。これらの因子は投薬形態からの活性物質の放出に影響するかもしれず、それ故、製品の貯蔵寿命中の患者の暴露の程度を変化させるかもしれない。それ故、単一担体賦形剤又は担体系中の活性物質の溶解性は物理的に安定な系の前提条件ではないであろう。
親油性担体系
親油性賦形剤は化学的に不安定な物質を保護するために水分バリヤー系として普通使用される。この目的のために、種々の脂肪又はワックスが固体投薬形態又はそれらの製造中間体に適用されて周囲の水蒸気又は酸素の移行を防止し、活性物質の化学安定性を改良し得る。親油性バインダーへの薬物のホットメルト封入体が同様に水分との接触を防止し得る。固体疎水性系は崩壊しにくいので、これらの系における薬物放出は、低粘度の液体脂質製剤中の薬物放出とは対照的に、遅延される。この遅延された薬物放出は変性された薬物送出系の活性物質の特定のプラスマプロフィールにより反映される (Ritschel W.ら, Die Tablette, 2002, 第2編, ECV, Aulendorf, p. 267f)。それ故、液体系の粘度が重要なパラメーターであり、適切な薬物放出を確実にするために慎重に調節される必要がある。
実際に、親油性製剤又は“脂質”製剤は広範囲の性質を有する多様なグループの製剤である。これらは純粋なトリグリセリド油から混合グリセリド、親油性界面活性剤、親水性界面活性剤及び水溶性補助溶媒に至る範囲の、最大5種類の賦形剤のブレンドから生じる。
製剤の性能はその相対的な生物学的利用能を測定することにより、即ち、その生物学的利用能を活性物質の水溶液の生物学的利用能と比較することにより評価し得る。系が溶解速度に関してではなく、薬物透過性に関して、匹敵する生物学的利用能を示す場合、活性物質のプレ全身(pre-systemic)又は全身代謝が全身暴露を決めるであろう。こうして、(脂質)懸濁液はまた生理条件内の活性物質の適切な溶解性のために患者の満足な暴露を示し得る。
この物質の化学構造が式(I)として以下に示される。
式(I)
本発明の更なる対象は、活性物質の懸濁液が担体、増粘剤そして必要により滑剤/可溶化剤を含む3-Z-[1-(4-(N-((4-メチル-ピペラジン-1-イル)-メチルカルボニル)-N-メチル-アミノ)-アニリノ)-1-フェニル-メチレン]-6-メトキシカルボニル-2-インドリノン-モノエタンスルホン酸塩の粘稠な懸濁液である上記製剤である。
本発明の好ましい実施態様において、担体は下記の脂質(親油性)担体から選ばれる:アセチル化モノグリセリド、トウモロコシ油グリセリド、中間鎖長トリグリセリド、中間鎖長部分グリセリド、カプリル酸/カプリン酸トリグリセリド、カプリル酸/カプリン酸/リノール酸トリグリセリド、カプリル酸/カプリン酸/コハク酸トリグリセリド、プロピレングリコールジカプリレート/ジカプレート、オレイン酸エチル、グリセロールモノ/ジオレエート、グリセロールモノリノレート、マクロゴールグリセロールカプリロカプレート、マクロゴールグリセロールリノレート、オレイン酸、ポリオキシルヒマシ油、ポリオキシル水添ヒマシ油、プロピレングリコールモノカプリレート、プロピレングリコールモノラウレート、精製された動物由来の油、精製大豆油、精製植物油、ソルビタンモノステアレート、又はこれらの混合物。
本発明の好ましい実施態様において、増粘剤はオレオゲル生成賦形剤(例えば、コロイドシリカもしくはベントナイト)、或いは高粘度の親油性もしくは両親媒性賦形剤(例えば、蜜蝋、グリセロールモノステアレート、水添植物油、部分水添植物油又は硬質脂肪)から選ばれる。
更に好ましい実施態様において、製剤は更に滑剤/可溶化剤を含む。
本発明の更なる対象は滑剤/可溶化剤がレシチンから選ばれる上記製剤である。
本発明の更なる対象はラウロイルマクロゴールグリセリド、リノレオイルマクロゴールグリセリド、マクロゴールグリセロールカプリロカプレート、マクロゴールグリセロールリノレート、オレオイルマクロゴールグリセリド、ポリオキシルヒマシ油、ポリオキシル水添ヒマシ油、ポリソルベート及びプロピレングリコールモノラウレートのような一種以上のマクロゴールグリセロール及び/又は可溶化剤を更に含む上記製剤である。
本発明の更なる対象はマクロゴールグリセロールがマクロゴールグリセロールヒドロキシステアレート又はマクロゴールグリセロールリシノレートから選ばれる、上記製剤である。
本発明の更なる対象はカプセル製剤が上記製剤を含むことを特徴とする、カプセルシェル及びカプセル製剤を含むカプセルである。
本発明の更なる対象はカプセルが軟質ゼラチンカプセルであることを特徴とする、上記カプセルである。
本発明の更なる対象はカプセル製剤が上記製剤を含むこと及びカプセルが必要によりシーリング又はバンディングにより、硬質ゼラチン若しくはヒドロキシプロピルメチルセルロース(HPMC)カプセル、ポリビニルアルコールポリマーカプセル又はプルランカプセルであることを特徴とする、カプセルシェル及びカプセル製剤を含むカプセルである。
本発明の更なる対象は薬物としての使用のための先に特定された製剤又は先に特定されたカプセルである。
本発明の更なる対象は抗増殖活性を有する医薬組成物としての使用のための先に特定された製剤又は先に特定されたカプセルである。
本発明の更なる対象は癌疾患、免疫疾患又は免疫成分を伴なう症状、及び線維症から選ばれた疾患又は症状の治療のための先に特定された製剤又は先に特定されたカプセルである。
本発明の更なる対象は有効量の先に特定された製剤又は先に特定されたカプセルを患者に毎日1回又は数回経口投与することを特徴とする、癌疾患、免疫疾患又は免疫成分を伴なう症状、及び線維症から選ばれた疾患又は症状を治療及び/又は予防する方法である。
本発明の更なる対象は体重1kg当り0.1mgから20mgまでの活性物質、好ましくは体重1kg当り0.5mgから4mgまでの活性物質の用量範囲の使用のための先に特定された製剤又は先に特定されたカプセルである。
本発明の更なる対象は一つ以上の先に特定されたカプセルを含む、カプセルの包装に適したガラス容器又は可撓性/硬質プラスチック容器である。
本発明の更なる対象は一つ以上の先に特定されたカプセルを含む、カプセルの包装に適したアルミニウムパウチ又は二重ポリバッグである。
本発明の更なる対象は必要によりアルミニウムパウチの過剰包装(オーバーパッケージング)とともに、一つ以上の先に特定されたカプセルを含む、カプセルの包装に適したプラスチック(例えば、PVC、PVDC又はアクラー(登録商標))ブリスターである。
本発明の更なる対象は一つ以上の先に特定されたカプセルを含む、カプセルの包装に適したアルミニウムブリスターである。
脂質懸濁液を含むこのような軟質ゼラチンカプセルの利点は製剤への水とり込みが非常に起こりそうもないことである。その投薬形態は三つの異なる区画、即ち、(a)親水性カプセルシェル及び(b)疎水性担体系(その中で、活性物質のわずかに吸湿性の粉末(c)が懸濁されている)に分けられる。周囲水分のために、水の含量がこれらの異なる区画内で変化し得る。平衡状態に達するまで、それが拡散により移行するであろう。含水量は薬物製品の種々の性質、例えば、活性物質の化学安定性(主として加水分解による)又はカプセルシェルの弾性に影響し得る。本系中の水とり込みは主としてカプセルシェル中である。これは水蒸気収着実験(図1に示される)だけでなく、カプセルの軟化との質量獲得の相関関係により示され得る。水とり込みは更に薬物物質の化学安定性に影響しない。これは、例えば、70℃で1ヶ月の応力安定性研究により、そして本発明の系についての長期(3年)及び促進(6ヶ月)安定性研究結果により確かめられる。
更に、これらの研究は密包装材料中で貯蔵された場合に本発明のカプセルについて質量増加又は粘着問題がないことを示していた。従って、このようなカプセルに推奨される包装は、例えば、alu/aluブリスター及びHDPEびんである。
既に前記されたように、本発明は活性物質3-Z-[1-(4-(N-((4-メチル-ピペラジン-1-イル)-メチルカルボニル)-N-メチル-アミノ)-アニリノ)-1-フェニル-メチレン]-6-メトキシカルボニル-2-インドリノン-モノエタンスルホン酸塩の脂質懸濁液製剤に関する。
本発明の好ましい実施態様において、活性物質3-Z-[1-(4-(N-((4-メチル-ピペラジン-1-イル)-メチルカルボニル)-N-メチル-アミノ)-アニリノ)-1-フェニル-メチレン]-6-メトキシカルボニル-2-インドリノン-モノエタンスルホン酸塩の脂質懸濁液製剤は、脂質担体、増粘剤及び滑剤/可溶化剤中の3-Z-[1-(4-(N-((4-メチル-ピペラジン-1-イル)-メチルカルボニル)-N-メチル-アミノ)-アニリノ)-1-フェニル-メチレン]-6-メトキシカルボニル-2-インドリノン-モノエタンスルホン酸塩の粘稠な懸濁液を含む。
本発明の更に好ましい実施態様において、3-Z-[1-(4-(N-((4-メチル-ピペラジン-1-イル)-メチルカルボニル)-N-メチル-アミノ)-アニリノ)-1-フェニル-メチレン]-6-メトキシカルボニル-2-インドリノン-モノエタンスルホン酸塩の量は脂質懸濁液製剤の1〜90質量%の範囲内、好ましくは10〜50質量%の範囲内で含まれる。
上記物理安定性の問題、例えば、再結晶又は粒子成長を避けるために、活性物質は担体に完全に不溶性であり、又は溶解される必要がある。親油性、親水性及び両親媒性の賦形剤並びに混合物の溶解性スクリーニングが本発明の脂質懸濁液を製剤化するための種々の潜在的な担体を明らかにした。本発明の脂質懸濁液のためのこれらの脂質担体の選択が本発明の更なる対象を表す。
安定性の問題、例えば、活性物質の加水分解は親水性担体成分によっても引き起こされるかもしれない。それ故、親水性ポリエチレングリコールをベースとする担体系は一般に一層疎水性の担体、例えば、脂質担体よりも劣る安定性を示すであろう。
本発明によれば、最も好ましい脂質担体は中間鎖長トリグリセリドである。それは脂質懸濁液製剤の1〜90質量%の範囲内、好ましくは10〜70質量%の範囲内で含まれる。好適な中間鎖長トリグリセリドは市販製品ミグリオール812(登録商標)、ミグリオール810(登録商標)、ミグリオール818(登録商標)、ミグリオール829(登録商標)又はミグリオール840(登録商標)であってもよい。
本発明によれば、最も好ましい増粘剤は硬質脂肪である。それは好ましくは懸濁液製剤の1〜30質量%の範囲内、最も好ましくは10〜30質量%の範囲内で含まれる。最適の硬質脂肪は30℃〜44℃の融解範囲、最も好ましくは33℃〜40℃の融解範囲を有する。好適な市販の製品はゲルシアー(登録商標)33/01、ウィテプソール(登録商標)W35又はソフチサン(登録商標)378である。硬質脂肪に最適の融解範囲の決定は図3に示されるように、経時のin-vitro溶解挙動に関する硬質脂肪の融解範囲の効果の測定により行ない得る。
レシチンは軟質ゼラチンカプセル中の担体系として一般的な賦形剤である。それはカプセル化中に高度に濃縮された懸濁液の滑剤として使用され、ダクト及びポンプの閉塞を防止し、カプセル化製剤の高い質量一様性を確実にする。更にレシチンは界面活性剤として作用し、これがin-vitro溶解試験中の製剤-液滴の分布だけでなく、薬物吸収のためのin-vivoの分布を改良し得る。更に、それはまた活性物質結晶の湿潤を改良し得る。好適なレシチンは市販製品トプシチン(登録商標)であってもよい。
驚くことに、或る含量までのレシチンは完成カプセルの溶解挙動を改良するのに有益であることがわかった。過剰量は、図2に示されるように、in-vitro溶解試験中に付加的な利益を示さない。
本発明の好ましい実施態様において、レシチンの量は脂質懸濁液製剤の0.1〜10質量%の範囲内、最も好ましくは0.25〜2.5質量%の範囲内で含まれる。
本発明の好ましい実施態様において、一種以上のマクロゴールグリセロールの量は脂質懸濁液製剤の0.1〜50質量%の範囲内、最も好ましくは0.3〜10質量%の範囲内で含まれる。3種の担体系(以下に記載される親水性P3、親油性P1及び界面活性剤を含む親油性P2半固体懸濁液製剤)が非臨床研究で生物学的利用能について試験され、それらの全てが活性物質3-Z-[1-(4-(N-((4-メチル-ピペラジン-1-イル)-メチルカルボニル)-N-メチル-アミノ)-アニリノ)-1-フェニル-メチレン]-6-メトキシカルボニル-2-インドリノン-モノエタンスルホン酸塩の経口投薬形態に適した選択肢であると同定された。
しかしながら、生物学的利用能の理由のために、図4に示された結果から明らかであるように、中間鎖長トリグリセリド、硬質脂肪及びレシチン中の3-Z-[1-(4-(N-((4-メチル-ピペラジン-1-イル)-メチルカルボニル)-N-メチル-アミノ)-アニリノ)-1-フェニル-メチレン]-6-メトキシカルボニル-2-インドリノン-モノエタンスルホン酸塩の粘稠な懸濁液を含む脂質(親油性)懸濁液製剤が好ましい。
それ故、図4は本発明の活性物質の水溶液(S)対種々の担体系(P1、P2及びP3)についての24時間にわたってラットで試験された絶対生物学的利用能(BA、%)の比較の結果を示す。その実験は以下に記載される。
下記の表は試験された担体系(半固体懸濁液製剤)の組成を示す。
半固体懸濁液が硬質ゼラチンカプセル(カプスゲル、no. Y0303490)に充填される。夫々のカプセルは製剤約15〜20mgを含む。カプセルが強制飼養と同様の特別な装置でラットに適用される。比較のために、0.5%ナトロソール250HXを含む水溶液が強制飼養により適用される。絶対生物学的利用能の計算のために、ラットの追加のグループが5%のグルコース溶液(水溶液(S))に溶解された化合物を静脈内投薬される。1グループ当たり5匹の雄のハン・ウィスターラット(系統: CrlGlxBrlHan:WI)が使用される。血液サンプリング時間は投薬後0.5時間、1時間、2時間、4時間、8時間、24時間であり、血漿が有効化HPLC/MS/MS方法により分析される。血漿レベルから、曲線下の時間曲線面積(AUC)が線形台形規則により計算される。経口製剤の用量標準化AUCが絶対生物学的利用能の計算のために静脈内製剤の用量標準化AUCにより割られる。図4に示された実験の結果からわかるように、生物学的利用能は水溶液(S:11%)及び活性物質の種々の担体系(P1:14%、P2:10%及びP3:10%)について同様であるが、個体間の変化(生物学的利用能の標準偏差)は水溶液(S)及び担体系(P1)の方が担体系(P2)及び(P3)よりも小さく(2.8及び4.1対7.4及び7.1)、溶液(S)に対する試験された製剤(P1、P2及びP3)での実用的に完全な相対生物学的利用能が示されるが、担体系(P2)及び(P3)における一層高い変化が示される。
硬質ゼラチンカプセル、ヒドロキシプロピルメチルセルロース(HPMC)カプセル、ポリビニルアルコールポリマーカプセル又はプルランカプセルの場合、カプセル中の充填物が更にシール又はバンディングされてもよい。
本発明の好ましい実施態様において、カプセルはカプセル製剤(又はカプセル充填物)が前記された脂質懸濁液製剤を含むことを特徴とする、ゼラチン、一種以上の可塑剤そして必要により更なる補助材料を含むカプセルシェル、及びカプセル製剤(又はカプセル充填物)からなる軟質ゼラチンカプセルである。
本発明のカプセル医薬投薬形態、特に軟質ゼラチンカプセルは、好適なガラス容器もしくは可撓性/硬質プラスチック容器(好ましくは非PVC材料をベースとする)、又は必要によりアルミニウムのオーバーパッケージング(アルミニウムパウチ)つきのプラスチック(例えば、PVC、PVDC又はアクラー(登録商標))ブリスター、或いは、例えば、PA/Al/PVCの下部ホイル及びアルミニウム蓋ホイル(後者は最高の水保護を与える)からなるアルミニウムブリスター中に貯蔵されてもよい。それ故、容器は本発明のカプセル医薬投薬形態、特に軟質ゼラチンカプセルに特別な保護を与えるように、例えば、それらを光、酸素又は水から保護するように設計されてもよい。可撓性プラスチック容器は追加の保護(例えば、追加のアルミニウムパッケージングの形態で)を含んでもよい。
脂質懸濁液製剤は文献から知られている製剤の通常の製造方法により、即ち、均一にされた懸濁液を得るために成分を前もって決められた温度で前もって決められた順序で混合することにより調製されてもよい。
また、脂質懸濁液製剤は実施例10に記載された操作(これはまた本発明の対象である)に従って調製されてもよい。
本発明の活性物質の脂質懸濁液製剤、それを含む完成軟質ゼラチンカプセル及び完成軟質ゼラチンカプセルの包装のための包装材料が以下の実施例及び図面により示される。実施例は純粋に例示として利用され、限定と見なされるべきではない。
全ての実施例における活性物質は3-Z-[1-(4-(N-((4-メチル-ピペラジン-1-イル)-メチルカルボニル)-N-メチル-アミノ)-アニリノ)-1-フェニル-メチレン]-6-メトキシカルボニル-2-インドリノン-モノエタンスルホン酸塩である。
脂質をベースとする担体系
付加的な界面活性剤を含む脂質をベースとする担体系
親水性担体系
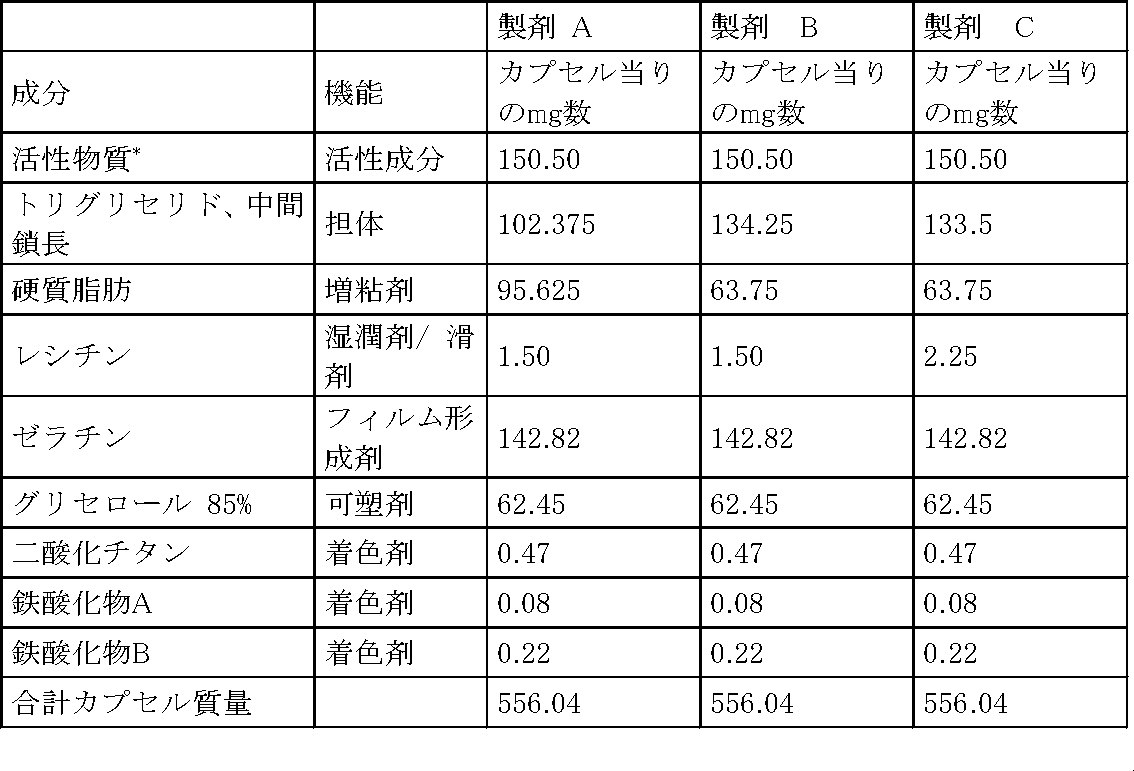
活性物質50mgを含む軟質ゼラチンカプセル
活性物質100mgを含む軟質ゼラチンカプセル
活性物質125mgを含む軟質ゼラチンカプセル
活性物質150mgを含む軟質ゼラチンカプセル
活性物質200mgを含む軟質ゼラチンカプセル
上記実施例4〜8の軟質ゼラチンカプセルの包装のための包装材料はガラス容器、可撓性/硬質プラスチック容器又は必要によりアルミニウムパウチ内の、PVC/PVDCブリスター、或いはalu/aluブリスターであってもよい。
[実施例10]
a:硬質脂肪及び中間鎖長トリグリセリドの一部を加工ユニット中で予備混合する。続いてレシチン、中間鎖長グリセリドの残部及び活性物質を添加する。その懸濁液を混合し、均一にし、脱気し、最後に篩分けて製剤(充填混合物)を製造する。
b.ゼラチンベースの塊成分(グリセロール、水及びゼラチン)を混合し、高温で溶解する。次いで、相当する着色剤を添加し、混合して、着色されたゼラチン塊を製造する。
c.カプセル化機械の調節後に、回転ダイ方法を使用して充填混合物及び着色されたゼラチン塊を軟質ゼラチンカプセルに加工する。この方法が、例えば、Swarbrick, Boylann, Encyclopedia of pharmaceutical technology, Marcel Dekker, 1990, 2巻, pp 269 ffに記載されている。
d.回転乾燥機を使用して初期乾燥を行なう。最終乾燥工程のために、カプセルをトレイに入れる。乾燥を15-26℃で低い相対湿度で行なう。
e.変形カプセル又は漏出しているカプセルを分離するためにカプセルの100%目視検査をした後に、カプセルをサイズ分類する。
f.最後に、オフセット印刷技術又はインクジェット印刷技術を使用して、カプセルを捺印する。また、リボン印刷技術(その技術では、ゼラチンバンドがカプセル化工程cの前に捺印される)を使用してカプセル捺印をすることもできる。
[1]
活性物質3-Z-[1-(4-(N-((4-メチル-ピペラジン-1-イル)-メチルカルボニル)-N-メチル-アミノ)-アニリノ)-1-フェニル-メチレン]-6-メトキシカルボニル-2-インドリノン-モノエタンスルホン酸塩の懸濁液を含む、前記活性物質の製剤。
[2]
活性物質の懸濁液が担体及び増粘剤を含む3-Z-[1-(4-(N-((4-メチル-ピペラジン-1-イル)-メチルカルボニル)-N-メチル-アミノ)-アニリノ)-1-フェニル-メチレン]-6-メトキシカルボニル-2-インドリノン-モノエタンスルホン酸塩の粘稠な懸濁液である、[1]記載の製剤。
[3]
担体が、アセチル化モノグリセリド、トウモロコシ油グリセリド、オレイン酸エチル、グリセロールモノ/ジオレエート、グリセロールモノリノレート、グリセロール、マクロゴールグリセロールカプリロカプレート、マクロゴールグリセロールリノレート、中間鎖長部分グリセリド、中間鎖長トリグリセリド、カプリル酸-カプリン酸トリグリセリド、カプリル酸/カプリン酸/リノール酸トリグリセリド、カプリル酸/カプリン酸/コハク酸トリグリセリド、プロピレングリコールジカプリレート/ジカプレート、オレイン酸、液体又は半固体の低粘度/中間粘度のポリエチレングリコール、ポリオキシルヒマシ油、ポリオキシル水添ヒマシ油、プロピレングリコールモノカプリレート、プロピレングリコールモノラウレート、精製された動物由来の油、精製大豆油、精製植物油、ソルビタンモノステアレート、トリアセチン、クエン酸トリエチル、又はこれらの混合物から選ばれる、[2]記載の製剤。
[4]
増粘剤が半固体の高度に粘稠なポリエチレングリコールもしくは固体のポリエチレングリコール、オレオゲル生成賦形剤、高粘度の親油性もしくは両親媒性賦形剤、及び硬質脂肪から選ばれる、[2]記載の製剤。
[5]
担体が脂質(親油性)担体である、[2]記載の製剤。
[6]
滑剤/可溶化剤を更に含む、[2]記載の製剤。
[7]
滑剤/可溶化剤がレシチンから選ばれる、[6]記載の製剤。
[8]
中間鎖長トリグリセリド、硬質脂肪及びレシチン中の3-Z-[1-(4-(N-((4-メチル-ピペラ
ジン-1-イル)-メチルカルボニル)-N-メチル-アミノ)-アニリノ)-1-フェニル-メチレン]-6-メトキシカルボニル-2-インドリノン-モノエタンスルホン酸塩の粘稠な懸濁液を含む、[7]記載の製剤。
[9]
一種以上のマクロゴールグリセロール及び/又は可溶化剤を更に含む、[1]から[8]のいずれか1項記載の製剤。
[10]
マクロゴールグリセロールがマクロゴールグリセロールヒドロキシステアレート又はマクロゴールグリセロールリシノレートから選ばれる、[9]記載の製剤。
[11]
カプセル製剤が[1]から[10]のいずれか1項記載の製剤を含むことを特徴とする、カプセルシェル及びカプセル製剤を含むカプセル。
[12]
カプセルが軟質ゼラチンカプセルであることを特徴とする、[11]記載のカプセル。
[13]
カプセルシェルがグリセロールを可塑剤として含むことを特徴とする、[11]記載のカプセル。
[14]
カプセルが、必要によりシーリング又はバンディングつきの、硬質ゼラチンもしくはヒドロキシプロピルメチルセルロース(HPMC)カプセル、ポリビニルアルコールポリマーカプセル又はプルランカプセルであることを特徴とする、[11]記載のカプセル。
[15]
薬物としての使用のための[1]から[10]のいずれか1項記載の製剤又は[11]から[14]のいずれか1項記載のカプセル。
[16]
抗増殖活性を有する医薬組成物としての使用のための[1]から[10]のいずれか1項記載の製剤又は[11]から[14]のいずれか1項記載のカプセル。
[17]
癌疾患、免疫疾患又は免疫成分を伴なう症状、及び線維症から選ばれた疾患又は症状の治療のための[1]から[10]のいずれか1項記載の製剤又は[11]から[14]のいずれか1項記載のカプセル。
[18]
癌疾患、免疫疾患又は免疫成分を伴なう症状、及び線維症から選ばれた疾患又は症状の治療のための薬物の調製のための[1]から[10]のいずれか1項記載の製剤又は[11]から[14]のいずれか1項記載のカプセルの使用。
[19]
有効量の[1]から[10]のいずれか1項記載の製剤又は[11]から[14]のいずれか1項記載のカプセルを患者に毎日1回又は数回経口投与することを特徴とする、癌疾患、免疫疾患又は免疫成分を伴なう症状、及び線維症から選ばれた疾患又は症状を治療及び/又は予防する方法。
[20]
体重1kg当り0.1mgから20mgの用量範囲の活性物質を使用するための[1]から[10]のいずれか1項記載の製剤又は[11]から[14]のいずれか1項記載のカプセル。
[21]
[11]から[14]のいずれか1項記載の一つ以上のカプセルを含む、カプセルの包装に適したガラス容器又は可撓性/硬質プラスチック容器。
[22]
[11]から[14]のいずれか1項記載の一つ以上のカプセルを含む、カプセルの包装に適した、必要によりアルミニウムのオーバーパッケージングつきのプラスチックブリスター、又はアルミニウムブリスター。
Claims (12)
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP08157748.8 | 2008-06-06 | ||
| EP08157748 | 2008-06-06 | ||
| PCT/EP2009/056878 WO2009147212A1 (en) | 2008-06-06 | 2009-06-04 | Capsule pharmaceutical dosage form comprising a suspension formulation of an indolinone derivative |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2014163667A Division JP5905542B2 (ja) | 2008-06-06 | 2014-08-11 | インドリノン誘導体の懸濁液製剤を含むカプセル医薬投薬形態 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2011522812A JP2011522812A (ja) | 2011-08-04 |
| JP5661031B2 true JP5661031B2 (ja) | 2015-01-28 |
Family
ID=40911908
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011512128A Active JP5661031B2 (ja) | 2008-06-06 | 2009-06-04 | インドリノン誘導体の懸濁液製剤を含むカプセル医薬投薬形態 |
| JP2014163667A Active JP5905542B2 (ja) | 2008-06-06 | 2014-08-11 | インドリノン誘導体の懸濁液製剤を含むカプセル医薬投薬形態 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2014163667A Active JP5905542B2 (ja) | 2008-06-06 | 2014-08-11 | インドリノン誘導体の懸濁液製剤を含むカプセル医薬投薬形態 |
Country Status (35)
| Country | Link |
|---|---|
| US (4) | US20110301177A1 (ja) |
| EP (1) | EP2299987B1 (ja) |
| JP (2) | JP5661031B2 (ja) |
| KR (2) | KR20170020557A (ja) |
| CN (2) | CN102056598B (ja) |
| AR (1) | AR072059A1 (ja) |
| AU (1) | AU2009254548B2 (ja) |
| BR (1) | BRPI0913434B8 (ja) |
| CA (1) | CA2726267C (ja) |
| CL (1) | CL2010001279A1 (ja) |
| CO (1) | CO6280467A2 (ja) |
| CY (1) | CY1120533T1 (ja) |
| DK (1) | DK2299987T3 (ja) |
| EA (1) | EA029996B1 (ja) |
| EC (1) | ECSP10010660A (ja) |
| ES (1) | ES2669469T3 (ja) |
| HR (1) | HRP20180709T1 (ja) |
| HU (1) | HUE039187T2 (ja) |
| IL (1) | IL208954A (ja) |
| LT (1) | LT2299987T (ja) |
| MA (1) | MA32385B1 (ja) |
| MX (2) | MX2010013203A (ja) |
| MY (1) | MY158930A (ja) |
| NO (1) | NO2299987T3 (ja) |
| NZ (1) | NZ603162A (ja) |
| PE (1) | PE20100254A1 (ja) |
| PL (1) | PL2299987T3 (ja) |
| PT (1) | PT2299987T (ja) |
| RS (1) | RS57142B1 (ja) |
| SI (1) | SI2299987T1 (ja) |
| TW (1) | TW201002691A (ja) |
| UA (1) | UA104590C2 (ja) |
| UY (1) | UY31879A (ja) |
| WO (1) | WO2009147212A1 (ja) |
| ZA (1) | ZA201007636B (ja) |
Families Citing this family (35)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| UA107560C2 (uk) * | 2008-06-06 | 2015-01-26 | Фармацевтична лікарська форма для негайного вивільнення похідної індолінону | |
| US20170065529A1 (en) | 2015-09-09 | 2017-03-09 | Boehringer Ingelheim International Gmbh | Pharmaceutical dosage form for immediate release of an indolinone derivative |
| MX2010013203A (es) | 2008-06-06 | 2011-02-25 | Boehringer Ingelheim Int | Forma de dosificacion farmaceutica en capsula que comprende una formulacion en suspension de un derivado de indolinona. |
| JO3659B1 (ar) * | 2010-06-02 | 2020-08-27 | Astellas Deutschland Gmbh | أشكال جرعات بينداموستين عن طريق الفم وإستخداماته العلاجية |
| US20130202693A1 (en) * | 2010-06-02 | 2013-08-08 | Astellas Deutschland Gmbh | Oral Dosage Forms of Bendamustine |
| GB201020032D0 (en) * | 2010-11-25 | 2011-01-12 | Sigmoid Pharma Ltd | Composition |
| JP2015532272A (ja) | 2012-09-28 | 2015-11-09 | ベーリンガー インゲルハイム インターナショナル ゲゼルシャフト ミット ベシュレンクテル ハフツング | 二重アンジオポエチン−2/Dll4結合剤および抗VEGF−R剤を含む薬学的組み合わせ |
| US20140350022A1 (en) | 2013-05-10 | 2014-11-27 | Boehringer Ingelheim International Gmbh | Efficacious treatment of NSCLC and predictive clinical marker of the responsiveness of a tumour to a treatment |
| JP6799201B2 (ja) | 2013-07-31 | 2020-12-16 | アヴァリン ファーマ インク. | エアロゾルチロシンキナーゼ阻害剤の化合物、及びその使用 |
| US20150209360A1 (en) * | 2014-01-30 | 2015-07-30 | Orbz, Llc | Oral caffeine delivery composition |
| CN106031716B (zh) * | 2015-03-13 | 2022-04-15 | 江苏豪森药业集团有限公司 | 含有吲哚满酮衍生物混悬液的药物制剂及其制备方法 |
| KR102643821B1 (ko) | 2015-06-06 | 2024-03-07 | 클라우드브레이크 테라퓨틱스, 엘엘씨 | 익상편을 치료하기 위한 조성물 및 방법 |
| CN107019697A (zh) * | 2016-02-02 | 2017-08-08 | 瑞阳(苏州)生物科技有限公司 | 预防或治疗纤维化疾病的药物组合物及其应用 |
| KR102657707B1 (ko) | 2016-06-02 | 2024-04-15 | 에이디에스 테라퓨틱스 엘엘씨 | 녹내장 수술 성공을 개선하기 위해 닌테다닙을 사용하는 조성물 및 방법 |
| US10561630B2 (en) * | 2016-10-25 | 2020-02-18 | Glykon Technologies Group, Llc | Hydroxycitric acid compounds and capsule liquid delivery |
| CN108066343A (zh) * | 2016-11-08 | 2018-05-25 | 瑞阳(苏州)生物科技有限公司 | 一种预防或治疗肾纤维化疾病的药物 |
| WO2018108669A1 (en) | 2016-12-12 | 2018-06-21 | Boehringer Ingelheim International Gmbh | Nintedanib for use in methods for the treatment of interstitial lung diseases by coadministration with olodaterol |
| EP3600322A1 (en) | 2017-03-28 | 2020-02-05 | Boehringer Ingelheim International GmbH | Nintedanib for use in methods for the treatment of muscular dystrophy |
| CN107184549B (zh) * | 2017-04-11 | 2020-11-20 | 江苏大学 | 一种尼达尼布自微乳制剂和其制成的软胶囊及制备方法 |
| ES3041129T3 (en) | 2017-10-23 | 2025-11-07 | Boehringer Ingelheim Int | New combination of active agents for the treatment of progressive fibrosing interstitial lung diseases (pf-ild) |
| WO2019106692A1 (en) * | 2017-11-29 | 2019-06-06 | Sun Pharmaceutical Industries Limited | Oral suspension of nintedanib esylate |
| PL3761980T3 (pl) | 2018-03-07 | 2024-06-10 | Pliant Therapeutics, Inc. | Związki aminokwasowe i sposoby zastosowania |
| CN113292537B (zh) | 2018-06-15 | 2024-04-05 | 汉达癌症医药责任有限公司 | 激酶抑制剂的盐类及其组合物 |
| CN113301884A (zh) * | 2018-09-13 | 2021-08-24 | 夫特弗制药私人有限公司 | 非水性化疗口服悬浮液 |
| AU2019363244B2 (en) | 2018-10-15 | 2024-10-03 | Cipla Limited | Pharmaceutical formulation |
| CN112386580B (zh) * | 2019-08-13 | 2022-07-08 | 齐鲁制药有限公司 | 具有改善的溶出度和稳定性的尼达尼布药物制剂、制备方法及其应用 |
| KR20220109439A (ko) | 2019-12-04 | 2022-08-04 | 이도르시아 파마슈티컬스 리미티드 | 섬유증 질환의 치료에서 사용하기 위한 아제티딘 lpa1 수용체 길항제와 피르페니돈 및/또는 닌테다닙의 조합 |
| WO2021198253A1 (en) | 2020-04-01 | 2021-10-07 | Boehringer Ingelheim International Gmbh | Use of biomarkers in the treatment of fibrotic conditions |
| EP4098246A1 (en) | 2021-05-31 | 2022-12-07 | Lotus Pharmaceutical Co., Ltd. | Formulation of nintedanib |
| CA3234791A1 (en) * | 2021-10-14 | 2023-04-20 | Eric Lefebvre | Integrin inhibitors and uses thereof in combination with other agents |
| CN114404382B (zh) * | 2022-01-24 | 2023-05-12 | 南京康川济医药科技有限公司 | 乙磺酸尼达尼布软胶囊及其制备方法 |
| CN119630395A (zh) | 2022-02-28 | 2025-03-14 | 努福米克斯技术有限公司 | 用于治疗特发性肺纤维化的组合物和方法 |
| JP2025525881A (ja) | 2022-08-16 | 2025-08-07 | ベーリンガー インゲルハイム インターナショナル ゲゼルシャフト ミット ベシュレンクテル ハフツング | 眼内使用するためのニンテダニブの医薬製剤 |
| TW202532079A (zh) * | 2024-02-05 | 2025-08-16 | 瑩碩生技醫藥股份有限公司 | 醫藥組成物及其用途 |
| WO2025254255A1 (ko) | 2024-06-05 | 2025-12-11 | 영진약품 주식회사 | 닌테다닙 또는 이의 약학적으로 허용가능한 염을 포함하는 개선된 용출률을 갖는 신규한 정제 및 이의 제조방법 |
Family Cites Families (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2870062A (en) | 1956-04-27 | 1959-01-20 | Scherer Corp R P | Gelatin composition for capsules |
| GB8305693D0 (en) | 1983-03-02 | 1983-04-07 | Scherer Ltd R P | Pharmaceutical compositions |
| EP0169398B1 (de) | 1984-07-24 | 1990-08-29 | R.P. Scherer GmbH | Oxytetracyclin-HC1-Weichgelatinekapseln und Verfahren zu ihrer Herstellung |
| GB9313329D0 (en) * | 1993-06-28 | 1993-08-11 | Scherer Ltd R P | Softgel capsule shell compositions |
| DE19603402A1 (de) | 1995-02-24 | 1996-08-29 | Basf Ag | Weichgelatinekapseln |
| US6762180B1 (en) | 1999-10-13 | 2004-07-13 | Boehringer Ingelheim Pharma Kg | Substituted indolines which inhibit receptor tyrosine kinases |
| GEP20053654B (en) * | 2001-05-01 | 2005-11-10 | Pfizer Prod Inc | Method For Manufacturing Low Dose Pharmaceutical Composition Having Uniform Drug Distribution |
| DE10233500A1 (de) * | 2002-07-24 | 2004-02-19 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | 3-Z-[1-(4-(N-((4-Methyl-piperazin-1-yl)-methylcarbonyl)-N-methyl-amino)-anilino)-1-phenyl-methylen]-6-methoxycarbonyl-2-indolinon-Monoethansulfonat und dessen Verwendung als Arzneimittel |
| US20050043233A1 (en) | 2003-04-29 | 2005-02-24 | Boehringer Ingelheim International Gmbh | Combinations for the treatment of diseases involving cell proliferation, migration or apoptosis of myeloma cells or angiogenesis |
| US20060058311A1 (en) * | 2004-08-14 | 2006-03-16 | Boehringer Ingelheim International Gmbh | Combinations for the treatment of diseases involving cell proliferation |
| PE20060777A1 (es) * | 2004-12-24 | 2006-10-06 | Boehringer Ingelheim Int | Derivados de indolinona para el tratamiento o la prevencion de enfermedades fibroticas |
| US20060293260A1 (en) * | 2005-05-24 | 2006-12-28 | Wyeth | Useful high load concentrate compositions for control of ecto-and endo-parasites |
| PL1948180T3 (pl) | 2005-11-11 | 2013-09-30 | Boehringer Ingelheim Int | Terapia skojarzona raka polegająca na podawaniu inhibitorów EGFR/HER2 |
| MX2010013203A (es) | 2008-06-06 | 2011-02-25 | Boehringer Ingelheim Int | Forma de dosificacion farmaceutica en capsula que comprende una formulacion en suspension de un derivado de indolinona. |
| PT2293795E (pt) * | 2008-06-06 | 2015-11-17 | Boehringer Ingelheim Int | Combinação farmacêutica |
| UA107560C2 (uk) * | 2008-06-06 | 2015-01-26 | Фармацевтична лікарська форма для негайного вивільнення похідної індолінону | |
| JP2012515184A (ja) | 2009-01-14 | 2012-07-05 | ベーリンガー インゲルハイム インターナショナル ゲゼルシャフト ミット ベシュレンクテル ハフツング | 大腸がんの治療方法 |
| US8802384B2 (en) | 2009-03-12 | 2014-08-12 | Boehringer Ingelheim International Gmbh | Method or system using biomarkers for the monitoring of a treatment |
| US20120142703A1 (en) | 2009-05-14 | 2012-06-07 | Boehringer Ingelheim International Gmbh | New combination therapy in treatment of oncological and fibrotic diseases |
-
2009
- 2009-06-04 MX MX2010013203A patent/MX2010013203A/es active IP Right Grant
- 2009-06-04 NZ NZ60316209A patent/NZ603162A/en unknown
- 2009-06-04 CN CN200980121067.8A patent/CN102056598B/zh not_active Ceased
- 2009-06-04 KR KR1020177004310A patent/KR20170020557A/ko not_active Withdrawn
- 2009-06-04 ES ES09757593.0T patent/ES2669469T3/es active Active
- 2009-06-04 SI SI200931833T patent/SI2299987T1/en unknown
- 2009-06-04 UA UAA201100098A patent/UA104590C2/ru unknown
- 2009-06-04 MX MX2014006908A patent/MX359229B/es unknown
- 2009-06-04 CA CA2726267A patent/CA2726267C/en active Active
- 2009-06-04 US US12/995,869 patent/US20110301177A1/en not_active Abandoned
- 2009-06-04 NO NO09757593A patent/NO2299987T3/no unknown
- 2009-06-04 EA EA201001856A patent/EA029996B1/ru not_active IP Right Cessation
- 2009-06-04 HR HRP20180709TT patent/HRP20180709T1/hr unknown
- 2009-06-04 HU HUE09757593A patent/HUE039187T2/hu unknown
- 2009-06-04 EP EP09757593.0A patent/EP2299987B1/en active Active
- 2009-06-04 PE PE2009000782A patent/PE20100254A1/es not_active Application Discontinuation
- 2009-06-04 JP JP2011512128A patent/JP5661031B2/ja active Active
- 2009-06-04 MY MYPI2010005645A patent/MY158930A/en unknown
- 2009-06-04 KR KR1020107027317A patent/KR101725469B1/ko active Active
- 2009-06-04 DK DK09757593.0T patent/DK2299987T3/en active
- 2009-06-04 PT PT97575930T patent/PT2299987T/pt unknown
- 2009-06-04 BR BRPI0913434A patent/BRPI0913434B8/pt active IP Right Grant
- 2009-06-04 WO PCT/EP2009/056878 patent/WO2009147212A1/en not_active Ceased
- 2009-06-04 RS RS20180491A patent/RS57142B1/sr unknown
- 2009-06-04 CN CN201510660732.8A patent/CN105193720B/zh not_active Ceased
- 2009-06-04 PL PL09757593T patent/PL2299987T3/pl unknown
- 2009-06-04 AU AU2009254548A patent/AU2009254548B2/en active Active
- 2009-06-04 LT LTEP09757593.0T patent/LT2299987T/lt unknown
- 2009-06-05 AR ARP090102039A patent/AR072059A1/es unknown
- 2009-06-05 TW TW098118825A patent/TW201002691A/zh unknown
- 2009-06-08 UY UY0001031879A patent/UY31879A/es not_active Application Discontinuation
-
2010
- 2010-10-26 IL IL208954A patent/IL208954A/en active IP Right Grant
- 2010-10-26 ZA ZA2010/07636A patent/ZA201007636B/en unknown
- 2010-11-22 CL CL2010001279A patent/CL2010001279A1/es unknown
- 2010-12-03 CO CO10152519A patent/CO6280467A2/es not_active Application Discontinuation
- 2010-12-03 EC EC2010010660A patent/ECSP10010660A/es unknown
- 2010-12-06 MA MA33402A patent/MA32385B1/fr unknown
-
2013
- 2013-08-30 US US14/015,186 patent/US20140004187A1/en not_active Abandoned
-
2014
- 2014-08-11 JP JP2014163667A patent/JP5905542B2/ja active Active
-
2015
- 2015-10-07 US US14/877,132 patent/US20160022672A1/en not_active Abandoned
-
2016
- 2016-07-07 US US15/204,277 patent/US9907756B2/en active Active
-
2018
- 2018-05-15 CY CY20181100499T patent/CY1120533T1/el unknown
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5661031B2 (ja) | インドリノン誘導体の懸濁液製剤を含むカプセル医薬投薬形態 | |
| JP5583119B2 (ja) | インドリノン誘導体の即時放出のための医薬投薬形態 | |
| US10105323B2 (en) | Pharmaceutical dosage form for immediate release of an indolinone derivative | |
| AU2015227503B2 (en) | Capsule pharmaceutical dosage form comprising a suspension formulation of an indolinone derivative | |
| HK1152477A (en) | Capsule pharmaceutical dosage form comprising a suspension formulation of an indolinone derivative | |
| HK1152641A (en) | Pharmaceutical dosage form for immediate release of an indolinone derivative | |
| AU2015210331A1 (en) | Pharmaceutical dosage form for immediate release of an indolinone derivative |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20101203 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20101203 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130221 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20130517 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20130524 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130819 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20140409 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140811 |
|
| C60 | Trial request (containing other claim documents, opposition documents) |
Free format text: JAPANESE INTERMEDIATE CODE: C60 Effective date: 20140811 |
|
| C11 | Written invitation by the commissioner to file amendments |
Free format text: JAPANESE INTERMEDIATE CODE: C11 Effective date: 20140820 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20140926 |
|
| C21 | Notice of transfer of a case for reconsideration by examiners before appeal proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C21 Effective date: 20140929 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20141104 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20141202 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5661031 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R153 | Grant of patent term extension |
Free format text: JAPANESE INTERMEDIATE CODE: R153 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R153 | Grant of patent term extension |
Free format text: JAPANESE INTERMEDIATE CODE: R153 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R153 | Grant of patent term extension |
Free format text: JAPANESE INTERMEDIATE CODE: R153 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |