JP4854825B1 - 糖尿病の治療又は予防のためのジペプチジルペプチダーゼ−iv阻害剤としてのアミノテトラヒドロピラン - Google Patents
糖尿病の治療又は予防のためのジペプチジルペプチダーゼ−iv阻害剤としてのアミノテトラヒドロピラン Download PDFInfo
- Publication number
- JP4854825B1 JP4854825B1 JP2011536433A JP2011536433A JP4854825B1 JP 4854825 B1 JP4854825 B1 JP 4854825B1 JP 2011536433 A JP2011536433 A JP 2011536433A JP 2011536433 A JP2011536433 A JP 2011536433A JP 4854825 B1 JP4854825 B1 JP 4854825B1
- Authority
- JP
- Japan
- Prior art keywords
- compounds
- dpp
- mmol
- pyran
- diabetes
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- PEXPXTIKHASWFI-RKSDUNRASA-N C[C@@H](C[C@H]1N)CO[C@H]1[AlH2] Chemical compound C[C@@H](C[C@H]1N)CO[C@H]1[AlH2] PEXPXTIKHASWFI-RKSDUNRASA-N 0.000 description 1
- 0 C[C@](C1)CO[C@](*)[C@]1N Chemical compound C[C@](C1)CO[C@](*)[C@]1N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D309/00—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only ring hetero atom, not condensed with other rings
- C07D309/16—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only ring hetero atom, not condensed with other rings having one double bond between ring members or between a ring member and a non-ring member
- C07D309/28—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only ring hetero atom, not condensed with other rings having one double bond between ring members or between a ring member and a non-ring member with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D309/30—Oxygen atoms, e.g. delta-lactones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/415—1,2-Diazoles
- A61K31/4162—1,2-Diazoles condensed with heterocyclic ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/1703—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates
- A61K38/1709—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates from mammals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/22—Hormones
- A61K38/26—Glucagons
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2022—Organic macromolecular compounds
- A61K9/205—Polysaccharides, e.g. alginate, gums; Cyclodextrin
- A61K9/2054—Cellulose; Cellulose derivatives, e.g. hydroxypropyl methylcellulose
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/06—Antihyperlipidemics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/04—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/04—Ortho-condensed systems
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Diabetes (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Obesity (AREA)
- Hematology (AREA)
- Gastroenterology & Hepatology (AREA)
- Zoology (AREA)
- Immunology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Endocrinology (AREA)
- Marine Sciences & Fisheries (AREA)
- Emergency Medicine (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
Description
本発明は、新規置換3−アミノテトラヒドロピランに関し、これは、ジペプチジルペプチダーゼ−IV酵素の阻害剤(「DPP−4阻害剤」)であり、糖尿病、特に2型糖尿病のような、ジペプチジルペプチダーゼ−IV酵素が関与する疾患の治療又は予防に有用である。本発明は、また、このような化合物を含む医薬組成物、並びにジペプチジルペプチダーゼ−IV酵素が関与する前記疾患の予防又は治療における、これらの化合物及び組成物の使用に関する。
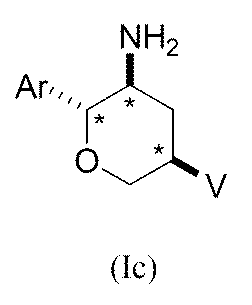
本発明は、ジペプチジルペプチダーゼ−IVの阻害剤として有用な新規置換3−アミノテトラヒドロピランに関する。本発明の化合物は、構造式I:
Arは、1〜5個のR1置換基で置換されていてもよいフェニルであり;
各R1は、独立して:
ハロゲン、
シアノ、
ヒドロキシ、
1〜5個のフッ素で置換されていてもよいC1−6アルキル、及び
1〜5個のフッ素で置換されていてもよいC1−6アルコキシ、からなる群から選択され;
各R2は、独立して:
水素、
ハロゲン、
シアノ、
アルコキシが独立してフッ素及びヒドロキシから選択される1〜5個の置換基で置換されていてもよい、C1−10アルコキシ、
アルキルが独立してフッ素及びヒドロキシから選択される1〜5個の置換基で置換されていてもよい、C1−10アルキル、
アルケニルが独立してフッ素及びヒドロキシから選択される1〜5個の置換基で置換されていてもよい、C2−10アルケニル、
アリールが独立してヒドロキシ、ハロゲン、シアノ、ニトロ、CO2H、C1−6アルキルオキシカルボニル、C1−6アルキル及びC1−6アルコキシから選択される1〜5個の置換基で置換されていてもよい、(CH2)n−アリール(ここで、アルキル及びアルコキシは1〜5個のフッ素で置換されていてもよい)、
ヘテロアリールが独立してヒドロキシ、ハロゲン、シアノ、ニトロ、CO2H、C1−6アルキルオキシカルボニル、C1−6アルキル及びC1−6アルコキシから選択される1〜3個の置換基で置換されていてもよい、(CH2)n−ヘテロアリール(ここで、アルキル及びアルコキシは1〜5個のフッ素で置換されていてもよい)、
ヘテロシクリルが独立してオキソ、ヒドロキシ、ハロゲン、シアノ、ニトロ、CO2H、C1−6アルキルオキシカルボニル、C1−6アルキル及びC1−6アルコキシから選択される1〜3個の置換基で置換されていてもよい、(CH2)n−ヘテロシクリル(ここで、アルキル及びアルコキシは1〜5個のフッ素で置換されていてもよい)、
シクロアルキルが独立してハロゲン、ヒドロキシ、シアノ、ニトロ、CO2H、C1−6アルキルオキシカルボニル、C1−6アルキル及びC1−6アルコキシから選択される1〜3個の置換基で置換されていてもよい、(CH2)n−C3−6シクロアルキル(ここで、アルキル及びアルコキシは1〜5個のフッ素で置換されていてもよい)、
(CH2)n−COOH、
(CH2)n−COOC1−6アルキル、
(CH2)n−NR4R5、
(CH2)n−CONR4R5、
(CH2)n−OCONR4R5、
(CH2)n−SO2NR4R5、
(CH2)n−SO2R6、
(CH2)n−NR7SO2R6、
(CH2)n−NR7CONR4R5、
(CH2)n−NR7COR7、及び
(CH2)n−NR7CO2R6、からなる群から選択され、
ここで、(CH2)n中の任意の個々のメチレン(CH2)炭素原子は、独立してフッ素、ヒドロキシ、C1−4アルキル及びC1−4アルコキシから選択される1〜2個の置換基で置換されていてもよく、アルキル及びアルコキシは1〜5個のフッ素で置換されていてもよく;
R3a及びR3bは、それぞれ独立して、水素又は1〜5個のフッ素で置換されていてもよいC1−4アルキルであり;
R4及びR5は、それぞれ独立して、
水素、
(CH2)m−フェニル、
(CH2)m−C3−6シクロアルキル、及び
C1−6アルキル、からなる群から選択され、
ここで、アルキルは、独立してフッ素及びヒドロキシから選択される1〜5個の置換基で置換されていてもよく、フェニル及びシクロアルキルは、独立してハロゲン、ヒドロキシ、C1−6アルキル、C1−6アルコキシから選択される1〜5個の置換基で置換されていてもよく、ここで、アルキル及びアルコキシは1〜5個のフッ素で置換されていてもよく;
又は、R4及びR5は、それらが結合する窒素原子と一緒になって、アゼチジン、ピロリジン、ピペリジン、ピペラジン及びモルホリンから選択される複素環を形成し、ここで、前記複素環は、独立してハロゲン、ヒドロキシ、C1−6アルキル及びC1−6アルコキシから選択される1〜3個の置換基で置換されていてもよく、アルキル及びアルコキシは1〜5個のフッ素で置換されていてもよく;
各R6は、独立してC1−6アルキルであり、ここでアルキルは、独立してフッ素及びヒドロキシルから選択される1〜5個の置換基で置換されていてもよく;
R7は、水素又はR6であり;
R8は:
−SO2C1−6アルキル、
−SO2C3−6シクロアルキル、
−SO2−アリール、
−SO2−ヘテロアリール、
−C(O)C1−6アルキル、
−C(O)C3−6シクロアルキル、
−C(O)−アリール、
−C(O)−ヘテロアリール、
−C(O)OC1−6アルキル、
−C(O)OC3−6シクロアルキル、
−C(O)O−アリール、
−C(O)O−ヘテロアリール、
−C(O)NHC1−6アルキル、
−C(O)NHC3−6シクロアルキル、
−C(O)NH−アリール、及び
−C(O)−NH−ヘテロアリール、からなる群から選択され、
ここで、アルキル及びシクロアルキルは、1〜5個のフッ素で置換されていてもよく、アリール及びヘテロアリールは、独立してヒドロキシ、ハロゲン、シアノ、ニトロ、CO2H、C1−6アルキルオキシカルボニル、C1−6アルキル及びC1−6アルコキシからなる群から選択される1〜5個の置換基で置換されていてもよく、アルキル及びアルコキシは1〜5個のフッ素で置換されていてもよく;
各nは独立して0、1、2又は3であり;そして
各mは独立して0、1又は2である]の化合物又は薬学的に許容されるその塩により記載される。
本発明の化合物の第4の実施態様においては、R8は、
−SO2C1−6アルキル、
−SO2C3−6シクロアルキル、
−SO2−アリール、及び
−SO2−ヘテロアリール、からなる群から選択され、
ここで、アルキル及びシクロアルキルは、1〜5個のフッ素で置換されていてもよく、アリール及びヘテロアリールは、独立してヒドロキシ、ハロゲン、シアノ、ニトロ、CO2H、C1−6アルキルオキシカルボニル、C1−6アルキル及びC1−6アルコキシからなる群から選択される1〜5個の置換基で置換されていてもよく、アルキル及びアルコキシは1〜5個のフッ素で置換されていてもよい。この第4の実施態様の一クラスにおいては、R8は、−SO2C1−6アルキル又は−SO2C3−6シクロアルキルであり、アルキル及びシクロアルキルは1〜5個のフッ素で置換されていてもよい。
水素、
アルキルが1〜5個のフッ素で置換されていてもよい、C1−6アルキル、及び
シクロアルキルが独立してハロゲン、ヒドロキシ、C1−4アルキル及びC1−4アルコキシから選択される1〜3個の置換基で置換されていてもよい、C3−6シクロアルキル(ここで、アルキル及びアルコキシは1〜5個のフッ素で置換されていてもよい)、からなる群から選択される。
(1)(i)グリタゾン類(例えば、ピオグリタゾン、ロシグリタゾン、ネトグリタゾン、リボグリタゾン及びバラグリタゾン)のようなPPARγアゴニスト、及び他のPPARリガンド((1)ムラグリタザル、アレグリタザル、ソデルグリタザル及びナバグリタザルのようなPPARα/γ二重アゴニスト、(2)フェノフィブリン酸誘導体(ゲムフィブロジル、クロフィブラート、シプロフィブラート、フェノフィブラート及びベザフィブラート)のようなPPARαアゴニスト、(3)WO02/060388、WO02/08188、WO2004/019869、WO2004/020409、WO2004/020408及びWO2004/066963に開示された化合物のような選択的PPARγモジュレータ(SPPARγM’s)及び(4)PPARγ部分アゴニスト);(ii)メトホルミン及び薬学的に許容されるその塩、特にメトホルミン塩酸塩のようなビグアニド類、並びにGlumetza(登録商標)、Fortamet(登録商標)及びGlucophageXR(登録商標)のような、それらの徐放製剤、(iii)タンパク質チロシンホスファターゼ−1B(PTP−1B)阻害剤、を含むインシュリン増感剤;
(2)インシュリンlispro、インシュリンdetemir、インシュリンglargine、インシュリンglulisine及びそれぞれの吸入可能製剤のような、インシュリン及びインシュリン類似体又は誘導体;
(3)メトレレプチンのような、レプチン及びレプチン誘導体、アゴニスト及び類似体;
(4)アミリン;ダバリンチドのようなアミリン類似体、及びプラムリンチドのようなアミリンアゴニスト;
(5)トルブタミド、グリブリド、グリピジド、グリメピリド、ミチグリニドのようなスルホニル尿素及び非スルホニル尿素インシュリン分泌促進剤、並びにナテグリニド及びレパグリニド等のメグリチニド類;
(6)α−グルコシダーゼ阻害剤(例えば、アカルボース、ボグリボース及びミグリトール):
(7)WO98/04528、WO99/01423、WO00/39088及びWO00/69810に開示された化合物のようなグルカゴン受容体アンタゴニスト;
(8)GLP−1、GLP−1類似体、誘導体及び模倣薬のようなインクレチン模倣薬(例えば、WO2008/011446、米国特許第5545618号、米国特許第6191102及び米国特許第56583111号を参照されたい);オキシントモジュリン、並びにその類似体及び誘導体(例えば、WO2003/022304、WO2006/134340、WO2007/100535を参照されたい)、グルカゴン、並びにその類似体及び誘導体(例えば、WO2008/101017を参照されたい)、鼻腔内、経皮及びそれらの週1回製剤、例えばエキセナチドQWを含む、エキセナチド、リラグルチド、タスポグルチド、アルビグルチド、AVE0010、CJC−1134−PC、NN9535、LY2189265、LY2428757及びBIM−51077のようなGLP−1受容体アゴニスト;
(9)(i)HMG−CoAレダクターゼ阻害剤(ロバスタチン、シンバスタチン、プラバスタチン、セリバスタチン、フルバスタチン、アトルバスタチン、ピタバスタチン及びロスバスタチン)、(ii)胆汁酸金属イオン封鎖剤(例えば、コレスチラミン、コレスチミド、塩酸コレセベラム、コレスチポール及び架橋デキストランのジアルキルアミノアルキル誘導体)、(iii)エゼチミブのようなコレステロール吸収の阻害剤、(iv)アバシミブのようなアシルCoA:コレステロールアシルトランスフェラーゼ阻害剤のような、LDLコレステロール低下剤;
(11)抗肥満化合物;
(12)アスピリン、非ステロイド抗炎症剤(NSAIDs)、グルココルチコイド及び選択的シクロオキシゲナーゼ−2(COX−2)阻害剤のような、炎症状態において用いられることを意図する薬剤;
(13)ACE阻害剤(例えば、エナラプリル、リシノプリル、ラミプリル、カプトプリル、キナプリル及びタンドラプリル)、A−II受容体遮断薬(例えば、ロサルタン、カンデサルタン、イルベサルタン、オルメサルタンメドキソミル、バルサルタン、テルミサルタン及びエプロサルタン)、レニン阻害剤(例えば、アリスキレン)、ベータ遮断薬(例えば、カルシウムチャンネル遮断薬)のような、抗高血圧薬;
(14)LY2599506のようなグルコキナーゼ活性化剤(GKAs);
(15)米国特許第6,730,690号;WO03/104207;及びWO04/058741に開示された化合物のような、11β−ヒドロキシステロイドデヒドロゲナーゼI型の阻害剤;
(16)トルセトラピブ及びMK−0859のような、コレステリルエステル転移タンパク質(CETP)の阻害剤;
(17)米国特許第6,054,587号;第6,110,903号;第6,284,748号;第6,399,782号及び第6,489,476号に開示された化合物のような、フルクトース1,6−ビスホスファターゼの阻害剤;
(18)アセチルCoAカルボキシラーゼ−1又は2(ACC1又はACC2)の阻害剤;
(19)AMP活性化蛋白質キナーゼ(AMPK)活性化剤;
(20)G−蛋白質共役受容体のアゴニスト:GPR−109、GPR−116、GPR−119及びGPR−40;
(21)WO2009/011836に開示された化合物のようなSSTR3アンタゴニスト;
(22)ニューロメジンU(NMU)及びニューロメジンS(NMS)並びにそれらの類似体及び誘導体を含むがこれらに限定されない、WO2007/109135及びWO2009/042053に開示された化合物のような、ニューロメジンU受容体1(NMUR1)及び/又はニューロメジンU受容体2(NMUR2)アゴニスト;
(23)ステアロイル−補酵素Aデルタ−9デサチュラーゼ(SCD)の阻害剤;
(24)WO2009/000087に開示された化合物のようなGPR−105(P2YR14)アンタゴニスト;
(25)SGLT−1のようなナトリウム−グルコーストランスポーター(SGLT)阻害剤及びその種々のアイソマー;ダパグリフロジン及びレモグリフロジンのようなSGLT−2;並びにSGLT−3のような、グルコース摂取の阻害剤;
(26)アシル補酵素A:ジアシルグリセロールアシルトランスフェラーゼ1及び2(DGAT−1及びDGAT−2)の阻害剤;
(27)脂肪酸シンターゼの阻害剤;
(28)アシル補酵素A:モノアシルグリセロールアシルトランスフェラーゼ1及び2(MGAT−1及びMGAT−2)の阻害剤;
(29)TGR5受容体のアゴニスト(GPBAR1、BG37、GPCR19、GPR131及びM−BARとしても知られている);
(30)ブロモクリプチンメシラート及びその急速放出製剤;
(31)ヒスタミンH3受容体アゴニスト、及び
(32)α2−アドレナリン作動性又はβ3−アドレナリン作動性受容体アゴニスト、
が含まれるが、これらに限定されない。
N−[4−((1S)−1−{3−(3,5−ジクロロフェニル)−5−[6−(トリフルオロメトキシ)−2−ナフチル]−1H−ピラゾール−1−イル}エチル)ベンゾイル]−β−アラニン;
N−[4−((1R)−1−{3−(3,5−ジクロロフェニル)−5−[6−(トリフルオロメトキシ)−2−ナフチル]−1H−ピラゾール−1−イル}エチル)ベンゾイル]−β−アラニン;
N−(4−{1−[3−(2,5−ジクロロフェニル)−5−(6−メトキシ−2−ナフチル)−1H−ピラゾール−1−イル]エチル}ベンゾイル)−β−アラニン;
N−(4−{(1S)−1−[3−(3,5−ジクロロフェニル)−5−(6−メトキシ−2−ナフチル)−1H−ピラゾール−1−イル]エチル}ベンゾイル)−β−アラニン;
N−(4−{(1S)−1−[(R)−(4−クロロフェニル)(7−フルオロ−5−メチル−1H−インドール−3−イル)メチル]ブチル}ベンゾイル)−β−アラニン、及び
N−(4−{(1S)−1−[(4−クロロフェニル)(6−クロロ−8−メチルキノリン−4−イル)メチル]ブチル}ベンゾイル)−β−アラニン;並びに薬学的に許容されるそれらの塩が含まれるが、これらに限定されない。
[5−(5−{4−[2−(トリフルオロメチル)フェノキシ]ピペリジン−1−イル}−1,3,4−チアジアゾール−2−イル)−2H−テトラゾール−2−イル]酢酸;
(2’−{4−[2−(トリフルオロメチル)フェノキシ]ピペリジン−1−イル}−2,5’−ビ−1,3−チアゾール−4−イル)酢酸;
(5−{3−[4−(2−ブロモ−5−フルオロフェノキシ)ピペリジン−1−イル]イソキサゾール−5−イル}−2H−テトラゾール−2−イル)酢酸;
(3−{3−[4−(2−ブロモ−5−フルオロフェノキシ)ピペリジン−1−イル]−1,2,4−オキサジアゾール−5−イル}−1H−ピロール−1−イル)酢酸;
(5−{5−[4−(2−ブロモ−5−フルオロフェノキシ)ピペリジン−1−イル]ピラジン−2−イル}−2H−テトラゾール−2−イル)酢酸、及び
(5−{2−[4−(5−ブロモ−2−クロロフェノキシ)ピペリジン−1−イル]ピリミジン−5−イル}−2H−テトラゾール−2−イル)酢酸;並びに薬学的に許容されるそれらの塩が含まれるが、これらに限定されない。
3−(6−エタンスルホニルピリジン−3−イルオキシ)−5−(2−ヒドロキシ−1−メチル−エトキシ)−N−(1−メチル−1H−ピラゾール−3−イル)ベンズアミド;
5−(2−ヒドロキシ−1−メチル−エトキシ)−3−(6−メタンスルホニルピリジン−3−イルオキシ)−N−(1−メチル−1H−ピラゾール−3−イル)ベンズアミド;
5−(1−ヒドロキシメチル−プロポキシ)−3−(6−メタンスルホニルピリジン−3−イルオキシ)−N−(1−メチル−1H−ピラゾール−3−イル)ベンズアミド;
3−(6−メタンスルホニルピリジン−3−イルオキシ)−5−(1−メトキシメチル−プロポキシ)−N−(1−メチル−1H−ピラゾール−3−イル)ベンズアミド;
5−イソプロポキシ−3−(6−メタンスルホニルピリジン−3−イルオキシ)−N−(1−メチル−1H−ピラゾール−3−イル)ベンズアミド;
5−(2−フルオロ−1−フルオロメチル−エトキシ)−3−(6−メタンスルホニルピリジン−3−イルオキシ)−N−(1−メチル−1H−ピラゾール−3−イル)ベンズアミド;
3−({4−[2−(ジメチルアミノ)エトキシ]フェニル}チオ)−N−(3−メチル−1,2,4−チアジアゾール−5−イル)−6−[(4−メチル−4H−1,2,4−トリアゾール−3−イル)チオ]ピリジン−2−カルボキサミド;
3−({4−[(1−メチルアゼチジン−3−イル)オキシ]フェニル}チオ)−N−(3−メチル−1,2,4−チアジアゾール−5−イル)−6−[(4−メチル−4H−1,2,4−トリアゾール−3−イル)チオ]ピリジン−2−カルボキサミド;
N−(3−メチル−1,2,4−チアジアゾール−5−イル)−6−[(4−メチル−4H−1,2,4−トリアゾール−3−イル)チオ]−3−{[4−(2−ピロリジン−1−イルエトキシ)フェニル]チオ}ピリジン−2−カルボキサミド、及び
3−[(4−{2−[(2R)−2−メチルピロリジン−1−イル]エトキシ}フェニル)チオ−N−(3−メチル−1,2,4−チアジアゾール−5−イル)−6−[(4−メチル−4H−1,2,4−トリアゾール−3−イル)チオ]ピリジン−2−カルボキサミド;並びに薬学的に許容されるそれらの塩が含まれるが、これらに限定されない。
rac−シス5−クロロ−2−{4−[2−(2−{[5−(メチルスルホニル)ピリジン−2−イル]オキシ}エチル)シクロプロピル]ピペリジン−1−イル}ピリミジン;
5−クロロ−2−{4−[(1R,2S)−2−(2−{[5−(メチルスルホニル)ピリジン−2−イル]オキシ}エチル)シクロプロピル]ピペリジン−1−イル}ピリミジン;
racシス−5−クロロ−2−[4−(2−{2−[4−(メチルスルホニル)フェノキシ]エチル}シクロプロピル)ピペリジン−1−イル]ピリミジン;
5−クロロ−2−[4−((1S,2R)−2−{2−[4−(メチルスルホニル)フェノキシ]エチル}シクロプロピル)ピペリジン−1−イル]ピリミジン;
5−クロロ−2−[4−((1R,2S)−2−{2−[4−(メチルスルホニル)フェノキシ]エチル}シクロプロピル)ピペリジン−1−イル]ピリミジン;
racシス−5−クロロ−2−[4−(2−{2−[3−(メチルスルホニル)フェノキシ]エチル}シクロプロピル)ピペリジン−1−イル]ピリミジン、及び
racシス−5−クロロ−2−[4−(2−{2−[3−(5−メチル−1,3,4−オキサジアゾール−2−イル)フェノキシ]エチル}シクロプロピル)ピペリジン−1−イル]ピリミジン;並びに薬学的に許容されるそれらの塩が含まれるが、これらに限定されない。
(2S)−2−({6−クロロ−3−[6−(4−クロロフェノキシ)−2−プロピルピリジン−3−イル]−1,2−ベンズイソキサゾール−5−イル}オキシ)プロパン酸;
(2S)−2−({6−クロロ−3−[6−(4−フルオロフェノキシ)−2−プロピルピリジン−3−イル]−1,2−ベンズイソキサゾール−5−イル}オキシ)プロパン酸;
(2S)−2−{[6−クロロ−3−(6−フェノキシ−2−プロピルピリジン−3−イル)−1,2−ベンズイソキサゾール−5−イル]オキシ}プロパン酸;
(2R)−2−({6−クロロ−3−[6−(4−クロロフェノキシ)−2−プロピルピリジン−3−イル]−1,2−ベンズイソキサゾール−5−イル}オキシ)プロパン酸;
(2R)−2−{3−[3−(4−メトキシ)ベンゾイル−2−メチル−6−(トリフルオロメトキシ)−1H−インドール−1−イル]フェノキシ}ブタン酸;
(2S)−2−{3−[3−(4−メトキシ)ベンゾイル−2−メチル−6−(トリフルオロメトキシ)−1H−インドール−1−イル]フェノキシ}ブタン酸;
2−{3−[3−(4−メトキシ)ベンゾイル−2−メチル−6−(トリフルオロメトキシ)−1H−インドール−1−イル]フェノキシ}−2−メチルプロパン酸、及び
(2R)−2−{3−[3−(4−クロロ)ベンゾイル−2−メチル−6−(トリフルオロメトキシ)−1H−インドール−1−イル]フェノキシ}プロパン酸;並びに薬学的に許容されるそれらの塩が含まれるが、これらに限定されない。
3−[1−(4−クロロフェニル)−トランス−3−フルオロシクロブチル]−4,5−ジシクロプロピル−r−4H−1,2,4−トリアゾール;
3−[1−(4−クロロフェニル)−トランス−3−フルオロシクロブチル]−4−シクロプロピル−5−(1−メチルシクロプロピル)−r−4H−1,2,4−トリアゾール;
3−[1−(4−クロロフェニル)−トランス−3−フルオロシクロブチル]−4−メチル−5−[2−(トリフルオロメトキシ)フェニル]−r−4H−1,2,4−トリアゾール;
3−[1−(4−クロロフェニル)シクロブチル]−4−メチル−5−[2−(トリフルオロメチル)フェニル]−4H−1,2,4−トリアゾール;
3−{4−[3−(エチルスルホニル)プロピル]ビシクロ[2.2.2]オクタ−1−イル}−4−メチル−5−[2−(トリフルオロメチル)フェニル]−4H−1,2,4−トリアゾール;
4−メチル−3−{4−[4−(メチルスルホニル)フェニル]ビシクロ[2.2.2]オクタ−1−イル}−5−[2−(トリフルオロメチル)フェニル]−4H−1,2,4−トリアゾール;
3−(4−{4−メチル−5−[2−(トリフルオロメチル)フェニル]−4H−1,2,4−トリアゾール−3−イル}ビシクロ[2.2.2]オクタ−1−イル)−5−(3,3,3−トリフルオロプロピル)−1,2,4−オキサジアゾール;
3−(4−{4−メチル−5−[2−(トリフルオロメチル)フェニル]−4H−1,2,4−トリアゾール−3−イル}ビシクロ[2.2.2]オクタ−1−イル)−5−(3,3,3−トリフルオロエチル)−1,2,4−オキサジアゾール;
5−(3,3−ジフルオロシクロブチル)−3−(4−{4−メチル−5−[2−(トリフルオロメチル)フェニル]−4H−1,2,4−トリアゾール−3−イル}ビシクロ[2.2.2]オクタ−1−イル)−1,2,4−オキサジアゾール;
5−(1−フルオロ−1−メチルエチル)−3−(4−{4−メチル−5−[2−(トリフルオロメチル)フェニル]−4H−1,2,4−トリアゾール−3−イル}ビシクロ[2.2.2]オクタ−1−イル)−1,2,4−オキサジアゾール;
2−(1,1−ジフルオロエチル)−5−(4−{4−メチル−5−[2−(トリフルオロメチル)フェニル]−4H−1,2,4−トリアゾール−3−イル}ビシクロ[2.2.2]オクタ−1−イル)−1,3,4−オキサジアゾール;
2−(3,3−ジフルオロシクロブチル)−5−(4−{4−メチル−5−[2−(トリフルオロメチル)フェニル]−4H−1,2,4−トリアゾール−3−イル}ビシクロ[2.2.2]オクタ−1−イル)−1,3,4−オキサジアゾール、及び
5−(1,1−ジフルオロエチル)−3−(4−{4−メチル−5−[2−(トリフルオロメチル)フェニル]−4H−1,2,4−トリアゾール−3−イル}ビシクロ[2.2.2]オクタ−1−イル)−1,2,4−オキサジアゾール;並びに薬学的に許容されるそれらの塩が含まれるが、これらに限定されない。
3−{1’−[(1−シクロプロピル−4−メトキシ−1H−インドール−6−イル)カルボニル]−4−オキソスピロ[クロマン−2,4’−ピペリジン]−6−イル}安息香酸;
5−{1’−[(1−シクロプロピル−4−メトキシ−1H−インドール−6−イル)カルボニル]−4−オキソスピロ[クロマン−2,4’−ピペリジン]−6−イル}ニコチン酸;
1’−[(1−シクロプロピル−4−メトキシ−1H−インドール−6−イル)カルボニル]−6−(1H−テトラゾール−5−イル)スピロ[クロマン−2,4’−ピペリジン]−4−オン;
1’−[(1−シクロプロピル−4−エトキシ−3−メチル−1H−インドール−6−イル)カルボニル]−6−(1H−テトラゾール−5−イル)スピロ[クロマン−2,4’−ピペリジン]−4−オン;
5−{1’−[(1−シクロプロピル−4−メトキシ−3−メチル−1H−インドール−6−イル)カルボニル]−4−オキソ−スピロ[クロマン−2,4’−ピペリジン]−6−イル}ニコチン酸;
4’−({6−(5−カルバモイルピリジン−2−イル)−4−オキソスピロ[クロマン−2,4’−ピペリジン]−1’−イル}カルボニル)−2’,6’−ジエトキシビフェニル−4−カルボン酸;
2’,6’−ジエトキシ−4’−{[6−(1−メチル−1H−ピラゾール−4−イル)−4−オキソスピロ[クロマン−2,4’−ピペリジン]−1’−イル]カルボニル}ビフェニル−4−カルボン酸;
2’,6’−ジエトキシ−3−フルオロ−4’−{[6−(1−メチル−1H−ピラゾール−4−イル)−4−オキソスピロ[クロマン−2,4’−ピペリジン]−1’−イル]カルボニル}ビフェニル−4−カルボン酸;
5−[4−({6−(3−カルバモイルフェニル)−4−オキソスピロ[クロマン−2,4’−ピペリジン]−1’−イル}カルボニル)−2,6−ジエトキシフェニル]ニコチン酸;
ナトリウム4’−({6−(5−カルバモイルピリジン−2−イル)−4−オキソスピロ[クロマン−2,4’−ピペリジン]−1’−イル}カルボニル)−2’,6’−ジエトキシビフェニル−4−カルボキシレート;
メチル4’−({6−(5−カルバモイルピリジン−2−イル)−4−オキソスピロ[クロマン−2,4’−ピペリジン]−1’−イル}カルボニル)−2’,6’−ジエトキシビフェニル−4−カルボキシレート;
1’−[(4,8−ジメトキシキノリン−2−イル)カルボニル]−6−(1H−テトラゾール−5−イル)スピロ[クロマン−2,4’−ピペリジン]−4−オン;
(5−{1’−[(4,8−ジメトキシキノリン−2−イル)カルボニル]−4−オキソスピロ[クロマン−2,4’−ピペリジン]−6−イル}−2H−テトラゾール−2−イル)メチルピバレート;
5−{1’−[(8−シクロプロピル−4−メトキシキノリン−2−イル)カルボニル]−4−オキソスピロ[クロマン−2,4’−ピペリジン]−6−イル}ニコチン酸;
1’−(8−メトキシ−4−モルホリン−4−イル−2−ナフトイル)−6−(1H−テトラゾール−5−イル)スピロ[クロマン−2,4’−ピペリジン]−4−オン、及び
1’−[(4−エトキシ−8−エチルキノリン−2−イル)カルボニル]−6−(1H−テトラゾール−5−イル)スピロ[クロマン−2,4’−ピペリジン]−4−オン;並びに薬学的に許容されるそれらの塩が含まれるが、これらに限定されない。
工程A:フェニル2,4,5−トリフルオロベンゾアート
フェノール(13.3g、141mmol)の無水ジクロロメタン(370mL)中の溶液を氷浴中で冷却し、N,N−ジイソプロピルエチルアミン(34mL、193mmol)で処理し、次いで、2,4,5−トリフルオロベンゾイルクロライド(25g、129mmol)を15分間かけて滴下して加えた。氷浴を取り除き、室温で撹拌を2時間継続し、次いで、溶液を分液漏斗に移し、有機層を塩酸溶液(2N、150mL)、飽和炭酸水素ナトリウム水溶液(150mL)及び食塩水(150mL)で連続的に洗浄し、無水硫酸ナトリウムで乾燥し、ろ過し、濃縮し、得られた固形生成物を、ヘキサン、次いでヘキサン中0〜5%エーテルの勾配様式で連続的に溶出し、シリカ上で何回に分けて精製し、フェニル2,4,5−トリフルオロベンゾアートを白色固体として得た。
水素化ナトリウム(12g、油中60%、297mmol)をヘキサンで洗浄し(4×100mL)、無水窒素を吹きつけ、N,N−ジメチルホルムアミド(350mL)中に懸濁し、次いでニトロメタン(44mL、81mmol)で処理した。得られた混合物を室温で2.5時間撹拌し、0℃まで冷却し、次いでフェニル2,4,5−トリフルオロベンゾアート(22.8g、90.0mmol)のN,N−ジメチルホルムアミド(180mL)中の溶液で2時間処理した。反応混合物を同じ温度に一晩維持し、室温で更に1時間、撹拌を続けた。混合物を濃塩酸(48mL)と一緒に氷(400g)に注ぎ入れた。水性混合物を酢酸エチル(3×250mL)で抽出した。一緒にした有機層を食塩水(40mL)で洗浄し、無水硫酸ナトリウムで乾燥し、ろ過し、減圧下で濃縮した。粗生成物をエーテル−ヘキサン(1:1、240mL)及び水(200mL)に溶解した。有機層を分離し、冷凍庫内に静置し、冷却して生成された結晶をろ過により回収し、乾燥し、2−ニトロ−1−(2,4,5−トリフルオロフェニル)エタノンを灰色がかった白色固体として得た。
3−クロロ−2−(クロロメチル)プロパ−1−エン(1.0g、8mmol)及びヨウ化ナトリウム(6.6g、44mmol)の混合物を、アセトン(60mL)中、室温で20時間撹拌し、減圧下で濃縮し、ジクロロメタン(150mL)及び水(50mL)に溶解した。有機層を硫酸ナトリウムで乾燥し、ろ過し、濃縮し、3−ヨード−2−(ヨードメチル)プロパ−1−エンを赤みがかった油状物質(2.45g)として得た。2−ニトロ−1−(2,4,5−トリフルオロフェニル)エタノン(110mg、0.5mmol)のN,N−ジメチルホルムアミド(3mL)及び3−ヨード−2−(ヨードメチル)プロパ−1−エン(170mg、0.55mmol)中の溶液にN,N−ジイソプロピルエチルアミン(0.20mL)を加え、混合物を60℃で2.5時間加熱し、濃縮し、Biotage Horizon(登録商標)システム上でクロマトグラフィー(シリカ、ヘキサン中0〜30%ジクロロメタンの勾配)により精製し、3−メチレン−5−ニトロ−6−(2,4,5−トリフルオロフェニル)−3,4−ジヒドロ−2H−ピランを得た。
3−メチレン−5−ニトロ−6−(2,4,5−トリフルオロフェニル)−3,4−ジヒドロ−2H−ピラン(798mg、2.94mmol)のクロロホルム(42mL)及びイソプロピルアルコール(7.8mL)中の溶液に、シリカゲル(5.1g)及び水素化ホウ素ナトリウム(420mg,11.1mmol)を加え、反応混合物を室温で30分間撹拌した。次いで、塩酸(6mL、2N)を滴下して加えることにより、反応混合物の反応を停止し、ろ過した。得られた固体の残渣を酢酸エチル(100mL)で洗浄した。一緒にしたろ液を、飽和炭酸水素ナトリウム水溶液及び食塩水で連続的に洗浄し、無水硫酸ナトリウムで乾燥し、濃縮した。得られた褐色の油状物質(802mg)をテトラヒドロフラン(15mL)に溶解し、1,8−ジアザビシクロ[5.4.0]ウンデカ−7−エン(DBU、40μL)を加えた。溶液を105分間撹拌し、次いで酢酸エチル(100mL)及び1N塩酸(50mL)を含む分液漏斗に移した。有機層を食塩水で洗浄し、水層を酢酸エチルで抽出した。一緒にした有機層を無水硫酸ナトリウムで乾燥し、ろ過し、濃縮し、粗生成物を得、これをフラッシュクロマトグラフィー(シリカ、ヘキサン中、8〜10%エーテル)により精製し、トランス−5−メチレン−3−ニトロ−2−(2,4,5トリフルオロフェニル)テトラヒドロ−2H−ピランを得た。この生成物(388mg)の一部をHPLC(ChiralCel OD、ヘプタン中1.5%イソプロピルアルコール)により分割し、遅く移動する鏡像異性体、(2R,3S)−5−メチレン−3−ニトロ−2−(2,4,5−トリフルオロフェニル)テトラヒドロ−2H−ピランを得た。
(2R,3S)−5−メチレン−3−ニトロ−2−(2,4,5−トリフルオロフェニル)テトラヒドロ−2H−ピラン(200mg、0.73mmol)及び亜鉛粉末(561mg、8.59mmol)のエタノール(7mL)中の激しく撹拌した懸濁液に6N塩酸(2.3mL、14mmol)を加えた。1時間後、混合物をエーテル(100mL)及び水酸化ナトリウム水溶液(2.5N、40mL)で処理した。有機層を飽和食塩水で洗浄し、無水硫酸ナトリウムで乾燥し、濃縮し、(2R,3S)−5−メチレン−2−(2,4,5−トリフルオロフェニル)テトラヒドロ−2H−ピラン−3−アミンを得、これは更に精製することなく次の工程で用いた。
(2R,3S)−5−メチレン−2−(2,4,5−トリフルオロフェニル)テトラヒドロ−2H−ピラン−3−アミン(177mg、0.73mmol)のジクロロメタン(5mL)中の溶液に、ジ−tert−ブチルジカルボネート(239mg、1.1mmol)を加え、混合物を室温で2.5時間撹拌した。減圧下で溶液を濃縮し、tert−ブチル[(2R,3S)−5−メチレン−2−(2,4,5−トリフルオロフェニル)テトラヒドロ−2H−ピラン−3−イル]カルバメートを白色固体として得た。これを、更に精製することなく次の工程で用いた。
tert−ブチル[(2R,3S)−5−メチレン−2−(2,4,5−トリフルオロフェニル)テトラヒドロ−2H−ピラン−3−イル]カルバメート(203mg、0.59mmol)のtert−ブチルアルコール(6mL)、アセトン(3mL)及び水(1.5mL)中の溶液に、四酸化オスミウム(tert−ブチルアルコール中2.5%溶液、0.113mL、0.009mmol)を加えた。得られた混合物を室温で10分間撹拌し、次いでN−メチルモルホリンN−オキシド(92mg、0.79mmol)で処理し、撹拌した。2日後、反応混合物を亜硫酸水素ナトリウム水溶液(5mL、2.0N)、10分後に酢酸エチルで処理した。有機層を、2N塩酸及び飽和炭酸水素ナトリウム水溶液で連続的に洗浄し、無水硫酸ナトリウムで乾燥し、ろ過し、濃縮し、tert−ブチル[(2R,3S)−5−ヒドロキシ−5−(ヒドロキシメチル)−2−(2,4,5−トリフルオロフェニル)テトラヒドロ−2H−ピラン−3−イル]カルバメートを得、これは更に精製することなく次の工程で用いた。
tert−ブチル[(2R,3S)−5−ヒドロキシ−5−(ヒドロキシメチル)−2−(2,4,5−トリフルオロフェニル)テトラヒドロ−2H−ピラン−3−イル]カルバメート(223mg、0.59mmol)のテトラヒドロフラン(4mL)中の溶液に、過ヨウ素酸ナトリウム(143mg,0.67mmol)の水(1.3mL)中の溶液を加え、混合物を3時間撹拌した。混合物を濃縮し、フラッシュクロマトグラフィー(シリカ、クロロホルム中5〜20%酢酸エチルの勾配)により精製し、tert−ブチル[(2R,3S)−5−オキソ−2−(2,4,5−トリフルオロフェニル)テトラヒドロ−2H−ピラン−3−イル]カルバメートを白色固体として得た。
中間体2
工程A:1−(2,5−ジフルオロフェニル)−2−ニトロエタノール
5℃で、水酸化ナトリウム(1N、3L)及びメタノール(1500mL)に、2,5−ジフルオロベンズアルデヒド(350g、2.46mol)及びニトロメタン(157mL、2.9mol)のメタノール(350mL)中の溶液を1時間かけて滴下して加えた。次いで、反応混合物を氷酢酸(165mL)で中和した。ジエチルエーテル(1500mL)を加え、層を分離した。有機層を、飽和炭酸ナトリウム水溶液(1000mL)及び飽和食塩水(1000mL)で連続的に洗浄した。有機層を無水硫酸マグネシウムで乾燥し、ろ過し、濃縮し、1−(2,5−ジフルオロフェニル)−2−ニトロエタノールを得、これは更に精製することなく工程Bで用いた。
10℃で、デス−マーチンペルヨージナン(125g)のジクロロメタン(600mL)中の溶液を、工程Aで製造したニトロアルコールの溶液(46.3g)に30分間かけて加えた。撹拌を2時間続け、次いで、反応混合物を、水(3L)中の炭酸水素ナトリウム(300g)及びチオ硫酸ナトリウム(333g)の混合物に注ぎ入れた。所望の生成物をメチルt−ブチルエーテル(MTBE)(2L)で抽出した。水層をHCl(2N、1.5L)で中和し、MTBE(3L)で抽出した。一緒にした有機層を無水硫酸マグネシウムで乾燥し、ろ過し、濃縮し、残渣をクロマトグラフィー(シリカゲル、ジクロロメタンで溶出)により精製し、所望のニトロケトンを得た。
3−クロロ−2−(クロロメチル)プロパ−1−エン(1.0g、8mmol)及びヨウ化ナトリウム(6.6g、44mmol)の混合物を、アセトン(60mL)中、室温で20時間撹拌し、減圧下で濃縮し、ジクロロメタン(150mL)及び水(50mL)で分配した。有機層を硫酸ナトリウムで乾燥し、ろ過し、濃縮し、3−ヨード−2−(ヨードメチル)プロパ−1−エンを赤みがかった油状物質として得た。
N,N−ジイソプロピルエチルアミン(184mL)を、2−ニトロ−1−(2,5−ジフルオロフェニル)エタノン(92.7g、461mmol)のN,N−ジメチルホルムアミド(1000mL)及び3−ヨード−2−(ヨードメチル)プロパ−1−エン(156g、507mmol)の溶液に加えた。混合物を60℃で2時間加熱し、濃縮し、クロマトグラフィー(シリカゲル、ヘキサン中0〜30%ジクロロメタンの勾配)により精製し、3−メチレン−5−ニトロ−6−(2,5−ジフルオロフェニル)−3,4−ジヒドロ−2H−ピランを得た。
この化合物は、3−メチレン−5−ニトロ−6−(2,5−トリフルオロフェニル)−3,4−ジヒドロ−2H−ピランを用い、中間体1、工程Dに記載されたのと同じ方法に従って製造した。
この化合物は、(2R,3S)−5−メチレン−3−ニトロ−2−(2,5−ジフルオロフェニル)テトラヒドロ−2H−ピランを用い、中間体1、工程Eに記載されたのと同じ方法に従って製造した。
この化合物は、(2R,3S)−5−メチレン−2−(2,5−ジフルオロフェニル)テトラヒドロ−2H−ピラン−3−アミンを用い、中間体1、工程Fに記載されたのと同じ方法に従って製造した。
この化合物は、tert−ブチル[(2R,3S)−5−メチレン−2−(2,5−ジフルオロフェニル)テトラヒドロ−2H−ピラン−3−イル]カルバメートを用い、中間体1、工程Gに記載されたのと同じ方法に従って製造した。
0℃で、tert−ブチル[(2R,3S)−5−ヒドロキシ−5−(ヒドロキシメチル)−2−(2,5−トリフルオロフェニル)テトラヒドロ−2H−ピラン−3−イル]カルバメート(10.5g)のメタノール(100mL)中の溶液に、ピリジン(7.8mL)及び四酢酸鉛(21.7g)を加えた。反応混合物を20分間撹拌した。酢酸エチルによる水性の処理により、粗生成物を与え、これをクロマトグラフィー(シリカ、0〜50%酢酸エチル/ヘプタン)により精製し、tert−ブチル[(2R,3S)−5−オキソ−2−(2,5−ジフルオロフェニル)テトラヒドロ−2H−ピラン−3−イル]カルバメートを白色固体として得た。
tert−ブチル3−オキソピロリジン−1−カルボキシレート(40g、216mmol)の溶液をDMF−DMA(267g、2241mmol)で処理し、105℃で40分間加熱した。溶液を冷却し、減圧下で濃縮し、得られた橙色の固体をヘキサン(200mL)で処理し、冷凍庫内で3日間冷却した。このようにして得られた黄褐色の固体をろ過により集め、乾燥し、更に精製することなく次の工程で用いた。
ヒドラジン(3mL)及びtert−ブチル(3Z)−3−[(ジメチルアミノ)メチレン]−4−オキソピロリジン−1−カルボキシレート(19.22g)のエタノール(40mL)中の溶液を、密封チューブ内、85℃で4時間加熱した。減圧下で溶媒を除去し、残渣をジクロロメタン(160mL)及び酢酸エチル(15mL)で粉砕した。得られた固体をろ過した。ろ液を濃縮し、得られた固体を再度粉砕し、ろ過した。一緒にした固体を、メタノール中の4N塩酸(250mL)で処理し、6時間撹拌した。反応混合物を濃縮し、乾燥させた。得られた固体を、メタノール中の4N塩酸(250mL)で、再度6時間処理した。濃縮し、乾燥させた後、得られた塩酸塩をメタノール中のアンモニア(2N、300mL)及び水中の水酸化アンモニウム溶液(28%、30mL)で処理し、濃縮し、乾燥させた。得られた固体をメタノール(70mL)及び水(5mL)で処理し、Biotage Horizon(登録商標)システム(シリカ、酢酸エチル中10%濃縮水酸化アンモニウムを含む5〜17%のメタノールの勾配)による3回のバッチで精製し、1,4,5,6−テトラヒドロピロロ[3,4−c]ピラゾールを得た。1H NMR(500MHz,CD3OD):δ4.04(d,4H);7.39(s,1H)。
1−(シクロペンチルスルホニル)−1,4,5,6−テトラヒドロピロロ[3,4−c]ピラゾール
2−(シクロペンチルスルホニル)−2,4,5,6−テトラヒドロピロロ[3,4−c]ピラゾール
N−Boc−ピラゾロピロリジン(中間体3、工程B)(316mg、1.51mmol)のジクロロメタン中の溶液に、N,N−ジイソプロピルエチルアミン(0.791mL)、次いでシクロペンタンスルホニルクロライド(0.299mL、2.265mmol)を加えた。混合物を室温で18時間撹拌した。反応混合物をBiotage(商標)カラムに乗せ、ヘキサン中の50%酢酸エチルでクロマトグラフに付し、中間体A及びBを、いずれも灰色がかった白色固体として得た。LC−MS:342.09(M+1)。
前記工程で調製した中間体A(84mg)を、ジクロロメタン(4.0mL)中、トリフルオロ酢酸(4.0mL)で室温で2時間処理した。反応混合物を濃縮し、ジクロロメタン中の2.5〜5%メタノール及び0.25〜0.5%水酸化アンモニウムで溶出するBiotage(商標)カラムにより精製し、標題の化合物を茶色のシロップとして得た。1H NMR(500MHz,CD3OD):δ1.60−1.81(m,4H);1.92−2.11(m,4H);3.92(m,2H);4.05(m,1H);4.12(m,2H);及び7.60(s,1H)。LC−MS:242.10(M+1)。
前記工程Aで調製した中間体B(275mg)を、ジクロロメタン(4.0mL)中、トリフルオロ酢酸(4.0mL)で、室温で2時間処理した。反応物を濃縮し、残渣を、ジクロロメタン中の5%メタノール及び0.5%水酸化アンモニウムで溶出するシリカゲルカラムで精製し、標題の化合物を茶色のシロップとして得た。1H NMR(500MHz,CD3OD):δ1.60−1.75(m,4H);1.89−2.07(m,4H);3.93−4.01(m,5H)及び7.84(s,1H)。LC−MS:242.05(M+1)。
工程A:tert−ブチル1−(メチルスルホニル)]−4,6−ジヒドロピロロ[3,4−c]ピラゾール−5(1H)−カルボキシレート(A)及びtert−ブチル2−(メチルスルホニル)]−2,6−ジヒドロピロロ[3,4−c]ピラゾール−5(4H)−カルボキシレート(B)
N−Boc−ピラゾロピロリジン(中間体3、工程B)(27.16g、130mmol)の無水アセトニトリル(1.0L)中の懸濁液を温度計及び添加漏斗を取り付けた2.0Lの三ツ口フラスコに入れ、窒素雰囲気下、水素化ナトリウム(油中、60%分散液、6.23g、156mmol)で一度に処理した。反応混合物を室温で2時間撹拌した。次いで、得られた白色の懸濁液を氷浴中で冷却し、塩化メタンスルホニル(25.2mL、324mmol)を添加漏斗を通してゆっくりと加えた。次いで、氷浴を取り除き、混合物を室温で1時間撹拌した。水(500mL)を用いて反応混合物の反応を停止し、層を分離した。次いで、水層を2×500mLのジクロロメタンで抽出した。一緒にした有機層を硫酸ナトリウムで乾燥し、減圧下で濃縮し、生成物A及びBの混合物を無色のシロップとして得た。CD3OD中のNMRは、生成物A中のピラゾール環のプロトンが7.70ppmに現れるが、生成物B中のプロトンが7.95ppmに現れる、2種の生成物の1:1混合物であることを示した。LC−MS:288.08(M+1)。
0℃で、前記工程で調製した中間体A及びB(48.4g、168mmol)をジクロロメタン(400mL)中に含む溶液に、トリフルオロ酢酸(200mL)をゆっくりと加えた。加えた後、冷却槽を取り除き、反応物を室温で2時間撹拌させた。減圧下で溶媒を除去し、次いで、得られたトリフルオロ酢酸塩を、ジクロロメタン中の25%メタノール及び2.5%水酸化アンモニウム500mLで中和した。溶媒を除去した後、ジクロロメタン中、2.5〜12.5%メタノール及び0.25〜1.25%水酸化アンモニウムで溶出するBiotage(商標)カラム(2×340g)によるクロマトグラフィーの後に、所望の中間体5を得た。LC−MS:109.85(M+1)。
1−(シクロプロピルスルホニル)−1,4,5,6−テトラヒドロピロロ[3,4−c]ピラゾール
2−(シクロプロピルスルホニル)−2,4,5,6−テトラヒドロピロロ[3,4−c]ピラゾール
室温で、窒素雰囲気下、水素化ナトリウム(油中、60%分散液、1.55g、38.7mmol)の無水アセトニトリル(200mL)中の懸濁液を、N−Boc−ピラゾロピロリジン(中間体3、工程B)(5.3g、25.5mmol)に一度に加えた。反応混合物を室温で2時間撹拌した。得られた白色の懸濁液に、シクロプロパンスルホニルクロライド(6.9g、49.1mmol)をゆっくりと加え、混合物を室温で18時間撹拌し、水(120mL)により反応を停止し、層を分離した。次いで、水層を2×100mLのジクロロメタンで抽出した。一緒にした有機層を硫酸ナトリウムで乾燥し、減圧下で濃縮した。シリカゲルクロマトグラフィー(300g Biotage(商標)カラム)により粗生成物を精製し、ヘキサン中15〜80%酢酸エチルで溶出して原料を精製し、化合物A及び化合物Bを、いずれも白色固体として得た。LC−MS:314.21(M+1)。
室温で、化合物A(60mg、0.19mmol)のジクロロメタン(1.0mL)中の溶液をトリフルオロ酢酸(1.0mL)で処理した。1.5時間後、反応物を濃縮し、ジクロロメタン中の5〜10%メタノール及び0.5〜1%NH4OHを用いるシリカゲルカラムにより精製し、標題の化合物を琥珀色の泡状物質として得た。1H NMR(500MHz,CD3OD):δ1.14−1.23(m,2H);1.31−1.38(m,2H);2.91−2.97(m,1H);4.01−4.05(m,2H);4.20−4.24(m,2H);7.60(s,1H)。LC−MS:214.13(M+1)。
工程A:tert−ブチル{(2R,3S,5R)−2−(2,5−ジフルオロフェニル)−5−[2−(メチルスルホニル)−2,6−ジヒドロピロロ[3,4−c]ピラゾール−5(4H)−イル]テトラヒドロ−2H−ピラン−3−イル}カルバメート
中間体2(26.3g、80mmol)及び2−(メチルスルホニル)−2,4,5,6−テトラヒドロピロロ[3,4−c]ピラゾール(中間体5)(15.07g、80mmol)の混合物を、無水メタノール(1.5L)中、室温で2時間撹拌した。得られた白色の懸濁液に、デカボラン(2.95g、24.15mmol)を加え、混合物を室温で一晩撹拌した。メタノールを除去し、残渣を、ジクロロメタン中5〜50%酢酸エチルで溶出する、2本の65i Biotage(商標)カラムにより精製し、標題の化合物を白色固体として得た。LC−MS:499.10(M+1)。
室温で、ジクロロメタン(200mL)中のトリフルオロ酢酸(100mL)を用い、工程A由来の生成物(13.78g、27.67mmol)中のBOC基の除去を実施した。2時間撹拌した後、反応物を濃縮し、ジクロロメタン中の25%MeOH及び2.5%水酸化アンモニウムで中和した。減圧下で溶媒を除去し、ジクロロメタン中の1.25〜5%MeOH及び0.125〜0.5%水酸化アンモニウムで溶出する65i Biotage(商標)カラムにより、得られた粗生成物を精製した。単離した物質を、60℃で5:1のEtOAc/CH2Cl2から再結晶することにより更に精製した。結晶性生成物を、冷却した2:1のEtOAc/ヘキサンで洗浄し、標題の化合物を淡褐色の固体として得た。1H NMR(500MHz,CD3OD):1.71(q,1H,J=12Hz),2.56−2.61(m,1H),3.11−3.18(m,1H),3.36−3.40(m,1H),3.48(t,1H,J=12Hz),3.88−3.94(m,4H),4.30−4.35(m,1H),4.53(d,1H,J=12Hz),7.14−7.23(m,2H),7.26−7.30(m,1H),7.88(s,1H)。LC−MS:399.04(M+1)。
工程A:tert−ブチル{(2R,3S,5R)−2−(2,4,5−トリフルオロフェニル)−5−[2−(メチルスルホニル)−2,6−ジヒドロピロロ[3,4−c]ピラゾール−5(4H)−イル]テトラヒドロ−2H−ピラン−3−イル}カルバメート
中間体1(516mg、1.5mmol)及び2−(メチルスルホニル)−2,4,5,6−テトラヒドロピロロ[3,4−c]ピラゾール(中間体5)(280mg、1.5mmol)の混合物を、無水メタノール(70mL)中、30分間撹拌した後、デカボラン(54.8mg、0.45mmol)を加えた。反応物を室温で18時間撹拌した。反応物を濃縮し、微量の異性体を洗い流すために、ジクロロメタン中0〜10%酢酸エチルで溶出し、ジクロロメタン中1.25%メタノールで溶出する40M Biotage(商標)シリカカラムにより精製し、白色固体として得られる標題の化合物を溶出した。LC/MS:517.05(M+1)。
室温で、前記工程Aで得られた中間体(379mg、0.734mmol)を、ジクロロメタン(20mL)中、トリフルオロ酢酸(10mL)で処理した。2時間後、反応物を濃縮し、ジクロロメタン中の10%NH4OHを含む0〜2%メタノールで溶出するシリカゲルカラム(40S Biotage(商標))により粗生成物を精製し、標題の化合物を白色固体として得た。1H NMR(500MHz,CD3OD):δ1.50(q,1H,J=12Hz);2.43−2.49(m,1H);2.88(td,1H,J=12,6Hz);3.11−3.18(m,1H);3.34(s,3H);3.40(t,1H,J=12Hz);3.48−3.92(m,4H);4.23−4.28(m,2H);7.14−7.20(m,1H);7.36−7.42(m,1H);7.86(s,1H)。LC−MS:417.12(M+1)。
工程A:tert−ブチル{(2R,3S,5R)−2−(2,5−ジフルオロフェニル)−5−[1−(シクロペンチルスルホニル)−2,6−ジヒドロピロロ[3,4−c]ピラゾール−5(4H)−イル]テトラヒドロ−2H−ピラン−3−イル}カルバメート
中間体2(50.1mg、0.15mmol)及び1−(シクロペンチルスルホニル)−2,4,5,6−テトラヒドロピロロ[3,4−c]ピラゾール(中間体4)(35mg、0.15mmol)の混合物を、無水メタノール(1.0mL)中、30分間撹拌した後、デカボラン(5.32mg、0.044mmol)を加えた。室温で18時間撹拌した後、反応混合物を濃縮し、ジクロロメタン中50%酢酸エチルで溶出する分取用薄層クロマトグラフィープレートにより精製し、標題の化合物を無色のフィルムとして得た。LC−MS:553.46(M+1)。
室温で、前記工程Aで得られた中間体(49mg、0.089mmol)のジクロロメタン(4mL)中の溶液をトリフルオロ酢酸(2mL)で処理した。1.5時間後、反応混合物を濃縮し、ジクロロメタン中の10%NH4OHを含む5%メタノールで溶出する分取用薄層クロマトグラフィーにより精製し、標題の化合物を得た。
1H NMR(500MHz,CD3OD):δ1.54(q,1H,J=12Hz);1.62−1.77(m,4H);1.92−2.08(m,4H);2.42−2.49(m,1H);2.98−3.06(m,1H);3.07−3.14(m,1H);3.40(t,1H,J=12Hz);3.87−3.91(m,2H);4.01−4.08(m,1H);4.09−4.17(m,2H);4.20−4.27(m,1H);4.34(d,1H,J=10Hz);7.08−7.18(m,2H);7.20−7.25(m,1H);7.64(s,1H)。LC−MS:453.10(M+1)。
工程A:tert−ブチル{(2R,3S,5R)−2−(2,5−ジフルオロフェニル)−5−[2−(シクロペンチルスルホニル)−2,6−ジヒドロピロロ[3,4−c]ピラゾール−5(4H)−イル]テトラヒドロ−2H−ピラン−3−イル}カルバメート
中間体2(92mg、0.28mmol)及び2−(シクロペンチルスルホニル)−2,4,5,6−テトラヒドロピロロ[3,4−c]ピラゾール(中間体4)(68mg、0.28mmol)の混合物を、無水メタノール(2.0mL)中、30分間撹拌した後、デカボラン(10.3mg、0.085mmol)を加えた。室温で18時間撹拌した後、反応混合物を濃縮し、ジクロロメタン中30%酢酸エチルで溶出する分取用薄層クロマトグラフィープレートにより精製し、標題の化合物を白色固体として得た。LC−MS:553.37(M+1)。
室温で、前記工程Aで得られた中間体(90mg、0.16mmol)のジクロロメタン(6mL)中の溶液をトリフルオロ酢酸(3mL)で処理した。1.5時間後、反応混合物を濃縮し、標題の化合物を得た。1H NMR(500MHz,CD3OD):δ1.61−1.74(m,4H);1.92−2.08(m,4H);2.11(q,1H,J=12Hz);2.78−2.84(m,1H);3.68(td,1H,J=12,4Hz);3.78(t,1H,J=12Hz);3.88−3.96(m,1H);4.02−4.10(m,1H);4.49−4.67(m,5H);4.71(d,1H,J=12Hz);7.19−7.27(m,2H);7.28−7.33(m,1H);8.09(s,1H)。LC−MS:453.04(M+1)。
工程A:tert−ブチル{(2R,3S,5R)−2−(2,4,5−トリフルオロフェニル)−5−[2−(シクロペンチルスルホニル)−2,6−ジヒドロピロロ[3,4−c]ピラゾール−5(4H)−イル]テトラヒドロ−2H−ピラン−3−イル}カルバメート
中間体1(97mg、0.28mmol)及び2−(シクロペンチルスルホニル)−2,4,5,6−テトラヒドロピロロ[3,4−c]ピラゾール(中間体4)(68mg、0.28mmol)の混合物を、無水メタノール(2.0mL)中、30分間撹拌した後、デカボラン(10.3mg、0.085mmol)を加えた。室温で18時間撹拌した後、反応混合物を濃縮し、ジクロロメタン中30%酢酸エチルで溶出する分取用薄層クロマトグラフィープレートにより精製し、標題の化合物を白色固体として得た。LC−MS:571.34(M+1)。
室温で、前記工程Aで得られた中間体(93mg、0.16mmol)のジクロロメタン(6mL)中の溶液をトリフルオロ酢酸(3mL)で処理した。1.5時間後、反応物を濃縮し、標題の化合物を得た。
1H NMR(500MHz,CD3OD):δ1.71−1.76(m,4H);1.92−2.08(m,4H);2.12(q,1H,J=12Hz);2.79−2.85(m,1H);3.64(td,1H,J=10,6Hz);3.79(t,1H,J=12Hz);3.90−3.98(m,1H);4.02−4.10(m,1H);4.48−4.54(m,1H);4.57−4.72(m,5H);7.24−7.33(m,1H);7.46−7.54(m,1H);8.10(s,1H)。LC−MS:471.04(M+1)。
工程A:tert−ブチル{(2R,3S,5R)−2−(2,5−ジフルオロフェニル)−5−[1−(シクロプロピルスルホニル)−2,6−ジヒドロピロロ[3,4−c]ピラゾール−5(4H)−イル]テトラヒドロ−2H−ピラン−3−イル}カルバメート
中間体2(26mg、0.08mmol)及び1−(シクロプロピルスルホニル)−2,4,5,6−テトラヒドロピロロ[3,4−c]ピラゾール(中間体6)(18mg、0.084mmol)の混合物を、無水メタノール(1.0mL)中、30分間撹拌した後、デカボラン(2.9mg、0.024mmol)を加えた。室温で18時間撹拌した後、反応混合物を濃縮し、ジクロロメタン中50%酢酸エチルで溶出する分取用薄層クロマトグラフィープレートにより精製し、標題の化合物を白色固体として得た。LC−MS:525.2(M+1)。
室温で、前記工程Aで得られた中間体(52mg、0.099mmol)のジクロロメタン(2mL)中の溶液をトリフルオロ酢酸塩(1mL)で処理した。1.5時間後、反応混合物を濃縮し、0.05TFAv/vを含むH2O/アセトニトリルを用いる逆相HPLCにより精製し、標題の化合物を得た。1H NMR(500MHz,CD3OD):δ1.21−1.27(m,2H);1.38−1.43(m,2H);2.06(q,1H,J=14Hz);2.73−2.79(m,1H);2.29−3.06(m,1H);3.57−3.64(m,1H);3.74(t,1H,J=12Hz);3.81−3.90(m,1H);4.44−4.54(m,3H);4.69(d,1H,J=12Hz);4.71−4.81(m,2H);7.18−7.26(m,2H);7.27−7.32(m,1H);7.74(s,1H)。LC−MS:425.21(M+1)。
工程A:tert−ブチル{(2R,3S,5R)−2−(2,5−ジフルオロフェニル)−5−[2−(シクロプロピルスルホニル)−2,6−ジヒドロピロロ[3,4−c]ピラゾール−5(4H)−イル]テトラヒドロ−2H−ピラン−3−イル}カルバメート
中間体2(1.10g、3.38mmol)及び2−(シクロプロピルスルホニル)−2,4,5,6−テトラヒドロピロロ[3,4−c]ピラゾール(中間体6)(600mg、2.81mmol)の混合物を、無水メタノール(80mL)中、30分間撹拌した後、デカボラン(206mg、1.7mmol)を加えた。室温で18時間撹拌した後、反応物を濃縮し、ジクロロメタン中の5%メタノール及び1%NH4OHで溶出する分取用薄層クロマトグラフィープレートにより精製し、標題の化合物を白色固体として得た。LC−MS:425.01(M+1)。
室温で、前記工程Aからの中間体(93mg、0.16mmol)のジクロロメタン(6mL)中の溶液をトリフルオロ酢酸(3mL)で処理した。1.5時間後、反応混合物を濃縮し、標題の化合物を得た。1H NMR(500MHz,CD3OD):δ1.17−1.23(m,2H);1.34−1.40(m,2H);2.08(q,1H,J=12Hz);2.80(d,1H,J=12Hz);2.91−2.97(m,1H);3.58−3.66(m,1H);3.76(t,1H,J=12Hz),3.82−3.90(m,1H);4.47−4.62(m,5H);4.70(d,1H,J=10Hz);7.18−7.26(m,2H);7.28−7.32(m,1H);8.05(s,1H)。LC−MS:425.01(M+1)。
工程A:tert−ブチル{(2R,3S,5R)−2−(2,4,5−トリフルオロフェニル)−5−[2−(シクロプロピルスルホニル)−2,6−ジヒドロピロロ[3,4−c]ピラゾール−5(4H)−イル]テトラヒドロ−2H−ピラン−3−イル}カルバメート
中間体1(94mg、0.27mmol)及び2−(シクロプロピルスルホニル)−2,4,5,6−テトラヒドロピロロ[3,4−c]ピラゾール(中間体6)(58mg、0.27mmol)の混合物を、無水メタノール中、30分間撹拌した後、デカボラン(10mg、0.083mmol)を加えた。室温で18時間撹拌した後、反応混合物を濃縮し、ジクロロメタン中50%酢酸エチルで溶出する分取用薄層クロマトグラフィープレートにより精製し、標題の化合物を白色固体として得た。LC−MS:543.30(M+1)。
室温で、前記工程Aで得られた生成物(74mg、0.14mmol)のジクロロメタン(6mL)中の溶液をトリフルオロ酢酸(3mL)で処理した。1.5時間後、反応混合物を濃縮し、標題の化合物を得た。1H NMR(500MHz,CD3OD):δ1.18−1.24(m,2H);1.35−1.40(m,2H);2.12(q,1H,J=12Hz);2.79−2.86(m,1H);2.92−2.98(m,1H);3.64(td,1H,J=12,6Hz);3.79(t,1H,J=12Hz);3.90−3.98(m,1H);4.48−4.54(m,1H);4.57−4.72(m,5H);7.25−7.32(m,1H);7.46−7.53(m,1H);8.08(s,1H)。LC−MS:443.04(M+1)。
経口医薬組成物の具体的な実施態様として、100mgの力価の錠剤を、実施例のいずれか1つに記載されたもの100mg、微結晶性セルロース268mg、クロスカルメロースナトリウム20mg及びステアリン酸マグネシウム4mgから構成する。活性成分、微結晶性セルロース及びクロスカルメロースを最初に混合する。次いで、ステアリン酸マグネシウムで混合物を滑沢とし、錠剤に圧縮する。
Claims (2)
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US19917908P | 2008-11-13 | 2008-11-13 | |
| US61/199,179 | 2008-11-13 | ||
| PCT/US2009/063976 WO2010056708A1 (en) | 2008-11-13 | 2009-11-11 | Aminotetrahydropyrans as dipeptidyl peptidase-iv inhibitors for the treatment or prevention of diabetes |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011150098A Division JP5537507B2 (ja) | 2008-11-13 | 2011-07-06 | 糖尿病の治療又は予防のためのジペプチジルペプチダーゼ−iv阻害剤としてのアミノテトラヒドロピラン |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP4854825B1 true JP4854825B1 (ja) | 2012-01-18 |
| JP2012508746A JP2012508746A (ja) | 2012-04-12 |
Family
ID=41559521
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011536433A Active JP4854825B1 (ja) | 2008-11-13 | 2009-11-11 | 糖尿病の治療又は予防のためのジペプチジルペプチダーゼ−iv阻害剤としてのアミノテトラヒドロピラン |
| JP2011150098A Active JP5537507B2 (ja) | 2008-11-13 | 2011-07-06 | 糖尿病の治療又は予防のためのジペプチジルペプチダーゼ−iv阻害剤としてのアミノテトラヒドロピラン |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011150098A Active JP5537507B2 (ja) | 2008-11-13 | 2011-07-06 | 糖尿病の治療又は予防のためのジペプチジルペプチダーゼ−iv阻害剤としてのアミノテトラヒドロピラン |
Country Status (39)
| Country | Link |
|---|---|
| US (8) | US8143289B2 (ja) |
| EP (4) | EP2676961B1 (ja) |
| JP (2) | JP4854825B1 (ja) |
| KR (2) | KR101260162B1 (ja) |
| CN (1) | CN102272136B (ja) |
| AR (1) | AR074306A1 (ja) |
| AU (1) | AU2009314191B2 (ja) |
| BR (1) | BRPI0921375B8 (ja) |
| CA (1) | CA2742783C (ja) |
| CL (1) | CL2011001082A1 (ja) |
| CO (1) | CO6382129A2 (ja) |
| CR (1) | CR20110257A (ja) |
| CY (1) | CY1114617T1 (ja) |
| DK (1) | DK2358717T3 (ja) |
| DO (1) | DOP2011000128A (ja) |
| EA (1) | EA018613B1 (ja) |
| EC (1) | ECSP11011044A (ja) |
| ES (1) | ES2432191T3 (ja) |
| GE (1) | GEP20135724B (ja) |
| HN (1) | HN2011001256A (ja) |
| HR (1) | HRP20130924T1 (ja) |
| IL (2) | IL212485A (ja) |
| JO (1) | JO2870B1 (ja) |
| MA (1) | MA32887B1 (ja) |
| MX (1) | MX2011005044A (ja) |
| MY (1) | MY150787A (ja) |
| NI (1) | NI201100081A (ja) |
| NZ (1) | NZ592826A (ja) |
| PA (1) | PA8848201A1 (ja) |
| PE (1) | PE20120027A1 (ja) |
| PL (1) | PL2358717T3 (ja) |
| PT (1) | PT2358717E (ja) |
| RS (1) | RS52946B (ja) |
| SI (1) | SI2358717T1 (ja) |
| SV (1) | SV2011003903A (ja) |
| TN (1) | TN2011000201A1 (ja) |
| TW (1) | TWI398443B (ja) |
| UA (1) | UA101414C2 (ja) |
| WO (1) | WO2010056708A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013503864A (ja) * | 2009-09-02 | 2013-02-04 | メルク・シャープ・エンド・ドーム・コーポレイション | 糖尿病の治療又は予防のためのジペプチジルペプチダーゼiv阻害剤としてのアミノテトラヒドロピラン |
Families Citing this family (57)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| BRPI0915720A2 (pt) | 2008-06-12 | 2015-08-04 | Janssen Pharmaceutica Nv | Moduladores de diaminopiridina, pirimidina, e piridazina do receptor de histamina h4 |
| JO2870B1 (en) | 2008-11-13 | 2015-03-15 | ميرك شارب اند دوهم كورب | Amino Tetra Hydro Pirans as Inhibitors of Peptide Dipeptide IV for the Treatment or Prevention of Diabetes |
| WO2011037793A1 (en) | 2009-09-25 | 2011-03-31 | Merck Sharp & Dohme Corp. | Substituted aminopiperidines as dipeptidyl peptidase-iv inhibitors for the treatment of diabetes |
| US8853212B2 (en) | 2010-02-22 | 2014-10-07 | Merck Sharp & Dohme Corp | Substituted aminotetrahydrothiopyrans and derivatives thereof as dipeptidyl peptidase-IV inhibitors for the treatment of diabetes |
| WO2011146358A1 (en) | 2010-05-21 | 2011-11-24 | Merck Sharp & Dohme Corp. | Substituted seven-membered heterocyclic compounds as dipeptidyl peptidase-iv inhibitors for the treatment of diabetes |
| WO2012078448A1 (en) | 2010-12-06 | 2012-06-14 | Schering Corporation | Tricyclic heterocycles useful as dipeptidyl peptidase-iv inhibitors |
| JP2014521594A (ja) * | 2011-05-25 | 2014-08-28 | アミリン・ファーマシューティカルズ,リミテッド・ライアビリティ・カンパニー | 長持続期間デュアルホルモンコンジュゲート |
| CA2838738A1 (en) * | 2011-06-29 | 2013-01-03 | Merck Sharp & Dohme Corp. | Novel crystalline forms of a dipeptidyl peptidase-iv inhibitor |
| EP2729468A4 (en) | 2011-07-05 | 2015-03-18 | Merck Sharp & Dohme | Tricyclic heterocycles useful as dipeptidyl peptidase-iv inhibitors |
| WO2013122920A1 (en) | 2012-02-17 | 2013-08-22 | Merck Sharp & Dohme Corp. | Dipeptidyl peptidase-iv inhibitors for the treatment or prevention of diabetes |
| EP2874622A4 (en) | 2012-07-23 | 2015-12-30 | Merck Sharp & Dohme | TREATMENT OF DIABETES WITH DIPEPTIDYLPEPTIDASE IV INHIBITORS |
| US9156848B2 (en) | 2012-07-23 | 2015-10-13 | Merck Sharp & Dohme Corp. | Treating diabetes with dipeptidyl peptidase-IV inhibitors |
| TWI500613B (zh) | 2012-10-17 | 2015-09-21 | Cadila Healthcare Ltd | 新穎之雜環化合物 |
| EP3038465B1 (en) * | 2013-08-30 | 2021-10-06 | Merck Sharp & Dohme Corp. | Oral pharmaceutical formulation of omarigliptin |
| ES2587585T3 (es) | 2014-03-20 | 2016-10-25 | F.I.S.- Fabbrica Italiana Sintetici S.P.A. | Procedimiento para la preparación de intermedios clave de omarigliptina |
| CN105037367A (zh) * | 2014-04-18 | 2015-11-11 | 四川海思科制药有限公司 | 氨基六元环类衍生物及其在医药上的应用 |
| CN105085528A (zh) * | 2014-05-15 | 2015-11-25 | 成都贝斯凯瑞生物科技有限公司 | 作为二肽基肽酶-iv抑制剂的氨基四氢吡喃衍生物 |
| CN105085530B (zh) * | 2014-05-23 | 2019-01-04 | 四川海思科制药有限公司 | 三元稠合环取代的氨基六元环类衍生物及其在医药上的应用 |
| MY181641A (en) * | 2014-06-17 | 2020-12-30 | Sichuan Haisco Pharmaceutical Co Ltd | Amino pyran ring derivative and composition and use thereof |
| CN105294694B (zh) * | 2014-06-18 | 2019-01-04 | 四川海思科制药有限公司 | 氨基六元环类衍生物及其在医药上的应用 |
| US9862725B2 (en) | 2014-07-21 | 2018-01-09 | Merck Sharp & Dohme Corp. | Process for preparing chiral dipeptidyl peptidase-IV inhibitors |
| CN105985357A (zh) * | 2015-02-12 | 2016-10-05 | 北京赛林泰医药技术有限公司 | 取代的氨基六元饱和杂脂环类长效dpp-iv抑制剂 |
| CN107250135B (zh) * | 2015-08-24 | 2020-05-26 | 四川科伦博泰生物医药股份有限公司 | 长效二肽基肽酶-ⅳ抑制剂、用途及其中间体的制备方法 |
| CN106478631B (zh) * | 2015-08-24 | 2019-04-05 | 四川科伦药物研究院有限公司 | 长效二肽基肽酶-iv抑制剂、用途及其中间体的制备方法 |
| WO2017032705A1 (en) | 2015-08-25 | 2017-03-02 | Sandoz Ag | Crystalline form of omarigliptin |
| TWI681962B (zh) * | 2015-08-26 | 2020-01-11 | 大陸商四川海思科製藥有限公司 | 胺基六員環類衍生物及其在醫藥上的應用 |
| TWI640524B (zh) * | 2015-08-27 | 2018-11-11 | 四川海思科製藥有限公司 | Aminopyran ring derivatives and compositions and uses thereof |
| CN105198847B (zh) * | 2015-10-28 | 2017-05-17 | 四川凯科医药科技有限公司 | 一种化合物的制备方法 |
| JP6475368B2 (ja) * | 2015-12-03 | 2019-02-27 | エッフェ・イ・エッセ − ファッブリカ・イタリアーナ・シンテテイチ・ソチエタ・ペル・アツィオーニF.I.S. − Fabbrica Italiana Sintetici S.p.A. | アミノテトラヒドロピラン類の製造方法 |
| CN105399744B (zh) * | 2015-12-17 | 2017-07-18 | 黄燕鸽 | 一种奥格列汀的合成方法 |
| EP3181565A1 (en) | 2015-12-18 | 2017-06-21 | Sandoz Ag | Crystalline omarigliptin salts |
| CN106916158A (zh) * | 2015-12-25 | 2017-07-04 | 四川海思科制药有限公司 | 一种吡喃衍生物盐酸盐水合物及其中间体的制备方法 |
| CN106916157A (zh) * | 2015-12-25 | 2017-07-04 | 四川海思科制药有限公司 | 取代的氨基吡喃衍生物的晶型 |
| CN106928228B (zh) * | 2015-12-29 | 2019-08-30 | 杭州普晒医药科技有限公司 | 奥格列汀盐及其晶型、它们的制备方法和药物组合物 |
| CN107337674B (zh) * | 2016-04-29 | 2019-09-20 | 江苏吉贝尔药业股份有限公司 | 用于dpp-iv抑制剂的四氢吡喃胺衍生物、其药物组合物和制剂以及用途 |
| CN109071551B (zh) * | 2016-05-25 | 2020-12-08 | 四川海思科制药有限公司 | 一种三氟甲基取代的吡喃衍生物的制备方法 |
| WO2017202365A1 (zh) * | 2016-05-25 | 2017-11-30 | 四川海思科制药有限公司 | 一种三氟甲基取代的吡喃衍生物制备方法 |
| CN107652291B (zh) * | 2016-07-26 | 2020-07-14 | 中国科学院上海药物研究所 | 一种制备手性四氢吡喃衍生物的方法 |
| WO2018028666A1 (zh) * | 2016-08-12 | 2018-02-15 | 正大天晴药业集团股份有限公司 | Dpp-iv长效抑制剂的结晶及其盐 |
| CN106674227B (zh) * | 2016-12-06 | 2019-03-19 | 上海博志研新药物技术有限公司 | 一种奥格列汀及其中间体的制备方法 |
| EP3335702A1 (en) | 2016-12-16 | 2018-06-20 | Hexal AG | Pharmaceutical compositions comprising omarigliptin |
| EP3335701A1 (en) | 2016-12-16 | 2018-06-20 | Hexal AG | Pharmaceutical composition comprising omarigliptin |
| EP3335703A1 (en) | 2016-12-16 | 2018-06-20 | Hexal AG | Pharmaceutical composition comprising omarigliptin |
| EP3335704A1 (en) | 2016-12-16 | 2018-06-20 | Hexal AG | Pharmaceutical composition comprising omarigliptin |
| CN107024590A (zh) * | 2017-03-13 | 2017-08-08 | 新疆医科大学 | 一种诊断1型和2型糖尿病的血清蛋白标志物组 |
| WO2018167589A1 (en) | 2017-03-16 | 2018-09-20 | Inventia Healthcare Private Limited | Pharmaceutical composition comprising dapagliflozin |
| ES2747768T3 (es) | 2017-03-20 | 2020-03-11 | Forma Therapeutics Inc | Composiciones de pirrolopirrol como activadores de quinasa de piruvato (PKR) |
| CN109796455B (zh) * | 2017-11-17 | 2021-02-26 | 四川海思科制药有限公司 | 一种氨基吡喃衍生物的盐、其晶型及其制备方法和用途 |
| CN116919952A (zh) * | 2018-02-06 | 2023-10-24 | 四川海思科制药有限公司 | 一种氨基吡喃衍生物的组合物 |
| ES2989438T3 (es) | 2018-09-19 | 2024-11-26 | Novo Nordisk Healthcare Ag | Activación de la piruvato cinasa R |
| US12053458B2 (en) | 2018-09-19 | 2024-08-06 | Novo Nordisk Health Care Ag | Treating sickle cell disease with a pyruvate kinase R activating compound |
| US12421269B2 (en) | 2019-07-26 | 2025-09-23 | Cgenetech (Suzhou, China) Co., Ltd. | SGLT2/DPP4 inhibitor and application thereof |
| CN110568100B (zh) * | 2019-09-12 | 2022-05-31 | 江西金水宝制药有限公司 | 一种米格列奈钙r-异构体的检测方法 |
| US20220378756A1 (en) | 2019-09-19 | 2022-12-01 | Forma Therapeutics, Inc. | Activating pyruvate kinase r |
| CN111793071B (zh) * | 2020-07-06 | 2021-06-04 | 四川凯科医药科技有限公司 | 奥格列汀的合成工艺 |
| US12128035B2 (en) | 2021-03-19 | 2024-10-29 | Novo Nordisk Health Care Ag | Activating pyruvate kinase R |
| CN119504764B (zh) * | 2024-11-26 | 2025-09-23 | 斯坦德药典标准物质研发(湖北)有限公司 | 一种Omarigliptin的制备方法 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20070232676A1 (en) * | 2006-03-28 | 2007-10-04 | Tesfaye Biftu | Aminotetrahydropyrans as dipeptidyl peptidase-IV inhibitors for the treatment or prevention of diabetes |
| WO2009014676A1 (en) * | 2007-07-23 | 2009-01-29 | Merck & Co., Inc. | Novel crystalline form of a dihydrochloride salt of a dipeptidyl peptidase-iv inhibitor |
Family Cites Families (68)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4166452A (en) | 1976-05-03 | 1979-09-04 | Generales Constantine D J Jr | Apparatus for testing human responses to stimuli |
| US4256108A (en) | 1977-04-07 | 1981-03-17 | Alza Corporation | Microporous-semipermeable laminated osmotic system |
| US4265874A (en) | 1980-04-25 | 1981-05-05 | Alza Corporation | Method of delivering drug with aid of effervescent activity generated in environment of use |
| US5232929A (en) | 1990-11-28 | 1993-08-03 | Pfizer Inc. | 3-aminopiperidine derivatives and related nitrogen containing heterocycles and pharmaceutical compositions and use |
| US5545618A (en) | 1990-01-24 | 1996-08-13 | Buckley; Douglas I. | GLP-1 analogs useful for diabetes treatment |
| IL111785A0 (en) | 1993-12-03 | 1995-01-24 | Ferring Bv | Dp-iv inhibitors and pharmaceutical compositions containing them |
| DE19616486C5 (de) | 1996-04-25 | 2016-06-30 | Royalty Pharma Collection Trust | Verfahren zur Senkung des Blutglukosespiegels in Säugern |
| AR008789A1 (es) | 1996-07-31 | 2000-02-23 | Bayer Corp | Piridinas y bifenilos substituidos |
| UA65549C2 (uk) | 1996-11-05 | 2004-04-15 | Елі Ліллі Енд Компані | Спосіб регулювання ожиріння шляхом периферійного введення аналогів та похідних glp-1 (варіанти) та фармацевтична композиція |
| TW492957B (en) | 1996-11-07 | 2002-07-01 | Novartis Ag | N-substituted 2-cyanopyrrolidnes |
| US6054587A (en) | 1997-03-07 | 2000-04-25 | Metabasis Therapeutics, Inc. | Indole and azaindole inhibitors of fructose-1,6-bisphosphatase |
| AU6452098A (en) | 1997-03-07 | 1998-09-22 | Metabasis Therapeutics, Inc. | Novel purine inhibitors of fructose-1,6-bisphosphatase |
| DE69819311T2 (de) | 1997-03-07 | 2004-07-29 | Metabasis Therapeutics Inc., San Diego | Neue benzimidazol inhibitoren der fructose-1,6-bisphosphatase |
| AU749271B2 (en) | 1997-07-01 | 2002-06-20 | Agouron Pharmaceuticals, Inc. | Glucagon antagonists/inverse agonists |
| US6613942B1 (en) | 1997-07-01 | 2003-09-02 | Novo Nordisk A/S | Glucagon antagonists/inverse agonists |
| PA8469501A1 (es) * | 1998-04-10 | 2000-09-29 | Pfizer Prod Inc | Hidroxamidas del acido (4-arilsulfonilamino)-tetrahidropiran-4-carboxilico |
| CA2331122A1 (en) | 1998-05-04 | 1999-11-11 | Point Therapeutics, Inc. | Hematopoietic stimulation |
| ATE246197T1 (de) | 1998-09-09 | 2003-08-15 | Metabasis Therapeutics Inc | Neue heteroaromatische fructose 1,6- bisphosphatase inhibitoren |
| CO5150173A1 (es) | 1998-12-10 | 2002-04-29 | Novartis Ag | Compuestos n-(glicilo sustituido)-2-cianopirrolidinas inhibidores de peptidasa de dipeptidilo-iv (dpp-iv) los cuales son efectivos en el tratamiento de condiciones mediadas por la inhibicion de dpp-iv |
| GB9906715D0 (en) | 1999-03-23 | 1999-05-19 | Ferring Bv | Compositions for promoting growth |
| WO2000069810A1 (en) | 1999-05-17 | 2000-11-23 | Novo Nordisk A/S | Glucagon antagonists/inverse agonists |
| WO2002008188A1 (en) | 2000-07-25 | 2002-01-31 | Merck & Co., Inc. | N-substituted indoles useful in the treatment of diabetes |
| KR20030096227A (ko) | 2000-10-27 | 2003-12-24 | 프로비오드룩 아게 | 신경 및 신경정신 질환의 치료방법 |
| WO2002060388A2 (en) | 2001-01-30 | 2002-08-08 | Merck & Co., Inc. | Acyl sulfamides for treatment of obesity, diabetes and lipid disorders |
| DE60221983T2 (de) | 2001-06-27 | 2008-05-15 | Smithkline Beecham Corp. | Fluorpyrrolidine als dipeptidyl-peptidase inhibitoren |
| UA74912C2 (en) | 2001-07-06 | 2006-02-15 | Merck & Co Inc | Beta-aminotetrahydroimidazo-(1,2-a)-pyrazines and tetratriazolo-(4,3-a)-pyrazines as inhibitors of dipeptylpeptidase for the treatment or prevention of diabetes |
| GB0121709D0 (en) | 2001-09-07 | 2001-10-31 | Imp College Innovations Ltd | Food inhibition agent |
| AR040241A1 (es) | 2002-06-10 | 2005-03-23 | Merck & Co Inc | Inhibidores de la 11-beta-hidroxiesteroide deshidrogrenasa 1 para el tratamiento de la diabetes obesidad y dislipidemia |
| WO2004020408A1 (en) | 2002-08-29 | 2004-03-11 | Merck & Co., Inc. | Indoles having anti-diabetic activity |
| WO2004019869A2 (en) | 2002-08-29 | 2004-03-11 | Merck & Co., Inc. | Indoles having anti-diabetic activity |
| WO2004037159A2 (en) | 2002-10-23 | 2004-05-06 | Obetherapy Biotechnology | Compounds, compositions and methods for modulating fat metabolism |
| US7192922B2 (en) | 2002-11-19 | 2007-03-20 | Allegheny-Singer Research Institute | Method of treating left ventricular dysfunction |
| JO2397B1 (en) | 2002-12-20 | 2007-06-17 | ميرك شارب اند دوم كوربوريشن | Terazol derivatives as beta-hydroxy steroid dihydrogenase-1 inhibitors |
| JP2007504285A (ja) | 2003-01-17 | 2007-03-01 | メルク エンド カムパニー インコーポレーテッド | N−シクロヘキシルアミノカルボニルベンゼンスルホンアミド誘導体 |
| WO2004091499A2 (en) | 2003-04-09 | 2004-10-28 | Neose Technologies, Inc. | Intracellular formation of peptide conjugates |
| US7145012B2 (en) * | 2003-04-23 | 2006-12-05 | Pfizer Inc. | Cannabinoid receptor ligands and uses thereof |
| US20040214856A1 (en) * | 2003-04-23 | 2004-10-28 | Pfizer Inc | Cannabinoid receptor ligands and uses thereof |
| WO2005030751A2 (en) * | 2003-09-08 | 2005-04-07 | Takeda Pharmaceutical Company Limited | Dipeptidyl peptidase inhibitors |
| WO2005061523A1 (en) | 2003-12-23 | 2005-07-07 | Progen Industries Limited | Glycosaminoglycan (gag) mimetics |
| AU2005265148B2 (en) * | 2004-06-21 | 2011-01-20 | Merck Sharp & Dohme Corp. | Aminocyclohexanes as dipeptidyl peptidase-IV inhibitors for the treatment or prevention of diabetes |
| WO2006020372A2 (en) | 2004-07-23 | 2006-02-23 | Neose Technologies, Inc. | Enzymatic modification of glycopeptides |
| US7718667B2 (en) * | 2004-09-28 | 2010-05-18 | Merck Sharp & Dohme Corp. | Fused aminopiperidines as dipeptidyl peptidase-IV inhibitors for the treatment or prevention of diabetes |
| AU2005292134B2 (en) | 2004-10-01 | 2010-12-23 | Merck Sharp & Dohme Corp. | Aminopiperidines as dipeptidyl peptidase-IV inhibitors for the treatment or prevention of diabetes |
| US20090253752A1 (en) | 2004-10-25 | 2009-10-08 | Bryan Burkey | Combination of dpp-iv inhibitor, ppar antidiabetic and metmorfin |
| JP4999698B2 (ja) | 2004-11-29 | 2012-08-15 | メルク・シャープ・エンド・ドーム・コーポレイション | 糖尿病の治療または予防用のジペプチジルペプチダーゼ−iv阻害剤としての縮合アミノピペリジン |
| CN101090888A (zh) | 2004-12-20 | 2007-12-19 | 霍夫曼-拉罗奇有限公司 | 4-氨基哌啶衍生物 |
| US7411093B2 (en) | 2004-12-20 | 2008-08-12 | Hoffman-La Roche Inc. | Aminocycloalkanes as DPP-IV inhibitors |
| EP1702916A1 (en) | 2005-03-18 | 2006-09-20 | Santhera Pharmaceuticals (Schweiz) GmbH | DPP-IV inhibitors |
| TWI357902B (en) * | 2005-04-01 | 2012-02-11 | Lg Life Science Ltd | Dipeptidyl peptidase-iv inhibiting compounds, meth |
| JP5069678B2 (ja) | 2005-05-25 | 2012-11-07 | メルク・シャープ・エンド・ドーム・コーポレイション | 糖尿病の治療又は予防のためのジペプチジルペプチダーゼiv阻害剤としてのアミノシクロヘキサン |
| RU2485135C2 (ru) | 2005-06-13 | 2013-06-20 | Импиэриэл Инноувейшнс Лимитид | Соединения оксинтомодулина (варианты), фармацевтическая композиция на их основе, способы лечения и профилактики ожирения и сопутствующих заболеваний (варианты) и лекарственное средство (варианты) |
| CA2619111C (en) | 2005-08-26 | 2013-04-09 | Merck & Co., Inc. | Fused aminopiperidines as dipeptidyl peptidase-iv inhibitors for the treatment or prevention of diabetes |
| US7943615B2 (en) | 2005-12-14 | 2011-05-17 | Merck Sharp & Dohme Corp. | Fused aminopiperidines as dipeptidyl peptidase-4 inhibitors for the treatment or prevention of diabetes |
| CA2636757A1 (en) * | 2006-01-25 | 2007-08-02 | Tesfaye Biftu | Aminocyclohexanes as dipeptidyl peptidase-iv inhibitors for the treatment or prevention of diabetes |
| WO2007097931A2 (en) | 2006-02-15 | 2007-08-30 | Merck & Co., Inc. | Aminotetrahydropyrans as dipeptidyl peptidase-iv inhibitors for the treatment or prevention of diabetes |
| CN101389648B (zh) | 2006-02-22 | 2013-07-17 | 默沙东公司 | 肽胃泌酸调节素衍生物 |
| KR20090005329A (ko) | 2006-03-20 | 2009-01-13 | 머크 앤드 캄파니 인코포레이티드 | 뉴로메딘 u 수용체 효능제 및 이의 용도 |
| AU2007254357B2 (en) | 2006-05-16 | 2011-07-21 | Merck Sharp & Dohme Corp. | Aminotetrahydropyrans as dipeptidyl peptidase-IV inhibitors for the treatment or prevention of diabetes |
| AU2007275294A1 (en) | 2006-07-18 | 2008-01-24 | Centocor, Inc. | Human GLP-1 mimetibodies, compositions, methods and uses |
| CA2668662A1 (en) * | 2006-11-14 | 2008-05-22 | Merck & Co., Inc. | Tricyclic heteroaromatic compounds as dipeptidyl peptidase-iv inhibitors for the treatment or prevention of diabetes |
| AU2008216265B2 (en) | 2007-02-15 | 2014-04-03 | Indiana University Research And Technology Corporation | Glucagon/GLP-1 receptor co-agonists |
| AU2008267724A1 (en) | 2007-06-28 | 2008-12-31 | Merck Frosst Canada Ltd | Substituted fused pyrimidines as antagonists of GPR105 activity |
| EP2178537A4 (en) | 2007-07-19 | 2011-08-17 | Merck Sharp & Dohme | BETA-CARBOLIN DERIVATIVES AS ANTIDIBLE COMPOUNDS |
| CA2696211C (en) | 2007-08-21 | 2015-05-26 | Merck Sharp & Dohme Corp. | Heterocyclic compounds as dipeptidyl peptidase-iv inhibitors for the treatment or prevention of diabetes |
| WO2009042053A2 (en) | 2007-09-21 | 2009-04-02 | Merck & Co., Inc. | Neuromedin u receptor agonists and uses thereof |
| US7902376B2 (en) * | 2008-01-23 | 2011-03-08 | Merck Sharp & Dohme Corp. | Process for preparing chiral dipeptidyl peptidase-IV inhibitor intermediates |
| CN102272135A (zh) | 2008-10-08 | 2011-12-07 | 百时美施贵宝公司 | 唑并吡咯酮黑色素浓集激素受体-1拮抗剂 |
| JO2870B1 (en) | 2008-11-13 | 2015-03-15 | ميرك شارب اند دوهم كورب | Amino Tetra Hydro Pirans as Inhibitors of Peptide Dipeptide IV for the Treatment or Prevention of Diabetes |
-
2009
- 2009-11-04 JO JO2009408A patent/JO2870B1/en active
- 2009-11-09 TW TW98137972A patent/TWI398443B/zh not_active IP Right Cessation
- 2009-11-09 AR ARP090104318 patent/AR074306A1/es unknown
- 2009-11-11 EA EA201170670A patent/EA018613B1/ru not_active IP Right Cessation
- 2009-11-11 SI SI200930757T patent/SI2358717T1/sl unknown
- 2009-11-11 PA PA8848201A patent/PA8848201A1/es unknown
- 2009-11-11 BR BRPI0921375A patent/BRPI0921375B8/pt active IP Right Grant
- 2009-11-11 EP EP13180593.9A patent/EP2676961B1/en active Active
- 2009-11-11 MY MYPI20112075 patent/MY150787A/en unknown
- 2009-11-11 MX MX2011005044A patent/MX2011005044A/es active IP Right Grant
- 2009-11-11 KR KR1020117010775A patent/KR101260162B1/ko active Active
- 2009-11-11 WO PCT/US2009/063976 patent/WO2010056708A1/en not_active Ceased
- 2009-11-11 JP JP2011536433A patent/JP4854825B1/ja active Active
- 2009-11-11 DK DK09756204T patent/DK2358717T3/da active
- 2009-11-11 PE PE2011001028A patent/PE20120027A1/es not_active Application Discontinuation
- 2009-11-11 EP EP20130180590 patent/EP2676959A1/en not_active Withdrawn
- 2009-11-11 NZ NZ592826A patent/NZ592826A/en not_active IP Right Cessation
- 2009-11-11 PT PT09756204T patent/PT2358717E/pt unknown
- 2009-11-11 AU AU2009314191A patent/AU2009314191B2/en active Active
- 2009-11-11 CN CN200980154484.2A patent/CN102272136B/zh active Active
- 2009-11-11 KR KR20127021008A patent/KR101454093B1/ko active Active
- 2009-11-11 PL PL09756204T patent/PL2358717T3/pl unknown
- 2009-11-11 HR HRP20130924AT patent/HRP20130924T1/hr unknown
- 2009-11-11 ES ES09756204T patent/ES2432191T3/es active Active
- 2009-11-11 UA UAA201107305A patent/UA101414C2/uk unknown
- 2009-11-11 CA CA 2742783 patent/CA2742783C/en active Active
- 2009-11-11 RS RSP20130426 patent/RS52946B/sr unknown
- 2009-11-11 EP EP13180592.1A patent/EP2676960B1/en active Active
- 2009-11-11 GE GEAP200912261A patent/GEP20135724B/en unknown
- 2009-11-11 EP EP20090756204 patent/EP2358717B1/en active Active
- 2009-11-12 US US12/616,831 patent/US8143289B2/en active Active
-
2011
- 2011-04-21 TN TN2011000201A patent/TN2011000201A1/fr unknown
- 2011-04-26 IL IL212485A patent/IL212485A/en not_active IP Right Cessation
- 2011-04-28 NI NI201100081A patent/NI201100081A/es unknown
- 2011-05-06 HN HN2011001256A patent/HN2011001256A/es unknown
- 2011-05-09 DO DO2011000128A patent/DOP2011000128A/es unknown
- 2011-05-11 EC ECSP11011044 patent/ECSP11011044A/es unknown
- 2011-05-12 SV SV2011003903A patent/SV2011003903A/es unknown
- 2011-05-12 CO CO11058568A patent/CO6382129A2/es active IP Right Grant
- 2011-05-12 CL CL2011001082A patent/CL2011001082A1/es unknown
- 2011-05-13 CR CR20110257A patent/CR20110257A/es unknown
- 2011-06-08 MA MA33925A patent/MA32887B1/fr unknown
- 2011-07-06 JP JP2011150098A patent/JP5537507B2/ja active Active
-
2012
- 2012-02-17 US US13/398,887 patent/US8415297B2/en active Active
-
2013
- 2013-02-07 US US13/761,407 patent/US8592371B2/en active Active
- 2013-03-13 IL IL225198A patent/IL225198A/en active IP Right Grant
- 2013-10-22 US US14/059,638 patent/US8772328B2/en active Active
- 2013-10-31 CY CY20131100966T patent/CY1114617T1/el unknown
-
2014
- 2014-06-02 US US14/293,031 patent/US8951965B2/en active Active
-
2015
- 2015-01-07 US US14/591,124 patent/US9138426B2/en active Active
- 2015-08-13 US US14/825,535 patent/US9278976B2/en active Active
-
2016
- 2016-01-26 US US15/006,220 patent/US9403790B2/en active Active
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20070232676A1 (en) * | 2006-03-28 | 2007-10-04 | Tesfaye Biftu | Aminotetrahydropyrans as dipeptidyl peptidase-IV inhibitors for the treatment or prevention of diabetes |
| WO2007126745A2 (en) * | 2006-03-28 | 2007-11-08 | Merck & Co., Inc. | Aminotetrahydropyrans as dipeptidyl peptidase-iv inhibitors for the treatment or prevention of diabetes |
| WO2009014676A1 (en) * | 2007-07-23 | 2009-01-29 | Merck & Co., Inc. | Novel crystalline form of a dihydrochloride salt of a dipeptidyl peptidase-iv inhibitor |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013503864A (ja) * | 2009-09-02 | 2013-02-04 | メルク・シャープ・エンド・ドーム・コーポレイション | 糖尿病の治療又は予防のためのジペプチジルペプチダーゼiv阻害剤としてのアミノテトラヒドロピラン |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4854825B1 (ja) | 糖尿病の治療又は予防のためのジペプチジルペプチダーゼ−iv阻害剤としてのアミノテトラヒドロピラン | |
| EP2473047B1 (en) | Aminotetrahydropyrans as dipeptidyl peptidase-iv inhibitors for the treatment or prevention of diabetes | |
| EP2538783B1 (en) | Substituted aminotetrahydrothiopyrans and derivatives thereof as dipeptidyl peptidase-iv inhibitors for the treatment of diabetes | |
| HK1187344A (en) | Combination drugs comprising aminotetrahydropyrans as dipeptidyl peptidase-iv inhibitors for the treatment or prevention of diabetes | |
| HK1187342A (en) | Combination drugs comprising aminotetrahydropyrans as dipeptidyl peptidase-iv inhibitors for the treatment or prevention of diabetes | |
| HK1187343A (en) | Combination drugs comprising aminotetrahydropyrans as dipeptidyl peptidase-iv inhibitors for the treatment or prevention of diabetes | |
| HK1154849B (en) | Aminotetrahydropyrans as dipeptidyl peptidase-iv inhibitors for the treatment or prevention of diabetes |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A975 | Report on accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A971005 Effective date: 20111006 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20111018 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20111025 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20141104 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 4854825 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| S111 | Request for change of ownership or part of ownership |
Free format text: JAPANESE INTERMEDIATE CODE: R313111 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20141104 Year of fee payment: 3 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R153 | Grant of patent term extension |
Free format text: JAPANESE INTERMEDIATE CODE: R153 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| S111 | Request for change of ownership or part of ownership |
Free format text: JAPANESE INTERMEDIATE CODE: R313111 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |