JP4773361B2 - 可溶性tcr分子とその使用方法 - Google Patents
可溶性tcr分子とその使用方法 Download PDFInfo
- Publication number
- JP4773361B2 JP4773361B2 JP2006539829A JP2006539829A JP4773361B2 JP 4773361 B2 JP4773361 B2 JP 4773361B2 JP 2006539829 A JP2006539829 A JP 2006539829A JP 2006539829 A JP2006539829 A JP 2006539829A JP 4773361 B2 JP4773361 B2 JP 4773361B2
- Authority
- JP
- Japan
- Prior art keywords
- cells
- cell
- 264sctcr
- fragment
- tcr
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K51/00—Preparations containing radioactive substances for use in therapy or testing in vivo
- A61K51/02—Preparations containing radioactive substances for use in therapy or testing in vivo characterised by the carrier, i.e. characterised by the agent or material covalently linked or complexing the radioactive nucleus
- A61K51/04—Organic compounds
- A61K51/08—Peptides, e.g. proteins, carriers being peptides, polyamino acids, proteins
- A61K51/10—Antibodies or immunoglobulins; Fragments thereof, the carrier being an antibody, an immunoglobulin or a fragment thereof, e.g. a camelised human single domain antibody or the Fc fragment of an antibody
- A61K51/1027—Antibodies or immunoglobulins; Fragments thereof, the carrier being an antibody, an immunoglobulin or a fragment thereof, e.g. a camelised human single domain antibody or the Fc fragment of an antibody against receptors, cell-surface antigens or cell-surface determinants
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/62—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being a protein, peptide or polyamino acid
- A61K47/64—Drug-peptide, drug-protein or drug-polyamino acid conjugates, i.e. the modifying agent being a peptide, protein or polyamino acid which is covalently bonded or complexed to a therapeutically active agent
- A61K47/6415—Toxins or lectins, e.g. clostridial toxins or Pseudomonas exotoxins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/62—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being a protein, peptide or polyamino acid
- A61K47/64—Drug-peptide, drug-protein or drug-polyamino acid conjugates, i.e. the modifying agent being a peptide, protein or polyamino acid which is covalently bonded or complexed to a therapeutically active agent
- A61K47/642—Drug-peptide, drug-protein or drug-polyamino acid conjugates, i.e. the modifying agent being a peptide, protein or polyamino acid which is covalently bonded or complexed to a therapeutically active agent the peptide or protein in the drug conjugate being a cytokine, e.g. IL2, chemokine, growth factors or interferons being the inactive part of the conjugate
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/62—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being a protein, peptide or polyamino acid
- A61K47/64—Drug-peptide, drug-protein or drug-polyamino acid conjugates, i.e. the modifying agent being a peptide, protein or polyamino acid which is covalently bonded or complexed to a therapeutically active agent
- A61K47/6425—Drug-peptide, drug-protein or drug-polyamino acid conjugates, i.e. the modifying agent being a peptide, protein or polyamino acid which is covalently bonded or complexed to a therapeutically active agent the peptide or protein in the drug conjugate being a receptor, e.g. CD4, a cell surface antigen, i.e. not a peptide ligand targeting the antigen, or a cell surface determinant, i.e. a part of the surface of a cell
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/62—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being a protein, peptide or polyamino acid
- A61K47/66—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being a protein, peptide or polyamino acid the modifying agent being a pre-targeting system involving a peptide or protein for targeting specific cells
- A61K47/665—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being a protein, peptide or polyamino acid the modifying agent being a pre-targeting system involving a peptide or protein for targeting specific cells the pre-targeting system, clearing therapy or rescue therapy involving biotin-(strept) avidin systems
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B82—NANOTECHNOLOGY
- B82Y—SPECIFIC USES OR APPLICATIONS OF NANOSTRUCTURES; MEASUREMENT OR ANALYSIS OF NANOSTRUCTURES; MANUFACTURE OR TREATMENT OF NANOSTRUCTURES
- B82Y5/00—Nanobiotechnology or nanomedicine, e.g. protein engineering or drug delivery
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/52—Cytokines; Lymphokines; Interferons
- C07K14/54—Interleukins [IL]
- C07K14/55—IL-2
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
- C07K14/70503—Immunoglobulin superfamily
- C07K14/7051—T-cell receptor (TcR)-CD3 complex
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/543—Immunoassay; Biospecific binding assay; Materials therefor with an insoluble carrier for immobilising immunochemicals
- G01N33/554—Immunoassay; Biospecific binding assay; Materials therefor with an insoluble carrier for immobilising immunochemicals the carrier being a biological cell or cell fragment, e.g. bacteria, yeast cells
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/566—Immunoassay; Biospecific binding assay; Materials therefor using specific carrier or receptor proteins as ligand binding reagents where possible specific carrier or receptor proteins are classified with their target compounds
- G01N33/567—Immunoassay; Biospecific binding assay; Materials therefor using specific carrier or receptor proteins as ligand binding reagents where possible specific carrier or receptor proteins are classified with their target compounds utilising isolate of tissue or organ as binding agent
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/574—Immunoassay; Biospecific binding assay; Materials therefor for cancer
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/574—Immunoassay; Biospecific binding assay; Materials therefor for cancer
- G01N33/57484—Immunoassay; Biospecific binding assay; Materials therefor for cancer involving compounds serving as markers for tumor, cancer, neoplasia, e.g. cellular determinants, receptors, heat shock/stress proteins, A-protein, oligosaccharides, metabolites
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/574—Immunoassay; Biospecific binding assay; Materials therefor for cancer
- G01N33/57484—Immunoassay; Biospecific binding assay; Materials therefor for cancer involving compounds serving as markers for tumor, cancer, neoplasia, e.g. cellular determinants, receptors, heat shock/stress proteins, A-protein, oligosaccharides, metabolites
- G01N33/57492—Immunoassay; Biospecific binding assay; Materials therefor for cancer involving compounds serving as markers for tumor, cancer, neoplasia, e.g. cellular determinants, receptors, heat shock/stress proteins, A-protein, oligosaccharides, metabolites involving compounds localized on the membrane of tumor or cancer cells
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
- G01N33/6875—Nucleoproteins
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/20—Fusion polypeptide containing a tag with affinity for a non-protein ligand
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/30—Non-immunoglobulin-derived peptide or protein having an immunoglobulin constant or Fc region, or a fragment thereof, attached thereto
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/32—Fusion polypeptide fusions with soluble part of a cell surface receptor, "decoy receptors"
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/435—Assays involving biological materials from specific organisms or of a specific nature from animals; from humans
- G01N2333/705—Assays involving receptors, cell surface antigens or cell surface determinants
- G01N2333/70503—Immunoglobulin superfamily, e.g. VCAMs, PECAM, LFA-3
- G01N2333/7051—T-cell receptor (TcR)-CD3 complex
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/435—Assays involving biological materials from specific organisms or of a specific nature from animals; from humans
- G01N2333/705—Assays involving receptors, cell surface antigens or cell surface determinants
- G01N2333/70503—Immunoglobulin superfamily, e.g. VCAMs, PECAM, LFA-3
- G01N2333/70539—MHC-molecules, e.g. HLA-molecules
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/70—Mechanisms involved in disease identification
- G01N2800/7023—(Hyper)proliferation
- G01N2800/7028—Cancer
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Chemical & Material Sciences (AREA)
- Immunology (AREA)
- Molecular Biology (AREA)
- Cell Biology (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Biomedical Technology (AREA)
- Urology & Nephrology (AREA)
- Hematology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biochemistry (AREA)
- Biotechnology (AREA)
- Physics & Mathematics (AREA)
- Microbiology (AREA)
- Food Science & Technology (AREA)
- Analytical Chemistry (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Pharmacology & Pharmacy (AREA)
- Oncology (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Epidemiology (AREA)
- Organic Chemistry (AREA)
- Hospice & Palliative Care (AREA)
- Biophysics (AREA)
- Toxicology (AREA)
- Gastroenterology & Hepatology (AREA)
- Zoology (AREA)
- Genetics & Genomics (AREA)
- Nanotechnology (AREA)
- General Engineering & Computer Science (AREA)
- Medical Informatics (AREA)
- Crystallography & Structural Chemistry (AREA)
- Optics & Photonics (AREA)
Description
本出願は、「可溶性TCR分子とその使用方法」の名称で2003年11月10日に出願された米国仮特許出願第60/518,790号の優先権を主張するものであり、その全てを本明細書取り込む。
本発明は、MHC又はHLA複合体として存在するペプチド抗原を含む細胞又は組織を検出するための組成物及び方法を特徴とする。本発明は、がん細胞を検出するための感度の高い方法を提供することを含む広範な適用を有する。
本発明は、米国立衛生研究所のグラント第1R43CA88615−01号及び第1R43CA105816−01号に基づき、一部米国政府の助成を受けてなされたものであり、米国政府は本発明に関して所定の権利を有する。
a)細胞又は組織を、存在しているペプチド抗原と可溶性TCR分子又はその断片が特異的な結合複合体を形成する条件下で、少なくとも一つの可溶性TCR分子又はその機能性断片に接触させる、
b)存在しているペプチド抗原に結合しなかったすべての可溶性TCR分子又はその断片を取り除くのに適した条件下で、細胞又は組織を洗浄する、及び
c)存在しているペプチド抗原を含む細胞又は組織の指標としての特異的な結合複合体を検出する、
工程のうち少なくとも一つ、好ましくはその全てを含む。
上記考察のように、本発明は一般に、MHC複合体として細胞又は組織に提示されるペプチド抗原を含む細胞又は組織を検出するための方法を含む。ある態様では、本発明は、存在しているペプチド抗原と可溶性TCR又はその断片が特異的に結合する複合体を形成する条件下で、少なくとも一つの可溶性TCR分子又はその機能的断片と細胞又は組織を接触させること、存在しているペプチド抗原に結合しなかったすべての可溶性TCR分子又はその断片を取り除くのに適した条件下で、細胞又は組織を洗浄すること、及び存在しているペプチド抗原を含む細胞又は組織の指標としての特異的な結合複合体を検出すること、を含む。
さらに他の態様に於いて、MHC複合体はHLA−A2限定性(restricted)である。
本発明で使用される特定のペプチド抗原は、p53(aa149〜157)又はp53(aa264〜272)を含む。
本発明の方法は、インビボ、エキソビボ、又はインビトロで実施することができる。
以下の実施例は、本発明を説明するものであり、何ら本発明を限定するものではない。
ヒトIL−2に融合したp53ペプチド抗原に特異的な、3つのドメインをもつ、HLA−A2.1限定性マウスTCRを含む融合タンパク質を産生した。TCR融合タンパク質構築物として、ヒトp53ペプチド(aa264〜272)に特異的なTCRsを産生するマウスT細胞株から単離したRNAのRT−PCRによりVα及びVβ/Cβ領域(region)を産生した。TCRα鎖(Vα3)可変領域のカルボキシル末端は、TCRの抗原結合部分を産生するために、柔軟なリンカー(G4S)4[文献21参照]を介して、Vβ(Vβ3)のN末端に結合した。Vβドメインに直接結合するCβドメインは、一本鎖の可溶性TCR分子を産生するために、最終システイン直前のアミノ酸残基で切断して膜貫通及び細胞質ドメインを除去した(図1A及び1B)。ヒトIL−2を、短いリンカー(アミノ酸配列 VNAKTTAPSVYPLAPV;配列番号1)を介してTCR部分に融合した。EE標識(アミノ酸配列EEEEYMPME;配列番号2)[文献11参照]は、必要であれば、TCR/IL−2融合タンパク質を抗EE標識mAbによって検出可能にするために、融合分子のIL−2部分のすぐ下流に挿入した。CMVプロモータによって哺乳動物細胞の発現を駆動し、抗体の軽鎖のリーダー配列によって分泌を方向付け、G418耐性にて選別した。
図1Aは、264scTCR/IL−2融合タンパク質のドメイン構造を模式的に示すものである。
図1Bは、264scTCR/IL−2融合タンパク質のアミノ酸配列である。
融合タンパク質のそれぞれのドメインのアミノ酸番号を図中に示す。
264scTCR/IL−2融合タンパク質の性状を検討するために、264scTCR/IL−2構築物を、CHO−K1細胞に安定に形質転換した。264scTCR/IL−2融合タンパク質を分泌する安定な形質転換体は、材料と方法の欄に記載されるようにELISAアッセイを用いて選択した。これらのELISAに於ける陽性シグナルは、形質転換した細胞が、抗マウスTCR及び抗ヒトIL−2抗体両方ともに認識される264scTCR/IL−2融合タンパク質を分泌していることを示し、更に分泌された264scTCR/IL−2が形質転換した細胞内で、適切に集合し、折りたたまれていること、及び細胞から分泌されたときに原型のままで存在すること、を示唆している。
CHO細胞を、264scTCR/IL−2発現ベクターで安定に形質転換した。分泌された融合タンパク質は、免疫親和性クロマトグラフィで精製し、図の上部に示されるように還元又は非還元条件下で、SDS−PAGE処理した。SDS−PAGEゲルは、クーマシーブリリアントブルーで染色した。
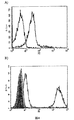
264scTCR/IL−2融合タンパク質のペプチドを収容したMHCへの結合能をフローサイトメトリーで測定した。p53(aa264〜272)又はp53(aa149〜157)(対照)ペプチドを収容したT2細胞を、264scTCR/IL−2融合タンパク質で染色した。p53(aa264〜272)を収容した細胞は、抗TCR CβmAb又は抗IL−2検出抗体のいずれかでの検出で、264scTCR/IL−2により陽性に染色された。p53(aa149〜157)対照ペプチドを収容した細胞は、抗TCR CβmAb又は抗IL−2検出抗体のいずれによっても染色されなかった。p53(aa149〜157)を収容したT2細胞が染色されないのは、p53(aa149〜157)ペプチドがHLA−A2に対し結合不能であるためではないことを証明するために、ペプチドを収容していないT2細胞、p53(aa149〜157)ペプチドを収容したT2細胞又はp53(aa264〜272)ペプチドを収容したT2細胞をそれぞれBB7.2αHLA−A2モノクローナル抗体で染色した。何れのp53ペプチドを収容した細胞も、ペプチドを収容しなかった細胞に比べて強く染色された。このことは、両ペプチドはHLA−A2分子に結合可能であることを示した(図3C)。また、T2細胞をIL−2受容体について調べるために染色したが、IL−2受容体を発現していないことが分かった。これらのデータは、264scTCR/IL−2融合タンパク質の結合が、融合タンパク質のTCR部分によって仲介されていることを示している。T2細胞が対照ペプチドを収容している場合に融合タンパク質によって染色されなかったこともまた、染色がTCR部分を介してなされること、及び、染色が適切なペプチドに特異的であることを示している。これらのデータは、264scTCR/IL−2融合タンパク質のTCR部分がその特異的なペプチドをHLA−A2として認識することが可能であることを示している。
図3A)264scTCR/IL−2融合タンパク質及び抗TCR CβmAbで染色されているか、又は
図3B)264scTCR/IL−2融合タンパク質及び抗IL−2mAbで染色されているかの何れかである。
図3C)p53(aa264〜272)ペプチド(暗い灰色の線)を収容したT2細胞、p53(aa149〜157)ペプチド(明るい灰色の線)を収容したT2細胞、又はペプチドを収容していない(黒い線)T2細胞は、抗HLA−A2 BB7.2mAbで、次いでFITC標識ヤギ抗マウスIgGで染色した。影をつけたピークは、染色されていないT2細胞である。
264scTCR/IL−2融合タンパク質のIL−2部分のIL−2受容体結合能は、フローサイトメトリーによって検討された。マウス初代脾臓細胞を単離し、T細胞芽細胞を産生するために、rIL−2及び抗CD3で刺激した。IL−2受容体を発現する刺激した脾臓細胞は、p53(aa264〜272)を収容したHLA−A2四量体で、264scTCR/IL−2融合タンパク質の存在下でのみ陽性に染色された(図4A)。同様に、CTLL−2マウス細胞傷害性のTリンパ細胞は、恒常的にIL−2受容体を発現しているが、264scTCR/IL−2融合タンパク質により、陽性に染色されたが、264scTCR/κ融合タンパク質では染色されなかった(図4B)。CTLL−2細胞をα−ヒトCD25ブロッキング抗体又はアイソタイプの対照抗体、次いで264scTCR/IL−2とインキュベートすると、細胞をブロッキング抗体とインキュベートしたときには染色は実質的に減少したが、アイソタイプの対照抗体では減少しなかった。264scTCR/マウスκ鎖融合タンパク質又はIL−2受容体ブロッキング抗体とインキュベートしたCTLL−2細胞からシグナルが欠如したことは、これらの細胞の染色が264scTCR/IL−2融合タンパク質のIL−2部分によって仲介されていることを示している。これらのデータは、264scTCR/IL−2融合タンパク質のIL−2部分が、IL−2受容体に結合できることを示唆している。
図4A)マウス脾臓細胞を、IL−2及び抗CD3εmAbで刺激し、その後、264scTCR/IL−2融合タンパク質の存在下(灰色の線)又は非存在下(黒い線)でインキュベートした。結合した融合タンパク質は、PE標識したHLA−A2p53(aa264〜272)四量体で検出された。
図4B)CTLL−2細胞を、α−ヒトCD25ブロッキング抗体又はアイソタイプの対照抗体、次いで264scTCR/IL−2又は264scTCR/κ融合タンパク質とインキュベートした。結合した融合タンパク質は、PE標識したα−TCR−Vβ3抗体で検出した。影のついたピークは、染色されていないCTLL−2細胞である。
黒い線:264scTCR/IL−2だけで染色したCTLL−2細胞。
灰色の点線:対照抗体に次いで264scTCR/IL−2で染色したCTLL−2細胞。
明るい灰色の線:α−ヒトCD25ブロッキング抗体、次いで264scTCR/IL−2でインキュベートしたCTLL−2細胞。
暗い灰色の線:264scTCR/κ融合タンパク質で染色したCTLL−2細胞。
黒いダッシュの線:α−TCR-Vβで染色したCTLL−2細胞。
264scTCR/IL−2融合タンパク質のIL−2部分の生物学的活性を実証するため、IL−2依存性のCTLL−2細胞を、様々な濃度の264scTCR/IL−2又は組み換えIL−2のいずれかと共に培養し、細胞の生存率をWST−1を用いて評価した。図5Aに示されるように、rIL−2又は264scTCR/IL−2のCTLL−2細胞の増殖を支援する能力は、投与量依存性であり、ここに於いて、組み換えIL−2又は264scTCR/IL−2のいずれかをより高濃度にしたときに、より多くの細胞増殖がみられた。さらに、組み換えIL−2又は264scTCR/IL−2のいずれかを同等モル量を使用したとき、細胞の増殖は同様のレベルであった。特異性に対する更なる対照として、CTLL−2細胞を、α−ヒトCD25ブロッキング抗体又はアイソタイプの対照とともに264scTCR/IL−2とインキュベートした。培養物にブロッキング抗体が含まれた場合、増殖はブロッキング抗体の濃度の減少とともに実質的に減少したが、CTLL−2細胞の増殖は、いずれの濃度の対照抗体の影響も受けなかった(図5B)。このデータは、264scTCR/IL−2のIL−2部分がインビトロで組み換えIL−2と同様な生物学的活性を有すること、及び融合タンパク質の増殖活性がその分子のIL−2部分に依存していること、を示している。
図5A)CTLL−2細胞を、264scTCR/IL−2(実線)又は組み換えIL−2(点線)と共に、図の下段に示されるような様々な濃度で培養した。
図5B)CTLL−2細胞を、図の下段に示されるような264scTCR/IL−2及びα−ヒトCD25ブロッキング抗体又はアイソタイプの対照抗体と共に、インキュベートした。細胞の生存率は、WST−1と共にインキュベートして測定し、吸光度は450nmで測定した。
Cab+5:5μg対照抗体;Cab+50:50μg対照抗体;Bab+5:5μgブロッキング抗体;Bab+50:50μgブロッキング抗体
264scTCR/IL−2融合タンパク質の有用な特性は、そのTCR及びサイトカイン部分の各々により、標的細胞及びエフェクター細胞を結合させる能力にある。264scTCR/IL−2融合タンパク質が細胞を効果的に結合させることができることを実証するために、T2細胞を、p53(aa264〜272)又はp53(aa149〜157)ペプチドのいずれかで収容し、その後ジヒドロエチジウム(HE)で標識した。CTLL−2細胞を、カルセインAMで標識し、二つの標識された細胞集団を、264scTCR/IL−2融合タンパク質の存在下又は非存在下で混合し、インキュベートした。試料を、フローサイトメトリーで分析した。二つの細胞集団を264scTCR/IL−2融合タンパク質の非存在下でインキュベートした時(図6A及び6B)、又はT2細胞に対照ペプチドを収容し、CTLL−2細胞と264scTCR/IL−2融合タンパク質の存在下でインキュベートした時(図6C)、フローサイトメトリーヒストグラム上では、細胞群は二つの異なる集団に含まれたが、総集団の約45%が各々(図6A、6B、及び6Cの領域1及び3に)示されており、総集団の約0.46%のみが、二重染色されたセルウィンドウ(図6A、6B、及び6Cの領域2)に示された。しかしながら、T2細胞をp53(aa264〜272)ペプチドを収容し、264scTCR/IL−2融合タンパク質の存在下で、CTLL−2細胞とインキュベートした場合(図6D)、2重染色された細胞集団は、全集団の4.1%(図6Dの領域2、結合細胞)であり、このことは、T2細胞が264scTCR/IL−2融合タンパク質を介してCTLL−2細胞に結合していることを示唆している。
T2細胞を、p53(aa264〜272)(図6B及び6D)又はp53(aa149〜157)(対照)ペプチド(図6A及び6C)のいずれかで収容し、その後HEで標識した。CTLL−2細胞を、カルセインAMで標識した。標識された細胞を、264scTCR/IL−2融合タンパク質の存在下(図6C及び6D)又は非存在下(図6A及び6B)で混合して、インキュベートし、次いで試料をフローサイトメトリーで分析した。収容に使用されたペプチド及び融合タンパク質の存在又は非存在といったアッセイ条件を、各ヒストグラムの下に示す。一重染色領域は、1及び3の番号で示され、2重染色された細胞集団は2番で示されている。
264scTCR/IL−2融合タンパク質の薬物速度論は、BLAB/cマウスを用いて測定した。薬物をマウスに、経静脈的に投与し、様々な経過時点での血清試料を回収した。264scTCR/IL−2融合タンパク質の血清レベルは、ELISAを用いて測定した。ELISA検出は、融合タンパク質がインビボで修飾されているか、又は切断されているかを決定するために、抗TCRmAb捕獲/抗IL−2Ab検出(図7A)、抗TCRmAb捕獲/抗TCRmAb検出(図7B)、又は抗IL−2mAb捕獲/抗IL−2ポリクローナルAb検出(図7C)を用いて実施した。264scTCR/IL−2融合タンパク質を注入されたマウスは、毒性の兆候をまったく示さなかった。これらのアッセイに於いて、使用したELISA形式により、見かけ上の血清中半減期が1.6〜3.0時間で、最大濃度0.75〜2.5μg/mLの264scTCR/IL−2が検出された(図7)。報告されているフリーのIL−2の血清中半減期は、約5分であるので[文献6参照]、これらのデータは、融合タンパク質がインビボで切断されておらず、その代わり血液中で比較的長期間にわたり原型のまま残存することを示している。これらの検討で測定された264scTCR/IL−2の半減期に於ける小さなぶれは、多分に、ELISAアッセイの感度の違いによるものである。
BALB/cマウスに、264scTCR/IL−2融合タンパク質を注入し、血清試料を、注入後15、30分、1、4、8、24時間後に集めた。264scTCR/IL−2の血清濃度は、以下の形式を用いて、ELISAにより測定した。
7A)抗TCRmAb捕獲/抗IL−2Ab検出;
7B)抗TCRmAb捕獲/抗TCRmAb検出;及び
7C)抗IL−2mAb捕獲/抗IL−2Ab検出
264scTCR/IL−2融合タンパク質が、標的の腫瘍細胞を認識し、結合できれば、有用である。264scTCR/IL−2が腫瘍細胞に結合することができるかどうかを試験するため、HLA−A2.1及びp53の両方を発現している、A375ヒトメラノーマ細胞を、264scTCR/IL−2又は無関係なTCR/IL−2融合タンパク質である3C8、のいずれかで染色した。融合タンパク質とインキュベートしていない細胞及び3C8とインキュベートした細胞は、H57−597検出抗体により陽性に染色されないが、264scTCR/IL−2とインキュベートした細胞は検出抗体で陽性に染色された(図8)。この結果から、264scTCR/IL−2融合タンパク質が、標的の腫瘍細胞を認識し、結合できること、そしてインビボ抗がん治療として役に立つことが示唆される。
A375ヒトメラノーマ細胞を、融合タンパク質なし(黒いダッシュの線)、5μgの3C8TCR/IL−2融合たんぱく質(対照)(点線)、又は5μgの264scTCR/IL−2融合タンパク質(黒い実線)とインキュベートし、次いで、H57−597mAbで染色した。染色されなかった細胞は、影のついた領域で示す。
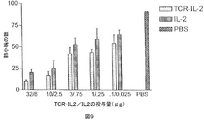
264scTCR/IL−2融合タンパク質がインビボで抗腫瘍効果を持つかどうかを決定するために、実験的転移アッセイを実施した。メスの胸腺欠損ヌードマウスに、高転移性A375ヒトメラノーマサブクローンであるA375−C15Nを注入し、様々な投与量の264scTCR/IL−2又は組み換えIL−2のいずれかで処置した。腫瘍細胞注入後42日で、肺の小塊をカウントした。264scTCR/IL−2と組み換えIL−2の両方とも、投与量依存的に肺転移を減少させた(図9)が、264scTCR/IL−2融合タンパク質の方が、全ての投与量に於いて、肺転移を大きく減少させた。このことは、サイトカインを腫瘍に標的化することは、がん治療として大きな効果をもたらすものであることが示唆される。
メスの胸腺欠損ヌードマウスに、高度に転移性のA375−C15N細胞を注入し、264scTCR/IL−2、組み換えIL−2、又はPBSで処理した。腫瘍細胞の注入の42日後、肺を摘出し、肺の小塊をカウントし、次いでPBS処理した対照群に対応する肺の小塊数の平均をプロットした。
様々な264scTCR融合タンパク質の単量体や多量体を調製し、それらのT2細胞に対する結合挙動を、以下のセクション11及び12に記載される方法で、フローサイトメトリーにより分析した。その結果、図10に示されるように、264scTCR融合タンパク質は、p53(aa264〜273)を収容したT2細胞を、p53(aa149〜157)を収容した細胞より強く染色した(図10A、10B)。図中では、染色されていないT2細胞は、T2 149非染色001と表示されたヒストグラム中に示されている;第2の試薬(H57−PE)で染色した、p53(aa149〜157)及びp53(aa264〜273)を収容したT2細胞は、それぞれ「T2 149 H57.002」及び「T2 264 H57.009」と表示されたヒストグラム中に示されている;多量体の264scTCR/IgG1に次いでH57−PEで染色した、p53(aa149〜157)及びp53(aa264〜273)を収容したT2細胞は、それぞれ「T2 149 IgG H57.003」及び「T2 264 IgG H57.010」と表示されたヒストグラム中に示されている;264scTCR/IL−2に次いでH57−PEで染色したp53(aa149〜157)及びp53(aa264〜273)を収容したT2細胞は、それぞれ「T2 149 IL2 H57.004」及び「T2 264 IL2 H57.011」と表示されたヒストグラム中に示されている;単量体の264scTCR/trunIgG1に次いでH57−PEで染色したp53(aa149〜157)及びp53(aa264〜273)を収容したT2細胞は、それぞれ「T2 149 trun H57.005」及び「T2 264 trun H57.012」と表示されたヒストグラム中に示されている;そして単量体の264scTCR/BirAに次いでH57−PEで染色したp53(aa149〜157)及びp53(aa264〜273)を収容したT2細胞は、それぞれ「T2 149 birA H57.006」及び「T2 264 birA H57.013」と表示されたヒストグラム中に示されている。この結果は、観察した染色がペプチド特異的であることを確証づけた。
264scTCR試薬が腫瘍細胞を染色する能力もまた試験された。培養したA375細胞を、10mMのEDTAを添加したPBS(pH7.4)で接着を剥がし、洗浄用緩衝液で2回洗浄した。細胞染色は、4μgの264scTCR/IgG1融合タンパク質を用いて、23℃にて45分間実行された。細胞を一回洗浄し、3μgのFITC結合のヤギ抗ヒトIgGFcのF(ab’)2断片(抗IgG−FITC)で染色した。2回洗浄した後、染色細胞を、再び縣濁し、次いでFACScanで分析した。抗IgG−FITC抗体のみで染色したA375細胞を、対照として用いた
。
考察のように、保存又は「固定された」試料のMHC/ペプチド複合体を検出することは、特に患者から取得した細胞、組織、又は他の生物学的試料を固定するのが通常である臨床又は他の医学的環境に於いて、有用性がある。しかしながら、MHC/ペプチド複合体は3つの分離したペプチド鎖からなる細胞表面抗原であるため、通常の固定化手順の後の可溶性TCRによる検出の際に、MHC/ペプチド複合体の完全な構造が十分原型をとどめていられるかどうか定かではない。可溶性TCRの染色が、固定された細胞上で実施できたかどうかを評価するために、ペプチドを収容したT2細胞及び遺伝子操作がなされていないA375細胞を、フローサイトメトリーで分析した。培養細胞A375は、10mMのEDTAを含むPBS(pH7.4)で接着を剥がし、洗浄用緩衝液で2回洗浄した。T2細胞は、50μMのp53(aa264〜273)で3時間インキュベートし、その後洗浄用緩衝液で2回洗浄した。両方の細胞は、3.7%のホルムアルデヒドで5分間固定し、2回洗浄した。細胞染色は、4μgの264scTCR/IgG1又はCMVscTCR/IgG1融合タンパク質を用いて、20μgのHLA−A2.1/p53(aa264〜272)四量体の存在下又は非存在下、23℃で45分間実施した。細胞を一回洗浄し、3μgのFITC結合ヤギ抗ヒトIgGFcのF(ab’)2断片で染色した。染色された細胞は、2回洗浄した後、再縣濁して、FACScanで分析した。
HLA−A2及びp53発現に於いて異なるいくつかの細胞株(すなわち、A375、HT29及びSaos2)を、分析のために選び、264scTCR/IgG1融合タンパク質又は対照の融合タンパク質CMVscTCR/IgG1のいずれかで染色した。細胞を、カバースリップ上で24時間培養し、その後3.7%のホルムアルデヒドで5分間固定し、次いで洗浄緩衝液(0.5%のBSA及び0.1%のアジ化ナトリウム入りPBS)で2回洗浄した。BSAは、非特異的なタンパク質結合を低減させるブロッキング試薬である。細胞を、5%の正常ヤギ血清(NGS)を含む200μLのPBS中の10μgの264scTCR/IgG1又はCMVscTCR/IgG1融合タンパク質で、23℃にて45分間染色した。NGSは、非特異的結合を低減させるブロッキング試薬である。細胞を2回洗浄し、3μgのFITC結合のヤギ抗ヒトIgGFcのF(ab’)2断片(Jackson ImmunoResearch, West Grove, PA)で染色した。細胞を、2回洗浄し、その後平衡化緩衝液(Molecular Probe, Eugene, OR)で1回洗浄した。カバースリップは、スライドガラス上に、グリセロール緩衝液中の色あせ防止試薬(Molecular Probe, Eugene, OR)でマウントし、ネイルオイルで密閉した。スライドを、SPOT RTカメラを有したニコン社製のエピ蛍光顕微鏡(Nikon, Tokyo, Japan)及びSPOT RTソフトウェアv3.2(Diagnostic Instrument, Sterling Heights, MI)を用いて、記録した。
ペプチドを収容したT2細胞に結合できる264scTCR複合体の数が、測定された。T2細胞を、様々な量のp53(aa264〜273)と共に3時間インキュベートし、その後、洗浄用緩衝液で2回洗浄した。3.7μgの264scTCR/BirA−ストレプトアビジン−PE四量体を用いて23℃にて45分間、細胞染色を実施した。2回洗浄後、染色された細胞を、再縣濁し、FACScanで分析した。一方、3.76μgの264scTCR/IgG1融合タンパク質を用いて23℃にて45分間、細胞染色を実施した。細胞を1回洗浄し、3μgのPE結合抗ヒトIgG抗体で染色した。2回洗浄後、染色された細胞を、再縣濁し、FACScanで分析した。
皮下腫瘍を産生するために、A375ヒトメラノーマ細胞(1x106)を、ヌードマウスの左肩に皮下注入した。腫瘍を、500mm3まで成長させ、マウスは人道的に犠牲にした。腫瘍を、覆っている皮膚とともに摘出し、中性緩衝液ホルマリン中で一晩固定させた。転移性の肺小塊を産生するために、MDA−MB−231細胞(1x106)を、ヌードマウスの側部尾静脈に注入し、転移性の肺小塊を発達させた。18日後、マウスを人道的に犠牲にして、肺を取り出し、次いで中性緩衝液ホルマリン中で固定した。固定された組織を、70%、90%、95%、100%(2回)エタノール中で連続的に30分のインキュベーションし、次いでキシレン中で30分間のインキュベーションを2回行い、脱水した。その後組織を、パラフィン中に包埋して、5μm切片を調製し、そして顕微鏡スライド上にマウントした。
ヒト腫瘍組織アレイは、商業的な供給元又はティッシュアレイリサーチプログラム(Tissue Array Research Program:NCI)から得られる。染色のために、組織アレイのスライドを、それぞれキシレン中で5分間のリンスを2回行い、次いで100%(2回)、95%、及び85%エタノールでそれぞれ2分間、連続的なインキュベーションにより、再度水和した。PBSによる5分間2回及び蒸留水による5分間1回の洗浄後、内因性のペルオキシダーゼを失活させるためにスライドを、3%の過酸化水素中で5分間インキュベートし、次いで蒸留水で5分間の洗浄を1回行った。スライドを、抗原回復溶液(Dako)中に置き、97℃にて20分間加熱した。スライドを、抗原回復溶液中で20分間室温まで冷却し、その後、PBSで5分間の洗浄を2回行った。非HRPで標識された二次試薬を用いる場合は、スライドをアビジン/ビオチンブロッキング溶液中でインキュベートし(それぞれの溶液で10分)、次いでPBS中で5分間の洗浄を2回する。スライドを、1%の正常ヤギ血清(NGS)を含むPBS中で室温にて30分間ブロッキングし、その後、264scTCR/IgG1融合タンパク質又はCMVscTCR/IgG1融合タンパク質(又は他の非結合scTCR試薬)の存在下、又は非存在下で室温にて45分間インキュベートする。PBS中で5分間の洗浄を2回行った後、スライドを、二次試薬(HRP標識されたヤギ抗ヒトIgG又はビオチン化された抗TCRCβ抗体のいずれか)中、室温にて45分間インキュベートする。スライドは、それぞれPBSで5分間の洗浄を2回行う。
発現ベクターは、GFP(緑色蛍光タンパク質)又はLuc(ホタル・ルシフェラーゼ)に融合した264scTCRを産生するために構築される。これらのベクターは、本明細書記載の264scTCR/IgG1発現ベクターから、IgG1遺伝子断片をGFP又はLucをコードする配列に置き換えることにより、産生できる。これらのコード配列は、商業的に入手可能である(例えば、GFP遺伝子に対してはpEGFP−C1(Clontech)、Luc遺伝子に対してはpSP−Luc(Promega))。ベクターは、標準的なPCR法により適切なDNA配列を単離するための鋳型として用いられる。対照TCR(すなわちCMVscTCR)のGFP及びLucへの融合物の発現ベクターは、同じ方法で産生可能である。ある適用では、これらの発現ベクターは、CHO細胞のような形質転換細胞に使用できる。そして結果として発現するタンパク質は、本明細書に記載されているようにして精製される。
HLA−A2/p53陽性の腫瘍細胞を保持する腫瘍部位に於ける264scTCR/Luc又は264scTCR/GFP試薬の、他の組織と比較して異なる検出を明らかにする画像化検討から得られる結果は、scTCR試薬が、インビボに於いて腫瘍を特異的に検出できることを示している。
別の態様に於いて、264scTCR融合タンパク質は、例えば、131Iによる直接のヨード化によって放射線標識される。ヨード化は、標準的な方法により実施される。HLA−A2及びp53発現に関して様々であるヒトの腫瘍細胞を、皮下又は静脈内のいずれかに注入し、腫瘍又は転移性の肺小塊を、記載されたように発達させる。マウスに放射線標識された264scTCR融合タンパク質を経静脈又は腹腔内投与し、放射線標識された264scTCR融合タンパク質を注入して、例えば、1、2、4、8、及び12時間後、そして1から14日後に、画像化する。全身スキャンするために、マウスを、ペントバルビタールナトリウム(100mg/kg)で麻酔して、例えばマイクロコンピュータと連結した、4mmピンホールのコリメーターを有した大きな視野のSopha DSXカメラで、画像化する。腫瘍部位に於ける放射線核種で標識された264scTCR試薬の、他の組織との比較により、差別化された検出を実践する画像化の検討から得られた結果は、それらの放射線標識されたscTCR試薬がインビボに於いて腫瘍を特異的に検出するために有用であることを示唆するものである。
以下の材料及び方法は、実施例に概説された実験を実施するために必要に応じて用いられた。
A2.1 264CTLクローン#5は、HLA−A2.1トランスジェニックマウス[文献49参照]に於いて産生されたヒトp53 264〜272ペプチドに特異的なCTLラインから限界希釈法[文献50参照]により得られた。CHO.K1チャイニーズハムスター卵巣、JurkatヒトTリンパ球、CTLL−2マウス細胞傷害性Tリンパ球、T2ヒトリンパ芽球、A375ヒトメラノーマ、H57−597ハイブリドーマ、及びBB7.2ハイブリドーマ細胞株は、アメリカンタイプカルチャーコレクション(ATCC:Rockville, MD)から得られた。T2ヒトリンパ芽球細胞は、HLA−A2.1に対し陽性であるが、外来性ペプチドを収容することができる空のMHC分子を提示するための、TAP1及び2タンパク質が欠損している[文献2参照]。A375ヒトメラノーマ細胞株は、本発明者らの研究室でHLA−A2.1及びp53に関して試験されて、両方の抗原に関して陽性であることが見出された。H57−597ハイブリドーマは、マウスのTCRβ定常領域に於けるエピトープを認識するモノクローナル抗体を産生し、BB7.2ハイブリドーマは、HLA−A2のα2ドメイン上のエピトープを特異的に認識するBB7.2モノクローナル抗体を産生する。ヒトメラノーマ細胞株A375の高度に転移性のサブクローン、A375−C15Nは、インビボに於ける転移性検討にしか使われないものであるが、以前に報告されたように維持された[文献53参照]。薬物速度論検討に於けるELISAに使用される、組み換えヒトIL−2及びビオチン化抗ヒトIL−2ポリクローナル抗体は、R&D Systems,Inc.(Minneapolis, MN)から購入された。抗TCR CβmAbH57−597、抗マウスTCR Vβ3mAb、抗マウスCD3εmAb、抗ヒトIL−2mAb、抗ヒトCD25ブロッキング抗体及びアイソタイプの対照抗体、及びFITC標識されたヤギ抗マウスIgGは、Pharmingen(San Diego, CA)から得られた。すべての細胞培養培地及び添加物は、CellGro(Herndon, VA)から購入され、他に記されない限り、すべての細胞培養材料は、Nunc(Rochester, NY)から購入された。すべてのマウスは、Harlan Labs(Indianapolis, IN)から購入された。
すべての細胞株は、10%熱不活性化FBS、2mMのL−グルタミン、及び1 mg/mLのG418(形質転換されたCHO細胞についてのみ)を添加されたIMDMを含む完全な培養培地中で、37℃にて5%のCO2下で維持された。CTLL−2細胞は、9U/mLの組み換えヒトIL−2を添加した同じ培地中で維持された。A375−C15N細胞は、10%熱不活性化FBS、ペニシリン及びストレプトマイシン(Life Technologies)を含むRPMI−1640中で維持された。
プライマー−オリゴヌクレオチドプライマーは、マウスT細胞受容体及びヒトIL−2遺伝子に適合する又は相補する配列から合成された:
KC228:5’−GAGGTGGCCCAGCCGGCCATGGCCCAGTCAGTGACGCAGC−3’;(配列番号3)
KC229:5’−GAGGTGACTAGTGTCTGGCTTTATAATTAG−3’;(配列番号4)
PRIB4:5’−GGGGGGCTCGAGCAATTCAAAAGTCATTCAGACTC−3’;(配列番号5)
KC176:5’−GAGGTGGAGCCCGGGGTCTGCTCGGCCCCAGGC−3’;(配列番号6)
ET−TCRF1:5’−CCCACCGGTCAGTCAGTGACGCAGCCC−3’;(配列番号7)
KC−170:5’−GTGGAGTTCGAAAAGGTGACTTACGTTTGTCTGCTCGGCCCCAG−3’;(配列番号8)
KC231:5’CGATAAGTGTACTTACGTTTTCATTATTCCATCGGCATGTACTCTTCTTCCTCTCG−3’;(配列番号9)
KC208:5’GTGGAGATCGATAAGTGTACTTACGTTTTCATTATCGCGATCCGGAGTTAACGTCTGCTCGGCCCCAG−3’;(配列番号10)
KC327B:5’−TAGGTGTCCGGAGCACCTACTTCAAGTTCTAC−3’;(配列番号11)
KC328B:5’−TAGGTGTCGCGAAGTTAGTGTTGAGATGATG−3’;(配列番号12)
AP2:5’−ACTCACTATAGGGCTCGAGCGGC−3’;(配列番号13)
CαHYB:5’GCTGTCCTGAGACCGAGGATCTTTTAACTG3’;(配列番号14)
CβHYB:5’−TTGTTTGTTTGCAATCTGTGCTTTTGATGG−3’;(配列番号15)
264scTCR/IL−2は、抗マウスTCRモノクローナル抗体H57−597を用いた免疫親和性クロマトグラフィにより、細胞培養物の上清液から精製された。なお、この抗マウスTCRモノクローナル抗体H57−597は、TCRβ鎖の不変領域にあるエピトープを認識して、セファロース4Bカラム(Amersham Pharmacia, Piscataway, NJ)に結合している。精製された試料は、その後、30kDaの分子量でカットオフする膜(Millipore, Bedford, MA)を有したUltrafree−15遠心性フィルターを用いて、濃縮され、PBSに緩衝液交換された。TCR融合タンパク質試料は、2〜8℃(短期間)又は−80℃(長期間)で生化学的及び機能的分析のために保存された。SDS−PAGEが、還元条件又は非還元条件のいずれかで、4〜12%のNu−PAGEポリアクリルアミドゲル(Novex, San Diego, CA)及びNovex EX−Cell IIシステムを用いて実施された。SDS−PAGEゲルは、クーマシーブルーで染色された。
すべてのELISAは、100〜200ng/wellの抗ヒトIL−2mAb又は抗マウスTCR Vβ3mAbでコートされたMaxisorb96ウェルプレート(Nunc, Rochester, NY)を用いて行われた。融合タンパク質は、ビオチン化された抗マウスTCRH57mAb、抗マウスTCRVβ3mAb、又は抗IL−2ポリクローナル抗体、次いでストレプトアビジン−HRP(Kirkegaard and Perry Laboratories, Gaithersburg, MD)、TMB基質、及び反応を停止させるための0.18MのH2SO4(BioFx, Owings Mills, MD)で検出された。吸光度は、96ウェルプレートリーダー(Bio-Tek Instruments, Inc., Winooski, VT)を用いて、450nmで測定された。
p53(aa149〜157)又はp53(aa264〜272)ペプチドのいずれかでパルスされたT2細胞は、1%のFBSを含むPBS中で、0.5μgの264scTCR/IL−2融合タンパク質と室温にて30分間インキュベートされた。細胞はその後、0.5μgの抗IL−2Ab又は0.5μgのビオチン化抗TCRH57−597mAbと、室温にて30分間インキュベートされ、次いで1μgの抗マウスκPE又は5ngのストレプトアビジン−PE(両方とも、Becton Dickenson, Franklin Lakes, NJ)とそれぞれインキュベートされた。試料は、FACScan分析(Becton Dickenson, Franklin Lakes, NJ)の前に1%のFBSを含むPBS中で、洗浄された。両p53ペプチドがHLA−A2に同様に結合するかどうかを決定するため、ペプチドを収容した細胞は、BB7.2を用いて室温にて30分間染色され、次いでFITCで標識されたヤギ抗マウスIgGで染色され、そしてFACScan機器で分析された。
p53(aa264〜272)ペプチド又はp53(aa149〜157)ペプチドのいずれかでパルスされたT2細胞は、7.88ng/mlのジヒドロエチジウム(HE)(Molecular Probes, Inc., Eugene, OR)で標識され、CTLL−2細胞は、50ng/mlのカルセインAM(Molecular Probes, Inc., Eugene, OR)で標識された。洗浄後、標識された細胞の二つの集団は、1対1の比率で、2μgの264scTCR/IL−2融合タンパク質の存在又は非存在下で、室温にて20分間一緒に混合された。細胞はその後、FACScanにより分析された。
CTLL−2細胞は、様々な濃度の組み換えIL−2又は264scTCR/IL−2のいずれかを含む100μLの培養培地中に、1ウェル当たり4x103細胞で撒かれ、37℃にて21時間、5%CO2下でインキュベートされた。特異性についての対照として、CTLL−2細胞は、5又は50μgの抗ヒトCD25ブロッキング抗体又はアイソタイプの対照抗体の存在又は非存在下で、264scTCR/IL−2と37℃にて21時間、5%CO2下でインキュベートされた。細胞増殖試薬WST−1(Roche Inc., Indianapolis, IN)が、1ウェル当たり20μL添加され、37℃にて4時間、5%CO2下でインキュベートされた。吸光度は、96ウェルプレートリーダー上450nmで測定された。
動物に関するすべての実験に於いて、適用可能なところでは、特定の国内法令と同様、研究室に於ける動物配慮の原則(NIH発行 No.85〜23,1985年改訂)に従った。メスのBALB/cマウスは、経静脈的に側部尾静脈を介して、100μLになるようにPBSで希釈した、32μgの264scTCR/IL−2融合タンパク質を注入した。血清は、バックグラウンドレベルを確立するために、264scTCR/IL−2を注入されていない一つのマウス集団から採取された。血清は、注入された集団から、15分、30分、1、2、4、8、及び24時間後に、尾の出血で採取された。血液試料は、14,000xgにて、4℃で10分間遠心され、血清は回収され、そして使用されるまで−80℃に保存された。264scTCR/IL−2濃度は、捕獲のため抗TCRVβ3又は抗IL−2モノクローナル抗体、及びビオチン化抗TCRH57モノクローナル又は抗IL−2モノクローナル抗体のいずれか、次いで、検出のためにストレプトアビジンHRPを用いて、ELISAにより決定された。
メスの胸腺欠損ヌードマウス(nu/nu)は、5.0x105のA375−C15N細胞を側部尾静脈を介して、注入された。動物は、様々な濃度の264scTCR/IL−2(全量100μlに32、10、3、1、又は0.1μg)又は組み換えヒトIL−2(全量100μlに8、2.5、0.75、0.25、又は0.025μg)を、腫瘍細胞投与後1、2、3、4、7、10、14、17、21、28、及び35日に注入された。腫瘍細胞注入後42日に、すべての動物は人道的に犠牲にされ、肺が取り出され、Bouin溶液中で固定され、肺表面腫瘍小塊が数えられた。それぞれの肺の腫瘍小塊は、二人の観察者によって数えられ、平均数が記録された。
TCR遺伝子は、記載されたようにT細胞クローンA2.1 264#5からクローン化された。このT細胞クローンから得られた一本鎖のTCRは、264scTCRと指定された。3ドメインの一本鎖264scTCRは、264scTCR/IL−2融合タンパク質構築物を鋳型として用いて、増幅された。264scTCR/IgG1発現構築物を産生するために、一本鎖のTCR断片は、抗体重鎖発現ベクターに結紮されて、抗体の可変領域を置き換え、一本鎖のTCRをヒトIgG1重鎖領域に結合させた。264scTCR/trunIgG1を産生するために、ジスルフィド結合を形成するヒンジ領域の前で切り取られたIgG1重鎖ドメインを含む発現ベクターに、TCR断片が結紮された。
264scTCR試薬が固定された及び固定されていない細胞を染色する能力は、いくつかの検討で特徴付けられた。細胞染色方法は、様々な検出可能ドメインを保持している264scTCR融合物の利用、及び様々な蛍光標識プローブでこれらの融合物の細胞レベルの相互作用を検出すること、を含む。いくつかの対照は、特異的な染色を評価するために用いられた。対照は、p53(aa264〜273)抗原を欠損している細胞を264scTCR試薬で染色すること、p53陽性細胞をCMVscTCR試薬で染色すること、p53陽性細胞を二次染色試薬だけで染色すること、及びp53陽性細胞を可溶性HLA−A2/p53多量体のような競合的ブロッキング試薬の存在下及び非存在下に於いて264scTCR試薬で染色すること、を含んでいる。
次の文献は、本発明の開示の全体を通して、(以下に示される番号によって)参照される。その各々は、参照して本明細書に取り込む。
1. Altman J D, Moss PA, Goulder PJ, Barouch DH, McHeyzer-Williams MG, Bell JI, McMichael AJ, Davis MM (1996) Phenotypic analysis of antigen-specific T lymphocytes. Science 274: 94
2. Anderson KS, Alexander J, Wei M, Cresswell P (1993) Intracellular transport of class I MHC molecules in antigen processing mutant cell lines. J Immunol 151: 3407
3. Bauer RJ, Dedrick RL, White ML, Murray MJ, Garovoy MR (1999) Population pharmacokinetics and pharmacodynamics of the anti-CD11a antibody hu1124 in human subjects with psoriasis. J Pharmacokinet Biopharm 27: 397
4. Becker JC, Varki N, Gillies SD, Furukawa K, Reisfeld RA (1996) Long-lived and transferable tumor immunity in mice after targeted interleukin-2 therapy. J Clin Invest 98: 2801
5. Chung S, Wucherpfennig KW, Friedman SM, Hafler DA, Strominger JL (1994) Functional three-domain single-chain T-cell receptors. Proc Natl Acad Sci USA 91: 12654
6. Donohue JH, Rosenberg SA (1983) The fate of interleukin-2 after in vivo administration. J Immunol 130: 2203
7. Dummer R, Gore ME, Hancock BW, Guillou PJ, Grobben HC, Becker JC, Oskam R, Dieleman JP, Burg G (1995) A multicenter phase II clinical trial using dacarbazine and continuous infusion interleukin-2 for metastatic melanoma. Clinical data and immunomonitoring. Cancer 75: 1038
8. Engel I, Ottenhoff TH, Klausner RD (1992) High-efficiency expression and solubilization of functional T cell antigen receptor heterodimers. Science 256: 1318
9. Gregoire C, Rebai N, Schweisguth F, Necker A, Mazza G, Auphan N, Millward A, Schmitt-Verhulst A M, Malissen B (1991) Engineered secreted T-cell receptor alpha beta heterodimers. Proc Natl Acad Sci USA 88: 8077
10. Grimm EA, Mazumder A, Zhang HZ, Rosenberg SA (1982) Lymphokine-activated killer cell phenomenon. Lysis of natural killer-resistant fresh solid tumor cells by interleukin 2-activated autologous human peripheral blood lymphocytes. J. Exp Med 155: 1823
11. Grussenmeyer T, Scheidtmann KH, Hutchinson MA, Eckhart W, Walter G (1985) Complexes of polyoma virus medium T antigen and cellular proteins. Proc Natl Acad Sci USA 82: 7952
12. Hank J A, Albertini MR, Schiller J, Sondel PM (1993) Activation of multiple effector mechanisms to enhance tumor immunotherapy. J. Immunother 14: 329
13. Hank JA, Robinson RR, Surfus J, Mueller BM, Reisfeld RA, Cheung NK, Sondel PM (1990a) Augmentation of antibody dependent cell mediated cytotoxicity following in vivo therapy with recombinant interleukin 2. Cancer Res 50: 5234
14. Hank JA, Sosman JA, Kohler PC, Bechhofer R, Storer B, Sondel PM (1990b) Depressed in vitro T cell responses concomitant with augmented interleukin-2 responses by lymphocytes from cancer patients following in vivo treatment with interleukin-2. J. Biol Response Mod 9: 5
15. Hank JA, Surfus J, Gan J, Chew TL, Hong R, Tans K, Reisfeld R, Seeger RC, Reynolds CP, Bauer M, et al. (1994) Treatment of neuroblastoma patients with antiganglioside GD2 antibody plus interleukin-2 induces antibody-dependent cellular cytotoxicity against neuroblastoma detected in vitro. J. Immunother 15: 29
16. Harvill ET, Fleming JM, Morrison SL (1996) In vivo properties of an IgG3-IL-2 fusion protein. A general strategy for immune potentiation. J Immunol 157: 3165
17. Harvill ET, Morrison SL (1995) An IgG3-IL2 fusion protein activates complement, binds Fc gamma R1, generates LAK activity and shows enhanced binding to the high affinity IL-2R. Immunotechnology 1: 95
18. Hilyard KL, Reyburn H, Chung S, Bell JI, Strominger JL (1994) Binding of soluble natural ligands to a soluble human T-cell receptor fragment produced in Escherichia coli. Proc Natl Acad Sci USA 91: 9057
19. Hinds PW, Finlay CA, Quartin RS, Baker SJ, Fearon ER., Vogelstein B, Levine A J (1990) Mutant p53 DNA clones from human colon carcinomas cooperate with ras in transforming primary rat cells: a comparison of the "hot spot" mutant phenotypes. Cell Growth Differ 1: 571
20. Hurford RK Jr, Dranoff G, Mulligan RC, Tepper RI (1995) Gene therapy of metastatic cancer by in vivo retroviral gene targeting. Nat Genet 10: 430
21. Huston JS, Levinson D, Mudgett-Hunter M, Tai MS, Novotny J, Margolies M N, Ridge RJ, Bruccoleri RE, Haber E, Crea R, et al (1988) Protein engineering of antibody binding sites: recovery of specific activity in an anti-digoxin single-chain Fv analogue produced in Escherichia coli. Proc Natl Acad Sci USA 85: 587
22. Iggo R, Gatter K, Bartek J, Lane D, Harris AL (1990) Increased expression of mutant forms of p53 oncogene in primary lung cancer. Lancet 335: 675
23. Kendra K, Gan J, Ricci M, Surfus J, Shaker A, Super M, Frost J D, Rakhmilevich A, Hank JA, Gillies SD, Sondel PM (1999) Pharmacokinetics and stability of the ch14.18-interleukin-2 fusion protein in mice. Cancer Immunol Immunother 48: 219
24. Klausner RD, Lippincott-Schwartz J, Bonifacino JS (1990) The T cell antigen receptor: insights into organelle biology. Annu Rev Cell Biol 6: 403
25. Lewis LD, Cole BF, Wallace PK, Fisher JL, Waugh M, Guyre PM, Fanger MW, Curnow RT, Kaufman PA, Ernstoff MS (2001) Pharmacokinetic-pharmacodynamic relationships of the bispecific antibody MDX-H210 when administered in combination with interferon gamma: a multiple-dose phase-I study in patients with advanced cancer which overexpresses HER-2/neu. J. Immunol Methods 248: 149
26. Lin AY, Devaux B, Green A, Sagerstrom C, Elliott JF, Davis MM (1990) Expression of T cell antigen receptor heterodimers in a lipid-linked form. Science 249: 677
27. Lode HN, Xiang R, Dreier T, Varki NM, Gillies SD, Reisfeld RA (1998) Natural killer cell-mediated eradication of neuroblastoma metastases to bone marrow by targeted interleukin-2 therapy. Blood 91: 1706
28. Lode HN, Xiang R, Varki NM, Dolman CS, Gillies SD, Reisfeld RA (1997) Targeted interleukin-2 therapy for spontaneous neuroblastoma metastases to bone marrow. J. Natl Cancer Inst 89: 1586
29. Lustgarten J, Marks J, Sherman LA (1999) Redirecting effector T cells through their IL-2 receptors. J. Immunol 162: 359
30. McLaughlin R, O'Hanlon D, McHale T, Connolly CE, Given HF (2001) Prognostic implications of p53 and bcl-2 expression in 108 women with stage two breast cancer. Ir J Med Sci 170: 11
31. Motzer RJ, Rakhit A, Ginsberg M, Rittweger K, Vuky J, Yu R, Fettner S, Hooftman L (2001) Phase I trial of 40-kd branched pegylated interferon alfa-2a for patients with advanced renal cell carcinoma. J. Clin Oncol 19: 1312
32. Motzer RJ, Rakhit A, Schwartz LH, Olencki T, Malone TM, Sandstrom K, Nadeau R, Parmar H, Bukowski R (1998) Phase I trial of subcutaneous recombinant human interleukin-12 in patients with advanced renal cell carcinoma. Clin Cancer Res 4: 1183
33. Nastala CL, Edington HD, McKinney TG, Tahara H, Nalesnik MA, Brunda MJ, Gately MK, Wolf SF, Schreiber RD, Storkus WJ, et al. (1994) Recombinant IL-12 administration induces tumor regression in association with IFN-gamma production. J. Immunol 153: 1697
34. Pardoll DM (1995) Paracrine cytokine adjuvants in cancer immunotherapy. Annu Rev Immunol 13: 399
35. Peng LS, Penichet ML, Morrison SL (1999) A single-chain IL-12 IgG3 antibody fusion protein retains antibody specificity and IL-12 bioactivity and demonstrates antitumor activity. J. Immunol 163: 250
36. Penichet ML, Harvill ET, Morrison SL (1997) Antibody-IL-2 fusion proteins: a novel strategy for immune protection. Hum Antibodies 8: 106
37. Posey JA, Raspet R, Verma U, Deo YM, Keller T, Marshall JL, Hodgson J, Mazumder A, Hawkins MJ (1999) A pilot trial of GM-CSF and MDX-H210 in patients with erbB-2-positive advanced malignancies. J. Immunother 22: 371
38. Pullarkat V, Deo Y, Link J, Spears L, Marty V, Curnow R, Groshen S, Gee C, Weber JS (1999) A phase I study of a HER2/neu bispecific antibody with granulocyte-colony-stimulating factor in patients with metastatic breast cancer that overexpresses HER2/neu. Cancer Immunol Immunother 48: 9
39. Reddy KR, Wright TL, Pockros PJ, Shiffman M, Everson G, Reindollar R, Fried MW, Purdum PP 3rd, Jensen D, Smith C, et al. (2001) Efficacy and safety of pegylated (40-kd) interferon alpha-2a compared with interferon alpha-2a in noncirrhotic patients with chronic hepatitis C. Hepatology 33: 433
40. Rosenberg SA, Lotze MT, Muul LM, Chang AE, Avis FP, Leitman S, Linehan WM, Robertson CN, Lee RE, Rubin JT, et al (1987) A progress report on the treatment of 157 patients with advanced cancer using lymphokine-activated killer cells and interleukin-2 or high-dose interleukin-2 alone. N Engl J. Med 316: 889
41. Rosenberg SA, Lotze MT, Yang JC, Aebersold PM, Linehan WM, Seipp CA, White D E (1989) Experience with the use of high-dose interleukin-2 in the treatment of 652 cancer patients. Ann Surg 210: 474
42. Rosenberg SA, Spiess PJ, Schwarz S (1983) In vivo administration of Interleukin-2 enhances specific alloimmune responses. Transplantation 35: 631
43. Rosenberg SA, Yang JC, White DE, Steinberg SM (1998) Durability of complete responses in patients with metastatic cancer treated with high-dose interleukin-2: identification of the antigens mediating response. Ann Surg 228: 307-
44. Royal RE, Steinberg SM, Krouse RS, Heywood G, White DE, Hwu P, Marincola FM, Parkinson DR, Schwartzentruber DJ, Topalian SL, et al. (1996) Correlates of Response to IL-2 Therapy in Patients Treated for Metastatic Renal Cancer and Melanoma. Cancer J. Sci Am 2: 91
45. Sherman LA, Hesse SV, Irwin MJ, La Face D, Peterson P (1992) Selecting T cell receptors with high affinity for self-MHC by decreasing the contribution of CD8. Science 258: 815
46. Sondel PM, Kohler PC, Hank JA, Moore KH, Rosenthal NS, Sosman JA, Bechhofer R, Storer B (1988) Clinical and immunological effects of recombinant interleukin 2 given by repetitive weekly cycles to patients with cancer. Cancer Res 48: 2561
47. Sosman JA, Hank JA, Moore KH, Borchert A, Schell K, Kohler PC, Goldstein D, Bechhofer R, Storer B, Albertini MR, et al. (1991) Prolonged interleukin-2 (IL-2) treatment can augment immune activation without enhancing antitumor activity in renal cell carcinoma. Cancer Invest 9: 35
48. Temmim L, Baker H, Sinowatz F (2001) Immunohistochemical detection of p53 protein expression in breast cancer in young Kuwaiti women. Anticancer Res 21: 743
49. Theobald M, Biggs J, Dittmer D, Levine AJ, Sherman LA (1995) Targeting p53 as a general tumor antigen. Proc Natl Acad Sci USA 92: 11993
50. Theobald M, Biggs J, Hernandez J, Lustgarten J, Labadie C, Sherman LA (1997) Tolerance to p53 by A2.1-restricted cytotoxic T lymphocytes. J. Exp Med 185: 833
51. thor Straten P, Guldberg P, Schrama D, Andersen MA, Moerch U, Seremet T, Siedel C, Reisfeld RA, Becker JC (2001) In situ cytokine therapy: redistribution of clonally expanded T cells. Eur J. Immunol 31: 250
52. Tsung K, Meko JB, Peplinski GR, Tsung YL, Norton JA (1997) IL-12 induces T helper 1-directed antitumor response. J. Immunol 158: 3359
53. van Golen KL, Risin S, Staroselsky A, Berger D, Tainsky MA, Pathak S, Price JE (1996) Predominance of the metastatic phenotype in hybrids formed by fusion of mouse and human melanoma clones. Clin Exp Metastasis. 14: 95
54. Weber S, Traunecker A, Oliveri F, Gerhard W, Karjalainen K (1992) Specific low-affinity recognition of major histocompatibility complex plus peptide by soluble T-cell receptor. Nature 356: 793
55. Weil-Hillman G, Voss SD, Fisch P, Schell K, Hank JA, Sosman JA, Sugamura K, Sondel P M (1990) Natural killer cells activated by interleukin 2 treatment in vivo respond to interleukin 2 primarily through the p75 receptor and maintain the p55 (TAC) negative phenotype. Cancer Res 50: 2683
56. Wiebke EA, Rosenberg SA, Lotze MT (1988) Acute immunologic effects of interleukin-2 therapy in cancer patients: decreased delayed type hypersensitivity response and decreased proliferative response to soluble antigens. J. Clin Oncol 6: 1440.
57. O'Herron SM, Lebowitz MS, Bieler JG, al-Ramadi BK, Utz U, Bothwell ALM and Schneck JP (1997) Analysis of the expression of peptide-major histocompatibility complexes using high affinity soluble divalent T cell receptors. J. Exp Med 186: 1333.
Claims (35)
- a)内因性のペプチド抗原が提示される細胞又は組織を、可溶性TCR分子又はその断片が特異的な結合複合体を形成する条件下で、少なくとも一つの可溶性TCR分子又はその断片に接触させる、
b)前記ペプチド抗原に結合しなかったすべての可溶性TCR分子又はその断片を取り除くのに適した条件下で、細胞又は組織を洗浄する、及び
c)前記ペプチド抗原を含む細胞又は組織の指標としての特異的な結合複合体を検出する、
工程を含む、MHC複合体として細胞又は組織上に提示される前記ペプチド抗原を含む細胞又は組織を検出するための方法であって、
前記可溶性TCR分子又はその断片が、V−α鎖、V−β鎖及びC−β鎖を含む一本鎖TCR分子であり、サイトカイン又は免疫グロブリンドメインと共有結合していることを特徴とする方法。 - サイトカインがインターロイキン2(IL−2)である、請求項1に記載の方法。
- 免疫グロブリンドメインがIgG1ドメインである、請求項1に記載の方法。
- 一本鎖TCR分子が野生型のTCRから構築される、請求項1〜3のいずれかに記載の方法。
- 細胞又は組織をさらに、少なくとも一つのブロッキング試薬と接触させる、請求項1〜4のいずれかに記載の方法。
- 可溶性TCR又はその断片と細胞との非特異的結合を減少させるために、工程aの前に細胞又は組織をブロッキング試薬と接触させることを更に含む、請求項5に記載の方法。
- ブロッキング試薬が過酸化物、血清蛋白質、抗体又はその断片である、請求項5又は6に記載の方法。
- 複合体に結合できる可溶性TCR又はその断片に競合的及び特異的に結合する条件下で、前記複合体を競合MHC分子又はその断片と接触させることを更に含む、請求項1〜7のいずれかに記載の方法。
- 競合複合体を形成するために、実質的にすべての可溶性TCR又はその断片が競合MHC分子又はその断片に結合している、請求項8に記載の方法。
- 競合複合体を検出すること及びMHC分子又は可溶性TCRの結合特異性を決定することを更に含む、請求項8又は9に記載の方法。
- MHC分子又はその断片が一本鎖である、請求項8〜10のいずれかに記載の方法。
- MHC分子又はその断片がペプチド抗原を収容している、請求項8〜11のいずれかに記載の方法。
- 細胞又は組織が懸濁されている、請求項1〜12のいずれかに記載の方法。
- 可溶性TCR分子又はその断片が、一本鎖のTCRを少なくとも一つ含む、請求項1〜13のいずれかに記載の方法。
- 可溶性TCR分子又はその断片が検出可能に標識されている、請求項1〜14のいずれかに記載の方法。
- 検出可能な標識が、ビオチン、ストレプトアビジン、酵素又はその触媒活性を有する断片、放射性核種、ナノ粒子、常磁性金属イオン、又は、蛍光、りん光若しくは化学発光分子である、請求項15に記載の方法。
- MHC複合体がHLA−A2限定性である、請求項1〜16のいずれかに記載の方法。
- 内因性ペプチド抗原を含まない細胞と可溶性TCR又はその断片の如何なる結合をも検出するための対照を用いることを更に含む、請求項1〜17のいずれかに記載の方法。
- インビボ、エキソビボ、又はインビトロで実行される、請求項1〜18のいずれかに記載の方法。
- 細胞又は組織が腫瘍細胞又は腫瘍組織である、請求項1〜19のいずれかに記載の方法。
- 内因性ペプチド抗原が、腫瘍関連ペプチド抗原である、請求項1〜20のいずれかに記載の方法。
- 内因性ペプチド抗原が、p53(aa149〜157)又はp53(aa264〜272)である、請求項1〜20のいずれかに記載の方法。
- 細胞又は組織を少なくとも一つの変性試薬と接触させることを更に含む、請求項1〜22のいずれかに記載の方法。
- 工程aの前に、細胞又は組織を変性試薬と接触させ、細胞又は組織を変性させる(固定させる)ことを更に含む、請求項23に記載の方法。
- 複数の細胞又は組織をアレイに搭載することを更に含む、請求項1〜24のいずれかに記載の方法。
- 細胞又は組織を搭載したアレイのそれぞれの要素に於いて実施される、請求項25に記載の方法。
- アレイのそれぞれの要素に於いて実質的に同時に実施される、請求項25又は26に記載の方法。
- 工程cが、アレイをスキャンすること、及び特異的な結合複合体の存在を示す画像情報を発生させることを更に含む、請求項25〜27のいずれかに記載の方法。
- 工程cが、リアルタイムに情報を利用者に出力すること、及び必要に応じて画像情報の保存画像に見出しをつけることを更に含む、請求項28に記載の方法。
- 細胞上に提示される内因性のペプチド抗原の量が、約100,000コピーより少ない、請求項1〜29のいずれかに記載の方法。
- 細胞上に提示される内因性のペプチド抗原の量が、約400コピーより少ない、請求項1〜30のいずれかに記載の方法。
- 可溶性TCR分子又はその断片を含有してなる、細胞又は組織中の、MHC複合体として細胞又は組織上に提示される内因性のペプチド抗原を検出するための検出用組成物であって、
前記可溶性TCR分子又はその断片が、V−α鎖、V−β鎖及びC−β鎖を含む一本鎖TCR分子であり、サイトカイン又は免疫グロブリンドメインと共有結合していることを特徴とする検出用組成物。 - 可溶性TCR分子又はその断片を含有してなる、腫瘍細胞又は腫瘍組織中の、MHC複合体として細胞又は組織上に提示される内因性の腫瘍関連ペプチド抗原を検出するための検出用組成物であって、
前記可溶性TCR分子又はその断片が、V−α鎖、V−β鎖及びC−β鎖を含む一本鎖TCR分子であり、サイトカイン又は免疫グロブリンドメインと共有結合していることを特徴とする検出用組成物。 - 可溶性TCR分子又はその断片が検出可能に標識されている、請求項32又は33に記載の検出用組成物。
- 検出可能な標識が、ビオチン、ストレプトアビジン、酵素又はその触媒活性を有する断片、放射性核種、ナノ粒子、常磁性金属イオン、又は蛍光、りん光若しくは化学発光分子である、請求項34に記載の検出用組成物。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US51879003P | 2003-11-10 | 2003-11-10 | |
| US60/518,790 | 2003-11-10 | ||
| PCT/US2004/037569 WO2005046449A2 (en) | 2003-11-10 | 2004-11-10 | Soluble tcr molecules and methods of use |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2007513326A JP2007513326A (ja) | 2007-05-24 |
| JP2007513326A5 JP2007513326A5 (ja) | 2007-12-27 |
| JP4773361B2 true JP4773361B2 (ja) | 2011-09-14 |
Family
ID=34590303
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2006539829A Active JP4773361B2 (ja) | 2003-11-10 | 2004-11-10 | 可溶性tcr分子とその使用方法 |
Country Status (8)
| Country | Link |
|---|---|
| US (4) | US8772451B2 (ja) |
| EP (1) | EP1691661B1 (ja) |
| JP (1) | JP4773361B2 (ja) |
| KR (1) | KR101131297B1 (ja) |
| CN (2) | CN105021814B (ja) |
| AU (1) | AU2004289316B2 (ja) |
| CA (1) | CA2544483C (ja) |
| WO (1) | WO2005046449A2 (ja) |
Families Citing this family (27)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2007085266A1 (en) * | 2006-01-30 | 2007-08-02 | Dako Denmark A/S | High-speed quantification of antigen specific t-cells in whole blood by flow cytometry |
| JP4748542B2 (ja) * | 2006-02-24 | 2011-08-17 | 古河電気工業株式会社 | フローサイトメトリーによる生体分子の定量システム、及び定量方法 |
| WO2008116468A2 (en) | 2007-03-26 | 2008-10-02 | Dako Denmark A/S | Mhc peptide complexes and uses thereof in infectious diseases |
| ES2470772T3 (es) | 2007-05-11 | 2014-06-24 | Altor Bioscience Corporation | Moléculas de fusión y variantes de IL-15 |
| EP3620465A1 (en) | 2007-07-03 | 2020-03-11 | Dako Denmark A/S | Improved methods for generation, labeling and use of mhc multimers |
| EP2197908A2 (en) | 2007-09-27 | 2010-06-23 | Dako Denmark A/S | Mhc multimers in tuberculosis diagnostics, vaccine and therapeutics |
| US10968269B1 (en) | 2008-02-28 | 2021-04-06 | Agilent Technologies, Inc. | MHC multimers in borrelia diagnostics and disease |
| US20110070191A1 (en) * | 2008-03-19 | 2011-03-24 | Wong Hing C | T cell receptor fusions and conjugates and methods of use there of |
| WO2010009735A2 (en) * | 2008-07-23 | 2010-01-28 | Dako Denmark A/S | Combinatorial analysis and repair |
| GB0817244D0 (en) * | 2008-09-20 | 2008-10-29 | Univ Cardiff | Use of a protein kinase inhibitor to detect immune cells, such as T cells |
| US10369204B2 (en) | 2008-10-02 | 2019-08-06 | Dako Denmark A/S | Molecular vaccines for infectious disease |
| EP2258719A1 (en) * | 2009-05-19 | 2010-12-08 | Max-Delbrück-Centrum für Molekulare Medizin (MDC) | Multiple target T cell receptor |
| US11053299B2 (en) | 2010-09-21 | 2021-07-06 | Immunity Bio, Inc. | Superkine |
| EP2918607B1 (en) | 2010-09-21 | 2017-11-08 | Altor BioScience Corporation | Multimeric il-15 soluble fusion molecules and methods of making and using same |
| WO2012058627A2 (en) * | 2010-10-29 | 2012-05-03 | Miqin Zhang | Pre-targeted nanoparticle system and method for labeling biological particles |
| US10654908B2 (en) | 2014-04-15 | 2020-05-19 | University Of Virginia Patent Foundation | Isolated T cell receptors and methods of use therefor |
| CN112494646A (zh) | 2014-06-30 | 2021-03-16 | 阿尔托生物科学有限公司 | 基于il-15的分子及其方法和用途 |
| US10865230B2 (en) | 2016-05-27 | 2020-12-15 | Altor Bioscience, Llc | Construction and characterization of multimeric IL-15-based molecules with CD3 binding domains |
| JP7012364B2 (ja) * | 2016-08-05 | 2022-02-14 | 国立大学法人東北大学 | T細胞受容体の認識機構を用いたがん又は感染症の治療及び診断 |
| AU2017345791B2 (en) | 2016-10-21 | 2020-10-22 | Altor Bioscience Corporation | Multimeric IL-15-based molecules |
| EP3592778A4 (en) | 2017-03-06 | 2021-01-13 | Altor BioScience Corporation | IL-15 FUSION PROTEINS SPECIFIC TO IL-12 AND IL-18 |
| TW202116798A (zh) * | 2017-03-08 | 2021-05-01 | 新加坡商新加坡科技研究局 | 類t細胞受體之抗體 |
| US20190048055A1 (en) | 2017-03-31 | 2019-02-14 | Altor Bioscience Corporation | Alt-803 in combination with anti-cd38 antibody for cancer therapies |
| CN111655716B (zh) | 2017-08-28 | 2024-03-08 | 艾尔特生物科技公司 | 基于il-15的与il-7和il-21的融合体 |
| JP2020535832A (ja) * | 2017-10-05 | 2020-12-10 | アメリカ合衆国 | マウス定常領域を伴うtcrを発現する細胞を選択的に増幅するための方法 |
| EP3773657A4 (en) | 2018-03-26 | 2021-12-08 | Altor Bioscience LLC | ANTI-PDL1, IL-15 AND TGF BETA RECEPTOR COMBINATION MOLECULES |
| US20220275043A1 (en) | 2018-07-17 | 2022-09-01 | Massachusetts Institute Of Technology | Soluble multimeric immunoglobulin-scaffold based fusion proteins and uses thereof |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2001090747A2 (en) * | 2000-05-25 | 2001-11-29 | Sunol Molecular Corporation | Modulation of t-cell receptor interactions |
| JP2002515243A (ja) * | 1998-05-19 | 2002-05-28 | アヴィデックス リミテッド | 多価t細胞受容体複合体 |
| JP2003518377A (ja) * | 1999-12-06 | 2003-06-10 | ボード オブ トラスティーズ オブ ザ ユニバーシティ オブ イリノイ | 高親和性tcrタンパク質および方法 |
| US20030144474A1 (en) * | 2000-06-05 | 2003-07-31 | Sunol Molecular Corporation | T cell receptor fusions and conjugates and methods of use thereof |
Family Cites Families (29)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US34513A (en) * | 1862-02-25 | Improvement in machines for stacking hay | ||
| US253632A (en) * | 1882-02-14 | Heney j | ||
| US82719A (en) * | 1868-10-06 | Improved mode of preserving fruits, meats, vegetables | ||
| US91079A (en) * | 1869-06-08 | Improvement in device for operating throttle-valves | ||
| US198144A (en) * | 1877-12-11 | Improvement in devices for decorating vases | ||
| US171552A (en) * | 1875-12-28 | Improvement in wash-boards | ||
| US144474A (en) * | 1873-11-11 | Improvement in the means for propelling vessels | ||
| US4384193A (en) | 1981-06-09 | 1983-05-17 | Immulok, Inc. | Incubating device for specimen mounted on glass slides in immunoassays |
| WO1988009344A1 (en) * | 1987-05-21 | 1988-12-01 | Creative Biomolecules, Inc. | Targeted multifunctional proteins |
| FR2698880B1 (fr) * | 1992-11-25 | 1995-02-24 | Inst Nat Sante Rech Med | Procédé de production de récepteurs T solubles, produits ainsi obtenus et leur utilisation dans des compositions diagnostiques ou thérapeutiques. |
| US7074904B2 (en) | 1994-07-29 | 2006-07-11 | Altor Bioscience Corporation | MHC complexes and uses thereof |
| WO1996018105A1 (en) | 1994-12-06 | 1996-06-13 | The President And Fellows Of Harvard College | Single chain t-cell receptor |
| US5869270A (en) * | 1996-01-31 | 1999-02-09 | Sunol Molecular Corporation | Single chain MHC complexes and uses thereof |
| DE19616997A1 (de) | 1996-04-27 | 1997-10-30 | Boehringer Mannheim Gmbh | Verfahren zur automatisierten mikroskopunterstützten Untersuchung von Gewebeproben oder Körperflüssigkeitsproben |
| EP1019439B1 (en) * | 1997-10-02 | 2011-11-16 | Altor BioScience Corporation | Soluble single-chain t-cell receptor proteins |
| US6232445B1 (en) | 1997-10-29 | 2001-05-15 | Sunol Molecular Corporation | Soluble MHC complexes and methods of use thereof |
| ES2293748T3 (es) * | 1998-10-21 | 2008-03-16 | Altor Bioscience Corporation | Moleculas de fijacion poliespecificas y usos de las mismas. |
| US6566063B1 (en) | 1999-05-14 | 2003-05-20 | Chiron Corporation | Methods for determining metastatic potential of breast cancer cells by detecting GSEF gene product expression |
| US6406840B1 (en) | 1999-12-17 | 2002-06-18 | Biomosaic Systems, Inc. | Cell arrays and the uses thereof |
| EP1118661A1 (en) | 2000-01-13 | 2001-07-25 | Het Nederlands Kanker Instituut | T cell receptor libraries |
| CA2400789A1 (en) | 2000-02-22 | 2001-08-30 | Genospectra, Inc. | Microarray fabrication techniques and apparatus |
| US20020058235A1 (en) * | 2000-02-29 | 2002-05-16 | Dinnerstein Mitchell Elliot | Jack switch talking block |
| US6466690C1 (en) | 2000-12-19 | 2008-11-18 | Bacus Res Lab Inc | Method and apparatus for processing an image of a tissue sample microarray |
| JP4447456B2 (ja) * | 2001-06-05 | 2010-04-07 | アルトール バイオサイエンス コーポレーション | P53結合t細胞受容体分子とその使用 |
| US6642661B2 (en) | 2001-08-28 | 2003-11-04 | Tokyo Electron Limited | Method to affect spatial distribution of harmonic generation in a capacitive discharge reactor |
| EP1567553A2 (en) * | 2002-12-03 | 2005-08-31 | Avidex Ltd. | Complexes of receptors |
| EP1796237B1 (de) * | 2005-12-13 | 2007-08-01 | Nexans, Societe Anonyme | Elektrische Durchführung zur Verbindung einer supraleitenden Einrichtung mit einer bei Raumtemperatur befindlichen Einrichtung |
| US20110070191A1 (en) * | 2008-03-19 | 2011-03-24 | Wong Hing C | T cell receptor fusions and conjugates and methods of use there of |
| TWM523243U (zh) | 2015-04-01 | 2016-06-01 | 嚴介宏 | 手機轉接裝置及系統 |
-
2004
- 2004-11-10 AU AU2004289316A patent/AU2004289316B2/en active Active
- 2004-11-10 EP EP04818691.0A patent/EP1691661B1/en active Active
- 2004-11-10 CN CN201510413443.8A patent/CN105021814B/zh active Active
- 2004-11-10 US US10/985,271 patent/US8772451B2/en active Active
- 2004-11-10 CA CA2544483A patent/CA2544483C/en active Active
- 2004-11-10 JP JP2006539829A patent/JP4773361B2/ja active Active
- 2004-11-10 CN CNA2004800401834A patent/CN1901839A/zh active Pending
- 2004-11-10 KR KR1020067011529A patent/KR101131297B1/ko active IP Right Grant
- 2004-11-10 WO PCT/US2004/037569 patent/WO2005046449A2/en active Application Filing
-
2014
- 2014-02-18 US US14/182,888 patent/US9290560B2/en active Active
-
2016
- 2016-02-10 US US15/040,724 patent/US20160199523A1/en not_active Abandoned
-
2019
- 2019-04-29 US US16/398,226 patent/US20190269807A1/en not_active Abandoned
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2002515243A (ja) * | 1998-05-19 | 2002-05-28 | アヴィデックス リミテッド | 多価t細胞受容体複合体 |
| JP2003518377A (ja) * | 1999-12-06 | 2003-06-10 | ボード オブ トラスティーズ オブ ザ ユニバーシティ オブ イリノイ | 高親和性tcrタンパク質および方法 |
| WO2001090747A2 (en) * | 2000-05-25 | 2001-11-29 | Sunol Molecular Corporation | Modulation of t-cell receptor interactions |
| US20030144474A1 (en) * | 2000-06-05 | 2003-07-31 | Sunol Molecular Corporation | T cell receptor fusions and conjugates and methods of use thereof |
Also Published As
| Publication number | Publication date |
|---|---|
| CN1901839A (zh) | 2007-01-24 |
| EP1691661B1 (en) | 2014-01-08 |
| US9290560B2 (en) | 2016-03-22 |
| US20190269807A1 (en) | 2019-09-05 |
| KR101131297B1 (ko) | 2012-03-30 |
| EP1691661A2 (en) | 2006-08-23 |
| WO2005046449A2 (en) | 2005-05-26 |
| US20160199523A1 (en) | 2016-07-14 |
| US20140378656A1 (en) | 2014-12-25 |
| EP1691661A4 (en) | 2008-02-20 |
| JP2007513326A (ja) | 2007-05-24 |
| CA2544483C (en) | 2013-09-10 |
| AU2004289316B2 (en) | 2011-03-31 |
| KR20070001909A (ko) | 2007-01-04 |
| AU2004289316A1 (en) | 2005-05-26 |
| CN105021814B (zh) | 2018-02-16 |
| CN105021814A (zh) | 2015-11-04 |
| US8772451B2 (en) | 2014-07-08 |
| CA2544483A1 (en) | 2005-05-26 |
| US20050214284A1 (en) | 2005-09-29 |
| WO2005046449A3 (en) | 2006-01-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4773361B2 (ja) | 可溶性tcr分子とその使用方法 | |
| US11479614B2 (en) | Methods for treating cancer or modulating T cells or NK cells in a subject with cancer by administering cells comprising chimeric cytokine receptors | |
| ES2251120T3 (es) | Glicoproteinas de superficie celular asociadas a los linfomas b humanos-ulbp, adn y polipeptidos. | |
| WO2008146911A9 (ja) | IL13Ra2に対する抗体およびこれを含む診断・治療薬 | |
| TW202126683A (zh) | T細胞調節多肽及其使用方法 | |
| US20220289820A1 (en) | Chimeric cytokine receptor | |
| WO2023073352A1 (en) | Chimeric cytokine receptor | |
| KR102669749B1 (ko) | 키메라 사이토카인 수용체 | |
| NZ739942B2 (en) | Chimeric cytokine receptor |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20071112 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20071112 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20100219 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20100316 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20100611 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20100618 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20100713 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20100721 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20100803 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20100810 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100915 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20101214 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20110308 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20110315 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110414 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20110531 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20110623 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20140701 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 Ref document number: 4773361 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |