JP4703075B2 - 外用貼付剤 - Google Patents
外用貼付剤 Download PDFInfo
- Publication number
- JP4703075B2 JP4703075B2 JP2001511904A JP2001511904A JP4703075B2 JP 4703075 B2 JP4703075 B2 JP 4703075B2 JP 2001511904 A JP2001511904 A JP 2001511904A JP 2001511904 A JP2001511904 A JP 2001511904A JP 4703075 B2 JP4703075 B2 JP 4703075B2
- Authority
- JP
- Japan
- Prior art keywords
- acid
- mass
- salt
- organic acid
- patch
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
- -1 organic acid salt Chemical class 0.000 claims abstract description 69
- 150000003839 salts Chemical class 0.000 claims abstract description 30
- 239000002253 acid Substances 0.000 claims abstract description 28
- 239000000203 mixture Substances 0.000 claims abstract description 25
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical compound [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 claims abstract description 16
- 239000001632 sodium acetate Substances 0.000 claims abstract description 16
- 235000017281 sodium acetate Nutrition 0.000 claims abstract description 16
- 150000001732 carboxylic acid derivatives Chemical class 0.000 claims abstract description 6
- 229910052751 metal Inorganic materials 0.000 claims abstract description 5
- 239000002184 metal Substances 0.000 claims abstract description 5
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 claims description 39
- 239000012790 adhesive layer Substances 0.000 claims description 34
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 15
- 238000002156 mixing Methods 0.000 claims description 12
- XIQVNETUBQGFHX-UHFFFAOYSA-N Ditropan Chemical compound C=1C=CC=CC=1C(O)(C(=O)OCC#CCN(CC)CC)C1CCCCC1 XIQVNETUBQGFHX-UHFFFAOYSA-N 0.000 claims description 9
- 229960005434 oxybutynin Drugs 0.000 claims description 9
- 238000013329 compounding Methods 0.000 claims description 7
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical compound [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 claims 1
- 239000003814 drug Substances 0.000 abstract description 45
- 150000007524 organic acids Chemical class 0.000 abstract description 33
- 125000004432 carbon atom Chemical group C* 0.000 abstract description 8
- 238000009472 formulation Methods 0.000 abstract description 5
- 150000001559 benzoic acids Chemical class 0.000 abstract 1
- 150000003870 salicylic acids Chemical class 0.000 abstract 1
- 229940079593 drug Drugs 0.000 description 21
- YGSDEFSMJLZEOE-UHFFFAOYSA-N salicylic acid Chemical compound OC(=O)C1=CC=CC=C1O YGSDEFSMJLZEOE-UHFFFAOYSA-N 0.000 description 14
- 238000002360 preparation method Methods 0.000 description 13
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 12
- 230000000052 comparative effect Effects 0.000 description 12
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 11
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 10
- 229920000346 polystyrene-polyisoprene block-polystyrene Polymers 0.000 description 10
- 229920005989 resin Polymers 0.000 description 10
- 239000011347 resin Substances 0.000 description 10
- 210000003491 skin Anatomy 0.000 description 10
- RSWGJHLUYNHPMX-UHFFFAOYSA-N Abietic-Saeure Natural products C12CCC(C(C)C)=CC2=CCC2C1(C)CCCC2(C)C(O)=O RSWGJHLUYNHPMX-UHFFFAOYSA-N 0.000 description 9
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 9
- 229920002367 Polyisobutene Polymers 0.000 description 9
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 9
- KHPCPRHQVVSZAH-HUOMCSJISA-N Rosin Natural products O(C/C=C/c1ccccc1)[C@H]1[C@H](O)[C@@H](O)[C@@H](O)[C@@H](CO)O1 KHPCPRHQVVSZAH-HUOMCSJISA-N 0.000 description 9
- ZWUKMNZJRDGCTQ-UHFFFAOYSA-N Tizanidine hydrochloride Chemical compound Cl.ClC=1C=CC2=NSN=C2C=1NC1=NCCN1 ZWUKMNZJRDGCTQ-UHFFFAOYSA-N 0.000 description 9
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 9
- 235000014113 dietary fatty acids Nutrition 0.000 description 9
- 229930195729 fatty acid Natural products 0.000 description 9
- 239000000194 fatty acid Substances 0.000 description 9
- 229960002388 tizanidine hydrochloride Drugs 0.000 description 9
- KHPCPRHQVVSZAH-UHFFFAOYSA-N trans-cinnamyl beta-D-glucopyranoside Natural products OC1C(O)C(O)C(CO)OC1OCC=CC1=CC=CC=C1 KHPCPRHQVVSZAH-UHFFFAOYSA-N 0.000 description 9
- 231100000245 skin permeability Toxicity 0.000 description 8
- 239000003431 cross linking reagent Substances 0.000 description 7
- FJKROLUGYXJWQN-UHFFFAOYSA-N papa-hydroxy-benzoic acid Natural products OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 7
- 229960004889 salicylic acid Drugs 0.000 description 7
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 6
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 6
- 238000010521 absorption reaction Methods 0.000 description 6
- 235000019441 ethanol Nutrition 0.000 description 6
- 239000010410 layer Substances 0.000 description 6
- 229940057995 liquid paraffin Drugs 0.000 description 6
- 238000000034 method Methods 0.000 description 6
- 239000000126 substance Substances 0.000 description 6
- 239000005711 Benzoic acid Substances 0.000 description 5
- 229920002799 BoPET Polymers 0.000 description 5
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 5
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 5
- 239000003522 acrylic cement Substances 0.000 description 5
- 230000001070 adhesive effect Effects 0.000 description 5
- 230000000202 analgesic effect Effects 0.000 description 5
- 230000003110 anti-inflammatory effect Effects 0.000 description 5
- 235000010233 benzoic acid Nutrition 0.000 description 5
- 235000010354 butylated hydroxytoluene Nutrition 0.000 description 5
- 239000003795 chemical substances by application Substances 0.000 description 5
- DNTGGZPQPQTDQF-XBXARRHUSA-N crotamiton Chemical compound C/C=C/C(=O)N(CC)C1=CC=CC=C1C DNTGGZPQPQTDQF-XBXARRHUSA-N 0.000 description 5
- 229960003338 crotamiton Drugs 0.000 description 5
- 230000007794 irritation Effects 0.000 description 5
- 239000004310 lactic acid Substances 0.000 description 5
- 235000014655 lactic acid Nutrition 0.000 description 5
- 239000004014 plasticizer Substances 0.000 description 5
- 102000005962 receptors Human genes 0.000 description 5
- 108020003175 receptors Proteins 0.000 description 5
- 239000011975 tartaric acid Substances 0.000 description 5
- 235000002906 tartaric acid Nutrition 0.000 description 5
- 238000012360 testing method Methods 0.000 description 5
- GLZPCOQZEFWAFX-UHFFFAOYSA-N Geraniol Chemical compound CC(C)=CCCC(C)=CCO GLZPCOQZEFWAFX-UHFFFAOYSA-N 0.000 description 4
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 4
- LCTONWCANYUPML-UHFFFAOYSA-N Pyruvic acid Chemical compound CC(=O)C(O)=O LCTONWCANYUPML-UHFFFAOYSA-N 0.000 description 4
- 239000003655 absorption accelerator Substances 0.000 description 4
- 239000002585 base Substances 0.000 description 4
- 235000015165 citric acid Nutrition 0.000 description 4
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 4
- 229940093915 gynecological organic acid Drugs 0.000 description 4
- FUZZWVXGSFPDMH-UHFFFAOYSA-N hexanoic acid Chemical compound CCCCCC(O)=O FUZZWVXGSFPDMH-UHFFFAOYSA-N 0.000 description 4
- 229920001600 hydrophobic polymer Polymers 0.000 description 4
- KQNPFQTWMSNSAP-UHFFFAOYSA-N isobutyric acid Chemical compound CC(C)C(O)=O KQNPFQTWMSNSAP-UHFFFAOYSA-N 0.000 description 4
- 239000012948 isocyanate Substances 0.000 description 4
- OSWPMRLSEDHDFF-UHFFFAOYSA-N methyl salicylate Chemical compound COC(=O)C1=CC=CC=C1O OSWPMRLSEDHDFF-UHFFFAOYSA-N 0.000 description 4
- WWZKQHOCKIZLMA-UHFFFAOYSA-N octanoic acid Chemical compound CCCCCCCC(O)=O WWZKQHOCKIZLMA-UHFFFAOYSA-N 0.000 description 4
- 235000005985 organic acids Nutrition 0.000 description 4
- 229920000139 polyethylene terephthalate Polymers 0.000 description 4
- 239000005020 polyethylene terephthalate Substances 0.000 description 4
- 229920000642 polymer Polymers 0.000 description 4
- 230000003637 steroidlike Effects 0.000 description 4
- BJEPYKJPYRNKOW-REOHCLBHSA-N (S)-malic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O BJEPYKJPYRNKOW-REOHCLBHSA-N 0.000 description 3
- LVYLCBNXHHHPSB-UHFFFAOYSA-N 2-hydroxyethyl salicylate Chemical compound OCCOC(=O)C1=CC=CC=C1O LVYLCBNXHHHPSB-UHFFFAOYSA-N 0.000 description 3
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerol Natural products OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 3
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 3
- 239000002202 Polyethylene glycol Substances 0.000 description 3
- 235000011054 acetic acid Nutrition 0.000 description 3
- 230000002378 acidificating effect Effects 0.000 description 3
- 239000000654 additive Substances 0.000 description 3
- 239000000853 adhesive Substances 0.000 description 3
- BJEPYKJPYRNKOW-UHFFFAOYSA-N alpha-hydroxysuccinic acid Natural products OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 3
- 239000003963 antioxidant agent Substances 0.000 description 3
- 235000006708 antioxidants Nutrition 0.000 description 3
- 230000015572 biosynthetic process Effects 0.000 description 3
- 230000008859 change Effects 0.000 description 3
- 239000013078 crystal Substances 0.000 description 3
- MTHSVFCYNBDYFN-UHFFFAOYSA-N diethylene glycol Chemical compound OCCOCCO MTHSVFCYNBDYFN-UHFFFAOYSA-N 0.000 description 3
- 230000000694 effects Effects 0.000 description 3
- 239000000945 filler Substances 0.000 description 3
- 230000004907 flux Effects 0.000 description 3
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 description 3
- 239000007788 liquid Substances 0.000 description 3
- 239000001630 malic acid Substances 0.000 description 3
- 235000011090 malic acid Nutrition 0.000 description 3
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 3
- 239000003921 oil Substances 0.000 description 3
- 235000019198 oils Nutrition 0.000 description 3
- 230000035699 permeability Effects 0.000 description 3
- 230000000704 physical effect Effects 0.000 description 3
- 229920001223 polyethylene glycol Polymers 0.000 description 3
- 239000003755 preservative agent Substances 0.000 description 3
- 239000010734 process oil Substances 0.000 description 3
- PRAKJMSDJKAYCZ-UHFFFAOYSA-N squalane Chemical compound CC(C)CCCC(C)CCCC(C)CCCCC(C)CCCC(C)CCCC(C)C PRAKJMSDJKAYCZ-UHFFFAOYSA-N 0.000 description 3
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 3
- XMGQYMWWDOXHJM-JTQLQIEISA-N (+)-α-limonene Chemical compound CC(=C)[C@@H]1CCC(C)=CC1 XMGQYMWWDOXHJM-JTQLQIEISA-N 0.000 description 2
- NOOLISFMXDJSKH-KXUCPTDWSA-N (-)-Menthol Chemical compound CC(C)[C@@H]1CC[C@@H](C)C[C@H]1O NOOLISFMXDJSKH-KXUCPTDWSA-N 0.000 description 2
- AXTGDCSMTYGJND-UHFFFAOYSA-N 1-dodecylazepan-2-one Chemical compound CCCCCCCCCCCCN1CCCCCC1=O AXTGDCSMTYGJND-UHFFFAOYSA-N 0.000 description 2
- HBKBEZURJSNABK-MWJPAGEPSA-N 2,3-dihydroxypropyl (1r,4ar,4br,10ar)-1,4a-dimethyl-7-propan-2-yl-2,3,4,4b,5,6,10,10a-octahydrophenanthrene-1-carboxylate Chemical compound C([C@@H]12)CC(C(C)C)=CC1=CC[C@@H]1[C@]2(C)CCC[C@@]1(C)C(=O)OCC(O)CO HBKBEZURJSNABK-MWJPAGEPSA-N 0.000 description 2
- FEDJGPQLLNQAIY-UHFFFAOYSA-N 2-[(6-oxo-1h-pyridazin-3-yl)oxy]acetic acid Chemical compound OC(=O)COC=1C=CC(=O)NN=1 FEDJGPQLLNQAIY-UHFFFAOYSA-N 0.000 description 2
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 2
- 239000005635 Caprylic acid (CAS 124-07-2) Substances 0.000 description 2
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 2
- 239000013032 Hydrocarbon resin Substances 0.000 description 2
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 2
- 239000004698 Polyethylene Substances 0.000 description 2
- 229920001328 Polyvinylidene chloride Polymers 0.000 description 2
- 239000004820 Pressure-sensitive adhesive Substances 0.000 description 2
- OFOBLEOULBTSOW-UHFFFAOYSA-N Propanedioic acid Natural products OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 2
- 206010040880 Skin irritation Diseases 0.000 description 2
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 2
- XLOMVQKBTHCTTD-UHFFFAOYSA-N Zinc monoxide Chemical compound [Zn]=O XLOMVQKBTHCTTD-UHFFFAOYSA-N 0.000 description 2
- 229940124532 absorption promoter Drugs 0.000 description 2
- NIXOWILDQLNWCW-UHFFFAOYSA-N acrylic acid group Chemical group C(C=C)(=O)O NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 2
- 150000001298 alcohols Chemical class 0.000 description 2
- 125000002723 alicyclic group Chemical group 0.000 description 2
- 125000001931 aliphatic group Chemical group 0.000 description 2
- 229920006271 aliphatic hydrocarbon resin Polymers 0.000 description 2
- 150000008064 anhydrides Chemical class 0.000 description 2
- TZCXTZWJZNENPQ-UHFFFAOYSA-L barium sulfate Chemical compound [Ba+2].[O-]S([O-])(=O)=O TZCXTZWJZNENPQ-UHFFFAOYSA-L 0.000 description 2
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 2
- OSGAYBCDTDRGGQ-UHFFFAOYSA-L calcium sulfate Chemical compound [Ca+2].[O-]S([O-])(=O)=O OSGAYBCDTDRGGQ-UHFFFAOYSA-L 0.000 description 2
- 150000001735 carboxylic acids Chemical class 0.000 description 2
- 239000004359 castor oil Substances 0.000 description 2
- 235000019438 castor oil Nutrition 0.000 description 2
- 150000001875 compounds Chemical class 0.000 description 2
- 230000001186 cumulative effect Effects 0.000 description 2
- GHVNFZFCNZKVNT-UHFFFAOYSA-N decanoic acid Chemical compound CCCCCCCCCC(O)=O GHVNFZFCNZKVNT-UHFFFAOYSA-N 0.000 description 2
- 210000004207 dermis Anatomy 0.000 description 2
- DOIRQSBPFJWKBE-UHFFFAOYSA-N dibutyl phthalate Chemical compound CCCCOC(=O)C1=CC=CC=C1C(=O)OCCCC DOIRQSBPFJWKBE-UHFFFAOYSA-N 0.000 description 2
- 229960005316 diltiazem hydrochloride Drugs 0.000 description 2
- LQZZUXJYWNFBMV-UHFFFAOYSA-N dodecan-1-ol Chemical compound CCCCCCCCCCCCO LQZZUXJYWNFBMV-UHFFFAOYSA-N 0.000 description 2
- POULHZVOKOAJMA-UHFFFAOYSA-N dodecanoic acid Chemical compound CCCCCCCCCCCC(O)=O POULHZVOKOAJMA-UHFFFAOYSA-N 0.000 description 2
- 239000003623 enhancer Substances 0.000 description 2
- 230000002708 enhancing effect Effects 0.000 description 2
- 150000002148 esters Chemical class 0.000 description 2
- 150000002170 ethers Chemical class 0.000 description 2
- RRAFCDWBNXTKKO-UHFFFAOYSA-N eugenol Chemical compound COC1=CC(CC=C)=CC=C1O RRAFCDWBNXTKKO-UHFFFAOYSA-N 0.000 description 2
- 150000004665 fatty acids Chemical class 0.000 description 2
- 235000011187 glycerol Nutrition 0.000 description 2
- ZEMPKEQAKRGZGQ-XOQCFJPHSA-N glycerol triricinoleate Natural products CCCCCC[C@@H](O)CC=CCCCCCCCC(=O)OC[C@@H](COC(=O)CCCCCCCC=CC[C@@H](O)CCCCCC)OC(=O)CCCCCCCC=CC[C@H](O)CCCCCC ZEMPKEQAKRGZGQ-XOQCFJPHSA-N 0.000 description 2
- 229960002389 glycol salicylate Drugs 0.000 description 2
- BXWNKGSJHAJOGX-UHFFFAOYSA-N hexadecan-1-ol Chemical compound CCCCCCCCCCCCCCCCO BXWNKGSJHAJOGX-UHFFFAOYSA-N 0.000 description 2
- IPCSVZSSVZVIGE-UHFFFAOYSA-N hexadecanoic acid Chemical compound CCCCCCCCCCCCCCCC(O)=O IPCSVZSSVZVIGE-UHFFFAOYSA-N 0.000 description 2
- 229920006270 hydrocarbon resin Polymers 0.000 description 2
- 150000002500 ions Chemical class 0.000 description 2
- 150000002513 isocyanates Chemical class 0.000 description 2
- 229920003049 isoprene rubber Polymers 0.000 description 2
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 2
- 239000011976 maleic acid Substances 0.000 description 2
- UQDUPQYQJKYHQI-UHFFFAOYSA-N methyl laurate Chemical compound CCCCCCCCCCCC(=O)OC UQDUPQYQJKYHQI-UHFFFAOYSA-N 0.000 description 2
- 229960001047 methyl salicylate Drugs 0.000 description 2
- 229960002446 octanoic acid Drugs 0.000 description 2
- 210000000056 organ Anatomy 0.000 description 2
- 235000006408 oxalic acid Nutrition 0.000 description 2
- XNGIFLGASWRNHJ-UHFFFAOYSA-N phthalic acid Chemical compound OC(=O)C1=CC=CC=C1C(O)=O XNGIFLGASWRNHJ-UHFFFAOYSA-N 0.000 description 2
- 229920000058 polyacrylate Polymers 0.000 description 2
- 229920001083 polybutene Polymers 0.000 description 2
- 229920000728 polyester Polymers 0.000 description 2
- 229920000573 polyethylene Polymers 0.000 description 2
- 229920000136 polysorbate Polymers 0.000 description 2
- 239000005033 polyvinylidene chloride Substances 0.000 description 2
- 230000002335 preservative effect Effects 0.000 description 2
- 235000019260 propionic acid Nutrition 0.000 description 2
- 229940107700 pyruvic acid Drugs 0.000 description 2
- IUVKMZGDUIUOCP-BTNSXGMBSA-N quinbolone Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)CC[C@@]21C)C1=CCCC1 IUVKMZGDUIUOCP-BTNSXGMBSA-N 0.000 description 2
- 229930195734 saturated hydrocarbon Natural products 0.000 description 2
- 230000036556 skin irritation Effects 0.000 description 2
- 231100000475 skin irritation Toxicity 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- 239000000021 stimulant Substances 0.000 description 2
- 210000000434 stratum corneum Anatomy 0.000 description 2
- 229920003048 styrene butadiene rubber Polymers 0.000 description 2
- 229920000468 styrene butadiene styrene block copolymer Polymers 0.000 description 2
- 150000003505 terpenes Chemical class 0.000 description 2
- 235000007586 terpenes Nutrition 0.000 description 2
- HLZKNKRTKFSKGZ-UHFFFAOYSA-N tetradecan-1-ol Chemical compound CCCCCCCCCCCCCCO HLZKNKRTKFSKGZ-UHFFFAOYSA-N 0.000 description 2
- MGSRCZKZVOBKFT-UHFFFAOYSA-N thymol Chemical compound CC(C)C1=CC=C(C)C=C1O MGSRCZKZVOBKFT-UHFFFAOYSA-N 0.000 description 2
- URAYPUMNDPQOKB-UHFFFAOYSA-N triacetin Chemical compound CC(=O)OCC(OC(C)=O)COC(C)=O URAYPUMNDPQOKB-UHFFFAOYSA-N 0.000 description 2
- 239000006097 ultraviolet radiation absorber Substances 0.000 description 2
- DTGKSKDOIYIVQL-WEDXCCLWSA-N (+)-borneol Chemical compound C1C[C@@]2(C)[C@@H](O)C[C@@H]1C2(C)C DTGKSKDOIYIVQL-WEDXCCLWSA-N 0.000 description 1
- CSTRPYAGFNTOEQ-MGMRMFRLSA-N (2r)-2-[(1s)-1,2-dihydroxyethyl]-3,4-dihydroxy-2h-furan-5-one;octadecanoic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O.CCCCCCCCCCCCCCCCCC(O)=O CSTRPYAGFNTOEQ-MGMRMFRLSA-N 0.000 description 1
- YYGNTYWPHWGJRM-UHFFFAOYSA-N (6E,10E,14E,18E)-2,6,10,15,19,23-hexamethyltetracosa-2,6,10,14,18,22-hexaene Chemical compound CC(C)=CCCC(C)=CCCC(C)=CCCC=C(C)CCC=C(C)CCC=C(C)C YYGNTYWPHWGJRM-UHFFFAOYSA-N 0.000 description 1
- ALSTYHKOOCGGFT-KTKRTIGZSA-N (9Z)-octadecen-1-ol Chemical compound CCCCCCCC\C=C/CCCCCCCCO ALSTYHKOOCGGFT-KTKRTIGZSA-N 0.000 description 1
- OYHQOLUKZRVURQ-NTGFUMLPSA-N (9Z,12Z)-9,10,12,13-tetratritiooctadeca-9,12-dienoic acid Chemical compound C(CCCCCCC\C(=C(/C\C(=C(/CCCCC)\[3H])\[3H])\[3H])\[3H])(=O)O OYHQOLUKZRVURQ-NTGFUMLPSA-N 0.000 description 1
- WRIDQFICGBMAFQ-UHFFFAOYSA-N (E)-8-Octadecenoic acid Natural products CCCCCCCCCC=CCCCCCCC(O)=O WRIDQFICGBMAFQ-UHFFFAOYSA-N 0.000 description 1
- DSSYKIVIOFKYAU-XCBNKYQSSA-N (R)-camphor Chemical compound C1C[C@@]2(C)C(=O)C[C@@H]1C2(C)C DSSYKIVIOFKYAU-XCBNKYQSSA-N 0.000 description 1
- WLRMANUAADYWEA-NWASOUNVSA-N (S)-timolol maleate Chemical compound OC(=O)\C=C/C(O)=O.CC(C)(C)NC[C@H](O)COC1=NSN=C1N1CCOCC1 WLRMANUAADYWEA-NWASOUNVSA-N 0.000 description 1
- PMGQWSIVQFOFOQ-BDUVBVHRSA-N (e)-but-2-enedioic acid;(2r)-2-[2-[1-(4-chlorophenyl)-1-phenylethoxy]ethyl]-1-methylpyrrolidine Chemical compound OC(=O)\C=C\C(O)=O.CN1CCC[C@@H]1CCOC(C)(C=1C=CC(Cl)=CC=1)C1=CC=CC=C1 PMGQWSIVQFOFOQ-BDUVBVHRSA-N 0.000 description 1
- RZPZLFIUFMNCLY-WLHGVMLRSA-N (e)-but-2-enedioic acid;1-(propan-2-ylamino)-3-[4-(2-propan-2-yloxyethoxymethyl)phenoxy]propan-2-ol Chemical compound OC(=O)\C=C\C(O)=O.CC(C)NCC(O)COC1=CC=C(COCCOC(C)C)C=C1 RZPZLFIUFMNCLY-WLHGVMLRSA-N 0.000 description 1
- WBYWAXJHAXSJNI-VOTSOKGWSA-M .beta-Phenylacrylic acid Natural products [O-]C(=O)\C=C\C1=CC=CC=C1 WBYWAXJHAXSJNI-VOTSOKGWSA-M 0.000 description 1
- VNJHUUNVDMYCRH-UHFFFAOYSA-N 1,1-diphenyl-3-piperidin-1-ylpropan-1-ol;methanesulfonic acid Chemical compound CS(O)(=O)=O.C=1C=CC=CC=1C(C=1C=CC=CC=1)(O)CCN1CCCCC1 VNJHUUNVDMYCRH-UHFFFAOYSA-N 0.000 description 1
- SQUNAWUMZGQQJD-UHFFFAOYSA-N 1-(4-ethylphenyl)-2-methyl-3-(piperidin-1-yl)propan-1-one Chemical compound C1=CC(CC)=CC=C1C(=O)C(C)CN1CCCCC1 SQUNAWUMZGQQJD-UHFFFAOYSA-N 0.000 description 1
- RZRNAYUHWVFMIP-KTKRTIGZSA-N 1-oleoylglycerol Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OCC(O)CO RZRNAYUHWVFMIP-KTKRTIGZSA-N 0.000 description 1
- SPSPIUSUWPLVKD-UHFFFAOYSA-N 2,3-dibutyl-6-methylphenol Chemical compound CCCCC1=CC=C(C)C(O)=C1CCCC SPSPIUSUWPLVKD-UHFFFAOYSA-N 0.000 description 1
- XFOQWQKDSMIPHT-UHFFFAOYSA-N 2,3-dichloro-6-(trifluoromethyl)pyridine Chemical compound FC(F)(F)C1=CC=C(Cl)C(Cl)=N1 XFOQWQKDSMIPHT-UHFFFAOYSA-N 0.000 description 1
- SMZOUWXMTYCWNB-UHFFFAOYSA-N 2-(2-methoxy-5-methylphenyl)ethanamine Chemical compound COC1=CC=C(C)C=C1CCN SMZOUWXMTYCWNB-UHFFFAOYSA-N 0.000 description 1
- FLPJVCMIKUWSDR-UHFFFAOYSA-N 2-(4-formylphenoxy)acetamide Chemical compound NC(=O)COC1=CC=C(C=O)C=C1 FLPJVCMIKUWSDR-UHFFFAOYSA-N 0.000 description 1
- GOXQRTZXKQZDDN-UHFFFAOYSA-N 2-Ethylhexyl acrylate Chemical compound CCCCC(CC)COC(=O)C=C GOXQRTZXKQZDDN-UHFFFAOYSA-N 0.000 description 1
- VRPJIFMKZZEXLR-HOSYLAQJSA-N 2-[(2-methylpropan-2-yl)oxycarbonylamino]acetic acid Chemical compound CC(C)(C)OC(=O)NC[13C](O)=O VRPJIFMKZZEXLR-HOSYLAQJSA-N 0.000 description 1
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 1
- SPCKHVPPRJWQRZ-UHFFFAOYSA-N 2-benzhydryloxy-n,n-dimethylethanamine;2-hydroxypropane-1,2,3-tricarboxylic acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O.C=1C=CC=CC=1C(OCCN(C)C)C1=CC=CC=C1 SPCKHVPPRJWQRZ-UHFFFAOYSA-N 0.000 description 1
- RFVNOJDQRGSOEL-UHFFFAOYSA-N 2-hydroxyethyl octadecanoate Chemical compound CCCCCCCCCCCCCCCCCC(=O)OCCO RFVNOJDQRGSOEL-UHFFFAOYSA-N 0.000 description 1
- HFCUBKYHMMPGBY-UHFFFAOYSA-N 2-methoxyethyl prop-2-enoate Chemical compound COCCOC(=O)C=C HFCUBKYHMMPGBY-UHFFFAOYSA-N 0.000 description 1
- QTWJRLJHJPIABL-UHFFFAOYSA-N 2-methylphenol;3-methylphenol;4-methylphenol Chemical compound CC1=CC=C(O)C=C1.CC1=CC=CC(O)=C1.CC1=CC=CC=C1O QTWJRLJHJPIABL-UHFFFAOYSA-N 0.000 description 1
- BGRXBNZMPMGLQI-UHFFFAOYSA-N 2-octyldodecyl tetradecanoate Chemical compound CCCCCCCCCCCCCC(=O)OCC(CCCCCCCC)CCCCCCCCCC BGRXBNZMPMGLQI-UHFFFAOYSA-N 0.000 description 1
- LQJBNNIYVWPHFW-UHFFFAOYSA-N 20:1omega9c fatty acid Natural products CCCCCCCCCCC=CCCCCCCCC(O)=O LQJBNNIYVWPHFW-UHFFFAOYSA-N 0.000 description 1
- OHXPGWPVLFPUSM-KLRNGDHRSA-N 3,7,12-trioxo-5beta-cholanic acid Chemical compound C1CC(=O)C[C@H]2CC(=O)[C@H]3[C@@H]4CC[C@H]([C@@H](CCC(O)=O)C)[C@@]4(C)C(=O)C[C@@H]3[C@]21C OHXPGWPVLFPUSM-KLRNGDHRSA-N 0.000 description 1
- AKUVRZKNLXYTJX-UHFFFAOYSA-N 3-benzylazetidine Chemical compound C=1C=CC=CC=1CC1CNC1 AKUVRZKNLXYTJX-UHFFFAOYSA-N 0.000 description 1
- MEAPRSDUXBHXGD-UHFFFAOYSA-N 3-chloro-n-(4-propan-2-ylphenyl)propanamide Chemical compound CC(C)C1=CC=C(NC(=O)CCCl)C=C1 MEAPRSDUXBHXGD-UHFFFAOYSA-N 0.000 description 1
- ALYNCZNDIQEVRV-UHFFFAOYSA-N 4-aminobenzoic acid Chemical class NC1=CC=C(C(O)=O)C=C1 ALYNCZNDIQEVRV-UHFFFAOYSA-N 0.000 description 1
- HIQIXEFWDLTDED-UHFFFAOYSA-N 4-hydroxy-1-piperidin-4-ylpyrrolidin-2-one Chemical compound O=C1CC(O)CN1C1CCNCC1 HIQIXEFWDLTDED-UHFFFAOYSA-N 0.000 description 1
- BSYNRYMUTXBXSQ-FOQJRBATSA-N 59096-14-9 Chemical compound CC(=O)OC1=CC=CC=C1[14C](O)=O BSYNRYMUTXBXSQ-FOQJRBATSA-N 0.000 description 1
- XZIIFPSPUDAGJM-UHFFFAOYSA-N 6-chloro-2-n,2-n-diethylpyrimidine-2,4-diamine Chemical compound CCN(CC)C1=NC(N)=CC(Cl)=N1 XZIIFPSPUDAGJM-UHFFFAOYSA-N 0.000 description 1
- VCCNKWWXYVWTLT-CYZBKYQRSA-N 7-[(2s,3r,4s,5s,6r)-4,5-dihydroxy-6-(hydroxymethyl)-3-[(2s,3r,4r,5r,6s)-3,4,5-trihydroxy-6-methyloxan-2-yl]oxyoxan-2-yl]oxy-5-hydroxy-2-(3-hydroxy-4-methoxyphenyl)chromen-4-one Chemical compound C1=C(O)C(OC)=CC=C1C(OC1=C2)=CC(=O)C1=C(O)C=C2O[C@H]1[C@H](O[C@H]2[C@@H]([C@H](O)[C@@H](O)[C@H](C)O2)O)[C@@H](O)[C@H](O)[C@@H](CO)O1 VCCNKWWXYVWTLT-CYZBKYQRSA-N 0.000 description 1
- QSBYPNXLFMSGKH-UHFFFAOYSA-N 9-Heptadecensaeure Natural products CCCCCCCC=CCCCCCCCC(O)=O QSBYPNXLFMSGKH-UHFFFAOYSA-N 0.000 description 1
- MKBLHFILKIKSQM-UHFFFAOYSA-N 9-methyl-3-[(2-methyl-1h-imidazol-3-ium-3-yl)methyl]-2,3-dihydro-1h-carbazol-4-one;chloride Chemical compound Cl.CC1=NC=CN1CC1C(=O)C(C=2C(=CC=CC=2)N2C)=C2CC1 MKBLHFILKIKSQM-UHFFFAOYSA-N 0.000 description 1
- LSNNMFCWUKXFEE-UHFFFAOYSA-M Bisulfite Chemical compound OS([O-])=O LSNNMFCWUKXFEE-UHFFFAOYSA-M 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- 239000005632 Capric acid (CAS 334-48-5) Substances 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical group [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- NPBVQXIMTZKSBA-UHFFFAOYSA-N Chavibetol Natural products COC1=CC=C(CC=C)C=C1O NPBVQXIMTZKSBA-UHFFFAOYSA-N 0.000 description 1
- WBYWAXJHAXSJNI-SREVYHEPSA-N Cinnamic acid Chemical compound OC(=O)\C=C/C1=CC=CC=C1 WBYWAXJHAXSJNI-SREVYHEPSA-N 0.000 description 1
- IROWCYIEJAOFOW-UHFFFAOYSA-N DL-Isoprenaline hydrochloride Chemical compound Cl.CC(C)NCC(O)C1=CC=C(O)C(O)=C1 IROWCYIEJAOFOW-UHFFFAOYSA-N 0.000 description 1
- NOOLISFMXDJSKH-UHFFFAOYSA-N DL-menthol Natural products CC(C)C1CCC(C)CC1O NOOLISFMXDJSKH-UHFFFAOYSA-N 0.000 description 1
- MQIUGAXCHLFZKX-UHFFFAOYSA-N Di-n-octyl phthalate Natural products CCCCCCCCOC(=O)C1=CC=CC=C1C(=O)OCCCCCCCC MQIUGAXCHLFZKX-UHFFFAOYSA-N 0.000 description 1
- AVZIYZHXZAYGJS-UHFFFAOYSA-N Difenidol hydrochloride Chemical compound Cl.C=1C=CC=CC=1C(C=1C=CC=CC=1)(O)CCCN1CCCCC1 AVZIYZHXZAYGJS-UHFFFAOYSA-N 0.000 description 1
- CTENFNNZBMHDDG-UHFFFAOYSA-N Dopamine hydrochloride Chemical compound Cl.NCCC1=CC=C(O)C(O)=C1 CTENFNNZBMHDDG-UHFFFAOYSA-N 0.000 description 1
- 239000005770 Eugenol Substances 0.000 description 1
- RXKMOPXNWTYEHI-RDRKJGRWSA-N Flunarizine hydrochloride Chemical compound Cl.Cl.C1=CC(F)=CC=C1C(C=1C=CC(F)=CC=1)N1CCN(C\C=C\C=2C=CC=CC=2)CC1 RXKMOPXNWTYEHI-RDRKJGRWSA-N 0.000 description 1
- ZIIJJOPLRSCQNX-UHFFFAOYSA-N Flurazepam hydrochloride Chemical compound Cl.Cl.N=1CC(=O)N(CCN(CC)CC)C2=CC=C(Cl)C=C2C=1C1=CC=CC=C1F ZIIJJOPLRSCQNX-UHFFFAOYSA-N 0.000 description 1
- 239000005792 Geraniol Substances 0.000 description 1
- GLZPCOQZEFWAFX-YFHOEESVSA-N Geraniol Natural products CC(C)=CCC\C(C)=C/CO GLZPCOQZEFWAFX-YFHOEESVSA-N 0.000 description 1
- 239000007995 HEPES buffer Substances 0.000 description 1
- 244000043261 Hevea brasiliensis Species 0.000 description 1
- DTGKSKDOIYIVQL-MRTMQBJTSA-N Isoborneol Natural products C1C[C@@]2(C)[C@H](O)C[C@@H]1C2(C)C DTGKSKDOIYIVQL-MRTMQBJTSA-N 0.000 description 1
- BJIOGJUNALELMI-ONEGZZNKSA-N Isoeugenol Natural products COC1=CC(\C=C\C)=CC=C1O BJIOGJUNALELMI-ONEGZZNKSA-N 0.000 description 1
- 239000005639 Lauric acid Substances 0.000 description 1
- CERQOIWHTDAKMF-UHFFFAOYSA-M Methacrylate Chemical compound CC(=C)C([O-])=O CERQOIWHTDAKMF-UHFFFAOYSA-M 0.000 description 1
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 1
- 241000699670 Mus sp. Species 0.000 description 1
- FXHOOIRPVKKKFG-UHFFFAOYSA-N N,N-Dimethylacetamide Chemical compound CN(C)C(C)=O FXHOOIRPVKKKFG-UHFFFAOYSA-N 0.000 description 1
- GLZPCOQZEFWAFX-JXMROGBWSA-N Nerol Natural products CC(C)=CCC\C(C)=C\CO GLZPCOQZEFWAFX-JXMROGBWSA-N 0.000 description 1
- 206010030113 Oedema Diseases 0.000 description 1
- 239000005642 Oleic acid Substances 0.000 description 1
- ZQPPMHVWECSIRJ-UHFFFAOYSA-N Oleic acid Natural products CCCCCCCCC=CCCCCCCCC(O)=O ZQPPMHVWECSIRJ-UHFFFAOYSA-N 0.000 description 1
- BPQQTUXANYXVAA-UHFFFAOYSA-N Orthosilicate Chemical compound [O-][Si]([O-])([O-])[O-] BPQQTUXANYXVAA-UHFFFAOYSA-N 0.000 description 1
- 235000021314 Palmitic acid Nutrition 0.000 description 1
- 235000019483 Peanut oil Nutrition 0.000 description 1
- OOSOWXQJLLTIAF-UHFFFAOYSA-N Perisoxal citrate Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O.C1=C(C=2C=CC=CC=2)ON=C1C(O)CN1CCCCC1.C1=C(C=2C=CC=CC=2)ON=C1C(O)CN1CCCCC1 OOSOWXQJLLTIAF-UHFFFAOYSA-N 0.000 description 1
- 229920001213 Polysorbate 20 Polymers 0.000 description 1
- HCBIBCJNVBAKAB-UHFFFAOYSA-N Procaine hydrochloride Chemical compound Cl.CCN(CC)CCOC(=O)C1=CC=C(N)C=C1 HCBIBCJNVBAKAB-UHFFFAOYSA-N 0.000 description 1
- UVMRYBDEERADNV-UHFFFAOYSA-N Pseudoeugenol Natural products COC1=CC(C(C)=C)=CC=C1O UVMRYBDEERADNV-UHFFFAOYSA-N 0.000 description 1
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- 239000002174 Styrene-butadiene Substances 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- BHEOSNUKNHRBNM-UHFFFAOYSA-N Tetramethylsqualene Natural products CC(=C)C(C)CCC(=C)C(C)CCC(C)=CCCC=C(C)CCC(C)C(=C)CCC(C)C(C)=C BHEOSNUKNHRBNM-UHFFFAOYSA-N 0.000 description 1
- 239000005844 Thymol Substances 0.000 description 1
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 description 1
- DOOTYTYQINUNNV-UHFFFAOYSA-N Triethyl citrate Chemical compound CCOC(=O)CC(O)(C(=O)OCC)CC(=O)OCC DOOTYTYQINUNNV-UHFFFAOYSA-N 0.000 description 1
- RSLNRVYIRDVHLY-UHFFFAOYSA-N Tulobuterol hydrochloride Chemical compound [Cl-].CC(C)(C)[NH2+]CC(O)C1=CC=CC=C1Cl RSLNRVYIRDVHLY-UHFFFAOYSA-N 0.000 description 1
- XTXRWKRVRITETP-UHFFFAOYSA-N Vinyl acetate Chemical compound CC(=O)OC=C XTXRWKRVRITETP-UHFFFAOYSA-N 0.000 description 1
- 206010047700 Vomiting Diseases 0.000 description 1
- KGUHOFWIXKIURA-VQXBOQCVSA-N [(2r,3s,4s,5r,6r)-6-[(2s,3s,4s,5r)-3,4-dihydroxy-2,5-bis(hydroxymethyl)oxolan-2-yl]oxy-3,4,5-trihydroxyoxan-2-yl]methyl dodecanoate Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](COC(=O)CCCCCCCCCCC)O[C@@H]1O[C@@]1(CO)[C@@H](O)[C@H](O)[C@@H](CO)O1 KGUHOFWIXKIURA-VQXBOQCVSA-N 0.000 description 1
- DOQPXTMNIUCOSY-UHFFFAOYSA-N [4-cyano-4-(3,4-dimethoxyphenyl)-5-methylhexyl]-[2-(3,4-dimethoxyphenyl)ethyl]-methylazanium;chloride Chemical compound [H+].[Cl-].C1=C(OC)C(OC)=CC=C1CCN(C)CCCC(C#N)(C(C)C)C1=CC=C(OC)C(OC)=C1 DOQPXTMNIUCOSY-UHFFFAOYSA-N 0.000 description 1
- YKTSYUJCYHOUJP-UHFFFAOYSA-N [O--].[Al+3].[Al+3].[O-][Si]([O-])([O-])[O-] Chemical compound [O--].[Al+3].[Al+3].[O-][Si]([O-])([O-])[O-] YKTSYUJCYHOUJP-UHFFFAOYSA-N 0.000 description 1
- 239000006096 absorbing agent Substances 0.000 description 1
- 150000001242 acetic acid derivatives Chemical class 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 230000032683 aging Effects 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 229920000180 alkyd Polymers 0.000 description 1
- 150000005215 alkyl ethers Chemical class 0.000 description 1
- DTOSIQBPPRVQHS-PDBXOOCHSA-N alpha-linolenic acid Chemical compound CC\C=C/C\C=C/C\C=C/CCCCCCCC(O)=O DTOSIQBPPRVQHS-PDBXOOCHSA-N 0.000 description 1
- 235000020661 alpha-linolenic acid Nutrition 0.000 description 1
- WUOACPNHFRMFPN-UHFFFAOYSA-N alpha-terpineol Chemical compound CC1=CCC(C(C)(C)O)CC1 WUOACPNHFRMFPN-UHFFFAOYSA-N 0.000 description 1
- 229960000852 alprenolol hydrochloride Drugs 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- WOLHOYHSEKDWQH-UHFFFAOYSA-N amantadine hydrochloride Chemical compound [Cl-].C1C(C2)CC3CC2CC1([NH3+])C3 WOLHOYHSEKDWQH-UHFFFAOYSA-N 0.000 description 1
- 229920003180 amino resin Polymers 0.000 description 1
- 229940035676 analgesics Drugs 0.000 description 1
- 239000000730 antalgic agent Substances 0.000 description 1
- RWZYAGGXGHYGMB-UHFFFAOYSA-N anthranilic acid Chemical class NC1=CC=CC=C1C(O)=O RWZYAGGXGHYGMB-UHFFFAOYSA-N 0.000 description 1
- 230000003474 anti-emetic effect Effects 0.000 description 1
- 230000001754 anti-pyretic effect Effects 0.000 description 1
- 239000000043 antiallergic agent Substances 0.000 description 1
- 239000002111 antiemetic agent Substances 0.000 description 1
- 239000000739 antihistaminic agent Substances 0.000 description 1
- 229940125715 antihistaminic agent Drugs 0.000 description 1
- 229940125684 antimigraine agent Drugs 0.000 description 1
- 239000002282 antimigraine agent Substances 0.000 description 1
- 230000003078 antioxidant effect Effects 0.000 description 1
- 239000000939 antiparkinson agent Substances 0.000 description 1
- 239000003908 antipruritic agent Substances 0.000 description 1
- 239000002221 antipyretic Substances 0.000 description 1
- 239000003420 antiserotonin agent Substances 0.000 description 1
- 230000004596 appetite loss Effects 0.000 description 1
- 230000006793 arrhythmia Effects 0.000 description 1
- 206010003119 arrhythmia Diseases 0.000 description 1
- 125000003118 aryl group Chemical group 0.000 description 1
- 235000010323 ascorbic acid Nutrition 0.000 description 1
- 229960005070 ascorbic acid Drugs 0.000 description 1
- 239000011668 ascorbic acid Substances 0.000 description 1
- 210000000467 autonomic pathway Anatomy 0.000 description 1
- 229960004335 azelastine hydrochloride Drugs 0.000 description 1
- YEJAJYAHJQIWNU-UHFFFAOYSA-N azelastine hydrochloride Chemical compound Cl.C1CN(C)CCCC1N1C(=O)C2=CC=CC=C2C(CC=2C=CC(Cl)=CC=2)=N1 YEJAJYAHJQIWNU-UHFFFAOYSA-N 0.000 description 1
- 230000004888 barrier function Effects 0.000 description 1
- 229960004916 benidipine Drugs 0.000 description 1
- QZVNQOLPLYWLHQ-ZEQKJWHPSA-N benidipine Chemical compound C1([C@H]2C(=C(C)NC(C)=C2C(=O)OC)C(=O)O[C@H]2CN(CC=3C=CC=CC=3)CCC2)=CC=CC([N+]([O-])=O)=C1 QZVNQOLPLYWLHQ-ZEQKJWHPSA-N 0.000 description 1
- 229960004365 benzoic acid Drugs 0.000 description 1
- 229960001510 betahistine mesylate Drugs 0.000 description 1
- SNHRLVCMMWUAJD-SUYDQAKGSA-N betamethasone valerate Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@H](C)[C@@](C(=O)CO)(OC(=O)CCCC)[C@@]1(C)C[C@@H]2O SNHRLVCMMWUAJD-SUYDQAKGSA-N 0.000 description 1
- 229960004311 betamethasone valerate Drugs 0.000 description 1
- BJQHLKABXJIVAM-UHFFFAOYSA-N bis(2-ethylhexyl) phthalate Chemical compound CCCCC(CC)COC(=O)C1=CC=CC=C1C(=O)OCC(CC)CCCC BJQHLKABXJIVAM-UHFFFAOYSA-N 0.000 description 1
- 229960005400 bisoprolol fumarate Drugs 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- CKDOCTFBFTVPSN-UHFFFAOYSA-N borneol Natural products C1CC2(C)C(C)CC1C2(C)C CKDOCTFBFTVPSN-UHFFFAOYSA-N 0.000 description 1
- 229960002802 bromocriptine Drugs 0.000 description 1
- NOJMTMIRQRDZMT-GSPXQYRGSA-N bromocriptine methanesulfonate Chemical compound CS(O)(=O)=O.C1=CC(C=2[C@H](N(C)C[C@@H](C=2)C(=O)N[C@]2(C(=O)N3[C@H](C(N4CCC[C@H]4[C@]3(O)O2)=O)CC(C)C)C(C)C)C2)=C3C2=C(Br)NC3=C1 NOJMTMIRQRDZMT-GSPXQYRGSA-N 0.000 description 1
- 229940124630 bronchodilator Drugs 0.000 description 1
- 239000000168 bronchodilator agent Substances 0.000 description 1
- QDHFHIQKOVNCNC-UHFFFAOYSA-N butane-1-sulfonic acid Chemical compound CCCCS(O)(=O)=O QDHFHIQKOVNCNC-UHFFFAOYSA-N 0.000 description 1
- GMTYREVWZXJPLF-AFHUBHILSA-N butorphanol D-tartrate Chemical compound OC(=O)[C@@H](O)[C@H](O)C(O)=O.N1([C@@H]2CC3=CC=C(C=C3[C@@]3([C@]2(CCCC3)O)CC1)O)CC1CCC1 GMTYREVWZXJPLF-AFHUBHILSA-N 0.000 description 1
- 229960001590 butorphanol tartrate Drugs 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- CZBZUDVBLSSABA-UHFFFAOYSA-N butylated hydroxyanisole Chemical compound COC1=CC=C(O)C(C(C)(C)C)=C1.COC1=CC=C(O)C=C1C(C)(C)C CZBZUDVBLSSABA-UHFFFAOYSA-N 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 229910000019 calcium carbonate Inorganic materials 0.000 description 1
- 239000010495 camellia oil Substances 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 150000001733 carboxylic acid esters Chemical class 0.000 description 1
- 239000000496 cardiotonic agent Substances 0.000 description 1
- RZMKWKZIJJNSLQ-UHFFFAOYSA-M carpronium chloride Chemical compound [Cl-].COC(=O)CCC[N+](C)(C)C RZMKWKZIJJNSLQ-UHFFFAOYSA-M 0.000 description 1
- 229950003631 carpronium chloride Drugs 0.000 description 1
- 229960000541 cetyl alcohol Drugs 0.000 description 1
- 229940074979 cetyl palmitate Drugs 0.000 description 1
- 229960001657 chlorpromazine hydrochloride Drugs 0.000 description 1
- BHQCQFFYRZLCQQ-OELDTZBJSA-N cholic acid Chemical class C([C@H]1C[C@H]2O)[C@H](O)CC[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CC[C@H]([C@@H](CCC(O)=O)C)[C@@]2(C)[C@@H](O)C1 BHQCQFFYRZLCQQ-OELDTZBJSA-N 0.000 description 1
- 239000002812 cholic acid derivative Substances 0.000 description 1
- 235000013985 cinnamic acid Nutrition 0.000 description 1
- 229930016911 cinnamic acid Natural products 0.000 description 1
- CCRCUPLGCSFEDV-UHFFFAOYSA-N cinnamic acid methyl ester Natural products COC(=O)C=CC1=CC=CC=C1 CCRCUPLGCSFEDV-UHFFFAOYSA-N 0.000 description 1
- BJIOGJUNALELMI-ARJAWSKDSA-N cis-isoeugenol Chemical compound COC1=CC(\C=C/C)=CC=C1O BJIOGJUNALELMI-ARJAWSKDSA-N 0.000 description 1
- 229960002689 clemastine fumarate Drugs 0.000 description 1
- 239000002131 composite material Substances 0.000 description 1
- 229920001577 copolymer Polymers 0.000 description 1
- 239000003218 coronary vasodilator agent Substances 0.000 description 1
- 150000001893 coumarin derivatives Chemical class 0.000 description 1
- 229930003836 cresol Natural products 0.000 description 1
- 125000004122 cyclic group Chemical group 0.000 description 1
- GVJHHUAWPYXKBD-UHFFFAOYSA-N d-alpha-tocopherol Natural products OC1=C(C)C(C)=C2OC(CCCC(C)CCCC(C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-UHFFFAOYSA-N 0.000 description 1
- 229960002997 dehydrocholic acid Drugs 0.000 description 1
- SQIFACVGCPWBQZ-UHFFFAOYSA-N delta-terpineol Natural products CC(C)(O)C1CCC(=C)CC1 SQIFACVGCPWBQZ-UHFFFAOYSA-N 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 230000018109 developmental process Effects 0.000 description 1
- FSBVERYRVPGNGG-UHFFFAOYSA-N dimagnesium dioxido-bis[[oxido(oxo)silyl]oxy]silane hydrate Chemical compound O.[Mg+2].[Mg+2].[O-][Si](=O)O[Si]([O-])([O-])O[Si]([O-])=O FSBVERYRVPGNGG-UHFFFAOYSA-N 0.000 description 1
- 150000002012 dioxanes Chemical class 0.000 description 1
- 229960004646 diphenhydramine tannate Drugs 0.000 description 1
- 229960005058 diphenidol hydrochloride Drugs 0.000 description 1
- SZXQTJUDPRGNJN-UHFFFAOYSA-N dipropylene glycol Chemical compound OCCCOCCCO SZXQTJUDPRGNJN-UHFFFAOYSA-N 0.000 description 1
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 1
- 208000035475 disorder Diseases 0.000 description 1
- DTGKSKDOIYIVQL-UHFFFAOYSA-N dl-isoborneol Natural products C1CC2(C)C(O)CC1C2(C)C DTGKSKDOIYIVQL-UHFFFAOYSA-N 0.000 description 1
- 229960001149 dopamine hydrochloride Drugs 0.000 description 1
- 238000001647 drug administration Methods 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 229950003102 efonidipine Drugs 0.000 description 1
- IKBJGZQVVVXCEQ-UHFFFAOYSA-N efonidipine hydrochloride Chemical compound Cl.CCO.CC=1NC(C)=C(C(=O)OCCN(CC=2C=CC=CC=2)C=2C=CC=CC=2)C(C=2C=C(C=CC=2)[N+]([O-])=O)C=1P1(=O)OCC(C)(C)CO1 IKBJGZQVVVXCEQ-UHFFFAOYSA-N 0.000 description 1
- 229920001971 elastomer Polymers 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 229960002565 eperisone Drugs 0.000 description 1
- 239000003822 epoxy resin Substances 0.000 description 1
- 229960004943 ergotamine Drugs 0.000 description 1
- OFKDAAIKGIBASY-VFGNJEKYSA-N ergotamine Chemical compound C([C@H]1C(=O)N2CCC[C@H]2[C@]2(O)O[C@@](C(N21)=O)(C)NC(=O)[C@H]1CN([C@H]2C(C3=CC=CC4=NC=C([C]34)C2)=C1)C)C1=CC=CC=C1 OFKDAAIKGIBASY-VFGNJEKYSA-N 0.000 description 1
- 229960001903 ergotamine tartrate Drugs 0.000 description 1
- XCGSFFUVFURLIX-UHFFFAOYSA-N ergotaminine Natural products C1=C(C=2C=CC=C3NC=C(C=23)C2)C2N(C)CC1C(=O)NC(C(N12)=O)(C)OC1(O)C1CCCN1C(=O)C2CC1=CC=CC=C1 XCGSFFUVFURLIX-UHFFFAOYSA-N 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 229960002217 eugenol Drugs 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 238000004299 exfoliation Methods 0.000 description 1
- 239000004744 fabric Substances 0.000 description 1
- 235000019197 fats Nutrition 0.000 description 1
- 150000002191 fatty alcohols Chemical class 0.000 description 1
- IVLVTNPOHDFFCJ-UHFFFAOYSA-N fentanyl citrate Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O.C=1C=CC=CC=1N(C(=O)CC)C(CC1)CCN1CCC1=CC=CC=C1 IVLVTNPOHDFFCJ-UHFFFAOYSA-N 0.000 description 1
- 229960004207 fentanyl citrate Drugs 0.000 description 1
- 238000010579 first pass effect Methods 0.000 description 1
- 229960002807 flunarizine hydrochloride Drugs 0.000 description 1
- 229960003628 flurazepam hydrochloride Drugs 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- 210000001035 gastrointestinal tract Anatomy 0.000 description 1
- 229940113087 geraniol Drugs 0.000 description 1
- 239000001087 glyceryl triacetate Substances 0.000 description 1
- 235000013773 glyceryl triacetate Nutrition 0.000 description 1
- 229960003607 granisetron hydrochloride Drugs 0.000 description 1
- LNEPOXFFQSENCJ-UHFFFAOYSA-N haloperidol Chemical compound C1CC(O)(C=2C=CC(Cl)=CC=2)CCN1CCCC(=O)C1=CC=C(F)C=C1 LNEPOXFFQSENCJ-UHFFFAOYSA-N 0.000 description 1
- PXDJXZJSCPSGGI-UHFFFAOYSA-N hexadecanoic acid hexadecyl ester Natural products CCCCCCCCCCCCCCCCOC(=O)CCCCCCCCCCCCCCC PXDJXZJSCPSGGI-UHFFFAOYSA-N 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- 150000004677 hydrates Chemical class 0.000 description 1
- 229930195733 hydrocarbon Natural products 0.000 description 1
- 229960000443 hydrochloric acid Drugs 0.000 description 1
- QYZRTBKYBJRGJB-UHFFFAOYSA-N hydron;1-methyl-n-(9-methyl-9-azabicyclo[3.3.1]nonan-3-yl)indazole-3-carboxamide;chloride Chemical compound Cl.C1=CC=C2C(C(=O)NC3CC4CCCC(C3)N4C)=NN(C)C2=C1 QYZRTBKYBJRGJB-UHFFFAOYSA-N 0.000 description 1
- JUMYIBMBTDDLNG-OJERSXHUSA-N hydron;methyl (2r)-2-phenyl-2-[(2r)-piperidin-2-yl]acetate;chloride Chemical compound Cl.C([C@@H]1[C@H](C(=O)OC)C=2C=CC=CC=2)CCCN1 JUMYIBMBTDDLNG-OJERSXHUSA-N 0.000 description 1
- 230000002209 hydrophobic effect Effects 0.000 description 1
- 230000000147 hypnotic effect Effects 0.000 description 1
- 150000002462 imidazolines Chemical class 0.000 description 1
- XZZXIYZZBJDEEP-UHFFFAOYSA-N imipramine hydrochloride Chemical compound [Cl-].C1CC2=CC=CC=C2N(CCC[NH+](C)C)C2=CC=CC=C21 XZZXIYZZBJDEEP-UHFFFAOYSA-N 0.000 description 1
- 229960002102 imipramine hydrochloride Drugs 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 229910017053 inorganic salt Inorganic materials 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- QXJSBBXBKPUZAA-UHFFFAOYSA-N isooleic acid Natural products CCCCCCCC=CCCCCCCCCC(O)=O QXJSBBXBKPUZAA-UHFFFAOYSA-N 0.000 description 1
- 229940074928 isopropyl myristate Drugs 0.000 description 1
- XUGNVMKQXJXZCD-UHFFFAOYSA-N isopropyl palmitate Chemical compound CCCCCCCCCCCCCCCC(=O)OC(C)C XUGNVMKQXJXZCD-UHFFFAOYSA-N 0.000 description 1
- 150000002576 ketones Chemical class 0.000 description 1
- YNQQEYBLVYAWNX-WLHGVMLRSA-N ketotifen fumarate Chemical compound OC(=O)\C=C\C(O)=O.C1CN(C)CCC1=C1C2=CC=CC=C2CC(=O)C2=C1C=CS2 YNQQEYBLVYAWNX-WLHGVMLRSA-N 0.000 description 1
- 229960003630 ketotifen fumarate Drugs 0.000 description 1
- 150000003903 lactic acid esters Chemical class 0.000 description 1
- 239000005001 laminate film Substances 0.000 description 1
- 229960004393 lidocaine hydrochloride Drugs 0.000 description 1
- YECIFGHRMFEPJK-UHFFFAOYSA-N lidocaine hydrochloride monohydrate Chemical compound O.[Cl-].CC[NH+](CC)CC(=O)NC1=C(C)C=CC=C1C YECIFGHRMFEPJK-UHFFFAOYSA-N 0.000 description 1
- 229960004488 linolenic acid Drugs 0.000 description 1
- KQQKGWQCNNTQJW-UHFFFAOYSA-N linolenic acid Natural products CC=CCCC=CCC=CCCCCCCCC(O)=O KQQKGWQCNNTQJW-UHFFFAOYSA-N 0.000 description 1
- 210000004185 liver Anatomy 0.000 description 1
- 239000003589 local anesthetic agent Substances 0.000 description 1
- 229960005015 local anesthetics Drugs 0.000 description 1
- 235000021266 loss of appetite Nutrition 0.000 description 1
- 208000019017 loss of appetite Diseases 0.000 description 1
- ZLNQQNXFFQJAID-UHFFFAOYSA-L magnesium carbonate Chemical compound [Mg+2].[O-]C([O-])=O ZLNQQNXFFQJAID-UHFFFAOYSA-L 0.000 description 1
- 239000001095 magnesium carbonate Substances 0.000 description 1
- 229910000021 magnesium carbonate Inorganic materials 0.000 description 1
- 239000000391 magnesium silicate Substances 0.000 description 1
- 229910052919 magnesium silicate Inorganic materials 0.000 description 1
- 235000019792 magnesium silicate Nutrition 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 230000007721 medicinal effect Effects 0.000 description 1
- 150000002736 metal compounds Chemical class 0.000 description 1
- 150000002739 metals Chemical class 0.000 description 1
- TWXDDNPPQUTEOV-FVGYRXGTSA-N methamphetamine hydrochloride Chemical compound Cl.CN[C@@H](C)CC1=CC=CC=C1 TWXDDNPPQUTEOV-FVGYRXGTSA-N 0.000 description 1
- 229960002532 methamphetamine hydrochloride Drugs 0.000 description 1
- CMUHZRATLMUDJI-UHFFFAOYSA-N methyl 2h-pyridine-1-carboxylate Chemical compound COC(=O)N1CC=CC=C1 CMUHZRATLMUDJI-UHFFFAOYSA-N 0.000 description 1
- LZULAZTXJLWELL-UHFFFAOYSA-N methyl hex-5-ynoate Chemical compound COC(=O)CCCC#C LZULAZTXJLWELL-UHFFFAOYSA-N 0.000 description 1
- WBYWAXJHAXSJNI-UHFFFAOYSA-N methyl p-hydroxycinnamate Natural products OC(=O)C=CC1=CC=CC=C1 WBYWAXJHAXSJNI-UHFFFAOYSA-N 0.000 description 1
- CCRCUPLGCSFEDV-BQYQJAHWSA-N methyl trans-cinnamate Chemical compound COC(=O)\C=C\C1=CC=CC=C1 CCRCUPLGCSFEDV-BQYQJAHWSA-N 0.000 description 1
- 229960001033 methylphenidate hydrochloride Drugs 0.000 description 1
- 229960001300 metoprolol tartrate Drugs 0.000 description 1
- 229930003658 monoterpene Natural products 0.000 description 1
- 235000002577 monoterpenes Nutrition 0.000 description 1
- 229960005195 morphine hydrochloride Drugs 0.000 description 1
- XELXKCKNPPSFNN-BJWPBXOKSA-N morphine hydrochloride trihydrate Chemical compound O.O.O.Cl.O([C@H]1[C@H](C=C[C@H]23)O)C4=C5[C@@]12CCN(C)[C@@H]3CC5=CC=C4O XELXKCKNPPSFNN-BJWPBXOKSA-N 0.000 description 1
- 239000003158 myorelaxant agent Substances 0.000 description 1
- 229940043348 myristyl alcohol Drugs 0.000 description 1
- 229940078812 myristyl myristate Drugs 0.000 description 1
- WQEPLUUGTLDZJY-UHFFFAOYSA-N n-Pentadecanoic acid Natural products CCCCCCCCCCCCCCC(O)=O WQEPLUUGTLDZJY-UHFFFAOYSA-N 0.000 description 1
- JXTPJDDICSTXJX-UHFFFAOYSA-N n-Triacontane Natural products CCCCCCCCCCCCCCCCCCCCCCCCCCCCCC JXTPJDDICSTXJX-UHFFFAOYSA-N 0.000 description 1
- 230000003533 narcotic effect Effects 0.000 description 1
- 229920003052 natural elastomer Polymers 0.000 description 1
- 229920001194 natural rubber Polymers 0.000 description 1
- 229960001499 neostigmine bromide Drugs 0.000 description 1
- LULNWZDBKTWDGK-UHFFFAOYSA-M neostigmine bromide Chemical compound [Br-].CN(C)C(=O)OC1=CC=CC([N+](C)(C)C)=C1 LULNWZDBKTWDGK-UHFFFAOYSA-M 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 229960002289 nicardipine hydrochloride Drugs 0.000 description 1
- AIKVCUNQWYTVTO-UHFFFAOYSA-N nicardipine hydrochloride Chemical compound Cl.COC(=O)C1=C(C)NC(C)=C(C(=O)OCCN(C)CC=2C=CC=CC=2)C1C1=CC=CC([N+]([O-])=O)=C1 AIKVCUNQWYTVTO-UHFFFAOYSA-N 0.000 description 1
- 239000000041 non-steroidal anti-inflammatory agent Substances 0.000 description 1
- 239000004745 nonwoven fabric Substances 0.000 description 1
- 230000037311 normal skin Effects 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 1
- KSCKTBJJRVPGKM-UHFFFAOYSA-N octan-1-olate;titanium(4+) Chemical compound [Ti+4].CCCCCCCC[O-].CCCCCCCC[O-].CCCCCCCC[O-].CCCCCCCC[O-] KSCKTBJJRVPGKM-UHFFFAOYSA-N 0.000 description 1
- 229940073665 octyldodecyl myristate Drugs 0.000 description 1
- ZQPPMHVWECSIRJ-KTKRTIGZSA-N oleic acid Chemical compound CCCCCCCC\C=C/CCCCCCCC(O)=O ZQPPMHVWECSIRJ-KTKRTIGZSA-N 0.000 description 1
- 235000021313 oleic acid Nutrition 0.000 description 1
- 229940055577 oleyl alcohol Drugs 0.000 description 1
- XMLQWXUVTXCDDL-UHFFFAOYSA-N oleyl alcohol Natural products CCCCCCC=CCCCCCCCCCCO XMLQWXUVTXCDDL-UHFFFAOYSA-N 0.000 description 1
- 239000004006 olive oil Substances 0.000 description 1
- 235000008390 olive oil Nutrition 0.000 description 1
- 229960000770 ondansetron hydrochloride Drugs 0.000 description 1
- 239000000312 peanut oil Substances 0.000 description 1
- UWCVGPLTGZWHGS-ZORIOUSZSA-N pergolide mesylate Chemical compound CS(O)(=O)=O.C1=CC([C@H]2C[C@@H](CSC)CN([C@@H]2C2)CCC)=C3C2=CNC3=C1 UWCVGPLTGZWHGS-ZORIOUSZSA-N 0.000 description 1
- 229960001511 pergolide mesylate Drugs 0.000 description 1
- 239000000810 peripheral vasodilating agent Substances 0.000 description 1
- 229960002116 peripheral vasodilator Drugs 0.000 description 1
- 229940083254 peripheral vasodilators imidazoline derivative Drugs 0.000 description 1
- 229950005491 perisoxal Drugs 0.000 description 1
- 239000003208 petroleum Substances 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- 229940127557 pharmaceutical product Drugs 0.000 description 1
- 239000005011 phenolic resin Substances 0.000 description 1
- 239000002504 physiological saline solution Substances 0.000 description 1
- 229920000647 polyepoxide Polymers 0.000 description 1
- 229920000098 polyolefin Polymers 0.000 description 1
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 1
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 1
- 229940068977 polysorbate 20 Drugs 0.000 description 1
- 229940068965 polysorbates Drugs 0.000 description 1
- 150000003097 polyterpenes Chemical class 0.000 description 1
- 229920002635 polyurethane Polymers 0.000 description 1
- 239000004814 polyurethane Substances 0.000 description 1
- 229920002689 polyvinyl acetate Polymers 0.000 description 1
- 239000011118 polyvinyl acetate Substances 0.000 description 1
- 229920000915 polyvinyl chloride Polymers 0.000 description 1
- 239000004800 polyvinyl chloride Substances 0.000 description 1
- 229960001309 procaine hydrochloride Drugs 0.000 description 1
- 229960002789 procaterol hydrochloride Drugs 0.000 description 1
- KCXFHTAICRTXLI-UHFFFAOYSA-N propane-1-sulfonic acid Chemical compound CCCS(O)(=O)=O KCXFHTAICRTXLI-UHFFFAOYSA-N 0.000 description 1
- 229960004604 propranolol hydrochloride Drugs 0.000 description 1
- AQHHHDLHHXJYJD-UHFFFAOYSA-N propranolol hydrochloride Natural products C1=CC=C2C(OCC(O)CNC(C)C)=CC=CC2=C1 AQHHHDLHHXJYJD-UHFFFAOYSA-N 0.000 description 1
- YKYONYBAUNKHLG-UHFFFAOYSA-N propyl acetate Chemical group CCCOC(C)=O YKYONYBAUNKHLG-UHFFFAOYSA-N 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 229960004063 propylene glycol Drugs 0.000 description 1
- 229940083082 pyrimidine derivative acting on arteriolar smooth muscle Drugs 0.000 description 1
- 150000003230 pyrimidines Chemical class 0.000 description 1
- HNJBEVLQSNELDL-UHFFFAOYSA-N pyrrolidin-2-one Chemical compound O=C1CCCN1 HNJBEVLQSNELDL-UHFFFAOYSA-N 0.000 description 1
- 229950002503 rilmazafone Drugs 0.000 description 1
- 190000007496 rilmazafone hydrochloride Chemical compound 0.000 description 1
- 239000005060 rubber Substances 0.000 description 1
- 229940058287 salicylic acid derivative anticestodals Drugs 0.000 description 1
- 150000003872 salicylic acid derivatives Chemical class 0.000 description 1
- 238000005070 sampling Methods 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- 229940125723 sedative agent Drugs 0.000 description 1
- 239000000932 sedative agent Substances 0.000 description 1
- 230000035807 sensation Effects 0.000 description 1
- 229940121356 serotonin receptor antagonist Drugs 0.000 description 1
- 229930004725 sesquiterpene Natural products 0.000 description 1
- RMAQACBXLXPBSY-UHFFFAOYSA-N silicic acid Chemical compound O[Si](O)(O)O RMAQACBXLXPBSY-UHFFFAOYSA-N 0.000 description 1
- 229910052710 silicon Inorganic materials 0.000 description 1
- 239000010703 silicon Substances 0.000 description 1
- 235000012239 silicon dioxide Nutrition 0.000 description 1
- 229940125706 skeletal muscle relaxant agent Drugs 0.000 description 1
- 229960004249 sodium acetate Drugs 0.000 description 1
- 239000000243 solution Substances 0.000 description 1
- 229940035044 sorbitan monolaurate Drugs 0.000 description 1
- 230000007480 spreading Effects 0.000 description 1
- 238000003892 spreading Methods 0.000 description 1
- 229940032094 squalane Drugs 0.000 description 1
- 229940031439 squalene Drugs 0.000 description 1
- TUHBEKDERLKLEC-UHFFFAOYSA-N squalene Natural products CC(=CCCC(=CCCC(=CCCC=C(/C)CCC=C(/C)CC=C(C)C)C)C)C TUHBEKDERLKLEC-UHFFFAOYSA-N 0.000 description 1
- 238000013112 stability test Methods 0.000 description 1
- 239000008117 stearic acid Substances 0.000 description 1
- 150000003431 steroids Chemical class 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 229940032085 sucrose monolaurate Drugs 0.000 description 1
- 230000009747 swallowing Effects 0.000 description 1
- 239000003784 tall oil Substances 0.000 description 1
- 229940116411 terpineol Drugs 0.000 description 1
- WUBVEMGCQRSBBT-UHFFFAOYSA-N tert-butyl 4-(trifluoromethylsulfonyloxy)-3,6-dihydro-2h-pyridine-1-carboxylate Chemical compound CC(C)(C)OC(=O)N1CCC(OS(=O)(=O)C(F)(F)F)=CC1 WUBVEMGCQRSBBT-UHFFFAOYSA-N 0.000 description 1
- TUNFSRHWOTWDNC-HKGQFRNVSA-N tetradecanoic acid Chemical compound CCCCCCCCCCCCC[14C](O)=O TUNFSRHWOTWDNC-HKGQFRNVSA-N 0.000 description 1
- DZKXJUASMGQEMA-UHFFFAOYSA-N tetradecyl tetradecanoate Chemical compound CCCCCCCCCCCCCCOC(=O)CCCCCCCCCCCCC DZKXJUASMGQEMA-UHFFFAOYSA-N 0.000 description 1
- 229920001187 thermosetting polymer Polymers 0.000 description 1
- 229960000790 thymol Drugs 0.000 description 1
- 229960005221 timolol maleate Drugs 0.000 description 1
- OGIDPMRJRNCKJF-UHFFFAOYSA-N titanium oxide Inorganic materials [Ti]=O OGIDPMRJRNCKJF-UHFFFAOYSA-N 0.000 description 1
- 235000010384 tocopherol Nutrition 0.000 description 1
- 229960001295 tocopherol Drugs 0.000 description 1
- 229930003799 tocopherol Natural products 0.000 description 1
- 239000011732 tocopherol Substances 0.000 description 1
- BJIOGJUNALELMI-UHFFFAOYSA-N trans-isoeugenol Natural products COC1=CC(C=CC)=CC=C1O BJIOGJUNALELMI-UHFFFAOYSA-N 0.000 description 1
- 229960002622 triacetin Drugs 0.000 description 1
- 239000001069 triethyl citrate Substances 0.000 description 1
- VMYFZRTXGLUXMZ-UHFFFAOYSA-N triethyl citrate Natural products CCOC(=O)C(O)(C(=O)OCC)C(=O)OCC VMYFZRTXGLUXMZ-UHFFFAOYSA-N 0.000 description 1
- 235000013769 triethyl citrate Nutrition 0.000 description 1
- QDWJJTJNXAKQKD-UHFFFAOYSA-N trihexyphenidyl hydrochloride Chemical compound Cl.C1CCCCC1C(C=1C=CC=CC=1)(O)CCN1CCCCC1 QDWJJTJNXAKQKD-UHFFFAOYSA-N 0.000 description 1
- 229960004479 trihexyphenidyl hydrochloride Drugs 0.000 description 1
- 229960004846 tulobuterol hydrochloride Drugs 0.000 description 1
- 229920006305 unsaturated polyester Polymers 0.000 description 1
- 230000002485 urinary effect Effects 0.000 description 1
- 235000015112 vegetable and seed oil Nutrition 0.000 description 1
- 239000008158 vegetable oil Substances 0.000 description 1
- 229960000881 verapamil hydrochloride Drugs 0.000 description 1
- 230000008673 vomiting Effects 0.000 description 1
- 239000011787 zinc oxide Substances 0.000 description 1
- NWONKYPBYAMBJT-UHFFFAOYSA-L zinc sulfate Chemical compound [Zn+2].[O-]S([O-])(=O)=O NWONKYPBYAMBJT-UHFFFAOYSA-L 0.000 description 1
- GVJHHUAWPYXKBD-IEOSBIPESA-N α-tocopherol Chemical compound OC1=C(C)C(C)=C2O[C@@](CCC[C@H](C)CCC[C@H](C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-IEOSBIPESA-N 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/70—Web, sheet or filament bases ; Films; Fibres of the matrix type containing drug
- A61K9/7023—Transdermal patches and similar drug-containing composite devices, e.g. cataplasms
- A61K9/703—Transdermal patches and similar drug-containing composite devices, e.g. cataplasms characterised by shape or structure; Details concerning release liner or backing; Refillable patches; User-activated patches
- A61K9/7038—Transdermal patches of the drug-in-adhesive type, i.e. comprising drug in the skin-adhesive layer
- A61K9/7046—Transdermal patches of the drug-in-adhesive type, i.e. comprising drug in the skin-adhesive layer the adhesive comprising macromolecular compounds
- A61K9/7053—Transdermal patches of the drug-in-adhesive type, i.e. comprising drug in the skin-adhesive layer the adhesive comprising macromolecular compounds obtained by reactions only involving carbon to carbon unsaturated bonds, e.g. polyvinyl, polyisobutylene, polystyrene
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/12—Carboxylic acids; Salts or anhydrides thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/70—Web, sheet or filament bases ; Films; Fibres of the matrix type containing drug
- A61K9/7023—Transdermal patches and similar drug-containing composite devices, e.g. cataplasms
- A61K9/703—Transdermal patches and similar drug-containing composite devices, e.g. cataplasms characterised by shape or structure; Details concerning release liner or backing; Refillable patches; User-activated patches
- A61K9/7038—Transdermal patches of the drug-in-adhesive type, i.e. comprising drug in the skin-adhesive layer
- A61K9/7046—Transdermal patches of the drug-in-adhesive type, i.e. comprising drug in the skin-adhesive layer the adhesive comprising macromolecular compounds
- A61K9/7053—Transdermal patches of the drug-in-adhesive type, i.e. comprising drug in the skin-adhesive layer the adhesive comprising macromolecular compounds obtained by reactions only involving carbon to carbon unsaturated bonds, e.g. polyvinyl, polyisobutylene, polystyrene
- A61K9/7061—Polyacrylates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/70—Web, sheet or filament bases ; Films; Fibres of the matrix type containing drug
- A61K9/7023—Transdermal patches and similar drug-containing composite devices, e.g. cataplasms
- A61K9/703—Transdermal patches and similar drug-containing composite devices, e.g. cataplasms characterised by shape or structure; Details concerning release liner or backing; Refillable patches; User-activated patches
- A61K9/7038—Transdermal patches of the drug-in-adhesive type, i.e. comprising drug in the skin-adhesive layer
- A61K9/7076—Transdermal patches of the drug-in-adhesive type, i.e. comprising drug in the skin-adhesive layer the adhesive comprising ingredients of undetermined constitution or reaction products thereof, e.g. rosin or other plant resins
Landscapes
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Dermatology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Epidemiology (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Medicinal Chemistry (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Botany (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Medicinal Preparation (AREA)
- Prostheses (AREA)
- Transition And Organic Metals Composition Catalysts For Addition Polymerization (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Description
本発明は、外用貼付剤に関する。本発明は、特に、塩基性薬物、有機酸および有機酸塩を含有し、経皮吸収性と安定性に優れた外用貼付剤に関する。
背景技術
従来より、薬物の投与方法として、経口投与、直腸投与、皮内投与、静脈内投与等、種々の方法が知られているが、経口投与が最も広く採用されている。しかし、経口投与には、薬物を吸収した後、肝臓での初回通過効果を受けやすいことや、投与後一時的に必要以上の血中濃度が認められる等の欠点を有している。また、経口投与においては、胃腸管障害、嘔吐感、食欲不振等の副作用も多く報告されている。さらに、近年の高齢化社会において、嚥下力の低下した患者が増加していることを考慮すると、より服用しやすい製剤が臨床上望まれている。従って、このような経口投与における欠点を解消し、より安全にしかも持続的に患者が服用しやすい製剤として、外用貼付剤の開発が積極的に進められ、製品も上市されている。
しかしながら、多くの薬物は経皮吸収性が低いため、外用貼付剤の開発が困難であり、外用貼付剤はその目的を未だ十分に達成し得ていない。すなわち、正常皮膚は本来、異物の体内への侵入を防ぐバリヤー機能を有しているため、通常の外用貼付剤に用いられる基剤では、薬物が十分に経皮吸収されないことが多い。
そのため、皮膚の角質層を介する薬物の経皮吸収性を高める工夫が求められており、いわゆる経皮吸収促進剤の基剤への配合が一般的に試みられている。例えば、低級アルキルアミドと組み合わせた吸収促進剤として、ジメチルアセトアミドとエチルアルコール、イソプロピルアルコール、イソプロピルパルミテート等を組み合わせた例(米国特許第3,472,931号公報)や、2−ピロリドンと適当なオイル、直鎖脂肪酸とアルコールのエステルを組み合わせた例(米国特許第4,017,641号公報)、また、低級アルコールと炭素数7〜20のアルコール、炭素数5〜30の脂肪酸炭化水素、炭素数19〜26の脂肪酸カルボン酸のアルコールエステル、炭素数10〜24のモノまたはジエーテル、炭素数11〜15のケトンと水を組み合わせた例(特開昭61−249934号公報)等がすでに提案されている。しかしながら、これら従来の吸収促進剤および吸収促進組成物は皮膚に対する安全性が十分ではない。また、塩基性薬物を酸付加塩の形態で含有した外用貼付剤においてはその効果はほとんど期待できなかった。
また、外用貼付剤として、薬物と有機酸を組み合わせる手法も報告されている。例えば、天然ゴム系粘着剤に、吉草酸ベタメタゾンと有機酸を組み合わせたテープ製剤の例(特開昭56−61312号公報)、アクリル系粘着剤に非ステロイド系消炎鎮痛剤と有機酸を組み合わせたテープ製剤の例(特開昭62−126119号公報)、また、スチレン−イソプレン−スチレンブロック共重合体ポリマーに、薬効成分としてサリチル酸メチル、乳化剤、有機酸、可塑剤、粘着付与樹脂および水を組み合わせたパップ型製剤の例(特開昭63−159315号公報)等がすでに提案されている。しかしながら、これらの公報において有機酸塩は使用されておらず、また有機酸の使用目的は、安定性の改善、溶解性の改善およびpH調整剤であり、経皮吸収性の向上を目的としたものではない。さらに、これらの公報における薬物は酸性または中性であるため、本発明のように、イオン対の形成を介して塩基性薬物の皮膚透過性及び安定性を向上させるために、有機酸を用いるものでもない。
また、塩基性の生理活性物質の皮膚透過性を向上させる手法も試みられている。例えば、アクリル系粘着剤に、クエン酸と塩酸イソプレテレノールを組み合わせたテープ製剤の例(特開昭63−79820号公報)、アクリル系粘着剤に有機酸とピンボセチンを組み合わせたテープ製剤の例(特開平5−25039号公報)等が報告されている。しかしながら、これらの製剤には、剥離時の刺激性の問題があり、薬物の放出量が治療に十分な効果をもたらすに至っていない。
また、経皮投与製剤として、薬物と有機酸を組み合わせた手法も報告されている。例えば、非ステロイド系の消炎鎮痛剤の塩に、有機酸およびグリコールを含有したもの(特開昭62−181226号公報)、アルカリ金属の塩形態を有する非ステロイド系消炎鎮痛剤および遊離状態の非ステロイド消炎鎮痛剤より強酸性の有機酸を含有する貼付剤(特公平7−47535号公報)がある。しかしながら、これらの提案は、酸性薬物に関するもので、塩基性薬物に関するものではない。また、塩基性薬物またはその塩、炭素原子数2〜5のアルコール炭素原子数2〜5の有機酸および炭素原子数16〜20のカルボン酸エステルの組み合わせの例があるものの、有機酸塩の使用に関する記載はない。
さらに、WO 96/16642には塩型の塩基性薬物に有機酸塩を含有させた貼付製剤の技術が開示されているが、有機酸と有機酸塩を組み合わせることによって薬物の皮膚透過性を向上させ、粘着物性や性状等の外用貼付剤の物理的安定性を高めることについては開示がない。
すなわち、塩基性薬物を酸付加塩の形態で外用貼付剤に含有させ、優れた安定性を有し、かつ期待する薬物の経皮吸収を得ることができる外用貼付剤は、未だ見出されていない。
発明の開示
本発明は上述した従来技術の課題を解決し、薬物の経皮吸収性が高く、しかも安定性に優れた、塩基性薬物含有の外用貼付剤を提供することを目的とするものである。
本発明者らは、上記の課題を解決すべく、鋭意研究を重ねた結果、塩基性薬物を酸付加塩型で含有する外用貼付剤に、特定量の有機酸と有機酸塩を含有させると、有機酸塩を単独で用いる場合より安定にイオン対を形成し、外用貼付剤中に皮膚透過性に優れた準安定状態が安定して保持されることを見出し、本発明を完成させた。
すなわち、本発明は、塩基性薬物、有機酸および有機酸塩を必須成分として含有することを特徴とする外用貼付剤である。
発明を実施するための最良の形態
以下、本発明について詳しく説明する。
本発明の外用貼付剤は、粘着層を含むものであることが望ましく、その他、例えば、粘着層を支持する支持体層、粘着層上に設けられる離型紙層を有するものであることができる。本発明の外用貼付剤において、塩基性薬物、有機酸および有機酸塩は上記粘着層中に含有されることが好ましい。
本発明の外用貼付剤の粘着層において使用される塩基性薬物としては、塩基性薬物の酸付加塩であることが望ましい。塩基性薬物の酸付加塩としては、特に限定はないが、例えば、催眠・鎮静剤(塩酸フルラゼパム、塩酸リルマザホン等)、解熱消炎鎮痛剤(酒石酸ブトルファノール、クエン酸ペリソキサール等)、抗片頭痛剤(酒石酸エルゴタミン、メシル酸エルゴタミン等)興奮・覚醒剤(塩酸メタンフェタミン、塩酸メチルフェニデート等)、精神神経用剤(塩酸クロルプロマジン、塩酸イミプラミン等)、局所麻酔剤(塩酸リドカイン、塩酸プロカイン等)、泌尿器官用剤(塩酸オキシブチニン等)、骨格筋弛緩剤(塩酸チザニジン、塩酸エペリゾン、メシル酸プリジノール等)、自律神経用剤(塩化カルプロニウム、臭化ネオスチグミン等)、抗パーキンソン剤(メシル酸ペルゴリド、メシル酸ブロモクリプチン、塩酸トリヘキシフェニジル、塩酸アマンタジン等)、抗ヒスタミン剤(フマル酸クレマスチン、タンニン酸ジフェンヒドラミン等)、気管支拡張剤(塩酸ツロブテロール、塩酸プロカテロール等)、強心剤(塩酸イソプレナリン、塩酸ドパミン等)、冠血管拡張剤(塩酸ジルチアゼム、塩酸ベラパミル等)、末梢血管拡張剤(クエン酸ニカメタート、塩酸トラゾリン等)、循環器官用剤(塩酸フルナリジン、塩酸ニカルジピン、塩酸ベニジピン、塩酸エホニジピン、フマル酸ビソプロロール、マレイン酸チモロール、塩酸ジルチアゼム、酒石酸メトプロロール等)、不整脈用剤(塩酸プロプラノロール、塩酸アルプレノロール等)、抗アレルギー剤(フマル酸ケトチフェン、塩酸アゼラスチン等)、鎮暈剤(メシル酸ベタヒスチン、塩酸ジフェニドール等)、セロトニン受容体拮抗制吐剤(塩酸オンダンセトロン、塩酸グラニセトロン等)、麻薬系の鎮痛剤(塩酸モルヒネ、クエン酸フェンタニル等)が挙げられる。
これらの塩基性薬物は、1種類を単独で用いても2種類以上を組み合わせて用いてもよく、無機塩または有機塩のいずれの形態の薬物であってもよい。また、これらの塩基性薬物の配合量は、外用貼付剤としての充分な透過量および粘着物性等への影響を考慮して、粘着層の組成全体の質量に基づいて、0.1〜20質量%とすることが好ましい。この配合量が0.1質量%未満となると、充分な薬効が得られず、20質量%を超えると、貼付剤としての物性が劣ったものとなる。
本発明の外用貼付剤の粘着層中において使用される有機酸は、特に限定されないが、炭素数2〜7のカルボン酸が好ましい。炭素数2〜7の有機酸としては、脂肪族(モノ、ジ、トリ)カルボン酸(例えば、酢酸、プロピオン酸、イソ酪酸、乳酸、マレイン酸、フマル酸、ピルビン酸、シュウ酸、コハク酸、酒石酸等)、芳香族カルボン酸(例えば、サリチル酸、安息香酸等)等が挙げられる。これらの中でも、特に酢酸、乳酸、酒石酸、クエン酸、リンゴ酸、安息香酸、サリチル酸が好ましい。
これらの有機酸は、1種類を単独で用いても2種類以上を組み合わせて用いてもよい。また、これらの有機酸の配合量は、外用貼付剤としての安定性および皮膚への刺激性を考慮すると、粘着剤層の組成全体の質量に基づいて、0.01〜20質量%であることが好ましく、さらに好ましくは0.1〜15質量%であり、特に好ましくは0.1〜10質量%である。有機酸の粘着層における配合量が、0.1質量%未満となると、安定性が劣ったものとなり、20質量%を超えると、皮膚刺激が生じる。
また、塩基性薬物の酸付加塩と有機酸の配合比は、5:1〜1:5(当量比)とすることが好ましい。この塩基性薬物の酸付加塩と有機酸の配合比が5:1〜1:5の範囲外となると、安定性が劣ったものとなったり、皮膚透過性が劣ったものとなる。
本発明の外用貼付剤の粘着層中において使用される有機酸塩は、特に限定されないが、例えば、脂肪族(モノ、ジ、トリ)カルボン酸(例えば、酢酸、プロピオン酸、イソ酪酸、カプロン酸、カプリル酸、乳酸、マレイン酸、ピルビン酸、シュウ酸、コハク酸、酒石酸等)、芳香族カルボン酸(例えば、フタル酸、サリチル酸、安息香酸、アセチルサリチル酸等)、アルキルスルホン酸(例えば、エタンスルホン酸、プロピルスルホン酸、ブタンスルホン酸、ポリオキシエチレンアルキルエーテルスルホン酸等)、アルキルスルホン酸誘導体(例えば、N−2−ヒドロキシエチルピペリジン−N’−2−エタンスルホン酸(以下、「HEPES」と略記する)等)、コール酸誘導体(例えば、デヒドロコール酸等)の各水溶性無機塩類を挙げることができる。これらの中でも、カルボン酸の金属塩が好ましく、特に酢酸ナトリウムが好ましい。また、これらの有機酸塩は無水物であっても水和物であってもよいが、疎水性の粘着層中に用いられる場合には無水物であることが好ましい。
これらの有機酸塩は、1種類を単独で用いても2種類以上を組み合わせて用いてもよい。また、これらの有機酸塩の配合量は、外用貼付剤としての充分な透過量および皮膚への刺激性を考慮すると、粘着層の組成全体の質量に基づいて、0.01〜20質量%とすることが好ましく、さらに好ましくは、0.1〜15質量%、特に好ましくは0.1〜10質量%である。有機酸塩の配合量が、0.01質量%未満となると、皮膚透過性が劣ったものとなり、20質量%を超えると、皮膚刺激が生じる。
また、塩基性薬物の酸付加塩と有機酸塩の配合比は5:1〜1:5(当量比)であることが好ましい。この塩基性薬物の酸付加塩と有機酸塩の配合比が5:1〜1:5の範囲外となると、皮膚透過性が劣ったものとなったり、物性が劣ったものとなる。
さらに、有機酸と有機酸塩の配合比は、3:1〜1:20(当量比)とすることが好ましく、さらに好ましくは2:1〜1:15(当量比)であり、特に好ましくは1:1〜1:10(当量比)である。この有機酸と有機酸塩の配合比が3:1〜1:20の範囲外となると、皮膚透過性が劣ったものとなったり、安定性が劣ったものとなる。
本発明の外用貼付剤の粘着層は、上記した必須成分としての塩基性薬物、有機酸および有機酸塩の他、吸収促進剤、可塑剤、脂溶性の疎水性高分子、粘着付与樹脂、および必要に応じて、その他の添加剤等を含有することができる。
吸収促進剤としては、皮膚での吸収促進作用が知られている化合物であればいずれのものも用いることができ、例えば、炭素鎖数6〜20の脂肪酸、脂肪族アルコール、脂肪酸エステルまたはエーテル類、芳香族系有機酸、芳香族系アルコール、芳香族系有機酸エステルまたはエーテル(以上は飽和、不飽和のいずれでもよく、環状、直鎖状分枝状のいずれでもよい)、さらに、乳酸エステル類、酢酸エステル類、モノテルペン系化合物、セスキテルペン系化合物、エイゾン(Azone)、エイゾン(Azone)誘導体、グリセリン脂肪酸エステル類、ソルビタン脂肪酸エステル類(Span系)ポリソルベート系(Tween系)、ポリエチレングリコール脂肪酸エステル類、ポリオキシエチレン硬化ヒマシ油系(HCO系)、ショ糖脂肪酸エステル類等が挙げられる。
上記吸収促進剤の好ましい例としては、カプリル酸、カプリン酸、カプロン酸、ラウリン酸、ミリスチン酸、パルミチン酸、ステアリン酸、オレイン酸、リノール酸、リノレン酸、ラウリルアルコール、ミリスチルアルコール、オレイルアルコール、セチルアルコール、ラウリン酸メチル、ミリスチン酸イソプロピル、ミリスチン酸ミリスチル、ミリスチン酸オクチルドデシル、パルミチン酸セチル、サリチル酸、サリチル酸メチル、サリチル酸エチレングリコール、ケイ皮酸、ケイ皮酸メチル、クレゾール、乳酸セチル、酢酸エチル、酢酸プロピル、ゲラニオール、チモール、オイゲノール、テルピネオール、l−メントール、ボルネオロール、d−リモネン、イソオイゲノール、イソボルネオール、ネロール、dl−カンフル、グリセリンモノラウレート、グリセリンモノオレエート、ソルビタンモノラウレート、ショ糖モノラウレート、ポリソルベート20、プロピレングリコール、ポリエチレングリコールモノラウレート、ポリエチレングリコールモノステアレート、HCO−60、ピロチオデカンが挙げられ、特に好ましい例としてラウリルアルコール、l−メントール、プロピレングリコール、ピロチオデカンが挙げられる。
これらの吸収促進剤は1種類を単独で用いても、2種類以上を組み合わせて用いてもよい。また、吸収促進剤の配合量は、外用貼付剤としての充分な透過性および発赤、浮腫等の皮膚への刺激性等を考慮して、粘着層の組成全体の質量に基づいて、0.01〜20質量%とすることが好ましく、さらに好ましくは0.05〜10質量%であり、特に好ましくは0.1〜5質量%の量である。
本発明の外用貼付剤の粘着層に用いることができる可塑剤としては、石油系オイル(例えば、パラフィン系プロセスオイル、ナフテン系プロセスオイル、芳香族系プロセスオイル等)、スクワラン、スクワレン、植物系オイル(例えば、オリーブ油、ツバキ油、ひまし油、 トール油、ラッカセイ油)、シリコンオイル、二塩基酸エステル(例えば、ジブチルフタレート、ジオクチルフタレート等)、液状ゴム(例えば、ポリブテン、液状イソプレンゴム)、ジエチレングリコール、ポリエチレングリコール、サリチル酸グリコール、プロピレングリコール、ジプロピレングリコール、トリアセチン、クエン酸トリエチル、クロタミトン、セバシン酸ジエチル等が挙げられる。これらの中でも、特に流動パラフィン、液状ポリブテン、サリチル酸グリコール、クロタミトンが好ましい。
これらの可塑剤は1種類を単独で用いても、2種類以上を組み合わせて用いてもよい。また、可塑剤の粘着層の組成全体に基づく配合量は、充分な透過性および貼付製剤としての充分な凝集力の維持を考慮して、合計で10〜70質量%とすることが好ましく、さらに好ましくは10〜60質量%であり、特に好ましくは10〜50質量%である。
本発明の外用貼付剤の粘着層に用いることができる脂溶性の疎水性高分子としては、スチレン−イソプレン−スチレンブロック共重合体(以下、「SIS」と略記する。)、イソプレンゴム、ポリイソブチレン(以下、「PIB」と略記する。)、スチレン−ブタジエン−スチレンブロック共重合体(以下、「SBS」と略記する。)、スチレン−ブタジエンゴム(以下、「SBR」と略記する。)アクリル系ポリマー(2−エチルヘキシルアクリレート、酢酸ビニル、メタクリレート、メトキシエチルアクリレートおよびアクリル酸からなる群から選ばれる少なくとも2種の共重合体)を挙げることができる。これらの中でも特に、SIS、PIB、これら2種のブレンドおよびアクリル系ポリマーが好ましい。
これらの疎水性高分子は1種類を単独で用いても、2種類以上を組み合わせて用いてもよい。また、疎水性高分子の粘着層の組成全体の質量に基づく配合量は、粘着剤層の形成および充分な透過性を考慮して、SIS、PIB等の場合は、10〜60質量%が好ましく、さらに好ましくは15〜50質量%であり、特に好ましくは18〜40質量%の量である。同様にアクリル系ポリマーの場合は、10〜98質量%が好ましく、さらに好ましくは20〜98質量%であり、特に好ましくは30〜98質量%である。
本発明の外用貼付剤の粘着層において用いることができる粘着付与樹脂としては、ロジン誘導体(例えば、ロジン、ロジンのグリセリンエステル、水添ロジン、水添ロジンのグリセリンエステル、ロジンのペンタエリストールエステル等)、脂環族飽和炭化水素樹脂、脂肪族系炭化水素樹脂、テルペン樹脂、マレイン酸レジン等が挙げられる。これらの中でも特に、水添ロジンのグリセリンエステル、脂環族飽和炭化水素樹脂、脂肪族系炭化水素樹脂、テルペン樹脂が好ましい。
これらの粘着付与樹脂は、1種類を単独で用いても2種類以上を組み合わせて用いてもよい。また、粘着付与樹脂の粘着層の組成全体に基づく配合量は、貼付剤としての充分な粘着力および剥離時の皮膚への刺激性を考慮して、10〜70質量%とすることが好ましく、さらに好ましくは15〜60質量%であり、特に好ましくは20〜50質量%である。
また、本発明の外用貼付剤の粘着層には、必要に応じて、抗酸化剤、充填剤、架橋剤、防腐剤、紫外線吸収剤等の添加剤を用いることができる。
抗酸化剤としては、トコフェロールおよびこれらのエステル誘導体、アスコルビン酸、アスコルビン酸ステアリン酸エステル、ノルジヒトログアヤレチン酸、ジブチルヒドロキシトルエン(BHT)、ブチルヒドロキシアニソール等を用いることができる。
充填剤としては、炭酸カルシウム、炭酸マグネシウム、ケイ酸塩(例えば、ケイ酸アルミニウム、ケイ酸マグネシウム等)、ケイ酸、硫酸バリウム、硫酸カルシウム、亜鉛酸カルシウム、酸化亜鉛、酸化チタン等を用いることができる。
架橋剤としては、アミノ樹脂、フェノール樹脂、エポキシ樹脂、アルキド樹脂、不飽和ポリエステル等の熱硬化性樹脂、イソシアネート化合物、ブロックイソシアネート化合物、有機系架橋剤、金属または金属化合物等の無機系架橋剤を用いることができる。
防腐剤としては、パラオキシ安息香酸エチル、パラオキシ安息香酸プロピル、パラオキシ安息香酸ブチル等を用いることができる。
紫外線吸収剤としては、p−アミノ安息香酸誘導体、アントラニル酸誘導体、サリチル酸誘導体、クマリン誘導体、アミノ酸系化合物、イミダゾリン誘導体、ピリミジン誘導体、ジオキサン誘導体等を用いることができる。
このような抗酸化剤、充填剤、架橋剤、防腐剤、紫外線吸収剤等の添加剤の配合量は、本発明の外用貼付剤の粘着層の組成全体の質量に基づいて、合計で、10質量%以下とすることが好ましく、さらに好ましくは5質量%以下であり、特に好ましくは2質量%以下である。
このような組成を有する本発明の外用貼付剤の製造方法は限定されず、いずれの方法によっても製造することができる。例えば、薬物を含む基剤組成を熱融解させ、離型紙または支持体に塗工後、支持体または離型紙と張り合わせて本外用貼付剤を得ることができる。また、薬物を含む基剤成分をトルエン、ヘキサン、酢酸エチル等の溶媒に溶解させ、離型紙または支持体上に伸展して溶剤を乾燥除去後、支持体または離型紙と張り合わせて本外用貼付剤を得ることができる。
本発明の外用貼付剤は水を含有しない非水系外用貼付剤であることが好ましい。
なお、本発明の外用貼付剤は、上記のような塩基性薬物、有機酸塩および有機酸を含むものであれば、その他の構成や各構成部分の素材は、いずれの種類のものであってもよい。
粘着層を支持するために設けることができる支持体層は、伸縮性または非伸縮性の支持体を用いて形成することができる。支持体としては、例えば布、不織布、ポリウレタン、ポリエステル、ポリ酢酸ビニル、ポリ塩化ビニリデン、ポリエチレン、ポリエチレンテレフタレート、アルミニウムシート等、またはそれらの複合素材から選択して用いることができる。
また粘着層上に設けることができる離型紙層は、例えば、粘着層との接触面にシリコーン処理されたポリエチレンテレフタレート、ポリエステル、ポリ塩化ビニル、ポリ塩化ビニリデン等のフィルム、または上質紙等とポリオレフィンとのラミネートフィルム等から選択して用いることができる。
実施例
以下、実施例を示して、本発明をさらに具体的に説明する。尚、実施例、比較例および試験例において、「%」は、全て「質量%」を意味するものとする。
(実施例1)
酢酸ナトリウム 1.0%
酒石酸 0.5%
アクリル系粘着ポリマー 93.5%
(PE−300:日本カーバイド社製)
イソシアネート系架橋剤 1.0%
(CK−100:日本カーバイド社製)
ピロチオデカン 2.0%
塩酸チザニジン 2.0%
−−−−−−−−−−−−−−−−−−−−−−−−−−−−−−−−−
全量 100.0%
これらの組成中、酒石酸、酢酸ナトリウム、ピロチオデカンおよび塩酸チザニジンを酢酸エチルに加え、室温で攪拌、溶解した後、アクリル系粘着ポリマー酢酸エチル溶液およびイソシアネート系架橋剤を添加して攪拌し、ポリエチレンテレフタレートフィルム(PET:30μm)上に伸展し、90℃で15分間熱架橋し、50μmの粘着層を得て、次いで本発明の外用貼付剤を得た。
(実施例2)
酢酸ナトリウム 9.0%
乳酸 2.0%
流動パラフィン 14.0%
ロジン系粘着付与剤 29.0%
(KE−311:荒川化学工業社製)
PIB 13.0%
SIS 18.0%
塩酸オキシブチニン 15.0%
−−−−−−−−−−−−−−−−−−−−−−−−−−−−−−−−
全量 100.0%
これらの組成中、酢酸ナトリウム、乳酸、塩酸オキシブチニン以外の成分をトルエンに溶解、混合した後、残りの成分を添加し、均一になるまで分散させた後、PETフィルム(30μm)上に粘着層が50μmとなるように伸展し、本発明の外用貼付剤を得た。
(実施例3)
酢酸ナトリウム 9.0%
クエン酸 2.5%
流動パラフィン 10.5%
ポリテルペン樹脂系粘着付与剤 32.0%
(アルコンP−100:荒川化学工業社製)
PIB 13.0%
SIS 18.0%
塩酸オキシブチニン 15.0%
−−−−−−−−−−−−−−−−−−−−−−−−−−−−−−−−
全量 100.0%
これらの組成中、酢酸ナトリウム、クエン酸および塩酸オキシブチニン以外の成分をトルエンに溶解、混合した後、残りの成分を添加し、均一になるまで分散させた後、PETフィルム(30μm)上に粘着層が50μmとなるように伸展し、本発明の外用貼付剤を得た。
(実施例4)
酢酸ナトリウム 1.0%
リンゴ酸 0.3%
流動パラフィン 27.4%
ロジン系粘着付与剤 27.5%
(KE−311:荒川化学工業社製)
PIB 12.0%
SIS 22.3%
ピロチオデカン 3.0%
クロタミトン 5.0%
BHT 0.5%
塩酸チザニジン 1.0%
−−−−−−−−−−−−−−−−−−−−−−−−−−−−−−−−
全量 100.0%
これらの組成中、酢酸ナトリウム、リンゴ酸、塩酸チザニジン以外の成分をシクロヘキサンに溶解、混合した後、残りの成分を添加し、均一になるまで分散させた後、PETフィルム(30μm)上に粘着層が50μmとなるように伸展し、本発明の外用貼付剤を得た。
(実施例5)
酢酸ナトリウム 1.0%
安息香酸 0.3%
流動パラフィン 27.4%
ロジン系粘着付与剤 27.5%
(KE−311:荒川化学工業社製)
PIB 12.0%
SIS 22.3%
ピロチオデカン 3.0%
クロタミトン 5.0%
BHT 0.5%
塩酸チザニジン 1.0%
−−−−−−−−−−−−−−−−−−−−−−−−−−−−−−−−−
全量 100.0%
これらの組成中、酢酸ナトリウム、安息香酸、塩酸チザニジン以外の成分をシクロヘキサンに溶解、混合した後、残りの成分を添加し、均一になるまで分散させた後、PETフィルム(30μm)上に粘着層が50μmとなるように伸展し、本発明の外用貼付剤を得た。
(実施例6)
酢酸ナトリウム 1.0%
サリチル酸 0.3%
流動パラフィン 27.4%
ロジン系粘着付与剤 27.5%
(KE−311:荒川化学工業社製)
PIB 12.0%
SIS 22.3%
ピロチオデカン 3.0%
クロタミトン 5.0%
BHT 0.5%
塩酸チザニジン 1.0%
−−−−−−−−−−−−−−−−−−−−−−−−−−−−−−−−
全量 100.0%
これらの組成中、酢酸ナトリウム、サリチル酸、塩酸チザニジン以外の成分をシクロヘキサンに溶解、混合した後、残りの成分を添加し、均一になるまで分散させた後、PETフィルム(30μm)上に粘着層が50μmとなるように伸展し、本発明の外用貼付剤を得た。
(比較例1〜6)
比較例1〜6はそれぞれ、実施例1〜6の各実施例に対応して行い、実施例1〜6において用いられた酢酸ナトリウムを配合しないこと以外は、それぞれ実施例1〜6と同様にして外用貼付剤を得た。
(比較例7〜9)
比較例7〜9はそれぞれ、実施例1〜3の各実施例に対応して行い、実施例1〜3において用いられた有機酸を配合しないこと以外は、それぞれ実施例1〜3と同様にして外用貼付剤を得た。
(比較例10)
比較例10は、実施例4に対応しており、実施例4において用いられた有機酸を配合しないこと以外は同様にして、外用貼付剤を得た。
(試験例1:In vitro経皮吸収性試験)
ヘアレスマウス(6〜9週齢)の背部皮膚を摘出した後、真皮側の脂肪を注意深く取り除き、真皮側がレセプター相となるように、フロースルーセルに装着した。尚、フロースルーセルには37℃の水をレセプター相の外周部に循環させた。この摘出皮膚の角質層側に実施例1〜6および比較例1〜10の各貼付剤(製剤の適用面積は5cm2)を貼付し、レセプター相である生理食塩水を1時間当たり約5mlで流した。2時間毎に24時間までサンプリングを行い、流出するレセプター相の流量を正確に測定した。その後、高速液体クロマトグラフ法によりレセプター相の薬物濃度を測定し、累積透過量[Q]を下記式に従い算出した。
累積透過量[Q](μg/cm2)
=[薬物濃度(μg/ml)×流量(ml)]/製剤の適用面積(cm2)
皮膚透過速度[flux]は、単位時間当たりの透過量の変化量として定義され、時間tにより
flux(μg/cm2/hr)=ΔQ(μg/cm2)/Δt(hr)
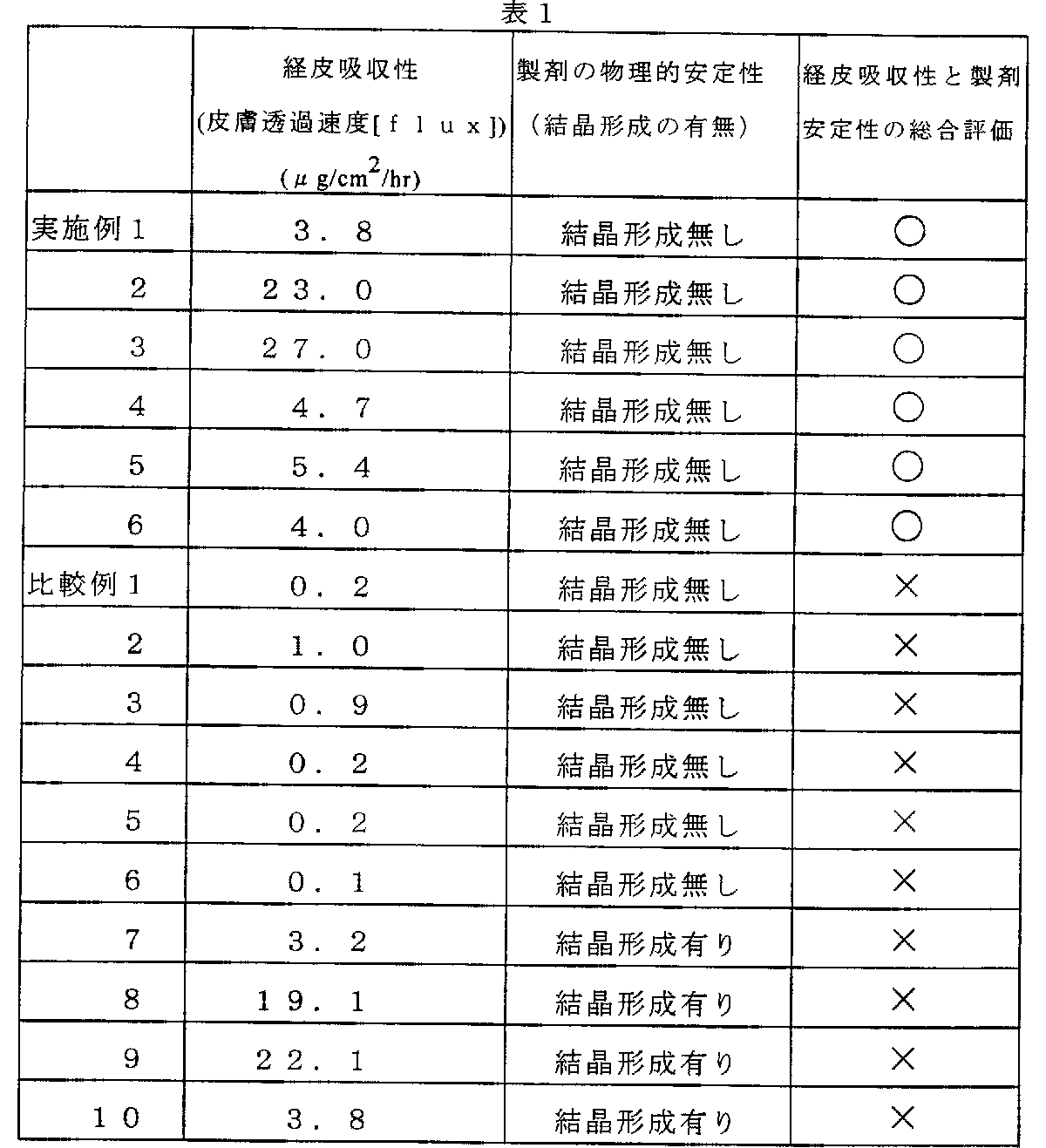
と表される。Flux値が大きい製剤は、経皮吸収性に優れたものと認められる。結果を表1に示す。
(試験例2:製剤安定性試験)
実施例1〜6および比較例1〜10で得られた各外用貼付剤を、25℃の条件下で3ヶ月保存した後、肉眼で観察し、結晶形成の有無を調べた。経時的に結晶が形成すると、貼付剤の品質の可否判断である外観の性状が変化するので、医薬品として安定なものとは認められない。また、結晶が形成すると、放出特性および粘着物性が変化するため、不安定な製剤と判断した。結果を表1に示す。
・経皮吸収性と製剤安定性の総合評価
実施例1〜6および比較例1〜10について、上記試験例1〜2の結果を鑑みて、経皮吸収性と安定性のどちらも良好なものを○、どちらか一方のみが良好なものといずれも良好でないものを×とした。結果を表1に示す。
表1に示される結果から明らかなように、塩基性薬物と有機酸と有機酸塩を組み合わせて用いた実施例1〜6の外用貼付剤は、経皮吸収性および安定性がともに優れたものであった。これに対して、塩基性薬物と有機酸のみを組み合わせて用いた比較例1〜6の外用貼付剤は、安定性は良好であったものの、経皮吸収性は著しく劣っていた。さらに、塩基性薬物と有機酸塩のみを組み合わせて用いた比較例7〜10の外用貼付剤は、経皮吸収性は良好であったものの、安定性が著しく劣っていた。
産業上の利用可能性
本発明によれば、薬物の経皮吸収性が高く、しかも安定性に優れた塩基性薬物含有の外用貼付剤が提供される。
Claims (17)
- オキシブチニン酸付加塩、クエン酸および有機酸塩を必須成分として含有することを特徴とする水を含有しない外用貼付剤。
- 有機酸塩が、カルボン酸の金属塩であることを特徴とする請求の範囲第1項に記載の水を含有しない外用貼付剤。
- 有機酸塩が、酢酸ナトリウムであることを特徴とする請求の範囲第1または2項に記載の水を含有しない外用貼付剤。
- 粘着層の組成全体の質量に基づいて、オキシブチニン酸付加塩0.1〜20質量%、クエン酸0.01〜20質量%および有機酸塩0.01〜20質量%を含有することを特徴とする請求の範囲第1項に記載の水を含有しない外用貼付剤。
- 粘着層の組成全体の質量に基づいて、オキシブチニン酸付加塩1〜15質量%、クエン酸0.3〜2.5質量%、および有機酸塩1.0〜9.0質量%を含有することを特徴とする請求の範囲第1項に記載の水を含有しない外用貼付剤。
- オキシブチニン酸付加塩と有機酸塩の配合比が、5:1〜1:5(当量比)であることを特徴とする請求の範囲第1項に記載の水を含有しない外用貼付剤。
- オキシブチニン酸付加塩とクエン酸の配合比が、5:1〜1:5(当量比)であることを特徴とする請求の範囲第1項に記載の水を含有しない外用貼付剤。
- クエン酸と有機酸塩の配合比が、3:1〜1:20(当量比)であることを特徴とする請求の範囲第1項に記載の水を含有しない外用貼付剤。
- オキシブチニン酸付加塩が、塩酸オキシブチニンであることを特徴とする請求項の範囲第1〜8項のいずれかに記載の水を含有しない外用貼付剤。
- オキシブチニン酸付加塩、クエン酸および有機酸塩を必須成分として得られることを特徴とする水を含有しない外用貼付剤。
- 有機酸塩が、カルボン酸の金属塩であることを特徴とする請求の範囲第10項に記載の水を含有しない外用貼付剤。
- 粘着層の組成全体の質量に基づいて、オキシブチニン酸付加塩0.1〜20質量%、クエン酸0.01〜20質量%および有機酸塩0.01〜20質量%を用いて得られることを特徴とする請求の範囲第10項に記載に水を含有しない外用貼付剤。
- 粘着層の組成全体の質量に基づいて、オキシブチニン酸付加塩1〜15質量%、クエン酸0.3〜2.5質量%、および有機酸塩1.0〜9.0質量%を必須成分として得られることを特徴とする請求の範囲第10項に記載の水を含有しない外用貼付剤。
- オキシブチニン酸付加塩と有機酸塩の配合比を、5:1〜1:5(当量比)として得られることを特徴とする請求の範囲第10項に記載の水を含有しない外用貼付剤。
- オキシブチニン酸付加塩とクエン酸の配合比を、5:1〜1:5(当量比)として得られることを特徴とする請求の範囲第10項に記載の水を含有しない外用貼付剤。
- クエン酸と有機酸塩の配合比を、3:1〜1:20(当量比)として得られることを特徴とする請求の範囲第10項に記載の水を含有しない外用貼付剤。
- オキシブチニン酸付加塩が、塩酸オキシブチニンであることを特徴とする請求の範囲第10〜16項のいずれかに記載の水を含有しない外用貼付剤。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2001511904A JP4703075B2 (ja) | 1999-07-27 | 2000-07-25 | 外用貼付剤 |
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP11-212921 | 1999-07-27 | ||
| JP21292199 | 1999-07-27 | ||
| JP1999212921 | 1999-07-27 | ||
| JP2001511904A JP4703075B2 (ja) | 1999-07-27 | 2000-07-25 | 外用貼付剤 |
| PCT/JP2000/004945 WO2001007018A1 (fr) | 1999-07-27 | 2000-07-25 | Bandes adhesives a usage externe |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010272021A Division JP5180277B2 (ja) | 1999-07-27 | 2010-12-06 | 外用貼付剤 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO2001007018A1 JPWO2001007018A1 (ja) | 2003-02-12 |
| JP4703075B2 true JP4703075B2 (ja) | 2011-06-15 |
Family
ID=16630500
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2001511904A Expired - Lifetime JP4703075B2 (ja) | 1999-07-27 | 2000-07-25 | 外用貼付剤 |
| JP2010272021A Expired - Lifetime JP5180277B2 (ja) | 1999-07-27 | 2010-12-06 | 外用貼付剤 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010272021A Expired - Lifetime JP5180277B2 (ja) | 1999-07-27 | 2010-12-06 | 外用貼付剤 |
Country Status (11)
| Country | Link |
|---|---|
| EP (1) | EP1201232B1 (ja) |
| JP (2) | JP4703075B2 (ja) |
| CN (1) | CN1222281C (ja) |
| AT (1) | ATE359767T1 (ja) |
| AU (1) | AU779027B2 (ja) |
| CA (1) | CA2378385C (ja) |
| DE (1) | DE60034458T2 (ja) |
| DK (1) | DK1201232T3 (ja) |
| ES (1) | ES2286028T3 (ja) |
| PT (1) | PT1201232E (ja) |
| WO (1) | WO2001007018A1 (ja) |
Families Citing this family (45)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| USRE44145E1 (en) | 2000-07-07 | 2013-04-09 | A.V. Topchiev Institute Of Petrochemical Synthesis | Preparation of hydrophilic pressure sensitive adhesives having optimized adhesive properties |
| US8840918B2 (en) | 2001-05-01 | 2014-09-23 | A. V. Topchiev Institute of Petrochemical Synthesis, Russian Academy of Sciences | Hydrogel compositions for tooth whitening |
| US20050215727A1 (en) | 2001-05-01 | 2005-09-29 | Corium | Water-absorbent adhesive compositions and associated methods of manufacture and use |
| US20050113510A1 (en) | 2001-05-01 | 2005-05-26 | Feldstein Mikhail M. | Method of preparing polymeric adhesive compositions utilizing the mechanism of interaction between the polymer components |
| WO2002087645A1 (en) | 2001-05-01 | 2002-11-07 | A.V. Topchiev Institute Of Petrochemical Synthesis | Hydrogel compositions |
| US8541021B2 (en) | 2001-05-01 | 2013-09-24 | A.V. Topchiev Institute Of Petrochemical Synthesis | Hydrogel compositions demonstrating phase separation on contact with aqueous media |
| US8206738B2 (en) | 2001-05-01 | 2012-06-26 | Corium International, Inc. | Hydrogel compositions with an erodible backing member |
| JP4865958B2 (ja) | 2001-05-23 | 2012-02-01 | 株式会社トクホン | 鎮痛抗炎症局所作用型の貼付剤 |
| JP4354678B2 (ja) * | 2002-08-28 | 2009-10-28 | 久光製薬株式会社 | 貼付剤 |
| JP4694967B2 (ja) * | 2003-07-31 | 2011-06-08 | 久光製薬株式会社 | 貼付剤 |
| JP4311728B2 (ja) * | 2003-12-10 | 2009-08-12 | ニチバン株式会社 | 経皮吸収型貼付剤 |
| WO2005074894A1 (en) | 2004-01-30 | 2005-08-18 | Corium International | Rapidly dissolving film for delivery of an active agent |
| JP4961207B2 (ja) * | 2004-04-21 | 2012-06-27 | 久光製薬株式会社 | 粘着基剤中の吸収促進剤の含有率を高めた外用貼付剤 |
| WO2005115355A1 (ja) * | 2004-05-28 | 2005-12-08 | Hisamitsu Pharmaceutical Co., Inc. | 貼付製剤 |
| WO2005117886A1 (ja) * | 2004-06-01 | 2005-12-15 | Hisamitsu Pharmaceutical Co., Inc. | 貼付剤 |
| JP5075334B2 (ja) * | 2004-11-22 | 2012-11-21 | 久光製薬株式会社 | 薬物含有貼付剤 |
| DE602005010812D1 (de) | 2004-11-22 | 2008-12-18 | Hisamitsu Pharmaceutical Co | Transdermales Pflaster enthaltend einen schmelzpunktsenkenden Hilfsstoff |
| US8771726B2 (en) | 2006-08-28 | 2014-07-08 | Hisamitsu Pharmaceutical Co., Inc | Nail patch |
| CA2703872C (en) | 2007-11-11 | 2015-11-03 | Medrx Co., Ltd. | Lidocaine tape preparation |
| AU2008327436B2 (en) | 2007-11-22 | 2013-09-05 | Medrx Co., Ltd. | External preparation composition comprising fatty acid-based ionic liquid as active ingredient |
| EP2258396B1 (en) * | 2008-03-03 | 2017-09-06 | Hisamitsu Pharmaceutical Co., Inc. | Transdermally absorbable preparation |
| EP2311498A4 (en) * | 2008-08-05 | 2013-07-24 | Medrx Co Ltd | EXTERNAL PREPARATION COMPRISING A FATTY ACID SALT OR A BENZOIC ACID SALT OF A PHARMACOLOGICALLY ACTIVE BASIC COMPONENT, AND PROCESS FOR PRODUCTION THEREOF |
| ITMI20081652A1 (it) * | 2008-09-16 | 2010-03-17 | Antica Ritrovati Medicinal I S A R M Srl Soc | Composizioni transdermiche per immunoterapia specifica iposensibilizzante |
| CA2751884C (en) | 2009-01-14 | 2018-09-25 | Corium International, Inc. | Transdermal administration of tamsulosin |
| AU2010331264B2 (en) | 2009-12-15 | 2014-05-01 | Teikoku Seiyaku Co., Ltd. | Transdermal preparation containing basic anti-inflammatory agent |
| WO2012029097A1 (ja) * | 2010-09-03 | 2012-03-08 | 株式会社ケイ・エム トランスダーム | 経皮吸収製剤 |
| JP6014813B2 (ja) * | 2010-09-03 | 2016-10-26 | 株式会社 ケイ・エム トランスダーム | 経皮吸収製剤および皮膚貼付用粘着シート |
| EP2700401B1 (en) | 2011-04-18 | 2020-01-15 | Hisamitsu Pharmaceutical Co., Inc. | Method for producing adhesive patch, and adhesive patch |
| US11123305B2 (en) | 2012-07-26 | 2021-09-21 | Hisamitsu Pharmaceutical Co., Inc. | Patch |
| US10493156B2 (en) | 2012-07-26 | 2019-12-03 | Hisamitsu Pharmaceutical Co., Inc. | Patch and method for producing the same |
| KR102013477B1 (ko) * | 2012-07-26 | 2019-08-22 | 히사미쓰 세이야꾸 가부시키가이샤 | 첩부제 |
| AU2013305563B2 (en) * | 2012-08-24 | 2018-09-27 | Integurx Therapeutics, Llc | Chemical compositions and methods for enhancing transdermal delivery of therapeutic agents |
| ES2710548T3 (es) * | 2012-10-11 | 2019-04-25 | Hisamitsu Pharmaceutical Co | Parche transdérmico |
| JP5270035B1 (ja) | 2012-12-06 | 2013-08-21 | 久光製薬株式会社 | 貼付剤及びその製造方法 |
| JP5307931B1 (ja) | 2012-12-27 | 2013-10-02 | 久光製薬株式会社 | 貼付剤及びその製造方法 |
| WO2014174564A1 (ja) * | 2013-04-22 | 2014-10-30 | 祐徳薬品工業株式会社 | メマンチン含有経皮吸収型貼付製剤 |
| JP5415645B1 (ja) | 2013-06-28 | 2014-02-12 | 久光製薬株式会社 | 貼付剤の製造方法、貼付剤及び包装体 |
| EP4122460A1 (en) | 2015-01-09 | 2023-01-25 | Chase Pharmaceuticals Corporation | Oxybutynin transdermal therapeutic system combination |
| JP6430871B2 (ja) * | 2015-03-23 | 2018-11-28 | 救急薬品工業株式会社 | 塩基性薬物塩含有経皮投与テープ剤の製造方法 |
| US9974858B2 (en) | 2015-08-29 | 2018-05-22 | Medrx Co., Ltd | Percutaneous absorption composition |
| WO2017037813A1 (ja) * | 2015-08-29 | 2017-03-09 | 株式会社メドレックス | 塩基性薬物とソルビン酸とを含有する経皮吸収組成物 |
| CN106344926A (zh) * | 2016-10-31 | 2017-01-25 | 魏舒畅 | 一种后交联凝胶贴膏基质及其制备含药物贴膏剂的方法 |
| JP6748237B2 (ja) | 2017-08-01 | 2020-08-26 | 久光製薬株式会社 | 貼付剤 |
| EP3960238A4 (en) * | 2019-04-24 | 2023-01-25 | MEDRx Co., Ltd. | Lidocaine-containing patch |
| JP7640498B2 (ja) * | 2021-08-04 | 2025-03-05 | 久光製薬株式会社 | ブロナンセリン含有貼付剤 |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0189861A2 (en) * | 1985-01-26 | 1986-08-06 | Showa Denko Kabushiki Kaisha | Percutaneous absorption accelerator for ionic water-soluble medicine |
| JPS62126119A (ja) * | 1985-11-26 | 1987-06-08 | Nitto Electric Ind Co Ltd | 消炎鎮痛用貼付剤 |
| JPH07157429A (ja) * | 1993-12-01 | 1995-06-20 | Hisamitsu Pharmaceut Co Inc | 貼付製剤 |
| WO1996016642A1 (en) * | 1994-11-29 | 1996-06-06 | Hisamitsu Pharmaceutical Co., Inc. | Matrix type patch preparation |
| WO1999024032A1 (en) * | 1997-11-10 | 1999-05-20 | Novo Nordisk A/S | Transdermal delivery of 3,4-diarylchromans |
| JP2933944B2 (ja) * | 1989-03-29 | 1999-08-16 | 日東電工株式会社 | 医療用貼付剤 |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4940456A (en) * | 1987-02-10 | 1990-07-10 | Dan Sibalis | Electrolytic transdermal delivery of proteins |
| JP3526887B2 (ja) * | 1993-04-23 | 2004-05-17 | 帝國製薬株式会社 | 消炎鎮痛外用貼付剤 |
| DE69528165T2 (de) * | 1994-04-21 | 2003-05-15 | Hisamitsu Pharmaceutical Co., Inc. | Transdermal verabreichbare grundlage und daraus hergestelltes transdermal verabreichbares arzneimittel |
| JP4167750B2 (ja) * | 1997-04-16 | 2008-10-22 | 久光製薬株式会社 | 経皮吸収用基剤及び該基剤を含有する経皮吸収製剤 |
| US7018647B1 (en) * | 1999-12-27 | 2006-03-28 | Teikoku Seiyaku Co., Ltd | Patches for external use |
-
2000
- 2000-07-25 DK DK00946484T patent/DK1201232T3/da active
- 2000-07-25 WO PCT/JP2000/004945 patent/WO2001007018A1/ja not_active Ceased
- 2000-07-25 AU AU60240/00A patent/AU779027B2/en not_active Expired
- 2000-07-25 JP JP2001511904A patent/JP4703075B2/ja not_active Expired - Lifetime
- 2000-07-25 EP EP00946484A patent/EP1201232B1/en not_active Expired - Lifetime
- 2000-07-25 PT PT00946484T patent/PT1201232E/pt unknown
- 2000-07-25 CN CN00812322.5A patent/CN1222281C/zh not_active Expired - Lifetime
- 2000-07-25 DE DE60034458T patent/DE60034458T2/de not_active Expired - Lifetime
- 2000-07-25 ES ES00946484T patent/ES2286028T3/es not_active Expired - Lifetime
- 2000-07-25 AT AT00946484T patent/ATE359767T1/de not_active IP Right Cessation
- 2000-07-25 CA CA002378385A patent/CA2378385C/en not_active Expired - Lifetime
-
2010
- 2010-12-06 JP JP2010272021A patent/JP5180277B2/ja not_active Expired - Lifetime
Patent Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0189861A2 (en) * | 1985-01-26 | 1986-08-06 | Showa Denko Kabushiki Kaisha | Percutaneous absorption accelerator for ionic water-soluble medicine |
| JPS62126119A (ja) * | 1985-11-26 | 1987-06-08 | Nitto Electric Ind Co Ltd | 消炎鎮痛用貼付剤 |
| JP2933944B2 (ja) * | 1989-03-29 | 1999-08-16 | 日東電工株式会社 | 医療用貼付剤 |
| JPH07157429A (ja) * | 1993-12-01 | 1995-06-20 | Hisamitsu Pharmaceut Co Inc | 貼付製剤 |
| WO1996016642A1 (en) * | 1994-11-29 | 1996-06-06 | Hisamitsu Pharmaceutical Co., Inc. | Matrix type patch preparation |
| JPH08157365A (ja) * | 1994-11-29 | 1996-06-18 | Hisamitsu Pharmaceut Co Inc | ケトチフェン含有経皮投与製剤 |
| WO1999024032A1 (en) * | 1997-11-10 | 1999-05-20 | Novo Nordisk A/S | Transdermal delivery of 3,4-diarylchromans |
Also Published As
| Publication number | Publication date |
|---|---|
| AU779027B2 (en) | 2005-01-06 |
| WO2001007018A1 (fr) | 2001-02-01 |
| JP2011079855A (ja) | 2011-04-21 |
| DE60034458D1 (de) | 2007-05-31 |
| CA2378385C (en) | 2009-01-27 |
| JP5180277B2 (ja) | 2013-04-10 |
| ATE359767T1 (de) | 2007-05-15 |
| DK1201232T3 (da) | 2007-08-13 |
| EP1201232A1 (en) | 2002-05-02 |
| CN1372463A (zh) | 2002-10-02 |
| PT1201232E (pt) | 2007-07-24 |
| ES2286028T3 (es) | 2007-12-01 |
| CA2378385A1 (en) | 2001-02-01 |
| DE60034458T2 (de) | 2008-01-03 |
| EP1201232B1 (en) | 2007-04-18 |
| CN1222281C (zh) | 2005-10-12 |
| EP1201232A4 (en) | 2004-02-25 |
| AU6024000A (en) | 2001-02-13 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4703075B2 (ja) | 外用貼付剤 | |
| JP4205778B2 (ja) | 貼付製剤 | |
| JP4643018B2 (ja) | 経皮吸収型製剤 | |
| US5866157A (en) | Matrix patch formulation | |
| US8420117B2 (en) | Patch formulation for external use | |
| JPWO2001007018A1 (ja) | 外用貼付剤 | |
| JP4057418B2 (ja) | 経皮吸収型製剤 | |
| KR100846642B1 (ko) | 첩부제 | |
| TWI428153B (zh) | Adhesive agent and its manufacturing method | |
| JPWO2005115355A1 (ja) | 貼付製剤 | |
| JP4694967B2 (ja) | 貼付剤 | |
| EP2258396A1 (en) | Transdermally absorbable preparation | |
| JPWO2007099966A1 (ja) | 経皮吸収型製剤 | |
| JP4961207B2 (ja) | 粘着基剤中の吸収促進剤の含有率を高めた外用貼付剤 | |
| JP2004083520A (ja) | 貼付剤 | |
| JP4271028B2 (ja) | 経皮吸収型製剤 | |
| JP4354678B2 (ja) | 貼付剤 | |
| JP4404251B2 (ja) | 経皮吸収型製剤 | |
| EP1679075A1 (en) | Transdermal preparations and method for relieving side effects in pergolide therapy |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20041207 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20080715 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20080912 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20090714 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20090911 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20100907 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20101206 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20110114 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20110301 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20110308 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 4703075 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20140318 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20210318 Year of fee payment: 10 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R153 | Grant of patent term extension |
Free format text: JAPANESE INTERMEDIATE CODE: R153 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| EXPY | Cancellation because of completion of term |