JP4489978B2 - 損傷細胞分類計数方法 - Google Patents
損傷細胞分類計数方法 Download PDFInfo
- Publication number
- JP4489978B2 JP4489978B2 JP2001002883A JP2001002883A JP4489978B2 JP 4489978 B2 JP4489978 B2 JP 4489978B2 JP 2001002883 A JP2001002883 A JP 2001002883A JP 2001002883 A JP2001002883 A JP 2001002883A JP 4489978 B2 JP4489978 B2 JP 4489978B2
- Authority
- JP
- Japan
- Prior art keywords
- damaged
- scattered light
- measured
- cells
- counting
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
- 238000000034 method Methods 0.000 title claims description 19
- 210000000265 leukocyte Anatomy 0.000 claims description 31
- 210000004027 cell Anatomy 0.000 claims description 24
- 210000003979 eosinophil Anatomy 0.000 claims description 12
- 210000004698 lymphocyte Anatomy 0.000 claims description 10
- 210000000440 neutrophil Anatomy 0.000 claims description 10
- 239000003219 hemolytic agent Substances 0.000 claims description 8
- 210000001616 monocyte Anatomy 0.000 claims description 8
- 239000002736 nonionic surfactant Substances 0.000 claims description 4
- 239000003093 cationic surfactant Substances 0.000 claims description 3
- 150000007524 organic acids Chemical class 0.000 claims description 3
- 239000007864 aqueous solution Substances 0.000 claims description 2
- 125000003118 aryl group Chemical group 0.000 claims description 2
- 239000000872 buffer Substances 0.000 claims description 2
- 238000004820 blood count Methods 0.000 claims 2
- 150000003839 salts Chemical class 0.000 claims 1
- 210000004369 blood Anatomy 0.000 description 25
- 239000008280 blood Substances 0.000 description 25
- 125000000217 alkyl group Chemical group 0.000 description 9
- 125000004432 carbon atom Chemical group C* 0.000 description 8
- 125000003342 alkenyl group Chemical group 0.000 description 7
- 238000005259 measurement Methods 0.000 description 5
- XNGIFLGASWRNHJ-UHFFFAOYSA-N phthalic acid Chemical compound OC(=O)C1=CC=CC=C1C(O)=O XNGIFLGASWRNHJ-UHFFFAOYSA-N 0.000 description 4
- 239000004065 semiconductor Substances 0.000 description 4
- 239000004094 surface-active agent Substances 0.000 description 4
- -1 urine Substances 0.000 description 4
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 201000010099 disease Diseases 0.000 description 3
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 3
- 210000003743 erythrocyte Anatomy 0.000 description 3
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 3
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 3
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- SNRUBQQJIBEYMU-UHFFFAOYSA-N Dodecane Natural products CCCCCCCCCCCC SNRUBQQJIBEYMU-UHFFFAOYSA-N 0.000 description 2
- QIAFMBKCNZACKA-UHFFFAOYSA-N N-benzoylglycine Chemical compound OC(=O)CNC(=O)C1=CC=CC=C1 QIAFMBKCNZACKA-UHFFFAOYSA-N 0.000 description 2
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 2
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical class C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 2
- 239000003146 anticoagulant agent Substances 0.000 description 2
- 229940127219 anticoagulant drug Drugs 0.000 description 2
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 2
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- 210000000170 cell membrane Anatomy 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 125000002704 decyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 2
- 238000010586 diagram Methods 0.000 description 2
- 125000003438 dodecyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 2
- 239000000203 mixture Substances 0.000 description 2
- 125000002347 octyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- 210000005259 peripheral blood Anatomy 0.000 description 2
- 239000011886 peripheral blood Substances 0.000 description 2
- 150000003242 quaternary ammonium salts Chemical class 0.000 description 2
- YGSDEFSMJLZEOE-UHFFFAOYSA-N salicylic acid Chemical compound OC(=O)C1=CC=CC=C1O YGSDEFSMJLZEOE-UHFFFAOYSA-N 0.000 description 2
- 238000000926 separation method Methods 0.000 description 2
- FDCJDKXCCYFOCV-UHFFFAOYSA-N 1-hexadecoxyhexadecane Chemical compound CCCCCCCCCCCCCCCCOCCCCCCCCCCCCCCCC FDCJDKXCCYFOCV-UHFFFAOYSA-N 0.000 description 1
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 1
- HVBSAKJJOYLTQU-UHFFFAOYSA-N 4-aminobenzenesulfonic acid Chemical compound NC1=CC=C(S(O)(=O)=O)C=C1 HVBSAKJJOYLTQU-UHFFFAOYSA-N 0.000 description 1
- 239000005711 Benzoic acid Substances 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 239000007995 HEPES buffer Substances 0.000 description 1
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 125000000304 alkynyl group Chemical group 0.000 description 1
- 238000002617 apheresis Methods 0.000 description 1
- XKRFYHLGVUSROY-UHFFFAOYSA-N argon Substances [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 1
- 229910052786 argon Inorganic materials 0.000 description 1
- 210000003651 basophil Anatomy 0.000 description 1
- 235000010233 benzoic acid Nutrition 0.000 description 1
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 1
- 238000010241 blood sampling Methods 0.000 description 1
- 238000009534 blood test Methods 0.000 description 1
- 210000001124 body fluid Anatomy 0.000 description 1
- 239000010839 body fluid Substances 0.000 description 1
- 210000001185 bone marrow Anatomy 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 238000003745 diagnosis Methods 0.000 description 1
- DDXLVDQZPFLQMZ-UHFFFAOYSA-M dodecyl(trimethyl)azanium;chloride Chemical compound [Cl-].CCCCCCCCCCCC[N+](C)(C)C DDXLVDQZPFLQMZ-UHFFFAOYSA-M 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 238000000684 flow cytometry Methods 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 125000005843 halogen group Chemical group 0.000 description 1
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 238000007689 inspection Methods 0.000 description 1
- 230000002934 lysing effect Effects 0.000 description 1
- QSHDDOUJBYECFT-UHFFFAOYSA-N mercury Chemical compound [Hg] QSHDDOUJBYECFT-UHFFFAOYSA-N 0.000 description 1
- 229910052753 mercury Inorganic materials 0.000 description 1
- 125000001421 myristyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- FJKROLUGYXJWQN-UHFFFAOYSA-N papa-hydroxy-benzoic acid Natural products OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 1
- 238000004321 preservation Methods 0.000 description 1
- 229960004889 salicylic acid Drugs 0.000 description 1
- 229950000244 sulfanilic acid Drugs 0.000 description 1
- 210000002700 urine Anatomy 0.000 description 1
- 238000011179 visual inspection Methods 0.000 description 1
Images
Landscapes
- Investigating Or Analysing Biological Materials (AREA)
Description
【発明の属する技術分野】
本発明はフローサイトメトリによる損傷細胞の分類計数に関する。
【0002】
【従来の技術】
臨床検査の分野において、白血球の分類計数を行うことは、疾患の診断を行う上できわめて有用な情報を得ることができる。例えば、通常、正常な末梢血中の白血球には、リンパ球、単球、好中球、好酸球、好塩基球の5つの正常白血球が一定の比率で存在する。疾患の存在により、これらの白血球の比率は変動されることがあり、これらの正常白血球を分類計数することにより、各白血球の比率を測定することは有用である。
【0003】
近年、医療費の削減により、一般病院では血液検査を検査センターなどに依頼することが多くなっている。従って、検査センターなどでは、採血後時間が経過した検体や保存状態が悪い検体が送られてくる場合がある。採血後時間が経過したり、保存状態が悪いと、白血球細胞は損傷を受けて、非常に細胞膜が壊れやすい状態になっている。
【0004】
従来、全自動白血球分類計数装置では、このような検体の白血球を正確に分類計数することができず、何らかの疾患の存在を認めるフラッグを出力していた。この場合、目視による再検を行う必要性が生じることになる。このようなことが頻繁に発生すると、検査の非効率化やコスト高を招く恐れがある。
【0005】
【発明が解決しようとする課題】
本発明は、採血後時間が経過した検体や保存状態が悪い検体でも、正確に白血球の分類計数が行うことができる方法を提供することを目的とする。
【0006】
【課題を解決するための手段】
本発明は以下の工程:
(1)試料を、血液試料中の赤血球を測定の障害とならない程度に溶解し、白血球および損傷細胞を測定に好適な状態にする溶血剤と混合する工程
(2)(1)で調製した試料をフローサイトメーターで測定し、少なくとも2つの散乱光を測定する工程
(3)(2)で測定した個々の細胞の散乱光信号から異なる散乱光を2軸として、2次元分布を得る工程、
(4)2次元分布から、正常な白血球を少なくとも4つに分類計数する工程
(5)2次元分布から、損傷リンパ球の領域を設定し、損傷リンパ球を分類計数する工程
(6)2次元分布から、損傷単球の領域を設定し、損傷単球を分類計数する工程
(7)2次元分布から、損傷好中球の領域を設定し、損傷好中球を分類計数する工程
(8)2次元分布から、損傷好酸球の領域を設定し、損傷好酸球を分類計数する工程
(9)(4)で測定したリンパ球数と(5)で測定した損傷リンパ球数を用いて、リンパ球数を補正する工程
(10)(4)で測定した単球数と(6)で測定した損傷単球数を用いて、単球数を補正する工程
(11)(4)で測定した好中球数と(7)で測定した損傷好中球数を用いて、好中球数を補正する工程
(12)(4)で測定した好酸球数と(8)で測定した損傷好酸球数を用いて、好酸球数を補正する工程。
からなる損傷細胞分類計数方法を提供する。
【0007】
【発明の実施の形態】
本発明でいう血液試料とは、末梢血液、骨髄液、尿、アフェレーシスで採取した血液試料など、白血球を含む体液試料をいう。
【0008】
本発明でいう損傷細胞とは、採血後時間が経過したり、保存状態が悪いために、細胞膜が壊れやすくなっている白血球のことをいう。
【0009】
本発明でいう、血液試料中の赤血球を測定の障害とならないように溶解し、白血球及び損傷細胞を測定に好適な状態にする溶血剤と混合する工程とは、血液試料を適当な溶血剤と混合する工程である。
【0010】
本工程の目的は、赤血球を測定の障害とならないように溶解するだけである。この目的に使用する溶血剤は、少なくとも一つのカチオン性界面活性剤、少なくとも一つのノニオン性界面活性剤、pHを一定に保つための緩衝剤を含むpH4.5〜11.0の水溶液である。
【0011】
カチオン性界面活性剤としては、4級アンモニウム塩型界面活性剤又はピリジニウム塩型界面活性剤が好ましい。4級アンモニウム塩型およびピリジニウム塩型界面活性剤は、
【0012】
【化1】
【0013】
〔R1は炭素数6〜18のアルキル又はアルケニル基、R2およびR3は炭素数1〜4のアルキル又はアルケニル基、R4は炭素数1〜4のアルキルおよびアルケニル基又はベンジル基、Xはハロゲン原子である。〕で表される全炭素数9〜30の界面活性剤が挙げられる。R1の炭素数6〜18のアルキル又はアルケニル基としてはへキシル、オクチル、デシル、ドデシル、テトラデシル等を挙げることができるが、とりわけオクチル、デシル、ドデシル等の直鎖のアルキル基が好ましい。また、R2およびR3の炭素数1〜4のアルキル、アルケニル基としては、メチル、エチル、プロピル、ブチル等を挙げることができるが、とりわけ、メチル、エチル、プロピル等の炭素数1〜3のアルキル基が好ましい。さらに、R4の炭素数1〜4のアルキルおよびアルケニル基としては、メチル、エチル、プロピル、ブチル等を挙げることができるが、とりわけ、メチル、エチル、プロピル等の炭素数1〜3のアルキル基が好ましい。
【0014】
ノニオン性界面活性剤としては以下の式のポリオキシエチレン系ノニオン界面活性剤が好ましい:R1−R2−(CH2CH2O)n−H〔式中、R1は炭素数8〜25のアルキル、アルケニル又はアルキニル基;R2はO、
【0015】
【化2】
またはCOO;nは10〜50の整数を表す。〕
【0016】
溶血剤の組成は特に限定されるものではないが、例えば、特開平6−20792号、特開平7−181177号に記載の溶血剤などが好適に使用される。
【0017】
さらに、少なくとも1つの、分子内に1つの芳香環を有する有機酸を含有することは、白血球および損傷細胞の散乱光強度分布を、分類に好適なように調整するために好適である。
【0018】
例えば、安息香酸、フタル酸、馬尿酸、サリチル酸、p−アミノベンゼンスルホン酸、ヘンゼンスルホン酸などが好適に使用できる。好ましくは0.1〜100mM、より好ましくは1〜50mM、さらに好ましくは10〜30mMの濃度範囲で使用できる。
【0019】
これらの有機酸を含有することにより、特に好酸球の散乱光強度が増加し、結果として、好中球と好酸球の分離が改善される。
【0020】
pHが4.5よりも低い場合、好酸球の分離が悪くなり、正常白血球を分画することが困難になる。pH11.0よりも高い場合は、白血球が損傷を受けやすくなり、好ましくない。
【0021】
本発明でいう散乱光とは、一般に市販されるフローサイトメーターで測定できる散乱光であり、側方散乱光、前方低角散乱光(受光角度0〜5度付近)、前方高角散乱光(5〜20度付近)等をいい、白血球の大きさもしくは内部構造情報を反映する散乱角度が選ばれる。
【0022】
異なる2つの散乱光の1つに前方散乱光(低角でも高角でもどちらでも良い)を使用すると、細胞の大きさに関する情報が得られる。
【0023】
フローサイトメーターの光源は、特に限定されず、例えば、アルゴンイオンレーザー、He/Neレーザー、赤色半導体レーザー、水銀アークランプなどが使用される。
【0024】
特に半導体レーザーは気体レーザーに比べ非常に安価であり、装置コストを大幅に下げることができるため、好適である。
【0025】
「測定した個々の細胞の散乱光信号から異なる散乱光を2軸として2次元分布を得る工程」とは、例えば、X軸に側方散乱光、Y軸に前方散乱光をとって2次元分布を描くことである。
【0026】
「2次元分布から、正常な白血球を少なくとも4つに分類計数する工程」とは、例えば、X軸に側方散乱光、Y軸に前方散乱光をとって、2次元分布を描くと、図1に示すように、各白血球細胞は細胞毎に集団を形成する。この集団を適当な解析ソフトで解析することにより、各白血球集団の数と割合を算出する。
【0027】
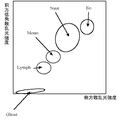
「2次元分布から、損傷白血球の領域を設定し、損傷白血球を分類計数する工程」とは、例えば、X軸に側方散乱光、Y軸に前方散乱光をとって、2次元分布を描くと、図2に示すように、損傷リンパ球(Damaged Lymph)は集団を形成する。この集団を適当な解析ソフトで解析することにより、損傷リンパ球集団の数と割合を算出する。損傷単球(Damaged Mono)、損傷好中球(Damaged Neut)、損傷好酸球(Damaged Eo)も同様にして、各集団の数と割合を算出する。
【0028】
【実施例】
実施例1 採血後時間が経過した場合
以下の組成の試薬を調製した。
HEPES(市販品) 10mM
フタル酸2Na(市販品) 20mM
BC30TX(ポリオキシエチレン(30)セチルエーテル) 1500ppm
(日光ケミカルズ(株))
ドデシルトリメチルアンモニウムクロライド(市販品) 550ppm
NaOHでpHを7.0に調整。
【0029】
上記試薬1.0mlに抗凝固剤処理した健常人の採血直後および採血後4℃で72時間経過した血液をそれぞれ30μlずつ加え、35℃で40秒間反応させた後、FCMで前方低角散乱光、側方散乱光を測定した。光源は633nmの赤色半導体レーザを使用した。
【0030】
図3にX軸に側方散乱光、Y軸に前方低角散乱光をとった採血直後のスキャッタグラムを示す。
【0031】
図4にX軸に側方散乱光、Y軸に前方低角散乱光をとった72時間後のスキャッタグラムを示す。
【0032】
図5に採血直後、本法による補正前、本法による補正後の各細胞比率を示す。本法による補正により採血後時間が経過した場合でも、採血直後と同様の結果が得られた。
【0033】
実施例2 保存状態が悪い場合
実施例1の試薬1.0mlに抗凝固剤処理した健常人の採血直後および室温で48時間保存した血液をそれぞれ30μlずつ加え、35℃で40秒間反応させた後、FCMで前方低角散乱光、側方散乱光を測定した。光源は633nmの赤色半導体レーザを使用した。
【0034】
図6にX軸に側方散乱光、Y軸に前方低角散乱光をとった採血直後のスキャッタグラムを示す。
【0035】
図7にX軸に側方散乱光、Y軸に前方低角散乱光をとった室温で保存した場合のスキャッタグラムを示す。
【0036】
図8に採血直後、本法による補正前、本法による補正後の各細胞比率を示す。本法による補正により保存状態が悪い場合でも、採血直後と同様の結果が得られた。
【0037】
【発明の効果】
本発明によれば、採血後時間が経過した検体や保存状態が悪い検体でも、正確に白血球の分類計数が行うことができる。
【図面の簡単な説明】
【図1】各白血球細胞の2次元分布図の模式図である。
【図2】損傷細胞が出現した場合の各白血球細胞の2次元分布図である。
【図3】本発明の実施例1における採血直後のスキャッタグラムである。
【図4】本発明の実施例1における4℃で72時間保存後のスキャッタグラムである。
【図5】本発明の実施例1における採血直後、本法による補正前、本法による補正後の各細胞比率である。
【図6】本発明の実施例2における採血直後のスキャッタグラムである。
【図7】本発明の実施例2における室温で48時間保存した場合のスキャッタグラムである。
【図8】本発明の実施例2における採血直後、本法による補正前、本法による補正後の各細胞比率である。
Claims (4)
- 以下の工程からなる損傷細胞分類計数方法。
(1)少なくとも一つのノニオン性界面活性剤、少なくとも一つのカチオン性界面活性剤、及びpHを一定に保つための緩衝剤を含むpH4.5〜11.0の水溶液である溶血剤と試料とを混合する工程
(2)(1)で調製した試料をフローサイトメータで測定し、少なくとも2つの散乱光を測定する工程
(3)(2)で測定した個々の細胞の散乱光信号から異なる散乱光を2軸として、2次元分布を得る工程、
(4)2次元分布から、正常な白血球を少なくとも4つに分類計数する工程
(5)2次元分布から、損傷細胞の領域を設定し、損傷細胞を分類計数する工程
(6)(4)で測定した白血球数と(5)で測定した損傷細胞数を用いて、白血球数を補正する工程。 - 白血球が、リンパ球、単球、好中球または好酸球であり、損傷細胞が、損傷リンパ球、損傷単球、損傷好中球または損傷好酸球である請求項1記載の損傷細胞分類計数方法。
- 溶血剤が、少なくとも1つの芳香環を有する有機酸もしくはその塩を含有する請求項1又は2に記載の損傷細胞分類計数方法。
- 散乱光の受光角度が、前方低角散乱光、前方高角散乱光、側方散乱光から選ばれる少なくとも2つである請求項1〜3のいずれか一項に記載の損傷細胞分類計数方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2001002883A JP4489978B2 (ja) | 2001-01-10 | 2001-01-10 | 損傷細胞分類計数方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2001002883A JP4489978B2 (ja) | 2001-01-10 | 2001-01-10 | 損傷細胞分類計数方法 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2002207038A JP2002207038A (ja) | 2002-07-26 |
| JP2002207038A5 JP2002207038A5 (ja) | 2008-02-14 |
| JP4489978B2 true JP4489978B2 (ja) | 2010-06-23 |
Family
ID=18871316
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2001002883A Expired - Lifetime JP4489978B2 (ja) | 2001-01-10 | 2001-01-10 | 損傷細胞分類計数方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP4489978B2 (ja) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2014209090A (ja) * | 2013-03-29 | 2014-11-06 | シスメックス株式会社 | 細胞分析方法及び装置 |
-
2001
- 2001-01-10 JP JP2001002883A patent/JP4489978B2/ja not_active Expired - Lifetime
Also Published As
| Publication number | Publication date |
|---|---|
| JP2002207038A (ja) | 2002-07-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP3886271B2 (ja) | 赤芽球の分類計数用試薬及び分類計数方法 | |
| JP4324552B2 (ja) | 白血球の分類計数方法 | |
| JP3048260B2 (ja) | 白血球分類計数用試料調製方法 | |
| JP4042925B2 (ja) | 幼若白血球の分類計数法 | |
| JP3830613B2 (ja) | 血液中の白血球及びヘモグロビン濃度測定試薬 | |
| US7749757B1 (en) | Stabilizing solution for cells and tissues | |
| JP5865009B2 (ja) | 活性化好中球の検出方法 | |
| JPH11507733A (ja) | 血液中の白血球の鑑別式決定のための試薬及び方法 | |
| EP3382035A1 (en) | Cellular analysis of body fluids | |
| JP2001258590A (ja) | 細菌の染色方法及び検出方法 | |
| JP2008003062A (ja) | 試料分析用試薬、試料分析用試薬キット及び試料分析方法 | |
| JP3345135B2 (ja) | 血液分析方法 | |
| JP2019090814A (ja) | サンプル分析のための方法、機器、及びシステム | |
| JP2002148261A (ja) | 異常細胞分類計数方法 | |
| JP4484375B2 (ja) | 異常細胞検出方法 | |
| Dervišević et al. | Red blood cell distribution width-to-platelet ratio inversely correlates with indicators of disease activity status in rheumatoid arthritis patients | |
| JP4338206B2 (ja) | 赤芽球の分類計数方法 | |
| JP4489978B2 (ja) | 損傷細胞分類計数方法 | |
| CN107976397A (zh) | 一种溶血剂的制备及其应用 | |
| JP2003344393A (ja) | 脳脊髄液などの体液試料をアッセイするための自動法およびそのための試薬 | |
| EP0259833B1 (en) | Reagent and method for classifying leukocytes by flow cytometry | |
| Burns et al. | Compendium of normal blood values for baboons, chimpanzees, and marmosets | |
| JP4107441B2 (ja) | 赤芽球の分類計数用試薬 | |
| JP4391489B2 (ja) | 血液中のヘモグロビン濃度測定方法 | |
| JP4354982B2 (ja) | 白血球の分類計数方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20071219 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20071219 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20100118 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20100126 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100209 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20100309 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20100401 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130409 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 4489978 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130409 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20160409 Year of fee payment: 6 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| EXPY | Cancellation because of completion of term |