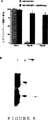JP4214239B2 - 二機能性レトロウイルス/アデノウイルス系 - Google Patents
二機能性レトロウイルス/アデノウイルス系 Download PDFInfo
- Publication number
- JP4214239B2 JP4214239B2 JP52385598A JP52385598A JP4214239B2 JP 4214239 B2 JP4214239 B2 JP 4214239B2 JP 52385598 A JP52385598 A JP 52385598A JP 52385598 A JP52385598 A JP 52385598A JP 4214239 B2 JP4214239 B2 JP 4214239B2
- Authority
- JP
- Japan
- Prior art keywords
- retroviral
- vector
- cells
- gene
- adenoviral
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 241000701161 unidentified adenovirus Species 0.000 title claims description 71
- 230000001588 bifunctional effect Effects 0.000 title claims description 50
- 241001430294 unidentified retrovirus Species 0.000 title description 81
- 239000013598 vector Substances 0.000 claims abstract description 325
- 230000001177 retroviral effect Effects 0.000 claims abstract description 304
- 108090000623 proteins and genes Proteins 0.000 claims abstract description 94
- 239000002245 particle Substances 0.000 claims abstract description 73
- 238000001727 in vivo Methods 0.000 claims abstract description 49
- 230000001225 therapeutic effect Effects 0.000 claims abstract description 13
- 238000012239 gene modification Methods 0.000 claims abstract 2
- 230000010076 replication Effects 0.000 claims description 21
- 230000002950 deficient Effects 0.000 claims description 20
- 108700008625 Reporter Genes Proteins 0.000 claims description 14
- 210000004072 lung Anatomy 0.000 claims description 12
- 102000004169 proteins and genes Human genes 0.000 claims description 10
- 108700004025 env Genes Proteins 0.000 claims description 8
- 239000003550 marker Substances 0.000 claims description 7
- 239000000203 mixture Substances 0.000 claims description 7
- 210000002216 heart Anatomy 0.000 claims description 6
- 208000019693 Lung disease Diseases 0.000 claims description 5
- 241000711975 Vesicular stomatitis virus Species 0.000 claims description 5
- 101150030339 env gene Proteins 0.000 claims description 5
- 208000019622 heart disease Diseases 0.000 claims description 5
- 208000014951 hematologic disease Diseases 0.000 claims description 5
- 238000010361 transduction Methods 0.000 abstract description 51
- 230000026683 transduction Effects 0.000 abstract description 51
- 238000004519 manufacturing process Methods 0.000 abstract description 33
- 238000011065 in-situ storage Methods 0.000 abstract description 17
- 230000002792 vascular Effects 0.000 abstract description 5
- 239000013603 viral vector Substances 0.000 abstract description 4
- 238000010276 construction Methods 0.000 abstract description 3
- 238000001476 gene delivery Methods 0.000 abstract 1
- 230000005017 genetic modification Effects 0.000 abstract 1
- 235000013617 genetically modified food Nutrition 0.000 abstract 1
- 238000004806 packaging method and process Methods 0.000 abstract 1
- 210000004027 cell Anatomy 0.000 description 258
- 230000010354 integration Effects 0.000 description 82
- 239000013612 plasmid Substances 0.000 description 54
- 230000014509 gene expression Effects 0.000 description 49
- 238000004458 analytical method Methods 0.000 description 38
- 238000000034 method Methods 0.000 description 37
- 239000005090 green fluorescent protein Substances 0.000 description 36
- 108020004414 DNA Proteins 0.000 description 34
- 108010043121 Green Fluorescent Proteins Proteins 0.000 description 34
- 102000004144 Green Fluorescent Proteins Human genes 0.000 description 34
- 238000012546 transfer Methods 0.000 description 28
- 238000001890 transfection Methods 0.000 description 24
- 208000015181 infectious disease Diseases 0.000 description 22
- 230000006698 induction Effects 0.000 description 21
- 239000006228 supernatant Substances 0.000 description 21
- 230000005540 biological transmission Effects 0.000 description 20
- 241000699666 Mus <mouse, genus> Species 0.000 description 18
- 241001465754 Metazoa Species 0.000 description 15
- 230000001566 pro-viral effect Effects 0.000 description 15
- 102000005962 receptors Human genes 0.000 description 14
- 230000001052 transient effect Effects 0.000 description 14
- 230000001404 mediated effect Effects 0.000 description 13
- 238000012761 co-transfection Methods 0.000 description 12
- 239000012634 fragment Substances 0.000 description 12
- 210000000056 organ Anatomy 0.000 description 12
- 239000013605 shuttle vector Substances 0.000 description 12
- 206010028980 Neoplasm Diseases 0.000 description 11
- 210000004185 liver Anatomy 0.000 description 10
- 241000700605 Viruses Species 0.000 description 9
- 210000005229 liver cell Anatomy 0.000 description 9
- 230000007774 longterm Effects 0.000 description 9
- 210000004872 soft tissue Anatomy 0.000 description 9
- OPIFSICVWOWJMJ-AEOCFKNESA-N 5-bromo-4-chloro-3-indolyl beta-D-galactoside Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1OC1=CNC2=CC=C(Br)C(Cl)=C12 OPIFSICVWOWJMJ-AEOCFKNESA-N 0.000 description 8
- 238000012937 correction Methods 0.000 description 8
- 239000003102 growth factor Substances 0.000 description 8
- 229930193140 Neomycin Natural products 0.000 description 7
- 238000003556 assay Methods 0.000 description 7
- 229960004927 neomycin Drugs 0.000 description 7
- 239000000047 product Substances 0.000 description 7
- 206010038997 Retroviral infections Diseases 0.000 description 6
- 239000002299 complementary DNA Substances 0.000 description 6
- 230000029087 digestion Effects 0.000 description 6
- 230000012010 growth Effects 0.000 description 6
- 238000000338 in vitro Methods 0.000 description 6
- 210000001519 tissue Anatomy 0.000 description 6
- 230000002463 transducing effect Effects 0.000 description 6
- 108090000288 Glycoproteins Proteins 0.000 description 5
- 102000003886 Glycoproteins Human genes 0.000 description 5
- 206010033128 Ovarian cancer Diseases 0.000 description 5
- 206010061535 Ovarian neoplasm Diseases 0.000 description 5
- 210000000981 epithelium Anatomy 0.000 description 5
- 238000002474 experimental method Methods 0.000 description 5
- 230000002068 genetic effect Effects 0.000 description 5
- 230000002688 persistence Effects 0.000 description 5
- 239000013641 positive control Substances 0.000 description 5
- 230000003362 replicative effect Effects 0.000 description 5
- 108091008146 restriction endonucleases Proteins 0.000 description 5
- 238000010186 staining Methods 0.000 description 5
- 230000002123 temporal effect Effects 0.000 description 5
- 238000013459 approach Methods 0.000 description 4
- 230000004663 cell proliferation Effects 0.000 description 4
- 238000011161 development Methods 0.000 description 4
- 230000000694 effects Effects 0.000 description 4
- 238000001415 gene therapy Methods 0.000 description 4
- 230000001744 histochemical effect Effects 0.000 description 4
- 230000001939 inductive effect Effects 0.000 description 4
- 238000011081 inoculation Methods 0.000 description 4
- 230000003993 interaction Effects 0.000 description 4
- 150000007523 nucleic acids Chemical class 0.000 description 4
- 238000011580 nude mouse model Methods 0.000 description 4
- 230000008569 process Effects 0.000 description 4
- 238000010561 standard procedure Methods 0.000 description 4
- 238000007400 DNA extraction Methods 0.000 description 3
- 102100027723 Endogenous retrovirus group K member 6 Rec protein Human genes 0.000 description 3
- 101710121417 Envelope glycoprotein Proteins 0.000 description 3
- 241000699660 Mus musculus Species 0.000 description 3
- 238000002105 Southern blotting Methods 0.000 description 3
- 230000000052 comparative effect Effects 0.000 description 3
- 108010078428 env Gene Products Proteins 0.000 description 3
- 210000002950 fibroblast Anatomy 0.000 description 3
- 238000001943 fluorescence-activated cell sorting Methods 0.000 description 3
- 239000001963 growth medium Substances 0.000 description 3
- 230000001976 improved effect Effects 0.000 description 3
- 239000002609 medium Substances 0.000 description 3
- 108020004707 nucleic acids Proteins 0.000 description 3
- 102000039446 nucleic acids Human genes 0.000 description 3
- 238000003752 polymerase chain reaction Methods 0.000 description 3
- 230000035755 proliferation Effects 0.000 description 3
- 238000000746 purification Methods 0.000 description 3
- 230000001988 toxicity Effects 0.000 description 3
- 231100000419 toxicity Toxicity 0.000 description 3
- 238000003146 transient transfection Methods 0.000 description 3
- 210000004881 tumor cell Anatomy 0.000 description 3
- 238000010200 validation analysis Methods 0.000 description 3
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 2
- 206010005003 Bladder cancer Diseases 0.000 description 2
- 208000003322 Coinfection Diseases 0.000 description 2
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 2
- 238000012413 Fluorescence activated cell sorting analysis Methods 0.000 description 2
- 101150066002 GFP gene Proteins 0.000 description 2
- 241001529936 Murinae Species 0.000 description 2
- 238000000636 Northern blotting Methods 0.000 description 2
- 238000010222 PCR analysis Methods 0.000 description 2
- 208000007097 Urinary Bladder Neoplasms Diseases 0.000 description 2
- 230000000692 anti-sense effect Effects 0.000 description 2
- 238000011717 athymic nude mouse Methods 0.000 description 2
- AIYUHDOJVYHVIT-UHFFFAOYSA-M caesium chloride Chemical compound [Cl-].[Cs+] AIYUHDOJVYHVIT-UHFFFAOYSA-M 0.000 description 2
- 230000001413 cellular effect Effects 0.000 description 2
- 238000010367 cloning Methods 0.000 description 2
- 244000144993 groups of animals Species 0.000 description 2
- 238000007901 in situ hybridization Methods 0.000 description 2
- 238000007912 intraperitoneal administration Methods 0.000 description 2
- 201000007270 liver cancer Diseases 0.000 description 2
- 208000014018 liver neoplasm Diseases 0.000 description 2
- 239000012528 membrane Substances 0.000 description 2
- 108020004999 messenger RNA Proteins 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 239000013642 negative control Substances 0.000 description 2
- 210000004940 nucleus Anatomy 0.000 description 2
- 230000002085 persistent effect Effects 0.000 description 2
- 230000010469 pro-virus integration Effects 0.000 description 2
- 230000002062 proliferating effect Effects 0.000 description 2
- 238000011002 quantification Methods 0.000 description 2
- 238000003753 real-time PCR Methods 0.000 description 2
- 230000035945 sensitivity Effects 0.000 description 2
- 238000012163 sequencing technique Methods 0.000 description 2
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 description 2
- 238000007920 subcutaneous administration Methods 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- 230000010474 transient expression Effects 0.000 description 2
- 238000002054 transplantation Methods 0.000 description 2
- 201000005112 urinary bladder cancer Diseases 0.000 description 2
- 210000002845 virion Anatomy 0.000 description 2
- 238000005406 washing Methods 0.000 description 2
- 239000013607 AAV vector Substances 0.000 description 1
- 208000010370 Adenoviridae Infections Diseases 0.000 description 1
- 206010060931 Adenovirus infection Diseases 0.000 description 1
- 102100026189 Beta-galactosidase Human genes 0.000 description 1
- 208000019838 Blood disease Diseases 0.000 description 1
- 108010001857 Cell Surface Receptors Proteins 0.000 description 1
- 241000282693 Cercopithecidae Species 0.000 description 1
- 102000029816 Collagenase Human genes 0.000 description 1
- 108060005980 Collagenase Proteins 0.000 description 1
- 241000702421 Dependoparvovirus Species 0.000 description 1
- 241000588724 Escherichia coli Species 0.000 description 1
- 101900264058 Escherichia coli Beta-galactosidase Proteins 0.000 description 1
- SXRSQZLOMIGNAQ-UHFFFAOYSA-N Glutaraldehyde Chemical compound O=CCCCC=O SXRSQZLOMIGNAQ-UHFFFAOYSA-N 0.000 description 1
- MVORZMQFXBLMHM-QWRGUYRKSA-N Gly-His-Lys Chemical compound NCCCC[C@@H](C(O)=O)NC(=O)[C@@H](NC(=O)CN)CC1=CN=CN1 MVORZMQFXBLMHM-QWRGUYRKSA-N 0.000 description 1
- 208000031220 Hemophilia Diseases 0.000 description 1
- 208000009292 Hemophilia A Diseases 0.000 description 1
- 229920000209 Hexadimethrine bromide Polymers 0.000 description 1
- 102000001706 Immunoglobulin Fab Fragments Human genes 0.000 description 1
- 108010054477 Immunoglobulin Fab Fragments Proteins 0.000 description 1
- 231100000002 MTT assay Toxicity 0.000 description 1
- 238000000134 MTT assay Methods 0.000 description 1
- 241000699670 Mus sp. Species 0.000 description 1
- 239000000020 Nitrocellulose Substances 0.000 description 1
- 108091028043 Nucleic acid sequence Proteins 0.000 description 1
- 108091034117 Oligonucleotide Proteins 0.000 description 1
- 238000012408 PCR amplification Methods 0.000 description 1
- 229930040373 Paraformaldehyde Natural products 0.000 description 1
- 229930182555 Penicillin Natural products 0.000 description 1
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 1
- 108700009124 Transcription Initiation Site Proteins 0.000 description 1
- 108700019146 Transgenes Proteins 0.000 description 1
- 208000011589 adenoviridae infectious disease Diseases 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 239000011543 agarose gel Substances 0.000 description 1
- 108010005774 beta-Galactosidase Proteins 0.000 description 1
- 230000008033 biological extinction Effects 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 210000004204 blood vessel Anatomy 0.000 description 1
- 239000001506 calcium phosphate Substances 0.000 description 1
- 229910000389 calcium phosphate Inorganic materials 0.000 description 1
- 235000011010 calcium phosphates Nutrition 0.000 description 1
- 244000309466 calf Species 0.000 description 1
- 201000011510 cancer Diseases 0.000 description 1
- 210000003855 cell nucleus Anatomy 0.000 description 1
- 108091092356 cellular DNA Proteins 0.000 description 1
- 108091092328 cellular RNA Proteins 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 229960002424 collagenase Drugs 0.000 description 1
- 238000004891 communication Methods 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 238000012790 confirmation Methods 0.000 description 1
- 230000021615 conjugation Effects 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 239000012228 culture supernatant Substances 0.000 description 1
- 238000012258 culturing Methods 0.000 description 1
- 231100000135 cytotoxicity Toxicity 0.000 description 1
- 230000003013 cytotoxicity Effects 0.000 description 1
- 230000007812 deficiency Effects 0.000 description 1
- 238000012217 deletion Methods 0.000 description 1
- 230000037430 deletion Effects 0.000 description 1
- 238000001514 detection method Methods 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 239000003623 enhancer Substances 0.000 description 1
- 230000002708 enhancing effect Effects 0.000 description 1
- 238000009585 enzyme analysis Methods 0.000 description 1
- 238000001976 enzyme digestion Methods 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 230000002349 favourable effect Effects 0.000 description 1
- 210000003754 fetus Anatomy 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 238000000799 fluorescence microscopy Methods 0.000 description 1
- 238000010230 functional analysis Methods 0.000 description 1
- 108700004026 gag Genes Proteins 0.000 description 1
- 210000004907 gland Anatomy 0.000 description 1
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 1
- 208000018706 hematopoietic system disease Diseases 0.000 description 1
- 230000006801 homologous recombination Effects 0.000 description 1
- 238000009396 hybridization Methods 0.000 description 1
- 230000000984 immunochemical effect Effects 0.000 description 1
- 230000002779 inactivation Effects 0.000 description 1
- 230000002458 infectious effect Effects 0.000 description 1
- 210000003292 kidney cell Anatomy 0.000 description 1
- 238000002372 labelling Methods 0.000 description 1
- 208000032839 leukemia Diseases 0.000 description 1
- 239000003446 ligand Substances 0.000 description 1
- 238000012886 linear function Methods 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- 238000013507 mapping Methods 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 210000004379 membrane Anatomy 0.000 description 1
- 102000006240 membrane receptors Human genes 0.000 description 1
- 230000002503 metabolic effect Effects 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 238000007479 molecular analysis Methods 0.000 description 1
- 238000010172 mouse model Methods 0.000 description 1
- 229920001220 nitrocellulos Polymers 0.000 description 1
- 238000005457 optimization Methods 0.000 description 1
- 229920002866 paraformaldehyde Polymers 0.000 description 1
- 229940049954 penicillin Drugs 0.000 description 1
- 239000013600 plasmid vector Substances 0.000 description 1
- 108700004029 pol Genes Proteins 0.000 description 1
- 229920000656 polylysine Polymers 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 230000006798 recombination Effects 0.000 description 1
- 230000003014 reinforcing effect Effects 0.000 description 1
- 210000001533 respiratory mucosa Anatomy 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 239000000523 sample Substances 0.000 description 1
- 239000012898 sample dilution Substances 0.000 description 1
- 230000009291 secondary effect Effects 0.000 description 1
- 238000013207 serial dilution Methods 0.000 description 1
- 210000002966 serum Anatomy 0.000 description 1
- 230000001568 sexual effect Effects 0.000 description 1
- 230000037432 silent mutation Effects 0.000 description 1
- 239000001488 sodium phosphate Substances 0.000 description 1
- 229910000162 sodium phosphate Inorganic materials 0.000 description 1
- 239000000243 solution Substances 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 239000012192 staining solution Substances 0.000 description 1
- 208000003265 stomatitis Diseases 0.000 description 1
- 229960005322 streptomycin Drugs 0.000 description 1
- 230000002459 sustained effect Effects 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 238000004448 titration Methods 0.000 description 1
- 238000003151 transfection method Methods 0.000 description 1
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 1
- RYFMWSXOAZQYPI-UHFFFAOYSA-K trisodium phosphate Chemical compound [Na+].[Na+].[Na+].[O-]P([O-])([O-])=O RYFMWSXOAZQYPI-UHFFFAOYSA-K 0.000 description 1
- 230000005740 tumor formation Effects 0.000 description 1
- 238000011144 upstream manufacturing Methods 0.000 description 1
- 238000012795 verification Methods 0.000 description 1
- 210000003501 vero cell Anatomy 0.000 description 1
- 230000003612 virological effect Effects 0.000 description 1
- 238000012800 visualization Methods 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/85—Vectors or expression systems specially adapted for eukaryotic hosts for animal cells
- C12N15/86—Viral vectors
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/005—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2710/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA dsDNA viruses
- C12N2710/00011—Details
- C12N2710/10011—Adenoviridae
- C12N2710/10311—Mastadenovirus, e.g. human or simian adenoviruses
- C12N2710/10341—Use of virus, viral particle or viral elements as a vector
- C12N2710/10344—Chimeric viral vector comprising heterologous viral elements for production of another viral vector
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2740/00—Reverse transcribing RNA viruses
- C12N2740/00011—Details
- C12N2740/10011—Retroviridae
- C12N2740/13011—Gammaretrovirus, e.g. murine leukeamia virus
- C12N2740/13022—New viral proteins or individual genes, new structural or functional aspects of known viral proteins or genes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2740/00—Reverse transcribing RNA viruses
- C12N2740/00011—Details
- C12N2740/10011—Retroviridae
- C12N2740/13011—Gammaretrovirus, e.g. murine leukeamia virus
- C12N2740/13041—Use of virus, viral particle or viral elements as a vector
- C12N2740/13043—Use of virus, viral particle or viral elements as a vector viral genome or elements thereof as genetic vector
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2810/00—Vectors comprising a targeting moiety
- C12N2810/50—Vectors comprising as targeting moiety peptide derived from defined protein
- C12N2810/60—Vectors comprising as targeting moiety peptide derived from defined protein from viruses
- C12N2810/6072—Vectors comprising as targeting moiety peptide derived from defined protein from viruses negative strand RNA viruses
- C12N2810/6081—Vectors comprising as targeting moiety peptide derived from defined protein from viruses negative strand RNA viruses rhabdoviridae, e.g. VSV
Landscapes
- Life Sciences & Earth Sciences (AREA)
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Genetics & Genomics (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Biophysics (AREA)
- Zoology (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- Molecular Biology (AREA)
- Wood Science & Technology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Engineering & Computer Science (AREA)
- Virology (AREA)
- Biomedical Technology (AREA)
- Biotechnology (AREA)
- Physics & Mathematics (AREA)
- Plant Pathology (AREA)
- Gastroenterology & Hepatology (AREA)
- Microbiology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Medicinal Chemistry (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Peptides Or Proteins (AREA)
Description
関連出願
本願は1996年11月19日出願の仮出願60/031,323及び1997年2月4日出願の仮出願60/037,081に基づくものである。
発明の分野
本願は一般的にはベクターの分子生物学及び遺伝子治療の分野に関するものである。より具体的には、本発明は二機能性アデノウイルス・ベクター系及びその利用法に関するものである。
関連技術の説明
心臓、肺、及び血液の疾患に対する多数の遺伝子治療は関連柔組織細胞の安定した遺伝子修正に基づいている。多くの場合、これはそれによって安定した形質導入が特定の箇所で達成される直接のイン・ビボ遺伝子伝達によってのみ達成することができる。この目的のために、種々のウイルス性ベクターが、安定した遺伝子性形質導入を達成するための手段としてその結合能力を向上させるために開発されている。このタイプのベクターとしては遺伝子組換えレトロウイルス及びアデノ関連ウイルス(AAV)などがあり、標的細胞の安定した遺伝子性修正を達成するためにイクス・ビボ遺伝子伝達方式によって用いられている。
これらのイクス・ビボ例でのレトロウイルス及びAAVベクターの利用性にも拘らず、直接イン・ビボ遺伝子伝達のためにこれらのベクターを用いるにはいくつかの問題がある。これに関連して、有効な力価及びイン・ビボでの安定性という問題が柔組織の直接特定箇所形質導入が必要となる多くの方式のためのこれらのベクターの利用性に限られたものにしている。一方、遺伝子組換えアデノウイルス性ベクターは高力価に調製することが可能で、イン・ビボでの安定性を有しており、両方の要素とも種々の標的細胞に対する直接イン・ビボ遺伝子伝達のためにそれらを用いることを可能にしている。しかしながら、アデノウイルス性ベクターの制約は誘導される異種遺伝子表現が一過性に過ぎないことである。これは、部分的にはアデノウイルス性ベクターによって形質導入された細胞が免疫的に宿主によって根絶されてしまうという事実に基づいている。加えて、親のアデノウイルスがそのゲノムを宿主クロモソームに結合させる能力を有していない。
先行技術は直接のイン・ビボでのベクター投与後の安定した遺伝子による細胞の修正を可能にしてくれるような有効なベクター系を欠いている点で不十分である。本発明はこの技術分野における長年望まれていたニーズと望みに応えるものである。
発明の要約
イン・ビボでの標的細胞の効率的で安定した形質導入を行うことができる系を誘導するために、アデノウイルス性ベクターで、レトロウイルス性結合機能をつくりだすことができる。本発明はレトロウイルス性ベクターの組み込み及びレトロウイルス性ベクター機能がアデノウイルス性ベクター構成物の中で機能することができ、結合性の子孫レトロウイルス性ベクターをうまく誘導することを示すものである。この方式においては、標的細胞はアデノウイルス性ベクターが媒介するレトロウイルス性ベクター配列の伝達とレトロウイルス性組み込み機能のアデノウイルス性ベクター表現との組み合わせによる一過性レトロウイルス性『プロデューサ細胞』として機能するように誘導される。このイン・ビボ状況では、レトロウイルス組み込み及びベクター機能の高効率な伝達は本来の場所でこれを達成するアデノウイルス性ベクターを介して柔組織個所で達成されるであろう。従って、その場所でつくりだされるレトロウイルス性ベクターは隣接細胞には二次的な影響を及ぼすだけで暗転した遺伝子性形質導入を達成することができるであろう。従って、各成分ベクターの好ましい性質をつくりだす『二機能性(chimeric)』ベクター系が開発されたのである。
本発明の目的はレトロウイルス性結合機能を含むアデノウイルス性ベクターを開発して、標的細胞の安定した形質導入のためにイン・ビトロでのその利用を最適化することである。
本発明の他の目的はこれらの二機能性ベクターを用いて心臓、肺、及び血液の疾患に関連した柔組織細胞の安定したイン・ビボでの遺伝子修正を行うことである。
結合能力を有するアデノウイルス性ベクターの開発はこれらのベクターがイン・ビボで導入遺伝子の安定した結合を可能にしてくれるであろう。こうした戦略は、従って、柔組織標的個所での安定した遺伝子表現を可能にする上で好ましい特性をつくりだし、心臓、肺及び血液の病気のための遺伝子治療に応用する上で効果的な遺伝子補正を行う可能性を大幅に改善してくれるであろう。
本発明のひとつの実施の形態においては、レトロウイルス性配列を含む少なくとも1つのアデノウイルス性ベクターで構成される二機能性のアデノウイルス性/レトロウイルス性ベクターが提供される。
本発明のひとつの実施の形態においては、本発明による上記の二機能性のアデノウイルス性/レトロウイルス性ベクターをそうした治療を必要とする個人に投与するステップを含む標的細胞に安定して形質導入する方法が提供される。
本発明の他の、そしてさらなる側面、特徴、及び利点は開示の目的で提供される本発明の現段階で好ましい実施の形態についての以下の説明を参照することで明らかになるであろう。
図面の説明
上に述べた、およびこれから明らかになる本発明の特徴、利点、及び目的を詳細に理解できるように、上に要約して述べた発明について、添付図面に示すそのいくつかの実施の形態を参照して、以下に具体的に説明する。これらの図面は明細書の一部を構成する。なお、添付図面は本発明の好ましい実施の形態を示すものであって、その範囲を限定することは意図していない。
図1は標的器官個所でのレトロウイルス性ベクターの局所的発生の図を示している。レトロウイルス性ベクター及び組み込み機能をコード表現するアデノウイルス性ベクターは標的柔組織細胞に対するイン・ビボでの遺伝子伝達を高効率で達成して、それらを一過性のレトロウイルス性プロデューサ細胞にしてしまう。局所的につくりだされるレトロウイルス性粒子は従って隣接細胞に直接影響を及ぼす場合がある。
図2Aはレトロウイルス性組み込み機能を含むアデノウイルス性シャトル・プラスミドのマップを示し、図2Bはレトロウイルス性ベクター機能を含むアデノウイルス性シャトル・プラスミドのマップを示す。
図3は分子分析を介してのアデノウイルス性ベクターの構造的検証を示す。
図4はイン・ビボでの標的細胞増殖を誘発するためのHGF及びKGFをコード表現する構成化アデノウイルス性ベクターのマップを示す。
図5は上記アデノウイルス性/レトロウイルス性の二機能性ベクター系を介して達成された持続性のある遺伝子表現を示す。標的細胞はAdLNCMVGFP+AdCMVmpgあるいはAdLNCMVGFPだけで感染されて、安定した遺伝子性形質導入が行われたかどうかについての分析が行われた。W162細胞におけるGFP表現はアデノウイルス性ベクターの感染後示されている時点で蛍光顕微鏡で分析された。
図6は、持続性のある遺伝子表現を示している。標的細胞はAdLNCMVGFP+AdCMVmpgあるいはAdLNCMVGFPだけで感染されて、安定した遺伝子性形質導入が行われたかどうかについての分析が行われた。図6Aは感染後の示された時点でのW162細胞におけるGFP表現のFASC分析を示している。図6Bは感染後30日目に取り出されたW162細胞から抽出されたゲノム性DNAの分析を示している。細胞のHMWDNAをMunIで消化して、レトロウイルス性ベクター部分でプローブした。レーン1のDNAはAdLNCMVGFP+AdCMVmpgで感染した細胞から取り出したもので、レーン2のDNAはAdLNCMVGFPだけで感染された細胞から抽出されたものであり、そしてレーン3はMunIで消化したAdLNCMVGFPゲノム性DNAを含む比較例である。
図7はアデノウイルス/レトロウイルス二機能性ベクターを介しての形質導入レトロウイルス粒子の誘導を示している。図に示されている細胞はAdLNCMVGFPだけか、あるいはAdLNCMVGFP+AdCMVmpgで処理され、上澄液をNIH−3T3細胞上に滴下してレトロウイルス性ベクターについて調べた。上澄液を処理した細胞は蛍光顕微鏡で20日目に分析した。
図8はアデノウイルス/レトロウイルス二機能性ベクターを介してのイン・ビボでの遺伝子伝達を示している。SKOV3ipl細胞を腹膜内に移植した。図8Aはヘマトサイクリンで染色した腹膜内腫瘍塊である。供試動物は図8Bに示すようにAdLNCMVGFPだけか、あるいは(図8Cに示すように)AdLNCMVGFPとAdCMVmpgで刺激を与えて、16日目にGFPが表現されているかどうかを蛍光顕微鏡で分析した。
図9はアデノウイルス/レトロウイルス二機能性ベクターを介してのイン・ビボ遺伝子伝達を示している。SKOV3ipl細胞をAdLNCMVGFP(図9B)又はAdLNCMVGFP+AdCMVmpg(図9C)で感染させて、バージン腫瘍細胞と混合し、ヌード・マウスの皮下に移植した。20日目に、腫瘍を取り出して、蛍光顕微鏡で分析した。(図9A)ヘマトサイクリンで染色された部分を2つのウイルス皮下塊から取り出した。SKOV3iplを腹膜内に移植して、動物にAdLNCMVGFPだけか(図9E)、あるいはAdLNCMVGFP+AdCMVmpg(図9F)で刺激を与えた。16日目にGFPの表現があるかどうかを蛍光顕微鏡で分析した。(図9D)ヘマトサイクリンで染色した腹膜内腫瘍塊。
発明の詳細な説明
本発明は血管投与後に効率的にイン・ビボ遺伝子伝達を行うと同時に異種遺伝子配列を結合して、形質導入後の安定した細胞の遺伝子的修正を行う能力を有するベクター系に関するものである。本発明の二機能性ベクターにおいては、細胞内にレトロウイルス性粒子を局所的に、本来の場所でつくりだす目的で、レトロウイルス性機能を伝達するためにアデノウイルス性ベクターが用いられる。これはレトロウイルス性『組み込み』機能(レトロウイルス性遺伝子gag,pol,env)かレトロウイルス性『ベクター』機能(『治療用』遺伝子を側鎖しているレトロウイルス性LTR配列)のいずれかを含んでいる複製不全アデノウイルス性・ベクターの構成によって達成される。これらのアデノウイルス性ベクターは血管を通じてのベクター投与後に効率的なイン・ビボ形質導入を達成することが知られているアデノウイルス性ベクターの能力に基づいて非常に効率的に細胞に対して遺伝子生成物を共伝達することができる。
これらのアデノウイルス性ベクターによって形質導入された肝臓細胞などの細胞は、その後、一過性のレトロウイルス性ベクター『プロデューサ細胞』にされる。これらの細胞はレトロウイルス性ベクターの機能を一過性的に表現する。従って、これらの細胞は治療用遺伝子を含んだレトロウイルス性粒子をつくりだすことができる。レトロウイルス性粒子の『局所的』で本来の場所での産出のおかげで、このつくりだされたレトロウイルス性粒子によって、隣接細胞の効率的な形質導入が達成される。従ってこうした方法は『遠位』血管投与に伴って起きるレトロウイルス性ベクターの損失を克服することができる。加えて、形質導入された『隣接』細胞はレトロウイルス性ベクターが形質導入を行うという事実のせいで、安定して修正される。この方法は、従って結合による形質導入イベントを可能にすることによってアデノウイルス性ベクターの重要な限界性を克服するものでもある。
この二機能性ウイルス・ベクター系の1つのユニークな特性は、有効な、本来の場所でのレトロウイルス性形質導入を達成するためのアデノウイルス性ベクター伝達要素をつくりだす点である。こうした考え方は『局所的に』つくりだされたレトロウイルス性ベクターに対して細胞をさらに敏感にしてしまう可能性のある他の遺伝子の伝達にも拡張して適用することができる。
本発明は、レトロウイルス性配列を含む少なくとも1つのアデノウイルス性ベクターで構成される二機能性アデノウイルス性/レトロウイルス性ベクターに関するものである。好ましくは、この二機能性アデノウイルス性/レトロウイルス性ベクターは、(a)レトロウイルス性ベクター機能を含む複製不全アデノウイルス性ベクターと、そして(b)少なくとも1つのレトロウイルス性組み込み機能を含む複製不全アデノウイルス性ベクターとを含んでいる。好ましくは、このレトロウイルス性ベクター機能は異種遺伝子を含んでおり、そうした遺伝子がレトロウイルスの長い末端反復によって側鎖されている。一般的に、このレトロウイルス性組み込み機能はgag,pol及びenv、あるいはそれらの組み合わせで構成されるグループから選択される。当業者であれば、ひとつの細胞により具体的に狙いをつけるために別のenv遺伝子を用いることができることは容易に分かるであろう。例えば、以下に詳細に述べるような小水泡性口内炎ウイルスG−糖蛋白は利用が可能なenv遺伝子である。好ましくは、異種遺伝子は治療用蛋白質をコード表現する遺伝子、選択可能なマーカー、そしてレポータ遺伝子で構成されるグループから選択される。当業者であれば、そうした蛋白質を置換したり、あるいは特定の生化学活性を増強したり抑制するために、例えば治療用蛋白質などの蛋白質をコード表現するいろいろな遺伝子を用いることができよう。
本発明はまた、そうした治療を必要とする個人に対して本発明による二機能性アデノウイルス性/レトロウイルス性ベクターを投与するステップを含む標的細胞を安定して形質導入する方法にも関連している。好ましくは、この二機能性アデノウイルス性/レトロウイルス性ベクターは、(a)レトロウイルス性ベクター機能を含む複製不全アデノウイルス性ベクターと、そして(b)少なくとも1つのレトロウイルス性組み込み機能を含む複製不全アデノウイルス性ベクターとを含んでいる。好ましくは、レトロウイルス性ベクター機能は異種遺伝子を含んでおり、そうした遺伝子はレトロウイルス性の長い末端反復によって側鎖されている。一般的に、レトロウイルス性組み込み機能はgap,pol及びenvあるいはそれらの組み合わせで構成されるグループから選択される。当業者であれば、ひとつの細胞により具体的に狙いをつけるために別のenv遺伝子を用いることができることは容易に分かるであろう。例えば、以下に詳細に述べるような小水泡性口内炎ウイルスG−糖蛋白は利用が可能なenv遺伝子である。好ましくは、異種遺伝子は治療用蛋白質をコード表現する遺伝子、選択可能なマーカー、そしてレポータ遺伝子で構成されるグループから選択される。当業者であれば、そうした蛋白質を置換したり、あるいは特定の生化学活性を増強したり抑制するために、例えば治療用蛋白質などの蛋白質をコード表現するいろいろな遺伝子を用いることができよう。以下に述べるような方法を用いて、レトロウイルス性ベクター機能を含む複製不全アデノウイルス性ベクターを投与することができ、そうしたレトロウイルス性組み込み機能を含む複製不全アデノウイルス性ベクターは宿主細胞内に形質導入されて、その内部でそうしたアデノウイルス・シャトル・ベクターによってコード表現された遺伝子の表現は上に述べた治療用遺伝子を含むレトロウイルス性粒子の産出をもたらし、さらにそのレトロウイルス性粒子は隣接細胞に感染し、その内部でレトロウイルス性粒子は上記宿主細胞のゲノム性DNA内にその治療遺伝子を結合させる。
当業者であれば種々の操作によって本発明による二機能性アデノウイルス性/レトロウイルス性ベクターを標的により特殊的に向かわせることができることは分かるであろう。例えば、細胞表面受容体を個別的に認識するリガンドを組み込むことによって、アデノウイルス性ベクターの繊維あるいはノブ成分を遺伝子的に修正することができる。また、この技術分野で知られているFabフラグメントの単鎖抗体を用いて免疫的にアデノウイルスを標的に向かわせることも可能であろう。
以下の実施例は本発明の種々の実施の形態を示すために提供されるものであって、いかなる意味でも本発明を限定することは意図していない。
実施例1
標的細胞の安定した形質導入のための、レトロウイルス性結合機能を含んだアデノウイルス性ベクターの利用
効率的なイン・ビボ遺伝子伝達の結果としての長期にわたる異種遺伝子表現を達成するために、レトロウイルスの結合特性をアデノウイルス性ベクター系に結合することができる。これは、複製不全アデノウイルス性ベクターを用いて細胞にその場所でレトロウイルスの組み込み機能としてレトロウイルス性ベクター配列の両方を伝達することによって行うことができる。そうすると、共形質導入された細胞はレトロウイルス性プロデューサ細胞として機能する。こうした方式においては、局所的につくりだされるレトロウイルス性粒子がそれを取り囲んでいる柔組織内の『隣接細胞』を安定して形質導入し、従って、遺伝子治療のために関連標的器官の導入遺伝子配列の効率的な統合を達成する。アデノウイルス性ベクターが標的遺伝子の効率的な形質導入のための適切なレトロウイルス性機能を伝達してレトロウイルス性プロデューサ細胞として機能する能力が示されている。
実施例2
プラスミド・ベクター及び細胞
アデノウイルス/レトロウイルス・キメラをつくりだすために、レトロウイルスのゲノム成分の個々の要素を最初にpCAAmpg及びpΔE1LNCXと命名されている2つの別のアデノウイルス性シャトル・ベクターに組み込んだ。シャトル・ベクターはレポータ遺伝子も含むようにつくられ、pΔE1LNCMVGFPとなったが、これは緑色蛍光蛋白質(GFP)cDNAとエスケリチア・コリβ−ガラクトシダーゼ(LacZ)をコード表現するpΔE1LNCMVLacZをコード表現する。
pCAAmgpの場合,レトロウイルス性gag/polと両性env遺伝子をコード表現するDNAフラグメントをpPAM3(Dusty A. Miller博士、Fred Hutchinson Cancer ResearchCenter, Seattle, WA提供)から、以下のような二段階手順で単離した。つまり、gag/pol転写開始箇所を含む133bp PCRフラグメントを、HindIIIサイトを含む上流プライマ、5’−gggaagcttatgggccagactgttaccac(SEQ ID No.1)と、内部PstIサイトにまたがる下流プライマー,5’−caaggcttcccaggtcacgatgtagg(SEQ ID No.2)を用いてpPAM3から増幅した。このフラグメントをHindIIIとPstIとを用いて消化してからクローニングを行った。残りの7.0kbのgag/pol/envセグメントはPstI−HpaI消化によってpPAM3から得た。これら2つのレトロウイルス性フラグメントをHindIII−EcoRVサイトでアデノウイルス性シャトル・ベクターpCA13(Microbix Biosystems Inc., Ontario, Canada)に三重結紮させて、pcAAmpgベクター(13.9kb)を得た。
レトロウイルス性統合配列、ネオマイシン抵抗性cDNA、CMVプロモータ、及び多重クローニング・サイトを含んだアデノウイルス性シャトル・ベクターを構成するために、レトロウイルス性ベクターpLNCX(A. Dusty Miller博士提供)をEcoRIとHindIIIサイトで部分的に消化して、3.6kbフラグメントを得た。このフラグメントをその後、pZero−1TM(Invitrogen, La Jolla, CA, USA)の修正版にサブクローンしたところ、EcoRVサイトとNotIサイトの間に沈黙突然変異によってClaIサイトが導入された。得られた構成物はpEH3.6と標識された。残りのレトロウイルス性ベクター配列はApaI及びHindIII消化で得、得られたフラグメントをHindIII及びEcoRVサイトでサブクローンしてpHA0.9を得た。pEH3.6からのこの3.6kbのClaI−HindIIIフラグメントとpHA0.9からの1.0kbのHindIII−XhoIフラグメントをClaI及びXhoIサイトでpΔElSPlA(Microbix, Biosystems Ic.)に三重結紮してpΔE1LNCXをつくった。0.9kbのGFP cDNAセグメントをHindIII−HpaI消化でpEGFP−NI(Clontech Inc., Palo Alto, CA, USA)から切り出して、HindIII及びHpaIサイトでpΔE1LNCXにサブクローンした。pΔE1LNCXからpΔE1LNCMVLacZを構成するために同様の方式を用いた。制限酵素分析によってシャトル・ベクター、pCAAmpg,pΔE1LNCX,pΔE1LNCMVGFP,pΔE1LNCMVLacZが確認され、USB70770配列キット(Amersham, Cleveland, Ohio, USA)を用いて部分的に配列決定を行った。
NIH−3T3線維芽腫、293細胞、EJ膀胱癌細胞(ATCC,Rockville, Maryland)、W162(Gary Ketner, Princeton University)及びSKOV3ipl細胞(Janct Price博士、M. D. Anderson Cancer Center, Houston, TX)を、10%仔ウシ血清(FBS、Hyclone;Logan, UT)、2mMグルタミン(Mediatech)、及びペニシリン/ストレプトマイシン(Cellgro Mediatech)で補強したダルベッコの修正イーグルMedium/Ham’s F12(DMEM/F12、Mediatech, Inc.;Washington, D. c)で構成された完全培養液内に保持した。すべての細胞は5%CO2下で37℃の温度で保持された。
実施例3
遺伝子組換えアデノウイルス性ベクターの生成
イン・ビトロ同種遺伝子組換え法によってE1A/B及びE3消去複製不全遺伝子組換えアデノウイルス性ベクターを生成させた。これらの研究で、pCAAmpg,pΔE1LNCMVLacZあるいはpΔE1LNCMVGFPシャトル・プラスミドをpBGH11(Microbix Biosystems Inc.)と共に293細胞内に共感染させてそれぞれAdCMVAmpg,AdLNCMVLacZあるいはAdLNCMVGFPをつくりだした。各アデノウイルスをプラーク精製を三回通過させて、その後、PCR分析及び制限酵素マッピングで確認した。遺伝子組換えアデノウイルスを許容293細胞株上で増殖させて、CsCl勾配遠心分離で二度精製して、標準的な方法でプラーク滴定した。
実施例4
レトロウイルス性粒子の生成と検出
細胞を10%FBSを含む完全培養液内で100−mm組織培養プレートに置いて(10 6 細胞/プレート)、5%CO2下で37℃の温度で一昼夜培養した。プラスミド構成物を最初にテストするために、293細胞をpΔE1LNCMCLacZ+pCAAmgpか、あるいはpLNCX及びpPAM3のいずれかを用いて燐酸カルシウム沈殿によってトランスフェクトさせた。翌日、細胞に新鮮な完全培養液を与えた。トランスフェクションから48時間後に、上澄液を取り出して、NIH−3T3細胞上でレトロウイルスの力価を判定するために用いた。アデノウイルス感染を行うために、培養液を抜き取って、DMEM/F12+AdCMVAmgpとAdLNCMVGFP、あるいはAdLNCMVGFPだけを含んだ2%FBSで、各グループあたり50プラーク形成単位(pfu)/細胞の割合で置換した。3時間培養した後、培養液を抜き取って、細胞をPBSで数回洗浄してから、完全培養液を与えた。感染48時間後に上澄液を滴下することによって直接的に、あるいはレトロウイルス感染に関して隣接細胞を観察することで間接的に判定した。安定した統合を行わせるための長期培養は8日間の間隔をおいて行われた。レトロウイルスの滴定はNIH−3T3細胞上で行われた。この分析のために、レトロウイルスプロデューサ細胞からの培養上澄液を取り出して、ろ過し(0.45μm)、受容細胞に1:1の割合で完全培養液+10mg/mlポリブレンに加えた。48時間後、LacZを表現している細胞をX−gal組織化学で視覚化し、総青色細胞/皿の定量で力価を判定した。力価は、感染性ヴリオン/mlとして表した。
実施例5
LacZ,GFP及び複製可能レトロウイルス(RCR)アッセイ
LacZの細胞表現についてX−gal(5−ブロモ−4−コロル−3−インドリリル−β−D−ガラクトシド)で染色して定量分析を行った。細胞を0.25%グルタルアルデヒド/0.1Mリン酸ナトリウムで15分間室温で固定してから、PBSで洗浄して、X−gal染色溶液(0.2%X−gal/2mM MgCl2/4mM K4Fe(CN)6/4mM K4Fe(CN)63H2OをPBSに溶解したもの)で室温で一昼夜培養した。X−gal陽性(青色)の細胞を光学顕微鏡で数えた。細胞のGFP表現FACS分析及びメーカー(Clontech, CA, USA)の指示する手順で蛍光顕微鏡を用いて視覚化することで定量的に分析した。
フェリンS+L-(PG-4)細胞をMcCoyの5A培養液(BioWhattaker, Walkersville, MD)+15%FBS内に蒔種し、60mm培養皿で約24時間培養してから接種した。5つの複製皿にサンプル希釈液を0.2mlずつ入れ、ポジティブ・コントロールとして両性ネズミ・レトロウィルス4070Aを1及び10核形成単位として用い、そして培養液はネガティブ・コントロールとして機能した。36±2℃で2時間吸収させ、新鮮な培養液を加えた後、必要に応じて4−5日培養すると、形質変換された細胞の核がポジティブ・コントロールの皿には十分に形成された。これらの皿を顕微鏡で調べて、核を数えた。ネガティブ・コントロールに核が観察されず、ポジティブ・コントロール希釈液がポジティブ・コントロール・ウイルス・ロットの有効平均力価の1ログ以内で平均力価を持っている場合に、アッセイは有効と考えられた。
実施例6
イン・ビボ実験及びプロウイルス統合
雌のヌード・マウス(生後4−6週間)に1×107SKOV3ipl細胞の割合で腹膜接種した。5日後、供試動物にAdCMVAmpg+AdLNCMVGFPか、あるいはAdLNCMVGFPだけを腹膜内接種した(各ウイルスあたりネズミ一匹につき1×109)。動物はアデノウイルス接種から16日目に致死させた。腫瘍結節を取り出して、4%パラホルムアルデヒド/PBS内で固定して、分解し、蛍光顕微鏡で分析した。皮下での混合を調べるために、SKOV3ipl細胞を細胞1個あたり50pfuの割合でイクス・ビボで感染させた。感染から16時間後に、細胞をPBSで二度洗浄してから、トリプシン化し、取り出して、数え、そして感染していないSKOV3ipl細胞と1:4の割合で混合した。全部で5×106の混合細胞がヌード・マウスのわき腹に皮下接種された。動物は接種後20日目に致死された。腫瘍結節を取り出して蛍光顕微鏡で分析した。
プロウイルス統合を検出するために、アデノウイルスで処理した細胞から高分子量画分DNAを取り出した。このDNAをMunIで消化して、0.8%アガロース・ゲルに溶解し、4.8kbから6.2kbのAdLNCMVGFPのPCR増幅によって得たレトロウィルス性ベクター配列を含む32Pでラベルした1.4kbフラグメントでプローブした。メーカー(Amersham)の決めた手順に従って、DNAラベリング、薄膜透過、交雑、そして洗浄手順を行った。
実施例7
隣接細胞を安定して形質導入するための柔組織標的部位でのレトロウィルス粒子の作成
本発明は遺伝子組換えアデノウイルス性ベクターの高効率イン・ビボ遺伝子伝達とレトロウィルスから誘導される結合能力とを合わせ持った『複合』ベクター系を開発した。これはアデノウイルス性ベクターに感染された標的細胞をアデノウイルス性ベクターに媒介されたレトロウィルスの組み込み機能とレトロウィルス・ベクター配列の伝達を介して一過性の『レトロウィルス・プロデューサ細胞』内に送り込むことによって達成される。こうした方法で、局所的につくりだされたレトロウィルス性ベクターは結合性ベクターを介して隣接柔組織細胞に感染することができる。こうした方式の概念的基礎を図1に示す。
こうした方式を実施するための最初のステップとして、レトロウィルス性ベクター配列とレトロウィルス性組み込み機能をコード表現するアデノウイルス性ベクターを誘導した。これらのアデノウイルス性ベクターの誘導は、その導入遺伝子を含んだアデノウイルス『シャトル』ベクターをアデノウイルス性組み込みプラスミドpJM17と共感染させる方法に基づいている。これらのプラスミド内部の同種領域の遺伝子組換えによって複製不全、EIA/B消去、アデノウイルス性ベクターがもたらされる。アデノウイルス・シャトル・プラスミドはアデノウイルス性ベクターの組み込み特性を有している無傷の表現カセットを含んでいるので、それらはアプリオリな導入遺伝子配列の機能的有用性検証を行うための手段を提供してくれる。こうした考え方に基づいて、適切なレトロウィルス性導入遺伝子配列を含んだ一連のアデノウイルス性シャトル・ベクターが誘導された。このようにして、アデノウイルス性シャトル・ベクターpCA13(図2)のポリリンカーにクローンされたレトロウィルス性機能gag/pol/env,gag/polあるいはenvを有する一連のプラスミドが誘導された。
これらのベクターは従ってCMV中間/初期エンハンサー−プロモータを介してレトロウィルス性組み込み機能の表現を可能にしてくれるであろう。加えて、レトロウィルス性ベクター配列をコード表現するアデノウイルス性シャトル・プラスミドが誘導された。この例では、その表現されたアデノウイルス性ベクターはコード表現された導入遺伝子配列の高効率伝達媒体としての機能を果たすであろう。これらのレトロウィルス性ベクター配列はその場合レトロウィルス性粒子内に組み込まれ、そのプロセスには標的細胞内でのベクター表現は必要とされないであろう。従って、これらの例においては、ネオマイシン選択可能マーカーと組み合わされたE.coli β−ガラクトシダーゼ(LacZ)か、あるいはこれもネオマイシン選択可能なマーカーと組み合わされたレポータ遺伝子緑色蛍光蛋白質(GFP)のいずれかをコード表現するレトロウィルス性ベクター配列が『プロモータを持たない』アデノウイルス性シャトル・ベクター(図2)のポリリンカーにクローンされた。
これらのレトロウィルス性ベクター遺伝子構成物は完全なレトロウィルス性長末端側面(LTR)で側鎖されたマーカー/レポータ配列を含んでいる。これが達成されたのは、これらの機能がレトロウィルス性ベクターの統合にin cisで必要となる最低限の配列だからである。これらのプラスミドはすべて構成後に制限エンドヌクレアーゼ消化による間接的分析と、ジデオキシ鎖末端配列決定による直接的分析の両方で確認された。
アデノウイルス性シャトル・プラスミドでのレトロウィルス性組み込み機能が発揮されることを確認するために、機能分析が行われた。この調査のために、レトロウィルス性組み込み機能を含むアデノウィルス性シャトル・プラスミド(pCAAmpg)の利用可能性を、マロニー白血病ウイルス(MLV)LTRの制御下でエコトロピックはレトロウィルス遺伝子gag/pol/envを含む標準組み込みプラスミド、pPAM3と比較した。これらのプラスミドをそれによってLacZレポータ遺伝子がレトロウィルス性LTRによって側鎖されるレトロウィルス性ベクター・カセットを含むコントロールのレトロウィルス性ベクター・プラスミドpLNCLZからレトロウィルス性ベクター配列を取り出す能力があるかどうかについての分析を行った。これらのプラスミドの293細胞への共感染後、上澄液を取り出して標準的な方法でネズミ線維芽腫細胞株NIH−3T3を感染するために用いた。これらの細胞は、その後、X−gal免疫化学的方法でLacZ生成物に対する染色を行ってから、感染後48時間で視覚化された。
レトロウィルス性組み込み機能を含んでいるアデノウイルス性シャトル・プラスミドの機能性検証を行ったところ、293細胞がCaPO4によってそのプラスミドで形質導入されたことが示され、上澄液を用いて標的NIH−3T3細胞を感染し、LacZ遺伝子の生成物を調べるために48時間後にX−gal染色を行った。トランスフェクションはa)pPAM3及びpLNCLZ,b)pPAM3,c)pLNCLZ、及びd)pCAAmpg及びpLNCLZで行われた。pPAM3及びpLNCLZによるトランスフェクションの結果はポジティブであった。pPAM3及びpLNCLZによるトランスフェクションの結果はネガティブであった。pCAAmpg及びpLNCLZによるトランスフェクションの結果はネガティブであった。
コントロールのpPAM3及びpLNCRZの共トランスフェクションはLacZポジティブNIH−3T3細胞の存在で示されるように、レトロウィルス性形質導入性粒子をつくりだした。対照的に、これらのプラスミドのどちらか一方だけでトランスフェクションを行った場合には形質導入性レトロウィルス性粒子はつくりだされなかった。次に、レトロウィルス性組み込み機能をコード表現するアデノウイルス性シャトル・ベクターとレトロウィルス性ベクター・プラスミドpLNCLZによる共トランスフェクションを行った。コントロール・プラスミド(pPAM3及びpLNCLZ)の両方を用いた共トランスフェクションに関しては、この分析でLacZレトロウィルス性粒子が誘導された。従って、レトロウィルス性組み込み機能をアデノウイルス性シャトル・プラスミドの存在下でのレトロウィルス性粒子誘導のためにつくりだすことができる。
レトロウィルス性ベクター配列をアデノウイルス性シャトル・ベクターから取り出すことができるかどうかについての研究が行われた。この分析のために、レトロウィルス性粒子が誘導され、形質導入性粒子を上に述べた方法で分析した。この分析のために用いられた組み込みプラスミドはpPAM3である。これは、レトロウィルス性LTRで側鎖されたLacZ遺伝子を含む通常のレトロウィルス性ベクター・プラスミド、pLNCLZか、あるいは同じLTR−neo−CMV−LacZ−LTRセグメント(pΔE1LNCMVLacZ)を含むアデノウイルス性シャトル・プラスミドのいずれかからレトロウィルス性粒子を取り出すために用いられた。上にも述べたように、pPAM3とpLNCLZによる293の共トランスフェクションはNIH−3T3インジケータ細胞のX−gal細胞によって示されるように、LacZ形質導入性レトロウィルス性粒子を発生させた。さらに、いずれのプラスミドも単独ではこの能力を示さなかった。重要なことは、レトロウィルス性ベクター配列を含んだアデノウイルス性シャトル・プラスミド、pΔE1LNCMVLacZとコントロールのレトロウィルス性組み込みプラスミド,pPAM3による共トランスフェクションがLacZ形質導入性レトロウィルス性粒子を発生させることが実証できたことである。
レトロウィルス性ベクター機能を含んだアデノウイルス性シャトル・プラスミドの機能検証が行われた。この分析の目的のために、293細胞をCaPO4によって示されたプラスミドでトランスフェクトし、上澄液を用いて標的のNIH−3T3細胞を感染して、48時間後にLacZ遺伝子の存在を確認するためにX−gal染色を行った。トランスフェクションはa)pPAM3及びpLNCLZ,b)pPAM3,c)pLNCLZ及びd)pPAM3及びpΔE1LNCMVLacZのいずれかで行った。pPAM3とpLNNCLZによるトランスフェクションの結果はポジティブであり、pPAM3によるトランスフェクションの結果はネガティブであり、pLNCLZによるトランスフェクションの結果はネガティブであり、そしてpPAM3及びpΔE1LNCMVLacZによるトランスフェクションの結果はポジティブであった。従って、形質導入性粒子の誘導のためにレトロウィルス性ベクターをレトロウィルス性シャトル・プラスミドから誘導することができる。
これらの研究はそれぞれ個別的に、レトロウィルス性組み込み及びベクター機能がアデノウイルス性シャトル・プラスミドの存在下で発揮されてイン・ビボのレトロウィルス性粒子の発生を可能にしてくれる。これらの機能が、両方ともアデノウイルス性シャトル・プラスミドの存在下で存在している場合に、これらの機能がレトロウィルス粒子を生み出す機能も発揮することは実証できたことは重要である。この分析のために、アデノウイルス性シャトル・ベクター・プラスミド、pΔE1LNCMVLacZの存在下でレトロウィルス性ベクター機能を取り出すレトロウィルス性組み込み機能の能力を評価した。pPAM3及びpLNCLZによるコントロール(比較)実験はこのアッセイで粒子を誘導する能力を実証した。さらに、pCAAmpgとpΔE1LNCMVLacZによる比較のためのトランスフェクションも独立で粒子を生み出すことはできなかった。しかしながら、これら2つのプラスミドの共トランスフェクションはポジティブ・コントロール研究で示されたように、LacZ形質導入性レトロウィルス性粒子をつくりだした。
レトロウィルス性ベクター機能を含んだアデノウイルス性シャトル・プラスミドの機能的検証を行った。トランスフェクション及び上澄液アッセイは上に述べた通りである。トランスフェクションは、a)pPAM3とpLNCLZ,b)pCAAmpg,c)pΔE1PLCMVLacZ及びd)pCAAmpg及びpΔE1LNCMVLacZによって行われた。pPAM3とpLNCLZによるトランスフェクションの結果はポジティブであり、pΔE1PLCMVLacZによるトランスフェクションの結果はネガティブであり、そしてpCAAmpgとpΔE1PLCMVLacZによるトランスフェクションの結果はネガティブであった。従って、この実験は必要最小限のレトロウィルス性機能を含んだアデノウイルス性シャトル・プラスミドからアデノウイルス性粒子が発生されることを確認した。この知見は従って、これをベースとして構成されるアデノウイルス性ベクターを誘導できる根拠を実証している。
こうした結果に基づいて、組み込み機能あるいはレトロウィルス性ベクター機能をコード表現するアデノウイルス性ベクターが構成された。これらのベクターは、上に述べたようなアデノウイルス性組み込みプラスミドpJM17で示されたシャトル・プラスミドを共トランスフェクションすることを介して通常の方法で発生された。取り出されたプラークを拡大して、ポリメラーゼ鎖反応(PCR)でその同一性を確認した後、3つのシリアル・パッセージでプラーク精製を行った。拡大後、ベクターの同一性をアデノウイルス性ゲノムのE1A領域の異種DNAセグメントの制限酵素による消化及びPCR分析で確認した。この確認の一例を図4に示す。これらのベクターはすべてE1A/B消去、複製不能アデノウイルス性ベクターであった。これらのベクターがレトロウィルス性組み込み及びベクター機能に関して利用できるかどうかを調べるために対応するシャトル・プラスミドに対して行ったのと同様にイン・ビトロで特徴付けを行った。アデノウイルス性ベクターの存在下でのこれらレトロウィルス性ベクターの機能的利用性の実証はイン・ビボ研究の実行を可能にしてくれる。
こうした考え方に基づき、本発明は増殖を誘発させるために関連する標的柔組織に成長因子を提供するためにアデノウイルス性ベクターが用いられる戦略を開示する。こうした方法はレトロウィルス性ベクター及び/又は組み込み機能のアデノウイルス媒介遺伝子伝達を介してのレトロウィルス性ベクターのその場所での発生と組み合わせて用いることができる。この方法では、アデノウイルスは適切な成長因子遺伝子の標的柔組織に対しての高効率のイン・ビボ遺伝子伝達を達成する。関連のあるサイトでの高効率伝達は成長因子の高い局所的濃縮を可能にしてくれ、標的細胞の増殖をさらに誘発してくれる。
アデノウイルス/レトロウィルス二機能性ベクターを構成して、その機能について検証した。レトロウィルス性ベクター配列、AdLNCMVLacZを含む遺伝子組換えアデノウイルスを構成して、機能的な検証を行った。アデノウイルス性ゲノムからレトロウィルス性ベクター配列を取り出せたかどうかを判定するためにレトロウィルス性組み込み機能を有する非293細胞の高度の、そして一過性のトランスフェクションを達成するための方針が考えられた。この必要性のために、アデノウイルス−ポリリシン・ベクタ(AdpL)を用いた。この研究のために、HeLa細胞をプラスミドpPAM3を含むAdpL複合体でトランスフェクトしたところ、レトロウィルス性組み込み機能の表現がもたらされ、その後、AdLNCCMLacZで感染された。比較のための実験は、AdpLを介してのpPAM3とPLNCLZでのHeLaの共トランスフェクションはレトロウィルス性粒子の産出をもたらした。対照的に、プラスミドPLCCLZのAdpL−トランスフェクションは何の結果ももたらさなかった。pPAM3によるAdpLトランスフェクションの後にAdLNCMVLacZでの感染を行ったところ、LacZ形質導入性レトロウィルス性粒子を得ることができた。HeLa細胞をAdpL/pPAM3で前処理しない場合は、そうしたレトロウィルス性粒子を得ることができなかったことは注目に値する。従って、標的細胞へのプロデユーサ細胞からのLacZコード表現アデノウイルスの『キャリー・オーバー』(譲り渡し)はこの結果を説明することにはならない。従って、レトロウィルス性ベクター配列をアデノウイルス性ベクターから取り出して、形質導入性レトロウィルス性粒子をうまく誘導することができる。
AdLNCMVLacZの機能的検証を行った。この分析を行うために、HeLa細胞をAdpL法でレトロウィルス性組み込み及び/又はベクター・プラスミドでトランスフェクトした。いくつかの例で、細胞はAdLNCMVLacZで感染させた。その後、上澄液を取り出して、前に述べたのと同様に、LacZ形質導入性レトロウィルス性粒子の存在に関する分析を行った。形質導入/感染条件は、a)pPAM3及びPLNCLZでの’AdpLトランスフェクション、b)PLNCNZでのAdpLトランスフェクション、c)pPAM3でAdpL感染に続いてのAdLNCMVLacZによる感染、d)AdLNCMVLacZだけでのAd感染であった。pPAM3及びPLNCLZでのAdpLトランスフェクションによる形質導入/感染の結果はポジティブであり、PLNCLZでのAdpLトランスフェクションの結果はネガティブであり、pPAM3でAdpLトランスフェクションを行い続いてAdLNCMVLacZによる感染を行った結果はポジティブ、そしてAdLNCMVLacZのみによるAd感染の結果はネガティブであった。これらの研究に用いられたすべてのベクターはE1 A/B消去、複製不能アデノウイルス性ベクターであった。
実施例8
アデノウイルス性ベクターで媒介された伝達で誘発されたレトロウィルス性プロデューサ細胞内での遺伝子表現のパターン
この戦略の基礎は、アデノウイルス性ベクター粒子からのレトロウィルス性ベクター配列の取り出しを可能にするための標的細胞内でのレトロウィルス性組み込み機能の効率的な表現である。レトロウィルス性組み込み機能gag/pol/envの遺伝子表現のパターンを種々の『従来の』組み込みシステムで評価して、これらの機能をコード表現するアデノウイルス性ベクターAdCMVAmpgによって達成されたパターンとの比較を行った。この点で、組み込み細胞株GP+Am12は安定して形質導入され、両性レトロウィルス性機能を表現し、レトロウィルス性ベクター組み込みのための効率的な媒体として確認されている。加えて、CaPO4微結晶粒子を介してのヒト胎児腎臓細胞293のkat組み込みプラスミドpKat2ampac及びPLNCLZによる一過性トランスフェクションは共形質導入されたレトロウィルス性ベクター・プラスミドを効率的に組み込むことが示されている。これら2つの細胞系をアデノウイルス性ベクターAdCMVAmpgで形質導入されたHeLa細胞と比較して、達成された組み込み機能の強度とパターンの分析を行った。
これらの分析のために、組み込み細胞株GP+Am12、プラスミドpKat2ampacでCaPO4を介して形質導入された293細胞、及びアデノウイルス性ベクターAdCMVAmpgで感染されたHeLa細胞に対して誘導後のいろいろな時点でノーザン・ブロット分析を行った。比較可能な量の抽出総細胞RNAをニトロセルロース薄膜上に移して、得られたブロットをレトロウィルスgag,polあるいはenv遺伝子に対応する32Pでラベルしたオリゴヌクレオチドでプローブした。得られたブロットはアデノウイルス伝達を介して達成されたレトロウィルス性組み込み遺伝子機能の強度及びパターンと従来の組み込み技術で達成されたレベルとの比較を可能にしてくれる。このデータを用いることによって、アデノウイルス性媒体を介しての標的細胞の一過性トランスフェクションからのレトロウィルス性ベクター産出を最適化することが可能になる。
実施例9
アデノウイルス性ベクターの媒介による遺伝子伝達によって誘発される一過性プロデューサ細胞を介してのレトロウィルス性ベクターの産出
レトロウィルスの遺伝子gag/pol/envをコード表現するアデノウイルス性ベクターから適切なレベルとパターンのレトロウィルス性組み込み機能を引き出すことができることを確認した後、形質導入性レトロウィルス粒子の産出を行った。プラスミドpLNCLZによる両性レトロウィルス・プロデューサ株GP+Am12の形質導入によってつくられた安定したレトロウィルス性プロデューサ細胞株を含む『従来の』レトロウィルス性組み込み系との比較が行われた。この株はLacZ/ネオマイシンをコード表現するレトロウィルス粒子を安定してつくりだす。さらに、レトロウィルス性ベクターが両性レトロウィルス性組み込みプラスミドpPAM3をレトロウィルス性ベクター・プラスミドPLNCLZと組み合わせて用いるCaPO4手順での293細胞の一過性共トランスフェクションを介してつくりだされた。比較のために、HeLa細胞を正規の量のレトロウィルス性組み込み機能かレトロウィルス性ベクター機能(AdLNCMVLacZ)をコード表現するアデノウイルス性ベクター(AdCMVmpg)を用いて共形質導入した。
導入48時間後に、標的細胞から上澄液を取り出して、つくられたレトロウィルス性粒子の中身を分析した。つくられたレトロウィルス性粒子の力価と機能を判定するために多数の分析が行われた。つくられた粒子の強度はノーザン・ブロットで直接判定してレトロウィルス性ベクター配列を調べるためにcDNAを介してプローブで上澄液の分析を行った。各上澄液のシリアル希釈液を公知の量のレトロウィルス性ベクター・プラスミドを含んだ標準と比較した。このアッセイは従って各組み込み系で産出されたレトロウィルス性粒子に組み込まれたレトロウィルス性ベクター配列のレベルに関する情報をつくりだす。さらに、つくりだされたレトロウィルス性ベクターの力価は2つの方法で直接判定された。第一に、上澄液を標準的な方法でインジケータ細胞株NIH−3T3に移した。48時間後に、これらの細胞を染色して、FDGによるLacZ遺伝子の生成物について調べ、形質導入頻度についてFACSで分析した。さらに、同様に感染されたNIH−3T3細胞をネオマイシン類似物G418の存在下で安定した選択にかけた。21日後、生き残っているコロニーを結晶性バイオレットで染色してスコアをとった。加えて、それらコロニーの一部を拡大して宿主ゲノム内でのレトロウィルス性ベクターDNAセグメントの状態を分析した。限定分析でDNAが統合しているか、あるいはエピソームとして存在しているかについて調べた。
これらの研究は従って一過性レトロウィルス性プロデューサ細胞がレトロウィルス性組み込み及びベクター機能のアデノウイルス性ベクターの媒介による伝達で誘導され得ることを裏づけている。さらに、プロウイルス性配列を含む導入遺伝子に基づいて標的細胞内に長期的な遺伝子表現を達成することができる形質導入能力を有するレトロウィルス性粒子をつくりだすことができる。加えて、レトロウィルス性組み込み株のアデノウイルス性ベクターが媒介する誘導を介して多数の機能性形質導入レトロウィルス性ベクターの比較を標準的な方法で行うことができる。
実施例10
アデノウイルス/レトロウィルス二機能性システムを介してのレトロウィルス性粒子の最適な産出のためのパラメータ
組み込み細胞からのレトロウィルス産出に影響を及ぼすパラメータは宿主細胞の因子、及び達成可能なレトロウィルス性組み込み/ベクター機能などである。この点で、アデノウイルス性ベクターが媒介する異種遺伝子表現のレベルは一般的には入力粒子数の線形関数である。この関係はアデノウイルス性ベクターに関連する毒性が形質導入された細胞によってつくられる異種遺伝子を減衰するまで続く。アデノウイルス/レトロウィルス二機能性システムを介しての最適化されたレトロウィルス産出の決定因子が示される。HeLa細胞は等分子量のレトロウィルス性組み込み機能(AdCMVAmpg)とレトロウィルス性ベクター機能(AdLNCMVLacZ)をコード表現するアデノウイルス性ベクターによって共形質導入された。前にも述べたのと同様に、上澄液を取り出してレトロウィルス性粒子が産出されているかどうかを調べた。レトロウィルス性ベクター産出との関連を調べるために入力アデノウイルス性ベクターの量は変えることができる。従って、HeLa細胞は細胞1個あたり、1,10,100,500及び1,000個の割合でアデノウイルス性ベクターによって感染された。レトロウィルス性プロデューサ細胞(HeLa)におけるアデノウイルス媒介細胞毒性は細胞増殖に関するMTTアッセイを用いて直接判定された。この分析に基づいて、毒性の制限及び/又は反応の線形性から示されるような入力アデノウイルス性ベクターと出力レトロウィルス性ベクターとの関係が判定された。
ウイルス粒子の出力に影響を及ぼす可能性のある別の要因はレトロウィルス性組み込み機能とレトロウィルス性プロデューサ細胞内につくりだされるレトロウィルス性ベクター配列の比率である。これは最高のレトロウィルス性力価を有するプロデューサ細胞を判定することで安定したレトロウィルス性プロデューサ細胞の存在下で経験的に達成される。この系の両方の成分を独立に調節することができるので、レトロウィルス性ベクター産出を可能にする組み込み及びベクター機能の最適の比率を判定することができる。HeLa細胞をレトロウィルス性組み込み機能(AdCMVAmpg)をコード表現するアデノウイルス性ベクターとレトロウィルス性ベクター機能(AdLNCMVLacZ)をコード表現するアデノウイルス性ベクターの両方を用いて共感染し、生成物のレトロウィルス性粒子の分析を行った。二つの粒子の線形比率(1:1,1:2,1:4など)で共感染を行って、形質導入性レトロウィルス性粒子の最終的な分析を行った。これらの研究はアデノウイルス/レトロウィルス二機能性システムの存在下でのベクター産出に最も適合したレトロウィルス性機能の正確な比率の判定を可能にした。
実施例11
マウス細胞株内でのアデノウイルス/レトロウィルス二機能性システムを介してのレトロウィルス産生
長期間の遺伝子表現をもたらす細胞固有伝達を行うための方法が気道上皮(肺)、血管上皮(心臓)、及び肝臓(代謝血液、血友病)に関して調べられた。レトロウィルス・プロデューサ細胞として機能するマウス肝臓細胞の能力について判定した。この分析のために、安定したレトロウィルス・プロデューサ細胞、レトロウィルス組み込み及びベクター・プラスミドで一過性的にトランスフェクトされた293細胞、及び組み込み及びベクター機能を有する等量のアデノウイルス・レトロウィルス・ベクターによって感染されたHeLa細胞及びマウス肝臓癌細胞の両方との間の直接的な比較が行われた。誘導されたレトロウィルス性粒子を分析した。この分析は関連する柔組織器官標的からのマウス細胞が一過性のレトロウィルス・プロデューサ細胞として機能できるレベルに関する直接の判定を示している。
マウス細胞は自己指向性及び両性レトロウィルス性ベクターによって感染させることができる。しかしながら、マウス細胞が自己指向性レトロウィルス性ベクターと両性レトロウィルス性ベクターに対してそれぞれ違って機能するのかどうかについてはまだはっきり分かっていない。本発明による方法はマウス柔組織細胞の存在下でのレトロウィルスの局所的産出を伴うので、アデノウイルス/レトロウィルス二機能性戦略による自己指向性レトロウィルス性ベクターと両性レトロウィルス性ベクターを産出するマウス肝臓癌細胞の能力が示された。これを達成するために、レトロウィルス粒子内のエンベロープ糖蛋白質を変性するための柔軟な方式が開発された。レトロウィルス組み込み機能gag及びpol(AdCMVGP)をコード表現するアデノウイルス性ベクターを開発した。さらに、自己指向性あるいは両性env糖蛋白質のいずれかをコード表現する別のアデノウイルス性ベクターを開発した。従って、AdLNCMVLacZとgag/pol(AdCMVGP)及び両性env(AdCMVEnva)をコード表現するアデノウイルス性ベクターによる標的細胞の共トランスフェクションによって両性レトロウィルス粒子を誘導したり、あるいはAdLNCMVLacZとgag/pol(AdCMVGP)及び自己指向性env(AnCMVEnve)をコード表現するアデノウイルス性ベクターによる標的細胞の共トランスフェクションによって本発明によるアデノウイルス/レトロウィルス二機能性システムを介して自己指向性レトロウィルス粒子を誘導することは実行可能である。
この分析のために、マウス肝臓癌細胞株をアデノウイルス性ベクターの適切な組み合わせで感染させて、遺伝子組換え自己指向性あるいは両性レトロウィルス性ベクターのいずれかの一過性プロデューサとして機能させた。誘導されたベクターはNIH−3T3に対する力価で分析して、LacZ遺伝子表現および新しい選択可能なクローンをスコアした。この分析はレトロウィルス・プロデューサ細胞として機能するマウス細胞に関する細胞の制約因子を明らかにする。この分析は自己指向性及び両性レトロウィルス性ベクターの産出に関連する具体的な問題の直接的判定についても寄与するであろう。
実施例12
マウス一次細胞でのアデノウイルス/レトロウィルス二機能性システムを介してのレトロウィルス性ベクター産出
肝臓細胞のマウス一次培養体をコラーゲナーゼ消化及び精製という標準的な方法でつくりだした。これらの細胞のレトロウィルス産出に関連するパラメータ、つまり、1)アデノウイルス/レトロウィルス二機能性システムによって誘発されるレトロウィルス組み込み機能のパターンと強度;2)アデノウイルス/レトロウィルス二機能性システムによって誘発されるレトロウィルス性ベクターの産出の強度、3)アデノウイルス/レトロウィルス二機能性システムによって誘発されるレトロウィルス性ベクターの産出に関するパラメータの最適化、4)アデノウイルス/レトロウィルス二機能性システムを介しての自己指向性及び両性レトロウィルス性ベクターの異なった産出などについての評価を行った。これらの研究は末端アッセイとしてLacZ組織化学陽性及びネオマイシン抵抗で評価される形質導入性レトロウィルス粒子の産出を用いる。これによって、イン・ビボ状況と最高度の類似性を有する適切な標的細胞の存在下のレトロウィルス性ベクター産出に関連した最適パラメータの判定が可能になる。
実施例13
アデノウイルス/レトロウィルス二機能性システムを介してのレトロウィルス形質導入を補強する手段としてレトロウィルス受容体の誘導
隣接柔組織細胞を形質導入するレトロウィルス性ベクターをその場所で発生させることはその安定した遺伝子修正を可能にしてくれる。一度アデノウイルス/レトロウィルス二機能性方式でアデノウイルス性ベクターの高度の局所的発生が行われると、他の因子が周辺の標的細胞の実際の形質導入に関与してくる。この点に関して、標的器官サイトでの安定したプロデューサ細胞がレトロウィルス性ベクターを介して起きるようにするためには、形質導入される細胞が増殖状態にあることが必要である。つくられるレトロウィルスに対する受容体の局所集中も隣接細胞が形質導入される有効性を示す因子であろう。自己指向性あるいは両性ベクターのための受容体レベルはこのベクターによる感染に対する標的細胞の全体的な感受性を示す限定的な因子である。さらに、同族レトロウィルス受容体の異種表現は、1)受容体−env相互作用に基づく有効な形質導入イベントの数を増大することにより標的細胞の感受性を増大し、そして/又は2)受容体−env相互作用を可能にする従来は不全であった機能を提供することによって、レトロウィルス感染に従来は抵抗性を示していた細胞をそれに対して感受性を示すようにしてくれる。レトロウィルス受容体群の調節はこれらのベクターによる形質導入の有効性の重要な決定因子であろう。
自己指向性レトロウィルス(eco−R)のエンベロープ糖蛋白質に対応する受容体と両性レトロウィルス(ampho−R)のエンベロープ糖蛋白質に対するcDNAクローンを得た。これらはアデノウイルス性ベクター内に組み入れられ、それによってレトロウィルス性ベクターがE1A/B消去、複製不能アデノウイルス性ベクターの存在下でCMV中間初期プロモータ/エンハンサを介して表現された。これらのベクターを用いて標準的な手順で一次マウス肝臓細胞に感染させた。これらの標的肝臓細胞は、その後、LacZ/neoカセットをコード表現する自己指向性及び両性ベクターによって感染させられた。レトロウィルスがコード表現したcDNAによって形質導入されていないマウス一次肝臓細胞との比較が行われた。上にも述べた通り、インジケータ細胞をスコアしてLacZ組織化学活性とネオマイシン抵抗性とのレトロウィルスによる誘発について調べた。さらに評価可能なパラメータとしてはレトロウィルス性ベクターの感受性に対する標的レトロウィルス受容体数の影響がある。加えて、ecoRとamphoR誘発のそれぞれの能力の比較が可能である。これらの調査はレトロウィルス受容体誘発が関連標的細胞のレトロウィルス形質導入を強化することが可能かどうかについて明らかにしてくれる。この戦略はその場所でのレトロウィルス受容体誘発を達成するためのアデノウイルス性ベクターの効率的なイン・ビボ遺伝子伝達特性をもたしてくれる。従って、アデノウイルス性ベクターはつくりだされたレトロウィルス粒子を介して隣接細胞を感染させるために標的器官サイトでプロデューサ細胞を発生させるために用いられる。隣接細胞でのレトロウィルス受容体の誘導を介してこのプロセスを強化することもアデノウイルス性ベクターが媒介する遺伝子伝達を可能にしてくれる。
実施例14
アデノウイルス/レトロウィルス二機能性システムによるVSV−G偽型化レトロウィルス性ベクターの産出
レトロウィルス性ベクターを介しての効率的な遺伝子伝達を達成するという流れのなかでの標的細胞レトロウィルス受容体の制約を克服するために偽型化レトロウィルスが用いられた。この点で、最も一般的には小水泡性口内炎ウイルスG−糖蛋白質(VSV−G)から誘導される、交互に繰り返されるenv糖蛋白質を含む二機能性レトロウィルス粒子を発生させることができる。そして、これらの二機能性レトロウィルス粒子はVSV−G糖蛋白質と標的細胞受容体との相互作用の効能によって細胞に感染するかもしれない。交互細胞侵入を可能にするこの手段は両性あるいは自己指向性env糖蛋白質に対する標的受容体の欠如を回避してくれる。こうしたやり方はレトロウィルス抵抗性細胞を感染させる目的と、形質導入効率を向上させるのとの両方の目的で用いられている。さらに、これら偽型化ベクターはイン・ビボでのより高いレベルの安定性を有しており、イン・ビボ伝達状況でのその場所でのより高いレベルの形質導入を可能にしてくれるであろう。これらのVSV−G偽型化レトロウィルスは両性あるいは自己指向性gag/polとVSV−G糖蛋白質との協調表現によって発生される。集合レトロウィルス粒子は両性あるいは自己指向性env対応物の代わりにVSV−Gを取り込む。この目的を達成するひとつの手段はレトロウィルス性gag/polをコード表現するプラスミド及びVSV−G+レトロウィルス性ベクター・プラスミドによる細胞の共トランスフェクションである。形質導入された細胞はレトロウィルス性偽型の一過性プロデューサにされる。この方法は望ましい偽型化レトロウィルス粒子をつくりだすことができるが、VSV−G糖蛋白質に関連した毒性がプロデューサ細胞内で示され、このことは産出量の低下、ひいては全体的な力価の低下という結果をもたらす。組み込み細胞株方式は調節可能な表現単位をつくりだすことで開発されてきている。構成的にレトロウィルスgag/polを表現し、同時に誘導可能な表現カセットにVSV−Gを含んだ安定した細胞が開発されている。レトロウィルス性ベクター・プラスミドによるこれらの細胞の形質導入に続いて、偽型化ベクターの誘導を可能にすべくVSV−G表現が誘発された。こうしたやり方は偽型化粒子を発生できる細胞株の安定した維持と向上されたレベルのベクター産出を可能にしてくれる。
標的細胞をVSV−G偽型の一過性プロデューサ内に入れるためにアデノウイルス/レトロウィルス二機能性システムを用いた。こうしたやり方はイン・ビボで隣接細胞を感染させる際に利点を有している。そうした補強された形質導入効率性は改良された標的細胞感染効率に反映する可能性がある。それとは別に、そうしたことは偽型化レトロウィルス粒子のより大きなイン・ビボ安定性に反映する可能性もある。この分析のために、標的細胞をより厳密さを向上させたモデル・システムとして用いた。従って、HeLa細胞、マウス肝臓細胞株BNL CL.2、そして最終的にマウス一次細胞をアデノウイルス/レトロウィルス二機能性システムによって一過性VSV−G偽型化レトロウィルス・プロデューサとして誘発した。
偽型化レトロウィルスの発生のために、細胞をレトロウィルス性gag/polを含むアデノウイルス性ベクター、CAdCMVGP、レトロウィルス性ベクター配列をコード表現するアデノウイルス(AdLNCMVLacZ)+VSV−G糖蛋白質をコード表現するアデノウイルスで共感染した。この後者のベクターはL. Prevec(McMaster University, Ontario, Canada)から入手した。これは種々の高レベルの真核性標的細胞でVSV−Gを表現することはできるE1A/B消去、複製不能アデノウイルス性ベクターである。これらの細胞はそれぞれAdCMVEnv e及びAdCMVEnvaを用いてアデノウイルス/レトロウィルス二機能性システムを介しての自己指向性及び両性レトロウィルス性ベクターの発生のためにも誘発された。感染後、細胞上澄液を取り出して、標的細胞を感染するために用いられた。最初に、NIH 3T3細胞を感染して、LacZ誘発及びネオマイシン選択可能性クローンをスコアした。この分析は、VSV−G偽型化に対して相対的な力価指数をつくりだして、それを両性及び自己指向性ベクターと比較する方法を可能にしてくれる。さらに、上澄液を用いてマウス肝臓一次細胞を感染させてLacZをスコアした。この分析は、偽型化方式がVSV−G標的細胞受領体相互作用に基づいて柔組織標的の感染性を増大させるかどうかを明らかにする。相関的研究は、VSV−G形質導入がベクターのプロウイルス性の統合に関連しているのかどうかについて反転した。VSV−Gは『偽形質導入』と関連づけられており、そのことによって異種遺伝子生成物の移送が標的細胞の安定した遺伝子修正の過程で起きるのであるから、これは重要なことである。さらに、VSV−G糖蛋白質の誘発された表現がアデノウイルス/レトロウィルス二機能性システムを介してベクター産出をさらに最適化することができるかどうかについて調べられた。この誘発性がより高い力価のVSV−G偽型の誘導を可能にするかどうかについての評価が行われた。これらの研究は、従ってアデノウイルス/レトロウィルス二機能性システムがVSV−G偽型化レトロウィルス粒子を生み出すように機能できるのかどうかについての判断を可能にしてくれる。さらに、これらの粒子がイン・ビトロでの関連柔組織標的のより増強された形質導入能力を有しているかどうかについても調べられた。
実施例15
イン・ビボで柔組織細胞を修正するアデノウイルス/レトロウィルス二機能性ベクター
本発明は標的細胞をアデノウイルス・プロデューサ細胞として機能させるためにアデノウイルス性ベクターを用いる方法を提供する。さらにこの方法は心臓、肺、及び血液の病気のモデルに関連した標的組織に対して最適化することができる。この方式をイン・ビボで用いて、標的柔組織サイトでの長期間の安定した統合を達成することができる。1)全身血管伝達による肝臓細胞形質導入と、そして2)内腔気道伝達による気道上皮の2つの状況で、イン・ビボ研究が行われた。これらのルーティング方式は関連柔組織の高効率のイン・ビボ形質導入が達成できる伝達ルートを示している。従って、イン・ビボでの遺伝子機能のレトロウィルスによる伝達効率は人をまごつかせるような要因ではない。標的細胞をレトロウィルス・プロデューサとして機能させるためにアデノウイルス性ベクターが用いられた。つくりだされたレトロウィルスは周囲の柔組織細胞に形質導入するように機能した。
実施例16
柔組織サイトでのレトロウィルス産出のイン・ビボ誘発後の標的細胞のその場所でのレトロウィルス感染
レトロウィルスがイン・ビボでつくりだされる程度及び範囲について調べた。つくりだされるウイルス粒子はその場所では発生後に実際的な方法で検出することはできないので、この分析では隣接細胞がレトロウィルス性ベクターによって安定的に形質導入された程度を強化することで、その結果を間接的に判定した。これらの研究のために、気道上皮か、あるいは肝臓細胞上皮のいずれかでの伝達を実現するためにレトロウィルス性ベクター機能をコード表現するアデノウイルス性ベクターとレトロウィルス性ベクター配列をコード表現するアデノウイルス性ベクターの両方でマウスに刺激を与えた。組み込み機能の表現と、誘導されたレトロウィルス性ベクター(LacZ/neo)の表現された生成物はmRNAトランスクリプト(gag/pol/env)の定量的ポリメラーゼ鎖反応及び/又はDNAコピー数(LTRLacZ/neo)によって標的器官でそれぞれ独立に確認された。さらに、特にこれらのレトロウィルス性成分をつくりだす標的細胞は肺及び肝臓から誘導されるこれらの部分のその本来の場所での雑種形成によって判定された。これらの研究はアデノウイルス性ベクターの伝達が標的器官サイトでレトロウィルス組み込み機能の表現を達成することができることを裏づけている。さらに、レトロウィルス・プロデューサ細胞として強力に機能する特定の細胞サブセットも識別することができる。
つくりだされるレトロウィルスによる標的細胞の形質導入によって統合が行われる程度の判定は宿主器官ゲノム性DNAの存在下でのプロウイルス性DNAの状態の分析によって行われる。レトロウィルス粒子の局所的な産出の後、周辺の細胞の形質導入はレトロウィルス・プロウイルス性ゲノムの統合化コピーを発生された。総DNAはアデノウイルス/レトロウィルス二機能性システムによる誘発の後に抽出されて、プロウイルス性DNAの状態の分析にかけられた。最初、組織物質に対してHirt DNA抽出が行われた。誘導されたDNAがサザン・ブロットで分析されて、アデノウイルス誘導配列の存在とその状態について調べられた。レトロウィルス性ベクターDNAの大部分はHirt画分内で非統合エピソームとして検出されるはずである。これはAdCMVAmpgゲノムと、少なくともAdLNCMVLacZゲノムの一部にも当てはまるであろう。次に、高分子量DNAを同様の方法で分析した。2つのアデノウイルス性ベクターのゲノムは、それらがエピソーム性で、Hirt抽出可能なDNAの存在する場所に移行するので、HMW DNA画分で検出されるはずである。対照的に、統合がいずれかの程度で行われるのであれば、AdLNCMVLacZのプロウイルス性成分はサザン・ブロット分析で高分子量画分で検出される。このことは、これら2つの標的器官サイトから誘導されたDNAのHirt画分及びHMW画分のサザン・ブロットと組み合わせた制限エンドヌクレアーゼ消化によって確認された。比較対照との比較が行われ、それによってレトロウィルス組み込み機能、あるいはレトロウィルス・ベクター機能のいずれか1つだけのアデノウイルスを介しての伝達が行われた。この分析は統合イベントがアデノウイルス/レトロウィルス二機能性システムによるその本来の場所でのレトロウィルス性ベクター形質導入の結果として起きたのかどうかを判定する感受性『スクリーン』として機能する。
その本来の場所でのレトロウィルス感染の追加的アッセイを標的サイトでのベクター・プロウイルス性DNAあるいはDNAコード表現配列の長さである。安定して、長期間の表現がこれらの表現の器官からその本来の場所でのレトロウィルス感染から誘導される。最初の例で、標的器官の柔組織細胞でのベクター・プロウイルスDNAの統合は宿主ゲノムDNAの存在下でのDNA配列の長期的持続として示されるであろう。従って、ベクター・プロウイルスDNAの一時的パターンについて検査した。この点で、前にも述べたのと同様、肺及び肝臓の形質導入についてAdCMVAmpg及びAdLNCMVLacZによって動物を検査した。処理後特定の時間的間隔をおいて、その器官を取り出して、Hirt DNA抽出及びHMW DNA抽出の両方を行った。アデノウイルス性ベクター・ゲノム性DNAとレトロウィルス性プロウイルスDNAの両方の分析を定量性PCRを用いて行って、各時点での宿主HMWゲノム性DNA内の統合レトロウィルス性ベクターDNAの絶対量を判定した。HMW画分内部の持続性プロウイルス性ベクター配列を示す一時的な特徴は安定した統合が起きた程度を示す。ベクター・プロウイルス統合に基づく持続性の別の指数が組織化学レポータを用いて求められた。LacZとGFPの両方を、その表現が適切に処理された組織部分の組織化学分析によって消去することができるレポータとして用いられた。レトロウィルス性ベクターの形質導入後に気道上皮及び肝臓に存在するこれらレポータ遺伝子の一過性表現特性についてはかなり資料として発表されている。従って、レポータ遺伝子の一時的パターンはその本来の場所でのレトロウィルス発生及びその結果としてのベクター・プロウイルス性DNAを示すものである。動物に肝臓及び肺での形質導入を行うためにAdLNCMVLacZ又はAdLNCMVGFPを用いて実験を行った。処理後のいろいろな時点で、関連する器官を取り出して、コード表現されたLacZ及びGFP遺伝子の生成物に関する組織化学分析を行った。この分析を補強するために、これらレポータ遺伝子のmRNA産出を調べるために組織部分の、その本来の場所での雑種形成を行って、追加的な定量的指数を得た。この分析では、アデノウイルスだけをコード表現するレポータとは比べて、その本来の場所のレトロウィルス性ベクター・グループ内で持続性パターンの違いが明らかにされるであろう。
実施例17
レトロウィルス組み込み及びベクター機能のイン・ビボでのアデノウイルスによる伝達を介しての、その本来の場所でのレトロウィルス感染の増強
局所的につくられたレトロウィルス性ベクターが標的細胞に安定して形質導入できる能力は局所的な細胞因子によって影響を受ける。これらの因子には標的細胞の増殖状態と、その局所的につくりだされたレトロウィルス性ベクターに対する受容体の数などがある。細胞増殖を調節するために、成長因子に基づく戦略が用いられた。標的細胞の増殖を強化するために成長因子誘発の戦略が用いられたが、成長因子KFG及び肝臓細胞成長因子(HGF)をコード表現する遺伝子成長物の肺及び肝臓に対する効率的なイン・ビボ伝達を達成するためにアデノウイルス性ベクターが用いられた。この方法によって達成されたこれら成長因子の高い局所的濃度はこれらの器官サイトで柔組織増殖の最適化された誘発をもたらし、これらの増殖誘発は局所的につくられたレトロウィルス性ベクターによる標的細胞の形質導入強化を可能にしてくれる。
動物に対して、初めに、その肺あるいは肝臓に対してKGFあるいはHGFをコード表現するアデノウイルス性ベクターを伝達することで刺激を与えた。増殖の最適な誘発のための一時的な特性が確立した後、動物に対してその本来の場所でのレトロウィルス発生のためにアデノウイルス/レトロウィルス二機能性ベクターAdCMVAmpg及びAdLNCMVLacZを与えた。その後、これらの動物を分析して統合されたプロウイルス性ベクター配列を判定した。これらの調査には肺と肝臓のHMWDNA画分内での統合プロウイルス配列の定量と、安定して形質導入された細胞の数を判定するための、その本来の場所での雑種形成とが含まれていた。相関的な研究は誘発された増殖がどの程度に本来の場所でのレトロウィルス形質導入の成功に寄与するかについて判定するものである。これらの研究をまとめると、成長因子遺伝子のアデノウイルス・ベクターに媒介された伝達を介して誘発される増殖が柔組織標的の安定した形質導入を達成する上で本来の場所で発生されたレトロウィルス性ベクターの能力にどの程度好ましい影響を及ぼすかを明らかにしてくれる。
実施例18
アデノウイルス性ベクターは標的細胞をレトロウイルス・プロデューサとして機能させることができる
標的細胞をアデノウイルス・ベクター、AdCMVAmpg及びAdLNCMVGFPの組み合わせ、あるいはAdLNCMVGFPだけで感染させた。標的細胞はサル・ベロ細胞株W162、マウス腺維芽細胞株NIH−3T3、ヒト膀胱癌細胞株EJ、あるいはヒト卵巣癌細胞株SKOV3ipl(データ示さず)であった。細胞は3時間適切なアデノウイルス性ベクターで感染させてから、洗浄してすべての遊離アデノウイルスを取り除いた。これらの細胞をいろいろな期間組織培養に入れて、蛍光活性化細胞ソーティング(FACS)あるいは蛍光顕微鏡で緑色蛍光蛋白質(GFP)の表現について分析した。
感染2日目のアデノウイルス性ベクター感染細胞の分析の結果、比較対称と推定されるレトロウィルス・プロデューサは高い頻度でGFPレポータ遺伝子の表現を示した(図5)。これは両方のグループで起きたAdLNCMVGFP感染の初期の高い頻度とも一致しており、その後のGFP遺伝子表現も両方のグループで同様に発生した。各グループのサブセットを8日間毎に通過させて、30日目と60日目に分析した。アデノウイルス性ベクター(AdCMVAmpg及びAdLNCMVGFP)の両方に露出させた細胞グループのFACS分析はAdLNCMVGFPだけに露出させた細胞と比較してかなり多い数のGFP−ポジティブ細胞を示した(図6A)。両方のウイルスに感染させたグループからのGFP−ポジティブ細胞は密集した状態で成長しており、これはレトロウィルスが局所的に分布していること、及び/又はクローンの発生原点を示している(図5)。これはGFP表現を失ってしまったAdLNCMVGFPだけで感染された細胞と著しい対称を示しており、標準的なアデノウイルス方式(図5及び6A)で伝達される遺伝子の公知の一過性表現と一致した傾向を示している。高分子量細胞DNAのレトロウィルス配列が示されたことでプロウイルス統合が確認された(図6B)。
実施例19
形質導入性レトロウィルス粒子の産出
NIH−3T3あるいはW162細胞をAdCMVAmpgとAdLNCMVGFP、あるいはAdLNCMVGFPだけで感染させて、その後、上に述べたような手順で洗浄した。上澄液を感染後48時間で取り出して、その後、レトロウィルスの力価を調べるためにNIH−3T3細胞を感染するために用いた。上澄液で感染された細胞を培養内に20日間保持して、GFP表現に関する分析を行った。AdLNCMVGFPウイルスから誘導された上澄液は標的細胞内で長期GFP表現を誘発することはできなかった(図7)。対称的に、AdCMVAmpg及びAdLNCMVGFP上澄液で感染された細胞は20日目で高い割合のGFP表現を示した。この研究はGFP誘発が最初のアデノウイルスで感染された標的細胞から誘導されたレトロウィルスによる感染からもたらされたことを裏づけるものである。これら長期的なGFP表現に関する調査はレトロウィルス産出によって媒介される安定した形質導入からの移転アデノウイルス一過性遺伝子表現(<2週間)を明確にするために考案されたものである。これらの結果は形質導入性レトロウィルス粒子が実際に標的内のアデノウイルス性ベクター伝達遺伝子によって発生されたことを示している。
こうした方法が複製能力を有するレトロウィルス(RCR)の有意な産出に関連しているかどうかについて判定するため、プラスミドに基づくトランスフェクション方法を介して誘導されるRCR発生とアデノウイルス/レトロウィルス二機能性ベクターの使用との比較が行われた。従って、HeLa細胞をpPAM3+pLNCLZでトランスフェクトするか、あるいはAdCMVAmpg又はAdLNCVGFP、又はAdCMVAmpg+AdLNCMVGFPによって感染された。これらの上澄液はその後複製能力を有するレトロウィルスがあるかどうかについて調べた。アデノウイルス/レトロウィルス二機能性によっては複製能力を有するレトロウィルスは検出されなかった(データ示さず)。従って、この方法による複製能力を有するレトロウィルスの発生は通常の方法を上回っているとは思われない。
実施例20
安定した統合によるイン・ビボ遺伝子伝達
こうした基本的な考え方を確立した後、安定した統合をもたらすイン・ビボ遺伝子伝達を行うためにこの方法を用いた。これは最も厳しい伝達状況でのこの方式の全体的な実用性について判定したために行われた。この分析のために、ヒト卵巣癌のマウス・モデルを用いた。無胸腺ヌード・マウスをヒト卵巣癌細胞株SKOV3iplによってオルソトピックな方法で異種間移植した。腹膜腫瘍プラークを確立した後、動物に腹膜ルートでベクターを与えた。動物のいくつかのグループにアデノウイルス/レトロウィルス二機能性ベクターかこのベクター+アデノウイルス/レトロウィルス二機能性組み込み機能のいずれかを与えた。前者のグループでは、用いられたベクター、AdLNCMVGFPはGFPレポータ遺伝子を含むレトロウィルス性ベクター配列を含んでいた。後者のグループでは、pCAAmpgから誘導されたアデノウイルス性ベクターAdCMVAmpgは、機能的に検証された組み込み機能を含んでいた。一方のウイルス・グループでは、GFP表現カセットのアデノウイルス性ベクター媒介伝達はイン・ビボ遺伝子表現をもたらし、非統合性異種遺伝子伝達に基づく急速な消滅という一時的な特性を有している。対称的に、これら2つのウイルスは腫瘍細胞の本来の場所での誘発を達成してレトロウィルス・プロデューサ細胞として機能させることが予想された。局所的につくられたレトロウィルス性ベクターは増殖性の隣接細胞、この場合にはSKOV3ipl腫瘍標的の安定した形質導入を行うことが予想されるであろう。これらの考察に基づけば、2つのオリジナル・グループは安定した形質導入を達成する別の能力に基づいてGFPレポータ遺伝子の表現の明確に異なった一時的特性を示すことが予想されるであろう。アデノウイルス/レトロウィルス二機能性ベクターAdLNCMVGFPによって処理された動物を伝達後の早い時点と時間が経ってからGFP表現を示す腫瘍細胞があるかどうかを示すために蛍光顕微鏡で分析した。この分析で、単一のベクターを受けた動物のグループは図8に示すように遅い時点では稀にしかポジティブ細胞を示さなかった。対称的に、アデノウイルス/レトロウィルス二機能性ベクター+アデノウイルス/レトロウィルス二機能性組み込み機能を与えられた動物は遅い時点ではっきりと異なったパターンを示した。この点で、このグループの分析はクラスター内でポジティブな細胞はより多く検出されている点が注目に値する。この知見は標的細胞の安定した形質導入がクローン表現で起きたとする考え方と一致している。
実施例21
アデノウイルス/レトロウィルス二機能体のイン・ビボでの有効性
卵巣癌細胞株SKOV3iplをAdCMVAmpg+AdLNCMVGFP、あるいはAdLNCMVGFPだけのいずれかでイン・ビトロで感染させた。感染されたレトロウィルス粒子のイン・ビボでの発生と隣接細胞の感染を確認するために、感染された細胞を未感染の細胞と、アデノウイルス性ベクターによって感染された細胞25%、そして未処理SKOV3ipl細胞75%の割合で混合して、腫瘍形成が行われるように無胸腺ヌード・マウス内に皮下接種した。移植から20日目に、両方の動物グループとも明白な腫瘍を有しており、この腫瘍を取り出してGFPレポータ遺伝子の持続性および表現を分析した。AdLNCMVGFPだけで感染されたグループは、稀に、孤立した蛍光細胞だけを有していた(図9B)。対照的に、2−ウイルス・グループから誘導された腫瘍はGFPポジティブ細胞の大きな膨張性クラスターを持っていた(図9C)。複数のフィールドでのポジティブ細胞を数えることによって、1−ウイルス・グループが80%以上のGFP−ポジティブ細胞を有しているという形質導入された細胞の推定を可能にしてくれた。従って、このグループでは、ポジティブ細胞の数は最初の移植混合体内のアデノウイルスで感染された細胞の割合よりかなり大きかった。2−ウイルス・グループでのGFP−ポジティブ細胞がかなり広く分布していることは、本来の場所のレトロウィルス性ベクターによる隣接細胞の安定した遺伝子修正を示唆している。
イン・ビボでのアデノウイルス性ベクター形質導入と本来の場所でのレトロウィルス・プロデューサ発生と結合させる可能性について検査した。ヌード・マウスにオルソトピックな方法でヒト卵巣癌細胞株SKOV3iplを移植した。移植後5日目に動物にAdLNCMVGFPだけか、あるいはAdLNCMVGFP+AdCMVAmpgのいずれかで腹膜内接種した。アデノウイルス接種16日後、動物を致死させて、腫瘍を分析した。1−ウイルス・グループではGFP−ポジティブ細胞は検出されなかった(図9E)。対照的に、両方のアデノウイルス性ベクターを受けたグループではGFP−ポジティブ細胞の島が検出された(図9F)。複数の顕微鏡フィールドの分析は1−ウイルス・グループの場合全体的な形質導入率が1%以下、そして2−ウイルス・グループの場合10−15%であることが示された。レトロウィルス組み込みの十分な誘発を可能にする2つのアデノウイルス性ベクターを受けたグループでのイン・ビボでのGFP表現の持続性は二次的につくりだされるレトロウィルス性ベクターに基づいて発生する安定した形質導入に関するイン・ビトロでの知見と一貫している。
実施例22
要約
イン・ビボで標的細胞の効率的で安定した遺伝子修正を行うための新しいベクター方式が開発された。これはアデノウイルスをレトロウイルス性ベクター及び組み込み成分のための伝達システムとして用い、それによって標的細胞に一過性の、本来の場所でのレトロウイルス性ベクターの一過性プロデューサとして機能させることによって達成された。従ってこの方式は、隣接細胞を感染させ、安定した形質導入を達成することができるレトロウイルス性ベクター粒子の発生を可能にした。この方式においては、2つの重要な要因がこのレベルの安定したイン・ビボでの形質導入を可能にしてくれた。第一に、標的細胞のサイトでのレトロウイルス性ベクターの局所的産出がレトロウイルス粒子の、その不活性化につながるような体液因子への露出による不都合な影響を克服してくれる。第二に、アデノウイルス性ベクターの能力を利用して本来の場所でのレトロウイルス・プロデューサ細胞の効率的なアデノウイルス性ベクターに標的細胞への有効なイン・ビボ伝達を達成させた。この戦略は成分ベクター系の望ましい諸側面を遺伝子伝達という目的のために結合させるという新しい概念に基づく方式を示している。
本明細書で述べられている特許あるいは出版物は本発明が関連する技術分野の当業者のレベルを示している。これらの特許及び出版物はそれらを参照することによって、個々の出版物が具体的、個別的に組み込まれるのと同じ程度に、全体として本明細書に組み込まれる。
当業者であれば、本発明がここで述べられている目的や利点や、それと本質的に関連している目的や利点を実行、達成するのによく適合していることは容易に理解できるであろう。ここに述べられた実施例は、その方法、手順、処理、分子、及び具体的な化合物も含めて好ましい実施の形態を示すものであり、具体例であって、本発明の範囲の限定を意図するものではない。その変更やその他の利用法は、権利請求の範囲で述べられるような本発明の範囲に含まれる技術分野の当業者なら容易に想起できるであろう。
配列リスト
(1) 一般的情報
(i) 出 願 人:Curiel, D.
(ii) 発明の名称:二機能性レトロウイルス/アデノウイルス系
(iii) 配列番号:2
(iv) 連絡住所
(A) 住所:Benjamin A. Adler, Ph. D, J. D.
(B) 通り:8011 Candle Ln.
(C) 都市:Houston
(D) 州:TX
(E) ZIP:77071
(v) コンピュータ読み取り形式
(A) メディア・タイプ:フロッピー・ディスク
(B) コンピュータ:Apple Macintosh
(C) オペレーティング・システム:Macintosh
(D) ソフトウエア:Microsoft WORD6.0
(vi) 現行出願データ
(A) 出願番号
(B) 出願日:
(C) 分類
(vii) 前回出願日
(A) 出願番号
(B) 出願日:
(viii) 弁理士に関する情報
(A) 氏名:Benjamin A. Adler
(B) 登録番号:35,423
(C) 参照・ドケット番号:D6015
(ix) 通信情報
(A) 電話:(713)777−2321
(B) FAX:(713)777−6908
(C) TELEX:
(2) 配列識別番号No.1に関する情報
(i) 配列特性:
(A) 長さ:29bp
(B) タイプ:核酸
(C) ストランド性:単一ストランド
(D) トポロジー:線形
(ii) 分子タイプ:
(A) 説明:他の核酸
(iii) 仮定:なし
(iv) 抗センス:なし
(v) フラグメント・タイプ
(vi) オリジナル・ソース
(vii) 緊急ソース:
(viii) ゲノムでの位置
(ix) 特徴
(x) 刊行物情報
(xi) 配列説明:配列識別番号:1
(3) 配列識別番号:2に関する情報
(i) 配列特性
(A) 長さ:26
(B) タイプ:核酸
(C) ストランド性:単一ストランド
(D) トポロジー:線形
(ii) 分子タイプ
(iv) 抗センス:なし
(v) フラグメント・タイプ
(vi) オリジナル・ソース
(vii) 緊急ソース:
(viii) ゲノムでの位置
(ix) 特徴
(x) 刊行物情報
(xi) 配列説明:配列識別番号:2
Claims (9)
- 二機能性(chimeric)アデノウイルス/レトロウイルスベクターシステムであって、前記システムが下記(a)及び(b):
(a)レトロウイルスの長端末反復(LTR)が両側に配置された異種遺伝子を含む第1の複製不全アデノウイルスベクター、及び
(b)1つ又はそれ以上の第2の複製不全アデノウイルスベクターであって、前記第2の複製不全アデノウイルスベクターはレトロウイルス遺伝子gag、pol及びenvを一緒にコード化するものである、
を含んでいることを特徴とするベクターシステム。 - 第2の複製不全アデノウイルスベクターが、gag、pol及びenvをコード化するアデノウイルスベクター、gag及びpolをコード化するアデノウイルスベクター、及びenvをコード化するアデノウイルスベクターから構成されるグループから選択され、前記第2の複製不全アデノウイルスベクターがレトロウイルス遺伝子gag、pol及びenvを一緒にコード化することを特徴とする請求項1記載のベクターシステム。
- env遺伝子が小水泡性口内炎ウイルスG−糖蛋白質である請求項1又は2記載のベクターシステム。
- 異種遺伝子が、治療用蛋白質をコード化する遺伝子、選択可能なマーカー及びレポータ遺伝子から構成されるグループから選択されることを特徴とする請求項1記載のベクターシステム。
- イン ビボで、心臓、肺、及び血液の疾患に関する柔組織細胞の遺伝子修正を達成するための二機能性アデノウイルス/レトロウイルスベクターシステムを含有する組成物であって、前記二機能性アデノウイルス/レトロウイルスベクターシステムが下記(a)及び(b):
(a)レトロウイルスの長端末反復(LTR)が両側に配置された異種遺伝子を含む第1の複製不全アデノウイルスベクター、及び
(b)1つ又はそれ以上の第2の複製不全アデノウイルスベクターであって、前記第2の複製不全アデノウイルスベクターはレトロウイルス遺伝子gag、pol及びenvを一緒にコード化するものである、
を含んでいることを特徴とする組成物。 - 第2の複製不全アデノウイルスベクターが、gag、pol及びenvをコード化するアデノウイルスベクター、gag及びpolをコード化するアデノウイルスベクター、及びenvをコード化するアデノウイルスベクターから構成されるグループから選択されことを特徴とする請求項5記載の組成物。
- env遺伝子が小水泡性口内炎ウイルスG−糖蛋白質である請求項5又は6記載の組成物。
- 異種遺伝子が、治療用蛋白質をコード化する遺伝子、選択可能なマーカー及びレポータ遺伝子から構成されるグループから選択されることを特徴とする請求項5記載の組成物。
- 第1及び第2の複製不全アデノウイルスベクターが、宿主細胞に共形質導入され、そうすることによって、前記第1の複製不全アデノウイルスベクターによってコード化された治療用遺伝子を含むレトロウイルス粒子の産出をもたらし、前記レトロウイルス粒子が隣接細胞に感染し、前記治療用遺伝子を宿主細胞のゲノムDNA内に安定して統合させる請求項5〜8のいずれか1項に記載の組成物。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US3132396P | 1996-11-19 | 1996-11-19 | |
| US60/031,323 | 1996-11-19 | ||
| US3708197P | 1997-02-04 | 1997-02-04 | |
| US60/037,081 | 1997-02-04 | ||
| PCT/US1997/021169 WO1998022143A1 (en) | 1996-11-19 | 1997-11-19 | Chimeric retrovirus/adenovirus system |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2001509009A JP2001509009A (ja) | 2001-07-10 |
| JP2001509009A5 JP2001509009A5 (ja) | 2005-03-10 |
| JP4214239B2 true JP4214239B2 (ja) | 2009-01-28 |
Family
ID=26707084
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP52385598A Expired - Fee Related JP4214239B2 (ja) | 1996-11-19 | 1997-11-19 | 二機能性レトロウイルス/アデノウイルス系 |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US6333030B1 (ja) |
| EP (1) | EP0956052B1 (ja) |
| JP (1) | JP4214239B2 (ja) |
| AT (1) | ATE292983T1 (ja) |
| AU (1) | AU728610B2 (ja) |
| CA (1) | CA2272121A1 (ja) |
| DE (1) | DE69733035T2 (ja) |
| WO (1) | WO1998022143A1 (ja) |
Families Citing this family (21)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20010006629A1 (en) * | 1993-10-25 | 2001-07-05 | Richard J. Gregory | Recombinant adenoviral vector and methods of use |
| ATE314482T1 (de) * | 1993-10-25 | 2006-01-15 | Canji Inc | Rekombinante adenoviren-vektor und verfahren zur verwendung |
| US6210939B1 (en) | 1993-10-25 | 2001-04-03 | Canji, Inc. | Recombinant adenoviral vector and methods of use |
| US20060275261A1 (en) * | 1993-10-25 | 2006-12-07 | Canji, Inc. | Adenoviral vectors having a protein IX deletion |
| US8703480B1 (en) | 1997-03-21 | 2014-04-22 | Enzo Therapeutics, Inc. | Biological function effecting viral vectors and chimeric cells useful as packaging cell lines and target cells |
| IL131979A0 (en) * | 1997-03-21 | 2001-03-19 | Enzo Therapeutics Inc | Vectors and viral vectors and packaging cell lines for propagating the same |
| AU6962698A (en) * | 1997-04-11 | 1998-11-11 | Government Of The United States Of America, As Represented By The Secretary Of The Department Of Health And Human Services, The | Transgenomic viruses and the use thereof |
| AU2796799A (en) * | 1998-03-03 | 1999-09-20 | Uab Research Foundation, The | Amplification of gene transfer and gene therapy by controlled replication |
| US20060183228A1 (en) * | 1998-03-24 | 2006-08-17 | Enzo Therapeutics, Inc. | Viral vectors with surface or envelope components |
| FR2778670B1 (fr) | 1998-05-18 | 2002-12-13 | Rhone Poulenc Rorer Sa | Methodes et compositions pour la production de particules virales |
| AU6149099A (en) * | 1998-09-22 | 2000-04-10 | Government Of The United States Of America, As Represented By The Secretary Of The Department Of Health And Human Services, The | Replication deficient retroviral vector system and methods of using |
| WO2001055362A2 (en) * | 2000-01-31 | 2001-08-02 | The Governement Of The United States Of America, As Represented By The Secretary, Departement Of Health & Human Services, The National Institutes Of Health | Hybrid adeno-retroviral vector for the transfection of cells |
| AU2001265219A1 (en) | 2000-05-31 | 2001-12-11 | Human Gene Therapy Research Institute | Methods and compositions for efficient gene transfer using transcomplementary vectors |
| WO2002061104A2 (en) | 2001-01-30 | 2002-08-08 | The Government Of The United States Of America, As Represented By The Secretary, Department Of Health & Human Services | Hybrid adenoviral vector |
| WO2002092619A2 (en) | 2001-05-14 | 2002-11-21 | The Gouvernment Of The United States Of America, Represented By The Secretary, Department Of Health And Human Services | Modified growth hormone |
| US20040086485A1 (en) * | 2001-10-04 | 2004-05-06 | Aguilar-Cordova Carlos Estuardo | Chemeric viral vectors for gene therapy |
| US20070037284A1 (en) * | 2003-06-04 | 2007-02-15 | Enzo Therapeutics, Inc. | Vectors for expressing exogenous gene or exogenous nucleic acid sequences |
| ES2292271B1 (es) * | 2004-05-20 | 2009-02-16 | Proyecto De Biomedicina Cima, S.L. | Un vector hibrido adenovirus-alfavirus para la administracion eficaz y expresion de genes terapeuticos en celulas tumorales. |
| WO2011123518A1 (en) | 2010-03-31 | 2011-10-06 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Adenosine receptor agonists for the treatment and prevention of vascular or joint capsule calcification disorders |
| EP4099989A4 (en) | 2020-02-06 | 2023-12-13 | University of Pittsburgh - Of the Commonwealth System of Higher Education | T CELL RECEPTORS TARGETING DEFECTIVE DNA REPAIR PROTEINS |
| US10822379B1 (en) | 2020-03-12 | 2020-11-03 | University of Pittsburgh—of the Commonwealth System of Higher Education | Molecules that bind to SARS-CoV-2 |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0927263A1 (en) * | 1996-01-05 | 1999-07-07 | Genetic Therapy, Inc. | Recombinase-mediated generation of adenoviral vectors |
-
1997
- 1997-11-19 AU AU54475/98A patent/AU728610B2/en not_active Ceased
- 1997-11-19 AT AT97948396T patent/ATE292983T1/de not_active IP Right Cessation
- 1997-11-19 JP JP52385598A patent/JP4214239B2/ja not_active Expired - Fee Related
- 1997-11-19 DE DE69733035T patent/DE69733035T2/de not_active Expired - Lifetime
- 1997-11-19 CA CA002272121A patent/CA2272121A1/en not_active Abandoned
- 1997-11-19 EP EP97948396A patent/EP0956052B1/en not_active Expired - Lifetime
- 1997-11-19 WO PCT/US1997/021169 patent/WO1998022143A1/en active IP Right Grant
- 1997-11-19 US US08/974,113 patent/US6333030B1/en not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| AU728610B2 (en) | 2001-01-11 |
| AU5447598A (en) | 1998-06-10 |
| DE69733035D1 (en) | 2005-05-19 |
| US6333030B1 (en) | 2001-12-25 |
| JP2001509009A (ja) | 2001-07-10 |
| EP0956052B1 (en) | 2005-04-13 |
| ATE292983T1 (de) | 2005-04-15 |
| EP0956052A1 (en) | 1999-11-17 |
| EP0956052A4 (en) | 2001-05-02 |
| WO1998022143A1 (en) | 1998-05-28 |
| DE69733035T2 (de) | 2005-11-24 |
| CA2272121A1 (en) | 1998-05-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4214239B2 (ja) | 二機能性レトロウイルス/アデノウイルス系 | |
| Feng et al. | Stable in vivo gene transduction via a novel adenoviral/retroviral chimeric vector | |
| US6156497A (en) | Recombinase-mediated generation of adenoviral vectors | |
| Beyer et al. | Oncoretrovirus and lentivirus vectors pseudotyped with lymphocytic choriomeningitis virus glycoprotein: generation, concentration, and broad host range | |
| JP2001517452A (ja) | 機能的スプライス・ドナー部位及び機能的スプライス・アクセプター部位を含むレトロウイルスベクター | |
| EP1059357A1 (en) | Replicating or semi-replicating retroviral constructs, preparation and uses for gene delivery | |
| EP0763120A1 (en) | Safe vectors for gene therapy | |
| WO1997025446A9 (en) | Recombinase-mediated generation of adenoviral vectors | |
| JP2002153278A (ja) | ウイルスベクターの製造に用いられる細胞、その製法およびその細胞を用いたウイルスベクターの製造方法 | |
| JP2001517453A (ja) | 方 法 | |
| US5710037A (en) | Retroviral vector particles | |
| US20100233125A1 (en) | Chimeric adenovirus, method for producing the same and pharmaceutical using the same | |
| JP2007530004A (ja) | 疾患を処置するためのサブグループbアデノウイルスベクター | |
| US6303380B1 (en) | Construction of retroviral producer cells from adenoviral and retroviral vectors | |
| JP2001500021A (ja) | 新規な内部リボソームエントリー部位およびそれを含有するベクター | |
| JP2002539797A (ja) | 機能的および非機能的なスプライス供与部位ならびにスプライス受容部位を含むレトロウイルスベクター | |
| US20020164583A1 (en) | Targeting viral vectors to specific cells | |
| JP2002514388A (ja) | 修飾エンベロープエスコート蛋白質を含むレトロウイルスベクター | |
| EP1059356A1 (en) | Replicating or semi-replicating retroviral constructs, preparation and uses for gene delivery | |
| JPH10510163A (ja) | 欠失レトロウイルスベクタのトランス補完用のパッケージング細胞及び発現ベクタ | |
| Schambach et al. | Retroviral vectors for cell and gene therapy | |
| EP1264892A2 (en) | Lentiviral vectors comprising endothelial cell specific promoters | |
| WO2023133400A2 (en) | Cytomegalovirus vectors and methods of use | |
| WO2002064805A2 (en) | Replication competent non-mammalian retroviral vectors | |
| Fu | Gene transfer by viral vectors |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20040608 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20040608 |
|
| RD02 | Notification of acceptance of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7422 Effective date: 20040608 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20061003 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20061219 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20070219 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20070330 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20080916 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20081010 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20111114 Year of fee payment: 3 |
|
| LAPS | Cancellation because of no payment of annual fees |