JP2022542828A - 組換え修飾アデノ随伴ウイルスのパッケージング効率を改善するための組換え修飾アデノ随伴ウイルスヘルパーベクターおよびそれらの使用 - Google Patents
組換え修飾アデノ随伴ウイルスのパッケージング効率を改善するための組換え修飾アデノ随伴ウイルスヘルパーベクターおよびそれらの使用 Download PDFInfo
- Publication number
- JP2022542828A JP2022542828A JP2022502941A JP2022502941A JP2022542828A JP 2022542828 A JP2022542828 A JP 2022542828A JP 2022502941 A JP2022502941 A JP 2022502941A JP 2022502941 A JP2022502941 A JP 2022502941A JP 2022542828 A JP2022542828 A JP 2022542828A
- Authority
- JP
- Japan
- Prior art keywords
- aav
- serotype
- promoter sequence
- native
- raav
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 239000013598 vector Substances 0.000 title claims abstract description 140
- 241000702421 Dependoparvovirus Species 0.000 title claims abstract description 90
- 238000004806 packaging method and process Methods 0.000 title abstract description 15
- 108090000623 proteins and genes Proteins 0.000 claims abstract description 152
- 238000004519 manufacturing process Methods 0.000 claims abstract description 125
- 102000004169 proteins and genes Human genes 0.000 claims abstract description 95
- 241000702423 Adeno-associated virus - 2 Species 0.000 claims description 158
- 239000013600 plasmid vector Substances 0.000 claims description 102
- 108091033319 polynucleotide Proteins 0.000 claims description 96
- 102000040430 polynucleotide Human genes 0.000 claims description 96
- 239000002157 polynucleotide Substances 0.000 claims description 96
- 210000004027 cell Anatomy 0.000 claims description 81
- 238000000034 method Methods 0.000 claims description 66
- 241001655883 Adeno-associated virus - 1 Species 0.000 claims description 63
- 241001634120 Adeno-associated virus - 5 Species 0.000 claims description 62
- 241001164823 Adeno-associated virus - 7 Species 0.000 claims description 56
- 241000972680 Adeno-associated virus - 6 Species 0.000 claims description 55
- 241000202702 Adeno-associated virus - 3 Species 0.000 claims description 40
- 241001164825 Adeno-associated virus - 8 Species 0.000 claims description 40
- 241000580270 Adeno-associated virus - 4 Species 0.000 claims description 34
- 108700019146 Transgenes Proteins 0.000 claims description 25
- 238000012258 culturing Methods 0.000 claims description 17
- 210000003292 kidney cell Anatomy 0.000 claims description 14
- 230000002068 genetic effect Effects 0.000 claims description 13
- 239000008194 pharmaceutical composition Substances 0.000 claims description 13
- 241000699800 Cricetinae Species 0.000 claims description 10
- 208000026350 Inborn Genetic disease Diseases 0.000 claims description 10
- 230000001225 therapeutic effect Effects 0.000 claims description 9
- 208000024556 Mendelian disease Diseases 0.000 claims description 8
- 208000028782 Hereditary disease Diseases 0.000 claims description 7
- 102000039446 nucleic acids Human genes 0.000 claims description 7
- 108020004707 nucleic acids Proteins 0.000 claims description 7
- 150000007523 nucleic acids Chemical class 0.000 claims description 7
- 239000003937 drug carrier Substances 0.000 claims description 6
- 241000238631 Hexapoda Species 0.000 claims description 5
- 208000016361 genetic disease Diseases 0.000 claims description 5
- 239000013612 plasmid Substances 0.000 description 83
- 101150066583 rep gene Proteins 0.000 description 48
- 230000014509 gene expression Effects 0.000 description 33
- 230000006870 function Effects 0.000 description 32
- 241000700605 Viruses Species 0.000 description 26
- 238000001890 transfection Methods 0.000 description 26
- 208000015181 infectious disease Diseases 0.000 description 23
- 101150044789 Cap gene Proteins 0.000 description 21
- 230000002458 infectious effect Effects 0.000 description 19
- 238000001415 gene therapy Methods 0.000 description 18
- MYWUZJCMWCOHBA-VIFPVBQESA-N methamphetamine Chemical compound CN[C@@H](C)CC1=CC=CC=C1 MYWUZJCMWCOHBA-VIFPVBQESA-N 0.000 description 18
- 108090000565 Capsid Proteins Proteins 0.000 description 16
- 102100023321 Ceruloplasmin Human genes 0.000 description 15
- 108700039691 Genetic Promoter Regions Proteins 0.000 description 15
- 210000000234 capsid Anatomy 0.000 description 12
- 101100524324 Adeno-associated virus 2 (isolate Srivastava/1982) Rep78 gene Proteins 0.000 description 11
- 239000002245 particle Substances 0.000 description 11
- 238000002360 preparation method Methods 0.000 description 11
- 241000701161 unidentified adenovirus Species 0.000 description 11
- 239000013607 AAV vector Substances 0.000 description 10
- 101100524321 Adeno-associated virus 2 (isolate Srivastava/1982) Rep68 gene Proteins 0.000 description 10
- 108010048367 enhanced green fluorescent protein Proteins 0.000 description 10
- 239000002609 medium Substances 0.000 description 10
- 230000004048 modification Effects 0.000 description 10
- 238000012986 modification Methods 0.000 description 10
- 108091030071 RNAI Proteins 0.000 description 9
- 230000009368 gene silencing by RNA Effects 0.000 description 9
- 238000013518 transcription Methods 0.000 description 9
- 230000035897 transcription Effects 0.000 description 9
- 108091033380 Coding strand Proteins 0.000 description 8
- 239000003814 drug Substances 0.000 description 8
- 239000000203 mixture Substances 0.000 description 8
- 230000010076 replication Effects 0.000 description 8
- 239000013603 viral vector Substances 0.000 description 8
- 230000003612 virological effect Effects 0.000 description 8
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 7
- 241000701022 Cytomegalovirus Species 0.000 description 7
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 7
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 7
- 230000001404 mediated effect Effects 0.000 description 7
- 230000008685 targeting Effects 0.000 description 7
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 6
- 229960000723 ampicillin Drugs 0.000 description 6
- AVKUERGKIZMTKX-NJBDSQKTSA-N ampicillin Chemical compound C1([C@@H](N)C(=O)N[C@H]2[C@H]3SC([C@@H](N3C2=O)C(O)=O)(C)C)=CC=CC=C1 AVKUERGKIZMTKX-NJBDSQKTSA-N 0.000 description 6
- 238000003556 assay Methods 0.000 description 6
- 230000007812 deficiency Effects 0.000 description 6
- 201000010099 disease Diseases 0.000 description 6
- 239000011780 sodium chloride Substances 0.000 description 6
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 6
- 108020004414 DNA Proteins 0.000 description 5
- 201000009342 Limb-girdle muscular dystrophy Diseases 0.000 description 5
- 241000700584 Simplexvirus Species 0.000 description 5
- 238000001727 in vivo Methods 0.000 description 5
- 210000003734 kidney Anatomy 0.000 description 5
- 239000000725 suspension Substances 0.000 description 5
- 238000004448 titration Methods 0.000 description 5
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 4
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 4
- 201000003533 Leber congenital amaurosis Diseases 0.000 description 4
- 210000003169 central nervous system Anatomy 0.000 description 4
- 230000000295 complement effect Effects 0.000 description 4
- 239000003085 diluting agent Substances 0.000 description 4
- 238000005259 measurement Methods 0.000 description 4
- 238000000746 purification Methods 0.000 description 4
- 230000001105 regulatory effect Effects 0.000 description 4
- 239000000243 solution Substances 0.000 description 4
- 229940124597 therapeutic agent Drugs 0.000 description 4
- 238000013519 translation Methods 0.000 description 4
- 101100524317 Adeno-associated virus 2 (isolate Srivastava/1982) Rep40 gene Proteins 0.000 description 3
- 101100524319 Adeno-associated virus 2 (isolate Srivastava/1982) Rep52 gene Proteins 0.000 description 3
- 108091033409 CRISPR Proteins 0.000 description 3
- 230000004543 DNA replication Effects 0.000 description 3
- 239000006145 Eagle's minimal essential medium Substances 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- 241000282412 Homo Species 0.000 description 3
- 206010028980 Neoplasm Diseases 0.000 description 3
- 108091034057 RNA (poly(A)) Proteins 0.000 description 3
- 108010083379 Sarcoglycans Proteins 0.000 description 3
- 239000003708 ampul Substances 0.000 description 3
- 230000015572 biosynthetic process Effects 0.000 description 3
- 239000001506 calcium phosphate Substances 0.000 description 3
- 229910000389 calcium phosphate Inorganic materials 0.000 description 3
- 235000011010 calcium phosphates Nutrition 0.000 description 3
- 201000011510 cancer Diseases 0.000 description 3
- 239000002775 capsule Substances 0.000 description 3
- 229940079593 drug Drugs 0.000 description 3
- 239000008103 glucose Substances 0.000 description 3
- 230000007246 mechanism Effects 0.000 description 3
- 239000002773 nucleotide Substances 0.000 description 3
- 125000003729 nucleotide group Chemical group 0.000 description 3
- 239000000047 product Substances 0.000 description 3
- 230000000069 prophylactic effect Effects 0.000 description 3
- 230000022532 regulation of transcription, DNA-dependent Effects 0.000 description 3
- 210000001519 tissue Anatomy 0.000 description 3
- 238000012546 transfer Methods 0.000 description 3
- 238000011282 treatment Methods 0.000 description 3
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 3
- 230000006490 viral transcription Effects 0.000 description 3
- VBICKXHEKHSIBG-UHFFFAOYSA-N 1-monostearoylglycerol Chemical compound CCCCCCCCCCCCCCCCCC(=O)OCC(O)CO VBICKXHEKHSIBG-UHFFFAOYSA-N 0.000 description 2
- 102100030686 Beta-sarcoglycan Human genes 0.000 description 2
- 241000282693 Cercopithecidae Species 0.000 description 2
- 102100021790 Delta-sarcoglycan Human genes 0.000 description 2
- 102000004190 Enzymes Human genes 0.000 description 2
- 108090000790 Enzymes Proteins 0.000 description 2
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 2
- 102100021792 Gamma-sarcoglycan Human genes 0.000 description 2
- 102100021519 Hemoglobin subunit beta Human genes 0.000 description 2
- 108091005904 Hemoglobin subunit beta Proteins 0.000 description 2
- 208000009292 Hemophilia A Diseases 0.000 description 2
- 208000032087 Hereditary Leber Optic Atrophy Diseases 0.000 description 2
- 208000001021 Hyperlipoproteinemia Type I Diseases 0.000 description 2
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 2
- 201000000639 Leber hereditary optic neuropathy Diseases 0.000 description 2
- 108010013563 Lipoprotein Lipase Proteins 0.000 description 2
- 102000043296 Lipoprotein lipases Human genes 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- 208000018737 Parkinson disease Diseases 0.000 description 2
- 229920002873 Polyethylenimine Polymers 0.000 description 2
- 241000288906 Primates Species 0.000 description 2
- 108010076504 Protein Sorting Signals Proteins 0.000 description 2
- 241000700618 Vaccinia virus Species 0.000 description 2
- 108020005202 Viral DNA Proteins 0.000 description 2
- 108700005077 Viral Genes Proteins 0.000 description 2
- 108010067390 Viral Proteins Proteins 0.000 description 2
- 201000001408 X-linked juvenile retinoschisis 1 Diseases 0.000 description 2
- 208000017441 X-linked retinoschisis Diseases 0.000 description 2
- 239000002671 adjuvant Substances 0.000 description 2
- 102000015395 alpha 1-Antitrypsin Human genes 0.000 description 2
- 108010050122 alpha 1-Antitrypsin Proteins 0.000 description 2
- 229940024142 alpha 1-antitrypsin Drugs 0.000 description 2
- 150000001413 amino acids Chemical class 0.000 description 2
- -1 antibodies Proteins 0.000 description 2
- 239000000427 antigen Substances 0.000 description 2
- 108091007433 antigens Proteins 0.000 description 2
- 102000036639 antigens Human genes 0.000 description 2
- 238000013459 approach Methods 0.000 description 2
- 239000007864 aqueous solution Substances 0.000 description 2
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 2
- AIYUHDOJVYHVIT-UHFFFAOYSA-M caesium chloride Chemical compound [Cl-].[Cs+] AIYUHDOJVYHVIT-UHFFFAOYSA-M 0.000 description 2
- 210000003986 cell retinal photoreceptor Anatomy 0.000 description 2
- 230000001413 cellular effect Effects 0.000 description 2
- 208000015114 central nervous system disease Diseases 0.000 description 2
- 210000000349 chromosome Anatomy 0.000 description 2
- 238000010367 cloning Methods 0.000 description 2
- 239000012141 concentrate Substances 0.000 description 2
- 230000002950 deficient Effects 0.000 description 2
- VYFYYTLLBUKUHU-UHFFFAOYSA-N dopamine Chemical compound NCCC1=CC=C(O)C(O)=C1 VYFYYTLLBUKUHU-UHFFFAOYSA-N 0.000 description 2
- 239000003995 emulsifying agent Substances 0.000 description 2
- 239000012091 fetal bovine serum Substances 0.000 description 2
- 238000001476 gene delivery Methods 0.000 description 2
- 239000001963 growth medium Substances 0.000 description 2
- 239000005556 hormone Substances 0.000 description 2
- 229940088597 hormone Drugs 0.000 description 2
- 230000005847 immunogenicity Effects 0.000 description 2
- 238000001802 infusion Methods 0.000 description 2
- 230000010354 integration Effects 0.000 description 2
- 239000003446 ligand Substances 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 230000004807 localization Effects 0.000 description 2
- 239000008176 lyophilized powder Substances 0.000 description 2
- 230000035800 maturation Effects 0.000 description 2
- 239000006179 pH buffering agent Substances 0.000 description 2
- 239000000546 pharmaceutical excipient Substances 0.000 description 2
- 230000008488 polyadenylation Effects 0.000 description 2
- 230000023603 positive regulation of transcription initiation, DNA-dependent Effects 0.000 description 2
- 239000000843 powder Substances 0.000 description 2
- 238000003753 real-time PCR Methods 0.000 description 2
- 108020003175 receptors Proteins 0.000 description 2
- 238000011084 recovery Methods 0.000 description 2
- 210000003583 retinal pigment epithelium Anatomy 0.000 description 2
- 201000007714 retinoschisis Diseases 0.000 description 2
- 230000035945 sensitivity Effects 0.000 description 2
- 208000002320 spinal muscular atrophy Diseases 0.000 description 2
- 238000006467 substitution reaction Methods 0.000 description 2
- 238000012385 systemic delivery Methods 0.000 description 2
- 230000014616 translation Effects 0.000 description 2
- 230000006656 viral protein synthesis Effects 0.000 description 2
- 239000011782 vitamin Substances 0.000 description 2
- 229940088594 vitamin Drugs 0.000 description 2
- 229930003231 vitamin Natural products 0.000 description 2
- 235000013343 vitamin Nutrition 0.000 description 2
- 238000009736 wetting Methods 0.000 description 2
- 239000000080 wetting agent Substances 0.000 description 2
- 108091005957 yellow fluorescent proteins Proteins 0.000 description 2
- NHBKXEKEPDILRR-UHFFFAOYSA-N 2,3-bis(butanoylsulfanyl)propyl butanoate Chemical compound CCCC(=O)OCC(SC(=O)CCC)CSC(=O)CCC NHBKXEKEPDILRR-UHFFFAOYSA-N 0.000 description 1
- 241000649045 Adeno-associated virus 10 Species 0.000 description 1
- 108010024878 Adenovirus E1A Proteins Proteins 0.000 description 1
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 1
- 208000024827 Alzheimer disease Diseases 0.000 description 1
- 108700019265 Aromatic amino acid decarboxylase deficiency Proteins 0.000 description 1
- 102000003823 Aromatic-L-amino-acid decarboxylases Human genes 0.000 description 1
- 108090000121 Aromatic-L-amino-acid decarboxylases Proteins 0.000 description 1
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 1
- 238000010354 CRISPR gene editing Methods 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- 241000283707 Capra Species 0.000 description 1
- 241000700199 Cavia porcellus Species 0.000 description 1
- 102100022641 Coagulation factor IX Human genes 0.000 description 1
- 102100026735 Coagulation factor VIII Human genes 0.000 description 1
- 108091026890 Coding region Proteins 0.000 description 1
- 208000006992 Color Vision Defects Diseases 0.000 description 1
- 102000053602 DNA Human genes 0.000 description 1
- SNRUBQQJIBEYMU-UHFFFAOYSA-N Dodecane Natural products CCCCCCCCCCCC SNRUBQQJIBEYMU-UHFFFAOYSA-N 0.000 description 1
- 108010067770 Endopeptidase K Proteins 0.000 description 1
- 241000283073 Equus caballus Species 0.000 description 1
- 201000003542 Factor VIII deficiency Diseases 0.000 description 1
- 241000282326 Felis catus Species 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 108700028146 Genetic Enhancer Elements Proteins 0.000 description 1
- 108010044091 Globulins Proteins 0.000 description 1
- 102000006395 Globulins Human genes 0.000 description 1
- 241000282575 Gorilla Species 0.000 description 1
- 108010043121 Green Fluorescent Proteins Proteins 0.000 description 1
- 102000004144 Green Fluorescent Proteins Human genes 0.000 description 1
- 208000031220 Hemophilia Diseases 0.000 description 1
- 208000005176 Hepatitis C Diseases 0.000 description 1
- 101000911390 Homo sapiens Coagulation factor VIII Proteins 0.000 description 1
- 102000002265 Human Growth Hormone Human genes 0.000 description 1
- 108010000521 Human Growth Hormone Proteins 0.000 description 1
- 239000000854 Human Growth Hormone Substances 0.000 description 1
- 241000598171 Human adenovirus sp. Species 0.000 description 1
- 241000701024 Human betaherpesvirus 5 Species 0.000 description 1
- 241000701806 Human papillomavirus Species 0.000 description 1
- 208000023105 Huntington disease Diseases 0.000 description 1
- 241000282596 Hylobatidae Species 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- 208000015439 Lysosomal storage disease Diseases 0.000 description 1
- 241000282567 Macaca fascicularis Species 0.000 description 1
- 201000011442 Metachromatic leukodystrophy Diseases 0.000 description 1
- 241000699666 Mus <mouse, genus> Species 0.000 description 1
- 241000699670 Mus sp. Species 0.000 description 1
- GXCLVBGFBYZDAG-UHFFFAOYSA-N N-[2-(1H-indol-3-yl)ethyl]-N-methylprop-2-en-1-amine Chemical compound CN(CCC1=CNC2=C1C=CC=C2)CC=C GXCLVBGFBYZDAG-UHFFFAOYSA-N 0.000 description 1
- BKAYIFDRRZZKNF-VIFPVBQESA-N N-acetylcarnosine Chemical compound CC(=O)NCCC(=O)N[C@H](C(O)=O)CC1=CN=CN1 BKAYIFDRRZZKNF-VIFPVBQESA-N 0.000 description 1
- 240000007594 Oryza sativa Species 0.000 description 1
- 235000007164 Oryza sativa Nutrition 0.000 description 1
- 241000282579 Pan Species 0.000 description 1
- 241001631646 Papillomaviridae Species 0.000 description 1
- 241000282520 Papio Species 0.000 description 1
- 241000701945 Parvoviridae Species 0.000 description 1
- 235000019483 Peanut oil Nutrition 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- BELBBZDIHDAJOR-UHFFFAOYSA-N Phenolsulfonephthalein Chemical compound C1=CC(O)=CC=C1C1(C=2C=CC(O)=CC=2)C2=CC=CC=C2S(=O)(=O)O1 BELBBZDIHDAJOR-UHFFFAOYSA-N 0.000 description 1
- 241000282405 Pongo abelii Species 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 108020004511 Recombinant DNA Proteins 0.000 description 1
- 108091028664 Ribonucleotide Proteins 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- 108020004682 Single-Stranded DNA Proteins 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- 101710172711 Structural protein Proteins 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- 238000011053 TCID50 method Methods 0.000 description 1
- AUYYCJSJGJYCDS-LBPRGKRZSA-N Thyrolar Chemical class IC1=CC(C[C@H](N)C(O)=O)=CC(I)=C1OC1=CC=C(O)C(I)=C1 AUYYCJSJGJYCDS-LBPRGKRZSA-N 0.000 description 1
- 102100038313 Transcription factor E2-alpha Human genes 0.000 description 1
- 235000021307 Triticum Nutrition 0.000 description 1
- 244000098338 Triticum aestivum Species 0.000 description 1
- 108091034131 VA RNA Proteins 0.000 description 1
- 101150003160 X gene Proteins 0.000 description 1
- 201000000761 achromatopsia Diseases 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 230000006978 adaptation Effects 0.000 description 1
- 101150063416 add gene Proteins 0.000 description 1
- 238000007792 addition Methods 0.000 description 1
- 230000001464 adherent effect Effects 0.000 description 1
- VREFGVBLTWBCJP-UHFFFAOYSA-N alprazolam Chemical compound C12=CC(Cl)=CC=C2N2C(C)=NN=C2CN=C1C1=CC=CC=C1 VREFGVBLTWBCJP-UHFFFAOYSA-N 0.000 description 1
- 230000003698 anagen phase Effects 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 210000004102 animal cell Anatomy 0.000 description 1
- 239000002246 antineoplastic agent Substances 0.000 description 1
- 230000006907 apoptotic process Effects 0.000 description 1
- 201000004001 aromatic L-amino acid decarboxylase deficiency Diseases 0.000 description 1
- 239000007640 basal medium Substances 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 210000004556 brain Anatomy 0.000 description 1
- 244000309464 bull Species 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 239000006143 cell culture medium Substances 0.000 description 1
- 210000003855 cell nucleus Anatomy 0.000 description 1
- 230000004663 cell proliferation Effects 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 230000002759 chromosomal effect Effects 0.000 description 1
- 238000000975 co-precipitation Methods 0.000 description 1
- 201000007254 color blindness Diseases 0.000 description 1
- 239000002872 contrast media Substances 0.000 description 1
- 210000003239 corneal fibroblast Anatomy 0.000 description 1
- 230000000120 cytopathologic effect Effects 0.000 description 1
- 210000000805 cytoplasm Anatomy 0.000 description 1
- 231100000433 cytotoxic Toxicity 0.000 description 1
- 229940127089 cytotoxic agent Drugs 0.000 description 1
- 230000001472 cytotoxic effect Effects 0.000 description 1
- 239000005547 deoxyribonucleotide Substances 0.000 description 1
- 125000002637 deoxyribonucleotide group Chemical group 0.000 description 1
- 238000011033 desalting Methods 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 230000018109 developmental process Effects 0.000 description 1
- 239000008121 dextrose Substances 0.000 description 1
- 208000035475 disorder Diseases 0.000 description 1
- 238000006073 displacement reaction Methods 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- 125000003438 dodecyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 229960003638 dopamine Drugs 0.000 description 1
- 238000012377 drug delivery Methods 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 239000003623 enhancer Substances 0.000 description 1
- 235000013312 flour Nutrition 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 238000012239 gene modification Methods 0.000 description 1
- 230000005017 genetic modification Effects 0.000 description 1
- 235000013617 genetically modified food Nutrition 0.000 description 1
- 238000010362 genome editing Methods 0.000 description 1
- YQEMORVAKMFKLG-UHFFFAOYSA-N glycerine monostearate Natural products CCCCCCCCCCCCCCCCCC(=O)OC(CO)CO YQEMORVAKMFKLG-UHFFFAOYSA-N 0.000 description 1
- SVUQHVRAGMNPLW-UHFFFAOYSA-N glycerol monostearate Natural products CCCCCCCCCCCCCCCCC(=O)OCC(O)CO SVUQHVRAGMNPLW-UHFFFAOYSA-N 0.000 description 1
- 239000005090 green fluorescent protein Substances 0.000 description 1
- 210000002216 heart Anatomy 0.000 description 1
- 208000009429 hemophilia B Diseases 0.000 description 1
- 208000005252 hepatitis A Diseases 0.000 description 1
- 208000002672 hepatitis B Diseases 0.000 description 1
- 230000003054 hormonal effect Effects 0.000 description 1
- 210000005260 human cell Anatomy 0.000 description 1
- 238000009396 hybridization Methods 0.000 description 1
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 description 1
- 239000012216 imaging agent Substances 0.000 description 1
- 238000003384 imaging method Methods 0.000 description 1
- 230000001900 immune effect Effects 0.000 description 1
- 230000028993 immune response Effects 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 230000000977 initiatory effect Effects 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 230000002452 interceptive effect Effects 0.000 description 1
- 229910052742 iron Inorganic materials 0.000 description 1
- RUTXIHLAWFEWGM-UHFFFAOYSA-H iron(3+) sulfate Chemical compound [Fe+3].[Fe+3].[O-]S([O-])(=O)=O.[O-]S([O-])(=O)=O.[O-]S([O-])(=O)=O RUTXIHLAWFEWGM-UHFFFAOYSA-H 0.000 description 1
- 229910000360 iron(III) sulfate Inorganic materials 0.000 description 1
- 229930027917 kanamycin Natural products 0.000 description 1
- 229960000318 kanamycin Drugs 0.000 description 1
- SBUJHOSQTJFQJX-NOAMYHISSA-N kanamycin Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CN)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](N)[C@H](O)[C@@H](CO)O2)O)[C@H](N)C[C@@H]1N SBUJHOSQTJFQJX-NOAMYHISSA-N 0.000 description 1
- 229930182823 kanamycin A Natural products 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 238000011031 large-scale manufacturing process Methods 0.000 description 1
- 239000010410 layer Substances 0.000 description 1
- 210000004185 liver Anatomy 0.000 description 1
- 210000004072 lung Anatomy 0.000 description 1
- 210000004962 mammalian cell Anatomy 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 108020004999 messenger RNA Proteins 0.000 description 1
- 235000010446 mineral oil Nutrition 0.000 description 1
- 239000002480 mineral oil Substances 0.000 description 1
- 238000004264 monolayer culture Methods 0.000 description 1
- 239000000178 monomer Substances 0.000 description 1
- 210000000663 muscle cell Anatomy 0.000 description 1
- 239000003921 oil Substances 0.000 description 1
- 235000019198 oils Nutrition 0.000 description 1
- 210000000496 pancreas Anatomy 0.000 description 1
- 230000001717 pathogenic effect Effects 0.000 description 1
- 239000000312 peanut oil Substances 0.000 description 1
- 230000002688 persistence Effects 0.000 description 1
- 239000003208 petroleum Substances 0.000 description 1
- 229940124531 pharmaceutical excipient Drugs 0.000 description 1
- 229960003531 phenolsulfonphthalein Drugs 0.000 description 1
- 108091008695 photoreceptors Proteins 0.000 description 1
- 239000006187 pill Substances 0.000 description 1
- 229920001184 polypeptide Polymers 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 102000004196 processed proteins & peptides Human genes 0.000 description 1
- 108090000765 processed proteins & peptides Proteins 0.000 description 1
- 230000001737 promoting effect Effects 0.000 description 1
- QQONPFPTGQHPMA-UHFFFAOYSA-N propylene Natural products CC=C QQONPFPTGQHPMA-UHFFFAOYSA-N 0.000 description 1
- 125000004805 propylene group Chemical group [H]C([H])([H])C([H])([*:1])C([H])([H])[*:2] 0.000 description 1
- 239000013646 rAAV2 vector Substances 0.000 description 1
- 230000009257 reactivity Effects 0.000 description 1
- 230000022983 regulation of cell cycle Effects 0.000 description 1
- 230000000717 retained effect Effects 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 206010039073 rheumatoid arthritis Diseases 0.000 description 1
- 239000002336 ribonucleotide Substances 0.000 description 1
- 125000002652 ribonucleotide group Chemical group 0.000 description 1
- 235000009566 rice Nutrition 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 239000000523 sample Substances 0.000 description 1
- 238000013207 serial dilution Methods 0.000 description 1
- 239000004017 serum-free culture medium Substances 0.000 description 1
- 239000008159 sesame oil Substances 0.000 description 1
- 235000011803 sesame oil Nutrition 0.000 description 1
- 239000000741 silica gel Substances 0.000 description 1
- 229910002027 silica gel Inorganic materials 0.000 description 1
- 239000002356 single layer Substances 0.000 description 1
- 210000002363 skeletal muscle cell Anatomy 0.000 description 1
- 235000020183 skimmed milk Nutrition 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- RYYKJJJTJZKILX-UHFFFAOYSA-M sodium octadecanoate Chemical compound [Na+].CCCCCCCCCCCCCCCCCC([O-])=O RYYKJJJTJZKILX-UHFFFAOYSA-M 0.000 description 1
- 239000003549 soybean oil Substances 0.000 description 1
- 235000012424 soybean oil Nutrition 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 239000008227 sterile water for injection Substances 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 238000004114 suspension culture Methods 0.000 description 1
- 238000013268 sustained release Methods 0.000 description 1
- 239000012730 sustained-release form Substances 0.000 description 1
- 208000011580 syndromic disease Diseases 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 239000003826 tablet Substances 0.000 description 1
- 239000000454 talc Substances 0.000 description 1
- 229910052623 talc Inorganic materials 0.000 description 1
- 238000011287 therapeutic dose Methods 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- 239000005495 thyroid hormone Substances 0.000 description 1
- 229940036555 thyroid hormone Drugs 0.000 description 1
- 230000005026 transcription initiation Effects 0.000 description 1
- 238000010361 transduction Methods 0.000 description 1
- 230000026683 transduction Effects 0.000 description 1
- 239000012096 transfection reagent Substances 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- 238000003146 transient transfection Methods 0.000 description 1
- 230000001228 trophic effect Effects 0.000 description 1
- 230000010415 tropism Effects 0.000 description 1
- 241000701447 unidentified baculovirus Species 0.000 description 1
- 241001430294 unidentified retrovirus Species 0.000 description 1
- 235000013311 vegetables Nutrition 0.000 description 1
- 239000003981 vehicle Substances 0.000 description 1
- 230000029812 viral genome replication Effects 0.000 description 1
- 230000001018 virulence Effects 0.000 description 1
- 230000003442 weekly effect Effects 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/85—Vectors or expression systems specially adapted for eukaryotic hosts for animal cells
- C12N15/86—Viral vectors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0601—Invertebrate cells or tissues, e.g. insect cells; Culture media therefor
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0684—Cells of the urinary tract or kidneys
- C12N5/0686—Kidney cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2750/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssDNA viruses
- C12N2750/00011—Details
- C12N2750/14011—Parvoviridae
- C12N2750/14111—Dependovirus, e.g. adenoassociated viruses
- C12N2750/14141—Use of virus, viral particle or viral elements as a vector
- C12N2750/14143—Use of virus, viral particle or viral elements as a vector viral genome or elements thereof as genetic vector
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2750/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssDNA viruses
- C12N2750/00011—Details
- C12N2750/14011—Parvoviridae
- C12N2750/14111—Dependovirus, e.g. adenoassociated viruses
- C12N2750/14151—Methods of production or purification of viral material
- C12N2750/14152—Methods of production or purification of viral material relating to complementing cells and packaging systems for producing virus or viral particles
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2800/00—Nucleic acids vectors
- C12N2800/40—Systems of functionally co-operating vectors
Landscapes
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Life Sciences & Earth Sciences (AREA)
- Genetics & Genomics (AREA)
- Biomedical Technology (AREA)
- Biotechnology (AREA)
- Chemical & Material Sciences (AREA)
- Zoology (AREA)
- Organic Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Wood Science & Technology (AREA)
- General Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Microbiology (AREA)
- Biochemistry (AREA)
- Cell Biology (AREA)
- Urology & Nephrology (AREA)
- Molecular Biology (AREA)
- Physics & Mathematics (AREA)
- Biophysics (AREA)
- Virology (AREA)
- Plant Pathology (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Abstract
Description
配列表の参照
AAVゲノムの3’ハーフは、VP1,VP2,VP3の3つのキャプシドタンパク質(VP)をコードするAAVキャプシド遺伝子(cap)を含む。3つのキャプシドタンパク質は、単一のプロモーター(AAV2の場合はP40)によって制御される単一のmRNA転写産物から翻訳される。AAVゲノムの3’ハーフは、また、AAVアセンブリ活性化タンパク質(AAP)をコードするAAP遺伝子を含む。60個のVPモノマー(約5コピーのVP1、5コピーのVP2、および50コピーのVP3を含む)がAAVゲノムの周囲で自己集合し、成熟ウイルス粒子の正二十面体のタンパク質の殻(キャプシド)を形成する(Buning,H.他(2019)“Capsid Modifications for Targeting and Improving the Efficacy of AAV Vectors,”Mol.Ther.Meth.Clin.Devel.12:P248-P265;Van Vliet K.M.他(2008)The Role of the Adeno-Associated Virus Capsid in Gene Transfer.In:Drug Delivery Systems,Jain,K.K.(編集),Meth.Molec.Biol.437:51-91).AAV AAPタンパク質は、新たに産生されたVPタンパク質を安定化し、細胞質から細胞核へ輸送するために必要であると考えられている。AAVゲノムの3’ハーフは、また、ゲノム複製をサポートするタンパク質をコードすると考えられているAAV X遺伝子を含む(Colella,P.他(2018)“Emerging Issues in AAV-Mediated In Vivo Gene Therapy,”Molec.Ther.Meth.Clin.Develop.8:87-104;Buning,H.他(2019)“Capsid Modifications for Targeting and Improving the Efficacy of AAV Vectors,”Mol.Ther.Meth.Clin.Devel.12:P248-P265;Cao,M.他(2014)“The X Gene Of Adeno-Associated Virus2(AAV2)Is Involved In Viral DNA Replication,”PLoS ONE 9,e104596:1-10)。
II.遺伝子治療におけるrAAVとその利用
III.rAAV製造の方法
IV.rAAVの精製および回収方法
(1)rAAV;
(2)上述の、さらに非AAVヘルパー機能提供ポリヌクレオチドを含む、組換え改変アデノ随伴ウイルス(AAV)ヘルパーベクター;
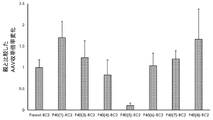
培養は、rAAVの産生を可能にするのに十分な条件下で、培地中で行われ、非天然AAV血清型P5またはP40プロモーター配列の存在は、細胞が、前記AAVヘルパー機能提供ポリヌクレオチドが天然血清型P5およびP40プロモーターを含有する場合に達成されるものと比較して、増加した産生力価で、前記rAAVの産生を引き起こす。
(1)rAAV;
(2)上述の、組換え改変アデノ随伴ウイルス(AAV)ヘルパーベクターのいずれか;および
(3)さらなるベクター、特に、非AAVヘルパー機能提供ポリヌクレオチを含む、プラスミドベクター;
培養は、rAAVの産生を可能にするのに十分な条件下で、培地中で行われ、非天然AAV血清型P5またはP40プロモーター配列の存在は、細胞が、前記AAVヘルパー機能提供ポリヌクレオチドが天然血清型P5およびP40プロモーターを含有する場合に達成されるものと比較して、増加した産生力価で、前記rAAVの産生を引き起こす。
(A)前記ベクターの前記AAVヘルパー機能提供ポリヌクレオチドは、AAV1 Capタンパク質をコードし、前記非天然AAV血清型プロモーター配列は、血清型AAV3、AAV4、AAV5、AAV6、AAV7またはAAV8、または前記血清型の1つ以上のハイブリッドのAAVのプロモーター配列である;
(B)前記ベクターの前記AAVヘルパー機能提供ポリヌクレオチドは、AAV2 Capタンパク質をコードし、前記非天然AAV血清型プロモーター配列は、血清型AAV1、AAV3、AAV4、AAV5、AAV6、AAV7またはAAV8、または前記血清型の1つ以上のハイブリッドのAAVのプロモーター配列である;
(C)前記ベクターの前記AAVヘルパー機能提供ポリヌクレオチドは、AAV3 Capタンパク質をコードし、前記非天然AAV血清型プロモーター配列は、血清型AAV1、AAV4、AAV5、AAV6、AAV7またはAAV8、または前記血清型の1つ以上のハイブリッドのAAVのプロモーター配列である;
(D)前記ベクターの前記AAVヘルパー機能提供ポリヌクレオチドは、AAV4 Capタンパク質をコードし、前記非天然AAV血清型プロモーター配列は、血清型AAV1、AAV3、AAV5、AAV6、AAV7またはAAV8、または前記血清型の1つ以上のハイブリッドのAAVのプロモーター配列である;
(E)前記ベクターの前記AAVヘルパー機能提供ポリヌクレオチドは、AAV5 Capタンパク質をコードし、前記非天然AAV血清型プロモーター配列は、血清型AAV1、AAV3、AAV4、AAV6、AAV7またはAAV8、または前記血清型の1つ以上のハイブリッドのAAVのプロモーター配列である;
(F)前記ベクターの前記AAVヘルパー機能提供ポリヌクレオチドは、AAV6 Capタンパク質をコードし、前記非天然AAV血清型プロモーター配列は、血清型AAV1、AAV3、AAV4、AAV5、AAV7またはAAV8、または前記血清型の1つ以上のハイブリッドのAAVのプロモーター配列である;
(G)前記ベクターの前記AAVヘルパー機能提供ポリヌクレオチドは、AAV7 Capタンパク質をコードし、前記非天然AAV血清型プロモーター配列は、血清型AAV1、AAV3、AAV4、AAV5、AAV6またはAAV8、または前記血清型の1つ以上のハイブリッドのAAVのプロモーター配列である;または
(H)前記ベクターの前記AAVヘルパー機能提供ポリヌクレオチドは、AAV8 Capタンパク質をコードし、前記非天然AAV血清型プロモーター配列は、血清型AAV1、AAV3、AAV4、AAV5、AAV6またはAAV7、または前記血清型の1つ以上のハイブリッドのAAVのプロモーター配列である。
本発明は、組換え型アデノ随伴ウイルス(rAAV)のパッケージング効率を高めることができる組換え型アデノ随伴ウイルス(AAV)ヘルパーベクター、およびそのようなrAAVのパッケージング効率を改善するためのそれらの使用に関する。本発明は、特に、そのようなrAAVによってコードされるRepタンパク質と天然に会合するP5および/またはP40プロモーター配列を、異なる血清型のrAAVのRepタンパク質と会合するAAV P5および/またはP40プロモーターと置換(または増強)するようにさらに改変された組換え改変アデノ随伴ウイルス(AAV)ヘルパーベクターに関する。このような代替または追加のプロモーター配列の使用は、組換え修飾アデノ随伴ウイルスの産生増加を引き起こす。
A.例示的なAAVヘルパー機能提供ポリヌクレオチド
1.プラスミドpAAV-RC1
プラスミドpAAV-RC1のコード鎖(配列番号1):
catggttttg ggacgtttcc tgagtcagat tcgcgaaaaa ctgattcaga gaatttaccg cgggatcgag ccgactttgc caaactggtt cgcggtcaca aagaccagaa atggcgccgg aggcgggaac aaggtggtgg atgagtgcta catccccaat tacttgctcc ccaaaaccca gcctgagctc cagtgggcgt ggactaatat ggaacagtat ttaagcgcct gtttgaatct cacggagcgt aaacggttgg tggcgcagca tctgacgcac gtgtcgcaga cgcaggagca gaacaaagag aatcagaatc ccaattctga tgcgccggtg atcagatcaa aaacttcagc caggtacatg gagctggtcg ggtggctcgt ggacaagggg attacctcgg agaagcagtg gatccaggag gaccaggcct catacatctc cttcaatgcg gcctccaact cgcggtccca aatcaaggct gccttggaca atgcgggaaa gattatgagc ctgactaaaa ccgcccccga ctacctggtg ggccagcagc ccgtggagga catttccagc aatcggattt ataaaatttt ggaactaaac gggtacgatc cccaatatgc ggcttccgtc tttctgggat gggccacgaa aaagttcggc aagaggaaca ccatctggct gtttgggcct gcaactaccg ggaagaccaa catcgcggag gccatagccc acactgtgcc cttctacggg tgcgtaaact ggaccaatga gaactttccc ttcaacgact gtgtcgacaa gatggtgatc tggtgggagg aggggaagat gaccgccaag gtcgtggagt cggccaaagc cattctcgga ggaagcaagg tgcgcgtgga ccagaaatgc aagtcctcgg cccagataga cccgactccc gtgatcgtca cctccaacac caacatgtgc gccgtgattg acgggaactc aacgaccttc gaacaccagc agccgttgca agaccggatg ttcaaatttg aactcacccg ccgtctggat catgactttg ggaaggtcac caagcaggaa gtcaaagact ttttccggtg ggcaaaggat cacgtggttg aggtggagca tgaattctac gtcaaaaagg gtggagccaa gaaaagaccc gcccccagtg acgcagatat aagtgagccc aaacgggtgc gcgagtcagt tgcgcagcca tcgacgtcag acgcggaagc ttcgatcaac tacgcagaca ggtaccaaaa caaatgttct cgtcacgtgg gcatgaatct gatgctgttt ccctgcagac aatgcgagag aatgaatcag aattcaaata tctgcttcac tcacggacag aaagactgtt tagagtgctt tcccgtgtca gaatctcaac ccgtttctgt cgtcaaaaag gcgtatcaga aactgtgcta cattcatcat atcatgggaa aggtgccaga cgcttgcact gcctgcgatc tggtcaatgt ggatttggat gactgcatct ttgaacaata aatgatttaa atcaggtatg gctgccgatg gttatcttcc agattggctc gaggacaacc tctctgaggg cattcgcgag tggtgggact tgaaacctgg agccccgaag cccaaagcca accagcaaaa gcaggacgac ggccggggtc tggtgcttcc tggctacaag tacctcggac ccttcaacgg actcgacaag ggggagcccg tcaacgcggc ggacgcagcg gccctcgagc acgacaaggc ctacgaccag cagctcaaag cgggtgacaa tccgtacctg cggtataacc acgccgacgc cgagtttcag gagcgtctgc aagaagatac gtcttttggg ggcaacctcg ggcgagcagt cttccaggcc aagaagcggg ttctcgaacc tctcggtctg gttgaggaag gcgctaagac ggctcctgga aagaaacgtc cggtagagca gtcgccacaa gagccagact cctcctcggg catcggcaag acaggccagc agcccgctaa aaagagactc aattttggtc agactggcga ctcagagtca gtccccgatc cacaacctct cggagaacct ccagcaaccc ccgctgctgt gggacctact acaatggctt caggcggtgg cgcaccaatg gcagacaata acgaaggcgc cgacggagtg ggtaatgcct caggaaattg gcattgcgat tccacatggc tgggcgacag agtcatcacc accagcaccc gcacctgggc cttgcccacc tacaataacc acctctacaa gcaaatctcc agtgcttcaa cgggggccag caacgacaac cactacttcg gctacagcac cccctggggg tattttgatt tcaacagatt ccactgccac ttttcaccac gtgactggca gcgactcatc aacaacaatt ggggattccg gcccaagaga ctcaacttca aactcttcaa catccaagtc aaggaggtca cgacgaatga tggcgtcaca accatcgcta ataaccttac cagcacggtt caagtcttct cggactcgga gtaccagctt ccgtacgtcc tcggctctgc gcaccagggc tgcctccctc cgttcccggc ggacgtgttc atgattccgc aatacggcta cctgacgctc aacaatggca gccaagccgt gggacgttca tccttttact gcctggaata tttcccttct cagatgctga gaacgggcaa caactttacc ttcagctaca cctttgagga agtgcctttc cacagcagct acgcgcacag ccagagcctg gaccggctga tgaatcctct catcgaccaa tacctgtatt acctgaacag aactcaaaat cagtccggaa gtgcccaaaa caaggacttg ctgtttagcc gtgggtctcc agctggcatg tctgttcagc ccaaaaactg gctacctgga ccctgttatc ggcagcagcg cgtttctaaa acaaaaacag acaacaacaa cagcaatttt acctggactg gtgcttcaaa atataacctc aatgggcgtg aatccatcat caaccctggc actgctatgg cctcacacaa agacgacgaa gacaagttct ttcccatgag cggtgtcatg atttttggaa aagagagcgc cggagcttca aacactgcat tggacaatgt catgattaca gacgaagagg aaattaaagc cactaaccct gtggccaccg aaagatttgg gaccgtggca gtcaatttcc agagcagcag cacagaccct gcgaccggag atgtgcatgc tatgggagca ttacctggca tggtgtggca agatagagac gtgtacctgc agggtcccat ttgggccaaa attcctcaca cagatggaca ctttcacccg tctcctctta tgggcggctt tggactcaag aacccgcctc ctcagatcct catcaaaaac acgcctgttc ctgcgaatcc tccggcggag ttttcagcta caaagtttgc ttcattcatc acccaatact ccacaggaca agtgagtgtg gaaattgaat gggagctgca gaaagaaaac agcaagcgct ggaatcccga agtgcagtac acatccaatt atgcaaaatc tgccaacgtt gattttactg tggacaacaa tggactttat actgagcctc gccccattgg cacccgttac cttacccgtc ccctgtaagg cgcgccaccg gttgcttgtt aatcaataaa ccgtttaatt cgtttcagtt gaactttggt ctctgcgtat ttctttctta tctagtttcc atgctctagg atccactagt aacggccgcc agtgtgctgg aattcggctt tgtagttaat gattaacccg ccatgctact tatctacgta gccatgctct agaggtcctg tattagaggt cacgtgagtg ttttgcgaca ttttgcgaca ccatgtggtc acgctgggta tttaagcccg agtgagcacg cagggtctcc attttgaagc gggaggtttg aacgcgcagc cgccaagccg aattctgcag atatccaaac actggcggcc gctcgactag agcggccgcc accgcggtgg agctccagct tttgttccct ttagtgaggg ttaattgcgc gcttggcgta atcatggtca tagctgtttc ctgtgtgaaa ttgttatccg ctcacaattc cacacaacat acgagccgga agcataaagt gtaaagcctg gggtgcctaa tgagtgagct aactcacatt aattgcgttg cgctcactgc ccgctttcca gtcgggaaac ctgtcgtgcc agctgcatta atgaatcggc caacgcgcgg ggagaggcgg tttgcgtatt gggcgctctt ccgcttcctc gctcactgac tcgctgcgct cggtcgttcg gctgcggcga gcggtatcag ctcactcaaa ggcggtaata cggttatcca cagaatcagg ggataacgca ggaaagaaca tgtgagcaaa aggccagcaa aaggccagga accgtaaaaa ggccgcgttg ctggcgtttt tccataggct ccgcccccct gacgagcatc acaaaaatcg acgctcaagt cagaggtggc gaaacccgac aggactataa agataccagg cgtttccccc tggaagctcc ctcgtgcgct ctcctgttcc gaccctgccg cttaccggat acctgtccgc ctttctccct tcgggaagcg tggcgctttc tcatagctca cgctgtaggt atctcagttc ggtgtaggtc gttcgctcca agctgggctg tgtgcacgaa ccccccgttc agcccgaccg ctgcgcctta tccggtaact atcgtcttga gtccaacccg gtaagacacg acttatcgcc actggcagca gccactggta acaggattag cagagcgagg tatgtaggcg gtgctacaga gttcttgaag tggtggccta actacggcta cactagaaga acagtatttg gtatctgcgc tctgctgaag ccagttacct tcggaaaaag agttggtagc tcttgatccg gcaaacaaac caccgctggt agcggtggtt tttttgtttg caagcagcag attacgcgca gaaaaaaagg atctcaagaa gatcctttga tcttttctac ggggtctgac gctcagtgga acgaaaactc acgttaaggg attttggtca tgagattatc aaaaaggatc ttcacctaga tccttttaaa ttaaaaatga agttttaaat caatctaaag tatatatgag taaacttggt ctgacagtta ccaatgctta atcagtgagg cacctatctc agcgatctgt ctatttcgtt catccatagt tgcctgactc cccgtcgtgt agataactac gatacgggag ggcttaccat ctggccccag tgctgcaatg ataccgcgag acccacgctc accggctcca gatttatcag caataaacca gccagccgga agggccgagc gcagaagtgg tcctgcaact ttatccgcct ccatccagtc tattaattgt tgccgggaag ctagagtaag tagttcgcca gttaatagtt tgcgcaacgt tgttgccatt gctacaggca tcgtggtgtc acgctcgtcg tttggtatgg cttcattcag ctccggttcc caacgatcaa ggcgagttac atgatccccc atgttgtgca aaaaagcggt tagctccttc ggtcctccga tcgttgtcag aagtaagttg gccgcagtgt tatcactcat ggttatggca gcactgcata attctcttac tgtcatgcca tccgtaagat gcttttctgt gactggtgag tactcaacca agtcattctg agaatagtgt atgcggcgac cgagttgctc ttgcccggcg tcaatacggg ataataccgc gccacatagc agaactttaa aagtgctcat cattggaaaa cgttcttcgg ggcgaaaact ctcaaggatc ttaccgctgt tgagatccag ttcgatgtaa cccactcgtg cacccaactg atcttcagca tcttttactt tcaccagcgt ttctgggtga gcaaaaacag gaaggcaaaa tgccgcaaaa aagggaataa gggcgacacg gaaatgttga atactcatac tcttcctttt tcaatattat tgaagcattt atcagggtta ttgtctcatg agcggataca tatttgaatg tatttagaaa aataaacaaa taggggttcc gcgcacattt ccccgaaaag tgccacctaa attgtaagcg ttaatatttt gttaaaattc gcgttaaatt tttgttaaat cagctcattt tttaaccaat aggccgaaat cggcaaaatc ccttataaat caaaagaata gaccgagata gggttgagtg ttgttccagt ttggaacaag agtccactat taaagaacgt ggactccaac gtcaaagggc gaaaaaccgt ctatcagggc gatggcccac tacgtgaacc atcaccctaa tcaagttttt tggggtcgag gtgccgtaaa gcactaaatc ggaaccctaa agggagcccc cgatttagag cttgacgggg aaagccggcg aacgtggcga gaaaggaagg gaagaaagcg aaaggagcgg gcgctagggc gctggcaagt gtagcggtca cgctgcgcgt aaccaccaca cccgccgcgc ttaatgcgcc gctacagggc gcgtcccatt cgccattcag gctgcgcaac tgttgggaag ggcgatcggt gcgggcctct tcgctattac gccagctggc gaaaggggga tgtgctgcaa ggcgattaag ttgggtaacg ccagggtttt cccagtcacg acgttgtaaa acgacggcca gtgagcgcgc gtaatacgac tcactatagg gcgaattggg taccgggccc cccctcgagg tcgacggtat cgggggagct cgcagggtct ccattttgaa gcgggaggtt tgaacgcgca gccgccatgc cggggtttta cgagattgtg attaaggtcc ccagcgacct tgacgagcat ctgcccggca tttctgacag ctttgtgaac tgggtggccg agaaggaatg ggagttgccg ccagattctg acatggatct gaatctgatt gagcaggcac ccctgaccgt ggccgagaag ctgcagcgcg actttctgac ggaatggcgc cgtgtgagta aggccccgga ggctcttttc tttgtgcaat ttgagaaggg agagagctac ttccacatgc acgtgctcgt ggaaaccacc ggggtgaaat c
2.プラスミドpAAV-RC2
プラスミドpAAV-RC2のコード鎖(配列番号2):
ccgggccccc cctcgaggtc gacggtatcg ggggagctcg cagggtctcc attttgaagc gggaggtttg aacgcgcagc cgccatgccg gggttttacg agattgtgat taaggtcccc agcgaccttg acgagcatct gcccggcatt tctgacagct ttgtgaactg ggtggccgag aaggaatggg agttgccgcc agattctgac atggatctga atctgattga gcaggcaccc ctgaccgtgg ccgagaagct gcagcgcgac tttctgacgg aatggcgccg tgtgagtaag gccccggagg ctcttttctt tgtgcaattt gagaagggag agagctactt ccacatgcac gtgctcgtgg aaaccaccgg ggtgaaatcc atggttttgg gacgtttcct gagtcagatt cgcgaaaaac tgattcagag aatttaccgc gggatcgagc cgactttgcc aaactggttc gcggtcacaa agaccagaaa tggcgccgga ggcgggaaca aggtggtgga tgagtgctac atccccaatt acttgctccc caaaacccag cctgagctcc agtgggcgtg gactaatatg gaacagtatt taagcgcctg tttgaatctc acggagcgta aacggttggt ggcgcagcat ctgacgcacg tgtcgcagac gcaggagcag aacaaagaga atcagaatcc caattctgat gcgccggtga tcagatcaaa aacttcagcc aggtacatgg agctggtcgg gtggctcgtg gacaagggga ttacctcgga gaagcagtgg atccaggagg accaggcctc atacatctcc ttcaatgcgg cctccaactc gcggtcccaa atcaaggctg ccttggacaa tgcgggaaag attatgagcc tgactaaaac cgcccccgac tacctggtgg gccagcagcc cgtggaggac atttccagca atcggattta taaaattttg gaactaaacg ggtacgatcc ccaatatgcg gcttccgtct ttctgggatg ggccacgaaa aagttcggca agaggaacac catctggctg tttgggcctg caactaccgg gaagaccaac atcgcggagg ccatagccca cactgtgccc ttctacgggt gcgtaaactg gaccaatgag aactttccct tcaacgactg tgtcgacaag atggtgatct ggtgggagga ggggaagatg accgccaagg tcgtggagtc ggccaaagcc attctcggag gaagcaaggt gcgcgtggac cagaaatgca agtcctcggc ccagatagac ccgactcccg tgatcgtcac ctccaacacc aacatgtgcg ccgtgattga cgggaactca acgaccttcg aacaccagca gccgttgcaa gaccggatgt tcaaatttga actcacccgc cgtctggatc atgactttgg gaaggtcacc aagcaggaag tcaaagactt tttccggtgg gcaaaggatc acgtggttga ggtggagcat gaattctacg tcaaaaaggg tggagccaag aaaagacccg cccccagtga cgcagatata agtgagccca aacgggtgcg cgagtcagtt gcgcagccat cgacgtcaga cgcggaagct tcgatcaact acgcagacag gtaccaaaac aaatgttctc gtcacgtggg catgaatctg atgctgtttc cctgcagaca atgcgagaga atgaatcaga attcaaatat ctgcttcact cacggacaga aagactgttt agagtgcttt cccgtgtcag aatctcaacc cgtttctgtc gtcaaaaagg cgtatcagaa actgtgctac attcatcata tcatgggaaa ggtgccagac gcttgcactg cctgcgatct ggtcaatgtg gatttggatg actgcatctt tgaacaataa atgatttaaa tcaggtatgg ctgccgatgg ttatcttcca gattggctcg aggacactct ctctgaagga ataagacagt ggtggaagct caaacctggc ccaccaccac caaagcccgc agagcggcat aaggacgaca gcaggggtct tgtgcttcct gggtacaagt acctcggacc cttcaacgga ctcgacaagg gagagccggt caacgaggca gacgccgcgg ccctcgagca cgacaaagcc tacgaccggc agctcgacag cggagacaac ccgtacctca agtacaacca cgccgacgcg gagtttcagg agcgccttaa agaagatacg tcttttgggg gcaacctcgg acgagcagtc ttccaggcga aaaagagggt tcttgaacct ctgggcctgg ttgaggaacc tgttaagacg gctccgggaa aaaagaggcc ggtagagcac tctcctgtgg agccagactc ctcctcggga accggaaagg cgggccagca gcctgcaaga aaaagattga attttggtca gactggagac gcagactcag tacctgaccc ccagcctctc ggacagccac cagcagcccc ctctggtctg ggaactaata cgatggctac aggcagtggc gcaccaatgg cagacaataa cgagggcgcc gacggagtgg gtaattcctc gggaaattgg cattgcgatt ccacatggat gggcgacaga gtcatcacca ccagcacccg aacctgggcc ctgcccacct acaacaacca cctctacaaa caaatttcca gccaatcagg agcctcgaac gacaatcact actttggcta cagcacccct tgggggtatt ttgacttcaa cagattccac tgccactttt caccacgtga ctggcaaaga ctcatcaaca acaactgggg attccgaccc aagagactca acttcaagct ctttaacatt caagtcaaag aggtcacgca gaatgacggt acgacgacga ttgccaataa ccttaccagc acggttcagg tgtttactga ctcggagtac cagctcccgt acgtcctcgg ctcggcgcat caaggatgcc tcccgccgtt cccagcagac gtcttcatgg tgccacagta tggatacctc accctgaaca acgggagtca ggcagtagga cgctcttcat tttactgcct ggagtacttt ccttctcaga tgctgcgtac cggaaacaac tttaccttca gctacacttt tgaggacgtt cctttccaca gcagctacgc tcacagccag agtctggacc gtctcatgaa tcctctcatc gaccagtacc tgtattactt gagcagaaca aacactccaa gtggaaccac cacgcagtca aggcttcagt tttctcaggc cggagcgagt gacattcggg accagtctag gaactggctt cctggaccct gttaccgcca gcagcgagta tcaaagacat ctgcggataa caacaacagt gaatactcgt ggactggagc taccaagtac cacctcaatg gcagagactc tctggtgaat ccgggcccgg ccatggcaag ccacaaggac gatgaagaaa agttttttcc tcagagcggg gttctcatct ttgggaagca aggctcagag aaaacaaatg tggacattga aaaggtcatg attacagacg aagaggaaat caggacaacc aatcccgtgg ctacggagca gtatggttct gtatctacca acctccagag aggcaacaga caagcagcta ccgcagatgt caacacacaa ggcgttcttc caggcatggt ctggcaggac agagatgtgt accttcaggg gcccatctgg gcaaagattc cacacacgga cggacatttt cacccctctc ccctcatggg tggattcgga cttaaacacc ctcctccaca gattctcatc aagaacaccc cggtacctgc gaatccttcg accaccttca gtgcggcaaa gtttgcttcc ttcatcacac agtactccac gggacaggtc agcgtggaga tcgagtggga gctgcagaag gaaaacagca aacgctggaa tcccgaaatt cagtacactt ccaactacaa caagtctgtt aatgtggact ttactgtgga cactaatggc gtgtattcag agcctcgccc cattggcacc agatacctga ctcgtaatct gtaattgctt gttaatcaat aaaccgttta attcgtttca gttgaacttt ggtctctgcg tatttctttc ttatctagtt tccatgctct aggatccact agtaacggcc gccagtgtgc tggaattcgg ctttgtagtt aatgattaac ccgccatgct acttatctac gtagccatgc tctagaggtc ctgtattaga ggtcacgtga gtgttttgcg acattttgcg acaccatgtg gtcacgctgg gtatttaagc ccgagtgagc acgcagggtc tccattttga agcgggaggt ttgaacgcgc agccgccaag ccgaattctg cagatatcca aacactggcg gccgctcgac tagagcggcc gccaccgcgg tggagctcca gcttttgttc cctttagtga gggttaattg cgcgcttggc gtaatcatgg tcatagctgt ttcctgtgtg aaattgttat ccgctcacaa ttccacacaa catacgagcc ggaagcataa agtgtaaagc ctggggtgcc taatgagtga gctaactcac attaattgcg ttgcgctcac tgcccgcttt ccagtcggga aacctgtcgt gccagctgca ttaatgaatc ggccaacgcg cggggagagg cggtttgcgt attgggcgct cttccgcttc ctcgctcact gactcgctgc gctcggtcgt tcggctgcgg cgagcggtat cagctcactc aaaggcggta atacggttat ccacagaatc aggggataac gcaggaaaga acatgtgagc aaaaggccag caaaaggcca ggaaccgtaa aaaggccgcg ttgctggcgt ttttccatag gctccgcccc cctgacgagc atcacaaaaa tcgacgctca agtcagaggt ggcgaaaccc gacaggacta taaagatacc aggcgtttcc ccctggaagc tccctcgtgc gctctcctgt tccgaccctg ccgcttaccg gatacctgtc cgcctttctc ccttcgggaa gcgtggcgct ttctcatagc tcacgctgta ggtatctcag ttcggtgtag gtcgttcgct ccaagctggg ctgtgtgcac gaaccccccg ttcagcccga ccgctgcgcc ttatccggta actatcgtct tgagtccaac ccggtaagac acgacttatc gccactggca gcagccactg gtaacaggat tagcagagcg aggtatgtag gcggtgctac agagttcttg aagtggtggc ctaactacgg ctacactaga agaacagtat ttggtatctg cgctctgctg aagccagtta ccttcggaaa aagagttggt agctcttgat ccggcaaaca aaccaccgct ggtagcggtg gtttttttgt ttgcaagcag cagattacgc gcagaaaaaa aggatctcaa gaagatcctt tgatcttttc tacggggtct gacgctcagt ggaacgaaaa ctcacgttaa gggattttgg tcatgagatt atcaaaaagg atcttcacct agatcctttt aaattaaaaa tgaagtttta aatcaatcta aagtatatat gagtaaactt ggtctgacag ttaccaatgc ttaatcagtg aggcacctat ctcagcgatc tgtctatttc gttcatccat agttgcctga ctccccgtcg tgtagataac tacgatacgg gagggcttac catctggccc cagtgctgca atgataccgc gagacccacg ctcaccggct ccagatttat cagcaataaa ccagccagcc ggaagggccg agcgcagaag tggtcctgca actttatccg cctccatcca gtctattaat tgttgccggg aagctagagt aagtagttcg ccagttaata gtttgcgcaa cgttgttgcc attgctacag gcatcgtggt gtcacgctcg tcgtttggta tggcttcatt cagctccggt tcccaacgat caaggcgagt tacatgatcc cccatgttgt gcaaaaaagc ggttagctcc ttcggtcctc cgatcgttgt cagaagtaag ttggccgcag tgttatcact catggttatg gcagcactgc ataattctct tactgtcatg ccatccgtaa gatgcttttc tgtgactggt gagtactcaa ccaagtcatt ctgagaatag tgtatgcggc gaccgagttg ctcttgcccg gcgtcaatac gggataatac cgcgccacat agcagaactt taaaagtgct catcattgga aaacgttctt cggggcgaaa actctcaagg atcttaccgc tgttgagatc cagttcgatg taacccactc gtgcacccaa ctgatcttca gcatctttta ctttcaccag cgtttctggg tgagcaaaaa caggaaggca aaatgccgca aaaaagggaa taagggcgac acggaaatgt tgaatactca tactcttcct ttttcaatat tattgaagca tttatcaggg ttattgtctc atgagcggat acatatttga atgtatttag aaaaataaac aaataggggt tccgcgcaca tttccccgaa aagtgccacc taaattgtaa gcgttaatat tttgttaaaa ttcgcgttaa atttttgtta aatcagctca ttttttaacc aataggccga aatcggcaaa atcccttata aatcaaaaga atagaccgag atagggttga gtgttgttcc agtttggaac aagagtccac tattaaagaa cgtggactcc aacgtcaaag ggcgaaaaac cgtctatcag ggcgatggcc cactacgtga accatcaccc taatcaagtt ttttggggtc gaggtgccgt aaagcactaa atcggaaccc taaagggagc ccccgattta gagcttgacg gggaaagccg gcgaacgtgg cgagaaagga agggaagaaa gcgaaaggag cgggcgctag ggcgctggca agtgtagcgg tcacgctgcg cgtaaccacc acacccgccg cgcttaatgc gccgctacag ggcgcgtccc attcgccatt caggctgcgc aactgttggg aagggcgatc ggtgcgggcc tcttcgctat tacgccagct ggcgaaaggg ggatgtgctg caaggcgatt aagttgggta acgccagggt tttcccagtc acgacgttgt aaaacgacgg ccagtgagcg cgcgtaatac gactcactat agggcgaatt gggta
3.プラスミドpAAV-RC5
プラスミドpAAV-RC5のコード鎖(配列番号3):
catggttttg ggacgtttcc tgagtcagat tcgcgaaaaa ctgattcaga gaatttaccg cgggatcgag ccgactttgc caaactggtt cgcggtcaca aagaccagaa atggcgccgg aggcgggaac aaggtggtgg atgagtgcta catccccaat tacttgctcc ccaaaaccca gcctgagctc cagtgggcgt ggactaatat ggaacagtat ttaagcgcct gtttgaatct cacggagcgt aaacggttgg tggcgcagca tctgacgcac gtgtcgcaga cgcaggagca gaacaaagag aatcagaatc ccaattctga tgcgccggtg atcagatcaa aaacttcagc caggtacatg gagctggtcg ggtggctcgt ggacaagggg attacctcgg agaagcagtg gatccaggag gaccaggcct catacatctc cttcaatgcg gcctccaact cgcggtccca aatcaaggct gccttggaca atgcgggaaa gattatgagc ctgactaaaa ccgcccccga ctacctggtg ggccagcagc ccgtggagga catttccagc aatcggattt ataaaatttt ggaactaaac gggtacgatc cccaatatgc ggcttccgtc tttctgggat gggccacgaa aaagttcggc aagaggaaca ccatctggct gtttgggcct gcaactaccg ggaagaccaa catcgcggag gccatagccc acactgtgcc cttctacggg tgcgtaaact ggaccaatga gaactttccc ttcaacgact gtgtcgacaa gatggtgatc tggtgggagg aggggaagat gaccgccaag gtcgtggagt cggccaaagc cattctcgga ggaagcaagg tgcgcgtgga ccagaaatgc aagtcctcgg cccagataga cccgactccc gtgatcgtca cctccaacac caacatgtgc gccgtgattg acgggaactc aacgaccttc gaacaccagc agccgttgca agaccggatg ttcaaatttg aactcacccg ccgtctggat catgactttg ggaaggtcac caagcaggaa gtcaaagact ttttccggtg ggcaaaggat cacgtggttg aggtggagca tgaattctac gtcaaaaagg gtggagccaa gaaaagaccc gcccccagtg acgcagatat aagtgagccc aaacgggtgc gcgagtcagt tgcgcagcca tcgacgtcag acgcggaagc ttcgatcaac tacgcagaca ggtaccaaaa caaatgttct cgtcacgtgg gcatgaatct gatgctgttt ccctgcagac aatgcgagag aatgaatcag aattcaaata tctgcttcac tcacggacag aaagactgtt tagagtgctt tcccgtgtca gaatctcaac ccgtttctgt cgtcaaaaag gcgtatcaga aactgtgcta cattcatcat atcatgggaa aggtgccaga cgcttgcact gcctgcgatc tggtcaatgt ggatttggat gactgcatct ttgaacaata aatgatttaa atcaggtatg tcttttgttg atcaccctcc agattggttg gaagaagttg gtgaaggtct tcgcgagttt ttgggccttg aagcgggccc accgaaacca aaacccaatc agcagcatca agatcaagcc cgtggtcttg tgctgcctgg ttataactat ctcggacccg gaaacggtct cgatcgagga gagcctgtca acagggcaga cgaggtcgcg cgagagcacg acatctcgta caacgagcag cttgaggcgg gagacaaccc ctacctcaag tacaaccacg cggacgccga gtttcaggag aagctcgccg acgacacatc cttcggggga aacctcggaa aggcagtctt tcaggccaag aaaagggttc tcgaaccttt tggcctggtt gaagagggtg ctaagacggc ccctaccgga aagcggatag acgaccactt tccaaaaaga aagaaggctc ggaccgaaga ggactccaag ccttccacct cgtcagacgc cgaagctgga cccagcggat cccagcagct gcaaatccca gcccaaccag cctcaagttt gggagctgat acaatgtctg cgggaggtgg cggcccattg ggcgacaata accaaggtgc cgatggagtg ggcaatgcct cgggagattg gcattgcgat tccacgtgga tgggggacag agtcgtcacc aagtccaccc gaacctgggt gctgcccagc tacaacaacc accagtaccg agagatcaaa agcggctccg tcgacggaag caacgccaac gcctactttg gatacagcac cccctggggg tactttgact ttaaccgctt ccacagccac tggagccccc gagactggca aagactcatc aacaactact ggggcttcag accccggtcc ctcagagtca aaatcttcaa cattcaagtc aaagaggtca cggtgcagga ctccaccacc accatcgcca acaacctcac ctccaccgtc caagtgttta cggacgacga ctaccagctg ccctacgtcg tcggcaacgg gaccgaggga tgcctgccgg ccttccctcc gcaggtcttt acgctgccgc agtacggtta cgcgacgctg aaccgcgaca acacagaaaa tcccaccgag aggagcagct tcttctgcct agagtacttt cccagcaaga tgctgagaac gggcaacaac tttgagttta cctacaactt tgaggaggtg cccttccact ccagcttcgc tcccagtcag aacctgttca agctggccaa cccgctggtg gaccagtact tgtaccgctt cgtgagcaca aataacactg gcggagtcca gttcaacaag aacctggccg ggagatacgc caacacctac aaaaactggt tcccggggcc catgggccga acccagggct ggaacctggg ctccggggtc aaccgcgcca gtgtcagcgc cttcgccacg accaatagga tggagctcga gggcgcgagt taccaggtgc ccccgcagcc gaacggcatg accaacaacc tccagggcag caacacctat gccctggaga acactatgat cttcaacagc cagccggcga acccgggcac caccgccacg tacctcgagg gcaacatgct catcaccagc gagagcgaga cgcagccggt gaaccgcgtg gcgtacaacg tcggcgggca gatggccacc aacaaccaga gctccaccac tgcccccgcg accggcacgt acaacctcca ggaaatcgtg cccggcagcg tgtggatgga gagggacgtg tacctccaag gacccatctg ggccaagatc ccagagacgg gggcgcactt tcacccctct ccggccatgg gcggattcgg actcaaacac ccaccgccca tgatgctcat caagaacacg cctgtgcccg gaaatatcac cagcttctcg gacgtgcccg tcagcagctt catcacccag tacagcaccg ggcaggtcac cgtggagatg gagtgggagc tcaagaagga aaactccaag aggtggaacc cagagatcca gtacacaaac aactacaacg acccccagtt tgtggacttt gccccggaca gcaccgggga atacagaacc accagaccta tcggaacccg ataccttacc cgaccccttt aaggcgcgcc accggttgct tgttaatcaa taaaccgttt aattcgtttc agttgaactt tggtctctgc gtatttcttt cttatctagt ttccatgctc taggatccac tagtaacggc cgccagtgtg ctggaattcg gctttgtagt taatgattaa cccgccatgc tacttatcta cgtagccatg ctctagaggt cctgtattag aggtcacgtg agtgttttgc gacattttgc gacaccatgt ggtcacgctg ggtatttaag cccgagtgag cacgcagggt ctccattttg aagcgggagg tttgaacgcg cagccgccaa gccgaattct gcagatatcc aaacactggc ggccgctcga ctagagcggc cgccaccgcg gtggagctcc agcttttgtt ccctttagtg agggttaatt gcgcgcttgg cgtaatcatg gtcatagctg tttcctgtgt gaaattgtta tccgctcaca attccacaca acatacgagc cggaagcata aagtgtaaag cctggggtgc ctaatgagtg agctaactca cattaattgc gttgcgctca ctgcccgctt tccagtcggg aaacctgtcg tgccagctgc attaatgaat cggccaacgc gcggggagag gcggtttgcg tattgggcgc tcttccgctt cctcgctcac tgactcgctg cgctcggtcg ttcggctgcg gcgagcggta tcagctcact caaaggcggt aatacggtta tccacagaat caggggataa cgcaggaaag aacatgtgag caaaaggcca gcaaaaggcc aggaaccgta aaaaggccgc gttgctggcg tttttccata ggctccgccc ccctgacgag catcacaaaa atcgacgctc aagtcagagg tggcgaaacc cgacaggact ataaagatac caggcgtttc cccctggaag ctccctcgtg cgctctcctg ttccgaccct gccgcttacc ggatacctgt ccgcctttct cccttcggga agcgtggcgc tttctcatag ctcacgctgt aggtatctca gttcggtgta ggtcgttcgc tccaagctgg gctgtgtgca cgaacccccc gttcagcccg accgctgcgc cttatccggt aactatcgtc ttgagtccaa cccggtaaga cacgacttat cgccactggc agcagccact ggtaacagga ttagcagagc gaggtatgta ggcggtgcta cagagttctt gaagtggtgg cctaactacg gctacactag aagaacagta tttggtatct gcgctctgct gaagccagtt accttcggaa aaagagttgg tagctcttga tccggcaaac aaaccaccgc tggtagcggt ggtttttttg tttgcaagca gcagattacg cgcagaaaaa aaggatctca agaagatcct ttgatctttt ctacggggtc tgacgctcag tggaacgaaa actcacgtta agggattttg gtcatgagat tatcaaaaag gatcttcacc tagatccttt taaattaaaa atgaagtttt aaatcaatct aaagtatata tgagtaaact tggtctgaca gttaccaatg cttaatcagt gaggcaccta tctcagcgat ctgtctattt cgttcatcca tagttgcctg actccccgtc gtgtagataa ctacgatacg ggagggctta ccatctggcc ccagtgctgc aatgataccg cgagacccac gctcaccggc tccagattta tcagcaataa accagccagc cggaagggcc gagcgcagaa gtggtcctgc aactttatcc gcctccatcc agtctattaa ttgttgccgg gaagctagag taagtagttc gccagttaat agtttgcgca acgttgttgc cattgctaca ggcatcgtgg tgtcacgctc gtcgtttggt atggcttcat tcagctccgg ttcccaacga tcaaggcgag ttacatgatc ccccatgttg tgcaaaaaag cggttagctc cttcggtcct ccgatcgttg tcagaagtaa gttggccgca gtgttatcac tcatggttat ggcagcactg cataattctc ttactgtcat gccatccgta agatgctttt ctgtgactgg tgagtactca accaagtcat tctgagaata gtgtatgcgg cgaccgagtt gctcttgccc ggcgtcaata cgggataata ccgcgccaca tagcagaact ttaaaagtgc tcatcattgg aaaacgttct tcggggcgaa aactctcaag gatcttaccg ctgttgagat ccagttcgat gtaacccact cgtgcaccca actgatcttc agcatctttt actttcacca gcgtttctgg gtgagcaaaa acaggaaggc aaaatgccgc aaaaaaggga ataagggcga cacggaaatg ttgaatactc atactcttcc tttttcaata ttattgaagc atttatcagg gttattgtct catgagcgga tacatatttg aatgtattta gaaaaataaa caaatagggg ttccgcgcac atttccccga aaagtgccac ctaaattgta agcgttaata ttttgttaaa attcgcgtta aatttttgtt aaatcagctc attttttaac caataggccg aaatcggcaa aatcccttat aaatcaaaag aatagaccga gatagggttg agtgttgttc cagtttggaa caagagtcca ctattaaaga acgtggactc caacgtcaaa gggcgaaaaa ccgtctatca gggcgatggc ccactacgtg aaccatcacc ctaatcaagt tttttggggt cgaggtgccg taaagcacta aatcggaacc ctaaagggag cccccgattt agagcttgac ggggaaagcc ggcgaacgtg gcgagaaagg aagggaagaa agcgaaagga gcgggcgcta gggcgctggc aagtgtagcg gtcacgctgc gcgtaaccac cacacccgcc gcgcttaatg cgccgctaca gggcgcgtcc cattcgccat tcaggctgcg caactgttgg gaagggcgat cggtgcgggc ctcttcgcta ttacgccagc tggcgaaagg gggatgtgct gcaaggcgat taagttgggt aacgccaggg ttttcccagt cacgacgttg taaaacgacg gccagtgagc gcgcgtaata cgactcacta tagggcgaat tgggtaccgg gccccccctc gaggtcgacg gtatcggggg agctcgcagg gtctccattt tgaagcggga ggtttgaacg cgcagccgcc atgccggggt tttacgagat tgtgattaag gtccccagcg accttgacga gcatctgccc ggcatttctg acagctttgt gaactgggtg gccgagaagg aatgggagtt gccgccagat tctgacatgg atctgaatct gattgagcag gcacccctga ccgtggccga gaagctgcag cgcgactttc tgacggaatg gcgccgtgtg agtaaggccc cggaggctct tttctttgtg caatttgaga agggagagag ctacttccac atgcacgtgc tcgtggaaac caccggggtg aaatc
4.プラスミドpAAV-RC6
プラスミドpAAV-RC6のコード鎖(配列番号4):
catggttttg ggacgtttcc tgagtcagat tcgcgaaaaa ctgattcaga gaatttaccg cgggatcgag ccgactttgc caaactggtt cgcggtcaca aagaccagaa atggcgccgg aggcgggaac aaggtggtgg atgagtgcta catccccaat tacttgctcc ccaaaaccca gcctgagctc cagtgggcgt ggactaatat ggaacagtat ttaagcgcct gtttgaatct cacggagcgt aaacggttgg tggcgcagca tctgacgcac gtgtcgcaga cgcaggagca gaacaaagag aatcagaatc ccaattctga tgcgccggtg atcagatcaa aaacttcagc caggtacatg gagctggtcg ggtggctcgt ggacaagggg attacctcgg agaagcagtg gatccaggag gaccaggcct catacatctc cttcaatgcg gcctccaact cgcggtccca aatcaaggct gccttggaca atgcgggaaa gattatgagc ctgactaaaa ccgcccccga ctacctggtg ggccagcagc ccgtggagga catttccagc aatcggattt ataaaatttt ggaactaaac gggtacgatc cccaatatgc ggcttccgtc tttctgggat gggccacgaa aaagttcggc aagaggaaca ccatctggct gtttgggcct gcaactaccg ggaagaccaa catcgcggag gccatagccc acactgtgcc cttctacggg tgcgtaaact ggaccaatga gaactttccc ttcaacgact gtgtcgacaa gatggtgatc tggtgggagg aggggaagat gaccgccaag gtcgtggagt cggccaaagc cattctcgga ggaagcaagg tgcgcgtgga ccagaaatgc aagtcctcgg cccagataga cccgactccc gtgatcgtca cctccaacac caacatgtgc gccgtgattg acgggaactc aacgaccttc gaacaccagc agccgttgca agaccggatg ttcaaatttg aactcacccg ccgtctggat catgactttg ggaaggtcac caagcaggaa gtcaaagact ttttccggtg ggcaaaggat cacgtggttg aggtggagca tgaattctac gtcaaaaagg gtggagccaa gaaaagaccc gcccccagtg acgcagatat aagtgagccc aaacgggtgc gcgagtcagt tgcgcagcca tcgacgtcag acgcggaagc ttcgatcaac tacgcagaca ggtaccaaaa caaatgttct cgtcacgtgg gcatgaatct gatgctgttt ccctgcagac aatgcgagag aatgaatcag aattcaaata tctgcttcac tcacggacag aaagactgtt tagagtgctt tcccgtgtca gaatctcaac ccgtttctgt cgtcaaaaag gcgtatcaga aactgtgcta cattcatcat atcatgggaa aggtgccaga cgcttgcact gcctgcgatc tggtcaatgt ggatttggat gactgcatct ttgaacaata aatgatttaa atcaggtatg gctgccgatg gttatcttcc agattggctc gaggacaacc tctctgaggg cattcgcgag tggtgggact tgaaacctgg agccccgaaa cccaaagcca accagcaaaa gcaggacgac ggccggggtc tggtgcttcc tggctacaag tacctcggac ccttcaacgg actcgacaag ggggagcccg tcaacgcggc ggatgcagcg gccctcgagc acgacaaggc ctacgaccag cagctcaaag cgggtgacaa tccgtacctg cggtataacc acgccgacgc cgagtttcag gagcgtctgc aagaagatac gtcttttggg ggcaacctcg ggcgagcagt cttccaggcc aagaagaggg ttctcgaacc ttttggtctg gttgaggaag gtgctaagac ggctcctgga aagaaacgtc cggtagagca gtcgccacaa gagccagact cctcctcggg cattggcaag acaggccagc agcccgctaa aaagagactc aattttggtc agactggcga ctcagagtca gtccccgacc cacaacctct cggagaacct ccagcaaccc ccgctgctgt gggacctact acaatggctt caggcggtgg cgcaccaatg gcagacaata acgaaggcgc cgacggagtg ggtaatgcct caggaaattg gcattgcgat tccacatggc tgggcgacag agtcatcacc accagcaccc gaacatgggc cttgcccacc tataacaacc acctctacaa gcaaatctcc agtgcttcaa cgggggccag caacgacaac cactacttcg gctacagcac cccctggggg tattttgatt tcaacagatt ccactgccat ttctcaccac gtgactggca gcgactcatc aacaacaatt ggggattccg gcccaagaga ctcaacttca agctcttcaa catccaagtc aaggaggtca cgacgaatga tggcgtcacg accatcgcta ataaccttac cagcacggtt caagtcttct cggactcgga gtaccagttg ccgtacgtcc tcggctctgc gcaccagggc tgcctccctc cgttcccggc ggacgtgttc atgattccgc agtacggcta cctaacgctc aacaatggca gccaggcagt gggacggtca tccttttact gcctggaata tttcccatcg cagatgctga gaacgggcaa taactttacc ttcagctaca ccttcgagga cgtgcctttc cacagcagct acgcgcacag ccagagcctg gaccggctga tgaatcctct catcgaccag tacctgtatt acctgaacag aactcagaat cagtccggaa gtgcccaaaa caaggacttg ctgtttagcc gggggtctcc agctggcatg tctgttcagc ccaaaaactg gctacctgga ccctgttacc ggcagcagcg cgtttctaaa acaaaaacag acaacaacaa cagcaacttt acctggactg gtgcttcaaa atataacctt aatgggcgtg aatctataat caaccctggc actgctatgg cctcacacaa agacgacaaa gacaagttct ttcccatgag cggtgtcatg atttttggaa aggagagcgc cggagcttca aacactgcat tggacaatgt catgatcaca gacgaagagg aaatcaaagc cactaacccc gtggccaccg aaagatttgg gactgtggca gtcaatctcc agagcagcag cacagaccct gcgaccggag atgtgcatgt tatgggagcc ttacctggaa tggtgtggca agacagagac gtatacctgc agggtcctat ttgggccaaa attcctcaca cggatggaca ctttcacccg tctcctctca tgggcggctt tggacttaag cacccgcctc ctcagatcct catcaaaaac acgcctgttc ctgcgaatcc tccggcagag ttttcggcta caaagtttgc ttcattcatc acccagtatt ccacaggaca agtgagcgtg gagattgaat gggagctgca gaaagaaaac agcaaacgct ggaatcccga agtgcagtat acatctaact atgcaaaatc tgccaacgtt gatttcactg tggacaacaa tggactttat actgagcctc gccccattgg cacccgttac ctcacccgtc ccctgtaagg cgcgccaccg gttgcttgtt aatcaataaa ccgtttaatt cgtttcagtt gaactttggt ctctgcgtat ttctttctta tctagtttcc atgctctagg atccactagt aacggccgcc agtgtgctgg aattcggctt tgtagttaat gattaacccg ccatgctact tatctacgta gccatgctct agaggtcctg tattagaggt cacgtgagtg ttttgcgaca ttttgcgaca ccatgtggtc acgctgggta tttaagcccg agtgagcacg cagggtctcc attttgaagc gggaggtttg aacgcgcagc cgccaagccg aattctgcag atatccaaac actggcggcc gctcgactag agcggccgcc accgcggtgg agctccagct tttgttccct ttagtgaggg ttaattgcgc gcttggcgta atcatggtca tagctgtttc ctgtgtgaaa ttgttatccg ctcacaattc cacacaacat acgagccgga agcataaagt gtaaagcctg gggtgcctaa tgagtgagct aactcacatt aattgcgttg cgctcactgc ccgctttcca gtcgggaaac ctgtcgtgcc agctgcatta atgaatcggc caacgcgcgg ggagaggcgg tttgcgtatt gggcgctctt ccgcttcctc gctcactgac tcgctgcgct cggtcgttcg gctgcggcga gcggtatcag ctcactcaaa ggcggtaata cggttatcca cagaatcagg ggataacgca ggaaagaaca tgtgagcaaa aggccagcaa aaggccagga accgtaaaaa ggccgcgttg ctggcgtttt tccataggct ccgcccccct gacgagcatc acaaaaatcg acgctcaagt cagaggtggc gaaacccgac aggactataa agataccagg cgtttccccc tggaagctcc ctcgtgcgct ctcctgttcc gaccctgccg cttaccggat acctgtccgc ctttctccct tcgggaagcg tggcgctttc tcatagctca cgctgtaggt atctcagttc ggtgtaggtc gttcgctcca agctgggctg tgtgcacgaa ccccccgttc agcccgaccg ctgcgcctta tccggtaact atcgtcttga gtccaacccg gtaagacacg acttatcgcc actggcagca gccactggta acaggattag cagagcgagg tatgtaggcg gtgctacaga gttcttgaag tggtggccta actacggcta cactagaaga acagtatttg gtatctgcgc tctgctgaag ccagttacct tcggaaaaag agttggtagc tcttgatccg gcaaacaaac caccgctggt agcggtggtt tttttgtttg caagcagcag attacgcgca gaaaaaaagg atctcaagaa gatcctttga tcttttctac ggggtctgac gctcagtgga acgaaaactc acgttaaggg attttggtca tgagattatc aaaaaggatc ttcacctaga tccttttaaa ttaaaaatga agttttaaat caatctaaag tatatatgag taaacttggt ctgacagtta ccaatgctta atcagtgagg cacctatctc agcgatctgt ctatttcgtt catccatagt tgcctgactc cccgtcgtgt agataactac gatacgggag ggcttaccat ctggccccag tgctgcaatg ataccgcgag acccacgctc accggctcca gatttatcag caataaacca gccagccgga agggccgagc gcagaagtgg tcctgcaact ttatccgcct ccatccagtc tattaattgt tgccgggaag ctagagtaag tagttcgcca gttaatagtt tgcgcaacgt tgttgccatt gctacaggca tcgtggtgtc acgctcgtcg tttggtatgg cttcattcag ctccggttcc caacgatcaa ggcgagttac atgatccccc atgttgtgca aaaaagcggt tagctccttc ggtcctccga tcgttgtcag aagtaagttg gccgcagtgt tatcactcat ggttatggca gcactgcata attctcttac tgtcatgcca tccgtaagat gcttttctgt gactggtgag tactcaacca agtcattctg agaatagtgt atgcggcgac cgagttgctc ttgcccggcg tcaatacggg ataataccgc gccacatagc agaactttaa aagtgctcat cattggaaaa cgttcttcgg ggcgaaaact ctcaaggatc ttaccgctgt tgagatccag ttcgatgtaa cccactcgtg cacccaactg atcttcagca tcttttactt tcaccagcgt ttctgggtga gcaaaaacag gaaggcaaaa tgccgcaaaa aagggaataa gggcgacacg gaaatgttga atactcatac tcttcctttt tcaatattat tgaagcattt atcagggtta ttgtctcatg agcggataca tatttgaatg tatttagaaa aataaacaaa taggggttcc gcgcacattt ccccgaaaag tgccacctaa attgtaagcg ttaatatttt gttaaaattc gcgttaaatt tttgttaaat cagctcattt tttaaccaat aggccgaaat cggcaaaatc ccttataaat caaaagaata gaccgagata gggttgagtg ttgttccagt ttggaacaag agtccactat taaagaacgt ggactccaac gtcaaagggc gaaaaaccgt ctatcagggc gatggcccac tacgtgaacc atcaccctaa tcaagttttt tggggtcgag gtgccgtaaa gcactaaatc ggaaccctaa agggagcccc cgatttagag cttgacgggg aaagccggcg aacgtggcga gaaaggaagg gaagaaagcg aaaggagcgg gcgctagggc gctggcaagt gtagcggtca cgctgcgcgt aaccaccaca cccgccgcgc ttaatgcgcc gctacagggc gcgtcccatt cgccattcag gctgcgcaac tgttgggaag ggcgatcggt gcgggcctct tcgctattac gccagctggc gaaaggggga tgtgctgcaa ggcgattaag ttgggtaacg ccagggtttt cccagtcacg acgttgtaaa acgacggcca gtgagcgcgc gtaatacgac tcactatagg gcgaattggg taccgggccc cccctcgagg tcgacggtat cgggggagct cgcagggtct ccattttgaa gcgggaggtt tgaacgcgca gccgccatgc cggggtttta cgagattgtg attaaggtcc ccagcgacct tgacgagcat ctgcccggca tttctgacag ctttgtgaac tgggtggccg agaaggaatg ggagttgccg ccagattctg acatggatct gaatctgatt gagcaggcac ccctgaccgt ggccgagaag ctgcagcgcg actttctgac ggaatggcgc cgtgtgagta aggccccgga ggctcttttc tttgtgcaat ttgagaaggg agagagctac ttccacatgc acgtgctcgt ggaaaccacc ggggtgaaat c
5.pAAV-RC7プラスミド
プラスミドpAAV-RC7のコード鎖(配列番号5):
catggttttg ggacgtttcc tgagtcagat tcgcgaaaaa ctgattcaga gaatttaccg cgggatcgag ccgactttgc caaactggtt cgcggtcaca aagaccagaa atggcgccgg aggcgggaac aaggtggtgg atgagtgcta catccccaat tacttgctcc ccaaaaccca gcctgagctc cagtgggcgt ggactaatat ggaacagtat ttaagcgcct gtttgaatct cacggagcgt aaacggttgg tggcgcagca tctgacgcac gtgtcgcaga cgcaggagca gaacaaagag aatcagaatc ccaattctga tgcgccggtg atcagatcaa aaacttcagc caggtacatg gagctggtcg ggtggctcgt ggacaagggg attacctcgg agaagcagtg gatccaggag gaccaggcct catacatctc cttcaatgcg gcctccaact cgcggtccca aatcaaggct gccttggaca atgcgggaaa gattatgagc ctgactaaaa ccgcccccga ctacctggtg ggccagcagc ccgtggagga catttccagc aatcggattt ataaaatttt ggaactaaac gggtacgatc cccaatatgc ggcttccgtc tttctgggat gggccacgaa aaagttcggc aagaggaaca ccatctggct gtttgggcct gcaactaccg ggaagaccaa catcgcggag gccatagccc acactgtgcc cttctacggg tgcgtaaact ggaccaatga gaactttccc ttcaacgact gtgtcgacaa gatggtgatc tggtgggagg aggggaagat gaccgccaag gtcgtggagt cggccaaagc cattctcgga ggaagcaagg tgcgcgtgga ccagaaatgc aagtcctcgg cccagataga cccgactccc gtgatcgtca cctccaacac caacatgtgc gccgtgattg acgggaactc aacgaccttc gaacaccagc agccgttgca agaccggatg ttcaaatttg aactcacccg ccgtctggat catgactttg ggaaggtcac caagcaggaa gtcaaagact ttttccggtg ggcaaaggat cacgtggttg aggtggagca tgaattctac gtcaaaaagg gtggagccaa gaaaagaccc gcccccagtg acgcagatat aagtgagccc aaacgggtgc gcgagtcagt tgcgcagcca tcgacgtcag acgcggaagc ttcgatcaac tacgcagaca ggtaccaaaa caaatgttct cgtcacgtgg gcatgaatct gatgctgttt ccctgcagac aatgcgagag aatgaatcag aattcaaata tctgcttcac tcacggacag aaagactgtt tagagtgctt tcccgtgtca gaatctcaac ccgtttctgt cgtcaaaaag gcgtatcaga aactgtgcta cattcatcat atcatgggaa aggtgccaga cgcttgcact gcctgcgatc tggtcaatgt ggatttggat gactgcatct ttgaacaata aatgatttaa atcaggtatg gctgccgatg gttatcttcc agattggctc gaggacaacc tctctgaggg cattcgcgag tggtgggacc tgaaacctgg agccccgaaa cccaaagcca accagcaaaa gcaggacaac ggccggggtc tggtgcttcc tggctacaag tacctcggac ccttcaacgg actcgacaag ggggagcccg tcaacgcggc ggacgcagcg gccctcgagc acgacaaggc ctacgaccag cagctcaaag cgggtgacaa tccgtacctg cggtataacc acgccgacgc cgagtttcag gagcgtctgc aagaagatac gtcatttggg ggcaacctcg ggcgagcagt cttccaggcc aagaagcggg ttctcgaacc tctcggtctg gttgaggaag gcgctaagac ggctcctgca aagaagagac cggtagagcc gtcacctcag cgttcccccg actcctccac gggcatcggc aagaaaggcc agcagcccgc cagaaagaga ctcaatttcg gtcagactgg cgactcagag tcagtccccg accctcaacc tctcggagaa cctccagcag cgccctctag tgtgggatct ggtacagtgg ctgcaggcgg tggcgcacca atggcagaca ataacgaagg tgccgacgga gtgggtaatg cctcaggaaa ttggcattgc gattccacat ggctgggcga cagagtcatt accaccagca cccgaacctg ggccctgccc acctacaaca accacctcta caagcaaatc tccagtgaaa ctgcaggtag taccaacgac aacacctact tcggctacag caccccctgg gggtattttg actttaacag attccactgc cacttctcac cacgtgactg gcagcgactc atcaacaaca actggggatt ccggcccaag aagctgcggt tcaagctctt caacatccag gtcaaggagg tcacgacgaa tgacggcgtt acgaccatcg ctaataacct taccagcacg attcaggtat tctcggactc ggaataccag ctgccgtacg tcctcggctc tgcgcaccag ggctgcctgc ctccgttccc ggcggacgtc ttcatgattc ctcagtacgg ctacctgact ctcaacaatg gcagtcagtc tgtgggacgt tcctccttct actgcctgga gtacttcccc tctcagatgc tgagaacggg caacaacttt gagttcagct acagcttcga ggacgtgcct ttccacagca gctacgcaca cagccagagc ctggaccggc tgatgaatcc cctcatcgac cagtacttgt actacctggc cagaacacag agtaacccag gaggcacagc tggcaatcgg gaactgcagt tttaccaggg cgggccttca actatggccg aacaagccaa gaattggtta cctggacctt gcttccggca acaaagagtc tccaaaacgc tggatcaaaa caacaacagc aactttgctt ggactggtgc caccaaatat cacctgaacg gcagaaactc gttggttaat cccggcgtcg ccatggcaac tcacaaggac gacgaggacc gctttttccc atccagcgga gtcctgattt ttggaaaaac tggagcaact aacaaaacta cattggaaaa tgtgttaatg acaaatgaag aagaaattcg tcctactaat cctgtagcca cggaagaata cgggatagtc agcagcaact tacaagcggc taatactgca gcccagacac aagttgtcaa caaccaggga gccttacctg gcatggtctg gcagaaccgg gacgtgtacc tgcagggtcc catctgggcc aagattcctc acacggatgg caactttcac ccgtctcctt tgatgggcgg ctttggactt aaacatccgc ctcctcagat cctgatcaag aacactcccg ttcccgctaa tcctccggag gtgtttactc ctgccaagtt tgcttcgttc atcacacagt acagcaccgg acaagtcagc gtggaaatcg agtgggagct gcagaaggaa aacagcaagc gctggaaccc ggagattcag tacacctcca actttgaaaa gcagactggt gtggactttg ccgttgacag ccagggtgtt tactctgagc ctcgccctat tggcactcgt tacctcaccc gtaatctgta aggcgcgcca ccggttgctt gttaatcaat aaaccgttta attcgtttca gttgaacttt ggtctctgcg tatttctttc ttatctagtt tccatgctct aggatccact agtaacggcc gccagtgtgc tggaattcgg ctttgtagtt aatgattaac ccgccatgct acttatctac gtagccatgc tctagaggtc ctgtattaga ggtcacgtga gtgttttgcg acattttgcg acaccatgtg gtcacgctgg gtatttaagc ccgagtgagc acgcagggtc tccattttga agcgggaggt ttgaacgcgc agccgccaag ccgaattctg cagatatcca aacactggcg gccgctcgac tagagcggcc gccaccgcgg tggagctcca gcttttgttc cctttagtga gggttaattg cgcgcttggc gtaatcatgg tcatagctgt ttcctgtgtg aaattgttat ccgctcacaa ttccacacaa catacgagcc ggaagcataa agtgtaaagc ctggggtgcc taatgagtga gctaactcac attaattgcg ttgcgctcac tgcccgcttt ccagtcggga aacctgtcgt gccagctgca ttaatgaatc ggccaacgcg cggggagagg cggtttgcgt attgggcgct cttccgcttc ctcgctcact gactcgctgc gctcggtcgt tcggctgcgg cgagcggtat cagctcactc aaaggcggta atacggttat ccacagaatc aggggataac gcaggaaaga acatgtgagc aaaaggccag caaaaggcca ggaaccgtaa aaaggccgcg ttgctggcgt ttttccatag gctccgcccc cctgacgagc atcacaaaaa tcgacgctca agtcagaggt ggcgaaaccc gacaggacta taaagatacc aggcgtttcc ccctggaagc tccctcgtgc gctctcctgt tccgaccctg ccgcttaccg gatacctgtc cgcctttctc ccttcgggaa gcgtggcgct ttctcatagc tcacgctgta ggtatctcag ttcggtgtag gtcgttcgct ccaagctggg ctgtgtgcac gaaccccccg ttcagcccga ccgctgcgcc ttatccggta actatcgtct tgagtccaac ccggtaagac acgacttatc gccactggca gcagccactg gtaacaggat tagcagagcg aggtatgtag gcggtgctac agagttcttg aagtggtggc ctaactacgg ctacactaga agaacagtat ttggtatctg cgctctgctg aagccagtta ccttcggaaa aagagttggt agctcttgat ccggcaaaca aaccaccgct ggtagcggtg gtttttttgt ttgcaagcag cagattacgc gcagaaaaaa aggatctcaa gaagatcctt tgatcttttc tacggggtct gacgctcagt ggaacgaaaa ctcacgttaa gggattttgg tcatgagatt atcaaaaagg atcttcacct agatcctttt aaattaaaaa tgaagtttta aatcaatcta aagtatatat gagtaaactt ggtctgacag ttaccaatgc ttaatcagtg aggcacctat ctcagcgatc tgtctatttc gttcatccat agttgcctga ctccccgtcg tgtagataac tacgatacgg gagggcttac catctggccc cagtgctgca atgataccgc gagacccacg ctcaccggct ccagatttat cagcaataaa ccagccagcc ggaagggccg agcgcagaag tggtcctgca actttatccg cctccatcca gtctattaat tgttgccggg aagctagagt aagtagttcg ccagttaata gtttgcgcaa cgttgttgcc attgctacag gcatcgtggt gtcacgctcg tcgtttggta tggcttcatt cagctccggt tcccaacgat caaggcgagt tacatgatcc cccatgttgt gcaaaaaagc ggttagctcc ttcggtcctc cgatcgttgt cagaagtaag ttggccgcag tgttatcact catggttatg gcagcactgc ataattctct tactgtcatg ccatccgtaa gatgcttttc tgtgactggt gagtactcaa ccaagtcatt ctgagaatag tgtatgcggc gaccgagttg ctcttgcccg gcgtcaatac gggataatac cgcgccacat agcagaactt taaaagtgct catcattgga aaacgttctt cggggcgaaa actctcaagg atcttaccgc tgttgagatc cagttcgatg taacccactc gtgcacccaa ctgatcttca gcatctttta ctttcaccag cgtttctggg tgagcaaaaa caggaaggca aaatgccgca aaaaagggaa taagggcgac acggaaatgt tgaatactca tactcttcct ttttcaatat tattgaagca tttatcaggg ttattgtctc atgagcggat acatatttga atgtatttag aaaaataaac aaataggggt tccgcgcaca tttccccgaa aagtgccacc taaattgtaa gcgttaatat tttgttaaaa ttcgcgttaa atttttgtta aatcagctca ttttttaacc aataggccga aatcggcaaa atcccttata aatcaaaaga atagaccgag atagggttga gtgttgttcc agtttggaac aagagtccac tattaaagaa cgtggactcc aacgtcaaag ggcgaaaaac cgtctatcag ggcgatggcc cactacgtga accatcaccc taatcaagtt ttttggggtc gaggtgccgt aaagcactaa atcggaaccc taaagggagc ccccgattta gagcttgacg gggaaagccg gcgaacgtgg cgagaaagga agggaagaaa gcgaaaggag cgggcgctag ggcgctggca agtgtagcgg tcacgctgcg cgtaaccacc acacccgccg cgcttaatgc gccgctacag ggcgcgtccc attcgccatt caggctgcgc aactgttggg aagggcgatc ggtgcgggcc tcttcgctat tacgccagct ggcgaaaggg ggatgtgctg caaggcgatt aagttgggta acgccagggt tttcccagtc acgacgttgt aaaacgacgg ccagtgagcg cgcgtaatac gactcactat agggcgaatt gggtaccggg ccccccctcg aggtcgacgg tatcggggga gctcgcaggg tctccatttt gaagcgggag gtttgaacgc gcagccgcca tgccggggtt ttacgagatt gtgattaagg tccccagcga ccttgacgag catctgcccg gcatttctga cagctttgtg aactgggtgg ccgagaagga atgggagttg ccgccagatt ctgacatgga tctgaatctg attgagcagg cacccctgac cgtggccgag aagctgcagc gcgactttct gacggaatgg cgccgtgtga gtaaggcccc ggaggctctt ttctttgtgc aatttgagaa gggagagagc tacttccaca tgcacgtgct cgtggaaacc accggggtga aatc
B.例示的な非AAVヘルパー機能提供ポリヌクレオチド
プラスミドpHelper-Kanのコード鎖(配列番号6)
C.例示的なrAAVプラスミドベクター
プラスミドpAV-CMV-EGFPのコード鎖(配列番号7):
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc ccgggcgtcg ggcgaccttt ggtcgcccgg ccctccagtg agcgagcgcg cagagaggga gtggccaact ccatcactag gggttcctgc ggccgcacgc gtctagttat taatagtaat cgaattcgtg ttactcataa ctagtaaggt cgggcaggaa gagggcctat ttcccatgat tccttcatat ttgcatatac gatacaaggc tgttagagag ataattagaa ttaatttgac tgtaaacaca aagatattag tacaaaatac gtgacgtaga aagtaataat ttcttgggta gtttgcagtt ttaaaattat gttttaaaat ggactatcat atgcttaccg taacttgaaa gtatttcgat ttcttgggtt tatatatctt gtggaaagga cgcgggatcc actggaccag gcagcagcgt cagaagactt ttttggaaaa gcttgactag taatactgta atagtaatca attacggggt cattagttca tagcccatat atggagttcc gcgttacata acttacggta aatggcccgc ctggctgacc gcccaacgac ccccgcccat tgacgtcaat aatgacgtat gttcccatag taacgccaat agggactttc cattgacgtc aatgggtgga gtatttacgg taaactgccc acttggcagt acatcaagtg tatcatatgc caagtacgcc ccctattgac gtcaatgacg gtaaatggcc cgcctggcat tatgcccagt acatgacctt atgggacttt cctacttggc agtacatcta cgtattagtc atcgctatta ccatggtgat gcggttttgg cagtacatca atgggcgtgg atagcggttt gactcacggg gatttccaag tctccacccc attgacgtca atgggagttt gttttgcacc aaaatcaacg ggactttcca aaatgtcgta acaactccgc cccattgacg caaatgggcg gtaggcgtgt acggtgggag gtctatataa gcagagctgg tttagtgaac cgtcagatcc gctagagatc cggtaccgag gagatctgcc gccgcgatcg ccggcgcgcc agatctcacg cttaactagc tagcggaccg acgcgtacgc ggccgctcga gatggtgagc aagggcgagg agctgttcac cggggtggtg cccatcctgg tcgagctgga cggcgacgta aacggccaca agttcagcgt gtccggcgag ggcgagggcg atgccaccta cggcaagctg accctgaagt tcatctgcac caccggcaag ctgcccgtgc cctggcccac cctcgtgacc accctgacct acggcgtgca gtgcttcagc cgctaccccg accacatgaa gcagcacgac ttcttcaagt ccgccatgcc cgaaggctac gtccaggagc gcaccatctt cttcaaggac gacggcaact acaagacccg cgccgaggtg aagttcgagg gcgacaccct ggtgaaccgc atcgagctga agggcatcga cttcaaggag gacggcaaca tcctggggca caagctggag tacaactaca acagccacaa cgtctatatc atggccgaca agcagaagaa cggcatcaag gtgaacttca agatccgcca caacatcgag gacggcagcg tgcagctcgc cgaccactac cagcagaaca cccccatcgg cgacggcccc gtgctgctgc ccgacaacca ctacctgagc acccagtccg ccctgagcaa agaccccaac gagaagcgcg atcacatggt cctgctggag ttcgtgaccg ccgccgggat cactctcggc atggacgagc tgtacaagta agtcgaggat tataaggatg acgacgataa attcgtcgag caccaccacc accaccacta ataaggttta tccgatccac cggatctaga taagatatcc gatccaccgg atctagataa ctgatcataa tcagccatac cacatttgta gaggttttac ttgctttaaa aaacctccca cacctccccc tgaacctgaa acataaaatg aatgcaattg ttgttgttaa cttgtttatt gcagcttata atggttacaa ataaagcaat agcatcacaa atttcacaaa taaagcattt ttttcactgc attctagttg tggtttgtcc aaactcatca atgtatctta acgcggtaac cacgtgcgga ccgagcggcc gcaggaaccc ctagtgatgg agttggccac tccctctctg cgcgctcgct cgctcactga ggccgggcga ccaaaggtcg cccgacgccc gggctttgcc cgggcggcct cagtgagcga gcgagcgcgc agctgcctgc aggggcgcct gatgcggtat tttctcctta cgcatctgtg cggtatttca caccgcatac gtcaaagcaa ccatagtacg cgccctgtag cggcgcatta agcgcggcgg gtgtggtggt tacgcgcagc gtgaccgcta cacctgccag cgccttagcg cccgctcctt tcgctttctt cccttccttt ctcgccacgt tcgccggctt tccccgtcaa gctctaaatc gggggctccc tttagggttc cgatttagtg ctttacggca cctcgacccc aaaaaacttg atttgggtga tggttcacgt agtgggccat cgccctgata gacggttttt cgccctttga cgttggagtc cacgttcttt aatagtggac tcttgttcca aactggaaca acactcaacc ctatctcggg ctattctttt gatttataag ggattttgcc gatttcggcc tattggttaa aaaatgagct gatttaacaa aaatttaacg cgaattttaa caaaatatta acgtttacaa ttttatggtg cactctcagt acaatctgct ctgatgccgc atagttaagc cagccccgac acccgccaac acccgctgac gcgccctgac gggcttgtct gctcccggca tccgcttaca gacaagctgt gaccgtctcc gggagctgca tgtgtcagag gttttcaccg tcatcaccga aacgcgcgag acgaaagggc ctcgtgatac gcctattttt ataggttaat gtcatgataa taatggtttc ttagacgtca ggtggcactt ttcggggaaa tgtgcgcgga acccctattt gtttattttt ctaaatacat tcaaatatgt atccgctcat gagacaataa ccctgataaa tgcttcaata atattgaaaa aggaagagta tgagtattca acatttccgt gtcgccctta ttcccttttt tgcggcattt tgccttcctg tttttgctca cccagaaacg ctggtgaaag taaaagatgc tgaagatcag ttgggtgcac gagtgggtta catcgaactg gatctcaaca gcggtaagat ccttgagagt tttcgccccg aagaacgttt tccaatgatg agcactttta aagttctgct atgtggcgcg gtattatccc gtattgacgc cgggcaagag caactcggtc gccgcataca ctattctcag aatgacttgg ttgagtactc accagtcaca gaaaagcatc ttacggatgg catgacagta agagaattat gcagtgctgc cataaccatg agtgataaca ctgcggccaa cttacttctg acaacgatcg gaggaccgaa ggagctaacc gcttttttgc acaacatggg ggatcatgta actcgccttg atcgttggga accggagctg aatgaagcca taccaaacga cgagcgtgac accacgatgc ctgtagcaat ggcaacaacg ttgcgcaaac tattaactgg cgaactactt actctagctt cccggcaaca attaatagac tggatggagg cggataaagt tgcaggacca cttctgcgct cggcccttcc ggctggctgg tttattgctg ataaatctgg agccggtgag cgtgggtctc gcggtatcat tgcagcactg gggccagatg gtaagccctc ccgtatcgta gttatctaca cgacggggag tcaggcaact atggatgaac gaaatagaca gatcgctgag ataggtgcct cactgattaa gcattggtaa ctgtcagacc aagtttactc atatatactt tagattgatt taaaacttca tttttaattt aaaaggatct aggtgaagat cctttttgat aatctcatga ccaaaatccc ttaacgtgag ttttcgttcc actgagcgtc agaccccgta gaaaagatca aaggatcttc ttgagatcct ttttttctgc gcgtaatctg ctgcttgcaa acaaaaaaac caccgctacc agcggtggtt tgtttgccgg atcaagagct accaactctt tttccgaagg taactggctt cagcagagcg cagataccaa atactgtcct tctagtgtag ccgtagttag gccaccactt caagaactct gtagcaccgc ctacatacct cgctctgcta atcctgttac cagtggctgc tgccagtggc gataagtcgt gtcttaccgg gttggactca agacgatagt taccggataa ggcgcagcgg tcgggctgaa cggggggttc gtgcacacag cccagcttgg agcgaacgac ctacaccgaa ctgagatacc tacagcgtga gctatgagaa agcgccacgc ttcccgaagg gagaaaggcg gacaggtatc cggtaagcgg cagggtcgga acaggagagc gcacgaggga gcttccaggg ggaaacgcct ggtatcttta tagtcctgtc gggtttcgcc acctctgact tgagcgtcga tttttgtgat gctcgtcagg ggggcggagc ctatggaaaa acgccagcaa cgcggccttt ttacggttcc tggccttttg ctggcctttt gctcacatgt
pAV-TBG-EGFPプラスミドのコード鎖(配列番号8):
cctgcaggca gctgcgcgct cgctcgctca ctgaggccgc ccgggcgtcg ggcgaccttt ggtcgcccgg cctcagtgag cgagcgagcg cgcagagagg gagtggccaa ctccatcact aggggttcct gcggccggtc gcgtctagta ctagtaggtt aatttttaaa aagcagtcaa aagtccaagt ggcccttggc agcatttact ctctctgttt gctctggtta ataatctcag gagcacaaac attccagatc caggttaatt tttaaaaagc agtcaaaagt ccaagtggcc cttggcagca tttactctct ctgtttgctc tggttaataa tctcaggagc acaaacattc cagatccggc gcgccagggc tggaagctac ctttgacatc atttcctctg cgaatgcatg tataatttct acagaaccta ttagaaagga tcacccagcc tctgcttttg tacaactttc ccttaaaaaa ctgccaattc cactgctgtt tggcccaata gtgagaactt tttcctgctg cctcttggtg cttttgccta tggcccctat tctgcctgct gaagacactc ttgccagcat ggacttaaac ccctccagct ctgacaatcc tctttctctt ttgttttaca tgaagggtct ggcagccaaa gcaatcactc aaagttcaaa ccttatcatt ttttgctttg ttcctcttgg ccttggtttt gtacatcagc tttgaaaata ccatcccagg gttaatgctg gggttaattt ataactaaga gtgctctagt tttgcaatac aggacatgct ataaaaatgg aaagatgttg ctttctgaga gacaggtacc gaggagatct gccgccgcga tcgccaccat ggtgagcaag ggcgaggagc tgttcaccgg ggtggtgccc atcctggtcg agctggacgg cgacgtaaac ggccacaagt tcagcgtgtc cggcgagggc gagggcgatg ccacttacgg caagctgacc ctgaagttca tctgcaccac cggcaagctg cccgtgccct ggcccaccct cgtgaccacc ctgacctacg gcgtgcagtg cttcagccgc taccccgacc acatgaagca gcacgacttc ttcaagtccg ccatgcccga aggctacgtc caggagcgca ccatcttctt caaggacgac ggcaactaca agacccgcgc cgaggtgaag ttcgagggcg acaccctggt gaaccgcatc gagctgaagg gcatcgactt caaggaggac ggcaacatcc tggggcacaa gctggagtac aactacaaca gccacaacgt ctatatcatg gccgacaagc agaagaacgg catcaaggtg aacttcaaga tccgccacaa catcgaggac ggcagcgtgc agctcgccga ccactaccag cagaacaccc ccatcggcga cggccccgtg ctgctgcccg acaaccacta cctgagcacc cagtccgccc tgagcaaaga ccccaacgag aagcgcgatc acatggtcct gctggagttc gtgaccgccg ccgggatcac tctcggcatg gacgagctgt acaagtagac gcgtacgcgg ccgctcgagg attataagga tgacgacgat aaattcgtcg agcaccacca ccaccaccac taataaggtt tatccgatcc accggatcta gataagatat ccgatccacc ggatctagat aactgatcat aatcagccat accacatttg tagaggtttt acttgcttta aaaaacctcc cacacctccc cctgaacctg aaacataaaa tgaatgcaat tgttgttgtt aacttgttta ttgcagctta taatggttac aaataaagca atagcatcac aaatttcaca aataaagcat ttttttcact gcattctagt tgtggtttgt ccaaactcat caatgtatct taacgcggta accacgtgcg gacccaacgg ccgcaggaac ccctagtgat ggagttggcc actccctctc tgcgcgctcg ctcgctcact gaggccgggc gaccaaaggt cgcccgacgc ccgggctttg cccgggcggc ctcagtgagc gagcgagcgc gcagctgcct gcaggggcgc ctgatgcggt attttctcct tacgcatctg tgcggtattt cacaccgcat acgtcaaagc aaccatagta cgcgccctgt agcggcacat taagcgcggc gggtgtggtg gttacgcgca gcgtgaccgc tacacctgcc agcgccttag cgcccgctcc tttcgctttc ttcccttcct ttctcgccac gttcgccggc tttccccgtc aagctctaaa tcgggggctc cctttagggt tccgatttag tgctttacgg cacctcgacc ccaaaaaact tgatttgggt gatggttcac gtagtgggcc atcgccctga tagacggttt ttcgcccttt gacgttggag tccacgttct ttaatagtgg actcttgttc caaactggaa caacactcaa ctctatctcg ggctattctt ttgatttata agggattttg ccgatttcgg tctattggtt aaaaaatgag ctgatttaac aaaaatttaa cgcgaatttt aacaaaatat taacgtttac aattttatgg tgcactctca gtacaatctg ctctgatgcc gcatagttaa gccagccccg acacccgcca acacccgctg acgcgccctg acgggcttgt ctgctcccgg catccgctta cagacaagct gtgaccgtct ccgggagctg catgtgtcag aggttttcac cgtcatcacc gaaacgcgcg agacgaaagg gcctcgtgat acgcctattt ttataggtta atgtcatgat aataatggtt tcttagacgt caggtggcac ttttcgggga aatgtgcgcg gaacccctat ttgtttattt ttctaaatac attcaaatat gtatccgctc atgagacaat aaccctgata aatgcttcaa taatattgaa aaaggaagag tatgagtatt caacatttcc gtgtcgccct tattcccttt tttgcggcat tttgccttcc tgtttttgct cacccagaaa cgctggtgaa agtaaaagat gctgaagatc agttgggtgc acgagtgggt tacatcgaac tggatctcaa cagcggtaag atccttgaga gttttcgccc cgaagaacgt tttccaatga tgagcacttt taaagttctg ctatgtggcg cggtattatc ccgtattgac gccgggcaag agcaactcgg tcgccgcata cactattctc agaatgactt ggttgagtac tcaccagtca cagaaaagca tcttacggat ggcatgacag taagagaatt atgcagtgct gccataacca tgagtgataa cactgcggcc aacttacttc tgacaacgat cggaggaccg aaggagctaa ccgctttttt gcacaacatg ggggatcatg taactcgcct tgatcgttgg gaaccggagc tgaatgaagc cataccaaac gacgagcgtg acaccacgat gcctgtagca atggcaacaa cgttgcgcaa actattaact ggcgaactac ttactctagc ttcccggcaa caattaatag actggatgga ggcggataaa gttgcaggac cacttctgcg ctcggccctt ccggctggct ggtttattgc tgataaatct ggagccggtg agcgtgggtc tcgcggtatc attgcagcac tggggccaga tggtaagccc tcccgtatcg tagttatcta cacgacgggg agtcaggcaa ctatggatga acgaaataga cagatcgctg agataggtgc ctcactgatt aagcattggt aactgtcaga ccaagtttac tcatatatac tttagattga tttaaaactt catttttaat ttaaaaggat ctaggtgaag atcctttttg ataatctcat gaccaaaatc ccttaacgtg agttttcgtt ccactgagcg tcagaccccg tagaaaagat caaaggatct tcttgagatc ctttttttct gcgcgtaatc tgctgcttgc aaacaaaaaa accaccgcta ccagcggtgg tttgtttgcc ggatcaagag ctaccaactc tttttccgaa ggtaactggc ttcagcagag cgcagatacc aaatactgtt cttctagtgt agccgtagtt aggccaccac ttcaagaact ctgtagcacc gcctacatac ctcgctctgc taatcctgtt accagtggct gctgccagtg gcgataagtc gtgtcttacc gggttggact caagacgata gttaccggat aaggcgcagc ggtcgggctg aacggggggt tcgtgcacac agcccagctt ggagcgaacg acctacaccg aactgagata cctacagcgt gagctatgag aaagcgccac gcttcccgaa gggagaaagg cggacaggta tccggtaagc ggcagggtcg gaacaggaga gcgcacgagg gagcttccag ggggaaacgc ctggtatctt tatagtcctg tcgggtttcg ccacctctga cttgagcgtc gatttttgtg atgctcgtca ggggggcgga gcctatggaa aaacgccagc aacgcggcct ttttacggtt cctggccttt tgctggcctt ttgctcacat gt
・AAV1 P5プロモーター配列は天然にAAV1のrep遺伝子の転写を制御し、AAV1 P40 プロモーター配列は天然にAAV1のrep遺伝子の中に見いだされる。したがって、AAV1 P5プロモーター配列およびAAV1 P40プロモーター配列はAAV1 rep遺伝子の天然AAV血清型プロモーター配列である;
・AAV2 P5プロモーター配列は天然にAAV2 のrep遺伝子の転写を制御し、AAV2 P40ロモーター配列は天然にAAV2のrep遺伝子の中に見いだされる。したがって、AAV2 P5プロモーター配列およびAAV2 P40プロモーター配列はAAV2 rep遺伝子の天然AAV血清型プロモーター配列である;
・AAV5 P5プロモーター配列は天然にAAV5のrep遺伝子を制御し、AAV5 P40プロモーター配列は天然にAAV5のrep遺伝子の中に見いだされる。したがって、AAV5 P5プロモーター配列およびAAV5 P40プロモーター配列はAAV5のrep遺伝子の天然AAV血清型プロモーター配列である;
・AAV6 P5プロモーター配列は天然にAAV6のrep遺伝子を制御し、AAV6 P40プロモーター配列は天然にAAV6のrep遺伝子の中に見いだされる。したがって、AAV6 P5プロモーター配列およびAAV6 P40プロモーター配列はAAV6遺伝子の天然AAV血清型プロモーター配列である;そして、
・AAV7 P5プロモーター配列は天然にAAVのrep遺伝子を制御し、AAV7 P40配列は天然にAAV7のrep遺伝子の中に見いだされる。したがって、AAV7 P5プロモーター配列およびAAV7 P40プロモーター配列はAAV7の天然AAV血清型プロモーター配列である。
(1)非天然AAV血清型プロモーター配列を有し、そのようなrAAVまたはrAAVプラスミドベクターによって天然に提供されないが、それらの産生に必要なタンパク質またはRNA分子を発現することができるAADヘルパーベクター。上述のように、このようなタンパク質またはRNA分子には、ベクター転写制御および複製、ならびにウイルスゲノムのウイルス被膜へのパッケージングに必要なReP52およびRep78タンパク質をコードする遺伝子、ならびに感染性粒子の形成に必要なVPキャプシドタンパク質をコードするキャップ遺伝子が含まれる;および
(2)そのようなrAAVまたはrAAVプラスミドベクターによって提供されないが、それらの産生に必要な、非AAVヘルパータンパク質(例えば、E1a、E1b、E2a、VA、E4)またはRNAを提供することができるAdヘルパーベクター。
(1)rAAV;
(2)AAVヘルパー機能を提供するポリヌクレオチドを含む組換え改変アデノ随伴ウイルス(rAAV)ヘルパーベクターであって、そのようなポリヌクレオチドは、天然AAV血清型プロモーター配列の置換またはそれに加えて、非天然AAV血清型P5またはP40プロモーター配列を含む、組換え改変アデノ随伴ウイルス(rAAV)ヘルパーベクター;および
(3)さらなるベクター、特に、非AAVヘルパー機能提供ポリヌクレオチを含む、プラスミドベクター;
培養は、rAAVの産生を可能にするのに十分な条件下で、培地中で行われ、非天然AAV血清型P5またはP40プロモーター配列の存在は、細胞が、前記AAVヘルパー機能提供ポリヌクレオチドが天然血清型P5およびP40プロモーターを含有する場合に達成されるものと比較して、増加した産生力価で、前記rAAVの産生を引き起こす。
(1)rAAV;および
(2)以下を含む組換え改変アデノ随伴ウイルス(rAAV)ヘルパーベクター:
(a)AAVヘルパー機能提供ポリヌクレオチドであって、そのようなポリヌクレオチドは、天然AAV血清型プロモーター配列の置換またはそれに加えて、非天然AAV血清型P5またはP40プロモーター配列を含む、AAVヘルパー機能提供ポリヌクレオチド;および
(b)非AAVヘルパー機能提供ポリヌクレオチド;
培養は、rAAVの産生を可能にするのに十分な条件下で、培地中で行われ、非天然AAV血清型P5またはP40プロモーター配列の存在は、細胞が、前記AAVヘルパー機能提供ポリヌクレオチドが天然血清型P5およびP40プロモーターを含有する場合に達成されるものと比較して、増加した産生力価で、前記rAAVの産生を引き起こす。
II.本発明の薬学的組成物
III.本発明の使用
IV.本発明の実施形態
E1.AAVヘルパー機能提供ポリヌクレオチドを含む組換え改変アデノ随伴ウイルス(AAV)ヘルパーベクターであって、ポリヌクレオチドが非天然AAV血清型P5またはP40プロモーター配列を含む、組換え改変アデノ随伴ウイルス(AAV)ヘルパーベクター。
E2.AAVヘルパー機能提供ポリヌクレオチドベクターが非天然AAV血清型P5プロモーター配列を含む、E1の組換え改変アデノ随伴ウイルス(AAV)ヘルパーベクター。
E3.AAVヘルパー機能提供ポリヌクレオチドベクターが非天然AAV血清型P40プロモーター配列を含む、E1またはE2のいずれかの組換え改変アデノ随伴ウイルス(AAV)ヘルパーベクター。
E4.ベクターがプラスミドベクターであるE1からE3のいずれかの組換え改変アデノ随伴ウイルス(AAV)ヘルパーベクター。
E5.非天然AAV血清型P5またはP40プロモーター配列が天然AAV血清型プロモーター配列を置換する、E1の組換え改変アデノ随伴ウイルス(AAV)ヘルパーベクター。
E6.ベクターが、非AAVヘルパー機能提供ポリヌクレオチドをさらに含む、E1からE6のいずれかの組換え改変アデノ随伴ウイルス(AAV)ヘルパーベクター。
E7.導入遺伝子カセットを含む組換え改変アデノ随伴ウイルス(rAAV)の産生力価を増加させる方法であって、該方法は、以下でトランスフェクトされた細胞を培養することを含み:
(1)rAAV;および
(2)E6の組換え改変アデノ随伴ウイルス(AAV)ヘルパーベクター、
培養は、rAAVの産生を可能にするのに十分な条件下で、培地中で行われ、非天然AAV血清型P5またはP40プロモーター配列の存在は、細胞が、前記AAVヘルパー機能提供ポリヌクレオチドが天然血清型P5およびP40プロモーターを含有する場合に達成されるものと比較して、増加した産生力価で、rAAVの産生を引き起こす、方法。
E8.導入遺伝子カセットを含む組換え改変アデノ随伴ウイルス(rAAV)の産生力価を増加させる方法であって、該方法は、以下でトランスフェクトされた細胞を培養することを含み:
(1)rAAV;
(2)E1からE6のいずれか組換え改変アデノ随伴ウイルス(AAV)ヘルパーベクター;および
(3)非AAVヘルパー機能提供ポリヌクレオチを含む、さらなるベクター、特にプラスミドベクター、
培養は、rAAVの産生を可能にするのに十分な条件下で、培地中で行われ、非天然AAV血清型P5またはP40プロモーター配列の存在は、細胞が、前記AAVヘルパー機能提供ポリヌクレオチドが天然血清型P5およびP40プロモーターを含有する場合に達成されるものと比較して、増加した産生力価で、rAAVの産生を引き起こす、方法。
E9.E7またはE8の方法であって、
(A)前記ベクターの前記AAVヘルパー機能提供ポリヌクレオチドは、AAV1 Capタンパク質をコードし、前記非天然AAV血清型プロモーター配列は、血清型AAV3、AAV4、AAV5、AAV6、AAV7またはAAV8、または前記血清型の1つ以上のハイブリッドのAAVのプロモーター配列である;
(B)前記ベクターの前記AAVヘルパー機能提供ポリヌクレオチドは、AAV2 Capタンパク質をコードし、前記非天然AAV血清型プロモーター配列は、血清型AAV1、AAV3、AAV4、AAV5、AAV6、AAV7またはAAV8、または前記血清型の1つ以上のハイブリッドのAAVのプロモーター配列である;
(C)前記ベクターの前記AAVヘルパー機能提供ポリヌクレオチドは、AAV3 Capタンパク質をコードし、前記非天然AAV血清型プロモーター配列は、血清型AAV1、AAV4、AAV5、AAV6、AAV7またはAAV8、または前記血清型の1つ以上のハイブリッドのAAVのプロモーター配列である;
(D)前記ベクターの前記AAVヘルパー機能提供ポリヌクレオチドは、AAV4 Capタンパク質をコードし、前記非天然AAV血清型プロモーター配列は、血清型AAV1、AAV3、AAV5、AAV6、AAV7またはAAV8、または前記血清型の1つ以上のハイブリッドのAAVのプロモーター配列である;
(E)前記ベクターの前記AAVヘルパー機能提供ポリヌクレオチドは、AAV5 Capタンパク質をコードし、前記非天然AAV血清型プロモーター配列は、血清型AAV1、AAV3、AAV4、AAV6、AAV7またはAAV8、または前記血清型の1つ以上のハイブリッドのAAVのプロモーター配列である;
(F)前記ベクターの前記AAVヘルパー機能提供ポリヌクレオチドは、AAV6 Capタンパク質をコードし、前記非天然AAV血清型プロモーター配列は、血清型AAV1、AAV3、AAV4、AAV5、AAV7またはAAV8、または前記血清型の1つ以上のハイブリッドのAAVのプロモーター配列である;
(G)前記ベクターの前記AAVヘルパー機能提供ポリヌクレオチドは、AAV7 Capタンパク質をコードし、前記非天然AAV血清型プロモーター配列は、血清型AAV1、AAV3、AAV4、AAV5、AAV6またはAAV8、または前記血清型の1つ以上のハイブリッドのAAVのプロモーター配列である;または
(H)前記ベクターの前記AAVヘルパー機能提供ポリヌクレオチドは、AAV8 Capタンパク質をコードし、前記非天然AAV血清型プロモーター配列は、血清型AAV1、AAV3、AAV4、AAV5、AAV6またはAAV7、または前記血清型の1つ以上のハイブリッドのAAVのプロモーター配列である、
方法。
E10.細胞がヒト胚性腎細胞、ベビーハムスター腎細胞またはsf9昆虫細胞であるE7からE9の方法。
E11.細胞がHEK293ヒト胚性腎細胞であるE10の方法。
E12.細胞がBHK21ベビーハムスター腎細胞であるE11の方法。
E13.導入遺伝子カセットが、タンパク質をコードするか、または転写された核酸を含み、それは遺伝子に関するまたは遺伝性の疾患または状態に対して治療的である、E7からE12のいずれか方法。
E14.E13の方法によって産生される組換え改変アデノ随伴ウイルス(rAAV)の調製物。
E15.E13の方法によって産生される組換え改変アデノ随伴ウイルス(rAAV)、および、薬学的に許容される担体を含む薬学的組成物。
E16. 遺伝性の疾患または状態を治療に使用するための、E14の組換え改変アデノ随伴ウイルス(rAAV)の調製物またはE15の薬学的組成物。
実施例1
非天然AAV血清型P5プロモーター配列を有するAAV RC2ヘルパープラスミドベクターでトランスフェクトした細胞によるrAAV産生力価の比較
(1)Parent-RC2
AAV2 rep遺伝子および完全なAAV2血清型P5プロモーター配列(配列番号10)の一部の部分、およびAAV2 cap遺伝子を含み、その発現が天然AAV2 P40プロモーター配列(配列番号18)によって制御されるpAAV-RC2(配列番号2);
(2)P5(1)-RC2
天然AAV血清型P5プロモーター配列をAAV血清型1のP5プロモーター配列(配列番号9)で置換したプラスミドベクターpAAV-RC2の誘導体;
(3)P5(2)-RC2
Parent-RC2の部分的AAV2血清型P5プロモーター配列をAAV血清型2の完全長P5プロモーター(配列番号10)で置換したプラスミドベクターpAAV-RC2の誘導体;
(4)P5(3)-RC2
天然AAV2血清型P5プロモーター配列をAAV血清型3のP5プロモーター配列(配列番号11)で置換したプラスミドベクターpAAV-RC2の誘導体;
(5)P5(4)-RC2
天然AAV2血清型P5プロモーター配列をAAV血清型4のP5プロモーター配列(配列番号12)で置換したプラスミドベクターpAAV-RC2の誘導体;
(6)P5(5)-RC2
天然AAV2血清型P5プロモーター配列をAAV血清型5のP5プロモーター配列(配列番号13)で置換したプラスミドベクターpAAV-RCの誘導体;
(7)P5(6)-RC2
天然AAV2血清型P5プロモーター配列をAAV血清型6のP5プロモーター配列(配列番号14)で置換したプラスミドベクターpAAV-RCの誘導体;
(8)P5(7)-RC2
天然AAV2血清型P5プロモーター配列をAAV血清型7のP5プロモーター配列(配列番号15)で置換したプラスミドベクターpAAV-RCの誘導体;および
(9)P5(8)-RC2
天然AAV2血清型P5プロモーター配列をAAV血清型8のP5プロモーター配列(配列番号16)で置換したプラスミドベクターpAAV-RCの誘導体。
図12Bは、P5プロモーターの血清型がrAAV産生力価に影響を及ぼすことを明らかにし、プラスミドベクターpAAV-RC2の天然のAAV2 P5プロモーターをAAV5血清型P5プロモーターへ置換することは、rAAV産生力価を大きく減少したこと、一方、プラスミドベクターpAAV-RC2の天然のAAV2 P5プロモーターのAAV血清型1、3、5、7または8のP5プロモーターでの置換は、rAAV産生力価を大きく増加したことを示す。
実施例2
非天然AAV血清型P40プロモーター配列を有するAAV RC2ヘルパープラスミドベクターでトランスフェクトした細胞によるrAAV産生力価の比較
(1)Parent-RC2
AAV2 rep遺伝子および完全なAAV2血清型P5プロモーター配列(配列番号10)の一部の部分、およびAAV2 cap遺伝子を含み、その発現が天然AAV2 P40プロモーター配列(配列番号18)によって制御されるpAAV-RC2(配列番号2);
(2)P40(1)-RC2
天然AAV2血清型P40プロモーター配列をAAV血清型1のP40プロモーター配列(配列番号17)で置換したプラスミドベクターpAAV-RC2の誘導体;
(3)P40(2)-RC2
Parent-RC2のAAV2血清型P40プロモーター配列をAAV血清型2のP40プロモーター配列(配列番号18)で置換したプラスミドベクターpAAV-RC2の誘導体;
(4)P40(3)-RC2
天然AAV2血清型P40プロモーター配列をAAV血清型3のP40プロモーター配列(配列番号19)で置換したプラスミドベクターpAAV-RC2の誘導体;
(5)P40(4)-RC2
天然AAV2血清型P40プロモーター配列をAAV血清型4のP40プロモーター配列(配列番号20)で置換したプラスミドベクターpAAV-RC2の誘導体;
(6)P40(5)-RC2
天然AAV2血清型P40プロモーター配列をAAV血清型5のP40プロモーター配列(配列番号21)で置換したプラスミドベクターpAAV-RC2の誘導体;
(7)P40(6)-RC2
天然AAV2血清型P40プロモーター配列をAAV血清型6のP40プロモーター配列(配列番号22)で置換したプラスミドベクターpAAV-RC2の誘導体;
(8)P40(7)-RC2
天然AAV2血清型P40プロモーター配列をAAV血清型7のP40プロモーター配列(配列番号23)で置換したプラスミドベクターpAAV-RC2の誘導体;および
(9)P40(8)-RC2
天然AAV2血清型P40プロモーター配列をAAV血清型8のP40プロモーター配列(配列番号24)で置換したプラスミドベクターpAAV-RC2の誘導体。
実施例3
非天然AAV血清型P5およびP40プロモーター配列を有するAAV RC2ヘルパープラスミドベクターでトランスフェクトした細胞によるrAAV産生力価の比較
(1)Parent-RC2
AAV2 rep遺伝子および完全なAAV2血清型P5プロモーター配列(配列番号10)の一部の部分、およびAAV2 cap遺伝子を含み、その発現が天然AAV2 P40プロモーター配列(配列番号18)によって制御されるpAAV-RC2(配列番号2);
(2)P5(2)-RC2
該一部のAAV2血清型P5プロモーター配列をAAV血清型2のP5プロモーター配列(配列番号10)で置換したプラスミドベクターpAAV-RC2の誘導体;
(3)P5(3)-RC2
天然AAV2血清型P5プロモーター配列をAAV血清型3のP5プロモーター配列(配列番号11)で置換したプラスミドベクターpAAV-RC2の誘導体;
(4)P5(5)-RC2
天然AAV2血清型P5プロモーター配列をAAV5血清型のP5プロモーター配列(配列番号13)で置換したプラスミドベクターpAAV-RC2の誘導体;
(5)P40(1)-RC2
天然AAV2血清型P40プロモーター配列をAAV1血清型のP40プロモーター配列(配列番号17)で置換したプラスミドベクターpAAV-RC2の誘導体;
(6)P5(2)/P40(1)-RC2
天然AAV2血清型P5プロモーター配列をAAV2のP5プロモーター配列(配列番号10)で置換し、天然P40プロモーター配列をAAV1のP40プロモーター配列(配列番号17)で置換したプラスミドベクターpAAV-RC2の誘導体;
(7)P5(3)/P40(1)-RC2
天然AAV2血清型P5プロモーター配列をAAV3のP5プロモーター配列(配列番号11)で置換し、天然P40プロモーター配列をAAV1のP40プロモーター配列(配列番号17)で置換したプラスミドベクターpAAV-RC2の誘導体;および
(8)P5(5)/P40(1)-RC2
天然AAV2血清型P5プロモーター配列をAAV5のP5プロモーター配列(配列番号13)で置換し、天然P40プロモーター配列をAAV1のP40プロモーター配列(配列番号17)で置換したプラスミドベクターpAAV-RC2の誘導体。
実施例4
非天然AAV血清型P5およびP40プロモーター配列を有するAAV RC6ヘルパープラスミドベクターでトランスフェクトした細胞によるrAAV産生力価の比較
(1)Parent-RC6
AAV2 rep遺伝子とその天然AAV2血清型P5プロモーター配列(配列番号10)およびAAV6 cap遺伝子を含み、その発現が天然AAV2 P40プロモーター配列(配列番号18)によって制御されるpAAV-RC6(配列番号4);
(2)P5(1)-RC6
天然AAV2血清型P5プロモーター配列をAAV1血清型のP5プロモーター配列(配列番号9)で置換したプラスミドベクターpAAV-RC6の誘導体;
(3)P5(2)-RC6
天然AAV2血清型P5プロモーター配列をAAV2血清型のP5プロモーター配列(配列番号10)で置換したプラスミドベクターpAAV-RC6の誘導体;
(4)P5(3)-RC6
天然AAV2血清型P5プロモーター配列をAAV3血清型のP5プロモーター配列(配列番号11)で置換したプラスミドベクターpAAV-RC6の誘導体;
(5)P5(7)-RC6
天然AAV2血清型P5プロモーター配列をAAV7血清型のP5プロモーター配列(配列番号15)で置換したプラスミドベクターpAAV-RC6の誘導体;および
(6)P5(8)-RC6
天然AAV2血清型P5プロモーター配列をAAV8血清型のP5プロモーター配列(配列番号16)で置換したプラスミドベクターpAAV-RC6の誘導体。
実施例5
非天然AAV血清型P5およびP40プロモーター配列を有するAAV RC1、AAV RC5またはAAV RC7ヘルパープラスミドベクターでトランスフェクトした細胞によるrAAV産生力価の比較
(1)Parent-RC1
AAV2 rep遺伝子とその天然AAV2血清型P5プロモーター配列(配列番号10)、およびAAV1 cap遺伝子を含み、その発現が天然AAV2 P40プロモーター配列(配列番号18)によって制御されるpAAV-RC1(配列番号1);
(2)Parent-RC5
AAV2 rep遺伝子とその天然AAV2血清型P5プロモーター配列(配列番号10)、およびAAV5 cap遺伝子を含み、その発現が天然AAV2 P40プロモーター配列(配列番号18)によって制御されるpAAV-RC5(配列番号3);
(3)Parent-RC7
AAV2 rep遺伝子とその天然AAV2血清型P5プロモーター配列(配列番号10)、およびAAV7 cap遺伝子を含み、その発現が天然AAV2 P40プロモーター配列(配列番号18)によって制御されるpAAV-RC7(配列番号5);
(4)P5(2)-RC1
天然AAV1血清型P5プロモーター配列がAAV2のP5プロモーター配列(配列番号10)で置換されたプラスミドベクターpAAV-RC1の誘導体;
(5)P5(7)-RC1
天然AAV1血清型P5プロモーター配列がAAV7のP5プロモーター配列(配列番号15)で置換されたプラスミドベクターpAAV-RC1の誘導体;
(6)P5(8)-RC1
天然AAV1血清型P5プロモーター配列がAAV8のP5プロモーター配列(配列番号16)で置換されたプラスミドベクターpAAV-RC1の誘導体;
(7)P5(7)-RC5
天然AAV5血清型P5プロモーター配列がAAV7のP5プロモーター配列(配列番号15)で置換されたプラスミドベクターpAAV-RC5の誘導体;
(8)P5(2)-RC7
天然AAV7血清型P5プロモーター配列がAAV2のP5プロモーター配列(配列番号10)で置換されたプラスミドベクターpAAV-RC7の誘導体;
(9)P5(7)-RC7
天然AAV7血清型P5プロモーター配列がAAV7のP5プロモーター配列(配列番号15)で置換されたプラスミドベクターpAAV-RC7の誘導体;および
(10)P5(8)-RC7
天然AAV7血清型P5プロモーター配列がAAV8のP5プロモーター配列(配列番号16)で置換されたプラスミドベクターpAAV-RC7の誘導体。
Claims (20)
- AAVヘルパー機能提供ポリヌクレオチドを含む組換え改変アデノ随伴ウイルス(AAV)ヘルパーベクターであって、前記ポリヌクレオチドが非天然AAV血清型P5またはP40プロモーター配列を含む、組換え改変アデノ随伴ウイルス(AAV)ヘルパーベクター。
- 前記AAVヘルパー機能提供ポリヌクレオチドベクターが非天然AAV血清型P5プロモーター配列を含む、請求項1に記載の組換え改変アデノ随伴ウイルス(AAV)ヘルパーベクター。
- 前記AAVヘルパー機能提供ポリヌクレオチドベクターが非天然AAV血清型P40プロモーター配列を含む、請求項1に記載の組換え改変アデノ随伴ウイルス(AAV)ヘルパーベクター。
- 前記ベクターがプラスミドベクターである請求項1に記載の組換え改変アデノ随伴ウイルス(AAV)ヘルパーベクター。
- 前記非天然AAV血清型P5またはP40プロモーター配列が天然AAV血清型プロモーター配列を置換する、請求項1に記載の組換え改変アデノ随伴ウイルス(AAV)ヘルパーベクター。
- 前記ベクターが、非AAVヘルパー機能提供ポリヌクレオチドをさらに含む、請求項1に記載の組換え改変アデノ随伴ウイルス(AAV)ヘルパーベクター。
- 導入遺伝子カセットを含む組換え改変アデノ随伴ウイルス(rAAV)の産生力価を増加させる方法であって、該方法は、以下でトランスフェクトされた細胞を培養することを含み:
(1)前記rAAV;および
(2)請求項6に記載の組換え改変アデノ随伴ウイルス(AAV)ヘルパーベクター、
前記培養は、前記rAAVの産生を可能にするのに十分な条件下で、培地中で行われ、前記非天然AAV血清型P5またはP40プロモーター配列の存在は、前記細胞が、前記AAVヘルパー機能提供ポリヌクレオチドが天然血清型P5およびP40プロモーターを含有する場合に達成されるものと比較して、増加した産生力価で、前記rAAVの産生を引き起こす、方法。 - 前記導入遺伝子カセットが、タンパク質をコードするか、または転写された核酸を含み、それは遺伝子に関するまたは遺伝性の疾患または状態に対して治療的である、請求項7に記載の組換え改変アデノ随伴ウイルス(rAAV)。
- 請求項7に記載の方法であって:
(A)前記ベクターの前記AAVヘルパー機能提供ポリヌクレオチドは、AAV1 Capタンパク質をコードし、前記非天然AAV血清型プロモーター配列は、血清型AAV3、AAV4、AAV5、AAV6、AAV7またはAAV8、または前記血清型の1つ以上のハイブリッドのAAVのプロモーター配列である;
(B)前記ベクターの前記AAVヘルパー機能提供ポリヌクレオチドは、AAV2 Capタンパク質をコードし、前記非天然AAV血清型プロモーター配列は、血清型AAV1、AAV3、AAV4、AAV5、AAV6、AAV7またはAAV8、または前記血清型の1つ以上のハイブリッドのAAVのプロモーター配列である;
(C)前記ベクターの前記AAVヘルパー機能提供ポリヌクレオチドは、AAV3 Capタンパク質をコードし、前記非天然AAV血清型プロモーター配列は、血清型AAV1、AAV4、AAV5、AAV6、AAV7またはAAV8、または前記血清型の1つ以上のハイブリッドのAAVのプロモーター配列である;
(D)前記ベクターの前記AAVヘルパー機能提供ポリヌクレオチドは、AAV4 Capタンパク質をコードし、前記非天然AAV血清型プロモーター配列は、血清型AAV1、AAV3、AAV5、AAV6、AAV7またはAAV8、または前記血清型の1つ以上のハイブリッドのAAVのプロモーター配列である;
(E)前記ベクターの前記AAVヘルパー機能提供ポリヌクレオチドは、AAV5 Capタンパク質をコードし、前記非天然AAV血清型プロモーター配列は、血清型AAV1、AAV3、AAV4、AAV6、AAV7またはAAV8、または前記血清型の1つ以上のハイブリッドのAAVのプロモーター配列である;
(F)前記ベクターの前記AAVヘルパー機能提供ポリヌクレオチドは、AAV6 Capタンパク質をコードし、前記非天然AAV血清型プロモーター配列は、血清型AAV1、AAV3、AAV4、AAV5、AAV7またはAAV8、または前記血清型の1つ以上のハイブリッドのAAVのプロモーター配列である;
(G)前記ベクターの前記AAVヘルパー機能提供ポリヌクレオチドは、AAV7 Capタンパク質をコードし、前記非天然AAV血清型プロモーター配列は、血清型AAV1、AAV3、AAV4、AAV5、AAV6またはAAV8、または前記血清型の1つ以上のハイブリッドのAAVのプロモーター配列である;または
(H)前記ベクターの前記AAVヘルパー機能提供ポリヌクレオチドは、AAV8 Capタンパク質をコードし、前記非天然AAV血清型プロモーター配列は、血清型AAV1、AAV3、AAV4、AAV5、AAV6またはAAV7、または前記血清型の1つ以上のハイブリッドであるAAVのプロモーター配列である、
方法。 - 前記細胞がヒト胚性腎細胞、ベビーハムスター腎細胞またはsf9昆虫細胞である請求項7に記載の方法。
- 前記細胞がHEK293ヒト胚性腎細胞である請求項10に記載の方法。
- 前記細胞がBHK21ベビーハムスター腎細胞である請求項10に記載の方法。
- 導入遺伝子カセットを含む組換え改変アデノ随伴ウイルス(rAAV)の産生力価を増加させる方法であって、該方法は、以下でトランスフェクトされた細胞を培養することを含み:
(1)前記rAAV;
(2)請求項1に記載の組換え改変アデノ随伴ウイルス(AAV)ヘルパーベクター;および
(3)非AAVヘルパー機能提供ポリヌクレオチを含む、さらなるベクター、特にプラスミドベクター;
前記培養は、前記rAAVの産生を可能にするのに十分な条件下で、培地中で行われ、前記非天然AAV血清型P5またはP40プロモーター配列の存在は、前記細胞が、前記AAVヘルパー機能提供ポリヌクレオチドが天然血清型P5およびP40プロモーターを含有する場合に達成されるものと比較して、増加した産生力価で、前記rAAVの産生を引き起こす、方法。 - 前記導入遺伝子カセットが、タンパク質をコードするか、または転写された核酸を含み、それは遺伝子に関するまたは遺伝性の疾患または状態に対して治療的である、請求項13に記載の方法。
- 請求項13に記載の方法であって、
(A)前記ベクターの前記AAVヘルパー機能提供ポリヌクレオチドは、AAV1 Capタンパク質をコードし、前記非天然AAV血清型プロモーター配列は、血清型AAV3、AAV4、AAV5、AAV6、AAV7またはAAV8、または前記血清型の1つ以上のハイブリッドのAAVのプロモーター配列である;
(B)前記ベクターの前記AAVヘルパー機能提供ポリヌクレオチドは、AAV2 Capタンパク質をコードし、前記非天然AAV血清型プロモーター配列は、血清型AAV1、AAV3、AAV4、AAV5、AAV6、AAV7またはAAV8、または前記血清型の1つ以上のハイブリッドのAAVのプロモーター配列である;
(C)前記ベクターの前記AAVヘルパー機能提供ポリヌクレオチドは、AAV3 Capタンパク質をコードし、前記非天然AAV血清型プロモーター配列は、血清型AAV1、AAV4、AAV5、AAV6、AAV7またはAAV8、または前記血清型の1つ以上のハイブリッドのAAVのプロモーター配列である;
(D)前記ベクターの前記AAVヘルパー機能提供ポリヌクレオチドは、AAV4 Capタンパク質をコードし、前記非天然AAV血清型プロモーター配列は、血清型AAV1、AAV3、AAV5、AAV6、AAV7またはAAV8、または前記血清型の1つ以上のハイブリッドのAAVのプロモーター配列である;
(E)前記ベクターの前記AAVヘルパー機能提供ポリヌクレオチドは、AAV5 Capタンパク質をコードし、前記非天然AAV血清型プロモーター配列は、血清型AAV1、AAV3、AAV4、AAV6、AAV7またはAAV8、または前記血清型の1つ以上のハイブリッドのAAVのプロモーター配列である;
(F)前記ベクターの前記AAVヘルパー機能提供ポリヌクレオチドは、AAV6 Capタンパク質をコードし、前記非天然AAV血清型プロモーター配列は、血清型AAV1、AAV3、AAV4、AAV5、AAV7またはAAV8、または前記血清型の1つ以上のハイブリッドのAAVのプロモーター配列である;
(G)前記ベクターの前記AAVヘルパー機能提供ポリヌクレオチドは、AAV7 Capタンパク質をコードし、前記非天然AAV血清型プロモーター配列は、血清型AAV1、AAV3、AAV4、AAV5、AAV6またはAAV8、または前記血清型の1つ以上のハイブリッドのAAVのプロモーター配列である;または
(H)前記ベクターの前記AAVヘルパー機能提供ポリヌクレオチドは、AAV8 Capタンパク質をコードし、前記非天然AAV血清型プロモーター配列は、血清型AAV1、AAV3、AAV4、AAV5、AAV6またはAAV7、または前記血清型の1つ以上のハイブリッドのAAVのプロモーター配列である、
方法。 - 前記細胞がヒト胚性腎細胞、ベビーハムスター腎細胞またはsf9昆虫細胞である請求項13に記載の方法。
- 前記細胞がHEK293ヒト胚性腎細胞である請求項16に記載の方法。
- 前記細胞がBHK21ベビーハムスター腎細胞である請求項16に記載の方法。
- 請求項6に記載の組換え改変アデノ随伴ウイルス(rAAV)、および、薬学的に許容される担体を含む薬学的組成物。
- 請求項13に記載の組換え改変アデノ随伴ウイルス(rAAV)、および、薬学的に許容される担体を含む薬学的組成物。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US16/512,194 | 2019-07-15 | ||
| US16/512,194 US10557149B1 (en) | 2019-07-15 | 2019-07-15 | Recombinantly-modified adeno-associated virus helper vectors and their use to improve the packaging efficiency of recombinantly-modified adeno-associated virus |
| PCT/US2020/014945 WO2021011029A1 (en) | 2019-07-15 | 2020-01-24 | Recombinantly-modified adeno-associated virus helper vectors and their use to improve the packaging efficiency of recombinantly-modified adeno-associated virus |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2022542828A true JP2022542828A (ja) | 2022-10-07 |
| JPWO2021011029A5 JPWO2021011029A5 (ja) | 2023-02-01 |
Family
ID=69410866
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022502941A Pending JP2022542828A (ja) | 2019-07-15 | 2020-01-24 | 組換え修飾アデノ随伴ウイルスのパッケージング効率を改善するための組換え修飾アデノ随伴ウイルスヘルパーベクターおよびそれらの使用 |
Country Status (7)
| Country | Link |
|---|---|
| US (3) | US10557149B1 (ja) |
| EP (1) | EP3999625A4 (ja) |
| JP (1) | JP2022542828A (ja) |
| KR (1) | KR20220034212A (ja) |
| CN (1) | CN114450393A (ja) |
| AU (1) | AU2020315770A1 (ja) |
| WO (1) | WO2021011029A1 (ja) |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3655041A4 (en) * | 2017-08-25 | 2021-04-21 | Ovid Therapeutics Inc | RECOMBINANT ADENO-ASSOCIATED VECTORS |
| US10557149B1 (en) * | 2019-07-15 | 2020-02-11 | Vigene Biosciences, Inc. | Recombinantly-modified adeno-associated virus helper vectors and their use to improve the packaging efficiency of recombinantly-modified adeno-associated virus |
| CN114657153A (zh) * | 2022-05-24 | 2022-06-24 | 上海健士拜生物科技有限公司 | rAAV重组包装质粒、用于rAAV包装的质粒系统和rAAV的制备方法 |
| WO2024160232A1 (zh) * | 2023-02-01 | 2024-08-08 | 纽福斯(苏州)生物科技有限公司 | 质粒包装系统及其应用 |
| CN117925663A (zh) * | 2023-12-04 | 2024-04-26 | 广州派真生物技术有限公司 | 一种用于重组腺相关病毒包装的质粒系统及其应用 |
| CN117660534B (zh) * | 2023-12-13 | 2024-05-07 | 广州派真生物技术有限公司 | 一种降低重组腺相关病毒中宿主细胞dna残留的辅助质粒及应用 |
Family Cites Families (53)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6342390B1 (en) | 1994-11-23 | 2002-01-29 | The United States Of America As Represented By The Secretary Of Health And Human Services | Lipid vesicles containing adeno-associated virus rep protein for transgene integration and gene therapy |
| US6093570A (en) | 1995-06-07 | 2000-07-25 | The University Of North Carolina At Chapel Hill | Helper virus-free AAV production |
| ES2210391T3 (es) * | 1995-08-03 | 2004-07-01 | Avigen, Inc. | Sistema auxiliar de alta eficacia para la produccion de vectores aav. |
| US6001650A (en) * | 1995-08-03 | 1999-12-14 | Avigen, Inc. | High-efficiency wild-type-free AAV helper functions |
| WO1997009441A2 (en) * | 1995-09-08 | 1997-03-13 | Genzyme Corporation | Improved aav vectors for gene therapy |
| WO1998011244A2 (en) | 1996-09-11 | 1998-03-19 | The Government Of The United States Of America, Represented By The Secretary, Department Of Health And Human Services | Aav4 vector and uses thereof |
| EP1007637B1 (en) * | 1997-04-14 | 2004-06-30 | Cell Genesys, Inc. | Methods for increasing the efficiency of recombinant aav product |
| US6566118B1 (en) | 1997-09-05 | 2003-05-20 | Targeted Genetics Corporation | Methods for generating high titer helper-free preparations of released recombinant AAV vectors |
| US6995006B2 (en) | 1997-09-05 | 2006-02-07 | Targeted Genetics Corporation | Methods for generating high titer helper-free preparations of released recombinant AAV vectors |
| IT1297074B1 (it) | 1997-11-21 | 1999-08-03 | Angeletti P Ist Richerche Bio | Forme ormone-dipendenti delle proteine rep del virus adeno-associato (aav-2), sequenze di dna codificanti per esse, vettori che le |
| ATE402254T1 (de) | 1998-05-28 | 2008-08-15 | Us Gov Health & Human Serv | Aav5 vektoren und deren verwendung |
| US6984517B1 (en) | 1998-05-28 | 2006-01-10 | The United States Of America As Represented By The Department Of Health And Human Services | AAV5 vector and uses thereof |
| US6759237B1 (en) | 1998-11-05 | 2004-07-06 | The Trustees Of The University Of Pennsylvania | Adeno-associated virus serotype 1 nucleic acid sequences, vectors and host cells containing same |
| US6759050B1 (en) | 1998-12-03 | 2004-07-06 | Avigen, Inc. | Excipients for use in adeno-associated virus pharmaceutical formulations, and pharmaceutical formulations made therewith |
| DE19905501B4 (de) | 1999-02-10 | 2005-05-19 | MediGene AG, Gesellschaft für molekularbiologische Kardiologie und Onkologie | Verfahren zur Herstellung eines rekombinanten Adeno-assoziierten Virus, geeignete Mittel hierzu sowie Verwendung zur Herstellung eines Arzneimittels |
| JP4693244B2 (ja) * | 1999-03-18 | 2011-06-01 | ザ・トラステイーズ・オブ・ザ・ユニバーシテイ・オブ・ペンシルベニア | 組換えアデノ随伴ウイルスのヘルパー無しの生産のための組成物および方法 |
| US6498244B1 (en) | 1999-05-28 | 2002-12-24 | Cell Genesys, Inc. | Adeno-associated virus capsid immunologic determinants |
| US7115391B1 (en) | 1999-10-01 | 2006-10-03 | Genovo, Inc. | Production of recombinant AAV using adenovirus comprising AAV rep/cap genes |
| US7208315B2 (en) | 2000-01-05 | 2007-04-24 | Fred Hutchinson Cancer Research Center | Compositions and methods for efficient AAV vector production |
| DE10066104A1 (de) * | 2000-09-08 | 2003-01-09 | Medigene Ag | Wirtszellen zur Verpackung von rekombinantem Adeno-assoziiertem Virus (rAAV), Verfahren zu ihrer Herstellung und deren Verwendung |
| WO2002053703A2 (en) | 2001-01-05 | 2002-07-11 | Children's Hospital, Inc. | Aav2 vectors and methods |
| US6841357B1 (en) | 2001-03-30 | 2005-01-11 | Stratagene California | Method and kits for titering adeno-associated virus vectors |
| US6723551B2 (en) | 2001-11-09 | 2004-04-20 | The United States Of America As Represented By The Department Of Health And Human Services | Production of adeno-associated virus in insect cells |
| AU2002360355B2 (en) | 2001-11-09 | 2005-07-07 | Government Of The United States Of America, Department Of Health And Human Services | Production of adeno-associated virus in insect cells |
| NZ618298A (en) * | 2001-11-13 | 2015-04-24 | Univ Pennsylvania | A method of detecting and/or identifying adeno-associated virus (aav) sequences and isolating novel sequences identified thereby |
| ES2975413T3 (es) | 2001-12-17 | 2024-07-05 | Univ Pennsylvania | Secuencias de serotipo 8 de virus adenoasociado (AAV), vectores que las contienen y usos de las mismas |
| WO2003104392A2 (en) * | 2001-12-18 | 2003-12-18 | University Of North Carolina At Chapel Hill | Improved reagents and methods for producing parvoviruses |
| US7419817B2 (en) | 2002-05-17 | 2008-09-02 | The United States Of America As Represented By The Secretary Department Of Health And Human Services, Nih. | Scalable purification of AAV2, AAV4 or AAV5 using ion-exchange chromatography |
| US7122348B2 (en) | 2002-12-11 | 2006-10-17 | City Of Hope | AAV2 Rep protein fusions |
| US9441244B2 (en) | 2003-06-30 | 2016-09-13 | The Regents Of The University Of California | Mutant adeno-associated virus virions and methods of use thereof |
| US9233131B2 (en) | 2003-06-30 | 2016-01-12 | The Regents Of The University Of California | Mutant adeno-associated virus virions and methods of use thereof |
| JP5054975B2 (ja) | 2003-09-30 | 2012-10-24 | ザ・トラステイーズ・オブ・ザ・ユニバーシテイ・オブ・ペンシルベニア | アデノ随伴ウイルス(aav)の同源系統群、配列、それらを含有するベクターおよびそれらの用途 |
| US7625570B1 (en) | 2005-03-10 | 2009-12-01 | The Regents Of The University Of California | Methods for purifying adeno-associated virus |
| JP5305913B2 (ja) | 2005-10-20 | 2013-10-02 | アムステルダム モレキュラー セラピューティクス ビー.ブイ. | 昆虫細胞で産生される改良されたaavベクター |
| CA2655957C (en) * | 2006-06-21 | 2016-05-03 | Amsterdam Molecular Therapeutics (Amt) B.V. | Vectors with modified initiation codon for the translation of aav-rep78 useful for production of aav in insect cells |
| WO2008024998A2 (en) | 2006-08-24 | 2008-02-28 | Virovek, Inc. | Expression in insect cells of genes with overlapping open reading frames, methods and compositions therefor |
| CN105861454B (zh) | 2009-06-16 | 2020-03-03 | 建新公司 | 用于纯化重组aav载体的改进方法 |
| US8663624B2 (en) | 2010-10-06 | 2014-03-04 | The Regents Of The University Of California | Adeno-associated virus virions with variant capsid and methods of use thereof |
| CN103502458B (zh) | 2011-02-17 | 2016-11-16 | 宾夕法尼亚大学托管会 | 用于改变组织特异性和改善aav9-介导的基因转移的组合物和方法 |
| EP2500434A1 (en) | 2011-03-12 | 2012-09-19 | Association Institut de Myologie | Capsid-free AAV vectors, compositions, and methods for vector production and gene delivery |
| US20140155469A1 (en) | 2011-04-19 | 2014-06-05 | The Research Foundation Of State University Of New York | Adeno-associated-virus rep sequences, vectors and viruses |
| PL2699270T3 (pl) | 2011-04-22 | 2017-12-29 | The Regents Of The University Of California | Wiriony wirusa towarzyszącego adenowirusom z różnymi kapsydami i sposoby ich zastosowania |
| WO2013009981A2 (en) * | 2011-07-12 | 2013-01-17 | University Of Rochester | Treating neurological disease or injury with a dynamin-related protein 1 (drp1) encoding nucleic acid |
| EP2771455B1 (en) | 2011-10-28 | 2016-10-05 | The University of North Carolina At Chapel Hill | Cell line for production of adeno-associated virus |
| HUE038850T2 (hu) | 2012-05-25 | 2018-11-28 | Univ California | Eljárások és kompozíciók cél-DNS RNS-irányított módosításához és transzkripció RNS-irányított modulálásához |
| EP3738974A1 (en) * | 2012-09-28 | 2020-11-18 | The University of North Carolina at Chapel Hill | Aav vectors targeted to oligodendrocytes |
| US8697359B1 (en) | 2012-12-12 | 2014-04-15 | The Broad Institute, Inc. | CRISPR-Cas systems and methods for altering expression of gene products |
| US10161011B2 (en) | 2013-11-29 | 2018-12-25 | Takara Bio Inc. | Method for quantifying adeno-associated virus |
| US10837027B2 (en) * | 2014-03-10 | 2020-11-17 | Uniqure Ip B.V. | Further improved AAV vectors produced in insect cells |
| WO2017112948A1 (en) | 2015-12-24 | 2017-06-29 | University Of Florida Research Foundation, Inc. | Improved aav production using suspension adapted cells |
| CA3012409A1 (en) * | 2016-01-29 | 2017-08-03 | Sirion Biotech Gmbh | Aav-based conditional expression system |
| US10294452B2 (en) | 2016-11-22 | 2019-05-21 | Dao-Yao He | Lysis, extraction and purification of adeno-associated virus and adenovirus from host cells |
| US10557149B1 (en) * | 2019-07-15 | 2020-02-11 | Vigene Biosciences, Inc. | Recombinantly-modified adeno-associated virus helper vectors and their use to improve the packaging efficiency of recombinantly-modified adeno-associated virus |
-
2019
- 2019-07-15 US US16/512,194 patent/US10557149B1/en active Active
- 2019-12-06 US US16/705,831 patent/US11001859B2/en active Active
-
2020
- 2020-01-24 EP EP20840038.2A patent/EP3999625A4/en active Pending
- 2020-01-24 CN CN202080064497.7A patent/CN114450393A/zh active Pending
- 2020-01-24 JP JP2022502941A patent/JP2022542828A/ja active Pending
- 2020-01-24 US US17/627,170 patent/US20220290178A1/en active Pending
- 2020-01-24 KR KR1020227004887A patent/KR20220034212A/ko unknown
- 2020-01-24 WO PCT/US2020/014945 patent/WO2021011029A1/en unknown
- 2020-01-24 AU AU2020315770A patent/AU2020315770A1/en active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| EP3999625A1 (en) | 2022-05-25 |
| US11001859B2 (en) | 2021-05-11 |
| AU2020315770A1 (en) | 2022-02-17 |
| KR20220034212A (ko) | 2022-03-17 |
| CN114450393A (zh) | 2022-05-06 |
| US10557149B1 (en) | 2020-02-11 |
| US20210017538A1 (en) | 2021-01-21 |
| EP3999625A4 (en) | 2023-08-30 |
| US20220290178A1 (en) | 2022-09-15 |
| WO2021011029A1 (en) | 2021-01-21 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US11001859B2 (en) | Recombinantly-modified adeno-associated virus helper vectors and their use to improve the packaging efficiency of recombinantly-modified adeno-associated virus | |
| KR102370675B1 (ko) | 표적 핵산의 변형을 위한 개선된 방법 | |
| AU2023226754A1 (en) | Compositions and methods for modifying genomes | |
| DK2087106T3 (en) | MUTATING DELTA8 DESATURATION GENES CONSTRUCTED BY TARGETED MUTAGENES AND USE THEREOF IN THE MANUFACTURE OF MULTI-Saturated FAT ACIDS | |
| KR20120099509A (ko) | 재조합 숙주 세포에서 육탄당 키나아제의 발현 | |
| CN109563505A (zh) | 用于真核细胞的组装系统 | |
| US20220282277A1 (en) | Use of ion concentrations to increase the packaging efficiency of recombinant adeno-associated virus | |
| CN115698297A (zh) | 多模块生物合成酶基因组合文库的制备方法 | |
| US20220257678A1 (en) | Recombinantly-modified adeno-associated virus (raav) having improved packaging efficiency | |
| KR20210118402A (ko) | 위스콧-알드리치(Wiskott-Aldrich) 증후군에 대한 조혈 줄기 세포-유전자 치료요법 | |
| CN111534542A (zh) | piggyBac转座子系统介导的真核生物转基因细胞系及构建方法 | |
| CN113637672B (zh) | 一种碱基编辑工具及其构建方法 | |
| CN114644581B (zh) | 含芳基硫酚或芳基硒酚经修饰的氨基酸、重组蛋白及其生物合成方法及应用 | |
| CN112209883B (zh) | 一种与rna特异性结合的荧光素染料及其应用 | |
| CN114645066B (zh) | 一种用于艾滋病基因治疗的核酸构建体 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A712 Effective date: 20220526 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20220526 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220916 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230116 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20230116 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20231227 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240116 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20240416 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240507 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20240827 |