JP2022017594A - デュシェンヌ型筋ジストロフィーおよび関連障害の処置のための組成物および方法 - Google Patents
デュシェンヌ型筋ジストロフィーおよび関連障害の処置のための組成物および方法 Download PDFInfo
- Publication number
- JP2022017594A JP2022017594A JP2021185544A JP2021185544A JP2022017594A JP 2022017594 A JP2022017594 A JP 2022017594A JP 2021185544 A JP2021185544 A JP 2021185544A JP 2021185544 A JP2021185544 A JP 2021185544A JP 2022017594 A JP2022017594 A JP 2022017594A
- Authority
- JP
- Japan
- Prior art keywords
- exon
- dystrophin
- myostatin
- seq
- sequence
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 238000000034 method Methods 0.000 title abstract description 240
- 206010013801 Duchenne Muscular Dystrophy Diseases 0.000 title abstract description 136
- 239000000203 mixture Substances 0.000 title abstract description 74
- 230000000692 anti-sense effect Effects 0.000 abstract description 330
- 108010069091 Dystrophin Proteins 0.000 abstract description 324
- 102000001039 Dystrophin Human genes 0.000 abstract description 294
- 108010056852 Myostatin Proteins 0.000 abstract description 280
- 102000004472 Myostatin Human genes 0.000 abstract description 276
- 239000003814 drug Substances 0.000 abstract description 194
- 229940124597 therapeutic agent Drugs 0.000 abstract description 172
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 abstract description 91
- 208000035475 disorder Diseases 0.000 abstract description 72
- 238000011282 treatment Methods 0.000 abstract description 70
- 210000003205 muscle Anatomy 0.000 abstract description 50
- 241000699670 Mus sp. Species 0.000 abstract description 44
- 230000001965 increasing effect Effects 0.000 abstract description 33
- 230000009885 systemic effect Effects 0.000 abstract description 5
- 238000010172 mouse model Methods 0.000 abstract description 2
- 230000008685 targeting Effects 0.000 description 238
- 125000003729 nucleotide group Chemical group 0.000 description 226
- 239000002773 nucleotide Substances 0.000 description 187
- -1 13 Chemical compound 0.000 description 139
- 239000002777 nucleoside Substances 0.000 description 132
- 108020004999 messenger RNA Proteins 0.000 description 130
- 230000000295 complement effect Effects 0.000 description 128
- 150000001875 compounds Chemical class 0.000 description 113
- OPTASPLRGRRNAP-UHFFFAOYSA-N cytosine Chemical compound NC=1C=CNC(=O)N=1 OPTASPLRGRRNAP-UHFFFAOYSA-N 0.000 description 108
- RWQNBRDOKXIBIV-UHFFFAOYSA-N thymine Chemical compound CC1=CNC(=O)NC1=O RWQNBRDOKXIBIV-UHFFFAOYSA-N 0.000 description 108
- 230000014509 gene expression Effects 0.000 description 105
- 229910052799 carbon Inorganic materials 0.000 description 94
- 229910052739 hydrogen Inorganic materials 0.000 description 93
- 239000002585 base Substances 0.000 description 91
- 108700024394 Exon Proteins 0.000 description 85
- ISAKRJDGNUQOIC-UHFFFAOYSA-N Uracil Chemical compound O=C1C=CNC(=O)N1 ISAKRJDGNUQOIC-UHFFFAOYSA-N 0.000 description 66
- 235000000346 sugar Nutrition 0.000 description 64
- 108090000623 proteins and genes Proteins 0.000 description 61
- 210000004027 cell Anatomy 0.000 description 56
- 150000003833 nucleoside derivatives Chemical class 0.000 description 56
- 102000004169 proteins and genes Human genes 0.000 description 55
- 108010051109 Cell-Penetrating Peptides Proteins 0.000 description 54
- 102000020313 Cell-Penetrating Peptides Human genes 0.000 description 54
- 229940104302 cytosine Drugs 0.000 description 54
- 235000018102 proteins Nutrition 0.000 description 54
- 229940113082 thymine Drugs 0.000 description 54
- 102000039446 nucleic acids Human genes 0.000 description 52
- 108020004707 nucleic acids Proteins 0.000 description 52
- 150000007523 nucleic acids Chemical class 0.000 description 52
- 108090000765 processed proteins & peptides Proteins 0.000 description 51
- 230000035772 mutation Effects 0.000 description 49
- 101000886562 Homo sapiens Growth/differentiation factor 8 Proteins 0.000 description 43
- 102000054677 human MSTN Human genes 0.000 description 43
- 239000012634 fragment Substances 0.000 description 42
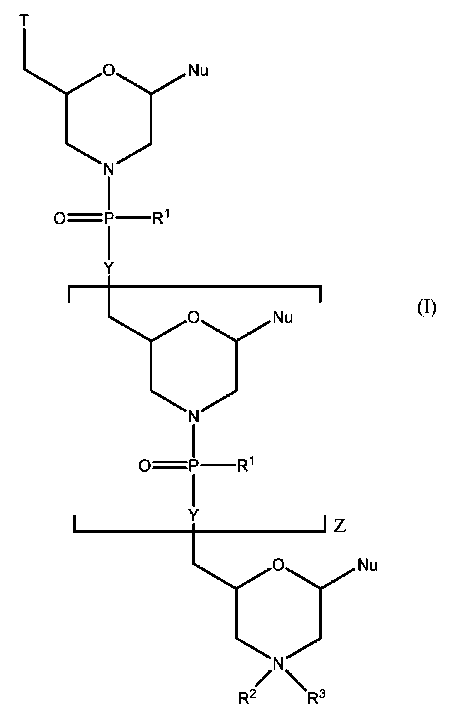
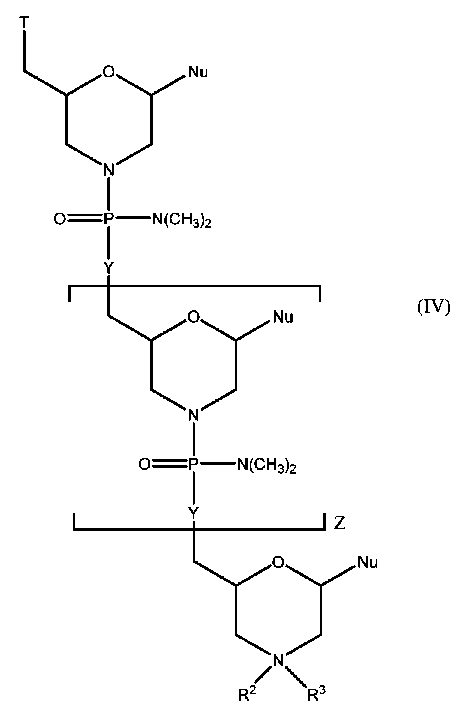
- 125000004573 morpholin-4-yl group Chemical group N1(CCOCC1)* 0.000 description 41
- 239000008194 pharmaceutical composition Substances 0.000 description 40
- 238000012545 processing Methods 0.000 description 39
- 150000003839 salts Chemical class 0.000 description 37
- 201000006938 muscular dystrophy Diseases 0.000 description 35
- 125000002147 dimethylamino group Chemical group [H]C([H])([H])N(*)C([H])([H])[H] 0.000 description 34
- 239000002502 liposome Substances 0.000 description 34
- 229940035893 uracil Drugs 0.000 description 33
- LRSASMSXMSNRBT-UHFFFAOYSA-N 5-methylcytosine Chemical compound CC1=CNC(=O)N=C1N LRSASMSXMSNRBT-UHFFFAOYSA-N 0.000 description 31
- 125000002091 cationic group Chemical group 0.000 description 31
- 125000003835 nucleoside group Chemical group 0.000 description 31
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 30
- 108091034117 Oligonucleotide Proteins 0.000 description 30
- 125000000217 alkyl group Chemical group 0.000 description 29
- 230000001225 therapeutic effect Effects 0.000 description 29
- 230000000694 effects Effects 0.000 description 28
- 230000002401 inhibitory effect Effects 0.000 description 28
- 150000001413 amino acids Chemical class 0.000 description 27
- 210000001519 tissue Anatomy 0.000 description 27
- 108020004414 DNA Proteins 0.000 description 26
- 108091093037 Peptide nucleic acid Proteins 0.000 description 26
- 125000002252 acyl group Chemical group 0.000 description 26
- 235000001014 amino acid Nutrition 0.000 description 26
- 229940024606 amino acid Drugs 0.000 description 25
- 230000001939 inductive effect Effects 0.000 description 25
- 125000005647 linker group Chemical group 0.000 description 25
- 125000002221 trityl group Chemical group [H]C1=C([H])C([H])=C([H])C([H])=C1C([*])(C1=C(C(=C(C(=C1[H])[H])[H])[H])[H])C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 25
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 24
- 101001053946 Homo sapiens Dystrophin Proteins 0.000 description 24
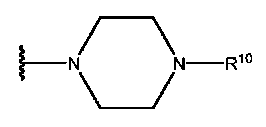
- GLUUGHFHXGJENI-UHFFFAOYSA-N Piperazine Chemical compound C1CNCCN1 GLUUGHFHXGJENI-UHFFFAOYSA-N 0.000 description 24
- 230000004048 modification Effects 0.000 description 24
- 238000012986 modification Methods 0.000 description 24
- 101710163270 Nuclease Proteins 0.000 description 22
- 230000027455 binding Effects 0.000 description 22
- FDGQSTZJBFJUBT-UHFFFAOYSA-N hypoxanthine Chemical compound O=C1NC=NC2=C1NC=N2 FDGQSTZJBFJUBT-UHFFFAOYSA-N 0.000 description 21
- 125000006239 protecting group Chemical group 0.000 description 21
- 238000012360 testing method Methods 0.000 description 21
- 108020005067 RNA Splice Sites Proteins 0.000 description 20
- 238000009472 formulation Methods 0.000 description 20
- 229910052757 nitrogen Inorganic materials 0.000 description 20
- 201000010099 disease Diseases 0.000 description 19
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 19
- 102000004196 processed proteins & peptides Human genes 0.000 description 19
- 238000013518 transcription Methods 0.000 description 18
- 230000035897 transcription Effects 0.000 description 18
- 230000003442 weekly effect Effects 0.000 description 18
- 239000003937 drug carrier Substances 0.000 description 17
- 239000000835 fiber Substances 0.000 description 17
- 229910052698 phosphorus Inorganic materials 0.000 description 17
- 108020003175 receptors Proteins 0.000 description 17
- 102000005962 receptors Human genes 0.000 description 17
- 239000004475 Arginine Substances 0.000 description 16
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical group N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 16
- ODKSFYDXXFIFQN-BYPYZUCNSA-P L-argininium(2+) Chemical compound NC(=[NH2+])NCCC[C@H]([NH3+])C(O)=O ODKSFYDXXFIFQN-BYPYZUCNSA-P 0.000 description 16
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 16
- 235000009697 arginine Nutrition 0.000 description 16
- UYTPUPDQBNUYGX-UHFFFAOYSA-N guanine Chemical compound O=C1NC(N)=NC2=C1N=CN2 UYTPUPDQBNUYGX-UHFFFAOYSA-N 0.000 description 16
- 238000001727 in vivo Methods 0.000 description 16
- 239000000178 monomer Substances 0.000 description 16
- 210000000663 muscle cell Anatomy 0.000 description 16
- 239000000047 product Substances 0.000 description 16
- 238000003757 reverse transcription PCR Methods 0.000 description 16
- 238000006243 chemical reaction Methods 0.000 description 15
- 241000699666 Mus <mouse, genus> Species 0.000 description 14
- 239000000074 antisense oligonucleotide Substances 0.000 description 14
- 238000012230 antisense oligonucleotides Methods 0.000 description 14
- 125000003118 aryl group Chemical group 0.000 description 14
- 229940079593 drug Drugs 0.000 description 14
- 208000024891 symptom Diseases 0.000 description 14
- 238000012384 transportation and delivery Methods 0.000 description 14
- 125000003710 aryl alkyl group Chemical group 0.000 description 13
- 125000004437 phosphorous atom Chemical group 0.000 description 13
- 239000000243 solution Substances 0.000 description 13
- 201000006935 Becker muscular dystrophy Diseases 0.000 description 12
- 230000015572 biosynthetic process Effects 0.000 description 12
- 229960005141 piperazine Drugs 0.000 description 12
- 229920001184 polypeptide Polymers 0.000 description 12
- 238000002360 preparation method Methods 0.000 description 12
- 230000002829 reductive effect Effects 0.000 description 12
- 238000006467 substitution reaction Methods 0.000 description 12
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 11
- UGQMRVRMYYASKQ-UHFFFAOYSA-N Hypoxanthine nucleoside Natural products OC1C(O)C(CO)OC1N1C(NC=NC2=O)=C2N=C1 UGQMRVRMYYASKQ-UHFFFAOYSA-N 0.000 description 11
- 239000002253 acid Substances 0.000 description 11
- 230000000875 corresponding effect Effects 0.000 description 11
- 239000003623 enhancer Substances 0.000 description 11
- 125000004433 nitrogen atom Chemical group N* 0.000 description 11
- 238000003786 synthesis reaction Methods 0.000 description 11
- 206010064571 Gene mutation Diseases 0.000 description 10
- 108091027305 Heteroduplex Proteins 0.000 description 10
- 210000004369 blood Anatomy 0.000 description 10
- 239000008280 blood Substances 0.000 description 10
- 101150015424 dmd gene Proteins 0.000 description 10
- 239000000839 emulsion Substances 0.000 description 10
- 230000006872 improvement Effects 0.000 description 10
- 150000002632 lipids Chemical class 0.000 description 10
- 229940002612 prodrug Drugs 0.000 description 10
- 239000000651 prodrug Substances 0.000 description 10
- 239000000523 sample Substances 0.000 description 10
- 239000000126 substance Substances 0.000 description 10
- RYYWUUFWQRZTIU-UHFFFAOYSA-K thiophosphate Chemical compound [O-]P([O-])([O-])=S RYYWUUFWQRZTIU-UHFFFAOYSA-K 0.000 description 10
- 229930024421 Adenine Natural products 0.000 description 9
- GFFGJBXGBJISGV-UHFFFAOYSA-N Adenine Chemical compound NC1=NC=NC2=C1N=CN2 GFFGJBXGBJISGV-UHFFFAOYSA-N 0.000 description 9
- 108091027974 Mature messenger RNA Proteins 0.000 description 9
- PYMYPHUHKUWMLA-LMVFSUKVSA-N Ribose Natural products OC[C@@H](O)[C@@H](O)[C@@H](O)C=O PYMYPHUHKUWMLA-LMVFSUKVSA-N 0.000 description 9
- 102000011856 Utrophin Human genes 0.000 description 9
- 108010075653 Utrophin Proteins 0.000 description 9
- 230000009471 action Effects 0.000 description 9
- 229960000643 adenine Drugs 0.000 description 9
- HMFHBZSHGGEWLO-UHFFFAOYSA-N alpha-D-Furanose-Ribose Natural products OCC1OC(O)C(O)C1O HMFHBZSHGGEWLO-UHFFFAOYSA-N 0.000 description 9
- 230000037396 body weight Effects 0.000 description 9
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 9
- 238000011260 co-administration Methods 0.000 description 9
- 238000010217 densitometric analysis Methods 0.000 description 9
- 238000009396 hybridization Methods 0.000 description 9
- 238000007911 parenteral administration Methods 0.000 description 9
- 230000032258 transport Effects 0.000 description 9
- UGQMRVRMYYASKQ-KQYNXXCUSA-N Inosine Chemical compound O[C@@H]1[C@H](O)[C@@H](CO)O[C@H]1N1C2=NC=NC(O)=C2N=C1 UGQMRVRMYYASKQ-KQYNXXCUSA-N 0.000 description 8
- JLCPHMBAVCMARE-UHFFFAOYSA-N [3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-hydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methyl [5-(6-aminopurin-9-yl)-2-(hydroxymethyl)oxolan-3-yl] hydrogen phosphate Polymers Cc1cn(C2CC(OP(O)(=O)OCC3OC(CC3OP(O)(=O)OCC3OC(CC3O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c3nc(N)[nH]c4=O)C(COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3CO)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cc(C)c(=O)[nH]c3=O)n3cc(C)c(=O)[nH]c3=O)n3ccc(N)nc3=O)n3cc(C)c(=O)[nH]c3=O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)O2)c(=O)[nH]c1=O JLCPHMBAVCMARE-UHFFFAOYSA-N 0.000 description 8
- 210000004899 c-terminal region Anatomy 0.000 description 8
- 230000015556 catabolic process Effects 0.000 description 8
- 238000007796 conventional method Methods 0.000 description 8
- 238000012217 deletion Methods 0.000 description 8
- 230000037430 deletion Effects 0.000 description 8
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 8
- 230000006870 function Effects 0.000 description 8
- 238000001502 gel electrophoresis Methods 0.000 description 8
- 238000000338 in vitro Methods 0.000 description 8
- 238000001802 infusion Methods 0.000 description 8
- 230000003834 intracellular effect Effects 0.000 description 8
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 8
- 239000004094 surface-active agent Substances 0.000 description 8
- KDCGOANMDULRCW-UHFFFAOYSA-N 7H-purine Chemical compound N1=CNC2=NC=NC2=C1 KDCGOANMDULRCW-UHFFFAOYSA-N 0.000 description 7
- MSSXOMSJDRHRMC-UHFFFAOYSA-N 9H-purine-2,6-diamine Chemical compound NC1=NC(N)=C2NC=NC2=N1 MSSXOMSJDRHRMC-UHFFFAOYSA-N 0.000 description 7
- 238000009825 accumulation Methods 0.000 description 7
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 description 7
- 238000006731 degradation reaction Methods 0.000 description 7
- ANCLJVISBRWUTR-UHFFFAOYSA-N diaminophosphinic acid Chemical compound NP(N)(O)=O ANCLJVISBRWUTR-UHFFFAOYSA-N 0.000 description 7
- 235000014113 dietary fatty acids Nutrition 0.000 description 7
- 239000002552 dosage form Substances 0.000 description 7
- 229930195729 fatty acid Natural products 0.000 description 7
- 239000000194 fatty acid Substances 0.000 description 7
- 238000004519 manufacturing process Methods 0.000 description 7
- 238000005259 measurement Methods 0.000 description 7
- 150000003230 pyrimidines Chemical class 0.000 description 7
- 230000004044 response Effects 0.000 description 7
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 description 6
- OISVCGZHLKNMSJ-UHFFFAOYSA-N 2,6-dimethylpyridine Chemical compound CC1=CC=CC(C)=N1 OISVCGZHLKNMSJ-UHFFFAOYSA-N 0.000 description 6
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 6
- 102100021886 Activin receptor type-2A Human genes 0.000 description 6
- 108020000948 Antisense Oligonucleotides Proteins 0.000 description 6
- HMFHBZSHGGEWLO-SOOFDHNKSA-N D-ribofuranose Chemical compound OC[C@H]1OC(O)[C@H](O)[C@@H]1O HMFHBZSHGGEWLO-SOOFDHNKSA-N 0.000 description 6
- 239000005977 Ethylene Substances 0.000 description 6
- 101000970954 Homo sapiens Activin receptor type-2A Proteins 0.000 description 6
- 108091092195 Intron Proteins 0.000 description 6
- 108091028043 Nucleic acid sequence Proteins 0.000 description 6
- 239000003795 chemical substances by application Substances 0.000 description 6
- 238000003776 cleavage reaction Methods 0.000 description 6
- 230000034994 death Effects 0.000 description 6
- 230000007423 decrease Effects 0.000 description 6
- 150000002148 esters Chemical class 0.000 description 6
- 150000004665 fatty acids Chemical class 0.000 description 6
- 230000005021 gait Effects 0.000 description 6
- 210000001087 myotubule Anatomy 0.000 description 6
- 108010082406 peptide permease Proteins 0.000 description 6
- 230000007017 scission Effects 0.000 description 6
- 102000040650 (ribonucleotides)n+m Human genes 0.000 description 5
- 239000004471 Glycine Substances 0.000 description 5
- 229930010555 Inosine Natural products 0.000 description 5
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 5
- YNAVUWVOSKDBBP-UHFFFAOYSA-N Morpholine Chemical group C1COCCN1 YNAVUWVOSKDBBP-UHFFFAOYSA-N 0.000 description 5
- CMVLJPNLCSZQGQ-UHFFFAOYSA-N NP(N)(N)=O.Cl.Cl Chemical compound NP(N)(N)=O.Cl.Cl CMVLJPNLCSZQGQ-UHFFFAOYSA-N 0.000 description 5
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 5
- CZPWVGJYEJSRLH-UHFFFAOYSA-N Pyrimidine Chemical compound C1=CN=CN=C1 CZPWVGJYEJSRLH-UHFFFAOYSA-N 0.000 description 5
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 5
- 125000003277 amino group Chemical group 0.000 description 5
- 239000000427 antigen Substances 0.000 description 5
- 108091007433 antigens Proteins 0.000 description 5
- 102000036639 antigens Human genes 0.000 description 5
- 235000003704 aspartic acid Nutrition 0.000 description 5
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 description 5
- 239000002775 capsule Substances 0.000 description 5
- 239000000969 carrier Substances 0.000 description 5
- 230000001413 cellular effect Effects 0.000 description 5
- 230000036755 cellular response Effects 0.000 description 5
- 239000003246 corticosteroid Substances 0.000 description 5
- 230000003247 decreasing effect Effects 0.000 description 5
- 230000007812 deficiency Effects 0.000 description 5
- 230000004761 fibrosis Effects 0.000 description 5
- 239000000499 gel Substances 0.000 description 5
- 239000001257 hydrogen Substances 0.000 description 5
- 229960003786 inosine Drugs 0.000 description 5
- 238000001990 intravenous administration Methods 0.000 description 5
- 230000003902 lesion Effects 0.000 description 5
- 230000000670 limiting effect Effects 0.000 description 5
- 239000007788 liquid Substances 0.000 description 5
- 230000001404 mediated effect Effects 0.000 description 5
- 230000035515 penetration Effects 0.000 description 5
- 125000002467 phosphate group Chemical group [H]OP(=O)(O[H])O[*] 0.000 description 5
- 230000006461 physiological response Effects 0.000 description 5
- 239000000843 powder Substances 0.000 description 5
- 238000011002 quantification Methods 0.000 description 5
- 238000011084 recovery Methods 0.000 description 5
- 210000002027 skeletal muscle Anatomy 0.000 description 5
- 239000011780 sodium chloride Substances 0.000 description 5
- 239000007787 solid Substances 0.000 description 5
- 238000007920 subcutaneous administration Methods 0.000 description 5
- 238000011200 topical administration Methods 0.000 description 5
- 230000000699 topical effect Effects 0.000 description 5
- 238000001262 western blot Methods 0.000 description 5
- ASJSAQIRZKANQN-CRCLSJGQSA-N 2-deoxy-D-ribose Chemical group OC[C@@H](O)[C@@H](O)CC=O ASJSAQIRZKANQN-CRCLSJGQSA-N 0.000 description 4
- QGJOPFRUJISHPQ-UHFFFAOYSA-N Carbon disulfide Chemical class S=C=S QGJOPFRUJISHPQ-UHFFFAOYSA-N 0.000 description 4
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 4
- 206010016654 Fibrosis Diseases 0.000 description 4
- 206010028289 Muscle atrophy Diseases 0.000 description 4
- 108010003723 Single-Domain Antibodies Proteins 0.000 description 4
- 150000007513 acids Chemical class 0.000 description 4
- 150000001412 amines Chemical class 0.000 description 4
- 238000010171 animal model Methods 0.000 description 4
- 238000003556 assay Methods 0.000 description 4
- 230000008901 benefit Effects 0.000 description 4
- 125000003236 benzoyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C(*)=O 0.000 description 4
- 239000003833 bile salt Substances 0.000 description 4
- 125000004432 carbon atom Chemical group C* 0.000 description 4
- 239000002299 complementary DNA Substances 0.000 description 4
- 201000006815 congenital muscular dystrophy Diseases 0.000 description 4
- 229960001334 corticosteroids Drugs 0.000 description 4
- 235000018417 cysteine Nutrition 0.000 description 4
- 230000002708 enhancing effect Effects 0.000 description 4
- 230000001815 facial effect Effects 0.000 description 4
- 125000000524 functional group Chemical group 0.000 description 4
- JYGXADMDTFJGBT-VWUMJDOOSA-N hydrocortisone Chemical compound O=C1CC[C@]2(C)[C@H]3[C@@H](O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 JYGXADMDTFJGBT-VWUMJDOOSA-N 0.000 description 4
- 238000002347 injection Methods 0.000 description 4
- 239000007924 injection Substances 0.000 description 4
- 238000001361 intraarterial administration Methods 0.000 description 4
- 230000033001 locomotion Effects 0.000 description 4
- 239000000463 material Substances 0.000 description 4
- 230000007659 motor function Effects 0.000 description 4
- 230000037257 muscle growth Effects 0.000 description 4
- 230000003387 muscular Effects 0.000 description 4
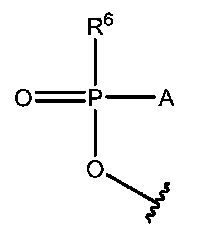
- PTMHPRAIXMAOOB-UHFFFAOYSA-L phosphoramidate Chemical compound NP([O-])([O-])=O PTMHPRAIXMAOOB-UHFFFAOYSA-L 0.000 description 4
- 239000011574 phosphorus Substances 0.000 description 4
- XHXFXVLFKHQFAL-UHFFFAOYSA-N phosphoryl trichloride Chemical compound ClP(Cl)(Cl)=O XHXFXVLFKHQFAL-UHFFFAOYSA-N 0.000 description 4
- 238000011160 research Methods 0.000 description 4
- 239000011347 resin Substances 0.000 description 4
- 229920005989 resin Polymers 0.000 description 4
- 210000003019 respiratory muscle Anatomy 0.000 description 4
- 201000009410 rhabdomyosarcoma Diseases 0.000 description 4
- 210000001324 spliceosome Anatomy 0.000 description 4
- 150000003431 steroids Chemical class 0.000 description 4
- 230000004083 survival effect Effects 0.000 description 4
- 239000000725 suspension Substances 0.000 description 4
- 238000011269 treatment regimen Methods 0.000 description 4
- ZIBGPFATKBEMQZ-UHFFFAOYSA-N triethylene glycol Chemical compound OCCOCCOCCO ZIBGPFATKBEMQZ-UHFFFAOYSA-N 0.000 description 4
- 239000003981 vehicle Substances 0.000 description 4
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 4
- 230000004584 weight gain Effects 0.000 description 4
- 235000019786 weight gain Nutrition 0.000 description 4
- 208000030507 AIDS Diseases 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- 102100027647 Activin receptor type-2B Human genes 0.000 description 3
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 3
- 108060002716 Exonuclease Proteins 0.000 description 3
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 3
- 101000937269 Homo sapiens Activin receptor type-2B Proteins 0.000 description 3
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 3
- 102100022745 Laminin subunit alpha-2 Human genes 0.000 description 3
- 208000021642 Muscular disease Diseases 0.000 description 3
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 3
- 239000002202 Polyethylene glycol Substances 0.000 description 3
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical group [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 3
- RYYWUUFWQRZTIU-UHFFFAOYSA-N Thiophosphoric acid Chemical class OP(O)(S)=O RYYWUUFWQRZTIU-UHFFFAOYSA-N 0.000 description 3
- 238000010521 absorption reaction Methods 0.000 description 3
- 125000003545 alkoxy group Chemical group 0.000 description 3
- 125000000539 amino acid group Chemical group 0.000 description 3
- 238000004458 analytical method Methods 0.000 description 3
- 239000005557 antagonist Substances 0.000 description 3
- 239000003242 anti bacterial agent Substances 0.000 description 3
- 238000013459 approach Methods 0.000 description 3
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 3
- 239000003613 bile acid Substances 0.000 description 3
- 230000004071 biological effect Effects 0.000 description 3
- 230000000903 blocking effect Effects 0.000 description 3
- 150000001732 carboxylic acid derivatives Chemical group 0.000 description 3
- 210000000170 cell membrane Anatomy 0.000 description 3
- 239000002738 chelating agent Substances 0.000 description 3
- 238000002512 chemotherapy Methods 0.000 description 3
- 235000015165 citric acid Nutrition 0.000 description 3
- 238000002648 combination therapy Methods 0.000 description 3
- 125000004122 cyclic group Chemical group 0.000 description 3
- 238000002716 delivery method Methods 0.000 description 3
- 230000007717 exclusion Effects 0.000 description 3
- 102000013165 exonuclease Human genes 0.000 description 3
- 239000003862 glucocorticoid Substances 0.000 description 3
- 235000013922 glutamic acid Nutrition 0.000 description 3
- 239000004220 glutamic acid Substances 0.000 description 3
- 230000005764 inhibitory process Effects 0.000 description 3
- 238000000185 intracerebroventricular administration Methods 0.000 description 3
- 238000007918 intramuscular administration Methods 0.000 description 3
- 238000007912 intraperitoneal administration Methods 0.000 description 3
- 238000007913 intrathecal administration Methods 0.000 description 3
- 238000010253 intravenous injection Methods 0.000 description 3
- 239000012528 membrane Substances 0.000 description 3
- 230000004060 metabolic process Effects 0.000 description 3
- 239000011859 microparticle Substances 0.000 description 3
- 238000001964 muscle biopsy Methods 0.000 description 3
- 230000004220 muscle function Effects 0.000 description 3
- 201000000585 muscular atrophy Diseases 0.000 description 3
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 3
- 239000002105 nanoparticle Substances 0.000 description 3
- 125000004430 oxygen atom Chemical group O* 0.000 description 3
- 230000002093 peripheral effect Effects 0.000 description 3
- 239000000546 pharmaceutical excipient Substances 0.000 description 3
- 239000012071 phase Substances 0.000 description 3
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 3
- 150000004713 phosphodiesters Chemical class 0.000 description 3
- 150000008299 phosphorodiamidates Chemical group 0.000 description 3
- 229920001223 polyethylene glycol Polymers 0.000 description 3
- 238000002203 pretreatment Methods 0.000 description 3
- 230000002265 prevention Effects 0.000 description 3
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 3
- 230000008569 process Effects 0.000 description 3
- 230000009467 reduction Effects 0.000 description 3
- 125000000548 ribosyl group Chemical group C1([C@H](O)[C@H](O)[C@H](O1)CO)* 0.000 description 3
- 210000002966 serum Anatomy 0.000 description 3
- 238000010254 subcutaneous injection Methods 0.000 description 3
- 239000007929 subcutaneous injection Substances 0.000 description 3
- 229910052717 sulfur Inorganic materials 0.000 description 3
- 239000011593 sulfur Substances 0.000 description 3
- 239000003826 tablet Substances 0.000 description 3
- 238000001890 transfection Methods 0.000 description 3
- MTCFGRXMJLQNBG-REOHCLBHSA-N (2S)-2-Amino-3-hydroxypropansäure Chemical compound OC[C@H](N)C(O)=O MTCFGRXMJLQNBG-REOHCLBHSA-N 0.000 description 2
- 125000001637 1-naphthyl group Chemical group [H]C1=C([H])C([H])=C2C(*)=C([H])C([H])=C([H])C2=C1[H] 0.000 description 2
- XWKFPIODWVPXLX-UHFFFAOYSA-N 2-methyl-5-methylpyridine Natural products CC1=CC=C(C)N=C1 XWKFPIODWVPXLX-UHFFFAOYSA-N 0.000 description 2
- 125000000094 2-phenylethyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])C([H])([H])* 0.000 description 2
- 102000010825 Actinin Human genes 0.000 description 2
- 108010063503 Actinin Proteins 0.000 description 2
- 108010052946 Activin Receptors Proteins 0.000 description 2
- 102000018918 Activin Receptors Human genes 0.000 description 2
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- 241000282472 Canis lupus familiaris Species 0.000 description 2
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical group [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 2
- 108020004705 Codon Proteins 0.000 description 2
- 108020004635 Complementary DNA Proteins 0.000 description 2
- 108020004394 Complementary RNA Proteins 0.000 description 2
- RGHNJXZEOKUKBD-SQOUGZDYSA-N D-gluconic acid Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C(O)=O RGHNJXZEOKUKBD-SQOUGZDYSA-N 0.000 description 2
- 102000053602 DNA Human genes 0.000 description 2
- 108010042407 Endonucleases Proteins 0.000 description 2
- 102000004190 Enzymes Human genes 0.000 description 2
- 108090000790 Enzymes Proteins 0.000 description 2
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 2
- JZNWSCPGTDBMEW-UHFFFAOYSA-N Glycerophosphorylethanolamin Natural products NCCOP(O)(=O)OCC(O)CO JZNWSCPGTDBMEW-UHFFFAOYSA-N 0.000 description 2
- AEMRFAOFKBGASW-UHFFFAOYSA-N Glycolic acid Chemical compound OCC(O)=O AEMRFAOFKBGASW-UHFFFAOYSA-N 0.000 description 2
- 206010019280 Heart failures Diseases 0.000 description 2
- 241000282412 Homo Species 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 2
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 2
- AVXURJPOCDRRFD-UHFFFAOYSA-N Hydroxylamine Chemical compound ON AVXURJPOCDRRFD-UHFFFAOYSA-N 0.000 description 2
- 108010021625 Immunoglobulin Fragments Proteins 0.000 description 2
- 102000008394 Immunoglobulin Fragments Human genes 0.000 description 2
- XUJNEKJLAYXESH-REOHCLBHSA-N L-Cysteine Chemical compound SC[C@H](N)C(O)=O XUJNEKJLAYXESH-REOHCLBHSA-N 0.000 description 2
- ONIBWKKTOPOVIA-BYPYZUCNSA-N L-Proline Chemical compound OC(=O)[C@@H]1CCCN1 ONIBWKKTOPOVIA-BYPYZUCNSA-N 0.000 description 2
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 description 2
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 2
- HNDVDQJCIGZPNO-YFKPBYRVSA-N L-histidine Chemical compound OC(=O)[C@@H](N)CC1=CN=CN1 HNDVDQJCIGZPNO-YFKPBYRVSA-N 0.000 description 2
- AGPKZVBTJJNPAG-WHFBIAKZSA-N L-isoleucine Chemical compound CC[C@H](C)[C@H](N)C(O)=O AGPKZVBTJJNPAG-WHFBIAKZSA-N 0.000 description 2
- ROHFNLRQFUQHCH-YFKPBYRVSA-N L-leucine Chemical compound CC(C)C[C@H](N)C(O)=O ROHFNLRQFUQHCH-YFKPBYRVSA-N 0.000 description 2
- KDXKERNSBIXSRK-YFKPBYRVSA-N L-lysine Chemical compound NCCCC[C@H](N)C(O)=O KDXKERNSBIXSRK-YFKPBYRVSA-N 0.000 description 2
- COLNVLDHVKWLRT-QMMMGPOBSA-N L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=CC=C1 COLNVLDHVKWLRT-QMMMGPOBSA-N 0.000 description 2
- AYFVYJQAPQTCCC-GBXIJSLDSA-N L-threonine Chemical compound C[C@@H](O)[C@H](N)C(O)=O AYFVYJQAPQTCCC-GBXIJSLDSA-N 0.000 description 2
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 description 2
- KZSNJWFQEVHDMF-BYPYZUCNSA-N L-valine Chemical compound CC(C)[C@H](N)C(O)=O KZSNJWFQEVHDMF-BYPYZUCNSA-N 0.000 description 2
- ROHFNLRQFUQHCH-UHFFFAOYSA-N Leucine Natural products CC(C)CC(N)C(O)=O ROHFNLRQFUQHCH-UHFFFAOYSA-N 0.000 description 2
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 2
- 239000004472 Lysine Substances 0.000 description 2
- 108010059343 MM Form Creatine Kinase Proteins 0.000 description 2
- 241000124008 Mammalia Species 0.000 description 2
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 2
- 108700011259 MicroRNAs Proteins 0.000 description 2
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 2
- 206010028980 Neoplasm Diseases 0.000 description 2
- 238000000636 Northern blotting Methods 0.000 description 2
- 229910019142 PO4 Inorganic materials 0.000 description 2
- 102000035195 Peptidases Human genes 0.000 description 2
- 108091005804 Peptidases Proteins 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- ONIBWKKTOPOVIA-UHFFFAOYSA-N Proline Natural products OC(=O)C1CCCN1 ONIBWKKTOPOVIA-UHFFFAOYSA-N 0.000 description 2
- 239000004365 Protease Substances 0.000 description 2
- 238000012228 RNA interference-mediated gene silencing Methods 0.000 description 2
- WNYXRWJUZBOMBX-UHFFFAOYSA-N SC(=O)c1ccc[pH]1 Chemical group SC(=O)c1ccc[pH]1 WNYXRWJUZBOMBX-UHFFFAOYSA-N 0.000 description 2
- 102000006308 Sarcoglycans Human genes 0.000 description 2
- 108010083379 Sarcoglycans Proteins 0.000 description 2
- MTCFGRXMJLQNBG-UHFFFAOYSA-N Serine Natural products OCC(N)C(O)=O MTCFGRXMJLQNBG-UHFFFAOYSA-N 0.000 description 2
- 108091027967 Small hairpin RNA Proteins 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- AYFVYJQAPQTCCC-UHFFFAOYSA-N Threonine Natural products CC(O)C(N)C(O)=O AYFVYJQAPQTCCC-UHFFFAOYSA-N 0.000 description 2
- 239000004473 Threonine Substances 0.000 description 2
- 108090001012 Transforming Growth Factor beta Proteins 0.000 description 2
- 102000004887 Transforming Growth Factor beta Human genes 0.000 description 2
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 2
- KZSNJWFQEVHDMF-UHFFFAOYSA-N Valine Natural products CC(C)C(N)C(O)=O KZSNJWFQEVHDMF-UHFFFAOYSA-N 0.000 description 2
- AJYQMCHCOGIXMR-IDTAVKCVSA-N [(2r,3s,4r,5r)-5-[6-(4-bromo-2,3-dioxobutyl)sulfanylpurin-9-yl]-3,4-dihydroxyoxolan-2-yl]methyl phosphono hydrogen phosphate Chemical compound O[C@@H]1[C@H](O)[C@@H](COP(O)(=O)OP(O)(O)=O)O[C@H]1N1C2=NC=NC(SCC(=O)C(=O)CBr)=C2N=C1 AJYQMCHCOGIXMR-IDTAVKCVSA-N 0.000 description 2
- 230000004913 activation Effects 0.000 description 2
- 239000004480 active ingredient Substances 0.000 description 2
- 239000000443 aerosol Substances 0.000 description 2
- 235000004279 alanine Nutrition 0.000 description 2
- 230000003110 anti-inflammatory effect Effects 0.000 description 2
- 229940088710 antibiotic agent Drugs 0.000 description 2
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 2
- 238000001574 biopsy Methods 0.000 description 2
- 101150006308 botA gene Proteins 0.000 description 2
- 238000004422 calculation algorithm Methods 0.000 description 2
- 201000011510 cancer Diseases 0.000 description 2
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 2
- 238000004113 cell culture Methods 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 239000003184 complementary RNA Substances 0.000 description 2
- 229940125898 compound 5 Drugs 0.000 description 2
- 239000000562 conjugate Substances 0.000 description 2
- 230000021615 conjugation Effects 0.000 description 2
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 2
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 description 2
- 150000001945 cysteines Chemical class 0.000 description 2
- GHVNFZFCNZKVNT-UHFFFAOYSA-N decanoic acid Chemical class CCCCCCCCCC(O)=O GHVNFZFCNZKVNT-UHFFFAOYSA-N 0.000 description 2
- 230000002950 deficient Effects 0.000 description 2
- 238000013461 design Methods 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 230000018109 developmental process Effects 0.000 description 2
- 239000003085 diluting agent Substances 0.000 description 2
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 2
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 2
- POULHZVOKOAJMA-UHFFFAOYSA-N dodecanoic acid Chemical class CCCCCCCCCCCC(O)=O POULHZVOKOAJMA-UHFFFAOYSA-N 0.000 description 2
- 238000001035 drying Methods 0.000 description 2
- 239000003792 electrolyte Substances 0.000 description 2
- 238000004520 electroporation Methods 0.000 description 2
- 229910001651 emery Inorganic materials 0.000 description 2
- 230000012202 endocytosis Effects 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- 125000001301 ethoxy group Chemical group [H]C([H])([H])C([H])([H])O* 0.000 description 2
- 230000000763 evoking effect Effects 0.000 description 2
- 210000003414 extremity Anatomy 0.000 description 2
- 230000004927 fusion Effects 0.000 description 2
- 108020001507 fusion proteins Proteins 0.000 description 2
- 102000037865 fusion proteins Human genes 0.000 description 2
- 230000009368 gene silencing by RNA Effects 0.000 description 2
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 2
- 235000004554 glutamine Nutrition 0.000 description 2
- 239000008187 granular material Substances 0.000 description 2
- IPCSVZSSVZVIGE-UHFFFAOYSA-N hexadecanoic acid Chemical compound CCCCCCCCCCCCCCCC(O)=O IPCSVZSSVZVIGE-UHFFFAOYSA-N 0.000 description 2
- 235000014304 histidine Nutrition 0.000 description 2
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 description 2
- 229960000890 hydrocortisone Drugs 0.000 description 2
- 230000007062 hydrolysis Effects 0.000 description 2
- 238000006460 hydrolysis reaction Methods 0.000 description 2
- 238000010166 immunofluorescence Methods 0.000 description 2
- 238000003364 immunohistochemistry Methods 0.000 description 2
- 230000001976 improved effect Effects 0.000 description 2
- 238000010348 incorporation Methods 0.000 description 2
- 239000003112 inhibitor Substances 0.000 description 2
- 230000002452 interceptive effect Effects 0.000 description 2
- 238000007917 intracranial administration Methods 0.000 description 2
- 238000010255 intramuscular injection Methods 0.000 description 2
- 239000007927 intramuscular injection Substances 0.000 description 2
- 239000007928 intraperitoneal injection Substances 0.000 description 2
- 235000014705 isoleucine Nutrition 0.000 description 2
- AGPKZVBTJJNPAG-UHFFFAOYSA-N isoleucine Natural products CCC(C)C(N)C(O)=O AGPKZVBTJJNPAG-UHFFFAOYSA-N 0.000 description 2
- 229960000310 isoleucine Drugs 0.000 description 2
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 2
- 210000002414 leg Anatomy 0.000 description 2
- 235000005772 leucine Nutrition 0.000 description 2
- 235000018977 lysine Nutrition 0.000 description 2
- 238000009115 maintenance therapy Methods 0.000 description 2
- 210000004962 mammalian cell Anatomy 0.000 description 2
- 239000003550 marker Substances 0.000 description 2
- 230000007246 mechanism Effects 0.000 description 2
- 239000002207 metabolite Substances 0.000 description 2
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 2
- 239000002679 microRNA Substances 0.000 description 2
- 150000007522 mineralic acids Chemical class 0.000 description 2
- 239000008185 minitablet Substances 0.000 description 2
- 238000012544 monitoring process Methods 0.000 description 2
- 125000002757 morpholinyl group Chemical group 0.000 description 2
- 230000009756 muscle regeneration Effects 0.000 description 2
- 239000006199 nebulizer Substances 0.000 description 2
- 239000013642 negative control Substances 0.000 description 2
- 210000005036 nerve Anatomy 0.000 description 2
- 238000007899 nucleic acid hybridization Methods 0.000 description 2
- 210000004940 nucleus Anatomy 0.000 description 2
- 239000003921 oil Substances 0.000 description 2
- 238000006384 oligomerization reaction Methods 0.000 description 2
- 238000011275 oncology therapy Methods 0.000 description 2
- 150000007524 organic acids Chemical class 0.000 description 2
- 239000012044 organic layer Substances 0.000 description 2
- 239000002245 particle Substances 0.000 description 2
- 108010043655 penetratin Proteins 0.000 description 2
- MCYTYTUNNNZWOK-LCLOTLQISA-N penetratin Chemical compound C([C@H](NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H]([C@@H](C)CC)NC(=O)[C@H](CCCCN)NC(=O)[C@@H](NC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](N)CCCNC(N)=N)[C@@H](C)CC)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCCN)C(N)=O)C1=CC=CC=C1 MCYTYTUNNNZWOK-LCLOTLQISA-N 0.000 description 2
- 239000000863 peptide conjugate Substances 0.000 description 2
- 230000008823 permeabilization Effects 0.000 description 2
- 239000000825 pharmaceutical preparation Substances 0.000 description 2
- 230000002974 pharmacogenomic effect Effects 0.000 description 2
- 230000000144 pharmacologic effect Effects 0.000 description 2
- COLNVLDHVKWLRT-UHFFFAOYSA-N phenylalanine Natural products OC(=O)C(N)CC1=CC=CC=C1 COLNVLDHVKWLRT-UHFFFAOYSA-N 0.000 description 2
- 235000008729 phenylalanine Nutrition 0.000 description 2
- 235000021317 phosphate Nutrition 0.000 description 2
- 239000002953 phosphate buffered saline Substances 0.000 description 2
- 150000008104 phosphatidylethanolamines Chemical class 0.000 description 2
- 150000008298 phosphoramidates Chemical group 0.000 description 2
- 150000003013 phosphoric acid derivatives Chemical class 0.000 description 2
- 125000003367 polycyclic group Chemical group 0.000 description 2
- 229920000642 polymer Polymers 0.000 description 2
- 239000013641 positive control Substances 0.000 description 2
- 229960004618 prednisone Drugs 0.000 description 2
- XOFYZVNMUHMLCC-ZPOLXVRWSA-N prednisone Chemical compound O=C1C=C[C@]2(C)[C@H]3C(=O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 XOFYZVNMUHMLCC-ZPOLXVRWSA-N 0.000 description 2
- 230000002028 premature Effects 0.000 description 2
- 235000013930 proline Nutrition 0.000 description 2
- 230000001737 promoting effect Effects 0.000 description 2
- 230000002685 pulmonary effect Effects 0.000 description 2
- 238000000746 purification Methods 0.000 description 2
- 238000012552 review Methods 0.000 description 2
- YGSDEFSMJLZEOE-UHFFFAOYSA-N salicylic acid Chemical compound OC(=O)C1=CC=CC=C1O YGSDEFSMJLZEOE-UHFFFAOYSA-N 0.000 description 2
- 235000004400 serine Nutrition 0.000 description 2
- 238000011947 six minute walk test Methods 0.000 description 2
- 239000004055 small Interfering RNA Substances 0.000 description 2
- 150000003384 small molecules Chemical class 0.000 description 2
- 239000007790 solid phase Substances 0.000 description 2
- 230000006641 stabilisation Effects 0.000 description 2
- 238000011105 stabilization Methods 0.000 description 2
- 125000003696 stearoyl group Chemical group O=C([*])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- 230000004936 stimulating effect Effects 0.000 description 2
- 125000000547 substituted alkyl group Chemical group 0.000 description 2
- 238000005987 sulfurization reaction Methods 0.000 description 2
- 239000000829 suppository Substances 0.000 description 2
- 229940037128 systemic glucocorticoids Drugs 0.000 description 2
- ZRKFYGHZFMAOKI-QMGMOQQFSA-N tgfbeta Chemical compound C([C@H](NC(=O)[C@H](C(C)C)NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CC(C)C)NC(=O)CNC(=O)[C@H](C)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@@H](NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](N)CCSC)C(C)C)[C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C)C(=O)N[C@@H](CC(C)C)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(O)=O)C1=CC=C(O)C=C1 ZRKFYGHZFMAOKI-QMGMOQQFSA-N 0.000 description 2
- 239000002562 thickening agent Substances 0.000 description 2
- 125000003396 thiol group Chemical group [H]S* 0.000 description 2
- 235000008521 threonine Nutrition 0.000 description 2
- 239000012049 topical pharmaceutical composition Substances 0.000 description 2
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 2
- 230000014616 translation Effects 0.000 description 2
- 230000005945 translocation Effects 0.000 description 2
- 235000002374 tyrosine Nutrition 0.000 description 2
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 description 2
- 235000014393 valine Nutrition 0.000 description 2
- 239000004474 valine Substances 0.000 description 2
- 239000013603 viral vector Substances 0.000 description 2
- 230000003612 virological effect Effects 0.000 description 2
- FDKWRPBBCBCIGA-REOHCLBHSA-N (2r)-2-azaniumyl-3-$l^{1}-selanylpropanoate Chemical compound [Se]C[C@H](N)C(O)=O FDKWRPBBCBCIGA-REOHCLBHSA-N 0.000 description 1
- RUDATBOHQWOJDD-UHFFFAOYSA-N (3beta,5beta,7alpha)-3,7-Dihydroxycholan-24-oic acid Chemical class OC1CC2CC(O)CCC2(C)C2C1C1CCC(C(CCC(O)=O)C)C1(C)CC2 RUDATBOHQWOJDD-UHFFFAOYSA-N 0.000 description 1
- 125000003088 (fluoren-9-ylmethoxy)carbonyl group Chemical group 0.000 description 1
- CITHEXJVPOWHKC-UUWRZZSWSA-N 1,2-di-O-myristoyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCCCCCCCCCCCC CITHEXJVPOWHKC-UUWRZZSWSA-N 0.000 description 1
- NRJAVPSFFCBXDT-HUESYALOSA-N 1,2-distearoyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCCCCCCCCCCCCCCCC NRJAVPSFFCBXDT-HUESYALOSA-N 0.000 description 1
- VUDQSRFCCHQIIU-UHFFFAOYSA-N 1-(3,5-dichloro-2,6-dihydroxy-4-methoxyphenyl)hexan-1-one Chemical compound CCCCCC(=O)C1=C(O)C(Cl)=C(OC)C(Cl)=C1O VUDQSRFCCHQIIU-UHFFFAOYSA-N 0.000 description 1
- HNEGJTWNOOWEMH-UHFFFAOYSA-N 1-fluoropropane Chemical group [CH2]CCF HNEGJTWNOOWEMH-UHFFFAOYSA-N 0.000 description 1
- MCTWTZJPVLRJOU-UHFFFAOYSA-N 1-methyl-1H-imidazole Chemical compound CN1C=CN=C1 MCTWTZJPVLRJOU-UHFFFAOYSA-N 0.000 description 1
- LAZQWLMVJAIYFE-UHFFFAOYSA-N 1-tritylpiperazine Chemical compound C1CNCCN1C(C=1C=CC=CC=1)(C=1C=CC=CC=1)C1=CC=CC=C1 LAZQWLMVJAIYFE-UHFFFAOYSA-N 0.000 description 1
- FUFLCEKSBBHCMO-UHFFFAOYSA-N 11-dehydrocorticosterone Natural products O=C1CCC2(C)C3C(=O)CC(C)(C(CC4)C(=O)CO)C4C3CCC2=C1 FUFLCEKSBBHCMO-UHFFFAOYSA-N 0.000 description 1
- OSUKSSHOHKZSJC-UHFFFAOYSA-N 12591-02-5 Chemical compound ClP(=O)=O OSUKSSHOHKZSJC-UHFFFAOYSA-N 0.000 description 1
- NRKYWOKHZRQRJR-UHFFFAOYSA-N 2,2,2-trifluoroacetamide Chemical compound NC(=O)C(F)(F)F NRKYWOKHZRQRJR-UHFFFAOYSA-N 0.000 description 1
- LDGWQMRUWMSZIU-LQDDAWAPSA-M 2,3-bis[(z)-octadec-9-enoxy]propyl-trimethylazanium;chloride Chemical compound [Cl-].CCCCCCCC\C=C/CCCCCCCCOCC(C[N+](C)(C)C)OCCCCCCCC\C=C/CCCCCCCC LDGWQMRUWMSZIU-LQDDAWAPSA-M 0.000 description 1
- PIINGYXNCHTJTF-UHFFFAOYSA-N 2-(2-azaniumylethylamino)acetate Chemical group NCCNCC(O)=O PIINGYXNCHTJTF-UHFFFAOYSA-N 0.000 description 1
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 description 1
- HPZXCYOKHIEMGN-OXQGGJHDSA-N 2-amino-9-[(2s,3r,4s,5r)-3,4-dihydroxy-5-(hydroxymethyl)-2-(2-phenylacetyl)oxolan-2-yl]-3h-purin-6-one Chemical compound C1=NC=2C(=O)NC(N)=NC=2N1[C@]1(C(=O)CC=2C=CC=CC=2)O[C@H](CO)[C@@H](O)[C@H]1O HPZXCYOKHIEMGN-OXQGGJHDSA-N 0.000 description 1
- 125000004777 2-fluoroethyl group Chemical group [H]C([H])(F)C([H])([H])* 0.000 description 1
- 125000000954 2-hydroxyethyl group Chemical group [H]C([*])([H])C([H])([H])O[H] 0.000 description 1
- 125000001622 2-naphthyl group Chemical group [H]C1=C([H])C([H])=C2C([H])=C(*)C([H])=C([H])C2=C1[H] 0.000 description 1
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 1
- BMYNFMYTOJXKLE-UHFFFAOYSA-N 3-azaniumyl-2-hydroxypropanoate Chemical compound NCC(O)C(O)=O BMYNFMYTOJXKLE-UHFFFAOYSA-N 0.000 description 1
- QOXOZONBQWIKDA-UHFFFAOYSA-N 3-hydroxypropyl Chemical group [CH2]CCO QOXOZONBQWIKDA-UHFFFAOYSA-N 0.000 description 1
- SSRFBERYIRRDJN-MWKWWEEBSA-N 4-amino-1-[(2s,3r,4s,5r)-2-benzoyl-3,4-dihydroxy-5-(hydroxymethyl)oxolan-2-yl]pyrimidin-2-one Chemical compound O=C1N=C(N)C=CN1[C@@]1(C(=O)C=2C=CC=CC=2)[C@H](O)[C@H](O)[C@@H](CO)O1 SSRFBERYIRRDJN-MWKWWEEBSA-N 0.000 description 1
- TXLINXBIWJYFNR-UHFFFAOYSA-N 4-phenylpyridine-2-carbonitrile Chemical compound C1=NC(C#N)=CC(C=2C=CC=CC=2)=C1 TXLINXBIWJYFNR-UHFFFAOYSA-N 0.000 description 1
- LQLQRFGHAALLLE-UHFFFAOYSA-N 5-bromouracil Chemical compound BrC1=CNC(=O)NC1=O LQLQRFGHAALLLE-UHFFFAOYSA-N 0.000 description 1
- KSNXJLQDQOIRIP-UHFFFAOYSA-N 5-iodouracil Chemical compound IC1=CNC(=O)NC1=O KSNXJLQDQOIRIP-UHFFFAOYSA-N 0.000 description 1
- 102000007469 Actins Human genes 0.000 description 1
- 108010085238 Actins Proteins 0.000 description 1
- 102000005606 Activins Human genes 0.000 description 1
- 108010059616 Activins Proteins 0.000 description 1
- 108010088751 Albumins Proteins 0.000 description 1
- 102000009027 Albumins Human genes 0.000 description 1
- PQSUYGKTWSAVDQ-UHFFFAOYSA-N Aldosterone Natural products C1CC2C3CCC(C(=O)CO)C3(C=O)CC(O)C2C2(C)C1=CC(=O)CC2 PQSUYGKTWSAVDQ-UHFFFAOYSA-N 0.000 description 1
- PQSUYGKTWSAVDQ-ZVIOFETBSA-N Aldosterone Chemical compound C([C@@]1([C@@H](C(=O)CO)CC[C@H]1[C@@H]1CC2)C=O)[C@H](O)[C@@H]1[C@]1(C)C2=CC(=O)CC1 PQSUYGKTWSAVDQ-ZVIOFETBSA-N 0.000 description 1
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 1
- 244000144725 Amygdalus communis Species 0.000 description 1
- 241000272525 Anas platyrhynchos Species 0.000 description 1
- 101710150620 Anionic peptide Proteins 0.000 description 1
- 108091023037 Aptamer Proteins 0.000 description 1
- 239000005711 Benzoic acid Substances 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- VOVIALXJUBGFJZ-KWVAZRHASA-N Budesonide Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@@H]2[C@@H]1[C@@H]1C[C@H]3OC(CCC)O[C@@]3(C(=O)CO)[C@@]1(C)C[C@@H]2O VOVIALXJUBGFJZ-KWVAZRHASA-N 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- 241000283707 Capra Species 0.000 description 1
- 239000005632 Capric acid (CAS 334-48-5) Chemical class 0.000 description 1
- KXDHJXZQYSOELW-UHFFFAOYSA-M Carbamate Chemical compound NC([O-])=O KXDHJXZQYSOELW-UHFFFAOYSA-M 0.000 description 1
- 208000002177 Cataract Diseases 0.000 description 1
- 102000009193 Caveolin Human genes 0.000 description 1
- 108050000084 Caveolin Proteins 0.000 description 1
- 241000700198 Cavia Species 0.000 description 1
- 108010009685 Cholinergic Receptors Proteins 0.000 description 1
- MFYSYFVPBJMHGN-ZPOLXVRWSA-N Cortisone Chemical compound O=C1CC[C@]2(C)[C@H]3C(=O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 MFYSYFVPBJMHGN-ZPOLXVRWSA-N 0.000 description 1
- MFYSYFVPBJMHGN-UHFFFAOYSA-N Cortisone Natural products O=C1CCC2(C)C3C(=O)CC(C)(C(CC4)(O)C(=O)CO)C4C3CCC2=C1 MFYSYFVPBJMHGN-UHFFFAOYSA-N 0.000 description 1
- 102000004420 Creatine Kinase Human genes 0.000 description 1
- 108010042126 Creatine kinase Proteins 0.000 description 1
- 241000699800 Cricetinae Species 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FDKWRPBBCBCIGA-UWTATZPHSA-N D-Selenocysteine Natural products [Se]C[C@@H](N)C(O)=O FDKWRPBBCBCIGA-UWTATZPHSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- RGHNJXZEOKUKBD-UHFFFAOYSA-N D-gluconic acid Natural products OCC(O)C(O)C(O)C(O)C(O)=O RGHNJXZEOKUKBD-UHFFFAOYSA-N 0.000 description 1
- 229920002307 Dextran Polymers 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- BWLUMTFWVZZZND-UHFFFAOYSA-N Dibenzylamine Chemical compound C=1C=CC=CC=1CNCC1=CC=CC=C1 BWLUMTFWVZZZND-UHFFFAOYSA-N 0.000 description 1
- 241000224495 Dictyostelium Species 0.000 description 1
- GZDFHIJNHHMENY-UHFFFAOYSA-N Dimethyl dicarbonate Chemical compound COC(=O)OC(=O)OC GZDFHIJNHHMENY-UHFFFAOYSA-N 0.000 description 1
- 102000007623 Dystroglycans Human genes 0.000 description 1
- 108010071885 Dystroglycans Proteins 0.000 description 1
- 238000002965 ELISA Methods 0.000 description 1
- 102100031780 Endonuclease Human genes 0.000 description 1
- 102000004533 Endonucleases Human genes 0.000 description 1
- 241000792859 Enema Species 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- 102000010834 Extracellular Matrix Proteins Human genes 0.000 description 1
- 108010037362 Extracellular Matrix Proteins Proteins 0.000 description 1
- 206010015866 Extravasation Diseases 0.000 description 1
- 102000001690 Factor VIII Human genes 0.000 description 1
- 108010054218 Factor VIII Proteins 0.000 description 1
- 108010008177 Fd immunoglobulins Proteins 0.000 description 1
- 241000282326 Felis catus Species 0.000 description 1
- 241000699694 Gerbillinae Species 0.000 description 1
- 229930186217 Glycolipid Natural products 0.000 description 1
- NYHBQMYGNKIUIF-UUOKFMHZSA-N Guanosine Chemical compound C1=NC=2C(=O)NC(N)=NC=2N1[C@@H]1O[C@H](CO)[C@@H](O)[C@H]1O NYHBQMYGNKIUIF-UUOKFMHZSA-N 0.000 description 1
- 102000008100 Human Serum Albumin Human genes 0.000 description 1
- 108091006905 Human Serum Albumin Proteins 0.000 description 1
- 206010020880 Hypertrophy Diseases 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 108060003951 Immunoglobulin Proteins 0.000 description 1
- 108010054477 Immunoglobulin Fab Fragments Proteins 0.000 description 1
- 102000001706 Immunoglobulin Fab Fragments Human genes 0.000 description 1
- 108010067060 Immunoglobulin Variable Region Proteins 0.000 description 1
- 102000017727 Immunoglobulin Variable Region Human genes 0.000 description 1
- 206010061218 Inflammation Diseases 0.000 description 1
- 102100034343 Integrase Human genes 0.000 description 1
- 101710203526 Integrase Proteins 0.000 description 1
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 description 1
- ZFOMKMMPBOQKMC-KXUCPTDWSA-N L-pyrrolysine Chemical compound C[C@@H]1CC=N[C@H]1C(=O)NCCCC[C@H]([NH3+])C([O-])=O ZFOMKMMPBOQKMC-KXUCPTDWSA-N 0.000 description 1
- QIVBCDIJIAJPQS-VIFPVBQESA-N L-tryptophane Chemical compound C1=CC=C2C(C[C@H](N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-VIFPVBQESA-N 0.000 description 1
- 239000005639 Lauric acid Substances 0.000 description 1
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 1
- 101150048453 MSTN gene Proteins 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- FQISKWAFAHGMGT-SGJOWKDISA-M Methylprednisolone sodium succinate Chemical compound [Na+].C([C@@]12C)=CC(=O)C=C1[C@@H](C)C[C@@H]1[C@@H]2[C@@H](O)C[C@]2(C)[C@@](O)(C(=O)COC(=O)CCC([O-])=O)CC[C@H]21 FQISKWAFAHGMGT-SGJOWKDISA-M 0.000 description 1
- 102000002151 Microfilament Proteins Human genes 0.000 description 1
- 108010040897 Microfilament Proteins Proteins 0.000 description 1
- 101000973497 Mus musculus E3 ubiquitin-protein ligase MIB2 Proteins 0.000 description 1
- 208000010428 Muscle Weakness Diseases 0.000 description 1
- 208000029578 Muscle disease Diseases 0.000 description 1
- 206010048654 Muscle fibrosis Diseases 0.000 description 1
- 206010028311 Muscle hypertrophy Diseases 0.000 description 1
- 206010049816 Muscle tightness Diseases 0.000 description 1
- 206010028372 Muscular weakness Diseases 0.000 description 1
- 206010052904 Musculoskeletal stiffness Diseases 0.000 description 1
- 241000282341 Mustela putorius furo Species 0.000 description 1
- 208000000112 Myalgia Diseases 0.000 description 1
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 description 1
- 108091005461 Nucleic proteins Proteins 0.000 description 1
- 108700026244 Open Reading Frames Proteins 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 208000001132 Osteoporosis Diseases 0.000 description 1
- 229910019213 POCl3 Inorganic materials 0.000 description 1
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 1
- 235000021314 Palmitic acid Nutrition 0.000 description 1
- 241000282579 Pan Species 0.000 description 1
- 241000282515 Papio hamadryas Species 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- ABLZXFCXXLZCGV-UHFFFAOYSA-N Phosphorous acid Chemical class OP(O)=O ABLZXFCXXLZCGV-UHFFFAOYSA-N 0.000 description 1
- 229920002873 Polyethylenimine Polymers 0.000 description 1
- 108010039918 Polylysine Proteins 0.000 description 1
- 241000282405 Pongo abelii Species 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- OFOBLEOULBTSOW-UHFFFAOYSA-N Propanedioic acid Natural products OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 208000004756 Respiratory Insufficiency Diseases 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- 108020004682 Single-Stranded DNA Proteins 0.000 description 1
- 206010041277 Sodium retention Diseases 0.000 description 1
- 102000005890 Spectrin Human genes 0.000 description 1
- 108010019965 Spectrin Proteins 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- 101100388071 Thermococcus sp. (strain GE8) pol gene Proteins 0.000 description 1
- 206010068872 Toe walking Diseases 0.000 description 1
- 108700019146 Transgenes Proteins 0.000 description 1
- 206010066901 Treatment failure Diseases 0.000 description 1
- QIVBCDIJIAJPQS-UHFFFAOYSA-N Tryptophan Natural products C1=CC=C2C(CC(N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-UHFFFAOYSA-N 0.000 description 1
- 208000003443 Unconsciousness Diseases 0.000 description 1
- 241000251539 Vertebrata <Metazoa> Species 0.000 description 1
- VTAPXODOLMOLNK-PCYKNENESA-N [(2s,3r,4s,5r)-2-(6-aminopurin-9-yl)-3,4-dihydroxy-5-(hydroxymethyl)oxolan-2-yl]-phenylmethanone Chemical compound C1=NC=2C(N)=NC=NC=2N1[C@]1(C(=O)C=2C=CC=CC=2)O[C@H](CO)[C@@H](O)[C@H]1O VTAPXODOLMOLNK-PCYKNENESA-N 0.000 description 1
- 210000001015 abdomen Anatomy 0.000 description 1
- 230000001594 aberrant effect Effects 0.000 description 1
- DHKHKXVYLBGOIT-UHFFFAOYSA-N acetaldehyde Diethyl Acetal Chemical group CCOC(C)OCC DHKHKXVYLBGOIT-UHFFFAOYSA-N 0.000 description 1
- 150000001242 acetic acid derivatives Chemical class 0.000 description 1
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 1
- 102000034337 acetylcholine receptors Human genes 0.000 description 1
- 239000003377 acid catalyst Substances 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 125000002015 acyclic group Chemical group 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 210000004404 adrenal cortex Anatomy 0.000 description 1
- 238000012382 advanced drug delivery Methods 0.000 description 1
- 229960002478 aldosterone Drugs 0.000 description 1
- 125000001931 aliphatic group Chemical group 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 150000001340 alkali metals Chemical class 0.000 description 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 1
- 150000001342 alkaline earth metals Chemical class 0.000 description 1
- 125000005036 alkoxyphenyl group Chemical group 0.000 description 1
- VREFGVBLTWBCJP-UHFFFAOYSA-N alprazolam Chemical compound C12=CC(Cl)=CC=C2N2C(C)=NN=C2CN=C1C1=CC=CC=C1 VREFGVBLTWBCJP-UHFFFAOYSA-N 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 229940059260 amidate Drugs 0.000 description 1
- 150000001408 amides Chemical class 0.000 description 1
- 125000006242 amine protecting group Chemical group 0.000 description 1
- 239000000908 ammonium hydroxide Substances 0.000 description 1
- 235000011114 ammonium hydroxide Nutrition 0.000 description 1
- 125000005428 anthryl group Chemical group [H]C1=C([H])C([H])=C2C([H])=C3C(*)=C([H])C([H])=C([H])C3=C([H])C2=C1[H] 0.000 description 1
- 230000000844 anti-bacterial effect Effects 0.000 description 1
- 229940121375 antifungal agent Drugs 0.000 description 1
- 239000003429 antifungal agent Substances 0.000 description 1
- 239000008346 aqueous phase Substances 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 239000007900 aqueous suspension Substances 0.000 description 1
- 125000002029 aromatic hydrocarbon group Chemical group 0.000 description 1
- 125000005160 aryl oxy alkyl group Chemical group 0.000 description 1
- 235000010323 ascorbic acid Nutrition 0.000 description 1
- 239000011668 ascorbic acid Substances 0.000 description 1
- 229960005070 ascorbic acid Drugs 0.000 description 1
- 125000004429 atom Chemical group 0.000 description 1
- 229910052788 barium Inorganic materials 0.000 description 1
- DSAJWYNOEDNPEQ-UHFFFAOYSA-N barium atom Chemical compound [Ba] DSAJWYNOEDNPEQ-UHFFFAOYSA-N 0.000 description 1
- 230000006399 behavior Effects 0.000 description 1
- 230000003542 behavioural effect Effects 0.000 description 1
- SRSXLGNVWSONIS-UHFFFAOYSA-N benzenesulfonic acid Chemical compound OS(=O)(=O)C1=CC=CC=C1 SRSXLGNVWSONIS-UHFFFAOYSA-N 0.000 description 1
- 229940092714 benzenesulfonic acid Drugs 0.000 description 1
- 235000010233 benzoic acid Nutrition 0.000 description 1
- 150000001558 benzoic acid derivatives Chemical class 0.000 description 1
- WGQKYBSKWIADBV-UHFFFAOYSA-O benzylaminium Chemical compound [NH3+]CC1=CC=CC=C1 WGQKYBSKWIADBV-UHFFFAOYSA-O 0.000 description 1
- 125000001584 benzyloxycarbonyl group Chemical group C(=O)(OCC1=CC=CC=C1)* 0.000 description 1
- 229960002537 betamethasone Drugs 0.000 description 1
- UREBDLICKHMUKA-DVTGEIKXSA-N betamethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O UREBDLICKHMUKA-DVTGEIKXSA-N 0.000 description 1
- 229940093761 bile salts Drugs 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 238000010876 biochemical test Methods 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 239000012472 biological sample Substances 0.000 description 1
- 230000036765 blood level Effects 0.000 description 1
- 210000001124 body fluid Anatomy 0.000 description 1
- 239000010839 body fluid Substances 0.000 description 1
- 230000036760 body temperature Effects 0.000 description 1
- 229960004436 budesonide Drugs 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 210000005252 bulbus oculi Anatomy 0.000 description 1
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 1
- 210000001217 buttock Anatomy 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 238000010804 cDNA synthesis Methods 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 239000001506 calcium phosphate Substances 0.000 description 1
- 229910000389 calcium phosphate Inorganic materials 0.000 description 1
- 235000011010 calcium phosphates Nutrition 0.000 description 1
- 150000001720 carbohydrates Chemical class 0.000 description 1
- 235000014633 carbohydrates Nutrition 0.000 description 1
- 150000001721 carbon Chemical group 0.000 description 1
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 1
- 239000001768 carboxy methyl cellulose Substances 0.000 description 1
- 125000002843 carboxylic acid group Chemical group 0.000 description 1
- 230000009084 cardiovascular function Effects 0.000 description 1
- 238000006555 catalytic reaction Methods 0.000 description 1
- 150000001767 cationic compounds Chemical class 0.000 description 1
- 210000001175 cerebrospinal fluid Anatomy 0.000 description 1
- 125000003636 chemical group Chemical group 0.000 description 1
- 210000000038 chest Anatomy 0.000 description 1
- 230000002759 chromosomal effect Effects 0.000 description 1
- 230000001684 chronic effect Effects 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 238000004891 communication Methods 0.000 description 1
- 239000008139 complexing agent Substances 0.000 description 1
- 229940126214 compound 3 Drugs 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 230000037020 contractile activity Effects 0.000 description 1
- 230000001276 controlling effect Effects 0.000 description 1
- 239000012059 conventional drug carrier Substances 0.000 description 1
- 229960004544 cortisone Drugs 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 239000006071 cream Substances 0.000 description 1
- DMSZORWOGDLWGN-UHFFFAOYSA-N ctk1a3526 Chemical compound NP(N)(N)=O DMSZORWOGDLWGN-UHFFFAOYSA-N 0.000 description 1
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 210000000805 cytoplasm Anatomy 0.000 description 1
- 210000004292 cytoskeleton Anatomy 0.000 description 1
- 230000001086 cytosolic effect Effects 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- 230000006735 deficit Effects 0.000 description 1
- 229960001145 deflazacort Drugs 0.000 description 1
- FBHSPRKOSMHSIF-GRMWVWQJSA-N deflazacort Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@@H]2[C@@H]1[C@@H]1C[C@H]3OC(C)=N[C@@]3(C(=O)COC(=O)C)[C@@]1(C)C[C@@H]2O FBHSPRKOSMHSIF-GRMWVWQJSA-N 0.000 description 1
- 239000007857 degradation product Substances 0.000 description 1
- 230000001934 delay Effects 0.000 description 1
- 229940124447 delivery agent Drugs 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 238000010511 deprotection reaction Methods 0.000 description 1
- 230000000368 destabilizing effect Effects 0.000 description 1
- 229960003957 dexamethasone Drugs 0.000 description 1
- UREBDLICKHMUKA-CXSFZGCWSA-N dexamethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O UREBDLICKHMUKA-CXSFZGCWSA-N 0.000 description 1
- 125000001028 difluoromethyl group Chemical group [H]C(F)(F)* 0.000 description 1
- 230000003292 diminished effect Effects 0.000 description 1
- BPHQZTVXXXJVHI-UHFFFAOYSA-N dimyristoyl phosphatidylglycerol Chemical compound CCCCCCCCCCCCCC(=O)OCC(COP(O)(=O)OCC(O)CO)OC(=O)CCCCCCCCCCCCC BPHQZTVXXXJVHI-UHFFFAOYSA-N 0.000 description 1
- 229960003724 dimyristoylphosphatidylcholine Drugs 0.000 description 1
- 231100000676 disease causative agent Toxicity 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 239000002612 dispersion medium Substances 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 229950000274 domagrozumab Drugs 0.000 description 1
- 239000006196 drop Substances 0.000 description 1
- 238000009509 drug development Methods 0.000 description 1
- 239000013583 drug formulation Substances 0.000 description 1
- 229940126534 drug product Drugs 0.000 description 1
- 230000004064 dysfunction Effects 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 239000007920 enema Substances 0.000 description 1
- 229940079360 enema for constipation Drugs 0.000 description 1
- 210000003979 eosinophil Anatomy 0.000 description 1
- 230000008029 eradication Effects 0.000 description 1
- RTZKZFJDLAIYFH-UHFFFAOYSA-N ether Substances CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 1
- 235000019439 ethyl acetate Nutrition 0.000 description 1
- 125000004494 ethyl ester group Chemical group 0.000 description 1
- NPUKDXXFDDZOKR-LLVKDONJSA-N etomidate Chemical compound CCOC(=O)C1=CN=CN1[C@H](C)C1=CC=CC=C1 NPUKDXXFDDZOKR-LLVKDONJSA-N 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 230000001747 exhibiting effect Effects 0.000 description 1
- 210000002744 extracellular matrix Anatomy 0.000 description 1
- 230000036251 extravasation Effects 0.000 description 1
- 235000019197 fats Nutrition 0.000 description 1
- 210000002950 fibroblast Anatomy 0.000 description 1
- 239000000796 flavoring agent Substances 0.000 description 1
- 125000004216 fluoromethyl group Chemical group [H]C([H])(F)* 0.000 description 1
- 229960002949 fluorouracil Drugs 0.000 description 1
- 239000006260 foam Substances 0.000 description 1
- 235000013355 food flavoring agent Nutrition 0.000 description 1
- 210000000245 forearm Anatomy 0.000 description 1
- 210000003194 forelimb Anatomy 0.000 description 1
- 150000004675 formic acid derivatives Chemical class 0.000 description 1
- 125000002485 formyl group Chemical group [H]C(*)=O 0.000 description 1
- 230000037433 frameshift Effects 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- 235000011087 fumaric acid Nutrition 0.000 description 1
- 230000005714 functional activity Effects 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 238000001415 gene therapy Methods 0.000 description 1
- 239000000174 gluconic acid Substances 0.000 description 1
- 235000012208 gluconic acid Nutrition 0.000 description 1
- 230000004153 glucose metabolism Effects 0.000 description 1
- 125000003827 glycol group Chemical group 0.000 description 1
- 208000037824 growth disorder Diseases 0.000 description 1
- 239000003102 growth factor Substances 0.000 description 1
- 229940093915 gynecological organic acid Drugs 0.000 description 1
- 125000005059 halophenyl group Chemical group 0.000 description 1
- 229940088597 hormone Drugs 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- 150000002430 hydrocarbons Chemical group 0.000 description 1
- 239000000017 hydrogel Substances 0.000 description 1
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 1
- 229920001477 hydrophilic polymer Polymers 0.000 description 1
- 230000002209 hydrophobic effect Effects 0.000 description 1
- 125000004029 hydroxymethyl group Chemical group [H]OC([H])([H])* 0.000 description 1
- 125000004464 hydroxyphenyl group Chemical group 0.000 description 1
- 238000010191 image analysis Methods 0.000 description 1
- 230000001900 immune effect Effects 0.000 description 1
- 230000003832 immune regulation Effects 0.000 description 1
- 230000028993 immune response Effects 0.000 description 1
- 238000003018 immunoassay Methods 0.000 description 1
- 238000003119 immunoblot Methods 0.000 description 1
- 102000018358 immunoglobulin Human genes 0.000 description 1
- 238000002991 immunohistochemical analysis Methods 0.000 description 1
- 238000013115 immunohistochemical detection Methods 0.000 description 1
- 239000007943 implant Substances 0.000 description 1
- 238000011065 in-situ storage Methods 0.000 description 1
- 125000003392 indanyl group Chemical group C1(CCC2=CC=CC=C12)* 0.000 description 1
- 229940060367 inert ingredients Drugs 0.000 description 1
- 208000015181 infectious disease Diseases 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 230000000977 initiatory effect Effects 0.000 description 1
- 229910001411 inorganic cation Inorganic materials 0.000 description 1
- 238000003780 insertion Methods 0.000 description 1
- 230000037431 insertion Effects 0.000 description 1
- 230000003434 inspiratory effect Effects 0.000 description 1
- 102000006495 integrins Human genes 0.000 description 1
- 108010044426 integrins Proteins 0.000 description 1
- 210000000876 intercostal muscle Anatomy 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000004491 isohexyl group Chemical group C(CCC(C)C)* 0.000 description 1
- 125000001972 isopentyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 230000009191 jumping Effects 0.000 description 1
- 210000003734 kidney Anatomy 0.000 description 1
- 238000009533 lab test Methods 0.000 description 1
- 239000004310 lactic acid Substances 0.000 description 1
- 235000014655 lactic acid Nutrition 0.000 description 1
- 239000010410 layer Substances 0.000 description 1
- 201000003723 learning disability Diseases 0.000 description 1
- 208000032839 leukemia Diseases 0.000 description 1
- 239000008206 lipophilic material Substances 0.000 description 1
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 1
- 229910052744 lithium Inorganic materials 0.000 description 1
- 210000004185 liver Anatomy 0.000 description 1
- 230000004807 localization Effects 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 239000006210 lotion Substances 0.000 description 1
- 210000004705 lumbosacral region Anatomy 0.000 description 1
- 210000004324 lymphatic system Anatomy 0.000 description 1
- 229920002521 macromolecule Polymers 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- 239000011976 maleic acid Substances 0.000 description 1
- 230000013011 mating Effects 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 238000002483 medication Methods 0.000 description 1
- PSGAAPLEWMOORI-PEINSRQWSA-N medroxyprogesterone acetate Chemical compound C([C@@]12C)CC(=O)C=C1[C@@H](C)C[C@@H]1[C@@H]2CC[C@]2(C)[C@@](OC(C)=O)(C(C)=O)CC[C@H]21 PSGAAPLEWMOORI-PEINSRQWSA-N 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- MYWUZJCMWCOHBA-VIFPVBQESA-N methamphetamine Chemical compound CN[C@@H](C)CC1=CC=CC=C1 MYWUZJCMWCOHBA-VIFPVBQESA-N 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- 229930182817 methionine Natural products 0.000 description 1
- 235000006109 methionine Nutrition 0.000 description 1
- 150000004702 methyl esters Chemical class 0.000 description 1
- 125000000325 methylidene group Chemical group [H]C([H])=* 0.000 description 1
- 229960004584 methylprednisolone Drugs 0.000 description 1
- 239000004530 micro-emulsion Substances 0.000 description 1
- 239000003094 microcapsule Substances 0.000 description 1
- 238000000520 microinjection Methods 0.000 description 1
- 239000004005 microsphere Substances 0.000 description 1
- 230000003278 mimic effect Effects 0.000 description 1
- 239000002395 mineralocorticoid Substances 0.000 description 1
- 230000037230 mobility Effects 0.000 description 1
- 238000000465 moulding Methods 0.000 description 1
- 230000012042 muscle hypertrophy Effects 0.000 description 1
- 208000013465 muscle pain Diseases 0.000 description 1
- 210000003365 myofibril Anatomy 0.000 description 1
- WQEPLUUGTLDZJY-UHFFFAOYSA-N n-Pentadecanoic acid Natural products CCCCCCCCCCCCCCC(O)=O WQEPLUUGTLDZJY-UHFFFAOYSA-N 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- XBXCNNQPRYLIDE-UHFFFAOYSA-M n-tert-butylcarbamate Chemical compound CC(C)(C)NC([O-])=O XBXCNNQPRYLIDE-UHFFFAOYSA-M 0.000 description 1
- 125000001624 naphthyl group Chemical group 0.000 description 1
- 229930014626 natural product Natural products 0.000 description 1
- 210000002569 neuron Anatomy 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 229910017604 nitric acid Inorganic materials 0.000 description 1
- 125000006574 non-aromatic ring group Chemical group 0.000 description 1
- 239000012457 nonaqueous media Substances 0.000 description 1
- 238000003199 nucleic acid amplification method Methods 0.000 description 1
- 238000003499 nucleic acid array Methods 0.000 description 1
- 125000000371 nucleobase group Chemical group 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 1
- 239000002674 ointment Substances 0.000 description 1
- 238000001543 one-way ANOVA Methods 0.000 description 1
- 238000011369 optimal treatment Methods 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 150000002892 organic cations Chemical class 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 230000008520 organization Effects 0.000 description 1
- 230000002018 overexpression Effects 0.000 description 1
- 235000006408 oxalic acid Nutrition 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- FJKROLUGYXJWQN-UHFFFAOYSA-N papa-hydroxy-benzoic acid Natural products OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 1
- 230000036961 partial effect Effects 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- 230000037361 pathway Effects 0.000 description 1
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 1
- 230000035699 permeability Effects 0.000 description 1
- 239000008177 pharmaceutical agent Substances 0.000 description 1
- 229940127557 pharmaceutical product Drugs 0.000 description 1
- 125000004934 phenanthridinyl group Chemical group C1(=CC=CC2=NC=C3C=CC=CC3=C12)* 0.000 description 1
- 125000005561 phenanthryl group Chemical group 0.000 description 1
- BSCCSDNZEIHXOK-UHFFFAOYSA-N phenyl carbamate Chemical compound NC(=O)OC1=CC=CC=C1 BSCCSDNZEIHXOK-UHFFFAOYSA-N 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- RLOWWWKZYUNIDI-UHFFFAOYSA-N phosphinic chloride Chemical compound ClP=O RLOWWWKZYUNIDI-UHFFFAOYSA-N 0.000 description 1
- 150000003904 phospholipids Chemical class 0.000 description 1
- FUWGSUOSJRCEIV-UHFFFAOYSA-N phosphonothioic O,O-acid Chemical class OP(O)=S FUWGSUOSJRCEIV-UHFFFAOYSA-N 0.000 description 1
- 235000011007 phosphoric acid Nutrition 0.000 description 1
- 238000000554 physical therapy Methods 0.000 description 1
- 230000004962 physiological condition Effects 0.000 description 1
- 230000035790 physiological processes and functions Effects 0.000 description 1
- 125000004193 piperazinyl group Chemical group 0.000 description 1
- 229940037129 plain mineralocorticoids for systemic use Drugs 0.000 description 1
- 229920000656 polylysine Polymers 0.000 description 1
- 238000003752 polymerase chain reaction Methods 0.000 description 1
- 238000010837 poor prognosis Methods 0.000 description 1
- 230000004481 post-translational protein modification Effects 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 229960005205 prednisolone Drugs 0.000 description 1
- OIGNJSKKLXVSLS-VWUMJDOOSA-N prednisolone Chemical compound O=C1C=C[C@]2(C)[C@H]3[C@@H](O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 OIGNJSKKLXVSLS-VWUMJDOOSA-N 0.000 description 1
- 230000003449 preventive effect Effects 0.000 description 1
- 230000000750 progressive effect Effects 0.000 description 1
- 125000001500 prolyl group Chemical group [H]N1C([H])(C(=O)[*])C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 230000000069 prophylactic effect Effects 0.000 description 1
- 235000019260 propionic acid Nutrition 0.000 description 1
- 230000004952 protein activity Effects 0.000 description 1
- 230000004853 protein function Effects 0.000 description 1
- 230000022558 protein metabolic process Effects 0.000 description 1
- 238000001742 protein purification Methods 0.000 description 1
- 230000006337 proteolytic cleavage Effects 0.000 description 1
- 230000002294 pubertal effect Effects 0.000 description 1
- 150000003212 purines Chemical class 0.000 description 1
- IUVKMZGDUIUOCP-BTNSXGMBSA-N quinbolone Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)CC[C@@]21C)C1=CCCC1 IUVKMZGDUIUOCP-BTNSXGMBSA-N 0.000 description 1
- 150000003254 radicals Chemical class 0.000 description 1
- 229950006653 ramatercept Drugs 0.000 description 1
- 238000003753 real-time PCR Methods 0.000 description 1
- 230000010837 receptor-mediated endocytosis Effects 0.000 description 1
- 230000011514 reflex Effects 0.000 description 1
- 238000011069 regeneration method Methods 0.000 description 1
- 230000000241 respiratory effect Effects 0.000 description 1
- 201000004193 respiratory failure Diseases 0.000 description 1
- 230000004202 respiratory function Effects 0.000 description 1
- 230000003938 response to stress Effects 0.000 description 1
- 230000004043 responsiveness Effects 0.000 description 1
- 239000002342 ribonucleoside Substances 0.000 description 1
- 125000002652 ribonucleotide group Chemical group 0.000 description 1
- 150000003290 ribose derivatives Chemical class 0.000 description 1
- 125000006413 ring segment Chemical group 0.000 description 1
- 230000000630 rising effect Effects 0.000 description 1
- 229960004889 salicylic acid Drugs 0.000 description 1
- 208000000943 scapulohumeral muscular dystrophy Diseases 0.000 description 1
- 206010039722 scoliosis Diseases 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 235000016491 selenocysteine Nutrition 0.000 description 1
- 229940055619 selenocysteine Drugs 0.000 description 1
- ZKZBPNGNEQAJSX-UHFFFAOYSA-N selenocysteine Natural products [SeH]CC(N)C(O)=O ZKZBPNGNEQAJSX-UHFFFAOYSA-N 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 231100000004 severe toxicity Toxicity 0.000 description 1
- 230000001568 sexual effect Effects 0.000 description 1
- 230000011664 signaling Effects 0.000 description 1
- 239000000741 silica gel Substances 0.000 description 1
- 229910002027 silica gel Inorganic materials 0.000 description 1
- 238000010898 silica gel chromatography Methods 0.000 description 1
- RMAQACBXLXPBSY-UHFFFAOYSA-N silicic acid Chemical compound O[Si](O)(O)O RMAQACBXLXPBSY-UHFFFAOYSA-N 0.000 description 1
- 235000012239 silicon dioxide Nutrition 0.000 description 1
- DRNXZGJGRSUXHW-UHFFFAOYSA-N silyl carbamate Chemical compound NC(=O)O[SiH3] DRNXZGJGRSUXHW-UHFFFAOYSA-N 0.000 description 1
- 239000002356 single layer Substances 0.000 description 1
- 238000009097 single-agent therapy Methods 0.000 description 1
- 108010062513 snake venom phosphodiesterase I Proteins 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 235000019812 sodium carboxymethyl cellulose Nutrition 0.000 description 1
- 229920001027 sodium carboxymethylcellulose Polymers 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 230000009870 specific binding Effects 0.000 description 1
- 108010068698 spleen exonuclease Proteins 0.000 description 1
- 230000002269 spontaneous effect Effects 0.000 description 1
- 239000007921 spray Substances 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 238000007619 statistical method Methods 0.000 description 1
- 239000008117 stearic acid Substances 0.000 description 1
- 239000003270 steroid hormone Substances 0.000 description 1
- 230000003637 steroidlike Effects 0.000 description 1
- 108010075210 streptolysin O Proteins 0.000 description 1
- 230000036435 stunted growth Effects 0.000 description 1
- 125000001424 substituent group Chemical group 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 150000008163 sugars Chemical class 0.000 description 1
- 230000008093 supporting effect Effects 0.000 description 1
- 230000002459 sustained effect Effects 0.000 description 1
- 238000013268 sustained release Methods 0.000 description 1
- 239000012730 sustained-release form Substances 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 235000020357 syrup Nutrition 0.000 description 1
- 239000006188 syrup Substances 0.000 description 1
- 238000007910 systemic administration Methods 0.000 description 1
- 239000007916 tablet composition Substances 0.000 description 1
- 229940095064 tartrate Drugs 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- XBXCNNQPRYLIDE-UHFFFAOYSA-N tert-butylcarbamic acid Chemical compound CC(C)(C)NC(O)=O XBXCNNQPRYLIDE-UHFFFAOYSA-N 0.000 description 1
- 125000001981 tert-butyldimethylsilyl group Chemical group [H]C([H])([H])[Si]([H])(C([H])([H])[H])[*]C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 125000001973 tert-pentyl group Chemical group [H]C([H])([H])C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 125000001712 tetrahydronaphthyl group Chemical group C1(CCCC2=CC=CC=C12)* 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 230000009261 transgenic effect Effects 0.000 description 1
- 238000013519 translation Methods 0.000 description 1
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 1
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 description 1
- UFTFJSFQGQCHQW-UHFFFAOYSA-N triformin Chemical compound O=COCC(OC=O)COC=O UFTFJSFQGQCHQW-UHFFFAOYSA-N 0.000 description 1
- JBWKIWSBJXDJDT-UHFFFAOYSA-N triphenylmethyl chloride Chemical compound C=1C=CC=CC=1C(C=1C=CC=CC=1)(Cl)C1=CC=CC=C1 JBWKIWSBJXDJDT-UHFFFAOYSA-N 0.000 description 1
- 210000000689 upper leg Anatomy 0.000 description 1
- 238000011144 upstream manufacturing Methods 0.000 description 1
- 210000002700 urine Anatomy 0.000 description 1
- RUDATBOHQWOJDD-UZVSRGJWSA-N ursodeoxycholic acid Chemical class C([C@H]1C[C@@H]2O)[C@H](O)CC[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CC[C@H]([C@@H](CCC(O)=O)C)[C@@]2(C)CC1 RUDATBOHQWOJDD-UZVSRGJWSA-N 0.000 description 1
- 230000002792 vascular Effects 0.000 description 1
- 239000013598 vector Substances 0.000 description 1
- 210000003462 vein Anatomy 0.000 description 1
- 230000003519 ventilatory effect Effects 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/177—Receptors; Cell surface antigens; Cell surface determinants
- A61K38/1774—Immunoglobulin superfamily (e.g. CD2, CD4, CD8, ICAM molecules, B7 molecules, Fc-receptors, MHC-molecules)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
- A61K48/005—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy characterised by an aspect of the 'active' part of the composition delivered, i.e. the nucleic acid delivered
- A61K48/0066—Manipulation of the nucleic acid to modify its expression pattern, e.g. enhance its duration of expression, achieved by the presence of particular introns in the delivered nucleic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/547—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom
- C07F9/6558—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom containing at least two different or differently substituted hetero rings neither condensed among themselves nor condensed with a common carbocyclic ring or ring system
- C07F9/65586—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom containing at least two different or differently substituted hetero rings neither condensed among themselves nor condensed with a common carbocyclic ring or ring system at least one of the hetero rings does not contain nitrogen as ring hetero atom
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/10—Type of nucleic acid
- C12N2310/11—Antisense
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/32—Chemical structure of the sugar
- C12N2310/323—Chemical structure of the sugar modified ring structure
- C12N2310/3233—Morpholino-type ring
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/35—Nature of the modification
- C12N2310/351—Conjugate
- C12N2310/3513—Protein; Peptide
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2320/00—Applications; Uses
- C12N2320/30—Special therapeutic applications
- C12N2320/31—Combination therapy
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2320/00—Applications; Uses
- C12N2320/30—Special therapeutic applications
- C12N2320/33—Alteration of splicing
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Genetics & Genomics (AREA)
- General Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Biomedical Technology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Molecular Biology (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Zoology (AREA)
- Biotechnology (AREA)
- Biochemistry (AREA)
- Epidemiology (AREA)
- Wood Science & Technology (AREA)
- General Engineering & Computer Science (AREA)
- Gastroenterology & Hepatology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Physics & Mathematics (AREA)
- Biophysics (AREA)
- Immunology (AREA)
- Plant Pathology (AREA)
- Microbiology (AREA)
- Cell Biology (AREA)
- Psychology (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Peptides Or Proteins (AREA)
Abstract
【課題】デュシェンヌ型筋ジストロフィーおよび関連障害の処置のための組成物および方法。【解決手段】本開示は、デュシェンヌ型筋ジストロフィーおよび関連障害の処置のための組成物および方法に関する。デュシェンヌ型筋ジストロフィーおよび関連障害の処置のための修飾アンチセンスオリゴマーが開示される。本開示は、少なくとも一部において、ミオスタチン治療剤と組み合わせたジストロフィン治療剤によるmdxマウス(デュシェンヌ型筋ジストロフィーのマウスモデル)の全身処置により、とりわけ、マウスにおける握力(筋力)が増加したという驚くべき発見に基づく。【選択図】なし
Description
背景
開示の分野
本発明は、デュシェンヌ型筋ジストロフィーおよび関連障害の処置のための組成物および方法に関する。
開示の分野
本発明は、デュシェンヌ型筋ジストロフィーおよび関連障害の処置のための組成物および方法に関する。
関連技術の説明
デュシェンヌ型筋ジストロフィー(DMD)は、タンパク質ジストロフィンの発現の欠陥に起因する。タンパク質をコードする遺伝子は、200万を超えるDNAのヌクレオチドにわたって広がる79のエクソンを含む。エクソンのリーディングフレームを変えるか、または停止コドンを導入するか、あるいはフレームがあっていない1もしくは複数のエクソン全体の除去または1もしくは複数のエクソンの重複により特徴付けられるいかなるエクソンの変異も、機能的なジストロフィンの産生を途絶させ、それによりDMDをもたらす可能性がある。
デュシェンヌ型筋ジストロフィー(DMD)は、タンパク質ジストロフィンの発現の欠陥に起因する。タンパク質をコードする遺伝子は、200万を超えるDNAのヌクレオチドにわたって広がる79のエクソンを含む。エクソンのリーディングフレームを変えるか、または停止コドンを導入するか、あるいはフレームがあっていない1もしくは複数のエクソン全体の除去または1もしくは複数のエクソンの重複により特徴付けられるいかなるエクソンの変異も、機能的なジストロフィンの産生を途絶させ、それによりDMDをもたらす可能性がある。
疾患の発症は、クレアチンキナーゼレベルの上昇により出生時に実証されることがあり、顕著な運動障害が生後1年で見られる場合がある。DMDを有する大部分の患者は7歳または8歳までに次第に足取りがぎこちなくなり、床から立ち上がり階段を登る能力を失い、10~14歳までにほとんどが車椅子に依存する。DMDは一様に致命的であり、罹患個体は、典型的には、10代後半または20代前半には呼吸および/または心不全により死亡する。DMDの持続的な進行は、疾患の全ての段階で治療的介入が可能であるが、処置は現在のところ糖質コルチコイドに限られており、それは体重増加、行動変化、思春期変化、骨粗鬆症、クッシング様顔貌、発育阻止および白内障を含む多くの副作用を伴う。
典型的には1または複数のエクソンの欠失である変異により、ジストロフィン転写物全体にわたって正しいリーディングフレームとなり、その結果、mRNAのタンパク質への翻訳が早まって終了しない場合には、本明細書で記載される関連障害である、低重症型の筋ジストロフィーであるベッカー型筋ジストロフィー(BMD)が発症することがわかっている。変異ジストロフィンプレmRNAのプロセシングにおいて、上流および下流エクソンの接合により遺伝子の正しいリーディングフレームが維持される場合、若干の活性が保持された、短い内部欠失を有するタンパク質をコードするmRNAが生じ、その結果、ベッカー型の表現型となる。
長年、ジストロフィンタンパク質のリーディングフレームを変えない1または複数のエクソンの欠失が、BMD表現型をもたらすが、フレームシフトが生じるエクソン欠失はDMDをもたらすことが公知である(Monaco、Bertelsonら、1988年)。一般に、リー
ディングフレームを変更し、したがって適切なタンパク質翻訳を中断する、点変異およびエクソン欠失を含むジストロフィン変異は、DMDをもたらす。また、一部のBMDおよびDMD患者は、複数のエクソンにまたがるエクソン欠失を有することに留意すべきである。
ディングフレームを変更し、したがって適切なタンパク質翻訳を中断する、点変異およびエクソン欠失を含むジストロフィン変異は、DMDをもたらす。また、一部のBMDおよびDMD患者は、複数のエクソンにまたがるエクソン欠失を有することに留意すべきである。
DMDの処置に対するスプライススイッチングオリゴヌクレオチド(SSO)の安全性および有効性を試験した最近の臨床試験は、スプライソソームの立体阻害によるプレmRNAの選択的スプライシングを誘導するSSO技術に基づく(Cirakら、2011年;Goemansら、2011年;Kinaliら、2009年;van Deutekomら、2007年)。しかし
ながら、これらの成功にもかかわらず、DMDの処置に利用できる薬理学的オプションは限られている。
ながら、これらの成功にもかかわらず、DMDの処置に利用できる薬理学的オプションは限られている。
ゆえに、DMDの処置のための改善された治療的アプローチに対する強いニーズが依然として存在する。
要旨
本開示は、少なくとも一部において、ミオスタチン治療剤と組み合わせたジストロフィン治療剤によるmdxマウス(デュシェンヌ型筋ジストロフィーのマウスモデル)の全身処置により、とりわけ、マウスにおける握力(筋力)が増加したという驚くべき発見に基づく。握力(筋力)の増加に加えて、この複合治療的アプローチはまた、単独治療のみと比較して、エクソンスキッピング効率およびタンパク質発現、ならびに他のin vivoおよびin vitroエンドポイントを増加させた。これらには、とりわけ、体重、筋肉量、特定の筋線維の肥大および筋肉の再生の改善が含まれる。
本開示は、少なくとも一部において、ミオスタチン治療剤と組み合わせたジストロフィン治療剤によるmdxマウス(デュシェンヌ型筋ジストロフィーのマウスモデル)の全身処置により、とりわけ、マウスにおける握力(筋力)が増加したという驚くべき発見に基づく。握力(筋力)の増加に加えて、この複合治療的アプローチはまた、単独治療のみと比較して、エクソンスキッピング効率およびタンパク質発現、ならびに他のin vivoおよびin vitroエンドポイントを増加させた。これらには、とりわけ、体重、筋肉量、特定の筋線維の肥大および筋肉の再生の改善が含まれる。
さらに驚くべき発見は、とりわけ本明細書で記載される方法および組合せによる処置に受容的な集団の年齢に関する。若齢のmdxマウスは、筋肉の成長および再生のより長い一定期間を経験し、ゆえにより穏やかな病変を示す傾向があることが一般的に公知である。例えば、McGreevyら、Disease Models & Mechanisms、8巻:195~213頁(2015年)を参照されたい。対照的に、老齢のmdxマウスは、筋肉の完全性および機能のより一層一貫した低下を示し、処置が困難であるより重症の病変により特徴付けられる。しかしながら、驚くべきことに、上記のin vivoおよびin vitroでの結果は、若齢のmdxマウスのみならず老齢のマウスでも生じることを見出した。これは、本明細書で記載される組成物および方法が、より重症の病変および予後不良を有する高齢患者(例えば、7歳またはこれを超える小児患者)の処置に有用であることを示す。
さらに驚くべき発見は、試験した処置集団における長い寿命および/または高い生存率に関する。若齢のmdxマウスは、ジストロフィン欠損であるにもかかわらず、臨床症状が最小であることが公知である(McGreevyら、2015年)。マウスが15カ月齢またはこれを超えるまで、臨床表現型、例えば筋肉の消耗、脊柱側弯症および心不全をよく表す重症のジストロフィーの表現型が現れない。しかし、mdxマウスの寿命は野生型マウスと比較し約25%短いため、早期死亡がこの時点でしばしば生じる。しかしながら、ここで本発明者らは驚くべきことに、本明細書の方法および組合せに従う処置が、このモデルにおける典型的な寿命/生存率をはるかに超える少なくとも約18~24カ月に、mdxマウスの生存を延長したことを見出した。本明細書の多様な態様および実施形態に従い、老齢のmdxマウスにおいて観察されたこれらの高い治療的利益および長い寿命は、驚くべきである。
したがって、本明細書に提示される多様な態様は、ジストロフィン治療剤とミオスタチン治療剤との組合せを投与することにより、被験体においてデュシェンヌ型筋ジストロフィーを処置する方法を含む。
多様な態様は、ジストロフィンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得るジストロフィン遺伝子における変異を有する、デュシェンヌ型筋ジストロフィーを有する被験体を処置する方法を含む。この方法は、前記被験体に、17~40サブユニットを含み、ヒトジストロフィンプレmRNAのエクソンを含む標的領域内の12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップを含み、前記アンチセンスオリゴマーが、前記エクソンのスキッピングを誘導し、前記オリゴマーが、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含み、前記被験体が、前記被験体におけるミオスタチン活性およびミオスタチン発現の一方または両方を阻害するミオスタチン治療剤を投与され、それによりデュシェンヌ型筋ジストロフィーを処置する。
多様な実施形態では、前記エクソンが、エクソン7、エクソン8、エクソン9、エクソン19、エクソン23、エクソン44、エクソン45、エクソン50、エクソン51、エクソン52、エクソン53またはエクソン55から選択される。一部の実施形態では、前記エクソンがエクソン23を含む。一部の実施形態では、前記エクソンがエクソン45を含む。一部の実施形態では、前記エクソンがエクソン51を含む。一部の実施形態では、前記エクソンがエクソン53を含む。一部の実施形態では、前記エクソンが、エクソン8、エクソン44、エクソン50、エクソン52またはエクソン55を含む。
多様な実施形態では、前記アンチセンスオリゴマーが、20~30サブユニットを含む。一部の実施形態では、前記アンチセンスオリゴマーが、配列番号76~配列番号3485から選択される配列を含む。さらなる実施形態では、前記アンチセンスオリゴマーが、配列番号76である。
多様な実施形態では、前記ターゲティング配列が、前記標的領域内の少なくとも15の連続ヌクレオチドと相補的である。一部の実施形態では、前記ターゲティング配列が、前記標的領域内の少なくとも17の連続ヌクレオチドと相補的である。さらなる実施形態では、前記ターゲティング配列が、前記標的領域と100%相補的である。
多様な実施形態では、前記ミオスタチン治療剤が、タンパク質または核酸である。一部の実施形態では、前記タンパク質が、抗ミオスタチン抗体である。一部の実施形態では、前記タンパク質が、可溶性受容体である。さらなる実施形態では、可溶性受容体が、ACVR2である。一部の実施形態では、前記核酸が、アンチセンスオリゴマーまたはsiRNAのうちの少なくとも1つである。
多様な実施形態では、前記アンチセンスオリゴマーが、12~40サブユニットを含み、ミオスタチンプレmRNAの標的領域内の12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含み、前記オリゴマーが、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含む。実施形態では、前記アンチセンスオリゴマーが、20~30サブユニットを含む。一部の実施形態では、前記ターゲティング配列が、前記標的領域内の少なくとも15の連続ヌクレオチドと相補的である。さらなる実施形態では、前記ターゲティング配列が、前記標的領域内の少なくとも17の連続ヌクレオチドと相補的である。実施形態では、前記ターゲティング配列が、前記標的領域と100%相補的である。実施形態では、前記標的領域が、配列番号1を含む。実施形態では、前記エクソンが、エクソン2を含む。
多様な実施形態では、前記標的領域が、(i)少なくとも1つのヌクレオチドが、イントロン1/エクソン2およびエクソン2/イントロン2に伴うスプライス接合部にわたるヌクレオチド配列、または、(ii)ヌクレオチドが、イントロン1/エクソン2およびエクソン2/イントロン2に伴うスプライス接合部にわたらないヌクレオチド配列から選択される。実施形態では、前記スプライス接合部が、スプライスアクセプター部位またはスプライスドナー部位を含む配列から選択される。実施形態では、前記スプライス接合部が、スプライスアクセプター部位またはスプライスドナー部位を含む配列から選択される。一部の実施形態では、前記スプライスアクセプター部位が、配列番号2の内部に存在し、前記スプライスドナー部位が配列番号3の内部に存在する。
多様な実施形態では、前記(i)のヌクレオチドが、配列番号16~43から選択される。実施形態では、前記(ii)のヌクレオチドが、配列番号44~70から選択される。
多様な実施形態では、前記被験体が、7歳またはこれを超える小児患者である。
多様な態様は、デュシェンヌ型筋ジストロフィーを処置する方法であって、
被験体に、12~40サブユニットを含み、ヒトミオスタチンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップを含み、前記オリゴマーが、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含み、前記被験体が、前記被験体内でのジストロフィンの発現を増加させるジストロフィン治療剤を投与され、それによりデュシェンヌ型筋ジストロフィーを処置する、方法を含む。
被験体に、12~40サブユニットを含み、ヒトミオスタチンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップを含み、前記オリゴマーが、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含み、前記被験体が、前記被験体内でのジストロフィンの発現を増加させるジストロフィン治療剤を投与され、それによりデュシェンヌ型筋ジストロフィーを処置する、方法を含む。
多様な実施形態では、前記被験体が、ヒトミオスタチンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得るジストロフィン遺伝子における変異を有する。
多様な実施形態では、前記アンチセンスオリゴマーが、20~30サブユニットを含む。実施形態では、前記ターゲティング配列が、標的領域内の少なくとも15の連続ヌクレオチドと相補的である。実施形態では、前記ターゲティング配列が、標的領域内の少なくとも17の連続ヌクレオチドと相補的である。実施形態では、前記アンチセンスオリゴマーが、標的領域と100%相補的である。実施形態では、前記標的領域が、配列番号1を含む。実施形態では、前記エクソンが、エクソン2を含む。
多様な実施形態では、前記標的領域が、(i)少なくとも1つのヌクレオチドがイントロン1/エクソン2およびエクソン2/イントロン2に伴うスプライス接合部にわたるヌクレオチド配列、または、(ii)ヌクレオチドがイントロン1/エクソン2およびエクソン2/イントロン2に伴うスプライス接合部にわたらないヌクレオチド配列から選択される。実施形態では、前記スプライス接合部が、スプライスアクセプター部位またはスプライスドナー部位を含む配列から選択される。実施形態では、前記スプライスアクセプター部位が、配列番号2の内部に存在し、前記スプライスドナー部位が、配列番号3の内部に存在する。
多様な実施形態では、前記ジストロフィン治療剤が、タンパク質または核酸のうちの1つまたは複数から選択される。実施形態では、前記核酸が、アンチセンスオリゴマーである。一部の実施形態では、前記アンチセンスオリゴマーが、20~50サブユニットを含み、ヒトジストロフィンプレmRNAのエクソンを含む標的領域内の10またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含み、前記オリゴマーが、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含む。
様々な態様および実施形態は、ジストロフィンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得るジストロフィン遺伝子における変異を有する被験体においてデュシェンヌ型筋ジストロフィーおよび関連障害を処置する方法を含む。様々な実施形態では、この方法は、被験体に、式(I):
を含むターゲティング配列または薬学的に許容されるその塩を投与するステップを含み、式中、
各Nuは、一緒になってターゲティング配列を形成するヌクレオ塩基であり;
Zは、8から48の整数であり;
各Yは、Oおよび-NR4から独立に選択され、式中、各R4は、H、C1~C6アルキル、アラルキル、C(=NH)NH2、C(O)(CH2)nNR5C(=NH)NH2、C(O)(CH2)2NHC(O)(CH2)5NR5C(=NH)NH2およびGから独立に選択され、式中、R5は、HおよびC1~C6アルキルから選択され、nは、1から5の整数であり;
Tは、OHおよび式:
の部分か選択され、式中、
Aは、-OH、-N(R7)2R8から選択され、式中、
各R7は、HおよびC1~C6アルキルから独立に選択され、
R8は、電子対およびHから選択され、そして
R6は、OH、-N(R9)CH2C(O)NH2および式:
の部分から選択され、式中、
R9は、HおよびC1~C6アルキルから選択され、
R10は、G、C(O)-R11OH、アシル、トリチル、4メトキシトリチル、C(=NH)NH2、C(O)(CH2)mNR12C(=NH)NH2およびC(O)(CH2)2NHC(O)(CH2)5NR12C(=NH)NH2から選択され、式中、
mは、1から5の整数であり、
R11は、式-(O-アルキル)y-を有し、式中、yは、3から10の整数であり、
y個のアルキル基の各々は、C2~C6アルキルから独立に選択され;
R12は、HおよびC1~C6アルキルから選択され;
R1の各例は、
-N(R13)2R14[式中、各R13は、HおよびC1~C6アルキルから独立に選択され、そしてR14は、電子対およびHから選択される];
式(II):
の部分[式中、
R15は、H、G、C1~C6アルキル、C(=NH)NH2、C(O)(CH2)qNR18C(=NH)NH2および-C(O)(CH2)2NHC(O)(CH2)5NR18C(=NH)NH2から選択され、式中、
R18は、HおよびC1~C6アルキルから選択され;
qは、1から5の整数であり、
R16は、電子対およびHから選択され;
各R17は、Hおよびメチルから独立に選択される];および
式(III):
の部分[式中、
R19は、H、C1~C6アルキル、C(=NH)NH2、-C(O)(CH2)rNR22C(=NH)NH2、-C(O)CH(NH2)(CH2)3NHC(=NH)NH2、-C(O)(CH2)2NHC(O)(CH2)5NR22C(=NH)NH2、-C(O)CH(NH2)(CH2)4NH2およびGから選択され、式中、
R22は、HおよびC1~C6アルキルから選択され;
rは、1から5の整数であり、
R20は、HおよびC1~C6アルキルから選択され;
R21は、電子対およびHから選択される]
から独立に選択され;
R2は、H、G、アシル、トリチル、4-メトキシトリチル、C1~C6アルキル、-C(=NH)NH2、-C(O)-R23、-C(O)(CH2)sNR24C(=NH)NH2、-C(O)(CH2)2NHC(O)(CH2)5NR24C(=NH)NH2、-C(O)CH(NH2)(CH2)3NHC(=NH)NH2および式:
の部分から選択され、式中、
R23は、式-(O-アルキル)v-OHを有し、式中、vは、3から10の整数であり、v個のアルキル基の各々は、C2~C6アルキルから独立に選択され;
R24は、HおよびC1~C6アルキルから選択され;
sは、1から5の整数であり;
Lは、-C(O)(CH2)6C(O)-および-C(O)(CH2)2S2(CH2)2C(O)-から選択され;
各R25は、式-(CH2)2OC(O)N(R26)2を有し、式中、各R26は、式-(CH2)6NHC(=NH)NH2を有し;
R3は、電子対、HおよびC1~C6アルキルから選択され、
ここで、Gは、-C(O)(CH2)5NH-CPP、-C(O)(CH2)2NH-CPP、-C(O)(CH2)2NHC(O)(CH2)5NH-CPPおよび-C(O)CH2NH-CPPから選択される細胞透過性ペプチド(「CPP」)およびリンカー部分であるか、またはGは、式:
を有し、式中、CPPは、Gの最大で1つの例が存在するという条件で、CPPのカルボキシ末端において、アミド結合により、リンカー部分に結合しており、
ここで、前記ターゲティング配列は、ヒトジストロフィンプレmRNAのエクソンを含む標的領域内の10またはこれを超える連続ヌクレオチドと相補的であり、
ここで、前記被験体は、ミオスタチン治療剤を投与されており、それにより、前記被験体におけるミオスタチン活性およびミオスタチン発現の一方または両方が抑制される。
を含むターゲティング配列または薬学的に許容されるその塩を投与するステップを含み、式中、
各Nuは、一緒になってターゲティング配列を形成するヌクレオ塩基であり;
Zは、8から48の整数であり;
各Yは、Oおよび-NR4から独立に選択され、式中、各R4は、H、C1~C6アルキル、アラルキル、C(=NH)NH2、C(O)(CH2)nNR5C(=NH)NH2、C(O)(CH2)2NHC(O)(CH2)5NR5C(=NH)NH2およびGから独立に選択され、式中、R5は、HおよびC1~C6アルキルから選択され、nは、1から5の整数であり;
Tは、OHおよび式:
の部分か選択され、式中、
Aは、-OH、-N(R7)2R8から選択され、式中、
各R7は、HおよびC1~C6アルキルから独立に選択され、
R8は、電子対およびHから選択され、そして
R6は、OH、-N(R9)CH2C(O)NH2および式:
の部分から選択され、式中、
R9は、HおよびC1~C6アルキルから選択され、
R10は、G、C(O)-R11OH、アシル、トリチル、4メトキシトリチル、C(=NH)NH2、C(O)(CH2)mNR12C(=NH)NH2およびC(O)(CH2)2NHC(O)(CH2)5NR12C(=NH)NH2から選択され、式中、
mは、1から5の整数であり、
R11は、式-(O-アルキル)y-を有し、式中、yは、3から10の整数であり、
y個のアルキル基の各々は、C2~C6アルキルから独立に選択され;
R12は、HおよびC1~C6アルキルから選択され;
R1の各例は、
-N(R13)2R14[式中、各R13は、HおよびC1~C6アルキルから独立に選択され、そしてR14は、電子対およびHから選択される];
式(II):
の部分[式中、
R15は、H、G、C1~C6アルキル、C(=NH)NH2、C(O)(CH2)qNR18C(=NH)NH2および-C(O)(CH2)2NHC(O)(CH2)5NR18C(=NH)NH2から選択され、式中、
R18は、HおよびC1~C6アルキルから選択され;
qは、1から5の整数であり、
R16は、電子対およびHから選択され;
各R17は、Hおよびメチルから独立に選択される];および
式(III):
の部分[式中、
R19は、H、C1~C6アルキル、C(=NH)NH2、-C(O)(CH2)rNR22C(=NH)NH2、-C(O)CH(NH2)(CH2)3NHC(=NH)NH2、-C(O)(CH2)2NHC(O)(CH2)5NR22C(=NH)NH2、-C(O)CH(NH2)(CH2)4NH2およびGから選択され、式中、
R22は、HおよびC1~C6アルキルから選択され;
rは、1から5の整数であり、
R20は、HおよびC1~C6アルキルから選択され;
R21は、電子対およびHから選択される]
から独立に選択され;
R2は、H、G、アシル、トリチル、4-メトキシトリチル、C1~C6アルキル、-C(=NH)NH2、-C(O)-R23、-C(O)(CH2)sNR24C(=NH)NH2、-C(O)(CH2)2NHC(O)(CH2)5NR24C(=NH)NH2、-C(O)CH(NH2)(CH2)3NHC(=NH)NH2および式:
の部分から選択され、式中、
R23は、式-(O-アルキル)v-OHを有し、式中、vは、3から10の整数であり、v個のアルキル基の各々は、C2~C6アルキルから独立に選択され;
R24は、HおよびC1~C6アルキルから選択され;
sは、1から5の整数であり;
Lは、-C(O)(CH2)6C(O)-および-C(O)(CH2)2S2(CH2)2C(O)-から選択され;
各R25は、式-(CH2)2OC(O)N(R26)2を有し、式中、各R26は、式-(CH2)6NHC(=NH)NH2を有し;
R3は、電子対、HおよびC1~C6アルキルから選択され、
ここで、Gは、-C(O)(CH2)5NH-CPP、-C(O)(CH2)2NH-CPP、-C(O)(CH2)2NHC(O)(CH2)5NH-CPPおよび-C(O)CH2NH-CPPから選択される細胞透過性ペプチド(「CPP」)およびリンカー部分であるか、またはGは、式:
を有し、式中、CPPは、Gの最大で1つの例が存在するという条件で、CPPのカルボキシ末端において、アミド結合により、リンカー部分に結合しており、
ここで、前記ターゲティング配列は、ヒトジストロフィンプレmRNAのエクソンを含む標的領域内の10またはこれを超える連続ヌクレオチドと相補的であり、
ここで、前記被験体は、ミオスタチン治療剤を投与されており、それにより、前記被験体におけるミオスタチン活性およびミオスタチン発現の一方または両方が抑制される。
多様な実施形態では、各Nuが、独立に、アデニン、グアニン、チミン、ウラシル、シトシン、イノシン、ヒポキサンチン、2,6-ジアミノプリン、5-メチルシトシン、C5-プロピニル修飾ピリミジンまたは10-(9-(アミノエトキシ)フェノキサジニル)である。
多様な実施形態では、前記標的領域が、(i)少なくとも1つのヌクレオチドが前記エクソンに伴うスプライス接合部にわたるヌクレオチド配列;または(ii)ヌクレオチドが前記エクソン接合部に伴うスプライス接合部にわたらないヌクレオチド配列から選択される。実施形態では、前記ターゲティング配列が、配列番号76~3485から選択される配列を含むか、配列番号76~3485から選択されるターゲティング配列の少なくとも10の連続ヌクレオチドの断片であるか、または配列番号76~3485から選択されるターゲティング配列と少なくとも90%の配列同一性を有する変異体である。
多様な実施形態では、
i)Yが、Oであり、R2が、HもしくはGから選択され、R3が、電子対もしくはHから選択されるか;
ii)R2が、Gであり、式中、前記CPPが配列番号3486~3501から選択される配列を有するか;
iii)各R1が、-N(CH3)2であるか;
iv)少なくとも1つのR1が、
から選択されるか;または
v)R1基の50~90%が、-N(CH3)2である。
i)Yが、Oであり、R2が、HもしくはGから選択され、R3が、電子対もしくはHから選択されるか;
ii)R2が、Gであり、式中、前記CPPが配列番号3486~3501から選択される配列を有するか;
iii)各R1が、-N(CH3)2であるか;
iv)少なくとも1つのR1が、
から選択されるか;または
v)R1基の50~90%が、-N(CH3)2である。
多様な態様は、ジストロフィンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得るジストロフィン遺伝子における変異を有する被験体においてデュシェンヌ型筋ジストロフィーおよび関連障害を処置する方法を含む。この方法は、被験体に、式(VI):
を含む化合物または薬学的に許容されるその塩を投与するステップを含み、式中、
各Nuは、一緒になってターゲティング配列を形成するヌクレオ塩基であり;
Zは、8から48の整数であり;
各Yは、Oおよび-NR4から独立に選択され、式中、各R4は、H、C1~C6アルキル、アラルキル、-C(=NH)NH2、-C(O)(CH2)nNR5C(=NH)NH2、-C(O)(CH2)2NHC(O)(CH2)5NR5C(=NH)NH2およびGから独立に選択され、式中、R5は、HおよびC1~C6アルキルから選択され、nは、1から5の整数であり;
Tは、OHおよび式:
の部分から選択され、式中、
Aは、-OHおよび-N(R7)2R8から選択され、式中
各R7は、HおよびC1~C6アルキルから独立に選択され、
R8は、電子対およびHから選択され、
R6は、OH、-N(R9)CH2C(O)NH2および式:
の部分から選択され、式中、
R9は、HおよびC1~C6アルキルから選択され、
R10は、G、-C(O)-R11OH、アシル、トリチル、4-メトキシトリチル、-C(=NH)NH2、-C(O)(CH2)mNR12C(=NH)NH2および-C(O)(CH2)2NHC(O)(CH2)5NR12C(=NH)NH2から選択され、式中、
mは、1から5の整数であり、
R11は、式-(O-アルキル)y-を有し、式中、yは、3から10の整数であり、
y個のアルキル基の各々は、C2~C6アルキルから独立に選択され;
R12は、HおよびC1~C6アルキルから選択され;
R2は、H、G、アシル、トリチル、4-メトキシトリチル、C1~C6アルキル、-C(=NH)NH2および-C(O)-R23から選択され;
R3は、電子対、HおよびC1~C6アルキルから選択され、
ここで、前記ターゲティング配列は、配列番号76~3485から選択される配列を含むか、
配列番号76~3485から選択されるか、配列番号76~3485から選択される配列の少なくとも10の連続ヌクレオチドの断片であるか、または配列番号76~3485から選択される配列と少なくとも90%の配列同一性を有する変異体である。
を含む化合物または薬学的に許容されるその塩を投与するステップを含み、式中、
各Nuは、一緒になってターゲティング配列を形成するヌクレオ塩基であり;
Zは、8から48の整数であり;
各Yは、Oおよび-NR4から独立に選択され、式中、各R4は、H、C1~C6アルキル、アラルキル、-C(=NH)NH2、-C(O)(CH2)nNR5C(=NH)NH2、-C(O)(CH2)2NHC(O)(CH2)5NR5C(=NH)NH2およびGから独立に選択され、式中、R5は、HおよびC1~C6アルキルから選択され、nは、1から5の整数であり;
Tは、OHおよび式:
の部分から選択され、式中、
Aは、-OHおよび-N(R7)2R8から選択され、式中
各R7は、HおよびC1~C6アルキルから独立に選択され、
R8は、電子対およびHから選択され、
R6は、OH、-N(R9)CH2C(O)NH2および式:
の部分から選択され、式中、
R9は、HおよびC1~C6アルキルから選択され、
R10は、G、-C(O)-R11OH、アシル、トリチル、4-メトキシトリチル、-C(=NH)NH2、-C(O)(CH2)mNR12C(=NH)NH2および-C(O)(CH2)2NHC(O)(CH2)5NR12C(=NH)NH2から選択され、式中、
mは、1から5の整数であり、
R11は、式-(O-アルキル)y-を有し、式中、yは、3から10の整数であり、
y個のアルキル基の各々は、C2~C6アルキルから独立に選択され;
R12は、HおよびC1~C6アルキルから選択され;
R2は、H、G、アシル、トリチル、4-メトキシトリチル、C1~C6アルキル、-C(=NH)NH2および-C(O)-R23から選択され;
R3は、電子対、HおよびC1~C6アルキルから選択され、
ここで、前記ターゲティング配列は、配列番号76~3485から選択される配列を含むか、
配列番号76~3485から選択されるか、配列番号76~3485から選択される配列の少なくとも10の連続ヌクレオチドの断片であるか、または配列番号76~3485から選択される配列と少なくとも90%の配列同一性を有する変異体である。
多様な態様は、ヒトミオスタチンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得るジストロフィン遺伝子における変異を有する被験体においてデュシェンヌ型筋ジストロフィーおよび関連障害を処置する方法お含む。実施形態では、この方法は、
被験体に、式(I):
を含む化合物または薬学的に許容されるその塩を投与するステップを含み、式中、
各Nuは、一緒になってターゲティング配列を形成するヌクレオ塩基であり;
Zは、8から48の整数であり;
各Yは、Oおよび-NR4から独立に選択され、式中、各R4は、H、C1~C6アルキル、アラルキル、C(=NH)NH2、C(O)(CH2)nNR5C(=NH)NH2、C(O)(CH2)2NHC(O)(CH2)5NR5C(=NH)NH2およびGから独立に選択され、式中、R5は、HおよびC1~C6アルキルから選択され、nは1から5の整数であり;
Tは、OHおよび式:
の部分から選択され、式中、
Aは、-OH、-N(R7)2R8から選択され、式中
R7は、HおよびC1~C6アルキルから独立に選択され、
R8は、電子対およびHから選択され、
R6は、OH、-N(R9)CH2C(O)NH2および式:
の部分から選択され、式中、
R9は、HおよびC1~C6アルキルから選択され;
R10は、G、C(O)-R11OH、アシル、トリチル、4メトキシトリチル、C(=NH)NH2、C(O)(CH2)mNR12C(=NH)NH2およびC(O)(CH2)2NHC(O)(CH2)5NR12C(=NH)NH2から選択され、式中、
mは、1から5の整数であり、
R11は、式-(O-アルキル)y-を有し、式中、yは、3から10の整数であり、
y個のアルキル基の各々は、C2~C6アルキルから独立に選択され;
R12は、HおよびC1~C6アルキルから選択され;
R1の各例は、
-N(R13)2R14[式中、各R13は、HおよびC1~C6アルキルから独立に選択され、R14は、電子対およびHから選択される];
式(II):
の部分[式中、
R15は、H、G、C1~C6アルキル、C(=NH)NH2、C(O)(CH2)qNR18C(=NH)NH2および-C(O)(CH2)2NHC(O)(CH2)5NR18C(=NH)NH2から選択され、式中、
R18は、HおよびC1~C6アルキルから選択され;
qは、1から5の整数であり、
R16は、電子対およびHから選択され;そして
各R17は、Hおよびメチルから独立に選択される];および
式(III):
の部分[式中、
R19は、H、C1~C6アルキル、C(=NH)NH2、-C(O)(CH2)rNR22C(=NH)NH2、-C(O)CH(NH2)(CH2)3NHC(=NH)NH2、-C(O)(CH2)2NHC(O)(CH2)5NR22C(=NH)NH2、-C(O)CH(NH2)(CH2)4NH2およびGから選択され、式中、
R22は、HおよびC1~C6アルキルから選択され;
rは、1から5の整数であり、
R20は、HおよびC1~C6アルキルから選択され;
R21は、電子対およびHから選択される]から独立に選択され;
R2は、H、G、アシル、トリチル、4-メトキシトリチル、C1~C6アルキル、-C(=NH)NH2、-C(O)-R23、-C(O)(CH2)sNR24C(=NH)NH2、-C(O)(CH2)2NHC(O)(CH2)5NR24C(=NH)NH2、-C(O)CH(NH2)(CH2)3NHC(=NH)NH2および式:
の部分から選択され、式中、
R23は、式-(O-アルキル)v-OHを有し、式中、vは、3から10の整数であり、v個のアルキル基の各々は、C2~C6アルキルから独立に選択され;
R24は、HおよびC1~C6アルキルから選択され;
sは、1から5の整数であり;
Lは、-C(O)(CH2)6C(O)-および-C(O)(CH2)2S2(CH2)2C(O)-から選択され、
各R25は、式-(CH2)2OC(O)N(R26)2を有し、式中、各R26は、式-(CH2)6NHC(=NH)NH2を有し;
R3は、電子対、HおよびC1~C6アルキルから選択され、
ここで、Gは、-C(O)(CH2)5NH-CPP、-C(O)(CH2)2NH-CPP、-C(O)(CH2)2NHC(O)(CH2)5NH-CPPおよび-C(O)CH2NH-CPPから選択される、細胞透過性ペプチド(「CPP」)およびリンカー部分であるか、またはGは、式:
を有し、式中、CPPは、Gの最大で1つの例が存在するという条件で、CPPのカルボキシ末端において、アミド結合により、リンカー部分に結合しており、
ここで、前記ターゲティング配列は、ヒトジストロフィンプレmRNAのエクソンを含む標的領域内の10またはこれを超える連続ヌクレオチドと相補的であり、
ここで、前記被験体は、ミオスタチン治療剤を投与されており、それにより、前記被験体におけるミオスタチン活性またはミオスタチン発現の一方または両方が抑制される。
被験体に、式(I):
を含む化合物または薬学的に許容されるその塩を投与するステップを含み、式中、
各Nuは、一緒になってターゲティング配列を形成するヌクレオ塩基であり;
Zは、8から48の整数であり;
各Yは、Oおよび-NR4から独立に選択され、式中、各R4は、H、C1~C6アルキル、アラルキル、C(=NH)NH2、C(O)(CH2)nNR5C(=NH)NH2、C(O)(CH2)2NHC(O)(CH2)5NR5C(=NH)NH2およびGから独立に選択され、式中、R5は、HおよびC1~C6アルキルから選択され、nは1から5の整数であり;
Tは、OHおよび式:
の部分から選択され、式中、
Aは、-OH、-N(R7)2R8から選択され、式中
R7は、HおよびC1~C6アルキルから独立に選択され、
R8は、電子対およびHから選択され、
R6は、OH、-N(R9)CH2C(O)NH2および式:
の部分から選択され、式中、
R9は、HおよびC1~C6アルキルから選択され;
R10は、G、C(O)-R11OH、アシル、トリチル、4メトキシトリチル、C(=NH)NH2、C(O)(CH2)mNR12C(=NH)NH2およびC(O)(CH2)2NHC(O)(CH2)5NR12C(=NH)NH2から選択され、式中、
mは、1から5の整数であり、
R11は、式-(O-アルキル)y-を有し、式中、yは、3から10の整数であり、
y個のアルキル基の各々は、C2~C6アルキルから独立に選択され;
R12は、HおよびC1~C6アルキルから選択され;
R1の各例は、
-N(R13)2R14[式中、各R13は、HおよびC1~C6アルキルから独立に選択され、R14は、電子対およびHから選択される];
式(II):
の部分[式中、
R15は、H、G、C1~C6アルキル、C(=NH)NH2、C(O)(CH2)qNR18C(=NH)NH2および-C(O)(CH2)2NHC(O)(CH2)5NR18C(=NH)NH2から選択され、式中、
R18は、HおよびC1~C6アルキルから選択され;
qは、1から5の整数であり、
R16は、電子対およびHから選択され;そして
各R17は、Hおよびメチルから独立に選択される];および
式(III):
の部分[式中、
R19は、H、C1~C6アルキル、C(=NH)NH2、-C(O)(CH2)rNR22C(=NH)NH2、-C(O)CH(NH2)(CH2)3NHC(=NH)NH2、-C(O)(CH2)2NHC(O)(CH2)5NR22C(=NH)NH2、-C(O)CH(NH2)(CH2)4NH2およびGから選択され、式中、
R22は、HおよびC1~C6アルキルから選択され;
rは、1から5の整数であり、
R20は、HおよびC1~C6アルキルから選択され;
R21は、電子対およびHから選択される]から独立に選択され;
R2は、H、G、アシル、トリチル、4-メトキシトリチル、C1~C6アルキル、-C(=NH)NH2、-C(O)-R23、-C(O)(CH2)sNR24C(=NH)NH2、-C(O)(CH2)2NHC(O)(CH2)5NR24C(=NH)NH2、-C(O)CH(NH2)(CH2)3NHC(=NH)NH2および式:
の部分から選択され、式中、
R23は、式-(O-アルキル)v-OHを有し、式中、vは、3から10の整数であり、v個のアルキル基の各々は、C2~C6アルキルから独立に選択され;
R24は、HおよびC1~C6アルキルから選択され;
sは、1から5の整数であり;
Lは、-C(O)(CH2)6C(O)-および-C(O)(CH2)2S2(CH2)2C(O)-から選択され、
各R25は、式-(CH2)2OC(O)N(R26)2を有し、式中、各R26は、式-(CH2)6NHC(=NH)NH2を有し;
R3は、電子対、HおよびC1~C6アルキルから選択され、
ここで、Gは、-C(O)(CH2)5NH-CPP、-C(O)(CH2)2NH-CPP、-C(O)(CH2)2NHC(O)(CH2)5NH-CPPおよび-C(O)CH2NH-CPPから選択される、細胞透過性ペプチド(「CPP」)およびリンカー部分であるか、またはGは、式:
を有し、式中、CPPは、Gの最大で1つの例が存在するという条件で、CPPのカルボキシ末端において、アミド結合により、リンカー部分に結合しており、
ここで、前記ターゲティング配列は、ヒトジストロフィンプレmRNAのエクソンを含む標的領域内の10またはこれを超える連続ヌクレオチドと相補的であり、
ここで、前記被験体は、ミオスタチン治療剤を投与されており、それにより、前記被験体におけるミオスタチン活性またはミオスタチン発現の一方または両方が抑制される。
多様な実施形態では、各Nuが、独立に、アデニン、グアニン、チミン、ウラシル、シトシン、イノシン、ヒポキサンチン、2,6-ジアミノプリン、5-メチルシトシン、C5-プロピニル修飾ピリミジンまたは10-(9-(アミノエトキシ)フェノキサジニル)である。
多様な実施形態では、前記ターゲティング配列が、配列番号16~75から選択される配列を含むか、配列番号16~75から選択されるターゲティング配列の少なくとも10の連続ヌクレオチドの断片であるか、または配列番号16~75から選択されるターゲティング配列と少なくとも90%の配列同一性を有する変異体である。
多様な実施形態では、
i)Yが、Oであり、R2が、HもしくはGから選択され、R3が、電子対もしくはHから選択されるか;
ii)R2が、Gであり、前記CPPが、配列番号3486~3501から選択される配列を有するか;
iii)各R1が、-N(CH3)2であるか;
iv)少なくとも1つのR1が、
から選択されるか、または
v)R1基の50~90%が、-N(CH3)2である。
i)Yが、Oであり、R2が、HもしくはGから選択され、R3が、電子対もしくはHから選択されるか;
ii)R2が、Gであり、前記CPPが、配列番号3486~3501から選択される配列を有するか;
iii)各R1が、-N(CH3)2であるか;
iv)少なくとも1つのR1が、
v)R1基の50~90%が、-N(CH3)2である。
多様な態様は、ミオスタチンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得るジストロフィン遺伝子における変異を有する被験体においてデュシェンヌ型筋ジストロフィーおよび関連障害を処置する方法を含む。多様な実施形態では、この方法は、被験体に、式(VI):
を含む化合物または薬学的に許容されるその塩を投与するステップを含み、式中、
各Nuは、一緒になってターゲティング配列を形成するヌクレオ塩基であり;
Zは、8から48の整数であり;
各Yは、Oおよび-NR4から独立に選択され、式中、R4は、H、C1~C6アルキル、アラルキル、-C(=NH)NH2、-C(O)(CH2)nNR5C(=NH)NH2、-C(O)(CH2)2NHC(O)(CH2)5NR5C(=NH)NH2およびGから独立に選択され、式中、R5は、HおよびC1~C6アルキルから選択され、nは、1から5の整数であり;
Tは、OHおよび式:
の部分から選択され、式中、
Aは、-OHおよび-N(R7)2R8から選択され、式中、
各R7は、HおよびC1~C6アルキルから独立に選択され、
R8は、電子対およびHから選択され、
R6は、OH、-N(R9)CH2C(O)NH2および式:
の部分から選択され、式中、
R9は、HおよびC1~C6アルキルから選択され;
R10は、G、-C(O)-R11OH、アシル、トリチル、4-メトキシトリチル、-C(=NH)NH2、-C(O)(CH2)mNR12C(=NH)NH2および-C(O)(CH2)2NHC(O)(CH2)5NR12C(=NH)NH2から選択され、式中、
mは、1から5の整数であり、
R11は、式-(O-アルキル)y-を有し、式中、yは、3から10の整数であり、
y個のアルキル基の各々は、C2~C6アルキルから独立に選択され;
R12は、HおよびC1~C6アルキルから選択され;
R2は、H、G、アシル、トリチル、4-メトキシトリチル、C1~C6アルキル、-C(=NH)NH2および-C(O)-R23から選択され;
R3は、電子対、HおよびC1~C6アルキルから選択され、
ここで、前記ターゲティング配列は、配列番号16~75から選択される配列を含むか、配列番号16~75から選択されるか、配列番号16~75から選択される配列の少なくとも10の連続ヌクレオチドの断片であるか、または配列番号16~75から選択される配列と少なくとも90%の配列同一性を有する変異体である。
を含む化合物または薬学的に許容されるその塩を投与するステップを含み、式中、
各Nuは、一緒になってターゲティング配列を形成するヌクレオ塩基であり;
Zは、8から48の整数であり;
各Yは、Oおよび-NR4から独立に選択され、式中、R4は、H、C1~C6アルキル、アラルキル、-C(=NH)NH2、-C(O)(CH2)nNR5C(=NH)NH2、-C(O)(CH2)2NHC(O)(CH2)5NR5C(=NH)NH2およびGから独立に選択され、式中、R5は、HおよびC1~C6アルキルから選択され、nは、1から5の整数であり;
Tは、OHおよび式:
の部分から選択され、式中、
Aは、-OHおよび-N(R7)2R8から選択され、式中、
各R7は、HおよびC1~C6アルキルから独立に選択され、
R8は、電子対およびHから選択され、
R6は、OH、-N(R9)CH2C(O)NH2および式:
R9は、HおよびC1~C6アルキルから選択され;
R10は、G、-C(O)-R11OH、アシル、トリチル、4-メトキシトリチル、-C(=NH)NH2、-C(O)(CH2)mNR12C(=NH)NH2および-C(O)(CH2)2NHC(O)(CH2)5NR12C(=NH)NH2から選択され、式中、
mは、1から5の整数であり、
R11は、式-(O-アルキル)y-を有し、式中、yは、3から10の整数であり、
y個のアルキル基の各々は、C2~C6アルキルから独立に選択され;
R12は、HおよびC1~C6アルキルから選択され;
R2は、H、G、アシル、トリチル、4-メトキシトリチル、C1~C6アルキル、-C(=NH)NH2および-C(O)-R23から選択され;
R3は、電子対、HおよびC1~C6アルキルから選択され、
ここで、前記ターゲティング配列は、配列番号16~75から選択される配列を含むか、配列番号16~75から選択されるか、配列番号16~75から選択される配列の少なくとも10の連続ヌクレオチドの断片であるか、または配列番号16~75から選択される配列と少なくとも90%の配列同一性を有する変異体である。
多様な態様は、12~40サブユニットのアンチセンスオリゴマー化合物と、薬学的に許容される担体とを含むミオスタチン関連医薬組成物であって、前記化合物が、
(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットと;
ヒトミオスタチンプレmRNAのエクソンを含む標的領域内の12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列と
を含むミオスタチン関連組成物と組み合わせた、
20~50サブユニットのアンチセンスオリゴマー化合物と、薬学的に許容される担体とを含むジストロフィン関連医薬組成物であって、前記化合物が、
(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または、(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットと;
ヒトジストロフィンプレmRNAのエクソンを含む標的領域内の10またはこれを超える連続ヌクレオチドと相補的なターゲティング配列と
を含むジストロフィン関連医薬組成物を含む。多様な実施形態では、前記ジストロフィン関連組成物と前記ミオスタチン関連組成物とが、同じ医薬組成物として提供される。
(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットと;
ヒトミオスタチンプレmRNAのエクソンを含む標的領域内の12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列と
を含むミオスタチン関連組成物と組み合わせた、
20~50サブユニットのアンチセンスオリゴマー化合物と、薬学的に許容される担体とを含むジストロフィン関連医薬組成物であって、前記化合物が、
(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または、(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットと;
ヒトジストロフィンプレmRNAのエクソンを含む標的領域内の10またはこれを超える連続ヌクレオチドと相補的なターゲティング配列と
を含むジストロフィン関連医薬組成物を含む。多様な実施形態では、前記ジストロフィン関連組成物と前記ミオスタチン関連組成物とが、同じ医薬組成物として提供される。
多様な態様は、ヒトミオスタチンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得る遺伝子変異を有する被験体においてミオスタチン発現をモジュレートするための方法であって、前記被験体に、12~40サブユニットを含み、ヒトミオスタチンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップであって、前記オリゴマーが、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含む、ステップと、ミオスタチンプレmRNA転写物内の標的領域に前記アンチセンスオリゴマーを結合させるステップと、前記標的領域のヒトミオスタチンmRNA転写物への転写を阻害するステップとを含み、前記被験体が、前記被験体におけるジストロフィン発現を増加させるジストロフィン治療剤を投与されている、方法を含む。
多様な態様は、ヒトミオスタチンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得る遺伝子変異を有する被験体においてエクソン2の発現を減少させるための方法であって、前記被験体に、12~40サブユニットを含み、ヒトミオスタチンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップと、ミオスタチンmRNA転写物内のエクソン2の転写を阻害するステップとを含み、前記被験体が、前記被験体におけるジストロフィン発現を増加させるジストロフィン治療剤を投与されている、方法を含む。多様な実施形態では、ミオスタチンmRNA転写物内のエクソン2の発現が、約5%、6%、7%、8%、9%、10%、11%、12%、13%、14%、15%、16%、17%、18%、19%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%または100%減少する。
多様な態様は、ヒトミオスタチンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得るジストロフィン遺伝子における変異を有する被験体の筋細胞または組織における機能的なミオスタチンタンパク質の蓄積を減少させるための方法であって、前記被験体に、12~40サブユニットを含み、ヒトミオスタチンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップと、ミオスタチンmRNA転写物内のエクソン2の転写を阻害するステップとを含み、前記被験体が、前記被験体におけるジストロフィン発現を増加させるジストロフィン治療剤を投与されている、方法を含む。
多様な態様は、デュシェンヌ型筋ジストロフィーおよび関連障害を処置するための医薬であって、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含み;ヒトミオスタチンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、12~40サブユニットを含むアンチセンスオリゴマー化合物と;ジストロフィンの発現を増加させるジストロフィン治療剤とを含む医薬を含む。
多様な態様は、ヒトミオスタチンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得るジストロフィン遺伝子における変異を有する被験体においてデュシェンヌ型筋ジストロフィーおよび関連障害の進行を阻害するための方法であって、前記被験体に、12~40サブユニットを含み、ヒトミオスタチンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップと、ミオスタチンmRNA転写物内のエクソン2の転写を阻害するステップとを含み、前記被験体が、前記被験体におけるジストロフィン発現を増加させるジストロフィン治療剤を投与され、それによりデュシェンヌ型筋ジストロフィーの進行を阻害する、方法を含む。
多様な態様は、デュシェンヌ型筋ジストロフィーおよび関連障害を有する被験体において機能的なミオスタチンタンパク質の蓄積を減少させる方法であって、前記被験体に、12~40サブユニットを含み、ヒトミオスタチンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップと、ミオスタチンmRNA転写物内のエクソン2の転写を阻害するステップとを含み、前記被験体における機能的なミオスタチンタンパク質の蓄積が減少し、前記被験体が、前記被験体内でジストロフィン発現を増加させるジストロフィン治療剤を投与されている、方法を含む。
多様な態様は、そのような処置を必要とする被験体においてデュシェンヌ型筋ジストロフィーおよび関連障害を処置するための方法であって、 前記被験体において少なくとも約200~400nMのアンチセンスオリゴマーのピークの血中濃度を得るための有効量でアンチセンスオリゴマーを投与するステップを含む方法を含む。
多様な態様は、ヒトミオスタチンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得るジストロフィン遺伝子における変異を有する被験体において骨格筋量不足を処置する方法であって、(a)前記被験体におけるミオスタチンタンパク質の血液中または組織中レベルを測定するステップと、(b)前記被験体に、12~40サブユニットを含み、ヒトミオスタチンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップと、(c)ミオスタチンmRNA転写物内のエクソン2の転写を阻害するステップと、(d)選択した時間以後、前記被験体におけるミオスタチンタンパク質レベルを測定するステップと、(e)(d)で測定された前記レベルを使用して前記の投与を反復するステップであって、投与されるアンチセンスオリゴマーの量の用量または投薬スケジュールを調整するステップとを含み、前記被験体におけるミオスタチンタンパク質の前記レベルが、前記アンチセンスオリゴマーの投与後に低下し、前記被験体が、前記被験体においてジストロフィン発現を増加させるジストロフィン治療剤を投与されている、方法を含む。
多様な態様は、ジストロフィンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得るジストロフィン遺伝子における変異を有する被験体においてデュシェンヌ型筋ジストロフィーおよび関連障害の進行を阻害する方法であって、前記被験体に、17~40サブユニットを含み、ヒトジストロフィンプレmRNAのエクソンを含む標的領域内の12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップを含み、前記アンチセンスオリゴマーが、前記エクソンのスキッピングを誘導し、前記オリゴマーが、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含み、前記被験体が、前記被験体におけるミオスタチンの活性および発現のうちの一方または両方を阻害するミオスタチン治療剤を投与され、それによりデュシェンヌ型筋ジストロフィーの進行を阻害する、方法を含む。
多様な態様は、デュシェンヌ型筋ジストロフィーの進行を阻害する方法であって、被験体に、12~40サブユニットを含み、ヒトミオスタチンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップを含み、前記オリゴマーが、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含み、前記被験体が、前記被験体においてジストロフィン発現を増加させるジストロフィン治療剤を投与され、それによりデュシェンヌ型筋ジストロフィーの進行を阻害する、方法を含む。
多様な態様および実施形態は、アンチセンスオリゴマーの3’末端または5’末端にコンジュゲートするアルギニンに富むペプチド配列をさらに含むアンチセンスオリゴマーを含み、前記アルギニンに富むペプチド配列が、配列番号3486~3501から選択される配列を含む。
多様な態様は、17~40サブユニットを含み、ヒトジストロフィンプレmRNAのエクソンを含む標的領域内の12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含むアンチセンスオリゴマーであって、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含む、ジストロフィンを標的とする前記オリゴマーと;12~40サブユニットを含み、ヒトミオスタチンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含むアンチセンスオリゴマーであって、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含む、ミオスタチンを標的とする前記オリゴマーとを含む組成物を含む。
多様な態様および実施形態は、ジストロフィン治療剤とミオスタチン治療剤を被験体に投与するステップを含み、前記被験体が、7歳またはこれを超える小児患者である。
多様な態様および実施形態は、ヒトミオスタチンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得る遺伝子変異を有する被験体においてジストロフィン発現をモジュレートするための方法であって、
前記被験体に、17~40サブユニットを含み、ヒトジストロフィンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップを含み、
前記オリゴマーが、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含み、
前記被験体が、前記被験体におけるミオスタチン活性およびミオスタチン発現の一方または両方を阻害するミオスタチン治療剤を投与されている、方法を含む。
前記被験体に、17~40サブユニットを含み、ヒトジストロフィンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップを含み、
前記オリゴマーが、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含み、
前記被験体が、前記被験体におけるミオスタチン活性およびミオスタチン発現の一方または両方を阻害するミオスタチン治療剤を投与されている、方法を含む。
DMDおよび関連障害を有する被験体において筋肉量をモジュレートする方法をさらに含む多様な態様および実施形態が提供される。
別の態様では、本開示は、DMDを有する患者を処置するための方法であって、被験体に、本明細書で記載されるいずれかのジストロフィン治療剤および本明細書で記載されるいずれかのミオスタチン治療剤の一方または両方を投与し、それによりDMDを処置するステップを含む方法を提供する。患者は、例えばエクソンスキッピングを誘導できるオリゴヌクレオチドを使用してエクソンスキッピングされ得るDMD遺伝子における変異を有する患者であり得る。一部の実施形態では、患者はエクソン51スキッピングされ得るDMD遺伝子における変異を有する。一部の実施形態では、患者はエクソン53スキッピングされ得るDMD遺伝子における変異を有する。一部の実施形態では、患者はエクソン45スキッピングされ得るDMD遺伝子における変異を有する。一部の実施形態では、患者はエクソン44スキッピングされ得るDMD遺伝子における変異を有する。一部の実施形態では、患者はエクソン52スキッピングされ得るDMD遺伝子における変異を有する。一部の実施形態では、患者はエクソン50スキッピングされ得るDMD遺伝子における変異を有する。一部の実施形態では、患者はエクソン8スキッピングされ得るDMD遺伝子における変異を有する。一部の実施形態では、患者はエクソン55スキッピングされ得るDMD遺伝子における変異を有する。
別の態様では、本開示は、本明細書で記載されるジストロフィン治療剤のいずれか1または複数と、本明細書で記載されるミオスタチン治療剤のいずれか1または複数とを含む組成物(例えば医薬組成物)を提供する。
本明細書で記載される方法または組成物の一部の実施形態では、ジストロフィン治療剤はエテプリルセンである。
本明細書で記載される方法または組成物の一部の実施形態では、ジストロフィン治療剤は、配列番号927に明示された配列を含まず、それからならない。
本明細書で記載される方法または組成物の一部の実施形態では、ジストロフィンはヒトジストロフィンである。本明細書で記載される方法または組成物の一部の実施形態では、ミオスタチンはヒトミオスタチンである。本明細書で記載される方法または組成物の一部の実施形態では、被験体はヒトである。
本明細書で記載される方法または組成物のいずれかの一部の実施形態では、被験体はヒト(例えばヒト患者)である。本明細書で記載される方法または組成物のいずれかの一部の実施形態では、被験体は男性被験体である。本明細書で記載される方法または組成物のいずれかの一部の実施形態では、被験体は小児患者である。本明細書で記載される方法または組成物のいずれかの一部の実施形態では、患者は7歳またはこれを超える。本明細書で記載される方法または組成物のいずれかの一部の実施形態では、患者は少なくとも7歳であるが、約21歳未満である。
本明細書で記載される方法または組成物のいずれかの一部の実施形態では、ジストロフィン治療剤およびミオスタチン治療剤の一方または両方は、例えば静脈内投与により被験体に全身的に送達される。本明細書で記載される方法または組成物のいずれかの一部の実施形態では、ジストロフィン治療剤は、被験体に全身的に送達される。本明細書で記載される方法または組成物のいずれかの一部の実施形態では、ミオスタチン治療剤は、被験体に全身的に送達される。
本明細書で記載される方法または組成物のいずれかの一部の実施形態では、ジストロフィン治療剤およびミオスタチン治療剤の一方または両方は、被験体に慢性的に投与される。例えば、本明細書で記載される方法または組成物のいずれかの一部の実施形態では、治療剤の一方または両方は、各々独立に、毎日、毎週、毎月、2週に1回または2カ月に1回投与され得る。本明細書で記載される方法または組成物のいずれかの一部の実施形態では、治療剤の一方または両方の治療有効量は、各々独立に、単回用量(例えば週1回用量)として、または複数回用量(例えば2回またはこれを超える、例えば3、4、5、6または7回用量)として、処置期間内に、例えば週1回(毎週)または週2回被験体に送達することができる。
本明細書で記載される方法のいずれかの一部の実施形態では、ジストロフィン治療剤は1回目に投与され、ミオスタチン治療剤は2回目に投与される。例えば、ジストロフィン治療剤(例えばエテプリルセン)は、ミオスタチン治療剤を被験体に投与する前に、1回目に、被験体の筋細胞内でジストロフィン産生を増加させるのに十分な量および期間投与され得る。したがって、一部の実施形態では、ジストロフィン治療剤(例えばエテプリルセン)は、ミオスタチン治療剤を投与する前に、週1回、ある期間(例えば6カ月、1年、18カ月、2年またはこれを超える)、被験体の体重1kgあたり約30mgで被験体に投与され、被験体の筋細胞内でジストロフィン発現が増加する。一部の実施形態では、ジストロフィン治療剤(例えばエテプリルセン)は、ミオスタチン治療剤を投与する前に、週1回、ある期間(例えば6カ月、1年、18カ月、2年またはこれを超える)、被験体の体重1kgあたり約30~約50mgで、被験体に投与され、被験体の筋細胞におけるジストロフィン発現が増加する。本明細書で記載される方法のいずれかの一部の実施形態では、ミオスタチン治療剤は1回目に投与され、ジストロフィン治療剤は2回目に投与される。
一部の実施形態では、本明細書で記載される組成物および方法に使用するためのアンチセンスオリゴヌクレオチド化合物は、細胞透過性ペプチドを含まない。
特定の実施形態では、例えば、以下が提供される:
(項目1)
ジストロフィンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得るジストロフィン遺伝子における変異を有する、デュシェンヌ型筋ジストロフィーおよび関連障害を有する被験体を処置する方法であって、
前記被験体に、17~40サブユニットを含み、ヒトジストロフィンプレmRNAのエクソンを含む標的領域内の12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップを含み、前記アンチセンスオリゴマーが、前記エクソンのスキッピングを誘導し、
前記オリゴマーが、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含み、
前記被験体が、前記被験体におけるミオスタチン活性およびミオスタチン発現の一方または両方を阻害するミオスタチン治療剤を投与され、それによりデュシェンヌ型筋ジストロフィーまたは関連障害のうちの少なくとも1つを処置する、方法。
(項目2)
前記エクソンが、エクソン7、エクソン8、エクソン9、エクソン19、エクソン23、エクソン44、エクソン45、エクソン50、エクソン51、エクソン52、エクソン53またはエクソン55から選択される、項目1に記載の方法。
(項目3)
前記エクソンがエクソン23を含む、項目2に記載の方法。
(項目4)
前記エクソンがエクソン45を含む、項目2に記載の方法。
(項目5)
前記エクソンがエクソン51を含む、項目2に記載の方法。
(項目6)
前記エクソンがエクソン53を含む、項目2に記載の方法。
(項目7)
前記エクソンが、エクソン8、エクソン44、エクソン50、エクソン52またはエクソン55を含む、項目2に記載の方法。
(項目8)
前記アンチセンスオリゴマーが、20~30サブユニットを含む、項目1に記載の方法。
(項目9)
前記アンチセンスオリゴマーが、配列番号76~配列番号3485から選択される配列を含む、項目1に記載の方法。
(項目10)
前記アンチセンスオリゴマーが、エテプリルセン(eteplirsen)である、項目9に記載の方法。
(項目11)
前記ターゲティング配列が、前記標的領域内の少なくとも15の連続ヌクレオチドと相補的である、項目1に記載の方法。
(項目12)
前記ターゲティング配列が、前記標的領域内の少なくとも17の連続ヌクレオチドと相補的である、項目11に記載の方法。
(項目13)
前記ターゲティング配列が、前記標的領域と100%相補的である、項目12に記載の方法。
(項目14)
前記ミオスタチン治療剤が、タンパク質または核酸のうちの1つまたは複数から選択される、項目1に記載の方法。
(項目15)
前記タンパク質が、抗ミオスタチン抗体である、項目14に記載の方法。
(項目16)
前記タンパク質が、可溶性受容体である、項目14に記載の方法。
(項目17)
可溶性受容体が、ACVR2である、項目14に記載の方法。
(項目18)
前記核酸が、アンチセンスオリゴマーまたはsiRNAのうちの少なくとも1つである、項目14に記載の方法。
(項目19)
前記アンチセンスオリゴマーが、12~40サブユニットを含み、ミオスタチンプレmRNAの標的領域内の12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含み、
前記オリゴマーが、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含む、項目18に記載の方法。
(項目20)
前記アンチセンスオリゴマーが、20~30サブユニットを含む、項目19に記載の方法。
(項目21)
前記ターゲティング配列が、前記標的領域内の少なくとも15の連続ヌクレオチドと相補的である、項目19に記載の方法。
(項目22)
前記ターゲティング配列が、前記標的領域内の少なくとも17の連続ヌクレオチドと相補的である、項目19に記載の方法。
(項目23)
前記ターゲティング配列が、前記標的領域と100%相補的である、項目19に記載の方法。
(項目24)
前記標的領域が、配列番号1を含む、項目19に記載の方法。
(項目25)
前記エクソンが、エクソン2を含む、項目19に記載の方法。
(項目26)
前記標的領域が、(i)少なくとも1つのヌクレオチドが、イントロン1/エクソン2およびエクソン2/イントロン2に伴うスプライス接合部にわたるヌクレオチド配列、または、(ii)ヌクレオチドが、イントロン1/エクソン2およびエクソン2/イントロン2に伴うスプライス接合部にわたらないヌクレオチド配列から選択される項目19に記載の方法。
(項目27)
前記スプライス接合部が、スプライスアクセプター部位またはスプライスドナー部位を含む配列から選択される、項目26に記載の方法。
(項目28)
前記スプライスアクセプター部位が、配列番号2の内部に存在し、前記スプライスドナー部位が配列番号3の内部に存在する、項目27に記載の方法。
(項目29)
前記(i)のヌクレオチドが、配列番号16~43から選択される、項目26に記載の方法。
(項目30)
前記(ii)のヌクレオチドが、配列番号44~70から選択される、項目26に記載の方法。
(項目31)
前記被験体が、7歳またはこれを超える、項目1に記載の方法。
(項目32)
デュシェンヌ型筋ジストロフィーおよび関連障害を処置する方法であって、
被験体に、12~40サブユニットを含み、ヒトミオスタチンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップを含み、
前記オリゴマーが、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含み、
前記被験体が、前記被験体の筋細胞内で機能的なジストロフィンタンパク質の発現を増加させるジストロフィン治療剤を投与され、それによりデュシェンヌ型筋ジストロフィーまたは関連障害のうちの少なくとも1つを処置する、方法。
(項目33)
前記被験体が、ヒトミオスタチンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得るジストロフィン遺伝子における変異を有する、項目32に記載の方法。
(項目34)
前記アンチセンスオリゴマーが、20~30サブユニットを含む、項目32に記載の方法。
(項目35)
前記ターゲティング配列が、標的領域内の少なくとも15の連続ヌクレオチドと相補的である、項目32に記載の方法。
(項目36)
前記ターゲティング配列が、標的領域内の少なくとも17の連続ヌクレオチドと相補的である、項目32に記載の方法。
(項目37)
前記アンチセンスオリゴマーが、標的領域と100%相補的である、項目32に記載の方法。
(項目38)
前記標的領域が、配列番号1を含む、項目32に記載の方法。
(項目39)
前記エクソンが、エクソン2を含む、項目32に記載の方法。
(項目40)
前記標的領域が、(i)少なくとも1つのヌクレオチドがイントロン1/エクソン2およびエクソン2/イントロン2に伴うスプライス接合部にわたるヌクレオチド配列、または、(ii)ヌクレオチドがイントロン1/エクソン2およびエクソン2/イントロン2に伴うスプライス接合部にわたらないヌクレオチド配列から選択される、項目32に記載の方法。
(項目41)
前記スプライス接合部が、スプライスアクセプター部位またはスプライスドナー部位を含む配列から選択される、項目40に記載の方法。
(項目42)
前記スプライスアクセプター部位が、配列番号2の内部に存在し、前記スプライスドナー部位が、配列番号3の内部に存在する、項目41に記載の方法。
(項目43)
前記(i)のヌクレオチドが、配列番号16~43から選択される、項目41に記載の方法。
(項目44)
前記(ii)のヌクレオチドが、配列番号44~70から選択される、項目41に記載の方法。
(項目45)
前記ジストロフィン治療剤が、タンパク質または核酸のうちの1つまたは複数から選択される、項目32に記載の方法。
(項目46)
前記核酸が、アンチセンスオリゴマーである、項目45に記載の方法。
(項目47)
前記アンチセンスオリゴマーが、20~50サブユニットを含み、ヒトジストロフィンプレmRNAのエクソンを含む標的領域内の10またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含み、
前記オリゴマーが、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含む、項目46に記載の方法。
(項目48)
前記エクソンが、エクソン7、エクソン8、エクソン9、エクソン19、エクソン23、エクソン44、エクソン45、エクソン50、エクソン51、エクソン52、エクソン53またはエクソン55から選択される、項目47に記載の方法。
(項目49)
前記エクソンが、エクソン23を含む、項目48に記載の方法。
(項目50)
前記エクソンが、エクソン45を含む、項目48に記載の方法。
(項目51)
前記エクソンが、エクソン51を含む、項目48に記載の方法。
(項目52)
前記エクソンが、エクソン53を含む、項目48に記載の方法。
(項目53)
前記エクソンが、エクソン8、エクソン44、エクソン50、エクソン52またはエクソン55を含む、項目48に記載の方法。
(項目54)
前記アンチセンスオリゴマーが、20~30サブユニットを含む、項目47に記載の方法。
(項目55)
前記アンチセンスオリゴマーが、配列番号76~配列番号3485から選択される配列を含む、項目47に記載の方法。
(項目56)
前記アンチセンスオリゴマーが、エテプリルセンである、項目55に記載の方法。
(項目57)
前記ターゲティング配列が、標的領域内の少なくとも15の連続ヌクレオチドと相補的である、項目46に記載の方法。
(項目58)
前記ターゲティング配列が、標的領域内の少なくとも17の連続ヌクレオチドと相補的である、項目46に記載の方法。
(項目59)
前記ターゲティング配列が、標的領域と100%相補的である、項目46に記載の方法。
(項目60)
ジストロフィンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得るジストロフィン遺伝子における変異を有する被験体においてデュシェンヌ型筋ジストロフィーおよび関連障害を処置する方法であって、
被験体に、式(I):
を含む化合物または薬学的に許容されるその塩を投与するステップを含み、式中、
各Nuは、一緒になってターゲティング配列を形成するヌクレオ塩基であり;
Zは、8から48の整数であり;
各Yは、Oおよび-NR4から独立に選択され、式中、各R4は、H、C1~C6アルキル、アラルキル、C(=NH)NH2、C(O)(CH2)nNR5C(=NH)NH2、C(O)(CH2)2NHC(O)(CH2)5NR5C(=NH)NH2およびGから独立に選択され、式中、R5は、HおよびC1~C6アルキルから選択され、nは、1から5の整数であり;
Tは、OHおよび式:
の部分か選択され、式中、
Aは、-OH、-N(R7)2R8から選択され、式中、
各R7は、HおよびC1~C6アルキルから独立に選択され、
R8は、電子対およびHから選択され、そして
R6は、OH、-N(R9)CH2C(O)NH2および式:
の部分から選択され、式中、
R9は、HおよびC1~C6アルキルから選択され、
R10は、G、C(O)-R11OH、アシル、トリチル、4メトキシトリチル、C(=NH)NH2、C(O)(CH2)mNR12C(=NH)NH2およびC(O)(CH2)2NHC(O)(CH2)5NR12C(=NH)NH2から選択され、式中、
mは、1から5の整数であり、
R11は、式-(O-アルキル)y-を有し、式中、yは、3から10の整数であり、
y個のアルキル基の各々は、C2~C6アルキルから独立に選択され;
R12は、HおよびC1~C6アルキルから選択され;
R1の各例は、
-N(R13)2R14[式中、各R13は、HおよびC1~C6アルキルから独立に選択され、そしてR14は、電子対およびHから選択される];
式(II):
の部分[式中、
R15は、H、G、C1~C6アルキル、C(=NH)NH2、C(O)(CH2)qNR18C(=NH)NH2および-C(O)(CH2)2NHC(O)(CH2)5NR18C(=NH)NH2から選択され、式中、
R18は、HおよびC1~C6アルキルから選択され;
qは、1から5の整数であり、
R16は、電子対およびHから選択され;
各R17は、Hおよびメチルから独立に選択される];および
式(III):
の部分[式中、
R19は、H、C1~C6アルキル、C(=NH)NH2、-C(O)(CH2)rNR22C(=NH)NH2、-C(O)CH(NH2)(CH2)3NHC(=NH)NH2、-C(O)(CH2)2NHC(O)(CH2)5NR22C(=NH)NH2、-C(O)CH(NH2)(CH2)4NH2およびGから選択され、式中、
R22は、HおよびC1~C6アルキルから選択され;
rは、1から5の整数であり、
R20は、HおよびC1~C6アルキルから選択され;
R21は、電子対およびHから選択される]
から独立に選択され;
R2は、H、G、アシル、トリチル、4-メトキシトリチル、C1~C6アルキル、-C(=NH)NH2、-C(O)-R23、-C(O)(CH2)sNR24C(=NH)NH2、-C(O)(CH2)2NHC(O)(CH2)5NR24C(=NH)NH2、-C(O)CH(NH2)(CH2)3NHC(=NH)NH2および式:
の部分から選択され、式中、
R23は、式-(O-アルキル)v-OHを有し、式中、vは、3から10の整数であり、v個のアルキル基の各々は、C2~C6アルキルから独立に選択され;
R24は、HおよびC1~C6アルキルから選択され;
sは、1から5の整数であり;
Lは、-C(O)(CH2)6C(O)-および-C(O)(CH2)2S2(CH2)2C(O)-から選択され;
各R25は、式-(CH2)2OC(O)N(R26)2を有し、式中、各R26は、式-(CH2)6NHC(=NH)NH2を有し;
R3は、電子対、HおよびC1~C6アルキルから選択され、
ここで、Gは、-C(O)(CH2)5NH-CPP、-C(O)(CH2)2NH-CPP、-C(O)(CH2)2NHC(O)(CH2)5NH-CPPおよび-C(O)CH2NH-CPPから選択される細胞透過性ペプチド(「CPP」)およびリンカー部分であるか、またはGは、式:
を有し、式中、CPPは、Gの最大で1つの例が存在するという条件で、CPPのカルボキシ末端において、アミド結合により、リンカー部分に結合しており、
ここで、前記ターゲティング配列は、ヒトジストロフィンプレmRNAのエクソンを含む標的領域内の12またはこれを超える連続ヌクレオチドと相補的であり、
ここで、前記被験体は、前記被験体におけるミオスタチン活性およびミオスタチン発現の一方または両方を阻害するミオスタチン治療剤を投与され、それによりデュシェンヌ型筋ジストロフィーまたは関連障害のうちの少なくとも1つを処置する、方法。
(項目61)
各Nuが、独立に、アデニン、グアニン、チミン、ウラシル、シトシン、イノシン、ヒポキサンチン、2,6-ジアミノプリン、5-メチルシトシン、C5-プロピニル修飾ピリミジンまたは10-(9-(アミノエトキシ)フェノキサジニル)である、項目60に記載の方法。
(項目62)
前記標的領域が、(i)少なくとも1つのヌクレオチドが前記エクソンに伴うスプライス接合部にわたるヌクレオチド配列;または(ii)ヌクレオチドが前記エクソン接合部に伴うスプライス接合部にわたらないヌクレオチド配列から選択される、項目60に記
載の方法。
(項目63)
前記ターゲティング配列が、配列番号76~3485から選択される配列を含むか、配列番号76~3485から選択されるターゲティング配列の少なくとも10の連続ヌクレオチドの断片であるか、または配列番号76~3485から選択されるターゲティング配列と少なくとも90%の配列同一性を有する変異体である、項目60に記載の方法。
(項目64)
i)Yが、Oであり、R2が、HもしくはGから選択され、R3が、電子対もしくはHから選択されるか;
ii)R2が、Gであり、式中、前記CPPが配列番号3486~3501から選択される配列を有するか;
iii)各R1が、-N(CH3)2であるか;
iv)少なくとも1つのR1が、
から選択されるか;または
v)R1基の50~90%が、-N(CH3)2である、項目60に記載の方法。
(項目65)
Tが、式:
を有し、式中、Aは、-N(CH3)2であり、R6は、式:
を有し、式中、R10は、-C(O)R11OHである、項目60に記載の方法。
(項目66)
各Yが、Oであり、Tが、
から選択される、項目60に記載の方法。
(項目67)
Tが、式:
を有する、項目60に記載の方法。
(項目68)
ジストロフィンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得るジストロフィン遺伝子における変異を有する被験体においてデュシェンヌ型筋ジストロフィーおよび関連障害を処置する方法であって、
被験体に、式(VI):
を含む化合物または薬学的に許容されるその塩を投与するステップを含み、式中、
各Nuは、一緒になってターゲティング配列を形成するヌクレオ塩基であり;
Zは、8から48の整数であり;
各Yは、Oおよび-NR4から独立に選択され、式中、各R4は、H、C1~C6アルキル、アラルキル、-C(=NH)NH2、-C(O)(CH2)nNR5C(=NH)NH2、-C(O)(CH2)2NHC(O)(CH2)5NR5C(=NH)NH2およびGから独立に選択され、式中、R5は、HおよびC1~C6アルキルから選択され、nは、1から5の整数であり;
Tは、OHおよび式:
の部分から選択され、式中、
Aは、-OHおよび-N(R7)2R8から選択され、式中
各R7は、HおよびC1~C6アルキルから独立に選択され、
R8は、電子対およびHから選択され、
R6は、OH、-N(R9)CH2C(O)NH2および式:
の部分から選択され、式中、
R9は、HおよびC1~C6アルキルから選択され、
R10は、G、-C(O)-R11OH、アシル、トリチル、4-メトキシトリチル、-C(=NH)NH2、-C(O)(CH2)mNR12C(=NH)NH2および-C(O)(CH2)2NHC(O)(CH2)5NR12C(=NH)NH2から選択され、式中、
mは、1から5の整数であり、
R11は、式-(O-アルキル)y-を有し、式中、yは、3から10の整数であり、
y個のアルキル基の各々は、C2~C6アルキルから独立に選択され;
R12は、HおよびC1~C6アルキルから選択され;
R2は、H、G、アシル、トリチル、4-メトキシトリチル、C1~C6アルキル、-C(=NH)NH2および-C(O)-R23から選択され;
R3は、電子対、HおよびC1~C6アルキルから選択され、
ここで、前記ターゲティング配列は、配列番号76~3485から選択される配列を含むか、
配列番号76~3485から選択されるか、配列番号76~3485から選択される配列の少なくとも10の連続ヌクレオチドの断片であるか、または配列番号76~3485から選択される配列と少なくとも90%の配列同一性を有する変異体であり、
ここで、前記被験体は、前記被験体におけるミオスタチン活性およびミオスタチン発現の一方または両方を阻害するミオスタチン治療剤を投与され、それによりデュシェンヌ型筋ジストロフィーまたは関連障害のうちの少なくとも1つを処置する、方法。
(項目69)
ヒトジストロフィンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得るジストロフィン遺伝子における変異を有する被験体においてデュシェンヌ型筋ジストロフィーおよび関連障害を処置する方法であって、
被験体に、式(I):
を含む化合物または薬学的に許容されるその塩を投与するステップを含み、式中、
各Nuは、一緒になってターゲティング配列を形成するヌクレオ塩基であり;
Zは、8から48の整数であり;
各Yは、Oおよび-NR4から独立に選択され、式中、各R4は、H、C1~C6アルキル、アラルキル、C(=NH)NH2、C(O)(CH2)nNR5C(=NH)NH2、C(O)(CH2)2NHC(O)(CH2)5NR5C(=NH)NH2およびGから独立に選択され、式中、R5は、HおよびC1~C6アルキルから選択され、nは1から5の整数であり;
Tは、OHおよび式:
の部分から選択され、式中、
Aは、-OH、-N(R7)2R8から選択され、式中
R7は、HおよびC1~C6アルキルから独立に選択され、
R8は、電子対およびHから選択され、
R6は、OH、-N(R9)CH2C(O)NH2および式:
の部分から選択され、式中、
R9は、HおよびC1~C6アルキルから選択され;
R10は、G、C(O)-R11OH、アシル、トリチル、4メトキシトリチル、C(=NH)NH2、C(O)(CH2)mNR12C(=NH)NH2およびC(O)(CH2)2NHC(O)(CH2)5NR12C(=NH)NH2から選択され、式中、
mは、1から5の整数であり、
R11は、式-(O-アルキル)y-を有し、式中、yは、3から10の整数であり、
y個のアルキル基の各々は、C2~C6アルキルから独立に選択され;
R12は、HおよびC1~C6アルキルから選択され;
R1の各例は、
-N(R13)2R14[式中、各R13は、HおよびC1~C6アルキルから独立に選択され、R14は、電子対およびHから選択される];
式(II):
の部分[式中、
R15は、H、G、C1~C6アルキル、C(=NH)NH2、C(O)(CH2)qNR18C(=NH)NH2および-C(O)(CH2)2NHC(O)(CH2)5NR18C(=NH)NH2から選択され、式中、
R18は、HおよびC1~C6アルキルから選択され;
qは、1から5の整数であり、
R16は、電子対およびHから選択され;そして
各R17は、Hおよびメチルから独立に選択される];および
式(III):
の部分[式中、
R19は、H、C1~C6アルキル、C(=NH)NH2、-C(O)(CH2)rNR22C(=NH)NH2、-C(O)CH(NH2)(CH2)3NHC(=NH)NH2、-C(O)(CH2)2NHC(O)(CH2)5NR22C(=NH)NH2、-C(O)CH(NH2)(CH2)4NH2およびGから選択され、式中、
R22は、HおよびC1~C6アルキルから選択され;
rは、1から5の整数であり、
R20は、HおよびC1~C6アルキルから選択され;
R21は、電子対およびHから選択される]から独立に選択され;
R2は、H、G、アシル、トリチル、4-メトキシトリチル、C1~C6アルキル、-C(=NH)NH2、-C(O)-R23、-C(O)(CH2)sNR24C(=NH)NH2、-C(O)(CH2)2NHC(O)(CH2)5NR24C(=NH)NH2、-C(O)CH(NH2)(CH2)3NHC(=NH)NH2および式:
の部分から選択され、式中、
R23は、式-(O-アルキル)v-OHを有し、式中、vは、3から10の整数であり、v個のアルキル基の各々は、C2~C6アルキルから独立に選択され;
R24は、HおよびC1~C6アルキルから選択され;
sは、1から5の整数であり;
Lは、-C(O)(CH2)6C(O)-および-C(O)(CH2)2S2(CH2)2C(O)-から選択され、
各R25は、式-(CH2)2OC(O)N(R26)2を有し、式中、各R26は、式-(CH2)6NHC(=NH)NH2を有し;
R3は、電子対、HおよびC1~C6アルキルから選択され、
ここで、Gは、-C(O)(CH2)5NH-CPP、-C(O)(CH2)2NH-CPP、-C(O)(CH2)2NHC(O)(CH2)5NH-CPPおよび-C(O)CH2NH-CPPから選択される、細胞透過性ペプチド(「CPP」)およびリンカー部分であるか、またはGは、式:
を有し、式中、CPPは、Gの最大で1つの例が存在するという条件で、CPPのカルボキシ末端において、アミド結合により、リンカー部分に結合しており、
ここで、前記ターゲティング配列は、ヒトジストロフィンプレmRNAのエクソンを含む標的領域内の10またはこれを超える連続ヌクレオチドと相補的であり、
ここで、前記被験体は、前記被験体におけるミオスタチン活性およびミオスタチン発現の一方または両方を阻害するミオスタチン治療剤を投与され、それによりデュシェンヌ型筋ジストロフィーまたは関連障害のうちの少なくとも1つを処置する、方法。
(項目70)
各Nuが、独立に、アデニン、グアニン、チミン、ウラシル、シトシン、イノシン、ヒポキサンチン、2,6-ジアミノプリン、5-メチルシトシン、C5-プロピニル修飾ピリミジンまたは10-(9-(アミノエトキシ)フェノキサジニル)である、項目69に記載の方法。
(項目71)
前記ターゲティング配列が、配列番号16~75から選択される配列を含むか、配列番号16~75から選択されるターゲティング配列の少なくとも10の連続ヌクレオチドの断片であるか、または配列番号16~75から選択されるターゲティング配列と少なくとも90%の配列同一性を有する変異体である、項目69に記載の方法。
(項目72)
i)Yが、Oであり、R2が、HもしくはGから選択され、R3が、電子対もしくはHから選択されるか;
ii)R2が、Gであり、前記CPPが、配列番号3486~3501から選択される配列を有するか;
iii)各R1が、-N(CH3)2であるか;
iv)少なくとも1つのR1が、
から選択されるか、または
v)R1基の50~90%が、-N(CH3)2である、項目69に記載の方法。
(項目73)
Tが、式:
を有し、式中、Aが、-N(CH3)2であり、R6が式:
を有し、式中、R10が、-C(O)R11OHである、項目69に記載の方法。
(項目74)
各Yが、Oであり、Tが、
から選択される、項目69に記載の方法。
(項目75)
Tが、式:
を有する、項目69に記載の方法。
(項目76)
被験体においてデュシェンヌ型筋ジストロフィーおよび関連障害を処置する方法であって、
被験体に、式(VI):
を含む化合物または薬学的に許容されるその塩を投与するステップを含み、式中、
各Nuは、一緒になってターゲティング配列を形成するヌクレオ塩基であり;
Zは、8から48の整数であり;
各Yは、Oおよび-NR4から独立に選択され、式中、R4は、H、C1~C6アルキル、アラルキル、-C(=NH)NH2、-C(O)(CH2)nNR5C(=NH)NH2、-C(O)(CH2)2NHC(O)(CH2)5NR5C(=NH)NH2およびGから独立に選択され、式中、R5は、HおよびC1~C6アルキルから選択され、nは、1から5の整数であり;
Tは、OHおよび式:
の部分から選択され、式中、
Aは、-OHおよび-N(R7)2R8から選択され、式中、
各R7は、HおよびC1~C6アルキルから独立に選択され、
R8は、電子対およびHから選択され、
R6は、OH、-N(R9)CH2C(O)NH2および式:
の部分から選択され、式中、
R9は、HおよびC1~C6アルキルから選択され;
R10は、G、-C(O)-R11OH、アシル、トリチル、4-メトキシトリチル、-C(=NH)NH2、-C(O)(CH2)mNR12C(=NH)NH2および-C(O)(CH2)2NHC(O)(CH2)5NR12C(=NH)NH2から選択され、式中、
mは、1から5の整数であり、
R11は、式-(O-アルキル)y-を有し、式中、yは、3から10の整数であり、
y個のアルキル基の各々は、C2~C6アルキルから独立に選択され;
R12は、HおよびC1~C6アルキルから選択され;
R2は、H、G、アシル、トリチル、4-メトキシトリチル、C1~C6アルキル、-C(=NH)NH2および-C(O)-R23から選択され;
R3は、電子対、HおよびC1~C6アルキルから選択され、
ここで、前記ターゲティング配列は、配列番号16~75から選択される配列を含むか、配列番号16~75から選択されるか、配列番号16~75から選択される配列の少なくとも10の連続ヌクレオチドの断片であるか、または配列番号16~75から選択される配列と少なくとも90%の配列同一性を有する変異体であり、
ここで、前記被験体は、前記被験体の筋細胞内で機能的なジストロフィンタンパク質の発現を増加させるジストロフィン治療剤を投与され、それによりデュシェンヌ型筋ジストロフィーまたは関連障害のうちの少なくとも1つを処置する、方法。
(項目77)
12~40サブユニットのアンチセンスオリゴマー化合物と、薬学的に許容される担体とを含むミオスタチン関連医薬組成物であって、前記化合物が、
(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットと;
ヒトミオスタチンプレmRNAのエクソンを含む標的領域内の12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列と
を含むミオスタチン関連組成物と組み合わせた、
17~40サブユニットのアンチセンスオリゴマー化合物と、薬学的に許容される担体とを含むジストロフィン関連医薬組成物であって、前記化合物が、
(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または、(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットと;
ヒトジストロフィンプレmRNAのエクソンを含む標的領域内の10またはこれを超える連続ヌクレオチドと相補的なターゲティング配列と
を含むジストロフィン関連医薬組成物。
(項目78)
前記ジストロフィン関連組成物と前記ミオスタチン関連組成物とが、同じ医薬組成物として提供される、77に記載の組成物。
(項目79)
ヒトミオスタチンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得る遺伝子変異を有する被験体においてミオスタチン発現をモジュレートするための方法であって、
前記被験体に、12~40サブユニットを含み、ヒトミオスタチンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップであって、
前記オリゴマーが、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含む、ステップと、
ミオスタチンプレmRNA転写物内の標的領域に前記アンチセンスオリゴマーを結合させるステップと、
前記標的領域のヒトミオスタチンmRNA転写物への転写を阻害するステップとを含み、
前記被験体が、前記被験体におけるジストロフィン発現を増加させるジストロフィン治療剤を投与されている、方法。
(項目80)
ヒトミオスタチンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得る遺伝子変異を有する被験体においてエクソン2の発現を減少させるための方法であって、
前記被験体に、12~40サブユニットを含み、ヒトミオスタチンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップと、ミオスタチンmRNA転写物内のエクソン2の転写を阻害するステップとを含み、
前記被験体が、前記被験体におけるジストロフィン発現を増加させるジストロフィン治療剤を投与されている、方法。
(項目81)
ミオスタチンmRNA転写物内のエクソン2の発現が、約5%、6%、7%、8%、9%、10%、11%、12%、13%、14%、15%、16%、17%、18%、19%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%または100%減少する、項目80に記載の方法。
(項目82)
ヒトミオスタチンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得るジストロフィン遺伝子における変異を有する被験体の筋細胞または組織における機能的なミオスタチンタンパク質の蓄積を減少させるための方法であって、
前記被験体に、12~40サブユニットを含み、ヒトミオスタチンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップと、
ミオスタチンmRNA転写物内のエクソン2の転写を阻害するステップとを含み、
前記被験体が、前記被験体におけるジストロフィン発現を増加させるジストロフィン治療剤を投与されている、方法。
(項目83)
デュシェンヌ型筋ジストロフィーおよび関連障害を処置するための医薬であって、
(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含み;ヒトミオスタチンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、12~40サブユニットを含むアンチセンスオリゴマー化合物と;
機能的なジストロフィンタンパク質の発現を増加させるジストロフィン治療剤とを含む医薬。
(項目84)
ヒトミオスタチンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得るジストロフィン遺伝子における変異を有する被験体においてデュシェンヌ型筋ジストロフィーおよび関連障害の進行を阻害するための方法であって、
前記被験体に、12~40サブユニットを含み、ヒトミオスタチンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップと、ミオスタチンmRNA転写物内のエクソン2の転写を阻害するステップとを含み、
前記被験体が、前記被験体におけるジストロフィン発現を増加させるジストロフィン治療剤を投与され、それによりデュシェンヌ型筋ジストロフィーの進行を阻害する、方法。
(項目85)
デュシェンヌ型筋ジストロフィーおよび関連障害を有する被験体において機能的なミオスタチンタンパク質の蓄積を減少させる方法であって、
前記被験体に、12~40サブユニットを含み、ヒトミオスタチンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップと、
ミオスタチンmRNA転写物内のエクソン2の転写を阻害するステップとを含み、
前記被験体における機能的なミオスタチンタンパク質の蓄積が減少し、
前記被験体が、前記被験体の筋細胞内で機能的なジストロフィンタンパク質の発現を増加させるジストロフィン治療剤を投与されている、方法。
(項目86)
そのような処置を必要とする被験体においてデュシェンヌ型筋ジストロフィーおよび関連障害を処置するための方法であって、
前記被験体において少なくとも約200~400nMのアンチセンスオリゴマーのピークの血中濃度を得るための有効量でアンチセンスオリゴマーを投与するステップを含む方法。
(項目87)
ヒトミオスタチンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得るジストロフィン遺伝子における変異を有する被験体において骨格筋量不足を処置する方法であって、
(a)前記被験体におけるミオスタチンタンパク質の血液中または組織中レベルを測定するステップと、
(b)前記被験体に、12~40サブユニットを含み、ヒトミオスタチンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップと、
(c)ミオスタチンmRNA転写物内のエクソン2の転写を阻害するステップと、
(d)選択した時間以後、前記被験体におけるミオスタチンタンパク質レベルを測定するステップと、
(e)(d)で測定された前記レベルを使用して前記の投与を反復するステップであって、投与されるアンチセンスオリゴマーの量の用量または投薬スケジュールを調整するステップとを含み、前記被験体におけるミオスタチンタンパク質の前記レベルが、前記アンチセンスオリゴマーの投与後に低下し、
前記被験体が、前記被験体の筋細胞において機能的なジストロフィン発現タンパク質の発現を増加させるジストロフィン治療剤を投与されている、方法。
(項目88)
ジストロフィンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得るジストロフィン遺伝子における変異を有する被験体においてデュシェンヌ型筋ジストロフィーおよび関連障害の進行を阻害する方法であって、
前記被験体に、17~40サブユニットを含み、ヒトジストロフィンプレmRNAのエクソンを含む標的領域内の12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップを含み、前記アンチセンスオリゴマーが、前記エクソンのスキッピングを誘導し、
前記オリゴマーが、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含み、
前記被験体が、前記被験体におけるミオスタチンの活性および発現のうちの一方または両方を阻害するミオスタチン治療剤を投与され、それによりデュシェンヌ型筋ジストロフィーまたは関連障害のうちの少なくとも1つの進行を阻害する、方法。
(項目89)
デュシェンヌ型筋ジストロフィーの進行を阻害する方法であって、
被験体に、12~40サブユニットを含み、ヒトミオスタチンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップを含み、
前記オリゴマーが、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含み、
前記被験体が、前記被験体の筋細胞において機能的なジストロフィンタンパク質の発現を増加させるジストロフィン治療剤を投与され、それによりデュシェンヌ型筋ジストロフィーの進行を阻害する、方法。
(項目90)
前記アンチセンスオリゴマーの3’末端または5’末端にコンジュゲートするアルギニンに富むペプチド配列をさらに含み、前記アルギニンに富むペプチド配列が、配列番号3486~3501から選択される配列を含む、前出の項目のいずれか一項に記載のアンチセンスオリゴマー。
(項目91)
R2が、Gであり、前記CPPが、配列番号3486~3501から選択される配列を含む、項目60から75のいずれか一項に記載の方法。
(項目92)
アンチセンスオリゴマーの3’末端にコンジュゲートするアルギニンに富むペプチド配列をさらに含み、前記アルギニンに富むペプチド配列が、配列番号3486~3501から選択される配列を含む、項目83に記載の医薬。
(項目93)
17~40サブユニットを含み、ヒトジストロフィンプレmRNAのエクソンを含む標的領域内の12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含むアンチセンスオリゴマーであって、
(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含む、ジストロフィンを標的とする前記オリゴマーと;
12~40サブユニットを含み、ヒトミオスタチンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含むアンチセンスオリゴマーであって、
(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含む、ミオスタチンを標的とする前記オリゴマーとを含む組成物。
(項目94)
ヒトジストロフィンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得る遺伝子変異を有する被験体においてジストロフィン発現をモジュレートするための方法であって、
前記被験体に、17~40サブユニットを含み、ヒトジストロフィンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップを含み、
前記オリゴマーが、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含み、
前記被験体が、前記被験体におけるミオスタチン活性およびミオスタチン発現の一方または両方を阻害するミオスタチン治療剤を投与されている、方法。
(項目95)
ヒトミオスタチンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得る遺伝子変異を有する被験体においてミオスタチン発現をモジュレートするための方法であって、
前記被験体に、12~40サブユニットを含み、ヒトミオスタチンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップを含み、
前記オリゴマーが、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含み、
前記被験体が、前記被験体の筋細胞内で機能的なジストロフィンタンパク質の発現を増加させるジストロフィン治療剤を投与されている、方法。
(項目96)
前記アンチセンスオリゴマー、ジストロフィン治療剤またはミオスタチン治療剤の少なくとも1つが、前記被験体に全身投与される、項目1から95のいずれかに記載の方法。
(項目97)
前記被験体が、ヒトである、項目96に記載の方法。
(項目98)
前記被験体が、7歳またはこれを超える、項目97に記載の方法。
(項目99)
アンチセンスオリゴマーまたはジストロフィン治療剤が、配列番号927を含まない、項目98に記載の方法。
特定の実施形態では、例えば、以下が提供される:
(項目1)
ジストロフィンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得るジストロフィン遺伝子における変異を有する、デュシェンヌ型筋ジストロフィーおよび関連障害を有する被験体を処置する方法であって、
前記被験体に、17~40サブユニットを含み、ヒトジストロフィンプレmRNAのエクソンを含む標的領域内の12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップを含み、前記アンチセンスオリゴマーが、前記エクソンのスキッピングを誘導し、
前記オリゴマーが、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含み、
前記被験体が、前記被験体におけるミオスタチン活性およびミオスタチン発現の一方または両方を阻害するミオスタチン治療剤を投与され、それによりデュシェンヌ型筋ジストロフィーまたは関連障害のうちの少なくとも1つを処置する、方法。
(項目2)
前記エクソンが、エクソン7、エクソン8、エクソン9、エクソン19、エクソン23、エクソン44、エクソン45、エクソン50、エクソン51、エクソン52、エクソン53またはエクソン55から選択される、項目1に記載の方法。
(項目3)
前記エクソンがエクソン23を含む、項目2に記載の方法。
(項目4)
前記エクソンがエクソン45を含む、項目2に記載の方法。
(項目5)
前記エクソンがエクソン51を含む、項目2に記載の方法。
(項目6)
前記エクソンがエクソン53を含む、項目2に記載の方法。
(項目7)
前記エクソンが、エクソン8、エクソン44、エクソン50、エクソン52またはエクソン55を含む、項目2に記載の方法。
(項目8)
前記アンチセンスオリゴマーが、20~30サブユニットを含む、項目1に記載の方法。
(項目9)
前記アンチセンスオリゴマーが、配列番号76~配列番号3485から選択される配列を含む、項目1に記載の方法。
(項目10)
前記アンチセンスオリゴマーが、エテプリルセン(eteplirsen)である、項目9に記載の方法。
(項目11)
前記ターゲティング配列が、前記標的領域内の少なくとも15の連続ヌクレオチドと相補的である、項目1に記載の方法。
(項目12)
前記ターゲティング配列が、前記標的領域内の少なくとも17の連続ヌクレオチドと相補的である、項目11に記載の方法。
(項目13)
前記ターゲティング配列が、前記標的領域と100%相補的である、項目12に記載の方法。
(項目14)
前記ミオスタチン治療剤が、タンパク質または核酸のうちの1つまたは複数から選択される、項目1に記載の方法。
(項目15)
前記タンパク質が、抗ミオスタチン抗体である、項目14に記載の方法。
(項目16)
前記タンパク質が、可溶性受容体である、項目14に記載の方法。
(項目17)
可溶性受容体が、ACVR2である、項目14に記載の方法。
(項目18)
前記核酸が、アンチセンスオリゴマーまたはsiRNAのうちの少なくとも1つである、項目14に記載の方法。
(項目19)
前記アンチセンスオリゴマーが、12~40サブユニットを含み、ミオスタチンプレmRNAの標的領域内の12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含み、
前記オリゴマーが、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含む、項目18に記載の方法。
(項目20)
前記アンチセンスオリゴマーが、20~30サブユニットを含む、項目19に記載の方法。
(項目21)
前記ターゲティング配列が、前記標的領域内の少なくとも15の連続ヌクレオチドと相補的である、項目19に記載の方法。
(項目22)
前記ターゲティング配列が、前記標的領域内の少なくとも17の連続ヌクレオチドと相補的である、項目19に記載の方法。
(項目23)
前記ターゲティング配列が、前記標的領域と100%相補的である、項目19に記載の方法。
(項目24)
前記標的領域が、配列番号1を含む、項目19に記載の方法。
(項目25)
前記エクソンが、エクソン2を含む、項目19に記載の方法。
(項目26)
前記標的領域が、(i)少なくとも1つのヌクレオチドが、イントロン1/エクソン2およびエクソン2/イントロン2に伴うスプライス接合部にわたるヌクレオチド配列、または、(ii)ヌクレオチドが、イントロン1/エクソン2およびエクソン2/イントロン2に伴うスプライス接合部にわたらないヌクレオチド配列から選択される項目19に記載の方法。
(項目27)
前記スプライス接合部が、スプライスアクセプター部位またはスプライスドナー部位を含む配列から選択される、項目26に記載の方法。
(項目28)
前記スプライスアクセプター部位が、配列番号2の内部に存在し、前記スプライスドナー部位が配列番号3の内部に存在する、項目27に記載の方法。
(項目29)
前記(i)のヌクレオチドが、配列番号16~43から選択される、項目26に記載の方法。
(項目30)
前記(ii)のヌクレオチドが、配列番号44~70から選択される、項目26に記載の方法。
(項目31)
前記被験体が、7歳またはこれを超える、項目1に記載の方法。
(項目32)
デュシェンヌ型筋ジストロフィーおよび関連障害を処置する方法であって、
被験体に、12~40サブユニットを含み、ヒトミオスタチンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップを含み、
前記オリゴマーが、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含み、
前記被験体が、前記被験体の筋細胞内で機能的なジストロフィンタンパク質の発現を増加させるジストロフィン治療剤を投与され、それによりデュシェンヌ型筋ジストロフィーまたは関連障害のうちの少なくとも1つを処置する、方法。
(項目33)
前記被験体が、ヒトミオスタチンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得るジストロフィン遺伝子における変異を有する、項目32に記載の方法。
(項目34)
前記アンチセンスオリゴマーが、20~30サブユニットを含む、項目32に記載の方法。
(項目35)
前記ターゲティング配列が、標的領域内の少なくとも15の連続ヌクレオチドと相補的である、項目32に記載の方法。
(項目36)
前記ターゲティング配列が、標的領域内の少なくとも17の連続ヌクレオチドと相補的である、項目32に記載の方法。
(項目37)
前記アンチセンスオリゴマーが、標的領域と100%相補的である、項目32に記載の方法。
(項目38)
前記標的領域が、配列番号1を含む、項目32に記載の方法。
(項目39)
前記エクソンが、エクソン2を含む、項目32に記載の方法。
(項目40)
前記標的領域が、(i)少なくとも1つのヌクレオチドがイントロン1/エクソン2およびエクソン2/イントロン2に伴うスプライス接合部にわたるヌクレオチド配列、または、(ii)ヌクレオチドがイントロン1/エクソン2およびエクソン2/イントロン2に伴うスプライス接合部にわたらないヌクレオチド配列から選択される、項目32に記載の方法。
(項目41)
前記スプライス接合部が、スプライスアクセプター部位またはスプライスドナー部位を含む配列から選択される、項目40に記載の方法。
(項目42)
前記スプライスアクセプター部位が、配列番号2の内部に存在し、前記スプライスドナー部位が、配列番号3の内部に存在する、項目41に記載の方法。
(項目43)
前記(i)のヌクレオチドが、配列番号16~43から選択される、項目41に記載の方法。
(項目44)
前記(ii)のヌクレオチドが、配列番号44~70から選択される、項目41に記載の方法。
(項目45)
前記ジストロフィン治療剤が、タンパク質または核酸のうちの1つまたは複数から選択される、項目32に記載の方法。
(項目46)
前記核酸が、アンチセンスオリゴマーである、項目45に記載の方法。
(項目47)
前記アンチセンスオリゴマーが、20~50サブユニットを含み、ヒトジストロフィンプレmRNAのエクソンを含む標的領域内の10またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含み、
前記オリゴマーが、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含む、項目46に記載の方法。
(項目48)
前記エクソンが、エクソン7、エクソン8、エクソン9、エクソン19、エクソン23、エクソン44、エクソン45、エクソン50、エクソン51、エクソン52、エクソン53またはエクソン55から選択される、項目47に記載の方法。
(項目49)
前記エクソンが、エクソン23を含む、項目48に記載の方法。
(項目50)
前記エクソンが、エクソン45を含む、項目48に記載の方法。
(項目51)
前記エクソンが、エクソン51を含む、項目48に記載の方法。
(項目52)
前記エクソンが、エクソン53を含む、項目48に記載の方法。
(項目53)
前記エクソンが、エクソン8、エクソン44、エクソン50、エクソン52またはエクソン55を含む、項目48に記載の方法。
(項目54)
前記アンチセンスオリゴマーが、20~30サブユニットを含む、項目47に記載の方法。
(項目55)
前記アンチセンスオリゴマーが、配列番号76~配列番号3485から選択される配列を含む、項目47に記載の方法。
(項目56)
前記アンチセンスオリゴマーが、エテプリルセンである、項目55に記載の方法。
(項目57)
前記ターゲティング配列が、標的領域内の少なくとも15の連続ヌクレオチドと相補的である、項目46に記載の方法。
(項目58)
前記ターゲティング配列が、標的領域内の少なくとも17の連続ヌクレオチドと相補的である、項目46に記載の方法。
(項目59)
前記ターゲティング配列が、標的領域と100%相補的である、項目46に記載の方法。
(項目60)
ジストロフィンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得るジストロフィン遺伝子における変異を有する被験体においてデュシェンヌ型筋ジストロフィーおよび関連障害を処置する方法であって、
被験体に、式(I):
各Nuは、一緒になってターゲティング配列を形成するヌクレオ塩基であり;
Zは、8から48の整数であり;
各Yは、Oおよび-NR4から独立に選択され、式中、各R4は、H、C1~C6アルキル、アラルキル、C(=NH)NH2、C(O)(CH2)nNR5C(=NH)NH2、C(O)(CH2)2NHC(O)(CH2)5NR5C(=NH)NH2およびGから独立に選択され、式中、R5は、HおよびC1~C6アルキルから選択され、nは、1から5の整数であり;
Tは、OHおよび式:
の部分か選択され、式中、
Aは、-OH、-N(R7)2R8から選択され、式中、
各R7は、HおよびC1~C6アルキルから独立に選択され、
R8は、電子対およびHから選択され、そして
R6は、OH、-N(R9)CH2C(O)NH2および式:
R9は、HおよびC1~C6アルキルから選択され、
R10は、G、C(O)-R11OH、アシル、トリチル、4メトキシトリチル、C(=NH)NH2、C(O)(CH2)mNR12C(=NH)NH2およびC(O)(CH2)2NHC(O)(CH2)5NR12C(=NH)NH2から選択され、式中、
mは、1から5の整数であり、
R11は、式-(O-アルキル)y-を有し、式中、yは、3から10の整数であり、
y個のアルキル基の各々は、C2~C6アルキルから独立に選択され;
R12は、HおよびC1~C6アルキルから選択され;
R1の各例は、
-N(R13)2R14[式中、各R13は、HおよびC1~C6アルキルから独立に選択され、そしてR14は、電子対およびHから選択される];
式(II):
の部分[式中、
R15は、H、G、C1~C6アルキル、C(=NH)NH2、C(O)(CH2)qNR18C(=NH)NH2および-C(O)(CH2)2NHC(O)(CH2)5NR18C(=NH)NH2から選択され、式中、
R18は、HおよびC1~C6アルキルから選択され;
qは、1から5の整数であり、
R16は、電子対およびHから選択され;
各R17は、Hおよびメチルから独立に選択される];および
式(III):
の部分[式中、
R19は、H、C1~C6アルキル、C(=NH)NH2、-C(O)(CH2)rNR22C(=NH)NH2、-C(O)CH(NH2)(CH2)3NHC(=NH)NH2、-C(O)(CH2)2NHC(O)(CH2)5NR22C(=NH)NH2、-C(O)CH(NH2)(CH2)4NH2およびGから選択され、式中、
R22は、HおよびC1~C6アルキルから選択され;
rは、1から5の整数であり、
R20は、HおよびC1~C6アルキルから選択され;
R21は、電子対およびHから選択される]
から独立に選択され;
R2は、H、G、アシル、トリチル、4-メトキシトリチル、C1~C6アルキル、-C(=NH)NH2、-C(O)-R23、-C(O)(CH2)sNR24C(=NH)NH2、-C(O)(CH2)2NHC(O)(CH2)5NR24C(=NH)NH2、-C(O)CH(NH2)(CH2)3NHC(=NH)NH2および式:
の部分から選択され、式中、
R23は、式-(O-アルキル)v-OHを有し、式中、vは、3から10の整数であり、v個のアルキル基の各々は、C2~C6アルキルから独立に選択され;
R24は、HおよびC1~C6アルキルから選択され;
sは、1から5の整数であり;
Lは、-C(O)(CH2)6C(O)-および-C(O)(CH2)2S2(CH2)2C(O)-から選択され;
各R25は、式-(CH2)2OC(O)N(R26)2を有し、式中、各R26は、式-(CH2)6NHC(=NH)NH2を有し;
R3は、電子対、HおよびC1~C6アルキルから選択され、
ここで、Gは、-C(O)(CH2)5NH-CPP、-C(O)(CH2)2NH-CPP、-C(O)(CH2)2NHC(O)(CH2)5NH-CPPおよび-C(O)CH2NH-CPPから選択される細胞透過性ペプチド(「CPP」)およびリンカー部分であるか、またはGは、式:
を有し、式中、CPPは、Gの最大で1つの例が存在するという条件で、CPPのカルボキシ末端において、アミド結合により、リンカー部分に結合しており、
ここで、前記ターゲティング配列は、ヒトジストロフィンプレmRNAのエクソンを含む標的領域内の12またはこれを超える連続ヌクレオチドと相補的であり、
ここで、前記被験体は、前記被験体におけるミオスタチン活性およびミオスタチン発現の一方または両方を阻害するミオスタチン治療剤を投与され、それによりデュシェンヌ型筋ジストロフィーまたは関連障害のうちの少なくとも1つを処置する、方法。
(項目61)
各Nuが、独立に、アデニン、グアニン、チミン、ウラシル、シトシン、イノシン、ヒポキサンチン、2,6-ジアミノプリン、5-メチルシトシン、C5-プロピニル修飾ピリミジンまたは10-(9-(アミノエトキシ)フェノキサジニル)である、項目60に記載の方法。
(項目62)
前記標的領域が、(i)少なくとも1つのヌクレオチドが前記エクソンに伴うスプライス接合部にわたるヌクレオチド配列;または(ii)ヌクレオチドが前記エクソン接合部に伴うスプライス接合部にわたらないヌクレオチド配列から選択される、項目60に記
載の方法。
(項目63)
前記ターゲティング配列が、配列番号76~3485から選択される配列を含むか、配列番号76~3485から選択されるターゲティング配列の少なくとも10の連続ヌクレオチドの断片であるか、または配列番号76~3485から選択されるターゲティング配列と少なくとも90%の配列同一性を有する変異体である、項目60に記載の方法。
(項目64)
i)Yが、Oであり、R2が、HもしくはGから選択され、R3が、電子対もしくはHから選択されるか;
ii)R2が、Gであり、式中、前記CPPが配列番号3486~3501から選択される配列を有するか;
iii)各R1が、-N(CH3)2であるか;
iv)少なくとも1つのR1が、
から選択されるか;または
v)R1基の50~90%が、-N(CH3)2である、項目60に記載の方法。
(項目65)
Tが、式:
を有し、式中、Aは、-N(CH3)2であり、R6は、式:
を有し、式中、R10は、-C(O)R11OHである、項目60に記載の方法。
(項目66)
各Yが、Oであり、Tが、
から選択される、項目60に記載の方法。
(項目67)
Tが、式:
を有する、項目60に記載の方法。
(項目68)
ジストロフィンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得るジストロフィン遺伝子における変異を有する被験体においてデュシェンヌ型筋ジストロフィーおよび関連障害を処置する方法であって、
被験体に、式(VI):
を含む化合物または薬学的に許容されるその塩を投与するステップを含み、式中、
各Nuは、一緒になってターゲティング配列を形成するヌクレオ塩基であり;
Zは、8から48の整数であり;
各Yは、Oおよび-NR4から独立に選択され、式中、各R4は、H、C1~C6アルキル、アラルキル、-C(=NH)NH2、-C(O)(CH2)nNR5C(=NH)NH2、-C(O)(CH2)2NHC(O)(CH2)5NR5C(=NH)NH2およびGから独立に選択され、式中、R5は、HおよびC1~C6アルキルから選択され、nは、1から5の整数であり;
Tは、OHおよび式:
の部分から選択され、式中、
Aは、-OHおよび-N(R7)2R8から選択され、式中
各R7は、HおよびC1~C6アルキルから独立に選択され、
R8は、電子対およびHから選択され、
R6は、OH、-N(R9)CH2C(O)NH2および式:
の部分から選択され、式中、
R9は、HおよびC1~C6アルキルから選択され、
R10は、G、-C(O)-R11OH、アシル、トリチル、4-メトキシトリチル、-C(=NH)NH2、-C(O)(CH2)mNR12C(=NH)NH2および-C(O)(CH2)2NHC(O)(CH2)5NR12C(=NH)NH2から選択され、式中、
mは、1から5の整数であり、
R11は、式-(O-アルキル)y-を有し、式中、yは、3から10の整数であり、
y個のアルキル基の各々は、C2~C6アルキルから独立に選択され;
R12は、HおよびC1~C6アルキルから選択され;
R2は、H、G、アシル、トリチル、4-メトキシトリチル、C1~C6アルキル、-C(=NH)NH2および-C(O)-R23から選択され;
R3は、電子対、HおよびC1~C6アルキルから選択され、
ここで、前記ターゲティング配列は、配列番号76~3485から選択される配列を含むか、
配列番号76~3485から選択されるか、配列番号76~3485から選択される配列の少なくとも10の連続ヌクレオチドの断片であるか、または配列番号76~3485から選択される配列と少なくとも90%の配列同一性を有する変異体であり、
ここで、前記被験体は、前記被験体におけるミオスタチン活性およびミオスタチン発現の一方または両方を阻害するミオスタチン治療剤を投与され、それによりデュシェンヌ型筋ジストロフィーまたは関連障害のうちの少なくとも1つを処置する、方法。
(項目69)
ヒトジストロフィンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得るジストロフィン遺伝子における変異を有する被験体においてデュシェンヌ型筋ジストロフィーおよび関連障害を処置する方法であって、
被験体に、式(I):
を含む化合物または薬学的に許容されるその塩を投与するステップを含み、式中、
各Nuは、一緒になってターゲティング配列を形成するヌクレオ塩基であり;
Zは、8から48の整数であり;
各Yは、Oおよび-NR4から独立に選択され、式中、各R4は、H、C1~C6アルキル、アラルキル、C(=NH)NH2、C(O)(CH2)nNR5C(=NH)NH2、C(O)(CH2)2NHC(O)(CH2)5NR5C(=NH)NH2およびGから独立に選択され、式中、R5は、HおよびC1~C6アルキルから選択され、nは1から5の整数であり;
Tは、OHおよび式:
の部分から選択され、式中、
Aは、-OH、-N(R7)2R8から選択され、式中
R7は、HおよびC1~C6アルキルから独立に選択され、
R8は、電子対およびHから選択され、
R6は、OH、-N(R9)CH2C(O)NH2および式:
の部分から選択され、式中、
R9は、HおよびC1~C6アルキルから選択され;
R10は、G、C(O)-R11OH、アシル、トリチル、4メトキシトリチル、C(=NH)NH2、C(O)(CH2)mNR12C(=NH)NH2およびC(O)(CH2)2NHC(O)(CH2)5NR12C(=NH)NH2から選択され、式中、
mは、1から5の整数であり、
R11は、式-(O-アルキル)y-を有し、式中、yは、3から10の整数であり、
y個のアルキル基の各々は、C2~C6アルキルから独立に選択され;
R12は、HおよびC1~C6アルキルから選択され;
R1の各例は、
-N(R13)2R14[式中、各R13は、HおよびC1~C6アルキルから独立に選択され、R14は、電子対およびHから選択される];
式(II):
の部分[式中、
R15は、H、G、C1~C6アルキル、C(=NH)NH2、C(O)(CH2)qNR18C(=NH)NH2および-C(O)(CH2)2NHC(O)(CH2)5NR18C(=NH)NH2から選択され、式中、
R18は、HおよびC1~C6アルキルから選択され;
qは、1から5の整数であり、
R16は、電子対およびHから選択され;そして
各R17は、Hおよびメチルから独立に選択される];および
式(III):
の部分[式中、
R19は、H、C1~C6アルキル、C(=NH)NH2、-C(O)(CH2)rNR22C(=NH)NH2、-C(O)CH(NH2)(CH2)3NHC(=NH)NH2、-C(O)(CH2)2NHC(O)(CH2)5NR22C(=NH)NH2、-C(O)CH(NH2)(CH2)4NH2およびGから選択され、式中、
R22は、HおよびC1~C6アルキルから選択され;
rは、1から5の整数であり、
R20は、HおよびC1~C6アルキルから選択され;
R21は、電子対およびHから選択される]から独立に選択され;
R2は、H、G、アシル、トリチル、4-メトキシトリチル、C1~C6アルキル、-C(=NH)NH2、-C(O)-R23、-C(O)(CH2)sNR24C(=NH)NH2、-C(O)(CH2)2NHC(O)(CH2)5NR24C(=NH)NH2、-C(O)CH(NH2)(CH2)3NHC(=NH)NH2および式:
の部分から選択され、式中、
R23は、式-(O-アルキル)v-OHを有し、式中、vは、3から10の整数であり、v個のアルキル基の各々は、C2~C6アルキルから独立に選択され;
R24は、HおよびC1~C6アルキルから選択され;
sは、1から5の整数であり;
Lは、-C(O)(CH2)6C(O)-および-C(O)(CH2)2S2(CH2)2C(O)-から選択され、
各R25は、式-(CH2)2OC(O)N(R26)2を有し、式中、各R26は、式-(CH2)6NHC(=NH)NH2を有し;
R3は、電子対、HおよびC1~C6アルキルから選択され、
ここで、Gは、-C(O)(CH2)5NH-CPP、-C(O)(CH2)2NH-CPP、-C(O)(CH2)2NHC(O)(CH2)5NH-CPPおよび-C(O)CH2NH-CPPから選択される、細胞透過性ペプチド(「CPP」)およびリンカー部分であるか、またはGは、式:
を有し、式中、CPPは、Gの最大で1つの例が存在するという条件で、CPPのカルボキシ末端において、アミド結合により、リンカー部分に結合しており、
ここで、前記ターゲティング配列は、ヒトジストロフィンプレmRNAのエクソンを含む標的領域内の10またはこれを超える連続ヌクレオチドと相補的であり、
ここで、前記被験体は、前記被験体におけるミオスタチン活性およびミオスタチン発現の一方または両方を阻害するミオスタチン治療剤を投与され、それによりデュシェンヌ型筋ジストロフィーまたは関連障害のうちの少なくとも1つを処置する、方法。
(項目70)
各Nuが、独立に、アデニン、グアニン、チミン、ウラシル、シトシン、イノシン、ヒポキサンチン、2,6-ジアミノプリン、5-メチルシトシン、C5-プロピニル修飾ピリミジンまたは10-(9-(アミノエトキシ)フェノキサジニル)である、項目69に記載の方法。
(項目71)
前記ターゲティング配列が、配列番号16~75から選択される配列を含むか、配列番号16~75から選択されるターゲティング配列の少なくとも10の連続ヌクレオチドの断片であるか、または配列番号16~75から選択されるターゲティング配列と少なくとも90%の配列同一性を有する変異体である、項目69に記載の方法。
(項目72)
i)Yが、Oであり、R2が、HもしくはGから選択され、R3が、電子対もしくはHから選択されるか;
ii)R2が、Gであり、前記CPPが、配列番号3486~3501から選択される配列を有するか;
iii)各R1が、-N(CH3)2であるか;
iv)少なくとも1つのR1が、
v)R1基の50~90%が、-N(CH3)2である、項目69に記載の方法。
(項目73)
Tが、式:
を有し、式中、Aが、-N(CH3)2であり、R6が式:
を有し、式中、R10が、-C(O)R11OHである、項目69に記載の方法。
(項目74)
各Yが、Oであり、Tが、
から選択される、項目69に記載の方法。
(項目75)
Tが、式:
を有する、項目69に記載の方法。
(項目76)
被験体においてデュシェンヌ型筋ジストロフィーおよび関連障害を処置する方法であって、
被験体に、式(VI):
を含む化合物または薬学的に許容されるその塩を投与するステップを含み、式中、
各Nuは、一緒になってターゲティング配列を形成するヌクレオ塩基であり;
Zは、8から48の整数であり;
各Yは、Oおよび-NR4から独立に選択され、式中、R4は、H、C1~C6アルキル、アラルキル、-C(=NH)NH2、-C(O)(CH2)nNR5C(=NH)NH2、-C(O)(CH2)2NHC(O)(CH2)5NR5C(=NH)NH2およびGから独立に選択され、式中、R5は、HおよびC1~C6アルキルから選択され、nは、1から5の整数であり;
Tは、OHおよび式:
の部分から選択され、式中、
Aは、-OHおよび-N(R7)2R8から選択され、式中、
各R7は、HおよびC1~C6アルキルから独立に選択され、
R8は、電子対およびHから選択され、
R6は、OH、-N(R9)CH2C(O)NH2および式:
の部分から選択され、式中、
R9は、HおよびC1~C6アルキルから選択され;
R10は、G、-C(O)-R11OH、アシル、トリチル、4-メトキシトリチル、-C(=NH)NH2、-C(O)(CH2)mNR12C(=NH)NH2および-C(O)(CH2)2NHC(O)(CH2)5NR12C(=NH)NH2から選択され、式中、
mは、1から5の整数であり、
R11は、式-(O-アルキル)y-を有し、式中、yは、3から10の整数であり、
y個のアルキル基の各々は、C2~C6アルキルから独立に選択され;
R12は、HおよびC1~C6アルキルから選択され;
R2は、H、G、アシル、トリチル、4-メトキシトリチル、C1~C6アルキル、-C(=NH)NH2および-C(O)-R23から選択され;
R3は、電子対、HおよびC1~C6アルキルから選択され、
ここで、前記ターゲティング配列は、配列番号16~75から選択される配列を含むか、配列番号16~75から選択されるか、配列番号16~75から選択される配列の少なくとも10の連続ヌクレオチドの断片であるか、または配列番号16~75から選択される配列と少なくとも90%の配列同一性を有する変異体であり、
ここで、前記被験体は、前記被験体の筋細胞内で機能的なジストロフィンタンパク質の発現を増加させるジストロフィン治療剤を投与され、それによりデュシェンヌ型筋ジストロフィーまたは関連障害のうちの少なくとも1つを処置する、方法。
(項目77)
12~40サブユニットのアンチセンスオリゴマー化合物と、薬学的に許容される担体とを含むミオスタチン関連医薬組成物であって、前記化合物が、
(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットと;
ヒトミオスタチンプレmRNAのエクソンを含む標的領域内の12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列と
を含むミオスタチン関連組成物と組み合わせた、
17~40サブユニットのアンチセンスオリゴマー化合物と、薬学的に許容される担体とを含むジストロフィン関連医薬組成物であって、前記化合物が、
(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または、(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットと;
ヒトジストロフィンプレmRNAのエクソンを含む標的領域内の10またはこれを超える連続ヌクレオチドと相補的なターゲティング配列と
を含むジストロフィン関連医薬組成物。
(項目78)
前記ジストロフィン関連組成物と前記ミオスタチン関連組成物とが、同じ医薬組成物として提供される、77に記載の組成物。
(項目79)
ヒトミオスタチンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得る遺伝子変異を有する被験体においてミオスタチン発現をモジュレートするための方法であって、
前記被験体に、12~40サブユニットを含み、ヒトミオスタチンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップであって、
前記オリゴマーが、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含む、ステップと、
ミオスタチンプレmRNA転写物内の標的領域に前記アンチセンスオリゴマーを結合させるステップと、
前記標的領域のヒトミオスタチンmRNA転写物への転写を阻害するステップとを含み、
前記被験体が、前記被験体におけるジストロフィン発現を増加させるジストロフィン治療剤を投与されている、方法。
(項目80)
ヒトミオスタチンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得る遺伝子変異を有する被験体においてエクソン2の発現を減少させるための方法であって、
前記被験体に、12~40サブユニットを含み、ヒトミオスタチンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップと、ミオスタチンmRNA転写物内のエクソン2の転写を阻害するステップとを含み、
前記被験体が、前記被験体におけるジストロフィン発現を増加させるジストロフィン治療剤を投与されている、方法。
(項目81)
ミオスタチンmRNA転写物内のエクソン2の発現が、約5%、6%、7%、8%、9%、10%、11%、12%、13%、14%、15%、16%、17%、18%、19%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%または100%減少する、項目80に記載の方法。
(項目82)
ヒトミオスタチンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得るジストロフィン遺伝子における変異を有する被験体の筋細胞または組織における機能的なミオスタチンタンパク質の蓄積を減少させるための方法であって、
前記被験体に、12~40サブユニットを含み、ヒトミオスタチンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップと、
ミオスタチンmRNA転写物内のエクソン2の転写を阻害するステップとを含み、
前記被験体が、前記被験体におけるジストロフィン発現を増加させるジストロフィン治療剤を投与されている、方法。
(項目83)
デュシェンヌ型筋ジストロフィーおよび関連障害を処置するための医薬であって、
(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含み;ヒトミオスタチンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、12~40サブユニットを含むアンチセンスオリゴマー化合物と;
機能的なジストロフィンタンパク質の発現を増加させるジストロフィン治療剤とを含む医薬。
(項目84)
ヒトミオスタチンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得るジストロフィン遺伝子における変異を有する被験体においてデュシェンヌ型筋ジストロフィーおよび関連障害の進行を阻害するための方法であって、
前記被験体に、12~40サブユニットを含み、ヒトミオスタチンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップと、ミオスタチンmRNA転写物内のエクソン2の転写を阻害するステップとを含み、
前記被験体が、前記被験体におけるジストロフィン発現を増加させるジストロフィン治療剤を投与され、それによりデュシェンヌ型筋ジストロフィーの進行を阻害する、方法。
(項目85)
デュシェンヌ型筋ジストロフィーおよび関連障害を有する被験体において機能的なミオスタチンタンパク質の蓄積を減少させる方法であって、
前記被験体に、12~40サブユニットを含み、ヒトミオスタチンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップと、
ミオスタチンmRNA転写物内のエクソン2の転写を阻害するステップとを含み、
前記被験体における機能的なミオスタチンタンパク質の蓄積が減少し、
前記被験体が、前記被験体の筋細胞内で機能的なジストロフィンタンパク質の発現を増加させるジストロフィン治療剤を投与されている、方法。
(項目86)
そのような処置を必要とする被験体においてデュシェンヌ型筋ジストロフィーおよび関連障害を処置するための方法であって、
前記被験体において少なくとも約200~400nMのアンチセンスオリゴマーのピークの血中濃度を得るための有効量でアンチセンスオリゴマーを投与するステップを含む方法。
(項目87)
ヒトミオスタチンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得るジストロフィン遺伝子における変異を有する被験体において骨格筋量不足を処置する方法であって、
(a)前記被験体におけるミオスタチンタンパク質の血液中または組織中レベルを測定するステップと、
(b)前記被験体に、12~40サブユニットを含み、ヒトミオスタチンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップと、
(c)ミオスタチンmRNA転写物内のエクソン2の転写を阻害するステップと、
(d)選択した時間以後、前記被験体におけるミオスタチンタンパク質レベルを測定するステップと、
(e)(d)で測定された前記レベルを使用して前記の投与を反復するステップであって、投与されるアンチセンスオリゴマーの量の用量または投薬スケジュールを調整するステップとを含み、前記被験体におけるミオスタチンタンパク質の前記レベルが、前記アンチセンスオリゴマーの投与後に低下し、
前記被験体が、前記被験体の筋細胞において機能的なジストロフィン発現タンパク質の発現を増加させるジストロフィン治療剤を投与されている、方法。
(項目88)
ジストロフィンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得るジストロフィン遺伝子における変異を有する被験体においてデュシェンヌ型筋ジストロフィーおよび関連障害の進行を阻害する方法であって、
前記被験体に、17~40サブユニットを含み、ヒトジストロフィンプレmRNAのエクソンを含む標的領域内の12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップを含み、前記アンチセンスオリゴマーが、前記エクソンのスキッピングを誘導し、
前記オリゴマーが、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含み、
前記被験体が、前記被験体におけるミオスタチンの活性および発現のうちの一方または両方を阻害するミオスタチン治療剤を投与され、それによりデュシェンヌ型筋ジストロフィーまたは関連障害のうちの少なくとも1つの進行を阻害する、方法。
(項目89)
デュシェンヌ型筋ジストロフィーの進行を阻害する方法であって、
被験体に、12~40サブユニットを含み、ヒトミオスタチンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップを含み、
前記オリゴマーが、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含み、
前記被験体が、前記被験体の筋細胞において機能的なジストロフィンタンパク質の発現を増加させるジストロフィン治療剤を投与され、それによりデュシェンヌ型筋ジストロフィーの進行を阻害する、方法。
(項目90)
前記アンチセンスオリゴマーの3’末端または5’末端にコンジュゲートするアルギニンに富むペプチド配列をさらに含み、前記アルギニンに富むペプチド配列が、配列番号3486~3501から選択される配列を含む、前出の項目のいずれか一項に記載のアンチセンスオリゴマー。
(項目91)
R2が、Gであり、前記CPPが、配列番号3486~3501から選択される配列を含む、項目60から75のいずれか一項に記載の方法。
(項目92)
アンチセンスオリゴマーの3’末端にコンジュゲートするアルギニンに富むペプチド配列をさらに含み、前記アルギニンに富むペプチド配列が、配列番号3486~3501から選択される配列を含む、項目83に記載の医薬。
(項目93)
17~40サブユニットを含み、ヒトジストロフィンプレmRNAのエクソンを含む標的領域内の12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含むアンチセンスオリゴマーであって、
(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含む、ジストロフィンを標的とする前記オリゴマーと;
12~40サブユニットを含み、ヒトミオスタチンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含むアンチセンスオリゴマーであって、
(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含む、ミオスタチンを標的とする前記オリゴマーとを含む組成物。
(項目94)
ヒトジストロフィンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得る遺伝子変異を有する被験体においてジストロフィン発現をモジュレートするための方法であって、
前記被験体に、17~40サブユニットを含み、ヒトジストロフィンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップを含み、
前記オリゴマーが、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含み、
前記被験体が、前記被験体におけるミオスタチン活性およびミオスタチン発現の一方または両方を阻害するミオスタチン治療剤を投与されている、方法。
(項目95)
ヒトミオスタチンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できるアンチセンスオリゴマーによって処置され得る遺伝子変異を有する被験体においてミオスタチン発現をモジュレートするための方法であって、
前記被験体に、12~40サブユニットを含み、ヒトミオスタチンプレmRNAのエクソンを含む12またはこれを超える連続ヌクレオチドと相補的なターゲティング配列をさらに含む、有効量のアンチセンスオリゴマーを投与するステップを含み、
前記オリゴマーが、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットを含み、
前記被験体が、前記被験体の筋細胞内で機能的なジストロフィンタンパク質の発現を増加させるジストロフィン治療剤を投与されている、方法。
(項目96)
前記アンチセンスオリゴマー、ジストロフィン治療剤またはミオスタチン治療剤の少なくとも1つが、前記被験体に全身投与される、項目1から95のいずれかに記載の方法。
(項目97)
前記被験体が、ヒトである、項目96に記載の方法。
(項目98)
前記被験体が、7歳またはこれを超える、項目97に記載の方法。
(項目99)
アンチセンスオリゴマーまたはジストロフィン治療剤が、配列番号927を含まない、項目98に記載の方法。
詳細な説明
以下の説明は、本質的に、単に例示的なものであり、本発明、その応用またはその使用を限定することを意図しない。図面全体を通じて、対応する参照番号は、類似または対応する部分および特徴を示すことを理解すべきである。本発明の多様な実施形態において示される具体例の記載は、説明のみを意図するものであり、本明細書で開示される発明の範囲を限定することを意図しない。さらに、述べられた特徴を有する複数の実施形態の説明は、さらなる特徴を有する他の実施形態、または述べられた特徴の異なる組合せが組み込まれた他の実施形態を除外することを意図しない。
以下の説明は、本質的に、単に例示的なものであり、本発明、その応用またはその使用を限定することを意図しない。図面全体を通じて、対応する参照番号は、類似または対応する部分および特徴を示すことを理解すべきである。本発明の多様な実施形態において示される具体例の記載は、説明のみを意図するものであり、本明細書で開示される発明の範囲を限定することを意図しない。さらに、述べられた特徴を有する複数の実施形態の説明は、さらなる特徴を有する他の実施形態、または述べられた特徴の異なる組合せが組み込まれた他の実施形態を除外することを意図しない。
さらに、本発明の多様な実施形態の詳細な説明は、例示として多様な実施形態を示す添付の図面を参照する。これらの実施形態は、当業者が本発明を実施することを可能にするのに十分詳細に記載されているが、他の実施形態が実現される可能性があり、本発明の思想および範囲から逸脱することなく、論理的および機構的変更をなし得ることを理解すべきである。このように、本明細書の詳細な説明は、限定を目的としてではなく、説明のみを目的として提示される。例えば、説明において挙げられるステップもしくは機能、いかなる方法、システムまたはプロセスも、いかなる順序で実施してもよく、提示される順序に限定されない。さらに、ステップまたはその機能のいずれかを、1または複数の第三者に外注または実行させてもよい。さらに、単数形へのいかなる言及も、複数の実施形態を含み、1つを超える構成要素に対するいかなる言及も、単数の実施形態を含み得る。
I.定義
そうでないことが規定されない限りにおいて、本明細書で使用される、全ての技術用語および科学用語は、本開示が属する技術分野の当業者により一般に理解される意味と同じ意味を有する。本明細書で記載される方法および材料と同様または同等な、任意の方法および材料を、本開示の主題の実施または試験において使用しうるが、好ましい方法および材料について記載する。本開示の目的で、下記では、以下の用語について規定する。
本明細書では、冠詞の「1つの(a)」および「1つの(an)」を、冠詞の文法的対象物の1つまたは1つを超える対象物(すなわち、少なくとも1つの対象物)を指すのに使用する。例を目的として述べると、「ある要素」とは、1つの要素または1つを超える要素を意味する。
用語「約」は、基準の数量、レベル、値、数、頻度、百分率、寸法、サイズ、量、重量、または長さに対して、30、25、20、15、10、9、8、7、6、5、4、3、2、または1%ほど変動する、数量、レベル、値、数、頻度、百分率、寸法、サイズ、量、重量、または長さを意味する。数値範囲に関して用語「約」を使用するとき、それは明示された数値の上下限値を拡張することによりその範囲を修正する。一般に、用語「約」は、述べられた値の上下≦10%の変動により数値を修飾することを意図する。
本開示を通して、文脈によりそうでないことが要請されない限り、「~を含む」、「~を含む」、および「~を含むこと」という語は、言明されるステップもしくは要素またはステップもしくは要素の群の包含を含意するが、他の任意のステップもしくは要素またはステップもしくは要素の群の除外は含意しないことが理解されるであろう。
用語「~からなること」は、「~からなること」という語句に後続するあらゆる語句を含み、かつ、これに限定されることを意味する。したがって、「~からなること」という語句は、列挙される要素が要請されるかまたは必須であり、他の要素は存在しえないことを指し示す。用語「~から本質的になること」は、この語句の後に列挙される任意の要素を含み、かつ、列挙される要素について、本開示で指定される活性または作用に干渉または寄与しない、他の要素に限定されることを意味する。したがって、「~から本質的になること」という語句は、列挙される要素が要請されるかまたは必須であるが、他の要素は任意選択であり、それらが列挙される要素の活性または作用に、実質的に影響を及ぼすのかどうかに応じて、存在してもよく、存在しなくてもよいことを示す。
「~を投与すること」または「~を投与する」という用語は、本開示の修飾アンチセンスオリゴマーを含む治療剤の、被験体への、局所投与または全身投与による送達を含む。投与は、局所投与(眼投与、ならびに膣送達および直腸送達を含む、粘膜への投与を含む)、例えば、噴霧器による投与を含む、粉末またはエアゾールによる吸入または送気による、肺投与、気管内投与、鼻腔内投与、表皮投与および経皮投与、経口投与、または非経口投与でありうる。非経口投与は、静脈内注射もしくは静脈内注入、動脈内注射もしくは動脈内注入、皮下注射もしくは皮下注入、腹腔内注射もしくは腹腔内注入、または筋内注射もしくは筋内注入;あるいは頭蓋内投与、例えば、髄腔内投与または脳室内投与を含む。
本発明で使用される「共投与」または「共投与すること」または「併用療法」は、一般的には、本明細書で開示される1または複数のミオスタチン治療用化合物と組み合わせた、DMDエクソンスキッピングアンチセンスオリゴヌクレオチドの投与を指す。言い換えると、用語「共投与すること」または「共投与」または「併用療法」は、薬学的に許容される下記の剤形で、本明細書で開示される1または複数のミオスタチン治療用化合物および任意選択で1または複数の糖質コルチコイドと同時にDMDエクソンスキッピングアンチセンスオリゴヌクレオチド、例えばエテプリルセンを投与することを意味する:(i)DMDエクソンスキッピングアンチセンスオリゴヌクレオチド、例えばエテプリルセンと、本明細書で開示される1または複数のミオスタチン治療用化合物と、任意選択で1または複数の糖質コルチコイドおよび薬学的に許容される担体とを含む医薬組成物を意味する、同じ剤形、例えば同じ錠剤または医薬組成物;(ii)投与方法が同じ別々の剤形、例えば、DMDエクソンスキッピングアンチセンスオリゴヌクレオチド、例えばエテプリルセンおよび薬学的に許容される担体を含む非経口投与に適する第1の医薬組成物と、本明細書で開示される1または複数のミオスタチン治療用化合物および薬学的に許容される担体を含む非経口投与に適する第2の医薬組成物と、任意選択で、本明細書で開示される1または複数の糖質コルチコイドおよび薬学的に許容される担体を含む非経口投与に適する第3の医薬組成物とを含むキット、ならびに(iii)投与方法が異なる別々の剤形、例えば、DMDエクソンスキッピングアンチセンスオリゴヌクレオチド、例えばエテプリルセンおよび薬学的に許容される担体を含む非経口投与に適する第1の医薬組成物と、本明細書で開示される1または複数のミオスタチン治療用化合物および薬学的に許容される担体を含む経口投与に適する第2の医薬組成物と、任意選択で、本明細書で開示される1または複数の糖質コルチコイドおよび薬学的に許容される担体を含む経口投与に適する第3の医薬組成物とを含むキット。
さらに、本開示の利益を受ける当業者は、本明細書で開示される1つを超えるミオスタチン治療用化合物が投与されるとき、当該薬剤は、同じ投与方法を共有する必要はなく、例えばDMDエクソンスキッピングアンチセンスオリゴヌクレオチド、例えばエテプリルセンおよび薬学的に許容される担体を含む非経口投与に適する第1の医薬組成物と、本明細書で開示される第1のミオスタチン治療用化合物および薬学的に許容される担体を含む経口投与に適する第2の医薬組成物と、本明細書で開示される第2の非ステロイド性抗炎症性化合物および薬学的に許容される担体を含む非経口投与に適する第3の医薬組成物とを含むキットがあり得ると察知するであろう。当業者は、「共投与すること」または「共投与」に関して上で言及された同時投与が、DMDエクソンスキッピングアンチセンスオリゴヌクレオチドを含む医薬組成物とミオスタチン治療用化合物を含む医薬組成物が、同じスケジュールに従い、すなわち同じ時間および日に、または異なるスケジュール、すなわち異なるが必ずしも明確に区別されないスケジュールに従い投与され得ることを意味すると察知するであろう。
そのことに関して、DMDエクソンスキッピングアンチセンスオリゴヌクレオチドを含む医薬組成物と、ミオスタチン治療用化合物を含む医薬組成物とが、異なるスケジュールに従い投与されるとき、かかる異なるスケジュールは、本明細書では「バックグラウンド」または「バックグラウンド投与」と称する場合もある。例えば、DMDエクソンスキッピングアンチセンスオリゴヌクレオチドを含む医薬組成物が1日2回、ある特定の剤形で投与され得、またミオスタチン治療用化合物を含む医薬組成物が1日1回投与され得、ゆえに、1日の投与のうちの1つの間に、DMDエクソンスキッピングアンチセンスオリゴヌクレオチドを含む医薬組成物が、ミオスタチン治療用化合物を含む医薬組成物と、必ずではないが同時に投与され得る。もちろん、「共投与すること」、「共投与」または「併用療法」に対する他の適切な変形は、本開示の利益を受ける当業者に容易に明らかであり、またこの用語の意味の一部である。
本明細書で使用される「慢性投与」は、持続的、定期的、長期的な治療的投与、すなわち実質的な中断のない定期的投与を指す。例えば、患者において筋ジストロフィーを処置する目的で、少なくとも数週間または数カ月または数年間、毎日の投与である。例えば、患者において筋ジストロフィーを処置する目的で、少なくとも数カ月または数年間、毎週の投与である(例えば少なくとも6週間で毎週、少なくとも12週間で毎週、少なくとも24週間で毎週、少なくとも48週間で毎週、少なくとも72週間で毎週、少なくとも96週間で毎週、少なくとも120週間で毎週、少なくとも144週間で毎週、少なくとも168週間で毎週、少なくとも180週間で毎週、少なくとも192週間で毎週、少なくとも216週間で毎週、または少なくとも240週間で毎週)。ある特定の実施形態では、DMDエクソンスキッピング化合物、例えばエテプリルセンは、本明細書で開示されるミオスタチン治療用化合物と組み合わせて、静脈内注入により毎週1回、30mg/kgで慢性投与される。
「細胞を接触させること」、「導入すること」、または「送達すること」という用語は、本開示の治療剤の、細胞への、当技術分野で慣例的な方法(例えば、トランスフェクション(例えば、リポソーム、リン酸カルシウム、ポリエチレンイミン)、電気穿孔(例えば、ヌクレオフェクション)、マイクロインジェクション)が挙げられる)による送達を含む。
「アルキル」という用語は、直鎖状(すなわち、非分枝状または非環式)、分枝状、環式、または多環式非芳香族の炭化水素基であって、任意選択で、1または複数の官能基により置換された炭化水素基を指す。そうでないことが指定されない限りにおいて、「アルキル」基は、1~8個の炭素原子を含有し、好ましくは、1~6個の炭素原子を含有する。C1~C6アルキルとは、少なくともC1アルキル基、C2アルキル基、C3アルキル基、C4アルキル基、C5アルキル基、およびC6アルキル基を含むことを意図する。低級アルキルとは、1~6個の炭素原子を含有するアルキル基を指す。アルキルの例は、メチル、エチル、n-プロピル、イソプロピル、シクロプロピル、ブチル、イソブチル、sec-ブチル、tert-ブチル、シクロブチル、ペンチル、イソペンチル、tert-ペンチル、シクロペンチル、ヘキシル、イソヘキシル、シクロヘキシルなどを含むがこれらに限定されない。アルキルは、置換アルキルの場合もあり、非置換アルキルの場合もある。例示的な置換アルキル基は、フルオロメチル、ジフルオロメチル、トリフルオロメチル、2-フルオロエチル、3-フルオロプロピル、ヒドロキシメチル、2-ヒドロキシエチル、3-ヒドロキシプロピル、ベンジル、置換ベンジル、フェネチル、置換フェネチルなどを含むがこれらに限定されない。
「アルコキシ」という用語は、アルキルのサブセットであって、上記で規定した、表示の数の炭素を伴うアルキル基が、酸素架橋を介して結合しているサブセットを指す。例えば、「アルコキシ」とは、直鎖状立体配置、分枝状立体配置、環式立体配置である、1~8個の炭素原子を含有する-O-アルキル基を指す。「アルコキシ」の例は、メトキシ、エトキシ、n-プロポキシ、i-プロポキシ、t-ブトキシ、n-ブトキシ、s-ペントキシなどを含むがこれらに限定されない。
単独で、または「アラルキル」、「アラルコキシ」、または「アリールオキシアルキル」における通り、より大型の部分の一部として使用される「アリール」という用語は、フェニル、1-ナフチル、2-ナフチル、1-アントラシル、および2-アントラシルなど、6~14個の環原子を有する芳香環基を指す。「アリール」環は、1または複数の置換基を含有しうる。「アリール」という用語は、「アリール環」という用語と互換的に使用することができる。「アリール」はまた、芳香環を1または複数の環へと縮合させた、縮合多環式芳香環系も含む。有用なアリール環基の非限定的な例は、フェニル、ヒドロキシフェニル、ハロフェニル、アルコキシフェニル、ジアルコキシフェニル、トリアルコキシフェニル、アルキレンジオキシフェニル、ナフチル、フェナントリル、アントリル、フェナントロなどのほか、1-ナフチル、2-ナフチル、1-アントラシル、および2-アントラシルを含む。本明細書で使用される「アリール」という用語の範囲内にはまた、芳香環を1または複数の非芳香環へと縮合させた基であって、ラジカルまたは結合点が芳香環上にある、インダニル、フェナントリジニル、またはテトラヒドロナフチルなどにおける基も含まれる。
「アシル」という用語は、C(O)R基(式中、Rは、上記で規定したH、アルキル、またはアリールを意味する)を指す。アシル基の例は、ホルミル、アセチル、ベンゾイル、フェニルアセチル、および類似の基を含む。
「同族化合物」という用語は、同じ化学基の逐次的付加により規則的に異なる化合物を指す。例えば、化合物の同族化合物は、1または複数の-CH2-基、アミノ酸残基、ヌクレオチド、またはヌクレオチド類似体の付加により異なりうる。
「細胞透過性ペプチド」(CPP)または「細胞取込みを増強するペプチド部分」という用語は、互換的に使用され、「輸送ペプチド」、「担体ペプチド」、または「ペプチド導入ドメイン」ともまた呼ばれる、カチオン性細胞透過性ペプチドを指す。例えば、ペプチドコンジュゲートホスホルアミデートまたはホスホロジアミデートモルホリノ(PPMO)は、本明細書で記載される、細胞取込みを増強する細胞透過性ペプチドまたは細胞透過性ペプチド部分を含みうる。多様な実施形態では、ペプチドは、修飾アンチセンスオリゴマーに共有結合させることができる。さらなる実施形態では、ペプチドは、修飾アンチセンスオリゴマーの3’末端または5’末端にコンジュゲートさせることができる。さらなる実施形態では、ペプチドは、3’末端のモルホリン環のピペラジニル部分または窒素原子へと連結することができる。一部の実施形態では、細胞取込みを増強する、細胞透過性ペプチドまたは細胞透過性ペプチド部分は、本明細書で記載される、アルギニンに富むペプチドを含みうる。非限定的な例において、本明細書で開示される通りの修飾アンチセンスオリゴマーは、(Arg)6Gly(オリゴヌクレオチドに結合する6つのアルギニンおよび1つのグリシン)などのアルギニンに富むペプチドに結合することができる。
本明細書で示されるペプチドは、全身投与されると、所与の細胞培養物集団の細胞のうちの約30%、40%、50%、60%、70%、80%、90%、もしくは100%、または少なくともほぼこれらの比率の細胞内の細胞透過を誘導し、in vivoにおいて、複数の組織内の高分子のトランスロケーションを可能とする能力を有する。一部の実施形態では、CPPは、式-[(C(O)CHR’NH)m]R’’[式中、R’は、天然に存在するアミノ酸、またはその1炭素同族化合物もしくは2炭素同族化合物の側鎖であり、R’’は、水素またはアシルから選択され、mは、最大で50の整数である]を有する。当技術分野では、さらなるCPPも周知であり、例えば、参照によりその全体において本明細書に組み込まれる、米国出願公開第20100016215号において開示されている。他の実施形態では、mは、1~50から選択される整数であり、ここで、mが1である場合、部分は、単一のアミノ酸またはその誘導体である。
「アミノ酸」という用語は、一級アミノ基、カルボン酸基、側鎖、および水素原子が結合している炭素原子を含む化合物を指す。例えば、「アミノ酸」という用語は、グリシン、アラニン、バリン、ロイシン、イソロイシン、アスパラギン、グルタミン、リシン、アスパラギン酸、ヒスチジン、メチオニン、プロリン、フェニルアラニン、トレオニン、トリプトファン、システイン、グルタミン酸、セリン、チロシン、ピロリシン、セレノシステイン、およびアルギニンを含むがこれらに限定されない。加えて、本明細書で使用される「アミノ酸」はまた、エステル、およびアミド、および塩など、アミノ酸の誘導体のほか、活性形態へと代謝されると薬理学的特性を有する誘導体を含む、他の誘導体も含む。したがって、「アミノ酸」という用語は、天然に存在するアミノ酸および天然に存在しないアミノ酸を含むことが理解される。
「電子対」という用語は、他の原子と結合しないかまたは共有されていない、電子の原子価対を指す。
「相同性」という用語は、2つもしくはこれを超えるアミノ酸配列または2つもしくはこれを超えるヌクレオチド配列の類似性の量または程度を指す。いくつかの例において、配列相同性には、1または複数の保存的置換であって、対象タンパク質の基本的な構造または機能に影響を及ぼさない当該1または複数の置換が含まれ得る。保存的ヌクレオチド置換には、1つの核酸の別の核酸への置換であって、そのコドンによりコードされるアミノ酸を変化させない置換が含まれ得る。保存的アミノ酸置換には、1つのアミノ酸の別のアミノ酸への置換であって、置換されたアミノ酸が置換をするアミノ酸と同じまたは類似の分類に属する置換、例えばある脂肪族アミノ酸の別の脂肪族アミノ酸による置換が含まれ得る。相同性は、GAPなどの配列比較プログラムを使用して決定することができる(Deverauxら、1984年、Nucleic Acids Research、12巻、387~395頁)。このようにして、本明細書で引例される配列と、類似の長さまたは実質的に異なる長さの配列を、アラインメントへのギャップの挿入により比較することができ、このようなギャップを、例えば、GAPにより使用される比較アルゴリズムにより決定する。
「単離された」という用語は、その生来の状態では通常それに随伴する成分を、実質的または本質的に含まない材料を指す。例えば、本明細書で使用される「単離オリゴヌクレオチド」または「単離オリゴマー」とは、天然に存在する状態ではそれを挟む配列から精製されるかまたは取り出されたオリゴマー、例えば、ゲノム内の断片に隣接する配列から取り出されたDNA断片を指す場合がある。細胞に関する場合の、「~を単離すること」という用語は、細胞(例えば、線維芽細胞、リンパ芽球)の、供給源となる被験体(例えば、オリゴヌクレオチドリピート病を伴う被験体)からの精製を指してもよい。mRNAまたはタンパク質の文脈では、「~を単離すること」とは、mRNAまたはタンパク質の、供給源、例えば、細胞からの回収を指してもよい。
「~をモジュレートする」という用語は、1または複数の定量化可能なパラメータを、任意選択で、規定された量および/または統計学的に有意な量で「増加」または「減少」させることを含む。「~を増加させる」もしくは「~を増加させること」、「~を増強する」もしくは「~を増強すること」、または「~を刺激する」もしくは「~を刺激すること」とは、一般に、1もしくは複数の修飾アンチセンスオリゴマー化合物もしくは組成物、および/または、1もしくは複数の治療剤が、細胞または被験体において、アンチセンスオリゴマー化合物および/もしくは治療剤を伴わずに引き起こされる応答、または対照化合物により引き起こされる応答と比べて、より大きな生理学的応答(例えば下流における効果)をもたらすかまたは引き起こす能力を指す。関係のある生理学的応答または細胞応答(in vivoまたはin vitro)は、当業者には明らかであり、ミオスタチンmRNAにおけるエクソン2の包含の減少(もしくはエクソン2の除外の増加)、および/または、例えばそれを必要とする被験体の細胞もしくは組織における機能的なミオスタチンタンパク質の発現の減少を含み得る。他の関係のある生理学的応答または細胞応答(in vivoまたはin vitro)は、ジストロフィンmRNAにおける遺伝子変異を有する1または複数のエクソンの包含の減少(もしくは除外の増加)、および/または、細胞もしくは組織における、機能的もしくは半機能的なジストロフィンタンパク質の発現の増加を含み得る。「減少された」または「低減された」量とは、典型的には、「統計学的に有意な」量であり、修飾アンチセンスオリゴマー化合物および/もしくは治療剤の投与の非存在下で、それを必要とする被験体によりもたらされる量(例えば特定の被験体またはコホートの、「生来」または「自然」の発現率)または対照化合物によりもたらされる量と比較して、1、2、3、4、5、6、7、8、9、10、15、20、30、40、50分の1またはこれ未満(例えば100、500、1000分の1)であって、全ての整数およびそれらの間にあり1より大きい小数(decimal point)(例えば1.1、1.2、1.3、1.4、1.5、1.6、1.7、1.8、1.9を含む)分数の減少を含み得る。「~を低減する」または「~を阻害する」という用語は一般に、1もしくは複数のアンチセンスオリゴマー化合物もしくは組成物、および/または、1もしくは複数の治療剤が、本明細書に記載される疾患または状態の症状などの関係のある生理学的応答または細胞応答であって、診断技術分野で慣例的な技法に従い、測定される応答を「減少させる」能力に関する場合がある。「増加した」または「増強された」量とは、典型的には、「統計学的に有意な」量であり、修飾アンチセンスオリゴマー化合物および/もしくは治療剤の非存在下でそれを必要とする被験体によりもたらされる量(例えば特定の被験体またはコホートの「生来の」または「天然の」発現率)または対照化合物によりもたらされる量と比較して、全ての整数およびそれらの間にあって1より大きい小数(例えば、1.1、1.2、1.3、1.4、1.5、1.6、1.7、1.8、1.9)を含めて1、2、3、4、5、6、7、8、9、10、15、20、30、40、50倍またはこれを超える(例えば100、500、1000倍)増加を含み得る。「~を増強する」という用語は、一般に、1もしくは複数の修飾アンチセンスオリゴマー化合物もしくは組成物、および/または、1もしくは複数の治療剤が、本明細書に記載される疾患または状態の症状などの関係のある生理学的応答または細胞応答を、診断技術分野における慣例的な技法に従って測定したとき「増加させる」能力に関し得る。
関係のある生理学的応答または細胞応答(in vivoまたはin vitro)は、当業者に明らかであり、デュシェンヌ型筋ジストロフィー(DMD)および関連障害、例えばベッカー型筋ジストロフィー(BMD)、肢帯筋ジストロフィー、先天性筋ジストロフィー、顔面肩甲上腕筋ジストロフィー、筋緊張性筋ジストロフィー、眼球咽頭筋ジストロフィー、末梢型筋ジストロフィー、エメリー・ドライフス筋ジストロフィー、筋肉消耗状態または障害、例えばAIDS、がんまたは化学療法関連の筋肉消耗、および線維症または線維症関連障害(例えば骨格筋線維症)などの症状または病変の減少を含み得る。他の実施形態では、例えば、症状または病変の軽減が、機能的なジストロフィンタンパク質の発現の増加および/または機能的なミオスタチンタンパク質の発現の減少に随伴するかまたはこれに関連し得る、デュシェンヌ型筋ジストロフィーおよび関連障害を処置する方法が提供される。応答の「増加」は、修飾アンチセンスオリゴマー化合物および/もしくは治療剤の投与の非存在下でそれを必要とする被験体によりもたらされる応答に比べて(例えば特定の被験体またはコホートの「生来の」または「天然の」発現率と比べて)または対照化合物と比べて「統計学的に有意」であり得、間にある全ての整数を含めて、1%、2%、3%、4%、5%、6%、7%、8%、9%、10%、11%、12%、13%、14%、15%、16%、17%、18%、19%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%または100%の増加を含み得る。
本明細書で使用される用語「治療剤」(「therapeutic」または「therapeutic agent」)とは、治療効果を生じさせることができる薬剤を意味する。一部の実施形態では、治療剤は、ポリペプチド、ポリペプチド類似体、核酸、核酸類似体、アプタマーもしくは小分子であるか、またはそれらを含む。「ポリペプチド」、「ペプチド」および「タンパク質」は、長さまたは翻訳後修飾に関係なく、交換可能に使用され、アミノ酸の任意のペプチド結合鎖を意味する。ポリペプチドは、野生型タンパク質、野生型タンパク質の機能的断片、または野生型タンパク質もしくは断片の変異体であってもよい。変異体は、1または複数のアミノ酸の置換、欠失または挿入を含んでもよい。置換は保存的であっても、非保存的であってもよい。保存的置換には、典型的には、以下の群内の置換が含まれる:グリシンおよびアラニン;バリン、イソロイシンおよびロイシン;アスパラギン酸およびグルタミン酸;アスパラギン、グルタミン、セリンおよびトレオニン;リシン、ヒスチジンおよびアルギニン;ならびにフェニルアラニンおよびチロシン。一部の実施形態では、タンパク質には抗体または可溶性受容体が含まれる。複数の実施形態では、可溶性受容体はACVR2(例えばACVR2B)である。一部の実施形態では、核酸はタンパク質、例えばジストロフィン、マイクロジストロフィンまたはミニジストロフィンをコードするものである。複数の実施形態では、核酸はアンチセンスオリゴマーまたはsiRNAである。一部の実施形態では、アンチセンスオリゴマーは本明細書で記載される通りの修飾アンチセンスオリゴマーである。
本明細書で使用される「抗体」という用語は、2つの軽鎖ポリペプチドと2つの重鎖ポリペプチドとを含む全抗体を指す。全抗体は、IgM、IgG、IgA、IgDおよびIgE抗体を含む異なる抗体アイソタイプを含む。「抗体」という用語は、ポリクローナル抗体、モノクローナル抗体、キメラ化されたもしくはキメラ抗体、ヒト化抗体、霊長類化抗体、脱免疫原性(deimmunized)抗体および完全ヒト抗体を含む。抗体は、例えば、哺乳動物、例えばヒト、非ヒト霊長類(例えばオランウータン、マントヒヒまたはチンパンジー)、ウマ、ウシ、ブタ、ヒツジ、ヤギ、イヌ、ネコ、ウサギ、モルモット、スナネズミ、ハムスター、ラットおよびマウスなどの種々の種のいずれかで作製でき、またはそれらに由来し得る。抗体は、精製された抗体または組換え抗体であり得る。
本明細書で使用するとき、用語「抗体断片」、「抗原結合断片」または類似の用語は、標的抗原と結合し、標的抗原の活性を阻害する能力を保持する抗体の断片を指す。かかる断片は、例えば単鎖抗体、単鎖Fv断片(scFv)、Fd断片、Fab断片、Fab’断片またはF(ab’)2断片を含む。scFv断片は、scFvが由来する抗体の重鎖可変領域および軽鎖可変領域の両方を含む単一のポリペプチド鎖である。さらに、細胞内抗体(intrabodies)、低分子化抗体(minibodies)、三重特異性抗体(triabodies)および二重特異性抗体(diabody)も抗体の定義に含まれ、本明細書で記載される方法での使用に適する。例えば、Todorovskaら、(2001年)J Immunol Methods 248巻(1号):47~66頁;HudsonおよびKortt(1999年)J Immunol Methods 231巻(1号):177~189頁;Poljak(19
94年)Structure 2巻(12号):1121~1123頁;RondonおよびMarasco(1997年)Annual Review of Microbiology 51巻:257~283頁を参照されたい。これらの各々は参照によりそれらの全体において本明細書に組み込まれる。
94年)Structure 2巻(12号):1121~1123頁;RondonおよびMarasco(1997年)Annual Review of Microbiology 51巻:257~283頁を参照されたい。これらの各々は参照によりそれらの全体において本明細書に組み込まれる。
本明細書で使用するとき、用語「抗体断片」はまた、例えばラクダ化(camelized)された単一ドメイン抗体などの単一ドメイン抗体を含む。例えば、Muyldermansら
(2001年)Trends Biochem Sci 26巻:230~235頁;Nuttallら(200
0年)Curr Pharm Biotech 1巻:253~263頁;Reichmannら(1999年)J Immunol Meth 231巻:25~38頁;PCT出願公開第WO94/04678号および第WO94/25591号;ならびに米国特許第6,005,079号を参照されたい。これらの各々は参照によりそれらの全体において本明細書に組み込まれる。一部の実施形態では、本開示は、単一ドメイン抗体が形成されるような修飾がなされた、2つのVHドメインを含む単一ドメイン抗体を提供する。
(2001年)Trends Biochem Sci 26巻:230~235頁;Nuttallら(200
0年)Curr Pharm Biotech 1巻:253~263頁;Reichmannら(1999年)J Immunol Meth 231巻:25~38頁;PCT出願公開第WO94/04678号および第WO94/25591号;ならびに米国特許第6,005,079号を参照されたい。これらの各々は参照によりそれらの全体において本明細書に組み込まれる。一部の実施形態では、本開示は、単一ドメイン抗体が形成されるような修飾がなされた、2つのVHドメインを含む単一ドメイン抗体を提供する。
一部の実施形態では、抗原結合断片は、重鎖ポリペプチドの可変領域と軽鎖ポリペプチドの可変領域とを含む。一部の実施形態では、本明細書で記載される抗原結合断片は、抗体の軽鎖および重鎖ポリペプチドのCDRを含む。
成長分化因子8(GDF-8)とも称されるミオスタチンは、トランスフォーミング成長因子ベータ(TGF-β)のスーパーファミリーに属する。ミオスタチンは、MSTN遺伝子によりコードされるタンパク質である。ミオスタチンのアミノ酸配列は、MQKLQLCVYIYLFMLIVAGPVDLNENSEQKENVEKEGLCNACTWRQNTKSSRIEAIKIQILSKLRLETAPNISKDVIRQLLPKAPPLRELIDQYDVQRDDSSDGSLEDDDYHATTETIITMPTESDFLMQVDGKPKCCFFKFSSKIQYNKVVKAQLWIYLRPVETPTTVFVQILRLIKPMKDGTRYTGIRSLKLDMNPGTGIWQSIDVKTVLQNWLKQPESNLGIEIKALDENGHDLAVTFPGPGEDGLNPFLEVKVTDTPKRSRRDFGLDCDEHSTESRCCRYPLTVDFEAFGWDWIIAPKRYKANYCSGECEFVFLQKYPHTHLVHQANPRGSAGPCCTPTKMSPINMLYFNGKEQIIYGKIPAMVVDRCGCS(配列番号3502)である。MS
TN遺伝子は主にヒト骨格筋で発現し、筋肉の成長の負の制御因子として作用する。例えば、ミオスタチン遺伝子を欠くように操作したマウスは、正常なマウスの2倍の筋肉量の発達を示す(McPherronら、(1997年)、Nature 387巻:83~90頁)。
TN遺伝子は主にヒト骨格筋で発現し、筋肉の成長の負の制御因子として作用する。例えば、ミオスタチン遺伝子を欠くように操作したマウスは、正常なマウスの2倍の筋肉量の発達を示す(McPherronら、(1997年)、Nature 387巻:83~90頁)。
複数の実施形態では、ミオスタチン治療剤は、被験体におけるミオスタチン活性およびミオスタチン発現の一方または両方を抑制できる。ミオスタチン治療剤は、ミオスタチンプレmRNAを標的とし、ミオスタチンプレmRNAの成熟mRNAへの転写に干渉する治療剤であってもよい。複数の実施形態では、ミオスタチン治療剤は、ヒトミオスタチンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できる。複数の実施形態では、ミオスタチン治療剤は、ミオスタチンプレmRNAにおけるエクソン2のスキッピングを誘導し、エクソン2を含むミオスタチンプレmRNAの発現を阻害する。ミオスタチン治療剤は、ミオスタチンタンパク質を標的とし、ミオスタチン受容体とのミオスタチンタンパク質の結合に干渉する治療剤であってもよい。ミオスタチン治療用タンパク質は、抗ミオスタチン抗体、例えば、抗GDF8(Abcam、ケンブリッジ、MA)、ドマグロズマブ(Domagrozumab)(PF-06252616、Pfizer Inc.);スタムルマブ(Stamulumab)(Cambridge Antibody Technology);PF-3446879(Pfizer Inc.);ランドグロズマブ(Landogrozumab)(LY-2495655;Eli Lilly);またはトレボグルマブ(Trevogrumab)(REGN-103;Regeneron)であってもよい。複数の実施形態では、ミオスタチン治療剤は、可溶性受容体がACVR2である可溶性受容体であってもよい(例えばACVR2B;MTAPWVALALLWGSLCAGSGRGEAETRECIYYNANWELERTNQSGLERCEGEQDKRLHCYASWRNSSGTIELVKKGCWLDDFNCYDRQECVATEENPQVYFCCCEGNFCNERFTHLPEAGGPEVTYEPPPTAPTLLTVLAYSLLPIGGLSLIVLLAFWMYRHRKPPYGHVDIHEDPGPPPPSPLVGLKPLQLLEIKARGRFGCVWKAQLMNDFVAVKIFPLQDKQSWQSEREIFSTPGMKHENLLQFIAAEKRGSNLEVELWLITAFHDKGSLTDYLKGNIITWNELCHVAETMSRGLSYLHEDVPWCRGEGHKPSIAHRDFKSKNVLLKSDLTAVLADFGLAVRFEPGKPPGDTHGQVGTRRYMAPEVLEGAINFQRDAFLRIDMYAMGLVLWELVSRCKAADGPVDEYMLPFEEEIGQHPSLEELQEVVVHKKMRPTIKDHWLKHPGLAQLCVTIEECWDHDAEARLSAGCVEERVSLIRRSVNGTTSDCLVSLVTSVTNVDLPPKESSI;配列番号3503)。一部の実施形態では、可溶性受容体(例えばACVR2B)は、異種性部分、例えば被験体において治療剤の循環半減期を増加させる部分とコンジュゲートする。一部の実施形態では、部分はイムノグロブリンのFc部分(例えばヒトIgG Fc)である。一部の実施形態では、部分はポリエチレングリコール部分である。一部の実施形態では、部分はアルブミンポリペプチド(例えばヒトアルブミン)の全体または一部を含む。一部の実施形態では、ミオスタチン治療剤は、ヒトACVR2-Fc融合体、例えばラマテルセプト(ramatercept)(Acceleron)である。ミオスタチン治療剤は、核酸がアンチセンスオリゴマーおよびsiRNAから選択される核酸を含む。アンチセンスオリゴマーは本明細書で記載される通りの修飾ミオスタチンアンチセンスオリゴマーであってもよい。一部の実施形態では、ミオスタチン治療剤は、小分子、例えばOSX-200(Ossianix Inc)またはSRK-015(Scholar Rock Inc.)である。
本明細書で記載される方法および組成物に有用なミオスタチンのアンタゴニストは、例えば、抗ミオスタチン抗体などのミオスタチンに直接結合する薬剤(GDF-8)を含む。かかる抗体は当技術分野において公知であり、例えば国際特許出願公開第WO2006116269号(Pfizer)、米国特許第8,066,996号(Eli Lilly)、米国特許第7,807,159号(Amgen)、米国特許第6,096,506号および米国特許第6,468,535号に記載されており、これらの各々の開示は参照によりそれらの全体において本明細書に組み込まれる。ミオスタチンアンタゴニストは、可溶性アクチビン(Activin)受容体タンパク質または、可溶性アクチビンタンパク質を含む融合タンパク質(例えばACVR2-Fc融合タンパク質)も含む。可溶性アクチビン受容体タンパク質は、例えば、国際特許出願公開第WO2010129406号(ジョンズホプキンス大学)、米国特許出願公開第20090005308号(Acceleron)、国際特許出願公開第WO2008/097541号(Acceleron)および国際特許出願公開第WO2010019261号(Acceleron)に記載されており、これらの各々の開示は参照により本明細書に組み込まれる。一部の実施形態では、ミオスタチンアンタゴニストは、短鎖干渉核酸(siNA)、短鎖干渉RNA(siRNA)、二本鎖RNA(dsRNA)、マイクロRNA(miRNA)、およびミオスタチンに対してRNA干渉(RNAi)を媒介できる短鎖ヘアピンRNA(shRNA)分子などの、ミオスタチンの発現を阻害する核酸である。かかる分子は、例えば米国特許出願公開第20050124566号および米国特許第7,887,793号に記載されており、これらの各々の開示は参照によりそれらの全体において本明細書に組み込まれる。一部の実施形態では、例えばAbbott Laboratoriesへの米国特許第6,284,882号に記載されている通り、核酸はミオスタチンプロモーターを阻害し、それによりミオスタチン発現を阻害する。ミオスタチンの阻害剤は、その受容体を経るミオスタチンシグナリングを阻害する薬、例えば抗ACVR2B抗体を含む(例えば、米国特許出願公開第20100272734号(Novartis)および国際特許出願公開第WO2014172448号(Anaptysbio)を参照されたい)。ミオスタチンのさらなる例示的な阻害剤は、国際特許出願公開第WO2006/083183号に記載されている。
一部の実施形態では、ジストロフィン治療剤は1回目に投与され、ミオスタチン治療剤は2回目に投与される。例えば、ジストロフィン治療剤は、治療剤が投与される被験体の筋肉において機能的なジストロフィンタンパク質の発現を促進し、回復させ、および/または増加させるのに十分な時間投与される。次に、ミオスタチン治療剤は、例えば被験体における筋肉量、筋力、および/または弾力性を強化するのに十分な時間で被験体に投与される。複数の実施形態では、ジストロフィン治療剤は、被験体におけるジストロフィンの発現を増加させることができる。ジストロフィン治療剤は、ジストロフィンまたは機能的もしくは半機能的な切断型(truncated)ジストロフィンの発現を増加させ得る。切断型ジストロフィンは、マイクロジストロフィンおよびミニジストロフィンを含むが、これらに限定されない(参照によりその全体において本明細書に組み込まれる欧州特許第2125006号で開示されている)。ジストロフィン治療剤は、ジストロフィンプレmRNAを標的とし、ジストロフィンプレmRNAの成熟mRNA、例えば本明細書で記載される修飾アンチセンスオリゴマーへの転写をモジュレートする治療剤であってもよい。複数の実施形態では、ジストロフィン治療剤は、ヒトジストロフィンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できる。複数の実施形態では、標的とされるジストロフィンプレmRNAは、1または複数の遺伝子変異を有してもよい。ジストロフィン治療剤が、エクソンスキッピングを誘導することにより、1または複数の遺伝子変異を含む1または複数のエクソンが、成熟mRNAへのプロセシングの間、ジストロフィンプレmRNAから除去される。得られる切断型mRNAは、機能的または半機能的なジストロフィンタンパク質に翻訳され得る。
一部の実施形態では、ジストロフィン治療剤は、機能的なジストロフィンタンパク質、例えばマイクロジストロフィンまたはミニジストロフィンタンパク質をコードする核酸であるか、またはそれを含む。一部の実施形態では、核酸はウイルス送達により被験体の筋細胞に導入される。一部の実施形態では、核酸からの機能的なジストロフィンタンパク質の発現は、筋肉特異的プロモーター、例えば筋肉クレアチンキナーゼ(MCK)のプロモーターにより駆動される。DMDの遺伝子治療のための、機能的なジストロフィンタンパク質を含むウイルスベクターの使用は、例えば、Shinら(2013年)Mol Ther 21
巻(4号):750~757頁;Rodino-Klapacら(2011年)Methods Mol Biol
709巻:287~298頁;Okadaら(2013年)Pharmaceuticals 6巻(7号):813~836頁;Rodino-Klapacら(2010年)Mol Ther 18巻(1号):109~117頁;Vincentら(1993年)Nature Genetics 5巻:130~134頁;Xu
ら(2007年)Neuromusc Disorders 17巻:209~220頁;Martinら(2009年)Am J Physiol Cell Physiol 296巻:476~488頁;国際特許出願公
開第WO2009/088895号および米国特許出願公開第2010003218号および同第20140323956号に記載されており、これらの各々の開示は参照によりそれらの全体において本明細書に組み込まれる。当業者はまた、目的の細胞への導入遺伝子の送達に使用できる他のベクター系も熟知している(例えば米国特許第5,707,618号;Verhaartら(2012年)Curr Opin Neurol 25巻(5号):588~596頁;Odomら(2011年)Mol Ther 19巻(1号):36~45頁;およびKoppanatiら(2010年)Gene Ther 17巻(11号):1355~1362)。機能的なジストロフィンタンパク質のトランスジェニック送達を評価している進行中の臨床試験は、例えば米国ClinicalTrials.gov識別番号NCT02376816(Nationwide Children’s Hospital)およびNCT00428935(Nationwide Children’s Hospital)、ならびにBowlesら(2012年)Mol Ther 20巻(2号):443~455頁によ
り記載された治験を含む。
巻(4号):750~757頁;Rodino-Klapacら(2011年)Methods Mol Biol
709巻:287~298頁;Okadaら(2013年)Pharmaceuticals 6巻(7号):813~836頁;Rodino-Klapacら(2010年)Mol Ther 18巻(1号):109~117頁;Vincentら(1993年)Nature Genetics 5巻:130~134頁;Xu
ら(2007年)Neuromusc Disorders 17巻:209~220頁;Martinら(2009年)Am J Physiol Cell Physiol 296巻:476~488頁;国際特許出願公
開第WO2009/088895号および米国特許出願公開第2010003218号および同第20140323956号に記載されており、これらの各々の開示は参照によりそれらの全体において本明細書に組み込まれる。当業者はまた、目的の細胞への導入遺伝子の送達に使用できる他のベクター系も熟知している(例えば米国特許第5,707,618号;Verhaartら(2012年)Curr Opin Neurol 25巻(5号):588~596頁;Odomら(2011年)Mol Ther 19巻(1号):36~45頁;およびKoppanatiら(2010年)Gene Ther 17巻(11号):1355~1362)。機能的なジストロフィンタンパク質のトランスジェニック送達を評価している進行中の臨床試験は、例えば米国ClinicalTrials.gov識別番号NCT02376816(Nationwide Children’s Hospital)およびNCT00428935(Nationwide Children’s Hospital)、ならびにBowlesら(2012年)Mol Ther 20巻(2号):443~455頁によ
り記載された治験を含む。
当業者であれば、ジストロフィン遺伝子における多様な変異が治療的なエクソンスキッピングを受け得ることを熟知している。例えば、エクソン51スキッピングされ得る以下のエクソン中の変異の非限定的な例は、例えば45~50、47~50、48~50、49~50、50、52、52~63を含む(Leiden Duchenne muscular dystrophy mutation database、Leiden University Medical Center、オランダ)。患者がDMD遺伝子中に、エクソンスキッピングされ得る変異を有するか否かを判定することも、十分に当業者の技量の範囲内である(例えば、Aartsma-Rusら(2009年)Hum Mut 30
巻:293~299頁およびAbbsら(2010年)Neuromusc Disorders 20巻:422~427頁を参照されたい。これらの各々の開示は参照によりそれらの全体において本明細書に組み込まれる)。
巻:293~299頁およびAbbsら(2010年)Neuromusc Disorders 20巻:422~427頁を参照されたい。これらの各々の開示は参照によりそれらの全体において本明細書に組み込まれる)。
エテプリルセン(例えば、参照によりその全体において本明細書に組み込まれる米国特許第7,807,816号を参照されたい)は、その安全性および効能を試験するための臨床試験の対象であり、また臨床開発が進行中である。エテプリルセンは、ホスホロジアミデートモルホリノ(PMO)アンチセンスオリゴヌクレオチドである。一部の実施形態では、ジストロフィン治療剤はエテプリルセンである。「AVN-4658」としても公知である「エテプリルセン」は、塩基配列5’-CTCCAACATCAAGGAAGATGGCATTTCTAG-3’(配列番号76)を有するPMOである。エテプリルセンは、CAS登録番号1173755-55-9として登録されている。化学名は、RNA、[P-デオキシ-P-(ジメチルアミノ)](2’,3’-ジデオキシ-2’,3’-イミノ-2’,3’-セコ)(2’a→5’)(C-m5U-C-C-A-A-C-A-m5U-C-A-A-G-G-A-A-G-A-m5U-G-G-C-A-m5U-m5U-m5U-C-m5U-A-G)(配列番号263)、5’-[P-[4-[[2-[2-(2-ヒドロキシエトキシ)エトキシ]エトキシ]カルボニル]-1-ピペラジニル]-N,N-ジメチルホスホンアミデート]およびP,2’,3’-トリデオキシ-P-(ジメチルアミノ)-5’-O-{P-[4-(10-ヒドロキシ-2,5,8-トリオキサデカノイル)ピペラジン-1-イル]-N,N-ジメチルホスホンアミドイル}-2’,3’-イミノ-2’,3’-セコシチジリル-(2’a→5’)-P,3’-ジデオキシ-P-(ジメチルアミノ)-2’,3’-イミノ-2’,3’-セコチミジリル-(2’a→5’)-P,2’,3’-トリデオキシ-P-(ジメチルアミノ)-2’,3’-イミノ-2’,3’-セコシチジリル-(2’a→5’)-P,2’,3’-トリデオキシ-P-(ジメチルアミノ)-2’,3’-イミノ-2’,3’-セコシチジリル-(2’a→5’)-P,2’,3’-トリデオキシ-P-(ジメチルアミノ)-2’,3’-イミノ-2’,3’-セコアデニリル-(2’a→5’)-P,2’,3’-トリデオキシ-P-(ジメチルアミノ)-2’,3’-イミノ-2’,3’-セコアデニリル-(2’a→5’)-P,2’,3’-トリデオキシ-P-(ジメチルアミノ)-2’,3’-イミノ-2’,3’-セコシチジリル-(2’a→5’)-P,2’,3’-トリデオキシ-P-(ジメチルアミノ)-2’,3’-イミノ-2’,3’-セコアデニリル-(2’a→5’)-P,3’-ジデオキシ-P-(ジメチルアミノ)-2’,3’-イミノ-2’,3’-セコチミジリル-(2’a→5’)-P,2’,3’-トリデオキシ-P-(ジメチルアミノ)-2’,3’-イミノ-2’,3’-セコシチジリル-(2’a→5’)-P,2’,3’-トリデオキシ-P-(ジメチルアミノ)-2’,3’-イミノ-2’,3’-セコアデニリル-(2’a→5’)-P,2’,3’-トリデオキシ-P-(ジメチルアミノ)-2’,3’-イミノ-2’,3’-セコアデニリル-(2’a→5’)-P,2’,3’-トリデオキシ-P-(ジメチルアミノ)-2’,3’-イミノ-2’,3’-セコグアニリル-(2’a→5’)-P,2’,3’-トリデオキシ-P-(ジメチルアミノ)-2’,3’-イミノ-2’,3’-セコグアニリル-(2’a→5’)-P,2’,3’-トリデオキシ-P-(ジメチルアミノ)-2’,3’-イミノ-2’,3’-セコアデニリル-(2’a→5’)-P,2’,3’-トリデオキシ-P-(ジメチルアミノ)-2’,3’-イミノ-2’,3’-セコアデニリル-(2’a→5’)-P,2’,3’-トリデオキシ-P-(ジメチルアミノ)-2’,3’-イミノ-2’,3’-セコグアニリル-(2’a→5’)-P,2’,3’-トリデオキシ-P-(ジメチルアミノ)-2’,3’-イミノ-2’,3’-セコアデニリル-(2’a→5’)-P,3’-ジデオキシ-P-(ジメチルアミノ)-2’,3’-イミノ-2’,3’-セコチミジリル-(2’a→5’)-P,2’,3’-トリデオキシ-P-(ジメチルアミノ)-2’,3’-イミノ-2’,3’-セコグアニリル-(2’a→5’)-P,2’,3’-トリデオキシ-P-(ジメチルアミノ)-2’,3’-イミノ-2’,3’-セコグアニリル-(2’a→5’)-P,2’,3’-トリデオキシ-P-(ジメチルアミノ)-2’,3’-イミノ-2’,3’-セコシチジリル-(2’a→5’)-P,2’,3’-トリデオキシ-P-(ジメチルアミノ)-2’,3’-イミノ-2’,3’-セコアデニリル-(2’a→5’)-P,3’-ジデオキシ-P-(ジメチルアミノ)-2’,3’-イミノ-2’,3’-セコチミジリル-(2’a→5’)-P,3’-ジデオキシ-P-(ジメチルアミノ)-2’,3’-イミノ-2’,3’-セコチミジリル-(2’a→5’)-P,3’-ジデオキシ-P-(ジメチルアミノ)-2’,3’-イミノ-2’,3’-セコチミジリル-(2’a→5’)-P,2’,3’-トリデオキシ-P-(ジメチルアミノ)-2’,3’-イミノ-2’,3’-セコシチジリル-(2’a→5’)-P,3’-ジデオキシ-P-(ジメチルアミノ)-2’,3’-イミノ-2’,3’-セコチミジリル-(2’a→5’)-P,2’,3’-トリデオキシ-P-(ジメチルアミノ)-2’,3’-イミノ-2’,3’-セコアデニリル-(2’a→5’)-2’,3’-ジデオキシ-2’,3’-イミノ-2’,3’-セコグアノシンを含む。
「ジストロフィン」は、桿状の細胞質タンパク質であり、細胞膜を通じて筋線維の細胞骨格を周囲の細胞外マトリックスへ連結するタンパク質複合体の非常に重要な部分であり、ジストロフィン(すなわちDMD)遺伝子によりコードされる。ジストロフィンは、複数の機能的ドメインを含む。例えば、ジストロフィンは、アミノ酸14~240周辺にアクチン結合ドメインを、およびアミノ酸253~3040周辺に中央桿状ドメインを含む。この大型の中央ドメインは、アルファ-アクチニンおよびスペクトリンとの相同性を有する、約109のアミノ酸からなる24個のスペクトリン様の3重ヘリックスエレメントで形成される。その繰り返しは典型的には、4つのプロリンに富む非繰り返しセグメント(ヒンジ領域とも呼ばれる)により中断される。繰り返し15および16は、ジストロフィンのタンパク質分解切断のための主要部位を提供すると考えられる18アミノ酸の伸長部により分離される。ほとんどの繰り返し同士の配列同一性は、10~25%の範囲である。1つの繰り返しは3つのアルファ-ヘリックス:1、2および3を含む。アルファ-ヘリックス1および3は各々、7つのヘリックスターンにより形成され、おそらく疎水性インタフェースを介してコイルドコイルとして相互作用している。アルファ-ヘリックス2はより複雑な構造を有し、4つおよび3つのヘリックスターンのセグメントにより形成され、グリシンまたはプロリン残基により分離される。各繰り返しは2つのエクソンによりコードされ、典型的にはアルファ-ヘリックス2の第1の部分におけるアミノ酸47と48との間のイントロンにより中断される。他のイントロンは、繰り返し中の異なる位置に存在し、通常、ヘリックス-3上に点在する。ジストロフィンはまた、アミノ酸3080~3360周辺に、粘菌(Dictyostelium discoideum)アルファ-アクチニンのC末端ドメインとの相同性を示す、システインに富むセグメント(すなわち280のアミノ酸のうち15のシステイン)などのシステインに富むドメインを含む。カルボキシ末端ドメインは、アミノ酸3361~3685周辺に存在する。
ジストロフィンのアミノ末端はF-アクチンと結合し、カルボキシ末端は筋細胞膜においてジストロフィン関連タンパク質複合体(DAPC)と結合する。DAPCはジストログリカン、サルコグリカン、インテグリンおよびカベオリンを含み、これらの構成要素のいずれかにおける変異により、常染色体遺伝性の筋ジストロフィーが発症する。ジストロフィンが存在しない場合、DAPCは不安定化し、それにより構成タンパク質のレベルが低下し、その結果、段階的な線維損傷および膜漏出に至る。デュシェンヌ型筋ジストロフィー(DMD)およびベッカー型筋ジストロフィー(BMD)などの多様な型の筋ジストロフィーにおいて、主に誤ったスプライシングに至る遺伝子配列の変異に起因して、筋細胞は、変形され、機能的に不完全な形状のジストロフィンを産生するか、またはジストロフィンを全く産生しなくなる。不完全なジストロフィンタンパク質のプレドミナントな発現、またはジストロフィンもしくはジストロフィン様タンパク質の完全な欠乏は、上記のように筋変性の急速な進行につながる。この点に関して、「不完全な」ジストロフィンタンパク質は、当技術分野において公知のように、DMDまたはBMDを有する特定の被験体において産生されるジストロフィンの形状により、または、検出可能なジストロフィンの欠如により特徴付けられ得る。
ジストロフィンタンパク質に関する「機能的」という用語は、野生型タンパク質とも称される、ジストロフィン遺伝子のエクソン1~79の全てに対応する配列を含むmRNA転写物に由来するタンパク質を含む。機能的なジストロフィンタンパク質とは、DMDまたは関連障害を有するある特定の被験体に存在する変形されたまたは「不完全な」形状のジストロフィンタンパク質と典型的に比較して、低減しなければデュシェンヌ型筋ジストロフィーに特徴的である筋組織の段階的分解を低減するのに十分な生物学的活性を有するジストロフィンタンパク質を一般に指す。機能的なジストロフィンタンパク質は、当技術分野で慣例的な技法により測定した場合に、野生型ジストロフィンのin vitroまたはin vivo生物学的活性の約10%、20%、30%、40%、50%、60%、70%、80%、90%または100%(それらの間の全ての整数を含む)を有し得る。1つの例として、in vitroでの筋肉培養物におけるジストロフィン関連活性は、筋管サイズ、筋原線維の組織化(または分裂)、収縮活性およびアセチルコリン受容体の自発的なクラスタリングにより測定できる(例えば、Brownら、Journal of Cell Science.112巻:209~216頁、1999年を参照されたい)。動物モデルも疾患の病因を検討するための有用な資源であり、ジストロフィン関連活性を試験する手段を提供する。DMD研究に最も広く使用されている動物モデルのうちの2つは、mdxマウスおよびゴールデンレトリバー筋ジストロフィー(GRMD)イヌであり、いずれもジストロフィンネガティブである(例えば、CollinsおよびMorgan、Int J Exp Pathol 84巻:165~172頁、2003年を参照されたい)。これらおよび他の動物モデルは、多様なジストロフィンタンパク質の機能的活性を測定するために使用できる。本発明のアンチセンスオリゴマー化合物のいくつかにより産生される形状などの切断型ジストロフィンも含まれる。
「機能的な」または「半機能的な」ジストロフィンタンパク質という用語は、切断型の転写物に対応する配列を含むmRNA転写物、例えばジストロフィン遺伝子のエクソン1~79のうちの全てではないエクソンを有するジストロフィンmRNA転写物に由来するタンパク質を含む。言い換えると、切断型のジストロフィンmRNAは、対応するジストロフィン遺伝子の1または複数のエクソンを除外し得る。切断型のジストロフィンmRNAは、マイクロジストロフィンタンパク質とも称される、切断または短縮型のジストロフィンタンパク質を発現し得る。
ミオスタチンタンパク質に関する「機能的な」という用語は、野生型タンパク質とも称される、ミオスタチン遺伝子のエクソン1、エクソン2およびエクソン3に対応する全ての配列を含むmRNA転写物に由来するタンパク質を含む。
非機能的、機能不全、または不活性なミオスタチンタンパク質は、エクソン1、エクソン2およびエクソン3の配列に対応する全長遺伝子の全部もしくは任意の一部を欠失するミオスタチンmRNA転写物に由来するタンパク質、または、イントロン1、イントロン2もしくは他のイントロン配列に対応する配列の全部もしくは一部を含むタンパク質、または、非機能的状態が、各エクソンに由来するような機能的な要素の欠失に関連する場合のタンパク質、または、さもなければ、その部分的または完全な配列を含む各イントロンを含むことに由来するタンパク質を含む。非機能的、機能不全、または不活性なミオスタチンタンパク質は、例えばエクソン2を除外するミオスタチンmRNA転写物に由来するタンパク質、および/または、野生型ミオスタチンタンパク質と比較して機能性が低下したタンパク質を含む。
このように、多様な実施形態では、機能的または半機能的なジストロフィンタンパク質の存在、発現または発現増加は、例えば修飾アンチセンスオリゴマーおよび/または本開示の治療剤により処置されたDMD患者由来の筋細胞の、例えばウェスタンブロット解析およびジストロフィン遺伝子の発現により決定できる。多様な実施形態では、修飾アンチセンスオリゴマーおよび/または本開示の治療剤による、DMDの処置を必要とするDMD筋細胞または被験体の処置は、例えば正常な細胞または正常な被験体で発現されるジストロフィンタンパク質の正常な量の約5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%または100%の量の機能的なジストロフィンタンパク質の発現をもたらし得る。
多様な実施形態では、DMDの処置を必要とする組織または被験体により発現されるジストロフィンまたは切断型ジストロフィンタンパク質の機能性は、例えば筋線維の数、筋肉量の増加、中心核を有する筋線維のパーセントおよび機能的なジストロフィンタンパク質の量の、未処置の同等物と比較した、免疫組織化学的分析によって決定し得る。DMDの処置を必要とする被験体のジストロフィンまたは切断型ジストロフィンタンパク質の機能性は、筋肉量および握力の測定を含む運動機能試験などの、物理的および生理学的試験によりさらに分析し得る。
一部の実施形態では、ジストロフィン治療剤は、目的の細胞におけるジストロフィン発現を回復させる。ジストロフィン合成または産生の「回復」という用語は、一般には、本明細書に記載されるエテプリルセンによる処置後に筋ジストロフィーを有する患者における、切断型ジストロフィンを含めたジストロフィンタンパク質の産生を指す。一部の実施形態では、処置により、患者における新規ジストロフィン産生の、1%、5%、10%、20%、30%、40%、50%、60%、70%、80%、90%または100%(これらの間の全ての整数を含む)の増加がもたらされる。一部の実施形態では、処置により、ジストロフィン陽性線維の数が、被験体において、正常値の少なくとも20%、約30%、約40%、約50%、約60%、約70%、約80%、約90%または約95%~100%に増加する。他の実施形態では、処置により、ジストロフィン陽性線維の数が、被験体において、正常値の約20%~約60%、または約30%~約50%に増加する。処置後の患者におけるジストロフィン陽性線維のパーセントは、公知の技法を使用して筋生検により決定できる。例えば、筋生検は適切な筋肉、例えば患者における上腕二頭筋から採取し得る。
陽性ジストロフィン線維のパーセンテージの分析は、処置前および/または処置後または一連の処置中の時点で行ってもよい。一部の実施形態では、処置後の生検は、処置前生検と対側の筋肉から採取される。処置前および処置後のジストロフィン発現の検討は、ジストロフィンに関するいかなる適切なアッセイを使用して行ってもよい。一実施形態では、筋生検から得た組織切片に対して、ジストロフィンのマーカーである抗体、例えばモノクローナルまたはポリクローナル抗体を使用して免疫組織化学的検出を実施する。例えば、ジストロフィンに対して非常に感受性の高いマーカーであるMANDYS106抗体が使用できる。いかなる適切な二次抗体も使用し得る。
一部の実施形態では、ジストロフィン陽性線維のパーセントは、計数される全ての線維で陽性線維数を除算することにより算出される。正常な筋肉試料は、ジストロフィン陽性線維が100%である。したがって、ジストロフィン陽性線維のパーセントは、正常値に対するパーセンテージとして表示できる。処置前筋肉ならびにリバータント(revertant)線維におけるジストロフィンの微量レベルの存在を補正(control)するため、処置後筋肉におけるジストロフィン陽性線維を計数するときには、各患者から得た処置前筋肉の切片を使用してベースラインを設定できる。これは、その患者における処置後筋肉の切片におけるジストロフィン陽性線維を計数するための閾値として使用され得る。他の実施形態では、抗体染色した組織切片は、Bioquant画像解析ソフトウェア(Bioquant Image Analysis Corporation、ナッシュビル、TN)を使用するジストロフィンの定量のために使用することもできる。ジストロフィンの蛍光シグナル強度の合計を、正常値に対するパーセンテージとして報告することができる。さらに、モノクローナルまたはポリクローナル抗ジストロフィン抗体によるウェスタンブロット解析を使用して、ジストロフィン陽性線維のパーセンテージを決定することができる。例えば、Novacastra製の抗ジストロフィン抗体NCL-Dys1を使用してもよい。ジストロフィン産生はまた、逆転写ポリメラーゼ連鎖反応(RT-PCR)によって測定することもできる。機能的なジストロフィンタンパク質を産生するジストロフィン遺伝子を測定するよう、プライマーを設計することができる。ジストロフィン陽性線維のパーセンテージはまた、サルコグリカン複合体(□□□)の構成要素および/またはニューロンのNOSの発現を測定することにより分析できる。
一部の実施形態では、処置により、処置を行わない場合に予想されるDMDを有する患者における、進行性の呼吸筋機能不全および/または呼吸筋不全が遅延され、または減少する。一部の実施形態では、処置により、DMDを有する患者における呼吸筋機能が安定する。一実施形態では、エテプリルセンによる処置により、処置を行わない場合に予想される換気援助の必要性が減少するか、または除去され得る。一実施形態では、疾患の経過を追跡するための呼吸機能の測定、ならびに治療的介入の可能性の評価は、最大吸気圧(MIP)、最大呼気圧(MEP)および努力性肺活量(FVC)を含む。MIPおよびMEPは、それぞれ、個人の吸入および呼息の間に発生しうる圧力のレベルを測定し、呼吸筋力の精度の高い測定法である。MIPは、横隔膜筋肉の脆弱性の測定法である。
一部の実施形態では、処置により、被験体の歩行能力が安定化し、維持され、改善され、または向上し得る(例えば歩行運動の安定化)。一部の実施形態では、処置により、例えば、McDonaldら(Muscle Nerve、2010年;42巻:966~74頁;Muscle Nerve、2010年;41巻:500~10頁、その内容は参照によりその全体において本明細書に組み込まれる)によって記載された6分間歩行試験(6MWT)によって測定した場合に、患者の安定な歩行距離が維持され、増加され、またはその減少が低減される。6MWTは、疾患状態の変化の表れとして経時的な歩行機能の変化を特徴付ける歩行運動に着目した臨床的に有意義なエンドポイントである。
6分間歩行距離(6MWD)の変化は、絶対値、変化パーセンテージまたは予測値(%)の変化として表され得る。健常者の典型的な能力に対する、6MWTにおけるDMD患者の能力は、予測値(%)を算出することによって決定できる。例えば、予測6MWD(%)は、男性の場合、以下の式を使用して算出され得る:196.72+(39.81×年齢)-(1.36×年齢2)+(132.28×身長(メートル))。女性の場合、予測6MWD(%)は、以下の式を使用して算出され得る:188.61+(51.50×年齢)-(1.86×年齢2)+(86.10×身長(メートル))(Henricsonら PLoS Curr.、2012年、2版、その内容は参照によりその全体において本明細書に組み込まれる)。
歩行運動は、ノーススター歩行能力評価(North Star Ambulatory Assessment)(NSAA)などの多様な方法により測定できる。NSAAは、DMDを有する歩行可能な男児を評価するために、North Start Clinical NetworkのPhysiotherapy Assessment and Evaluation Groupにより開発され、2~0でスコア化される活動リストを提供する(正常:2および「独立して達成できない」:0)(2006~2011年 MDC/North Star Clinical Network)。これらの活動は、最低3秒立っていられる~箱を上り下りできる~走れる、にわたる。ある特定の実施形態では、エテプリルセンによる処置により、例えばNSAAによって決定した場合に、歩行運動が維持、安定化、上昇または改善され得る。
本発明では、修飾アンチセンスオリゴマーなどの治療剤を使用することで、エクソン2を含むミオスタチンmRNAの減少が誘導され、デュシェンヌ型筋ジストロフィーの症状(例えば機能的なミオスタチンタンパク質の減少)が、未処置と比較して、約30%~約100%の範囲、または機能性に関して上記で開示したパーセンテージで改善される。症状のかかる改善は、ミクロのレベル(例えば、免疫組織化学、免疫蛍光法、ウェスタンブロット解析などにより測定されるミオスタチンタンパク質発現の減少;筋肉の成長の増加;筋肉機能の回復)および生理学的なレベル(例えば、身体検査により評価される運動機能の改善)で観察され得る。
修飾アンチセンスオリゴマーは、ジストロフィンプレmRNAのプロセシングの間にエクソンスキッピングを誘導するために使用されるが、その際、ジストロフィンプレmRNAは、1もしくは複数の遺伝子変異を有するエクソンを含むか、またはジストロフィン遺伝子の1もしくは複数の領域が削除されており、それにより、デュシェンヌ型筋ジストロフィーに関連する症状および関連障害が改善される(例えば機能的または半機能的なジストロフィンタンパク質の回復)。機能的または半機能的なジストロフィンタンパク質は、未処置と比較して、約30%~約100%の範囲、または機能性に関して上記で開示したパーセンテージで増加し得る。症状のかかる改善は、ミクロのレベル(例えば、免疫組織化学、免疫蛍光法、ウェスタンブロット解析などにより測定されるジストロフィンタンパク質発現の増加;筋肉の成長の増加;筋肉機能の回復)および生理学的なレベル(例えば、身体検査により評価される運動機能の改善)で観察され得る。
「ヌクレオチド」という用語は、ヌクレオ塩基と、糖と、少なくとも1つのリン酸基(例えば、ホスホジエステル連結基)とを含む、天然に存在するヌクレオチドを指す。
「ヌクレオチド類似体」という用語は、天然に存在するヌクレオチドの誘導体、または天然に存在するヌクレオチドに対する修飾、例えば、少なくとも1つの修飾を含むヌクレオチドを指す。このような修飾は、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せのうちの少なくとも1つを含みうる。当業者は、修飾を、ヌクレオチドサブユニットのうちの任意の1つの構成要素(例えば、修飾糖)に関して指定する場合、ヌクレオチドサブユニットのうちの、指定されていない部分は、依然として非修飾(例えば、非修飾ヌクレオシド間連結、非修飾ヌクレオ塩基)でありうることを察知すると予想される。
「オリゴヌクレオチド」、「オリゴマー」、「オリゴ」、「アンチセンスオリゴヌクレオチド」、「アンチセンスオリゴマー」、「修飾アンチセンスオリゴマー」および「アンチセンスオリゴ」という用語、ならびにこれらの他の適切な組合せおよび派生語は、ヌクレオチドまたはヌクレオチド類似体の直鎖状配列であって、1または複数のヌクレオ塩基が、ワトソン-クリック塩基対合により、標的配列と称される、オリゴマーが指向される標的RNAの部分とハイブリダイズして、標的配列内で、オリゴマー:RNAヘテロ二重鎖を形成しうる直鎖状配列を指す。具体的に、「アンチセンス」、「オリゴヌクレオチド」、「オリゴマー」、「オリゴ」、および「化合物」という用語は、このようなオリゴマーを指すように、多様な組合せで、かつ、互換的に使用することができる。ヌクレオチドの部分を含む環式サブユニットは、リボースまたは別の五炭糖、糖類似体に基づく場合もあり、ある特定の実施形態では、修飾糖、例えば、モルホリノ基である場合もある(下記のモルホリノベースのオリゴマーについての記載を参照されたい)。
オリゴマーに言及する場合の、「修飾された」、「天然に存在しない」、または「類似体」という用語、ならびにこれらの他の適切な組合せおよび派生形は、(i)修飾ヌクレオシド間連結、例えば、天然に存在するオリゴヌクレオチド内に見出される、標準的なホスホジエステル連結以外のヌクレオシド間連結、(ii)修飾糖部分、例えば、天然に存在するオリゴヌクレオチド内に見出される、リボース部分もしくはデオキシリボース部分以外の部分、または(iii)前出の組合せから選択される、少なくとも1つの修飾を有する、1または複数のヌクレオチドサブユニットを有するオリゴマーを指す。多様な実施形態では、修飾ヌクレオシド間連結は、ホスホロチオエートヌクレオシド間連結、ホスホルアミデートヌクレオシド間連結、ホスホロジアミデートヌクレオシド間連結およびホスホロトリアミデートヌクレオシド間連結から選択される。さらなる実施形態では、ホスホロジアミデートヌクレオシド間連結は、(1,4-ピペラジン)-1-イル部分、置換(1,4-ピペラジン)-1-イル部分、4-アミノピペリジン-1-イル部分、または置換4-アミノピペリジン-1-イル部分に共有結合したリン原子を含む。多様な実施形態では、修飾糖部分は、ペプチド核酸(PNA)サブユニット、ロックト核酸(LNA)サブユニット、2’O,4’C-エチレン架橋核酸(ENA)サブユニット、トリシクロDNA(tc-DNA)サブユニット、2’O-メチルサブユニット、2’O-メトキシエチルサブユニット、2’-フルオロサブユニット、2’-O-[2-(N-メチルカルバモイル)エチル]サブユニット、およびモルホリノサブユニットから選択される。
ヌクレオシド間連結への修飾は、オリゴマーの、少なくとも2つの糖部分および/または修飾糖部分の間の修飾でありうる。ヌクレオチド類似体は、ワトソン-クリック塩基対合により、天然に存在するオリゴヌクレオチド塩基への水素結合が可能な塩基を担い、ここで、類似体は、オリゴマー類似体分子と、天然に存在するオリゴヌクレオチド(例えば、一本鎖RNAまたは一本鎖DNA)内の塩基との間で、配列特異的に、このような水素結合を可能とするように、塩基を提示する。例示的な類似体は、実質的に非荷電の、リンを含有するヌクレオシド間連結を有する類似体である。
「ヌクレアーゼ耐性」オリゴマーとは、そのヌクレオシド間連結が、非ハイブリダイズ形態でも、ハイブリダイズ形態でも、ヌクレアーゼによる切断であって、体内の、一般的な、細胞外ヌクレアーゼおよび細胞内ヌクレアーゼによる(例えば、3’-エクソヌクレアーゼなどのエクソヌクレアーゼ、エンドヌクレアーゼ、RNアーゼHによる)切断に対して実質的に耐性であるオリゴマーを指す;すなわち、オリゴマーは、オリゴマーが曝露される、体内の正常なヌクレアーゼ条件下で、ヌクレアーゼによる切断を、ほとんどまたは全く示さない。「ヌクレアーゼ耐性ヘテロ二重鎖」とは、ヘテロ二重鎖が、細胞内ヌクレアーゼおよび細胞外ヌクレアーゼによる、in vivoにおける分解であって、二本鎖RNA/RNA複合体または二本鎖RNA/DNA複合体を切断することが可能な分解に対して、実質的に耐性となるように、修飾アンチセンスオリゴマーの、その相補的な標的への結合により形成されるヘテロ二重鎖を指す。「ヘテロ二重鎖」とは、修飾アンチセンスオリゴマーと、標的RNAの相補的部分との二重鎖を指す。例えば、ヌクレアーゼ耐性オリゴマーは、本明細書で記載される修飾アンチセンスオリゴマーでありうる。
「ヌクレオ塩基」(Nu)、「塩基対合部分」、または「塩基」という用語は、自然発生または「生来」のDNAまたはRNA(例えば、ウラシル、チミン、アデニン、シトシン、およびグアニン)のほか、天然に存在するプリンおよびピリミジンの類似体であって、結合アフィニティーなど、改善された特性を、オリゴマーへと付与する類似体において見出される、プリン塩基またはピリミジン塩基を指すように、互換的に使用される。例示的な類似体は、ヒポキサンチン(ヌクレオシドであるイノシンの塩基成分);2,6-ジアミノプリン;5-メチルシトシン;C5-プロピニル修飾ピリミジン;10-(9-(アミノエトキシ)フェノキサジニル(Gクランプ)などを含む。
塩基対合部分のさらなる例は、それらのそれぞれのアミノ基を、アシル保護基で保護した、ウラシル、チミン、アデニン、シトシン、グアニン、およびヒポキサンチン(イノシン)、2-フルオロウラシル、2-フルオロシトシン、5-ブロモウラシル、5-ヨードウラシル、2,6-ジアミノプリン、アザシトシン、シュードイソシトシンおよびシュードウラシルなどのピリミジン類似体、ならびに8-置換プリン、8-置換キサンチン、または8-置換ヒポキサンチン(後者の2つは、天然の分解産物である)など、他の修飾ヌクレオ塩基を含むがこれらに限定されない。それらの内容が参照により本明細書に組み込まれる、ChiuおよびRana、RNA、2003年、9巻、1034~1048頁、Limbachら、Nucleic Acids Research、1994年、22巻、2183~2196頁;ならびにRevankarおよびRao、Comprehensive Natural Products Chemistry、1999年、7巻、313頁において開示されている修飾ヌクレオ塩基もまた想定される。
塩基対合部分のさらなる例は、1または複数のベンゼン環を付加したサイズ拡大型ヌクレオ塩基を含むがこれらに限定されない。核塩基置換(nucleic base replacement)は、以下の例に記載されている:Glen Researchのカタログ(www.glenresearch.com);Krueger ATら、Acc. Chem. Res.、2007年、40巻、141~150頁;Kool, ET、Acc. Chem. Res.、2002年、35巻、936~943頁;Benner S.A.ら、Nat. Rev. Genet.、2005年、6巻、553~543頁;Romesberg, F.E.ら、Curr. Opin. Chem. Biol.、2003年、7巻、723~733頁;Hirao, I.、Curr. Opin. Chem. Biol.、2006年、10巻、622~627頁(各例の内容は、本明細書において参考として援用される)。これらは、本明細書で記載される多様なオリゴマーの合成に有用であると想定される。サイズ拡大型ヌクレオ塩基の例を、下記:
に示す。
に示す。
リボース、糖類似体、修飾糖、またはモルホリノに共有結合的に連結されたヌクレオ塩基は、ヌクレオシドを含む。「ヌクレオチド」は、少なくとも1つの連結リン酸基と併せたヌクレオシドを含む。リン酸基は、オリゴマーを形成するように、隣接するヌクレオチドへの共有結合的連結を含む。こうして、ヌクレオチドのリン酸基は一般に、「ヌクレオシド間連結」を形成すると称する。したがって、ヌクレオチドは、本明細書でさらに記載されるヌクレオシドと、ヌクレオシド間連結とを含む。一部の実施形態では、本開示の修飾アンチセンスオリゴマーは、サブユニットを含み、ここで、「サブユニット」は、天然に存在するヌクレオチド、本明細書で記載されるヌクレオチド類似体、およびこれらの組合せを含む。ある特定の実施形態では、本開示の修飾アンチセンスオリゴマーは、サブユニットを含み、ここで、少なくとも1つのサブユニットは、ヌクレオチド類似体である。
「配列同一性」、「配列相同性」および「相補性」という用語(例えば「~と50%同一な配列」、「~と50%相同な配列」および「~と50%相補的な配列」)は、核酸に関しては、配列が、ヌクレオチド対ヌクレオチドベースで、比較ウィンドウにわたり同一である程度を指す。「同一性百分率」、「相同性百分率」および「~と~百分率相補的な」は、2つの最適にアラインメントされた配列を、比較ウィンドウにわたり比較し、両方の配列内で、同一な核酸塩基(例えば、A、T、C、G、I)が生じる位置の数を決定して、マッチさせた位置の数をもたらし、マッチさせた位置の数を、比較ウィンドウ内の位置の総数(すなわち、ウィンドウサイズ)で除し、結果に100を乗じて、配列同一性の百分率をもたらすことにより計算することができる。比較ウィンドウをアラインメントするための、配列の最適のアラインメントは、コンピュータへのアルゴリズム(Wisconsin Genetics Software Package Release 7.0、Genetics Computer Group、575 Science Drive Madison、Wis.、USAにおける、GAP、BESTFIT、FASTA、およびTFASTA)の実行により行うこともでき、精査と、選択される多様な方法のうちのいずれかにより生成される、最良のアラインメント(すなわち、比較ウィンドウにわたり最高の相同性百分率をもたらすアラインメント)とにより行うこともできる。また、例えば、Altschulら、Nucl. Acids Res.、25巻:3389頁、1997年により開示されている通り、BLASTファミリーのプログラムも参照することができる。多様な実施形態では、本開示の修飾アンチセンスオリゴマーは、表1(配列番号1~3)および表2(配列番号4~15)におけるターゲティング配列に対して、少なくとも70%、75%、80%、85%、90%、95%、99%、または100%の配列同一性を有しうる。
本明細書で使用される通り、融点(Tm)が、40℃、45℃、50℃を実質的に超え、多様な実施形態では、60℃~80℃またはこれを超える生理学的条件下で、オリゴマーのターゲティング配列が、標的領域とハイブリダイズする場合に、オリゴマーは、オリゴヌクレオチドの標的領域と、「特異的にハイブリダイズする」。このようなハイブリダイゼーションは、ストリンジェントなハイブリダイゼーション条件に対応することが好ましい。所与のイオン強度およびpHにおいて、Tmは、ターゲティング配列のうちの50%が、標的領域における相補的な配列とハイブリダイズする温度である。このようなハイブリダイゼーションは、修飾アンチセンスオリゴマーの、標的領域への「ほぼ(near)」または「実質的な」相補性により生じうるほか、正確な相補性によっても生じうる。一部の実施形態では、オリゴマーは、標的領域と、約50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、99%、または100%でハイブリダイズしうる。
本明細書で使用される、「サブユニット」という用語は、天然に存在するヌクレオチド、または少なくとも1つの修飾を含む、天然に存在するヌクレオチドを指す。修飾は、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せのうちの少なくとも1つを含みうる。さらなる実施形態では、修飾は、修飾ヌクレオ塩基を含みうる。
本明細書で使用するとき、「十分な長さ」という用語は、プレmRNA内の標的領域内の少なくとも20~50の連続ヌクレオ塩基と相補的である修飾アンチセンスオリゴマーを指し、かかる相補性は、エクソン内の標的領域の完全に内部に存在してもよく、または、イントロン/エクソンもしくはエクソン/イントロン領域を横切るスプライス接合部にわたってもよい。複数の実施形態では、十分な長さは、プレmRNA内の標的領域の少なくとも12の連続ヌクレオ塩基と相補的である修飾アンチセンスオリゴマーを指す場合があり、かかる相補性は、エクソン内の標的領域の完全に内部に存在してもよく、または、イントロン/エクソンもしくはエクソン/イントロン領域を横切るスプライス接合部にわたってもよい。
例えば、修飾ミオスタチンアンチセンスオリゴマーは、ミオスタチンプレmRNAのイントロン1/エクソン2、エクソン2、またはエクソン2/イントロン2と相補的であってもよい。多様な実施形態では、修飾ミオスタチンアンチセンスオリゴマーは、ミオスタチンプレmRNA配列の標的領域と特異的にハイブリダイズすることが可能な少なくともいくつかのヌクレオチドを含む。好ましくは、十分な長さのオリゴマーは、これらの範囲の間の全ての整数を含めて、12~40ヌクレオチド、12~30ヌクレオチド、12~15ヌクレオチド、12~20ヌクレオチド、15~20ヌクレオチド、15~22ヌクレオチド、12~22ヌクレオチドの長さである。一部の実施形態では、ミオスタチンアンチセンスオリゴマーは、約12~約40または約12~約30塩基の長さである。一部の実施形態では、アンチセンスオリゴマーは、約12~約25、約15~約25または約15~約20塩基の長さである。一部の実施形態では、ミオスタチンアンチセンスオリゴマー配列は、少なくとも約12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39または40の連続塩基または非連続塩基であって、表1の標的配列(例えば、配列番号1、配列番号2または配列番号3、または配列番号X、配列番号Yまたは配列番号Zの少なくとも一部にわたる配列)と相補的な連続塩基または非連続塩基を含む。
修飾ジストロフィンアンチセンスオリゴマーは、エクソン7、エクソン8、エクソン9、エクソン19、エクソン23、エクソン44、エクソン45、エクソン50、エクソン51、エクソン52、エクソン53またはエクソン55内に完全にある標的領域と相補的であってもよい。多様な実施形態では、修飾ジストロフィンアンチセンスオリゴマーは、ジストロフィンプレmRNA配列の標的領域と特異的にハイブリダイズすることが可能な少なくともいくつかのヌクレオチドを含む。十分な長さのオリゴマーは、17~50ヌクレオチド、17~40ヌクレオチド、14~25ヌクレオチド、15~30ヌクレオチド、17~30ヌクレオチド、17~27ヌクレオチド、10~27ヌクレオチド、10~25ヌクレオチドまたは10~20ヌクレオチドの長さであることが、これらの間の全ての整数を含めて、好ましい。一部の実施形態では、アンチセンスオリゴマーは、約17~約40または約10~約30塩基の長さである。一部の実施形態では、アンチセンスオリゴマーは、約14~約25または約17~約27塩基の長さである。一部の実施形態では、アンチセンスオリゴマー配列は、少なくとも約10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39または40の連続塩基または非連続塩基であって、表2の標的配列(例えば配列番号4~15)と相補的な連続塩基または非連続塩基を含む。
本明細書で使用するとき、「被験体」または「それを必要とする被験体」という用語は、ヒト被験体などの哺乳動物被験体を含む。例示的な哺乳動物被験体は、デュシェンヌ型筋ジストロフィーおよび関連障害を有するか、またはこれを有する危険性がある。本明細書で使用するとき、「筋ジストロフィー」、「デュシェンヌ型筋ジストロフィー」および「関連障害」という用語は、ミオスタチンタンパク質の過剰発現、または罹患個体におけるジストロフィン遺伝子の遺伝子変異を多くの場合特徴とするヒト常染色体劣性疾患を指す。一部の実施形態では、デュシェンヌ型筋ジストロフィーおよび関連障害は、ベッカー型筋ジストロフィー、肢帯筋ジストロフィー、先天性筋ジストロフィー、顔面肩甲上腕筋ジストロフィー、筋緊張性筋ジストロフィー、眼球咽頭筋ジストロフィー、末梢型筋ジストロフィー、エメリー・ドライフス筋ジストロフィー、筋肉消耗状態または障害、例えばAIDS、がんまたは化学療法関連の筋肉消耗、および線維症または線維症関連障害(例えば骨格筋線維症)を含むが、これらに限定されない。
本明細書で使用される「患者」は、本明細書で記載される通りに処置され得る症状を呈示するかまたは症状を呈示する危険性がある任意の個人、例えば、DMDもしくはBMD、またはこれらの状態に関連する症状のいずれか(例えば筋線維損失)を有するか、またはそれを有する危険性がある被験体などを含む。
本明細書で使用される「小児患者」は、1~21歳(上下限値を含む)の患者である。一部の実施形態では、小児患者は7~21歳(例えば7、8、9、10、11、12、13、14、15、16、17、18、19、20または21歳)の患者である。一部の実施形態では、小児患者は7歳未満の患者である。一部の実施形態では、小児患者は7歳またはこれを超える患者である。
本明細書で使用するとき、「標的」または「標的領域」という用語は、ミオスタチンまたはジストロフィンプレmRNAなどのプレmRNA転写物内の領域を指す。多様な実施形態では、ミオスタチン標的領域は、ミオスタチンプレmRNAのイントロン1/エクソン2、エクソン2、またはエクソン2/イントロン2を含む領域である。多様な実施形態では、ジストロフィン標的領域は、エクソン7、エクソン8、エクソン9、エクソン19、エクソン23、エクソン44、エクソン45、エクソン50、エクソン51、エクソン52、エクソン53またはエクソン55のうちの1または複数を含む領域である。
多様な実施形態では、「ターゲティング配列」という用語は、修飾アンチセンスオリゴマー内または修飾アンチセンスオリゴマー類似体内の配列であって、プレmRNA転写物内の標的配列と相補的な配列を指す。修飾アンチセンスオリゴマーの全配列が、標的配列と相補的な場合もあり、修飾アンチセンスオリゴマーの一部分だけが、標的配列と相補的な場合もある。例えば、12~50塩基を有するオリゴマー内の、約7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49または50個は、プレmRNA転写物内の標的領域と相補的な配列(例えば、「ターゲティング配列」)を含有しうる。ターゲティング配列は、オリゴマー内の連続塩基から形成されることが典型的であるが、代替的に、例えば、オリゴマーの反対側の末端から一体とされると、標的配列にわたる配列を構成する非連続配列から形成される場合もある。
「ターゲティング配列」は、標的配列に対して「ほぼ」または「実質的な」相補性を有し得、それでもなお、その意図した目的のため、例えば、遺伝子変異を有する1または複数のエクソンを排除したジストロフィンmRNA発現のレベルを上昇させる、または機能的もしくは半機能的なジストロフィンタンパク質の発現を増加させるために機能し得る。ミオスタチンの場合、ターゲティング配列は、エクソン2を含むミオスタチンmRNAの発現レベルを低下させるか、または機能的なミオスタチンタンパク質の発現を減少させるように機能し得る。本開示における修飾アンチセンスオリゴマー化合物は、標的配列に対して、多くても10ヌクレオチドに1つのミスマッチ、または20ヌクレオチドに1つのミスマッチを有することが好ましい。あるいは、本明細書の修飾アンチセンスオリゴマーは、本明細書で示す例示的な標的配列に対する、少なくとも90%の配列相同性、少なくとも95%の配列相同性、少なくとも99%の配列相同性または100%の配列相同性を有する。
ジストロフィンの場合、ターゲティング配列は、配列番号76~3485から選択される配列を含み得るか、配列番号76~3485から選択されるか、配列番号76~3485から選択される配列の少なくとも10の連続ヌクレオチドの断片であるか、または配列番号76~3485から選択される配列に対する少なくとも90%の配列同一性を有する変異体であり、各Xはウラシル(U)またはチミン(T)から独立に選択され、各Yはシトシン(C)または5-メチルシトシン(5mC)から独立に選択される。一部の実施形態では、配列番号76~3485の各Xはチミン(T)であり、配列番号76~3485の各Yはシトシン(C)である。一部の実施形態では、ターゲティング配列は、配列番号76を含み得る。
ミオスタチンの場合、ターゲティング配列は、配列番号16~75から選択される配列を含み得るか、配列番号16~75から選択されるか、配列番号16~75から選択される配列の少なくとも10の連続ヌクレオチドの断片であるか、または配列番号16~75から選択される配列に対する少なくとも90%の配列同一性を有する変異体であり、各Xはウラシル(U)またはチミン(T)から独立に選択され、各Yはシトシン(C)または5-メチルシトシン(5mC)から独立に選択される。一部の実施形態では、配列番号16~75の各Xはチミン(T)であり、配列番号16~75の各Yはシトシン(C)である。
一部の実施形態では、ミオスタチンターゲティング配列は、
a)配列番号71(YYAGYYYAXYXXYXYYXGGXYYXGG)[Zは25である];
b)配列番号72(YAYXXAYYAGYYYAXYXXYXYYXGG)[Zは25である];
c)配列番号73(YYAYXXGYAXXAGAAAAXYAGY)[Zは22である];
d)配列番号74(GYATTAGAAAATYAGYTATAAATG)[Zは24である];および
e)配列番号75(YYATYYGYTTGYATTAGAAAGTYAGY)[Zは26である]
から選択され、各Xはウラシル(U)またはチミン(T)から独立に選択され、各Yはシトシン(C)または5-メチルシトシン(5mC)から独立に選択される。一部の実施形態では、配列番号71~75の各Xはチミン(T)であり、配列番号71~75の各Yはシトシン(C)である。
a)配列番号71(YYAGYYYAXYXXYXYYXGGXYYXGG)[Zは25である];
b)配列番号72(YAYXXAYYAGYYYAXYXXYXYYXGG)[Zは25である];
c)配列番号73(YYAYXXGYAXXAGAAAAXYAGY)[Zは22である];
d)配列番号74(GYATTAGAAAATYAGYTATAAATG)[Zは24である];および
e)配列番号75(YYATYYGYTTGYATTAGAAAGTYAGY)[Zは26である]
から選択され、各Xはウラシル(U)またはチミン(T)から独立に選択され、各Yはシトシン(C)または5-メチルシトシン(5mC)から独立に選択される。一部の実施形態では、配列番号71~75の各Xはチミン(T)であり、配列番号71~75の各Yはシトシン(C)である。
多様な実施形態では、ターゲティング配列の少なくとも1つのXはTである。多様な実施形態では、ターゲティング配列の各XはTである。
多様な実施形態では、ターゲティング配列の少なくとも1つのXはUである。多様な実施形態では、ターゲティング配列の各XはUである。
多様な実施形態では、ターゲティング配列の少なくとも1つのYは5mCである。多様な実施形態では、ターゲティング配列の各Yは5mCである。
多様な実施形態では、ターゲティング配列の少なくとも1つのYはCである。多様な実施形態では、ターゲティング配列の各YはCである。
多様な実施形態では、配列番号16~75および配列番号76~3485の少なくとも1つのXはTである。多様な実施形態では、配列番号16~75および配列番号76~3485の各XはTである。
多様な実施形態では、ターゲティング配列の少なくとも1つのXはUである。多様な実施形態では、配列番号16~75および配列番号76~3485の各XはUである。
多様な実施形態では、配列番号16~75および配列番号76~3485の少なくとも1つのYは5mCである。多様な実施形態では、配列番号16~75および配列番号76~3485の各Yは5mCである。
多様な実施形態では、配列番号16~75および配列番号76~3485の少なくとも1つのYはCである。多様な実施形態では、配列番号16~75および配列番号76~3485の各YはCである。
本明細書で使用される「TEG」、「トリエチレングリコールテール」または「EG3」という用語は、例えば、その3’末端または5’末端でオリゴマーにコンジュゲートしたトリエチレングリコール部分を指す。例えば、一部の実施形態では、「TEG」は、例えば、式(I)、(IV)、(V)、(VI)、(VII)および(VIII)の化合物のTが、式:
のものであるものを含む。
のものであるものを含む。
本明細書で使用される、治療剤または組成物の「治療有効量」または「有効量」という用語は、組成物が有効な処置のために、障害の防止または処置において有効な量を指す。「障害」とは、BMD、肢帯筋ジストロフィー、先天性筋ジストロフィー、顔面肩甲上腕筋ジストロフィー、筋緊張性筋ジストロフィー、眼球咽頭筋ジストロフィー、末梢型筋ジストロフィー、エメリー・ドライフス筋ジストロフィー、筋肉消耗状態または障害、例えばAIDS、がんまたは化学療法関連の筋肉消耗、および線維症または線維化関連障害(例えば骨格筋線維症)などのあらゆるデュシェンヌ型筋ジストロフィーまたは関連障害を指す。
本明細書で使用される「~を定量化すること」、「定量化」という用語、または他の類縁の語は、核酸、オリゴヌクレオチド、オリゴマー、ペプチド、ポリペプチド、またはタンパク質の、数量、質量、または単位容量中の濃度を決定することを指す。
多様な実施形態では、本明細書で使用される「処置」という用語は、被験体(例えば、ヒトなどの哺乳動物)または細胞の処置(処理)であって、被験体または細胞の現在の経過を変更する処置を含む。処置は、医薬組成物の投与を含むがこれに限定されず、予防的に実施することもでき、病理学的事象の開始または病因作用物質との接触に後続して実施することもできる。また、処置される疾患もしくは状態の進行速度の低減、この疾患もしくは状態の発症の遅延、またはその発症の重症度の軽減を指向しうる「予防的」処置も含まれる。「処置」または「予防」とは、必ずしも、疾患もしくは状態、またはこれらの関連する症状の、完全な根絶、治癒、または防止を指し示すものではない。
II.プレmRNA転写物のスプライシングのモジュレーション
例示を目的とし、理論に束縛されずに述べると、治療剤が修飾アンチセンスオリゴマーである場合、これらは、スプライソソームの作用および成熟mRNA転写物の産生を阻害するなどにより、プレmRNAのプロセシングの遮断、阻害、またはモジュレーションを促進すると考えられ、また、標的としたmRNAの分解も誘導しうる。一部の例では、スプライソソーム(spliceosome)がエクソン/イントロンスプライス接合部に結合するの
を阻害して、エクソン/イントロンスプライス接合部がスキップされ、mRNA転写物から1つまたは複数のエクソンが除去されるようにすることができる。野生型mRNA転写物より1つまたは複数少ないエクソンを有する成熟mRNA転写物は、オープンリーディングフレームを保持するmRNA転写物をもたらし得、それにより、mRNA転写物は、分解されるのでなく、機能的なタンパク質へと翻訳されうる。野生型mRNAより少ないエクソンを有するmRNA転写物から翻訳されたタンパク質は、結果として、野生型mRNA転写物から転写されたタンパク質より少ないアミノ酸残基を含む転写タンパク質となり得る。野生型タンパク質より少ないアミノ酸残基で構成された機能的なタンパク質は、野生型タンパク質と同じまたは同様の活性/機能性を有し得る。修飾アンチセンスオリゴマーは、それがハイブリダイズする標的配列または標的領域「を指向する」またはこれら「に対してターゲティングされた」ということができる。ある特定の実施形態では、標的配列はプレmRNAの3’スプライス接合部位もしくは5’スプライス接合部位を含む領域、分岐点、エクソンのスプライシングエンハンサー(ESE)もしくはイントロンのスプライシングエンハンサー(ISE)、またはスプライシングの調節に関与する他の配列を含む。イントロン内では、ドナー部位(イントロンの5’末端)およびアクセプター部位(イントロンの3’末端)が、スプライシングに必要である。スプライスドナー部位は、イントロンの5’末端にあるほとんど不変の配列GUを、より大きい、それほど高度に保存されていない領域内に含む。イントロンの3’末端にあるスプライスアクセプター部位は、ほとんど不変のAG配列によってイントロンを終結させる。標的配列は、エクソン内に完全にあり標的配列のいかなる部分もプライス接合部にわたらないか、エクソン/イントロンスプライス接合部内にあるか、またはエクソン/イントロンスプライス接合部にわたる、配列を含み得る。標的配列は、エクソン/イントロンドナースプライス部位を含み得る。
例示を目的とし、理論に束縛されずに述べると、治療剤が修飾アンチセンスオリゴマーである場合、これらは、スプライソソームの作用および成熟mRNA転写物の産生を阻害するなどにより、プレmRNAのプロセシングの遮断、阻害、またはモジュレーションを促進すると考えられ、また、標的としたmRNAの分解も誘導しうる。一部の例では、スプライソソーム(spliceosome)がエクソン/イントロンスプライス接合部に結合するの
を阻害して、エクソン/イントロンスプライス接合部がスキップされ、mRNA転写物から1つまたは複数のエクソンが除去されるようにすることができる。野生型mRNA転写物より1つまたは複数少ないエクソンを有する成熟mRNA転写物は、オープンリーディングフレームを保持するmRNA転写物をもたらし得、それにより、mRNA転写物は、分解されるのでなく、機能的なタンパク質へと翻訳されうる。野生型mRNAより少ないエクソンを有するmRNA転写物から翻訳されたタンパク質は、結果として、野生型mRNA転写物から転写されたタンパク質より少ないアミノ酸残基を含む転写タンパク質となり得る。野生型タンパク質より少ないアミノ酸残基で構成された機能的なタンパク質は、野生型タンパク質と同じまたは同様の活性/機能性を有し得る。修飾アンチセンスオリゴマーは、それがハイブリダイズする標的配列または標的領域「を指向する」またはこれら「に対してターゲティングされた」ということができる。ある特定の実施形態では、標的配列はプレmRNAの3’スプライス接合部位もしくは5’スプライス接合部位を含む領域、分岐点、エクソンのスプライシングエンハンサー(ESE)もしくはイントロンのスプライシングエンハンサー(ISE)、またはスプライシングの調節に関与する他の配列を含む。イントロン内では、ドナー部位(イントロンの5’末端)およびアクセプター部位(イントロンの3’末端)が、スプライシングに必要である。スプライスドナー部位は、イントロンの5’末端にあるほとんど不変の配列GUを、より大きい、それほど高度に保存されていない領域内に含む。イントロンの3’末端にあるスプライスアクセプター部位は、ほとんど不変のAG配列によってイントロンを終結させる。標的配列は、エクソン内に完全にあり標的配列のいかなる部分もプライス接合部にわたらないか、エクソン/イントロンスプライス接合部内にあるか、またはエクソン/イントロンスプライス接合部にわたる、配列を含み得る。標的配列は、エクソン/イントロンドナースプライス部位を含み得る。
標的プレmRNA配列に対する配列相補性であって、標的RNAのスプライシングをモジュレートするのに十分な配列相補性を有する修飾アンチセンスオリゴマーは、スプライソソーム複合体に対する結合部位の遮蔽または妨害を誘発するのに十分な配列であって、他の点で、このようなスプライシングに影響を及ぼし、かつ/または、他の点で、ターゲティングされたプレmRNAの三次元構造の変更を含む配列を有する修飾アンチセンスオリゴマーを含む。
A.ミオスタチンプレmRNAのスプライシングのモジュレーション
多様な態様は、ミオスタチンプレmRNAのイントロンおよびエクソンのスプライシングをモジュレートするための方法に関する。さらなる態様は、ミオスタチンプレmRNAのイントロン1/エクソン2とエクソン2/イントロン2のスプライス接合部位でのスプライシングを阻害することに関する。さらなる態様では、所与の試料(例えば、血清試料、血漿試料、組織試料、細胞試料など)において、ミオスタチンエクソン2をコードするmRNAの発現は、例えばエクソン2野生型mRNAと比較して、阻害される。多様な方法は、ミオスタチンプレmRNA内の標的領域と相補的なターゲティング配列を含む本明細書で記載されるアンチセンスオリゴマーを投与するステップを含み、ミオスタチンエクソン2のmRNAの発現が、エクソン2野生型(すなわち対照)mRNAの発現と比較して阻害される。
多様な態様は、ミオスタチンプレmRNAのイントロンおよびエクソンのスプライシングをモジュレートするための方法に関する。さらなる態様は、ミオスタチンプレmRNAのイントロン1/エクソン2とエクソン2/イントロン2のスプライス接合部位でのスプライシングを阻害することに関する。さらなる態様では、所与の試料(例えば、血清試料、血漿試料、組織試料、細胞試料など)において、ミオスタチンエクソン2をコードするmRNAの発現は、例えばエクソン2野生型mRNAと比較して、阻害される。多様な方法は、ミオスタチンプレmRNA内の標的領域と相補的なターゲティング配列を含む本明細書で記載されるアンチセンスオリゴマーを投与するステップを含み、ミオスタチンエクソン2のmRNAの発現が、エクソン2野生型(すなわち対照)mRNAの発現と比較して阻害される。
多様な実施形態では、修飾アンチセンスオリゴマーのターゲティング配列は、十分な長さおよびミオスタチンプレmRNAの標的領域内の配列に対して十分な相補性を有する。多様な実施形態では、修飾アンチセンスオリゴマー内のターゲティング配列は、エクソン2内に完全にありターゲティング配列のいかなる部分もスプライス接合部にわたらない標的配列の領域、あるいはミオスタチンプレmRNAのイントロン/エクソンまたはエクソン/イントロンスプライス接合部にわたる領域、例えばミオスタチンプレmRNAのイントロン2/エクソン2の+24/-01もしくは+18/-07領域、またはエクソン2/イントロン2の-01/+21、-01/+25もしくは-09/+15の領域とハイブリダイズする。一部の実施形態では、修飾アンチセンスオリゴマーは、約12塩基~約40塩基の場合もあり、ターゲティング配列が、標的配列へのハイブリダイゼーション時に、スプライスモジュレーションを行うのに十分に相補的であり、任意選択で、プレmRNAと共に、Tmが45℃またはこれを超える、ヘテロ二重鎖を形成する限り、少数のミスマッチを含む。
多様な実施形態では、アンチセンスターゲティング配列と標的配列との相補性の程度は、安定的な二重鎖を形成するのに十分である。修飾アンチセンスオリゴマーの、標的配列との相補性の領域は、12~15塩基という短い領域であり得るが、12~20塩基またはこれを超える領域であることが可能であり、例えば、これらの範囲の間の全ての整数を含む、12~40塩基、12~30塩基、12~25塩基、12~22塩基、15~25塩基、15~22塩基または15~20塩基であり得る。ある特定の実施形態では、本明細書で論じられる、必須の結合Tmを達成するのに、最小の長さの相補塩基が要請され得る。
B.ジストロフィンプレmRNAのスプライシングのモジュレーション
多様な態様は、ジストロフィンプレmRNAのイントロンおよびエクソンのスプライシングをモジュレートするための方法に関する。さらなる態様は、ジストロフィンプレmRNAのイントロン/エクソンのスプライス接合部位およびエクソン/イントロンスプライス接合部におけるスプライシングを阻害することに関する。さらなる態様では、所与の試料(例えば血清試料、血漿試料、組織試料、細胞試料など)において切断型のジストロフィンコードmRNAの発現は、例えば、全長野生型ジストロフィンmRNAと比較して強化される。多様な方法は、ジストロフィンプレmRNA内の標的領域と相補的なターゲティング配列を含む、本明細書で記載されるアンチセンスオリゴマーを投与するステップを含み、切断型ジストロフィンmRNAの発現が、全長野生型(すなわち対照)mRNAの発現と比較して強化される。
多様な態様は、ジストロフィンプレmRNAのイントロンおよびエクソンのスプライシングをモジュレートするための方法に関する。さらなる態様は、ジストロフィンプレmRNAのイントロン/エクソンのスプライス接合部位およびエクソン/イントロンスプライス接合部におけるスプライシングを阻害することに関する。さらなる態様では、所与の試料(例えば血清試料、血漿試料、組織試料、細胞試料など)において切断型のジストロフィンコードmRNAの発現は、例えば、全長野生型ジストロフィンmRNAと比較して強化される。多様な方法は、ジストロフィンプレmRNA内の標的領域と相補的なターゲティング配列を含む、本明細書で記載されるアンチセンスオリゴマーを投与するステップを含み、切断型ジストロフィンmRNAの発現が、全長野生型(すなわち対照)mRNAの発現と比較して強化される。
多様な実施形態では、アンチセンスオリゴマーは、ジストロフィンプレmRNAのエクソン内部の標的領域と結合する。複数の実施形態では、アンチセンスオリゴマーは、エクソン7、エクソン8、エクソン9、エクソン19、エクソン23、エクソン44、エクソン45、エクソン50、エクソン51、エクソン52、エクソン53またはエクソン55から選択されるエクソンと結合する。複数の実施形態では、標的領域は、ジストロフィンプレmRNAのエクソン内に完全にあり、ターゲティング配列のいかなる部分もスプライス接合部にわたらない、またはイントロン/エクソンもしくはエクソン/イントロンスプライス接合部にわたる領域である。複数の実施形態では、ジストロフィンプレmRNAの1または複数のエクソンは、1または複数の遺伝子変異を有する。複数の実施形態では、アンチセンスオリゴマーは、1または複数の遺伝子変異を有するエクソンを標的とし、それにより、エクソンが、プロセシングの間、プレmRNA転写物から成熟mRNAにスプライシングされ、短縮または切断型のジストロフィンmRNAとなる。
多様な実施形態では、修飾アンチセンスオリゴマーのターゲティング配列は、十分な長さおよびジストロフィンプレmRNAの標的領域内の配列への十分な相補性を有する。多様な実施形態では、修飾アンチセンスオリゴマー内のターゲティング配列は、1または複数のエクソン内に完全にありターゲティング配列のいかなる部分もスプライス接合部にわたらない標的配列の領域、または、ジストロフィンプレmRNAのイントロン/エクソンもしくはエクソン/イントロンのスプライス接合部にわたる領域とハイブリダイズする。一部の実施形態では、修飾アンチセンスオリゴマーは、約8塩基~約50塩基の場合もあり、ターゲティング配列が、標的配列へのハイブリダイゼーション時にスプライスモジュレーションを行うのに十分に相補的であり、任意選択で、RNAと共に、Tmが45℃またはこれを超えるヘテロ二重鎖を形成する限り、少数のミスマッチを含む。
多様な実施形態では、アンチセンスターゲティング配列と標的配列との相補性の程度は、安定的な二重鎖を形成するのに十分である。修飾アンチセンスオリゴマーの、標的配列との相補性の領域は、8~15塩基という短い領域であり得るが、8~20塩基またはこれを超える領域であることが可能であり、例えば、これらの範囲の間の全ての整数を含む、8~40塩基、8~30塩基、8~25塩基、8~22塩基、8~25塩基、8~22塩基、8~20塩基、17~20塩基、17~22塩基、17塩基~25塩基、17~30塩基、17~40塩基または20~30塩基であり得る。ある特定の実施形態では、本明細書で論じられる、必須の結合Tmを達成するのに、最小の長さの相補塩基が要請され得る。
多様な態様では、オリゴマーを、バイオアベイラビリティー、安定性、細胞更新(cellular update)、およびヌクレアーゼ分解に対する耐性を含むがこれらに限定されない、さらなる機能性のために構成する。一般に、50塩基を含むオリゴマーは、適切である可能性があり、ここで、少なくとも最小数の塩基、例えば、8または12塩基は、標的配列と相補的である。多様な態様では、オリゴマーを、促進された細胞取込みまたは能動的な細胞取込みを増強するように構成する。多様な態様では、改変アンチセンスオリゴマーは、1または複数のホスホルアミデートモルホリノ単量体サブユニットまたはホスホロジアミデートモルホリノ単量体サブユニットを含む。多様な実施形態では、改変アンチセンスオリゴマーは、約8~50ホスホルアミデートモルホリノ単量体サブユニットまたはホスホロジアミデートモルホリノ単量体サブユニットを含む。多様な実施形態では、改変アンチセンスオリゴマーは、約8~30ホスホルアミデートモルホリノ単量体サブユニットまたはホスホロジアミデートモルホリノ単量体サブユニットを含む。多様な実施形態では、改変アンチセンスオリゴマーは、約17~40ホスホルアミデートモルホリノ単量体サブユニットまたはホスホロジアミデートモルホリノ単量体サブユニットを含む。多様な実施形態では、改変アンチセンスオリゴマーは、約12~25ホスホルアミデートモルホリノ単量体サブユニットまたはホスホロジアミデートモルホリノ単量体サブユニットを含む。多様な実施形態では、改変アンチセンスオリゴマーは、約15~25ホスホルアミデートモルホリノ単量体サブユニットまたはホスホロジアミデートモルホリノ単量体サブユニットを含む。多様な実施形態では、改変アンチセンスオリゴマーは、約15~22ホスホルアミデートモルホリノ単量体サブユニットまたはホスホロジアミデートモルホリノ単量体サブユニットを含む。
多様な態様では、修飾アンチセンスオリゴマーは、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットと、プレmRNA内の10またはこれを超える連続ヌクレオチドの標的領域と相補的なターゲティング配列とを任意選択で含む、8~50サブユニットを含むか、これらからなるか、またはこれらから本質的になる。多様な実施形態では、標的領域は、1または複数のエクソン内に完全にありターゲティング配列のいかなる部分もスプライス接合部にわたらないか、またはミオスタチンもしくはジストロフィン遺伝子のイントロン/エクソンもしくはエクソン/イントロンのスプライス接合部にわたる領域内の、10、12またはこれを超える連続ヌクレオチドを含む。
多様な実施形態では、ミオスタチンプレmRNAの標的領域は、ミオスタチンプレmRNAのエクソン2、イントロン1/エクソン2、または、エクソン2/イントロン2内の領域を含む。さらなる実施形態では、標的領域は、ミオスタチンプレmRNAのイントロン2/エクソン2の+24/-01もしくは+18/-07領域、または、エクソン2/イントロン2の-01/+21、-01/+25もしくは-09/+15領域を含む。
多様な実施形態では、ジストロフィンプレmRNAの標的領域は、ジストロフィンプレmRNAのエクソン7、エクソン8、エクソン9、エクソン19、エクソン23、エクソン44、エクソン45、エクソン50、エクソン51、エクソン52、エクソン53またはエクソン55から選択されるエクソンのうちの1または複数内の領域を含む。
多様な態様では、修飾アンチセンスオリゴマーは、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットと、配列番号16~75および配列番号76~3485から選択される配列を含むか、これらからなるか、またはこれらから本質的になるターゲティング配列とを任意選択で含む、10~50サブユニットを含むか、これからなるか、またはこれから本質的になる。一部の態様では、修飾アンチセンスオリゴマーは、配列番号71~75および配列番号76から選択される配列を含むことが好ましい。
さらなる態様は、ミオスタチンまたはジストロフィンプレmRNA内の標的領域と特異的にハイブリダイズする、8~50サブユニットの修飾アンチセンスオリゴマーを含む。
多様な実施形態では、ミオスタチンプレmRNA内の標的領域は、ミオスタチン遺伝子のエクソン2、イントロン1/エクソン2、または、エクソン2/イントロン2(またはスプライス接合部にわたる領域)内の領域を含む。多様な実施形態では、標的領域は、ミオスタチンプレmRNAのエクソン2内に完全にある領域を含む。多様な実施形態では、標的領域は、イントロン1/エクソン2またはエクソン2/イントロン2内の領域を含む。多様な実施形態では、標的領域は、イントロン1/エクソン2またはエクソン2/イントロン2のスプライス接合部にわたる領域を含む。さらなる実施形態では、標的領域は、ミオスタチンプレmRNAのイントロン2/エクソン2の+24/-01もしくは+18/-07領域、または、エクソン2/イントロン2の-01/+21、-01/+25もしくは-09/+15領域を含む。
さらなる態様は、修飾糖部分を含む、ヌクレオチド類似体サブユニットを有する、修飾アンチセンスオリゴマーを含む。多様な実施形態では、修飾糖部分は、ペプチド核酸(PNA)サブユニット、ロックト核酸(LNA)サブユニット、2’O,4’C-エチレン架橋核酸(ENA)サブユニット、トリシクロDNA(tc-DNA)サブユニット、2’O-メチルサブユニット、2’O-メトキシエチルサブユニット、2’-フルオロサブユニット、2’-O-[2-(N-メチルカルバモイル)エチル]サブユニット、およびモルホリノサブユニットから選択される。
さらなる態様は、修飾ヌクレオシド間連結を含む、ヌクレオチド類似体サブユニットを有する、修飾アンチセンスオリゴマーを含む。多様な実施形態では、修飾ヌクレオシド間連結は、ホスホロチオエートヌクレオシド間連結、ホスホルアミデートヌクレオシド間連結、ホスホロジアミデートヌクレオシド間連結およびホスホロトリアミデートヌクレオシド間連結から選択される。さらなる実施形態では、ホスホロジアミデートヌクレオシド間連結は、(1,4-ピペラジン)-1-イル部分、置換(1,4-ピペラジン)-1-イル部分、4-アミノピペリジン-1-イル部分、または置換4-アミノピペリジン-1-イル部分に共有結合したリン原子を含む。
さらなる態様は、修飾糖部分と修飾ヌクレオシド間連結の少なくとも1つの組合せを含むヌクレオチド類似体サブユニットを有する修飾アンチセンスオリゴマーを含み、多様な実施形態では、1または複数のサブユニットは、
任意選択でホスホルアミデートヌクレオシド間連結、ホスホロジアミデートヌクレオシド間連結、ホスホロトリアミデートヌクレオシド間連結またはホスホロチオエートヌクレオシド間連結で置換されたモルホリノサブユニット、
任意選択でホスホルアミデートヌクレオシド間連結、ホスホロジアミデートヌクレオシド間連結またはホスホロチオエートヌクレオシド間連結で置換された2’O-メチルサブユニット、
任意選択でホスホルアミデートヌクレオシド間連結、ホスホロジアミデートヌクレオシド間連結またはホスホロチオエートヌクレオシド間連結で置換される2’O-メトキシエチルサブユニット、
任意選択でホスホルアミデートヌクレオシド間連結、ホスホロジアミデートヌクレオシド間連結またはホスホロチオエートヌクレオシド間連結で置換された2’-フルオロサブユニット、
任意選択でホスホルアミデートヌクレオシド間連結、ホスホロジアミデートヌクレオシド間連結またはホスホロチオエートヌクレオシド間連結で置換された2’O,4’C-エチレン架橋核酸サブユニット、
任意選択でホスホルアミデートヌクレオシド間連結、ホスホロジアミデートヌクレオシド間連結またはホスホロチオエートヌクレオシド間連結で置換された2’-O-[2-(N-メチルカルバモイル)エチル]サブユニット、
任意選択でホスホルアミデートヌクレオシド間連結、ホスホロジアミデートヌクレオシド間連結またはホスホロチオエートヌクレオシド間連結で置換されたトリシクロDNAサブユニット、
任意選択でホスホルアミデートヌクレオシド間連結、ホスホロジアミデートヌクレオシド間連結またはホスホロチオエートヌクレオシド間連結で置換されたロックト核酸サブユニット、
ホスホロジアミデートのリン原子がモルホリノ環の窒素原子に共有結合し、(1,4-ピペラジン)-1-イル部分または置換(1,4-ピペラジン)-1-イル部分に共有結合する、ホスホロジアミデートヌクレオシド間連結をさらに含むモルホリノサブユニット、
ホスホロジアミデートのリン原子が4-アミノピペリジン-1-イル部分または置換4-アミノピペリジン-1-イル部分に共有結合する、ホスホロジアミデートヌクレオシド間連結をさらに含むモルホリノサブユニット、
ホスホロジアミデートのリン原子がモルホリノ環の窒素原子に共有結合し、ジメチルアミノ部分に共有結合する、ホスホロジアミデートヌクレオシド間連結をさらに含むモルホリノサブユニット、
ホスホロチオエートヌクレオシド間またはホスホルアミデートヌクレオシド間連結で置換されたリボース糖サブユニット、
ホスホロチオエートヌクレオシド間連結またはホスホルアミデートヌクレオシド間連結で置換されたデオキシリボース糖サブユニット、
任意選択で置換されたペプチド核酸サブユニット、
または前出の任意の組合せから選択される。
任意選択でホスホルアミデートヌクレオシド間連結、ホスホロジアミデートヌクレオシド間連結、ホスホロトリアミデートヌクレオシド間連結またはホスホロチオエートヌクレオシド間連結で置換されたモルホリノサブユニット、
任意選択でホスホルアミデートヌクレオシド間連結、ホスホロジアミデートヌクレオシド間連結またはホスホロチオエートヌクレオシド間連結で置換された2’O-メチルサブユニット、
任意選択でホスホルアミデートヌクレオシド間連結、ホスホロジアミデートヌクレオシド間連結またはホスホロチオエートヌクレオシド間連結で置換される2’O-メトキシエチルサブユニット、
任意選択でホスホルアミデートヌクレオシド間連結、ホスホロジアミデートヌクレオシド間連結またはホスホロチオエートヌクレオシド間連結で置換された2’-フルオロサブユニット、
任意選択でホスホルアミデートヌクレオシド間連結、ホスホロジアミデートヌクレオシド間連結またはホスホロチオエートヌクレオシド間連結で置換された2’O,4’C-エチレン架橋核酸サブユニット、
任意選択でホスホルアミデートヌクレオシド間連結、ホスホロジアミデートヌクレオシド間連結またはホスホロチオエートヌクレオシド間連結で置換された2’-O-[2-(N-メチルカルバモイル)エチル]サブユニット、
任意選択でホスホルアミデートヌクレオシド間連結、ホスホロジアミデートヌクレオシド間連結またはホスホロチオエートヌクレオシド間連結で置換されたトリシクロDNAサブユニット、
任意選択でホスホルアミデートヌクレオシド間連結、ホスホロジアミデートヌクレオシド間連結またはホスホロチオエートヌクレオシド間連結で置換されたロックト核酸サブユニット、
ホスホロジアミデートのリン原子がモルホリノ環の窒素原子に共有結合し、(1,4-ピペラジン)-1-イル部分または置換(1,4-ピペラジン)-1-イル部分に共有結合する、ホスホロジアミデートヌクレオシド間連結をさらに含むモルホリノサブユニット、
ホスホロジアミデートのリン原子が4-アミノピペリジン-1-イル部分または置換4-アミノピペリジン-1-イル部分に共有結合する、ホスホロジアミデートヌクレオシド間連結をさらに含むモルホリノサブユニット、
ホスホロジアミデートのリン原子がモルホリノ環の窒素原子に共有結合し、ジメチルアミノ部分に共有結合する、ホスホロジアミデートヌクレオシド間連結をさらに含むモルホリノサブユニット、
ホスホロチオエートヌクレオシド間またはホスホルアミデートヌクレオシド間連結で置換されたリボース糖サブユニット、
ホスホロチオエートヌクレオシド間連結またはホスホルアミデートヌクレオシド間連結で置換されたデオキシリボース糖サブユニット、
任意選択で置換されたペプチド核酸サブユニット、
または前出の任意の組合せから選択される。
多様な態様および実施形態では、本開示の修飾アンチセンスオリゴマーは、修飾アンチセンスオリゴマーに共有結合したペプチドをさらに含む。多様な実施形態では、アルギニンに富む細胞透過性ペプチドを、修飾アンチセンスオリゴマーの3’末端または5’末端にコンジュゲートさせる。
多様な実施形態では、修飾アンチセンスオリゴマーは、これらの範囲の間の全ての整数を含む、約8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49もしくは50塩基、または8~50、8~40、8~30、8~25、8~20、8~18、12~30、12~25、10~20、10~18、15~30、15~25、15~20、15~18、17~20、17~30、17~40、18~30、18~25または18~20の範囲の塩基からなる場合がある。一部の実施形態では、修飾アンチセンスオリゴマーは、約8~約50、約8~約40または約8~約30塩基の長さである。一部の実施形態では、修飾アンチセンスオリゴマーは、約12~約25塩基の長さである。一部の実施形態では、修飾アンチセンスオリゴマー配列は、例えばミオスタチンプレmRNAのエクソン2、イントロン1/エクソン2もしくはエクソン2/イントロン2、またはジストロフィンプレmRNAのエクソン7、エクソン8、エクソン9、エクソン19、エクソン23、エクソン44、エクソン45、エクソン50、エクソン51、エクソン52、エクソン53もしくはエクソン55のうちの1もしくは複数、またはミオスタチンもしくはジストロフィンプレmRNAの少なくとも一部にわたる配列などの、ミオスタチンまたはジストロフィンプレmRNA内の標的配列と相補的である、少なくとも約8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49または50の連続または非連続塩基を含む。
修飾アンチセンスオリゴマーは、典型的には、ミオスタチンタンパク質のミオスタチンプレmRNA配列のエクソン2、イントロン1/エクソン2、または、エクソン2/イントロン2内の配列または領域と十分に相補的である塩基配列を含み得る。下記の表1は、エクソン2、イントロン1/エクソン2およびエクソン2/イントロン2中の配列または領域を示す。
修飾アンチセンスオリゴマーは、典型的には、ジストロフィンタンパク質のジストロフィンプレmRNA配列のエクソン7、エクソン8、エクソン9、エクソン19、エクソン23、エクソン44、エクソン45、エクソン50、エクソン51、エクソン52、エクソン53またはエクソン55のうちの1または複数のエクソン内の配列または領域と十分に相補的な塩基配列を含み得る。下記の表2は、エクソン7、エクソン8、エクソン9、エクソン19、エクソン23、エクソン44、エクソン45、エクソン50、エクソン51、エクソン52、エクソン53およびエクソン55のエクソン内の配列または領域を示す。
修飾アンチセンスオリゴマーは、エクソン、例えばエクソン2の発現を効果的に減少させ、それにより機能的なミオスタチンタンパク質の発現を減少させることが好ましい。修飾ジストロフィンアンチセンスオリゴマーは、ジストロフィンプレmRNAの異常なスプライシングを効果的にモジュレートし、それにより機能的または半機能的なジストロフィンタンパク質の発現を増加させることが好ましい。この要件は、任意選択で、オリゴマー化合物が、哺乳動物細胞により能動的に取り込まれ、取り込まれると、標的mRNAと共に、任意選択で、Tmが、約40℃または45℃を超える、安定的な二重鎖(またはヘテロ二重鎖)を形成する能力を有する場合に満たされる。
本明細書で使用される「相補的(complementary)」または「相補的(complementary)」とは、標的配列と相補的なヌクレオチドターゲティング配列のうちの、約90%~約100%を有する修飾アンチセンスオリゴマーのターゲティング配列を指す。複数の実施形態では、相補的なヌクレオチドターゲティング配列は、標的配列と特異的にハイブリダイズして、所望の効果、例えば、本明細書で記載される治療効果を誘導する。ある特定の実施形態では、修飾アンチセンスオリゴマーのターゲティング配列は、オリゴマーターゲティング配列と標的配列との間に形成されるヘテロ二重鎖が、細胞ヌクレアーゼの作用、およびin vivoにおいて生じうる、他の様態の分解に抗するのに十分に安定である限りにおいて、標的配列と100%相補的な場合もあり、例えば、改変体を擁するように、ミスマッチを含む場合もある。よって、ある特定のオリゴマーターゲティング配列は、オリゴマーターゲティング配列と、標的配列との間の、約90%または少なくとも約90%の配列相補性、例えば、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%、または100%の配列相補性を意味する、実質的な相補性を有しうる。本明細書では、ヌクレアーゼによる切断を受けにくいオリゴマーのヌクレオシド間連結が提供される。ミスマッチは、存在する場合、ハイブリッド二重鎖の中央部より、末端領域に向かって、より不安定化しにくくなることが典型的である。許容されるミスマッチの数は、よく理解されている、二重鎖安定性の原理に従い、オリゴマーの長さ、二重鎖内のG:C塩基対の百分率、および二重鎖内のミスマッチの位置に依存すると予想される。このような改変アンチセンスオリゴマーは必ずしも、標的配列に対する、100%の相補性を含むわけではないが、標的プレmRNAのスプライシングを十分にモジュレートする、例えば、本明細書で記載される治療効果を達成するように、標的配列に、有効に、安定的に、かつ特異的に結合するのに十分な相補性を有するべきである。
理論に束縛されずに述べると、オリゴマーと、標的配列との間で形成される二重鎖の安定性は、結合Tmと、二重鎖の、細胞酵素による切断の受けやすさとの関数であると考えられる。相補配列であるRNA二重鎖との関連における、オリゴマーのTmは、Hamesら、「Nucleic Acid Hybridization」、IRL Press、1985年、107~108頁により記載されている方法、またはMiyada C. G.およびWallace R. B.、1987年、「Oligomer Hybridization Techniques」、Methods Enzymol.、154巻、94~107頁(この内容は、本明細書中に参考として援用される)において記載されている方法など、従来の方法により測定することができる。多様な実施形態では、改変アンチセンスオリゴマーは、相補配列であるRNA二重鎖との関連における結合Tmであって、例えば、約45℃または50℃を超えるなど、体温を超えるTmを有する。60~80℃またはこれを超える範囲のTmもまた含まれる。周知の原理に従い、相補性ベースのRNAハイブリッド二重鎖との関連における、オリゴマーのTmは、二重鎖内のC:G対合塩基の比を増加させ、かつ/またはヘテロ二重鎖の長さ(塩基対での)を増加させることにより、上昇させることができる。
ある特定の修飾アンチセンスオリゴマーは、このように、表3の配列(例えば配列番号16~75)を含むか、これからなるか、もしくはこれから本質的になるか、配列番号16~75から選択されるか、配列番号16~75から選択される配列の少なくとも12の連続ヌクレオチドの断片であるか、または配列番号16~75から選択される配列に対する少なくとも90%の配列同一性を有する変異体であり、各Xはウラシル(U)またはチミン(T)から独立に選択され、各Yはシトシン(C)または5-メチルシトシン(5mC)から独立に選択される。例えば、ある特定の修飾アンチセンスオリゴマーは、配列番号16~75のいずれかの、約または少なくとも約12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39または40の連続または非連続ヌクレオチドを含む。非連続部分においては、介在するヌクレオチドを削除できるか、もしくは異なるヌクレオチドで置換でき、または介在ヌクレオチドを追加できる。変異体のさらなる例は、配列番号16~75のいずれかの全長に対して、約または少なくとも約90%の配列同一性または相同性、例えば90%、91%、92%、93%、94%、95%、96%、97%、98%、99%または100%の配列同一性または相同性を有するオリゴマーを含む。ある特定の実施形態では、ターゲティング配列は、配列番号16~75から選択される。
ジストロフィン遺伝子を標的とするオリゴヌクレオチドは、WO2006/000057、WO2011/057350、WO2010/048586、WO2014/100714、WO2014/153220、米国出願第US20140315862号、米国出願第US20140323544号、米国出願第US20120202752号、米国出願第US20030235845号、米国出願第US20110312086号、米国出願第US20090312532号、米国出願第US20090269755号、米国出願第US20130211062号、米国出願第US20140343266号、米国出願第US20120059042号、米国出願第US20110294753号、米国出願第US20140113955号、米国出願第US20150166996号、米国出願第US20150203849号、米国出願第US20150045413号および米国出願第US20140057964号に開示されており、これらは参照によりそれらの全体において本明細書に組み込まれる。
ある特定の修飾アンチセンスオリゴマーは、このように、表4の配列(例えば配列番号76~3485)を含むか、これからなるか、もしくはこれから本質的になるか、配列番号76~3485から選択されるか、配列番号76~3485から選択される配列の少なくとも10の連続ヌクレオチドの断片であるか、または配列番号76~3485から選択される配列に対する少なくとも90%の配列同一性を有する変異体であり、各Xはウラシル(U)またはチミン(T)から独立に選択され、各Yはシトシン(C)または5-メチルシトシン(5mC)から独立に選択される。例えば、ある特定の修飾アンチセンスオリゴマーは、配列番号76~3485のいずれかの、約または少なくとも約8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39または40の連続または非連続ヌクレオチドを含む。非連続部分においては、介在するヌクレオチドを削除でき、もしくは異なるヌクレオチドで置換でき、または介在ヌクレオチドを追加できる。改変体のさらなる例は、約90%または少なくとも約90%の配列同一性または配列相同性、例えば、配列番号76~3485のいずれかの全長にわたる、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%、または100%の配列同一性または配列相同性を有するオリゴマーを含む。ある特定の実施形態では、ターゲティング配列は、配列番号76~3485から選択される。一部の実施形態では、ターゲティング配列は配列番号76を含みうる。
改変アンチセンスオリゴマーおよびその改変体の活性/機能性は、当技術分野における慣例的な技法に従いアッセイすることができる。例えば、サーベイされるRNAのスプライス形態および発現レベルを、転写される核酸またはタンパク質のスプライス形態および/または発現を検出するための、多種多様な周知の方法のうちのいずれかにより評価することができる。このような方法の非限定的な例は、RNAのスプライシング形態についてのRT-PCRに続く、PCR産物のサイズによる分離、核酸ハイブリダイゼーション法、例えば、ノーザンブロット、ならびに/または核酸アレイ;核酸増幅法;タンパク質を検出するための免疫学的方法;タンパク質精製法;およびタンパク質機能アッセイまたはタンパク質活性アッセイの使用を含む。
RNA発現レベルは、mRNA/cDNA(すなわち、転写されるオリゴヌクレオチド)を、細胞、組織、または生物体から調製し、mRNA/cDNAを、アッセイされる核酸またはその断片の相補体である基準オリゴヌクレオチドとハイブリダイズさせることにより評価することができる。cDNAは、任意選択で、相補的オリゴヌクレオチドとのハイブリダイゼーションの前に、様々なポリメラーゼ連鎖反応またはin vitroにおける転写法のうちのいずれかを使用して増幅することもできるが;増幅しないことが好ましい。1または複数の転写物の発現はまた、転写物の発現レベルについて評価する、定量的PCRを使用して検出することもできる。
III.改変アンチセンスオリゴマー化学
A.一般的特徴
多様な態様および実施形態では、改変アンチセンスオリゴマーは、ミオスタチンプレmRNA内のターゲティング領域と特異的にハイブリダイズする。例示的な改変アンチセンスオリゴマーは、表3に明示されたターゲティング配列、表3のターゲティング配列のうちの、少なくとも12連続ヌクレオチドの断片、または表3のターゲティング配列に対する、少なくとも90%の配列同一性を有する改変体を含む。他の例示的な改変アンチセンスオリゴマーは、表3に明示されたターゲティング配列からなるか、またはこれらから本質的になる。
A.一般的特徴
多様な態様および実施形態では、改変アンチセンスオリゴマーは、ミオスタチンプレmRNA内のターゲティング領域と特異的にハイブリダイズする。例示的な改変アンチセンスオリゴマーは、表3に明示されたターゲティング配列、表3のターゲティング配列のうちの、少なくとも12連続ヌクレオチドの断片、または表3のターゲティング配列に対する、少なくとも90%の配列同一性を有する改変体を含む。他の例示的な改変アンチセンスオリゴマーは、表3に明示されたターゲティング配列からなるか、またはこれらから本質的になる。
多様な態様および実施形態では、修飾アンチセンスオリゴマーは、ジストロフィンプレmRNA内の標的領域と特異的にハイブリダイズする。例示的な修飾アンチセンスオリゴマーは、表4に明示されたターゲティング配列、表4のターゲティング配列の少なくとも10の連続ヌクレオチドの断片、または表4のターゲティング配列に対する少なくとも90%の配列同一性を有する変異体を含む。他の例示的な修飾アンチセンスのオリゴマーは、表4に明示されたターゲティング配列からなるか、またはこれから本質的になる。
さらなる態様では、ヌクレアーゼ耐性改変アンチセンスオリゴマーが提供される。多様な実施形態では、1または複数のヌクレオシド間連結の修飾を含む改変アンチセンスオリゴマーが提供される。他の実施形態では、1または複数の修飾糖部分を含む改変アンチセンスオリゴマーが提供される。他の実施形態では、1または複数の修飾ヌクレオシド間連結と、1または複数の修飾糖部分との組合せを含む、改変アンチセンスオリゴマーが提供される。他の実施形態では、修飾ヌクレオ塩基単独、または修飾ヌクレオシド間連結もしくは修飾糖部分のうちのいずれかと組み合わせた修飾ヌクレオ塩基を含む、改変アンチセンスオリゴマーが提供される。
多様な実施形態では、改変アンチセンスオリゴマーは、完全に修飾されたヌクレオシド間連結を有するオリゴマーを含むことが可能であり、例えば、ヌクレオシド間連結の100%が修飾されている(例えば、25merの改変アンチセンスオリゴマーは、本明細書で記載される修飾のうちの1つまたはこれらの任意の組合せで修飾された、24のヌクレオシド間連結を含む)。多様な実施形態では、改変アンチセンスオリゴマーは、そのヌクレオシド間連結の約100%~2.5%が修飾されたものを含みうる。多様な実施形態では、改変アンチセンスオリゴマーは、そのヌクレオシド間連結のうちの約99%、95%、90%、85%、80%、75%、70%、65%、60%、55%、50%、45%、40%、35%、30%、25%、20%、15%、10%、5%、または2.5%、およびその間の整数(iteration)の%が修飾されたものを含みうる。他の実施形態では、改変アンチセンスオリゴマーは、本明細書で記載される修飾の任意の組合せを含みうる。
修飾ヌクレオシド間連結のパーセントについての実施形態と組み合わせた実施形態を含む、多様な実施形態では、改変アンチセンスオリゴマーは、完全修飾糖部分を有するオリゴマーを含むことが可能であり、例えば、糖部分の100%が修飾されている(例えば、25merの改変アンチセンスオリゴマーは、本明細書で記載される修飾のうちの1つまたはこれらの任意の組合せで修飾された、25の糖部分を含む)。多様な実施形態では、改変アンチセンスオリゴマーは、その糖部分の約100%~2.5%が修飾されたものを含みうる。多様な実施形態では、改変アンチセンスオリゴマーは、その糖部分のうちの約99%、95%、90%、85%、80%、75%、70%、65%、60%、55%、50%、45%、40%、35%、30%、25%、20%、15%、10%、5%、または2.5%、およびその間の整数の%が修飾されたものを含みうる。他の実施形態では、改変アンチセンスオリゴマーは、本明細書で記載される修飾の任意の組合せを含みうる。
多様な実施形態では、改変アンチセンスオリゴマーは、実質的に非荷電であり、任意選択で、細胞膜を横切る、能動的な輸送または促進された輸送のための基質として適する。一部の実施形態では、全てのヌクレオシド間連結は、非荷電である。オリゴマーが、標的プレmRNAと共に、安定的な二重鎖を形成する能力はまた、標的との関連における、改変アンチセンスオリゴマーの相補性の長さおよび程度、G:C塩基マッチの、A:T塩基マッチに対する比、ならびに任意のミスマッチ塩基の位置を含む、オリゴマーの他の特色にも関しうる。改変アンチセンスオリゴマーが、細胞ヌクレアーゼに抵抗する能力は、薬剤の存続および細胞質への最終的な送達を促進しうる。
多様な実施形態では、改変アンチセンスオリゴマーは、生理学的pHで正に荷電しているか、またはカチオン性である、少なくとも1つのヌクレオシド間連結を有する。さらなる実施形態では、改変アンチセンスオリゴマーは、約5.5~約12の間のpKaを呈示する、少なくとも1つのヌクレオシド間連結を有する。さらなる実施形態では、改変アンチセンスオリゴマーは、約1つ、2つ、3つ、4つ、5つ、6つ、7つ、8つ、9つ、もしくは10のヌクレオシド間連結、少なくともほぼこれらの数のヌクレオシド間連結、またはほぼこれらの数を超えないヌクレオシド間連結であって、約4.5~約12の間のpKaを呈示するヌクレオシド間連結を含有する。一部の実施形態では、改変アンチセンスオリゴマーは、約10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、もしくは100%のヌクレオシド間連結、または少なくともほぼこれらの比率のヌクレオシド間連結であって、約4.5~約12の間のpKaを呈示するヌクレオシド間連結を含有する。任意選択で、改変アンチセンスオリゴマーは、塩基性の窒素と、アルキル基、アリール基、またはアラルキル基との両方を伴う、少なくとも1つのヌクレオシド間連結を有する。特定の実施形態では、1または複数のカチオン性ヌクレオシド間連結は、4-アミノピペリジン-1-イル(APN)基またはその誘導体を含む。一部の実施形態では、改変アンチセンスオリゴマーは、モルホリノ環を含む。理論に束縛されるわけではないが、オリゴマー内の、1または複数のカチオン性連結(例えば、APN基またはAPN誘導体)の存在は、標的ヌクレオチド内の、負に荷電したホスフェートへの結合を促進することが考えられる。こうして、変異体RNAと、カチオン性連結を含有するオリゴマーとの間のヘテロ二重鎖の形成は、イオン性引力およびワトソン-クリック塩基対合の両方により一体に保持されうる。
多様な実施形態では、カチオン性連結の数は、少なくとも2つであり、全ヌクレオシド間連結の約半分を超えず、例えば、約1つ、2つ、3つ、4つ、5つ、6つ、7つ、8つ、9つ、10、11、12、13、14、15、16、17、18、19、20のカチオン性連結、またはほぼこれらを超えないカチオン性連結である。一部の実施形態では、しかし、ヌクレオシド間連結のうちの、最大で全ては、カチオン性連結であり、例えば、全ヌクレオシド間連結のうちの約1つ、2つ、3つ、4つ、5つ、6つ、7つ、8つ、9つ、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、もしくは40、または少なくともほぼこれらの数は、カチオン性連結である。さらなる実施形態では、約19~20単量体サブユニットのオリゴマーは、2つ~10、例えば、4~8つのカチオン性連結と、残りの非荷電連結とを有しうる。他の具体的な実施形態では、14~15サブユニットのオリゴマーは、2~7つ、例えば、2つ、3つ、4つ、5つ、6つ、または7つのカチオン性連結と、残りの非荷電連結とを有しうる。こうして、オリゴマー内のカチオン性連結の総数は、約1~10~18~20~30またはこれを超えて(間の全ての整数を含む)変動することが可能であり、オリゴマー全体にわたり散在しうる。
一部の実施形態では、改変アンチセンスオリゴマーは、10の非荷電連結ごとに約4つ~5つまたは4つもしくは5つなど、2つ~5つまたは2つ、3つ、4つ、もしくは5つの非荷電連結ごとに約1つのカチオン性連結または最大で約1つのカチオン性連結を有しうる。
ある特定の実施形態は、約10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、または100%のカチオン性連結を含有する改変アンチセンスオリゴマーを含む。ある特定の実施形態では、アンチセンス活性の最適な改善は、ヌクレオシド間連結のうちの約25%がカチオン性である場合に見ることができる。ある特定の実施形態では、増強は、少数(例えば、10~20%)のカチオン性連結に関して見ることもでき、カチオン性連結の数が、約60%など、50~80%の範囲内にある場合に見ることもできる。
さらなる実施形態では、カチオン性連結を、ヌクレオシド間連結に沿って散在させる。このようなオリゴマーは任意選択で、少なくとも2つの連続非荷電連結を含有する;すなわち、オリゴマーは任意選択で、その全長に沿って、厳密に交互のパターンを有さない。具体的な場合では、各1つまたは2つのカチオン性連結は、ヌクレオシド間連結に沿って、少なくとも1つ、2つ、3つ、4つ、もしくは5つの非荷電連結により隔てられる。
また、カチオン性連結のブロックと、非荷電連結のブロックとを有するオリゴマーも含まれる。例えば、中央の非荷電連結のブロックが、カチオン性連結のブロックに挟まれる場合もあり、この逆の場合もある。一部の実施形態では、オリゴマーは、ほぼ等長の5’領域、3’領域、および中央領域を有し、中央領域内のカチオン性連結の百分率は、カチオン性連結の総数のうちの、約50%、60%、70%、または80%を超える。
ある特定の改変アンチセンスオリゴマーでは、カチオン性連結のバルク(例えば、カチオン性連結のうちの70、75%、80%、90%)は、ヌクレオシド間連結の「中央領域」、例えば、6つ、7つ、8つ、9つ、10、11、12、13、14、または15の真ん中の連結(centermost linkage)に近接して分布する。例えば、16、17、18、19、20、21、22、23、または24merのオリゴマーは、全カチオン性連結のうちの、少なくとも50%、60%、70%、または80%を、8つ、9つ、10、11、または12の真ん中の連結へと局在化させうる。
B.化学の特色
改変アンチセンスオリゴマーは、様々なヌクレオチド類似体サブユニットを含有しうる。さ
らなる例は、
ホスホルアミデートを含有するオリゴマー、
ホスホロジアミデートを含有するオリゴマー、
ホスホロトリアミデートを含有するオリゴマー、
ホスホロチオエートを含有するオリゴマー、
モルホリノを含有するオリゴマーであって、任意選択で、ホスホルアミデートヌクレオシド間連結またはホスホロジアミデートヌクレオシド間連結で置換されたオリゴマー、
2’O-メチルを含有するオリゴマーであって、任意選択で、ホスホロチオエートヌクレオシド間連結で置換されたオリゴマー、
ロックト核酸(LNA)を含有するオリゴマーであって、任意選択で、ホスホロチオエートヌクレオシド間連結で置換されたオリゴマー、
2’O-メトキシエチル(MOE)を含有するオリゴマーであって、任意選択で、ホスホロチオエートヌクレオシド間連結で置換されたオリゴマー、
2’-フルオロを含有するオリゴマーであって、任意選択で、ホスホロチオエートヌクレオシド間連結で置換されたオリゴマー、
2’O,4’C-エチレン架橋核酸(ENA)を含有するオリゴマーであって、任意選択で、ホスホロチオエートヌクレオシド間連結で置換されたオリゴマー、
トリシクロDNA(tc-DNA)を含有するオリゴマーであって、任意選択で、ホスホロチオエートヌクレオシド間連結で置換されたオリゴマー、
2’-O-[2-(N-メチルカルバモイル)エチル]を含有するオリゴマーであって、任意選択で、ホスホロチオエートヌクレオシド間連結で置換されたオリゴマー、
モルホリノを含有するオリゴマーであって、ホスホロジアミデートヌクレオシド間連結をさらに含み、ホスホロジアミデートのリン原子を、モルホリノ環の窒素原子に共有結合させ、かつ、(1,4-ピペラジン)-1-イル部分、または置換(1,4-ピペラジン)-1-イル(PMOプラス)部分に共有結合させたオリゴマー、
モルホリノを含有するオリゴマーであって、ホスホロジアミデートヌクレオシド間連結をさらに含み、ホスホロジアミデートのリン原子を、モルホリノ環の窒素原子に共有結合させ、かつ、4-アミノピペリジン-1-イル部分(すなわち、APN)または置換4-アミノピペリジン-1-イル(PMO-X)部分に共有結合させたオリゴマー、
モルホリノサブユニットであって、ホスホロジアミデートヌクレオシド間連結をさらに含み、ホスホロジアミデートのリン原子を、モルホリノ環の窒素原子に共有結合させ、かつ、ジメチルアミノ部分に共有結合させたオリゴマー、
リボース糖を含有するオリゴマーであって、ホスホロチオエートヌクレオシド間連結またはホスホルアミデートヌクレオシド間連結をさらに含むオリゴマー、
デオキシリボース糖を含有するオリゴマーであってホスホロチオエートヌクレオシド間連結オリゴマーまたはホスホルアミデートヌクレオシド間連結をさらに含むオリゴマー、
任意選択でさらに置換された、ペプチドコンジュゲートホスホロジアミデートモルホリノ含有オリゴマー(PPMO)、
さらなる置換を含む、任意選択でさらに置換された、ペプチド核酸(PNA)オリゴマー、
および前出のうちのいずれかの組合せを含む。
改変アンチセンスオリゴマーは、様々なヌクレオチド類似体サブユニットを含有しうる。さ
らなる例は、
ホスホルアミデートを含有するオリゴマー、
ホスホロジアミデートを含有するオリゴマー、
ホスホロトリアミデートを含有するオリゴマー、
ホスホロチオエートを含有するオリゴマー、
モルホリノを含有するオリゴマーであって、任意選択で、ホスホルアミデートヌクレオシド間連結またはホスホロジアミデートヌクレオシド間連結で置換されたオリゴマー、
2’O-メチルを含有するオリゴマーであって、任意選択で、ホスホロチオエートヌクレオシド間連結で置換されたオリゴマー、
ロックト核酸(LNA)を含有するオリゴマーであって、任意選択で、ホスホロチオエートヌクレオシド間連結で置換されたオリゴマー、
2’O-メトキシエチル(MOE)を含有するオリゴマーであって、任意選択で、ホスホロチオエートヌクレオシド間連結で置換されたオリゴマー、
2’-フルオロを含有するオリゴマーであって、任意選択で、ホスホロチオエートヌクレオシド間連結で置換されたオリゴマー、
2’O,4’C-エチレン架橋核酸(ENA)を含有するオリゴマーであって、任意選択で、ホスホロチオエートヌクレオシド間連結で置換されたオリゴマー、
トリシクロDNA(tc-DNA)を含有するオリゴマーであって、任意選択で、ホスホロチオエートヌクレオシド間連結で置換されたオリゴマー、
2’-O-[2-(N-メチルカルバモイル)エチル]を含有するオリゴマーであって、任意選択で、ホスホロチオエートヌクレオシド間連結で置換されたオリゴマー、
モルホリノを含有するオリゴマーであって、ホスホロジアミデートヌクレオシド間連結をさらに含み、ホスホロジアミデートのリン原子を、モルホリノ環の窒素原子に共有結合させ、かつ、(1,4-ピペラジン)-1-イル部分、または置換(1,4-ピペラジン)-1-イル(PMOプラス)部分に共有結合させたオリゴマー、
モルホリノを含有するオリゴマーであって、ホスホロジアミデートヌクレオシド間連結をさらに含み、ホスホロジアミデートのリン原子を、モルホリノ環の窒素原子に共有結合させ、かつ、4-アミノピペリジン-1-イル部分(すなわち、APN)または置換4-アミノピペリジン-1-イル(PMO-X)部分に共有結合させたオリゴマー、
モルホリノサブユニットであって、ホスホロジアミデートヌクレオシド間連結をさらに含み、ホスホロジアミデートのリン原子を、モルホリノ環の窒素原子に共有結合させ、かつ、ジメチルアミノ部分に共有結合させたオリゴマー、
リボース糖を含有するオリゴマーであって、ホスホロチオエートヌクレオシド間連結またはホスホルアミデートヌクレオシド間連結をさらに含むオリゴマー、
デオキシリボース糖を含有するオリゴマーであってホスホロチオエートヌクレオシド間連結オリゴマーまたはホスホルアミデートヌクレオシド間連結をさらに含むオリゴマー、
任意選択でさらに置換された、ペプチドコンジュゲートホスホロジアミデートモルホリノ含有オリゴマー(PPMO)、
さらなる置換を含む、任意選択でさらに置換された、ペプチド核酸(PNA)オリゴマー、
および前出のうちのいずれかの組合せを含む。
ある特定の実施形態では、ホスホロジアミデート連結のリン原子を、(1,4-ピペラジン)-1-イル部分、置換(1,4-ピペラジン)-1-イル部分、4-アミノピペリジン-1-イル部分、または置換4-アミノピペリジン-1-イル部分で、さらに置換する。
一般に、PNA化学およびLNA化学は、PMOおよび2’O-Meオリゴマーと比べた、それらの比較的高度な標的結合強度のために、より短いターゲティング配列を活用しうる。ホスホロチオエート化学と、2’O-Me化学とを組み合わせて、2’O-Me-ホスホロチオエート類似体を作出することができる。例えば、参照によりそれらの全体において本明細書に組み込まれる、PCT公開第WO/2013/112053号および同第WO/2009/008725号を参照されたい。
場合によって、ホスホロジアミデートモルホリノオリゴマー(PMO)などの改変アンチセンスオリゴマーを、細胞透過性ペプチド(CPP)にコンジュゲートさせて、細胞内送達を促進することができる。ペプチドコンジュゲートPMOは、PPMOと呼ばれ、ある特定の実施形態は、参照によりその全体において本明細書に組み込まれる、PCT公開第WO/2012/150960号において記載されているPPMOを含む。一部の実施形態では、例えば、本明細書で記載される改変アンチセンスオリゴマーの3’末端にコンジュゲートまたは連結させた、アルギニンに富むペプチド配列を使用することができる。
1.ペプチド核酸(PNA)
ペプチド核酸(PNA)とは、骨格が、デオキシリボース骨格と構造的に同形である、DNAの類似体であって、ピリミジン塩基またはプリン塩基を結合させた、N-(2-アミノエチル)グリシン単位からなる類似体である。天然のピリミジン塩基およびプリン塩基を含有するPNAは、ワトソン-クリック塩基対合則に従う相補的オリゴマーとハイブリダイズし、塩基対認識の点で、DNAを模倣する(Egholm、Buchardtら、1993年)。PNAのヌクレオシド間連結は、ホスホジエステル結合ではなく、ペプチド結合により形成されることから、アンチセンス適用(下記の構造を参照されたい)に良好に適する。骨格が非荷電である結果として、通常を超える熱安定性を呈示する、PNA/DNA二重鎖またはPNA/RNA二重鎖がもたらされる。PNAは、ヌクレアーゼによっても、プロテアーゼによっても認識されない。PNAサブユニットを含むPNAオリゴマーの非限定的な例を、下記:
に描示する。
ペプチド核酸(PNA)とは、骨格が、デオキシリボース骨格と構造的に同形である、DNAの類似体であって、ピリミジン塩基またはプリン塩基を結合させた、N-(2-アミノエチル)グリシン単位からなる類似体である。天然のピリミジン塩基およびプリン塩基を含有するPNAは、ワトソン-クリック塩基対合則に従う相補的オリゴマーとハイブリダイズし、塩基対認識の点で、DNAを模倣する(Egholm、Buchardtら、1993年)。PNAのヌクレオシド間連結は、ホスホジエステル結合ではなく、ペプチド結合により形成されることから、アンチセンス適用(下記の構造を参照されたい)に良好に適する。骨格が非荷電である結果として、通常を超える熱安定性を呈示する、PNA/DNA二重鎖またはPNA/RNA二重鎖がもたらされる。PNAは、ヌクレアーゼによっても、プロテアーゼによっても認識されない。PNAサブユニットを含むPNAオリゴマーの非限定的な例を、下記:
に描示する。
天然構造に対する大幅な構造変化にもかかわらず、PNAは、ヘリックス形態による、DNAまたはRNAへの配列特異的結合が可能である。PNAの特徴は、相補的なDNAまたはRNAに対する高結合アフィニティー、単一塩基ミスマッチにより引き起こされる不安定化効果、ヌクレアーゼおよびプロテアーゼに対する耐性、塩濃度に依存しない、DNAまたはRNAとのハイブリダイゼーション、およびホモプリンDNAとの三重鎖形成を含む。PANAGENE(Daejeon、Korea)は、Bts PNA単量体(Bts;ベンゾチアゾール-2-スルホニル基)と、オリゴマー化工程とを開発している。Bts PNA単量体を使用する、PNAのオリゴマー化は、脱保護、カップリング、およびキャッピングの反復的サイクルから構成される。PNAは、当技術分野で公知の任意の技法を使用して、合成により作製することができる。例えば、米国特許第6,969,766号、同第7,211,668号、同第7,022,851号、同第7,125,994号、同第7,145,006号、および同第7,179,896号を参照されたい。PNAの調製についてはまた、米国特許第5,539,082号;同第5,714,331号;および同第5,719,262号も参照されたい。PNA化合物についてのさらなる教示は、Nielsenら、Science、254巻:1497~1500頁、1991年においても見出すことができる。前出の各々は、参照によりその全体において本明細書に組み込まれる。
2.ロックト核酸(LNA)
改変アンチセンスオリゴマー化合物はまた、「ロックト核酸」サブユニット(LNA)も含有しうる。「LNA」とは、架橋核酸(BNA)と呼ばれる修飾のクラスのメンバーである。BNAは、リボース環のコンフォメーションを、C30-エンド(ノーザン)糖パッカー(sugar pucker)にロックする共有結合的連結を特徴とする。LNAでは、架橋は、2’-O位と4’-C位との間のメチレンから構成される。LNAは、骨格の事前組織化(preorganization)および塩基スタッキングを増強して、ハイブリダイゼーションおよび熱安定性を増加させる。
改変アンチセンスオリゴマー化合物はまた、「ロックト核酸」サブユニット(LNA)も含有しうる。「LNA」とは、架橋核酸(BNA)と呼ばれる修飾のクラスのメンバーである。BNAは、リボース環のコンフォメーションを、C30-エンド(ノーザン)糖パッカー(sugar pucker)にロックする共有結合的連結を特徴とする。LNAでは、架橋は、2’-O位と4’-C位との間のメチレンから構成される。LNAは、骨格の事前組織化(preorganization)および塩基スタッキングを増強して、ハイブリダイゼーションおよび熱安定性を増加させる。
LNAの構造は、例えば、参照によりそれらの全体において本明細書に組み込まれる、Wengelら、Chemical Communications(1998年)、455巻;Tetrahedron(1998年)、54巻:3607頁、およびAccounts of Chem. Research(1999年)、32巻:301頁);Obikaら、Tetrahedron Letters(1997年)、38巻:8735頁;(1998年)、39巻:5401頁、ならびにBioorganic Medicinal Chemistry(2008年)、16巻:9230頁において見出すことができる。LNAサブユニットと、ホスホジエステルヌクレオシド間連結とを含む、LNAオリゴマーの非限定的な例を、下記:
に描示する。
に描示する。
本開示の化合物には、1または複数のLNAを組み込むことができ、場合によって、化合物を、LNAから完全に構成することもできる。個別のLNAヌクレオシドサブユニットの合成およびオリゴマーへのそれらの組込みのための方法については、例えば、参照によりそれらの全体において本明細書に組み込まれる、米国特許第7,572,582号、同第7,569,575号、同第7,084,125号、同第7,060,809号、同第7,053,207号、同第7,034,133号、同第6,794,499号、および同第6,670,461号において記載されている。典型的なヌクレオシド間リンカーは、ホスホジエステル部分およびホスホロチオエート部分を含み、代替的に、リン非含有リンカーを使用することもできる。さらなる実施形態は、LNA含有化合物を含み、各LNAサブユニットは、DNAサブユニットで隔てられている。ある特定の化合物は、交互のLNAサブユニットおよびDNAサブユニットから構成され、ヌクレオシド間リンカーは、ホスホロチオエートである。
ENAオリゴマーおよびそれらの調製については、参照によりその全体において本明細書に組み込まれる、Obikaら、Tetrahedron Ltt、38巻(50号):8735頁において記載されている。本開示の化合物には、1または複数のENAサブユニットを組み込むことができる。
3.ホスホロチオエート
「ホスホロチオエート」(またはS-オリゴ)とは、生来DNAまたは生来RNAの改変体であって、ホスホジエステルヌクレオシド間連結の非架橋酸素のうちの1つを、硫黄で置きかえた改変体である。デオキシリボースサブユニットと、ホスホロチオエートヌクレオシド間連結とを含む、ホスホロチオエートDNA(左)、および、リボースサブユニットと、ホスホロチオエート(phosophorothioate)ヌクレオシド間連結とを含む、ホスホロチオエートRNA(右)の非限定的な例を、下記:
に描示する。
「ホスホロチオエート」(またはS-オリゴ)とは、生来DNAまたは生来RNAの改変体であって、ホスホジエステルヌクレオシド間連結の非架橋酸素のうちの1つを、硫黄で置きかえた改変体である。デオキシリボースサブユニットと、ホスホロチオエートヌクレオシド間連結とを含む、ホスホロチオエートDNA(左)、および、リボースサブユニットと、ホスホロチオエート(phosophorothioate)ヌクレオシド間連結とを含む、ホスホロチオエートRNA(右)の非限定的な例を、下記:
に描示する。
ヌクレオシド間結合の硫黄化(sulfurization)は、5’-3’および3’-5’DNA POL 1エクソヌクレアーゼ、ヌクレアーゼS1およびP1、RNアーゼ、血清ヌクレアーゼ、ならびにヘビ毒ホスホジエステラーゼを含む、エンドヌクレアーゼおよびエクソヌクレアーゼの作用を低減する。ホスホロチオエートは、2つの主要な経路:ホスホン酸水素上の炭素ジスルフィド内の硫黄元素の溶解作用、または亜リン酸トリエステルを、テトラエチルチウラムジスルフィド(TETD)もしくは3H-1,2-ベンゾジチオール-3-オン1,1-ジオキシド(3H-1,2-bensodithiol-3-one 1,1-dioxide;BDTD)で硫黄化する方法(例えば、参照によりそれらの全体において本明細書に組み込まれる、Iyerら、J. Org. Chem.55巻、4693~4699頁、1990年を参照されたい)により作製し得る。後者の方法は、大半の有機溶媒中の硫黄元素の不溶性および炭素ジスルフィドの毒性の問題を回避する。TETD法およびBDTD法はまた、高純度のホスホロチオエートももたらす。
4.トリシクロDNAおよびトリシクロホスホロチオエートヌクレオチド
トリシクロDNA(tc-DNA)とは、各ヌクレオチドを、シクロプロパン環の導入により修飾して、骨格のコンフォメーション可撓性を制約し、ねじれ角γの骨格形状を最適化した、拘束DNA類似体のクラスである。ホモ塩基性のアデニン含有tc-DNAおよびチミン含有tc-DNAは、相補的なRNAと共に、極めて安定的なA-T塩基対を形成する。トリシクロDNAおよびそれらの合成については、参照によりその全体において本明細書に組み込まれる、PCT公開第WO2010/115993号において記載されている。本開示の化合物には、1または複数のトリシクロDNAサブユニットを組み込むことができ、場合によって、化合物は、トリシクロDNAサブユニットから完全に構成されうる。
トリシクロDNA(tc-DNA)とは、各ヌクレオチドを、シクロプロパン環の導入により修飾して、骨格のコンフォメーション可撓性を制約し、ねじれ角γの骨格形状を最適化した、拘束DNA類似体のクラスである。ホモ塩基性のアデニン含有tc-DNAおよびチミン含有tc-DNAは、相補的なRNAと共に、極めて安定的なA-T塩基対を形成する。トリシクロDNAおよびそれらの合成については、参照によりその全体において本明細書に組み込まれる、PCT公開第WO2010/115993号において記載されている。本開示の化合物には、1または複数のトリシクロDNAサブユニットを組み込むことができ、場合によって、化合物は、トリシクロDNAサブユニットから完全に構成されうる。
トリシクロホスホロチオエートヌクレオチドとは、ホスホロチオエートヌクレオシド間連結を伴うトリシクロDNAサブユニットである。トリシクロホスホロチオエートヌクレオチドおよびそれらの合成については、参照によりその全体において本明細書に組み込まれる、PCT公開第WO2013/053928号において記載されている。本開示の化合物には、1または複数のトリシクロDNAサブユニットを組み込むことができ、場合によって、化合物は、トリシクロDNAヌクレオチドから完全に構成されうる。トリシクロDNA/三環系(tricycle)サブユニットおよびホスホジエステルヌクレオシド間連結の非限定的な例を、下記:
に描示する。
に描示する。
5. 2’O-メチルオリゴマー、2’O-MOEオリゴマー、および2’-Fオリゴマー
「2’O-Meオリゴマー」分子は、リボース分子の2’-OH残基において、メチル基を保有するサブユニットを含む。2’-O-Me-RNAは、DNAと同じ(または類似の)挙動を示すが、ヌクレアーゼによる分解に対して保護されている。2’-O-Me-RNAはまた、さらなる安定化のために、ホスホロチオエートオリゴマー(PTO)と組み合わせることもできる。2’O-Meオリゴマー(2’-OMeサブユニットが、ホスホジエステルヌクレオシド間連結またはホスホロチオエートヌクレオシド間連結により接続されている)は、当技術分野における慣例的な技法(例えば、参照によりその全体において本明細書に組み込まれる、Yooら、Nucleic Acids Res.、32巻:2008~16頁、2004年を参照されたい)に従い、合成することができる。2’-OMeサブユニットおよびホスホジエステルサブユニット間連結を含む2’O-Meオリゴマーの非限定的な例を、下記:
に描示する。
「2’O-Meオリゴマー」分子は、リボース分子の2’-OH残基において、メチル基を保有するサブユニットを含む。2’-O-Me-RNAは、DNAと同じ(または類似の)挙動を示すが、ヌクレアーゼによる分解に対して保護されている。2’-O-Me-RNAはまた、さらなる安定化のために、ホスホロチオエートオリゴマー(PTO)と組み合わせることもできる。2’O-Meオリゴマー(2’-OMeサブユニットが、ホスホジエステルヌクレオシド間連結またはホスホロチオエートヌクレオシド間連結により接続されている)は、当技術分野における慣例的な技法(例えば、参照によりその全体において本明細書に組み込まれる、Yooら、Nucleic Acids Res.、32巻:2008~16頁、2004年を参照されたい)に従い、合成することができる。2’-OMeサブユニットおよびホスホジエステルサブユニット間連結を含む2’O-Meオリゴマーの非限定的な例を、下記:
に描示する。
2’O-Meオリゴマーはまた、ホスホロチオエート連結(2’O-Meホスホロチオエートオリゴマー)も含みうる。2’O-Meオリゴマーなどの2’O-メトキシエチルオリゴマー(2’-O MOE)は、リボース分子の2’-OH残基において、メトキシエチル基を保有するサブユニットを含み、参照によりその全体において本明細書に組み込まれる、Martinら、Helv. Chim. Acta、78巻、486~504頁、1995年において論じられている。2’O-MOEサブユニットの非限定的な例を、下記:
に描示する。
に描示する。
前出のアルキル化2’OHリボース誘導体と対照的に、2’-フルオロオリゴマーは、2’位において、2’OHの代わりにフルオロラジカルを有するサブユニットを含む。2’-Fサブユニットおよびホスホジエステルヌクレオシド間連結を含む2’-Fオリゴマーの非限定的な例を、下記:
に描示する。
に描示する。
2’-フルオロオリゴマーについては、参照によりその全体において本明細書に組み込まれる、WO2004/043977においてさらに記載されている。本開示の化合物には、1または複数の2’O-メチルサブユニット、2’O-MOEサブユニット、および2’-Fサブユニットを組み込むことができ、本明細書で記載されるヌクレオシド間連結のうちのいずれかを活用することができる。場合によって、本開示の化合物は、2’O-メチル、2’O-MOE、または2’Fサブユニットから完全に構成しうると予想される。本開示の化合物についての一実施形態は、2’O-メチルサブユニットから完全に構成される。
6. 2’-O-[2-(N-メチルカルバモイル)エチル]オリゴマー(MCE)
MCEは、本開示の化合物中で有用な、2’O修飾リボヌクレオチドの別の例である。この例では、2’OHを、2-(N-メチルカルバモイル)エチル部分へと誘導体化して、ヌクレアーゼ耐性を増加させる。MCEサブユニットおよびホスホジエステルヌクレオシド間連結を含むMCEオリゴマーの非限定的な例を、下記:
に描示する。
MCEは、本開示の化合物中で有用な、2’O修飾リボヌクレオチドの別の例である。この例では、2’OHを、2-(N-メチルカルバモイル)エチル部分へと誘導体化して、ヌクレアーゼ耐性を増加させる。MCEサブユニットおよびホスホジエステルヌクレオシド間連結を含むMCEオリゴマーの非限定的な例を、下記:
に描示する。
MCEおよびそれらの合成については、参照によりその全体において本明細書に組み込まれる、Yamadaら、J. Org. Chem.、76巻(9号):3042~53頁において記載されている。本開示の化合物には、1または複数のMCEサブユニットを組み込むことができる。
7.モルホリノベースのオリゴマー
モルホリノベースのオリゴマーとは、ヌクレオ塩基を支持するモルホリノサブユニットを含むオリゴマーを指し、リボースの代わりに、モルホリニル環を含有する。例示的なヌクレオシド間連結は、例えば、1つのモルホリノサブユニットのモルホリニル環窒素を、隣接するモルホリノサブユニットの4’環外炭素に接合する、ホスホルアミデートヌクレオシド間連結またはホスホロジアミデートヌクレオシド間連結を含む。各モルホリノサブユニットは、塩基特異的水素結合により、オリゴヌクレオチド内の塩基に結合するのに有効な、プリンまたはピリミジンのヌクレオ塩基を含む。
モルホリノベースのオリゴマーとは、ヌクレオ塩基を支持するモルホリノサブユニットを含むオリゴマーを指し、リボースの代わりに、モルホリニル環を含有する。例示的なヌクレオシド間連結は、例えば、1つのモルホリノサブユニットのモルホリニル環窒素を、隣接するモルホリノサブユニットの4’環外炭素に接合する、ホスホルアミデートヌクレオシド間連結またはホスホロジアミデートヌクレオシド間連結を含む。各モルホリノサブユニットは、塩基特異的水素結合により、オリゴヌクレオチド内の塩基に結合するのに有効な、プリンまたはピリミジンのヌクレオ塩基を含む。
モルホリノベースのオリゴマー(改変アンチセンスオリゴマーを含む)については、参照によりそれらの全体において本明細書に組み込まれる、米国特許第5,698,685号;同第5,217,866号;同第5,142,047号;同第5,034,506号;同第5,166,315号;同第5,185,444号;同第5,521,063号;同第5,506,337号;ならびに係属中の米国特許出願第12/271,036号;同第12/271,040号;およびPCT公開第WO/2009/064471号および同第WO/2012/043730号;ならびにSummertonら、1997年、「Antisense and Nucleic Acid Drug Development」、7巻、187~195頁において詳述されている。「モルホリノサブユニット」という用語は、Summertonらに記載されている通りに使用される。
オリゴマー構造内で、リン酸基は一般に、オリゴマーの「ヌクレオシド間連結」を形成する基として言及される。RNAおよびDNAの天然に存在するヌクレオシド間連結は、3’-5’ホスホジエステル連結である。「ホスホルアミデート」基が、3つの結合酸素原子と、1つの結合窒素原子とを有するリンを含むのに対し、「ホスホロジアミデート」基は、2つの結合酸素原子と、2つの結合窒素原子とを有するリンを含む。「ホスホロトリアミデート」基(またはリン酸トリアミド基)は、1個の結合する酸素原子および3個の結合する窒素原子を有するリンを含む。本明細書で記載されるモルホリノベースのオリゴマーの非荷電ヌクレオシド間連結またはカチオン性ヌクレオシド間連結では、1つの窒素は常に、連結鎖に対してペンダントであるものである。ホスホロジアミデート連結における第2の窒素は、モルホリノ環構造内の環窒素であることが典型的である。
「PMO」とは、(i)モルホリノ環の窒素原子への共有結合、および(ii)ジメチルアミノの窒素への第2の共有結合を伴うリン原子を有する、ホスホロジアミデートモルホリノベースのオリゴマーを指す。「PMO-X」とは、(i)モルホリノ環の窒素原子への共有結合、および(ii)例えば、4-アミノピペリジン-1-イル(すなわちAPN)または4-アミノピペリジン-1-イルの誘導体の環窒素への第2の共有結合を伴うリン原子を有するホスホロジアミデートモルホリノベースのオリゴマーを指す。例示的なPMO-Xオリゴマーについては、参照によりそれらの全体において本明細書に組み込まれる、PCT出願第PCT/US2011/38459号およびPCT公開第WO2013/074834号において開示されている。PMO-Xは、リン原子を、モルホリノ基、および4-アミノピペリジン-1-イル(すなわち、APN)の環窒素へと連結する、少なくとも1つのヌクレオシド間連結を含む、PMO-Xオリゴマーを指す、「PMO-apn」、「PMO-APN」または「APN」を含む。具体的な実施形態では、表3および表4に明示されたターゲティング配列を含む修飾アンチセンスオリゴマーは、少なくとも1つのAPNを含有する連結またはAPN誘導体を含有する連結を含む。多様な実施形態は、モルホリノベースのオリゴマーであって、約10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、または100%の、APN/APN誘導体を含有する連結を有し、残りの連結(100%未満である場合)が、非荷電連結であり、例えば、全ヌクレオシド間連結のうちの約1つ、2つ、3つ、4つ、5つ、6つ、7つ、8つ、9つ、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49または50、または少なくともほぼこれらの数が、APN/APN誘導体を含有する連結であるオリゴマーを含む。
多様な実施形態では、修飾アンチセンスオリゴマーは、式(I):
の化合物または薬学的に許容されるその塩であり、式中、
各Nuは、一緒になってターゲティング配列を形成するヌクレオ塩基であり;
Zは、8から48の整数であり;
各Yは、Oおよび-NR4から独立に選択され、式中、各R4は、H、C1~C6アルキル、アラルキル、C(=NH)NH2、C(O)(CH2)nNR5C(=NH)NH2、C(O)(CH2)2NHC(O)(CH2)5NR5C(=NH)NH2およびGから独立に選択され、式中、R5は、HおよびC1~C6アルキルから選択され、nは、1から5の整数であり;
Tは、OHおよび式:
の部分か選択され、式中、
Aは、-OH、-N(R7)2R8から選択され、式中、
各R7は、HおよびC1~C6アルキルから独立に選択され、
R8は、電子対およびHから選択され、そして
R6は、OH、-N(R9)CH2C(O)NH2および式:
の部分から選択され、式中、
R9は、HおよびC1~C6アルキルから選択され、
R10は、G、C(O)-R11OH、アシル、トリチル、4メトキシトリチル、C(=NH)NH2、C(O)(CH2)mNR12C(=NH)NH2およびC(O)(CH2)2NHC(O)(CH2)5NR12C(=NH)NH2から選択され、式中、
mは、1から5の整数であり、
R11は、式-(O-アルキル)y-を有し、式中、yは、3から10の整数であり、
y個のアルキル基の各々は、C2~C6アルキルから独立に選択され;
R12は、HおよびC1~C6アルキルから選択され;
R1の各例は、
-N(R13)2R14[式中、各R13は、HおよびC1~C6アルキルから独立に選択され、そしてR14は、電子対およびHから選択される];
式(II):
の部分[式中、
R15は、H、G、C1~C6アルキル、C(=NH)NH2、C(O)(CH2)qNR18C(=NH)NH2および-C(O)(CH2)2NHC(O)(CH2)5NR18C(=NH)NH2から選択され、式中、
R18は、HおよびC1~C6アルキルから選択され;
qは、1から5の整数であり、
R16は、電子対およびHから選択され;
各R17は、Hおよびメチルから独立に選択される];および
式(III):
の部分[式中、
R19は、H、C1~C6アルキル、C(=NH)NH2、-C(O)(CH2)rNR22C(=NH)NH2、-C(O)CH(NH2)(CH2)3NHC(=NH)NH2、-C(O)(CH2)2NHC(O)(CH2)5NR22C(=NH)NH2、-C(O)CH(NH2)(CH2)4NH2およびGから選択され、式中、
R22は、HおよびC1~C6アルキルから選択され;
rは、1から5の整数であり、
R20は、HおよびC1~C6アルキルから選択され;
R21は、電子対およびHから選択される]
から独立に選択され;
R2は、H、G、アシル、トリチル、4-メトキシトリチル、C1~C6アルキル、-C(=NH)NH2、-C(O)-R23、-C(O)(CH2)sNR24C(=NH)NH2、-C(O)(CH2)2NHC(O)(CH2)5NR24C(=NH)NH2、-C(O)CH(NH2)(CH2)3NHC(=NH)NH2および式:
の部分から選択され、式中、
R23は、式-(O-アルキル)v-OHを有し、式中、vは、3から10の整数であり、v個のアルキル基の各々は、C2~C6アルキルから独立に選択され;
R24は、HおよびC1~C6アルキルから選択され;
sは、1から5の整数であり;
Lは、-C(O)(CH2)6C(O)-および-C(O)(CH2)2S2(CH2)2C(O)-から選択され;
各R25は、式-(CH2)2OC(O)N(R26)2を有し、式中、各R26は、式-(CH2)6NHC(=NH)NH2を有し;
R3は、電子対、HおよびC1~C6アルキルから選択され、
ここで、Gは、-C(O)(CH2)5NH-CPP、-C(O)(CH2)2NH-CPP、-C(O)(CH2)2NHC(O)(CH2)5NH-CPPおよび-C(O)CH2NH-CPPから選択される細胞透過性ペプチド(「CPP」)およびリンカー部分であるか、またはGは、式:
を有し、式中、CPPは、Gの最大で1つの例が存在するという条件で、CPPのカルボキシ末端において、アミド結合により、リンカー部分に結合している。
の化合物または薬学的に許容されるその塩であり、式中、
各Nuは、一緒になってターゲティング配列を形成するヌクレオ塩基であり;
Zは、8から48の整数であり;
各Yは、Oおよび-NR4から独立に選択され、式中、各R4は、H、C1~C6アルキル、アラルキル、C(=NH)NH2、C(O)(CH2)nNR5C(=NH)NH2、C(O)(CH2)2NHC(O)(CH2)5NR5C(=NH)NH2およびGから独立に選択され、式中、R5は、HおよびC1~C6アルキルから選択され、nは、1から5の整数であり;
Tは、OHおよび式:
の部分か選択され、式中、
Aは、-OH、-N(R7)2R8から選択され、式中、
各R7は、HおよびC1~C6アルキルから独立に選択され、
R8は、電子対およびHから選択され、そして
R6は、OH、-N(R9)CH2C(O)NH2および式:
の部分から選択され、式中、
R9は、HおよびC1~C6アルキルから選択され、
R10は、G、C(O)-R11OH、アシル、トリチル、4メトキシトリチル、C(=NH)NH2、C(O)(CH2)mNR12C(=NH)NH2およびC(O)(CH2)2NHC(O)(CH2)5NR12C(=NH)NH2から選択され、式中、
mは、1から5の整数であり、
R11は、式-(O-アルキル)y-を有し、式中、yは、3から10の整数であり、
y個のアルキル基の各々は、C2~C6アルキルから独立に選択され;
R12は、HおよびC1~C6アルキルから選択され;
R1の各例は、
-N(R13)2R14[式中、各R13は、HおよびC1~C6アルキルから独立に選択され、そしてR14は、電子対およびHから選択される];
式(II):
の部分[式中、
R15は、H、G、C1~C6アルキル、C(=NH)NH2、C(O)(CH2)qNR18C(=NH)NH2および-C(O)(CH2)2NHC(O)(CH2)5NR18C(=NH)NH2から選択され、式中、
R18は、HおよびC1~C6アルキルから選択され;
qは、1から5の整数であり、
R16は、電子対およびHから選択され;
各R17は、Hおよびメチルから独立に選択される];および
式(III):
の部分[式中、
R19は、H、C1~C6アルキル、C(=NH)NH2、-C(O)(CH2)rNR22C(=NH)NH2、-C(O)CH(NH2)(CH2)3NHC(=NH)NH2、-C(O)(CH2)2NHC(O)(CH2)5NR22C(=NH)NH2、-C(O)CH(NH2)(CH2)4NH2およびGから選択され、式中、
R22は、HおよびC1~C6アルキルから選択され;
rは、1から5の整数であり、
R20は、HおよびC1~C6アルキルから選択され;
R21は、電子対およびHから選択される]
から独立に選択され;
R2は、H、G、アシル、トリチル、4-メトキシトリチル、C1~C6アルキル、-C(=NH)NH2、-C(O)-R23、-C(O)(CH2)sNR24C(=NH)NH2、-C(O)(CH2)2NHC(O)(CH2)5NR24C(=NH)NH2、-C(O)CH(NH2)(CH2)3NHC(=NH)NH2および式:
の部分から選択され、式中、
R23は、式-(O-アルキル)v-OHを有し、式中、vは、3から10の整数であり、v個のアルキル基の各々は、C2~C6アルキルから独立に選択され;
R24は、HおよびC1~C6アルキルから選択され;
sは、1から5の整数であり;
Lは、-C(O)(CH2)6C(O)-および-C(O)(CH2)2S2(CH2)2C(O)-から選択され;
各R25は、式-(CH2)2OC(O)N(R26)2を有し、式中、各R26は、式-(CH2)6NHC(=NH)NH2を有し;
R3は、電子対、HおよびC1~C6アルキルから選択され、
ここで、Gは、-C(O)(CH2)5NH-CPP、-C(O)(CH2)2NH-CPP、-C(O)(CH2)2NHC(O)(CH2)5NH-CPPおよび-C(O)CH2NH-CPPから選択される細胞透過性ペプチド(「CPP」)およびリンカー部分であるか、またはGは、式:
を有し、式中、CPPは、Gの最大で1つの例が存在するという条件で、CPPのカルボキシ末端において、アミド結合により、リンカー部分に結合している。
多様な実施形態では、ターゲティング配列は、ミオスタチンプレmRNA内の標的領域と相補的である。一部の実施形態では、ターゲティング配列は、エクソン2内に完全にありターゲティング配列のいかなる部分もスプライス接合部にわたらない標的領域内の、または、ミオスタチンプレmRNAのイントロン/エクソンもしくはエクソン/イントロンスプライス接合部にわたる領域(例えば配列番号2~3)の、12またはこれを超える連続ヌクレオチドと相補的である。
多様な実施形態では、ターゲティング配列は、ジストロフィンプレmRNA内の標的領域と相補的である。一部の実施形態では、ターゲティング配列は、エクソン7、エクソン8、エクソン9、エクソン19、エクソン23、エクソン44、エクソン45、エクソン50、エクソン51、エクソン52、エクソン53またはエクソン55から選択されるジストロフィンプレmRNAのエクソン内の標的領域内の、10またはこれを超える連続ヌクレオチドと相補的である。複数の実施形態では、標的領域は、ジストロフィンプレmRNAのエクソン内に完全にありターゲティング配列のいかなる部分もスプライス接合部にわたらないか、または、ジストロフィンプレmRNAのイントロン/エクソンもしくはエクソン/イントロンスプライス接合部にわたる領域である。
多様な実施形態では、ミオスタチンターゲティング配列は、配列番号16~75のうちの1つを含むか、配列番号16~75のうちの1つから選択されるか、配列番号16~75のうちの少なくとも1つから選択される配列の少なくとも12の連続ヌクレオチドの断片であるか、または、配列番号16~75のうちの少なくとも1つから選択される配列に対する少なくとも90%の配列同一性を有する変異体であり、各Xはウラシル(U)またはチミン(T)から独立に選択され、各Yはシトシン(C)または5-メチルシトシン(5mC)から独立に選択される。一部の実施形態では、配列番号16~75の各Xはチミン(T)であり、配列番号16~75の各Yはシトシン(C)である。
一部の実施形態では、式(I)のミオスタチンターゲティング配列は、
a)配列番号71(YYAGYYYAXYXXYXYYXGGXYYXGG)[Zは25である];
b)配列番号72(YAYXXAYYAGYYYAXYXXYXYYXGG)[Zは25である];
c)配列番号73(YYAYXXGYAXXAGAAAAXYAGY)[Zは22である];
d)配列番号74(GYATTAGAAAATYAGYTATAAATG)[Zは24である];および
e)配列番号75(YYATYYGYTTGYATTAGAAAGTYAGY)[Zは26である]
から選択され、各Xはウラシル(U)またはチミン(T)から独立に選択され、各Yはシトシン(C)または5-メチルシトシン(5mC)から独立に選択される。一部の実施形態では、配列番号71~75の各Xはチミン(T)であり、配列番号71~75の各Yはシトシン(C)である。
a)配列番号71(YYAGYYYAXYXXYXYYXGGXYYXGG)[Zは25である];
b)配列番号72(YAYXXAYYAGYYYAXYXXYXYYXGG)[Zは25である];
c)配列番号73(YYAYXXGYAXXAGAAAAXYAGY)[Zは22である];
d)配列番号74(GYATTAGAAAATYAGYTATAAATG)[Zは24である];および
e)配列番号75(YYATYYGYTTGYATTAGAAAGTYAGY)[Zは26である]
から選択され、各Xはウラシル(U)またはチミン(T)から独立に選択され、各Yはシトシン(C)または5-メチルシトシン(5mC)から独立に選択される。一部の実施形態では、配列番号71~75の各Xはチミン(T)であり、配列番号71~75の各Yはシトシン(C)である。
多様な実施形態では、ジストロフィンターゲティング配列は、配列番号76~3485のうちの1つを含むか、配列番号76~3485のうちの1つから選択されるか、配列番号76~3485のうちの少なくとも1つから選択される配列の少なくとも10の連続ヌクレオチドの断片であるか、または、配列番号76~3485のうちの少なくとも1つから選択される配列に対する少なくとも90%の配列同一性を有する変異体であり、各Xはウラシル(U)またはチミン(T)から独立に選択され、各Yはシトシン(C)または5-メチルシトシン(5mC)から独立に選択される。一部の実施形態では、配列番号76~3485の各Xはチミン(T)であり、配列番号76~3485の各Yはシトシン(C)である。一部の実施形態では、ターゲティング配列は、配列番号76を含み得る。
多様な実施形態では、ターゲティング配列の少なくとも1つのXはTである。多様な実施形態では、ターゲティング配列の各XはTである。
多様な実施形態では、ターゲティング配列の少なくとも1つのXはUである。多様な実施形態では、ターゲティング配列の各XはUである。
多様な実施形態では、ターゲティング配列の少なくとも1つのYは5mCである。多様な実施形態では、ターゲティング配列の各Yは5mCである。
多様な実施形態では、ターゲティング配列の少なくとも1つのYはCである。多様な実施形態では、ターゲティング配列の各YはCである。
多様な実施形態では、配列番号16~75および配列番号76~3485の少なくとも1つのXはTである。多様な実施形態では、配列番号16~75および配列番号76~3485の各XはTである。
多様な実施形態では、ターゲティング配列の少なくとも1つのXはUである。多様な実施形態では、配列番号16~75および配列番号76~3485の各XはUである。
多様な実施形態では、配列番号16~75および配列番号76~3485の少なくとも1つのYは5mCである。多様な実施形態では、配列番号16~75および配列番号76~3485の各Yは5mCである。
多様な実施形態では、配列番号16~75および配列番号76~3485の少なくとも1つのYはCである。多様な実施形態では、配列番号16~75および配列番号76~3485の各YはCである。
一部の実施形態では、R3は式:
の部分である[式中、Lは、-C(O)(CH2)6C(O)-または-C(O)(CH2)2S2(CH2)2C(O)-から選択され、
各R25は、式-(CH2)2OC(O)N(R26)2を有し、各R26は、式-(CH2)6NHC(=NH)NH2を有する。かかる部分は、参照によりその全体において本明細書に組み込まれる米国特許第7,935,816号でさらに記載されている。
の部分である[式中、Lは、-C(O)(CH2)6C(O)-または-C(O)(CH2)2S2(CH2)2C(O)-から選択され、
各R25は、式-(CH2)2OC(O)N(R26)2を有し、各R26は、式-(CH2)6NHC(=NH)NH2を有する。かかる部分は、参照によりその全体において本明細書に組み込まれる米国特許第7,935,816号でさらに記載されている。
多様な実施形態では、各YはOであり、R2はHまたはGから選択され、R3は、電子対またはHから選択される。一部の実施形態では、R2はGであり、CPPは配列番号3486~3501から選択される配列を有する。ある特定の実施形態では、R2はHである。
ある特定の実施形態では、各R1は-N(CH3)2である。一部の実施形態では、R1基の約50~90%はジメチルアミノ(すなわち-N(CH3)2)である。ある特定の実施形態では、R1基の約70%~約80%はジメチルアミノである。ある特定の実施形態では、R1基の約75%はジメチルアミノである。ある特定の実施形態では、R1基の約66%はジメチルアミノである。
多様な実施形態では、各YはOであり、R2はHまたはGから選択され、R3は電子対またはHから選択される。一部の実施形態では、R2はGであり、CPPは、後述する配列番号3486~3501から選択される配列を有する。
他の実施形態では、修飾アンチセンスオリゴマーは、式(IV):
の化合物または薬学的に許容されるその塩であり、式中、
各Nuは、一緒になってターゲティング配列を形成するヌクレオ塩基であり;
Zは、8から48の整数であり;
各Yは、Oおよび-NR4から独立に選択され、式中、各R4は、H、C1~C6アルキル、アラルキル、-C(=NH)NH2、-C(O)(CH2)nNR5C(=NH)NH2、-C(O)(CH2)2NHC(O)(CH2)5NR5C(=NH)NH2およびGから独立に選択され、式中、R5は、HおよびC1~C6アルキルから選択され、nは、1から5の整数であり;
Tは、OHおよび式:
の部分から選択され、式中、
Aは、-OHおよび-N(R7)2R8から選択され、式中
各R7は、HおよびC1~C6アルキルから独立に選択され、
R8は、電子対およびHから選択され、
R6は、OH、-N(R9)CH2C(O)NH2および式:
の部分から選択され、式中、
R9は、HおよびC1~C6アルキルから選択され、
R10は、G、-C(O)-R11OH、アシル、トリチル、4-メトキシトリチル、-C(=NH)NH2、-C(O)(CH2)mNR12C(=NH)NH2および-C(O)(CH2)2NHC(O)(CH2)5NR12C(=NH)NH2から選択され、式中、
mは、1から5の整数であり、
R11は、式-(O-アルキル)y-を有し、式中、yは、3から10の整数であり、
y個のアルキル基の各々は、C2~C6アルキルから独立に選択され;
R12は、HおよびC1~C6アルキルから選択され;
R2は、H、G、アシル、トリチル、4-メトキシトリチル、C1~C6アルキル、-C(=NH)NH2および-C(O)-R23から選択され;
R3は、電子対、HおよびC1~C6アルキルから選択される。
の化合物または薬学的に許容されるその塩であり、式中、
各Nuは、一緒になってターゲティング配列を形成するヌクレオ塩基であり;
Zは、8から48の整数であり;
各Yは、Oおよび-NR4から独立に選択され、式中、各R4は、H、C1~C6アルキル、アラルキル、-C(=NH)NH2、-C(O)(CH2)nNR5C(=NH)NH2、-C(O)(CH2)2NHC(O)(CH2)5NR5C(=NH)NH2およびGから独立に選択され、式中、R5は、HおよびC1~C6アルキルから選択され、nは、1から5の整数であり;
Tは、OHおよび式:
の部分から選択され、式中、
Aは、-OHおよび-N(R7)2R8から選択され、式中
各R7は、HおよびC1~C6アルキルから独立に選択され、
R8は、電子対およびHから選択され、
R6は、OH、-N(R9)CH2C(O)NH2および式:
の部分から選択され、式中、
R9は、HおよびC1~C6アルキルから選択され、
R10は、G、-C(O)-R11OH、アシル、トリチル、4-メトキシトリチル、-C(=NH)NH2、-C(O)(CH2)mNR12C(=NH)NH2および-C(O)(CH2)2NHC(O)(CH2)5NR12C(=NH)NH2から選択され、式中、
mは、1から5の整数であり、
R11は、式-(O-アルキル)y-を有し、式中、yは、3から10の整数であり、
y個のアルキル基の各々は、C2~C6アルキルから独立に選択され;
R12は、HおよびC1~C6アルキルから選択され;
R2は、H、G、アシル、トリチル、4-メトキシトリチル、C1~C6アルキル、-C(=NH)NH2および-C(O)-R23から選択され;
R3は、電子対、HおよびC1~C6アルキルから選択される。
多様な実施形態では、ターゲティング配列は、ミオスタチンプレmRNA内の標的領域と相補的である。一部の実施形態では、ターゲティング配列は、エクソン2内に完全にありターゲティング配列のいかなる部分もスプライス接合部にわたらない標的領域内の12またはこれを超える連続ヌクレオチド、または、ミオスタチンプレmRNAのイントロン/エクソンもしくはエクソン/イントロンのスプライス接合部(例えば配列番号1~3)にわたる領域と相補的である。
多様な実施形態では、ターゲティング配列は、ジストロフィンプレmRNA内の標的領域と相補的である。一部の実施形態では、ターゲティング配列は、エクソン7、エクソン8、エクソン9、エクソン19、エクソン23、エクソン44、エクソン45、エクソン50、エクソン51、エクソン52、エクソン53またはエクソン55から選択されるジストロフィンプレmRNAのエクソン内の標的領域内の10またはこれを超える連続ヌクレオチドと相補的である。複数の実施形態では、標的領域は、ジストロフィンプレmRNAのエクソン内に完全にありターゲティング配列のいかなる部分もスプライス接合部にわたらないか、または、ジストロフィンプレmRNAのイントロン/エクソンもしくはエクソン/イントロンのスプライス接合部にわたる領域(例えば配列番号76~3485)である。
多様な実施形態では、ミオスタチンターゲティング配列は、配列番号4~15のうちの1つを含むか、配列番号4~15のうちの1つから選択されるか、配列番号4~15のうちの少なくとも1つから選択される配列の少なくとも12の連続ヌクレオチドの断片であるか、または、配列番号4~15のうちの少なくとも1つから選択される配列に対する少なくとも90%の配列同一性を有する変異体であり、各Xはウラシル(U)またはチミン(T)から独立に選択され、各Yはシトシン(C)または5-メチルシトシン(5mC)から独立に選択される。一部の実施形態では、配列番号4~15の各Xはチミン(T)であり、配列番号4~15の各Yはシトシン(C)である。
一部の実施形態では、式(IV)のミオスタチンターゲティング配列は、
a)配列番号71(YYAGYYYAXYXXYXYYXGGXYYXGG)[Zは25である];
b)配列番号72(YAYXXAYYAGYYYAXYXXYXYYXGG)[Zは25である];
c)配列番号73(YYAYXXGYAXXAGAAAAXYAGY)[Zは22である];
d)配列番号74(GYATTAGAAAATYAGYTATAAATG)[Zは24である];および
e)配列番号75(YYATYYGYTTGYATTAGAAAGTYAGY)[Zは26である]
から選択され、各Xはウラシル(U)またはチミン(T)から独立に選択され、各Yはシトシン(C)または5-メチルシトシン(5mC)から独立に選択される。一部の実施形態では、配列番号71~75の各Xはチミン(T)であり、配列番号71~75の各Yはシトシン(C)である。
a)配列番号71(YYAGYYYAXYXXYXYYXGGXYYXGG)[Zは25である];
b)配列番号72(YAYXXAYYAGYYYAXYXXYXYYXGG)[Zは25である];
c)配列番号73(YYAYXXGYAXXAGAAAAXYAGY)[Zは22である];
d)配列番号74(GYATTAGAAAATYAGYTATAAATG)[Zは24である];および
e)配列番号75(YYATYYGYTTGYATTAGAAAGTYAGY)[Zは26である]
から選択され、各Xはウラシル(U)またはチミン(T)から独立に選択され、各Yはシトシン(C)または5-メチルシトシン(5mC)から独立に選択される。一部の実施形態では、配列番号71~75の各Xはチミン(T)であり、配列番号71~75の各Yはシトシン(C)である。
多様な実施形態では、ジストロフィンターゲティング配列は、配列番号76~3485のうちの1つを含むか、配列番号76~3485のうちの1つから選択されるか、配列番号76~3485のうちの少なくとも1つから選択される配列の少なくとも10の連続ヌクレオチドの断片であるか、または、配列番号76~3485のうちの少なくとも1つから選択される配列に対する少なくとも90%の配列同一性を有する変異体であり、各Xはウラシル(U)またはチミン(T)から独立に選択され、各Yはシトシン(C)または5-メチルシトシン(5mC)から独立に選択される。一部の実施形態では、配列番号76~3485の各Xはチミン(T)であり、配列番号76~3485の各Yはシトシン(C)である。一部の実施形態では、ターゲティング配列は、配列番号76を含み得る。
多様な実施形態では、YはOであり、R2はHまたはGから選択され、R3は電子対またはHから選択される。一部の実施形態では、R2はGであり、CPPは配列番号9~24から選択される配列を有する。ある特定の実施形態では、R2はHである。
他の実施形態では、改変アンチセンスオリゴマーは、式(V):
の化合物または薬学的に許容されるその塩であり、式中、
各Nuは、一緒になってターゲティング配列を形成するヌクレオ塩基であり;
Zは、8から48の整数であり;
各Yは、Oおよび-NR4から独立に選択され、式中、各R4は、H、C1~C6アルキル、アラルキル、C(=NH)NH2、C(O)(CH2)nNR5C(=NH)NH2、C(O)(CH2)2NHC(O)(CH2)5NR5C(=NH)NH2およびGから独立に選択され、式中、R5は、HおよびC1~C6アルキルから選択され、nは1から5の整数であり;
Tは、OHおよび式:
の部分から選択され、式中、
Aは、-OH、-N(R7)2R8から選択され、式中
R7は、HおよびC1~C6アルキルから独立に選択され、
R8は、電子対およびHから選択され、
R6は、OH、-N(R9)CH2C(O)NH2および式:
の部分から選択され、式中、
R9は、HおよびC1~C6アルキルから選択され;
R10は、G、C(O)-R11OH、アシル、トリチル、4メトキシトリチル、C(=NH)NH2、C(O)(CH2)mNR12C(=NH)NH2およびC(O)(CH2)2NHC(O)(CH2)5NR12C(=NH)NH2から選択され、式中、
mは、1から5の整数であり、
R11は、式-(O-アルキル)y-を有し、式中、yは、3から10の整数であり、
y個のアルキル基の各々は、C2~C6アルキルから独立に選択され;
R12は、HおよびC1~C6アルキルから選択され;
ここで、Gは、-C(O)(CH2)5NH-CPP、-C(O)(CH2)2NH-CPP、-C(O)(CH2)2NHC(O)(CH2)5NH-CPPおよび-C(O)CH2NH-CPPから選択される、細胞透過性ペプチド(「CPP」)およびリンカー部分であるか、またはGは、式:
を有し、式中、CPPは、Gの最大で1つの例が存在するという条件で、CPPのカルボキシ末端において、アミド結合により、リンカー部分に結合している。
の化合物または薬学的に許容されるその塩であり、式中、
各Nuは、一緒になってターゲティング配列を形成するヌクレオ塩基であり;
Zは、8から48の整数であり;
各Yは、Oおよび-NR4から独立に選択され、式中、各R4は、H、C1~C6アルキル、アラルキル、C(=NH)NH2、C(O)(CH2)nNR5C(=NH)NH2、C(O)(CH2)2NHC(O)(CH2)5NR5C(=NH)NH2およびGから独立に選択され、式中、R5は、HおよびC1~C6アルキルから選択され、nは1から5の整数であり;
Tは、OHおよび式:
Aは、-OH、-N(R7)2R8から選択され、式中
R7は、HおよびC1~C6アルキルから独立に選択され、
R8は、電子対およびHから選択され、
R6は、OH、-N(R9)CH2C(O)NH2および式:
の部分から選択され、式中、
R9は、HおよびC1~C6アルキルから選択され;
R10は、G、C(O)-R11OH、アシル、トリチル、4メトキシトリチル、C(=NH)NH2、C(O)(CH2)mNR12C(=NH)NH2およびC(O)(CH2)2NHC(O)(CH2)5NR12C(=NH)NH2から選択され、式中、
mは、1から5の整数であり、
R11は、式-(O-アルキル)y-を有し、式中、yは、3から10の整数であり、
y個のアルキル基の各々は、C2~C6アルキルから独立に選択され;
R12は、HおよびC1~C6アルキルから選択され;
ここで、Gは、-C(O)(CH2)5NH-CPP、-C(O)(CH2)2NH-CPP、-C(O)(CH2)2NHC(O)(CH2)5NH-CPPおよび-C(O)CH2NH-CPPから選択される、細胞透過性ペプチド(「CPP」)およびリンカー部分であるか、またはGは、式:
を有し、式中、CPPは、Gの最大で1つの例が存在するという条件で、CPPのカルボキシ末端において、アミド結合により、リンカー部分に結合している。
多様な実施形態では、ターゲティング配列は、ミオスタチンプレmRNA内の標的領域と相補的である。一部の実施形態では、ターゲティング配列は、エクソン2内に完全にありターゲティング配列のいかなる部分もスプライス接合部にわたらない標的領域内の12もしくはこれを超える連続ヌクレオチド、または、ミオスタチンプレmRNAのイントロン/エクソンもしくはエクソン/イントロンのスプライス接合部(例えば配列番号1~3)にわたる領域と相補的である。
多様な実施形態では、ターゲティング配列は、ジストロフィンプレmRNA内の標的領域と相補的である。一部の実施形態では、ターゲティング配列は、エクソン7、エクソン8、エクソン9、エクソン19、エクソン23、エクソン44、エクソン45、エクソン50、エクソン51、エクソン52、エクソン53またはエクソン55から選択される、ジストロフィンプレmRNAのエクソン内の標的領域内の10またはこれを超える連続ヌクレオチドと相補的である。複数の実施形態では、標的領域は、ジストロフィンプレmRNAのエクソン内に完全にありターゲティング配列のいかなる部分もスプライス接合部にわたらないか、またはジストロフィンプレmRNAのイントロン/エクソンもしくはエクソン/イントロンのスプライス接合部(例えば配列番号4~15)にわたる領域である。
多様な実施形態では、ミオスタチンターゲティング配列は、配列番号16~75のうちの1つを含むか、配列番号16~75のうちの1つから選択されるか、配列番号16~75のうちの少なくとも1つから選択される配列の少なくとも12の連続ヌクレオチドの断片であるか、または、配列番号16~75のうちの少なくとも1つから選択される配列に対する少なくとも90%の配列同一性を有する変異体であり、各Xはウラシル(U)またはチミン(T)から独立に選択され、各Yはシトシン(C)または5-メチルシトシン(5mC)から独立に選択される。一部の実施形態では、配列番号16~75の各Xはチミン(T)であり、配列番号16~75の各Yはシトシン(C)である。
一部の実施形態では、式(V)のミオスタチンターゲティング配列は、
a)配列番号71(YYAGYYYAXYXXYXYYXGGXYYXGG)[Zは25である];
b)配列番号72(YAYXXAYYAGYYYAXYXXYXYYXGG)[Zは25である];
c)配列番号73(YYAYXXGYAXXAGAAAAXYAGY)[Zは22である];
d)配列番号74(GYATTAGAAAATYAGYTATAAATG)[Zは24である];および
e)配列番号75(YYATYYGYTTGYATTAGAAAGTYAGY)[Zは26である]
から選択され、各Xはウラシル(U)またはチミン(T)から独立に選択され、各Yはシトシン(C)または5-メチルシトシン(5mC)から独立に選択される。一部の実施形態では、配列番号71~75の各Xはチミン(T)であり、配列番号71~75の各Yはシトシン(C)である。
a)配列番号71(YYAGYYYAXYXXYXYYXGGXYYXGG)[Zは25である];
b)配列番号72(YAYXXAYYAGYYYAXYXXYXYYXGG)[Zは25である];
c)配列番号73(YYAYXXGYAXXAGAAAAXYAGY)[Zは22である];
d)配列番号74(GYATTAGAAAATYAGYTATAAATG)[Zは24である];および
e)配列番号75(YYATYYGYTTGYATTAGAAAGTYAGY)[Zは26である]
から選択され、各Xはウラシル(U)またはチミン(T)から独立に選択され、各Yはシトシン(C)または5-メチルシトシン(5mC)から独立に選択される。一部の実施形態では、配列番号71~75の各Xはチミン(T)であり、配列番号71~75の各Yはシトシン(C)である。
多様な実施形態では、ジストロフィンターゲティング配列は、配列番号76~3485のうちの1つを含むか、配列番号76~3485のうちの1つから選択されるか、配列番号76~3485のうちの少なくとも1つから選択される配列の少なくとも10の連続ヌクレオチドの断片であるか、または、配列番号76~3485のうちの少なくとも1つから選択される配列に対する少なくとも90%の配列同一性を有する変異体であり、各Xはウラシル(U)またはチミン(T)から独立に選択され、各Yはシトシン(C)または5-メチルシトシン(5mC)から独立に選択される。一部の実施形態では、配列番号76~3485の各Xはチミン(T)であり、配列番号76~3485の各Yはシトシン(C)である。一部の実施形態では、ターゲティング配列は、配列番号76を含み得る。
ある特定の実施形態では、本開示のアンチセンスオリゴマーは、式(VI):
の化合物または薬学的に許容されるその塩であり、式中、
各Nuは、一緒になってターゲティング配列を形成するヌクレオ塩基であり、
Zは、15~25の整数であり、
各Yは、Oであり、
各R1は、
から独立に選択される。
の化合物または薬学的に許容されるその塩であり、式中、
各Nuは、一緒になってターゲティング配列を形成するヌクレオ塩基であり、
Zは、15~25の整数であり、
各Yは、Oであり、
各R1は、
から独立に選択される。
多様な実施形態では、少なくとも1つのR1は-N(CH3)2である。一部の実施形態では、各R1は-N(CH3)2である。
多様な実施形態では、ターゲティング配列は、ミオスタチンプレmRNA内の標的領域と相補的である。一部の実施形態では、ターゲティング配列は、エクソン2内に完全にありターゲティング配列のいかなる部分もスプライス接合部にわたらない標的領域内の12またはこれを超える連続ヌクレオチド、または、ミオスタチンプレmRNAのイントロン/エクソンもしくはエクソン/イントロンのスプライス接合部(例えば配列番号1~3)にわたる領域と相補的である。
多様な実施形態では、ターゲティング配列は、ジストロフィンプレmRNA内の標的領域と相補的である。一部の実施形態では、ターゲティング配列は、エクソン7、エクソン8、エクソン9、エクソン19、エクソン23、エクソン44、エクソン45、エクソン50、エクソン51、エクソン52、エクソン53またはエクソン55から選択される、ジストロフィンプレmRNAのエクソン内の標的領域内の10またはこれを超える連続ヌクレオチドと相補的である。一部の実施形態では、標的領域は、ジストロフィンプレmRNAのエクソン内に完全にありターゲティング配列のいかなる部分もスプライス接合部にわたらないか、またはジストロフィンプレmRNAのイントロン/エクソンもしくはエクソン/イントロンのスプライス接合部(例えば配列番号4~15)にわたる領域である。
多様な実施形態では、ミオスタチンターゲティング配列は、配列番号16~75のうちの1つを含むか、配列番号16~75のうちの1つから選択されるか、配列番号16~75のうちの少なくとも1つから選択される配列の少なくとも12の連続ヌクレオチドの断片であるか、または、配列番号16~75のうちの少なくとも1つから選択される配列に対する少なくとも90%の配列同一性を有する変異体であり、各Xはウラシル(U)またはチミン(T)から独立に選択され、各Yはシトシン(C)または5-メチルシトシン(5mC)から独立に選択される。一部の実施形態では、配列番号16~75の各Xはチミン(T)であり、配列番号16~75の各Yはシトシン(C)である。
一部の実施形態では、式(VI)のミオスタチンターゲティング配列は、
a)配列番号71(YYAGYYYAXYXXYXYYXGGXYYXGG)[Zは25である];
b)配列番号72(YAYXXAYYAGYYYAXYXXYXYYXGG)[Zは25である];
c)配列番号73(YYAYXXGYAXXAGAAAAXYAGY)[Zは22である];
d)配列番号74(GYATTAGAAAATYAGYTATAAATG)[Zは24である];および
e)配列番号75(YYATYYGYTTGYATTAGAAAGTYAGY)[Zは26である]
から選択され、各Xはウラシル(U)またはチミン(T)から独立に選択され、各Yはシトシン(C)または5-メチルシトシン(5mC)から独立に選択される。一部の実施形態では、配列番号71~75の各Xはチミン(T)であり、配列番号71~75の各Yはシトシン(C)である。
a)配列番号71(YYAGYYYAXYXXYXYYXGGXYYXGG)[Zは25である];
b)配列番号72(YAYXXAYYAGYYYAXYXXYXYYXGG)[Zは25である];
c)配列番号73(YYAYXXGYAXXAGAAAAXYAGY)[Zは22である];
d)配列番号74(GYATTAGAAAATYAGYTATAAATG)[Zは24である];および
e)配列番号75(YYATYYGYTTGYATTAGAAAGTYAGY)[Zは26である]
から選択され、各Xはウラシル(U)またはチミン(T)から独立に選択され、各Yはシトシン(C)または5-メチルシトシン(5mC)から独立に選択される。一部の実施形態では、配列番号71~75の各Xはチミン(T)であり、配列番号71~75の各Yはシトシン(C)である。
多様な実施形態では、ジストロフィンターゲティング配列は、配列番号76~3485のうちの1つを含むか、配列番号76~3485のうちの1つから選択されるか、配列番号76~3485のうちの少なくとも1つから選択される配列の少なくとも10の連続ヌクレオチドの断片であるか、または、配列番号76~3485のうちの少なくとも1つから選択される配列に対する少なくとも90%の配列同一性を有する変異体であり、各Xはウラシル(U)またはチミン(T)から独立に選択され、各Yはシトシン(C)または5-メチルシトシン(5mC)から独立に選択される。一部の実施形態では、配列番号76~3485の各Xはチミン(T)であり、配列番号76~3485の各Yはシトシン(C)である。一部の実施形態では、ターゲティング配列は、配列番号76を含み得る。
一部の実施形態では、アンチセンスオリゴマーは式(VII):
の化合物または薬学的に許容されるその塩であり、式中、
各Nuは、一緒になってターゲティング配列を形成するヌクレオ塩基であり、
Zは、8~48の整数であり、
各Yは、Oであり、
各R1は、
から選択され、
R2は、H、アシル、トリチル、4-メトキシトリチル、C1~C6アルキル、-C(=NH)NH2および-C(O)-R23から選択され;
R3は電子対、HおよびC1~C6アルキルから選択される。
の化合物または薬学的に許容されるその塩であり、式中、
各Nuは、一緒になってターゲティング配列を形成するヌクレオ塩基であり、
Zは、8~48の整数であり、
各Yは、Oであり、
各R1は、
から選択され、
R2は、H、アシル、トリチル、4-メトキシトリチル、C1~C6アルキル、-C(=NH)NH2および-C(O)-R23から選択され;
R3は電子対、HおよびC1~C6アルキルから選択される。
多様な実施形態では、ターゲティング配列は、ミオスタチンプレmRNA内の標的領域と相補的である。一部の実施形態では、ターゲティング配列は、ミオスタチンプレmRNAのエクソン内に完全にある標的領域内の12もしくはこれを超える連続ヌクレオチド、または、ミオスタチンプレmRNAのイントロン/エクソンもしくはエクソン/イントロンのスプライス接合部(例えば配列番号1~3)にわたる領域と相補的である。
多様な実施形態では、ターゲティング配列は、ジストロフィンプレmRNA内の標的領域と相補的である。一部の実施形態では、ターゲティング配列は、エクソン7、エクソン8、エクソン9、エクソン19、エクソン23、エクソン44、エクソン45、エクソン50、エクソン51、エクソン52、エクソン53またはエクソン55から選択されるジストロフィンプレmRNAのエクソン内の標的領域内の10またはこれを超える連続ヌクレオチドと相補的である。複数の実施形態では、標的領域は、ジストロフィンプレmRNAのエクソン内に完全にありターゲティング配列のいかなる部分もスプライス接合部にわたらないか、またはジストロフィンプレmRNAのイントロン/エクソンもしくはエクソン/イントロンのスプライス接合部(例えば配列番号4~15)にわたる領域である。
多様な実施形態では、ミオスタチンターゲティング配列は、配列番号16~75のうちの1つを含むか、配列番号16~75のうちの1つから選択されるか、配列番号16~75のうちの少なくとも1つから選択される配列の少なくとも12の連続ヌクレオチドの断片であるか、または、配列番号16~75のうちの少なくとも1つから選択される配列に対する少なくとも90%の配列同一性を有する変異体であり、各Xはウラシル(U)またはチミン(T)から独立に選択され、各Yはシトシン(C)または5-メチルシトシン(5mC)から独立に選択される。一部の実施形態では、配列番号16~75の各Xはチミン(T)であり、配列番号16~75の各Yはシトシン(C)である。
一部の実施形態では、式(VII)のミオスタチンターゲティング配列は、
a)配列番号71(YYAGYYYAXYXXYXYYXGGXYYXGG)[Zは25である];
b)配列番号72(YAYXXAYYAGYYYAXYXXYXYYXGG)[Zは25である];
c)配列番号73(YYAYXXGYAXXAGAAAAXYAGY)[Zは22である];
d)配列番号74(GYATTAGAAAATYAGYTATAAATG)[Zは24である];および
e)配列番号75(YYATYYGYTTGYATTAGAAAGTYAGY)[Zは26である]
から選択され、各Xはウラシル(U)またはチミン(T)から独立に選択され、各Yはシトシン(C)または5-メチルシトシン(5mC)から独立に選択される。一部の実施形態では、配列番号71~75の各Xはチミン(T)であり、配列番号71~75の各Yはシトシン(C)である。
a)配列番号71(YYAGYYYAXYXXYXYYXGGXYYXGG)[Zは25である];
b)配列番号72(YAYXXAYYAGYYYAXYXXYXYYXGG)[Zは25である];
c)配列番号73(YYAYXXGYAXXAGAAAAXYAGY)[Zは22である];
d)配列番号74(GYATTAGAAAATYAGYTATAAATG)[Zは24である];および
e)配列番号75(YYATYYGYTTGYATTAGAAAGTYAGY)[Zは26である]
から選択され、各Xはウラシル(U)またはチミン(T)から独立に選択され、各Yはシトシン(C)または5-メチルシトシン(5mC)から独立に選択される。一部の実施形態では、配列番号71~75の各Xはチミン(T)であり、配列番号71~75の各Yはシトシン(C)である。
多様な実施形態では、ジストロフィンターゲティング配列は、配列番号76~3485のうちの1つを含むか、配列番号76~3485のうちの1つから選択されるか、配列番号76~3485のうちの少なくとも1つから選択される配列の少なくとも10の連続ヌクレオチドの断片であるか、または、配列番号76~3485のうちの少なくとも1つから選択される配列に対する少なくとも90%の配列同一性を有する変異体であり、各Xはウラシル(U)またはチミン(T)から独立に選択され、各Yはシトシン(C)または5-メチルシトシン(5mC)から独立に選択される。一部の実施形態では、配列番号76~3485の各Xはチミン(T)であり、配列番号76~3485の各Yはシトシン(C)である。一部の実施形態では、ターゲティング配列は、配列番号76を含み得る。
多様な実施形態では、ターゲティング配列の少なくとも1つのXはTである。多様な実施形態では、ターゲティング配列の各XはTである。
多様な実施形態では、ターゲティング配列の少なくとも1つのXはUである。多様な実施形態では、ターゲティング配列の各XはUである。
多様な実施形態では、ターゲティング配列の少なくとも1つのYは5mCである。多様な実施形態では、ターゲティング配列の各Yは、5mCである。
多様な実施形態では、ターゲティング配列の少なくとも1つのYはCである。多様な実施形態では、ターゲティング配列の各YはCである。
多様な実施形態では、配列番号16~75および配列番号76~3485の少なくとも1つのXはTである。多様な実施形態では、配列番号16~75および配列番号76~3485の各XはTである。
多様な実施形態では、ターゲティング配列の少なくとも1つのXはUである。多様な実施形態では、配列番号16~75および配列番号76~3485の各XはUである。
多様な実施形態では、配列番号16~75および配列番号76~3485の少なくとも1つのYは5mCである。多様な実施形態では、配列番号16~75および配列番号76~3485の各Yは5mCである。
多様な実施形態では、配列番号16~75および配列番号76~3485の少なくとも1つのYはCである。多様な実施形態では、配列番号16~75および配列番号76~3485の各YはCである。
ある特定の実施形態では、アンチセンスオリゴマーは、式(VIII):
の化合物または薬学的に許容されるその塩であり、式中、
各Nuは、一緒になってターゲティング配列を形成するヌクレオ塩基であり、
Zは、8~48の整数である。
の化合物または薬学的に許容されるその塩であり、式中、
各Nuは、一緒になってターゲティング配列を形成するヌクレオ塩基であり、
Zは、8~48の整数である。
多様な実施形態では、ターゲティング配列は、ミオスタチンプレmRNA内の標的領域と相補的である。一部の実施形態では、ターゲティング配列は、エクソン/イントロンスプライス接合部位内の標的領域内の12もしくはこれを超える連続ヌクレオチド、または、ミオスタチンプレmRNAのイントロン/エクソンもしくはエクソン/イントロンのスプライス接合部(例えば配列番号1~3)にわたる領域と相補的である。
多様な実施形態では、ターゲティング配列は、ジストロフィンプレmRNA内の標的領域と相補的である。一部の実施形態では、ターゲティング配列は、エクソン7、エクソン8、エクソン9、エクソン19、エクソン23、エクソン44、エクソン45、エクソン50、エクソン51、エクソン52、エクソン53またはエクソン55から選択される、ジストロフィンプレmRNAのエクソン内の標的領域内の10またはこれを超える連続ヌクレオチドと相補的である。複数の実施形態では、標的領域は、ジストロフィンプレmRNAのエクソン内に完全にありターゲティング配列のいかなる部分もスプライシング接合部にわたらないか、またはジストロフィンプレmRNAのイントロン/エクソンもしくはエクソン/イントロンのスプライス接合部(例えば配列番号4~15)にわたる領域である。
多様な実施形態では、ミオスタチンターゲティング配列は、配列番号16~75のうちの1つを含むか、配列番号16~75のうちの1つから選択されるか、配列番号16~75のうちの少なくとも1つから選択される配列の少なくとも12の連続ヌクレオチドの断片であるか、または、配列番号16~75のうちの少なくとも1つから選択される配列に対する少なくとも90%の配列同一性を有する変異体であり、各Xはウラシル(U)またはチミン(T)から独立に選択され、各Yはシトシン(C)または5-メチルシトシン(5mC)から独立に選択される。一部の実施形態では、配列番号16~75の各Xはチミン(T)であり、配列番号16~75の各Yはシトシン(C)である。
一部の実施形態では、ミオスタチンターゲティング配列は、
a)配列番号71(YYAGYYYAXYXXYXYYXGGXYYXGG)[Zは25である];
b)配列番号72(YAYXXAYYAGYYYAXYXXYXYYXGG)[Zは25である];
c)配列番号73(YYAYXXGYAXXAGAAAAXYAGY)[Zは22である];
d)配列番号74(GYATTAGAAAATYAGYTATAAATG)[Zは24である];および
e)配列番号75(YYATYYGYTTGYATTAGAAAGTYAGY)[Zは26である]
から選択され、各Xはウラシル(U)またはチミン(T)から独立に選択され、各Yはシトシン(C)または5-メチルシトシン(5mC)から独立に選択される。一部の実施形態では、配列番号71~75の各Xはチミン(T)であり、配列番号71~75の各Yはシトシン(C)である。
a)配列番号71(YYAGYYYAXYXXYXYYXGGXYYXGG)[Zは25である];
b)配列番号72(YAYXXAYYAGYYYAXYXXYXYYXGG)[Zは25である];
c)配列番号73(YYAYXXGYAXXAGAAAAXYAGY)[Zは22である];
d)配列番号74(GYATTAGAAAATYAGYTATAAATG)[Zは24である];および
e)配列番号75(YYATYYGYTTGYATTAGAAAGTYAGY)[Zは26である]
から選択され、各Xはウラシル(U)またはチミン(T)から独立に選択され、各Yはシトシン(C)または5-メチルシトシン(5mC)から独立に選択される。一部の実施形態では、配列番号71~75の各Xはチミン(T)であり、配列番号71~75の各Yはシトシン(C)である。
多様な実施形態では、ジストロフィンターゲティング配列は、配列番号76~3485のうちの1つを含むか、配列番号76~3485のうちの1つから選択されるか、配列番号76~3485のうちの少なくとも1つから選択される配列の少なくとも10の連続ヌクレオチドの断片であるか、または、配列番号76~3485のうちの少なくとも1つから選択される配列に対する少なくとも90%の配列同一性を有する変異体であり、各Xはウラシル(U)またはチミン(T)から独立に選択され、各Yはシトシン(C)または5-メチルシトシン(5mC)から独立に選択される。一部の実施形態では、配列番号76~3485の各Xはチミン(T)であり、配列番号76~3485の各Yはシトシン(C)である。一部の実施形態では、ターゲティング配列は、配列番号76を含み得る。
一部の実施形態では、式(I)、(IV)、(V)、(VI)、(VII)、および(VIII)の化合物を含む本開示のアンチセンスオリゴマーの各Nuは、アデニン、グアニン、チミン、ウラシル、シトシン、ヒポキサンチン(イノシン)、2,6-ジアミノプリン、5-メチルシトシン、C5-プロピニル修飾ピリミジン、および10-(9-(アミノエトキシ)フェノキサジニル)から独立に選択される。一部の実施形態では、式(I)、(IV)、(V)、(VI)、(VII)、および(VIII)の化合物を含む本開示のアンチセンスオリゴマーのターゲティング配列は、配列番号2、3、4もしくは6から選択される配列を含むか、配列番号2、3、4もしくは6から選択されるか、配列番号2、3、4もしくは6から選択される配列のうちの、少なくとも12連続ヌクレオチドの断片であるか、または、配列番号2、3、4もしくは6から選択される配列に対する、少なくとも90%の配列同一性を有する改変体であり、ここで、Xは、ウラシル(U)またはチミン(T)から選択され、Iは、イノシンである。
本開示に従い使用されうる、さらなる改変アンチセンスオリゴマー/化学は、参照によりそれらの全体において本明細書に組み込まれる、以下の特許および特許公報:PCT公開第WO2007/002390号;同第WO2010/120820号;および同第WO2010/148249号;米国特許第7,838,657号;ならびに米国特許出願第2011/0269820号において記載されているアンチセンスオリゴマー/化学を含む。
C.モルホリノサブユニットおよびホスホルアミデートヌクレオシド間リンカーの調製
モルホリノ単量体サブユニット、修飾ヌクレオシド間連結、およびこれらを含むオリゴマーは、例えば、参照によりそれらの全体において本明細書に組み込まれる、米国特許第5,185,444号および同第7,943,762号において記載されている通りに調製することができる。モルホリノサブユニットは、以下の一般的な反応スキームIに従い調製することができる。
モルホリノ単量体サブユニット、修飾ヌクレオシド間連結、およびこれらを含むオリゴマーは、例えば、参照によりそれらの全体において本明細書に組み込まれる、米国特許第5,185,444号および同第7,943,762号において記載されている通りに調製することができる。モルホリノサブユニットは、以下の一般的な反応スキームIに従い調製することができる。
反応スキーム1[式中、Bは、塩基対合部分を表し、PGは、保護基を表す]を参照すると、モルホリノサブユニットは、示される通り、対応するリボヌクレオシド(1)から調製することができる。モルホリノサブユニット(2)は、任意選択で、適切な保護基前駆体、例えば、トリチルクロリドを伴う反応により保護することができる。下記でより詳細に記載される通り、3’保護基は一般に、固体オリゴマー合成時に除去する。塩基対合部分は、固相オリゴマー合成に適するように保護することができる。適切な保護基は、アデニンおよびシトシンのためのベンゾイル、グアニンのためのフェニルアセチル、およびヒポキサンチン(I)のためのピバロイルオキシメチルを含む。ピバロイルオキシメチル基は、ヒポキサンチン複素環塩基のN1位へと導入することができる。非保護のヒポキサンチンサブユニットも使用しうるが、塩基を保護する場合の活性化反応の収率は、はるかに優れている。他の適切な保護基は、参照によりその全体において本明細書に組み込まれる、米国特許第8,076,476号において開示されている保護基を含む。
活性化リン化合物4を伴う化合物3の反応は、所望の連結部分である化合物5を有するモルホリノサブユニットをもたらす。構造4の化合物は、任意の数の、当業者に公知の方法を使用して調製することができる。例えば、このような化合物は、対応するアミンと、オキシ塩化リン(phosphorous oxychloride)との反応により調製することができる。この点で、アミン出発材料は、当技術分野で公知の任意の方法、例えば、実施例、ならびに参照によりその全体が本明細書に組み込まれる、米国特許第5,185,444号、同第7,943,762号、および同第8,779,128号において記載されている方法を使用して調製することができる。
構造5の化合物は、ヌクレオシド間連結を含むオリゴマーを調製するための固相自動式オリゴマー合成において使用することができる。このような方法は、当技術分野で周知である。略述すると、構造5の化合物は、固体支持体へのリンカーを含有するように、5’末端において修飾することができる。例えば、化合物5は、L11およびL15を含むリンカーにより、固体支持体へと連結することができる。支持がなされたら、保護基(例えば、トリチル)を除去し、遊離アミンを、第2の構造5の化合物の活性化リン部分と反応させる。このシークエンスを、所望の長さのオリゴが得られるまで繰り返す。5’末端における保護基は、除去することもでき、5’修飾が望ましい場合は、残すこともできる。オリゴは、任意の数の方法、例えば、DTTによる処理に続く、水酸化アンモニウムによる処理を使用して、固体支持体から除去することができる。
修飾モルホリノサブユニットおよびモルホリノベースのオリゴマーの調製については、実施例においてより詳細に記載する。本明細書で記載される方法、当技術分野で公知であり、かつ/または参照により本明細書で記載される方法を使用して、任意の数の修飾連結を含有するモルホリノベースのオリゴマーを調製することができる。実施例ではまた、既に記載されている(例えば、参照によりその全体において本明細書に組み込まれる、PCT公開第WO2008/036127号を参照されたい)通りに調製された、モルホリノベースのオリゴマーの全般的な修飾についても記載する。
「保護基」という用語は、化合物の一部または全部の反応性部分をブロックし、保護基を除去するまで、このような部分が、化学反応に参与することを防止する化学的部分、例えば、T.W. Greene、P.G.M. Wuts、「Protective Groups in Organic Synthesis」、3版、John Wiley & Sons(1999年)(その全体が本明細書において参考として援用される)において列挙および記載されている部分を指す。異なる保護基を使用する場合、各(異なる)保護基が、異なる手段により除去可能であることは、有利でありうる。完全に非対応の反応条件下で切断される保護基は、このような保護基の示差的な除去を可能とする。例えば、保護基は、酸、塩基、および加水分解により除去することができる。トリチル、ジメトキシトリチル、アセタール、およびtert-ブチルジメチルシリルなどの基は、酸不安定性であり、加水分解により除去可能なCbz基、および塩基不安定性のFmoc基で保護されるアミノ基の存在下で、カルボキシ反応性部分およびヒドロキシ反応性部分を保護するのに使用することができる。カルボン酸部分は、限定なしに述べると、メチルまたはエチルなどの塩基不安定性基でブロックすることができ、ヒドロキシ反応性部分は、tert-ブチルカルバメートなどの酸不安定性基、または酸安定性であり、かつ、塩基安定性であるが、加水分解により除去可能なカルバメートでブロックされるアミンの存在下では、アセチルなどの塩基不安定性基でブロックすることができる。
カルボン酸反応性部分およびヒドロキシル反応性部分はまた、ベンジル基など、加水分解により除去可能な保護基でブロックしうるのに対し、アミン基は、Fmocなどの塩基不安定性基でブロックすることができる。式(I)の化合物を合成するのに、特に有用なアミン保護基は、トリフルオロアセトアミドである。カルボン酸反応性部分が、2,4-ジメトキシベンジルなど、酸化により除去可能な保護基(protective group)でブロックしうるのに対し、共存するアミノ基は、フルオリド不安定性シリルカルバメートでブロックすることができる。
アリルブロッキング基は、酸保護基および塩基保護基の存在下において、前者が、安定であり、その後、金属またはパイ-酸触媒により除去されうるので、有用である。例えば、アリルでブロックされたカルボン酸は、酸不安定性t-ブチルカルバメートまたは塩基不安定性アセテートアミン保護基の存在下で、パラジウム(0)触媒反応により脱保護することができる。保護基のさらに別の形態は、化合物または中間体が結合しうる樹脂である。残基が樹脂に結合する限りにおいて、その官能基は、ブロックされており、反応することができない。樹脂から放出されると、官能基は、反応に利用可能である。
そうでないことが注記されない限りにおいて、全ての化学物質は、Sigma-Aldrich-Fluka(St.Louis、MO)から得た。ベンゾイルアデノシン、ベンゾイルシチジン、およびフェニルアセチルグアノシンは、Carbosynth Limited(Berkshire、UK)から得た。
本明細書で記載される、さらなる連結修飾を含有する、PMO、PMOプラス、PPMO、およびPMO-Xの合成は、当技術分野で公知であり、参照によりそれらの全体において本明細書に組み込まれる、米国特許出願第12/271,036号および同第12/271,040号ならびにPCT公開第WO2009/064471号において記載されている方法を使用して行った。
3’トリチル修飾を伴うPMOは、脱トリチル化(detritylation)ステップを省くことを除き、本質的に、PCT公開第WO2009/064471号において記載されている通りに合成する。
D.細胞透過性ペプチド
本開示の改変アンチセンスオリゴマー化合物は、本明細書ではまた、細胞透過性ペプチド(CPP)とも称するペプチドにコンジュゲートしていてもよい。ある特定の好ましい実施形態では、ペプチドは、化合物の、細胞への輸送を増強するのに有効な、アルギニンに富むペプチド輸送部分である。輸送部分は、オリゴマーの末端に、結合させることが好ましい。ペプチドは、全身投与されると、所与の細胞培養物集団の細胞のうちの30%、40%、50%、60%、70%、80%、90%、または100%であって、間の全ての整数を含む%の細胞内の細胞透過を誘導し、in vivoにおいて、複数の組織内の高分子のトランスロケーションを可能とする能力を有する。一実施形態では、細胞透過性ペプチドは、アルギニンに富むペプチド輸送体でありうる。別の実施形態では、細胞透過性ペプチドは、ペネトラチンまたはTatペプチドでありうる。当技術分野では、これらのペプチドが周知であり、例えば、参照によりその全体において本明細書に組み込まれる、米国公開第2010-0016215A1号において開示されている。ペプチドの、本開示の改変アンチセンスオリゴマーへのコンジュゲーションのための1つの手法は、参照によりその全体において本明細書に組み込まれる、PCT公開第WO2012/150960号において見出すことができる。本開示のペプチドコンジュゲートオリゴマーについての一部の実施形態は、CPPと、改変アンチセンスオリゴマーとの間のリンカーとして、グリシンを活用する。例えば、本開示のペプチドコンジュゲートPMOは、R6-G-PMOからなる。
本開示の改変アンチセンスオリゴマー化合物は、本明細書ではまた、細胞透過性ペプチド(CPP)とも称するペプチドにコンジュゲートしていてもよい。ある特定の好ましい実施形態では、ペプチドは、化合物の、細胞への輸送を増強するのに有効な、アルギニンに富むペプチド輸送部分である。輸送部分は、オリゴマーの末端に、結合させることが好ましい。ペプチドは、全身投与されると、所与の細胞培養物集団の細胞のうちの30%、40%、50%、60%、70%、80%、90%、または100%であって、間の全ての整数を含む%の細胞内の細胞透過を誘導し、in vivoにおいて、複数の組織内の高分子のトランスロケーションを可能とする能力を有する。一実施形態では、細胞透過性ペプチドは、アルギニンに富むペプチド輸送体でありうる。別の実施形態では、細胞透過性ペプチドは、ペネトラチンまたはTatペプチドでありうる。当技術分野では、これらのペプチドが周知であり、例えば、参照によりその全体において本明細書に組み込まれる、米国公開第2010-0016215A1号において開示されている。ペプチドの、本開示の改変アンチセンスオリゴマーへのコンジュゲーションのための1つの手法は、参照によりその全体において本明細書に組み込まれる、PCT公開第WO2012/150960号において見出すことができる。本開示のペプチドコンジュゲートオリゴマーについての一部の実施形態は、CPPと、改変アンチセンスオリゴマーとの間のリンカーとして、グリシンを活用する。例えば、本開示のペプチドコンジュゲートPMOは、R6-G-PMOからなる。
上記で記載した輸送部分は、結合オリゴマーの細胞移入を、結合輸送部分の非存在下におけるオリゴマーの取込みと比べて大幅に増強することが示されている。取込みは、非コンジュゲート化合物と比べて、少なくとも10倍増強することが好ましく、20倍増強することがより好ましい。
アルギニンに富むペプチド輸送体(すなわち、細胞透過性ペプチド)の使用は、本開示を実施するのに特に有用である。ある特定のペプチド輸送体は、アンチセンス化合物の、筋細胞を含む初代細胞への送達において、高度に有効であることが示されている(参照によりそれらの全体において本明細書に組み込まれる、Marshall, Odaら、2007年;Jearawiriyapaisarn, Moultonら、2008年;Wu, Moultonら、2008年)。さらに、ペネトラチンおよびTatペプチドなど、他の公知のペプチド輸送体と比較して、本明細書で記載されるペプチド輸送体は、アンチセンスPMOにコンジュゲートさせると、複数の遺伝子転写物のスプライシングを変更する能力の増強を裏付ける(参照によりその全体において本明細書に組み込まれる、Marshall, Odaら、2007年)。
多様な実施形態では、G(式I、IV、およびVで列挙された)は、以下:
-C(O)(CH2)5NH-CPP、-C(O)(CH2)2NH-CPP、-C(O)(CH2)2NHC(O)(CH2)5NH-CPP、および-C(O)CH2NH-CPPから選択される細胞透過性ペプチド(「CPP」)およびリンカー部分であるか、またはGは、式:
のものであり、式中、CPPは、CPPのカルボキシ末端において、アミド結合により、リンカー部分に結合している。一部の実施形態では、CPPは、配列番号3486~3501から選択される。
-C(O)(CH2)5NH-CPP、-C(O)(CH2)2NH-CPP、-C(O)(CH2)2NHC(O)(CH2)5NH-CPP、および-C(O)CH2NH-CPPから選択される細胞透過性ペプチド(「CPP」)およびリンカー部分であるか、またはGは、式:
のものであり、式中、CPPは、CPPのカルボキシ末端において、アミド結合により、リンカー部分に結合している。一部の実施形態では、CPPは、配列番号3486~3501から選択される。
一部の実施形態では、G(式I、IV、およびVにおいて列挙する通り)は、式:
であり、Raは、H、アセチル、ベンゾイル、およびステアロイルから選択され、Jは、4~9の整数である。ある特定の実施形態では、Jは、6である。
であり、Raは、H、アセチル、ベンゾイル、およびステアロイルから選択され、Jは、4~9の整数である。ある特定の実施形態では、Jは、6である。
一部の実施形態では、CPP(式I、IV、およびVにおいて列挙する通り)は、式:
であり、Raは、H、アセチル、ベンゾイル、およびステアロイルから選択され、Jは、4~9の整数である。ある特定の実施形態では、CPPは、配列番号15である。多様な実施形態では、Jは、6である。一部の実施形態では、Raは、Hおよびアセチルから選択される。例えば、一部の実施形態では、Raは、Hである。ある特定の実施形態では、Raは、アセチルである。
であり、Raは、H、アセチル、ベンゾイル、およびステアロイルから選択され、Jは、4~9の整数である。ある特定の実施形態では、CPPは、配列番号15である。多様な実施形態では、Jは、6である。一部の実施形態では、Raは、Hおよびアセチルから選択される。例えば、一部の実施形態では、Raは、Hである。ある特定の実施形態では、Raは、アセチルである。
IV.製剤
本開示の化合物はまた、取込み、分布、および/または吸収を支援するために、例えば、リポソーム、受容体にターゲティングされた分子、経口製剤、直腸製剤、局所製剤、または他の製剤として、他の分子、分子構造、または化合物の混合物と混合するか、これらと共に封入するか、これらにコンジュゲートさせるか、またはこれらと他の形で会合させることもできる。このような取込み支援製剤、分布支援製剤、および/または吸収支援製剤の調製について教示する、代表的な米国特許は、参照によりそれらの全体において本明細書に組み込まれる、米国特許第5,108,921号;同第5,354,844号;同第5,416,016号;同第5,459,127号;同第5,521,291号;同第5,543,158号;同第5,547,932号;同第5,583,020号;同第5,591,721号;同第4,426,330号;同第4,534,899号;同第5,013,556号;同第5,108,921号;同第5,213,804号;同第5,227,170号;同第5,264,221号;同第5,356,633号;同第5,395,619号;同第5,416,016号;同第5,417,978号;同第5,462,854号;同第5,469,854号;同第5,512,295号;同第5,527,528号;同第5,534,259号;同第5,543,152号;同第5,556,948号;同第5,580,575号および同第5,595,756号を含むがこれらに限定されない。
本開示の化合物はまた、取込み、分布、および/または吸収を支援するために、例えば、リポソーム、受容体にターゲティングされた分子、経口製剤、直腸製剤、局所製剤、または他の製剤として、他の分子、分子構造、または化合物の混合物と混合するか、これらと共に封入するか、これらにコンジュゲートさせるか、またはこれらと他の形で会合させることもできる。このような取込み支援製剤、分布支援製剤、および/または吸収支援製剤の調製について教示する、代表的な米国特許は、参照によりそれらの全体において本明細書に組み込まれる、米国特許第5,108,921号;同第5,354,844号;同第5,416,016号;同第5,459,127号;同第5,521,291号;同第5,543,158号;同第5,547,932号;同第5,583,020号;同第5,591,721号;同第4,426,330号;同第4,534,899号;同第5,013,556号;同第5,108,921号;同第5,213,804号;同第5,227,170号;同第5,264,221号;同第5,356,633号;同第5,395,619号;同第5,416,016号;同第5,417,978号;同第5,462,854号;同第5,469,854号;同第5,512,295号;同第5,527,528号;同第5,534,259号;同第5,543,152号;同第5,556,948号;同第5,580,575号および同第5,595,756号を含むがこれらに限定されない。
本開示のアンチセンス化合物は、任意の薬学的に許容される塩、エステル、もしくはこのようなエステルの塩、またはヒトを含む動物へと投与されると、生物学的に活性の代謝物もしくはその残余物をもたらす(直接的または間接的に)ことが可能な、他の任意の化合物を包含する。したがって、例えば、本開示はまた、本開示の化合物のプロドラッグおよび薬学的に許容される塩、このようなプロドラッグの薬学的に許容される塩、および他の生物学的同等物へも導かれる。
「プロドラッグ」という用語は、内因性酵素または他の化学物質および/もしくは条件の作用により、体内またはその細胞内で活性形態(すなわち、薬物)へと転換される、不活性形態で調製された治療剤を指し示す。特に、本開示のオリゴマーのプロドラッグバージョンは、参照によりそれらの全体において本明細書に組み込まれる、1993年12月9日に公開された、GosselinらによるPCT公開第WO1993/24510号またはImbachらによる、PCT公開第WO1994/26764号および米国特許第5,770,713号において開示されている方法に従い、SATE[(S-アセチル-2-チオエチル)ホスフェート]誘導体として調製される。
「薬学的に許容される塩」という用語は、本開示の化合物の、生理学的かつ薬学的に許容される塩:すなわち、親化合物の望ましい生物学的活性を保持し、望ましくない毒性効果をこれに付与しない塩を指す。オリゴマーについては、薬学的に許容される塩およびそれらの使用の例については、その全体において本明細書に参考として援用される、米国特許第6,287,860号においてさらに記載されている。
本開示はまた、本開示のアンチセンス化合物を含む医薬組成物および製剤も含む。本開示の医薬組成物は、局所処置が望ましいのか、全身処置が望ましいのか、および処置される領域に応じて、多数の方式で投与することができる。投与は、局所投与(眼投与および膣送達および直腸送達を含む粘膜への投与を含む)、肺投与、例えば、噴霧器による投与を含む、散剤またはエアゾールによる吸入または送気による投与;気管内投与、鼻腔内投与、表皮投与および経皮投与、経口投与、または非経口投与でありうる。非経口投与は、静脈内注射もしくは静脈内注入、動脈内注射もしくは動脈内注入、皮下注射もしくは皮下注入、腹腔内注射もしくは腹腔内注入、または筋内注射もしくは筋内注入;あるいは頭蓋内投与、例えば、髄腔内投与または脳室内投与を含む。少なくとも1つの2’-O-メトキシエチル修飾を伴うオリゴマーは、経口投与に特に有用であると考えられる。局所投与のための医薬組成物および製剤は、経皮パッチ、軟膏、ローション、クリーム、ゲル、ドロップ、坐剤、スプレー、液剤(liquid)、および散剤を含みうる。従来の医薬担体、水性、粉末、または油性の基剤、増粘剤などが、必要であるかまたは望ましい場合がある。コーティングされたコンドーム、手袋などもまた、有用でありうる。
単位剤形で提示されると好都合でありうる本開示の医薬製剤は、製薬業界で周知の従来の技法に従い調製することができる。このような技法は、有効成分を、医薬担体または賦形剤と会合させるステップを含む。一般に、製剤は、有効成分を、液体担体もしくは微細に分割された固体担体、またはこれらの両方と、均一かつ十分に会合させ、次いで、必要な場合、生成物を成形することにより調製する。
本開示の組成物は、錠剤、カプセル、ゲルカプセル、液体シロップ、軟質ゲル、坐剤、および浣腸剤(enema)などであるがこれらに限定されない、多くの可能な剤形のうちのいずれかへと製剤化することができる。本開示の組成物はまた、水性媒体中、非水性媒体中、または混合媒体中の懸濁物としても製剤化することができる。水性懸濁物は、懸濁物の粘性を増加させる物質であって、例えば、カルボキシメチルセルロースナトリウム、ソルビトール、および/またはデキストランを含む物質をさらに含有しうる。懸濁物はまた、安定化剤も含有しうる。
本開示の医薬組成物は、溶液、エマルジョン、泡沫、およびリポソームを含有する製剤を含むがこれらに限定されない。本開示の医薬組成物および製剤は、1または複数の浸透増強剤、担体、賦形剤、または他の活性成分もしくは不活性成分を含みうる。
エマルジョンは、通常0.1μmの直径を超える液滴の形態で、別の液体中に分散させた1つの液体による不均質系であることが典型的である。エマルジョンは、分散相に加えたさらなる成分と、水相中、油相中の溶液、または分離相としてのそれ自体として存在しうる活性薬物とを含有しうる。マイクロエマルジョンは、本開示の実施形態として含まれる。当技術分野では、エマルジョンおよびそれらの使用が周知であり、その全体において本明細書に参考として援用される、米国特許第6,287,860号においてさらに記載されている。
本開示の製剤は、リポソーム製剤を含む。本開示で使用される「リポソーム」という用語は、1または複数の球状の二重層内に配置された、両親媒性脂質から構成される小胞を意味する。リポソームとは、親油性材料から形成された膜と、送達される組成物を含有する水性の内部とを有する、単層または多重層の小胞である。カチオン性リポソームは、正に荷電したリポソームであり、負に荷電したDNA分子と相互作用して、安定的な複合体を形成すると考えられる。pH感受性であるか、または負に荷電したリポソームは、DNAと複合体化するのではなく、DNAを捕獲すると考えられる。カチオン性リポソームおよび非カチオン性リポソームのいずれも、DNAを、細胞へと送達するのに使用されている。
リポソームはまた、本明細書で使用される用語であって、1または複数の特殊化された脂質を含むリポソームを指す、「立体安定化」リポソームも含み、この脂質は、リポソームへと組み込まれると、このような特殊化された脂質を欠くリポソームと比べて、循環寿命の増強を結果としてもたらす。立体安定化リポソームの例は、リポソームの小胞形成脂質部分の一部が、1もしくは複数の糖脂質を含むか、またはリポソームの小胞形成脂質部分の一部を、ポリエチレングリコール(PEG)部分など、1もしくは複数の親水性ポリマーで誘導体化した立体安定化リポソームである。リポソームおよびそれらの使用については、その全体において本明細書に参考として援用される、米国特許第6,287,860号においてさらに記載されている。
本開示の医薬製剤および医薬組成物はまた、界面活性剤も含みうる。当技術分野では、薬物製品中、製剤中、およびエマルジョン中の界面活性剤の使用が周知である。界面活性剤およびそれらの使用については、その全体において本明細書に参考として援用される、米国特許第6,287,860号においてさらに記載されている。
一部の実施形態では、本開示は、多様な浸透増強剤を使用して、核酸、特に、オリゴマーの効率的な送達を行う。細胞膜を横切る非親油性薬物の拡散の支援に加えて、浸透増強剤はまた、親油性薬物の透過性も増強する。浸透増強剤は、5つの大きな類別、すなわち、界面活性剤、脂肪酸、胆汁酸塩、キレート化剤、および非キレート化非界面活性剤のうちの1つに属するものとして分類することができる。浸透増強剤およびそれらの使用については、その全体において本明細書に参考として援用される、米国特許第6,287,860号においてさらに記載されている。
当業者は、製剤が、それらの意図される使用、すなわち、投与経路に従い、慣例的にデザインされることを認識するであろう。
局所投与のための製剤は、本開示のオリゴマーを、脂質、リポソーム、脂肪酸、脂肪酸エステル、ステロイド、キレート化剤、および界面活性剤など、局所送達剤と混合した製剤を含む。脂質およびリポソームは、中性(例えば、ジオレオイルホスファチジルエタノールアミンDOPE、ジミリストイルホスファチジルコリンDMPC、ジステアロイルホスファチジルコリン)、陰性(例えば、ジミリストイルホスファチジルグリセロールDMPG)、およびカチオン性(例えば、ジオレオイルテトラメチルアミノプロピルDOTAPおよびジオレオイルホスファチジルエタノールアミンDOTMA)を含む。
局所投与または他の投与のために、本開示のオリゴマーを含む治療剤を、リポソーム内に封入することもでき、リポソーム、特に、カチオン性リポソームとの複合体を形成することもできる。代替的に、治療剤は、脂質、特に、カチオン性脂質と複合体化させることもできる。脂肪酸およびエステル、薬学的に許容されるそれらの塩、ならびにそれらの使用については、その全体において本明細書に参考として援用される、米国特許第6,287,860号においてさらに記載されている。局所製剤については、それらの全体において本明細書に参考として援用される、1999年5月20日に出願された、米国特許出願第09/315,298号およびMourichら,2009, J. Invest.
Dermatol., 129(8):1945-53において詳細に記載されている。
Dermatol., 129(8):1945-53において詳細に記載されている。
経口投与のための組成物および製剤は、粉末または顆粒、マイクロ粒子、ナノ粒子、水中または非水性媒体中の懸濁物または溶液、カプセル、ゲルカプセル、小袋(sachet)、錠剤またはミニ錠剤(minitablet)を含む。増粘剤、矯味矯臭剤、希釈剤、乳化剤、分散助剤、または結合剤が望ましい場合がある。経口製剤は、本開示のオリゴマーを、1または複数の浸透増強剤、界面活性剤、およびキレート剤と共に投与する経口製剤である。界面活性剤は、脂肪酸および/またはそのエステルもしくは塩、胆汁酸および/またはその塩を含む。胆汁酸/塩および脂肪酸ならびにそれらの使用については、その全体において本明細書に参考として援用される、米国特許第6,287,860号においてさらに記載されている。一部の実施形態では、本開示は、浸透増強剤の組合せ、例えば、胆汁酸/塩と組み合わせた脂肪酸/塩を提示する。例示的な組合せは、ラウリン酸、カプリン酸、およびUDCAのナトリウム塩である。さらなる浸透増強剤は、ポリオキシエチレン-9-ラウリルエーテル、ポリオキシエチレン-20-セチルエーテルを含む。本開示のオリゴマーは、経口送達することもでき、噴霧乾燥粒子を含む顆粒形態で送達することもでき、マイクロ粒子またはナノ粒子を形成するように複合体化させることもできる。オリゴマー複合体化剤およびそれらの使用については、その全体において本明細書に参考として援用される、米国特許第6,287,860号においてさらに記載されている。オリゴマーのための経口製剤およびそれらの調製については、それらの全体において本明細書に参考として援用される、米国出願第09/108,673号(1998年7月1日に出願された)、同第09/315,298号(1999年5月20日に出願された)、および同第10/071,822号(2002年2月8日に出願された)において詳細に記載されている。
非経口投与、髄腔内投与、または脳室内投与のための組成物および製剤は、浸透増強剤、担体化合物、および他の薬学的に許容される担体または賦形剤などであるがこれらに限定されない、緩衝液、希釈剤および他の適切な添加剤もまた含有しうる、滅菌水溶液を含みうる。
別の関連する実施形態では、本開示の組成物は、第1の核酸へとターゲティングされた、1または複数のアンチセンス化合物、特にオリゴマーと、第2の核酸標的へとターゲティングされた、1または複数のさらなるアンチセンス化合物とを含有しうる。代替的に、本開示の組成物は、同じ核酸標的の異なる領域へとターゲティングされた、2つまたはこれを超えるアンチセンス化合物を含有しうる。当技術分野では、アンチセンス化合物の多数の例が公知である。2つまたはこれを超える組合せ化合物を、併せて使用することもでき、逐次的に使用することもできる。
V.使用方法
ある特定の態様は、ミオスタチン治療剤を受けている被験体に、ジストロフィン治療剤も投与するステップを含む、デュシェンヌ型筋ジストロフィーまたは関連障害を有する被験体を処置する方法に関する。
ある特定の態様は、ミオスタチン治療剤を受けている被験体に、ジストロフィン治療剤も投与するステップを含む、デュシェンヌ型筋ジストロフィーまたは関連障害を有する被験体を処置する方法に関する。
複数の態様では、治療剤は、DMDまたは関連障害を有する被験体に投与される。複数の実施形態では、1または複数の治療剤は、本明細書で記載される通りの修飾アンチセンスオリゴマーによる処置の前に被験体に投与され得る。複数の実施形態では、1または複数の治療剤は、修飾アンチセンスオリゴマーの投与前、それと同時、または投与後に被験体に投与され得る。複数の実施形態では、治療剤はタンパク質または核酸である。一部の実施形態では、タンパク質は抗体または可溶性受容体である。複数の実施形態では、可溶性受容体はACVR2である。複数の実施形態では、核酸はアンチセンスオリゴマーまたはsiRNAである。一部の実施形態では、アンチセンスオリゴマーは、本明細書で記載される通りの修飾アンチセンスオリゴマーである。
複数の実施形態では、治療剤は、被験体におけるミオスタチン活性またはミオスタチン発現のうちの一方または両方を抑制できるミオスタチン治療剤である。ミオスタチン治療剤は、ミオスタチンプレmRNAを標的とし、ミオスタチンプレmRNAの成熟mRNAへの転写に干渉する治療剤であり得る。複数の実施形態では、ミオスタチン治療剤は、ヒトミオスタチンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できる。複数の実施形態では、ミオスタチン治療剤は、ミオスタチンプレmRNAにおけるエクソン2のスキッピングを誘導し、エクソン2を含むミオスタチンプレmRNAの発現を阻害する。ミオスタチン治療剤は、ミオスタチンタンパク質を標的とし、ミオスタチン受容体とのミオスタチンタンパク質の結合に干渉する治療剤であり得る。
ミオスタチン治療剤は、タンパク質および核酸から選択される。タンパク質は、抗ミオスタチン抗体、例えば、抗GDF8(Abcam、ケンブリッジ MA)、または可溶性受容体であり得る。複数の実施形態では、可溶性受容体はACVR2である。核酸は、アンチセンスオリゴマーおよびsiRNAから選択される。アンチセンスオリゴマーは、本明細書で記載される通りの修飾ミオスタチンアンチセンスオリゴマーであり得る。
複数の実施形態では、治療剤は、被験体においてジストロフィンを増加させることができるジストロフィン治療剤である。ジストロフィン治療剤は、機能的または半機能的なジストロフィンまたは切断型ジストロフィンの発現を増加させ得る。切断型ジストロフィンは、マイクロジストロフィンおよびミニジストロフィン(参照によりその全体において本明細書に組み込まれる欧州特許第2125006号に開示)を含むが、これらに限定されない。ジストロフィン治療剤は、ジストロフィンプレmRNAを標的とし、ジストロフィンプレmRNAの成熟mRNAへの転写をモジュレートする治療剤であり得る。複数の実施形態では、ジストロフィン治療剤は、ヒトジストロフィンプレmRNAのプロセシングの間、エクソンスキッピングを誘導できる。複数の実施形態では、標的とされるジストロフィンプレmRNAは、1または複数の遺伝子変異を有する。ジストロフィン治療剤は、エクソンスキッピングを誘導し、それにより、1または複数の遺伝子変異を含む1または複数のエクソンは、成熟mRNAへのプロセシングの間、ジストロフィンプレmRNAから除去される。得られる切断型mRNAは、機能的または半機能的なジストロフィンタンパク質への翻訳が可能である。
一部の態様では、修飾ジストロフィンアンチセンスオリゴマーは、ジストロフィン遺伝子のプレmRNA内で領域と特異的にハイブリダイズするのに十分な長さおよび相補性のヌクレオチド配列を含み、修飾アンチセンスオリゴマーが当該領域に結合することにより、ジストロフィンプレmRNAのプロセシングの間、エクソンスキッピングが誘導される。複数の実施形態では、ジストロフィンプレmRNAのプロセシングの間のエクソンスキッピングにより、遺伝子変異を有する1または複数のエクソンがプレmRNAから除去される。複数の実施形態では、遺伝子変異を有する1または複数のエクソンのジストロフィンプレmRNAからの除去により、細胞および/または被験体の組織における非変異ジストロフィンプレmRNAのレベルが上昇する。被験体における非変異ジストロフィンプレmRNAのレベルの上昇は、機能的または半機能的なジストロフィンタンパク質の発現の増加にさらにつながり得る。このように、本開示は、本明細書で記載される通りの修飾ジストロフィンアンチセンスオリゴマーを使用して、非変異ジストロフィンmRNAのレベルを上昇させることにより、機能的または半機能的なジストロフィンタンパク質を増加させる方法に関する。
一部の態様では、修飾ミオスタチンアンチセンスオリゴマーは、ミオスタチン遺伝子のプレmRNA内の領域と特異的にハイブリダイズするのに十分な長さおよび相補性のヌクレオチド配列を含み、修飾アンチセンスオリゴマーが当該領域に結合することにより、ミオスタチンプレmRNAのプロセシングの間、エクソンスキッピングが誘導される。複数の実施形態では、修飾ミオスタチンオリゴマーが当該領域に結合することにより、細胞および/または被験体の組織におけるエクソン2含有ミオスタチンmRNAのレベルが低下する。被験体におけるエクソン2含有ミオスタチンmRNAのレベルの低下は、機能的なミオスタチンタンパク質の発現の減少にさらにつながり得る。
方法は、治療剤と組み合わせて、有効量の本開示の修飾アンチセンスオリゴマーを被験体に投与することを含む、デュシェンヌ型筋ジストロフィー(DMD)もしくは関連障害に罹患している、またはそれを発症する危険性がある個体を処置するステップを含む。修飾アンチセンスオリゴマーは、同じ組成物中にあってもなくてもよく、また、被験体に共投与されてもされなくてもよい。多様な実施形態では、修飾アンチセンスオリゴマーは、治療剤と同時に、またはほぼ同時に投与される。さらなる実施形態では、修飾アンチセンスオリゴマーは、治療剤とは実質的に異なる時間に投与される。本明細書で記載される通りの修飾アンチセンスオリゴマーにより標的とされる例示的な配列を、表1および2に示す。
また、DMDもしくは関連障害を処置するための、または、DMDもしくは関連障害の処置のための医薬の調製に使用するための、治療剤および修飾アンチセンスオリゴマーが含まれ、処置または医薬には治療剤が含まれる。複数の実施形態では、医薬は、本明細書で記載される通りの修飾アンチセンスオリゴマーを含み、例えば、修飾アンチセンスオリゴマーは、(i)修飾ヌクレオシド間連結、(ii)修飾糖部分、または(iii)前出の組合せを有するヌクレオチド類似体である少なくとも1つのサブユニットと、ジストロフィンまたはミオスタチンプレmRNA内の標的領域内の10またはこれを超える連続ヌクレオチドと相補的なターゲティング配列とを任意選択で有する10~50サブユニットを含む。
多様な実施形態では、ターゲティング配列は、ミオスタチンプレmRNA内の標的領域と相補的である。一部の実施形態では、ターゲティング配列は、エクソン2内に完全にありターゲティング配列のいかなる部分もスプライス接合部にわたらない標的領域内の12もしくはこれを超える連続ヌクレオチド、または、ミオスタチンプレmRNAのイントロン/エクソンもしくはエクソン/イントロンのスプライス接合部(例えば配列番号1~3)にわたる領域と相補的である。一部の実施形態では、修飾アンチセンスオリゴマーのターゲティング配列は、(a)配列番号16~75から選択される配列を含むか、(b)配列番号16~75から選択されるか、(c)配列番号16~75から選択される配列の少なくとも12の連続ヌクレオチドの断片であるか、または、(d)配列番号16~75から選択される配列に対する少なくとも90%の配列同一性を有する変異体であり、Xはウラシル(U)またはチミン(T)から選択され、Cはシトシン(C)または5-メチルシトシン(5mC)から選択される。
多様な実施形態では、ターゲティング配列は、ジストロフィンプレmRNA内の標的領域と相補的である。一部の実施形態では、ターゲティング配列は、エクソン7、エクソン8、エクソン9、エクソン19、エクソン23、エクソン44、エクソン45、エクソン50、エクソン51、エクソン52、エクソン53またはエクソン55から選択される、ジストロフィンプレmRNAのエクソン内で、標的領域内の10またはこれを超える連続ヌクレオチドと相補的である。複数の実施形態では、標的領域は、ジストロフィンプレmRNAのエクソン内に完全にありターゲティング配列のいかなる部分もスプライス接合部にわたらないか、またはジストロフィンプレmRNAのイントロン/エクソンもしくはエクソン/イントロンのスプライス接合部(例えば配列番号4~15)にわたる領域である。一部の実施形態では、修飾アンチセンスオリゴマーのターゲティング配列は、(a)配列番号76~3485から選択される配列を含むか、(b)配列番号76~3485から選択されるか、(c)配列番号76~3485から選択される配列の少なくとも10の連続ヌクレオチドの断片であるか、または、(d)配列番号76~3485から選択される配列に対する少なくとも90%の配列同一性を有する変異体であり、Xはウラシル(U)またはチミン(T)から選択され、Cはシトシン(C)または5-メチルシトシン(5mC)から選択される。
一部の実施形態では、DMDもしくは関連障害を処置する方法、またはDMDもしくは関連障害を処置するための医薬は、修飾糖部分を含むヌクレオチド類似体サブユニットを有する修飾アンチセンスオリゴマーを含む。修飾糖部分は、ペプチド核酸(PNA)サブユニット、ロックト核酸(LNA)サブユニット、2’O,4’C-エチレン架橋核酸(ENA)サブユニット、トリシクロDNA(tc-DNA)サブユニット、2’O-メチルサブユニット、2’O-メトキシエチルサブユニット、2’-フルオロサブユニット、2’-O-[2-(N-メチルカルバモイル)エチル]サブユニット、およびモルホリノサブユニットから選択されうる。
これらのさらなる態様および実施形態は、修飾ヌクレオシド間連結を含む、ヌクレオチド類似体サブユニットを有する、修飾アンチセンスオリゴマーを含む。多様な実施形態では、修飾ヌクレオシド間連結は、ホスホロチオエートヌクレオシド間連結、ホスホルアミデートヌクレオシド間連結、ホスホロジアミデートヌクレオシド間連結から選択される。さらなる実施形態では、ホスホロジアミデートヌクレオシド間連結は、(1,4-ピペラジン)-1-イル部分、置換(1,4-ピペラジン)-1-イル部分、4-アミノピペリジン-1-イル部分、または置換4-アミノピペリジン-1-イル部分に共有結合したリン原子を含む。
これらのさらなる態様および実施形態は、修飾糖部分と修飾ヌクレオシド間連結との少なくとも1つの組合せを含む、ヌクレオチド類似体サブユニットを有する、修飾アンチセンスオリゴマーを含む。
一部の実施形態では、修飾アンチセンスオリゴマーは、哺乳動物細胞により能動的に取り込まれる。さらなる実施形態では、かかる取り込みを促進するために、本明細書で記載される通り修飾アンチセンスオリゴマーを輸送部分(例えば輸送ペプチドまたはCPP)とコンジュゲートさせてもよい。多様な態様は、本明細書で記載される通りの修飾アンチセンスオリゴマーを使用して、細胞、組織および/または被験体における、エクソン2含有ミオスタチンmRNA転写物および/または機能的なミオスタチンタンパク質の発現を減少させる方法に関する。一部の場合では、エクソン2含有ミオスタチンmRNA転写物および/または機能的なミオスタチンタンパク質は、対照、例えば対照細胞/被験体(例えばデュシェンヌ型筋ジストロフィーまたは関連障害を有さない被験体)、修飾アンチセンスオリゴマーを含まない対照組成物、処置の欠如および/または当初の時点と比較して、約または少なくとも約5%、6%、7%、8%、9%、10%、11%、12%、13%、14%、15%、16%、17%、18%、19%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%または100%減少するか、または低下する。また、健常対照、例えば、デュシェンヌ型筋ジストロフィーまたは関連障害を有さない被験体のレベルと比較して、エクソン2含有mRNA転写物または機能的なミオスタチンタンパク質の発現を減少させる方法が含まれる。本明細書で使用するとき、「有効量」または「治療的な量」とは、被験体に投与されたとき、ミオスタチンプレmRNA転写物の標的領域と結合し、対照細胞/被験体と比較して、増加に関して開示したパーセンテージの範囲で、エクソン2含有ミオスタチンmRNA転写物および機能的なミオスタチンタンパク質の発現を減少させることができる、修飾アンチセンスオリゴマーの用量を指す。
多様な態様は、本明細書で記載される通りの修飾アンチセンスオリゴマーを使用して、ジストロフィンプレmRNAのイントロンおよびエクソンのスプライシングをモジュレートし、細胞、組織および/または被験体におけるジストロフィンまたは切断型ジストロフィンプレmRNAの発現を増加させる方法に関する。さらなる態様では、例えば全長野生型ジストロフィンプレmRNAと比較して、切断型ジストロフィンプレmRNAの発現が強化される。一部の場合において、ジストロフィンmRNA転写物および/または機能的もしくは半機能的なジストロフィンタンパク質は、対照、例えば、対照細胞/被験体(例えば、デュシェンヌ型筋ジストロフィーまたは関連障害を有さない被験体)、修飾アンチセンスオリゴマーを含まない対照組成物、処置の欠如および/または当初の時点と比較して、約または少なくとも約5%、6%、7%、8%、9%、10%、11%、12%、13%、14%、15%、16%、17%、18%、19%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%または100%増加するか、または強化される。方法はまた、健常対照、例えばデュシェンヌ型筋ジストロフィーまたは関連障害を有さない被験体のレベルと比較して、ジストロフィンmRNA転写物または機能的もしくは半機能的なジストロフィンタンパク質の発現を増加させるステップを含む。本明細書で使用するとき、「有効量」または「治療的な量」は、被験体に投与されたとき、ジストロフィンプレmRNA転写物の標的領域と結合し、対照細胞/被験体と比較て、増加に関して開示したパーセンテージの範囲で、ジストロフィンまたは切断型ジストロフィンmRNA転写物、および機能的なジストロフィンタンパク質の発現を増加させることができる、修飾アンチセンスオリゴマーの用量を指す。
方法はまた、本明細書で記載される通り、細胞、組織および/または被験体における機能的/活性型ミオスタチンタンパク質の発現を減少させるステップを含む。ある特定の場合において、機能的/活性型ミオスタチンタンパク質のレベルは、対照、例えば、対照細胞/被験体(例えばデュシェンヌ型筋ジストロフィーまたは関連障害を有する被験体)、治療剤を含まない対照組成物、処置の欠如および/または当初の時点と比較して、約または少なくとも約5%、6%、7%、8%、9%、10%、11%、12%、13%、14%、15%、16%、17%、18%、19%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%または100%減少する。方法はまた、影響を受けた対照、例えばデュシェンヌ型筋ジストロフィーまたは関連障害を有する被験体のレベルと比較して、機能的/活性型ミオスタチンタンパク質の発現を減少させるステップを含む。
方法はまた、本明細書で記載される通り、細胞、組織および/または被験体における機能的または半機能的/活性型ジストロフィンタンパク質の発現を増加させるステップを含む。ある特定の場合において、機能的または半機能的/活性型ジストロフィンタンパク質のレベルは、対照、例えば、対照細胞/被験体(例えばデュシェンヌ型筋ジストロフィーまたは関連障害を有さない被験体)、治療剤を含まない対照組成物、処置の欠如および/または当初の時点と比較して、約または少なくとも約5%、6%、7%、8%、9%、10%、11%、12%、13%、14%、15%、16%、17%、18%、19%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%または100%増加する。方法はまた、影響を受けた対照、例えば、デュシェンヌ型筋ジストロフィーまたは関連障害を有する被験体のレベルと比較して、機能的または半機能的/活性型ジストロフィンタンパク質の発現を増加させるステップを含む。
方法はまた、本明細書で記載される通りのアンチセンスオリゴマーと組み合わせて治療剤を使用して、被験体におけるデュシェンヌ型筋ジストロフィーおよび関連障害の進行を阻害するステップを含む。
一部の実施形態では、治療剤および修飾アンチセンスオリゴマーを、1または複数の適切な医薬担体中で、DMDまたは関連障害の1または複数の症状を呈示する被験体に投与する。本明細書で使用するとき、「処置」という用語は、DMDもしくは関連障害、またはDMDもしくは関連障害に関連する少なくとも1つの識別可能な症状の改善を指す。一部の実施形態では、「処置」は、被験体によって必ずしも識別可能ではない少なくとも1つの測定可能な物理的および/または生物学的パラメータの改善を指す。被験体は、例えば筋力および協調の物理的な改善を経験する場合がある。それらのパラメータは、例えば自己評価試験、医師の検査、物理的および生理学的測定のための実験室検査、ならびに被験体からの試料の生物学的試験により評価され得る。別の実施形態では、「処置」とは、DMDまたは関連障害の進行を遅延させるか、または進行を逆転させることを指す。本明細書で使用するとき、「予防する」または「阻害する」は、DMDまたは関連障害の発症を遅延させるか、またはそれが発症する危険性を低下させることを指す。
方法は、それを必要とする被験体において、DMDおよび関連障害の1または複数の症状を適宜、軽減または改善するステップを含む。具体的な例は、頻繁な転倒、臥位または座位からの立ち上がりの困難さ、走行および跳躍の困難さ、アヒル歩行、つま先歩行、ヒラメ筋肉肥大、筋肉の痛みおよび凝りおよび学習障害などの、段階的筋衰弱の症状を含む。
方法はまた、被験体における骨格筋量を増加させるステップを含む。方法はまた、健常な被験体または疾患、障害もしくは症状に罹患する被験体において、被験体の筋肉量の減少を処置または予防するステップを含む。方法はまた、疾患、障害または状態に罹患する被験体の骨格筋量不足を処置するステップを含む。多様な実施形態では、ミオスタチンおよびジストロフィンタンパク質の一方または両方の血液中または組織レベルは、治療剤および本明細書で記載されるアンチセンスオリゴマーの一方または両方の投与前に患者において測定する。有効量の、治療剤および本明細書のアンチセンスオリゴマーの一方または両方が被験体に投与される。ミオスタチンおよびジストロフィンタンパク質の一方または両方の血液中または組織中レベルは、選択した時間およびアンチセンスオリゴマーの投与の後、被験体において測定する。任意選択で、治療剤およびアンチセンスオリゴマーの一方または両方の投与量および/または投薬スケジュールは、測定により調整し、例えば、一方または両方の治療的な量が被験体において存在することを確実にするために投与量を増加させる。選択した時間は、本明細書で記載される治療剤およびアンチセンスオリゴマーのうちの一方または両方の投与後の、血流中への吸収ならびに/または肝臓および他の代謝プロセスによる代謝に要する時間を見越した時間の量を含み得る。一部の実施形態では、選択した時間は、投与後約1、2、3、4、5、6、7、8、9、10、11、12、15、18、20、22または24時間であり得る。一部の実施形態では、選択した時間は、投与後約12、18または24時間であり得る。他の実施形態では、選択した時間は、投与後約1、2、3、4、5、6または7日であり得る。
このような処置と共に、ゲノム薬理学(すなわち、個体の遺伝子型と、外来化合物または薬物へのその個体の応答との関係についての研究)について考慮することもできる。治療剤の代謝の差違は、薬理学的な活性薬物の用量と血中濃度との関係を変更することにより、重度の毒性または治療の失敗をもたらしうる。こうして、医師または臨床医は、治療剤を投与すべきなのかどうかの決定においてのほか、治療剤による処置の投与量および/または治療レジメンの調整においても関与性のゲノム薬理学研究において得られる知見の適用について考慮することができる。
修飾アンチセンスオリゴマーを含む治療剤の、標的核酸への有効な投与および送達は、さらなる側面である。治療剤の送達経路は、経口経路および非経口経路を含む、多様な全身経路、例えば、静脈内送達、皮下送達、腹腔内送達、および筋内送達のほか、吸入送達、経皮送達、および局所送達を含むがこれらに限定されない。適切な経路は、当業者が、処置下にある被験体の状態に適切な経路として決定することができる。血管循環または血管外循環の、血液またはリンパ系、および脳脊髄液は、RNAを導入しうる、一部の非限定的な部位である。
特定の実施形態では、治療剤を、被験体に、静脈内(IV)または皮下(SC)投与する、すなわち、アンチセンスオリゴマーを、静脈へと静脈内投与もしくは静脈内送達するか、または皮膚と筋肉との間の脂肪層へと皮下投与もしくは皮下送達する。静脈内注射部位の非限定的な例は、腕、手、脚、または足の静脈を含む。皮下注射部位の非限定的な例は、腹部、大腿部、下方背部(lower back)、または上腕部を含む。例示的な実施形態では、修飾アンチセンスオリゴマーのPMO形態、PMO-X形態、またはPPMO形態を、IV投与またはSC投与する。他の実施形態では、修飾アンチセンスオリゴマーを、被験体に、筋内内(IM)投与する、例えば、アンチセンスオリゴマーを、腕部の三角筋、脚部の外側広筋、腰部の腹側臀筋(ventrogluteal muscle)、臀部の背側臀筋(dorsogluteal muscle)、胸郭の横隔膜筋および内肋間筋へと投与または送達する。
ある特定の実施形態では、本開示の治療剤は、経皮的な方法により(例えば、このような修飾アンチセンスオリゴマーを、任意選択で、リポソームへとパッケージングする、修飾アンチセンスオリゴマーの、例えば、エマルジョンへの組込みを介して)送達することができる。送達のこのような経皮的な方法およびエマルジョン/リポソーム媒介型の方法は、修飾アンチセンスオリゴマーの送達について、当技術分野、例えば、それらの全体において本明細書に参考として援用される、米国特許第6,965,025号において記載されている。
本明細書で記載される治療剤はまた、植込み可能なデバイスを介して送達することもできる。このようなデバイスのデザインは、当技術分野で認知された工程であって、例えば、それらの全体において本明細書に参考として援用される、米国特許第6,969,400号において記載されている、例えば、合成インプラントデザインを伴う工程である。
当技術分野で認知された技法(例えば、トランスフェクション、電気穿孔、融合、リポソーム、コロイド状ポリマー性粒子、およびウイルスベクターおよび非ウイルスベクターのほか、当技術分野で公知の他の手段)を使用して、治療剤を、細胞へと導入することができる。選択される送達法は、例えば、オリゴマー化学、処置(処理)される細胞、および細胞の場所に依存し、そして当業者には明らかであろう。例えば、局在化は、表面上にリポソームを方向づける特異的なマーカーを伴うリポソーム、標的細胞を含有する組織への直接的な注射、特異的な受容体媒介型の取込みなどにより達成することができる。
当技術分野で公知の通り、治療剤は、例えば、リポソーム媒介型の取込み、脂質コンジュゲート、ポリリシン媒介型の取込み、ナノ粒子媒介型の取込み、および受容体媒介型のエンドサイトーシスのほか、マイクロインジェクション、透過化(例えば、ストレプトリジンOによる透過化、アニオン性ペプチドによる透過化)、電気穿孔、およびエンドサイトーシス以外の多様な非侵襲性送達法であって、当技術分野で公知の送達法など、エンドサイトーシス以外のさらなる送達方式(参照によりその全体において本明細書に組み込まれる、DokkaおよびRojanasakul、Advanced Drug Delivery Reviews、44巻、35~49頁(2000)を参照されたい)を伴う方法を使用して送達することができる。
治療剤は、生理学的および/または薬学的に許容される、任意の好都合なビヒクルまたは担体により投与することができる。このような組成物は、薬学的に許容される、様々な標準的担体であって、当業者により使用される担体のうちのいずれかを含みうる。例は、食塩水、リン酸緩衝食塩水(PBS)、水、水性エタノール、油/水エマルジョンまたはトリグリセリドエマルジョンなどのエマルジョン、錠剤、およびカプセルを含むがこれらに限定されない。生理学的に許容される適切な担体の選出は、選び出される投与方式に応じて変動するであろう。「薬学的に許容される担体」は、薬学的投与に適合性の担体など、任意で全ての溶媒、分散媒、コーティング、抗菌剤および抗真菌剤、等張剤および吸収遅延剤を含むことを意図する。当技術分野では、薬学的に活性な物質のための、このような媒体および薬剤の使用が周知である。任意の従来の媒体または薬剤が、活性化合物に不適合性である場合を除き、組成物中のその使用が想定される。補充の活性化合物もまた、組成物へと組み込むことができる。
本開示の修飾アンチセンスオリゴマーは一般に、遊離酸または遊離塩基として活用することができる。代替的に、本開示の化合物は、酸付加塩または塩基付加塩の形態で使用することもできる。本開示の遊離アミノ化合物の酸付加塩は、当技術分野で周知の方法により調製することができ、有機酸および無機酸から形成することができる。適切な有機酸は、マレイン酸、フマル酸、安息香酸、アスコルビン酸、コハク酸、メタンスルホン酸、酢酸、トリフルオロ酢酸、シュウ酸、プロピオン酸、酒石酸、サリチル酸、クエン酸、グルコン酸、乳酸、マンデル酸、ケイ皮酸、アスパラギン酸、ステアリン酸、パルミチン酸、グリコール酸、グルタミン酸、およびベンゼンスルホン酸を含む。
適切な無機酸は、塩酸、臭化水素酸、硫酸、リン酸、および硝酸を含む。塩基付加塩は、カルボン酸アニオンと共に形成される塩を含み、さらに、アルカリ金属およびアルカリ土類金属(例えば、リチウム、ナトリウム、カリウム、マグネシウム、バリウム、およびカルシウム)から選択されるもののほか、アンモニウムイオンおよびその置換誘導体(例えば、ジベンジルアンモニウム、ベンジルアンモニウム、2-ヒドロキシエチルアンモニウムなど)などの、有機カチオンおよび無機カチオンと共に形成される塩を含む。こうして、「薬学的に許容される塩」という用語は、任意で全ての許容される塩形態を包含することを意図する。
加えて、本開示の文脈にはまた、プロドラッグも含まれる。プロドラッグとは、このようなプロドラッグを、患者へと投与すると、in vivoにおいて、化合物を放出する、共有結合した任意の担体である。プロドラッグは一般に、慣例的な操作により、またはin vivoにおいて、修飾が切断されて、親化合物をもたらすように、官能基を修飾することにより調製する。プロドラッグは、例えば、本開示の化合物であって、ヒドロキシ基、アミン基、またはスルフヒドリル基を、患者へと投与されると、切断されて、ヒドロキシ基、アミン基、またはスルフヒドリル基を形成する任意の基に結合させた化合物を含む。こうして、プロドラッグの代表例は、本開示の修飾アンチセンスオリゴマーのアルコール官能基およびアミン官能基の、酢酸誘導体、ギ酸誘導体、および安息香酸誘導体を含む(がこれらに限定されない)。さらに、カルボン酸(-COOH)の場合は、メチルエステル、エチルエステルなどのエステルも使用することができる。
場合によって、リポソームを使用して、修飾アンチセンスオリゴマーの、細胞への取込みを促進することもできる(例えば、Williams, S.A.、Leukemia、10巻(12号):1980~1989頁、1996年;Lappalainenら、Antiviral Res.、23巻:119頁、1994年;Uhlmannら、「modified antisense oligomers: a new therapeutic principle」、Chemical Reviews、90巻、4号、25 544~584頁、1990年;Gregoriadis, G.、14章、「Liposomes, Drug Carriers in Biology and Medicine」、287~341頁、Academic Press、1979年を参照されたい)。例えば、PCT公開番号WO1993/01286において記載されている通り、ヒドロゲルもまた、修飾アンチセンスオリゴマーを投与するためのビヒクルとして使用することができる。代替的に、オリゴマーは、マイクロスフェアまたはマイクロ粒子により投与することもできる(例えば、Wu, G.Y.およびWu, C.H.、J. Biol. Chem.、262巻:4429~4432頁、30 1987年を参照されたい)。代替的に、米国特許第6,245,747号において記載されている通り、修飾アンチセンスオリゴマーと複合体化させたガス充填マイクロバブルの使用によっても、標的組織への送達を増強することができる。持続放出組成物もまた、使用することができる。これらは、フィルムまたはマイクロカプセルなどの成形品の形態にある半透性ポリマーマトリクスを含みうる。かかる文献の各々は、その全体が本明細書において参考として援用される。
一部の実施形態では、治療剤を、少なくとも200~400nMの治療剤のピーク血中濃度を結果としてもたらすのに有効な量および様式で投与する。一般に、約1~2週間にわたり、定期的な間隔で、1または複数の用量の治療剤が投与されることが典型的である。経口投与に好ましい用量は、70kg当たりのオリゴマー約1~1000mgである。場合によって、患者1人当たりのオリゴマー1000mgを超える用量が必要でありうる。i.v.投与では、好ましい用量は、70kg当たりのオリゴマー約0.5mg~1000mgである。治療剤は、短期間にわたり、定期的な間隔で、例えば、2週間またはこれ未満にわたり、毎日投与することができる。しかし、場合によって、治療剤を、より長期間にわたり、間欠的に投与する。投与は、抗生剤または他の治療的処置の投与が後続する場合もあり、これらと共時的な場合もある。処置レジメンは、処置下の被験体についての、イムノアッセイ、他の生化学的検査および生理学的精査の結果に基づき指し示される通りに、調整することができる(用量、頻度、経路など)。
本開示の治療剤を使用する、in vivoにおける有効な処置レジメンは、持続期間、用量、頻度、および投与経路のほか、処置下の被験体の状態(すなわち、限局感染または全身感染に応答した投与と対比した予防的投与)に従い変化させることができる。したがって、このようなin vivoにおける治療は、最適な治療転帰を達成するために、処置下にある特定の種類の障害に適切な検査によるモニタリング、および用量または処置レジメンにおける対応する調整を要請することが多いであろう。
処置は、例えば当技術分野において公知の疾患の一般的な指標によりモニターされ得る。in vivo投与された治療剤の効能は、治療剤の投与前、その間、およびその後に被験体から採取した生体試料(組織、血液、尿など)から決定され得る。治療剤が修飾アンチセンスオリゴマーである、かかる試料のアッセイは、(1)当業者に公知の手順、例えば、電気泳動ゲル移動度アッセイを使用して、標的配列および非標的配列によるヘテロ二重鎖の形成の有無をモニターすること;(2)参照エクソン2含有ミオスタチンmRNAに関する、ミオスタチンエクソン2を含まないmRNAの量をモニターすること;または(3)RT-PCR、ノザンブロッティング、ELISAもしくはウェスタンブロット法などの標準的な技法により決定される、1または複数の遺伝子変異を含む参照ジストロフィンmRNAに関する、1または複数の遺伝子変異を有する1または複数のエクソンを含むジストロフィンmRNAを含まないmRNAの量をモニターすることを含む。一部の実施形態では、処置は症状評価によりモニターされる。それらの評価は、自己評価、医師の検査、筋肉のサイズ、筋肉量、筋力、反射、無意識筋運動の測定を含む運動機能テスト(例えば握力試験)、電気生理学的試験、筋線維および中心核を有する線維の数、ならびに心電図(EKGまたはEGG)などの心血管機能試験を含む。
一部の実施形態では、本明細書で記載される方法はまた、別の治療剤と組み合わせた投与を含む。このさらなる治療剤は、本発明の治療剤(単数または複数)の投与の前に、それと並行して、または並行せずに、例えば、その後投与され得る。例えば、治療剤はステロイドおよび/または抗生物質と組み合わせて投与され得る。別の例では、患者は、エテプリルセンの投与の前に、コルチコステロイドを用いて処置(例えば4~6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、または24週もしくはこれを超える週、一定用量のコルチコステロイド)されている。ステロイドは、糖質コルチコイドまたはプレドニゾンであってもよい。コルチゾールなどの糖質コルチコイドは、炭水化物、脂肪およびタンパク質代謝を制御し、リン脂質の放出を防止することにより抗炎症性であり、それにより好酸球作用およびいくつかの他の作用機序を減少させる。アルドステロンなどの鉱質コルチコイドは、主に腎臓におけるナトリウム貯留を促進することにより、電解質および水分のレベルを制御する。コルチコステロイドは、脊椎動物の副腎皮質で天然に産生されるステロイドホルモン、および実験室で合成されるこれらのホルモンの類似体を含む、化学物質の種類である。コルチコステロイドは、ストレス応答、免疫応答、ならびに炎症、糖質代謝、タンパク質異化、血中電解質レベルおよび挙動の調節など、広範囲にわたる生理学的プロセスに関与する。コルチコステロイドは、ベタメタゾン、ブデソニド、コルチゾン、デキサメタゾン、ヒドロコルチゾン、メチルプレドニゾロン、プレドニゾロンおよびプレドニゾンを含むが、これらに限定されない。本発明の組成物の投与の前に、それと並行して、またはその後に投与され得る、目的の、1つの特定のステロイドは、デフラザコルト(deflazacort)およびその製剤である(例えばMP-104、Marathon Pharmaceuticals LLC)。
一部の実施形態では、治療剤(例えばエテプリルセンなどの治療用オリゴヌクレオチド)の投与量は、DMDを処置するのに十分な期間中、約30mg/kgである。一部の実施形態では、治療剤は、患者に、例えば週1回、約25mg/kg~約50mg/kg(例えば約25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49または50mg/kg)の用量で投与される。一部の実施形態では、治療剤は、患者に、例えば週1回、約25mg/kg~約50mg/kg(例えば約30mg/kg~約50mg/kg、約25mg/kg~約40mg/kg、約28mg/kg~約32mg/kgまたは約30mg/kg~約40mg/kg)の用量で投与される。
一部の実施形態では、治療剤は週1回静脈内投与される。ある特定の実施形態では、注入時間は約15分から約4時間までである。一部の実施形態では、注入時間は約30分から約3時間までである。一部の実施形態では、注入時間は約30分から約2時間までである。一部の実施形態では、注入時間は約1時間から約2時間までである。一部の実施形態では、注入時間は約30分から約1時間までである。一部の実施形態では、注入時間は約60分である。一部の実施形態では、注入時間は35~60分である。
VI.投薬
治療用組成物の製剤化およびそれらのその後における投与(投薬)は、当業者の技術の範囲内にあると考えられる。投薬は、処置される疾患状態の重症度および応答性に依存し、処置の過程は、数日間から数カ月間にわたり持続するか、または治癒がなされるか、もしくは疾患状態の減殺が達成されるまで持続する。最適の投薬スケジュールは、患者の体内の薬物蓄積の測定値から計算することができる。当業者は、最適の投与量、投薬法、および反復速度を容易に決定することができる。最適の投与量は、個々のオリゴマーの相対的効力に応じて変動させることができ、一般に、in vitroおよびin vivoの動物モデルにおいて有効であることが見出されているEC50に基づき推定することができる。一般に、投与量は、体重1kg当たり0.01μg~100gであり、毎日、毎週、毎月、もしくは毎年1回もしくは複数回にわたり、なおまたは2~20年間ごとに1回施すことができる。当業者は、体液中または組織内の、薬物の測定された滞留時間および濃度に基づき、投薬の反復速度を、容易に推定することができる。処置が成功した後、患者に、疾患状態の再発を防止する維持療法であって、オリゴマーを、経口投与のためには、体重70kg当たり1~1000mgのオリゴマー、またはi.v.投与のためには、体重70kg当たり0.5mg~1000mgのオリゴマーの範囲の維持用量で、毎日1回または複数回~20年ごとに1回投与する維持療法を受けさせることが望ましい場合がある。
治療用組成物の製剤化およびそれらのその後における投与(投薬)は、当業者の技術の範囲内にあると考えられる。投薬は、処置される疾患状態の重症度および応答性に依存し、処置の過程は、数日間から数カ月間にわたり持続するか、または治癒がなされるか、もしくは疾患状態の減殺が達成されるまで持続する。最適の投薬スケジュールは、患者の体内の薬物蓄積の測定値から計算することができる。当業者は、最適の投与量、投薬法、および反復速度を容易に決定することができる。最適の投与量は、個々のオリゴマーの相対的効力に応じて変動させることができ、一般に、in vitroおよびin vivoの動物モデルにおいて有効であることが見出されているEC50に基づき推定することができる。一般に、投与量は、体重1kg当たり0.01μg~100gであり、毎日、毎週、毎月、もしくは毎年1回もしくは複数回にわたり、なおまたは2~20年間ごとに1回施すことができる。当業者は、体液中または組織内の、薬物の測定された滞留時間および濃度に基づき、投薬の反復速度を、容易に推定することができる。処置が成功した後、患者に、疾患状態の再発を防止する維持療法であって、オリゴマーを、経口投与のためには、体重70kg当たり1~1000mgのオリゴマー、またはi.v.投与のためには、体重70kg当たり0.5mg~1000mgのオリゴマーの範囲の維持用量で、毎日1回または複数回~20年ごとに1回投与する維持療法を受けさせることが望ましい場合がある。
その実施形態のうちのいくつかに従い、本開示について具体的に記載してきたが、以下の実施例は、本開示を例示することだけに資するものであり、これを限定することを意図するものではない。本出願で列挙される、参考文献、特許、特許出願、GenBank受託番号などの各々は、参照によりその全体において本明細書に組み込まれる。
VI.実施例
以下の実施例は、例示を目的として使用することができ、本発明の範囲を狭めるものと考えるべきではない。
以下の実施例は、例示を目的として使用することができ、本発明の範囲を狭めるものと考えるべきではない。
本開示の修飾アンチセンスオリゴマー(図1A~1Gに図示)を、ジストロフィンまたはミオスタチンプレmRNA転写物内の標的領域と結合するようデザインし、以下のプロトコールを使用して調製した。
ジクロロメタン中の撹拌溶液6(1当量)に、POCl3(1.1当量)を添加し、続いて0℃でジイソプロピルエチルアミン(3当量)を添加し、氷浴で冷却した。15分後、氷浴を除去し、溶液を1時間室温へと温めた。反応が完了したら、反応溶液をジクロロメタンで希釈し、10%のクエン酸水溶液で3回洗浄した。MgSO4で乾燥させた後、有機層をシリカゲルプラグに通し、減圧中で濃縮した。得られるホスホロアミドジクロリド(4)をさらに精製せずに次のステップで直接使用した。
ホスホロアミドジクロリド(4)(1当量)の溶液に、ジクロロメタン中の2,6-ルチジン(1当量)、Mo(Tr)T(7)(0.5当量)/ジクロロメタン溶液を添加し、続いてN-メチルイミダゾール(0.2当量)を添加した。反応液を室温で終夜撹拌した。反応が完了したら、反応溶液をジクロロメタンで希釈し、10%のクエン酸水溶液で3回洗浄した。MgSO4で乾燥させた後、有機層を濾過し、次いで濃縮した。生成物(8)をシリカゲルクロマトグラフィー(酢酸エチル/ヘキサンの勾配で溶出)により精製し、次いで-20℃で保存した。LCMS分析により構造を確認した。
ジクロロメタン中のPOCl3(1.1当量)溶液に、2,6-ルチジン(2当量)を添加し、続いて0℃でMo(Tr)T(7)(1当量)/ジクロロメタン溶液を滴下添加した。1時間後、反応溶液をジクロロメタンで希釈し、10%のクエン酸水溶液で3回、手早く洗浄した。MgSO4で乾燥させ、溶媒を蒸発させた後、所望のホスホジクロリデート(9)を得た。
ジクロロメタン中のホスホジクロリデート(1当量)溶液に、0℃でアミン(1当量)/ジクロロメタンを溶液への滴下により添加した。15分後、反応混合物を約1時間、室温へと温めた。反応が完了したら、ヘキサンを添加して沈殿させ、続いて濾過することによって、白色固体としての生成物(8)を回収した。生成物を減圧下で乾燥させた後、-20℃で保存した。LCMS分析により構造を確認した。
(実施例1)
((2S,6R)-6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチルホスホロジクロリデート
(実施例1)
((2S,6R)-6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチルホスホロジクロリデート
オキシ塩化リン(2.12mL、22.7mmol)の冷却(氷/水浴)DCM溶液(20mL)に、2,6-ルチジン(4.82mL、41.4mmol)を滴下添加し、次いで、Mo(Tr)T(2)(10.0g、20.7mmol)のDCM溶液(20mL)を15分にわたり滴下添加し(内部温度:0~10℃)、次いで浴槽を除去し、20分間周囲温度で撹拌を継続させた。反応物をクエン酸溶液(40mL×3、10%w/v水溶液)で洗浄し、乾燥させ(MgSO4)、濾過し、白色泡状物(9.79g)となるまで濃縮し、次いで以下の手順に直接使用した。
(実施例2)
(6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチル(4-(ジメチルアミノ)ピペリジン-1-イル)ホスホノクロリデート
(実施例2)
(6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチル(4-(ジメチルアミノ)ピペリジン-1-イル)ホスホノクロリデート
実施例1で得たジクロロホスフェート(5.00g、5.00mmol)の冷却(氷/水浴)DCM溶液(5mL)に、ピペリジン(0.61g、4.76mmol)のDCM溶液(5mL)を滴下添加し、次いで浴槽を除去し、周囲温度で30分間撹拌を継続させた。反応物をカラム上に直接ロードした。[SiO2カラム(40g)、DCM/EtOH溶出液(勾配1:0~1:1)]でのクロマトグラフィーにより、白色泡状物として表題化合物(2.5g)を得た。1(4ニトロフェニル)ピペラジン誘導体C46H55N8O7PのESI/MS:計算値862.4、実測値m/z=863.6(M+1)。
(実施例3)
1-(1-(クロロ((6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メトキシ)ホスホリル)ピペリジン-4-イル)-1-メチルピロリジン-1-イウムクロリド
(実施例3)
1-(1-(クロロ((6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メトキシ)ホスホリル)ピペリジン-4-イル)-1-メチルピロリジン-1-イウムクロリド
実施例2に記載の方法と類似の方法で表題化合物を合成し、白色固体として表題化合物(0.6g)を得た。1-(4-ニトロフェニル)ピペラジン誘導体C49H60N8O7PのESI/MS:計算値903.4、実測値m/z=903.7(M+)。
(実施例4)
((2S,6R)-6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチル(4-メチルピペラジン-1-イル)ホスホノクロリデート
(実施例4)
((2S,6R)-6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチル(4-メチルピペラジン-1-イル)ホスホノクロリデート
オキシ塩化リン(1.02mL、11.0mmol)の冷却(氷/水浴)DCM溶液(10mL)に、2,6-ルチジン(3.49mL、29.9mmol)を滴下添加し、次いでメチルピペラジン(1.00g、10.0mmol)のDCM溶液(10mL)を滴下添加し、1時間撹拌を継続させた。Mo(Tr)T(2)(4.82、10.0mmol)およびNMI(79μL、1.0mmol)のDCM溶液(10mL)を添加し、4時間撹拌し、次いでカラム上に直接ロードした。
(SiO2カラム(80g)、DCM/アセトン(勾配1:0~0:1)、2%のTEA溶出液)でのクロマトグラフィーにより、白色泡状物として表題化合物(0.8g)を得た。1-(4-ニトロフェニル)ピペラジン誘導体C43H48N7O8PのESI/MS:計算値834.4、実測値m/z=835.5(M+1)。
(実施例5)
((2S,6R)-6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチル(4-エチルピペラジン-1-イル)ホスホノクロリデート
(実施例5)
((2S,6R)-6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチル(4-エチルピペラジン-1-イル)ホスホノクロリデート
実施例4に記載の方法と類似の方法で表題化合物を合成し、白色泡状物として表題化合物(11.5g)を得た。1-(4-ニトロフェニル)ピペラジン誘導体C45H53N8O7PのESI/MS:計算値848.4、実測値m/z=849.7(M+1)。
(実施例6)
((2S,6R)-6-(6-ベンズアミド-9H-プリン-9-イル)-4-トリチルモルホリン-2-イル)メチル(4-エチルピペラジン-1-イル)ホスホノクロリデート
(実施例6)
((2S,6R)-6-(6-ベンズアミド-9H-プリン-9-イル)-4-トリチルモルホリン-2-イル)メチル(4-エチルピペラジン-1-イル)ホスホノクロリデート
実施例4に記載の方法と類似の方法で表題化合物を合成し、白色泡状物として表題化合物(4.5g)を得た。1-(4-ニトロフェニル)ピペラジン誘導体C52H56N11O6PのESI/MS:計算値961.4、実測値m/z=962.8(M+1)。
(実施例7)
((2S,6R)-6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチル(4-イソプロピルピペラジン-1-イル)ホスホノクロリデート
(実施例7)
((2S,6R)-6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチル(4-イソプロピルピペラジン-1-イル)ホスホノクロリデート
実施例4に記載の方法と類似の方法で表題化合物を合成し、白色泡状物として表題化合物(3.5g)を得た。1-(4-ニトロフェニル)ピペラジン誘導体C46H55N8O7PのESI/MS:計算値862.4、実測値m/z=863.7(M+1)。
(実施例8)
((2S,6R)-6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチルメチル(2-(2,2,2-トリフルオロアセトアミド)エチル)ホスホルアミドクロリデート
(実施例8)
((2S,6R)-6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチルメチル(2-(2,2,2-トリフルオロアセトアミド)エチル)ホスホルアミドクロリデート
実施例4に記載の方法と類似の方法により表題化合物を合成し、白色泡状物として表題化合物(1.0g)を得た。1-(4-ニトロフェニル)ピペラジン誘導体C44H48F3N8O8PのESI/MS:計算値904.3、実測値m/z=903.7(M-1)。
(実施例9)
((2S,6R)-6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチルメチル(2-(2,2,2-トリフルオロ-N-メチルアセトアミド)エチル)ホスホルアミドクロリデート
(実施例9)
((2S,6R)-6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチルメチル(2-(2,2,2-トリフルオロ-N-メチルアセトアミド)エチル)ホスホルアミドクロリデート
実施例4に記載の方法と類似の方法で表題化合物を合成し、白色泡状物として表題化合物(1.8g)を得た。1-(4-ニトロフェニル)ピペラジン誘導体C45H50F3N8O8PのESI/MS:計算値918.3、実測値m/z=1836.6(2M+)。
(実施例10)
((2S,6R)-6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチル(4-(2,2,2-トリフルオロアセトアミド)ピペリジン-1-イル)ホスホノクロリデート
(実施例10)
((2S,6R)-6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチル(4-(2,2,2-トリフルオロアセトアミド)ピペリジン-1-イル)ホスホノクロリデート
DCM(190mL)中のオキシ塩化リン(17.7mL、190mmol)冷却溶液(氷/水浴)に、2,6-ルチジン(101mL、864mmol)を滴下添加し、次いでMo(Tr)T(2)(83.5g、173mmol)を15分にわたり一部ずつ添加し(内部温度0~10℃)、撹拌した。30分後、4-アミノピペリジンモノトリフルオロアセトアミド(48.9g、約190mmol)を15分にわたり滴下添加し(内部温度0~8℃)、撹拌した。1時間後、DIPEA(50mL)を滴下添加し(内部温度0~10℃)、1時間撹拌した。反応物をクエン酸溶液(500mL×3、10%w/v水溶液)で洗浄し、乾燥させ(MgSO4)、濾過し、濃縮して粘稠な油状物を得、それをカラムに直接ロードした。[SiO2カラム(330g)、ヘキサン/EtOAc溶出液(勾配1:0~0:1)]でのクロマトグラフィーにより、白色泡状物として表題化合物(91.3g、70%の収率)を得た。1-(4-ニトロフェニル)ピペラジン誘導体C43H48N7O8PのESI/MS:計算値930.9、実測値m/z=954.4(M+Na)。
実施例11~14は、上記手順Aにより調製した。
(実施例11)
(6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチル(4-(1-(2,2,2-トリフルオロアセチル)ピペリジン-4-イル)ピペラジン-l-イル)ホスホノクロリデート
(実施例12)
(6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチル(4-モルホリノピペリジン-1-イル)ホスホノクロリデート
(実施例13)
(6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチルビス(3-(2,2,2-トリフルオロアセトアミド)プロピル)ホスホルアミドクロリデート
(実施例14)
(6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチル[1,4’-ビピペリジン]-1’-イルホスホノクロリデート
以下の実施例15から20は、上記の手順Bにより調製した。
(実施例15)
(6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチル(4-(ピリミジン-2-イル)ピペラジン-1-イル)ホスホノクロリデート
(実施例16)
(6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチル(4-(2-(ジメチルアミノ)エチル)ピペラジン-1-イル)ホスホノクロリデート
(実施例17)
(6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチル(4-フェニルピペラジン-1-イル)ホスホノクロリデート
(実施例18)
(6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチル(4-(2,2,2-トリフルオロ-N-メチルアセトアミド)ピペリジン-1-イル)ホスホノクロリデート
(実施例19)
(6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチルメチル(3-(2,2,2-トリフルオロ-N-メチルアセトアミド)プロピル)ホスホルアミドクロリデート
(実施例20)
((2S,6R)-6-(6-ベンズアミド-9H-プリン-9-イル)-4-トリチルモルホリン-2-イル)メチル(4-(2,2,2-トリフルオロアセトアミド)ピペリジン-1-イル)ホスホノクロリデート
(実施例21)
(4-(ピロリジン-1-イル)ピペリジン-1-イル)ホスホニックジクロリド塩酸塩
(実施例11)
(6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチル(4-(1-(2,2,2-トリフルオロアセチル)ピペリジン-4-イル)ピペラジン-l-イル)ホスホノクロリデート
(実施例12)
(6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチル(4-モルホリノピペリジン-1-イル)ホスホノクロリデート
(実施例13)
(6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチルビス(3-(2,2,2-トリフルオロアセトアミド)プロピル)ホスホルアミドクロリデート
(実施例14)
(6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチル[1,4’-ビピペリジン]-1’-イルホスホノクロリデート
以下の実施例15から20は、上記の手順Bにより調製した。
(実施例15)
(6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチル(4-(ピリミジン-2-イル)ピペラジン-1-イル)ホスホノクロリデート
(実施例16)
(6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチル(4-(2-(ジメチルアミノ)エチル)ピペラジン-1-イル)ホスホノクロリデート
(実施例17)
(6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチル(4-フェニルピペラジン-1-イル)ホスホノクロリデート
(実施例18)
(6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチル(4-(2,2,2-トリフルオロ-N-メチルアセトアミド)ピペリジン-1-イル)ホスホノクロリデート
(実施例19)
(6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチルメチル(3-(2,2,2-トリフルオロ-N-メチルアセトアミド)プロピル)ホスホルアミドクロリデート
(実施例20)
((2S,6R)-6-(6-ベンズアミド-9H-プリン-9-イル)-4-トリチルモルホリン-2-イル)メチル(4-(2,2,2-トリフルオロアセトアミド)ピペリジン-1-イル)ホスホノクロリデート
(実施例21)
(4-(ピロリジン-1-イル)ピペリジン-1-イル)ホスホニックジクロリド塩酸塩
DCM(30mL)中のオキシ塩化リン(5.70mL、55.6mmol)冷却(氷/水浴)溶液に、2,6-ルチジン(19.4mL、167mmol)および4-(1-ピロリジニル)-ピペリジン(8.58g、55.6mmol)のDCM溶液(30mL)を添加し、1時間撹拌した。懸濁液を濾過し、固体を過剰量のジエチルエーテルで洗浄し、白色固体として表題のピロリジン(17.7g、91%の収率)を得た。1-(4-ニトロフェニル)ピペラジン誘導体C19H30N5O4PのESI/MS:計算値423.2、実測値m/z=422.2(M-1)。
(実施例22)
((2S,6R)-6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチル(4-(ピロリジン-1-イル)ピペリジン-1-イル)ホスホノクロリデート塩酸塩
(実施例22)
((2S,6R)-6-(5-メチル-2,4-ジオキソ-3,4-ジヒドロピリミジン-1(2H)-イル)-4-トリチルモルホリン-2-イル)メチル(4-(ピロリジン-1-イル)ピペリジン-1-イル)ホスホノクロリデート塩酸塩
DCM(100mL)中の実施例21で得たジクロロホスホルアミデート(17.7g、50.6mmol)撹拌冷却(氷/水浴)溶液に、Mo(Tr)T(2)(24.5g、50.6mmol)、2,6-ルチジン(17.7mL、152mmol)および1-メチルイミダゾール(0.401mL、5.06mmol)のDCM溶液(100mL)を10分にわたり滴下添加した。懸濁液を撹拌しながら、浴槽を周囲温度へと温めた。6時間後、懸濁液をジエチルエーテル(1L)上に注ぎ、15分間撹拌し、濾過し、固体をさらなるエーテルで洗浄し、白色固体(45.4g)を得た。粗生成物をクロマトグラフィー[SiO2カラム(120グラム)、DCM/MeOH溶出液(勾配1:0~6:4)]により精製し、合わせた画分をジエチルエーテル(2.5L)上に注ぎ、15分間撹拌し、濾過し、得られた固体を、さらなるエーテルで洗浄し、白色固体として表題化合物(23.1g、60%の収率)を得た。1-(4-ニトロフェニル)ピペラジン誘導体C48H57N8O7PのESI/MS:計算値888.4、実測値m/z=887.6(M-1)。
(実施例23)
修飾アンチセンスオリゴマーおよび例示的な修飾アンチセンスオリゴマーのデザインおよび製造
トリチルピペラジンフェニルカルバメート35の調製(図2A):ジクロロメタン中の化合物11の冷却懸濁物(6mL/gの11)に、水中の炭酸カリウム(3.2当量)溶液(4mL/gの炭酸カリウム)を添加した。この2相混合物に、ジクロロメタン中のクロロギ酸フェニル(1.03当量)溶液(2g/gのクロロギ酸フェニル)を、ゆっくりと添加した。反応混合物を、20℃へと温めた。反応が完了したら(1~2時間)、層を分離した。有機層を、水で洗浄し、無水炭酸カリウムで乾燥させた。生成物35を、アセトニトリルからの結晶化により単離した。
修飾アンチセンスオリゴマーおよび例示的な修飾アンチセンスオリゴマーのデザインおよび製造
トリチルピペラジンフェニルカルバメート35の調製(図2A):ジクロロメタン中の化合物11の冷却懸濁物(6mL/gの11)に、水中の炭酸カリウム(3.2当量)溶液(4mL/gの炭酸カリウム)を添加した。この2相混合物に、ジクロロメタン中のクロロギ酸フェニル(1.03当量)溶液(2g/gのクロロギ酸フェニル)を、ゆっくりと添加した。反応混合物を、20℃へと温めた。反応が完了したら(1~2時間)、層を分離した。有機層を、水で洗浄し、無水炭酸カリウムで乾燥させた。生成物35を、アセトニトリルからの結晶化により単離した。
カルバメートアルコール36の調製:水素化ナトリウム(1.2当量)を、1-メチル-2-ピロリジノン(32mL/gの水素化ナトリウム)中に懸濁させた。この懸濁物に、トリエチレングリコール(10.0当量)および化合物35(1.0当量)を添加した。結果として得られるスラリーを、95℃へと加熱した。反応が完了したら(1~2時間)、混合物を、20℃へと冷却した。この混合物に、30%のジクロロメタン/メチルtert-ブチルエーテル(v:v)および水を添加した。生成物を含有する有機層を、水性NaOH、水性コハク酸、および飽和水性塩化ナトリウムで、逐次洗浄した。生成物36を、ジクロロメタン/メチルtert-ブチルエーテル/ヘプタンからの結晶化により単離した。
テール型酸(Tail acid)37の調製:テトラヒドロフラン中の化合物36の溶液(7mL/gの36)に、無水コハク酸(2.0当量)およびDMAP(0.5当量)を添加した。混合物を、50℃へと加熱した。反応が完了したら(5時間)、混合物を、20℃へと冷却し、水性NaHCO3により、pH8.5へと調整した。メチルtert-ブチルエーテルを添加し、生成物を、水性層へと抽出した。ジクロロメタンを添加し、混合物を、水性クエン酸により、pH3へと調整した。生成物を含有する有機層を、クエン酸緩衝液と、飽和水性塩化ナトリウムとの、pH=3の混合物で洗浄した。この37のジクロロメタン溶液を、単離せずに、化合物38の調製において使用した。
38の調製:化合物37の溶液に、N-ヒドロキシ-5-ノルボルネン-2,3-ジカルボン酸イミド(HONB)(1.02当量)、4-ジメチルアミノピリジン(DMAP)(0.34当量)を添加し、次いで、1-(3-ジメチルアミノプロピル)-N’-エチルカルボジイミドヒドロクロリド(EDC)(1.1当量)を添加した。混合物を、55℃へと加熱した。反応が完了したら(4~5時間)、混合物を、20℃へと冷却し、1:1の0.2Mクエン酸/ブラインおよびブラインで、逐次洗浄した。ジクロロメタン溶液に、アセトンへの溶媒交換、次いで、N,N-ジメチルホルムアミドへの溶媒交換を施し、生成物を、アセトン/N,N-ジメチルホルムアミドからの、飽和水性塩化ナトリウムへの沈殿により単離した。粗生成物を、水中で、複数回にわたり、再スラリー化させて、残留するN,N-ジメチルホルムアミドおよび塩を除去した。
活性化「テール」の、アンカーロード樹脂への導入は、固相合成におけるサブユニットの組込みのために使用される手順により、ジメチルイミダゾリジノン(DMI)中で実施した。
モルホリノベースのオリゴマーの合成のための固体支持体の調製:この手順は、粗い多孔性(40~60μm)のガラスフリット、オーバーヘッド撹拌機、および、フリットを介してN2を沸騰させるかまたは真空抽出を可能とする、Teflon製の三方止め栓を伴う、シラン化、ジャケット付きのペプチド容器(ChemGlass、NJ、USA)内で実施した。
以下の手順における樹脂処理/洗浄ステップは、2つの基本的な操作からなる:樹脂流動化または撹拌床樹脂反応器および溶媒/溶液抽出。樹脂の流動化のために、フリットを通ってN2の逆流(flow up)を可能とするように、止め栓を位置付け、指定の樹脂処理/洗浄液を、反応器へと添加し、樹脂を透過化させ、完全に湿潤させた。次いで、混合を開始し、指定の回数にわたり、樹脂スラリーを混合した。溶媒/溶液抽出のために、混合およびN2の流れを停止させ、真空ポンプを始動させ、次いで、樹脂処理/洗浄液を排出して廃棄することを可能とするように、止め栓を位置付けた。そうでないことが注記されない限りにおいて、樹脂処理/洗浄液の全容量は、樹脂1g当たり15mLであった。
シラン化、ジャケット付きのペプチド容器内のアミノメチルポリスチレン樹脂(100~200メッシュ;窒素置換に基づき、1g当たり約1.0mmolのロード;75g、1当量、Polymer Labs、UK、型番:1464-X799)に、1-メチル-2-ピロリジノン(NMP;樹脂1g当たり20ml)を添加し、樹脂を、混合しながら、1~2時間にわたり膨潤させた。膨潤溶媒(swell solvent)の排出後、樹脂を、ジクロロメタン(2×1~2分間)、25%のイソプロパノール/ジクロロメタン中に5%のジイソプロピルエチルアミン(2×3~4分間)、およびジクロロメタン(2×1~2分間)で洗浄した。最終洗浄液を排出した後、樹脂を、1-メチル-2-ピロリジノン中の、ジスルフィドアンカー34溶液(0.17M;樹脂1g当たり15mL、約2.5当量)で処理し、樹脂/試薬混合物を、45℃で60時間にわたり加熱した。反応が完了したら、加熱を中断し、アンカー溶液を排出し、樹脂を、1-メチル-2-ピロリジノン(4×3~4分間)およびジクロロメタン(6×1~2分間)で洗浄した。樹脂を、ジクロロメタン中に10%(v/v)のジエチルジカーボネート溶液(16mL/g;2×5~6分間)で処理し、次いで、ジクロロメタン(6×1~2分間)で洗浄した。樹脂39(図2B)を、N2流下で、1~3時間にわたり、次いで、真空下で、一定の重量(±2%)まで乾燥させた。収率:元の樹脂重量の110~150%。
アミノメチルポリスチレン-ジスルフィド樹脂のローディングの決定:樹脂のローディング(潜在的に利用可能な反応性部位の数)は、分光アッセイにより、樹脂1グラム当たりのトリフェニルメチル(トリチル)基の数について決定する。
公知の重量(25±3mg)の乾燥樹脂を、25mlのシラン化メスフラスコへと移し、ジクロロメタン中に2%(v/v)のトリフルオロ酢酸約5mLを添加する。内容物を、静かな回旋により混合し、次いで、30分間にわたり静置する。容量を、ジクロロメタン中に2%(v/v)の、さらなるトリフルオロ酢酸により、25mLへと増量し、内容物を、完全に混合した。容積型ピペット(positive displacement
pipette)を使用して、トリチル含有溶液(500μL)のアリコートを、10mLのメスフラスコへと移し、容量を、メタンスルホン酸により、10mLへと増量する。
pipette)を使用して、トリチル含有溶液(500μL)のアリコートを、10mLのメスフラスコへと移し、容量を、メタンスルホン酸により、10mLへと増量する。
最終溶液中のトリチルカチオン含量は、431.7nmにおけるUV吸光度により測定し、樹脂のローディングは、適切な容量、希釈率、消衰係数(ε:41μmol-1cm-1)、および樹脂重量を使用して、樹脂1グラム当たりのトリチル基(μmol/g)により計算する。アッセイは、三連で実施し、平均ローディングを計算する。
本実施例における樹脂のローディング手順により、約500μmol/gのローディングを有する樹脂を提供する。ジスルフィドアンカーの組込みステップを、室温で24時間にわたり実施する場合、μmol/g単位で300~400のローディングが得られた。
テールローディング:アミノメチルポリスチレン-ジスルフィド樹脂を調製するための設定および容量と同じ設定および容量を使用して、テールを、固体支持体へと導入することができる。アンカーロード樹脂をまず、酸性条件下で脱保護し、結果として得られる材料を中性化させてから、カップリングした。カップリングステップのために、ジスルフィドアンカー溶液の代わりに、4-エチルモルホリン(NEM、0.4M)を含有するDMI中の、38の溶液(0.2M)を使用した。45℃で2時間後、樹脂39を、25%のイソプロパノール/ジクロロメタン中に5%のジイソプロピルエチルアミンで2回にわたり洗浄し、DCMで1回洗浄した。樹脂に、安息香酸無水物(0.4M)およびNEM(0.4M)の溶液を添加した。25分後、反応器ジャケットを、室温へと冷却し、樹脂を、25%のイソプロパノール/ジクロロメタン中に5%のジイソプロピルエチルアミンで、2回にわたり洗浄し、DCMで、8回にわたり洗浄した。樹脂40を濾過し、高真空下で乾燥させた。樹脂40に対するローディングは、テールローディングにおいて使用した、元のアミノメチルポリスチレン-ジスルフィド樹脂39のローディングであると規定する。
固相合成:モルホリノベースのオリゴマーは、Gilson AMS-422 Automated Peptide Synthesizer上、2mLのGilsonポリプロピレン反応カラム(型番:3980270)内で調製した。カラムを合成器に静置するときに、カラムの周囲に、水流のためのチャネルを伴うアルミニウム製のブロックを入れた。AMS-422は、代替的に、試薬/洗浄液を添加し、指定された時間にわたり保持し、真空を使用して、カラムを排気する。
最大で約25サブユニットの長さの範囲のオリゴマーでは、ローディングを、樹脂1g当たり約500μmolとする、アミノメチルポリスチレン-ジスルフィド樹脂が好ましい。より大型のオリゴマーでは、ローディングを、樹脂1g当たり300~400μmolとする、アミノメチルポリスチレン-ジスルフィド樹脂が好ましい。5’テールを伴う分子が所望される場合も、同じローディング指針により、テールでローディングした樹脂を選択する。
以下の試薬溶液を調製した。
脱トリチル化溶液:4:1ジクロロメタン/アセトニトリル中に、10%のシアノ酢酸(w/v);中性化溶液:3:1のジクロロメタン/イソプロパノール中に、5%のジイソプロピルエチルアミン;カップリング溶液:所望の塩基型および連結型を有する、0.18M(または20サブユニットより長くなったオリゴマーには、0.24M)の活性化モルホリノサブユニット、ならびに1,3-ジメチルイミダゾリジノン中に、0.4MのNエチルモルホリン。ジクロロメタン(DCM)を、異なる試薬溶液の洗浄を隔てる、一過性洗浄液として使用した。
ブロックを42℃に設定した合成器上で、30mgのアミノメチルポリスチレン-ジスルフィド樹脂(またはテール樹脂)を含有する各カラムに、2mLの1-メチル-2-ピロリジノンを添加し、室温で、30分間にわたり静置した。2mLのジクロロメタンで、2回にわたる洗浄の後、以下の合成サイクルを使用した。
各カラムが、適正な配列の、適正なカップリング溶液(A、C、G、T、I)を受容するように、個々のオリゴマーの配列を、合成器へとプログラムした。カラム内のオリゴマーが、その最終的なサブユニットの組込みを完了したら、カラムを、ブロックから取り出し、0.89Mの4-エチルモルホリンを含有する、4-メトキシトリフェニルメチルクロリド(DMI中に0.32M)を含むカップリング溶液により、最終サイクルを、手動で実施した。
樹脂からの切断ならびに塩基および保護基の除去:メトキシトリチル化の後、樹脂を、2mLの1-メチル-2-ピロリジノンで、8回にわたり洗浄した。1-メチル-2-ピロリジノン中に、0.1Mの1,4-ジチオトレイトール(DTT)および0.73Mのトリエチルアミンを含む、1mLの切断溶液を添加し、カラムに蓋をし、室温で、30分間にわたり静置した。この時間の後、溶液を、12mLのWheatonバイアルへと排出した。大幅に縮んだ樹脂を、300μLの切断溶液で、2回にわたり洗浄した。溶液に、4.0mLの濃縮アンモニア水(-20℃で保存された)を添加し、バイアルにきつく蓋をし(テフロン(登録商標)加工のねじ蓋により)、混合物を回旋にかけて、溶液をミックスした。バイアルを、45℃のオーブンに、16~24時間にわたり入れて、塩基および保護基の切断を行った。
粗生成物の精製:バイアルに入れた(vialed)アンモノリシス溶液を、オーブンから取り出して、室温へと冷却した。溶液を、20mLの0.28%の水性アンモニアで希釈し、Macroprep HQ樹脂(BioRad)を含有する、2.5×10cmのカラムに通した。塩勾配(A:0.28%のアンモニアに、B:0.28%のアンモニア中に1Mの塩化ナトリウムを伴う;60分間でBを0~100%とする)を使用して、メトキシトリチルを含有するピークを溶出させた。合わせた画分をプールし、所望される生成物に応じて、さらに加工した。
モルホリノベースのオリゴマーの脱メトキシトリチル化:Macroprepによる精製からプールされた画分を、1MのH3PO4で処理して、pHを2.5へと低下させた。初期の混合の後、試料を、室温で4分間にわたり静置し、この時間に、それらを、2.8%のアンモニア/水で、pH10~11へと中性化させる。生成物は、固相抽出(SPE)により精製した。
SPEカラムのパッキングおよびコンディショニング:Amberchrome CG-300M(Rohm and Haas;Philadelphia、PA)(3mL)を、20mLのフリットカラム(BioRad Econo-Pac Chromatography Columns(732~1011))へとパッキングし、樹脂を、3mLの以下のもの:0.28%のNH4OH/80%のアセトニトリル;0.5MのNaOH/20%のエタノール;水;50mMのH3PO4/80%のアセトニトリル;水;0.5のNaOH/20%のエタノール;水;0.28%のNH4OHですすいだ。
SPEの精製:脱メトキシトリチル化からの溶液を、カラムへとロードし、樹脂を、0.28%の水性アンモニア3~6mLで、3回にわたりすすいだ。Wheatonバイアル(12mL)を、カラムの下に置き、生成物を、0.28%の水性アンモニア中に、45%のアセトニトリル2mLで2回にわたる洗浄により溶出させた。
生成物の単離:溶液を、ドライアイス内で凍結させ、バイアルを凍結乾燥機に入れて、綿毛状の白色粉末をもたらした。試料を、水中に溶解させ、シリンジを使用して、0.22ミクロンのフィルター(Pall Life Sciences、Acrodisc 25mmシリンジフィルターに、0.2ミクロンのHT Tuffryn膜を伴う)を通して濾過し、UV分光光度計上で、光学濃度(OD)を測定して、存在するオリゴマーのOD単位を決定したほか、試料を解析のために分注した。次いで、凍結乾燥させるために、溶液を、Wheatonバイアルに戻した。
MALDIによる、モルホリノベースのオリゴマーについての解析:MALDI-TOF質量分析を、使用して、精製物中の画分の組成を決定したほか、オリゴマーの正体の証拠(分子量)ももたらした。マトリックスとしての、3,5-ジメトキシ-4-ヒドロキシケイ皮酸(シナピン酸)、3,4,5-トリヒドロキシアセトフェノン(THAP)、またはアルファ-シアノ-4-ヒドロキシケイ皮酸(HCCA)の溶液による希釈後に、試料を試行にかけた。
(実施例24)
PMOミオスタチン配列のin vivoスクリーニング
ミオスタチンエクソン2をスキップするようにデザインされたPMO配列をスクリーニングした。ヒト横紋筋肉腫(RD)およびマウス筋芽細胞(正常:C2C12、およびジストロフィー:H2Kbmdx)細胞の両方において、in vitroでPMO配列の有効性を試験した。次に、RD細胞において、ミオスタチンエクソン2の5’末端を標的とする4つのヒト特異的なPMOをスクリーニングした。
PMOミオスタチン配列のin vivoスクリーニング
ミオスタチンエクソン2をスキップするようにデザインされたPMO配列をスクリーニングした。ヒト横紋筋肉腫(RD)およびマウス筋芽細胞(正常:C2C12、およびジストロフィー:H2Kbmdx)細胞の両方において、in vitroでPMO配列の有効性を試験した。次に、RD細胞において、ミオスタチンエクソン2の5’末端を標的とする4つのヒト特異的なPMOをスクリーニングした。
Nucleofection(Neonトランスフェクションシステム、Life technologies、カールズバッド、CA)によって、製造業者の標準的なプロトコールに従い、PMOをトランスフェクトした。RT-PCR産物のゲル電気泳動結果のデンシトメトリー分析に従い、スキップされた産物およびスキップされなかった産物の総密度に対するスキップされた産物の密度のパーセンテージとして、半定量的RT-PCRにより、PMOのスキッピング効率を評価した。配列を表7に列挙する。
配列PMO39(配列番号48)、PMO42(配列番号16)、PMO43(配列番号49)、PMO44(配列番号17)、PMO45(配列番号18)およびPMO124を、マウスおよびヒトミオスタチンエクソン2の両方と結合するようにデザインした。PMOは、4つの用量(0.25、0.5、1および2μM)で3回ずつ試験した。上記のようにRT-PCR(図3A)およびRT-PCR産物のデンシトメトリー分析により、スキップされた産物およびスキップされなかった産物の総強度に対するスキップされた産物の強度のパーセンテージとして、ミオスタチンエクソン2のスキッピング効率を評価した。統計解析は、PMOの効率を、個々の用量において、ミオスタチンエクソン2をスキップする有効なPMOとして示されたPMO28(GeneToolsにより合成)のそれと比較する一方向分散分析により実施した(図3B)。
ヒトミオスタチンエクソン2の5’末端と結合するように全てデザインされた4つのヒト特異的PMO(PMO40、PMO46(配列番号21)、PMO47(配列番号20)、PMO48(配列番号19))を分析した。PMOは、1μMの用量で3回試験し、3’末端を標的とするPMOと同じ濃度で比較した。これらのPMOがエクソン2スキッピングを誘導すると予想されたので、それらの有効性を、確立したRT-PCRプロトコールにより、上記のようなデンシトメトリー分析に従い評価した。RT-PCT産物の結果を図4Aに示し、デンシトメトリー分析を図4Bに示す。
ミオスタチンエクソン2の3’末端を標的とするPMOのうち、PMO44(配列番号17)およびPMO45(配列番号18)(ならびにより高い濃度でPMO39(配列番号48))は、特に低い濃度で、他よりも一貫したスキッピングを誘導した(図4B)。ミオスタチンエクソン2の5’末端を標的とするPMOを使用したとき、スキッピング有効性はさらに高く、PMO46(配列番号21)はほぼ100%のスキッピングを誘導し、PMO40および48(配列番号19)は約80%のスキッピングを誘導した(図4B)。
マウスミオスタチンのエクソン2のスキッピング用のPMOのスクリーニング:C2C12およびH2Kbmdx細胞におけるPMO39、42、43、44、45、124の用量反応試験
マウスミオスタチンのエクソン2のスキッピング用のPMOのスクリーニング:C2C12およびH2Kbmdx細胞におけるPMO39、42、43、44、45、124の用量反応試験
mdxマウスモデルにおける特異的および再現可能なエクソンスキッピングの最初の例が、Wiltonら(Wilton、Lloydら1999年、その内容は参照によりその全体において本
明細書に組み込まれる)により報告された。アンチセンス分子をドナースプライス部位に指向させることにより、培養細胞の6時間以内の処理で、一貫したおよび効果的なエクソン23のスキッピングがジストロフィンmRNAにおいて誘導された。Wiltonらはまた、より長いアンチセンスオリゴヌクレオチドを用いた、マウスジストロフィンプレmRNAのアクセプター領域のターゲッティングについて記載している。イントロン23のドナースプライス部位を指向する第1のアンチセンスオリゴヌクレオチドが初代培養筋芽細胞において一貫したエクソンスキッピングを誘導した一方で、この化合物が、より高いレベルのジストロフィンを発現する不死化細胞培養ではそれ程効率的でないことがわかった。しかしながら、ターゲッティングおよびアンチセンスオリゴヌクレオチドのデザインを改良することにより、特異的なエクソン除去の効率がほぼ1桁増加した(Mann、Honeymanら、2002年、その内容は参照によりその全体において本明細書に組み込まれる)。
明細書に組み込まれる)により報告された。アンチセンス分子をドナースプライス部位に指向させることにより、培養細胞の6時間以内の処理で、一貫したおよび効果的なエクソン23のスキッピングがジストロフィンmRNAにおいて誘導された。Wiltonらはまた、より長いアンチセンスオリゴヌクレオチドを用いた、マウスジストロフィンプレmRNAのアクセプター領域のターゲッティングについて記載している。イントロン23のドナースプライス部位を指向する第1のアンチセンスオリゴヌクレオチドが初代培養筋芽細胞において一貫したエクソンスキッピングを誘導した一方で、この化合物が、より高いレベルのジストロフィンを発現する不死化細胞培養ではそれ程効率的でないことがわかった。しかしながら、ターゲッティングおよびアンチセンスオリゴヌクレオチドのデザインを改良することにより、特異的なエクソン除去の効率がほぼ1桁増加した(Mann、Honeymanら、2002年、その内容は参照によりその全体において本明細書に組み込まれる)。
最初に、マウス筋芽細胞C2C12細胞において、0.25、0.5、1、2および5μMの用量で各4回、PMOを試験した(図5Aおよび図5C)。PMO配列ならびに0.5および2μMの用量を用いて、スキッピングの変動が反復的に観察された。代わりに筋芽細胞ジストロフィー細胞モデルであるH2Kbmdx細胞においてスクリーニングを行った結果、より一貫した、信頼性が高い結果が示された(図5Aおよび図5B)。
試験したH2Kbmdx細胞培養において、PMO28は、高濃度で最高のPMOであり、低濃度で最も効率的なPMOの1つであった(PMO45(配列番号18)およびPMO39(配列番号48)と同程度)(図5B)。
mdxマウスにおける、非コンジュゲートPMO-MSTN配列の予備的in vivoスクリーニング
mdxマウスにおける、非コンジュゲートPMO-MSTN配列の予備的in vivoスクリーニング
in vitroの結果に基づき、PMO39(配列番号48)、44(配列番号17)および45(配列番号18)を本試験用に選択した。PMO124を対照として使用した。PMO124の最適用量である3nmol(18×1014分子に相当)を、8週齢のmdxマウスの各前脛骨(TA)筋に注射した。他のPMOの量は、注射したPMO124の同じ分子数に対して正規化した。2匹のマウスの両方のTA筋に、25μlの最終量(食塩水で希釈)で、各PMO(群あたりn=4)を注射した。注射の2週後に筋肉を採取した。結果を図6A、図6Bおよび図6Cに図示する。
PMO用量の算出:
a)PMO39(配列番号48(18mer))=18.5μg(2匹のマウス、4つのTA)
b)PMO44(配列番号17(25mer))=25.4μg(2匹のマウス、4つのTA)
c)PMO45(配列番号18(25mer))=25.5μg(2匹のマウス、4つのTA)
d)PMO124(28mer)=28.8μg(2匹のマウス、4つのTA)
これらのμg量は、各PMOにつき18×1014個の分子に対応する。
PMO用量の算出:
a)PMO39(配列番号48(18mer))=18.5μg(2匹のマウス、4つのTA)
b)PMO44(配列番号17(25mer))=25.4μg(2匹のマウス、4つのTA)
c)PMO45(配列番号18(25mer))=25.5μg(2匹のマウス、4つのTA)
d)PMO124(28mer)=28.8μg(2匹のマウス、4つのTA)
これらのμg量は、各PMOにつき18×1014個の分子に対応する。
試験した全てのPMOは、in vivoで生物学的に活性であった。スキッピング効率は、PMO124で処理した筋肉において最も高く、PMO45(配列番号18)で処理した筋肉において最も低かった(図6C)。しかしながら、かかる効率は筋肉重量の増加と相関していなかった。PMO45(配列番号18)で処理した筋肉は、未処理の、またはPMO124もしくは44(配列番号17)で処理された筋肉より重かったが、差が有意でなかった(図6B)。
mdxマウスにおけるPMOの全身注射
mdxマウスにおけるPMOの全身注射
また、PMO39(配列番号48)、44(配列番号17)、45(配列番号18)および124を、全身的なスキッピング有効性について試験した。8週齢のmdxマウスにおいて尾静脈内注射を通じてスクリーニングを実施した。PMO124を対照として、200μlの食塩水で希釈した200mg/kgの用量(12.53×1018の分子または20.8μmolに相当)で使用した。他のPMOの量は、注射したPMO124の分子数に対して正規化した。群あたり3匹のマウスを使用した。注射の2週後、横隔膜-DIA、長指伸筋-EDL、腓腹筋-GAS、ヒラメ筋-SOLおよび前脛骨-TAを含む筋肉を回収した。結果を図7A、図7B、図7Cおよび図7Dに図示する。
PMO用量の算出:
a)PMO124(28mer)=200mg/kg(3匹のマウス)
b)PMO45(配列番号18(25mer))=176.2μg(3匹のマウス)
c)PMO44(配列番号17(25mer))=176.8μg(3匹のマウス)
d)PMO39(配列番号48(28mer))=128.6μg(3匹のマウス)
これらのμg量は、各PMOにつき12.53×1018個の分子(20.8μmol)に対応する。
PMO用量の算出:
a)PMO124(28mer)=200mg/kg(3匹のマウス)
b)PMO45(配列番号18(25mer))=176.2μg(3匹のマウス)
c)PMO44(配列番号17(25mer))=176.8μg(3匹のマウス)
d)PMO39(配列番号48(28mer))=128.6μg(3匹のマウス)
これらのμg量は、各PMOにつき12.53×1018個の分子(20.8μmol)に対応する。
スキッピング結果は、1匹のマウスから採取した筋肉間、および異なるマウスからの同じタイプの筋肉間で変動していた(図7Aおよび図7B)。しかしながら、全てのPMOは、1回のIV注射後、ジストロフィーの筋肉において生物学的に活性であった。GASおよびTAは、PMO45(配列番号18)または124の注射後、食塩水を注射されたマウスの、同じタイプの筋肉と比較して、重量が増加する傾向を示した(最終体重に対して正規化、図7D)。
C57マウスにおける、BペプチドコンジュゲートPMOのin vivoスクリーニング
C57マウスにおける、BペプチドコンジュゲートPMOのin vivoスクリーニング
前のin vitroおよびin vivoスクリーニングから選抜されたPMO D30(配列番号16)、PMO39(配列番号48)およびPMO45(配列番号18)を、PMOの3’末端でBペプチド(RAhxRRBRRAhxRRBRAhxB:配列番号3499およびペプチドのカルボキシ末端におけるAhxBリンカー部分)とコンジュゲートさせ、全身尾静脈注射で毎週、14週間にわたり送達した。BペプチドコンジュゲートPMO(以下「BPMO」とも称する)を、12週齢のC57マウス(群あたり10匹のマウス)において実施した。10または20mg/kgの2つの用量で試験した。最終の注射後、握力試験により前肢の筋力を測定した(図9Aおよび図9B)。10mg/kgのBPMOで処理したマウスのTA筋の最大筋力を、in situで電気生理学的に測定した(図9C)。筋肉量およびミオスタチンエクソンスキッピングの評価のため、心臓、DIAおよび4つの骨格筋(EDL、GAS、SOL、TA)を回収した。
20mg/kgのBPMO-39およびBPMO-D30処理群のマウスの何匹かは、尾静脈がほとんど見えなかったため、最後の4~6週の間、IV注射を受けなかった。その代わりに、これらのマウスにはIP注射を行った。BPMO-39、20mg/kgの処理群において、2匹のマウスは、本試験の間に死亡した。
結果:
結果:
1)体重および筋肉量の増加:BPMO-39処理群(10または20mg/kg)におけるマウスの体重は、食塩水およびスクランブルBPMOを注射した動物のいずれの体重と比較しても、有意に増加した(図8Aおよび図8C)。BPMO-D30は、20mg/kgで使用したとき、非常に効果的な体重増加を誘導した(図8C)。投与される投与量および検討した筋肉に依存して、筋肉量の変動(初期体重に対して正規化)が観察された(図8Bおよび図8D)。BPMO-39は、TA(10または20mg/kgの処理、図8Bおよび図8D)およびGAS(10mg/kgの処理、図8B)において最も一貫した筋肉増加を示し、一方、BPMO-D30または-45は、TA(10mg/kgの処理、図8B)またはGAS(20mg/kgの処理、図8D)において質量増加を誘導した。20mg/kgの処理を受けたマウスのDIAでは、試験したBPMOの全てが有意な筋肉重量増加を誘導した(図8D)。最後の数回の注射の際に使用したIP送達経路は、この結果に対する影響を有した可能性がある。
2)握力の分析:前肢力の測定は、両方のBPMO用量で処理したマウスで実施した(図9Aおよび図9B)。BPMO-39は、食塩水群と比較して、また10mg/kgの処理でのみ、筋力強化を示す唯一の候補であった(図9A)。スクランブルBPMOは、予想外にも、また説明不能であるが、10および20mg/kgの用量の両方で、食塩水処理マウスと比較して有意に異なって、その処理マウスの前肢の筋力を増加させた(図9Aおよび図9B)。
3)in situにおける筋肉の生理学的試験:10mg/kgのBPMOで処理したマウスのTAを、電気生理学的評価を使用して分析した。BPMO-D30は、スクランブルPMOおよび他の試験したBPMOと比較して、発生する最大かつ比筋力を有意に増加させた(図9C)。
4)エクソンスキッピングの定量:DIA(図10Aおよび図10B)ならびにTA(図10Cおよび図10D)の筋肉のミオスタチンスキッピング効率を分析した。20mg/kgの処理を受けた筋肉のスキッピングレベルは、10mg/kgで処理した筋肉でのレベルより3~4倍高かった(図10Bおよび図10D)。BPMO-D30および-45は、使用した20mg/kgの用量(DIA、図10BとTA、図10D)または10mg/kgの用量(TA、図10D)では、BPMO-39よりも有意に効率が高かった。
in vivoスクリーニングの暫定的結果:BPMO-D30およびBPMO-45は、筋肉重量、筋力およびエクソンスキッピング効率に対する全体的な効果を考慮して、最も有効な分子であった。(筋線維の断面分析に関する有力なデータとして)組織学的分析を行う。
(実施例25)
BPMOの誘導による二重エクソンスキッピング:ミオスタチンおよびジストロフィンによる組合せ処理
若齢のジストロフィーマウスにおけるジストロフィンリーディングフレームのレスキュー+ミオスタチンのノックダウン。
(実施例25)
BPMOの誘導による二重エクソンスキッピング:ミオスタチンおよびジストロフィンによる組合せ処理
若齢のジストロフィーマウスにおけるジストロフィンリーディングフレームのレスキュー+ミオスタチンのノックダウン。
PMO M23D(配列番号937)を、PMOの3’末端においてBペプチド(RAhxRRBRRAhxRRBRAhxB:配列番号3499およびペプチドのカルボキシ末端のAhxBリンカー部分)とコンジュゲートさせ、BPMO-M23Dと命名した。BPMO-M23D(10mg/kg)および/またはBPMO-MSTN(D30、10mg/kg)を200μlの食塩水で希釈し、6週齢のmdxマウスまたはC57BL10マウスの尾静脈を通して注射した。10週間にわたり、注射を毎週繰り返した。10匹のマウスを各処理に使用した。5つのマウスの群の詳細は以下の通りである:
a)C57BL10マウス+食塩水(陽性対照)
b)Mdxマウス+食塩水(陰性対照)
c)Mdxマウス+BPMO-M23D(配列番号937)(10mg/kg)
d)Mdxマウス+BPMO-M23D(配列番号937)(10mg/kg)およびBPMO-MSTN(配列番号16)(10mg/kg)
e)Mdxマウス+BPMO-MSTN(配列番号16)(10mg/kg)
結果:
a)C57BL10マウス+食塩水(陽性対照)
b)Mdxマウス+食塩水(陰性対照)
c)Mdxマウス+BPMO-M23D(配列番号937)(10mg/kg)
d)Mdxマウス+BPMO-M23D(配列番号937)(10mg/kg)およびBPMO-MSTN(配列番号16)(10mg/kg)
e)Mdxマウス+BPMO-MSTN(配列番号16)(10mg/kg)
結果:
12週間の処理の後、処理を受けたmdxマウスにおいて、食塩水を注射された動物と比較した体重の有意な増加が観察されなかった(図11A)。前肢の筋力を測定する握力分析は、BPMO-M23Dの注射が、mdxマウスと比較して、筋力の有意な増加を誘導する一方、BPMO-M23DおよびBPMO-MSTNの共注射は、筋力をC57マウスの筋力に対して正常化したことを明らかにした(図11B)。BPMO-MSTN処理単独では、食塩水を注射されたmdxマウスと比較して、処理を受けたマウスの筋力を変化させなかった(図11B)。上で報告された握力試験を、以下の通りにさらに実施した。3日連続で(アクティビティケージ評価に従い)試験を実施した。各試験では、5回の読取値/マウスの値を記録した。各値は、2回の読取値間のインターバルを30秒間とし、30秒以内に測定される前肢の筋力の最も高い値とした。合計15回の読取値/マウス(図18A)として、または、3×5回の読取値の平均/マウス/試験(図18B)として、または、3×5回の読取値の最高値/マウス/試験(図18C)としてデータを示す。統計解析は、一方向分散分析およびボンフェローニ事後検定(群あたりn=10)により行った。エラーバーは、SEMを表す。
BPMO-M23D処理は、単独で、またはBPMO-MSTNとの組合せで、心臓における約25%のスキッピングを除き、分析した全ての筋肉において、70~80%のジストロフィン再フレーミングとなる非常に効率的なジストロフィンエクソンスキッピングを誘導した(図12A)。BPMO-MSTNとBPMO-M23Dとの組合せによる処理は、BPMO-M23D単独による処理よりも、高いDMDエクソンスキッピング効率をもたらした。次にジストロフィンタンパク質の回復をウェスタンブロット解析により確認し、骨格筋での発現はC57マウスのレベルの30~100%の間の範囲のであった(図12B)。免疫組織化学によりジストロフィン発現を再確認した。ミオスタチンエクソン2のスキッピングは、二重処理を受けたマウスにおいても効率的であり、試験した全ての筋肉において、平均スキッピングが約55%であった(図12C)。
筋線維肥大および再生に対する処理の効果を試験するため、採取した筋肉においてさらなる組織学的分析を実施した。中心核線維の頻度に加え、筋線維の数および直径を調査した。EDL、GAS、SOLおよびTA筋における治療的利益を評価した。TA線維分析の結果を代表として報告する(図13Aおよび図13B)。BPMO-MSTN単独による処理は、ジストロフィーの表現型を変化させなかったが、BPMO-M23DおよびBPMO-M23D+BPMO-D30処理は、未処理のmdxの筋肉と比較して、筋線維の断面領域の変動(図13A)および中心核線維の存在(図13B)の減少により病変を部分的に改善した。この効果は、基本的に、mdxの筋肉の偽性肥大および筋肉の変性プロセスの両方を低下させるジストロフィンの回復に起因するものであった。
老齢のmdxマウスにおけるミオスタチンのジストロフィンリーディングフレームのレスキュー+ノックダウン
老齢のmdxマウスにおけるミオスタチンのジストロフィンリーディングフレームのレスキュー+ノックダウン
BPMO-MSTNおよびBPMO-M23Dを、上で報告したように、同一の用量レジメンおよび投与経路を使用して、ヒトで観察されるジストロフィー疾患を(若齢のmdxマウスと比較して)より正確に再現する老齢(>18カ月齢)のmdxマウスに注射した。10mg/kgのBPMO-M23D(n=5)またはBPMOM23D(10mg/kg)とBPMO-MSTN(10mg/kg)(n=5)または、20mg/kgのスクランブルBPMO(n=4)により、週1回で10週間、マウスに注射した。最終の注射の1週後、前肢の筋力を調査するため、マウスの握力分析を行った。筋肉を採取する前に、処理を受けたマウスのTA筋を、次の週に電気生理学的に分析した。
結果:
結果:
処理を受けたマウスの体重の(スクランブル群と比較した)有意な変化が、7週目以降に観察された(図14A)。スクランブル、BPMO-M23DおよびBPMO-M23D+BPMO-MSTNで処理したマウスの、DIA、EDL、GAS、SOL、TAおよび心筋の筋肉量を試験した(図14B)。しかしながら、スクランブルを注射したマウスが徐々に死亡し、本試験終了時には1匹のマウスしか生存しなかったため、体重または筋肉重量に関する統計解析は行わなかった。BPMO-M23Dで、またはBPMO-M23D+BPMO-MSTNで処理したマウスは全て、試験期間中生存した。握力分析は、BPMO-M23Dで、またはBPMO-M23D+BPMO-MSTNで処理されたマウスが、スクランブルBPMOで処理されたマウスよりも強いことを示した(図14C)。単一処理と二重処理との間の、TA筋の最大および比筋力をさらに比較した結果、組合せ処理群において良好な効果が見られ、筋肉損傷性の延長収縮(伸張性収縮)に対する抵抗力の有意な改善が示された(図14D)。
次に、全ての筋肉においてジストロフィン再フレーミングの顕著なレベルを示したジストロフィンのエクソン23のスキッピング効率を評価するため、RT-PCRを実施した(図15A)。若齢のmdxマウスで観察されるように、BPMO-MSTNの追加により一貫してBPMO-M23Dのスキッピング効率が上昇した(図15B)。ジストロフィンエクソンスキッピングの結果は、分析した全ての筋肉におけるタンパク質発現の有意な増加と相関していた(図16A)。さらに、BPMO-MSTNとBPMO-M23Dとの組合せによる処理が、M23D単独による処理よりもジストロフィンレベルを上昇させることが示された(図16B)。
採取した全ての筋肉におけるミオスタチンエクソン2のスキッピングを、RT-PCRにより評価した(図17A)。スキッピングのレベルは、分析した筋肉のタイプに応じて5%~40%の間で変動した。全ての筋肉の結果を総合して得られる平均値は約20%であった(図17B)。
上に明示した開示は、独立した有用性を伴う少なくとも1つの別個の発明を含むと考えられる。本発明は、例示的な形態で開示されているが、多くの変形が可能であるため、本明細書に開示および例示される通りのその特定の実施形態は、限定的な意味で考慮されるべきでない。多様な実施形態、材料、組成物および方法の均等な変更、修飾およびバリエーションが、本発明の範囲内で実質的に類似の結果をもたらす態様で実施され得る。本発明の主題は、本明細書で開示される様々な要素、特徴、機能および/または特性の全ての新規かつ非自明な組合せおよびサブコンビネーションを包含する。
本明細書では、特定の実施形態に関する利益、他の利点および課題解決手段を記載した。しかしながら、利益、利点、課題解決手段、および任意の利益、利点、または解決手段をもたらすまたはより明らかにし得る任意の要素または要素の組合せは、本発明のいずれかまたは全ての請求項の決定的な、必要な、または不可欠な特徴または要素として解釈されるべきでない。本発明の範囲内における多くの変更および修飾は、全てのそのような修飾を包含する。下記の特許請求の範囲における、全ての要素の対応する構造、材料、操作および均等物は、具体的に特許請求された通りの他の請求項の要素と組み合わせて機能を発揮するあらゆる構造、材料または操作を包含することを意図するものである。本発明の範囲は、上記で示される実施例よりはむしろ、添付の特許請求の範囲およびそれらの法的均等物により決定されるべきである。
実施形態では、本明細書で記載される通りの修飾アンチセンスオリゴマーのいずれかにおけるいかなるウラシル(U)またはチミン(T)ヌクレオチドも、Xまたはnで置換され得る。実施形態では、各Xまたはnは、ウラシル(U)またはチミン(T)から独立に選択される。
Claims (1)
- 明細書に記載の発明。
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201562239812P | 2015-10-09 | 2015-10-09 | |
| US62/239,812 | 2015-10-09 | ||
| PCT/US2016/056093 WO2017062835A2 (en) | 2015-10-09 | 2016-10-07 | Compositions and methods for treating duchenne muscular dystrophy and related disorders |
| JP2018517603A JP2018530560A (ja) | 2015-10-09 | 2016-10-07 | デュシェンヌ型筋ジストロフィーおよび関連障害の処置のための組成物および方法 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018517603A Division JP2018530560A (ja) | 2015-10-09 | 2016-10-07 | デュシェンヌ型筋ジストロフィーおよび関連障害の処置のための組成物および方法 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2022017594A true JP2022017594A (ja) | 2022-01-25 |
Family
ID=58488705
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018517603A Withdrawn JP2018530560A (ja) | 2015-10-09 | 2016-10-07 | デュシェンヌ型筋ジストロフィーおよび関連障害の処置のための組成物および方法 |
| JP2021185544A Pending JP2022017594A (ja) | 2015-10-09 | 2021-11-15 | デュシェンヌ型筋ジストロフィーおよび関連障害の処置のための組成物および方法 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018517603A Withdrawn JP2018530560A (ja) | 2015-10-09 | 2016-10-07 | デュシェンヌ型筋ジストロフィーおよび関連障害の処置のための組成物および方法 |
Country Status (9)
| Country | Link |
|---|---|
| US (1) | US20190177723A1 (ja) |
| EP (2) | EP3359668A4 (ja) |
| JP (2) | JP2018530560A (ja) |
| CN (1) | CN108699555A (ja) |
| BR (1) | BR112018007066A2 (ja) |
| EA (1) | EA201890908A1 (ja) |
| IL (2) | IL258069A (ja) |
| MA (1) | MA45819A (ja) |
| WO (1) | WO2017062835A2 (ja) |
Families Citing this family (55)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ES2852549T3 (es) | 2005-02-09 | 2021-09-13 | Sarepta Therapeutics Inc | Composición antisentido para tratamiento de la atrofia muscular |
| TWI541024B (zh) | 2010-09-01 | 2016-07-11 | 日本新藥股份有限公司 | 反義核酸 |
| US20130085139A1 (en) | 2011-10-04 | 2013-04-04 | Royal Holloway And Bedford New College | Oligomers |
| MA41795A (fr) | 2015-03-18 | 2018-01-23 | Sarepta Therapeutics Inc | Exclusion d'un exon induite par des composés antisens dans la myostatine |
| US20190262375A1 (en) * | 2016-06-30 | 2019-08-29 | Sarepta Therapeutics, Inc. | Exon skipping oligomers for muscular dystrophy |
| CN109757108A (zh) * | 2016-07-05 | 2019-05-14 | 比奥马林技术公司 | 具有治疗遗传疾病的改善特征的包含双环支架部分的前体mRNA剪接转换或调节寡核苷酸 |
| KR102646318B1 (ko) | 2016-12-19 | 2024-03-12 | 사렙타 쎄러퓨틱스 인코퍼레이티드 | 근육 이상증에 대한 엑손 스킵핑 올리고머 결합체 |
| KR102810425B1 (ko) * | 2016-12-19 | 2025-05-21 | 사렙타 쎄러퓨틱스 인코퍼레이티드 | 근육 이상증에 대한 엑손 스킵핑 올리고머 결합체 |
| HRP20240705T1 (hr) * | 2016-12-19 | 2024-08-30 | Sarepta Therapeutics, Inc. | Oligomerni konjugati koji preskaču egzon za mišićnu distrofiju |
| AR112538A1 (es) * | 2017-08-31 | 2019-11-06 | Sarepta Therapeutics Inc | Métodos para el tratamiento de distrofia muscular |
| EA201991450A1 (ru) * | 2017-09-22 | 2019-12-30 | Сарепта Терапьютикс, Инк. | Конъюгаты олигомеров для пропуска экзона при мышечной дистрофии |
| TWI812647B (zh) * | 2017-09-25 | 2023-08-21 | 美商薩羅塔治療公司 | 經由速流合成以製備磷醯二胺嗎啉代寡聚物之製程 |
| US20200384084A1 (en) | 2017-12-01 | 2020-12-10 | Merus N.V. | Use of bispecific antibody and il-15 for combination therapy |
| BR112020015617A2 (pt) * | 2018-01-31 | 2021-01-05 | The Board Of Regents Of The University Of Texas System | Composições e métodos para correção de mutações da distrofina em cardiomiócitos humanos |
| BR112020020670A2 (pt) | 2018-04-12 | 2021-03-02 | Wave Life Sciences Ltd. | composição de oligonucleotídeo, composição farmacêutica, método para alterar o splicing de uma transcrição alvo, método para tratar distrofia muscular, método para preparar um oligonucleotídeo ou uma composição de oligonucleotídeo do mesmo e oligonucleotídeo |
| EP3784248A4 (en) * | 2018-04-26 | 2022-08-10 | Sarepta Therapeutics, Inc. | EXON-SKIPPING OLIGOMERS AND OLIGOMER CONJUGATES FOR MUSCULAR DYSTROPHY |
| TWI844541B (zh) * | 2018-05-11 | 2024-06-11 | 新加坡商波濤生命科學有限公司 | 寡核苷酸組成物及其使用方法 |
| US10765760B2 (en) * | 2018-05-29 | 2020-09-08 | Sarepta Therapeutics, Inc. | Exon skipping oligomer conjugates for muscular dystrophy |
| EP3806868A4 (en) * | 2018-06-13 | 2022-06-22 | Sarepta Therapeutics, Inc. | EXON SKIPPING OLIGOMERS FOR MUSCULAR DYSTROPHY |
| WO2019241385A2 (en) * | 2018-06-13 | 2019-12-19 | Sarepta Therapeutics, Inc. | Exon skipping oligomers for muscular dystropy |
| WO2019241470A2 (en) * | 2018-06-14 | 2019-12-19 | Sarepta Therapeutics, Inc. | Exon skipping oligomers and oligomer conjugates for muscular dystrophy |
| TW202449155A (zh) * | 2018-07-27 | 2024-12-16 | 美商薩羅塔治療公司 | 用於肌肉萎縮症之外顯子跳躍寡聚物 |
| US12018087B2 (en) | 2018-08-02 | 2024-06-25 | Dyne Therapeutics, Inc. | Muscle-targeting complexes comprising an anti-transferrin receptor antibody linked to an oligonucleotide and methods of delivering oligonucleotide to a subject |
| AU2019316103B2 (en) | 2018-08-02 | 2026-02-19 | Dyne Therapeutics, Inc. | Muscle targeting complexes and uses thereof for treating facioscapulohumeral muscular dystrophy |
| US11168141B2 (en) | 2018-08-02 | 2021-11-09 | Dyne Therapeutics, Inc. | Muscle targeting complexes and uses thereof for treating dystrophinopathies |
| WO2020028832A1 (en) | 2018-08-02 | 2020-02-06 | Dyne Therapeutics, Inc. | Muscle targeting complexes and uses thereof for treating dystrophinopathies |
| GB201812972D0 (en) | 2018-08-09 | 2018-09-26 | Univ Oxford Innovation Ltd | Cell-penetrating peptides |
| GB201812980D0 (en) | 2018-08-09 | 2018-09-26 | Univ Oxford Innovation Ltd | Cell-penetrating peptides |
| EP3874044A1 (en) * | 2018-11-02 | 2021-09-08 | BioMarin Technologies B.V. | Bispecific antisense oligonucleotides for dystrophin exon skipping |
| AU2019392928A1 (en) * | 2018-12-06 | 2021-06-17 | Wave Life Sciences Ltd. | Oligonucleotide compositions and methods thereof |
| EP3890783A1 (en) | 2018-12-07 | 2021-10-13 | Oxford University Innovation Limited | Linkers |
| SG11202104960PA (en) * | 2018-12-13 | 2021-06-29 | Sarepta Therapeutics Inc | Exon skipping oligomer conjugates for muscular dystrophy |
| GB201821269D0 (en) * | 2018-12-28 | 2019-02-13 | Nippon Shinyaku Co Ltd | Myostatin signal inhibitor |
| US12215382B2 (en) | 2019-03-01 | 2025-02-04 | The General Hospital Corporation | Liver protective MARC variants and uses thereof |
| WO2020209285A1 (ja) * | 2019-04-08 | 2020-10-15 | 国立大学法人東京医科歯科大学 | 筋疾患治療用医薬組成物 |
| EP3959319A4 (en) | 2019-04-25 | 2023-06-07 | Avidity Biosciences, Inc. | NUCLEIC ACID COMPOSITIONS AND METHODS FOR MULTI-EXON SKIPPING |
| BR112021022208A2 (pt) * | 2019-05-06 | 2022-01-11 | Antisense Therapeutics Ltd | Métodos para tratamento de distrofia muscular usando oligonucleotídeos inibidores para cd49d |
| US20220282247A1 (en) * | 2019-08-02 | 2022-09-08 | Research Institute At Nationwide Children's Hospital | Exon 44-targeted nucleic acids and recombinant adeno-associated virus comprising said nucleic acids for treatment of dystrophin-based myopathies |
| AU2020368539A1 (en) | 2019-10-16 | 2022-04-28 | Massachusetts Institute Of Technology | Engineered muscle targeting compositions |
| CN115348883B (zh) * | 2019-11-27 | 2024-11-15 | 诺华股份有限公司 | 用于治疗杜兴氏肌营养不良症的化合物和方法 |
| AU2020411964A1 (en) * | 2019-12-26 | 2022-06-16 | National Center Of Neurology And Psychiatry | Antisense nucleic acid that induces skipping of exon 50 |
| UY39444A (es) * | 2020-09-30 | 2022-04-29 | Biomarin Tech Bv | Oligonucleótido |
| EP4299743A4 (en) * | 2021-02-26 | 2025-01-29 | KNC Laboratories Co., Ltd. | NUCLEIC ACID MEDICINAL PRODUCT EXPRESSING A SPLICE VARIANT OF MYOSTATIN |
| WO2022192749A2 (en) * | 2021-03-12 | 2022-09-15 | Pepgen Inc. | Methods of treating duchenne muscular dystrophy using peptide-oligonucleotide conjugates |
| US11638761B2 (en) | 2021-07-09 | 2023-05-02 | Dyne Therapeutics, Inc. | Muscle targeting complexes and uses thereof for treating Facioscapulohumeral muscular dystrophy |
| JP2024525608A (ja) | 2021-07-09 | 2024-07-12 | ダイン セラピューティクス,インコーポレーテッド | ジストロフィン異常症を処置するための筋標的化複合体および製剤 |
| US11969475B2 (en) | 2021-07-09 | 2024-04-30 | Dyne Therapeutics, Inc. | Muscle targeting complexes and uses thereof for treating facioscapulohumeral muscular dystrophy |
| US11771776B2 (en) | 2021-07-09 | 2023-10-03 | Dyne Therapeutics, Inc. | Muscle targeting complexes and uses thereof for treating dystrophinopathies |
| JP2025509438A (ja) * | 2022-03-17 | 2025-04-11 | サレプタ セラピューティクス, インコーポレイテッド | ホスホロジアミデートモルホリノオリゴマーコンジュゲート |
| US12071621B2 (en) | 2022-04-05 | 2024-08-27 | Avidity Biosciences, Inc. | Anti-transferrin receptor antibody-PMO conjugates for inducing DMD exon 44 skipping |
| IL316143A (en) | 2022-04-15 | 2024-12-01 | Dyne Therapeutics Inc | Muscle targeting complexes and formulations for the treatment of myotonic dystrophy |
| US20250288641A1 (en) * | 2022-04-27 | 2025-09-18 | The Curators Of The University Of Missouri | Micro-dystrophin for heart protection |
| WO2025072246A1 (en) * | 2023-09-26 | 2025-04-03 | Entrada Therapeutics, Inc. | Compounds and methods for skipping exon 50 in duchenne muscular dystrophy |
| CN120648680A (zh) * | 2024-03-15 | 2025-09-16 | 迦进生物医药(上海)有限公司 | 治疗杜兴型肌营养不良症和贝克型肌营养不良症的药物 |
| WO2025262186A2 (en) * | 2024-06-20 | 2025-12-26 | MAX-PLANCK-Gesellschaft zur Förderung der Wissenschaften e.V. | Therapeutic oligonucleotides for treating diseases being associated with or caused by a missense, nonsense or in-frame indel mutation |
Family Cites Families (118)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4534899A (en) | 1981-07-20 | 1985-08-13 | Lipid Specialties, Inc. | Synthetic phospholipid compounds |
| US4426330A (en) | 1981-07-20 | 1984-01-17 | Lipid Specialties, Inc. | Synthetic phospholipid compounds |
| AU5661386A (en) | 1985-03-15 | 1986-10-13 | Stirchak, E. | Stereoregular polynucleotide-binding polymers |
| US5506337A (en) | 1985-03-15 | 1996-04-09 | Antivirals Inc. | Morpholino-subunit combinatorial library and method |
| US5166315A (en) | 1989-12-20 | 1992-11-24 | Anti-Gene Development Group | Sequence-specific binding polymers for duplex nucleic acids |
| US5217866A (en) | 1985-03-15 | 1993-06-08 | Anti-Gene Development Group | Polynucleotide assay reagent and method |
| US5185444A (en) | 1985-03-15 | 1993-02-09 | Anti-Gene Deveopment Group | Uncharged morpolino-based polymers having phosphorous containing chiral intersubunit linkages |
| US5521063A (en) | 1985-03-15 | 1996-05-28 | Antivirals Inc. | Polynucleotide reagent containing chiral subunits and methods of use |
| US5034506A (en) | 1985-03-15 | 1991-07-23 | Anti-Gene Development Group | Uncharged morpholino-based polymers having achiral intersubunit linkages |
| US5354844A (en) | 1989-03-16 | 1994-10-11 | Boehringer Ingelheim International Gmbh | Protein-polycation conjugates |
| US5108921A (en) | 1989-04-03 | 1992-04-28 | Purdue Research Foundation | Method for enhanced transmembrane transport of exogenous molecules |
| US5227170A (en) | 1989-06-22 | 1993-07-13 | Vestar, Inc. | Encapsulation process |
| US5013556A (en) | 1989-10-20 | 1991-05-07 | Liposome Technology, Inc. | Liposomes with enhanced circulation time |
| US5356633A (en) | 1989-10-20 | 1994-10-18 | Liposome Technology, Inc. | Method of treatment of inflamed tissues |
| US5527528A (en) | 1989-10-20 | 1996-06-18 | Sequus Pharmaceuticals, Inc. | Solid-tumor treatment method |
| US5469854A (en) | 1989-12-22 | 1995-11-28 | Imarx Pharmaceutical Corp. | Methods of preparing gas-filled liposomes |
| US5580575A (en) | 1989-12-22 | 1996-12-03 | Imarx Pharmaceutical Corp. | Therapeutic drug delivery systems |
| US5264618A (en) | 1990-04-19 | 1993-11-23 | Vical, Inc. | Cationic lipids for intracellular delivery of biologically active molecules |
| JP3220180B2 (ja) | 1991-05-23 | 2001-10-22 | 三菱化学株式会社 | 薬剤含有タンパク質結合リポソーム |
| US5719262A (en) | 1993-11-22 | 1998-02-17 | Buchardt, Deceased; Ole | Peptide nucleic acids having amino acid side chains |
| US5539082A (en) | 1993-04-26 | 1996-07-23 | Nielsen; Peter E. | Peptide nucleic acids |
| US5714331A (en) | 1991-05-24 | 1998-02-03 | Buchardt, Deceased; Ole | Peptide nucleic acids having enhanced binding affinity, sequence specificity and solubility |
| WO1993001286A2 (en) | 1991-06-28 | 1993-01-21 | Massachusetts Institute Of Technology | Localized oligonucleotide therapy |
| US5521291A (en) | 1991-09-30 | 1996-05-28 | Boehringer Ingelheim International, Gmbh | Conjugates for introducing nucleic acid into higher eucaryotic cells |
| NZ244306A (en) | 1991-09-30 | 1995-07-26 | Boehringer Ingelheim Int | Composition for introducing nucleic acid complexes into eucaryotic cells, complex containing nucleic acid and endosomolytic agent, peptide with endosomolytic domain and nucleic acid binding domain and preparation |
| FR2692265B1 (fr) | 1992-05-25 | 1996-11-08 | Centre Nat Rech Scient | Composes biologiquement actifs de type phosphotriesters. |
| US6005079A (en) | 1992-08-21 | 1999-12-21 | Vrije Universiteit Brussels | Immunoglobulins devoid of light chains |
| EP1498427B1 (en) | 1992-08-21 | 2009-12-16 | Vrije Universiteit Brussel | Immunoglobulins devoid of light chains |
| US5583020A (en) | 1992-11-24 | 1996-12-10 | Ribozyme Pharmaceuticals, Inc. | Permeability enhancers for negatively charged polynucleotides |
| JP3351476B2 (ja) | 1993-01-22 | 2002-11-25 | 三菱化学株式会社 | リン脂質誘導体及びそれを含有するリポソーム |
| US5395619A (en) | 1993-03-03 | 1995-03-07 | Liposome Technology, Inc. | Lipid-polymer conjugates and liposomes |
| US5994618A (en) | 1997-02-05 | 1999-11-30 | Johns Hopkins University School Of Medicine | Growth differentiation factor-8 transgenic mice |
| ES2201076T3 (es) | 1993-03-19 | 2004-03-16 | The Johns Hopkins University School Of Medicine | Factor-8 de diferenciacion del crecimiento. |
| US5462854A (en) | 1993-04-19 | 1995-10-31 | Beckman Instruments, Inc. | Inverse linkage oligonucleotides for chemical and enzymatic processes |
| DK0698097T3 (da) | 1993-04-29 | 2001-10-08 | Unilever Nv | Produktion af antistoffer eller (funktionaliserede) fragmenter deraf afledt af Camelidae-immunoglobuliner med tung kæde |
| FR2705099B1 (fr) | 1993-05-12 | 1995-08-04 | Centre Nat Rech Scient | Oligonucléotides phosphorothioates triesters et procédé de préparation. |
| US5534259A (en) | 1993-07-08 | 1996-07-09 | Liposome Technology, Inc. | Polymer compound and coated particle composition |
| US5543158A (en) | 1993-07-23 | 1996-08-06 | Massachusetts Institute Of Technology | Biodegradable injectable nanoparticles |
| US5417978A (en) | 1993-07-29 | 1995-05-23 | Board Of Regents, The University Of Texas System | Liposomal antisense methyl phosphonate oligonucleotides and methods for their preparation and use |
| US5595756A (en) | 1993-12-22 | 1997-01-21 | Inex Pharmaceuticals Corporation | Liposomal compositions for enhanced retention of bioactive agents |
| US5543152A (en) | 1994-06-20 | 1996-08-06 | Inex Pharmaceuticals Corporation | Sphingosomes for enhanced drug delivery |
| US5591721A (en) | 1994-10-25 | 1997-01-07 | Hybridon, Inc. | Method of down-regulating gene expression |
| US5512295A (en) | 1994-11-10 | 1996-04-30 | The Board Of Trustees Of The Leland Stanford Junior University | Synthetic liposomes for enhanced uptake and delivery |
| US5707618A (en) | 1995-03-24 | 1998-01-13 | Genzyme Corporation | Adenovirus vectors for gene therapy |
| DK2111876T3 (da) | 1995-12-18 | 2011-12-12 | Angiodevice Internat Gmbh | Tværbundne polymerpræparater og fremgangsmåder til anvendelse deraf |
| US6245747B1 (en) | 1996-03-12 | 2001-06-12 | The Board Of Regents Of The University Of Nebraska | Targeted site specific antisense oligodeoxynucleotide delivery method |
| WO1999002667A1 (en) * | 1997-07-14 | 1999-01-21 | University Of Liege | Mutations in the myostation gene cause double-muscling in mammals |
| US7572582B2 (en) | 1997-09-12 | 2009-08-11 | Exiqon A/S | Oligonucleotide analogues |
| US6794499B2 (en) | 1997-09-12 | 2004-09-21 | Exiqon A/S | Oligonucleotide analogues |
| US7084125B2 (en) | 1999-03-18 | 2006-08-01 | Exiqon A/S | Xylo-LNA analogues |
| AU776362B2 (en) | 1999-05-04 | 2004-09-09 | Roche Innovation Center Copenhagen A/S | L-ribo-LNA analogues |
| US6284882B1 (en) | 1999-06-10 | 2001-09-04 | Abbott Laboratories | Myostatin gene promoter and inhibition of activation thereof |
| US6287860B1 (en) | 2000-01-20 | 2001-09-11 | Isis Pharmaceuticals, Inc. | Antisense inhibition of MEKK2 expression |
| EP1191097A1 (en) | 2000-09-21 | 2002-03-27 | Leids Universitair Medisch Centrum | Induction of exon skipping in eukaryotic cells |
| US20050124566A1 (en) | 2001-05-18 | 2005-06-09 | Sirna Therapeutics, Inc. | RNA interference mediated inhibition of myostatin gene expression using short interfering nucleic acid (siNA) |
| CA2459347C (en) | 2001-09-04 | 2012-10-09 | Exiqon A/S | Locked nucleic acid (lna) compositions and uses thereof |
| US6965025B2 (en) | 2001-12-10 | 2005-11-15 | Isis Pharmaceuticals, Inc. | Antisense modulation of connective tissue growth factor expression |
| KR100464261B1 (ko) | 2002-01-24 | 2005-01-03 | 주식회사 파나진 | Pna 올리고머를 합성하기 위한 신규한 단량체 및 그의제조방법 |
| KR20030084444A (ko) | 2002-04-26 | 2003-11-01 | 주식회사 파나진 | Pna 올리고머를 합성하기 위한 신규한 단량체 및 그의제조방법 |
| US7569575B2 (en) | 2002-05-08 | 2009-08-04 | Santaris Pharma A/S | Synthesis of locked nucleic acid derivatives |
| WO2004044140A2 (en) | 2002-11-05 | 2004-05-27 | Isis Pharmaceticals, Inc. | 2’-substituted oligomeric compounds and compositions for use in gene modulations |
| AU2003225410A1 (en) | 2003-03-21 | 2004-10-11 | Academisch Ziekenhuis Leiden | Modulation of exon recognition in pre-mrna by interfering with the secondary rna structure |
| ES2351976T3 (es) * | 2003-04-29 | 2011-02-14 | Avi Biopharma, Inc. | Composiciones para mejorar el transporte y la eficacia antisentido de análogos de ácidos nucleicos en células. |
| US7211668B2 (en) | 2003-07-28 | 2007-05-01 | Panagene, Inc. | PNA monomer and precursor |
| SI2206781T1 (sl) | 2004-06-28 | 2016-05-31 | The University Of Western Australia | Protismiselni oligonukleotidi za induciranje preskakovanja eksona in postopki njihove uporabe |
| US7838657B2 (en) | 2004-12-03 | 2010-11-23 | University Of Massachusetts | Spinal muscular atrophy (SMA) treatment via targeting of SMN2 splice site inhibitory sequences |
| NZ538097A (en) | 2005-02-07 | 2006-07-28 | Ovita Ltd | Method and compositions for improving wound healing |
| ES2852549T3 (es) * | 2005-02-09 | 2021-09-13 | Sarepta Therapeutics Inc | Composición antisentido para tratamiento de la atrofia muscular |
| CA2605512A1 (en) | 2005-04-22 | 2006-10-26 | Academisch Ziekenhuis Leiden | Modulation of exon recognition in pre-mrna by interfering with the binding of sr proteins and by interfering with secondary rna structure. |
| BRPI0610248A2 (pt) | 2005-04-25 | 2010-06-08 | Pfizer | anticorpos contra miostatina, composição farmacêutica compreendendo os mesmos, linhas celulares que os produzem , moléculas de ácido nucleico codificantes dos mesmos bem como seus usos |
| CA2538208A1 (en) | 2005-05-04 | 2006-11-04 | Universite Laval | Modulation of myostatin and use thereof in cell transplantation-based treatment of muscle disease |
| DE202005008426U1 (de) | 2005-05-31 | 2005-09-15 | Ricon Sieb Und Foerdertechnik | Fördervorrichtung mit Fördertuch |
| US8361977B2 (en) | 2005-06-23 | 2013-01-29 | Isis Pharmaceuticals, Inc. | Compositions and methods for modulation of SMN2 splicing |
| WO2007003216A1 (en) | 2005-07-06 | 2007-01-11 | Universidad Autónoma de Madrid | Anti-ccr7 receptor antibodies for the treatment of cancer |
| ES2657400T3 (es) | 2006-05-10 | 2018-03-05 | Sarepta Therapeutics, Inc. | Análogos de oligonucleótidos que tienen enlaces intersubunitarios catiónicos |
| EP1857548A1 (en) | 2006-05-19 | 2007-11-21 | Academisch Ziekenhuis Leiden | Means and method for inducing exon-skipping |
| US8097596B2 (en) * | 2006-06-30 | 2012-01-17 | Lakewood-Amedex, Inc. | Compositions and methods for the treatment of muscle wasting |
| WO2008088895A2 (en) | 2007-01-18 | 2008-07-24 | University Of Missouri-Columbia | Synthetic mini/micro-dystrophin genes to restore nnos to the sarcolemma |
| TW201940502A (zh) | 2007-02-02 | 2019-10-16 | 美商艾瑟勒朗法瑪公司 | 衍生自ActRIIB的變體與其用途 |
| US20100016215A1 (en) | 2007-06-29 | 2010-01-21 | Avi Biopharma, Inc. | Compound and method for treating myotonic dystrophy |
| AU2008271050B2 (en) * | 2007-06-29 | 2014-11-06 | Sarepta Therapeutics, Inc. | Tissue specific peptide conjugates and methods |
| WO2009008725A2 (en) | 2007-07-12 | 2009-01-15 | Prosensa Technologies B.V. | Molecules for targeting compounds to various selected organs, tissues or tumor cells |
| US7935816B2 (en) | 2007-10-25 | 2011-05-03 | Gene Tools, Llc | Molecular transporter compositions comprising dendrimeric oligoguanidine with a triazine core that facilitate delivery into cells in vivo |
| DK2203173T3 (en) | 2007-10-26 | 2016-02-29 | Academisch Ziekenhuis Leiden | Materials and methods for prevention of muscle diseases |
| US8076476B2 (en) | 2007-11-15 | 2011-12-13 | Avi Biopharma, Inc. | Synthesis of morpholino oligomers using doubly protected guanine morpholino subunits |
| CA2884340C (en) | 2007-11-15 | 2017-07-25 | Sarepta Therapeutics, Inc. | Method of synthesis of morpholino oligomers |
| CA2711302C (en) | 2008-01-04 | 2016-11-08 | Cue Acoustics, Inc. | Audio device with integrated switching power supply |
| EP2119783A1 (en) | 2008-05-14 | 2009-11-18 | Prosensa Technologies B.V. | Method for efficient exon (44) skipping in Duchenne Muscular Dystrophy and associated means |
| US8236557B2 (en) | 2008-05-28 | 2012-08-07 | University Of Missouri-Columbia | Hybrid-AAV vectors to deliver large gene expression cassette |
| LT3750552T (lt) | 2008-08-14 | 2023-06-26 | Acceleron Pharma Inc. | Gdf gaudyklės |
| US8084601B2 (en) | 2008-09-11 | 2011-12-27 | Royal Holloway And Bedford New College Royal Holloway, University Of London | Oligomers |
| EP2762567B1 (en) | 2008-10-24 | 2016-07-13 | Sarepta Therapeutics, Inc. | Multiple exon skipping compositions for DMD |
| CN102625840A (zh) | 2009-04-10 | 2012-08-01 | 肌肉学研究协会 | 用于治疗疾病的三环dna反义寡核苷酸、组合物和方法 |
| WO2010120820A1 (en) | 2009-04-13 | 2010-10-21 | Isis Pharmaceuticals, Inc. | Compositions and methods for modulation of smn2 splicing |
| ES2593836T3 (es) | 2009-04-24 | 2016-12-13 | Biomarin Technologies B.V. | Oligonucleótido que comprende una inosina para tratar la DMD |
| EA027071B1 (ru) | 2009-04-27 | 2017-06-30 | Новартис Аг | АНТИТЕЛО К ActRIIB И СОДЕРЖАЩАЯ ЕГО КОМПОЗИЦИЯ |
| WO2010129406A2 (en) * | 2009-05-04 | 2010-11-11 | The Johns Hopkins University | Methods of promoting muscle growth |
| PT3449926T (pt) | 2009-06-17 | 2019-11-12 | Cold Spring Harbor Laboratory | Composições e métodos de modulação de excisões de smn2 em um sujeito |
| SMT201800579T1 (it) | 2009-11-12 | 2019-01-11 | Univ Western Australia | Molecole antisenso e metodi per trattare patologie |
| US8802642B2 (en) | 2010-04-28 | 2014-08-12 | Iowa State University Research Foundation, Inc. | Spinal muscular atrophy treatment via targeting SMN2 catalytic core |
| JP2013530154A (ja) | 2010-05-28 | 2013-07-25 | サレプタ セラピューティクス, インコーポレイテッド | 修飾されたサブユニット間結合および/または末端基を有するオリゴヌクレオチドアナログ |
| TWI541024B (zh) | 2010-09-01 | 2016-07-11 | 日本新藥股份有限公司 | 反義核酸 |
| PL2623507T3 (pl) | 2010-09-30 | 2017-03-31 | Nippon Shinyaku Co., Ltd. | Pochodna kwasu morfolinonukleinowego |
| EP2672977A1 (en) | 2011-02-08 | 2013-12-18 | The Charlotte-Mecklenburg Hospital Authority d/b/a Carolina Healthcare System | Antisense oligonucleotides |
| WO2012150960A1 (en) | 2011-05-05 | 2012-11-08 | Avi Biopharma, Inc. | Peptide oligonucleotide conjugates |
| US20130085139A1 (en) * | 2011-10-04 | 2013-04-04 | Royal Holloway And Bedford New College | Oligomers |
| ES2535654T3 (es) | 2011-10-13 | 2015-05-13 | Association Institut De Myologie | ADN triciclo-fosforotioato |
| BR112014011875B1 (pt) | 2011-11-18 | 2022-01-04 | Sarepta Therapeutics, Inc | Oligonucleotídeos funcionalmente modificados e subunidades dos mesmos |
| US9434928B2 (en) | 2011-11-23 | 2016-09-06 | Nationwide Children's Hospital, Inc. | Recombinant adeno-associated virus delivery of alpha-sarcoglycan polynucleotides |
| CN108611349A (zh) | 2011-12-28 | 2018-10-02 | 日本新药株式会社 | 反义核酸 |
| ES2907250T3 (es) | 2012-01-27 | 2022-04-22 | Biomarin Tech Bv | Oligonucleótidos de modulación de ARN con características mejoradas para el tratamiento de la distrofia muscular de Duchenne y de Becker |
| AU2013285698A1 (en) * | 2012-07-03 | 2015-02-19 | Biomarin Technologies B.V. | Oligonucleotide for the treatment of muscular dystrophy patients |
| KR20150099804A (ko) | 2012-12-20 | 2015-09-01 | 사렙타 쎄러퓨틱스 인코퍼레이티드 | 근위축증을 치료하기 위한 개선된 엑손 스키핑 조성물 |
| AU2014236140B2 (en) | 2013-03-14 | 2019-10-03 | Sarepta Therapeutics, Inc. | Exon skipping compositions for treating muscular dystrophy |
| NZ732507A (en) * | 2013-03-15 | 2018-08-31 | Sarepta Therapeutics Inc | Improved compositions for treating muscular dystrophy |
| WO2014172448A2 (en) | 2013-04-17 | 2014-10-23 | Anaptysbio, Inc. | Antibodies directed against activin receptor type ii (actrii) |
| IL282239B2 (en) * | 2013-09-05 | 2023-10-01 | Sarepta Therapeutics Inc | Antisense-induced exon2 inclusion in acid alpha-glucosidase |
| US10867398B2 (en) | 2017-11-21 | 2020-12-15 | Reliance Core Consulting LLC | Methods, systems, apparatuses and devices for facilitating motion analysis in an environment |
-
2016
- 2016-10-07 WO PCT/US2016/056093 patent/WO2017062835A2/en not_active Ceased
- 2016-10-07 EA EA201890908A patent/EA201890908A1/ru unknown
- 2016-10-07 BR BR112018007066A patent/BR112018007066A2/pt not_active Application Discontinuation
- 2016-10-07 EP EP16854468.2A patent/EP3359668A4/en not_active Withdrawn
- 2016-10-07 EP EP21151113.4A patent/EP3858993A1/en not_active Withdrawn
- 2016-10-07 US US15/765,466 patent/US20190177723A1/en not_active Abandoned
- 2016-10-07 JP JP2018517603A patent/JP2018530560A/ja not_active Withdrawn
- 2016-10-07 CN CN201680072146.4A patent/CN108699555A/zh active Pending
- 2016-10-07 MA MA045819A patent/MA45819A/fr unknown
-
2018
- 2018-03-13 IL IL258069A patent/IL258069A/en unknown
-
2021
- 2021-11-15 JP JP2021185544A patent/JP2022017594A/ja active Pending
-
2022
- 2022-01-27 IL IL290160A patent/IL290160A/en unknown
Also Published As
| Publication number | Publication date |
|---|---|
| JP2018530560A (ja) | 2018-10-18 |
| IL290160A (en) | 2022-03-01 |
| MA45819A (fr) | 2018-08-15 |
| BR112018007066A2 (pt) | 2018-10-23 |
| US20190177723A1 (en) | 2019-06-13 |
| EP3858993A1 (en) | 2021-08-04 |
| WO2017062835A3 (en) | 2017-06-08 |
| WO2017062835A2 (en) | 2017-04-13 |
| EP3359668A2 (en) | 2018-08-15 |
| EP3359668A4 (en) | 2019-06-05 |
| IL258069A (en) | 2018-05-31 |
| CN108699555A (zh) | 2018-10-23 |
| EA201890908A1 (ru) | 2018-10-31 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2022017594A (ja) | デュシェンヌ型筋ジストロフィーおよび関連障害の処置のための組成物および方法 | |
| JP6503031B2 (ja) | デュシェンヌ型及びベッカー型筋ジストロフィーの治療のための改善された特徴を有するrna調節オリゴヌクレオチド | |
| CN105793422B (zh) | 酸性α-葡糖苷酶中反义诱导的外显子2纳入 | |
| US20220090084A1 (en) | Antisense-induced exon exclusion in myostatin | |
| TW202332470A (zh) | 用於肌肉萎縮症之外顯子跳躍寡聚物結合物 | |
| US12121532B2 (en) | Modified antisense oligomers for exon inclusion in spinal muscular atrophy | |
| JP2023053352A (ja) | アンチセンスオリゴマー化合物 | |
| US20240415857A1 (en) | Antisense-induced exon exclusion in type vii collagen | |
| CN114127288A (zh) | 晚期糖基化终产物受体rna的调节剂和调节 | |
| HK40069896A (en) | Modulators and modulation of the receptor for advanced glycation end-products rna |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20211115 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20221115 |