JP2018537414A - ゲルマイクロスフェアの作製及び使用のためのシステム及び方法 - Google Patents
ゲルマイクロスフェアの作製及び使用のためのシステム及び方法 Download PDFInfo
- Publication number
- JP2018537414A JP2018537414A JP2018519002A JP2018519002A JP2018537414A JP 2018537414 A JP2018537414 A JP 2018537414A JP 2018519002 A JP2018519002 A JP 2018519002A JP 2018519002 A JP2018519002 A JP 2018519002A JP 2018537414 A JP2018537414 A JP 2018537414A
- Authority
- JP
- Japan
- Prior art keywords
- fluid
- gel
- polymer
- droplets
- carrier fluid
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q19/00—Preparations for care of the skin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
- A61K9/1682—Processes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/54—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic compound
- A61K47/549—Sugars, nucleosides, nucleotides or nucleic acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/56—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule
- A61K47/59—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes
- A61K47/60—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes the organic macromolecular compound being a polyoxyalkylene oligomer, polymer or dendrimer, e.g. PEG, PPG, PEO or polyglycerol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/69—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit
- A61K47/6903—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being semi-solid, e.g. an ointment, a gel, a hydrogel or a solidifying gel
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/69—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit
- A61K47/6921—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a particulate, a powder, an adsorbate, a bead or a sphere
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/02—Cosmetics or similar toiletry preparations characterised by special physical form
- A61K8/04—Dispersions; Emulsions
- A61K8/044—Suspensions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/72—Cosmetics or similar toiletry preparations characterised by the composition containing organic macromolecular compounds
- A61K8/84—Cosmetics or similar toiletry preparations characterised by the composition containing organic macromolecular compounds obtained by reactions otherwise than those involving only carbon-carbon unsaturated bonds
- A61K8/86—Polyethers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/72—Cosmetics or similar toiletry preparations characterised by the composition containing organic macromolecular compounds
- A61K8/84—Cosmetics or similar toiletry preparations characterised by the composition containing organic macromolecular compounds obtained by reactions otherwise than those involving only carbon-carbon unsaturated bonds
- A61K8/87—Polyurethanes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
- A61K9/1605—Excipients; Inactive ingredients
- A61K9/1629—Organic macromolecular compounds
- A61K9/1635—Organic macromolecular compounds obtained by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyvinyl pyrrolidone, poly(meth)acrylates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/5005—Wall or coating material
- A61K9/5021—Organic macromolecular compounds
- A61K9/5026—Organic macromolecular compounds obtained by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyvinyl pyrrolidone, poly(meth)acrylates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/5089—Processes
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J13/00—Colloid chemistry, e.g. the production of colloidal materials or their solutions, not otherwise provided for; Making microcapsules or microballoons
- B01J13/0052—Preparation of gels
- B01J13/0065—Preparation of gels containing an organic phase
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J13/00—Colloid chemistry, e.g. the production of colloidal materials or their solutions, not otherwise provided for; Making microcapsules or microballoons
- B01J13/0052—Preparation of gels
- B01J13/0069—Post treatment
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J13/00—Colloid chemistry, e.g. the production of colloidal materials or their solutions, not otherwise provided for; Making microcapsules or microballoons
- B01J13/02—Making microcapsules or microballoons
- B01J13/06—Making microcapsules or microballoons by phase separation
- B01J13/14—Polymerisation; cross-linking
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J13/00—Colloid chemistry, e.g. the production of colloidal materials or their solutions, not otherwise provided for; Making microcapsules or microballoons
- B01J13/02—Making microcapsules or microballoons
- B01J13/20—After-treatment of capsule walls, e.g. hardening
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2800/00—Properties of cosmetic compositions or active ingredients thereof or formulation aids used therein and process related aspects
- A61K2800/10—General cosmetic use
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2800/00—Properties of cosmetic compositions or active ingredients thereof or formulation aids used therein and process related aspects
- A61K2800/40—Chemical, physico-chemical or functional or structural properties of particular ingredients
- A61K2800/41—Particular ingredients further characterized by their size
- A61K2800/412—Microsized, i.e. having sizes between 0.1 and 100 microns
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2800/00—Properties of cosmetic compositions or active ingredients thereof or formulation aids used therein and process related aspects
- A61K2800/80—Process related aspects concerning the preparation of the cosmetic composition or the storage or application thereof
- A61K2800/81—Preparation or application process involves irradiation
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2800/00—Properties of cosmetic compositions or active ingredients thereof or formulation aids used therein and process related aspects
- A61K2800/80—Process related aspects concerning the preparation of the cosmetic composition or the storage or application thereof
- A61K2800/95—Involves in-situ formation or cross-linking of polymers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/10—Dispersions; Emulsions
- A61K9/107—Emulsions ; Emulsion preconcentrates; Micelles
- A61K9/113—Multiple emulsions, e.g. oil-in-water-in-oil
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2219/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J2219/00049—Controlling or regulating processes
- B01J2219/00177—Controlling or regulating processes controlling the pH
Abstract
Description
本出願は、Weitzらによる「ゲルマイクロスフェアの作製及び使用のためのシステム及び方法」と題する2015年10月13日に出願された米国仮特許出願第62/241,079号に基づく優先権を主張し、参照によりその全体を本明細書に組み込む。
本発明は、米国国立科学財団によって付与された許可番号NMR−1310266による政府の支援によりなされた。政府は、本発明において一定の権利を有する。
本発明は概して、マイクロ流体小滴(microfluidic droplets)、特に、多重(又は複数の:multiple)エマルジョンマイクロ流体小滴に関する。
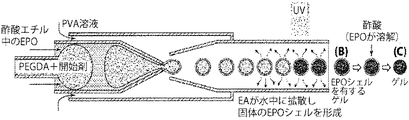
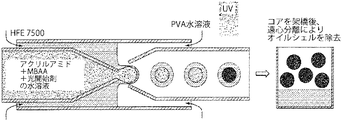
本発明は概して、マイクロ流体小滴、特に、多重エマルジョンマイクロ流体小滴に関する。ある態様では、ゲル粒子などの粒子は、水性小滴から水性キャリア(又は非水性小滴から非水性キャリア)の中に調製することができる。例えば、いくつかの実施形態では、キャリア流体中に含まれる、第2の流体によって囲まれた第1の流体のダブルエマルジョン小滴が調製されてもよく、そこでは第1の流体がゲルを形成し、第2の流体が除去される。例えば、第2の流体をキャリア流体中に溶解させてもよく、又は、例えばpHの変化により第2の流体を硬化させてから除去してもよい。本発明の他の実施形態は概して、そのようなマイクロ流体小滴を含むキット、そのようなマイクロ流体小滴を作製するためのマイクロ流体デバイス等を対象とする。
For example, if the outer shell comprises a polymer, the polymer may be degradable hydrolytically, enzymatically, photolytically, mechanically, etc.
別の例として、ポリマーは、その融点を超える温度でポリマーを加熱することによって液化され得る。例えば、外部シェルはアガロースゲルを含んでもよい。さらに別の例では、メタクリレートは、例えば酸性条件(例えば、pHが7未満、6未満、5未満、4未満、3未満など)までのpH変化で除去することができ、それによってキャリア流体中に含まれるゲルを残す。pHは、例えば適切な酸又は塩基を加えることによって変えることができる。pHは、例えば、少なくとも約2、3、4又はそれ以上のpH単位で変化されてもよい。適切な酸の非限定的な例として、任意の適切な希釈又は濃度で、酢酸、HCl、H2SO4、HNO3などを含む。適切な塩基の非限定的な例として、NaOH又はKOHを含む。
Claims (46)
- キャリア流体中に含まれる第2の流体によって囲まれた、ポリマーを含む第1の流体の小滴を供給する工程と、
前記第2の流体を固化させる工程と、
前記第1の流体中のポリマーでゲルを形成する工程と、
固化した第2の流体を除去する工程であって、それによって前記キャリア流体中に前記ゲルの懸濁液を形成する、除去する工程と、と含む方法。 - 前記ポリマーでゲルを形成する工程は、前記ポリマーを架橋させて前記ゲルを形成させるために紫外線を照射することを含む請求項1に記載の方法。
- 前記ポリマーでゲルを形成する工程は、前記キャリア流体にTEMEDを適用することを含み、それによって前記TEMEDは前記第1の流体中に拡散することができる、請求項1又は2に記載の方法。
- 前記第2の流体は、溶媒と第2のポリマーとを含み、
前記第2の流体を固化させる工程は、前記第2のポリマーが固体を形成するように、前記溶媒を前記キャリア流体に入れることを含む請求項1〜3のいずれか1つに記載の方法。 - 前記第2の流体を固化させる工程は、前記第2の流体の温度を変更することによって前記第2の流体を固化させることを含む請求項1〜4のいずれか1つに記載の方法。
- 前記固化した第2の流体はゲルである請求項1〜5のいずれか1つに記載の方法。
- 前記固化した第2の流体を除去する工程は、前記固化した第2の流体を前記キャリア流体中に溶解させるように前記キャリア流体のpHを低下させることを含む請求項1〜6のいずれか1つに記載の方法。
- 前記キャリア流体のpHを変化させる工程は、前記キャリア流体の前記pHを、少なくとも約2pHの単位で低下させることを含む請求項7に記載の方法。
- 前記キャリア流体のpHを変化させる工程は、前記キャリア流体の前記pHを5以下まで低下させることを含む請求項7又は8に記載の方法。
- 前記キャリア流体のpHを変化させる工程は、前記キャリア流体に酸を添加することを含む請求項7〜9のいずれか1つに記載の方法。
- 前記固化した第2の流体を除去する工程は、前記固化した第2の流体を機械的に除去することを含む請求項1〜10のいずれか1つに記載の方法。
- 前記第1の流体は開始剤をさらに含む請求項1〜11のいずれか1つに記載の方法。
- 前記開始剤はイルガキュア2559を含む請求項12に記載の方法。
- 前記ポリマーはポリ(エチレングリコール)ジアクリレートを含む請求項1〜13のいずれか1つに記載の方法。
- 前記第2の流体はアクリレート又はメタクリレートを含む請求項1〜14のいずれか1つに記載の方法。
- 前記第2の流体はジメチルアミノエチルメタクリレートを含む請求項1〜15のいずれか1つに記載の方法。
- 前記第2の流体はブチルメタクリレートを含む請求項1〜16のいずれか1つに記載の方法。
- 前記第2の流体はメチルメタクリレートを含む請求項1〜17のいずれか1つに記載の方法。
- 前記小滴は約1mm以下の平均直径を有する請求項1〜18のいずれか1つに記載の方法。
- 前記小滴は、前記小滴の少なくとも90%が、前記小滴の前記平均直径の90%よりも大きく110%よりも小さい直径を有するような直径分布を有する請求項1〜19のいずれか1つに記載の方法。
- 前記キャリア流体は水性である請求項1〜20のいずれか1つに記載の方法。
- 前記キャリア流体と前記第2の流体は実質的に非混和である請求項1〜21のいずれか1つに記載の方法。
- 前記第1の流体と前記第2の流体は実質的に非混和である請求項1〜22のいずれか1つに記載の方法。
- 種を前記ゲル中に取り込むために、前記種を前記ゲルにさらす工程をさらに含む請求項1〜23のいずれか1つに記載の方法。
- 前記種を前記ゲルに結合させる工程を含む請求項24に記載の方法。
- 前記種を前記ゲルに共有結合させる工程を含む請求項25に記載の方法。
- 前記種は核酸を含む請求項24〜26のいずれか1つに記載の方法。
- 前記種はDNAを含む請求項27に記載の方法。
- EDCの結合反応を用いて前記DNAを前記ゲルに結合させる工程を含む請求項27又は28に記載の方法。
- キャリア流体中に含まれる溶媒とポリマーとを含む小滴を供給する工程と、
前記ポリマーでゲルを形成する工程と、
前記ゲルからの前記溶媒を除去する工程であって、それによって前記キャリア流体中に前記ゲルの懸濁液を形成する、除去する工程と、を含む方法。 - 前記ポリマーでゲルを形成する工程は、前記ポリマーを架橋させて前記ゲルを形成させるように紫外線を照射する工程を含む請求項30に記載の方法。
- 前記ポリマーでゲルを形成する工程は、キャリア流体にTEMEDを適用することを含み、それによって前記TEMEDは前記第1の流体中に拡散することができる、請求項30又は30に記載の方法。
- 前記小滴は開始剤をさらに含む請求項30〜32のいずれか1つに記載の方法。
- 前記開始剤はイルガキュア2559を含む請求項33に記載の方法。
- 前記ポリマーはポリ(エチレングリコール)ジアクリレートを含む請求項30〜34のいずれか1つに記載の方法。
- 前記溶媒は、前記キャリア流体にさらされたとき、分離相を形成することができる、請求項30〜35のいずれか1つに記載の方法。
- 前記ゲルからの前記溶媒を除去する工程は、前記溶媒を前記キャリア流体に入れることを含む請求項30〜36のいずれか1つに記載の方法。
- 前記キャリア流体は水性の流体である請求項30〜37のいずれか1つに記載の方法。
- 前記キャリア流体は水である請求項30〜38のいずれか1つに記載の方法。
- 前記溶媒は約1g/ml未満の水溶解度を有する請求項30〜39のいずれか1つに記載の方法。
- 種を前記ゲル中に取り込むために、前記種を前記ゲルにさらす工程をさらに含む請求項30〜40のいずれか1つに記載の方法。
- 前記種を前記ゲルに結合させる工程を含む請求項41に記載の方法。
- 前記種を前記ゲルに共有結合させる工程を含む請求項42に記載の方法。
- 前記種は核酸を含む請求項30〜43のいずれか1つに記載の方法。
- 前記種はDNAを含む請求項44に記載の方法。
- EDCの結合反応を用いて前記DNAを前記ゲルに結合させる工程を含む、請求項44又は45に記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201562241079P | 2015-10-13 | 2015-10-13 | |
| US62/241,079 | 2015-10-13 | ||
| PCT/US2016/056509 WO2017066231A1 (en) | 2015-10-13 | 2016-10-12 | Systems and methods for making and using gel microspheres |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2018537414A true JP2018537414A (ja) | 2018-12-20 |
| JP2018537414A5 JP2018537414A5 (ja) | 2019-11-21 |
Family
ID=58518551
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018519002A Pending JP2018537414A (ja) | 2015-10-13 | 2016-10-12 | ゲルマイクロスフェアの作製及び使用のためのシステム及び方法 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US11123297B2 (ja) |
| EP (1) | EP3362032A4 (ja) |
| JP (1) | JP2018537414A (ja) |
| CN (1) | CN108289797B (ja) |
| AU (1) | AU2016338907B2 (ja) |
| CA (1) | CA3001679A1 (ja) |
| WO (1) | WO2017066231A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR102581886B1 (ko) * | 2022-05-30 | 2023-09-26 | 윤상훈 | 수성 페인트용 마이크로 비드 수분산체, 내오염성이 우수한 수성 페인트 조성물 및 이를 이용한 페인트 도장 시공 방법 |
Families Citing this family (35)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2010033200A2 (en) | 2008-09-19 | 2010-03-25 | President And Fellows Of Harvard College | Creation of libraries of droplets and related species |
| WO2015069634A1 (en) | 2013-11-08 | 2015-05-14 | President And Fellows Of Harvard College | Microparticles, methods for their preparation and use |
| US9824068B2 (en) | 2013-12-16 | 2017-11-21 | 10X Genomics, Inc. | Methods and apparatus for sorting data |
| CN106795553B (zh) | 2014-06-26 | 2021-06-04 | 10X基因组学有限公司 | 分析来自单个细胞或细胞群体的核酸的方法 |
| WO2017066231A1 (en) | 2015-10-13 | 2017-04-20 | President And Fellows Of Harvard College | Systems and methods for making and using gel microspheres |
| US10550429B2 (en) | 2016-12-22 | 2020-02-04 | 10X Genomics, Inc. | Methods and systems for processing polynucleotides |
| US10837047B2 (en) | 2017-10-04 | 2020-11-17 | 10X Genomics, Inc. | Compositions, methods, and systems for bead formation using improved polymers |
| SG11201913654QA (en) | 2017-11-15 | 2020-01-30 | 10X Genomics Inc | Functionalized gel beads |
| WO2019157529A1 (en) | 2018-02-12 | 2019-08-15 | 10X Genomics, Inc. | Methods characterizing multiple analytes from individual cells or cell populations |
| US11639928B2 (en) | 2018-02-22 | 2023-05-02 | 10X Genomics, Inc. | Methods and systems for characterizing analytes from individual cells or cell populations |
| US11932899B2 (en) | 2018-06-07 | 2024-03-19 | 10X Genomics, Inc. | Methods and systems for characterizing nucleic acid molecules |
| US11703427B2 (en) | 2018-06-25 | 2023-07-18 | 10X Genomics, Inc. | Methods and systems for cell and bead processing |
| JP2021528443A (ja) | 2018-06-29 | 2021-10-21 | ザ プロクター アンド ギャンブル カンパニーThe Procter & Gamble Company | 二相製品 |
| KR20210008853A (ko) * | 2018-06-29 | 2021-01-25 | 더 프록터 앤드 갬블 캄파니 | 이중상 제품 분배기 |
| WO2020006327A1 (en) | 2018-06-29 | 2020-01-02 | The Procter & Gamble Company | Dual phase products |
| US20200032335A1 (en) | 2018-07-27 | 2020-01-30 | 10X Genomics, Inc. | Systems and methods for metabolome analysis |
| CN109021947B (zh) * | 2018-09-14 | 2020-12-04 | 兰州理工大学 | 一种高强度小粒径调剖剂及其制备方法与应用 |
| CN109482111B (zh) * | 2018-11-07 | 2021-05-04 | 四川大川合颐生物科技有限公司 | 子弹状非球形微颗粒和微囊及其制备方法 |
| CN113227344A (zh) * | 2018-12-31 | 2021-08-06 | 美国圣戈班性能塑料公司 | 含有可降解载体的容器 |
| US11845983B1 (en) | 2019-01-09 | 2023-12-19 | 10X Genomics, Inc. | Methods and systems for multiplexing of droplet based assays |
| US11851683B1 (en) | 2019-02-12 | 2023-12-26 | 10X Genomics, Inc. | Methods and systems for selective analysis of cellular samples |
| US11655499B1 (en) | 2019-02-25 | 2023-05-23 | 10X Genomics, Inc. | Detection of sequence elements in nucleic acid molecules |
| WO2020185791A1 (en) | 2019-03-11 | 2020-09-17 | 10X Genomics, Inc. | Systems and methods for processing optically tagged beads |
| CN110307929B (zh) * | 2019-07-08 | 2020-08-25 | 上海交通大学 | 一种基于压力敏感薄膜的流体压力测量系统及方法 |
| CN110316935B (zh) * | 2019-07-19 | 2022-03-08 | 清远市清新区谷城矿业开发投资有限公司 | 一种废泥处理方法 |
| CN110665555A (zh) * | 2019-09-30 | 2020-01-10 | 大连理工大学 | 一种同轴毛细管微流控芯片及其制备方法 |
| US20210291129A1 (en) * | 2020-03-23 | 2021-09-23 | Mark A. Gray | Capillary tube droplet generation systems and methods |
| GB202004515D0 (en) * | 2020-03-27 | 2020-05-13 | Univ Oxford Innovation Ltd | Method |
| US11851700B1 (en) | 2020-05-13 | 2023-12-26 | 10X Genomics, Inc. | Methods, kits, and compositions for processing extracellular molecules |
| AU2022227563A1 (en) | 2021-02-23 | 2023-08-24 | 10X Genomics, Inc. | Probe-based analysis of nucleic acids and proteins |
| CN114191848B (zh) * | 2021-12-06 | 2022-12-30 | 武汉瑞法医疗器械有限公司 | 琼脂糖微球的清洗方法 |
| WO2023129514A2 (en) * | 2021-12-28 | 2023-07-06 | The Texas A&M University System | Environmental biospecimen recovery after in-droplet gel encapsulation |
| CN114534590B (zh) * | 2022-02-26 | 2023-06-09 | 四川大学 | 一种可控制备单分散双重乳液的旋转式套管微流控装置及方法 |
| CN114534531A (zh) * | 2022-03-08 | 2022-05-27 | 南京工业大学 | 一种不使用乳化剂制备w/o和o/w乳状液的方法 |
| CN116715805B (zh) * | 2023-08-01 | 2023-10-27 | 苏州大学 | 一种富含双膦酸基团多功能凝胶微球及其制备方法和应用 |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2008535644A (ja) * | 2005-03-04 | 2008-09-04 | プレジデント・アンド・フエローズ・オブ・ハーバード・カレツジ | 多重エマルジョンの形成のための方法および装置 |
| WO2010104604A1 (en) * | 2009-03-13 | 2010-09-16 | President And Fellows Of Harvard College | Method for the controlled creation of emulsions, including multiple emulsions |
| WO2012156744A2 (en) * | 2011-05-17 | 2012-11-22 | Cambridge Enterprise Limited | Gel beads in microfluidic droplets |
| US20140199731A1 (en) * | 2007-03-07 | 2014-07-17 | President And Fellows Of Harvard College | Assay and other reactions involving droplets |
| JP2014522718A (ja) * | 2011-07-06 | 2014-09-08 | プレジデント アンド フェローズ オブ ハーバード カレッジ | 多相エマルションおよび多相エマルション形成法 |
Family Cites Families (190)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE3230289A1 (de) | 1982-08-14 | 1984-02-16 | Bayer Ag, 5090 Leverkusen | Herstellung von pharmazeutischen oder kosmetischen dispersionen |
| US5100933A (en) | 1986-03-31 | 1992-03-31 | Massachusetts Institute Of Technology | Collapsible gel compositions |
| US4732930A (en) | 1985-05-20 | 1988-03-22 | Massachusetts Institute Of Technology | Reversible, discontinuous volume changes of ionized isopropylacrylamide cells |
| US4916070A (en) | 1986-04-14 | 1990-04-10 | The General Hospital Corporation | Fibrin-specific antibodies and method of screening for the antibodies |
| US4743507A (en) | 1986-09-12 | 1988-05-10 | Franses Elias I | Nonspherical microparticles and method therefor |
| JPH075743B2 (ja) | 1986-12-22 | 1995-01-25 | ダイキン工業株式会社 | テトラフルオロエチレン系共重合体粉末およびその製造法 |
| US5525464A (en) | 1987-04-01 | 1996-06-11 | Hyseq, Inc. | Method of sequencing by hybridization of oligonucleotide probes |
| US5202231A (en) | 1987-04-01 | 1993-04-13 | Drmanac Radoje T | Method of sequencing of genomes by hybridization of oligonucleotide probes |
| US5149625A (en) | 1987-08-11 | 1992-09-22 | President And Fellows Of Harvard College | Multiplex analysis of DNA |
| JPH0694483B2 (ja) | 1988-01-29 | 1994-11-24 | 三田工業株式会社 | 粒径の増大した単分散重合体粒子の製造方法 |
| US5055390A (en) | 1988-04-22 | 1991-10-08 | Massachusetts Institute Of Technology | Process for chemical manipulation of non-aqueous surrounded microdroplets |
| US5326692B1 (en) | 1992-05-13 | 1996-04-30 | Molecular Probes Inc | Fluorescent microparticles with controllable enhanced stokes shift |
| GB9021061D0 (en) | 1990-09-27 | 1990-11-07 | Unilever Plc | Encapsulating method and products containing encapsulated material |
| US5120349A (en) | 1990-12-07 | 1992-06-09 | Landec Labs, Inc. | Microcapsule having temperature-dependent permeability profile |
| US5216096A (en) | 1991-09-24 | 1993-06-01 | Japan Synthetic Rubber Co., Ltd. | Process for the preparation of cross-linked polymer particles |
| AU3816993A (en) | 1992-03-19 | 1993-10-21 | Regents Of The University Of California, The | Multiple tag labeling method for DNA sequencing |
| AU5895994A (en) | 1993-10-04 | 1995-05-01 | Mark Chasin | Controlled release microspheres |
| US5512131A (en) | 1993-10-04 | 1996-04-30 | President And Fellows Of Harvard College | Formation of microstamped patterns on surfaces and derivative articles |
| US20030044777A1 (en) | 1993-10-28 | 2003-03-06 | Kenneth L. Beattie | Flowthrough devices for multiple discrete binding reactions |
| US5834252A (en) | 1995-04-18 | 1998-11-10 | Glaxo Group Limited | End-complementary polymerase reaction |
| US5583162A (en) | 1994-06-06 | 1996-12-10 | Biopore Corporation | Polymeric microbeads and method of preparation |
| EP0812434B1 (en) | 1995-03-01 | 2013-09-18 | President and Fellows of Harvard College | Microcontact printing on surfaces and derivative articles |
| WO1996041011A1 (en) | 1995-06-07 | 1996-12-19 | Lynx Therapeutics, Inc. | Oligonucleotide tags for sorting and identification |
| CN1146668C (zh) | 1995-06-07 | 2004-04-21 | 林克斯治疗公司 | 用于分选和鉴定的寡核苷酸标记物 |
| US5851769A (en) | 1995-09-27 | 1998-12-22 | The Regents Of The University Of California | Quantitative DNA fiber mapping |
| US5736330A (en) | 1995-10-11 | 1998-04-07 | Luminex Corporation | Method and compositions for flow cytometric determination of DNA sequences |
| US6051377A (en) | 1995-11-30 | 2000-04-18 | Pharmaseq, Inc. | Multiplex assay for nucleic acids employing transponders |
| US5736332A (en) | 1995-11-30 | 1998-04-07 | Mandecki; Wlodek | Method of determining the sequence of nucleic acids employing solid-phase particles carrying transponders |
| US6001571A (en) | 1995-11-30 | 1999-12-14 | Mandecki; Wlodek | Multiplex assay for nucleic acids employing transponders |
| US6355198B1 (en) | 1996-03-15 | 2002-03-12 | President And Fellows Of Harvard College | Method of forming articles including waveguides via capillary micromolding and microtransfer molding |
| JP3633091B2 (ja) | 1996-04-09 | 2005-03-30 | 旭硝子株式会社 | 微小無機質球状中実体の製造方法 |
| US6022501A (en) | 1996-08-15 | 2000-02-08 | American Cyanamid Company | pH-sensitive microcapsules |
| US20050042625A1 (en) | 1997-01-15 | 2005-02-24 | Xzillion Gmbh & Co. | Mass label linked hybridisation probes |
| US20020034737A1 (en) | 1997-03-04 | 2002-03-21 | Hyseq, Inc. | Methods and compositions for detection or quantification of nucleic acid species |
| US6297006B1 (en) | 1997-01-16 | 2001-10-02 | Hyseq, Inc. | Methods for sequencing repetitive sequences and for determining the order of sequence subfragments |
| US6391622B1 (en) | 1997-04-04 | 2002-05-21 | Caliper Technologies Corp. | Closed-loop biochemical analyzers |
| US6143496A (en) | 1997-04-17 | 2000-11-07 | Cytonix Corporation | Method of sampling, amplifying and quantifying segment of nucleic acid, polymerase chain reaction assembly having nanoliter-sized sample chambers, and method of filling assembly |
| CA2291180A1 (en) | 1997-05-23 | 1998-11-26 | Lynx Therapeutics, Inc. | System and apparatus for sequential processing of analytes |
| US20040241759A1 (en) | 1997-06-16 | 2004-12-02 | Eileen Tozer | High throughput screening of libraries |
| DK1019496T3 (da) | 1997-07-07 | 2005-01-10 | Medical Res Council | In vitro-sorteringsmetode |
| GB9714716D0 (en) | 1997-07-11 | 1997-09-17 | Brax Genomics Ltd | Characterising nucleic acids |
| CA2300940A1 (en) | 1997-08-15 | 1999-02-25 | Hyseq, Inc. | Methods and compositions for detection or quantification of nucleic acid species |
| WO1999014368A2 (en) | 1997-09-15 | 1999-03-25 | Whitehead Institute For Biomedical Research | Methods and apparatus for processing a sample of biomolecular analyte using a microfabricated device |
| US20020092767A1 (en) | 1997-09-19 | 2002-07-18 | Aclara Biosciences, Inc. | Multiple array microfluidic device units |
| WO1999018438A1 (en) | 1997-10-02 | 1999-04-15 | Aclara Biosciences, Inc. | Capillary assays involving separation of free and bound species |
| AU737174B2 (en) | 1997-10-10 | 2001-08-09 | President & Fellows Of Harvard College | Replica amplification of nucleic acid arrays |
| US6511803B1 (en) | 1997-10-10 | 2003-01-28 | President And Fellows Of Harvard College | Replica amplification of nucleic acid arrays |
| US6485944B1 (en) | 1997-10-10 | 2002-11-26 | President And Fellows Of Harvard College | Replica amplification of nucleic acid arrays |
| KR20010031140A (ko) | 1997-10-14 | 2001-04-16 | 루미넥스 코포레이션 | 정밀 형광염료 입자 및 그의 제조방법 그리고 그의 사용 |
| JP4318859B2 (ja) | 1997-12-04 | 2009-08-26 | ジーイー・ヘルスケア・ユーケイ・リミテッド | 複合アッセイ方法 |
| AU2460399A (en) | 1998-01-20 | 1999-08-02 | Packard Bioscience Company | Gel pad arrays and methods and systems for making them |
| WO1999052708A1 (en) | 1998-04-13 | 1999-10-21 | Luminex Corporation | Liquid labeling with fluorescent microparticles |
| DE69931497T2 (de) | 1998-08-07 | 2007-05-03 | Cellay LLC, Cambridge | Gel mikrotropfen für die genetische analyse |
| US6489096B1 (en) | 1998-10-15 | 2002-12-03 | Princeton University | Quantitative analysis of hybridization patterns and intensities in oligonucleotide arrays |
| WO2000026412A1 (en) | 1998-11-02 | 2000-05-11 | Kenneth Loren Beattie | Nucleic acid analysis using sequence-targeted tandem hybridization |
| GB9900298D0 (en) | 1999-01-07 | 1999-02-24 | Medical Res Council | Optical sorting method |
| US6635419B1 (en) | 1999-02-16 | 2003-10-21 | Applera Corporation | Polynucleotide sequencing method |
| ATE556149T1 (de) | 1999-02-23 | 2012-05-15 | Caliper Life Sciences Inc | Manipulation von mikropartikeln in mikrofluidischen systemen |
| US6908737B2 (en) | 1999-04-15 | 2005-06-21 | Vitra Bioscience, Inc. | Systems and methods of conducting multiplexed experiments |
| JP3815969B2 (ja) | 1999-05-12 | 2006-08-30 | アクララ バイオサイエンシーズ, インコーポレイテッド | 微量流体デバイスにおける多重方式蛍光検出 |
| US6380297B1 (en) | 1999-08-12 | 2002-04-30 | Nexpress Solutions Llc | Polymer particles of controlled shape |
| US6524456B1 (en) | 1999-08-12 | 2003-02-25 | Ut-Battelle, Llc | Microfluidic devices for the controlled manipulation of small volumes |
| EP1248853A2 (en) | 1999-08-20 | 2002-10-16 | Luminex Corporation | Liquid array technology |
| US6982146B1 (en) | 1999-08-30 | 2006-01-03 | The United States Of America As Represented By The Department Of Health And Human Services | High speed parallel molecular nucleic acid sequencing |
| CA2403708A1 (en) | 2000-03-22 | 2001-09-27 | Quantum Dot Corporation | Methods of using semiconductor nanocrystals in bead-based nucleic acid assays |
| US6413548B1 (en) | 2000-05-10 | 2002-07-02 | Aveka, Inc. | Particulate encapsulation of liquid beads |
| US6800298B1 (en) | 2000-05-11 | 2004-10-05 | Clemson University | Biological lubricant composition and method of applying lubricant composition |
| US6645432B1 (en) | 2000-05-25 | 2003-11-11 | President & Fellows Of Harvard College | Microfluidic systems including three-dimensionally arrayed channel networks |
| US6632606B1 (en) | 2000-06-12 | 2003-10-14 | Aclara Biosciences, Inc. | Methods for single nucleotide polymorphism detection |
| US7892854B2 (en) | 2000-06-21 | 2011-02-22 | Bioarray Solutions, Ltd. | Multianalyte molecular analysis using application-specific random particle arrays |
| AU2001290879A1 (en) | 2000-09-15 | 2002-03-26 | California Institute Of Technology | Microfabricated crossflow devices and methods |
| IL150020A0 (en) | 2000-10-10 | 2002-12-01 | Diversa Corp | High throughput or capillary-based screening for a bioactivity or biomolecule |
| US20040096515A1 (en) | 2001-12-07 | 2004-05-20 | Bausch Andreas R. | Methods and compositions for encapsulating active agents |
| EP1385488A2 (en) | 2000-12-07 | 2004-02-04 | President And Fellows Of Harvard College | Methods and compositions for encapsulating active agents |
| JP3746766B2 (ja) | 2001-02-23 | 2006-02-15 | 独立行政法人科学技術振興機構 | エマルションの製造方法およびその装置 |
| US7572642B2 (en) | 2001-04-18 | 2009-08-11 | Ambrigen, Llc | Assay based on particles, which specifically bind with targets in spatially distributed characteristic patterns |
| EP1399580B1 (en) | 2001-05-26 | 2008-10-08 | One Cell Systems, Inc. | Secretion of proteins by encapsulated cells |
| US6613523B2 (en) | 2001-06-29 | 2003-09-02 | Agilent Technologies, Inc. | Method of DNA sequencing using cleavable tags |
| US6767731B2 (en) | 2001-08-27 | 2004-07-27 | Intel Corporation | Electron induced fluorescent method for nucleic acid sequencing |
| AU2002337803A1 (en) | 2001-10-03 | 2003-04-14 | Glaxo Group Limited | Sustained release pharmaceutical compositions |
| EP1448789A4 (en) | 2001-10-30 | 2007-01-03 | Nanomics Biosystems Pty Ltd | DEVICE AND METHOD FOR THE TARGETED SYNTHESIS OF CHEMICAL LIBRARIES |
| US20030099954A1 (en) | 2001-11-26 | 2003-05-29 | Stefan Miltenyi | Apparatus and method for modification of magnetically immobilized biomolecules |
| US20030170698A1 (en) | 2002-01-04 | 2003-09-11 | Peter Gascoyne | Droplet-based microfluidic oligonucleotide synthesis engine |
| EP1488006B1 (en) | 2002-03-20 | 2008-05-28 | InnovativeBio.Biz | Microcapsules with controlable permeability encapsulating a nucleic acid amplification reaction mixture and their use as reaction compartments for parallels reactions |
| US7901939B2 (en) | 2002-05-09 | 2011-03-08 | University Of Chicago | Method for performing crystallization and reactions in pressure-driven fluid plugs |
| JP2006507921A (ja) | 2002-06-28 | 2006-03-09 | プレジデント・アンド・フェロウズ・オブ・ハーバード・カレッジ | 流体分散のための方法および装置 |
| IL151660A0 (en) | 2002-09-09 | 2003-04-10 | Univ Ben Gurion | Method for isolating and culturing unculturable microorganisms |
| ES2338654T5 (es) | 2003-01-29 | 2017-12-11 | 454 Life Sciences Corporation | Amplificación de ácidos nucleicos en emulsión de perlas |
| US7041481B2 (en) | 2003-03-14 | 2006-05-09 | The Regents Of The University Of California | Chemical amplification based on fluid partitioning |
| GB0307403D0 (en) | 2003-03-31 | 2003-05-07 | Medical Res Council | Selection by compartmentalised screening |
| US20060078893A1 (en) | 2004-10-12 | 2006-04-13 | Medical Research Council | Compartmentalised combinatorial chemistry by microfluidic control |
| GB0307428D0 (en) | 2003-03-31 | 2003-05-07 | Medical Res Council | Compartmentalised combinatorial chemistry |
| EP2266687A3 (en) | 2003-04-10 | 2011-06-29 | The President and Fellows of Harvard College | Formation and control of fluidic species |
| WO2004102204A1 (en) | 2003-05-16 | 2004-11-25 | Global Technologies (Nz) Ltd | Method and apparatus for mixing sample and reagent in a suspension fluid |
| WO2004103565A2 (de) | 2003-05-19 | 2004-12-02 | Hans-Knöll-Institut für Naturstoff-Forschung e.V. | Vorrichtung und verfahren zur strukturierung von flüssigkeiten und zum zudosieren von reaktionsflüssigkeiten zu in separationsmedium eingebetteten flüssigkeitskompartimenten |
| WO2004105734A1 (en) | 2003-05-28 | 2004-12-09 | Valorisation Recherche, Societe En Commandite | Method of preparing microcapsules |
| JP3875653B2 (ja) | 2003-06-05 | 2007-01-31 | 正昭 川橋 | 小滴の状態計測装置、及び状態計測方法 |
| WO2005010145A2 (en) | 2003-07-05 | 2005-02-03 | The Johns Hopkins University | Method and compositions for detection and enumeration of genetic variations |
| US8796030B2 (en) | 2003-07-12 | 2014-08-05 | Parallel Synthesis Technologies, Inc. | Methods for optically encoding an object with upconverting materials and compositions used therein |
| JP4630870B2 (ja) | 2003-08-27 | 2011-02-09 | プレジデント アンド フェロウズ オブ ハーバード カレッジ | 流体種の電子的制御 |
| US20070275080A1 (en) | 2003-10-31 | 2007-11-29 | Engineered Release Systems Inc. | Polymer-Based Microstructures |
| EP1691792A4 (en) | 2003-11-24 | 2008-05-28 | Yeda Res & Dev | COMPOSITIONS AND METHODS FOR IN VITRO / I SORTING OF MOLECULAR AND CELLULAR BANKS |
| US7309500B2 (en) | 2003-12-04 | 2007-12-18 | The Board Of Trustees Of The University Of Illinois | Microparticles |
| US20050181379A1 (en) | 2004-02-18 | 2005-08-18 | Intel Corporation | Method and device for isolating and positioning single nucleic acid molecules |
| WO2005082098A2 (en) | 2004-02-27 | 2005-09-09 | President And Fellows Of Harvard College | Polony fluorescent in situ sequencing beads |
| US7595155B2 (en) | 2004-02-27 | 2009-09-29 | Hitachi Chemical Research Center | Multiplex detection probes |
| US20050221339A1 (en) | 2004-03-31 | 2005-10-06 | Medical Research Council Harvard University | Compartmentalised screening by microfluidic control |
| US20060020371A1 (en) | 2004-04-13 | 2006-01-26 | President And Fellows Of Harvard College | Methods and apparatus for manipulation and/or detection of biological samples and other objects |
| WO2005103106A1 (en) | 2004-04-23 | 2005-11-03 | Eugenia Kumacheva | Method of producing polymeric particles with selected size, shape, morphology and composition |
| US7799553B2 (en) | 2004-06-01 | 2010-09-21 | The Regents Of The University Of California | Microfabricated integrated DNA analysis system |
| US7892731B2 (en) | 2004-10-01 | 2011-02-22 | Radix Biosolutions, Ltd. | System and method for inhibiting the decryption of a nucleic acid probe sequence used for the detection of a specific nucleic acid |
| US7968287B2 (en) | 2004-10-08 | 2011-06-28 | Medical Research Council Harvard University | In vitro evolution in microfluidic systems |
| WO2007001448A2 (en) | 2004-11-04 | 2007-01-04 | Massachusetts Institute Of Technology | Coated controlled release polymer particles as efficient oral delivery vehicles for biopharmaceuticals |
| US20080004436A1 (en) | 2004-11-15 | 2008-01-03 | Yeda Research And Development Co. Ltd. At The Weizmann Institute Of Science | Directed Evolution and Selection Using in Vitro Compartmentalization |
| WO2006078841A1 (en) | 2005-01-21 | 2006-07-27 | President And Fellows Of Harvard College | Systems and methods for forming fluidic droplets encapsulated in particles such as colloidal particles |
| WO2006089192A2 (en) | 2005-02-18 | 2006-08-24 | Canon U.S. Life Sciences, Inc. | Devices and methods for identifying genomic dna of organisms |
| US20070054119A1 (en) | 2005-03-04 | 2007-03-08 | Piotr Garstecki | Systems and methods of forming particles |
| JP2006289250A (ja) | 2005-04-08 | 2006-10-26 | Kao Corp | マイクロミキサー及びそれを用いた流体混合方法 |
| JP2006349060A (ja) | 2005-06-16 | 2006-12-28 | Ntn Corp | ボールねじ |
| WO2007002490A2 (en) | 2005-06-22 | 2007-01-04 | The Research Foundation Of State University Of New York | Massively parallel 2-dimensional capillary electrophoresis |
| FR2888912B1 (fr) | 2005-07-25 | 2007-08-24 | Commissariat Energie Atomique | Procede de commande d'une communication entre deux zones par electromouillage, dispositif comportant des zones isolables les unes des autres et procede de realisation d'un tel dispositif |
| WO2007024840A2 (en) | 2005-08-22 | 2007-03-01 | Critical Therapeutics, Inc. | Method of quantitating nucleic acids by flow cytometry microparticle-based array |
| US7932037B2 (en) | 2007-12-05 | 2011-04-26 | Perkinelmer Health Sciences, Inc. | DNA assays using amplicon probes on encoded particles |
| WO2007081386A2 (en) | 2006-01-11 | 2007-07-19 | Raindance Technologies, Inc. | Microfluidic devices and methods of use |
| US7537897B2 (en) | 2006-01-23 | 2009-05-26 | Population Genetics Technologies, Ltd. | Molecular counting |
| US20070195127A1 (en) | 2006-01-27 | 2007-08-23 | President And Fellows Of Harvard College | Fluidic droplet coalescence |
| JP4921829B2 (ja) | 2006-03-30 | 2012-04-25 | 株式会社東芝 | 微粒子の製造装置、乳化剤保持部、微粒子の製造方法および分子膜の製造方法 |
| WO2007114794A1 (en) | 2006-03-31 | 2007-10-11 | Nam Trung Nguyen | Active control for droplet-based microfluidics |
| JP2009538123A (ja) | 2006-04-19 | 2009-11-05 | アプライド バイオシステムズ, エルエルシー | ゲル非含有ビーズベースの配列決定のための試薬、方法およびライブラリー |
| JP4774517B2 (ja) | 2006-04-28 | 2011-09-14 | 国立大学法人埼玉大学 | 粒子計測装置および方法 |
| US7811603B2 (en) | 2006-05-09 | 2010-10-12 | The Regents Of The University Of California | Microfluidic device for forming monodisperse lipoplexes |
| US20080014589A1 (en) | 2006-05-11 | 2008-01-17 | Link Darren R | Microfluidic devices and methods of use thereof |
| WO2007133807A2 (en) | 2006-05-15 | 2007-11-22 | Massachusetts Institute Of Technology | Polymers for functional particles |
| ES2620398T3 (es) | 2006-05-22 | 2017-06-28 | Nanostring Technologies, Inc. | Sistemas y métodos para analizar nanoindicadores |
| CA2653321A1 (en) | 2006-05-26 | 2007-12-06 | Althea Technologies, Inc. | Biochemical analysis of partitioned cells |
| FR2901717A1 (fr) | 2006-05-30 | 2007-12-07 | Centre Nat Rech Scient | Procede de traitement de gouttes dans un circuit microfluidique. |
| EP2038427A4 (en) | 2006-06-19 | 2010-07-07 | Univ Johns Hopkins | SINGLE MOLECULE PCR ON MICROPARTICLES IN WATER-IN-OIL EMULSIONS |
| EP2077912B1 (en) | 2006-08-07 | 2019-03-27 | The President and Fellows of Harvard College | Fluorocarbon emulsion stabilizing surfactants |
| US8841116B2 (en) | 2006-10-25 | 2014-09-23 | The Regents Of The University Of California | Inline-injection microdevice and microfabricated integrated DNA analysis system using same |
| WO2008058297A2 (en) | 2006-11-10 | 2008-05-15 | Harvard University | Non-spherical particles |
| US20080176768A1 (en) | 2007-01-23 | 2008-07-24 | Honeywell Honeywell International | Hydrogel microarray with embedded metal nanoparticles |
| FI20075124A0 (fi) | 2007-02-21 | 2007-02-21 | Valtion Teknillinen | Menetelmä ja testikitti nukleotidivariaatioiden toteamiseksi |
| US7776927B2 (en) * | 2007-03-28 | 2010-08-17 | President And Fellows Of Harvard College | Emulsions and techniques for formation |
| US20100130369A1 (en) | 2007-04-23 | 2010-05-27 | Advanced Liquid Logic, Inc. | Bead-Based Multiplexed Analytical Methods and Instrumentation |
| US20100255556A1 (en) | 2007-06-29 | 2010-10-07 | President And Fellows Of Harvard College | Methods and apparatus for manipulation of fluidic species |
| US20090068170A1 (en) | 2007-07-13 | 2009-03-12 | President And Fellows Of Harvard College | Droplet-based selection |
| US8592150B2 (en) | 2007-12-05 | 2013-11-26 | Complete Genomics, Inc. | Methods and compositions for long fragment read sequencing |
| JP5738597B2 (ja) | 2007-12-21 | 2015-06-24 | プレジデント アンド フェローズ オブ ハーバード カレッジ | 核酸の配列決定のためのシステムおよび方法 |
| US20090191276A1 (en) | 2008-01-24 | 2009-07-30 | Fellows And President Of Harvard University | Colloidosomes having tunable properties and methods for making colloidosomes having tunable properties |
| JP5468271B2 (ja) | 2008-02-08 | 2014-04-09 | 花王株式会社 | 微粒子分散液の製造方法 |
| US8802027B2 (en) | 2008-03-28 | 2014-08-12 | President And Fellows Of Harvard College | Surfaces, including microfluidic channels, with controlled wetting properties |
| KR20110042050A (ko) | 2008-06-05 | 2011-04-22 | 프레지던트 앤드 펠로우즈 오브 하바드 칼리지 | 폴리머좀, 콜로이드좀, 리포좀 및 유체 액적과 관련된 다른 종 |
| WO2010009365A1 (en) | 2008-07-18 | 2010-01-21 | Raindance Technologies, Inc. | Droplet libraries |
| WO2010033200A2 (en) | 2008-09-19 | 2010-03-25 | President And Fellows Of Harvard College | Creation of libraries of droplets and related species |
| US9156010B2 (en) | 2008-09-23 | 2015-10-13 | Bio-Rad Laboratories, Inc. | Droplet-based assay system |
| EP2373812B1 (en) | 2008-12-19 | 2016-11-09 | President and Fellows of Harvard College | Particle-assisted nucleic acid sequencing |
| CN101759882B (zh) | 2008-12-25 | 2012-02-29 | 陕西北美基因股份有限公司 | 交联葡聚糖磁性复合微粒及其制备方法及其使用 |
| CN103952482A (zh) | 2009-04-02 | 2014-07-30 | 弗卢伊蒂格姆公司 | 用于对目标核酸进行条形码化的多引物扩增方法 |
| EP4019977A1 (en) | 2009-06-26 | 2022-06-29 | President and Fellows of Harvard College | Fluid injection |
| EP2467479B1 (en) | 2009-08-20 | 2016-01-06 | Population Genetics Technologies Ltd | Compositions and methods for intramolecular nucleic acid rearrangement |
| KR20120089662A (ko) | 2009-09-02 | 2012-08-13 | 바스프 에스이 | 연접을 이용하여 생성된 다중 에멀젼 |
| US20120211084A1 (en) | 2009-09-02 | 2012-08-23 | President And Fellows Of Harvard College | Multiple emulsions created using jetting and other techniques |
| WO2011041496A1 (en) | 2009-09-30 | 2011-04-07 | Massachusetts Institute Of Technology | Phototriggered nanoparticles for cell and tissue targeting |
| JP5791621B2 (ja) | 2009-10-27 | 2015-10-07 | プレジデント アンド フェローズ オブ ハーバード カレッジ | 液滴生成技術 |
| WO2011056872A2 (en) | 2009-11-03 | 2011-05-12 | Gen9, Inc. | Methods and microfluidic devices for the manipulation of droplets in high fidelity polynucleotide assembly |
| US8835358B2 (en) | 2009-12-15 | 2014-09-16 | Cellular Research, Inc. | Digital counting of individual molecules by stochastic attachment of diverse labels |
| US10837883B2 (en) | 2009-12-23 | 2020-11-17 | Bio-Rad Laboratories, Inc. | Microfluidic systems and methods for reducing the exchange of molecules between droplets |
| AR080405A1 (es) | 2010-03-17 | 2012-04-04 | Basf Se | Emulsificacion para fundir |
| CA2767182C (en) | 2010-03-25 | 2020-03-24 | Bio-Rad Laboratories, Inc. | Droplet generation for droplet-based assays |
| US9138659B2 (en) | 2010-08-23 | 2015-09-22 | Massachusetts Institute Of Technology | Compositions, methods, and systems relating to controlled crystallization and/or nucleation of molecular species |
| DK2625320T3 (da) | 2010-10-08 | 2019-07-01 | Harvard College | High-throughput enkeltcellestregkodning |
| WO2012112804A1 (en) | 2011-02-18 | 2012-08-23 | Raindance Technoligies, Inc. | Compositions and methods for molecular labeling |
| WO2012162296A2 (en) | 2011-05-23 | 2012-11-29 | President And Fellows Of Harvard College | Control of emulsions, including multiple emulsions |
| CN103764272A (zh) | 2011-08-30 | 2014-04-30 | 哈佛学院院长等 | 壳包囊的体系和方法 |
| CA2848304A1 (en) | 2011-09-09 | 2013-03-14 | The Board Of Trustees Of The Leland Stanford Junior University | Methods for sequencing a polynucleotide |
| EP2788114B1 (en) | 2011-12-07 | 2021-03-24 | Givaudan SA | Process of making microcapsules |
| WO2013177220A1 (en) | 2012-05-21 | 2013-11-28 | The Scripps Research Institute | Methods of sample preparation |
| US20150005200A1 (en) | 2012-08-14 | 2015-01-01 | 10X Technologies, Inc. | Compositions and methods for sample processing |
| US9701998B2 (en) | 2012-12-14 | 2017-07-11 | 10X Genomics, Inc. | Methods and systems for processing polynucleotides |
| WO2014028537A1 (en) | 2012-08-14 | 2014-02-20 | 10X Technologies, Inc. | Microcapsule compositions and methods |
| US20140378349A1 (en) | 2012-08-14 | 2014-12-25 | 10X Technologies, Inc. | Compositions and methods for sample processing |
| EP3862435A1 (en) | 2013-02-08 | 2021-08-11 | 10X Genomics, Inc. | Polynucleotide barcode generation |
| WO2015069634A1 (en) | 2013-11-08 | 2015-05-14 | President And Fellows Of Harvard College | Microparticles, methods for their preparation and use |
| WO2015160919A1 (en) | 2014-04-16 | 2015-10-22 | President And Fellows Of Harvard College | Systems and methods for producing droplet emulsions with relatively thin shells |
| US20170224849A1 (en) | 2014-10-14 | 2017-08-10 | President And Fellows Of Harvard College | Microcapsules and uses thereof |
| EP3224419A4 (en) | 2014-11-24 | 2018-06-27 | President and Fellows of Harvard College | Multiple emulsions comprising rigidified portions |
| JP2017537776A (ja) | 2014-11-24 | 2017-12-21 | ザ プロクター アンド ギャンブル カンパニー | 液滴及び他の区画内での活性物質のカプセル化のためのシステム |
| US10258191B2 (en) | 2015-09-18 | 2019-04-16 | Starbucks Corporation | Beverage dispensing systems and methods |
| WO2017066231A1 (en) | 2015-10-13 | 2017-04-20 | President And Fellows Of Harvard College | Systems and methods for making and using gel microspheres |
| US20200197894A1 (en) | 2017-08-21 | 2020-06-25 | President And Fellow Of Harvard College | Poly(acid) microcapsules and related methods |
-
2016
- 2016-10-12 WO PCT/US2016/056509 patent/WO2017066231A1/en active Application Filing
- 2016-10-12 AU AU2016338907A patent/AU2016338907B2/en active Active
- 2016-10-12 CN CN201680068910.0A patent/CN108289797B/zh active Active
- 2016-10-12 CA CA3001679A patent/CA3001679A1/en not_active Abandoned
- 2016-10-12 EP EP16856059.7A patent/EP3362032A4/en active Pending
- 2016-10-12 JP JP2018519002A patent/JP2018537414A/ja active Pending
- 2016-10-12 US US15/768,135 patent/US11123297B2/en active Active
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2008535644A (ja) * | 2005-03-04 | 2008-09-04 | プレジデント・アンド・フエローズ・オブ・ハーバード・カレツジ | 多重エマルジョンの形成のための方法および装置 |
| US20140199731A1 (en) * | 2007-03-07 | 2014-07-17 | President And Fellows Of Harvard College | Assay and other reactions involving droplets |
| WO2010104604A1 (en) * | 2009-03-13 | 2010-09-16 | President And Fellows Of Harvard College | Method for the controlled creation of emulsions, including multiple emulsions |
| WO2012156744A2 (en) * | 2011-05-17 | 2012-11-22 | Cambridge Enterprise Limited | Gel beads in microfluidic droplets |
| JP2014522718A (ja) * | 2011-07-06 | 2014-09-08 | プレジデント アンド フェローズ オブ ハーバード カレッジ | 多相エマルションおよび多相エマルション形成法 |
Non-Patent Citations (1)
| Title |
|---|
| AICHE ANNUAL MEETING, JPN6021016848, 2007, pages 1 - 3, ISSN: 0004501036 * |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR102581886B1 (ko) * | 2022-05-30 | 2023-09-26 | 윤상훈 | 수성 페인트용 마이크로 비드 수분산체, 내오염성이 우수한 수성 페인트 조성물 및 이를 이용한 페인트 도장 시공 방법 |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2017066231A1 (en) | 2017-04-20 |
| CN108289797B (zh) | 2022-01-28 |
| EP3362032A4 (en) | 2019-05-01 |
| AU2016338907B2 (en) | 2022-07-07 |
| US11123297B2 (en) | 2021-09-21 |
| AU2016338907A1 (en) | 2018-05-10 |
| US20180296488A1 (en) | 2018-10-18 |
| CA3001679A1 (en) | 2017-04-20 |
| CN108289797A (zh) | 2018-07-17 |
| EP3362032A1 (en) | 2018-08-22 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2018537414A (ja) | ゲルマイクロスフェアの作製及び使用のためのシステム及び方法 | |
| US10738337B2 (en) | Assays and other reactions involving droplets | |
| Choi et al. | Recent advances in engineering microparticles and their nascent utilization in biomedical delivery and diagnostic applications | |
| US7776927B2 (en) | Emulsions and techniques for formation | |
| WO2016085743A1 (en) | Methods and systems for encapsulation of actives within droplets and other compartments | |
| JP2013525087A (ja) | 融解乳化 | |
| JP2013503742A (ja) | ジャンクションを使用して生成された多重エマルジョン | |
| WO2009061372A1 (en) | Systems and methods for creating multi-phase entities, including particles and/or fluids | |
| WO2016085746A1 (en) | Multiple emulsions comprising rigidified portions | |
| KR101654790B1 (ko) | 다중성분 마이크로입자의 제조방법 | |
| Martins et al. | Microfluidics as a Tool for the Synthesis of Advanced Drug Delivery Systems |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20191010 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20191010 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20201027 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210126 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20210511 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20211130 |