JP2017206751A - ニッケル粉末の製造方法 - Google Patents
ニッケル粉末の製造方法 Download PDFInfo
- Publication number
- JP2017206751A JP2017206751A JP2016101059A JP2016101059A JP2017206751A JP 2017206751 A JP2017206751 A JP 2017206751A JP 2016101059 A JP2016101059 A JP 2016101059A JP 2016101059 A JP2016101059 A JP 2016101059A JP 2017206751 A JP2017206751 A JP 2017206751A
- Authority
- JP
- Japan
- Prior art keywords
- nickel
- liquid
- powder
- aqueous solution
- mol
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Landscapes
- Manufacture Of Metal Powder And Suspensions Thereof (AREA)
- Powder Metallurgy (AREA)
Abstract
【課題】 ニッケル塩の水溶液とニッケルイオンに対して還元性を有する水溶液とを用いる湿式還元反応において、反応後のニッケル粒子に残留する炭素を始めとする不純物含有量を少なくさせ、かつ狭い粒度分布を有する平均粒径0.05μm〜0.45μmの球状ニッケル粉末を提供する。【解決手段】 ニッケル塩と、アンモニウムイオンと、ニッケルよりも貴な金属塩とを含む水溶液である第1液と、ニッケル及びニッケルよりも貴な金属に対して還元作用を有する水溶液である第2液と、ヒドロキシル基を有するアルカリ性の水溶液である第3液と、をすべて混合することで反応液とし、この反応液中でニッケルを晶析させるニッケル粉末の製造方法である。好ましくは反応液とする前の液の温度を10℃〜55℃とし、反応液を昇温させて55℃〜85℃とする。【選択図】 なし
Description
本発明は、積層セラミックコンデンサの内部電極材料となるニッケル粉末に関するものであって、ニッケル塩とニッケル塩の還元剤を用いる湿式還元反応によるニッケル粉末の製造に関する。
ニッケル粉末は、厚膜導電体を作製するための導電ペーストの材料として使用されている。厚膜導電体は、電気回路の形成や、積層セラミックコンデンサおよび多層セラミック基板等の積層セラミック部品の電極などに用いられている。
積層セラミック部品である積層セラミックコンデンサは、次のように製造されている。まず、ニッケル粉末とエチルセルロース等の樹脂とターピネオール等の有機溶剤等とを混練した導電ペーストを誘電体グリーンシート上にスクリーン印刷する。印刷された導電ペーストが交互に重なるように誘電体グリーンシートを積層し圧着する。その後、積層体を所定の大きさにカットし、有機バインダとして使用したエチルセルロース等の樹脂の燃焼、除去を行う脱バインダ処理を行って、1300℃まで高温焼成する。そして、このセラミック体に外部電極を取り付けて積層セラミックコンデンサとする。
近年、小型化、高容量化が求められている積層セラミックコンデンサは、内部電極、誘電体ともに薄層化が進められており、内部電極層と誘電体層が薄層化するに従って、内部電極層に使用されるニッケル粉末、誘電体層に使用されるチタン酸バリウム等は微粒化する傾向にある。
こうした背景を受け、気相法や湿式法による各種ニッケル粉末の開発が検討されている。
気相法において得られるニッケル粉末は、粒度分布が広くなりやすい傾向にあるものの、有機物を使用せず高温で合成するために残留炭素は無く、残留炭素に起因するコンデンサ特性の劣化やコンデンサ製造時のクラックなどは起きにくい。また粒度分布が広くなることによって発生する粗大粒子は、分級によって除去すれば良いが、歩留まり悪化によりコストが高くなる傾向にある。
気相法において得られるニッケル粉末は、粒度分布が広くなりやすい傾向にあるものの、有機物を使用せず高温で合成するために残留炭素は無く、残留炭素に起因するコンデンサ特性の劣化やコンデンサ製造時のクラックなどは起きにくい。また粒度分布が広くなることによって発生する粗大粒子は、分級によって除去すれば良いが、歩留まり悪化によりコストが高くなる傾向にある。
液体中で還元しニッケル粉末を得る湿式法においては、塩化ニッケルや硫酸ニッケルといったニッケル塩の水溶液と、水素化ホウ素ナトリウムやヒドラジンといった還元剤の水溶液と、水酸化ナトリウムやアンモニウム水溶液といったアルカリ性の水溶液と、特許文献1に開示されているように、必要に応じて更にクエン酸三ナトリウムといった錯化剤や、特許文献2や3に開示されているように核として有機系の保護コロイド剤を含む貴金属コロイドとを混合しニッケル粉末を得る方法が提案されている。
一般的に湿式法によって得られるニッケル粉末は、粒度分布が狭く単一粒子が得られやすく、気相法によるニッケル粉末のように分級を必要とせず、低コスト化しやすい。
しかし、ニッケル粉末の単分散性を高めること、粒度分布をシャープにすること等を目的として、還元反応系内に有機化合物である錯化剤などを添加している場合、ニッケル粉末中に炭素が残留し炭素含有量が高くなりやすい。特許文献4には、ニッケル粉末中の炭素含有量が高くなると、脱バインダ処理の際に残留炭素量が多くなり、積層セラミックコンデンサ特性の劣化やクラックが発生しやすくなることが記載されている)。
しかし、ニッケル粉末の単分散性を高めること、粒度分布をシャープにすること等を目的として、還元反応系内に有機化合物である錯化剤などを添加している場合、ニッケル粉末中に炭素が残留し炭素含有量が高くなりやすい。特許文献4には、ニッケル粉末中の炭素含有量が高くなると、脱バインダ処理の際に残留炭素量が多くなり、積層セラミックコンデンサ特性の劣化やクラックが発生しやすくなることが記載されている)。
一方で、有機化合物を添加せず、塩化ニッケルや硫酸ニッケルといったニッケル塩の水溶液と、水素化ホウ素ナトリウムやヒドラジンといった還元剤の水溶液と、水酸化ナトリウムやアンモニウム水溶液といったアルカリ性の水溶液のみを用いた際には、平均粒子径が0.3μm以上のニッケル粉末、もしくは粒度分布が比較的均一であるものの連結粗大粒子が存在しており更に均一で単分散にする余地があるニッケル粉末しか得られていない。更には、特許文献5にはニッケル100gに対して60%水加ヒドラジンを500mL使用することが実施例に示されたり、特許文献6には還元剤の推奨量が5〜15モル/ニッケルイオンであることが開示されたりと、ニッケルの還元に対して理論量よりも、かなり過剰な還元剤量を使用しており、高コストである。
また特許文献7には、水酸化ニッケルを生成させ、水酸化ニッケル粉末を焙焼し酸化ニッケルを得た後に、水素ガスによる還元雰囲気で還元しニッケル粉末を得る方法が提案されている(文献7)。この方法によるニッケル粉末は、有機物を使用していないために残留炭素は存在していないが、ニッケル粉末の形状が不均一であり、その製造時に精密な制御を必要とする内部電極が薄層化された積層セラミックコンデンサを製造することは困難である。
また特許文献7には、水酸化ニッケルを生成させ、水酸化ニッケル粉末を焙焼し酸化ニッケルを得た後に、水素ガスによる還元雰囲気で還元しニッケル粉末を得る方法が提案されている(文献7)。この方法によるニッケル粉末は、有機物を使用していないために残留炭素は存在していないが、ニッケル粉末の形状が不均一であり、その製造時に精密な制御を必要とする内部電極が薄層化された積層セラミックコンデンサを製造することは困難である。
こうしたことから、低コストで粒度分布が狭い球状ニッケル粉末を得ることが容易な湿式法において、炭素を始めとした残留不純物が少ないニッケル粉末が求められており、湿式法において炭素を含む原材料を使用せず、かつ、容易に0.4μm〜0.5μm以下の微粒化ができ、粒度が均一となるニッケル粉末の合成方法が求められている。
積層セラミックコンデンサ用のニッケル粉末を得るためにニッケル塩の水溶液とニッケルイオンに対して還元性を有する水溶液とを用いる湿式還元反応において、反応後のニッケル粒子に残留する炭素を始めとする不純物含有量を少なくさせ、かつ狭い粒度分布を有する平均粒径0.05μm〜0.45μmの球状ニッケル粉末を提供することにある。
本発明の第1の発明は、ニッケル塩と、アンモニウムイオンと、ニッケルよりも貴な金属塩とを含む水溶液である第1液と、ニッケル及びニッケルよりも貴な金属に対して還元作用を有する水溶液である第2液と、ヒドロキシル基を有するアルカリ性の水溶液である第3液と、をすべて混合することで反応液とし、この反応液中でニッケルを晶析させることを特徴とするニッケル粉末の製造方法である。
本発明の第2の発明は、第1の発明において反応液とする前の第1液、第2液、第3液、及び第1液から第3液の任意の2液を混合させた混合液の温度が、10℃〜55℃であることを特徴とするニッケル粉末の製造方法である。
本発明の第3の発明は、第2の発明における反応液を昇温させて55℃〜85℃とすることを特徴とするニッケル粉末の製造方法である。
本発明の第4の発明は、第1〜3のいずれかの発明において、ニッケル及びニッケルよりも貴な金属に対して還元作用を有する水溶液が、ヒドラジンまたはその水化物の水溶液であることを特徴とするニッケル粉末の製造方法である。
本発明の第5の発明は、第4の発明において、ニッケルよりも貴な金属の総量がニッケルに対して1質量ppm〜10000質量ppmであり、アンモニウムイオン量が1〜6モル/ニッケルイオン1モルであり、ヒドラジンまたはその水化物の水溶液がヒドラジン量で1.3〜5.5モル/ニッケルイオン1モルであり、ヒドロキシル基を有するアルカリ性水溶液が水酸化物イオン量で2.0〜10モル/ニッケルイオン1モルであることを特徴とするニッケル粉末の製造方法である。
本発明の第6の発明は、第5の発明におけるニッケル塩が、塩化ニッケル、硫酸ニッケルのいずれか若しくはそれらの混合物であることを特徴とするニッケル粉末の製造方法である。
本発明の第7の発明は、第5、6の発明におけるアンモニウムイオン源が、アンモニア水であることを特徴とするニッケル粉末の製造方法である。
本発明の第8の発明は、第5〜7のいずれかの発明におけるニッケルよりも貴な金属が、パラジウム、銀、銅のいずれか若しくはそれらの混合物であることを特徴とするニッケル粉末の製造方法である。
本発明の第9の発明は、第5〜8のいずれかの発明におけるヒドロキシル基を有するアルカリ性水溶液が、水酸化ナトリウム、水酸化カリウムの少なくともいずれかを含む水溶液であることを特徴とするニッケル粉末の製造方法である。
本発明の製造方法により得られたニッケル粉末は、平均粒径が0.05μm〜0.45μmで炭素を始めとする不純物含有量が少なく、球状でシャープな粒度分布を有している。このニッケル粉末を積層セラミックコンデンサの内部電極に用いれば、薄層化された積層セラミックコンデンサにおいても特性の劣化やクラック等を起こさずに製造することができる。
本発明のニッケル粉末は、ニッケルイオン源としてのニッケル塩とアンモニウムイオンとニッケルよりも貴な金属塩を含む水溶液(第1液)と、ニッケル及びニッケルよりも貴な金属に対して還元作用を有する水溶液(第2液)と、ヒドロキシル基を有するアルカリ性水溶液(第3液)とを混合することによって反応液とし、ニッケルを晶析させる。晶析したニッケル(以降ニッケル晶析粉とすることもある)は粒子が容易に解される程度に結合した凝集体を形成し、そのニッケル晶析粉の凝集体を洗浄、固液分離し、比較的軽度の機械的なせん断力で解して(解砕)から乾燥することでニッケル粉末とする手順で製造される。ここで以降の説明では、第1液から第3液の任意の2液を混合させた液を混合液、第1液から第3液のすべての液を混合させた液を反応液と区別している。もちろん回分式反応器で行う場合は、これらの操作では十分に撹拌された状態で行うのが望ましい。流通式管型反応器で行う場合は、第1液から第三液が決まった順序や混合割合で混合できれば良い。
第1液と第2液と第3液の混合順序は、特に限定しない。例えば、第1液に第2液を添加して混合液とした後に第3液を混合して反応液とする方法、第3液に第2液を添加して混合液とした後に第1液を添加して反応液とする方法などがある。
最も望ましい添加順序は、第1液と第2液とを混合し、その後、第1液と第2液の混合液に第3液を添加する方法である。その理由としては、第1液に含まれるニッケルとニッケルよりも貴な金属は、全てアンモニウム錯体となり均一な水溶液であり、その中に、ニッケル及びニッケルよりも貴な金属に対して還元作用を有する水溶液を入れても固体が析出することなく均一な液にすることができ、その後、反応開始の駆動力になるアルカリ性を有する水溶液を添加することで、より系内が均一な状態で反応させることができるためである。また、第2液としてヒドラジンを用いた場合は、自己分解してしまうためニッケルの還元に必要な理論値よりも多くの量を添加する必要があるが、本添加順序であれば自己分解によるヒドラジン消費を抑制できニッケルの還元にヒドラジンが効率よく使用され、ニッケルに対するヒドラジン添加量を大幅に減らすことが可能である。
最も望ましい添加順序は、第1液と第2液とを混合し、その後、第1液と第2液の混合液に第3液を添加する方法である。その理由としては、第1液に含まれるニッケルとニッケルよりも貴な金属は、全てアンモニウム錯体となり均一な水溶液であり、その中に、ニッケル及びニッケルよりも貴な金属に対して還元作用を有する水溶液を入れても固体が析出することなく均一な液にすることができ、その後、反応開始の駆動力になるアルカリ性を有する水溶液を添加することで、より系内が均一な状態で反応させることができるためである。また、第2液としてヒドラジンを用いた場合は、自己分解してしまうためニッケルの還元に必要な理論値よりも多くの量を添加する必要があるが、本添加順序であれば自己分解によるヒドラジン消費を抑制できニッケルの還元にヒドラジンが効率よく使用され、ニッケルに対するヒドラジン添加量を大幅に減らすことが可能である。
第1液を構成するニッケルよりも貴な金属塩の水溶液は、ニッケルに対して還元作用を有する水溶液(第2液)やニッケル水酸化物を形成させるヒドロキシル基を有するアルカリ性水溶液(第3液)を添加する前に、ニッケル塩の水溶液またはニッケル塩とアンモニウムが含まれる水溶液と混合することが望ましい。ニッケルよりも貴な金属塩は、後述するよう核剤としてニッケル晶析粉生成の核として用いるが、その理由は、還元作用を有する第2液を添加した後に、ニッケルよりも貴な金属塩の水溶液を添加すると、ニッケルよりも貴な金属イオンが系内で均一な状態になる前に還元してしまい、ニッケルよりも貴な金属の核が成長して大きくなり核数が減少してしまい、必要な核数を得るためにニッケルよりも貴な金属塩を多量に添加する必要がでてしまうためである。また、第3液をニッケル塩の水溶液に添加してニッケル水酸化物を形成させた後にニッケルよりも貴な金属塩の水溶液を添加すると、系内でニッケル水酸化物と核剤が不均一な状態で存在してしまい、還元で得られたニッケル粉末の粒度分布が広くなるためである。
第1液と第2液と第3液とを混合する際には、反応液とする前の混合前の各液と第1液から第3液の任意の2液を混合させた混合液の温度を10℃〜55℃とするのが望ましい。55℃よりも高い温度で混合すると、所定量の第1液と第2液と第3液とを混合させた反応液が均一な状態となる前に、ニッケルへの還元が開始され、不均一な液の状態となり粒度分布が広くなったり、連結粒子や粗大粒子が発生したりするためである。また、高温にすると、特に第1液を構成するアンモニウムイオン源としてアンモニア水を用いる場合には、アンモニア水が沸騰してしまい、蒸発気化して量が減ってしまう。10℃よりも低い場合は、ニッケルイオンがニッケルまで還元される反応が起きるまでに時間がかかり生産性が低下する。
第1液から第3液のすべてを混合して反応液とした後の液温は、混合前の10℃〜55℃で保持してもよいが、反応液とした後で昇温して55℃〜85℃とするのがさらに望ましい。反応液とした後で均一な液な状態でニッケルへの還元が開始し、その後で昇温することで、得られるニッケル粉末は狭い粒度分布を維持しながら反応が促進され生産性が向上する。しかし反応液は85℃を超えて昇温させると、反応速度が速くなりすぎて粒度分布が広くなることがある。
第1液であるニッケル塩とニッケルよりも貴な金属塩とアンモニウムイオンとを混合した水溶液の作製においては、ニッケル塩とニッケルよりも貴な金属塩とアンモニウムイオンの混合の仕方は特に限定しない。例えば、ニッケル塩の水溶液に、ニッケルよりも貴な金属塩の水溶液を添加した後にアンモニウムイオン源を添加する方法、アンモニウムイオン源にニッケル塩の水溶液を添加した後に、ニッケルよりも貴な金属の水溶液を添加する方法などが挙げられる。
ニッケルよりも貴な金属塩は、ニッケル粉末中のニッケルに対してニッケルよりも貴な金属が、1質量ppm〜10000質量ppmとなるように添加することで平均粒径が0.05μm〜0.45μmのニッケル粉末を得ることができる。ニッケルより貴な金属塩は反応液中でニッケル晶析時の核剤として働き、添加量が増加するに従いニッケル粉末は微細化されて平均粒径は低下するが、1質量ppm未満ではこの微細化の効果が十分に得られない。上限については特に限定されないが、10000質量ppmを超えて添加したとしても、更なる微細化の効果は得られない。
ニッケル塩は、塩化ニッケル、硫酸ニッケル、硝酸ニッケル、及びそれらの混合物が望ましく、更には塩化ニッケル、硫酸ニッケルが望ましい。硝酸ニッケルの場合、反応後液において硝酸イオンが加えられ反応後液の窒素処理負荷が増すことになる。酢酸ニッケルのような有機系ニッケル化合物の使用は、ニッケル粉末に炭素が残留しやすくなるので避けることが望ましい。
ニッケルよりも貴な金属塩としては、銅、パラジウム、白金、イリジウム、銀などが望ましく、比較的安価であるパラジウム、銀、銅が更には望ましい。これらの金属塩は、各々の単体で添加しても良いし、混合物で添加してもよい。
アンモニウムイオンは、反応液中のニッケルイオンに対して1モル〜6モル/ニッケルイオン1モルとなるように添加することが望ましく、2.5モル〜4モル/ニッケルイオン1モルが更に望ましい。1モル/ニッケルイオン1モル未満であると、還元剤を入れた際に還元剤とニッケルによる化合物が析出してしまい系内が不均一状態となり歪な粒子しか得られない。ニッケルはアンモニウムイオンと錯体を形成してヘキサアンミンニッケルイオン等のアンモニウム錯体となり、最大6配位になるので、アンモニウムイオンを6モル/ニッケルイオン1モルよりも多量に入れても、反応に寄与しないアンモニウムイオンが増えるだけで得られたニッケル粉末において特別な性能は得られず廃液処理コストが増加するだけである。更には、アンモニウムイオンが2.5モル〜4モル/ニッケルイオン1モルの範囲であると、ニッケルのアンモニウム錯体は反応液中で過飽和度が高くなりやすく、ニッケルよりも貴な金属である核剤量を比較的に少ない条件でも容易に微粒化することができ、核剤コストを抑えることができる。
アンモニウムイオン源としては、アンモニア水、炭酸アンモニウム、塩化アンモニウム、硝酸アンモニウム等、アンモニア水または無機アンモニウム化合物、及びそれらの混合物が望ましい。得られるニッケル粉末の不純物含有量の観点から、アンモニア水を用いるのが更に望ましい。第2液であるニッケル及びニッケルよりも貴な金属に対して還元作用を有する水溶液は、還元作用を有する物質であれば良いが、ニッケル粉末の不純物含有量の観点から無機物のヒドラジンまたはその水化物、水素化ホウ素ナトリウム、及びそれらの混合物の水溶液が望ましく、窒素と水素のみの元素で構成されているヒドラジンまたはその水化物の水溶液が不純物含有量の観点で更に望ましい。
ヒドラジンは、反応液中のニッケルイオンに対して1.3モル〜5.5モル/ニッケルイオン1モルであることが望ましく、更には1.3モル〜2モル/ニッケルイオン1モルであることが望ましい。その理由としては、5.5モル/ニッケルイオン1モルよりも多い量を添加すると、連結したニッケル粉末や粗大化したニッケル粉末が発生してしまい、粒度分布が狭いニッケル粉末を得ることができないためである。また、1.3モル〜5.5モル/ニッケルイオン1モルであると、反応液中で0.05μm〜0.45μmのニッケル晶析粉を形成した後にこれらが数百μmの凝集体を形成し固液分離が容易になること、その凝集体が比較的軽度の機械的なせん断力で容易に解れ0.05〜0.45μmの単分散のニッケル粒子にすることができること、ニッケル粉末の製造費用に占めるヒドラジン費用を低減することができるためである。還元剤が1.3モル/ニッケルイオン1モルよりも少ない場合、一部凝集体を形成するが、一部未凝集で分散状態である。そのため反応終了後の液が黒色であり、次工程以降での固液分離の際に、ニッケル晶析粉が液側に分配されやすくロスが発生しやすい。また、場合によっては一部未還元のニッケルが存在してしまう場合もある。
第3液であるヒドロキシル基を有するアルカリ性水溶液は、強アルカリであればよく、水酸化アルカリである水酸化ナトリウム、水酸化カリウム、水酸化リチウムなどの水溶液が挙げられるが、特に広く一般的に使われ、残留不純物が少ない水酸化ナトリウム、水酸化カリウムの少なくともいずれかを含む水溶液が望ましい。
ヒドロキシル基を有するアルカリ性水溶液は、反応液中のニッケルイオンに対して水酸化物イオン量で2.0〜10モル/ニッケルイオン1モルが望ましい。この量よりも少ない場合、反応液中で過飽和度が低くなり生成する核数が少なくなりニッケル粉末が大きくなりやすい。またニッケル粉末の形状も悪化し、球状性が低下する。10モル/ニッケルイオンよりも多い場合も、ニッケル粒子が大きくなりやすい。理由は不明だが、ニッケル晶析粉の凝集体も得られ難くなることから、ニッケルよりも貴な金属の核が凝集しやすくなり、見かけ上、核数が減少するためと思われる。
ヒドロキシル基を有するアルカリ性水溶液は、反応液中のニッケルイオンに対して水酸化物イオン量で2.0〜10モル/ニッケルイオン1モルが望ましい。この量よりも少ない場合、反応液中で過飽和度が低くなり生成する核数が少なくなりニッケル粉末が大きくなりやすい。またニッケル粉末の形状も悪化し、球状性が低下する。10モル/ニッケルイオンよりも多い場合も、ニッケル粒子が大きくなりやすい。理由は不明だが、ニッケル晶析粉の凝集体も得られ難くなることから、ニッケルよりも貴な金属の核が凝集しやすくなり、見かけ上、核数が減少するためと思われる。
このようにして反応液からニッケル晶析粉の凝集体を生成させた後、洗浄、固液分離して凝集体を取出し、この凝集体を解してから乾燥させることでニッケル粉末とする。
洗浄は、特にその方法は限定されることはなく公知の方法を用いればよいが、反応液中のニッケル晶析粉の凝集体を静置沈降させた後、上澄み液を除去してから洗浄液を添加し、一定時間撹拌してから再度ニッケル晶析粉の凝集体を静置沈降させる手順とすることができる。またこの手順を複数回繰り返してもよい。
洗浄は、特にその方法は限定されることはなく公知の方法を用いればよいが、反応液中のニッケル晶析粉の凝集体を静置沈降させた後、上澄み液を除去してから洗浄液を添加し、一定時間撹拌してから再度ニッケル晶析粉の凝集体を静置沈降させる手順とすることができる。またこの手順を複数回繰り返してもよい。
洗浄液についても特に限定されることはないが、純水やエタノール等を用いればよい。洗浄温度についても特に限定されることはないが、15℃〜40℃とするのが望ましい。
固液分離は、ニッケル晶析粉の凝集体の量などを勘案して、公知のろ過方法を適宜選択すればよい。
固液分離は、ニッケル晶析粉の凝集体の量などを勘案して、公知のろ過方法を適宜選択すればよい。
固液分離後に凝集体を解すために解砕処理を行う。解砕とは、粒子が弱く結合した凝集体を対象として、その個々の粒子にダメージを与えないように比較的軽度の機械的せん断力(外力)を加えることで、弱く結合した凝集体から個々の粒子を分離する処理である。その方法は公知の方法を用いればよく、例えばニッケル晶析粉の凝集体の量が少ない場合には、薬さじを用いて行ってもよい。量が多くなれば、公知の解砕装置を用いることとなるが、ニッケル晶析粉にダメージを与えないような条件設定とすればよい。また、解砕処理を行った後に、再度洗浄をしてもよい。
最後に乾燥させてニッケル粉末とする。乾燥方法についても特に限定されることはなく、公知の温風乾燥、減圧乾燥、真空乾燥等を用いればよい。
このようにして得られたニッケル粉末は、球状で、平均粒径が0.05μm〜0.45μmであり、粒度分布も狭くなる。さらに、反応液中に有機物を用いていないので、不純物含有量、特に炭素含有量を低減することができる。
以下、各実施例及び比較例によって本発明を詳細に説明するが、本発明は、これらの実施例及び比較例によって何ら限定されるものではない。なお、実施例及び比較例でそれぞれ得られたニッケル粉末の粒子形状、平均粒径、粒度分布、炭素等の不純物含有量の測定方法は、以下に示す通りである。
(1)ニッケル粉末の粒子形状、平均粒径、粒度分布
ニッケル粉末を、走査型電子顕微鏡(SEM:Scanning Electron Microscope、日本電子社製、JSM−5510)を用いて、倍率20000倍で観察して粒子形状を測定した。また平均粒径は、その観察像の写真(縦19.2μm×横25.6μm)を撮影し、写真中の粒子形状の全様が見える粒子の面積を測定し、面積から各粒子の直径を求め、その平均値により定めた。さらに粒度分布は各粒子の直径の標準偏差を、その平均値で除した値が0.2以下の場合を「狭い」、0.2を超えた場合を「広い」とした。
ニッケル粉末を、走査型電子顕微鏡(SEM:Scanning Electron Microscope、日本電子社製、JSM−5510)を用いて、倍率20000倍で観察して粒子形状を測定した。また平均粒径は、その観察像の写真(縦19.2μm×横25.6μm)を撮影し、写真中の粒子形状の全様が見える粒子の面積を測定し、面積から各粒子の直径を求め、その平均値により定めた。さらに粒度分布は各粒子の直径の標準偏差を、その平均値で除した値が0.2以下の場合を「狭い」、0.2を超えた場合を「広い」とした。
(2)ニッケル粉末の酸素、炭素、硫黄の含有量
ニッケル粉の硫黄と炭素の含有量は分析装置(LECO社製、CS−600)にて測定した。ニッケル粉末の酸素の含有量は分析装置(LECO社製、TC−436AR)にて測定した。
ニッケル粉の硫黄と炭素の含有量は分析装置(LECO社製、CS−600)にて測定した。ニッケル粉末の酸素の含有量は分析装置(LECO社製、TC−436AR)にて測定した。
(3)塩素の含有量
硝酸水溶液に過酸化水素を添加した後に試料を添加し、加熱冷却した後に硝酸とよう化カリウムと硝酸銀を添加し固液分離し、固形物を蛍光X線分析にて測定した。
硝酸水溶液に過酸化水素を添加した後に試料を添加し、加熱冷却した後に硝酸とよう化カリウムと硝酸銀を添加し固液分離し、固形物を蛍光X線分析にて測定した。
(4)ナトリウムの含有量
硝酸水溶液に試料を添加し加熱分解した後に、イットリウムと水を添加し、その後硝酸を添加し、原子吸光分析にて測定した。
硝酸水溶液に試料を添加し加熱分解した後に、イットリウムと水を添加し、その後硝酸を添加し、原子吸光分析にて測定した。
(実施例1)
28℃のニッケル濃度100g/Lの塩化ニッケル水溶液500mLを5Lビーカーに計量し、塩化ニッケル中のニッケルに対してパラジウムが10質量ppm含まれるように計量した10℃の塩化パラジウム水溶液1mLを添加し撹拌した。その後、撹拌しながら28℃の25%アンモニア水(比重0.91g/mL)を200mL(3.14モル/ニッケルイオン1モル)添加して第1液とした。アンモニア水を添加した時点で発熱するが、冷却し28℃とした後に、この第1液に第2液である28℃の60%抱水ヒドラジン(比重1.03g/mL)100mL(2.59モル/ニッケルイオン1モル)を添加した。この混合液に第3液として28℃の365g/Lの水酸化ナトリウム水溶液300mL(水酸化物イオン3.21モル/ニッケルイオン1モル)を添加して反応液とし、反応液を80℃まで昇温させながら、ニッケル晶析粉を生成させた。ニッケル晶析終了時には、ニッケル晶析粉は凝集体を形成して沈降し、反応液は透明であった。
得られたニッケル晶析粉をさらに静置沈降させて上澄液を除去した後に1L純水を加え撹拌し、上澄液を除去した後に、ヌッチェにて固液分離を行い、凝集体を薬さじで解し圧密した後に、0.5Lの純水で掛け水洗浄を行った。その後、150℃で真空乾燥を24時間した後に、大気圧まで空気導入しニッケル粉末回収した。
28℃のニッケル濃度100g/Lの塩化ニッケル水溶液500mLを5Lビーカーに計量し、塩化ニッケル中のニッケルに対してパラジウムが10質量ppm含まれるように計量した10℃の塩化パラジウム水溶液1mLを添加し撹拌した。その後、撹拌しながら28℃の25%アンモニア水(比重0.91g/mL)を200mL(3.14モル/ニッケルイオン1モル)添加して第1液とした。アンモニア水を添加した時点で発熱するが、冷却し28℃とした後に、この第1液に第2液である28℃の60%抱水ヒドラジン(比重1.03g/mL)100mL(2.59モル/ニッケルイオン1モル)を添加した。この混合液に第3液として28℃の365g/Lの水酸化ナトリウム水溶液300mL(水酸化物イオン3.21モル/ニッケルイオン1モル)を添加して反応液とし、反応液を80℃まで昇温させながら、ニッケル晶析粉を生成させた。ニッケル晶析終了時には、ニッケル晶析粉は凝集体を形成して沈降し、反応液は透明であった。
得られたニッケル晶析粉をさらに静置沈降させて上澄液を除去した後に1L純水を加え撹拌し、上澄液を除去した後に、ヌッチェにて固液分離を行い、凝集体を薬さじで解し圧密した後に、0.5Lの純水で掛け水洗浄を行った。その後、150℃で真空乾燥を24時間した後に、大気圧まで空気導入しニッケル粉末回収した。
得られたニッケル粉末をSEM観察し、平均粒径、粒子形状、粒度分布を測定した。SEM観察より、固液分離後の薬さじによる解しでも十分に凝集体が解され、単分散したニッケル粉末であることが確認された。続けてニッケル粉末中の不純物(酸素、炭素、および原材料起因のナトリウムと塩素)含有量を測定した。これらを表1に示す。
(実施例2)
第1液の塩化ニッケル水溶液の液温を10℃としたこと、第1液に第2液を添加した混合液を10℃とした後に、第3液として10℃の水酸化ナトリウム水溶液を添加したこと以外は、実施例1と同様の手順で実施した。
ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
第1液の塩化ニッケル水溶液の液温を10℃としたこと、第1液に第2液を添加した混合液を10℃とした後に、第3液として10℃の水酸化ナトリウム水溶液を添加したこと以外は、実施例1と同様の手順で実施した。
ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
(実施例3)
第1液の塩化ニッケル水溶液の液温を55℃としたこと、第1液に第2液を添加した混合液を55℃とした後に、第3液として55℃の水酸化ナトリウム水溶液を添加したこと以外は、以外は、実施例1と同様の手順で実施した。
ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
第1液の塩化ニッケル水溶液の液温を55℃としたこと、第1液に第2液を添加した混合液を55℃とした後に、第3液として55℃の水酸化ナトリウム水溶液を添加したこと以外は、以外は、実施例1と同様の手順で実施した。
ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
(実施例4)
第1液の塩化パラジウム水溶液の液温を28℃としたこと、第1液に第2液を添加した混合液を混合後に45℃まで加温した後に、第3液として28℃の水酸化ナトリウム水溶液を添加したこと以外は、実施例1と同様の手順で実施した。
ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
第1液の塩化パラジウム水溶液の液温を28℃としたこと、第1液に第2液を添加した混合液を混合後に45℃まで加温した後に、第3液として28℃の水酸化ナトリウム水溶液を添加したこと以外は、実施例1と同様の手順で実施した。
ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
(実施例5)
第2液として28℃の60%抱水ヒドラジン(比重1.03g/mL)100mL(2.59モル/ニッケルイオン1モル)を5Lビーカーに計量し、更に第3液として28℃の365g/Lの水酸化ナトリウム水溶液300mL(水酸化物イオン3.21モル/ニッケルイオン1モル)を加え撹拌し混合液とした。また、別の容器に第1液として、28℃のニッケル濃度100g/Lの塩化ニッケル水溶液500mLを2Lビーカーに計量し、ニッケルに対してパラジウムが10質量ppm含まれる塩化パラジウム水溶液1mLを添加し撹拌し、撹拌しながら28℃の25%アンモニア水(比重0.91g/mL)を200mL(3.14モル/ニッケルイオン1モル)添加した。この第1液を、室温にて、水酸化ナトリウムとヒドラジンを含む混合液に添加して反応液とし、撹拌しながら80℃まで昇温させ、ニッケル晶析粉を生成させた。
その後の手順は実施例1と同様の手順で実施した。
ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
第2液として28℃の60%抱水ヒドラジン(比重1.03g/mL)100mL(2.59モル/ニッケルイオン1モル)を5Lビーカーに計量し、更に第3液として28℃の365g/Lの水酸化ナトリウム水溶液300mL(水酸化物イオン3.21モル/ニッケルイオン1モル)を加え撹拌し混合液とした。また、別の容器に第1液として、28℃のニッケル濃度100g/Lの塩化ニッケル水溶液500mLを2Lビーカーに計量し、ニッケルに対してパラジウムが10質量ppm含まれる塩化パラジウム水溶液1mLを添加し撹拌し、撹拌しながら28℃の25%アンモニア水(比重0.91g/mL)を200mL(3.14モル/ニッケルイオン1モル)添加した。この第1液を、室温にて、水酸化ナトリウムとヒドラジンを含む混合液に添加して反応液とし、撹拌しながら80℃まで昇温させ、ニッケル晶析粉を生成させた。
その後の手順は実施例1と同様の手順で実施した。
ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
(実施例6)
第1液として、28℃のニッケル濃度100g/Lの塩化ニッケル水溶液500mLを5Lビーカーに計量し、ニッケルに対してパラジウムが10質量ppm含まれる28℃の塩化パラジウム水溶液1mLを添加し撹拌し、撹拌しながら28℃の25%アンモニア水(比重0.91g/mL)を200mL(3.14モル/ニッケルイオン1モル)添加した。その後、この第1液に撹拌しながら第3液である28℃の365g/Lの水酸化ナトリウム水溶液300mL(水酸化物イオン3.21モル/ニッケルイオン1モル)を添加して混合液とした。その後、更にこの混合液に第2液として28℃の60%抱水ヒドラジン(比重1.03g/mL)100mL(2.59モル/ニッケルイオン1モル)を添加して反応液とし、撹拌しながら80℃まで昇温させ、ニッケル晶析粉を生成させた。
その後の手順は実施例1と同様の手順で実施した。
第1液として、28℃のニッケル濃度100g/Lの塩化ニッケル水溶液500mLを5Lビーカーに計量し、ニッケルに対してパラジウムが10質量ppm含まれる28℃の塩化パラジウム水溶液1mLを添加し撹拌し、撹拌しながら28℃の25%アンモニア水(比重0.91g/mL)を200mL(3.14モル/ニッケルイオン1モル)添加した。その後、この第1液に撹拌しながら第3液である28℃の365g/Lの水酸化ナトリウム水溶液300mL(水酸化物イオン3.21モル/ニッケルイオン1モル)を添加して混合液とした。その後、更にこの混合液に第2液として28℃の60%抱水ヒドラジン(比重1.03g/mL)100mL(2.59モル/ニッケルイオン1モル)を添加して反応液とし、撹拌しながら80℃まで昇温させ、ニッケル晶析粉を生成させた。
その後の手順は実施例1と同様の手順で実施した。
ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
(実施例7)
第1液として28℃のニッケル濃度100g/Lの硫酸ニッケル水溶液500mLを5Lビーカーに計量し、ニッケルに対してパラジウムが10質量ppm含まれる28℃の塩化パラジウム水溶液1mLを添加し撹拌した。その後、撹拌しながら28℃の25%アンモニア水(比重0.91g/mL)を200mL(3.14モル/ニッケルイオン1モル)添加した。この第1液に、撹拌しながら第2液として28℃の60%抱水ヒドラジン(比重1.03g/mL)100mL(2.59モル/ニッケルイオン1モル)を添加して混合液とした。その後、更にこの混合液に第3液として28℃の365g/Lの水酸化ナトリウム水溶液300mL(水酸化物イオン3.21モル/ニッケルイオン1モル)を添加して反応液とし、撹拌しながら80℃まで昇温させ、ニッケル晶析粉を生成させた。
その後の手順は実施例1と同様の手順で実施した。
第1液として28℃のニッケル濃度100g/Lの硫酸ニッケル水溶液500mLを5Lビーカーに計量し、ニッケルに対してパラジウムが10質量ppm含まれる28℃の塩化パラジウム水溶液1mLを添加し撹拌した。その後、撹拌しながら28℃の25%アンモニア水(比重0.91g/mL)を200mL(3.14モル/ニッケルイオン1モル)添加した。この第1液に、撹拌しながら第2液として28℃の60%抱水ヒドラジン(比重1.03g/mL)100mL(2.59モル/ニッケルイオン1モル)を添加して混合液とした。その後、更にこの混合液に第3液として28℃の365g/Lの水酸化ナトリウム水溶液300mL(水酸化物イオン3.21モル/ニッケルイオン1モル)を添加して反応液とし、撹拌しながら80℃まで昇温させ、ニッケル晶析粉を生成させた。
その後の手順は実施例1と同様の手順で実施した。
ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。なおニッケル塩として塩化ニッケルの替わりに硫酸ニッケルを用いたため、不純物含有量の測定では塩素の替わりに硫黄を対象とした。
(実施例8)
第1液として28℃のニッケル濃度100g/Lの塩化ニッケル水溶液500mLを5Lビーカーに計量し、その中に、ニッケルに対してパラジウムが10質量ppm含まれる28℃のジクロロテトラアンミンパラジウム水溶液1mLとニッケルに対して銀が1質量ppm含まれる28℃のジクロロジアンミン銀水溶液1mLとの混合液を添加、撹拌し、撹拌しながら28℃の25%アンモニア水(比重0.91g/mL)を200mL(3.14モル/ニッケルイオン1モル)添加した。その後、この第1液に撹拌しながら第3液として28℃の365g/Lの水酸化ナトリウム水溶液300mL(水酸化物イオン3.21モル/ニッケルイオン1モル)を添加して混合液とした。その後、この混合液に更に第2液として28℃の60%抱水ヒドラジン(比重1.03g/mL)100mL(2.59モル/ニッケルイオン1モル)を添加して反応液とし、撹拌しながら80℃まで昇温させ、ニッケル晶析粉を生成させた。
その後の手順は実施例1と同様の手順で実施した。
第1液として28℃のニッケル濃度100g/Lの塩化ニッケル水溶液500mLを5Lビーカーに計量し、その中に、ニッケルに対してパラジウムが10質量ppm含まれる28℃のジクロロテトラアンミンパラジウム水溶液1mLとニッケルに対して銀が1質量ppm含まれる28℃のジクロロジアンミン銀水溶液1mLとの混合液を添加、撹拌し、撹拌しながら28℃の25%アンモニア水(比重0.91g/mL)を200mL(3.14モル/ニッケルイオン1モル)添加した。その後、この第1液に撹拌しながら第3液として28℃の365g/Lの水酸化ナトリウム水溶液300mL(水酸化物イオン3.21モル/ニッケルイオン1モル)を添加して混合液とした。その後、この混合液に更に第2液として28℃の60%抱水ヒドラジン(比重1.03g/mL)100mL(2.59モル/ニッケルイオン1モル)を添加して反応液とし、撹拌しながら80℃まで昇温させ、ニッケル晶析粉を生成させた。
その後の手順は実施例1と同様の手順で実施した。
ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
(実施例9)
パラジウムを10000質量ppmとしたこと以外は、実施例1と同様としてニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
パラジウムを10000質量ppmとしたこと以外は、実施例1と同様としてニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
(実施例10)
パラジウムを200質量ppmとしたこと以外は、実施例1と同様としてニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
パラジウムを200質量ppmとしたこと以外は、実施例1と同様としてニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
(実施例11)
パラジウムを50質量ppmとしたこと以外は、実施例1と同様としてニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
パラジウムを50質量ppmとしたこと以外は、実施例1と同様としてニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
(実施例12)
パラジウムを2質量ppmとしたこと以外は、実施例1と同様としてニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
パラジウムを2質量ppmとしたこと以外は、実施例1と同様としてニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
(実施例13)
塩化パラジウム水溶液と25%アンモニア水の添加順序を逆にしたこと以外は、実施例4と同様としてニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
塩化パラジウム水溶液と25%アンモニア水の添加順序を逆にしたこと以外は、実施例4と同様としてニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
(実施例14)
第2液であるヒドラジンを添加した水溶液を、第3液である水酸化ナトリウム水溶液に添加して混合液とし、この混合液を第1液に添加したこと以外は実施例4と同様としてニッケル粉末を得た。
ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
第2液であるヒドラジンを添加した水溶液を、第3液である水酸化ナトリウム水溶液に添加して混合液とし、この混合液を第1液に添加したこと以外は実施例4と同様としてニッケル粉末を得た。
ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
(実施例15)
水酸化ナトリウムを190mL(水酸化物イオン2.04モル/ニッケルイオン1モル)としたこと以外は、実施例4と同様としてニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
水酸化ナトリウムを190mL(水酸化物イオン2.04モル/ニッケルイオン1モル)としたこと以外は、実施例4と同様としてニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
(実施例16)
水酸化ナトリウムを900mL(水酸化物イオン9.64モル/ニッケルイオン1モル)としたこと以外は、実施例4と同様としてニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
水酸化ナトリウムを900mL(水酸化物イオン9.64モル/ニッケルイオン1モル)としたこと以外は、実施例4と同様としてニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
(実施例17)
ヒドラジンを60mL(1.55モル/ニッケルイオン1モル)としたこと以外は、実施例4と同様とした。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
ヒドラジンを60mL(1.55モル/ニッケルイオン1モル)としたこと以外は、実施例4と同様とした。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
(実施例18)
ヒドラジンを200mL(5.18モル/ニッケルイオン1モル)としたこと以外は、実施例4と同様としてニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
ヒドラジンを200mL(5.18モル/ニッケルイオン1モル)としたこと以外は、実施例4と同様としてニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
(実施例19)
アンモニア水を70mL(1.10モル/ニッケルイオン1モル)としたこと以外は、実施例4と同様としてニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
アンモニア水を70mL(1.10モル/ニッケルイオン1モル)としたこと以外は、実施例4と同様としてニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
(実施例20)
アンモニア水を370mL(5.81モル/ニッケルイオン1モル)としたこと以外は、実施例4と同様としてニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
アンモニア水を370mL(5.81モル/ニッケルイオン1モル)としたこと以外は、実施例4と同様としてニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
(比較例1)
アンモニウム水を50mL(0.79モル/ニッケルイオン1モル)としたこと以外は、実施例1と同様として、ニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
アンモニウム水を50mL(0.79モル/ニッケルイオン1モル)としたこと以外は、実施例1と同様として、ニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
(比較例2)
パラジウム添加をしなかったこと以外は、実施例1と同様として、ニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
パラジウム添加をしなかったこと以外は、実施例1と同様として、ニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
(比較例3)
パラジウムを11000質量ppmとしたこと以外は、実施例1と同様として、ニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
パラジウムを11000質量ppmとしたこと以外は、実施例1と同様として、ニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
(比較例4)
ヒドラジン量を54mL(1.40モル/ニッケルイオン1モル)としたこと以外は、実施例1と同様として、ニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
ヒドラジン量を54mL(1.40モル/ニッケルイオン1モル)としたこと以外は、実施例1と同様として、ニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
(比較例5)
ヒドラジン量を227mL(5.88モル/ニッケルイオン1モル)としたこと以外は、実施例1と同様として、ニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
ヒドラジン量を227mL(5.88モル/ニッケルイオン1モル)としたこと以外は、実施例1と同様として、ニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
(比較例6)
水酸化ナトリウム量を150mL(水酸化物イオン1.61モル/ニッケルイオン1モル)としたこと以外は、実施例1と同様として、ニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
水酸化ナトリウム量を150mL(水酸化物イオン1.61モル/ニッケルイオン1モル)としたこと以外は、実施例1と同様として、ニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
(比較例7)
水酸化ナトリウム量を1000mL(水酸化物イオン10.71モル/ニッケルイオン1モル)としたこと以外は、実施例1と同様として、ニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
水酸化ナトリウム量を1000mL(水酸化物イオン10.71モル/ニッケルイオン1モル)としたこと以外は、実施例1と同様として、ニッケル粉末を得た。ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
(比較例8)
特開2004−332055にあるように、水酸化ナトリウム130gを純水2.5Lに溶解混合し、これに60%抱水ヒドラジン500mLを添加し、撹拌調製した。このアルカリ性ヒドラジン水溶液3Lを75℃に加温して保持した。これを撹拌しながら、予め塩化パラジウム水溶液を添加して調製しておいた、パラジウム濃度20mg/L及びニッケル濃度100g/Lの塩化ニッケル水溶液1Lを滴下して還元を行い、ニッケル晶析粉を生成させた。その後の手順は実施例1と同様の手順として、ニッケル粉末を得た。
ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
特開2004−332055にあるように、水酸化ナトリウム130gを純水2.5Lに溶解混合し、これに60%抱水ヒドラジン500mLを添加し、撹拌調製した。このアルカリ性ヒドラジン水溶液3Lを75℃に加温して保持した。これを撹拌しながら、予め塩化パラジウム水溶液を添加して調製しておいた、パラジウム濃度20mg/L及びニッケル濃度100g/Lの塩化ニッケル水溶液1Lを滴下して還元を行い、ニッケル晶析粉を生成させた。その後の手順は実施例1と同様の手順として、ニッケル粉末を得た。
ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
(比較例9)
特開2007−138291にあるように、純水6Lにゼラチン0.005gを溶解させた後、ヒドラジン濃度が0.02g/Lとなるようにヒドラジンを混合した。次に、ニッケルに対してパラジウムが5質量ppmとなるようにジクロロテトラアンミンパラジウムとニッケルに対して銀が0.05質量ppmとなるクロロジアンミン銀とを含む混合水溶液を作製しゼラチンとヒドラジンが含まれる前記溶液に滴下してコロイド溶液を得た。このコロイド溶液に、水酸化ナトリウムを添加し、pHを10以上とした後、更にヒドラジン濃度が26g/Lとなるまでヒドラジンを添加して、パラジウムと微量の銀からなる複合コロイド粒子が混合されたアルカリ性ヒドラジン溶液を作製し、ニッケルを還元するためのアルカリ性ヒドラジン溶液とした。そして、このアルカリ性コロイド溶液に、ニッケルン水溶液としてニッケル濃度100g/Lの塩化ニッケル水溶液を0.5L滴下して、ニッケルの還元を行いニッケル晶析粉を生成させた。
特開2007−138291にあるように、純水6Lにゼラチン0.005gを溶解させた後、ヒドラジン濃度が0.02g/Lとなるようにヒドラジンを混合した。次に、ニッケルに対してパラジウムが5質量ppmとなるようにジクロロテトラアンミンパラジウムとニッケルに対して銀が0.05質量ppmとなるクロロジアンミン銀とを含む混合水溶液を作製しゼラチンとヒドラジンが含まれる前記溶液に滴下してコロイド溶液を得た。このコロイド溶液に、水酸化ナトリウムを添加し、pHを10以上とした後、更にヒドラジン濃度が26g/Lとなるまでヒドラジンを添加して、パラジウムと微量の銀からなる複合コロイド粒子が混合されたアルカリ性ヒドラジン溶液を作製し、ニッケルを還元するためのアルカリ性ヒドラジン溶液とした。そして、このアルカリ性コロイド溶液に、ニッケルン水溶液としてニッケル濃度100g/Lの塩化ニッケル水溶液を0.5L滴下して、ニッケルの還元を行いニッケル晶析粉を生成させた。
その後の手順は実施例1と同様の手順として、ニッケル粉末を得た。
ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
ニッケル晶析終了時のニッケル晶析粉、反応液の液色、最終的に得られたニッケル粉末のSEM観察と観察像の評価結果、およびニッケル粉末の不純物含有量を測定した。これらの結果をまとめて表1に示す。
(比較例10)
ニッケル濃度60g/Lの塩化ニッケル水溶液と、24質量%の水酸化ナトリウム水溶液をpH8.3で一定となるように調整しながら反応槽に連続的に添加することで、水酸化ニッケルを生成させた。生成した水酸化ニッケル粉をろ過し、スラリー濃度100g/Lとなるように純水に再スラリー化することで水洗した。その後、大気乾燥機を用いて120℃で24時間乾燥し、水酸化ニッケル粉末を得た。得られた水酸化ニッケル粉末を、空気中380℃で2時間加熱し酸化ニッケル粉末を得た。得られた酸化ニッケル粉末を、水素雰囲気中400℃で3時間還元し、ニッケル還元粉を得た。
ニッケル濃度60g/Lの塩化ニッケル水溶液と、24質量%の水酸化ナトリウム水溶液をpH8.3で一定となるように調整しながら反応槽に連続的に添加することで、水酸化ニッケルを生成させた。生成した水酸化ニッケル粉をろ過し、スラリー濃度100g/Lとなるように純水に再スラリー化することで水洗した。その後、大気乾燥機を用いて120℃で24時間乾燥し、水酸化ニッケル粉末を得た。得られた水酸化ニッケル粉末を、空気中380℃で2時間加熱し酸化ニッケル粉末を得た。得られた酸化ニッケル粉末を、水素雰囲気中400℃で3時間還元し、ニッケル還元粉を得た。
残留塩素を除去するために、得られたニッケル還元粉1kgを採取し、0.13質量%の硫酸水溶液4L(ニッケルに対して0.52質量%)に懸濁させ、30℃で30分間撹拌を実施した。洗浄後30分間静置沈降しデカンテーションを行い、次いでニッケル還元粉スラリーを吸引ろ過により固液分離した。分離されたニッケル還元粉を含む組成物を4Lの純水中で30分間撹拌して水洗し、吸引ろ過を行った。吸引ろ過後のニッケル還元粉を含む組成物の含水率は18質量%であった。その後、大気乾燥機を用いて120℃で12時間乾燥し、150μm開口径の篩にかけ、ニッケル粉末を得た。
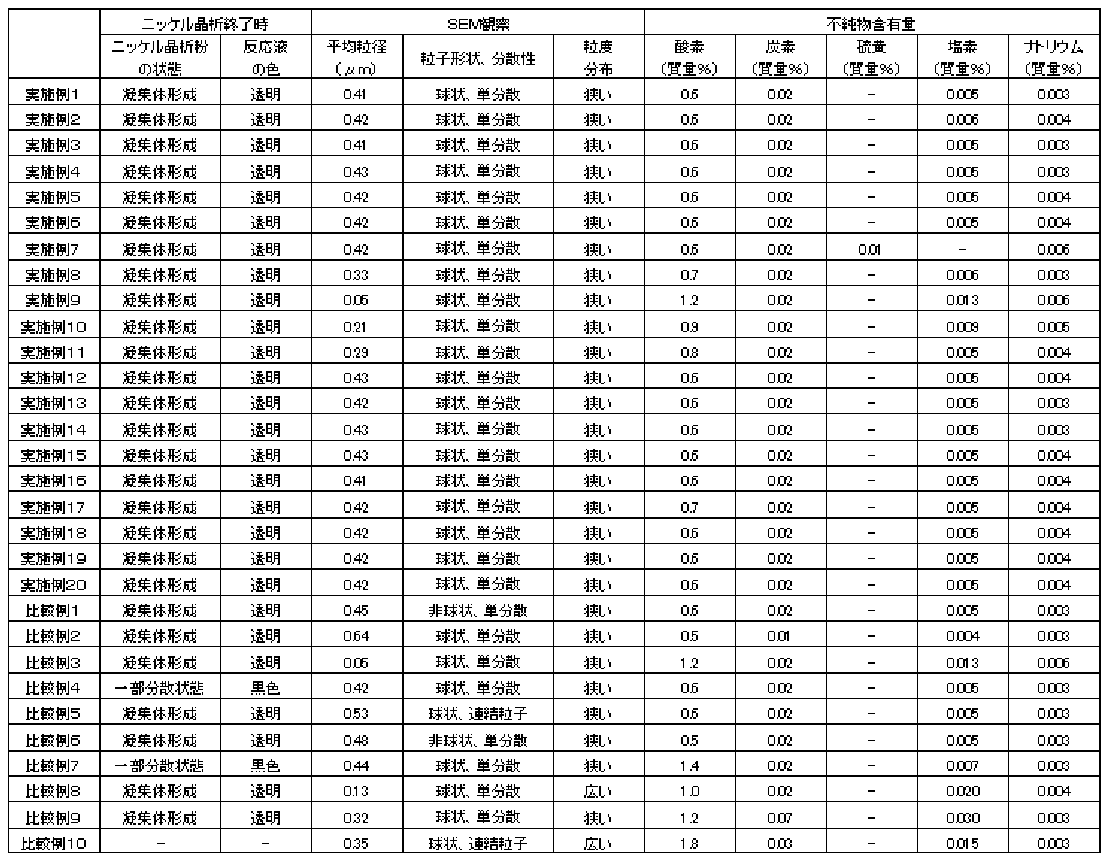
実施例1〜20は、平均粒径は0.05μm〜0.43μmの球状で単分散したニッケル粉末であり、粒度分布は狭く、炭素を始めとする不純物含有量も低い。
これらに対し、比較例1は非球状である。比較例2は粒径が大きい。比較例3は実施例9よりも多く貴金属を添加しているが微粒化効果が得られていない。比較例4は、反応後のスラリーが黒色で、完全な凝集体が得られていない。比較例5は連結粒子となっている。比較例6は非球状である。比較例7は、反応後のスラリーが黒色で、完全な凝集体が得られていない。比較例8は残留塩素が高い。比較例9は、残留塩素および炭素が高い。比較例10は連結粒子が多く、粒度分布が広く、残留塩素が高い。
これらに対し、比較例1は非球状である。比較例2は粒径が大きい。比較例3は実施例9よりも多く貴金属を添加しているが微粒化効果が得られていない。比較例4は、反応後のスラリーが黒色で、完全な凝集体が得られていない。比較例5は連結粒子となっている。比較例6は非球状である。比較例7は、反応後のスラリーが黒色で、完全な凝集体が得られていない。比較例8は残留塩素が高い。比較例9は、残留塩素および炭素が高い。比較例10は連結粒子が多く、粒度分布が広く、残留塩素が高い。
Claims (9)
- ニッケル塩と、アンモニウムイオンと、ニッケルよりも貴な金属塩と、を含む水溶液である第1液と、
ニッケル及びニッケルよりも貴な金属に対して還元作用を有する水溶液である第2液と、
ヒドロキシル基を有するアルカリ性の水溶液である第3液と、
をすべて混合することで反応液とし、該反応液中でニッケルを晶析させることを特徴とするニッケル粉末の製造方法。 - 反応液とする前の前記第1液、前記第2液、前記第3液、及び前記第1液から前記第3液の任意の2液を混合させた混合液の温度が、10℃〜55℃であることを特徴とする請求項1に記載のニッケル粉末の製造方法。
- 前記反応液を昇温させて55℃〜85℃とすることを特徴とする請求項2に記載のニッケル粉末の製造方法。
- 前記ニッケル及びニッケルよりも貴な金属に対して還元作用を有する水溶液が、ヒドラジンまたはその水化物の水溶液であることを特徴とする請求項1〜3のいずれかに記載のニッケル粉末の製造方法。
- 前記ニッケルよりも貴な金属の総量がニッケルに対して1質量ppm〜10000質量ppmであり、
前記アンモニウムイオン量が1〜6モル/ニッケルイオン1モルであり、
前記ヒドラジンまたはその水化物の水溶液が、ヒドラジン量で1.3〜5.5モル/ニッケルイオン1モルであり、
前記ヒドロキシル基を有するアルカリ性水溶液が、水酸化物イオン量で2.0〜10モル/ニッケルイオン1モルであることを特徴とする請求項4に記載のニッケル粉末の製造方法。 - 前記ニッケル塩が、塩化ニッケル、硫酸ニッケルのいずれか若しくはそれらの混合物であることを特徴とする請求項5に記載のニッケル粉末の製造方法。
- 前記アンモニウムイオン源が、アンモニア水であることを特徴とする請求項5または6に記載のニッケル粉末の製造方法。
- 前記ニッケルよりも貴な金属が、パラジウム、銀、銅のいずれか若しくはそれらの混合物であることを特徴とする請求項5〜7のいずれかに記載のニッケル粉末の製造方法。
- ヒドロキシル基を有するアルカリ性水溶液が、水酸化ナトリウム、水酸化カリウムの少なくともいずれかを含む水溶液であることを特徴とする請求項5〜8のいずれかに記載のニッケル粉末の製造方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2016101059A JP2017206751A (ja) | 2016-05-20 | 2016-05-20 | ニッケル粉末の製造方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2016101059A JP2017206751A (ja) | 2016-05-20 | 2016-05-20 | ニッケル粉末の製造方法 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2017206751A true JP2017206751A (ja) | 2017-11-24 |
Family
ID=60414808
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016101059A Pending JP2017206751A (ja) | 2016-05-20 | 2016-05-20 | ニッケル粉末の製造方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2017206751A (ja) |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2019151891A (ja) * | 2018-03-02 | 2019-09-12 | 本多電子株式会社 | 金属ナノ粒子の粒径制御方法、粒径分散値制御方法、粒子形状制御方法、金属ナノ粒子の製造方法 |
| JP2020041197A (ja) * | 2018-09-12 | 2020-03-19 | 住友金属鉱山株式会社 | ニッケル粉末およびニッケル粉末の製造方法 |
| JP2022151722A (ja) * | 2021-03-25 | 2022-10-07 | 住友金属鉱山株式会社 | 金属ニッケル粉末の析出反応の解析方法 |
| JP2023079721A (ja) * | 2021-11-29 | 2023-06-08 | 住友金属鉱山株式会社 | ニッケル粉末の製造方法 |
| JP2023079720A (ja) * | 2021-11-29 | 2023-06-08 | 住友金属鉱山株式会社 | ニッケル粉末の製造方法 |
-
2016
- 2016-05-20 JP JP2016101059A patent/JP2017206751A/ja active Pending
Cited By (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2019151891A (ja) * | 2018-03-02 | 2019-09-12 | 本多電子株式会社 | 金属ナノ粒子の粒径制御方法、粒径分散値制御方法、粒子形状制御方法、金属ナノ粒子の製造方法 |
| JP7069513B2 (ja) | 2018-03-02 | 2022-05-18 | 本多電子株式会社 | 中空状金ナノ粒子の製造方法 |
| JP2020041197A (ja) * | 2018-09-12 | 2020-03-19 | 住友金属鉱山株式会社 | ニッケル粉末およびニッケル粉末の製造方法 |
| JP7293591B2 (ja) | 2018-09-12 | 2023-06-20 | 住友金属鉱山株式会社 | ニッケル粉末およびニッケル粉末の製造方法 |
| JP2022151722A (ja) * | 2021-03-25 | 2022-10-07 | 住友金属鉱山株式会社 | 金属ニッケル粉末の析出反応の解析方法 |
| JP2023079721A (ja) * | 2021-11-29 | 2023-06-08 | 住友金属鉱山株式会社 | ニッケル粉末の製造方法 |
| JP2023079720A (ja) * | 2021-11-29 | 2023-06-08 | 住友金属鉱山株式会社 | ニッケル粉末の製造方法 |
| JP7697357B2 (ja) | 2021-11-29 | 2025-06-24 | 住友金属鉱山株式会社 | ニッケル粉末の製造方法 |
| JP7697356B2 (ja) | 2021-11-29 | 2025-06-24 | 住友金属鉱山株式会社 | ニッケル粉末の製造方法 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5820202B2 (ja) | 導電性ペースト用銅粉およびその製造方法 | |
| JP2017206751A (ja) | ニッケル粉末の製造方法 | |
| JP6135935B2 (ja) | 湿式ニッケル粉末の製造方法 | |
| WO2013122244A1 (ja) | 球状銀粉およびその製造方法 | |
| CN103079726A (zh) | 银粒子及其制备方法 | |
| JP2006336060A (ja) | ニッケル微粒子粉末及びその製造方法 | |
| JP2019108610A (ja) | 球状銀粉およびその製造方法 | |
| KR900004108B1 (ko) | 고용체를 형성하는 방법 | |
| CN108025366B (zh) | 贵金属粉末的制造方法 | |
| JP4100244B2 (ja) | ニッケル粉末とその製造方法 | |
| JP2017039991A (ja) | 銀コート銅粉とその製造方法、及びそれを用いた導電性ペースト | |
| KR20070043661A (ko) | 니켈 분말과 그의 제조방법 | |
| JP5756694B2 (ja) | 扁平金属粒子 | |
| CN103930226B (zh) | 银粉 | |
| JP2017039990A (ja) | 銅粉とその製造方法、及びそれを用いた導電性ペースト | |
| JP6985219B2 (ja) | 球状銀粉の製造方法 | |
| JP5835077B2 (ja) | ニッケル粉及びその製造方法 | |
| WO1989004736A1 (fr) | Procede de production de poudre de particules metalliques | |
| JP5063624B2 (ja) | ニッケル微粒子の製造方法 | |
| KR100508693B1 (ko) | 니켈 나노분말의 합성 방법 | |
| JP6031571B2 (ja) | 導電性ペースト用銅粉およびその製造方法 | |
| JP2004323884A (ja) | 超微粒子のニッケル粉末及びその製造方法 | |
| JP6201818B2 (ja) | チタン及びバリウム含有ニッケル粉末の製造方法 | |
| TWI695897B (zh) | 金屬粉末 | |
| JP6201817B2 (ja) | チタン含有ニッケル粉末の製造方法 |