JP2014517841A - 半フッ化アルカンを基礎にした局所薬学的組成物 - Google Patents
半フッ化アルカンを基礎にした局所薬学的組成物 Download PDFInfo
- Publication number
- JP2014517841A JP2014517841A JP2014511893A JP2014511893A JP2014517841A JP 2014517841 A JP2014517841 A JP 2014517841A JP 2014511893 A JP2014511893 A JP 2014511893A JP 2014511893 A JP2014511893 A JP 2014511893A JP 2014517841 A JP2014517841 A JP 2014517841A
- Authority
- JP
- Japan
- Prior art keywords
- skin
- composition according
- composition
- semi
- active ingredient
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/10—Dispersions; Emulsions
- A61K9/107—Emulsions ; Emulsion preconcentrates; Micelles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/045—Hydroxy compounds, e.g. alcohols; Salts thereof, e.g. alcoholates
- A61K31/07—Retinol compounds, e.g. vitamin A
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/35—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having six-membered rings with one oxygen as the only ring hetero atom
- A61K31/352—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having six-membered rings with one oxygen as the only ring hetero atom condensed with carbocyclic rings, e.g. methantheline
- A61K31/353—3,4-Dihydrobenzopyrans, e.g. chroman, catechin
- A61K31/355—Tocopherols, e.g. vitamin E
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/4353—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems
- A61K31/436—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems the heterocyclic ring system containing a six-membered ring having oxygen as a ring hetero atom, e.g. rapamycin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
- A61K31/57—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids substituted in position 17 beta by a chain of two carbon atoms, e.g. pregnane or progesterone
- A61K31/573—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids substituted in position 17 beta by a chain of two carbon atoms, e.g. pregnane or progesterone substituted in position 21, e.g. cortisone, dexamethasone, prednisone or aldosterone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0014—Skin, i.e. galenical aspects of topical compositions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/06—Ointments; Bases therefor; Other semi-solid forms, e.g. creams, sticks, gels
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/08—Solutions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/10—Dispersions; Emulsions
- A61K9/107—Emulsions ; Emulsion preconcentrates; Micelles
- A61K9/1075—Microemulsions or submicron emulsions; Preconcentrates or solids thereof; Micelles, e.g. made of phospholipids or block copolymers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/04—Antipruritics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/06—Antipsoriatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/10—Anti-acne agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/12—Keratolytics, e.g. wart or anti-corn preparations
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/14—Drugs for dermatological disorders for baldness or alopecia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/10—Antimycotics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/08—Antiallergic agents
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Engineering & Computer Science (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- Dermatology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Dispersion Chemistry (AREA)
- Immunology (AREA)
- Molecular Biology (AREA)
- Biophysics (AREA)
- Communicable Diseases (AREA)
- Oncology (AREA)
- Rheumatology (AREA)
- Virology (AREA)
- Pain & Pain Management (AREA)
- Transplantation (AREA)
- Pulmonology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicinal Preparation (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
【選択図】なし
Description
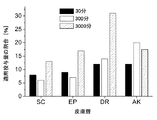
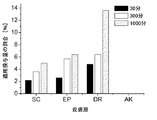
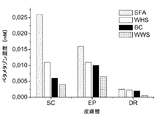
− 10μm厚の1枚の薄片(角質層に対応する)
− 各々20μmの4枚の薄片(生きている表皮に対応する)
− 各々40μmの5×5枚の薄片(真皮の5つの層に対応する)。
Claims (15)
- 皮膚または皮膚付属器に影響を及ぼす疾患または症状の防止または処置に用いるための局所薬学的組成物であり、有効量の活性成分、および次式:
RFRH
(式中、RFは、4〜12個の炭素原子を有する線状過フッ化炭化水素セグメントであり、そしてRHは、4〜8個の炭素原子を有する線状アルキル基である)
で表わされる半フッ化アルカンを含む組成物であって、皮膚または皮膚付属器に投与される組成物。 - 前記半フッ化アルカンが、F4H5、F4H6、F4H8、F6H6およびF6H8(ここで、Fは過フッ化炭化水素セグメントを意味し、Hは非フッ化セグメントを意味し、そして数字はそれぞれのセグメントの炭素原子の数である)から選択される請求項2記載の組成物。
- 液体、半固体溶液、乳濁液またはマイクロエマルションの形態である前記請求項のいずれかに記載の組成物。
- 好ましくは、エタノール、アセトン、酢酸エチル、イソプロピルアルコール、グリセロール、プロピレングリコール、ペンチレングリコール、ポリエチレングリコール、液体パラフィン、トリグリセリド油、ヒドロフルオロカーボン:例えばHFA134aおよび/またはHFA227、および液体モノまたはジグリセリドから選択される生理学的に許容可能な共溶媒を含む前記請求項のいずれかに記載の組成物。
- 前記皮膚または皮膚付属器が、乾癬、皮膚炎、紅斑、湿疹、アレルギー、座瘡、光線性角化症、真菌感染症、細菌感染症、ウイルス感染症、疣または酒さから選択される疾患または症状により影響を及ぼされる、前記請求項のいずれかに記載の組成物。
- 前記疾患または症状が、皮膚の生きている表皮、真皮および/または皮下組織に影響を及ぼす、前記請求項のいずれかに記載の組成物。
- 前記皮膚が乾癬により影響を及ぼされ、前記活性成分が免疫抑制剤またはレチノイドから選択される前記請求項のいずれかに記載の組成物。
- 前記免疫抑制剤が、タクロリムス、シロリムス、エベロリムス、タクロリムス、ピメクロリムス、リダフォロリムス、テムシロリムス、ゾタロリムスおよびシクロスポリンAから選択される請求項7記載の組成物。
- 前記レチノイドが、レチノール、レチナール、トレチノイン、イソトレチノイン、アリトレチノイン、エトレチネート、アシトレチン、タザロテン、ベキサロテンおよびアダパレンから選択される請求項7記載の組成物。
- 前記皮膚が座瘡により影響を及ぼされ、前記活性成分がレチノイドまたは抗感染薬から選択される請求項1〜6のいずれかに記載の組成物。
- 前記レチノイドが、レチノール、レチナール、トレチノイン、イソトレチノイン、アリトレチノイン、エトレチネート、アシトレチン、タザロテン、ベキサロテンおよびアダパレンから選択される請求項10記載の組成物。
- 前記抗感染薬が、アジスロマイシン、エリスロマイシン、クリンダマイシンまたはミノサイクリンから選択される請求項10記載の組成物。
- 前記皮膚が光線性角化症により影響を及ぼされ、そして前記活性成分が、好ましくはジクロフェナク、5−フルオロウラシルおよびイミキモドから選択される請求項1〜6のいずれかに記載の組成物。
- 前記皮膚または皮膚付属器の疾患または症状により影響を及ぼされた患者を処置するための方法であって、前記請求項のいずれかに記載の薬学的組成物を前記皮膚または皮膚付属器に局所投与することを包含する方法。
- 皮膚の生きている表皮、真皮および/または皮下組織に活性成分を送達するための請求項1〜13記載の組成物の使用。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP11167552.6 | 2011-05-25 | ||
| EP11167552 | 2011-05-25 | ||
| EP11167732.4 | 2011-05-26 | ||
| EP11167732 | 2011-05-26 | ||
| PCT/EP2012/059787 WO2012160179A2 (en) | 2011-05-25 | 2012-05-24 | Topical pharmaceutical composition based on semifluorinated alkanes |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016215748A Division JP6306126B2 (ja) | 2011-05-25 | 2016-11-03 | 半フッ化アルカンを基礎にした局所薬学的組成物 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2014517841A true JP2014517841A (ja) | 2014-07-24 |
| JP2014517841A5 JP2014517841A5 (ja) | 2015-07-09 |
| JP6039145B2 JP6039145B2 (ja) | 2016-12-07 |
Family
ID=46168482
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2014511893A Active JP6039145B2 (ja) | 2011-05-25 | 2012-05-24 | 半フッ化アルカンを基礎にした局所薬学的組成物 |
| JP2016215748A Active JP6306126B2 (ja) | 2011-05-25 | 2016-11-03 | 半フッ化アルカンを基礎にした局所薬学的組成物 |
| JP2018040265A Active JP6901421B2 (ja) | 2011-05-25 | 2018-03-07 | 半フッ化アルカンを基礎にした局所薬学的組成物 |
Family Applications After (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016215748A Active JP6306126B2 (ja) | 2011-05-25 | 2016-11-03 | 半フッ化アルカンを基礎にした局所薬学的組成物 |
| JP2018040265A Active JP6901421B2 (ja) | 2011-05-25 | 2018-03-07 | 半フッ化アルカンを基礎にした局所薬学的組成物 |
Country Status (13)
| Country | Link |
|---|---|
| US (4) | US10130707B2 (ja) |
| EP (3) | EP2714010B1 (ja) |
| JP (3) | JP6039145B2 (ja) |
| KR (2) | KR20170122282A (ja) |
| CN (4) | CN103596554A (ja) |
| AU (3) | AU2012260787B2 (ja) |
| CA (1) | CA2834855C (ja) |
| DK (2) | DK2714010T3 (ja) |
| ES (3) | ES2808051T3 (ja) |
| HK (1) | HK1247116A1 (ja) |
| PL (2) | PL2714010T3 (ja) |
| PT (2) | PT3192501T (ja) |
| WO (1) | WO2012160179A2 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2020517622A (ja) * | 2017-04-21 | 2020-06-18 | ノバリック ゲーエムベーハー | ヨウ素組成物 |
Families Citing this family (42)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8911494B2 (en) | 2009-05-04 | 2014-12-16 | Valtech Cardio, Ltd. | Deployment techniques for annuloplasty ring |
| EP2506777B1 (en) | 2009-12-02 | 2020-11-25 | Valtech Cardio, Ltd. | Combination of spool assembly coupled to a helical anchor and delivery tool for implantation thereof |
| PL2547323T3 (pl) | 2010-03-17 | 2016-07-29 | Novaliq Gmbh | Kompozycja farmaceutyczna do leczenia podwyższonego ciśnienia wewnątrzgałkowego |
| EP2575685B1 (en) | 2010-06-07 | 2019-02-13 | Valtech Cardio, Ltd. | Apparatus for guide-wire based advancement of a rotation assembly |
| EP2444063A1 (en) | 2010-10-20 | 2012-04-25 | Novaliq GmbH | Liquid pharmaceutical compositions for the delivery of active ingredients |
| EP2462921A1 (en) | 2010-11-11 | 2012-06-13 | Novaliq GmbH | Liquid pharmaceutical compositions for the treatment of a posterior eye disease |
| DK2714010T3 (en) | 2011-05-25 | 2017-06-12 | Novaliq Gmbh | TOPICAL PHARMACEUTICAL COMPOSITION BASED ON SEMIFLUORED ALKANES |
| JP6023181B2 (ja) | 2011-05-25 | 2016-11-09 | ノバリック ゲーエムベーハー | 爪に投与するための医薬組成物 |
| KR101989648B1 (ko) | 2012-01-23 | 2019-06-14 | 노바리크 게엠베하 | 부분불소화 알칸에 기초한 안정화된 단백질 조성물 |
| CN113679699B (zh) | 2012-09-12 | 2022-10-28 | 诺瓦利克有限责任公司 | 包含半氟化烷烃的混合物的组合物 |
| AU2013314303B2 (en) * | 2012-09-12 | 2018-01-18 | Novaliq Gmbh | Semifluorinated alkane compositions |
| AU2014209141B2 (en) | 2013-01-24 | 2018-05-10 | Palvella Therapeutics, Inc. | Compositions for transdermal delivery of mTOR inhibitors |
| PT3024484T (pt) | 2013-07-23 | 2018-10-24 | Novaliq Gmbh | Composições de anticorpo estabilizadas |
| US9522189B2 (en) * | 2013-12-20 | 2016-12-20 | Johnson & Johnson Consumer Inc. | Topical gel compositions including poly(monostearoyl glycerol-co-succinate) polymer and methods for enhancing the topical application of a benefit agent |
| EP2944324A1 (de) * | 2014-05-13 | 2015-11-18 | LTS LOHMANN Therapie-Systeme AG | Verwendung von semifluorierten Alkanen in transdermalen therapeutischen Systemen |
| US11154513B2 (en) | 2015-09-30 | 2021-10-26 | Novaliq Gmbh | Semifluorinated compounds |
| CN110403923B (zh) | 2015-09-30 | 2021-09-21 | 诺瓦利克有限责任公司 | 半氟化化合物和其组合物 |
| CN105663027B (zh) * | 2016-04-01 | 2018-12-18 | 中国人民解放军广州军区武汉总医院 | 西罗莫司外用制剂、其制备方法及用途 |
| PT3442480T (pt) | 2016-06-23 | 2019-12-23 | Novaliq Gmbh | Método de administração tópica |
| CA3036297C (en) | 2016-09-22 | 2023-09-05 | Novaliq Gmbh | Pharmaceutical compositions for use in the therapy of blepharitis |
| WO2018055101A1 (en) | 2016-09-23 | 2018-03-29 | Novaliq Gmbh | Ophthalmic compositions comprising ciclosporin |
| US10751295B2 (en) * | 2016-11-09 | 2020-08-25 | Specialty Drug and Device, LLC | Compositions and methods for the removal of ear wax |
| BR112019012568A2 (pt) | 2016-12-22 | 2019-11-26 | Novaliq Gmbh | composições compreendendo tacrolimus para o tratamento de doenças intraoculares inflamatórias |
| EP4374851B1 (en) | 2016-12-23 | 2026-04-15 | Novaliq GmbH | Ophthalmic composition for treatment of dry eye disease |
| EP3565520B1 (en) | 2017-01-06 | 2026-02-25 | Palvella Therapeutics, Inc. | Anhydrous compositions of mtor inhibitors and methods of use |
| US11278503B2 (en) | 2017-05-12 | 2022-03-22 | Novaliq Gmbh | Pharmaceutical compositions comprising semifluorinated alkanes for the treatment of contact lense-related conditions |
| WO2018215638A1 (en) | 2017-05-26 | 2018-11-29 | Novaliq Gmbh | Pharmaceutical compositions comprising azithromycin |
| MX2020003534A (es) | 2017-09-27 | 2020-07-29 | Novaliq Gmbh | Composiciones oftalmicas que comprenden latanoprost para usarse en el tratamiento de las enfermedades oculares. |
| WO2019068763A1 (en) | 2017-10-04 | 2019-04-11 | Novaliq Gmbh | OPHTHALMIC COMPOSITIONS COMPRISING F6H8 |
| KR20200128407A (ko) | 2018-03-02 | 2020-11-12 | 노바리크 게엠베하 | 네비볼롤을 포함하는 약제학적 조성물 |
| SG11202007860XA (en) | 2018-03-28 | 2020-09-29 | Novaliq Gmbh | Pharmaceutical composition comprising timolol |
| CN112153970A (zh) | 2018-04-27 | 2020-12-29 | 诺瓦利克有限责任公司 | 用于治疗青光眼的包含他氟前列素的眼用组合物 |
| US11000513B2 (en) | 2018-07-02 | 2021-05-11 | Palvella Therapeutics, Inc. | Anhydrous compositions of mTOR inhibitors and methods of use |
| EP3856124A1 (en) * | 2018-09-27 | 2021-08-04 | Novaliq GmbH | Lipid barrier repair |
| CA3111870C (en) * | 2018-09-27 | 2022-04-12 | Novaliq Gmbh | Topical sunscreen formulation |
| SG11202102820VA (en) | 2018-10-12 | 2021-04-29 | Novaliq Gmbh | Ophthalmic composition for treatment of dry eye disease |
| EP3923907B1 (en) | 2019-02-13 | 2024-09-25 | Novaliq GmbH | Compositions and methods for the treatment of ocular neovascularization |
| KR20220058577A (ko) | 2019-09-06 | 2022-05-09 | 노바리크 게엠베하 | 포도막염 치료를 위한 안과용 조성물 |
| EP3861857A1 (en) * | 2020-02-07 | 2021-08-11 | Novaliq GmbH | Antiparasitic compositions |
| CN117982412B (zh) * | 2024-02-04 | 2024-09-17 | 济川(上海)医学科技有限公司 | 一种醋克利定眼用组合物及其药物制剂和用途 |
| WO2026003129A1 (en) * | 2024-06-26 | 2026-01-02 | Novaliq Gmbh | Stabilization of (r)-ruxolitinib |
| WO2026037894A1 (en) | 2024-08-15 | 2026-02-19 | Dermaliq Therapeutics, Inc. | Semifluorinated alkane compositions for cleaning the skin |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0670159A1 (de) * | 1994-02-22 | 1995-09-06 | Hoechst Aktiengesellschaft | Fluorkohlenwasserstoffe enthaltende Ölemulsionen |
| JP2000511157A (ja) * | 1995-09-29 | 2000-08-29 | マイネルト,ハッソ | セミフルオロアルカン及びその使用 |
| JP2008518891A (ja) * | 2004-11-02 | 2008-06-05 | スイッチ バイオテック アーゲー | Tリンパ球の増殖および/またはケラチノサイトの過剰増殖を特徴とする疾患、特にアトピー性皮膚炎および乾癬を処置するための、ピルリンドールの使用 |
| WO2011009436A2 (de) * | 2009-07-24 | 2011-01-27 | Mika Pharma Gesellschaft Für Die Entwicklung Und Vermarktung Pharmazeutischer Produkte Mbh | Verfahren zur entwicklung einer als schaum auf die haut zu applizierende flüssige zusammensetzung sowie eine topisch applizierbare zusammensetzung |
Family Cites Families (103)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10022A (en) | 1853-09-13 | Lard-lamp | ||
| US2616927A (en) | 1950-05-12 | 1952-11-04 | Minnesota Mining & Mfg | Fluorocarbon tertiary amines |
| JPS5721312A (en) | 1980-07-12 | 1982-02-04 | Green Cross Corp:The | Breathable ointment |
| US4452818A (en) | 1982-03-19 | 1984-06-05 | Haidt Sterling J | Extraocular method of treating the eye with liquid perfluorocarbons |
| US5077036A (en) | 1986-01-14 | 1991-12-31 | Alliance Pharmaceutical Corp. | Biocompatible stable fluorocarbon emulsions for contrast enhancement and oxygen transport comprising 40-125% wt./volume fluorocarbon combined with a phospholipid |
| JPH0764702B2 (ja) | 1986-04-23 | 1995-07-12 | 鐘紡株式会社 | 多相乳化型化粧料 |
| JPS6452722A (en) | 1987-05-01 | 1989-02-28 | Anjierini Pharmaceut Inc | Ophthalmic composition |
| JP3046346B2 (ja) | 1990-03-12 | 2000-05-29 | 昭和電工株式会社 | 外用剤基剤又は補助剤とそれを含有する人又は動物の外用剤 |
| US5518731A (en) | 1990-09-27 | 1996-05-21 | Allergan, Inc. | Nonaqueous fluorinated drug delivery vehicle suspensions |
| US6458376B1 (en) | 1990-09-27 | 2002-10-01 | Allergan, Inc. | Nonaqueous fluorinated drug delivery suspensions |
| US5152997A (en) | 1990-12-11 | 1992-10-06 | Theratech, Inc. | Method and device for transdermally administering testosterone across nonscrotal skin at therapeutically effective levels |
| US5326566A (en) | 1991-05-17 | 1994-07-05 | Bristol-Myers Squibb Company | Use of dibutyl adipate and isopropyl myristate in topical and transdermal products |
| FR2679150A1 (fr) | 1991-07-17 | 1993-01-22 | Atta | Preparations comprenant un fluorocarbure ou compose hautement fluore et un compose organique lipophile-fluorophile, et leurs utilisations. |
| US5336175A (en) | 1992-10-29 | 1994-08-09 | Mames Robert N | Method for the treatment of retinal detachments |
| FR2720943B1 (fr) | 1994-06-09 | 1996-08-23 | Applic Transferts Technolo | Emulsions inverses stables à forte concentration en composé(s) fluoré(s) et leur utilisation pour l'administration pulmonaire de médicaments et pour la fabrication d'émulsions multiples. |
| US6294563B1 (en) | 1994-10-27 | 2001-09-25 | Allergan Sales, Inc. | Combinations of prostaglandins and brimonidine or derivatives thereof |
| US5696164A (en) | 1994-12-22 | 1997-12-09 | Johnson & Johnson Consumer Products, Inc. | Antifungal treatment of nails |
| US5667809A (en) * | 1995-06-07 | 1997-09-16 | Alliance Pharmaceutical Corp. | Continuous fluorochemical microdispersions for the delivery of lipophilic pharmaceutical agents |
| US5874481A (en) | 1995-06-07 | 1999-02-23 | Alliance Pharmaceutical Corp. | Fluorochemical solutions for the delivery of lipophilic pharmaceutical agents |
| US5874469A (en) | 1996-01-05 | 1999-02-23 | Alcon Laboratories, Inc. | Fluoroalkyl hydrocarbons for administering water insoluble or unstable drugs |
| RU2111738C1 (ru) | 1996-06-24 | 1998-05-27 | Акционерное общество "НИЗАР" | Средство для усиления солнцезащитной активности фотозащитных агентов |
| FR2752161B1 (fr) | 1996-08-07 | 1998-09-25 | Atta | Emulsions multiples de type hydrocarbure-dans-eau-dans- fluorocarbone pour le transport de substances medicamenteuses hydrophiles et/ou lipophiles |
| US5863560A (en) * | 1996-09-11 | 1999-01-26 | Virotex Corporation | Compositions and methods for topical application of therapeutic agents |
| IN184589B (ja) | 1996-10-16 | 2000-09-09 | Alza Corp | |
| DE19709704C2 (de) | 1997-03-10 | 1999-11-04 | Michael Georgieff | Verwendung einer flüssigen Präparation von Xenon zur intravenösen Verabreichung bei Einleitung und/oder Aufrechterhaltung der Anaesthesie |
| US5980936A (en) | 1997-08-07 | 1999-11-09 | Alliance Pharmaceutical Corp. | Multiple emulsions comprising a hydrophobic continuous phase |
| US5851544A (en) | 1997-12-18 | 1998-12-22 | Chesebrough-Pond's Usa Co., Division Of Conopco, Inc. | Cosmetic skin or hair care compositions containing fluorocarbons infused with carbon dioxide |
| US5981607A (en) | 1998-01-20 | 1999-11-09 | Allergan | Emulsion eye drop for alleviation of dry eye related symptoms in dry eye patients and/or contact lens wearers |
| CA2278328C (en) | 1998-02-09 | 2008-07-22 | Macrochem Corporation | Antifungal nail lacquer and method using same |
| DE19861012A1 (de) | 1998-03-18 | 1999-09-30 | Pharm Pur Gmbh | Behandlungsmittel für die Ophthalmologie |
| DE69912441T2 (de) | 1998-08-19 | 2004-08-19 | Skyepharma Canada Inc., Verdun | Injizierbare wässerige propofoldispersionen |
| US6140374A (en) | 1998-10-23 | 2000-10-31 | Abbott Laboratories | Propofol composition |
| US6159977A (en) | 1998-11-16 | 2000-12-12 | Astan, Inc. | Therapeutic anti-fungal nail preparation |
| CA2361424C (en) | 1999-02-08 | 2009-04-28 | Intarcia Therapeutics, Inc. | Stable non-aqueous single phase viscous vehicles and formulations utilizing such vehicles |
| US7258869B1 (en) | 1999-02-08 | 2007-08-21 | Alza Corporation | Stable non-aqueous single phase viscous vehicles and formulations utilizing such vehicle |
| EP1124416A1 (en) | 1999-03-15 | 2001-08-22 | John Claude Krusz | Treatment of acute headaches and chronic pain using rapidly-cleared anesthetic drug at sub-anesthetic dosages |
| US6177477B1 (en) | 1999-03-24 | 2001-01-23 | American Home Products Corporation | Propofol formulation containing TRIS |
| US6239113B1 (en) | 1999-03-31 | 2001-05-29 | Insite Vision, Incorporated | Topical treatment or prevention of ocular infections |
| DE19926890C1 (de) | 1999-06-12 | 2000-07-27 | Pharm Pur Gmbh | Verwendung eines hochfluorierten oligomeren Alkans in der Ophthalmologie |
| DE19938668B4 (de) | 1999-08-14 | 2006-01-26 | Bausch & Lomb Inc. | Tränenersatzmittel |
| US6528086B2 (en) * | 1999-09-28 | 2003-03-04 | Zars, Inc. | Methods and apparatus for drug delivery involving phase changing formulations |
| JP2001158734A (ja) | 1999-12-02 | 2001-06-12 | Lion Corp | 眼科用組成物及びソフトコンタクトレンズに対する吸着抑制方法 |
| US20030018044A1 (en) | 2000-02-18 | 2003-01-23 | Peyman Gholam A. | Treatment of ocular disease |
| DE10024413A1 (de) | 2000-05-19 | 2001-12-06 | Mika Pharma Gmbh | Pharmazeutische und/oder kosmetische Zubereitung |
| DE10042412B4 (de) | 2000-08-30 | 2005-12-22 | Lts Lohmann Therapie-Systeme Ag | Transdermales therapeutisches System zur Abgabe von Venlafaxin, und seine Verwendung |
| US6399087B1 (en) | 2000-12-20 | 2002-06-04 | Amphastar Pharmaceuticals, Inc. | Propofol formulation with enhanced microbial inhibition |
| CA2446060A1 (en) | 2001-05-07 | 2002-11-14 | Corium International | Compositions and delivery systems for administration of a local anesthetic agent |
| CZ301310B6 (cs) | 2001-09-04 | 2010-01-13 | Trommsdorff Gmbh & Co. Kg Arzneimittel | Náplast |
| JP2005523252A (ja) | 2002-01-26 | 2005-08-04 | マイクロ サイエンス テック コーポレーション リミテッド | 牧丹皮抽出物を有効成分として含む組成物 |
| EP2977043A3 (en) * | 2003-08-25 | 2016-04-06 | Foamix Pharmaceuticals Ltd. | Penetrating pharmaceutical foam |
| US20050079210A1 (en) | 2003-10-09 | 2005-04-14 | Gupta Shyam K. | Liposomal delivery system for topical pharmaceutical, cosmeceutical, and cosmetic ingredients |
| ATE534373T1 (de) | 2003-10-10 | 2011-12-15 | Antares Pharma Ipl Ag | Transdermale pharmazeutische formulierung zur minimierung von rückständen auf der haut |
| JP2007511616A (ja) | 2003-11-19 | 2007-05-10 | バーンズ−ジューイッシュ ホスピタル | 増強された薬物送達 |
| GB0408164D0 (en) | 2004-04-13 | 2004-05-19 | Immune Targeting Systems Ltd | Antigen delivery vectors and constructs |
| WO2005099718A1 (en) | 2004-04-19 | 2005-10-27 | Centre National De La Recherche Scientifique (C.N.R.S.) | Lung surfactant supplements |
| MXPA06014425A (es) | 2004-06-08 | 2007-05-23 | Ocularis Pharma Inc | Composiciones oftalmicas hidrofobas y metodo de uso. |
| AU2005262392A1 (en) | 2004-07-01 | 2006-01-19 | Johnson & Johnson Vision Care, Inc. | Compositions and methods for treating eye disorders and conditions |
| US20060078580A1 (en) | 2004-10-08 | 2006-04-13 | Mediquest Therapeutics, Inc. | Organo-gel formulations for therapeutic applications |
| US7740875B2 (en) | 2004-10-08 | 2010-06-22 | Mediquest Therapeutics, Inc. | Organo-gel formulations for therapeutic applications |
| GB0511499D0 (en) * | 2005-06-06 | 2005-07-13 | Medpharm Ltd | Topical ungual formulations |
| ATE420625T1 (de) | 2005-08-05 | 2009-01-15 | Bharat Serums & Vaccines Ltd | Intravenöse propofol-emulsionszusammensetzungen mit konservierendem effekt |
| FR2892023B1 (fr) | 2005-10-14 | 2009-09-25 | Galderma Sa | Composition pharmaceutique a base d'amorolfine et d'agent filmogene hydrosoluble pour application ungueale et peri-ungueale |
| DE102005050431A1 (de) | 2005-10-21 | 2007-04-26 | Lts Lohmann Therapie-Systeme Ag | Transdermales therapeutisches System zur Verabreicherung lipophiler und/oder wenig hautpermeabler Wirkstoffe |
| DE102005055811A1 (de) * | 2005-11-23 | 2007-05-31 | Novaliq Gmbh | Verwendung einer Zusammensetzung zur Konservierung von Organen und Gliedmaßen |
| TWI376239B (en) | 2006-02-01 | 2012-11-11 | Andrew Xian Chen | Vitamin e succinate stabilized pharmaceutical compositions, methods for the preparation and the use thereof |
| EP2070518A2 (en) | 2006-07-25 | 2009-06-17 | Osmotica Corp. | Ophthalmic solutions |
| EP2068828A2 (en) | 2006-09-29 | 2009-06-17 | SurModics, Inc. | Biodegradable ocular implants and methods for treating ocular conditions |
| DE102007055046A1 (de) | 2007-11-19 | 2009-05-28 | Fluoron Gmbh | Infusionslösung |
| US20090136430A1 (en) * | 2007-11-27 | 2009-05-28 | Dugger Harry A | Antihistamine/Corticosteroid preparations for the treatment of atopic dermatitis |
| ES2377152T3 (es) | 2008-04-18 | 2012-03-22 | Novaliq Gmbh | Uso inhalativo e instilativo de alcanos semifluorados como vehículos de principios activos en la región intrapulmonar |
| US20100189765A1 (en) | 2008-11-26 | 2010-07-29 | Erickson Signe R | Implantable ocular drug delivery device and methods |
| JP4642905B2 (ja) | 2009-01-22 | 2011-03-02 | 株式会社資生堂 | 乳化化粧料 |
| US8501800B2 (en) | 2009-03-05 | 2013-08-06 | Insite Vision Incorporated | Controlled-release ophthalmic vehicles |
| IT1393419B1 (it) | 2009-03-19 | 2012-04-20 | Medivis S R L | Composizioni oftalmiche a base di acidi grassi polinsaturi omega-3 e omega-6. |
| WO2010146536A1 (en) | 2009-06-18 | 2010-12-23 | Koninklijke Philips Electronics N.V. | Suspension of particles with drug |
| JP5736635B2 (ja) | 2009-06-25 | 2015-06-17 | ライオン株式会社 | ドライアイ治療剤 |
| US9012503B2 (en) | 2009-06-25 | 2015-04-21 | Lion Corporation | Ophthalmic composition |
| EP2332525A1 (en) | 2009-11-23 | 2011-06-15 | Novaliq GmbH | Pharmaceutical composition comprising propofol |
| EP2335735A1 (en) | 2009-12-14 | 2011-06-22 | Novaliq GmbH | Pharmaceutical composition for treatment of dry eye syndrome |
| US20110223208A1 (en) | 2010-03-09 | 2011-09-15 | Beth Hill | Non-Aqueous High Concentration Reduced Viscosity Suspension Formulations |
| PL2547323T3 (pl) | 2010-03-17 | 2016-07-29 | Novaliq Gmbh | Kompozycja farmaceutyczna do leczenia podwyższonego ciśnienia wewnątrzgałkowego |
| DE102010022567A1 (de) | 2010-06-02 | 2011-12-08 | Fluoron Gmbh | Zubereitung |
| EP2444063A1 (en) | 2010-10-20 | 2012-04-25 | Novaliq GmbH | Liquid pharmaceutical compositions for the delivery of active ingredients |
| EP2462921A1 (en) | 2010-11-11 | 2012-06-13 | Novaliq GmbH | Liquid pharmaceutical compositions for the treatment of a posterior eye disease |
| ES2711760T3 (es) | 2011-01-04 | 2019-05-07 | Novaliq Gmbh | Emulsiones de aceite/agua que comprenden alcanos semifluorados |
| US20120219640A1 (en) | 2011-02-25 | 2012-08-30 | Wright Kenneth W | Anti-infective solution for athlete's foot |
| DK2714010T3 (en) | 2011-05-25 | 2017-06-12 | Novaliq Gmbh | TOPICAL PHARMACEUTICAL COMPOSITION BASED ON SEMIFLUORED ALKANES |
| JP6023181B2 (ja) | 2011-05-25 | 2016-11-09 | ノバリック ゲーエムベーハー | 爪に投与するための医薬組成物 |
| US8758826B2 (en) | 2011-07-05 | 2014-06-24 | Wet Inc. | Cannabinoid receptor binding agents, compositions, and methods |
| KR101989648B1 (ko) | 2012-01-23 | 2019-06-14 | 노바리크 게엠베하 | 부분불소화 알칸에 기초한 안정화된 단백질 조성물 |
| AU2013314303B2 (en) | 2012-09-12 | 2018-01-18 | Novaliq Gmbh | Semifluorinated alkane compositions |
| CN113679699B (zh) | 2012-09-12 | 2022-10-28 | 诺瓦利克有限责任公司 | 包含半氟化烷烃的混合物的组合物 |
| EP2783703A1 (en) | 2013-03-25 | 2014-10-01 | B. Braun Melsungen AG | Semifluorocarbon compound containing contrast agent |
| PT3024484T (pt) | 2013-07-23 | 2018-10-24 | Novaliq Gmbh | Composições de anticorpo estabilizadas |
| EP2944324A1 (de) | 2014-05-13 | 2015-11-18 | LTS LOHMANN Therapie-Systeme AG | Verwendung von semifluorierten Alkanen in transdermalen therapeutischen Systemen |
| US11154513B2 (en) | 2015-09-30 | 2021-10-26 | Novaliq Gmbh | Semifluorinated compounds |
| CN110403923B (zh) | 2015-09-30 | 2021-09-21 | 诺瓦利克有限责任公司 | 半氟化化合物和其组合物 |
| CN106176937A (zh) | 2016-08-24 | 2016-12-07 | 刘艺鹏 | 湿疹、痤疮软膏 |
| CA3058097C (en) | 2017-04-21 | 2024-01-02 | Novaliq Gmbh | Iodine compositions |
| EP3856124A1 (en) | 2018-09-27 | 2021-08-04 | Novaliq GmbH | Lipid barrier repair |
| CA3111870C (en) | 2018-09-27 | 2022-04-12 | Novaliq Gmbh | Topical sunscreen formulation |
| JP2022543402A (ja) | 2019-08-09 | 2022-10-12 | ノバリック ゲーエムベーハー | プロスタグランジンアナログを含む局所組成物 |
| EP3861857A1 (en) | 2020-02-07 | 2021-08-11 | Novaliq GmbH | Antiparasitic compositions |
-
2012
- 2012-05-24 DK DK12723683.4T patent/DK2714010T3/en active
- 2012-05-24 PT PT171548373T patent/PT3192501T/pt unknown
- 2012-05-24 US US14/122,044 patent/US10130707B2/en active Active
- 2012-05-24 CN CN201280025366.3A patent/CN103596554A/zh active Pending
- 2012-05-24 PT PT127236834T patent/PT2714010T/pt unknown
- 2012-05-24 CA CA2834855A patent/CA2834855C/en active Active
- 2012-05-24 CN CN201810165933.4A patent/CN108283623A/zh active Pending
- 2012-05-24 EP EP12723683.4A patent/EP2714010B1/en active Active
- 2012-05-24 KR KR1020177030042A patent/KR20170122282A/ko not_active Ceased
- 2012-05-24 AU AU2012260787A patent/AU2012260787B2/en active Active
- 2012-05-24 ES ES17154837T patent/ES2808051T3/es active Active
- 2012-05-24 WO PCT/EP2012/059787 patent/WO2012160179A2/en not_active Ceased
- 2012-05-24 EP EP17201124.9A patent/EP3311802B1/en active Active
- 2012-05-24 EP EP17154837.3A patent/EP3192501B1/en active Active
- 2012-05-24 ES ES12723683.4T patent/ES2623233T3/es active Active
- 2012-05-24 KR KR1020137033325A patent/KR101790388B1/ko active Active
- 2012-05-24 JP JP2014511893A patent/JP6039145B2/ja active Active
- 2012-05-24 ES ES17201124T patent/ES2962524T3/es active Active
- 2012-05-24 PL PL12723683T patent/PL2714010T3/pl unknown
- 2012-05-24 DK DK17154837.3T patent/DK3192501T3/da active
- 2012-05-24 CN CN201710375364.1A patent/CN107397718A/zh active Pending
- 2012-05-24 CN CN201810782938.1A patent/CN109260193A/zh active Pending
- 2012-05-24 PL PL17154837T patent/PL3192501T3/pl unknown
-
2016
- 2016-11-03 JP JP2016215748A patent/JP6306126B2/ja active Active
-
2017
- 2017-01-31 AU AU2017200622A patent/AU2017200622B2/en active Active
- 2017-09-29 US US15/721,259 patent/US10813999B2/en active Active
-
2018
- 2018-03-07 JP JP2018040265A patent/JP6901421B2/ja active Active
- 2018-05-25 HK HK18106802.5A patent/HK1247116A1/zh unknown
- 2018-07-20 AU AU2018206812A patent/AU2018206812B2/en active Active
-
2020
- 2020-10-16 US US17/072,923 patent/US11844836B2/en active Active
-
2022
- 2022-04-04 US US17/713,082 patent/US20220218828A1/en not_active Abandoned
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0670159A1 (de) * | 1994-02-22 | 1995-09-06 | Hoechst Aktiengesellschaft | Fluorkohlenwasserstoffe enthaltende Ölemulsionen |
| JP2000511157A (ja) * | 1995-09-29 | 2000-08-29 | マイネルト,ハッソ | セミフルオロアルカン及びその使用 |
| JP2008518891A (ja) * | 2004-11-02 | 2008-06-05 | スイッチ バイオテック アーゲー | Tリンパ球の増殖および/またはケラチノサイトの過剰増殖を特徴とする疾患、特にアトピー性皮膚炎および乾癬を処置するための、ピルリンドールの使用 |
| WO2011009436A2 (de) * | 2009-07-24 | 2011-01-27 | Mika Pharma Gesellschaft Für Die Entwicklung Und Vermarktung Pharmazeutischer Produkte Mbh | Verfahren zur entwicklung einer als schaum auf die haut zu applizierende flüssige zusammensetzung sowie eine topisch applizierbare zusammensetzung |
Non-Patent Citations (1)
| Title |
|---|
| JPN5014007221; HENDRIK HARDUNG: 'SEMIFLUORIERTE UND PERFLUORIERTE VERBINDUNGEN ZUR TOPISCHEN UND PARENTERALEN ANWENDUNG' [ONLINE] , 20080818 * |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2020517622A (ja) * | 2017-04-21 | 2020-06-18 | ノバリック ゲーエムベーハー | ヨウ素組成物 |
| JP7072582B2 (ja) | 2017-04-21 | 2022-05-20 | ノバリック ゲーエムベーハー | ヨウ素組成物 |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6306126B2 (ja) | 半フッ化アルカンを基礎にした局所薬学的組成物 | |
| KR101773648B1 (ko) | 조갑에 투여를 위한 제약학적 조성물 | |
| AU2012260787A1 (en) | Topical pharmaceutical composition based on semifluorinated alkanes | |
| HK40002180A (en) | Topical pharmaceutical composition based on semifluorinated alkanes | |
| HK1254443A1 (en) | Topical pharmaceutical composition based on semifluorinated alkanes | |
| HK1254443B (en) | Topical pharmaceutical composition based on semifluorinated alkanes | |
| HK1241277B (en) | Topical pharmaceutical composition based on semifluorinated alkanes | |
| HK1241277A1 (en) | Topical pharmaceutical composition based on semifluorinated alkanes |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150520 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20150520 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20160329 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20160408 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20160707 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20160901 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20161007 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20161103 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6039145 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| S111 | Request for change of ownership or part of ownership |
Free format text: JAPANESE INTERMEDIATE CODE: R313113 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |