JP2012502015A - 必要がある患者に医薬組成物を送達するための方法 - Google Patents
必要がある患者に医薬組成物を送達するための方法 Download PDFInfo
- Publication number
- JP2012502015A JP2012502015A JP2011525623A JP2011525623A JP2012502015A JP 2012502015 A JP2012502015 A JP 2012502015A JP 2011525623 A JP2011525623 A JP 2011525623A JP 2011525623 A JP2011525623 A JP 2011525623A JP 2012502015 A JP2012502015 A JP 2012502015A
- Authority
- JP
- Japan
- Prior art keywords
- dose
- administered
- esomeprazole
- hours
- time
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2072—Pills, tablets, discs, rods characterised by shape, structure or size; Tablets with holes, special break lines or identification marks; Partially coated tablets; Disintegrating flat shaped forms
- A61K9/2086—Layered tablets, e.g. bilayer tablets; Tablets of the type inert core-active coat
- A61K9/209—Layered tablets, e.g. bilayer tablets; Tablets of the type inert core-active coat containing drug in at least two layers or in the core and in at least one outer layer
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/192—Carboxylic acids, e.g. valproic acid having aromatic groups, e.g. sulindac, 2-aryl-propionic acids, ethacrynic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/415—1,2-Diazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4427—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems
- A61K31/4439—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems containing a five-membered ring with nitrogen as a ring hetero atom, e.g. omeprazole
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0053—Mouth and digestive tract, i.e. intraoral and peroral administration
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/28—Dragees; Coated pills or tablets, e.g. with film or compression coating
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/04—Centrally acting analgesics, e.g. opioids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
Landscapes
- Health & Medical Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Epidemiology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Organic Chemistry (AREA)
- Physical Education & Sports Medicine (AREA)
- Rheumatology (AREA)
- Pain & Pain Management (AREA)
- Physiology (AREA)
- Nutrition Science (AREA)
- Biomedical Technology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Immunology (AREA)
- Neurosurgery (AREA)
- Neurology (AREA)
- Medicinal Preparation (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
本開示は、単位用量形態の医薬組成物の製造におけるナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩の使用に向けられ、ここで該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、特定のpHで該単位用量形態から放出され、ここで特定の薬物動的プロファイルを標的とするために、一つの単位用量形態はAM用量として投与され、そして第二の単位用量形態はPM用量として約10時間後に投与される。
Description
本開示は、必要がある患者に医薬組成物を送達するための方法であって、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与する、上記方法に向けられている。
1500万人以上の米国人が、疼痛または炎症の治療として、非ステロイド系抗炎症薬(NSAID)を毎日服用する。残念ながら、多くのNSAIDは、高頻度で消化管の合併症(胃炎、消化不良、胃十二指腸潰瘍、穿孔、および出血を含む)を伴う。消化管病変の発生をもたらす多くの因子は、胃および上部小腸における酸の存在と考えられる。
近年、例えば、プロトンポンプ阻害薬のような胃酸分泌を阻害する薬剤をNSAIDと共に投与することにより、NSAIDの服用に伴う胃腸障害の危険性を減らす試みが行われている。例えば、特許文献1は、NSAID後に患者の消化管のpHを上昇させるプロトンポンプ阻害薬を含む少なくとも1つの薬物投薬形態に関する。この製剤、および類似する製剤は、所望の薬力学反応および薬物動態値(pharmacokinetic value)を生じるエソメプラゾールおよびナプロキセンの投薬を介して、NSAID耐性を改善するのに有効であり得る。所望の薬力学反応および薬物動態値に影響を及ぼし得るパラメータとしては、例えば、個々の投薬量;薬物吸収の程度;薬物分布の程度、および薬物投与期間が挙げられるが、これらに限定されない。
約4以上の胃内(instragastric)pHおよび有効なナプロキセンの血漿レベルを達成するのに十分な期間、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物をその必要がある患者に送達する、臨床的に有効な治療が必要である。
(発明の要旨)
1つの局面において、本開示は、単位用量形態の医薬組成物の製造におけるナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩の使用に関し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から標的に放出され:少なくとも約41%の、胃内pHが約24時間、約4.0以上のままである平均%時間。
1つの局面において、本開示は、単位用量形態の医薬組成物の製造におけるナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩の使用に関し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から標的に放出され:少なくとも約41%の、胃内pHが約24時間、約4.0以上のままである平均%時間。
別の実施形態において、胃内pHが約24時間、約4.0以上のままである平均%時間は、少なくとも約60%、少なくとも約71%、または少なくとも約77%である。
別の実施形態において、医薬組成物は、ナプロキセンについて、約76μg/mlまたは約79μg/mlの平均最大血漿濃度(Cmax)を有する薬物動態(pk)プロファイルをさらに標的とする。
別の実施形態において、医薬組成物は、エソメプラゾールについて、約1500hr*μg/mL、約2134hr*μg/mLまたは約4911hr*μg/mLの、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイルを標的とする。
1つの局面において、本開示は、その必要がある患者に送達するための単位用量形態の医薬組成物の製造におけるナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩の使用に関し、ここで、第一の単位用量形態はAM用量(AM dose)として標的に投与され、そして第二の単位用量形態はPM用量(PM dose)として、約10時間後に投与される:
i)ナプロキセンについての薬物動態(pk)プロファイル:
a)AM用量は約81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は約76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;および
ii)エソメプラゾールについての薬物動態(pk)プロファイル:
a)AM用量は、約850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、約650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する。
i)ナプロキセンについての薬物動態(pk)プロファイル:
a)AM用量は約81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は約76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;および
ii)エソメプラゾールについての薬物動態(pk)プロファイル:
a)AM用量は、約850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、約650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する。
1つの実施形態において、医薬組成物は、以下を提供する:
a)ナプロキセンの前記AM用量についてのCmaxの平均値が、約86.2μg/mLまたは約80.9μg/mLであり、そして前記Tmaxの中央値が約3.0時間であり;そして
a)前記PM用量についてのCmaxの平均値が、約76.8μg/mLまたは約76.2μg/mLであり、そして前記Tmaxの中央値が約10時間である。
a)ナプロキセンの前記AM用量についてのCmaxの平均値が、約86.2μg/mLまたは約80.9μg/mLであり、そして前記Tmaxの中央値が約3.0時間であり;そして
a)前記PM用量についてのCmaxの平均値が、約76.8μg/mLまたは約76.2μg/mLであり、そして前記Tmaxの中央値が約10時間である。
別の実施形態において、上記の医薬組成物は、以下を提供する:
a)エソメプラゾールの前記AM用量について、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)が約1216hr*μg/mLまたは約2779hr*μg/mLであり、そして
b)エソメプラゾールの前記PM用量について、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)が、約919hr*μg/mLまたは約2066hr*μg/mLである。
a)エソメプラゾールの前記AM用量について、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)が約1216hr*μg/mLまたは約2779hr*μg/mLであり、そして
b)エソメプラゾールの前記PM用量について、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)が、約919hr*μg/mLまたは約2066hr*μg/mLである。
別の実施形態において、医薬組成物は、エソメプラゾールについて、約1500hr*μg/mL、約2000hr*μg/mL、または約4911hr*μg/mLの、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイルを標的とする。
医薬組成物は、少なくとも約41%、約60%、約71%、または約77%の、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間をさらに標的とする、請求項19〜26のいずれか1項に記載の使用。
1つの実施形態において、用量形態が、少なくとも1種のコアならびに少なくとも第一の層および第二の層を含む多層錠であり、ここで:
i)該コアは、ナプロキセン、またはそれらの薬学的に受容可能な塩を含み;
ii)該第一の層は、周囲媒質のpHが約3.5以上である場合に、ナプロキセン、またはそれらの薬学的に受容可能な塩を少なくとも放出し始めるコーティングであり;そして
iii)該第二の層は、エソメプラゾールを含み、ここで、前記エソメプラゾールは約0以上のpHで放出される。
i)該コアは、ナプロキセン、またはそれらの薬学的に受容可能な塩を含み;
ii)該第一の層は、周囲媒質のpHが約3.5以上である場合に、ナプロキセン、またはそれらの薬学的に受容可能な塩を少なくとも放出し始めるコーティングであり;そして
iii)該第二の層は、エソメプラゾールを含み、ここで、前記エソメプラゾールは約0以上のpHで放出される。
別の実施形態において、用量形態は、約1以上のpH、約0〜約2のpH、または約2〜4のpHでエソメプラゾールの放出をもたらす。別の実施形態において、エソメプラゾール、またはそれらの薬学的に受容可能な塩の少なくとも一部分は、腸溶コーティングでコートされていない。別の実施形態において、第一の層が腸溶コーティングである。なお別の実施形態において、多層錠は、重炭酸ナトリウムを実質的に含まない。1つの実施形態において、第一の層は、周囲媒質のpHが約4.0または約4.5以上である場合に、ナプロキセンを放出し始める。
別の実施形態において、単位用量形態の医薬組成物は、約500mgの前記ナプロキセン、またはそれらの薬学的に受容可能な塩、および約20mgまたは約30mgの前記エソメプラゾール、またはそれらの薬学的に受容可能な塩を含む。
別の実施形態において、医薬組成物は、1日に2回を少なくとも約6日間または1日に2回を少なくとも9日間投与される。
別の実施形態において、医薬組成物は、危険な状態にある患者に投与される。
危険な状態にある患者は、疼痛および炎症から選択される疾患または障害の治療を受けている患者であり得るか、または変形性関節症、関節リウマチ、強直性脊椎炎、またはそれらの組み合わせの治療を受けている患者であり得る。
1つの局面において、本開示は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から標的に放出され:少なくとも約41%の、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間。
別の局面において、本開示は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から放出され、ここで、ある単位用量形態が標的にAM用量として投与され、そして第二の用量がPM用量として約10時間後に投与され
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、約81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、約76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;および
ii)エソメプラゾールについてのpkプロファイル:
a)AM用量は、約850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)
を有し、そして
b)PM用量は、約650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する。
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、約81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、約76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;および
ii)エソメプラゾールについてのpkプロファイル:
a)AM用量は、約850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)
を有し、そして
b)PM用量は、約650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する。
なお別の局面は、疼痛および炎症から選択される疾患または障害の治療を受けている患者に、本明細書中に開示される薬力学反応および/または薬物動態値を提供する単位用量形態の医薬組成物を送達することに関する。
さらなる局面は、変形性関節症、関節リウマチ、強直性脊椎炎、またはそれらの組み合わせの治療を受けている患者に、本明細書中に開示される薬力学反応および/または薬物動態値を提供する単位用量形態の医薬組成物を送達することに関する。
なおさらなる局面は、危険な状態にある患者に、本明細書中に開示される薬力学反応および/または薬物動態値を提供する単位用量形態の医薬組成物を送達することに関する。
別の局面は、疼痛および炎症から選択される疾患または障害の治療を受けている危険な状態にある患者に、本明細書中に開示される薬力学反応および/または薬物動態値を提供する単位用量形態の医薬組成物を送達することに関する。
さらなる局面は、変形性関節症、関節リウマチ、強直性脊椎炎、またはそれらの組み合わせの治療を受けている危険な状態にある患者に、本明細書中に開示される薬力学反応および/または薬物動態値を提供する単位用量形態の医薬組成物を送達することに関する。
なお別の局面は、少なくとも1種のコアならびに少なくとも第一の層および第二の層を含む多層錠を介して、本明細書中に開示される薬力学反応および/または薬物動態値を提供する単位投薬形態の医薬組成物を送達することに関し、ここで:
i)該コアは、ナプロキセン、またはそれらの薬学的に受容可能な塩を含み;
ii)該第一の層は、周囲媒質のpHが約3.5以上である場合に、ナプロキセン、またはそれらの薬学的に受容可能な塩を少なくとも放出し始めるコーティングであり;そして
iii)該第二の層は、エソメプラゾール、またはそれらの薬学的に受容可能な塩であり、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は約0以上のpHで放出される。
i)該コアは、ナプロキセン、またはそれらの薬学的に受容可能な塩を含み;
ii)該第一の層は、周囲媒質のpHが約3.5以上である場合に、ナプロキセン、またはそれらの薬学的に受容可能な塩を少なくとも放出し始めるコーティングであり;そして
iii)該第二の層は、エソメプラゾール、またはそれらの薬学的に受容可能な塩であり、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は約0以上のpHで放出される。
本明細書中で使用され得る略語および/または特殊用語は、表1および以下の本文中に示される。
用語「危険な状態にある患者」とは、年齢または胃潰瘍の確認された病歴、またはLDA(低用量アスピリン)の同時投与に起因して、NSAID関連潰瘍の危険がある患者をいう。1つの実施形態において、危険な状態にある患者は、50歳以上の年齢に起因して、NSAID関連潰瘍の危険がある患者である。別の実施形態において、危険な状態にある患者は、アスピリンの併用に起因して、NSAID関連潰瘍の危険がある患者である。なお別の実施形態において、危険な状態にある患者は、上部消化管(UGI)の潰瘍または出血の病歴に起因して、NSAID関連潰瘍の危険がある患者である。
本明細書中で使用される場合、用語「薬学的に受容可能な」とは、「薬学的に受容可能」として同定された材料が、患者/被験者への投与に適切であり、かつ生理学的に受容可能であることを意味する。例えば、用語「薬学的に受容可能な塩」とは、適切でかつ生理学的に受容可能な塩を意味する。
語句「ナプロキセン、またはそれらの薬学的に受容可能な塩」とは、ナプロキセンの遊離塩基、ナプロキセンの薬学的に受容可能な塩、および/またはナプロキセンの遊離塩基および少なくとも1種のナプロキセンの薬学的に受容可能な塩の混合物をいう。
語句「エソメプラゾール、またはそれらの薬学的に受容可能な塩」とは、エソメプラゾールの遊離塩基、エソメプラゾールの薬学的に受容可能な塩、および/またはエソメプラゾールの遊離塩基および少なくとも1種のエソメプラゾールの薬学的に受容可能な塩の混合物をいう。
本明細書中で使用される場合、用語「単位投薬形態」(または「単位用量形態」)とは、薬物投与のための単一体をいう。例えば、エソメプラゾールおよびナプロキセンの両方を含む単一錠剤またはカプセル剤は、単位投薬形態である。本開示の単位投薬形態は、胃内pHを上昇させ、そして胃十二指腸粘膜に対するナプロキセンの有害効果を減らす方法で連続的な薬物放出を提供する、すなわち、エソメプラゾールが初めに放出され、そしてGI管中のpHが3.5以上に上昇するまで、ナプロキセンの放出が先延ばしされる。「単位投薬形態」(または「単位用量形態」)はまた、「固定投薬形態」(または「固定用量形態」)または固定投薬混合剤(fixed dosage combination)(または「固定用量混合剤(fixed dose combination)」)ともいい、そして他と互換性である。
本明細書中に示される値について、用語「約」とは、所定の数が少なくとも5%変更され得ることを意味し、10%、15%または20%の変動が可能である。
本明細書中に示される薬物動態および/または薬力学の値に関して、変動の程度は、SDおよび%CV値で表される。%CV=SD/平均×100;SD=(%CV×平均)÷100。患者の約68%が、1つの平均値のSD内にあり、そして患者の約95%が2つの平均値のSD内にあることが期待され得る。本明細書中に示される薬物動態および薬力学の値は、小数点第1位で四捨五入して整数にした平均値であり、そして複数の個人から得た結果に基づく。結果として、本明細書中に示される値は、患者によって異なり得る。この変動量は、用語「約」で表される。
ナプロキセン、またはそれらの薬学的に受容可能な塩および/またはエソメプラゾール、またはそれらの薬学的に受容可能な塩の各投薬量に関して、用語「約」とは、当該分野で受容可能な明確に同定された投薬量からの変動量を表すことを意味する。
本明細書中で言及される期間に関して、用語「約」とは、当該分野で受容可能な明確に同定された期間からの変動量を表すことを意味する。
本明細書中で使用される%変動係数および/または範囲に関して、用語「約」とは、規定された数として実質的に同じ結果を達成し得る規定された数値および/または範囲の上下の変動量を表すことを意味する。
本明細書中で言及されるpH値および/または範囲に関して、用語「約」とは、規定された数として実質的に同じ結果を達成し得る規定された数の上下の変動量を捕捉することを意味する。
語句「実質的に含まない」と共に使用される用語数値に関して、用語は、規定された数として実質的に同じ結果を達成し得る規定された数の上下の変動量を捕捉することを意味する。
語句「実質的に含まない」とは、約95%〜約99.99%含まないことを意味する。1つの実施形態において、実質的に含まないとは、約95%含まないことを意味する。別の実施形態において、用語、実質的に含まないとは、約96%含まないことを意味する。なお別の実施形態において、用語、実質的に含まないとは、約97%含まないことを意味する。なお別の実施形態において、用語、実質的に含まないとは、約98%含まないことを意味する。さらなる実施形態において、用語、実質的に含まないとは、約99%含まないことを意味する。なおさらなる実施形態において、用語、実質的に含まないとは、約99.99%含まないことを意味する。
本開示において、それぞれ、様々に規定された範囲は、各範囲の規定された最小値と最大値との間の各数値パラメータを包含するように連続的であることを意味する。例えば、約1〜約4の範囲は、約1、1、約2、2、約3、3、約4、および4を包含する。
1つの実施形態において、本開示は、単位用量形態の医薬組成物の製造におけるナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩の使用に関し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から標的に放出される:少なくとも約41%の、約24時間、胃内pHが約4.0以上のままである平均%時間。
別の実施形態において、約24時間、胃内pHが約4.0以上のままである平均%時間は、少なくとも約60%、少なくとも約71%、または少なくとも約77%である。
別の実施形態において、医薬組成物は、ナプロキセンについて約76μg/mlまたは約79μg/mlの平均最大血漿濃度(Cmax)を有する薬物動態(pk)プロファイルをさらに標的とする。
別の実施形態において、医薬組成物は、エソメプラゾールについて、約1500hr*μg/mL、約2134hr*μg/mLまたは約4911hr*μg/mLの、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイルを標的とする。
1つの局面において、本開示は、その必要がある患者に送達するための単位用量形態の医薬組成物の製造におけるナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩の使用に関し、ここで、第一の単位用量形態が標的にAM用量として投与され、そして第二の単位用量形態がPM用量として約10時間後に投与される:
i)ナプロキセンについての薬物動態(pk)プロファイル:
a)AM用量は、約81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、約76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;および
ii)エソメプラゾールについての薬物動態(pk)プロファイル:
a)AM用量は、約850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、約650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する。
i)ナプロキセンについての薬物動態(pk)プロファイル:
a)AM用量は、約81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、約76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;および
ii)エソメプラゾールについての薬物動態(pk)プロファイル:
a)AM用量は、約850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、約650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する。
1つの実施形態において、医薬組成物は以下を提供する:
a)ナプロキセンの前記AM用量についてのCmaxの平均値が約86.2μg/mLまたは約80.9μg/mLであり、そして前記Tmaxの中央値が約3.0時間であり;そして
b)前記PM用量についてのCmaxの平均値が約76.8μg/mLまたは約76.2μg/mL であり、そして前記Tmaxの中央値が約10時間である。
a)ナプロキセンの前記AM用量についてのCmaxの平均値が約86.2μg/mLまたは約80.9μg/mLであり、そして前記Tmaxの中央値が約3.0時間であり;そして
b)前記PM用量についてのCmaxの平均値が約76.8μg/mLまたは約76.2μg/mL であり、そして前記Tmaxの中央値が約10時間である。
別の実施形態において、上記の医薬組成物は以下を提供する:
a)エソメプラゾールの前記AM用量について、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)が約1216hr*μg/mLまたは約2779hr*μg/mLであり、そして
b)エソメプラゾールの前記PM用量について、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)が約919hr*μg/mLまたは約2066hr*μg/mLである。
a)エソメプラゾールの前記AM用量について、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)が約1216hr*μg/mLまたは約2779hr*μg/mLであり、そして
b)エソメプラゾールの前記PM用量について、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)が約919hr*μg/mLまたは約2066hr*μg/mLである。
別の実施形態において、医薬組成物は、エソメプラゾールについて、約1500hr*μg/mL、約2000hr*μg/mL、または約4911hr*μg/mLの、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイルを標的とする。
医薬組成物が、少なくとも約41、約60%、約71%、または約77%の、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間をさらに標的とする、請求項19〜26のいずれか1項に記載の使用。
一般に、本明細書中に開示される単位用量形態の医薬組成物の[1日に2回の]送達後、約4〜5日、約5〜6日、約6〜7日、約7〜8日、約8〜9日、または約9〜10日でナプロキセンまたはエソメプラゾールの定常状態レベルに達する。他の実施形態において、約4日、約5日、約6日、約7日、約8日、約9日、または約10日でナプロキセンまたはエソメプラゾールの定常状態レベルに達する。
1つの実施形態において、用量形態は、少なくとも1種のコアならびに少なくとも第一の層および第二の層を含む多層錠であり、ここで:
i)該コアは、ナプロキセン、またはそれらの薬学的に受容可能な塩を含み;
ii)該第一の層は、周囲媒質のpHが約3.5以上である場合に、ナプロキセン、またはそれらの薬学的に受容可能な塩を少なくとも放出し始めるコーティングであり;そして
iii)該第二の層は、エソメプラゾールを含み、ここで、前記エソメプラゾール
は約0以上のpHで放出される。
i)該コアは、ナプロキセン、またはそれらの薬学的に受容可能な塩を含み;
ii)該第一の層は、周囲媒質のpHが約3.5以上である場合に、ナプロキセン、またはそれらの薬学的に受容可能な塩を少なくとも放出し始めるコーティングであり;そして
iii)該第二の層は、エソメプラゾールを含み、ここで、前記エソメプラゾール
は約0以上のpHで放出される。
別の実施形態において、用量形態は、約1以上のpH、約0〜約2のpH、または約2〜4のpHで、エソメプラゾールの放出をもたらす。別の実施形態において、エソメプラゾール、またはそれらの薬学的に受容可能な塩の少なくとも一部は、腸溶コーティングでコーティングされていない。別の実施形態において、第一の層は、腸溶コーティングである。なお別の実施形態において、多層錠は重炭酸ナトリウムを実質的に含まない。1つの実施形態において、第一の層は、周囲媒質のpHが約4.0または約4.5以上である場合に、ナプロキセンを放出し始める。
別の実施形態において、単位用量形態の医薬組成物は、約500mgの前記ナプロキセン、またはそれらの薬学的に受容可能な塩、および約20mgまたは約30mgの前記エソメプラゾール、またはそれらの薬学的に受容可能な塩を含む。
別の実施形態において、医薬組成物は、1日に2回を少なくとも約6日間または1日に2回を少なくとも9日間投与される。
別の実施形態において、医薬組成物は危険な状態にある患者に投与される。危険な状態にある患者は、疼痛および炎症から選択される疾患または障害の治療を受けている患者であり得るか、または変形性関節症、関節リウマチ、強直性脊椎炎、またはそれらの組み合わせの治療を受けている患者であり得る。
1つの実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から標的に放出される:少なくとも約41%の、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間。
他の実施形態において、定常状態に達した後、24時間、胃内pHが約4.0以上のままである平均%時間は、少なくとも約40%、約45%、約50%、約55%、約60%、約65%、約70%、約71%、約75%、約77%、約80%、約85%、約90%、または約95%である。
別の実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から標的に放出される:少なくとも約41%の、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間およびナプロキセンについて、17〜23の%変動係数範囲で、少なくとも76μg/mLの平均最大血漿濃度(Cmax)を有する薬物動態(pk)プロファイル。
さらなる実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から標的に放出される:少なくとも約41%の、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間およびナプロキセンについて、約76μg/mLの平均最大血漿濃度(Cmax)を有する薬物動態(pk)プロファイル。
なお別の実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで前記エソメプラゾール、またはそれらの薬学的に受容可能な塩は、pH0以上で該単位用量形態から標的に放出される:少なくとも約41%の、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間およびエソメプラゾールについて、40〜80の%変動係数範囲で、少なくとも1500hr*μg/mLの、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイル。
なおさらなる実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、0以上のpHで該単位用量形態から標的に放出される:少なくとも約41%の、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間およびエソメプラゾールについて、約1500hr*μg/mLの第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイル。
なお別の実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から標的に放出される:少なくとも約41%の、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間;およびナプロキセンについて、17〜23の%変動係数範囲で、少なくとも76μg/mLの平均最大血漿濃度(Cmax)およびエソメプラゾールについて、40〜80の%変動係数範囲で、少なくとも1500hr*μg/mLの第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイル。
さらになお別の実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から標的に放出される:少なくとも約41%の、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間;およびナプロキセンについて、約76μg/mLの平均最大血漿濃度(Cmax)およびエソメプラゾールについて、約1500hr*μg/mLの、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイル。
なおさらなる実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から標的に放出される:ナプロキセンについて、17〜23の%変動係数範囲で、少なくとも76μg/mLの平均最大血漿濃度(Cmax)を有する薬物動態(pk)プロファイル。
なおさらなる実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から標的に放出される:ナプロキセンについて、約76μg/mLの平均最大血漿濃度(Cmax)を有する薬物動態(pk)プロファイル。
なおさらなる実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から標的に放出される:およびエソメプラゾールについて、40〜80の%変動係数範囲で、少なくとも1500hr*μg/mLの第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイル。
なおさらなる実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から標的に放出される:およびエソメプラゾールについて、約1500hr*μg/mLの、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイル。
さらなる実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から放出され、ここである単位用量形態は標的にAM用量として投与され、そして第二の用量が、PM用量として約10時間後に投与される:
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、22〜23の%変動係数範囲で、少なくとも81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、18〜23の%変動係数範囲で、少なくとも76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;および
ii)エソメプラゾールについてのpkプロファイル:
a)AM用量は、45〜70の%変動係数範囲で、少なくとも850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、50〜85の%変動係数範囲で、少なくとも650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する。
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、22〜23の%変動係数範囲で、少なくとも81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、18〜23の%変動係数範囲で、少なくとも76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;および
ii)エソメプラゾールについてのpkプロファイル:
a)AM用量は、45〜70の%変動係数範囲で、少なくとも850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、50〜85の%変動係数範囲で、少なくとも650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する。
なおさらなる実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、0以上のpHで該単位用量形態から放出され、ここで、ある単位用量形態は標的にAM用量として投与され、そして第二の用量が、PM用量として約10時間後に投与される:
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、約81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、約76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;および
ii)エソメプラゾールについてのpkプロファイル:
a)AM用量は、約850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、約650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する。
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、約81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、約76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;および
ii)エソメプラゾールについてのpkプロファイル:
a)AM用量は、約850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、約650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する。
なおさらなる実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から放出され、ここで、ある単位用量形態は、標的にAM用量として投与され、そして第二の用量は、PM用量として約10時間後に投与される:
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、22〜23の%変動係数範囲で、少なくとも81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、18〜23の%変動係数範囲で、少なくとも76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する。
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、22〜23の%変動係数範囲で、少なくとも81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、18〜23の%変動係数範囲で、少なくとも76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する。
なおさらなる実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から放出され、ここで、ある単位用量形態は、標的にAM用量として投与され、そして第二の用量は、PM用量として約10時間後に投与される:
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、約81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、約76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する。
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、約81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、約76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する。
なおさらなる実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から放出され、ここで、ある単位用量形態は、標的にAM用量として投与され、そして第二の用量は、PM用量として約10時間後に投与される:
i)エソメプラゾールについてのpkプロファイル:
a)AM用量は、45〜70の%変動係数範囲で、少なくとも850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、50〜85の%変動係数範囲で、少なくとも650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する。
i)エソメプラゾールについてのpkプロファイル:
a)AM用量は、45〜70の%変動係数範囲で、少なくとも850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、50〜85の%変動係数範囲で、少なくとも650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する。
さらなる実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から放出され、ここで、ある単位用量形態は、標的にAM用量として投与され、そして第二の用量は、PM用量として約10時間後に投与される:
i)エソメプラゾールについてのpkプロファイル:
a)AM用量は、約850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、約650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する。
i)エソメプラゾールについてのpkプロファイル:
a)AM用量は、約850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、約650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する。
なおさらなる実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から放出され、ここで、ある単位用量形態は、標的にAM用量として投与され、そして第二の用量は、PM用量として約10時間後に投与される:
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、22〜23の%変動係数範囲で、少なくとも81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、18〜23の%変動係数範囲で、少なくとも76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;
ii)エソメプラゾールについてのpkプロファイル:
a)AM用量は、45〜70の%変動係数範囲で、少なくとも850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、50〜85の%変動係数範囲で、少なくとも650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する;および
iii)少なくとも約41%の、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間。
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、22〜23の%変動係数範囲で、少なくとも81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、18〜23の%変動係数範囲で、少なくとも76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;
ii)エソメプラゾールについてのpkプロファイル:
a)AM用量は、45〜70の%変動係数範囲で、少なくとも850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、50〜85の%変動係数範囲で、少なくとも650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する;および
iii)少なくとも約41%の、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間。
なおさらなる実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から放出され、ここで、ある単位用量形態は、標的にAM用量として投与され、そして第二の用量は、PM用量として約10時間後に投与される:
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、少なくとも約(about least)81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、約76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;
ii)エソメプラゾールについてのpkプロファイル:
a)AM用量は、約850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、約650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する;および
iii)少なくとも約41%の、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間。
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、少なくとも約(about least)81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、約76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;
ii)エソメプラゾールについてのpkプロファイル:
a)AM用量は、約850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、約650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する;および
iii)少なくとも約41%の、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間。
なおさらに別の実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から放出され、ここで、ある単位用量形態は、標的にAM用量として投与され、そして第二の用量は、PM用量として約10時間後に投与される:
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、22〜23の%変動係数範囲で、少なくとも81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、18〜23の%変動係数範囲で、少なくとも76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;および
ii)少なくとも約41%の、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間。
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、22〜23の%変動係数範囲で、少なくとも81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、18〜23の%変動係数範囲で、少なくとも76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;および
ii)少なくとも約41%の、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間。
なおさらなる実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から放出され、ここで、ある単位用量形態は、標的にAM用量として投与され、そして第二の用量は、PM用量として約10時間後に投与される:
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、約81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、約76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;および
ii)少なくとも約41%の、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間。
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、約81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、約76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;および
ii)少なくとも約41%の、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間。
なおさらなる実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾールは、0以上のpHで該単位用量形態から放出され、ここで、ある単位用量形態は、標的にAM用量として投与され、そして第二の用量は、PM用量として約10時間後に投与される:
i)エソメプラゾールについてのpkプロファイル:
a)AM用量は、45〜70の%変動係数範囲で、少なくとも850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、50〜85の%変動係数範囲で、少なくとも650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する;および
ii)少なくとも約41%の、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間。
i)エソメプラゾールについてのpkプロファイル:
a)AM用量は、45〜70の%変動係数範囲で、少なくとも850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、50〜85の%変動係数範囲で、少なくとも650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する;および
ii)少なくとも約41%の、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間。
なおさらなる実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾールは、0以上のpHで該単位用量形態から放出され、ここで、ある単位用量形態は、標的にAM用量として投与され、そして第二の用量は、PM用量として約10時間後に投与される:
i)エソメプラゾールについてのpkプロファイル:
a)AM用量は、約850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、約650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する;および
ii)少なくとも約41%の、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間。
i)エソメプラゾールについてのpkプロファイル:
a)AM用量は、約850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、約650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する;および
ii)少なくとも約41%の、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間。
なおさらなる実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から放出され、ここで、ある単位用量形態は、標的にAM用量として投与され、そして第二の用量は、PM用量として約10時間後に投与される:
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、22〜23の%変動係数範囲で、少なくとも81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、18〜23の%変動係数範囲で、少なくとも76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;
ii)エソメプラゾールについてのpkプロファイル:
a)AM用量は、45〜70の%変動係数範囲で、少なくとも850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、50〜85の%変動係数範囲で、少なくとも650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する;
iii)少なくとも約41%の、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間;および
iv)エソメプラゾールについて、40〜80の%変動係数範囲で、少なくとも1500hr*μg/mLの、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイル。
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、22〜23の%変動係数範囲で、少なくとも81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、18〜23の%変動係数範囲で、少なくとも76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;
ii)エソメプラゾールについてのpkプロファイル:
a)AM用量は、45〜70の%変動係数範囲で、少なくとも850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、50〜85の%変動係数範囲で、少なくとも650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する;
iii)少なくとも約41%の、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間;および
iv)エソメプラゾールについて、40〜80の%変動係数範囲で、少なくとも1500hr*μg/mLの、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイル。
別の実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から放出され、ここで、ある単位用量形態は、標的にAM用量として投与され、そして第二の用量は、PM用量として約10時間後に投与される:
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、少なくとも約(about least)81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、約76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;
ii)エソメプラゾールについてのpkプロファイル:
a)AM用量は、約850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、約650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する;
iii)少なくとも約41%の、定常状態に達した後、24時間、胃内pHが約4.0以上のままである平均%時間;および
iv)エソメプラゾールについて、約1500hr*μg/mLの、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイル。
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、少なくとも約(about least)81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、約76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;
ii)エソメプラゾールについてのpkプロファイル:
a)AM用量は、約850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、約650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する;
iii)少なくとも約41%の、定常状態に達した後、24時間、胃内pHが約4.0以上のままである平均%時間;および
iv)エソメプラゾールについて、約1500hr*μg/mLの、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイル。
さらなる実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から放出され、ここで、ある単位用量形態は、標的にAM用量として投与され、そして第二の用量は、PM用量として約10時間後に投与される:
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、22〜23の%変動係数範囲で、少なくとも81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、18〜23の%変動係数範囲で、少なくとも76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;
ii)エソメプラゾールについてのpkプロファイル:
a)AM用量は、45〜70の%変動係数範囲で、少なくとも850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、50〜85の%変動係数範囲で、少なくとも650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する;および
iii)エソメプラゾールについて、40〜80の%変動係数範囲で、少なくとも1500hr*μg/mLの、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイル。
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、22〜23の%変動係数範囲で、少なくとも81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、18〜23の%変動係数範囲で、少なくとも76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;
ii)エソメプラゾールについてのpkプロファイル:
a)AM用量は、45〜70の%変動係数範囲で、少なくとも850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、50〜85の%変動係数範囲で、少なくとも650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する;および
iii)エソメプラゾールについて、40〜80の%変動係数範囲で、少なくとも1500hr*μg/mLの、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイル。
なおさらなる実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から放出され、ここで、ある単位用量形態は、標的にAM用量として投与され、そして第二の用量は、PM用量として約10時間後に投与される:
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、約81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、約76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;
ii)エソメプラゾールについてのpkプロファイル:
a)AM用量は、約850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、約650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する;および
iii)エソメプラゾールについて、約1500hr*μg/mLの、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイル。
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、約81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、約76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;
ii)エソメプラゾールについてのpkプロファイル:
a)AM用量は、約850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、約650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する;および
iii)エソメプラゾールについて、約1500hr*μg/mLの、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイル。
なおさらなる実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から放出され、ここで、ある単位用量形態は、標的にAM用量として投与され、そして第二の用量は、PM用量として約10時間後に投与される:
i)エソメプラゾールについてのpkプロファイル:
a)AM用量は、45〜70の%変動係数範囲で、少なくとも850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、50〜85の%変動係数範囲で、少なくとも650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する;および
ii)エソメプラゾールについて、40〜80の%変動係数範囲で、少なくとも1500hr*μg/mLの、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイル。
i)エソメプラゾールについてのpkプロファイル:
a)AM用量は、45〜70の%変動係数範囲で、少なくとも850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、50〜85の%変動係数範囲で、少なくとも650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する;および
ii)エソメプラゾールについて、40〜80の%変動係数範囲で、少なくとも1500hr*μg/mLの、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイル。
なおさらなる実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から放出され、ここで、ある単位用量形態は、標的にAM用量として投与され、そして第二の用量は、PM用量として約10時間後に投与される:
i)エソメプラゾールについてのpkプロファイル:
a)AM用量は、約850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、約650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する;および
ii)エソメプラゾールについて、約1500hr*μg/mLの、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイル。
i)エソメプラゾールについてのpkプロファイル:
a)AM用量は、約850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、約650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する;および
ii)エソメプラゾールについて、約1500hr*μg/mLの、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイル。
なお別の実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から放出され、ここで、ある単位用量形態は、標的にAM用量として投与され、そして第二の用量は、PM用量として約10時間後に投与される:
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、22〜23の%変動係数範囲で、少なくとも81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、18〜23の%変動係数範囲で、少なくとも76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;および
ii)エソメプラゾールについて、40〜80の%変動係数範囲で、少なくとも1500hr*μg/mLの、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイル。
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、22〜23の%変動係数範囲で、少なくとも81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、18〜23の%変動係数範囲で、少なくとも76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;および
ii)エソメプラゾールについて、40〜80の%変動係数範囲で、少なくとも1500hr*μg/mLの、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイル。
なおさらに別の実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から放出され、ここで、ある単位用量形態は、標的にAM用量として投与され、そして第二の用量は、PM用量として約10時間後に投与される:
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、約81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、約76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;および
ii)エソメプラゾールについて、約1500hr*μg/mLの、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイル。
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、約81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、約76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;および
ii)エソメプラゾールについて、約1500hr*μg/mLの、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイル。
なおさらなる実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から放出され、ここで、ある単位用量形態は、標的にAM用量として投与され、そして第二の用量は、PM用量として約10時間後に投与される:
i)エソメプラゾールについてのpkプロファイル:
a)AM用量は、45〜70の%変動係数範囲で、少なくとも850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、50〜85の%変動係数範囲で、少なくとも650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する;
ii)少なくとも約41%の、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間;および
iii)エソメプラゾールについて、40〜80の%変動係数範囲で、少なくとも1500hr*μg/mLの、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイル。
i)エソメプラゾールについてのpkプロファイル:
a)AM用量は、45〜70の%変動係数範囲で、少なくとも850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、50〜85の%変動係数範囲で、少なくとも650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する;
ii)少なくとも約41%の、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間;および
iii)エソメプラゾールについて、40〜80の%変動係数範囲で、少なくとも1500hr*μg/mLの、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイル。
なおさらなる実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から放出され、ここで、ある単位用量形態は、標的にAM用量として投与され、そして第二の用量は、PM用量として約10時間後に投与される:
i)エソメプラゾールについてのpkプロファイル:
a)AM用量は、約850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、約650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する;
ii)少なくとも約41%の、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間;および
iii)エソメプラゾールについて、約1500hr*μg/mLの、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイル。
i)エソメプラゾールについてのpkプロファイル:
a)AM用量は、約850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、約650hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する;
ii)少なくとも約41%の、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間;および
iii)エソメプラゾールについて、約1500hr*μg/mLの、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイル。
なお別の実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から放出され、ここで、ある単位用量形態は、標的にAM用量として投与され、そして第二の用量は、PM用量として約10時間後に投与される:
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、22〜23の%変動係数範囲で、少なくとも81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、18〜23の%変動係数範囲で、少なくとも76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;
ii)少なくとも約41%の、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間;および
iii)エソメプラゾールについて、40〜80の%変動係数範囲で、少なくとも1500hr*μg/mLの、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイル。
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、22〜23の%変動係数範囲で、少なくとも81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、18〜23の%変動係数範囲で、少なくとも76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;
ii)少なくとも約41%の、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間;および
iii)エソメプラゾールについて、40〜80の%変動係数範囲で、少なくとも1500hr*μg/mLの、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイル。
なおさらに別の実施形態は、その必要がある患者に医薬組成物を送達するための方法に関し、該方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を該患者に投与することを包含し、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0以上のpHで該単位用量形態から放出され、ここで、ある単位用量形態は、標的にAM用量として投与され、そして第二の用量は、PM用量として約10時間後に投与される:
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、約81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、約76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;
ii)少なくとも約41%の、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間;そして
iii)エソメプラゾールについて、約1500hr*μg/mLの、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイル。
i)ナプロキセンについてのpkプロファイル:
a)AM用量は、約81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、約76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有する;
ii)少なくとも約41%の、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間;そして
iii)エソメプラゾールについて、約1500hr*μg/mLの、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイル。
別の実施形態において、ナプロキセンは、約500mgからの量で遊離塩基として存在し得る。
なお別の実施形態において、ナプロキセンは、約500mgの量で遊離塩基として存在し得る。
なお別の実施形態において、ナプロキセンは、当量のナプロキセンの薬学的に受容可能な塩、例えば、ナプロキセンナトリウムで存在し得る。
さらなる実施形態において、エソメプラゾールは、マグネシウム塩として存在し得る。
なおさらなる実施形態において、エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約10mg〜約30mgのエソメプラゾールを提供する量で存在し得る。
さらなる実施形態において、エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約15mgのエソメプラゾールを提供する量で存在し得る。
なおさらなる実施形態において、エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約20mgのエソメプラゾールを提供する量で存在し得る。
なおさらに別の実施形態において、エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約30mgのエソメプラゾールを提供する量で存在し得る。
なお別の実施形態において、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間は、少なくとも約60%である。
なお別の実施形態において、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間は、少なくとも約71%である。
なおさらなる実施形態において、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間は、少なくとも約77%である。
なおさらなる実施形態において、ナプロキセンについて、平均最大血漿濃度(Cmax)は、17〜23の%変動係数範囲で、少なくとも79μg/mLである。
さらなる実施形態において、ナプロキセンについて、平均最大血漿濃度(Cmax)は、約79μg/mLである。
なおさらなる実施形態において、エソメプラゾールについて、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)は、74の%変動係数で、2134hr*μg/mLである。
別の実施形態において、エソメプラゾールについて、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)は、約2134hr*μg/mLである。
なお別の実施形態において、エソメプラゾールについて、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)は、40〜80の%変動係数範囲で、約2000hr*μg/mLである。
なお別の実施形態において、エソメプラゾールについて、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)は、約2000hr*μg/mLである。
なお別の実施形態において、エソメプラゾールについて、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)は、約1500hr*μg/mLである。
なおさらなる実施形態において、エソメプラゾールについて、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)は、42の%変動係数で、4911hr*μg/mLである。
なおさらなる実施形態において、エソメプラゾールについて、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)は約4911hr*μg/mLである。
1つの実施形態において、単位用量形態の医薬組成物は、約500mgの前記ナプロキセン、またはそれらの薬学的に受容可能な塩、および約20mgの前記エソメプラゾール、またはそれらの薬学的に受容可能な塩を含む。
別の実施形態において、単位用量形態の医薬組成物は、約500mgの前記ナプロキセン、またはそれらの薬学的に受容可能な塩、および約30mgの前記エソメプラゾール、またはそれらの薬学的に受容可能な塩を含む。
なお別の実施形態において、単位用量形態は、1日に2回を少なくとも6日間投与される。
なお別の実施形態において、単位用量形態は、1日に2回を少なくとも9日間投与される。
なおさらに別の実施形態において、その必要がある患者は、危険な状態にある患者である。
なお別の実施形態において、危険な状態にある患者は、疼痛および炎症から選択される疾患または障害の治療を受けている。
さらなる実施形態において、危険な状態にある患者は、変形性関節症、関節リウマチ、強直性脊椎炎、またはそれらの組み合わせの治療を受けている。
別の実施形態において、その必要がある患者は、疼痛および炎症から選択される疾患または障害の治療を受けている。
なお別の実施形態において、その必要がある患者は、変形性関節症、関節リウマチ、強直性脊椎炎、またはそれらの組み合わせの治療を受けている。
なお別の実施形態において、ナプロキセンの前記AM用量についてのCmaxの平均値が22の%変動係数で、86.2μg/mLであり、そして前記Tmaxの中央値が約3.0時間であり;そして前記PM用量についてのCmaxの平均値が18の%変動係数で、76.8μg/mLであり、そして前記Tmaxの中央値が約10時間である。
別の実施形態において、ナプロキセンの前記AM用量についてのCmaxの平均値が約86.2μg/mLであり、そして前記Tmaxの中央値が約3.0時間であり;そして前記PM用量についてのCmaxの平均値が約76.8μg/mLであり、そして前記Tmaxの中央値が約10時間である。
なお別の実施形態において、ナプロキセンの前記AM用量についてのCmaxの平均値が23の%変動係数で、80.9μg/mLであり、そして前記Tmaxの中央値が約3.0時間であり;そしてb)前記PM用量についてのCmaxの平均値が23の%変動係数で、76.2μg/mLであり、そして前記Tmaxの中央値が約10.4時間である。
なおさらに別の実施形態において、ナプロキセンの前記AM用量についてのCmaxの平均値が約80.9μg/mLであり、そして前記Tmaxの中央値が約3.0時間であり;そしてb)前記PM用量についてのCmaxの平均値が約76.2μg/mLであり、そして前記Tmaxの中央値が約10.4時間である。
なおさならる別の実施形態において、エソメプラゾールの前記AM用量について、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)が、69の%変動係数で、1216hr*μg/mLであり、そしてエソメプラゾールの前記PM用量について、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)が、84の%変動係数で、919hr*μg/mLである。
さらなる実施形態において、PM用量は、50〜85の%変動係数範囲で、少なくとも900hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する。
なおさらなる実施形態において、PM用量は、約900hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する。
なおさらなる実施形態において、PM用量は、約2100hr*μg/mLの、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する。
なお別の実施形態において、エソメプラゾールの前記AM用量について、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)は約1216hr*μg/mLであり、そしてエソメプラゾールの前記PM用量について、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)は約919hr*μg/mLである。
なおさらなる実施形態において、AM用量は、45〜70の%変動係数範囲で、少なくとも1200hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有する。
なおさらなる実施形態において、AM用量は、約1200hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有する。
なおさらなる実施形態において、AM用量は、約2800hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有する。
なおさらなる実施形態において、エソメプラゾールの前記AM用量について、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)は、45の%変動係数で、2779hr*μg/mLであり、そしてエソメプラゾールの前記PM用量について、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)は、53の%変動係数で、2066hr*μg/mLである。
なおさらなる実施形態において、エソメプラゾールの前記AM用量について、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)は、約2779hr*μg/mLであり、そしてエソメプラゾールの前記PM用量について、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)は約2066hr*μg/mLである。
なおさらなる実施形態において、単位用量形態の医薬組成物は、少なくとも1種のコアならびに少なくとも第一の層および第二の層を含む多層錠であり、ここで、該コアは、ナプロキセン、またはそれらの薬学的に受容可能な塩を含み;該第一の層は、周囲媒質のpHが約3.5以上である場合に、ナプロキセン、またはそれらの薬学的に受容可能な塩を少なくとも放出し始めるコーティングであり;該第二の層は、エソメプラゾール、またはそれらの薬学的に受容可能な塩であり、ここで、該エソメプラゾール、またはそれらの薬学的に受容可能な塩は約0以上のpHで放出される。
なおさらなる実施形態において、エソメプラゾール、またはそれらの薬学的に受容可能な塩は、0以上のpHで放出される。
別の実施形態において、エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約1以上のpHで放出される。
さらなる実施形態において、エソメプラゾール、またはそれらの薬学的に受容可能な塩は、1以上のpHで放出される。
なお別の実施形態において、エソメプラゾール、またはそれらの薬学的に受容可能な塩は、約0〜約2のpHで放出される。
なおさらなる実施形態において、エソメプラゾール、またはそれらの薬学的に受容可能な塩は、0〜2のpHで放出される。
なおさらなる別の実施形態において、前記エソメプラゾール、またはそれらの薬学的に受容可能な塩の少なくとも一部は、腸溶コーティングでコーティングされていない。
なおさらなる別の実施形態において、第一の層は、腸溶コーティングである。
なおさらなる実施形態において、単位用量形態の医薬組成物は、ナプロキセン、またはそれらの薬学的に受容可能な塩を含むコア、および周囲媒質のpHが約3.5以上である場合に、ナプロキセンを少なくとも放出し始めるコーティングを含む第一の層およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む第二の層(該エソメプラゾール、またはそれらの薬学的に受容可能な塩の少なくとも一部は、腸溶コーティングで囲まれていない)を含む多層錠である。
別の実施形態において、第一の層は、周囲媒質のpHが約4.0、4.5、5.0以上である場合に、ナプロキセンを少なくとも放出し始めるコーティングである。
なおさらに別の実施形態において、前記第一の層は、周囲媒質のpHが約4.0以上である場合に、ナプロキセンを放出し始める。
さらなる実施形態において、前記第一の層は、周囲媒質のpHが約4.5以上である場合に、ナプロキセンを放出し始める。
なおさらなる実施形態において、前記第一の層は、周囲媒質のpHが約5.0以上である場合に、ナプロキセンを放出し始める。
1つの実施形態において、少なくとも約95%のエソメプラゾール、またはそれらの薬学的に受容可能な塩は、腸溶コーティングで囲まれていない。
別の実施形態において、少なくとも約99%のエソメプラゾール、またはそれらの薬学的に受容可能な塩は、腸溶コーティングで囲まれていない。なお別の実施形態において、少なくとも約99.5%のエソメプラゾール、またはそれらの薬学的に受容可能な塩は、腸溶コーティングで囲まれていない。
なお別の実施形態において、多層錠は、重炭酸ナトリウムを実質的に含まない。
なお別の実施形態において、多層錠は、重炭酸ナトリウムを全く(すなわち、100%)含まない。
1つの実施形態において、投与計画は、1日に2回である。
別の実施形態において、投薬は、少なくとも約10時間の間隔が開けられ得る。
別の実施形態において、単位用量形態の医薬組成物は、患者が食事を摂取する約1時間前に投与される。
別の実施形態において、本開示の医薬組成物は、短期間または長期間にわたって(例えば、慢性的に)、患者に治療的に投与され得る。
他の実施形態において、本明細書中に開示される医薬組成物の長期または慢性投与は、短期投与に対して、24時間当たりより高い%時間で、少なくとも約4.0以上の胃内pHをもたらし得る。例えば、特定の医薬組成物の投与は、治療の日1に対して、日9の治療では、約4.0以上の胃内pHのより高い%時間をもたらし得る。
別の実施形態において、その必要がある患者に医薬組成物を送達ための方法は、ナプロキセン、またはそれらの薬学的に受容可能な塩、およびエソメプラゾール、またはそれらの薬学的に受容可能な塩を含む単位用量形態の医薬組成物を患者に投与することを包含し、ここで、胃内pHは、投与の1時間以内に少なくとも約4.0まで上昇する。
別の実施形態において、胃内pHは、投与の30または45分以内に少なくとも約4.0以上まで上昇する。
本明細書中に開示される医薬組成物としては、例えば、当該分野で標準的な方法に従って製造され得る錠剤およびカプセル剤が挙げられるが、これらに限定されない(例えば、Remington’s Pharmaceutical Sciences,16th ed.,A Oslo editor,Easton,Pa.(1980)を参照のこと)。
適切な担体としては、以下が挙げられるが、これらに限定されない:水;食塩水;アルコール;アラビアゴム;植物油;ベンジルアルコール;ポリエチレングリコール;ゼラチン;炭水化物(例えば、ラクトース、アミロースまたはデンプン);ステアリン酸マグネシウム;タルク;ケイ酸;パラフィン;香油;脂肪酸エステル;ヒドロキシメチルセルロース;ポリビニルピロリドン;など。
本明細書中に開示される医薬組成物は、滅菌され得、必要に応じて、例えば、例えば、保存料;安定化剤;緩衝剤;着色料;および香味剤のような助剤と混合され得る。
1つの実施形態において、本明細書中に開示される医薬組成物を含む少なくとも一方の層は、標準的なコーティング技術を使用して塗付され得る。層材料は、有機または水性溶媒中に溶解されるか、または分散され得る。層材料は、例えば、1種またはそれ以上の以下の材料を含み得るが、これらに限定されない:メタクリル酸共重合体、セラック、ヒドロキシプロピルメチルセルロースフタレート(hydroxypropylmethcellulose phthalate)、ポリビニルアセテートフタレート、ヒドロキシプロピルメチルセルローストリメリテート、カルボキシメチルエチル−セルロース、酢酸フタル酸セルロース、および/または他の適切なポリマー。第一の層が溶解するpHは、選択されるポリマーまたはポリマーの組み合わせ、および/またはペンダント基の割合によって制御され得る。例えば、エステル基に対する遊離カルボキシル基の割合によって、ポリマーフィルムの溶解特性を変更し得る。層はまた、例えば、クエン酸トリエチル、フタル酸ジブチル、トリアセチン、ポリエチレングリコール、ポリソルベートまたはその他の可塑剤ような薬学的に受容可能な可塑剤を含み得る。例えば、分散剤、着色料、付着防止剤(anti−adhering)、および消泡剤のような添加物をまた使用し得る。
1つの実施形態において、本明細書中に開示される医薬組成物は、二層錠または多層錠の形態であり得る。二層錠において、錠剤の第一の部分/層は、適切な添加剤、溶解を補助する薬剤、滑沢剤、充填剤などと共に必要な用量でエソメプラゾール、またはそれらの薬学的に受容可能な塩を含み;そして錠剤の第二の部分/層は、他の添加剤、溶解剤、滑沢剤、充填剤などと共に必要な用量でNSAIDを含む。
別の実施形態において、ナプロキセン部分/層は、少なくとも約3.5以上のpHで溶解するポリマーコーティングで囲まれる。
なお別の実施形態において、ナプロキセン部分/層は、少なくとも約4以上のpHで溶解するポリマーコーティングで囲まれる。
ナプロキセン、またはそれらの薬学的に受容可能な塩は、遷延性の(slugging)造粒法、低または高せん断造粒法、湿式造粒法、または流動層造粒のような方法により粒状にされ得る。これらのプロセスのうち、遷延性の造粒法が、一般に、堅くなく、かつよりもろい錠剤を製造する。低せん断造粒法、高せん断造粒法、湿式造粒法および流動層造粒が、一般に、より堅く、もろくない錠剤を製造する。
本発明は、以下の実施例においてさらに明確にされる。当然のことながら、実施例は例証の目的でのみ示される。前記の議論および実施例から、当業者は、本発明の本質的特徴を確認し得、そしてその趣旨および範囲から逸脱することなく、種々の用途および状態に対して本発明を適合させるために様々に変更し、そして改変し得る。結果として、本発明は、以下に示される例証的な実施例によっては限定されず、むしろ本明細書に添付した特許請求の範囲により定められる。
実施例1
腸溶コーティングなしのナプロキセン錠剤500mgの1日に2回の別個の経口投与およびECエソメプラゾール(20mg)カプセル剤(Nexium(R) 20mgカプセル剤)の1日1回の別個の経口投与に対する3つのPN 400製剤(腸溶コーティングなしのエソメプラゾール10、20、または30mgと組み合わせの腸溶コーティングのナプロキセン500mg)の1日に2回の経口投与の健常者の24時間胃内pHおよび薬物動態パラメータ(すなわち、Cmax、Tmax、AUC0-10,am、AUC0-14,pm、AUC0-24、AUC0-t,am、およびAUC0-t,pm)に及ぼす日1および日9の効果を評価するための無作為化非盲検4−ウェイクロスオーバー試験。PN400錠剤は、腸溶コーティングを含む第一層および腸溶コーティングなしのエソメプラゾールを含む第二の層で囲まれた内部コアにナプロキセンを含む多層錠である。
腸溶コーティングなしのナプロキセン錠剤500mgの1日に2回の別個の経口投与およびECエソメプラゾール(20mg)カプセル剤(Nexium(R) 20mgカプセル剤)の1日1回の別個の経口投与に対する3つのPN 400製剤(腸溶コーティングなしのエソメプラゾール10、20、または30mgと組み合わせの腸溶コーティングのナプロキセン500mg)の1日に2回の経口投与の健常者の24時間胃内pHおよび薬物動態パラメータ(すなわち、Cmax、Tmax、AUC0-10,am、AUC0-14,pm、AUC0-24、AUC0-t,am、およびAUC0-t,pm)に及ぼす日1および日9の効果を評価するための無作為化非盲検4−ウェイクロスオーバー試験。PN400錠剤は、腸溶コーティングを含む第一層および腸溶コーティングなしのエソメプラゾールを含む第二の層で囲まれた内部コアにナプロキセンを含む多層錠である。
試験は、1日に2回(BID)投与の腸溶コーティングなしのナプロキセンおよび1日1回投与のECエソメプラゾール(20mg)の組み合わせに対する3つのPN 400製剤のBID投与の日9の胃内pHの薬力学(PD)測定(pH>4.0の%時間)を比較するために設計された。
試験はまた、BID投与の腸溶コーティングなしのナプロキセンおよび1日1回投与のECエソメプラゾールの組み合わせに対する3つのPN400製剤のBID投与の、日1の胃内pHのPD測定(pH>4.0の%時間)を比較するために設計され;そして各治療群における日1および日9のエソメプラゾールおよびナプロキセンの薬物動態を評価した。
これは、28人の成人健常者における単一施設試験であった。この試験は、4回の9日間の治療期間からなる。第一、第二および第三治療期間の後に、少なくとも12日間のウォッシュアウト期間を設けた。適格な被験者は、スクリーニングの日0のPMに第1相試験ユニット(Phase 1 unit)に報告された。
スクリーニング手順は、インフォームドコンセントの受領、病歴および薬歴、健康診断、バイタルサイン、12誘導心電図(ECG)、臨床検査(clinical laboratory testing)、尿中薬物スクリーニング、出産可能な女性の妊娠テスト、およびヘリコバクターピロリの呼気検査を含んだ。臨床検査、健康診断、および生命徴候の測定は、スクリーニングおよび最終来院時に行なった。12誘導心電図(ECG)およびヘリコバクターピロリ感染の可能性について検査するための13C−尿素呼気試験をスクリーニング時に行なった。全ての被験者についての尿素薬物スクリーニングおよび出産可能な女性の尿妊娠テスト(urine pregnancy test)を、各治療期間の日0および日8に行なった。各治療期間の日1および日9に、薬物動態(PK)評価のために24時間採血を行なった。被験者は、スクリーニング手順の開始から14日内に第1相試験ユニットに報告するように指示された。
28人の被験者が、計画の対象とされ、無作為化され、そして治療を受け、そして25人の被験者のデータが、パープロトコル(PP)集団として解析され;包括解析(ITT)、安全性およびPK集団は、28人の全被験者を含んだ。被験者は、BMI値が19〜32kg/m2である18〜55歳の健常な男性または授乳しておらず、妊娠していない女性であり、ヘリコバクターピロリ(H.pylori)陰性であり、そして消化性潰瘍疾患または他の酸関連胃腸(GI)症状の病歴がなく概ね健康であった。
被験者の登録および内訳を表2に要約する。28人の被験者を無作為化し、そして1つの臨床試験実施センター(investigational center)で治療した;これらの被験者がPK集団を構成した。1人の被験者は、3回の治療期間(治療A[PN 400/E30]、B[PN 400/E20]およびD[EC E20+ナプロキセン])を終えた後、個人的な理由で試験から脱落した。PP集団は、25人の被験者を含んだ。
スクリーニングでのITT集団の人口統計学的特性を表3に要約する。試験集団は68%が男性であり、そして平均年齢は約25歳であった。被験者の全員が、ヒスパニック系でない白人であった。
スクリーニング中のいずれかの時点で、しかし少なくとも第一治療期間の日1よりも前に、被験者は、pHプローブの正確な位置を決定するために下部食道括約筋(LES)位置決めを行なった。
被験者に以下の毎日の治療計画の9日コースの各々をクロスオーバー形式で投与するために、第一治療期間の日1に彼らを4つの投薬シーケンス(dosing sequences)のうちの1つに無作為化した:
治療A:1錠 PN 400/E30(ECナプロキセン 500mgおよび非−ECエソメプラゾール 30mg)BID。
治療B:1錠 PN 400/E20(ECナプロキセン 500mgおよび非−ECエソメプラゾール 20mg)BID。
治療C:1錠 PN 400/E10(ECナプロキセン 500mgおよび非−ECエソメプラゾール 10mg)BID。
治療D:EC E20+ナプロキセン(AMに1錠 非−ECナプロキセン 500mgおよび1カプセル ECエソメプラゾール 20mg、ならびにPMに1錠 非−ECナプロキセン 500mg)。
治療A:1錠 PN 400/E30(ECナプロキセン 500mgおよび非−ECエソメプラゾール 30mg)BID。
治療B:1錠 PN 400/E20(ECナプロキセン 500mgおよび非−ECエソメプラゾール 20mg)BID。
治療C:1錠 PN 400/E10(ECナプロキセン 500mgおよび非−ECエソメプラゾール 10mg)BID。
治療D:EC E20+ナプロキセン(AMに1錠 非−ECナプロキセン 500mgおよび1カプセル ECエソメプラゾール 20mg、ならびにPMに1錠 非−ECナプロキセン 500mg)。
全ての治療剤は、食事の60分前に試験担当者により投与された(すなわち、投与は9日間、朝食の60分前(AM用量のため、一晩の絶食後)および/または夕食の60分前(PM用量のため)に受けた)。BID投与される試験薬物を、約10時間開けて投与した。試験薬物の日1のAM用量の投与前に、24時間胃内pHをモニターするためにpHプローブを配置した。LESロケーターを使用して、そして/または治験責任医師による正規の食道マノメトリーの使用により、遠位電極(distal electrode)をLESの10cm下に配置し、近位電極(proximal electrode)をLESの5cm上に配置した。鼻腔からの電極距離の位置を、24時間の胃内pH評価を容易にするために記録した。
さらに、AM用量前の血液サンプルを採取した。PK評価のために、AM用量後の血液サンプルを、約:10、20、30および45分、ならびに1、1.5、2、2.5、3、4、6、8、10(PM用量前血液サンプル)、10.17、10.33、10.5、10.75、11、11.5、12、12.5、13、14、16、18、20および24時間に採取した。被験者は、日2のAM用量後、第1相試験ユニットから退院し、そして日2のPMに次の投薬のために戻り、日3〜8にAMおよびPM服用量を受けることを指示された。被験者は、日9の24時間PKおよびpH評価に備えて、日8のPMに第1相試験ユニットに拘束された。日9のpHのモニタリングおよび血液サンプル採取は、日1の上述した通りに行われた。pHプローブを日10のAMに取り出した。最終PKサンプルを日10のAMに採取した。
被験者は、後続の治療期間のために第1相試験ユニットに戻ることを指示され、そして次の治療期間の時期を伝えられた(すなわち、治療間の少なくとも12日間のウォッシュアウト期間)。後続の各治療期間において、第一期間と同様の手順が行なわれ、そして最後の試験手順は、最終治療期間の日10に、または被験者が試験を中断したときにその都度行われた。
この試験において使用したPK測定は、第1相試験で一般に使用される評価である。
胃内pHの測定
胃内pHを測定するために使用した手順は、制酸薬の薬力学的効果を評価するのに一般に使用される標準法である。Medtronics Digitrapper pHデータロガー(Medtronics,Minneapolis,MN)を使用して、pHを記録した。24時間pH評価を、日1および日9に行なった。pH記録システムは、プローブのチップ中の記録電極と参照電極との間の電位差を測定し、そして数秒毎にこの値を保存した。pHデータを、治療群の割付けを伏せて第三者に提供した。第三者は、データを評価して以下の診断基準に基づいて、pH記録の有効性を決定した:少なくとも20時間分の有効なpHデータが予め特定された参照範囲内にあること;pH記録に技術的な失敗が見られないこと;および連続1時間以上pHデータが参照範囲から外れていないこと。
胃内pHを測定するために使用した手順は、制酸薬の薬力学的効果を評価するのに一般に使用される標準法である。Medtronics Digitrapper pHデータロガー(Medtronics,Minneapolis,MN)を使用して、pHを記録した。24時間pH評価を、日1および日9に行なった。pH記録システムは、プローブのチップ中の記録電極と参照電極との間の電位差を測定し、そして数秒毎にこの値を保存した。pHデータを、治療群の割付けを伏せて第三者に提供した。第三者は、データを評価して以下の診断基準に基づいて、pH記録の有効性を決定した:少なくとも20時間分の有効なpHデータが予め特定された参照範囲内にあること;pH記録に技術的な失敗が見られないこと;および連続1時間以上pHデータが参照範囲から外れていないこと。
サンプルの採取
PK血液サンプルを、6mLのヘパリンナトリウムVACUTAINER管に採取し、そしてサンプル採取の30分以内に、約4℃で維持した冷凍遠心器中、約10分間、3000rpm(約1800×g)で遠心分離するまで、氷上に貯蔵した。血漿上清を回収し、そして回収の60分以内に−20℃またはそれ以下に凍結した。サンプルを2当量のアリコートに分け、一方の管をナプロキセン分析に使用し、そして他方をエソメプラゾール分析に使用した。サンプルを−20℃で凍結したまま、試験の終わりに解析するためPPD Development,Richmond VAに一夜で輸送した。
PK血液サンプルを、6mLのヘパリンナトリウムVACUTAINER管に採取し、そしてサンプル採取の30分以内に、約4℃で維持した冷凍遠心器中、約10分間、3000rpm(約1800×g)で遠心分離するまで、氷上に貯蔵した。血漿上清を回収し、そして回収の60分以内に−20℃またはそれ以下に凍結した。サンプルを2当量のアリコートに分け、一方の管をナプロキセン分析に使用し、そして他方をエソメプラゾール分析に使用した。サンプルを−20℃で凍結したまま、試験の終わりに解析するためPPD Development,Richmond VAに一夜で輸送した。
血漿中のエソメプラゾールの分析
アッセイ方法
エソメプラゾールは光学的に安定であり、そしてヒトにおいてSからRエナンチオマーへの変換の程度はごくわずかである。従って、エソメプラゾールについてのサンプル分析を、オメプラゾール用にバリデートされた(validated)高速液体クロマトグラフィータンデム質量分析(HPLC/MS/MS)法を使用して行なった。この方法は、PPD Development,Richmond,VAにより開発され、そして検証された。
アッセイ方法
エソメプラゾールは光学的に安定であり、そしてヒトにおいてSからRエナンチオマーへの変換の程度はごくわずかである。従って、エソメプラゾールについてのサンプル分析を、オメプラゾール用にバリデートされた(validated)高速液体クロマトグラフィータンデム質量分析(HPLC/MS/MS)法を使用して行なった。この方法は、PPD Development,Richmond,VAにより開発され、そして検証された。
アッセイ方法は概ね、本明細書中以下に本質的に記載されるように行なった:
抗凝固剤(ヘパリンナトリウム)および被検体を含むヒト血漿のアリコート(100μL)に内部標準(オメプラゾールの重水素化されたアナログ)を強化した(fortify)。被検体をPhenomenex Strata−X(10mg)96−ウェルSPEプレートを使用して、固相抽出(SPE)で単離した。Micromass Quattro Micro、トリプル四重極計器を使用して、最終抽出物をMS/MS検出器を備えるHPLCで分析した。被検体のクロマトグラフ保持および分離を、勾配移動相プログラムを使用するBetasil Silica−100分析カラム(3×50mm、5μm粒経)上で行った。移動相Aは、アセトニトリル中0.1% ギ酸からなり、そして移動相Bは0.1% ギ酸からなる。被検体は、多重反応モニタリング(MRM)モードのポジティブエレクトロスプレーイオン化(positive electrospray ionization)を備えるMS/MSにより検出され、イオンはオメプラゾール(m/z 346→198)および重水素化オメプラゾール(m/z 349→198)についてモニターした。
抗凝固剤(ヘパリンナトリウム)および被検体を含むヒト血漿のアリコート(100μL)に内部標準(オメプラゾールの重水素化されたアナログ)を強化した(fortify)。被検体をPhenomenex Strata−X(10mg)96−ウェルSPEプレートを使用して、固相抽出(SPE)で単離した。Micromass Quattro Micro、トリプル四重極計器を使用して、最終抽出物をMS/MS検出器を備えるHPLCで分析した。被検体のクロマトグラフ保持および分離を、勾配移動相プログラムを使用するBetasil Silica−100分析カラム(3×50mm、5μm粒経)上で行った。移動相Aは、アセトニトリル中0.1% ギ酸からなり、そして移動相Bは0.1% ギ酸からなる。被検体は、多重反応モニタリング(MRM)モードのポジティブエレクトロスプレーイオン化(positive electrospray ionization)を備えるMS/MSにより検出され、イオンはオメプラゾール(m/z 346→198)および重水素化オメプラゾール(m/z 349→198)についてモニターした。
定量化は、被検体対内部標準のピーク面積比によるものであった。定量化の線形範囲はヒト血漿において1〜1000ng/mLであり、定量化の下限値(LLOQ)は1ng/mLであった。アッセイを特異性、精度(precision)、真度(accuracy)、およびサンプル安定性に関して検証した。
アッセイ性能
1.00〜1000ng/mLの範囲の8つの較正標準および各被検体を5つの異なる濃度(2.60、8.00、30.0、130、および750ng/mL)で含む品質管理(QC)サンプルを調製し、そして−20℃で保存した。QCサンプルの分析についてのバッチ間精度および真度を、この試験における臨床サンプルのバッチ分析から決定した。精度を、各QCレベルについて得られた一連の値の%変動係数(%CV)として測定した。真度を、各QCレベルでの理論濃度から平均値の%差として表した。
1.00〜1000ng/mLの範囲の8つの較正標準および各被検体を5つの異なる濃度(2.60、8.00、30.0、130、および750ng/mL)で含む品質管理(QC)サンプルを調製し、そして−20℃で保存した。QCサンプルの分析についてのバッチ間精度および真度を、この試験における臨床サンプルのバッチ分析から決定した。精度を、各QCレベルについて得られた一連の値の%変動係数(%CV)として測定した。真度を、各QCレベルでの理論濃度から平均値の%差として表した。
オメプラゾールラン(run)についてのQCのアッセイ間(inter−assay)CVは、3.44%〜5.88%の範囲であり、理論値(theoretical)との平均%差は0.32 9%〜1.80%の範囲であった。公称の値と逆算による較正曲線の値との差は−2.87%〜1.54%の範囲であった。希釈された被験者サンプルを含む分析ランについては、研究サンプルの希釈を検証するのと同様の様式で、適正レベル品質管理プールを希釈し、そして分析した。このランにおける希釈QCの%CVは、0.599%〜2.74%の範囲であり、理論値との平均%差は、−1.24%〜3.99%の範囲であった。
血漿中のナプロキセンの分析
アッセイ方法
ヒト血漿中のナプロキセンの濃度は、概ね本明細書以下に本質的に記載されるようにして、PPD Development,Richmond,VAで開発され、そして検証された蛍光検出を用いるバリデートされたHPLC法を使用して決定した。
アッセイ方法
ヒト血漿中のナプロキセンの濃度は、概ね本明細書以下に本質的に記載されるようにして、PPD Development,Richmond,VAで開発され、そして検証された蛍光検出を用いるバリデートされたHPLC法を使用して決定した。
ヘパリンナトリウムおよび被検体を含むヒト血漿のアリコート(100μL)を、内部標準溶液(2−ナフチル酢酸)と混合し、そして塩化カリウムで希釈した。液−液抽出を使用して、被検体および内部標準を分離した。被検体のクロマトグラフ保持および分離を、45% アセトニトリル:55% 14.8mM リン酸緩衝液からなる定組織移動相を使用するSymmetry C18カラム(4.6×150mm、5μm粒経)で行った。それぞれ、230nmおよび370nmの励起波長および発光波長を使用する蛍光により被検体を検出した。
定量化は、被検体対内部標準のピーク高さ比によるものであった。この方法の公称の範囲は、ヒト血漿におけるナプロキセンについて0.10〜100μg/mLであり、LLOQは0.10μg/mLであった。
アッセイ性能
0.1〜100ng/mLの範囲の8つの較正基準および被検体を5つの異なる濃度(0.28、0.80、3.0、12.0および76.0μg/mL)で含むQCサンプルを調製し、そして−20℃で保存した。QCサンプルの分析についてのバッチ間精度および真度を、この試験における臨床サンプルのバッチ分析から決定した。精度を、各QCレベルについて得られた一連の値の%CVとして測定した。真度を、各QCレベルでの理論濃度から平均値の%差として示した。
0.1〜100ng/mLの範囲の8つの較正基準および被検体を5つの異なる濃度(0.28、0.80、3.0、12.0および76.0μg/mL)で含むQCサンプルを調製し、そして−20℃で保存した。QCサンプルの分析についてのバッチ間精度および真度を、この試験における臨床サンプルのバッチ分析から決定した。精度を、各QCレベルについて得られた一連の値の%CVとして測定した。真度を、各QCレベルでの理論濃度から平均値の%差として示した。
ナプロキセンランのQCのアッセイ間CVは、2.22%〜9.59%の範囲であり、理論値との平均%差異は−3.59%〜0.933%の範囲であった。公称の値と逆算による較正曲線値との差異は−4.73%〜3.79%の範囲であった。希釈された被験者サンプルを含む分析ランについては、試験サンプルの希釈を検証するのと同様の様式で、適正レベルのQCサンプルを希釈し、そして分析した。このランにおける希釈QCの%CVは、4.12%であり、理論値との平均%差は、−1.54%の範囲であった。
統計および解析
データは、分類的および序数的な測定については各分類における被験者の数および割合を、そして連続的な測定については平均、標準偏差または標準誤差、中央値、および範囲を報告することにより要約した。全ての統計解析およびデータリストは、SAS(R) system,version8.2またはそれ以上を使用して仕上げた。
データは、分類的および序数的な測定については各分類における被験者の数および割合を、そして連続的な測定については平均、標準偏差または標準誤差、中央値、および範囲を報告することにより要約した。全ての統計解析およびデータリストは、SAS(R) system,version8.2またはそれ以上を使用して仕上げた。
分析のために3つの解析集団を使用した:
1)包括解析(ITT)集団:少なくとも1つの治療期間に関する有効なpHデータを有する全ての無作為化された被験者。被験者がプロトコル毎の試験医薬の全投薬を受け、臨床治験責任医師により決定された有効なpHデータを少なくとも20時間有し、pH記録の技術的失敗がなく、そして参照範囲外のpHデータを連続1時間以上有さない場合、被験者は、各治療期間について、有効なpHデータを有するとした。
2)パープロトコル(PP)集団:4つ全ての治療期間に関する有効なpHデータを有し、そしてPD評価項目の評価に有意な影響を与えるかたちでプロトコルから逸脱しなかった全てのITT被験者。
3)PK集団:少なくとも1つの治療期間の間、試験医薬の全投薬を受け、そしてその試験薬物のPKパラメータを決定するのに十分な採血が行われた全ての無作為化された被験者。
1)包括解析(ITT)集団:少なくとも1つの治療期間に関する有効なpHデータを有する全ての無作為化された被験者。被験者がプロトコル毎の試験医薬の全投薬を受け、臨床治験責任医師により決定された有効なpHデータを少なくとも20時間有し、pH記録の技術的失敗がなく、そして参照範囲外のpHデータを連続1時間以上有さない場合、被験者は、各治療期間について、有効なpHデータを有するとした。
2)パープロトコル(PP)集団:4つ全ての治療期間に関する有効なpHデータを有し、そしてPD評価項目の評価に有意な影響を与えるかたちでプロトコルから逸脱しなかった全てのITT被験者。
3)PK集団:少なくとも1つの治療期間の間、試験医薬の全投薬を受け、そしてその試験薬物のPKパラメータを決定するのに十分な採血が行われた全ての無作為化された被験者。
薬力学的評価項目
各Digitrapperセッションにおいて、各被験者について食道pHおよび胃内pHの記録の別々のプロットを作成し、そして有効でないpHデータについて検討した。0.6〜8.0の範囲外の記録されたpH値に特に注意を払った。その方法において合理的に予想されるばらつきにより生じたとは考え難いと治験責任医師により判断され、そして計器の一時的な信頼性の低下の可能性を示唆していると思われる程度に続いた値を特定し、データベースから削除した。他の明らかな「フラット−ライニング(flat−lining)」のpH記録もまた、有効でないデータとみなした。
各Digitrapperセッションにおいて、各被験者について食道pHおよび胃内pHの記録の別々のプロットを作成し、そして有効でないpHデータについて検討した。0.6〜8.0の範囲外の記録されたpH値に特に注意を払った。その方法において合理的に予想されるばらつきにより生じたとは考え難いと治験責任医師により判断され、そして計器の一時的な信頼性の低下の可能性を示唆していると思われる程度に続いた値を特定し、データベースから削除した。他の明らかな「フラット−ライニング(flat−lining)」のpH記録もまた、有効でないデータとみなした。
PD評価項目を治療毎に集約し、そして分散分析(ANOVA)により解析した。ANOVAモデルには、母数効果としてのシーケンス、期間、および治療、ならびに変量効果としてのシーケンス内の被験者が含まれた。各治療についての最小二乗(LS)平均、各PN 400治療と実対照薬との間のLS平均の差、および全ての治療差異の95%信頼区間(CI)が計算された。ITTおよびPP集団の両方が、PD解析に使用された。PP集団が、主な解析集団であった。さらに、日1および日9のpH>3.0および>5.0の%時間が、pH>4.0の%時間と同様の様式で解析された。日1および日9の24時間にわたる平均pHデータが、治療毎にプロットされた。
予備的試験から、pH>4.0の%時間の被験者内標準偏差(SD)は10%であった。本研究は、解析のために評価可能な被験者を24人とすることを目標として、28人の被験者を登録するよう計画した。合計24人の被験者は、24時間にわたるpH>4.0の%時間における各PN 400治療と実対照薬との間の差が≦−8%であるという帰無仮説を片側有意水準0.05のペアワイズt検定(pairwise t−test)を使用して棄却するための検出力80%を提供する。
主要薬力学的評価項目:日9の胃内pH>4.0の%時間
日9の結果を表4に示す。日9にPN 400/E30およびPN 400/E20治療の両方が、EC E20+ナプロキセンでの治療よりも大きな胃内pH>4.0の%時間をもたらした。PN 400/E10は、最も低い胃内pH>4.0の%時間を有し、そしてまた、表4において高い%CVからも明らかなように最も変動がある治療であった。
日9の結果を表4に示す。日9にPN 400/E30およびPN 400/E20治療の両方が、EC E20+ナプロキセンでの治療よりも大きな胃内pH>4.0の%時間をもたらした。PN 400/E10は、最も低い胃内pH>4.0の%時間を有し、そしてまた、表4において高い%CVからも明らかなように最も変動がある治療であった。
日1に、胃内pH>4.0のLS平均%時間は、PN 400/E10の13%〜PN 400/E30の28%の範囲であった。EC E20+ナプロキセンと比較した治療差は、小さかった。PN 400/E30(28%)だけが、EC E20+ナプロキセン(21%)と比較して、統計的に有意なより大きいpH>4.0の%時間を有した。
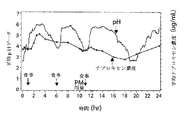
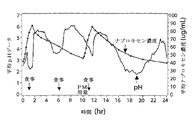
図1に示されるように、1日を通して3回のpHの上昇があり、これは、それぞれ、朝食、昼食および夕食の1、6および11時間での食物摂取と関連していた。全ての治療について、各食事の約1時間後にpHの上昇が起こった。日9のPN 400のAM用量後、食事により誘導されるpHの上昇よりも約1時間早く、pHの上昇が起こった(図2もまた参照のこと)。EC E20+ナプロキセンのAM用量後、PN 400よりも少なくとも30分遅く、pH上昇が起こった。
日9のpHプロファイルは全体として、食物摂取の影響を上回る胃内pHに対するエソメプラゾール投薬関連の効果を示した。胃内pHプロファイルに対する効果は、PN 400/E30とPN 400/E 20間で類似しており、各これらの治療は、PN400/E10またはEC E20+ナプロキセン治療のどちらよりも、食物摂取後の胃内容物の低pHレベルへのより緩やかな戻りを反映している。
ITT集団についての日9の結果は、PP集団からの結果と類似していた。全治療における日9の最初のpH測定は、一晩の絶食後の平均胃内pHが2.0〜3.0であったことを示し、これは日1の最初のpHよりも高かった(1.0〜2.0)(図2)。
図4に示されるように、この試験の主要PD応答、すなわち、日9の胃内pH>4.0の%時間は、PN400治療におけるエソメプラゾール量と共に増加した。しかし、エソメプラゾール量をPN 400において10から20mgに増加させた場合は、さらに大きな主要PD応答の増加が観察された(すなわち、40.9から76.5%へ)。エソメプラゾール量をPN 400において20から30mgに増加した場合では、胃内pH>4.0は71.4から76.5%への小さい増加のみであった。
副次的薬力学的評価項目:日1の胃内pH>4.0の%時間
日1の結果を表5に示す。胃内pH>4.0のLS平均%時間は、PN 400/E10の約13%〜PN 400/E30の約28%の範囲であった。
日1の結果を表5に示す。胃内pH>4.0のLS平均%時間は、PN 400/E10の約13%〜PN 400/E30の約28%の範囲であった。
日1の24時間にわたる平均pHデータを図2に示す。日1のpHプロファイルは、一晩の絶食後、いずれの治療前の平均ベースラインの胃内pHが1.0〜2.0で低いことを示した。1日を通してpH4.0を超える3回のpH上昇があり、これは、1、6および11時間での食物摂取と関連していた。胃内pHの上昇は、全治療について各食事の約1時間後に起こった。治療の日1の初めの24時間を通して、食事の効果を超える程度の胃内pHに対する効果はいずれの試験治療においてもほとんど認められなかった。
他の薬力学的所見
日9のpH>3.0および>5.0の%時間の解析は、PP集団についての日9のpH>4の%時間の主要評価項目のものと統計的に類似のパターンをもたらし、PN400/E30およびPN400/E20は、EC E20+ナプロキセンよりも大きな制酸能力(acid−reducing capacity)を示し、これはLS平均差および95% CIに基づけばPN400/E10よりも大きな能力であった。日1のpH>3.0および>5.0の%時間の解析結果は、PP集団に基づけば、日1のpH>4の%時間の主要評価効果の結果と類似していた。ITT集団の結果は、PP集団のものと類似していた。
日9のpH>3.0および>5.0の%時間の解析は、PP集団についての日9のpH>4の%時間の主要評価項目のものと統計的に類似のパターンをもたらし、PN400/E30およびPN400/E20は、EC E20+ナプロキセンよりも大きな制酸能力(acid−reducing capacity)を示し、これはLS平均差および95% CIに基づけばPN400/E10よりも大きな能力であった。日1のpH>3.0および>5.0の%時間の解析結果は、PP集団に基づけば、日1のpH>4の%時間の主要評価効果の結果と類似していた。ITT集団の結果は、PP集団のものと類似していた。
PN 400をBID投薬する場合、この投薬計画に対応する個々の時間間隔、すなわち、0〜10時間および10〜24時間を、日9の胃内pH>4.0の%時間について解析した。0〜10時間について、PN 400/E30治療は、EC E20+ナプロキセン(71%)での治療よりも大きな胃内pH>4.0の%時間(84%)をもたらしたことを、この結果が示した。PN 400/E20はまた、胃内pH>4.0の高い%時間(79%)を有したが、結果はEC E20+ナプロキセン治療と統計的に有意な差ではなかった。PN400/E30およびPN400/E20のBID投薬はどちらも、10〜24時間の治療間隔で、EC E20+ナプロキセンでの治療(47%)と比較して、より大きな胃内pH>4.0の%時間(それぞれ、71%および66%)を有した。PN400/E10治療は、0〜10時間(52%)および10〜24時間(33%)の両方の治療間隔で、EC E20+ナプロキセンでの治療と比較して、より低い胃内pH>4.0の%時間を有した。
薬物動態評価項目
日1に、PN 400/E30、PN 400/E20およびEC E20+ナプロキセンを終了する28人の被験者;およびPN 400/E10を終了する27人の被験者から得たエソメプラゾールおよびナプロキセン血漿プロファイルについて、PKデータ解析を行なった。
日1に、PN 400/E30、PN 400/E20およびEC E20+ナプロキセンを終了する28人の被験者;およびPN 400/E10を終了する27人の被験者から得たエソメプラゾールおよびナプロキセン血漿プロファイルについて、PKデータ解析を行なった。
日9に、PN 400/E30およびEC E20+ナプロキセンを終了する28人の被験者、ならびにPN 400/E20およびPN 400/E10を終了する27人の被験者からのエソメプラゾールまたはナプロキセン血漿プロファイルについて、PKデータ解析を行なった。
3つの異なるPN 400治療後にエソメプラゾールについてのPKパラメータを決定し、そして各4つの治療後にナプロキセンについてのPKパラメータを決定し、このPKパラメータには、日1および日9のピーク血漿濃度(Cmax);日1および日9のピーク血漿濃度までの時間(tmax);日1および日9の時間0から薬物濃度が測定可能な最終時点までの血漿中濃度時間曲線下面積(AUC0-t);および可能な場合、日1および日9のAMおよびPM用量の両方後の消失半減期(terminal half−life)(t1/2)が含まれる。さらに、日1および日9に、時間0(投薬時)からAM用量10時間後のAUC(AUC0-10,am)および時間0(投薬時)からPM用量14時間後のAUC(AUC0-14,pm)ならびに一日の総AUC(AUC0-24)を決定した。EC E20+ナプロキセン後のエソメプラゾールについてのPKパラメータには、日1および日9の両日のAM用量後のCmax、tmax、AUC0-t、t1/2、およびAUC0-24が含まれる。
ナプロキセンおよびエソメプラゾールの両方についての以下のパラメータ:Cmax,am、Cmax,pm、AUC0-10,am、AUC0-14,pm、およびAUC0-24についての日9対日1の比率の推定値および90% CIを決定するために、分散分析(ANOVA)を使用して、統計解析を行なった。
血漿エソメプラゾールおよびナプロキセン濃度時間データを、治療、試験の日および被験者によりリストアップする。平均値、SD、%CV、中央値、最小値および最大値を含む記述統計学を使用して、治療および試験の日の各公称の(または予定された)採取時間により、濃度データを要約した。LLOQ(すなわち、エソメプラゾールについて1ng/mL、およびナプロキセンについて0.10μg/mL)を下回る血漿濃度は、記述統計学の計算上、0値として処理された。LLOQを下回る(BQL)値を1またはそれ以上有する時点の平均/中央値は、その平均/中央値がアッセイのLLOQを下回らない限り報告し、下回る場合は、その値をBQLとして報告した。個々の被験者の血漿中濃度時間曲線を実際の採取時間に対してプロットし、そして平均/中央値の血漿中濃度時間曲線を治療による公称の採取時間に対してプロットした。
WinNonlinバージョン4.1(Pharsight Corporation,Mountain View,CA)を使用して、各被検体の血漿中濃度時間データを、非コンパートメント解析に供した。各サンプルについての実際の採血時間を、PKデータ解析に使用した。BID投薬、すなわち、治療A、B、およびCにおけるエソメプラゾールまたは4つ全ての治療におけるナプロキセンから得られた被検体濃度について、AMおよびPM用量後に得られた血漿プロファイルについて別々にPK解析を行なった。従って、PM用量後の濃度時間プロファイルについての実際の投薬後採取時間は、PM用量の実際の投薬時間からの経過時間に基づいて計算された。
PK解析について、各被検体の個々のプロファイルにおいてLLOQを下回る血漿濃度(BQL値)を以下のように処理した。その値がプロファイルに現れたのが、そのプロファイルの吸収相(absorptive phase)の間、すなわち、そのプロファイルにおいて最大濃度を観察する前である場合、0濃度の値を代入した。プロファイルの吸収相ではなく2つの測定可能な被検体濃度間に生じた単一のBQL値は、原則的に省かれた。2またはそれ以上のBQL値が連続してピーク時間後(または排出相の間)に生じた場合、そのプロファイルは、そのプロファイルの測定可能な被検体濃度が得られた最後の時点で終了したと決定した。
日1および日9に、エソメプラゾールについて(各3つのPN400治療後)、およびナプロキセンについて(各4つの治療後)計算したPKパラメータには以下が含まれる:AM用量後(Cmax,am)およびPM用量後(Cmax,pm)に観察された最大血漿濃度;AM用量後(tmax,am)およびPM用量後(tmax,pm)のピーク血漿濃度までの時間;AM用量後(tlag,am)およびPM用量後(tlag,pm)の最初に測定可能な血漿濃度までの時間;WinNonlinにおいてリニアアップ(linear−up)およびログダウン(log−down)台形法を使用して計算した、AM用量後(AUC0-t,am)およびPM用量後(AUC0-t,pm)の時間0から薬物濃度が測定可能な最終時点(tlast)までの血漿中濃度時間曲線下面積(AUC);データが認められる場合、少なくとも3つの時点を使用して、血漿薬物濃度時間曲線の見掛けの最終対数線形相(terminal log−linear phase)の傾きにより決定される見かけの一次消失速度定数(λz,amおよびλz,pm);データが認められる場合、AMおよびPM用量後の0.693/λzとして決定される見かけの血中濃度半減期(t1/2)、すなわち、それぞれ、t1/2,amおよびt1/2,pm;必要ならば、tlastからAM用量10時間後までのλz,am推量を使用する外挿法を用いる時間0(AM用量の時間)からAM用量10時間後までのAUC(AUC0-10,am);必要ならば、tlastからPM用量14時間後までのλz,pm推量を使用する外捜法を用いる時間0(PM用量の時間)からPM用量14時間後までのAUC(AUC0-14,pm);およびAUC0-10,am+AUC0-14,pmとして決定される時間0(AM用量の時間)からAM用量24時間後までの1日の総AUC(AUC0-24)。
日1および日9に、治療DのエソメプラゾールについてAM用量後に計算したPKパラメータには、Cmax、tmax、AUC0-t、t1/2およびAUC0-24が含まれた。上記と同じ方法を適用した。
治療および試験の日に、ナプロキセンおよびエソメプラゾールの全PKパラメータについて記述統計学(平均、SD、%CV、中央値、最小値および最大値を含む)を計算した。幾何平均および関連95%信頼区間(CI)をまた、tmaxを除いて全PKパラメータについて計算した。
以下のパラメータについての日9対日1の比率の推定値および関連90% CIを決定するために、ANOVAを使用して、統計解析を行なった:各3つのPN400治療におけるエソメプラゾールデータについて、および各4つの治療におけるナプロキセンデータについて、Cmax,am、Cmax,pm、AUC0-10,am、AUC0-14,pm、およびAUC0-24。治療Dからのエソメプラゾールデータについて、CmaxおよびAUC0-24についての日9対
日1の比率を決定した。自然対数変換CmaxおよびAUC値を解析に使用し、これによって、各パラメータについての幾何最小二乗平均比(geometric least−squares mean ratio)を決定した。
日1の比率を決定した。自然対数変換CmaxおよびAUC値を解析に使用し、これによって、各パラメータについての幾何最小二乗平均比(geometric least−squares mean ratio)を決定した。
3つのPN400治療からのエソメプラゾールのCmax,am、Cmax,pm、AUC0-10,am、AUC0-14,pm、およびAUC0-24における用量比例性を、以下のような検出力モデルを使用して、日1および日9に別々に解析した:
y=a*(用量)b
ln(y)=ln(a)+ b*ln(用量)
ここで、yはPKパラメータ値であり、そしてlnは自然対数である。検出力モデルには、母数効果としてのln(用量)および期間ならびに変量効果としての被験者が含まれた。
y=a*(用量)b
ln(y)=ln(a)+ b*ln(用量)
ここで、yはPKパラメータ値であり、そしてlnは自然対数である。検出力モデルには、母数効果としてのln(用量)および期間ならびに変量効果としての被験者が含まれた。
エソメプラゾール
表6は、それぞれ、日1および日9のPN 400/E30およびEC E20+ナプロキセン治療を終えた28人の被験者ならびにPN 400/E10治療を終えた27人の被験者;ならびに、日1および日9のPN 400/E20治療を終えた28、および27人の被験者についてのエソメプラゾール血漿中濃度時間データについて行なった、PK解析からの結果を要約する。
表6は、それぞれ、日1および日9のPN 400/E30およびEC E20+ナプロキセン治療を終えた28人の被験者ならびにPN 400/E10治療を終えた27人の被験者;ならびに、日1および日9のPN 400/E20治療を終えた28、および27人の被験者についてのエソメプラゾール血漿中濃度時間データについて行なった、PK解析からの結果を要約する。
日1のPN 400の経口投与後、エソメプラゾール濃度は、AM用量10分後、およびPM用量20〜30分後に測定可能となった。PM用量後の血漿エソメプラゾール濃度は、両日ともにAM用量後よりも低かった。エソメプラゾールのCmaxおよびAUCは、日1のAM用量後、ほぼ用量比例で増加したが、日1のPM用量ならびに日9のAMおよびPM用量後、用量比例を上回った。エソメプラゾール濃度は、各PN 400治療の日1よりも日9でかなり高かった。日9対日1の幾何最小二乗平均AUC0-24比は、PN 400/E30、PN 400/E20、およびPN 400/E10での治療について、それぞれ、7.13、4.10、および2.26であった。
EC E20+ナプロキセン治療後、最初に測定可能なエソメプラゾール濃度は、投薬の0.5〜1.5時間後であった。EC E20+ナプロキセン治療群におけるEC E20に対して、PN400/E20治療群におけるエソメプラゾールの効果を評価するために、PN400/E20およびEC E20+ナプロキセン治療群からのPKパラメータを比較した。日1のエソメプラゾールCmax,amの平均値は、PN400/E20およびEC E20+ナプロキセン治療とほぼ等しかった(それぞれ、292および282ng/mL)。PN400/E20治療の日1のAUC0-10の平均値は、EC E20+ナプロキセン治療の約3分の2であった(それぞれ、350対520hr・ng/mL)。しかし、日9のPN400/E20治療群についてのエソメプラゾールAUC0-10は、EC
E20+ナプロキセン治療群よりも大きく(それぞれ、1216対1046hr・ng/mL)、そしてPN400/E20治療群についてのCmax,amは、EC E20+ナプロキセン治療群のほぼ2倍であった(それぞれ、715対435ng/mL)。
E20+ナプロキセン治療群よりも大きく(それぞれ、1216対1046hr・ng/mL)、そしてPN400/E20治療群についてのCmax,amは、EC E20+ナプロキセン治療群のほぼ2倍であった(それぞれ、715対435ng/mL)。
4つ全ての治療後の血漿エソメプラゾール濃度時間プロファイルの平均および中央値をプロットし、そして平均プロットを図3および4に示す。これらの図は、日1または日9のAMまたはPM用量後のエソメプラゾール濃度が、PN 400治療におけるエソメプラゾール量と共に増加したことを示す。さらに、日1および日9の両日のAM用量後のエソメプラゾール濃度は、各PN 400治療のPM用量後よりも高かった。EC E20+ナプロキセン治療後の平均プロファイルは、PN 400と比較して、日1および日9の両日で遅れた吸収ピークを示す。さらに、EC E20+ナプロキセン治療後のピークエソメプラゾール濃度は、特に日9のPN 400/E20後よりも低かった(約50%低い)。
各治療群の日1および日9のAMおよびPM用量後のエソメプラゾールの薬物動態パラメータを、以下の表7から10に要約する。
ナプロキセン
表11は、それぞれ、日1および日9のPN 400/E30およびEC E20+ナプロキセン治療を終えた28人の被験者ならびにPN 400/E10治療を終えた27人の被験者;ならびに、日1および日9のPN 400/E20治療を終えた28、および27人の被験者についてのナプロキセン血漿中濃度時間データについて行なった、PK解析からの結果を要約する。
表11は、それぞれ、日1および日9のPN 400/E30およびEC E20+ナプロキセン治療を終えた28人の被験者ならびにPN 400/E10治療を終えた27人の被験者;ならびに、日1および日9のPN 400/E20治療を終えた28、および27人の被験者についてのナプロキセン血漿中濃度時間データについて行なった、PK解析からの結果を要約する。
日1のPN 400の経口投与後、最初に測定可能なナプロキセン濃度は、AM用量約2時間後に生じた。ナプロキセンに対する血漿暴露は、3つのPN400治療間で同程度であった。PN 400の反復投与後、日9対日1のナプロキセン濃度比は、ナプロキセンの半減期推量に基づいて期待された蓄積量と一致した。AMとPM用量間のナプロキセンAUCにおける変動性は、日1よりも日9でより小さく、これはナプロキセンレベルが反復投与によりほぼ定常状態になったことを示す。Cmax値は、日9と比較して、日1のAMおよびPM用量間でよりやや可変であり、平均AMレベルは、日1の全ての治療についての平均PMレベルよりも低く、そして平均AMレベルは、日9の全ての治療についての平均PMレベルよりも少し高かった。
日1の治療Dの初めの(AM)投薬後、血漿ナプロキセン濃度は、初めの採取時間、すなわち、投薬の10分後からAM用量24時間後(またはPM用量の14時間)まで全ての被験者で測定可能であり、これは腸溶コーティングされていないナプロキセンの典型的な性能を示した。
4つ全ての治療後の血漿ナプロキセン濃度対時間プロファイルの平均および中央値を図5および6に示す。
各治療について、日1および日9のAMおよびPM用量後のナプロキセンのPKパラメータを、以下の表12から15に要約した。
薬力学測定に関連する薬物濃度または薬物動態
図7に示されるように、エソメプラゾールに対する平均総血漿暴露、すなわち、日9のAUC0-24(定常状態暴露を示す)、と日9の胃内pH>4.0の平均%時間(主要PD評価項目)との関係を、以下に定義される典型的な薬理学的最大反応(pharmacological maximal response)(Emax)モデルにより表し得る:
作用=(Emax *AUC0-24)/(EC50+AUC0-24)、ここで、
作用=日9の胃内pH>4.0の平均%時間(エソメプラゾールAUC0-24 が0である場合、胃内pH>4.0も0時間であると仮定する)
Emax=最大作用
EC50=最大作用の50%を示すのに必要な血漿平均AUC0-24
Emaxは、定常状態で1日の胃内pH>4.0時間の90.4%であると見積もられた。最大反応の半分(または50%)を達成するのに必要なAUC0-24値は、713hr*ng/mLであると見積もられた。PN 400/E20後、PD反応は、最大反応の約80%に達しており、これはPN 400/E30により達成されるものよりもわずかに低いだけであった(Emaxの85%)。
図7に示されるように、エソメプラゾールに対する平均総血漿暴露、すなわち、日9のAUC0-24(定常状態暴露を示す)、と日9の胃内pH>4.0の平均%時間(主要PD評価項目)との関係を、以下に定義される典型的な薬理学的最大反応(pharmacological maximal response)(Emax)モデルにより表し得る:
作用=(Emax *AUC0-24)/(EC50+AUC0-24)、ここで、
作用=日9の胃内pH>4.0の平均%時間(エソメプラゾールAUC0-24 が0である場合、胃内pH>4.0も0時間であると仮定する)
Emax=最大作用
EC50=最大作用の50%を示すのに必要な血漿平均AUC0-24
Emaxは、定常状態で1日の胃内pH>4.0時間の90.4%であると見積もられた。最大反応の半分(または50%)を達成するのに必要なAUC0-24値は、713hr*ng/mLであると見積もられた。PN 400/E20後、PD反応は、最大反応の約80%に達しており、これはPN 400/E30により達成されるものよりもわずかに低いだけであった(Emaxの85%)。
PN 400/E30およびPN 400/E20の反復投与は、EC E20+ナプロキセン(投薬約1.5時間後)よりもより早い胃内pHの上昇の出現をもたらした(投薬約1時間後)(図1)。
図8Aに示されるように、PN 400からのナプロキセンの放出は、AM用量の1.5〜2時間後に生じた。ナプロキセンがPN 400治療後のピーク濃度に吸収される前に、すでに、胃内pHはpH 4.0を優に上回る高レベルに達していた(図8A)。実際、食事の1時間前に行われたPN 400/E20のBID計画により、胃内pHは、24時間の間の70%以上で4.0以上を維持し、この間にこの日の全ての血漿ナプロキセン濃度の上昇が含まれる。
対照的に、EC E20+ナプロキセンは、胃内pHの上昇よりも前にピークナプロキセン濃度を示した(図8B)。実際、ピークナプロキセン濃度は投薬の1〜2時間後に生じ、これは胃内pHが最低である期間と一致していた(図8B)。
実施例2
PN400、腸溶コーティングナプロキセン 500mg+腸溶コーティングエソメプラゾール 20mg、腸溶コーティングナプロキセン 500mg単独、および腸溶コーティングエソメプラゾール 20mg単独の経口投与後の、健常者におけるナプロキセンおよびエソメプラゾール血漿レベルを評価するために、無作為化非盲検4−ウェイクロスオーバー試験を行った。この試験は、少なくとも12日間のウォッシュアウト期間を含む4回の単回投与治療期間からなる。被験者は、10時間の一晩絶食後、バランスの取れた治療シーケンスを含む無作為化スケジュールに基づいたクロスオーバー形式で、以下の各4つの治療の単回投与を受けた。
PN400、腸溶コーティングナプロキセン 500mg+腸溶コーティングエソメプラゾール 20mg、腸溶コーティングナプロキセン 500mg単独、および腸溶コーティングエソメプラゾール 20mg単独の経口投与後の、健常者におけるナプロキセンおよびエソメプラゾール血漿レベルを評価するために、無作為化非盲検4−ウェイクロスオーバー試験を行った。この試験は、少なくとも12日間のウォッシュアウト期間を含む4回の単回投与治療期間からなる。被験者は、10時間の一晩絶食後、バランスの取れた治療シーケンスを含む無作為化スケジュールに基づいたクロスオーバー形式で、以下の各4つの治療の単回投与を受けた。
各治療後、投薬後72時間にわたる頻回採血の解析から、ナプロキセンの血漿濃度対時間プロファイルを得た。治療A(PN 400)、治療B(ECナプロキセン+ECエソメプラゾール)、および治療D(ECエソメプラゾール単独)後、投薬後12時間にわたる採血の解析から、エソメプラゾールの血漿濃度時間プロファイルを得た。
非コンパートメント法を使用して、血漿濃度対時間プロファイルからナプロキセンおよびエソメプラゾールの薬物動態(PK)パラメータを決定した。PKパラメータには、最大血漿濃度(Cmax)、最大濃度までの時間(tmax)、吸収における遅延時間(tlag)、時間0から薬物濃度が測定可能な最終時点までの血漿濃度時間曲線下面積(AUC0-t)、外捜法を用いた時間0から無限までのAUC(AUC0-inf)、薬物濃度が測定可能な最終時点から無限までを外捜するAUC0-infの%(%AUCextrap)、および終末相消失半減期(terminal elimination half−life)(t1/2)が含まれた。
治療A対治療B、および治療A対治療DについてのエソメプラゾールのAUC0-t、AUC0-inf、およびCmaxの比率により、PN 400からのエソメプラゾールの相対的バイオアベイラビリティを決定した。治療A対治療B、および治療A対治療CについてのナプロキセンのAUC0-t、AUC0-inf、およびCmaxの比率により、PN 400からのナプロキセンの相対的バイオアベイラビリティを決定した。母数効果としてのシーケンス、期間、および治療、ならびに変量効果としてのシーケンス内の被験者を用いて、loge−変換パラメータの分散分析(ANOVA)から比率を見積もった。各治療比較についての治療とAUCおよびCmaxに対する関連90%信頼区間との幾何最小二乗平均(GLSM)比を計算した。
全員で40人の被験者が登録され、そして37人の被験者が、4つ全ての治療受けて計画通りに研究を終えた。血漿濃度時間プロファイルは、それぞれ、治療A、B、C、およびDを終えた38人、39人、39人、および39人の被験者から入手できた。5人の被験者が、1または3の投薬期間の間、投薬前血漿サンプルにおいて、測定可能なナプロキセン濃度(>0.1μg/mL)を有した。最も大きな測定可能な投薬前濃度は、各プロファイルにおける最大濃度の5%未満であり、そしてこれらはPKパラメータ推定値にほとんど影響を与えないので、PK解析に含まれた。しかし、2人の被験者(被験者1003および1018)は、1または3つ全ての投薬期間において、プロファイルの最大濃度の>5%である測定可能な投薬前ナプロキン濃度を有した。これら2人の被験者において、各プロファイルにおける各時点でのナプロキセン濃度は、測定濃度から残留濃度を減算することにより補正した(時間0(投薬前)濃度からの減衰曲線に基づいて計算した)。その後、PKデータ解析は、これら2人の被験者において補正されたナプロキセン濃度に基づいた。
一般に、血漿ナプロキセン濃度は、治療Aを受けた大多数の被験者において、投薬2時間後の前、または治療BまたはCを受けた大多数の被験者において、投薬後1.5時間前の採取時間では測定可能でなかった。血漿ナプロキセン濃度は、各治療後、全ての被験者において投薬72時間後まで測定可能であった。3つ全ての治療は、非常に類似した血漿ナプロキセンプロファイルの平均/中央値を示し、治療A(PN 400)は、わずかに右方向にシフトした(遅延した)プロファイルを示す(図9を参照のこと)。
1人の被験者を除いて1つの投薬期間において、投薬前血漿サンプルのどれもが定量化可能なエソメプラゾール濃度を有さなかった(全て<1ng/mLであった)。治療A(PN 400)後、概ね、38人の被験者のうち32人において、最初の採取時間(投薬10分後)で血漿エソメプラゾール濃度が血漿中に直ちに現れた。治療Aの投薬20分後、全ての被験者において、血漿エソメプラゾール濃度は測定可能であった。しかし、治療BまたはD後、血漿エソメプラゾール濃度は、概ね、投薬0.75〜1.0時間後まで測定可能でなかった。血漿において測定可能なエソメプラゾール濃度の持続時間は、治療A後の約8時間であり、そして治療BまたはDの投薬後の10〜11時間までであった。
被験者1036(治療Bを受けた)および被験者1037(治療Dを受けた)について、期間4の間に採取された投薬8時間後サンプルは、心ならずも取り違えられたようであった。しかし、このサンプル取り違えの可能性は証明できなかったので、両方の被験者において、この時点を含めたり、除外したりすることによりPKデータ解析を実施した。治療A(PN 400)では、エソメプラゾール血漿プロファイルにおいて即時放出型特性を示し、そして治療BおよびDでは、右方向にシフトした曲線でエソメプラゾール血漿プロファイルにおいて遅延放出特性を示した(図10を参照のこと)。
治療によるナプロキセンおよびエソメプラゾールのPKパラメータの要約を以下の表16および17に示す。
PN 400の経口投薬後、エソメプラゾールはわずかな遅延時間もなく直ちに吸収された。予想通りに、ECエソメプラゾール単独またはECナプロキセンとの組み合わせ投与後、エソメプラゾールの遅延吸収があった。ECエソメプラゾール製剤の投与後のエソメプラゾールのtmaxの中央値は、エソメプラゾールの即時放出型製剤を含むPN 400の投与後よりも約2時間長かった。エソメプラゾールのCmaxおよびAUC値において、被験者間の大きな変動性はあったが、全ての治療についてt1/2の値ではなかった。
全ての治療比較について、ナプロキセンおよびエソメプラゾールのバイオアベイラビリティパラメータの統計解析結果を、以下の表18〜20に示す。
プロファイルのCmaxが投薬前ナプロキセン濃度>5%である2人の被験者(1003および1018)を除くことにより、以下の表19に示され得るように、類似の結果が得られた。
全ての治療比較について、ナプロキセンのAUC0-infおよびCmaxの幾何最小二乗法平均(GLSM)比の90%信頼区間(CI)は、0.80〜1.25限界の範囲内にあり、これはナプロキセンバイオアベイラビリティパラメータに関して、治療間の生物学的同等性を示した。
治療B対治療Dについて、エソメプラゾールのAUC0-infのGLSM比(試験/参照)の90% CIは、0.80〜1.25限界の範囲内にあり、これはECエソメプラゾール(ナプロキセンを併用するか、または併用しない)での2つの治療についてのエソメプラゾールAUC値が生物学的に同等であることを示した。推定値および90% CIに基づいて、治療A(PN 400中即時放出型エソメプラゾール)について、エソメプラゾールのAUC0-infは、単回投薬後の治療BまたはD(すなわち、ECエソメプラゾール)よりも約50%低かった。
有害(aderse)事象(AE)の慨説を以下の表21に表示する。重篤な有害事象(SAE)もなく、またAEによる脱落もなかった。全てのAEの罹患率は、治療Cの3%から治療Bの15%の範囲であった。最も頻度の高いAEは、目眩、頭痛、および吐き気または咽喉の疼痛であった。ほとんどのAEにおいて、重症度は軽度であった。
器官別大分類(SOC)によりAEデータを要約し、そして以下の表22に示す。総合的な発生率は、他の治療(3〜8%)よりも治療B(15%)が特に大きかった。治療期間あたり1人より多い被験者で生じたAEは、目眩(これは、治療Bで2人の被験者(5%)で生じた);頭痛(これは、治療Bで2人の被験者で生じた);および咽喉の疼痛(これは、治療Bで3人(8%)の被験者で生じた)のみであった。
治験責任医師によって治療関連として判断されたAEは、一人の被験者における吐き気、目眩および頭痛ならびに別の被験者における頭痛および発熱のみであり、それぞれ治療B中に生じた。
Claims (20)
- 単位用量形態の医薬組成物の製造におけるナプロキセンまたはその薬学的に受容可能な塩、およびエソメプラゾールまたはその薬学的に受容可能な塩の使用であって、ここで、該エソメプラゾールまたはその薬学的に受容可能な塩は約0又はそれより大きいpHで該単位用量形態から放出され、ここで、
i)ナプロキセンについての薬物動態(pk)プロファイル:
a)AM用量は、約81μg/mLのCmaxの平均値および約2.5〜約4時間の最大濃度までの時間(Tmax)の中央値を有し、そして
b)PM用量は、約76.2μg/mLのCmaxの平均値および約10〜約14時間のTmaxの中央値を有し;そして
ii)エソメプラゾールについての薬物動態(pk)プロファイル:
a)AM用量は、約850hr*μg/mLの、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)を有し、そして
b)PM用量は、約650hr*μg/mLのPM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)を有する:を標的とするため、第一の単位用量形態がAM用量として投与され、そして第二の単位用量形態がPM用量として約10時間後に投与される、上記使用。 - a)ナプロキセンの前記AM用量についてのCmaxの平均値が約86.2μg/mLであり、前記Tmaxの中央値が約3.0時間であり;そして
b)前記PM用量についてのCmaxの平均値が約76.8μg/mLであり、そして前記Tmaxの中央値が約10時間である、請求項1に記載の使用。 - a)ナプロキセンの前記AM用量についてのCmaxの平均値が約80.9μg/mLであり、そして前記Tmaxの中央値が約3.0時間であり;そして
b)前記PM用量についてのCmaxの平均値が約76.2μg/mLであり、そして前記Tmaxの中央値が約10.4時間である、請求項1に記載の使用。 - a)エソメプラゾールの前記AM用量について、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)が約1216hr*μg/mLであり、そして
b)エソメプラゾールの前記PM用量について、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)が約919hr*μg/mLである、請求項1〜3のいずれか1項に記載の使用。 - a)エソメプラゾールの前記AM用量について、AM用量が投与される時間0からAM用量が投与された約10時間後までの平均血漿中濃度時間曲線下面積(AUC0-10,am)が約2779hr*μg/mLであり、そして
b)エソメプラゾールの前記PM用量について、PM用量が投与される時間0からPM用量が投与された約14時間後までの平均血漿中濃度時間曲線下面積(AUC0-14,pm)が約2066hr*μg/mLである、請求項1〜3のいずれか1項に記載の使用。 - 医薬組成物が、エソメプラゾールについて、約1500hr*μg/mLの、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)を有する薬物動態(pk)プロファイルをさらに標的とする、請求項1〜5のいずれか1項に記載の使用。
- エソメプラゾールについて、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)が約2000hr*μg/mLである、請求項6に記載の使用。
- エソメプラゾールについて、第一の用量が投与される時間0から第一の用量が投与された約24時間後までの平均血漿中濃度時間曲線下面積(AUC0-24)が約4911hr*μg/mLである、請求項6に記載の使用。
- 医薬組成物が、少なくとも約41%の、定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間をさらに標的とする、請求項1〜8のいずれか1項に記載の使用。
- 定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間が少なくとも約60%である、請求項9に記載の使用。
- 定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間が少なくとも約71%である、請求項9に記載の使用。
- 定常状態に達した後、約24時間、胃内pHが約4.0以上のままである平均%時間が少なくとも約77%である、請求項9に記載の使用。
- 単位用量形態の医薬組成物が、約500mgのナプロキセンおよび約20mgのエソメプラゾールを含む、請求項1〜11のいずれか1項に記載の使用。
- 単位用量形態が少なくとも約6日間投与される、請求項1〜13のいずれか1項に記載の使用。
- 単位用量形態が少なくとも約9日間投与される、請求項1〜14のいずれか1項に記載の使用。
- 必要がある患者が、疼痛および炎症から選択される疾患または障害の治療を受けている、請求項1〜15のいずれか1項に記載の使用。
- 必要がある患者が、変形性関節症、関節リウマチ、強直性脊椎炎、またはそれらの併発の治療を受けている、請求項1〜15のいずれか1項に記載の使用。
- 単位用量形態が、少なくとも1種のコアならびに少なくとも第一の層および第二の層を含む多層錠であり、ここで:
i)該コアは、ナプロキセン、またはそれらの薬学的に受容可能な塩を含み;
ii)該第一の層は、周囲媒質のpHが約3.5以上である場合に、ナプロキセン、またはそれらの薬学的に受容可能な塩を少なくとも放出し始めるコーティングであり;そして
iii)該第二の層は、エソメプラゾールを含み、ここで、該エソメプラゾールは約0以上のpHで放出される、請求項1〜17のいずれか1項に記載の使用。 - エソメプラゾールが約0〜約2のpHで放出される、請求項18に記載の使用。
- 多層錠が、重炭酸ナトリウムを実質的に含まない、請求項18または19に記載の使用。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US9558408P | 2008-09-09 | 2008-09-09 | |
| US61/095,584 | 2008-09-09 | ||
| PCT/GB2009/051108 WO2010029335A1 (en) | 2008-09-09 | 2009-09-03 | Method for delivering a pharmaceutical composition to patient in need thereof |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2012502015A true JP2012502015A (ja) | 2012-01-26 |
| JP2012502015A5 JP2012502015A5 (ja) | 2012-10-18 |
Family
ID=41217579
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011525623A Pending JP2012502015A (ja) | 2008-09-09 | 2009-09-03 | 必要がある患者に医薬組成物を送達するための方法 |
Country Status (13)
| Country | Link |
|---|---|
| US (3) | US9220698B2 (ja) |
| EP (1) | EP2344139A1 (ja) |
| JP (1) | JP2012502015A (ja) |
| KR (1) | KR20110079641A (ja) |
| CN (1) | CN102209529A (ja) |
| AU (1) | AU2009290712A1 (ja) |
| BR (1) | BRPI0918492A2 (ja) |
| CA (1) | CA2736547C (ja) |
| EA (1) | EA201100313A1 (ja) |
| MA (1) | MA32692B1 (ja) |
| MX (1) | MX2011002515A (ja) |
| WO (1) | WO2010029335A1 (ja) |
| ZA (1) | ZA201102645B (ja) |
Families Citing this family (82)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8206741B2 (en) | 2001-06-01 | 2012-06-26 | Pozen Inc. | Pharmaceutical compositions for the coordinated delivery of NSAIDs |
| US9265732B2 (en) * | 2006-03-06 | 2016-02-23 | Pozen Inc. | Dosage forms for administering combinations of drugs |
| AU2009290712A1 (en) | 2008-09-09 | 2010-03-18 | Astrazeneca Ab | Method for delivering a pharmaceutical composition to patient in need thereof |
| US20100305163A1 (en) * | 2009-05-20 | 2010-12-02 | Pramod Dattatray Yedurkar | Pharmaceutical formulations comprising nsaid and proton pump inhibitor drugs |
| CA2764963C (en) * | 2009-06-25 | 2016-11-01 | Astrazeneca Ab | Method for treating a patient at risk for developing an nsaid-associated ulcer |
| CN102638978A (zh) * | 2009-06-25 | 2012-08-15 | 波曾公司 | 用于治疗需要阿司匹林治疗之患者的方法 |
| BR112014016085A8 (pt) | 2011-12-28 | 2017-07-04 | Pozen Inc | composições aprimoradas e métodos para distribuição de omeprazol mais ácido acetilsalicílico |
| US9590889B2 (en) | 2014-10-08 | 2017-03-07 | Dell Products L.P. | Multicast routing via non-minimal paths |
| US11607456B2 (en) | 2015-02-10 | 2023-03-21 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US10058614B2 (en) | 2015-02-10 | 2018-08-28 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US10933136B2 (en) | 2015-02-10 | 2021-03-02 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US10729774B1 (en) | 2015-02-10 | 2020-08-04 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US10799588B2 (en) | 2015-02-10 | 2020-10-13 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US10512692B2 (en) | 2015-02-10 | 2019-12-24 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US11013806B2 (en) | 2015-02-10 | 2021-05-25 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US10702602B2 (en) | 2015-02-10 | 2020-07-07 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US10653777B2 (en) | 2015-02-10 | 2020-05-19 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US10532101B1 (en) | 2015-02-10 | 2020-01-14 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US10758618B2 (en) | 2015-02-10 | 2020-09-01 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US12485176B2 (en) | 2015-02-10 | 2025-12-02 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US10517950B1 (en) | 2015-02-10 | 2019-12-31 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US10537642B1 (en) | 2015-02-10 | 2020-01-21 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US11738085B2 (en) | 2015-02-10 | 2023-08-29 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US10780166B2 (en) | 2015-02-10 | 2020-09-22 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US10722583B2 (en) | 2015-02-10 | 2020-07-28 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US10933137B2 (en) | 2015-02-10 | 2021-03-02 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US10695429B2 (en) | 2015-02-10 | 2020-06-30 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US10729773B2 (en) | 2015-02-10 | 2020-08-04 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US11602563B2 (en) | 2015-02-10 | 2023-03-14 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US10695430B2 (en) | 2015-02-10 | 2020-06-30 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US11045549B2 (en) | 2015-02-10 | 2021-06-29 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US11110173B2 (en) | 2015-02-10 | 2021-09-07 | Axsome Therapeutics, Inc | Pharmaceutical compositions comprising meloxicam |
| US10780165B2 (en) | 2015-02-10 | 2020-09-22 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US11013805B2 (en) | 2015-02-10 | 2021-05-25 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US10821181B2 (en) | 2015-02-10 | 2020-11-03 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| EP3416976A2 (en) | 2016-02-16 | 2018-12-26 | Yale University | Compositions for enhancing targeted gene editing and methods of use thereof |
| KR101884230B1 (ko) * | 2016-02-29 | 2018-08-01 | 주식회사 유영제약 | 에소메프라졸을 포함하는 제제 |
| US11207327B2 (en) | 2017-01-04 | 2021-12-28 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US10729696B2 (en) | 2017-01-04 | 2020-08-04 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US10940153B2 (en) | 2017-01-04 | 2021-03-09 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US11471465B2 (en) | 2017-01-04 | 2022-10-18 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US10894053B2 (en) | 2017-01-04 | 2021-01-19 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| CA3121746A1 (en) | 2017-01-04 | 2018-07-12 | Herriot TABUTEAU | Pharmaceutical compositions comprising meloxicam |
| US10821182B2 (en) | 2017-06-29 | 2020-11-03 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US10561664B1 (en) | 2017-01-04 | 2020-02-18 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US11806354B2 (en) | 2017-01-04 | 2023-11-07 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US11433078B2 (en) | 2017-01-04 | 2022-09-06 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US11433079B2 (en) | 2017-01-04 | 2022-09-06 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US11266657B2 (en) | 2017-01-04 | 2022-03-08 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US10471014B2 (en) | 2017-01-04 | 2019-11-12 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US10729697B2 (en) | 2017-01-04 | 2020-08-04 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US10905693B2 (en) | 2017-01-04 | 2021-02-02 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US11801250B2 (en) | 2017-01-04 | 2023-10-31 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US10583144B2 (en) | 2017-01-04 | 2020-03-10 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US11617755B2 (en) | 2017-01-04 | 2023-04-04 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US10583088B2 (en) | 2017-01-04 | 2020-03-10 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US20200113821A1 (en) | 2017-04-04 | 2020-04-16 | Yale University | Compositions and methods for in utero delivery |
| US11759522B2 (en) | 2017-06-29 | 2023-09-19 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US10987358B2 (en) | 2017-06-29 | 2021-04-27 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US10512693B2 (en) | 2017-06-29 | 2019-12-24 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US10918722B2 (en) | 2017-06-29 | 2021-02-16 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US10758617B2 (en) | 2017-06-29 | 2020-09-01 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US11617756B2 (en) | 2017-06-29 | 2023-04-04 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US10688185B2 (en) | 2017-06-29 | 2020-06-23 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US11510927B2 (en) | 2017-06-29 | 2022-11-29 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US11865117B2 (en) | 2017-06-29 | 2024-01-09 | Axsome Therapeutics, Inc | Pharmaceutical compositions comprising meloxicam |
| US11219626B2 (en) | 2017-06-29 | 2022-01-11 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US11185550B2 (en) | 2017-06-29 | 2021-11-30 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US11617791B2 (en) | 2017-06-29 | 2023-04-04 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US10688102B2 (en) | 2017-06-29 | 2020-06-23 | Axsome Therapeutics, Inc. | Combination treatment for migraine and other pain |
| KR102080023B1 (ko) | 2018-01-29 | 2020-02-21 | 주식회사 종근당 | 에스오메프라졸 및 탄산수소나트륨을 포함하는 안정한 약제학적 조성물 |
| KR102006777B1 (ko) | 2018-01-29 | 2019-10-08 | 주식회사 종근당 | 에스오메프라졸 및 탄산수소나트륨을 포함하는 약제학적 제제 |
| MX2021001905A (es) | 2018-08-23 | 2021-04-28 | Chong Kun Dang Pharmaceutical Corp | Preparacion farmaceutica que tiene excelentes propiedades de disolucion, que contiene esomeprazol y bicarbonato de sodio. |
| DE102019100527A1 (de) * | 2019-01-10 | 2020-07-16 | Hans-Peter Wilfer | Abdeckelement zur Abdeckung einer in einer planen Geräteoberfläche verbauten LED |
| KR102290295B1 (ko) * | 2019-07-26 | 2021-08-17 | 주식회사 종근당 | 에스오메프라졸 및 탄산수소나트륨을 포함하는 안정한 약제학적 조성물 |
| US20240058354A1 (en) | 2020-04-06 | 2024-02-22 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US12128052B2 (en) | 2020-05-28 | 2024-10-29 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| JP2024502041A (ja) | 2020-12-31 | 2024-01-17 | アクスサム セラピューティクス インコーポレイテッド | メロキシカムを含む医薬組成物 |
| US12370196B2 (en) | 2020-12-31 | 2025-07-29 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| CN113450890B (zh) * | 2021-02-02 | 2022-07-05 | 中南大学湘雅医院 | 药品数据库创建方法、装置、计算机设备和存储介质 |
| US12005118B2 (en) | 2022-05-19 | 2024-06-11 | Axsome Therapeutics, Inc. | Pharmaceutical compositions comprising meloxicam |
| US12544383B1 (en) | 2025-01-30 | 2026-02-10 | Axsome Therapeutics, Inc. | Methods of treating migraines with a combination of a meloxicam and a rizatriptan |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2004536809A (ja) * | 2001-06-01 | 2004-12-09 | ポーゼン インコーポレイテッド | Nsaidを協調的に送達するための薬剤組成物 |
Family Cites Families (170)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SE7804231L (sv) * | 1978-04-14 | 1979-10-15 | Haessle Ab | Magsyrasekretionsmedel |
| CH647676A5 (fr) * | 1978-12-22 | 1985-02-15 | Donald E Panoz | Formes galeniques a usage oral, a liberation programmee et leurs procedes de preparation. |
| US4198390A (en) * | 1979-01-31 | 1980-04-15 | Rider Joseph A | Simethicone antacid tablet |
| FR2470599A1 (fr) * | 1979-12-07 | 1981-06-12 | Panoz Donald | Perfectionnements apportes aux procedes de preparation de formes galeniques a action retard et a liberation programmee et formes galeniques de medicaments ainsi obtenus |
| US4344929A (en) * | 1980-04-25 | 1982-08-17 | Alza Corporation | Method of delivering drug with aid of effervescent activity generated in environment of use |
| CY1398A (en) | 1981-09-04 | 1987-12-18 | Glaxo Group Ltd | Pharmaceutical compositions containing non-steroidal anti-inflammatory agents |
| SE8301182D0 (sv) | 1983-03-04 | 1983-03-04 | Haessle Ab | Novel compounds |
| JPS59227870A (ja) * | 1983-06-07 | 1984-12-21 | Yamanouchi Pharmaceut Co Ltd | 新規2−グアニジノチアゾリン誘導体ならびにその製造法 |
| US4554276A (en) * | 1983-10-03 | 1985-11-19 | Pfizer Inc. | 2-Amino-5-hydroxy-4-methylpyrimidine derivatives |
| SE442264B (sv) | 1983-12-23 | 1985-12-16 | Bengt Gustavsson | Ampull |
| US4522826A (en) | 1984-02-08 | 1985-06-11 | Richardson-Vicks Inc. | Analgesic and anti-inflammatory compositions comprising diphenhydramine and methods of using same |
| US4552899A (en) * | 1984-04-09 | 1985-11-12 | Analgesic Associates | Cough/cold mixtures comprising non-steroidal anti-inflammatory drugs |
| IL75400A (en) | 1984-06-16 | 1988-10-31 | Byk Gulden Lomberg Chem Fab | Dialkoxypyridine methyl(sulfinyl or sulfonyl)benzimidazoles,processes for the preparation thereof and pharmaceutical compositions containing the same |
| IT1196190B (it) | 1984-07-12 | 1988-11-10 | Lisapharma Spa | Forma farmaceutica solida orale ad azione sequenziale per la somministrazione di farmaci ad effetto collaterale ulcerogeno |
| JPS6150978A (ja) | 1984-08-16 | 1986-03-13 | Takeda Chem Ind Ltd | ピリジン誘導体およびその製造法 |
| AU4640985A (en) | 1984-08-31 | 1986-03-06 | Nippon Chemiphar Co. Ltd. | Benzimidazole derivatives |
| US4766117A (en) * | 1984-10-11 | 1988-08-23 | Pfizer Inc. | Antiinflammatory compositions and methods |
| US4676984A (en) * | 1985-08-14 | 1987-06-30 | American Home Products Corp. | Rehydratable antacid composition |
| US4704278A (en) * | 1984-10-17 | 1987-11-03 | American Home Products Corp (Del) | Fluidized magaldrate suspension |
| DE3603576A1 (de) * | 1986-02-06 | 1987-08-13 | Code Kaffee Handel | Verwendung von gerbstoffen und/oder chlorogensaeure sowie nahrungs-, genuss- und/oder arzneimittel mit gerbstoff- und/oder chlorogensaeurezusatz |
| CA1327010C (en) * | 1986-02-13 | 1994-02-15 | Tadashi Makino | Stabilized solid pharmaceutical composition containing antiulcer benzimidazole compound and its production |
| US5043358A (en) * | 1986-03-04 | 1991-08-27 | Bristol-Myers Squibb Company | Gastroprotective process |
| US5037815A (en) * | 1986-03-04 | 1991-08-06 | Bristol-Myers Squibb Co. | Non-steroidal anti-inflammatory compositions protected against gastrointestinal injury with a combination of certain H1 - and H2 -receptor blockers |
| US4965065A (en) * | 1986-04-29 | 1990-10-23 | Bristol-Myers Squibb Company | Gastroprotective process and compositions |
| US4757060A (en) | 1986-03-04 | 1988-07-12 | Bristol-Myers Company | Non-steroidal anti-inflammatory compositions protected against gastrointestinal injury with a combination of certain H1 and H2, receptor blockers |
| GB2189698A (en) * | 1986-04-30 | 1987-11-04 | Haessle Ab | Coated omeprazole tablets |
| GB2189699A (en) | 1986-04-30 | 1987-11-04 | Haessle Ab | Coated acid-labile medicaments |
| US5260333A (en) * | 1986-08-08 | 1993-11-09 | Bristol Myers Squibb Company | Effect of a combination of a terbutaline, diphenhydramine and ranitidine composition on gastrointestinal injury produced by nonsteroidal anti-inflammatory compositions |
| US5026560A (en) * | 1987-01-29 | 1991-06-25 | Takeda Chemical Industries, Ltd. | Spherical granules having core and their production |
| EP0320550A1 (en) | 1987-12-18 | 1989-06-21 | Bristol-Myers Company | Non steroidal anti-inflammatory drug composition containing H1 blockers, H2 blockers, beta adrenergic agonists or combinations thereof and an alkalizing agent |
| GB8805268D0 (en) | 1988-03-04 | 1988-04-07 | Glaxo Group Ltd | Medicaments |
| JPH0768125B2 (ja) * | 1988-05-18 | 1995-07-26 | エーザイ株式会社 | 酸不安定化合物の内服用製剤 |
| SE8804629D0 (sv) | 1988-12-22 | 1988-12-22 | Ab Haessle | New therapeutically active compounds |
| US4948581A (en) * | 1989-02-17 | 1990-08-14 | Dojin Iyaku-Kako Co., Ltd. | Long acting diclofenac sodium preparation |
| US5204118A (en) * | 1989-11-02 | 1993-04-20 | Mcneil-Ppc, Inc. | Pharmaceutical compositions and methods for treating the symptoms of overindulgence |
| NZ235877A (en) | 1989-11-02 | 1992-09-25 | Mcneil Ppc Inc | Composition comprising acetaminophen or nsaid and an h 1 or h 2 receptor blocker and/or proton pump inhibitor for treating overindulgence |
| WO1991016886A1 (en) | 1990-05-03 | 1991-11-14 | G.D. Searle & Co. | Pharmaceutical composition containing ibuprofen and a prostaglandin |
| WO1991016896A1 (en) | 1990-05-03 | 1991-11-14 | G.D. Searle & Co. | Pharmaceutical composition for use in treating pain |
| EP0527887B1 (en) * | 1990-05-03 | 1995-04-26 | G.D. Searle & Co. | Pharmaceutical composition |
| SE9002206D0 (sv) | 1990-06-20 | 1990-06-20 | Haessle Ab | New compounds |
| AU649456B2 (en) | 1990-06-20 | 1994-05-26 | Astra Aktiebolag | Dialkoxy-pyridinyl-benzimidazole derivatives, process for their preparation and their pharmaceutical use |
| DE4035455A1 (de) | 1990-11-08 | 1992-05-14 | Byk Gulden Lomberg Chem Fab | Enantiomerentrennung |
| WO1992015332A1 (en) * | 1991-03-04 | 1992-09-17 | Warner-Lambert Company | Novel salts/ion pairs of non-steroidal anti-inflammatory drugs in various dosage forms |
| US5409709A (en) * | 1991-11-29 | 1995-04-25 | Lion Corporation | Antipyretic analgesic preparation containing ibuprofen |
| ES2130152T3 (es) * | 1991-12-06 | 1999-07-01 | Glaxo Group Ltd | Medicamentos para tratar dolencias inflamatorias o para analgesia que contienen un nsaid y ranitidina/citrato de bismuto. |
| EP0661966B1 (en) | 1991-12-17 | 2000-07-19 | Biovail Technologies Ltd. | Ulcer prevention and treatment composition and method |
| WO1993012817A1 (en) | 1991-12-20 | 1993-07-08 | Warner-Lambert Company | Therapeutic combinations useful in the treatment of gastroesophageal reflux disease |
| US5294433A (en) * | 1992-04-15 | 1994-03-15 | The Procter & Gamble Company | Use of H-2 antagonists for treatment of gingivitis |
| GR1002332B (el) * | 1992-05-21 | 1996-05-16 | Mcneil-Ppc Inc. | Νεες φαρμακευτικες συνθεσεις που περιεχουν σιμεθεικονη. |
| WO1994007541A1 (en) | 1992-09-29 | 1994-04-14 | Merck & Co., Inc. | Ibuprofen-h2 antagonist combinations |
| CA2110313C (en) * | 1992-12-01 | 2004-10-26 | Edward John Roche | Pharmaceutical compositions containing a guanidinothiazole compound and antacids |
| US5686105A (en) * | 1993-10-19 | 1997-11-11 | The Procter & Gamble Company | Pharmaceutical dosage form with multiple enteric polymer coatings for colonic delivery |
| SE9301830D0 (sv) * | 1993-05-28 | 1993-05-28 | Ab Astra | New compounds |
| US6875872B1 (en) | 1993-05-28 | 2005-04-05 | Astrazeneca | Compounds |
| US5877192A (en) | 1993-05-28 | 1999-03-02 | Astra Aktiebolag | Method for the treatment of gastric acid-related diseases and production of medication using (-) enantiomer of omeprazole |
| DK66493D0 (da) * | 1993-06-08 | 1993-06-08 | Ferring A S | Praeparater, isaer til brug ved behandling af inflammatoriske tarmsygdomme eller til at opnaa forbedret saarheling |
| SE9302395D0 (sv) | 1993-07-09 | 1993-07-09 | Ab Astra | New pharmaceutical formulation |
| SE9302396D0 (sv) * | 1993-07-09 | 1993-07-09 | Ab Astra | A novel compound form |
| WO1995011024A1 (en) * | 1993-10-19 | 1995-04-27 | The Procter & Gamble Company | Picosulphate dosage form |
| US5514663A (en) * | 1993-10-19 | 1996-05-07 | The Procter & Gamble Company | Senna dosage form |
| US5643960A (en) * | 1994-04-15 | 1997-07-01 | Duke University | Method of delaying onset of alzheimer's disease symptoms |
| US6025395A (en) * | 1994-04-15 | 2000-02-15 | Duke University | Method of preventing or delaying the onset and progression of Alzheimer's disease and related disorders |
| FR2719999B1 (fr) * | 1994-05-17 | 1996-08-02 | Georges Serge Grimberg | Composition pharmaceutique à base de gomme de guar et d'un antiacide neutralisant, à laquelle peut être ajoutée une série de principes actifs thérapeutiques. |
| TNSN95062A1 (fr) | 1994-05-27 | 1996-02-06 | Astra Ab | Nouveaux derives dialkoxy-pyridinyle-benzimidazole |
| PT1078628E (pt) * | 1994-07-08 | 2009-01-27 | Astrazeneca Ab | Forma de dosagem em comprimidos com unidades múltiplas |
| US5702723A (en) * | 1994-08-02 | 1997-12-30 | Griffin; David | Multi-stage delivery system for ingestible medications or nutrients |
| WO1996005199A1 (de) | 1994-08-12 | 1996-02-22 | Byk Gulden Lomberg Chemische Fabrik Gmbh | Imidazopyridinsalz |
| CN1102144C (zh) | 1994-08-13 | 2003-02-26 | 株式会社柳韩洋行 | 新的嘧啶衍生物及其制备方法 |
| ZA959469B (en) | 1994-11-15 | 1996-05-15 | South African Druggists Ltd | Pharmaceutical composition |
| DE69621773T2 (de) | 1995-01-27 | 2003-01-02 | Board Of Regents, The University Of Texas System | Verfahren zur erhöhung der therapeutischen wirkung von nsaids und dazu verwendbare zwitterionische phospholipidhaltige zusammensetungen |
| SE9500422D0 (sv) * | 1995-02-06 | 1995-02-06 | Astra Ab | New oral pharmaceutical dosage forms |
| SE9500478D0 (sv) * | 1995-02-09 | 1995-02-09 | Astra Ab | New pharmaceutical formulation and process |
| US5955451A (en) | 1995-05-12 | 1999-09-21 | The University Of Texas System Board Of Regents | Methods of enhancing the therapeutic activity of NSAIDS and compositions of zwitterionic phospholipids useful therein |
| US6132768A (en) * | 1995-07-05 | 2000-10-17 | Byk Gulden Lomberg Chemische Fabrik Gmbh | Oral pharmaceutical composition with delayed release of active ingredient for reversible proton pump inhibitors |
| CA2231550A1 (en) | 1995-09-27 | 1997-04-03 | Merck Frosst Canada Inc. | Compositions for treating inflammation containing certain prostaglandins and a selective cyclooxygenase-2 inhibitor |
| US5840737A (en) * | 1996-01-04 | 1998-11-24 | The Curators Of The University Of Missouri | Omeprazole solution and method for using same |
| US6489346B1 (en) * | 1996-01-04 | 2002-12-03 | The Curators Of The University Of Missouri | Substituted benzimidazole dosage forms and method of using same |
| US6699885B2 (en) | 1996-01-04 | 2004-03-02 | The Curators Of The University Of Missouri | Substituted benzimidazole dosage forms and methods of using same |
| US20050054682A1 (en) * | 1996-01-04 | 2005-03-10 | Phillips Jeffrey O. | Pharmaceutical compositions comprising substituted benzimidazoles and methods of using same |
| US6645988B2 (en) | 1996-01-04 | 2003-11-11 | Curators Of The University Of Missouri | Substituted benzimidazole dosage forms and method of using same |
| SE9600071D0 (sv) | 1996-01-08 | 1996-01-08 | Astra Ab | New oral formulation of two active ingredients I |
| SE9600070D0 (sv) | 1996-01-08 | 1996-01-08 | Astra Ab | New oral pharmaceutical dosage forms |
| SE9600072D0 (sv) * | 1996-01-08 | 1996-01-08 | Astra Ab | New oral formulation of two active ingredients II |
| US6231888B1 (en) | 1996-01-18 | 2001-05-15 | Perio Products Ltd. | Local delivery of non steroidal anti inflammatory drugs (NSAIDS) to the colon as a treatment for colonic polyps |
| US8022095B2 (en) | 1996-08-16 | 2011-09-20 | Pozen, Inc. | Methods of treating headaches using 5-HT agonists in combination with long-acting NSAIDs |
| US5872145A (en) | 1996-08-16 | 1999-02-16 | Pozen, Inc. | Formulation of 5-HT agonist and NSAID for treatment of migraine |
| US6077539A (en) | 1996-11-12 | 2000-06-20 | Pozen, Inc. | Treatment of migraine headache |
| CA2271799A1 (en) | 1996-11-22 | 1998-05-28 | The Procter & Gamble Company | Compositions for the treatment of gastrointestinal disorders containing bismuth, and nsaid and one or more antimicrobials |
| HUP9904073A3 (en) | 1996-11-22 | 2000-04-28 | Procter & Gamble | Compositions for the treatment of gastrointestinal disorders containing bismuth and nsaid |
| SE510666C2 (sv) * | 1996-12-20 | 1999-06-14 | Astra Ab | Nya Kristallmodifikationer |
| US6160020A (en) | 1996-12-20 | 2000-12-12 | Mcneill-Ppc, Inc. | Alkali metal and alkaline-earth metal salts of acetaminophen |
| SE510650C2 (sv) | 1997-05-30 | 1999-06-14 | Astra Ab | Ny förening |
| SE510643C2 (sv) | 1997-06-27 | 1999-06-14 | Astra Ab | Termodynamiskt stabil omeprazol natrium form B |
| DE69819351D1 (de) | 1997-09-11 | 2003-12-04 | Nycomed Danmark As Roskilde | Aus mehreren einzeleinheiten zusammengesetzte arzneimittel mit nicht-steroidalen wirkstoffen (nsaids) |
| AU747099B2 (en) | 1997-10-31 | 2002-05-09 | Pharmacia Corporation | Gellan gum tablet coating |
| DK1037607T3 (da) | 1997-12-08 | 2004-06-21 | Altana Pharma Ag | Hidtil ukendt suppositoriumsform, der omfatter en syrelabil aktiv forbindelse |
| SE9704870D0 (sv) | 1997-12-22 | 1997-12-22 | Astra Ab | New pharmaceutical formulation I |
| FR2772615B1 (fr) | 1997-12-23 | 2002-06-14 | Lipha | Comprime multicouche pour la liberation instantanee puis prolongee de substances actives |
| DE19801811B4 (de) | 1998-01-19 | 2004-12-23 | Stada Arzneimittel Ag | Pharmazeutische Zubereitung zur oralen Verabreichung |
| CA2320963A1 (en) * | 1998-01-30 | 1999-08-05 | Sepracor, Inc. | R-lansoprazole compositions and methods |
| AU2481899A (en) * | 1998-01-30 | 1999-08-16 | Sepracor, Inc. | S-lansoprazole compositions and methods |
| US6350470B1 (en) | 1998-04-29 | 2002-02-26 | Cima Labs Inc. | Effervescent drug delivery system for oral administration |
| GB9814215D0 (en) | 1998-07-01 | 1998-09-02 | Norton Healthcare Ltd | Anti-inflammatory pharmaceutical formulations |
| US6093734A (en) * | 1998-08-10 | 2000-07-25 | Partnership Of Michael E. Garst, George Sachs, And Jai Moo Shin | Prodrugs of proton pump inhibitors |
| WO2000015195A1 (en) | 1998-09-10 | 2000-03-23 | Nycomed Danmark A/S | Quick release pharmaceutical compositions of drug substances |
| US6387410B1 (en) | 1998-09-10 | 2002-05-14 | Norton Healthcare Ltd | Anti-inflammatory pharmaceutical formulations |
| US20020090395A1 (en) * | 1998-09-10 | 2002-07-11 | Austen John Woolfe | Anti-inflammatory pharmaceutical formulations |
| US8231899B2 (en) * | 1998-09-10 | 2012-07-31 | Nycomed Danmark Aps | Quick release pharmaceutical compositions of drug substances |
| KR100695562B1 (ko) | 1998-09-28 | 2007-03-15 | 워너-램버트 캄파니 엘엘씨 | Hpmc 캡슐을 이용한 장 및 결장에의 전달방법 |
| US6485747B1 (en) | 1998-10-30 | 2002-11-26 | Monsanto Company | Coated active tablet(s) |
| SE9803772D0 (sv) | 1998-11-05 | 1998-11-05 | Astra Ab | Pharmaceutical formulation |
| US6797283B1 (en) | 1998-12-23 | 2004-09-28 | Alza Corporation | Gastric retention dosage form having multiple layers |
| DE19901687B4 (de) | 1999-01-18 | 2006-06-01 | Grünenthal GmbH | Opioide Analgetika mit kontrollierter Wirkstofffreisetzung |
| US6183779B1 (en) | 1999-03-22 | 2001-02-06 | Pharmascience Inc. | Stabilized pharmaceutical composition of a nonsteroidal anti-inflammatory agent and a prostaglandin |
| CZ20013455A3 (cs) | 1999-03-26 | 2003-02-12 | Pozen Inc. | Vysoce účinné dihydroergotaminové prostředky |
| IL145220A0 (en) | 1999-05-20 | 2002-06-30 | Par Pharmaceutical Inc | Stabilized composition based on pyridinyl-sulfinyl-benzimidazoles and process |
| TWI243672B (en) | 1999-06-01 | 2005-11-21 | Astrazeneca Ab | New use of compounds as antibacterial agents |
| US6632451B2 (en) | 1999-06-04 | 2003-10-14 | Dexcel Pharma Technologies Ltd. | Delayed total release two pulse gastrointestinal drug delivery system |
| SE9902386D0 (sv) | 1999-06-22 | 1999-06-22 | Astra Ab | New formulation |
| CA2277407A1 (en) | 1999-07-14 | 2001-01-14 | Bernard Charles Sherman | Pharmaceutical tablet comprising an nsaid and misoprostol |
| GB9923436D0 (en) | 1999-10-04 | 1999-12-08 | American Home Prod | Pharmaceutical compositions |
| US6787164B2 (en) | 2000-02-23 | 2004-09-07 | Bioselect Innovations, Inc. | Composition and method for treating the effects of diseases and maladies |
| SE0000773D0 (sv) | 2000-03-08 | 2000-03-08 | Astrazeneca Ab | New formulation |
| US20020044962A1 (en) * | 2000-06-06 | 2002-04-18 | Cherukuri S. Rao | Encapsulation products for controlled or extended release |
| SE0002476D0 (sv) | 2000-06-30 | 2000-06-30 | Astrazeneca Ab | New compounds |
| US7029701B2 (en) | 2000-09-11 | 2006-04-18 | Andrx Pharmaceuticals, Llc | Composition for the treatment and prevention of ischemic events |
| US6544556B1 (en) | 2000-09-11 | 2003-04-08 | Andrx Corporation | Pharmaceutical formulations containing a non-steroidal antiinflammatory drug and a proton pump inhibitor |
| US20020045184A1 (en) * | 2000-10-02 | 2002-04-18 | Chih-Ming Chen | Packaging system |
| US6749867B2 (en) | 2000-11-29 | 2004-06-15 | Joseph R. Robinson | Delivery system for omeprazole and its salts |
| AU2002257582A1 (en) | 2001-02-14 | 2002-09-04 | Glaxo Wellcome S.A. | Pharmaceutical formulation |
| SE0101379D0 (sv) * | 2001-04-18 | 2001-04-18 | Diabact Ab | Komposition som hämmar utsöndring av magsyra |
| US20100172983A1 (en) * | 2001-06-01 | 2010-07-08 | Plachetka John R | Pharmaceutical Compositions for the Coordinated Delivery of Naproxen and Esomeprazole |
| US8206741B2 (en) | 2001-06-01 | 2012-06-26 | Pozen Inc. | Pharmaceutical compositions for the coordinated delivery of NSAIDs |
| US20030068356A1 (en) * | 2001-07-10 | 2003-04-10 | Pather S. Indiran | Sequential drug delivery systems |
| AR036354A1 (es) | 2001-08-31 | 2004-09-01 | Takeda Chemical Industries Ltd | Preparacion solida |
| US6930099B2 (en) | 2001-09-07 | 2005-08-16 | Advanced Medical Instruments | Composition for the treatment and prevention of endothelial dysfunction |
| SE0203065D0 (sv) | 2002-10-16 | 2002-10-16 | Diabact Ab | Gastric acid secretion inhibiting composition |
| FR2845917B1 (fr) * | 2002-10-21 | 2006-07-07 | Negma Gild | Composition pharmaceutique associant le tenatoprazole et un anti-inflammatoire |
| US20040131676A1 (en) * | 2002-12-20 | 2004-07-08 | Rajneesh Taneja | Dosage forms containing a PPI, NSAID, and buffer |
| US20070243251A1 (en) * | 2002-12-20 | 2007-10-18 | Rajneesh Taneja | Dosage Forms Containing A PPI, NSAID, and Buffer |
| US20040121004A1 (en) * | 2002-12-20 | 2004-06-24 | Rajneesh Taneja | Dosage forms containing a PPI, NSAID, and buffer |
| EP1575566B1 (en) | 2002-12-26 | 2012-02-22 | Pozen, Inc. | Multilayer dosage forms containing naproxen and triptans |
| WO2004062552A2 (en) | 2003-01-09 | 2004-07-29 | Galephar M/F | Pharmaceutical composition containing a nsaid and a benzimidazole derivative |
| WO2004064815A1 (en) | 2003-01-21 | 2004-08-05 | Smartrix Technologies Inc. | Oral dosage formulation |
| JP2005145894A (ja) | 2003-11-17 | 2005-06-09 | Takeda Chem Ind Ltd | 固形製剤 |
| US20050163847A1 (en) * | 2004-01-21 | 2005-07-28 | Andrx Pharmaceuticals, Llc | Pharmaceutical formulations containing a non-steroidal antiinflammatory drug and an antiulcerative drug |
| WO2005074930A1 (en) | 2004-01-28 | 2005-08-18 | Altana Pharma Ag | Pharmaceutical combinations of (s) -pantoprazole with nsaid or corticosteroids |
| WO2005074536A2 (en) | 2004-01-30 | 2005-08-18 | Eisai Co., Ltd. | Compositions and methods using proton pump inhibitors |
| EP1718303A4 (en) * | 2004-02-10 | 2010-09-01 | Santarus Inc | COMBINATION OF INHIBITOR OF PROTON PUMP, BUFFER AND NON-STEROIDAL ANTI-INFLAMMATORY DRUG |
| US20050227949A1 (en) * | 2004-04-07 | 2005-10-13 | Nasrola Edalatpour | Compositions and methods for treatment of viral and bacterial infections |
| WO2006044202A2 (en) | 2004-10-19 | 2006-04-27 | State Of Oregon Acting By And Through The State Board Of Higher Education On Behalf Of Oregon State University | Enteric coated compositions that release active ingredient(s) in gastric fluid and intestinal fluid |
| US20060165797A1 (en) * | 2005-01-12 | 2006-07-27 | Pozen Inc. | Dosage form for treating gastrointestinal disorders |
| US20060178348A1 (en) * | 2005-01-24 | 2006-08-10 | Pozen Inc. | Compositions and therapeutic methods utilizing a combination of a protein extravasation inhibitor and an NSAID |
| US20060178349A1 (en) * | 2005-01-24 | 2006-08-10 | Pozen Inc. | Compositions and therapeutic methods utilizing a combination of a 5-HT1F inhibitor and an NSAID |
| US20060177504A1 (en) * | 2005-02-08 | 2006-08-10 | Renjit Sundharadas | Combination pain medication |
| EP1726300A1 (en) | 2005-05-24 | 2006-11-29 | Flamel Technologies | Oral pharmaceutical formulation for the prevention and/or the treatment of cardiovascular and inflammatory diseases |
| EP1726301A1 (en) | 2005-05-24 | 2006-11-29 | Flamel Technologies | Oral pharmaceutical composition for treating a COX-2 mediated condition |
| AR057181A1 (es) * | 2005-11-30 | 2007-11-21 | Astra Ab | Nueva forma de dosificacion de combinacion |
| EP1965774A2 (en) * | 2005-12-30 | 2008-09-10 | Cogentus Pharmaceuticals, Inc. | Oral pharmaceutical formulations containing non-steroidal anti-inflammatory drugs and acid inhibitors |
| MX2008011441A (es) | 2006-03-06 | 2008-11-18 | Pozen Inc | Formas de dosificacion para administrar combinaciones de farmacos. |
| AU2007257652A1 (en) | 2006-06-15 | 2007-12-21 | Novartis Ag | Compositions comprising tegaserod alone or in combination with a proton pump inhibitor for treating or preventing gastric injury |
| WO2008057802A2 (en) * | 2006-10-27 | 2008-05-15 | The Curators Of The University Of Missouri | Compositions comprising at least one acid labile proton pump inhibiting agents, optionally other pharmaceutically active agents and methods of using same |
| WO2008101064A1 (en) * | 2007-02-14 | 2008-08-21 | Logical Therapeutics, Inc. | Method of treating arthritis, pain or inflammation with naproxen 2(methanesulfonyl)ethyl ester and an h2 receptor antagonist |
| US20080031950A1 (en) * | 2007-04-27 | 2008-02-07 | Nectid Inc. | Novel anelgesic combination |
| WO2009012393A1 (en) | 2007-07-18 | 2009-01-22 | The Curators Of The University Of Missouri | Pharmaceutical composition comprising a proton pump inhibitor and protein component |
| US20090280173A1 (en) | 2008-05-09 | 2009-11-12 | Ishwar Chauhan | Multilayer Omeprazole Tablets |
| CA2740974A1 (en) | 2008-05-30 | 2009-12-03 | Pozen Inc. | Dosage forms for the rapid and sustained elevation of gastric ph |
| AU2009290712A1 (en) | 2008-09-09 | 2010-03-18 | Astrazeneca Ab | Method for delivering a pharmaceutical composition to patient in need thereof |
| CA2764963C (en) * | 2009-06-25 | 2016-11-01 | Astrazeneca Ab | Method for treating a patient at risk for developing an nsaid-associated ulcer |
| CN102638978A (zh) | 2009-06-25 | 2012-08-15 | 波曾公司 | 用于治疗需要阿司匹林治疗之患者的方法 |
-
2009
- 2009-09-03 AU AU2009290712A patent/AU2009290712A1/en not_active Abandoned
- 2009-09-03 KR KR1020117008107A patent/KR20110079641A/ko not_active Withdrawn
- 2009-09-03 EP EP09785567A patent/EP2344139A1/en not_active Withdrawn
- 2009-09-03 CN CN2009801444257A patent/CN102209529A/zh active Pending
- 2009-09-03 JP JP2011525623A patent/JP2012502015A/ja active Pending
- 2009-09-03 EA EA201100313A patent/EA201100313A1/ru unknown
- 2009-09-03 CA CA2736547A patent/CA2736547C/en active Active
- 2009-09-03 BR BRPI0918492A patent/BRPI0918492A2/pt not_active Application Discontinuation
- 2009-09-03 MX MX2011002515A patent/MX2011002515A/es not_active Application Discontinuation
- 2009-09-03 US US12/553,107 patent/US9220698B2/en active Active
- 2009-09-03 WO PCT/GB2009/051108 patent/WO2010029335A1/en not_active Ceased
-
2011
- 2011-04-05 MA MA33745A patent/MA32692B1/fr unknown
- 2011-04-08 ZA ZA2011/02645A patent/ZA201102645B/en unknown
-
2015
- 2015-12-28 US US14/980,639 patent/US9393208B2/en active Active
-
2016
- 2016-07-12 US US15/207,623 patent/US9801824B2/en not_active Expired - Fee Related
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2004536809A (ja) * | 2001-06-01 | 2004-12-09 | ポーゼン インコーポレイテッド | Nsaidを協調的に送達するための薬剤組成物 |
Non-Patent Citations (2)
| Title |
|---|
| JPN6013057018; A 6-Month, Phase 3, Randomized, Double-Blind, Parallel-Group, Controlled, Multi-Center Study to Eval * |
| JPN6013057019; A 12-Month, Phase 3, Open-Label, Multi-Center Study to Evaluate the Long-Term Safety of PN 400 * |
Also Published As
| Publication number | Publication date |
|---|---|
| CN102209529A (zh) | 2011-10-05 |
| US20100062064A1 (en) | 2010-03-11 |
| MX2011002515A (es) | 2011-04-07 |
| CA2736547C (en) | 2016-11-01 |
| WO2010029335A1 (en) | 2010-03-18 |
| US20160106678A1 (en) | 2016-04-21 |
| EP2344139A1 (en) | 2011-07-20 |
| US9393208B2 (en) | 2016-07-19 |
| BRPI0918492A2 (pt) | 2015-12-01 |
| MA32692B1 (fr) | 2011-10-02 |
| ZA201102645B (en) | 2014-03-26 |
| US9220698B2 (en) | 2015-12-29 |
| CA2736547A1 (en) | 2010-03-18 |
| US9801824B2 (en) | 2017-10-31 |
| AU2009290712A1 (en) | 2010-03-18 |
| KR20110079641A (ko) | 2011-07-07 |
| EA201100313A1 (ru) | 2011-10-31 |
| US20170071861A1 (en) | 2017-03-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2012502015A (ja) | 必要がある患者に医薬組成物を送達するための方法 | |
| US10603283B2 (en) | Compositions and methods for delivery of omeprazole plus acetylsalicylic acid | |
| AU2017312660B2 (en) | Methods of treating eosinophilic esophagitis | |
| Danvish et al. | Comparison of equivalent doses of fentanyl buccal tablets and arteriovenous differences in fentanyl pharmacokinetics | |
| JP2012531409A (ja) | Nsaid関連潰瘍を発症するリスクがある患者の処置方法 | |
| BRPI0708059A2 (pt) | formulação de niacina de baixo rubor | |
| PT2043637E (pt) | Métodos e medicamentos para administração de ibuprofeno | |
| Gresele et al. | Effect on walking distance and atherosclerosis progression of a nitric oxide-donating agent in intermittent claudication | |
| PT1807156T (pt) | Novas formulações farmacêuticas úteis no tratamento de insónia | |
| JP2018516267A (ja) | 代謝性疾患を治療するためのサクビトリルおよびバルサルタン | |
| KR20160091348A (ko) | 부종없이 통증을 완화시키기 위한 고정된 용량의 복합제 | |
| HK1162345A (en) | Method for delivering a pharmaceutical composition to patient in need thereof | |
| CN115989031A (zh) | 用于抑制透析转化或肾死亡的药剂 | |
| DK2651392T3 (en) | Solid compositions containing flurbiprofen, processes for their preparation, and their use | |
| Souza et al. | Evaluation of the relative bioavailability between two formulations of olmesartan medoxomil 40mg, in orodispersible tablet form and coated tablet form, in healthy participants of both sexes | |
| US20130078287A1 (en) | Pharmaceutical compositions of ibuprofen and an h2 receptor antagonist | |
| US20190125727A1 (en) | Fixed dose combination for pain relief without edema | |
| Van Nieuwenhoven et al. | Efficacy of 20 mg oral rabeprazole vs. 40 mg omeprazole intravenously on 24 h gastric pH in healthy volunteers: a randomized, double-blind, placebo-controlled, cross-over study | |
| Bothe et al. | Randomized clinical trial: Randomized, controlled, single-blind, three-way crossover study to evaluate the efficacy and safety of a new preparation for post-prandial heartburn |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120829 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20120829 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20140422 |