JP2010095523A - カルバゾール誘導体の製造方法 - Google Patents
カルバゾール誘導体の製造方法 Download PDFInfo
- Publication number
- JP2010095523A JP2010095523A JP2009216398A JP2009216398A JP2010095523A JP 2010095523 A JP2010095523 A JP 2010095523A JP 2009216398 A JP2009216398 A JP 2009216398A JP 2009216398 A JP2009216398 A JP 2009216398A JP 2010095523 A JP2010095523 A JP 2010095523A
- Authority
- JP
- Japan
- Prior art keywords
- light
- layer
- phenyl
- carbazole
- compound
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- WYCSINSMWHKJER-UHFFFAOYSA-N C1c(cc(cc2)-c(cc3)ccc3-c(cc3)cc(c4ccccc44)c3[n]4-c(cc3)ccc3-c3c(cccc4)c4c(-c4ccccc4)c4c3cccc4)c2-c2c1cccc2 Chemical compound C1c(cc(cc2)-c(cc3)ccc3-c(cc3)cc(c4ccccc44)c3[n]4-c(cc3)ccc3-c3c(cccc4)c4c(-c4ccccc4)c4c3cccc4)c2-c2c1cccc2 WYCSINSMWHKJER-UHFFFAOYSA-N 0.000 description 1
- IEIXPUMKRIPJOP-UHFFFAOYSA-N CC(C)(C)c(cc1)ccc1-c(cc1)cc(c2ccccc22)c1[n]2-c(cc1)ccc1-c1c(cccc2)c2c(-c2ccccc2)c2c1cccc2 Chemical compound CC(C)(C)c(cc1)ccc1-c(cc1)cc(c2ccccc22)c1[n]2-c(cc1)ccc1-c1c(cccc2)c2c(-c2ccccc2)c2c1cccc2 IEIXPUMKRIPJOP-UHFFFAOYSA-N 0.000 description 1
- HTXXJLHTIFIOHO-UHFFFAOYSA-N CC1(C)c2cc(-c(cc3)ccc3-c(cc3)cc(c4ccccc44)c3[n]4-c(cc3)ccc3-c3c(cccc4)c4c(-c4ccccc4)c4c3cccc4)ccc2-c2ccccc12 Chemical compound CC1(C)c2cc(-c(cc3)ccc3-c(cc3)cc(c4ccccc44)c3[n]4-c(cc3)ccc3-c3c(cccc4)c4c(-c4ccccc4)c4c3cccc4)ccc2-c2ccccc12 HTXXJLHTIFIOHO-UHFFFAOYSA-N 0.000 description 1
- LRBBLSCXBIMSFI-UHFFFAOYSA-N Cc(cc1)ccc1-c(cc1)cc(c2ccccc22)c1[n]2-c(cc1)ccc1-c1c(cccc2)c2c(-c2ccccc2)c2c1cccc2 Chemical compound Cc(cc1)ccc1-c(cc1)cc(c2ccccc22)c1[n]2-c(cc1)ccc1-c1c(cccc2)c2c(-c2ccccc2)c2c1cccc2 LRBBLSCXBIMSFI-UHFFFAOYSA-N 0.000 description 1
- FTLCFHPVOYEKHT-UHFFFAOYSA-N Cc(cc1C)cc(C)c1-c(cc1)cc(c2ccccc22)c1[n]2-c(cc1)ccc1-c1c(cccc2)c2c(-c2ccccc2)c2c1cccc2 Chemical compound Cc(cc1C)cc(C)c1-c(cc1)cc(c2ccccc22)c1[n]2-c(cc1)ccc1-c1c(cccc2)c2c(-c2ccccc2)c2c1cccc2 FTLCFHPVOYEKHT-UHFFFAOYSA-N 0.000 description 1
- XIVDYNYVHRSJDV-UHFFFAOYSA-N Cc(cc1C)cc(C)c1-c(cc1)ccc1-c(cc1)cc(c2ccccc22)c1[n]2-c(cc1)ccc1-c1c(cccc2)c2c(-c2ccccc2)c2c1cccc2 Chemical compound Cc(cc1C)cc(C)c1-c(cc1)ccc1-c(cc1)cc(c2ccccc22)c1[n]2-c(cc1)ccc1-c1c(cccc2)c2c(-c2ccccc2)c2c1cccc2 XIVDYNYVHRSJDV-UHFFFAOYSA-N 0.000 description 1
- GMPHGUFBZKWOJH-UHFFFAOYSA-N FC(c(cc1)ccc1-c(cc1)ccc1-c(cc1)cc(c2ccccc22)c1[n]2-c(cc1)ccc1-c1c(cccc2)c2c(-c2ccccc2)c2c1cccc2)(F)F Chemical compound FC(c(cc1)ccc1-c(cc1)ccc1-c(cc1)cc(c2ccccc22)c1[n]2-c(cc1)ccc1-c1c(cccc2)c2c(-c2ccccc2)c2c1cccc2)(F)F GMPHGUFBZKWOJH-UHFFFAOYSA-N 0.000 description 1
- DVPAOLHDEOLAHP-UHFFFAOYSA-N FC(c(cc1)ccc1-c(cc1c2c3cccc2)ccc1[n]3-c(cc1)ccc1-c1c(cccc2)c2c(-c2ccccc2)c2c1cccc2)(F)F Chemical compound FC(c(cc1)ccc1-c(cc1c2c3cccc2)ccc1[n]3-c(cc1)ccc1-c1c(cccc2)c2c(-c2ccccc2)c2c1cccc2)(F)F DVPAOLHDEOLAHP-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6572—Polycyclic condensed heteroaromatic hydrocarbons comprising only nitrogen in the heteroaromatic polycondensed ring system, e.g. phenanthroline or carbazole
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/56—Ring systems containing three or more rings
- C07D209/80—[b, c]- or [b, d]-condensed
- C07D209/82—Carbazoles; Hydrogenated carbazoles
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/56—Ring systems containing three or more rings
- C07D209/80—[b, c]- or [b, d]-condensed
- C07D209/82—Carbazoles; Hydrogenated carbazoles
- C07D209/86—Carbazoles; Hydrogenated carbazoles with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to carbon atoms of the ring system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/56—Ring systems containing three or more rings
- C07D209/80—[b, c]- or [b, d]-condensed
- C07D209/82—Carbazoles; Hydrogenated carbazoles
- C07D209/88—Carbazoles; Hydrogenated carbazoles with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to carbon atoms of the ring system
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/626—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing more than one polycyclic condensed aromatic rings, e.g. bis-anthracene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K99/00—Subject matter not provided for in other groups of this subclass
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Physics & Mathematics (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Optics & Photonics (AREA)
- Indole Compounds (AREA)
Abstract
【解決手段】カルバゾール骨格の3位に活性部位を有する9−[4−(10−フェニル−9−アントリル)フェニル]−9H−カルバゾールと、活性部位を有する芳香族化合物とを、カップリングすることを特徴とする特定なカルバゾール誘導体の製造方法。
【選択図】なし
Description
また、それらの誘導体が電気化学的安定性に富むことも既に知られており、勿論それら誘導体の製造方法も既知である(特許文献1及び2参照)。
その第1の既知方法を具体的に示すと下記のとおりであり、反応式(K−1)、反応式(K−2)及び反応式(K−3)の三段階からなる。
その反応式(K−1)においてX2はハロゲンを表し、ハロゲンとしてはヨウ素、臭素が好ましいが、その反応式(K−1)において臭素化する場合、用いることができる臭素化剤は、臭素、N−ブロモコハク酸イミドなどである。
その際に用いることができる溶媒はクロロホルム、四塩化炭素などのハロゲン系溶媒であるが、臭素化剤にN−ブロモコハク酸イミドを用いる場合には、溶媒は酢酸エチル、テトラヒドロフラン、ジメチルホルムアミド、酢酸、水等などである。
反応式(K−2)において、X2はハロゲンを表し、ハロゲンとしては、ヨウ素、臭素が好ましい。また、反応式(K−2)において、X2がトリフラート基である化合物を用いてもよい。なお、R101及びR102が水素の時、化合物K3で表される有機ホウ素化合物をアリールボロン酸とよぶ。
反応式(K−2)において、用いることができるパラジウム触媒の配位子としては、トリ(オルトートリル)ホスフィンや、トリフェニルホスフィンや、トリシクロヘキシルホスフィン等である。
反応式(K−3)において、ハートウィック・ブッフバルト反応を行う場合、用いることができるパラジウム触媒としては、ビス(ジベンジリデンアセトン)パラジウム(0)、酢酸パラジウム(II)等である。
その際に用いることができる塩基としては、炭酸カリウム等の無機塩基が挙げられる。
なお、反応式(K−4)の出発原料である、化合物K4は、反応式(K−1)及び反応式(K−2)の二段階の反応を経ることにより得られるものであるから、第2の既知方法は厳密には更に二段階の反応プロセスが増加することになる。
反応式(K−4)において、X4及びX5はハロゲンまたは、トリフラート基を表し、X4及びX5がハロゲンである場合、ヨウ素、臭素、塩素が好ましい。また、X4及びX5は同じであっても異なっていてもよい。反応式(K−4)において、Ar1は炭素数6−13の置換基を有していてもよいアリール基を表す。
また、用いることができる塩基としては、ナトリウム tert−ブトキシド等の有機塩基や、炭酸カリウム等の無機塩基等であり、用いることができる溶媒としては、トルエン、キシレン、ベンゼン、テトラヒドロフラン等である。
また、R111がヨウ素であるヨウ化銅(I)、又はR112がアセチル基である酢酸銅(II)が好ましい。また、銅化合物の他に銅を用いることもできる。
その反応式(K−5)において、X5はハロゲン又はトリフラート基を表し、ハロゲンとしてはヨウ素、臭素、塩素が好ましく、Ar1は炭素数6−13の置換基を有していてもよいアリール基を表す。
また、化合物K8のボロン酸をエチレングリコールやピナコールにより保護してから次の反応に用いてよい。
また、アルキルリチウム試薬は、R50がn−ブチル基であるn−ブチルリチウムや、R50がt−ブチル基であるt−ブチルリチウムや、R50がメチル基であるメチルリチウム等である。さらに、ホウ素試薬としては、R51がメチル基であるホウ酸トリメチルや、R51がイソプロピル基であるホウ酸トリイソプロピルなどである。
その反応式(K−6)において、X6はハロゲンまたはトリフラート基を表し、X6がハロゲンである場合、ヨウ素、臭素、塩素が好ましい。
その際のパラジウム触媒の配位子としては、トリ(オルト−トリル)ホスフィンや、トリフェニルホスフィンや、トリシクロヘキシルホスフィン等である。
その反応式において、用いることができる塩基としては、ナトリウム tert−ブトキシド等の有機塩基や、炭酸カリウム等の無機塩基等が挙げられる。
なお、化合物K8に代えて化合物K8のボロン酸をエチレングリコールやピナコールにより保護した有機ホウ素化合物を用いてもよい。
また、その一般式(1)の化合物は、アントラセン骨格とカルバゾール骨格との結合したものであり、そのカルバゾール骨格の3位の位置にアリール基が結合した構造となっている。
また、本願発明の一態様の製造方法及び既知の製造方法のいずれにおいても製造対象物質である一般式(1)の誘導体におけるアリール基(Ar1)には各種アリール基が採用でき、それら製造方法においては各種バリエーションのカルバゾール誘導体を製造することができるが、既知の製造方法においてはアントラセン骨格とカルバゾール骨格との結合が行われる前にカルバゾールの3位の位置に結合するアリール基の導入が行われており、そのため各種バリエーションのカルバゾール誘導体を製造するには優れた方法とは言い難いところがある。
その結果、第1の既知方法では、アリール基導入反応と、その後に続く両骨格の結合反応とが導入されたアリール基の種類によって影響を受け、目的物質の収率、純度等が導入されたアリール基によって差異が生ずるという問題がある。
そのため、それぞれの段階で置換されたアリール基によって反応の進行が影響を受けることになるので、出発物質に導入されているアリール基の種類によって、目的物質の収率、純度等に大きな差異が生ずることになる。
すなわち、本願発明は、簡潔かつ単純なプロセスで、しかも導入されたアリール基の種類によって生ずる目的物質の収率及び純度等の差異を極力低減した各種バリエーションのカルバゾール誘導体の製造方法を提供することを発明の解決すべき課題とするものである。
すなわち、カルバゾール骨格の3位に活性部位を有する9−[4−(10−フェニル−9−アントリル)フェニル]−9H−カルバゾールと、化合物(A1)で表される活性部位を有する芳香族化合物とを、金属触媒を用いてカップリングすることを特徴とする、一般式(1a)で表されるカルバゾール誘導体の製造方法である。
すなわち、カルバゾール骨格の3位に活性部位を有する9−[4−(10−フェニル−9−アントリル)フェニル]−9H−カルバゾールと、化合物(A2)で表される有機ホウ素化合物とを、パラジウム触媒を用いてカップリングすることを特徴とする、一般式(1b)で表されるカルバゾール誘導体の製造方法である。なお、化合物(A2)の一般式において、R101及びR102が水素の時、化合物(A2)で表される有機ホウ素化合物をアリールボロン酸とよぶ。
したがって、本願発明は、簡潔かつ単純なプロセスで各種のカルバゾール誘導体を製造する優れた方法を提供するものである。
また、本願発明は、各種バリエーションのカルバゾール誘導体を製造する際に、既知方法のように、カルバゾール骨格の3位に、様々なバリエーションのアリール基(Ar1)の官能基を導入した後に2以上の複数の反応工程を経ることがないので、カルバゾール基に導入されるアリール基の種類によって発生する目的物質の収率あるいは純度等の低減を極力抑制することができる。
但し、本発明は以下の説明に限定されない。従って、本発明の趣旨及びその範囲から逸脱することなくその形態及び詳細を様々に変更し得ることは当業者であれば容易に理解される。なお、以下においては、本発明の製造方法により作製した目的物質を用いた利用態様等に関しても詳述する。
その製造方法の前段となる、3位に活性部位を有する9−[4−(10−フェニル−9−アントリル)フェニル]−9H−カルバゾールの形成工程と、それに続くカップリング工程とを反応式で示すと下記の反応式1及び反応式2のとおりである。
そのAr1のアリール基としては、フェニル基、ナフチル基、フルオレニル基等が例示でき、それが更に置換基を有する場合の置換基としては炭素数1〜4のアルキル基、炭素数1のハロアルキル基、フェニル基、ナフチル基、フルオレニル基等が例示できる。なお、Ar1が置換基を有する場合には、置換基同士が互いに結合して環を形成してもよく、その場合の環構造としてはスピロ環も含むものとする。なお、その場合のスピロ環を形成する炭素は環を形成するということになる。
また、フルオレニル基で、かつ置換基を有する場合の具体例が置換基(S−17)ないし(S−19)である。なお、置換基同士が互いに結合してスピロ環を形成する場合の具体例が置換基(S−18)である。
すなわち、カルバゾール骨格の3位に活性部位を有する9−[4−(10−フェニル−9−アントリル)フェニル]−9H−カルバゾールと、前記した化合物(A1)で表される活性部位を有するアリール基とを、金属触媒を用いてカップリングすることを特徴とする、前記した一般式(1a)で表されるカルバゾール誘導体の製造方法である。
反応に用いる金属触媒としては、パラジウム触媒、ニッケル触媒などの金属触媒を挙げることができる。また、金属触媒は、銅、鉄などの金属、ヨウ化銅(I)等の金属化合物であってもよい。
すなわち、カルバゾール骨格の3位に活性部位を有する9−[4−(10−フェニル−9−アントリル)フェニル]−9H−カルバゾールと、前記した化合物(A2)で表される有機ホウ素化合物とを、パラジウム触媒を用いてカップリングすることを特徴とする、前記した一般式(1b)で表されるカルバゾール誘導体の製造方法である。なお、化合物(A2)の一般式において、R101及びR102が水素の時、化合物(A2)で表される有機ホウ素化合物をアリールボロン酸とよぶ。
それら化合物の一部について、化合物名で具体的に示すと下記のとおりである。
3−フェニル−9−[4−(10−フェニル−9−アントリル)フェニル]−9H−カルバゾール(略称:CzPAP、構造式1の化合物)、3−[4−(1−ナフチル)フェニル]−9−[4−(10−フェニル−9−アントリル)フェニル]−9H−カルバゾール(略称:CzPAαNP、構造式2の化合物)。
本願発明製造方法の形態に関し以下において詳述する。
本願発明の一態様の製造方法は、前記したとおりカルバゾール骨格の3位に活性部位を有する9−[4−(10−フェニル−9−アントリル)フェニル]−9H−カルバゾールと、活性部位を有する芳香族化合物とを、カップリングすることを特徴とするものである。
前記反応式2のカップリング反応において、鈴木・宮浦カップリングを行う場合には、化合物2のX7がハロゲンもしくはトリフレートであり、化合物3のX8がボロン酸もしくは有機ホウ素化合物であることが好ましい。または、化合物2のX7がボロン酸もしくは有機ホウ素化合物であり、X8がハロゲンもしくはトリフレートであることが好ましい。また、パラジウム触媒を用いることが好ましい。
本実施の形態においては、化合物2のX7がハロゲン又はトリフレートであり、化合物3のX8がボロン酸又は有機ホウ素化合物である場合を例に説明する。
なお、本実施の形態の製造方法に係るカップリング反応としては、右田・小杉・スティルカップリング、熊田・玉尾カップリング又は根岸カップリング等を用いることができる。
すなわち、第1段階では、反応式M1により、9−[4−(10−フェニル−9−アントリル)フェニル]−9H−カルバゾール(化合物1、略称:CzPA)を直接ハロゲン化することにより、CzPAのカルバゾール骨格の3位がハロゲン化された化合物M1を得るものである。
臭素を用いて臭素化する場合に用いることができる溶媒は、クロロホルム、四塩化炭素などのハロゲン系溶媒が挙げられるが、これらに限られるものではない。N−ブロモコハク酸イミドを用いて臭素化する場合に用いることができる溶媒は、酢酸エチル、テトラヒドロフラン、ジメチルホルムアミド、酢酸、水等が挙げられる。
なお、反応式M1で示すハロゲン化以外の方法を用いてもよく、CzPAのカルバゾール骨格の3位にトリフラート基を置換した化合物を合成してもよい。
その反応はCzPAのカルバゾール骨格の3位がハロゲン化された化合物M1と、化合物M2である有機ホウ素化合物とを、パラジウム触媒を用いた鈴木・宮浦反応によりカップリングして、目的物である一般式(1)で表されるCzPA誘導体を得る。なお、R101及びR102が水素の時、化合物M2で表される有機ホウ素化合物をアリールボロン酸とよぶ。
また、その反応式において、Ar1は炭素数6−13の置換基を有していてもよいアリール基を表し、置換基同士が互いに結合して環を形成していてもよく、環構造としてはスピロ環も含む物とする。
さらに、その反応式の化合物(M2)の一般式において、R101とR102は、水素又は炭素数1−6のアルキル基を表し、R101とR102は互いに結合して環構造を形成していてもよい。
さらに、その反応式において、用いることができる塩基としては、ナトリウム tert−ブトキシド等の有機塩基や、炭酸カリウム等の無機塩基等が挙げられる。
本願発明製造方法により製造したカルバゾール誘導体を用いて作製した発光素子の一形態について図1(A)を用いて以下に説明する。
この発光素子は、一対の電極間に少なくとも発光物質を含む層(発光層ともいう)を有するEL層を挟持して形成される。
そのEL層は発光物質を含む層の他に複数の層を有してもよい。当該複数の層は、電極から離れたところに発光領域が形成されるように、つまり電極から離れた部位でキャリアの再結合が行われるように、キャリア注入性の高い物質やキャリア輸送性の高い物質からなる層を組み合わせて積層されたものである。
前記のように第1の層103として有機化合物と無機化合物とを複合してなる複合材料を用いた場合、第1の電極102とオーム接触をすることが可能となるため、仕事関数に関わらず第1の電極を形成する材料を選ぶことができる。
さらに、ポリ(N−ビニルカルバゾール)(略称:PVK)やポリ(4−ビニルトリフェニルアミン)(略称:PVTPA)等の高分子化合物を用いることもできる。
さらに、PMMAのような電気的に不活性な高分子化合物に、正孔輸送性材料を添加してもよい。
また、実施の形態1の製造方法で得られたカルバゾール誘導体(以下、「本発明の一態様に係るカルバゾール誘導体」と略称することもある)は、第3の層105においてホストとして用いることもでき、そのカルバゾール誘導体に発光物質となるドーパントを分散させた構成とすることで、発光物質となるドーパントからの発光を得ることができる。
さらに、(アセチルアセトナト)ビス[2,3−ビス(4−フルオロフェニル)キノキサリナト]イリジウム(III)(略称:Ir(Fdpq)2(acac))、2,3,7,8,12,13,17,18−オクタエチル−21H,23H−ポルフィリン白金(II)(略称:PtOEP)などの燐光を発光する燐光発光物質を用いることができる。
本発明の一態様に係るカルバゾール誘導体を溶媒に溶解した溶液状の組成物を用いて湿式法によって薄膜を形成する場合、前記カルバゾール誘導体及び溶媒を含む溶液状の組成物を被形成領域に付着させ、溶媒を除去し固化させることによって薄膜として形成する。
それらに加えて、成膜した膜の性質を向上させるために、さらにバインダーを含んでいてもよい。バインダーとしては、電気的に不活性な高分子化合物を用いることが好ましい。具体的には、ポリメチルメタクリレート(略称:PMMA)や、ポリイミドなどを用いることができる。
その発光は、第1の電極102または第2の電極107のいずれか一方または両方を通って外部に取り出される。従って、第1の電極102または第2の電極107のいずれか一方または両方は、透光性を有する物質で成る。
つまり、層の積層構造については特に限定されず、電子輸送性の高い物質または正孔輸送性の高い物質、電子注入性の高い物質、正孔注入性の高い物質、バイポーラ性の物質(電子及び正孔の輸送性の高い物質)、正孔ブロック材料等から成る層を、本発明の一態様に係るカルバゾール誘導体により形成される発光層と自由に組み合わせて構成すればよい。
本実施の形態の発光素子は一対の電極間にEL層が挟持される構造となっている。EL層は少なくとも本発明の一態様に係るカルバゾール誘導体を用いて形成された発光物質を有する層(発光層ともいう)を含む。そのEL層には、発光物質を含む層の他に機能層(正孔注入層、正孔輸送層、電子輸送層、電子注入層など)を含んでもよい。電極(第1の電極及び第2の電極)、発光物質を含む層、及び機能層は液滴吐出法(インクジェット法)、スピンコート法、印刷法などの湿式法を用いて形成してもよく、真空蒸着法、CVD法、スパッタリング法などの乾式法を用いて形成してもよい。
また、そのカルバゾール誘導体は、バンドギャップが広く、電子及び正孔の輸送性の高いバイポーラ材料である。したがって、本発明の一態様に係るカルバゾール誘導体を発光素子に用いることにより、キャリアバランスのよい高信頼性の発光素子を得ることができる。
さらに、その誘導体を用いることにより、高信頼性の発光装置および電子機器を得ることができる。
本実施の形態では、実施の形態2で示した構成と異なる構成の発光素子について図3(A)(B)を用いて説明する。
この実施の形態では、図3(A)に示すように電子輸送層である第4の層106と発光層である第3の層105(発光層105とも記す)との間に電子キャリアの移動を制御する層130を設ける構成を有する。このように電子輸送層と発光層との間に電子キャリアの移動を制御する層を設けても良い。
例えば、第1の発光層105aと第2の発光層105bを正孔輸送層である第2の層104側から順に積層して発光層105とする場合、第1の発光層105aのホスト材料として正孔輸送性を有する物質を用い、第2の発光層105bとして電子輸送性を有する物質を用いる構成などがある。
そのカルバゾール誘導体をホストとして用いる場合、本発明の一態様に係るカルバゾール誘導体に発光物質となるドーパントを分散させた構成とすることで、発光物質となるドーパントからの発光を得ることができる。
他方、本発明の一態様に係るカルバゾール誘導体をドーパントとして用いる場合、その誘導体よりも大きなバンドギャップを有する材料(ホスト)よりなる層中に添加した構成とすることで、本発明の一態様に係るカルバゾール誘導体からの発光を得ることができる。
前記誘導体は、第1の発光層105a、第2の発光層105bには、単独で発光層として用いてもよいし、ホスト材料、ドーパント材料として用いてもよい。単独で発光層、又はホスト材料として用いる場合はそのキャリア輸送性によって、正孔輸送性の第1の発光層105aか、電子輸送性の第2の発光層105bに用いるか決定すればよい。
なお、本実施の形態は、他の実施の形態と適宜組み合わせることが可能である。
本実施の形態は、実施の形態2に記載の発光素子を1ユニットとし、その複数のユニットを積層した構成の発光素子(以下、積層型素子という)の態様であり、それに関し図4を参照して説明する。この発光素子は、第1の電極と第2の電極との間に、複数の発光ユニットを有する発光素子である。
なお、この複数のユニットを積層した構成の発光素子を形成する際には、ユニット間に位置する電極は取り除いた構造となっている。
なお、本実施の形態は、他の実施の形態と適宜組み合わせることが可能である。
本実施の形態は、本発明の一態様に係るカルバゾール誘導体を用いて作製された発光装置(以下、「本発明の一態様に係る発光装置」と略称することもある)について示すものであるが、それに関し図5を用いて説明する。
図5(A)は、発光装置を示す上面図、図5(B)は図5(A)をA−BおよびC−Dで切断した断面図である。点線で示された601は駆動回路部(ソース側駆動回路)、602は画素部、603は駆動回路部(ゲート側駆動回路)である。また、604は封止基板、605はシール材であり、シール材605で囲まれた内側は、空間607になっている。
そのソース側駆動回路601はnチャネル型TFT623とpチャネル型TFT624とを組み合わせたCMOS回路が形成され、駆動回路を形成するTFTは、種々のCMOS回路、PMOS回路もしくはNMOS回路で形成しても良い。なお、本実施の形態では、基板上に駆動回路を形成したドライバ一体型を示すが、必ずしもその必要はなく、駆動回路を基板上ではなく外部に形成することもできる。
そのシール材605にはエポキシ系樹脂を用いるのが好ましい。また、これらの材料はできるだけ水分や酸素を透過しない材料であることが望ましい。
以上のようにして、本発明の一態様に係るカルバゾール誘導体を用いて作製された発光装置を得ることができる。
また、本発明の一態様に係るカルバゾール誘導体を用いることにより、高信頼性の発光装置および電子機器を得ることができる。
図6には、本発明の一態様に係るカルバゾール誘導体を用いて作製したパッシブマトリクス型の発光装置の斜視図を示す。図6において、基板951上には、電極952と電極956との間には発光物質を含む層955が設けられている。電極952の端部は絶縁層953で覆われている。そして、絶縁層953上には隔壁層954が設けられている。
本実施の形態では、実施の形態5に示す発光装置をその一部に含む電子機器について示す。本実施の形態の電子機器は、実施の形態1に示したカルバゾール誘導体を含み、高信頼性の表示部を有する。
また、本発明の一態様に係る発光装置は、照明装置として用いることもできる。本発明の一態様に係る発光素子を照明装置として用いる態様を、図8を用いて示す。
図10は、本発明の一態様に係る発光装置を、室内の照明装置3001として用いた例である。本発明の一態様に係る発光装置は大面積化も可能であるため、大面積の照明装置として用いることができる。また、本発明の一態様に係る発光装置は、薄型であるため、薄型化の照明装置として用いることが可能となる。
以下に、本発明の一態様のカルバゾール誘導体の製造方法について、実施例1ないし7の7例を示すが、本発明はこれらの実施例によって何等限定されるものではなく、特許請求の範囲の記載によって特定されるものであることはいうまでもない。
本実施例では、前記構造式1で表される3−フェニル−9−[4−(10−フェニル−9−アントリル)フェニル]−9H−カルバゾール(略称:CzPAP)を製造する例を示す。その合成反応はステップ1及び2の2段階からなる。
このステップは3−ブロモ−9−[4−(10−フェニル−9−アントリル)フェニル]−9H−カルバゾールの合成工程であり、そのステップ1を反応式(E1−1)に示すと共にそのステップの反応に関し以下において詳述する。
このステップは3−フェニル−9−[4−(10−フェニル−9−アントリル)フェニル]−9H−カルバゾール(略称:CzPAP)の合成工程であり、そのステップを反応式(E1−2)に示すと共にそのステップの反応に関し以下において詳述する。
得られたろ液を濃縮して得た油状物をシリカゲルカラムクロマトグラフィー(展開溶媒 ヘキサン:トルエン=5:1)により精製したところ、淡黄色固体を得た。
得られた淡黄色粉末1.3gをトレインサブリメーション法により昇華精製した。昇華精製条件は、減圧下で、アルゴンガスを流量4.0mL/minで流しながら、270℃で淡黄色粉末を加熱した。昇華精製後、目的の化合物の淡黄色固体を1.2g、収率89%で得た。
得られた化合物の1H NMRの測定データを以下に示す。
1H NMR(CDCl3,300MHz):δ=7.35−7.66(m,14H),7.69−7.78(m,9H),7.86(d,J=8.1Hz,4H),8.25(d,J=7.8Hz,1H),8.42(s,1H)
また、1H NMRチャートを図11(A)、(B)に示す。なお、図11(B)は、図11(A)における7.1ppm〜8.5ppmの範囲を拡大して表したチャートである。
そのCV測定における溶液は、溶媒として脱水ジメチルホルムアミド(DMF)((株)アルドリッチ製、99.8%、カタログ番号;22705−6)を用いた。
また、作用電極としては白金電極(ビー・エー・エス(株)製、PTE白金電極)を、補助電極としては白金電極(ビー・エー・エス(株)製、VC−3用Ptカウンター電極(5cm))を、参照電極としてはAg/Ag+電極(ビー・エー・エス(株)製、RE5非水溶媒系参照電極)をそれぞれ用いた。なお、測定は室温で行った。
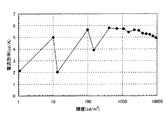
CzPAPの還元反応特性については次のようにして調べた。基準電極に対する作用電極の電位を−1.45Vから−2.35Vまで変化させた後、−2.35Vから−1.45Vまで変化させる走査を1サイクルとし、100サイクル測定した。なお、CV測定のスキャン速度は0.1V/sに設定した。
本例では、前記したとおり構造式1で表される3−フェニル−9−[4−(10−フェニル−9−アントリル)フェニル]−9H−カルバゾール(略称:CzPAP)を既知製造方法である前記第1の既知方法による製造例を示す。
このステップは、3−フェニル−9H−カルバゾールの合成工程であり、そのステップを反応式(R1−1)に示すと共にそのステップの反応に関し以下において詳述する。
このステップは、3−フェニル−9−[4−(10−フェニル−9−アントリル)フェニル]−9H−カルバゾール(略称:CzPAP)の合成工程であり、そのステップを反応式(R1−2)に示すと共にそのステップの反応に関し以下において詳述する。
本例では、前記したとおり構造式1で表される3−フェニル−9−[4−(10−フェニル−9−アントリル)フェニル]−9H−カルバゾール(略称:CzPAP)を既知製造方法である前記第2の既知方法による製造例を示す。
このステップは、9−(4−ブロモフェニル)−3−フェニル−9H−カルバゾールの合成工程であり、そのステップを反応式(R2−1)に示すと共にそのステップの反応に関し以下において詳述する。
このステップは、4−(3−フェニル−9H−カルバゾール−9−イル)フェニルボロン酸の合成工程であり、そのステップを反応式(R2−2)に示すと共にそのステップの反応に関し以下において詳述する。
このステップは、3−フェニル−9−[4−(10−フェニル−9−アントリル)フェニル]−9H−カルバゾール(略称:CzPAP)の合成工程であり、そのステップを反応式(R2−3)に示すと共にそのステップの反応に関し以下において詳述する。
この目的物をCzPAPの製造例と同様に、核磁気共鳴法(NMR)によって、この化合物が目的物である3−フェニル−9−[4−(10−フェニル−9−アントリル)フェニル]−9H−カルバゾール(略称:CzPAP)であることを確認した。
本実施例では、前記構造式2で表される3−[4−(1−ナフチル)フェニル]−9−[4−(10−フェニル−9−アントリル)フェニル]−9H−カルバゾール(略称:CzPAαNP)を製造する例を反応式(E2)で示すと共にその反応に関し以下において詳述する。
得られた淡黄色粉末2.3gをトレインサブリメーション法により昇華精製した。昇華精製条件は、減圧下で、アルゴンガスを流量4.0mL/minで流しながら、340℃で加熱した。昇華精製後、目的の化合物の淡黄色固体を2.2g、収率95%で得た。
核磁気共鳴法(NMR)によって、この化合物が目的物である3−[4−(1−ナフチル)フェニル]−9−[4−(10−フェニル−9−アントリル)フェニル]−9H−カルバゾール(略称:CzPAαNP)であることを確認した。
1H NMR(CDCl3,300MHz):δ=7.37−7.67(m,17H),7.70−7.80(m,6H),7.85−7.96(m,9H),8.06(d,J=8.1Hz,1H),8.29(d,J=7.8Hz,1H),8.52(d,J=0.90Hz,1H)
また、1H NMRチャートを図18(A)、(B)に示す。なお、図18(B)は、図18(A)における7.2ppm〜8.4ppmの範囲を拡大して表したチャートである。
本実施例では、前記構造式4で表される3−(1−ナフチル)−9−[4−(10−フェニル−9−アントリル)フェニル]−9H−カルバゾール(略称:CzPAαN)を製造する例を反応式(E3)で示すと共にその反応に関し以下において詳述する。
得られたろ液を濃縮して得られた油状物を、シリカゲルカラムクロマトグラフィー(展開溶媒 ヘキサン:トルエン=5:1)により精製し、淡黄色油状物を得た。
この油状物をトルエンとヘキサンの混合溶媒により再結晶したところ、目的物の淡黄色粉末を1.8g、収率60%で得た。
核磁気共鳴法(NMR)によって、この化合物が3−(1−ナフチル)−9−[4−(10−フェニル−9−アントリル)フェニル]−9H−カルバゾール(略称:CzPAαN)であることを確認した。
1H NMR(CDCl3,300MHz):δ=7.34−7.67(m,16H),7.72−7.81(m,6H),7.85−7.96(m,6H),8.07(d,J=8.4Hz,1H),8.20(d,J=7.8Hz,1H),8.32(d,J=1.5Hz,1H)
また、1H NMRチャートを図19(A)、図19(B)に示す。なお、図19(B)は、図19(A)における7.0ppm〜8.5ppmの範囲を拡大して表したチャートである。
本実施例では、前記構造式5で表される3−(2−ナフチル)−9−[4−(10−フェニル−9−アントリル)フェニル]−9H−カルバゾール(略称:CzPAβN)を製造する例を反応式(E4)で示すと共にその反応に関し以下において詳述する。
核磁気共鳴法(NMR)によって、この化合物が目的物である3−(2−ナフチル)−9−[4−(10−フェニル−9−アントリル)フェニル]−9H−カルバゾール(略称:CzPAβN)であることを確認した。
1H NMR(CDCl3,300MHz):δ=7.37−7.66(m,13H),7.70−7.80(m,6H),7.85−8.00(m,9H),8.20(s,1H),8.30(d,J=4.8Hz,1H),8.54(s,1H)。
また、1H NMRチャートを図20(A)、図20(B)に示す。なお、図20(B)は、図20(A)における7.0ppm〜9.0ppmの範囲を拡大して表したチャートである。
本実施例では、前記構造式6で表される3−(ビフェニル−4−イル)−9−[4−(10−フェニル−9−アントリル)フェニル]−9H−カルバゾール(略称:CzPApB)を製造する例を反応式(E5)で示すと共にその反応に関し以下において詳述する。
核磁気共鳴法(NMR)によって、この化合物が目的物である3−(ビフェニル−4−イル)−9−[4−(10−フェニル−9−アントリル)フェニル]−9H−カルバゾール(略称:CzPApB)であることを確認した。
1H NMR(CDCl3,300MHz):δ=7.35−7.80(m,25H)、7.82−7.88(m,6H)、8.27(d,J=7.8Hz,1H)、8.47(d,J=1.5Hz,1H)
また、1H NMRチャートを図21(A)、(B)に示す。なお、図21(B)は、図21(A)における7.0ppm〜8.5ppmの範囲を拡大して表したチャートである。
本実施例では、下記構造式8で表される3−(ビフェニル−2−イル)−9−[4−(10−フェニル−9−アントリル)フェニル]−9H−カルバゾール(略称:CzPAoB)を製造する例を反応式(E6)で示すと共にその反応に関し以下において詳述する。
核磁気共鳴法(NMR)によって、この化合物が目的物である3−(ビフェニル−2−イル)−9−[4−(10−フェニル−9−アントリル)フェニル]−9H−カルバゾール(略称:CzPAoB)であることを確認した。
1H NMR(DMSO−d6,300MHz):δ=7.14−7.27(m,6H),7.33(t,J=7.5Hz,1H),7.45−7.81(m,22H),7.87(d,J=8.1Hz,2H),8.21(d,J=9.0Hz,2H)
また、1H NMRチャートを図22(A)、(B)に示す。なお、図22(B)は、図22(A)における7.0ppm〜8.5ppmの範囲を拡大して表したチャートである。
核磁気共鳴法(NMR)によって、この化合物が目的物である3−(9,9−ジメチルフルオレン−2−イル)−9−[4−(10−フェニル−9−アントリル)フェニル]−9H−カルバゾール(略称:CzPAFL)であることを確認した。
1H NMR(CDCl3,300MHz):δ=1.61(s,6H),7.34−7.54(m,11H),7.57−7.66(m,3H),7.70−7.81(m,10H),7.84−7.89(m,5H),8.30(d,J=7.5Hz,1H),8.47(s,1H)
また、1H NMRチャートを図23(A)、(B)に示す。なお、図23(B)は、図23(A)における7.1ppm〜8.6ppmの範囲を拡大して表したチャートである。
本作製例では、実施の形態1の製造方法により製造されたカルバゾール誘導体を用いて発光素子を作製する例を示す。この作製例を図24を用いて説明する。
また、この作製例で作製した発光素子1及び発光素子2の素子構成を表1に示す。その表1では、混合比は全て重量比で表している。
まず、発光素子1の作製例を示す。その発光素子1では、ガラス基板2101上に、酸化珪素を含むインジウム錫酸化物(ITSO)をスパッタリング法にて成膜し、第1の電極2102を形成した。なお、その膜厚は110nmとし、電極面積は2mm×2mmとした。
なお、上述した蒸着過程において、蒸着は全て抵抗加熱法を用いた。また、NPB、PCBAPA、2PCAPA、DPQd、Alq、及びBphen構造式を下記に示す。
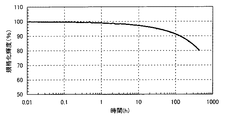
図33に示すように、発光素子1は、430時間後でも初期輝度の80%の輝度を保っており、時間経過による輝度の低下が起こりにくく、長寿命な発光素子であることがわかった。また、図34に示すように、発光素子2は、570時間後でも初期輝度の82%の輝度を保っており、時間経過による輝度の低下が起こりにくく、長寿命な発光素子であることがわかった。
本作製例により、本発明の一態様に係るカルバゾール誘導体を用いて作製した発光素子が、発光素子としての特性が得られ、十分機能することが確認できた。また信頼性試験の結果から、発光素子を連続点灯させた場合であっても、膜の欠陥等に由来する短絡が生じることがなく、信頼性の高い発光素子が得られたことがわかった。
発光素子1の作製例で使用した4−(10−フェニル−9−アントリル)−4’−(9−フェニル−9H−カルバゾール−3−イル)トリフェニルアミン(略称:PCBAPA)は新規物質であり、下記の構造を有するものである。その製造方法に関し、以下において発光素子の作製例に使用した化学物質の製造例として具体的に示す。
その製造工程は、3つの反応工程からなり、それぞれの工程に関し、以下において具体的な製造プロセスを示す。
上記第2の工程で得られた固体を核磁気共鳴分光法(NMR)により測定した。
1H NMR(DMSO−d6,300MHz):δ=6.81−6.86(m,1H),7.12(dd,J1=0.9Hz,J2=8.7Hz、2H),7.19(d、J=8.7Hz,2H)、7.23−7.32(m、3H)、7.37−7.47(m、3H)、7.51−7.57(m,1H)、7.61−7.73(m、7H)8.28(s,1H)、8.33(d、J=7.2Hz,1H)、8.50(d、J=1.5Hz,1H)
1H NMR(CDCl3,300MHz):δ=7.09−7.14(m,1H),7.28−7.72(m、33H)、7.88(d,J=8.4Hz、2H),8.19(d,J=7.2Hz、1H)、8.37(d,J=1.5Hz,1H)
102 第1の電極
103 第1の層
104 第2の層
105 第3の層
105a 発光層
105b 発光層
106 第4の層
107 第2の電極
108 EL層
130 層
301 基板
302 第1の電極
303 第1の層
304 第2の層
305 第3の層
306 第4の層
307 第2の電極
308 EL層
501 第1の電極
502 第2の電極
511 第1の発光ユニット
512 第2の発光ユニット
513 電荷発生層
601 ソース側駆動回路
602 画素部
603 ゲート側駆動回路
604 封止基板
605 シール材
607 空間
608 配線
609 FPC(フレキシブルプリントサーキット)
610 素子基板
611 スイッチング用TFT
612 電流制御用TFT
613 第1の電極
614 絶縁物
616 発光物質を含む層
617 第2の電極
618 発光素子
623 nチャネル型TFT
624 pチャネル型TFT
901 筐体
902 液晶層
903 バックライト
904 筐体
905 ドライバIC
906 端子
951 基板
952 電極
953 絶縁層
954 隔壁層
955 発光物質を含む層
956 電極
2001 筐体
2002 光源
3001 照明装置
8001 筐体
8002 支持台
8003 表示部
8004 スピーカー部
8005 ビデオ入力端子
8102 筐体
8103 表示部
8104 キーボード
8105 外部接続ポート
8106 マウス
8202 表示部
8204 外部接続ポート
8205 リモコン受信部
8206 受像部
8209 操作キー
8403 表示部
8404 音声入力部
8405 音声出力部
8406 操作キー
8407 外部接続ポート
Claims (3)
- カルバゾール骨格の3位に活性部位を有する9−[4−(10−フェニル−9−アントリル)フェニル]−9H−カルバゾールと、化合物(A1)で表される活性部位を有する芳香族化合物とを、金属触媒を用いてカップリングすることを特徴とする、一般式(1a)で表されるカルバゾール誘導体の製造方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2009216398A JP5624296B2 (ja) | 2008-09-19 | 2009-09-18 | カルバゾール誘導体の製造方法 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008240299 | 2008-09-19 | ||
| JP2008240299 | 2008-09-19 | ||
| JP2009216398A JP5624296B2 (ja) | 2008-09-19 | 2009-09-18 | カルバゾール誘導体の製造方法 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2014196103A Division JP5955916B2 (ja) | 2008-09-19 | 2014-09-26 | 化合物及びその製造方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010095523A true JP2010095523A (ja) | 2010-04-30 |
| JP5624296B2 JP5624296B2 (ja) | 2014-11-12 |
Family
ID=41202816
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2009216398A Expired - Fee Related JP5624296B2 (ja) | 2008-09-19 | 2009-09-18 | カルバゾール誘導体の製造方法 |
| JP2014196103A Expired - Fee Related JP5955916B2 (ja) | 2008-09-19 | 2014-09-26 | 化合物及びその製造方法 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2014196103A Expired - Fee Related JP5955916B2 (ja) | 2008-09-19 | 2014-09-26 | 化合物及びその製造方法 |
Country Status (6)
| Country | Link |
|---|---|
| US (2) | US8669373B2 (ja) |
| EP (2) | EP2330097B1 (ja) |
| JP (2) | JP5624296B2 (ja) |
| KR (1) | KR101661328B1 (ja) |
| CN (1) | CN101676265B (ja) |
| AT (1) | ATE517088T1 (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013082742A (ja) * | 2010-09-27 | 2013-05-09 | Semiconductor Energy Lab Co Ltd | 化合物 |
| JP2017085107A (ja) * | 2015-10-30 | 2017-05-18 | 株式会社半導体エネルギー研究所 | 有機化合物、発光素子、発光装置、電子機器及び照明装置 |
Families Citing this family (26)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN101184732B (zh) | 2005-03-28 | 2012-05-16 | 株式会社半导体能源研究所 | 蒽衍生物、发光元件用材料、发光元件、发光装置和电子器件 |
| CN101506163B (zh) * | 2006-08-30 | 2012-05-02 | 株式会社半导体能源研究所 | 合成蒽衍生物的方法和蒽衍生物、发光元件、发光装置、电子装置 |
| US7723722B2 (en) * | 2007-03-23 | 2010-05-25 | Semiconductor Energy Laboratory Co., Ltd. | Organic compound, anthracene derivative, and light-emitting element, light-emitting device, and electronic device using anthracene derivative |
| US20080286445A1 (en) * | 2007-05-17 | 2008-11-20 | Semiconductor Energy Laboratory Co., Ltd. | Composition, and method of fabricating light-emitting element |
| CN101903346B (zh) * | 2007-12-21 | 2013-06-12 | 株式会社半导体能源研究所 | 蒽衍生物和发光材料,发光元件,发光器件及使用发光器件的电子器件 |
| WO2010005066A1 (en) * | 2008-07-08 | 2010-01-14 | Semiconductor Energy Laboratory Co., Ltd. | Carbazole derivative, light-emitting element material, light-emitting element, and light-emitting device |
| US8283855B2 (en) * | 2010-01-11 | 2012-10-09 | Semiconductor Energy Laboratory Co., Ltd. | Method for synthesis of anthracene derivative |
| KR101898499B1 (ko) | 2010-08-20 | 2018-09-13 | 로디아 오퍼레이션스 | 중합체 조성물, 중합체 막, 중합체 겔, 중합체 발포제, 및 이러한 막, 겔, 및 발포제를 포함하는 전자장치 |
| CN107814821A (zh) | 2012-01-12 | 2018-03-20 | Udc 爱尔兰有限责任公司 | 具有二苯并[f,h]喹喔啉的金属配合物 |
| CN102584678B (zh) * | 2012-01-16 | 2012-12-26 | 山东盛华电子新材料有限公司 | 一种n-苯基-3-(4-溴苯基)咔唑的合成方法 |
| US9005357B2 (en) * | 2012-05-24 | 2015-04-14 | Agency For Science, Technology And Research | Method of preparing molybdenum oxide films |
| EP2930762B1 (en) | 2012-12-10 | 2020-09-16 | Konica Minolta, Inc. | Material for organic electroluminescent element, organic electroluminescent element, illumination device, and display device |
| KR101597901B1 (ko) * | 2013-09-26 | 2016-02-25 | 주식회사 엘지화학 | 헤테로환 화합물 및 이를 이용한 유기 발광 소자 |
| JP6567875B2 (ja) * | 2014-05-22 | 2019-08-28 | イー・アイ・デュポン・ドウ・ヌムール・アンド・カンパニーE.I.Du Pont De Nemours And Company | 電子用途において有用な印刷可能なインクおよびこれに関する方法 |
| TWI690534B (zh) | 2014-08-08 | 2020-04-11 | 愛爾蘭商Udc愛爾蘭責任有限公司 | 電致發光咪唑并喹噁啉碳烯金屬錯合物 |
| KR102512938B1 (ko) | 2014-11-18 | 2023-03-23 | 유디씨 아일랜드 리미티드 | 유기 발광 다이오드에 사용하기 위한 Pt- 또는 Pd-카르벤 착체 |
| CN105037253A (zh) * | 2015-05-27 | 2015-11-11 | 上海应用技术学院 | 一种超声逼晶法提纯化合物的方法 |
| KR102537438B1 (ko) | 2015-11-24 | 2023-05-30 | 삼성디스플레이 주식회사 | 화합물 및 이를 포함하는 유기 발광 소자 |
| KR102552273B1 (ko) | 2015-11-26 | 2023-07-07 | 삼성디스플레이 주식회사 | 축합환 화합물 및 이를 포함한 유기 발광 소자 |
| KR102546673B1 (ko) * | 2015-12-03 | 2023-06-23 | 삼성디스플레이 주식회사 | 유기 발광 소자 및 이를 포함하는 표시 장치 |
| KR20170074170A (ko) | 2015-12-21 | 2017-06-29 | 유디씨 아일랜드 리미티드 | 삼각형 리간드를 갖는 전이 금속 착체 및 oled에서의 이의 용도 |
| KR20170101128A (ko) | 2016-02-26 | 2017-09-05 | 가부시키가이샤 한도오따이 에네루기 켄큐쇼 | 유기 화합물, 발광 소자, 발광 장치, 전자 기기, 및 조명 장치 |
| KR20180010136A (ko) | 2016-07-20 | 2018-01-30 | 가부시키가이샤 한도오따이 에네루기 켄큐쇼 | 유기 화합물, 발광 소자, 발광 장치, 전자 기기, 및 조명 장치 |
| KR102567674B1 (ko) | 2017-02-09 | 2023-08-16 | 가부시키가이샤 한도오따이 에네루기 켄큐쇼 | 유기 화합물, 발광 소자, 발광 장치, 전자 기기, 및 조명 장치 |
| CN107417627A (zh) * | 2017-05-12 | 2017-12-01 | 上海开荣化工科技有限公司 | 嘧菌酯的提纯方法 |
| CN113061236B (zh) * | 2021-03-26 | 2023-09-15 | 辽宁大学 | 一种超疏水共价有机骨架材料及其制备方法和应用 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007039431A (ja) * | 2005-03-28 | 2007-02-15 | Semiconductor Energy Lab Co Ltd | アントラセン誘導体、発光素子用材料、発光素子、発光装置及び電子機器 |
| JP2007131722A (ja) * | 2005-11-10 | 2007-05-31 | Toray Ind Inc | 発光素子材料および発光素子 |
| JP2010168345A (ja) * | 2008-07-08 | 2010-08-05 | Semiconductor Energy Lab Co Ltd | カルバゾール誘導体、発光素子用材料、発光素子、発光装置及び電子機器 |
Family Cites Families (46)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5811834A (en) * | 1996-01-29 | 1998-09-22 | Toyo Ink Manufacturing Co., Ltd. | Light-emitting material for organo-electroluminescence device and organo-electroluminescence device for which the light-emitting material is adapted |
| AUPP649498A0 (en) * | 1998-10-14 | 1998-11-05 | Commonwealth Scientific And Industrial Research Organisation | Organoboron derivatives and coupling thereof |
| CN1962810A (zh) * | 1998-12-28 | 2007-05-16 | 出光兴产株式会社 | 用于有机场致发光装置的材料 |
| FR2794742B1 (fr) * | 1999-06-11 | 2005-06-03 | Sanofi Synthelabo | Nouveaux derives du benzene, un procede pour leur preparation et les compositions pharmaceutiques les contenant |
| CA2386074A1 (en) | 1999-09-30 | 2001-04-05 | Merck Patent Gesellschaft Mit Beschraenkter Haftung | Method for producing indole derivatives on a solid phase |
| US6998487B2 (en) * | 2001-04-27 | 2006-02-14 | Lg Chem, Ltd. | Double-spiro organic compounds and organic electroluminescent devices using the same |
| JP2003031371A (ja) | 2001-07-17 | 2003-01-31 | Mitsubishi Chemicals Corp | 有機電界発光素子及び青色発光素子 |
| JP3883854B2 (ja) | 2001-11-29 | 2007-02-21 | 株式会社半導体エネルギー研究所 | 表示装置、コンピュータ、ナビゲーションシステム、ゲーム機器、及び携帯情報端末 |
| JP4080213B2 (ja) | 2002-02-01 | 2008-04-23 | 三井化学株式会社 | 有機電界発光素子 |
| JP4381645B2 (ja) | 2002-02-22 | 2009-12-09 | 出光興産株式会社 | 新規アントラセン化合物およびそれを用いた有機エレクトロルミネッセンス素子 |
| EP1489155A4 (en) * | 2002-03-22 | 2006-02-01 | Idemitsu Kosan Co | MATERIAL FOR ORGANIC ELECTROLUMINESCENT DEVICES AND ORGANIC ELECTROLUMINESCENT DEVICES PRODUCED WITH THIS MATERIAL |
| JP4170655B2 (ja) * | 2002-04-17 | 2008-10-22 | 出光興産株式会社 | 新規芳香族化合物及びそれを利用した有機エレクトロルミネッセンス素子 |
| US20030205696A1 (en) * | 2002-04-25 | 2003-11-06 | Canon Kabushiki Kaisha | Carbazole-based materials for guest-host electroluminescent systems |
| JP4078922B2 (ja) | 2002-08-28 | 2008-04-23 | 富士ゼロックス株式会社 | 有機電界発光素子 |
| JP4164317B2 (ja) * | 2002-08-28 | 2008-10-15 | キヤノン株式会社 | 有機発光素子 |
| JP4311707B2 (ja) | 2002-08-28 | 2009-08-12 | キヤノン株式会社 | 有機発光素子 |
| JP2004091334A (ja) | 2002-08-29 | 2004-03-25 | Mitsubishi Chemicals Corp | 2,6−アリールアミノアントラセン系化合物、電荷輸送材料及び有機電界発光素子 |
| DE10247633A1 (de) * | 2002-10-11 | 2004-04-29 | Studiengesellschaft Kohle Mbh | Mischungen von chiralen Monophosphor-Verbindungen als Ligandensysteme für die asymmetrische Übergangsmetallkatalyse |
| EP2765174B1 (en) * | 2002-11-26 | 2018-05-30 | Konica Minolta Holdings, Inc. | Organic electroluminescent element, and display and illuminator |
| AU2003302925A1 (en) * | 2002-12-11 | 2004-06-30 | Eli Lilly And Company | Novel mch receptor antagonists |
| KR100624407B1 (ko) * | 2003-01-02 | 2006-09-18 | 삼성에스디아이 주식회사 | 디페닐안트라센 유도체 및 이를 채용한 유기 전계 발광 소자 |
| WO2004072205A2 (en) * | 2003-02-12 | 2004-08-26 | Koninklijke Philips Electronics N.V. | Carbazole compounds and use of such compounds in organic electroluminescent devices |
| US7541097B2 (en) * | 2003-02-19 | 2009-06-02 | Lg Display Co., Ltd. | Organic electroluminescent device and method for fabricating the same |
| US7651787B2 (en) * | 2003-02-19 | 2010-01-26 | Lg Display Co., Ltd. | Organic electroluminescent device |
| US7161185B2 (en) * | 2003-06-27 | 2007-01-09 | Semiconductor Energy Laboratory Co., Ltd. | Display device and electronic device |
| US7745988B2 (en) * | 2003-09-05 | 2010-06-29 | Ricoh Company, Limited | 3, 6-diphenylcarbazole compound and organic electroluminescent device |
| JP2005170911A (ja) * | 2003-12-15 | 2005-06-30 | Idemitsu Kosan Co Ltd | 芳香族化合物およびそれを用いた有機エレクトロルミネッセンス素子 |
| KR100787425B1 (ko) * | 2004-11-29 | 2007-12-26 | 삼성에스디아이 주식회사 | 페닐카바졸계 화합물 및 이를 이용한 유기 전계 발광 소자 |
| TWI373506B (en) | 2004-05-21 | 2012-10-01 | Toray Industries | Light-emitting element material and light-emitting material |
| TWI327563B (en) * | 2004-05-24 | 2010-07-21 | Au Optronics Corp | Anthracene compound and organic electroluminescent device including the anthracene compound |
| US8324403B2 (en) | 2004-12-24 | 2012-12-04 | Pioneer Corporation | Organic compound, charge-transporting material, and organic electroluminescent element |
| JP5089063B2 (ja) * | 2005-03-23 | 2012-12-05 | 株式会社半導体エネルギー研究所 | 複合材料および複合材料を用いた発光素子並びに発光装置 |
| US7649197B2 (en) | 2005-03-23 | 2010-01-19 | Semiconductor Energy Laboratory Co., Ltd. | Composite material, and light emitting element and light emitting device using the composite material |
| CN101184732B (zh) * | 2005-03-28 | 2012-05-16 | 株式会社半导体能源研究所 | 蒽衍生物、发光元件用材料、发光元件、发光装置和电子器件 |
| WO2007013537A1 (en) * | 2005-07-27 | 2007-02-01 | Semiconductor Energy Laboratory Co., Ltd. | Anthracene derivative, material for light emitting element, light emitting element, light emitting device, and electronic appliance |
| WO2007026626A1 (en) * | 2005-08-31 | 2007-03-08 | Semiconductor Energy Laboratory Co., Ltd. | Carbazole derivative, material for light emitting element, light emitting element, light emitting device, and electronic device |
| EP1928828B1 (en) * | 2005-09-02 | 2012-03-14 | Semiconductor Energy Laboratory Co., Ltd. | Anthracene derivative |
| KR20070036910A (ko) * | 2005-09-30 | 2007-04-04 | 삼성에스디아이 주식회사 | 전자 방출 표시 디바이스의 제조 방법 |
| US20070215889A1 (en) * | 2006-03-20 | 2007-09-20 | Semiconductor Energy Laboratory Co., Ltd. | Aromatic amine compound, and light-emitting element, light-emitting device, and electronic appliance using the aromatic amine compound |
| EP2084123B1 (en) * | 2006-04-28 | 2014-08-27 | Semiconductor Energy Laboratory Co., Ltd. | Anthracene derivative, and light-emitting element, light-emitting device, electronic device using anthracene derivative |
| JP2009536656A (ja) * | 2006-05-09 | 2009-10-15 | ユニバーシティ オブ ワシントン | 有機発光装置向けの架橋可能な正孔輸送物質 |
| JP5179805B2 (ja) | 2006-08-30 | 2013-04-10 | 株式会社半導体エネルギー研究所 | アントラセン誘導体、発光素子および発光装置 |
| CN101506163B (zh) * | 2006-08-30 | 2012-05-02 | 株式会社半导体能源研究所 | 合成蒽衍生物的方法和蒽衍生物、发光元件、发光装置、电子装置 |
| US7723722B2 (en) * | 2007-03-23 | 2010-05-25 | Semiconductor Energy Laboratory Co., Ltd. | Organic compound, anthracene derivative, and light-emitting element, light-emitting device, and electronic device using anthracene derivative |
| JP4958597B2 (ja) | 2007-03-26 | 2012-06-20 | 日新製鋼株式会社 | 住宅用床小梁 |
| CN101200634B (zh) | 2007-11-06 | 2011-07-06 | 华南理工大学 | 可溶性树枝取代的蒽分子蓝光材料及其制备方法与应用 |
-
2009
- 2009-09-04 AT AT09169453T patent/ATE517088T1/de not_active IP Right Cessation
- 2009-09-04 KR KR1020090083531A patent/KR101661328B1/ko active IP Right Grant
- 2009-09-04 EP EP11000870A patent/EP2330097B1/en not_active Not-in-force
- 2009-09-04 EP EP09169453A patent/EP2166001B1/en not_active Not-in-force
- 2009-09-16 US US12/560,903 patent/US8669373B2/en not_active Expired - Fee Related
- 2009-09-17 CN CN200910169057.3A patent/CN101676265B/zh not_active Expired - Fee Related
- 2009-09-18 JP JP2009216398A patent/JP5624296B2/ja not_active Expired - Fee Related
-
2014
- 2014-03-07 US US14/201,123 patent/US20140187791A1/en not_active Abandoned
- 2014-09-26 JP JP2014196103A patent/JP5955916B2/ja not_active Expired - Fee Related
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007039431A (ja) * | 2005-03-28 | 2007-02-15 | Semiconductor Energy Lab Co Ltd | アントラセン誘導体、発光素子用材料、発光素子、発光装置及び電子機器 |
| JP2007131722A (ja) * | 2005-11-10 | 2007-05-31 | Toray Ind Inc | 発光素子材料および発光素子 |
| JP2010168345A (ja) * | 2008-07-08 | 2010-08-05 | Semiconductor Energy Lab Co Ltd | カルバゾール誘導体、発光素子用材料、発光素子、発光装置及び電子機器 |
Cited By (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013082742A (ja) * | 2010-09-27 | 2013-05-09 | Semiconductor Energy Lab Co Ltd | 化合物 |
| US9040720B2 (en) | 2010-09-27 | 2015-05-26 | Semiconductor Energy Laboratory Co., Ltd. | Organic compound, light-emitting element, light-emitting device, electronic device, and lighting device |
| US9614164B2 (en) | 2010-09-27 | 2017-04-04 | Semiconductor Energy Laboratory Co., Ltd. | Organic compound, light-emitting element, light-emitting device, electronic device, and lighting device |
| US20170162798A1 (en) | 2010-09-27 | 2017-06-08 | Semiconductor Energy Laboratory Co., Ltd. | Organic compound, light-emitting element, light-emitting device, electronic device, and lighting device |
| US10263195B2 (en) | 2010-09-27 | 2019-04-16 | Semiconductor Energy Laboratory Co., Ltd. | Organic compound, light-emitting element, light-emitting device, electronic device, and lighting device |
| US10497880B2 (en) | 2010-09-27 | 2019-12-03 | Semiconductor Energy Laboratory Co., Ltd. | Organic compound, light-emitting element, light-emitting device, electronic device, and lighting device |
| JP2017085107A (ja) * | 2015-10-30 | 2017-05-18 | 株式会社半導体エネルギー研究所 | 有機化合物、発光素子、発光装置、電子機器及び照明装置 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP5955916B2 (ja) | 2016-07-20 |
| EP2330097B1 (en) | 2013-01-23 |
| ATE517088T1 (de) | 2011-08-15 |
| US20100076201A1 (en) | 2010-03-25 |
| JP5624296B2 (ja) | 2014-11-12 |
| US20140187791A1 (en) | 2014-07-03 |
| CN101676265B (zh) | 2014-04-30 |
| EP2330097A1 (en) | 2011-06-08 |
| US8669373B2 (en) | 2014-03-11 |
| KR101661328B1 (ko) | 2016-09-29 |
| KR20100033340A (ko) | 2010-03-29 |
| JP2015017120A (ja) | 2015-01-29 |
| EP2166001A1 (en) | 2010-03-24 |
| EP2166001B1 (en) | 2011-07-20 |
| CN101676265A (zh) | 2010-03-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5955916B2 (ja) | 化合物及びその製造方法 | |
| JP6684317B2 (ja) | 有機化合物の合成方法 | |
| JP6463547B1 (ja) | 発光装置 | |
| JP5552270B2 (ja) | カルバゾール誘導体、発光素子用材料、発光素子、発光装置及び電子機器 | |
| JP6874183B2 (ja) | カルバゾール誘導体、発光素子、発光装置、電子機器、照明装置 | |
| JP5459903B2 (ja) | アントラセン誘導体、発光素子、発光装置、電子機器、及び照明装置 | |
| JP5577132B2 (ja) | 複素環化合物、及び発光素子 | |
| JP5489632B2 (ja) | 有機化合物、アントラセン誘導体、およびアントラセン誘導体を用いた発光素子、発光装置 | |
| JP5586936B2 (ja) | アントラセン誘導体 | |
| JP5179805B2 (ja) | アントラセン誘導体、発光素子および発光装置 | |
| JP2008106063A (ja) | アントラセン誘導体、およびアントラセン誘導体を用いた発光素子、発光装置、電子機器 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20120830 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20131205 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20131217 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140213 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20140415 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140527 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20140909 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20140926 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5624296 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |