JP2010090070A - β−1,3−1,6−D−グルカンを用いた消化管粘膜保護剤または下痢抑制剤 - Google Patents
β−1,3−1,6−D−グルカンを用いた消化管粘膜保護剤または下痢抑制剤 Download PDFInfo
- Publication number
- JP2010090070A JP2010090070A JP2008262823A JP2008262823A JP2010090070A JP 2010090070 A JP2010090070 A JP 2010090070A JP 2008262823 A JP2008262823 A JP 2008262823A JP 2008262823 A JP2008262823 A JP 2008262823A JP 2010090070 A JP2010090070 A JP 2010090070A
- Authority
- JP
- Japan
- Prior art keywords
- glucan
- diarrhea
- protective agent
- gastrointestinal
- gastrointestinal mucosa
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Landscapes
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Polysaccharides And Polysaccharide Derivatives (AREA)
- Coloring Foods And Improving Nutritive Qualities (AREA)
Abstract
【解決手段】β−D−グルカンを含む消化管粘膜保護剤および下痢抑制剤を提供する。
【選択図】なし
Description
しかしながら、消化管粘膜細胞は代謝回転が盛んで、治療目的で投与された薬剤、例えば、抗癌剤や抗生物質等の種々の組織障害因子の影響を顕著に受けることが知られている。
消化管粘膜細胞が障害を受ければ、水分、栄養素等の吸収が損なわれるだけでなく、消化管でのバリアーが破綻し、細菌等が消化管粘膜を通過して臓器内に移行し、感染症の原因ともなる。
したがって、消化管粘膜細胞の保護は、生体機能の維持に重要である。
しかしながら、これら物質は、経口投与不可能である。また、単一純粋な物質でない等の欠点を有する。
しかしながら、β-1,3-1,6-D-グルカンが、消化管粘膜保護作用を発揮することは未だ報告されていない。
また、黒酵母由来のβ-1,3-1,6-D-グルカンは、工業的規模で精製できることも報告されている(特許文献3参照)。
さらには、優れた下痢抑制剤を提供することも目的とする。
好ましくは、代謝拮抗剤により惹起される消化管粘膜障害から消化管粘膜を保護する、β-1,3-1,6-D-グルカンを含む消化管粘膜保護剤に関する。
消化管粘膜は、腸管粘膜であり得に好ましくは、小腸粘膜である。
β-1,3-1,6-D-グルカンは黒酵母が産生するものが好ましく、オーレオバシジウム・プルランス(Aureobasidium pullulans)が産生するものがより好ましい。さらに好ましくは、オーレオバシジウム・プルランスGM-NH-1A1株、又はGM-NH-1A2株(独立行政法人産業技術研究所特許生物寄託センターにそれぞれFERM P-19285及びFERM P-19286として寄託済み)が産生するものが好ましい。
さらにより好ましくは、β-1,3-1,6-D-グルカンは、以下の(1)−(2)の性質:
(1)1N水酸化ナトリウム重水溶液を溶媒とする溶液の1H NMRスペクトルが約4.7ppm及び約4.5ppmの2つのシグナルを有する;
(2)水溶液の30℃、pH5.0、濃度0.5(w/v%)における粘度が200cP(mPa・s)以下である、
を有する。
本発明のβ-1,3-1,6-D-グルカンを含む消化管粘膜保護剤は、好ましくは、経口投与可能な製剤である。
好ましくは、消化管粘膜障害により惹起される下痢の発症を抑制する、β-1,3-1,6-D-グルカンを含む下痢抑制剤に関する。
消化管粘膜障害は、代謝拮抗薬により惹起され得る。
消化管粘膜は、腸管粘膜であり得に好ましくは、小腸粘膜である。
β-1,3-1,6-D-グルカンは黒酵母が産生するものが好ましく、オーレオバシジウム・プルランス(Aureobasidium pullulans)が産生するものがより好ましい。さらに好ましくは、オーレオバシジウム・プルランスGM-NH-1A1株、又はGM-NH-1A2株(独立行政法人産業技術研究所特許生物寄託センターにそれぞれFERM P-19285及びFERM P-19286として寄託済み)が産生するものが好ましい。
さらにより好ましくは、β-1,3-1,6-D-グルカンは、以下の(1)−(2)の性質:
(1)1N水酸化ナトリウム重水溶液を溶媒とする溶液の1H NMRスペクトルが約4.7ppm及び約4.5ppmの2つのシグナルを有する;
(2)水溶液の30℃、pH5.0、濃度0.5(w/v%)における粘度が200cP(mPa・s)以下である、
を有する。
本発明のβ-1,3-1,6-D-グルカンを含む下痢抑制剤は、好ましくは、経口投与可能な製剤である。
本発明は、β-1,3-1,6-D-グルカンを含む消化管粘膜保護剤および下痢抑制剤を提供する。
消化管粘膜は、消化管の内腔を覆う上皮と粘膜固有層、粘膜筋板を含むものであり、臓器は特に限定されないが、好ましくは、腸管粘膜、より好ましくは小腸粘膜である。
本発明に係るβ-1,3-1,6-D-グルカンを含む消化管粘膜保護剤は、組織障害因子により惹起される消化管粘膜障害から、消化管粘膜を保護することができるが、組織障害因子は、特に限定されず、あらゆる消化管粘膜障害を惹起する物質を包含する。組織障害因子の例としては、各種抗癌剤、抗生物質が挙げられ、例えば、5−FU、テガフール・ウラシル(UFT)、テガフール・ギメラシル・オテラシル(TS−1またはS−1)を含むピリミジン系代謝拮抗剤、メルカプトプリン、フルダラビンを含むプリン系代謝拮抗剤、メトトレキサート等の葉酸拮抗剤、イリノテカン、エトポシド等のトポイソメラーゼ阻害剤、シスプラチン、カルボプラチン等の白金製剤が挙げられる。また、インドメタシン、アスピリン等の抗炎症剤も組織障害因子に含まれる。
代謝拮抗剤として好ましくは、5−FU、テガフール・ウラシル(UFT)、テガフール・ギメラシル・オテラシル(TS−1またはS−1)を含むピリミジン系代謝拮抗剤、メルカプトプリン、フルダラビンを含むプリン系代謝拮抗剤、メトトレキサート等の葉酸拮抗剤が挙げられる。さらに好ましくは、5−FU、テガフール・ウラシル(UFT)、テガフール・ギメラシル・オテラシル(TS−1またはS−1)を含むピリミジン系代謝拮抗剤が挙げられる。
オーレオバシジウム属の微生物が産生するβ-1,3-1,6-D-グルカンは、菌体外に分泌されるために回収が容易であり、また水溶性である点で好ましいものである。オーレオバシジウム属の微生物は、分子量が100万以上の高分子量のβ-1,3-1,6-D-グルカンから分子量が数万程度の低分子のβ-1,3-1,6-D-グルカンまでを培養条件に応じて産生することができる。
β-1,3-1,6-D-グルカンは、例えば、これを産生する微生物の培養上清に有機溶媒を添加することにより沈殿物として得ることができる。
上記の高粘度のβ-1,3-1,6-D-グルカンを含む培養液を、常温で攪拌しながら、これにアルカリを添加すると、急激に粘度が低下する。
本発明の消化管粘膜保護剤および下痢抑制剤において、β-1,3-1,6-D-グルカンは、必要に応じて薬学的に許容される担体とともに適当な製剤とすることができる。このような担体として、賦形剤、結合剤、崩壊剤、潤沢剤、付湿剤等が挙げられる。また、酸化防止剤のような慣用の添加剤なども含まれていてよい。
投与
本発明の消化管粘膜保護剤および下痢抑制剤は、消化管粘膜障害または下痢を発症している、または発症する可能性の高いヒトを含む哺乳動物に好適に投与できる。この中には、他の疾患を併発している患者も含まれる。さらに、β-1,3-1,6-D-グルカンは安全な天然成分であることから、消化管粘膜障害または下痢の予防を目的として健常人も適時又は常時摂取することができる。
したがって、本発明に関するβ-1,3-1,6-D-グルカンは、消化管粘膜障害または下痢の治療および/または予防を目的として投与され得る。
また、本発明に関するβ-1,3-1,6-D-グルカンは、経口投与によっても消化管粘膜保護作用および下痢抑制作用を発揮するので、本発明の消化管粘膜保護剤および下痢抑制剤は経口投与され得るが、他の投与法(静脈内投与、腹腔内投与を含む)によっても投与され得る。
本発明の消化管粘膜保護剤および下痢抑制剤が投与される対象としては、例えば、抗癌剤等の組織障害因子を投与される、または投与される予定のヒトが含まれる。
また、本発明の下痢抑制剤は、下痢を抑制する。ここで「抑制」とは、下痢の発症を完全に阻止することのみならず、その程度を抑制すること、発症を遅らせること、並びに既に発症した症状を緩和すること、進行を止める、あるいは遅らせることも含むものとする。
また、本発明の消化管粘膜保護剤および下痢抑制剤は、一態様として、組織障害因子、例えば、抗癌剤等の代謝拮抗剤を投与されるヒトに対して、該組織障害因子と同時に投与され得る。
本発明の消化管粘膜保護剤および下痢抑制剤の投与の時期は、組織障害因子、例えば、抗癌剤等の代謝拮抗剤の投与時期等を考慮に入れて適切な時期に投与されればよく、投与量も適宜設定されることができる。
本発明に関するβ-1,3-1,6-D-グルカンは、免疫賦活作用を有し、白血球数を増加させ、さらに抗癌作用を有するので、抗癌剤と併用すれば、相加または相乗的な抗癌効果が発揮できる。さらに、本願発明に関するβ-1,3-1,6-D-グルカンは、抗癌剤により惹起される、消化管粘膜障害、下痢を含む副作用を抑制または回避できるので、本発明に関するβ−1,3−1,6−D−グルカンと抗癌剤を併用することにより、癌患者のQOL(Quality of Life;生活の質)を改善しつつ、相加または相乗的な抗癌効果が発揮できる。
このような知見から、抗癌剤の中に、本発明に関するβ-1,3-1,6-D-グルカンを含め合剤とすることもできる。
本発明の飲食品組成物は、β-1,3-1,6-D-グルカン、好ましくは、オーレオバシジウム属(Aureobasidium sp.)に属する微生物に由来するβ-1,3-1,6-D-グルカンを含む。このβ-1,3-1,6-D-グルカンは、さらに好ましくは、1N水酸化ナトリウム重水溶液を溶媒とする溶液の1H NMRスペクトルが約4.7ppm及び約4.5ppmの2つのシグナルを有し、かつ水溶液の30℃、pH5.0、濃度0.5(w/v%)における粘度が好ましくは200cP(mPa・s)以下、より好ましくは100cP(mPa・s)以下、さらに好ましくは50cP(mPa・s)以下、よりさらに好ましくは10cP以下のものである。この飲食品組成物は、β-1,3-1,6-D-グルカンを含むことから消化管粘膜保護作用および下痢抑制作用を有するため、健康食品、機能性食品、又は栄養機能食品又は特定保健用食品のような保健機能食品として好適に使用できる。ここで、本発明における健康食品は、一般に「健康によい」として売られている食品全般、又は消費者が健康に良いと積極的な効果を期待して摂取する医薬品以外の食品を含み、健康補助食品を含む。また、本発明における機能性食品は、生体調節機能を充分に効率よく発現するように設計した食品を含む。
次に実施例及び試験例を挙げて本発明を詳細に説明するが、本発明はこれらの実施例に限定されるものではない。
(1-1)β-1,3-1,6-D-グルカンの培養産生
後掲の表1に示す組成を有する液体培地100mlを500ml容量の肩付きフラスコに入れ、121℃で、15分間、加圧蒸気滅菌を行った後、オーレオバシジウム・プルランス(Aureobasidium pullulans)GM-NH-1A1株(FERM P-19285)を同培地組成のスラントより無菌的に1白金耳植菌し、130rpmの速度で通気攪拌しつつ、30℃で24時間培養することにより種培養液を調製した。
<多糖濃度測定>
多糖濃度は、培養液を数mlサンプリングし、菌体を遠心分離除去した後、その上清に最終濃度が66%(v/v)となるようにエタノールを加えて多糖を沈殿させて回収した後、イオン交換水に溶解し、フェノール硫酸法で定量した。
<置換スルホ含量測定>
同様にして菌体を除去した培養上清にエタノールを最終濃度が66%となるように添加し、β-1,3-1,6-D-グルカンを沈殿回収した。その後、再度イオン交換水に溶解し、再度遠心分離後、その上清に最終濃度が0.9%になるように食塩を加えた後、再度66%エタノールでβ-1,3-1,6-D-グルカンを回収した。このβ-1,3-1,6-D-グルカン回収精製操作を更に2回繰り返し、得られたβ-1,3-1,6-D-グルカン水溶液をイオン交換水で透析後、凍結乾燥によりβ-1,3-1,6-D-グルカン粉末を得た。
上記のようにして得られた培養液の粘度はBM型回転粘度計(東京計器製)を用いて、30℃、12rpmで測定したところ、1500cP((mPa・s))であった。測定に用いるロータは粘度にあわせて適当なものを選択した。
上記のβ-1,3-1,6-D-グルカン水溶液(培養ろ液)を0.3%に希釈後、限外ろ過(UF)膜(分子量カット5万、日東電工社製)を用いて脱塩を行い、最終的にナトリウムイオン濃度を20mg/100mlに落とした後、50%(w/v)クエン酸水溶液によりpHを3.5に調整した。
<硫黄含有量の測定>
また、得られたβ-1,3-1,6-D-グルカン水溶液をイオン交換水で透析後、凍結乾燥によりβ-1,3-1,6-D-グルカン粉末を得た。本β-1,3-1,6-D-グルカンの組成分析結果からS含量は330mg/kgであり、これから計算される置換スルホ酢酸含量は0.12%であった。
<結合状態の確認>
また、脱塩を行った上記培養ろ液について、コンゴーレッド法によって、480nmから525nm付近への波長シフトを確認することができたのでβ−1,3結合を含むグルカンを含有していることが証明された(K. Ogawa, Carbohydrate Research, 67, 527-535 (1978)、今中忠行 監修, 微生物利用の大展開, 1012-1015, エヌ・ティー・エス(2002))。そのときの極大値へのシフト差分はΔ0.48/500μg多糖であった。
<粒度測定>
次に、レ−ザ回折/散乱式粒度分布測定装置(HORIBA製LA−920)を用いて培養液の粒度を測定したところ、粒子としては0.3μmと100μm程度の大きさのところにピ−クが見られた。続いて、超音波を照射しながら、粒度測定を行うと、100μmのピ−クはみるみるうちに消失し、0.3μmのピ−クが増え、最終的に0.3μmのみとなった。超音波照射したときの培養液の粒度分布を図10に示す。
<分子量測定>
また、東ソー社製のトーヨーパールHW65(カラムサイズ75cm×φ1cm、排除分子量250万(デキストラン))を用いて、0.1Mの水酸化ナトリウム水溶液を溶離液としてゲルろ過クロマトグラフィーを行い、溶解β-1,3-1,6-D-グルカンとβ-1,3-1,6-D-グルカンの1次粒子とを含む溶液の分子量を測定したところ、溶解β-1,3-1,6-D-グルカンに由来する2〜30万のピークの低分子画分と、1次粒子に由来する見かけ上50〜250万の高分子画分との二種類が検出された。分子量のマーカーとしてShodex社製のプルランを用いた。
(1)において、アルカリ処理および菌体除去処理により調製された微粒子β-1,3-1,6-D-グルカンを含むβ-1,3-1,6-D-グルカン水溶液に、最終濃度が66%(v/v)となるようにエタノールを添加して、多糖グルカンを沈殿させ、遠心分離法により回収した。次いで凍結乾燥法によりエタノールと水分を除去し、乾燥β-1,3-1,6-D-グルカンを得た。そのときの収率はエタノール沈殿前の全糖濃度と比較して95%以上であった。
(1)においてアルカリ処理を行い低粘度化した培養液(多糖濃度0.5%(5mg/ml))90Lを50%クエン酸水溶液9kgで中和後、濾過助剤(日本製紙ケミカル製粉末セルロ−スKCフロック)を1.8kgプレコートした薮田式濾過圧搾機40D-4を通して、菌体を取り除いた。ろ液を限外濾過スパイラルエレメント(日東電工製NTU3150−S4)で9Lまで濃縮した。本濃縮液を攪拌しながら、pHを3.0-3.5にクエン酸により調整して、エタノール18Lを加え、β-1,3-1,6-D-グルカン/エタノール/水スラリーを得た。スラリーの粘度はBM型粘度計で22mPa・s(30℃)であった。室温で3時間静置し、上澄み液(エタノール/水)約17Lを取り除いた。残ったスラリーの粘度は45mPa・s(30℃)であった。本濃縮スラリー10Lを坂本技研型の噴霧乾燥装置R-3を用いて噴霧乾燥し、360gのβ-1,3-1,6-D-グルカン粉末を得た(回収率80%)。得られたβ-1,3-1,6-D-グルカンの純度はNMRスペクトルの解析の結果、90%以上であった。
なお、得られたβ-1,3-1,6-D-グルカン粉末を1N水酸化ナトリウム重水溶液に溶解させ、NMRスペクトルを測定したところ、1H NMRスペクトルが約4.7ppm及び約4.5ppmの2つのシグナルを得た。また、得られたβ-1,3-1,6-D-グルカン粉末の濃度0.5(w/v%)の水溶液の粘度は200cP以下であった(pH5.0、30℃)。
●材料および方法
1. 実験材料
黒酵母由来β-1,3-1,6-D-グルカン粉末(LMW-βグルカン)は上記により製造したものを使用した。
β-1,3-1,6-D-グルカン粉末(LMW-βグルカン)「以下、β−グルカンまたはβ−glucanとも称す」は25 mg/kg、50 mg/kgおよび100 mg/kgの投与量となるように蒸留水で溶解した。
代謝拮抗剤であるガン化学療法剤UFTの構成成分、テガフールおよびウラシルはSigma社および和光純薬工業(株)から購入し、UFTを調整し、50 mg/kgの投与量となるように蒸留水で懸濁した。GOT/GPTの測定は和光純薬工業のキットを用いて測定した。
2. 実験動物
Balb/c雄性マウス(5週齢)は日本SLC(株)から購入し、1週間予備飼育した後、健康なマウスを実験に使用した。マウスは1群7匹を使用し、実験構成は、(1)正常群、(2)Colon 26移植マウス群、(3)Colon 26移植マウス+UFT(50 mg/kg)投与群、(4)Colon 26移植マウス+UFT+β−グルカン(25 mg/kg)投与群、(5)Colon 26移植マウス+UFT+β−グルカン(50 mg/kg)投与群および(6)Colon 26移植マウス+UFT+β−グルカン(100 mg/kg)投与群の6群とした。
3. ガン細胞
マウス大腸ガン細胞Colon 26は、東北大学抗加齢研究所から供与されたものを用いた。
4. ガン移植マウスの作成、β−グルカンとUFTとの併用による抗腫瘍効果および副作用(体重減少、下痢、白血球および血小板減少、肝臓障害)の測定
a)Colon 26 (1 x 105細胞数/マウス)をBalb/cマウスの背部皮下に移植し、ガン移植1週間後の背部に固形腫瘍が確認された後に、UFT(50 mg/kg)を朝(8:00)1回経口投与し、14日間投与した。β−グルカン(25、50および100 mg/kg)は朝(8:00)、夕(20:00)2回、14日間経口投与した。
b)体重測定はガン移植翌日から各日に測定した。
c)腫瘍容積量はガン移植9日目から各日に測定した。
d)下痢の観察および摂食量の測定はUFTおよびβ−グルカン投与後から開始した。
e)ガン移植から21日目に各マウスは、エーテル麻酔下、下大静脈から血液を採取し、腫瘍組織、肝臓、脾臓、胸腺および小腸を摘出し、各重量を測定した。採取した血液中の赤血球、白血球、血小板数、ヘモグロビン量およびヘマトクリット値は、自動血球測定装置を用いて測定した。
1.代謝拮抗剤UFTとβ−グルカン併用における抗腫瘍効果
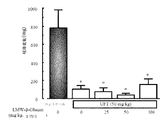
UFT(50 mg/kg)投与によって、腫瘍の増加は抑制された。β−グルカン(50および100 mg/kg)の併用においてUFTの抗腫瘍効果を維持し、もしくは有意な差は認めらなかったが、UFTによる抗腫瘍効果を減弱することなしに、抗腫瘍効果の増強傾向が認められた(図1)。 最終の腫瘍組織重量も、UFTによる抗腫瘍効果を維持していることが判明した(図2)。
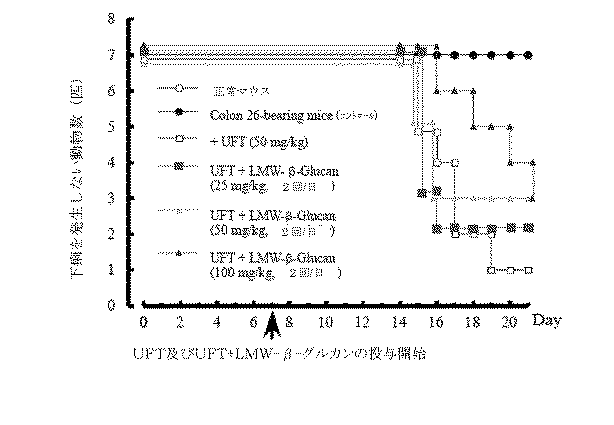
UFT投与開始12日目(ガン移植18日目)から体重は、正常群およびColon 26移植マウス群と比較して有意に低下した。β−グルカン併用した群では体重の低下がUFT投与群と比較して有意ではないけれど、わずかに抑制する傾向が認められた(図3)。摂食量もUFT投与開始9日目(ガン移植15日目)から低下したが、β−グルカン(50および100mg/kg)の併用はUFTによる摂食量の低下を回復した(図4)。下痢もUFT投与開始10日目(ガン移植16日目)から発生した。UFTによる下痢の発生はβ−グルカン(50および100mg/kg)の併用によって抑制された(図5)。
表2に示すように、UFT投与よって、肝臓、脾臓および胸腺重量は低下したが、β−グルカンの併用によっても回復されなかった。UFTによって肝臓重量の低下が認められたが、肝臓障害の指標となるGOTおよびGPT値には影響を及ぼさなかった。
処方例1(クッキー)
粉末β-1,3-1,6-D-グルカン 1重量%
殺菌乳酸菌末 0.2重量%
カテキン 1重量%
クッキー生地 残量
処方例2(サプリメント)
粉末β-1,3-1,6-D-グルカン 1重量%
コラーゲンペプチド 42重量%
ヒアルロン酸 0.06重量%
殺菌乳酸菌末 1重量%
ビタミンC 10重量%
ビタミンB2 0.03重量%
ビタミンB6 0.03重量%
賦形剤(でんぷんなど) 残量
処方例3(サプリメント)
粉末β-1,3-1,6-D-グルカン 1重量%
コラーゲンペプチド 42重量%
ヒアルロン酸 0.06重量%
殺菌乳酸菌末 1重量%
ビタミンC 10重量%
ビタミンB2 0.03重量%
ビタミンB6 0.03重量%
ナイアシン 0.15重量%
賦形剤(でんぷんなど) 残量
処方例4(ドリンク剤)
β-1,3-1,6-D-グルカン水溶液
(0.2重量%β-グルカン水溶液) 61.5重量%
殺菌乳酸菌末 0.03重量%
ミルクトオリゴ糖 0.8重量%
ラクトフェリン 0.09重量%
甘味料(スクラロース) 0.03重量%
クエン酸 0.22重量%
香料 0.37重量%
水 残部
処方例5(ドリンク剤)
β-1,3-1,6-D-グルカン水溶液
(0.2重量%β-グルカン水溶液) 61.5重量%
殺菌乳酸菌末 0.03重量%
テアニン 0.8重量%
GABA 0.09重量%
甘味料(スクラロース) 0.03重量%
クエン酸 0.22重量%
香料 0.37重量%
水 残部
処方例6(ドリンク剤)
粉末β-1,3-1,6-D-グルカン
(オーレオバシジウム属由来) 0.2重量%
紅花エキス 7%
イチョウ葉エキス 7%
高麗人参エイキ 7%
ザクロエキス 3.5%
天草エキス 3.5%
桂皮エキス 3.5%
陳皮エキス 3.5%
ウコンエキス 2.1%
生姜エキス 1%
ハチミツ 3%
水 残部
Claims (12)
- β-1,3-1,6-D-グルカンを含む消化管粘膜保護剤。
- 代謝拮抗剤により惹起される消化管粘膜障害から消化管粘膜を保護する、請求項1に記載の消化管粘膜保護剤。
- β-1,3-1,6-D-グルカンを含む下痢抑制剤。
- 消化管粘膜障害により惹起される下痢の発症を抑制する、請求項3に記載の下痢抑制剤。
- 消化管粘膜障害が、代謝拮抗剤により惹起される、請求項4に記載の下痢抑制剤。
- 消化管粘膜が小腸粘膜である、請求項1、2、4または5に記載の消化管粘膜保護剤または下痢抑制剤。
- β-1,3-1,6-D-グルカンが黒酵母由来である、請求項1−6のいずれかに記載の消化管粘膜保護剤または下痢抑制剤。
- 黒酵母が、オーレオバシジウム・プルランスGM-NH-1A1株(FERM BP-10294)、又はオーレオバシジウム・プルランスGM-NH-1A2株(FERM BP-10295)である、請求項7に記載の消化管粘膜保護剤または下痢抑制剤。
- β-1,3-1,6-D-グルカンが、以下の(1)−(2)の性質:
(1)1N水酸化ナトリウム重水溶液を溶媒とする溶液の1H NMRスペクトルが約4.7ppm及び約4.5ppmの2つのシグナルを有する;
(2)水溶液の30℃、pH5.0、濃度0.5(w/v%)における粘度が200cP(mPa・s)以下である、
を有する、請求項1−8のいずれかに記載の消化管粘膜保護剤または下痢抑制剤。 - 経口投与用である、請求項1−9のいずれかに記載の消化管粘膜保護剤または下痢抑制剤。
- 請求項1−9のいずれかに記載の消化管粘膜保護剤または下痢抑制剤を含む食品。
- 消化管粘膜保護および/または下痢抑制のために用いられる旨の表示を付した、請求項10に記載の食品。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008262823A JP5320965B2 (ja) | 2008-10-09 | 2008-10-09 | β−1,3−1,6−D−グルカンを用いた消化管粘膜保護剤または下痢抑制剤 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008262823A JP5320965B2 (ja) | 2008-10-09 | 2008-10-09 | β−1,3−1,6−D−グルカンを用いた消化管粘膜保護剤または下痢抑制剤 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010090070A true JP2010090070A (ja) | 2010-04-22 |
| JP5320965B2 JP5320965B2 (ja) | 2013-10-23 |
Family
ID=42253169
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008262823A Active JP5320965B2 (ja) | 2008-10-09 | 2008-10-09 | β−1,3−1,6−D−グルカンを用いた消化管粘膜保護剤または下痢抑制剤 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP5320965B2 (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013095702A (ja) * | 2011-11-01 | 2013-05-20 | Daiso Co Ltd | β−1,3−グルカンを含む過敏性腸症候群の下痢抑制剤、腹痛改善剤、及び大腸における痛覚過敏改善剤 |
| JP2017522308A (ja) * | 2014-07-21 | 2017-08-10 | ネステク ソシエテ アノニム | 安全な嚥下を促進する嚥下障害者用栄養製品 |
Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS61146192A (ja) * | 1984-12-17 | 1986-07-03 | Satoshi Shinohara | フラクトオリゴ糖とβ―1.3―1.6グルカンを主成分とする飲食物の製造方法 |
| JPH11501691A (ja) * | 1995-03-13 | 1999-02-09 | ノボゲン リサーチ ピーティーワイ.リミテッド. | グルカンの製造方法、及びグルカンの治療用途 |
| JP2001506129A (ja) * | 1996-12-19 | 2001-05-15 | ザ、ユニバーシティ、オブ、ニュー、サウス、ウェイルズ | プレバイオテックスおよびプロバイオテックス |
| JP2005307150A (ja) * | 2004-03-26 | 2005-11-04 | Asahi Denka Kogyo Kk | βグルカン |
| JP2006028307A (ja) * | 2004-07-14 | 2006-02-02 | Asahi Denka Kogyo Kk | βグルカン |
| JP2006104439A (ja) * | 2004-03-29 | 2006-04-20 | Daiso Co Ltd | β−1,3−1,6−D−グルカンおよびその用途 |
| JP2006137719A (ja) * | 2004-11-12 | 2006-06-01 | Daiso Co Ltd | β−1,3−1,6−D−グルカンを用いた腸管免疫活性化剤 |
| JP2007267718A (ja) * | 2006-03-31 | 2007-10-18 | Daiso Co Ltd | 精製β−D−グルカンの製造方法 |
| JP2011503161A (ja) * | 2007-11-13 | 2011-01-27 | バイオテック・ファルマコン・アーエスアー | 腸管の炎症性疾患を処置または予防する方法 |
-
2008
- 2008-10-09 JP JP2008262823A patent/JP5320965B2/ja active Active
Patent Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS61146192A (ja) * | 1984-12-17 | 1986-07-03 | Satoshi Shinohara | フラクトオリゴ糖とβ―1.3―1.6グルカンを主成分とする飲食物の製造方法 |
| JPH11501691A (ja) * | 1995-03-13 | 1999-02-09 | ノボゲン リサーチ ピーティーワイ.リミテッド. | グルカンの製造方法、及びグルカンの治療用途 |
| JP2001506129A (ja) * | 1996-12-19 | 2001-05-15 | ザ、ユニバーシティ、オブ、ニュー、サウス、ウェイルズ | プレバイオテックスおよびプロバイオテックス |
| JP2005307150A (ja) * | 2004-03-26 | 2005-11-04 | Asahi Denka Kogyo Kk | βグルカン |
| JP2006104439A (ja) * | 2004-03-29 | 2006-04-20 | Daiso Co Ltd | β−1,3−1,6−D−グルカンおよびその用途 |
| JP2006028307A (ja) * | 2004-07-14 | 2006-02-02 | Asahi Denka Kogyo Kk | βグルカン |
| JP2006137719A (ja) * | 2004-11-12 | 2006-06-01 | Daiso Co Ltd | β−1,3−1,6−D−グルカンを用いた腸管免疫活性化剤 |
| JP2007267718A (ja) * | 2006-03-31 | 2007-10-18 | Daiso Co Ltd | 精製β−D−グルカンの製造方法 |
| JP2011503161A (ja) * | 2007-11-13 | 2011-01-27 | バイオテック・ファルマコン・アーエスアー | 腸管の炎症性疾患を処置または予防する方法 |
Non-Patent Citations (3)
| Title |
|---|
| JPN6011016580; FUJII,N. et al: 'Polysaccharide product of Aureobasidium pullulans FERM-P4257. Part 7. Effects of polysaccharide cult' Miyazaki Daigaku Nogakubu Kenkyu Hokoku Vol.39, No.1, 1992, p.57-61 * |
| JPN6013016310; 機能性食品と薬理栄養 1(4), 2003, pp.201-206 * |
| JPN6013016315; Biotherapy 21(4), 2007, pp.265-273 * |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013095702A (ja) * | 2011-11-01 | 2013-05-20 | Daiso Co Ltd | β−1,3−グルカンを含む過敏性腸症候群の下痢抑制剤、腹痛改善剤、及び大腸における痛覚過敏改善剤 |
| JP2017522308A (ja) * | 2014-07-21 | 2017-08-10 | ネステク ソシエテ アノニム | 安全な嚥下を促進する嚥下障害者用栄養製品 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP5320965B2 (ja) | 2013-10-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US8686053B2 (en) | Alginic acid with low molecular weight, its salts, uses, preparative methods, pharmaceutical compositions and foods | |
| EP2222311B1 (en) | Liquid nucleotides/nucleosides-containing product | |
| Torres et al. | Fucoidans: The importance of processing on their anti-tumoral properties | |
| JP5585769B2 (ja) | 腸管免疫賦活能を有する乳酸菌に対する効果促進剤 | |
| JP5740072B2 (ja) | β−1,3−1,6−D−グルカンを用いたストレス緩和剤 | |
| JP4369258B2 (ja) | 免疫賦活剤 | |
| JP5320965B2 (ja) | β−1,3−1,6−D−グルカンを用いた消化管粘膜保護剤または下痢抑制剤 | |
| JP4967420B2 (ja) | β−1,3−1,6−D−グルカンを用いた便秘の予防又は改善剤 | |
| JP2010111646A (ja) | 潰瘍性大腸炎治療剤 | |
| JP4974453B2 (ja) | β−1,3−1,6−D−グルカンを用いた腸管免疫活性化剤 | |
| JP2012051830A (ja) | 胃粘膜保護剤 | |
| KR101915715B1 (ko) | 면역기능 증진 활성이 있는 당근박 유래 다당 분획물 및 이의 제조방법 | |
| KR20150093640A (ko) | 미토콘드리아 활성화를 위한 조성물 | |
| JP6257031B2 (ja) | 尿路感染症の予防又は治療 | |
| JP4975947B2 (ja) | 健康飲料 | |
| JP2003048839A (ja) | 免疫反応性NO合成を誘導するiNOS酵素を刺激する組成剤およびその製造方法 | |
| JP5928774B2 (ja) | β−1,3−グルカンを含む過敏性腸症候群の下痢抑制剤、腹痛改善剤、及び大腸における痛覚過敏改善剤 | |
| JP2009120502A (ja) | キトサン含有組成物 | |
| JP2009298768A (ja) | β−1,3−1,6−D−グルカンを用いたメタボリックシンドローム改善剤 | |
| JP2006206474A (ja) | 機能性食品及び医薬 | |
| US20120129803A1 (en) | Composition containing chitooligosaccharide for recovering from fatigue | |
| EP4097126A1 (en) | Compositions comprising pig stomach mucins and uses thereof | |
| Kazemi et al. | Evaluation the effect of royal jelly on the growth of two members of gut microbiota; Bacteroides fragillis and Bacteroides thetaiotaomicron. | |
| JP2018002620A (ja) | 骨吸収抑制剤 | |
| KR101905009B1 (ko) | 면역기능 증진 활성이 있는 케일박 유래 다당 분획물 및 이의 제조방법 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20110531 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130409 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130530 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20130618 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20130701 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5320965 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| S533 | Written request for registration of change of name |
Free format text: JAPANESE INTERMEDIATE CODE: R313533 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |