JP2007016020A - 経皮吸収製剤 - Google Patents
経皮吸収製剤 Download PDFInfo
- Publication number
- JP2007016020A JP2007016020A JP2006156586A JP2006156586A JP2007016020A JP 2007016020 A JP2007016020 A JP 2007016020A JP 2006156586 A JP2006156586 A JP 2006156586A JP 2006156586 A JP2006156586 A JP 2006156586A JP 2007016020 A JP2007016020 A JP 2007016020A
- Authority
- JP
- Japan
- Prior art keywords
- parts
- drug
- sensitive adhesive
- chloride
- pressure
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Landscapes
- Medicinal Preparation (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Abstract
【解決手段】セレギリン及び塩酸セレギリンを除く薬物、金属塩化物並びに粘着剤を含有し、架橋処理が施されてなる粘着剤層が、支持体の少なくとも片面に形成されてなる経皮吸収製剤。
【選択図】なし
Description
すなわち、本発明は以下の通りである。
(1)セレギリン及び塩酸セレギリンを除く薬物、金属塩化物並びに粘着剤を含有し、架橋処理が施されてなる粘着剤層が、支持体の少なくとも片面に形成されてなる経皮吸収製剤。
(2)架橋処理が金属キレート化合物によって施されてなる、(1)記載の経皮吸収製剤。
(3)薬物が塩基性薬物である、(1)または(2)記載の経皮吸収製剤。
(4)粘着剤がアクリル系重合体を含むアクリル系粘着剤である(1)〜(3)のいずれか1つに記載の経皮吸収製剤。
(5)金属塩化物が、塩化ナトリウム、塩化カルシウム、塩化アルミニウム、塩化第一スズ、および塩化第二鉄から選ばれる少なくとも1つの無機金属塩化物である、(1)〜(4)のいずれか1つに記載の経皮吸収製剤。
(6)金属塩化物が塩化ナトリウムである、(1)〜(4)のいずれか1つに記載の経皮吸収製剤。
(7)金属塩化物が薬物の塩酸塩を塩基性化合物で中和して生じさせた塩である、(1)〜(6)のいずれか1つに記載の経皮吸収製剤。
(8)粘着剤層が、液状可塑剤をさらに含有する(1)〜(7)のいずれか1つに記載の経皮吸収製剤。
(9)液状可塑剤が、炭素数12〜16の高級脂肪酸と炭素数1〜4の低級1価アルコールからなる脂肪酸エステルである、(8)記載の経皮吸収製剤。
本発明の経皮吸収製剤は、セレギリン及び塩酸セレギリンを除く薬物、金属塩化物並びに粘着剤を含み、架橋処理が施されてなる粘着剤層が、支持体の少なくとも片面に形成されてなる経皮吸収製剤である。
液状可塑剤は、それ自体室温で液状であり、可塑化作用を示し、上記の粘着性ポリマーと相溶するものであれば特に限定されない。液状可塑剤は、薬物の経皮吸収性、保存安定性を向上させるものが好ましく、粘着剤中への薬物溶解性等をさらに高める目的でも配合することができる。薬物の経皮吸収性、保存安定性を向上させるという観点では、通常、ミリスチン酸イソプロピル、ラウリン酸エチル、パルミチン酸イソプロピル等の炭素数12〜16の高級脂肪酸と炭素数1〜4の低級1価アルコールからなる脂肪酸エステル;炭素数8〜10の脂肪酸;エチレングリコール、ジエチレングリコール、トリエチレングリコール、ポリエチレングリコール、プロピレングリコール、ポリプロピレングリコール等のグリコール類;オリーブ油、ヒマシ油、スクアレン、ラノリン等の油脂類;酢酸エチル、エチルアルコール、ジメチルデシルスルホキシド、デシルメチルスルホキシド、ジメチルスルホキシド、ジメチルホルムアミド、ジメチルアセトアミド、ジメチルラウリルアミド、ドデシルピロリドン、イソソルビトール、オレイルアルコール、ラウリン酸等の有機溶剤;液状の界面活性剤;ジイソプロピルアジペート、フタル酸エステル、ジエチルセバケート等の従来より公知の可塑剤;流動パラフィン等の炭化水素類;その他、エトキシ化ステアリルアルコール、グリセリンエステル(室温で液状の物)、ミリスチン酸イソトリデシル、N−メチルピロリドン、オレイン酸エチル、オレイン酸、アジピン酸ジイソプロピル、パルミチン酸オクチル、1、3−プロパンジオール、グリセリン等が挙げられる。これらの中から常温で液状のものが使用される。また、これらの液状可塑剤は単独でまたは2種以上の組み合わせで使用される。
該脂肪酸エステルの炭素数12〜16の高級脂肪酸は飽和及び不飽和脂肪酸を包含するが、飽和脂肪酸が好ましく、また炭素数1〜4の低級1価アルコールは直鎖でも分岐鎖でもよい。炭素数12〜16の高級脂肪酸の好適な例としては、ラウリン酸(C12)、ミリスチン酸(C14)、パルミチン酸(C16)が挙げられ、炭素数1〜4の低級1価アルコールの好適な例としては、イソプロピルアルコール、エチルアルコール、メチルアルコール、プロピルアルコール等が挙げられる。これらのうち、好適な脂肪酸エステルとしては、ミリスチン酸イソプロピルが例示される。
なお、薬物を、粘着剤(例えばアクリル系共重合体粘着剤等)、架橋剤、並びに必要に応じて液状可塑剤やその他の添加剤等と共に、溶媒または分散媒に溶解または分散して、薬物含有溶液を調製した後、得られた溶液に金属塩化物を混合攪拌し、支持体の片面もしくは剥離シートの剥離処理面に塗布し、乾燥して粘着剤層を形成し、その後、剥離シートもしくは支持体を貼り合わせてもよい。
(アクリル系共重合体粘着剤Aの調製)
不活性ガス雰囲気下、アクリル酸2−エチルへキシル75部、N−ビニル−2−ピロリドン22部、アクリル酸3部およびアゾビスイソブチロニトリル0.2部を酢酸エチル中60℃にて溶液重合させてアクリル系共重合体粘着剤Aの溶液を調製した。
(アクリル系共重合体粘着剤Bの調製)
不活性ガス雰囲気下、アクリル酸2−エチルへキシル95部、アクリル酸5部および過酸化ベンゾイル0.2部を酢酸エチル中60℃にて溶液重合させてアクリル系共重合体粘着剤Bの溶液を調製した。
アクリル系共重合体粘着剤A49部、ミリスチン酸イソプロピル40部、ガロパミル10部を容器中で均一になるように混合攪拌を行った。その後エタノールに分散した塩化ナトリウム1部を先のアクリル系共重合体粘着剤A溶液に添加、攪拌を行い、エチルアセトアセテートアルミニウムジイソプロピレート0.3部(粘着剤固形分に対して)を添加、酢酸エチルで粘度を調整し、ポリエステルフィルム(75μm厚)に乾燥後の厚みが80μmになるように調整を行い、乾燥してポリエステルフィルム(12μm厚)に貼りあわせた後、70℃で48時間エージング処理を行い、ガロパミルの経皮吸収製剤を得た。
アクリル系共重合体粘着剤A47部、ミリスチン酸イソプロピル40部、ガロパミル10部を容器中で均一になるように混合攪拌を行った。その後エタノールに分散した塩化ナトリウム3部を先のアクリル系共重合体粘着剤A溶液に添加、攪拌を行い、エチルアセトアセテートアルミニウムジイソプロピレート0.3部(粘着剤固形分に対して)を添加、酢酸エチルで粘度を調整し、実施例1と同様の操作を行いガロパミルの経皮吸収製剤を得た。
アクリル系共重合体粘着剤A45部、ミリスチン酸イソプロピル40部、ガロパミル10部を容器中で均一になるように混合攪拌を行った。その後エタノールに分散した塩化ナトリウム5部を先のアクリル系共重合体粘着剤A溶液に添加、攪拌を行い、エチルアセトアセテートアルミニウムジイソプロピレート0.3部(粘着剤固形分に対して)を添加、酢酸エチルで粘度を調整し、実施例1と同様の操作を行いガロパミルの経皮吸収製剤を得た。
アクリル系共重合体粘着剤A48.42部、ミリスチン酸イソプロピル40部を容器中で均一になるように混合攪拌を行い、別な容器で、塩酸ガロパミル10.75部、エタノールに溶解した水酸化ナトリウム(10重量%)0.83部を混合攪拌し生成した塩化ナトリウムとガロパミルフリー体を先のアクリル系共重合体粘着剤A溶液に添加、攪拌を行い、エチルアセトアセテートアルミニウムジイソプロピレート0.3部(粘着剤固形分に対して)を添加、酢酸エチルで粘度を調整し、ポリエステルフィルム(75μm厚)に乾燥後の厚みが80μmになるように調整を行い、乾燥してポリエステルフィルム(12μm厚)に貼りあわせた後、70℃で48時間エージング処理を行い、ガロパミルの経皮吸収製剤を得た。
アクリル系共重合体粘着剤A36.84部、ミリスチン酸イソプロピル40部を容器中で均一になるように混合攪拌を行い、別な容器で、塩酸ガロパミル21.5部、エタノールに溶解した水酸化ナトリウム(10重量%)1.66部を混合攪拌し生成した塩化ナトリウムとガロパミルフリー体を先のアクリル系共重合体粘着剤A溶液に添加、攪拌を行い、エチルアセトアセテートアルミニウムジイソプロピレート0.3部(粘着剤固形分に対して)を添加、酢酸エチルで粘度を調整し、ポリエステルフィルム(75μm厚)に乾燥後の厚みが80μmになるように調整を行い、乾燥してポリエステルフィルム(12μm厚)に貼りあわせた後、70℃で48時間エージング処理を行い、ガロパミルの経皮吸収製剤を得た。
アクリル系共重合体粘着剤B47部、ミリスチン酸イソプロピル40部、ガロパミル10部を容器中で均一になるように混合攪拌を行った。その後エタノールに分散した塩化ナトリウム3部を先のアクリル系共重合体粘着剤B溶液に添加、攪拌を行い、エチルアセトアセテートアルミニウムジイソプロピレート0.3部(粘着剤固形分に対して)を添加、酢酸エチルで粘度を調整し、実施例1と同様の操作を行いガロパミルの経皮吸収製剤を得た。
アクリル系共重合体粘着剤A48.16部、ミリスチン酸イソプロピル40部を容器中で均一になるように混合攪拌を行い、別な容器で、塩酸ジルチアゼム10.88部、エタノールに溶解した水酸化ナトリウム(10重量%)0.96部を混合攪拌し生成した塩化ナトリウムとジルチアゼムフリー体を先のアクリル系共重合体粘着剤A溶液に添加、攪拌を行い、エチルアセトアセテートアルミニウムジイソプロピレート0.3部(粘着剤固形分に対して)を添加、酢酸エチルで粘度を調整し、ポリエステルフィルム(75μm厚)に乾燥後の厚みが80μmになるように調整を行い、乾燥してポリエステルフィルム(12μm厚)に貼りあわせた後、70℃で48時間エージング処理を行い、ジルチアゼムの経皮吸収製剤を得た。
アクリル系共重合体粘着剤A51部、ミリスチン酸イソプロピル40部、ガロパミル4部、グリセリン5部を容器中で均一になるように混合攪拌を行い、エチルアセトアセテートアルミニウムジイソプロピレート0.3部(粘着剤固形分に対して)を添加、酢酸エチルで粘度を調整し、実施例1と同様の操作を行いガロパミルの経皮吸収製剤を得た。
アクリル系共重合体粘着剤A50部、ミリスチン酸イソプロピル40部、ガロパミル10部を容器中で均一になるように混合攪拌を行い、エチルアセトアセテートアルミニウムジイソプロピレート0.3部(粘着剤固形分に対して)を添加、酢酸エチルで粘度を調整し、実施例1と同様の操作を行いガロパミルの経皮吸収製剤を得た。
アクリル系共重合体粘着剤A45部、ミリスチン酸イソプロピル40部、ガロパミル10部、グリセリン5部を容器中で均一になるように混合攪拌を行い、エチルアセトアセテートアルミニウムジイソプロピレート0.3部(粘着剤固形分に対して)を添加、酢酸エチルで粘度を調整し、実施例1と同様の操作を行いガロパミルの経皮吸収製剤を得た。
アクリル系共重合体粘着剤B50部、ミリスチン酸イソプロピル40部、ガロパミル10部を容器中で均一になるように混合攪拌を行い、エチルアセトアセテートアルミニウムジイソプロピレート0.3部(粘着剤固形分に対して)を添加、酢酸エチルで粘度を調整し、実施例1と同様の操作を行いガロパミルの経皮吸収製剤を得た。
アクリル系共重合体粘着剤B45部、ミリスチン酸イソプロピル40部、ガロパミル10部、グリセリン5部を容器中で均一になるように混合攪拌を行い、エチルアセトアセテートアルミニウムジイソプロピレート0.3部(粘着剤固形分に対して)を添加、酢酸エチルで粘度を調整し、実施例1と同様の操作を行いガロパミルの経皮吸収製剤を得た。
アクリル系共重合体粘着剤A43.5部、ミリスチン酸イソプロピル40部、グリセリン3部を容器中で均一になるように混合攪拌を行い、別な容器で、塩酸ガロパミル10.75部、ジイソプロパノールアミン2.75部(いずれも2−プロパノール溶液で10wt%に調整)を混合攪拌し、その後先のアクリル系共重合体粘着剤A溶液に添加、攪拌を行い、エチルアセトアセテートアルミニウムジイソプロピレート0.3部(粘着剤固形分に対して)を添加、酢酸エチルで粘度を調整し、実施例1と同様の操作を行いガロパミルの経皮吸収製剤を得た。
アクリル系共重合体粘着剤A30部、ミリスチン酸イソプロピル40部、グリセリン3部を容器中で均一になるように混合攪拌を行い、別な容器で、塩酸ガロパミル21.5部、ジイソプロパノールアミン5.5部(いずれも2−プロパノール溶液で10wt%に調整)を混合攪拌し、その後先のアクリル系共重合体粘着剤A溶液に添加、攪拌を行い、エチルアセトアセテートアルミニウムジイソプロピレート0.3部(粘着剤固形分に対して)を添加、酢酸エチルで粘度を調整し、実施例1と同様の操作を行いガロパミルの経皮吸収製剤を得た。
アクリル系共重合体粘着剤A42.99部、ミリスチン酸イソプロピル40部、グリセリン5部を容器中で均一になるように混合攪拌を行い、別な容器で、塩酸ガロパミル10.75部、モノエタノールアミン1.26部(いずれも2−プロパノール溶液で10wt%に調整)を混合攪拌し、その後先のアクリル系共重合体粘着剤A溶液に添加、攪拌を行い、エチルアセトアセテートアルミニウムジイソプロピレート0.3部(粘着剤固形分に対して)を添加、酢酸エチルで粘度を調整し、実施例1と同様の操作を行いガロパミルの経皮吸収製剤を得た。
アクリル系共重合体粘着剤B42.99部、ミリスチン酸イソプロピル40部、グリセリン5部を容器中で均一になるように混合攪拌を行い、別な容器で、塩酸ガロパミル10.75部、モノエタノールアミン1.26部(いずれも2−プロパノール溶液で10wt%に調整)を混合攪拌し、その後先のアクリル系共重合体粘着剤B溶液に添加、攪拌を行い、エチルアセトアセテートアルミニウムジイソプロピレート0.3部(粘着剤固形分に対して)を添加、酢酸エチルで粘度を調整し、実施例1と同様の操作を行いガロパミルの経皮吸収製剤を得た。
アクリル系共重合体粘着剤A45部、ミリスチン酸イソプロピル40部、ジルチアゼム10部、グリセリン5部を容器中で均一になるように混合攪拌を行い、エチルアセトアセテートアルミニウムジイソプロピレート0.3部(粘着剤固形分に対して)を添加、酢酸エチルで粘度を調整し、実施例1と同様の操作を行いジルチアゼムの経皮吸収製剤を得た。
上記各実施例および各比較例にて作製したガロパミル、ジルチアゼム経皮吸収製剤について、以下に示すゲル分率測定実験、及び浸漬試験を行った。
実験例1(ゲル分率測定試験)
製剤内に残存する酢酸エチルに不溶なゲル成分の割合を次の方法を用いて求めた。
得られた製剤を25cm2(5cm×5cm)に打ち抜き、2枚を予め重量を測定した多孔性テトラフルオロエチレンフィルム(20cm×10cm)(基材)に貼付した。内容物がこぼれない様に折りたたみ、重量を測定した。これをビーカーに入れ、2種類の溶媒(タイプ1:酢酸エチル、タイプ2:0.4wt%乳酸入り酢酸エチル)にて、基材が完全に漬かるまで加えた。その翌日に中の溶液を捨て、前日と同じ組成の溶媒を添加し、1日ごとに交換し、3回交換後ビーカー中の溶液を捨て、乾燥後、重量を測定した。ゲル分率は以下の式にて算出する。
実際の皮膚に貼付された場合を想定し、粘着剤層の凝集力を次の方法で評価した。
得られた製剤を約10cm2(3.16cm×3.16cm)に打ち抜いた。0.4wt%乳酸を含む生理食塩水をガラス製シャーレに5mL添加し、そこに打ち抜かれた製剤を、セパレーターを剥がし粘着面が下になるように浸漬した(浮かせた)。浸漬24時間後にその製剤を取り出し、表面を乾燥させた後、指で触ることにより評価した。
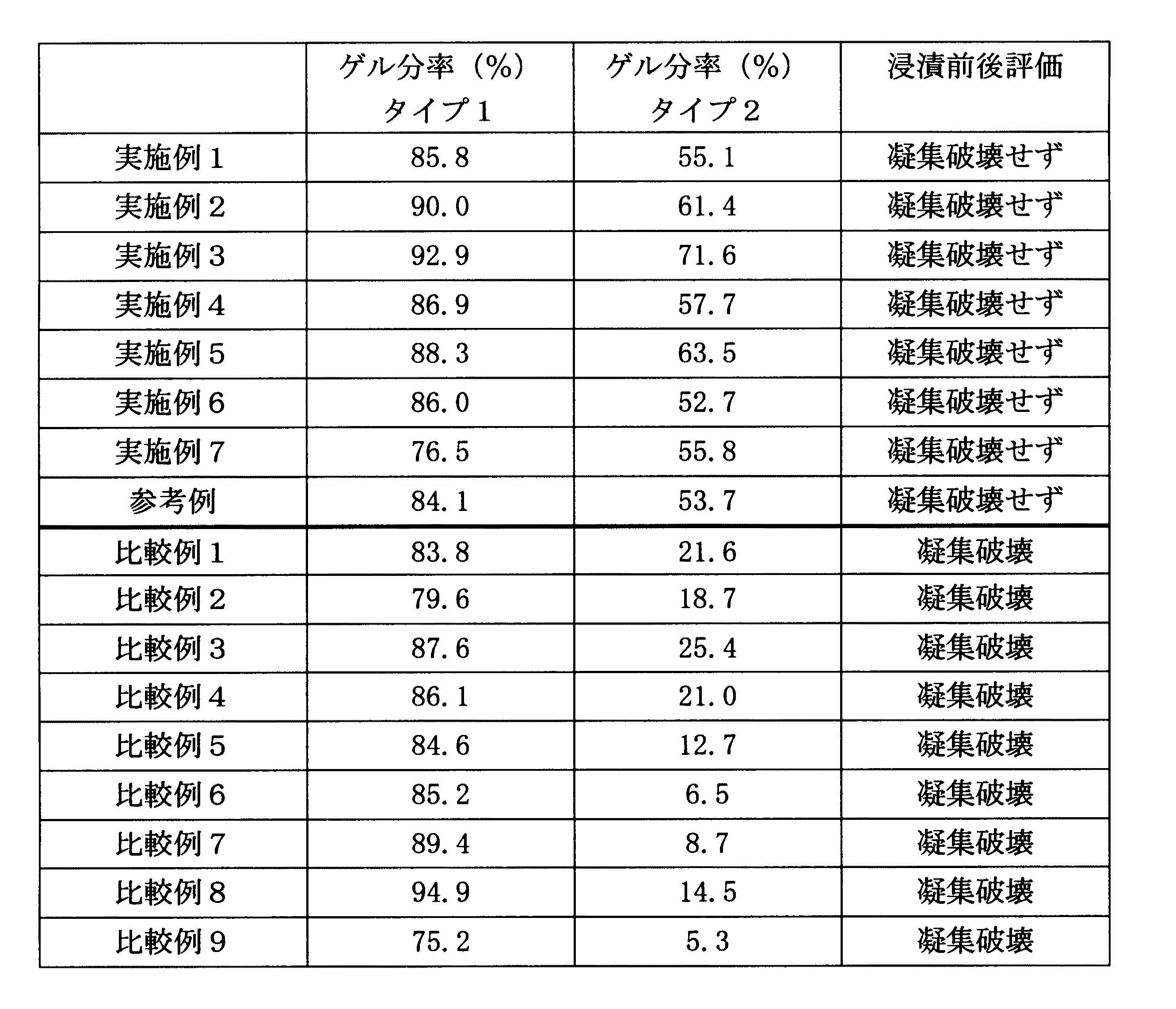
実験例1および2の結果を表1に示した。
参考例の様に、塩基性薬物の濃度が比較的低い場合はグリセリンによる効果も確認されるが、これに対して、塩基性薬物の濃度が倍以上になると(比較例1〜4)、もはやグリセリンによる効果も利用できずに凝集破壊することが確認された。
グリセリンは添加されているが、塩化ナトリウムのない比較例2、4についてもその値が顕著に低下し、また凝集破壊を引き起こすことも解った。
水酸化ナトリウムではなく、塩基性化合物に有機アミンを添加した場合の比較例5〜8の値についても、先の比較例と同様に、タイプ2の場合のゲル分率の値が顕著に低下し、また凝集破壊を引き起こすことが確認された。
塩基性薬物の濃度が高い場合、実施例4、5の場合では濃度の増加と共に生成する塩化ナトリウムの量も増加し、さらに凝集力の高い粘着剤層が形成されることに反して、比較例6では薬物濃度の増加に伴い、タイプ2でのゲル分率も低下し、凝集破壊を抑制できないことが確認された。
実施例7および比較例9の結果から、塩酸塩を有する塩基性薬物には有効であることが確認された。
Claims (9)
- セレギリン及び塩酸セレギリンを除く薬物、金属塩化物並びに粘着剤を含有し、架橋処理が施されてなる粘着剤層が、支持体の少なくとも片面に形成されてなる経皮吸収製剤。
- 架橋処理が金属キレート化合物によって施されてなる、請求項1に記載の経皮吸収製剤。
- 薬物が塩基性薬物である、請求項1または2に記載の経皮吸収製剤。
- 粘着剤がアクリル系重合体を含むアクリル系粘着剤である、請求項1〜3のいずれか1項に記載の経皮吸収製剤。
- 金属塩化物が、塩化ナトリウム、塩化カルシウム、塩化アルミニウム、塩化第一スズ、および塩化第二鉄から選ばれる少なくとも1つの金属塩化物である、請求項1〜4のいずれか1項に記載の経皮吸収製剤。
- 金属塩化物が塩化ナトリウムである、請求項1〜4のいずれか1項に記載の経皮吸収製剤。
- 金属塩化物が、薬物の塩酸塩を塩基性化合物で中和して生じさせた塩である、請求項1〜6のいずれか1項に記載の経皮吸収製剤。
- 粘着剤層が、液状可塑剤をさらに含有する請求項1〜7のいずれか1項に記載の経皮吸収製剤。
- 液状可塑剤が、炭素数12〜16の高級脂肪酸と炭素数1〜4の低級1価アルコールからなる脂肪酸エステルである、請求項8に記載の経皮吸収製剤。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2006156586A JP5025998B2 (ja) | 2005-06-06 | 2006-06-05 | 経皮吸収製剤 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2005165213 | 2005-06-06 | ||
| JP2005165213 | 2005-06-06 | ||
| JP2006156586A JP5025998B2 (ja) | 2005-06-06 | 2006-06-05 | 経皮吸収製剤 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2007016020A true JP2007016020A (ja) | 2007-01-25 |
| JP5025998B2 JP5025998B2 (ja) | 2012-09-12 |
Family
ID=37753488
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2006156586A Expired - Fee Related JP5025998B2 (ja) | 2005-06-06 | 2006-06-05 | 経皮吸収製剤 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP5025998B2 (ja) |
Cited By (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2009107479A1 (ja) * | 2008-02-27 | 2009-09-03 | 久光製薬株式会社 | 貼付製剤 |
| WO2009107478A1 (ja) | 2008-02-27 | 2009-09-03 | 久光製薬株式会社 | 貼付剤及び包装体 |
| JP2010111598A (ja) * | 2008-11-04 | 2010-05-20 | Nitto Denko Corp | 貼付剤及び貼付製剤 |
| JP5421252B2 (ja) * | 2008-05-30 | 2014-02-19 | エーザイ・アール・アンド・ディー・マネジメント株式会社 | 経皮吸収製剤 |
| JP5615899B2 (ja) * | 2010-02-24 | 2014-10-29 | 久光製薬株式会社 | 経皮吸収製剤 |
| JP5615898B2 (ja) * | 2010-02-24 | 2014-10-29 | 久光製薬株式会社 | 貼付剤 |
Citations (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH01178566A (ja) * | 1987-12-29 | 1989-07-14 | Nippon Synthetic Chem Ind Co Ltd:The | 感圧性接着剤組成物 |
| JPH04178323A (ja) * | 1990-11-09 | 1992-06-25 | Teikoku Seiyaku Co Ltd | 経皮投与製剤 |
| JPH08291056A (ja) * | 1995-04-25 | 1996-11-05 | Sekisui Chem Co Ltd | 貼付剤 |
| JPH09132525A (ja) * | 1995-11-08 | 1997-05-20 | Nippon Carbide Ind Co Inc | 医療用粘着剤組成物 |
| JPH1160475A (ja) * | 1997-06-26 | 1999-03-02 | Verteq Inc | 高可塑薬剤の経皮配給用接着剤混合物 |
| JPH11209271A (ja) * | 1998-01-23 | 1999-08-03 | Nitto Denko Corp | 経皮吸収製剤 |
| JPH11209270A (ja) * | 1998-01-22 | 1999-08-03 | Nitto Denko Corp | 経皮吸収製剤 |
| JP2000355535A (ja) * | 1999-04-13 | 2000-12-26 | Nitto Denko Corp | 経皮吸収型製剤 |
| JP2002509878A (ja) * | 1998-03-30 | 2002-04-02 | エルティエス ローマン テラピー−ズュステーメ アーゲー | パーキンソン症候群の治療のためのd2−アゴニスト含有経皮吸収治療システムおよびその製造方法 |
| JP2002258044A (ja) * | 2001-03-02 | 2002-09-11 | Nitto Denko Corp | 粘着型光学フィルムおよび光学フィルム用粘着剤 |
| JP2003155252A (ja) * | 2001-11-19 | 2003-05-27 | Toagosei Co Ltd | パップ剤基剤 |
| WO2004078165A1 (ja) * | 2003-03-07 | 2004-09-16 | Toagosei Co., Ltd. | 貼付剤用基剤及びそれを用いた貼付剤 |
-
2006
- 2006-06-05 JP JP2006156586A patent/JP5025998B2/ja not_active Expired - Fee Related
Patent Citations (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH01178566A (ja) * | 1987-12-29 | 1989-07-14 | Nippon Synthetic Chem Ind Co Ltd:The | 感圧性接着剤組成物 |
| JPH04178323A (ja) * | 1990-11-09 | 1992-06-25 | Teikoku Seiyaku Co Ltd | 経皮投与製剤 |
| JPH08291056A (ja) * | 1995-04-25 | 1996-11-05 | Sekisui Chem Co Ltd | 貼付剤 |
| JPH09132525A (ja) * | 1995-11-08 | 1997-05-20 | Nippon Carbide Ind Co Inc | 医療用粘着剤組成物 |
| JPH1160475A (ja) * | 1997-06-26 | 1999-03-02 | Verteq Inc | 高可塑薬剤の経皮配給用接着剤混合物 |
| JPH11209270A (ja) * | 1998-01-22 | 1999-08-03 | Nitto Denko Corp | 経皮吸収製剤 |
| JPH11209271A (ja) * | 1998-01-23 | 1999-08-03 | Nitto Denko Corp | 経皮吸収製剤 |
| JP2002509878A (ja) * | 1998-03-30 | 2002-04-02 | エルティエス ローマン テラピー−ズュステーメ アーゲー | パーキンソン症候群の治療のためのd2−アゴニスト含有経皮吸収治療システムおよびその製造方法 |
| JP2000355535A (ja) * | 1999-04-13 | 2000-12-26 | Nitto Denko Corp | 経皮吸収型製剤 |
| JP2002258044A (ja) * | 2001-03-02 | 2002-09-11 | Nitto Denko Corp | 粘着型光学フィルムおよび光学フィルム用粘着剤 |
| JP2003155252A (ja) * | 2001-11-19 | 2003-05-27 | Toagosei Co Ltd | パップ剤基剤 |
| WO2004078165A1 (ja) * | 2003-03-07 | 2004-09-16 | Toagosei Co., Ltd. | 貼付剤用基剤及びそれを用いた貼付剤 |
Cited By (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9155725B2 (en) | 2008-02-27 | 2015-10-13 | Hisamitsu Pharmaceutical Co., Inc. | Adhesive skin patch and packaged product |
| WO2009107478A1 (ja) | 2008-02-27 | 2009-09-03 | 久光製薬株式会社 | 貼付剤及び包装体 |
| WO2009107476A1 (ja) | 2008-02-27 | 2009-09-03 | 久光製薬株式会社 | 貼付製剤 |
| WO2009107477A1 (ja) | 2008-02-27 | 2009-09-03 | 久光製薬株式会社 | 貼付製剤 |
| WO2009107479A1 (ja) * | 2008-02-27 | 2009-09-03 | 久光製薬株式会社 | 貼付製剤 |
| JPWO2009107478A1 (ja) * | 2008-02-27 | 2011-06-30 | 久光製薬株式会社 | 貼付剤及び包装体 |
| US8580281B2 (en) | 2008-02-27 | 2013-11-12 | Hisamitsu Pharmaceutical Co., Inc. | Medicated patch |
| JP5485135B2 (ja) * | 2008-02-27 | 2014-05-07 | 久光製薬株式会社 | 貼付製剤 |
| JP5546013B2 (ja) * | 2008-02-27 | 2014-07-09 | 久光製薬株式会社 | 貼付剤及び包装体 |
| US8871249B2 (en) | 2008-02-27 | 2014-10-28 | Hisamitso Pharmaceutical Co., Inc. | Medicated patch |
| JP6054013B2 (ja) * | 2008-02-27 | 2016-12-27 | 久光製薬株式会社 | 貼付製剤 |
| JP5421252B2 (ja) * | 2008-05-30 | 2014-02-19 | エーザイ・アール・アンド・ディー・マネジメント株式会社 | 経皮吸収製剤 |
| JP2010111598A (ja) * | 2008-11-04 | 2010-05-20 | Nitto Denko Corp | 貼付剤及び貼付製剤 |
| JP5615898B2 (ja) * | 2010-02-24 | 2014-10-29 | 久光製薬株式会社 | 貼付剤 |
| US9370495B2 (en) | 2010-02-24 | 2016-06-21 | Hisamitsu Pharmaceutical Co., Inc. | Adhesive patch |
| JP5615899B2 (ja) * | 2010-02-24 | 2014-10-29 | 久光製薬株式会社 | 経皮吸収製剤 |
| US9707188B2 (en) | 2010-02-24 | 2017-07-18 | Hisamitsu Pharmaceutical Co., Inc. | Transdermal preparation |
Also Published As
| Publication number | Publication date |
|---|---|
| JP5025998B2 (ja) | 2012-09-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5237112B2 (ja) | 経皮吸収製剤 | |
| JP4999366B2 (ja) | 経皮吸収製剤 | |
| JP5037523B2 (ja) | ドネペジル含有貼付製剤の着色を抑制する方法、およびドネペジルの類縁物質の生成量を低減する方法 | |
| JP5547784B2 (ja) | 安定化されたドネペジル含有貼付製剤 | |
| CA2549516C (en) | Percutaneous absorption-type pharmaceutical preparation | |
| JP5421252B2 (ja) | 経皮吸収製剤 | |
| JP5025998B2 (ja) | 経皮吸収製剤 | |
| RU2432179C2 (ru) | Фармацевтический препарат абсорбционного типа для чрезкожного введения | |
| TWI415636B (zh) | Bisoprolol transdermal device | |
| JP5623102B2 (ja) | セレギリン含有貼付製剤 | |
| JP5037522B2 (ja) | 安定化されたドネペジル含有貼付製剤 | |
| JP2008239603A (ja) | 薬物含有貼付製剤 | |
| JP5281973B2 (ja) | ビソプロロール含有貼付剤 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20081110 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20111014 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20111018 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20111216 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120403 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120530 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20120619 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20120620 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20150629 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 Ref document number: 5025998 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |