JP2006101875A - L−グルタミン酸生産菌及びl−グルタミン酸の製造方法 - Google Patents
L−グルタミン酸生産菌及びl−グルタミン酸の製造方法 Download PDFInfo
- Publication number
- JP2006101875A JP2006101875A JP2005262178A JP2005262178A JP2006101875A JP 2006101875 A JP2006101875 A JP 2006101875A JP 2005262178 A JP2005262178 A JP 2005262178A JP 2005262178 A JP2005262178 A JP 2005262178A JP 2006101875 A JP2006101875 A JP 2006101875A
- Authority
- JP
- Japan
- Prior art keywords
- amino acid
- seq
- gene
- mutation
- acid sequence
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N1/00—Microorganisms, e.g. protozoa; Compositions thereof; Processes of propagating, maintaining or preserving microorganisms or compositions thereof; Processes of preparing or isolating a composition containing a microorganism; Culture media therefor
- C12N1/20—Bacteria; Culture media therefor
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/0004—Oxidoreductases (1.)
- C12N9/0008—Oxidoreductases (1.) acting on the aldehyde or oxo group of donors (1.2)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P13/00—Preparation of nitrogen-containing organic compounds
- C12P13/04—Alpha- or beta- amino acids
- C12P13/08—Lysine; Diaminopimelic acid; Threonine; Valine
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P13/00—Preparation of nitrogen-containing organic compounds
- C12P13/04—Alpha- or beta- amino acids
- C12P13/14—Glutamic acid; Glutamine
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Health & Medical Sciences (AREA)
- Genetics & Genomics (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biotechnology (AREA)
- Microbiology (AREA)
- General Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Biochemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Biomedical Technology (AREA)
- Medicinal Chemistry (AREA)
- Molecular Biology (AREA)
- Tropical Medicine & Parasitology (AREA)
- Virology (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Enzymes And Modification Thereof (AREA)
Abstract
【解決手段】L−グルタミン酸生産能を有するコリネ型細菌であって、生育が非改変株または野生株と同等以上であり、かつ染色体上のα−ケトグルタル酸デヒドロゲナーゼのサブユニットをコードするodhA遺伝子のコード領域内、または発現制御領域内に変異が導入されたことにより、菌体内α−ケトグルタル酸デヒドロゲナーゼ活性が、非改変株または野生株の菌体内α−ケトグルタル酸デヒドロゲナーゼ活性の二分の一以下に低下したことを特徴とするコリネ型細菌を培地で培養して、L−グルタミン酸を該培地中又は菌体内に生成蓄積させ、該培地又は菌体よりL−グルタミン酸を回収する。
【選択図】図5
Description
(1)L−グルタミン酸生産能を有するコリネ型細菌であって、生育が非改変株または野生株と同等以上であり、かつ染色体上のα−ケトグルタル酸デヒドロゲナーゼのE1oサブユニットをコードするodhA遺伝子のコード領域内、または発現制御領域内に変異が導入されたことにより、菌体内α−ケトグルタル酸デヒドロゲナーゼ活性が、非改変株または野生株の菌体内α−ケトグルタル酸デヒドロゲナーゼ活性の二分の一以下に低下したこと
を特徴とするコリネ型細菌。
(2)前記odhA遺伝子が以下の(A)〜(D)のいずれかに記載のタンパク質をコードする遺伝子である、(1)のコリネ型細菌:
(A)配列番号10に示すアミノ酸配列を有するタンパク質、
(B)配列番号10に示すアミノ酸配列において1若しくは数個のアミノ酸が置換、欠失、挿入、または付加されたアミノ酸配列を有し、かつα−ケトグルタル酸デヒドロゲナーゼのE1oサブユニット活性を示すタンパク質。
(C)配列番号10に示すアミノ酸配列のアミノ酸番号37〜1257のアミノ酸配列を有するタンパク質、
(D)配列番号10に示すアミノ酸配列のアミノ酸番号37〜1257のアミノ酸配列において1若しくは数個のアミノ酸が置換、欠失、挿入、または付加されたアミノ酸配列を有し、かつα−ケトグルタル酸デヒドロゲナーゼのE1oサブユニット活性を示すタンパク質。
(3)前記数個が2〜20個である、(2)のコリネ型細菌。
(4)前記odhA遺伝子が以下の(a)〜(d)のいずれかに記載の遺伝子である、(1)のコリネ型細菌:
(a)配列番号9に示す塩基配列の塩基番号443〜4213の塩基配列を有する遺伝子、
(b)配列番号9に示す塩基配列の塩基番号443〜4213の塩基配列を有するポリヌクレオチド又は同塩基配列から調製され得るプローブとストリンジェントな条件下でハイブリダイズし、かつα−ケトグルタル酸デヒドロゲナーゼのE1oサブユニット活性を示すタンパク質をコードする遺伝子。
(c)配列番号9に示す塩基配列の塩基番号551〜4213の塩基配列を有する遺伝子、
(d)配列番号9に示す塩基配列の塩基番号551〜4213の塩基配列を有するポリヌクレオチド又は同塩基配列から調製され得るプローブとストリンジェントな条件下でハイブリダイズし、かつα−ケトグルタル酸デヒドロゲナーゼのE1oサブユニット活性を示すタンパク質をコードする遺伝子。
(5)前記変異が前記odhA遺伝子のチアミンピロリン酸結合部位をコードする領域に導入されたことを特徴とする(1)〜(4)のいずれかのコリネ型細菌。
(6)前記変異が、配列番号9に記載の塩基配列において、2534-2548番目の領域に導入されたことを特徴とする、(1)〜(4)のいずれかのコリネ型細菌。
(7)前記変異が、配列番号10に記載のアミノ酸配列において、698−702番目のアミノ酸残基のうちいずれか1以上のアミノ酸残基を欠失させる変異である、(1)〜(4)のいずれかのコリネ型細菌。
(8)前記変異が配列番号10に記載のアミノ酸配列において、698番目のLys残基、699番目のLeu残基、700番目のArg残基, 702のTyr残基から選択される残基を他のアミノ酸に置換する変異である、(1)〜(4)のいずれかのコリネ型細菌。
(9)前記変異が、配列番号9に記載の塩基配列において、1094-1111番目の領域に導入されたことを特徴とする、(1)〜(4)のいずれかのコリネ型細菌。
(10)前記変異が、配列番号10に記載のアミノ酸配列において、218〜224番目のアミノ酸残基のうちの1または2以上のアミノ酸残基を欠失させる変異である、(1)〜(4)のいずれかのコリネ型細菌。
(11)(1)〜(10)のいずれかのコリネ型細菌を培地で培養して、L−グルタミン酸を該培地中又は菌体内に生成蓄積させ、該培地又は菌体からL−グルタミン酸を回収することを特徴とするL−グルタミン酸の製造法。
(12)下記(e)〜(f)のいずれかに記載の遺伝子である、変異型α−ケトグルタル酸デヒドロゲナーゼ遺伝子:
(e)配列番号11、13、もしくは15の塩基番号443〜4213、または配列番号44、46、もしくは48の塩基番号443〜4210に示す塩基配列を有する遺伝子
、
(f)配列番号11、13、もしくは15の塩基番号443〜4213、または配列番号44、46、もしくは48の塩基番号443〜4210に示す塩基配列を有するポリヌクレオチド又は同塩基配列から調製され得るプローブとストリンジェントな条件下でハイブリダイズし、かつ、α−ケトグルタル酸デヒドロゲナーゼのE2o及びE3サブユニットタンパク質と複合体を形成することにより、野生株または非改変株のα−ケトグルタル酸デヒドロゲナーゼ複合体の二分の一以下のα−ケトグルタル酸デヒドロゲナーゼ活性を示すタンパク質をコードする遺伝子。
(g)配列番号11、13、もしくは15の塩基番号551〜4213、または配列番号44、46、もしくは48に示す塩基配列の塩基番号551〜4210の塩基配列を有する遺伝子、又は
(h)配列番号11、13、もしくは15の塩基番号551〜4213、または配列番号44、46、もしくは48に示す塩基配列の塩基番号551〜4210の塩基配列を有するポリヌクレオチド又は同塩基配列から調製され得るプローブとストリンジェントな条件下でハイブリダイズし、かつ、α−ケトグルタル酸デヒドロゲナーゼのE2o及びE3サブユニットタンパク質と複合体を形成することにより、野生株または非改変株のα−ケトグルタル酸デヒドロゲナーゼ複合体の二分の一以下のα−ケトグルタル酸デヒドロゲナーゼ活性を示すタンパク質をコードする遺伝子。
(13)下記(E)〜(H)のいずれかに記載のタンパク質である変異型α−ケトグルタル酸デヒドロゲナーゼ:
(E)配列番号12、14、16、45、47又は49に示すアミノ酸配列を有するタンパク質、
(F)配列番号12、14、16、45、47又は49に示すアミノ酸配列において、1または数個のアミノ酸が置換、欠失、または付加されたアミノ酸配列を有し、かつ、α−ケトグルタル酸デヒドロゲナーゼのE2o及びE3サブユニットタンパク質と複合体を形成することにより、野生株または非改変株のα−ケトグルタル酸デヒドロゲナーゼ複合体の二分の一以下のα−ケトグルタル酸デヒドロゲナーゼ活性を示すタンパク質、
(G)配列番号12、45、47又は49に示すアミノ酸配列のアミノ酸番号37〜1256のアミノ酸配列、配列番号14に示すアミノ酸配列のアミノ酸番号37〜1255のアミノ酸配列、または配列番号16に示すアミノ酸配列のアミノ酸番号37〜1254のアミノ酸配列を有するタンパク質、
(H)配列番号12、45、47又は49に示すアミノ酸配列のアミノ酸番号37〜1256のアミノ酸配列、配列番号14に示すアミノ酸配列のアミノ酸番号37〜1255のアミノ酸配列、または配列番号16に示すアミノ酸配列のアミノ酸番号37〜1254のアミノ酸配列において、1または数個のアミノ酸が置換、欠失、または付加されたアミノ酸配列を有し、かつ、α−ケトグルタル酸デヒドロゲナーゼのE2o及びE3サブユニットタンパク質と複合体を形成することにより、野生株または非改変株のα−ケトグルタル酸デヒドロゲナーゼ複合体の二分の一以下のα−ケトグルタル酸デヒドロゲナーゼ活性を示すタンパク質。
本発明のコリネ型細菌は、L−グルタミン酸生産能を有するコリネ型細菌であって、生育が非改変株または野生株と同等以上であり、かつ染色体上のα−ケトグルタル酸デヒドロゲナーゼ(以下、α−KGDHとも呼ぶ)のE1oサブユニットをコードするodhA遺伝子のコード領域内、または発現制御領域内に変異が導入されたことにより、菌体内α−KGDH活性が、非改変株または野生株の菌体内α−KGDH活性の二分の一以下に低下したことを特徴とするコリネ型細菌である。
コリネバクテリウム・アセトグルタミカム
コリネバクテリウム・アルカノリティカム
コリネバクテリウム・カルナエ
コリネバクテリウム・グルタミカム
コリネバクテリウム・リリウム
コリネバクテリウム・メラセコーラ
コリネバクテリウム・サーモアミノゲネス (コリネバクテリウム・エフィシエンス)
コリネバクテリウム・ハーキュリス
ブレビバクテリウム・ディバリカタム
ブレビバクテリウム・フラバム
ブレビバクテリウム・インマリオフィラム
ブレビバクテリウム・ラクトファーメンタム(コリネバクテリウム・グルタミカム)
ブレビバクテリウム・ロゼウム
ブレビバクテリウム・サッカロリティカム
ブレビバクテリウム・チオゲニタリス
コリネバクテリウム・アンモニアゲネス
ブレビバクテリウム・アルバム
ブレビバクテリウム・セリヌム
ミクロバクテリウム・アンモニアフィラム
具体的には、下記のような菌株を例示することができる。
コリネバクテリウム・アセトグルタミカム ATCC15806
コリネバクテリウム・アルカノリティカム ATCC21511
コリネバクテリウム・カルナエ ATCC15991
コリネバクテリウム・グルタミカム ATCC13020, ATCC13032, ATCC13060, ATCC13869
コリネバクテリウム・リリウム ATCC15990
コリネバクテリウム・メラセコーラ ATCC17965
コリネバクテリウム・サーモアミノゲネス AJ12340(FERM BP-1539)
コリネバクテリウム・ハーキュリス ATCC13868
ブレビバクテリウム・ディバリカタム ATCC14020
ブレビバクテリウム・フラバム ATCC13826, ATCC14067, AJ12418(FERM BP-2205)
ブレビバクテリウム・インマリオフィラム ATCC14068
ブレビバクテリウム・ラクトファーメンタム (コリネバクテリウム・グルタミカム)
ATCC13869
ブレビバクテリウム・ロゼウム ATCC13825
ブレビバクテリウム・サッカロリティカム ATCC14066
ブレビバクテリウム・チオゲニタリス ATCC19240
コリネバクテリウム・アンモニアゲネス ATCC6871、ATCC6872
ブレビバクテリウム・アルバム ATCC15111
ブレビバクテリウム・セリヌム ATCC15112
ミクロバクテリウム・アンモニアフィラム ATCC15354
以上のような方法により、クエン酸シンターゼ遺伝子、フォスフォエノールピルベートカルボキシラーゼ遺伝子、及び/又はグルタミン酸デヒドロゲナーゼ遺伝子の発現が増強
するように改変された微生物としては、特開平2001-333769号公報、特開2000-106869号公報、特開2000-189169号公報、特開2001-333769等に記載された微生物が例示できる。
上記のような酵素の活性を低下または欠損させるには、通常の変異処理法によって、染色体上の上記酵素の遺伝子に、細胞中の当該酵素の活性が低下または欠損するような変異を導入すればよい。例えば、遺伝子組換えによって、染色体上の酵素をコードする遺伝子を欠損させたり、プロモーターやシャインダルガルノ(SD)配列等の発現調節配列を改変したりすることなどによって達成される。また、染色体上の酵素をコードする領域にアミノ酸置換(ミスセンス変異)を導入すること、また終始コドンを導入すること(ナンセンス変異)、1〜2塩基を付加または欠失させるフレームシフト変異を導入すること、遺伝子の一部分を欠失させることによっても達成出来る。(Journal of biological Chemistry 272:8611-8617(1997))また、コード領域が欠失したような変異酵素をコードする遺伝子を構築し、相同組換えなどによって、該遺伝子で染色体上の正常遺伝子を置換することによっても酵素活性を低下または欠損させることができる。
このような耐性菌の具体例としては、下記のような菌株が挙げられる。
ブレビバクテリウム・フラバムAJ11355(FERM P−5007;特開昭56−1889号公報参照)
コリネバクテリウム・グルタミカムAJ11368(FERM P− P−5020;特開昭56−1889号公報参照)
ブレビバクテリウム・フラバムAJ11217(FERM P−4318;特開昭57−2689号公報参照)
コリネバクテリウム・グルタミカムAJ11218(FERM−P4319;特開昭57−2689号公報参照)
ブレビバクテリウム・フラバムAJ11564(FERM P−5472;特開昭56−140895公報参照)
ブレビバクテリウム・フラバムAJ11439(FERM P−5136;特開昭56−35981号公報参照)
コリネバクテリウム・グルタミカムH7684(FERM BP−3004;特開平04−88994号公報参照)
−ケトグルタル酸(2−オキソグルタル酸)を酸化的に脱炭酸し、サクシニル−CoA(succinyl-CoA)を生成する反応を触媒する活性を意味する。上記反応は、α−ケトグルタル酸デヒドロゲナーゼ(E1o EC1.2.4.2)、ジヒドロリポアミドS−サクシニルトランスフェラーゼ(E2o dihydrolipoamide-S-succinyltransferase EC:2.3.1.61)、ジヒドロリポアミドデヒドロゲナーゼ(E3 dihydrolipoamide dehydrogenase EC:1.8.1.4)の3種の酵素によって触媒される。すなわち、これらの3種類のサブユニットはそれぞれ以下の反応を触媒し、これら3つの反応をあわせた反応を触媒する活性をα−KDGH活性という。
E1o: 2-oxoglutarate + [dihydrolipoyllysine-residue succinyltransferase]lipoyllysine = [dihydrolipoyllysine-residue succinyltransferase]S-succinyldihydrolipoyllysine + CO2
E2o:CoA + enzymeN6-(S-succinyldihydrolipoyl)lysine=succinyl-CoA + enzyme N6-(dihydrolipoyl)lysine
E3: protein N6-(dihydrolipoyl)lysine + NAD+ = protein N6-(lipoyl)lysine+ NADH + H+
エシェリヒア・コリ等では、この3種それぞれの酵素活性を有するサブユニットタンパク質が複合体を形成している。
なお、α−ケトグルタル酸デヒドロゲナーゼは、オキソグルタル酸デヒドロゲナーゼ(oxoglutarate dehydrogenase)、2-オキソグルタル酸デヒドロゲナーゼ(2-oxoglutarate dehydrogenase)とも呼ばれる。
また、α−KGDHのE1oサブユニット活性を示すタンパク質であって、配列番号10、配列番号10のアミノ酸番号37〜1257のアミノ酸配列、または配列番号51のアミノ酸配列において、1または数個のアミノ酸が置換されたアミノ酸配列を有するタンパク質をコードする遺伝子であってもよい。ここで、数個とは、2〜20個が好ましく、2〜10個がより好ましく、2〜5個が特に好ましい。
より具体的には、配列番号9に示す塩基配列の塩基番号443〜4213、配列番号9に示す塩基配列の塩基番号551〜4213の塩基配列、または配列番号50の塩基配列を有する遺伝子を挙げることができる。また、Genbankやゲノムデータベースに登録されているコリネ型細菌のodhA遺伝子あるいは、sucA遺伝子を挙げることが出来る。(Genban
k Accession No.NCgl1084, CE1190)
また、コリネ型細菌の種や菌株によってodhA遺伝子の塩基配列に差異が存在することがあるため、α−KGDHのE1oサブユニット活性を示すタンパク質をコードする限り、配列番号9に示す塩基配列の塩基番号443〜4213、配列番号9の塩基番号551〜4213、もしくは配列番号50の塩基配列を有するポリヌクレオチドまたは該塩基配列の一部を有するプローブとストリンジェントな条件下でハイブリダイズする遺伝子であってもよい。ここでストリンジェントな条件としては例えば、通常のサザンハイブリダイゼーションの洗いの条件が挙げられ、具体的には、60℃、1×SSC,0.1%SDS、好ましくは、0.1×SSC、0.1%SDSに相当する塩濃度で、1回より好ましくは2〜3回洗浄する条件が挙げられる。なお、α−KGDHのE1oサブユニット単独の活性は、Masseyらの方法(Biochim. Biophys. Acta 38,447-460)によって測定することができる。
上記のような変異はodhA遺伝子のコード領域だけでなく、発現調節領域に導入されてもよい。発現調節領域とは、プロモーターやオペレーターなどの領域を含む。odhAの発現を直接支配する発現制御領域は、odhAの開始コドン直前の領域であり、配列番号9に示す塩基配列の塩基番号1〜442の領域が挙げられ、中でもプロモーターやSD配列に変異を導入することが有効である。プロモーター領域やSD配列は、GENETYX等の遺伝子解析ソフトを用いることや、Prokaryotic promoters in biotechnology. Biotechnol. Annu. Rev., 1995, 1, 105-128等に記載されている方法で検索できる。
なお、α−KGDH(複合体)活性は、Shiioらの方法(Isamu Shiio and Kyoko Ujigawa-Takeda, Agric.Biol.Chem.,44(8),1897-1904,1980)に従って測定することができる。
後に出現するコロニーの数に基いて算出することができる。
なお、本発明のコリネ型細菌の生育は少なくともある特定の温度(例えば低温)において野生株または非改変株と同等であればよい。すなわち、後述の実施例で示すGN2-2株のように、低温(例えば25〜30℃)で野生株または非改変株と同等の生育を示すが、高温(例えば、34〜40℃)では野生株または非改変株よりも生育が低下したコリネ型細菌も、本発明のコリネ型細菌に含まれる。
Sci. USA, 2000, vol. 97, No. 12, p6640−6645)の直鎖状DNAを用いる方法や温度感受性複製起点を含むプラスミドを用いる方法などがある(米国特許第6303383号明細書、または特開平05−007491号公報)。また、上述のような相同組換えを利用した遺伝子置換による遺伝子破壊は、宿主で複製能力を持たないプラスミドや、コリネ型細菌に接合伝達可能なプラスミドを用いて行うことが出来る。
中央第6)に受託番号FERM P-11763として寄託され、1991年8月26日にブダペスト条約に基づく国際寄託に移管され、FERM BP-3524の受託番号で寄託されている
)があり、バチルス・ズブチルスについて報告されているような、増殖段階の細胞からコンピテントセルを調整しDNAを導入する方法(Dancan,C.H., Wilson,G.A and Young,F.E , Gene ,1,153(1977) )がある。あるいは、バチルス・ズブチルス、放線菌類及び酵母について知られているようなDNA受容菌の細胞を組換えDNAをDNA受容菌に導入する方法(Chang.S. and Choen,S.N., Molec. Gen. Genet., 168, 111 (1979); Bibb,M.J., Ward,J.M. and Hopwood,O.A., Nature, 274, 398 (1978); Hinnen,A., Hicks,J.B. and Fink,G.R., Proc. Natl. Acad. Sci. USA, 75 1929 (1978))も応用できる。また、コリネ型細菌の形質転換は、電気パルス法(杉本ら、特開平2−207791号公報)によっても行うことができる。
バチルス・アミロリキュファシエンス:sacB GenBank Accession Number X52988
ザイモモナス・モビリス:sacB GenBank Accession Number L33402
バチルス・ステアロサ−モフィラス:surB GenBank Accession Number U34874
ラクトバチルス・サンフランシセンシス:frfA GenBank Accession Number AJ508391
アセトバクタ−・キシリナス:lsxA GenBank Accession Number AB034152
グルコンアセトバクタ−・ジアゾトロフィカス:lsdA GenBank Accession Number L41732
染色体上のα−KGDHのサブユニットをコードするodhA遺伝子における変異は、菌体内α−KGDH活性を、非改変株または野生株の菌体内α−ケトグルタル酸デヒドロゲナーゼ活性の二分の一以下に低下させる変異であって、該変異を含むα−KGDH遺伝子を保持する細菌が野生株と同等に生育できる変異である。本発明の変異型odhA遺伝子がコードする変異型α−KGDH E1oサブユニットは、α−KGDHのE2oサブユニットおよびE3サブユニットタンパク質と複合体を形成することにより、野生型α−KGDH(複合体)または非改変型α−KGDH(複合体)の二分の一以下のα−KGDH活性を示す。さらに、変異型odhAがコードする該タンパク質をコリネ型細菌に保持させた場合に、該コリネ型細菌が野生株と同等の生育を示すようなタンパク質が好ましい。
例えば、具体例には以下のような変異が挙げられる。
この変異は、補酵素であるチアミンピロリン酸の結合領域に導入された変異であり、チアミンピロリン酸結合領域とは、odhA遺伝子(配列番号9)の2498番目〜2584番目の塩基によってコードされる領域(配列番号10の686G-714D)をいう。配列番号10の686〜688番目のGly-Leu-Gly残基、および713-714番目のAsn-Asn残基がチアミンピロリン酸結合部位であり、このチアミンピロリン酸結合部位や、チアミンピロリン酸結合部位の間の配列に変異を導入することが好ましい。
700番目のArg残基は、塩基性アミノ酸残基以外(Lys,His)以外のアミノ酸残基に、702番目のTyr残基は、ヒドロキシル基を有するアミノ酸以外(Ser,Thr)のアミノ酸残基に置換
することが望ましい。
中でも、698番目のLys残基は、脂肪族疎水性アミノ酸残基(Ile,Leu,Val)に置換することが望ましく、699番目のLeu残基は、側鎖にヒドロキシル基を持つSer,Thr,Tyr残基に置換することが望ましく、700番目のArg残基は、側鎖にS原子を有するCys,Met残基に置換することが望ましく、また、702番目のTyr残基は、脂肪族疎水性アミノ酸残(Ile,Leu,Val)に置換することが望ましい。
これらの残基が置換された変異型odhA遺伝子をコードする遺伝子の塩基配列を配列番号44,46,48の塩基番号443〜4210に(または配列番号44、46、48の塩基番号551〜4210)、変異型OdhAのアミノ酸配列を配列番号45,47,49(または配列番号45、47、49のアミノ酸番号37〜1256)に示す。該GN型変異と同じアミノ酸置換及びアミノ酸欠失を生じさせる変異、すなわち、染色体上のodhA遺伝子塩基配列を、配列番号14のアミノ酸配列をコードする塩基配列にするその他の変異も本発明の範囲に含まれる。
この変異は、odhA遺伝子(配列番号9)の1094-1111番目の領域に導入されたものであり、好ましくは、配列番号10に記載のアミノ酸配列の218-224番目のアミノ酸残基(Asp-Val-Ile-Asp-Gly-Lys-Pro)のうち1または2以上のアミノ酸残基を欠失させる変異及び/又は1または2以上のアミノ酸残基を置換する変異である。より好ましくは、odhA遺伝子(配列番号9)の1094−1098番目のgacgtを欠失させ、かつ、1110−1111番のagをggccに置換する変異である。この変異を有するodhA遺伝子の塩基配列を配列番号11の塩基番号443〜4213(または配列番号11の塩基番号551〜4213)に示す。該遺伝子にコードされる変異型odhAのアミノ酸配列を配列番号12(または配列番号12のアミノ酸番号37〜1256)に示す。
アミノ酸残基の欠失を伴う変異としては、配列番号10に記載のアミノ酸残基の218番目のAsp残基を欠失させる変異が好ましい。この変異を有するodhA遺伝子の塩基配列を配列番号11の塩基番号443〜4213(または配列番号11の塩基番号551〜4213)に示す。該遺伝子にコードされる変異型odhAのアミノ酸配列を配列番号12(または配列番号12のアミノ酸番号37〜1256)に示す。
置換されるアミノ酸残基は、219-221番目のアミノ酸残基は、塩基性アミノ酸残基への置換(His,Arg,Lys)が望ましく、222番目のGly残基は、側鎖にアミド基を持つアミノ酸残基(Asp,Gln)、223番目のLys残基は単純構造のアミノ酸残基(Gly,Ala)に置換することが望ましい。
なお、該2-2型変異と同じアミノ酸置換及びアミノ酸欠失を生じさせる変異、すなわち、染色体上のodhA遺伝子塩基配列を、配列番号12のアミノ酸配列をコードする塩基配列
にするその他の変異も本発明の範囲に含まれる。
この変異は上記GN型変異と2-2型変異の両方を含む変異である。この変異を有するα−KGDH遺伝子の塩基配列及び該遺伝子にコードされる変異酵素のアミノ酸配列の一例を、それぞれ配列番号15の塩基番号443〜4213(または配列番号15の塩基番号551〜4213)に示す。該遺伝子にコードされる変異型α−KGDHのアミノ酸配列を配列番号16(または配列番号16のアミノ酸番号37〜1254)に示す。
なお、該GN+2−2型変異と同じアミノ酸置換及びアミノ酸欠失を生じさせる変異、すなわち、染色体上のodhA遺伝子塩基配列を、配列番号16のアミノ酸配列をコードする塩基配列にするその他の変異も本発明の範囲に含まれる。
への置換、pheからtrp、tyr、met、ile又はleuへの置換、serからthr又はalaへの置換、thrからser又はalaへの置換、trpからphe又はtyrへの置換、tyrからhis、phe又はtrpへの置換、及び、valからmet、ile又はleuへの置換が例示される。
なお、α−KGDH複合体とは、E1oサブユニットとE2oサブユニットがodhA遺伝子にコードされている場合、配列番号10のタンパク質及び配列番号18のタンパク質からなる複合体を挙げることができ、E1oサブユニットがodhA遺伝子に、E2oサブユニットが配列番号27の遺伝子にコードされている場合、配列番号10のタンパク質、配列番号18のタンパク質及び配列番号28のタンパク質からなる複合体を挙げることができる。
本発明の変異型odhA遺伝子は、上述の変異を有し、α−KGDHのE2oサブユニットおよびE3サブユニットタンパク質と複合体を形成することにより、野生株または非改変株のα−KGDH複合体の二分の一以下のα−KGDH活性を示す限りにおいて、配列番号11,13,もしくは15の塩基番号443〜4213,または配列番号44,46,もしくは48の塩基番号443〜4210(または配列番号11,13,もしくは15の塩基番号551〜4213,または配列番号44,46,もしくは48の塩基番号551〜4210)の塩基配列を有するポリヌクレオチドとストリンジェントな条件下でハイブリダイズする遺伝子であってもよい。ここでストリンジェントな条件としては例えば、通常のサザンハイブリダイゼーションの洗いの条件が挙げられ、具体的には、60℃、1×SSC,0.1%SDS、好ましくは、0.1×SSC、0.1%SDSに相当する塩濃度で、1回より好ましくは2〜3回洗浄する条件が挙げられる。
本発明のコリネ型細菌を培地に培養し、培地中にL−グルタミン酸を生成蓄積せしめ、L−グルタミン酸を該培地から採取することにより、L−グルタミン酸を製造することが出来る。本発明の製造方法においては、本発明のコリネ型細菌を、例えば、20〜45℃で、8〜120時間培養する。なお、実施例に示すGN2-2株のような低温では野生株と同等の生育を示すが、高温では生育が低下した本発明のコリネ型細菌を用いる場合、該コリネ型細菌を低温、例えば、25〜30℃で8〜30時間培養して増殖させ、ついで、得られた菌体を、高温、例えば、34〜40℃で、16〜48時間保持することによってL−グルタミン酸を生産させることが好ましい。
以下、実施例を挙げて本発明を具体的に説明する。ただし、本発明は以下の実施例に限定されない。
(A)pBS3の構築
sacB遺伝子(配列番号19)をバチルス・ズブチリスの染色体DNAを鋳型として配列番号21と22をプライマーとして用いて、PCRにより取得した。PCR反応は、LA taq(TaKaRa)を用い、94 ℃で5分保温を1サイクル行った後、変性94℃ 30秒、会合49℃ 30秒、伸長72℃ 2分からなるサイクルを25回繰り返した。生成したPCR産物を常法により精製後BglIIとBamHIで消化し、平滑化した。この断片をpHSG299のAvaIIで消化後、平滑化した部位に挿入した。このDNAを用いて、エシェリヒア・コリJM109のコンピテントセル(宝バイオ社製)を用いて形質転換を行い、カナマイシン(以下、Kmと略す)25μg/mlを含むLB培地に塗布し、一晩培養した。その後、出現したコロニーを釣り上げ、単コロニーを分離し形質転換体を得た。得られた形質転換体よりプラスミドを抽出し、目的のPCR産物が挿入されていたものをpBS3と命名した。pBS3の構築過程を図1に示す。
pBS3上に存在するカナマイシン耐性遺伝子配列中のSmaI部位をアミノ基置換を伴わない塩基置換によりカナマイシン耐性遺伝子を破壊したプラスミドをクロスオーバーPCRで取得した。まず、pBS3を鋳型として配列番号23,24の合成DNAをプライマーとしてPCRを行い、カナマイシン耐性遺伝子のN末端側の増幅産物を得る。一方Km耐性遺伝子のC末端側の増幅産物を得るためにpBS3を鋳型として配列番号25,26の合成DNAを鋳型としてPCRを行った。PCR反応はPyrobest DNA Polymerase(宝バイオ社製)を用い、98 ℃で5分保温を1サイクル行った後、変性98℃ 10秒、会合57℃ 30秒、伸長72℃ 1分からなるサイクルを25回繰り返すことにより目的のPCR産物を得ることができる。配列番号24と25は部分的に相補的であり、またこの配列内に存在するSmaI部位はアミノ酸置換を伴わない塩基置換を施すことにより破壊されている。次にSmaI部位が破壊された変異型カナマイシン耐性遺伝子断片を得るために、上記カナマイシン耐性遺伝子N末端側及びC末端側の遺伝子産物を、それぞれほぼ等モルとなるように混合し、これを鋳型として配列番号23,26の合成DNAをプライマーとしてPCRを行い変異導入されたKm耐性遺伝子増幅産物を得た。PCR反応はPyrobest DNA
Polymerase(宝バイオ社)を用い、98 ℃で5分保温を1サイクル行った後、変性98℃ 10秒、会合57℃ 30秒、伸長72℃ 1.5分からなるサイクルを25回繰り返すことにより目的のPCR産物を得ることができる。
コリネ型細菌のα−ケトグルタル酸デヒドロゲナーゼをコードしているodhAの配列は既に明らかになっている(Microbiology 142, 3347-3354, (1996)、GenBank accession No.D84102)。
本発明者らが育種に成功したL−グルタミン酸生産菌GN株は、odhA遺伝子(配列番号9)内の遺伝子番号2538番、2543−2547番の遺伝子が欠失していることが塩基配列の解析によりわかった(表1)。
ース10g/lに変更した組成)に塗布した。S10プレート上で生育し、且つカナマイシン感受性を示す株を数株選択後、これら株のodhA配列に目的通りの変異が導入されているのか、Sangerの方法(J.Mol.Biol.,143, 161, (1980))にて確認を行った。具体的な塩基配列の決定はBigDye terminator sequencing kit(Applied Biosystems製)を用いて、genietic
Analyzer ABI310(Applied Biosystems製)で解析した。このようにして取得した変異導入株をATCC13869 OAGNと命名した。
本発明者らが育種に成功したL−グルタミン酸生産菌2-2株は、odhA遺伝子内の遺伝子番号1094−1098番の塩基が欠失し、1110−1111番のagがggccに置換された配列を保持していることが塩基配列の解析によりわかった(表2)。
実施例1の<2>にて作製したATCC13869 OAGN株に、実施例1の<3>にて構築したプラスミドpBSOA2-2を用いて、実施例11の<2>に記載した手順と同様の操作を行い、2-2型変異が導入されたATCC13869 OAGN2-2株を取得した。以下、2-2変異とGN変異の二重変異をGN2-2変異とも言う。
を含むプラスミドを構築する。次にこの断片をBamHIで切り出しpBS4Sベクターに搭載すればpBSOAGNと同様のプラスミドを構築出来る。
同様に、2-2変異を導入するためには、上記と同様の方法で5'末端がリン酸化された配列番号7の合成DNAの代わりに5'末端がリン酸化された配列番号8の合成DNAを用いることでpBSOA2-2と同様のプラスミドが構築できる。またGN2-2変異を導入する為には、前述の方法で構築したpBSOAGNもしくはpBSOA2-2より変異型odhA断片を切り出して再度pKF19kにクローニングし、もう一方の変異をさらに導入すればよい。
野生型odhAを保持する株は、培地中のグルタミン酸を資化するが、odhA遺伝子がコードしているα−ケトグルタル酸デヒドロゲナーゼ活性が弱化あるいは欠失株では、そのグルタミン酸分解能力が低下することが推定される。この性質を利用し、実施例1の<2>〜<4>において作製したodhA変異株ATCC13869 OAGN、OA2-2、OAGN2-2のグルタミン酸分解能を測定した。各菌株をCM-Dexプレートで一昼夜25℃にて培養し、グルタミン酸ナトリウム 20g/l、(NH4)2SO4 2.64g/l、KH2PO4 0.5g/l、K2HPO4 0.5g/l、MgSO4・7H2O 0.25g/l、FeSO4・7H2O 0.01g/l、MnSO4・4-5H2O 0.01g/l、CaCl2 0.01g/l、CuSO4 0.02mg/l、MOPS 40g/l、プロトカテク酸 0.03g/l、ビタミンB1 200μg/l、ビオチン 300μg/l(NaOHを用いてpH6.7に調整)の組成からなる液体培地に接種後、25℃及び34℃にて50時間培養を行った。培養開始前、25、50時間後のグルタミン酸量を測定し、グルタミン酸の分解量を25℃、34℃で培養した菌体で比較した。その結果を表3に記載した。特にGN2-2変異株は培養温度を34℃に上げることによりグルタミン酸の分解量は低下したことから、GN2-2変異の導入によりα−ケトグルタル酸デヒドロゲナーゼ活性が高温でより弱化する性質を付与できることが示唆された。
後述の実施例4にて培養した培養液(培養開始4時間後)を用いてATCC13869 OAGN、OA2-2、OAGN2-2のα−ケトグルタル酸デヒドロゲナーゼ活性の測定を行った。活性測定方法については、Agric.Biol.Chem.,44(8), p1897 (1980)に従った。具体的には、菌体を0.2%
塩化カリウムにて洗浄後、100mM TES-NaOH(pH7.5)、30%グリセロール溶液に懸濁した。Bioruptorを用いて超音波破砕後、遠心分離(1000xg、30分)を行って未破砕菌体を取り除き、Sephadex-G25を用いて同バッファーにてゲルろ過した。このようにして調製したものを粗酵素液とした。100mM TES-NaOH(pH7.7)、5mM MgCl2、0.2mM CoA、 0.3mMコカルボキシラーゼ、1mM α−ケトグルタル酸、3mM L-システイン、1mM アセチルピリジン−アデニン−ジヌクレオチドを含む反応系に粗酵素液を添加し、31.5℃における365nmの吸収を日立分光光度計U-2001にて測定した。粗酵素液のタンパク質濃度の測定には、Protein Assay(Bio-Rad製)を用い、標準タンパク質には牛血清アルブミンを用いた。
活性測定の結果を表4に記載した。GN型変異、2-2型変異、GN2-2型変異を導入することにより、α−ケトグルタル酸デヒドロゲナーゼ活性はATCC13869と比較して低下し、特にG
N2-2変異導入株においては、顕著な活性低下が認められた。以上のことからGN型変異、2-2型変異、GN2-2型変異はα−ケトグルタル酸デヒドロゲナーゼ活性を弱化させる変異であることが明らかとなった。
ATCC13869 OAGN、OA2-2、OAGN2-2のL−グルタミン酸生産能をジャーファーメンターで検証した。まず、上記4株をCM-Dex寒天培地で25℃で一昼夜培養を行い、滅菌したシード培地(グルコース60g/l、H3PO4 1.54g/l、KOH 1.45g/l、MgSO4・7H2O 0.9g/l、FeSO4・7H2O 0.01g/l、ビタミンB1 670μg/l、ビオチン 3200μg/l、DL-Met 0.28g/L、大豆蛋白加水分解液1.54g/l、消泡剤AZ-20R 0.1ml/l)300mlに接種し、25℃で糖を完全に消費するまで培養した。なお、培養中は1/1VVM通気で溶存酸素濃度が5%以下とならないように攪拌し、培養時のpHはアンモニアガスを用いてpH7.2となるように制御した。次に、得られたシード培養液30mlを滅菌した本培養培地(グルコース80g/l、KH2PO4 3.46g/l、MgSO4・7H2O 1.0g/l、FeSO4・7H2O 0.01g/l、MnSO4・4-5H2O 0.01g/l、ビタミンB1 230μg/l、ビオチン 525μg/l、大豆蛋白加水分解液0.35g/l、消泡剤AZ-20R 0.2ml/l)270mlに接種し25℃または34℃で培養した。なお、通気は1/1VVMで行い、溶存酸素濃度が5%以下とならないように攪拌し、培養時のpHはアンモニアガスを用いてpH7.3となるように制御した。
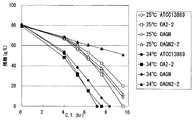
培養開始後約7.5時間目のL−グルタミン酸蓄積を表5に、培養経時のL−グルタミン酸蓄積、菌体量、残糖の変化を図5,6,7にそれぞれ示した。ATCC13869はどの培養温度においてもL−グルタミン酸を蓄積しないが、OAGN、OAGN2-2変異導入株ではL−グルタミン酸を蓄積するようになり、特に34℃で培養を行うと、L−グルタミン酸蓄積量が増大した。また、各変異導入株の低温での生育は野生型と同程度であった。
以上より、GN型変異、2-2型変異、GN2-2型変異はL−グルタミン酸生成向上に効果があり、特にGN2-2型変異は、最も高いL−グルタミン酸生成向上効果を付与する変異であることを確認出来た。
<L30型YggB変異株の構築>
まず、ATCC13869株よりyggB遺伝子に変異をもつ株を構築した。yggB遺伝子のL30型変異は、野生型yggB遺伝子(C.glutamicumの野生型遺伝子を配列番号29に示す)の1768番目のCがTに置換された変異である。この変異が導入された変異型yggB遺伝子の塩基配列を配列番号31に、該遺伝子にコードされる変異型YggBのアミノ酸配列を配列番号32に示す。
実施例1と同様の方法にて、L30型変異が導入されたyggB変異株を構築した。具体的には、配列番号33に示す合成DNAと配列番号34に示す合成DNAをプライマーとして、ATCC13869株の染色体DNAを鋳型としてPCRを行い、yggB遺伝子のN末端側断片を調製した。同様に配列番号35と配列番号36の合成DNAをプライマーとして、yggB遺伝子のC末端側断片を調製した。続いてN末端側断片とC末端側断片を等量混合したものを鋳型として、配列番号37と配列番号35の合成DNAをプライマーとしてPCRを行うことによりL30型yggB遺伝子の部分断片を取得した。得られた変異型yggB遺伝子断片をSacIで処理してpBS4SのSacI部位に挿入することにより、変異導入用のプラスミドを構築した。このようにして得られたpBS4 YggB-Lを実施例1記載の方法と同様にATCC13869株の染色体に挿入した後、脱落させた。得られたカナマイシン感受性株のyggB遺伝子の配列を決定し、L30型に置換された株を選択することにより、L30型変異を有する株を得た。配列番号31のyggB遺伝子の配列を持つ株をATCC13869-L株とした。
このATCC13869-L株は変異型odhA遺伝子のスクリーニング及び評価に用いることができる。
次に、ATCC13869-L株のodhA遺伝子に表6に示す変異を導入した株を構築した。なお、表6では、配列番号9の塩基番号2528〜2562に相当する領域の配列を示した。また、表7では配列番号10のアミノ酸番号696〜707に相当する領域の配列を示した。
配列番号42の塩基配列を有する変異型odhA遺伝子が導入されたL30sucA8株を構築するには以下のようにすればよい。まず配列番号2と配列番号5に示す合成DNAをプライマーとしてPCRを行い、odhA断片を調整する。得られたodhA断片をBamHI処理して、タカラバイオ製Mutan-Super Express Kmに付属のプラスミドpKF19mのBamHI部位にクローニングした後、5'末端がリン酸化された配列番号38の合成DNAとMutan-Super Express Kmに添付されているセレクションプライマーを用いてPCRを行い、得られたPCR産物でsup0のE.coli例えばMV1184株を形質転換することで変異型odhA断片を含むプラスミドを構築する。次にこの断片をBamHIで切り出し、pBS4SのBamHI部位に挿入することで変異導入用プラスミドが構築できる。このプラスミドを用いて実施例1記載の方法と同様にしてATCC13869-L株を形質転換し、染色体に変異導入用プラスミドが挿入された株を取得する。次に、これらの染色体にプラスミドが挿入された株から、スクロースに耐性を示し、かつカナマイシンに感受性を示す株を分離する。さらにodhAの配列を確認し、目的フレームシフトが導入された株を選択することによりodhA遺伝子が欠損したL30sucA8(odhA8)株が構築できる。
配列番号44の塩基配列を有する変異型odhA遺伝子が導入されたL30sucA801株の取得には、5'末端がリン酸化された配列番号38の合成DNAの代わりに5'末端がリン酸化された配列番号39の合成DNAを用いて上記方法を適用すればよい。
配列番号46の塩基配列を有する変異型odhA遺伝子が導入されたL30sucA805株の取得には、5'末端がリン酸化された配列番号38の合成DNAの代わりに5'末端がリン酸化された配列番号40の合成DNAを用いて上記方法を適用すればよい。
配列番号48の塩基配列を有する変異型odhA遺伝子が導入されたL30sucA77株の取得には、5'末端がリン酸化された配列番号38の合成DNAの代わりに5'末端がリン酸化された
配列番号41の合成DNAを用いて上記方法を適用すればよい。
これらのodhA改変株のL-グルタミン酸生産能を、坂口フラスコを用いた培養を行うことにより検証した。表4に示した株をCM-Dex寒天培地で31.5℃で一昼夜培養を行い、フラスコ培地(グルコース60g/l、硫安22.5g/l、KH2PO4 1g/l、MgSO4・7H2O 0.4g/l、FeSO4・7H2O 0.01g/l、MnSO4・4-5H2O 0.01g/l、ビタミンB1 200μg/l、大豆蛋白加水分解液0.48g/l、ビオチン300μg/l、KOHを用いてpH8.0に調整)20mlに1/6プレート分の菌体を接種し、予め乾熱滅菌しておいた炭酸カルシウム1gを添加した後、31.5℃、速度115rpmで振とう培養を行った。培養開始19時間目のL-グルタミン酸蓄積を表8に示した。odhA改変株の中には、ATCC13869-L株とほぼ同等のL-グルタミン酸蓄積のものも含まれていたが、sucA801, sucA805,sucA77株はsucA8株よりも高いL-グルタミン酸蓄積を示した。これらの結果から、L-グルタミン酸の効率よい生産にはαKGDH活性のファインチューニングが有効であり、そのためにはodhA遺伝子のチアミンピロリン酸結合部位近傍に変異を導入する方法が有効であることが示された。
Claims (13)
- L−グルタミン酸生産能を有するコリネ型細菌であって、生育が非改変株または野生株と同等以上であり、かつ染色体上のα−ケトグルタル酸デヒドロゲナーゼのE1oサブユニットをコードするodhA遺伝子のコード領域内、または発現制御領域内に変異が導入されたことにより、菌体内α−ケトグルタル酸デヒドロゲナーゼ活性が、非改変株または野生株の菌体内α−ケトグルタル酸デヒドロゲナーゼ活性の二分の一以下に低下したことを特徴とするコリネ型細菌。
- 前記odhA遺伝子が以下の(A)〜(D)のいずれかに記載のタンパク質をコードする遺伝子である、請求項1に記載のコリネ型細菌:
(A)配列番号10に示すアミノ酸配列を有するタンパク質、
(B)配列番号10に示すアミノ酸配列において1若しくは数個のアミノ酸が置換、欠失、挿入、または付加されたアミノ酸配列を有し、かつα−ケトグルタル酸デヒドロゲナーゼのE1oサブユニット活性を示すタンパク質。
(C)配列番号10に示すアミノ酸配列のアミノ酸番号37〜1257のアミノ酸配列を有するタンパク質、
(D)配列番号10に示すアミノ酸配列のアミノ酸番号37〜1257のアミノ酸配列において1若しくは数個のアミノ酸が置換、欠失、挿入、または付加されたアミノ酸配列を有し、かつα−ケトグルタル酸デヒドロゲナーゼのE1oサブユニット活性を示すタンパク質。 - 前記数個が2〜20個である、請求項2に記載のコリネ型細菌。
- 前記odhA遺伝子が以下の(a)〜(d)のいずれかに記載の遺伝子である、請求項1に記載のコリネ型細菌:
(a)配列番号9に示す塩基配列の塩基番号443〜4213の塩基配列を有する遺伝子、
(b)配列番号9に示す塩基配列の塩基番号443〜4213の塩基配列を有するポリヌクレオチド又は同塩基配列から調製され得るプローブとストリンジェントな条件下でハイブリダイズし、かつα−ケトグルタル酸デヒドロゲナーゼのE1oサブユニット活性を示すタンパク質をコードする遺伝子。
(c)配列番号9に示す塩基配列の塩基番号551〜4213の塩基配列を有する遺伝子、
(d)配列番号9に示す塩基配列の塩基番号551〜4213の塩基配列を有するポリヌクレオチド又は同塩基配列から調製され得るプローブとストリンジェントな条件下でハイブリダイズし、かつα−ケトグルタル酸デヒドロゲナーゼのE1oサブユニット活性を示すタンパク質をコードする遺伝子。 - 前記変異が前記odhA遺伝子のチアミンピロリン酸結合領域をコードする領域に導入されたことを特徴とする請求項1〜4のいずれか1項に記載のコリネ型細菌。
- 前記変異が、配列番号9に記載の塩基配列において、2534-2548番目の領域に導入されたことを特徴とする、請求項1〜4のいずれか1項に記載のコリネ型細菌。
- 前記変異が、配列番号10に記載のアミノ酸配列において、698−702番目のアミノ酸残基のうちいずれか1以上のアミノ酸残基を欠失させる変異である、請求項1〜4のいずれか1項に記載のコリネ型細菌。
- 前記変異が配列番号10に記載のアミノ酸配列において、698番目のLys残基、699番目のL
eu残基、700番目のArg残基, 702のTyr残基から選択される残基を他のアミノ酸に置換する変異である、請求項1〜4のいずれか1項に記載のコリネ型細菌。 - 前記変異が、配列番号9に記載の塩基配列において、1094-1111番目の領域に導入されたことを特徴とする、請求項1〜4のいずれか1項に記載のコリネ型細菌。
- 前記変異が、配列番号10に記載のアミノ酸配列において、218〜224番目のアミノ酸残基のうちの1または2以上のアミノ酸残基を欠失させる変異である、請求項1〜4のいずれか1項に記載のコリネ型細菌。
- 請求項1〜10のいずれか1項に記載のコリネ型細菌を培地で培養して、L−グルタミン酸を該培地中又は菌体内に生成蓄積させ、該培地又は菌体からL−グルタミン酸を回収することを特徴とするL−グルタミン酸の製造法。
- 下記(e)〜(f)のいずれかに記載の遺伝子である、変異型α−ケトグルタル酸デヒドロゲナーゼ遺伝子:
(e)配列番号11、13、もしくは15の塩基番号443〜4213、または配列番号44、46、もしくは48の塩基番号443〜4210に示す塩基配列を有する遺伝子、
(f)配列番号11、13、もしくは15の塩基番号443〜4213、または配列番号44、46、もしくは48の塩基番号443〜4210に示す塩基配列を有するポリヌクレオチド又は同塩基配列から調製され得るプローブとストリンジェントな条件下でハイブリダイズし、かつ、α−ケトグルタル酸デヒドロゲナーゼのE2o及びE3サブユニットタンパク質と複合体を形成することにより、野生株または非改変株のα−ケトグルタル酸デヒドロゲナーゼ複合体の二分の一以下のα−ケトグルタル酸デヒドロゲナーゼ活性を示すタンパク質をコードする遺伝子。
(g)配列番号11、13、もしくは15の塩基番号551〜4213、または配列番号44、46、もしくは48に示す塩基配列の塩基番号551〜4210の塩基配列を有する遺伝子、又は
(h)配列番号11、13、もしくは15の塩基番号551〜4213、または配列番号44、46、もしくは48に示す塩基配列の塩基番号551〜4210の塩基配列を有するポリヌクレオチド又は同塩基配列から調製され得るプローブとストリンジェントな条件下でハイブリダイズし、かつ、α−ケトグルタル酸デヒドロゲナーゼのE2o及びE3サブユニットタンパク質と複合体を形成することにより、野生株または非改変株のα−ケトグルタル酸デヒドロゲナーゼ複合体の二分の一以下のα−ケトグルタル酸デヒドロゲナーゼ活性を示すタンパク質をコードする遺伝子。 - 下記(E)〜(H)のいずれかに記載のタンパク質である変異型α−ケトグルタル酸デヒドロゲナーゼ:
(E)配列番号12、14、16、45、47又は49に示すアミノ酸配列を有するタンパク質、
(F)配列番号12、14、16、45、47又は49に示すアミノ酸配列において、1または数個のアミノ酸が置換、欠失、または付加されたアミノ酸配列を有し、かつ、α−ケトグルタル酸デヒドロゲナーゼのE2o及びE3サブユニットタンパク質と複合体を形成することにより、野生株または非改変株のα−ケトグルタル酸デヒドロゲナーゼ複合体の二分の一以下のα−ケトグルタル酸デヒドロゲナーゼ活性を示すタンパク質、
(G)配列番号12、45、47又は49に示すアミノ酸配列のアミノ酸番号37〜1256のアミノ酸配列、配列番号14に示すアミノ酸配列のアミノ酸番号37〜1255のアミノ酸配列、または配列番号16に示すアミノ酸配列のアミノ酸番号37〜1254のアミノ酸配列を有するタンパク質、
(H)配列番号12、45、47又は49に示すアミノ酸配列のアミノ酸番号37〜1256のアミノ酸配列、配列番号14に示すアミノ酸配列のアミノ酸番号37〜1255のアミノ酸配列、または配列番号16に示すアミノ酸配列のアミノ酸番号37〜1254のアミノ酸配列において、1または数個のアミノ酸が置換、欠失、または付加されたアミノ酸配列を有し、かつ、α−ケトグルタル酸デヒドロゲナーゼのE2o及びE3サブユニットタンパク質と複合体を形成することにより、野生株または非改変株のα−ケトグルタル酸デヒドロゲナーゼ複合体の二分の一以下のα−ケトグルタル酸デヒドロゲナーゼ活性を示すタンパク質。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2005262178A JP2006101875A (ja) | 2004-09-10 | 2005-09-09 | L−グルタミン酸生産菌及びl−グルタミン酸の製造方法 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2004264458 | 2004-09-10 | ||
| JP2005262178A JP2006101875A (ja) | 2004-09-10 | 2005-09-09 | L−グルタミン酸生産菌及びl−グルタミン酸の製造方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2006101875A true JP2006101875A (ja) | 2006-04-20 |
| JP2006101875A5 JP2006101875A5 (ja) | 2008-08-21 |
Family
ID=35734913
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2005262178A Pending JP2006101875A (ja) | 2004-09-10 | 2005-09-09 | L−グルタミン酸生産菌及びl−グルタミン酸の製造方法 |
Country Status (6)
| Country | Link |
|---|---|
| EP (1) | EP1786899B1 (ja) |
| JP (1) | JP2006101875A (ja) |
| KR (1) | KR100930842B1 (ja) |
| CN (1) | CN101010423B (ja) |
| BR (1) | BRPI0515035A (ja) |
| WO (1) | WO2006028298A2 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2017516488A (ja) * | 2014-06-03 | 2017-06-22 | シージェイ チェイルジェダン コーポレーション | O−スクシニルホモセリンまたはコハク酸の生産能を有する微生物、及びそれを利用したコハク酸またはo−スクシニルホモセリンの生産方法 |
Families Citing this family (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AU2005320486B2 (en) * | 2004-12-28 | 2009-08-13 | Ajinomoto Co., Inc. | L-glutamic acid-producing microorganism and a method for producing L-glutamic acid |
| JP2010041920A (ja) | 2006-12-19 | 2010-02-25 | Ajinomoto Co Inc | L−アミノ酸の製造法 |
| JP2010130899A (ja) | 2007-03-14 | 2010-06-17 | Ajinomoto Co Inc | L−グルタミン酸系アミノ酸生産微生物及びアミノ酸の製造法 |
| WO2009103547A1 (en) | 2008-02-21 | 2009-08-27 | Basf Se | Process for the production of gamma-aminobutyric acid |
| WO2013069634A1 (ja) | 2011-11-11 | 2013-05-16 | 味の素株式会社 | 発酵法による目的物質の製造法 |
| JP2016165225A (ja) | 2013-07-09 | 2016-09-15 | 味の素株式会社 | 有用物質の製造方法 |
| JP2016192903A (ja) | 2013-09-17 | 2016-11-17 | 味の素株式会社 | 海藻由来バイオマスからのl−アミノ酸の製造方法 |
| CN108250278B (zh) * | 2016-12-29 | 2021-06-22 | 廊坊梅花生物技术开发有限公司 | 生产l-谷氨酸的菌株和生产l-谷氨酸的方法 |
| KR102008673B1 (ko) * | 2017-12-07 | 2019-08-09 | 대상 주식회사 | 락토바실러스 퍼멘텀 c-7a 균주 및 이의 용도 |
| CN113637699B (zh) * | 2020-04-27 | 2023-05-30 | 中国科学院分子植物科学卓越创新中心 | 一种提高氨基酸产生菌生产能力的方法 |
| CA3191344A1 (en) * | 2020-09-09 | 2022-03-17 | Nara Kwon | A recombinant microorganism for producing l-glutamic acid and a method for producing l-glutamic acid using the same |
| CN112646767B (zh) * | 2020-12-30 | 2022-08-09 | 宁夏伊品生物科技股份有限公司 | 具有增强的l-谷氨酸生产力的菌株及其构建方法与应用 |
| KR102665227B1 (ko) * | 2021-06-30 | 2024-05-10 | 씨제이제일제당 주식회사 | 고농도 l-글루탐산을 생산하기 위한 균주 및 이를 이용한 l-글루탐산 생산방법 |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1995034672A1 (fr) * | 1994-06-14 | 1995-12-21 | Ajinomoto Co., Inc. | GENE A DESHYDROGENASE α-CETOGLUTARIQUE |
-
2005
- 2005-09-09 KR KR1020077008186A patent/KR100930842B1/ko not_active IP Right Cessation
- 2005-09-09 BR BRPI0515035-3A patent/BRPI0515035A/pt not_active IP Right Cessation
- 2005-09-09 JP JP2005262178A patent/JP2006101875A/ja active Pending
- 2005-09-09 CN CN2005800298560A patent/CN101010423B/zh not_active Expired - Fee Related
- 2005-09-09 WO PCT/JP2005/017098 patent/WO2006028298A2/en active Application Filing
- 2005-09-09 EP EP05783597A patent/EP1786899B1/en not_active Not-in-force
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1995034672A1 (fr) * | 1994-06-14 | 1995-12-21 | Ajinomoto Co., Inc. | GENE A DESHYDROGENASE α-CETOGLUTARIQUE |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2017516488A (ja) * | 2014-06-03 | 2017-06-22 | シージェイ チェイルジェダン コーポレーション | O−スクシニルホモセリンまたはコハク酸の生産能を有する微生物、及びそれを利用したコハク酸またはo−スクシニルホモセリンの生産方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP1786899A2 (en) | 2007-05-23 |
| CN101010423A (zh) | 2007-08-01 |
| KR20070053321A (ko) | 2007-05-23 |
| EP1786899B1 (en) | 2012-06-27 |
| CN101010423B (zh) | 2012-06-27 |
| WO2006028298A3 (en) | 2006-04-27 |
| WO2006028298A2 (en) | 2006-03-16 |
| BRPI0515035A (pt) | 2008-07-01 |
| KR100930842B1 (ko) | 2009-12-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2006101875A (ja) | L−グルタミン酸生産菌及びl−グルタミン酸の製造方法 | |
| US7205132B2 (en) | L-glutamic acid-producing microorganism and a method for producing L-glutamic acid | |
| JP3716427B2 (ja) | α−ケトグルタル酸デヒドロゲナーゼ遺伝子 | |
| JP4560998B2 (ja) | 発酵法によるl−グルタミンの製造法及びl−グルタミン生産菌 | |
| JP4595506B2 (ja) | L−アミノ酸生産菌及びl−アミノ酸の製造方法 | |
| KR101233739B1 (ko) | L-글루탐산 생산 미생물 및 l-글루탐산의 제조방법 | |
| JP4035855B2 (ja) | L−リジンの製造法 | |
| EP1010755B1 (en) | Method for producing L-Glutamic acid by fermentation | |
| JP5343303B2 (ja) | L−グルタミン酸生産菌及びl−グルタミン酸の製造方法 | |
| WO2007024010A1 (ja) | L−グルタミン酸生産菌及びl−グルタミン酸の製造方法 | |
| AU742609B2 (en) | Process for producing L-glutamic acid by fermentation method | |
| CN1316011C (zh) | 生产l-谷氨酰胺的方法和生产l-谷氨酰胺的细菌 | |
| JP2000201692A (ja) | 発酵法によるl―グルタミン酸の製造法 | |
| US8110381B2 (en) | L-glutamic acid-producing bacterium and method for production of L-glutamic acid | |
| JP2004187684A (ja) | L−グルタミンの製造法及びl−グルタミン生産菌 | |
| WO2004113550A1 (ja) | L−グルタミン酸の製造法 | |
| JP2007175016A (ja) | L−グルタミン酸生産菌及びl−グルタミン酸の製造方法 | |
| JP2010161970A (ja) | L−グルタミン酸生産菌及びl−グルタミン酸の製造方法 | |
| JP4239334B2 (ja) | 発酵法によるl−グルタミン酸の製造法 | |
| JP7549665B2 (ja) | L-分枝鎖アミノ酸生産能が強化された微生物及びそれを用いてl-分枝鎖アミノ酸を生産する方法 | |
| KR20230016505A (ko) | LacI 계열 DNA 결합 전사 조절자의 활성이 약화된 미생물 및 이를 이용한 L-글루탐산의 생산방법 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20060615 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20080704 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20080704 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20110510 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20111025 |