ES2828503T3 - Bloqueadores de los canales de sodio, método de preparación de los mismos y uso de los mismos - Google Patents
Bloqueadores de los canales de sodio, método de preparación de los mismos y uso de los mismos Download PDFInfo
- Publication number
- ES2828503T3 ES2828503T3 ES13846541T ES13846541T ES2828503T3 ES 2828503 T3 ES2828503 T3 ES 2828503T3 ES 13846541 T ES13846541 T ES 13846541T ES 13846541 T ES13846541 T ES 13846541T ES 2828503 T3 ES2828503 T3 ES 2828503T3
- Authority
- ES
- Spain
- Prior art keywords
- benzenesulfonamide
- thiazol
- oxy
- fluoro
- cyano
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- UBCKNKHYDRISKE-AKDWUGJWSA-N CN/C(/c1nc(-c(c(F)n2)ccc2F)ccc1Oc(c(Cl)c1)cc(F)c1S(Nc1c[s]cn1)(=O)=O)=C\C=N Chemical compound CN/C(/c1nc(-c(c(F)n2)ccc2F)ccc1Oc(c(Cl)c1)cc(F)c1S(Nc1c[s]cn1)(=O)=O)=C\C=N UBCKNKHYDRISKE-AKDWUGJWSA-N 0.000 description 1
- OOHQWMUSIRSPEV-UHFFFAOYSA-N C[n]1ncc(-c2cc(-c3ccnc(F)c3)ncc2Oc(c(Cl)c2)cc(F)c2S(Nc2c[s]cn2)(=O)=O)c1 Chemical compound C[n]1ncc(-c2cc(-c3ccnc(F)c3)ncc2Oc(c(Cl)c2)cc(F)c2S(Nc2c[s]cn2)(=O)=O)c1 OOHQWMUSIRSPEV-UHFFFAOYSA-N 0.000 description 1
- UOPBQJNBNDGVLC-UHFFFAOYSA-N C[n]1ncc(-c2nc(-c3cccc(F)c3)ccc2Oc(ccc(S(Nc2ncc[s]2)(=O)=O)c2)c2C#N)c1 Chemical compound C[n]1ncc(-c2nc(-c3cccc(F)c3)ccc2Oc(ccc(S(Nc2ncc[s]2)(=O)=O)c2)c2C#N)c1 UOPBQJNBNDGVLC-UHFFFAOYSA-N 0.000 description 1
- FLXLGCULLANAKJ-UHFFFAOYSA-N C[n]1ncc(-c2nc(-c3cccnc3F)ccc2Oc(c(C#N)c2)ccc2S(C)(Nc2ncc[s]2)(O)=O)c1 Chemical compound C[n]1ncc(-c2nc(-c3cccnc3F)ccc2Oc(c(C#N)c2)ccc2S(C)(Nc2ncc[s]2)(O)=O)c1 FLXLGCULLANAKJ-UHFFFAOYSA-N 0.000 description 1
- UNLOXDNMGOCIGH-UHFFFAOYSA-N C[n]1nccc1-c1cc(-c2cccnc2)ncc1Oc(c(F)c1)ccc1S(Nc1ncc[s]1)(=O)=O Chemical compound C[n]1nccc1-c1cc(-c2cccnc2)ncc1Oc(c(F)c1)ccc1S(Nc1ncc[s]1)(=O)=O UNLOXDNMGOCIGH-UHFFFAOYSA-N 0.000 description 1
- GGDRJZPMAJTCDG-UHFFFAOYSA-N C[n]1nccc1-c1cc(Cl)ccc1C(c(c(F)c1)ccc1S(Nc1ncc[s]1)(=O)=O)O Chemical compound C[n]1nccc1-c1cc(Cl)ccc1C(c(c(F)c1)ccc1S(Nc1ncc[s]1)(=O)=O)O GGDRJZPMAJTCDG-UHFFFAOYSA-N 0.000 description 1
- WVKAYDVCKHUMDL-UHFFFAOYSA-N N#Cc(cc(cc1)S(Nc2ncc[s]2)(=O)=O)c1Oc(c(-c(cccn1)c1F)c1)cnc1-c1ccccc1 Chemical compound N#Cc(cc(cc1)S(Nc2ncc[s]2)(=O)=O)c1Oc(c(-c(cccn1)c1F)c1)cnc1-c1ccccc1 WVKAYDVCKHUMDL-UHFFFAOYSA-N 0.000 description 1
- NEPGOBMQIRAJEP-UHFFFAOYSA-N N#Cc(cc(cc1)S(Nc2ncc[s]2)(=O)=O)c1Oc(c(-c1c[nH]nc1)c1)cnc1-c1ccccc1 Chemical compound N#Cc(cc(cc1)S(Nc2ncc[s]2)(=O)=O)c1Oc(c(-c1c[nH]nc1)c1)cnc1-c1ccccc1 NEPGOBMQIRAJEP-UHFFFAOYSA-N 0.000 description 1
- MYFPQHXXFPEIFK-UHFFFAOYSA-N N#Cc(cc(cc1)S(Nc2ncc[s]2)(=O)=O)c1Oc(c(-c1c[o]cc1)c1)cnc1-c(cn1)ccc1F Chemical compound N#Cc(cc(cc1)S(Nc2ncc[s]2)(=O)=O)c1Oc(c(-c1c[o]cc1)c1)cnc1-c(cn1)ccc1F MYFPQHXXFPEIFK-UHFFFAOYSA-N 0.000 description 1
- HNMQFDZCDGRWAQ-UHFFFAOYSA-N N#Cc(cc(cc1)S(Nc2ncc[s]2)(=O)=O)c1Oc(c(-c1c[o]cc1)c1)cnc1-c1ccnc(F)c1 Chemical compound N#Cc(cc(cc1)S(Nc2ncc[s]2)(=O)=O)c1Oc(c(-c1c[o]cc1)c1)cnc1-c1ccnc(F)c1 HNMQFDZCDGRWAQ-UHFFFAOYSA-N 0.000 description 1
- JQXDQYJMHMNWKR-UHFFFAOYSA-N N#Cc(cc(cc1)S(Nc2ncc[s]2)(=O)=O)c1Oc(c(-c1c[s]c(C2CC2)n1)c1)cnc1-c1ccccc1 Chemical compound N#Cc(cc(cc1)S(Nc2ncc[s]2)(=O)=O)c1Oc(c(-c1c[s]c(C2CC2)n1)c1)cnc1-c1ccccc1 JQXDQYJMHMNWKR-UHFFFAOYSA-N 0.000 description 1
- DGETVUPHYGUSLN-UHFFFAOYSA-N N#Cc(cc(cc1)S(Nc2ncc[s]2)(O)=O)c1Oc(c(-c(cc1)cnc1F)c1)cnc1-c1ccccc1 Chemical compound N#Cc(cc(cc1)S(Nc2ncc[s]2)(O)=O)c1Oc(c(-c(cc1)cnc1F)c1)cnc1-c1ccccc1 DGETVUPHYGUSLN-UHFFFAOYSA-N 0.000 description 1
- PLIYGMVQFZBOTB-UHFFFAOYSA-N O=S(c(c(F)c1)cc(Cl)c1Oc(c(-c1c[o]cc1)c1)cnc1-c1ccnc(F)c1)(Nc1c[s]cn1)=O Chemical compound O=S(c(c(F)c1)cc(Cl)c1Oc(c(-c1c[o]cc1)c1)cnc1-c1ccnc(F)c1)(Nc1c[s]cn1)=O PLIYGMVQFZBOTB-UHFFFAOYSA-N 0.000 description 1
- HJXZTLGRWABPRL-UHFFFAOYSA-N O=S(c(c(F)c1)cc(F)c1Oc(c(-c1cccnc1)c1)cnc1-c(cc1F)ccc1F)(Nc1c[s]cn1)=O Chemical compound O=S(c(c(F)c1)cc(F)c1Oc(c(-c1cccnc1)c1)cnc1-c(cc1F)ccc1F)(Nc1c[s]cn1)=O HJXZTLGRWABPRL-UHFFFAOYSA-N 0.000 description 1
- DTQVDTLACAAQTR-UHFFFAOYSA-N OC(C(F)(F)F)=O Chemical compound OC(C(F)(F)F)=O DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 1
- ZLZAOSYKDFEZNA-UHFFFAOYSA-N OC(c(cc1)ccc1S(Nc1ncc[s]1)(=O)=O)c(c(-c1c[o]cc1)c1)ccc1Cl Chemical compound OC(c(cc1)ccc1S(Nc1ncc[s]1)(=O)=O)c(c(-c1c[o]cc1)c1)ccc1Cl ZLZAOSYKDFEZNA-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing three or more hetero rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/425—Thiazoles
- A61K31/427—Thiazoles not condensed and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4427—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4427—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems
- A61K31/443—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems containing a five-membered ring with oxygen as a ring hetero atom
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P23/00—Anaesthetics
Abstract
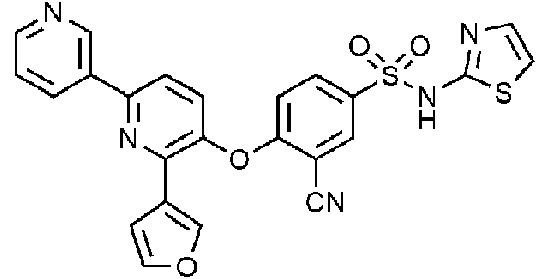
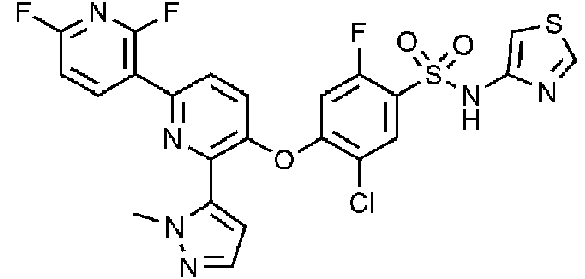
Un compuesto representado por la siguiente Fórmula 1 o una sal farmacéuticamente aceptable del mismo: **(Ver fórmula)** en el que R1 es arilo o heteroarilo seleccionado del grupo que consiste en fenilo, piridinilo, pirimidinilo, furanilo, isoxazolilo, pirazolilo y tienilo, en el que el arilo o heteroarilo no está sustituido o está sustituido con uno o dos sustituyentes seleccionados independientemente del grupo que consiste en C1-4 alquilo, C1-4 haloalquilo y halógeno, R2 es arilo o heteroarilo seleccionado del grupo que consiste en furanilo, imidazolilo, isoxazolilo, pirazolilo, piridinilo, pirimidinilo, tiazolilo y tienilo, en el que el arilo o heteroarilo no está sustituido o está sustituido con uno o dos sustituyentes seleccionados independientemente del grupo que consiste en C1-4 alquilo, C3-6 cicloalquilo, halógeno, morfolino, piperazinilo, piperidinilo, piridinilo y pirrolidinilo, R3 es tiazolilo o tiadiazolilo, X1 es CH y X2 es N, o X1 es N y X2 es CH, Y es O, Z es CR4, R4 es H, halógeno o CN, R5 es H o halógeno.
Description
DESCRIPCIÓN
Bloqueadores de los canales de sodio, método de preparación de los mismos y uso de los mismos
Campo técnico
La presente invención se refiere a un compuesto que tiene un efecto de bloqueo contra los canales iónicos de sodio, particularmente Nav1.7, un método de preparación del mismo y uso del mismo.
Antecedentes de la técnica
Varios canales (sensores moleculares) están presentes en el terminal de los nervios nociceptivos y varios canales de Na+ dependientes de voltaje (canales Nav) y canales de K+ (canales Kav) están presentes en los troncos nerviosos. Además, el potencial de membrana (es decir, el potencial generador) está presente en la terminal nerviosa por varios canales. Cuando dichos canales Nav se despolarizan por el potencial generador en la terminal nerviosa, juegan un papel importante en la generación de voltaje de acción. Así, los canales Nav juegan un papel importante en diversas enfermedades, incluida la epilepsia (ver Yogeeswari y otros, Curr. Drug Targets, 5(7):589-602 (2004)), arritmia (ver Noble D., Proc. Nail. Acad. Sci. USA, 99(9):5755-6 (2002)), miotonía (ver Cannon, S. C. y otros, Kidney Int., 57(3):772-9(2000)), ataxia (ver Meisler, M. H. y otros, Novartis Found Symp., 241:72-81 (2002)), esclerosis múltiple (ver Black, J. A. y otros, Proc. Nail. Acad. Sci. Us a , 97(21): 11598-11602 (2000) y Renganathan, M. M. y otros, Brain Res., 959 (2): 235-242 (2003)), síndrome del intestino irritable (ver Laird, J. M. y otros, J. Neurosci., 22(19):8352-3856 (2002)), incontinencia urinaria y dolor visceral (ver Yoshimura, N. S. y otros, J. Neurosci., 21(21): 8690-8696 (2001)), depresión (ver Hurley, S. C. y otros, Ann, Pharmacother, 36(5):860-873 (2002)) y dolor (ver Wood, J. N. y otros, J. Neurobiol., 61(1):55-71 (2004)). Actualmente, en humanos se encuentran diez canales Nav (Nav1.1-1.9 y Nax). Entre ellos, se sabe que cuatro canales (Nav1.3, Nav1.7, Nav1.8 y Nav1.9) tienen una estrecha conexión con la transmisión de señales de dolor y, por lo tanto, se reconocen como importantes objetivos analgésicos.
Existe un total de diez canales Nav conocidos que se resumen en la Tabla 1 a continuación. Entre los diez canales, nueve canales (Nav1.1-NaV1.9) forman canales (ver Goldin, A. L. y otros, Annu. Rev. Physiol., 63:871-894 (2001)). Entre ellos, Nav1.3, Nav1.6, Nav1.7, Nav1.8 y Nav1.9 se expresan en DRG.
Tabla 1
[Tabla 1]
En particular, se sabe que Nav1.7 se expresa principalmente en los ganglios de la raíz dorsal (DRG) y los ganglios simpáticos (ver Toledo-Aral, J. J. y otros, Proc. Natl. Acad. Sci. USA., 94:1527-1532 (1997), y Rush, A. M. y otros Proc. Natl. Acad. Sci. USA., 103:8245-8250 (2006)). En los GRD que son ganglios sensoriales, el canal Nav1.7 se expresa en neuronas de fibra A o C, pero con frecuencia se distribuye en neuronas pequeñas que tienen una conexión profunda con el dolor. Particularmente, el 85 % de los DRG están presentes en células definidas como nociceptores (ver Djouhri, L. y otros, J. Physiol., 546: 565-576 (2003)). Este hecho indica que Nav1.7 tiene una estrecha relación con el dolor.
El hecho de que el canal Nav1.7 tenga una estrecha conexión con el dolor está bien demostrado en los resultados no solo de estudios en animales, sino también de estudios de enfermedades humanas. Los resultados de estudios en animales indicaron que, cuando se produce inflamación, la transcripción genética de Nav1.7 aumenta significativamente y también aumenta la expresión de proteínas. Se cree que este aumento en la transcripción es atribuible a un aumento en el NGF. Se cree que el aumento de la expresión de Nav1.7 es la causa directa de un
aumento de la excitabilidad de las células sensoriales. En particular, cuando se elimina o reduce el gen del canal Nav1.7, el dolor inflamatorio se reduce considerablemente. Sin embargo, los estudios en animales no indican que la eliminación o reducción del gen del canal Nav1.7 reduzca el dolor neuropático. Sin embargo, hay mucha evidencia de que Nav1.7 está involucrado en el dolor neuropático en humanos.
Los resultados de experimentos de linajes que sienten dolor severo o ningún dolor proporcionan muchas respuestas para la investigación del dolor. Particularmente, estos resultados indican directamente la importancia de Nav1.7 para provocar dolor. Existen dos tipos de enfermedades hereditarias que causan dolor intenso. En el caso de eritromelalgia o eritermalgia entre estas enfermedades, a veces se siente un dolor intenso durante unas horas cuando el cuerpo está ligeramente caliente o se ejercita. En algunos casos, la piel se enrojece y la mano, el pie o la cara se hinchan. Los resultados de la investigación genética indicaron que SCN9A (el nombre del gen humano Nav1.7) está presente en sitios cromosómicos asociados con enfermedades. Hasta ahora se han encontrado nueve mutaciones de Nav1.7. Estas mutaciones reducen el umbral de activación o dan como resultado una desactivación lenta del canal. Por lo tanto, estas mutaciones pueden generar fácilmente un potencial de acción incluso tras la despolarización de algunas neuronas (ver Dib-Hajj, SD. y otros, Trends in Neurosci.,30,555-563:(2007)).
En el caso del trastorno de dolor paroxístico intenso (PEPD) que es otra enfermedad hereditaria, el dolor se siente en el transcurso de la vida diaria y se produce cuando se evacuan los intestinos o se estimula la región anal. Además del dolor, la pierna se enrojece. Como se conoce en la técnica, en el PEPD, ocurren ocho mutaciones en Nav1.7. Estas mutaciones ocurren principalmente en sitios que causan inactivación. El canal Nav tiene una bola de inactivación en el enlazador entre los dominios III y IV y una región receptora de péptidos en el enlazador entre los segmentos S5 y S6 de los dominios III y IV. Curiosamente, todas las mutaciones que causan PEPD ocurren en estas dos regiones. Estas causan un problema en la inactivación de Nav1.7. Como se esperaba, estas mutaciones provocan un problema en la inactivación de Nav1.7, resultando en una desactivación lenta del canal (ver Fertleman, C. R. y otros, Neuron, 52, 767-774 (2006)). Por lo tanto, aumenta la cantidad de corriente eléctrica que entra por el canal.
Aún otra enfermedad hereditaria es la indiferencia congénita al dolor (CIP). Esta enfermedad es el resultado de la mutación del canal Nav1.7 y existe en los linajes de Pakistán y China. Las personas que padecen esta enfermedad no sienten dolor (ver Cox, J. J. y otros, Nature, 444, 894-898 (2006)). Específicamente, las personas que padecen esta enfermedad no sienten casi ningún dolor, incluido el dolor causado por una quemadura y dolores de órganos (ver Cox, J. J. y otros, Nature, 444, 894-898 (2006)). La CIP provoca la pérdida de función del canal Nav1.7. Particularmente, una mutación en este canal inhibe la expresión de este canal. Por lo tanto, este canal no se expresa (ver Cox, J. J. y otros, Nature, 444, 894-898 (2006)). Curiosamente, el knock-out de Nav1.7 no influye en otras sensaciones (ver Dib-Hajj, SD. y otros, Trends in Neurosci., 30, 555-563 (2007)). Sin embargo, influye en la sensación olfativa. Este hecho indica directamente que Nav1.7 no se superpone con otros canales en la transmisión del dolor y que la función del mismo no se compensa con otros canales Nav.
Como se describió para las enfermedades anteriores, cuando una mutación en el canal Nav1.7 causa una ganancia de función, se siente un dolor intenso y cuando causa una pérdida de la función, el dolor se alivia. Este es un buen ejemplo clínico que muestra directamente que el canal Nav1.7 es la principal causa de dolor. Por tanto, se considera que un antagonista que inhibe este canal dará como resultado naturalmente un efecto analgésico.
Sin embargo, si el antagonista del canal Nav1.7 inhibe una pluralidad de canales Nav, incluido el canal Nav1.7, puede mostrar efectos adversos de diversas alteraciones del SNC, como visión borrosa, mareos, vómitos y depresión. Particularmente, si inhibe el canal Nav1.5, puede causar arritmia cardíaca e insuficiencia cardíaca, lo que puede resultar fatal. Por estas razones, la inhibición selectiva de los canales Nav1.7 es muy importante.
El dolor se puede clasificar en gran medida en tres tipos: dolor agudo, dolor inflamatorio y dolor neuropático. El dolor agudo desempeña una función protectora importante para mantener la seguridad de los organismos frente a los estímulos que pueden causar lesiones tisulares. Por lo tanto, generalmente es temporal e intenso. Por otro lado, el dolor inflamatorio puede ser persistente y su intensidad aumenta aún más. El dolor inflamatorio es mediado por diversas sustancias que se liberan durante la inflamación, incluida la sustancia P, histamina, ácidos, prostaglandina, bradicinina, CGRP, citocinas, ATP y otras sustancias (ver Julius, D. y otros, Nature, 413 (6852):203-210 (2001)). El tercer dolor es neuropático e involucra una lesión nerviosa o una lesión nerviosa causada por una infección viral. Provoca la reconstitución de circuitos con proteínas neuronales para provocar una "sensibilización" patológica, que puede resultar en un dolor crónico que dura varios años. Este tipo de dolor no ofrece la ventaja de la adaptabilidad y es difícil de tratar con los métodos terapéuticos actuales.
Particularmente, el dolor neuropático y el dolor intratable son grandes problemas médicos que no se han resuelto. Varios cientos de millones de pacientes padecen un dolor severo que no se inhibe bien con los métodos terapéuticos actuales. Los fármacos que se usan actualmente para el tratamiento del dolor incluyen AINE, inhibidores de la COX-2, opioides, antidepresivos tricíclicos y anticonvulsivos. El dolor neuropático es particularmente difícil de tratar, porque no responde bien a los opioides hasta que se alcanza una dosis alta. Actualmente, la gabapentina se usa más ampliamente como agente terapéutico contra el dolor neuropático, pero solo es eficaz en el 60 % de los pacientes y, por tanto, no es muy eficaz. Este fármaco es generalmente seguro, pero es problemático en términos de acción sedante en dosis altas.
En consecuencia, los estudios sobre el descubrimiento de nuevos reguladores del canal Nav1.7 (ver Wiffen, P. S. y otros, Cochrane Database Syst. Rev 3., (2000); Guay, D. R., Pharmacotherapy, 21(9):1070-1081 (2001)) y su uso para el tratamiento del dolor agudo (ver Wiffen, P. S. y otros, Cochrane Database Syst. Rev3., (2000)), agudo crónico (ver Guay, D. R., Pharmacotherapy, 21(9):1070-1081 (2001)), dolor inflamatorio (ver Gold, M. S., Proc. Natl. Acad. Sci. USA., 96(14): 7645-7649 (1999)) y dolor neuropático (Sandner-Kiesling, A. G. y otros, Acta. Anaesthesiol Scand., 46(10):1261-1264 (2002)) han sido llevados a cabo activamente por compañías farmacéuticas globales, incluidas Merck, AstraZeneca y similares (ver WO-A-2005/013914; WO-A-2005/054176; WO-A-2008/118758; EP-A-1088819; WO-A-2009/012242; US2010/0197655 A1; US7858786 B2; US7989481 B2; WO-A-2012/04743).
En consecuencia, los presentes inventores han realizado estudios sobre nuevos compuestos y como resultado, han encontrado que los compuestos que tienen estructuras químicas diferentes a las de los bloqueadores de los canales de sodio reportados hasta la fecha tienen excelentes efectos de bloqueo de los canales de sodio, completando así la presente invención. Los compuestos que caen dentro del alcance de la presente invención tienen principalmente actividad bloqueadora de los canales de sodio, pero no se excluye que los productos producidos por un entorno especial in vivo o un proceso metabólico después de la absorción de los compuestos in vivo actúen como agonistas y exhiban una acción farmacológica eficaz.
Divulgación de la invención
Problema técnico
Un objeto de la presente invención es proporcionar compuestos que tengan un efecto de bloqueo contra los canales iónicos de sodio, particularmente Nav1.7, un método de preparación de los mismos y el uso de los mismos.
Solución al problema
Para lograr el objeto anterior, la presente invención proporciona un compuesto representado por la siguiente Fórmula 1 o una sal farmacéuticamente aceptable del mismo:
en el que
R1 es arilo o heteroarilo seleccionado del grupo que consiste en fenilo, piridinilo, pirimidinilo, furanilo, isoxazolilo, pirazolilo y tienilo,
en el que el arilo o heteroarilo no está sustituido o está sustituido con uno o dos sustituyentes seleccionados independientemente del grupo que consiste en C1-4 alquilo, C1-4 haloalquilo y halógeno,
R2 es arilo o heteroarilo seleccionado del grupo que consiste en furanilo, imidazolilo, isoxazolilo, fenilo, pirazolilo, piridinilo, pirimidinilo, tiazolilo y tienilo,
en el que el arilo o heteroarilo no está sustituido o está sustituido con uno o dos sustituyentes seleccionados independientemente del grupo que consiste en C1-4 alquilo, C3-6 cicloalquilo, halógeno, morfolino, piperazinilo, piperidinilo, piridinilo y pirrolidinilo,
R3 es tiazolilo o tiadiazolilo,
X 1 es CH y X2 es N, o X 1 es N y X2 es CH,
Y es O,
Z es CR4 ,
R4 es H, halógeno o CN,
R5 es H o halógeno,
Preferentemente, R1 es fenilo no sustitudo o sustituido con uno o dos sustituyentes seleccionados independientemente del grupo que consiste en C1-4 haloalquilo y halógeno; piridinilo no sustituido o sustituido con uno o dos halógenos;
pirimidinilo no sustituido; furanilo no sustituido; isoxazolilo no sustituido; pirazolilo no sustituido o sustituido por C1-4 alquilo; o tienilo no sustituido.
Preferentemente, R1 es fenilo no sustitudo o sustituido con uno o dos sustituyentes seleccionados independientemente del grupo que consiste en CF3 , F y Cl; piridinilo no sustituido o sustituido por uno o dos F; pirimidinilo no sustituido; furanilo no sustituido; isoxazolilo no sustituido; pirazolilo no sustituido o sustituido por metilo; o tienilo no sustituido. Preferentemente, R2 es furanilo no sustituido; imidazolilo sustituido por piridinilo; isoxazolilo sustituido por dos C1-4 alquilo; fenilo no sustituido; pirazolilo no sustituido o sustituido por C1-4 alquilo o C3-6 cicloalquilo; piridinilo no sustituido o sustituido por uno o dos sustituyentes seleccionados del grupo que consiste en C1-4 alquilo, halógeno, morfolino, piperidinilo y pirrolidinilo; pirimidinilo no sustituido o sustituido por piperazinilo; tiazolilo sustituido por C3-6 cicloalquilo; o tienilo sustituido por uno o dos C1-4 alquilo.
Preferentemente, R2 es furanilo no sustituido; imidazolilo sustituido por piridinilo; isoxazolilo sustituido por dos metilo; fenilo no sustituido; pirazolilo no sustituido o sustituido por metilo o ciclopropilo; piridinilo no sustituido o sustituido por uno o dos sustituyentes seleccionados del grupo que consiste en metilo, F, Cl, morfolino, piperidinilo y pirrolidinilo; pirimidinilo no sustituido o sustituido por piperazinilo; tiazolilo sustituido por ciclopropilo; o tienilo sustituido por uno o dos metilo.
Preferentemente, R4 es H, F, Cl o CN.
Preferentemente, R5 es H o F.
Preferentemente,
R1 es arilo o heteroarilo seleccionado del grupo que consiste en fenilo, piridinilo, pirimidinilo, furanilo, isoxazolilo, pirazolilo y tienilo,
en el que el arilo o heteroarilo no está sustituido o está sustituido con uno o dos sustituyentes seleccionados independientemente del grupo que consiste en C1-4 alquilo, C1-4 haloalquilo y halógeno,
R2 es arilo o heteroarilo seleccionado del grupo que consiste en furanilo, imidazolilo, isoxazolilo, pirazolilo, piridinilo, pirimidinilo, tiazolilo y tienilo,
en el que el arilo o heteroarilo no está sustituido o está sustituido con uno o dos sustituyentes seleccionados independientemente del grupo que consiste en C1-4 alquilo, C3-6 cicloalquilo, halógeno, morfolino, piperazinilo, piperidinilo, piridinilo y pirrolidinilo,
R3 es tiazolilo o tiadiazolilo,
X 1 es CH y X2 es N, o X 1 es N y X2 es CH,
Y es O,
Z es CR4 ,
R4 es H, halógeno o CN,
R5 es H o halógeno.
Los compuestos representativos representados por la siguiente Fórmula 1 son los siguientes:
1) 3-ciano-4-((4-(furan-3-il)-6-fenilpiridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
2) 3-ciano-4-((4-(1-metil-1H-pirazol-5-il)-6-fenilpiridin-3-il)oxi)-N-(tiazol-2-il) bencenosulfonamida,
3) 3-ciano-4-((4-(furan-3-il)-6-fenilpiridin-3-il)oxi)-N-(1,2,4-tiadiazol-5-il)bencenosulfonamida,
4) 3-ciano-4-((4-(1-metil-1H-pirazol-5-il)-6-fenilpiridin-3-il)oxi)-N-(1,2,4-tiadiazol-5-il)bencenosulfonamida,
5) 3-ciano-4-(6-(3-fluorofenil)-4-(furan-3-il)piridin-3-iloxi)-N-(tiazol-2-il)benceno sulfonamida,
6) 3-ciano-4-(6-(2-fluorofenil)-4-(furan-3-il)piridin-3-iloxi)-N-(tiazol-2-il)benceno sulfonamida,
7) 3-ciano-4-(6-(4-fluorofenil)-4-(furan-3-il)piridin-3-iloxi)-N-(tiazol-2-il)benceno sulfonamida,
8) 3-ciano-4-(4-(furan-3-il)-6-(3-(trifluorometil)fenil)piridin-3-iloxi)-N-(tiazol-2-il)bencenosulfonamida,
) 3-ciano-4-(2'-fluoro-4-(furan-3-il)-2,4'-bipiridin-5-iloxi)-N-(tiazol-2-il)bencenosulfonamida, 0) 3-ciano-4-(2'-fluoro-4-(furan-3-il)-2,3'-bipiridin-5-iloxi)-N-(tiazol-2-il)bencenosulfonamida,
1) 3-ciano-4-(6'-fluoro-4-(furan-3-il)-2,3'-bipiridin-5-iloxi)-N-(tiazol-2-il)bencenosulfonamida,
2) 3-ciano-4-(2',6'-difluoro-4-(furan-3-il)-2,3'-bipiridin-5-iloxi)-N-(tiazol-2-il)bencenosulfonamida,
3) 3-ciano-4-(4-(furan-3-il)-2,3'-bipiridin-5-iloxi)-N-(tiazol-2-il)bencenosulfonamida,
4) 3-ciano-4-(4-(furan-3-il)-2,4'-bipiridin-5-iloxi)-N-(tiazol-2-il)bencenosulfonamida,
5) 3-ciano-4-(4-(furan-3-il)-6-(pirimidin-5-il)piridin-3-iloxi)-N-(tiazol-2-il)benceno sulfonamida,
6) 3-ciano-4-((4,6-di(furan-3-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
7) 4-((4,6-di(furan-3-il)piridin-3-il)oxi)-3-fluoro-N-(tiazol-2-il)bencenosulfonamida,
8) 3-ciano-4-((2'-fluoro-4-(1-metil-1H-pirazol-5-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida, 9) 3-ciano-4-((6'-fluoro-4-(1-metil-1H-pirazol-5-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida, 0) 3-ciano-4-((4-(furan-3-il)-6-(tiofen-3-il)piridin-3-il)oxi)-N-(tiazol-2-il)benceno sulfonamida,
1) 3-fluoro-4-((4-(1-metil-1H-pirazol-5-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida, 2) 3-fluoro-4-((4-(1-metil-1H-pirazol-5-il)-6-(tiofen-3-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida, 3) 3-ciano-4-((6-(4-fluorofenil)-4-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida, 4) 3-ciano-4-((6-(2-fluorofenil)-4-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida, 5) 3-ciano-4-((6-(furan-3-il)-4-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida, 6) 3-ciano-4-((6-(3-fluorofenil)-4-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida, 7) 3-ciano-4-((2'-fluoro-4-(1-metil-1H-pirazol-5-il)-[2,4'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida, 8) 4-((4,6-di(furan-3-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
9) 3-ciano-4-((2-fluoro-6'-fenil-[3,4'-bipiridin]-3'-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
0) 3-ciano-4-((6-fluoro-6'-fenil-[3,4'-bipiridin]-3'-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
1) 3-ciano-4-((2'-fluoro-6-fenil-[4,4'-bipiridin]-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
2) 3-ciano-4-((6-fluoro-5-metil-6'-fenil-[3,4'-bipiridin]-3'-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
3) 3-ciano-4-((6'-fenil-[3,4'-bipiridin]-3'-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
4) 3-ciano-4-((6-fenil-4-(pirimidin-5-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
5) 4-((3'-cloro-6-fenil-[4,4'-bipiridin]-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida,
6) 3-ciano-4-((2',3'-dicloro-6-fenil-[4,4'-bipiridin]-3-il)oxi)-N-(tiazol-2-il)benceno sulfonamida,
7) 3-ciano-4-((4-(3,5-dimetilisoxazol-4-il)-6-fenilpiridin-3-il)oxi)-N-(tiazol-2-il) bencenosulfonamida, 8) 3-ciano-4-((4-(1-metil-1H-pirazol-4-il)-6-fenilpiridin-3-il)oxi)-N-(tiazol-2-il) bencenosulfonamida, 9) 3-ciano-4-((6-fenil-4-(1H-pirazol-4-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosu lfonamida,
0) 3-ciano-4-((6-fenil-[4,4'-bipiridin]-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
1) 3-ciano-4-((4-(2,5-dimetiltiofen-3-il)-6-fenilpiridin-3-il)oxi)-N-(tiazol-2-il) bencenosulfonamida,
) 3-ciano-4-((4-(5-metiltiofen-2-il)-6-fenilpiridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
) 3-ciano-4-((4-(2-ciclopropiltiazol-4-il)-6-fenilpiridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
) 3-ciano-4-((4-(1-ciclopropil-1H-pirazol-4-il)-6-fenilpiridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
) 3-ciano-4-((4-(furan-3-il)-6-(1H-pirazol-4-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
) 3-ciano-4-((4-(furan-3-il)-6-(1-metil-1H-pirazol-4-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
) 3-fluoro-4-((2'-fluoro-4-(furan-3-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)benceno sulfonamida,
) 3-fluoro-4-((6'-fluoro-4-(furan-3-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)benceno sulfonamida,
) 3-ciano-4-((6-fluoro-[3,2':4',3"-terpiridin]-5'-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
) 3-ciano-4-((6'-(3-fluorofenil)-[3,4'-bipiridin]-3'-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
) 3-ciano-4-((2-fluoro-[3,2':4',3"-terpiridin]-5'-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
) 3-ciano-4-((6'-(2-fluorofenil)-[3,4'-bipiridin]-3'-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
) 3-ciano-4-((2,6-difluoro-[3,2':4',4"-terpiridin]-5'-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
) 4-((4,6-bis(1-metil-1H-pirazol-4-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida,
) 4-((4,6-bis(1-metil-1H-pirazol-4-il)piridin-3-il)oxi)-3-ciano-N-(1,2,4-tiadiazol-5-il)bencenosulfonamida,
) 5-cloro-2-fluoro-4-((2'-fluoro-4-(furan-3-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
) 5-cloro-2-fluoro-4-((6'-fluoro-4-(furan-3-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
) 5-cloro-4-((2',6'-difluoro-4-(furan-3-il)-[2,3'-bipiridin]-5-il)oxi)-2-fluoro-N-(tiazol -4-il)bencenosulfonamida, ) 5-cloro-2-fluoro-4-((6-(3-fluorofenil)-4-(furan-3-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
) 5-cloro-2-fluoro-4-((6-(2-fluorofenil)-4-(furan-3-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
) 5-cloro-2-fluoro-4-((6-(4-fluorofenil)-4-(furan-3-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
) 5-cloro-2-fluoro-4-((2'-fluoro-4-(furan-3-il)-[2,4'-bipiridin]-5-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
) 5-cloro-2-fluoro-4-((6-(2-fluorofenil)-4-(1-metil-1H-pirazol-4-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida .2- trifluoroacetato,
) 5-cloro-2-fluoro-4-((6-(3-fluorofenil)-4-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida, ) 5-cloro-2-fluoro-4-((6-(4-fluorofenil)-4-(1-metil-1H-pirazol-4-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida .2- trifluoroacetato,
) 5-cloro-4-((6-(2,4-difluorofenil)-4-(1-metil-1H-pirazol-4-il)piridin-3-il)oxi)-2-fluoro-N-(tiazol-4-il)bencenosulfonamida .2- trifluoroacetato,
) 5-cloro-4-((6-(3,4-difluorofenil)-4-(1-metil-1H-pirazol-4-il)piridin-3-il)oxi)-2-fluoro-N-(tiazol-4-il)bencenosulfonamida .2- trifluoroacetato,
) 5-cloro-2-fluoro-4-((2'-fluoro-4-(1-metil-1H-pirazol-4-il)-[2,4'-bipiridin]-5-il)oxi )-N-(tiazol-4-il)bencenosulfonamida .2- trifluoroacetato,
) 5-cloro-2-fluoro-4-((2'-fluoro-4-(1-metil-1H-pirazol-4-il)-[2,3'-bipiridin]-5-il)oxi )-N-(tiazol-4-il)bencenosulfonamida .2- trifluoroacetato,
) 5-cloro-2-fluoro-4-((6'-fluoro-4-(1-metil-1H-pirazol-4-il)-[2,3'-bipiridin]-5-il)oxi )-N-(tiazol-4-il)bencenosulfonamida .2- trifluoroacetato,
) 5-cloro-2-fluoro-4-((6-(3-fluorofenil)-4-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
72) 5-cloro-2-fluoro-4-((6-(3-fluorofenil)-4-(2-(piperazin-1-il)pirimidin-4-il)piridin-3 -il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
73) 5-cloro-2-fluoro-4-((6'-(3-fluorofenil)-[3,4'-bipiridin]-3'-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
74) 5-cloro-2-fluoro-4-((6'-(3-fluorofenil)-[3,4'-bipiridin]-3'-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
75) 5-cloro-2-fluoro-4-((2"-fluoro-[3,4':2',4"-terpiridin]-5'-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
76) 5-cloro-2-fluoro-4-((6-(3-fluorofenil)-4-(pirimidin-5-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida, 77) 5-cloro-2-fluoro-4-((2'-fluoro-4-(pirimidin-5-il)-[2,4'-bipiridin]-5-il)oxi)-N-(tiazol -4-il)bencenosulfonamida, 78) 5-cloro-2-fluoro-4-((6-(3-fluorofenil)-4-(1H-pirazol-4-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida, 79) 5-cloro-2-fluoro-4-((2'-fluoro-6-(3-fluorofenil)-[4,4'-bipiridin]-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida, 80) 5-cloro-4-((6-(3,4-difluorofenil)-2'-fluoro-[4,4'-bipiridin]-3-il)oxi)-2-fluoro-N-(tiazol-4-il)bencenosulfonamida, 81) 5-cloro-4-((6'-(5-cloro-2-fluorofenil)-[3,4'-bipiridin]-3'-il)oxi)-2-fluoro-N-(tiazol-4-il)bencenosulfonamida, 82) 5-cloro-4-((6'-(3,4-difluorofenil)-[3,4'-bipiridin]-3'-il)oxi)-2-fluoro-N-(tiazol-4-il)bencenosulfonamida,
83) 3-ciano-4-((6-(3-fluorofenil)-4-(1H-pirazol-4-il)piridin-3-il)oxi)-N-(tiazol-4-il) bencenosulfonamida,
84) 3-ciano-4-((6'-(3-fluorofenil)-[3,4'-bipiridin]-3'-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
85) 3-ciano-4-((6'-(3,4-difluorofenil)-[3,4'-bipiridin]-3'-il)oxi)-N-(tiazol-4-il)benceno sulfonamida,
86) 3-ciano-4-((6'-(3-fluoro-4-(trifluorometil)fenil)-[3,4'-bipiridin]-3'-il)oxi)-N-(tiazol-4-il)bencenosulfonamida, 87) 2,5-difluoro-4-((6'-(3-fluorofenil)-[3,4'-bipiridin]-3'-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
88) 4-((6'-(3,4-difluorofenil)-[3,4'-bipiridin]-3'-il)oxi)-2,5-difluoro-N-(tiazol-4-il)bencenosulfonamida,
89) 2,5-difluoro-4-((6'-(3-fluoro-4-(trifluorometil)fenil)-[3,4'-bipiridin]-3'-il)oxi)-N-(tiazol-4-il)bencenosulfonamida, 90) 3-ciano-4-((6-(4-fluorofenil)-4-(1H-pirazol-4-il)piridin-3-il)oxi)-N-(tiazol-4-il) bencenosulfonamida,
91) 3-ciano-4-((6-(3,4-difluorofenil)-4-(1H-pirazol-4-il)piridin-3-il)oxi)-N-(tiazol-4 -il)bencenosulfonamida,
92) 3-ciano-4-((6-(3-fluorofenil)-4-(pirimidin-5-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
93) 3-ciano-4-((6-(3,4-difluorofenil)-4-(pirimidin-5-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
94) 3-ciano-4-((6-(3-fluoro-4-(trifluorometil)fenil)-4-(pirimidin-5-il)piridin-3-il)oxi )-N-(tiazol-4-il)bencenosulfonamida, 95) 2,5-difluoro-4-((6-(3-fluorofenil)-4-(pirimidin-5-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
96) 4-((6-(3,4-difluorofenil)-4-(pirimidin-5-il)piridin-3-il)oxi)-2,5-difluoro-N-(tiazol-4-il)bencenosulfonamida, 97) 2,5-difluoro-4-((6-(3-fluoro-4-(trifluorometil)fenil)-4-(pirimidin-5-il)piridin-3-il) oxi)-N-(tiazol-4-il)bencenosulfonamida,
98) 5-cloro-4-((6-(3,4-difluorofenil)-4-(1H-pirazol-4-il)piridin-3-il)oxi)-2-fluoro-N-( tiazol-4-il)bencenosulfonamida, 99) 5-cloro-2-fluoro-4-((6'-(3-fluorofenil)-5-(pirrolidin-1-il)-[3,4'-bipiridin]-3'-il)oxi) -N-(tiazol-4-il)bencenosulfonamida, 100) 5-cloro-2-fluoro-4-((6-(3-fluorofenil)-4-(1-(piridin-3-il)-1H-imidazol-4-il)piridin -3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
101) 5-cloro-2-fluoro-4-((6-(3-fluorofenil)-2'-morfolino-[4,4'-bipiridin]-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida, 102) 5-cloro-2-fluoro-4-((6-(3-fluorofenil)-2'-(piperidin-1-il)-[4,4'-bipiridin]-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida, 103) 3-ciano-4-((2'-fluoro-6-(furan-3-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)benceno sulfonamida,
104) 3-ciano-4-((6'-fluoro-6-(furan-3-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)benceno sulfonamida, 105) 3-ciano-4-((6-(furan-3-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
106) 3-ciano-4-((2-(furan-3-il)-6-(pirimidin-5-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
107) 3-ciano-4-((2'-fluoro-6-(1-metil-1H-pirazol-5-il)-[2,4'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida, 108) 3-ciano-4-((6-(2-fluorofenil)-2-(furan-3-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
109) 3-ciano-4-((6-(4-fluorofenil)-2-(furan-3-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
110) 3-ciano-4-((6-(3-fluorofenil)-2-(furan-3-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
111) 3-ciano-4-((6-(furan-3-il)-[2,4'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
112) 3-ciano-4-((2'-fluoro-6-(furan-3-il)-[2,4'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)benceno sulfonamida,
113) 3-ciano-4-((2-(furan-3-il)-6-(tiofen-3-il)piridin-3-il)oxi)-N-(tiazol-2-il)benceno sulfonamida,
114) 3-ciano-4-((2,6-di(furan-3-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
115) 3-ciano-4-((6'-fluoro-6-(1-metil-1H-pirazol-5-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida, 116) 3-ciano-4-((2'-fluoro-6-(1-metil-1H-pirazol-5-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida, 117) 3-ciano-4-((6-(3-fluorofenil)-2-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida, 118) 3-ciano-4-((6-(2-fluorofenil)-2-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida, 119) 3-ciano-4-((2-(1-metil-1H-pirazol-5-il)-6-(tiofen-3-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
120) 3-ciano-4-((6-(1-metil-1H-pirazol-4-il)-2-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida, 121) 3-ciano-4-((6-(isoxazol-4-il)-2-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida, 122) 3-ciano-4-((6-(3-fluorofenil)-2-(1-metil-1H-pirazol-4-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida, 123) 3-ciano-4-((2'-fluoro-6-(1-metil-1H-pirazol-4-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida, 124) 3-ciano-4-((6'-fluoro-6-(1-metil-1H-pirazol-4-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida, 125) 3-ciano-4-((2'-fluoro-6-(1-metil-1H-pirazol-4-il)-[2,4'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida, 126) 3-ciano-4-((2',6'-difluoro-6-(1-metil-1H-pirazol-4-il)-[2,3'-bipiridin]-5-il)oxi)-N-( tiazol-2-il)bencenosulfonamida, 127) 3-ciano-4-((2',6'-difluoro-6-(furan-3-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
128) 3-ciano-4-((2',6'-difluoro-6-(1-metil-1H-pirazol-5-il)-[2,3'-bipiridin]-5-il)oxi)-N-( tiazol-2-il)bencenosulfonamida, 129) 5-cloro-4-((2',6'-difluoro-6-(furan-3-il)-[2,3'-bipiridin]-5-il)oxi)-2-fluoro-N-(tiazol -4-il)bencenosulfonamida, 130) 5-cloro-2-fluoro-4-((6'-fluoro-6-(furan-3-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
131) 5-cloro-2-fluoro-4-((6-(4-fluorofenil)-2-(furan-3-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
132) 5-cloro-2-fluoro-4-((2'-fluoro-6-(furan-3-il)-[2,4'-bipiridin]-5-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
133) 5-cloro-2-fluoro-4-((6-(2-fluorofenil)-2-(furan-3-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
134) 5-cloro-4-((2',6'-difluoro-6-(1-metil-1H-pirazol-5-il)-[2,3'-bipiridin]-5-il)oxi)-2-fluoro-N-(tiazol-4-il)bencenosulfonamida,
135) 5-cloro-2-fluoro-4-((6-(4-fluorofenil)-2-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida, 136) 5-cloro-2-fluoro-4-((6-(2-fluorofenil)-2-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
137) 5-cloro-2-fluoro-4-((6'-fluoro-6-(1-metil-1H-pirazol-5-il)-[2,3'-bipiridin]-5-il)oxi )-N-(tiazol-4-il)bencenosulfonamida, Los compuestos 138-157 no caen bajo la Fórmula (1) y son ejemplos de referencia.
138) 4-((4-cloro-2-(1-metil-1H-pirazol-5-il)fenil)(hidroxi)metil)-N-(tiazol-2-il)bencenosulfonamida,
139) 4-((4-cloro-2-(1H-pirazol-4-il)fenil)(hidroxi)metil)-3-fluoro-N-(tiazol-2-il)bencenosulfonamida,
140) 4-((4-cloro-2-(furan-3-il)fenil)(hidroxi)metil)-3-fluoro-N-(tiazol-2-il)bencenosulfonamida,
141) 4-((2,4-di(furan-3-il)fenil)(hidroxi)metil)-3-fluoro-N-(tiazol-2-il)bencenosulfonamida,
142) 3-fluoro-4-(hidroxi(2-(1-metil-1H-pirazol-5-il)fenil)metil)-N-(tiazol-2-il)bencenosulfonamida,
143) 4-((4-cloro-2-(furan-3-il)fenil)(hidroxi)metil)-N-(tiazol-2-il)bencenosulfonamida,
144) 4-((4-cloro-2-(1-metil-1H-pirazol-5-il)fenil)(hidroxi)metil)-3-fluoro-N-(tiazol-2-il)bencenosulfonamida,
145) 4-((4-cloro-2-(piridin-3-il)fenil)(hidroxi)metil)-3-fluoro-N-(tiazol-2-il)bencenosulfonamida,
146) 4-((4-cloro-2-(piridin-4-il)fenil)(hidroxi)metil)-3-fluoro-N-(tiazol-2-il)bencenosulfonamida,
147) 4-((4-cloro-2-(piridin-4-il)fenil)(hidroxi)metil)-N-(tiazol-2-il)bencenosulfonamida,
148) 4-((4-cloro-2-(piridin-3-il)fenil)(hidroxi)metil)-N-(tiazol-2-il)bencenosulfonamida,
149) 4-((2,4-di(furan-3-il)fenil)(hidroxi)metil)-N-(tiazol-2-il)bencenosulfonamida,
150) 4-((4-(2-fluoropiridin-3-il)-2-(furan-3-il)fenil)(hidroxi)metil)-N-(tiazol-2-il)bencenosulfonamida,
151) 4-((4-(6-fluoropiridin-3-il)-2-(furan-3-il)fenil)(hidroxi)metil)-N-(tiazol-2-il)bencenosulfonamida,
152) 4-((2'-fluoro-3-(furan-3-il)-[1,1'-bifenil]-4-il)(hidroxi)metil)-N-(tiazol-2-il)bencenosulfonamida,
153) 4-((3'-fluoro-3-(furan-3-il)-[1,1'-bifenil]-4-il)(hidroxi)metil)-N-(tiazol-2-il)bencenosulfonamida,
154) 4-((4'-fluoro-3-(furan-3-il)-[1,1'-bifenil]-4-il)(hidroxi)metil)-N-(tiazol-2-il)bencenosulfonamida,
155) 3-fluoro-4-((2-(furan-3-il)piridin-3-il)(hidroxi)metil)-N-(tiazol-2-il)bencenosulfonamida,
156) 4-((2-(furan-3-il)piridin-3-il)(hidroxi)metil)-N-(tiazol-2-il)bencenosulfonamida, y
157) 3-fluoro-4-(hidroxi(2-fenilpiridin-3-il)metil)-N-(tiazol-2-il)bencenosulfonamida.
La presente invención proporciona un método para preparar el compuesto representado por la Fórmula 1.
Por ejemplo, la presente invención proporciona un método para preparar un compuesto representado por la Fórmula 1 en el que Y es O, el método es el que se muestra en el siguiente Esquema de reacción 1:
(en donde R1 , R2 , R3 , R5 , X 1 , X2 y Z son como se definieron anteriormente y X es un halógeno. Preferentemente, X es fluoro.)
En la reacción anterior, se deja que un compuesto representado por la Fórmula 2-1 reaccione con un compuesto representado por la Fórmula 2-2. La reacción se lleva a cabo preferentemente en presencia de Cs2CO3 y un solvente para la reacción es preferentemente DMF.
Por ejemplo, la presente descripción también proporciona un método para preparar un compuesto representado por la Fórmula 1 en el que Y es CH (OH), el método es el que se muestra en el siguiente Esquema de reacción 2:
(en donde Ri , R2 , R3 , R5 , X i , X2 y Z son como se definieron anteriormente y X es un halógeno. Preferentemente, X es cloro.)
En la reacción que se muestra en el Esquema de reacción 2, se deja que un compuesto representado por la Fórmula 2-3 reaccione con un compuesto representado por la Fórmula 2-4. La reacción se lleva a cabo preferentemente en presencia de n-BuLi y un solvente para la reacción es preferentemente THF.
Por ejemplo, la presente invención también proporciona un método para preparar un compuesto representado por la Fórmula 1 en donde R1 es arilo o heteroarilo seleccionado del grupo que consiste en fenilo, piridinilo, pirimidinilo, furanilo, isoxazolilo, pirazolilo y tienilo (en donde el arilo o heteroarilo no está sustituido o está sustituido con uno o dos sustituyentes seleccionados independientemente del grupo que consiste en C1-4 alquilo, C1-4 haloalquilo y halógeno), el método es el que se muestra en el siguiente Esquema de reacción 3:
(en el que R2 , R3 , R5 , X 1 , X2 , Y y Z son como se definieron anteriormente y X es un halógeno. Preferentemente, X es cloro.)
En la reacción que se muestra en el Esquema de reacción 3, se deja que un compuesto representado por la Fórmula 2-5 reaccione con un compuesto representado por la Fórmula 2-6. La reacción se lleva a cabo preferentemente en presencia de Pd(PPh3)4 y Na2CO3 , un solvente para el la reacción es preferentemente DMF.
Además, se puede obtener una sal de metal farmacéuticamente aceptable del compuesto representado por la Fórmula 1 usando una base de acuerdo con un método convencional. Por ejemplo, se puede obtener una sal de metal farmacéuticamente aceptable del compuesto representado por la Fórmula 1 al disolver el compuesto de Fórmula 1 en un exceso de una solución de hidróxido de metal alcalino o de hidróxido de metal alcalinotérreo, filtrando la sal del compuesto no disuelto, evaporando y secando el filtrado. En la presente descripción, la sal metálica preparada es particularmente de preferencia una sal de sodio, potasio o calcio y esta sal metálica se puede hacer reaccionar con una sal adecuada (por ejemplo, nitrato).
Una sal o solvato farmacéuticamente no aceptable del compuesto representado por la Fórmula 1 se puede usar como intermedio en la preparación del compuesto representado por la Fórmula 1 o una sal o solvato farmacéuticamente aceptable del mismo.
Los compuestos de la invención representados por la Fórmula 1 incluyen, además de sus sales farmacéuticamente aceptables, posibles solvatos e hidratos que pueden prepararse a partir de ellos, así como todos los posibles estereoisómeros. Los solvatos, hidratos y estereoisómeros de los compuestos representados por la Fórmula 1 pueden prepararse a partir de los compuestos de la Fórmula 1 usando métodos convencionales.
Además, el compuesto de la invención representado por la Fórmula 1 puede prepararse en forma cristalina o amorfa. Cuando el compuesto representado por la Fórmula 1 se prepara en forma cristalina, éste puede hidratarse o solvatarse opcionalmente. La presente invención incluye dentro de su alcance hidratos estequiométricos de los compuestos representados por la Fórmula 1 así como compuestos que contienen cantidades variables de agua. Los solvatos de los compuestos de la invención representados por la Fórmula 1 incluyen todos los solvatos estequiométricos y solvatos no estequiométricos.
La presente invención proporciona una composición farmacéutica para prevenir o tratar una enfermedad relacionada con los bloqueadores de los canales de sodio que comprende el compuesto representado por la Fórmula 1 o una sal, hidrato, solvato o isómero farmacéuticamente aceptables del mismo como ingrediente activo. Además, la presente
invención proporciona un método para tratar o prevenir una enfermedad relacionada con los bloqueadores de los canales de sodio, que comprende administrar a un sujeto que lo necesite una composición farmacéutica que comprende el compuesto representado por la Fórmula 1 o una sal, hidrato, solvato o isómero farmacéuticamente aceptables del mismo como ingrediente activo. Además, la presente invención proporciona una composición farmacéutica para su uso en la prevención o el tratamiento de una enfermedad relacionada con los bloqueadores de los canales de sodio, que comprende el compuesto representado por la Fórmula 1 o una sal, hidrato, solvato o isómero farmacéuticamente aceptables del mismo como ingrediente activo. Además, la presente invención proporciona el uso de una composición farmacéutica que comprende el compuesto representado por la Fórmula 1 o una sal, hidrato, solvato o isómero farmacéuticamente aceptables del mismo como ingrediente activo, para la fabricación de un medicamento para prevenir o tratar una enfermedad relacionada con los bloqueadores de los canales de sodio.
En la presente descripción, las enfermedades incluyen dolor agudo, dolor crónico, dolor neuropático, dolor postoperatorio, migraña, artralgia, neuropatía, lesión nerviosa, neuropatía diabética, enfermedad neuropática, epilepsia, arritmia, miotonía, ataxia, esclerosis múltiple, síndrome del intestino irritable, incontinencia urinaria, dolor visceral, depresión, eritromelalgia, trastorno de dolor paroxístico intenso (PEPD) y similares.
La composición farmacéutica de la presente invención puede formularse en formas de dosificación oral o parenteral de acuerdo con los estándares farmacéuticos estándar. Estas formulaciones pueden contener, además del ingrediente activo, aditivos tales como un portador, adyuvante o diluyente farmacéuticamente aceptables. Los ejemplos de portadores adecuados incluyen, pero no se limitan a, solución salina fisiológica, polietilenglicol, etanol, aceite vegetal y miristato de isopropilo y los ejemplos de diluyentes adecuados incluyen, pero no se limitan a, lactosa, dextrosa, sacarosa, manitol, sorbitol, celulosa y/o glicina. Además, los compuestos de la presente invención pueden disolverse en aceite, propilenglicol u otros disolventes, que se usan generalmente en la preparación de soluciones inyectables. Además, los compuestos de la presente invención pueden formularse en pomadas o cremas para aplicación tópica.
A continuación, se describirán los métodos de formulación y los excipientes, pero el alcance de la presente invención no se limita a estos ejemplos.
Los compuestos de la presente invención se pueden usar en forma de sales o solvatos farmacéuticamente aceptables y también pueden usarse solos o en asociación apropiada, así como en combinación con otros compuestos farmacéuticamente activos.
Los compuestos de la presente invención pueden formularse en inyecciones disolviendo, suspendiendo o emulsionando solventes solubles en agua como solución salina o dextrosa al 5 %, o en solventes insolubles en agua como aceites vegetales, glicéridos de ácidos grasos sintéticos, ésteres de ácidos grasos superiores o propilenglicol. Las formulaciones de la presente invención pueden incluir cualquiera de los aditivos convencionales tales como agentes disolventes, agentes isotónicos, agentes de suspensión, emulsionantes, estabilizantes y conservantes.
La dosis preferida del compuesto de la presente invención varía dependiendo del estado y el peso del paciente, la gravedad de la enfermedad, la forma del fármaco, la vía y la duración de la administración y los expertos en la técnica pueden seleccionarla adecuadamente. Sin embargo, para lograr los efectos deseados, el compuesto de la presente invención se puede administrar a una dosis diaria de 0,0001-100 mg/kg (peso) y preferentemente 0,001-100 mg/kg (peso). El compuesto de la presente invención puede administrarse por vía oral o parenteral en una sola dosis en una sola dosis o en múltiples dosis diarias.
La composición de la presente invención puede contener el compuesto de la presente invención en una cantidad del 0,001 al 99 % en peso y preferentemente del 0,01 al 60 % en peso, dependiendo del modo de administración.
La composición farmacéutica de la presente invención puede administrarse a mamíferos, incluidas ratas, ratones, seres humanos, animales domésticos y similares, por diversas vías. Se pueden contemplar todas las vías de administración y, por ejemplo, la composición se puede administrar por vía oral, intrarrectal o mediante inyección intravenosa, intramuscular, subcutánea, intrauterina, intratecal o intracerebroventricular.
Efectos ventajosos de la invención
Como se describió anteriormente, el compuesto de la invención representado por la Fórmula 1 o una sal, hidrato, solvato o estereoisómero farmacéuticamente aceptables del mismo puede usarse eficazmente para la prevención o el tratamiento del dolor, por ejemplo, dolor agudo, dolor crónico, dolor neuropático, postoperatorio. dolor, migraña, artralgia, neuropatía, lesión nerviosa, neuropatía diabética, enfermedad neuropática, epilepsia, arritmia, miotonía, ataxia, esclerosis múltiple, síndrome del intestino irritable, incontinencia urinaria, dolor visceral, depresión, eritromelalgia o trastorno de dolor extremo paroxismal (PEPD).
Modo para la llevar a cabo la invención
A continuación, la presente invención se describirá con más detalle con referencia a los ejemplos de preparación y ejemplos. Debe entenderse, sin embargo, que estos ejemplos de preparación y ejemplos tienen fines ilustrativos y no pretenden limitar el alcance de la presente invención.
Ejemplo 1: Preparación de 3-ciano-4-(4-(furan-3-il)-6-fenilpiridin-3-iloxi)-N-(tiazol-2-il)bencenosolfonamida
10 mg (0,04 mmol) de 4-(furan-3-il)-6-fenilpiridin-3-ol se disolvió en 1,5 mL de N,N-dimetilformamida y 27 mg (0,08 mmol) de Cs2CO3 se añadieron a esto, seguido por agitación a temperatura ambiente durante 10 minutos. Después, 15 mg (0,04 mmol) de 3-ciano-4-fluoro-N-(tiazol-2-il)bencenosulfonamida se añadió a esto y la solución se agitó a temperatura ambiente durante 3 horas. Después del completamiento de la reacción comprobado por TLC, el solvente se eliminó y el material restante se diluyó con acetato de etilo y se lavó con cloruro de sodio saturado. La capa orgánica se recogió, se secó con sulfato de magnesio para eliminar el agua y se concentró a presión reducida y el residuo se purificó por cromatografía de columna (solvente de desarrollo: acetato de etilo = 100 %) para obtener 16,0 mg (80 % de rendimiento) del compuesto del título.
1H NMR (CDCl3, 500MHz) 58,48 (1H), 7,98 (3H), 7,93 (1H), 7,91 (1H), 7,51 (3H), 7,46 (1H), 7,13 (1H), 6,82 (2H), 6,59 (1H)
Ejemplo 2: Preparación de 3-ciano-4-((4-(1-metil-1H-pirazol-5-il)-6-fenilpiridin-3-iloxi)-N-(tiazol-2-il)bencenosulfonamida
10 mg (0,04 mmol) de 4-(1-metil-1H-pirazol-5-il)-6-fenilpiridin-3-ol se disolvió en 1,5 mL de N,N-dimetilformamida y 26 mg (0,08 mmol) de Cs2CO3 se añadieron a esto, seguido por agitación a temperatura ambiente durante 10 minutos. Después, 15 mg (0,04 mmol) de 3-ciano-4-fluoro-N-(tiazol-2-il)bencenosulfonamida se añadió a esto y la solución se agitó a temperatura ambiente durante 3 horas. Después del completamiento de la reacción comprobado por TLC, el solvente se eliminó y el material restante se diluyó con acetato de etilo y se lavó con cloruro de sodio saturado. La capa orgánica se recogió, se secó con sulfato de magnesio para eliminar el agua y se concentró a presión reducida y el residuo se purificó por cromatografía de columna (solvente de desarrollo: acetato de etilo = 100 %) para obtener 17,1 mg (83 % de rendimiento) del compuesto del título.
1H NMR (CDCls, 500MHz) 558,61 (1H), 8,13 (1H), 8,01 (2H), 7,92 (1H), 7,81 (1H), 7,66 (1H), 7,48 (3H), 7,12 (1H), 6,73 (1H), 6,59 (1H), 6,35 (1H), 3,93 (3H)
Ejemplo 3: Preparación de 3-ciano-4-(4-(furan-3-il)-6-fenilpiridin-3-iloxi)-N-(1,2,4-tiadiazol-5-il)bencenosulfonamida
17,6 mg (88 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 1, excepto que se usó 3-ciano-4-fluoro-N-(1,2,4-tiadiazol-5-il)bencenosulfonamida en lugar de 3-ciano-4-fluoro-N-(tiazol-2-il)bencenosulfonamida.1
1H NMR (CDCls , 500MHz) 58,49 (1H), 8,23 (1H), 8,16 (1H), 8,11 (1H), 8,07 (2H), 7,99 (2H), 7,60 (1H), 7,51 (2H), 7,46 (1H), 7,01 (1H), 6,92 (1H)
Ejemplo 4: Preparación de 3-ciano-4-((4-(1-metil-1H-pirazol-5-il)-6-fenilpiridin-3-il)oxi)-N-(1,2,4-tiadiazol-5-il)bencenosulfonamida
16,7 mg (81 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 2, excepto que se usó 3-ciano-4-fluoro-N-(1,2,4-tiadiazol-5-il)bencenosulfonamida en lugar de 3-ciano-4-fluoro-N-(tiazol-2-il)bencenosulfonamida. 1H NMR (CDCh, 500MHz) 58,71 (1H), 8,10 (3H), 8,08 (1H), 7,97 (1H), 7,94 (1H), 7,51 (2H), 7,48 (1H), 7,38 (1H), 6,93 (1H), 6,37 (1H), 3,89 (3H)
Ejemplo 5: Preparación de 3-ciano-4-(6-(3-fluorofenil)-4-(furan-3-il)piridin-3-iloxi)-N-(tiazol-2-il)bencenosulfonamida
100 mg (0,22 mmol) de 4-((6-cloro-4-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida se disolvió en 2,4 mL de 1,4-dioxano y 33,6 mg (0,24 mmol) de ácido (3-fluorofenil)borónico se añadió a esto y luego 8,3 mg (3 % en mol) de Pd(PPh3) 4, 76,2 mg (0,72 mmol) de Na2CO3 y 2,4 mL de H2O se añadieron a esto. Después de reaccionar en el reactor de microondas a 120 °C durante 5 minutos, el solvente se eliminó y el material restante se diluyó con acetato de etilo y la capa orgánica se separó y se lavó con cloruro de sodio saturado. La capa orgánica se recogió, se secó con sulfato de magnesio para eliminar el agua y se concentró a presión reducida y el residuo se purificó por cromatografía de columna (solvente de desarrollo, hexa no: acetato de etilo = 1:1) para obtener 80 mg (70 % de rendimiento) del compuesto del título. 1H NMR (CDCh, 500MHz) 58,51 (s, 1H), 8,23 (s, 1H), 8,06 (s, 1H), 7,96 (d 1H), 7,92 (s, 1H), 7,79 (d, 1H), 7,73 (d, 1H), 7,54 (s, 1H), 7,49 (m, 1H), 7,18 (m, 1H), 7,11 (s, 1H), 6,90 (d, 1H), 6,86 (s, 1H), 6,58 (s, 1H)
Ejemplo 6: Preparación de 3-ciano-4-(6-(2-fluorofenil)-4-(furan-3-il)piridin-3-iloxi)-N-(tiazol-2-il)bencenosulfonamida
68 mg (60 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usó ácido (2-fluorofenil)borónico en lugar de ácido (3-fluorofenil)borónico. 1H NMR (CD3OD/CDQ3 , 500MHz) 58,22(s, 1H), 7,98(s, 1H), 7,87(s, 2H), 7,74(d, 1H), 7,53(t, 1H), 7,29(s, 1H), 7,22(m, 1H), 7,05(t, 1H), 7,98(t, 1H), 6,73(d, 1H), 6,70(d, 1H), 6,64(s, 1H), 6,34(d, 1H)
Ejemplo 7: Preparación de 3-ciano-4-(6-(4-fluorofenil)-4-(furan-3-il)piridin-3-iloxi)-N-(tiazol-2-il)bencenosulfonamida
74 mg (65 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usó ácido (4-fluorofenil)borónico en lugar de ácido (3-fluorofenil)borónico. 1H NMR (CD3OD/CDQ3 , 500MHz) 58,19 (s, 1H), 7,99 (s, 1H), 7,92 (d, 2H), 7,75 (d, 2H), 7,50 (d, 1H), 7,68 (m, 2H), 6,98 (t, 1H), 6,73 (m, 3H), 6,35 (d, 1H)
Ejemplo 8: Preparación de 3-ciano-4-(4-(furan-3-il)-6-(3-(trifluorometil)fenil)piridin-3-iloxi)-N-(tiazol-2-il)bencenosulfonamida
63 mg (50 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usó ácido (3-(trifluorometil)fenil)borónico en lugar de ácido (3-fluorofenil)borónico.
1H NMR (CDCl3, 500MHz) 58,49 (s, 1H), 8,28 (s, 1H), 8,22 (m, 2H), 8,08 (s, 1H), 7,97 (s, 1H), 7,94 (d, 1H), 7,73 (d, 1H), 7,60 (m, 1H), 7,01 (d, 1H), 6,88 (s, 1H), 6,85 (d, 1H), 6,53 (d, 1H)
Ejemplo 9: Preparación de 3-ciano-4-(2'-fluoro-4-(furan-3-il)-2,4'-bipiridin-5-iloxi)-N-(tiazol-2-il)bencenosulfonamida
74 mg (65 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usó ácido (2-fluoropiridin-4-il)borónico en lugar de ácido (3-fluorofenil)borónico.
1H NMR (CD3OD/CDG3 , 500MHz) 58,19 (s, 1H), 8,00 (d, 1H), 7,95 (s, 1H), 7,90 (s, 1H), 7,78 (s, 1H), 7,68 (d, 1H), 7,63 (d, 1H), 7,40 (s, 1H), 6,70 (d, 1H), 6,66 (s, 1H), 6,58 (d, 1H), 6,33 (d, 1H)
Ejemplo 10: Preparación de 3-ciano-4-(2'-fluoro-4-(furan-3-il)-2,3'-bipiridin-5-iloxi)-N-(tiazol-2-il)bencenosulfonamida
63 mg (55 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usó ácido (2-fluoropiridin-3-il)borónico en lugar de ácido (3-fluorofenil)borónico.
1H NMR (CDCls, 500MHz) 58,59 (t, 1H), 8,50 (s, 1H), 8,32 (d, 1H), 8,26 (d, 1H), 8,06 (s, 1H), 8,99 (d, 1H), 7,53 (s, 1H), 7,40 (t, 1H), 7,10 (d, 1H), 6,87 (d, 1H), 6,86 (s, 1H), 6,59 (d, 1H)
Ejemplo 11: Preparación de 3-ciano-4-(6'-fluoro-4-(furan-3-il)-2,3'-bipiridin-5-iloxi)-N-(tiazol-2-il)bencenosulfonamida
69 mg (60 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usó ácido (6-fluoropiridin-3-il)borónico en lugar de ácido (3-fluorofenil)borónico.
1H NMR (CDCI3 , 500MHz) 58,84 (s, 1H), 8,51 (t, 1H), 8,48 (s, 1H), 8,24 (s, 1H), 8,06 (s, 1H), 7,97 (d, 1H), 7,92 (s, 1H), 7,54 (s, 1H), 7,09 (m, 2H), 6,87 (m, 2H), 6,59 (d, 1H)
Ejemplo 12: Preparación de 3-ciano-4-(2,,6,-difluoro-4-(furan-3-il)-2,3,-bipiridin-5-iloxi)-N-(tiazol-2-il)bencenosulfonamida
59 mg (50 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usó ácido (2,6-difluoropiridin-3-il)borónico en lugar de ácido (3-fluorofenil)borónico.
1H NMR (CDCl3, 500MHz) 58,73 (q, 1H), 8,48 (s, 1H), 8,25 (d, 1H), 8,11 (s, 1H), 8,06 (s, 1H), 7,99 (dd, 1H), 7,67 (m, 1H), 7,11 (d, 1H), 7,04 (dd, 1H), 6,88 (d, 1H), 6,85 (s, 1H), 6,60 (d, 1H)
Ejemplo 13: Preparación de 3-ciano-4-(4-(furan-3-il)-2,3'-bipiridin-5-iloxi)-N-(tiazol-2-il)bencenosulfonamida
66 mg (60 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usó ácido piridin-3-ilborónico en lugar de ácido (3-fluorofenil)borónico. 1H NMR (CD3OD/CDQ3 , 500MHz) 59,67 (s, 1H), 9,20 (d, 1H), 8,79 (d, 1H), 8,42 (s, 1H), 8,34 (s, 1H), 8,21 (s, 1H), 8,08 (s, 1H), 8,05 (d, 1H), 7,94 (d, 1H), 7,47 (s, 1H), 6,98 (s, 1H), 6,88 (s, 1H), 6,79 (d, 1H), 6,48 (d, 1H)
Ejemplo 14: Preparación de 3-ciano-4-(4-(furan-3-il)-2,4'-bipiridin-5-iloxi)-N-(tiazol-2-il)bencenosulfonamida
61 mg (55 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usó ácido piridin-4-ilborónico en lugar de ácido (3-fluorofenil)borónico.
1H NMR (CD3OD/CDCl3, 500MHz) 58,76 (d, 2H), 8,57 (s, 1H), 8,43 (s, 1H), 8,37 (d, 2H), 8,29 (d, 1H), 8,17 (s, 1H), 8,03 (d, 1H), 7,62 (s, 1H), 7,10 (d, 1H), 7,07 (s, 1H), 7,00 (d, 1H), 6,73 (d, 1H)
Ejemplo 15: Preparación de 3-ciano-4-(4-(furan-3-il)-6-(pirimidin-5-il)piridin-3-iloxi)-N-(tiazol-2-il)bencenosulfonamida
66 mg (60 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usó ácido (pirimidin-5-il)borónico en lugar de ácido (3-fluorofenil)borónico. 1H NMR (CD3OD/CDCl3,
500MHz) 59,38 (s, 2H), 9,22 (s, 1H), 8,43 (s, 1H), 8,20 (s, 1H), 8,00 (s, 2H), 7,92 (m, 1H), 7,46 (s, 1H), 6,87 (s, 2H), 6,84 (s, 1H), 6,76 (m, 1H), 6,48 (s, 1H)
Ejemplo 16: Preparación de 3-ciano-4-((4,6-di(furan-3-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
20,0 mg de 4,6-di(furan-3-il)piridin-3-ol y 24,9 mg de 3-ciano-4-fluoro-N-(tiazol-2-il)bencenosulfonamida se disolvieron en DMF y 86,0 mg(3,0eq) de Cs2CO3(86,0mg, 3,0eq) se añadió a esto. Después de reaccionar a temperatura ambiente durante 2 horas, la mezcla resultante se hizo reaccionar a 60 °C durante 16 horas. El solvente se eliminó por concentración a presión reducida. Cuando se trató con EA/H 2O, la capa de acetato de etilo se trató con sulfato de magnesio y se concentró a presión reducida. El residuo se separó por PLC (solvente de desarrollo, EA:n-Hex = 1:4) para obtener 10,1 mg (24 % de rendimiento) del compuesto del título.
1H NMR (CDs OD/CDCls , 500MHz) 58,39 (s, 1H), 8,24 (s, 2H), 8,09 (s, 1H), 8,00 (s, 1H), 7,96 (s, 1H), 7,63 (s, 1H), 7,60 (s, 1H), 7,10 (d, 1H), 7,07 (s, 1H), 7,01 (s, 1H), 6,89 (m, 1H), 6,71 (s, 1H)
Ejemplo 17: Preparación de 4-((4,6-di(furan-3-il)piridin-3-il)oxi)-3-fluoro-N-(tiazol-2-il)bencenosulfonamida
7,8 mg (18 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 16, excepto que se usó N-(terc-butil)-3,4-fluoro-N-(tiazol-2-il)bencenosulfonamida en lugar de 3-ciano-4-fluoro-N-(tiazol-2-il)bencenosulfonamida.
1H NMR (CDCls, 500MHz) 58,41 (s, 1H), 8,21 (s, 1H), 8,18 (s, 1H), 7,81 (d, 1H), 7,76 (s, 1H), 7,69 (d, 1H), 7,58 (s, 1H), 7,54 (s, 1H), 7,18 (m, 1H), 7,12 (d, 1H), 7,06 (s, 1H), 6,90 (s, 1H), 6,58 (d, 1H)
Ejemplo 18: Preparación de 3-ciano-4-((2'-fluoro-4-(1-metil-1H-pirazol-5-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
10 mg de 4-((6-cloro-4-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida se disolvió en DMF/H2O=1:1 (0,46 mL) y 3,2 mg de ácido (2-fluoropiridin-3-il)borónico, 0,8 mg de Pd(PPh3)4 y 7,4 mg de Na2CO3 se añadieron a esto. Después de reaccionar en el reactor de microondas a 120 °C durante 5 minutos, el DMF se eliminó por concentración a presión reducida. Después de extraer con EA, el extracto se trató con MgSO4 y se concentró a presión reducida. El residuo se separó por PLC (solvente de desarrollo, EA) para obtener 3,2 mg (28 % de rendimiento) del compuesto del título.1
1H NMR (CD3OD, 500MHz) 58,79 (s, 1H), 8,63 (t, 1H), 8,31 (d, 1H), 8,14 (d, 1H), 8,07 (s, 1H), 7,98 (dd, 1H), 7,52 (t, 1H), 7,39 (d, 1H), 7,14 (d, 1H), 7,00 (d, 1H), 6,76 (d, 1H), 6,41 (d, 1H), 3,89 (s, 3H)
Ejemplo 19: Preparación de 3-ciano-4-((6'-fluoro-4-(1-metil-1H-pirazol-5-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
4,2 mg (37 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 18, excepto que se usó ácido (6-fluoropiridin-3-il)borónico en lugar de ácido (2-fluoropiridin-3-il)borónico.
1H NMR (CD3OD, 500MHz) 58,95 (s, 1H), 8,75 (s, 1H), 8,67 (t, 1H), 8,13 (s, 1H), 7,96 (m, 2H), 7,39 (s, 1H), 7,22 (d, 1H), 7,14 (d, 1H), 6,98 (d, 1H), 6,76 (d, 1H), 6,40 (d, 1H), 3,88 (s, 3H)
Ejemplo 20: Preparación de 3-ciano-4-((4-(furan-3-il)-6-(tiofen-3-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
34 mg (31 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usó ácido (tiofen-3-il)borónico en lugar de ácido (3-fluorofenil)borónico.
1H NMR (CD3OD, 500MHz) 58,43 (s, 1H), 8,26 (s, 1H), 8,13 (s, 2H), 8,10 (s, 1H), 8,00 (dd, 1H), 7,79 (d, 1H), 7,61 (s, 1H), 7,54 (dd, 1H), 7,12 (d, 1H), 7,02 (s, 1H), 6,94 (d, 1H), 6,75 (d, 1H)
Ejemplo 21: Preparación de 3-fluoro-4-((4-(1-metil-1H-pirazol-5-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
10 mg (0,02 mmol) de 4-((6-cloro-4-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-3-fluoro-N-(tiazol-2-il)bencenosulfonamida se disolvió en 3 mL de N,N-dimetilformamida y 3,9 mg (0,03 mmol) de ácido (piridin-3-il)borónico se añadió a esto y luego 2,4 mg (10 % en mol) de Pd(PPh3)4 , 6,8 mg (0,64 mmol) de Na2CO3 y 1 mL de H2O se añadieron a esto. Después de reaccionar en el reactor de microondas a 120 °C 10 minutos, el solvente se eliminó y el material restante se diluyó con acetato de etilo y la capa orgánica se separó y se lavó con cloruro de sodio saturado. La capa orgánica se recogió, se secó con sulfato de magnesio para eliminar el agua y se concentró a presión reducida y el residuo se purificó por cromatografía de columna (solvente de desarrollo, hexano:acetato de etilo = 3:1) para obtener 5 mg (45 % de rendimiento) del compuesto del título. 1H NMR (CD3OD, 500MHz) 59,23 (s, 1H), 8,80 (d, 1H), 8,60 (s, 1H), 8,53 (m, 1H), 8,10 (s, 1H), 7,70 (m, 1H), 7,67(m, 1H), 7,62 (m, 1H), 7,43 (s, 1H), 7,13 (m, 2H), 6,76 (m, 1H), 6,45 (s, 1H), 3,87 (s, 3H)
Ejemplo 22: Preparación de 3-fluoro-4-((4-(1-metil-1H-pirazol-5-il)-6-(tiofen-3-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
5 mg (45 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 21, excepto que se usó ácido (tiofen-3-il)borónico en lugar de ácido (piridin-3-il)borónico.1
1H NMR (CD3OD/CDG3 , 500MHz) 58,45 (s, 1H), 8,23 (s, 1H), 8,09 (s,1H), 7,92 (m, 1H), 7,59(m, 4H), 7,40 (s, 1H), 7,12 (m, 1H), 7,03 (m, 1H), 6,76 (m, 1H), 6,40 (s, 1H), 3,85 (s, 3H)
Ejemplo 23: Preparación de 3-ciano-4-((6-(4-fluorofenil)-4-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-N-( tiazol-2-il)bencenosulfonamida
10 mg (0,02 mmol) de 4-((6-cloro-4-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida se disolvió en 3 mL de N,N-dimetilformamida y 4,4 mg (0,03 mmol) de ácido (4-fluorofenil)borónico se añadió a esto y luego 2,4 mg (10 % en mol) de Pd(PPh3)4 , 6,7 mg (0,6 mmol) de Na2CO3 y 1 mL de H2O se añadieron a esto. Después de reaccionar en el reactor de microondas a 120 °C durante 10 minutos, el solvente se eliminó y el material restante se diluyó con acetato de etilo y la capa orgánica se separó y se lavó con cloruro de sodio saturado. La capa orgánica se recogió, se secó con sulfato de magnesio para eliminar el agua y se concentró a presión reducida y el residuo se purificó por cromatografía de columna (solvente de desarrollo, hexano:acetato de etilo = 3:1) para obtener 5 mg (45 % de rendimiento) del compuesto del título. 1H NMR (CD3OD, 500MHz) 58,72 (s, 1H), 8,14 (m, 3H), 8,03 (s, 1H), 7,94 (m, 1H), 7,37 (d, 1H), 7,23 (m, 2H), 7,13 (m, 1H), 6,94 (m, 1H), 6,74 (d, 1H), 3,87 (s, 3H)
Ejemplo 24: Preparación de 3-ciano-4-((6-(2-fluorofenil)-4-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-N-( tiazol-2-il)bencenosulfonamida
5 mg (45 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 23, excepto que se usó ácido (piridin-2-il)borónico en lugar de ácido (4-fluorofenil)borónico. 1H NMR (CD3OD/CDCl3, 500MHz) 58,79 (s, 1H), 8,12 (s, 1H), 7,98 (m, 3H), 7,52 (m, 1H), 7,38 (m, 2H), 7,29 (m, 1H), 7,13 (m, 1H), 6,99 (m, 1H), 6,75 (d, 1H), 6,39 (s, 1H), 3,88 (s, 3H)
Ejemplo 25: Preparación de 3-ciano-4-((6-(furan-3-il)-4-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
5 mg (47 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 23, excepto que se usó ácido (furan-3-il)borónico en lugar de ácido (4-fluorofenil)borónico. 1H NMR (CD3OD/CDCl3, 500MHz) 58,61 (s, 1H), 8,23 (s, 1H), 8,11 (s, 1H), 7,93 (m, 1H), 7,84 (s, 1H), 7,62 (s, 1H), 7,36(d, 1H), 7,13 (d, 1H), 7,05 (d, 1H), 6,92 (d, 1H), 6,75 (d, 1H), 6,35 (d, 1H), 3,86 (s, 3H)
Ejemplo 26: Preparación de 3-ciano-4-((6-(3-fluorofenil)-4-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-N-( tiazol-2-il)bencenosulfonamida
5 mg (45 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 23, excepto que se usó ácido (piridin-3-il)borónico en lugar de ácido (4-fluorofenil)borónico.
1H NMR (CD3OD/CDCI3 , 500MHz) 58,72 (s, 1H), 7,95 (d, 2H), 7,93 (m, 3H), 7,50 (m, 1H), 7,37 (s, 1H), 7,22 (m, 1H), 7,13 (m, 1H), 6,95 (d, 1H), 6,75 (d, 1H), 6,39 (s, 1H), 3,88 (s, 3H)
Ejemplo 27: Preparación de 3-ciano-4-((2,-fluoro-4-(1-metil-1H-pirazol-5-il)-[2,4,-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
5 mg (44 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 23, excepto que se usó ácido (2-fluoropiridin-4-il)borónico en lugar de ácido (4-fluorofenil)borónico. 1H n Mr (CD3OD/CDCl3, 500MHz) 58,78 (s, 1H), 8,33 (m, 1H), 8,26 (s, 1H), 8,14 (d, 1H), 8,06 (m, 1H), 7,98 (m, 1H), 7,83 (s, 1H), 7,39 (m, 1H), 7,12 (d, 1H), 6,99 (d, 1H), 6,73 (m, 1H), 6,41 (d, 1H), 3,88 (s, 3H)
Ejemplo 28: Preparación de 4-((4,6-di(furan-3-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
2,8 mg (78 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 16, excepto que se usó N-(terc-butil)-4-fluoro-N-(tiazol-2-il)bencenosulfonamida en lugar de 3-ciano-4-fluoro-N-(tiazol-2-il)bencenosulfonamida.
1H NMR (CD3OD, 500MHz) 58,22 (s, 1H), 8,16 (s, 1H), 7,96 (s, 1H), 7,91 (s, 1H), 7,87 (d, 2H), 7,58 (s, 1H), 7,55 (s, 1H), 7,05 (m, 3H), 7,00 (dd, 2H), 6,66 (d, 1H)
Ejemplo 29: Preparación de 3-ciano-4-((2-fluoro-6'-fenil-[3,4'-bipiridin]-3,-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
10 mg (0,02 mmol) de 3-ciano-4-((4-yodo-6-fenilpiridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida se disolvió en 3 mL de N,N-dimetilformamida y 3,7 mg (0,03 mmol) de ácido (2-fluoropiridin-3-il)borónico se añadió a esto y luego 2,0 mg (10 % en mol) de Pd(PPh3)4 , 5,6 mg (0,6 mmol) de Na2CO3 y 1 mL de H2O se añadieron a esto. Después de reaccionar en el reactor de microondas a 120 °C durante 5 minutos, el solvente se eliminó y el material restante se diluyó con acetato de etilo y la capa orgánica se separó y se lavó con cloruro de sodio saturado. La capa orgánica se recogió, se secó con sulfato de magnesio para eliminar el agua y se concentró a presión reducida y el residuo se purificó por cromatografía de columna (solvente de desarrollo, hexano:acetato de etilo = 3:1) para obtener 3 mg (30 % de rendimiento) del compuesto del título.
1H NMR (CD3OD, 500MHz) 58,61 (s, 1H), 8,08 (m, 3H), 8,04 (m, 1H), 7,84 (m, 2H), 7,52 (m, 4H), 7,15 (m, 1H), 6,77 (m, 2H), 6,64 (m, 1H)
Ejemplo 30: Preparación de 3-ciano-4-((6-fluoro-6'-fenil-[3,4'-bipiridin]-3,-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
3 mg (30 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 29, excepto que se usó ácido (2-fluoropiridin-5-il)borónico en lugar de ácido (2-fluoropiridin-3-il)borónico.
1H NMR (CD3OD/CDCl3, 500MHz) 58,52 (s, 1H), 8,35 (m, 1H), 8,15 (m, 1H), 8,05 (m, 2H), 7,99 (m, 1H), 7,92 (m, 1H), 7,86 (m, 1H), 7,52 (m, 2H), 7,45 (m, 1H), 7,11 (m, 1H), 6,86 (m, 1H), 6,72 (m, 1H), 6,64 (m, 1H)
Ejemplo 31: Preparación de 3-ciano-4-((2,-fluoro-6-fenil-[4,4,-bipiridin]-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
3 mg (30 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 29, excepto que se usó ácido (2-fluoropiridin-4-il)borónico en lugar de ácido (2-fluoropiridin-3-il)borónico.
1H NMR (CD3OD/CDCL3, 500MHz) 58,63 (s, 1H), 8,11 (m, 1H), 8,08 (m, 2H), 8,02 (m, 2H), 7,93 (m, 1H), 7,52 (m, 3H), 7,12 (m, 1H), 6,91 (m, 1H), 6,71 (m, 3H)
Ejemplo 32: Preparación de 3-ciano-4-((6-fluoro-5-metil-6'-fenil-[3,4,-bipiridin]-3,-il)oxi)-N-(tiazol-2-il )bencenosulfonamida
3 mg (30 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 29, excepto que se usó ácido (6-fluoro-5-metilpiridin-3-il)borónico en lugar de ácido (2-fluoropiridin-3-il)borónico. 1H NMR (CDsOD/CDCls, 500MHz) 58,57 (s, 1H), 8,22 (m, 1H), 8,13 (m, 1H), 8,07 (m, 2H), 8,05 (m, 1H), 8,01 (m, 1H), 7,91 (m, 1H), 7,52 (m, 3H), 7,11 (m, 1H), 6,85 (m, 1H), 6,72 (m, 1H), 2,29 (s, 3H)
Ejemplo 33: Preparación de 3-ciano-4-((6'-fenil-[3,4'-bipiridin]-3,-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
3 mg (30 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 29, excepto que se usó ácido piridin-3-ilborónico en lugar de ácido (2-fluoropiridin-3-il)borónico.1
1H NMR (CDs OD/CDCls , 500MHz) 58,05 (m, 1H), 8,65 (s, 1H), 8,50 (m, 1H), 8,12 (m, 5H), 7,92 (m, 1H), 7,48 (m, 4H), 7,12 (m, 1H), 6,98 (d, 1H), 6,74 (d, 1H)
Ejemplo 34: Preparación de 3-ciano-4-((6-fenil-4-(pirimidin-5-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
3 mg (30 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 29, excepto que se usó ácido (pirimidin-5-il)borónico en lugar de ácido (2-fluoropiridin-3-il)borónico.
1H NMR (CD3OD/CDCl3, 500MHz) 59,13 (m, 3H), 8,65 (s, 1H), 8,19 (m, 2H), 8,12 (m, 2H), 7,99 (m, 1H), 7,51 (m, 3H), 7,10 (m, 1H), 7,06 (m, 1H), 6,72 (m, 1H)
Ejemplo 35: Preparación de 4-((3'-cloro-6-fenil-[4,4'-bipiridin]-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida
3 mg (30 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 29, excepto que se usó ácido (3-cloropiridin-4-il)borónico en lugar de ácido (2-fluoropiridin-3-il)borónico.
1H NMR (CD3OD/CDG3 , 500MHz) 58,55 (m, 1H), 8,26 (m, 1H), 8,10 (m, 1H), 7,99 (m, 3H), 7,72 (m, 1H), 7,66 (m, 1H), 7,57 (m, 1H), 7,50 (m, 2H), 7,44 (m, 1H), 7,13 (m, 2H), 6,75 (m, 1H)
Ejemplo 36: Preparación de 3-ciano-4-((2',3'-dicloro-6-fenil-[4,4'-bipiridin]-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
3 mg (30 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 29, excepto que se usó ácido (2,3-dicloropiridin-4-il)borónico en lugar de ácido (2-fluoropiridin-3-il)borónico.
1H NMR (CDsOD/CDCls, 500MHz) 58,54 (m, 1H), 8,26 (m, 1H), 8,08 (m, 1H), 7,99 (m, 3H), 7,72 (m, 1H), 7,56 (m, 1H), 7,49 (m, 2H), 7,43 (m, 1H), 7,12 (m, 2H), 6,73 (m, 1H)
Ejemplo 37: Preparación de 3-ciano-4-((4-(3,5-dimetilisoxazol-4-il)-6-fenilpiridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
3 mg (30 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 29, excepto que se usó ácido (3,5-dimetilisoxazol-4-il)borónico en lugar de ácido (2-fluoropiridin-3-il)borónico.
1H NMR (CD3OD/CDCI3 , 500MHz) 58,66 (s, 1H), 8,15 (m, 1H), 8,05 (m, 2H), 7,99 (m, 2H), 7,49 (m, 4H), 7,10 (m, 1H), 6,89 (m, 1H), 6,71 (m, 1H), 2,34 (s, 3H), 2,23 (s, 3H)
Ejemplo 38: Preparación de 3-ciano-4-((4-(1-metil-1H-pirazol-4-il)-6-fenilpiridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
3 mg (30 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 29, excepto que se usó 1-metil-4-(4,4,5,5-tetrametil-1,3,2-dioxaboran-2-il)-1H-pirazol en lugar de ácido (2-fluoropiridin-3-il)borónico.
1H NMR (CDsOD/CDCls, 500MHz) 58,45 (m, 1H), 8,27 (m, 1H), 8,20 (m, 2H), 8,05 (m, 3H), 7,98 (m, 1H), 7,50 (m, 2H), 7,47 (m, 1H), 7,10 (m, 1H), 6,94 (m, 1H), 6,71 (m, 1H), 3,89 (s, 2H)
Ejemplo 39: Preparación de 3-ciano-4-((6-fenil-4-(1H-pirazol-4-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
3 mg (30 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 29, excepto que se usó terc-butil 4-(4,4,5,5-tetrametil-1,3,2-dioxaboran-2-il)-1 H-pirazol-1-carboxilato en lugar de ácido (2-fluoropiridin-3-il)borónico.
1H NMR (CDs OD/CDCls , 500MHz) 58,47 (s, 1H), 8,24 (m, 4H), 8,05 (m, 2H), 7,97 (m, 1H), 7,52 (m, 2H), 7,49 (m, 1H), 7,10 (m, 1H), 6,93 (m, 1H), 6,71 (m, 1H)
Ejemplo 40: Preparación de 3-ciano-4-((6-fenil-[4,4'-bipiridin]-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
3 mg (30 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 29, excepto que se usó ácido (piridin-4-il)borónico en lugar de ácido (2-fluoropiridin-3-il)borónico.
1H NMR (CD3OD/CDCh, 500MHz) 58,67 (s, 1H), 8,59 (m, 2H), 8,14 (m, 1H), 8,09 (m, 3H), 7,94 (m, 1H), 7,70 (m, 2H), 7,52 (m, 2H), 7,47 (m, 1H), 7,12 (m, 1H), 6,99 (m, 1H), 6,76 (m, 1H)
Ejemplo 41: Preparación de 3-ciano-4-((4-(2,5-dimetiltiofen-3-il)-6-fenilpiridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
3 mg (30 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 29, excepto que se usó ácido (2,5-dimetiltiofen-3-il)borónico en lugar de ácido (2-fluoropiridin-3-il)borónico.
1H NMR (CD3OD/CDG3 , 500MHz) 58,64 (s, 1H), 8,06 (m, 3H), 7,89 (m, 2H), 7,50 (m, 2H), 7,46 (m, 2H), 7,16 (d, 1H), 6,81 (m, 2H), 6,63 (s, 1H), 2,27 (s, 6H)
Ejemplo 42: Preparación de 3-ciano-4-((4-(5-metiltiofen-2-il)-6-fenilpiridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
3 mg (30 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 29, excepto que se usó ácido (5-metiltiofen-2-il)borónico en lugar de ácido (2-fluoropiridin-3-il)borónico.
1H NMR (CD3OD/CDG3 , 500MHz) 58,54 (s, 1H), 8,27 (s, 1H), 8,10 (m, 1H), 8,07 (m, 3H), 7,74 (m, 1H), 7,72 (m, 2H), 7,50 (m, 1H), 7,47 (m, 1H), 7,45 (m, 2H), 7,13 (m, 1H), 6,75 (d, 1H), 2,13 (s, 3H)
Ejemplo 43: Preparación de 3-ciano-4-((4-(2-ciclopropiltiazol-4-il)-6-fenilpiridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
3 mg (30 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 29, excepto que se usó 2-ciclopropil-4-(4,4,5,5-tetrametil-1,3,2-dioxaboran-2-il)tiazol en lugar de ácido (2-fluoropiridin-3-il)borónico.
1H NMR (CDsOD/CDCls, 500MHz) 58,54 (s, 1H), 8,48 (s, 1H), 8,24 (s, 1H), 8,05 (d, 1H), 7,97 (m, 1H), 7,88 (s, 1H), 7,64 (m, 1H), 7,55 (m, 2H), 7,50 (m, 1H), 7,13 (d, 1H), 6,93 (d, 1H), 6,74 (m, 1H), 2,33 (m, 1H), 1,61 (m, 4H) Ejemplo 44: Preparación de 3-ciano-4-((4-(1-ciclopropil-1H-pirazol-4-il)-6-fenilpiridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
3 mg (30 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 29, excepto que se usó 1-ciclopropil-4-(4,4,5,5-tetrametil-1,3,2-dioxaboran-2-il)-1 H-pirazol en lugar de ácido (2-fluoropiridin-3-il)borónico.
1H NMR (CDs OD/CDCls , 500MHz) 58,56 (s, 1H), 8,23 (s, 1H), 8,08 (m, 1H), 8,00 (m, 2H), 7,74 (m, 1H), 7,72 (m, 1H), 7,66 (m, 1H), 7,56 (m, 2H), 7,29 (m, 1H), 7,13 (m, 2H), 6,75 (d, 1H), 2,32 (m, 1H), 1,61 (m, 4H)
Ejemplo 45: Preparación de 3-ciano-4-((4-(furan-3-il)-6-(1H-pirazol-4-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
32 mg (30 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usó ácido (1H-pirzol-4-il)borónico en lugar de ácido (3-fluorofenil)borónico.
1H NMR (CDCl3, 500MHz) ó 8,53 (t, 1H), 8,36 (s, 1H), 8,28 (s, 1H), 8,09 (d, 2H), 7,80 (d, 1H), 7,67 (d, 1H), 7,52 (s, 1H), 7,36 (t, 1H), 7,09 (d, 1H), 7,00 (t, 1H), 6,87 (s, 1H), 6,56 (d, 1H)
Ejemplo 46: Preparación de 3-ciano-4-((4-(furan-3-il)-6-(1-metil-1H-pirazol-4-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
29 mg (26 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usó 1-metil-4-(4,4,5,5-tetrametil-1,3,2-dioxaboran-2-il)-1H-pirazol en lugar de ácido (3-fluorofenil)borónico.
1H NMR (CDsOD, 500MHz) ó 8,89 (s, 1H), 8,61 (m, 1H), 8,33 (s, 1H), 8,23 (s, 1H), 8,20 (s, 1H), 7,79 (dd, 1H), 7,68 (d, 1H), 7,63 (s, 1H), 7,20 (dd, 1H), 7,13 (m, 3H), 6,75 (d, 1H)
Ejemplo 47: Preparación de 3-fluoro-4-((2'-fluoro-4-(furan-3-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
10,0 mg de 4-((6-cloro-4-(furan-3-il)piridin-3-il)oxi)-3-fluoro-N-(tiazol-2-il)bencenosulfonamida se disolvió en 1,4-dioxano/H2O=1:1 (0,48 mL) y 3,2 mg de ácido 2-fluoropiridin-3-il)borónico, 0,84 mg de Pd(PPh3)4 y 7,7 mg de Na2CO3 , se añadieron a esto. Después de reaccionar en el reactor de microondas a 120 °C durante 5 minutos, 1,4-dioxano se eliminó por concentración a presión reducida. Después de extraer con acetato de etilo, el extracto se trató con MgSO4 y se concentró a presión reducida. El residuo se purificó por PLC (solvente de desarrollo, EA:n-Hex = 2:1) para obtener 3,9 mg (34 % de rendimiento) del compuesto del título.
1H NMR (CD3OD, 500MHz) ó 8,39 (s, 1H), 8,27 (s, 2H), 8,10 (s, 1H), 8,06 (s, 1H), 7,99 (d, 1H), 7,83 (s, 1H), 7,63 (s, 1H), 7,60 (s, 1H), 7,54 (s, 1H), 7,10 (d, 1H), 7,02 (s, 1H), 6,93 (d, 1H), 6,73 (d, 1H)
Ejemplo 48: Preparación de 3-fluoro-4-((6'-fluoro-4-(furan-3-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
3,9 mg (34 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 47, excepto que se usó ácido (6-fluoropiridin-3-il)borónico en lugar de ácido (2-fluoropiridin-3-il)borónico. 1H NMR (CDCl3, 500MHz) ó 8,29 (s, 1H), 8,00 (s, 1H), 7,97 (s, 1H), 7,94 (s, 1H), 7,71 (d, 1H), 7,66 (d, 1H), 7,62 (s, 1H), 7,56 (t, 1H), 7,54 (s, 1H), 7,38 (d, 1H), 6,89 (t, 1H), 6,83 (s, 1H), 3,98 (s, 3H)
Ejemplo 49: Preparación de 3-ciano-4-((6-fluoro-[3,2':4',3"-terpiridin]-5'-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
10 mg (0,02 mmol) de 4-((6'-cloro-[3,4'-bipiridin]-3'-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida se disolvió en 3 mL de N,N-dimetilformamida y 4,5 mg (0,03 mmol) de ácido (6-fluoropiridin-3-il)borónico se añadió a esto y luego 2,4 mg (10 % en mol) de Pd(PPh3)4, 6,7 mg (0,6 mmol) de Na2CO3 y 1 mL de H2O se añadieron a esto. Después de reaccionar en el reactor de microondas a 120 °C durante 10 minutos, el solvente se eliminó y el material restante se diluyó con acetato de etilo y la capa orgánica se separó y se lavó con cloruro de sodio saturado. La capa orgánica se recogió, se secó con sulfato de magnesio para eliminar el agua y se concentró a presión reducida y el residuo se purificó por cromatografía de columna (solvente de desarrollo, hexano:acetato de etilo = 3:1) para obtener 3 mg (27 % de rendimiento) del compuesto del título.
1H NMR (CD3OD, 500MHz) 58,97 (d, 1H), 8,82 (s, 1H), 8,70 (m, 2H), 8,52 (m, 1H), 8,21 (m, 1H), 8,13 (m, 2H), 7,79 (m, 1H), 7,39 (m, 1H), 7,48 (m, 1H), 7,23 (m, 1H), 7,14 (m, 1H), 7,00 (d, 1H), 6,75 (d, 1H)
Ejemplo 50: Preparación de 3-ciano-4-((6'-(3-fluorofenil)-[3,4'-bipiridin]-3'-il)oxi)-N-(tiazol-2-il)benceno sulfonamida
3 mg (30 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 49, excepto que se usó ácido (3-fluorofenil)borónico en lugar de ácido (6-fluoropiridin-3-il)borónico.
1H NMR (CDsOD/CDCls, 500MHz) 58,80 (d, 1H), 8,67 (s, 1H), 8,50 (m, 1H), 8,15 (m, 3H), 7,94 (m, 3H), 7,52 (m, 2H), 7,22 (m, 1H), 7,13 (m, 1H), 6,99 (d, 1H), 6,75 (d, 1H)
Ejemplo 51: Preparación de 3-ciano-4-((2-fluoro-[3,2':4',3"-terpiridin]-5'-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
3 mg (30 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 49, excepto que se usó ácido (2-fluoropiridin-3-il)borónico en lugar de ácido (6-fluoropiridin-3-il)borónico.
1H NMR (CDs OD/CDCls , 500MHz) 58,79 (s, 1H), 8,74 (s, 1H), 8,62 (m, 1H), 8,52 (m, 1H), 8,30 (m, 1H), 8,14 (m, 3H), 7,96 (m, 1H), 7,51 (m, 2H), 7,13 (d, 1H), 7,03 (d, 1H), 6,74 (d, 1H)
Ejemplo 52: Preparación de 3-ciano-4-((6'-(2-fluorofenil)-[3,4'-bipiridin]-3'-il)oxi)-N-(tiazol-2-il)benceno sulfonamida
3 mg (30 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 49, excepto que se usó ácido (2-fluorofenil)borónico en lugar de ácido (6-fluoropiridin-3-il)borónico.
1H NMR (CD3OD/CDCl3, 500MHz) 58,78 (m, 1H), 8,69 (s, 1H), 8,51 (d, 1H), 8,13 (s, 1H), 8,09 (d, 1H), 8,03 (m, 2H), 7,96 (m, 1H), 7,49 (m, 2H), 7,45 (m, 1H), 7,34 (m, 1H), 7,10 (m, 1H), 7,00 (d, 1H), 6,71 (m, 1H)
Ejemplo 53: Preparación de 3-ciano-4-((2,6-difluoro-[3,2':4',4"-terpiridin]-5'-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
10 mg (0,02 mmol) de 4-((6-cloro-[4,4'-bipiridin]-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida se disolvió en 3 mL de N,N-dimetilformamida y 5 mg (0,03 mmol) de ácido (2,6-difluoropiridin-3-il)borónico se añadió a esto y luego 2,4 mg (10 % en mol) de Pd(PPh3)4, 6,7 mg (0,6 mmol) de Na2CO3 y 1 mL de H2O se añadieron a esto. Después de reaccionar en el reactor de microondas a 120 °C durante 10 minutos, el solvente se eliminó y el material restante se diluyó con acetato de etilo y la capa orgánica se separó y se lavó con cloruro de sodio saturado. La capa orgánica se recogió, se secó con sulfato de magnesio para eliminar el agua y se concentró a presión reducida y el residuo se purificó por cromatografía de columna (solvente de desarrollo, hexano:acetato de etilo = 3:1) para obtener 2 mg (19 % de rendimiento) del compuesto del título.
1H NMR (CD3OD, 500MHz) 58,76 (m, 2H), 8,59 (m, 2H), 8,15 (s, 1H), 8,10 (s, 1H), 7,96 (d, 1H), 7,66 (m, 2H), 7,20 (m, 1H), 7,12 (m, 1H), 7,04 (d, 1H), 6,74 (m, 1H)
Ejemplo 54: Preparación de 4-((4,6-bis(1-metil-1H-pirazol-4-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida
10 mg (0,04 mmol) de 4,6-bis(1-metil-1H-pirazol-4-il)piridin-3-ol se disolvió en 3 mL de N,N-dimetilformamida y 32 mg (0,1 mmol) de Cs2CO3 se añadieron a esto, seguido por agitación a temperatura ambiente durante 10 minutos. Después, 11 mg (0,04 mmol) de 3-ciano-4-fluoro-N-(tiazol-2-il)bencenosulfonamida se añadió a esto y la solución se agitó a temperatura ambiente durante 3 horas. Después del completamiento de la reacción comprobado por TLC, el solvente se eliminó y el material restante se diluyó con acetato de etilo y se lavó con cloruro de sodio saturado. La capa orgánica se recogió, se secó con sulfato de magnesio para eliminar el agua y se concentró a presión reducida y el residuo se purificó por cromatografía de columna (solvente de desarrollo, hexano:acetato de etilo = 3:1) para obtener 16,0 mg (80 % de rendimiento) del compuesto del título.
1H NMR (CDCls, 500MHz) 58,34 (s, 1H), 8,24 (s, 1H), 8,20 (s, 1H), 8,14 (s, 1H), 8,08 (s, 1H), 7,98 (m, 3H), 7,10 (d, 1H), 6,90 (d, 1H), 6,71 (d, 1H), 3,96 (s, 3H), 3,88 (s, 3H)
Ejemplo 55: Preparación de 4-((4,6-bis(1-metil-1H-pirazol-4-il)piridin-3-il)oxi)-3-ciano-N-(1,2,4-tiadiazo l-5-il)bencenosulfonamida
16 mg (80 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 54, excepto que se usó 3-ciano-4-fluoro-N-(1,2,4-tiadiazol-5-il)bencenosulfonamida en lugar de 3-ciano-4-fluoro-N-(tiazol-2-il)bencenosulfonamida.
1H NMR (CD3OD/CDCl3, 500MHz) 58,31 (s, 1H), 8,22 (m, 2H), 8,13 (s, 1H), 8,09 (s, 1H), 7,96 (m, 3H), 7,92 (s, 1H), 6,86 (d, 1H), 3,96 (s, 3H), 3,87 (s, 3H)
Ejemplo 56: Preparación de 5-cloro-2-fluoro-4-((2,-fluoro-4-(furan-3-il)-[2,3,-bipiridin]-5-il)oxi)-N-(tiazol-4-il)bencenosulfonamida
10 mg de terc-butil ((5-cloro-4-((6-cloro-4-(furan-3-il)piridin-3-il)oxi)-2-fluorofenil)sulfonil)(tiazol-4-il)carbamato se disolvió en 1,4-dioxano/H2O=1:1 (0,38 mL) y 3,5 mg de ácido (2-fluoropiridin-3-il)borónico, 0,65 mg (3 % en mol) de Pd(PPh3)4 y 5,96 mg de Na2 CO3 se añadieron a esto. Después de reaccionar en el reactor de microondas a 120 °C durante 5 minutos, 1,4-dioxano se eliminó por concentración a presión reducida. Después de extraer con acetato de etilo, el extracto se trató con MgSO4 y se concentró a presión reducida. El residuo se separó por PLC (solvente de desarrollo, EA:n-Hex = 1:1) para obtener 6,7 mg (72 % de rendimiento) del compuesto del título.
1H NMR (CDCls , 500MHz) 59,49 (s, 1H), 8,64 (s, 1H), 8,58 (t, 1H), 8,43 (s, 1H), 8,29 (s, 1H), 8,12 (s, 1H), 8,00 (d, 2H), 7,50 (s, 1H), 7,37 (t, 1H), 7,04 (s, 1H), 6,82 (s, 1H), 6,50 (d, 1H)
Ejemplo 57: Preparación de 5-cloro-2-fluoro-4-((6'-fluoro-4-(furan-3-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-4-il)bencenosulfonamida
9,1 mg (97 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 56, excepto que se usó ácido (6-fluoropiridin-3-il)borónico en lugar de ácido (2-fluoropiridin-3-il)borónico.
1H NMR (CDCls, 500MHz) 5 10,3 (s, 1H), 8,80 (s, 1H), 8,68 (s, 1H), 8,45 (m, 1H), 8,43 (s, 1H), 8,00 (d, 1H), 7,99 (s, 1H), 7,85 (s, 1H), 7,50 (s, 1H), 7,05 (d, 1H), 7,00 (s, 1H), 6,81 (s, 1H), 6,47 (d, 1H)
Ejemplo 58: Preparación de 5-cloro-4-((2',6'-difluoro-4-(furan-3-il)-[2,3,-bipiridin]-5-il)oxi)-2-fluoro-N-(tiazol-4-il)bencenosulfonamida
8,6 mg (89 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 56, excepto que se usó ácido (2,6-difluoropiridin-3-il)borónico en lugar de ácido (2-fluoropiridin-3-il)borónico.
1H NMR (CDCI3 , 500MHz) 5 10,1 (s, 1H), 8,70 (s, 1H), 8,67 (s, 1H), 8,40 (s, 1H), 8,06 (s, 1H), 8,01 (s, 1H), 7,99 (s, 1H), 7,50 (s, 1H), 7,01 (s, 1H), 6,99 (s, 1H), 6,81 (s, 1H), 6,48 (d, 1H)
Ejemplo 59: Preparación de 5-cloro-2-fluoro-4-((6-(3-fluorofenil)-4-(furan-3-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida
8,7 mg (93 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 56, excepto que se usó ácido (3-fluorofenil)borónico en lugar de ácido (2-fluoropiridin-3-il)borónico.
1H NMR (CDCl3, 500MHz) 59,75 (s, 1H), 8,66 (d, 1H), 8,40 (d, 1H), 7,99 (d, 1H), 7,98 (d, 1H), 7,86 (d, 1H), 7,76 (dd, 1H), 7,72 (d, 1H), 7,50 (s, 1H), 7,46 (d, 1H), 7,14 (t, 1H), 7,02 (d, 1H), 6,81 (s, 1H), 6,46 (dd, 1H)
Ejemplo 60: Preparación de 5-cloro-2-fluoro-4-((6-(2-fluorofenil)-4-(furan-3-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida
9,0 mg (97 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 56, excepto que se usó ácido (2-fluorofenil)borónico en lugar de ácido (2-fluoropiridin-3-il)borónico.
1H NMR (CDCl3, 500MHz) 59,98 (s, 1H), 8,66 (s, 1H), 8,43 (s, 1H), 7,99 (m, 3H), 7,96 (s, 1H), 7,47 (s, 1H), 7,41 (m, 1H), 7,29 (m, 1H), 7,19 (m, 1H), 7,00 (s, 1H), 6,79 (s, 1H), 6,48 (d, 1H)
Ejemplo 61: Preparación de 5-cloro-2-fluoro-4-((6-(4-fluorofenil)-4-(furan-3-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida
8,2 mg (88 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 56, excepto que se usó ácido (4-fluorofenil)borónico en lugar de ácido (2-fluoropiridin-3-il)borónico.
1H NMR (CDCl3 , 500MHz) 5 10,2 (s, 1H), 8,67 (s, 1H), 8,38 (s, 1H), 7,97 (m, 4H), 7,82 (s, 1H), 7,49 (s, 1H), 7,17 (t, 2H), 6,99 (d, 1H), 6,80 (s, 1H), 6,44 (d, 1H)
Ejemplo 62: Preparación de 5-cloro-2-fluoro-4-((2'-fluoro-4-(furan-3-il)-[2,4'-bipiridin]-5-il)oxi)-N-(tiazol-4-il)bencenosulfonamida
8,3 mg (89 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 56, excepto que se usó ácido (2-fluoropiridin-4-il)borónico en lugar de ácido (2-fluoropiridin-3-il)borónico. 1H NMR (CDCl3, 500MHz) 59,57 (s, 1H), 8,66 (s, 1H), 8,42 (s, 1H), 8,35 (d, 1H), 8,02 (s, 1H), 8,00 (s, 1H), 7,95 (s, 1H), 7,79 (d, 1H), 7,56 (d, 1H), 7,53 (d, 1H), 7,04 (d, 1H), 6,83 (d, 1H), 6,51 (d, 1H)
Ejemplo 63: Preparación de 5-cloro-2-fluoro-4-((6-(2-fluorofenil)-4-(1-metil-1H-pirazol-4-il)piridin-3-il )oxi)-N-(tiazol-4-il)bencenosulfonamida 2,2,2-trifluoroacetato
20 mg (0,03 mmol) de terc-butil ((5-cloro-2-fluoro-4-((6-(2-fluorofenil)-4-(1-metil-1H-pirazol-4-il)piridin-3-il)oxi)fenil)sulfonil)(tiazol-4-il)carbamato se disolvió en 3 mL de diclorometano y 30 uL de ácido trifluoroacético se añadieron a esto, seguido por agitación a temperatura ambiente durante 5 horas. Después del completamiento de la reacción comprobado por TLC, el solvente se eliminó para obtener 7,0 mg (35 % de rendimiento) del compuesto del título.
1H NMR (CDCls, 500MHz) 58,75 (m, 1H), 8,52 (s, 1H), 8,39 (d, 1H), 8,35 (d, 1H), 8,14 (m, 1H), 8,07 (m, 1H), 7,84 (m, 1H), 7,61 (m, 1H), 7,39 (m, 2H), 7,10 (m, 2H), 3,93 (s, 3H)
Ejemplo 64: Preparación de 5-cloro-2-fluoro-4-((6-(3-fluorofenil)-4-(1-metil-1H-pirazol-5-il)piridin-3-il )oxi)-N-(tiazol-2-il)bencenosulfonamida
10 mg (0,02 mmol) de 5-cloro-4-((6-cloro-4-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-2-fluoro-N-(tiazol-2-il)bencenosulfonamida se disolvió en 3 mL de N,N-dimetilformamida y 4,2 mg (0,03 mmol) de ácido (3-fluorofenil)borónico se añadió a esto y luego 2,3 mg (10 % en mol) de Pd(PPh3)4 , 6,3 mg (0,6 mmol) de Na2CO3 y 1 mL de H2O se añadieron a esto. Después de reaccionar en el reactor de microondas a 120 °C durante 10 minutos, el solvente se eliminó y el material restante se diluyó con acetato de etilo y la capa orgánica se separó y se lavó con cloruro de sodio saturado. La capa orgánica se recogió, se secó con sulfato de magnesio para eliminar el agua y se concentró a presión reducida y el residuo se purificó por cromatografía de columna (solvente de desarrollo, hexano:acetato de etilo = 3:1) para obtener 4 mg (36 % de rendimiento) del compuesto del título.
1H NMR (CD3OD, 500MHz) 58,51 (s, 1H), 8,06 (s, 2H), 7,98 (m, 1H), 7,89 (m, 2H), 7,49 (m, 3H), 7,18 (m, 1H), 7,00 (m, 1H), 6,52 (s, 1H), 3,92 (s, 3H)
Ejemplo 65: Preparación de 5-cloro-2-fluoro-4-((6-(4-fluorofenil)-4-(1-metil-1H-pirazol-4-il)piridin-3-il )oxi)-N-(tiazol-4-il)bencenosulfonamida 2,2,2-trifluoroacetato
16 mg (80 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 63, excepto que se usó terc-butil ((5-cloro-2-fluoro-4-((6-(4-fluorofenil)-4-(1-metil-1H-pirazol-4-il)piridin-3-il)oxi)fenil)sulfonil)(tiazol-4-il)carbamato en lugar de terc-butil ((5-cloro-2-fluoro-4-((6-(2-fluorofenil)-4-(1-metil-1H-pirazol-4-il)piridin-3-il)oxi)fenil)sulfonil)(tiazol-4-il)carbamato.
1H NMR (CD3OD, 500MHz) 58,73 (s, 1H), 8,45 (s, 1H), 8,36 (s, 2H), 8,17 (m, 1H), 8,05 (m, 3H), 7,34 (m, 2H), 7,09 (m, 1H), 7,01 (m, 1H), 3,93 (s, 3H)
Ejemplo 66: Preparación de 5-cloro-4-((6-(2,4-difluorofenil)-4-(1-metil-1H-pirazol-4-il)piridin-3-il)oxi) -2-fluoro-N-(tiazol-4-il)bencenosulfonamida 2,2,2-trifluoroacetato
16 mg (80 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 63, excepto que se usó terc-butil ((5-cloro-4-((6-(2,4-difluorofenil)-4-(1 -metil-1 H-pirazol-4-il)piridin-3-il)oxi)-2-fluorofenil)sulfonil)(tiazol-4-il)carbamato en lugar de terc-butil ((5-cloro-2-fluoro-4-((6-(2-fluorofenil)-4-(1 -metil-1 H-pirazol-4-il)piridin-3-il)oxi)fenil)sulfonil)(tiazol-4-il)carbamato.
1H NMR (CD3OD, 500MHz) 58,73 (s, 1H), 8,40 (s, 1H), 8,30 (s, 1H), 8,24 (s, 1H), 8,08 (m, 2H), 7,92 (m, 1H), 7,20 (m, 2H), 7,09 (s, 1H), 6,99 (m, 1H)
Ejemplo 67: Preparación de 5-cloro-4-((6-(3,4-difluorofenil)-4-(1-metil-1H-pirazol-4-il)piridin-3-il)oxi) -2-fluoro-N-(tiazol-4-il)bencenosulfonamida 2,2,2-trifluoroacetato
16 mg (80 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 63, excepto que se usó terc-butil ((5-cloro-4-((6-(3,4-difluorofenil)-4-(1 -metil-1 H-pirazol-4-il)piridin-3-il)oxi)-2-fluorofenil)sulfonil)(tiazol-4-il)carbamato en lugar de terc-butil ((5-cloro-2-fluoro-4-((6-(2-fluorofenil)-4-(1-metil-1 H-pirazol-4-il)piridin-3-il)oxi)fenil)sulfonil)(tiazol-4-il)carbamato.
1H NMR (CD3OD, 500MHz) 58,73 (d, 1H), 8,40 (s, 1H), 8,29 (m, 2H), 8,10 (m, 1H), 8,03 (m, 2H), 7,89 (m, 1H), 7,43 (m, 1H), 7,08 (m, 1H), 6,87 (d, 1H), 3,91 (s, 3H)
Ejemplo 68: Preparación de 5-cloro-2-fluoro-4-((2'-fluoro-4-(1-metil-1H-pirazol-4-il)-[2,4'-bipiridin]-5-il) oxi)-N-(tiazol-4-il)bencenosulfonamida 2,2,2-trifluoroacetato
16 mg (80 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 63, excepto que se usó terc-butil ((5-cloro-2-fluoro-4-((2'-fluoro-4-(1-metil-1H-pirazol-4-il)-[2,4'-bipiridin]-5-il)oxi)fenil)sulfonil)(tiazol-4-il)carbamato en lugar de terc-butil ((5-cloro-2-fluoro-4-((6-(2-fluorofenil)-4-(1-metil-1 H-pirazol-4-il)piridin-3-il)oxi)fenil)sulfonil)(tiazol-4-il)carbamato.
1H NMR (CD3OD, 500MHz) 58,73 (s, 1H), 8,40 (s, 2H), 8,32 (m, 1H), 8,25 (d, 1H), 8,10 (m, 1H), 8,03 (m, 1H), 7,81 (s, 1H), 7,08 (s, 1H), 6,85 (d, 1H), 3,92 (s, 3H)
Ejemplo 69: Preparación de 5-cloro-2-fluoro-4-((2,-fluoro-4-(1-metil-1H-pirazol-4-il)-[2,3,-bipiridin]-5-il) oxi)-N-(tiazol-4-il)bencenosulfonamida 2,2,2-trifluoroacetato
16 mg (80 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 63, excepto que se usó terc-butil ((5-cloro-2-fluoro-4-((2'-fluoro-4-(1-metil-1H-pirazol-4-il)-[2,3'-bipiridin]-5-il)oxi)fenil)sulfonil)(tiazol-4-il)carbamato en lugar de terc-butil ((5-cloro-2-fluoro-4-((6-(2-fluorofenil)-4-(1-metil-1H-pirazol-4-il)piridin-3-il)oxi)fenil)sulfonil)(tiazol-4-il)carbamato.
1H NMR (CD3OD, 500MHz) 58,73 (s, 1H), 8,46 (m, 2H), 8,30 (m, 1H), 8,25 (m, 2H), 8,03 (m, 2H), 7,50 (s, 1H), 7,08 (s, 1H), 6,90 (m, 1H), 3,91 (s, 3H)
Ejemplo 70: Preparación de 5-cloro-2-fluoro-4-((6'-fluoro-4-(1-metil-1H-pirazol-4-il)-[2,3'-bipiridin]-5-il) oxi)-N-(tiazol-4-il)bencenosulfonamida 2,2,2-trifluoroacetato
16 mg (80 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 63, excepto que se usó terc-butil ((5-cloro-2-fluoro-4-((6'-fluoro-4-(1-metil-1H-pirazol-4-il)-[2,3'-bipiridin]-5-il)oxi)fenil)sulfonil)(tiazol-4-il)carbamato en lugar de terc-butil ((5-cloro-2-fluoro-4-((6-(2-fluorofenil)-4-(1-metil-1H-pirazol-4-il)piridin-3-il)oxi)fenil)sulfonil)(tiazol-4-il)carbamato.
1H NMR (CD3OD, 500MHz) 58,91 (m, 1H), 8,72 (m, 1H), 8,61 (m, 1H), 8,41 (m, 1H), 8,31 (m, 1H), 8,25 (m, 1H), 8,09 (m, 2H), 7,22 (m, 1H), 7,07 (m, 1H), 6,82 (m, 1H), 3,90 (s, 3H)
Ejemplo 71: Preparación de 5-cloro-2-fluoro-4-((6-(3-fluorofenil)-4-(1-metil-1H-pirazol-5-il)piridin-3-il )oxi)-N-(tiazol-4-il)bencenosulfonamida
20 mg (0,03 mmol) de terc-butil ((5-cloro-4-((6-cloro-4-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-2-fluorofenil)sulfonil)(tiazol-4-il)carbamato se disolvió en 3 mL de N,N-dimetilformamida y 6,9 mg (0,05 mmol) de ácido (3-fluorofenil)borónico se añadió a esto y luego 3,8 mg (10 % en mol) de Pd(PPh3)4 , 10,5 mg (0,1 mmol) de Na2CO3 y 1 mL de H2O se añadieron a esto. Después de reaccionar en el reactor de microondas a 120 °C durante 10 minutos, el solvente se eliminó y el material restante se diluyó con acetato de etilo y la capa orgánica se separó y se lavó con cloruro de sodio saturado. La capa orgánica se recogió, se secó con sulfato de magnesio para eliminar el agua y se concentró a presión reducida y el residuo se purificó por cromatografía de columna (solvente de desarrollo, hexano:acetato de etilo = 3:1) para obtener 5 mg (27 % de rendimiento) del compuesto del título.
1H NMR (CD3OD, 500MHz) 58,72 (s, 1H), 8,59 (s, 1H), 8,05 (s, 1H), 7,89 (m, 3H), 7,52 (m, 1H), 7,41 (m, 1H), 7,21 (m, 1H), 7,02 (m, 1H), 6,82 (m, 1H), 6,41 (s, 1H), 3,87 (s, 3H)
Ejemplo 72: Preparación de 5-cloro-2-fluoro-4-((6-(3-fluorofenil)-4-(2-(piperazin-1-il)pirimidin-4-il)pirid in-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida
1000 mg (1 eq) de 6-cloropiridin-3-ol se disolvió en 50 mL de N,N-dimetilformamida y 370 mg (1,2 eq) de hidruro de sodio se añadieron a esto, seguido por agitación a temperatura ambiente por 1 hora. Después, 688 uL (1,1 eq) de cloro(metoxi)metano se añadió lentamente al mismo y la solución se agitó a temperatura ambiente durante 2 horas. La N,N-dimetilformamida se eliminó por concentración a presión reducida. Después de extraer con acetato de etilo, el extracto se trató con sulfato de magnesio anhidro y se concentró a presión reducida. El residuo se separó mediante cromatografía de columna (solvente de desarrollo, hexano:acetato de etilo = 9:1) para obtener 1200 mg de 2-cloro-5-(metoximetoxi)piridina.
200 mg (1,0 eq) de la 2-cloro-5-(metoximetoxi)piridina obtenida se disolvió en N,N-dimetilformamida/H2O = 5:1 (16 mL), 193 mg (1,2 eq) de ácido (3-fluorofenil)borónico, 48 mg (3 % en mol) de Pd(PPh3)4 y 586 mg (4,0 eq) de Na 2CO3 se añadieron. Después de reaccionar en el reactor de microondas a 120 °C durante 30 minutos, N,N-dimetilformamida se eliminó por concentración a presión reducida. Después de extraer con acetato de etilo, el extracto se trató con sulfato de magnesio anhidro y se concentró a presión reducida. El residuo se separó mediante cromatografía de columna (solvente de desarrollo, hexano:acetato de etilo = 9:1) para obtener 220 mg de 2-(3-fluorofenil)-5-(metoximetoxi)piridina.
100 mg (1,0 eq) de la 2-(3-fluorofenil)-5-(metoximetoxi)piridina obtenida se disolvió en 4,3 mL de tetrahidrofurano. Después de enfriar a -78 °C, se añadió lentamente solución de terc-butillitio 1,7 M (0,5 mL, 2,0 eq). La mezcla se agitó a la misma temperatura durante 30 minutos. 121 mg (1,5 eq) de B(O-iPr)3 se disolvió en 2,1 mL de tetrahidrofurano y se añadió a la mezcla anterior. La mezcla se agitó a la misma temperatura durante 1 hora y se agitó durante 3 horas mientras se calentaba a temperatura ambiente. Después de inactivar mediante la adición de agua destilada, se añadió solución de tetrahidrofurano y se lavó con salmuera. La solución de reacción se secó con sulfato de magnesio para eliminar el agua, se concentró a presión reducida y se cristalizó con cloruro de metilo para obtener 50 mg de ácido (2-(3-fluorofenil)-5-hidroxipiridin-4-il)borónico como sólido blanco.
15.0 mg (1,0 eq) del ácido (2-(3-fluorofenil)-5-hidroxipiridin-4-il)borónico obtenido se disolvieron en 4,3 mL de 1,4-dioxano/H2O = 1:1 (1,0 mL) y 11,7 mg (1,0 eq) de ácido (2-(3-fluorofenil)-5-hidroxipiridin-4-il)borónico, 1,74 mg (3 % en mol) de Pd(PPhs)4 y 16,0 mg (3,0 eq) de Na2CO3 se añadieron. Después de reaccionar en el reactor de microondas a 120 °C durante 5 minutos, 1,4-dioxano se eliminó por concentración a presión reducida. Después de extraer con acetato de etilo, el extracto se trató con sulfato de magnesio anhidro y se concentró a presión reducida. El residuo se separó mediante cromatografía de columna (solvente de desarrollo, hexano:acetato de etilo = 4:1) para obtener 10,0 mg de terc-butil 4-(4-(2-(3-fluorofenil)-5-hidroxipiridin-4-il)pirimidin-2-il)piperazin-1 -carboxilato.
10.0 mg (1,0 eq) del terc-butil 4-(4-(2-(3-fluorofenil)-5-hidroxipiridin-4-il)pirimidin-2-il)piperazin-1-carboxilato obtenido y 9,1 mg (1,0 eq) del terc-butil ((5-cloro-2,4-difluorofenil)sulfonil)(tiazol-4-il)carbamato obtenido se disolvieron en 0,2 mL de N,N-dimetilformamida 0,2 mL, luego 21,6 mg (3,0 eq) de Cs2CO3 se añadió a esto. La mezcla se hizo reaccionar a temperatura ambiente durante 16 horas. El solvente se eliminó por concentración a presión reducida. El residuo se separó mediante PLC (solvente de desarrollo, hexano:acetato de etilo = 2:1) para obtener 10 mg de terc-butil 4-(4-(5-(4-(N-(tert-butoxicarbonil)-N-(tiazol-4-il)sulfamoil)-2-cloro-5-fluorofen oxi)-2-(3-fluorofenil)piridin-4-il)pirimidin-2-il)piperazin-1-carboxilato.
10 mg (1,0 eq) del terc-butil 4-(4-(5-(4-(N-(tert-butoxicarbonil)-N-(tiazol-4-il)sulfamoil)-2-cloro-5-fluorofen oxi)-2-(3-fluorofenil)piridin-4-il)pirimidin-2-il)piperazin-1-carboxilato obtenido se disolvió en 0,2 mL de dicloruro de metilo y 0,2 mL de ácido trifluoroacético se añadió a esto. La mezcla se hizo reaccionar a temperatura ambiente durante 2 horas. El solvente se eliminó por concentración a presión reducida. El residuo se separó mediante PLC (solvente de desarrollo, dicloruro de metilo:metanol = 15:1) para obtener 2,0 mg de 5-cloro-2-fluoro-4-((6-(3-fluorofenil)-4-(2-(piperazin-1-il)pirimidin-4-il)piridin-3 -il)oxi)-N-(tiazol-4-il)bencenosulfonamida.
1H NMR (CDCl3, 500MHz) 58,70 (s, 1H), 8,59 (s, 1H), 8,47 (d, 1H), 8,25 (s, 1H), 7,93 (m, 2H), 7,87 (d, 1H), 7,53 (q, 1H), 7,21 (m, 1H), 7,11 (d, 1H), 6,85 (d, 1H), 6,76 (d, 1H), 4,62 (br, 1H), 3,80 (br, 4H), 3,07 (t, 4H)
Ejemplo 73: Preparación de 5-cloro-2-fluoro-4-((6,-(3-fluorofenil)-[3,4,-bipiridin]-3,-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
20 mg (0,03 mmol) de terc-butil ((5-cloro-4-((6'-cloro-[3,4'-bipiridin]-3'-il)oxi)-2-fluorofenil)sulfonil)(tiazol-2-il)carbamato se disolvió en 3 mL de N,N-dimetilformamida y 7 mg (0,05 mmol) de ácido (3-fluorofenil)borónico se añadió a esto y luego 3,8 mg (10 % en mol) de Pd(PPh3)4 , 10,6 mg (0,10 mmol) de Na2CO3 y 1 mL de H2O se añadieron a esto. Después de reaccionar en el reactor de microondas a 120 °C durante 10 minutos, el solvente se eliminó y el material restante se diluyó con acetato de etilo y la capa orgánica se separó y se lavó con cloruro de sodio saturado. La capa orgánica se recogió, se secó con sulfato de magnesio para eliminar el agua y se concentró a presión reducida y el residuo se purificó por cromatografía de columna (solvente de desarrollo, hexano:acetato de etilo = 3:1) para obtener 5 mg (27 % de rendimiento) del compuesto del título.
1H NMR (CD3OD, 500MHz) 58,88 (m, 1H), 8,60 (s, 1H), 8,55 (m, 1H), 8,18 (m, 1H), 8,07 (s, 1H), 7,93 (m, 1H), 7,90 (m, 1H), 7,54 (m, 3H), 7,21 (m, 1H), 6,97 (m, 1H), 6,71 (s, 1H)
Ejemplo 74: Preparación de 5-cloro-2-fluoro-4-((6,-(3-fluorofenil)-[3,4,-bipiridin]-3,-il)oxi)-N-(tiazol-4-il)bencenosulfonamida
20 mg (0,03 mmol) de terc-butil ((5-cloro-4-((6'-cloro-[3,4'-bipiridin]-3'-il)oxi)-2-fluorofenil)sulfonil)(tiazol-4-il)carbamato se disolvió en 3 mL de N,N-dimetilformamida y 3,8 mg (10 % en mol) de ácido (3-fluorofenil)borónico se añadió a esto y luego 8,3 mg(3 % en mol) de Pd(PPh3)4 , 10,6 mg (0,10 mmol) de Na2CO3 y 1 mL de H2O se añadieron a esto. Después de reaccionar en el reactor de microondas a 120 °C durante 10 minutos, el solvente se eliminó y el material restante se diluyó con acetato de etilo y la capa orgánica se separó y se lavó con cloruro de sodio saturado. La capa orgánica se recogió, se secó con sulfato de magnesio para eliminar el agua y se concentró a presión reducida y el residuo se purificó por cromatografía de columna (solvente de desarrollo, hexano:acetato de etilo = 3:1) para obtener 5 mg (27 % de rendimiento) del compuesto del título.
1H NMR (CD3OD, 500MHz) 58,82 (m, 1H), 8,72 (m, 1H), 8,54 (m, 2H), 8,13 (m, 2H), 7,92 (m, 3H), 7,62 (m, 1H), 7,54 (m, 1H), 7,20 (m, 1H), 7,00 (m, 1H), 6,82 (d, 1H)
Ejemplo 75: Preparación de 5-cloro-2-fluoro-4-((2M-fluoro-[3,4':2,,4"-terpiridin]-5,-il)oxi)-N-(tiazol-4-il)bencenosulfonamida
16 mg (80 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 74, excepto que se usó ácido (2-fluoropiridin-4-il)borónico en lugar de ácido (3-fluorofenil)borónico.
1H NMR (CD3OD/CDCL3, 500MHz) 58,82 (s, 1H), 8,73 (s, 1H), 8,60 (s, 1H), 8,56 (m, 1H), 8,32 (m, 2H), 8,15 (m, 1H), 8,07 (m, 1H), 7,91 (m, 1H), 7,84 (s, 1H), 7,50 (m, 1H), 7,01 (s, 1H), 6,89 (d, 1H)
Ejemplo 76: Preparación de 5-cloro-2-fluoro-4-((6-(3-fluorofenil)-4-(pirimidin-5-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida
20 mg (0,03 mmol) de terc-butil ((5-cloro-4-((6-cloro-4-(pirimidin-5-il)piridin-3-il)oxi)-2-fluorofenil)sulfonil)(tiazol-4-il)carbamato se disolvió en 3 mL de N,N-dimetilformamida y 7 mg (0,05 mmol) de ácido (3-fluorofenil)borónico se añadió a esto y luego 3,8 mg (10 % en mol) de Pd(PPh3)4 , 10,6 mg (0,10 mmol) de Na2CO3 y 1 mL de H2O se añadieron a esto. Después de reaccionar en el reactor de microondas a 120 °C durante 10 minutos, el solvente se eliminó y el material restante se diluyó con acetato de etilo y la capa orgánica se separó y se lavó con cloruro de sodio saturado. La capa orgánica se recogió, se secó con sulfato de magnesio para eliminar el agua y se concentró a presión reducida y el residuo se purificó por cromatografía de columna (solvente de desarrollo, hexano:acetato de etilo = 3:1) para obtener 5 mg (27 % de rendimiento) del compuesto del título.
1H NMR (CD3OD, 500MHz) 59,17 (s, 1H), 9,11 (m, 2H), 8,74 (m, 1H), 8,54 (s, 1H), 8,21 (s, 1H), 7,93 (m, 3H), 7,52 (m, 1H), 7,20 (m, 1H), 7,04 (m, 1H), 6,95 (d, 1H)
Ejemplo 77: Preparación de 5-cloro-2-fluoro-4-((2,-fluoro-4-(pirimidin-5-il)-[2,4,-bipiridin]-5-il)oxi)-N-(tiazol-4-il)bencenosulfonamida
16 mg (80 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 76, excepto que se usó ácido (2-fluoropiridin-4-il)borónico en lugar de ácido (3-fluorofenil)borónico.
1H NMR (CDsOD/CDCls, 500MHz) 59,19 (s, 1H), 9,14 (s, 2H, 8,74 (m, 1H), 8,59 (s, 1H), 8,39 (m, 1H), 8,33 (m, 1H), 8,06 (m, 1H), 7,95 (m, 1H), 7,85 (m, 1H), 7,05 (m, 2H)
Ejemplo 78: Preparación de 5-cloro-2-fluoro-4-((6-(3-fluorofenil)-4-(1H-pirazol-4-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida
13,9 mg (0,03 mmol) de 5-cloro-4-((6-cloro-4-(1H-pirazol-4-il)piridin-3-il)oxi)-2-fluoro-N-(tiazol-4-il)bencenosulfonamida se disolvió en 1 mL de 1,4-dioxano y 6,3 mg (0,05 mmol) de ácido (3-fluorofenil)borónico se añadió a esto y luego 3,5 mg (10 % en mol)de Pd(PPh3 )4 , 12,4 mg (0,09 mmol) de Na2CO3 y 0,2 mL de H2O se añadieron a esto. Después de reaccionar en el reactor de microondas a 120 °C durante 20 minutos, el solvente se eliminó y el material restante se diluyó con acetato de etilo y la capa orgánica se separó y se lavó con cloruro de sodio saturado. La capa orgánica se recogió, se secó con sulfato de magnesio para eliminar el agua y se concentró a presión reducida y el residuo se purificó por cromatografía de columna (solvente de desarrollo, dicloruro de metilo:etanol = 15:1) para obtener 3,2 mg (19,7 % de rendimiento) del compuesto del título.
1H NMR (CD3OD, 500MHz) 56,73 (1H), 7,05 (1H), 7,19 (1H), 7,51 (1H), 7,85 (1H), 7,91 (1H), 8,00 (1H), 8,23 (3H), 8,39 (1H), 7,81 (1H)
Ejemplo 79: Preparación de 5-cloro-2-fluoro-4-((2'-fluoro-6-(3-fluorofenil)-[4,4'-bipiridin]-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida
20 mg (0,03 mmol) de terc-butil ((5-cloro-4-((6-cloro-2'-fluoro-[4,4'-bipiridin]-3-il)oxi)-2-fluorofenil)sulfonil)(tiazol-4-il)carbamato se disolvió en 3 mL de N,N-dimetilformamida y 6,8 mg (0,05 mmol) de ácido (3-fluorofenil)borónico se añadió a esto y luego 3,7 mg (10 % en mol) de Pd(PPh3)4 , 10 mg (0,10 mmol) de Na2CO3 y 1 mL de H2O se añadieron a esto. Después de reaccionar en el reactor de microondas a 120 °C durante 5 minutos, el solvente se eliminó y el material restante se diluyó con acetato de etilo y la capa orgánica se separó y se lavó con cloruro de sodio saturado. La capa orgánica se recogió, se secó con sulfato de magnesio para eliminar el agua y se concentró a presión reducida y el residuo se purificó por cromatografía de columna (solvente de desarrollo, hexano:acetato de etilo = 3:1) para obtener 5 mg (27 % de rendimiento) del compuesto del título.
1H NMR (CD3OD, 500MHz) 58,72 (m, 1H), 8,54 (s, 1H), 8,24 (d, 1H), 8,12 (m, 1H), 7,87 (m, 3H), 7,57 (m, 1H), 7,52 (m, 1H), 7,49 (m, 1H), 7,21 (m, 1H), 7,02 (m, 1H), 6,87 (d, 1H)
Ejemplo 80: Preparación de 5-cloro-4-((6-(3,4-difluorofenil)-2,-fluoro-[4,4,-bipiridin]-3-il)oxi)-2-fluoro-N-(tiazol-4-il)bencenosulfonamida
16 mg (80 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 79, excepto que se usó ácido (3,4-fluorofenil)borónico en lugar de ácido (3-fluorofenil)borónico.
1H NMR (CDsOD/CDCls, 500MHz) 58,72 (s, 1H), 8,53 (s, 1H), 8,24 (m, 1H), 8,11 (m, 2H), 7,91 (m, 2H), 7,56 (m, 1H), 7,40 (m, 2H), 7,01 (s, 1H), 6,88 (d, 1H)
Ejemplo 81: Preparación de 5-cloro-4-((6'-(5-cloro-2-fluorofenil)-[3,4,-bipiridin]-3,-il)oxi)-2-fluoro-N-(tiazol-4-il)bencenosulfonamida
16 mg (80 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 74, excepto que se usó ácido (5-cloro-2-fluorofenil)borónico en lugar de ácido (3-fluorofenil)borónico.
1H NMR (CDs OD/CDCls , 500MHz) 58,96 (s, 1H), 8,87 (s, 1H), 8,70 (s, 1H), 8,58 (m, 1H), 8,12 (m, 4H), 7,70 (s, 1H), 7,52 (m, 2H), 7,30 (m, 1H), 6,98 (d, 1H)
Ejemplo 82: Preparación de 5-cloro-4-((6'-(3,4-difluorofenil)-[3,4'-bipiridin]-3,-il)oxi)-2-fluoro-N-(tiazol -4-il)bencenosulfonamida
16 mg (80 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 74, excepto que se usó ácido (3,4-fluorofenil)borónico en lugar de ácido (3-fluorofenil)borónico.
1H NMR (CD3OD/CDCl3, 500MHz) 58,82 (s, 1H), 8,71 (s, 1H), 8,53 (s, 2H), 8,11 (m, 3H), 7,94 (m, 1H), 7,87 (d, 1H), 7,47 (m, 1H), 7,40 (m, 1H), 6,95 (s, 1H), 6,80 (d, 1H)
Ejemplo 83: Preparación de 3-ciano-4-((6-(3-fluorofenil)-4-(1H-pirazol-4-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida
25,0 mg (0,05 mmol) de 4-((6-cloro-4-(1H-pirazol-4-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-4-il)bencenosulfonamida se disolvió en 1,5 mL de 1,4-dioxano y 10,5 mg (0,08 mmol) de ácido (3-fluorofenil)borónico se añadió a esto y luego 5,8 mg (10 % en mol) de Pd(PPh 3)4 , 20,7 mg (0,15 mmol) de K2CO3 y 0,3 mL de H2O se añadieron a esto. Después de reaccionar en el reactor de microondas a 120 °C durante 20 minutos, el solvente se eliminó y el material restante se diluyó con acetato de etilo y la capa orgánica se separó y se lavó con cloruro de sodio saturado. La capa orgánica se recogió, se secó con sulfato de magnesio para eliminar el agua y se concentró a presión reducida y el residuo se purificó por cromatografía de columna (solvente de desarrollo, hexano:acetato de etilo = 1:1) para obtener 9,0 mg (31,9 % de rendimiento) del compuesto del título.
1H NMR (CD3OD, 500MHz) 56,92 (1H), 7,07 (1H), 7,19 (1H), 7,53 (1H), 7,86 (1H), 7,92 (2H), 8,26 (4H), 8,49 (1H), 8,71 (1H)
Ejemplo 84: Preparación de 3-ciano-4-((6'-(3-fluorofenil)-[3,4'-bipiridin]-3'-il)oxi)-N-(tiazol-4-il)benceno sulfonamida
10 mg (0,03 mmol) de terc-butil ((4-((6'-cloro-[3,4'-bipiridin]-3'-il)oxi)-3-cianofenil)sulfonil)(tiazol-4-il)carbam ate se disolvió en 3 mL de N,N-dimetilformamida y 3,7 mg (0,03 mmol) de ácido (3-fluorofenil)borónico se añadió a esto y luego 2 mg (10 % en mol) de Pd(PPh3) 4, 5,6 mg (0,05 mmol) de Na2CO3 y 1 mL de H2O se añadieron a esto. Después de reaccionar en el reactor de microondas a 120 °C durante 5 minutos, el solvente se eliminó y el material restante se diluyó con acetato de etilo y la capa orgánica se separó y se lavó con cloruro de sodio saturado. La capa orgánica se recogió, se secó con sulfato de magnesio para eliminar el agua y se concentró a presión reducida y el residuo se purificó por cromatografía de columna (solvente de desarrollo, hexano:acetato de etilo = 3:1) para obtener 5 mg (27 % de rendimiento) del compuesto del título.
1H NMR (CD3OD, 500MHz) 58,79 (s, 1H), 8,71 (m, 1H), 8,67 (s, 1H), 8,52 (m, 1H), 8,13 (m, 3H), 7,91 (m, 3H), 7,51 (m, 1H), 7,48 (m, 1H), 7,21 (m, 1H), 7,19 (m, 1H), 6,95 (d, 1H)
Ejemplo 85: Preparación de 3-ciano-4-((6'-(3,4-difluorofenil)-[3,4'-bipiridin]-3'-il)oxi)-N-(tiazol-4-il)bencenosulfonamida
16 mg (80 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 84, excepto que se usó ácido (3,4-fluorofenil)borónico en lugar de ácido (3-fluorofenil)borónico.
1H NMR (CD3OD/CDCL3, 500MHz) 58,78 (s, 1H), 8,72 (s, 1H), 8,65 (s, 1H), 8,52 (m, 1H), 8,12 (m, 4H), 7,99 (m, 1H), 7,88 (m, 1H), 7,46 (m, 1H), 7,39 (m, 1H), 7,02 (s, 1H), 6,93 (d, 1H)
Ejemplo 86: Preparación de 3-ciano-4-((6,-(3-fluoro-4-(trifluorometil)fenil)-[3,4,-bipiridin]-3,-il)oxi)-N-( tiazol-4-il)bencenosulfonamida
16 mg (80 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 84, excepto que se usó ácido (3-fluoro-4-(trifluorometil)fenil)borónico en lugar de ácido (3-fluorofenil)borónico.
1H NMR (CD3OD/CDG3 , 500MHz) 58,81 (s, 1H), 8,71 (s, 2H), 8,53 (m, 1H), 8,27 (m, 1H), 8,12 (m, 4H), 7,88 (m, 2H), 7,49 (m, 1H), 7,01 (m, 2H)
Ejemplo 87: Preparación de 2,5-difluoro-4-((6'-(3-fluorofenil)-[3,4,-bipiridin]-3,-il)oxi)-N-(tiazol-4-il)bencenosulfonamida
10 mg (0,03 mmol) de terc-butil ((4-((6'-cloro-[3,4'-bipiridin]-3'-il)oxi)-2,5-difluorofenil)sulfonil)(tiazol-4-il)carbamato se disolvió en 3 mL de N,N-dimetilformamida y 3,7 mg (0,03 mmol) de ácido (3-fluorofenil)borónico se añadió a esto y luego 2 mg (10 % en mol) de Pd(PPh3) 4 , 5,5 mg (0,05 mmol) de Na2CO3 y 1 mL de H2O se añadieron a esto. Después de reaccionar en el reactor de microondas a 120 °C durante 10 minutos, el solvente se eliminó y el material restante se diluyó con acetato de etilo y la capa orgánica se separó y se lavó con cloruro de sodio saturado. La capa orgánica se recogió, se secó con sulfato de magnesio para eliminar el agua y se concentró a presión reducida y el residuo se purificó por cromatografía de columna (solvente de desarrollo, hexano:acetato de etilo = 3:1) para obtener 5 mg (27 % de rendimiento) del compuesto del título.
1H NMR (CD3OD, 500MHz) 58,81 (m, 1H), 8,73 (m, 1H), 8,54 (m, 2H), 8,12 (m, 2H), 7,91 (d, 1H), 7,86 (m, 1H), 7,68 (m, 1H), 7,50 (m, 2H), 7,19 (m, 1H), 6,99 (m, 1H), 6,94 (m, 1H)
Ejemplo 88: Preparación de 4-((6'-(3,4-difluorofenil)-[3,4'-bipiridin]-3,-il)oxi)-2,5-difluoro-N-(tiazol-4-il) bencenosulfonamida
16 mg (80 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 87, excepto que se usó ácido (3,4-fluorofenil)borónico en lugar de ácido (3-fluorofenil)borónico.
1H NMR (CD3OD/CDG3 , 500MHz) 58,81 (s, 1H), 8,73 (s, 1H), 8,54 (m, 2H), 8,12 (m, 3H), 7,93 (m, 1H), 7,67 (m, 1H), 7,50 (m, 1H), 7,39 (m, 1H), 7,00 (s, 1H), 6,91 (m, 1H)
Ejemplo 89: Preparación de 2,5-difluoro-4-((6'-(3-fluoro-4-(trifluorometil)fenil)-[3,4'-bipiridin]-3'-il)oxi)-N-(tiazol-4-il)bencenosulfonamida
16 mg (80 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 87, excepto que se usó ácido (3-fluoro-4-(trifluorometil)fenil)borónico en lugar de ácido (3-fluorofenil)borónico.
1H NMR (CD3OD/CDCl3, 500MHz) 58,83 (m, 1H), 8,78 (m, 1H), 8,56 (m, 2H), 8,21 (s, 1H), 8,12 (m, 3H), 7,81 (m, 1H), 7,68 (m, 1H), 7,51 (m, 1H), 6,96 (m, 2H)
Ejemplo 90: Preparación de 3-ciano-4-((6-(4-fluorofenil)-4-(1H-pirazol-4-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida
5,5 mg (29,5 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 83, excepto que se usaron 4-((6-cloro-4-(1H-pirazol-4-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-4-il)bencenosulfonamida y ácido (4-fluorofenil)borónico en lugar de 4-((6-cloro-4-(1 H-pirazol-4-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-4-il)bencenosulfonamida y ácido (3-fluorofenil)borónico.
1H NMR (CDsOD, 500MHz) 56,91 (1H), 7,05 (1H), 7,24 (2H), 7,92 (1H), 8,12 (3H), 8,24 (3H), 8,47 (1H), 8,70 (1H)
Ejemplo 91: Preparación de 3-ciano-4-((6-(3,4-difluorofenil)-4-(1H-pirazol-4-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida
5,7 mg (29,5 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 83, excepto que se usó ácido (3,4-difluorofenil)borónico en lugar de ácido (3-fluorofenil)borónico.
1H NMR (CDs OD, 500MHz) 56,91 (1H), 7,06 (1H), 7,40 (1H), 7,94 (2H), 8,07 (1H), 8,23 (4H), 8,49 (1H), 8,71 (1H)
Ejemplo 92: Preparación de 3-ciano-4-((6-(3-fluorofenil)-4-(pirimidin-5-il)piridin-3-il)oxi)-N-(tiazol-4-il )bencenosulfonamida
10 mg (0,02 mmol) de terc-butil ((4-((6-cloro-4-(pirimidin-5-il)piridin-3-il)oxi)-3-cianofenil)sulfonil)(tiazol-4-il)carbamato se disolvió en 3 mL de N,N-dimetilformamida y 3,7 mg (0,03 mmol) de ácido (3-fluorofenil)borónico se añadió a esto y luego 2 mg (10 % en mol) de Pd(PPh3)4, 5,5 mg (0,05 mmol) de Na2CO3 y 1 mL de H2O se añadieron a esto. Después
de reaccionar en el reactor de microondas a 120 °C durante 10 minutos, el solvente se eliminó y el material restante se diluyó con acetato de etilo y la capa orgánica se separó y se lavó con cloruro de sodio saturado. La capa orgánica se recogió, se secó con sulfato de magnesio para eliminar el agua y se concentró a presión reducida y el residuo se purificó por cromatografía de columna (solvente de desarrollo, hexano:acetato de etilo = 3:1) para obtener 80 mg (70 % de rendimiento) del compuesto del título.
1H NMR (CD3OD, 500MHz) 59,15 (s, 1H), 9,08 (s, 2H), 8,73 (s, 1H), 8,67 (s, 1H), 8,23 (s, 1H), 8,18 (m, 1H), 7,97 (m, 1H), 7,93 (m, 2H), 7,53 (m, 1H), 7,21 (m, 1H), 7,05 (m, 2H)
Ejemplo 93: Preparación de 3-ciano-4-((6-(3,4-difluorofenil)-4-(pirimidin-5-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida
16 mg (80 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 92, excepto que se usó ácido (3,4-fluorofenil)borónico en lugar de ácido (3-fluorofenil)borónico.
1H NMR (CD3OD/CDG3 , 500MHz) 59,16 (s, 1H), 9,08 (s, 2H), 8,72 (s, 1H), 8,66 (s, 1H), 8,22 (s, 1H), 8,18 (s, 1H), 8,11 (m, 1H), 7,98 (m, 1H), 7,91 (m, 1H), 7,42 (m, 1H), 7,05 (m, 2H)
Ejemplo 94: Preparación de 3-ciano-4-((6-(3-fluoro-4-(trifluorometil)fenil)-4-(pirimidin-5-il)piridin-3-il) oxi)-N-(tiazol-4-il)bencenosulfonamida
16 mg (80 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 92, excepto que se usó ácido (3-fluoro-4-(trifluorometil)fenil)borónico en lugar de ácido (3-fluorofenil)borónico.
1H NMR (CDsOD/CDCls, 500MHz) 59,17 (s, 1H), 9,10 (s, 2H), 8,73 (m, 2H), 8,35 (s, 1H), 8,19 (m, 3H), 7,94 (m, 1H), 7,83 (m, 1H), 7,09 (m, 2H)
Ejemplo 95: Preparación de 2,5-difluoro-4-((6-(3-fluorofenil)-4-(pirimidin-5-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida
10 mg (0,02 mmol) de terc-butil ((4-((6-cloro-4-(pirimidin-5-il)piridin-3-il)oxi)-2,5-difluorofenil)sulfonil)(tiazol-4-il)carbamato se disolvió en 3 mL de N,N-dimetilformamida y 3,6 mg (0,03 mmol) de ácido (3-fluorofenil)borónico se añadió a esto y luego 2 mg (10 % en mol) de Pd(PPh3)4, 5,4 mg (0,05 mmol) de Na2CO3 y 1 mL de H2O se añadieron a esto. Después de reaccionar en el reactor de microondas a 120 °C durante 10 minutos, el solvente se eliminó y el material restante se diluyó con acetato de etilo y la capa orgánica se separó y se lavó con cloruro de sodio saturado. La capa orgánica se recogió, se secó con sulfato de magnesio para eliminar el agua y se concentró a presión reducida y el residuo se purificó por cromatografía de columna (solvente de desarrollo, hexano:acetato de etilo = 3:1) para obtener 5 mg (27 % de rendimiento) del compuesto del título.
1H NMR (CD3OD, 500MHz) 59,18 (s, 1H), 9,10 (s, 2H), 8,73 (s, 1H), 8,54 (s, 1H), 8,19 (s, 1H), 7,92 (m, 2H), 7,72 (m, 1H), 7,52 (m, 1H), 7,21 (m, 1H), 7,09 (m, 1H), 7,01 (s, 1H)
Ejemplo 96: Preparación de 4-((6-(3,4-difluorofenil)-4-(pirimidin-5-il)piridin-3-il)oxi)-2,5-difluoro-N-(tiazol-4-il)bencenosulfonamida
16 mg (80 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 95, excepto que se usó ácido (3,4-difluorofenil)borónico en lugar de ácido (3-fluorofenil)borónico.
1H NMR (CD3OD/CDG3 , 500MHz) 59,18 (s, 1H), 9,10 (s, 2H), 8,73 (s, 1H), 8,53 (s, 1H), 8,17 (s, 1H), 8,08 (m, 1H), 7,95 (m, 1H), 7,73 (m, 1H), 7,38 (m, 1H), 7,08 (m, 1H), 7,01 (s, 1H)
Ejemplo 97: Preparación de 2,5-difluoro-4-((6-(3-fluoro-4-(trifluorometil)fenil)-4-(pirimidin-5-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida
16 mg (80 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 95, excepto que se usó ácido (3-fluoro-4-(trifluorometil)fenil)borónico en lugar de ácido (3-fluorofenil)borónico.
1H NMR (CDsOD/CDCls, 500MHz) 59,19 (s, 1H), 9,12 (s, 2H), 8,73 (s, 1H), 8,57 (s, 1H), 8,30 (s, 1H), 8,14 (m, 2H), 7,82 (m, 1H), 7,77 (m, 1H), 7,14 (m, 1H), 7,02 (s, 1H)
Ejemplo 98: Preparación de 5-cloro-4-((6-(3,4-difluorofenil)-4-(1H-pirazol-4-il)piridin-3-il)oxi)-2-fluoro-N-(tiazol-4-il)bencenosulfonamida
15,0 mg (0,03 mmol) de 5-cloro-4-((6-cloro-4-(1H-pirazol-4-il)piridin-3-il)oxi)-2-fluoro-N-(tiazol-4-il)bencenosulfonamida se disolvió en 1,5 mL de 1,4-dioxano y 7,1 mg (0,05 mmol) de ácido (3,4-difluorofenil)borónico se añadió a esto y luego 3,5 mg (10 % en mol) de Pd(PPh3)4 , 12,4 mg (0,09 mmol) de K2CO3 y 0,3 mL de H2O se añadieron a esto. Después de reaccionar en el reactor de microondas a 150 °C durante 30 minutos, el solvente se eliminó y el material restante se diluyó con acetato de etilo y la capa orgánica se separó y se lavó con cloruro de sodio saturado. La capa orgánica se recogió, se secó con sulfato de magnesio para eliminar el agua y se concentró a presión reducida y el residuo se purificó por cromatografía de columna (solvente de desarrollo, dicloruro de metilo:metanol = 20:1) para obtener 9,0 mg (31,9 % de rendimiento) del compuesto del título.
1H NMR (DMSO-d6 , 500MHz) 58,86 (1H), 8,59 (1H), 8,35 (1H), 8,04 (2H), 7,88 (3H), 7,37 (1H), 7,17 (1H), 6,31 (1H)
Ejemplo 99: Preparación de 5-cloro-2-fluoro-4-((6'-(3-fluorofenil)-5-(pirrolidin-1-il)-[3,4'-bipiridin]-3'-il) oxi)-N-(tiazol-4-il)bencenosulfonamida
30 mg (0,05 mmol) de 5-cloro-2-fluoro-4-((6-(3-fluorofenil)-4-yodipiridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida se disolvió en 0,9 mL de N,N-dimetilformamida y 13,2 mg (0,05 mmol) de ácido (5-(pirrolidin-1-il)piridin-3-il)borónico se añadió a esto y luego 5,3 mg (10 % en mol) de Pd(PPh3)4 , 14,5 mg (0,15 mmol) de Na2CO3 y 0,1 mL de H2O se añadieron a esto. Después de reaccionar en el reactor de microondas a 120 °C durante 10 minutos, el solvente se eliminó y el material restante se diluyó con acetato de etilo y la capa orgánica se separó y se lavó con cloruro de sodio saturado. La capa orgánica se recogió, se secó con sulfato de magnesio para eliminar el agua y se concentró a presión reducida y el residuo se purificó por cromatografía de columna (solvente de desarrollo, hexano:acetato de etilo = 1 :2) para obtener 5,0 mg (17,5 % de rendimiento) del compuesto del título.
1H NMR (CD3OD, 500MHz) 58,71 (1H), 8,70 (1H), 8,56 (1H), 8,08 (1H), 7,87 (4H), 7,51 (1H), 7,19 (1H), 7,12 (1H), 6,97 (1H), 6,73 (1H), 2,00 (4H)
Ejemplo 100: Preparación de 5-cloro-2-fluoro-4-((6-(3-fluorofenil)-4-(1-(piridin-3-il)-1H-imidazol-4-il)piri din-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida
3,0 mg (10,5 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 99, excepto que se usó 3-(4-(4,4,5,5,-tetrametil-1,3,2-dioxaboran-2-il)-1H-imidazol-1-il)piridina en lugar de ácido (5-(pirrolidin-1-il)piridin-3-il)borónico.
1H NMR (CD3OD, 500MHz) 58,30 (1H), 8,11 (1H), 7,78 (3H), 7,67 (3H), 7,56 (3H), 7,45 (1H), 7,11 (1H)
Ejemplo 101: Preparación de 5-cloro-2-fluoro-4-((6-(3-fluorofenil)-2'-morfolino-[4,4'-bipiridin]-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida
4,5 mg (15,4 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 99, excepto que se usó ácido (2-morfolinopiridin-4-il)borónico en lugar de ácido (5-(pirrolidin-1-il)piridin-3-il)borónico.
1H NMR (CD3OD, 500MHz) 58,71 (1H), 8,56 (1H), 8,11 (1H), 8,06 (1H), 7,92 (1H), 7,87 (2H), 7,53 (1H), 7,20 (1H), 6,94 (2H), 6,86 (1H), 6,72 (1H), 3,75 (4H), 3,46 (4H)
Ejemplo 102: Preparación de 5-cloro-2-fluoro-4-((6-(3-fluorofenil)-2'-(piperidin-1-il)-[4,4'-bipiridin]-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida
4,8 mg (16,4 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 99, excepto que se usó ácido (2-(piperidin-1-il)piridin-4-il)borónico en lugar de ácido (5-(pirrolidin-1-il)piridin-3-il)borónico.
1H NMR (CD3OD, 500MHz) 58,71 (1H), 8,55 (1H), 8,05 (2H), 7,91 (1H), 7,87 (2H), 7,52 (1H), 7,20 (1H), 6,94 (1H), 6,87 (1H), 6,77 (1H), 6,72 (1H), 3,49 (4H), 1,65 (2H), 1,56 (4H)
Ejemplo 103: Preparación de 3-ciano-4-((2,-fluoro-6-(furan-3-il)-[2,3,-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
2,5 mg (22,1 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usaron 4-((6-cloro-2-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (2-fluoropiridin-3-il)borónico en lugar de 4-((6-cloro-4-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (3-fluorofenil)borónico.
1H NMR (DMSO-d6, 500MHz) 56,87 (1H), 7,18 (2H), 7,28 (1H), 7,56 (1H), 7,89 (2H), 7,99 (1H), 7,28 (2H), 8,34 (1H), 8,70 (1H)
Ejemplo 104: Preparación de 3-ciano-4-((6'-fluoro-6-(furan-3-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
2,5 mg (11,0 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usaron 4-((6-cloro-2-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (6-fluoropiridin-3-il)borónico en lugar de 4-((6-cloro-4-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (3-fluorofenil)borónico.
1H NMR (CD3OD, 500MHz) 56,86 (1H), 7,10 (1H), 7,20 (1H), 7,28 (1H), 7,34 (1H), 7,81 (1H), 7,92 (1H), 7,96 (1H), 8,08 (1H), 8,28 (2H), 8,77 (1H), 9,10 (1H)
Ejemplo 105: Preparación de 3-ciano-4-((6-(furan-3-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
2,5 mg (11,5 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usaron 4-((6-cloro-4-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (3-fluorofenil)borónico en lugar de 4-((6-cloro-2-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (piridin-3-il)borónico.
1H NMR (CDsOD, 500MHz) 56,73 (1H), 7,04 (1H), 7,11 (1H), 7,21 (1H), 7,59 (2H), 7,71 (1H), 7,95 (1H), 8,05 (1H), 8,19 (1H), 8,30 (1H), 8,61 (2H), 9,31 (1H)
Ejemplo 106: Preparación de 3-ciano-4-((2-(furan-3-il)-6-(pirimidin-5-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
2,4 mg (11,0 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usaron 4-((6-cloro-2-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (pirimidin-5-il)borónico en lugar de 4-((6-cloro-4-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (3-fluorofenil)borónico.
1H NMR (DMSO-d6, 500MHz) 56,74 (1H), 7,08 (1H), 7,12 (1H), 7,22 (1H), 7,60 (1H), 7,73 (1H), 8,00 (1H), 8,06 (1H), 8,22 (1H), 8,31 (1H), 9,22 (1H), 9,52 (2H)
Ejemplo 107: Preparación de 3-ciano-4-((2'-fluoro-6-(1-metil-1H-pirazol-5-il)-[2,4'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
2,0 mg (15,2 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usaron 4-((6-cloro-2-(1 -metil-1H-pirazol-5-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (2-fluoropiridin-4-il)borónico en lugar de 4-((6-cloro-4-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (3-fluorofenil)borónico.
1H NMR (DMSO-d6, 500MHz) 54,10 (3H), 6,61 (1H), 6,88 (1H), 7,15 (1H), 7,29 (1H), 7,47 (1H), 7,92 (2H), 8,12 (2H), 8,23 (1H), 8,39 (2H), 12,88 (1H)
Ejemplo 108: Preparación de 3-ciano-4-((6-(2-fluorofenil)-2-(furan-3-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
3,0 mg (13,2 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usaron 4-((6-cloro-2-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (2-fluorofenil)borónico en lugar de 4-((6-cloro-4-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (3-fluorofenil)borónico.
1H NMR (DMSO-d6, 500MHz) 56,86 (1H), 7,14 (2H), 7,28 (1H), 7,37 (2H), 7,52 (1H), 7,79 (2H), 7,86 (1H), 7,98 (1H), 8,10 (1H), 8,30 (2H)
Ejemplo 109: Preparación de 3-ciano-4-((6-(4-fluorofenil)-2-(furan-3-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
4,5 mg (19,7 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usaron 4-((6-cloro-2-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (4-fluorofenil)borónico en lugar de 4-((6-cloro-4-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (3-fluorofenil)borónico.
1H NMR (DMSO-d6, 500MHz) 56,86 (1H), 7,08 (1H), 7,16 (1H), 7,27 (1H), 7,34 (2H), 7,80 (1H), 7,86 (1H), 7,97 (2H), 8,25 (4H)
Ejemplo 110: Preparación de 3-ciano-4-((6-(3-fluorofenil)-2-(furan-3-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
4.3 mg (18,9 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usaron 4-((6-cloro-2-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (3-fluorofenil)borónico en lugar de 4-((6-cloro-4-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (3-fluorofenil)borónico.
1H NMR (DMSO-d6, 500MHz) 56,86 (1H), 7,10 (1H), 7,19 (1H), 7,28 (2H), 7,56 (1H), 7,80 (1H), 7,87 (1H), 7,96 (1H), 8.04 (3H), 8,27 (2H)
Ejemplo 111: Preparación de 3-ciano-4-((6-(furan-3-il)-[2,4'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
2,5 mg (11,3 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usaron 4-((6-cloro-2-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (piridin-4-il)borónico en lugar de 4-((6-cloro-4-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (3-fluorofenil)borónico.
1H NMR (CDsOD, 500MHz) 56,76 (1H), 7,08 (1H), 7,13 (1H), 7,24 (1H), 7,61 (1H), 7,73 (1H), 8,05 (2H), 8,21 (3H), 8,32 (1H), 8,68 (2H)
Ejemplo 112: Preparación de 3-ciano-4-((2'-fluoro-6-(furan-3-il)-[2,4'-bipiridin]-5-il)oxi)-N-(tiazol-2-iljbencenosulfonamida
2,5 mg (11,0 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usaron 4-((6-cloro-2-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (2-fluoropiridin-4-il)borónico en lugar de 4-((6-cloro-4-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (3-fluorofenil)borónico.
1H NMR (CD3OD, 500MHz) 56,75 (1H), 7,09 (1H), 7,13 (1H), 7,24 (1H), 7,61 (1H), 7,72 (1H), 7,85 (1H), 7,94 (3H), 8,23 (1H), 8,33 (1H)
Ejemplo 113: Preparación de 3-ciano-4-((2-(furan-3-il)-6-(tiofen-3-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
3.0 mg (13,4 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usaron 4-((6-cloro-2-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (tiofen-3-il)borónico en lugar de 4-((6-cloro-4-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (3-fluorofenil)borónico.
1H NMR (CD3OD, 500MHz) 56,75 (1H), 6,95 (1H), 7,14 (1H), 7,52 (1H), 7,56 (1H) 7,61 (1H), 7,76 (1H), 7,80 (1H), 8.01 (1H), 8,11 (2H), 8,30 (1H)
Ejemplo 114: Preparación de 3-ciano-4-((2,6-di(furan-3-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
3,2 mg (14,8 % de rendimiento) del compuesto del titulo se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usaron 4-((6-cloro-2-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (furan-3-il)borónico en lugar de 4-((6-cloro-4-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (3-fluorofenil)borónico.
1H NMR (CD3OD, 500MHz) 56,71 (1H), 6,92 (1H), 7,05 (1H), 7,09 (1H), 7,12 (1H), 7,58 (4H), 8,01 (1H), 8,09 (1H), 8,20 (1H), 8,27 (1H)
Ejemplo 115: Preparación de 3-ciano-4-((6'-fluoro-6-(1-metil-1H-pirazol-5-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
2,4 mg (18,2 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usaron 4-((6-cloro-2-(1 -metil-1H-pirazol-5-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (6-fluoropiridin-3-il)borónico en lugar de 4-((6-cloro-4-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (3-fluorofenil)borónico.
1H NMR (CD3OD, 500MHz) 54,11 (3H), 6,69 (1H), 6,76 (1H), 7,02 (1H), 7,13 (1H), 7,23 (1H), 7,44 (1H), 7,89 (1H), 8,00 (1H), 8,11 (1H), 8,20 (1H), 8,68 (1H), 8,98 (1H)
Ejemplo 116: Preparación de 3-ciano-4-((2'-fluoro-6-(1-metil-1H-pirazol-5-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
1,9 mg (13,7 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usaron 4-((6-cloro-2-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (2-fluoropiridin-3-il)borónico en lugar de 4-((6-cloro-4-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (3-fluorofenil)borónico.
1H NMR (CD3OD, 500MHz) 54,10 (3H), 6,71 (1H), 6,76 (1H), 7,05 (1H), 7,13 (1H), 7,45 (1H), 7,51 (1H), 7,90 (1H), 8,02 (1H), 8,08 (1H), 8,22 (1H), 8,32 (1H), 8,65 (1H),
Ejemplo 117: Preparación de 3-ciano-4-((6-(3-fluorofenil)-2-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-N-( tiazol-2-il)bencenosulfonamida
1,5 mg (17,6 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usaron 4-((6-cloro-2-(1 -metil-1H-pirazol-5-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (3-fluorofenil)borónico en lugar de 4-((6-cloro-4-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (3-fluorofenil)borónico.
1H NMR (CD3OD, 500MHz) 54,12 (3H), 6,68 (1H), 6,76 (1H), 6,99 (1H), 7,13 (1H), 7,20 (1H), 7,44 (1H), 7,53 (1H), 7,89 (2H), 7,96 (1H), 7,99 (1H), 8,08 (1H), 8,20 (1H)
Ejemplo 118: Preparación de 3-ciano-4-((6-(2-fluorofenil)-2-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-N-( tiazol-2-il)bencenosulfonamida
1,3 mg (15,3 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usaron 4-((6-cloro-2-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (2-fluorofenil)borónico en lugar de 4-((6-cloro-4-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (3-fluorofenil)borónico.
1H NMR (CD3OD, 500MHz) 54,09 (3H), 6,68 (1H), 6,75 (1H), 7,01 (1H), 7,13 (1H), 7,28 (1H), 7,35 (1H), 7,43 (1H), 7,85 (1H), 8,00 (3H), 8,20 (1H)
Ejemplo 119: Preparación de 3-ciano-4-((2-(1-metil-1H-pirazol-5-il)-6-(tiofen-3-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
4,5 mg (20,4 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usaron 4-((6-cloro-2-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (tiofen-3-il)borónico en lugar de 4-((6-cloro-4-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (3-fluorofenil)borónico.
1H NMR (DMSO-d6, 500MHz) 54,09 (3H), 6,53 (1H), 6,80 (1H), 7,02 (1H), 7,22 (1H), 7,43 (1H), 7,70 (1H), 7,82 (1H), 7,89 (1H), 7,97 (1H), 8,05 (1H), 8,18 (1H), 8,31 (1H)
Ejemplo 120: Preparación de 3-ciano-4-((6-(1-metil-1H-pirazol-4-il)-2-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
2,5 mg (11,4 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usaron 4-((6-cloro-2-(1 -metil-1H-pirazol-5-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (1-metil-1H-pirazol-4-il)borónico en lugar de 4-((6-cloro-4-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (3-fluorofenil)borónico.
1H NMR (CDsOD, 500MHz) 53,97 (3H), 4,09 (3H), 6,61 (1H), 6,73 (1H), 6,92 (1H), 7,12 (1H), 7,76 (1H), 7,97 (1H), 8,07 (1H), 8,17 (1H), 8,25 (1H)
Ejemplo 121: Preparación de 3-ciano-4-((6-(isoxazol-4-il)-2-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
3,0 mg (14,0 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usaron 4-((6-cloro-2-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (isoxazol-4-il)borónico en lugar de 4-((6-cloro-4-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (3-fluorofenil)borónico.
1H NMR (CDs OD, 500MHz) 53,90 (3H), 6,48 (1H), 6,75 (1H), 6,89 (1H), 7,12 (1H), 7,40 (1H), 7,64 (1H), 7,79 (1H), 7,96 (1H), 8,13 (1H), 8,84 (1H), 9,08 (1H)
Ejemplo 122: Preparación de 3-ciano-4-((6-(3-fluorofenil)-2-(1-metil-1H-pirazol-4-il)piridin-3-il)oxi)-N-( tiazol-2-il)bencenosulfonamida
10 mg (0,02 mmol) de 4-((6-cloro-2-(1-metil-1H-pirazol-4-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida se disolvieron en 3 mL de N,N-dimetilformamida y 4,4 mg (0,03 mmol) de ácido (3-fluorofenil)borónico se añadió a esto y luego 2,4 mg (10 % en mol) de Pd(PPh3)4, 6,7 mg (0,63 mmol) de Na2CO3 y 1 mL de H2O se añadieron a esto. Después de reaccionar en el reactor de microondas a 120 °C durante 10 minutos, el solvente se eliminó y el material restante se diluyó con acetato de etilo y la capa orgánica se separó y se lavó con cloruro de sodio saturado. La capa orgánica se recogió, se secó con sulfato de magnesio para eliminar el agua y se concentró a presión reducida y el
residuo se purificó por cromatografía de columna (solvente de desarrollo, hexano:acetato de etilo = 3:1) para obtener 5 mg (45 % de rendimiento) del compuesto del título.
1H NMR (CD3OD, 500MHz) 58,30 (s, 1H), 8,27 (s, 1H), 8,10 (s, 1H), 8,02 (d, 1H), 7,96 (m, 1H), 7,84 (d, 1H), 7,66 (d, 1H), 7,52 (m, 1H), 7,18 (m, 1H), 7,12 (d, 1H), 6,99 (d, 1H), 6,76 (d, 1H), 3,92 (s, 3H)
Ejemplo 123: Preparación de 3-ciano-4-((2,-fluoro-6-(1-metil-1H-pirazol-4-il)-[2,3,-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
5 mg (45 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 122, excepto que se usó ácido (2-fluorofenil-4-il)borónico en lugar de ácido (3-fluorofenil)borónico.
1H NMR (CD3OD/CDCl3, 500MHz) 58,79 (m, 1H), 8,33 (s, 1H), 8,30 (m, 2H), 8,15 (s, 1H), 8,08 (d, 1H), 7,88 (d, 1H), 7,72 (d, 1H), 7,55 (m, 1H), 7,15 (d, 1H), 7,08 (d, 1H), 4,65 (s, 2H), 3,92 (s, 3H)
Ejemplo 124: Preparación de 3-ciano-4-((6'-fluoro-6-(1-metil-1H-pirazol-4-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
5 mg (45 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 122, excepto que se usó ácido (6-fluoropiridin-3-il)borónico en lugar de ácido (3-fluorofenil)borónico.
1H NMR (CDsOD/CDCls, 500MHz) 58,99 (s, 1H), 8,76 (m, 1H), 8,30 (m, 2H), 8,14 (s, 1H), 8,07 (d, 1H), 7,89 (d, 1H), 7,68 (m, 5H), 7,59 (m, 3H), 7,25 (m, 1H), 7,16 (d, 1H), 7,05 (d, 1H), 6,78 (d, 1H), 3,94 (s, 3H)
Ejemplo 125: Preparación de 3-ciano-4-((2'-fluoro-6-(1-metil-1H-pirazol-4-il)-[2,4'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
5 mg (45 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 122, excepto que se usó ácido (2-fluoropiridin-4-il)borónico en lugar de ácido (3-fluorofenil)borónico.
1H NMR (CDs OD/CDCls , 500MHz) 58,36 (m, 1H), 8,18 (s, 1H), 8,10 (m, 2H), 8,00 (d, 1H), 7,88 (s, 1H), 7,72 (d, 1H), 7,62 (m, 2H), 7,15 (m, 1H), 7,10 (m, 1H), 6,78 (d, 1H), 3,96 (s, 3H)
Ejemplo 126: Preparación de 3-ciano-4-((2',6'-difluoro-6-(1-metil-1H-pirazol-4-il)-[2,3,-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
5 mg (45 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 122, excepto que se usó ácido (2,6-difluoropiridin-3-il)borónico en lugar de ácido (3-fluorofenil)borónico.
1H NMR (CD3OD/CDCl3, 500MHz) 58,86 (m, 1H), 8,31 (s, 1H), 8,11 (s, 1H), 8,05 (m, 1H), 7,82 (m, 1H), 7,69 (m, 1H), 7,62 (m, 2H), 7,19 (m, 1H), 7,13 (m, 1H), 7,06 (d, 1H), 6,76 (d, 1H), 3,92 (s, 3H)
Ejemplo 127: Preparación de 3-ciano-4-((2,,6,-difluoro-6-(furan-3-il)-[2,3,-bipiridin]-5-il)oxi)-N-(tiazol-2-il) bencenosulfonamida
17,4 mg (29,7 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usaron 4-((6-cloro-2-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (2,6-difluoropiridin-3-il)borónico en lugar de 4-((6-cloro-4-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (3-fluorofenil)borónico.
1H NMR (CDsOD, 500MHz) 56,75 (1H), 6,76 (1H), 7,13 (1H), 7,18 (2H), 7,58 (1H), 7,71 (1H), 7,86 (1H), 7,05 (1H), 8,18 (1H), 8,30 (1H), 8,87 (1H)
Ejemplo 128: Preparación de 3-ciano-4-((2',6,-difluoro-6-(1-metil-1H-pirazol-5-il)-[2,3,-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida
12,0 mg (34,3 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usaron 4-((6-cloro-2-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (2,6-difluoropiridin-3-il)borónico en lugar de 4-((6-cloro-4-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (3-fluorofenil)borónico.
1H NMR (CDs OD, 500MHz) 54,09 (3H), 6,70 (1H), 6,76 (1H), 7,04 (1H), 7,13 (1H), 7,18 (1H), 7,44 (1H), 7,89 (1H), 8,01 (2H), 8,21 (1H), 8,75 (1H)
Ejemplo 129: Preparación de 5-cloro-4-((2',6,-difluoro-6-(furan-3-il)-[2,3,-bipiridin]-5-il)oxi)-2-fluoro-N-(tiazol-4-il)bencenosulfonamida
4,4 mg (22,8 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usaron terc-butil ((5-cloro-4-((6-cloro-2-(furan-3-il)piridin-3-il)oxi)-2
fluorofenil)sulfonil)(tiazol-4-il)carbamato y ácido (2,6-difluoropiridin-3-il)borónico en lugar de 4-((6-cloro-4-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (3-fluorofenil)borónico.
1H NMR (CD3OD, 500MHz) 56,92 (1H), 7,08 (1H), 7,17 (2H), 7,57 (2H), 7,82 (1H), 8,05 (1H), 8,18 (1H), 8,74 (1H), 8,86 (1H)
Ejemplo 130: Preparación de 5-cloro-2-fluoro-4-((6,-fluoro-6-(furan-3-il)-[2,3,-bipiridin]-5-il)oxi)-N-(tiazol-4-il)bencenosulfonamida
4,5 mg (24,2 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usaron terc-butil ((5-cloro-4-((6-cloro-2-(furan-3-il)piridin-3-il)oxi)-2-fluorofenil)sulfonil)(tiazol-4-il)carbamato y ácido (6-fluoropiridin-3-il)borónico en lugar de 4-((6-cloro-4-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (3-fluorofenil)borónico.
1H NMR (CD3OD, 500MHz) 56,88 (1H), 7,78 (1H), 7,21 (2H), 7,58 (2H), 7,86 (1H), 7,05 (1H), 8,17 (1H), 8,71 (2H), 8,94 (1H)
Ejemplo 131: Preparación de 5-cloro-2-fluoro-4-((6-(4-fluorofenil)-2-(furan-3-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida
5,7 mg (30,6 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usaron terc-butil ((5-cloro-4-((6-cloro-2-(furan-3-il)piridin-3-il)oxi)-2-fluorofenil)sulfonil)(tiazol-4-il)carbamato y ácido (4-fluorofenil)borónico en lugar de 4-((6-cloro-4-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (3-fluorofenil)borónico.
1H NMR (CD3OD, 500MHz) 56,79 (1H), 7,06 (1H), 7,21 (3H), 7,55 (2H), 7,80 (1H), 8,03 (1H), 8,14 (3H), 8,75 (1H)
Ejemplo 132: Preparación de 5-cloro-2-fluoro-4-((2'-fluoro-6-(furan-3-il)-[2,4'-bipiridin]-5-il)oxi)-N-(tiazol-4-il)bencenosulfonamida
4,1 mg (22,0 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usaron terc-butil ((5-cloro-4-((6-cloro-2-(furan-3-il)piridin-3-il)oxi)-2-fluorofenil)sulfonil)(tiazol-4-il)carbamato y ácido (2-fluoropiridin-4-il)borónico en lugar de 4-((6-cloro-4-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (3-fluorofenil)borónico.
1H NMR (CD3OD, 500MHz) 56,99 (1H), 7,09 (1H), 7,25 (1H), 7,55 (1H), 7,61 (1H), 7,83 (1H), 7,98 (1H), 8,07 (2H), 8,23 (1H), 8,32 (1H), 8,74 (1H)
Ejemplo 133: Preparación de 5-cloro-2-fluoro-4-((6-(2-fluorofenil)-2-(furan-3-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida
4,0 mg (21,5 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usaron terc-butil ((5-cloro-4-((6-cloro-2-(furan-3-il)piridin-3-il)oxi)-2-fluorofenil)sulfonil)(tiazol-4-il)carbamato y ácido (2-fluorofenil)borónico en lugar de 4-((6-cloro-4-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (3-fluorofenil)borónico.
1H NMR (CD3OD, 500MHz) 56,86 (1H), 7,06 (1H), 7,16 (1H), 7,24 (1H), 7,34 (1H), 7,46 (1H), 7,55 (2H), 7,79 (1H), 8,04 (1H), 8,12 (2H), 8,74 (1H)
Ejemplo 134: Preparación de 5-cloro-4-((2,,6,-difluoro-6-(1-metil-1H-pirazol-5-il)-[2,3,-bipiridin]-5-il)oxi)-2-fluoro-N-(tiazol-4-il)bencenosulfonamida
6,0 mg (41,4 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usaron terc-butil ((5-cloro-4-((6-cloro-2-(1 -metil-1 H-pirazol-5-il)piridin-3-il)oxi)-2-fluorofenil)sulfonil)(tiazol-4-il)carbamato y ácido (2,6-difluoropiridin-3-il)borónico en lugar de 4-((6-cloro-4-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (3-fluorofenil)borónico.
1H NMR (CD3OD, 500MHz) 54,11 (3H), 6,72 (1H), 6,94 (1H), 7,05 (1H), 7,17 (1H), 7,45 (1H), 7,74 (1H), 7,98 (2H), 8,74 (2H)
Ejemplo 135: Preparación de 5-cloro-2-fluoro-4-((6-(4-fluorofenil)-2-(1-metil-1H-pirazol-5-il)piridin-3-il )oxi)-N-(tiazol-4-il)bencenosulfonamida
6,0 mg (42,8 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usaron terc-butil ((5-cloro-4-((6-cloro-2-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-2-fluorofenil )sulfonil)(tiazol-4-il)carbamato y ácido (4-fluorofenil)borónico en lugar de 4-((6-cloro-4-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (3-fluorofenil)borónico.
1H NMR (CD3OD, 500MHz) 54,14 (3H), 6,78 (1H), 6,82 (1H), 7,03 (1H), 7,23 (2H), 7,43 (1H), 7,69 (1H), 7,96 (2H), 8,14 (2H), 8,73 (1H)
Ejemplo 136: Preparación de 5-cloro-2-fluoro-4-((6-(2-fluorofenil)-2-(1-metil-1H-pirazol-5-il)piridin-3-il )oxi)-N-(tiazol-4-il)bencenosulfonamida
6,0 mg (42,8 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usaron terc-butil ((5-cloro-4-((6-cloro-2-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-2-fluorofenil
)sulfonil)(tiazol-4-il)carbamato y ácido (2-fluorofenil)borónico en lugar de 4-((6-cloro-4-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (3-fluorofenil)borónico.
1H NMR (CD3OD, 500MHz) 54,16 (3H), 6,77 (1H), 6,95 (1H), 7,28 (1H), 7,35 (1H), 7,48 (2H), 7,72 (1H), 7,84 (1H), 8,03 (2H), 8,19 (1H), 8,96 (1H)
Ejemplo 137: Preparación de 5-cloro-2-fluoro-4-((6,-fluoro-6-(1-metil-1H-pirazol-5-il)-[2,3,-bipiridin]-5-il) oxi)-N-(tiazol-4-il)bencenosulfonamida
6,0 mg (42,8 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 5, excepto que se usaron terc-butil ((5-cloro-4-((6-cloro-2-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-2-fluorofenil )sulfonil)(tiazol-4-il)carbamato y ácido (6-fluoropiridin-3-il)borónico en lugar de 4-((6-cloro-4-(furan-3-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida y ácido (3-fluorofenil)borónico.
1H NMR (CD3OD, 500MHz) 54,14 (3H), 6,72 (1H), 6,90 (1H), 7,03 (1H), 7,22 (1H), 7,45 (1H), 7,96 (1H), 8,06 (1H), 8,66 (1H), 8,73 (1H), 8,95 (1H)
Los siguientes Ejemplos 138-157 son ejemplos de referencia.
Ejemplo 138: Preparación de 4-((4-cloro-2-(1-metil-1H-pirazol-5-il)fenil)(hidroxi)metil)-N-(tiazol-2-il)bencenosulfonamida
192 mg (0,46 mmol) de terc-butil (4-bromofenil)sulfonil(tiazol-2-il)carbamato se disolvió en 1,5 mL de tetrahidrofurano bajo gas nitrógeno y se enfrió a -78 °C. Después de añadir 0,4 mL (0,64 mmol) de n-butillitio (1 ,6M en tetrahidrofurano) lentamente, la mezcla se agitó durante 30 minutos mientras se mantenía a -78 °C. 50,0 mg (0,23 mmol) de 4-cloro-2-(1-metil-1H-pirazol-5-il)benzaldehído se disolvió en 0,5 mL de tetrahidrofurano y se añadió a la solución de reacción anterior. A medida que se calienta de -78 °C a temperatura ambiente, la solución de reacción se agitó durante 24 horas. A la solución de reacción se añadieron acetato de etilo y agua/1N-clorhidrato y esta se agitó. Después de separar las capas, solo se recogió la capa orgánica y se concentró a presión reducida. El residuo obtenido se separó mediante cromatografía de columna (solvente de desarrollo, hexano:acetato de etilo = 1:2) para obtener 10,0 mg (9,6 % de rendimiento) del compuesto del título.
1H NMR (CD3OD, 500MHz) 57,80 (1H), 7,73 (2H), 7,55 (1H), 7,50 (1H), 7,23 (1H), 7,07 (3H), 6,70 (1H), 6,26 (1H), 5,72 (1H)
Ejemplo 139: Preparación de 4-((4-cloro-2-(1H-pirazol-4-il)fenil)(hidroxi)metil)-3-fluoro-N-(tiazol-2-il )bencenosulfonamida
5,77 mg (5,4 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 138, excepto que se usaron terc-butil (4-bromo-3-fluorofenil)sulfonil(tiazol-2-il)carbamato,
terc-butil-4-(5-cloro-2-formilfenil)-1H-pirazol-1-carboxilato en lugar de terc-butil (4-bromofenil)sulfonil(tiazol-2-il)carbamato y 4-cloro-2-(1-metil-1H-pirazol-5-il)benzaldehído.
1H NMR (CD3OD, 500MHz) 57,67 (1H), 7,53 (3H), 7,34 (3H), 7,25 (1H), 7,02 (1H), 6,95 (1H), 6,60 (1H)
Ejemplo 140: Preparación de 4-((4-cloro-2-(furan-3-il)fenil)(hidroxi)metil)-3-fluoro-N-(tiazol-2-il)bencenosulfonamida
5,45 mg (5,1 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 139, excepto que se usó 4-cloro-2-(furan-3-il)benzaldehído en lugar de terc-butil-4-(5-cloro-2-formilfenil)-1H-pirazol-1-carboxilato.
1H NMR (CD3OD, 500MHz) 57,70 (1H), 7,61 (2H), 7,53 (1H), 7,45 (1H), 7,31 (1H), 7,26 (2H), 7,07 (1H), 6,67 (1H), 6,52 (1H), 6,15 (1H)
Ejemplo 141: Preparación de 4-((2,4-di(furan-3-il)fenil)(hidroxi)metil)-3-fluoro-N-(tiazol-2-il)bencenosulfonamida
5,46 mg (5,0 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 139, excepto que se usó 2,4-di(furan-3-il)benzaldehído en lugar de terc-butil-4-(5-cloro-2-formilfenil)-1H-pirazol-1-carboxilato.
1H NMR (CD3OD, 500MHz) 57,90 (1H), 7,45 (9H), 7,28 (1H), 7,07 (1H), 6,79 (1H), 6,66 (1H), 6,55 (1H), 6,19 (1H)
Ejemplo 142: Preparación de 3-fluoro-4-(hidroxi(2-(1-metil-1H-pirazol-5-il)fenil)metil)-N-(tiazol-2-il) bencenosulfonamida
4,40 mg (4,3 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 139, excepto que se usó 2-(1-metil-1H-pirazol-5-il)benzaldehído en lugar de terc-butil-4-(5-cloro-2-formilfenil)-1H-pirazol-1-carboxilato.
1H NMR (CD3OD, 500MHz) 57,58 (1H), 7,48 (1H), 7,42 (6H), 7,21 (1H), 7,06 (1H), 6,67 (1H), 6,18 (1H), 5,97 (1H), 3,34 (3H)
Ejemplo 143: Preparación de 4-((4-cloro-2-(furan-3-il)fenil)(hidroxi)metil)-N-(tiazol-2-il)bencenosulfonamida
192 mg (0,46 mmol) de terc-butil (4-bromofenil)sulfonil(tiazol-2-il)carbamato se disolvió en 2 mL de tetrahidrofurano bajo gas nitrógeno y se enfrió a -78 °C. Después de añadir 0,4 mL (0,64 mmol) de n-butillitio (1,6 M en tetrahidrofurano)
lentamente, la mezcla se agitó durante 30 minutos mientras se mantenía a -78 °C. 47,5 mg (0,23 mmol) de 4-cloro-2-(furan-3-il)benzaldehído se disolvió en 0,5 mL de tetrahidrofurano y se añadió a la solución de reacción anterior. A medida que se calienta de -78 °C a temperatura ambiente, la solución de reacción se agitó durante 24 horas. A la solución de reacción se añadieron acetato de etilo y agua/1N-clorhidrato y esta se agitó. Después de separar las capas, solo se recogió la capa orgánica y se concentró a presión reducida. El residuo obtenido se separó mediante cromatografía de columna (solvente de desarrollo, hexano:acetato de etilo = 1:1) para obtener 9,9 mg (9,6 % de rendimiento) del compuesto del título.
1H NMR (CD3OD, 500MHz) 57,78 (m, 2H), 7,56 (s, 2H), 7,35 (m, 1H), 7,31 (m, 4H), 7,06 (m, 1H), 6,67 (m, 1H), 6,53 (s, 1H), 6,00 (s, 1H)
Ejemplo 144: Preparación de 4-((4-cloro-2-(1-metil-1H-pirazol-5-il)fenil)(hidroxi)metil)-3-fluoro-N-(tiazol-2-il)bencenosulfonamida
10,0 mg (9,6 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 139, excepto que se usó 4-cloro-2-(1-metil-1H-pirazol-5-il)benzaldehído en lugar de terc-butil-4-(5-cloro-2-formilfenil)-1H-pirazol-1-carboxilato.
1H NMR (CD3OD, 500MHz) 57,58 (1H), 7,48 (1H), 7,42 (5H), 7,21 (1H), 7,06 (1H), 6,67 (1H), 6,18 (1H), 5,97 (1H), 3,34 (3H)
Ejemplo 145: Preparación de 4-((4-cloro-2-(piridin-3-il)fenil)(hidroxi)metil)-3-fluoro-N-(tiazol-2-il)bencenosulfonamida
10,0 mg (9,6 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 139, excepto que se usó 4-cloro-2-(piridin-3-il)benzaldehído en lugar de terc-butil-4-(5-cloro-2-formilfenil)-1H-pirazol-1-carboxilato.
1H NMR (CDCls, 500MHz) 58,73 (1H), 8,26 (1H), 7,87 (1H), 7,66 (4H), 7,43 (2H), 7,10 (3H), 6,88 (1H), 6,55 (1H)
Ejemplo 146: Preparación de 4-((4-cloro-2-(piridin-4-il)fenil)(hidroxi)metil)-3-fluoro-N-(tiazol-2-il)bencenosulfonamida
10,0 mg (9,6 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 139, excepto que se usó 4-cloro-2-(piridin-2-il)benzaldehído en lugar de terc-butil-4-(5-cloro-2-formilfenil)-1H-pirazol-1-carboxilato.
1H NMR (CDCls , 500MHz) 58,42 (1H), 7,88 (1H), 7,84 (1H), 7,34 (4H), 7,16 (1H), 6,95 (1H), 6,85 (1H), 6,52 (1H)
Ejemplo 147: Preparación de 4-((4-cloro-2-(piridin-4-il)fenil)(hidroxi)metil)-N-(tiazol-2-il)bencenosulfonamida
10,0 mg (9,6 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 138, excepto que se usó -cloro-2-(piridin-2-il)benzaldehído en lugar de 4-cloro-2-(1-metil-1 H-pirazol-5-il)benzaldehído.
1H NMR (CDCl3, 500MHz) 58,50 (1H), 7,72 (2H), 7,54 (1H), 7,47 (1H), 7,31 (2H), 7,24 (1H), 7,18 (2H), 7,09 (1H), 6,71 (1H)
Ejemplo 148: Preparación de 4-((4-cloro-2-(piridin-3-il)fenil)(hidroxi)metil)-N-(tiazol-2-il)bencenosulfonamida
8,6 mg (4,1 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 138, excepto que se usó 4-cloro-2-(piridin-3-il)benzaldehído en lugar de 4-cloro-2-(1-metil-1H-pirazol-5-il)benzaldehído.
1H NMR (CD3OD, 500MHz) 58,52 (dd, 1H), 8,44 (s, 1H), 7,73 (d, 2H), 7,66 (d, 1H), 7,56 (d, 1H), 7,47 (dd, 1H), 7,39 (m, 1H), 7,26 (d, 1H), 7,16 (d, 2H), 7,09 (d, 1H), 6,71 (d, 1H), 5,76 (s, 1H)
Ejemplo 149: Preparación de 4-((2,4-di(furan-3-il)fenil)(hidroxi)metil)-N-(tiazol-2-il)bencenosulfonamida
5,2 mg (2,4 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 138, excepto que se usó 2,4-di(furan-3-il)benzaldehído en lugar de 4-cloro-2-(1-metil-1 H-pirazol-5-il)benzaldehído.
1H NMR (CD3OD, 500MHz) 57,92 (s, 1H), 7,80 (d, 2H), 7,59-7,50 (m, 5H), 7,36 (d, 3H), 7,08 (d, 1H), 6,81 (s, 1H), 6,70 (d, 1H), 6,59 (s, 1H), 6,05 (s, 1H)
Ejemplo 150: Preparación de 4-((4-(2-fluoropiridin-3-il)-2-(furan-3-il)fenil)(hidroxi)metil)-N-(tiazol-2-il )bencenosulfonamida
6,9 mg (2,9 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 138, excepto que se usó 4-(2-fluoropiridin-3-il)-2-(furan-3-il)benzaldehído en lugar de 4-cloro-2-(1-metil-1H-pirazol-5-il)benzaldehído.
1H NMR (CD3OD, 500MHz) 58,18 (d, 1H), 8,08 (t, 1H), 7,81 (d, 2H), 7,60-7,51 (m, 5H), 7,42-7,37 (m, 3H), 7,08 (d, 1H), 6,70 (d, 1H), 6,60 (s, 1H), 6,11 (s, 1H)
Ejemplo 151: Preparación de 4-((4-(6-fluoropiridin-3-il)-2-(furan-3-il)fenil)(hidroxi)metil)-N-(tiazol-2-il )bencenosulfonamida
5,8 mg (2,5 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 138, excepto que se usó 4-(6-fluoropiridin-3-il)-2-(furan-3-il)benzaldehído en lugar de 4-cloro-2-(1-metil-1H-pirazol-5-il)benzaldehído.
1H NMR (CD3OD, 500MHz) 58,61 (d, 1H), 8,08 (t, 1H), 7,81 (d, 2H), 7,60-7,51 (m, 5H), 7,42-7,37 (m, 3H), 7,08 (d, 1H), 6,70 (d, 1H), 6,60 (s, 1H), 6,11 (s, 1H)
Ejemplo 152: Preparación de 4-((2'-fluoro-3-(furan-3-il)-[1,1'-bifenil]-4-il)(hidroxi)metil)-N-(tiazol-2-il) bencenosulfonamida
5,2 mg (2,2 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 138, excepto que se usó 2'-fluoro-3-(furan-3-il)-[1,1'-bifenil]-4-carbaldehído en lugar de 4-cloro-2-(1-metil-1H-pirazol-5-il)benzaldehído.
1H NMR (CD3OD, 500MHz) 57,81 (d, 2H), 7,57 (d, 2H), 7,47-7,44 (m, 4H), 7,39-7,34 (m, 3H), 7,24-7,14 (m, 2H), 7,07 (d, 1H), 6,68 (d, 1H), 6,58 (s, 1H), 6,10 (s, 1H)
Ejemplo 153: Preparación de 4-((3'-fluoro-3-(furan-3-il)-[1,1'-bifenil]-4-il)(hidroxi)metil)-N-(tiazol-2-il) bencenosulfonamida
4,0 mg (1,7 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 138, excepto que se usó 3'-fluoro-3-(furan-3-il)-[1,1'-bifenil]-4-carbaldehído en lugar de 4-cloro-2-(1-metil-1H-pirazol-5-il)benzaldehído.
1H NMR (CD3OD, 500MHz) 57,81 (d, 2H), 7,61-7,55 (m, 4H), 7,48-7,43 (m, 3H), 7,37 (d, 3H), 7,08 (d, 2H), 6,70 (d, 1H), 6,61 (s, 1H), 6,10 (s, 1H)
Ejemplo 154: Preparación de 4-((4'-fluoro-3-(furan-3-il)-[1,1'-bifenil]-4-il)(hidroxi)metil)-N-(tiazol-2-il) bencenosulfonamida
4,6 mg (2,0 % de rendimiento) del compuesto del título se obtuvieron de la misma manera que se describió en el Ejemplo 138, excepto que se usó 4'-fluoro-3-(furan-3-il)-[1,1'-bifenil]-4-carbaldehído en lugar de 4-cloro-2-(1-metil-1H-pirazol-5-il)benzaldehído.
1H NMR (CD3OD, 500MHz) ó 7,81 (d, 2H), 7,58-7,53 (m, 6H), 7,45 (d, 1H), 7,38 (d, 2H), 7,16 (t, 2H), 7,09 (d, 1H), 6,71 (d, 1H), 6,61 (d, 1H), 6,09 (s, 1H)
Ejemplo 155: Preparación de 3-fluoro-4-((2-(furan-3-il)piridin-3-il)(hidroxi)metil)-N-(tiazol-2-il)bencenosulfonamida
100 mg (0,26 mmol) de terc-butil ((3,4-difluorofenil)sulfonil)(tiazol-2-il)carbamato se disolvió en 5 mL de tetrahidrofurano bajo gas nitrógeno y se enfrió a -78 °C. Después de añadir 0,25 mL (0,39 mmol) de n-butillitio (1,6 M en tetrahidrofurano) lentamente, la mezcla se agitó durante 30 minutos mientras se mantenía a -78 °C. 23 mg (0,13 mmol) de 2-(furan-3-il)nicotinaldehído se disolvió en 0,5 mL de tetrahidrofurano y se se añadió a la solución de reacción anterior. A medida que se calienta de -78 °C a temperatura ambiente, la solución de reacción se agitó durante 24 horas. A la solución de reacción se añadieron acetato de etilo y agua/1N-clorhidrato y esta se agitó. Después de separar las capas, solo se recogió la capa orgánica y se concentró a presión reducida. El residuo obtenido se separó mediante cromatografía de columna (solvente de desarrollo, hexano:acetato de etilo = 1:1) para obtener 7 mg (6,1 % de rendimiento) del compuesto del título.
1H NMR (CD3OD, 500MHz) ó 8,48 (m, 1H), 7,84 (s, 1H), 7,72 (m, 3H), 7,59 (m, 1H), 7,47 (m, 1H), 7,32 (m, 1H), 7,70 (m, 1H), 6,73 (m, 2H), 6,24 (s, 1H)
Ejemplo 156: Preparación de 4-((2-(furan-3-il)piridin-3-il)(hidroxi)metil)-N-(tiazol-2-il)bencenosulfonamida
100 mg (0,28 mmol) de terc-butil ((4-fluorofenil)sulfonil)(tiazol-2-il)carbamato se disolvió en 5 mL de tetrahidrofurano bajo gas nitrógeno y se enfrió a -78 °C. Después de añadir 0,26 mL (0,42 mmol) de n-butillitio (1,6 M en tetrahidrofurano) lentamente, la mezcla se agitó durante 30 minutos mientras se mantenía a -78 °C. 23 mg (0,13 mmol) de 2-(furan-3-il)nicotinaldehído se disolvieron en 0,5 mL de tetrahidrofurano y se añadió a la solución de reacción anterior. A medida que se calienta de -78 °C a temperatura ambiente, la solución de reacción se agitó durante 24 horas. A la solución de reacción se añadieron acetato de etilo y agua/ 1N-clorhidrato y esta se agitó. Después de separar las capas, solo se recogió la capa orgánica y se concentró a presión reducida. El residuo obtenido se separó mediante cromatografía de columna (solvente de desarrollo, hexano:acetato de etilo = 1:1) para obtener 6 mg (5,2 % de rendimiento) del compuesto del título.
1H NMR (CD3OD, 500MHz) ó 8,48 (m, 1H), 7,81 (m, 4H), 7,59 (m, 1H), 7,36 (m, 3H), 7,09 (m, 1H), 6,73 (m, 2H), 6,09 (s, 1H)
Ejemplo 157: Preparación de 3-fluoro-4-(hidroxi(2-fenilpiridin-3-il)metil)-N-(tiazol-2-il)bencenosulfonamida
100 mg (0,26 mmol) de terc-butil ((3,4-difluorofenil)sulfonil)(tiazol-2-il)carbamato se disolvió en 5 mL de tetrahidrofurano bajo gas nitrógeno y se enfrió a -78 °C. Después de añadir 0,25 mL (0,39 mmol) de n-butillitio (1,6 M en tetrahidrofurano) lentamente, la mezcla se agitó durante 30 minutos mientras se mantenía a -78 °C. 24,3 mg (0,13 mmol) de 2-fenilnicotinaldehído se disolvieron en 0,5 mL de tetrahidrofurano y se añadió a la solución de reacción
anterior. A medida que se calienta de -78 °C a temperatura ambiente, la solución de reacción se agitó durante 24 horas. A la solución de reacción se añadieron acetato de etilo y agua/1N-clorhidrato y esta se agitó. Después de separar las capas, solo se recogió la capa orgánica y se concentró a presión reducida. El residuo obtenido se separó mediante cromatografía de columna (solvente de desarrollo, hexano:acetato de etilo = 1:1) para obtener 9 mg (7,6 % de rendimiento) del compuesto del título.
1H NMR (CD3OD, 500MHz) 58,49 (m, 1H), 7,95 (m, 1H), 7,64 (m, 1H), 7,52 (m, 1H), 7,42 (m, 1H), 7,37 (m, 6H), 7,12 (m, 1H), 6,74 (m, 1H), 6,09 (s, 1H)
Ejemplo Experimental: Experimento sobre el efecto de bloqueo contra el canal iónico de sodio (Nav1.7)
Para medir las actividades de los compuestos de la invención como antagonistas, se llevó a cabo un experimento sobre un efecto de bloqueo contra el canal iónico de sodio (Nav1.7) como sigue.
1) Cultivo celular
La línea celular HEK293 hNav1.7 usada fue una línea celular que tiene un gen del canal iónico de sodio humano 1.7 (subunidad alfa del canal de sodio dependiente de voltaje tipo IX) (subunidad alfa del canal de sodio dependiente de voltaje tipo IX) en 293 células de riñón embrionario humano (HEK) y se adquirió de Millipore. El medio usado se preparó por adición de 1 % de 100X NEAA y 10 % de FBS inactivadas por calor a DMEM F-12 y la adición de 1 % P/S como un antibiótico a esto. G-418 como una enzima de restricción se añadió durante el subcultivo y las células HEK293 hNav1.7 se cultivaron hasta una confluencia de aproximadamente 80 % en un matraz T75 en una incubadora de CO2 al 5 % a 37 °C durante 2 o 3 días y se separaron del matraz mediante tratamiento con una solución de tripsina al 0,25 %. Después, las células se recogieron por centrifugación y se usaron en el experimento.
2) Preparación de muestras de compuestos
Los compuestos preparados en los Ejemplos de la presente invención se disolvieron en dimetilsulfóxido (DMSO) y se usaron en el experimento. Se prepararon soluciones madre de DMSO 90 mM y 10 mM DMSO de cada uno de los compuestos y se diluyeron en una solución extracelular (4 mM de KCl, 138 mM de NaCl, 1 mM de MgCh, 1,8 mM de CaCl2 , 5,6 mM de glucosa, 10 mM de HEPES, pH 7,45) a diversas concentraciones, de modo que la concentración final de cada compuesto en DMSO fuera del 0,3 % o menos.
3) Medición de los efectos de bloqueo de los canales iónicos de sodio
Para medir el efecto de bloqueo del canal iónico de sodio, se usó un sistema de pinzamiento zonal IonFlux16 Auto (Fluxion, Inc.) y una placa de uso exclusivo. Las células se distribuyeron en una solución extracelular (4 mM de KCl, 138 mM de NaCl, 1 mM de MgCl2 , 1,8 mM de CaCl2, 5,6 mM de glucosa, 10 mM de HEPES, pH 7,45) y luego se dispensaron en las regiones especificadas de la placa y cada una de las muestras de compuestos preparadas se diluyó a varias concentraciones y luego se dispensó en la región especificada de la placa. Después de la dispensación de las células, las muestras del compuesto y una solución intracelular (100 mM de CsF, 45 mM de CsCl, 5 mM de NaCl, 5 mM de EGTA, 10 mM de HEPES, pH 7,2) en la placa se ha completado, la placa se montó en el sistema de pinzamiento zonal y se midió si los compuestos inhibían el canal iónico de acuerdo con un programa establecido y un protocolo de pulso.
Específicamente, se establecieron ocho concentraciones por compuesto y el porcentaje de inhibición se determinó calculando el porcentaje de inhibición de la corriente máxima, generada después de tratar las células con cada concentración del compuesto durante 50 segundos, en relación con la corriente máxima generada antes del tratamiento con el compuesto y el valor IC50 se calculó mediante el uso del programa Sigma plot. Los resultados del cálculo se muestran en las Tablas 2-4 a continuación. En las Tablas 2-4 a continuación, el porcentaje de inhibición de Nav1.7 se clasifica de la siguiente manera:
Nav1.7 IC50 : (>100 nM), + (51-100 nM) y ++ (<50 nM)
Tabla 2
[Tabla 2]
Tabla 3
[Tabla 3]
Tabla 4
[Tabla 4]
Claims (137)
- REIVINDICACIONESi. Un compuesto representado por la siguiente Fórmula 1 o una sal farmacéuticamente aceptable del mismo:en el queR1 es arilo o heteroarilo seleccionado del grupo que consiste en fenilo, piridinilo, pirimidinilo, furanilo, isoxazolilo, pirazolilo y tienilo,en el que el arilo o heteroarilo no está sustituido o está sustituido con uno o dos sustituyentes seleccionados independientemente del grupo que consiste en C1-4 alquilo, C1-4 haloalquilo y halógeno,R2 es arilo o heteroarilo seleccionado del grupo que consiste en furanilo, imidazolilo, isoxazolilo, pirazolilo, piridinilo, pirimidinilo, tiazolilo y tienilo,en el que el arilo o heteroarilo no está sustituido o está sustituido con uno o dos sustituyentes seleccionados independientemente del grupo que consiste en C1-4 alquilo, C3-6 cicloalquilo, halógeno, morfolino, piperazinilo, piperidinilo, piridinilo y pirrolidinilo,R3 es tiazolilo o tiadiazolilo,X 1 es CH y X2 es N, o X 1 es N y X2 es CH,Y es O,Z es CR4 ,R4 es H, halógeno o CN,R5 es H o halógeno.
- 2. El compuesto o sal farmacéuticamente aceptable del mismo de la reivindicación 1, en el que R1 es fenilo no sustitudo o sustituido con uno o dos sustituyentes seleccionados independientemente del grupo que consiste en C1-4 haloalquilo y halógeno; piridinilo no sustituido o sustituido con uno o dos halógenos; pirimidinilo no sustituido; furanilo no sustituido; isoxazolilo no sustituido; pirazolilo no sustituido o sustituido por C1-4 alquilo; o tienilo no sustituido.
- 3. El compuesto o sal farmacéuticamente aceptable del mismo de la reivindicación 2, en el que R1 es fenilo no sustitudo o sustituido con uno o dos sustituyentes seleccionados independientemente del grupo que consiste en CF3 , F y Cl; piridinilo no sustituido o sustituido por uno o dos F; pirimidinilo no sustituido; furanilo no sustituido; isoxazolilo no sustituido; pirazolilo no sustituido o sustituido por metilo; o tienilo no sustituido.
- 4. El compuesto o sal farmacéuticamente aceptable del mismo de la reivindicación 1, en el que R2 es furanilo no sustituido; imidazolilo sustituido por piridinilo; isoxazolilo sustituido por dos C1-4 alquilo; fenilo no sustituido; pirazolilo no sustituido o sustituido por C1-4 alquilo o C3-6 cicloalquilo; piridinilo no sustituido o sustituido por uno o dos sustituyentes seleccionados del grupo que consiste en C1-4 alquilo, halógeno, morfolino, piperidinilo y pirrolidinilo; pirimidinilo no sustituido o sustituido por piperazinilo; tiazolilo sustituido por C3-6 cicloalquilo; o tienilo sustituido por uno o dos C1-4 alquilo.
- 5. El compuesto o sal farmacéuticamente aceptable del mismo de la reivindicación 4, en el que R2 es furanilo no sustituido; imidazolilo sustituido por piridinilo; isoxazolilo sustituido por dos metilo; fenilo no sustituido; pirazolilo no sustituido o sustituido por metilo o ciclopropilo; piridinilo no sustituido o sustituido por uno o dos sustituyentes seleccionados del grupo que consiste en metilo, F, Cl, morfolino, piperidinilo y pirrolidinilo; pirimidinilo no sustituido o sustituido por piperazinilo; tiazolilo sustituido por ciclopropilo; o tienilo sustituido por uno o dos metilo.6. El compuesto o sal farmacéuticamente aceptable del mismo de la reivindicación 1, en el que R4 es H, F, Cl o CN.7. El compuesto o sal farmacéuticamente aceptable del mismo de la reivindicación 1, en el que R5 es H o F.8. Un compuesto o una sal farmacéuticamente aceptable del mismo, en el que el compuesto se selecciona del grupo que consiste en1) 3-ciano-4-((4-(furan-3-il)-6-fenilpiridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,2) 3-ciano-4-((4-(1-metil-1H-pi razol-5-il)-6-fenilpiridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida, 3) 3-ciano-4-((4-(furan-3-il)-6-fenilpiridin-3-il)oxi)-N-(1,2,4-tiadiazol-5-il)bencenosulfonamida,4) 3-ciano-4-((4-(1-metil-1H-pi razol-5-il)-6-fenilpiridin-3-il)oxi)-N-(1,2,4-tiadiazol-5-il)bencenosulfonamida, 5) 3-ciano-4-(6-(3-fluorofenil)-4-(furan-3-il)pi ridin-3-iloxi)-N-(tiazol-2-il)bencenosulfonamida,
- 6) 3-ciano-4-(6-(2-fluorofenil)-4-(furan-3-il)pi ridin-3-iloxi)-N-(tiazol-2-il)bencenosulfonamida,
- 7) 3-ciano-4-(6-(4-fluorofenil)-4-(furan-3-il)pi ridin-3-iloxi)-N-(tiazol-2-il)bencenosulfonamida,
- 8) 3-ciano-4-(4-(furan-3-il)-6-(3-(trifluorometil)fenil)piridin-3-iloxi)-N-(tiazol-2-il)bencenosulfonamida,
- 9) 3-ciano-4-(2'-fluoro-4-(furan-3-il)-2,4'-bipiridin-5-iloxi)-N-(tiazol-2-il)bencenosulfonamida,
- 10) 3-ciano-4-(2'-fluoro-4-(furan-3-il)-2,3'-bipiridin-5-iloxi)-N-(tiazol-2-il)bencenosulfonamida,
- 11) 3-ciano-4-(6'-fluoro-4-(furan-3-il)-2,3'-bipiridin-5-iloxi)-N-(tiazol-2-il)bencenosulfonamida,
- 12) 3-ciano-4-(2',6'-difluoro-4-(furan-3-il)-2,3'-bipiridin-5-iloxi)-N-(tiazol-2-il)bencenosulfonamida,
- 13) 3-ciano-4-(4-(furan-3-il)-2,3'-bipiridin-5-iloxi)-N-(tiazol-2-il)bencenosulfonamida,
- 14) 3-ciano-4-(4-(furan-3-il)-2,4'-bipiridin-5-iloxi)-N-(tiazol-2-il)bencenosulfonamida,
- 15) 3-ciano-4-(4-(furan-3-il)-6-(pirimidin-5-il)piridin-3-iloxi)-N-(tiazol-2-il)bencenosulfonamida,
- 16) 3-ciano-4-((4,6-di(furan-3-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 17) 4-((4,6-di(furan-3-il)piridin-3-il)oxi)-3-fluoro-N-(tiazol-2-il)bencenosulfonamida,
- 18) 3-ciano-4-((2'-fluoro-4-(1-metil-1H-pirazol-5-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 19) 3-ciano-4-((6'-fluoro-4-(1-metil-1H-pirazol-5-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 20) 3-ciano-4-((4-(furan-3-il)-6-(tiofen-3-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 21) 3-fluoro-4-((4-(1-metil-1H-pirazol-5-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 22) 3-fluoro-4-((4-(1-metil-1H-pirazol-5-il)-6-(tiofen-3-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 23) 3-ciano-4-((6-(4-fluorofenil)-4-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 24) 3-ciano-4-((6-(2-fluorofenil)-4-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 25) 3-ciano-4-((6-(furan-3-il)-4-(1-metil-1H-pirazol-5-il)pi ridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 26) 3-ciano-4-((6-(3-fluorofenil)-4-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 27) 3-ciano-4-((2'-fluoro-4-(1-metil-1H-pirazol-5-il)-[2,4'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 28) 4-((4,6-di(furan-3-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 29) 3-ciano-4-((2-fluoro-6'-fenil-[3,4'-bipiridin]-3'-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 30) 3-ciano-4-((6-fluoro-6'-fenil-[3,4‘bipiridin]-3'-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 31) 3-ciano-4-((2'-fluoro-6-fenil-[4,4'-bipiridin]-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 32) 3-ciano-4-((6-fluoro-5-metil-6'-fenil-[3,4'-bipiridin]-3'-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 33) 3-ciano-4-((6'-fenil-[3,4'-bipiridin]-3'-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 34) 3-ciano-4-((6-fenil-4-(pirimidin-5-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 35) 4-((3'-cloro-6-fenil-[4,4'-bipiridin]-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida,
- 36) 3-ciano-4-((2',3'-dicloro-6-fenil-[4,4'-bipiridin]-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 37) 3-ciano-4-((4-(3,5-dimetilisoxazol-4-il)-6-fenilpiridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 38) 3-ciano-4-((4-(1-metil-1H-pirazol-4-il)-6-fenilpiridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 39) 3-ciano-4-((6-fenil-4-(1H-pirazol-4-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 40) 3-ciano-4-((6-fenil-[4,4'-bipiridin]-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 41) 3-ciano-4-((4-(2,5-dimetiltiofen-3-il)-6-fenilpiridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 42) 3-ciano-4-((4-(5-metiltiofen-2-il)-6-fenilpiridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 43) 3-ciano-4-((4-(2-ciclopropiltiazol-4-il)-6-fenilpiridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 44) 3-ciano-4-((4-(1-ciclopropil-1h-pirazol-4-il)-6-fenilpiridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 45) 3-ciano-4-((4-(furan-3-il)-6-(1H-pirazol-4-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 46) 3-ciano-4-((4-(furan-3-il)-6-(1-metil-1H-pirazol-4-il)pi ridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 47) 3-fluoro-4-((2'-fluoro-4-(furan-3-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 48) 3-fluoro-4-((6'-fluoro-4-(furan-3-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 49) 3-ciano-4-((6-fluoro-[3,2':4',3"-terpiridin]-5'-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 50) 3-ciano-4-((6'-(3-fluorofenil)-[3,4'-bipiridin]-3'-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 51) 3-ciano-4-((2-fluoro-[3,2':4',3"-terpiridin]-5'-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 52) 3-ciano-4-((6'-(2-fluorofenil)-[3,4'-bipiridin]-3'-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 53) 3-ciano-4-((2,6-difluoro-[3,2':4',4"-terpiridin]-5'-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 54) 4-((4,6-bis(1-metil-1H-pi razol-4-il)piridin-3-il)oxi)-3-ciano-N-(tiazol-2-il)bencenosulfonamida,
- 55) 4-((4,6-bis(1-metil-1H-pi razol-4-il)piridin-3-il)oxi)-3-ciano-N-(1,2,4-tiadiazol-5-il)bencenosulfonamida,
- 56) 5-cloro-2-fluoro-4-((2'-fluoro-4-(furan-3-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 57) 5-cloro-2-fluoro-4-((6'-fluoro-4-(furan-3-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 58) 5-cloro-4-((2',6'-difluoro-4-(furan-3-il)-[2,3'-bipiridin]-5-il)oxi)-2-fluoro-N-(tiazol-4-il)bencenosulfonamida,
- 59) 5-cloro-2-fluoro-4-((6-(3-fluorofenil)-4-(furan-3-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 60) 5-cloro-2-fluoro-4-((6-(2-fluorofenil)-4-(furan-3-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 61) 5-cloro-2-fluoro-4-((6-(4-fluorofenil)-4-(furan-3-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 62) 5-cloro-2-fluoro-4-((2'-fluoro-4-(furan-3-il)-[2,4'-bipiridin]-5-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 63) 5-cloro-2-fluoro-4-((6-(2-fluorofenil)-4-(1-metil-1H-pirazol-4-il)pi ridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida 2,2,2-trifluoroacetato,
- 64) 5-cloro-2-fluoro-4-((6-(3-fluorofenil)-4-(1-metil-1H-pi razol-5-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 65) 5-cloro-2-fluoro-4-((6-(4-fluorofenil)-4-(1-metil-1H-pirazol-4-il)pi ridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida 2,2,2-trifluoroacetato,
- 66) 5-cloro-4-((6-(2,4-difluorofenil)-4-(1-metil-1H-pirazol-4-il)piridin-3-il)oxi)-2-fluoro-N-(tiazol-4-il)bencenosulfonamida 2,2,2-trifluoroacetato,
- 67) 5-cloro-4-((6-(3,4-difluorofenil)-4-(1-metil-1H-pirazol-4-il)piridin-3-il)oxi)-2-fluoro-N-(tiazol-4-il)bencenosulfonamida 2,2,2-trifluoroacetato,
- 68) 5-cloro-2-fluoro-4-((2'-fluoro-4-(1-metil-1H-pirazol-4-il)-[2,4'-bipiridin]-5-il)oxi)-N-(tiazol-4-il)bencenosulfonamida 2,2,2-trifluoroacetato,
- 69) 5-cloro-2-fluoro-4-((2'-fluoro-4-(1-metil-1H-pirazol-4-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-4-il)bencenosulfonamida 2,2,2-trifluoroacetato,
- 70) 5-cloro-2-fluoro-4-((6'-fluoro-4-(1-metil-1H-pirazol-4-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-4-il)bencenosulfonamida 2,2,2-trifluoroacetato,
- 71) 5-cloro-2-fluoro-4-((6-(3-fluorofenil)-4-(1-metil-1H-pirazol-5-il)pi ridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 72) 5-cloro-2-fluoro-4-((6-(3-fluorofenil)-4-(2-(piperazin-1-il)pirimidin-4-il)pi ridi n-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 73) 5-cloro-2-fluoro-4-((6'-(3-fluorofenil)-[3,4'-bipiridin]-3'-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 74) 5-cloro-2-fluoro-4-((6'-(3-fluorofenil)-[3,4'-bipiridin]-3'-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 75) 5-cloro-2-fluoro-4-((2"-fluoro-[3,4':2',4"-terpiridin]-5'-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 76) 5-cloro-2-fluoro-4-((6-(3-fluorofenil)-4-(pirimidin-5-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 77) 5-cloro-2-fluoro-4-((2'-fluoro-4-(pirimidin-5-il)-[2,4'-bipiridin]-5-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 78) 5-cloro-2-fluoro-4-((6-(3-fluorofenil)-4-(1H-pirazol-4-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 79) 5-cloro-2-fluoro-4-((2'-fluoro-6-(3-fluorofenil)-[4,4'-bipiridin]-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 80) 5-cloro-4-((6-(3,4-difluorofenil)-2'-fluoro-[4,4'-bipiridin]-3-il)oxi)-2-fluoro-N-(tiazol-4-il)bencenosulfonamida,
- 81) 5-cloro-4-((6'-(5-cloro-2-fluorofenil)-[3,4'-bipiridin]-3'-il)oxi)-2-fluoro-N-(tiazol-4-il)bencenosulfonamida,
- 82) 5-cloro-4-((6'-(3,4-difluorofenil)-[3,4'-bipiridin]-3'-il)oxi)-2-fluoro-N-(tiazol-4-il)bencenosulfonamida,
- 83) 3-ciano-4-((6-(3-fluorofenil)-4-(1H-pirazol-4-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 84) 3-ciano-4-((6'-(3-fluorofenil)-[3,4'-bipiridin]-3'-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 85) 3-ciano-4-((6'-(3,4-difluorofenil)-[3,4'-bipiridin]-3'-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 86) 3-ciano-4-((6'-(3-fluoro-4-(trifluorometil)fenil)-[3,4'-bipi ridin]-3'-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 87) 2,5-difluoro-4-((6'-(3-fluorofenil)-[3,4'-bipiridin]-3'-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 88) 4-((6'-(3,4-difluorofenil)-[3,4'-bipiridin]-3'-il)oxi)-2,5-difluoro-N-(tiazol-4-il)bencenosulfonamida,
- 89) 2,5-difluoro-4-((6'-(3-fluoro-4-(trifluorometil)fenil)-[3,4'-bipiridin]-3'-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 90) 3-ciano-4-((6-(4-fluorofenil)-4-(1H-pirazol-4-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 91) 3-ciano-4-((6-(3,4-difluorofenil)-4-(1H-pirazol-4-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 92) 3-ciano-4-((6-(3-fluorofenil)-4-(pirimidin-5-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 93) 3-ciano-4-((6-(3,4-difluorofenil)-4-(pirimidin-5-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 94) 3-ciano-4-((6-(3-fluoro-4-(trifluorometil)fenil)-4-(pirimidin-5-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 95) 2,5-difluoro-4-((6-(3-fluorofenil)-4-(pirimidin-5-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 96) 4-((6-(3,4-difluorofenil)-4-(pirimidin-5-il)piridin-3-il)oxi)-2,5-difluoro-N-(tiazol-4-il)bencenosulfonamida,
- 97) 2,5-difluoro-4-((6-(3-fluoro-4-(trifluorometil)fenil)-4-(pirimidin-5-il)pi ridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 98) 5-cloro-4-((6-(3,4-difluorofenil)-4-(1H-pirazol-4-il)piridin-3-il)oxi)-2-fluoro-N-(tiazol-4-il)bencenosulfonamida,
- 99) 5-cloro-2-fluoro-4-((6'-(3-fluorofenil)-5-(pirrolidin-1-il)-[3,4'-bipiridin]-3'-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 100) 5-cloro-2-fluoro-4-((6-(3-fluorofenil)-4-(1-(piridin-3-il)-1H-imidazol-4-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 101) 5-cloro-2-fluoro-4-((6-(3-fluorofenil)-2'-morfolino-[4,4'-bipiridin]-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 102) 5-cloro-2-fluoro-4-((6-(3-fluorofenil)-2'-(piperidin-1-il)-[4,4'-bipiridin]-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 103) 3-ciano-4-((2'-fluoro-6-(furan-3-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 104) 3-ciano-4-((6'-fluoro-6-(furan-3-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 105) 3-ciano-4-((6-(furan-3-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 106) 3-ciano-4-((2-(furan-3-il)-6-(pirimidin-5-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 107) 3-ciano-4-((2'-fluoro-6-(1-metil-1H-pirazol-5-il)-[2,4'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 108) 3-ciano-4-((6-(2-fluorofenil)-2-(furan-3-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 109) 3-ciano-4-((6-(4-fluorofenil)-2-(furan-3-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 110) 3-ciano-4-((6-(3-fluorofenil)-2-(furan-3-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 111) 3-ciano-4-((6-(furan-3-il)-[2,4'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 112) 3-ciano-4-((2'-fluoro-6-(furan-3-il)-[2,4'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 113) 3-ciano-4-((2-(furan-3-il)-6-(tiofen-3-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 114) 3-ciano-4-((2,6-di(furan-3-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 115) 3-ciano-4-((6'-fluoro-6-(1-metil-1H-pirazol-5-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 116) 3-ciano-4-((2'-fluoro-6-(1-metil-1H-pirazol-5-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 117) 3-ciano-4-((6-(3-fluorofenil)-2-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 118) 3-ciano-4-((6-(2-fluorofenil)-2-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 119) 3-ciano-4-((2-(1-metil-1H-pirazol-5-il)-6-(tiofen-3-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 120) 3-ciano-4-((6-(1-metil-1H-pirazol-4-il)-2-(1-metil-1H-pirazol-5-il)piridin-3-M)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 121) 3-ciano-4-((6-(isoxazol-4-il)-2-(1-metil-1H-pirazol-5-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 122) 3-ciano-4-((6-(3-fluorofenil)-2-(1-metil-1H-pirazol-4-il)piridin-3-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 123) 3-ciano-4-((2'-fluoro-6-(1-metil-1H-pirazol-4-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 124) 3-ciano-4-((6'-fluoro-6-(1-metil-1H-pirazol-4-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 125) 3-ciano-4-((2'-fluoro-6-(1-metil-1H-pirazol-4-il)-[2,4'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 126) 3-ciano-4-((2',6'-difluoro-6-(1-metil-1H-pirazol-4-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 127) 3-ciano-4-((2',6'-difluoro-6-(furan-3-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 128) 3-ciano-4-((2',6'-difluoro-6-(1-metil-1H-pi razol-5-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-2-il)bencenosulfonamida,
- 129) 5-cloro-4-((2',6'-difluoro-6-(furan-3-il)-[2,3'-bipiridin]-5-il)oxi)-2-fluoro-N-(tiazol-4-il)bencenosulfonamida,
- 130) 5-cloro-2-fluoro-4-((6'-fluoro-6-(furan-3-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 131) 5-cloro-2-fluoro-4-((6-(4-fluorofenil)-2-(furan-3-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 132) 5-cloro-2-fluoro-4-((2'-fluoro-6-(furan-3-il)-[2,4'-bipiridin]-5-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 133) 5-cloro-2-fluoro-4-((6-(2-fluorofenil)-2-(furan-3-il)piridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 134) 5-cloro-4-((2',6'-difluoro-6-(1-metil-1H-pirazol-5-il)-[2,3'-bipiridin]-5-il)oxi)-2-fluoro-N-(tiazol-4-il)bencenosulfonamida,
- 135) 5-cloro-2-fluoro-4-((6-(4-fluorofenil)-2-(1-metil-1H-pirazol-5-il)pi ridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida,
- 136) 5-cloro-2-fluoro-4-((6-(2-fluorofenil)-2-(1-metil-1H-pirazol-5-il)pi ridin-3-il)oxi)-N-(tiazol-4-il)bencenosulfonamida, and
- 137) 5-chloro-2-fluoro-4-((6'-fluoro-6-(1-metil-1H-pi razol-5-il)-[2,3'-bipiridin]-5-il)oxi)-N-(tiazol-4-il)bencenosulfonamida.Una composición farmacéutica para su uso en la prevención o el tratamiento de una enfermedad relacionada con los bloqueadores de los canales de sodio que comprende el compuesto o sal farmacéuticamente aceptable del mismo de cualquiera de las reivindicaciones 1 a 8 como ingrediente activo en el que la enfermedad relacionada con los bloqueadores de los canales de sodio se selecciona del grupo que consiste en dolor agudo, dolor crónico, dolor neuropático, dolor posoperatorio, migraña, artralgia, neuropatía, lesión nerviosa, neuropatía diabética, enfermedad neuropática, epilepsia, arritmia, miotonía, ataxia, esclerosis múltiple, síndrome del intestino irritable, incontinencia urinaria, dolor visceral, depresión, eritromelalgia y trastorno paroxístico de dolor extremo (PEPD).
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR20120114414 | 2012-10-15 | ||
| PCT/KR2013/009206 WO2014061970A1 (en) | 2012-10-15 | 2013-10-15 | Sodium channel blockers, preparation method thereof and use thereof |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2828503T3 true ES2828503T3 (es) | 2021-05-26 |
Family
ID=50488472
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES13846541T Active ES2828503T3 (es) | 2012-10-15 | 2013-10-15 | Bloqueadores de los canales de sodio, método de preparación de los mismos y uso de los mismos |
| ES18198388T Active ES2798138T3 (es) | 2012-10-15 | 2013-10-15 | Bloqueadores de los canales de sodio, método de preparación de los mismos y uso de los mismos |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES18198388T Active ES2798138T3 (es) | 2012-10-15 | 2013-10-15 | Bloqueadores de los canales de sodio, método de preparación de los mismos y uso de los mismos |
Country Status (14)
| Country | Link |
|---|---|
| US (1) | US9376429B2 (es) |
| EP (2) | EP3444249B1 (es) |
| JP (1) | JP6251275B2 (es) |
| KR (1) | KR102038607B1 (es) |
| CN (1) | CN104718205B (es) |
| AU (1) | AU2013332648B2 (es) |
| BR (1) | BR112015008508B1 (es) |
| CA (1) | CA2887845C (es) |
| ES (2) | ES2828503T3 (es) |
| IL (1) | IL238296B (es) |
| MX (1) | MX2015004765A (es) |
| MY (1) | MY177422A (es) |
| RU (1) | RU2645711C2 (es) |
| WO (1) | WO2014061970A1 (es) |
Families Citing this family (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB201417497D0 (en) * | 2014-10-03 | 2014-11-19 | Convergence Pharmaceuticals | Novel use |
| RU2705578C1 (ru) * | 2015-11-13 | 2019-11-08 | Даевунг Фармасьютикал Ко., Лтд. | Блокатор натриевых каналов |
| CA3008611A1 (en) | 2015-12-18 | 2017-06-22 | Merck Sharp & Dohme Corp. | Hydroxyalkylamine- and hydroxycycloalkylamine-substituted diamine-arylsulfonamide compounds with selective activity in voltage-gated sodium channels |
| CN108430969B (zh) * | 2016-02-03 | 2020-06-02 | 上海海雁医药科技有限公司 | 杂环取代的n-磺酰基苯甲酰胺衍生物、其制法与医药上的用途 |
| SG11201809702SA (en) | 2016-05-20 | 2018-12-28 | Xenon Pharmaceuticals Inc | Benzenesulfonamide compounds and their use as therapeutic agents |
| SG10201912372XA (en) * | 2016-12-09 | 2020-02-27 | Xenon Pharmaceuticals Inc | Benzenesulfonamide compounds and their use as therapeutic agents |
| PE20211389A1 (es) | 2018-06-13 | 2021-07-27 | Xenon Pharmaceuticals Inc | Compuestos de bencenosulfonamida y su uso como agentes terapeuticos |
| JP7383012B2 (ja) | 2018-08-31 | 2023-11-17 | ゼノン・ファーマシューティカルズ・インコーポレイテッド | ヘテロアリール置換スルホンアミド化合物、およびナトリウムチャネル阻害剤としてのその使用 |
| PE20211066A1 (es) | 2018-08-31 | 2021-06-09 | Xenon Pharmaceuticals Inc | Compuestos de sulfonamida sustituidos con heteroarilo y su uso como agentes terapeuticos |
| CN113527281B (zh) * | 2020-04-20 | 2023-12-22 | 昆山彭济凯丰生物科技有限公司 | 杂环化合物及其制备方法和应用 |
| CN111920796A (zh) * | 2020-08-28 | 2020-11-13 | 南京医科大学 | 化合物在制备治疗癫痫药物中的应用 |
| WO2023122494A1 (en) * | 2021-12-23 | 2023-06-29 | Veralox Therapeutics | Compositions and methods of use to treat 12-lipoxygenase (12-lox) mediated diseases |
Family Cites Families (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DK1088819T3 (da) | 1999-09-30 | 2005-09-12 | Pfizer Prod Inc | 6-azauracilderivater som thyroidreceptorligander |
| JP2007501804A (ja) | 2003-08-08 | 2007-02-01 | バーテックス ファーマシューティカルズ インコーポレイテッド | 電位開口型のナトリウムチャネルのインヒビターとして有用な組成物 |
| ES2299906T3 (es) | 2003-11-25 | 2008-06-01 | Eli Lilly And Company | Moduladores de receptores activados por proliferadores de peroxisomas. |
| WO2006119451A1 (en) | 2005-05-04 | 2006-11-09 | Vertex Pharmaceuticals Incorporated | Pyrimidines and pyrazines useful as modulators of ion channels |
| WO2006133459A1 (en) | 2005-06-09 | 2006-12-14 | Vertex Pharmaceuticals Incorporated | Indane derivatives as modulators of ion channels |
| DE602008000809D1 (de) | 2007-03-23 | 2010-04-29 | Icagen Inc | Ionenkanal-Hemmer |
| CA2693588C (en) | 2007-07-13 | 2015-11-17 | Icagen, Inc. | Sodium channel inhibitors |
| WO2009157399A1 (ja) * | 2008-06-23 | 2009-12-30 | アステラス製薬株式会社 | スルホンアミド化合物又はその塩 |
| DK2385938T3 (en) * | 2009-01-12 | 2015-04-27 | Pfizer Ltd | Sulfonamidderivater |
| EP2590972B1 (en) * | 2010-07-09 | 2015-01-21 | Pfizer Limited | N-sulfonylbenzamides as inhibitors of voltage-gated sodium channels |
| WO2012004714A2 (en) * | 2010-07-09 | 2012-01-12 | Pfizer Limited | Chemical compounds |
| ES2533065T3 (es) * | 2010-07-09 | 2015-04-07 | Pfizer Limited | Bencenosulfonamidas útiles como inhibidores de los canales de sodio |
-
2013
- 2013-10-15 ES ES13846541T patent/ES2828503T3/es active Active
- 2013-10-15 AU AU2013332648A patent/AU2013332648B2/en active Active
- 2013-10-15 KR KR1020130122783A patent/KR102038607B1/ko active IP Right Grant
- 2013-10-15 MX MX2015004765A patent/MX2015004765A/es active IP Right Grant
- 2013-10-15 MY MYPI2015000978A patent/MY177422A/en unknown
- 2013-10-15 EP EP18198388.3A patent/EP3444249B1/en active Active
- 2013-10-15 CN CN201380053790.3A patent/CN104718205B/zh active Active
- 2013-10-15 JP JP2015536720A patent/JP6251275B2/ja active Active
- 2013-10-15 RU RU2015113333A patent/RU2645711C2/ru active
- 2013-10-15 ES ES18198388T patent/ES2798138T3/es active Active
- 2013-10-15 CA CA2887845A patent/CA2887845C/en active Active
- 2013-10-15 WO PCT/KR2013/009206 patent/WO2014061970A1/en active Application Filing
- 2013-10-15 US US14/435,473 patent/US9376429B2/en active Active
- 2013-10-15 EP EP13846541.4A patent/EP2906558B1/en active Active
- 2013-10-15 BR BR112015008508-3A patent/BR112015008508B1/pt active IP Right Grant
-
2015
- 2015-04-14 IL IL238296A patent/IL238296B/en active IP Right Grant
Also Published As
| Publication number | Publication date |
|---|---|
| ES2798138T3 (es) | 2020-12-09 |
| JP6251275B2 (ja) | 2017-12-20 |
| IL238296A0 (en) | 2015-06-30 |
| MY177422A (en) | 2020-09-15 |
| CA2887845C (en) | 2020-12-15 |
| AU2013332648A1 (en) | 2015-04-30 |
| EP2906558A4 (en) | 2016-07-27 |
| IL238296B (en) | 2018-01-31 |
| BR112015008508A2 (pt) | 2020-01-07 |
| US20150336944A1 (en) | 2015-11-26 |
| WO2014061970A1 (en) | 2014-04-24 |
| EP3444249B1 (en) | 2020-05-13 |
| KR102038607B1 (ko) | 2019-10-30 |
| AU2013332648B2 (en) | 2017-09-07 |
| RU2645711C2 (ru) | 2018-02-28 |
| EP3444249A1 (en) | 2019-02-20 |
| BR112015008508B1 (pt) | 2022-06-07 |
| JP2015536917A (ja) | 2015-12-24 |
| CN104718205B (zh) | 2017-12-01 |
| MX2015004765A (es) | 2015-08-14 |
| US9376429B2 (en) | 2016-06-28 |
| CA2887845A1 (en) | 2014-04-24 |
| EP2906558B1 (en) | 2020-09-02 |
| KR20140048059A (ko) | 2014-04-23 |
| RU2015113333A (ru) | 2016-12-10 |
| EP2906558A1 (en) | 2015-08-19 |
| CN104718205A (zh) | 2015-06-17 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2828503T3 (es) | Bloqueadores de los canales de sodio, método de preparación de los mismos y uso de los mismos | |
| US10266548B2 (en) | Substituted benzylindazoles for use as Bub1 kinase inhibitors in the treatment of hyperproliferative diseases | |
| AU2014233414B2 (en) | N-acyl-N'-(pyridin-2-yl) ureas and analogs exhibiting anti-cancer and anti-proliferative activities | |
| ES2958954T3 (es) | Compuestos de piridazinona y usos de los mismos | |
| KR102399891B1 (ko) | 항암 및 항-증식 활성을 나타내는 2-아미노피리미딘-6-온 및 유사체 | |
| ES2728759T3 (es) | Compuestos de sulfonamida de cetona bicíclica | |
| AU2015317332B2 (en) | Inhibiting the transient receptor potential A1 ion channel | |
| EA031678B1 (ru) | 2-(морфолин-4-ил)-1,7-нафтиридины | |
| ES2918337T3 (es) | Bloqueadores de los canales de sodio | |
| TW200914458A (en) | Inhibitors of protein tyrosine kinase activity | |
| CN114072395A (zh) | 杂环化合物及其治疗蠕虫感染和疾病的用途 | |
| US20210139505A1 (en) | PIKfyve Inhibitors | |
| CN103539784A (zh) | 杂环苯甲酰胺类化合物、药用组合物及其应用 | |
| AU2014367283A1 (en) | Maleimide derivatives as modulators of WNT pathway | |
| ES2915583T3 (es) | Novedoso derivado de fenilpiridina y composición farmacéutica que contiene el mismo | |
| ES2821962T3 (es) | Bloqueador de canales de sodio | |
| ES2963508T3 (es) | Derivados de 5-hidroxi-7-oxabiciclo[2.2.1]heptano-2-carboxamida para inducir condrogénesis para el tratamiento del daño articular |