ES2808610T3 - Composiciones oftálmicas - Google Patents
Composiciones oftálmicas Download PDFInfo
- Publication number
- ES2808610T3 ES2808610T3 ES11726486T ES11726486T ES2808610T3 ES 2808610 T3 ES2808610 T3 ES 2808610T3 ES 11726486 T ES11726486 T ES 11726486T ES 11726486 T ES11726486 T ES 11726486T ES 2808610 T3 ES2808610 T3 ES 2808610T3
- Authority
- ES
- Spain
- Prior art keywords
- contact lens
- composition
- bioflavonoids
- bioflavonoid
- test
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L12/00—Methods or apparatus for disinfecting or sterilising contact lenses; Accessories therefor
- A61L12/08—Methods or apparatus for disinfecting or sterilising contact lenses; Accessories therefor using chemical substances
- A61L12/14—Organic compounds not covered by groups A61L12/10 or A61L12/12
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/35—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having six-membered rings with one oxygen as the only ring hetero atom
- A61K31/352—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having six-membered rings with one oxygen as the only ring hetero atom condensed with carbocyclic rings, e.g. methantheline
- A61K31/353—3,4-Dihydrobenzopyrans, e.g. chroman, catechin
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N65/00—Biocides, pest repellants or attractants, or plant growth regulators containing material from algae, lichens, bryophyta, multi-cellular fungi or plants, or extracts thereof
- A01N65/08—Magnoliopsida [dicotyledons]
- A01N65/36—Rutaceae [Rue family], e.g. lime, orange, lemon, corktree or pricklyash
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K36/00—Medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicines
- A61K36/18—Magnoliophyta (angiosperms)
- A61K36/185—Magnoliopsida (dicotyledons)
- A61K36/75—Rutaceae (Rue family)
- A61K36/752—Citrus, e.g. lime, orange or lemon
-
- C—CHEMISTRY; METALLURGY
- C11—ANIMAL OR VEGETABLE OILS, FATS, FATTY SUBSTANCES OR WAXES; FATTY ACIDS THEREFROM; DETERGENTS; CANDLES
- C11D—DETERGENT COMPOSITIONS; USE OF SINGLE SUBSTANCES AS DETERGENTS; SOAP OR SOAP-MAKING; RESIN SOAPS; RECOVERY OF GLYCEROL
- C11D3/00—Other compounding ingredients of detergent compositions covered in group C11D1/00
- C11D3/0005—Other compounding ingredients characterised by their effect
- C11D3/0078—Compositions for cleaning contact lenses, spectacles or lenses
-
- C—CHEMISTRY; METALLURGY
- C11—ANIMAL OR VEGETABLE OILS, FATS, FATTY SUBSTANCES OR WAXES; FATTY ACIDS THEREFROM; DETERGENTS; CANDLES
- C11D—DETERGENT COMPOSITIONS; USE OF SINGLE SUBSTANCES AS DETERGENTS; SOAP OR SOAP-MAKING; RESIN SOAPS; RECOVERY OF GLYCEROL
- C11D7/00—Compositions of detergents based essentially on non-surface-active compounds
- C11D7/22—Organic compounds
- C11D7/26—Organic compounds containing oxygen
- C11D7/267—Heterocyclic compounds
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Natural Medicines & Medicinal Plants (AREA)
- Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Wood Science & Technology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Animal Behavior & Ethology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Biotechnology (AREA)
- Mycology (AREA)
- Pharmacology & Pharmacy (AREA)
- Microbiology (AREA)
- Medicinal Chemistry (AREA)
- Botany (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Organic Chemistry (AREA)
- Alternative & Traditional Medicine (AREA)
- Medical Informatics (AREA)
- Emergency Medicine (AREA)
- Agronomy & Crop Science (AREA)
- Plant Pathology (AREA)
- Dentistry (AREA)
- Zoology (AREA)
- Environmental Sciences (AREA)
- General Chemical & Material Sciences (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicinal Preparation (AREA)
Abstract
Un método para almacenar o desinfectar una lente de contacto que comprende poner dicha lente de contacto en contacto con una composición, con una composición de desinfección y/o almacenamiento de lentes de contacto antimicrobiana acuosa que comprende al menos un bioflavonoide, seleccionado de naringina, neohesperidina y sus mezclas, opcionalmente junto con otros bioflavonoides, de modo que la naringina y la neohesperidina comprenden más del 75 % en p/p del bioflavonoide, en donde la composición comprende además ácido cítrico.
Description
DESCRIPCIÓN
Composiciones oftálmicas
Campo de la invención
La presente invención se refiere a composiciones y métodos para el cuidado de ojos y lentes de contacto. Más particularmente, la invención se refiere a una composición acuosa adecuada para su uso como una solución de lentes de contacto con agente antimicrobiano, que comprende una mezcla de bioflavonoides, en donde la naringina y la neohesperidina comprenden más del 75 % en p/p de la mezcla de bioflavonoides y en donde la composición comprende además ácido cítrico y un componente de tonicidad que comprende el 0,1-1% de cloruro de sodio.
Antecedentes de la invención
Los productos para la desinfección de lentes de contacto por medios químicos están destinados a reducir la contaminación microbiana introducida durante el uso y la eliminación de lentes, la limpieza y almacenamiento y deben contener agentes antimicrobianos capaces de lograr esto. Las lentes de contacto normalmente están sujetas a un régimen de limpieza y desinfección de lentes de contacto entre períodos de uso. Las soluciones acuosas que contienen agentes de limpieza y/o desinfección se usan comúnmente para este propósito.
Hay disponibles muchas soluciones multipropósito que se pueden usar para limpiar, desinfectar y humedecer lentes de contacto, seguido de la inserción directa en el ojo. Las soluciones multipropósito deben ser lo suficientemente fuertes como para destruir los microorganismos dañinos que pueden estar presentes o crecer en las lentes, mientras que son lo suficientemente suaves como para usar en los ojos. Tal solución también debe ser compatible con los muchos materiales de lentes de contacto en uso, que incluye lentes rígidas permeables a los gases, lentes blandas hidrofílicas tradicionales (de alto y bajo contenido de agua) y lentes de hidrogel de silicona. Las medidas de compatibilidad de lentes de contacto incluyen la decoloración de lentes de contacto, el cambio de parámetro físico, la fragilidad y absorción/liberación de componentes de la solución, especialmente agentes antimicrobianos. Soluciones para el cuidado de lentes de contacto, tales como las soluciones multipropósito (SMP) (a veces llamadas soluciones "todo en uno"), intentan equilibrar la capacidad de limpieza y desinfección con seguridad y comodidad en los ojos. La adición de agentes desinfectantes más eficaces generalmente tiene el efecto de reducir la compatibilidad del material de las lentes de contacto o la comodidad ocular de la solución. Una forma de lograr compatibilidad y comodidad adicionales del material es reducir la cantidad de agente desinfectante. Sin embargo, el conocimiento convencional dicta que esto da como resultado una menor eficacia antimicrobiana. Existe la necesidad de un antimicrobiano oftálmico que presente una eficacia biocida amplia y fuerte, mientras que causa irritación ocular mínima o molestias para el usuario. Las composiciones y métodos desvelados abordan esta necesidad proporcionando un complejo soluble acuoso que contiene al menos un bioflavonoide.
Se conocen ciertas composiciones que comprenden bioflavonoides que tienen alguna actividad antibacteriana y antivírica.
El documento US2007/0207116, se refiere a composiciones oftálmicas que comprenden al menos un agente antioxidante elegido de un carotenoide, glutatión, glutatión reducido, potenciadores de glutatión, un ácido lipoico, un bioflavonoide, un ácido oleanoico, palmitato de ascorbilo, extracto de aloe vera, un ácido graso omega-6, melatonina y acetato de vitamina E.
El documento WO2008/061536, se refiere a composiciones que comprenden al menos un bioflavonoide para el tratamiento o la mejora de una enfermedad o trastorno del ojo y/o los anexos del ojo en un sujeto animal, incluyendo un ser humano.
El documento WO02/20028, se refiere a composiciones y métodos para prevenir trastornos oculares al proteger las células de los efectos dañinos de los radicales libres. Los métodos implican administrar a un sujeto una composición que comprende ácido alfa lipoico, tocoferoles mixtos naturales, vitamina C, bioflavonoides cítricos, extracto de corteza de pino, luteína, carotenoides mixtos naturales y vitamina A.
El documento WO2008/009958, se refiere a una composición oral que tiene un pH en el intervalo de 3 a 8,5, que comprende: (a) en el intervalo del 0,1 % a < 10 % en p/p (basado en el peso total de la composición oral) de una solución madre que comprende una mezcla de bioflavonoides y ácidos de frutas o sales de los mismos; y (b) agua; y, opcionalmente, (c) un vehículo farmacéuticamente aceptable para el mismo.
El documento EP2198862, se refiere a bioflavonoides para su uso en el tratamiento de infecciones parasitarias.
Sumario de la divulgación
La presente invención se refiere a composiciones y métodos para el cuidado de ojos y lentes de contacto. En el primer aspecto de la invención, se proporciona una composición acuosa adecuada para su uso como una solución de lentes
de contacto con agente antimicrobiano, que comprende una mezcla de bioflavonoides, en donde la naringina y la neohesperidina comprenden más del 75 % en p/p de la mezcla de bioflavonoides y en donde la composición comprende además ácido cítrico y un componente de tonicidad que comprende el 0,1-1% de cloruro de sodio.
Además, se proporciona un método para almacenar o desinfectar una lente de contacto que comprende poner dicha lente de contacto en contacto con dicha composición anterior, preferentemente durante al menos 1 hora.
La lente de contacto se desinfecta con respecto a la colonización real o potencial por uno o más microorganismos seleccionados de Acanthamoeba sp, Aspergillus niger, Bacillus cereus, Clostridium difficile, Staphylococcus aureus, Pseudomonas aeruginosa, Staphylococcus epidermidis, Staphylococcus aureus resistente a la meticilina (SARM) y Fusarium solani. Con respecto a la colonización real o potencial por el microorganismo Acanthamoeba, la desinfección afecta a los trofozoítos y/o quistes.
Además, se proporciona el uso de una composición según el primer aspecto de la invención para almacenar o desinfectar una lente de contacto, preferentemente durante al menos 1 hora, por ejemplo durante al menos 6 horas, por ejemplo durante la noche. El almacenamiento será típicamente a temperatura ambiente, por ejemplo, a una temperatura de 18 a 24 °C, por ejemplo, alrededor de 20 °C.
De acuerdo con un aspecto adicional de la invención, se proporciona el uso de al menos un bioflavonoide, seleccionado de naringina, neohesperidina y sus mezclas, opcionalmente junto con otros bioflavonoides, de modo que la naringina y la neohesperidina comprenden más del 75 % en p/p del bioflavonoide, en donde la composición comprende además ácido cítrico, tal como un conservante para una composición oftálmica.
De acuerdo con un aspecto adicional de la invención, se proporciona un método para preservar una composición acuosa oftálmica que comprende el uso de al menos un bioflavonoide, seleccionado de naringina, neohesperidina y sus mezclas, opcionalmente junto con otros bioflavonoides, de modo que la naringina y la neohesperidina comprenden más del 75 % en p/p del bioflavonoide, en donde la composición comprende además ácido cítrico, en dicha composición oftálmica como conservante.
El uso o método de acuerdo con los aspectos previos de la invención para la preservación es preferentemente con respecto a la colonización real o potencial por uno o más microorganismos seleccionados de Acanthamoeba sp, Aspergillus niger, Bacillus cereus, Clostridium difficile, Staphylococcus aureus, Pseudomonas aeruginosa, Staphylococcus epidermidis, Staphylococcus aureus resistente a la meticilina (SARM) y Fusarium solani. Con respecto a la colonización real o potencial por el microorganismo Acanthamoeba, la desinfección afecta tanto a los trofozoítos y/o a los quistes
De acuerdo con un aspecto adicional de la invención, se proporciona una composición acuosa que comprende al menos un bioflavonoide, seleccionado de naringina, neohesperidina y sus mezclas, opcionalmente junto con otros bioflavonoides, de modo que la naringina y la neohesperidina comprenden más del 75 % en p/p del bioflavonoide, y en donde la composición comprende además ácido cítrico, para el almacenamiento y/o la desinfección de lentes de contacto para su uso en el tratamiento o prevención de infección o colonización del ojo por uno o más microorganismos seleccionados de Acanthamoeba sp, Aspergillus niger, Bacillus cereus, Clostridium difficile, Staphylococcus aureus, Pseudomonas aeruginosa, Staphylococcus epidermidis, Staphylococcus aureus resistente a la meticilina (SARM) y Fusarium solani.
Además, se proporciona un método para tratar o prevenir la infección o colonización del ojo de un sujeto por uno o más microorganismos seleccionados de Acanthamoeba sp, Aspergillus niger, Bacillus cereus, Clostridium difficile, Staphylococcus aureus, Pseudomonas aeruginosa, Staphylococcus epidermidis, Staphylococcus aureus resistente a la meticilina (SARM) y Fusarium solani que comprende administrar a dicho sujeto una composición tal como se describe en la reivindicación 1. Con respecto a la infección o colonización por el microorganismo Acanthamoeba, el tratamiento o la prevención afecta tanto a los trofozoítos y/o a los quistes. También se proporciona un método para reducir las poblaciones de las formas de trofozoítos y/o quistes de Acanthamoeba sp. que comprende administrar a dicho sujeto una composición según lo requerido por la reivindicación 10.
Descripción de figuras
Figura 1. El efecto desinfectante de la adición de la Formulación 1 a la Solución 1 de lentes de contacto en una población de Staphylococcus aureus resistente a la meticilina (SARM) en presencia o ausencia de suciedad orgánica.
Figura 2. El efecto desinfectante de la adición de la Formulación 1 a la Solución de lentes de contacto 2 en una población de Staphylococcus aureus resistente a la meticilina (SARM).
Figura 3. El efecto desinfectante de la adición de la Formulación 1 a la Solución de lentes de contacto 2 en una población de Staphylococcus aureus resistente a la meticilina (SARM) en presencia de suciedad orgánica.
Figura 4. El efecto desinfectante de la adición de la formulación 1 a la solución de lentes de contacto 1 en una población de Candida albicans.
Figura 5. El efecto desinfectante de la adición de la formulación 1 a la solución de lentes de contacto 1 en una población de Candida albicans en presencia de suciedad orgánica.
Figura 6. El efecto desinfectante de la adición de la formulación 1 a la solución de lentes de contacto 2 en una población de Candida albicans.
Figura 7. El efecto desinfectante de la adición de la formulación 1 a la solución de lentes de contacto 2 en una población de Candida albicans en presencia de suciedad orgánica.
Figura 8. El efecto desinfectante de la adición de la formulación 1 a la solución de lentes de contacto 1 en una población de Fusarium solani
Figura 9. El efecto desinfectante de la adición de la formulación 1 a la solución de lentes de contacto 2 en una población de Fusarium solani
Figura 10. El efecto desinfectante de la adición de la Formulación 1 a la Solución de lentes de contacto 1 en una población de trofozoítos de Acanthamoeba castellanii.
Figura 11. El efecto desinfectante de la adición de la formulación 1 a la solución de lentes de contacto 2 en una población de trofozoítos de Acanthamoeba castellanii.
Figura 12. El efecto desinfectante de la adición de la Formulación 1 a la Solución de lentes de contacto 1 en una población de quistes de Acanthamoeba castellanii.
Figura 13. El efecto desinfectante de la adición de la Formulación 1 a la Solución de lentes de contacto 1 en una población de quistes de Acanthamoeba castellanii en presencia de suciedad orgánica.
Figura 14. El efecto desinfectante de la adición de la formulación 1 a la solución de lentes de contacto 2 en una población de quistes de Acanthamoeba castellanii.
Figura 15. El efecto desinfectante de la adición de la formulación 1 a la solución de lentes de contacto 2 en una población de quistes de Acanthamoeba castellanii en presencia de suciedad orgánica.
Descripción detallada de la invención
El término "bioflavonoide" se refiere a una clase de metabolitos secundarios de plantas que tienen una estructura de polihidroxipolifenol a menudo como glucósidos. El término cubre los flavonoides derivados de la estructura 2-fenilcromen-4-ona (2-fenil-1,4-benzopi-rona) (ejemplos: quercetina, rutina), isoflavonoides, derivados de la estructura 3-fenilcromen-4-ona (3-fenil-1,4-ben-zopirona), neoflavonoides, derivados de la estructura 4-fenilcumarina (4-fenil-1,2-benzopirona), flavanonas, derivados de 2,3-dihidro-2-fenilcromen-4-ona (ejemplos hesperidina, naringina) y flavan-3-oles (catequinas).
El al menos un bioflavonoide de cualquiera de los aspectos anteriores de las invenciones proviene preferentemente de frutos de las especies de Citrus, lo más preferentemente, el al menos un bioflavonoide proviene de la médula de las naranjas amargas inmaduras, Citrus aurantium L. El al menos un bioflavonoide de cualquiera de los aspectos anteriores de las invenciones puede ser uno de una mezcla compleja de bioflavonoides. Por ejemplo, una mezcla de bioflavonoides obtenidos de los frutos de Citrus aurantium contiene al menos nueve flavonoides. La mezcla de flavonoides puede contener adecuadamente uno o más (o 2 o 3 o 4 o 5 o 6 o 7 u 8 o más, o los 9) de neoeriocitrina, isonaringina, naringina, hesperidina, neohesperidina, neodiosmina, naringenina, poncirina y riofolina. Tal mezcla de flavonoides se puede obtener de naranjas amargas, véase, por ejemplo, el documento WO2008/009956.
Actualmente se cree que las mezclas de tales flavonoides tienen ventajas sobre el uso de un solo flavonoide. Es particularmente ventajoso que se pueda emplear extracto de naranjas amargas sin la necesidad de aislar flavonoides individuales si se desea.
Uno o más bioflavonoides pueden, sin embargo, estar parcialmente o completamente purificados, si se desea, con respecto a las sustancias con las que están naturalmente asociadas (incluidos otros bioflavonoides).
Convenientemente, la mezcla de flavonoides comprenderá al menos el 25 %, más adecuadamente al menos el 40 % y preferentemente al menos el 50 % de naringina. Más convenientemente, la mezcla contendrá hasta un 65 % de naringina. Convenientemente, la mezcla de flavonoides comprenderá al menos el 15 %, más adecuadamente al menos el 20 % y preferentemente al menos el 25 % de neohesperidina. Más convenientemente, la mezcla contendrá hasta un 35 % de neohesperidina. En una forma preferida, la mezcla contendrá al menos el 75 % de neohesperidina y
naringina. Los valores de % mencionados anteriormente son en p/p.
Convenientemente, la mezcla de bioflavonoides será soluble en agua.
Convenientemente, la mezcla de bioflavonoides comprende bioflavonoides solubles en agua en asociación con la biomasa resultante del proceso de extracción; por consiguiente, la mezcla de bioflavonoides puede estar asociada con hasta el 40-70 % en p/p, preferentemente aproximadamente el 55 % p/p, de biomasa (basada en el peso de la mezcla de bioflavonoides). Los flavonoides son preferentemente glucósidos, especialmente aquellos seleccionados de neoeriocitrina, isonaringina, naringina, hesperidina, neohesperidina, neodiosmina, naringenina, poncirina y riofolina, y más preferentemente cada uno de estos está presente en la mezcla. Se prefiere especialmente cuando la mayor parte de la mezcla de bioflavonoides (es decir, más del 50 %) comprende naringina y neohesperidina, como cuando estos comprenden más del 75 % del componente bioflavonoide (excluyendo la biomasa). Adecuadamente, otros bioflavonoides (tales como flavonol, crisina, hesperetina) están sustancialmente ausentes de la mezcla de bioflavonoides y, por lo tanto, el componente de bioflavonoides consiste esencialmente en los bioflavonoides solubles en agua enumerados anteriormente, aunque pueden estar presentes trazas de otros bioflavonoides.
Una fuente adecuada de dicha mezcla de bioflavonoides solubles en agua se denomina en el presente documento 'HPLC 45', de los cuales aproximadamente el 45 % en p/p (de la composición total de HPLC 45) comprende dichos bioflavonoides, comprendiendo el resto (aproximadamente el 55 %) biomasa tal como pectinas, azúcares y ácidos orgánicos menores. Tal como se ha indicado anteriormente, especialmente preferido es cuando la mayor parte de la mezcla de bioflavonoides comprende naringina y neohesperidina, tal como cuando estos comprenden más del 35 % del componente bioflavonoide en una mezcla con biomasa tal como HPLC 45. El documento WO2008/009958, describe el proceso para la producción de HPLC45. La siguiente tabla proporciona una composición típica de HPLC 45.
Constituyente
% en p/p
Neoeriocitrina 1,1
Isonaringina 1,2
Naringina 23,4
Hesperidina 1,4
Neohesperidina 12,5
Neodiosmina 1,4
Naringenina 1,5
Poncirina 2,0
Riofolina 0,5
Contenido total de bioflavonoides 45%
El HPLC 45 está disponible de Exquim (la división de alimentos del Grupo Ferrer) como complejo de bioflavonoides cítricos del 45 % de HPLC.
Otra fuente adecuada de bioflavonoides solubles en agua es un extracto de té verde (un extracto de Camellia sinensis). Por lo general, el extracto contiene los galatos de epigalocatequina de bioflavonoides, epigalocatequina, galato de epicatequina y epi-catequina, de los cuales, el galato de epigalocatequina representa más del 40 % en p/p del contenido total. Otros componentes incluyen otros tres flavonoides adicionales, kaempferol, quercetina y miricetina.
Otro ejemplo de una fuente adecuada de bioflavonoides solubles en agua es un extracto de gingko (Gingko biloba) que contiene aproximadamente el 24 % de flavonoides, que consta de 33 bioflavonoides identificados.
En algunas realizaciones, puede ser deseable que la composición que contiene uno o más bioflavonoides de la presente invención comprenda además ácidos de frutas. Tal como se ha señalado en los ejemplos, la presencia de ácidos frutales en la composición puede mejorar la actividad antimicrobiana. Los ejemplos de ácidos de frutas incluyen ácido málico, ascórbico, cítrico y tartárico opcionalmente en forma de una sal. Por ejemplo, el ácido ascórbico se puede emplear como ascorbato de colina. Los ácidos de frutas, si están presentes, se pueden incluir a una concentración del 0,0001 al 1 % en p/v.
Aplicaciones de almacenamiento/esterilización de lentes de contacto
Las composiciones de acuerdo con la invención para su uso en el almacenamiento y la esterilización de lentes de contacto típicamente contendrán bioflavonoides a una concentración del 0,000001 al 0,04 % en p/v. Las soluciones de almacenamiento y esterilización de lentes de contacto típicamente contienen modificadores de tonicidad, por ejemplo, se basan en solución salina fisiológica (por ejemplo, NaCl al 0,9 % en p/v en agua) y pueden contener otros componentes. Conservantes adicionales tales como policuaternio-1, miristamidopropil dimetilamina, poliaminopropil biguanida y polihexametilen biguanida se pueden incluir, por ejemplo, en una cantidad del 0,000005 - 0,001 % en p/v. aunque preferentemente no están incluidos. Otros componentes que pueden estar presentes deseablemente incluyen agentes potenciadores de la viscosidad tales como hidroxipropilmetilcelulosa o un carbómero, por ejemplo, en una
cantidad del 0,001 - 0,1 % en p/v. Se pueden incluir tensioactivos tales como un poloxómero, es decir, poloxamina o poloxómero 407, tetronic 1304 o Surfac APG PC en una cantidad del 0,001 - 0,1 % en p/v. Se pueden incluir agentes quelantes, tales como EDTA, edentato disodio o ácido nonanoiletilendiaminotriacético. También se pueden usar agentes humectantes tales como el propilenglicol, glicerol (glicerina) o hidroxialquilfosfonato. Las composiciones para su uso en el almacenamiento y la esterilización de lentes de contacto también pueden ser adecuadas para humedecer lentes de contacto para la inserción en el ojo (es decir, son soluciones todo en uno). Ciertos de los componentes adicionales mencionados anteriormente son más adecuados cuando la composición está destinada a humedecer lentes de contacto. El pH de las soluciones de esterilización es típicamente entre 7,0 y 7,4. para una máxima compatibilidad con el ojo, aunque se puede tolerar un pH de 5 a 8. El pH se puede ajustar según sea necesario mediante la adición de ácido o base. Típicamente un sistema de tampón, por ejemplo, un sistema tampón basado en citrato y/o borato y/o fosfato, tal como un tampón de cítrico/borato, un borato o un tampón cítrico/fosfato, se empleará para mantener el intervalo de pH. También se puede añadir hidróxido de colina.
Se pueden proporcionar las soluciones de esterilización de lentes de contacto ya preparadas con bioflavonoides o bien se pueden proporcionar como un kit de modo que el bioflavonoide se suministre como una concentración para la dilución en otros componentes de la solución en el momento del uso.
Aplicaciones de preservación de soluciones oftálmicas
Las soluciones oftálmicas típicamente contienen modificadores de tonicidad, por ejemplo, se basan en solución salina fisiológica (por ejemplo, NaCl al 0,9 % en p/v en agua) y pueden contener otros componentes. Los componentes se pueden incluir tal como se mencionó anteriormente en "aplicaciones de lentes de contacto". Se pueden incluir otros componentes de acuerdo con el propósito, por ejemplo, se pueden incluir componentes farmacéuticamente activos (ingredientes activos antialérgicos tales como inhibidores de la liberación de mastocitos, antihistamínicos, etc). Las soluciones oftálmicas se pueden proporcionar ya preparadas con bioflavonoides o bien se pueden proporcionar como un kit para que el bioflavonoide se suministre como una concentración para la dilución en otros componentes de la solución en el momento del uso. La concentración de bioflavonoides en la solución oftálmica final es típicamente del 0,000001 al 0,4 % en p/v.
Composiciones farmacéuticas para el tratamiento de la infección ocular
Para el tratamiento de la infección ocular, las composiciones contendrán típicamente bioflavonoides a una concentración del 0,00001 al 0,4 % en p/v. Otros componentes que pueden estar presentes en la composición, incluidos los tampones, modificadores de la tonicidad, agentes modificadores de la viscosidad y tensioactivos como se mencionó anteriormente en "aplicaciones de lentes de contacto". El pH de tales composiciones será típicamente de 5,5 a 8,0, por ejemplo, 7,0 a 7,4.
Para el tratamiento de la infección ocular, típicamente las composiciones se pueden aplicar hasta 4 veces al día, preferentemente 2 veces al día, más preferentemente una vez al día. Convenientemente, el tratamiento consistirá en la aplicación de entre una y doce gotas, lo que equivale a aproximadamente 0,5 ml en cada período de dosis, o en el caso de una formulación de gel, la aplicación de una cantidad de "tamaño de guisante" en cada período de dosis.
Asuntos generales
Las composiciones de cualquiera de los aspectos de la invención se pueden envasar adecuadamente en recipientes de vidrio o plástico de tamaño adecuado, preferentemente en recipientes de plástico. Ejemplos de los tipos de plástico adecuados pueden ser polietileno de alta densidad (HDPE), polietileno de baja densidad (LDPE), polipropileno (PP) y tereftalato de polietileno (PET). El tamaño del envase dependerá de la aplicación. Por ejemplo, las lentes de contacto se pueden envasar en tamaños de 60 ml, 330 ml, 600 ml y, por ejemplo, las gotas antimicrobianas se pueden envasar en tamaños de 0,5 ml hasta 30 ml.
Las composiciones para uso oftálmico, incluidas las aplicaciones de lentes de contacto, se proporcionan típicamente como formulaciones estériles. La esterilización puede ser por llenado aséptico en recipientes esterilizados o por esterilización terminal después del llenado, ya sea mediante el uso de calor (tratamiento en autoclave) o irradiación.
A continuación, se ilustrará la presente invención mediante los siguientes ejemplos.
Ejemplo 1 - Preparación de soluciones madre
a) Preparación del complejo de bioflavonoides de Citrus
La médula de las naranjas amargas inmaduras (Citrus aurantium) se muele y luego se tritura en agua o agua/etanol.
La mezcla resultante se filtra para dejar una biomasa soluble en agua, que se retiene y una biomasa insoluble, que se desecha. La biomasa soluble en agua se somete luego a concentración y filtración fina para proporcionar los bioflavonoides solubles en agua. La solución se concentra y se seca al vacío para dejar un polvo higroscópico de color marrón del Complejo de Bioflavonoides de Citrus (CBC). El Complejo de Bioflavonoides de Citrus también está
disponible comercialmente, por ejemplo de Exquim SA, Ferrer Group. Típicamente, el Complejo de Bioflavonoides de Citrus contiene alrededor del 45 % de bioflavonoides, con naringina y neohesperidina siendo los componentes principales. Los componentes no bioflavonoides son típicamente pectinas al 10-15 % en p/p, proteínas al 10-15 % y carbohidratos al 5-6 %.
b) Composición y preparación de las formulaciones 1, 2, 3 y 4
Las composiciones de las formulaciones 1,2, 3 y 4 se dan en la T abla 1. Para preparar una solución madre, se agrega agua desmineralizada a una licuadora y se calienta a 50 °C. La glicerina y el ascorbato de colina (si se especifica) se agrega mientras se mezcla. La solución se mezcla durante 30 minutos, luego se añaden el Complejo de Bioflavonoides de Citrus, ácido cítrico, ácido málico, ácido ascórbico (si se especifica) y tensioactivo (si se especifica) mientras se mezcla. El producto luego se transfiere a contenedores adecuados y se controla la calidad.
Tabla 1 Constituyentes de las formulaciones 1, 2, 3 y 4
Constituyente Fórmula 1 Fórmula 2 Fórmula 3 Fórmula 4
% en p/p % en p/p % en p/p % en p/p Complejo de Bioflavonoides de Citrus 3,3 3,3 3,25 3,25$ Ácido málico 4,5 4,5 8,75 8,75 Ácido cítrico 4,5 4,5 8,75 8,75 Ácido ascórbico 1,5 - - -Ascorbato de colina - 6,0 4,0 4,0 Glicerina 7,5 - 0,83 0,83 Berol LFG 61 - 13,3 - -Propilenglicolfl - 7,5 - -Surfac APG PC t - - 3,0 3,0 Agua 78,6 60,9 71,42 71,42
pH 1,5 a 1,75 1,5 a 1,75 2,2 2,39
Contenido total de bioflavonoides
(ppm)_________________________ 14850 14850 14625 20000 Berol LFG 61, un tensioactivo alcoxilato es una combinación de tensioactivos de alquil glucósido y etoxilato t Surfac APG PC, un alquil poliglucósido, es un leve tensioactivo no iónico de origen natural
$ Contenido de flavonoides = 61 %
Ejemplo 2: prueba de suspensión cuantitativa para la evaluación de la actividad bactericida
Usando el estándar BS EN1276 Prueba cuantitativa de suspensión para la evaluación de la actividad bactericida de desinfectantes químicos y antisépticos utilizados en alimentos, zonas industriales, domésticas e institucionales, se probaron las formulaciones 1, 3 y 4 después de la dilución con agua dura estéril y se demostró que son eficaces contra varias bacterias en "condiciones sucias", es decir, en presencia de albúmina de suero bovino al 0,3 % en p/v. Las Tablas 2, 3 y 4 muestran la reducción microbiana proporcionada por la Formulación 1, 3 y 4, respectivamente, contra los organismos de pruebafl
Tabla 2 Efecto de la Formulación 1 sobre microorganismos utilizando la prueba EN 1276 en condiciones sucias
Concentración (% en Concentración de Reducción Organismo de prueba v/v) bioflavonoides (ppm) microbiana Campylobacter jejuni NCTC 11322 0,2 29,70 3,26 x 105 Enterococcus faecalis NCTC 8213 0,60 89,10 >1,32 x 106 Enterococcus hirae ATCC 8043 0,20 29,70 > 2,29 x 106 Escherichia coli NCTC 10418 0,20 29,70 >4,05 x 106 Lactobacillus acidophilus ATCC
4356 0,20 29,70 1,17 x 105 Legionella pneumophila NCTC
11192 0,60 89,10 ¥1,90 x 104 Mycobacterium fortuitum NCTC
8573 0,60 89,10 ¥9,15 x 103 Pseudomonas aeruginosa ATCC 29,70 1,9 x 10615442
(continuaci ón)
Concentración (% en Concentración de Reducción Organismo de prueba v/v) bioflavonoides (ppm) microbiana Staphylococcus aureus NCTC
6571 0,20 29,70 > 1,34 x 106 Vibro parahaemolyticus ATTC
17802 0,20 29,70 3,50 x 105 ¥- actividad bacteriana en 15 minutos a 20 °C en condiciones
sucias
Tabla 3 Efecto de la Formulación 3 sobre microorganismos utilizando la prueba EN 1276 en condiciones sucias
Concentración de Reducción Organismo de prueba Conc (% en v/v) bioflavonoides (ppm) microbiana Bacillus subtillus 10262 1 146,25 1,34 x 105 Enterococcus hirae ATCC 8043 0,2 29,25 >4,40 x 106 Escherichia coli NCTC 10418 0,2 29,25 >3,00 x 106 Pseudomonas aeruginosa ATCC
15442 0,2 29,25 >2,40 x 106 Staphylococcus aureus NCTC 6571 0,2 29,25 >5,58 x 106
Tabla 4 Efecto de la Formulación 4 sobre microorganismos utilizando la prueba EN 1276 en condiciones sucias
Conc(% Concentración de Reducción Organismo de prueba en v/v) bioflavonoides (ppm) microbiana Enterococcus hirae ATCC 8043 1 169 >4,02 x 106 Escherichia coli NCTC 10418 1 169 >5,49 x 106 Pseudomonas aeruginosa ATCC 15442 1 169 >7,16 x 104 Staphylococcus aureus NCTC 6571 1 169 >4,30 x 106
Este ejemplo muestra que incluso a concentraciones de 30 ppm, las composiciones de bioflavonoides son eficaces para destruir una variedad de especies de bacterias y cumplen los requisitos de_BS EN1276 Prueba cuantitativa de suspensión para la evaluación de la actividad bactericida de desinfectantes químicos y antisépticos utilizados en alimentos, zonas industriales, domésticas e institucionales.
Ejemplo 3 - Prueba cuantitativa de suspensión para la evaluación de la actividad esporicida y fungicida
Usando los estándares BS EN 13704 Prueba cuantitativa de suspensión para la evaluación de la actividad esporicida de los desinfectantes químicos utilizados en los alimentos, zonas industriales, domésticas e institucionales y BS EN 1650 Ensayo cuantitativo de suspensión para evaluar la actividad fungicida o levadicida de los desinfectantes químicos utilizados en los alimentos, zonas industriales, domésticas e institucionales, se probó la formulación 1 y demostró ser eficaz contra Bacillus cereus, dos especies de Clostridium sp., tres especies de hongos y una levadura. La Tabla 5 muestra la reducción microbiana proporcionada por la Formulación 1 después de la dilución con agua dura estéril contra los organismos de prueba en 'condiciones sucias', es decir, en presencia de albúmina de suero bovino al 0,3 % en p/v (Prueba EN 13704) o suspensión de levadura al 5 % en p/v (Prueba EN 1650).
Tabla 5 Efecto de la Solución 1 sobre los microorganismos utilizando las pruebas EN 13704 y EN 1650 en condiciones sucias
Concentración Concentración de Reducción Organismo de prueba (% en v/v) bioflavonoides (ppm) Ensayot microbiana Aspergillus niger NCPF 2275 1,0 146,3 EN 1650 8,71 x 103 Bacillus cereus ATCC 12826 0,5 73,1 EN13704 1,73 x 103 Candida albicans NCPF
3179 1,0 146,3 EN 1650 2,24 x 104 Clostridium difficile ATCC
11437 0,40 58,5 EN13704 3,93 x 103 Clostridium perfringens 0,40 58,5 EN13704 1,08 x 104 Penicillium digitatum 1,50 219,4 EN 1650 2,16 x 106 Phytophthora ramorum 0,50 73,1 EN 1650 2,76 x 104 t 30 minutos a 20 °C en condiciones sucias
Este ejemplo muestra que a concentraciones de 60 - 220 ppm, la composición de bioflavonoides es eficaz para destruir una variedad de especies de hongos y levaduras, y cumple con los requisitos de_BS EN 13704 Prueba cuantitativa de suspensión para la evaluación de la actividad esporicida de los desinfectantes químicos utilizados en los alimentos, zonas industriales, domésticas e institucionales y BS EN 1650 Ensayo cuantitativo de suspensión para evaluar la
actividad fungicida o levadicida de los desinfectantes químicos utilizados en los alimentos, zonas industriales, domésticas e institucionales
Ejemplo 4 - Mejora de la actividad antibacteriana de bioflavonoides usando ácidos de frutas
Se realizó un estudio comparando la actividad de una mezcla de bioflavonoide y un ácido de fruta contra los componentes individuales. Usando el estándar BS EN1276 Prueba cuantitativa de suspensión para la evaluación de la actividad bactericida de desinfectantes químicos y antisépticos utilizados en alimentos, zonas industriales, domésticas e institucionales, una solución acuosa de ácido cítrico, se comparó una solución acuosa del Complejo de Bioflavonoides de Citrus y una combinación de ácido cítrico y Complejo de Bioflavonoides de Citrus. La Tabla 6 muestra la actividad de las tres muestras de prueba contra cuatro bacterias.
Tabla 6 Efecto del ácido cítrico, complejo de bioflavonoides de Citrus y una combinación de los dos en _______________ microorganismos utilizando la prueba EN 1276 en condiciones sucias_______________ Organismo de prueba Artículo de prueba Reducción microbiana Bacillus subtillus 10262 Ácido cítrico 2,29 x 103 Bacillus subtillus 10262 CBC 6,46 x 103 Bacillus subtillus 10262 CBC ácido cítrico 3,80 x 105 Escherichia coli 11867 Ácido cítrico 6,46 x 102 Escherichia coli 11867 CBC 7,08 x 103 Escherichia coli 11867 CBC ácido cítrico 9,55 x 105 Pseudomonas aeruginosa ATCC 15442 Ácido cítrico 2,69 x 103 Pseudomonas aeruginosa ATCC 15442 CBC 1,95 x 104 Pseudomonas aeruginosa ATCC 15442 CBC ácido cítrico 3,72 x 106 Staphylococcus aureus NCTC 6571 Ácido cítrico 3,02 x 102 Staphylococcus aureus NCTC 6571 CBC 2,04 x 102 Staphylococcus aureus NCTC 6571 CBC ácido cítrico 4,17 x 105
La Tabla 6 muestra que las tres muestras de prueba presentaron actividad antibacteriana, teniendo la combinación un efecto mejorado.
Ejemplo 5 - Efectos de la formulación 4 en Acanthamoeba polyphaga
El propósito del estudio es evaluar la eficacia de la Formulación 4 contra la forma de trofozoíto de la ameba patógena ocular de vida libre Acanthamoeba. Las lentes de contacto normalmente están sujetas a un régimen de limpieza y desinfección entre períodos de uso. Si bien es un requisito que se demuestre que las soluciones para la desinfección de lentes de contacto tienen actividad contra bacterias y hongos, la eficacia contra la ameba de vida libre Acanthamoeba actualmente no es un requisito del estándar internacional para probar productos de cuidado de lentes de contacto. Sin embargo, Acanthamoeba es un patógeno ocular raro pero grave, con hasta el 90 % de los casos reportados en usuarios de lentes de contacto.
La concentración mínima de amebicida con trofozoíto (MTAC) y la concentración mínima de quisticida (MCC) de soluciones antimicrobianas contra la ameba patógena ocular de vida libre Acanthamoeba polyphaga se evaluó utilizando el método de microdilución en caldo.
La formulación 4 (1 ml) se diluyó con solución salina (0,9 % en p/v, 8 ml), se ajustó con NaOH 5 M a pH = 7, se preparó hasta 10 ml con más solución salina y se filtró para proporcionar una dilución del 10 % de la formulación (Solución de prueba 1). Esto equivale a 1,6 mg/ml de bioflavonoides. Por el mismo método, se produjo una muestra adicional que se ajustó a pH = 5 (solución de prueba 2).
Preparación del organismo
Trofozoítos de Acanthamoeba
La cepa de Acanthamoeba polyphaga (Ros) obtenida de la colección de cultivo de laboratorio se cultivó en medio Ac#6 a la temperatura apropiada. Una vez que se produjo un crecimiento confluente, los trofozoítos se recolectaron y se lavaron con solución de Ringer de % de fuerza. La concentración de trofozoítos se ajustó a 2 x 104 trofozoítos/ml utilizando medio Ac#6.
Quistes de Acanthamoeba
La cepa de Acanthamoeba polyphaga (Ros) obtenida de la colección de cultivo de laboratorio se cultivó en medio Ac#6 a la temperatura apropiada. Una vez que se produjo un crecimiento confluente, Los trofozoítos se recolectaron y se lavaron con medio de enquistamiento. Los trofozoítos se resuspendieron en medio de enquistamiento y se incubaron con agitación a la temperatura apropiada durante 5-7 días. Los quistes resultantes se recolectaron y se lavaron con una solución de Ringer de fuerza U. La concentración del quiste se ajustó a 2 x 104 quistes/ml utilizando solución de
Ringer de % de concentración antes de su uso.
Preparación de muestras de prueba y de control
Cada solución de prueba se probó por triplicado contra trofozoítos o quistes preparados tal como se detalla anteriormente. Para ensayos de trofozoítos, se añadió medio Ac#6 a los pocillos 2-12 de las filas A, B, C, F, G y H de una placa de microtitulación de fondo plano de 96 pocillos. Para los ensayos de quistes, la solución de Ringer de resistencia en U añadida a los pocillos 2-12 de las filas A, B, C, F, G y H de una placa de microtitulación de fondo plano de 96 pocillos. La solución de prueba 2 se añadió a los pocillos A1, B1 y C1, y la solución de prueba 1 se añadió a los pocillos F1, G1 y H1. Se realizaron diluciones en serie de 2 veces de las soluciones de prueba a través de la placa de microtitulación de las filas 2-11. La dilución y concentración de bioflavonoides en cada pocillo se proporciona en la Tabla 7 a continuación.
Tabla 7
El organismo de prueba calibrado se añadió a los pocillos de prueba y control de las filas A, B, C, F, G y H. Las placas se cubrieron y se incubaron a la temperatura adecuada durante 24 horas para los trofozoítos de Acanthamoeba.
Después de 24 horas de incubación, se inspeccionaron los pocillos con un microscopio óptico invertido. Los trofozoítos en los pocillos de prueba se compararon con los de los pocillos de control. La concentración mínima de amebicida con trofozoítos (MTAC) para el compuesto de prueba se determinó como la concentración más baja del compuesto de prueba que proporciona lisis o degeneración completa de los trofozoítos.
Quistes de Acanthamoeba
Después de 24 horas de incubación, se descartó el contenido de los pocillos. Los pocillos se rellenaron con solución de Ringer de 1/4 de concentración y se dejaron durante 15 minutos a temperatura ambiente. El procedimiento de lavado se repitió dos veces más. Luego, los pocillos se llenaron con una solución de Ringer con resistencia en U que contenía Escherichia coli. La placa se cubrió y se incubó a la temperatura apropiada durante 14 días. Los quistes en los pocillos de prueba se compararon con los de los pocillos de control utilizando un microscopio óptico invertido. La concentración mínima de quisticida (CCM) se determinó como la concentración más baja del compuesto de prueba que no produjo excreción ni replicación de trofozoítos.
Los resultados se muestran en la Tabla 8.
Tabla 8. Resultados de los ensayos de MTAC y MCC contra los trofozoítos y quistes de Acanthamoeba l h R
La Tabla 8 muestra que ambas soluciones de prueba son eficaces para destruir trofozoítos y quistes de Acanthamoeba polyphaga (Ros), un patógeno ocular raro pero grave.
Ejemplo 6 - La susceptibilidad in vitro de bacterias, hongos y levaduras
La susceptibilidad in vitro de bacterias, hongos y levaduras a compuestos antimicrobianos se evaluó de acuerdo con los procedimientos publicados por el Instituto de Normas Clínicas y de Laboratorio (CLSI). La concentración mínima inhibitoria (CMI) de soluciones antimicrobianas contra patógenos oculares bacterianos y fúngicos se evaluó utilizando el método de microdilución en caldo.
La formulación 4 (1 ml) se diluyó con solución salina (0,9 % en p/v, 8 ml), se ajustó con NaOH 5 M a pH = 7, se preparó hasta 10 ml con más solución salina y se filtró para proporcionar una dilución del 10 % de la formulación (Solución de prueba 1). Esto equivale a 1,6 mg/ml de bioflavonoides. Por el mismo método, se produjo una muestra adicional que se ajustó a pH = 5 (solución de prueba 2).
Preparación del organismo
Los organismos dados en la Tabla 9 se incubaron en el medio de crecimiento apropiado de acuerdo con los métodos estándar del CLSI, luego se recolectaron y se diluyeron para permitir suspensiones de soluciones madre de trabajo en los intervalos dados en la Tabla 10. Los números viables reales se confirmaron haciendo diluciones de la preparación de la solución madre y realizando recuentos de placas en espiral.
Tabla 9
Tabla 10
Preparación de muestras de prueba y de control
Cada solución de prueba se probó por triplicado contra cada organismo preparado tal como se detalla anteriormente.
Para pruebas bacterianas, se añadió caldo Mueller-Hinton ajustado a cationes (CAMHB) y para pruebas de levadura y hongos, se añadió medio de Roswell Park Memorial Institute (RPMI-1640) a los pocillos 2-12 de las filas A, B, C, F, G y H de una placa de microtitulación de fondo redondo de 96 pocillos, de acuerdo con los métodos estándar del CLSI
La solución de prueba 2 se añadió a los pocillos A1, B1 y C1, y la solución de prueba 1 se añadió a los pocillos F1, G1 y H1. Se realizaron diluciones en serie de 2 veces de las soluciones de prueba a través de la placa de microtitulación de las filas 2-11. La dilución y concentración de bioflavonoides en cada pocillo se proporciona en la Tabla a continuación.
Tabla 11
El organismo de prueba calibrado se añadió a los pocillos de prueba y control de las filas A, B, C, F, G y H. La placa se cubrió y se incubó a la temperatura apropiada durante 24 horas (bacterias y levadura) o 48 horas (hongos).
Se inspeccionaron las placas y se registró la CMI visual. La CMI es la concentración más baja de la solución que inhibe el crecimiento visible del organismo. Los pocillos que contenían la concentración mínima inhibitoria se colocaron en placas junto con los pocillos de control en los medios sólidos apropiados para cuantificar los niveles de desinfección de los pocillos de prueba de CMI. En singlete, los pocillos de prueba a las concentraciones superiores a la CMI se colocaron en placas para determinar la concentración mínima letal (CML) para cada microorganismo. La CML se define como la concentración más baja de la solución requerida para destruir al organismo, es decir, no hay crecimiento en medios sólidos.
Los resultados se muestran en las Tablas 12 y 13.
Tabla 12. Resultados de ensa os de CMI contra bacterias
Tabla 13. Resultados de ensa os de CMI contra levaduras hon os
Las Tablas 12 y 13 muestran que ambas soluciones de prueba son eficaces para inhibir el crecimiento de bacterias, levaduras y hongos que se sabe que causan infecciones en el ojo. Hay una dependencia del pH con algunos organismos, de modo que la solución de prueba que fue neutra fue más eficaz que esa solución de prueba con pH = 5.
Ejemplo 7 - Adición de la formulación 1 a soluciones de lentes de contacto
El propósito del presente estudio es evaluar la capacidad de las soluciones desinfectantes de lentes de contacto para reducir las poblaciones microbianas. Las soluciones para la desinfección de lentes de contacto están destinadas a reducir la población microbiana introducida durante el uso, retirada, limpieza y almacenaje de las lentes. La eficacia de los regímenes de lentes de contacto se puede determinar mediante el uso del Documento de orientación de la Notificación previa a la comercialización (510K) de la FDA 1997 para productos para el cuidado de lentes de contacto y la óptica oftálmica ISO14729 -Productos para el cuidado de lentes de contacto- Requisitos microbiológicos y métodos de prueba para productos y regímenes para el manejo higiénico de lentes de contacto. Las soluciones de lentes de contacto existentes se añadieron con varias concentraciones de Formulación 1 para determinar si se puede ver una actividad potenciada.
Muestras
Las muestras de prueba se proporcionaron tal como se detalla en la Tabla 14
_____ Tabla 14. Soluciones de prueba________________________________ Soluciones de prueba________ Contenidos______________________________________________________ Solución base 1 Hidroxialquilfosfonato (0,03 %), poloxamina (1 %), poliaminopropil biguanida (0,0001 %), ácido bórico, borato de sodio, cloruro de sodio, edetato disódico Solución base 1 0,25 % como arriba con el 0,0042 % de bioflavonoides
Formulación 1
Solución base 1 0,10 % como arriba con el 0,0017 % de bioflavonoides
Formulación 1
Solución base 1 0,05 % como arriba con el 0,0009 % de bioflavonoides
Formulación 1
Solución base 1 en presencia del
10 % de p/v de suciedad
orgánica
Solución base 1 0,25 % de como arriba con el 0,0042 % de bioflavonoides
Formulación 1 en presencia del
10 % en p/v de suciedad
orgánica_____________________
Solución base 2 TETRONIC® 1304, ácido nonanoil etilendiaminotriacético, polyquarter-1 (0,001
%), miristamidopropildimetilamina (0,0005 %)
Solución base 2 0,25 % como arriba con el 0,0042 % de bioflavonoides
Formulación 1
(continuación)
Soluciones de prueba Contenidos
Solución base 2 0,10 % como arriba con el 0,0017 % de bioflavonoides
Formulación 1
Solución base 2+ 0,05 % como arriba con el 0,0009 % de bioflavonoides
Formulación 1
Solución base 2 en presencia del
10 % de p/v de suciedad orgánica
Solución base 2 el 0,25 % de como arriba con el 0,0042 % de bioflavonoides
Formulación 1 en presencia del
10 % en p/v de suciedad orgánica
Los valores de % en esta tabla son en v/v excepto cuando se menciona lo contrario
Preparación del organismo
Los organismos dados en la Tabla 15 se incubaron en el medio de crecimiento apropiado de acuerdo con los métodos estándar ISO14729, luego se recolectaron y se diluyeron para permitir suspensiones de soluciones madre de trabajo en los intervalos dados en la Tabla 16.
Tabla 15
Tabla 16
Preparación de muestras de prueba y de control
Cada solución de prueba se probó por triplicado contra cada organismo preparado tal como se detalla anteriormente.
Los resultados se muestran en las Tablas 17-32 y se presentan en las Figuras 1 - 15
Tabla 17. Resultados de Staphylococcus aureus, SARM, infección del torrente sanguíneo con la Solución Base 1
continuación
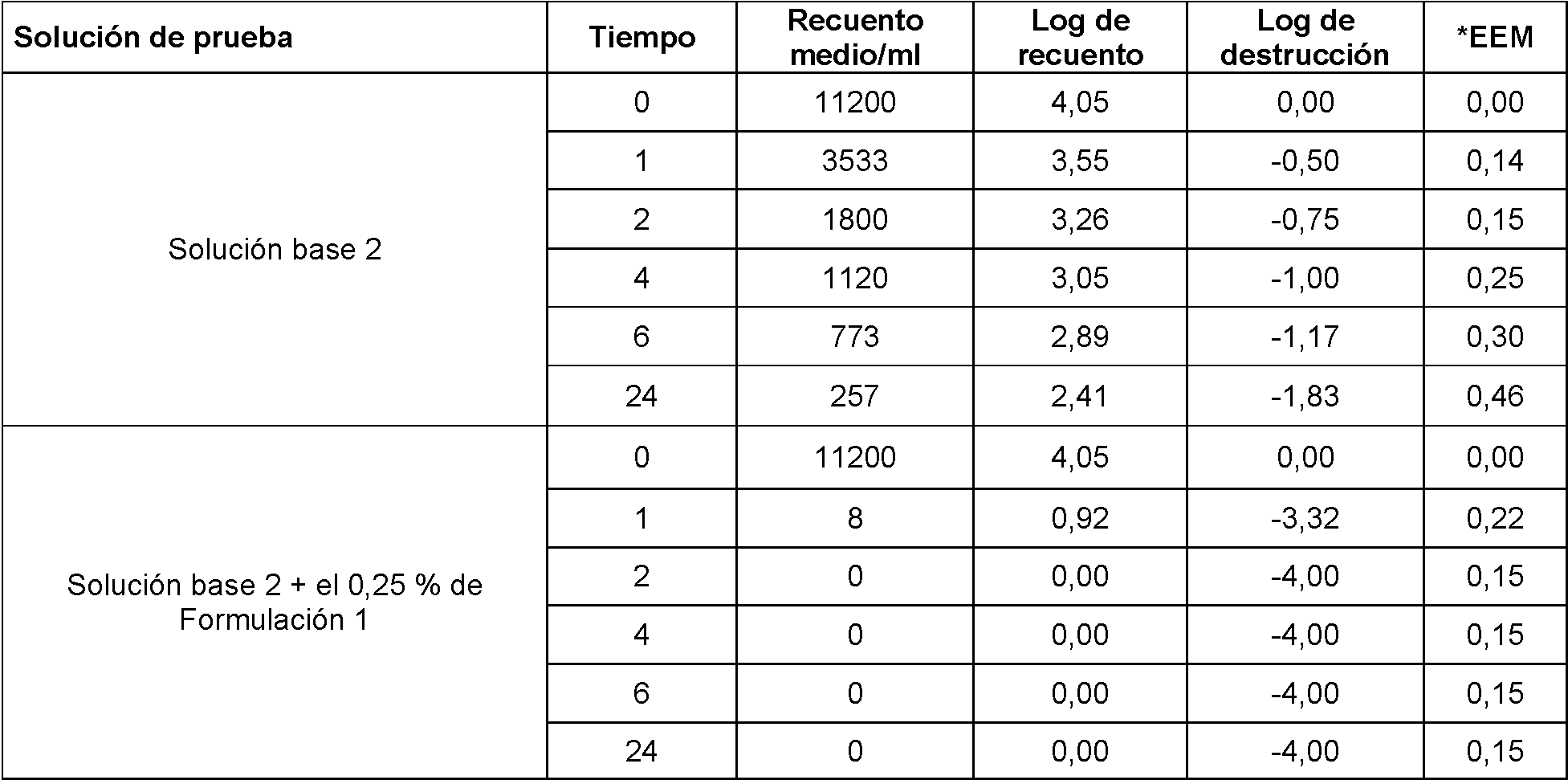
Tabla 18. Resultados de Staphylococcus aureus, SARM, infección del torrente sanguíneo con la Solución Base 2
Tabla 19. Resultados de Staphylococcus aureus, SARM, infección del torrente sanguíneo con la Solución B 1 n r n i l 1 n v i r ni
Tabla 20. Resultados de Staphylococcus aureus, SARM, infección del torrente sanguíneo con la Solución B 2 n r n i l 1 n v i r ni
Tabla 21. Resultados de Candida albicans ATCC 10231 con solución base 1
continuación
Tabla 22. Resultados de Candida albicans ATCC 10231 con solución base 2
continuación
Tabla 23. Resultados de Candida albicans, ATCC 10231 con solución base 1 en presencia del 10 % en p/v de suciedad or ánica
Tabla 24. Resultados de Candida albicans, ATCC 10231 con solución base 2 en presencia del 10 % en p/v de suciedad or ánica
Tabla 25. Resultados de Fusarium solani ATCC 36031 con solución base 1
Tabla 26. Resultados de Fusarium solani ATCC 36031 con solución base 2
Tabla 27. Resultados de trofozoítos de Acanthamoeba castellanii ATCC 50370 con solución base 1
continuación
Tabla 28. Resultados de trofozoítos de Acanthamoeba castellanii ATCC 50370 con solución base 2
T l 2. R l i A nh m ll nii AT 7 n l i n 1
continuación
Tabla 30. Resultados de uistes de Acanthamoeba castellanii ATCC 50370 con solución base 2
Tabla 31. Resultados de quistes de Acanthamoeba castellanii (ATCC 50370) con solución base 1 en r n i l 1 n v i r ni
Tabla 32 Resultados de quistes de Acanthamoeba castellanii (ATCC 50370) con solución base 2 en presencia l 1 n v i r ni
En resumen, de estas tablas se puede concluir que la adición de la Formulación 1 a las soluciones estándar de lentes de contacto mejora la actividad antimicrobiana contra Staphylococcus aureus, Candida albicans, Fusarium solani y Acanthamoeba castellanii (trofozoítos y quistes).
Ejemplo 8 Compatibilidad con lentes de contacto
La formulación 4 diluida al 0,5 % en v/v con solución salina al 0,9 % en p/v se probó para la compatibilidad de lentes de contacto. Se descubrió que para el material rígido permeable al gas evaluado, Óptimo confort, las lentes no parecían mostrar ningún cambio notable en comparación con las lentes de control. Esto se observa para las lentes en tres grupos de potencia. El efecto de la solución en lentes hidrofílicas blandas tradicionales se investigó mediante el uso de materiales con bajo contenido de agua (% de CF38) y alto contenido de agua (% de IG67). El material CF38 es un producto típico de poli(HEMA) (clasificación de la FDA como polimacon) y se utilizó una versión con un tinte de manipulación azul para el presente estudio. No se registraron cambios significativos en los parámetros de la lente para
las lentes de prueba en comparación con las lentes de control para ninguno de los tres grupos de potencia investigados. El material IG67 es típico de un material tradicional con alto contenido de agua y utiliza vinilpirrolidona como componente hidrofílico principal. Nuevamente, no se observaron diferencias significativas en los parámetros de la lente para los tres grupos de potencia con exposición a la solución de prueba en comparación con las lentes de control. Para las lentes definitivas de hidrogel de silicona, no se observaron cambios significativos para las lentes en cada uno de los grupos de potencia.
Ejemplo 9 - Prueba de eficacia conservativa de las formulaciones 3 y 4
Antes de la prueba, los microorganismos se cultivan en medios apropiados para el organismo y se recolectan para proporcionar suspensiones de cultivo a aproximadamente 108 ufc/ml. Se extrae una muestra de cada suspensión y se diluye en serie para los controles de enumeración y validación.
Para cada una de las muestras de prueba, se dispensaron 10 ml en un vaso universal para cada organismo. También se inició un control en blanco para cada organismo. Las suspensiones de microorganismos (108 ufc/ml, 0,1 ml) se añadieron a los universales y el producto se mezcló para garantizar la homogeneidad. Los controles se realizaron usando una dilución de 1:100 del producto en caldo, así como el caldo en blanco que luego se enriqueció con un pico de organismo de bajo nivel y se sembró para asegurar la neutralización adecuada de cualquier conservante.
Las soluciones del producto inoculado se incubaron a 20-25 °C en ausencia de luz. En los puntos de tiempo relevantes para el organismo bajo prueba (0, 6 h, 24 h, 7 días, 28 días para bacterias y 0, 7, 14 y 28 días para levaduras y mohos), se extrajo una muestra (1 ml), se diluyó según correspondiese y se sembró en placas para determinar el número de microorganismos viables. El log10 de la reducción se calculó a partir de los niveles de inóculo y el nivel de recuperación final del organismo, compensando cualquier dilución realizada durante la prueba.
El número de microorganismos viables en las suspensiones de cultivo se da en la Tabla 33.
Tabla 33 Recuentos de viables de suspensiones de cultivo
Organismo Recuento (log10 ufc/ml)
Aspergillus niger 7,6
Candida albicans 7,8
Zygosachharomyces rouxii 7,7
Pseudomonas aeruginosa 7,6
Staphylococcus aureus 8,0
Escherichia coli 8,1
Los recuentos de recuperación para los controles con picos de bajo nivel pasaron todos los criterios de validación. Los recuentos de recuperación en los puntos de tiempo específicos para el 0,5 % de la Formulación 3, el 1 % de la Formulación 3, el 0,5 % de la Formulación 4 y el 1 % de la Formulación 4 se dan en las Tablas 34, 35, 36 y 37 respectivamente.
Tabla 34 Recuentos de recuperación después de la incubación con el 0,5 % en v/v de la Formulación 3 Organismo log10 de recuperación Log10 de reducción
0 h 6 h 24 h 7 días 14 días 28 días
A. niger 5,3 nd nd 1,0 1,0 1,2
Z. rouxii >5,5 nd nd >4,7 >4,7 >4,7 P. aeruginosa 5,2 2,4 >4,7 >4,7 nd >4,7 S. aureus 4,8 >5,0 >5,0 >5,0 nd >5,0
nd = no determinado
Tabla 35 Recuentos de recuperación después de la incubación con el 1,0 % en v/v de la Formulación 3 Organismo log10 de recuperación Log10 de reducción
0 h 6 h 24 h 7 días 14 días 28 días
A. niger 5,1 nd nd 1,8 2,1 2,2
Z. rouxii >5,5 nd nd >4,7 >4,7 >4,7 P. aeruginosa 5,3 >4,7 >4,7 >4,7 nd >4,7 S. aureus 3,7 >5,0 >5,0 >5,0 nd >5,0 E. coli 5,4 >5,1 >5,1 >5,1 nd >5,1 nd = no determinado
Tabla 36 Recuentos de recuperación después de la incubación con el 0,5 % en v/v de la Formulación 4 Organismo log10 de recuperación Log10 de reducción
0 h 6 h 24 h 7 días 14 días 28 días
A. niger 5,0 nd nd >4,6 >4,6 >4,6
Z. rouxii 5,1 nd nd >4,7 >4,7 >4,7 P. aeruginosa 4,5 >4,7 >4,7 >4,7 nd >4,7 S. aureus <1 >5,0 >5,0 >5,0 nd >5,0
nd = no determinado
Tabla 37 Recuentos de recuperación después de la incubación con el 1 % en v/v de la Formulación 4 Organismo log10 de recuperación Log10 de reducción
0 h 6 h 24 h 7 días 14 días 28 días
A. niger 4,9 nd nd 4,6 4,6 >4,6
Z. rouxii 4,8 nd nd >4,7 >4,7 >4,7 P. aeruginosa 4,8 >4,7 >4,7 >4,7 nd >4,7 S. aureus 2,1 >5,0 >5,0 >5,0 nd >5,0
nd = no determinado
Se descubrió que tanto la Formulación 3 como la 4 al 0,5 y al 1,0 % en p/v son conservantes antimicrobianos eficaces.
Ejemplo 10 - Tolerancia ocular en conejos
Después de múltiples instilaciones de Formulación 3 en (a) el 3 % en v/v o (b) el 1 % en v/v o (c) diluciones del 2 % en v/v con solución salina al 0,9 % en el ojo derecho de conejos albinos durante 6 días, no se observaron reacciones oculares significativas. La concentración del 1 % parecía ser ligeramente más irritante que las otras dos concentraciones o el vehículo solo. Sin embargo, dado que claramente no hubo hallazgos dependientes de la dosis y los ojos no tratados mostraron hallazgos similares, esta evidente diferencia no se considera significativa o clínicamente significativa.
Por lo tanto, en estas condiciones experimentales, la formulación 3 fue macroscópicamente muy bien tolerada a las concentraciones del 1 %, del 2 % y del 3 % en v/v.
A menos que se indique lo contrario, los valores de % tal como se usan en el presente documento son valores de % en p/p.
Lo anterior describe ampliamente la presente invención, sin limitación. Las variaciones y modificaciones que serán fácilmente evidentes para los expertos en esta técnica están destinadas a ser incluidas dentro del alcance de la presente solicitud y patentes posteriores.
A lo largo de la memoria descriptiva y de las reivindicaciones que la siguen, a no ser que el contexto requiera lo contrario, el término "comprender" y sus variantes tales como "comprende" y "que comprende", se entenderá que implican la inclusión de un elemento, etapa, grupo de elementos o grupo de etapas indicados pero sin excluir ningún otro elemento, etapa, grupo de elementos o grupo de etapas.
Todas las patentes y solicitudes de patentes mencionadas a lo largo de la memoria descriptiva de la presente invención se incorporan en el presente documento en su totalidad a modo de referencia.
La invención abarca todas las combinaciones de grupos preferidos y más preferidos y grupos y realizaciones adecuados y más adecuados de los grupos mencionados anteriormente.
Claims (1)
- REIVINDICACIONES1. Un método para almacenar o desinfectar una lente de contacto que comprende poner dicha lente de contacto en contacto con una composición, con una composición de desinfección y/o almacenamiento de lentes de contacto antimicrobiana acuosa que comprende al menos un bioflavonoide, seleccionado de naringina, neohesperidina y sus mezclas, opcionalmente junto con otros bioflavonoides, de modo que la naringina y la neohesperidina comprenden más del 75 % en p/p del bioflavonoide, en donde la composición comprende además ácido cítrico.2. Un método de acuerdo con la reivindicación 1, en donde la lente de contacto está en contacto con la composición durante al menos 1 hora.3. Un método de acuerdo con una cualquiera de las reivindicaciones 1 o 2, en donde el al menos un bioflavonoide se obtiene de frutos de especies de Citrus, opcionalmente de la médula de las naranjas amargas, Citrus aurantium. 4. Un método de acuerdo con una cualquiera de las reivindicaciones 1 a 3, en donde la composición tiene un pH entre 5 y 8.5. Un método de acuerdo con una cualquiera de las reivindicaciones 1 a 4 en el que dicha lente de contacto se desinfecta con respecto a la colonización real o potencial por uno o más microorganismos seleccionados de Acanthamoeba sp, Aspergillus niger, Bacillus cereus, Clostridium difficile, Staphylococcus aureus, Pseudomonas aeruginosa, Staphylococcus epidermidis, Staphylococcus aureus resistente a la meticilina (SARM) y Fusarium solani.6. Un método de acuerdo con la reivindicación 5 en el que dicha lente de contacto se desinfecta con respecto a la presencia real o potencial de trofozoítos y/o quistes de Acanthamoeba sp.7. Un método de acuerdo con una cualquiera de las reivindicaciones 1 a 6, en el que la composición comprende además un componente de tonicidad que comprende el 0,1-1 % de cloruro de sodio.8. Uso de una composición antimicrobiana acuosa que comprende al menos un bioflavonoide, seleccionado de naringina, neohesperidina y sus mezclas, opcionalmente junto con otros bioflavonoides, de modo que la naringina y la neohesperidina comprenden más del 75 % en p/p del bioflavonoide, y en donde la composición comprende además ácido cítrico, para el almacenamiento y/o la desinfección de lentes de contacto.9. Uso de una composición antimicrobiana acuosa de acuerdo con la reivindicación 8, en donde la composición además comprende un componente de tonicidad que comprende el 0,1-1 % de cloruro de sodio.10. Una composición acuosa adecuada para su uso como una solución de lentes de contacto de agente antimicrobiano, que comprende una mezcla de bioflavonoides, en donde la naringina y la neohesperidina comprenden más del 75 % en p/p de la mezcla de bioflavonoides y en donde la composición comprende además ácido cítrico y un componente de tonicidad que comprende el 0,1-1% de cloruro de sodio.
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| PCT/GB2011/051105 WO2012172274A1 (en) | 2011-06-13 | 2011-06-13 | Ophthalmic compositions |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2808610T3 true ES2808610T3 (es) | 2021-03-01 |
Family
ID=44627286
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES11726486T Active ES2808610T3 (es) | 2011-06-13 | 2011-06-13 | Composiciones oftálmicas |
Country Status (12)
| Country | Link |
|---|---|
| US (1) | US9931428B2 (es) |
| EP (1) | EP2717690B1 (es) |
| DK (1) | DK2717690T3 (es) |
| ES (1) | ES2808610T3 (es) |
| HR (1) | HRP20201108T1 (es) |
| HU (1) | HUE049844T2 (es) |
| LT (1) | LT2717690T (es) |
| PL (1) | PL2717690T3 (es) |
| PT (1) | PT2717690T (es) |
| RS (1) | RS60624B1 (es) |
| SI (1) | SI2717690T1 (es) |
| WO (1) | WO2012172274A1 (es) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8557868B2 (en) | 2000-11-04 | 2013-10-15 | Fxs Ventures, Llc | Ophthalmic and contact lens solutions using low molecular weight amines |
| GR20180100568A (el) * | 2018-12-27 | 2020-07-16 | Μαριανα Γεωργιου Χατζαρα | Συνθεση με βαση το δικταμο κατα του βακτηριου ακανθαμοεμπα που προσβαλλει τους οφθαλμους |
| CN111616292A (zh) * | 2020-05-25 | 2020-09-04 | 广州素旺生物科技有限公司 | 一种杀菌抑菌消毒剂及其制备方法 |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| NL1002484C2 (nl) * | 1996-02-29 | 1997-09-01 | Christianus Hendrikus Mattias | Oftalmologisch bruikbare samenstelling, daarmee bereide oogvloeistoffen en contactlensverzorgingsmiddelen, en werkwijze voor het reinigen/des- infecteren van contactlenzen. |
| US20030086986A1 (en) * | 1998-08-06 | 2003-05-08 | Bruijn Chris De | Ophthalmic, pharmaceutical and other healthcare preparations with naturally occurring plant compounds, extracts and derivatives |
| WO2002020028A2 (en) | 2000-09-06 | 2002-03-14 | Braswell A Glenn | Method and composition for enhancing vision |
| WO2002092028A2 (en) * | 2001-05-15 | 2002-11-21 | The Procter & Gamble Company | Oral care compositions |
| US20070207116A1 (en) | 2006-03-01 | 2007-09-06 | Brown David C | Antioxidant compositions for the eye |
| JPWO2007125731A1 (ja) * | 2006-04-28 | 2009-09-10 | 株式会社メニコン | ソフトコンタクトレンズ用溶液及びそれを用いて得られる薬剤徐放性ソフトコンタクトレンズ並びにその製造方法 |
| GB0614353D0 (en) * | 2006-07-20 | 2006-08-30 | Oraldent Ltd | Oral compositions, their preparation and use |
| US20100209536A1 (en) | 2006-09-26 | 2010-08-19 | The Brigham And Women's Hospital, Inc. | Methods and Kits for Use in the Treatment and Prevention of Diseases or Conditions of the Immune System or Infectious Diseases |
| WO2008061536A1 (en) | 2006-11-22 | 2008-05-29 | Ocumedic Aps | Compositions and methods of using same for treatment of a disease or disorder of the eye and/or the adnexa of the eye |
| JP5346454B2 (ja) * | 2007-09-21 | 2013-11-20 | 花王株式会社 | 抗菌性洗浄剤組成物 |
| EP2198862A1 (en) | 2008-12-18 | 2010-06-23 | Citrox Limited | Use of flavonoids to treat parasitic infection |
-
2011
- 2011-06-13 US US14/125,427 patent/US9931428B2/en active Active
- 2011-06-13 HU HUE11726486A patent/HUE049844T2/hu unknown
- 2011-06-13 EP EP11726486.1A patent/EP2717690B1/en active Active
- 2011-06-13 ES ES11726486T patent/ES2808610T3/es active Active
- 2011-06-13 SI SI201131896T patent/SI2717690T1/sl unknown
- 2011-06-13 PT PT117264861T patent/PT2717690T/pt unknown
- 2011-06-13 RS RS20200832A patent/RS60624B1/sr unknown
- 2011-06-13 WO PCT/GB2011/051105 patent/WO2012172274A1/en active Application Filing
- 2011-06-13 DK DK11726486.1T patent/DK2717690T3/da active
- 2011-06-13 LT LTEP11726486.1T patent/LT2717690T/lt unknown
- 2011-06-13 PL PL11726486T patent/PL2717690T3/pl unknown
-
2020
- 2020-07-15 HR HRP20201108TT patent/HRP20201108T1/hr unknown
Also Published As
| Publication number | Publication date |
|---|---|
| EP2717690A1 (en) | 2014-04-16 |
| PT2717690T (pt) | 2020-08-11 |
| SI2717690T1 (sl) | 2020-09-30 |
| HUE049844T2 (hu) | 2020-11-30 |
| DK2717690T3 (da) | 2020-07-27 |
| RS60624B1 (sr) | 2020-09-30 |
| LT2717690T (lt) | 2020-09-25 |
| PL2717690T3 (pl) | 2020-11-02 |
| WO2012172274A1 (en) | 2012-12-20 |
| HRP20201108T1 (hr) | 2020-10-30 |
| EP2717690B1 (en) | 2020-04-15 |
| US20140186474A1 (en) | 2014-07-03 |
| US9931428B2 (en) | 2018-04-03 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2374607T3 (es) | Composiciones oftálmicas con un tensioactivo anfótero y ácido hialurónico. | |
| ES2443548T3 (es) | Composiciones farmacéuticas acuosas que contienen complejos de borato-poliol | |
| US20030086986A1 (en) | Ophthalmic, pharmaceutical and other healthcare preparations with naturally occurring plant compounds, extracts and derivatives | |
| PL187339B1 (pl) | Zastosowanie soli benzylolaurylodwumetyloamoniowych jako środków konserwujących do wytwarzania kompozycji ocznych i zastosowanie kompozycji ocznych do wytwarzania preparatów | |
| CN106572662A (zh) | 抗微生物‑抗生物膜组合物及其作为个人护理产品的使用方法 | |
| ES2808610T3 (es) | Composiciones oftálmicas | |
| AU2023219973A1 (en) | Antimicrobial compositions containing polyquaternium | |
| JP5401113B2 (ja) | メントール類を含有する亜塩素酸類化合物含有水性組成物 | |
| Padzik et al. | Evaluation of in vitro effect of selected contact lens solutions conjugated with nanoparticles in terms of preventive approach to public health risk generated by Acanthamoeba strains | |
| KR101726029B1 (ko) | 알콕실화된 천연 왁스를 갖는 안과용 조성물 | |
| BR112020000750A2 (pt) | composição antimicrobiana, método de tratamento e/ou prevenção de infecção por bactérias e/ou fungos | |
| ES2569085T3 (es) | Composición de desinfectante | |
| ES2652505T3 (es) | Composiciones oftálmicas con biguanida y ésteres de PEG-glicerol | |
| JP2006201247A (ja) | コンタクトレンズ用消毒保存溶液 | |
| ES2229160T3 (es) | Antiseptico para heridas y membranas mucosas. | |
| CN106900733B (zh) | 一种超分子杀菌剂及其制备方法和杀菌方法 | |
| ES2902585T3 (es) | Composición que tiene actividad antimicrobiana | |
| JP2007513951A (ja) | 医薬品組成物の抗菌活性を増強する有機緩衝剤の使用 | |
| KR102637031B1 (ko) | 콘택트렌즈용 관리용액 조성물 | |
| ES2695180T3 (es) | Composiciones oftálmicas sinérgicas para desinfectar lentes de contacto | |
| RU2476199C1 (ru) | Состав для дезинфекции и очистки съемных пластиночных протезов | |
| ES2579838T3 (es) | Soluciones únicas para el cuidado de lentes de contacto que comprenden camomila | |
| ES2366839B1 (es) | Composicion para el cuidado de lentes de contacto | |
| KR20110133764A (ko) | 키토산을 함유한 천연 살균소독제 및 그로 처리된 항균 티슈 | |
| KR20240000763A (ko) | 플라즈마 라디칼 용액과 천연 유래 추출물이 함유된 항균제 조성물 |