ES2804199T3 - Compuestos compatibles con silicona - Google Patents
Compuestos compatibles con silicona Download PDFInfo
- Publication number
- ES2804199T3 ES2804199T3 ES16884306T ES16884306T ES2804199T3 ES 2804199 T3 ES2804199 T3 ES 2804199T3 ES 16884306 T ES16884306 T ES 16884306T ES 16884306 T ES16884306 T ES 16884306T ES 2804199 T3 ES2804199 T3 ES 2804199T3
- Authority
- ES
- Spain
- Prior art keywords
- alkyl
- phenyl
- group
- sil
- compound
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 150000001875 compounds Chemical class 0.000 title claims abstract description 95
- 229920001296 polysiloxane Polymers 0.000 title claims description 78
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims abstract description 51
- 125000000217 alkyl group Chemical group 0.000 claims abstract description 24
- 239000001257 hydrogen Substances 0.000 claims abstract description 16
- 229910052739 hydrogen Inorganic materials 0.000 claims abstract description 16
- 125000004648 C2-C8 alkenyl group Chemical group 0.000 claims abstract description 13
- 125000000753 cycloalkyl group Chemical group 0.000 claims abstract description 13
- 125000001153 fluoro group Chemical group F* 0.000 claims abstract description 13
- 125000003545 alkoxy group Chemical group 0.000 claims abstract description 11
- -1 phenyl C1-C3 alkyl Chemical group 0.000 claims abstract description 10
- 125000004435 hydrogen atom Chemical class [H]* 0.000 claims abstract description 9
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 claims abstract description 6
- 229910052731 fluorine Inorganic materials 0.000 claims abstract description 6
- 239000011737 fluorine Substances 0.000 claims abstract description 6
- 239000000203 mixture Substances 0.000 claims description 68
- 229910052799 carbon Inorganic materials 0.000 claims description 17
- 125000003342 alkenyl group Chemical group 0.000 claims description 16
- 238000000034 method Methods 0.000 claims description 15
- 230000005855 radiation Effects 0.000 claims description 15
- 229920005573 silicon-containing polymer Polymers 0.000 claims description 14
- 230000000977 initiatory effect Effects 0.000 claims description 10
- 238000004519 manufacturing process Methods 0.000 claims description 10
- NIXOWILDQLNWCW-UHFFFAOYSA-N acrylic acid group Chemical group C(C=C)(=O)O NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 claims description 9
- 238000006460 hydrolysis reaction Methods 0.000 claims description 9
- 229910004298 SiO 2 Inorganic materials 0.000 claims description 8
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 8
- 238000000016 photochemical curing Methods 0.000 claims description 8
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical group CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 claims description 5
- 239000004205 dimethyl polysiloxane Substances 0.000 claims description 5
- 229920000435 poly(dimethylsiloxane) Polymers 0.000 claims description 5
- 238000006482 condensation reaction Methods 0.000 claims description 4
- 230000009977 dual effect Effects 0.000 claims description 3
- 239000011521 glass Substances 0.000 claims description 3
- 230000000269 nucleophilic effect Effects 0.000 claims description 3
- 238000006467 substitution reaction Methods 0.000 claims description 3
- 238000012360 testing method Methods 0.000 claims description 3
- WSDQIHATCCOMLH-UHFFFAOYSA-N phenyl n-(3,5-dichlorophenyl)carbamate Chemical compound ClC1=CC(Cl)=CC(NC(=O)OC=2C=CC=CC=2)=C1 WSDQIHATCCOMLH-UHFFFAOYSA-N 0.000 claims description 2
- 230000002194 synthesizing effect Effects 0.000 claims description 2
- SCPYDCQAZCOKTP-UHFFFAOYSA-N silanol Chemical compound [SiH3]O SCPYDCQAZCOKTP-UHFFFAOYSA-N 0.000 claims 2
- 125000003837 (C1-C20) alkyl group Chemical group 0.000 abstract description 3
- 125000004400 (C1-C12) alkyl group Chemical group 0.000 abstract description 2
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 abstract 2
- 101000836873 Homo sapiens Nucleotide exchange factor SIL1 Proteins 0.000 abstract 1
- 102100027096 Nucleotide exchange factor SIL1 Human genes 0.000 abstract 1
- 229910004738 SiO1 Inorganic materials 0.000 abstract 1
- 229910020489 SiO3 Inorganic materials 0.000 abstract 1
- 101000880156 Streptomyces cacaoi Subtilisin inhibitor-like protein 1 Proteins 0.000 abstract 1
- 229910052681 coesite Inorganic materials 0.000 abstract 1
- 229910052906 cristobalite Inorganic materials 0.000 abstract 1
- 239000000377 silicon dioxide Substances 0.000 abstract 1
- 235000012239 silicon dioxide Nutrition 0.000 abstract 1
- 229910052682 stishovite Inorganic materials 0.000 abstract 1
- 229910052905 tridymite Inorganic materials 0.000 abstract 1
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 24
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 21
- 239000000047 product Substances 0.000 description 18
- 239000012043 crude product Substances 0.000 description 15
- 229910052786 argon Inorganic materials 0.000 description 12
- 238000001723 curing Methods 0.000 description 12
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 12
- 238000006243 chemical reaction Methods 0.000 description 10
- 230000015572 biosynthetic process Effects 0.000 description 9
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 9
- 239000012044 organic layer Substances 0.000 description 9
- 239000002904 solvent Substances 0.000 description 9
- VHYFNPMBLIVWCW-UHFFFAOYSA-N 4-Dimethylaminopyridine Chemical compound CN(C)C1=CC=NC=C1 VHYFNPMBLIVWCW-UHFFFAOYSA-N 0.000 description 8
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 8
- PCLIMKBDDGJMGD-UHFFFAOYSA-N N-bromosuccinimide Chemical compound BrN1C(=O)CCC1=O PCLIMKBDDGJMGD-UHFFFAOYSA-N 0.000 description 8
- 238000003786 synthesis reaction Methods 0.000 description 8
- 239000007858 starting material Substances 0.000 description 7
- 238000004383 yellowing Methods 0.000 description 7
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 6
- 239000007832 Na2SO4 Substances 0.000 description 6
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 6
- ISAOCJYIOMOJEB-UHFFFAOYSA-N benzoin Chemical group C=1C=CC=CC=1C(O)C(=O)C1=CC=CC=C1 ISAOCJYIOMOJEB-UHFFFAOYSA-N 0.000 description 6
- 238000004440 column chromatography Methods 0.000 description 6
- 239000000706 filtrate Substances 0.000 description 6
- 230000007062 hydrolysis Effects 0.000 description 6
- 239000010410 layer Substances 0.000 description 6
- 239000012074 organic phase Substances 0.000 description 6
- 238000000746 purification Methods 0.000 description 6
- 229910052938 sodium sulfate Inorganic materials 0.000 description 6
- 235000011152 sodium sulphate Nutrition 0.000 description 6
- 230000005670 electromagnetic radiation Effects 0.000 description 5
- 150000002431 hydrogen Chemical class 0.000 description 5
- OZAIFHULBGXAKX-UHFFFAOYSA-N 2-(2-cyanopropan-2-yldiazenyl)-2-methylpropanenitrile Chemical compound N#CC(C)(C)N=NC(C)(C)C#N OZAIFHULBGXAKX-UHFFFAOYSA-N 0.000 description 4
- 229960000549 4-dimethylaminophenol Drugs 0.000 description 4
- OZAIFHULBGXAKX-VAWYXSNFSA-N AIBN Substances N#CC(C)(C)\N=N\C(C)(C)C#N OZAIFHULBGXAKX-VAWYXSNFSA-N 0.000 description 4
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 4
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical group [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 4
- KPUWHANPEXNPJT-UHFFFAOYSA-N disiloxane Chemical group [SiH3]O[SiH3] KPUWHANPEXNPJT-UHFFFAOYSA-N 0.000 description 4
- 235000019439 ethyl acetate Nutrition 0.000 description 4
- 150000002430 hydrocarbons Chemical group 0.000 description 4
- 239000007788 liquid Substances 0.000 description 4
- 239000000178 monomer Substances 0.000 description 4
- 229910052710 silicon Inorganic materials 0.000 description 4
- 239000000243 solution Substances 0.000 description 4
- 244000028419 Styrax benzoin Species 0.000 description 3
- 235000000126 Styrax benzoin Nutrition 0.000 description 3
- 235000008411 Sumatra benzointree Nutrition 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- 229960000583 acetic acid Drugs 0.000 description 3
- 230000032683 aging Effects 0.000 description 3
- 239000008346 aqueous phase Substances 0.000 description 3
- 239000012267 brine Substances 0.000 description 3
- 229950005499 carbon tetrachloride Drugs 0.000 description 3
- 238000001816 cooling Methods 0.000 description 3
- 238000009472 formulation Methods 0.000 description 3
- 239000012362 glacial acetic acid Substances 0.000 description 3
- 235000019382 gum benzoic Nutrition 0.000 description 3
- 230000008642 heat stress Effects 0.000 description 3
- 229920000642 polymer Polymers 0.000 description 3
- 238000002360 preparation method Methods 0.000 description 3
- 150000003254 radicals Chemical class 0.000 description 3
- 239000011541 reaction mixture Substances 0.000 description 3
- 229920002050 silicone resin Polymers 0.000 description 3
- CQLFBEKRDQMJLZ-UHFFFAOYSA-M silver acetate Chemical compound [Ag+].CC([O-])=O CQLFBEKRDQMJLZ-UHFFFAOYSA-M 0.000 description 3
- 229940071536 silver acetate Drugs 0.000 description 3
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 3
- VZGDMQKNWNREIO-UHFFFAOYSA-N tetrachloromethane Chemical compound ClC(Cl)(Cl)Cl VZGDMQKNWNREIO-UHFFFAOYSA-N 0.000 description 3
- 0 *c1c(*)c(*)c(C(P(*)(c2ccccc2)=O)=O)c(*)c1* Chemical compound *c1c(*)c(*)c(C(P(*)(c2ccccc2)=O)=O)c(*)c1* 0.000 description 2
- WHNPOQXWAMXPTA-UHFFFAOYSA-N 3-methylbut-2-enamide Chemical compound CC(C)=CC(N)=O WHNPOQXWAMXPTA-UHFFFAOYSA-N 0.000 description 2
- SFHYNDMGZXWXBU-LIMNOBDPSA-N 6-amino-2-[[(e)-(3-formylphenyl)methylideneamino]carbamoylamino]-1,3-dioxobenzo[de]isoquinoline-5,8-disulfonic acid Chemical compound O=C1C(C2=3)=CC(S(O)(=O)=O)=CC=3C(N)=C(S(O)(=O)=O)C=C2C(=O)N1NC(=O)N\N=C\C1=CC=CC(C=O)=C1 SFHYNDMGZXWXBU-LIMNOBDPSA-N 0.000 description 2
- KWOLFJPFCHCOCG-UHFFFAOYSA-N Acetophenone Chemical compound CC(=O)C1=CC=CC=C1 KWOLFJPFCHCOCG-UHFFFAOYSA-N 0.000 description 2
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 2
- BLRPTPMANUNPDV-UHFFFAOYSA-N Silane Chemical group [SiH4] BLRPTPMANUNPDV-UHFFFAOYSA-N 0.000 description 2
- 125000003118 aryl group Chemical group 0.000 description 2
- 229960002130 benzoin Drugs 0.000 description 2
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 2
- 229910052794 bromium Inorganic materials 0.000 description 2
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 2
- 239000011247 coating layer Substances 0.000 description 2
- 238000000576 coating method Methods 0.000 description 2
- 239000008393 encapsulating agent Substances 0.000 description 2
- 125000000524 functional group Chemical group 0.000 description 2
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 2
- 239000011159 matrix material Substances 0.000 description 2
- 238000005580 one pot reaction Methods 0.000 description 2
- 239000003504 photosensitizing agent Substances 0.000 description 2
- 230000008569 process Effects 0.000 description 2
- 238000010992 reflux Methods 0.000 description 2
- 239000000565 sealant Substances 0.000 description 2
- 229910000077 silane Inorganic materials 0.000 description 2
- 239000007787 solid Substances 0.000 description 2
- 239000000758 substrate Substances 0.000 description 2
- 238000002834 transmittance Methods 0.000 description 2
- 125000006273 (C1-C3) alkyl group Chemical group 0.000 description 1
- ONLFBNDNPYLPCT-UHFFFAOYSA-N 1-phosphorosoethene Chemical compound C=CP=O ONLFBNDNPYLPCT-UHFFFAOYSA-N 0.000 description 1
- XRUGBBIQLIVCSI-UHFFFAOYSA-N 2,3,4-trimethylphenol Chemical compound CC1=CC=C(O)C(C)=C1C XRUGBBIQLIVCSI-UHFFFAOYSA-N 0.000 description 1
- NIXOWILDQLNWCW-UHFFFAOYSA-M Acrylate Chemical compound [O-]C(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-M 0.000 description 1
- 239000004971 Cross linker Substances 0.000 description 1
- WOBHKFSMXKNTIM-UHFFFAOYSA-N Hydroxyethyl methacrylate Chemical compound CC(=C)C(=O)OCCO WOBHKFSMXKNTIM-UHFFFAOYSA-N 0.000 description 1
- WHNWPMSKXPGLAX-UHFFFAOYSA-N N-Vinyl-2-pyrrolidone Chemical compound C=CN1CCCC1=O WHNWPMSKXPGLAX-UHFFFAOYSA-N 0.000 description 1
- 101100084053 Neurospora crassa (strain ATCC 24698 / 74-OR23-1A / CBS 708.71 / DSM 1257 / FGSC 987) ppi-2 gene Proteins 0.000 description 1
- 230000006750 UV protection Effects 0.000 description 1
- XTXRWKRVRITETP-UHFFFAOYSA-N Vinyl acetate Chemical compound CC(=O)OC=C XTXRWKRVRITETP-UHFFFAOYSA-N 0.000 description 1
- VLEZFMLEQVGQSW-UHFFFAOYSA-N [(4-ethenylphenyl)-phenylphosphoryl]-(2,4,6-trimethylphenyl)methanone Chemical compound CC1=CC(C)=CC(C)=C1C(=O)P(=O)(C=1C=CC(C=C)=CC=1)C1=CC=CC=C1 VLEZFMLEQVGQSW-UHFFFAOYSA-N 0.000 description 1
- 150000008062 acetophenones Chemical class 0.000 description 1
- 230000002730 additional effect Effects 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 230000005540 biological transmission Effects 0.000 description 1
- 239000006227 byproduct Substances 0.000 description 1
- 125000004432 carbon atom Chemical group C* 0.000 description 1
- 239000003054 catalyst Substances 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 239000012141 concentrate Substances 0.000 description 1
- 238000009833 condensation Methods 0.000 description 1
- 230000005494 condensation Effects 0.000 description 1
- 230000018044 dehydration Effects 0.000 description 1
- 238000006297 dehydration reaction Methods 0.000 description 1
- 238000006356 dehydrogenation reaction Methods 0.000 description 1
- 238000006704 dehydrohalogenation reaction Methods 0.000 description 1
- RQLOSVWWQDTFSU-UHFFFAOYSA-N diphenylphosphoryl-(4-ethenyl-2,6-dimethylphenyl)methanone Chemical compound CC1=CC(C=C)=CC(C)=C1C(=O)P(=O)(C=1C=CC=CC=1)C1=CC=CC=C1 RQLOSVWWQDTFSU-UHFFFAOYSA-N 0.000 description 1
- VGLPAGIOBFMGJH-UHFFFAOYSA-N diphenylphosphoryl-(4-ethenylphenyl)methanone Chemical compound C1=CC(C=C)=CC=C1C(=O)P(=O)(C=1C=CC=CC=1)C1=CC=CC=C1 VGLPAGIOBFMGJH-UHFFFAOYSA-N 0.000 description 1
- 238000003683 electrophilic halogenation reaction Methods 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 230000008570 general process Effects 0.000 description 1
- 125000005843 halogen group Chemical group 0.000 description 1
- 230000003301 hydrolyzing effect Effects 0.000 description 1
- 238000006459 hydrosilylation reaction Methods 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- 125000005647 linker group Chemical group 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- QSHDDOUJBYECFT-UHFFFAOYSA-N mercury Chemical compound [Hg] QSHDDOUJBYECFT-UHFFFAOYSA-N 0.000 description 1
- 229910052753 mercury Inorganic materials 0.000 description 1
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- AUONHKJOIZSQGR-UHFFFAOYSA-N oxophosphane Chemical compound P=O AUONHKJOIZSQGR-UHFFFAOYSA-N 0.000 description 1
- 230000002165 photosensitisation Effects 0.000 description 1
- 238000006116 polymerization reaction Methods 0.000 description 1
- 230000001737 promoting effect Effects 0.000 description 1
- 238000010526 radical polymerization reaction Methods 0.000 description 1
- 238000007348 radical reaction Methods 0.000 description 1
- 229920005989 resin Polymers 0.000 description 1
- 239000011347 resin Substances 0.000 description 1
- 239000006120 scratch resistant coating Substances 0.000 description 1
- 150000004756 silanes Chemical class 0.000 description 1
- 239000010703 silicon Substances 0.000 description 1
- 150000003377 silicon compounds Chemical class 0.000 description 1
- 239000004447 silicone coating Substances 0.000 description 1
- 239000004590 silicone sealant Substances 0.000 description 1
- 150000003384 small molecules Chemical class 0.000 description 1
- 238000007655 standard test method Methods 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic System
- C07F9/02—Phosphorus compounds
- C07F9/28—Phosphorus compounds with one or more P—C bonds
- C07F9/30—Phosphinic acids R2P(=O)(OH); Thiophosphinic acids, i.e. R2P(=X)(XH) (X = S, Se)
- C07F9/32—Esters thereof
- C07F9/3205—Esters thereof the acid moiety containing a substituent or a structure which is considered as characteristic
- C07F9/3247—Esters of acids containing the structure -C(=X)-P(=X)(R)(XH) or NC-P(=X)(R)(XH), (X = O, S, Se)
- C07F9/3252—Esters of acids containing the structure -C(=X)-P(=X)(R)(XH) or NC-P(=X)(R)(XH), (X = O, S, Se) containing the structure -C(=X)-P(=X)(R)(XR), (X = O, S, Se)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic System
- C07F9/02—Phosphorus compounds
- C07F9/28—Phosphorus compounds with one or more P—C bonds
- C07F9/50—Organo-phosphines
- C07F9/53—Organo-phosphine oxides; Organo-phosphine thioxides
- C07F9/5337—Phosphine oxides or thioxides containing the structure -C(=X)-P(=X) or NC-P(=X) (X = O, S, Se)
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F2/00—Processes of polymerisation
- C08F2/46—Polymerisation initiated by wave energy or particle radiation
- C08F2/48—Polymerisation initiated by wave energy or particle radiation by ultraviolet or visible light
- C08F2/50—Polymerisation initiated by wave energy or particle radiation by ultraviolet or visible light with sensitising agents
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G77/00—Macromolecular compounds obtained by reactions forming a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon in the main chain of the macromolecule
- C08G77/04—Polysiloxanes
- C08G77/06—Preparatory processes
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G77/00—Macromolecular compounds obtained by reactions forming a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon in the main chain of the macromolecule
- C08G77/04—Polysiloxanes
- C08G77/06—Preparatory processes
- C08G77/08—Preparatory processes characterised by the catalysts used
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G77/00—Macromolecular compounds obtained by reactions forming a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon in the main chain of the macromolecule
- C08G77/04—Polysiloxanes
- C08G77/20—Polysiloxanes containing silicon bound to unsaturated aliphatic groups
Abstract
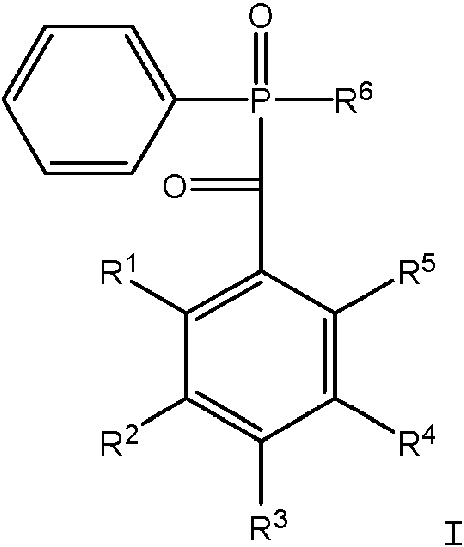
Un compuesto de la fórmula general I: **(Ver fórmula)** en la que: R1, R2, R3, R4, y R5 son iguales o diferentes y se seleccionan del grupo que consiste en SIL1-X, hidrógeno, alquilo C1- C20, alquenilo C2-C8, cicloalquilo C5-C8, fenil alquilo C1-C3 y flúor; X es opcional, y si está presente es alquilo C1-C12; SIL1 tiene la fórmula general: (R7 SiO3/2)a(R72 SiO2/2)b(R73 SiO1/2)c en la que: R7 se selecciona del grupo que consiste en alquilo C1-C20, alquenilo C2-C8, cicloalquilo C5-C8, alcoxilo, fenilo y fenil alquilo C1-C3; a es un número positivo, b es 0 o un número positivo, c es 0 o un número positivo, b/a es desde 0 hasta 100, y c/a es desde 0 hasta 10, en la que al menos uno de R1, R2, R3, R4, y R5 es SIL1-X; y R6 se selecciona del grupo que consiste en alquilo C1-C20, alquenilo C2-C8, cicloalquilo C5-C8, fenilo, fenil alquilo C1-C3 y flúor.
Description
DESCRIPCIÓN
Compuestos compatibles con silicona
Antecedentes
Campo
La presente invención se refiere a novedosos compuestos compatibles con silicona con base en una unidad estructural a-hidroxi-alquilfenona unido químicamente a una silicona, la producción de los mismos mediante un esquema de reacción simple y su uso como fotoiniciadores. Los compuestos de la invención absorben luz en el rango de luz ultravioleta más largo (UVV (es decir, longitudes de onda de aproximadamente 390 nanómetros o más), que no son absorbidas por las capas de cobertura en aplicaciones de visualización ópticamente transparentes. Los compuestos de la invención también son transparentes y altamente solubles en siliconas. Por lo tanto, los compuestos de la invención son particularmente útiles para iniciar el fotocurado de composiciones que comprenden siliconas que tienen grupos funcionales curables por radicales libres insaturados. Debido a su notable estabilidad, los compuestos de la invención no dan lugar a turbidez o amarillamiento y pueden ser utilizados, por ejemplo, en la preparación de selladores y recubrimientos de silicona ópticamente transparentes y pantallas ópticamente transparentes.
Breve descripción de la tecnología relacionada.
La polimerización fotoinducida de monómeros u oligómeros que comprenden grupos funcionales propensos a reacciones radicales es una técnica ampliamente utilizada en la producción de polímeros. Para iniciar la reacción, usualmente se añaden fotoiniciadores a los monómeros u oligómeros y la mezcla se expone luego a radiación electromagnética. Hay muchos fotoiniciadores disponibles que son fácilmente solubles en resinas orgánicas insaturadas, y los curan de manera efectiva. Sin embargo, muchos de estos fotoiniciadores tienen poca solubilidad y, por lo tanto, una efectividad de curado insatisfactoria en siliconas. Tales fotoiniciadores se separan de la matriz de silicona durante el almacenamiento, causando una turbidez severa en cualquier producto curado producido. Esto no es aceptable si los productos están destinados a ser utilizados para aplicaciones de visualización transparente óptica. Con el fin de aumentar la solubilidad y, por lo tanto, la compatibilidad con las siliconas, se ha propuesto unir químicamente los fotoiniciadores con organopolisiloxanos o silanos.
El documento Pat. U.S. 4,273,907 divulga una novedosa clase de compuestos de organopolisiloxano que comprende al menos un grupo benzoína unido químicamente a un átomo de silicio de la molécula de organopolisiloxano. Tales compuestos pueden prepararse mediante la reacción de condensación por deshidrohalogenación, deshidrogenación, deshidratación o desalcoholación entre un organopolisiloxano correspondiente que tiene átomos de halógeno unidos a silicio, átomos de hidrógeno, grupos hidroxilo o grupos alcoxi y un compuesto de benzoína en presencia de un promotor de reacción adecuado o un catalizador de condensación. Son solubles en composiciones de silicona y útiles como fotosensibilizadores en composiciones de organopolisiloxano fotocurables. Sin embargo, los compuestos no muestran suficiente estabilidad y tienden a amarillear tras la exposición al calor y/o radiación UV durante un período más largo. Por lo tanto, no son adecuados para ser utilizados en recubrimientos transparentes, encapsulantes o selladores de alto rendimiento.
El documento U.S. Pat. 4,391,963 también divulga novedosos fotosensibilizadores, que son compuestos de organopolisiloxano que portan al menos un grupo de benzoína unido químicamente. Aquí, sin embargo, los compuestos se preparan por hidrosililación de una benzoína sustituida con alquenilo y un compuesto de silicio que contiene al menos un átomo de hidrógeno unido a silicio. Por lo tanto, la unidad estructural organopolisiloxano y el grupo benzoína están unidos mediante un grupo hidrocarburo divalente. Esto da como resultado una mayor estabilidad frente a la hidrólisis, sin embargo, requiere un proceso de preparación comparativamente elaborado ya que las benzoínas sustituidas con alquenilo no están fácilmente disponibles, pero tienen que ser sintetizadas en una etapa de reacción separada.
El documento U.S. Pat. 4,536,265 también divulga fotoiniciadores de organopolisiloxano. Al menos una unidad de siloxano por molécula comprende una unidad estructural de foto acetofenona unida al átomo de silicio de la unidad de siloxano a través de un grupo hidrocarburo divalente que tiene entre 2 y 10 átomos de carbono. Tal grupo de unión muestra una alta estabilidad frente a la hidrólisis. Sin embargo, las acetofenonas sustituidas con alquenilo no están disponibles fácilmente, pero deben ser sintetizadas en una etapa de reacción separada, haciendo que el proceso general para producir el fotoiniciador de organopolisiloxano sea complejo. Además, las unidades estructurales de acetofenona tienden a amarillear tras la exposición al calor y/o la radiación UV durante un período más prolongado.
De Groot et al. Hydrophilic Polymeric Acylphospine Oxide Photoinitiators/Crosslinkers for in Vivo Blue-Light Photopolymerization, Biomacromolecules, US, (20011201), Vol. 2, No. 4 describe la síntesis de tres monómeros fotoiniciadores de óxido de fosfina funcionalizados con vinilo: óxido de 4-vinilbenzoildifenilfosfina (VBPO); Óxido de 2,6-dimetil-4-vinilbenzoildifenilfosfina (DMVBPO); y óxido de 2,4,6-trimetilbenzoilfenil-4-vinilfenilfosfina (TMBVPO). De estos monómeros, VBPO se copolimerizó con vinilpirrolidona o acetato de vinilo (polímero PPI-1a) y dimetilacrilamida (PPI-1b). DMVBPO y TMBVPO fueron ambos copolimerizados con dimetilacrilamida (PPI-2 y PPI-3, respectivamente).
Se demostró que la selección de óxido de vinilfosfina y comonómeros tiene una influencia significativa en las propiedades de los polímeros resultantes y su estabilidad tanto en solución acuosa como en solución en metacrilato de 2-hidroxietilo (HEMA).
El documento U.S. Pat. 5,776,658 describe fotoiniciadores compatibles con silicona que comprenden un residuo de silano u organopolisiloxano que porta un radical químicamente unido de un compuesto que tiene una o más de una actividad fotoiniciadora o fotosensibilizadora y que tiene al menos un grupo carbonilo ubicado en un núcleo aromático. Nuevamente, la unión del residuo de silano u organopolisiloxano y la unidad fotounidad estructural se efectúa mediante un grupo hidrocarburo divalente. Este grupo hidrocarburo divalente está unido a un átomo de carbono aromático que está posicionado orto al grupo carbonilo de la fotounidad estructural. Los fotoiniciadores muestran buena estabilidad frente a la hidrólisis. Los ejemplos divulgan la preparación de los fotoiniciadores mediante una reacción de un recipiente. Sin embargo, la mezcla de producto resultante necesita ser concentrada y elaborada por cromatografía. Por lo tanto, el proceso general es complejo y requiere mucho tiempo. Además, los rendimientos del fotoiniciador son bastante bajos, por ejemplo solo el 17 % en el ejemplo 5.
El documento EP 1072326 A2 proporciona fotoiniciadores con actividad de superficie que contienen siloxano que se concentran en la superficie de la formulación. Estos fotoiniciadores se utilizan en un método para producir recubrimientos resistentes a los rasguños a partir de formulaciones que contienen compuestos etilénicos. La fotounidad estructural comprende un anillo aromático que está enlazado a través de una unidad puente (Y) a un átomo de silicio del residuo de siloxano. Debido a las propiedades con actividad de superficie de estos fotoiniciadores, no se distribuirán de manera homogénea en toda la formulación y, por lo tanto, no son adecuados para recubrimientos, encapsulantes o selladores transparentes de alto rendimiento.
La publicación de la Solicitud de Patente U.S. 2015/0266907 proporciona fotoiniciadores compatibles con silicona que se producen a partir de materiales de partida fácilmente disponibles a través de una simple reacción en una sola etapa. Estos fotoiniciadores son altamente solubles en siliconas fotocurables y estables contra el estrés térmico, la radiación UV y la hidrólisis para evitar el amarillamiento de cualquier producto curado. Sin embargo, estos fotoiniciadores absorben la luz en el rango más corto de luz ultravioleta (es decir, longitudes de onda inferiores a 390 nanómetros). Las capas de recubrimiento de pantallas ópticamente transparentes pueden interferir con la transmisión de estas longitudes de onda más cortas al silicio fotocurable que se encuentra entre las capas de recubrimiento. Por consiguiente, estos fotoiniciadores pueden ser menos efectivos para promover el curado de siliconas fotocurables cuando se usan en aplicaciones de visualización ópticamente transparentes.
Sería ventajoso fabricar y usar compuestos que sean claros y altamente solubles en siliconas fotocurables y estables contra el estrés térmico, la radiación UV y la hidrólisis para evitar el turbidez y el amarillamiento del producto curado, y para los cuales las longitudes de onda ultravioleta de aproximadamente 390 nanómetros o más son efectivas en la iniciación del curado de las siliconas fotocurables.
Resumen
La presente invención proporciona novedosos compuestos, que pueden actuar como fotoiniciadores compatibles con silicona, accesibles desde materiales de partida fácilmente disponibles a través de un esquema de reacción simple. Son transparentes y altamente solubles en siliconas fotocurables y estables contra el estrés térmico, la radiación UV y la hidrólisis para evitar la turbidez y el amarillamiento de cualquier producto curado, incluidos tales fotoiniciadores. Además, los compuestos de la invención no producen subproductos de moléculas pequeñas durante el curado debido a la inclusión de las cadenas laterales de silicona. Por lo tanto, los compuestos de la invención no contribuyen a la turbidez y al amarillamiento del producto curado. Tales compuestos son particularmente útiles, por ejemplo, como fotoiniciadores en la producción de pantallas ópticamente transparentes.
Las capas de cobertura de las pantallas ópticamente transparentes a menudo absorben longitudes de onda más cortas de luz ultravioleta (es decir, longitudes de onda inferiores a 390 nanómetros). Sin embargo, los novedosos compuestos compatibles con silicona de la presente invención absorben longitudes de onda más largas de luz ultravioleta (UVV) (es decir, longitudes de onda de aproximadamente 390 nanómetros o más). Por consiguiente, esta propiedad adicional hace que los compuestos de la presente invención sean particularmente útiles como fotoiniciadores en la producción de pantallas ópticamente transparentes.
Los inventores encontraron que los compuestos específicos con base en unidades estructurales de foto ahidroxialquilfenl unidas en el grupo fenilo a una cadena lateral de silicona proporcionan las propiedades deseadas.
En un aspecto de la invención, se proporciona un compuesto representado por la siguiente Fórmula I:
en la que:
R1, R2 , R3 , R4 , y R5 son iguales o diferentes y se seleccionan del grupo que consiste en SILi -X, hidrógeno, alquilo Ci -C20 , alquenilo C2-C8 , cicloalquilo C5-C8 , fenil alquilo C1-C3 y flúor;
X es opcional, y si está presente es alquilo C1-C12;
SIL1 tiene la fórmula general:
(R7 SiO3/2)a (R72 SiO2/2)b(R73 SiO1/2)c
en la que:
R7 se selecciona del grupo que consiste en alquilo C1-C20, alquenilo C2-C8 , cicloalquilo C5-C8 , alcoxilo, fenilo y fenil alquilo C1-C3 ;
a es un número positivo,
b es 0 o un número positivo,
c es 0 o un número positivo,
b/a es desde 0 hasta 100, y
c/a es desde 0 hasta 10,
en la que al menos uno de R1, R2 , R3 , R4 , y R5 es SIL1-X; y
R6 se selecciona del grupo que consiste en alquilo C1-C20, alquenilo C2-C8 , cicloalquilo C5-C8 , fenilo, fenil alquilo C1-C3 y flúor.
En otro aspecto de la invención, se proporciona un método para sintetizar un compuesto representado por la siguiente Fórmula I:
en la que:
R1, R2 , R3 , R4 , y R5 son iguales o diferentes y se seleccionan del grupo que consiste en SIL1-X, hidrógeno, alquilo C1-C20 , alquenilo C2-C8 , cicloalquilo C-5-C8 , fenil alquilo C1-C3 y flúor;
X es opcional, y si está presente es alquilo C1-C12;
SIL1 tiene la fórmula general:
(R7 SiO3/2)a (R72 SiO2/2)b(R73 SiO1/2)c
en la que:
R7 se selecciona del grupo que consiste en alquilo C1-C20 , alquenilo C2-C8 , cicloalquilo C5-C8 , alcoxilo y fenil alquilo C1-C3 ;
a es un número positivo,
b es 0 o un número positivo,
c es 0 o un número positivo,
b/a es desde 0 hasta 100, y
c/a es desde 0 hasta 10,
en la que al menos uno de R1, R2 , R3 , R4 , y R5 es SIL1-X; y R6 se selecciona del grupo que consiste en alquilo C1-C20, alquenilo C2-C8 , cicloalquilo C5-C8 , fenilo, fenil alquilo C1-C3 , y flúor,
que comprende las etapas de:
1) Activar un compuesto de Fórmula A:
en la que R1, R2 , R3 , R4 , y R5 son como más arriba, pero ninguno puede ser SIL1-X,
para producir un compuesto de Fórmula B:
2) Someter el compuesto de Fórmula B a una reacción de sustitución de acetato nucleofílico para producir un compuesto de Fórmula C:
3) Someter el compuesto de Fórmula C a una reacción de hidrólisis. para producir un compuesto de Fórmula D:
y
4) Someter el compuesto de Fórmula D a una reacción de condensación con un compuesto que tiene la fórmula SIL1-X-Cl o SIL1-X-H para producir el compuesto de Fórmula 1.
En un aspecto adicional de la invención, se proporciona una composición que comprende:
a) aproximadamente 70 hasta aproximadamente 99.9 por ciento en peso de una silicona fotocurable; y
b) aproximadamente 0.1 hasta aproximadamente 10.0 por ciento en peso de un compuesto representado por la siguiente fórmula I:
en la que:
R1, R2 , R3 , R4 , y R5 son iguales o diferentes y se seleccionan del grupo que consiste en SIL1-X, hidrógeno, alquilo C1-C20 , alquenilo C2-C8 , cicloalquilo C5-C8 , fenil alquilo C1-C3 y flúor;
X es opcional, y si está presente es alquilo C1-C12;
SIL1 tiene la fórmula general:
(R7 SÍO3/2)a (R72 SÍO2/2) b(R73 SiOl /2)c
en la que:
R7 se selecciona del grupo que consiste en alquilo C1-C20, alquenilo C2-C8 , cicloalquilo C5-C8 , alcoxilo, fenilo y fenil alquilo C1-C3 ;
a es un número positivo,
b es 0 o un número positivo,
c es 0 o un número positivo,
b/a es desde 0 hasta 100, y
c/a es desde 0 hasta 10,
en la que al menos uno de R1, R2 , R3 , R4 , y R5 es SIL1-X; y
R6 se selecciona del grupo que consiste en alquilo C1-C20, alquenilo C2-C8 , cicloalquilo C-5-C8 , fenilo, fenil alquilo C1-C3 y flúor.
En otro aspecto de la invención, se proporciona un método para fabricar un producto de polímero de silicona, que comprende las etapas de:
A) Proporcionar una composición de silicona fotocurable que comprende:
i) aproximadamente 70 hasta aproximadamente 99.9 por ciento en peso de una silicona fotocurable; y
ii) aproximadamente 0.1 hasta aproximadamente 10.0 por ciento en peso de un compuesto representado por la siguiente fórmula I:
en la que:
R1, R2 , R3 , R4 , y R5 son iguales o diferentes y se seleccionan del grupo que consiste en SIL1-X, hidrógeno, alquilo C1-C20 , alquenilo C2-C8 , cicloalquilo C5-C8 , fenil alquilo C1-C3 y flúor;
X es opcional, y si está presente es alquilo C1-C12;
SIL1 tiene la fórmula general:
(R7 SiO3/2)a (R72 SiO2/2)b(R73 SiO1/2)c
en la que:
R7 se selecciona del grupo que consiste en alquilo C1-C20, alquenilo C2-C8 , cicloalquilo C5-C8 , alcoxilo, fenilo y fenil alquilo C1-C3 ;
a es un número positivo,
b es 0 o un número positivo,
c es 0 o un número positivo,
b/a es desde 0 hasta 100, y
c/a es desde 0 hasta 10,
en la que al menos uno de R1, R2, R3, R4, y R5 es SIL1-X; y
R6 se selecciona del grupo que consiste en alquilo C1-C20, alquenilo C2-C8 , cicloalquilo C5-C8 , fenilo, fenil alquilo C1-C3 , y flúor; y
B) Exponer la composición de silicona fotocurable a radiación ultravioleta o luz visible para iniciar el fotocurado de la composición de silicona fotocurable para producir el producto de polímero de silicona.
Descripción detallada
Los compuestos de acuerdo con la invención pueden usarse como fotoiniciadores y son particularmente efectivos si se usan en composiciones basadas en siliconas fotocurables.
El grupo SIL1-X en el compuesto de la presente invención está representado por la fórmula:
(R7 SiO3/2)a (R72 SiO2/2)b(R73 SiO1/2)c
en la que R7 es un grupo alquilo C1-C20 , alquenilo C2-C8 , cicloalquilo C5-C8 , alcoxilo, fenilo o fenil alquilo C1-C3. Además, a es un número positivo, b es 0 o un número positivo, c es 0 o un número positivo, b/a es desde 0 hasta 100, y c/a es desde 0 hasta 10. X es opcional, y si está presente es un grupo alquilo C1-C12.
Preferiblemente, X no está presente, R7 es un grupo metilo o un grupo metoxi, a es 1, b es 0 y c es 2 o 3.
Los compuestos de la presente invención pueden contener hasta 5 grupos SIL1-X, uno cada uno en R1 a R5. Preferiblemente, los compuestos de la presente invención contienen 1,2 o 3 grupos SIL1-X en uno o más de R1, R2 o R3. En una realización, los compuestos de la presente invención contienen un solo grupo SIL1-X en R3. Preferiblemente, si no está ocupado por un grupo SIL1-X, R1 y R5 son grupos metilo y R2 y R4 son hidrógeno.
Los compuestos de acuerdo con la invención muestran propiedades ventajosas si R3 es SIL1-X y el SIL1-X es:
R1 y R5 son grupos metilo, y R2 y R4 son hidrógeno.
R6 es un grupo alquilo C1-C20 , un grupo alquenilo C2-C8 , un grupo cicloalquilo C5-C8 , un grupo fenilo, un grupo fenil alquilo C1-C3 , un grupo trimetilfenol o flúor. Preferiblemente, R6 es un grupo fenilo, grupo CH3CH2O.
Los compuestos de acuerdo con la invención muestran propiedades particularmente ventajosas si R3 es SIL1-X y el SIL1-X es:
R1 y R5 son grupos metilo, R2 y R4 son hidrógeno, y R6 es un grupo fenilo, grupo CH3CH2O.
Preferiblemente, el compuesto de la presente invención es uno de los siguientes:
Estos compuestos pueden emplearse solos o en combinación en las composiciones y métodos de la presente invención.
Los compuestos de la presente invención pueden sintetizarse a través de un proceso de cuatro etapas personalizables para permitir la diversidad en los posibles fotoiniciadores compatibles con silicona que pueden producirse. Las cuatro etapas de la síntesis pueden describirse generalmente de la siguiente manera:
Etapa 1) El grupo fenilo del material de partida de a-hidroxi-alquilfenona se activa mediante la adición de un bromo al grupo fenilo mediante halogenación electrofílica;
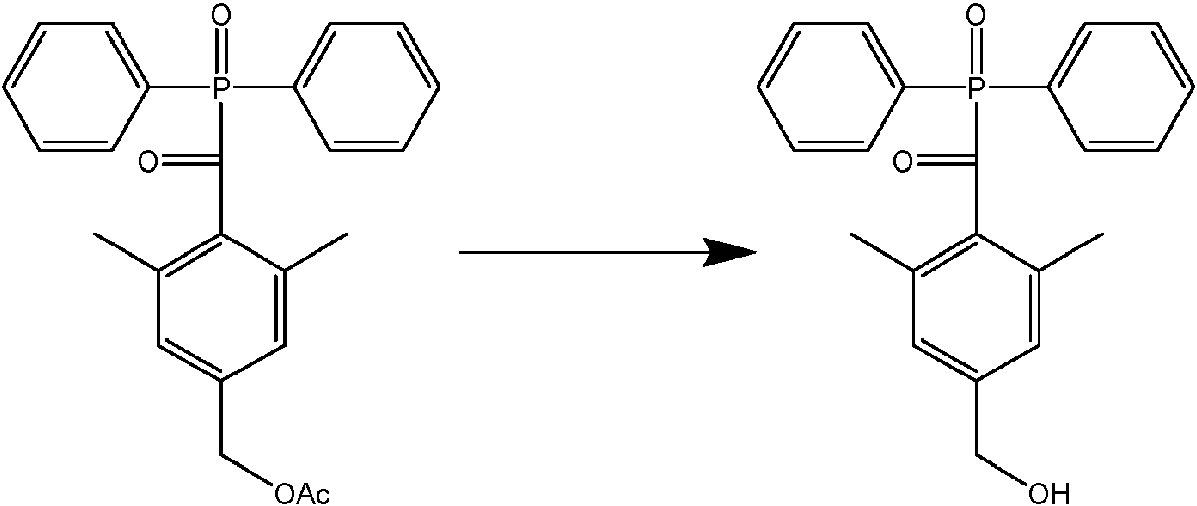
Etapa 2) El bromo se sustituye luego con acetato mediante una reacción de sustitución de acetato nucleofílico; Etapa 3) El acetato se hidroliza luego a un grupo hidroxi a través de una reacción de hidrólisis; y
Etapa 4) La cadena lateral de silicona se une luego al grupo fenilo de la a-hidroxi-alquilfenona a través de una reacción de condensación para producir el compuesto de la invención.
El esquema de reacción para la síntesis de los compuestos de la presente invención se puede representar generalmente como sigue:
ETAPA 1
NBS, AIBN
CCI4,
THF
DMAP Imidizol
CH2CI Cadena lateral de silicona Cl
Compuesto de la invención
Los parámetros generales preferidos para la síntesis de los compuestos de la presente invención se muestran en la Tabla 1.
Tabla 1
De manera deseable, los materiales de partida para la síntesis de los compuestos de la presente invención son las ahidroxialquilfenonas, cuyos ejemplos pueden estar representados por el compuesto de Fórmula A:
en la que R1, R2 , R3 , R4 y R5 son los mismos que en los compuestos de la presente invención (como se describe anteriormente), pero ninguno puede ser SIL1-X, y R6 es el mismo que en los compuestos de la presente invención . Preferiblemente, R1, R2 , R3 , R4 y R5 son independientemente grupos hidrógeno o metilo. En los materiales de partida preferidos R1, R3 y R5 son grupos metilo y R2 y R4 son hidrógeno. Preferiblemente, R6 es un grupo fenilo o un grupo CH3CH2O - en el material de partida.
Los materiales de partida preferidos incluyen los siguientes compuestos:
Un aspecto adicional de la invención es el uso de estos compuestos como fotoiniciadores. Un aspecto particular de la invención es un método para usar los compuestos de acuerdo con la invención como fotoiniciadores que incluyen las etapas de mezclar el compuesto con una silicona fotocurable, tal como un organopolisiloxano o resina de silicona fotopolimerizables, y exponer la mezcla resultante a radiación electromagnética.
Aunque no existe una limitación particular con respecto a la silicona fotocurable, se prefiere agregar el compuesto de acuerdo con la invención a una composición con base solamente o predominantemente en (met)acriloxisiloxanos, por ejemplo, polidimetilsiloxano terminado en silanol protegido en el extremo con (met)acrílico, ya que fotocurar tales mezclas da como resultado productos que tienen un grado de turbidez de menos de aproximadamente 2, preferiblemente menos de aproximadamente 1, un grado de amarillamiento de menos de aproximadamente 2,
preferiblemente menos de aproximadamente 1, y muestran muy buena estabilidad térmica, hidrolítica y UV. Preferiblemente, la silicona fotocurable es un organopolisiloxano o resina de silicona, una silicona protegida en el extremo con (met)acrílico, un (met)acriloxisiloxano, o un polidimetilsiloxano terminado en silanol protegido en el extremo con (met)acrílico.
La radiación electromagnética útil es cualquier radiación que provocará la formación de radicales y, por lo tanto, comenzará la polimerización por radicales libres de la silicona fotocurable. Un ejemplo de tal radiación electromagnética es la radiación UVV (luz ultravioleta a longitudes de onda de aproximadamente 390 nanómetros o más).
Un aspecto adicional de la invención es una composición que comprende: a) al menos una silicona fotocurable y b) un compuesto de acuerdo con la invención. Preferiblemente, la silicona fotocurable es un organopolisiloxano o resina de silicona, una silicona protegida en el extremo con (met)acrílico, un (met)acriloxisiloxano, o un polidimetilsiloxano terminado en silanol protegido en el extremo con (met)acrílico. Las siliconas fotocurables preferidas incluyen organosiliconas curables por ultravioleta y siliconas de curado dual por ultravioleta y humedad.
La cantidad del compuesto de acuerdo con la invención en tales composiciones puede variar dentro de amplios límites. Preferiblemente, la composición de la invención comprende el compuesto de acuerdo con la invención o una mezcla de varios compuestos de acuerdo con la invención en una cantidad total de 0.1 a 30 % en peso, preferiblemente de 0.2 a 15 % en peso, más preferiblemente de 0.5 a 10 % en peso, con base en el peso de la composición. El resto generalmente consiste solamente o predominantemente en la silicona fotocurable.
Aún otro aspecto de la invención es el método de hacer un producto de polímero de silicona exponiendo una composición que incluye a) al menos una silicona fotocurable y b) un compuesto de acuerdo con la invención para radiación electromagnética para iniciar el fotocurado para producir el producto de polímero de silicona. Preferiblemente, la radiación electromagnética es radiación UVV (luz ultravioleta a longitudes de onda de aproximadamente 390 nanómetros o más), más preferiblemente radiación ultravioleta a una longitud de onda de aproximadamente 405 nanómetros.
En realizaciones preferidas, el método para fabricar un producto de polímero de silicona incluye la etapa adicional de colocar la composición de silicona fotocurable en contacto con al menos una capa de una composición ópticamente transparente antes del inicio del fotocurado. Por lo tanto, cuando la composición de silicona fotocurable se cura, el producto de polímero de silicona es adecuado para su uso en una pantalla ópticamente transparente. Preferiblemente, el método para fabricar un producto de polímero de silicona de la invención incluye la etapa de colocar la composición de silicona fotocurable entre dos capas de una composición ópticamente transparente antes del inicio del fotocurado.
Las composiciones ópticamente transparentes para su uso en los métodos de la invención incluyen cualquier material que proporcione una transmitancia de luz visible mayor que aproximadamente 95 %, preferiblemente mayor que aproximadamente 98 %, incluso más preferiblemente mayor que aproximadamente 99 %. Preferiblemente, la composición ópticamente transparente es vidrio.
Preferiblemente, los productos poliméricos de la invención exhiben una claridad excelente y mantienen tal claridad incluso ante largos períodos de envejecimiento. Preferiblemente, los productos de polímero de silicona de la invención tienen un valor de turbidez de aproximadamente 2 o menos, más preferiblemente de aproximadamente 1 o menos, y un valor de amarillez de aproximadamente 2 o menos, más preferiblemente de aproximadamente 1 o menos, en un espacio de 750 micrómetros entre capas de composición ópticamente transparente, cuando se envejecen durante 500 horas en una máquina de prueba QUV o cuando se envejecen durante 500 horas en un horno a 85 °C y 85 % de humedad relativa. Preferiblemente, los productos de polímero de silicona de la invención proporcionan una transmitancia de luz visible mayor que aproximadamente 95 %, preferiblemente mayor que aproximadamente 98 %, incluso más preferiblemente mayor que aproximadamente 99 %.
A continuación se muestra una descripción de aspectos particulares de la presente invención utilizando una serie de ejemplos, sin embargo, la presente invención no se limita de ninguna manera a los ejemplos presentados a continuación.
Ejemplos
Ejemplo de síntesis 1
Etapa 1:
Se cargó una mezcla de Darocur TPO (17.5 g, 50.3 mmol), N-bromosuccinimida (12.5 g, 70.4 mmol), AIBN (201 mg) y tetraclorometano (100 ml) en un matraz de tres cuellos de 250 ml y se sometió a reflujo a 80 °C durante 5 horas bajo argón. La mezcla de reacción se filtró después de enfriar. El filtrado se evaporó para obtener un producto crudo. Etapa 2:
Una mezcla del producto crudo de la Etapa 1 (sin purificación adicional), acetato de plata (10.07 g, 60.35 mmol) y 150 ml de ácido acético glacial se cargó en un matraz de tres cuellos de 500 ml y se sometió a reflujo a 100 °C durante 3 horas bajo argón. La mezcla se filtró y se añadieron 500 ml de agua al filtrado. La mezcla resultante se extrajo con CH2Cl2 (50 ml) 3 veces. La capa orgánica combinada se lavó con 50 ml de agua, se secó sobre Na2SO4 anhidro, y el disolvente se eliminó bajo presión reducida. El producto crudo se purificó por cromatografía en columna (50 % EtOAc en hexano) para producir 7.4 g de compuesto intermedio (36 % de rendimiento para las Etapas 1 y 2 combinadas). Etapa 3:
Se cargó una mezcla del intermedio purificado de la Etapa 2 (7.4 g, 18.2 mmol), THF (44 ml), HCl (10.5 ml) y agua (52 ml) en un matraz de tres bocas de 250 ml y se sometió a reflujo a 80 °C durante la noche bajo argón. El THF se eliminó bajo presión reducida y se añadieron 15 ml de agua. La mezcla resultante se extrajo con CH2Cl2 (30 ml) 3 veces. La capa orgánica combinada se lavó con 10 ml de agua. La capa orgánica se secó sobre Na2SO4 anhidro, y el disolvente se evaporó. Este producto crudo (9.1 g, sólido amarillo) se usó en la siguiente etapa sin purificación adicional.
Etapa 4:
Una solución del producto crudo de la Etapa 3 (9 g, 24.7 mmol), imidazol (3.36 g, 49.4 mmol) y DMAP (40 mg) en CH2CI2 (100 ml) se cargó en un matraz de tres cuellos de 250 ml y se añadió ClSi (CH3SiO)39.82 g, 29.63 mmol). La mezcla se agitó a temperatura ambiente durante la noche bajo argón. La reacción se detuvo mediante la adición de agua. La fase acuosa se extrajo con CH2Cl2 (20 ml) 3 veces. La fase orgánica combinada se lavó con agua y salmuera. La fase orgánica se secó con Mg2SO4 anhidro. Después de eliminar el disolvente bajo presión reducida, el residuo se purificó por cromatografía en columna para producir 10.98 g del compuesto de la invención (rendimiento del 67 %, sólido de color amarillo claro).
Ejemplo de síntesis 2
Etapa 1:
Una mezcla del Compuesto A2 (arriba) (12.65 g, 40.0 mmol), N-bromosuccinimida (8.54 g, 48.0 mmol), AIBN (160.0 mg) y tetraclorometano (80 ml) se cargó en un matraz de tres cuellos de 250 ml y se sometió a reflujo a 80 °C durante 5 horas bajo argón. La mezcla de reacción se filtró después de enfriar. El filtrado se evaporó para obtener un producto crudo.
Etapa 2:
Una mezcla del producto crudo de la Etapa 1 (sin purificación adicional), acetato de plata (8.01 g, 48.0 mmol) y 100 ml de ácido acético glacial se cargó en un matraz de tres cuellos de 250 ml y se sometió a reflujo a 120 °C durante 3 horas bajo argón La mezcla se filtró y se añadieron 500 ml de agua al filtrado. La mezcla resultante se extrajo con CH2Cl2 (50 ml) 3 veces. La capa orgánica combinada se lavó con 50 ml de agua, se secó sobre Na2SO4 anhidro, y el disolvente se eliminó bajo presión reducida. El producto crudo se purificó por cromatografía en columna (50 % EtOAc en hexano) para producir 6.18 g de compuesto intermedio (41 % de rendimiento para las Etapas 1 y 2 combinadas). Etapa 3:
Se cargó una mezcla del intermedio purificado de la Etapa 2 (6.18 g, 16.5 mmol), THF (40 ml), HCl (9.5 ml) y agua (47 ml) en un matraz de tres cuellos de 250 ml y se sometió a reflujo a 80 °C durante la noche bajo argón. El THF se eliminó bajo presión reducida y se añadieron 15 ml de agua. La mezcla resultante se extrajo con CH2Cl2 (30 ml) 3 veces. La capa orgánica combinada se lavó con 10 ml de agua. La capa orgánica se secó sobre Na2SO4 anhidro, y el disolvente se evaporó. Este producto crudo (4.8 g, líquido amarillo) se usó en la siguiente etapa sin purificación adicional.
Etapa 4:
Una solución del producto crudo de la Etapa 3, imidazol (2.24 g 33.5 mmol), DMAP (25 mg) en CH2Cl2 (60 ml) se cargó en un matraz de tres bocas de 250 ml y se añadió ClSi (CH3SiO)3 (8.2 g, 27.4 mmol). La mezcla se agitó a temperatura ambiente durante la noche bajo argón. La reacción se detuvo mediante la adición de agua. La fase acuosa se extrajo con CH2Cl2 (20 ml) 3 veces. La fase orgánica combinada se lavó con agua y salmuera. La fase orgánica se secó con Mg2SO4 anhidro. Después de la eliminación del disolvente bajo presión reducida, el residuo se purificó por cromatografía en columna (EtOAc al 20 % en hexano) para producir 4.76 g del compuesto de la invención (rendimiento del 45 %, líquido de color amarillo claro).
Ejemplo de síntesis 3
Etapa 1:
Una mezcla de Compuesto A2 (arriba) (12.65 g, 40.0 mmol), N-bromosuccinimida (8.54 g, 48.0 mmol), AIBN (160.0 mg) y tetraclorometano (80 ml) se cargó en un matraz de tres cuellos de 250 ml y a reflujo a 80 °C durante 5 horas bajo argón. La mezcla de reacción se filtró después de enfriar. El filtrado se evaporó para obtener un producto crudo. Etapa 2:
Una mezcla del producto crudo de la Etapa 1 (sin purificación adicional), acetato de plata (8.01 g, 48.0 mmol) y 100 ml de ácido acético glacial se cargó en un matraz de tres cuellos de 250 ml y se sometió a reflujo a 120 °C durante 3 horas bajo argón. La mezcla se filtró y se añadieron 500 ml de agua al filtrado. La mezcla resultante se extrajo con CH2Cl2 (50 ml) 3 veces. La capa orgánica combinada se lavó con 50 ml de agua, se secó sobre Na2SO4 anhidro, y el disolvente se eliminó bajo presión reducida. El producto crudo se purificó por cromatografía en columna (50 % EtOAc en hexano) para producir 6.18 g de compuesto intermedio (41 % de rendimiento para las Etapas 1 y 2 combinadas). Etapa 3:
Se cargó una mezcla del intermedio purificado de la Etapa 2 (6.18 g, 16.5 mmol), THF (40 ml), HCl (9.5 ml) y agua (47 ml) en un matraz de tres cuellos de 250 ml y se sometió a reflujo a 80 °C durante la noche bajo argón. El THF se eliminó bajo presión reducida y se añadieron 15 ml de agua. La mezcla resultante se extrajo con CH2Cl2 (30 ml) 3 veces. La capa orgánica combinada se lavó con 10 ml de agua. La capa orgánica se secó sobre Na2SO4 anhidro, y el disolvente se evaporó. Este producto crudo (4.8 g, líquido de color amarillo) se usó en la siguiente etapa sin purificación adicional.
Etapa 4:
Una solución del producto crudo de la Etapa 3 (3.0 g, 9.0mmol), imidazol (1.36 g, 20.0mmol) y DMAP (20 mg) en tolueno (40 ml) se cargó en un matraz de tres cuellos de 250 ml y se añadió (CH3SiO)2SiCH3H (18.0mmol). La mezcla se agitó a temperatura ambiente durante la noche bajo argón. La reacción se detuvo mediante la adición de agua (30 ml). La fase acuosa se extrajo con CH2Cl2 (30 ml) 3 veces. La fase orgánica combinada se lavó con agua y salmuera. La fase orgánica se secó con Mg2SO4 anhidro. Después de eliminar el disolvente bajo presión reducida, el residuo se purificó por cromatografía en columna (PE: EA = 5: 1) para producir 3.55 g del compuesto de la invención (71 % de rendimiento, líquido de color amarillo claro).
Ejemplo 4
Evaluación de fotoiniciadores
Los compuestos de los Ejemplos 2 y 3 anteriores y fotoiniciadores comparativos Darocur TPO y SPI-7 se evaluaron para determinar la fuente de inicio de curado aplicable, resistencia a los rayos UV, propiedades anti-amarillento y antiturbidez. Darocur TPO es un fotoiniciador que se sabe que se usa con radiación UVV para curado. SPI-7 es un fotoiniciador UVA sustituido con silicona. La estructura de cada uno de los compuestos se muestra a continuación. Compuesto del Ejemplo 2:
Compuesto del Ejemplo 3:
Darocur TPO:
SPI-7:
El sustrato utilizado fue matriz de silicona de acrilato (15MDMA: 60DMA = 6.4). Los fotoiniciadores se mezclaron cada uno por separado con el sustrato. Estas mezclas se colocaron luego entre 2 capas de vidrio separadas por 750 micrómetros y expuestas a la luz ultravioleta. El inicio del curado se evaluó con radiación UV utilizando la cámara UV del Sistema de arco de mercurio de presión media (MPMA) durante 30 segundos a 75 mW/cm2 dos veces para producir el curado. Por separado, el inicio del curado también se evaluó utilizando una fuente de luz LED de 405 nanómetros. Después del curado, las muestras se envejecieron en una máquina de prueba QUV durante 500 horas. Después del envejecimiento, se midieron la turbidez y el amarillamiento de cada muestra utilizando un aparato Datacolor 650, disponible de Datacolor Corporation, de conformidad con el Método de prueba estándar ASTM D1003.
Las fuentes de luz capaces de iniciar el curado y los resultados para la turbidez y el amarillamiento se informan en la Tabla 2.
Tabla 2
Los valores de turbidez y amarillamiento se determinaron a una brecha de 750 micrómetros. Los valores de turbidez y amarillamiento de aproximadamente 2 o menos se consideraron aceptables, y los valores de aproximadamente 1 o menos se consideraron excelentes.
Con base en los resultados informados en la Tabla 2, solamente los compuestos de la invención produjeron valores aceptables de turbidez y amarillamiento y pudieron iniciar el curado usando luz ultravioleta de 405 nm. El compuesto del Ejemplo 2 mostró valores excelentes tanto para la turbidez como para el amarillamiento. Darocur TPO, que está libre de cadenas laterales de silicona, produjo una turbidez inaceptable al envejecer, y el curado no pudo iniciarse utilizando luz ultravioleta de 405 nm con SPI-7.
Claims (15)
1. Un compuesto de la fórmula general I:
en la que:
R1, R2 , R3 , R4 , y R5 son iguales o diferentes y se seleccionan del grupo que consiste en SIL1-X, hidrógeno, alquilo C1-C20 , alquenilo C2-C8 , cicloalquilo C5-C8 , fenil alquilo C1-C3 y flúor;
X es opcional, y si está presente es alquilo C1-C12;
SIL1 tiene la fórmula general:
(R7 SiO3/2)a (R72 SiO2/2)b(R73 SiO1/2)c
en la que:
R7 se selecciona del grupo que consiste en alquilo C1-C20, alquenilo C2-C8 , cicloalquilo C5-C8 , alcoxilo, fenilo y fenil alquilo C1-C3 ;
a es un número positivo,
b es 0 o un número positivo,
c es 0 o un número positivo,
b/a es desde 0 hasta 100, y
c/a es desde 0 hasta 10,
en la que al menos uno de R1, R2 , R3 , R4 , y R5 es SIL1-X; y
R6 se selecciona del grupo que consiste en alquilo C1-C20, alquenilo C2-C8 , cicloalquilo C5-C8 , fenilo, fenil alquilo C1-C3 y flúor.
2. El compuesto de acuerdo con la reivindicación 1, en el que R3 es SIL1-X y el SIL1-X es:
en la que R1 y R5 son preferiblemente grupos metilo y R2 y R4 son hidrógeno, y, en donde R6 se selecciona preferiblemente del grupo que consiste en un grupo fenilo y un grupo CH3CH2O-.
3. Un compuesto seleccionado del grupo que consiste en:
y combinaciones del mismo.
4. Un método para sintetizar un compuesto de la fórmula general I:
en la que:
R1, R2 , R3 , R4 , y R5 son iguales o diferentes y se seleccionan del grupo que consiste en SIL1-X, hidrógeno, alquilo C1-C20 , alquenilo C2-C8 , cicloalquilo C5-C8 , fenil alquilo C1-C3 y flúor;
X es opcional, y si está presente es alquilo C1-C12;
SIL1 tiene la fórmula general:
(R7 SiO3/2)a(R72 SiO2/2)b(R73 SiO1/2)c
en la que:
R7 se selecciona del grupo que consiste en alquilo C1-C20 , alquenilo C2-C8 , cicloalquilo C5-C8 , alcoxilo y fenil alquilo C1-C3 ;
a es un número positivo,
b es 0 o un número positivo,
c es 0 o un número positivo,
b/a es desde 0 hasta 100, y
c/a es desde 0 hasta 10,
en la que al menos uno de R1, R2 , R3 , R4 , y R5 es SIL1-X; y
R6 se selecciona del grupo que consiste en alquilo C1-C20, alquenilo C2-C8 , cicloalquilo C5-C8 , fenilo, fenil alquilo C1-C3 y flúor,
que comprende las etapas de:
1) Activar un compuesto de Fórmula A:
en la que R1, R2 , R3 , R4 , y R5 son como más arriba, pero ninguno puede ser SIL1-X,
para producir un compuesto de Fórmula B:
4) Someter el compuesto de Fórmula D a una reacción de condensación con un compuesto que tiene la fórmula SIL1-X-Cl o SIL1-X-H para producir el compuesto de Fórmula 1.
5. Una composición que comprende:
a) 70 hasta 99.9 por ciento en peso de una silicona fotocurable; y,
b) 0.1 hasta 10.0 por ciento en peso de un compuesto de la Fórmula general I:
en la que:
R1, R2 , R3 , R4 , y R5 son iguales o diferentes y se seleccionan del grupo que consiste en SIL1-X, hidrógeno, alquilo C1-C20 , alquenilo C2-C8 , cicloalquilo C5-C8 , fenil alquilo C1-C3 y flúor;
X es opcional, y si está presente es alquilo C1-C12;
SIL1 tiene la fórmula general:
(R78SiOs /2)a(R72SiO2/2)b(R73 SiOi/2)c
en la que:
R7 se selecciona del grupo que consiste en alquilo C1-C20, alquenilo C2-C8 , cicloalquilo C5-C8 , alcoxilo, fenilo y fenil alquilo C1-C3 ;
a es un número positivo,
b es 0 o un número positivo,
c es 0 o un número positivo,
b/a es desde 0 hasta 100, y
c/a es desde 0 hasta 10,
en la que al menos uno de R1, R2, R3, R4, y R5 es SIL1-X; y
R6 se selecciona del grupo que consiste en alquilo C1-C20, alquenilo C2-C8 , cicloalquilo C5-C8 , fenilo, fenil alquilo C1-C3 y flúor.
7. La composición de acuerdo con la reivindicación 5, en la que la silicona fotocurable es una organosilicona curable por UV o una silicona de curado dual por UV y humedad, en la que la silicona fotocurable es preferiblemente una silicona protegida en el extremo con (met)acrílico, o la silicona fotocurable es preferiblemente un polidimetilsiloxano terminado en silanol protegida en el extremo con (met)acrílico.
9. Un método para hacer un producto de polímero de silicona, que comprende las etapas de:
A) Proporcionar una composición de silicona fotocurable que comprende:
i) 70 hasta 99.9 por ciento en peso de una silicona fotocurable; y
ii) 0.1 hasta 10.0 por ciento en peso de un compuesto de la Fórmula general I:
en la que:
R1, R2 , R3 , R4 , y R5 son iguales o diferentes y se seleccionan del grupo que consiste en SIL1-X, hidrógeno, alquilo C1-C20 , alquenilo C2-C8 , cicloalquilo C5-C8 , fenil alquilo C1-C3 y flúor;
X es opcional, y si está presente es alquilo C1-C12;
SIL1 tiene la fórmula general:
(R7 SiO3/2)a (R72SiO2/2)b(R73 SiO1/2)c
en la que:
R7 se selecciona del grupo que consiste en alquilo C1-C20, alquenilo C2-C8 , cicloalquilo C5-C8 , alcoxilo, fenilo y fenil alquilo C1-C3 ;
a es un número positivo,
b es 0 o un número positivo,
c es 0 o un número positivo,
b/a es desde 0 hasta 100, y
c/a es desde 0 hasta 10,
en la que al menos uno de R1, R2 , R3 , R4 , y R5 es SIL1-X; y
R6 se selecciona del grupo que consiste en alquilo C1-C20, alquenilo C2-C8 , cicloalquilo C5-C8 , fenilo, fenil alquilo C1-C3 y flúor; y
B) Exponer la composición de silicona fotocurable a radiación ultravioleta o luz visible para iniciar el fotocurado de la composición de silicona fotocurable para producir el producto de polímero de silicona.
10. El método de acuerdo con la reivindicación 9, en el que la silicona fotocurable es una organosilicona curable por UV o una silicona de curado dual por UV y humedad, en el que la silicona fotocurable es preferiblemente una silicona protegida en el extremo con (met)acrílico o la silicona fotocurable es preferiblemente un polidimetilsiloxano terminado en silanol protegido en el extremo con (met)acrílico.
11. El método de acuerdo con la reivindicación 10, en el que la radiación ultravioleta tiene una longitud de onda de 390 nanómetros o mayor, preferiblemente una longitud de onda de 405 nanómetros.
12. El método de acuerdo con la reivindicación 9, que comprende además la etapa de colocar la composición de silicona fotocurable en contacto con al menos una capa de una composición ópticamente transparente antes del inicio del fotocurado, en el que cuando la composición de silicona fotocurable es curada, el producto de polímero de silicona es adecuado para usar en una pantalla ópticamente transparente.
13. El método de acuerdo con la reivindicación 12, en el que la composición ópticamente transparente es vidrio.
14. El método de acuerdo con la reivindicación 13, que comprende además la etapa de colocar la composición de silicona fotocurable entre dos capas de una composición ópticamente transparente antes del inicio del fotocurado, en el que cuando la composición de silicona fotocurable es curada, el producto de polímero de silicona es adecuado para uso en una pantalla ópticamente transparente.
15. El método de acuerdo con la reivindicación 13, en el que el producto de polímero de silicona tiene un valor de turbidez de 1 o menos y un valor de amarillez de 1 o menos en una brecha de 750 micrómetros entre las dos capas de la composición ópticamente transparente cuando se envejece durante 500 horas. en una máquina de prueba Q-panel Laboratory Ultraviolet (QUV) o cuando se envejece durante 500 horas en un horno a 85 °C y 85 % de humedad relativa.
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| PCT/CN2016/070609 WO2017120743A1 (en) | 2016-01-11 | 2016-01-11 | Silicone-compatible compounds |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2804199T3 true ES2804199T3 (es) | 2021-02-04 |
Family
ID=59310512
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES16884306T Active ES2804199T3 (es) | 2016-01-11 | 2016-01-11 | Compuestos compatibles con silicona |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US10597413B2 (es) |
| EP (1) | EP3402829B1 (es) |
| JP (1) | JP6703118B2 (es) |
| KR (1) | KR102575896B1 (es) |
| CN (1) | CN108779192B (es) |
| ES (1) | ES2804199T3 (es) |
| TW (1) | TWI712610B (es) |
| WO (1) | WO2017120743A1 (es) |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| TWI782066B (zh) | 2017-08-03 | 2022-11-01 | 德商漢高股份有限及兩合公司 | 可固化的聚矽氧光學透明黏著劑及其用途 |
| CN111527170B (zh) | 2017-12-27 | 2022-12-09 | 汉高股份有限及两合公司 | 光学透明的压敏粘合剂及其用途 |
| KR20210054010A (ko) * | 2018-10-01 | 2021-05-12 | 다우 도레이 캄파니 리미티드 | 광-경화성 오르가노폴리실록산 조성물 및 이의 경화물 |
| TW202340221A (zh) | 2022-04-06 | 2023-10-16 | 美商陶氏全球科技公司 | 醯基膦氧化物光起始劑 |
| TW202340331A (zh) * | 2022-04-06 | 2023-10-16 | 美商陶氏全球科技公司 | 聚矽氧可溶性醯基膦氧化物光起始劑 |
| JP2023160306A (ja) * | 2022-04-22 | 2023-11-02 | 信越化学工業株式会社 | 光反応性オルガノポリシロキサン、その製造方法および光硬化性組成物 |
Family Cites Families (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4273907A (en) * | 1979-07-18 | 1981-06-16 | Shin-Etsu Chemical Co., Ltd. | Benzoin-bonded organopolysiloxanes and method for the preparation thereof |
| JPS57207622A (en) | 1981-06-18 | 1982-12-20 | Toray Silicone Co Ltd | Photopolymerization sensitizer and its preparation |
| US4536265A (en) | 1984-04-19 | 1985-08-20 | Loctite Corporation | Siloxane polyphotoinitiators of the substituted acetophenone type |
| DE4435487A1 (de) | 1994-10-04 | 1996-04-11 | Hoechst Ag | Mit Silikonen kompatible Photoinitiatoren und diese enthaltende lichtempfindliche Gemische |
| US6376568B1 (en) | 1999-07-29 | 2002-04-23 | Ciba Specialty Chemicals Corporation | Surface-active photoinitiators |
| GB2360283B (en) * | 2000-02-08 | 2002-08-21 | Ciba Sc Holding Ag | Monoacylarylphosphines and acylphosphine oxides and sulphides |
| US6627672B1 (en) * | 2001-05-16 | 2003-09-30 | Henkel Loctite Corporation | UV/moisture dual cure silicone potting compound with improved depth of cure |
| US7618766B2 (en) * | 2005-12-21 | 2009-11-17 | E. I. Du Pont De Nemours And Company | Flame retardant photoimagable coverlay compositions and methods relating thereto |
| JP2010217438A (ja) * | 2009-03-16 | 2010-09-30 | Fuji Xerox Co Ltd | 電子写真感光体、プロセスカートリッジ、及び画像形成装置 |
| CN102924509A (zh) | 2011-08-09 | 2013-02-13 | 陈婷 | 双膦酰膦酸酯化合物 |
| WO2014086000A1 (en) | 2012-12-05 | 2014-06-12 | Henkel (China) Company Limited | Silicone-compatible photoinitiators |
| CN114181249A (zh) * | 2012-12-19 | 2022-03-15 | Igm集团公司 | 双酰基次膦酸的衍生物、其制备及其作为光敏引发剂的用途 |
| CN103333276B (zh) * | 2013-06-08 | 2015-07-29 | 新丰博兴聚合材料有限公司 | 一种含硅氧烷基团的长波吸收光引发剂及其制备方法 |
| US20150116415A1 (en) * | 2013-10-30 | 2015-04-30 | Xerox Corporation | Photocurable inks for indirect printing |
| KR102336227B1 (ko) * | 2014-08-29 | 2021-12-07 | 헨켈 아게 운트 코. 카게아아 | 유기규소 개질된 광개시제 및 그의 광경화성 접착제 조성물 |
| CN104829841B (zh) * | 2015-05-21 | 2017-11-10 | 山东大学 | 一种有机硅高分子材料及其制备方法 |
-
2016
- 2016-01-11 EP EP16884306.8A patent/EP3402829B1/en active Active
- 2016-01-11 CN CN201680078591.1A patent/CN108779192B/zh active Active
- 2016-01-11 JP JP2018536176A patent/JP6703118B2/ja active Active
- 2016-01-11 KR KR1020187019346A patent/KR102575896B1/ko active IP Right Grant
- 2016-01-11 ES ES16884306T patent/ES2804199T3/es active Active
- 2016-01-11 WO PCT/CN2016/070609 patent/WO2017120743A1/en active Application Filing
-
2017
- 2017-01-10 TW TW106100745A patent/TWI712610B/zh active
-
2018
- 2018-07-10 US US16/031,023 patent/US10597413B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| WO2017120743A1 (en) | 2017-07-20 |
| EP3402829A4 (en) | 2019-06-05 |
| JP6703118B2 (ja) | 2020-06-03 |
| EP3402829B1 (en) | 2020-06-17 |
| TW201739754A (zh) | 2017-11-16 |
| CN108779192A (zh) | 2018-11-09 |
| CN108779192B (zh) | 2021-01-26 |
| JP2019502717A (ja) | 2019-01-31 |
| KR20180103877A (ko) | 2018-09-19 |
| US10597413B2 (en) | 2020-03-24 |
| TWI712610B (zh) | 2020-12-11 |
| EP3402829A1 (en) | 2018-11-21 |
| US20180312532A1 (en) | 2018-11-01 |
| KR102575896B1 (ko) | 2023-09-07 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2804199T3 (es) | Compuestos compatibles con silicona | |
| JP5654050B2 (ja) | 新規のフッ素化化合物、これを含む組成物、これを利用した成形体、及び成形体の製造方法 | |
| TWI616459B (zh) | 矽可相容光引發劑 | |
| WO2019216008A1 (ja) | 光学樹脂組成物及び光学レンズ | |
| TWI603949B (zh) | 新穎肟酯聯苯基化合物、及含彼之光起始劑與光敏樹脂組合物 | |
| US10189867B2 (en) | Organosilicon modified photoinitiator and a photo-curable adhesive composition comprising the same | |
| KR100523295B1 (ko) | 광중합성 조성물 및 이로부터 제조된 광중합성 막 | |
| KR100680264B1 (ko) | 가교 가능한 포스핀옥사이드화합물과 이를 함유한 광중합성조성물 및 이를 이용한 광중합성 막 | |
| JP4846267B2 (ja) | 水酸基を有するシリコーン共重合体及びその製造方法 | |
| TW202039608A (zh) | 光硬化性聚矽氧樹脂組成物及由其硬化成的聚矽氧樹脂成形體以及該成形體的製造方法 | |
| JP2003327626A (ja) | 光硬化性シルフェニレン組成物およびその硬化物 | |
| KR20160117723A (ko) | 고굴절률 경화성 화합물, 이를 포함하는 광학부재용 점착제 조성물 및 이를 포함하는 광학시트용 조성물 | |
| KR100873986B1 (ko) | 방향족 아크릴계 화합물 및 이의 제조방법, 이를 포함하는중합성 수지 조성물 | |
| KR100612960B1 (ko) | 가교 가능한 포스핀옥사이드 화합물 및 이를 이용한광중합성 조성물 | |
| JP5677760B2 (ja) | 多面体骨格を有するポリシロキサン化合物の製造方法 |