ES2767352T3 - Métodos para producir combustibles, aditivos de gasolina y lubricantes - Google Patents
Métodos para producir combustibles, aditivos de gasolina y lubricantes Download PDFInfo
- Publication number
- ES2767352T3 ES2767352T3 ES14736519T ES14736519T ES2767352T3 ES 2767352 T3 ES2767352 T3 ES 2767352T3 ES 14736519 T ES14736519 T ES 14736519T ES 14736519 T ES14736519 T ES 14736519T ES 2767352 T3 ES2767352 T3 ES 2767352T3
- Authority
- ES
- Spain
- Prior art keywords
- formula
- catalyst
- reaction
- ketones
- metal
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D307/00—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom
- C07D307/02—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom not condensed with other rings
- C07D307/34—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D307/38—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with substituted hydrocarbon radicals attached to ring carbon atoms
- C07D307/40—Radicals substituted by oxygen atoms
- C07D307/46—Doubly bound oxygen atoms, or two oxygen atoms singly bound to the same carbon atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C1/00—Preparation of hydrocarbons from one or more compounds, none of them being a hydrocarbon
- C07C1/20—Preparation of hydrocarbons from one or more compounds, none of them being a hydrocarbon starting from organic compounds containing only oxygen atoms as heteroatoms
- C07C1/207—Preparation of hydrocarbons from one or more compounds, none of them being a hydrocarbon starting from organic compounds containing only oxygen atoms as heteroatoms from carbonyl compounds
- C07C1/2076—Preparation of hydrocarbons from one or more compounds, none of them being a hydrocarbon starting from organic compounds containing only oxygen atoms as heteroatoms from carbonyl compounds by a transformation in which at least one -C(=O)- moiety is eliminated
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C1/00—Preparation of hydrocarbons from one or more compounds, none of them being a hydrocarbon
- C07C1/20—Preparation of hydrocarbons from one or more compounds, none of them being a hydrocarbon starting from organic compounds containing only oxygen atoms as heteroatoms
- C07C1/22—Preparation of hydrocarbons from one or more compounds, none of them being a hydrocarbon starting from organic compounds containing only oxygen atoms as heteroatoms by reduction
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C29/00—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom not belonging to a six-membered aromatic ring
- C07C29/17—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom not belonging to a six-membered aromatic ring by hydrogenation of carbon-to-carbon double or triple bonds
- C07C29/175—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom not belonging to a six-membered aromatic ring by hydrogenation of carbon-to-carbon double or triple bonds with simultaneous reduction of an oxo group
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C45/00—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds
- C07C45/61—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by reactions not involving the formation of >C = O groups
- C07C45/65—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by reactions not involving the formation of >C = O groups by splitting-off hydrogen atoms or functional groups; by hydrogenolysis of functional groups
- C07C45/66—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by reactions not involving the formation of >C = O groups by splitting-off hydrogen atoms or functional groups; by hydrogenolysis of functional groups by dehydration
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C45/00—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds
- C07C45/61—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by reactions not involving the formation of >C = O groups
- C07C45/67—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by reactions not involving the formation of >C = O groups by isomerisation; by change of size of the carbon skeleton
- C07C45/68—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by reactions not involving the formation of >C = O groups by isomerisation; by change of size of the carbon skeleton by increase in the number of carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C45/00—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds
- C07C45/61—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by reactions not involving the formation of >C = O groups
- C07C45/67—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by reactions not involving the formation of >C = O groups by isomerisation; by change of size of the carbon skeleton
- C07C45/68—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by reactions not involving the formation of >C = O groups by isomerisation; by change of size of the carbon skeleton by increase in the number of carbon atoms
- C07C45/70—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by reactions not involving the formation of >C = O groups by isomerisation; by change of size of the carbon skeleton by increase in the number of carbon atoms by reaction with functional groups containing oxygen only in singly bound form
- C07C45/71—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by reactions not involving the formation of >C = O groups by isomerisation; by change of size of the carbon skeleton by increase in the number of carbon atoms by reaction with functional groups containing oxygen only in singly bound form being hydroxy groups
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C45/00—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds
- C07C45/61—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by reactions not involving the formation of >C = O groups
- C07C45/67—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by reactions not involving the formation of >C = O groups by isomerisation; by change of size of the carbon skeleton
- C07C45/68—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by reactions not involving the formation of >C = O groups by isomerisation; by change of size of the carbon skeleton by increase in the number of carbon atoms
- C07C45/72—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by reactions not involving the formation of >C = O groups by isomerisation; by change of size of the carbon skeleton by increase in the number of carbon atoms by reaction of compounds containing >C = O groups with the same or other compounds containing >C = O groups
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C45/00—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds
- C07C45/61—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by reactions not involving the formation of >C = O groups
- C07C45/67—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by reactions not involving the formation of >C = O groups by isomerisation; by change of size of the carbon skeleton
- C07C45/68—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by reactions not involving the formation of >C = O groups by isomerisation; by change of size of the carbon skeleton by increase in the number of carbon atoms
- C07C45/72—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by reactions not involving the formation of >C = O groups by isomerisation; by change of size of the carbon skeleton by increase in the number of carbon atoms by reaction of compounds containing >C = O groups with the same or other compounds containing >C = O groups
- C07C45/74—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by reactions not involving the formation of >C = O groups by isomerisation; by change of size of the carbon skeleton by increase in the number of carbon atoms by reaction of compounds containing >C = O groups with the same or other compounds containing >C = O groups combined with dehydration
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10G—CRACKING HYDROCARBON OILS; PRODUCTION OF LIQUID HYDROCARBON MIXTURES, e.g. BY DESTRUCTIVE HYDROGENATION, OLIGOMERISATION, POLYMERISATION; RECOVERY OF HYDROCARBON OILS FROM OIL-SHALE, OIL-SAND, OR GASES; REFINING MIXTURES MAINLY CONSISTING OF HYDROCARBONS; REFORMING OF NAPHTHA; MINERAL WAXES
- C10G3/00—Production of liquid hydrocarbon mixtures from oxygen-containing organic materials, e.g. fatty oils, fatty acids
- C10G3/50—Production of liquid hydrocarbon mixtures from oxygen-containing organic materials, e.g. fatty oils, fatty acids in the presence of hydrogen, hydrogen donors or hydrogen generating compounds
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10L—FUELS NOT OTHERWISE PROVIDED FOR; NATURAL GAS; SYNTHETIC NATURAL GAS OBTAINED BY PROCESSES NOT COVERED BY SUBCLASSES C10G OR C10K; LIQUIFIED PETROLEUM GAS; USE OF ADDITIVES TO FUELS OR FIRES; FIRE-LIGHTERS
- C10L1/00—Liquid carbonaceous fuels
- C10L1/04—Liquid carbonaceous fuels essentially based on blends of hydrocarbons
- C10L1/06—Liquid carbonaceous fuels essentially based on blends of hydrocarbons for spark ignition
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10L—FUELS NOT OTHERWISE PROVIDED FOR; NATURAL GAS; SYNTHETIC NATURAL GAS OBTAINED BY PROCESSES NOT COVERED BY SUBCLASSES C10G OR C10K; LIQUIFIED PETROLEUM GAS; USE OF ADDITIVES TO FUELS OR FIRES; FIRE-LIGHTERS
- C10L1/00—Liquid carbonaceous fuels
- C10L1/04—Liquid carbonaceous fuels essentially based on blends of hydrocarbons
- C10L1/08—Liquid carbonaceous fuels essentially based on blends of hydrocarbons for compression ignition
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10L—FUELS NOT OTHERWISE PROVIDED FOR; NATURAL GAS; SYNTHETIC NATURAL GAS OBTAINED BY PROCESSES NOT COVERED BY SUBCLASSES C10G OR C10K; LIQUIFIED PETROLEUM GAS; USE OF ADDITIVES TO FUELS OR FIRES; FIRE-LIGHTERS
- C10L1/00—Liquid carbonaceous fuels
- C10L1/10—Liquid carbonaceous fuels containing additives
- C10L1/14—Organic compounds
- C10L1/16—Hydrocarbons
- C10L1/1608—Well defined compounds, e.g. hexane, benzene
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10L—FUELS NOT OTHERWISE PROVIDED FOR; NATURAL GAS; SYNTHETIC NATURAL GAS OBTAINED BY PROCESSES NOT COVERED BY SUBCLASSES C10G OR C10K; LIQUIFIED PETROLEUM GAS; USE OF ADDITIVES TO FUELS OR FIRES; FIRE-LIGHTERS
- C10L1/00—Liquid carbonaceous fuels
- C10L1/10—Liquid carbonaceous fuels containing additives
- C10L1/14—Organic compounds
- C10L1/18—Organic compounds containing oxygen
- C10L1/182—Organic compounds containing oxygen containing hydroxy groups; Salts thereof
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10M—LUBRICATING COMPOSITIONS; USE OF CHEMICAL SUBSTANCES EITHER ALONE OR AS LUBRICATING INGREDIENTS IN A LUBRICATING COMPOSITION
- C10M127/00—Lubricating compositions characterised by the additive being a non- macromolecular hydrocarbon
- C10M127/02—Lubricating compositions characterised by the additive being a non- macromolecular hydrocarbon well-defined aliphatic
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10M—LUBRICATING COMPOSITIONS; USE OF CHEMICAL SUBSTANCES EITHER ALONE OR AS LUBRICATING INGREDIENTS IN A LUBRICATING COMPOSITION
- C10M129/00—Lubricating compositions characterised by the additive being an organic non-macromolecular compound containing oxygen
- C10M129/02—Lubricating compositions characterised by the additive being an organic non-macromolecular compound containing oxygen having a carbon chain of less than 30 atoms
- C10M129/04—Hydroxy compounds
- C10M129/06—Hydroxy compounds having hydroxy groups bound to acyclic or cycloaliphatic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2523/00—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group C07C2521/00
- C07C2523/38—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group C07C2521/00 of noble metals
- C07C2523/40—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group C07C2521/00 of noble metals of the platinum group metals
- C07C2523/42—Platinum
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2523/00—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group C07C2521/00
- C07C2523/38—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group C07C2521/00 of noble metals
- C07C2523/40—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group C07C2521/00 of noble metals of the platinum group metals
- C07C2523/44—Palladium
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2523/00—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group C07C2521/00
- C07C2523/38—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group C07C2521/00 of noble metals
- C07C2523/40—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group C07C2521/00 of noble metals of the platinum group metals
- C07C2523/46—Ruthenium, rhodium, osmium or iridium
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2601/00—Systems containing only non-condensed rings
- C07C2601/06—Systems containing only non-condensed rings with a five-membered ring
- C07C2601/08—Systems containing only non-condensed rings with a five-membered ring the ring being saturated
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2601/00—Systems containing only non-condensed rings
- C07C2601/06—Systems containing only non-condensed rings with a five-membered ring
- C07C2601/10—Systems containing only non-condensed rings with a five-membered ring the ring being unsaturated
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10L—FUELS NOT OTHERWISE PROVIDED FOR; NATURAL GAS; SYNTHETIC NATURAL GAS OBTAINED BY PROCESSES NOT COVERED BY SUBCLASSES C10G OR C10K; LIQUIFIED PETROLEUM GAS; USE OF ADDITIVES TO FUELS OR FIRES; FIRE-LIGHTERS
- C10L2200/00—Components of fuel compositions
- C10L2200/04—Organic compounds
- C10L2200/0407—Specifically defined hydrocarbon fractions as obtained from, e.g. a distillation column
- C10L2200/0415—Light distillates, e.g. LPG, naphtha
- C10L2200/0423—Gasoline
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10L—FUELS NOT OTHERWISE PROVIDED FOR; NATURAL GAS; SYNTHETIC NATURAL GAS OBTAINED BY PROCESSES NOT COVERED BY SUBCLASSES C10G OR C10K; LIQUIFIED PETROLEUM GAS; USE OF ADDITIVES TO FUELS OR FIRES; FIRE-LIGHTERS
- C10L2200/00—Components of fuel compositions
- C10L2200/04—Organic compounds
- C10L2200/0407—Specifically defined hydrocarbon fractions as obtained from, e.g. a distillation column
- C10L2200/0438—Middle or heavy distillates, heating oil, gasoil, marine fuels, residua
- C10L2200/0446—Diesel
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10L—FUELS NOT OTHERWISE PROVIDED FOR; NATURAL GAS; SYNTHETIC NATURAL GAS OBTAINED BY PROCESSES NOT COVERED BY SUBCLASSES C10G OR C10K; LIQUIFIED PETROLEUM GAS; USE OF ADDITIVES TO FUELS OR FIRES; FIRE-LIGHTERS
- C10L2270/00—Specifically adapted fuels
- C10L2270/02—Specifically adapted fuels for internal combustion engines
- C10L2270/023—Specifically adapted fuels for internal combustion engines for gasoline engines
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10L—FUELS NOT OTHERWISE PROVIDED FOR; NATURAL GAS; SYNTHETIC NATURAL GAS OBTAINED BY PROCESSES NOT COVERED BY SUBCLASSES C10G OR C10K; LIQUIFIED PETROLEUM GAS; USE OF ADDITIVES TO FUELS OR FIRES; FIRE-LIGHTERS
- C10L2270/00—Specifically adapted fuels
- C10L2270/02—Specifically adapted fuels for internal combustion engines
- C10L2270/026—Specifically adapted fuels for internal combustion engines for diesel engines, e.g. automobiles, stationary, marine
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10M—LUBRICATING COMPOSITIONS; USE OF CHEMICAL SUBSTANCES EITHER ALONE OR AS LUBRICATING INGREDIENTS IN A LUBRICATING COMPOSITION
- C10M2203/00—Organic non-macromolecular hydrocarbon compounds and hydrocarbon fractions as ingredients in lubricant compositions
- C10M2203/02—Well-defined aliphatic compounds
- C10M2203/022—Well-defined aliphatic compounds saturated
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10M—LUBRICATING COMPOSITIONS; USE OF CHEMICAL SUBSTANCES EITHER ALONE OR AS LUBRICATING INGREDIENTS IN A LUBRICATING COMPOSITION
- C10M2203/00—Organic non-macromolecular hydrocarbon compounds and hydrocarbon fractions as ingredients in lubricant compositions
- C10M2203/04—Well-defined cycloaliphatic compounds
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10M—LUBRICATING COMPOSITIONS; USE OF CHEMICAL SUBSTANCES EITHER ALONE OR AS LUBRICATING INGREDIENTS IN A LUBRICATING COMPOSITION
- C10M2207/00—Organic non-macromolecular hydrocarbon compounds containing hydrogen, carbon and oxygen as ingredients in lubricant compositions
- C10M2207/02—Hydroxy compounds
- C10M2207/021—Hydroxy compounds having hydroxy groups bound to acyclic or cycloaliphatic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10N—INDEXING SCHEME ASSOCIATED WITH SUBCLASS C10M RELATING TO LUBRICATING COMPOSITIONS
- C10N2070/00—Specific manufacturing methods for lubricant compositions
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P30/00—Technologies relating to oil refining and petrochemical industry
- Y02P30/20—Technologies relating to oil refining and petrochemical industry using bio-feedstock
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- General Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Health & Medical Sciences (AREA)
- Emergency Medicine (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Catalysts (AREA)
- Lubricants (AREA)
Abstract
Un método para producir una o más cetonas poniendo en contacto un compuesto de fórmula (I) con un catalizador básico y uno o más alcoholes o aldehídos de fórmula (II) para producir una o más cetonas seleccionadas del grupo que consiste en:**Fórmula** y cualquiera de las mezclas de los mismos, en donde el compuesto de fórmula (I) y el compuesto de fórmula (II) tienen las siguientes estructuras:**Fórmula** en las que: R7 se selecciona entre alquilo, arilo, alquenilo, alquinilo, furilo, 5-metilfurilo, 5-hidroximetilfurilo y heteroarilo; X es OH u O; y la línea discontinua representa un doble enlace opcional que está presente cuando X es O, comprendiendo el método además hidrogenar la una o más cetonas a uno o más alcanos. en el que el término "alquilo" también incluye "cicloalquilo".
Description
DESCRIPCIÓN
Métodos para producir combustibles, aditivos de gasolina y lubricantes
Campo
La presente divulgación generalmente se refiere a la producción de combustibles, aditivos de gasolina y/o lubricantes, y a precursores de los mismos.
Antecedentes
La producción de combustibles y otros productos químicos de valor añadido, tales como aditivos de gasolina y lubricantes a partir de fuentes renovables, se ha vuelto cada vez más importante como medio para reducir la producción de gases de efecto invernadero y reducir las importaciones de petróleo. Véase L. D. Gómez, C. G. Steele-King, S. J. McQueen-Mason, New Phytologist, 2008, 178, 473-485. La biomasa lignocelulósica está compuesta normalmente de celulosa, hemicelulosa y lignina. Estos componentes de biomasa son polímeros ricos en carbohidratos no comestibles que pueden servir como fuente renovable de energía. Normalmente representan hasta al menos el 70 % del peso seco de la biomasa. Como tales, la conversión de estos componentes de biomasa no comestibles en biocombustibles y otros productos químicos de valor añadido de fuentes renovables es de interés continuo que puede beneficiar al medio ambiente y reducir las importaciones de petróleo. Véase A. Demirbas, Energy Sources, Parte B: Economics, Planning and Policy, 2008, 3, 177-185. La biomasa se puede convertir primero en compuestos intermedios, tales como azúcares, que luego se pueden convertir en otras moléculas precursoras que se pueden convertir en combustibles (por ejemplo, gasolina o diésel), aditivos de gasolina y/o lubricantes.
El documento WO2012/166267 desvela métodos para producir cetonas adecuadas para su uso como combustibles y lubricantes mediante la conversión catalítica de una mezcla de producto de fermentación de acetona-butanoletanol (ABE) que puede derivarse de la biomasa.
Breve sumario
En un aspecto, se proporciona un método para producir una o más cetonas poniendo en contacto un compuesto de fórmula (I) con un catalizador básico y uno o más alcoholes o aldehídos de fórmula (II) para producir la una o más cetonas seleccionadas del grupo que consiste en:
y cualquiera de las mezclas de los mismos,
en el que el compuesto de fórmula (I) y el compuesto de fórmula (II) tienen las siguientes estructuras:
en las que:
R7 se selecciona entre alquilo, arilo, alquenilo, alquinilo, furilo, 5-metilfurilo, 5-hidroximetilfurilo y heteroarilo; X es OH u O; y
la línea discontinua representa un doble enlace opcional que está presente cuando X es O, comprendiendo el método además hidrogenar la una o más cetonas a uno o más alcanos. en los que el término "alquilo" también incluye "cicloalquilo".
En otro aspecto, se proporciona un método para producir uno o más alcanos C24-C36, mediante: (a) poner en contacto un aldehído y uno o más alcoholes con catalizador metálico y, opcionalmente, base para producir uno o más aldehídos superiores; (b) hidrogenar el uno o más aldehídos superiores a uno o más alcoholes superiores; y (c) convertir el uno o más alcoholes superiores en uno o más alcanos C24-C36. En algunas realizaciones, los aldehidos superiores tienen una mayor cantidad de átomos de carbono que la cantidad de átomos de carbono en la cetona utilizada en la etapa (a) como material de partida.
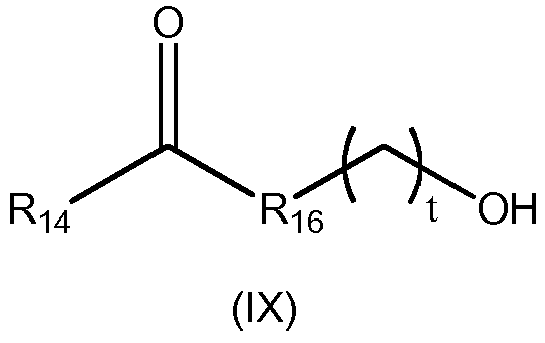
En el presente documento se desvela un método para producir uno o más compuestos de fórmula (IX), poniendo en contacto una cetona de fórmula (VII) con un diol de fórmula (VIII) para producir uno o más compuestos de fórmula (IX),
en la que:
la cetona de fórmula (VII) tiene la siguiente estructura:
(V il)
en la que:
R14 es H o alquilo; y
R15 es metilo;
el diol de fórmula (VIII) tiene la siguiente estructura:
HO
^ Í
t
n
OH
(VIH)
en la que t es un número entero mayor o igual a 4; y
el uno o más compuestos de fórmula (IX) tienen la siguiente estructura:
en la que:
R14 es como se ha descrito anteriormente para la fórmula (VII)
R16 es -CH2-; y
t es como se ha descrito anteriormente para la fórmula (VIII).
En otro aspecto más, se proporciona un método para producir un alcano cíclico, mediante: (a) poner en contacto una dicetona con catalizador básico para producir una cetona cíclica; y (b) hidrogenar la cetona cíclica para producir el alcano cíclico. También se desvela un método para producir un alcohol cíclico o mezclas de un alcohol cíclico y un alcano cíclico, mediante: (a) poner en contacto una dicetona con catalizador básico para producir una cetona cíclica; e (b) hidrogenar la cetona cíclica para producir el alcohol cíclico o mezclas de un alcohol cíclico y un alcano cíclico. También se proporciona una composición que incluye: un combustible diésel, un aditivo de gasolina o un lubricante, o cualquier mezcla de los mismos; y uno o más alcanos, alcanos cíclicos o alcoholes cíclicos producidos de acuerdo con cualquiera de los métodos descritos anteriormente.
Descripción de las figuras
La presente solicitud puede entenderse haciendo referencia a la siguiente descripción tomada junto con las figuras de los dibujos adjuntos, en los que se hace referencia a partes similares con números similares.
La figura 1 representa los datos obtenidos para la condensación aldólica cruzada de 2,5-hexanodiona y furfural a 25 °C, 50 °C y 80 °C.
La figura 2 representa los datos obtenidos para la condensación aldólica cruzada de 2,5-hexanodiona y furfural a diferentes cargas de catalizador básico.
La figura 3 representa los datos obtenidos para la condensación aldólica cruzada de 2,5-hexanodiona y 5-metilfurfural a diferentes cargas de catalizador básico.
La figura 4 representa los datos obtenidos para la condensación aldólica cruzada de 2,5-hexanodiona y furfural en diferentes proporciones de furfural:2,5-hexanodiona.
Descripción detallada
La siguiente descripción establece numerosas configuraciones de ejemplo, procesos, parámetros y similares. Debe reconocerse, sin embargo, que dicha descripción no pretende ser una limitación del alcance de la presente divulgación, sino que, en su lugar, se proporciona como una descripción de realizaciones de ejemplo.
Definiciones
"Alquilo" se refiere a una cadena de hidrocarbono saturado monorradical no ramificado o ramificado. En algunas realizaciones de los compuestos desvelados en el presente documento, el alquilo tiene de 1 a 20 átomos de carbono (es decir, alquilo C1-C20), de 1 a 10 átomos de carbono (es decir, alquilo C1-C10), de 1 a 8 átomos de carbono (es decir, alquilo C1-C8), de 1 a 6 átomos de carbono (es decir, alquilo C1-C6) o de 1 a 4 átomos de carbono (es decir,
alquilo C1-C4). Los ejemplos de grupos alquilo incluyen metilo, etilo, propilo, isopropilo, n-butilo, sec-butilo, ferc-butilo, pentilo, 2 -pentilo, isopentilo, neopentilo, hexilo, 2 -hexilo, 3-hexilo y 3-metilpentilo. Cuando se nombra un resto alquilo que tiene un número especificado de carbonos, se abarcan todos los isómeros geométricos que tienen ese número de carbonos; por lo tanto, por ejemplo, "butilo" puede incluir n-butilo, sec-butilo, isobutilo y t-butilo; "propilo" puede incluir n-propilo e isopropilo. El término "alquilo" también incluye compuestos de "cicloalquilo". "Cicloalquilo" se refiere a un grupo alquilo cíclico. En algunas realizaciones de los compuestos de fórmula (I), el cicloalquilo tiene de 3 a 2 0 átomos de carbono en el anillo (es decir, cicloalquilo C3-C20), o de 3 a 12 átomos de carbono en el anillo (es decir, cicloalquilo C3-C12), o de 3 a 8 átomos de carbono en el anillo (es decir, cicloalquilo C3-C8). Los ejemplos de grupos cicloalquilo incluyen ciclopropilo, ciclobutilo, ciclopentilo y ciclohexilo.
"Alquenilo" se refiere a un grupo hidrocarbonado insaturado que tiene al menos un sitio de insaturación olefínica (es decir, con al menos un resto de la fórmula C=C).
"Alquinilo" se refiere a un grupo hidrocarbonado insaturado que tiene al menos un sitio de insaturación acetilénico (es decir, con al menos un resto de la fórmula C=C).
"Arilo" se refiere a un grupo carbocíclico aromático que tiene un solo anillo (por ejemplo, fenilo), múltiples anillos (por ejemplo, bifenilo) o múltiples anillos fusionados (por ejemplo, naftilo, fluorenilo y antrilo). En ciertas realizaciones de los compuestos desvelados en el presente documento, arilo tiene de 6 a 2 0 átomos de carbono en el anillo (es decir, arilo C6-C20), o de 6 a 12 átomos de carbono en el anillo (es decir, arilo C6-C12).
"Heteroarilo" se refiere a un grupo arilo, en el que al menos un átomo de carbono del grupo carbocíclico designado ha sido reemplazado por un heteroátomo seleccionado de N, O y S. El término también incluye anillos heteroaromáticos de cinco miembros, tales como, por ejemplo, furanos e imidazoles.
En el presente documento se proporcionan métodos para producir aditivos de gasolina, diésel, y/o lubricantes, y precursores de los mismos. En algunas realizaciones, una dicetona puede sufrir condensación aldólica cruzada con un aldehído o alcohol para producir precursores diésel, que podría ser hidrogenada para formar diésel de alto valor. Los productos de la condensación aldólica cruzada también podrían someterse a otros tipos de química, tal como química de Guerbet, para producir lubricantes. En otras realizaciones, una dicetona puede sufrir una ciclación intramolecular para formar un precursor de gasolina, que podría hidrogenarse para formar aditivos de gasolina. Las reacciones para producir aditivos de gasolina, diésel y/o lubricantes, y precursores de los mismos, se describen cada una con más detalle a continuación.
Condensación aldólica cruzada de compuestos de fórmula (I) y compuestos de fórmula (II)
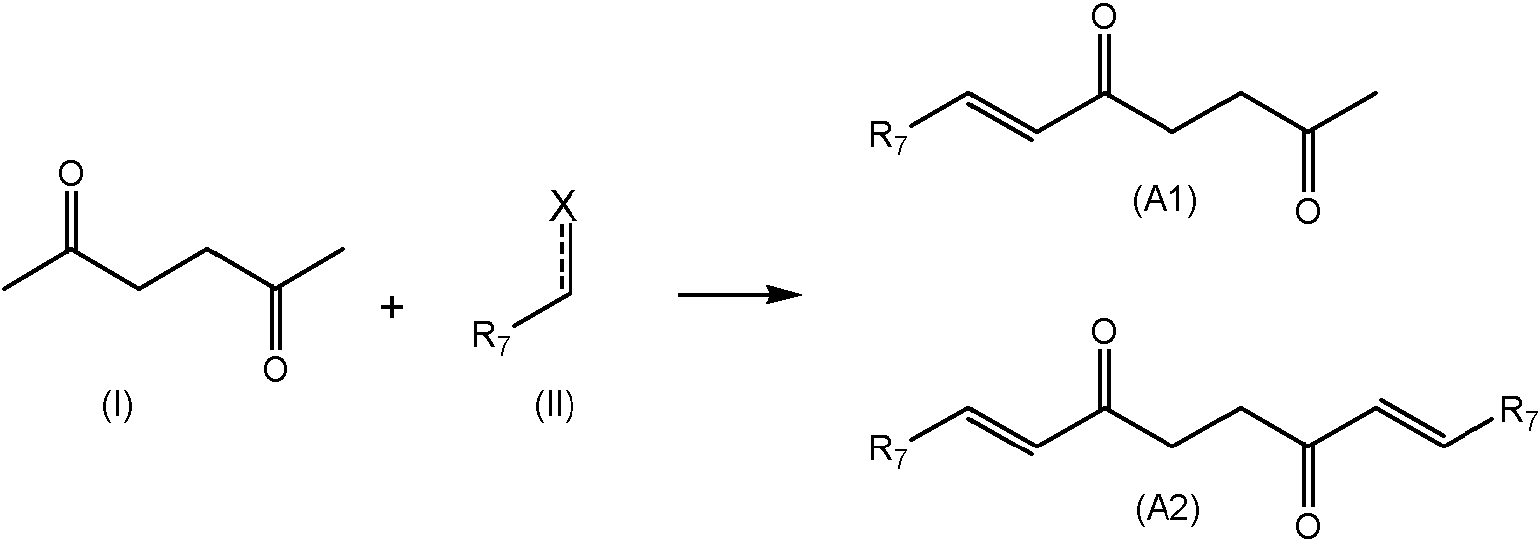
En un aspecto, se proporciona un método para producir una o más cetonas poniendo en contacto un compuesto de fórmula (I) con un catalizador básico y uno o más alcoholes o aldehídos de fórmula (II) para producir las una o más cetonas:
en las que:
R7 se selecciona entre alquilo, arilo, alquenilo, alquinilo, furilo, 5-metilfurilo, 5-hidroximetilfurilo y heteroarilo; X es OH u O; y
la línea discontinua representa un doble enlace opcional que está presente cuando X es O.
Debería entenderse que, con respecto a los alcoholes o aldehídos de fórmula (II), la línea discontinua representa un doble enlace opcional que está presente cuando X es O, o un doble enlace opcional que no está presente cuando X es OH.
a) Compuestos de Fórmula (I)
Los compuestos de fórmula (I) tienen la estructura:
Los compuestos de fórmula (I) pueden obtenerse de cualquier fuente disponible comercialmente o de acuerdo con cualquier método conocido por un experto en la materia. Los compuestos de fórmula (I) pueden obtenerse a partir de biomasa. Por ejemplo, la celulosa o la hemicelulosa se pueden convertir primero en glucosa o xilosa, que luego pueden convertirse en 5-hidroximetilfufural o furfural. El 5-hidroximetilfurfural se puede convertir en 2,5-dimetilfurano, que puede hidrolizarse en condiciones ácidas para producir 2,5-hexanodiona. Véase, por ejemplo, Thananatthanachon y Rauchfuss, Angewandte Chemie-Edición internacional 2010, 49 (37), 6616-6618; Kuhlmann, et al., The Journal of Organic Chemistry 1994, 59 (11), 3098-3101.
b) Compuestos de Fórmula (II)
Los compuestos de fórmula (II) tienen la estructura:
en la que:
R7 es alquilo C1-C20, arilo C6-C20, alquenilo C2-C20, alquinilo C2-C20 y heteroarilo C4-C21;
X es OH u O; y
la línea discontinua representa un doble enlace opcional que no está presente cuando X es OH.
En algunas realizaciones, X es OH y el compuesto de fórmula (II) es un compuesto de fórmula (II-A):
(ll-A)
En otras realizaciones, X es O y el compuesto de fórmula (II) es un compuesto de fórmula (II-B):
(ll-B)
En algunas realizaciones, R7 es alquilo C1-C20, arilo C6-C22, alquenilo C2-C20, alquinilo C2-C20 y heteroarilo C4-C21. En ciertas realizaciones, R7 es alquilo C1-C10, arilo C6-C22, alquenilo C2-C10, alquinilo C2-C10 y heteroarilo C4-C21. En
ciertas realizaciones, R7 es alquilo C1-C10. En una realización, R7 es alquilo C4. En otras realizaciones, R7 es heteroarilo. En una realización, R7 es furanilo. En otras realizaciones, R7 es furilo, 5-metilfurilo o 5-hidroximetilfurilo. En una realización, el compuesto de fórmula (II) es:
Los compuestos de fórmula (II) pueden obtenerse de cualquier fuente disponible comercialmente o de acuerdo con cualquier método conocido por un experto en la materia. Por ejemplo, el furfural se puede obtener de cualquier fuente de biomasa. Véase, por ejemplo, Huber et al., Chem. Rev. 2006, 106 (9), 4044-4098.
c) Productos de condensación aldólica cruzada
Se producen una o más cetonas cuando un compuesto de fórmula (I) se pone en contacto con uno o más alcoholes o aldehídos de fórmula (II) y un catalizador básico. Dependiendo de varios factores, las cetonas producidas pueden ser el resultado de una reacción intermolecular entre los compuestos de fórmulas (I) y (II), una reacción intramolecular que implica la ciclación del compuesto de fórmula (I), o una combinación de los mismos.
Reacción intermolecular
Cuando las cetonas producidas son el resultado de una reacción intermolecular, tales cetonas pueden ser adecuadas para su uso como precursores diésel, incluyendo, por ejemplo, precursores diésel de C11-C16. Tal reacción intermolecular se puede representar de la siguiente manera:
En algunas realizaciones, la reacción intermolecular es:
o cualquier mezcla de las mismas.
En ciertas realizaciones, la reacción intermolecular puede producir productos de 1 adición, incluyendo, por ejemplo:
Debería entenderse, sin embargo, que los productos también pueden sufrir una mayor condensación aldólica para formar otros oligómeros si el producto contiene carbonos enolizables que pueden continuar reaccionando.
Por ejemplo, los productos de 1 adición pueden reaccionar aún más para producir varios productos de 2 adiciones:
En otro ejemplo, los productos de 2 adición pueden reaccionar aún más para producir varios productos de 3
adiciones:
En otro ejemplo más, los productos de 3 adición pueden reaccionar aún más para producir varios productos de 4 adiciones:
Cuando las cetonas producidas son el resultado de una reacción intramolecular, tales cetonas pueden ser adecuadas para su uso como precursores de aditivos de gasolina, tales como compuestos de fórmula (B):
En algunas realizaciones, cuando los aditivos de gasolina son los productos deseados, el compuesto de fórmula (I) se convertirá en compuestos de fórmula B con el catalizador básico en ausencia de cualquier compuesto de fórmula (II). En algunas realizaciones en reacciones con compuestos de fórmula (I) y fórmula (II), las cetonas producidas por reacción intramolecular del compuesto de fórmula (I) pueden reaccionar adicionalmente con un compuesto de fórmula (II) para producir compuestos de fórmula (C) que se seleccionan de:
y cualquiera de las mezclas de los mismos.
Se entenderá que los compuestos mostrados anteriormente se formarán en una reacción de ejemplo en la que el compuesto de fórmula (I) es 2,5-hexanodiona. La 2,5-hexanodiona puede sufrir una ciclación intramolecular seguida de condensación con un compuesto de fórmula (II).
Debe entenderse que las reacciones intermoleculares e intramoleculares son reacciones competitivas y la formación del producto puede ajustarse controlando uno o más factores. Tales factores pueden incluir, por ejemplo, la cantidad de compuesto de fórmula (II) presente en el sistema de reacción, el tipo de catalizador, la carga del catalizador, la temperatura y el disolvente. En algunas realizaciones, los compuestos ramificados se pueden formar con preferencia a los compuestos lineales. En algunas realizaciones, al menos un 5 %, 10 %, 20 %, 30 %, 40 %, 50 %, 60 %, 70 %, 80% o 90 % de la una o más cetonas producidas por la reacción del compuesto de fórmula (I) y fórmula (II) son cetonas ramificadas. En algunas realizaciones, al menos el 70 % de la una o más cetonas producidas por la reacción del compuesto de fórmula (I) y fórmula (II) son cetonas ramificadas. En algunas realizaciones, al menos el 80 % de la una o más cetonas producidas por la reacción del compuesto de fórmula (I) y fórmula (II) son cetonas ramificadas. En algunas realizaciones, al menos el 90 % de la una o más cetonas producidas por la reacción del compuesto de fórmula (I) y fórmula (II) son cetonas ramificadas.
d) Catalizador básico
Los compuestos de fórmula (I) y uno o más alcoholes o aldehídos de fórmula (II) se ponen en contacto con el catalizador básico para producir una o más cetonas, por reacción intermolecular y/o reacción intramolecular.
En algunas realizaciones, el catalizador básico es una base inorgánica o una base orgánica. Los ejemplos de bases inorgánicas pueden incluir hidróxido de potasio, hidróxido de bario, hidróxido de cesio, hidróxido sódico, hidróxido de estroncio, hidróxido de calcio, hidróxido de litio, hidróxido de rubidio e hidróxido de magnesio. En algunas realizaciones, la base es K3PO4. Los ejemplos de bases orgánicas pueden incluir trietilamina, trimetilamina, piridina y metilamina. En algunas realizaciones, las aminas pueden estar ancladas a un soporte heterogéneo.
El catalizador básico puede ser homogéneo en el sistema de reacción o heterogéneo en el sistema de reacción. En
una realización, el catalizador básico es heterogéneo, permitiendo una fácil recuperación del catalizador del sistema de reacción. En algunas realizaciones, el catalizador heterogéneo comprende uno o más metales seleccionados del grupo que consiste en Mg, Al, Ar, Ti, Ce, B, Y, y cualquier mezcla de los mismos. En algunas realizaciones, el catalizador heterogéneo comprende además oxígeno. En una realización, el catalizador heterogéneo puede derivarse de un material de hidrotalcita. La basicidad de las hidrotalcitas se puede ajustar variando la relación magnesio-aluminio, rehidratando la hidrotalcita calcinada y dopando la hidrotalcita con Na y K. En algunas realizaciones, las hidrotalcitas se preparan por coprecipitación de sales de metales alcalinotérreos y/o nitratos de aluminio en una solución que incluye urea o amoníaco y carbonato de amonio o hidróxido de potasio y carbonato de potasio o hidróxido de sodio y carbonato de sodio. Por lo general, el material de hidrotalcita se calcina a temperaturas de aproximadamente 400 °C a aproximadamente 800 °C antes de su uso en las reacciones descritas en el presente documento. Después de la calcinación, el material de hidrotalcita se puede denominar óxido de metal mixto.
En algunas realizaciones, el catalizador básico es un óxido metálico. En algunas realizaciones, el óxido metálico comprende un metal seleccionado del grupo que consiste en Mg, Al, Ar, Ti, Ce, B e Y. En algunas realizaciones, se pueden combinar uno o más óxidos metálicos como se usa como catalizador básico. Los ejemplos de óxidos metálicos incluyen ThO2, ZrO2, ZnO, TiO2, MgO y cualquier mezcla de los mismos. En algunas realizaciones, el catalizador básico es un óxido metálico mixto que contiene uno o más metales. En algunas realizaciones, el catalizador básico es el óxido metálico mixto MgAlO o MgZrO. En algunas realizaciones, el catalizador básico es el óxido metálico mixto MgAlO. En algunas realizaciones, los óxidos metálicos mixtos comprenden al menos dos metales seleccionados del grupo que consiste en Mg, Al, Ar, Ti, Ce, B e Y.
En algunas realizaciones, los catalizadores incluyen uno o más metales y un soporte básico. En ciertas realizaciones, el catalizador básico es KF en alúmina.
La basicidad de los catalizadores heterogéneos puede determinarse mediante diversas técnicas conocidas en la materia. Por ejemplo, la basicidad del catalizador heterogéneo se puede medir mediante la desorción programada con temperatura de CO2 (TPD). En algunas realizaciones, la TPD de CO2 se lleva a cabo adsorbiendo CO2 al catalizador a temperatura ambiente y calentando hasta 773 K (o un ensayo similar). En algunas realizaciones, los catalizadores heterogéneos preferidos tienen densidades de sitio de base medidas por TPD de CO2 de al menos 50 micromoles/gramo de catalizador. En otras realizaciones, todos los catalizadores heterogéneos preferidos de todos los tipos tienen densidades de sitio de base por TPD de CO2 de al menos 10 micromoles/gramo de catalizador. La basicidad del catalizador heterogéneo también se puede medir usando la determinación de carga cero (Regalbuto), o usando el método del indicador Hammett.
En algunas realizaciones, los catalizadores básicos tienen un pKa de 10 a 16. En otras realizaciones, los catalizadores metálicos tienen un pKa de 11 a 15. En algunas realizaciones, el catalizador básico tiene una desorción de CO2 de al menos 200 °C. La determinación cuantitativa del pKa y otros métodos para caracterizar la basicidad de un soporte de catalizador tal como hidrotalcita se conocen en la materia. Véase, por ejemplo, A. Corma, et al., J. of Catalysis, 1992, 134, 58 y D. Debecker, et al., Chem. Eur. J., 2009, 15c.
Debe entenderse que el catalizador metálico puede prepararse por cualquier método conocido por un experto en la materia. Por ejemplo, la impregnación (por ejemplo, impregnación a humedad incipiente) es una técnica de ejemplo que se puede utilizar. En un ejemplo, un soporte, tal como la hidrotalcita) y la sal metálica, tal como cloruro de paladio o acetato de cobre) pueden combinarse y se añade un disolvente, tal como agua. Se permite que la sal metálica y el soporte reaccionen durante un período de tiempo entre 1 y 24 horas a una temperatura entre temperatura ambiente y 200 °C, o más específicamente, entre 50 y 120 °C. La mezcla de reacción se puede agitar en una atmósfera de hidrógeno. A continuación, el catalizador sólido se filtra y se lava con grandes cantidades de disolvente. A continuación, el sólido se puede secar al vacío a una temperatura entre 80 y 150 °C. Opcionalmente, se pueden añadir otros aditivos a la mezcla de reacción, tales como sales de metales alcalinos (por ejemplo, cloruro de sodio o cloruro de potasio) o una base como se ha descrito anteriormente.
El catalizador metálico también se puede preparar por impregnación (por ejemplo, impregnación a humedad incipiente) de sales metálicas sobre soportes básicos, seguido de calcinación a temperaturas superiores a 300 °C en aire o gases inertes y/o reducción en mezclas de hidrógeno y gases inertes. Como alternativa, el catalizador metálico puede prepararse sintetizando nanopartículas metálicas ex situ y soportando dichas nanopartículas en el soporte metálico básico usando un disolvente. En algunas realizaciones, el catalizador metálico preparado por impregnación (por ejemplo, impregnación a humedad incipiente) incluye al menos dos metales. En algunas realizaciones, el catalizador metálico contiene Pd y Cu. En algunas realizaciones, el catalizador metálico contiene Pd/Cu. Por ejemplo, la relación de Pd y Cu puede variar, en la que el Pd puede estar en un exceso molar de Cu (por ejemplo, en una relación molar de 2:1), o el Cu puede estar en un exceso molar de Pd (por ejemplo, en una relación molar de 1:2).
El catalizador metálico también se puede preparar usando los métodos mencionados anteriormente para soportar metales sobre soportes básicos, con la diferencia de que los soportes son inertes e incluyen SiO2 y carbono. Los soportes básicos también se preparan como se ha mencionado anteriormente, pero no hay metal soportado en ellos.
Los soportes básicos y los catalizadores metálicos se mezclan físicamente antes de la reacción.
El catalizador metálico también se puede preparar por impregnación simultánea o sucesiva (por ejemplo, impregnación a humedad incipiente) de soluciones de sales de nitrato o acetato de metales alcalinos o alcalinotérreos y sales o complejos apropiados de los metales desvelados en el presente documento sobre soportes inertes, seguido de calcinación y reducción en las condiciones mencionadas anteriormente. Como alternativa, el catalizador metálico puede prepararse por impregnación (por ejemplo, impregnación a humedad incipiente) de sales alcalinas sobre soportes inertes, seguido de calcinación e impregnación (por ejemplo, impregnación a humedad incipiente) de nanopartículas metálicas sintetizadas ex situ.
Ejemplos de catalizadores
El catalizador puede incluir hidrotalcita. En ciertas realizaciones, el catalizador incluye hidrotalcita y uno o más metales o dos o más metales. Los uno o más metales, o dos o más metales, pueden incluir, por ejemplo, paladio (Pd), cobre (Cu), níquel (Ni), cinc (Zn), rutenio (Ru), cobalto (Co) y platino (Pt). La hidrotalcita puede usarse como parte del catalizador de una o más formas. Por ejemplo, en una realización, la hidrotalcita puede incluir uno o más metales depositados mediante coprecipitación o impregnación (por ejemplo, impregnación a humedad incipiente). Tales ejemplos pueden incluir Pd/HT, Cu/HT y Pd-Cu/HT. En otra realización, la hidrotalcita se puede coprecipitar o impregnar sobre un soporte de carbono (por ejemplo, HT/C) y uno o más metales se pueden coprecipitar o impregnar sobre dicho soporte de carbono. Tales ejemplos pueden incluir Pd/HT/C o Pd-Cu/HT/C. En ciertas realizaciones, la hidrotalcita se puede mezclar con carbono para producir un soporte (por ejemplo, HT-C) y uno o más metales pueden coprecipitarse o impregnarse en dicho soporte de carbono. Dichos ejemplos pueden incluir Pd/HT-C o Pd-Cu/HT-C. En aún otra realización, la hidrotalcita se puede usar sola o en combinación con otros catalizadores, de forma que la HT es un catalizador de una mezcla de catalizadores usados. Tal ejemplo puede incluir una mezcla de catalizadores: Cu/SiO2 y Pd/C y HT.
En algunas realizaciones, el catalizador incluye: (i) uno o más, o dos o más, metales tales como paladio (Pd), cobre (Cu), o una combinación de los mismos; e (i) hidrotalcita. En ciertas realizaciones, el Pd, Cu, o una combinación de los mismos se pueden coprecipitar o impregnar sobre la hidrotalcita mediante métodos conocidos en la técnica. En ciertas realizaciones, la hidrotalcita se puede impregnar sobre soporte de carbono mediante métodos conocidos en la técnica. En aún otras realizaciones, el catalizador puede incluir además TiO 2. Por ejemplo, los catalizadores adecuados pueden incluir Pd-Cu/HT; Pd-Cu/HT-C; Pd-Cu/HT y TiO2; o Pd-Cu/HT-C y TiO2.
El catalizador puede incluir óxido de lantano (La2O3). El La2O3 puede prepararse mediante cualquier método adecuado conocido en la técnica. Por ejemplo, el La2O3 puede prepararse a partir de la calcinación de La2(C2O4)3 o La2(NO3)3 a o por encima de 500 °C. En ciertas realizaciones, el catalizador incluye La2O3 y uno o más metales. El uno o más metales pueden incluir, por ejemplo, paladio (Pd), cobre (Cu), níquel (Ni), cinc (Zn), rutenio (Ru), cobalto (Co) y platino (Pt). El La2O3 puede usarse como parte del catalizador de una o más formas. Por ejemplo, en una realización, el La2O3 puede incluir uno o más metales depositados mediante coprecipitación o impregnación (por ejemplo, impregnación a humedad incipiente). En otra realización, el La2O3 puede coprecipitarse o impregnarse sobre soporte de carbono (por ejemplo, La2O3/C). En otra realización más, el La2O3 se puede usar en combinación con otros catalizadores, de manera que el La2O3 sea un catalizador de una mezcla de catalizadores utilizados. Por ejemplo, el La2O3 puede usarse en una mezcla con uno o más catalizadores que contienen metales. Tales ejemplos pueden incluir una mezcla de catalizadores: Cu/SiO2 y Pd/C y La2O3/C; o Cu/ZnO/Al2O3 y Pd/C y La2O3 y TO 2; o Cu/ZnO/Al2O3 y La2O3.
El catalizador puede incluir óxido de magnesio (MgO). En ciertas realizaciones, el catalizador incluye MgO y uno o más metales. El uno o más metales pueden incluir, por ejemplo, paladio (Pd), cobre (Cu), níquel (Ni), cinc (Zn), rutenio (Ru), cobalto (Co) y platino (Pt). El MgO puede usarse como parte del catalizador de una o más formas. Por ejemplo, en una realización, el MgO puede incluir uno o más metales (incluido uno o más óxidos metálicos) depositados por coprecipitación o impregnación (por ejemplo, impregnación a humedad incipiente). Tales ejemplos pueden incluir Cu/MgO, SrO/MgO o CaO/MgO. En otra realización, el MgO puede coprecipitarse o impregnarse sobre soporte de carbono o soporte de sílice. Tales ejemplos incluyen MgO/C y MgO/SiO2. En otra realización más, el MgO puede usarse en combinación con otros catalizadores, de modo que el MgO es un catalizador de una mezcla de catalizadores usados. Por ejemplo, el MgO puede usarse en una mezcla con uno o más catalizadores que contienen metales. Tales ejemplos pueden incluir una mezcla de catalizadores: Cu/ZnO/Al2O3 y MgO/SiO2 ; o Cu/ZnO/Al2O3 y SrO/MgO; o Cu/ZnO/A^O3 y CaO/MgO; o Cu/SiO2 y CaO/MgO; o PdCu-CaO/MgO; o Cu/ZnO/A^O3 y MgO; o Cu/ZnO/AhO3, Pd/C y MgO.
El catalizador puede incluir dióxido de titanio (TO 2). En ciertas realizaciones, el catalizador incluye TiO2 y uno o más metales. El uno o más metales pueden incluir, por ejemplo, paladio (Pd), cobre (Cu), níquel (Ni), cinc (Zn), rutenio (Ru), cobalto (Co) y platino (Pt). El TiO2 puede usarse como parte del catalizador de una o más formas. Por ejemplo, en una realización, el TiO2 puede incluir uno o más metales depositados por coprecipitación o impregnación (por ejemplo, impregnación a humedad incipiente). En otra realización, el TiO2 puede coprecipitarse o impregnarse sobre soporte de carbono (por ejemplo, TiO2/C). En otra realización más, el TiO2 se puede usar en combinación con otros catalizadores, de manera que el TiO2 sea un catalizador de una mezcla de catalizadores utilizados. Por ejemplo, el
TÍO2 puede usarse en una mezcla con uno o más catalizadores que contienen metales. Tales ejemplos pueden incluir una mezcla de catalizadores: Pd-Cu/HT y TO 2; Pd-Cu/HT-C y TO 2; Cu/ZnO/A^O3 y Pd/C y La2O3 y TO 2; o Cu/ZnO/Al2O3 y Pd/C y CeO2 y TiO2; o Cu/ZnO/Al2O3 y Pd/C y MgO y TO 2.
En ciertas realizaciones, el catalizador incluye Pd-Cu/HT, Pd-Cu/HT-C, Pd-Cu/HT/C, Pd/HT, Cu/HT, Cu/ZnO/AhO3 , hidroxiapatita, perovskita, Cu/MgO, (Cu/ZnO/Al2Oa)/HT, BaO/SiO2, MgO/SiO2 , SrO/SiO2, CaO/SiO2 , SrO/MgO, CaO/MgO, Pd-Cu/NiHT, Cu/NiHT, PdCu/ZnHT, Cu/ZnHT, PdCu/ZnHT, Ru/HT, Cu-Ru/HT, Co/HT, Pt/HT, Pt-Cu/HT, Cu/SiO2, Pd/C, CaO/C, SrO/C, BaO/C, La2Oa/C, CeO2/C, HT/C, HT, CeO2 , La2O3, TiO2 o ceolita. Para una mayor claridad, debe entenderse que "Pd-Cu/HT-C" se refiere a paladio y cobre impregnados en un soporte de hidrotalcita mezclada con carbono, donde como "Pd-Cu/HT/C" se refiere a paladio y cobre impregnados en un soporte de hidrotalcita impregnado en carbono. También debe entenderse que puede usarse cualquier combinación de los catalizadores anteriores. En ciertas realizaciones, se puede usar cualquier combinación de los catalizadores anteriores, siempre que al menos un metal (incluyendo, por ejemplo, al menos un óxido metálico) está presente en el catalizador.
En una realización, el catalizador incluye:
Pd-Cu/HT;
Pd-Cu/HT/C;
Pd-Cu/HT y ceolita;
Pd-Cu/HT/C y ceolita;
Pd-Cu/HT y TiO2;
Pd-Cu/HT-C y TiO2;
Pd-Cu/HT/C y TiO2;
Pd/HT;
Cu/HT;
Pd/C y HT
Pd-Cu/C y HT
Pd/HT-C;
Pd/HT/C;
Pd-Cu/HT-C;
Cu/ZnO/Al2O3 e hidroxiapatita;
Cu/ZnO/Al2O3 y perovskita;
Cu/MgO;
Cu/ZnO/Al2O3 y HT;
Cu/ZnO/Al2O3 y BaO/SiO2 ;
Cu/ZnO/Al2O3 y MgO/SiO2;
Cu/ZnO/Al2O3 y SrO/SiO2;
Cu/ZnO/Al2O3 y CaO/SiO2;
Cu/ZnO/Al2O3 y SrO/MgO;
Cu/ZnO/Al2O3 y CaO/MgO;
Cu/SiO2 y CaO/MgO;
Pd-Cu/CaO-MgO;
Pd-Cu/NiHT;
Cu/NiHT;
Pd-Cu/ZnHT;
Cu/ZnHT;
Ru/HT;
Cu-Ru/HT;
Co/HT;
Pt/HT;
Pt-Cu/HT;
Cu/SiO2, Pd/C y CaO/C;
Cu/SiO2, Pd/C y SrO/C;
Cu/SiO2, Pd/C y BaO/C;
Cu/SiO2, Pd/C y La2O3/C;
Cu/SiO2, Pd/C y CeO2/C;
Cu/SiO2, Pd/C y HT/C;
Cu/SiO2, Pd/C y HT;
Cu/ZnO/Al2O3, Pd/C y HT;
Cu/ZnO/Al2O3 y CeO2;
Cu/ZnO/Al2O3, Pd/C y CeO2;
Cu/ZnO/Al2O3 y La2O3;
Cu/ZnO/Al2O3, Pd/C y La2O3 ;
Cu/ZnO/Al2O3, Pd/C, La2O3, y TiO2;
Cu/ZnO/Al2O3, Pd/C y CeO2;
Cu/ZnO/Al2Oa, Pd/C, CeO2 y TÍO2,
Pd-Cu/ZnO/HT;
Cu/ZnO/HT;
Cu/ZnO/Al2O3 y MgO;
Cu/ZnO/Al2O3, Pd/C y MgO; o
Cu/ZnO/Al2O3, Pd/C, MgO y TÍO2.
Debe entenderse que los catalizadores de ejemplo descritos anteriormente pueden usarse para cualquiera de los métodos descritos en el presente documento para producir una o más cetonas a partir de compuestos de fórmula (I) y alcoholes o aldehídos de fórmula (II).
e) Disolvente y condiciones de reacción
Disolvente
Por lo general, tanto las reacciones intermoleculares como las intramoleculares descritas anteriormente pueden llevarse a cabo en un disolvente acuoso, orgánico o bifásico acuoso y orgánico. En algunas realizaciones, el sistema de disolvente bifásico acuoso y orgánico puede dar altas conversiones y altas selectividades para productos particulares. Los ejemplos de disolventes orgánicos que se pueden usar en un sistema de disolvente de un solo componente o en un sistema de disolvente bifásico incluyen tolueno, trimetil-acetonitrilo, dimetilformamida, acetato de propilo, dioxano, butanol, hexanol, octanol y cualquier mezcla de los mismos. En algunas realizaciones, el disolvente orgánico utilizado en el sistema de disolvente bifásico es un disolvente aromático, tal como, por ejemplo, tolueno.
Temperatura de reacción
Las temperaturas de funcionamiento utilizadas en los métodos descritos en el presente documento para producir una o más cetonas pueden variar. El intervalo de temperatura de funcionamiento se refiere al intervalo de temperaturas en una zona de reacción.
En algunas realizaciones, la temperatura de funcionamiento es la temperatura de reflujo del disolvente si se usa uno. En otras realizaciones, la mezcla de reacción que contiene los compuestos de fórmula (I) y/o fórmula (II) y el catalizador básico se calienta a un intervalo de temperatura de funcionamiento adecuado para aumentar la selectividad para una o más cetonas ramificadas.
El intervalo de temperatura de funcionamiento seleccionado puede variar dependiendo de varios factores, incluyendo el disolvente y el catalizador básico utilizado. En algunas realizaciones, el intervalo de temperatura de funcionamiento está entre aproximadamente 25 °C y aproximadamente 400 °C, entre aproximadamente 50 °C y aproximadamente 350 °C, o entre aproximadamente 60 °C y aproximadamente 200 °C.
En algunas realizaciones, en el sistema de reacción donde se utiliza un sistema de disolvente bifásico como tolueno y agua como disolvente, el intervalo de temperatura de funcionamiento está entre aproximadamente 25 °C y aproximadamente 250 °C, o entre aproximadamente 50 °C y 200 °C.
En algunas realizaciones, la reacción puede ser exotérmica y se puede utilizar enfriamiento entre etapas para mantener la temperatura a la temperatura de funcionamiento.
Tiempo de reacción
En algunas realizaciones, la reacción puede llevarse a cabo durante 24 horas, pero el tiempo de reacción también variará con las condiciones de reacción (por ejemplo, la temperatura de reacción), la actividad catalizadora, el rendimiento deseado y la conversión deseada (por ejemplo, baja conversión con reciclado). En algunas realizaciones, el tiempo de reacción está determinado por la velocidad de conversión del material de partida o materiales de partida. En otras realizaciones, el tiempo de reacción está determinado por la velocidad de formación de productos particulares, tales como productos ramificados. En otras realizaciones, la mezcla de reacción se calienta durante de 10 a 30 horas. En otras realizaciones, la mezcla de reacción se calienta durante de 10 a 20 horas. En aún otras realizaciones, la mezcla de reacción se calienta durante de 1 a 10 horas. En aún otras realizaciones, la mezcla de reacción se calienta durante de 30 minutos a 10 horas.
Presión de funcionamiento
La presión de funcionamiento de los métodos descritos en el presente documento para producir las una o más cetonas puede variar. La presión de funcionamiento se refiere a la presión a través de una zona de reacción. En algunas realizaciones, la presión es entre 1 atm. y 60 atm.
Producción de diésel
Las cetonas de fórmula (A) producidas por reacción intermolecular entre los compuestos de las fórmulas (I) y (II) pueden ser adecuadas para su uso como precursores de diésel. Dichas cetonas se pueden hidrogenar para producir alcanos adecuados para su uso como diésel.
Una reacción general de ejemplo para producir diésel es:
Otras reacciones de ejemplo pueden incluir, por ejemplo:
En algunas realizaciones, los compuestos de fórmula (A) pueden hidrogenarse para producir alcanos con al menos seis átomos de carbono. En ciertas realizaciones, los compuestos de fórmula (A) pueden hidrogenarse para producir alcanos C11-C16. En otras realizaciones, los compuestos de fórmula (A) pueden hidrogenarse para producir alcanos con un índice de cetano de al menos 50, al menos 60, al menos 70 o al menos 80. En una realización, los alcanos tienen un índice de cetano de 83 o 100.
En una realización, los alcanos se seleccionan de:
y cualquiera de las mezclas de los mismos.
La formación de productos de condensación en los que los productos ramificados se forman con hexanodiona proporciona alcanos ramificados. Los alcanos ramificados reducen el punto de turbidez del combustible sin disminuciones significativas del índice de cetano.
En algunas realizaciones, la hidrogenación puede tener lugar con o sin descarbonilación.
Cualquier método adecuado conocido en la técnica puede usarse en compuestos hidrogenados de fórmula (A) para producir alcanos. Por ejemplo, véase He y Wang, Catalysis for Sustainable Energy, 2012, 1, 28-52; West, et al., Catalysis for Sustainable Energy, 2008, 1, 417-424.
Producción de lubricantes
a) Cetonas y alcoholes en lubricantes, no es parte de la invención
Ciertas cetonas y alcoholes se pueden combinar para formar precursores de lubricantes. En algunos ejemplos de referencia, la cetona puede ser una metilcetona. En una variación del ejemplo de referencia, la cetona es acetona. En algunas realizaciones, el alcohol es 2-etilhexanol:
En algunas realizaciones, la cetona formada (tal como la cetona C11 representada en el esquema de ejemplo anterior) puede hidrogenarse y deshidratarse para formar el alqueno (tal como un alqueno C11). A continuación, el alqueno se puede oligomerizar para formar alcanos como se muestra en el siguiente esquema de reacción de ejemplo:
Las reacciones de hidrogenación, deshidratación y oligomerización pueden llevarse a cabo usando procedimientos conocidos en la técnica. En algunas realizaciones, un catalizador de hidrogenación que comprende uno o más metales seleccionados del grupo que consiste en Cu, Ni, Pt, Pd, Rh, Ru e Ir pueden usarse en la reacción de hidrogenación. En algunas realizaciones, el catalizador de hidrogenación es Pd/C, Pd/AhOa, Pt/C, Pt/AhO3, Ru/C, Ru/Al2O3, Rh/C, Rh/Al2O3 o mezclas de los mismos. En algunas realizaciones, el catalizador de hidrogenación es Pd/C o Pt/C.
En algunas realizaciones, el catalizador de hidrogenación también puede causar descarbonilación.
En el presente documento también se proporcionan métodos para producir uno o más compuestos de fórmula (IX), poniendo en contacto una cetona de fórmula (VII) con un diol de fórmula (VIII) para producir uno o más compuestos de fórmula (IX).
La cetona de fórmula (VII) tiene la siguiente estructura:
en la que:
R14 es alquilo; y
R15 es H o metilo.
En algunas realizaciones de la cetona de fórmula (VII), R14 es alquilo C1-20, alquilo C1-15, alquilo C1-10 o alquilo C1-5. En ciertas realizaciones, R14 es metilo, etilo, propilo o butilo. En ciertas realizaciones, R14 es H.
El diol de fórmula (VIII) tiene la siguiente estructura:
en la que t es un número entero mayor o igual a 4.
En algunas realizaciones, t es 4-30, 4-25, 4-20, 4-15 o 4-10. En ciertas realizaciones, el diol de fórmula (VIII) es hexanodiol o heptanodiol.
El uno o más compuestos de fórmula (IX) tienen la siguiente estructura:
en la que:
R14 es como se ha descrito anteriormente para la fórmula (VII)
R16 es -CH2-; y
t es como se ha descrito anteriormente para la fórmula (VIII).
Con referencia a los métodos para producir uno o más compuestos de fórmula (IX), en una reacción de ejemplo, la cetona es 2-butanona y el diol es 1,6-hexanodiol:
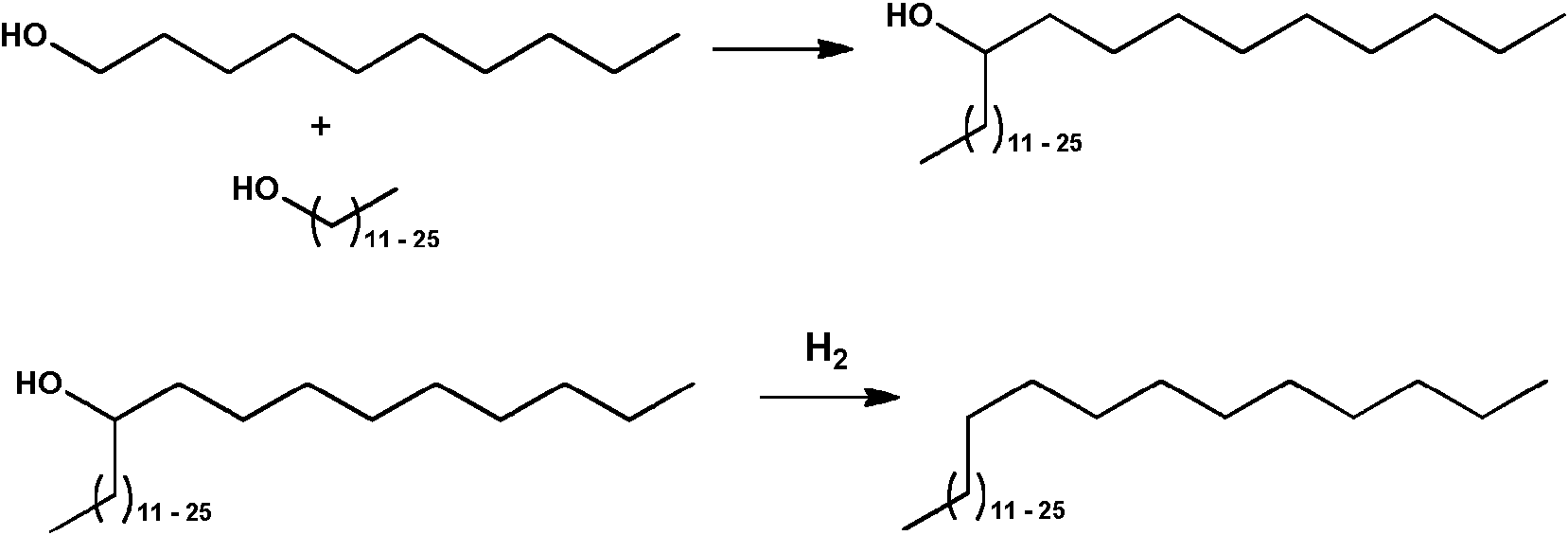
En algunas realizaciones de referencia, la reacción se lleva a cabo con un exceso de la cetona (por ejemplo, 2-butanona, anterior) de modo que el compuesto C10 es el producto principal. Este resultado es inesperado, ya que un experto en la materia esperaría que se llevara a cabo la reacción con un exceso de alcohol (por ejemplo, 1 ,6 -hexanodiol) conduciría al compuesto C10 como producto principal. En algunas realizaciones, el compuesto C10 se puede hidrogenar y el alcohol secundario preferentemente se hidrogena para dar 1 -decanol usando procedimientos conocidos en la técnica. En algunas realizaciones, el 1-decanol se puede convertir en 1-deceno que, a continuación, se oligomeriza a lubricantes C30 usando procedimientos conocidos en la técnica como se muestra en el esquema de reacción de ejemplo:
Como alternativa, una reacción de Guerbet con el alcohol C10 y un alcohol C12-C26 producirá lubricantes C24-C36 como se muestra en el siguiente esquema de reacción de ejemplo:
En algunas realizaciones, las cetonas de fórmula (A) o las cetonas de fórmula (C) descritas anteriormente pueden hacerse reaccionar con los uno o más alcoholes para formar los lubricantes. Se entenderá que cualquier combinación de cetonas y alcoholes que contenga el número apropiado de carbonos se puede combinar para formar lubricantes C24-C36. La reacción de Guerbet se puede llevar a cabo utilizando catalizador metálico y, opcionalmente, un base. En algunas realizaciones, el catalizador metálico y, opcionalmente, una base puede ser el mismo catalizador y base que la reacción de la cetona con uno o más alcoholes. En otras realizaciones, el catalizador metálico, y opcionalmente una base, puede ser un catalizador y una base diferentes como la reacción de la cetona con uno o más alcoholes.
En algunas realizaciones, una cetona puede reaccionar con dos alcoholes para formar una cetona superior. A continuación, la cetona superior se hidrogena a un alcohol de fórmula (C1). A continuación, el alcohol de fórmula (C1) se hace reaccionar con uno o más alcoholes en una reacción de Guerbet para formar un alcohol de fórmula (C2). El alcohol de fórmula (C2) se puede hidrogenar después a los lubricantes C24-C36.
En algunas realizaciones, la hidrogenación puede tener lugar con o sin descarbonilación.
En algunas realizaciones, los alcoholes utilizados en el esquema de reacción anterior serán dioles, tal como 1,6-hexanodiol. Se entenderá que, en algunas realizaciones, se pueden producir alcanos C24-C36 a partir de la hidrogenación de alcohol (C1) sin la necesidad de reacciones posteriores de Guerbet dependiendo del número de átomos de carbono presentes en R8, R9 y R10. También se entenderá que, en algunas realizaciones, el alcohol (C1) puede reaccionar con solo un alcohol adicional en lugar de dos moléculas de alcohol como se ha mostrado anteriormente. En algunas realizaciones, un catalizador de hidrogenación que comprende uno o más metales seleccionados del grupo que consiste en Cu, Ni, Pt, Pd, Rh, Ru e Ir pueden usarse en la reacción de hidrogenación. En algunas realizaciones, el catalizador de hidrogenación es Pd/C, Pd/Al2O3 , Pt/C, Pt/AhO3, Ru/C, Ru/A^O3, Rh/C, Rh/Al2O3 o mezclas de los mismos. En algunas realizaciones, el catalizador de hidrogenación es Pd/C o Pt/C.
b) Aldehídos y alcoholes a lubricantes, no es parte de la invención
En algunas realizaciones de referencia, un aldehído puede reaccionar con uno o más alcoholes, catalizador metálico y, opcionalmente, una base para formar precursores de lubricantes que luego pueden convertirse en lubricantes. En algunas realizaciones, los lubricantes formados están en el intervalo de C24-C36. En algunas realizaciones, se puede hacer reaccionar un aldehído de fórmula (V) con uno o más alcoholes de fórmula (VI), catalizador metálico y, opcionalmente, una base para formar uno o más precursores lubricantes de fórmula (E) de acuerdo con el siguiente esquema de reacción de ejemplo:
en el que cada R12 y R13 se seleccionan independientemente entre el grupo que consiste en alquilo, arilo, alquenilo, alquinilo y heteroarilo.
En algunas realizaciones, cada R12 y R13 se selecciona independientemente del grupo que consiste en hidrógeno y alquilo C1-C20, arilo C6-C20, alquenilo C2-C20, alquinilo C2-C20 y heteroarilo C4-C21. En ciertas realizaciones, cada R12 y R13 se selecciona independientemente del grupo que consiste en hidrógeno y alquilo C1-C10, arilo C6-C20, alquenilo C2-C10, alquinilo C2-C10 y heteroarilo C4-C21.
En algunas realizaciones, el alcohol es un diol, tal como 1,6-hexanodiol, como se muestra en la siguiente reacción de ejemplo con acetaldehído:
Se entenderá que se pueden formar diversos productos debido a las reacciones de autocondensación de aldol con el aldehído y la reacción de alquilación con el alcohol. Por ejemplo, los productos formados en la reacción de ejemplo de 1,6-hexanodiol con butiraldehído pueden incluir los siguientes:
En algunas realizaciones, el aldehído C10 formado se puede hidrogenar a 1,10-decanodiol. En otras realizaciones, el 1,10-decanodiol se puede hidrogenar a 1-decanol. En algunas realizaciones, un catalizador de hidrogenación que comprende uno o más metales seleccionados del grupo que consiste en Cu, Ni, Pt, Pd, Rh, Ru e Ir pueden usarse en la reacción de hidrogenación. En algunas realizaciones, el catalizador de hidrogenación es Pd/C, Pd/AhO3, Pt/C, Pt/Al2O3, Ru/C, Ru/Al2O3, Rh/C, Rh/Al2O3 o mezclas de los mismos. En algunas realizaciones, el catalizador de hidrogenación es Pd/C o Pt/C. En algunas realizaciones, el 1-decanol se puede convertir en 1-deceno que luego se
convierte en lubricantes C30 mediante procesos conocidos en la técnica. En otras realizaciones, el 1-decanol puede hacerse reaccionar con uno o más alcoholes en una reacción de Guerbet para formar alcoholes C24-C36 que se convierten en los lubricantes C24-C36. La reacción de Guerbet se puede llevar a cabo utilizando catalizador metálico y, opcionalmente, un base. El catalizador metálico y opcionalmente una base puede ser el mismo catalizador y base que la reacción de la cetona o aldehído con uno o más alcoholes.
En algunas realizaciones, el aldehído C10 se puede descarbonilar para formar un alcohol Cg. El alcohol Cg se convierte después en un alqueno y se oligomeriza para formar un alcano C27, o el alcohol Cg puede someterse a química de Guerbet, seguida de hidrogenación para formar un alcano C27.
c) Condiciones de reacción para la producción de lubricantes
El catalizador metálico
Ciertos catalizadores metálicos que pueden catalizar la reacción de la cetona o los aldehidos con uno o más alcoholes pueden emplearse en los métodos descritos en el presente documento. Ciertos catalizadores metálicos que pueden catalizar la reacción de Guerbet pueden emplearse en los métodos descritos en el presente documento. Los catalizadores metálicos que pueden catalizar la reacción de la cetona o los aldehidos con el uno o más alcoholes y los catalizadores metálicos que pueden catalizar la reacción de Guerbet pueden ser iguales o diferentes. En algunas realizaciones, el catalizador metálico que cataliza la reacción de la cetona o los aldehidos con uno o más alcoholes y el catalizador metálico que cataliza la reacción de Guerbet son los mismos, tales como, por ejemplo, Pd/C o Pt/C. En algunas realizaciones, el catalizador metálico que cataliza la reacción de la cetona o los aldehidos con uno o más alcoholes y el catalizador metálico que cataliza la reacción de Guerbet son diferentes. Se entenderá que incluso si los catalizadores son los mismos, la base, el disolvente, la temperatura, el tiempo de reacción y todas las demás variables de reacción posibles pueden necesitar optimizarse para obtener los rendimientos más altos y las selectividades más altas para el producto deseado (por ejemplo, cetonas superiores, aldehidos superiores o productos Guerbet).
En algunas realizaciones, el catalizador metálico incluye un metal de transición. En algunas realizaciones, el catalizador a base de metal incluye un metal de transición tardia. En algunas realizaciones, el catalizador metálico incluye un metal seleccionado del grupo que consiste en rutenio, hierro, paladio, platino, cobalto y cobre. También se contemplan mezclas de estos metales, incluyendo, por ejemplo, aleaciones metálicas. En algunas realizaciones preferidas, el metal es paladio.
En otras realizaciones, el catalizador metálico puede incluir metales de transición, tales como niquel, rutenio, rodio, paladio, renio, iridio o platino. En otras realizaciones, el catalizador metálico incluye paladio o platino. En ciertas realizaciones, el catalizador metálico es [Ir(COD)Cl]2, RuCh(COD), PtCh(COD), [Rh(COD)Cl]2, Ni/si-Alúmina, Ru/C, Rh/C, Pt/C o Pd/C.
En algunas realizaciones, el catalizador metálico es un óxido metálico de un solo componente, un óxido de metal alcalinotérreo u óxido de tierras raras (por ejemplo, ThO2 , ZrO2, ZnO, TO 2).
En aún otras realizaciones, el catalizador metálico es un catalizador a base de paladio. Los catalizadores a base de paladio pueden incluir metal de paladio y complejos de ligandos adecuados, incluidos aquellos que contienen átomos de P y/o N para coordinar los átomos de paladio y otras sales de paladio simples, ya sea en presencia o ausencia de ligandos. Los catalizadores a base de paladio también pueden incluir paladio y complejos de paladio soportados o fijados sobre soportes sólidos, tales como paladio sobre carbono (Pd/C), asi como negro de paladio, racimos de paladio o racimos de paladio que contienen otros metales. Los ejemplos adecuados de catalizadores a base de paladio pueden incluir Pd(OAc)2, Pd2(dba)3 , Pd(OH)2/C, Pd/C, Pd/CaCO3, Pd/Alúmina y Pd-polietileniminas sobre silice.
Soporte de catalizador
En algunas realizaciones, el catalizador metálico puede ser un catalizador metálico con soporte sólido. Un catalizador metálico con soporte sólido usado en el presente documento normalmente es un catalizador metálico en el que el metal se deposita o se impregna sobre un soporte.
En algunas realizaciones, el soporte se selecciona del grupo que consiste en hidrotalcita, óxidos metálicos monocomponente, óxidos alcalinotérreos, óxidos de metales alcalinos, óxidos de tierras raras, ThO2, MgO, MgO dopado con Na, SrO, BaO, CaO, ZnO, La2O3 , TO 2 , ZrO2, A^O3, hidroxiapatita, fluorapatita, terc-butoxiapatita, sepiolita, ceolitas básicas, ceolitas de intercambio iónico alcalino, ceolitas con iones alcalinos añadidos, Pd/NaY ceolita, Pd/NH4-p ceolita, iones de metales alcalinos soportados, iones de metales alcalinos sobre alúmina, iones de metales alcalinos sobre silice, metal alcalino sobre óxido de alcalinotérreo, metales alcalinos e hidróxidos de metales alcalinos sobre alúmina, Metal/SiO2, Na/SiO2 Pd/Na/SiO2 , Na/Ca/SiO2 , Na/Ca/SiO2, Cs/SiO2 , ceolita soportada sobre metal, óxido de potasio soportado sobre ceolita Y, crisotilos sintéticos, Mg3(OH)4Si4O5, crisotilo sustituido con cobalto (II), silice mesoporosa con funcionalidad amino, MCM-41 con funcionalidad amino, silice mesoporosa con
intercambio de iones alcalinos, SBA-15 con intercambio de iones alcalinos, MgO soportado en líquido iónico, aluminofosfato amorfo, talcos sintéticos, organosilicatos de magnesio, KF soportado sobre alúmina, lantánido imida sobre ceolita y lantánido nitruro sobre ceolita. En algunas realizaciones, el soporte es una ceolita con intercambio alcalino, tal como NaY, KY, RbY, CsY, NaX, KX, RbX y CsX. En algunas realizaciones, un metal, tal como Pd o Cu, se deposita sobre la ceolita intercambiada con álcali y se usa como catalizador a base de metal, tal como, por ejemplo, Pd/CsY y Cu/CsY. En algunas realizaciones, se añaden iones de metales alcalinos al soporte (por ejemplo, iones de metales alcalinos sobre alúmina, iones de metales alcalinos sobre sílice, metal alcalino sobre óxido de alcalinotérreo, metales alcalinos e hidróxidos de metales alcalinos sobre alúmina).
En algunas realizaciones, el soporte es una hidrotalcita o un material derivado de una hidrotalcita. En algunas realizaciones, la hidrotalcita o material derivado de una hidrotalcita comprende uno o más metales seleccionados del grupo que consiste en magnesio, aluminio, litio, cinc, cobre y níquel. En algunas realizaciones, la hidrotalcita o material derivado de una hidrotalcita comprende uno o más metales seleccionados del grupo que consiste en Mg, Al, Li, Zn, Cu y Ni. La basicidad de las hidrotalcitas se puede ajustar variando la relación magnesio-aluminio, rehidratando la hidrotalcita calcinada o dopando la hidrotalcita con Na y K. En algunas realizaciones, las hidrotalcitas se preparan por coprecipitación de sales de metales alcalinotérreos y/o nitratos de aluminio en una solución que incluye urea o amoníaco y carbonato de amonio o hidróxido de potasio y carbonato de potasio o hidróxido de sodio y carbonato de sodio. En algunas realizaciones, los soportes de metal alcalinotérreo pueden prepararse por descomposición de nitrato, sales de carbonato o ácido dicarboxílico a temperaturas elevadas, de 450 °C a 900 °C. Catalizadores básicos
En algunas realizaciones, los catalizadores incluyen uno o más metales y un soporte básico.
La basicidad del catalizador puede medirse mediante diversas técnicas conocidas por un experto en la materia. Por ejemplo, la basicidad del catalizador se puede medir mediante la desorción programada por temperatura de CO2 (TPD). En algunas realizaciones, la TPD de CO2 se lleva a cabo adsorbiendo CO2 al catalizador a temperatura ambiente y calentando hasta 773 K (o un ensayo similar). En algunas realizaciones, para catalizadores no ceolíticos, los catalizadores preferidos tienen densidades de sitio de base medidas por TPD de CO2 de al menos 50 micromoles/gramo de catalizador. En otras realizaciones, para catalizadores de ceolita, los catalizadores preferidos tienen densidades de sitio de base por TPD de CO2 de al menos 10 micromoles/gramo de catalizador. En otras realizaciones, todos los catalizadores preferidos de todos los tipos tienen densidades de sitio de base por TPD de CO2 de al menos 10 micromoles/gramo de catalizador.
La basicidad del catalizador también se puede medir usando la determinación de carga cero (Regalbuto), o usando el método del indicador Hammett.
En algunas realizaciones, los catalizadores metálicos tienen un pKa de 10 a 16. En otras realizaciones, los catalizadores metálicos tienen un pKa de 11 a 15. En algunas realizaciones, los catalizadores metálicos tienen una desorción de CO2 de al menos 200 °C. La determinación cuantitativa del pKa y otros métodos para caracterizar la basicidad de un soporte de catalizador tal como hidrotalcita son conocidos en la técnica. Véase, por ejemplo, A. Corma, et al., J. of Catalysis, 1992, 134, 58 y D. Debecker, et al., Chem. Eur. J., 2009, 15, 3920.
Debe entenderse que el catalizador metálico puede prepararse por cualquier método conocido por un experto en la materia. Por ejemplo, la impregnación a humedad incipiente es una técnica de ejemplo que se puede utilizar. En un ejemplo, se puede combinar un soporte, tal como hidrotalcita y sal metálica, tal como cloruro de paladio o acetato de cobre y se añade un disolvente, tal como agua. Se permite que la sal metálica y el soporte reaccionen durante un período de tiempo entre 1 y 24 horas a una temperatura entre temperatura ambiente y 200 °C, o más específicamente, entre 50 y 120 °C. La mezcla de reacción se puede agitar en una atmósfera de hidrógeno. A continuación, el catalizador sólido se filtra y se lava con grandes cantidades de disolvente. A continuación, el sólido se puede secar al vacío a una temperatura entre 80 y 150 °C. Opcionalmente, se pueden añadir otros aditivos a la mezcla de reacción tales como sales de metales alcalinos (por ejemplo, cloruro de sodio o cloruro de potasio) o una base como se ha descrito anteriormente.
El catalizador metálico también se puede preparar por impregnación a humedad incipiente de sales metálicas sobre soportes básicos, seguido de calcinación a temperaturas superiores a 300 °C en aire o gases inertes y/o reducción en mezclas de hidrógeno y gases inertes. Como alternativa, el catalizador metálico puede prepararse sintetizando nanopartículas metálicas ex situ y soportando dichas nanopartículas en el soporte metálico básico usando un disolvente. En algunas realizaciones, el catalizador metálico preparado por impregnación a humedad incipiente incluye al menos dos metales.
El catalizador metálico también se puede preparar usando los métodos mencionados anteriormente para soportar metales sobre soportes básicos, con la diferencia de que los soportes son inertes e incluyen SiO2 y carbono. Los soportes básicos también se preparan como se ha mencionado anteriormente, pero no hay metal soportado en ellos. Los soportes básicos y los catalizadores metálicos se mezclan físicamente antes de la reacción.
El catalizador metálico también se puede preparar por impregnación simultánea o sucesiva a humedad incipiente de soluciones de sales de nitrato o acetato de metales alcalinos o alcalinotérreos y sales o complejos apropiados de los metales desvelados en el presente documento sobre soportes inertes, seguido de calcinación y reducción en las condiciones mencionadas anteriormente. Como alternativa, el catalizador metálico puede prepararse por impregnación a humedad incipiente de sales alcalinas sobre soportes inertes, seguido de calcinación e impregnación a humedad incipiente de nanopartículas metálicas sintetizadas ex situ.
Base
En algunas realizaciones, se usa una base en combinación con el catalizador metálico para convertir la cetona o el aldehído y uno o más alcoholes en una o más cetonas o aldehídos superiores (por ejemplo, precursores de lubricantes) que luego se hidrogenan para formar lubricantes. Debería entenderse que, en ciertas realizaciones, incluso cuando el catalizador metálico tiene un soporte básico, la base puede añadirse adicionalmente a la mezcla de reacción.
Se pueden usar bases que promueven la alquilación de la cetona o aldehído con uno o más alcoholes. En determinadas realizaciones preferidas, la base es K3PO4. En algunas realizaciones, la base y el catalizador metálico son dos componentes separados que pueden combinarse y ponerse en contacto con los reactivos. En otras realizaciones, la base se soporta primero o se impregna en un material de soporte que normalmente contiene el catalizador metálico y se pone en contacto con los reactivos.
Las bases adecuadas pueden incluir bases inorgánicas (por ejemplo, hidróxidos de metales alcalinos y metales alcalinotérreos) y bases orgánicas. Los ejemplos de bases inorgánicas pueden incluir hidróxido de potasio, hidróxido de bario, hidróxido de cesio, hidróxido sódico, hidróxido de estroncio, hidróxido de calcio, hidróxido de litio, hidróxido de rubidio e hidróxido de magnesio. Los ejemplos de bases orgánicas pueden incluir trietilamina, trimetilamina, piridina y metilamina.
En algunas realizaciones, la base tiene un pKa de 10 a 16. En otras realizaciones, la base tiene un pKa de 11 a 15. En ciertas realizaciones, la base es KOH, Ba(OH)2.8 H2O, K2CO3 , KOAc, KH2PO4, Na2HPO4, piridina o Et3N.
El tipo de base utilizado puede determinarse por la resistencia deseada de la base y su capacidad para promover la alquilación de una cetona o aldehído, sin producir reacciones secundarias o productos secundarios indeseables. La cantidad de base seleccionada puede afectar al rendimiento global de la reacción y la proporción de productos alquilados. En ciertas realizaciones, el tipo de base utilizado puede determinarse por la resistencia deseada de la base y su capacidad para promover la alquilación de la cetona o aldehído, sin producir reacciones secundarias o productos secundarios indeseables. La cantidad de base seleccionada puede afectar al rendimiento general de la reacción.
En aún otras realizaciones, la base utilizada puede calcinarse. En dichas realizaciones, la base se puede tratar previamente a una temperatura alta para obtener un material más activo. Por ejemplo, en una realización en la que K3PO4 es la base utilizada, el K3PO4 se puede calentar a aproximadamente 600 °C para obtener un material que sea más activo en la promoción de la reacción de alquilación descrita en el presente documento.
Disolvente
En algunas realizaciones, los métodos para producir los precursores de lubricantes se realizan de forma ordenada, es decir, sin adición de disolvente. Sin embargo, en otras realizaciones, los métodos para producir los precursores de lubricantes pueden realizarse con un disolvente.
Cualquier disolvente que promueva la alquilación de la cetona o aldehído puede emplearse en el proceso descrito en el presente documento. Por ejemplo, el disolvente puede ser un disolvente orgánico. Los disolventes orgánicos pueden incluir compuestos aromáticos (por ejemplo, tolueno, benceno), cetonas (por ejemplo, acetona o metiletilcetona), acetatos (por ejemplo, acetato de etilo o acetato de isopropilo), nitrilos (por ejemplo, acetonitrilo), alcoholes (por ejemplo, butanol, etanol, isopropanol) o éteres (por ejemplo, diglima, monoglima, diglibu, THF). Como se usa en el presente documento, "diglima" se refiere a éter dimetílico de dietilenglicol. Como se usa en el presente documento, "diglibu" se refiere a éter dibutílico de dietilenglicol.
Temperatura de funcionamiento
Las temperaturas de funcionamiento utilizadas en los métodos descritos en el presente documento para producir los precursores de lubricantes pueden variar. El intervalo de temperatura de funcionamiento se refiere al intervalo de temperaturas en una zona de reacción. En algunas realizaciones, la temperatura de funcionamiento es la temperatura de reflujo del disolvente si se usa uno. El intervalo de temperatura de funcionamiento seleccionado puede variar dependiendo de varios factores, incluyendo el disolvente, la base y el catalizador utilizados. En algunas realizaciones, el intervalo de temperatura de funcionamiento está entre aproximadamente 100 °C y aproximadamente 400 °C, entre aproximadamente 190 °C y aproximadamente 350 °C, o entre aproximadamente
220 °C y aproximadamente 270 °C.
En algunas realizaciones, en el sistema de reacción en el que se usa tolueno como disolvente, el intervalo de temperatura de funcionamiento está entre aproximadamente 110 °C y aproximadamente 250 °C, o entre aproximadamente 180 °C y 250 °C.
En algunas realizaciones, la reacción puede ser exotérmica y se puede utilizar enfriamiento entre etapas para mantener la temperatura a la temperatura de funcionamiento.
Presión de funcionamiento
La presión de funcionamiento de los métodos descritos en el presente documento para producir las cetonas de hidrocarbono puede variar. La presión de funcionamiento se refiere a la presión a través de una zona de reacción. En algunas realizaciones, la presión es entre 1 atm. y 60 atm.
Tiempo de reacción
En algunas realizaciones, la reacción puede llevarse a cabo durante 24 horas, pero el tiempo de reacción también variará con las condiciones de reacción (por ejemplo, la temperatura de reacción), la actividad catalizadora, el rendimiento deseado y la conversión deseada (por ejemplo, baja conversión con reciclado). En algunas realizaciones, el tiempo de reacción está determinado por la velocidad de conversión del material de partida. En otras realizaciones, la mezcla de reacción se calienta durante de 10 a 30 horas. En otras realizaciones, la mezcla de reacción se calienta durante de 10 a 20 horas. En aún otras realizaciones, la mezcla de reacción se calienta durante de 1 a 10 horas. En aún otras realizaciones, la mezcla de reacción se calienta durante de 30 minutos a 10 horas. d) Otras vías a los lubricantes
Otras reacciones de ejemplo para producir lubricantes pueden incluir, por ejemplo:
La hidrogenación puede tener lugar mediante procesos conocidos en la técnica. En algunas realizaciones, la hidrogenación puede tener lugar con o sin descarbonilación.
En algunas realizaciones, un catalizador de hidrogenación que comprende uno o más metales seleccionados del grupo que consiste en Cu, Ni, Pt, Pd, Rh, Ru e Ir pueden usarse en la reacción de hidrogenación. En algunas realizaciones, el catalizador de hidrogenación es Pd/C, Pd/A^Oa, Pt/C, Pt/A^Oa, Ru/C, Ru/A^Oa, Rh/C, Rh/A^Oa o mezclas de los mismos. En algunas realizaciones, el catalizador de hidrogenación es Pd/C o Pt/C.
Producción de aditivos de gasolina
Las cetonas de fórmula (B) producidas por reacción intramolecular de los compuestos de fórmula (I) pueden ser adecuadas para su uso como precursores de gasolina. Dichas cetonas se pueden hidrogenar para producir cicloalcanos adecuados para su uso como aditivos de gasolina.
Una reacción de referencia de ejemplo para producir aditivos de gasolina es:
En una realización, los aditivos de gasolina son
0 cualquier mezcla de las mismas.
Se puede usar cualquier método adecuado conocido en la técnica para la hidrogenación para producir cicloalcanos (opcionalmente sustituidos con -OH) adecuados para su uso como aditivos de gasolina. En algunas realizaciones, un catalizador de hidrogenación que comprende uno o más metales seleccionados del grupo que consiste en Cu, Ni, Pt, Pd, Rh, Ru e Ir pueden usarse en la reacción de hidrogenación. En algunas realizaciones, el catalizador de hidrogenación es Pd/C, Pd/AhOa, Pt/C, Pt/AhOa, Ru/C, Ru/A^Oa, Rh/C, Rh/AhOa o mezclas de los mismos. En algunas realizaciones, el catalizador de hidrogenación es Pd/C o Pt/C.
Como se usa en el presente documento, el término "aproximadamente" se refiere a una aproximación de un valor establecido dentro de un intervalo aceptable. Preferentemente, el intervalo es /-10 % del valor indicado.
Ejemplos
Los siguientes ejemplos son meramente ilustrativos y no pretenden limitar ningún aspecto de la presente divulgación de ninguna manera.
Ejemplo 1
Calcinación y caracterización de materiales de hidrotalcita
Se pesó un plato Pyrex a 180,82 g antes de la adición de hidrotalcita sintética (CHiaAhMgaO-ig 4 H2O; Aldrich: 652288-1 kg). Se añadieron aproximadamente 100,59 g de hidrotalcita al plato antes de la calcinación en el horno de calcinaciones de aire estático del primer piso. La calcinación se programó para 2 °C/min hasta 700 °C y se mantuvo durante 2 horas a temperatura. El material se enfrió después en el horno y se retiró después de enfriar a TA. Después del enfriamiento, se recuperaron 56,50 g de material. El material calcinado es Mg6A^Og (PM 343,76). Por lo tanto, la recuperación teórica sería de 56,94 g suponiendo una transferencia completa.
Ejemplo 2
Desorción programada por temperatura (TPD) de CO
2
en material derivado de hidrotalcita a 600 °C
Se midieron 200,0 mg de hidrotalcita sintética (CH16Al2Mg6O1g4H2O; Aldrich: 652288-1 kg) que se habían calcinado a 600 °C (2 °C/min) y mantenido durante 1 hora. El material se calentó a la temperatura de calcinación a 2 °C/min (perfil 4) bajo flujo de 10,0 ml/min de He (86,2 kPa (12,5 psi) en el inyector) con ventilación a la atmósfera. El material se mantuvo a la temperatura de calcinación durante 1 hora y luego se enfrió. A continuación se adsorbió el CO2 ajustando la temperatura del horno a 50 °C y la válvula inferior para ventilar a la atmósfera. Se hizo fluir CO2 sobre el lecho de catalizador (aproximadamente 200 mg) a 40 ml/min (punto de ajuste del rotámetro - 57) durante 1 hora. A continuación, el flujo de CO2 se volvió a cambiar a He. Después, el material se calentó a 100 °C a 10 °C/min bajo un flujo de He de 18,3 ml/min (137,9 kPa (20 psi) en el inyector). El material se mantuvo a temperatura durante 1 hora. La TPD se midió añadiendo una columna Drierite® al fondo del reactor. Se cargó el método TPD (1050 °C TPD) y se inyectó una sola muestra. El programa de temperatura del horno comenzó a 0 °C y se calentó a 10 °C/min hasta 1050 °C. La temperatura se mantuvo durante 30 minutos a 1050 °C. Luego se enfrió el horno. Después de completar la TPD, la masa de material recuperable fue de 185,0 mg con algo de material restante en el tubo. Esto indica que el material tenía baja humedad inicial o absorción de carbono. Los resultados se resumen en la Tabla 1 que se expone a continuación.
Tabla 1.
Ejemplo 3
Síntesis de catalizador de MgZrO a partir de nitrato de magnesio y oxicloruro de circonilo
Se añadió 1 l de agua nanopura a un matraz Erlenmeyer de 1 l. Se añadieron 50,9003 g de hexahidrato de nitrato de magnesio y 5,8517 g de octahidrato de oxicloruro de circonilo a 1 l de agua nanopura. La solución se agitó y luego se transfirió a un vaso de precipitados de 2 l. Se preparó una solución de NaOH 1 M de 900 ml mediante la adición de 35,9973 g de gránulos de NaOH a 900 ml de agua nanopura en una botella de pyrex de 1000 ml. La solución de NaOH 1 M se añadió por pipeta a la solución de MgO/ZrO2 con agitación hasta que el pH alcanzó 10. El pH inicial de la solución fue de 1,81 y se añadieron 400 ml de NaOH 1 M para alcanzar un pH de 10. Se formó un gel blanco turbio (rpm 600) que se agitó durante 2 horas. El material se dejó en reposo sin agitar durante 70 horas adicionales para envejecimiento. La formación de gel comenzó inmediatamente después de la adición de NaOH a la solución de MgO/ZrO2.
El procedimiento anterior se repitió en una segunda reacción. En esta reacción, el polvo blanco se separó en gran medida en una capa acuosa y sólida tras la adición de NaOH a la solución de MgO/ZrO2. La capa acuosa se eliminó. La capa sólida se filtró inicialmente; sin embargo, la filtración fue extremadamente lenta debido al taponamiento del filtro y al grosor del gel. La capa sólida/líquida se transfirió a catorce tubos de centrífuga de 50 ml. Los tubos se centrifugaron a 4.000 RPM durante 5 minutos para producir una separación limpia entre fases. Se recogieron aproximadamente 10 ml de sólido de cada uno de los tubos y se vertió la capa acuosa de 40 ml y se recogió. Cada tubo tenía agua Milipure fresca añadida a 50 ml y se agitó manualmente con una microespátula para obtener una buena dispersión. Los tubos se agitaron después y se centrifugaron nuevamente. De nuevo, se recuperaron 10 ml de sólido de cada tubo. Se repitió la adición de agua seguida de centrifugación. Después de esta repetición, quedaron aproximadamente 5 ml de sólido en cada tubo. La centrifugación durante 5 minutos produjo una dispersión del sólido en la fase líquida y un granulado sólido. La capa líquida combinada se recogió y se dejó durante la noche. El pH de la mezcla permaneció cerca de 10.
La capa líquida combinada del día anterior se volvió a centrifugar en 12 tubos de centrífuga durante 15 minutos, dando una separación limpia. Cada tubo contenía aproximadamente 3 ml de sólido. La capa líquida eliminada del material recentrifugado se filtró a través de un filtro de poliétersulfona de 0,22 pm, produciendo una capa líquida transparente. La pequeña capa de sólido se recogió y se combinó con los sólidos restantes. Los sólidos combinados de los 14 tubos originales se combinaron en 3 tubos con una microespátula. La transferencia completa se aseguró con dos lavados de 5-10 ml de cada tubo con agua Milipure. Los sólidos de los 12 tubos recentrifugados se combinaron de la misma manera en un tubo. El volumen sólido de los cuatro tubos de centrífuga combinados fue de aproximadamente 40 ml de sólidos totales. Los tubos combinados se centrifugaron durante 25 minutos a 4.000 RPM produciendo una buena separación de fases. A continuación, el material se filtró a través de un filtro de poliétersulfona de 0,22 pm produciendo un líquido transparente. Los tubos se enjuagaron tres veces con 10 ml de agua para garantizar una buena transferencia. El material se enjuagó por última vez con 150 ml de agua Milipure para eliminar cualquier NaOH restante. El pH del lavado final fue de 9,73. Una muestra de la capa líquida se almacenó en un vial de centelleo de 20 ml. El sólido se transfirió después de que se completó la filtración al vacío en un plato de pyrex que pesaba 180,82 g. Los sólidos añadidos pesaron aproximadamente 39,8 g. El sólido se puso luego en un horno de mufla a 120 °C y se secó durante 24 horas. Después de secarse, se recuperaron 12,25 g de sólido. Aproximadamente 100 mg de este material seco se almacenaron para pruebas adicionales. A continuación, el sólido restante se cubrió con parafilm y se almacenó para calcinación.
El material seco se colocó en un plato Pyrex y se calentó a 873 K en una rampa de 3 horas y se mantuvo a temperatura durante 3 horas en aire. Luego se enfrió a ~ 50 °C bajo enfriamiento convectivo natural y se recuperó 14 horas después de que comenzaron las calcinaciones. El material sólido se molió finamente en un mortero y una mano. Después de recoger el material finamente molido, se recolectó un total de 9,244 g de material y se colocó en una botella ámbar y se selló con parafilm para su uso posterior.
Ejemplo 4
Condensación aldólica de 2,5-hexanodiona a 25 °C y 50 °C
Se usaron tolueno (Fisher), 2,5-hexanodiona (Aldrich), dodecano (Aldrich) y furfural (Aldrich) tal como se recibieron. El MgAlO se calcinó como se describe en el Ejemplo 1. Una mezcla de 3,277 g de furfural, 1,123 g de DD, 1,769 g de 2,5-hexanodiona y 22,62 g de tolueno se prepararon en un vaso de precipitados pequeño. Una porción de esta mezcla, agua y el catalizador básico se añadió a un vial de centelleo como se expone en la Tabla 2 a continuación.
Tabla 2.
Reactor Ct. Mezcla (g) Ct. de agua (g) Cantidad base (mg) Tiempo de reacción (h) Temp. (°C) 1 2,215 g 2,00 g 50,0 de MgAlO 24 25 2 2,215 g 2,00 g 100,0 de MgAlO 24 25 3 2,215 g 2,00 g 200,0 de MgAlO 24 25 4 2,215 g 2,00 g 25,0 gl de NaOH 2M 24 25 5 2,215 g 2,00 g 200,0 gl de NaOH 2M 24 25 6 1,107 g 0,870 g de tolueno
fresco 2,00 g 100,0 de MgAlO 24 25 7 2,215 g 2,00 g 50,0 de MgAlO 24 50 8 2,215 g 2,00 g 100,0 de MgAlO 24 50 9 2,215 g 2,00 g 200,0 de MgAlO 24 50 10 2,215 g 2,00 g 25,0 gl de NaOH 2M 24 50 11 2,215 g 2,00 g 200,0 gl de NaOH 2M 24 50 12 1,107 g 0,870 g de tolueno
fresco 2,00 g 100,0 de MgAlO 24 50
Los reactores se colocaron en placas de agitación precalentadas y se agitaron a 800 RPM. Para cada reactor, todo el material se transfirió a un tubo de centrífuga de 15 ml y se centrifugó a 4.000 RPM. La capa orgánica se recogió en un segundo tubo de centrífuga de 15 ml. La fase acuosa se lavó 3 veces más con 4 ml de EtOAc y se centrifugó. Las fracciones orgánicas se combinaron y se secaron sobre Na2SO4. Una muestra de la capa orgánica se analizó por GC. Los resultados se resumen en la Tabla 3 que se expone a continuación.
Tabla 3.
Conv.
Catalizador de Conv. de 1-Ad. 2-Ad. 2-Ad.-illo Suma de HD furfural Rendimiento
de MCP (%) Rendimiento Rendimiento an
cerrado producto
(%) (%) (%)
(%) (%) (%) 50 mg de AlMgO 77,2 50,8 0,5 46,9 4,4 0,2 51,6 100 mg de AlMgO 91,3 65,8 0,5 48,8 7,9 0,5 57,2 200 mg de AlMgO 99,8 91,5 0,4 31,2 17,6 0,8 49,5 25 gl de NaOH 2 M 68,0 40,3 0,6 47,5 1,2 0,1 48,8 200 gl de NaOH 2 M 100,0 90,6 0,5 22,2 34,9 4,1 61,2 100 mg de
AlMnO/(semiconc ) 95,2 69,2 0,5 51,8 9,5 0,6 61,9
Ejemplo 5
Condensación aldólica de 2,5-hexanodiona a 80 °C
Se usaron tolueno (Fisher), 2,5-hexanodiona (Fluka) y dodecano (Aldrich) tal como se recibieron. Furfural (Aldrich) se destiló recientemente antes de su uso. El MgAlO se calcinó como se describe en el Ejemplo 1. "Mezcla 1" de 1,639 g (126 mg (1,312 mmol)/reactor) furfural, 561,5 mg de dodecano (43,2 mg/reactor), 884,5 mg de 2,5-hexanodiona (68,0 mg (0,597 mmol)/reactor) y 11,31 g de tolueno se prepararon en un vial de centelleo. "Mezcla 2" de 1,878 g (144 mg (1,312 mmol)/reactor) 5-metilfurfural, 561,5 mg de dodecano (43,2 mg/reactor), 884,5 mg de 2,5-hexanodiona (68,0 mg (0,597 mmol)/reactor) y 11,31 g de tolueno se prepararon en un vial de centelleo. "Mezcla 3" de 224,6 mg de dodecano (43,2 mg/reactor), 353,8 mg de 2,5-hexanodiona (68,0 mg (0,597 mmol)/reactor) y 4,524 (0,87 g/reactor) g de tolueno se prepararon en un vial de centelleo. Una porción de cada mezcla, agua y el catalizador básico se añadió a un vial de centelleo como se expone en la Tabla 4 a continuación.
Tabla 4.
R eactor Ct. M ezcla. 1 (q) Ct. de aqua (q) C antidad base (mq) T iem po de reacción (h) Tem p. (°C) 1 1,108 g 1,00 g 10,0 de MgAlO 25 80 2 1,108 g 1,00 g 25,0 de MgAlO 25 80 3 1,108 g 1,00 g 50,0 de MgAlO 25 80 4 1,108 g 1,00 g 100,0 de MgAlO 25 80 5 1,108 g 1,00 g 150,0 de MgAlO 25 80 6 1,107 g 0,8
fre
7
s
0
co g de tolueno 1,00 g 200,0 de MgAlO 25 80 7 1,108 g 1,00 g 12,5 |jl de NaOH 2M 25 80 8 1,108 g 1,00 g 25,0 jl de NaOH 2M 25 80 9 1,108 g 0,95 g 50,0 jl de NaOH 2M 25 80 10 1,108 g 0,90 g 100,0 jl de NaOH 2M 25 80 11 1,107 g 0,870 g de tolueno
fresco - 25,0 de MgAlO 25 80 12 1,107 g 0,870 g de tolueno
fresco - 50,0 de MgAlO 25 80 Ct. M ezcla. 2 (q)
13 1,126 g 1,00 g 10,0 de MgAlO 25 80 14 1,126 g 1,00 g 25,0 de MgAlO 25 80 15 1,126 g 1,00 g 50,0 de MgAlO 25 80 16 1,126 g 1,00 g 100,0 de MgAlO 25 80 17 1,126 g 1,00 g 150,0 de MgAlO 25 80 18 1,126 g 1,00 g 200,0 de MgAlO 25 80 19 1,126 g 1,00 g 12,5 jl de NaOH 2M 25 80 20 1,126 g 1,00 g 25,0 jl de NaOH 2M 25 80 21 1,126 g 0,95 g 50,0 jl de NaOH 2M 25 80 22 1,126 g 0,90 g 100,0 jl de NaOH 2M 25 80
23 0,981 g 1,00 g 25,0 de MgAlO 25 80 24 0,981 g 1,00 g 50,0 de MgAlO 25 80 25 0,981 g 0,870 g de tolueno
fresco - 25,0 de MgAlO 25 80 26 0,981 g 0,870 g
fresco de tolueno - 50,0 de MgAlO 25 80
Los reactores se colocaron en placas de agitación precalentadas y se agitaron a 800 RPM. Para cada reactor, todo el material se transfirió a un tubo de centrífuga de 15 ml. La transferencia se completó con 2 x 2 ml de etanol lavado. La mezcla de 6 ml se agitó y se convirtió en una fase. La mezcla se centrifugó a 4.000 RPM. La capa orgánica se recogió en un segundo tubo de centrífuga de 15 ml. Una muestra de la capa orgánica se analizó por GC. Una comparación de los datos de 25 °C, 50 °C y 80 °C se muestran en la figura 1. Los resultados para furfural se resumen en la figura 2. Los resultados para 5-metilfurfural se resumen en la figura 3.
Ejemplo 6
Condensación aldólica de 2,5-hexanodiona y 0-6 equivalentes de furfural a 170 °C
Se usaron tolueno (Fisher), 2,5-hexanodiona (Fluka) y dodecano (Aldrich) tal como se recibieron. Furfural (Aldrich) se destiló recientemente antes de su uso. Se preparó una mezcla de 561,6 mg de dodecano (86,4 mg/reactor), 884,7 mg de 2,6-hexanodiona (136,1 mg (1,19 mmol)/reactor) y 11,31 g (1,74 g/reactor) de tolueno en un vaso de precipitados pequeño. Las cantidades de la mezcla y el catalizador de MgAlO (calcinado como se describe en el Ejemplo 1) como se expone en la Tabla 5 a continuación se añadieron a cada tubo Q (el catalizador se añadió primero).
Tabla 5.
Reactor Ct. Mezcla Ct. de Cantidad de furfural (mg) Cantidad de Tiempo de Temp.
(g) agua (g) (equivalente molar) MgAlO (mg) reacción (h) (°C) 1 1,9625 2 , 0 0 g 0 ( 0 eq.) 2 0 0 , 0 4 170 2 1,9625 2 , 0 0 g 57,1 (0,5) 2 0 0 , 0 4 170 3 1,9625 2 , 0 0 g 114,2 (1) 2 0 0 , 0 4 170 4 1,9625 2 , 0 0 g 228,5 (2) 2 0 0 , 0 4 170 5 1,9625 2 , 0 0 g 457,0 (4) 2 0 0 , 0 4 170 6 1,9625 2 , 0 0 g 685,4 (6 ) 2 0 0 , 0 4 170 Los reactores se colocaron en placas de agitación precalentadas y se agitaron a 800 RPM. Para cada reactor, todo el material se transfirió a un tubo de centrífuga de 15 ml y se centrifugó a 4.000 RPM. La capa orgánica se recogió en un segundo tubo de centrífuga de 15 ml. La fase acuosa se lavó 3 veces más con 4 ml de EtOAc y se centrifugó. Las fracciones orgánicas se combinaron y se secaron con Na2SO4. Los resultados se resumen en la figura 4.
Ejemplo 7
Condensación aldólica cruzada de 2,5-hexanodiona con butanal
El butanol (Mallinckrodt Chemicals), K3PO4 (Acros), 2,5-hexanodiona (Aldrich) y dodecano (Aldrich) se usaron tal como se recibieron. Los reactivos expuestos en la Tabla 6 a continuación se añadieron en viales de vidrio con espacio aéreo.
Tabla 6.
Reactor Ct. Disolvente Sec. Disolvente DD HD (mg) (2,385 Butanal K
3
PO
4
(50 % Temp.
(g) (g) (mg) mmol) (mg) mol) (mg) (°C) A 3,48 g - tolueno Ninguna 172,7 272,2 343,9 253,1 100 B 3,48 g - tolueno Ninguna 172,7 272,2 687,9 253,1 100 C 3,24 g -Butanol Ninguna 172,7 272,2 343,9 253,1 100 D 3,24 g - Butanol Ninguna 172,7 272,2 687,9 253,1 100 E 4,00 g - Agua Ninguna 172,7 272,2 343,9 253,1 100 F 4,00 g - Agua 3,24 (Butanol) 172,7 272,2 343,9 253,1 100 Inic. 3,48 g - tolueno Ninguna 172,7 272,2 343,9 0 25 Los viales se calentaron a 100 °C y se agitaron a 600 RPM durante dos horas. Al final de la reacción, los viales se enfriaron. Las reacciones se analizaron mediante GC. Se observaron productos de aldol cruzado, productos de degradación de butanal y productos de autoaldolización.
Ejemplo de referencia 8
Estudio del catalizador de condensación autoaldólica de 2,5-hexanodiona a 3-metilciclopent-2-enona (MCP) El tolueno obtenido de Fisher, la 2,5-hexanodiona obtenida de Fluka y el dodecano obtenido de Sigma Aldrich se usaron tal como se recibieron. Los catalizadores de MgAlO, MgZrOx y MgO se calcinaron a 700 °C, 600 °C y 450 °C, respectivamente. El A^O3 (Fisher 60-325 malla), K3PO4 (tribásico, 97 % de pureza, anhidro, Acros) y el TiO2 (anatasa nanoestructurada) se usaron tal como se recibieron.
Una mezcla de 22,62 g de tolueno (4 ml/3,48 g por reactor), 561,6 mg de dodecano (86,4 mg por reactor) y 884,7 mg de 2,5-hexanodiona (1,19 mmol/136,1 mg por reactor) se prepararon en un vaso de precipitados pequeño. Se añadieron 3,703 g de la mezcla a siete tubos de reactor individuales en un sistema de reactor de vidrio de alta presión para una reacción de hasta 1379 kPa (200 psi) (sistema Q-Tube). Se añadieron 25 mg de catalizador a cada tubo del reactor. Los reactores se agitaron a 800 RPM y se calentaron a 180 °C durante 0,75 o 2 horas. Tras el enfriamiento, todo el material se transfirió desde un tubo del reactor a un tubo de centrífuga de 15 ml. El tubo se centrifugó a 4000 RPM durante 10 minutos. Una muestra de la capa orgánica separada se analizó por GC. Los resultados se resumen en la Tabla 7 que se expone a continuación.
Tabla 7.
Tiempo Temp. Catalizador (40 Conversión HD Rendimie Sel. Entrada (hora) (°C) mg) Disolvente (%) MCP (%) CP (%) 1 0,75 180 K3PO4 Tolueno 35 31 89 2 0,75 180 Al2O3 básico Tolueno 94 78 84 3 0,75 180 TiO2 Tolueno 74 53 71 4 0,75 180 MgO Tolueno 99 78 78 5 0,75 180 MgZrO Tolueno 89 82 93 6 0,75 180 MgAlO Tolueno 94 75 80 7 2 180 MgAlO Agua/tolueno 85,2 84,5 99 8 2 180 MgAlO (50 mg) Agua/tolueno 95,7 94,3 99 Ejemplo de referencia 9
Efecto de la temperatura de calcinación sobre los materiales derivados de hidrotalcita en la ciclación de 2,5-hexanodiona a 3-metilciclopent-2-enona (MCP)
25,00 g de hidrotalcita sintética obtenida de Aldrich (CH16Al2Mg6O-i9-4H2O; Catálogo: 652288-1 kg) se midieron en un bote de cerámica. La temperatura del horno de calcinación se calentó a 2 °C/min (perfil 4) bajo aire hasta la temperatura final. El horno se mantuvo a la temperatura final durante 1 hora, luego se enfrió a 250 °C y se mantuvo a temperatura. La hidrotalcita caliente se retiró del horno y se cubrió hasta que se enfrió. La hidrotalcita calcinada se acumuló y se almacenó para su uso posterior. Las masas finales de hidrotalcita se resumen en la Tabla 8 a continuación.
Tabla 8.
Temperatura de calcinación (°C) Masa final de MgAlO (g)
650 14,113
450 14,816
500 14,429
550 14,272
600 14,178
700 13,939
La reacción de ciclación de 2,5-hexanodiona se llevó a cabo como se describe en el Ejemplo 8, anteriormente, a 180 °C, 1,5 horas, 1,19 mmol de 2,5-hexanodiona, 4 ml de tolueno y 40 mg de MgAlO. La calcinación en el intervalo de 500-550 °C proporcionó una actividad catalítica óptima (90-95 % de conversión de 2,5-hexanodiona) en el sistema orgánico monofásico. Sin embargo, la reacción de ciclación de 2,5-hexanodiona se realizó en un sistema bifásico como se describe en el Ejemplo 8, anteriormente, a 180 °C, 1,5 horas, 1,19 mmol de 2,5-hexanodiona, 2 ml de tolueno, 2 ml de agua y 20 mg de MgAlO. La calcinación a 700 °C para una retención de 2 horas tuvo la mayor conversión en aproximadamente 50 %.
Ejemplo de referencia 10
Condensación autoaldólica de 2,5-hexanodiona a 3-metilciclopent-2-enona (MCP) MgAlO y MgO en tolueno Una mezcla de 29,0 g de tolueno, 1,44 g de dodecano y 2,269 g de 2,5-hexanodiona se prepararon en un vaso de precipitados pequeño. Se añadieron 3,925 g de la mezcla a ocho tubos individuales a reactor en un sistema Q-Tube. Se añadieron 40 mg de catalizador (MgAlO calcinado a 450-700 °C o MgO calcinado a 450 °C) a cada tubo del reactor. Los reactores se agitaron a 800 RPM y se calentaron a 180 ° C durante 2,0 horas. Tras el enfriamiento, todo el material se transfirió desde un tubo del reactor a un tubo de centrífuga de 15 ml. El tubo se centrifugó a 4.000 RPM. La capa orgánica se recogió en un segundo tubo de centrífuga de 15 ml. La fase acuosa se lavó tres veces más con 4 ml de EtOAc, se centrifugó y todos los extractos orgánicos se combinaron y se secaron con sulfato de sodio. Una muestra de la capa orgánica separada se analizó por GC. Los resultados se resumen en la Tabla 9 que se expone a continuación.
Tabla 9.
Catalizador CDonv. de HD Rendimiento de MCP (% Cuant. Mayor rendimiento de producción (%) molar) (% en masa)
MgAlO -450 °C 83,0 70,8 8,5
MgAlO - 500 °C 91,8 75,2 11,2
MgAlO - 550 °C 92,0 75,0 11,0
MgAlO - 600 °C 86,7 70,8 10,4
MgAlO - 650 °C 83,7 69,6 9,5
MgAlO - 700 °C 84,7 69,3 9,7
MgAlO - 700 °C (lote 2) 76,3 62,7 8,7
MgO -450 °C 41,9 36,5 1,7
Ejemplo de referencia 11
Condensación autoaldólica de 2,5-hexanodiona a 3-metilciclopent-2-enona (MCP) MgAlO y MgO en tolueno y agua
Una mezcla de 14,5 g de tolueno, 0,720 g de dodecano y 1,135 g de 2,5-hexanodiona se prepararon en un vaso de precipitados pequeño. Se añadieron 1,963 g de la mezcla a ocho tubos individuales a reactor en un sistema Q-Tube. Se añadieron 20 mg de catalizador (MgAlO calcinado a 450-700 °C o MgO calcinado a 450 °C) a cada tubo del reactor. Se añadieron 2.000 g de agua a cada tubo del reactor. Los reactores se agitaron a 800 RPM y se calentaron a 180 ° C durante 1,5 horas. Tras el enfriamiento, todo el material se transfirió desde un tubo del reactor a un tubo de centrífuga de 15 ml. El tubo se centrifugó a 4.000 RPM. La capa orgánica se recogió en un segundo tubo de centrífuga de 15 ml. La fase acuosa se lavó tres veces más con 4 ml de EtOAc, se centrifugó y todos los extractos orgánicos se combinaron y se secaron con sulfato de sodio. Una muestra de la capa orgánica separada se analizó por GC. Los resultados se resumen en la Tabla 10 que se expone a continuación.
Tabla 10.
Conv. de HD Rendimiento de MCP (% Cuant. Mayor rendimiento de Catalizador
(%) molar) producción (% en masa) MgAlO -450 °C 17,6 17,1 0,1
MgAlO - 500 °C 16,1 15,7 0,1
MgAlO - 550 °C 22,0 21,4 0,2
MgAlO - 600 °C 24,7 24,5 0,2
MgAlO - 650 °C 24,8 24,7 0,1
MgAlO - 700 °C 40,5 40,3 0,5
MgAlO - 700 °C (lote 2) 49,0 48,1 0,4
MgO -450 °C 2,8 2,8 0,1
Ejemplo de referencia 12
Hidrogenación de 3-metilciclopent-2-enona (MCP)
La 3-metilciclopent-2-enona (MCP, Aldrich), el octanol (Fluka Analytical), el diclorometano (Sigma Aldrich) y el dodecano (Sigma Aldrich) se usaron tal como se recibieron. Pd/C (Acros), Pd/AhO3 (Aldrich), Pt/C (Acros), Pt/Al2O3 (Aldrich), Ru/C (Acros), Ru/AhO3 (Aldrich), Rh/C (Aldrich) y Rh/AhOs (Aldrich) se secaron durante 2 horas a alto vacío a 60 °C antes de su uso. Se usó un reactor HEL ChemSCAN para la reacción. Un reactor HEL es un sistema de autoclave múltiple. Cada uno de los 8 autoclaves hastelloy en el sistema tiene una capacidad de 15 ml y se agita magnéticamente. Cada reactor también puede tener presión y temperatura variadas independientemente entre sí. En cada reactor HEL, 100 mg de dodecano, 100 g de dodecano, 1,8 g de octanol y el catalizador se añadieron como se expone en la Tabla 11 a continuación.
Tabla 11.
Reactor Temp. (grados C) Presión (PSI) Mezcla (g) Catalizador (mg) 1 70 150 2 11,1 - Pd/C 2 70 150 2 22,1 - Pd/Al2Os 3 70 150 2 40,6 - Pt/C 4 70 150 2 40,6 - Pt/Al2Os 5 70 150 2 21,0 - Ru/C 6 70 150 2 21,0 - Ru/Al2Os 7 70 150 2 21,4 - Rh/C 8 70 150 2 21,4 - Rh/Al2Os (en la Tabla 11: 150 psi corresponden a 1034 kPa).
El reactor se inició con 2 purgas de N2 y 2 purgas de H2. La agitación se inició a 500 RPM al comienzo de la reacción para evitar que el catalizador se sedimente. La temperatura se ajustó a 70 °C, presión a 1034 kPa (150 psi) y agitación a 500 RPM. Tras 5 horas, los reactores se enfriaron y se ventilaron. El sólido y el líquido combinados se transfirieron a un tubo de centrífuga de 15 ml y se centrifugaron durante 20 minutos a 4000 RPM. Una muestra de la capa orgánica se analizó por GC. Los resultados se resumen en la Tabla 12 que se expone a continuación.
Tabla 12.
Conv. de MCP Rendimiento de cetona Rendimiento de alcohol Rendimiento de Catalizador
(%) (% mol) (% mol) alcanos (% mol) Pd/C 100,0 98,8 2,9 0 , 0 Pd/Al2Os 100,0 91,6 9,2 0 , 0
Pt/C 100,0 81,5 7,2 7,8 Pt/Al2O3 100,0 0,2 76,4 4,8
Ru/C 100,0 0,5 81,9 0 ,1 Ru/AhO3 100,0 41,0 46,8 1,4
Rh/C 100,0 22,6 39,2 3,1 Rh/Al2O3 100 71,9 24,0 0 , 0 Ejemplo 13
Hidrogenólisis de referencia de MCP
3-metilciclopent-2-enona (MCP, Aldrich), octanol (Fluka Analytical), Se usaron diclorometano (Sigma Aldrich) y dodecano (Sigma Aldrich) como se recibieron. Pt/C (Acros), Ru/C (Acros) y Amberlyst 70 (Dow) se secaron durante 2 horas a alto vacío a 60 °C antes de su uso. En cada reactor HEL, se añadieron los componentes expuestos en la Tabla 13 a continuación.
Tabla 13.
Reactor Temp. Disolvente (g) Presión Catalizador Catalizador ácido (grados C) (PSI) metálico (mg) A-70 (mg) 1 170 1,8 g de tolueno 450 40,6 - Pt/C 8,2 mg-A-70 2 170 1,8 g de octanol 450 40,6 - Pt/C 8,2 mg-A-70 3 170 1,8 g de tolueno 450 40,6 - Pt/C -4 170 1,8 g de octanol 450 40,6 - Pt/C -5 170 1,8 de Agua/1,292 de Octano 450 40,6 - Pt/C 8,2 mg-A-70 6 170 1,8 de Agua/1,566 de Tolueno 450 40,6 - Pt/C 8,2 mg-A-70 7 170 1,8 de
0
A
,9
gu
de
a/
A
1,
g
4
u
8
a
3
/0
d
,
e
78
O
3 ctanol 450 40,6 - Pt/C 8,2 mg - A-70 8 170 Tolueno 450 20,3 - Pt/C 4,1 mg-A-70 (en la Tabla 13: 450 psi corresponden a 3103 kPa).
El reactor se inició con 2 purgas de N2 y 2 purgas de H2. La agitación se inició a 500 RPM al comienzo de la reacción
para evitar que el catalizador se sedimente. La temperatura se ajustó a 170 °C, presión a 3103 kPa (450 psi) y agitación a 500 RPM. Tras 6 horas, los reactores se enfriaron y se ventilaron. El sólido y el líquido combinados se transfirieron a un tubo de centrífuga de 15 ml y se centrifugaron durante 5 minutos a 4000 RPM. Una muestra de la capa orgánica se analizó por GC. Los resultados se resumen en la Tabla 14 que se expone a continuación.
Tabla 14.
Sistema Sistema de Conv. de Rendimiento de Rendimiento de Rendimiento de catalizador disolvente MCP (%) cetona (% mol) alcohol (% mol) alcanos (% mol) Pt/C Tolueno 100,0 3,5 75,6 11,6 Pt/C A-70 Tolueno 100,0 0 ,1 0 , 0 81,3 Pt/C Octanol 100,0 57,2 19,9 12,1 Pt/C A-70 Octanol 99,9 7,5 3,9 47,9 Pt/C A-70 Agua/Octano
Agua/ 100,0 2,5 9,2 55,9 Pt/C A-70 Agua de tolueno/ 100,0 1,2 28,2 45,5 Ru/C A-70 Agua octanol/ 100,0 60,5 11,7 16,7 Pt/C A-70 Tolueno 100,0 1,3 33,7 38,2 Ejemplo de referencia 14
Reacción de Guerbet de 1-tetradecanol a alcohol C
28
La reacción de Guerbet se llevó a cabo en un mini reactor 4560 Parr. En un reactor de 50 ml, se añadieron 1-tetradecanol (10 g, 47 mmol), 5% sobre carbono (que contenía 50 % de agua, 0,06 mg, 0,14 mmol), fosfato de potasio tribásico (3,5 g, 16,5 mmol), tolueno (15 ml). El recipiente de reacción se selló y la mezcla se agitó a 220 °C durante 6 días. El análisis GC de la mezcla cruda reveló que la mezcla consistía principalmente en alcohol C28 y material de partida sin reaccionar en una relación 1 : 1. La mezcla de reacción se filtró sobre celite y se lavó con EtOH. El disolvente se evaporó y se añadió un nuevo lote de paladio al 5 % sobre carbono (que contenía 50 % de agua, 0,06 mg, 0,14 mmol), fosfato de potasio tribásico (3,5 g, 16,5 mmol), tolueno (15 ml). La mezcla de reacción se agitó adicionalmente durante 6 días.
La mezcla se filtró sobre celite para proporcionar C28-OH con un rendimiento global del 75 %.
Ejemplo de referencia 15
2-Butanona y 1,6-Hexanodiol en cetona C
10
En un tubo Q de 12 ml (tubo de presión) se colocaron 5 % de paladio sobre carbono (que contenía 50 % de agua, 5,5 mg, 0,0013 mmol), fosfato de potasio tribásico (34 mg, 0,16 mmol) y una barra de agitación magnética. Al tubo se añadió 1,0 ml de tolueno seguido de 2-butanona (360,5 mg, 5,0 mmol), 1,6-hexanodiol (118,2 mg, 1,0 mmol) y dodecano (patrón interno). El tubo Q se selló y la mezcla de reacción se agitó a 145 °C en el bloque de metal precalentado durante 20 h a la misma temperatura, después de lo cual el tubo se enfrió a temperatura ambiente. La muestra diluida con análisis de THF y GC de la mezcla de reacción produjo la cantidad de producto (57 % de rendimiento).
La reacción descrita anteriormente en este Ejemplo se repitió usando otros dioles, incluyendo 1,3-propanodiol, 1,4-butanodiol y 1,5-pentanodiol. No se observó producto cetoalcohol en tales reacciones usando paladio sobre carbono como catalizador, fosfato de potasio tribásico como base y tolueno como disolvente.
Ejemplo de referencia 16
En un tubo Q de 12 ml (tubo de presión) se colocaron 5 % de paladio sobre carbono (que contenía 50 % de agua, 11 mg, 0,0026 mmol), fosfato de potasio tribásico ( 68 mg, 0,32 mmol) y una barra de agitación magnética. Al tubo se añadieron butiraldehído (72,1 mg, 1,0 mmol), 1,6-hexanodiol (177 mg, 1,5 mmol), tolueno (1 ml) y dodecano (patrón interno). El tubo se selló y la mezcla de reacción se agitó durante 20 horas a 145 °C en el bloque de metal precalentado. La mezcla de reacción se enfrió a temperatura ambiente y la muestra se diluyó con THF. El análisis por GC de la mezcla de reacción mostró la formación de compuestos de mayor peso molecular cuyas estructuras fueron asignadas de forma provisional.
Ejemplo de referencia 17
Acetona y 2-Etilhexanol en cetona C
11
En un tubo Q de 12 ml (tubo de presión) se colocaron 5 % de paladio sobre carbono (que contenía 50 % de agua, 2,0 mg), fosfato de potasio tribásico (64 mg) y barra de agitación magnética. Al tubo se añadieron 1,0 ml de tolueno seguido de 2-etilhexanol (1,0 mmol), acetona (2,2 mmol) y dodecano (patrón interno). El tubo Q se selló y la mezcla de reacción se agitó a 200 °C en el bloque de metal precalentado durante 20 h a la misma temperatura, después de lo cual el tubo se enfrió a temperatura ambiente. La muestra diluida con análisis THF y GC de la mezcla de reacción produjo la cantidad de producto C11 (rendimiento del 25 %) y algo de producto C19 (rendimiento del 8 %).
Ejemplo 18
Referencia 2-Butanona y 1,6-hexanodiol en cetona C
10
La reacción representada anteriormente se realizó de acuerdo con el procedimiento descrito en el Ejemplo 15 anterior. Las cantidades de 2-butanona y hexanodiol, el tipo y la cantidad de metal y base, el tipo de disolvente y la temperatura de la reacción se especifican en la Tabla 15 a continuación. La Tabla 15 a continuación también resume el rendimiento de la cetona C10 producida.
Tabla 15.
2-butanona Hexanodiol Metal Base Disolvente Temp. (°C) Rendimiento 1 mmol 1,2 mmol Pd/C, 5,5 mg K3PO4, 68 mg Tolueno 145 20 % 2,2 mmol 1 mmol Pd/C, 5,5 mg K3PO4, 68 mg Tolueno 145 47 % 2,2 mmol 1 mmol Pd/C, 5,5 mg K3PO4, 136 mg Tolueno 145 14 % 2,2 mmol 1 mmol Pd/C, 5,5 mg K3PO4, 68 mg Tolueno 120 21 % 2,2 mmol 1 mmol Pd/C, 5,5 mg K3PO4, 34 mg Tolueno 120 24 % 2,2 mmol 1 mmol Pd/C, 11 mg K3PO4, 68 mg Tolueno 145 48 % 4,4 mmol 1 mmol Pd/C, 11 mg K3PO4, 68 mg Tolueno 145 38 % 5 mmol 1 mmol Pd/C, 5,5 mg K3PO4, 21 mg Tolueno 145 55 % 5 mmol 1 mmol Pd/C, 5,5 mg K3PO4, 34 mg Tolueno 145 57 % 5 mmol 1 mmol Pd/C, 5,5 mg K3PO4, 42 mg Tolueno 145 52 % 5 mmol 1 mmol Pd/C, 5,5 mg K3PO4, 68 mg Tolueno 145 40 % 2,2 mmol 1 mmol KOH, 18 mg K3PO4, 68 mg Tolueno 145 NR 2,2 mmol 1 mmol KOH, 18 mg K3PO4, 68 mg Dioxano 145 NR 5 mmol 1 mmol Pd/C, 5,5 mg K3PO4, 34 mg Dioxano 145 34 % NR = trazas de productos observadas
Claims (11)
1. Un método para producir una o más cetonas poniendo en contacto un compuesto de fórmula (I) con un catalizador básico y uno o más alcoholes o aldehídos de fórmula (II) para producir una o más cetonas seleccionadas del grupo que consiste en:
y cualquiera de las mezclas de los mismos,
en donde el compuesto de fórmula (I) y el compuesto de fórmula (II) tienen las siguientes estructuras:
en las que:
R7 se selecciona entre alquilo, arilo, alquenilo, alquinilo, furilo, 5-metilfurilo, 5-hidroximetilfurilo y heteroarilo;
X es OH u O; y
la línea discontinua representa un doble enlace opcional que está presente cuando X es O,
comprendiendo el método además hidrogenar la una o más cetonas a uno o más alcanos.
en el que el término "alquilo" también incluye "cicloalquilo".
3. El método de las reivindicaciones 1 o 2, en el que R7 se selecciona entre el grupo que consiste en furilo, 5-metilfurilo y 5-hidroximetilfurilo.
5. El método de una cualquiera de las reivindicaciones 1 a 4, en el que el catalizador básico comprende un hidróxido de metal alcalino, un hidróxido de metal alcalinotérreo o un óxido de metal mixto.
6. El método de la reivindicación 5, en el que el óxido de metal mixto comprende MgZrO o MgAlO.
7. El método de una cualquiera de las reivindicaciones 1 a 4, en el que el catalizador básico comprende La2O3 , TO 2, MgO o CeO2.
8. El método de una cualquiera de las reivindicaciones 1 a 7, en el que el compuesto de fórmula (I) se pone en contacto con el catalizador básico en un disolvente acuoso, un solvente orgánico o un disolvente bifásico acuoso y orgánico.
9. El método de la reivindicación 8, en el que el disolvente orgánico comprende tolueno, trimetilacetonitrilo, dimetilformamida, acetato de propilo, dioxano, butanol, hexanol, octanol o cualquier mezcla de los mismos.
10. El método de una cualquiera de las reivindicaciones 1 a 9, en el que al menos el 70 % de la una o más cetonas son cetonas ramificadas.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201361830586P | 2013-06-03 | 2013-06-03 | |
| PCT/US2014/040760 WO2014197514A1 (en) | 2013-06-03 | 2014-06-03 | Methods for producing fuels, gasoline additives, and lubricants |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2767352T3 true ES2767352T3 (es) | 2020-06-17 |
Family
ID=51136790
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES14736519T Active ES2767352T3 (es) | 2013-06-03 | 2014-06-03 | Métodos para producir combustibles, aditivos de gasolina y lubricantes |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US9738617B2 (es) |
| EP (1) | EP3004072B1 (es) |
| CN (1) | CN105392782A (es) |
| BR (1) | BR112015030209A2 (es) |
| EA (1) | EA201592251A1 (es) |
| ES (1) | ES2767352T3 (es) |
| WO (1) | WO2014197514A1 (es) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US11157564B2 (en) * | 2018-03-02 | 2021-10-26 | Thoughtspot, Inc. | Natural language question answering systems |
| CN110845312A (zh) * | 2019-11-27 | 2020-02-28 | 万华化学集团股份有限公司 | 一种制备甲基庚烯酮的方法 |
| CN113046160B (zh) * | 2021-03-25 | 2022-04-22 | 清华大学 | 一种多羟基功能化离子液体润滑剂及制备方法 |
| CN115558535A (zh) * | 2022-10-28 | 2023-01-03 | 中国科学院兰州化学物理研究所 | 一种改性二氧化钛复合材料及其制备方法、电流变液及其制备方法和应用 |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE4005163A1 (de) | 1990-02-17 | 1991-08-22 | Basf Ag | Verfahren zur herstellung von acrolein |
| US5763664A (en) | 1995-12-01 | 1998-06-09 | Albemarle Corporation | Process for preparing cyclopentenones |
| CN102019177B (zh) * | 2009-09-18 | 2013-02-13 | 中国石油天然气股份有限公司 | 一种羟醛缩合反应固体碱催化剂及应用 |
| CN102600827A (zh) | 2011-01-08 | 2012-07-25 | 中国科学院成都有机化学有限公司 | 一种用于羟醛缩合反应的催化剂及其制备方法 |
| CN102188967B (zh) | 2011-03-24 | 2012-08-15 | 宁波千衍新材料科技有限公司 | 一种羟醛缩合催化剂及其制备方法和用途 |
| WO2012166267A2 (en) * | 2011-05-27 | 2012-12-06 | The Regents Of The University Of California | Method to convert fermentation mixture into fuels |
| CN102389829A (zh) * | 2011-09-16 | 2012-03-28 | 中国科学院广州能源研究所 | 一种糠醛和丙酮羟醛合成航空燃料中间体的固体碱催化剂及制备方法与用途 |
-
2014
- 2014-06-03 EP EP14736519.1A patent/EP3004072B1/en active Active
- 2014-06-03 WO PCT/US2014/040760 patent/WO2014197514A1/en not_active Ceased
- 2014-06-03 ES ES14736519T patent/ES2767352T3/es active Active
- 2014-06-03 BR BR112015030209A patent/BR112015030209A2/pt not_active Application Discontinuation
- 2014-06-03 CN CN201480041136.5A patent/CN105392782A/zh active Pending
- 2014-06-03 EA EA201592251A patent/EA201592251A1/ru unknown
- 2014-06-03 US US14/895,851 patent/US9738617B2/en not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| BR112015030209A2 (pt) | 2017-07-25 |
| CN105392782A (zh) | 2016-03-09 |
| US9738617B2 (en) | 2017-08-22 |
| US20160115143A1 (en) | 2016-04-28 |
| WO2014197514A1 (en) | 2014-12-11 |
| EP3004072A1 (en) | 2016-04-13 |
| EP3004072B1 (en) | 2019-11-27 |
| EA201592251A1 (ru) | 2016-05-31 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US10618856B2 (en) | Methods for producing cyclic and acyclic ketones | |
| JP7062836B2 (ja) | 1,2-ペンタンジオール製造用触媒およびこれを用いた1,2-ペンタジオールの製造方法 | |
| ES2767352T3 (es) | Métodos para producir combustibles, aditivos de gasolina y lubricantes | |
| CN104711007A (zh) | 一种航空煤油或柴油范围液态烷烃的制备方法 | |
| ES2924482T3 (es) | Proceso para la producción de alquenoles y uso del mismo para la producción de 1,3-butadieno | |
| ES2462872A1 (es) | Catalizador y proceso catalítico para la eterificación/reducción de furfuril derivados a tetrahidro-furfuril éteres | |
| KR20200005291A (ko) | 1,2-펜탄디올 제조용 촉매 및 이를 이용한 1,2-펜탄디올의 제조방법 | |
| KR101855876B1 (ko) | 에탄올을 생산하고 메탄올을 공동생산하는 방법 | |
| KR101220326B1 (ko) | 산-염기 복합 촉매계를 이용하여 고산가 바이오 오일로부터 바이오 디젤을 제조하는 방법 | |
| Li et al. | La-doped Zr-Beta zeolite as efficient catalyst for reduction of cyclohexanone to cyclohexanol via the MPV process | |
| US20210188735A1 (en) | Production Of Cyclopentadiene From Furfural | |
| CN102863335B (zh) | 一种丁二酸二酯的制备方法 | |
| CN108102683A (zh) | 一种可再生十二醇和航空煤油范围内的支链烷烃的制备方法 | |
| KR102153514B1 (ko) | 기상반응에 의한 1,2-펜탄디올의 제조방법 | |
| KR100904058B1 (ko) | 합성가스로부터 디메틸에테르 직접합성용 촉매 및 이의제조방법 | |
| CN108002993B (zh) | 一种由丁醇制备4-庚酮的方法 | |
| JP2014534167A (ja) | 三元混合酸化物上でのアルコール及びエーテルの触媒脱水 | |
| CN112898135A (zh) | 一种制备2-戊酮的方法 | |
| CN112898142A (zh) | 制备2-戊酮的方法 | |
| ES2638719A1 (es) | Procedimiento para la valorización de compuestos oxigenados presentes en fracciones acuosas derivadas de biomasa | |
| CN112694459B (zh) | 一种由糠醇一步法连续制备γ-戊内酯的方法 | |
| KR101525943B1 (ko) | 디메틸에테르와 아세트산의 동시 제조용 불균일계 구리촉매 | |
| CN103962173A (zh) | 一种从碳水化合物制备c5,c6轻质烷烃的催化剂 | |
| EP4470668A1 (en) | Catalyst for methane oxidation reaction, method for preparing same, and methane oxidation method using same | |
| CN107963959A (zh) | 一步法合成2,6,8-三甲基-4-壬醇的工艺方法 |