ES2762479T3 - Comprimido que incluye 7-[4-(4-benzo[b]tiofen-4-il-piperazin-1-il)butoxi]-1H-quinolin-2-ona o sal de la misma - Google Patents
Comprimido que incluye 7-[4-(4-benzo[b]tiofen-4-il-piperazin-1-il)butoxi]-1H-quinolin-2-ona o sal de la misma Download PDFInfo
- Publication number
- ES2762479T3 ES2762479T3 ES12840025T ES12840025T ES2762479T3 ES 2762479 T3 ES2762479 T3 ES 2762479T3 ES 12840025 T ES12840025 T ES 12840025T ES 12840025 T ES12840025 T ES 12840025T ES 2762479 T3 ES2762479 T3 ES 2762479T3
- Authority
- ES
- Spain
- Prior art keywords
- tablet
- weight
- salt
- binder
- disintegrant
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 150000003839 salts Chemical class 0.000 title claims abstract description 33
- ZKIAIYBUSXZPLP-UHFFFAOYSA-N brexpiprazole Chemical compound C1=C2NC(=O)C=CC2=CC=C1OCCCCN(CC1)CCN1C1=CC=CC2=C1C=CS2 ZKIAIYBUSXZPLP-UHFFFAOYSA-N 0.000 title claims abstract description 11
- 229920002153 Hydroxypropyl cellulose Polymers 0.000 claims abstract description 29
- 235000010977 hydroxypropyl cellulose Nutrition 0.000 claims abstract description 29
- 239000001863 hydroxypropyl cellulose Substances 0.000 claims abstract description 28
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 claims abstract description 26
- 239000000546 pharmaceutical excipient Substances 0.000 claims abstract description 22
- 239000011230 binding agent Substances 0.000 claims abstract description 21
- 239000007884 disintegrant Substances 0.000 claims abstract description 20
- 239000000314 lubricant Substances 0.000 claims abstract description 20
- 229920000168 Microcrystalline cellulose Polymers 0.000 claims abstract description 15
- 235000019813 microcrystalline cellulose Nutrition 0.000 claims abstract description 15
- 239000008108 microcrystalline cellulose Substances 0.000 claims abstract description 15
- 229940016286 microcrystalline cellulose Drugs 0.000 claims abstract description 15
- 229920002261 Corn starch Polymers 0.000 claims abstract description 14
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 claims abstract description 14
- 239000008120 corn starch Substances 0.000 claims abstract description 14
- 239000008101 lactose Substances 0.000 claims abstract description 14
- 235000019359 magnesium stearate Nutrition 0.000 claims abstract description 13
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 claims abstract description 12
- 229920002785 Croscarmellose sodium Polymers 0.000 claims abstract description 11
- 229960001681 croscarmellose sodium Drugs 0.000 claims abstract description 11
- 235000010947 crosslinked sodium carboxy methyl cellulose Nutrition 0.000 claims abstract description 11
- 239000004480 active ingredient Substances 0.000 claims abstract description 9
- 229940031703 low substituted hydroxypropyl cellulose Drugs 0.000 claims abstract description 7
- 239000011734 sodium Substances 0.000 claims abstract description 7
- 229910052708 sodium Inorganic materials 0.000 claims abstract description 7
- 229920002472 Starch Polymers 0.000 claims abstract description 5
- 235000019698 starch Nutrition 0.000 claims abstract description 5
- 239000008107 starch Substances 0.000 claims abstract description 5
- UQSXHKLRYXJYBZ-UHFFFAOYSA-N Iron oxide Chemical compound [Fe]=O UQSXHKLRYXJYBZ-UHFFFAOYSA-N 0.000 claims description 26
- 238000000034 method Methods 0.000 claims description 20
- 239000011247 coating layer Substances 0.000 claims description 19
- 239000011248 coating agent Substances 0.000 claims description 18
- -1 4-benzo [b] thiophene-4-ylpiperazin-1-yl Chemical group 0.000 claims description 16
- 239000000203 mixture Substances 0.000 claims description 16
- 238000000576 coating method Methods 0.000 claims description 12
- 239000003086 colorant Substances 0.000 claims description 9
- 239000007788 liquid Substances 0.000 claims description 8
- 238000002156 mixing Methods 0.000 claims description 5
- WHNWPMSKXPGLAX-UHFFFAOYSA-N N-Vinyl-2-pyrrolidone Chemical compound C=CN1CCCC1=O WHNWPMSKXPGLAX-UHFFFAOYSA-N 0.000 claims description 3
- 238000004519 manufacturing process Methods 0.000 claims description 3
- 229940083542 sodium Drugs 0.000 claims description 3
- 235000015424 sodium Nutrition 0.000 claims description 3
- 238000005550 wet granulation Methods 0.000 claims description 3
- 125000004106 butoxy group Chemical group [*]OC([H])([H])C([H])([H])C(C([H])([H])[H])([H])[H] 0.000 claims description 2
- 229960000913 crospovidone Drugs 0.000 claims description 2
- 235000013809 polyvinylpolypyrrolidone Nutrition 0.000 claims description 2
- 229920000523 polyvinylpolypyrrolidone Polymers 0.000 claims description 2
- 239000000126 substance Substances 0.000 claims description 2
- 239000008187 granular material Substances 0.000 claims 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 claims 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 claims 1
- 229940069328 povidone Drugs 0.000 claims 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 abstract description 3
- 125000002057 carboxymethyl group Chemical group [H]OC(=O)C([H])([H])[*] 0.000 abstract 1
- 239000003826 tablet Substances 0.000 description 123
- 150000001875 compounds Chemical class 0.000 description 40
- OGIDPMRJRNCKJF-UHFFFAOYSA-N titanium oxide Inorganic materials [Ti]=O OGIDPMRJRNCKJF-UHFFFAOYSA-N 0.000 description 15
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 description 14
- 238000003860 storage Methods 0.000 description 12
- 229940099112 cornstarch Drugs 0.000 description 11
- 235000013980 iron oxide Nutrition 0.000 description 11
- 238000006467 substitution reaction Methods 0.000 description 9
- AQLLBJAXUCIJSR-UHFFFAOYSA-N OC(=O)C[Na] Chemical compound OC(=O)C[Na] AQLLBJAXUCIJSR-UHFFFAOYSA-N 0.000 description 7
- 239000001866 hydroxypropyl methyl cellulose Substances 0.000 description 7
- 235000010979 hydroxypropyl methyl cellulose Nutrition 0.000 description 7
- 229920003088 hydroxypropyl methyl cellulose Polymers 0.000 description 7
- 229960001375 lactose Drugs 0.000 description 7
- 229940080313 sodium starch Drugs 0.000 description 7
- 239000000654 additive Substances 0.000 description 6
- 238000007922 dissolution test Methods 0.000 description 6
- 238000005469 granulation Methods 0.000 description 6
- 230000003179 granulation Effects 0.000 description 6
- 239000000454 talc Substances 0.000 description 6
- 229910052623 talc Inorganic materials 0.000 description 6
- 238000012360 testing method Methods 0.000 description 6
- 239000000975 dye Substances 0.000 description 5
- 239000000576 food coloring agent Substances 0.000 description 5
- 229960003943 hypromellose Drugs 0.000 description 5
- GQHTUMJGOHRCHB-UHFFFAOYSA-N 2,3,4,6,7,8,9,10-octahydropyrimido[1,2-a]azepine Chemical compound C1CCCCN2CCCN=C21 GQHTUMJGOHRCHB-UHFFFAOYSA-N 0.000 description 4
- PNEYBMLMFCGWSK-UHFFFAOYSA-N Alumina Chemical compound [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 4
- 235000010980 cellulose Nutrition 0.000 description 4
- 229920002678 cellulose Polymers 0.000 description 4
- 238000001035 drying Methods 0.000 description 4
- WTFXARWRTYJXII-UHFFFAOYSA-N iron(2+);iron(3+);oxygen(2-) Chemical compound [O-2].[O-2].[O-2].[O-2].[Fe+2].[Fe+3].[Fe+3] WTFXARWRTYJXII-UHFFFAOYSA-N 0.000 description 4
- SZVJSHCCFOBDDC-UHFFFAOYSA-N iron(II,III) oxide Inorganic materials O=[Fe]O[Fe]O[Fe]=O SZVJSHCCFOBDDC-UHFFFAOYSA-N 0.000 description 4
- 238000004898 kneading Methods 0.000 description 4
- 238000005259 measurement Methods 0.000 description 4
- NDLPOXTZKUMGOV-UHFFFAOYSA-N oxo(oxoferriooxy)iron hydrate Chemical compound O.O=[Fe]O[Fe]=O NDLPOXTZKUMGOV-UHFFFAOYSA-N 0.000 description 4
- QZAYGJVTTNCVMB-UHFFFAOYSA-N serotonin Chemical compound C1=C(O)C=C2C(CCN)=CNC2=C1 QZAYGJVTTNCVMB-UHFFFAOYSA-N 0.000 description 4
- HMUNWXXNJPVALC-UHFFFAOYSA-N 1-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]piperazin-1-yl]-2-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)N1CCN(CC1)C(CN1CC2=C(CC1)NN=N2)=O HMUNWXXNJPVALC-UHFFFAOYSA-N 0.000 description 3
- VZSRBBMJRBPUNF-UHFFFAOYSA-N 2-(2,3-dihydro-1H-inden-2-ylamino)-N-[3-oxo-3-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)propyl]pyrimidine-5-carboxamide Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C(=O)NCCC(N1CC2=C(CC1)NN=N2)=O VZSRBBMJRBPUNF-UHFFFAOYSA-N 0.000 description 3
- ZWEHNKRNPOVVGH-UHFFFAOYSA-N 2-Butanone Chemical compound CCC(C)=O ZWEHNKRNPOVVGH-UHFFFAOYSA-N 0.000 description 3
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 3
- WMFOQBRAJBCJND-UHFFFAOYSA-M Lithium hydroxide Chemical compound [Li+].[OH-] WMFOQBRAJBCJND-UHFFFAOYSA-M 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- SJRJJKPEHAURKC-UHFFFAOYSA-N N-Methylmorpholine Chemical compound CN1CCOCC1 SJRJJKPEHAURKC-UHFFFAOYSA-N 0.000 description 3
- 239000002202 Polyethylene glycol Substances 0.000 description 3
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 3
- 239000007864 aqueous solution Substances 0.000 description 3
- 239000001913 cellulose Substances 0.000 description 3
- 239000003795 chemical substances by application Substances 0.000 description 3
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 3
- 239000012535 impurity Substances 0.000 description 3
- JEIPFZHSYJVQDO-UHFFFAOYSA-N iron(III) oxide Inorganic materials O=[Fe]O[Fe]=O JEIPFZHSYJVQDO-UHFFFAOYSA-N 0.000 description 3
- 229960003511 macrogol Drugs 0.000 description 3
- 229920001223 polyethylene glycol Polymers 0.000 description 3
- 239000000843 powder Substances 0.000 description 3
- 238000005507 spraying Methods 0.000 description 3
- FCEHBMOGCRZNNI-UHFFFAOYSA-N 1-benzothiophene Chemical compound C1=CC=C2SC=CC2=C1 FCEHBMOGCRZNNI-UHFFFAOYSA-N 0.000 description 2
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 2
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 2
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 2
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 2
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 2
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 2
- SMWDFEZZVXVKRB-UHFFFAOYSA-N Quinoline Chemical compound N1=CC=CC2=CC=CC=C21 SMWDFEZZVXVKRB-UHFFFAOYSA-N 0.000 description 2
- AUNGANRZJHBGPY-SCRDCRAPSA-N Riboflavin Chemical compound OC[C@@H](O)[C@@H](O)[C@@H](O)CN1C=2C=C(C)C(C)=CC=2N=C2C1=NC(=O)NC2=O AUNGANRZJHBGPY-SCRDCRAPSA-N 0.000 description 2
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 2
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 2
- 229910052783 alkali metal Inorganic materials 0.000 description 2
- 229910052791 calcium Inorganic materials 0.000 description 2
- 239000011575 calcium Substances 0.000 description 2
- 201000010099 disease Diseases 0.000 description 2
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 2
- UFVKGYZPFZQRLF-UHFFFAOYSA-N hydroxypropyl methyl cellulose Chemical compound OC1C(O)C(OC)OC(CO)C1OC1C(O)C(O)C(OC2C(C(O)C(OC3C(C(O)C(O)C(CO)O3)O)C(CO)O2)O)C(CO)O1 UFVKGYZPFZQRLF-UHFFFAOYSA-N 0.000 description 2
- VBMVTYDPPZVILR-UHFFFAOYSA-N iron(2+);oxygen(2-) Chemical class [O-2].[Fe+2] VBMVTYDPPZVILR-UHFFFAOYSA-N 0.000 description 2
- LDHBWEYLDHLIBQ-UHFFFAOYSA-M iron(3+);oxygen(2-);hydroxide;hydrate Chemical compound O.[OH-].[O-2].[Fe+3] LDHBWEYLDHLIBQ-UHFFFAOYSA-M 0.000 description 2
- 239000002609 medium Substances 0.000 description 2
- 239000008194 pharmaceutical composition Substances 0.000 description 2
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 2
- 229940076279 serotonin Drugs 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- 238000013112 stability test Methods 0.000 description 2
- 229940032147 starch Drugs 0.000 description 2
- VZGDMQKNWNREIO-UHFFFAOYSA-N tetrachloromethane Chemical compound ClC(Cl)(Cl)Cl VZGDMQKNWNREIO-UHFFFAOYSA-N 0.000 description 2
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 2
- GETQZCLCWQTVFV-UHFFFAOYSA-N trimethylamine Chemical compound CN(C)C GETQZCLCWQTVFV-UHFFFAOYSA-N 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- LNAZSHAWQACDHT-XIYTZBAFSA-N (2r,3r,4s,5r,6s)-4,5-dimethoxy-2-(methoxymethyl)-3-[(2s,3r,4s,5r,6r)-3,4,5-trimethoxy-6-(methoxymethyl)oxan-2-yl]oxy-6-[(2r,3r,4s,5r,6r)-4,5,6-trimethoxy-2-(methoxymethyl)oxan-3-yl]oxyoxane Chemical compound CO[C@@H]1[C@@H](OC)[C@H](OC)[C@@H](COC)O[C@H]1O[C@H]1[C@H](OC)[C@@H](OC)[C@H](O[C@H]2[C@@H]([C@@H](OC)[C@H](OC)O[C@@H]2COC)OC)O[C@@H]1COC LNAZSHAWQACDHT-XIYTZBAFSA-N 0.000 description 1
- SCYULBFZEHDVBN-UHFFFAOYSA-N 1,1-Dichloroethane Chemical compound CC(Cl)Cl SCYULBFZEHDVBN-UHFFFAOYSA-N 0.000 description 1
- SGUVLZREKBPKCE-UHFFFAOYSA-N 1,5-diazabicyclo[4.3.0]-non-5-ene Chemical compound C1CCN=C2CCCN21 SGUVLZREKBPKCE-UHFFFAOYSA-N 0.000 description 1
- LDXJRKWFNNFDSA-UHFFFAOYSA-N 2-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)-1-[4-[2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidin-5-yl]piperazin-1-yl]ethanone Chemical compound C1CN(CC2=NNN=C21)CC(=O)N3CCN(CC3)C4=CN=C(N=C4)NCC5=CC(=CC=C5)OC(F)(F)F LDXJRKWFNNFDSA-UHFFFAOYSA-N 0.000 description 1
- MFGOFGRYDNHJTA-UHFFFAOYSA-N 2-amino-1-(2-fluorophenyl)ethanol Chemical compound NCC(O)C1=CC=CC=C1F MFGOFGRYDNHJTA-UHFFFAOYSA-N 0.000 description 1
- BSKHPKMHTQYZBB-UHFFFAOYSA-N 2-methylpyridine Chemical compound CC1=CC=CC=N1 BSKHPKMHTQYZBB-UHFFFAOYSA-N 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 description 1
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 1
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical compound [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 description 1
- AUNGANRZJHBGPY-UHFFFAOYSA-N D-Lyxoflavin Natural products OCC(O)C(O)C(O)CN1C=2C=C(C)C(C)=CC=2N=C2C1=NC(=O)NC2=O AUNGANRZJHBGPY-UHFFFAOYSA-N 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- 229940096895 Dopamine D2 receptor agonist Drugs 0.000 description 1
- 239000004097 EU approved flavor enhancer Substances 0.000 description 1
- 239000001856 Ethyl cellulose Substances 0.000 description 1
- ZZSNKZQZMQGXPY-UHFFFAOYSA-N Ethyl cellulose Chemical compound CCOCC1OC(OC)C(OCC)C(OCC)C1OC1C(O)C(O)C(OC)C(CO)O1 ZZSNKZQZMQGXPY-UHFFFAOYSA-N 0.000 description 1
- BDAGIHXWWSANSR-UHFFFAOYSA-M Formate Chemical compound [O-]C=O BDAGIHXWWSANSR-UHFFFAOYSA-M 0.000 description 1
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-N Hydrogen bromide Chemical compound Br CPELXLSAUQHCOX-UHFFFAOYSA-N 0.000 description 1
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 1
- JVTAAEKCZFNVCJ-UHFFFAOYSA-M Lactate Chemical compound CC(O)C([O-])=O JVTAAEKCZFNVCJ-UHFFFAOYSA-M 0.000 description 1
- OFOBLEOULBTSOW-UHFFFAOYSA-L Malonate Chemical compound [O-]C(=O)CC([O-])=O OFOBLEOULBTSOW-UHFFFAOYSA-L 0.000 description 1
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 1
- 229920000881 Modified starch Polymers 0.000 description 1
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 1
- JLTDJTHDQAWBAV-UHFFFAOYSA-N N,N-dimethylaniline Chemical compound CN(C)C1=CC=CC=C1 JLTDJTHDQAWBAV-UHFFFAOYSA-N 0.000 description 1
- NIPNSKYNPDTRPC-UHFFFAOYSA-N N-[2-oxo-2-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethyl]-2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidine-5-carboxamide Chemical compound O=C(CNC(=O)C=1C=NC(=NC=1)NCC1=CC(=CC=C1)OC(F)(F)F)N1CC2=C(CC1)NN=N2 NIPNSKYNPDTRPC-UHFFFAOYSA-N 0.000 description 1
- AFCARXCZXQIEQB-UHFFFAOYSA-N N-[3-oxo-3-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)propyl]-2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidine-5-carboxamide Chemical compound O=C(CCNC(=O)C=1C=NC(=NC=1)NCC1=CC(=CC=C1)OC(F)(F)F)N1CC2=C(CC1)NN=N2 AFCARXCZXQIEQB-UHFFFAOYSA-N 0.000 description 1
- 229910002651 NO3 Inorganic materials 0.000 description 1
- NHNBFGGVMKEFGY-UHFFFAOYSA-N Nitrate Chemical compound [O-][N+]([O-])=O NHNBFGGVMKEFGY-UHFFFAOYSA-N 0.000 description 1
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-L Phosphate ion(2-) Chemical compound OP([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-L 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 description 1
- 239000003082 abrasive agent Substances 0.000 description 1
- 239000002250 absorbent Substances 0.000 description 1
- 230000002745 absorbent Effects 0.000 description 1
- VJHCJDRQFCCTHL-UHFFFAOYSA-N acetic acid 2,3,4,5,6-pentahydroxyhexanal Chemical compound CC(O)=O.OCC(O)C(O)C(O)C(O)C=O VJHCJDRQFCCTHL-UHFFFAOYSA-N 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 239000000674 adrenergic antagonist Substances 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 229910000288 alkali metal carbonate Inorganic materials 0.000 description 1
- 150000008041 alkali metal carbonates Chemical class 0.000 description 1
- 150000008044 alkali metal hydroxides Chemical class 0.000 description 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 1
- 125000000217 alkyl group Chemical group 0.000 description 1
- OENHQHLEOONYIE-UKMVMLAPSA-N all-trans beta-carotene Natural products CC=1CCCC(C)(C)C=1/C=C/C(/C)=C/C=C/C(/C)=C/C=C/C=C(C)C=CC=C(C)C=CC1=C(C)CCCC1(C)C OENHQHLEOONYIE-UKMVMLAPSA-N 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 150000003863 ammonium salts Chemical class 0.000 description 1
- 239000002518 antifoaming agent Substances 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 235000006708 antioxidants Nutrition 0.000 description 1
- 239000002585 base Substances 0.000 description 1
- 239000011648 beta-carotene Substances 0.000 description 1
- 235000013734 beta-carotene Nutrition 0.000 description 1
- TUPZEYHYWIEDIH-WAIFQNFQSA-N beta-carotene Natural products CC(=C/C=C/C=C(C)/C=C/C=C(C)/C=C/C1=C(C)CCCC1(C)C)C=CC=C(/C)C=CC2=CCCCC2(C)C TUPZEYHYWIEDIH-WAIFQNFQSA-N 0.000 description 1
- 229960002747 betacarotene Drugs 0.000 description 1
- 229960001210 brexpiprazole Drugs 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- FJDQFPXHSGXQBY-UHFFFAOYSA-L caesium carbonate Chemical compound [Cs+].[Cs+].[O-]C([O-])=O FJDQFPXHSGXQBY-UHFFFAOYSA-L 0.000 description 1
- 229910000024 caesium carbonate Inorganic materials 0.000 description 1
- HUCVOHYBFXVBRW-UHFFFAOYSA-M caesium hydroxide Inorganic materials [OH-].[Cs+] HUCVOHYBFXVBRW-UHFFFAOYSA-M 0.000 description 1
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 1
- 229950008138 carmellose Drugs 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 210000003169 central nervous system Anatomy 0.000 description 1
- 239000002738 chelating agent Substances 0.000 description 1
- 229940001468 citrate Drugs 0.000 description 1
- 238000004040 coloring Methods 0.000 description 1
- 238000006731 degradation reaction Methods 0.000 description 1
- 238000007907 direct compression Methods 0.000 description 1
- 239000002270 dispersing agent Substances 0.000 description 1
- 239000002612 dispersion medium Substances 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- 239000002288 dopamine 2 receptor stimulating agent Substances 0.000 description 1
- 238000007908 dry granulation Methods 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- CCIVGXIOQKPBKL-UHFFFAOYSA-M ethanesulfonate Chemical compound CCS([O-])(=O)=O CCIVGXIOQKPBKL-UHFFFAOYSA-M 0.000 description 1
- 235000019325 ethyl cellulose Nutrition 0.000 description 1
- 229920001249 ethyl cellulose Polymers 0.000 description 1
- 229960004667 ethyl cellulose Drugs 0.000 description 1
- 239000007941 film coated tablet Substances 0.000 description 1
- 235000019264 food flavour enhancer Nutrition 0.000 description 1
- 235000003599 food sweetener Nutrition 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 229930195712 glutamate Natural products 0.000 description 1
- 150000008282 halocarbons Chemical class 0.000 description 1
- 239000003112 inhibitor Substances 0.000 description 1
- 150000002576 ketones Chemical class 0.000 description 1
- 229940001447 lactate Drugs 0.000 description 1
- XGZVUEUWXADBQD-UHFFFAOYSA-L lithium carbonate Chemical compound [Li+].[Li+].[O-]C([O-])=O XGZVUEUWXADBQD-UHFFFAOYSA-L 0.000 description 1
- 229910052808 lithium carbonate Inorganic materials 0.000 description 1
- 229910000032 lithium hydrogen carbonate Inorganic materials 0.000 description 1
- HQRPHMAXFVUBJX-UHFFFAOYSA-M lithium;hydrogen carbonate Chemical compound [Li+].OC([O-])=O HQRPHMAXFVUBJX-UHFFFAOYSA-M 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 159000000003 magnesium salts Chemical class 0.000 description 1
- 229940049920 malate Drugs 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- BJEPYKJPYRNKOW-UHFFFAOYSA-N malic acid Chemical compound OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 229920000609 methyl cellulose Polymers 0.000 description 1
- 239000001923 methylcellulose Substances 0.000 description 1
- 235000010981 methylcellulose Nutrition 0.000 description 1
- 229960002900 methylcellulose Drugs 0.000 description 1
- 235000019426 modified starch Nutrition 0.000 description 1
- PSHKMPUSSFXUIA-UHFFFAOYSA-N n,n-dimethylpyridin-2-amine Chemical compound CN(C)C1=CC=CC=N1 PSHKMPUSSFXUIA-UHFFFAOYSA-N 0.000 description 1
- 239000006191 orally-disintegrating tablet Substances 0.000 description 1
- SOQBVABWOPYFQZ-UHFFFAOYSA-N oxygen(2-);titanium(4+) Chemical class [O-2].[O-2].[Ti+4] SOQBVABWOPYFQZ-UHFFFAOYSA-N 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- 239000008363 phosphate buffer Substances 0.000 description 1
- 229940075930 picrate Drugs 0.000 description 1
- OXNIZHLAWKMVMX-UHFFFAOYSA-M picrate anion Chemical compound [O-]C1=C([N+]([O-])=O)C=C([N+]([O-])=O)C=C1[N+]([O-])=O OXNIZHLAWKMVMX-UHFFFAOYSA-M 0.000 description 1
- 239000004014 plasticizer Substances 0.000 description 1
- 238000005498 polishing Methods 0.000 description 1
- 229920002451 polyvinyl alcohol Polymers 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 229910000027 potassium carbonate Inorganic materials 0.000 description 1
- 159000000001 potassium salts Chemical class 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 208000020016 psychiatric disease Diseases 0.000 description 1
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 1
- 239000002151 riboflavin Substances 0.000 description 1
- 235000019192 riboflavin Nutrition 0.000 description 1
- 229960002477 riboflavin Drugs 0.000 description 1
- 201000000980 schizophrenia Diseases 0.000 description 1
- 239000002400 serotonin 2A antagonist Substances 0.000 description 1
- 239000003772 serotonin uptake inhibitor Substances 0.000 description 1
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 1
- 235000017557 sodium bicarbonate Nutrition 0.000 description 1
- 229910000029 sodium carbonate Inorganic materials 0.000 description 1
- 239000000243 solution Substances 0.000 description 1
- 238000001228 spectrum Methods 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-L succinate(2-) Chemical compound [O-]C(=O)CCC([O-])=O KDYFGRWQOYBRFD-UHFFFAOYSA-L 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 239000003765 sweetening agent Substances 0.000 description 1
- 229940095064 tartrate Drugs 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 239000010936 titanium Substances 0.000 description 1
- 229910052719 titanium Inorganic materials 0.000 description 1
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 1
- IMNIMPAHZVJRPE-UHFFFAOYSA-N triethylenediamine Chemical compound C1CN2CCN1CC2 IMNIMPAHZVJRPE-UHFFFAOYSA-N 0.000 description 1
- 238000005303 weighing Methods 0.000 description 1
- OENHQHLEOONYIE-JLTXGRSLSA-N β-Carotene Chemical compound CC=1CCCC(C)(C)C=1\C=C\C(\C)=C\C=C\C(\C)=C\C=C\C=C(/C)\C=C\C=C(/C)\C=C\C1=C(C)CCCC1(C)C OENHQHLEOONYIE-JLTXGRSLSA-N 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/496—Non-condensed piperazines containing further heterocyclic rings, e.g. rifampin, thiothixene or sparfloxacin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0053—Mouth and digestive tract, i.e. intraoral and peroral administration
- A61K9/0056—Mouth soluble or dispersible forms; Suckable, eatable, chewable coherent forms; Forms rapidly disintegrating in the mouth; Lozenges; Lollipops; Bite capsules; Baked products; Baits or other oral forms for animals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2013—Organic compounds, e.g. phospholipids, fats
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2013—Organic compounds, e.g. phospholipids, fats
- A61K9/2018—Sugars, or sugar alcohols, e.g. lactose, mannitol; Derivatives thereof, e.g. polysorbates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2022—Organic macromolecular compounds
- A61K9/205—Polysaccharides, e.g. alginate, gums; Cyclodextrin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2022—Organic macromolecular compounds
- A61K9/205—Polysaccharides, e.g. alginate, gums; Cyclodextrin
- A61K9/2054—Cellulose; Cellulose derivatives, e.g. hydroxypropyl methylcellulose
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2022—Organic macromolecular compounds
- A61K9/205—Polysaccharides, e.g. alginate, gums; Cyclodextrin
- A61K9/2059—Starch, including chemically or physically modified derivatives; Amylose; Amylopectin; Dextrin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/28—Dragees; Coated pills or tablets, e.g. with film or compression coating
- A61K9/2806—Coating materials
- A61K9/2813—Inorganic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/18—Antipsychotics, i.e. neuroleptics; Drugs for mania or schizophrenia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/28—Dragees; Coated pills or tablets, e.g. with film or compression coating
- A61K9/2806—Coating materials
- A61K9/2833—Organic macromolecular compounds
- A61K9/286—Polysaccharides, e.g. gums; Cyclodextrin
- A61K9/2866—Cellulose; Cellulose derivatives, e.g. hydroxypropyl methylcellulose
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Chemical & Material Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Epidemiology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Molecular Biology (AREA)
- Biophysics (AREA)
- Physiology (AREA)
- Inorganic Chemistry (AREA)
- Nutrition Science (AREA)
- Zoology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- Psychiatry (AREA)
- Neurosurgery (AREA)
- Neurology (AREA)
- Biomedical Technology (AREA)
- Medicinal Preparation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Supply Of Fluid Materials To The Packaging Location (AREA)
- Basic Packing Technique (AREA)
Abstract
Comprimido que comprende 7-[4-(4-benzo[b]tiofen-4-il-piperazin-1-il)butoxi]-1H-quinolin-2-ona o una sal de la misma como principio activo, un excipiente (a), un aglutinante (b), un disgregante (c) y un lubricante (d), en el que el excipiente (a) es al menos un miembro seleccionado del grupo que consiste en lactosa, almidón de maíz y celulosa microcristalina; el aglutinante (b) es hidroxipropilcelulosa; el disgregante (c) es al menos un miembro seleccionado del grupo que consiste en hidroxipropilcelulosa de baja sustitución, croscarmelosa de sodio y carboximetil almidón de sodio; y el lubricante (d) es estearato de magnesio.
Description
DESCRIPCIÓN
Comprimido que incluye 7-[4-(4-benzo[b]tiofen-4-il-piperazin-1-il)butoxi]-1H-quinolin-2-ona o sal de la misma Campo técnico
La presente invención se refiere a un comprimido que comprende 7-[4-(4-benzo[b]tiofen-4-il-piperazin-1-il)butoxi]-1H-quinolin-2-ona o una sal de la misma como principio activo.
Antecedentes de la técnica
Se sabe que 7-[4-(4-benzo[b]tiofen-4-il-piperazin-1-il)butoxi]-1H-quinolin-2-ona (en adelante denominada compuesto (I)) o una sal de la misma actúa como un agonista parcial del receptor D2 de la dopamina, un antagonista del receptor 5-HT2A de la serotonina y un antagonista del receptor a1-adrenérgico, así como un inhibidor de la captación de serotonina (o un inhibidor de la recaptación de serotonina) (documento de patente 1), y posee una amplio espectro terapéutico en el tratamiento de enfermedades del sistema nervioso central (en particular, esquizofrenia).
Lista de referencias
Bibliografía de patentes
PTL 1: publicación de patente japonesa no examinada n.° 2006-316052
El documento US 2011/152286 se refiere a compuestos que incluyen 7-[4-(4-benzo[b]tiofen-4-il-piperazin-1-il)butoxi]-1H-quinolin-2-ona (brexpiprazol) y otros para su uso en el tratamiento de trastornos mentales. Se describe además que el compuesto puede incluirse en una composición farmacéutica tal como un comprimido, junto con excipientes, un aglutinante, un agente disgregante y/o un lubricante. El comprimido también puede recubrirse.
El documento WO 2012/13797 es un derecho anterior según el artículo 54(3) EPC y se refiere a composiciones farmacéuticas que incluyen una combinación de 7-[4-(4-benzo[b]tiofen-4-il-piperazin-1-il)butoxi]-1H-quinolin-2-ona y otro principio activo. La combinación puede formularse como un comprimido, que puede comprender uno o más excipientes, disgregantes, aglutinantes y/o lubricantes.
Sumario de la invención
Problema técnico
Un objeto de la presente invención es proporcionar un comprimido que comprende el compuesto (I) o una sal del mismo como principio activo y que tiene excelente capacidad de disgregación, estabilidad en almacenamiento y alta fotoestabilidad.
Solución al problema
Los presentes inventores realizaron una investigación intensiva para lograr el objeto anterior y encontraron que un comprimido que comprende el compuesto (I) o una sal del mismo como principio activo y que comprende además lactosa, almidón de maíz, celulosa microcristalina o un excipiente similar; hidroxipropilcelulosa de baja sustitución, croscarmelosa de sodio, carboximetil almidón de sodio o un disgregante similar; e hidroxipropilcelulosa o un aglutinante similar muestra una excelente capacidad de disgregación y estabilidad en almacenamiento. Los presentes inventores encontraron además que puede lograrse una fotoestabilidad mayor aplicando una capa de recubrimiento que contiene un colorante. La presente invención se completó a través de estudios adicionales basados en este hallazgo, y se define por las reivindicaciones.
Efectos ventajosos de la invención
El comprimido de la presente invención muestra una excelente capacidad de disgregación, estabilidad en almacenamiento y alta fotoestabilidad, de manera que puede usarse de manera eficaz en el campo médico.
Breve descripción de los dibujos
La figura 1 es un gráfico que muestra los resultados de la prueba de disolución de los comprimidos obtenidos en los ejemplos 1-1 a 1-3 y los ejemplos 2-1 a 2-3.
Descripción de las realizaciones
El comprimido de la presente invención comprende el compuesto (I) o una sal del mismo como principio activo.
En este caso, el comprimido de la presente invención puede ser un comprimido no recubierto que no tiene una capa de recubrimiento aplicada sobre el mismo o un comprimido recubierto que tiene una capa de recubrimiento sobre la superficie del mismo. Además, el comprimido de la presente invención puede usarse como un comprimido de disgregación por vía oral.
El compuesto (I) o una sal del mismo puede producirse mediante un método conocido, por ejemplo, el divulgado en la publicación de patente japonesa no examinada n.° 2006-316052 o un método basado en el mismo.
Las sales del compuesto (I) no están particularmente limitadas siempre que sean farmacológicamente aceptables. Los ejemplos preferibles de las mismas incluyen: sales de metales tales como sales de metales alcalinos (por ejemplo, sales de sodio y sales de potasio), sales de metales alcalinotérreos (por ejemplo, sales de calcio y sales de magnesio), sales de bases inorgánicas tales como sales de amonio, carbonatos de metales alcalinos (por ejemplo, carbonato de litio, carbonato de potasio, carbonato de sodio y carbonato de cesio), hidrogenocarbonatos de metales alcalinos (por ejemplo, hidrogenocarbonato de litio, hidrogenocarbonato de sodio e hidrogenocarbonato de potasio), e hidróxidos de metales alcalinos (por ejemplo, hidróxido de litio, hidróxido de sodio, hidróxido de potasio e hidróxido de cesio); sales de bases orgánicas tales como trialquil(inferior)aminas (por ejemplo, trimetilamina, trietilamina y N-etildiisopropilamina), piridina, quinolina, piperidina, imidazol, picolina, dimetilaminopiridina, dimetilanilina, N-alquil(inferior)-morfolina (por ejemplo, N-metilmorfolina), 1,5-diazabiciclo[4.3.0]non-5-eno (DBN), 1,8-diazabiciclo[5.4.0]undec-7-eno (DBU), 1,4-diazabiciclo[2.2.2]octano (DABCO); sales de ácidos inorgánicos tales como clorhidrato, bromhidrato, sulfato, nitrato y fosfato; sales de ácidos orgánicos tales como formiato, acetato, propionato, oxalato, malonato, succinato, fumarato, maleato, lactato, malato, citrato, tartrato, carbonato, picrato, metanosulfonato, etanosulfonato, p-toluenosulfonato y glutamato; y similares.
El compuesto (I) o una sal del mismo en las formas anteriores puede usarse de manera individual o en una combinación de dos o más.
El contenido del compuesto (I) o una sal del mismo es preferiblemente de aproximadamente el 0,05 al 25% en peso, y más preferiblemente de aproximadamente el 0,1 al 15% en peso con respecto al peso del comprimido (el peso de un comprimido no recubierto antes de aplicar un recubrimiento cuando el comprimido es un comprimido recubierto).
El comprimido de la presente invención comprende aditivos tales como un excipiente (a), un aglutinante (b), un disgregante (c) y un lubricante (d).
El excipiente (a) es al menos un miembro seleccionado de lactosa, almidón de maíz y celulosa microcristalina.
El contenido de excipiente (a) no está particularmente limitado, y es preferiblemente de aproximadamente el 10 al 98,5% en peso con respecto al peso del comprimido (cuando el comprimido está recubierto, el peso del comprimido no recubierto), más preferiblemente de aproximadamente el 20 al 95%, y todavía más preferiblemente de aproximadamente el 30 al 90% en peso.
La cantidad de excipiente (a) no está particularmente limitada, y es preferiblemente de aproximadamente 1 a 2000 partes en peso por 1 parte en peso del compuesto (I) o una sal del mismo, y más preferiblemente de aproximadamente 3 a 1800 partes en peso.
Ajustando el contenido y la cantidad del excipiente (a) tal como se describió anteriormente, puede mejorarse la productividad.
El aglutinante (b) es hidroxipropilcelulosa.
El contenido de aglutinante (b) no está particularmente limitado, y es preferiblemente de aproximadamente el 0,1 al 20% en peso con respecto al peso del comprimido (cuando el comprimido está recubierto, el peso del comprimido no recubierto), y más preferiblemente de aproximadamente el 0,5 al 5% en peso.
La cantidad de aglutinante (b) no está particularmente limitada, y es preferiblemente de aproximadamente 0,01 a 100 partes en peso por 1 parte en peso del compuesto (I) o una sal del mismo, y más preferiblemente de aproximadamente 0,1 a 50 partes en peso. Ajustando el contenido y la cantidad del aglutinante (b) tal como se describió anteriormente, pueden mejorarse la productividad y la capacidad de disgregación.
El disgregante (c) es al menos un miembro seleccionado del grupo que consiste en carboximetil almidón de sodio, carmelosa de calcio, croscarmelosa de sodio e hidroxipropilcelulosa de baja sustitución. Cabe destacar que, cuando se contiene crospovidona, el comprimido obtenido tiende a tener fotoestabilidad y estabilidad en almacenamiento reducidas. Por tanto, es más preferible si no se contiene sustancialmente este componente.
En este caso, en la presente memoria descriptiva, “hidroxipropilcelulosa de baja sustitución” es un derivado de celulosa que incluye grupos hidroxipropoxilo en de aproximadamente el 5 al 16%. La cantidad de los grupos hidroxipropoxilo en la hidroxipropilcelulosa de baja sustitución puede medirse mediante un método enumerado en,
por ejemplo, la Farmacopea Japonesa. La hidroxipropilcelulosa de baja sustitución puede producirse mediante un método conocido en la técnica, o también puede usarse un producto comercialmente disponible de la misma. Los ejemplos de productos comercialmente disponibles de la hidroxipropilcelulosa de baja sustitución incluyen, pero no se limitan a, la “serie LH” y la “serie NBD” fabricadas por Shin-Etsu Chemical Co., Ltd.
Además, en la presente memoria descriptiva, “hidroxipropilcelulosa” es un derivado de celulosa que incluye grupos hidroxipropoxilo en de aproximadamente el 50 al 85%. La cantidad de grupos hidroxipropoxilo en la hidroxipropilcelulosa puede medirse mediante un método enumerado en, por ejemplo, la Farmacopea Japonesa. La hidroxipropilcelulosa puede producirse mediante un método conocido en la técnica, o también puede usarse un producto comercialmente disponible de la misma. Los ejemplos de productos comercialmente disponibles de la hidroxipropilcelulosa incluyen, pero no se limitan a, la “serie HPC” fabricada por Nippon Soda Co., Ltd.; y la “serie Klucel” fabricada por Hercules Inc.
En la presente memoria descriptiva, “carboximetil almidón de sodio” es un derivado de almidón que incluye sodio de aproximadamente el 6 al 11%.
El contenido de disgregante (c) no está particularmente limitado, y es preferiblemente de aproximadamente el 1 al 25% en peso con respecto al peso del comprimido (cuando el comprimido está recubierto, el peso del comprimido no recubierto), más preferiblemente de aproximadamente el 2 al 20% en peso, y todavía más preferiblemente de aproximadamente el 3 al 15% en peso.
Además, la cantidad de disgregante (c) no está particularmente limitada, y es preferiblemente de aproximadamente 0,1 a 500 partes en peso por 1 parte en peso del compuesto (I) o una sal del mismo, más preferiblemente de aproximadamente 1 a 500 partes en peso, y todavía más preferiblemente de aproximadamente 1 a 250 partes en peso. Ajustando el contenido y la cantidad del disgregante (c) tal como se describió anteriormente, puede mejorarse la capacidad de disgregación.
El lubricante (d) es estearato de magnesio.
El contenido de lubricante (d) no está particularmente limitado, y es preferiblemente de aproximadamente el 0,1 al 10% en peso con respecto al peso del comprimido (cuando el comprimido está recubierto, el peso del comprimido no recubierto), más preferiblemente de aproximadamente el 0,2 al 8% en peso, y todavía más preferiblemente de aproximadamente el 0,3 al 7% en peso.
La cantidad de lubricante (d) no está particularmente limitada, y es preferiblemente de aproximadamente 0,01 a 50 partes en peso por 1 parte en peso del compuesto (I) o una sal del mismo, y más preferiblemente de aproximadamente 0,02 a 30 partes en peso. Ajustando el contenido y la cantidad del lubricante (d) tal como se describió anteriormente, puede mejorarse la capacidad de formación de comprimidos.
El comprimido de la presente invención puede comprender otros componentes además del excipiente (a), el aglutinante (b), el disgregante (c) y el lubricante (d). Los ejemplos de otros componentes incluyen diversos aditivos aplicables a comprimidos, tales como colorantes, ajustadores de pH, conservantes, absorbefacientes, potenciadores del sabor, antioxidantes, tampones, agentes quelantes, abrasivos, disolventes, agentes de endurecimiento, tensioactivos, edulcorantes, fluidizadores, agentes de abrillantamiento y aromatizantes. Esos componentes pueden usarse en una cantidad que no afecte negativamente a la presente invención.
El comprimido de la presente invención puede usarse como un comprimido no recubierto que comprende los componentes descritos anteriormente pero que no tiene una capa de recubrimiento proporcionada sobre el mismo. Un comprimido recubierto (comprimido recubierto con película) proporcionado con una capa de recubrimiento es preferible para lograr una estabilidad en almacenamiento a largo plazo y prevenir la degradación debida a la luz o similares.
La capa de recubrimiento puede comprender aditivos farmacéuticos, tales como un agente de recubrimiento, un plastificante, un dispersante, agente antiespumante, y similares, habitualmente usados para recubrir (para proporcionar un recubrimiento a) preparaciones farmacéuticas administrables por vía oral.
Los ejemplos de aditivos incluyen celulosas tales como celulosa microcristalina, metilcelulosa, etilcelulosa, carmelosa de sodio, hidroxipropilcelulosa e y hidroxipropil metil celulosa (hipromelosa) y derivados de los mismos; polietilenglicol (macrogol); poli(alcohol vinílico); óxido de titanio; y talco. Estos aditivos pueden usarse de manera individual o en una combinación de dos o más.
Entre estos, es preferible una combinación de hidroxipropil metil celulosa (hipromelosa), talco y óxido de titanio, que son componentes para el agente de recubrimiento. Cabe destacar que, cuando existe polietilenglicol (macrogol) en la capa de recubrimiento, el comprimido obtenido tiende a tener fotoestabilidad y estabilidad en almacenamiento reducidas. Por tanto, es más preferible si no se contiene sustancialmente polietilenglicol (macrogol).
Además, con respecto al comprimido recubierto, puede suministrarse fotoestabilidad al comprimido recubierto coloreando la capa de recubrimiento. Por tanto, se añade preferiblemente un colorante (e) al agente de recubrimiento para recubrir el comprimido.
Los ejemplos de colorantes (e) incluyen: óxidos de hierro tales como óxido férrico rojo, óxido férrico amarillo y óxido de hierro negro; óxido de titanio; beta-caroteno; colorante alimenticio azul n.° 2; colorante alimenticio azul n.° 2 aluminio lago; y riboflavina.
Entre estos, contener un óxido de hierro es más preferible desde el punto de vista de no sólo añadir un color al comprimido sino también mejorar adicionalmente la fotoestabilidad del comprimido.
El colorante (e) puede seleccionarse de manera adecuada, o usarse en combinación, dependiendo del color del comprimido recubierto preparado. Por ejemplo, para obtener un comprimido recubierto blanco, se usa óxido de titanio; para obtener un comprimido recubierto rojo, se usa una combinación de óxido de titanio y óxido férrico rojo; para obtener un comprimido recubierto amarillo, se usa una combinación de óxido de titanio y óxido férrico amarillo; para obtener un comprimido recubierto azul, se usa una combinación de óxido de titanio y colorante alimenticio azul n.° 2 aluminio lago; para obtener un comprimido recubierto naranja, se usa una combinación de óxido de titanio, óxido férrico rojo y óxido férrico amarillo; para obtener un comprimido recubierto verde, se usa una combinación de óxido de titanio, óxido férrico amarillo y óxido de hierro negro, o una combinación de óxido de titanio, óxido férrico amarillo y colorante alimenticio azul n.° 2 aluminio lago; y para obtener un comprimido recubierto morado, se usa una combinación de óxido de titanio, óxido férrico rojo y óxido de hierro negro, o una combinación de óxido de titanio, óxido férrico rojo y colorante alimenticio azul n.° 2 aluminio lago. Tal como se describió anteriormente, un comprimido recubierto puede elaborarse en diversos colores.
El contenido de colorante (e) es preferiblemente de aproximadamente el 0,1 al 3% en peso con respecto al peso total del comprimido recubierto, y de aproximadamente el 5 al 50% en peso con respecto al peso de la capa de recubrimiento del comprimido recubierto.
La cantidad de una capa de recubrimiento en el comprimido que se recubre usando el agente de recubrimiento y un colorante (e) que está contenido, si es necesario, es preferiblemente de aproximadamente 1 a 10 partes en peso por 100 partes en peso de un comprimido (comprimido no recubierto) antes de tener un recubrimiento proporcionado sobre el mismo.
Desde un punto de vista de productividad y capacidad de disgregación, estos aditivos se usan en una combinación de: como excipiente (a), al menos un miembro seleccionado del grupo que consiste en lactosa, almidón de maíz y celulosa microcristalina; como aglutinante (b), hidroxipropilcelulosa; como disgregante (c), al menos un miembro seleccionado del grupo que consiste en hidroxipropilcelulosa de baja sustitución, croscarmelosa de sodio y carboximetil almidón de sodio; y, como lubricante (d), estearato de magnesio.
El contenido y la cantidad de cada uno de los componentes en un modo preferible adicional del comprimido de la presente invención se muestran a continuación.
Contenido de cada uno de los componentes en el comprimido
Compuesto (I) o una sal del mismo: del 0,1 al 15% en peso
Lactosa: del 30 al 60% en peso
Almidón de maíz: del 10 al 30% en peso
Celulosa microcristalina: del 5 al 20% en peso
Hidroxipropilcelulosa: del 0,5 al 10% en peso
Al menos un miembro seleccionado del grupo que
consiste en hidroxipropilcelulosa de baja sustitución, del 2 al 15% en peso
croscarmelosa de sodio y carboximetil almidón de sodio:
Estearato de magnesio: del 0,1 al 10% en peso
Cantidad de cada uno de los componentes en el comprimido por 1 parte en peso del compuesto (I) o una sal del mismo
Lactosa: de 2 a 500 partes en peso
Almidón de maíz: de 2 a 200 partes en peso
Celulosa microcristalina: de 0,5 a 100 partes en peso
Hidroxipropilcelulosa: de 0,05 a 50 partes en peso
Al menos un miembro seleccionado del grupo que
consiste en hidroxipropilcelulosa de baja sustitución, de 1 a 250 partes en peso
croscarmelosa de sodio y carboximetil almidón de sodio:
Estearato de magnesio: de 0,05 a 30 partes en peso
Cuando el comprimido de la presente invención es un comprimido recubierto, los ejemplos preferibles de los aditivos contenidos en el comprimido recubierto incluyen, como los componentes para un comprimido no recubierto antes de recubrirse: el excipiente (a), el aglutinante (b) el disgregante (c) y el lubricante (d) tal como se definió anteriormente, y como componentes para la capa de recubrimiento: derivados de celulosa, talco, óxidos de titanio y óxidos de hierro como colorante (e).
Además, cuando el comprimido de la presente invención es un comprimido recubierto, una combinación más preferible es una formulación obtenida aplicando una capa de recubrimiento sobre un comprimido no recubierto; en la que el comprimido no recubierto contiene el compuesto (I) o una sal del mismo, lactosa, almidón de maíz, celulosa microcristalina, hidroxipropilcelulosa de baja sustitución, hidroxipropilcelulosa y estearato de magnesio, y la capa de recubrimiento contiene hipromelosa, talco, óxido de titanio y al menos un colorante (e) (óxido de hierro) seleccionado del grupo que consiste en óxido férrico rojo, óxido férrico amarillo y óxido de hierro negro.
El contenido y la cantidad preferibles de cada uno de los componentes, y el contenido y la cantidad preferibles adicionalmente de cada uno de los componentes en un modo preferible del comprimido recubierto se muestran a continuación.
Contenido de cada uno de los componentes en el comprimido no recubierto
Compuesto (I) o una sal del mismo: del 0,1 al 15% en peso
Lactosa: del 30 al 60% en peso
Almidón de maíz: del 10 al 30% en peso
Celulosa microcristalina: del 5 al 20% en peso
Hidroxipropilcelulosa: del 0,5 al 10% en peso
Al menos un miembro seleccionado del grupo que
consiste en hidroxipropilcelulosa de baja sustitución, del 2 al 15% en peso
croscarmelosa de sodio y carboximetil almidón de sodio:
Estearato de magnesio: del 0,1 al 10% en peso
Contenido de cada uno de los componentes en la capa de recubrimiento (por comprimido recubierto completo) Hipromelosa: del 1,5 al 4% en peso
Talco: del 0,2 al 0,5% en peso
Óxido de titanio: del 0,2 al 1% en peso
Óxido de hierro: del 0,02 al 0,5% en peso
Cantidad de cada uno de los componentes en el comprimido recubierto por 1 parte en peso del compuesto (I) o una sal del mismo
Lactosa: de 2 a 500 partes en peso
Almidón de maíz: de 2 a 200 partes en peso
Celulosa microcristalina: de 0,5 a 100 partes en peso
Hidroxipropilcelulosa: de 0,05 a 50 partes en peso
Al menos un miembro seleccionado del grupo que
consiste en hidroxipropilcelulosa de baja sustitución, de 1 a 250 partes en peso
croscarmelosa de sodio y carboximetil almidón de sodio:
Estearato de magnesio: de 0,05 a 30 partes en peso
Hipromelosa: de 0,2 a 40 partes en peso
Talco: de 0,02 a 8 partes en peso
Óxido de titanio: de 0,02 a 15 partes en peso
Óxido de hierro: de 0,001 a 2,5 partes en peso
El método para producir el comprimido de la presente invención no está particularmente limitado; por ejemplo, el comprimido de la presente invención puede producirse mediante una etapa de formar, en un comprimido, una mezcla que contiene el compuesto (I) o una sal del mismo, y componentes distintos del compuesto (I) o una sal del mismo necesarios para formar un comprimido (es decir, un excipiente (a), un aglutinante (b), un disgregante (c), un lubricante (d) y similares). Alternativamente, el comprimido de la presente invención puede producirse mediante el método que comprende: granular una mezcla que contiene el compuesto (I) o una sal del mismo, un excipiente (a), un aglutinante (b) y un disgregante (c), y mezclar adicionalmente con la misma un lubricante (d); y formar la mezcla obtenida en un comprimido.
El método de granulación usado para formar la sustancia granulada en un comprimido no está particularmente limitado. Los ejemplos del mismo incluyen métodos de granulación en seco y métodos de granulación en húmedo (por ejemplo, un método de granulación en lecho fluidizado y un método de granulación por amasado). Entre estos, se usan preferiblemente métodos de granulación en húmedo para la producción, desde el punto de vista de la posibilidad de mezclar de manera uniforme el principio activo y otros componentes en el comprimido, y la posibilidad
de obtener un comprimido cuyos componentes se distribuyen de manera uniforme en el mismo.
Los ejemplos de métodos de formación de comprimidos incluyen la formación de comprimidos, tal como formación de comprimidos por compresión directa, formación de comprimidos en seco, formación de comprimidos en húmedo y formación de comprimidos por lubricación externa.
El comprimido recubierto de la presente invención puede producirse mezclando un agente de recubrimiento, un colorante (e) y un medio líquido; pulverizando la mezcla líquida obtenida sobre la superficie del comprimido no recubierto obtenido mediante el método descrito anteriormente; y secándolo sucesivamente.
Los ejemplos del medio líquido (por ejemplo, un medio de dispersión) usado en la etapa descrita anteriormente incluyen: agua; metanol, etanol, isopropanol, y alcoholes inferiores similares; acetona, metil etil cetona, y cetonas similares; diclorometano, dicloroetano, cloroformo, tetracloruro de carbono e hidrocarburos halogenados similares; y mezclas de estos disolventes.
El comprimido de la presente invención preferiblemente comprende el compuesto (I), que es un principio activo, o una sal del mismo, en una cantidad de aproximadamente 0,05 a 25 mg calculados como compuesto (I).
La dosis del comprimido de la presente invención se selecciona de manera adecuada según el uso previsto; la edad, el sexo y otras condiciones del paciente; la gravedad de la enfermedad; y similares. La dosis se selecciona preferiblemente de manera que la cantidad del compuesto (I) (es decir, el principio activo) o una sal del mismo tomada es de aproximadamente 0,05 a 6 mg por día calculada como compuesto (I).
Ejemplos
La presente invención se explica en detalle a continuación con referencia a los ejemplos. Sin embargo, el alcance de la presente invención no se limita a estos ejemplos. Obsérvese que en todos los ejemplos descritos a continuación, el compuesto (I) era “7-[4-(4-benzo[b]tiofen-4-il-piperazin-1-il)butoxi]-1H-quinolin-2-ona”.
Ejemplo 1
Se produjeron comprimidos no recubiertos (un comprimido no proporcionado con una capa de recubrimiento) del compuesto (I) usando los componentes y las cantidades mostrados en la tabla 1, siguiendo los procedimientos descritos a continuación.
Ejemplo 1-1
Se pesaron y mezclaron compuesto (I), lactosa, almidón de maíz, celulosa microcristalina (CEOLUS PH-301) e hidroxipropilcelulosa de baja sustitución (LH-11, fabricada por Shin-Etsu Chemical Co., Ltd., contenido de grupos hidroxipropoxilo: del 10,0 al 12,9%). Se añadió una disolución acuosa preparada de manera separada de hidroxipropilcelulosa a la mezcla en polvo, seguido por granulación por amasado en húmedo. Después del secado y de la calibración del resultado, se añadió estearato de magnesio a la misma y se mezcló. Se sometió a compresión la mezcla resultante usando una máquina de formación de comprimidos individuales equipada con un punzón de 6,5 mm de diámetro de tal manera que el peso del comprimido se convirtió en 100 mg, obteniendo comprimidos no recubiertos que contenían 10 mg del compuesto (I) por comprimido.
Ejemplo 1-2
Se pesaron y mezclaron compuesto (I), lactosa, almidón de maíz, celulosa microcristalina y croscarmelosa de sodio. Se añadió una disolución acuosa preparada de manera separada de hidroxipropilcelulosa a la mezcla en polvo, seguido por granulación por amasado en húmedo. Después del secado y de la calibración del resultado, se añadió estearato de magnesio a la misma y se mezcló. Se sometió a compresión la mezcla resultante usando una máquina de formación de comprimidos individuales equipada con un punzón de 6,5 mm de diámetro de tal manera que el peso del comprimido se convirtió en 100 mg, obteniendo comprimidos no recubiertos que contenían 10 mg del compuesto (I) por comprimido.
Ejemplo 1-3
Se pesaron y mezclaron compuesto (I), lactosa, almidón de maíz, celulosa microcristalina y carboximetil almidón de sodio. Se añadió una disolución acuosa preparada de manera separada de hidroxipropilcelulosa a la mezcla en polvo, seguido por granulación por amasado en húmedo. Después del secado y de la calibración del resultado, se añadió estearato de magnesio a la misma y se mezcló. Se sometió a compresión la mezcla resultante usando una máquina de formación de comprimidos individuales equipada con un punzón de 6,5 mm de diámetro de tal manera que el peso del comprimido se convirtió en 100 mg, obteniendo comprimidos no recubiertos que contenían 10 mg del compuesto (I) por comprimido.
Tabla 1
La tabla 2 muestra las propiedades de comprimido de comprimidos no recubiertos obtenidos en los ejemplos 1-1 a 1-3.
Tabla 2
Los resultados de medición del tiempo de disgregación (prueba de disgregación) muestran los resultados de medición de seis comprimidos de cada ejemplo. La prueba se realizó usando agua como líquido de prueba según la prueba de disgregación de la Farmacopea Japonesa (sin un disco auxiliar).
Ejemplos 2-1 a 2-3
Los comprimidos no recubiertos producidos en los ejemplos 1-1 a 1-3 que tenían cada uno un peso de 100 mg y que contenían 10 mg del compuesto (I) se sometieron a recubrimiento pulverizando un líquido de recubrimiento que comprendía los componentes de capa de recubrimiento cuyas cantidades se muestran en la tabla 3, obteniéndose de ese modo comprimidos recubiertos.
Tabla 3
Las mediciones del tiempo de disgregación (prueba de disgregación) se realizaron para los comprimidos recubiertos producidos en los ejemplos 2-1 a 2-3 de la misma manera que en el ejemplo 1-1. La tabla 4 muestra los resultados. No se observó retraso en el tiempo de disgregación debido al recubrimiento en los comprimidos recubiertos producidos en los ejemplos 2-1 a 2-3.
Tabla 4
Las pruebas de disolución se realizaron para los comprimidos no recubiertos producidos en los ejemplos 1-1 a 1-3, y los comprimidos recubiertos producidos en los ejemplos 2-1 a 2-3. La figura 1 muestra los resultados.
Los resultados de la prueba de disolución muestran los valores promedio de los resultados de medición de dos comprimidos de cada ejemplo. La prueba de disolución se realizó según el método de prueba de disolución (método
de paletas; 50 rpm) de la Farmacopea Japonesa, usando una disolución tampón de hidrogenofosfato de disodioácido cítrico (900 ml) con pH 4,5 como líquido de prueba.
Los resultados de la prueba de disolución confirman unos excelentes perfiles de disolución de los comprimidos no recubiertos producidos en los ejemplos 1-1 a 1-3 y los comprimidos recubiertos producidos en los ejemplos 2-1 a 2 3.
Además, se realizó una prueba de estabilidad para los comprimidos no recubiertos producidos en los ejemplos 1-1 a 1-3 y los comprimidos recubiertos producidos en los ejemplos 2-1 a 2-3 en las condiciones de almacenamiento de irradiación de luz (luz visible: iluminancia total de 1,8x106 lux h; luz ultravioleta: intensidad total de 300 W h/m2) y un sistema cerrado a 40°C (sellado en frascos durante un mes o tres meses). Se midieron los contenidos del compuesto (I) y las impurezas después del almacenamiento en cada condición. La tabla 5 muestra los resultados. Obsérvese que después del almacenamiento en las condiciones de irradiación de luz anteriores, se observó una coloración amarilla en los comprimidos no recubiertos producidos en los ejemplos 1-1 a 1-3.
Tabla 5
Ejemplo 3-1
Usando los componentes y las cantidades mostrados en la tabla 6, se produjeron comprimidos no recubiertos que contenían 0,25 mg del compuesto (I) por comprimido de la misma manera que en el ejemplo 1-1, excepto que se usó una máquina de formación de comprimidos rotatoria equipada con un punzón de 6,0 mm de diámetro para obtener los comprimidos no recubiertos que tenían cada uno un peso de 90 mg.
Tabla 6
Ejemplos 3-2 a 3-9
Los comprimidos no recubiertos producidos en el ejemplo 3-1 que tenían cada uno un peso de 90 mg y que contenían 0,25 mg del compuesto (I) se sometieron a recubrimiento pulverizando un líquido de recubrimiento que comprendía los componentes de capa de recubrimiento cuyas cantidades se muestran en la tabla 7, obteniéndose de ese modo comprimidos recubiertos.
Tabla 7
Además, se realizó una prueba de estabilidad para los comprimidos no recubiertos producidos en el ejemplo 3-1 y los comprimidos recubiertos producidos en los ejemplos 3-2 a 3-9 en las condiciones de almacenamiento de irradiación de luz (luz visible: iluminancia total de 1,8x106 luxh; luz ultravioleta: intensidad total de 300 W h/m2) y un sistema abierto a 40°C/el 75% de HR (tres meses, seis meses), es decir, condiciones iguales o más rigurosas que las de los ejemplos 1-1 a 1-3 y los ejemplos 2-1 a 2-3. Se midieron los contenidos de impurezas después del almacenamiento en cada condición. La tabla 8 muestra los resultados.
No se observó un aumento en las impurezas en los comprimidos de los ejemplos 3-5 y 3-7, incluso después de la irradiación de luz.
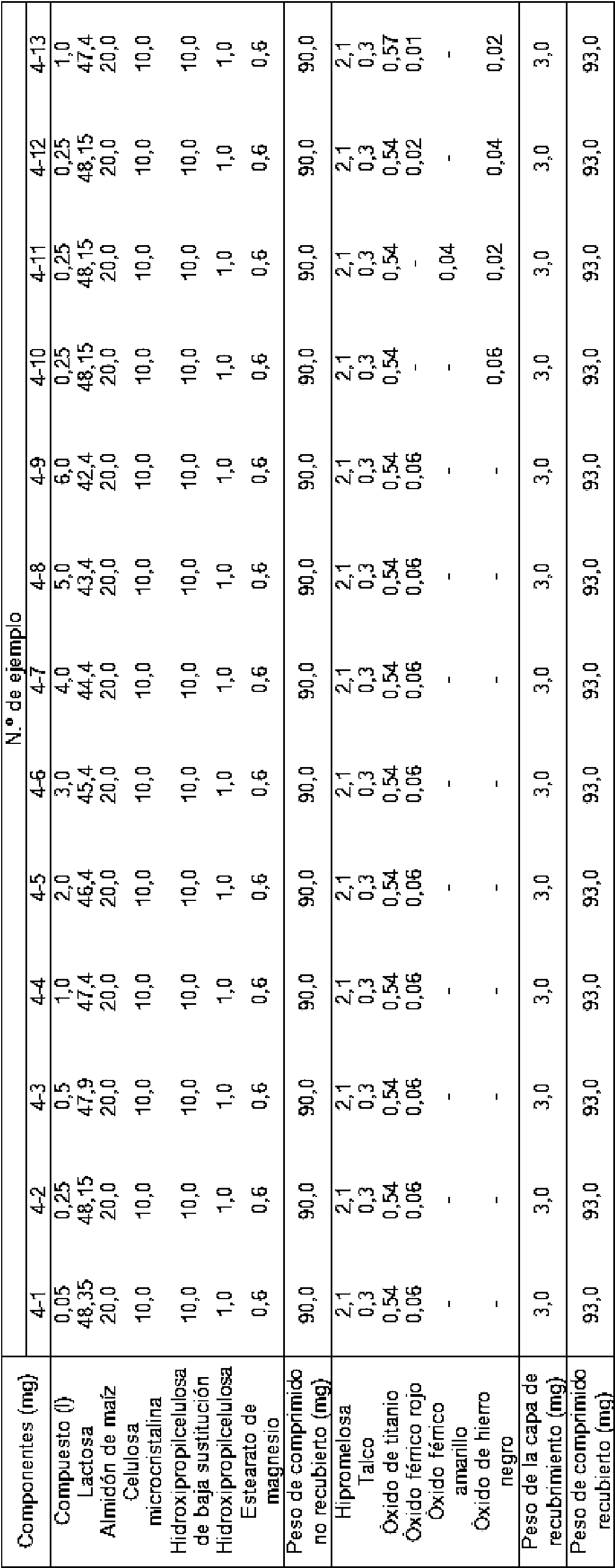
Ejemplos 4-1 a 4-13
Se produjeron comprimidos recubiertos del compuesto (I) de los ejemplos 4-1 a 4-13 que comprendían los componentes y las cantidades mostrados en la tabla 9 de la misma manera que en el ejemplo 3-2.
Aplicabilidad industrial
El comprimido de la presente invención que comprende compuesto de benzotiofeno (I) o una sal del mismo tiene excelente capacidad de disgregación, estabilidad en almacenamiento y fotoestabilidad. Por tanto, el comprimido de la presente invención es altamente utilizable en el campo médico.
Claims (9)
1. Comprimido que comprende 7-[4-(4-benzo[b]tiofen-4-il-piperazin-1-il)butoxi]-1H-quinolin-2-ona o una sal de la misma como principio activo, un excipiente (a), un aglutinante (b), un disgregante (c) y un lubricante (d), en el que el excipiente (a) es al menos un miembro seleccionado del grupo que consiste en lactosa, almidón de maíz y celulosa microcristalina;
el aglutinante (b) es hidroxipropilcelulosa;
el disgregante (c) es al menos un miembro seleccionado del grupo que consiste en hidroxipropilcelulosa de baja sustitución, croscarmelosa de sodio y carboximetil almidón de sodio; y
el lubricante (d) es estearato de magnesio.
2. Comprimido según la reivindicación 1, en el que el comprimido es un comprimido no recubierto que comprende:
del 0,05 al 25% en peso de 7-[4-(4-benzo[b]tiofen-4-il-piperazin-1-il)butoxi]-1H-quinolin-2-ona o una sal de la misma;
del 10 al 98,5% en peso del excipiente (a);
del 0,1 al 20% en peso del aglutinante (b);
del 1 al 25% en peso del disgregante (c); y
del 0,1 al 10% en peso del lubricante (d), con respecto al peso del comprimido no recubierto.
3. Comprimido según la reivindicación 1 ó 2, en el que por 1 parte en peso de 7-[4-(4-benzo[b]tiofen-4-ilpiperazin-1-il)butoxi]-1H-quinolin-2-ona o una sal de la misma, el comprimido comprende:
de 1 a 2000 partes en peso del excipiente (a);
de 0,01 a 100 partes en peso del aglutinante (b);
de 0,1 a 500 partes en peso del disgregante (c); y
de 0,01 a 50 partes en peso del lubricante (d).
4. Comprimido según una cualquiera de las reivindicaciones 1 a 3, que comprende además una capa de recubrimiento sobre la superficie del mismo.
5. Comprimido según la reivindicación 4, que comprende además el colorante (e) en la capa de recubrimiento, en el que el colorante (e) contiene un óxido de hierro, y
el comprimido contiene del 0,1 al 50% en peso del colorante (e) con respecto al peso de la capa de recubrimiento.
6. Comprimido según una cualquiera de las reivindicaciones 1 a 5, que se obtiene formando, en un comprimido, una sustancia granulada obtenida a través de granulación en húmedo.
7. Comprimido según una cualquiera de las reivindicaciones 1 a 6, en el que el comprimido no contiene povidona o crospovidona.
8. Método para producir un comprimido, comprendiendo el método las etapas de:
(1) granular una mezcla que contiene 7-[4-(4-benzo[b]tiofen-4-il-piperazin-1-il)butoxi]-1H-quinolin-2-ona o una sal de la misma, un excipiente (a), un aglutinante (b) y un disgregante (c), y mezclar adicionalmente con la misma un lubricante (d); y
(2) formar la mezcla obtenida en un comprimido,
en el que el excipiente (a) es al menos un miembro seleccionado del grupo que consiste en lactosa, almidón de maíz y celulosa microcristalina;
el aglutinante (b) es hidroxipropilcelulosa;
el disgregante (c) es al menos un miembro seleccionado del grupo que consiste en hidroxipropilcelulosa de baja sustitución, croscarmelosa de sodio y carboximetil almidón de sodio; y
el lubricante (d) es estearato de magnesio.
9. Método para producir el comprimido según la reivindicación 8, que comprende además la etapa de:
(3) mezclar un agente de recubrimiento, un colorante (e) y un medio líquido para obtener una mezcla de recubrimiento, y recubrir la superficie del comprimido usando la mezcla de recubrimiento.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2011227057 | 2011-10-14 | ||
| PCT/JP2012/076415 WO2013054872A1 (ja) | 2011-10-14 | 2012-10-12 | 7-[4-(4-ベンゾ[b]チオフェン-4-イル-ピペラジン-1-イル)ブトキシ]-1H-キノリン-2-オン又はその塩を含む錠剤 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| ES2762479T3 true ES2762479T3 (es) | 2020-05-25 |
| ES2762479T5 ES2762479T5 (en) | 2025-05-30 |
Family
ID=48081918
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES12840025T Active ES2762479T5 (en) | 2011-10-14 | 2012-10-12 | Tablet comprising 7-[4-(4-benzo[b]thiophen-4-yl-piperazin-1-yl) butoxy]-1h-quinolin-2-one or a salt thereof |
Country Status (34)
| Country | Link |
|---|---|
| US (8) | US20140234417A1 (es) |
| EP (1) | EP2767285B2 (es) |
| JP (2) | JP6084161B2 (es) |
| KR (1) | KR102072371B1 (es) |
| CN (2) | CN107397730A (es) |
| AP (1) | AP2014007564A0 (es) |
| AR (1) | AR088319A1 (es) |
| AU (1) | AU2012321723C1 (es) |
| BR (1) | BR112014008603A2 (es) |
| CA (1) | CA2851588C (es) |
| CL (1) | CL2014000909A1 (es) |
| CO (1) | CO6950480A2 (es) |
| CY (1) | CY1122460T1 (es) |
| DK (1) | DK2767285T4 (es) |
| EA (1) | EA032930B1 (es) |
| ES (1) | ES2762479T5 (es) |
| FI (1) | FI2767285T4 (es) |
| HR (1) | HRP20200037T4 (es) |
| HU (1) | HUE047493T2 (es) |
| IL (1) | IL231513B (es) |
| IN (1) | IN2014DN02055A (es) |
| JO (1) | JO3753B1 (es) |
| LT (1) | LT2767285T (es) |
| MX (1) | MX376092B (es) |
| MY (1) | MY173370A (es) |
| PH (1) | PH12014500607A1 (es) |
| PL (1) | PL2767285T5 (es) |
| PT (1) | PT2767285T (es) |
| SG (2) | SG2014013783A (es) |
| SI (1) | SI2767285T2 (es) |
| TW (1) | TWI634908B (es) |
| UA (1) | UA114411C2 (es) |
| WO (1) | WO2013054872A1 (es) |
| ZA (1) | ZA201402333B (es) |
Families Citing this family (21)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| TWI320783B (en) | 2005-04-14 | 2010-02-21 | Otsuka Pharma Co Ltd | Heterocyclic compound |
| JO3753B1 (ar) * | 2011-10-14 | 2021-01-31 | Otsuka Pharma Co Ltd | قرص يتألف من 7-[4-(4-بينزو[بي]ثيوفين-4-ايل-ببرازين-1-1ايل)بوتكسيل]-1اتش-كوينولين-2-وان أو ملح منه |
| JOP20200109A1 (ar) | 2012-04-23 | 2017-06-16 | Otsuka Pharma Co Ltd | مستحضر قابل للحقن |
| JP5936732B1 (ja) * | 2015-03-05 | 2016-06-22 | 日本カラコン合同会社 | フィルムコーティング組成物 |
| CN105106142B (zh) * | 2015-09-22 | 2018-05-22 | 成都欣捷高新技术开发有限公司 | 一种含有依匹哌唑的冻干口服制剂及其制备方法 |
| CN106994119A (zh) * | 2016-01-22 | 2017-08-01 | 浙江华海药业股份有限公司 | 含有依匹哌唑或其盐的口腔崩解片及其制备方法 |
| EP3417861B1 (en) * | 2016-02-19 | 2020-09-23 | Jiangsu Hengrui Medicine Co., Ltd. | Pharmaceutical composition containing jak kinase inhibitor or pharmaceutically acceptable salt thereof |
| JP7020688B2 (ja) * | 2016-06-28 | 2022-02-16 | 株式会社日本抗菌総合研究所 | 賦形剤及び錠剤 |
| JP7060878B2 (ja) * | 2016-07-27 | 2022-04-27 | 日本臓器製薬株式会社 | メトトレキサート含有フィルムコーティング錠 |
| EP3500247B1 (en) | 2016-08-16 | 2020-05-27 | H e x a l Aktiengesellschaft | Immediate release tablet of a benzothiophene compound |
| EP3500249A1 (en) | 2016-08-16 | 2019-06-26 | Hexal Aktiengesellschaft | Pharmaceutical compositions of a benzothiophene compound |
| CN106496206A (zh) * | 2016-08-31 | 2017-03-15 | 安徽省润生医药股份有限公司 | 一种依匹哌唑新的制备方法 |
| NZ755349A (en) * | 2017-02-23 | 2025-03-28 | Boehringer Ingelheim Int | New medical use of compound iii |
| JP7166754B2 (ja) | 2017-11-22 | 2022-11-08 | 沢井製薬株式会社 | ダサチニブ無水物含有製剤 |
| EP3501506B1 (en) | 2017-12-19 | 2019-10-09 | Alfred E. Tiefenbacher (GmbH & Co. KG) | Pharmaceutical tablet composition comprising brexpiprazole |
| EP3545950A1 (en) | 2018-03-26 | 2019-10-02 | Adamed sp. z o.o. | Pharmaceutical composition comprising brexpiprazole |
| JPWO2021029020A1 (es) * | 2019-08-13 | 2021-02-18 | ||
| WO2021095092A1 (ja) * | 2019-11-11 | 2021-05-20 | 大塚製薬株式会社 | 口腔内崩壊錠 |
| CN112168794A (zh) * | 2020-10-27 | 2021-01-05 | 浙江诺得药业有限公司 | 一种布瑞哌唑片的制备方法 |
| WO2022218358A1 (zh) * | 2021-04-13 | 2022-10-20 | 上海博志研新药物技术有限公司 | 一种布瑞哌唑物口腔薄膜剂、其制备方法及应用 |
| EP4374856A1 (en) | 2022-11-23 | 2024-05-29 | Sanovel Ilac Sanayi Ve Ticaret A.S. | A process for tablets comprising brexpiprazole |
Family Cites Families (22)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6562375B1 (en) * | 1999-08-04 | 2003-05-13 | Yamanouchi Pharmaceuticals, Co., Ltd. | Stable pharmaceutical composition for oral use |
| WO2003055467A1 (en) * | 2001-12-18 | 2003-07-10 | Synthon B.V. | Simvastatin dosage forms |
| BR0309875A (pt) * | 2002-05-03 | 2007-04-10 | Israel Inst For Biolog Res Isr | métodos e composições para tratamento de distúrbios do sistema nervoso periférico e novos compostos úteis para isto |
| MXPA05011643A (es) | 2003-04-29 | 2005-12-15 | Pfizer Ltd | 5,7-diaminopirazolo[4,3-d]pirimidinas en el tratamiento de hipertension. |
| US7247596B2 (en) * | 2003-06-09 | 2007-07-24 | Dow Global Technologies Inc. | Stabilized organoborane polymerization initiators and polymerizable compositions |
| JP2006061067A (ja) * | 2004-08-26 | 2006-03-09 | Asahi Kasei Life & Living Corp | 酸素インジケーター |
| GB0504203D0 (en) * | 2005-03-01 | 2005-04-06 | Novartis Ag | Organic compounds |
| CA2600542A1 (en) | 2005-03-17 | 2006-09-21 | Synthon B.V. | Pharmaceutical tablets of crystalline type ii aripiprazole |
| JP4315393B2 (ja) | 2005-04-14 | 2009-08-19 | 大塚製薬株式会社 | 複素環化合物 |
| TWI320783B (en) * | 2005-04-14 | 2010-02-21 | Otsuka Pharma Co Ltd | Heterocyclic compound |
| EP2036545A1 (en) | 2006-01-05 | 2009-03-18 | Teva Pharmaceutical Industries Ltd. | Aripiprazole tablets |
| JP4806595B2 (ja) * | 2006-07-05 | 2011-11-02 | 富士フイルム株式会社 | 固体撮像素子駆動装置及びデジタルカメラ |
| JP4540700B2 (ja) * | 2006-10-13 | 2010-09-08 | 大塚製薬株式会社 | 医薬 |
| WO2008106059A1 (en) * | 2007-02-26 | 2008-09-04 | Merck & Co., Inc. | Formulations for cathepsin k inhibitors |
| US7994183B2 (en) * | 2007-03-13 | 2011-08-09 | Takeda Pharmaceutical Company Limited | Solid preparation comprising 2-[[6-[(3R)-3-amino-1-piperidinyl]-3,4-dihydro-3-methyl-2,4-dioxo-1(2H)-pyrimidinyl]methyl]-4-fluorobenzonitrile |
| KR20100016270A (ko) * | 2007-05-11 | 2010-02-12 | 산텐 세이야꾸 가부시키가이샤 | 비맥각계의 선택적 d2 수용체 작용제를 유효 성분으로서 함유하는 후안부 질환의 예방 또는 치료제 |
| BRPI0818323A2 (pt) * | 2007-10-12 | 2017-05-16 | Astrazeneca Ab | composição farmacêutica, uso de uma composição farmacêutica, e, método para tratar câncer. |
| JP5463564B2 (ja) * | 2009-05-22 | 2014-04-09 | 国立大学法人信州大学 | 耐熱性及び耐塩性セルラーゼ製剤 |
| TR201000948A1 (tr) | 2010-02-09 | 2011-08-22 | Sanovel İlaç San.Ve Ti̇c.A.Ş. | Aripiprazol formülasyonları. |
| AR085840A1 (es) * | 2011-04-05 | 2013-10-30 | Otsuka Pharma Co Ltd | Medicamento que contiene un compuesto que es 7-[4-(4-benzo[b]tiofen-4-il-piperazin-1-il)butoxi]-1h-quinolin-2-ona |
| EP3173096A1 (en) | 2011-04-06 | 2017-05-31 | Biovaxim Limited | Pharmaceutical compositions for preventing and/or treating an hiv disease in humans |
| JO3753B1 (ar) * | 2011-10-14 | 2021-01-31 | Otsuka Pharma Co Ltd | قرص يتألف من 7-[4-(4-بينزو[بي]ثيوفين-4-ايل-ببرازين-1-1ايل)بوتكسيل]-1اتش-كوينولين-2-وان أو ملح منه |
-
2012
- 2012-10-04 JO JOP/2012/0301A patent/JO3753B1/ar active
- 2012-10-09 TW TW101137267A patent/TWI634908B/zh active
- 2012-10-12 MX MX2014004135A patent/MX376092B/es active IP Right Grant
- 2012-10-12 BR BR112014008603A patent/BR112014008603A2/pt not_active Application Discontinuation
- 2012-10-12 SI SI201231718T patent/SI2767285T2/sl unknown
- 2012-10-12 AU AU2012321723A patent/AU2012321723C1/en active Active
- 2012-10-12 MY MYPI2014700632A patent/MY173370A/en unknown
- 2012-10-12 JP JP2013538582A patent/JP6084161B2/ja active Active
- 2012-10-12 ES ES12840025T patent/ES2762479T5/es active Active
- 2012-10-12 PT PT128400256T patent/PT2767285T/pt unknown
- 2012-10-12 LT LTEP12840025.6T patent/LT2767285T/lt unknown
- 2012-10-12 UA UAA201405029A patent/UA114411C2/uk unknown
- 2012-10-12 CN CN201710266863.7A patent/CN107397730A/zh active Pending
- 2012-10-12 AR ARP120103801A patent/AR088319A1/es not_active Application Discontinuation
- 2012-10-12 AP AP2014007564A patent/AP2014007564A0/xx unknown
- 2012-10-12 WO PCT/JP2012/076415 patent/WO2013054872A1/ja active Application Filing
- 2012-10-12 HR HRP20200037TT patent/HRP20200037T4/hr unknown
- 2012-10-12 EA EA201490783A patent/EA032930B1/ru active Protection Beyond IP Right Term
- 2012-10-12 PH PH1/2014/500607A patent/PH12014500607A1/en unknown
- 2012-10-12 CN CN201280050586.1A patent/CN103889425B/zh active Active
- 2012-10-12 SG SG2014013783A patent/SG2014013783A/en unknown
- 2012-10-12 PL PL12840025.6T patent/PL2767285T5/pl unknown
- 2012-10-12 US US14/351,325 patent/US20140234417A1/en not_active Abandoned
- 2012-10-12 CA CA2851588A patent/CA2851588C/en active Active
- 2012-10-12 FI FIEP12840025.6T patent/FI2767285T4/fi active
- 2012-10-12 DK DK12840025.6T patent/DK2767285T4/da active
- 2012-10-12 SG SG10201608412SA patent/SG10201608412SA/en unknown
- 2012-10-12 HU HUE12840025A patent/HUE047493T2/hu unknown
- 2012-10-12 KR KR1020147010656A patent/KR102072371B1/ko active Active
- 2012-10-12 EP EP12840025.6A patent/EP2767285B2/en active Active
-
2014
- 2014-03-13 IL IL231513A patent/IL231513B/en active IP Right Grant
- 2014-03-19 IN IN2055DEN2014 patent/IN2014DN02055A/en unknown
- 2014-03-28 ZA ZA2014/02333A patent/ZA201402333B/en unknown
- 2014-04-10 CL CL2014000909A patent/CL2014000909A1/es unknown
- 2014-05-07 CO CO14098041A patent/CO6950480A2/es unknown
-
2016
- 2016-02-09 US US15/019,874 patent/US20160158227A1/en not_active Abandoned
-
2017
- 2017-01-20 JP JP2017008854A patent/JP2017088610A/ja active Pending
- 2017-02-27 US US15/444,113 patent/US20170165258A1/en not_active Abandoned
- 2017-09-22 US US15/713,427 patent/US10307419B2/en active Active
-
2019
- 2019-04-12 US US16/383,488 patent/US20190240215A1/en not_active Abandoned
-
2020
- 2020-01-08 CY CY20201100009T patent/CY1122460T1/el unknown
- 2020-10-01 US US17/061,394 patent/US20210023078A1/en not_active Abandoned
-
2022
- 2022-03-07 US US17/653,838 patent/US20220331311A1/en not_active Abandoned
-
2023
- 2023-12-18 US US18/543,053 patent/US20240277703A1/en active Pending
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2762479T3 (es) | Comprimido que incluye 7-[4-(4-benzo[b]tiofen-4-il-piperazin-1-il)butoxi]-1H-quinolin-2-ona o sal de la misma | |
| ES2988678T3 (es) | Un comprimido que comprende un derivado de metoxiurea y partículas de manitol | |
| US20190046452A1 (en) | Preparation containing 6,7-unsaturated-7-carbamoyl morphinan derivatives | |
| ES2674811T3 (es) | Composiciones estables de fesoterodina | |
| KR20230124655A (ko) | 경구 고형 제제 | |
| US10034855B2 (en) | Solid composition of pyrrole carboxamide | |
| US20170202777A1 (en) | Solid preparation | |
| HK1195740B (en) | TABLET COMPRISING 7-[4-(4-BENZO[b]THIOPHEN-4-YL-PIPERAZIN-1-YL)BUTOXY]-1H-QUINOLIN-2-ONE OR A SALT THEREOF | |
| HK1195740A (en) | TABLET COMPRISING 7-[4-(4-BENZO[b]THIOPHEN-4-YL-PIPERAZIN-1-YL)BUTOXY]-1H-QUINOLIN-2-ONE OR A SALT THEREOF | |
| NZ622639B2 (en) | TABLET COMPRISING 7-[4-(4-BENZO[b]THIOPHEN-4-YL-PIPERAZIN-1-YL) BUTOXY]-1H-QUINOLIN-2-ONE OR A SALT THEREOF | |
| NZ735026B2 (en) | Solid preparations of N-(4-(1-(2,6-difluorobenzyl)-5-((dimethyl amino)methyl)-3-(6-methoxy-3-pyridazinyl)-2,4-dioxo-1,2,3,4-tetrahydrothieno[2,3-d]pyrimidine-6-yl)phenyl)-N'-methoxyurea or a salt thereof, and methods of preparing same | |
| HK1247826B (en) | Solid composition of pyrrole carboxamide |