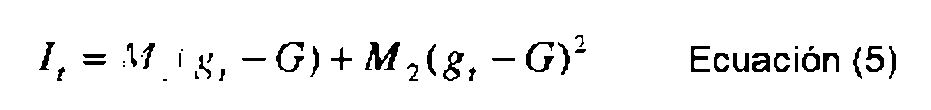ES2716235T3 - Sistemas para gestionar dispositivos de suministro de medicamentos - Google Patents
Sistemas para gestionar dispositivos de suministro de medicamentos Download PDFInfo
- Publication number
- ES2716235T3 ES2716235T3 ES10838319T ES10838319T ES2716235T3 ES 2716235 T3 ES2716235 T3 ES 2716235T3 ES 10838319 T ES10838319 T ES 10838319T ES 10838319 T ES10838319 T ES 10838319T ES 2716235 T3 ES2716235 T3 ES 2716235T3
- Authority
- ES
- Spain
- Prior art keywords
- patient
- therapy
- specific
- delivery system
- drug delivery
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- G—PHYSICS
- G16—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR SPECIFIC APPLICATION FIELDS
- G16H—HEALTHCARE INFORMATICS, i.e. INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR THE HANDLING OR PROCESSING OF MEDICAL OR HEALTHCARE DATA
- G16H20/00—ICT specially adapted for therapies or health-improving plans, e.g. for handling prescriptions, for steering therapy or for monitoring patient compliance
- G16H20/10—ICT specially adapted for therapies or health-improving plans, e.g. for handling prescriptions, for steering therapy or for monitoring patient compliance relating to drugs or medications, e.g. for ensuring correct administration to patients
- G16H20/17—ICT specially adapted for therapies or health-improving plans, e.g. for handling prescriptions, for steering therapy or for monitoring patient compliance relating to drugs or medications, e.g. for ensuring correct administration to patients delivered via infusion or injection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M2205/00—General characteristics of the apparatus
- A61M2205/35—Communication
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M2205/00—General characteristics of the apparatus
- A61M2205/35—Communication
- A61M2205/3507—Communication with implanted devices, e.g. external control
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M2205/00—General characteristics of the apparatus
- A61M2205/35—Communication
- A61M2205/3546—Range
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M2205/00—General characteristics of the apparatus
- A61M2205/35—Communication
- A61M2205/3546—Range
- A61M2205/3561—Range local, e.g. within room or hospital
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M2205/00—General characteristics of the apparatus
- A61M2205/35—Communication
- A61M2205/3576—Communication with non implanted data transmission devices, e.g. using external transmitter or receiver
-
- G—PHYSICS
- G16—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR SPECIFIC APPLICATION FIELDS
- G16H—HEALTHCARE INFORMATICS, i.e. INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR THE HANDLING OR PROCESSING OF MEDICAL OR HEALTHCARE DATA
- G16H50/00—ICT specially adapted for medical diagnosis, medical simulation or medical data mining; ICT specially adapted for detecting, monitoring or modelling epidemics or pandemics
- G16H50/50—ICT specially adapted for medical diagnosis, medical simulation or medical data mining; ICT specially adapted for detecting, monitoring or modelling epidemics or pandemics for simulation or modelling of medical disorders
Landscapes
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Chemical & Material Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Medicinal Chemistry (AREA)
- Epidemiology (AREA)
- General Health & Medical Sciences (AREA)
- Medical Informatics (AREA)
- Primary Health Care (AREA)
- Public Health (AREA)
- Infusion, Injection, And Reservoir Apparatuses (AREA)
Abstract
Un método para transferir la administración de una terapia desde un primer sistema médico a un segundo sistema médico, comprendiendo el método: un primer sistema de suministro de medicamentos electrónico que se conecta a un paciente que recibe un identificador de paciente que corresponde con el paciente; el primer sistema de suministro de medicamentos electrónico que estima las variables de control subyacentes específicas del paciente en base a (i) la terapia proporcionada a un paciente y (ii) la respuesta específica del paciente observada a la terapia, en donde las variables de control subyacentes específicas del paciente permiten la determinación de una dosis en base a un modelo; en base a (i) las variables de control subyacentes específicas del paciente, (ii) la respuesta específica del paciente a la terapia observada, y (iii) el objetivo de la terapia, el primer sistema de suministro de medicamentos que proporciona una terapia actualizada para el paciente para adaptar la terapia al paciente; el primer sistema de suministro de medicamentos electrónico transfiere a un sistema remoto un registro de la terapia actualizada proporcionada al paciente y las variables de control subyacentes específicas del paciente estimadas; tras conectar un segundo sistema de suministro de medicamentos al paciente, el segundo sistema de suministro de medicamentos electrónico recibe el identificador del paciente; el segundo sistema de suministro de medicamentos electrónico se comunica con el sistema remoto para acceder al registro de la terapia actualizada y las variables de control subyacentes específicas del paciente estimadas asociadas con el identificador del paciente; determinar el momento en que se interrumpió la terapia por el primer sistema de suministro de medicamentos electrónico y determinar en base al tiempo la cantidad en la que hay que reducir la terapia que se proporcionada; y ajustar el registro de la terapia actualizada para tener en cuenta la cantidad en que ajustar la terapia que será proporcionada por el segundo sistema de suministro de medicamentos electrónico.
Description
DESCRIPCIÓN
Sistemas para gestionar dispositivos de suministro de medicamentos
Referencia cruzada a las solicitudes relacionadas
Campo
La presente solicitud se relaciona con la automatización de una terapia de medicamentos, y más particularmente, con los sistemas y métodos para gestionar y suministrar la terapia al paciente a través de sistemas de suministro de medicamentos electrónicos, que incluyen una bomba de infusión y un sensor, monitor, o medidor para medir las características fisiológicas del paciente o la respuesta a la terapia, por ejemplo.
Antecedentes
El tratamiento de pacientes hospitalizados frecuentemente implica el control de uno o más parámetros fisiológicos en concierto con la administración de fluidos, de productos farmacéuticos y de la nutrición a través de bombas de infusión intravenosa (IV). Los sistemas actuales dependen de la intervención de personal clínico que ajustan de manera manual las tasas de infusión en base a las variables monitorizadas y los protocolos en “papel”, que se derivan de la experiencia y/o la evidencia según se presenta en la bibliografía médica.
Sin embargo, el proceso de control (o valoración) manual es una carga para los profesionales sanitarios y puede no lograr el cuidado óptimo del paciente. En parte, esto es debido a la complejidad del problema del control fisiológico, los limitados recursos disponibles para monitorizar el estado del paciente, y la naturaleza estática de los protocolos de ajuste. La intervención manual proporciona también oportunidades a la introducción de errores médicos durante el cálculo, la entrada de datos, o la programación de la bomba IV, por ejemplo. Además, los protocolos en papel y/o los nomogramas usados por la enfermera de cabecera pueden ser necesariamente simples y pueden no ser capaces de compensar la amplia variedad de sensibilidades farmacológicas del paciente, las características no lineales de la respuesta a los medicamentos, y la naturaleza dinámica a lo largo del tiempo.
Como un ejemplo de una condición que requiere tratamiento posiblemente usando intervención manual, la hiperglucemia o el alto nivel de azúcar en sangre es una condición en la que circula una cantidad excesiva de glucosa en el plasma sanguíneo. La hiperglucemia pronunciada se produce en aproximadamente el 75% de los pacientes gravemente enfermos y se asocia con un aumento significativo en la morbilidad y la mortalidad. Los estudios han mostrado que mantener niveles de glucosa en sangre normales a través de la infusión intravenosa (IV) de insulina puede llevar a mejorar los resultados en los pacientes gravemente enfermos. Por tanto, el tratamiento de la hiperglucemia requiere la eliminación de la causa subyacente si es posible, por ejemplo, el tratamiento de la diabetes cuando la diabetes es la causa, y en la mayoría de los casos, se usa la administración directa de la insulina, bajo supervisión médica. Sin embargo, las prácticas clínicas actuales para el tratamiento de la hiperglucemia que implican una terapia de insulina intensiva son una actividad pesada que implica frecuentes mediciones de la glucosa en sangre (1-2 horas) seguidas del ajuste manual de la tasa de infusión IV de insulina. Los cambios en la infusión de la insulina son dirigidos por protocolos que pueden fallar al representar de manera adecuada las diferencias entre paciente y paciente y presentar un alto riesgo de hipoglucemia. Por tanto, la supervisión manual por personal médico puede aumentar las posibilidades de error humano y a menudo no consideran las respuestas específicas de los pacientes a la terapia farmacológico.
Compendio
En los métodos ejemplares descritos en la presente memoria, se proporciona un método para gestionar y suministrar la terapia del paciente a través de sistemas de suministro de medicamentos electrónicos, que pueden incluir una bomba de infusión y un sensor, monitor, o medidor para medir una característica fisiológica del paciente o respuesta a la terapia. El método incluye un primer sistema de suministro de medicamentos que se conecta a un paciente recibiendo el identificador de paciente que corresponde al paciente, y estimando el primer sistema de suministro de medicamentos las variables de control subyacentes específicas del paciente en base a (i) la terapia proporcionada para el paciente y (ii) la respuesta específica del paciente a la terapia. En base a (i) las variables de control subyacentes específicas del paciente, (i) la respuesta específica del paciente a la terapia observada, y (iii) el objetivo de la terapia, el primer sistema de suministro de medicamentos proporciona una terapia actualizada para el paciente. El método además incluye el primer sistema de suministro de medicamentos que transfiere a un sistema remoto, que puede incluir uno o más ordenadores, interfaces y bases de datos, un registro de la terapia actualizada proporcionada al paciente y las variables de control subyacentes específicas del paciente estimadas. Tras conectar un segundo sistema de suministro de medicamentos al paciente, el segundo sistema de suministro de medicamentos recibe el identificador del paciente, y el segundo sistema de suministro de medicamentos se comunica con el sistema remoto para acceder al registro de la terapia actualizada y de las variables de control subyacentes específicas del paciente estimadas asociadas con el identificador del paciente.
Usando los métodos de ejemplo descritos más adelante, el segundo sistema de suministro de medicamentos recibe el registro de la terapia y las variables de control subyacentes específicas del paciente estimadas asociadas con el
identificador del paciente desde el sistema remoto, y continua la terapia del paciente en el punto en el que la terapia fue reportada anteriormente o de manera opcional interrumpida por el primer sistema de suministro de medicamentos.
En otros aspectos, los sistemas ejemplares descritos en la presente memoria se proporcionan para gestionar y suministrar la terapia del paciente a través de los sistemas de suministro de medicamentos. El sistema incluye un primer sistema de suministro de medicamentos conectado a un paciente que recibe un identificador de paciente que corresponde al paciente, y en base a (i) las variables de control subyacentes específicas del paciente estimadas (i) la respuesta específica del paciente observada a la terapia, y (iii) el objetivo de la terapia, el primer sistema de suministro de medicamentos proporciona una terapia actualizada para el paciente. El primer sistema de suministro de medicamentos transfiere a un sistema remoto un registro de la terapia actualizada proporcionada al paciente y las variables de control subyacentes específicas del paciente estimadas. El sistema también incluye un segundo sistema de suministro de medicamentos que recibe el identificador del paciente y se comunica con el sistema remoto para acceder al registro de la terapia actualizada y las variables de control subyacentes específicas del paciente estimadas asociadas con el identificador del paciente.
En aún otros aspectos, se proporciona un medio legible por un ordenador que tiene almacenado en éste instrucciones ejecutables por un dispositivo de computación para provocar que el dispositivo de computación realice ciertas funciones. Las funciones incluyen la recepción desde un primer sistema de suministro de medicamentos electrónico de un registro de las variables de control subyacentes específicas del paciente estimadas de un paciente. Las variables de control subyacentes específicas del paciente se basan en (i) una terapia proporcionada a un paciente y (ii) la respuesta específica del paciente observada a la terapia. Las funciones incluyen también la recepción desde el primer sistema de suministro de medicamentos electrónico de la terapia actualizada proporcionada al paciente. Estando la terapia actualizada basada en (i) las variables de control subyacentes específicas del paciente estimadas, (i) la respuesta específica del paciente a la terapia, y (iii) el objetivo de la terapia. Las funciones incluyen también la transferencia a un segundo sistema de suministro de medicamentos electrónico de un registro de la terapia actualizada proporcionada al paciente y las variables de control subyacentes específicas del paciente estimadas asociadas con el paciente.
El compendio anterior es sólo ilustrativo y no está destinado a ser limitante de ninguna manera. Además de los aspectos ilustrativos, las realizaciones, y las características descritas anteriormente, aspectos, realizaciones, y características adicionales resultarán evidentes mediante la referencia a los dibujos y la descripción detallada siguiente.
El Documento de los EE.UU. 2005/055242 A1 describe un sistema para el seguimiento, análisis y reporte de los datos médicos, para un sistema de cuidado de la salud. En concreto D1 describe en el párrafo [0021] que un dispositivo médico puede almacenar de manera local información y en una base de datos separada en un servidor, por ejemplo. Si el dispositivo falla, o el paciente se mueve a un segundo dispositivo, se puede transferir la información a un segundo dispositivo de manera tal que el segundo dispositivo pueda reanudar una terapia compleja en el punto en que la dejó el dispositivo médico inicial.
El Documento WO 2009/023634 A2 describe un sistema para controlar los dispositivos médicos y describe los cambios de terapia en las páginas 29-31 y las actualizaciones de orden de la terapia en las páginas 67-71. Sin embargo, ambos documentos fallan al describir
(i) determinar el tiempo que la terapia fue interrumpida,
(ii) determinar la cantidad en la que reducir la terapia y
(iii) ajustar el registro de la terapia actualizada... que será proporcionado por el segundo sistema de suministro de medicamentos electrónico
Breve descripción de los dibujos
La Figura 1 ilustra una configuración ejemplar para gestionar y suministrar la terapia a un paciente a través de los sistemas de suministro de medicamentos.
La Figura 2 ilustra otra configuración ejemplar para gestionar y suministrar la terapia a un paciente a través de los sistemas de suministro de medicamentos.
La Figura 3 ilustra aún otra configuración ejemplar para gestionar y suministrar la terapia a un paciente a través de los sistemas de suministro de medicamentos.
La Figura 4 ilustra un método ejemplar para suministrar la terapia de medicamentos usando un dispositivo médico. La Figura 5 ilustra un ejemplo de una configuración para transferir datos desde un dispositivo médico a otro.
La Figura 6 ilustra otro ejemplo de una configuración para transferir datos desde un dispositivo médico a otro.
La Figura 7 ilustra un ejemplo de una memoria para almacenar el registro de datos de un paciente y los registros de variables específicas de un paciente.
La Figura 8 ilustra un diagrama de bloques que incluye un dispositivo médico ejemplar con un controlador a bordo integrado para modelar la respuesta de un paciente a la terapia y calcular las variables de control subyacentes específicas del paciente.
Descripción detallada
En la siguiente descripción detallada, se hace referencia a los dibujos adjuntos, que forman parte de la misma. En los dibujos, símbolos similares identifican normalmente componentes similares, a menos que el contexto dictamine lo contrario. Las realizaciones ilustrativas descritas en la descripción detallada, los dibujos, y las reivindicaciones no están destinadas a ser limitantes. Otras realizaciones se pueden utilizar, y otros cambios se pueden hacer.
Se entenderá fácilmente que los aspectos de la presente descripción, tal y como se describen de manera general en la presente memoria, y se ilustran en la Figuras, se pueden disponer, sustituir, combinar, y diseñar en una amplia variedad de configuraciones diferentes, todas las cuales se contemplan de manera explícita y forman parte de esta descripción.
La automatización de los sistemas de terapia, tales como el sistema de infusión, proporciona oportunidades para mejorar el flujo de trabajo, reducir los errores de usuario, y permitir el resultado deseado de la terapia. Por ejemplo, se puede incluir un algoritmo del protocolo de infusión en una bomba de infusión para la automatización adicional del sistema para reducir los errores de entrada, mejorar el flujo de trabajo, y mejorar la eficiencia. Además, los dispositivos de infusión, prueba, y monitorización se pueden interconectar entre sí con servidores y otros ordenadores en un entorno hospitalario para permitir que se transfiera la información a los dispositivos. Dicha información incluye información de la medicación, de las tasas de medicación, del volumen a ser infundido, de la duración, de la frecuencia, del cuidador, de los identificadores del dispositivo y del paciente, de los valores monitorizados, y de los datos de prueba del punto de atención, por ejemplo.
En los métodos y sistemas ejemplares descritos, un dispositivo médico puede almacenar información de manera local y en una base de datos separada en un servidor, por ejemplo. Si el dispositivo falla, o un paciente se mueve a un segundo dispositivo puede reanudar la terapia compleja en el punto en el que lo dejó el dispositivo médico inicial. Los datos necesarios para volver a iniciar el sistema de terapia complejo (por ejemplo iterativo o recursivo) pueden incluir ciertas variables o parámetros de control subyacentes específicas del paciente calculadas o estimadas según un modelo que captura la respuesta fisiológica del paciente a la medicación en cuestión. Como resultado, es posible para el segundo dispositivo iniciar la compleja terapia en cualquier punto en la línea de tiempo en la que el primer dispositivo estaba modelando o aprendiendo sobre de la respuesta del paciente y usar esa información en lugar de tener que volver a iniciar el segundo dispositivo en la compleja terapia a partir de un conjunto de suposiciones iniciales de referencia. De manera alternativa, una parte de o todo el historial acumulativo de la terapia desde el primer dispositivo se puede transferir o transmitir al segundo dispositivo y las variables de control específicas del paciente se pueden volver a calcular por el segundo dispositivo usando la información histórica.
Referente ahora a las figuras, la Figura 1 ilustra un ejemplo de configuración para gestionar y suministrar la terapia del paciente a través de sistemas de suministro de medicamentos electrónicos. Se proporciona un sistema 102 de información hospitalaria para soportar la admisión, descarga, y transferencia de los datos de los pacientes a través de un hospital o comunidad médica, por ejemplo. El sistema 102 de información hospitalaria puede existir en forma de un servidor u otro tipo de estación de trabajo, y se puede conectar a una base de datos 104 a través de una red u otra interfaz, por ejemplo. La base de datos 104 puede incluir información específica del paciente relacionada con el tratamiento para el paciente. Una estación de trabajo 106 puede estar conectada también a la base de datos 104 para ser usada por un administrador o enfermera del hospital para introducir los datos del paciente, y para proporcionar la capacidad de generar reportes, generar e imprimir órdenes de dosificación de insulina subcutánea, y modificar los parámetros de configuración, por ejemplo. El sistema 102 de información hospitalaria, la base de datos 104, y la estación de trabajo 106 se pueden ubicar en un hospital o también fuera de éste.
Un dispositivo 108 médico ubicado en la cabecera del paciente puede estar en comunicación con el sistema 102 de información hospitalaria, la base de datos 104, o la estación de trabajo 106 usando una red con ya sea una conexión inalámbrica o por cable para recibir los datos específicos del paciente, que pueden incluir los datos de Transferencia de Alta de Admisión, del Sistema de Información Farmacéutica, o de los Sistemas de Información del Laboratorio, y para suministrar la terapia del paciente a una paciente 110. Una enfermera 112 u otro personal del hospital puede introducir los ajustes en el dispositivo 108 médico para suministrar la terapia al paciente 110 al que se conecta el dispositivo 108 médico. La unidad 114 de medición se puede conectar de manera operativa para, asociada con o usada en el paciente 110 a medir, monitorizar o medir la característica fisiológica del paciente o la respuesta a la terapia. Se puede extraer sangre u otros fluidos del paciente y ser examinados o analizados por la unidad 114 de medición. Por ejemplo, la unidad 114 de medición puede incluir un monitor de presión sanguínea, un monitor de glucosa en sangre, u otro monitor/medidor según sea necesario para medir una característica deseada del paciente
En un ejemplo, el dispositivo 108 médico puede ser una bomba de infusión que controla el nivel de glucosa en un paciente usando un algoritmo de software que incluye un mecanismo de retroalimentación para el control del azúcar en sangre para, pacientes estresados y en estado crítico. Por ejemplo, el dispositivo 108 médico puede ser un sistema, bomba o infusor de infusión Symbiq ®, disponible de Hospira, Inc. de Lake Forest, Illinois, que ejecuta un software, tal como el Endo Tool ® disponible también de Hospira, Inc., para realizar un método para calcular las tasas/dosis de insulina apropiadas y los intervalos de medición de glucosa para proporcionar una terapia de insulina intensiva. El método puede proporcionar al personal clínico con una dosis de insulina, dosis D50W (Dextrosa al 50% en agua), y recomendaciones de la frecuencia de comprobación (el momento de la siguiente comprobación de la glucosa) a través de una interfaz de la bomba, por ejemplo. Después de que el personal clínico haya confirmado o modificado la tasa de infusión de insulina recomendada, la tasa de infusión de la bomba se puede cambiar de manera automática.
Además de proporcionar una tasa recomendada para la infusión de insulina, el dispositivo 108 médico puede indicar el momento de la siguiente medición de glucosa. La medición de glucosa se puede proporcionar tal y como se describe anteriormente o la unidad 114 de medición puede incluir un medidor de glucosa de mano transportado por el personal clínico. La unidad 114 de medición puede estar en comunicación con el dispositivo 108 médico a través de una conexión por cable o inalámbrica o la unidad 114 de medición puede proporcionar al personal clínico las mediciones a introducir de manera manual en la bomba. Se puede recordar al personal clínico en momentos designados a través de la interfaz de la bomba actualizar el nivel de glucosa en sangre del paciente a través de la interfaz. Una serie de alertas y/o alarmas son generadas por el dispositivo 108 médico si no se recibe la medición de glucosa en el momento designado.
El dispositivo 108 médico puede ser capaz de un funcionamiento autónomo sin conexión con un servidor o cualquier sistema 102 de información hospitalaria, la base de datos 104, o la estación de trabajo 106. Sin embargo, el dispositivo 108 médico puede ser configurado usando la estación de trabajo 106 o por la enfermera 112 usando una interfaz en el dispositivo 108 médi
(CCA) y las específicas del hospital u otros datos del paciente.
La Figura 2 ilustra otro ejemplo de configuración para gestionar y suministrar la terapia al paciente a través de sistemas de suministro de medicamentos. En esta configuración, un sistema 202 de información hospitalaria se conecta a una base de datos 204, y una estación de trabajo 206 se puede conectar también a la base de datos 204 de una manera similar a la descrita con respecto de la Figura 1. El sistema 202 de información hospitalaria, la base de datos 204, y la estación de trabajo 206 se pueden ubicar en el hospital o también fuera de éste y conectarse a través de una red, por ejemplo.
Un servidor 208 de la red médica se puede conectar a la base de datos 204 para acceder y recibir los datos específicos del paciente. La información CCA, u otra información útil para el personal del hospital. El servidor 208 de la red médica se puede conectar también a una base de datos 210. El servidor 208 de la red médica y la base de datos 210 se pueden ubicar en el hospital, alejados de la cabecera del paciente, en la habitación del paciente, o también fuera de ésta.
Se puede proporcionar también un dispositivo 212 médico para suministrar la terapia de medicamentos a un paciente 214. El dispositivo médico puede estar en comunicación con el servidor 212 de la red médica para recibir información de la biblioteca de medicamentos, y para enviar información demográfica, de estado, y de los eventos del paciente al servidor 212 de la red médica, por ejemplo. En un ejemplo, el dispositivo 212 médico puede ser una bomba de infusión tal como se describe anteriormente. Se puede proporcionar también una unidad 216 de medición como se describe anteriormente.
El servidor 208 de la red médica puede soportar la transferencia de los parámetros de configuración desde bien las bases de datos 204 o 210 hasta el dispositivo 212 médico. El servidor 208 de la red médica pude agregar todos los datos relacionados con y usados por el dispositivo 212 médico para llenar las bases de datos 204 o 210. Por ejemplo, los datos centrados en el paciente, los datos centrados en el CCA, y el informe de registro de eventos pueden ser proporcionados a través del servidor 208 de la red médica al igual que la generación de órdenes de dosis de insulina subcutánea.
La Figura 3 ilustra aún otro ejemplo de configuración para gestionar y suministrar la terapia del paciente a través de los sistemas de suministro de medicamentos. En esta configuración, el sistema 302 de información hospitalaria se conecta al servidor 304 de la red médica, de manera similar a la configuración en la Figura 2. Sin embargo, sólo se proporciona una base datos 306 conectada al servidor 304 de la red médica. Un dispositivo 308 médico se comunica con el servidor 304 de la red médica para suministrar la terapia de medicamentos al paciente 310. El dispositivo 308 médico puede funcionar de manera similar a los dispositivos médicos de las Figuras 1 o 2, por ejemplo. La configuración tal como se muestra en la Figura 3 puede incluir también una unidad de medición (no mostrada) conectada al paciente y en comunicación con el dispositivo 308 médico y/o el servidor 304 de la red médica, por ejemplo.
En cualquiera de las configuraciones de las Figuras 1, 2, o 3, un dispositivo médico administra la terapia de medicamentos a un paciente, y se puede comunicar con los servidores y las bases de datos para enviar y recibir la
información específica del paciente, la información de suministro de los medicamentos, o los registros de eventos, por ejemplo.
Referente de nuevo a la Figura 1, el dispositivo 108 médico se hace funcionar para controlar el suministro de medicamentos al paciente 110. El dispositivo 108 médico se puede conectar al paciente a través de líneas intravenosas, por ejemplo. La Figura 4 ilustra un método ejemplar para suministrar la terapia de medicamentos usando el dispositivo 108 médico.
Inicialmente, como se muestra en el bloque 402, el dispositivo 108 médico puede recibir un identificador de paciente (ID) que corresponde al paciente. El ID del paciente se puede incluir en una pulsera en un paciente que puede ser recibido escaneando la pulsera, por ejemplo. El dispositivo 108 médico puede usar después el ID del paciente para recuperar la información específica del paciente de la base de datos 104 o del sistema 102 de información hospitalaria.
El dispositivo 108 médico puede iniciar entonces la terapia de medicamentos al paciente 110. Para hacer esto, como se muestra en el bloque 404, el dispositivo médico puede estimar las variables de control subyacentes específicas del paciente (por ejemplo, los niveles de glucosa en sangre) en base a la terapia calculada para el paciente 110, y en base a la respuesta específica del paciente observada (es decir, medida) a la terapia. La terapia se puede calcular dependiendo de todas las variables específicas del paciente, tales como la altura, el peso, etc., y se determina el tratamiento apropiado para la condición del paciente.
Ya que el dispositivo 108 médico observa la respuesta del paciente a la terapia, el dispositivo 108 médico puede actualizar la terapia para abordar mejor las necesidades del paciente. Por tanto, como se muestra en el bloque 406, en base a las variables de control subyacentes específicas del paciente, la respuesta específica del paciente observada a la terapia, y el objetivo de la terapia, el dispositivo 108 médico proporciona una terapia actualizada para el paciente.
El dispositivo 108 médico continuará monitorizando y observando la respuesta de paciente a la terapia y actualizará de manera continua la terapia según sea necesario. El dispositivo 108 médico puede transferir a un sistema remoto, tal como la base de datos 104 por ejemplo, un registro de la terapia actualizada proporcionada al paciente y las variables de control subyacentes específicas del paciente estimadas, como se muestra en el bloque 408. La información de terapia transferida desde el dispositivo 108 médico a la base de datos 104 puede incluir también las respuestas medidas del paciente y los tiempos en los que se tomaron las mediciones. Por supuesto, los datos de la medición se pueden transferir también de manera directa desde la unidad 114 de medición a la base de datos 104. Por tanto, la información actualizada de la terapia se puede almacenar en un dispositivo alternativo como respaldo, o transferir el control de la terapia a otro dispositivo. Por ejemplo tras conectar un segundo sistema de suministro de medicinas al paciente, el segundo sistema de suministro de medicinas puede recibir el identificador del paciente, como se muestra en el bloque 410, y el segundo sistema de suministro de medicinas puede comunicarse con el sistema remoto para acceder al registro de la terapia actualizada y a las variables de control subyacentes específicas del paciente estimadas asociadas con el identificador del paciente, como se muestra en el bloque 412. El segundo sistema de suministro de medicinas puede continuar entonces la terapia del paciente. Si el dispositivo 108 médico se desconecta posteriormente del paciente, el segundo sistema de suministro de medicinas puede continuar la terapia en el punto en que el dispositivo médico lo dejó. De esta manera, no se ha de volver a empezar la terapia desde el punto de comienzo inicial, sino que en su lugar, el segundo sistema de suministro de medicinas puede usar la información recopilada por el primer dispositivo 108 médico para mantener y continuar la terapia actualizada. La Figura 5 ilustra un ejemplo de una configuración para transferir datos desde un dispositivo médico a otro. Como se explicó con referencia al método 400 de la Figura 4, el dispositivo 108 médico puede transferir la terapia actualizada y las variables de control subyacentes específicas del paciente estimadas a la base de datos 104. Antes, durante, o después de conectar un segundo dispositivo 114 médico al paciente 110, el segundo dispositivo 114 médico puede recuperar la terapia actualizada y las variables de control subyacentes específicas del paciente estimadas de la base de datos 104 para continuar la terapia.
La Figura 6 ilustra otro ejemplo de un método para transferir datos desde un dispositivo médico a otro. Inicialmente, como se muestra en el bloque 602, las variables de control subyacentes específicas de paciente se estiman usando un primer dispositivo médico, y se transfieren a un servidor remoto. Las variables de control subyacentes específicas de paciente estimadas se pueden transferir de forma continua, o en un estado específico o un punto de informe de registro, o tras la terminación de la terapia por el primer dispositivo médico, por ejemplo. Una vez que la terapia proporcionada por el primer dispositivo médico se termina, como se muestra en el bloque 604, se elimina la autorización de terapia del primer dispositivo, como se muestra en el bloque 606. Por ejemplo, un servidor puede enviar un mensaje de control al primer dispositivo médico dando instrucciones al primer dispositivo médico para interrumpir la terapia al paciente.
Un segundo dispositivo médico puede recibir el ID del paciente para continuar la terapia al paciente, como se muestra en el bloque 608. Una enfermera puede conectar el segundo dispositivo médico al paciente, y puede introducir el ID del paciente y seleccionar la terapia para su tratamiento. El segundo dispositivo puede consultar entonces un servidor de la red médica (por ejemplo, un servidor remoto) en busca de las variables de control
subyacentes específicas del paciente estimadas, como se muestra en el bloque 610. Si las variables de control subyacentes específicas del paciente estimadas se encuentran en el servidor remoto de la red médica o en una base de datos conectada a éste, como se muestra en el bloque 612, la información se transfiere al segundo dispositivo médico a través de una interfaz inalámbrica o por cable.
La transferencia de los datos de la terapia se confirma en el segundo dispositivo, como se muestra en el bloque 614. Por ejemplo, el segundo dispositivo puede enviar una señal de confirmación al servidor de la red médica indicando la recepción de los datos, o una enfermera puede confirmar de manera manual la recepción de los datos en el segundo dispositivo. El servidor de la red médica autorizará entonces que la terapia empiece a usar el segundo dispositivo, y la red médica transferirá las variables de control al segundo dispositivo, como se muestra en el bloque 616. Posteriormente, la terapia puede reanudarse y continuar desde la petición anterior usando el segundo dispositivo, como se muestra en el bloque 618.
Puede ser deseable transferir la administración de la terapia desde un dispositivo médico a otro en muchas situaciones. Por ejemplo, en un entorno hospitalario, un paciente puede ser transferido entre habitaciones, y cada habitación puede incluir un dispositivo médico diferente. Para continuar la retroalimentación relacionada con el tratamiento en la segunda habitación del hospital, los datos recopilados por el primer dispositivo médico se transfieren al segundo dispositivo médico en la segunda habitación del hospital para reanudar el tratamiento en el punto que se dejó. Por tanto, en un ejemplo en el que un paciente es transferido desde una unidad de cuidados intensivos (ICU) a un ala general del hospital/consultorio y se ha de continuar la terapia, puede ser deseable configurar una bomba en la segunda habitación antes de cambiar a usar la segunda bomba. La terapia sólo será administrada por una bomba en cada momento dado; sin embargo, los datos se pueden transferir a la segunda bomba para iniciar el procedimiento de configuración o para poner la segunda bomba en modo de espera, por ejemplo. De esta manera, el cuidado del paciente es independiente de la ubicación o el dispositivo específico, y se puede mantener la continuidad del cuidado.
Además, puede ser deseable transferir los datos de la terapia desde un dispositivo médico a otro en los casos en los que la terapia depende de los datos que continuamente se actualizan de una forma iterativa o recursiva. Por tanto, si la terapia comenzó usando en una etapa inicial un primer dispositivo médico y se llevó a cabo durante unos pocos días, la terapia habrá cambiado en el tiempo en base a la respuesta del paciente a la terapia. Si posteriormente el paciente es movido a otra habitación y es transferido a un segundo dispositivo médico, sería beneficioso transferir los datos así como continuar, reanudar, o recalcular la terapia usando los datos actualizados en lugar de volver a comenzar la terapia en la etapa inicial.
Finalmente, puede ser deseable transferir los datos de la terapia desde un dispositivo médico a otro en los casos en los que se proporciona una terapia nueva pero relacionada en el nuevo dispositivo que es dependiente de la terapia suministrada a través del primer dispositivo. Por ejemplo, el primer dispositivo se puede usar para suministrar medicamentos de manera IV para una terapia concreta mientras que el segundo dispositivo continúa la misma terapia pero con una ruta de suministro de los medicamentos diferente. Como un ejemplo específico, una bomba de suministro de insulina intravenosa se puede reemplazar con una bomba de insulina subcutánea justo antes de que el paciente abandone el hospital.
Dependiendo del tipo de terapia que se proporciona al paciente, los datos que se transfieren desde un primer dispositivo médico a un segundo dispositivo médico pueden incluir muchas variables comunes y variables específicas del paciente. Dichas variables comunes puede incluir la identificación de la terapia, tal como por ejemplo, la gestión de glucosa, la gestión de heparina, la gestión de los fluidos, la gestión del dolor, la resucitación de la sepsis, el control cardiovascular, etc. Otras variables comunes incluyen un identificador del paciente o un número de registro médico (MRN), la información de identificación de la bomba, una fecha y hora, y el estado de la terapia tal como el estado de infusión (dosis de infusión de insulina) y la respuesta del paciente (último nivel de glucosa). Aún otras variables pueden incluir un reloj de sistema o un temporizador de la terapia administrada y de las mediciones tomadas.
Las variables de control subyacentes específicas de paciente estimadas que se pueden transferir desde un primer dispositivo médico a un segundo dispositivo médico pueden incluir dicha información así como la sensibilidad Si a la insulina, una tasa estimada de suministro basal de insulina (BR) (una tasa del suministro de insulina continuo necesario para dichos propósitos de controlar la glucosa celular y el consumo de aminoácidos), las ganancias de retroalimentación estimadas, los parámetros estimados del modelo, la tasa Pi estimada de aclaramiento de insulina, la producción estimada de glucosa endógena, y los términos de saturación estimados. Se puede transferir más información dependiendo del tipo de terapia que se proporcione, y los ejemplos de información adicional pueden incluir cualquiera de las variables encontradas dentro de cualquiera de las Ecuaciones (1)-(9) descritas más adelante.
En los métodos ejemplares, se usan los algoritmos y los controladores adaptativos con las variables del paciente para descubrir la respuesta del paciente a la terapia para personalizar las decisiones de la terapia y permitir recomendaciones de dosificación. Un dispositivo médico se puede hacer funcionar usando un sistema de software que gestione y suministre la terapia del paciente de una manera que haga descubrir las variables de control específicas del paciente estimadas.
La variables de control representan un modelo de la respuesta del paciente a una medicación concreta y se calculan a lo largo del tiempo. Por ejemplo, se pueden calcular dos variables de manera recursiva en una serie de tiempos de mediciones de glucosa y tasas de infusión. Según los parámetros de control calculados convergen a valores óptimos, mejora la calidad de gestión de la glucosa.
En una terapia ejemplar, un conjunto de variables de control, pV, proporciona la información para gestionar la glucosa en el futuro en base de la historia observada de lecturas de insulina, las concentraciones de glucosa, y los eventos relacionados de la terapia. Por ejemplo, la insulina estimada, pV.SI, y el aclaramiento de glucosa endógena, pV.PG, permiten la estimación y control de la concentración de glucosa. De manera alternativa, la variables del paciente pueden incluir la tasa de filtración glomerular (GFR), los antecedentes o la tasa de infusión basal, y los factores de multiplicación adicionales para los términos de dosificación no lineales.
El proceso de aprendizaje de las variables del paciente puede ser lento y costoso ya que el proceso se realiza en base a la información de diagnóstico en combinación con la información de infusión de los medicamentos. Existen gastos directos relacionados con las mediciones diagnósticas así como costes indirectos asociados con el flujo de trabajo del personal clínico y el malestar del paciente. De manera adicional, el contenido de información de los datos recopilados puede estar limitado por el tiempo de respuesta de los medicamentos y la frecuencia de las mediciones. Por ejemplo, en el caso de la gestión de la glucosa, el perfil de glucosa del paciente a lo largo del tiempo se registra a menudo en base a dolorosas e inconvenientes extracciones de sangre. Esta serie de tiempos de valores de diagnóstico y la insulina infundida registrada se usa para calcular las variables del paciente.
Ya que el proceso de recopilación y procesamiento de las variables específicas del paciente puede ser costoso, tanto en términos de tiempo como de dolor para el paciente, sería útil transferir dicha información desde un primer dispositivo médico a un segundo dispositivo médico cuando se ha de continuar el tratamiento en el segundo dispositivo médico, por ejemplo.
Más adelante hay modelos ejemplares que usan variables específicas del paciente para tratar a los pacientes. Existen muchos otros modelos dependiendo de la terapia que se proporciona a un paciente, por ejemplo.
Ejemplo 1: Modelo de entradas exógenas con movimiento de autoregresión (ARX) que define los parámetros de control específicos del paciente usados con el control de modelo predictivo.
En el caso de la gestión de la glucosa, es beneficioso desarrollar un modelo empírico de la respuesta de glucosa del paciente a la terapia de insulina ya que el modelo se puede usar para determinar una dosis de infusión de insulina óptima. El modelo describe cómo se relaciona una medición de la glucosa actual con las concentraciones anteriores de glucosa y la insulina que se ha infundido, y el modelo se parametriza de manera que sea específico para el paciente que recibe el tratamiento. Más concretamente, en un ejemplo, se usa un modelo de entradas exógenas con autoregresión (ARX) para representar la respuesta concreta del paciente a la terapia de insulina a través de la ecuación:
donde St es la concentración estimada de glucosa en el momento t, £t es la concentración de glucosa medida en el momento t, ut es la insulina infundida en el momento t, p representa el número total de parámetros a¡ de autoregresión, q es el número total de términos de entrada exógenos, y ai y P¡ son respectivamente los parámetros de control subyacentes específicos del paciente asociados con la i-ésima medición de glucosa anterior y la dosis de insulina. En este ejemplo los parámetros del modelo, a¡ y p¡ se seleccionan para permitir el cálculo de la glucosa del paciente en el momento t, , en base al historial de las p mediciones de glucosa anteriores y las q dosis de insulina anteriores.
De manera alternativa, la ecuación anterior se puede escribir:
donde 0t es el vector de parámetros ai y pi en el momento t, T es el operador de transposición y $t es el vector de mediciones de glucosa y dosis de insulina anteriores. De manera específica,
y
En cada momento, t, 0t se actualiza usando un estimador de mínimos cuadrados recursivo:
donde A es un factor de olvido (constante positiva) que representa el horizonte de memoria del algoritmo actualizado, K es una matriz de ganancia, P es una matriz de convarianza, I en la matriz unidad, <j)t se define más arriba, r| es un tamaño de paso de la ecuación actualizada para 0t, y et es el error entre la St observada y la concentración de glucosa estimada.
Por lo tanto, en cada punto en el tiempo, los parámetros de control subyacentes específicos del paciente, 0t, se adaptan al paciente que recibe la terapia hasta que el modelo sea capaz de predecir de manera precisa la respuesta de glucosa futura del paciente para una terapia de insulina concreta. Por ejemplo, 0t, se actualiza en base al tamaño de paso y el error et observado hasta dicho punto en el tiempo done 0t en un momento presente sustancialmente es igual que la medición 0t anterior, o está dentro de una cantidad de error aceptable.
En el tiempo, el modelo según se expresa en las Ecuaciones (1)-(3) resulta más preciso ya que el modelo se personaliza para el paciente y proporciona una estimación óptima de la glucosa en sangre a lo largo del tiempo y en el futuro para el paciente.
El modelo tal como se muestra en las ecuaciones (1)-(3) se puede usar en un controlador de modelo predictivo o de otro modelo bien conocido basado en el esquema de control adaptativo para determinar una entrada óptima de insulina. Fundamentalmente, la calidad de la recomendación de insulina puede estar directamente relacionada con la calidad del modelo y la presión de los parámetros estimados de manera recursiva, 0t.
Dado un valor beneficioso de las variables de control específicas de paciente y un coste de cálculo de las variables, las aplicaciones de soporte de la decisión proporcionadas en la interfaz de la bomba de infusión pueden registrar un conjunto de variables de paciente en un archivo, una base de datos, o una ubicación de memoria. Cuando el dispositivo de infusión se reemplaza, el proceso de volver a calcular las variables de control específicas del paciente no se tiene que volver a iniciar si las variables de control específicas del paciente son transferidas a un segundo dispositivo.
Las características específicas del paciente relacionadas con las terapias se pueden representar a través de un conjunto de variables de control específicas del paciente que pueden ser usadas mediante el reemplazo de un dispositivo de infusión sin perder información que es beneficiosa para la terapia objetivo.
Un paciente conectado a un primer sistema de infusión que recibe una terapia es proporcionado con un registro de terapias del paciente que incluye al menos un identificador del paciente (ID), tal como un número de registro médico (MRN) y se le calculan las variables de control específicas del paciente, tales como la GFR, el aclaramiento de glucosa, las constantes de utilización de insulina, los términos de saturación, y las variables descritas anteriormente en las Ecuaciones (1)-(3), por ejemplo. Un registro de la terapia del paciente incluye variables adicionales, tales como, la frecuencia de medición, las decisiones de terapia recomendadas, las mediciones de glucosa y los tiempos de muestreo asociados, las tasas de infusión y los tiempos de ajuste asociados, el peso del paciente, el género del paciente, el tipo de diabetes del paciente, el nivel de creatinina del suero del paciente, el uso de esteroides del paciente, la edad del paciente, los eventos del paciente, y los tiempos relacionados con los elementos de datos, por ejemplo.
La Figura 7 ilustra un ejemplo de una memoria 702 para almacenar un registro 704 de datos del paciente y unos registros 706-714 variables específicos del paciente. La memoria 702 se puede incluir dentro de cualquier número de dispositivos, tales como un sistema de información hospitalaria, un servidor, una base de datos, o un dispositivo médico, por ejemplo.
Tal como se mencionó anteriormente, el registro 704 de datos del paciente incluye un ID del paciente, y otra información relacionada con las características del paciente. Los registros 706-714 variables específicos del paciente incluyen información específica de un paciente en base a la respuesta del paciente a lo largo del tiempo que se proporciona la terapia. La memoria 702 puede almacenar nuevas variables 706-714 específicas del paciente en intervalos de tiempo predeterminados (para almacenar la respuesta actualizada del paciente), y cada registro posterior puede incluir la información actualizada. Por ejemplo, el registro 714 puede incluir las variables específicas
del paciente actuales y los registros 712-706 pueden incluir las variables específicas del paciente progresivamente más antiguas.
Las variables de control específicas del paciente calculadas proporcionan una base para la personalización de la terapia al individuo, y por lo tanto se registran. Aunque el ejemplo anterior es específico para la gestión de la glucosa, se reconoce que las variables de control, tales como los parámetros del modelo, que se calculan en base a los datos del paciente representan información que es específica del paciente y se pueden usar para personalizar casi cualquier terapia en la cabecera.
De manera continua y periódica, los registros 706-714 de variables específicas del paciente se pueden transferir a un sistema remoto y ser registrados en una base de datos. El registro 714 de variable específica del paciente más actual se puede transferir en cada periodo de transferencia, o los N registros 706-714 de variables específicas del paciente se pueden transferir en cada periodo de transferencia. En el ejemplo ilustrado, N=5, pero N se puede adaptar para cumplir las necesidades del algoritmo del modelo del paciente concreto. La transferencia puede producirse en incrementos de tiempo que se aproximan a la comunicación continua o de manera periódica en una base de minuto a minuto. Además, la transferencia puede ser asimétrica y ocurrir en conjunción con las actualizaciones de la terapia.
Por ejemplo, cuando se confirma una terapia en el dispositivo médico, el dispositivo médico puede enviar la información demográfica del paciente y los registros de las variables específicas del paciente al servidor remoto. Cuando la terapia está ajustada, se envía la misma información o información actualizada (por ejemplo, nuevas mediciones de glucosa) al servidor remoto. Los datos se pueden enviar como un mensaje codificado XML que usa una interfaz de comunicación inalámbrica o por cable hasta un sistema remoto, por ejemplo.
Si los registros 706-714 de variables específicas del paciente se almacenan en un dispositivo médico que administra la terapia a un paciente, el dispositivo médico puede transferir los registros 706-714 a un servidor o a otro dispositivo médico, por ejemplo. El dispositivo médico puede almacenar un nuevo registro de variables específicas del paciente a intervalos de tiempo predeterminados, y puede mantener el almacenamiento de todos los registros de variables específicos del paciente recopilados. Sin embargo, al realizar una transferencia de los registros de variables específicos del paciente a un servidor, el dispositivo médico sólo puede transferir los cinco registros 706-714 de variables específicos de paciente más recientes al servidor, por ejemplo, para enviar las cinco lecturas de glucosa anteriores, las tasas basales, etc, al servidor o a otro dispositivo médico por lo que la terapia puede ser reanudada/continuada en el punto en que la terapia se interrumpió usando el primer dispositivo médico.
Los registros 706-714 se pueden registrar como una unidad de datos única y transferirse de manera remota en intervalos específicos o dividirse en componentes normalizados que se transfieren cuando se producen actualizaciones o cambios. Sin embargo, la transferencia remota de los registros de las variables específicas del paciente permite una representación continua de las variables de control específicas del paciente calculadas para ser guardadas para su uso por otros sistemas y otros dispositivos.
Los registros 706-714 se pueden transferir mediante el dispositivo médico hasta un servidor, o desde el servidor a un dispositivo médico usando cualquier número de protocolos de transferencia de datos. Por ejemplo, los registros 706 714 se pueden transferir usando el protocolo de datagramas de usuario (UDP), el protocolo de control de la transmisión (TCP), el protocolo de transferencia de archivos (FTP), u otro protocolo propietario según se desee. Además, los registros 706-714 se pueden transferir usando cualquier número de técnicas por cable o inalámbricas, y por tanto, el dispositivo médico o el servidor pueden incluir una interfaz por cable o inalámbrica (por ejemplo, un receptor/transmisor) para realizar la transferencia de los datos.
Antes de o después de desconectar un primer dispositivo de infusión del paciente, un usuario puede iniciar un comando de detención seguido por una transferencia del registro de variables específicas del paciente al sistema remoto, por ejemplo. Sin embargo, el primer dispositivo de infusión puede perder energía o fallar por razones desconocidas. Por consiguiente, se pueden realizar frecuentes actualizaciones de los cambios de las variables específicas del paciente para asegurar un respaldo apropiado y un registro de la información de la terapia del paciente.
Después de la transferencia de los registros 706-714 de variables específicas del paciente, un primer dispositivo de infusión se puede desconectar del paciente y ser reemplazado por un segundo dispositivo. El personal clínico proporciona el identificador del paciente al segundo dispositivo. Esto se puede lograr a través de la entrada manual de un número de registro médico, un escáner de códigos de barras, o un identificador de frecuencias de radio (RFID). De manera alternativa, se puede usar una métrica de identificación biométrica para asociar el segundo dispositivo con un identificador concreto del paciente. El segundo dispositivo puede acceder al sistema remoto e identificar las terapias anteriores asociadas con el paciente. El segundo dispositivo entonces presenta una selección de terapias disponibles asociadas con los registros de las variables del paciente registradas. De manera alternativa, después de identificar el paciente, el usuario selecciona la terapia deseada.
El segundo dispositivo consulta al sistema remoto, identifica la variable o las variables de control del paciente asociadas, y pregunta al usuario para confirmar la inicialización usando las variables de control de la terapia
anteriormente estimadas. El segundo dispositivo puede proporcionar también información respecto al momento en que la variable o las variables de control del paciente fueron actualizadas por última vez para asegurar que la información de la terapia es suficientemente reciente, por ejemplo.
Tras la confirmación, los registros 706-714 de variables específicas del paciente se transfieren desde el sistema remoto al segundo dispositivo y se usan para comenzar la terapia en el punto en que la terapia se interrumpió anteriormente en el primer dispositivo.
Si la variable o las variables de control de la terapia del paciente no se encuentran o no están disponibles, el sistema proporciona unos medios para la entrada manual de las variables específicas del paciente que se pueden obtener de la interfaz del sistema remoto.
Reconociendo que la transferencia desde un sistema de infusión a otro implica la interrupción de la terapia, se puede proporcionar también una característica adicional de seguridad que permita la reducción en el medicamento recomendado o infundido de manera automática. El proceso implica determinar el momento en que la terapia se interrumpió, un límite de tiempo, y una regla de reducción que puede considerar o no el tiempo total de interrupción. Por ejemplo, en el caso de la gestión de la glucosa, una interrupción de la terapia mayor de 30 minutos puede producir una reducción automática de la insulina infundida del 80%.
Ejemplo 2: Ecuación de Dosificación con los Parámetros de Control Específicos del Paciente.
Una calculadora de dosis de glucosa puede tener la forma de:
donde t es el tiempo, lt es una dosis calculada de insulina en el momento t, A-i es la dosis suministrada de insulina en el periodo de tiempo anterior, £> es una medición de glucosa en el momento t, es un vector de los parámetros de control subyacentes específicos del paciente calculados, G es un conjunto de concentraciones de glucosa objetivo, y f es una función que hace corresponder o traduce los parámetros en dosis de insulina recomendadas. El vector de parámetros puede estar referido a las variables o los parámetros de control subyacentes específicos del paciente. Los parámetros de control permiten la determinación de la dosis de insulina específica del paciente ya que los parámetros de control se calculan en base a la respuesta de glucosa observada a la dosis de insulina.
Más específicamente, la función f de la Ecuación (4) se puede definir y el cálculo de It se puede realizar en base a la siguiente ecuación no lineal:
donde It es mayor que cero, y M1, M2 son constantes de multiplicación estimadas en el tiempo en base al error entre una respuesta de glucosa observada y la deseada a la dosis de insulina. En esencia, Mi y M2 son parámetros o elementos de control subyacentes específicos del paciente de &i. El método de cálculo de las variables de control subyacentes específicas del paciente se puede realizar usando un estimador de mínimos cuadrados recursivo, un estimador de Bayes, o reglas de control basadas en un nivel y un cambio de la concentración de glucosa del paciente en el tiempo, por ejemplo.
Como un ejemplo, el método de cálculo de las variables de control subyacentes específicas del paciente se puede realizar usando métodos establecidos de estimación de parámetros, tales como el filtrado Kalman extendido, la estimación de mínimos cuadrados recursiva, la estimación Bayesiana, o las reglas de control proporcional que se usan para ajustar M1 y M2 en base al error calculado, tal como una diferencia entre las concentraciones de glucosa observada y esperada. Por ejemplo, véase Goodwin y Sin, Filtrado Adaptativo, Predicción y Control, 1984.
Como un ejemplo ilustrativo específico, bajo la suposición de que la derivada parcial de una concentración de glucosa observada con respecto a una tasa de insulina calculada es negativa (esto es, los niveles de glucosa disminuyen al aumentar la insulina), se puede usar un pseudo algoritmo de disminución del gradiente para determinar M1 y M2 en base a la diferencia entre las lecturas de glucosa observada y deseada. Por ejemplo, dado el error:
donde S t es una concentración de glucosa objetivo o deseada en el momento t, los parámetros Mi y M2 se actualizan según lo siguiente:
M j = M v - a - e ,
Ecuación (7)
M t = M 2 - p - e ,
donde a y p son constantes positivas que se pueden sintonizar. En cada medición, las variables de control subyacentes se actualizan según la Ecuación (5) y, a tiempo, resultan personalizadas a la respuesta de insulinaglucosa del paciente.
La Figura 8 ilustra un diagrama de bloques que incluye un dispositivo 802 médico ejemplar para calcular las variables de control subyacentes específicas del paciente. El dispositivo 802 médico incluye un controlador 804 y un estimador 806 de parámetros. El dispositivo 802 médico se conecta a un paciente 808. El dispositivo 802 médico incluye además una interfaz 810, que puede ser una interfaz por cable o inalámbrica para comunicarse con otros dispositivos de red, por ejemplo.
En funcionamiento, se determina la respuesta objetivo a la terapia y el correspondiente conjunto de concentraciones de glucosa objetivo, G , es seleccionado por el médico o el director médico. Por ejemplo, la terapia objetivo se puede seleccionar como aproximadamente 120 mg/dL o en el intervalo de aproximadamente 100 hasta aproximadamente 150 mg/dL. El conjunto de concentraciones de glucosa objetivo, G, es proporcionado al controlador 804 y al estimador 806 de parámetros. Además, el controlador 804 y el estimador 806 de parámetros reciben la medición de glucosa en el momento t, ®f, tal y como se registró del paciente 808. El estimador 806 de parámetros emite un vector de parámetros de control subyacentes específicos del paciente calculados, 9 al controlador 804. A su vez, el controlador 804 emite la dosis de insulina calculada en el momento t, A I -i, calculada según cualquiera de las Ecuaciones (4)-(7) anteriores, al estimador 806 de parámetros y administra la dosis de insulina calculada al paciente 808.
El controlador 804 y el estimador 806 de parámetros pueden representar un módulo, un segmento, o una parte del código de programa, que incluye una o más instrucciones ejecutables por un procesador para implementar funciones lógicas específicas o pasos en el proceso. El código de programa se puede almacenar en cualquier tipo de medio legible por ordenador, por ejemplo, tal como un dispositivo de almacenamiento que incluye una unidad de disco o de disco duro. Además, el controlador 804 y el estimador 806 de parámetros pueden representar circuitería que se cablea para realizar las funciones lógicas específicas en el proceso, o un procesador para ejecutar las funciones lógicas específicas. Se incluyen implementaciones alternativas dentro del alcance de las realizaciones ejemplares de la presente solicitud en las que las funciones se pueden ejecutar fuera del orden que se muestra o discute, incluyendo sustancialmente un orden concurrente o al revés, dependiendo de la funcionalidad involucrada, como sería entendido por aquellos razonablemente expertos en la técnica.
El dispositivo 802 médico puede almacenar cualquier de las variables de control subyacentes específicas del paciente h-y , ®f, 9, y G en memoria (no mostrada). El dispositivo 802 médico puede transferir entonces cualquiera de estos datos a un servidor u otro dispositivo médico usando la interfaz 810, por ejemplo.
Ejemplo 3: Modelo Fármaco-Cinético Fármaco-Dinámico (PK-PD) con parámetros de control específicos del paciente usados con un regulador auto sintonizable para lograr un intervalo de tiempo de tromboplastina parcial activado (aPTT) objetivo.
La heparina se usa para el tratamiento y la prevención de enfermedades tromboembólicas, tales como la trombosis venosa profunda, el embolismo pulmonar, el ictus y la cardiopatía isquémica. Además, la Heparina es un anticoagulante frecuentemente asociado con los errores médicos. Un objetivo del tratamiento es proporcionar interferencia terapéutica con el mecanismo de coagulación del paciente para evitar o tratar la trombosis o el embolismo. Aunque la terapia es común dentro del entorno del cuidado agudo, la dosificación de los anticoagulantes, y en concreto de la heparina no fraccionada, es complicado debido a las diferencias entre paciente y paciente en cuanto a la eficacia de las medicinas, la variación en el tiempo, el impacto de la interferencia, y el aumento de los riesgos asociados con las condiciones de tratamiento sub y supra terapéuticas.
Como resultado, el efecto de la anticoagulación de la heparina no fraccionada se puede monitorizar a través del tiempo de tromboplastina parcial activado (aPTT), que se determina mediante el análisis de laboratorio que sigue a una extracción de sangre. Se puede ajustar entonces la dosis de heparina no fraccionada para lograr un tiempo de coagulación objetivo en base a los protocolos que aumente o disminuya la tasa de infusión en base a la diferencia entre el aPTT observado y el objetivo. Sin embargo, los nomogramas comúnmente usados proporcionan unos resultados de la terapia relativamente pobres con estudios reportando resultados tan bajos como sólo el 40% de los pacientes con el aPTT en un intervalo terapéutico, por ejemplo.
Un método alternativo para determinar la dosis de heparina no fraccionada puede ser calcular la respuesta específica del paciente a las medicinas en base a los modelos PK-PD conocidos que se han ajustado para
representar al paciente. Por ejemplo, un sistema que incluye un algoritmo de control para modelar la respuesta del paciente a la heparina no fraccionada en base de las lecturas del aPTT automatizadas y haciendo ajustes se presenta en “Sistema de Suministro de Heparina Automatizado para Controlar el Tiempo de Tromboplastina Parcial Activado: Evaluación en Voluntarios normales”, por Cannon, C., J. Dingemanse, C. Kleinbloesem, T. Jannett, K. Curry y C. Valcke, Circulación 1999; 99; 751-756.
Dicho sistema puede mejorar la seguridad del paciente y permite al personal clínico lograr niveles de aPTT terapéuticos más rápidos que con los nomogramas tradicionales basados en el peso empleando un controlador adaptativo para personalizar rápidamente las decisiones de terapia en base a cómo responde el paciente a la administración de la heparina. Además los elementos del ciclo de gestión de la heparina se pueden automatizar para reducir la carga de trabajo clínico así como los potenciales errores de medicación.
Usar los métodos y sistemas descritos en la presente memoria permite la transferencia de lecturas del aPTT desde un laboratorio centralizado a un sistema de infusión equipado con un controlador avanzado para recomendar cambios en la dosificación de la heparina no fraccionada. Específicamente, después de recibir una notificación de un nuevo valor del laboratorio, el algoritmo del sistema de infusión calcula una tasa de infusión de heparina no fraccionada y proporciona una alerta si fuera necesaria la intervención del personal clínico.
Si el valor del aPTT está dentro de un intervalo terapéutico, no se envía una alerta ya que no es necesaria la acción inmediata de una enfermera. Si el valor del laboratorio está fuera del intervalo (esto es, los intervalos de los valores del laboratorio se pueden almacenar también en la biblioteca de medicamentos), se emite una alarma. Por tanto, los sistemas descritos en la presente memoria proporcionan un servidor centralizado para gestionar los datos del paciente o los parámetros de control subyacentes específicos del paciente estimados, y proporcionar una transferencia automática de la terapia personalizada desde un dispositivo a otro, por ejemplo.
Además de proporcionar una tasa recomendada para la infusión de la heparina, el dispositivo de infusión puede presentar el tiempo hasta la siguiente extracción de sangre y análisis del aPTT. El personal clínico es recordado en momentos designados a través de una interfaz de usuario y/o un sistema de notificación remoto para comprobar el nivel del aPTT en la sangre del paciente para que una tasa de infusión de heparina actualizada pueda ser determinada por el algoritmo. Se generan una serie de alarmas crecientes si no se recibe una medición de heparina en el tiempo designado.
Las variables de control subyacentes específicas del paciente estimadas se calculan a través de un controlador de retroalimentación que se incrusta en el sistema de infusión. Después del cálculo de la dosis inicial, el algoritmo funciona como un controlador de retroalimentación proporcionando bolo y/o continuas actualizaciones de infusión de heparina y el tiempo hasta la siguiente lectura del aPTT en base al historial de diferencias entre las lecturas del aPTT y el intervalo objetivo. Cuando los tiempos de coagulación son menores que un intervalo objetivo, se aumenta la tasa de infusión de heparina. Al contrario, los tiempos de coagulación mayores que los tiempos deseados resultan en una disminución en la tasa de infusión de heparina recomendada. Una vez que la lectura del aPTT está en el intervalo terapéutico, la tasa de infusión de heparina no se cambia y el tiempo entre mediciones del aPTT se aumenta hasta las 24 horas.
Se proporciona la dosificación inicial en base a la edad, peso, género, historial de fumador, y nivel de creatinina en suero del paciente, por ejemplo. Un algoritmo de dosificación inicial multi variable, basado en un análisis PK-PD de población a priori, se optimiza para lograr una respuesta cercana a la terapéutica en 6 horas según la modalidad de tratamiento concreto. Las lecturas posteriores se usan para actualizar las variables de control subyacentes específicas del paciente calculadas asociadas con un modelo PK-PD de dinámicas de heparina usando ya sea un algoritmo de optimización Bayesiano, un filtro Kalman extendido, u otra técnica de estimación de parámetros.
El modelo PK-PD se relaciona con la respuesta aPTT a la heparina y los parámetros de control subyacentes específicos del paciente, θ¡, a través de las siguientes ecuaciones:
donde R(t) es la respuesta aPTT modelada a la administración de la heparina, aPTTo es la medición del aPTT de referencia, Sn es la sensibilidad a la heparina, a1 y a2 son constantes asociadas con el mecanismo saturable de eliminación de la heparina, A es la constante de tasa de eliminación, u(t) es la tasa de infusión de heparina, y Vd es el volumen de distribución.
Con la adición de cada nueva medición del aPTT del sistema de información del laboratorio, se actualiza 9 mediante técnicas de estimación Bayesiana u otras de manera tal que R(t) coincida más estrechamente con las observaciones.
Finalmente, 9 se utiliza para ajustar la tasa de infusión de heparina a través del modelo de control predictivo en el que la predicción del aPTT, R(t t ) donde t es el tiempo actual y t >0, se usa para determinar la tasa de infusión óptima recomendada.
En cada punto de actualización, los parámetros de control, 9 , junto con el historial de observaciones del aPTT, las infusiones de heparina, la información de identificación del paciente, y los índices de tiempo se pueden transferir desde el dispositivo de infusión al sistema remoto y ser registrados en una base de datos SQL, por ejemplo. Dicha información se puede transferir también a otros puntos a tiempo también. Esta información constituye un registro de información para reanudar la terapia en otro dispositivo de infusión debido al fallo del dispositivo actual o la necesidad de reemplazo, por ejemplo. Además, la información se puede transferir de manera directa a otro dispositivo médico para iniciar o reanudar la terapia usando el otro dispositivo médico.
Ejemplo 4: Algoritmo de Suministro de Glucosa en Sangre Controlado por Ordenador.
La insulina intravenosa es un método de control de la diabetes, y los métodos para administrar la insulina pueden ser complejos y limitados a las unidades de cuidados intensivos. Se puede usar un algoritmo controlado por ordenador para el asesoramiento del suministro de la insulina intravenosa que es flexible en la temporización de la glucosa en sangre y aconseja la dosificación de la insulina de manera gradual para mantener el control glucémico. El protocolo de insulina intravenosa incluye la fórmula:
Dosis de insulina/h = (glucosa en sangre - 60) x (multiplicador) Ecuación (9)
Los estudios han demostrado que un multiplicador que empieza en aproximadamente 0,02 proporciona los resultados deseados. El multiplicador se puede modificar de manera progresiva hasta que la fórmula de dosificación de la insulina controle la glucosa dentro de un intervalo objetivo.
Para iniciar el método, se toma una medición del valor de glucosa en sangre y se introduce en un dispositivo médico, y se calcula una tasa de infusión de insulina inicial según la Ecuación (9), con el multiplicador fijado a aproximadamente 0,02. En base a la tasa de cambio del nivel de glucosa, el dispositivo médico puede notificar a la enfermera cuando es necesario el siguiente valor de glucosa en sangre (por ejemplo, entre aproximadamente 20 minutos y aproximadamente 120 minutos). Por ejemplo, para un nivel de glucosa en sangre de 295 mg/dl, un multiplicador de 0,02 indica una tasa inicial de insulina de 4,7 unidades/hr. Si el segundo nivel de glucosa en sangre disminuye hasta 256 mg/dl (por ejemplo, menos que el 15%), el multiplicados se puede aumentar un 25% para aumentar la dosis de insulina a 4,9 unidades/hr. Si los posteriores niveles de glucosa en sangre medidos en serie disminuyen de manera satisfactoria (por ejemplo, 205 mg/dl seguido por 3,6 unidades/hr, 168 mg/dl seguido por 2,7 unidades/hr, y 115 mg/dl seguido por 1,5 unidades/hr) hasta que el nivel de glucosa en sangre sea menor que un valor objetivo inferior (por ejemplo, 69 mg/dl seguido por 0,2 unidades/hr), entonces, en ese momento, el multiplicador se desplaza hacia abajo y los siguientes dos niveles de glucosa y dosis de insulina (por ejemplo 98 mg/dl seguido por 0,8 unidades/hr y 110 mg/dl seguido por 1 unidad/hr) se pueden centrar en un intervalo objetivo. Un objetivo superior para el nivel de glucosa en sangre puede estar entre aproximadamente 120 hasta aproximadamente 140 mg/dl, y un objetivo inferior puede estar entre aproximadamente 80 hasta aproximadamente 100 mg/dl. En la ecuación (9), el multiplicador se puede iniciar en aproximadamente 0,01 hasta aproximadamente 0,02, y la duración máxima del tiempo entre mediciones de glucosa es de aproximadamente 120 minutos. La frecuencia de la monitorización de la glucosa en sangre se fija a un intervalo predicho para evitar que el nivel de glucosa en sangre caiga por debajo de aproximadamente 60 mg/dl, por ejemplo, Cuando los valores de glucosa en sangre son estables, el intervalo entre monitorizaciones del nivel de glucosa en sangre aumentará al intervalo máximo prefijado.
Como se muestra en el ejemplo anterior, se pueden necesitar múltiples mediciones de la glucosa en sangre y una considerable cantidad de tiempo antes se encontrar el multiplicador que logre el nivel de glucosa en sangre objetivo. El multiplicador por tanto es una variable de control subyacente específica del paciente que se puede determinar a lo largo del tiempo, y se puede transferir entre dispositivo médicos para mantener el servicio continuo a un paciente sin tener que volver a empezar la terapia de insulina desde los valores iniciales, por ejemplo. Además, los multiplicadores anteriores, las mediciones de glucosa en sangre, y las tasas de dosis de insulina forman un historial de la terapia proporcionada al paciente y puede presentar también información valiosa al dispositivo médico que administra la terapia al paciente. Por tanto, dicha información histórica se puede transferir también entre dispositivos médicos para mantener un servicio continuo al paciente sin tener que volver a empezar la terapia de insulina desde los valores iniciales, por ejemplo.
Los métodos, dispositivos, y sistemas descritos en la presente memoria proporcionan una manera de utilizar las variables de control específicas del paciente asociadas con una terapia para propósitos de diagnóstico o para
alternar y relacionar terapias. Los métodos proporcionan una manera semi automática de tomar decisiones terapéuticas en las que se mitiga el nivel de riesgo.
Cualquiera de los servidores o dispositivos médicos descritos en la presente memoria pueden incluir o tener funciones realizadas por un módulo, un segmento, o una parte del código de programa, que incluye una o más instrucciones ejecutables por un procesador para implementar funciones lógicas específicas o pasos en el proceso. El código de programa se puede almacenar en cualquier tipo de medio legible por un ordenador, por ejemplo, tal como un dispositivo de almacenamiento que incluye una unidad de disco o de disco duro. Además, los servidores o los dispositivos médicos descritos en la presente memoria pueden incluir circuitería que se cablea para realizar las funciones lógicas específicas en el proceso, o un procesador para ejecutar las funciones lógicas específicas. Implementaciones alternativas se incluyen dentro del alcance de las realizaciones ejemplares de la presente solicitud en las que las funciones se pueden ejecutar fuera del orden que se muestra o discute, incluyendo un orden sustancialmente concurrente o al contrario, dependiendo de la funcionalidad involucrada, como sería entendido por aquellos de experiencia razonable en la técnica.
Aunque se han descrito diversos aspectos y realizaciones en la presente memoria, otros aspectos y realizaciones serán evidentes a aquellos expertos en la técnica. Los diversos aspectos y realizaciones descritos en la presente memoria son para propósitos de ilustración y no están destinados a ser limitantes, con el alcance real que es indicado por las siguientes reivindicaciones.
Claims (14)
1. Un método para transferir la administración de una terapia desde un primer sistema médico a un segundo sistema médico, comprendiendo el método:
un primer sistema de suministro de medicamentos electrónico que se conecta a un paciente que recibe un identificador de paciente que corresponde con el paciente;
el primer sistema de suministro de medicamentos electrónico que estima las variables de control subyacentes específicas del paciente en base a (i) la terapia proporcionada a un paciente y (ii) la respuesta específica del paciente observada a la terapia, en donde las variables de control subyacentes específicas del paciente permiten la determinación de una dosis en base a un modelo;
en base a (i) las variables de control subyacentes específicas del paciente, (ii) la respuesta específica del paciente a la terapia observada, y (iii) el objetivo de la terapia, el primer sistema de suministro de medicamentos que proporciona una terapia actualizada para el paciente para adaptar la terapia al paciente;
el primer sistema de suministro de medicamentos electrónico transfiere a un sistema remoto un registro de la terapia actualizada proporcionada al paciente y las variables de control subyacentes específicas del paciente estimadas; tras conectar un segundo sistema de suministro de medicamentos al paciente, el segundo sistema de suministro de medicamentos electrónico recibe el identificador del paciente;
el segundo sistema de suministro de medicamentos electrónico se comunica con el sistema remoto para acceder al registro de la terapia actualizada y las variables de control subyacentes específicas del paciente estimadas asociadas con el identificador del paciente;
determinar el momento en que se interrumpió la terapia por el primer sistema de suministro de medicamentos electrónico y determinar en base al tiempo la cantidad en la que hay que reducir la terapia que se proporcionada; y ajustar el registro de la terapia actualizada para tener en cuenta la cantidad en que ajustar la terapia que será proporcionada por el segundo sistema de suministro de medicamentos electrónico.
2. El método de la reivindicación 1, en donde las variables de control subyacentes específicas del paciente se seleccionan de un grupo consistente de la sensibilidad a la insulina, la tasa de filtración glomerular (GFR), la tasa de infusión basal, los factores de multiplicación, el aclaramiento de la insulina, las constantes de utilización de la insulina, los términos de saturación, la sensibilidad a los medicamentos, la función renal, y las tasas de aclaramiento de los medicamentos.
3. El método de la reivindicación 1, que comprende además el primer sistema de suministro de medicamentos electrónico que transfiere al sistema remoto el registro de la terapia actualizada proporcionada al paciente y las variables de control subyacentes específicas del paciente estimadas de una manera periódica.
4. El método de la reivindicación 1, que comprende además el primer sistema de suministro de medicamentos que transfiere al sistema remoto el registro de la terapia actualizada proporcionada al paciente y las variables de control subyacentes específicas del paciente estimadas al menos en cada caso de un cambio en una de las variables de control subyacentes específicas del paciente estimadas.
5. El método de la reivindicación 1, que comprende además recibir un comando de detención en el primer sistema de suministro de medicamentos que indique interrumpir la terapia del paciente y transferir como respuesta las variables actuales de control subyacentes específicas del paciente estimadas y el registro de la terapia actualizada al sistema remoto antes de que el primer sistema de suministro de medicamentos electrónico se desconecte del paciente.
6. El método de la reivindicación 1, comprendiendo además el segundo sistema de suministro de medicamentos electrónico recibir el registro de la terapia y las variables de control subyacentes específicas del paciente estimadas asociadas con el identificador del paciente desde el sistema remoto y continuar la terapia del paciente en el punto en que la terapia fue interrumpida anteriormente por el primer sistema de suministro de medicamentos electrónico.
7. El método de la reivindicación 1, que comprende además que el primer sistema de suministro de medicamentos electrónico almacene (i) el registro de la terapia actualizada proporcionada al paciente y (ii) las variables de control subyacentes específicas del paciente estimadas de una manera periódica.
8. El método de la reivindicación 1, en donde la terapia proporcionada al paciente está basada en una función en la forma de, donde t es el tiempo lt es la dosis de insulina calculada en el momento t, es una dosis de insulina suministrada en el periodo anterior de tiempo, £> es la medición de glucosa en el momento t, es un vector de las variables de control subyacentes específicas del paciente estimadas, y es un conjunto de concentraciones de glucosa objetivo.
9. El método de la reivindicación 1, en donde la terapia proporcionada al paciente incluye la dosificación de anticoagulantes que incluyen la heparina no fraccionada, y en donde la respuesta específica del paciente observada a la terapia incluye el efecto de anticoagulación de la heparina no fraccionada monitorizado a través del tiempo de tromboplastina parcial observado (aPTT).
10. El método de la reivindicación 9, en donde la terapia actualizada incluye los ajustes a la dosis de heparina no fraccionada para lograr un tiempo de coagulación objetivo en base al aPTT observado y objetivo.
11. El método de la reivindicación 9, en donde las variables de control subyacentes específicas del paciente se seleccionan de un grupo consistente de las actualizaciones de infusión de heparina, el tiempo hasta la siguiente lectura del aPTT, la sensibilidad a la heparina, o el nivel del mecanismo saturable de eliminación de la heparina.
12. Un sistema para controlar y suministrar la terapia al paciente a través de los sistemas de suministro de medicamentos, comprendiendo el sistema:
un primer sistema de suministro de medicamentos conectado a un paciente y que recibe el identificador del paciente que corresponde al paciente, y en base a (i) las variables de control subyacentes específicas del paciente estimadas, (ii) la respuesta específica del paciente observada a la terapia, y (iii) el objetivo de la terapia, el primer sistema de suministro de medicamentos proporciona una terapia actualizada al paciente para adaptar la terapia al paciente, en donde las variables de control subyacentes específicas del paciente permiten la determinación de una dosis en base a un modelo, y el primer sistema de suministro de medicamentos transfiere a un sistema remoto un registro de la terapia actualizada proporcionada al paciente y las variables de control subyacentes específicas del paciente estimadas; y
el segundo sistema de suministro de medicamentos que recibe el identificador del paciente y se comunica con el sistema remoto para acceder al registro de la terapia actualizada y a las variables de control subyacentes específicas del paciente estimadas asociadas con el identificador del paciente, en donde el segundo sistema de suministro de medicamentos se configura además para determinar el momento en que la terapia fue interrumpida por el primer sistema de suministro de medicamentos y en base a ese momento y a la cantidad en la que reducir la terapia que se proporcionó, ajustar el registro de la terapia actualizada para tener en cuenta la cantidad en la que ajustar la terapia que será proporcionada por el segundo sistema de suministro de medicamentos electrónico.
13. El sistema de la reivindicación 12, en donde el segundo sistema de suministro de medicamentos electrónico recibe el registro de la terapia y las variables de control subyacentes específicas del paciente actualizadas asociadas con el identificador del paciente desde el sistema remoto y continua la terapia del paciente en el punto que fue interrumpida anteriormente por el primer sistema de suministro de medicamentos.
14. Un medio legible por un ordenador que tiene almacenado en éste las instrucciones ejecutables por un dispositivo de computación para provocar que el dispositivo de computación realice las funciones de:
recibir desde un primer sistema de suministro de medicamentos electrónico un registro de las variables de control subyacentes específicas del paciente estimadas para un paciente, estando las variables de control subyacentes específicas del paciente basadas en (i) una terapia proporcionada para un paciente y (ii) la respuesta específica del paciente observada a la terapia, en donde las variables de control subyacentes específicas del paciente permiten la determinación de una dosis en base a un modelo;
recibir desde el primer sistema de suministro de medicamentos electrónico una terapia actualizada proporcionada al paciente para adaptar la terapia al paciente, estando la terapia actualizada en base a (i) las variables de control subyacentes específicas del paciente estimadas, (ii) la respuesta específica del paciente observada a la terapia, y (iii) el objetivo de la terapia;
transferir a un segundo sistema de suministro de medicamentos electrónico un registro de la terapia actualizada proporcionada al paciente y las variables de control subyacentes específicas del paciente estimadas asociadas con el paciente
determinar el momento en que la terapia fue interrumpida por el primer sistema de suministro de medicamentos electrónico y en base a ese momento calcular una cantidad en la que reducir la terapia que se proporcionó; y ajustar el registro de la terapia actualizada para tener en cuenta la cantidad en la que ajustar la terapia que será proporcionada por el segundo sistema de suministro de medicamentos electrónico.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US28757909P | 2009-12-17 | 2009-12-17 | |
| US12/970,777 US8771251B2 (en) | 2009-12-17 | 2010-12-16 | Systems and methods for managing and delivering patient therapy through electronic drug delivery systems |
| PCT/US2010/061127 WO2011075687A1 (en) | 2009-12-17 | 2010-12-17 | Systems for managing drug delivery devices |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2716235T3 true ES2716235T3 (es) | 2019-06-11 |
Family
ID=44152116
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES10838319T Active ES2716235T3 (es) | 2009-12-17 | 2010-12-17 | Sistemas para gestionar dispositivos de suministro de medicamentos |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US8771251B2 (es) |
| EP (1) | EP2516671B1 (es) |
| JP (1) | JP5699161B2 (es) |
| AU (1) | AU2010330746B2 (es) |
| CA (1) | CA2784143C (es) |
| ES (1) | ES2716235T3 (es) |
| WO (1) | WO2011075687A1 (es) |
Families Citing this family (69)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8065161B2 (en) | 2003-11-13 | 2011-11-22 | Hospira, Inc. | System for maintaining drug information and communicating with medication delivery devices |
| US9123077B2 (en) | 2003-10-07 | 2015-09-01 | Hospira, Inc. | Medication management system |
| US20080091466A1 (en) | 2006-10-16 | 2008-04-17 | Hospira, Inc. | System and method for comparing and utilizing activity information and configuration information from multiple device management systems |
| US8517990B2 (en) | 2007-12-18 | 2013-08-27 | Hospira, Inc. | User interface improvements for medical devices |
| US10089443B2 (en) | 2012-05-15 | 2018-10-02 | Baxter International Inc. | Home medical device systems and methods for therapy prescription and tracking, servicing and inventory |
| US8271106B2 (en) | 2009-04-17 | 2012-09-18 | Hospira, Inc. | System and method for configuring a rule set for medical event management and responses |
| US9089292B2 (en) | 2010-03-26 | 2015-07-28 | Medtronic Minimed, Inc. | Calibration of glucose monitoring sensor and/or insulin delivery system |
| US9913599B2 (en) | 2011-02-11 | 2018-03-13 | Abbott Diabetes Care Inc. | Software applications residing on handheld analyte determining devices |
| EP2745204A4 (en) | 2011-08-19 | 2015-01-07 | Hospira Inc | SYSTEMS AND METHOD FOR A GRAPHIC INTERFACE WITH A GRAPHICAL PRESENTATION OF MEDICAL DATA |
| ES2959510T3 (es) | 2011-10-21 | 2024-02-26 | Icu Medical Inc | Sistema de actualización de dispositivos médicos |
| WO2013090709A1 (en) | 2011-12-16 | 2013-06-20 | Hospira, Inc. | System for monitoring and delivering medication to a patient and method of using the same to minimize the risks associated with automated therapy |
| TW201333870A (zh) * | 2011-12-21 | 2013-08-16 | 艾登工具股份有限公司 | 決定病人胰島素療法的系統及方法 |
| AU2013239778B2 (en) | 2012-03-30 | 2017-09-28 | Icu Medical, Inc. | Air detection system and method for detecting air in a pump of an infusion system |
| CA2880156C (en) | 2012-07-31 | 2020-10-13 | Hospira, Inc. | Patient care system for critical medications |
| US20140213998A1 (en) * | 2013-01-30 | 2014-07-31 | Glucome Ltd. | System and method for administering insulin |
| US9641432B2 (en) | 2013-03-06 | 2017-05-02 | Icu Medical, Inc. | Medical device communication method |
| US10303851B2 (en) * | 2013-03-15 | 2019-05-28 | Md24 Patent Technology, Llc | Physician-centric health care delivery platform |
| US10046112B2 (en) | 2013-05-24 | 2018-08-14 | Icu Medical, Inc. | Multi-sensor infusion system for detecting air or an occlusion in the infusion system |
| EP3003442B1 (en) | 2013-05-29 | 2020-12-30 | ICU Medical, Inc. | Infusion system and method of use which prevents over-saturation of an analog-to-digital converter |
| EP3003441B1 (en) | 2013-05-29 | 2020-12-02 | ICU Medical, Inc. | Infusion system which utilizes one or more sensors and additional information to make an air determination regarding the infusion system |
| AU2014312122A1 (en) | 2013-08-30 | 2016-04-07 | Icu Medical, Inc. | System and method of monitoring and managing a remote infusion regimen |
| US9662436B2 (en) | 2013-09-20 | 2017-05-30 | Icu Medical, Inc. | Fail-safe drug infusion therapy system |
| US10311972B2 (en) | 2013-11-11 | 2019-06-04 | Icu Medical, Inc. | Medical device system performance index |
| WO2015077320A1 (en) | 2013-11-19 | 2015-05-28 | Hospira, Inc. | Infusion pump automation system and method |
| WO2015085276A1 (en) * | 2013-12-06 | 2015-06-11 | Biogen Idec Ma Inc. | Population pharmacokinetics tools and uses thereof |
| US9898585B2 (en) | 2014-01-31 | 2018-02-20 | Aseko, Inc. | Method and system for insulin management |
| US9486580B2 (en) | 2014-01-31 | 2016-11-08 | Aseko, Inc. | Insulin management |
| US10293103B2 (en) | 2014-02-11 | 2019-05-21 | Smiths Medical Asd, Inc. | Pump startup algorithms and related systems and methods |
| ES2776363T3 (es) | 2014-02-28 | 2020-07-30 | Icu Medical Inc | Sistema de infusión y método que utiliza detección óptica de aire en línea de doble longitud de onda |
| JP6853669B2 (ja) | 2014-04-30 | 2021-03-31 | アイシーユー・メディカル・インコーポレーテッド | 条件付きの警報転送を用いた患者治療システム |
| CA2947045C (en) | 2014-05-29 | 2022-10-18 | Hospira, Inc. | Infusion system and pump with configurable closed loop delivery rate catch-up |
| US9724470B2 (en) | 2014-06-16 | 2017-08-08 | Icu Medical, Inc. | System for monitoring and delivering medication to a patient and method of using the same to minimize the risks associated with automated therapy |
| US10682478B2 (en) | 2014-08-04 | 2020-06-16 | Koninklijke Philips N.V. | Translating respiratory therapy parameters |
| US9539383B2 (en) | 2014-09-15 | 2017-01-10 | Hospira, Inc. | System and method that matches delayed infusion auto-programs with manually entered infusion programs and analyzes differences therein |
| WO2016069475A1 (en) | 2014-10-27 | 2016-05-06 | Aseko, Inc. | Subcutaneous outpatient management |
| US11081226B2 (en) | 2014-10-27 | 2021-08-03 | Aseko, Inc. | Method and controller for administering recommended insulin dosages to a patient |
| US11344668B2 (en) | 2014-12-19 | 2022-05-31 | Icu Medical, Inc. | Infusion system with concurrent TPN/insulin infusion |
| US9942091B2 (en) | 2015-02-27 | 2018-04-10 | Roche Diabetes Care, Inc. | Pump configuration software wizard for configuring parameters of a handheld insulin pump |
| US10850024B2 (en) | 2015-03-02 | 2020-12-01 | Icu Medical, Inc. | Infusion system, device, and method having advanced infusion features |
| US20160321400A1 (en) * | 2015-03-30 | 2016-11-03 | Zoll Medical Corporation | Clinical Data Handoff in Device Management and Data Sharing |
| WO2016189417A1 (en) | 2015-05-26 | 2016-12-01 | Hospira, Inc. | Infusion pump system and method with multiple drug library editor source capability |
| JP6858751B2 (ja) | 2015-08-20 | 2021-04-14 | アセコー インコーポレイテッド | 糖尿病管理療法アドバイザ |
| JP2018534701A (ja) | 2015-11-23 | 2018-11-22 | コーニンクレッカ フィリップス エヌ ヴェKoninklijke Philips N.V. | 有効性評価を使用して薬物投与スケジュールを評価し更新するためのパルスオキシメータ統合 |
| WO2017096511A1 (zh) * | 2015-12-07 | 2017-06-15 | 香港商台北市生活智能科技有限公司 | 自动获取治疗纪录的系统 |
| WO2017114949A1 (en) * | 2015-12-31 | 2017-07-06 | Koninklijke Philips N.V. | Automatically communicating between a non-mri compatible iv pump and a mri compatible iv pump |
| CA3013053A1 (en) | 2016-01-28 | 2017-08-03 | Savor Labs, Inc. | Method and apparatus for tracking of food intake and other behaviors and providing relevant feedback |
| EP3454922B1 (en) | 2016-05-13 | 2022-04-06 | ICU Medical, Inc. | Infusion pump system with common line auto flush |
| EP3468635B1 (en) | 2016-06-10 | 2024-09-25 | ICU Medical, Inc. | Acoustic flow sensor for continuous medication flow measurements and feedback control of infusion |
| WO2018013842A1 (en) | 2016-07-14 | 2018-01-18 | Icu Medical, Inc. | Multi-communication path selection and security system for a medical device |
| EP3504652B1 (en) * | 2016-08-25 | 2024-02-28 | Novo Nordisk A/S | Starter kit for basal insulin titration |
| CN110012675B (zh) | 2016-11-29 | 2024-02-27 | 诺和诺德股份有限公司 | 用于基础率滴定的起始套件 |
| USD853583S1 (en) | 2017-03-29 | 2019-07-09 | Becton, Dickinson And Company | Hand-held device housing |
| ES2866980T3 (es) * | 2017-12-12 | 2021-10-20 | Hoffmann La Roche | Procedimiento para operar un sistema de suministro de fármaco y sistema de suministro de fármaco |
| US10089055B1 (en) | 2017-12-27 | 2018-10-02 | Icu Medical, Inc. | Synchronized display of screen content on networked devices |
| US20190385728A1 (en) * | 2018-06-18 | 2019-12-19 | Bigfoot Biomedical, Inc. | Presenting insulin therapy setting recommendations associated with a therapy insight for a person with diabetes (pwd) and related methods |
| CA3106519A1 (en) | 2018-07-17 | 2020-01-23 | Icu Medical, Inc. | Systems and methods for facilitating clinical messaging in a network environment |
| US11152108B2 (en) | 2018-07-17 | 2021-10-19 | Icu Medical, Inc. | Passing authentication token to authorize access to rest calls via web sockets |
| US11139058B2 (en) | 2018-07-17 | 2021-10-05 | Icu Medical, Inc. | Reducing file transfer between cloud environment and infusion pumps |
| NZ771914A (en) | 2018-07-17 | 2023-04-28 | Icu Medical Inc | Updating infusion pump drug libraries and operational software in a networked environment |
| US10692595B2 (en) | 2018-07-26 | 2020-06-23 | Icu Medical, Inc. | Drug library dynamic version management |
| EP3827337A4 (en) | 2018-07-26 | 2022-04-13 | ICU Medical, Inc. | MEDICATION LIBRARY MANAGEMENT SYSTEM |
| US11645093B2 (en) | 2018-08-30 | 2023-05-09 | Express Scripts Strategic Development, Inc. | Systems and methods for user interface adaptation for per-user metrics |
| US10896048B1 (en) | 2018-08-30 | 2021-01-19 | Express Scripts Strategie Development, Inc. | Systems and methods for user interface adaptation for per-user metrics |
| US11367516B2 (en) | 2018-10-31 | 2022-06-21 | Medtronic Minimed, Inc. | Automated detection of a physical behavior event and corresponding adjustment of a medication dispensing system |
| US11278671B2 (en) | 2019-12-04 | 2022-03-22 | Icu Medical, Inc. | Infusion pump with safety sequence keypad |
| US20210178067A1 (en) * | 2019-12-13 | 2021-06-17 | Medtronic Minimed, Inc. | Translating therapy parameters of an insulin therapy system to translated therapy parameters for use at a different insulin therapy system |
| WO2022020184A1 (en) | 2020-07-21 | 2022-01-27 | Icu Medical, Inc. | Fluid transfer devices and methods of use |
| US11135360B1 (en) | 2020-12-07 | 2021-10-05 | Icu Medical, Inc. | Concurrent infusion with common line auto flush |
| WO2023233898A1 (ja) * | 2022-06-03 | 2023-12-07 | 株式会社レナサイエンス | 糖尿病治療薬の投与量の予測を支援する方法、予測支援装置、予測支援システム、及び予測支援プログラム |
Family Cites Families (193)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6241704B1 (en) | 1901-11-22 | 2001-06-05 | Sims Deltec, Inc. | Drug pump systems and methods |
| US5935099A (en) * | 1992-09-09 | 1999-08-10 | Sims Deltec, Inc. | Drug pump systems and methods |
| US5669877A (en) * | 1994-03-07 | 1997-09-23 | Sims Deltec, Inc. | Systems and methods for automated testing of medical equipment |
| US5338157B1 (en) * | 1992-09-09 | 1999-11-02 | Sims Deltec Inc | Systems and methods for communicating with ambulat |
| US4370983A (en) * | 1971-01-20 | 1983-02-01 | Lichtenstein Eric Stefan | Computer-control medical care system |
| US4055175A (en) * | 1976-05-07 | 1977-10-25 | Miles Laboratories, Inc. | Blood glucose control apparatus |
| US4151845A (en) * | 1977-11-25 | 1979-05-01 | Miles Laboratories, Inc. | Blood glucose control apparatus |
| US4559037A (en) * | 1977-12-28 | 1985-12-17 | Siemens Aktiengesellschaft | Device for the pre-programmable infusion of liquids |
| US4240438A (en) * | 1978-10-02 | 1980-12-23 | Wisconsin Alumni Research Foundation | Method for monitoring blood glucose levels and elements |
| US4308866A (en) * | 1978-11-02 | 1982-01-05 | University Of Southern California | Infusion controlling apparatus and method |
| US4731051A (en) * | 1979-04-27 | 1988-03-15 | The Johns Hopkins University | Programmable control means for providing safe and controlled medication infusion |
| US4373527B1 (en) * | 1979-04-27 | 1995-06-27 | Univ Johns Hopkins | Implantable programmable medication infusion system |
| DE3018641C2 (de) * | 1980-05-16 | 1986-05-28 | Hans 8228 Freilassing Rodler | Automatische Infusionspumpe |
| AU546785B2 (en) * | 1980-07-23 | 1985-09-19 | Commonwealth Of Australia, The | Open-loop controlled infusion of diabetics |
| DE3035670A1 (de) * | 1980-09-22 | 1982-04-29 | Siemens AG, 1000 Berlin und 8000 München | Vorrichtung zur infusion von fluessigkeiten in den menschlichen oder tierischen koerper |
| DE3112762A1 (de) | 1981-03-31 | 1983-01-13 | Jürgen Dr.med. 8700 Würzburg Schrezenmeir | Doppellumen-blutentnahme-einfachlumen-infusions-subclavia-katheterset |
| JPS57211361A (en) * | 1981-06-23 | 1982-12-25 | Terumo Corp | Liquid injecting apparatus |
| US4392849A (en) * | 1981-07-27 | 1983-07-12 | The Cleveland Clinic Foundation | Infusion pump controller |
| US4529401A (en) * | 1982-01-11 | 1985-07-16 | Cardiac Pacemakers, Inc. | Ambulatory infusion pump having programmable parameters |
| US4515584A (en) * | 1982-07-06 | 1985-05-07 | Fujisawa Pharmaceutical Co., Ltd. | Artificial pancreas |
| US4498843A (en) * | 1982-08-02 | 1985-02-12 | Schneider Philip H | Insulin infusion pump |
| US4464170A (en) * | 1982-09-29 | 1984-08-07 | Miles Laboratories, Inc. | Blood glucose control apparatus and method |
| US4526568A (en) * | 1982-09-29 | 1985-07-02 | Miles Laboratories, Inc. | Diagnostic method and apparatus for clamping blood glucose concentration |
| DE3372073D1 (en) * | 1982-10-18 | 1987-07-23 | Siemens Ag | Medicine-delivering apparatus |
| US4624661A (en) * | 1982-11-16 | 1986-11-25 | Surgidev Corp. | Drug dispensing system |
| US4679562A (en) * | 1983-02-16 | 1987-07-14 | Cardiac Pacemakers, Inc. | Glucose sensor |
| IT1170375B (it) * | 1983-04-19 | 1987-06-03 | Giuseppe Bombardieri | Apparecchio che infonde insulina o glucosio nel soggetto diabetico sulla base di determinazioni di concentrazioni di glucosio ottenute senza bisogno di prelievi del sangue del paziente |
| US4543955A (en) * | 1983-08-01 | 1985-10-01 | Cordis Corporation | System for controlling body implantable action device |
| DD230730A3 (de) | 1984-01-02 | 1985-12-11 | Zentralinstitut Fuer Diabetes | Einrichtung zur prospektiven automatischen bestimmung individualspezifischer glukoseregulationsparameter |
| US4685903A (en) * | 1984-01-06 | 1987-08-11 | Pacesetter Infusion, Ltd. | External infusion pump apparatus |
| IL74236A (en) * | 1984-02-08 | 1990-07-12 | Omni Flow Inc | Infusion system having plural fluid input ports and at least one patient output port |
| US5100380A (en) * | 1984-02-08 | 1992-03-31 | Abbott Laboratories | Remotely programmable infusion system |
| EP0158683B1 (de) * | 1984-04-14 | 1988-10-05 | Ferring Biotechnik GmbH | Vorrichtung zum intermittierenden Applizieren flüssiger Arzneimittel |
| US4741732A (en) * | 1984-05-10 | 1988-05-03 | The University Of Melbourne | Open-loop control of drug infusion |
| US4634427A (en) * | 1984-09-04 | 1987-01-06 | American Hospital Supply Company | Implantable demand medication delivery assembly |
| US4634426A (en) * | 1984-12-11 | 1987-01-06 | Baxter Travenol Laboratories | Medical infusion controller and user interface |
| US4676776A (en) * | 1985-01-18 | 1987-06-30 | Intelligent Medicine, Inc. | Device and method for effecting application of a therapeutic agent |
| US4756706A (en) * | 1985-01-23 | 1988-07-12 | American Hospital Supply Corporation | Centrally managed modular infusion pump system |
| US4838857A (en) * | 1985-05-29 | 1989-06-13 | Becton, Dickinson And Company | Medical infusion device |
| US5364346A (en) * | 1985-12-20 | 1994-11-15 | Schrezenmeir Juergen | Process for the continuous and discontinuous administration of insulin to the human body |
| US4714462A (en) * | 1986-02-03 | 1987-12-22 | Intermedics Infusaid, Inc. | Positive pressure programmable infusion pump |
| US5216597A (en) * | 1987-05-01 | 1993-06-01 | Diva Medical Systems Bv | Diabetes therapy management system, apparatus and method |
| WO1988010383A1 (en) * | 1987-06-19 | 1988-12-29 | The University Of Melbourne | Infusion pump and drive systems therefore |
| US4838856A (en) * | 1987-07-02 | 1989-06-13 | Truckee Meadows Research & Development | Fluid infusion flow control system |
| US5041086A (en) * | 1987-12-04 | 1991-08-20 | Pacesetter Infusion, Ltd. | Clinical configuration of multimode medication infusion system |
| US4898578A (en) * | 1988-01-26 | 1990-02-06 | Baxter International Inc. | Drug infusion system with calculator |
| US5131816A (en) * | 1988-07-08 | 1992-07-21 | I-Flow Corporation | Cartridge fed programmable ambulatory infusion pumps powered by DC electric motors |
| US5000739A (en) * | 1988-07-12 | 1991-03-19 | Pinewood Medical, Inc. | Programmable infusion pump |
| US4943279A (en) * | 1988-09-30 | 1990-07-24 | C. R. Bard, Inc. | Medical pump with infusion controlled by a detachable coded label |
| US5190522A (en) * | 1989-01-20 | 1993-03-02 | Institute Of Biocybernetics And Biomedical Engineering P.A.S. | Device for monitoring the operation of a delivery system and the method of use thereof |
| US5153827A (en) * | 1989-01-30 | 1992-10-06 | Omni-Flow, Inc. | An infusion management and pumping system having an alarm handling system |
| US5010473A (en) * | 1989-08-31 | 1991-04-23 | Duke University | Method and apparatus for model-based control of an open-loop process |
| US5084828A (en) * | 1989-09-29 | 1992-01-28 | Healthtech Services Corp. | Interactive medication delivery system |
| US5104374A (en) * | 1990-01-16 | 1992-04-14 | Bishko Jay R | Electronic fluid flow rate controller for controlling the infusion of intravenous drugs into a patient |
| US5109850A (en) * | 1990-02-09 | 1992-05-05 | Massachusetts Institute Of Technology | Automatic blood monitoring for medication delivery method and apparatus |
| AU7854891A (en) | 1990-04-26 | 1991-11-11 | Markwell Medical Institute, Inc. | Wearable blood glucose monitor |
| US5078683A (en) * | 1990-05-04 | 1992-01-07 | Block Medical, Inc. | Programmable infusion system |
| AT398694B (de) * | 1990-07-19 | 1995-01-25 | Avl Verbrennungskraft Messtech | Vorrichtung zur bestimmung der konzentration von zumindest einer in organischem gewebe vorliegenden substanz |
| US5256156A (en) * | 1991-01-31 | 1993-10-26 | Baxter International Inc. | Physician closed-loop neuromuscular blocking agent system |
| US5256157A (en) * | 1991-01-31 | 1993-10-26 | Baxter International Inc. | Automated infusion pump with replaceable memory cartridges |
| US5181910A (en) * | 1991-02-28 | 1993-01-26 | Pharmacia Deltec, Inc. | Method and apparatus for a fluid infusion system with linearized flow rate change |
| US5486286A (en) * | 1991-04-19 | 1996-01-23 | Althin Medical, Inc. | Apparatus for performing a self-test of kidney dialysis membrane |
| US5221268A (en) * | 1991-12-06 | 1993-06-22 | Block Medical, Inc. | Multiple dose control apparatus |
| US5244463A (en) * | 1991-12-06 | 1993-09-14 | Block Medical, Inc. | Programmable infusion pump |
| IL104365A0 (en) * | 1992-01-31 | 1993-05-13 | Gensia Pharma | Method and apparatus for closed loop drug delivery |
| JPH05277181A (ja) * | 1992-04-03 | 1993-10-26 | Sharp Corp | 輸液装置 |
| FR2690622B1 (fr) * | 1992-04-29 | 1995-01-20 | Chronotec | Système de pompe à perfusion ambulatoire programmable. |
| SE500122C2 (sv) * | 1992-08-27 | 1994-04-18 | Rudolf Valentin Sillen | Förfarande och anordning för individuellt styrd, adaptiv medicinering |
| US5330634A (en) * | 1992-08-28 | 1994-07-19 | Via Medical Corporation | Calibration solutions useful for analyses of biological fluids and methods employing same |
| US5788669A (en) * | 1995-11-22 | 1998-08-04 | Sims Deltec, Inc. | Pump tracking system |
| US5376070A (en) * | 1992-09-29 | 1994-12-27 | Minimed Inc. | Data transfer system for an infusion pump |
| ES2154651T3 (es) * | 1992-10-15 | 2001-04-16 | Gen Hospital Corp | Bomba de infusion con biblioteca de medicamentos cargable electronicamente. |
| US5956501A (en) * | 1997-01-10 | 1999-09-21 | Health Hero Network, Inc. | Disease simulation system and method |
| US5910252A (en) * | 1993-02-12 | 1999-06-08 | Cobe Laboratories, Inc. | Technique for extracorporeal treatment of blood |
| AU7323994A (en) * | 1993-07-13 | 1995-02-13 | Sims Deltec, Inc. | Medical pump and method of programming |
| US5368562A (en) * | 1993-07-30 | 1994-11-29 | Pharmacia Deltec, Inc. | Systems and methods for operating ambulatory medical devices such as drug delivery devices |
| US5423748A (en) * | 1993-08-16 | 1995-06-13 | Uhala; Dominic | Pain comforter system |
| US5389078A (en) * | 1993-10-06 | 1995-02-14 | Sims Deltec, Inc. | Programmable infusion pump for administering medication to patients |
| US5520637A (en) * | 1995-01-31 | 1996-05-28 | Pager; David | Closed-loop system for infusing oxytocin |
| US5941846A (en) * | 1995-03-13 | 1999-08-24 | Alaris Medical Systems, Inc. | Method and apparatus for power connection in a modular patient care system |
| US5713856A (en) * | 1995-03-13 | 1998-02-03 | Alaris Medical Systems, Inc. | Modular patient care system |
| US7384410B2 (en) | 1995-03-13 | 2008-06-10 | Cardinal Health 303, Inc. | System and method for managing patient care |
| US5772635A (en) * | 1995-05-15 | 1998-06-30 | Alaris Medical Systems, Inc. | Automated infusion system with dose rate calculator |
| US6671563B1 (en) | 1995-05-15 | 2003-12-30 | Alaris Medical Systems, Inc. | System and method for collecting data and managing patient care |
| US5781442A (en) * | 1995-05-15 | 1998-07-14 | Alaris Medical Systems, Inc. | System and method for collecting data and managing patient care |
| US5665065A (en) * | 1995-05-26 | 1997-09-09 | Minimed Inc. | Medication infusion device with blood glucose data input |
| US5995860A (en) * | 1995-07-06 | 1999-11-30 | Thomas Jefferson University | Implantable sensor and system for measurement and control of blood constituent levels |
| US5782805A (en) * | 1996-04-10 | 1998-07-21 | Meinzer; Randolph | Medical infusion pump |
| US6517482B1 (en) * | 1996-04-23 | 2003-02-11 | Dermal Therapy (Barbados) Inc. | Method and apparatus for non-invasive determination of glucose in body fluids |
| US5885245A (en) * | 1996-08-02 | 1999-03-23 | Sabratek Corporation | Medical apparatus with remote virtual input device |
| US6689091B2 (en) | 1996-08-02 | 2004-02-10 | Tuan Bui | Medical apparatus with remote control |
| US8734339B2 (en) | 1996-12-16 | 2014-05-27 | Ip Holdings, Inc. | Electronic skin patch for real time monitoring of cardiac activity and personal health management |
| US7267665B2 (en) | 1999-06-03 | 2007-09-11 | Medtronic Minimed, Inc. | Closed loop system for controlling insulin infusion |
| US5954643A (en) | 1997-06-09 | 1999-09-21 | Minimid Inc. | Insertion set for a transcutaneous sensor |
| US6558351B1 (en) * | 1999-06-03 | 2003-05-06 | Medtronic Minimed, Inc. | Closed loop system for controlling insulin infusion |
| US6000828A (en) * | 1997-08-22 | 1999-12-14 | Power Med Incorporated | Method of improving drug treatment |
| US6721582B2 (en) | 1999-04-06 | 2004-04-13 | Argose, Inc. | Non-invasive tissue glucose level monitoring |
| US7899518B2 (en) | 1998-04-06 | 2011-03-01 | Masimo Laboratories, Inc. | Non-invasive tissue glucose level monitoring |
| US6175752B1 (en) * | 1998-04-30 | 2001-01-16 | Therasense, Inc. | Analyte monitoring device and methods of use |
| US7308894B2 (en) | 1998-06-03 | 2007-12-18 | Scott Laboratories, Inc. | Apparatuses and methods for providing a conscious patient relief from pain and anxiety associated with medical or surgical procedures according to appropriate clinical heuristics |
| EP1082056B1 (en) | 1998-06-03 | 2007-11-14 | Scott Laboratories, Inc. | Apparatus for providing a conscious patient relief from pain and anxiety associated with medical or surgical procedures |
| US6554798B1 (en) | 1998-08-18 | 2003-04-29 | Medtronic Minimed, Inc. | External infusion device with remote programming, bolus estimator and/or vibration alarm capabilities |
| DE19840965A1 (de) | 1998-09-08 | 2000-03-09 | Disetronic Licensing Ag | Vorrichtung zur Selbstverabreichung eines Produktfluids |
| WO2000013580A1 (en) | 1998-09-11 | 2000-03-16 | Amira Medical | Device for determination of an analyte in a body fluid intergrated with an insulin pump |
| US7931642B2 (en) | 1998-09-18 | 2011-04-26 | Codman Neuro Sciences Sarl | Infusion pump comprising a computer for calculating the respective maximum permissible dosage |
| DE19844252A1 (de) | 1998-09-26 | 2000-03-30 | Hendrik Lehnert | Modulare Vorrichtung zur computergesteuerten Insulin- und Glukoseinfusion |
| US6540672B1 (en) * | 1998-12-09 | 2003-04-01 | Novo Nordisk A/S | Medical system and a method of controlling the system for use by a patient for medical self treatment |
| JP2002531884A (ja) | 1998-11-30 | 2002-09-24 | ノボ ノルディスク アクティーゼルスカブ | 複数の動作を含む自己治療においてユーザを支援するための方法及びシステム |
| DE59913262D1 (de) | 1999-07-08 | 2006-05-11 | Leonhardt Steffen | Vorrichtung zur messung des menschlichen blutzuckerspiegels |
| US6923763B1 (en) | 1999-08-23 | 2005-08-02 | University Of Virginia Patent Foundation | Method and apparatus for predicting the risk of hypoglycemia |
| US7933780B2 (en) * | 1999-10-22 | 2011-04-26 | Telaric, Llc | Method and apparatus for controlling an infusion pump or the like |
| US6694191B2 (en) | 2000-01-21 | 2004-02-17 | Medtronic Minimed, Inc. | Ambulatory medical apparatus and method having telemetry modifiable control software |
| DE10006044A1 (de) | 2000-02-10 | 2001-08-16 | Roche Diagnostics Gmbh | Anordnung und Verfahren zur Dosierung eines die Blutglukose eines Patienten regulierenden Hormons |
| US6572542B1 (en) * | 2000-03-03 | 2003-06-03 | Medtronic, Inc. | System and method for monitoring and controlling the glycemic state of a patient |
| US6599281B1 (en) | 2000-05-03 | 2003-07-29 | Aspect Medical Systems, Inc. | System and method for adaptive drug delivery |
| EP1316048A2 (en) | 2000-05-18 | 2003-06-04 | ALARIS Medical Systems, Inc. | Distributed remote asset and medication management drug delivery system |
| US7860583B2 (en) | 2004-08-25 | 2010-12-28 | Carefusion 303, Inc. | System and method for dynamically adjusting patient therapy |
| CA2421133C (en) | 2000-09-08 | 2012-06-26 | Insulet Corporation | Devices, systems and methods for patient infusion |
| US6575905B2 (en) | 2000-09-22 | 2003-06-10 | Knobbe, Lim & Buckingham | Method and apparatus for real-time estimation of physiological parameters |
| WO2002028454A2 (en) * | 2000-10-04 | 2002-04-11 | Insulet Corporation | Data collection assembly for patient infusion system |
| US6749587B2 (en) | 2001-02-22 | 2004-06-15 | Insulet Corporation | Modular infusion device and method |
| AUPR632301A0 (en) | 2001-07-11 | 2001-08-02 | Chee, Frederick Howe-Hui | Infusion apparatus for regulating blood glucose levels |
| US6544212B2 (en) * | 2001-07-31 | 2003-04-08 | Roche Diagnostics Corporation | Diabetes management system |
| WO2003011358A2 (en) | 2001-07-31 | 2003-02-13 | Scott Laboratories, Inc. | Apparatuses and methods for titrating drug delivery |
| US20040147034A1 (en) | 2001-08-14 | 2004-07-29 | Gore Jay Prabhakar | Method and apparatus for measuring a substance in a biological sample |
| US6740072B2 (en) | 2001-09-07 | 2004-05-25 | Medtronic Minimed, Inc. | System and method for providing closed loop infusion formulation delivery |
| US8152789B2 (en) | 2001-10-23 | 2012-04-10 | Medtronic Minimed, Inc. | System and method for providing closed loop infusion formulation delivery |
| US6827702B2 (en) | 2001-09-07 | 2004-12-07 | Medtronic Minimed, Inc. | Safety limits for closed-loop infusion pump control |
| EP1455878B1 (en) | 2001-12-06 | 2006-03-08 | Alaris Medical Systems, Inc. | Co2 monitored drug infusion system |
| US7204823B2 (en) | 2001-12-19 | 2007-04-17 | Medtronic Minimed, Inc. | Medication delivery system and monitor |
| US7399277B2 (en) | 2001-12-27 | 2008-07-15 | Medtronic Minimed, Inc. | System for monitoring physiological characteristics |
| US20030125662A1 (en) | 2002-01-03 | 2003-07-03 | Tuan Bui | Method and apparatus for providing medical treatment therapy based on calculated demand |
| US6985870B2 (en) | 2002-01-11 | 2006-01-10 | Baxter International Inc. | Medication delivery system |
| US20030140928A1 (en) | 2002-01-29 | 2003-07-31 | Tuan Bui | Medical treatment verification system and method |
| US20030141981A1 (en) | 2002-01-29 | 2003-07-31 | Tuan Bui | System and method for operating medical devices |
| US20030143746A1 (en) | 2002-01-31 | 2003-07-31 | Sage Burton H. | Self-calibrating body anayte monitoring system |
| US20030212379A1 (en) | 2002-02-26 | 2003-11-13 | Bylund Adam David | Systems and methods for remotely controlling medication infusion and analyte monitoring |
| US6852104B2 (en) | 2002-02-28 | 2005-02-08 | Smiths Medical Md, Inc. | Programmable insulin pump |
| US7108680B2 (en) | 2002-03-06 | 2006-09-19 | Codman & Shurtleff, Inc. | Closed-loop drug delivery system |
| GB0206792D0 (en) * | 2002-03-22 | 2002-05-01 | Leuven K U Res & Dev | Normoglycemia |
| US20050055242A1 (en) * | 2002-04-30 | 2005-03-10 | Bryan Bello | System and method for medical data tracking, analysis and reporting for healthcare system |
| US7238164B2 (en) | 2002-07-19 | 2007-07-03 | Baxter International Inc. | Systems, methods and apparatuses for pumping cassette-based therapies |
| US7278983B2 (en) | 2002-07-24 | 2007-10-09 | Medtronic Minimed, Inc. | Physiological monitoring device for controlling a medication infusion device |
| US7060059B2 (en) | 2002-10-11 | 2006-06-13 | Becton, Dickinson And Company | System and method for initiating and maintaining continuous, long-term control of a concentration of a substance in a patient using a feedback or model-based controller coupled to a single-needle or multi-needle intradermal (ID) delivery device |
| US8771183B2 (en) | 2004-02-17 | 2014-07-08 | Abbott Diabetes Care Inc. | Method and system for providing data communication in continuous glucose monitoring and management system |
| AU2004225145B2 (en) | 2003-03-28 | 2010-05-20 | Carefusion 303, Inc. | Infusion data communication system |
| CA2520880A1 (en) | 2003-04-18 | 2004-11-04 | Insulet Corporation | User interface for infusion pump remote controller and method of using the same |
| US8460243B2 (en) | 2003-06-10 | 2013-06-11 | Abbott Diabetes Care Inc. | Glucose measuring module and insulin pump combination |
| US8998808B2 (en) | 2003-06-19 | 2015-04-07 | Wayne State University | System for identifying patient response to anesthesia infusion |
| US7591801B2 (en) | 2004-02-26 | 2009-09-22 | Dexcom, Inc. | Integrated delivery device for continuous glucose sensor |
| JP4318984B2 (ja) * | 2003-08-12 | 2009-08-26 | 株式会社トプコン | 診療支援システム、診療支援装置、診療支援方法、その方法をコンピュータに実行させるためのプログラム、及びそのプログラムを記憶したコンピュータ読み取り可能な情報記録媒体 |
| US20060100907A1 (en) | 2003-10-07 | 2006-05-11 | Holland Geoffrey N | Medication management system |
| KR100567837B1 (ko) | 2003-10-24 | 2006-04-05 | 케이제이헬스케어 주식회사 | 혈당측정이 가능한 이동통신단말기와 결합되는 인슐린펌프와, 인슐린 펌프의 제어정보 전송을 위한 네트워크시스템 |
| DE10352456A1 (de) | 2003-11-07 | 2005-07-28 | Basibüyük, Halil | Verfahren und Vorrichtung zur Verabreichung von flüssigen Medikamenten an einem Patienten |
| US8020564B2 (en) | 2003-12-01 | 2011-09-20 | Carefusion 303, Inc. | System and method for analyzing medical treatment data |
| WO2005056087A1 (en) | 2003-12-05 | 2005-06-23 | Cardinal Health 303, Inc. | Patient-controlled analgesia with patient monitoring system |
| US20050137522A1 (en) | 2003-12-17 | 2005-06-23 | Thomas Aoki | System for infusing insulin to a subject to improve impaired hepatic glucose processing |
| US8808228B2 (en) | 2004-02-26 | 2014-08-19 | Dexcom, Inc. | Integrated medicament delivery device for use with continuous analyte sensor |
| WO2005084257A2 (en) | 2004-02-26 | 2005-09-15 | Vpn Solutions, Llc | Composite thin-film glucose sensor |
| US7905710B2 (en) | 2004-03-26 | 2011-03-15 | Hospira, Inc. | System and method for improved low flow medical pump delivery |
| US20060009727A1 (en) | 2004-04-08 | 2006-01-12 | Chf Solutions Inc. | Method and apparatus for an extracorporeal control of blood glucose |
| US20060009734A1 (en) | 2004-07-07 | 2006-01-12 | Martin James F | Dosage control for drug delivery system |
| US8359338B2 (en) | 2004-07-30 | 2013-01-22 | Carefusion 303, Inc. | System and method for managing medical databases for patient care devices |
| US20060079831A1 (en) | 2004-08-18 | 2006-04-13 | Gilbert Gregory F | Quantitative chronological medical infusion device |
| US20060047270A1 (en) | 2004-08-27 | 2006-03-02 | Shelton Brian M | Drug delivery apparatus and method for automatically reducing drug dosage |
| US8398592B2 (en) | 2004-09-07 | 2013-03-19 | Thomas Leibner-Druska | Medication data transfer system and method for patient infusions |
| US20060173260A1 (en) | 2005-01-31 | 2006-08-03 | Gmms Ltd | System, device and method for diabetes treatment and monitoring |
| US7547281B2 (en) | 2005-02-01 | 2009-06-16 | Medtronic Minimed, Inc. | Algorithm sensor augmented bolus estimator for semi-closed loop infusion system |
| SG158906A1 (en) | 2005-02-11 | 2010-02-26 | Cardinal Health 303 Inc | Identification system and method for medication management |
| WO2006102412A2 (en) | 2005-03-21 | 2006-09-28 | Abbott Diabetes Care, Inc. | Method and system for providing integrated medication infusion and analyte monitoring system |
| US20090054754A1 (en) | 2007-08-21 | 2009-02-26 | Mcmahon Dave | Clinician-controlled semi-automated medication management |
| US7509156B2 (en) | 2005-05-18 | 2009-03-24 | Clarian Health Partners, Inc. | System for managing glucose levels in patients with diabetes or hyperglycemia |
| US7713240B2 (en) | 2005-09-13 | 2010-05-11 | Medtronic Minimed, Inc. | Modular external infusion device |
| US7927284B2 (en) | 2005-09-16 | 2011-04-19 | Cardiac Pacemakers, Inc. | Quantifying hemodynamic response to drug therapy using implantable sensor |
| US20070078314A1 (en) | 2005-09-30 | 2007-04-05 | Grounsell Richard L | System and method for measuring and predicting insulin dosing rates |
| US20070088333A1 (en) | 2005-10-13 | 2007-04-19 | G&L Consulting, Llc | Method and system for infusing an osmotic solute into a patient and providing feedback control of the infusing rate |
| US7704226B2 (en) | 2005-11-17 | 2010-04-27 | Medtronic Minimed, Inc. | External infusion device with programmable capabilities to time-shift basal insulin and method of using the same |
| EP1801718A1 (de) | 2005-12-21 | 2007-06-27 | F. Hoffmann-La Roche AG | Verfahren zum Betrieb einer computergesteuerten Dosiervorrichtung für flüssige Medikamente bei reisebedingter Zeitverschiebung |
| US7785463B2 (en) | 2006-03-17 | 2010-08-31 | Children's Hospital Medical Center | Extracorporeal renal replacement modeling system |
| US20070233049A1 (en) * | 2006-03-28 | 2007-10-04 | Hospira, Inc. | Medication administration and management system and method |
| WO2007138154A1 (en) | 2006-05-29 | 2007-12-06 | Wristop Technologies Oy | Apparatus and method for dosing drug and wireless remote control of a drug pump |
| ATE553695T1 (de) | 2006-06-13 | 2012-05-15 | Carefusion 303 Inc | System und verfahren zur optimierten steuerung von pca- und pcea-systemen |
| US9056165B2 (en) | 2006-09-06 | 2015-06-16 | Medtronic Minimed, Inc. | Intelligent therapy recommendation algorithm and method of using the same |
| US20080091466A1 (en) * | 2006-10-16 | 2008-04-17 | Hospira, Inc. | System and method for comparing and utilizing activity information and configuration information from multiple device management systems |
| US20080214919A1 (en) | 2006-12-26 | 2008-09-04 | Lifescan, Inc. | System and method for implementation of glycemic control protocols |
| US8417311B2 (en) | 2008-09-12 | 2013-04-09 | Optiscan Biomedical Corporation | Fluid component analysis system and method for glucose monitoring and control |
| US20080300572A1 (en) | 2007-06-01 | 2008-12-04 | Medtronic Minimed, Inc. | Wireless monitor for a personal medical device system |
| CN101821741B (zh) | 2007-06-27 | 2013-12-04 | 霍夫曼-拉罗奇有限公司 | 用于被调用事件的医学诊断、治疗和预后系统及其方法 |
| EP2171630A1 (en) | 2007-06-27 | 2010-04-07 | F. Hoffmann-Roche AG | System and method for developing patient specific therapies based on modeling of patient physiology |
| JP6017758B2 (ja) | 2007-06-27 | 2016-11-02 | エフ ホフマン−ラ ロッシュ アクチェン ゲゼルシャフト | 治療システムのための患者情報入力インターフェイス |
| US9483615B2 (en) * | 2007-08-10 | 2016-11-01 | Smiths Medical Asd, Inc. | Communication of original and updated pump parameters for a medical infusion pump |
| US20090221890A1 (en) | 2008-02-28 | 2009-09-03 | Daniel Saffer | Diabetes Management System |
| US20100036310A1 (en) * | 2008-08-05 | 2010-02-11 | Hillman Robert S | Integrated patient management and control system for medication delivery |
-
2010
- 2010-12-16 US US12/970,777 patent/US8771251B2/en active Active
- 2010-12-17 ES ES10838319T patent/ES2716235T3/es active Active
- 2010-12-17 WO PCT/US2010/061127 patent/WO2011075687A1/en active Application Filing
- 2010-12-17 JP JP2012544916A patent/JP5699161B2/ja active Active
- 2010-12-17 AU AU2010330746A patent/AU2010330746B2/en active Active
- 2010-12-17 CA CA2784143A patent/CA2784143C/en active Active
- 2010-12-17 EP EP10838319.1A patent/EP2516671B1/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| AU2010330746A1 (en) | 2012-07-05 |
| US20110152830A1 (en) | 2011-06-23 |
| CA2784143C (en) | 2016-08-09 |
| US8771251B2 (en) | 2014-07-08 |
| CA2784143A1 (en) | 2011-06-23 |
| WO2011075687A1 (en) | 2011-06-23 |
| AU2010330746B2 (en) | 2016-02-25 |
| EP2516671A4 (en) | 2015-08-05 |
| EP2516671A1 (en) | 2012-10-31 |
| JP2013514834A (ja) | 2013-05-02 |
| EP2516671B1 (en) | 2019-02-20 |
| JP5699161B2 (ja) | 2015-04-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2716235T3 (es) | Sistemas para gestionar dispositivos de suministro de medicamentos | |
| JP7482968B2 (ja) | インスリン・デリバリ量の調節 | |
| US10188796B2 (en) | Method and system for management of diabetes with a glucose monitor and infusion pump to provide feedback on bolus dosing | |
| TWI671094B (zh) | 用於控制人工胰臟中之封閉迴路控制器因感測器更換後之調諧因子的系統 | |
| US9486578B2 (en) | Method and system for tuning a closed-loop controller for an artificial pancreas | |
| US7398183B2 (en) | Medication management system | |
| US9123077B2 (en) | Medication management system | |
| US20160310668A1 (en) | System for managing glucose levels in patients with diabetes or hyperglycemia | |
| US12112842B2 (en) | System and method for improving the drug therapy management | |
| US20090054754A1 (en) | Clinician-controlled semi-automated medication management | |
| TW201503921A (zh) | 用於人工胰臟之混合式控制至目標及控制至範圍模型預測控制的方法及系統 | |
| RU2778069C2 (ru) | Учет остаточного количества активного инсулина в системе искусственной поджелудочной железы | |
| Dubauskienė et al. | Challenges of Close Loop Electronic Medical Systems |