DE60029833T2 - Nahrungsmittelergänzungen zur Verbesserung des Knorpelzustandes sowie Herstellungsmethoden - Google Patents
Nahrungsmittelergänzungen zur Verbesserung des Knorpelzustandes sowie Herstellungsmethoden Download PDFInfo
- Publication number
- DE60029833T2 DE60029833T2 DE60029833T DE60029833T DE60029833T2 DE 60029833 T2 DE60029833 T2 DE 60029833T2 DE 60029833 T DE60029833 T DE 60029833T DE 60029833 T DE60029833 T DE 60029833T DE 60029833 T2 DE60029833 T2 DE 60029833T2
- Authority
- DE
- Germany
- Prior art keywords
- juice
- drink
- cartilage
- solution
- base
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
- 210000000845 cartilage Anatomy 0.000 title claims abstract description 47
- 235000015872 dietary supplement Nutrition 0.000 title abstract description 7
- 238000004519 manufacturing process Methods 0.000 title description 7
- 230000006872 improvement Effects 0.000 title description 3
- 239000013589 supplement Substances 0.000 claims abstract description 47
- 235000013361 beverage Nutrition 0.000 claims abstract description 25
- KIUKXJAPPMFGSW-DNGZLQJQSA-N (2S,3S,4S,5R,6R)-6-[(2S,3R,4R,5S,6R)-3-Acetamido-2-[(2S,3S,4R,5R,6R)-6-[(2R,3R,4R,5S,6R)-3-acetamido-2,5-dihydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-2-carboxy-4,5-dihydroxyoxan-3-yl]oxy-5-hydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-3,4,5-trihydroxyoxane-2-carboxylic acid Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](O[C@H]3[C@@H]([C@@H](O)[C@H](O)[C@H](O3)C(O)=O)O)[C@H](O)[C@@H](CO)O2)NC(C)=O)[C@@H](C(O)=O)O1 KIUKXJAPPMFGSW-DNGZLQJQSA-N 0.000 claims abstract description 7
- 229920002674 hyaluronan Polymers 0.000 claims abstract description 7
- 229960003160 hyaluronic acid Drugs 0.000 claims abstract description 7
- SQDAZGGFXASXDW-UHFFFAOYSA-N 5-bromo-2-(trifluoromethoxy)pyridine Chemical compound FC(F)(F)OC1=CC=C(Br)C=N1 SQDAZGGFXASXDW-UHFFFAOYSA-N 0.000 claims abstract description 6
- 229920001287 Chondroitin sulfate Polymers 0.000 claims abstract description 6
- 229940059329 chondroitin sulfate Drugs 0.000 claims abstract description 6
- 238000000034 method Methods 0.000 claims description 33
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 30
- 235000011389 fruit/vegetable juice Nutrition 0.000 claims description 26
- 150000001720 carbohydrates Chemical class 0.000 claims description 18
- 235000014633 carbohydrates Nutrition 0.000 claims description 18
- 239000000203 mixture Substances 0.000 claims description 17
- 239000004615 ingredient Substances 0.000 claims description 12
- 238000002156 mixing Methods 0.000 claims description 12
- 238000009928 pasteurization Methods 0.000 claims description 10
- 230000008569 process Effects 0.000 claims description 10
- 235000013343 vitamin Nutrition 0.000 claims description 9
- 239000011782 vitamin Substances 0.000 claims description 9
- 229940088594 vitamin Drugs 0.000 claims description 9
- 229930003231 vitamin Natural products 0.000 claims description 9
- 235000014058 juice drink Nutrition 0.000 claims description 7
- 235000018102 proteins Nutrition 0.000 claims description 7
- 108090000623 proteins and genes Proteins 0.000 claims description 7
- 102000004169 proteins and genes Human genes 0.000 claims description 7
- MSWZFWKMSRAUBD-IVMDWMLBSA-N 2-amino-2-deoxy-D-glucopyranose Chemical compound N[C@H]1C(O)O[C@H](CO)[C@@H](O)[C@@H]1O MSWZFWKMSRAUBD-IVMDWMLBSA-N 0.000 claims description 6
- MSWZFWKMSRAUBD-UHFFFAOYSA-N beta-D-galactosamine Natural products NC1C(O)OC(CO)C(O)C1O MSWZFWKMSRAUBD-UHFFFAOYSA-N 0.000 claims description 6
- 229960002442 glucosamine Drugs 0.000 claims description 6
- 229910052500 inorganic mineral Inorganic materials 0.000 claims description 6
- 239000011707 mineral Substances 0.000 claims description 6
- 235000010755 mineral Nutrition 0.000 claims description 6
- 239000003925 fat Substances 0.000 claims description 5
- 235000019197 fats Nutrition 0.000 claims description 5
- 238000002360 preparation method Methods 0.000 claims description 4
- 239000008369 fruit flavor Substances 0.000 claims description 3
- 235000015203 fruit juice Nutrition 0.000 claims description 3
- 239000003755 preservative agent Substances 0.000 claims description 3
- 229920002567 Chondroitin Polymers 0.000 claims description 2
- 239000008122 artificial sweetener Substances 0.000 claims description 2
- 235000021311 artificial sweeteners Nutrition 0.000 claims description 2
- DLGJWSVWTWEWBJ-HGGSSLSASA-N chondroitin Chemical compound CC(O)=N[C@@H]1[C@H](O)O[C@H](CO)[C@H](O)[C@@H]1OC1[C@H](O)[C@H](O)C=C(C(O)=O)O1 DLGJWSVWTWEWBJ-HGGSSLSASA-N 0.000 claims description 2
- 150000002301 glucosamine derivatives Chemical class 0.000 claims 2
- 235000021559 Fruit Juice Concentrate Nutrition 0.000 claims 1
- 235000021096 natural sweeteners Nutrition 0.000 claims 1
- DYIOQMKBBPSAFY-BENRWUELSA-N Palmityl myristoleate Chemical compound CCCCCCCCCCCCCCCCOC(=O)CCCCCCC\C=C/CCCC DYIOQMKBBPSAFY-BENRWUELSA-N 0.000 abstract description 18
- 229940093532 cetyl myristoleate Drugs 0.000 abstract description 18
- DYIOQMKBBPSAFY-UHFFFAOYSA-N palmityl myristoleate Natural products CCCCCCCCCCCCCCCCOC(=O)CCCCCCCC=CCCCC DYIOQMKBBPSAFY-UHFFFAOYSA-N 0.000 abstract description 18
- MTDHILKWIRSIHB-UHFFFAOYSA-N (5-azaniumyl-3,4,6-trihydroxyoxan-2-yl)methyl sulfate Chemical compound NC1C(O)OC(COS(O)(=O)=O)C(O)C1O MTDHILKWIRSIHB-UHFFFAOYSA-N 0.000 abstract description 8
- 229960002849 glucosamine sulfate Drugs 0.000 abstract description 8
- 235000011888 snacks Nutrition 0.000 abstract description 3
- 239000000243 solution Substances 0.000 description 44
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 21
- 239000000047 product Substances 0.000 description 13
- 230000035622 drinking Effects 0.000 description 9
- 244000228451 Stevia rebaudiana Species 0.000 description 8
- 229920002527 Glycogen Polymers 0.000 description 7
- 229940096919 glycogen Drugs 0.000 description 7
- 238000004806 packaging method and process Methods 0.000 description 7
- 239000000843 powder Substances 0.000 description 7
- HELXLJCILKEWJH-NCGAPWICSA-N rebaudioside A Chemical compound O([C@H]1[C@H](O)[C@@H](CO)O[C@H]([C@@H]1O[C@H]1[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O1)O)O[C@]12C(=C)C[C@@]3(C1)CC[C@@H]1[C@@](C)(CCC[C@]1([C@@H]3CC2)C)C(=O)O[C@H]1[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O1)O)[C@@H]1O[C@H](CO)[C@@H](O)[C@H](O)[C@H]1O HELXLJCILKEWJH-NCGAPWICSA-N 0.000 description 7
- 238000012546 transfer Methods 0.000 description 7
- 208000006820 Arthralgia Diseases 0.000 description 6
- 239000007788 liquid Substances 0.000 description 6
- 235000000346 sugar Nutrition 0.000 description 6
- CBOJBBMQJBVCMW-BTVCFUMJSA-N (2r,3r,4s,5r)-2-amino-3,4,5,6-tetrahydroxyhexanal;hydrochloride Chemical compound Cl.O=C[C@H](N)[C@@H](O)[C@H](O)[C@H](O)CO CBOJBBMQJBVCMW-BTVCFUMJSA-N 0.000 description 5
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 5
- 239000003995 emulsifying agent Substances 0.000 description 5
- 239000008103 glucose Substances 0.000 description 5
- WXMKPNITSTVMEF-UHFFFAOYSA-M sodium benzoate Chemical compound [Na+].[O-]C(=O)C1=CC=CC=C1 WXMKPNITSTVMEF-UHFFFAOYSA-M 0.000 description 5
- 235000010234 sodium benzoate Nutrition 0.000 description 5
- 239000004299 sodium benzoate Substances 0.000 description 5
- 239000003765 sweetening agent Substances 0.000 description 5
- 235000013305 food Nutrition 0.000 description 4
- 235000003599 food sweetener Nutrition 0.000 description 4
- 238000009472 formulation Methods 0.000 description 4
- 238000011084 recovery Methods 0.000 description 4
- LUEWUZLMQUOBSB-FSKGGBMCSA-N (2s,3s,4s,5s,6r)-2-[(2r,3s,4r,5r,6s)-6-[(2r,3s,4r,5s,6s)-4,5-dihydroxy-2-(hydroxymethyl)-6-[(2r,4r,5s,6r)-4,5,6-trihydroxy-2-(hydroxymethyl)oxan-3-yl]oxyoxan-3-yl]oxy-4,5-dihydroxy-2-(hydroxymethyl)oxan-3-yl]oxy-6-(hydroxymethyl)oxane-3,4,5-triol Chemical compound O[C@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@@H](O[C@@H]2[C@H](O[C@@H](OC3[C@H](O[C@@H](O)[C@@H](O)[C@H]3O)CO)[C@@H](O)[C@H]2O)CO)[C@H](O)[C@H]1O LUEWUZLMQUOBSB-FSKGGBMCSA-N 0.000 description 3
- 244000247812 Amorphophallus rivieri Species 0.000 description 3
- 235000001206 Amorphophallus rivieri Nutrition 0.000 description 3
- 229920002581 Glucomannan Polymers 0.000 description 3
- 229920002752 Konjac Polymers 0.000 description 3
- 230000000386 athletic effect Effects 0.000 description 3
- 235000021557 concentrated beverage Nutrition 0.000 description 3
- 229940046240 glucomannan Drugs 0.000 description 3
- 230000035876 healing Effects 0.000 description 3
- 239000000252 konjac Substances 0.000 description 3
- 235000010485 konjac Nutrition 0.000 description 3
- 235000016709 nutrition Nutrition 0.000 description 3
- 201000008482 osteoarthritis Diseases 0.000 description 3
- 239000006187 pill Substances 0.000 description 3
- 230000000153 supplemental effect Effects 0.000 description 3
- YWWVWXASSLXJHU-AATRIKPKSA-N (9E)-tetradecenoic acid Chemical compound CCCC\C=C\CCCCCCCC(O)=O YWWVWXASSLXJHU-AATRIKPKSA-N 0.000 description 2
- 241000894006 Bacteria Species 0.000 description 2
- 241000196324 Embryophyta Species 0.000 description 2
- 206010023230 Joint stiffness Diseases 0.000 description 2
- 244000299461 Theobroma cacao Species 0.000 description 2
- 238000010521 absorption reaction Methods 0.000 description 2
- 206010003246 arthritis Diseases 0.000 description 2
- 235000014171 carbonated beverage Nutrition 0.000 description 2
- 239000003795 chemical substances by application Substances 0.000 description 2
- 235000019219 chocolate Nutrition 0.000 description 2
- 235000008504 concentrate Nutrition 0.000 description 2
- 210000002808 connective tissue Anatomy 0.000 description 2
- 235000014113 dietary fatty acids Nutrition 0.000 description 2
- 239000003814 drug Substances 0.000 description 2
- 239000003792 electrolyte Substances 0.000 description 2
- 239000000194 fatty acid Substances 0.000 description 2
- 229930195729 fatty acid Natural products 0.000 description 2
- 150000004665 fatty acids Chemical class 0.000 description 2
- 239000012467 final product Substances 0.000 description 2
- 239000000796 flavoring agent Substances 0.000 description 2
- 235000019634 flavors Nutrition 0.000 description 2
- 239000012530 fluid Substances 0.000 description 2
- 229960001911 glucosamine hydrochloride Drugs 0.000 description 2
- 150000004676 glycans Chemical class 0.000 description 2
- BXWNKGSJHAJOGX-UHFFFAOYSA-N hexadecan-1-ol Chemical compound CCCCCCCCCCCCCCCCO BXWNKGSJHAJOGX-UHFFFAOYSA-N 0.000 description 2
- 230000002779 inactivation Effects 0.000 description 2
- 239000000314 lubricant Substances 0.000 description 2
- 235000012054 meals Nutrition 0.000 description 2
- 239000003921 oil Substances 0.000 description 2
- 229920001282 polysaccharide Polymers 0.000 description 2
- 239000005017 polysaccharide Substances 0.000 description 2
- 235000009561 snack bars Nutrition 0.000 description 2
- 235000011496 sports drink Nutrition 0.000 description 2
- 230000001954 sterilising effect Effects 0.000 description 2
- 238000004659 sterilization and disinfection Methods 0.000 description 2
- 238000003756 stirring Methods 0.000 description 2
- 150000008163 sugars Chemical class 0.000 description 2
- 208000024891 symptom Diseases 0.000 description 2
- 150000003722 vitamin derivatives Chemical class 0.000 description 2
- HSINOMROUCMIEA-FGVHQWLLSA-N (2s,4r)-4-[(3r,5s,6r,7r,8s,9s,10s,13r,14s,17r)-6-ethyl-3,7-dihydroxy-10,13-dimethyl-2,3,4,5,6,7,8,9,11,12,14,15,16,17-tetradecahydro-1h-cyclopenta[a]phenanthren-17-yl]-2-methylpentanoic acid Chemical compound C([C@@]12C)C[C@@H](O)C[C@H]1[C@@H](CC)[C@@H](O)[C@@H]1[C@@H]2CC[C@]2(C)[C@@H]([C@H](C)C[C@H](C)C(O)=O)CC[C@H]21 HSINOMROUCMIEA-FGVHQWLLSA-N 0.000 description 1
- YWWVWXASSLXJHU-UHFFFAOYSA-N 9E-tetradecenoic acid Natural products CCCCC=CCCCCCCCC(O)=O YWWVWXASSLXJHU-UHFFFAOYSA-N 0.000 description 1
- 244000215068 Acacia senegal Species 0.000 description 1
- WBZFUFAFFUEMEI-UHFFFAOYSA-M Acesulfame k Chemical compound [K+].CC1=CC(=O)[N-]S(=O)(=O)O1 WBZFUFAFFUEMEI-UHFFFAOYSA-M 0.000 description 1
- 244000208874 Althaea officinalis Species 0.000 description 1
- 235000006576 Althaea officinalis Nutrition 0.000 description 1
- 108010011485 Aspartame Proteins 0.000 description 1
- WQZGKKKJIJFFOK-QTVWNMPRSA-N D-mannopyranose Chemical compound OC[C@H]1OC(O)[C@@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-QTVWNMPRSA-N 0.000 description 1
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 1
- IAJILQKETJEXLJ-UHFFFAOYSA-N Galacturonsaeure Natural products O=CC(O)C(O)C(O)C(O)C(O)=O IAJILQKETJEXLJ-UHFFFAOYSA-N 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 229920000084 Gum arabic Polymers 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 208000001953 Hypotension Diseases 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- OVRNDRQMDRJTHS-UHFFFAOYSA-N N-acelyl-D-glucosamine Natural products CC(=O)NC1C(O)OC(CO)C(O)C1O OVRNDRQMDRJTHS-UHFFFAOYSA-N 0.000 description 1
- OVRNDRQMDRJTHS-FMDGEEDCSA-N N-acetyl-beta-D-glucosamine Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O OVRNDRQMDRJTHS-FMDGEEDCSA-N 0.000 description 1
- 208000008589 Obesity Diseases 0.000 description 1
- 208000002193 Pain Diseases 0.000 description 1
- 235000006092 Stevia rebaudiana Nutrition 0.000 description 1
- UEDUENGHJMELGK-HYDKPPNVSA-N Stevioside Chemical compound O([C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@H]1O[C@]12C(=C)C[C@@]3(C1)CC[C@@H]1[C@@](C)(CCC[C@]1([C@@H]3CC2)C)C(=O)O[C@H]1[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O1)O)[C@@H]1O[C@H](CO)[C@@H](O)[C@H](O)[C@H]1O UEDUENGHJMELGK-HYDKPPNVSA-N 0.000 description 1
- LEHOTFFKMJEONL-UHFFFAOYSA-N Uric Acid Chemical compound N1C(=O)NC(=O)C2=C1NC(=O)N2 LEHOTFFKMJEONL-UHFFFAOYSA-N 0.000 description 1
- TVWHNULVHGKJHS-UHFFFAOYSA-N Uric acid Natural products N1C(=O)NC(=O)C2NC(=O)NC21 TVWHNULVHGKJHS-UHFFFAOYSA-N 0.000 description 1
- 240000001717 Vaccinium macrocarpon Species 0.000 description 1
- 235000012545 Vaccinium macrocarpon Nutrition 0.000 description 1
- 235000002118 Vaccinium oxycoccus Nutrition 0.000 description 1
- 239000006096 absorbing agent Substances 0.000 description 1
- 239000000205 acacia gum Substances 0.000 description 1
- 235000010489 acacia gum Nutrition 0.000 description 1
- 239000000619 acesulfame-K Substances 0.000 description 1
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 238000013019 agitation Methods 0.000 description 1
- AEMOLEFTQBMNLQ-WAXACMCWSA-N alpha-D-glucuronic acid Chemical compound O[C@H]1O[C@H](C(O)=O)[C@@H](O)[C@H](O)[C@H]1O AEMOLEFTQBMNLQ-WAXACMCWSA-N 0.000 description 1
- 150000001413 amino acids Chemical class 0.000 description 1
- 230000003110 anti-inflammatory effect Effects 0.000 description 1
- 235000015197 apple juice Nutrition 0.000 description 1
- IAOZJIPTCAWIRG-QWRGUYRKSA-N aspartame Chemical compound OC(=O)C[C@H](N)C(=O)N[C@H](C(=O)OC)CC1=CC=CC=C1 IAOZJIPTCAWIRG-QWRGUYRKSA-N 0.000 description 1
- 239000000605 aspartame Substances 0.000 description 1
- 229960003438 aspartame Drugs 0.000 description 1
- 235000010357 aspartame Nutrition 0.000 description 1
- 239000002585 base Substances 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- 239000003613 bile acid Substances 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 230000036772 blood pressure Effects 0.000 description 1
- 230000003177 cardiotonic effect Effects 0.000 description 1
- 229940071162 caseinate Drugs 0.000 description 1
- 230000007248 cellular mechanism Effects 0.000 description 1
- 229960000541 cetyl alcohol Drugs 0.000 description 1
- HVYWMOMLDIMFJA-DPAQBDIFSA-N cholesterol Chemical compound C1C=C2C[C@@H](O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCCC(C)C)[C@@]1(C)CC2 HVYWMOMLDIMFJA-DPAQBDIFSA-N 0.000 description 1
- 229960004106 citric acid Drugs 0.000 description 1
- 229940110456 cocoa butter Drugs 0.000 description 1
- 235000019868 cocoa butter Nutrition 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 239000012141 concentrate Substances 0.000 description 1
- 238000010276 construction Methods 0.000 description 1
- 235000004634 cranberry Nutrition 0.000 description 1
- 230000001351 cycling effect Effects 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 235000020930 dietary requirements Nutrition 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 150000002016 disaccharides Chemical class 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 230000004064 dysfunction Effects 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 235000015897 energy drink Nutrition 0.000 description 1
- 230000002708 enhancing effect Effects 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- 238000009207 exercise therapy Methods 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 239000010408 film Substances 0.000 description 1
- 235000014106 fortified food Nutrition 0.000 description 1
- 238000007710 freezing Methods 0.000 description 1
- 230000008014 freezing Effects 0.000 description 1
- 235000015270 fruit-flavoured drink Nutrition 0.000 description 1
- 230000002496 gastric effect Effects 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 239000012213 gelatinous substance Substances 0.000 description 1
- 239000003349 gelling agent Substances 0.000 description 1
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 1
- 235000019674 grape juice Nutrition 0.000 description 1
- 235000015201 grapefruit juice Nutrition 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 239000000416 hydrocolloid Substances 0.000 description 1
- 230000036543 hypotension Effects 0.000 description 1
- 210000000987 immune system Anatomy 0.000 description 1
- 230000000415 inactivating effect Effects 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 239000002075 main ingredient Substances 0.000 description 1
- 235000001035 marshmallow Nutrition 0.000 description 1
- 230000000813 microbial effect Effects 0.000 description 1
- 210000003205 muscle Anatomy 0.000 description 1
- 229950006780 n-acetylglucosamine Drugs 0.000 description 1
- 235000015097 nutrients Nutrition 0.000 description 1
- 238000011903 nutritional therapy Methods 0.000 description 1
- 235000020824 obesity Nutrition 0.000 description 1
- 235000015205 orange juice Nutrition 0.000 description 1
- 230000008520 organization Effects 0.000 description 1
- 238000012856 packing Methods 0.000 description 1
- 210000000496 pancreas Anatomy 0.000 description 1
- 235000013944 peach juice Nutrition 0.000 description 1
- 235000021400 peanut butter Nutrition 0.000 description 1
- 239000001814 pectin Substances 0.000 description 1
- 235000010987 pectin Nutrition 0.000 description 1
- 229920001277 pectin Polymers 0.000 description 1
- 230000002335 preservative effect Effects 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 210000002966 serum Anatomy 0.000 description 1
- 230000035939 shock Effects 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 229940013618 stevioside Drugs 0.000 description 1
- OHHNJQXIOPOJSC-UHFFFAOYSA-N stevioside Natural products CC1(CCCC2(C)C3(C)CCC4(CC3(CCC12C)CC4=C)OC5OC(CO)C(O)C(O)C5OC6OC(CO)C(O)C(O)C6O)C(=O)OC7OC(CO)C(O)C(O)C7O OHHNJQXIOPOJSC-UHFFFAOYSA-N 0.000 description 1
- 235000019202 steviosides Nutrition 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 235000021092 sugar substitutes Nutrition 0.000 description 1
- 239000002562 thickening agent Substances 0.000 description 1
- 230000032258 transport Effects 0.000 description 1
- UFTFJSFQGQCHQW-UHFFFAOYSA-N triformin Chemical compound O=COCC(OC=O)COC=O UFTFJSFQGQCHQW-UHFFFAOYSA-N 0.000 description 1
- 229940116269 uric acid Drugs 0.000 description 1
- 235000012773 waffles Nutrition 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L2/00—Non-alcoholic beverages; Dry compositions or concentrates therefor; Their preparation
- A23L2/02—Non-alcoholic beverages; Dry compositions or concentrates therefor; Their preparation containing fruit or vegetable juices
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L2/00—Non-alcoholic beverages; Dry compositions or concentrates therefor; Their preparation
- A23L2/52—Adding ingredients
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L33/00—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof
- A23L33/10—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof using additives
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L33/00—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof
- A23L33/10—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof using additives
- A23L33/115—Fatty acids or derivatives thereof; Fats or oils
- A23L33/12—Fatty acids or derivatives thereof
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L7/00—Cereal-derived products; Malt products; Preparation or treatment thereof
- A23L7/10—Cereal-derived products
- A23L7/101—Addition of antibiotics, vitamins, amino-acids, or minerals
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L7/00—Cereal-derived products; Malt products; Preparation or treatment thereof
- A23L7/10—Cereal-derived products
- A23L7/117—Flakes or other shapes of ready-to-eat type; Semi-finished or partly-finished products therefor
- A23L7/122—Coated, filled, multilayered or hollow ready-to-eat cereals
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L7/00—Cereal-derived products; Malt products; Preparation or treatment thereof
- A23L7/10—Cereal-derived products
- A23L7/117—Flakes or other shapes of ready-to-eat type; Semi-finished or partly-finished products therefor
- A23L7/126—Snacks or the like obtained by binding, shaping or compacting together cereal grains or cereal pieces, e.g. cereal bars
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/715—Polysaccharides, i.e. having more than five saccharide radicals attached to each other by glycosidic linkages; Derivatives thereof, e.g. ethers, esters
- A61K31/726—Glycosaminoglycans, i.e. mucopolysaccharides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/715—Polysaccharides, i.e. having more than five saccharide radicals attached to each other by glycosidic linkages; Derivatives thereof, e.g. ethers, esters
- A61K31/726—Glycosaminoglycans, i.e. mucopolysaccharides
- A61K31/728—Hyaluronic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/715—Polysaccharides, i.e. having more than five saccharide radicals attached to each other by glycosidic linkages; Derivatives thereof, e.g. ethers, esters
- A61K31/737—Sulfated polysaccharides, e.g. chondroitin sulfate, dermatan sulfate
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/02—Nutrients, e.g. vitamins, minerals
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23V—INDEXING SCHEME RELATING TO FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES AND LACTIC OR PROPIONIC ACID BACTERIA USED IN FOODSTUFFS OR FOOD PREPARATION
- A23V2002/00—Food compositions, function of food ingredients or processes for food or foodstuffs
Description
- Die vorliegende Erfindung bezieht sich auf Getränkeergänzungsmittel, wie beispielsweise Getränke, die mit einem oder mehreren Knorpelergänzungsmitteln angereichert sind.
- Hintergrund
- Nährstoffriegel und Energiedrinks sind praktische Nährstoffergänzungsmittel, speziell für die Personen, die zu beschäftigt sind, regelmäßige Mahlzeiten einzunehmen, und für Wanderer, Radfahrer, Läufer oder andere Athleten, die abgepackte, fertige, energiereiche Snacks benötigen, während sie trainieren. Diese Riegel und Getränke sind ebenso geeignete Nährstoffergänzungsmittel für die Älteren, die abgepackte, fertige Snacks benötigen. Außerdem können diese Nahrungsergänzungsmittel die Verbraucher mit den notwendigen Vitaminen und Mineralien versorgen, die in der empfohlenen Tagesmenge, empfohlen von der US-Regierung, spezifiziert sind.
- Beispielsweise offenbart US-Patent Nr. 4,543,262 einen proteinreichen, laktosearmen oder -freien, Vitamin- und Mineral-angereicherten, nährstoffausgeglichenen Snackriegel. Außerdem lehrt US-Patent Nr. 3,814,819 einen Protein-angereicherten Nahrungsriegel, bestehend aus mehreren knusprig gebackenen Waffeln, die übereinander liegen, mit einer cremigen Füllung dazwischen. Die cremige Füllung enthält zusätzliche Vitamine, die fünfundzwanzig Prozent (25%) der empfohlenen Tagesmenge an Vitaminen und Mineralien bereitstellt. US-Patent Nr. 4,152,462 lehrt einen nährstoffreichen Protein- und Vitamin-angereicherten Nahrungsriegel mit Marshmallow-Grundlage. Schließlich offenbart US-Patent Nr. 3,901,799 einen proteinreichen Schokoladenriegel. Caseinat und Erdnußbutter werden zu einem Gemisch aus Schokolade und Kakaobutter zugegeben. Vitamine, die mit den Inhaltsstoffen kompatibel sind, können, wie offenbart, zu dem Snackriegel zugegeben werden.
- Getränkeformulierungen und Verfahren zu deren Herstellung sind ebenso entwickelt worden. Es sind Energie steigernde Getränke und Verfahren entwickelt worden, wie beispielsweise in US-Patent Nr. 3,894,148 offenbart, die sich auf Ernährungs- und Bewegungstherapien zur Maximierung der Speicherung von Glykogen im Muskelgewebe beziehen. Proteinanreicherungsgetränke sind in US-Patent Nr. 4,309,417 beschrieben worden. Kohlenhydrat- und Elektrolytgetränke sind in US-Patent Nr. 4,312,856 und 4,322,407 beschrieben worden. Die Patentzusammenfassung von
JP 11092385 JP 62224268 DE 203387 offenbart eine Zusammensetzung, umfassend Glucosaminhydrochlorid. - Seit langem ist bekannt, daß Nahrungsknorpelergänzungsmittel die Symptome von Gelenkschmerzen effektiv verringern. (Drovani, Clinical Therapeutics, (1980)). Ein Aminosäurekomplex, der Glutamin mit Glucosaminsulfat kombiniert, ist der Bestandteil, der vom Körper zum Aufbau von Knorpel- und Bindegewebe genutzt wird, die die Gelenke im Körper polstern und schmieren. Bisher sind über 6.000 Patienten in 20 klinischen Versuchen untersucht worden. Diese Studien sind alle zu dem Schluß gekommen, daß Glucosaminsulfatergänzungen Schmerz lindern und die Heilung bei Osteoarthritispatienten stimulieren. Tatsächlich hat die World Health Organization Glucosaminsulfat offiziell als ein langsam wirkendes Arzneimittel zur Behandlung von Osteoarthritis klassifiziert. Typischerweise wird Glucosaminsulfat in Form einer Pille oder eines Pulvers eingenommen.
- Chondroitinsulfat ist eine andere Verbindung, die verbreitet als ein Mittel zur Behandlung der Symptome für Gelenkschmerzen verkauft wird. In zwei Studien ist jedoch herausgefunden worden, daß seine Heilungseigenschaften als ein Nahrungsergänzungsmittel geringer sind als die Heilungseigenschaften von Glucosaminsulfat. Chondroitinsulfat wird auch in Form einer Pille oder eines Pulvers eingenommen.
- Hyaluronsäure ist ein Polysaccharid, das eine Hauptkomponente der gelartigen Substanz bildet, die im Bindegewebe von Säugetieren zu finden ist. Hinsichtlich der Struktur besteht es aus einem sich wiederholenden Disaccharid, bestehend aus N-Acetyl-D-glucosamin und D-Glucuronsäure. Funktionell betrachtet dient es als ein Schmiermittel und Stoßdämpfer in Säugergelenken. Hyaluronsäure wird auch in Form einer Pille oder eines Pulvers eingenommen und soll zur Behandlung von Gelenkschmerzen wirksam sein.
- Cetylmyristoleat (CM) ist ein neu anerkanntes Mittel, das potentiell zur Behandlung von Gelenkschmerzen nützlich ist. CM ist ein Ester einer Fettsäure, die Bausteine von Fetten und Ölen. CM wird durch die Vereinigung der Fettsäure Myristolsäure mit Cetylalkohol, einem langkettigen Alkohol, hergestellt. CM scheint im Körper auf drei Wegen zu fungieren. Erstens zeigt es eine entzündungshemmende Wirkung. Zweitens scheint es als ein Schmiermittel für die Gelenke zu agieren. Drittens fungiert CM als ein Immunsystemmodulator.
- Doktoren berichteten über signifikante Verbesserungen bei Patienten mit Osteoarthritis, die CM einnahmen. 1996 zeigten in einer einmonatigen klinischen Multi-Center-Studie, die 431 Patienten mit unterschiedlichen Formen von Arthritis umfaßte, dreiundsechzig Prozent (63%) derer, die CM einnahmen, eine Verbesserung, im vergleich zu vierzehn Prozent (14%) bei der Kontrollgruppe. CM wird typischerweise oral in Form eines Öls eingenommen.
- Konjac-Pulver ist ein löslicher Ballaststoff, der hinsichtlich der Struktur und der Funktion Pektin ähnelt und typischerweise als ein Verdickungsmittel, Emulgator, Geliermittel, Filmbildner und Stabilisator verwendet wird. Glucomannan, der Hauptbestandteil von Konjac-Pulver, ist ein leicht verzweigtes hydrokolloides Polysaccharid mit B1–4-verknüpften Untereinheiten von Glucose und Mannose und einem Molekulargewicht im Bereich von 200.000 bis 2.000.000 Dalton. Acetylgruppen, die alle 9–19 Untereinheiten entlang der Glucomannanhauptkette angeordnet sind, sind bei der Auflösung des Moleküls behilflich. Neben einem Nahrungsmittel ist Glucomannan an Menschen prinzipiell als ein Mittel zur Senkung des Serumcholesterins, des Gallen säureniveaus und des Serumtriglycerids getestet worden. Die Studien zeigten, daß Glucomannan die Glucosetoleranz und die Glucoseabsorption beeinträchtigen kann.
- Stevia (Stevia rebaudiana bectoni) ist eine natürliche, nicht kalorische süß schmekkende Pflanze, die typischerweise in medizinischen Anwendungen zur Inhibierung der Fettabsorption und zur Senkung des Blutdruckes sowie in der Lebensmittelindustrie als ein Süßstoff verwendet wird. Steviosid ist die Komponente von Stevia, die der Pflanze ihre Süße verleiht. Als ein Zuckerersatz ist es als konzentrierte Flüssigkeit, zerstoßene Blätter oder konzentriertes weißes Pulver erhältlich. Menschen, die keine Zucker oder andere Süßungsmittel vertragen, verwenden oftmals Stevia. Medizinisch betrachtet, zeigen Studien, daß Stevia bei der Regulierung der Pankreas behilflich ist und die Blutzuckerniveaus im Körper stabilisieren kann. Stevia gibt ebenso Anzeichen als ein Kardiotonikum, für Fettleibigkeit, zur Verringerung der Magenazidität, zur Verringerung von Gas, für Hypotonie und zur Verringerung der Urinsäureniveaus. Die Forschung hat ebenso ergeben, daß Stevia zur Verringerung von Bakterien beitragen kann.
- Während Kohlenhydrate, Proteine und Fette in der menschlichen Nahrung alle wichtig sind, sind Kohlenhydrate für ein athletisches Leistungsvermögen besonders wichtig. Kohlenhydrate sind eine allgemein bekannte Energiequelle, die vom Körper ohne weiteres absorbiert wird. Beispielsweise „speichern" Marathonläufer und andere Athleten typischerweise einen Tag vor dem Rennen Kohlenhydrate, indem sie große Mengen an Kohlenhydraten zu sich nehmen. Überdies benötigen Athleten bei Ausdauerwettbewerben eine Energiequelle, die vom Körper schnell absorbiert wird, um die kleiner werdenden Glucose- und Glycogenlager, die während des Wettbewerbs auftreten, zu ersetzen. Letztlich konsumieren Athleten typischerweise große Mengen an Kohlenhydraten unmittelbar nach einem Rennen, um die Glycogenniveaus, die durch das Ereignis abgereichert wurden, aufzufüllen. Somit ist die durch Kohlenhydrate bereitgestellte Energiequelle für Athleten vor, während und nach dem Rennen wichtig.
- Typischerweise liegen Kohlenhydrate zwischen komplexen Kohlenhydraten und einfachen Zuckern. Strukturell gesehen unterscheiden sich diese Kohlenhydrate in der Anzahl an Zuckern in dem Molekül und dem Verzweigungsgrad. Funktionell betrachtet unterscheiden sie sich dahingehend, wie schnell der Körper sie absorbieren und verarbeiten kann, um Energie daraus zu ziehen. Daher kann das richtige Verhältnis der unterschiedlichen Arten von Kohlenhydraten für Kurzzeit-, Mittelzeit- und Langzeit-Energieversorgung für den Körper sorgen.
- Während athletischer Wettbewerbe, insbesondere Ausdauerwettbeweben wie Marathonläufen, Triathalons und Langstreckenradfahren, können Athleten viele, wenn nicht sogar alle ihrer Glycogenreserven aufbrauchen. Daher ist es wichtig, daß Athleten ihre verbrauchten Glycogenreserven aus einer Kohlenhydratquelle auffüllen. Typischerweise ist der Zellmechanismus, der zur Umwandlung von Glucose zu Glycogen verwendet wird, in den Stunden unmittelbar nach dem athletischen Wettbewerb, der sogenannten Erholungsdauer, am effektivsten. Neben der Ausschöpfung ihrer Glycogenreserven können Athleten ihren Körpergelenken vorrübergehende und manchmal dauerhafte Schäden zufügen. Typischerweise wird diese Schädigung als schmerzende und steife Gelenke wahrgenommen. In einigen Formen liefert die vorliegende Erfindung eine qualitative Kohlenhydratquelle, die während der Erholungsdauer wichtig ist. Die Erfindung liefert außerdem Ergänzungen für die Kohlenhydratquelle. Gemäß der Erfindung umfassen diese Ergänzungen eines oder mehrere Knorpelergänzungsmittel, das/die ebenso zur Genesung beiträgt/beitragen, indem es Gelenkschmerzen und -steifheit verringert, und/oder Konjac-Pulver- und/oder Stevia-Ergänzungsmittel. Die Ergänzungsmittel werden allein oder in Kombination mit CM bereitgestellt.
- Ein anderes Ziel der Erfindung ist die Bereitstellung einer Formel für ein Getränk, umfassend eines oder mehrere Knorpelergänzungsmittel, die die Knorpeldysfunktion ansprechen. Ein weiteres Ziel der Erfindung ist die Bereitstellung eines Getränks, daß eine Quelle für qualitative Kohlenhydrate und eines oder mehrer Knorpelergänzungsmittel ist.
- Noch ein anderes Ziel der Erfindung ist die Bereitstellung eines Verfahrens zur Herstellung eines Getränks, enthaltend eines oder mehrere Knorpelergänzungsmittel.
- Zusammenfassung der Erfindung
- Die vorliegende Erfindung liefert ein Getränk zum menschlichen Verzehr gemäß dem Verfahren von Anspruch 1, wobei die in den Ansprüchen 2–16 definierten Merkmale bevorzugt sind.
- Ein Aspekt der Erfindung liefert ein Verfahren zur Herstellung eines Getränks zum menschlichen Verzehr, umfassend die Schritte des Bereitstellens einer Trinkgrundlage, wobei die Trinkgrundlage eine Lösung auf Wasser-Basis ist, umfassend eine Trinklösung mit Fruchtaroma, hergestellt unter Verwendung eines Pasteurisierungsverfahrens bei einer relativ hohen Temperatur; des Bereitstellens einer Knorpelergänzungsmittel-Lösung auf Wasser-Basis, umfassend ein Knorpel-Ergänzungsmittel, wobei die Knorpelergänzungsmittel-Lösung bei einer relativ niedrigen Temperatur in einem Bereich, der die Inaktivierung des Knorpelergänzungsmittels minimiert, hergestellt worden ist; und Bilden eines Gemisches durch Mischen der Gelenktrinkgrundlage und der Knorpelergänzungsmittel-Lösung.
- In einem bevorzugten Verfahren zur Herstellung der Getränke einer Ausführungsform der Erfindung wird ein „Kaltmisch"-Verfahren verwendet. Gemäß diesem Verfahren ist die Safttrinkgrundlage in einer der oben genannten bevorzugten Formen, am stärksten bevorzugt ein Saft mit Fruchtaroma. Die Safttrinkgrundlage kann alternativ aber auch Wasser ohne Aroma sein.
- Ein Getränkt zum menschlichen oder tierischen Verzehr wird aus einem Gemisch aus einer Safttrinkgrundlage und einer Knorpelergänzungsmittel-enthaltenden Lösung hergestellt. Die Safttrinkgrundlage ist eine Lösung auf Wasser-Basis und bevorzugt ein aromatisierter (und am stärksten bevorzugt mit natürlichem oder künstlichem Fruchtaroma) Saft. In einer Ausführungsform wird die Safttrinkgrundlage unter Verwendung eines Pasteurisierungsverfahrens bei einer relativ hohen Temperatur hergestellt. Die hohe Temperatur ist natürlich oder künstlich zur Tötung von Bakterien ausreichend. Die Knorpelergänzungsmittel-enthaltende Lösung ist eine Lösung auf Wasser-Basis, die ein oder mehrere Knorpelergänzungsmittel (wie Glucosamin, Chondroitin, Hyalauronsäure oder Gemische davon) umfaßt, hergestellt bei einer relativ niedrigen Temperatur. Die niedrige Temperatur liegt in einem Bereich, der die Inaktivierung des Knorpelergänzungsmittels minimiert. Das Getränk kann karbonisiert oder nicht karbonisiert sein, ferner kann das Getränk in konzentrierter Form zur späteren Verdünnung durch den Verbraucher oder trinkfertig vorliegen.
- Ausführliche Beschreibung der bevorzugten Ausführungsformen
- In einer anderen bevorzugten Ausführungsform werden die Knorpelergänzungsmittel, entweder allein oder Kombination mit dem CM, in Form eines Getränks geliefert. Anhand eines nicht einschränkenden Beispiels umfassen Getränke, die zur Verwendung in der vorliegenden Erfindung geeignet sind, Wasser oder Fruchtsäfte wie Apfelsaft, Orangensaft, Grapefruitsaft, Preiselbeersaft, Pfirsichsaft, Traubensaft und Gemische davon. Andere Getränke, die zur Verwendung in der vorliegenden Erfindung geeignet sind, umfassen kommerziell erhältlich Sportdrinks wie GATORADETM- und POWERADETM-Getränke. Im allgemeinen liefern diese Sportdrinks Kalorien im wesentlichen nur in Form von Kohlenhydraten und liefern Elektrolytersatzmittel, die zur Erholung nach dem Training beitragen sollen. Letztlich sind kommerziell erhältliche nutritiv ausgeglichene Getränke, wie zum Beispiel ENSURETM-Getränke, zur Verwendung in der vorliegenden Erfindung geeignet. Diese nutritiv ausgeglichenen Getränke versorgen den Verbraucher im allgemeinen mit Kohlenhydraten, Proteinen, Fett, Vitaminen und Mineralien und dienen oftmals als Mahlzeitenersatz.
- Gemäß der Erfindung sind alle drei Knorpelergänzungsmittel, entweder allein oder in Kombination, in Getränken wie den oben angegebenen Getränken vorhanden. Für den Fall das CM enthalten ist, muß jedoch angemerkt werden, daß CM eine ölige Substanz ist und daher mit den wasserbasierenden Getränken wahrscheinlich nicht ohne weiters mischbar ist. Wenn demgemäß CM einem Getränkt gemäß der vorliegenden Erfindung zugegeben wird, wird es zunächst emulgiert. Emulgatoren und Verfahren, die einem Fachmann bekannt sind, sind zur Verwendung in der vorliegenden Erfindung geeignet. Der ausgewählte Emulgator ist für den menschlichen Verzehr geeignet. Geeignete Emulgatoren umfassen Gummiarabikum und Gelatine. Die Emulsionen werden durch das Schütteln zweier Flüssigkeiten oder durch Zugabe einer Phase tropfenweise zu der anderen unter etwas Bewegung wie Bestrahlung mit Ultraschallwellen mit hoher Intensität hergestellt.
- In einem bevorzugten Verfahren werden die gemäß der vorliegenden Erfindung hergestellten Getränke zur Verbesserung des Knorpelzustandes unter Verwendung eines Mehrschrittverfahrens hergestellt. Im ersten Schritt wird eine Safttrinkgrundlage hergestellt. Wasser, Aromastoffe und Konservierungsmittel werden in vorbestimmten Mengen miteinander vermischt. Die Lösung wird wärmepasteurisiert und auf Umgebungstemperatur abgekühlt. Die Saftgrundlage kann zur späteren Verwendung hergestellt und gelagert werden oder unmittelbar bei der Produktion der endgültigen Getränkeprodukte verwendet werden.
- Im zweiten Schritt wird eine zweite Lösung aus „Knorpelergänzungsmittel-Lösung", die das Knorpelergänzungsmittel, und wenn und falls gewünscht, zusätzliche Aromastoffe und Kohlenhydrate enthält, bei Temperaturen unten denen, die in dem Wärmepasteurisierungsverfahren verwendet wurden, bevorzugt, aber nicht notwendigerweise bei Umgebungstemperaturen oder niedriger, hergestellt. Im dritten Schritt wird eine Trinkgrundlage mit der Knorpelergänzungsmittel-Lösung bei Umgebungstemperaturen kombiniert. Die kombinierte Lösung wird hinsichtlich der Azidität eingestellt und bevorzugt, aber nicht notwendigerweise, auf Temperaturen unter Umgebung und über dem Gefrierpunkt abgekühlt und karbonisiert. Das Mehrschrittverfahren stellt sicher, daß das Knorpelergänzungsmittel durch die Herstellung und/oder das Flaschenabfüllverfahren nicht beeinträchtigt wird. Als Alternative können der zweite und dritte Schritt kombiniert werden, wobei die Inhaltsstoffe für die Knorpelergänzungsmittel-Lösung direkt zu der Safttrinkgrundlage zugegeben werden, ihr pH eingestellt wird und sie, je nach Bedarf, karbonisiert werden. Der kombinierte zweite und dritte Schritt werden bevorzugt, aber nicht notwendigerweise bei Temperaturen unter denen, die in einem Wärmepasteurisierungsverfahren verwendet werden, durchgeführt.
- In einer anderen Ausführungsform wird ein Getränkekonzentrat hergestellt. Die Saftgrundlage, das Süßungsmittel, Wasser, Konservierungsmittel und gegebenenfalls Vitamine und/oder Mineralien werden in einem Mischtank gemischt und pasteurisiert. Das resultierende Produkt wird durch Transferleitungen aus dem Mischtank zum Verpacken überführt. Das Produkt kühlt in den Transferleitungen ab, wenn es von dem Mischtank zum Verpacken fließt. Die Temperatur des Produkts wird abgesenkt, indem es während des Fließens durch die Transferleitungen strahlungsgekühlt wird, oder gegebenenfalls die Leitungen gekühlt werden.
- Bevorzugt wird die Knorpelergänzungsmittel-Lösung an einem Punkt in den Transferleitungen, bevorzugt mit einem gewissen Abstand zum Mischtank, wo die Temperatur der fließenden Flüssigkeit niedriger ist als die Temperatur in dem Mischtank, in den flüssigen Strom eingeführt. So kann die Knorpel-Lösung bei Temperaturen unter der Pasteurisierungstemperatur und wenn die Getränkelösung während des Transportes kontinuierlich abgekühlt wird in das Produkt gemischt werden. Beim Verpakken werden die Behälter verschlossen und mit kaltem Wasser besprüht oder übergossen, um die Temperatur des Endproduktes auf ungefähr Umgebungstemperatur abzusenken.
- In dieser Ausführungsform ist die Gesamtverweilzeit der Knorpellösung bei erhöhten Temperaturen minimal, wodurch jegliche Wärmeinaktivierung des Knorpelergänzungsmittels minimiert wird. Beispielsweise kann die Produkttemperatur im Mischtank nahe 90,5°C (195°F) liegen. Da die Flüssigkeit in den Transferleitungen fortschreitet, kann der Punkt, bei dem Glucosamin zugegeben wird, 65,5°C (150°F) oder weniger betragen. Wenn die Lösung zum Verpacken überführt wird, wird sie kontinuierlich abgekühlt, so daß die Lösungstemperatur zum Zeitpunkt des Verpakkens ungefähr 37,8°C (100°F) bis 26,7°C (80°F) beträgt. Nach dem Verpacken wird das Endprodukt auf Umgebungstemperatur abgekühlt. Somit kann in diesem Beispiel die Gesamtverweilzeit von Glucosamin nahe den Pasteurisierungstemperaturen nur etwa 30 Sekunden betragen, während es kontinuierlich gekühlt wird.
- Das Wärmepasteurisierungsverfahren für die Saftgrundlage hängt sowohl von der eingesetzten Temperatur als auch der Verweilzeit der Lösung bei dieser Temperatur ab. Im allgemeinen, und in einem gewissen Bereich, gilt, je geringer die verwendete Temperatur, um so länger sollte die Lösung verarbeitet werden, um eine adäquate mikrobielle Kontrolle sicherstellen zu können. Die Pasteurisierungsparameter können von niedrig bei etwa 73,9°C (165°F) für 3 Minuten bis etwa 93,3°C (200°F) für weniger als 40 Sekunden reichen. Die bevorzugten Parameter sind 90,5 ± 2°C (195 ± 4°F) für 42 ± 4 Sekunden.
- In einer noch anderen Ausführungsform kann das Knorpelergänzungsmittel dem Mischtank mit der Saftgrundlage und anderen Bestandteilen zugegeben werden, und das Produkt kann unter Verwendung von Pasteurisierungsverfahren, die keine Wärmeverarbeitung umfassen, wie zum Beispiel, aber nicht beschränkt auf, Filtersterilisation oder Strahlungssterilisation, pasteurisiert werden.
- Die Saftgrundlagen, das vorkarbonisierte Produkt und konzentrierte Getränkelösungen werden hinsichtlich des Brix (ein Maß für lösliche Feststoffe) und des titrierbaren Säuregrads (TA) gemessen und unter Verwendung von Wasser bzw. Zitronensäure wie erforderlich eingestellt. Das vorkarbonisierte trinkfertige Produkt und das konzentrierte Getränkeprodukt werden kurz vor der Karbonisierung bzw. der Verpackung auch hinsichtlich des pHs eingestellt.
- Die durch diese verschiedenen Ausführungsformen hergestellten Getränke, umfassen, sind aber nicht beschränkt auf trinkfertige karbonisierte Getränke, trinkfertige nicht karbonisierte Getränke und konzentrierte Getränkemischungen, das heißt, Mischungen, die vom Verbraucher auf eine trinkbare Konzentration (mit Wasser, Saft, karbonisiertem Wasser und dergleichen) verdünnt werden.
- Beispiel 1
- Das Getränk der vorliegenden Erfindung, das Knorpelergänzungsmittel enthält, wurde folgendermaßen hergestellt:
Zunächst wurde ein Volumen an GATORADE in einem konventionellen Flüssigkeitsmischer aliquotiert. Hyaluronsäure und/oder Glucosaminsulfat und/oder Chondroitinsulfat wurden als nächstes zu der Lösung auf eine Endkonzentration von vier Prozent (4%) (Gewicht zu Volumen) von jeder Komponente zugegeben. Die Lösung wurde dann gemischt, bis die hinzugefügten Inhaltsstoffe löslich gemacht waren. Die Lösung wurde dann aseptisch in einzelne abnehmerfreundliche Flaschen von ungefähr fünfhundert Milliliter (500 ml) gefüllt. - Beispiel 2
- Das Getränk der vorliegenden Erfindung, das Knorpelergänzungsmittel und CM enthält, wurde folgendermaßen hergestellt:
Zunächst wurde CM mit irgendeinem bekannten Emulgator, der für den menschlichen Verzehr geeignet ist, emulgiert. Dann wurde ein Volumen an ENSURE in einem konventionellen Flüssigkeitsmischer aliquotiert. Das emulgierte CM wurde auf eine Endkonzentration von zwei Prozent (2%) (Volumen zu Volumen) zugegeben. Dann wurden Hyaluronsäure, Glucosaminsulfat und Chondroitinsulfat zu der Lösung auf eine Endkonzentration von vier Prozent (4%) (Gewicht zu Volumen) zugegeben. Die Lösung wurde gemischt, bis die hinzugefügten Knorpelergänzungsmittel löslich gemacht waren. Die Lösung wurde dann aseptisch in einzelne abnehmerfreundliche Flaschen von ungefähr fünfhundert Milliliter (500 ml) gefüllt. - Beispiele 3 bis 5
- Herstellung der Safttrinkgrundlage
- Safttrinkgrundlage-Lösungen, enthaltend die in Tabelle 1 gezeigten Inhaltsstoffe und Anteile, wurden hergestellt und zur späteren Verwendung bei der Formulierung der fertigen Getränkeprodukte gelagert.
- Für jedes Aroma wurden die obigen Inhaltsstoffe unter Verwendung von 90% Wasser zusammengemischt. Der Brix, der titrierbare Säuregrad und der pH wurden unter Verwendung der restlichen 10% Wasser eingestellt. Die resultierende Lösung wurde durch Erhitzen der Lösung auf 90,5°C (195°F) und Halten bei dieser Temperatur für ungefähr 40 Sekunden pasteurisiert. Dann wurde die Lösung auf Umgebungstemperatur abgekühlt, um die Herstellung der Trinkgrundlage zu beenden. In diesen Beispielen für die Safttrinkgrundlage wurden die Brixwerte und Werte des titrierbaren Säuregrads auf die in Tabelle 2 gezeigten Bereiche eingestellt. Diese Werte können um etwa ±5 Prozent variieren. Die Saftgrundlage wurde dann zur späteren Verwendung bei der Formulierung der Endprodukte gelagert.
- Beispiele 6 bis 8
- Herstellung von trinkfertigen Getränken:
- Trinkfertige, den Knorpelzustand verbessernde Ergänzungsmittelgetränke wurden bei Umgebungstemperatur unter Verwendung der in Tabelle 3 gezeigten Inhaltsstoffe (und Anteile) hergestellt.
- Anfangs wurde Natriumbenzoat zu 50% des gesamten Wassers zugegeben und bei Umgebungstemperatur gemischt, bis das Natriumbenzoat gelöst war. Diese Lösung wurde unter kontinuierlichem Rühren gehalten. Das Glucosamin-HCl, Zitronensäure, Safttrinkgrundlage und Isomeratzucker wurden jeweils separat zu der Lösung zugegeben und gründlich gemischt. Neunzig Prozent (90%) des restlichen Wassers wurden dann zugegeben und die Lösung wurde für 15 Minuten gemischt. Der Brix, der titrierbare Säuregrad und der pH wurden unter Verwendung des restlichen Wassers und, wenn notwendig, unter Verwendung von zusätzlicher Zitronensäure eingestellt. Die resultierende Lösung wurde dann in einem Portionierer (1 + 4) bei 40°F auf 3,0 Volumen karbonisiert. Das resultierende Getränk war dann für die Abfüllung bereit.
- Die akzeptablen Bereiche für den Brix und den TA in den Getränken vor und nach der Karbonisierung und der pH nach der Karbonisierung werden in Tabelle 4 gezeigt.
- Beispiele 9 bis 11
- Herstellung von zuckerfreien, trinkfertigen Getränken:
- Zuckerfreie (diätische) trinkfertige, den Knorpelzustand verbessernde Ergänzungsmittelgetränke wurden bei Umgebungstemperatur unter Verwendung der in Tabelle 5 gezeigten Inhaltsstoffe (und Anteile) hergestellt.
- Anfangs wurde Natriumbenzoat zu 50% des Gesamtwassers zugegeben und bei Umgebungstemperatur gemischt, bis das Natriumbenzoat gelöst war. Diese Lösung wurde unter kontinuierlichem Rühren gehalten. Das Glucosamin-HCl, Zitronensäure, Aspartam, Acesulfam K und die Saftgrundlage wurden jeweils separat zu der Lösung gegeben und gründlich gemischt. Neunzig Prozent (90%) des restlichen Wassers wurden dann zugegeben und die Lösung wurde für 15 Minuten gemischt. Der Brix, der titrierbare Säuregrad und der pH wurden unter Verwendung des restlichen Wassers und, wenn notwendig, unter Verwendung von zusätzlicher Zitronensäure eingestellt. Die resultierende Lösung wurde dann in einem Portionierer (1 + 4) auf 3,0 Volumen karbonisiert, und der pH weiter eingestellt. Das resultierende Getränk war dann für die Abfüllung bereit.
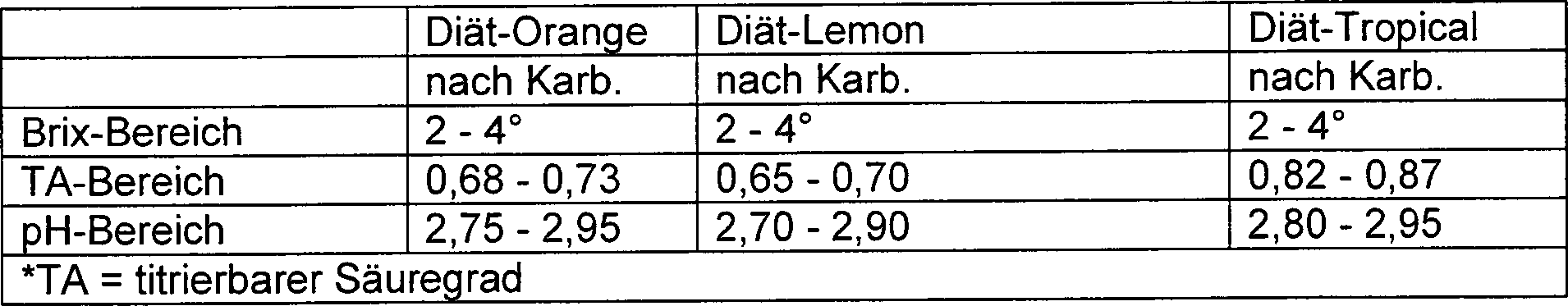
- Der Brix, der TA und der pH der Getränke wurden vor und nach der Karbonisierung gemessen. Tabelle 6 zeigt die akzeptablen Bereiche nach der Karbonisierung.
- Beispiele 12 bis 15
- Herstellung konzentrierter Saftgrundlagen
- Unter Verwendung der in Tabelle 7 gezeigten Inhaltsstoffe (und Anteile) wurden konzentrierte, den Knorpelzustand verbessernde Ergänzungsgetränke hergestellt.
- Herstellung eines konzentrierten Getränks:
- Anfangs wurden 50% des Wassers in den Mischtank gepumpt. Natriumbenzoat wurde zu dem Wasser zugegeben und gründlich gemischt. Zitronensäure, Süßstoffe (Isomeratzucker oder künstliche Süßstoffe) und Saftgrundlage wurden zu der Lösung gegeben und gründlich gemischt. Der Brix und der TA wurden unter Verwendung einer abgemessenen Menge des restlichen Wassers bzw. der Zitronensäure eingestellt. Die konzentrierten Saftgrundlagen wurden bei ungefähr 90,5°C (195°F) für etwa 42 Sekunden wärmepasteurisiert.
- Die Lösung wurde durch Transferleitungen zum Verpacken gepumpt. Glucosamin-HCl (gelöst in einer abgemessenen Menge an Wasser) wurde in den Flüssigkeitsstrom in den Transferleitungen eingeführt. Der Brix, der TA und der pH wurden an dem fertigen Produkt getestet, und die Chargenparameter wurden ungefähr eingestellt, wie in Tabelle 8 gezeigt. Die Verpackungen wurden verschlossen und mit Wasser bei Umgebungstemperatur gespült. Ausbeute: ungefähr 7.060 Zweiunzen-Packungen in Abhängigkeit des Aromas.
Claims (15)
- Verfahren zur Herstellung eines Getränks zum menschlichen Verzehr, umfassend die Schritte: A. das Bereitstellen einer Safttrinkgrundlage, wobei die Safttrinkgrundlage eine Lösung auf Wasser-Basis ist, umfassend einen Fruchtaromasaft, hergestellt unter Verwendung eines Pasteurisierungsverfahrens, bei einer relativ hohen Temperatur von oberhalb 87,8°C (190°F); B. das Bereitstellen einer Knorpelergänzungsmittel-Lösung auf Wasserbasis, umfassend ein Knorpel-Ergänzungsmittel, wobei die Knorpelergänzungsmittel-Lösung bei einer relativ niedrigen Temperatur von unterhalb 71,1°C (160°F) hergestellt worden ist; und C. das Bilden eines Gemisches durch Mischen der Safttrinkgrundlage und der Knorpelergänzungsmittel-Lösung.
- Getränk gemäß Anspruch 1, umfassend den weiteren Schritt D. des Einstellen des pH-Wertes des Gemisches in dem Bereich von 2,2 bis 4,6 nach Schritt C.
- Verfahren gemäß Anspruch 1 oder 2, wobei das Knorpelergänzungsmittel Glucosamin ist.
- Verfahren gemäß Anspruch 3, wobei das Knorpelergänzungsmittel aus Glucosaminsalzen, Glucosaminderivaten und Kombinationen davon, ausgewählt ist.
- Verfahren nach einem der Ansprüche 3 oder 4, wobei das Knorpelergänzungsmittel Glucosamin in Verbindung mit einem Gegenion in Kombination mit einem Knorpelergänzungsmittel, ausgewählt aus der Gruppe, bestehend aus einer Hyaluronsäure, Chondroitin, Chondroitinsulfat und Kombinationen davon, ist.
- Verfahren gemäß Anspruch 1, wobei das Gemisch bei einer Mischungstemperatur von zwischen 4,4°C (40°F) und 71,1°C (160°F) gebildet wird.
- Verfahren gemäß Anspruch 1, wobei der Mischungsschritt bei Raumtemperatur durchgeführt wird.
- Verfahren gemäß Anspruch 1, wobei das Getränk ein kohlensäurehaltiges ist, und die niedrige Temperatur oberhalb etwa 1,7°C (35°F) und unterhalb Raumtemperatur ist.
- Verfahren gemäß einem der Ansprüche 1 bis 8, wobei die Safttrinkgrundlage aus der Gruppe, bestehend aus Wasser, aromatisiertem Wasser, Fruchsaftkonzentrat, Fruchsaft, Fruchtaromasaft und Kombinationen davon, ausgewählt ist.
- Verfahren gemäß einem der Ansprüche 1 bis 9, wobei das Getränk weiter Bestandteile, ausgewählt aus der Gruppe, bestehend aus Proteinen, Fetten, Kohlenhydraten, Vitaminen, Mineralien und Kombinationen davon, einschließt.
- Verfahren gemäß einem der Ansprüche 1 bis 10, wobei das Getränk weiter Bestandteile, ausgewählt aus natürlichen Süßstoffen, künstlichen Süßstoffen, Konservierungsmitteln und Kombinationen davon, einschließt.
- Verfahren gemäß einem der Ansprüche 1 bis 11, wobei die Schritte B und C gleichzeitig durchgeführt werden.
- Verfahren gemäß einem der Ansprüche 1 bis 12, wobei die Schritte B, C und D gleichzeitig durchgeführt werden.
- Verfahren gemäß einem der Ansprüche 1 bis 7 oder 11 bis 13, umfassend den weiteren Schritt des Karbonisierens des Gemisches.
- Verfahren gemäß einem der Ansprüche 1 bis 14, wobei das Getränk zwischen etwa 1% bis etwa 10%, bezogen auf das Gewicht, an Knorpelergänzungsmitteln aufweist.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US09/338,021 US6391864B1 (en) | 1998-08-19 | 1999-06-22 | Food supplement containing a cartilage supplement |
| US338021 | 1999-06-22 | ||
| PCT/US2000/040267 WO2000078320A1 (en) | 1999-06-22 | 2000-06-21 | Cartilage enhancing food supplements and methods of preparing the same |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| DE60029833D1 DE60029833D1 (de) | 2006-09-14 |
| DE60029833T2 true DE60029833T2 (de) | 2007-03-01 |
Family
ID=23323065
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE60029833T Expired - Lifetime DE60029833T2 (de) | 1999-06-22 | 2000-06-21 | Nahrungsmittelergänzungen zur Verbesserung des Knorpelzustandes sowie Herstellungsmethoden |
Country Status (10)
| Country | Link |
|---|---|
| US (2) | US6391864B1 (de) |
| EP (1) | EP1263418B1 (de) |
| JP (1) | JP2003530072A (de) |
| AT (1) | ATE334604T1 (de) |
| AU (1) | AU7132000A (de) |
| CA (1) | CA2377627C (de) |
| DE (1) | DE60029833T2 (de) |
| ES (1) | ES2269175T3 (de) |
| MX (1) | MXPA01013301A (de) |
| WO (1) | WO2000078320A1 (de) |
Families Citing this family (110)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7906153B2 (en) | 1998-04-08 | 2011-03-15 | Theta Biomedical Consulting & Development Co., Inc. | Anti-inflammatory compositions for treating multiple sclerosis |
| US6984667B2 (en) * | 1998-04-08 | 2006-01-10 | Theta Biomedical Consulting And Development Co. | Synergistic proteoglycan compositions for inflammatory conditions |
| US20050220909A1 (en) | 2004-03-30 | 2005-10-06 | Theoharides Theoharis C | Composition for protection against superficial vasodilator flush syndrome |
| US7799766B2 (en) | 1998-04-08 | 2010-09-21 | Theta Biomedical Consulting & Development Co., Inc. | Composition for treating hormonally-dependent cancers |
| US6391864B1 (en) | 1998-08-19 | 2002-05-21 | Joint Juice, Inc. | Food supplement containing a cartilage supplement |
| CA2361268C (en) | 1999-02-01 | 2014-06-10 | Dermal Research Laboratories, Inc. | A pharmaceutical composition of complex carbohydrates and essential oils and methods of using the same |
| US7851458B2 (en) * | 1999-06-22 | 2010-12-14 | Joint Juice, Inc. | Cartilage enhancing food supplements and methods of preparing the same |
| US6677321B1 (en) * | 1999-12-09 | 2004-01-13 | Bruce Levin | Methods and compositions for treatment of inflammatory disease |
| AU2001266648A1 (en) * | 2000-06-02 | 2001-12-17 | The Procter And Gamble Company | Kits and methods for optimizing the efficacy of chondroprotective compositions |
| BR0111292A (pt) * | 2000-06-02 | 2003-06-10 | Procter & Gamble | Composições com baixo teor de carboidrato, kits destas e métodos de uso |
| EP1289384A2 (de) * | 2000-06-02 | 2003-03-12 | The Procter & Gamble Company | Wässrige chondroprotektive zusammensetzungen mit definierter ph-begrenzung zur effizienten abgabe |
| WO2001093832A2 (en) * | 2000-06-02 | 2001-12-13 | The Procter & Gamble Company | Aqueous chondroprotective compositions having defined dosage requirements for efficacious delivery |
| US7879824B2 (en) | 2001-07-31 | 2011-02-01 | Dermal Research Laboratories, Inc. | Methods of preventing or treating diseases and conditions using complex carbohydrates |
| EP1222863A1 (de) * | 2000-12-29 | 2002-07-17 | EnergyBalance AG | Viatmin angereicherte Lebensmittel |
| JP5025045B2 (ja) * | 2001-02-02 | 2012-09-12 | マルホ株式会社 | 多硫酸化多糖類によるtimp産生の亢進 |
| US8222232B2 (en) * | 2001-02-16 | 2012-07-17 | Cargill, Incorporated | Glucosamine and N-acetylglucosamine compositions and methods of making the same fungal biomass |
| US7923437B2 (en) * | 2001-02-16 | 2011-04-12 | Cargill, Incorporated | Water soluble β-glucan, glucosamine, and N-acetylglucosamine compositions and methods for making the same |
| US7816514B2 (en) | 2001-02-16 | 2010-10-19 | Cargill, Incorporated | Glucosamine and method of making glucosamine from microbial biomass |
| US6902739B2 (en) * | 2001-07-23 | 2005-06-07 | Nutracea | Methods for treating joint inflammation, pain, and loss of mobility |
| US20030203072A1 (en) * | 2002-04-26 | 2003-10-30 | Team Nrg, Inc. | Rehydration beverage |
| US20040029774A1 (en) * | 2002-08-06 | 2004-02-12 | Aly Gamay | Composition and methods for the treatment of musculoskeletal disorders and collagen and elastin deficiencies |
| US20040026447A1 (en) * | 2002-08-08 | 2004-02-12 | Jeffrey Badin | Any protein and energy powder supplement cold dispensing coin operated vending machine |
| US6979458B1 (en) * | 2002-09-11 | 2005-12-27 | Kenneth A. Martin | Beverage and additive for wellness |
| CA2408023C (en) * | 2002-10-15 | 2012-01-03 | Purepharm Inc. | Glucosamine as a food and beverage additive |
| US7504387B2 (en) * | 2002-10-16 | 2009-03-17 | Arthrodynamic Technologies, Animal Health Division, Inc. | Glycosaminoglycan composition and method for treatment and prevention of interstitial cystitis |
| US7485629B2 (en) * | 2002-10-16 | 2009-02-03 | Arthrodynamic Technologies, Animal Health Division, Inc. | Composition and method for treatment of joint damage |
| US7803787B2 (en) | 2002-10-16 | 2010-09-28 | Arthrodynamic Technologies, Animal Health Division, Inc. | Composition and method for treating connective tissue damage by transmucosal administration |
| ATE525076T1 (de) * | 2002-10-16 | 2011-10-15 | Arthrodynamic Technologies Animal Health Division Inc | Behandlung von traumatischer synovitis und geschädigtem gelenkknorpel |
| US8455458B2 (en) | 2002-10-16 | 2013-06-04 | Arthrodynamic Technologies, Animal Health Division, Inc. | Composition and method for treating connective tissue damage |
| US20070259094A1 (en) * | 2002-10-21 | 2007-11-08 | Willem Wassenaar | N-acetylglucosamine as a food and beverage additive |
| US20060058263A1 (en) * | 2002-11-01 | 2006-03-16 | Rogers Brent D | Heat pasturized liquids containing glucosamine |
| US20060003965A1 (en) * | 2002-11-01 | 2006-01-05 | Fosdick Lawrence D | N-acetyl-d-glucosamine (nag) supplemented food products and beverages |
| AU2003286807A1 (en) * | 2002-11-01 | 2004-06-07 | Cargill, Incorporated | Multiple component food product useful for delivering glucosamine and/or nacetyl-d-glucosamine |
| JP4143387B2 (ja) * | 2002-11-21 | 2008-09-03 | 株式会社アセロラフーズ | 健康食品 |
| CN1314361C (zh) * | 2003-04-02 | 2007-05-09 | 李安虎 | 一种关节保健饮品或食品及其制备方法 |
| US20040253344A1 (en) * | 2003-04-11 | 2004-12-16 | Novozymes A/S | Dairy product comprising hyaluronic acid |
| WO2004089098A1 (en) * | 2003-04-11 | 2004-10-21 | Novozymes A/S | Dairy product comprising hyaluronic acid |
| US8633247B2 (en) | 2003-08-11 | 2014-01-21 | Hill's Pet Nutrition, Inc. | Method for decreasing cartilage damage in dogs |
| US8633246B2 (en) | 2003-08-11 | 2014-01-21 | Hill's Pet Nutrition, Inc. | Omega-3 fatty acids for osteoarthritis |
| US20050058763A1 (en) | 2003-09-12 | 2005-03-17 | Therese Cetrulo | Reduced sugar citrus juice beverages |
| US20050064068A1 (en) * | 2003-09-24 | 2005-03-24 | Shukla Triveni P. | Emulsified liquid shortening compositions comprising dietary fiber gel, water and lipid |
| CZ13928U1 (cs) * | 2003-10-08 | 2004-01-20 | Cpn Spol. S R.O. | Dietetický přípravek pro prevenci a léčbu osteoporózy |
| JP2005118231A (ja) * | 2003-10-15 | 2005-05-12 | Fu Sheng Industrial Co Ltd | ゴルフクラブヘッドの構造 |
| US20050084588A1 (en) * | 2003-10-20 | 2005-04-21 | Shukla Triveni P. | Snack foods comprising emulsified liquid shortening compositions comprising dietary fiber gel, water and lipid |
| US20050084584A1 (en) * | 2003-10-20 | 2005-04-21 | Shukla Triveni P. | Cookies comprising emulsified liquid shortening compositions comprising dietary fiber gel, water and lipid |
| US20050084585A1 (en) * | 2003-10-20 | 2005-04-21 | Shukla Triveni P. | Breads comprising emulsified liquid shortening compositions comprising dietary fiber gel, water and lipid |
| US20070031569A1 (en) * | 2003-10-20 | 2007-02-08 | Z Trim Holdings, Inc. | Snack foods comprising emulsified liquid shortening compositions |
| US20050113287A1 (en) * | 2003-10-21 | 2005-05-26 | Motion Potion, Inc. | Composition to enhance joint function and repair |
| US20050147715A1 (en) * | 2003-12-17 | 2005-07-07 | Novozymes Biopolymer A/S | Dairy product comprising texturizers |
| CA2547761A1 (en) * | 2003-12-17 | 2005-06-30 | Novozymes Biopolymer A/S | Method for preparing a food product comprising texturizers |
| US20050147732A1 (en) * | 2003-12-17 | 2005-07-07 | Novozymes Biopolymer A/S | Method for preparing a food product comprising texturizers |
| US7923043B2 (en) | 2004-03-30 | 2011-04-12 | Theta Biomedical Consulting & Development Co., Inc. | Method for protecting humans against superficial vasodilator flush syndrome |
| JP4634757B2 (ja) * | 2004-08-11 | 2011-02-16 | 焼津水産化学工業株式会社 | 乳化液状経腸栄養剤 |
| US20060093592A1 (en) * | 2004-10-04 | 2006-05-04 | Nutracea | Synbiotics |
| US7897192B2 (en) * | 2004-10-07 | 2011-03-01 | Next Proteins, Inc. | High energy carbonated protein drink and method of making |
| US7906160B2 (en) * | 2004-10-07 | 2011-03-15 | Next Proteins, Inc. | Protein beverage and method of making the same |
| US7799363B2 (en) * | 2004-10-07 | 2010-09-21 | Next Proteins, Inc. | Protein beverage and protein beverage concentrate and methods of making the same |
| US20080206415A1 (en) * | 2004-10-07 | 2008-08-28 | Next Proteins, Inc. | Protein beverage and method of making the same |
| US7794770B2 (en) * | 2004-10-07 | 2010-09-14 | Next Proteins, Inc. | Protein beverage and method of making the same |
| US20080050498A1 (en) * | 2004-10-07 | 2008-02-28 | Next Proteins, Inc. | Powdered protein beverage mix and methods of making the same |
| US7205018B2 (en) * | 2004-10-07 | 2007-04-17 | Next Proteins, Inc. | Carbonated protein drink and method of making |
| US20110183052A1 (en) * | 2004-10-07 | 2011-07-28 | Next Proteins, Inc. | Protein beverage and method of making the same |
| US9220292B2 (en) | 2004-10-07 | 2015-12-29 | Next Problems, Inc. | Protein beverage and method of making same |
| ZA200704133B (en) * | 2004-11-23 | 2008-09-25 | Alcon Inc | Triple natural polymer viscoelastic composition |
| US20060286223A1 (en) * | 2005-06-15 | 2006-12-21 | Carol Long | Reduced sugar RTE cereals with maltodextrin |
| US20070026112A1 (en) * | 2005-08-01 | 2007-02-01 | Cadbury Adams Usa Llc | Container combining beverage and secondary consumable product |
| US9492381B1 (en) | 2005-11-10 | 2016-11-15 | Reyn Pharma, Llc | Method of administering hyaluronan formulation for preventing and ameliorating osteoarthritis |
| US8598144B1 (en) | 2005-11-10 | 2013-12-03 | Reyn Pharma, Llc | Method of administering hyaluronan formulation for the amelioration of osteoarthritis |
| US8956677B2 (en) | 2005-11-23 | 2015-02-17 | The Coca-Cola Company | High-potency sweetener composition with glucosamine and compositions sweetened therewith |
| JP2007161688A (ja) * | 2005-12-16 | 2007-06-28 | Hiroshima Univ | 軟骨生成促進剤 |
| TW200743492A (en) * | 2006-05-29 | 2007-12-01 | Ching-Chuan Jiang | Hyaluronic acid used for purpose of anti-oxidation and proliferation on cartilage cells |
| JP4712746B2 (ja) * | 2006-09-15 | 2011-06-29 | キユーピー株式会社 | 酸性飲料 |
| US9877500B2 (en) * | 2007-03-14 | 2018-01-30 | Concentrate Manufacturing Company Of Ireland | Natural beverage products |
| US8084073B2 (en) | 2007-03-14 | 2011-12-27 | Concentrate Manufacturing Company Of Ireland | Anisic acid modified steviol glycoside sweetened beverage products |
| US20080226800A1 (en) * | 2007-03-14 | 2008-09-18 | Concentrate Manufacturing Company Of Ireland | Diet cola beverages |
| US20080226803A1 (en) * | 2007-03-14 | 2008-09-18 | Concentrate Manufacturing Company Of Ireland | Natural flavoring agent for sugar-sweetened tea beverage to taste like high fructose corn syrup-sweetened beverage |
| US20080226802A1 (en) * | 2007-03-14 | 2008-09-18 | Concentrate Manufacturing Company Of Ireland | Beverage having natural sweeteners with one or more stevia components and source of berry |
| US20080226789A1 (en) * | 2007-03-14 | 2008-09-18 | Concentrate Manufacturing Company Of Ireland | Beverage products with non-nutritive sweetener and bitterant |
| US20080226799A1 (en) * | 2007-03-14 | 2008-09-18 | Concentrate Manufacturing Company Of Ireland | Diet Cola Beverages |
| US9314048B2 (en) * | 2007-03-14 | 2016-04-19 | The Concentrate Manufacturing Company Of Ireland | Beverage products with non-nutritive sweetener and bitterant |
| US8277861B2 (en) | 2007-03-14 | 2012-10-02 | Concentrate Manufacturing Company Of Ireland | Beverage products having steviol glycosides and at least one acid |
| US20080226790A1 (en) * | 2007-03-14 | 2008-09-18 | Concentrate Manufacturing Company Of Ireland | Long chain fatty acids for reducing off-taste of non-nutritive sweeteners |
| US20080226773A1 (en) * | 2007-03-14 | 2008-09-18 | Concentrate Manufacturing Company Of Ireland | Beverage Sweetened with Rebaudioside A |
| US20080226798A1 (en) * | 2007-03-14 | 2008-09-18 | Concentrate Manufacturing Company Of Ireland | Cola Beverages |
| US8277862B2 (en) | 2007-03-14 | 2012-10-02 | Concentrate Manufacturing Company Of Ireland | Beverage products having steviol glycosides and at least one acid |
| US8029846B2 (en) * | 2007-03-14 | 2011-10-04 | The Concentrate Manufacturing Company Of Ireland | Beverage products |
| JP4818177B2 (ja) * | 2007-03-27 | 2011-11-16 | ユニテックフーズ株式会社 | 高齢者向け骨・筋肉増強促進組成物 |
| US8617544B2 (en) * | 2007-05-01 | 2013-12-31 | Richard L. Kozlenko | Compositions and methods for controlling lipid metabolism |
| US9186375B2 (en) | 2007-06-21 | 2015-11-17 | Arthrodynamic Technologies, Animal Health Division, Inc. | Glycosaminoglycan compositions in combination with stem cells |
| US20090162499A1 (en) * | 2007-12-21 | 2009-06-25 | The Quaker Oats Company | Grain products having a potent natural sweetener and a bulking agent |
| US20090162487A1 (en) * | 2007-12-21 | 2009-06-25 | The Concentrate Manufacturing Company Of Ireland | Beverage products and flavor systems having a non-sweetening amount of rebaudioside a |
| US20090162488A1 (en) * | 2007-12-21 | 2009-06-25 | The Concentrate Manufacturing Company Of Ireland | Beverage products and flavor systems having a non-sweetening amount of monatin |
| US20090162484A1 (en) * | 2007-12-21 | 2009-06-25 | The Concentrate Manufacturing Company Of Ireland | Beverage having a non-sweetening amount of a potent natural sweetener |
| US20090162500A1 (en) * | 2007-12-21 | 2009-06-25 | The Quaker Oats Company | Grain products having a potent natural sweetener |
| US20090162498A1 (en) * | 2007-12-21 | 2009-06-25 | The Quaker Oats Company | Grain products having a non-sweetening amount of a potent sweetener |
| JP4838791B2 (ja) * | 2007-12-27 | 2011-12-14 | アサヒビール株式会社 | 混合果汁又は果汁飲料の製造方法 |
| JP4973528B2 (ja) * | 2008-02-05 | 2012-07-11 | ユーハ味覚糖株式会社 | 油脂加工食品及びその製造方法 |
| EP2247290A1 (de) * | 2008-02-25 | 2010-11-10 | Nestec S.A. | Polyphenole zur behandlung von knorpelerkrankungen |
| US20100112101A1 (en) * | 2008-05-06 | 2010-05-06 | Laila Impex | Bio-availability/bio-efficacy enhancing activity of stevia rebaudiana and extracts and fractions and compounds thereof |
| US8163716B1 (en) | 2008-06-30 | 2012-04-24 | Smith James D | Method of administering hyaluronan formulation for the amelioration of osteophytes |
| US8178511B1 (en) | 2008-07-02 | 2012-05-15 | Smith James D | Method of administering hyaluronan formulation for the amelioration of osteopenia |
| RU2469608C2 (ru) * | 2008-08-29 | 2012-12-20 | Тропикана Продактс, Инк. | Натурально подслащенные соковые продукты с бета-глюканом |
| RU2487644C2 (ru) * | 2008-08-29 | 2013-07-20 | Тропикана Продактс, Инк. | Натурально подслащенные соковые продукты |
| US8242180B2 (en) * | 2008-10-20 | 2012-08-14 | Susan B. Roberts, Llc | Use of high satiety, low calorie solid food product in controlling body weight |
| US9176146B2 (en) | 2009-08-03 | 2015-11-03 | Theta Biomedical Consulting & Development Co., Inc. | Methods of treating autism spectrum disorders and compositions for same |
| US9050275B2 (en) | 2009-08-03 | 2015-06-09 | Theta Biomedical Consulting & Development Co., Inc. | Methods of screening for and treating autism spectrum disorders and compositions for same |
| US20110039928A1 (en) * | 2009-08-13 | 2011-02-17 | Golini Jeffrey M | Cetylated fatty acid and alkali buffered creatine anti-inflammatory composition |
| RU2012126629A (ru) * | 2009-11-27 | 2014-01-10 | Нестек С.А. | Зерновой батончик с высоким содержанием молока |
| EP2886104A1 (de) | 2013-12-11 | 2015-06-24 | Patir, Suleyman | Intraartikuläres Gel |
| CZ26523U1 (cs) | 2014-01-23 | 2014-02-24 | Contipro Biotech S.R.O. | Výživová kompozice na bázi hyaluronanu pro kloubní výživu |
Family Cites Families (29)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3679660A (en) | 1969-06-09 | 1972-07-25 | Agatha C Magnus | Glucosamine-alkylsulfonate and process |
| DE2103387C3 (de) * | 1971-01-26 | 1982-05-06 | Johann G.W. Opfermann & Sohn, 5070 Bergisch-Gladbach | Verwendung des Hydrochlorids von Glukosamin zur Herstellung von pharmazeutischen Präparaten |
| US3814819A (en) | 1971-03-10 | 1974-06-04 | Pillsbury Co | High protein food bar |
| US3901799A (en) | 1973-10-29 | 1975-08-26 | Maxie C Adkison | Cyclone separator |
| AR207237A1 (es) * | 1974-02-25 | 1976-09-22 | Thomas A | Procedimiento para obtener extractos biologicos estables liofilizados solubles constituidos por complejos proteicos termorresistentes |
| US3894148A (en) | 1974-03-22 | 1975-07-08 | Vitose Corp | Process for enhancing the energy metabolism of an athlete |
| US4152463A (en) | 1976-08-02 | 1979-05-01 | The Quaker Oats Company | Highly nutritious, protein and vitamin enriched food bar |
| US4322407A (en) | 1978-12-11 | 1982-03-30 | Vitapharm Pharmaceutical Pty. Ltd. | Electrolyte drink |
| SE427983B (sv) | 1980-02-15 | 1983-05-30 | Pripps Bryggerier Ab | Dryckesprodukt |
| US4309417A (en) | 1980-07-10 | 1982-01-05 | Stauffer Chemical Company | Protein fortified isotonic beverages |
| US4466958A (en) * | 1981-03-18 | 1984-08-21 | Morrison L M | Food supplement |
| US4543262A (en) | 1983-03-30 | 1985-09-24 | Nabisco Brands, Inc. | Process for making a nutritional bar |
| US4647453A (en) | 1984-10-18 | 1987-03-03 | Peritain, Ltd. | Treatment for tissue degenerative inflammatory disease |
| DE3681779D1 (de) | 1985-11-15 | 1991-11-07 | Sports Drink Inc | Hypotonisches energiereiches getraenk fuer sportler. |
| US4766209A (en) | 1986-03-10 | 1988-08-23 | Nestec S. A. | Amino sugar carbonating agents and their preparation |
| JPS62224268A (ja) | 1986-03-26 | 1987-10-02 | Rooman Kogyo:Kk | 飲料 |
| EP0587972A1 (de) | 1992-09-18 | 1994-03-23 | The Procter & Gamble Company | Sportgetränk ohne zugesetzten Zucker oder künstliches Süssungsmittel |
| TW293036B (de) * | 1992-11-27 | 1996-12-11 | Takeda Pharm Industry Co Ltd | |
| US5364845C1 (en) * | 1993-03-31 | 2002-09-10 | Nutramax Lab Inc | Glusosamine chondroitin and manganese composition for the protection and repair of connective tissue |
| GB9402950D0 (en) | 1994-02-16 | 1994-04-06 | Univ Leeds Innovations Ltd | Sports drink |
| GB2286528B (en) * | 1994-02-17 | 1998-09-16 | Robert John Woodward | Dietary supplement |
| US5569676A (en) * | 1995-05-24 | 1996-10-29 | Diehl; Harry W. | Method for the treatment of osteoarthritis |
| KR0178893B1 (ko) * | 1995-10-04 | 1999-05-15 | 김광호 | 노트북 컴퓨터의 액정 화면부 결합 힌지장치 |
| NO962728A (no) | 1996-06-27 | 1997-11-17 | Jan Oxholm Gordeladze | Energidrikk |
| US5795576A (en) | 1996-07-08 | 1998-08-18 | Diaz; Jose A. | Chemical composition for aiding the absorption, binding and elimination of undigested fat |
| US5843919A (en) | 1996-11-25 | 1998-12-01 | Burger; John A. | Composition and method for the treatment of arthritis |
| JP3587665B2 (ja) * | 1997-09-19 | 2004-11-10 | 甲陽ケミカル株式会社 | グルコサミン塩含有ドリンク剤 |
| US6391864B1 (en) | 1998-08-19 | 2002-05-21 | Joint Juice, Inc. | Food supplement containing a cartilage supplement |
| US20030069202A1 (en) * | 2000-06-02 | 2003-04-10 | Kern Kenneth Norman | Compositions, kits, and methods for promoting defined health benefits |
-
1999
- 1999-06-22 US US09/338,021 patent/US6391864B1/en not_active Expired - Lifetime
-
2000
- 2000-06-21 AT AT00960108T patent/ATE334604T1/de not_active IP Right Cessation
- 2000-06-21 ES ES00960108T patent/ES2269175T3/es not_active Expired - Lifetime
- 2000-06-21 EP EP00960108A patent/EP1263418B1/de not_active Expired - Lifetime
- 2000-06-21 MX MXPA01013301A patent/MXPA01013301A/es active IP Right Grant
- 2000-06-21 WO PCT/US2000/040267 patent/WO2000078320A1/en active IP Right Grant
- 2000-06-21 JP JP2001504383A patent/JP2003530072A/ja active Pending
- 2000-06-21 AU AU71320/00A patent/AU7132000A/en not_active Abandoned
- 2000-06-21 DE DE60029833T patent/DE60029833T2/de not_active Expired - Lifetime
- 2000-06-21 CA CA2377627A patent/CA2377627C/en not_active Expired - Fee Related
- 2000-06-21 US US09/598,634 patent/US6432929B1/en not_active Expired - Lifetime
Also Published As
| Publication number | Publication date |
|---|---|
| AU7132000A (en) | 2001-01-09 |
| EP1263418A4 (de) | 2003-03-12 |
| EP1263418A2 (de) | 2002-12-11 |
| DE60029833D1 (de) | 2006-09-14 |
| WO2000078320A1 (en) | 2000-12-28 |
| US6391864B1 (en) | 2002-05-21 |
| ATE334604T1 (de) | 2006-08-15 |
| WO2000078320A8 (en) | 2001-05-25 |
| MXPA01013301A (es) | 2003-09-04 |
| ES2269175T3 (es) | 2007-04-01 |
| JP2003530072A (ja) | 2003-10-14 |
| US6432929B1 (en) | 2002-08-13 |
| CA2377627A1 (en) | 2000-12-28 |
| CA2377627C (en) | 2011-06-07 |
| EP1263418B1 (de) | 2006-08-02 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE60029833T2 (de) | Nahrungsmittelergänzungen zur Verbesserung des Knorpelzustandes sowie Herstellungsmethoden | |
| DE69837821T2 (de) | Zusammensetzung zur Ernährung von Diabetikern | |
| US6436446B1 (en) | Composition for increasing bone density | |
| DE60305331T2 (de) | Gelförmige getränkezusammensetzung | |
| DE69935946T2 (de) | Vitaminpulver zur verwendung für getränke | |
| DE60008238T2 (de) | Zusammensetzungen die kreatin in form einer suspension enthalten | |
| DE60128179T2 (de) | Nahrungsmittel enthaltend Vitamin k2 | |
| DE69632742T2 (de) | Verfahren zum Suspendieren von Einschlüssen | |
| US20080131561A1 (en) | Formulation of supplemented carrageenan jelly and manufacturing process | |
| US20030124200A1 (en) | Cartilage enhancing food supplements with sucralose and methods of preparing the same | |
| DE60019239T3 (de) | Fettlösliche Vitamine enthaltende Zusammensetzungen | |
| US7851458B2 (en) | Cartilage enhancing food supplements and methods of preparing the same | |
| DE3151245A1 (de) | Zur enteralen ernaehrung geeignete nahrungszusammensetzung | |
| KR20050083894A (ko) | 근육 증가용 제제 | |
| DE69823661T2 (de) | Funktionelle lebensmittelzubereitung | |
| CA2708764C (en) | Induced viscosity nutritional emulsions comprising a carbohydrate-surfactant complex | |
| DE60215312T2 (de) | Zusammensetzung enthaltend kreatin und kreatinin | |
| DE60222491T2 (de) | Lebensmittel mit verlängerter Energiefreisetzung | |
| DE60201681T2 (de) | Isotonisches energiegetränk und verfahren zu seiner herstellung | |
| WO2006018301A1 (de) | Liponsäure-konzentrat | |
| DE60132698T2 (de) | Verstreichbare maissirupzusammensetzungen mit reduziertem fettgehalt sowie verfahren zu deren herstellung | |
| EP1414312B1 (de) | Gelierzucker und verfahren zu dessen herstellung | |
| DE3139920A1 (de) | "mittel in granulatform auf basis von polysaccharid-gummen, verfahren zu seiner herstellung und verwendung" | |
| KR102125628B1 (ko) | 로즈힙을 함유하는 연골손상방지 내지 재생용 조성물 | |
| AU2005203619B2 (en) | Cartilage enhancing food supplements and methods of preparing the same |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 8364 | No opposition during term of opposition |