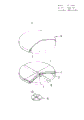CN85106361B - 培养细菌的培养皿及其用途 - Google Patents
培养细菌的培养皿及其用途 Download PDFInfo
- Publication number
- CN85106361B CN85106361B CN85106361A CN85106361A CN85106361B CN 85106361 B CN85106361 B CN 85106361B CN 85106361 A CN85106361 A CN 85106361A CN 85106361 A CN85106361 A CN 85106361A CN 85106361 B CN85106361 B CN 85106361B
- Authority
- CN
- China
- Prior art keywords
- culture dish
- substratum
- sheet
- aperture
- petri dish
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/02—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving viable microorganisms
- C12Q1/04—Determining presence or kind of microorganism; Use of selective media for testing antibiotics or bacteriocides; Compositions containing a chemical indicator therefor
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M23/00—Constructional details, e.g. recesses, hinges
- C12M23/02—Form or structure of the vessel
- C12M23/10—Petri dish
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Wood Science & Technology (AREA)
- Engineering & Computer Science (AREA)
- Zoology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- Microbiology (AREA)
- Biotechnology (AREA)
- Genetics & Genomics (AREA)
- General Engineering & Computer Science (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biomedical Technology (AREA)
- Clinical Laboratory Science (AREA)
- Sustainable Development (AREA)
- Toxicology (AREA)
- Physics & Mathematics (AREA)
- Analytical Chemistry (AREA)
- Biophysics (AREA)
- Immunology (AREA)
- Molecular Biology (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
Abstract
本发明是关于培养细菌的培养皿(Petti dish)和用这种培养皿检查从临床样品等分离出的或分离后纯培养出的细菌的药敏性的方法。至少用一个片将培养皿本体的上端面盖住,在该培养皿的底部至少开一个小孔。如果需要,可以安装几个隔板。使用渗透片作培养表面的、被分隔成几部分的培养皿,本发明的方法把在每一部分中接种了细菌的种类彼此不同的培养基,含不同种类的药物的培养基或含有同一种药物但浓度不同的培养基进行拼配。
Description
本发明涉及培养细菌的培养皿(Petri dish),它可用于细菌分离、增殖培养、药敏性试验等,和用这种培养皿从临床样品的分离细菌或其纯培养物中检查细菌药敏性的方法。
在医院里做细菌检查时,为了鉴别引起传染病的病原体,必须对被检物中的细菌进行分离培养和增殖培养等操作。特别是,由于传染病的病理性的并发症,当前从临床诊断推断致病的细菌更加困难,由于此趋向,由检查细菌的方法得到的结果变得重要起来。
根据细菌种类的不同,适于细菌生长的培养基是多种多样的。因此,鉴别致病细菌的时候,需要制备一种这样的培养基,它对被检物中可能被测出的每一种致病细菌都是合适的。在血液样品中可能发现的细菌被载明的有:葡萄球菌(staphylococcus)、链球菌(streptococcus)、肺炎球菌属(pneumococcus)、肠道球菌(enterococcus)、嗜血杆菌(haemophilus)、沙门氏菌(salmonella)、大肠杆菌(escherichia coli)、绿脓杆菌(pseudomonas aeruginosa)、厌氧菌(anaerobic bacterium)、campylobacter、布鲁氏菌属(brucella)等等。为了分离这些细菌的任一种,通常对每一样品都需要制备血液琼脂培养基、巧克力琼脂培养基、厌氧菌分离培养基、增殖培养的培养基等等。此外,可以从排泄物中测出沙门氏菌属、痢疾杆菌(dysentery bacillus)、致病大肠杆菌(pathogenic coli)、yersinia、enterocolitica、klebsiella oxytoca、弧菌属(vibrio)、葡萄球菌、蜡状芽胞杆菌(bacillus cereus)等等,因此,需要制备BTB乳糖琼脂培养基、DHL琼脂培养基、SS琼脂培养基、厌氧菌分离培养基、增殖培养基等,作为任一种这些细菌的培养基。
然而,在细菌培养中用常规的培养皿制备这些培养基时,需要将溶液进行长时间的加热,因为培养基中含有琼脂,并且还应将培养皿水平静置到琼脂培养基凝固为止,因此需要进行一种复杂的操作。此外,几乎所有用于细菌培养的常规培养皿每一个都只含有一种培养基,因此增加了一个样品所需培养皿的数目,还需要一个一个地进行培养皿的接种操作,以致不可避免使有关的操作复杂化。在这一点上,虽然可以设想一种方法,将几种培养基分别注入用隔板隔成几部分的培养皿中,但由于制备培养基时培养皿中各部分培养基的水平不同,因此,接种操作必需是一个部分接一个部分地进行。这种方法和上述的一种培养基一个培养皿的方法之间没有改进的变化。
此外,为了用常规培养皿培养细菌而制备各种平板培养基时,不仅需要复杂的操作,例如溶解、消毒、分别灌注、培养基组分的凝固等,各步操作还必须尽可能地在无菌条件下进行。通常,一种培养基分别注入每一个培养皿增加了每一样品所需的培养皿数,以致在医院的试验室中基本上不可能准备适量的培养基,因为在医院中样品数量和需处理的细菌种类不是一定的。因此,许多门诊部一次制作或购买预定期间内所需估计量的培养基,并且不可避免地采用逐步使用这些培养基的方法,并在冰箱中贮存培养基,在这种情况下,贮存和购买只能在培养基容器的周围盖一个盖子的状态下进行,因此存在湿度和各种细菌污染培养基的问题。
在使用一般的培养基之前,进行干燥操作是必不可少的,但在贮存期间或在购买时处在脱气状态的培养基在干燥操作中会溶解空气中的氧。因此,如果处理厌氧菌,在干燥过程之后需要将它单独移到一个无氧的容器中。
其次,在对细菌传染病使用化学疗法的情况下,对引起这种病的细菌选择和使用最有效的药物是值得推荐的。然而,在近年来对这些细菌有效的药物的种类和浓度需根据细菌的种类而定,而且化学疗法在近年来普及引起了抗药菌株(抗药性细菌)的出现。这种抗药菌株对通常的有效药物表现出抗性,因此,如果鉴定出任一引起传染病的细菌,采用一种有效药物基本上是不可能的。为此之故,为把适于临床的、合理的疗法投入实践目的,不应忘记在检查细菌时,药敏性检查是一个重要的项目。
稀释法、扩散法和浊度测定法都可以用作检查细菌药敏性的方法;使用琼脂培养基的琼脂平皿稀释法和肉汤稀释法属于上述稀释法,扩散法中有敏感片剂法、敏感圆片法、斜面平皿法和垂直扩散法。然而,就检查细菌的实际位点而言,操作中主要使用琼脂平皿稀释法和敏感圆片法。
敏感圆片法是在被试细菌生物抑制圈或抑制带的基础上进行判断,在预定的时间,在不含药物的培养基上放入一浸渍了药物的圆纸片,培养基上面提前接种了被试的细菌,然后进行细菌培养,随着药物的扩散而出现抑制带或抑制圈。虽然这是一种广泛使用的方法,它容易操作且可对许多药物和浓度进行试验并且只用一个培养皿就行,但是使用这种方法时,放了圆纸片的培养基的厚度、倾角和性质很容易引起抑制圈大小的波动,因此这种方法通常重复性不好。另一方面,虽然有时使用3一浓度圆片法(不基于抑制圈的大小判断效果,仅依其存在进行判断),但由于药物浓度的调整幅度更大,这种方法不适于测定被试细菌的最小抑制浓度(MIC)。
预先含有预定浓度药物的培养基的琼脂平皿稀释法在重复性方面较好,并能自由地安排药物的浓度。但这种方法需要对每种药物及其系列浓度中的每一种采用一种培养基,则不得不对每种培养基进行接种操作,因此这一方法也是很复杂的。
一般的药敏性检查(其目的是取得治疗法则)把抑制全部细菌生长的药物浓度看得很重要,但并不注意对应于每一药物浓度的被试菌株的药敏性。然而,为了得到正在趋向复杂的传染病的更适当的治疗法则,需要进一步掌握引起这种疾病的细菌的详细情报。
本发明的目的是解决培养细菌的上述一般培养皿存在的问题,即为了准备培养基不仅必须完成复杂的操作,而且一次操作仅可将细菌接种到一种培养基中,因而操作效率十分低。
通过本发明要达到的进一步的目的是解决培养基干燥的问题,或是在储存和运输中被湿度和各种细菌污染的问题。
本发明更进一步的目的是解决这样的问题,即常规检查法中为制备培养基和接种必需的复杂操作和敏感圆片法的低重复性。
为上述目的,本发明至少用一个薄片覆盖培养皿的上端面,在培养皿的底部至少开一个小孔,并且,如果需要的话,装几个其高度为培养皿底部和上述薄片之间的距离的隔板,在上述小孔上装密封盖。
上述的薄片可以是一种对充满培养皿的培养基组分可渗透的薄片(下称渗透片),并可使其适于附着细菌。配上一个对培养基组分不能渗透的薄片(下称非渗透片)也是可以的,在这种情况下,这种非渗透片需要能够可拆卸地覆盖培养皿本体。可以配上对水和氧也不能通过的非渗透片。进一步也可用非渗透片可拆卸地覆盖在渗透片的外面。
在本发明的方法中,使用具有可作为培养表面的渗透片并被分隔成几部分的培养皿,将不同种类的培养基、将含有不同种类药物的培养基或含有同种药物但浓度不同的培养基在每个分隔中分开,并在其中接种细菌,从而解决了上述的一般方法中存在的问题。
由于使用上述方法的结果,可以方便地在无菌条件下制备培养基,即从开在培养皿底部的小孔分别注入培养基,进行接种操作时,由于该薄片的作用培养基表面的高度是一致的,因此通过一次操作就可以在被分隔成几部分的培养基的全区域上接种细菌。
在使用非渗透片的情况下,培养基不会变得干燥或者在贮存和运输中不会受到湿度和各种细菌的污染。由于培养基是被封闭的,不会直接与空气接触,因而防止培养基由于氧化而变质。在接种操作的时候,虽然培养基被分隔开了,揭开非渗透片也可获得在同一平面上的培养基表面,从而一次操作就可将细菌接种到这种分隔培养基的全部范围。
本发明的实施例的描述是和附图的描述一起进行的。
图1到图6说明用渗透片的实施例。
实施例1
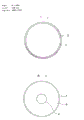
(1)是培养皿本体,培养皿本体(1)是用塑料或玻璃之类材料制造的,并且最好是透明的。培养皿本体(1)的上端面用渗透片(2)覆盖,底(3)设置小孔(4)。上述的渗透片(2)必须具有一些细孔或间隙,通过这些细孔和间隙在培养皿本体(1)和渗透片(2)之间充满的培养基组分可通过这些细孔和间隙沥滤到渗透片(2)的表面。作为渗透片的材料,多孔膜或多孔橡胶膜或包括纤维素酯类、聚丙烯类、聚碳酸酯类、聚偏二氟乙烯、属于芳烃类的聚合物等的合成树脂之类的薄膜是可取的材料。在培养皿被含琼脂之类的固化剂的培养基充满的情况下,可以用织物和纸(它们的间隙比较大)作为渗透性材料。当然,在那种情况下,如果所使用的合成树脂膜是疏水性的,那么,事先要进行亲水性处理。就渗透片(2)的强度而论,全部要求在于足以使培养基具有平整的表面。在培养皿灌装培养基的时候,如果材料需要某些增强的话,合成纤维等可起这类作用,或在固体培养基的情况下,即把平的增强膜插入渗透片(2)和培养皿盖(5)之间的间隙(这将在下面提及),直到培养基被固化并起增强的作用为止。此外,在培养皿底(3)上的小孔(4)最好设置可拆卸的密封盖(6),但在充满培养皿的培养基含有如琼脂之类的固化剂的情况下,可使已消毒的培养皿(1)内部保持无菌状态,因此这种需要有时差不多减少到零。
(5)是培养皿盖,用塑料或玻璃制造,且最好是透明的。培养皿盖的内部周边设置环形突出物(7)。这个突出物(7)提供形成渗透片(2)与培养皿盖(5)之间的间隙,当培养皿盖(5)与培养皿本体(1)配合的时候,防止在渗透片(2)的表面生长的细菌菌落附着到培养皿盖(5)的内表面上,并对外界保持足够的密封性。当上述突出物(7)提供的位置没有必要限制于培养皿盖(5)的内周边时,将它设置在渗透片(2)的周边上或设置在培养皿本体(1)的上端面的周边上是可行的。
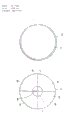
上述的培养皿本体(1)可以设置几块隔板(8),隔板(8)的高度为培养皿底(3)与渗透片(2)之间的距离。在这种情况下,被隔板(8)分隔成的各个部分(9)可以分别设置小孔(4)。例如,如同图4到图6所示分隔成四个部分的情况,在培养皿底(3)的中心设置小孔(4),隔板(8)在小孔(4)上交叉以使它和培养皿的每个部分(9)相通。此外,密封盖(6)可以采用具有十字形开口(10)的堵头,如同所示的那样。
实施例3~5
参考图7到图11,说明用非渗透片的实施例。在培养皿本体(1)的上端面用可拆卸的非渗透片(11)覆盖。非渗透片(11)的厚度没有任何限制,而要求它对水和氧是非渗透性的。作为非渗透材料,对氧具有较高的屏障性能的合成树脂膜或薄膜,例如聚丙烯腈、尼龙、聚甲基丙烯腈、乙烯-乙烯基醇聚合物,聚偏二氯乙烯、聚对苯二甲酸乙酯、聚氯乙烯等是可取的材料。以及在其上面压制了对氧具有较高屏障性能的上述树脂膜或金属箔如铝箔等的其他材料可满足要求,当然,这些材料必须能够达到有关的效果。当培养皿充满培养基的时候,非渗透片(11)的厚度根据材料而定,只有当它的强度达到使培养基保持平面的程度才满足要求。在固体培养基情况下,把平的增强膜插入非渗透片(11)和培养皿盖(5)之间的间隙,直到培养基被固化并由此起增强的作用。而且,如果在培养皿底(3)上的小孔(4)设置可拆卸的密封盖(6),最好是在已经被消毒的培养皿本体(1)的内部,实现无菌状态的条件。如果是这样的话,把培养基分别注入这个培养皿的时候,当然与一般的培养皿相似,这个培养皿的内部也保持无菌状态。
图9和图10所示的一个实施例中,培养皿的底(3)可以这样设置,以便从培养皿本体(1)的周边到小孔(4)具有一个倾斜度。在这种情况下,当把培养基分别注入这个培养皿的时候,就可能用培养基充满这个培养皿而不会产生泡沫。
图11说明用几块隔板(8)把培养皿本体(1)分隔成4份的情况,在那个实施例中,被分隔成的4份中的每一个部分(9)都设置小孔(4),通过小孔(4)把培养基分别注入每个部分(9)。小孔(4)可用密封盖(6)分别密封,因此,具有减小细菌污染的危险性的优点。
实施例6~7
图12到图15说明同时用前述的渗透片(2)和非渗透片(11)的实施例。在培养皿本体(1)的上端面用渗透片(2)覆盖,又用可拆卸的非渗透片(11)覆盖。
本发明用于培养细菌的培养皿,可用于除了液体或半流体培养基之外的各种琼脂培养基。
其次,根据本发明描述的实施例,检验细菌对药物敏感性的方法如下:
在这个实施例中,所用的培养皿如同图4到图6所示的那样,即分隔成了4份的培养皿本体(1)的上端面上用渗透片(2)覆盖,培养皿本体(1)设置隔板(8),它的高度为培养皿的底(3)和渗透片(2)之间的距离,这个培养皿的底(3)设置小孔(4),而小孔(4)和被隔板(8)分隔成的培养皿的每个部分相通,并且小孔(4)设置密封盖(6)。
上述的渗透片(2)使用多孔的聚偏二氟乙烯膜(孔径:0.45μ,μ=微米)。用Muller-Hinton琼脂培养基作为培养基,每批药物稀释液以固定量加入培养基。以便得到如同表1中所示的药物浓度,留下培养皿中的一个分隔用于对照,培养基通过3步分别注入培养皿的其余三部分(9),并在那里根据药物的浓度固化(在一个培养皿中操作达3次,四个培养皿需要操作12次)。作为对照培养基,Muller-Hinton培养基也是分别注入的。
首先,把病人的脓液作为试样,手工接种在上述被分隔成了四份的培养皿的渗透片(2)上。
其次,用螺旋形自动平板接种仪(spiral plater)(由美国Spiral System Instruments制造)通过直接的方法从病人的脓液接种。这种螺旋形自动平板接种仪是并入自动系统的接种装置,用来测量活的细菌的数目,它是美国食品药物管理局研究设计的。其接种过程中,使被试材料成螺旋形涂抹在培养基上,而被试材料根据从培养基中心的距离得出密度梯度值。
为此,根据本发明的方法,如果被试材料是以预定的密度梯度接种涂抹在渗透片(2)上,那么,仅仅测量每一个固定区域的隔离的菌落数目便可计算出包含在单位被试材料中的活细菌的总数。而且,除了根据一般标准的药物敏感度值外,引起疾病的细菌对每种药物的不同浓度的敏感性模式也可容易而迅速地获得。
使用上述的螺旋形自动平板接种仪,用金黄色葡萄球菌作为试样中的病原菌,分离率为2.8×104菌落形成单位/毫升(Colony Forming Unit)。
使用以生长的存在为基础的一般鉴定标准,可以由表1作出如下判断:对上述分离出的细菌,ABPC的MIC值是1.56μg/ml,CTM的MIC值是0.78μg/ml,此外CZX、GM和NFLX的MIC值分别是6.25,50以上,3.13μg/ml。
从表中各种药物的不同浓度的菌落数目变化看来,根据常规标准,可认为GM的MIC值超过50μg/ml,但实际上当浓度为6.25μg/ml时,大约50%的被试细菌就已对药物显示出敏感性。
表1
病原菌:金黄色葡萄球菌
对照培养基:Muller-Hinton 培养基(2.8×104CFU/ml)
药物名称 ABPC CTM CZX GM NFLX
药物浓度 (CFU/ml) (CFU/ml) (CFU/ml) (CFU/ml) (CFU/ml)
μg/ml
0.025 2.7×104 2.9×104 2.8×104 2.9×104 2.8×104
0.05 2.8×104 2.6×104 2.9×104 2.6×104 2.8×104
0.1 2.9×104 2.9×104 2.7×104 2.9×104 2.6×104
0.2 2.6×104 2.6×104 3.0×104 2.6×104 2.9×104
0.39 4.3×103 1.8×104 2.7×104 2.6×104 2.8×104
0.78 1.2×102 0 2.5×104 2.9×104 2.7×104
1.56 0 0 5.8×103 2.9×104 3.5×103
3.13 0 0 3.6×102 2.6×104 0
6.25 0 0 0 1.7×104 0
12.5 0 0 0 8.0×103 0
25 0 0 0 6.8×103 0
50 0 0 0 6.2×103 0
ABPC:氨必西林 CTM:cefotiam
czx:ceftizoxime GM:艮他霉素 NFLX:norfloxacin
由于本发明的用于培养细菌的培养皿具有前述的结构,因此用培养基充满培养皿本体(1)时就不需要打开培养皿盖(5),培养基可以分别注入。当装配上培养皿盖(5)时,使培养皿倒转,培养基可分别从培养皿的底(3)的小孔(4)注入。因此,由于培养皿盖(5)没有打开,当分别注入培养基的时候,和一般的方法相比,培养基分别注入的方法更加减少了被各种细菌污染的危险。同样,在使用渗透片(2)的情况下,培养基在作为底面的渗透片(2)上固化,渗透片(2)作为培养面,当培养基用来接种和培养细菌的时候,培养基的固化并不需要通常需要的一个平工作台,在固化时振动并不会引起培养基的表面上产生扰动。在使用非渗透片(11)的情况下,将非渗透片(11)揭开,即可将培养基用于接种和培养细菌并同样产生上述效果。
根据本发明,在使用分隔成几部分的培养皿的情况下,因为被培养基充满了的每部分的培养面的高度由渗透片(2)或非渗透片(11)保持均一,便可通过自动接种装置例如螺旋形自动平板接种仪接种。在一般的被分隔了的用培养基充满的培养皿中,由于隔板之间的各个培养基不在同一水平上,上述操作就会产生问题,同样在手工接种的情况下,通过一次操作把细菌接种到大部分培养基中也是可能的。
另外,采用渗透片(2)的培养皿,因为充满培养皿本体(1)的培养基的形状通过培养皿本体(1)和渗透片(2)被限定,在培养皿本体(1)中,借助于含有聚丙烯酸苏打、聚丙烯酸淀粉、聚乙烯乙酸酯等的吸水性较高的树脂,或含有来源于天然物质的藻酸和羧甲基纤维素的固化剂被密封在培养皿本体(1)中,充满液体培养基也是可能的。因此,需要传统复杂操作的含药物培养基的制备能容易地进行。此外,如果培养皿本体(1)的每一部分(9)用某些含不同浓度的药物的培养基充满的话,这些培养基用于药物敏感性试验将是便利的培养基。
在使用非渗透片(11)的培养皿情况下,在用培养基充满了培养皿之后,由于在贮存或在运输中,培养基被密封在非渗透片(11)和培养皿本体(1)之间,因此,培养基不会和空气接触,这样便可防止培养基干燥和由于氧化作用引起变质,防止由于湿气使培养表面潮湿,还可防止在贮存中由各种细菌产生污染。在与空气隔绝的情况下,培养基分别注入到培养皿里面贮存是可能的。当培养厌氧细菌的时候,如果培养基事先经过减压脱气、煮沸、超声波处理等,然后分别注入的话,就可以提供比一般的培养基有更少溶解氧的适当的培养基。
再者,本发明的用于培养细菌的培养皿,也可以通过在培养皿的各部分注入适当的培养基的方法,用多个培养皿来筛选病原菌。
根据本发明方法,利用渗透片(2)作为培养面就能够得到极平的培养面(尽管采用了被分隔的培养皿),此外,进行手工细菌接种也比较容易。也可利用象螺旋形自动平板接种仪这样的自动接种装置。
图1是本发明用于培养细菌的培养皿的实施例1的局部剖视的透视图,用的是渗透片;图2是实施例1的培养皿盖的仰视图;图3是实施例1的培养皿本体的仰视图;图4是实施例2的局部剖视的透视图;图5是实施例2的培养皿盖的仰视图;图6是实施例2的培养皿本体的仰视图;图7是用非渗透片的实施例3的培养皿本体的仰视图;图8是图7的A-A线处的剖视图;图9是实施例4的培养皿本体的仰视图;图10是图9在B-B线处的剖视图;图11是实施例5的局部剖视的透视图;图12是实施例6的同时用渗透片和非渗透片的局部剖视的透视图;图13是实施例6的培养皿本体的仰视图;图14是图13在C-C线处的剖视图;图15是实施例7的局部剖视的透视图。
Claims (14)
1、一种培养细菌的培养皿,该培养皿本体的上端面是开口的,内部充满培养基,其特征在于:
所说培养皿本体的上端面至少用一个片覆盖,以便这一个片或多个片可以形成一个平面或多个平面,当培养皿充满培养基时,所说的这一个片或多个片具有能保持该培养基的表面平展的强度,
所说的培养皿本体被隔板分隔成几部分,隔板高为所说培养皿的底部至所说的一个片或多个片之间的距离,
所说的培养皿的底部至少开一个小孔,通过这个小孔可使培养基充满被隔板分隔的几部分的内部,
所说的一个小孔或几个小孔分别装有一个或几个可拆卸的密封盖。
2、权利要求1的培养皿,其中所说的片是包括合成树脂或橡皮的一个多孔膜,通过它,充满所说培养皿本体内部的培养基的组分可以沥滤到片的表面。
3、权利要求1的培养皿,其中所说的片是一个对氧气具有较高的屏障性能的合成树脂膜,且该片可拆卸地覆盖所说的培养皿。
4、权利要求2的培养皿,其中所说的多孔膜用另一个片可拆卸地盖住,所说另一个片是一个对氧气具有较高的屏障性能的合成树脂膜。
5、权利要求3或4的培养皿,其中所说合成树脂膜包括下述合成树脂,如聚丙烯腈、尼龙、聚甲基丙烯腈、乙烯-乙烯基醇聚合物,聚偏二氯乙烯、聚对苯二甲酸乙酯、聚氯乙烯。
6、权利要求2的培养皿,其中所说多孔膜包括下述合成树脂,如纤维素酯类,聚丙烯类、聚碳酸酯类、聚偏二氟乙烯,属于芳烃类的聚合物。
7、权利要求1的培养皿,其中所说的培养皿的底部在大约中心位置有一个小孔,该孔与所有各分隔的部分相通。
8、权利要求1的培养皿,其中所说培养皿的底部有多个小孔,所述的这些小孔分别与各个分隔的部分相通。
9、权利要求7的培养皿,其中所说的培养皿的底部从培养皿本体的周边至小孔的周边向下倾斜。
10、权利要求1所述的培养皿用于检查细菌药敏性。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP59212163A JPS6192561A (ja) | 1984-10-09 | 1984-10-09 | 細菌培養用シヤ−レ |
| JP59-212163 | 1984-10-09 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN85106361A CN85106361A (zh) | 1986-04-10 |
| CN85106361B true CN85106361B (zh) | 1988-01-20 |
Family
ID=16617946
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN85106361A Expired CN85106361B (zh) | 1984-10-09 | 1985-08-24 | 培养细菌的培养皿及其用途 |
Country Status (8)
| Country | Link |
|---|---|
| US (2) | US4775628A (zh) |
| EP (1) | EP0181075B1 (zh) |
| JP (1) | JPS6192561A (zh) |
| KR (1) | KR890003945B1 (zh) |
| CN (1) | CN85106361B (zh) |
| AU (1) | AU567225B2 (zh) |
| CA (1) | CA1252375A (zh) |
| DE (1) | DE3565997D1 (zh) |
Families Citing this family (29)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5202262A (en) * | 1984-01-31 | 1993-04-13 | Millipore Corporation | Apparatus for microbiological testing of liquids |
| FI72741C (fi) * | 1986-02-21 | 1987-07-10 | Valio Meijerien | Foerfarande foer bestaemning mikrobkoncentrationer medelst en smaeltagarmetod samt daeri anvaenda skaolar. |
| JPH0640813B2 (ja) * | 1988-02-17 | 1994-06-01 | ダイキン工業株式会社 | 培養器 |
| GB8905001D0 (en) * | 1989-03-04 | 1989-04-19 | Univ Leicester | Screening for natural products of microbial metabolism |
| US5190879A (en) * | 1990-05-08 | 1993-03-02 | Bowolfe, Inc. | Controlled environment animal isolation systems |
| WO1992007061A1 (de) * | 1990-10-17 | 1992-04-30 | Fritz Reulecke | Behälter für kulturmedien und verwendung des behälters |
| CH686521A5 (fr) * | 1991-05-23 | 1996-04-15 | Eduard Dr Engelbrecht | Support pour milieux de culture compartimente et milieux de culture électifs complémentaires. |
| US5463223A (en) * | 1994-01-24 | 1995-10-31 | Patwong Technologies, Inc. | Disposable all purpose micro sample holder |
| US5593891A (en) * | 1994-11-10 | 1997-01-14 | Banes; Albert J. | Culture plate with splash guard |
| US6001586A (en) * | 1996-03-29 | 1999-12-14 | Genencor International, Inc. | Compartmentalization method for screening microorganisms |
| JP2003225083A (ja) * | 2002-02-05 | 2003-08-12 | Sony Corp | 円盤状培養媒体 |
| US7384599B2 (en) * | 2003-01-30 | 2008-06-10 | Randy Brewer | Apparatus for drug testing |
| US20050239200A1 (en) * | 2004-04-23 | 2005-10-27 | Beckwith Scott W | Devices for culturing anaerobic microorganisms and methods of using the same |
| JP4740584B2 (ja) * | 2004-12-14 | 2011-08-03 | オリンパス株式会社 | 観察装置 |
| JP4810093B2 (ja) * | 2004-12-28 | 2011-11-09 | オリンパス株式会社 | 培養観察装置および標本トレー保温装置および蓋 |
| WO2007149525A2 (en) * | 2006-06-22 | 2007-12-27 | Manhattan Diagnostics Corp. | Petri dish with filter |
| US8921283B2 (en) * | 2006-10-30 | 2014-12-30 | Washington University | Method for generating microscopic patterns of protein and other macromolecules |
| WO2008149914A2 (en) * | 2007-05-30 | 2008-12-11 | Nikon Corporation | Incubation container |
| US7968062B1 (en) | 2007-07-06 | 2011-06-28 | Richard Carle Putnam | Drug disposal and verification device |
| DE102007059199A1 (de) * | 2007-12-08 | 2009-06-10 | Cognis Ip Management Gmbh | Hautmodell |
| US8163540B2 (en) * | 2008-07-18 | 2012-04-24 | Carlo Acosta | Filtered petri dish |
| EP2776550B1 (en) | 2011-11-07 | 2018-01-10 | Rapid Micro Biosystems, Inc. | Cassette for sterility testing |
| CA3171698A1 (en) * | 2012-04-16 | 2013-10-24 | Rapid Micro Biosystems, Inc. | Cell culturing device |
| US9695458B2 (en) | 2013-08-27 | 2017-07-04 | Parker-Hannifin Corporation | Sample dish and compressed gas microbial test unit |
| JP7002329B2 (ja) * | 2014-08-14 | 2022-01-20 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツング | 膜濾過を用いた、液体の微生物学的調査のためのペトリディッシュおよび方法 |
| CN107090401A (zh) * | 2017-06-09 | 2017-08-25 | 天津施特雷生物科技股份有限公司 | 一种干制一次性无菌微生物培养皿 |
| CN109679833B (zh) * | 2019-01-10 | 2021-10-26 | 航天神舟生物科技集团有限公司 | 多因素一体化筛选平板及其制作工具和制作方法 |
| CN109679828B (zh) * | 2019-02-22 | 2020-06-09 | 胥振国 | 一种细菌培养用培养皿及使用方法 |
| WO2024080882A1 (en) * | 2022-10-10 | 2024-04-18 | Farm Medix Limited | Improved microbiological media container |
Family Cites Families (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE839245C (de) * | 1949-04-15 | 1952-05-19 | Ewald Dr Med Kanz | Verfahren und Einrichtung zur Zuechtung von Kleinlebewesen |
| US2677646A (en) * | 1952-03-22 | 1954-05-04 | Lovell Chemical Company | Unit for bacterial analysis |
| US2954327A (en) * | 1955-08-02 | 1960-09-27 | Kanz Ewald | Container for nutrient media |
| US2874091A (en) * | 1956-07-23 | 1959-02-17 | Hyland Lab | Disposable culturing device |
| US3073750A (en) * | 1959-05-07 | 1963-01-15 | Talb Ind Inc | Culture dish |
| US3055808A (en) * | 1959-07-23 | 1962-09-25 | Baltimore Biolog Lab Inc | Hermetically sealed petri dish |
| DE1210129B (de) * | 1964-12-03 | 1966-02-03 | St Luke S Hospital Res Foundat | Zum Zuechten anaerober Kulturen dienende abdeckbare Flachschale |
| US3630849A (en) * | 1969-04-24 | 1971-12-28 | David B Land | Surface micro-organism contamination assays |
| US3729382A (en) * | 1970-12-09 | 1973-04-24 | Becton Dickinson Co | Microorganism sampling dish |
| US3809617A (en) * | 1972-11-15 | 1974-05-07 | American Cyanamid Co | Device for detecting anticholinesterase materials |
| SE403382B (sv) * | 1974-03-12 | 1978-08-14 | Orion Yhtyme Oy Orion Diagnost | Sett vid undersokning av effekten av ett biologiskt aktivt emne pa tillvexten av mikroorganismer som odlas pa ett fast eller gelformigt odlingsmedium |
| US4030980A (en) * | 1975-05-15 | 1977-06-21 | Corning Glass Works | Apparatus and method for identification of selected clinical yeast |
| US4271270A (en) * | 1977-10-27 | 1981-06-02 | Lukacsek Patricia A | Apparatus for culturing and examining fungi |
| DE3102571A1 (de) * | 1981-01-27 | 1982-09-16 | C.A. Greiner und Söhne GmbH & Co KG, 7440 Nürtingen | Petrischale |
| JPS5863382A (ja) * | 1981-10-13 | 1983-04-15 | Terumo Corp | 多層微生物培養検査器 |
| US4435508A (en) * | 1981-11-20 | 1984-03-06 | Gabridge Michael G | Tissue culture vessel |
| DE3218532A1 (de) * | 1982-05-17 | 1983-11-17 | C.A. Greiner und Söhne GmbH & Co KG, 7440 Nürtingen | Mit einem naehrboden gefuellte schale zur zuechtung von bakterien und kleinpilzen |
-
1984
- 1984-10-09 JP JP59212163A patent/JPS6192561A/ja active Granted
-
1985
- 1985-07-23 KR KR1019850005241A patent/KR890003945B1/ko not_active IP Right Cessation
- 1985-08-08 AU AU45918/85A patent/AU567225B2/en not_active Ceased
- 1985-08-20 CA CA000489085A patent/CA1252375A/en not_active Expired
- 1985-08-24 CN CN85106361A patent/CN85106361B/zh not_active Expired
- 1985-09-11 US US06/774,757 patent/US4775628A/en not_active Expired - Lifetime
- 1985-09-23 DE DE8585306742T patent/DE3565997D1/de not_active Expired
- 1985-09-23 EP EP85306742A patent/EP0181075B1/en not_active Expired
-
1987
- 1987-11-20 US US07/123,141 patent/US4801548A/en not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| JPH0558705B2 (zh) | 1993-08-27 |
| KR860003345A (ko) | 1986-05-23 |
| US4775628A (en) | 1988-10-04 |
| US4801548A (en) | 1989-01-31 |
| KR890003945B1 (ko) | 1989-10-13 |
| DE3565997D1 (en) | 1988-12-08 |
| CN85106361A (zh) | 1986-04-10 |
| CA1252375A (en) | 1989-04-11 |
| AU4591885A (en) | 1986-04-17 |
| EP0181075B1 (en) | 1988-11-02 |
| AU567225B2 (en) | 1987-11-12 |
| JPS6192561A (ja) | 1986-05-10 |
| EP0181075A1 (en) | 1986-05-14 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN85106361B (zh) | 培养细菌的培养皿及其用途 | |
| CA1077814A (en) | Storage stable antibiotic susceptibility test kit | |
| US3992265A (en) | Antibiotic susceptibility testing | |
| US5817510A (en) | Device and method for evaluating microorganisms | |
| US3787290A (en) | Method and means for assaying biological factors demonstrating quantal response | |
| FI67725B (fi) | Foerfarande foer framstaellning av enheter avsedda foer bestaemning av antibiotika- och sulfarester i biologiska vaetskor och framstaellda enheter | |
| Marrie et al. | Influence of mucoidy on antibody coating of Pseudomonas aeruginosa | |
| Gwynn et al. | Regrowth of Pseudomonas aeruginosa and other bacteria after the bactericidal action of carbenicillin and other β-lactam antibiotics | |
| US3728228A (en) | Device for indication of bacterial sensitivity to antibiotics | |
| Lee et al. | Phagocytosis by polymorphonuclear leukocytes of Staphylococcus aureus and Pseudomonas aeruginosa adherent to plastic, agar, or glass | |
| Carey | Clinical comparison of the Isolator 1.5 microbial tube and the BACTEC radiometric system for detection of bacteremia in children | |
| Bonventre et al. | Autoradiographic evidence for the impermeability of mouse peritoneal macrophages to tritiated streptomycin | |
| EP0346732A1 (en) | Biological sample collection and transport device | |
| Qiu et al. | Batch culture formulation of live biotherapeutic products | |
| Yrios et al. | Survival of anaerobic and aerobic bacteria on cotton swabs in three transport systems | |
| CN112831539A (zh) | 一种需氧微生物的体外检测试剂盒 | |
| Mowjood et al. | Small-colony forms of enteric bacteria after exposure to aminoglycosides | |
| CN105255718A (zh) | 一种检验棉拭子及其制备方法和检验方法 | |
| Blair | Laboratory diagnosis of staphylococcal infections | |
| CN209443016U (zh) | 一种干细胞培养装置 | |
| Flowers | Use of sensitivity discs as primary antibiotic standards in MIC determination. | |
| CN219861298U (zh) | 一种具有分层培养功能的二氧化碳培养箱 | |
| Shyrobokov et al. | Study guide of the practical classes course part І | |
| CN102220234A (zh) | 万古霉素耐药金黄色葡萄球菌快速检测试剂盒及其制备方法 | |
| Paull et al. | A new method for the determination of bactericidal antibiotic synergy |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C13 | Decision | ||
| GR02 | Examined patent application | ||
| C14 | Grant of patent or utility model | ||
| GR01 | Patent grant | ||
| C19 | Lapse of patent right due to non-payment of the annual fee | ||
| CF01 | Termination of patent right due to non-payment of annual fee |