CN103764659A - 抑制胶质母细胞瘤的化合物及其用途 - Google Patents
抑制胶质母细胞瘤的化合物及其用途 Download PDFInfo
- Publication number
- CN103764659A CN103764659A CN201280028960.8A CN201280028960A CN103764659A CN 103764659 A CN103764659 A CN 103764659A CN 201280028960 A CN201280028960 A CN 201280028960A CN 103764659 A CN103764659 A CN 103764659A
- Authority
- CN
- China
- Prior art keywords
- glioblastoma multiforme
- compound
- cell
- gene
- coding
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D493/00—Heterocyclic compounds containing oxygen atoms as the only ring hetero atoms in the condensed system
- C07D493/12—Heterocyclic compounds containing oxygen atoms as the only ring hetero atoms in the condensed system in which the condensed system contains three hetero rings
- C07D493/18—Bridged systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D493/00—Heterocyclic compounds containing oxygen atoms as the only ring hetero atoms in the condensed system
- C07D493/12—Heterocyclic compounds containing oxygen atoms as the only ring hetero atoms in the condensed system in which the condensed system contains three hetero rings
- C07D493/20—Spiro-condensed systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/35—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having six-membered rings with one oxygen as the only ring hetero atom
- A61K31/352—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having six-membered rings with one oxygen as the only ring hetero atom condensed with carbocyclic rings, e.g. methantheline
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/4164—1,3-Diazoles
- A61K31/4188—1,3-Diazoles condensed with other heterocyclic ring systems, e.g. biotin, sorbinil
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D493/00—Heterocyclic compounds containing oxygen atoms as the only ring hetero atoms in the condensed system
- C07D493/02—Heterocyclic compounds containing oxygen atoms as the only ring hetero atoms in the condensed system in which the condensed system contains two hetero rings
- C07D493/06—Peri-condensed systems
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/574—Immunoassay; Biospecific binding assay; Materials therefor for cancer
- G01N33/57484—Immunoassay; Biospecific binding assay; Materials therefor for cancer involving compounds serving as markers for tumor, cancer, neoplasia, e.g. cellular determinants, receptors, heat shock/stress proteins, A-protein, oligosaccharides, metabolites
- G01N33/57492—Immunoassay; Biospecific binding assay; Materials therefor for cancer involving compounds serving as markers for tumor, cancer, neoplasia, e.g. cellular determinants, receptors, heat shock/stress proteins, A-protein, oligosaccharides, metabolites involving compounds localized on the membrane of tumor or cancer cells
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/435—Assays involving biological materials from specific organisms or of a specific nature from animals; from humans
- G01N2333/705—Assays involving receptors, cell surface antigens or cell surface determinants
- G01N2333/70596—Molecules with a "CD"-designation not provided for elsewhere in G01N2333/705
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/52—Predicting or monitoring the response to treatment, e.g. for selection of therapy based on assay results in personalised medicine; Prognosis
Abstract
本发明涉及用于治疗胶质母细胞瘤的抑制胶质母细胞瘤之化合物,特别地涉及藤黄酸酰胺及其衍生物。此外,本申请公开了用于确定使用本发明化合物的治疗是否适用于患者的方法。
Description
本发明涉及用于治疗胶质母细胞瘤(glioblastoma)的抑制胶质母细胞瘤之化合物,特别地涉及藤黄酸酰胺及其衍生物。此外,本申请公开了用于确定使用本发明化合物的治疗是否适用于患者的方法。
背景技术
胶质母细胞瘤(GBM;世界卫生组织第IV级胶质瘤)是成人中最常见的原发性脑肿瘤。即使采用本领域中当前最先进的手术前和手术中神经成像技术的积极手术切除术(aggressive surgical resection)以及手术后放射治疗和化学治疗近来的进展,GBM患者的预后仍然不良。在当前最佳手术后治疗方案下的中位存活率(median survival rate)仅为15个月(Stupp等,2005)。因此,当务之急是鉴定新的候选治疗剂。定义新治疗方法的一个挑战是GBM的异质性。瘤内异质性源自遗传性和非遗传性表观遗传因素。此外,新兴的概念提出了异质肿瘤细胞表型产生自由小亚组的干细胞样细胞(stem-like cell)启动的连续进行异常和恶性分化过程。这些干细胞样细胞通过其以下能力来定义:(i)自我更新(self-renewal);(ii)在多种异种移植范例中的肿瘤启动和增殖;和(iii)多潜能性(multipotency),即其分化为星形细胞(astrocyte)、少突细胞(oligodendrocyte)和神经元的能力(Singh等,2004)。另外,假设这些细胞耐受当前大多数放射治疗及化学治疗,并且认为针对干细胞样细胞的治疗可以改善目前常规治疗的可怕记录(Dirks,2008;Chalmers,2007)。基于该考虑,已开始使通常应用于干细胞研究领域的体外技术适用于分离、扩增以及更好地表征具有干细胞特征的肿瘤细胞(Pardal等,2003,Glas等,2010)。细胞在贴附条件下作为单层培养物增殖,与“球状体(sphereoid)”培养物相比,其可提供显著的优点(Lee等,2006;Pollard等,2009)。
因此,可以将本发明的根本问题视为提供用于改善胶质母细胞瘤之化学治疗的新化合物。
发明概述
在第一方面,本发明涉及根据式I、II或III的化合物:
其用于治疗胶质母细胞瘤,其中:
X是羰基、亚甲基、羟基次甲基(hydroxymethinyl)、烷氧基次甲基(alkoxymethinyl)、氨基次甲基(aminomethinyl)、肟、腙、芳基腙或缩氨基脲(semicarbazone);
Y是羰基、亚甲基、羟基次甲基、烷氧基次甲基、氨基次甲基、肟、腙、芳基腙或缩氨基脲;
R1是氢、经取代的烷基、酰基(RaCO)、氨基甲酰基(RbRcNCO)或磺酰基(RdSO2);其中Ra是氢、经取代的低级烷基、经取代的芳基、经取代的低级芳烷基或N-琥珀酰亚胺基;Rb和Rc独立地为氢、经取代的杂烷基、经取代的低级烷基、经取代的芳基、经取代的杂芳基或经取代的低级芳烷基;
R2是异戊二烯基或氢;并且
R3如果存在,则为氢、卤素、羟基、经取代的烷基、环烷基、烷氧基、烷基硫基或氨基。
在另一个方面,本发明涉及包含根据式I、II或III之化合物的药物组合物,其用于治疗胶质母细胞瘤,所述式中X、Y、R1、R2以及R3具有上述含义。
在另一个方面,本发明涉及用于确定使用根据式I、II或III之化合物(其中X、Y、R1、R2以及R3具有上述含义)的治疗是否适用于患者的方法,所述方法包括以下步骤:
a)测定患者的肿瘤组织或肿瘤细胞样品中CD133的表达水平;
b)将步骤a)中测定的表达水平与参考值进行比较;以及
c)基于步骤b)的比较结果确定使用根据式I、II或III之化合物的治疗是否适用于患者,其中过表达表示所述治疗适用于所述患者。
发明详述
除非另有指明,否则本文使用的全部技术和科学术语与本领域普通技术人员通常理解的含义相同。
优选地,本文使用的术语如“A multilingual glossary ofbiotechnological terms:(IUPAC Recommendations)”,Leuenberger,H.G.W,Nagel,B.和Klbl,H编著(1995),Helvetica Chimica Acta,CH-4010Basel,Switzerland)中所述来定义。
在本说明书和所附权利要求书全文中,除非上下文另有需要,否则词语“包含(comprise)”及变体例如“包含(comprises)”和“包含(comprising)”将理解为表示包括指出的整数或步骤或者整数或步骤的组,但并不排除任何其他整数或步骤或者整数或步骤的组。
在本说明书全文中引用了多个文件。无论在上文还是下文中,本文所引用的每个文件(包括所有的专利、专利申请、科学出版物、制造商说明书、说明书等)均通过引用整体并入本文。本文不应被解释为承认本发明无权凭借在先发明而先于这些公开内容。
在本发明所涉及的研究中,背景技术中所述的改进的培养条件已被用于对4种患者特异性GBM细胞的原代培养物筛选其对多种化合物之施用的代谢应答。基于分析,31种化合物示出完全代谢应答。采用药效学测定、凋亡的膜联蛋白V(Annexin V)分析、生长动力学的研究、自我更新的量化、多能(multipotent)CSC、干细胞标志物的表达谱以及特定作用模式的研究来对最令人感兴趣的抗GBM化合物(即,藤黄酸酰胺、藤黄酸、扁蒴藤素(pristimerin)、盐酸表柔比星(epirubicinhydrochloride)、吐根碱(emetine)和氯硝柳胺(niclosamide))进行进一步验证。数据表明,这些物质是高效的抗GBM治疗剂。
因此,通过提供选自以下的用于治疗胶质母细胞瘤的化合物解决本发明的根本问题:藤黄酸酰胺、柔红霉素(daunorubicine)、藤黄酸、硫柳汞(thimerosal)、盐酸米托蒽醌(mitoxanthrone hydrochloride)、醋酸苯汞(phenylmercuric acetate)、放线菌素D(dactinomycin)、扁蒴藤素、盐酸表柔比星、硫酸长春新碱(vincristine sulfate)、吐根碱、紫杉醇(paclitaxel)、10-羟基喜树碱(10-hydroxycamptothecin)、多柔比星(doxorubicine)、秋水仙碱(colchicine)、喜树碱(camptothecin)、替尼泊苷(teniposide)、硫酸长春花碱(vinblastine sulfate)、丝裂霉素C(mitomycin C)、氟尿苷(floxuridine)、哇巴因(ouabain)、盐酸安西他滨(ancitabine hydrochloride)、盐酸奎纳克林(quinacrinehydrochloride)、氯硝柳胺、安吖啶(amsacrine)、硫鸟嘌呤(thioguanine)、鱼藤酮(rotenone)、盐酸阿克拉菌素(aklavine hydrochloride)、阿糖胞苷、氨甲喋呤以及苦鬼臼毒素(picropodophyllotoxin)。
在一个优选实施方案中,所述化合物是根据式I、II或III的化合物或其盐:
其中:
X是羰基、亚甲基、羟基次甲基、烷氧基次甲基、氨基次甲基、肟、腙、芳基腙或缩氨基脲,优选为羰基;
Y是羰基、亚甲基、羟基次甲基、烷氧基次甲基、氨基次甲基、肟、腙、芳基腙或缩氨基脲,优选为羰基;
R1是氢、经取代的烷基、酰基(RaCO-)或氨基甲酰基(RbRcNCO-);其中Ra是氢、经取代的低级烷基、经取代的芳基、经取代的低级芳烷基或N-琥珀酰亚胺基;Rb和Rc独立地为氢、经取代的杂烷基、经取代的低级烷基、经取代的芳基、经取代的杂芳基或经取代的低级芳烷基,优选为氢;
R2是异戊二烯基或氢,优选为异戊二烯基;并且
R3是氢、卤素、羟基、经取代的烷基、环烷基、烷氧基、烷基硫基或氨基,优选为氢。
优选地,烷基是直链或支链C1至C10烷基,更优选为C1至C6烷基。将包含不超过6个碳原子的烷基称为“低级烷基”。优选的烷基包括甲基、乙基、丙基、异丙基、丁基、仲丁基、叔丁基、3-戊基、己基以及辛基。
优选的烷氧基包含被上述烷基之一所取代的氧,优选地被甲基、乙基、丙基、异丙基、丁基、仲丁基、叔丁基、3-戊基、己基以及辛基取代,更优选地被甲基取代。
优选的烷基硫基基团包含被上述烷基之一取代的硫,优选地被甲基、乙基、丙基、异丙基、丁基、仲丁基、叔丁基、3-戊基、己基以及辛基取代,更优选地被甲基、亚砜和砜取代。
优选的氨基包括-NH2、-NHR11、-NR11R12,其中R11和R12是C1至C10烷基,优选地选自甲基、乙基、丙基、异丙基、丁基、仲丁基、叔丁基、3-戊基、己基以及辛基,最优选甲基或环烷基;或者R11和R12与N组合以形成环结构,优选5至7元环结构,例如哌啶;或者R11和R12与N及其他杂原子组合以形成饱和的、经取代的的或者部分饱和的5至7元杂环基团。优选的杂原子包括O、N和S。
烷基的优选取代基包含卤素、羟基、羧基、烷氧基羰基、氨基、硝基、氰基、C1至C6酰基氨基、C1至C6氨基酰基、C1至C6酰基氧基、C1至C6烷氧基、芳基氧基、烷基硫基、C6至C10芳基、C4至C7环烷基、C2至C6烯基以及C2至C6炔基中的至少一个。
芳基、芳烷基和杂芳基的优选取代基包含酰基、亚烷基二氧基(-OCH2O-)、卤素、C1至C6卤代烷基、C6至C10芳基、C4至C7环烷基、C1至C6烷基、C2至C6烯基、C2至C6炔基、C1至C6羟基烷基、硝基、氨基、脲基、氰基、C1至C6酰基氨基、巯基、羟基、C1至C6烷氧基、C1至C6酰基氧基、叠氮基以及羧基中的至少一个。
优选的杂烷基包含1至10个碳原子和1至3个杂原子。杂烷基可以被取代。优选的取代基包含酰基、亚烷基二氧基(-OCH2O-)、卤素、C1至C6卤代烷基、C6至C10芳基、C4至C7环烷基、C1至C6烷基、C2至C6烯基、C2至C6炔基、C1至C6羟基烷基、硝基、氨基、氰基、C1至C6酰基氨基、巯基、羟基、C1至C6烷氧基、C1至C6酰基氧基、叠氮基以及羧基中的至少一个。
优选的芳基包括C6至C14芳基,更特别地C6至C10芳基。更优选地,芳基是苯基、萘基(naphtyl)、菲基、蒽基、茚基、甘菊环基、联苯基(bephenyl)、联苯基烯基或芴基。
优选的卤素包含氟、碘、氯和溴。
优选的环烷基是C3至C8环烷基,特别是环戊基、环己基、环庚基和环辛基。还优选相应的环烯基,特别是环戊烯基、环己烯基、环庚烯基和环辛烯基。
优选的芳烷基包括被任意上述C6至C14芳基取代的任意上述C1至C10烷基。特别优选苄基、苯乙基和萘甲基。
优选的杂芳基包括:噻吩基、苯并[b]噻吩基、萘并[2,3-b]噻吩基、噻蒽基、呋喃基、吡喃基、异苯并呋喃基、苯并吡喃基、呫吨基(xanthenyl)、氧硫杂蒽基(phenoxanthiinyl)、2H-吡咯基、吡咯基、咪唑基、吡唑基、吡啶基、吡嗪基、嘧啶基、哒嗪基、吲嗪基、异吲哚基、3H-吲哚基、吲哚基、吲唑基、嘌呤基、4H-喹嗪基、异喹啉基、喹啉基、酞嗪基(phtalzinyl)、萘啶基(naphthyridinyl)、喹喔啉基(quinozalinyl)、噌啉基、蝶啶基、咔唑基、β-咔啉基、菲啶基(phenanthridinyl)、吖啶基、permidinyl、邻二氮杂菲基(phenanthrolinyl)、吩嗪基、异噻唑基、吩噻嗪酮基(phenothiazonyl)、异唑基、呋吖基、吩嗪基、1,4-二氢喹喔啉-2,3-二酮、7-氨基异香豆素、吡啶并[1,2a]嘧啶-4-酮、1,2-苯并异唑-3-基、苯并咪唑基、2-羟吲哚基以及2-氧代苯并咪唑基。杂芳基的优选取代基包括杂芳基、杂环、烷基、芳烷基、环烷基、烷氧基羰基、氨基甲酰基、芳基以及C1至C6氨基酰基中的至少一个。
在一个更优选的实施方案中,所述化合物选自:如式I所定义的化合物,其中R1是氢,R2是异戊二烯基,X是羰基,Y是羰基;如式II所定义的化合物,其中R1是氢,R2是异戊二烯基,R3是氢,X和Y是羟基次甲基;如式II所定义的化合物,其中R1是氢,R2是异戊二烯基,X是羰基,Y是羟基次甲基;如式I所定义的化合物,其中R1是乙酰基,R2是异戊二烯基,X是羰基,Y是羰基;以及如式III所定义的化合物,其中R1是氢,R2是异戊二烯基,X是羰基。
优选地,根据式(I)和(II)的化合物具有式(Ia)和(IIa)所示的立体化学结构:
在大多数优选实施方案中,所述化合物如式(I)或式(Ia)所定义,并且R1是氢,R2是异戊二烯基,X是羰基,Y是羰基。将由式(Ia)表征的化合物称为“藤黄酸酰胺”。
术语“胶质母细胞瘤”或“多形性胶质母细胞瘤”是指涉及胶质细胞的原发性脑肿瘤。优选地,基于增殖性胶质瘤细胞(proliferative glialtumor cell)、血管增生和优先坏死组织区域(preferentially necrotic tissuearea)的组织学存在来诊断胶质母细胞瘤(进一步分类请见:Louis,D.N.,Ohgaki,H.,Wiestler,O.D.,Cavenee,W.K.,Burger,P.C.,Jouvet,A.,Scheithauer,B.W.,以及Kleihues,P.2007.The2007WHO classification oftumours of the central nervous system.Acta Neuropathol114:97-109)。
本发明所涉及的研究证实,本发明的化合物对以下肿瘤同样有效:同一患者的原发性和复发性胶质母细胞瘤、基因O6-甲基鸟嘌呤-甲基转移酶(methylguanin-methyltransferase,MGMT)启动子之甲基化增加和减少的胶质母细胞瘤、具有以及不具有突变之p53的胶质母细胞瘤;以及具有野生型B细胞抑制剂中核因子κ轻链多肽基因增强子(nuclear factorof kappa light polypeptide gene enhancer in B-cells inhibitor,NFKBIA)以及NFKBIA杂合缺失(heterocygous deletion)的胶质母细胞瘤。
因此,优选地,术语“胶质母细胞瘤”是指:与MGMT-启动子的甲基化状态无关的胶质母细胞瘤、具有和不具有突变之p53的胶质母细胞瘤、编码NFKBIA之基因发生改变或未发生改变的胶质母细胞瘤、编码表皮生长因子受体(epidermal growth factor receptor,EGFR)之基因发生改变和未发生改变的胶质母细胞瘤、编码血小板衍生生长因子受体之基因发生改变和未发生改变(alterations of the gene encodingplatelet-derived growth factor receptor,PDGFRA)的胶质母细胞瘤、编码异柠檬酸脱氢酶1(isocitrate dehydrogenase1,IDHI)之基因发生改变和未发生改变的胶质母细胞瘤以及编码1型神经纤维瘤(neurofibromatosis type1,NF1)之基因发生改变和未发生改变的胶质母细胞瘤。应理解,术语“胶质母细胞瘤”还包括特征在于上述特征中之至少两种任意组合的胶质母细胞瘤。
术语“改变”是指所讨论之基因的突变、缺失和其他拷贝的存在。突变和缺失可以是纯合的或杂合的。术语“胶质母细胞瘤”还指原发性以及复发性疾病。
在一个优选实施方案中,胶质母细胞瘤包含具有干细胞样性质的细胞。优选地,具有干细胞样性质的细胞通过以下三个特征来定义:(i)多潜能性;(ii)自我更新的能力和(iii)致瘤性(tumorigenicity)。可以优选地通过测定选自以下的至少一种基因的表达状态来检测具有前述特征的细胞:CD133、ATP-结合盒亚家族G成员2(ATP-binding cassettesub-family G member2,ABCG2)、醛脱氢酶1(dehydrogenase1,ALDH1A1)、musashi同源物1(musashi homolog1,MSI-1)、巢蛋白(nestin)和性别决定区Y-box2(sex determining region Y-box2,SOX-2)。根据本发明,最优选的标志物是CD133。
在本发明的一个特别优选的实施方案中,胶质母细胞瘤所包含的具有干细胞样性质之细胞的比例大于通常见于胶质母细胞瘤中的比例。优选地,通过测量所述细胞占有代表性的胶质母细胞瘤数目的平均比例来定义通常见于胶质母细胞瘤中的干细胞样细胞的比例。优选地,该平均比例基于在至少20、至少50或至少100个胶质母细胞瘤中干细胞样细胞的比例来确定。优选地,随机选择用于定义干细胞样细胞之平均比例的胶质母细胞瘤。
优选地,通过以下来表征具有干细胞样性质的细胞:与不具有干细胞样性质之细胞相比较,所引用的上述基因中的至少一种过表达。因为肿瘤中干细胞样细胞之比例通常较小(低于1%),所以还可以将肿瘤活检之任意选择的部分中所讨论基因的表达用作比较的基础。
一种优选的用于测定上述基因在细胞或细胞组中的表达状态的方法是流式细胞术。该方法对于本领域技术人员而言是公知的。其良好适用于区分在至少一个基因(优选地在细胞表面上)的表达方面不同的细胞群体。基于该结果,可以确定定义某一基因在所讨论之细胞或细胞组中是否过表达的合适的阈值。
可以通过进行对照实验来测试所确定阈值的正确性,所述对照实验示出根据流式细胞术指定为“干细胞样”的细胞事实上具有以下特性:(i)多潜能性;(ii)自我更新的能力和(iii)致瘤性。根据本发明,不需要每个指定为“干细胞样”的细胞具有所述能力而未指定为“干细胞样”的细胞均不具有所述能力。但是,需要的是与未指定为“干细胞样”的细胞群体相比,在统计学上显著较高比例的“干细胞样”细胞具有所述性质。这可以通过公知的统计学测试例如t检验来确认。
优选地,术语“过表达”是指与来自相同肿瘤的不具有干细胞样性质的细胞相比或者与肿瘤之一部分中基因的平均表达相比,表达提高至少2倍、至少3倍或至少4倍。在一个更优选的实施方案中,上述基因中至少之一的任意表达表明所讨论的细胞或细胞组具有干细胞样性质。
在本发明的一个实施方案中,上述化合物表示为可药用盐。术语“可药用盐”是指本发明化合物的盐。本发明化合物的合适的可药用盐包括酸加成盐,例如其可以通过将本发明化合物的溶液与可药用酸的溶液混合来形成,所述可药用酸例如盐酸、硫酸、富马酸、马来酸、琥珀酸、乙酸、苯甲酸、柠檬酸、酒石酸、碳酸或磷酸。此外,其中本发明化合物具有酸性部分,其合适的可药用盐可以包括碱金属盐(例如,钠盐或钾盐);碱土金属盐(例如,钙盐或镁盐);以及与合适的有机配体形成的盐(例如使用反阴离子例如卤素、氢氧根、羧酸根、硫酸根、磷酸根、硝酸根、烷基磺酸根和芳基磺酸根形成的铵、季铵以及胺阳离子)。可药用盐的示例性实例包括但不限于:乙酸盐、己二酸盐、藻酸盐、抗坏血酸盐、天冬氨酸盐、苯磺酸盐、苯甲酸盐、碳酸氢盐、硫酸氢盐、酒石酸氢盐、硼酸盐、溴化物、丁酸盐、乙二胺四乙酸钙、樟脑酸盐、樟脑磺酸盐、右旋樟脑磺酸盐(camsylate)、碳酸盐、氯化物、柠檬酸盐、克拉维酸盐、环戊烷丙酸盐、二葡糖酸盐、二盐酸盐、十二烷基硫酸盐、乙二胺四乙酸盐、乙二磺酸盐、依托酸盐(estolate)、乙磺酸盐(esylate)、乙烷磺酸盐、甲酸盐、富马酸盐、葡庚糖酸盐(gluceptate)、葡庚糖酸盐(glucoheptonate)、葡糖酸盐、谷氨酸盐、甘油磷酸盐、羟乙酰氨基苯胂酸盐(glycolylarsanilate)、半硫酸盐(hemisulfate)、庚酸盐、己酸盐、己基间苯二酚盐、海巴明、氢溴酸盐、盐酸盐、氢碘酸盐、2-羟基-乙烷磺酸盐、羟基萘甲酸盐、碘化物、异硫氰酸盐、乳酸盐、乳糖酸盐、月桂酸盐、月桂基硫酸盐、苹果酸盐、马来酸盐、丙二酸盐、扁桃酸盐、甲磺酸盐、甲烷磺酸盐、甲基硫酸盐、粘酸盐(mucate)、2-萘磺酸盐、萘磺酸盐(napsylate)、烟酸盐、硝酸盐、N-甲基葡糖胺铵盐、油酸盐、草酸盐、双羟萘酸盐(恩波酸盐(embonate))、棕榈酸盐、泛酸盐、果胶酸盐、过硫酸盐、3-苯基丙酸盐、磷酸盐/二磷酸盐、苦味酸盐、新戊酸盐、聚半乳糖醛酸盐、丙酸盐、水杨酸盐、硬脂酸盐、硫酸盐、碱式乙酸盐(subacetate)、琥珀酸盐、鞣酸盐、酒石酸盐、茶氯酸盐(teoclate)、甲苯磺酸盐、三乙基碘、十一烷酸盐、戊酸盐等(参见,例如,Berge,S.M.等,“Pharmaceutical Salts”,Journalof Pharmaceutical Science,1977,66,1-19)。本发明的某些特定化合物包含碱性官能性和酸性官能性二者,其允许化合物转化为碱加成盐或酸加成盐。
可以通过用常规方式使盐与碱或酸接触并分离母体化合物来再生成所述化合物的中性形式。所述化合物的母体形式在某些物理性质方面(例如,在极性溶剂中的溶解度)不同于多种盐形式,但在其他方面所述盐出于本发明的目的而等同于所述化合物的母体形式。
除盐形式之外,本发明还提供前药形式的化合物。本文所述化合物的前药是在生理条件下易于经历化学变化以提供通式(I)至(III)的化合物的那些化合物。前药是药理学活性的或失活的化合物,在向患者施用前药之后前药通过体内生理作用(例如,水解、代谢等)化学修饰成本发明化合物。此外,可以在离体环境中通过化学或生化方法将前药转化为本发明的化合物。例如,当与合适的酶一起置于透皮贴剂储库(reservoir)中时,前药可以缓慢地转化为本发明的化合物。本领域技术人员公知制备和使用前药所涉及的合适性和技术。对于涉及酯之前药的一般性讨论,参见Svensson和Tunek,Drug Metabolism Reviews16.5(1988)以及Bundgaard,Design of Prodrugs,Elsevier(1985)。掩饰的(masked)酸性阴离子的实例包括多种酯,例如烷基(例如甲基、乙基)酯、环烷基(例如,环己基)酯、芳烷基(例如,苄基、对甲氧基苄基)酯和烷基羰基氧基烷基(例如,新戊酰基氧基甲基)酯。已将胺掩饰为经芳基羰基氧基甲基取代的衍生物,其在体内被酯酶切割,释放游离药物和甲醛(BungaardJ.Med.Chem.2503(1989))。此外,用N-酰氧基甲基基团掩饰含酸性NH基团(例如咪唑、酰亚胺、吲哚等)的药物(Bundgaard Design of Prodrugs,Elsevier(1985))。已将羟基掩饰为酯和醚。EP 0 039 051(Sloan and Little,Apr.11,1981)公开了曼尼希碱(Mannich-base)异羟肟酸前药、其制备及用途。
本发明化合物以及根据本发明用于其制备的原料可以按照本文所示来合成,或者在本领域技术人员已知并且适用于所述反应的条件下,通过本领域技术人员已知的方法和标准步骤来合成,即,如文献(例如,标准工作中的,例如Houben-Weyl,Methoden der organischen Chemie[Methods of Organic Chemistry],Georg-Thieme-Verlag,Stuttgart)中所述。
如果期望的话,还可以通过以下所述来原位形成原料:不将原料与反应混合物分离,而是立即将其进一步转化为本发明的化合物。另一方面,可以逐步实施反应。应注意,当涉及具有非特异性立体化学之化合物的制备时,示出一般步骤。但是,这样的过程一般适用于具有特定立体化学的那些化合物,例如,其中立体中心处的立体化学为(S)或(R)。此外,具有一种立体化学(例如,(R))的化合物可以常常用于使用公知方法(例如,通过反转(inversion))产生具有相反立体化学(即,(S))的那些化合物。
本发明的某些化合物可以以未溶剂化形式以及溶剂化形式(包括水合形式)存在。一般来说,溶剂化形式等同于未溶剂化形式,并且旨在被包括在本发明的范围内。本发明的某些化合物可以以多晶型或无定形形式存在。一般来说,对于本发明所包括的用途而言,所有物理形式是等同的,并且旨在被包括在本发明的范围内。
本发明的某些化合物具有不对称碳原子(光学中心)或双键。外消旋体、对映体、非对映体、几何异构体以及单个异构体均旨在被包括在本发明的范围内。因此,本发明的化合物包括立体异构体的混合物,尤其是对映体的混合物;以及经纯化的立体异构体,尤其是经纯化的对映体;或者富含立体异构体的混合物,尤其是富含对映体的混合物。由下式(I)至(III)所示的化合物的单个异构体及其任何完全或部分平衡的混合物也被包括在本发明的范围内。本发明还包括由下式所示化合物的单个异构体及其异构体(其中一个或更多个手性中心是反转的)的混合物。此外,应理解,式(I)至(III)的化合物的所有互变异构体和互变异构体的混合物被包括在式(I)至(III)(并且优选其相应的式和子式)之化合物的范围内。
可以通过本身已知的方法机械地或化学地将所得外消旋体拆分为异构体。非对映体优选地通过与光学活性拆分剂反应而由外消旋混合物形成。
合适的拆分剂的实例是光学活性酸,例如酒石酸、二乙酰基酒石酸、二苯甲酰基酒石酸、扁桃酸、苹果酸、乳酸或多种光学活性樟脑磺酸(例如,樟脑磺酸)的D和L形式。同样有利的是借助于填充有光学活性拆分剂(例如二硝基苯甲酰基苯基甘氨酸)的柱的对映体拆分;合适的洗脱剂的实例是己烷/异丙醇/乙腈混合物。
还可以通过标准纯化方法(例如,色谱或分级结晶)来实施非对映体拆分。
还可以使用已为光学活性的原料通过上述方法获得式(I)至(III)的光学活性化合物。
在另一方面,本发明涉及包含根据式I、Ia、II、IIa或III(其中X、Y、R1、R2以及R3具有上述含义和优选的含义)之化合物的药物组合物,其用于治疗胶质母细胞瘤。
本申请所提及的“药物组合物”包含至少一种本发明的化合物和至少一种可药用载体。
就由本发明的化合物制备药物组合物而言,可药用载体可以为固体或液体。固体形式制剂包括散剂、片剂、丸剂、胶囊剂、扁囊剂、栓剂和可分散颗粒剂。固体载体可以是一种或更多种物质,其还可以作为稀释剂、矫味剂、粘合剂、防腐剂、片剂崩解剂或包封材料。
在散剂中,载体是细粒状的固体,其处于与细粒状的活性组分的混合物中。在片剂中,活性组分与具有必要粘合性质的载体以合适的比例混合并且以期望的形状和大小来压制。
所述散剂和片剂优选地包含5%至80%、更优选20%至70%的活性化合物。合适的载体是碳酸镁、硬脂酸镁、滑石粉、糖、乳糖、果胶、糊精、淀粉、明胶、西黄蓍胶、甲基纤维素、羧甲基纤维素钠、低熔点蜡、可可脂等。
术语“制备”旨在包括配制活性化合物与作为载体的包封材料以提供胶囊剂,其中,载体包围活性组分(具有或不具有其他载体)并且因此与其缔合。类似地,包括扁囊剂和锭剂(lozenge)。可以将片剂、散剂、胶囊剂、丸剂、扁囊剂和锭剂用作适用于经口施用的固体剂型。
就制备栓剂而言,首先熔化低熔点蜡(例如脂肪酸甘油酯或可可脂的混合物),并使活性成分在其中均匀分散(例如通过搅拌)。然后,将熔融的均匀混合物倒入合适大小的模件中使其冷却,从而固化。
液体形式制剂包括溶液剂、混悬剂和乳剂,例如水或水/丙二醇溶液。液体形式特别优选用于局部施用于眼。就肠胃外注射而言,液体制剂可以在溶液中配制为丙二醇水溶液。
适用于经口使用的水溶液可以通过以下来制备:将活性组分溶解于水中,并根据需要来添加合适的着色剂、矫味剂、稳定剂和增稠剂。适用于经口使用的水性混悬剂可通过以下来制备:将细粒状的活性组分与粘性材料以及其他公知的助悬剂一起分散于水中,所述粘性材料例如天然的或合成的树胶、树脂、甲基纤维素、羧甲基纤维素钠。
还包括固体形式制剂,其旨在在使用之前不久将液体形式制剂转化用于经口施用。这样的液体形式包括溶液剂、混悬剂和乳剂。除活性组分外,这些制剂还可包含着色剂、矫味剂、稳定剂、缓冲剂、人工的和天然的甜味剂、分散剂、增稠剂、增溶剂等。
药物制剂优选地为单位剂型。在这样的形式中,制剂细粒状为含有适量活性组分的单位计量。单位剂型可以为包装制剂,所述包装包含离散量的制剂,例如小瓶中或安瓿中的包装片剂、胶囊剂和散剂。此外,单位剂型可以是胶囊剂、片剂、扁囊剂或锭剂本身,或者其可以为合适数目的任意的这些包装形式。
在本发明的一个优选实施方案中,所述药物组合物还包含至少一种其他的抑制细胞生长的化合物或细胞毒性化合物。所述其他化合物选自:替莫唑胺、柔红霉素、藤黄酸酰胺、藤黄酸、硫柳汞、盐酸米托蒽醌、醋酸苯汞、放线菌素D、扁蒴藤素、盐酸表柔比星、硫酸长春新碱、吐根碱、紫杉醇、10-羟基喜树碱、多柔比星、秋水仙碱、喜树碱、替尼泊苷、硫酸长春花碱、丝裂霉素C、氟尿苷、哇巴因、盐酸安西他滨、盐酸奎纳克林、氯硝柳胺、安吖啶、硫鸟嘌呤、鱼藤酮、盐酸阿克拉菌素、阿糖胞苷、氨甲喋呤以及苦鬼臼毒素。
另一些优选的其他抑制细胞生长的化合物或细胞毒性化合物包括抗雌激素物(anti-estrogen)例如氟维司群、他莫西芬或雷洛昔芬;拓扑异构酶I或II的任何抑制剂,例如喜树碱(拓扑I)或依托泊苷(拓扑II);通过抑制芳香化酶活性起作用的任何化合物,例如阿那曲唑或来曲唑;干扰HER2信号转导的任何制剂,例如赫赛汀;与DNA相互螯合的任何化合物,例如多柔比星。特别优选的抑制细胞生长的药物或细胞毒性药物(其可以与本发明化合物组合)是烷基化物质、抗代谢物、抗生素、埃博霉素、核受体激动剂和拮抗剂、抗雄激素物、抗雌激素物、铂化合物、激素和抗激素、干扰素和细胞周期依赖性蛋白激酶(cell cycle-dependent proteinkinase,CDK)抑制剂、环氧合酶和/或脂氧合酶的抑制剂、生物源的脂肪酸和脂肪酸衍生物(包括前列腺素和白三烯)、蛋白激酶抑制剂、蛋白质磷酸酶抑制剂、脂质激酶抑制剂、铂配位复合物、乙烯亚氨(ethyleneimene)、甲基三聚氰胺、三嗪(trazine)、长春花生物碱、嘧啶类似物、嘌呤类似物、烷基磺酸盐,叶酸类似物、蒽二酮、经取代的脲、甲基肼衍生物(特别是醋地砜(acediasulfone))、阿克拉霉素、安巴腙、氨鲁米特、L-天冬酰胺酶、硫唑嘌呤、博来霉素、白消安、亚叶酸钙、卡铂、卡培他滨、卡莫司汀、塞来考昔、苯丁酸氮芥、顺铂、克拉屈滨、环磷酰胺、阿糖胞苷、达卡巴嗪、更生霉素氨苯砜、柔红霉素、双溴丙脒、二乙基己烯雌酚(diethylstilbestrole)、多西他赛、多柔比星、烯二炔类、表柔比星、埃坡霉素B、埃坡霉素D、磷酸雌莫司汀(estramucinphosphate)、雌激素、乙炔雌二醇、依托泊苷、夫拉平度、氟尿苷、氟达拉滨、氟尿嘧啶、氟甲睾酮、氟他胺磷雌酚(fosfestrol)、呋喃唑酮、吉西他滨、促性腺激素释放激素类似物、六甲密胺、羟基脲(hydroxycarbamide)、羟甲基硝基呋喃妥因、己酸羟孕酮(hydroxyprogesteronecaproat)、羟基脲、伊达比星、碘苷、异环磷酰胺、干扰素γ、伊立替康、亮丙瑞林(leuprolide)、洛莫司汀、勒托替康(lurtotecan)、硫酸磺胺米隆乙醇酰胺(olamide)、氮芥、醋酸甲羟孕酮、醋酸甲地孕酮(megastrolacetate)、美法仑、米帕林、巯基嘌呤、氨甲蝶呤、甲硝唑、丝裂霉素C、米托鬼臼肼、米托坦、米托蒽醌、光神霉素、萘啶酸、硝呋拉太(nifuratel)、硝呋酚酰肼、硝呋三嗪(nifuralazine)、硝呋替莫、嘧啶亚硝脲、尼莫拉唑(ninorazole)、硝基呋喃妥因、氮芥(nitrogen mustard)、卵粘蛋白(oleomucin)、喹酸(oxolinic acid)、喷他脒、喷司他丁、非那吡啶、酞磺胺噻唑、哌泊溴烷、泼尼莫司汀、强的松、preussin、甲苄肼、乙胺嘧啶、雷替曲塞、雷帕霉素、罗非考昔(rofecoxib)、罗格列酮、柳氮磺胺吡啶、氯化scriflavinium、司莫司汀链脲霉素、磺胺脲、磺胺醋酰、磺胺氯达嗪(sulfachlopyridazine)、磺胺嘧啶、磺胺戊烯、磺胺地索辛、磺胺乙二唑、磺胺异唑、磺胺胍、磺胺胍诺、磺胺甲二唑、磺胺甲基异唑、磺胺甲唑、磺胺甲氧二嗪、磺胺甲氧嗪、磺胺唑、磺胺、磺胺培苯、磺胺苯吡唑、磺胺噻唑、磺胺索嘧啶、星形孢菌素、他莫西芬、紫杉醇、替尼泊苷、特替泊苷(tertiposide)、睾内酯、丙酸睾酮、硫鸟嘌呤、塞替派、替硝唑、拓扑替康、三亚胺醌(triaziquone)、曲奥舒凡(treosulfan)、甲氧苄啶、曲磷胺(trofosfamide)、UCN-01、长春碱、长春新碱、长春地辛、长春碱、长春瑞滨以及佐柔比星,或其各自的衍生物或类似物。
在本发明的一个特别优选的实施方案中,所述其他抑制细胞生长的化合物或细胞毒性化合物是替莫唑胺。
盐/酯
根据本发明组合物中的化合物或可以使用的化合物可以作为盐或酯存在,特别是可药用盐或酯。本发明化合物的可药用盐包括其合适的酸加成盐或碱盐。合适的可药用盐的综述可见于Berge等,J Pharm Sci,66,1-19(1977)中。例如,与以下形成盐:强无机酸,例如矿物酸,例如硫酸、磷酸或氢卤酸;强有机羧酸,例如具有1至4个碳原子的烷烃羧酸(例如,乙酸),其未被取代或者被取代(例如,被卤素取代);饱和的或不饱和的二元羧酸,例如草酸、丙二酸、琥珀酸、马来酸、富马酸、邻苯二甲酸或四邻苯二甲酸;羟基羧酸,例如抗坏血酸、乙醇酸、乳酸、苹果酸、酒石酸或柠檬酸;氨基酸,例如天冬氨酸或谷氨酸;苯甲酸;或有机磺酸,例如(C1-C4)-烷基-或芳基-磺酸,其未被取代或者被取代(例如被卤素取代),例如甲磺酸或对甲苯磺酸。
根据被酯化的官能团,使用有机酸或醇/氢氧化物形成酯。有机酸包括羧酸,例如具有1至12个碳原子的烷烃羧酸,其未被取代或者被取代(例如,被卤素取代),例如乙酸;饱和的或不饱和的二元羧酸,例如草酸、丙二酸、琥珀酸、马来酸、富马酸、邻苯二甲酸或四邻苯二甲酸;羟基羧酸,例如抗坏血酸、乙醇酸、乳酸、苹果酸、酒石酸或柠檬酸;氨基酸,例如天冬氨酸或谷氨酸;苯甲酸;或有机磺酸,例如(C1-C4)-烷基-或芳基-磺酸,其未被取代或者被取代(例如被卤素取代),例如甲磺酸或对甲苯磺酸。合适的氢氧化物包括无机氢氧化物,例如氢氧化钠、氢氧化钾、氢氧化钙、氢氧化铝。醇包括具有1至12个碳原子的烷烃醇,其可以是未被取代的或被取代的,例如,被卤素取代。
同位素
本发明的化合物还可在构成所述化合物之一个或更多个原子处包含非天然比例的原子同位素。本发明试剂或其可药用盐的同位素变化定义如下:其中至少一个原子被具有相同原子序数但原子量不同于天然常见之原子量的原子所替代。可并入所述试剂及其可药用盐的同位素的实例包括氢、碳、氮、氧、磷、硫、氟和氯的同位素,分别例如2H、3H、13C、14C、15N、17O、18O、31P、32P、35S、18F以及36Cl。所述试剂及其可药用盐的某些同位素变化(例如,其中并入放射性同位素例如3H或14C的那些)可用于药物和/或底物组织分布研究。特别优选氚化的(即,3H)和碳-14(即,14C)同位素,这是因为它们的易于制备性和可检测性。此外,用同位素(例如,氘,即3H)取代可以提供由较大代谢稳定性导致的某些治疗优点,例如,体内半衰期增加或剂量需求降低,因此在某些情形下可以是优选的。本发明试剂和本发明的其可药用盐的同位素变化一般可以通过常规方法使用合适试剂的适当同位素变化来制备。
本发明化合物和组合物的所有同位素改变(无论是否为放射性的)均旨在被包括在本发明范围内。
溶剂合物
本发明还包括根据本发明可以使用的任意通式(I)至(III)的组合物或化合物中的化合物的溶剂合物形式。权利要求中使用的术语包括这些形式。
多晶型
本发明还涉及本发明组合物中的化合物或者根据本发明可以使用之式(I)的化合物的多种结晶形式、多晶型形式和无水/含水形式。在制药工业中已良好建立了以下事实:可以通过对从所述化合物合成制备所用溶剂中纯化和/或分离的方法进行稍微改变,以分离任意这些形式的化合物。
施用
根据本发明的化合物可以通过多种公知途径来施用,包括经口施用、直肠施用、胃内施用、颅内施用和肠胃外施用,例如静脉内、肌内、鼻内、皮内、皮下以及类似的施用途径。优选肠胃外施用,特别是静脉内施用,优选地通过积存注射(depot injection)。根据施用途径,需要不同药物制剂,并且其中一些可能需要将保护性包衣施用于药物制剂以防止本发明化合物例如在消化道中降解。
因此,优选地,本发明化合物被配制为糖浆剂、输注溶液剂或注射溶液剂、片剂、胶囊剂、囊片(capslet)、锭剂、脂质体、栓剂、硬膏剂(plaster)、创可贴(band-aid)、延迟胶囊剂(retard capsule)、散剂或缓慢释放制剂。优选地,稀释剂是水、缓冲剂、缓冲盐溶液或盐溶液,载体优选地选自可可脂和vitebesole。
用于施用本发明化合物的特别优选的药物形式是适合于可注射使用的形式并且包括用于临时制备无菌可注射溶液或分散剂的无菌水溶液或分散剂和无菌散剂。在所有情况下,这些最终的溶液或分散剂形式必须是无菌的并且是流体。通常,这样的溶液或分散剂将包含溶剂或分散介质,其包括例如水缓冲的水溶液,例如生物可相容的缓冲剂;乙醇;多元醇,例如甘油、丙二醇、聚乙二醇、其合适的混合物;表面活性剂或植物油。还可以将本发明化合物配制为脂质体,特别地用于肠胃外施用。如果与游离药物相比,则脂质体提供如下优点:增加的循环半衰期和延长的封闭药物的更均匀释放。
可以通过本领域已知的许多技术来完成输注溶液或注射溶液的灭菌,所述技术包括但不限于添加防腐剂例如抗细菌剂或抗真菌剂,例如尼泊金(parabene)、氯丁醇、苯酚、山梨酸或硫柳汞(thimersal)。此外,可以在输注溶液或注射溶液中加入等渗剂,例如糖或盐,特别是氯化钠。
含有一种或若干种本发明化合物的无菌注射溶液的生产通过以下来完成:在合适的溶剂中根据需要加入所需量的各种化合物和上文列举的多种成分,之后灭菌。为了获得无菌粉末,上述溶液必要时经真空干燥或冻干。本发明的优选稀释剂是水、生理上可接受的缓冲液、生理上可接受的缓冲盐溶液或盐溶液。优选的载体是可可脂和vitebesole。除上文已提到的优选赋形剂外,待与本发明化合物的多种药物形式一起使用的赋形剂可非限制性地选自以下物质:
a)粘合剂,例如乳糖、甘露醇、结晶山梨醇、二碱式磷酸盐(dibasicphosphate)、磷酸钙、糖、微晶纤维素、羧甲基纤维素、羟乙基纤维素、聚乙烯吡咯烷酮等;
b)润滑剂,例如硬脂酸镁、滑石粉、硬脂酸钙、硬脂酸锌、硬脂酸、氢化植物油、亮氨酸、甘油酯和硬脂酰富马酸钠;
c)崩解剂,例如淀粉、交联羧甲纤维素(croscaramellose)、甲基纤维素钠、琼脂、膨润土、藻酸、羧甲基纤维素、聚乙烯吡咯烷酮等。
其他合适的赋形剂可见于American Pharmaceutical Association出版的Handbook of Pharmaceutical Excipients,其通过引用并入本文。
应理解,根据疾病的严重程度和可以使用本发明化合物之一治疗的特定类型以及待治疗的各个患者(例如患者的一般健康状态)等,需要不同剂量的各种化合物来引起治疗或预防作用。适当剂量的确定在主治医生的判断范围内。
如本领域已知的,药物有效量的给定组合物还将取决于施用途径。一般来说,如果通过胃肠道施用,则所需量较高;例如通过栓剂、直肠或者通过胃内探针(intragastric probe),如果施用途径为肠胃外(例如,静脉内),则所需量较低。
在本发明的含义范围内,只要取代或变化的组合导致稳定的或化学可行的化合物,就可允许这样的组合。稳定的化合物或化学可行的化合物是在不存在水分或其他化学反应性的条件下,在40℃或更低的温度下保持至少一周而基本上不改变的化合物。本发明还设想本文公开的化合物的任何含碱性氮之基团的季铵化。可以通过这样的季铵化获得水溶性或油溶性或可分散性产物。
本发明的另一个实施方案涉及用于确定使用根据式I、II或III的化合物(其中,X、Y、R1、R2以及R3具有上述含义)的治疗是否适用于患者的方法,其包括以下步骤:
a)测定患者的肿瘤组织或肿瘤细胞样品中选自以下之基因的表达水平:CD133、ATP-结合盒亚家族G成员2(ABCG2)、醛脱氢酶1(ALDH1A1)、musashi同源物1(MSI-1)、巢蛋白和性别决定区Y-box2(SOX-2);
b)将步骤a)中所测定的表达水平与参考值进行比较;以及
c)基于步骤b)的比较结果确定用根据式I、II或III的化合物的治疗是否适用于患者,其中过表达表示所述治疗适用于患者。
优选地,本发明的方法在体外进行。优选地,所述患者患有胶质母细胞瘤。
用于确定基因表达水平的方法对于本领域技术人员而言是公知的。可以通过测量所讨论之基因的mRNA-转录物的量来确定基因表达,并且其还可以通过测量由所述基因编码之蛋白质的量来确定。基于所产生的mRNA-转录物之量的测量的优选方法包括实时定量PCR和基于例如微阵列之技术的杂交。用于测量特定蛋白质之量的优选方法包括免疫方法例如酶联免疫吸附测定(ELISA)。尤其优选的是使用允许确定单个细胞之基因表达水平的方法,这是因为在通常情况下,肿瘤中只有很少的细胞是干细胞样细胞。确定大量细胞中之基因表达的方法产生平均值,其可包括小的亚群体干细胞样细胞之偏差值。
因此,标记探针与转录物的杂交或用抗体检测由所讨论之基因编码的蛋白质以及由单个细胞产生的信号强度的后续确定是一种用于确定基因表达的优选方法。出于该目的,优选用合适抗体标记之细胞的流式细胞术。
上文描述了用于定义和确认定义过表达之合适阈值的方法。过表达至少一种上述基因之细胞的存在表示用根据式I、II或III之化合物的治疗适用于所述患者。
在本发明的一个优选实施方案中,确定了过表达至少一种上述基因的肿瘤细胞的比例。如果所述细胞在单个肿瘤中的比例高于存在于代表性数目之肿瘤中的平均比例,则用根据式I、II或III之化合物的治疗特别适用于所述患者。
本发明的另一些优选实施方案在下文的条目1至11中给出。
1.用于抑制人患者特异性胶质母细胞瘤细胞的方法,所述方法包括:使所述胶质母细胞瘤细胞与至少一种选自以下的化合物接触:细胞毒性化合物和/或抑制细胞生长的化合物,其中所述化合物在体外表现出比替莫唑胺对所述胶质母细胞瘤细胞的作用更高的抑制代谢活性作用。
2.根据条目1所述的方法,其中所述使所述胶质母细胞瘤细胞与所述细胞毒性化合物和/或抑制细胞生长的化合物相接触诱导所述胶质母细胞瘤细胞凋亡,抑制NF-kB信号传导并且诱导HSp70的表达。
3.根据条目1所述的方法,其中所述细胞毒性化合物和/或抑制细胞生长的化合物为选自以下的至少一种:柔红霉素、藤黄酸酰胺、藤黄酸、硫柳汞、盐酸米托蒽醌、醋酸苯汞、放线菌素D、扁蒴藤素、盐酸表柔比星、硫酸长春新碱、吐根碱、紫杉醇、10-羟基喜树碱、多柔比星、秋水仙碱、喜树碱、替尼泊苷、硫酸长春花碱、丝裂霉素C、氟尿苷、哇巴因、盐酸安西他滨、盐酸奎纳克林、氯硝柳胺、安吖啶、硫鸟嘌呤、鱼藤酮、盐酸阿克拉菌素、阿糖胞苷、氨甲喋呤以及苦鬼臼毒素。
4.根据条目3所述的方法,其中所述细胞毒性化合物和/或抑制细胞生长的化合物是选自以下的至少一种:藤黄酸酰胺、藤黄酸、扁蒴藤素、盐酸表柔比星、吐根碱、哇巴因、盐酸安西他滨、盐酸奎纳克林、氯硝柳胺、安吖啶、盐酸阿克拉菌素以及苦鬼臼毒素。
5.根据条目4所述的方法,其中所述细胞毒性化合物和/或抑制细胞生长的化合物是扁蒴藤素,其中所述扁蒴藤素以约0.1μM至约10μM、特别是约0.9μM至约1.3μM的浓度范围添加。
6.根据条目1所述的方法,其中所述胶质母细胞瘤细胞包含一个亚组的干细胞样细胞。
7.根据条目1所述的方法,其中所述使所述胶质母细胞瘤细胞与所述细胞毒性化合物和/或抑制细胞生长的化合物接触将所述胶质母细胞瘤细胞的细胞生长延迟多至所述接触之后10天。
8.抑制胶质母细胞瘤生长的化合物,其为选自以下的至少一种化合物:细胞毒性化合物和抑制细胞生长的化合物,其中所述化合物在体外表现出比替莫唑胺对所述胶质母细胞瘤患者之作用更高的抑制代谢活性作用。
9.根据条目8所述的化合物,其中所述化合物诱导所述胶质母细胞瘤细胞凋亡,抑制NF-kB信号转导并且诱导HSp70的表达。
10.根据条目8所述的化合物,其中所述细胞毒性化合物和/或抑制细胞生长的化合物为选自以下的至少一种:柔红霉素、藤黄酸酰胺、藤黄酸、硫柳汞、盐酸米托蒽醌、醋酸苯汞、放线菌素D、扁蒴藤素、盐酸表柔比星、硫酸长春新碱、吐根碱、紫杉醇、10-羟基喜树碱、多柔比星、秋水仙碱、喜树碱、替尼泊苷、硫酸长春花碱、丝裂霉素C、氟尿苷、哇巴因、盐酸安西他滨、盐酸奎纳克林、氯硝柳胺、安吖啶、硫鸟嘌呤、鱼藤酮、盐酸阿克拉菌素、阿糖胞苷、氨甲喋呤以及苦鬼臼毒素。
11.根据条目10所述的化合物,其中所述细胞毒性化合物和/或抑制细胞生长的化合物是选自以下的至少一种:藤黄酸酰胺、藤黄酸、扁蒴藤素、盐酸表柔比星、吐根碱、哇巴因、盐酸安西他滨、盐酸奎纳克林、氯硝柳胺、安吖啶、盐酸阿克拉菌素以及苦鬼臼毒素。
下述实施例和图仅为本发明的举例说明,而不应以任何方式被解释为限制如由所附权利要求书指明的本发明的范围。
附图描述
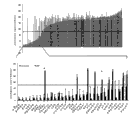
图1:(上图)160种化合物(x-轴)的排序图,其示出它们在单剂量施用(每种1μM)5天后对代谢活性的作用(数据平均值来自四种患者特异性的GBM原代培养物相对于经DMSO处理的细胞)。基于测定,我们鉴定了将相对代谢活性降低至<50%的31种“目标(hit)”化合物。作为参考,用50μM(桔色线)和500μM替莫唑胺(TMZ;蓝色线)处理细胞。(插图)31种目标化合物的详细数据示出。误差线表示三次重复测定结果的标准偏差。
图2:(上图)我们的四种患者特异性GBM样品与U87胶质瘤细胞系应答于160种化合物的平均相对代谢活性的比较图。(插图)与由U87胶质瘤细胞系(右方的柱)分析获得的结果相比,31种患者特异性“目标”化合物(左方的柱)的详细数据。误差线表示三次重复测定结果的标准偏差。
图3:(上图)四种患者特异性GBM样品和#155细胞应答于160种化合物的平均相对代谢活性的比较图。(插图)31种“目标”化合物的详细数据。GBM原代细胞的平均相对代谢活性以深灰色柱表示,#155细胞的平均相对代谢活性以浅灰色柱表示。误差线表示三次重复测定结果的标准偏差。
图4:(a)扁蒴藤素的化学结构。
图5:扁蒴藤素对多种患者特异性GBM原代细胞的药效学分析。基于化合物在体外施用5天后的分析来量化测定。(b)购自独立供应商的扁蒴藤素得出类似的结果。Microsource化合物(实线)和Sigma化合物(虚线)的ICM50中值分别为580nm和430nm。(c)研究了患者特异性GBM样品的ICM50值。MS=Microsource,S=Sigma,ICM50=将代谢活性细胞的量抑制了50%的浓度。每个数据点代表三次重复分析的平均值。
图6:基于膜联蛋白V的FACS分析。在单剂量施用1μM扁蒴藤素(黑色柱)或0.01%DMSO(白色柱)5天后获得结果。插图示出平均值。
图7:生长动力学分析(数据表示患者样品#035、#046、#078、#081和#106的平均值)。在对照条件(0.01%DMSO)下,GBM原代细胞以对数级(logarithmic scale)线性扩增(三角形)。在所研究的每种情况下,施用1μM扁蒴藤素之后发现斜率降低(正方形)。
图8:在两个独立的GBM原代细胞培养实验(035=三角形;046=正方形)中,施用1μM扁蒴藤素(虚线)之后细胞汇合度的长期监测(实线,0.1%DMSO)。使用CellaVista系统根据其说明书(Roche Diagnostics)进行活细胞成像。
图9:(a)单剂量施用1μM扁蒴藤素之后,NSA中一级、二级和三级神经球(neurosphere)的相对频率(数据表示046、078和106的情况下的平均值)。(b)NSA中对照和经处理一级神经球的明场外观。(c)来自对照和经处理三级神经球之细胞的平板接种和分化导致表达GFAP的星形细胞和表达β-微管蛋白的神经元示出形成神经球之细胞的多潜能性。
图10:用扁蒴藤素或用0.01%DMSO将GBM原代细胞(#046)处理5天。通过用特异性抗体进行western印迹分析来检测蛋白质提取物。确认与β-肌动蛋白抗体孵育加载有等量蛋白质的膜。
图11:在贴附(实线)相对于未贴附(虚线)条件下GBM原代细胞的抑制。结果表示各浓度的3种不同样品的三次重复孔分析的平均值(046、078、106)。
图12:单剂量施用1mM扁蒴藤素之后,来自复发的GBM肿瘤之两种原代细胞培养物的相对代谢活性。在处理5天之后以三次重复孔进行测定。
图13:用于如由制造商提供的本验证研究的藤黄酸(a)和藤黄酸酰胺(b)的结构组合物。注释:Enzo Life Sciences在其网页上列举了作为TrkA配体“藤黄酸酰胺(gambogig amide)”的产品。
图14:药效学分析。(A)藤黄酸和藤黄酸酰胺有效地抑制pGBM的代谢活性并且达到相当的程度。(B)但是,数据表明,藤黄酸酰胺抑制活性的诱导发生在较早的时间点。这些图示出化合物暴露(所示浓度)之后,在第1(菱形)、2(正方形)或5(三角形)天,pGBM(所示#)的相对代谢活性。数据为三次重复的平均值±SD。
图15:细胞毒性研究。向pGBM(所示#)施用DMSO对照、IMC50或1μM浓度的各化合物5天之后的基于cPARP的FACS分析。藤黄酸和藤黄酸酰胺似乎在类似程度上为其赋予细胞毒性作用。
图16:细胞周期分析。将pGBM(所示#)暴露于DMSO对照或分别为IMC50或1μM之浓度的化合物5天。采用标准方案进行流式细胞分析。PI:碘化丙啶;n.d.:未测定(由于在各化合物浓度下的大量细胞损失)。
图17:神经球测定。该测定用于评估pGBM中自我更新和多能细胞之合并物的潜在变化(n=3:#046;106;138;对所有样品进行三次重复分析)。用所示浓度的化合物单次预处理之后确定一级(1°)、二级(2°)和三级(3°)神经球的频率。(A)藤黄酸预处理未改变自我更新细胞的频率。(B)相比之下,藤黄酸酰胺预处理导致所研究pGBM中自我更新细胞的相当程度的减少。
图18:藤黄酸酰胺降低了pGBM的肿瘤启动潜力。将pGBM(#046)用IMC50浓度的各化合物在体外处理5天。然后,收集106种存活的活细胞(vital cell),并将其注入成年免疫受损小鼠的纹状体中(就每个实验而言,n=5)。(A)Kaplan-Meier曲线示出在注射经藤黄酸(虚线)相对于DMSO对照(实线)预处理的pGBM之后不显著的存活率优势。(B)相比之下,经藤黄酸酰胺预处理的(虚线)pGBM与各对照(DMSO;固体)相比示出显著较低的致瘤性。
图19:藤黄酸酰胺对CD133+GBM细胞的优选靶向。(A)基于FACS的鉴定和CD133+子群体与pGBM的分类(#106,上图;#058,下图)。注释:CD133+细胞的各频率示于图中。(B)在单一暴露于藤黄酸(IMC50,上图)和藤黄酸酰胺(IMC50,下图)5天之后确定的CD133-阳性相对于CD133阴性pGBM细胞的相对代谢活性和细胞汇合度。记录CD133+细胞应答于藤黄酸酰胺之施用的选择敏感性。
图20:藤黄酸酰胺有效地抑制广泛pGBM的细胞生存力。在化合物暴露(所示浓度)5天后,17种pGBM(所示#)的药效学分析。IMC50值为78nM至514nM。
图21:藤黄酸酰胺之药效学分析数据的分层(stratification)。(A)示出将代谢活性降低至50%对照水平的浓度的IMC50值谱。从市售胶质瘤/GBM细胞系(蓝色:LN229、T98G、U87、U138和U373细胞)以及17种pGBM收集的数据。(B)根据临床相关患者亚组之pGBM数据的分层。该图描绘来自以下之pGBM中各IMC50值逐对比较(形状编码的(shape-coded)):肿瘤中心相对于周围;原发性疾病相对于复发性疾病;超甲基化的MGMT启动子相对于未甲基化的样品;p53野生型(wt)相对于突变的p53;以及NFKBIA野生型(wt)相对于NFKBIA缺失的基因型。记录这些亚组的藤黄酸酰胺的IMC50值不显著改变,表明化合物的广泛适用性。
实施例
实施例1
组织样品
肿瘤组织获自波恩大学医学中心神经外科系的GBM手术。该研究经当地伦理委员会批准;所有患者都提供了知情同意书。基于世界卫生组织的现有分类(Louis等,ActaNPT2007)对所有生物活检样品进行了组织学,并且由波恩大学医学中心(神经外科的国家参考中心)神经外科系的两名独立的神经病理学家确认。
表1
表1:用于化合物筛选的四种原代GBm培养物的患者数据和特征。分别测定NSA中1°/2°/3°神经球的神经球频率。通过以下来测定多潜能性:将2°和3°神经球平板接种,接着进行21天分化过程,用特征性地表达于神经元(βIII微管蛋白)、星形细胞(GFAP)和少突细胞(CNPase)中的标志物进行免疫细胞化学。年龄:进行手术时的患者年龄;dpts:移植后天数;性别:M=男性;f=女性。
组织操作和原代培养
在切除术之后30至60分钟获得生物活检样品,然后在无菌条件下将组织切割为三个代表性的部分。一部分用4%多聚甲醛(PFA)固定以用于组织学分析,第二部分在液氮中经历迅速冷冻用于分子分析,第三部分使用0.25%胰蛋白酶缓冲液和火焰磨光的巴斯德吸管轻柔吹吸以制备单细胞混悬液。将单细胞混悬液置于贴附培养条件下用于细胞在6cm层粘连蛋白/聚-L-鸟氨酸包被的塑性培养皿中的增殖培养基(PROL;根据Lee等,2006的组合物)中的扩增。在平板接种之后提供20ng/ml EGF/bFGF,然后隔天添加10ng/ml EGF/bFGF。贴壁细胞通过在每4至7天以1:2或1:3的比例连续传代而增殖。
神经球测定
基于之前的研究(Scheffler等,2005),在含1%甲基纤维素的PROL培养基(提供有20ng/ml EGF/bFGF)中稀释1×104个细胞/cm2的单细胞混悬液,并接种入非贴附性培养皿中。然后隔天添加10ng/ml EGF/bFGF。在培养的第21天量化神经球,吹吸为单细胞混悬液,其在相同条件下用于平板接种,并分析二级或更高级神经球的形成。就多潜能性的分析而言,使用了代表性的部分3°神经球。将神经球平板接种到层粘连蛋白/聚-L-鸟氨酸包被的玻璃盖玻片上,贴壁之后,提供不含分裂素的PROL培养基,以在PFA固定和免疫荧光分析之前在培养时分化2至3周。
荧光分析
根据标准方案(Scheffler等,2005;Goetz等,2006)使用抗pHI微管蛋白的抗体(Promega,Mannheim,Germany;单克隆小鼠,1:1000)、抗CNPase的抗体(Millipore,Schwalbach,Germany;单克隆小鼠,1:300)和抗GFAP的抗体(DAKO,Hamburg,Germany;多克隆兔,1:600)对4%PFA固定的样品进行培养细胞的免疫荧光分析。通过用DAPI(Sigma)标记来使细胞核可视化。
Western印迹分新
用所示浓度的化合物将细胞孵育24小时。制备细胞提取物并按照所述(Wiechen等,2001)进行处理。将Western印迹膜在4℃与Cyclin-D1(1:1000;BD Pharmingen,Heidelberg,Germany)、Hsp-70(1:1000)、经切割的Notch1(1:1000)、磷酸化的S6蛋白(1:1000)、plkB(1:1000)、磷酸化的连环蛋白(Ser33/37/Thr41)(1:1000)、磷酸化的IKBa(Ser32)(1:1000)以及p85/p55-PI3K抗体(1:1000,all Cell signaling,Frankfurtam Main,Germany)孵育过夜。在充分清洗之后,添加过氧化酶偶联的二抗(SantaCruz,Heidelberg,Germany),保持1小时。清洗之后,使用ECL系统(AmershamPharmacia,Buckingshamshire,UK)将印迹显影。为了确认等量加载,用p-肌动蛋白抗体(Sigma,Deisenhofen,Germany)再次探测印迹。
增殖动力学
在6cm培养皿中处理5天之后,将47,000个活细胞平板接种到3.5cm层粘连蛋白/聚-L-鸟氨酸包被的塑性培养皿中。在平板接种之后提供20ng/ml EGF/bFGF,之后隔天添加10ng/ml EGF/bFGF。4至6天后,用胰蛋白酶消化贴壁细胞,收集,计数,并以4.7×104个细胞的密度进行平板接种。将该过程重复4至5代。示出平均值和标准误差。
流式细胞术
在6 cm培养皿中用化合物处理4天后收集细胞。通过离心沉淀1×105个细胞,在100μl膜联蛋白V缓冲液(BD Bioscience,Heidelberg,Germany)中重悬,并在室温下用5μl膜联蛋白V-FITC(BD Bioscience,Heidelberg,Germany)孵育1小时。为了区分活细胞和死细胞,用1.2μg/ml双苯酰亚胺H33258(Invitrogen,Karlsruhe,Germany)标记。采用标准条件在装配有FACSDiva软件(BD Bioscience,Heidelberg,Germany)的LSRII中测定表达。就每个测量而言,对20.000个细胞进行计数。将膜联蛋白V阳性细胞、膜联蛋白V和H33258阳性细胞和H33258阳性细胞称为非活细胞(avital cell)。
药物筛选
对获自Microsource Discovery Systems,Inc.,Gayordsville,CT,USA的多种化合物进行筛选。在筛选之前,分别对每个细胞系的细胞数目进行滴定以确保在整个实验过程中细胞增殖保持在线性-指数期。将2至3×103个细胞/孔接种到层粘连蛋白/聚-L-鸟氨酸包被的96孔板中,24小时之后,用2 nM、1 μM或10 μM的每种化合物(储液10 mM于DMSO中)处理原代培养物。作为参考,我们用50 μM和500 μM替莫唑胺(TMZ,SigmaAldrich,Taufkirchen,Germany;储液100 mM于DMSO中)处理细胞。用0.5%至0.01%DMSO处理对照细胞。施加6天之后,采用测定根据制造商建议(Invitrogen,Karlsruhe,Germany)测定细胞生存力。使用Infinite200酶标仪(microplate reader)(Tecan,Crailsheim,Germany)在Xex=540 nm和Xem=590 nm处测量荧光。对于每个样品,实验以三次重复进行。
对于扁蒴藤素和氯硝柳胺的药效学分析,将5×104个细胞平板接种在12孔板中,24小时之后,用所示浓度对它们进行处理。处理5天之后,通过测定监测细胞生存力。实验以三次重复进行。ICM50是在实验条件下将代谢活性降低50%的试剂浓度。
对于进一步实验,将原代GBM细胞以40%至50%的汇合度平板接种在层粘连蛋白/聚-L-鸟氨酸包被的6cm培养皿中。用所示浓度的扁蒴藤素和氯硝柳胺处理细胞。用0.1%DMSO处理对照细胞。
结果和讨论
为了鉴定细胞毒性化合物和抑制细胞生长的化合物,我们对四种不同的患者特异性原代GBM培养物进行了体外药物筛选测定(研究样品的基本特征参见表1)。
以三种不同浓度(10μM、1μM、2nM)筛选化合物文库。在用化合物孵育5天之后测定相对代谢活性。(1μM)数据组示于图1中。在该浓度,有31种化合物成为目标化合物,因为它们将相对代谢活性降低至低于经DMSO处理之对照的50%(图1上图;红色柱)。作为参考,我们向我们的细胞施加了50μM(报告的血浆峰浓度)和500μM的替莫唑胺(TMZ,如Beier等2008中所述)(替莫唑胺是现有标准化学治疗GBM的药物)。50μM TMZ的施加导致17%(桔色线)的降低,而500μM TMZ将我们的四种患者特异性原代细胞的相对代谢活性降低至63%的水平(数据平均值,蓝线;图1上图)。因此,与浓度为500μM(相对于50μM)的TMZ相比,在浓度为1μM时,61种筛选化合物中有39种在我们的患者特异性GBM细胞代谢活性方面产生更强的降低。但是,初级筛选设置中的“目标”被定义为相对代谢活性降低为低于经DMSO处理之对照细胞的50%的水平。基于从我们的四种患者特异性GBM原代细胞获得的数据平均值分析,所筛选的化合物收集中有31种满足了该定义(图1)。但是,研究了单个研究样本之间代谢抑制程度的改变。在31种“目标”化合物中仅有26种化合物在每个患者特异性案例中将代谢活性降低至高于50%(图1,下图)。
就与我们的四种患者特异性原代GBM细胞样品相比较而言,我们采用了市售胶质瘤细胞系U87,其常常在药物发现设定中进行研究(图2)。令人感兴趣的是,患者特异性“目标”化合物中有9种(即,扁蒴藤素、替尼泊苷、氟尿苷、盐酸安西他滨、氯硝柳胺、硫鸟嘌呤、鱼藤酮、甲氨蝶呤、苦鬼臼毒素)未导致U87的相对代谢活性降低>50%(图2,下图)。相比之下,只有一种化合物(Physicion)示出对U87代谢活性的显著影响而不影响原代GBM细胞。
作为一个替代对照,评价获自患有药物耐受型癫痫之患者(患者#155)的原代细胞。如同U87细胞系,当暴露于31种“目标”化合物时,155细胞示出一般更耐受的表型(图3)。这些化合物中有11种(即,5硫酸长春新碱、吐根碱、紫杉醇、10-羟基喜树碱、喜树碱、替尼泊苷、氟尿苷、氯硝柳胺、硫鸟嘌呤、鱼藤酮、甲氨蝶呤和苦鬼臼毒素)对#155细胞的代谢活性示出非常小的作用(图3,下图)。4种化合物(即,松胞菌素D、豆蔻酸-乙酸佛波酯(phorbol myristate acetate)、斑蝥素、2,3-二氯-5,8-二羟基萘醌)显著降低#155细胞的代谢活性,但对GBM原代细胞无显著作用(图3,上图)。
从其他验证中排除了31种“目标”化合物中的若干化合物,其为(i)正在/已用于胶质瘤治疗的临床应用,即柔红霉素、盐酸米托蒽醌、硫酸长春新碱、紫杉醇、10-羟基喜树碱、多柔比星、替尼泊苷、硫酸长春花碱、氟尿苷、硫鸟嘌呤和甲氨蝶呤;(ii)正在/已在胶质瘤的临床试验中研究的,即,放线菌素D、10-羟基喜树碱、丝裂霉素C和阿糖胞苷;或(iii)已示出对人或动物有显著毒性的,即,硫柳汞、乙酸苯汞、秋水仙碱、喜树碱和鱼藤酮。
12种候选化合物仍需进行进一步验证实验(即,藤黄酸酰胺、藤黄酸、扁蒴藤素、盐酸表柔比星、吐根碱、哇巴因、盐酸安西他滨、盐酸奎纳克林、氯硝柳胺、安吖啶、盐酸阿克拉菌素、苦鬼臼毒素)。所有这些均代表用于GBM化学治疗设定的新的潜在候选物。
扁蒴藤素验证实验
扁蒴藤素是天然的三萜类化合物(triterpenoid)(图4),其可见于卫矛科(Celastraceae)和翅子藤科(Hippocrateaceae)家族(Buffa Filho等,2002;Chenag等,2003;Niampoka等,2005)。其可诱导抗炎性、抗氧化、抗疟疾和杀虫过程(Sassa等,1994,Dirsch等,1997;Figueiredo等,1998;Avilla等,2000;Luo等,2005)。以剂量依赖性方式,三萜类化合物可诱导细胞保护、肿瘤分化、增殖停滞和凋亡作用(Suh等,1999;Suh等,2003;Ji等,2006)。扁蒴藤素可阻断骨髓瘤中的NF-κB信号转导(Tiedemann等,2009;Lu等,2010)。NF-κB信号转导参与细胞增殖、炎症、迁移和凋亡,并且NF-κB信号转导途径的组成型活化已被描述为GBM的特征(Yamamoto等,2000;Nozell等,2008)。此外,已提出了参与放疗耐受和化疗耐受的细胞机制(Eyler和Rich,2008)。因此,我们假设扁蒴藤素通过抑制NF-κB信号转导级联来发挥其抗GBM活性。
扁蒴藤素在GBM原代细胞中诱导凋亡。向四种患者特异性GBM细胞样品施用扁蒴藤素在所有情况下导致非常强的代谢活性降低(023=90%;035=97%;046=78%;106=97%;图1,下图)。因为尚未知扁蒴藤素的峰血浆浓度,所以我们研究了70nM至10μM的浓度范围(图5)。在这些条件下,扁蒴藤素在约500nM的中值ICM50(代谢活性的半数最大抑制浓度)时具有强效的细胞毒性(图5a、b、d)。
基于购自独立供应商的扁蒴藤素的分析(其产生类似的结果),可以将这些作用验证为化合物特异性的(Sigma;图1b)。对于进一步实验而言,以1μM的扁蒴藤素浓度施用(图1c)。基于膜联蛋白V的FACS分析证实,5天的扁蒴藤素暴露导致凋亡的强烈诱导。在8种研究的患者特异性GBM原代细胞的7种中,大于50%的全部细胞可以被归类为非活的(图6;***p<0.001,与其各自的经DMSO处理之对照细胞相比)。
但是,扁蒴藤素的单剂量施用从未导致细胞生长的完全停止。从扁蒴藤素施用中存活下来的细胞以对数级线性地扩增。细胞生长的初始延迟持续最多10天。但是,之后,我们所研究的每种患者特异性GBM原代细胞及其各自的DMSO对照迄今仍继续增殖(图7)。
我们采用CellaVistasystem(Roche Diagnostics,Mannheim)作为代理分析工具来监测细胞汇合度。与生长动力学分析相当,单剂量扁蒴藤素的施用导致细胞汇合度的较强初始降低。在化合物施用后10天以前,存活细胞不示出增殖活性(图8)。
此外,单剂量的扁蒴藤素将克隆源性(即,神经球形成)细胞的频率降低30%至60%(图9a,b)。在浓度为1mM时从未观察到克隆源性细胞的耗尽。克隆源性细胞总是能够自我更新并且形成更高级的神经球,其产生不成熟的神经元和星形细胞(图9c)。这些发现表明,扁蒴藤素不选择性地抑制GBM癌干细胞。扁蒴藤素以剂量依赖性方式降低具有及不具有干细胞特征之GBM细胞的活性。
接下来,进行Western印迹分析以揭示诱导凋亡的机制。数据表明,扁蒴藤素的施用导致可检测细胞周期蛋白D1和磷酸化的lκBa信号的损失(图10)。同样并且与骨髓瘤的研究(Tiedemann等,2009)相当,在我们的样品中观察到了热休克蛋白(HSP70)表达的强力诱导(图10)。
在3D培养系统(即,非贴附生长条件)中确认扁蒴藤素的GBM抑制活性(图11)。在撤回锚定(anchorage-withdrawal)的条件下,来自神经球的GBM细胞及其代谢应答形式的研究示出更有抗性的表型。但是,可以用扁蒴藤素的单剂量施用高效地抑制在这些培养条件下培养的GBM细胞(平均ICM50=1.1μM)。
最后,因为已提出来自复发性疾病的GBM细胞是放疗抗性和化疗抗性的原因(Rao等,2003),所以我们研究了两个独立的患者特异性案例(患者#91RZ和118RZ)。在这两种情况下,1μM扁蒴藤素的单剂量施用均导致代谢活性的几乎完全剥夺(图12)。
结论
总之,我们的数据建立了31种化合物作为用于GBM治疗的潜在新候选物。其中,12种化合物特别适用于验证实验(即,藤黄酸酰胺、藤黄酸、扁蒴藤素、盐酸表柔比星、吐根碱、哇巴因、盐酸安西他滨、盐酸奎纳克林、氯硝柳胺、安吖啶、盐酸阿克拉菌素、苦鬼臼毒素)。特别地,藤黄酸、藤黄酸酰胺、扁蒴藤素、盐酸表柔比星、吐根碱和氯硝柳胺是高度高效的抗GBM治疗剂。化合物扁蒴藤素代表在原发性和复发性疾病的设置中用于GBM治疗的极佳新候选物。人患者特异性GBM细胞的有效抑制可以以约1μM的浓度引发。扁蒴藤素诱导具有及不具有干细胞特征的GBM细胞凋亡,其抑制NF-κB信号转导,并且其诱导HSp70表达。
实施例2
选择两种结构相关的分子(即,藤黄酸酰胺(gambogig acid amide,GAA)和藤黄酸(Gambogig acid,GA))用于验证。GAA和GA二者都示出在以1μM的浓度施用时将患者特异性原代人胶质母细胞瘤细胞(pGBM)抑制为低于50%对照水平的能力。
为了验证获自初步筛选的结果,这些化合物均购自独立供应商(图13)。通过测定将pGBM的代谢活性降低至50%对照水平(IMC50)的浓度进行药效学分析。在记录与之相当的剂量响应曲线时,GAA的抑制活性在较低浓度下持续存在(图14),对每个样品进行三次重复分析。就进一步分析而言,在体外施用单剂量的各化合物5天之后,收集pGBM。流式细胞分析揭示了两种化合物的强细胞毒性和仅中度的抑制细胞生长的抗pGBM作用(图15和16)。
在下一系列的实验中,我们的目的是确定化合物对肿瘤启动细胞(tumor-initiating cell,TIC)之活性的影响。TIC表现出肿瘤内异质性的严重功能后果,这是因为至少在人胶质母细胞瘤中,预期它们表现为小亚群体的干细胞样细胞,即自我更新细胞和多能细胞(例如,Sties和Rowitch,2008;Zhou等,2009)。在之前的工作中,我们建立了其在培养代数为5至10的pGBM中0.25%至1%的频率(参见Glas等,2010)。为了评估pGBM中自我更新细胞和多能细胞之合并物的潜在化合物诱导的改变,按照近来所述(Scheffler等,2005;Glas等,2010)来实施神经球测定(neurosphere assay,NSA)。将异质性pGBM样品(#046、078、106)暴露于化合物,在第5天收集活细胞,并在非贴附条件下于NSA(神经球测定,参见方法)中处理。该测定中的一级、二级和三级球的量化和分化未示出GA-诱导的改变。相比之下,GAA的单一施用出乎意料地揭示pGBM中自我更新多能细胞的大大降低的频率(图17)。来自经DMSO对照或各化合物预处理的3°神经球的平板接种和分化揭示了表达GFAP的星形细胞和表达βIII微管蛋白的神经元表型。这些结果示出存活细胞的未改变的多能能力。
因此,试图推断仅GAA降低了致瘤细胞占pGBM的百分比。原位异种移植(orthotopic xenotransplantation)研究事实上证实了该假设(图18)。统计学分析示出接受经GAA预处理的pGBM的动物的显著提高的存活率。该作用对经GA预处理的细胞不明显。这些数据一起表明,与GA相比,GAA缺失的干细胞样癌细胞/TIC有效引起pGBM中肿瘤启动活性的显著降低。
为了进一步确证GAA的癌干细胞特异性抑制活性,我们选择来自pGBM的CD133阳性及阴性细胞群体(图19)。已知CD133+细胞在胶质母细胞瘤样品中代表少数致瘤性干细胞样表型(Singh等,2004)。由GAA和GA对CD133+相对于CD133-pGBM细胞诱导的抑制作用的比较评价证实了我们的假设。与分离自同一患者样品的CD133-群体相比,GAA的施用在CD133+细胞中导致显著更强的细胞生长与活力的下降(三次重复分析)。就GA而言无法揭示类似的选择抑制作用。
这些数据一起揭示GAA作为癌干细胞特异性细胞毒性化合物。
考虑到表征GBM的细胞和遗传多样性,接下来我们研究了GAA对来自11名患者的17种pGBM样品的药效学作用(样品和患者数据列表参见表2)。在全部所研究的细胞系中都可以表明GAA的强抑制活性,其IMC50为78nM(#132)至514nM(#106)(图20)。与之相当的结果获自用作参考的五种市售胶质瘤/GBM细胞系(LN229、T98G、U87、U138以及U373,参见方法)。接下来,对pGBM进行GAA药效学的逐对比较,以根据关键临床群组对结果进行分层(Bredel等,2011;Glas等,2010;Simpson等,2006;Weller等,2010)。胶质母细胞瘤样品得自:(i)肿瘤中心相对于同一患者的周围区域;(ii)同一患者的原发性疾病相对于复发性疾病;(iii)超甲基化的MGMT启动子相对于未甲基化的组织;(iv)p53野生型相对于突变的p53样品;以及(v)NFKBIA野生型相对于NFKBIA缺失的基因型。GAA似乎将所有这些样品抑制至类似的程度(图21)。
表2
表2:本研究中所研究的患者和组织样本列表。A:患者拒绝进一步治疗;B:手术后并发症;C:由于临床恶化的治疗中止;D:从成对的GBM生物活检样品分离的细胞,其代表相同样品的中心和周围,均为脑肿瘤;E:从GBM生物活检样品分离的细胞,其示出同一患者的原发性疾病和复发性疾病;R:肿瘤切除;RT:标准放射治疗;RT/TMZ:RT加上每日连续替莫唑胺(伴随(concomitant));TMZ:替莫唑胺(5/28:28天周期中的第1至5天);PFS:无进展存活;OS:总体存活;meth:甲基化的MGMT启动子;unmet:未甲基化的MGMT启动子。
这些数据一起确认和验证了我们的初步筛选结果,指明GAA作为高度有效的细胞毒性抗pGBM化合物,优先靶向致瘤的癌干细胞样表型。
试剂
为该研究购买了以下试剂:碘化丙啶、可固定死细胞染色试剂盒和Hoechst33342(Life Technologies);藤黄酸(Sigma-Aldrich);藤黄酸酰胺(Enzo Life Sciences)。
小鼠
波恩大学医学中心的伦理委员会批准了全部涉及动物的研究。Rag2Il2rg-/-小鼠获自Taconic Farm Inc.,其为国家过敏症与传染病研究所的立契约方(Cao等,1995)。
组织样品
肿瘤组织得自GBM手术。患者特征详细描述于补充表1中。当地伦理委员会分别批准了这些研究;所有患者都提供了知情同意书。基于世界卫生组织的现有分类(Louis等,2007)对组织进行诊断和分级,并且由波恩大学医学中心(神经外科的国家参考中心)神经外科系的两名独立的神经病理学家确认。
组织操作和原代细胞培养
按照近来所述地进行新鲜生物活检样品的处理和pGBM的获取(Glas等,2010)。用于pGBM样品的介质条件描述于(Glas等,2010;Lee等,2006)中。数据产生自培养代数7至10。
药效学分析
就药效学分析而言,将5×104个细胞平板接种在12孔板中,24小时后施用化合物系列。在处理5天后进行基于的分析。实验重复进行三次。IMC50被定义为与对照条件相比将代谢活性降低50%的化合物浓度,并且通过数据分析在GraphPad Prism4.0中确定。
细胞周期分析
将细胞(5×104个每孔)培养在12孔板中,并在处理后的所述时间进行收集。将细胞重悬于磷酸盐缓冲液(PBS)中,用冰冷的甲醇固定并在4℃孵育最少24小时。通过离心收集细胞沉淀并在PBS溶液(含50μg/ml碘化丙啶和50μg/ml RNase)中重悬。在37℃孵育30分钟之后,使用FACScaliber流式细胞仪(BD Bioscience)分析细胞的DNA含量。
基于cPARP的FACS分析
在化合物施用5天后收集1×105个细胞,通过离心沉淀,重悬于100μlLIVE/DEAD fixable dead Stain FarRed中,并在4℃孵育30分钟。然后将细胞在PBS中的冰冷4%(w/v)多聚甲醛中固定10分钟,并用0.5%Triton X-100通透5分钟。然后在室温下,用FITC偶联的cPARP抗体(BD Bioscience;1:5稀释)将细胞悬液染色30分钟。为了区分活细胞和死细胞,使用1.2μg/ml Hoechst33258进行标记。在装配有FACSDiva软件的LSRII(BD Bioscience)中采用标准条件测定表达。在每次测量中对20.000个细胞进行计数。
神经球测定
根据建立的方案(Glas等,2010;Scheffler等,2005)进行神经球测定以评估自我更新克隆源性细胞的频率。在培养的第21天量化神经球,吹吸为单细胞悬液,再次进行平板接种以分析二级和三级神经球。通过以下来测定多潜能性:将3°神经球代表性部分平板接种到层粘连蛋白/聚-L-鸟氨酸包被的玻璃盖玻片上,分化2至3周,然后在4%多聚甲醛(PFA)中固定。
荧光分析
根据标准方案(Scheffler等,2005)使用抗bIII微管蛋白的抗体(Promega;单克隆小鼠,1:1000)和抗GFAP的抗体(DAKO;多克隆兔,1:600)对PFA固定的样品进行免疫荧光分析。用DAPI(Sigma)来使细胞核可视化。
CD133
+
与CD133
-
细胞的分离
就荧光活化的细胞分离(FACS)而言,用CD133/2-PE或用CD133/2-APC(二者均为1:20;Miltenyi Biotech)对细胞进行染色,并在BD FACS DiVa细胞分选器(Becton Dickinson)上进行分选。
肿瘤异种移植实验
收获细胞,计数并在0.1%DNase/PBS中重悬。通过台盼蓝排除法(trypan blue exclusion)确定细胞生存力。将经DMSO对照、藤黄酸或藤黄酸酰胺预处理的106个pGBM定向地注入12周龄的Rag2Il2rg-/-小鼠纹状体(前部0.8mm,侧面2mm,深度3mm)中。每日监测小鼠,并且在呈现出不适/神经症状或显著体重减轻之特征后进行安乐死。对于后续的组织学分析,移除脑,防止冷冻,在低温保持器(Leica)上以20μm的厚度连续切割。每5个区段经历常规的H&E染色以用于肿瘤形成的组织学分析。
参考文献
Avilla,J.;Teixido,A.;Velazquez,C.;Alvarenga,N.;Ferro,E.and Canela,R.(2000):Insecticidal activity of Maytenus species(Celastraceae)nortriterpene quinonemethides against codling moth,Cydia pomonella(L.)(Lepidoptera:tortricidae),JAgric Food Chem(vol.48),No.1,pp.88-92.
Beier,D.;Rohrl,S.;Pillai,D.R.;Schwarz,S.;Kunz-Schughart,L.A.;Leukel,P.;Proescholdt,M.;Brawanski,A.;Bogdahn,U.;Trampe-Kieslich,A.;Giebel,B.;Wischhusen,J.;Reifenberger,G.;Hau,P.and Beier,C.P.(2008):Temozolomidepreferentially depletes cancer stem cells in glioblastoma,Cancer Res(vol.68),No.14,pp.5706-15.
Bredel,M.,Scholtens,D.M.,Yadav,A.K.,Alvarez,A.A.,Renfrow,J.J.,Chandler,J.P.,Yu,I.L.,Carro,M.S.,Dai,F.,Tagge,M.J.,et al.2011.NFKBIA deletion in glioblastomas.N Engl J Med364:627-637.
Buffa Filho,W.;Corsino,J.;Bolzani da,S.V.;Furlan,M.;Pereira,A.M.and Franca,S.C.(2002):Quantitativedetermination for cytotoxic Friedo-nor-oleanane derivatives fromfive morphological types of Maytenus ilicifolia(Celastraceae)by reverse-phasehigh-performance liquid chromatography,Phytochem Anal(vol.13),No.2,pp.75-8.
Cao,X.,Shores,E.W.,Hu-Li,J.,Anver,M.R.,Kelsall,B.L.,Russell,S.M.,Drago,J.,Noguchi,M.,Grinberg,A.,Bloom,E.T.,et al.1995.Defective lymphoid development in mice lackingexpression of the common cytokine receptor gamma chain.Immunity2:223-238.
Chalmers,A.J.(2007):Radioresistant glioma stem cells-therapeutic obstacle or promisingtarget?,DNA Repair(Amst)(vol.6),No.9,pp.1391-4.
Chang,F.R.;Hayashi,K.;Chen,I.H.;Liaw,C.C.;Bastow,K.F.;Nakanishi,Y.;Nozaki,H.;Cragg,G.M.;Wu,Y.C.and Lee,K.H.(2003):Antitumor agents.228.five new agarofurans,ReissantinsA-E,and c少otoxic principles from Reissantiabuchananii,J Nat Prod(vol.66),No.11,pp.1416-20.
Dirks,P.B.(2008):Brain tumor stem cells:bringing order to the chaos of braincancer,J Clin Oncol(vol.26),No.17,pp.2916-24.
Dirsch,V.M.;Kiemer,A.K.;Wagner,H.and Vollmar,A.M.(1997):The triterpenoidquinonemethide pristimerin inhibits induction of inducible nitric oxide synthase in murinemacrophages,Eur J Pharmacol(vol.336),No.2-3,pp.211-7.
Figueiredo,J.N.;Raz,B.and Sequin,U.(1998):Novel quinone methides from Salaciakraussii with in vitro antimalarial activity,J Nat Prod(vol.61),No.6,pp.718-23.
Glas,M.;Rath,B.H.;Simon,M.;Reinartz,R.;Schramme,A.;Trageser,D.;Eisenreich,R.;Leinhaas,Keller,M.;Schildhaus,H.U.;Garbe,S.;Steinfarz,B.;Pietsch,T.;Steindler,D.A.;Schramm,J.;Herrlinger,U.;Brustle,and Scheffler,B.Residual tumor cells areunique cellular targets in glioblastoma,Ann Neurol(vol.68),No.2,pp.264-9.
Goetz,A.K.;Scheffler,B.;Chen,H.X.;Wang,S.;Suslov,O.;Xiang,H.;Brustle,O.;Roper,S.N.and Steindler,D.A.(2006):Temporally restricted substrate interactions directfate and specification of neural precursors derived from embryonic stem cells,Proc NatlAcad Sci USA(vol.103),No.29,pp.11063-8.
Honda,T.;Rounds,B.V.;Bore,L.;Favaloro,F.G.,Jr.;Gribble,G.W.;Suh,N.;Wang,Y.and Spor,M.(1999):Novel synthetic oleanane triterpenoids:a series of highly activeinhibitors of nitric oxide production in mouse macrophages,Bioorg Med Chem Lett(vol.9),No.24,pp.3429-34.
Ji,Y.;Lee,H.J.;Goodman,C.;Uskokovic,M.;Liby,K.;Sporn,M.and Suh,N.(2006):The synthetic triterpenoid CDDO-imidazolide induces monocytic differentiation by activatingthe Smad and ERK signaling pathways in HL60leukemia cells,Mol Cancer Ther(vol.5),No.6,pp.1452-8.
Lee,J.;Kotliarova,S.;Kotliarov,Y.;Li,A.;Su,Q.;Donin,N.M.;Pastorino,S.;Purow,B.W.;Christopher,N.;Zhang,W.;Park,J.K.and Fine,H.A.(2006):Tumor stem cellsderived from glioblastomas cultured in bFGF and EGF more closely mirror the phenotypeand genotype of primary tumors than do serum-cultured cell lines,Cancer Cell(vol.9),No.5,pp.39l-403.
Louis,D.N.;Ohgaki,H.;Wiestler,O.D.;Cavenee,W.K.;Burger,P.;Jouvet,A.;Scheithauer,B.W.and Kleihues,P.(2007):The2007WHO classification of tumoursof the central nervous system,Acta Neuropathol(vol.114),No.2,pp.97-109.
Lu,Z.;Jin,Y.;Chen,C.;Li,J.;Cao,Q.and Pan,J.Pristimerin induces apoptosis inimatinib-resistant chronic myelogenous leukemia cells harboring T315I mutation byblocking NF-kappaB signaling and depleting Bcr-Abl,Mol Cancer(vol.9),p.112.
Luo,D.Q.;Wang,H.;Tian,X.;Shao,H.J.and Liu,J.K.(2005):Antifungal properties ofpristimerin and celastrol isolated from Celastrus hypoleucus,Pest Manag Sci(vol.61),No.1,pp.8590.
Niampoka,C.;Suttisri,R.;Bavovada,R.;Takayama,H.and Aimi,N.(2005):Potentiallycytotoxic triterpenoids from the root bark of Siphonodon celastrineus Griff,Arch PharmRes(vol.28),No.5,pp.546-9.
Pardal,R.;Clarke,M.F.and Morrison,S.J.(2003):Applying the principles of stem-cellbiology to cancer,Nat Rev Cancer(vol.3),No.12,pp.895-902.
Pollard,S.M.;Yoshikawa,K.;Clarke,I.D.;Danovi,D.;Stricker,S.;Russell,R.;Bayani,J.;Head,R.;Lee,M.;Bernstein,M.;Squire,J.A.;Smith,A.and Dirks,P.(2009):Glioma stem celllines expanded in adherent culture have tumor-specific phenotypes andare suitable for chemical and genetic screens,Cell Stern Cell(vol.4),No.6,pp.568-80.
Rao,J.S.(2003):Molecular mechanisms of glioma invasiveness:the role of proteases,Nat Rev Cancer(vol.3),No.7,pp.489-501.
Sassa,H.;Kogure,K.;Takaishi,Y.and Terada,H.(1994):Structural basis of potentantiperoxidation activity of the triterpene celastrol in mitochondria:effect of negativemembrane surface charge on Iipid peroxidation,Free Radic Biol Med(vol.17),No.3,pp.201-7.
Scheffler,B.;Walton,N.M.;Lin,D.D.;Goetz,A.K.;Enikolopov,G.;Roper,S.N.andSteindler,D.A.(2005):Phenotypic and functional characterization of adult brainneuropoiesis,Proc Natl Acad Sci USA(vol.102),No.26,pp.9353-8.
Simpson,L.,and Galanis,E.2006.Recurrent glioblastoma multiforme:advances intreatment and promising drug candidates.Expert Rev Anticancer Ther6:1593-1607.
Singh,S.K.;Hawkins,C.;Clarke,I.D.;Squire,J.A.;Bayani,J.;Hide,T.;Henkelman,R.M.;Cusimano,M.D.and Dirks,P.B.(2004):Identification of human brain tumourinitiating cells,Nature(vol.432),No.7015,pp.396-401.
Stiles,C.D.,and RoWitch,D.H.2008.Glioma stem cells:a midtern exam.Neuron58:832-846.
Stupp,R.;Mason,W.P.;van den Bent,M.J;Weller,M.;Fisher,B.;Taphoorn,M.J.;Belanger,K.;Brandes,A.A.;Marosi,C.;Bogdahn,U.;Curschmann,J.;Janzer,R.C.;Ludwin,S.K.;Gorlia,T.;Allgeier,A.;Lacombe,D.;Cairncross,J.G.;Eisenhauer,E.andMirimanoff,R.O.(2005):Radiotherapy plus concomitant and adjuvant temozolomide forglioblastoma,N Engl J Med(vol.352),No.pp.987-96.
Suh,N.;Roberts,A.B.;Birkey Reffey,S.;Miyazono,K.;Itoh,S.;ten Dijke,P.;Heiss,E.H.;Place,A.E.;Risingsong,R.;Williams,C.R.;Honda,T.;Gribble,G.W.and Spom,M.B.(2003):Synthetic triterpenoids enhance transfoorning growth factor beta/Smadsignaling,Cancer Res(vol.63),No.6,pp.1371-6.
Suh,W.S.;Kim,Y.S.;Schimmer,A.D.;Kitada,S.;Minden,M.;Andreeff,M.;Suh,N.;Spom,M.and Reed,J.C.(2003):Synthetic triterpenoids activate a pathway for apoptosisinAML cells involving downregulation of FLIP and sensitization to TRAIL,Leukemia(vol.17),No.11,pp.2122-9.
Tiedemann,R.E.;Schmidt,J.;Keats,J.J.;Shi,C.X.;Zhu,Y.X.;Palmer,S.E.;Mao,X.;Schimmer,A.D.and Stewart,A.K.(2009):Identification of a potent natural triterpenoidinhibitor of proteosome chymotrypsin-like activity and NF-kappaB with antimyeloma activityin vitro and in vivo,Blood(vol.113),No.17,pp.4027-37.
Weller,M.,Stupp,R.,Reifenberger,G.,Brandes,A.A.,van den Bent,M.J.,Wick,W.,andHegi,M.E.2010.MGMT promoter methylation in malignant gliomas:ready forpersonalized medicine?NatRev Neurol6:39-51.
Wiechen,K.;Diatchenko,L.;Agoulnik,A.;Scharff,K.M.;Schober,H.;Arlt,K.;Zhumabayeva,B.;Siebert,P.D.;Dietel,M.;Schafer,R.and Sers,C.(2001):Caveolin-1isdown-regulated in human ovarian carcinoma and acts as a candidate tumor suppressor gene,Am J Pathol(vol.159),No.5,pp.1635-43.
Yamamoto,M.;Fukushima,T.;Hayashi,S.;Ikeda,K.;Tsugu,H.;Kimura,H.;Soma,G.and Tomonaga,M.(2000):Correlation of the expression of nuclear factor-kappa B,tumornecrosis factor receptor type1(TNFR1)and c-Myc with the clinical course in the treatmentof malignant astrocytomas with recombinant mutant human tumor necrosis factor-alpha(TNF-SAM2),Anticancer Res(vol.20),No.1C,pp.611-8.
Zhou,B.B.,Zhang,H.,Damelin,M.,Geles,K.G.,Grindley,J.C.,and Dirks,P.B.2009.Tumour-initiating cells:challenges and opportunities for anticancer drug discovery.NatRev Drug Discov8:806-823.
Claims (13)
1.根据式I、II或III的化合物或其盐:
其用于治疗胶质母细胞瘤,其中:
X是羰基、亚甲基、羟基次甲基、烷氧基次甲基、氨基次甲基、肟、腙、芳基腙或缩氨基脲;
Y是羰基、亚甲基、羟基次甲基、烷氧基次甲基、氨基次甲基、肟、腙、芳基腙或缩氨基脲;
R1是氢、经取代的烷基、酰基(RaCO-)或氨基甲酰基(RbRcNCO-);其中Ra是氢、经取代的低级烷基、经取代的芳基、经取代的低级芳烷基或N-琥珀酰亚胺基;Rb和Rc独立地为氢、经取代的杂烷基、经取代的低级烷基、经取代的芳基、经取代的杂芳基或经取代的低级芳烷基;
R2是异戊二烯基或氢;并且
R3如果存在,则为氢、卤素、羟基、经取代的烷基、环烷基、烷氧基、烷基硫基或氨基。
2.根据权利要求1所述的化合物,其中:
(i)所述化合物由式I定义,并且R1是氢,R2是异戊二烯基,X是羰基,Y是羰基;或者
(ii)所述化合物由式II定义,并且R1是氢,R2是异戊二烯基,R3是氢,X和Y是羟基次甲基;或者
(iii)所述化合物由式I定义,并且R1是氢,R2是异戊二烯基,X是羰基,Y是羟基次甲基;或者
(iv)所述化合物由式I定义,并且R1是乙酰基,R2是异戊二烯基,X是羰基,Y是羰基;或者
(v)所述化合物由式III定义,并且R1是氢,R2是异戊二烯基,X是羰基。
3.根据权利要求1或2所述的化合物,其中待治疗的胶质母细胞瘤选自:原发性胶质母细胞瘤、复发性胶质母细胞瘤、基因O6-甲基鸟嘌呤-甲基转移酶(MGMT)之启动子的甲基化增加的胶质母细胞瘤、MGMT之启动子的甲基化未增加的胶质母细胞瘤、具有突变之p53的胶质母细胞瘤、不具有突变之p53的胶质母细胞瘤、编码B细胞抑制剂中κ轻链多肽基因增强子(NFKBIA)的基因发生改变的胶质母细胞瘤、编码NFKBIA的基因未发生改变的胶质母细胞瘤、编码表皮生长因子受体(EGFR)的基因发生改变的胶质母细胞瘤、编码EGFR的基因未发生改变的胶质母细胞瘤、编码血小板衍生生长因子受体(PDGFRA)的基因发生改变的胶质母细胞瘤、编码PDGFRA的基因未发生改变的胶质母细胞瘤、编码异柠檬酸脱氢酶1(IDHI)的基因发生改变的胶质母细胞瘤、编码IDHI的基因未发生改变的胶质母细胞瘤、编码1型神经纤维瘤(NF1)的基因发生改变的胶质母细胞瘤以及编码NF1的基因未发生改变的胶质母细胞瘤。
4.根据权利要求1或2所述的化合物,其中所述胶质母细胞瘤包含过表达或表达选自以下之基因的细胞:CD133、ATP-结合盒亚家族G成员2(ABCG2)、醛脱氢酶1(ALDH1A1)、musashi同源物1(MSI-1)、巢蛋白以及性别决定区Y-box2(SOX-2)。
5.根据权利要求1至4中任一项所述的化合物,其中所述胶质母细胞瘤包含干细胞样细胞的亚组。
6.根据权利要求1至5中任一项所述的化合物,其中所述化合物在施用后将所述胶质母细胞瘤细胞的细胞生长延迟多至10天。
7.药物组合物,其用于治疗胶质母细胞瘤,其包含根据式I、II或III的化合物,其中X、Y、R1、R2以及R3具有权利要求1中给出的含义。
8.根据权利要求7所述的药物组合物,其中:
(i)所述化合物由式I定义,并且R1是氢,R2是异戊二烯基,X是羰基,Y是羰基;或者
(ii)所述化合物由式II定义,并且R1是氢,R2是异戊二烯基,R3是氢,X和Y是羟基次甲基;或者
(iii)所述化合物由式I定义,并且R1是氢,R2是异戊二烯基,X是羰基,Y是羟基次甲基;或者
(iv)所述化合物由式I定义,并且R1是乙酰基,R2是异戊二烯基,X是羰基,Y是羰基;或者
(v)所述化合物由式III定义,并且R1是氢,R2是异戊二烯基,X是羰基。
9.根据权利要求7或8所述的药物组合物,其中待治疗的胶质母细胞瘤选自:原发性胶质母细胞瘤、复发性胶质母细胞瘤、基因O6-甲基鸟嘌呤-甲基转移酶(MGMT)之启动子的甲基化增加的胶质母细胞瘤、MGMT之启动子的甲基化未增加的胶质母细胞瘤、具有突变之p53的胶质母细胞瘤、不具有突变之p53的胶质母细胞瘤、编码B细胞抑制剂中κ轻链多肽基因增强子(NFKBIA)的基因发生改变的胶质母细胞瘤、编码NFKBIA的基因未发生改变的胶质母细胞瘤、编码表皮生长因子受体(EGFR)的基因发生改变的胶质母细胞瘤、编码EGFR的基因未发生改变的胶质母细胞瘤、编码血小板衍生生长因子受体(PDGFRA)的基因发生改变的胶质母细胞瘤、编码PDGFRA的基因未发生改变的胶质母细胞瘤、编码异柠檬酸脱氢酶1(IDHI)的基因发生改变的胶质母细胞瘤、编码IDHI的基因未发生改变的胶质母细胞瘤、编码1型神经纤维瘤(NF1)的基因发生改变的胶质母细胞瘤以及编码NF1的基因未发生改变的胶质母细胞瘤。
10.根据权利要求7或8所述的药物组合物,其中所述胶质母细胞瘤包含过表达或表达选自以下之基因的细胞:CD133、ATP-结合盒亚家族G成员2(ABCG2)、醛脱氢酶1(ALDH1A1)、musashi同源物1(MSI-1)、巢蛋白以及性别决定区Y-box2(SOX-2)。
11.根据权利要求7至10中任一项所述的药物组合物,其还包含至少一种具有抗癌活性的其他化合物。
12.根据权利要求11所述的药物组合物,其中所述至少一种其他化合物是替莫唑胺或其盐。
13.用于确定使用根据式I、II或III的化合物的治疗是否适用于患者的方法,所述式中X、Y、R1、R2以及R3具有权利要求1中给出的含义,所述方法包括以下步骤:
a)测定所述患者的肿瘤组织或肿瘤细胞样品中CD133的表达水平;
b)将步骤a)中测定的表达水平与参考值进行比较;以及
c)基于步骤b)的比较结果确定使用根据式I、II或III的化合物的治疗是否适用于患者,其中过表达表示所述治疗适用于所述患者。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201161497215P | 2011-06-15 | 2011-06-15 | |
| US61/497,215 | 2011-06-15 | ||
| PCT/EP2012/061485 WO2012172069A1 (en) | 2011-06-15 | 2012-06-15 | Glioblastoma inhibiting compounds and their use |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN103764659A true CN103764659A (zh) | 2014-04-30 |
Family
ID=46319762
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201280028960.8A Pending CN103764659A (zh) | 2011-06-15 | 2012-06-15 | 抑制胶质母细胞瘤的化合物及其用途 |
Country Status (13)
| Country | Link |
|---|---|
| US (1) | US9573960B2 (zh) |
| EP (1) | EP2721035B1 (zh) |
| JP (1) | JP6228113B2 (zh) |
| CN (1) | CN103764659A (zh) |
| AU (1) | AU2012268984B2 (zh) |
| BR (1) | BR112013032360A2 (zh) |
| CA (1) | CA2838945A1 (zh) |
| CL (1) | CL2013003563A1 (zh) |
| IL (1) | IL229767A0 (zh) |
| MX (1) | MX340816B (zh) |
| RU (1) | RU2014101070A (zh) |
| WO (1) | WO2012172069A1 (zh) |
| ZA (1) | ZA201309365B (zh) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN105796549A (zh) * | 2016-04-22 | 2016-07-27 | 中国医学科学院基础医学研究所 | 藤黄酰胺用于制备治疗人神经胶质瘤的药物的用途 |
| CN105802928A (zh) * | 2016-03-30 | 2016-07-27 | 苏州偲聚生物材料有限公司 | 用于检测血清中mgmt抗体的多肽,检测器件和检测试剂盒 |
| CN117538458A (zh) * | 2024-01-09 | 2024-02-09 | 中国医学科学院北京协和医院 | 同时定量分析14种单糖/二糖的液相色谱串联质谱分析方法 |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2014023329A1 (en) * | 2012-08-06 | 2014-02-13 | Life And Brain Gmbh | Niclosamide and its derivatives for use in the treatment of solid tumors |
| EP3313388A4 (en) | 2015-06-24 | 2019-05-15 | Duke University | CHEMICAL MODULATORS OF SIGNALING PATHWAYS AND THERAPEUTIC USE |
| WO2017023277A1 (en) * | 2015-07-31 | 2017-02-09 | Swedish Health Services | Methods and compositions for characterization of glioblastoma multiforme tumors and cancer stem cells |
| US11499972B2 (en) | 2015-09-15 | 2022-11-15 | Swedish Health Services | Methods and panels of compounds for characterization of glioblastoma multiforme tumors and cancer stem cells thereof |
| CN107475213A (zh) * | 2016-06-08 | 2017-12-15 | 中国科学院苏州纳米技术与纳米仿生研究所 | 用于检测血清中mgmt抗体的多肽,检测器件和检测试剂盒 |
| US11311606B2 (en) | 2018-03-13 | 2022-04-26 | Georgetown University | Enhancing chemotherapy in medulloblastoma and glioblastoma with high basal p53 levels |
| CN110433154A (zh) * | 2019-08-12 | 2019-11-12 | 昆明理工大学 | 藤黄酸的新用途 |
| WO2023183463A1 (en) * | 2022-03-23 | 2023-09-28 | University Of Cincinnati | Methods of potentiating temozolomide activity against glioblastoma cells |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1300403A1 (en) * | 2001-10-02 | 2003-04-09 | Aventis Pharma S.A. | Process for the manufacture of hypoxyxylerone derivatives |
| US20030078292A1 (en) * | 1999-05-21 | 2003-04-24 | Cytovia, Inc. | Gambogic acid, analogs and derivatives as activators of caspases and inducers of apoptosis |
| CN101289482A (zh) * | 2007-09-29 | 2008-10-22 | 辽宁利锋科技开发有限公司 | 藤黄酸苷衍生物和类似物及其制备方法和用途 |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2000045165A1 (en) * | 1999-02-01 | 2000-08-03 | Cytovia, Inc. | Methods of identifying therapeutically effective antineoplastic agents with cultured cells having intact cell membranes and corresponding products |
| JP3904364B2 (ja) | 2000-03-03 | 2007-04-11 | 独立行政法人科学技術振興機構 | 抗マラリア活性を有する新規化合物 |
| WO2008148008A1 (en) * | 2007-05-23 | 2008-12-04 | Emory University | High throughput bioassay for identifying selective trka receptor agonists, and gambogic amide, a selective trka agonist with neuroprotective activity |
| PA8851101A1 (es) * | 2008-12-16 | 2010-07-27 | Lilly Co Eli | Compuesto amino pirazol |
-
2012
- 2012-06-15 WO PCT/EP2012/061485 patent/WO2012172069A1/en active Application Filing
- 2012-06-15 JP JP2014515214A patent/JP6228113B2/ja not_active Expired - Fee Related
- 2012-06-15 RU RU2014101070/04A patent/RU2014101070A/ru not_active Application Discontinuation
- 2012-06-15 CN CN201280028960.8A patent/CN103764659A/zh active Pending
- 2012-06-15 BR BR112013032360A patent/BR112013032360A2/pt not_active IP Right Cessation
- 2012-06-15 AU AU2012268984A patent/AU2012268984B2/en not_active Expired - Fee Related
- 2012-06-15 EP EP12728260.6A patent/EP2721035B1/en not_active Not-in-force
- 2012-06-15 CA CA2838945A patent/CA2838945A1/en not_active Abandoned
- 2012-06-15 US US14/126,512 patent/US9573960B2/en active Active
- 2012-06-15 MX MX2013014708A patent/MX340816B/es active IP Right Grant
-
2013
- 2013-12-02 IL IL229767A patent/IL229767A0/en unknown
- 2013-12-11 ZA ZA2013/09365A patent/ZA201309365B/en unknown
- 2013-12-12 CL CL2013003563A patent/CL2013003563A1/es unknown
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20030078292A1 (en) * | 1999-05-21 | 2003-04-24 | Cytovia, Inc. | Gambogic acid, analogs and derivatives as activators of caspases and inducers of apoptosis |
| EP1300403A1 (en) * | 2001-10-02 | 2003-04-09 | Aventis Pharma S.A. | Process for the manufacture of hypoxyxylerone derivatives |
| CN101289482A (zh) * | 2007-09-29 | 2008-10-22 | 辽宁利锋科技开发有限公司 | 藤黄酸苷衍生物和类似物及其制备方法和用途 |
Non-Patent Citations (2)
| Title |
|---|
| PENG JIN-YONG等: "Separation of Two New Prenylated Dihydroflavonoids from Dolichos tenuicaulis (Baker) Craib by High-speed Counter-current Chromatography", 《CHINESE JOURNAL OF ANALYTICAL CHEMISTRY》, vol. 35, no. 10, 31 October 2007 (2007-10-31), pages 1444 - 1448, XP022857804, DOI: 10.1016/S1872-2040(07)60087-5 * |
| 冯锋等: "藤黄酸衍生物的研究", 《中国药科大学学报》, vol. 36, no. 4, 31 December 2005 (2005-12-31), pages 302 - 305 * |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN105802928A (zh) * | 2016-03-30 | 2016-07-27 | 苏州偲聚生物材料有限公司 | 用于检测血清中mgmt抗体的多肽,检测器件和检测试剂盒 |
| CN105796549A (zh) * | 2016-04-22 | 2016-07-27 | 中国医学科学院基础医学研究所 | 藤黄酰胺用于制备治疗人神经胶质瘤的药物的用途 |
| WO2017181799A1 (zh) * | 2016-04-22 | 2017-10-26 | 中国医学科学院基础医学研究所 | 藤黄酰胺用于制备治疗人神经胶质瘤的药物的用途 |
| CN117538458A (zh) * | 2024-01-09 | 2024-02-09 | 中国医学科学院北京协和医院 | 同时定量分析14种单糖/二糖的液相色谱串联质谱分析方法 |
| CN117538458B (zh) * | 2024-01-09 | 2024-03-29 | 中国医学科学院北京协和医院 | 同时定量分析14种单糖/二糖的液相色谱串联质谱分析方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| MX340816B (es) | 2016-07-26 |
| EP2721035A1 (en) | 2014-04-23 |
| CA2838945A1 (en) | 2012-12-20 |
| MX2013014708A (es) | 2014-08-18 |
| US9573960B2 (en) | 2017-02-21 |
| ZA201309365B (en) | 2015-11-25 |
| CL2013003563A1 (es) | 2014-06-06 |
| NZ618170A (en) | 2015-04-24 |
| WO2012172069A1 (en) | 2012-12-20 |
| RU2014101070A (ru) | 2015-07-20 |
| JP6228113B2 (ja) | 2017-11-08 |
| AU2012268984B2 (en) | 2016-07-14 |
| EP2721035B1 (en) | 2018-06-13 |
| BR112013032360A2 (pt) | 2017-06-13 |
| JP2014517025A (ja) | 2014-07-17 |
| US20150148390A1 (en) | 2015-05-28 |
| IL229767A0 (en) | 2014-01-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN103764659A (zh) | 抑制胶质母细胞瘤的化合物及其用途 | |
| KR102099159B1 (ko) | 아크릴산 유도체, 그의 제조방법 및 의약에 있어서의 그의 사용방법 | |
| AU2012268984A1 (en) | Glioblastoma inhibiting compounds and their use | |
| JP5492565B2 (ja) | Janusキナーゼ阻害剤としての置換複素環 | |
| US9844522B2 (en) | Niclosamide and its derivatives for use in the treatment of solid tumors | |
| US7332502B2 (en) | Phenanthroindolizidine alkaloids | |
| JPWO2016152907A1 (ja) | 胆管癌治療剤 | |
| KR20080007443A (ko) | c-MET 자기 인산화 저해 작용을 갖는 티에노피리딘유도체, 퀴놀린 유도체, 및 퀴나졸린 유도체 | |
| EP1991215A1 (en) | Use of inhibitors of scavenger receptor class proteins for the treatment of infectious diseases | |
| KR20140109498A (ko) | 폴리하이드록시 크로메논 화합물의 합성 및 이의 항종양 효과 | |
| CN102361853A (zh) | 甲苯胺磺酰胺及其用途 | |
| Byczek-Wyrostek et al. | Simple 2 (5H)-furanone derivatives with selective cytotoxicity towards non-small cell lung cancer cell line A549–Synthesis, structure-activity relationship and biological evaluation | |
| CN101827851A (zh) | 用于治疗肿瘤的5-氰基噻吩并吡啶 | |
| CN102015724A (zh) | 噻吩并嘧啶类 | |
| CN101341151A (zh) | 二氮杂䓬酮类 | |
| CA3003554A1 (en) | Pyrropyrimidine compounds as mnks inhibitors | |
| KR102205656B1 (ko) | 암의 예방 또는 치료용 약학적 조성물 | |
| NZ618170B2 (en) | Glioblastoma inhibiting compounds and their use | |
| Lee et al. | HS-133, a novel fluorescent phosphatidylinositol 3-kinase inhibitor as a potential imaging and anticancer agent for targeted therapy | |
| KR101457638B1 (ko) | 피라졸릴나프탈레놀 유도체, 그 제법 및 그것을 포함하는 항암 조성물 | |
| US20220119399A1 (en) | Compounds and compositions that cause mycn and/or cmyc degradation and methods of use thereof | |
| KR20170043958A (ko) | 항암효능을 보이는 나프탈레닐페닐피라조린 유도체 | |
| KR20230161639A (ko) | 제주쑥 추출물을 함유하는 항암용 조성물 | |
| CN114026098A (zh) | 苯并吡喃基化合物、方法及其用途 | |
| KR101524770B1 (ko) | 세포주기 조절을 통한 항암 효과를 보이는 폴리페놀 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| WD01 | Invention patent application deemed withdrawn after publication | ||
| WD01 | Invention patent application deemed withdrawn after publication |
Application publication date: 20140430 |