CN103200955A - 包含肽和病毒神经氨酸酶抑制剂的组合物 - Google Patents
包含肽和病毒神经氨酸酶抑制剂的组合物 Download PDFInfo
- Publication number
- CN103200955A CN103200955A CN2011800554632A CN201180055463A CN103200955A CN 103200955 A CN103200955 A CN 103200955A CN 2011800554632 A CN2011800554632 A CN 2011800554632A CN 201180055463 A CN201180055463 A CN 201180055463A CN 103200955 A CN103200955 A CN 103200955A
- Authority
- CN
- China
- Prior art keywords
- peptide
- inhibitor
- compositions
- aminoacid
- natural
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/04—Peptides having up to 20 amino acids in a fully defined sequence; Derivatives thereof
- A61K38/10—Peptides having 12 to 20 amino acids
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K7/00—Peptides having 5 to 20 amino acids in a fully defined sequence; Derivatives thereof
- C07K7/64—Cyclic peptides containing only normal peptide links
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/16—Amides, e.g. hydroxamic acids
- A61K31/165—Amides, e.g. hydroxamic acids having aromatic rings, e.g. colchicine, atenolol, progabide
- A61K31/167—Amides, e.g. hydroxamic acids having aromatic rings, e.g. colchicine, atenolol, progabide having the nitrogen of a carboxamide group directly attached to the aromatic ring, e.g. lidocaine, paracetamol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/35—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having six-membered rings with one oxygen as the only ring hetero atom
- A61K31/351—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having six-membered rings with one oxygen as the only ring hetero atom not condensed with another ring
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/04—Peptides having up to 20 amino acids in a fully defined sequence; Derivatives thereof
- A61K38/12—Cyclic peptides, e.g. bacitracins; Polymyxins; Gramicidins S, C; Tyrocidins A, B or C
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/19—Cytokines; Lymphokines; Interferons
- A61K38/191—Tumor necrosis factors [TNF], e.g. lymphotoxin [LT], i.e. TNF-beta
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/007—Pulmonary tract; Aromatherapy
- A61K9/0073—Sprays or powders for inhalation; Aerolised or nebulised preparations generated by other means than thermal energy
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
- A61P31/16—Antivirals for RNA viruses for influenza or rhinoviruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Organic Chemistry (AREA)
- Virology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Gastroenterology & Hepatology (AREA)
- Immunology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Pulmonology (AREA)
- General Chemical & Material Sciences (AREA)
- Molecular Biology (AREA)
- Zoology (AREA)
- Communicable Diseases (AREA)
- Oncology (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Pain & Pain Management (AREA)
- Otolaryngology (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Peptides Or Proteins (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicinal Preparation (AREA)
Abstract
描述了一种组合物,其包含-肽和-病毒神经氨酸酶的抑制剂,所述肽由7-17个相邻的氨基酸组成,且包含六聚体TX1EX2X3E,其中X1、X2和X3每个均可以是天然的或非天然的氨基酸,其中所述肽是不具有TNF-受体-结合活性并且是环化的。
Description
本发明涉及用于治疗流感的药物组合物。
在人类中,流感是由流感病毒造成的呼吸道和整个生物体的严重疾病。流感病毒属于正粘病毒科,其特征在于以负链取向的分段RNA基因组。与人类有关的类型是流感-A和-B病毒,其中已知尤其是亚型A是呼吸道的高热病的病原体。除了兽医学重要性以外,所有流感病毒具有人兽互传(zoonitic)潜力,即存在从鸡或猪转移到人类的可能性。
流感作为大流行病周期性地出现,其在大多数情况下起源于东南亚和中国,并从这些地方向全世界传播。流感病毒的大流行与高死亡数目有关,不仅涉及老年人,而且涉及青少年。根据世界卫生组织(WHO),每年的季节性流感导致全世界约300万至500万例严重疾病的发病病例,其中死亡率为250,000至500,000。最常见的死因是引起肺衰竭的流感性肺炎,但是也可能发生心血管损伤诸如心肌炎(心肌炎症)或心包炎(心包囊的炎症)。其它相对常见的死因可以是脑或脑膜的炎症(脑膜脑炎)或其它器官系统(尤其是肾)的损伤。
一般而言,潜伏期是4-5天,但也可能更短。该疾病开始于头痛、发冷、寒战和咳嗽的突然发作。这之后是最高达41℃的高热、肌肉疼痛、失去食欲和全身性乏力感。该阶段持续约3天,此后发热减退,并且在大多数情况下从第6天开始回落至正常值,病毒从体内消除。咳嗽可能持续数周。
如果在上述征状之后发展成初始病毒性间质性(经常出血性) 肺炎,则出现严重的危及生命的流感。除了虚弱的人以外,它也发生在大约25%的健康人或以前未受损伤的人中,且可以持续最多2周。通过肺重量的增加,可以检测出这样的肺炎。
肺炎也可能通过细菌(尤其是肺炎链球菌、金黄色葡萄球菌和流感嗜血杆菌)超感染二次产生。这些并发症的促进因素尤其是,其它肺疾病(例如哮喘)、免疫缺陷、年龄(婴幼儿和老年人)、糖尿病、肺损伤、吸烟。因此,具有这些并发症的人是疫苗接种的首要目标群。
流感病毒通过飞沫传染到达生物体,并通过HA蛋白结合在口、鼻和咽粘膜的上皮细胞上的末端神经氨酸残基上进行感染。从这里,它们传播至下呼吸道。可以在纤毛上皮和在呼吸道的所有区域的生粘液皮肤层中观察到细胞的破坏。如果形成原发性间质性肺炎,病毒会传染至肺实质的细胞。发现肺泡壁强烈肿胀,肺泡壁的上皮由于细胞破坏经常完全蚀落。通过肺重量的增加,可以检测出肺组织的这样的肿胀。
存在着预防性和治疗性处理。可使用针对流感-A和-B感染的疫苗。这些疫苗是在鸡蛋和/或细胞培养物中培养的被杀死的病毒。在疫苗接种以后大约2周,疫苗保护已经达到它的完全功效。但是,由于流感病毒的高变异性,必须每年针对当前流传的病毒亚型或亚型变体改进疫苗。
另外使用病毒神经氨酸酶的抑制剂(扎那米韦、奥司他韦),它们会阻止新复制的病毒颗粒从宿主细胞脱离。它们优选地在流感病毒感染发生和检测出以后不久使用,以便在感染的早期阶段抑制所述病毒的传播(WO
2003/026567 A2)。
但是,病毒神经氨酸酶的抑制剂仅仅干预病毒的增殖,却不会灭活已经存在于体内的病毒。神经氨酸酶抑制剂仅可以有助于将疾病持续时间微小地缩短(平均而言,在成人的情况中缩短1天)。
本发明的目标是,显著地增加这样的病毒增殖抑制剂的治疗效果。用本发明应提供改进的用于治疗流感病毒感染的药物组合物。
因此,本发明涉及尤其是用于预防和治疗流感的组合物,其包含
- 肽,其由7-17个相邻的氨基酸组成,且包含六聚体TX1EX2X3E,其中X1、X2和X3每个均可以是天然的或非天然的氨基酸,其中所述肽不具有TNF-受体-结合活性,且是环化的,和
- 病毒神经氨酸酶的抑制剂。
根据本发明现已发现,如果将如上定义的肽与神经氨酸酶抑制剂组合使用,用于治疗流感感染,则可以令人惊讶地提高神经氨酸酶抑制剂的作用。由此也表明了根据本发明的化合物的预防性用途。已经证实,本发明在治疗由流感病毒导致的肺炎中是特别有效的。
根据本发明待使用的肽例如由欧洲专利EP 1 264 599 B1 (或由US 2007/299003 A、WO
94/18325 A1或WO 2008/148545 A1)已知,且已经在现有技术中用于治疗水积(肺水肿),并尤其是用于重吸收这些水积。但是,令人惊奇地,这些肽也适合用于影响经由毛细血管内皮进入肺上皮中的反向流体流动,且因此也可以用于预防和治疗上皮细胞以及内皮细胞的渗透性过高(WO
2010/099556 A)。
这些肽(其本身是已知的,且根据本发明与神经氨酸酶抑制剂一起使用)不具有TNF-受体-结合活性(Hribar等人, Eur. J. Immunol. 1999; Elia等人, AJRCCM 2003;也参见:下面的实施例部分),且是环化的。这些肽的优选变体由7-17个相邻的氨基酸组成,且含有六聚体TPEGAE
(SEQ ID Nr. 4)。
但是WO 2010/099556 A1和EP 1
264 599 A1靶向肺中的某些病理学征状的治疗,而非靶向由某种病原体造成的疾病的预防和治疗,而根据本发明的应用则是完全不同的。
正如在本发明的研究的过程中已经证实的,根据权利要求(尤其根据WO
2010/099556 A1)所述的肽以协同方式促进在根据本发明的组合制品中的神经氨酸酶抑制剂的作用。因而,根据本发明的应用直接地靶向由于流感病毒引起的感染,而非靶向可能由几种不同病原体引起的一般征状(例如在WO 2010/099556 A1或在EP 1
264 599 A1中的情况)。
尽管在本领域技术人员看来,显而易见的是,神经氨酸酶抑制剂仅能抑制流感病毒的增殖,但是不会由此减少已经存在的病毒;然而,完全令人惊奇并且没有为现有技术所建议的是,神经氨酸酶抑制剂和根据本发明的肽的组合流感防治的显著改善。本领域技术人员在现有技术中没有获得对该组合的任何建议,相反:
在WO 2003/026567 A2中叙称,用于治疗流感的神经氨酸酶抑制剂也适合预防与流感关联的细菌感染。基于该文件,本领域技术人员根本不会认识到给神经氨酸酶抑制剂添加改善抗病毒效果或流感治疗功效的其它添加剂的任何理由。
在本发明的一个特别优选的实施方式中,根据本发明的组合物包含环化肽,所述环化肽由选自下述的彼此相继的氨基酸序列组成:
- QRETPEGAEAKPWY (SEQ ID Nr. 5)
- PKDTPEGAELKPWY (SEQ ID Nr. 6)
- CGQRETPEGAEAKPWYC (SEQ ID Nr. 1),和
- CGPKDTPEGAELKPWYC (SEQ ID Nr. 7)
及其至少7个氨基酸的片段,所述片段具有六聚体TPEGAE的片段。
优选地,在所述组合物中的肽包含氨基酸序列CGQRETPEGAEAKPWYC (SEQ ID Nr. 1),且经由C-残基环化。因而,该特别优选的肽具有下述氨基酸序列(SEQ ID Nr.
1) (NH2) Cys-Gly-Gln-Arg-Glu-Thr-Pro-Glu-Gly-Ala-Glu-Ala-Lys-Pro-Trp-Tyr-Cys
(COOH)。该肽也被称作“AP301”。
在此,根据本发明的肽的环化可以如下实现:例如,经由在N端和C端处的2个C-残基之间的二硫键而直接环化,或者通过经由2个半胱氨酸使所述肽偶联在载体物质上。在这种情况下,在根据本发明的肽中,优选在分子的起始处和终点处具有半胱氨酸残基。也可以使用能实现肽环化的其它官能团,例如通过酸基团与胺或醇导致生酰胺-或酯环合(在此例如,氨基酸天门冬氨酸和谷氨酸可以与丝氨酸、苏氨酸、酪氨酸、天冬酰胺、谷氨酰胺或赖氨酸优选地进行分子内环化)。所述肽的环化优选地通过所述肽的C-残基之间的二硫键(如果存在的话)来实现。
因而,根据本发明的其它优选的肽是例如CGQKETPEGAEAKPWYC (SEQ ID Nr. 8)、CGQRETPEGAEARPWYC
(SEQ ID Nr. 9)、CGQRETPEGAEAKPC
(SEQ ID Nr. 10)、CQRETPEGAEAKPWYC (SEQ ID Nr.
11)或CGQRETPEGAEAKFWYC (SEQ ID Nr. 12)。
但是,所述环化还可以通过使所述肽结合在载体物质上来实现。作为这类环化的载体物质,所有常规的药学上可用的物质都是合适的,其能够例如与半胱氨酸的SH基(或与所述肽的其它天然存在的或人工引入的化学反应性基团) 共价结合,其中常见的载体蛋白诸如钥孔戚血蓝素(KLH)、破伤风毒素等特别合适。在载体上也可以具有相邻的双功能残基(例如紧邻胺或醇基的酸基团)。在该背景下,重要的是“环化”既包括分子内环合与包括载体(结合的肽从所述载体伸出(通过肽的N端和C端结合在所述载体上))的键合;由此,这样环化的肽呈现环状空间结构,且相应地被稳定化。
病毒神经氨酸酶的抑制剂是已知的,且其本身已经在流感的预防和治疗中证实有效。这样的病毒神经氨酸酶抑制剂(例如扎那米韦(Zanamivir)、奥司他韦(Oseltamivir)、拉尼米韦(Laninamivir)或培拉米韦(Peramivir)) 会阻止新复制的病毒颗粒从宿主细胞分离。尤其是它们可以在流感病毒感染发生和检测出之后不久在感染早期抑制病毒传播。
但是,这些神经氨酸酶抑制剂仅仅干预病毒的增殖,却不会灭活已经存在于体内的病毒,因而,通常仅可以将疾病持续时间微小地缩短(平均而言,在成人的情况中缩短1天)。但是,首要的是,通常不能足够有效地防治或预防流感征状,特别是肺炎,其在大多数情况下导致特殊的并发症。
神经氨酸酶是对于流感病毒复制而言一种重要的酶,且已经被描述为负责释放病毒的“分子剪刀”。
神经氨酸酶抑制剂包含唾液酸的类似物,所述类似物代表一类新的第二代抗病毒剂,其显示出对流感A和B病毒的效力。根据本发明的神经氨酸酶抑制剂可以是迄今为止所有建议用于此的化合物,如在例如US
2008/0063722 A1中所总结的物质(以及这样的物质的优选药物制剂)。这些物质可以抑制A型或B型流感病毒粒子的强毒株的神经氨酸酶蛋白的至少一种酶活动。这样的物质可以用于预防和治疗流感;但是,与根据本发明的上面定义的肽相组合,会显著提高该作用。
在例如美国专利号5,453,533、5,763,483、5,952,375、5,958,973、5,512,596、5,886,213、5,602,277、6,410,594、5,360,817、5,866,601、6,340,702、6,451,766、6,455,571、6,593,314、6,509,359、6,518,305和6,831,096中描述了可以在本发明的组合物中使用的神经氨酸酶抑制剂的例子。已经用于人类(或至少处于临床试验中)且因此特别优选的是例如CS-8958(RI 18958;US 2008/0063722
A1),扎那米韦(GG167,RELENZA®),培拉米韦(RWJ-270201,BCX-1812),磷酸奥司他韦(Ro64-0796,GS4104),羧酸奥司他韦(Ro64-0802,GS4071),或奥司他韦(GS4104,达菲®)。当然,根据本发明包括神经氨酸酶抑制剂的所有有效化学形式,即作为盐、外消旋形式、光学纯的形式和/或无盐形式(也以例如对映异构体或非对映异构体的形式)。
优选地,病毒神经氨酸酶的抑制剂是扎那米韦或奥司他韦;这些物质是优选的,因为它们已经特别成功地用于人类的治疗中。
优选地,根据本发明的组合物包含药学上可接受的载体,且以适合施用给人类的药物组合物的形式制备。
表述“药物组合物”表示,包含神经氨酸酶抑制剂和如上定义的肽(当然,也表示这样的物质的合适的(即不会彼此负面干扰的)混合物)的组合物,所述组合物预防、改善或治愈在本文中所描述的病症。表述“药物组合物”具体地表示这样的组合物:其具有神经氨酸酶抑制剂和如上所述的肽,以及药学上可接受的载体或赋形剂(两种表述可以可互换地使用)。本领域技术人员已知的载体或赋形剂的适当实例是:水、食盐溶液、磷酸钠、醋酸钠、碳酸钠、柠檬酸盐、甘氨酸、甘氨酰甘氨酸、组氨酸、赖氨酸、精氨酸、TRIS和柠檬酸钠或它们的混合物。当然,也可以采用林格溶液、葡萄糖溶液或非还原糖的溶液;因此,甘露醇、海藻糖、蔗糖、山梨醇、果糖、麦芽糖、乳糖或葡聚糖、Hank溶液、固定油、油酸乙酯、在食盐溶液中的5% 葡萄糖、改善等张性和化学稳定性的物质、缓冲剂和防腐剂也适合作为这样的载体。其它合适的载体包括,其本身不会诱导抗体(其对要施用所述组合物的个体有害)的产生的任何载体,诸如蛋白、多糖、聚乳酸、聚乙醇酸、聚合氨基酸和氨基酸共聚物。在配制根据本发明的组合物时,当然必须符合有关的指南(例如(欧洲或美国)药典)。由此,也可以使要在根据本发明的组合物中提供的肽通过直接共价结合在这些载体上而环化。
根据本发明的药物组合物可以(作为药物)用本领域技术人员已知的任何适当方法来施用,特别优选的是,将根据本发明待使用的肽或根据本发明的组合物施用进肺中。虽然流感也在动物中起某种作用,并且根据本发明的组合物当然也可以用于预防和治疗动物,但是本发明的重点是预防和治疗人类,即已经被流感感染的人,或处于被该病毒感染的危险中的人(特别是流感流行病或-大流行病)。优选的施用途径是吸入(经由气雾剂),也可以是静脉内给药、滴注、口服给药或它们的组合。在吸入、肠胃外或口服给药中,将本发明的药物与上面定义的药学上可接受的赋形剂相组合配制成剂量单位剂型,如作为溶液、混悬液或乳剂。但是在个别情况下,剂量和给药形式当然也可以取决于各个个体。
因此,将在每种情况下需要的有效量施用给需要给药的个体。在此,“有效量”应当理解为这样的量:其足以有效地实现预期的治疗或预防效果,即例如阻止疾病的进一步传播,或有效地治疗疾病。在此,在大多数情况下,以一般患者为出发点;但是,可以以考虑到给药形式和患者的年龄、体重、状况以及疾病的程度和进展的方式(例如借助于适当的常规药理学方案),配制在所述组合物中的组分的实际有效量。
因此,在根据本发明的组合物中的药学上可接受的载体优选选自:水(特别优选: 注射用水)、食盐、磷酸钠、醋酸钠、碳酸钠、柠檬酸盐、甘氨酸、甘氨酰甘氨酸、组氨酸、赖氨酸、精氨酸、TRIS、柠檬酸钠、林格溶液、葡萄糖、甘露醇、海藻糖、蔗糖、山梨醇、果糖、麦芽糖、乳糖或葡聚糖、Hank溶液、固定油、油酸乙酯、改善等张性和化学稳定性的物质、防腐剂、药学上可接受的蛋白、多糖、聚乳酸、聚乙醇酸、聚合氨基酸和氨基酸共聚物。
也可以如下提供根据本发明的组合物:通过将2种活性组分,即以空间上分开的形式即作为套装提供神经氨酸酶抑制剂和如上所述的肽,所述套装包含至少一种神经氨酸酶抑制剂和肽(各自在单独的容器中)。因此,本发明也涉及一种套装,其包含至少一种神经氨酸酶抑制剂和肽(各自在单独的容器中)。由此能够分开施用(在空间上,但是也在时间上)所述肽和所述抑制剂,这尤其在下述情况下是优选的:如果有关的患者希望根据本发明的2种活性组分以不同给药途径。例如,奥司他韦在大多数情况下口服给药,而根据本发明待使用的肽主要通过吸入来施用。但是,在许多情况下,希望同时给药;例如,扎那米韦同样通过吸入来给药。当然,也可以指明借助于吸入来全身性地提供口服抑制剂。在某些情况下,根据本发明待使用的肽可能难于与神经氨酸酶抑制剂共混,例如如果静脉内地或口服地施用抑制剂且吸入来施用肽。但是,在许多情况下,所述抑制剂和所述肽可以共同吸入施用,由此所述抑制剂直接地到达肺中,且可能通过肺进入血液中(流感病毒首先存在于肺组织中)。
在包含分开的神经氨酸酶-和肽组分的这样的根据本发明的套装中,在本文中所述的特征和所述混合的组合物的优选实施方案当然可以以本领域技术人员可设想的所有组合来提供。
根据本发明的药物例如可以如此来施用,以至于以1µg/kg至10
mg/kg、更优选10µg/kg至5
mg/kg之间和最优选0.1至2
mg/kg之间的剂量来施用本发明的肽。优选地,它作为大丸剂剂量(Bolus-Dosis)来施用。但也可以连续吸入或输注或借助于重复剂量给药来使用。
特别优选的根据本发明的组合物含有-彼此独立地-:
- 所述肽,其量为1µg至10 g、优选10µg至1 g、尤其是1 mg至100 mg,和
- 病毒神经氨酸酶的抑制剂,其量为1µg至10 g、优选100µg至1 g、尤其是1 mg至200 mg。
特别优选的呈液体形式的根据本发明的组合物含有-彼此独立地-:
- 所述肽,其量为1µg至10 g、优选10µg至1 g、尤其是1 mg至100 mg,和
- 病毒神经氨酸酶的抑制剂,其量为1µg至10 g、优选100µg至1 g、尤其是1 mg至200 mg,
并且具有0.5-10 ml的体积、尤其具有1-5
ml的体积。
根据本发明的组合物优选地也可以以干燥形式借助于粉末吸入器来施用。可用于本发明的这样的粉末吸入器的例子描述在美国专利4,995,385和4,069,819中;已经确定的产品是SPINHALER®、ROTAHALER®、FLOWCAPS®、INHALATOR®、DISKHALER®和AEROLIZER®。
根据本发明的组合物优选也可以作为气溶胶借助于液体喷雾器来施用。这样的液体喷雾器的例子是确定的产品,诸如Aeroneb®和Pari®。
根据一个优选的实施方式,根据本发明的组合物的特征在于,所述肽和/或所述病毒神经氨酸酶的抑制剂存在于可雾化的粉末制剂中或存在于可雾化的流体制剂中。
根据本发明的组合物优选地用于治疗和预防流感病毒A型和B型、尤其是A型的感染。但是原则上,所述组合物也适合预防或治疗由任何可能的可以在动物中或在人类中引起疾病的流感病毒株的感染。关于不同流感类型的信息的相关数据库是本领域技术人员众所周知的;具体地,描述了或者甚至测序了许多分离的A型病毒株。
将通过下述实施例和附图更详细地解释本发明,当然,本发明不限于此。
其中:
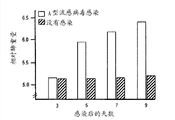
在图1中显示了在感染A型流感以后第3、5、7和9天或没有感染(作为对照)的C57BL/6-小鼠的相对肺重量;
在图2中显示了在感染A型流感感染以后第5、7和9天并用奥司他韦治疗、用根据本发明的组合物治疗和没有治疗(用PBS,作为对照)的C57BL/6-小鼠的相对肺重量;
在图3中显示了在感染A型流感感染以后第7和9天并用扎那米韦治疗、用根据本发明的组合物治疗和没有治疗(用PBS,作为对照)的C57BL/6-小鼠的相对肺重量。
实施例
用本发明的实施例在公认的实验小鼠模型中证实,通过给已经被流感病毒感染的小鼠施用神经氨酸酶抑制剂和神经氨酸酶抑制剂与合成肽AP301
(SEQ ID Nr. 1)的组合,已经实现了本发明的目标。
实施例1
流感病毒感染会造成肺炎的发展
用A型流感株(PR8/34)和150 PFU的剂量经鼻感染实验室小鼠(C57BL/6品系,8周龄)。在感染后第3、5、7和9天,分别取出8只小鼠的肺,并确定相对肺重量,作为肺炎的度量。
检查表明,随小鼠被流感病毒感染以后的持续时间增长,与对照肺相比的肺重量增加越多。结果图示于图1中。
实施例2
通过施用神经氨酸酶抑制剂或施用神经氨酸酶抑制剂和肽AP301的组合来治疗肺炎
用A型流感株(PR8/34)和150 PFU的剂量经鼻感染实验室小鼠(C57BL/6品系,8周龄)。随后,试验动物分别接受10 mg/kg奥司他韦(神经氨酸酶抑制剂)的口服给药和10µg肽AP301/试验动物的气管内给药。在第2和4试验天,重复所述治疗。
在感染后第5、7和9天,分别取出30只小鼠的肺,并确定相对肺重量,作为肺炎的度量。结果图示于图2中。
检查表明,通过测量肺重量,神经氨酸酶抑制剂仅仅产生中度的减轻肺炎的效应。但是,如果除了神经氨酸酶抑制剂以外还将肽AP301施用给被流感病毒感染的小鼠,会显著更大幅度地减轻肺炎。
实施例3
在人全血中先体内后体外地评估AP301肽的促炎性能
在人全血中进行了关于AP301肽的先体内后体外-安全性药理学研究,以确定AP301肽是否会导致从新鲜全血释放促炎标志物白介素-6
(IL-6)(即APN 301是否会表现出TNF-特异性的炎症活性(即TNF-受体-结合活性))。在本研究中,已经使用了新鲜全血,它是公认的用于评估体内炎症应答的预测模型。
方法概要
本研究的目标是,确定AP301肽的促炎信号传递能力。在此使用全血培养物,并借助于ELISA定量白介素-6 (IL-6)的分泌,所述白介素-6是促炎刺激的一种非常灵敏的标志物。
试验体系
试验体系 在试验中使用25 ml从5位健康受试者(GP)新鲜采集的肝素化的血液。
试验项目
鉴定:AP301肽(剂量:1 ng/ml至10µg/ml;在溶液中单次施用)
描述:白色粉末,纯度96%
全血培养
全血(VB) 培养通过将1 ml
VB吸量进24孔板的孔中进行。在每个实验中,包括未刺激的和刺激的对照-培养。
如果可能的话,总是将要研究的物质和刺激物以相同的体积用于给定实验的每个孔中,所述体积不超过孔中总体积的10%。未刺激的对照用PBS实现。同样用PBS进行不同处理的体积调节和稀释。
混合每个孔的内容物,并将平板在37℃和5% CO2下温育24小时。在温育后,将每个孔的内容物转移至新鲜的1.5
ml微管中,并在8,000-9,000 x g下离心15分钟。将每个样品的上清液逐个地分配至2个1.5 ml微管,并在-20℃保存备用。
白介素-6的检测
借助于特异性的ELISA (人IL-6
ELISA-Set, BD Biosciences, 目录号555220),使用抗-人IL-6抗体作为捕获抗体,使用生物素化的抗-人IL-6检测抗体、抗生物素蛋白-辣根过氧化物酶缀合物作为酶试剂,和使用重组IL-6作为标准品,定量白介素-6。使用Packard FusionReader,在450
nm下进行吸光度测量。
数据分析
存储每个板的结果,并使用FusionDataAnalysis软件进行评价。
研究结果总结
本研究的目标是,确定肽AP301的促炎信号传递能力。使用了全血培养物,并借助于ELISA定量IL-6的分泌,所述IL-6是促炎刺激的一种非常灵敏的标志物。
将5位健康受试者的全血样品保持未刺激(阴性对照)、用高和低剂量的LPS刺激(阳性对照)、或者用肽,在从10µg/ml至1 ng/ml.的9种半对数稀释中温育。结果显示在下表中:
表:在添加肽AP301和LPS的情况下,白介素-6从新鲜全血的释放
AP301肽
阳性对照(LPS)
浓度
IL-6的浓度(pg/ml, n = 5)
0 (阴性对照) 小于0.5
小于0.5
10 mg/ml 小于0.5
195.640
1 mg/ml
小于0.5
108.370
3 ng/ml
小于0.5
34.867
1 ng/ml
小于0.5
未测定
结果清楚地揭示,AP301肽在任何试验浓度下都没有诱导任何可检测水平的IL-6分泌。阳性对照(LPS) 导致IL-6分泌的强诱导。
讨论
已经进行实验来评估AP301肽是否会介导促炎级联的诱导。读出参数是得自5位健康供体的全血培养物中诱导的IL-6分泌。结果清楚地表明,AP301肽在供体的培养物中没有诱导可检测水平的IL-6。由此证实了,AP301肽在选择的先体内后体外模型中没有诱导促炎症应答,并因而不具有TNF-受体-结合活性。
实施例4
通过施用神经氨酸酶抑制剂(扎那米韦)或施用神经氨酸酶抑制剂(扎那米韦)和肽AP301的组合来治疗肺炎
用A型流感株(PR8/34)和150 PFU的剂量经鼻感染实验室小鼠(C57BL/6品系,8周龄)。随后,试验动物分别接受1.5 mg/kg扎那米韦(神经氨酸酶抑制剂)的鼻给药和50µg肽AP301/试验动物的气管内给药。在第2和4试验天,重复所述治疗。
在感染后第7和9天,分别取出20只小鼠的肺,并确定相对肺重量,作为肺炎的度量。结果图示于图3中。
检查表明,通过肺重量测量,神经氨酸酶抑制剂(扎那米韦)仅仅产生中度的减轻肺炎的效应。但是,如果除了神经氨酸酶抑制剂以外还将肽AP301施用给被流感病毒感染的小鼠,会显著更大幅度地减轻肺炎。
总结
与神经氨酸酶抑制剂相组合的根据本发明的肽在流感感染的治疗中具有协同效应。
在WO 2010/099556 A1中,如所述的,记载了不同肺征状的治疗,其靶向这样的肺病中的上皮细胞和内皮细胞的渗透性过高。根据WO
2010/099556 A1,证实了要求保护的肽非常适合用于预防和治疗这些征状。尽管根据WO 2010/099556
A1,还可以治疗在流感病毒感染的情况下上皮细胞和内皮细胞的渗透性过高(在该感染形成肺炎的范围内),但是其当然没有建议本发明。用包含该肽的组合制品一般地治疗流感的可能性,是关于所述肽用于治疗-任意的-随流感出现的征状的适用性的一种全新的且创造性的教导。
通过查看根据WO 2010/099556 A1的详述实验,也得出根本区别:在WO
2010/099556 A1的实施例中,通过实验证实,所述肽在肺组织中:
i)影响活性氧的含量,
ii)革兰氏阳性细菌毒素“李斯特菌溶血素(Listeriolysin)”和“肺炎链球菌溶血素(Pneumolysin)”的作用影响渗透性过高,尤其通过调节磷酸化的肌球蛋白轻链的含量、白血球的渗入、活化的蛋白激酶C,
iii)影响流感感染以后的体重,
iv)影响流感感染以后的体温,
v)影响流感感染以后试验动物的存活率。
但是,贯穿整个WO 2010/099556 A1,没有关于流感病毒对试验动物的感染会导致相对肺重量的改变以及关于通过施用所述肽来阻止和治疗这样的过程的实验暗示。尤其仅本发明证实,流感病毒对试验动物肺的感染会导致相对肺重量的大幅增加。
肺是最重要的器官之一。如果出现相对肺重量增加,则其与肺功能的损伤有关,且所述损伤不能由任何其它器官来补偿。健康肺的一种特性是,含有尽可能多的空气填充的空间(肺泡)。在相对肺重量增加时,可认为,空气填充的肺泡的比例将严重地下降,并因此限制了肺的功能。因此,相对肺重量是流感治疗的一个重要因素。因此,借助于非常关键的且有关的参数,以包含于本申请中的实验显示的结果令人影响深刻地证实了根据本发明的组合制品的协同效应。
迄今为止从神经氨酸酶抑制剂已知,这些抑制剂可抑制流感病毒的增殖。神经氨酸酶抑制剂未导致活流感病毒的减少。在现有技术中迄今为止不能证实,流感病毒导致相对肺重量的增加。本发明才令人惊讶地证实,在感染流感以后施用神经氨酸酶抑制剂会减轻肺重量的相对重量增加。另外,本发明首次证实,用神经氨酸酶抑制剂和根据WO
2010/099556 A1的肽的组合同时治疗被流感病毒感染的试验动物导致对相对肺重量的明显且不可预见的协同效应。尽管神经氨酸酶抑制剂将抑制流感病毒增殖,但不会减少既有的活病毒,但是神经氨酸酶抑制剂和根据本发明的肽的协同组合显而易见地导致流感治疗的显著改善。每种单独施用的药物(神经氨酸酶抑制剂和根据本发明的肽)自己独自均没有产生本发明证实的效果。
因此,从在WO 2010/099556 A1中公开的结果不能以任何方式导致本发明。
序列总结:
SEQ ID Nr. 1 CGQRETPEGAEAKPWYC
SEQ ID Nr. 2 KSPGGQRETPEGAEAKPWYE
SEQ ID Nr. 3 CGQREAPAGAAAKPWYC
SEQ ID Nr. 4 TPEGAE
SEQ ID Nr. 5 QRETPEGAEAKPWY
SEQ ID Nr. 6 PKDTPEGAELKPWY
SEQ ID Nr. 7 CGPKDTPEGAELKPWYC
SEQ ID Nr. 8 CGQKETPEGAEAKPWYC
SEQ ID Nr. 9 CGQRETPEGAEARPWYC
SEQ ID Nr. 10 CGQRETPEGAEAKPC
SEQ ID Nr. 11 CQRETPEGAEAKPWYC
SEQ ID Nr. 12 CGQRETPEGAEAKFWYC
序列表
<110> Apeptico Forschung und Entwicklung GmbH
<120> 包含肽和病毒神经氨酸酶抑制剂的组合物
<130> R 57719
<140> R 60211
<141> 15.11.2011
<150> A 1908/2010
<151> 18.11.2010
<160> 12
<170> PatentIn 3.5版
<210> 1
<211> 17
<212> PRT
<213> 人工序列
<220>
<223> 合成肽
<400> 1
Cys Gly Gln Arg Glu Thr Pro Glu
Gly Ala Glu Ala Lys Pro Trp Tyr
1 5 10 15
Cys
<210> 2
<211> 20
<212> PRT
<213> 人工序列
<220>
<223> 合成肽
<400> 2
Lys Ser Pro Gly Gly Gln Arg Glu
Thr Pro Glu Gly Ala Glu Ala Lys
1 5 10 15
Pro Trp Tyr Glu
20
<210> 3
<211> 17
<212> PRT
<213> 人工序列
<220>
<223> 合成肽
<400> 3
Cys Gly Gln Arg Glu Ala Pro Ala
Gly Ala Ala Ala Lys Pro Trp Tyr
1 5 10 15
Cys
<210> 4
<211> 6
<212> PRT
<213> 人工序列
<220>
<223> 合成肽
<400> 4
Thr Pro Glu Gly Ala Glu
1 5
<210> 5
<211> 14
<212> PRT
<213> 人工序列
<220>
<223> 合成肽
<400> 5
Gln Arg Glu Thr Pro Glu Gly Ala
Glu Ala Lys Pro Trp Tyr
1 5 10
<210> 6
<211> 14
<212> PRT
<213> 人工序列
<220>
<223> 合成肽
<400> 6
Pro Lys Asp Thr Pro Glu Gly Ala
Glu Leu Lys Pro Trp Tyr
1 5 10
<210> 7
<211> 17
<212> PRT
<213> 人工序列
<220>
<223> 合成肽
<400> 7
Cys Gly Pro Lys Asp Thr Pro Glu
Gly Ala Glu Leu Lys Pro Trp Tyr
1 5 10 15
Cys
<210> 8
<211> 17
<212> PRT
<213> 人工序列
<220>
<223> 合成肽
<400> 8
Cys Gly Gln Lys Glu Thr Pro Glu
Gly Ala Glu Ala Lys Pro Trp Tyr
1 5 10 15
Cys
<210> 9
<211> 17
<212> PRT
<213> 人工序列
<220>
<223> 合成肽
<400> 9
Cys Gly Gln Arg Glu Thr Pro Glu
Gly Ala Glu Ala Arg Pro Trp Tyr
1 5 10 15
Cys
<210> 10
<211> 15
<212> PRT
<213> 人工序列
<220>
<223> 合成肽
<400> 10
Cys Gly Gln Arg Glu Thr Pro Glu
Gly Ala Glu Ala Lys Pro Cys
1 5 10 15
<210> 11
<211> 16
<212> PRT
<213> 人工序列
<220>
<223> 合成肽
<400> 11
Cys Gln Arg Glu Thr Pro Glu Gly
Ala Glu Ala Lys Pro Trp Tyr Cys
1 5 10 15
<210> 12
<211> 17
<212> PRT
<213> 人工序列
<220>
<223> 合成肽
<400> 12
Cys Gly Gln Arg Glu Thr Pro Glu
Gly Ala Glu Ala Lys Phe Trp Tyr
1
5 10 15
Cys
Claims (16)
1.组合物,其包含
- 肽,其由7-17个相邻的氨基酸组成,且包含六聚体TX1EX2X3E,其中X1、X2和X3每个均可以是天然的或非天然的氨基酸,其中所述肽不具有TNF-受体-结合活性并且是环化的,和
- 病毒神经氨酸酶的抑制剂。
2.根据权利要求1所述的组合物,其中所述肽由7-17个相邻的氨基酸组成,且包含六聚体TPEGAE。
3.根据权利要求1或2所述的组合物,其中所述环化肽由选自下述的彼此相继的氨基酸序列组成:QRETPEGAEAKPWY、PKDTPEGAELKPWY、CGQRETPEGAEAKPWYC、CGPKDTPEGAELKPWYC及其至少7个氨基酸的片段,所述片段具有六聚体TPEGAE。
4.根据权利要求1-3中的任一项所述的组合物,其特征在于,所述肽包含氨基酸序列CGQRETPEGAEAKPWYC,且经由C-残基环化。
5.根据权利要求1-4中的任一项所述的组合物,其特征在于,所述肽通过所述C-残基之间的二硫键环化。
6.根据权利要求1-5中的任一项所述的组合物,其特征在于,所述病毒神经氨酸酶的抑制剂是扎那米韦或奥司他韦。
7.根据权利要求1-6中的任一项所述的组合物,其特征在于,所述组合物包含药学上可接受的载体,且被制备为适合于施用给人类的药物组合物。
8.根据权利要求1-7中的任一项所述的组合物,其特征在于,所述组合物包含药学上可接受的载体,所述载体选自:水、尤其是注射用水、食盐、磷酸钠、醋酸钠、碳酸钠、柠檬酸盐、甘氨酸、甘氨酰甘氨酸、组氨酸、赖氨酸、精氨酸、TRIS、柠檬酸钠、林格溶液、葡萄糖、甘露醇、海藻糖、蔗糖、山梨醇、果糖、麦芽糖、乳糖或葡聚糖、Hank溶液、固定油、油酸乙酯、改善等张性和化学稳定性的物质、防腐剂、药学上可接受的蛋白、多糖、聚乳酸、聚乙醇酸、聚合氨基酸和氨基酸共聚物。
9.根据权利要求1-8中的任一项所述的组合物,其特征在于,所述组合物包含-彼此独立地-
- 所述肽,其量为1µg至10 g、优选10µg至1 g、尤其是1 mg至100 mg,和
- 病毒神经氨酸酶的抑制剂,其量为1µg至10 g、优选100µg至1 g、尤其是1 mg至200 mg。
10.根据权利要求1-9中的任一项所述的组合物,其特征在于,所述组合物以液体形式存在,且包含-彼此独立地-
- 所述肽,其量为1µg至10 g、优选10µg至1 g、尤其是1 mg至100 mg,和
- 病毒神经氨酸酶的抑制剂,其量为1µg至10 g、优选100µg至1 g, 尤其是1 mg至200 mg,
并且以0.5-10 ml的体积、尤其是1-5 ml的体积存在。
11.根据权利要求1-10中的任一项所述的组合物,其特征在于,所述肽和/或所述病毒神经氨酸酶抑制剂存在于可雾化的粉末制剂中或存在于可雾化的液体制剂中。
12.套装,其包含下述的,各自提供于彼此分开的容器中的组分:
- 肽,其由7-17个相邻的氨基酸组成,且包含六聚体TX1EX2X3E,其中X1、X2和X3每个均可以是天然的或非天然的氨基酸,其中所述肽不具有TNF-受体-结合活性并且是环化的,和
- 病毒神经氨酸酶的抑制剂。
13.根据权利要求12所述的套装,其特征在于,所述各自提供于彼此分开的容器中的组分如在权利要求1-11中的任一项中所定义。
14.用于预防和治疗流感的组合物,其包含
- 肽,其由7-17个相邻的氨基酸组成,且包含六聚体TX1EX2X3E,其中X1、X2和X3每个均可以是天然的或非天然的氨基酸,其中所述肽不具有TNF-受体-结合活性并且是环化的,和
- 病毒神经氨酸酶的抑制剂。
15.用于由流感造成的肺炎的组合物,其包含
- 肽,其由7-17个相邻的氨基酸组成,且包含六聚体TX1EX2X3E,其中X1、X2和X3每个均可以是天然的或非天然的氨基酸,其中所述肽不具有TNF-受体-结合活性并且是环化的,和
- 病毒神经氨酸酶的抑制剂。
16.用于预防和治疗流感的套装,其包含下述的各自提供于彼此分开的容器中的组分:
- 肽,其由7-17个相邻的氨基酸组成,且包含六聚体TX1EX2X3E,其中X1、X2和X3每个均可以是天然的或非天然的氨基酸,其中所述肽不具有TNF-受体-结合活性并且是环化的,和
- 病毒神经氨酸酶的抑制剂。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN202011515592.2A CN112717122A (zh) | 2010-11-18 | 2011-11-15 | 包含肽和病毒神经氨酸酶抑制剂的组合物 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| ATA1908/2010A AT510585B1 (de) | 2010-11-18 | 2010-11-18 | Zusammensetzung umfassend ein peptid und ein hemmstoff der viralen neuraminidase |
| ATA1908/2010 | 2010-11-18 | ||
| PCT/AT2011/000462 WO2012065201A1 (de) | 2010-11-18 | 2011-11-15 | Zusammensetzung umfassend ein peptid und ein hemmstoff der viralen neuraminidase |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202011515592.2A Division CN112717122A (zh) | 2010-11-18 | 2011-11-15 | 包含肽和病毒神经氨酸酶抑制剂的组合物 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN103200955A true CN103200955A (zh) | 2013-07-10 |
Family
ID=45001564
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202011515592.2A Pending CN112717122A (zh) | 2010-11-18 | 2011-11-15 | 包含肽和病毒神经氨酸酶抑制剂的组合物 |
| CN2011800554632A Pending CN103200955A (zh) | 2010-11-18 | 2011-11-15 | 包含肽和病毒神经氨酸酶抑制剂的组合物 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202011515592.2A Pending CN112717122A (zh) | 2010-11-18 | 2011-11-15 | 包含肽和病毒神经氨酸酶抑制剂的组合物 |
Country Status (14)
| Country | Link |
|---|---|
| US (2) | US10344055B2 (zh) |
| EP (1) | EP2640410B1 (zh) |
| JP (1) | JP5970465B2 (zh) |
| KR (1) | KR101872218B1 (zh) |
| CN (2) | CN112717122A (zh) |
| AT (1) | AT510585B1 (zh) |
| AU (1) | AU2011331891A1 (zh) |
| BR (1) | BR112013011076A2 (zh) |
| CA (1) | CA2817787C (zh) |
| DK (1) | DK2640410T3 (zh) |
| ES (1) | ES2525758T3 (zh) |
| MX (1) | MX2013005391A (zh) |
| RU (1) | RU2596785C2 (zh) |
| WO (1) | WO2012065201A1 (zh) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN106456707A (zh) * | 2014-03-18 | 2017-02-22 | 阿佩普蒂科研究和开发有限责任公司 | 干粉肽药剂 |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9788539B2 (en) | 2011-05-17 | 2017-10-17 | Velico Medical, Inc. | Platelet protection solution having beta-galactosidase and sialidase inhibitors |
| EP2679239A1 (de) | 2012-06-28 | 2014-01-01 | Apeptico Forschung und Entwicklung GmbH | Pharmazeutische Zusammensetzung zur Behandlung der durch Sauerstoffarmut und verringerten Luftdruck vermittelten pulmonalen Form der Höhenkrankheit |
| CA2887083A1 (en) | 2012-10-05 | 2014-04-10 | Velico Medical, Inc. | Platelet additive solution having a beta-galactosidase inhibitor |
| KR102217476B1 (ko) * | 2013-04-23 | 2021-02-19 | 아펩티코 포어슝 운트 엔트빅크룽 게엠베하 | 식 x₁-gqretpegaeakpwy-x₂의 고리 펩티드를 함유하는 동결건조물 |
| JP6335279B2 (ja) * | 2013-04-23 | 2018-05-30 | アペプティコ フオルシユング ウント アントウィクラング ゲーエムベーハー | 式x1−gqretpegaeakpwy−x2の環状ペプチドを含んでなる医薬組成物および体外肺処置のための使用 |
| US20170014472A1 (en) * | 2014-03-04 | 2017-01-19 | Apeptico Forschung Und Entwicklung Gmbh | Attenuation of intrapulmonary inflammation |
| IL294894A (en) | 2020-05-08 | 2022-09-01 | Apeptico Forschung & Entwicklung Gmbh | A peptide for the prevention or treatment of covid-19 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN101487016A (zh) * | 2007-09-30 | 2009-07-22 | 浙江中奇生物药业股份有限公司 | 禽流感疫苗及其制备方法 |
| WO2010099556A1 (de) * | 2009-03-05 | 2010-09-10 | Apeptico Forschung Und Entwicklung Gmbh | Verfahren zur vermeidung und zur behandlung einer hyperpermeabilität |
Family Cites Families (34)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4069819A (en) | 1973-04-13 | 1978-01-24 | Societa Farmaceutici S.P.A. | Inhalation device |
| JPS60243016A (ja) * | 1984-05-17 | 1985-12-03 | Tsumura Juntendo Inc | 抗インフルエンザウイルス剤 |
| IT1228459B (it) | 1989-02-23 | 1991-06-19 | Phidea S R L | Inalatore con svuotamento regolare e completo della capsula. |
| SK282950B6 (sk) | 1990-04-24 | 2003-01-09 | Biota Scientific Management Pty Ltd | Deriváty alfa-D-neuramínovej kyseliny, spôsob ich prípravy, ich použitie a farmaceutické prípravky na ich báze |
| US5186166A (en) * | 1992-03-04 | 1993-02-16 | Riggs John H | Powder nebulizer apparatus and method of nebulization |
| US5891679A (en) * | 1993-02-03 | 1999-04-06 | N.V. Innogenetics S.A. | TNF-alpha muteins and a process for preparing them |
| US5958973A (en) | 1993-09-03 | 1999-09-28 | Gilead Sciences, Inc. | Polyhydroxy benzoic acid derivatives and their use as neuraminidase inhibitors |
| US5453533A (en) | 1994-04-14 | 1995-09-26 | The University Of Alabama At Birmingham | Inhibitors of influenza virus neuraminidase and methods of making and using the same |
| US5512596A (en) | 1994-09-02 | 1996-04-30 | Gilead Sciences, Inc. | Aromatic compounds |
| US5866601A (en) | 1995-02-27 | 1999-02-02 | Gilead Sciences, Inc. | Carbocyclic compounds |
| BR9607098A (pt) | 1995-02-27 | 1997-11-04 | Gilead Sciences Inc | Novos inibidores seletivos de neuraminidas virais ou bacterianas |
| US5602277A (en) | 1995-03-30 | 1997-02-11 | Biocryst Pharmaceuticals, Inc. | Substituted benzene derivatives useful as neuraminidase inhibitors |
| US5763483A (en) | 1995-12-29 | 1998-06-09 | Gilead Sciences, Inc. | Carbocyclic compounds |
| ES2263179T3 (es) | 1996-06-14 | 2006-12-01 | Biocryst Pharmaceuticals Inc. | Compuestos de clopentano sustituido como inhibidores de la neuraminidasa. |
| US6451766B1 (en) | 1996-07-22 | 2002-09-17 | Sankyo Company, Limited | Neuraminic acid derivatives, their preparation and their medical use |
| US6340702B1 (en) | 1996-07-22 | 2002-01-22 | Sankyo Company, Limited | Neuraminic acid derivatives, their preparation and their medical use |
| US5886213A (en) | 1997-08-22 | 1999-03-23 | Gilead Sciences, Inc. | Preparation of carbocyclic compounds |
| ZA988469B (en) | 1997-09-17 | 1999-03-17 | Biocryst Pharm Inc | Pyrrolidin-2-one compounds and their use as neuraminidase inhibitors |
| US6518305B1 (en) | 1998-04-23 | 2003-02-11 | Abbott Laboratories | Five-membered carbocyclic and heterocyclic inhibitors of neuraminidases |
| US6455571B1 (en) | 1998-04-23 | 2002-09-24 | Abbott Laboratories | Inhibitors of neuraminidases |
| DE69937206T2 (de) | 1998-08-14 | 2008-06-19 | Rudolf Lucas | TNF-Peptide und deren Verwendung zur Behandlung von Ödemen |
| US6419934B1 (en) * | 1999-02-24 | 2002-07-16 | Edward L. Tobinick | TNF modulators for treating neurological disorders associated with viral infection |
| US6593314B1 (en) | 1999-10-19 | 2003-07-15 | Abbott Laboratories | Neuraminidase inhibitors |
| PL203216B1 (pl) | 2000-07-28 | 2009-09-30 | Immupharm Aps | Zastosowanie lecznicze hydroksyetylorutozydów, kompozycja farmaceutyczna zawierająca hydroksyetylorutozydy oraz sól Zn²⁺ i/lub kompleks Zn²⁺, zestaw zawierający hydroksyetylorutozydy oraz sól Zn²⁺ i/lub kompleks Zn²⁺, oraz zastosowanie lecznicze kompozycji farmaceutycznej lub zestawu zawierającego hydroksyetylorutozydy oraz sól Zn²⁺ i/lub kompleks Zn²⁺ |
| WO2003026567A2 (en) * | 2001-09-27 | 2003-04-03 | St. Jude Children's Research Hospital, Inc. | Use of neuraminidase inhibitors to prevent flu associated bacterial infections |
| US20060035859A1 (en) * | 2003-05-16 | 2006-02-16 | Hemispherx Biopharma | Treating severe and acute viral infections |
| ES2339954T3 (es) * | 2004-08-06 | 2010-05-27 | Nycomed Gmbh | Composicion que comprende un agente tensioactivo pulmonar y un peptido derivado de tnf. |
| US20080063722A1 (en) | 2006-09-08 | 2008-03-13 | Advanced Inhalation Research, Inc. | Composition of a Spray-Dried Powder for Pulmonary Delivery of a Long Acting Neuraminidase Inhibitor (LANI) |
| SI2123276T1 (sl) * | 2007-02-16 | 2013-03-29 | Toyama Chemical Co., Ltd. | Farmacevtska sestava, vsebujoča derivat pirazina,in postopek z uporabo derivata pirazina v kombinaciji |
| US7981930B2 (en) * | 2007-03-13 | 2011-07-19 | Adamas Pharmaceuticals, Inc. | Compositions and kits for treating influenza |
| EP2009023A1 (en) * | 2007-06-04 | 2008-12-31 | Rentschler Beteiligungs GmbH | Novel peptides and their use for the treatment of edema |
| AT506150B1 (de) | 2007-12-12 | 2010-01-15 | Apeptico Forschung Und Entwick | Zyklisches und cystein-freies peptid |
| JP2010138081A (ja) * | 2008-12-09 | 2010-06-24 | Kansai Univ | インフルエンザウイルス免疫賦活剤、および抗インフルエンザウイルス剤 |
| WO2010099566A1 (en) | 2009-03-02 | 2010-09-10 | Manfred Imand Kurmis | A sealing member for a closure |
-
2010
- 2010-11-18 AT ATA1908/2010A patent/AT510585B1/de not_active IP Right Cessation
-
2011
- 2011-11-15 AU AU2011331891A patent/AU2011331891A1/en not_active Abandoned
- 2011-11-15 BR BR112013011076A patent/BR112013011076A2/pt not_active IP Right Cessation
- 2011-11-15 DK DK11785277.2T patent/DK2640410T3/da active
- 2011-11-15 WO PCT/AT2011/000462 patent/WO2012065201A1/de active Application Filing
- 2011-11-15 CN CN202011515592.2A patent/CN112717122A/zh active Pending
- 2011-11-15 CN CN2011800554632A patent/CN103200955A/zh active Pending
- 2011-11-15 CA CA2817787A patent/CA2817787C/en active Active
- 2011-11-15 US US13/885,705 patent/US10344055B2/en active Active
- 2011-11-15 KR KR1020137011221A patent/KR101872218B1/ko active IP Right Grant
- 2011-11-15 ES ES11785277.2T patent/ES2525758T3/es active Active
- 2011-11-15 RU RU2013127402/15A patent/RU2596785C2/ru active
- 2011-11-15 MX MX2013005391A patent/MX2013005391A/es active IP Right Grant
- 2011-11-15 JP JP2013539088A patent/JP5970465B2/ja active Active
- 2011-11-15 EP EP11785277.2A patent/EP2640410B1/de active Active
-
2019
- 2019-05-21 US US16/418,265 patent/US20190309021A1/en not_active Abandoned
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN101487016A (zh) * | 2007-09-30 | 2009-07-22 | 浙江中奇生物药业股份有限公司 | 禽流感疫苗及其制备方法 |
| WO2010099556A1 (de) * | 2009-03-05 | 2010-09-10 | Apeptico Forschung Und Entwicklung Gmbh | Verfahren zur vermeidung und zur behandlung einer hyperpermeabilität |
Non-Patent Citations (1)
| Title |
|---|
| 杨令芝等: "流感病毒神经氨酸酶的表达及其在药物筛选中的应用", 《中国生物工程杂志》, vol. 29, no. 5, 31 December 2009 (2009-12-31), pages 6 - 10 * |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN106456707A (zh) * | 2014-03-18 | 2017-02-22 | 阿佩普蒂科研究和开发有限责任公司 | 干粉肽药剂 |
| CN106456707B (zh) * | 2014-03-18 | 2020-08-11 | 阿佩普蒂科研究和开发有限责任公司 | 干粉肽药剂 |
| US10925924B2 (en) | 2014-03-18 | 2021-02-23 | Apeptico Forschung Und Entwicklung Gmbh | Dry-powder peptide medicament |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2014501718A (ja) | 2014-01-23 |
| US20130261048A1 (en) | 2013-10-03 |
| US20190309021A1 (en) | 2019-10-10 |
| WO2012065201A1 (de) | 2012-05-24 |
| KR101872218B1 (ko) | 2018-06-28 |
| AT510585A4 (de) | 2012-05-15 |
| KR20130139966A (ko) | 2013-12-23 |
| RU2013127402A (ru) | 2014-12-27 |
| EP2640410B1 (de) | 2014-10-29 |
| CA2817787C (en) | 2019-03-05 |
| BR112013011076A2 (pt) | 2017-06-20 |
| EP2640410A1 (de) | 2013-09-25 |
| ES2525758T3 (es) | 2014-12-30 |
| DK2640410T3 (da) | 2014-11-10 |
| MX2013005391A (es) | 2013-07-29 |
| AU2011331891A1 (en) | 2013-04-11 |
| RU2596785C2 (ru) | 2016-09-10 |
| US10344055B2 (en) | 2019-07-09 |
| JP5970465B2 (ja) | 2016-08-17 |
| CA2817787A1 (en) | 2012-05-24 |
| AT510585B1 (de) | 2012-05-15 |
| CN112717122A (zh) | 2021-04-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN103200955A (zh) | 包含肽和病毒神经氨酸酶抑制剂的组合物 | |
| US20070116785A1 (en) | Nitric oxide as an anti-viral agent, vaccine and vaccine adjuvant | |
| JP2009523722A (ja) | ポリイノシン酸−ポリシチジル酸を基礎としたアジュバントを含む粘膜免疫原性物質 | |
| RU2554745C2 (ru) | Рекомбинантный человеческий белок сс10 для лечения гриппа | |
| US20230079150A1 (en) | Methods for prevention or treatment of virus-induced organ injury or failure with il-22 dimer | |
| US9884032B2 (en) | Esters of short chains fatty acids for use in the treatment of immunogenic disorders | |
| CN103429610A (zh) | 用于抑制炎症的肽 | |
| CN104151403B (zh) | 一类多肽或其衍生物、及其在流感病毒感染中的应用 | |
| CN107708718A (zh) | 用于治疗2型糖尿病的肠内递送的苦味寡肽 | |
| CN1267091C (zh) | 抗流感药物 | |
| CN109996554A (zh) | 新型抗微生物和抗癌疗法 | |
| US20140287997A1 (en) | Use of growth hormone or growth hormone receptor agonists to prevent or treat stress-sensitive psychiatric illness | |
| US11161881B2 (en) | Composition comprising a peptide and an inhibitor of viral neuraminidase | |
| CA3190278A1 (en) | Antiviral use of liraglutide and gefitinib | |
| US20230181694A1 (en) | Treatment of respiratory viral infections | |
| CN116406273A (zh) | 氮卓斯汀用作抗病毒治疗 | |
| WO2023125432A1 (en) | Antiviral peptides and methods of use thereof | |
| US20230226136A1 (en) | A synergistic formulation for management of respiratory pathogens including coronaviruses | |
| CN113521117A (zh) | 雪松针叶提取物在抑制禽类动物h9n2 aiv增殖中的应用 | |
| WO2022139764A2 (en) | Development of an innovative inhalation formulation of nafamostat mesylate for the management of covid-19 | |
| US20090297559A1 (en) | Use of tight junction agonists to facilitate pulmonary delivery of therapeutic agents | |
| WO2024096742A1 (en) | SARS-CoV-2 BINDING POLYPEPTIDE | |
| Vivo | Functional Antagonism of Chemokine | |
| Oxford et al. | Common Cold–SARS–Pandemic Influenza Novel strategies to fight respiratory viral diseases | |
| Tyrrell | General Virology and Targets for Therapy: of the role played |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination |