CN102137675A - 通过阳离子脂质的对映体刺激免疫应答 - Google Patents
通过阳离子脂质的对映体刺激免疫应答 Download PDFInfo
- Publication number
- CN102137675A CN102137675A CN200980121761XA CN200980121761A CN102137675A CN 102137675 A CN102137675 A CN 102137675A CN 200980121761X A CN200980121761X A CN 200980121761XA CN 200980121761 A CN200980121761 A CN 200980121761A CN 102137675 A CN102137675 A CN 102137675A
- Authority
- CN
- China
- Prior art keywords
- antigen
- lipid
- cation lipid
- dotap
- cell
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/66—Phosphorus compounds
- A61K31/683—Diesters of a phosphorus acid with two hydroxy compounds, e.g. phosphatidylinositols
- A61K31/685—Diesters of a phosphorus acid with two hydroxy compounds, e.g. phosphatidylinositols one of the hydroxy compounds having nitrogen atoms, e.g. phosphatidylserine, lecithin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/04—Immunostimulants
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Chemical & Material Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Immunology (AREA)
- Epidemiology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Communicable Diseases (AREA)
- Oncology (AREA)
- Virology (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Medicinal Preparation (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Peptides Or Proteins (AREA)
Abstract
在体外激活免疫细胞或者在受试者中诱发免疫应答的组合物和方法,包括包含至少一种手性阳离子脂质的组合物。在一个实施方案中所述手性阳离子脂质包括具有式(I)表示感谢的结构的非甾体阳离子脂质;其中R1是季铵基团,Y1是选自下列的间隔子:烃链、酯、酮和肽,C*是手性碳,R2和R3独立地选自饱和脂肪酸、不饱和脂肪酸、酯连接的烃、磷-二酯及其组合。
Description
交叉引用相关申请
本申请要求于2008年4月17日提交的Elizabeth Vasievich,
Weihsu Chen, Kenya Toney, Gregory Conn, Frank Bedu-Addo和Leaf Huang的并且标题为“通过阳离子脂质的对映体刺激免疫应答”的美国临时申请No. 61/045,837的优先权,其公开内容以其整体通过引用并入本文。
发明领域
本发明一般地涉及刺激免疫应答,更特别地涉及脂质的R和S对映体在刺激免疫应答中的用途。
发明背景
本部分的目的在于给读者介绍本领域的许多方面,这些方面与本发明下面描述和/或权利主张的各个方面相关。相信此讨论能帮助给读者提供背景信息,以有助于更好地理解本发明的各个方面。相应地,应当理解,这些说明是以其观点阅读,而不是作为对在先技术的认可。
安全有效的人用免疫治疗法的开发仍然是全球患者的急迫的医学需求。为了引发适当的免疫应答,增强、引导或促进免疫应答的免疫调节剂("免疫调节剂")可用于疫苗设计或免疫治疗[Gregoriadis, G., Immunological
adjuvants:a role for liposomes.
Immunol Today 11:89 (1990)]。例如,疫苗可以包括刺激免疫应答的抗原。然而,一些包含抗原的有效疫苗是免疫应答的弱刺激物,因为该疫苗不能有效地将该抗原投递给免疫系统的抗原递呈细胞("APC"),和/或该抗原免疫原性弱。因此,给APC有效投递抗原并且刺激该免疫系统对抗原的应答的免疫治疗法是需要的,免疫调节剂有可能发挥作为免疫治疗法的功能。此类免疫治疗法可能具有这些和其它益处。例如,当包括作为治疗性疫苗的一部分时,免疫调节剂应当至少:(1)改善抗原投递和/或在APC中的处理[Wang, R, F., and Wang, H.
Y. Enhancement of antitumor immunity by prolonging antigen presentation on
dendritic cells. Nat Biotechnol 20:149 (2002)],(2)诱发免疫调节细胞因子的产生,该免疫调节细胞因子偏好对疫苗抗原的免疫应答的发展,由此促进细胞介导的免疫,包括细胞毒性T-淋巴细胞("CTL"),(3)减少免疫接种的次数或者有效疫苗所需的抗原量[Vogel, F. R. Improving
vaccine performance with adjuvants. Clin Infect Dis 30 Suppl 3:S266 (2000)],(4)增加疫苗抗原的生物学或免疫学半衰期,和(5)通过抑制抑制因子克服对抗原的免疫耐受性[Baecher-Allan, C, and
Anderson, D. E. Immune regulation in tumor-bearing hosts. Curr Opin Immunol 18:214 (2006)]。
近来,用于增强抗原例如肽或蛋白抗原在引发免疫应答中的有效性的主要类型的药剂是佐剂,例如油包水乳剂、明矾(alum)和增强抗应答的其它化学品;然而,这些佐剂不是上文所述的免疫调节剂,因为它们不具有自身的直接免疫调节作用[Vogel, F. R., and Powell,
M. F. A compendium of vaccine adjuvants and excipients, Pharm Biotechnol 6:141 (1995)]。几种此类佐剂可有效用于动物,并且其中一些已测试用于临床。除了常规佐剂例如铝盐外,已上市的有例如下列的产品:流行性感冒病毒小体[Gtuck, R., and Walti, E.
2000. Biophysical validation of Epaxal Berna, a hepatitis A vaccine adjuvanted
with immunopotentiating reconstituted influenza virosomes (IRIV). Dev Biol
(Basel) 103 :189 (2000)],以及Chiron's MF59 [Kahn, J.
O., et al. Clinical and immunologic responses to human immunodeficiency virus
(HIV) type ISF2 gp120 subunit vaccine combined with MF59 adjuvant with or
without muramyl tripeptide dipalmitoyl phosphatidylethanolamine in non-HIV-infected
human volunteers. J Infect Dis 170:1288 (1994)],它们具有内在的免疫作用。例如,MF59(其是亚微粒乳剂基佐剂)被内陷到树状突细胞[Dupuis, M., et al.,
dendritic cells internalize vaccine adjuvant after intramuscular injection.
Cell Immunol 186:18 (1998)]。然而,根据关于HSV和流行性感冒疫苗的临床试验报道[Jones, C. A., and Cunningham, A. L. Vaccination
strategies to prevent genital herpes and neonatal herpes simplex virus (HSV)
disease. Herpes 11:12 (2004);Minutello, M. et al., Safety and immunogenicity of an inactivated subunit
influenza virus vaccine combined with MF59 adjuvant emulsion in elderly
subjects, immunized for three consecutive influenza seasons. Vaccine 17:99 (1999)],来自动物模型的证据表明,MF59佐剂会增强中和抗体的产生而不会增强T细胞应答。因此需要有刺激细胞介导的免疫应答的新方法。
此外,如上文提到的,有一些抗是免疫应答的弱刺激子。因此,除了与刺激免疫应答的物质共同施用抗原以外,如上文所述的,可以调节弱的免疫原性抗原以增加其免疫原性. 例如,弱免疫原性抗原可以与免疫原性肽、多糖或脂质偶联以增加其免疫原性。然而,使弱免疫原性抗原与这些类型的化合物偶联可能不足以引发免疫应答。例如,所得免疫应答可以指向偶联的化合物上的免疫原性表位而不是该弱抗原,或者该偶联的抗原可能不能有效地传递免疫系统的APC。因此,需要有其它方法来刺激对弱免疫原性的抗原的免疫应答。
发明概述
本发明某些示例性的方面说明于下文。应当理解,提供这些方面仅是给读者提供本发明可采取的某些形式的简单概况,并且这些方面不是要限制本发明的范围。事实上,本发明可包括可能未在下文明确说明的各个方面。
本发明涉及阳离子脂质的手征性以及R和S阳离子脂质的对映体的用途,其在某些剂量和组合物的条件下充当新类型的免疫刺激剂,以使其(1)给该免疫系统有效提供或投递抗原,和(2)刺激免疫系统对抗原的应答。
脂质体已被广泛用于投递小分子量药物、质粒DNA、寡核苷酸、蛋白和肽。与用于减活疫苗或病毒载体例如牛痘苗或流感病毒的传统免疫接种相比,使用脂质体介质作为非病毒抗原载体的疫苗是优选的。本申请受让人的美国专利申请No. 12/049,957公开了简单然而有效的脂质基免疫治疗法,其包括具有两个分子即阳离子脂质和抗原的阳离子脂质/抗原复合物,以及脂质剂量对产生免疫应答的作用。报道的结果证实,与抗原复合的阳离子脂质体用于刺激免疫应答并引起树突状细胞(APC)与T-细胞的相互作用。
在本发明中,用所选阳离子脂质的两个对映体进行的附加研究发现,在不同条件下阳离子脂质的R和S对映体发挥有效免疫活性剂的能力方面存在差异。在与抗原组合时,含有R对映体的阳离子脂质/抗原复合物在各种剂量条件下(包括低剂量条件)会诱发特异性针对配制在该复合物中的抗原的强烈免疫应答,并导致肿瘤退化。然而,包含S-DOTAP和抗原的复合物仅能够诱发有限的肿瘤退化,但在R-DOTAP有效的所有剂量下却不会。然而,DOTAP的两种对映体在诱发树状突细胞的成熟和活化方面是等效的,这是诱发细胞免疫应答的第一步。
因此,本发明的一个方面提供了其量足以在受试者中诱发免疫应答的阳离子脂质的至少一种对映体的组合物。
本发明另一方面提供了在受试者中通过给该受试者施用阳离子脂质的特定对映体或对映体混合物来诱发免疫应答的方法。
本发明另一方面提供了其量足以在受试者中诱发免疫应答的阳离子脂质的R或S对映体的组合物。
本发明其它方面涉及给R或S对映体添加至少一种抗原以形成阳离子脂质/抗原复合物,在此情况下该免疫应答是抗原特异性的。
附图说明
当结合附图阅读以下详述时,本发明的各种特征、方面和益处将变得更好理解,其中:
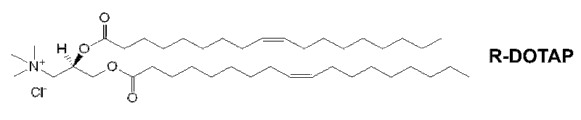
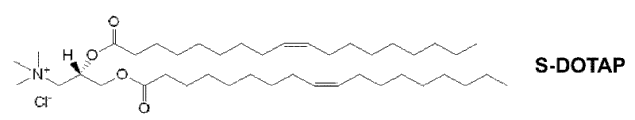
图1A和1B描绘了1,2-二油酰基-3-三甲基铵丙烷("DOTAP")的手征性。
图2是描绘通过R-DOTAP、S-DOTAP和外消旋混合物RS-DOTAP活化人树状突细胞导致辅刺激分子CD 80的表达的图。
图3是描绘通过R-DOTAP、S-DOTAP和外消旋混合物RS-DOTAP活化人树状突细胞导致辅刺激分子CD 83的表达的图。
图4是描绘通过R-DOTAP、S-DOTAP和外消旋混合物RS-DOTAP活化人树状突细胞导致辅刺激分子CD 86的表达的图。
图5是描绘通过R-DOTAP、S-DOTAP和外消旋混合物RS-DOTAP刺激人树状突细胞导致趋化因子CCL-3产生的图。
图6是描绘通过R-DOTAP、S-DOTAP和外消旋混合物RS-DOTAP刺激人树状突细胞导致趋化因子CCL-4产生的图。
图7是描绘通过R-DOTAP、S-DOTAP和外消旋混合物RS-DOTAP刺激人树状突细胞导致趋化因子CCL-5产生的图。
图8是描绘通过R-DOTAP、S-DOTAP和外消旋混合物RS-DOTAP刺激人树状突细胞导致趋化因子CCL-19产生的图。
图9是描绘通过R-DOTAP、S-DOTAP和外消旋混合物RS-DOTAP刺激人树状突细胞导致细胞因子IL-2产生的图。
图10是描绘通过R-DOTAP、S-DOTAP和外消旋混合物RS-DOTAP刺激人树状突细胞导致细胞因子IL-8产生的图。
图11是描绘通过R-DOTAP、S-DOTAP和外消旋混合物RS-DOTAP刺激人树状突细胞导致细胞因子IL-12产生的图。
图12是根据注射后肿瘤大小和时间证实不同剂量阳离子脂质/抗原复合物的体内抗肿瘤作用的图。
图13是证实S-DOTAP剂量对阳离子脂质/抗原复合物的体内抗肿瘤效能的作用的图。
图14是证实R-DOTAP剂量对阳离子脂质/抗原复合物的体内抗肿瘤效能的作用的图。
Fig-15是描绘DOTAP的外消旋混合物、R-DOTAP和S-DOTAP对阳离子脂质/抗原复合物的体内抗肿瘤免疫应答的脂质剂量应答作用物图,抗原剂量为20μg。还证实了DOTAP的外消旋混合物抗原剂量的作用。R-DOTAP相比于S-DOTAP:* p<0.05,** p<0.01,n=5-6。
发明详述
本发明一个或多个特别的实施方案将描述于下文。在提供这些实施方案的简要说明的努力中,所有确切实施方案的特征可能未描述于说明书中,应当理解,在开发任意这种确切实施方案中,许多特定实施方案的论断有必要做出以实现开发者的特定目标,其可以在不同的实施方案之间变化。此外,应当理解,这种开发的努力可能是复杂和耗时的,然而对于具有本发明公开益处的常规技术的那些是常规性的。
当介绍本发明的要素时(例如,其示例性实施方案),冠词“一”、“一个”、“该”和“所述”将表示存在有一个或多个要素。术语“包含”、“包括”和“具有”将是包涵性的并且表示除了所罗列的要素以外还有其它要素。
本发明的一个方面提供了在哺乳动物中刺激免疫应答以预防或治疗疾病的阳离子脂质的对映体。该个别的手性脂质可以通过激活MAP激酶信号途径的各种组分以剂量依赖性的方式独立地发挥免疫调节剂的功能,例如用于产生趋化因子和/或细胞因子。观察到有效诱导免疫应答的剂量范围在R和S对映体之间是不同的,并且在不同哺乳动物物种之间亦是不同的。例如,在啮齿目动物中,DOTAP的R-对映体在约30 nmol至约400 nmol的范围内有效减弱肿瘤生长。相反,DOTAP的S-对映体在相同的啮齿目动物中在同样剂量范围内是有效的,尽管其低于R-对映体。在另一方面,该手性阳离子脂质可能与用于给免疫系统的细胞提供抗原或药物同时刺激强抗原特异性免疫应答有关。在本发明的一些方面,该抗原是脂肽。
通过引用并入本文的美国专利No.7,303,881公开了与疾病相关抗原复合的复合阳离子脂质,其显示刺激防止特定疾病(例如,HPV-阳性癌症)的预防性免疫应答,以及杀灭表达特定抗原的细胞并产生对疾病的有效治疗的治疗性免疫应答。目前,通过使用DOTAP的R和S对映体进行研究,以进一步理解手征性对阳离子脂质的免疫刺激能力的作用。 (DOTAP的R和S对映体显示于图1A和1B)。这些研究发现,有(或无)抗原时,个别阳离子脂质的对映体可独立地发挥免疫调节剂的功能以刺激免疫应答。此外,当阳离子脂质的对映体与抗原复合时,产生抗原特异性免疫应答。在阳离子脂质的R和S对映体之间疾病特异性免疫应答的程度显著不同。
在另一方面,手性阳离子脂质以足以刺激免疫应答的剂量与一种或多种抗原组合施用。在此情况下,该阳离子脂质/抗原组合能够产生免疫应答,该免疫应答对于与阳离子脂质组合投予的一种或多种抗原是特异性的。产生的应答可包括产生特异性细胞毒性T细胞、记忆T细胞或B细胞,造成对与一种或多种抗原相关的特定疾病的预防或治疗性应答。
本发明的手性阳离子脂质可以呈阳离子脂质复合物的形式。该阳离子脂质复合物可以呈各种小囊泡的形式,例如脂质体、胶束或乳液。该阳离子脂质复合物可以是单层的或者多层的。当包含有抗原时,该抗原可以包囊在该阳离子脂质复合物中,或者可以是未包囊的。包囊的理解为表示该抗原可被包含在该复合物的内部空间和/或掺入到该复合物的脂质壁中。
本发明另一方面涉及生产这些复合物的方法,其中该方法可任选包括从过量单一组分中纯化这些成分的步骤。
在某些实施方案中,该阳离子脂质复合物在pH 6.0-8.0处具有净正电荷和/或荷正电的表面。
可以与本发明阳离子脂质复合物包括的任选“抗原”可以是核酸、肽、脂肽、蛋白、脂蛋白、多糖以及其它可能直接与阳离子脂质直接复合的大分子物质。然而,阳离子药物(例如,大阳离子蛋白)可以直接与阴离子脂质复合,或者接着首先与阴离子脂质或聚合物通过手性阳离子脂质复合。应用此方法可以通过本发明复合物将荷阳性或中性电荷的药物投递到细胞。
本发明一个方面涉及手性阳离子脂质复合物的应用,以活化树状突细胞,以及刺激趋化因子和细胞因子的产生。趋化因子和细胞因子是免疫应答的重要调节剂。趋化因子最初鉴定为有效的化学引诱剂以用于炎症细胞,包括中性粒细胞、嗜酸性细胞和单核细胞/巨噬细胞。后来的研究揭示,趋化因子对通过调节树状突细胞和其它淋巴细胞运输进入淋巴样器官的免疫反应具有极深的影响。树状突细胞是移动细胞, 其使组织中的样品抗移动到引流淋巴节并发育成熟以刺激T细胞应答。CC趋化因子的膜CCL2最初鉴定为一种单核细胞/巨噬细胞的趋化因子和活化因子。后来的研究表明,其还可以影响T细胞、自然杀伤细胞和中性粒细胞的功能。进一步探索发现,当存在Th1细胞因子、白介素-12 ("IL- 12")和干扰素-γ (“IFN- γ”)时,CCL2是CD8+细胞毒性T淋巴细胞(“CTL”)活性的最有效的活性剂。这可以通过CCL2与IFN-γ系统之间的正性相互作用来解释。细胞因子或趋化因子任一种的缺乏可以干扰Th1极化以及后续的特异性肿瘤免疫性生成。另一种CC趋化因子CCL-4亦显示在体内补充和扩张树状突细胞并赋予质粒DNA疫苗的免疫原性。最近,已经表明,趋化因子通过引导naϊve
CD8+ T细胞到CD4+ T细胞-树状突细胞相互作用的位点而增强免疫性,并促进记忆CD8+ T细胞增殖。可通过本发明阳离子脂质复合物刺激的少数趋化因子的实例是CCL-2、CCL-3和CCL-4。可通过本发明阳离子脂质复合物刺激的细胞因子的实例是IL-2、IL-8、IL- 12和IFN-γ。本发明人注意到,本发明阳离子脂质复合物除了本说明书公开的那些以外还可以刺激趋化因子和细胞因子。
脂质
本发明手性阳离子脂质复合物可以形成任选与抗原混合的脂质体,并且可以单独含有手性阳离子脂质或者与天然脂质组合的手性阳离子脂质。适宜的手性阳离子脂质种类包括但不限于下列的R和S对映体:3-β[4N-(1N,
8-二胍基精脒)-氨基甲酰基]胆固醇(BGSC);3-β[N,N-二胍基乙基-氨基乙烷)-氨基甲酰基]胆固醇(BGTC);N,N1N2N3四-甲基四棕榈基精胺(cellfectin);N-叔丁基-N'-四癸基-3-四癸基-氨基丙-脒(CLONfectin);二甲基二十八烷基铵溴化物(DDAB);1,2-二肉豆蔻基氧基丙基-3-二甲基- 羟基乙基铵溴化物(DMRIE);2,3-二油酰基氧基-N-[2(精胺羧基氨基)乙基]-N,N-二甲基-1-丙铵三氟乙酸盐) (DOSPA);1,3-二油酰基氧基-2-(6-羧基精基)-丙基酰胺(DOSPER);4-(2,3-二-棕榈酰基氧基-丙基)-1-甲基-1H-咪唑(DPIM) N,N,N',N'-四甲基-N,N'-二(2-羟基乙基)-2,3-二油酰基氧基-1,4-丁二铵碘化物) (Tfx-50);N-1-(2,3-二油酰基氧基) 丙基-N,N,N-三甲基铵氯化物(DOTMA)或者其它N-(N,N-1-二烷氧基)-烷基-N,N,N-三取代的铵表面活性剂;1,2-二油酰基-3-(4'-三甲基铵)丁醇-sn-甘油(DOBT)或胆固醇基(4'三甲基铵)丁酸盐(ChOTB),其中该三甲基铵基是通过丁醇间隔臂连接到双链(对于DOTB)或者胆固醇基(对于ChOTB);DOR1 (DL-1,2-二油酰基-3-二甲基氨基丙基-β-羟基乙基铵)或者DORIE (DL-1,2-O-二油酰基-3-二甲基氨基丙基-β-羟基乙基铵) (DORIE)或者如WO 93/03709公开的其类似物;1,2-二油酰基-3-琥珀酰基-sn-甘油胆碱酯(DOSC);胆固醇基半琥珀酸酯(ChOSC);脂多胺类(lipopolyamines)例如二十八烷基氨基甘氨酰精胺(DOGS)和二棕榈酰基磷脂酰乙醇戊基精胺(DPPES)或者公开于美国专利No. 5,283,185的阳离子脂质,胆固醇基-3β-羧基-氨基-亚乙基三甲基铵碘化物,1-二甲基氨基-3-三甲基铵基-DL-2-丙基-胆固醇基羧酸碘,胆固醇基-3-O-羧基氨基亚乙基胺,胆固醇基-3-β-氧基琥珀酰氨基-亚乙基三甲基铵碘化物,1-二甲基氨基-3-三甲基铵-DL-2-丙基-胆固醇基-3-β-氧基琥珀酸碘,2-(2-三甲基铵)-乙基甲基氨基乙基-胆固醇基-3-β-氧基琥珀酸碘,3-β-N-(N',N'-二甲基氨基乙烷) 氨基甲酰基胆固醇(DC-chol),和3-β-N-(聚乙烯亚胺)-氨基甲酰基胆固醇;O,O'-二肉豆蔻基-N-赖氨酰基天冬氨酸盐(DMKE);O,O'-二肉豆蔻基-N-赖氨酰基-二肉豆蔻基-N-赖氨酰基(DMKD);1,2-二肉豆蔻基氧基丙基-3-二甲基-羟基乙基铵溴化物(DMRIE);1,2-二月桂酰基-sn-甘油-3-乙基磷酸胆碱(DLEPC);1,2-二肉豆蔻基-sn-甘油-3-乙基磷酸胆碱(DMEPC);1,2-二油酰基-sn-甘油-3-乙基磷酸胆碱(DOEPC);1,2-二棕榈酰基-sn--甘油-3-乙基磷酸胆碱(DPEPC);1,2-二硬脂酰基-sn- 甘油-3-乙基磷酸胆碱(DSEPC);1,2-二油酰基-3-三甲基铵丙烷(DOTAP);二油酰基二甲基氨基丙烷(DODAP);1,2-棕榈酰基-3-三甲基铵丙烷(DPTAP);1,2-二硬脂酰基-3-三甲基铵丙烷(DSTAP),1,2-肉豆蔻基-3-三甲基铵丙烷(DMTAP);和十二烷基硫酸钠(SDS)。本发明考虑本申请公开的阳离子脂质的结构变异和衍生物的应用。
本发明的某些方面包括非甾体手性阳离子脂质,其具有下式表示的结构:
其中R1是季铵基团,Y1选自烃链、酯、酮和肽,C*是手性碳,R2和R3独立地选自饱和脂肪酸、不饱和脂肪酸、酯连接的烃、磷-二酯、及其组合。DOTAP、DMTAP、DSTAP、DPTAP、DPEPC、DSEPC、DMEPC、DLEPC、DOEPC、DMKE、DMKD、DOSPA、DOTMA是具有此通式结构的脂质的实例。
在一个实施方案中,本发明的手性阳离子脂质是这样的脂质,其中亲脂性基团与氨基基团之间的键在水溶液中是稳定的。因此,本发明复合物的特征在于其在贮存期间稳定(即,它们在形成后的时间能够保持小的直径并且保持生物学活性)。用于阳离子脂质的此类键包括酰胺键、酯键、醚键和氨基甲酰基键。本领域技术人员容易理解,含有一种以上种类的阳离子脂质的脂质体可用于制备本发明的复合物。例如,包含两种阳离子脂质(赖氨酰-磷脂酰乙醇胺和β-内氨酰胆固醇酯)的脂质体已被公开用于某些药物投递的应用[Brunette, E. et al.,
Nucl. Acids Res., 20:1151 (1992)]。
还应理解,在考虑适用于本发明并任选与抗原混合的手性阳离子脂质时,本发明方法不仅限于上文所文字阳离子脂质的应用,更确切地,任何脂质组合物均可使用,只要制备阳离子脂质体并且所得阳离子荷电密度足以活化并诱发免疫应答。
因此,除了手性阳离子脂质以外,本发明复合物还可以含有其它脂质。这些脂质包括但不限于,实例有溶血磷脂胆碱 (1-油酰基溶血磷脂胆碱)的溶解性脂质,胆固醇,中性磷脂其包括二油酰基磷脂酰乙醇胺(DOPE)或二油酰基磷脂酰胆碱(DOPC)以及包含聚乙二醇部分的的各种亲脂性表面活性剂,其实例有Tween-80和PEG-PE。
本发明的手性阳离子脂质复合物还可含有负电荷脂质以及阳离子脂质,只有所形成的复合物的净电荷是正的,和/或该复合物的表面是正电荷。本发明的负电荷脂质是这样的,它们包含至少一种脂质,所述脂质在生理pH值处或接近生理pH值处具有净负电荷。适宜种类的负电荷脂质包括但不限于CHEMS(胆甾醇半琥珀酸酯)、NGPE (N-戊二酰磷脂酰乙醇胺)\ 磷脂酰甘油和磷脂酸或相似的磷脂酸类似物。
制备用于制备包含本发明药物投递复合物的脂质的脂质体的方法是本领域技术人员已知的。脂质体制备方法的综述可见于:Liposome Technology (CFC
Press New York 1984);Ostro的Liposome (Marcel Dekker,
1987);Methods Biochem Anal. 33 :337-462 (1988)以及美国专利No. 5,283,185。这些方法包括冷冻-融化挤出和声裂法。单层脂质体(平均直径小于约200 nm)和多层脂质体(平均直径大于约300 nm)可用作起始成分以生产本发明复合物。
在用于制备本发明阳离子脂质复合物的阳离子脂质体中,该手性阳离子脂质是以脂质体为总脂质体脂质的约10mol%至约100mol%的量存在,或者为约20mol%至约80mol%。中性脂质(当包括在该脂质体中时)可以以总脂质体脂质的约0mol%至约90mol%的浓度存在,或者为约20mol%至约80mol%,或者为40mol%至80mol%。负电荷脂质(当包括在该脂质体中时)可以以总脂质体脂质的约0mol%至约49mol%的浓度范围存在,或者约0mol%至约40mol%。在一个实施方案中,该脂质体含有手性阳离子和中性脂质,比率为约2:8至约6:4。
还应理解,本发明的复合物可以含有修饰的脂质、蛋白、多聚阳离子或受体配体,其发挥使该复合物引向特定组强或细胞类型的靶向因子的功能。靶向因子的实例包括但不限于,无唾液酸糖蛋白、胰岛素、低密度脂蛋白(LDL)、叶酸盐/酯和对抗细胞表面分子的单克隆和多克隆抗体。此外,为改变该复合物的循环半衰期,通过掺入含有聚乙二醇部分的亲脂性表面活性剂可在空间上隔离该正表面电荷。
在从蔗糖梯度中收集之后,该阳离子脂质复合物可以贮存在等渗蔗糖或葡萄糖溶液中,或者它们可以冷冻干燥,然后在临用前复溶于等渗溶液中。在一个实施方案中,该阳离子脂质复合物贮存在溶液中。本发明阳离子脂质复合物的稳定性是通过测定该阳离子脂质复合物经时贮存的物理稳定性和生物学活性的特殊测定法来测定的。该阳离子脂质复合物的物理稳定性是通过测定该阳离子脂质复合物的直径和电荷来测定的,测定方法是本领域技术人员已知的那些,包括例如例如,电子显微镜法、凝胶过滤色谱法,或者如实施例所述使用例如Coulter N4SD粒度分析仪的准弹性光散射的方式。当贮存的阳离子脂质复合物的直径未增加到超过该阳离子脂质复合物纯化时测定的该阳离子脂质复合物的直径的100%、或50%、或30%时,该阳离子脂质复合物的物理稳定性是“基本未变化”的。
虽然手性阳离子脂质可能以纯的或基本上纯的形式施用,其优选以药物组合物、配方或制剂存在。使用本发明手性阳离子脂质复合物的药物配方可包括在生理相应性无菌缓冲溶液中的该阳离子脂质复合物,所述缓冲溶液例如磷酸盐缓冲盐水、等渗盐水或低低离子强度缓冲溶液例如乙酸盐或Hepes (示例性的pH的范围为约3.0至约8.0)。该手性阳离子脂质复合物可以以气溶胶或液体溶液施用,以供供瘤内、动脉内、静脉内、气管内、腹膜内、皮下和肌内施用。
本发明的配方可以掺入本领域已知的任何稳定剂。示例性的稳定剂是胆固醇和有助于脂质体双层硬化并防止双层分解或脱稳定化的其它固醇类。其它药剂例如聚乙二醇、多糖或单糖可以掺入到脂质体中,以修饰脂质体表面并防止其因为与血液成分相互作用而脱稳定化。其它示例性的稳定剂是蛋白质、糖类、无机酸或有机酸,其可以其本身使用或以混合物使用。
许多药学方法可用于控制、改变或延长免疫刺激的持续时间。控制释放制剂可以通过使用聚合物复合物例如聚酯类、聚氨基酸、甲基纤维素、聚乙烯、聚(乳酸)和水凝胶来实现,以将该阳离子脂质包裹或包埋并使其缓慢释放。类似的聚合物亦可用于吸附脂质体。该脂质体可以包含在乳液配方中,以便改变该刺激剂的释放模式。或者,刺激剂存在于血液循环中的持续时间可以通过用化合物包裹该脂质体的表面来增加,所述化合物例如聚乙二醇或其它聚合物,以及其它物质例如糖类,其能够增加脂质体和乳液的循环时间或半衰期。
当需要口服制剂时,手性阳离子脂质可以与本领域已知的典型药物载体例如蔗糖、乳糖、甲基纤维素、羧甲基纤维素或阿拉伯胶等组合。阳离子脂质还可以被包衰在胶囊或片剂中以供全身投药。
本发明的手性阳离子脂质的施用可以是预防目的或治疗目的。当要提供预防时,在任何情况或疾病症状下预先提供阳离子脂质。当要提供治疗时,在疾病发生时或发生后提供阳离子脂质。免疫刺激剂的治疗性施用可用于减弱或者治愈疾病。为了两种目的时,阳离子脂质可以与其它治疗剂或抗原施用,可以产生抑制特定疾病的预防或治疗作用。
本发明的配方(不论是兽用还是人用)包括上文所述单独的手性阳离子脂质,R和S对映体的混合物,或者还任选包括一种或多种其它治疗成分例如抗原或药物分子。所述配方可以方便地以单位剂型提供,并且可通过制药领域已知的任何方法来制备。
抗原
在一个实施方案中,手性阳离子脂质不与任何其它药剂施用,以便提高或降低各种免疫应答,包括产生其它免疫调节剂,以及提供对所要战胜的疾病的免疫应答。在其它实施方案中,该手性阳离子脂质与一种或多种抗原组合施用。在此情况下,目的是产生免疫应答,该免疫应答对于与阳离子脂质组合投递的所述抗原是特异性的。产生的应答可包括产生导致对与这些抗原有关的特定疾病的预防或治疗应答的特定的细胞毒性T-细胞、记忆T-细胞或B-细胞。该抗原可以是任何肿瘤相关抗原或者微生物抗原或者本领域技术人员已知的任何其它抗原。
本文所用的"肿瘤相关抗原"是一种分子或化合物(例如,蛋白质、肽、多肽、脂蛋白、脂肽、糖蛋白、糖肽、脂质、糖脂、碳水化合物、RNA和/或DNA),其与肿瘤或癌细胞有关,并且当在主要组织相容性复合物("MHC")分子的背景下在抗原递呈细胞表面表达时其能够激起免疫应答(体液的和/或细胞的)。肿瘤相关抗原包括自身抗原,以及与癌症无特定关系的其它抗原,但是在施用于动物时会增强对肿瘤细胞或癌细胞的免疫应答和/或减低肿瘤细胞或癌细胞的生长。本文提供了更具体的实施方案。
本文所用的"微生物抗原"是一种微生物的抗原,其包括但不限于传染性病毒、传染性细菌、传染性寄生虫和传染性真菌。微生物抗原可以是完整的微生物,以及天然的分离物、片段或共衍生物,与天然的微生物抗原相同或相似的合成化合物,并且优选地,会引起对相应微生物(由其产生天然微生物抗原)的特异性免疫应答。在优选的实施方案中,如果化合物诱发类似于天然微生物抗原相似的免疫应答(体液的和/或细胞的),则该化合物类似于天然微生物抗原。类似于天然微生物抗原的化合物或抗原是本领域技术人员已知的,例如蛋白、肽、多肽、脂蛋白、脂肽、糖蛋白、糖肽、脂质、糖脂、碳水化合物、RNA和/或DNA。类似于天然微生物抗原的化合物的另一非限制性实例是多糖抗原的肽拟似物。本文提供了更具体的实施方案。
术语"抗原"将进一步包括已知或野生型抗原的肽或蛋白类似物,例如本说明书中描述的那些。所述类似物比之于野生型抗原可以是更易溶解或更稳定的,并且亦可含有使该抗原更具免疫活性的突变或修饰。抗原可以以任何方式被修饰,例如加入脂质或糖部分、突变肽或蛋白氨基酸序列、突变DNA或RNA序列,或者本领域技术人员已知的任何其它修饰。可以使用本领域技术人员已知的标准方法修饰抗原。
本发明组合物和方法中还有用的是具有与期望抗原的氨基酸序列同源的氨基酸序列的肽或蛋白,其中该同源抗原诱导对各个肿瘤、微生物或受感染细胞的免疫应答。
在一个实施方案中,在该阳离子脂质复合物中的抗原包括与肿瘤或癌症相关的抗原(即肿瘤相关抗原)以制备疫苗来预防或治疗肿瘤。这样,在一个实施方案中,本发明的肿瘤或癌症疫苗进一步包括至少一种肿瘤相关抗原的至少一种抗原决定簇。在另一优选的实施方案中,本发明的肿瘤或癌症疫苗进一步包括来自一种或多种肿瘤相关抗原的多种抗原决定簇。发现用于本发明阳离子脂质复合物和方法的肿瘤相关抗原可以是内在免疫原性的,或者无免疫原性,或者是轻微免疫原性。如本文所证实的,甚至肿瘤相关自身抗原亦可以有利地用于治疗作用的本发明疫苗,因为该本发明组成能够破坏抑制例如抗原的免疫耐受性。示例性的抗原包括但不限于合成抗原、重组抗原、外来抗原或同源抗原,并且抗原性物质可包括但不限于蛋白、肽、多肽、脂蛋白、脂肽、脂质、糖脂、碳水化合物、RNA和DNA。此类疫苗的实例包括但不限于用于治疗或预防下列的那些:乳癌、头颈癌、黑素瘤、子宫颈癌、肺癌,前列腺癌、消化道癌,或者使用与肿瘤相关抗原复合的阳离子脂质的本领域已知的任何其它癌症。还可能使抗原与阳离子脂质配制而不将其包裹在脂质体中。因此,本发明的阳离子脂质复合物可用于治疗或预防癌的方法。在此情况下,可以给被免疫的哺乳动物注射含有包裹抗原的脂质体的药物配方。
适用于本发明的肿瘤相关抗原包括天然存在的以及修饰的分子,其可以是单一肿瘤类型的表型,若干肿瘤类型中共有的表型,和/或与正常细胞相比唯一表达或过表达于肿瘤细胞中的表型。除了蛋白、糖蛋白、脂蛋白、肽和脂肽以外,碳水化合物、神经节苷酯、糖脂和粘蛋白的表达的肿瘤特异性模式 亦已被证明。用于癌症疫苗的示例性肿瘤相关抗原包括致癌基因、肿瘤抑制基因和具有对肿瘤细胞独特地突变或重排的蛋白产物,再活化胚胎基因产物,癌胚抗原,组织特异性(但不是肿瘤特异性)分化抗原,生长因子受体,细胞表面碳水化合物残基,外来病毒蛋白和一些其它自身蛋白。
肿瘤相关抗原的具体实施方案包括,例如,突变或修饰抗原例如Ras p21原癌基因、肿瘤抑制基因p53和HER-2/neu和BCR-abl致癌基因的蛋白产物,以及CDK4、MUM1、半胱天冬酶8和β连环蛋白;过表达的抗原例如半乳凝素4、半乳凝素9、碳酸酐酶、醛缩酶A、PRAME、Her2/neu、ErbB-2和KSA,癌胚抗原例如α胎儿蛋白(AFP)、人体绒毛膜促性腺激素(hCG);自身抗原例如癌胚抗原(CEA)和黑素细胞分化抗原例如Mart 1/Melan A、gp100、gp75、酪氨酸酶、TRP1和TRP2;前列腺相关抗原例如PSA、PAP、PSMA、PSM-P1和PSM- P2;再活化胚胎基因产物例如MAGE 1、MAGE 3、MAGE 4、GAGE 1、GAGE 2、BAGE、RAGE和其它癌症睾丸抗原例如NY-ESO1、SSX2和SCP1;粘蛋白例如Muc-1和Muc-2;神经节苷酯例如GM2、GD2和GD3,中性糖脂质和糖蛋白例如Lewis (y)和globo-H;以及糖蛋白例如Tn、Thompson-Freidenreich 抗原(TF)和sTn。还包括在本文中肿瘤相关抗原是全细胞和肿瘤细胞溶胞产物和其免疫原性蛋白,以及表达于B淋巴细胞的单克隆增殖物上用于抑制B细胞淋巴瘤的免疫球蛋白特异型。
肿瘤相关抗原和它们各自的肿瘤细胞靶包括例如细胞角蛋白,特别是细胞角蛋白8、18和19,作为癌症的抗原。上皮膜抗原(EMA)、人胚胎抗原(HEA-125)、人牛奶脂肪球、MBr1、MBr8、Ber-EP4、17-1 A、C26和T16亦是已知的癌抗原。结合蛋白和肌肉特异性肌动蛋白是肌原性肉瘤的抗原。胎盘碱性磷酸酶、β-人绒毛膜促性腺激素和α胎儿蛋白是滋养层和生殖细胞肿瘤的抗原。前列腺特异性抗原是前列腺癌的抗原,结肠腺癌的癌胚抗原。HMB-45是黑素瘤的抗原。在子宫颈癌中,有用的抗原可通过人乳头状瘤病毒来编码。嗜铬粒蛋白-A和突触素是神经内分泌和神经外胚层肿瘤的抗原。特别感兴趣的是侵袭性肿瘤,其形成具有坏死区域的实质瘤块。这种坏死细胞的溶化是抗原-呈递细胞的抗原的丰富来源,并且此本发明治疗可发现有利地用于与常规化学治疗和/或放射治疗相结合。
在一个实施方案中,使用人乳头瘤病毒属HPV 抗原。用作肿瘤相关抗原的特异性HPV抗原是HPV亚型16 E7。HPV E7抗原-阳离子脂质复合物在预防和治疗子宫颈癌中是有效的。此外,具有抗原活性但不致瘤活性的遗传工程化E7蛋白即E7m蛋白是有效的肿瘤相关抗原。E7m-阳离子脂质复合物诱发细胞免疫以引起已建立肿瘤的完全消退,并因此可用作有效的抗-子宫颈癌疫苗。
肿瘤相关抗原可通过本领域公知的方法来制备。例如,这些抗原可以从癌细胞通过制备癌细胞的粗提物(例如,如描述于Cohen et al, Cancer Res.,
54:1055 (1994)中的),通过使该抗原部分纯化,通过重组技术,或通过已知抗原的从新合成来制备。该抗原亦可以是编码抗原肽的核酸形式,该抗原肽呈适合于在受试者中表达并呈递给被免疫的受试者的免疫系统的形式。此外,该抗原可以是完全抗原,或者其可以是包含至少一种抗原决定簇的完全抗原的片段。
得自已知易感染某些癌症的病原体的抗原亦可以有利地包括在本发明的癌症疫苗中。据估计,全球癌症发生率中接近16%可能归因于感染病原体;并且许多恶性肿瘤的特征在于特异性病毒基因产和的表达。因此,包括来自涉及引发癌症的病原体的一种或多种抗原可以有助于拓宽宿主的免疫应答并增加该癌症疫苗的预防或治疗效果。用于本文提供的癌症疫苗的特别感兴趣的病原体包括乙型肝炎病毒(肝细胞癌),丙型肝炎病毒(heptomas),Epstein Barr-病毒(EBV) (伯基特淋巴瘤、鼻咽癌、免疫抑制个体中的PTLD),HTLVL (成人型T细胞性白血病),16、18、33、45型致瘤性人乳头状瘤病毒(成人子宫颈癌),和细菌幽门螺旋杆菌(B细胞胃淋巴瘤)。可以在哺乳动物特别是人中作为抗原的其它医学上有关的微生物广泛描述于文献中,例如C. G. A Thomas, Medical
Microbiology, Bailliere Tindall, Great Britain 1983,其全部内容通过引用并入本文。
在另一实施方案中,该阳离子脂质复合物的抗原包括得自病原体或与病原体有关的抗原,即微生物抗原。这样,在一个实施方案中,本发明的病原体疫苗进一步包括至少一种微生物抗原的至少一种抗原决定簇。可通过本发明疫苗靶向的病原体包括但不限于,病毒、细菌、寄生虫和真菌。在另一实施方案中,本发明的病原体疫苗进一步包括来自一种或多种微生物抗原的多种抗原决定簇。
发现用于该阳离子脂质复合物和方法的微生物抗原可以是内在免疫原性、非免疫原性、或微免疫原性的。示例性的抗原包括但不限于合成的、重组的、外源的、或同源的抗原,并且抗原性物质可包括但不限于蛋白、肽、多肽、脂蛋白、脂肽、脂质、糖脂、碳水化合物、RNA和DNA。
示例性的病毒性病原体包括但不限于感染哺乳动物特别是人的病毒。病毒的实例包括但不限于:逆转录病毒科(例如,人类免疫缺陷病毒),例如HIV-1 (亦称为HTLV-UI、LAV或HTLV-III/LAV),或者HIV-III;以及其它分离物例如HIV-LP;小核糖核酸病毒科(例如脊髓灰质炎病毒、甲肝病毒;肠道病毒、人类柯萨奇病毒、鼻病毒属、埃可病毒);Calciviridae (例如引起胃肠炎的病毒株);披膜病毒科(例如马脑炎病毒、风疹病毒);Flaviridae (例如登革热病毒、脑炎病毒、黄热病病毒);日冕形病毒科(例如冠形病毒);弹状病毒科(例如疱疹性口炎病毒、狂犬病病毒);日冕形病毒科(例如冠形病毒);弹状病毒科(例如疱疹性口炎病毒、狂犬病病毒);纤丝病毒科(例如依波拉病毒);副粘病毒科(例如副流感病毒、腮腺炎病毒、麻疹病毒、呼吸道合胞病毒);正粘病毒科(例如流感病毒);Bungaviridae (例如汉坦病毒、Bunga病毒、静脉病毒和Nairo病毒);沙粒病毒科(出血热病毒);呼肠孤病毒科(例如呼肠病毒、orbiviurses和轮状病毒);双RNA病毒;肝DNA病毒科(乙型肝炎病毒);细小病毒科(细小病毒组);乳多空病毒科(乳头状瘤病毒、多瘤病毒);腺病毒科(大多数腺病毒);疱疹病毒科单纯疱疹病毒(HSV) 1和2、水痘-带状疱疹病毒、细胞巨化病毒(CMV)、疱疹病毒;Poxyiridae (类天花病毒、痘苗病毒、痘病毒);和虹彩病毒科(例如非洲猪瘟病毒);和未分类的病毒(例如海绵状脑病的病原因子、丁型病毒性肝炎的因子(认为是乙型肝炎病毒的缺陷随体(satellite))、非-A非-B肝炎因子(1类=内部穿透的;2类=胃肠外穿透的(即丙型肝炎);Norwalk和相关病毒,以及星状病毒)。
此外,革兰氏阴性菌和革兰氏阳性菌可通过本发明组合物和方法在脊椎动物靶向。此类革兰氏阳性菌包括但不限于巴斯德菌属,葡萄球菌属和链球菌属。革兰氏阴性菌包括但不限于大肠杆菌、假单胞菌属和沙门氏菌属。传染性细胞的具体实例包括但不限于包括但不限于:幽门螺旋杆菌、博氏疏螺旋体、军团杆菌属嗜肺性军团病菌、分枝杆菌属(例如结核分支杆菌、鸟型分枝杆菌、细胞内分枝杆菌、堪萨斯分枝杆菌、戈登分枝杆菌),金黄色葡萄球菌,淋病奈瑟氏菌,脑膜炎萘瑟氏菌,单核细胞增多性李司忒菌,化脓性链球菌(A组链球菌属),无乳链球菌(B组链球菌属),链球菌属(viridans组),粪链球菌,牛链球菌,链球菌属(厌氧菌属),肺炎链球菌,病原体性弯曲杆菌属,肠球菌属,流感嗜血杆菌,炭疽芽孢杆菌,白喉杆菌,棒状杆菌属,猪丹毒丹毒丝菌,产气荚膜梭状芽胞杆菌,破伤风梭状芽胞杆菌,产气肠杆菌,肺炎克雷伯杆菌,多杀巴斯德菌,拟杆菌属,核粒梭杆菌,念珠状链杆菌、梅毒密螺旋体,细弱密螺旋体,钩端螺旋体属,立克次体和衣氏放线菌。
发现在本发明组合物中用作微生物抗原来源的细菌性病原体的多肽包括但不限于铁调节外膜蛋白("IROMP")、外膜蛋白("OMP")和引起疖病的杀鲑气单胞菌的A-蛋白, 引起细菌性肾脏疾病("BKD")的沙门肾杆菌的p57 蛋白,主要表面相关抗原("msa"),表面表达的细胞毒素("mpr"),表面表达的("ish"),和耶尔森菌病鞭毛抗原;细胞外蛋白("ECP"),铁调节外膜蛋白("IROMP"),和巴斯德氏菌病的结构蛋白;鳗弧菌和病海弧菌的OMP和鞭毛蛋白;鞭毛蛋白,OMP 蛋白,不动性爱德华菌和迟钝爱德华菌的aroA和purA;小瓜虫属的表面抗原;和柱状噬纤维菌(Cytophaga columnari)的结构和调节蛋白;和立克次体的结构和调节蛋白。此类抗原可以分离或者重组法制备或者通过本领域已知的任何其它方法制备。
病原体的实例进一步包括但不限于感染动物特别是人的真菌。真菌的实例包括但不限于:,新型隐球菌,夹膜组织胞浆菌,粗球孢子菌,皮炎芽生菌,沙眼衣原体和白色念珠菌。感染性寄生虫的实例包括疟原虫例如镰状疟原虫,三日疟原虫,卵形疟原虫和间日疟原虫。其它感染性有机体(即原生生物)包括鼠弓形体。寄生性病原体的多肽包括但不限于小瓜虫属的表面抗原。
在哺乳动物特别是人中用作抗原的其它医学相关微生物广泛描述于文献中(例如,参见C. G. A Thomas, Medical
Microbiology, Bailliere Tindall, Great Britain 1983)。除了治疗感染性人类疾病和人类病原体外,本发明的组合物和方法可用于治疗非人类哺乳动物的感染。用于治疗非人类哺乳动物的许多疫苗公开于Bennett, K. Compendium of
Veterinary Products, 3rd ed. North American Compendiums, Inc., 1995;亦见于WO 02/069369,其公开内容以其整体通过引用清楚地并入本文。
示例性的非人类病原体包括但不限于小鼠乳腺瘤病毒 ("MMTV")、劳斯氏肉瘤病毒("RSV")、禽白血病病毒("ALV")、鸟类成髓细胞白血病病毒("AMV")、鼠白血病病毒("MLV")、猫白血病病毒("FeLV")、鼠肉瘤病毒("MSV")、长臂猿白血病病毒("GALV")、脾坏死病毒("SNV")、禽网状内皮组织增生病毒("RV")、猿猴肉瘤病毒("SSV")、梅森-菲舍猴病毒("MPMV")、1型猿猴逆转录病毒("SRV-1"),慢病毒属例如HIV-1、HIV-2、SIV、绵羊髓鞘脱落病毒、猫免疫缺损病毒("FIV")和马感染性贫血病毒("EIAV")、T细胞白血病病毒例如HTLV-1、HTLV-II、猿猴T细胞白血病病毒("STLV")和牛白血病病毒("BLV"),以及泡沫病毒例如人泡沫病毒("HFV")、猴泡沫病毒("SFV")和牛泡沫病毒("BFV")。
在一些实施方案中,所及感染性病原体的本文所用"治疗"、"治疗"和"治疗"是指预防性治疗,该预防性治疗增加受试者对病原体感染的抵抗性或者减低该受试者被该病原体感染的可能性;和/或受试者被感染之后的治疗以便战胜该感染,例如减少或消除感染或者预防其变恶化。
微生物抗原可通过本领域公知的方法制备。例如,这些抗原直接从病毒和细菌制备,其方式是通过制备粗提物、通过部分纯化该抗原,或者另选地通过重组技术或者通过已知抗原的重新合成。该抗原亦可以适合于在受试者中表达并呈递到被免疫受试者的免疫系统中的形式呈编码抗原肽的核酸形式。此外,该抗原可以是完全抗原,或者其可以是包含至少一种抗原决定簇的完全抗原。
为了提高抗原掺入到手性阳离子脂质囊泡中并提高投递到免疫系统的细胞,该抗原可以与脂质链结合以便提高其在阳离子脂质的疏水性酰基链中的溶解度,同时保持分子的抗原性质。脂质化抗原可以是脂蛋白或脂肽及其组合。脂质化抗原可以具有脂质和抗原之间结合的连接子,例如,N-末端α或ε-棕榈酰赖氨酸可以通过二肽Ser-Ser连接子连接到抗原。美国申请No. 12/049,957公开了,与DOTAP/E7配方相比,DOTAP/E7-脂肽复合物显示增强的功能抗原特异性CD8+ T淋巴细胞应答,并因此提供了优良的抗肿瘤效果。
根据以下实施例将进一步理解本发明。
实施例
通过阳离子脂质的对映体有效刺激免疫系统
1. 细胞系和肽
TC-1细胞是C57BL/6小鼠肺上皮细胞,其已用HPV16 E6和E7致癌基因和活化的H-ras转化。使细胞生长于RPMI培养基(商购自Invitrogen,Carlsbad, CA),该培养基补充了10%胎牛血清和100 U/ml青霉素,以及100 mg/ml链霉素。来自HPV 16 E7 蛋白的I型MHC限制性肽(氨基酸11至20,YMLDLQPETT [SEQ. ID. NO.
1])是通过匹兹堡大学肽合成实验室使用Advanced ChemTech模型200肽合成器并通过HPLC纯化经固相合成法合成的。
2.脂质/抗原复合物的制备和物理性质的测定
DOTAP的对映体由瑞士Merck AG (EPROVA)提供。所有其它的脂质购自Avanti Polar Lipids
(Alabaster, AL)。小单层DOTAP脂质体是通过薄膜水合法接着挤出来制备的。氯仿中的脂质是在玻璃管中在氮气流下以薄层干燥的。使该薄膜真空干燥2-3小时,然后重新水化于含有E7 肽的细胞培养级水中(商业得自Walkersville的Cambrex,MD)或缓冲液(此缓冲液虽本领域技术人员公知的)中,达到每mL含有0.7mg脂质和0.1mg E7的最终浓度 per mL (摩尔比=11:1)。使该脂质分散体依次通过孔径0.4、0.2和0.1 μm的聚碳酸酯膜挤出。没有除去未包埋的肽。使该脂质体保存于4℃直到使用。与脂质体缔合的E7肽是通过测定脂质体-结合肽的百分数来确定的。简而言之,通过Microcon® 离心过滤装置(Millipore, Bedford, MA)分离来自R-DOTAP/E7、S-DOTAP/E7或RS- DOTAP/E7 复合物的未结合的E7 肽,再通过Micro BCA™蛋白分析试剂盒(Pierce, Rockford, IL)测定未结合的肽的浓度。肽缔合的效能是以未结合肽的百分数确定的。还可以使用本领域技术人员公知的用于一般而论脂质体制备的其它方法。
3. 统计分析
数据是以至少3个独立试验的均值± SD提供的。使用双侧Student氏t检验来评价均值差异的统计学显著性。显著设定为p<0.05。
4. 阳离子脂质的单一R和S对映体/E7 复合物活化人树状突细胞与DOATP外消旋混合物相似。
如上文所述制备阳离子脂质体。用于配方的E7抗原是经鉴别的被HLA-A*0201限制的人E7 肽[HPV-16 E7,氨基酸11-20,YMLDLQPETT (SEQ. ID. NO.
1)]。通过匹兹堡PA的匹兹堡大学分子医学研究所合成该肽。人HLA-A2人树状突细胞得自Lonza (Walkersville,MD)。使冷冻的冷冻小瓶融化,再使树状突细胞培养于LGM-3培养基(购自Lonza,Walkersville, MD)中,该培养基补充了50微克/ml IL-4和GM-CSF,37°C和5% CO2,初始辅板密度为125,000细胞/cm2,在12孔组织培养皿的2 ml培养基中。使细胞在培养物中生长3天,通过显微镜检查显示为粘附和圆形细胞的混合物。
用新配的50 微克/ml的IL-4和GM-CSF (全部孔)在第3天处理细胞,测试孔用下列任一混合物处理:10 ng/ml的白细胞介素1-β("IL-β")、白细胞介素6 ("IL-6")和TNF-α,和10 μg/ml的前列腺素E2 ("PGE-2") (用于激活的阳性对照),未处理(阴性激活对照),以及2.5、10和40微摩尔最终浓度的S-DOTAP/E7,以及2.5、10和40微摩尔最终浓度的R-DOTAP/E7。使处理的树状突细胞保持在培养物中达24小时,采集细胞表面标记染色并用流式细胞计量术分析。通过血细胞计数器计数收获的细胞,再将10μl的下列抗体结合物连续加至各样品中以用于标记表面标记:CD80-FITC、CD83-APC和CD86-PE (BD Biosciences)。该表面标记的细胞接着通过流式细胞计量法使用BD FACxcaliber流式细胞测定器分析,监测共刺激树状突细胞标记分子CD80、CD83和CD86,它们是在激活时产生的。如图2、3和4所示,用两种阳离子脂质对映体/E7复合物处理的主要的人树状突细胞均使全部三种共刺激树状突细胞活化的标记的表达上调节,评价并要求成功地使抗原呈递到T-细胞,这类似于阳离子脂质的外消旋混合物(RS-DOTAP)所观察到并报道于本申请的申请人的美国申请No. 12/049,957中的。
5. 含有单个R和S对映体的阳离子脂质/E7复合物在活化人树状突细胞以诱导趋化因子和细胞因子产生中显示出不同的效能
如上文所述对人HLA-A2 树状突细胞(Lonza,Walkersville, MD)进行处理并生长于培养物中。在第3天,使细胞用40微摩尔DOTAP/E7复合物或者50微摩尔浓度的有效的免疫刺激剂脂多糖(LPS)(阳性对照)进行处理。除去来自分析孔中的培养基,再在microfuge中以1300 rpm离心5分钟成片状的未附着的树状突细胞。除去上清液,再用10微升/ml的Calbiochem (La Jolla, CA) 蛋白酶抑制剂鸡尾酒组I (Cat. No. 539131)处理,再在分析之前冷冻贮存。通过Searchlight Protein Array
Multiplex ELISA分析法[Pierce Biotechnology (Woburn, MA)]分析针对趋化因子和细胞因子表达分析样品。
评价选择的已知在细胞免疫应答中是必要的趋化因子的产生CCL3、CCL4、CCL5和CCL19,并评价IL-2、11-8和IL-12的产生(图5-11,它们说明了R-DOTAP/E7和S-DOTAP/E7诱发 CCL3、CCL4、CCL5、CCL-19、IL-2、IL-8和IL-12产生的能力)。这些图说明,含有单个DOTAP的对映体的DOTAP/E7复合物通过人树状突细胞诱发产生细胞因子和趋化因子。然而,两种对映体均不同程度地活化免疫系统,其中R-对映体显示更高的效能。
6. 在不同剂量的DOTAP外消旋混合物下用DOTAP/E7组合物治疗的小鼠中TC-1 HPV-阳性肿瘤生长的动力学。
在图12中,在第0天给小鼠皮下注射TC-1细胞,以诱发HPV-阳性肿瘤的生长。DOTAP/E7组合物包含DOTAP的外消旋混合物。在第6天,小鼠在腹部对侧皮下接受含有10 μg E7肽的DOTAP/E7组合物。在该复合物中的DOTAP脂质浓度在3至600 nmol间变化(3、15、30、75、150、300和600 nmol)。在第23天,与未治疗的对照相比,低剂量的DOTAP (15 nmol)显示出部分的肿瘤抑制作用(P < 0.05),而30、150或300 nmol的DOTAP显示出提高的效能(P < 0.01)。75nmol的DOTAP显示最显著的肿瘤退化作用(P < 0.001)。此外,给予高剂量DOTAP (600 nmol)的小鼠未显示抗肿瘤活性,证实高剂量下DOTAP 脂质体可能会诱发对免疫应答的负调节。此外,100 nmol剂量的DOTAP 脂质体(无E7肽)未显示肿瘤生长的显著抑制作用,表明该抗肿瘤作用是抗原特异性的。进一步地,150 nmol的1,2-二油酰基-sn-甘油-3-磷酸甘油(DOPG,一种阴离子脂质)的脂质体与抗原施用未能显著抑制肿瘤生长。
7. 在用不同剂量的R和S的DOTAP的R-DOTAP/E7和S-DOTAP组合物治疗的小鼠中TC-1 HPV-阳性肿瘤生长的动力学。
在图13和14中,在第0天给小鼠皮下注射TC-1细胞,以便诱发HPV-阳性肿瘤的生长。在第6天,使小鼠在腹部的对侧皮下接受R和S- DOTAP /E7组合物,其中含有20 μg E7 肽。在该复合物中的R或S-DOTAP脂质浓度范围为3至600 nmol (3、15、30、75、100、125、150、300和600 nmol)。与DOTAP的外消旋混合物(图12)不同,S-DOTAP 复合物未显示出抑制肿瘤生长的能力并且未观察到肿瘤退化(图13)。然而,观察到了剂量应答作用,并且在第23天与对照相比,600 nmol的S-DOTAP剂量诱发最慢的肿瘤生长(P < 0.05)。参见图14,含有R-DOTAP和抗原的复合物的抗肿瘤作用与在外消旋混合物(图12)中观察到的结果相似。在第23天与对照相比,75-150 nmol剂量的R-DOTAP显示出部分肿瘤抑制作用(P < 0.001)。此外,给予高剂量的R-DOTAP (600 nmole)的小鼠未显示出显著的抗肿瘤活性,证实高剂量的R-DOTAP 脂质体会诱发对免疫应答的负调节。单独的E7肽未显示出肿瘤生长的任何抑制作用(未示出)。图15显示了不同的阳离子脂质/E7抗原复合物DOTAP、S-DOTAP和R-DOTAP(20μg的抗原)以及DOTAP(10 μg的抗原)的肿瘤退化效能的脂质剂量应答曲线。
8. 通过S-DOTAP和R-DOTAP组合物诱发T细胞增生
我们在以前的归于本申请的申请人的美国临时专利申请No. 60/983,799中证实, DOTAP/E7直接与人T淋巴细胞相互作用,导致克隆细胞表达和T细胞活化。这些研究检测了DOTAP的外消旋混合物刺激T细胞的克隆细胞表达的能力。在这些研究中,从HLA-A2+健康供者获得的浓缩的人淋巴细胞是直接通过培养基、单独的DOTAP、单独的肽或DOTAP/hE7刺激的。以7-天的间隔重复该刺激3次。第三次刺激之后3天,与在培养基对照中的非克隆扩张相比,用DOTAP或DOTAP/E7处理的淋巴细胞在培养基中显示T细胞克隆的广泛扩张。该扩张的T-细胞还证实了显著的CTL活性。
在这些研究中,DOTAP-介导的T细胞活化通过T细胞中的ERK磷酸化而被进一步确证。还观察到在人T淋巴细胞中辅刺激分子CD86的DOTAP-诱导的表达。这些结果表明,DOTAP通过MAP激酶介导的细胞增殖而对T细胞活化有直接影响。
在本研究中,使用得自Lonza, MA的纯化的T-细胞研究并确证了通过DOTAP的R和S对映体诱导的人T-细胞增殖。与S-DOTAP相比R-DOTAP诱发更多的T-细胞增殖,并且活性类似于DOTAP外消旋混合物。
讨论
如美国专利No. 7,303,881所讨论的,广泛种类的阳离子脂质可以与抗原作为有效的免疫刺激剂,以疾病的治疗中产生抗原特异性免疫应答。例如,美国专利No. 7,303,881公开了包含阳离子脂质的脂质体活化树状突细胞,这是通过辅刺激分子CD80/CD86对DC2.4 树状突细胞的表达的阳离子脂质来刺激所证实的(图14A和14B)。如美国专利No. 7,303,881的图14A所示,通过不同阳离子脂质体对DC2.4细胞刺激CD80/CD86的表达的能力非常不同。Lipofectamine.RTM.(一种聚阳离子脂质2,3-二油酰基氧基-N-[2(精胺羧基氨基)乙基]-N,N-二甲基-1-丙烷铵三氟乙酸盐(DOSPA)和中性脂质二油酰基磷脂酰乙醇胺(DOPE)的3:1 (w/w)脂质体配方)以及从O,O'-二肉豆蔻基-N-赖氨酰天冬氨酸酯(DMKE)和O,O'-二肉豆蔻基-N-赖氨酰-谷氨酸酯(DMKD)制备的脂质体通过CD2.4细胞强烈地刺激CD80/CD86的表达。
如在美国专利No. 7,303,881中进一步公开的,不同的阳离子脂质经CD2.4细胞刺激CD 80的表面的能力是不同的。该脂质的亲水性头部和亲脂性尾部均显著影响此种能力。例如,具有乙基磷酸胆碱(EPC)头部基团的DXEPC脂质通常显示比之于具有三甲基铵丙烷(TAP) 头部基团的DXTAP 脂质更为有效。在带有一个特别的头部基团结构的脂质中,具有更短的(1,2-二月桂酰基-sn-甘油-3-乙基磷酸胆碱(DLEPC-12:0)、1,2-二肉豆蔻酰基-sn-甘油-3-乙基磷酸胆碱(DMEPC-14:0))或者不饱和的(1,2-二油酰基-sn-甘油-3-乙基磷酸胆碱(DOEPC-18:1))酰基链的脂质显示比之于具有更长(1,2-二棕榈酰基-sn-甘油-3-乙基磷酸胆碱(DPEPC-16:0))或者饱和的(1,2- 二硬脂酰基-sn-甘油-3-乙基磷酸胆碱(DSEPC-16:0))酰基链的那些更为有效。然而,这些数据证实,多种阳离子脂质能够刺激树状突细胞活化。美国申请No. 12/049,957中报道的研究强调通过阳离子脂质作为免疫刺激剂的机制。
来自上述研究的数据已得到这样的观察,即:该阳离子脂质不但靶向免疫系统的APC并投递抗原的载体到免疫系统的APC,而且在低剂量组合物下作为有效佐剂功能在MAP激酶依赖信号途径的整个活化中直接延伸到影响免疫系统功能,结果产生免疫系统调节分子包括细胞因子和趋化因子。一种明确的阳离子脂质对该配方的免疫刺激能力的剂量-应答作用已补充证实。其证实,在接受脂质/抗原复合物后,该粒子主要被树状突细胞吸收,该树状突细胞是主要的专业抗原递呈细胞。树状突细胞活化开始并迁移到引流淋巴结促进对抗抗原特异性TC-1肿瘤的免疫应答,这已被证实。功能性CD8+ T淋巴细胞是在小鼠中在接受DOTAP/E7注射时产生的,肿瘤大小减小并且显示增加的编程性细胞死亡,原因是在肿瘤微环境中浸润T细胞的数量增加。得到的钟形(在高于和低于最佳剂量下活性减小)阳离子脂质剂量应答曲线证实了在非常低的剂量下的活性,这表明,阳离子脂质作为佐剂或免疫刺激剂的活性是如此有效以致于EC50低到约15 nmol/注射。高剂量的阳离子脂质消除了免疫刺激活性。我们还证实,当将抗原例如卵白蛋白掺入到阳离子脂质体中并以单次皮下注射施用时,产生的抑制该抗原的有效抗体。阳离子脂质体还能诱发辅刺激分子CD80和CD83的表达并活化人树状突细胞。人们清楚,在最佳剂量组合物下,阳离子脂质和阳离子脂质/抗原复合物除了有效投递到树状突细胞以外还是有效的免疫系统活化剂,并且提供简单、安全和非常有效的免疫治疗法以用于预防和治疗疾病。
根据对免疫刺激机制的理解,进行进一步研究以评价阳离子脂质中的手征性的作用以及阳离子脂质的免疫刺激能力。为达到此效果,使用纯合成的DOTAP的R和S对映体,并与通常使用的外消旋混合物比较。关于树状突细胞的活化和成熟方面,DOTAP的R和S对映体二者均证实具有类似于外消旋DOTAP的能力。所有三种脂质诱发树状突细胞表达辅刺激分子CD 80、CD 83和CD 86。
诱发细胞对疾病的免疫应答的免疫刺激能力的重要特征是其能够诱发产生关键的趋化因子和细胞因子。如在实施例中所报道的,DOTAP的R和S对映体之间在其诱发趋化因子和细胞因子产生方面观察到显著差异。观察到R-DOTAP是一种比S-DOTAP更有效的免疫活化剂。在所有情况下,R-DOTAP的效能等于或高于DOATP外消旋混合物的效能。
为了确定细胞因子诱导作用的体外效能是否可以转化到体内治疗效能,对三种配方(R-DOTAP/E7、S-DOTAP/E7和DOTAP/E7(外消旋混合物))评价它们在荷瘤小鼠中根除HPV-E7阳性肿瘤的能力。每种配方是以多种脂质剂量评价的。如在图12-15中所证实的,含有R-DOTAP和DOTAP的两种配方均显示钟形的脂质-剂量应答,在特异性最佳剂量范围内强烈的E7特异性活性导致肿瘤退化。含有S-DOTAP的配方在任何观察的条件下均未诱发肿瘤退化,尽管高脂质配方减缓了肿瘤生长。
由此证明,DOTAP的R对映体是所观察到的DOTAP的佐剂作用的主要原因。然而,两种对映体均是树状突细胞引起成熟的有效活性剂。
以上报道的研究表明,包含手性脂质或手性脂质的混合物的阳离子脂质的特别独特的组合物和应用,能够对其利用以发开简单、价廉和更为需要的免疫治疗法以用于多种虚弱性疾病。
在上述方面和示例性的实施方案中可以进行许多变化而不会脱离本发明的范围,期望的是,包含于以上说明中的所有内容将解释为说明性的而非限制性的含义。这样,虽然实话例主要讨论了阳离子脂质 DOTAP的对映体,本领域技术人员理解,这种阳离子脂质仅是示例性的,并且该方法和机制能够用于其它阳离子脂质。
Claims (16)
1.一种组合物,其包含至少一种手性阳离子脂质,其剂量足以在生物体外激活免疫系统的细胞,或者激活受试者的免疫系统并且在该受试者中诱发免疫应答。
3.权利要求2的组合物,其中所述手性阳离子脂质选自DOTAP、DOTMA、DOEPC、及其组合。
4.权利要求1的组合物,其进一步包含至少一种抗原以形成阳离子脂质/抗原复合物,其中所述阳离子脂质/抗原复合物刺激抗原特异性作用或免疫应答。
5.权利要求4的组合物,其中所述至少一种抗原选自肿瘤相关抗原、病毒抗原、微生物抗原、及其组合。
6.权利要求4的组合物,其中所述至少一种抗原包括脂质化抗原或者被修饰以增加其疏水性的抗原,并且其可在所述抗原和连接的疏水基之间含有氨基酸连接子序列。
7.权利要求6的组合物,其中所述至少一种抗原选自脂蛋白、脂肽、被具有疏水性增加的氨基酸序列修饰的蛋白或肽、及其组合。
8.权利要求4的组合物,其中所述至少一种抗原包括共价连接到氨基酸序列的至少一种抗原,所述氨基酸序列使该抗原具有与母体蛋白中存在序列不同的氨基酸序列。
9.在生物体外激活免疫细胞或者在受试者中诱发免疫应答的方法,该方法包括给受试者以足以激活该细胞或者在受试者中诱发免疫应答的剂量施用至少一种手性阳离子脂质。
11.权利要求10的方法,其中所述手性阳离子脂质选自DOTAP、DOTMA、DOEPC、及其组合。
12.权利要求9的方法,其进一步包含至少一种抗原以形成阳离子脂质/抗原复合物,其中所述阳离子脂质/抗原复合物刺激抗原特异性免疫应答。
13. 权利要求12的方法,其中所述至少一种抗原选自肿瘤相关抗原、病毒抗原、微生物抗原、及其组合。
14.权利要求12的方法,其中所述至少一种抗原包括脂质化抗原或者被修饰以增加其疏水性的抗原,并且其可在所述抗原和连接的疏水基之间含有氨基酸连接子序列。
15.权利要求12的方法,其中所述至少一种抗原选自脂蛋白、脂肽、被具有疏水性增加的氨基酸序列修饰的蛋白或肽、及其组合。
16.通过用手性阳离子脂质或者阳离子脂质/抗原复合物处理T-细胞以诱发T-细胞增殖的方法,其中所述阳离子脂质包括手性脂质或手性脂质的混合物。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201811312211.3A CN110075113A (zh) | 2008-04-17 | 2009-04-14 | 通过阳离子脂质的对映体刺激免疫应答 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US4583708P | 2008-04-17 | 2008-04-17 | |
| US61/045837 | 2008-04-17 | ||
| PCT/US2009/040500 WO2009129227A1 (en) | 2008-04-17 | 2009-04-14 | Stimulation of an immune response by enantiomers of cationic lipids |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201811312211.3A Division CN110075113A (zh) | 2008-04-17 | 2009-04-14 | 通过阳离子脂质的对映体刺激免疫应答 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN102137675A true CN102137675A (zh) | 2011-07-27 |
Family
ID=41199446
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201811312211.3A Pending CN110075113A (zh) | 2008-04-17 | 2009-04-14 | 通过阳离子脂质的对映体刺激免疫应答 |
| CN200980121761XA Pending CN102137675A (zh) | 2008-04-17 | 2009-04-14 | 通过阳离子脂质的对映体刺激免疫应答 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201811312211.3A Pending CN110075113A (zh) | 2008-04-17 | 2009-04-14 | 通过阳离子脂质的对映体刺激免疫应答 |
Country Status (13)
| Country | Link |
|---|---|
| US (4) | US9789129B2 (zh) |
| EP (1) | EP2276495B1 (zh) |
| JP (1) | JP5971945B2 (zh) |
| CN (2) | CN110075113A (zh) |
| AU (1) | AU2009236306B2 (zh) |
| BR (1) | BRPI0910464B1 (zh) |
| CA (1) | CA2721366C (zh) |
| ES (1) | ES2712505T3 (zh) |
| IL (1) | IL208713A (zh) |
| PL (1) | PL2276495T3 (zh) |
| RU (1) | RU2530555C2 (zh) |
| TW (1) | TWI449534B (zh) |
| WO (1) | WO2009129227A1 (zh) |
Cited By (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN104066444A (zh) * | 2011-09-12 | 2014-09-24 | Pds生物科技公司 | 微粒疫苗制剂 |
| CN105101991A (zh) * | 2012-09-21 | 2015-11-25 | Pds生物科技公司 | 改进的疫苗组合物和使用方法 |
| CN105163753A (zh) * | 2012-06-15 | 2015-12-16 | Pds生物科技公司 | 阳离子脂质疫苗组合物和使用方法 |
| CN110461355A (zh) * | 2016-10-31 | 2019-11-15 | 艾金株式会社 | 包含免疫调控剂和阳离子脂质体的免疫增强的组合物及其用途 |
| US11612652B2 (en) | 2015-11-13 | 2023-03-28 | Pds Biotechnology Corporation | Lipids as synthetic vectors to enhance antigen processing and presentation ex-vivo in dendritic cell therapy |
| US11801257B2 (en) | 2008-04-17 | 2023-10-31 | Pds Biotechnology Corporation | Stimulation of an immune response by enantiomers of cationic lipids |
| US11911359B2 (en) | 2007-03-22 | 2024-02-27 | Pds Biotechnology Corporation | Stimulation of an immune response by cationic lipids |
Families Citing this family (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE10347710B4 (de) | 2003-10-14 | 2006-03-30 | Johannes-Gutenberg-Universität Mainz | Rekombinante Impfstoffe und deren Verwendung |
| DE102005046490A1 (de) | 2005-09-28 | 2007-03-29 | Johannes-Gutenberg-Universität Mainz | Modifikationen von RNA, die zu einer erhöhten Transkriptstabilität und Translationseffizienz führen |
| WO2011109294A1 (en) * | 2010-03-01 | 2011-09-09 | Dicerna Pharmaceuticals, Inc. | Lipid delivery formulations |
| JP2011184344A (ja) * | 2010-03-08 | 2011-09-22 | Kao Corp | p21発現促進剤 |
| RU2625546C2 (ru) | 2010-07-06 | 2017-07-14 | Новартис Аг | Катионные эмульсии "масло-в-воде" |
| CN103608033B (zh) | 2011-05-24 | 2016-06-15 | 生物技术公司 | 用于癌症的个体化疫苗 |
| CN103796639B (zh) | 2011-07-06 | 2017-05-31 | 诺华股份有限公司 | 阳离子水包油乳液 |
| JP6059220B2 (ja) | 2011-07-06 | 2017-01-18 | ノバルティス アーゲー | 核酸を含む水中油型エマルジョン |
| WO2013143555A1 (en) | 2012-03-26 | 2013-10-03 | Biontech Ag | Rna formulation for immunotherapy |
| EP2925348B1 (en) | 2012-11-28 | 2019-03-06 | BioNTech RNA Pharmaceuticals GmbH | Individualized vaccines for cancer |
| WO2014180490A1 (en) | 2013-05-10 | 2014-11-13 | Biontech Ag | Predicting immunogenicity of t cell epitopes |
| CN105873941A (zh) * | 2013-12-16 | 2016-08-17 | 默克专利有限公司 | 生存素导向的癌症疫苗治疗 |
| WO2016045732A1 (en) | 2014-09-25 | 2016-03-31 | Biontech Rna Pharmaceuticals Gmbh | Stable formulations of lipids and liposomes |
| WO2016128060A1 (en) | 2015-02-12 | 2016-08-18 | Biontech Ag | Predicting t cell epitopes useful for vaccination |
| WO2017059902A1 (en) | 2015-10-07 | 2017-04-13 | Biontech Rna Pharmaceuticals Gmbh | 3' utr sequences for stabilization of rna |
| JP2019500021A (ja) * | 2015-11-13 | 2019-01-10 | ピーディーエス バイオテクノロジー コーポレイションPds Biotechnology Corporation | 樹状細胞療法においてex vivoでの抗原のプロセシングと提示を亢進させるための合成ベクターとしての脂質 |
| US20180221475A1 (en) * | 2016-10-05 | 2018-08-09 | Pds Biotechnology Corporation | Methods to alter the tumor microenvironment for effective cancer immunotherapy |
| AU2018378588A1 (en) * | 2017-12-05 | 2020-06-25 | Pds Biotechnology Corporation | Methods and compositions comprising cationic lipids for stimulating type 1 interferon genes |
| JP2023551444A (ja) * | 2020-11-20 | 2023-12-08 | ピーディーエス バイオテクノロジー コーポレイション | 腫瘍内直接注射による免疫療法のための、方法及び陽イオン性脂質を含む組成物 |
| WO2024086290A2 (en) * | 2022-10-19 | 2024-04-25 | Pds Biotechnology Corporation | Novel t cell activating immunotherapeutic for treatment of mucin 1 protein expressing human cancers |
Family Cites Families (123)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2167480A (en) | 1927-11-02 | 1939-07-25 | Rca Corp | Signaling |
| US4703004A (en) | 1984-01-24 | 1987-10-27 | Immunex Corporation | Synthesis of protein with an identification peptide |
| JPS6440808A (en) | 1987-08-05 | 1989-02-13 | Canon Kk | Zoom lens |
| US5703055A (en) | 1989-03-21 | 1997-12-30 | Wisconsin Alumni Research Foundation | Generation of antibodies through lipid mediated DNA delivery |
| US6214804B1 (en) | 1989-03-21 | 2001-04-10 | Vical Incorporated | Induction of a protective immune response in a mammal by injecting a DNA sequence |
| US5264618A (en) | 1990-04-19 | 1993-11-23 | Vical, Inc. | Cationic lipids for intracellular delivery of biologically active molecules |
| US6183745B1 (en) | 1990-12-12 | 2001-02-06 | The University Of Queensland | Subunit papilloma virus vaccine and peptides for use therein |
| DE69207603T2 (de) | 1991-08-16 | 1996-09-12 | Vical Inc | Zusammensetzung und verfahren zur behandlung von zystischer fibrose |
| IL102964A0 (en) | 1991-08-26 | 1993-01-31 | Cytel Corp | Hla-restricted hepatitis b virus ctl epitopes |
| US6419931B1 (en) * | 1991-08-26 | 2002-07-16 | Epimmune Inc. | Compositions and methods for eliciting CTL immunity |
| US5283185A (en) | 1991-08-28 | 1994-02-01 | University Of Tennessee Research Corporation | Method for delivering nucleic acids into cells |
| IL105554A (en) | 1992-05-05 | 1999-08-17 | Univ Leiden | Peptides of human papillomavirus for use in preparations elicit a human T cell response |
| CA2134773A1 (en) | 1992-06-04 | 1993-12-09 | Robert J. Debs | Methods and compositions for in vivo gene therapy |
| US7105574B1 (en) | 1999-03-26 | 2006-09-12 | Vical Incorporated | Adjuvant compositions and methods for enhancing immune responses to polynucleotide-based vaccines |
| US5334761A (en) | 1992-08-28 | 1994-08-02 | Life Technologies, Inc. | Cationic lipids |
| US9266930B1 (en) | 1993-03-05 | 2016-02-23 | Epimmune Inc. | Inducing cellular immune responses to Plasmodium falciparum using peptide and nucleic acid compositions |
| JPH09502086A (ja) | 1993-08-06 | 1997-03-04 | サイテル コーポレイション | 完全mage1遺伝子のクローニング及び特性決定 |
| AUPM500494A0 (en) | 1994-04-12 | 1994-05-05 | Minister For Agriculture & Rural Affairs For The State Of New South Wales, The | Composition for use in increasing mucosal immunity |
| FR2726764B1 (fr) | 1994-11-14 | 1997-01-31 | Pasteur Merieux Serums Vacc | Adjuvant pour composition vaccinale |
| US6008202A (en) | 1995-01-23 | 1999-12-28 | University Of Pittsburgh | Stable lipid-comprising drug delivery complexes and methods for their production |
| FR2732895B1 (fr) | 1995-04-11 | 1997-05-16 | Pasteur Merieux Serums Vacc | Utilisation d'un compose amphipathique cationique comme agent de transfection, comme adjuvant de vaccin, ou comme medicament |
| CA2227065A1 (en) | 1995-07-21 | 1997-02-06 | Rhone-Poulenc Rorer Pharmaceuticals Inc. | Adeno-associated viral liposomes and their use in transfecting dendritic cells to stimulate specific immunity |
| WO1998000110A1 (en) | 1996-07-03 | 1998-01-08 | University Of Pittsburgh | Emulsion formulations for hydrophilic active agents |
| US7288266B2 (en) | 1996-08-19 | 2007-10-30 | United States Of America As Represented By The Secretary, Department Of Health And Human Services | Liposome complexes for increased systemic delivery |
| US7001614B2 (en) | 1996-08-19 | 2006-02-21 | The United States Of America As Represented By The Department Of Health And Human Services | Liposome complexes for increased systemic delivery |
| US20030229040A1 (en) | 1997-03-21 | 2003-12-11 | Georgetown University | Cationic liposomal delivery system and therapeutic use thereof |
| US6977074B2 (en) | 1997-07-10 | 2005-12-20 | Mannkind Corporation | Method of inducing a CTL response |
| US6693086B1 (en) | 1998-06-25 | 2004-02-17 | National Jewish Medical And Research Center | Systemic immune activation method using nucleic acid-lipid complexes |
| US20030022854A1 (en) | 1998-06-25 | 2003-01-30 | Dow Steven W. | Vaccines using nucleic acid-lipid complexes |
| AU2870300A (en) | 1999-02-05 | 2000-08-25 | Genzyme Corporation | Use of cationic lipids to generate anti-tumor immunity |
| JP2002537102A (ja) | 1999-02-26 | 2002-11-05 | カイロン コーポレイション | 吸着された高分子および微粒子を有するミクロエマルジョン |
| ES2308069T3 (es) | 1999-03-26 | 2008-12-01 | Vical Incorporated | Composiciones adyuvantes para realzar inmunorespuestas a las vacunas polinucleotido-basadas. |
| CA2370690A1 (en) | 1999-04-20 | 2000-10-26 | The University Of British Columbia | Cationic peg-lipids and methods of use |
| US6852334B1 (en) | 1999-04-20 | 2005-02-08 | The University Of British Columbia | Cationic peg-lipids and methods of use |
| US6649170B1 (en) | 1999-05-12 | 2003-11-18 | Statens Serum Institut | Adjuvant combinations for immunization composition and vaccines |
| FR2794370B1 (fr) | 1999-06-03 | 2003-10-17 | Biovector Therapeutics | Fragments proteiques polyepitopiques, leur obtention et leurs utilisations notamment en vaccination |
| EP1185662B1 (fr) | 1999-06-10 | 2011-03-02 | Merial | Vaccins adn pour les chiens |
| CA2309313A1 (en) | 1999-08-05 | 2001-02-05 | Board Of Trustees Of The University Of Arkansas | Stimulation of the immune response by human dendritic cell manipulation |
| PT1214097E (pt) | 1999-09-16 | 2009-10-19 | Eisai Inc | Ácidos nucleicos que codificam polipéptidos de poliepitopos |
| US20030008813A1 (en) | 1999-12-17 | 2003-01-09 | Felgner Philip L. | Intracellular protein delivery compositions and methods of use |
| EP1259592A1 (en) | 2000-01-11 | 2002-11-27 | Maxygen, Inc. | Monocyte-derived dendritic cell subsets |
| WO2001057068A1 (en) * | 2000-02-01 | 2001-08-09 | The Austin Research Institute | Mucin-1 derived antigens and their use in immunotherapy |
| JP2004508012A (ja) | 2000-04-20 | 2004-03-18 | ザ ユニバーシティ オブ ブリティッシュ コロンビア | エンドソーム膜不安定剤を用いたsplp媒介性トランスフェクションの強化方法 |
| DE60134421D1 (de) | 2000-12-08 | 2008-07-24 | Coley Pharmaceuticals Gmbh | Cpg-artige nukleinsäuren und verfahren zu ihrer verwendung |
| US20020187105A1 (en) | 2001-02-01 | 2002-12-12 | Yiyu Zou | Polymer combinations that result in stabilized aerosols for gene delivery to the lungs |
| EP1425039A4 (en) | 2001-03-23 | 2005-02-02 | Us Gov Health & Human Serv | PEPTIDES THAT GIVE AN IMMUNE REACTION WITH THE HUMAN PAPILLOMA VIRUS |
| FR2824326B1 (fr) | 2001-05-04 | 2004-03-19 | Commissariat Energie Atomique | Melange de peptides issus des proteines e6 et/ou e7 de papillomavirus et leurs applications |
| CN100384480C (zh) | 2001-05-30 | 2008-04-30 | 斯克里普斯研究学院 | 核酸传递系统 |
| EP1409009A1 (en) * | 2001-06-15 | 2004-04-21 | Nordic Vaccine Technology A/S | Therapeutical vaccination |
| US20060165708A1 (en) | 2001-06-29 | 2006-07-27 | Chugai Seiyaku Kabushiki Kaisha | Cancer vaccine containing cancer antigen based on tumor suppressor gene wt1 product and cationic liposomes |
| EP2263465A1 (en) * | 2001-07-06 | 2010-12-22 | Sloan-Kettering Institute for Cancer Research | Polyvalent conjugate vaccine for cancer |
| GB0118517D0 (en) * | 2001-07-30 | 2001-09-19 | Mitsubishi Tokyo Pharm Inc | Compound |
| CA2469738A1 (en) | 2001-11-07 | 2003-08-07 | Mannkind Corporation | Expression vectors encoding epitopes of target-associated antigens and methods for their design |
| US7598421B2 (en) | 2002-05-08 | 2009-10-06 | Ucl Biomedica Plc | Materials for the delivery of biologically-active material to cells |
| RU2311911C2 (ru) | 2002-07-05 | 2007-12-10 | Липоксен Текнолоджиз Лимитед | Способ усиления иммунного ответа при вакцинации нуклеиновой кислотой |
| JP4619121B2 (ja) | 2002-08-12 | 2011-01-26 | ザ カウンシル オブ ザ クイーンズランド インスティテュート オブ メディカル リサーチ | Tヘルパーエピトープおよび細胞傷害性tリンパ球(ctl)エピトープを含む新規な免疫原性リポペプチド |
| US20050031587A1 (en) | 2002-10-04 | 2005-02-10 | Yamanouchi Pharmaceutical Co., Ltd. | Immune response induction method |
| AU2003284239B2 (en) | 2002-10-21 | 2008-08-21 | Eisai Inc. | Compositions and methods for treating human papillomavirus-mediated disease |
| SE0301109D0 (sv) | 2003-04-14 | 2003-04-14 | Mallen Huang | Nucleotide vaccine composition |
| WO2004110493A2 (en) | 2003-05-30 | 2004-12-23 | Alza Corporation | Method of pulmonary administration of an agent |
| WO2005000889A1 (en) | 2003-06-05 | 2005-01-06 | The Government Of The United States Of America As Represented By The Secretary Of The Department Of Health And Human Services | Immunogenic peptides for the treatment of prostate and breast cancer |
| EP1638610B1 (en) | 2003-06-18 | 2015-03-18 | Yissum Research Development Company Of The Hebrew University Of Jerusalem | Sphingoid polyalkylamine conjugates for vaccination |
| US7906122B2 (en) | 2003-06-18 | 2011-03-15 | Yissum Research Development Company Of The Hebrew University Of Jersusalem | Sphingoid polyalkylamine conjugates for Hepatitis B virus vaccination |
| US8592197B2 (en) | 2003-07-11 | 2013-11-26 | Novavax, Inc. | Functional influenza virus-like particles (VLPs) |
| US20060182793A1 (en) | 2003-07-22 | 2006-08-17 | Cytos Biotechnology Ag | Cpg-packaged liposomes |
| JP5097400B2 (ja) | 2003-09-03 | 2012-12-12 | デンドリセラピューティクス、インク. | 複合ワクチン |
| CN1609617B (zh) * | 2003-09-29 | 2012-02-15 | 香港中文大学 | 诊断与预防严重急性呼吸道综合症(sars)的组合物和方法 |
| AU2004298991A1 (en) | 2003-12-10 | 2005-06-30 | Canji, Inc | Methods and compositions for treatment of interferon-resistant tumors |
| CN1559607A (zh) | 2004-02-20 | 2005-01-05 | �й�ũҵ��ѧ | 一种核酸物质与蛋白质类组合物及其生产方法和在免疫调节中的应用 |
| KR20070008625A (ko) | 2004-04-05 | 2007-01-17 | 화이자 프로덕츠 인코포레이티드 | 미세유체화된 수중유 유화액 및 백신 조성물 |
| GB0716992D0 (en) | 2007-08-31 | 2007-10-10 | Immune Targeting Systems Its L | Influenza antigen delivery vectors and constructs |
| US7303881B2 (en) * | 2004-04-30 | 2007-12-04 | Pds Biotechnology Corporation | Antigen delivery compositions and methods of use |
| AU2005251403B2 (en) | 2004-06-07 | 2011-09-01 | Arbutus Biopharma Corporation | Cationic lipids and methods of use |
| EP1778283A2 (en) * | 2004-06-30 | 2007-05-02 | ID Biomedical Corporation of Quebec | Vaccine compositions for treating coronavirus infection |
| WO2006007712A1 (en) | 2004-07-19 | 2006-01-26 | Protiva Biotherapeutics, Inc. | Methods comprising polyethylene glycol-lipid conjugates for delivery of therapeutic agents |
| DE102004057303A1 (de) * | 2004-11-26 | 2006-06-01 | Merck Patent Gmbh | Stabile Kristallmodifikationen von DOTAP Chlorid |
| EP1838330A4 (en) | 2004-12-13 | 2010-07-07 | Peplin Research Pty Ltd | TREATMENT OF SOLID TUMORS |
| EP1833838A2 (en) * | 2004-12-14 | 2007-09-19 | Applera Corporation, Applied Biosystems Group | Cationic liposomes comprising a charge neutral compound and a cationic phospholipid |
| JP2008528508A (ja) | 2005-01-21 | 2008-07-31 | イントロジェン・セラピューティクス,インコーポレイテッド | 標的細胞の治療および予防核酸への持続性の曝露を可能とする局所投与 |
| EP1957045A2 (en) | 2005-03-14 | 2008-08-20 | Board of Regents, The University of Texas System | Bioactive fus1 peptides and nanoprticle-polypeptide complexes |
| CA2599829C (en) | 2005-03-18 | 2013-08-06 | Widex A/S | Remote control system for a hearing aid |
| KR20160045151A (ko) | 2005-04-08 | 2016-04-26 | 아르고스 쎄라퓨틱스 인코포레이티드 | 수지상 세포 조성물 및 방법 |
| KR20080052509A (ko) | 2005-04-11 | 2008-06-11 | 더 거버먼트 오브 더 유나이티드 스테이츠 오브 아메리카, 애즈 레프리젠티드 바이 더 세크러테리, 디파트먼트 오브 헬쓰 앤드 휴먼 서비시즈, 센터스 포 디지즈 컨트롤 앤드 프리벤션 | 유행성 독감 바이러스에 대한 백신 |
| US20060275777A1 (en) | 2005-06-03 | 2006-12-07 | Waelti Ernst R | Novel strategies for protein vaccines |
| US20070059318A1 (en) | 2005-08-15 | 2007-03-15 | Balu-Iyer Sathy V | Lipid nano particulates containing antigens as cancer vaccines |
| US20110305713A1 (en) | 2005-10-21 | 2011-12-15 | Medical College Of Georgia Research Institute, Inc | Methods and compositions to enhance vaccine efficacy by reprogramming regulatory t cells |
| EP1969001A2 (en) | 2005-11-22 | 2008-09-17 | Novartis Vaccines and Diagnostics, Inc. | Norovirus and sapovirus antigens |
| WO2007106073A2 (en) * | 2006-03-02 | 2007-09-20 | University Of Massachusetts | Modified pathogens for use as vaccines |
| JP2007238559A (ja) | 2006-03-10 | 2007-09-20 | Nagoya City Univ | 未成熟樹状細胞活性化剤及びその使用 |
| CN101426811A (zh) | 2006-04-21 | 2009-05-06 | 特朗斯吉恩股份有限公司 | 基于hpv-16的乳头瘤病毒疫苗 |
| US20080014251A1 (en) | 2006-07-14 | 2008-01-17 | Advanced Vascular Dynamics | Hemostatic compound and its use |
| EP1894941A1 (en) | 2006-09-01 | 2008-03-05 | Institut Pasteur | Treatment of cervical carcinoma with a recombinant adenylate cyclase carrying HPV antigens |
| EP2084267B1 (en) | 2006-09-26 | 2018-04-11 | Cedars-Sinai Medical Center | Cancer stem cell antigen vaccines and methods |
| US20100099745A1 (en) | 2006-10-18 | 2010-04-22 | Suryaprakash Sambhara | Enhancing disease resistance against rna viral infections with intracytoplasmic pathogen sensors |
| KR100817024B1 (ko) | 2006-11-09 | 2008-03-26 | 재단법인 목암생명공학연구소 | 핵산 또는 약물을 간에 특이적으로 전달하는 복합체 및이를 포함하는 약학적 조성물 |
| US8877206B2 (en) | 2007-03-22 | 2014-11-04 | Pds Biotechnology Corporation | Stimulation of an immune response by cationic lipids |
| EP2167480A2 (en) | 2007-05-23 | 2010-03-31 | Vical Incorporated | Cationic lipids compositions and methods for enhancing immune responses to vaccines |
| US7832751B2 (en) * | 2007-06-29 | 2010-11-16 | Harley-Davidson Motor Company Group, Inc. | Rear fender assembly |
| CN113559253B (zh) | 2007-11-02 | 2024-09-17 | 约翰霍普金斯大学 | 用于治疗或预防人乳头瘤病毒感染的多型hpv肽的组合物和方法 |
| EP2276495B1 (en) | 2008-04-17 | 2018-11-21 | PDS Biotechnology Corporation | Stimulation of an immune response by enantiomers of cationic lipids |
| CA2724408A1 (en) | 2008-05-19 | 2009-11-26 | The University Of North Carolina At Chapel Hill | Methods and compositions comprising novel cationic lipids |
| US20100086584A1 (en) | 2008-09-18 | 2010-04-08 | Juvaris Biotherapeutics, Inc. | VACCINE COMPOSITIONS OF M2e, HA0 AND BM2 MULTIPLE ANTIGENIC PEPTIDES |
| CA2754826A1 (en) | 2009-03-06 | 2010-09-10 | Mount Sinai School Of Medicine | Live attenuated influenza virus vaccines comprising microrna response elements |
| WO2010132867A1 (en) | 2009-05-15 | 2010-11-18 | Irx Therapeutics, Inc. | Vaccine immunotherapy |
| WO2011109294A1 (en) | 2010-03-01 | 2011-09-09 | Dicerna Pharmaceuticals, Inc. | Lipid delivery formulations |
| EP3900740A1 (en) | 2010-03-30 | 2021-10-27 | Icahn School of Medicine at Mount Sinai | Influenza virus vaccines and uses thereof |
| JP5902616B2 (ja) | 2010-04-28 | 2016-04-13 | 協和発酵キリン株式会社 | カチオン性脂質 |
| AU2012286690A1 (en) | 2011-07-27 | 2014-03-06 | Baylor Research Institute | Dendritic cell (DC)-vaccine therapy for pancreatic cancer |
| ES2689799T3 (es) | 2011-09-12 | 2018-11-15 | Pds Biotechnology Corporation | Formulaciones de vacunas particuladas |
| EP2638896A1 (en) | 2012-03-14 | 2013-09-18 | Bioneer A/S | Cationic liposomal drug delivery system for specific targeting of human cd14+ monocytes in whole blood |
| EP2639299A1 (en) | 2012-03-16 | 2013-09-18 | Invectys | Universal cancer peptides derived from telomerase |
| EP3632464A1 (en) | 2012-06-15 | 2020-04-08 | PDS Biotechnology Corporation | Cationic lipid vaccine compositions and methods of use |
| US20150250872A1 (en) | 2012-09-21 | 2015-09-10 | Frank Bedu-Addo | Vaccine compositions and methods of use |
| HUE046469T2 (hu) | 2013-08-21 | 2020-03-30 | Curevac Ag | Készítmény és vakcina tüdõrák kezelésére |
| JP6788500B2 (ja) | 2013-10-23 | 2020-11-25 | アメリカ合衆国 | Muc1−c癌タンパク質のhla−a24アゴニストエピトープ及び組成物及び使用方法 |
| CN104189897A (zh) | 2014-05-21 | 2014-12-10 | 深圳先进技术研究院 | 一种树突状细胞高效负载抗原的制备方法 |
| SG11201707540QA (en) | 2015-03-16 | 2017-10-30 | Max-Delbrück-Centrum Für Molekulare Medizin In Der Helmholtz-Gemeinschaft | Method of detecting new immunogenic t cell epitopes and isolating new antigen-specific t cell receptors by means of an mhc cell library |
| CN105920599B (zh) | 2015-09-17 | 2020-02-11 | 武汉生物制品研究所有限责任公司 | 以阳离子脂质体dotap为佐剂的疫苗及其制备方法 |
| AU2016354590B2 (en) | 2015-11-13 | 2023-11-23 | Pds Biotechnology Corporation | Lipids as synthetic vectors to enhance antigen processing and presentation ex-vivo in dendritic cell therapy |
| US20180221475A1 (en) | 2016-10-05 | 2018-08-09 | Pds Biotechnology Corporation | Methods to alter the tumor microenvironment for effective cancer immunotherapy |
| MX2019003961A (es) | 2016-10-05 | 2019-08-26 | Pds Biotechnology Corp | Vacunas novedosas del vph16 con celulas t no restringidas por hla, composiciones y metodos de uso de las mismas. |
| AU2018378588A1 (en) | 2017-12-05 | 2020-06-25 | Pds Biotechnology Corporation | Methods and compositions comprising cationic lipids for stimulating type 1 interferon genes |
| CN111217918B (zh) * | 2020-03-04 | 2020-11-10 | 中山大学 | 一种基于2,4-二氧四氢喋啶合酶的新型冠状病毒s蛋白双区域亚单位纳米疫苗 |
-
2009
- 2009-04-14 EP EP09733034.4A patent/EP2276495B1/en active Active
- 2009-04-14 RU RU2010146655/15A patent/RU2530555C2/ru active
- 2009-04-14 CN CN201811312211.3A patent/CN110075113A/zh active Pending
- 2009-04-14 AU AU2009236306A patent/AU2009236306B2/en active Active
- 2009-04-14 WO PCT/US2009/040500 patent/WO2009129227A1/en active Application Filing
- 2009-04-14 JP JP2011505132A patent/JP5971945B2/ja active Active
- 2009-04-14 PL PL09733034T patent/PL2276495T3/pl unknown
- 2009-04-14 CN CN200980121761XA patent/CN102137675A/zh active Pending
- 2009-04-14 BR BRPI0910464-0A patent/BRPI0910464B1/pt active IP Right Grant
- 2009-04-14 ES ES09733034T patent/ES2712505T3/es active Active
- 2009-04-14 CA CA2721366A patent/CA2721366C/en active Active
- 2009-04-14 US US12/988,236 patent/US9789129B2/en active Active
- 2009-04-17 TW TW098112878A patent/TWI449534B/zh active
-
2010
- 2010-10-14 IL IL208713A patent/IL208713A/en active IP Right Grant
-
2017
- 2017-09-12 US US15/702,063 patent/US10702541B2/en active Active
-
2020
- 2020-06-12 US US16/899,763 patent/US11801257B2/en active Active
-
2021
- 2021-03-25 US US17/212,051 patent/US20210308157A1/en active Pending
Cited By (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US11911359B2 (en) | 2007-03-22 | 2024-02-27 | Pds Biotechnology Corporation | Stimulation of an immune response by cationic lipids |
| US11801257B2 (en) | 2008-04-17 | 2023-10-31 | Pds Biotechnology Corporation | Stimulation of an immune response by enantiomers of cationic lipids |
| CN104066444A (zh) * | 2011-09-12 | 2014-09-24 | Pds生物科技公司 | 微粒疫苗制剂 |
| CN110075292A (zh) * | 2011-09-12 | 2019-08-02 | Pds生物科技公司 | 微粒疫苗制剂 |
| CN105163753A (zh) * | 2012-06-15 | 2015-12-16 | Pds生物科技公司 | 阳离子脂质疫苗组合物和使用方法 |
| CN105163753B (zh) * | 2012-06-15 | 2018-12-21 | Pds生物科技公司 | 阳离子脂质疫苗组合物和使用方法 |
| CN113144188A (zh) * | 2012-09-21 | 2021-07-23 | Pds生物科技公司 | 改进的疫苗组合物和使用方法 |
| US11904015B2 (en) | 2012-09-21 | 2024-02-20 | Pds Biotechnology Corporation | Vaccine compositions and methods of use |
| CN105101991A (zh) * | 2012-09-21 | 2015-11-25 | Pds生物科技公司 | 改进的疫苗组合物和使用方法 |
| US11911465B2 (en) | 2012-09-21 | 2024-02-27 | Pds Biotechnology Corporation | Vaccine compositions and methods of use |
| US11612652B2 (en) | 2015-11-13 | 2023-03-28 | Pds Biotechnology Corporation | Lipids as synthetic vectors to enhance antigen processing and presentation ex-vivo in dendritic cell therapy |
| US11638753B2 (en) | 2015-11-13 | 2023-05-02 | PDS Biotechnology Corporalion | Lipids as synthetic vectors to enhance antigen processing and presentation ex-vivo in dendritic cell therapy |
| CN110461355B (zh) * | 2016-10-31 | 2023-06-09 | 艾金株式会社 | 包含免疫调控剂和阳离子脂质体的免疫增强的组合物及其用途 |
| CN110461355A (zh) * | 2016-10-31 | 2019-11-15 | 艾金株式会社 | 包含免疫调控剂和阳离子脂质体的免疫增强的组合物及其用途 |
Also Published As
| Publication number | Publication date |
|---|---|
| RU2010146655A (ru) | 2012-05-27 |
| EP2276495B1 (en) | 2018-11-21 |
| US9789129B2 (en) | 2017-10-17 |
| US20180015114A1 (en) | 2018-01-18 |
| RU2530555C2 (ru) | 2014-10-10 |
| ES2712505T3 (es) | 2019-05-13 |
| EP2276495A4 (en) | 2013-05-15 |
| IL208713A0 (en) | 2010-12-30 |
| US11801257B2 (en) | 2023-10-31 |
| TW201000124A (en) | 2010-01-01 |
| BRPI0910464A2 (pt) | 2018-03-27 |
| TWI449534B (zh) | 2014-08-21 |
| US20200330491A1 (en) | 2020-10-22 |
| EP2276495A1 (en) | 2011-01-26 |
| JP5971945B2 (ja) | 2016-08-17 |
| JP2011518170A (ja) | 2011-06-23 |
| CA2721366C (en) | 2017-06-06 |
| AU2009236306A1 (en) | 2009-10-22 |
| US20210308157A1 (en) | 2021-10-07 |
| WO2009129227A1 (en) | 2009-10-22 |
| PL2276495T3 (pl) | 2019-05-31 |
| CA2721366A1 (en) | 2009-10-22 |
| IL208713A (en) | 2016-10-31 |
| US10702541B2 (en) | 2020-07-07 |
| CN110075113A (zh) | 2019-08-02 |
| BRPI0910464B1 (pt) | 2021-08-10 |
| AU2009236306B2 (en) | 2015-04-02 |
| US20110110972A1 (en) | 2011-05-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US11801257B2 (en) | Stimulation of an immune response by enantiomers of cationic lipids | |
| US20210346333A1 (en) | Stimulation of an immune response by cationic lipids | |
| US11638753B2 (en) | Lipids as synthetic vectors to enhance antigen processing and presentation ex-vivo in dendritic cell therapy |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| RJ01 | Rejection of invention patent application after publication |
Application publication date: 20110727 |
|
| RJ01 | Rejection of invention patent application after publication |