CN101056656A - 在治疗肥胖症和糖尿病中降低er应力 - Google Patents
在治疗肥胖症和糖尿病中降低er应力 Download PDFInfo
- Publication number
- CN101056656A CN101056656A CNA2005800388745A CN200580038874A CN101056656A CN 101056656 A CN101056656 A CN 101056656A CN A2005800388745 A CNA2005800388745 A CN A2005800388745A CN 200580038874 A CN200580038874 A CN 200580038874A CN 101056656 A CN101056656 A CN 101056656A
- Authority
- CN
- China
- Prior art keywords
- medicine
- stress
- insulin
- cell
- xbp
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/13—Amines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/192—Carboxylic acids, e.g. valproic acid having aromatic groups, e.g. sulindac, 2-aryl-propionic acids, ethacrynic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/21—Esters, e.g. nitroglycerine, selenocyanates
- A61K31/215—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids
- A61K31/22—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids of acyclic acids, e.g. pravastatin
- A61K31/225—Polycarboxylic acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/365—Lactones
- A61K31/366—Lactones having six-membered rings, e.g. delta-lactones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
- A61K31/401—Proline; Derivatives thereof, e.g. captopril
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/02—Drugs for disorders of the nervous system for peripheral neuropathies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/04—Anorexiants; Antiobesity agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
- A61P5/48—Drugs for disorders of the endocrine system of the pancreatic hormones
- A61P5/50—Drugs for disorders of the endocrine system of the pancreatic hormones for increasing or potentiating the activity of insulin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
Landscapes
- Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Medicinal Chemistry (AREA)
- Chemical & Material Sciences (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Organic Chemistry (AREA)
- Diabetes (AREA)
- Emergency Medicine (AREA)
- Obesity (AREA)
- Endocrinology (AREA)
- Hematology (AREA)
- Cardiology (AREA)
- Neurosurgery (AREA)
- Vascular Medicine (AREA)
- Urology & Nephrology (AREA)
- Ophthalmology & Optometry (AREA)
- Biomedical Technology (AREA)
- Neurology (AREA)
- Heart & Thoracic Surgery (AREA)
- Child & Adolescent Psychology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Investigating Or Analysing Biological Materials (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
Abstract
已发现内质网应力与肥胖症有关。因此,降低或抑制ER应力的药物可用于治疗与肥胖症有关的疾病,包括外周胰岛素抗性、高血糖症和2型糖尿病。已显示降低ER应力和降低血糖水平的两种化合物包括4-苯基丁酸(PBA)、牛熊去氧胆酸(TUDCA)和三甲胺N-氧化物(TMAO)。用于降低ER应力的其它化合物是化学陪伴分子,如三甲胺N-氧化物和甘油。本发明提供使用ER应力减低剂(如PBA、TUDCA和TMAO)治疗患有下列疾病的患者的方法:肥胖症、高血糖症、2型糖尿病或胰岛素抗性。本发明还提供通过在ER加压细胞中鉴定降低ER应力标记药物来筛选ER应力减低剂的方法。这些药物可在治疗与肥胖症有关的疾病的方法和组合物中发现用途。
Description
相关申请
[0001]本申请依据35 U.S.C.§119(e),要求2004年9月15日提交的美国临时专利申请USSN 60/610,093的权益,其在此通过引用结合到本文中。本申请还涉及2004年9月15日提交的、题目为“用于治疗代谢性疾病的XBP-1活性的调节(Modulation of XBP-1 activityfor treatment of metabolic disorders)”的美国临时专利申请U.S.S.N.60/610,286;2005年9月15日提交的、题目为“用于治疗代谢性疾病的XBP-1活性的调节(Modulation of XBP-1 activity for treatment ofmetabolic disorders)”的美国临时专利申请U.S.S.N.XX/XXX,XXX;以及2003年9月2日提交的、题目为“用于调节XBP-1活性的方法和组合物(Methods and Compositions for Modulating XBP-1 Activity”的美国临时申请U.S.S.N.10/655,620,所述各申请均在此)通过引用结合到本文中。
政府支持
[0002]本发明所述的工作部分受到国立卫生研究所(the NationalInstitutes of Health)资助的第32412号项目的支持。美国政府可拥有本发明的某些权利。
发明背景
[0003]世界大部分地区肥胖症的发病率的戏剧性增加促成胰岛素抗性、2型糖尿病和心血管疾病发病率的增加。这些与肥胖症有关的疾病已对人体健康构成严重威胁。
[0004]现已发现肥胖症与细胞应力(stress)信号途径的激活有关(Uysal等,Nature 389:610,1997;Hirosumi等,Nature 420:333,2003;Yuan等,Science 293:1673,2001;均通过引用结合到本文中)。细胞应力响应中一参与成分(player)是内质网(ER),即在分泌和膜蛋白的合成和处理过程中发挥功能的一种膜状网络。ER负责真核细胞的大多数分泌性和膜内在蛋白质的处理和易位过程。ER的内腔为这些蛋白质的翻译后修饰和折叠提供了一种专门的环境。适当折叠的蛋白从ER的出口清除并进行到分泌途径,而未折叠或错折叠蛋白被ER-相关蛋白降解结构去除。细胞处理的蛋白质的负载依据细胞类型和细胞生理状态不同而有相当大的变化。可通过调节其ER处理蛋白和合成的蛋白的负载的能力来调节细胞。ER负载和折叠能力之间的平衡失调被称为ER应力(Harding等,Diabetes 51(Supp.3):S455,2002;通过引用结合到本文中)。已显示ER应力通过低氧、低血糖、暴露于扰乱ER功能的天然毒素以及各种影响患者蛋白折叠能力的突变所触发(Lee,Trends Biochem.Sci.26:504-510,2001;Lee,Curr.Opin.CellBiol.4:267-273,1992;其各自通过引用结合到本文中)。
[0005]现已显示某些病理性病症破坏ER体内平衡,从而导致ER内腔内未折叠或错折叠蛋白的聚集(Hampton Curr.Biol.10:R518,2000;Mori Cell 101:451,2000;Harding et al.Annu.Rev.Cell Dev.Biol.18:575,2002;其各自通过引用结合到本文中)。为解决ER应力,细胞激活将ER内腔与细胞质和细胞核连接的信号传导系统,称之为未折叠蛋白响应(UPR)(Hampton Curr.Biol.10:R518,2000;Mori Cell101:451,2000;Harding et al.Annu.Rev.Cell Dev.Biol.18:575,2002;其各自通过引用结合到本文中)。触发ER应力的条件包括葡萄糖和营养物丧失、病毒感染、分泌性蛋白质的合成增加以及突变体或错折叠蛋白的表达(Ma et al.Cell 107:827,2001;Kaufman et al.Nat.Rev.MoI.Cell Biol.3:411,2002;其各自通过引用结合到本文中)。
发明概述
[0006]现已发现很多呈现出触发ER应力的病症都出现于肥胖症以及诸如2型糖尿病、高血糖症和胰岛素抗性的相关疾病中。例如,肥胖症增加很多分泌器官系统内细胞的合成结构的要求,并且也与细胞内能量流和营养可用性的异常有关。本发明认为:很多这些与肥胖症有关的疾病引起ER应力,尤其在外周组织中,并且ER应力与触发胰岛素抗性和2型糖尿病(肥胖症的两种后遗症)有关。因此,能降低ER应力的药物可用于治疗肥胖症、外周胰岛素抗性、高血糖症和2型糖尿病。用于治疗这些疾病的药物包括小分子、蛋白质、核酸以及已知能降低或阻止ER应力的任何其它化学化合物。这些药物以任何能降低或阻止ER应力的方式发挥作用,例如降低或产生突变体或错折叠蛋白质、增加ER陪伴分子的表达、增加蛋白质的稳定性、推进ER的处理能力等。尤其有用的药物包括化学陪伴分子,如4-苯基丁酸(PBA)、牛熊去氧胆酸(tauroursodeoxycholic acid)(TUDCA)、三甲胺N-氧化物(TMAO)、甘油、D2O、二甲亚砜、甘氨酸三甲铵乙内酯(glycine betaine)、甲胺和甘油磷酸胆碱。特别是,已显示PBA和TUDCA能在动物中调节ER应力,其通过PERK磷酸化降低来测定,并显示它们能降低JNK的激活以及降低IRE-Iα的磷酸化,其通过在用本发明化合物治疗动物后进行的蛋白质印迹测定。另外,PBA和TUDCA能在动物中调节胰岛素受体信号,其可通过增加的胰岛素受体、胰岛素底物1-IRS-1和IRS-1酪氨酸磷酸化以及增加的Akt的丝氨酸磷酸化来测定。当将TMAO给予患有胰岛素抗性和2型糖尿病的动物时,TMAO在体内已呈现出抗糖尿病药物作用,降低葡萄糖和胰岛素水平。将所述药物或该药物的药用组合物以降低ER应力的有效剂量给予患者(例如人、狗、猫、哺乳动物、动物),从而降低肥胖症、胰岛素抗性和2型糖尿病的体征、症状和后遗症。本发明还提供通过给予降低ER应力的药物来治疗和/或预防肥胖症、胰岛素抗性、2型糖尿病和高血糖症的方法。虽然优选将所述药物口服或非肠道给药,但可将以药物传递领域已知的任何方式给予所述药物。这些药物的剂量范围依据所要传递的药物以及其它因素而变化,但一般为10mg/kg/日-10g/kg/日。
[0007]在某些实施方案中,用于降低ER应力的药物为4-苯基丁酸(PBA)。
已显示PBA能调节ER应力并能调节胰岛素信号。给予患者苯基丁酸(PBA)或其衍生物或盐以用于降低ER应力,尤其可用于治疗肥胖症、2型糖尿病、胰岛素抗性并用于降低血糖。PBA能有效降低血糖并增加胰岛素敏感性(图4和5)。PBA或其药用组合物的给药剂量范围为10mg/kg/日-2g/kg/日,优选100mg/kg/日-1g/kg/日,更优选500mg/kg/日-1g/kg/日。
[0008]在另一实施方案中,牛熊去氧胆酸(TUDCA),一种胆汁酸,是用于降低ER应力的药物。
已显示TUDCA能调节ER应力并能调节胰岛素信号。本发明提供给予患者牛熊去氧胆酸(TUDCA)或其盐或衍生物以降低ER应力。已发现TUDCA能降低血糖并增加胰岛素敏感性,使其可用于治疗肥胖症、2型糖尿病和胰岛素抗性(图6)。TUDCA或其药用组合物的给药剂量范围为10mg/kg/日-2g/kg/日,优选100mg/kg/日-1g/kg/日,更优选250mg/kg/日-750mg/kg/日。
[0009]在另一实施方案中,TMAO是用于降低ER应力的药物。
已显示TMAO能在体内作为抗糖尿病药物(见图7)。本发明提供给予患者TMAO或其盐或衍生物以降低ER应力。已发现TUDCA能有效降低血糖水平并增加胰岛素敏感性,使其可用于治疗肥胖症、2型糖尿病和胰岛素抗性(图7)。TMAO或其药用组合物的给药剂量范围为100mg/kg/日-0.01g/kg/日,优选10mg/kg/日-0.1g/kg/日,更优选5mg/kg/日-0.5mg/kg/日。
[0010]本发明还提供包括能降低ER应力的药物以及药学上可接受的赋形剂的药用组合物。可将药用组合物制成供口服、非肠道或透皮传递的制剂。还可将所述ER应力降低剂与其它药物联合使用,如胰岛素、抗糖尿病药、降血糖药、降胆固醇药、食欲抑制剂、阿司匹林、维生素、矿物质和抗高血压药。例如,可将PBA与二甲双胍组合或结合给药。可将所述各药物混合在同一药用组合物中或者可保持独立(即在两个单独制剂中)且在一个药剂盒中一起提供。所述药剂盒还可包括供医师和/或患者使用的说明书、注射器、针头、盒子、瓶子、管形瓶等。
[0011]在另一方面,本发明提供一种筛选能降低ER应力的药物的方法。所鉴定的药物用于治疗疗肥胖症、2型糖尿病、高血糖症和胰岛素抗性。将所筛选的药物与正经历ER应力的细胞接触。细胞经历的ER应力可通过遗传改造或用已知能引起ER应力的化学化合物(如衣霉素、毒胡萝卜素thapsigargin)处理来引发。特别用于本发明筛选的细胞包括肝细胞和脂肪细胞。然后测定ER应力标记的水平以鉴定能降低ER应力的药物。ER应力的标记的实例包括剪接形式的XBP-1、磷酸化状态的PERK(Thr980)和eIF2α(Ser51)、mRNA和蛋白水平的GRP78/BIP以及JNK活性。将与未处理的对照细胞比较,当与具有ER应力的细胞接触时能引起ER应力的标记降低的药物鉴定为能降低应力的药物。ER应力标记水平的降低表明药物可用于治疗与ER应力有关的疾病,如肥胖症、2型糖尿病、胰岛素抗性、高血糖症、囊性纤维化和阿尔茨海默氏病。用本发明方法鉴定的药物是本发明的部分。可对这些药物进一步测试在药用组合物中的用途。
[0012]在另一方面,本发明提供一种通过测定ER应力标记的表达水平而诊断胰岛素抗性、高血糖症或2型糖尿病的方法。可在本发明诊断方法中分析的标记包括剪接形式的XBP-1、磷酸化状态的PERK、磷酸化的eIF2α、mRNA水平的GRP78/BIP、蛋白水平的GRP78/BIP和JNK活性。也可使用已知能指示ER应力的任何其它细胞标记。这些标记的水平可通过本领域已知的任何方法测定,包括蛋白质印迹法、RNA印迹法、免疫测定法或酶测定法。ER应力标记水平的增加表明受试者面临胰岛素抗性、高血糖症或2型糖尿病的风险。
定义
[0013]“动物”:此处所用的术语动物指人或非人动物,包括例如哺乳动物、鸟类、爬行类动物、两栖类动物和鱼类。非人动物优选为哺乳动物(例如啮齿类动物、小鼠、大鼠、兔、猴、狗、猫、灵长类动物或猪)。在某些实施方案中,所述动物为人。
[0014]“化学陪伴分子”:“化学陪伴分子”是一种已知能抵抗蛋白质变性(如化学变性、热变性)而稳定蛋白质构象的化合物,因此保护蛋白质结构和功能的化合物(Welch et al.Cell Stress Chaperones1:109-115,1996;通过引用结合到本文中)。在某些实施方案中,“化学陪伴分子”是一种小分子或低分子量化合物。“化学陪伴分子”优选不是蛋白质。“化学陪伴分子”的实例包括如甘油、重水(D2O)、二甲亚砜(DMSO)、三甲胺N-氧化物(TMAO)、甘氨酸三甲铵乙内酯(甜菜碱)、甘油磷酸胆碱(GPC)(Burg等,Am.J.Physiol.(RenalPhysiol.43):F762-F765,1998;通过引用结合到本文中)、4-苯基丁酸盐或4-苯基丁酸(PBA)、甲胺和牛熊去氧胆酸(TUDCA)。化学陪伴分子可用于影响细胞中蛋白质的折叠。已显示化学陪伴分子在某些情况下能改正诸如囊性纤维化(Fischer等,Am.J.Physiol.Lung Cell MoI.Physiol.281:L52-L57,2001;通过引用结合到本文中)、蛋白感染素相关的疾病、肾性尿崩症和癌症等此类疾病中观察到的折叠/运输缺陷(Bai et al.Journal of Pharmacological and Toxicological Methods40(1):39-45,July 1998;通过引用结合到本文中)。化学陪伴分子还发现在降低ER应力中的用途,以及可用于治疗肥胖症、2型糖尿病、胰岛素抗性和高血糖症。
[0015]“有效量”:通常活性药物(如ER应力降低剂或其药用组合物)的“有效量”指引发所要求的生物学响应所必需的量。本领域普通技术人员清楚,能降低或阻止ER应力的药物的有效量可依据诸如所要求的生物学结果、正在传递的药物、正在治疗的疾病、所治疗的患者等这些因素而变化。例如,用于治疗高血糖症或2型糖尿病的药物的有效量是能导致血糖水平降低至少约10%、20%、30%、40%或50%的量。在其它实施方案中,ER应力调节剂的有效量降低至少一种ER应力标记(例如剪接形式的XBP-1、磷酸化状态的PERK、磷酸化的eIF2α、mRNA水平的GRP78/BIP、蛋白水平的GRP78/BIP和JNK活性)的水平。在某些实施方案中,可降低至少2、3、4或更多种ER应力标记的水平。可将ER应力标记降低大约10%、20%、30%、40%、50%、60%、70%、80%、90%、95%、98%、99%或100%。
[0016]“肽”或“蛋白质”:根据本发明,“肽”或“蛋白质”包括一股由肽键连接在一起的至少三个氨基酸。可将“肽”或“蛋白质”互换使用。虽然作为选择可使用非天然氨基酸(即不存在于自然界,但可加入多肽链中的化合物)和/或本领域已知的氨基酸类似物,但本发明的肽优选仅包含天然氨基酸。还可将发明肽中的一或多个氨基酸进行修饰,例如通过加入化学实体,如碳水化合物基团、磷酸根、法呢基、异法呢基、脂肪酸基、结合连接物(linker)、官能化或其它修饰等。在一优选的实施方案中,肽的修饰使得形成一种更稳定的肽(例如,体内更长的半衰期)。这些修饰可包括肽的环合、D-氨基酸的结合等。所述各修饰基本上不应干扰所述肽的所要求的生物学活性。
[0017]“多核苷酸”或“寡核苷酸”指核苷酸聚合物。聚合物可包括天然核苷酸(即腺苷、胸苷、鸟苷、胞苷、尿苷、去氧腺苷、脱氧胸苷、脱氧鸟苷和脱氧胞苷)、核苷类似物(如2-硫代胸苷、肌苷、吡咯并-嘧啶、3-甲基腺苷、5-甲基胞苷、2-氨基腺苷、C5-溴尿苷、C5-氟尿苷、C5-碘尿苷、C5-丙炔基尿苷、C5-丙炔基-胞苷、C5-甲基胞苷、7-去氮杂腺苷、7-去氮杂鸟苷、8-氧代腺苷、8-氧代鸟苷、O(6)-甲基鸟嘌呤、4-乙酰基胞苷、5-(羧基羟基甲基)尿苷、二氢尿苷、甲基假尿苷、1-甲基腺苷、1-甲基鸟苷、N6-甲基腺苷和2-硫代胞苷)、化学修修饰碱、生物修饰碱(例如甲基化碱基)、插入的碱、修饰的糖(如2’-氟核糖、核糖、2’-去氧核糖、2’-O-甲基胞苷、阿拉伯糖和己糖)或者修饰的磷酸根基(如硫代磷酸根(phosphorothioates)和5’-N-亚磷酰胺(phosphoramidite)键)。
[0018]“小分子”:本文所用术语“小分子”指不论是天然存在或人工生成(例如通过化学合成)的有机化合物,其具有相对低的分子量并且不是蛋白质、多肽或核酸。小分子具有的分子量通常小于约1500g/mol。小分子一般具有多个碳-碳键。已知天然存在的小分子包括,但不限于青霉素、红霉素、紫杉醇、环孢菌素和雷帕霉素。已知的合成小分子包括,但不限于氨苄西林、甲氧苯青霉素、新诺明和磺胺类药物。
附图简述
[0019]图1证实在肥胖症中观察到的增加的内质网应力。使用饮食性(高脂肪饮食诱发的)和遗传性(ob/ob)小鼠肥胖模型来检查肝组织中ER应力标记,并与年龄和性别匹配的瘦的对照组小鼠比较。对由保持在标准或高脂肪食谱下16周的雄性小鼠(C57BL/6)的肝值得的样本进行以上ER应力标记检查,ER应力标记包括剪接形式的XBP-1(XBP-1s)、磷酸化的eIF2α(ser51,p-eIF2a)、磷酸化的PERK(p-PERK)、mRNA表达水平的GRP78和JNK活性。用100μg蛋白质进行各免疫印迹(图1a)。对12-14周龄的雄性、ob/ob和野生型小鼠的肝中相同ER应力标记进行检查(图1b)。肝中GRP78 mRNA的表达水平通过根据RNA印迹分析法,在与图1a和1b中所述的类似组别的瘦的和肥胖动物中进行检测(图1c)。
[0020]图2显示ER应力的诱导作用如何通过JNK-介导的IRS-1的磷酸化作用损害肝细胞中胰岛素的作用。用毒胡萝卜素(thap,300nM,4小时)或衣霉素(tun,10μg/ml,2小时)在Fao细胞中诱导ER应力,接着将细胞用胰岛素(ins)刺激。在IRS-1免疫沉淀(IP)后,检测在毒胡萝卜素-或衣霉素处理的细胞中所刺激的胰岛素、IRS-1酪氨酸磷酸化和总蛋白水平,接着用对抗磷酸-酪氨酸(pY)的抗体进行免疫印迹(IB)(a)。在毒胡萝卜素-或衣霉素处理的细胞中胰岛素刺激的胰岛素受体(IR)酪氨酸磷酸化和总蛋白水平(b)。用毒胡萝卜素刺激2小时后,在Fao细胞中IRS-1的ser307残基的磷酸化(c)。用毒胡萝卜素刺激后,JNK-I抑制剂SP600125(JNKi)对ser307磷酸化的抑制作用(d)。通过用肽抑制剂(JNKi)阻断JNK活性,对IRS-1的胰岛素刺激的酪氨酸磷酸化(pY)的衣霉素诱导的抑制作用的逆转。在这些实验中,免疫沉淀和免疫印迹均采用抗磷酸酪氨酸抗体进行(e)。
[0021]图3显示IRE-I如何在ER应力介导的JNK激活作用、IRS-1的ser307磷酸化作用以及胰岛素受体信号的抑制作用中发挥关键作用。使用体外激酶试验并利重组c-jun作为底物,在IREIα+/+和IRE-Iα-/-成纤维细胞中用衣霉素处理后,在指定时间点测定JNK活性。JNK活性和总JNK水平(a)。在用衣霉素处理,接着用IRS-1磷酸丝氨酸307特异性抗体IRS-1免疫沉淀(IP)和免疫印迹(IB)后,IREIα+/+和IRE-Iα-/-成纤维细胞中ser307残基上IRS-1的磷酸化(b)。在IREIα+/+和IRE-Iα-/-成纤维细胞中用衣霉素处理后,胰岛素(ins)-刺激的IRS-1酪氨酸磷酸化和总IRS-1水平。各涂点下的图显示在各处理时间点上相对于总IRS-1水平的IRS-1酪氨酸磷酸化的校正密度(c)。
[0022]图4显示经非肠道途径给予的4-苯基丁酸盐(4-PBA)如何在体内增加胰岛素敏感性并降低糖尿病小鼠的血糖水平。使用遗传性(ob/ob)小鼠肥胖模型分析4-苯基丁酸盐(4-PBA)对胰岛素敏感性和高血糖症的作用。10-12周龄的瘦素(leptin)缺乏雄性小鼠来源于Jackson Labs,注射PBS三次(每日3次)共4日使之适应,然后用腹腔内注射4-PBA(1g/kg/日,以三个分剂量)或磷酸盐缓冲液(PBS)(3剂量的100μl)处理7日。在试验的第三日和第七日测进食血糖水平(mg/dl)(a)。在第一次注射之后第七日进行胰岛素抗性试验(ITT)(b)。
[0023]图5显示经口服途径给予的4-苯基丁酸盐(4-PBA)如何在体内增加胰岛素敏感性并降低糖尿病小鼠的血糖水平。使用遗传性小鼠肥胖模型(ob/ob)分析4-苯基丁酸盐(4-PBA)对胰岛素敏感性和高血糖症的作用。8-10周龄的瘦素缺乏雄性小鼠来源于Jackson Labs,注射PBS(每日2次)共4日使之适应,然后用4-PBA(500mg/kg/日,以二个分剂量)或磷酸盐缓冲液(PBS)(2剂量的200μl)处理20日。治疗之间的体重(a)。在试验的第0日和第20日禁食后6小时的血糖水平(mg/dl)(b)。在试验的第0日和第20日的胰岛素水平(ng/ml)(c)。在治疗的第15日进行胰岛素抗性试验(d)。
[0024]图6显示用牛熊去氧胆酸(TUDCA)治疗ob/ob小鼠能增强胰岛素敏感性病并能逆转糖尿病。使用9-10周龄ob/ob以及与其年龄和性别匹配的瘦对照组小鼠来分析TUDCA对葡萄糖代谢和糖尿病的影响。用PBS注射(每日一次,200μl腹腔注射)适应4日后,给小鼠腹膜内注射TUDCA(一日一次,500mg/kg在200μl PBS中)(瘦组n=6,ob/ob组n=7)和PBS(200μl)(瘦组n=6,ob/ob组n=7)。第一次注射后第4、7和10日的血糖水平(a)。第一次注射后第10日的ITT(b)。
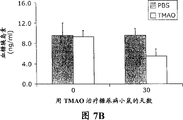
[0025]图7显示三甲胺N-氧化物(TMAO)的抗糖尿病作用。实验采用肥胖症和胰岛素抗性的ob/ob遗传模型(C57BL/6J-Lep-ob小鼠,购自Jackson Laboratory,Bar Harbor,ME)进行。在七周龄时,给予PBS适应5日后开始治疗。该期间过后,将TMAO(Sigma,T0514)溶解于PBS中,以每日1g/kg的剂量每24小时腹膜内(IP)注射给予。在指定日内,在8:00AM,使用自动血糖测量仪(glucometer)系统测定餐时血糖水平。为进行胰岛素测定,可在禁食6小时后收集血液样本,使用特异性ELISA(Crystal Chem,90060)确定血清胰岛素水平。每次试验时每组实验动物包含至少6只动物。
[0026]图8显示4-苯基丁酸盐和二甲双胍在治疗糖尿病中的有效组合。实验采用肥胖症和胰岛素抗性的ob/ob遗传模型(C57B6.V-Lepob/OlaHsd小鼠,购自Harlan Teklad,Madison,WI)进行。在七周龄时,给予PBS适应5日后开始治疗。该期间过后,每日通过管饲法,分别给予四个独立实验组小鼠(每组至少6只小鼠)PBS、4-苯基丁酸钠(200mg/kg/日)、二甲双胍(200mg/kg/日)和4-苯基丁酸钠+二甲双胍(各200mg/kg/日)。在这些剂量中,仅有4-苯基丁酸钠和二甲双胍组合显示能作为一种有效的降低血糖用药方案,而单一药物对血糖不具任何作用。在8:00AM,在喂食时测定血糖水平。
[0027]图9显示体外葡萄糖和体内高血糖对GRP78表达的调节作用。(A)将Fao细胞用各种剂量的葡萄糖(0、5、10、25和75mM)处理24小时。通过RNA印迹法,采用从这些细胞中分离的总RNAs,测定GRP78的mRNA水平。所显示的溴化乙锭染色法为一种装填和整合RNA的对照。(B)向雄性小鼠腹膜内注射链唑霉素(streptozotocin)(STZ,200mg/kg)。注射3日后,测定血糖水平以确定STZ-诱发高血糖症。注射10日后,收集肝,通过RNA印迹分析,采用肝总RNA测定GRP78表达。
[0028]图10显示肥胖小鼠的脂肪组织中的ER应力指示器。使用饮食性(高脂肪饮食-诱导)和遗传性(ob/ob)小鼠肥胖模型来检测脂肪组织中ER应力的标记,并与年龄和性别匹配的瘦型小鼠对照组比较。(A)对保持在标准饮食(RD)或高脂肪饮食(HFD)下16周的雄性小鼠(C57BL/6)的脂肪样本测定PERK磷酸化作用(p-PERK)和JNK活性。(B)12-14周龄的雄性ob/ob和WT瘦小鼠的脂肪组织中PERK磷酸化作用和JNK活性。(C)通过RNA印迹分析,在WT瘦型和ob/ob动物的脂肪组织中,检测GRP78的mRNA水平。所显示的溴化乙锭染色法为一种装填和整合RNA的对照。
[0029]图11显示ER应力的诱导作用通过JNK介导的IRS-1磷酸化损害胰岛素作用。(A)Fao肝细胞中ER应力通过用5μg/ml衣霉素(Tun)处理3小时诱导。接着用胰岛素(Ins)刺激细胞。使用免疫沉淀(IP),接着通过免疫印迹(IB)法或者直接免疫印迹法,测定IRS-1酪氨酸和丝氨酸(Ser307)磷酸化、Akt磷酸化(Ser473)、胰岛素受体(IR)酪氨酸磷酸化和它们的总蛋白水平。(B)在(A)中所述的实验条件下,用对各分子蛋白水平的归一化,对IRS-1(酪氨酸和Ser307)、Akt(Ser473)和IR(酪氨酸)磷酸化进行定量。(C)JNK-I抑制剂,SP600125(JNKi,25μM)对ER应力诱导的(300nM毒胡萝卜素,4小时)IRS-1的Ser307磷酸化的抑制作用。(D)在(C)中所述的条件下,对IRS-1Ser307磷酸化的定量。(E)JNK抑制剂对IRS-1的胰岛素刺激的酪氨酸磷酸化(pY)的ER诱导的抑制作用的逆转。(F)按(E)中所述,对胰岛素诱导的IRS-1酪氨酸磷酸化水平定量。(G)在IRE-1α+/+和IRE-Iα-/-成纤维细胞中,在用衣霉素处理(Tun,10μg/ml,1小时)后各指定时间点处的JNK活性、IRS-1的Ser307磷酸化和总IRS-1水平。(H)在IRE-1α+/+和IRE-Iα-/-成纤维细胞中,在用衣霉素处理(Tun,10μg/ml,1小时)后胰岛素刺激的IRS-1酪氨酸磷酸化和总IRS-1水平。在小图(panel)的底部显示IRE-1α+/+和IRE-Iα-/-细胞中定量的胰岛素诱导的IRS-1酪氨酸磷酸化水平。所有图表显示的平均值±SEM至少来源于两个独立实验,用*表示与对照组比较的具有p<0.005的统计学意义。
[0030]图12显示毒胡萝卜素诱导的ER应力对胰岛素受体信号的抑制作用以及Ca水平对IRS-1丝氨酸磷酸化的作用。(A)在Fao细胞中通过用300nM毒胡萝卜素(Thap)处理1小时诱导ER应力,接着将细胞用胰岛素(Ins)刺激。利用免疫沉淀法(IP),接着通过免疫印迹法(IB)或者直接用免疫印迹法,检测IRS-1酪氨酸磷酸化(pY)和丝氨酸磷酸化(pSer307)、胰岛素受体(IR)酪氨酸磷酸化以及总蛋白水平。(B)在暴露或不暴露于300nM毒胡萝卜素(Thap)另外1小时下,将Fao细胞用舒林酸硫化物(SS:0、7.5、30和60μM)处理45分钟。如上所述测定IRS-1丝氨酸磷酸化和总IRS-1蛋白水平。
[0031]图13表示通过控制XBP-1水平而使得ER应力响应的改变导致胰岛素受体信号的改变。ER应力在XBP-1s过度表达细胞(即XBP-1-/-细胞)和其对照细胞中响应。(A)小鼠胚胎成纤维细胞(MEF)中在除去脱氧土霉素下XBP-1s表达的诱导。(B)对XBP-1-/-MEF细胞及其WT对照细胞的野型(9.4kb)和定向(6.5kb)等位基因的蛋白质印迹分析。(C)衣霉素处理(Tun,2μg/ml)后,XBP-1s过度表达细胞及其对照细胞(分别为-Dox和+Dox)中PERK磷酸化(p-PERK)和JNK活性。(D)低剂量衣霉素处理(Tun,0.5μg/ml)后,XBP-1s过度表达细胞及其WT对照细胞中PERK磷酸化和JNK活性。(E)衣霉素处理(Tun,2μg/ml)后,XBP-1s过度表达细胞及其对照细胞(分别为-Dox和+Dox)中IRS-1 Ser307磷酸化,通过使用IRS-1的免疫沉淀法,接着用IRS-1磷酸丝氨酸307-特异性抗体的免疫印迹法检测。紧靠印迹图的图显示在小图E中所述的条件下,IRS-1 Ser307磷酸化的定量。(F)在有或无衣霉素处理(Tun,2μg/ml)下,XBP-1s过度表达细胞和对照细胞中IRS-1的胰岛素刺激的酪氨酸磷酸化。概括各独立试验的IRS-1酪氨酸磷酸化与总IRS-1水平的比率,并在表中给出。(G)按小图C中所述检测用衣霉素(Tun,0.5μg/ml)处理后,XBP-1-/-细胞及其WT对照细胞中IRS-1 Ser307的磷酸化。紧靠印迹图的图显示在图12G中所述的条件下,IRS-1 Ser307磷酸化的定量。(H)在有或无衣霉素处理(Tun,0.5μg/ml)下,XBP-1-/-细胞及其WT对照细胞中IRS-1的胰岛素刺激的酪氨酸磷酸化。概括各独立试验的IRS-1酪氨酸磷酸化与总IRS-1水平的比率,并在表中给出。所有图表显示的平均值±SEM至少来源于两个独立实验,用*表示与对照组比较的具有p<0.005的统计学意义。
[0032]图14显示在XBP-1过度表达和XBP-1-缺陷细胞中的胰岛素诱导的胰岛素受体的自磷酸化作用。(A)将XBP-1过度表达细胞及其对照MEF细胞(分别为-Dox和+Dox)用2μg/ml衣霉素(Tun)处理不同时间(0、0.5、1、2、3和4小时)。通过用抗IR抗体的免疫沉淀法(IP),接着用抗IR或磷酸酪氨酸(pY)的抗体进行免疫印迹(IB),在那些细胞中测定胰岛素诱导的胰岛素受体(IR)酪氨酸磷酸化(pY)和总IR水平。(B)将XBP-1-/-MEF细胞及其WT对照细胞用0.5μg/ml衣霉素处理不同时间(0、0.5、1、2、3和4小时)。按小图A的方法测定胰岛素诱导的胰岛素受体(IR)酪氨酸磷酸化(pY)和总IR水平。
[0033]图15显示高脂肪饮食中XBP-1+/-小鼠的葡萄糖的体内平衡。断奶后,立即将XBP-1+/-(◇)和XBP-1+/+(■)小鼠置于高脂肪饮食(HFD)下。在HFD过程中,在XBP-1+/-和XBP-1+/+小鼠中测定总体重(A)、禁食血胰岛素(B)、C-肽(C)和葡萄糖(D)水平。在XBP-1+/-和XBP-1+/+小鼠中,在HFD间,在第7(E)和16(F)周后进行葡萄糖耐量试验。在XBP-1+/-和XBP-1+/+小鼠中,n=11 XBP-1+/-小鼠;n=8XBP-1+/+小鼠;在HFD间,在第8(G)和17(H)周后进行胰岛素耐量试验。数据以平均值±SEM表示。*表示双尾student t检验的统计学意义p≤0.05,**表示p≤0.005,而***表示p≤0.0005。将XBP-1+/-和XBP-1+/+组别通过ANOVA(小图A-H)比较。
[0034]图16显示XBP-1+/-小鼠中ER应力和胰岛素受体信号。在高脂肪饮食16周后,检测XBP-1+/-和XBP-1+/+小鼠的肝中PERK磷酸化(p-PERK)(A)、JNK活性(p-c-Jun)(B)和IRS-1 Ser307(IRS-1pSer307)(C)。门静脉输注胰岛素(1U/kg)后,在高脂肪饮食16周的XBP-1+/-和XBP-1+/+小鼠的肝中,检测胰岛素受体(IR)酪氨酸磷酸化(pY)(D)、IRS-1酪氨酸磷酸化(E)、IRS-2酪氨酸磷酸化(F)和Akt Ser473磷酸化(G)。
[0035]图17是XBP-1+/-和XBP-1+/+小鼠中胰岛的特征。从正常饮食(A-D)或HFD(E-H)的XBP-1+/-和XBP-1+/+小鼠获得的胰脏部分中的胰岛形态学、体积以及对胰岛素和高血糖素的免疫组织化学染色。高脂肪饮食的XBP-1+/-和XBP-1+/+小鼠中的葡萄糖刺激的胰岛素分泌。在置于高脂肪饮食下16周的XBP-1+/-和WT小鼠中,检测葡萄糖刺激的胰岛素分泌(I)。给各基因型小鼠腹膜内给予葡萄糖,在指定时间点收集血液样本以测定胰岛素。在这些试验中,在XBP-1+/-岛中未检测到异常,并且在标准条件下基因型之间没有显著差异。在HFD下,XBP-1+/-和XBP-1+/+小鼠都呈现小岛超常增生。这种对HFD的预期响应在基因型之间类似,增生性组分(岛体积>150μM)在XBP-1+/-中占所有岛的40%,而在HFD下的WT小鼠中占所有岛的43%。在测定HFD下的XBP-1+/-和WT小鼠中葡萄糖刺激的胰岛素分泌的各试验中,XBP-1+/-小鼠对葡萄糖的响应比胰岛素分泌响应更强,其有效地消除它们显型下分离的岛的缺陷。因此,这些数据表明XBP-1+/-小鼠的显型不能通过缺陷性岛及甚至HFD16周后来解释,所述各岛在各显型之间未呈现差别。
[0036]图18显示XBP-1+/-小鼠中ER应力和胰岛素受体信号。在高脂肪饮食16周的XBP-1+/-和XBP-1+/+小鼠的肝中,检测PERK磷酸化(p-PERK)(A)、JNK活性(p-c-Jun)(B)和IRS-1 Ser307(IRS-1pSer307)(C)。门静脉输注胰岛素(1U/kg)后,在高脂肪饮食16周的XBP-1+/-和XBP-1+/+小鼠的肝中,检测胰岛素受体(IR)酪氨酸磷酸化(pY)(D)、IRS-1酪氨酸磷酸化(E)、IRS-2酪氨酸磷酸化(F)和Akt Ser473磷酸化(G)。
[0037]图19显示在正常饮食的XBP-1+/-和XBP-1+/+小鼠的肝和脂肪组织中完整的胰岛素受体信号。门静脉输注胰岛素(1U/kg)后,在正常饮食的XBP-1+/-和XBP-1+/+小鼠的肝(A)和脂肪组织(B)中,检测胰岛素受体(IR)酪氨酸磷酸化(pY)、IRS-1酪氨酸磷酸化、IRS-2酪氨酸磷酸化、Akt Ser473磷酸化和它们的总蛋白水平。
[0038]图20显示了高脂肪饮食的XBP-1+/-和XBP-1+/+小鼠的脂肪组织中胰岛素受体信号的降低。(A)门静脉输注胰岛素(1U/kg)后,在给予高脂肪饮食16周的XBP-1+/-和XBP+/+小鼠的脂肪组织中,检测胰岛素受体(IR)酪氨酸磷酸化(pY)、IRS-1酪氨酸磷酸化、IRS-2酪氨酸磷酸化、Akt Ser473磷酸化和它们的总蛋白水平。(B)在高脂肪饮食16周的XBP-1+/-和XBP+/+小鼠的脂肪组织中,进行JNK激酶测试。
[0039]图21显示肥胖小鼠肝组织中JNK活性的增加,以及随后的用PBA处理后JNK活性的归一化(normalization)。
本发明某些优选实施例的详细描述
[0040]已发现内质网(ER)应力对多种疾病的发病机理很重要,所述疾病包括α1-抗-胰蛋白酶缺陷、尿循环障碍、1型糖尿病和囊性纤维化。本发明认为ER应力涉及诸如肥胖症、外周胰岛素抗性、高血糖症和2型糖尿病等疾病的发病机制(Ozcan等,″EndoplasmicReticulum Stress Link Obesity,Insulin Action,and Type 2 Diabetes″Science 306:457-461,2004;通过引用结合到本文中)。基于这种发现,已显示能降低或阻止ER应力的药物可用于治疗肥胖症、胰岛素抗性、高血糖症和2型糖尿病。
[0041]已知能降低或调节ER应力的任何药物都可用于治疗这些代谢性疾病。这些药物可以任何方式发挥减少或防止ER应力的作用。在某些实施方案中,所述药物可增加ER处理蛋白质的能力(例如增加ER陪伴分子的表达、增加后翻译机构的水平)。在其它实施方案中,所述药物能降低ER处理的蛋白质的量(例如降低细胞中产生的蛋白质的总水平,降低ER处理的蛋白质的水平、降低突变蛋白质的水平、降低错折叠蛋白的水平)。然而,其它药物可能引起错折叠/突变蛋白从ER中的释放。所述药物可在细胞中作用,或者所述作用可限定于某些细胞类型(例如分泌细胞、上皮细胞、肝细胞、脂肪细胞、内分泌细胞等)。在某些实施方案中,所述药物尤其可用于降低脂肪细胞中ER应力。在其它实施方案中,所述药物尤其可用于降低肝细胞中ER应力。所述药物可作用在转录、翻译、翻译后或蛋白水平上,以降低或阻止ER应力。
[0042]给予患者有效治疗或预防肥胖症、胰岛素抗性、2型糖尿病、高血糖症或其它相关疾病的量的ER应力调节剂或包括ER应力调节剂的联合药物可以治愈正在治疗的疾病、缓解或降低至少一种正在治疗的疾病的体征和症状、降低疾病的短期后遗症、降低疾病的长期后遗症,或者提供对患者的某些其它的暂时的有益作用。在某些实施方案中,本发明疗法增加胰岛素敏感性。在其它实施方案中,本发明疗法降低血糖水平。在其它实施方案中,本发明疗法预防糖尿病的长期后遗症,包括动脉粥样硬化、糖尿病性视网膜病、外周性神经病等。在某些实施方案中,本发明疗法降低细胞(例如脂肪细胞、肝细胞)中ER应力标记的水平(例如剪接形式的XBP-1、磷酸化状态的PERK、磷酸化的eIF2α、mRNA水平的GRP78/BIP、蛋白水平的GRP78/BIP和JNK活性)。在某些实施方案中,本发明疗法增加胰岛素作用。在其它实施方案中,本发明疗法增加胰岛素受体信号(例如胰岛素受体、IRS-1、IRS-2、akt的磷酸化)。在某些实施方案中,本发明疗法抑制食欲。在其它实施方案中,本发明疗法抑制体重增加或促进体重降低。在某些实施方案中,本发明疗法预防2型糖尿病的发展。在某些实施方案中,本发明的疗法预防肥胖症的发展。在某些实施方案中,本发明治疗方法预防高血糖症的发展。
[0043]所述药物可以是任何类型的化学化合物。所述药物可以是小分子、有机金属复合物、无机化合物、蛋白质、糖蛋白、肽、碳水化合物、脂质或核酸。在某些实施方案中,所述药物为小分子。特别有用的药物为化学陪伴分子,已知其能稳定蛋白质以防止变性,由此保护蛋白质的结构和功能。化学陪伴分子包括甘油、D2O、二甲亚砜(DMSO)、4-苯基丁酸盐(PBA)、牛熊去氧胆酸(TUDCA)、甘氨酸三甲铵乙内酯(甜菜碱)、甘油磷酸胆碱(GPC)、甲胺类和三甲胺N-氧化物(TMAO)。在某些实施方案中,可使用一或多种化学陪伴分子。可将这些化学陪伴分子以剂量范围为10mg/kg/日-10g/kg/日的剂量给药,优选100mg/kg/日-5g/kg/日,更优选500mg/kg/日-3g/kg/日。在某些实施方案中,可将药物以分剂量给予(例如每日2次,每日3次,每日4次,每日5次)。在其它实施方案中,将药物以单日单次剂量给药。
[0044]可将所述药物与一或多种其它药物,尤其是治疗糖尿病、肥胖症或胰岛素抗性中传统使用的药物联合给药。与ER应力调节剂(例如PBA、TUDCA、TMAO或其衍生物)联合使用的药物名单包括在附录A中。该名单包括通用名称、商品名称和制造商。与ER应力降低剂联合使用的示例性药物包括,但不限于抗糖尿病药(例如胰岛素、降血糖药(例如口服降血糖药,如磺酰脲类、甲苯磺丁脲、二甲双胍、氯磺丙脲、醋磺环己脲、妥拉磺脲(tolazamide)、格列本脲等))、抗肥胖症药、抗血脂紊乱药或抗动脉粥样硬化药(例如降胆固醇药(例如HMg-CoA还原酶抑制剂,如洛伐他丁、阿托伐他丁、辛伐他丁、普伐他丁、氟伐他丁等、阿司匹林)、抗肥胖症药(例如食欲抑制药)、维生素、矿物质和抗高血压药。
[0045]在某些实施方案中,可将化学陪伴分子或ER应力调节剂(例如PBA、TUDCA、TMAO或其衍生物)与抗糖尿病药联合使用。抗糖尿病药的实例包括双胍类(例如二甲双胍)、磺酰脲类(例如格列美脲、优降糖、格列本脲、格列吡嗪、格列齐特)、胰岛素和胰岛素类似物(例如赖脯胰岛素(insulin lispro)、甘精胰岛素(insulin glargine)、exubera、AERx胰岛素糖尿病管理系统、AIR吸入胰岛素、oralin、地特胰岛素(insulin detemir)、insulin glulisine)、过氧化物酶体增殖子激活的受体-γ激动剂(例如罗格列酮、匹格列酮、isaglitazone、rivoglitazone、T-131、MBX-102、R-483 CLX-0921)、双重PPAR激动剂和PPAR pan激动剂(例如BMS-398585、tesaglitazar、muraglitazar、naveglitazar、TAK-559、netoglitazone、GW-677594、AVE-0847、LY-929、ONO-5129)、联合疗法(例如二甲双胍/格列苯脲、二甲双胍/罗格列酮、二甲双胍/格列吡嗪)、氯茴苯酸类(例如瑞格列奈、那格列奈)、α-葡糖苷酶抑制剂(例如阿卡玻糖、米格列醇、伏格列波糖)、高血糖素样肽-1(GLP-I)类似物和激动剂(例如Exenatide、ExenatideLAR、Liraglutide、CJC-1131、AVE-0010、BIM-51077、NN-2501、SUN-E7001)、二肽基肽酶IV(DPP-IV)抑制剂(例如LAF-237、MK-431(Merck and Co)、PSN-9301(Probiodrug Prosidion)、815541(GlaxoSmithKline-Tanabe)、823093(GlaxoSmithKline)、825964(GlaxoSmithKline)、BMS-477118)、胰脂肪酶抑制剂(例如奥利斯特)、Na+-葡糖共转运蛋白(SGLT)抑制剂(例如T-1095(Tanabe-J&J)、AVE-2268、869682(GlaxoSmithKline-Kissei))和糊精类似物(例如普兰林肽)。
[0046]在其它实施方案中,可将化学陪伴分子或ER应力调节剂(例如PBA、TUDCA、TMAO或其衍生物)与抗肥胖症药联合使用。抗肥胖症药的实例包括胰脂肪酶抑制剂(例如奥利斯特)、5-羟色胺和去甲肾上腺素再摄取抑制剂(例如西布曲明)、去甲肾上腺素能减食欲剂(例如苯丁胺、氯苯咪吲哚)、外周作用药(例如ATL-962(Alizyme)、HMR-1426(Aventis)、GI-181771(GlaxoSmithKline))、中枢作用药(例如重组人睫状节神经细胞营养因子、利莫那班(SR-141716)(Sanofi-Synthélabo)、BVT-933(GlaxoSmithKline/Biovitrum)、安非他酮(Bupropion)SR(GlaxoSmithKline)、P-57(Phytopharm))、热量生成剂(例如TAK-677(AJ-9677)(Dainippon/Takeda))、大麻素CB1拮抗剂(例如acomplia、SLV319)、缩胆囊素(CCK)激动剂(例如GI 181771(GSK))、脂质代谢调节剂(例如AOD9604(MonashUniversity/Metabolic Pharmaceuti-cals)、高血糖素样肽1激动剂(例如AC137(Amylin))、瘦素激动剂(例如第二代瘦素(Amgen)、β-3肾上腺素能激动剂(例如SR 58611(Sanofi-Aventis)、CP 331684(Pfizer)、LY377604(Eli Lilly)、n5984(Nisshin Kyorin Pharmaceutical))、肽激素(例如肽YY[3-36](Nastech))、CNS调节剂(例如S2367(Shionogi & Co.Ltd.))、神经细胞营养因子(例如peg axokine)和5HT2C 5-羟色胺受体激动剂(例如APD356)。其它抗肥胖症药包括盐酸脱氧麻黄碱、1426(Sanofi-Aventis)、1954(Sanofi-Aventis)、c-2624(Merck & Co)、c-5093(Merck & Co)和T71(Tularik)。
[0047]在另外的其它实施方案中,可将化学陪伴分子或ER应力调节剂(例如PBA、TUDCA、TMAO或其衍生物)与抗血脂紊乱药或抗动脉粥样硬化药联合使用。抗血脂紊乱药或抗动脉粥样硬化药的实例包括HMG-CoA还原酶抑制剂(例如阿伐他汀、普伐他丁、辛伐他汀、洛伐他丁、氟伐他丁、西立伐他汀、罗苏伐他汀、匹伐他汀)、贝特类(fibrates)(例如环丙贝特、苯扎贝特、氯贝特、非诺贝特、吉非贝齐(gemfibrozil)、胆汁酸多价螯合剂(例如考来烯胺、考来替泊、考来维仑)、烟酸(速释和控释)、抗血小板剂(例如阿司匹林、氯吡格雷(clopidogrel)、噻氯匹定)、血管紧张素转换酶(ACE)抑制剂(例如雷米普利、伊拉普利)、血管紧缩素II受体拮抗剂(例如氯沙坦钾)、脂酰辅酶A胆固醇乙酰转移酶(ACAT)抑制剂(例如阿伐麦布(avasimibe)、eflucimibe、CS-505(Sankyo and Kyoto)、SMP-797(Sumito))、胆固醇吸收抑制剂(例如依泽替米贝(ezetimibe)、帕马苷(pamaqueside))、烟酸衍生物(例如烟酸)、胆固醇酯转移蛋白(CETP)抑制剂(例如CP-529414(Pfizer)、JTT-705(Japan Tobacco)、CETi-I、torcetrapib)、微粒体甘油三酯转移蛋白(MTTP)抑制剂(例如英普他派(implitapide)、R-103757、CP-346086(Pfizer))、其它胆固醇调节剂(例如NO-1886(Otsuka/TAP Pharmaceutical)、CI-1027(Pfizer)、WAY-135433(Wyeth-Ayerst))、胆汁酸调节剂(例如GT1 02-279(GelTex/Sankyo)、HBS-107(Hisamitsu/Banyu)、BTG-511(BritishTechnology Group)、BARI-1453(Aventis)、S-8921(Shionogi)、SD-5613(Pfizer),AZD-7806(AstraZeneca))、过氧化物酶体增殖活化受体(PPAR)激动剂(例如Tesaglitazar(AZ-242)(AstraZeneca)、Netoglitazone(MCC-555)(Mitsubishi/Johnson & Johnson)、GW-409544(LigandPharmaceuticals/GlaxoSmithKline),GW-501516(LigandPharmaceuticals/GlaxoSmithKline)、LY-929(Ligand Pharmaceuticals andEli Lilly)、LY-465608(Ligand Pharmaceuticals and Eli Lilly)、LY-518674(Ligand Pharmaceuticals and Eli Lilly)、MK-767(Merck and Kyorin))、基于基因的疗法(例如AdGVVEGF 121.10(GenVec)、ApoAl(UCBPharma/Groupe Fournier)、EG-004(Trinam)(Ark Therapeutics)、ATP-结合盒式转运蛋白-Al(ABCAl)(CV Therapeutics/Incyte,Aventis,Xenon))、复合血管保护剂(例如AGI-1067(Atherogenics))、BO-653(Chugai)、糖蛋白Ilb/IIIa抑制剂(例如罗昔非班(Roxifiban)(Bristol-Myers Squibb)、更托非班(Gantofiban)(Yamanouchi)、Cromafiban(Millennium Pharmaceuti-cals))、阿司匹林及其类似物(例如控释阿司匹林制剂(asacard)、缓释阿司匹林、帕米格雷(pamicogrel))、联合疗法(例如烟酸/洛伐他丁、阿洛地平(amlodipine)/阿托伐他丁、辛伐他丁/依泽替米贝)、IBAT抑制剂(例如S-89-21(Shionogi))、角鲨烯合酶抑制剂(例如BMS-188494 I(Bristol-Myers Squibb)、CP-210172(Pfizer)、CP-295697(Pfizer)、CP-294838(Pfizer)、TAK-475(Takeda))、单核细胞化学诱引蛋白(MCP-I)抑制剂(例如RS-504393(RocheBioscie-nce)、其它MCP-I抑制剂(GlaxoSmithKline,Teijin和Bristol-Myers Squibb))、肝X受体激动剂(例如GW-3965(GlaxoSmithKline),TU-0901317(Tularik))和其它新途径(例如MBX-102(Metabolex),NO-1886(Otsuka)、Gemcabene(Pfizer))。
[0048]在另外的其它实施方案中,可将化学陪伴分子或ER应力调节剂(例如PBA、TUDCA、TMAO或其衍生物)与抗高血压药联合使用。抗高血压药的实例包括利尿剂(例如氯噻酮、美扎拉宗、吲达帕胺、布美他尼、依他尼酸、呋塞米、托塞米(torsemide)、盐酸阿米洛利、螺内酯、氨苯蝶啶)、α-阻滞剂(例如甲磺酸喹唑嗪(doxazosin)、盐酸哌唑嗪、盐酸特拉唑嗪(terazosin))、β-阻滞剂(例如醋丁洛尔、阿替洛尔、倍他洛尔、富马酸比索洛尔(bisoprolol)、盐酸卡替洛尔、酒石酸美托洛尔(metoprolol)、琥珀酸美托洛尔、纳多洛尔、硫酸喷布洛尔、吲哚洛尔、盐酸普萘洛尔、马来酸噻吗洛尔、卡维地洛(carvedilol))、Ca+2通道阻滞剂(例如苯磺酸氨氯地平、非洛地平、依拉地平(isradipine)、尼卡地平、硝苯地平、尼索地平(nisoldipine)、盐酸地尔硫、盐酸维拉帕米、阿折地平(azelnidipine)、普拉地平(pranidipine)、分级(graded)地尔硫制剂、(s)-氨氯地平(amlodipine)、氯维地平(clevidipine))、血管紧张素转换酶(ACE)抑制剂(例如盐酸贝那普利(benazepril)、卡托普利、马来酸依那普利、福辛普利(fosinopril)钠、赖诺普利(lisinopril)、莫昔普利(moexipril)、哌道普利(perindopril)、盐酸喹那普利(quinapril)、雷米普利、群多普利)、血管紧张素II(AT-II)拮抗剂(例如氯沙坦(losartan)、缬沙坦(valsartan)、依贝沙坦(irbesartan)、坎地沙坦(candesartan)、替米沙坦(telnisartan)、依普沙坦(eprosartan)、奥美沙坦(olmesarta)、YM-358(Yamanouchi))、血管肽酶抑制剂(例如奥马曲拉(omapatrilat)、gemopatrilat、法西多曲(fasidotril)、山帕曲拉(sampatrilat)、AVE 7688(Aventis)、M100240(Aventis)、Z13752A(Zambon/GSK)、796406(Zambon/GSK))、双重中性肽链内切酶和内皮素(enotheline)转化酶(NEP/ECE)抑制剂(例如SLV306(Solvay)、NEP抑制剂(例如依卡曲尔(ecadotril))、醛固酮拮抗剂(例如依普利酮(eplerenone))、肾素抑制剂(例如阿利吉仑(Aliskiren)(Novartis)、SPP 500(Roche/Speedel)、SPP600(Speedel)、SPP 800(Locus/Speedel))、血管紧张素疫苗(例如PMD-3117(Protherics))、ACE/NEP抑制剂(例如AVE-7688(Aventis)、GW-660511(ZambonSpA))、Na+/K+ATP酶调节剂(例如PST-2238(Prassis-Sigma-Tau)、内皮素拮抗剂(例如PD-156707(Pfizer))、血管扩张剂(例如NCX-4016(NicOx)、LP-805(Pola/Wyeth))、天然肽(例如BDNP(MayoFounda-tion))、血管紧张素受体阻滞剂(ARBs)(例如pratosartan)、ACE交联破碎剂(例如alagebrium chloride)、内皮素受体激动剂(例如替唑生坦(tezosentan)(Genentech)、ambrisentan(Myogen)、BMS 193884(BMS)、西他生坦(Encysive Pharmaceuticals)、SPP301(Roche/Speedel)、达卢生坦(darusentan)(Myogen/Abbott)、J104132(Banyu/Merck & Co.)、TBC3711(Encysive Pharmaceuticals)、SB 234551(GSK/Shionogi))、联合疗法(例如盐酸贝那普利/氢氯噻嗪、卡托普利/氢氯噻嗪、马来酸伊拉普利/氢氯噻嗪、赖诺普利/氢氯噻嗪、氯沙坦/氢氯噻嗪、阿替洛尔/氯噻酮、富马酸比索洛尔/氢氯噻嗪、酒石酸美多洛尔/氢氯噻嗪、氨氯地平苯磺酸盐/盐酸贝那普利、费乐地平/马来酸依那普利、盐酸维拉帕米/群多普利、乐卡地平和伊拉普利、奥美沙坦/氢氯噻嗪、依普沙坦/氢氯噻嗪、氨氯地平苯磺酸盐/阿伐他汀、尼群地平/伊拉普利)和MC4232(University of Manitoba/Medicure)。
[0049]在某些实施方案中,可将化学陪伴分子或ER应力调节剂(例如PBA、TUDCA、TMAO或其衍生物)与维生素、矿物质或其它营养补充剂联合使用。
[0050]在某些实施方案中,将ER应力调节剂(如PBA、TUDCA、TMAO或其衍生物)以亚-最适量(例如当在不存在第二种药物下给药时,不能呈现可检测的治疗益处的量)给药。在这些情况下,与另一药物联合,这种亚-最适量的ER应力调节剂的给药能产生协同作用。ER应力调节剂与其它药物一起作用产生治疗益处。在其它实施方案中,将其它药物(即不是ER应力调节剂)以亚-最适剂量给药。在与ER应力调节剂联合用药时,联合用药呈现治疗效果。在另外的其它实施方案中,将ER应力调节剂和其它药物都以亚治疗剂量给药,且当联合产生治疗效果时。其它药物的剂量可以低于本领域的那些标准剂量。
[0051]抗糖尿病药、抗肥胖症药、抗血脂紊乱药或抗动脉粥样硬化药、维生素、矿物质和抗高血压药(以上所列)的给药剂量、给药途径、剂型等都是本领域已知的。治疗医生或卫生保健专家可以查阅诸如Physician′s Desk Reference(59th Ed.,2005)或Mosby′s DrugConsult and Interacations(2005)的有关信息。应清楚治疗医生将根据其专业判断来确定针对具体患者的剂量安排。
[0052]本发明提供治疗2型糖尿病、胰岛素抗性、肥胖症和其它相关症状的体系和方法,它提供一种比单独给予ER应力形式或其它治疗形式更好的治疗方式。在某些实施方案中,治疗效果更高。在某些实施方案中,联合用药具有协同作用。在其它实施方案中,联合疗法具有累加效应。联合治疗方案的给药可降低或甚至避免某些不需要的或有害的副作用。在其它实施方案中,可将联合给药的各药物以较低的剂量给予,以较低的频率给予或者以较低频率和较低的剂量给药。因此,具有上述益处的联合疗法可增加患者的顺从性、提供治疗和/或降低不需要的或有害的副作用。
[0053]在某些实施方案中,可将化学陪伴分子(例如PBA、TUDCA、TMAO或其衍生物)与降血糖药联合使用。例如,可将胰岛素、高血糖素、双胍降血糖剂(例如二甲双胍、苯乙双胍或丁二胍)、噻唑烷二酮降血糖剂(例如环格列酮(ciglitazone)、匹格列酮)、磺酰脲类降血糖剂(例如甲苯磺丁脲、氯磺丙脲、醋磺环己脲、妥拉磺脲、格列本脲、格列吡嗪或格列齐特)、α-葡糖苷酶抑制剂(例如阿卡玻糖)或者二氮嗪与甘油、D2O、二甲亚砜(DMSO)、4-苯基丁酸盐(PBA)、牛熊去氧胆酸(TUDCA)、甘氨酸三甲铵乙内酯(甜菜碱)、甘油磷酸胆碱(GPC)、甲胺类和三甲胺N-氧化物(TMAO)联合使用。某些具体的示例性联合疗法包括胰岛素和PBA、胰岛素和TUDCA、胰岛素和甜菜碱、胰岛素和GPC、胰岛素和TMAO、二甲双胍和PBA、二甲双胍和TUDCA、二甲双胍和甜菜碱、二甲双胍和GPC、二甲双胍和TMAO、噻唑烷二酮降血糖剂和PBA、噻唑烷二酮降血糖剂和TUDCA、噻唑烷二酮降血糖剂和甜菜碱、噻唑烷二酮降血糖剂和GPC、噻唑烷二酮降血糖剂和TMAO。在某些实施方案中,用于治疗或预防糖尿病、胰岛素抗性、高血糖症或2型糖尿病的联合用药是4-苯基丁酸盐(PBA)和二甲双胍。对于联合疗法来讲,无论它们是化学陪伴分子的组合、ER应力调节剂的组合或者是化学陪伴分子/ER应力调节剂与其它诸如降血糖药的组合,都可将各药物同时或连续给药。在某些实施方案中,将化学陪伴分子或ER应力调节剂在其它药物之前给药。在其它实施方案中,将化学陪伴分子或ER应力调节剂在其它药物之后给药。
[0054]在某些实施方案中,显示降低ER应力的小分子药物包括4-苯基丁酸盐(PBA)、牛熊去氧胆酸(TUDCA)和三甲胺N-氧化物(TMAO)。PBA目前用于治疗α1-抗胰蛋白酶缺陷、尿循环障碍和囊性纤维化。PBA、TUDCA或TMAO的衍生物、盐(例如钠、钾、镁、铵等)、前药、酯、异构体和立体异构体也可用于治疗肥胖症、高血糖症、2型糖尿病和胰岛素抗性。虽然不希望受任何具体理论的束缚,但现认为这些化合物通过使ER更好地处理错折叠和/或ER处理突变蛋白而发挥作用。
[0055]在某些实施方案中,用于本发明的4-苯基丁酸盐的衍生物,或其药学上可接受的盐或其混合物具有下式:
其中n是1或2;
R0是芳基、杂芳基或苯氧基,其中所述芳基、杂芳基和苯氧基为未取代的或独立地被一或多个卤素、羟基或低级烷基(C1-C6)基团取代;
R1和R2独立为H、低级烷氧基、羟基、低级烷基或卤素;
R3和R4独立为H、低级烷基、低级烷氧基或卤素。
在某些实施方案中,R0是取代的或未取代的苯基环。在某些实施方案中,R0是未取代的苯基环。在其它实施方案中,R0是单取代的苯环。在另一些其它实施方案中,R0是双取代的苯环。在又一些其它实施方案中,R0是三取代的苯环。在某些实施方案中,R0是被1、2、3或4个卤原子取代的苯环。在某些实施方案中,R0是取代的或未取代的杂芳基环。在某些实施方案中,R0是萘基环。在某些实施方案中,R0是5或6元环,优选6元环。在某些实施方案中,R1和R2都是H。在某些实施方案中,n是1。在其它实施方案中,n是2。在某些实施方案中,R3和R4都是H。在其它实施方案中,R3或R4至少一个是H。在某些实施方案中,所用的化合物为盐的形式(钠盐、钾盐、镁盐、铵盐等)。本发明使用的其它衍生物在通过引用结合到本文中的美国专利5,710,178中描述。4-苯基丁酸盐或其衍生物可由商业来源获得或者通过全合成或半合成制备。
[0056]在某些实施方案中,本发明所用的TUDCA衍生物是具有下式的化合物或其药学上可接受的盐或衍生物:
其中R是-H或C1-C4烷基;
R1是-CH2-SO3R3以及R2是-H;或者R1是-COOH以及R2是-CH2-CH2-CONH2、-CH2-CONH2、-CH2-CH2-SCH3或-CH2-S-CH2-COOH;以及
R3是-H或碱性氨基酸残基。
在某些实施方案中,所述衍生物的立体化学根据以下结构所示定义:
在某些实施方案中,R是H。在其它实施方案中,R是甲基、乙基、正丙基、异丙基、正丁基、异丁基或叔丁基,优选为甲基。在某些实施方案中,R1或R2是氢。在某些实施方案中,R1是-CH2-SO3R3和R2是-H。在其它实施方案中,R1是-COOH和R2是-CH2-CH2-CONH2、-CH2-CONH2、-CH2-CH2-SCH3或-CH2-S-CH2-COOH。在某些实施方案中,R3是氢。在某些实施方案中,R3是赖氨酸、精氨酸、鸟氨酸或组氨酸。TUDCA和熊脱氧胆酸的衍生物可由商业来源获得、由全合成制备或者半合成获得。在某些实施方案中,所述衍生物可如美国专利5,550,421和4,865,765中所述的方法经半合成制备,所述各专利通过引用结合到本文中。
[0057]在某些实施方案中,本发明可用的三甲胺N-氧化物的衍生物为下式化合物其药学上可接受的盐或其混合物:
其中
R1、R2和R3独立地为氢、卤素或低级C1-C6烷基。在某些实施方案中,R1、R2和R3相同。在其它实施方案中,R1、R2和R3至少一个是不同的。在另一些其它各实施方案中,R1、R2和R3都不相同。在某些实施方案中,R1、R2和R3独立为氢或低级C1-C6烷基。在另一些其它各实施方案中,R1、R2和R3独立为低级C1-C6烷基。在另一些其它各实施方案中,R1、R2和R3独立地为甲基、乙基或丙基。在某些实施方案中,R1、R2和R3为乙基。TMAO的衍生物可由商业来源获得或者可通过全合成或半合成制备。
[0058]在其它实施方案中,所述药物为核酸,例如抑制的RNA,如siRNA。在其它实施方案中,所述药物为蛋白质,例如抗体或抗体片段。在另一些其它实施方案中,所述药物为肽。
[0059]在治疗患有肥胖症、外周胰岛素抗性、高血糖症或2型糖尿病的动物中,可通过能获得所要求的生物学结果的任何途径,给予患者治疗有效量的药物。可使用的任何途径包括口服、非肠道、静脉内、动脉内、肌内、皮下、直肠、阴道、经皮、腹膜内和鞘内途径。在某些实施方案中,经非肠道给药。在其它实施方案中,口服进行给药。
[0060]在使用PBA、TUDCA或TMAO中,优选口服给药;但是,还可使用以上所列的任何给药途径。在某些实施方案中,可将PBA、TUDCA或TMAO非肠道给药。PBA的给药剂量范围为10mg/kg/日-5g/kg/日,优选100mg/kg/日-1g/kg/日,更优选250mg/kg/日-750mg/kg/日。TUDCA的给药剂量范围为10mg/kg/日至5g/kg/日,优选100mg/kg/日至1g/kg/日,更优选250mg/kg/日至750mg/kg/日。TMAO的给药剂量范围为10g/kg/日至0.1g/kg/日,优选5g/kg/日至0.5g/kg/日,更优选2.5g/kg/日至500mg/kg/日。在某些实施方案中,可将药物以分剂量给予(例如每日2次、每日3次,每日4次、每日5次)。在其它实施方案中,将药物以每日单剂量给药。
药用组合物
[0061]本发明的药用组合物和本发明药用组合物的用途可包括药学上可接受的赋形剂或载体。本文所用的术语“药学上可接受的载体”指无毒、惰性固体、半固体或液体填充剂、稀释剂、包囊材料或任何类型的制剂辅助剂。用作药学上可接受的载体的物质的某些实例是糖,如乳糖、葡萄糖和蔗糖;淀粉,如玉米淀粉和马铃薯淀粉;纤维素及其衍生物,如羧甲基纤维素钠、乙基纤维素和乙酸纤维素;粉末化黄耆胶;麦芽、明胶;滑石粉;赋形剂如可可脂和栓剂蜡;油如花生油、棉籽油、红花油、芝麻油、橄榄油、玉米油和大豆油;二醇类,如丙二醇;酯类,如油酸乙酯和月桂酸乙酯;琼脂;除污剂,如吐温80;缓冲剂,如氢氧化镁和氢氧化铝;藻酸;无热原水;等渗盐水;林格氏溶液;乙醇;人工脑脊髓液(CSF)和磷酸盐缓冲溶液,以及其它非毒性可配伍的润滑剂,如十二烷基硫酸钠和硬脂酸镁,以及着色剂、释放剂、包衣剂、甜味剂、矫味剂和香料,根据制剂者的判断,防腐剂和抗菌剂也可存在于组合物中。可将本发明的药用组合物经以下途径给予人和/或动物:口服、直肠、非肠道、脑池内、阴道内、鼻腔内、腹膜内、局部(如通过散剂、霜剂、软膏剂或滴剂)、经皮、皮下、颊内或者口腔或鼻内喷雾剂。
[0062]注射制剂,如无菌注射水性或油性混悬剂,可根据已知的技术,采用适当的分散剂或湿润剂以及悬浮剂制备。无菌注射剂也可以是一种在无毒性非肠道上可接受的稀释剂或溶剂中的无菌注射溶液、混悬液或乳液,如1,3-丁二醇中的溶液。可使用的所述可接受的介质和溶剂是水、林格氏溶液(U.S.P.)和等渗氯化钠溶液。另外,一般可将无菌的不挥发性油类用作溶剂或悬浮介质。为此,可使用任何温和的不挥发性油,包括合成的单-或二-甘油酯。另外,在制备注射剂中,可使用脂肪酸如油酸。
[0063]可通过诸如下列方法将注射剂灭菌:通过截菌滤器过滤、或者通过将灭菌剂加入到无菌固体组合物中,该组合物在使用前将其溶解或分散于无菌水和其它无菌注射介质中来应用。
[0064]可将本发明的药用组合物与其它用于治疗糖尿病、胰岛素抗性或肥胖症的药物一起以药剂盒的形式提供。所述药剂盒可包括供医师和/或患者使用的说明书,该说明书可包括给药剂量信息、安全信息、副作用目录、药物的化学式、作用机理等。在某些实施方案中,药剂盒可包括供给予药用组合物的物质。例如,药剂盒可包括供注射剂给药的注射器、针头、酒精交换物等。在某些实施方案中,当药剂盒中提供两种或两种以上的药物时,可将各活性组分制成各自单一制剂或配制在一起。例如,药剂盒可包括两个容器,第一个容器装有ER应力调节剂(例如PBA、TUDCA、TMAO或其衍生物),第二个容器装有用于治疗2型糖尿病、胰岛素抗性、高血糖症、肥胖症或相关疾病的第二种药物(例如如上所述的抗糖尿病药、抗肥胖症药、抗血脂紊乱药或抗动脉粥样硬化药、维生素、矿物质和抗高血压药)。在某些实施方案中,可将各活性组分各自制成制剂。在其它实施方案中,可将各活性组分配制在一起。
ER应力降低剂的筛选
[0065]如本发明所示,已证明ER应力可作为治疗包括肥胖症、2型糖尿病、胰岛素抗性和高血糖症的各种疾病的靶标。ER应力的标记也被鉴定出来。由于对降低或预防ER应力的新的药物的需求,所以需要鉴定或筛选ER应力调节剂的方法。
[0066]在某些实施方案中,将化合物或化合物收集物进行分析测定,以鉴定能够在体内或体外(优选体内)降低或调节ER应力的化合物。这些化合物可以是任何类型的化学化合物,包括小分子、蛋白质、肽、多核苷酸、碳水化合物、脂质等。在某些实施方案中,使用本发明的方法筛选化合物的组合。这些收集物可以是过去的源自制药公司的化合物的库存。所述收集物也可以是化学化合物的组合库。所述收集物可包括至少5、10、50、100、500、1000、10000、100000或1000000个化合物。
[0067]可将所述化合物与细胞接触。细胞可以是具有内质网的任何类型的细胞。细胞可以是动物细胞、植物细胞或真菌细胞。在某些实施方案中,优选哺乳动物细胞,尤其是人体细胞。这些细胞可源自任何器官系统。在某些实施方案中,优选源自脂肪组织和肝组织的细胞。
[0068]在筛选降低ER应力的药物中,将实验化合物与已体验ER应力的细胞接触。细胞中的ER应力可通过本领域已知的任何技术引起。例如,ER应力可归因于细胞中遗传变更(例如XBP-1突变)或者用已知能引发ER应力的化学化合物处理(例如衣霉素、毒胡萝卜素)。在加入实验化合物之前和之后测定ER应力标记的水平,以确定化合物是否降低ER应力。本发明方法中可测定的ER应力的标记包括剪接形式的XBP-1、磷酸化状态的PERK(如Thr980)、磷酸化的eIF2α(如Ser51)、mRNA和/或蛋白水平的GRP78/BIP和JNK活性。在某些实施方案中,可测定一种ER标记。在其它实施方案中,可测定2、3、4、5、6或更多种ER应力标记的组合的水平。将能降低ER应力标记水平至少约10%、20%、30%、40%、50%、60%、70%、80%、90%、95%、99%或100%,优选至少25%,更优选至少50%的实验化合物认定为能用于临床上评估ER应力的降低剂。本领域技术人员将清楚,可在各种浓度以及在各种条件下(例如各种细胞类型、各种原因的ER应力(遗传性对化学性)、各种制剂)测试实验化合物。
[0069]在另一方面,本发明提供一种鉴别能预防ER应力的化合物的方法。在筛选预防ER应力的化合物中,细胞在与试验化合物接触之前未经历ER应力。使细胞与试验化合物接触之后,向细胞中加入已知能引起ER应力的药物,然后测定至少一种ER标记的水平,以确定化合物是否能预防ER应力。如本领域技术人员清楚的一样,可在各种浓度和各种条件下测定试验化合物。
[0070]可将通过本发明方法鉴定的药物进一步进行体内毒性、药代动力学性质、用途等试验,以使得可将它们制成制剂并在临床上用于治疗肥胖症、2型糖尿病、高血糖症和胰岛素抗性。还可发现所鉴定的药物在治疗与ER应力有关的其它疾病中的用途。
诊断与ER应力有关的病症
[0071]各种ER应力标记的鉴定能诊断与ER应力有关的病症并能筛选面临发生与ER应力有关的病症的患者。已显示肥胖症、高血糖症、2型糖尿病和胰岛素抗性都与ER应力有关。因此,测定患者中ER应力标记的水平即考虑到确定是否患者面临任何这些疾病的风险。可使用测定ER应力标记的水平来确定发生与ER应力有关的任何病症(例如囊性纤维化、阿尔茨海默氏病)的风险。
[0072]已被鉴定的ER应力标记包括剪接形式的XBP-1、磷酸化状态的PERK、磷酸化的eIF2α、mRNA水平的GRP78/BIP、蛋白水平的GRP78/BIP和JNK活性。可使用本领域已知的测定mRNA水平、蛋白水平、蛋白活性或磷酸化状态的任何技术测定这些ER应力标记。测定ER应力标记的示例性技术包括蛋白质印迹分析、RNA印迹分析、免疫测定法、PCR定量分析和酶活性试验(这些技术的更详细说明请参见Ausubel等Current Protocols in Molecular Biology(John Wiley & Sons,Inc.,New York,1999);Molecular Cloning:ALaboratory Manual,2nd Ed.,ed.by Sambrook,Fritsch,and Maniatis(Cold Spring Harbor Laboratory Press:1989);各自通过引用结合到本文中)。
[0073]在测定患者是否面临与ER应力有关的病症的风险时,可测定1、2、3、4、5或6种ER应力标记的水平。在某些实施方案中,仅测定一种ER应力标记的水平。在其它实施方案中,测定至少两种ER标记的水平。在另外的其它实施方案中,测定至少三种ER应力标记的水平。
[0074]一般地,如果所测定的ER应力标记水平比正常对照组增加,那么即认为所测定的患者面临胰岛素抗性、肥胖症、高血糖症或2型糖尿病的风险。然后将所鉴定的患者进行进一步的测试,可以开始治疗,或者可注意患者与胰岛素抗性、肥胖症、高血糖症或2型糖尿病的有关的症状和体征的进一步发展。下一行动过程一般在与患者商量后由患者的保健提供者确定。
[0075]可测定患者体内的任何细胞的ER应力标记的水平。优选将细胞与所试验的病症联系起来。例如在测定诸如肥胖症、2型糖尿病、胰岛素抗性或高血糖症的病症中,可使用肝细胞和脂肪细胞。在某些实施方案中,使用肝细胞。在其它实施方案中,所述细胞为脂肪细胞。在肝细胞情况下,细胞可通过肝脏活组织检查从患者中获得。脂肪细胞可通过患者的活组织检查获得。
[0076]本发明还提供用于测定患者各种ER应力标记水平的试剂盒和系统。试剂盒包括引发剂、杂交探针、多核苷酸、抗体、抗体片段、凝胶、缓冲剂、酶底物、ATP或其它核苷酸、用于从患者中获得细胞或活组织检查的工具、说明书、软件等。一般可将这些用于进行诊断方法的材料包装,以供医生、科学家、病理学家、护士、实验室技术人员或保健专家使用。
[0077]本发明的这些和其它方面通过下列实施例被进一步解释说明,所述实施例用于说明本发明的某些具体的实施方案,但并不构成对本发明范围的限定,本发明范围通过权利要求书界定。
实施例
实施例1:内质网应力与肥胖症、胰岛素作用以及2型糖尿病的联系肥胖症中ER应力的诱导作用
[0078]为检测ER应力在肥胖症中是否增加,我们在小鼠肥胖的饮食性(高脂肪饮食诱发)和遗传性(ob/ob)模型中研究了ER应力的几种分子指示器的表达模式。胰ER激酶或PKR样激酶(PERK)是ER跨膜蛋白激酶,其在响应于ER应力下使翻译起始因子2的α亚单位(eIF2α)磷酸化(Shi等,MoI.Cell Biol.18,7499(1998);Harding等,Nature 397,271(Jan 21,1999);其各自通过引用结合到本文中)。因此,PERK和eIF2α的磷酸化状态是ER应力存在的关键指示器。我们使用磷酸特异性抗体测定PERK(Thr980)和eIF2α(Ser51)的磷酸化状态。这些实验表明:与瘦的小鼠对照组比较,肥胖小鼠肝提取物中PERK和eIF2α磷酸化增加(图1A和1B)。ER应力还导致JNK活性。与早期发现(J.Hirosumi等,Nature 420,333(2002);通过引用结合到本文中)一致的是,通过c-Jun磷酸化指示的总JNK活性也在肥胖小鼠中极大地增高(图1A和1B)。
[0079]78kDa葡萄糖调节/结合Ig蛋白(GRP78/BIP)是一种其表达随ER应力增加的ER陪伴分子。与匹配的瘦对照小鼠相比,肥胖小鼠肝组织中GRP78/BIP mRNA水平升高(图1C和ID)。由于GRP78表达对葡萄糖做迅即响应,因此我们检测这种上调节是否简单地由于葡萄糖水平增加。用高水平葡萄糖处理培养的大鼠Fao肝细胞导致GRP78表达降低(图9A)。类似的GRP78水平在高血糖症小鼠模型中不增加(图9B),其表明肥胖症中的调节不可能只与血糖有关。
[0080]我们还对脂肪和肌肉组织,即对代谢体内平衡、肥胖症中ER应力的指征重要的部位进行了试验。与肝类似,与瘦的对照组比较,在肥胖动物的脂肪组织中PERK磷酸化、JNK活性和GRP78表达都明显增加(图10A-C)。但是,在肥胖动物的肌肉组织中没有出现明显的ER应力指征(数据未显示)。综上所述,这些结果表明肥胖症与主要在肝和脂肪组织中的ER应力的诱导有关。
ER应力抑制肝细胞中的胰岛素作用
[0081]为研究ER应力是否干扰胰岛素作用,我们用通常用于诱导ER应力的试剂衣霉素和毒胡萝卜素预处理Fao肝细胞。衣霉素明显降低IRS-1的胰岛素刺激的酪氨酸磷酸化(图11A和11B),并且还使IRS-1的分子量增加(图11A)。IRS-1是胰岛素受体酪氨酸激酶的底物,而IRS-1的丝氨酸磷酸化,尤其通过JNK介导,能降低胰岛素受体信号(Hirosumi等,Nature 420:333(2002);通过引用结合到本文中)。用衣霉素预处理的Fao细胞使得IRS-1的丝氨酸磷酸化明显增加(图11A和11B)。衣霉素预处理还抑制胰岛素诱导的Akt磷酸化,胰岛素受体信号途径中更为远侧的事件(图11A和11B)。类似的结果也在用毒胡萝卜素处理后得到(图12A),其与细胞钙水平中的改变无关(图12B)。
[0082]然后,我们检测了JNK对IRS-1丝氨酸磷酸化的作用以及ER应力对胰岛素刺激的IRS-1酪氨酸磷酸化的抑制作用(图11C和11D)。用合成抑制剂SP600125抑制JNK活性逆转ER应力诱导的IRS-1的丝氨酸磷酸化(图11C和11D)。用源于JNK结合蛋白JIP(Barr等,J.Biol.Chem.277:10987(2002);通过引用结合到本文中)的高特异性抑制肽预处理Fao细胞也完全保护暴露于衣霉素的细胞中的胰岛素受体信号(图11E和11F)。用合成JNK抑制剂SP600125也得到类似的结果(数据未显示)。这些结果表明ER应力促进IRS-1的JNK-依赖性丝氨酸磷酸化,然后依次抑制胰岛素受体信号。
IRE-I在胰岛素受体信号中发挥关键作用
[0083]在ER应力存在下,需要激酶-1α(IRE-1α)的肌醇的磷酸化的增高导致TNF-α受体-相关因子2(TRAF2)蛋白的复原并激活JNK(Urano等,Science 287:664(2000);通过引用结合到本文中)。为确定ER应力诱发的胰岛素抗性是否依赖完整的IRE-1α,我们在暴露于衣霉素的IRE-1α-/-和野型(WT)成纤维细胞中测定JNK活性、IRS-1丝氨酸磷酸化以及胰岛素受体信号。在WT但非IRE-1α-/-细胞中,衣霉素诱导的ER应力导致强烈的JNK激活(图11G)。衣霉素还刺激WT中(图11G)但非IRE-1α-/-成纤维细胞(图11E)中的Ser307残基上的磷酸化。重要的是,衣霉素在WT细胞中抑制IRS-1的胰岛素刺激的酪氨酸磷酸化,然而在IRE-1α-/-细胞中未检测到这种结果(图11H)。尽管总IRS-1蛋白水平较低,但IRS-1的胰岛素刺激的酪氨酸磷酸化的水平在IRE-1α-/-细胞中特别高(图11H)。这些结果表明ER应力-诱导的胰岛素作用的抑制作用由IRE-1α-JNK-依赖性蛋白激酶级联所介导。
XBP-1水平的控制改变胰岛素受体信号
[0084]转录因子XBP-1是bZIP蛋白。剪接或处理形式的XBP-1(XBP-1s)是分子陪伴分子的转录调节中的关键因素,并增强代偿性UPR(Calfon等,Nature 415,92(2002);Shen等,Cell 107:893(2001);Yoshida等,Cell 107:881(2001);Lee等,Mol.Cell Biol.23:7448(2003);各自通过引用结合到本文中)。因此,我们证实细胞中XBP-1s水平的调节应该通过其对ER应力反应的强度而改变胰岛素作用。为测定这种可能性,我们建立XBP-1功能-获得和-丧失细胞模型。首先,我们建立一种诱导基因表达系统,其中外源性XBP-1s仅在四环素/脱氧土霉素不存在时表达(图13A)。平行地,我们还研究源于XBP-1-/-小鼠胚胎中的MEFs(Lee等,MoI.Cell Biol.23,7448(2003);A.M.Reimold等,Genes Dev.14,152(2000);Reimold等,Nature 412,300(2001);各自通过引用结合到本文中)(图13B)。在无外源性XBP-1s表达的成纤维细胞中,衣霉素处理(2μg/ml)30分钟开始导致强力的PERK磷酸化,在3-4小时达到与PERK磷酸化的位移迁移率(mobilityshift)变动特性有关的峰值(图13C)。在这些细胞中,对ER应力响应还呈现快速和有力的JNK活化(图13C)。在XBP-1s表达的诱导下,衣霉素处理后,PERK磷酸化和JNK活化都明显降低(图13C)。因此,XBP-1s的过度表达致使WT细胞抗拒ER应力。在XBP-1-/-MEFs中所进行的类似实验显示出相反的模式(图13D)。甚至当用低剂量衣霉素(0.5μg/ml)处理时,XBP-1-/-MEFs也有强烈的ER应力反应,其在WT细胞中不能明显刺激ER应力(图13D)。在这些条件下,XBP-1-/-MEFs中PERK磷酸化和JNK活性水平比WT对照组中所观察到的明显更高(图13D),表明XBP-1-/-细胞倾向于ER应力。因此,细胞XBP-1s蛋白的水平的改变导致ER应力反应改变。
[0085]然后,我们检测了ER应力反应中的这些差别是否在胰岛素作用中产生变更,这可通过IRS-1丝氨酸磷酸化和胰岛素刺激的IRS-1酪氨酸磷酸化评估。与对照细胞相比,在外源性表达XBP-1s的成纤维细胞中,衣霉素诱导的IRS-1丝氨酸磷酸化明显降低(图13E)。在胰岛素刺激时,与对照组比较,在过度表达XBP-1s的细胞中,IRS-1酪氨酸磷酸化的程度明显较高(图13F)。相反地,与XBP-1+/+对照组比较,甚至在低剂量(0.5μg/ml)的衣霉素处理下,IRS-1丝氨酸磷酸化都由XBP-1-/-MEFs强烈地诱导(图13G)。胰岛素刺激后,与衣霉素处理的WT对照组比较,在衣霉素处理的XBP-1-/-细胞中,IRS-1酪氨酸磷酸化水平明显降低(图13H)。在这些细胞中,胰岛素受体的胰岛素刺激的酪氨酸磷酸化正常(图14)。
XBP-1+/-小鼠呈现受损的葡萄糖体内平衡
[0086]完全XBP-1缺陷导致胚胎死亡(Reimold等,Genes Dev.14:152,2000;通过引用结合到本文中)。为研究XBP-1对体内ER应力、胰岛素敏感性和系统葡萄糖代谢的作用,我们研究在一XBP-1等位基因上具有无效突变的Balb/C-XBP-1+/-小鼠。我们在Balb/C遗传背景下研究小鼠,因为这种品系小鼠对系统葡萄糖代谢中肥胖诱导的改变具有强烈的抗性。基于我们对细胞系统的效果,我们假定XBP-1缺陷易于使小鼠产生胰岛素抗性和2型糖尿病。
[0087]将3周龄的的XBP-1+/-小鼠及其WT同窝小鼠(littermates)用高脂肪饮食(HFD)喂饲。平行地,将两种遗传型的对照小鼠置于日常饮食下。正常饮食下,两种基因型的总体重类似,直至保持到HFD下的12周龄。这段期间后,HFD下的XBP-1+/-小鼠呈现出很小但明显的体重增加(图15A)。16周的HFD后,在两种遗传型之间所测定的瘦素(leptin)、脂联素(adiponectin)和甘油三酯的血清水平不呈现任何统计学上的明显差异(图16)。
[0088]在HFD下,XBP-1+/-小鼠早在4周时,即发生持续性和递增性的明显高胰岛素血症(图15B)。实验期间,XBP-1+/-小鼠的胰岛素水平持续增加。XBP-1+/+小鼠中的血胰岛素水平比XBP-1+/-同窝小鼠中的明显低下(图15B)。如图15C中所示,与WT对照组比较,XBP-1+/-小鼠中C-肽水平也明显较高。8周开始,HFD下XBP-1+/-小鼠中,血糖水平也开始升高,并一直保持高水平直至20周时作出实验结论(图15D)。这种方式在禁食(图15D)和喂食(未出现数据)状态相同。血糖在HFD下的小鼠中升高是发生外周胰岛素抗性的强有力的指征。
[0089]为研究系统性胰岛素的敏感性,我们对XBP-1+/-小鼠和XBP-1+/+对照组进行葡萄糖(GTT)和胰岛素(ITT)的耐受试验。暴露于HFD导致XBP-1+/-小鼠明显葡萄糖耐受不良。HFD 7周后进行葡萄糖激发,XBP-1+/-小鼠显示出比XBP-1+/+小鼠明显高的葡萄糖水平(图15E)。HFD 16周后,与WT小鼠比较,在XBP-1+/-小鼠中,这种葡萄糖耐受不良持续明显(图15F)。在ITT过程中,与HFD 8周的XBP-1+/+同窝小鼠比较,在XBP-1+/-小鼠中,对胰岛素的低血糖反应也明显降低(图15G),HFD 17周后,这种降低的反应性持续出现(图15H)。在基因型之间进行对小岛形态学和功能的检测,未显示明显差异(图17)。因此,XBP-1等位基因的丧失易使小鼠产生食物诱发的胰岛素抗性和糖尿病。
XBP-1+/-小鼠中ER应力增加和胰岛素信号受损
[0090]我们的培养细胞试验证实在XBP-1缺陷细胞中ER应力增加及胰岛素信号能力降低,并且在高水平XBP-1s表达下这些显型逆转。如果该机理是XBP-1+/-小鼠中所观测到的胰岛素抗性的基础,那么这些动物呈现与受损的胰岛素受体信号偶合的高水平ER应力。为进行这种检测,我们首先在肥胖的XBP-1+/-和WT小鼠的肝中通过测定PERK磷酸化和JNK活性而评估ER应力。这些试验显示:与HFD下的WT对照组比较,肥胖的XBP-1+/-小鼠中PERK水平增加,并且肝PERK磷酸化也似乎增加(图18A)。与WT对照组比较,XBP-1+/-小鼠中JNK活性也明显增加(图18B)。与这些结果一致的是,与HFD下的WT对照组比较,肥胖的XBP-1+/-小鼠中IRS-1的丝氨酸307磷酸化也增加(图18C)。最后,我们研究这些小鼠中体内胰岛素刺激的胰岛素受体信号能力。在正常饮食的显型之间,肝和脂肪组织中任何胰岛素受体信号组分都无能检测到的差别(图19)。但是,暴露于HFD后,与WT对照组比较,XBP-1+/-小鼠的肝中的胰岛素受体信号的主要成分,包括胰岛素-刺激的IR、IRS-1和IRS-2酪氨酸-和Akt丝氨酸-磷酸化都降低(图18D-G)。与HFD下的XBP-1+/+小鼠相比,在XBP-1+/-小鼠的脂肪组织中也出现类似的胰岛素受体信号的抑制(图20)。XBP-1+/-小鼠中IR酪氨酸磷酸化的抑制与在XBP-1-/-细胞中所作的观察不同,其中ER应力在受体后水平上抑制胰岛素作用。这很可能反映体内慢性高血糖症对胰岛素受体的作用。因此,我们的数据表明体内ER应力和胰岛素作用之间又关,但在确定胰岛素受体信号途径中的准确位置上(通过该机理靶向作用点)尚不明确。
讨论
[0091]在该研究中,我们认定ER应力是肥胖症、胰岛素作用退化和2型糖尿病发展之间的一种分子连结体。
[0092]我们的发现针对由ER和胰岛素作用抑制的肥胖诱发的代谢性应力的分子传感下的基本机理,其中所述代谢性应力最终导致胰岛素抗性和2型糖尿病。我们假定ER应力是肥胖症和系统性葡萄糖体内平衡的整体衰退中应力和炎症响应的出现的基础(Shi等,Sonenberg,Endocr.Rev.24:91(2003);通过引用结合到本文中)。我们的发现与本领域先前对ER应力与1型糖尿病关联的研究完全不同,表明ER应力是一种有关胰岛素抗性和2型糖尿病的整体机理。
[0093]胰岛素作用中ER应力响应的关键作用可能代表一种进化性的保守机理,其将应力信号与代谢性调整途经整合在一起。通过ER应力的此种整合作用具有多种优点,原因是在急性应力、病原体侵入和免疫反应过程中,能量流的适当调整和主要合成代谢途径的抑制(如胰岛素作用)可能是有用的。但是,在慢性ER应力(如肥胖症)存在下,ER应力和代谢性调节之间这种紧密的关联将导致产生胰岛素抗性,并最终产生2型糖尿病。最后,如果通过ER应力的应力信号和代谢体内平衡的整合对存活率具有潜在的积极作用,那么可对高响应性系统进行选择。这种选择可能是一种当今时代代谢疾病戏剧性高度流行的可能的潜在机制,原因是接触过度热量负载将产生持续的ER应力。从治疗方面来看,我们的发现提出对ER应力响应的控制为预防和治疗2型糖尿病提供了新的机遇。
材料和方法
[0094]生化试剂:Anti-IRS-1、anti-phospho-IRS-1(Ser307)和anti-IRS-2抗体来源于Upstate Biotechnology(Charlottesville,VA)。对抗磷酸酪氨酸、eIF2α、胰岛素受体β亚单位以及XBP-1的抗体均源自Santa Cruz Biotechnology(Santa Cruz,CA)。抗-phospho-PERK、抗-Akt和抗-phospho-Akt抗体以及c-Jun蛋白来源于Cell SignalingTechnology(Beverly,MA)。抗-phospho-eIF2α抗体购自Stressgen(Victoria,British Columbia,Canada)。抗胰岛素抗体和C-肽RIA药剂盒购自Linco Research(St.Charles,MO)。抗高血糖素抗体来源于Zymed(San Francisco,CA)。PERK抗血清由Dr.David Ron(New YorkUniversity School of Medicine)友好提供。德克萨斯红轭合的驴抗豚鼠IgG和荧光素轭合的(FITC-轭合)羊抗-兔IgG来源于Jackson ImmunoResearch Laboratories(West Grove,PA)。毒胡萝卜素、衣霉素和JNK抑制剂来源于Calbiochem(San Diego,CA)。胰岛素、葡萄糖和舒林酸硫化物来源于Sigma(St.Louis,MO)。超敏感大鼠胰岛素ELISA药剂盒来源于Crystal Chem Inc.(Downers Grove,IL)。
[0095]细胞:将大鼠Fao肝细胞用含有10%胎牛血清(FBS)的RPMI 1640(Gibco,Grand Island,NY)培养。在70-80%融合时,将细胞在除去血清下(serum depleted)培养12小时,然后开始试验。将包括衣霉素、毒胡萝卜素和JNK抑制剂的试剂逐渐加入到培养箱中的培养皿内,以防止任何环境应力。加入JNK抑制剂,1小时后进行衣霉素/毒胡萝卜素处理。将XBP-1-/-小鼠胚胎成纤维细胞(MEF)(A.H.Lee,N.N.Iwakoshi,L.H.Glimcher,MoI.Cell Biol.23:7448(2003);通过引用结合到本文中)、IRE-1α-/-MEF细胞(由Dr.David Ron,New York University School of Medicine友好提供)和它们的野生型对照细胞在含有10%FBS的Dulbecco′s改良Eagle培养基(DMEM)(Gibco,Grand Island,NY)中培养。MEF细胞试验按照类似方案进行,但细胞除去血清仅6小时。
[0096]MEFs中XBP-1的过度表达:将MEF-tet-off细胞(BDBiosciences Clontech,Palo Alto,CA)在含有100μg/ml G418和1μg/ml脱氧土霉素的DMEM中培养。MEF-tet-off细胞表达外源性tTA(四环素控制的反式作用子)蛋白,其与TRE(四环素响应元素)结合,并且仅在四环素和脱氧土霉素不存在下激活转录。将剪接形式的XBP-1的cDNA连接到pTRE2hyg2质粒(BD Biosciences Clontech,Palo Alto,CA)上。将MEF-tet-off细胞用TRE2hyg2-XBP-1s质粒转染,接着在400μg/ml潮霉素B存在下选择。分离稳定转染子的个体克隆,然后通过免疫印迹法确认与脱氧土霉素相关的XBP-1s的表达。
[0097]RNA印迹分析:用Trizol试剂(Invitrogen,Carlsbad,CA),从小鼠肝中分离总RNA,通过1%琼脂糖凝胶分离,然后转移至BrightStar Plus(增加发光痕迹)的尼龙膜上(Ambion,Austin,TX)。通过RT-PCR,使用下列引发剂5’-TGGAGTTCCCCAGATTGAAG-3’和5’-CCTGACCCACCTTTTTCTCA-3’,从小鼠肝总cDNAs中制备GRP78cDNA探针。使用随机DNA引物标记药剂盒(Roche,Indianapolis,IN),用32P-dCTP对DNA探针进行标记。根据制造商(Ambion,Austin,TX)的实验方案进行杂化,并根据Versa Doc成像系统3000(BioRad,Hercules,CA)显像。
[0098]细胞中的蛋白提取物:在各处理结束时,将细胞立即在液氮中冷冻,并在-80℃下保持。用包含25mM Tris-HCl(pH7.4)、2mMNa3VO4、10mM NaF、10mM Na4P2O7、1mM EGTA、1mM EDTA、1%NP-40、5μg/ml亮抑酶肽、5μg/ml抑肽酶、10nM冈田酸和1mM苯甲磺酰氟(PMSF)的溶胞缓冲液制备蛋白提取物。分别用750μg和75μg总蛋白进行免疫沉淀和免疫印迹试验。
[0099]动物研究和肥胖症模型:成年(10-12周龄)雄性ob/ob小鼠和它们的野生型(WT)同窝出生的小鼠购自Jackson Labs。饮食诱发的肥胖症模型中使用的小鼠为雄性C57BL/6。断奶后(在约3周),即可使所有小鼠处于高脂肪饮食(HFD:35.5%脂肪、20%蛋白质、32.7%碳水化合物、Bio-Serve)。XBP-1+/-和XBP-1+/+小鼠处于Balb/C遗传背景下。如前所述,进行胰岛素和葡萄糖抗性试验(Hirosumi等,Nature420:333(2002);通过引用结合到本文中)。根据制造商说明书,使用小鼠标准物,进行胰岛素和C-肽ELISA(Crystal Chem Inc.,DownersGrove,IL)。将从16周龄小鼠中分离的胰脏在布安氏液和福尔马林中固化,将石蜡切片用豚鼠抗-胰岛素和兔抗-高血糖素抗体进行双重染色。将德克萨斯红染料轭合的驴抗豚鼠IgG和FITC-轭合的羊抗-兔IgG用做第二抗体。
[00100]胰岛素输注和组织蛋白的提取:如前所述,经门静脉注射胰岛素(Uysal等,Nature 389:610(1997);Hirosumi et al.,Nature420:333(2002);各自通过引用结合到本文中)。胰岛素输注3分钟后,移出肝,在液氮中冷冻,在-80℃下保持直至处理。为进行蛋白提取,将肝组织(~0.3g)置于包含25mM Tris-HCl(pH7.4)、10mM Na3VO4、100mM NaF、50mM Na4P2O7、10mM EGTA、10mM EDTA、1%NP-40、5μg/ml亮抑酶肽、5μg/ml抑肽酶、10nM冈田酸和2mM PMSF的10ml溶胞缓冲液中。在冰上匀浆化后,在4℃下,以4,000rpm速度,将组织溶胞产物离心15分钟,接着在4℃下,以55,000rpm速度离心1小时。将其中总组织蛋白的1毫克用于免疫沉淀作用,然后进行免疫印迹,其中100-150μg总蛋白直接用于免疫印迹(Hirosumi等,Nature 420:333(2002);通过引用结合到本文中)。
其它实施方案
[00101]前述是对本发明的某些非限定优选实施方案的说明。本领域普通技术人员将清楚在不背离以下权利要求书中界定的本发明的精神和范围下,可对本说明进行各种改变和修改。
附件A
与ER应力调节剂联合使用的药物
抗糖尿病药物
过氧化物酶体增殖子-激活的受体-γ激动剂
·罗格列酮(GlaxoSmithKline′s Avandia)
·匹格列酮(Takeda/Eli Lilly′s Actos)
·Isaglitazone(Mitsubishi Pharma)
·rivoglitazone(Sankyo′s CS-O11)
·T-131(Amgen)
·MBX-102(Metabolex)
·R-483(Roche Chugai)
·CLX-0921(Calyx)
双胍类
·二甲双胍(Bristol-Myers Squibb′s Glucophage,generics,Bristol-Myers Squibb′s Glucophage XR)
磺酰脲类
·格列美脲(Aventis′s Amaryl)
·优降糖/格列本脲(Aventis′s Diabeta,Pharmacia′s Micronase,generics,Pharmacia′s Glynase)
·格列吡嗪(Pfizer′s Glucotrol,generics,Pfizer′s Glucotrol XL)
·格列齐特(Servier′s Diamicron,Molteni & CF.LLI Alitti′sDiabrezide,Irex-Synthélabo′s Glycemirex,Dainippon′s Glimicron,generics)
联合药物
·二甲双胍/格列苯脲(Bristol-Myers Squibb′s Glucovance,Hoechst′s Suguan M)
·二甲双胍/罗格列酮(GlaxoSmithKline′s Avandamet)
·二甲双胍/格列吡嗪(Bristol-Myers Squibb′s Metaglip)
氯茴苯酸类
·瑞格列奈(Novo Nordisk′s Prandin/NovoNorm)
·那格列奈(Novartis′s Starlix/Starsis)
α-葡萄糖苷酶抑制剂
·阿卡玻糖(Bayer′s Precose/Glucobay,generics)
·米格列醇(Pharmacia′s Glyset)
·伏格列波糖(Takeda′s Basen)
胰岛素和胰岛素类似物
·赖脯胰岛素(Eli Lilly′s Humalog)
·甘精胰岛素(Aventis′s Lantus)
·Exubera(Nektar/Pflzer/Aventis)
·AERx胰岛素糖尿病管理系统(Aradigm/Novo Nordisk)
·AIR吸入胰岛素(Eli Lilly/Alkermes)
·Oralin(Generex)
·地特胰岛素(NN-304)(Novo Nordisk)
·Insulin glulisine(Aventis)
双重PPAR激动剂和PPAR pan激动剂
·BMS-298585(Bristol-Myers Squibb/Merck)
·Tesaglitazar(AstraZeneca′s Galida)
·muraglitazar(BMS-Merck and Co)
·naveglitazar(Lilly-Ligand′s LY-818)
·TAK-559(Takeda)
·netoglitazone(Mitsubishi)
·GW-677594(GSK)
·AVE-0847(Aventis)
·LY-929(Lilly-Ligand)
·ONO-5129(ONO)
高血糖素样肽-1(GLP-I)类似物和激动剂
·Exenatide(AC-2993)(Eli Lilly/Amylin Pharmaceuticals)
·Exenatide LAR(AC-2993 LAR)(Amylin Pharmaceuticals/Alkermes/Eli Lilly)
·Liraglutide(促胰岛素/NN-2211)(Scios/Novo Nordisk)
·CJC-1131(ConjuChem)
·AVE-0010(A ventis-Zealand)
·BIM-51077(Roche-Teij in-Ipsen)
·NN-2501(Novo Nordisk)
·SUN-E7001(Daiichi Suntory-Sankyo)
二肽基肽酶IV(DPP-IV)抑制剂
·LAF-237(Novartis)
·MK-431(Merck and Co)
·PSN-9301(Probiodrug Prosidion)
·815541(GlaxoSmithKline-Tanabe)
·823093(GlaxoSmithKline)
·825964(GlaxoSmithKline)
·BMS-477118(BMS)
胰脂肪酶抑制剂
·奥利斯特(Roche Holding)
Na+-葡糖(Sodium Glucose)共传递载体(SGLT)抑制剂
·T-1095(Tanabe-J&J)
·AVE-2268(Aventis)
·869682(GlaxoSmithKline-Kissei)
糊精类似物
·普兰林肽(Amylin′s Symlin)
PDR的其它药物:
适应症=高血糖症
Actos片(Takeda)
盐酸匹格列酮
Amaryl片(Sanofi-Aventis)
格列美脲
Apidra注射剂(Sanofi-Aventis)
胰岛素Glulisine
Avandamet片(GlaxoSmithKline)
盐酸二甲双胍、马来酸罗格列酮
Avandia片(Glaxo SmithKline)
马来酸罗格列酮
DiaBeta片(Sanofi-Aventis)
格列苯脲
Fortamet控释片(Andrx Labs)
盐酸二甲双胍
Glucotrol XL控释片(Pfizer)
格列吡嗪
Metaglip片(Bristol-Myers Squibb)
格列吡嗪、盐酸二甲双胍
Prandin片(0.5,1,and 2mg)(Novo Nordisk)
瑞格列奈
Precose片(Bayer)
阿卡玻糖
Starlix片(Novartis)
那格列奈
PDR的其它药物:
适应症=胰岛素依赖型糖尿病
赖脯胰岛素注射剂(Lilly)
赖脯胰岛素,人
Humalog Mix 75/25-Pen(Lilly)
赖脯胰岛素鱼精蛋白,人、赖脯胰岛素,人
优泌林50/50,100单位(Lilly)
胰岛素,正常人和人NPH的混合物
优泌林70/30笔芯注射剂(Lilly)
胰岛素,正常人和人NPH的混合物
优泌林L,100单位(Lilly)
胰岛素,人、锌混悬液
优泌林N,100单位(Lilly)
胰岛素,人NPH
常规优泌林(U-500)(Lilly)
胰岛素,正常人
常规优泌林,100 Units(Lilly)
胰岛素,正常人
重组U,100单位(Lilly)
胰岛素,人、锌混悬液
优泌林N笔芯(Humulin N Pen)注射剂(Lilly)
胰岛素,人NPH
Innovo(Novo Nordisk)
设备
Lantus注射剂(Sanofi-Aventis)
甘精胰岛素
Novolin 70/30人胰岛素10ml药瓶(Novo Nordisk)
胰岛素,正常人和人NPH的混合物
Novolin 70/30胰岛素笔芯注射剂(PenFill)3ml药筒(Novo Nordisk)
胰岛素,正常人和人NPH的混合物
Novolin N人胰岛素10ml药瓶(Novo Nordisk)
胰岛素,人NPH
Novolin N胰岛素笔芯注射剂3ml药筒(Novo Nordisk)
胰岛素,人NPH
Novolin R人胰岛素10ml药瓶(Novo Nordisk)
胰岛素,正常人
Novolin R胰岛素笔芯(PenFill)注射剂1.5ml药筒(Novo Nordisk)
胰岛素,正常人
Novolin R胰岛素笔芯注射剂3ml药筒(Novo Nordisk)
胰岛素,正常人
NovoLog注射剂(Novo Nordisk)
速效胰岛素制剂,正常人
NovoLog Mix 70/30(Novo Nordisk)
速效胰岛素制剂鱼精蛋白,人、速效胰岛素制剂,正常人
PDR的其它药物:
适应症=非胰岛素依赖型糖尿病
Actos片(Takeda)
盐酸匹格列酮
Amaryl片(Sanofi-Aventis)
格列美脲
Avandamet片(GlaxoSmithKline)
盐酸二甲双胍、马来酸罗格列酮
Avandia片(Glaxo SmithKline)
马来酸罗格列酮
DiaBeta片(Sanofi-Aventis)
格列苯脲
Glucotrol XL延释片(Pfizer)
格列吡嗪
Lantus注射剂(Sanofi-Aventis)
甘精胰岛素
Metaglip片(Bristol-Myers Squibb)
格列吡嗪、盐酸二甲双胍
Prandin片(0.5,1,and 2mg)(Novo Nordisk)
瑞格列奈
Precose片(Bayer)
阿卡玻糖
Starlix片(Novartis)
那格列奈
PDR的其它药物:
适应症=1型糖尿病
Lantus注射剂(Sanofi-Aventis)
甘精胰岛素
Novolin 70/30 InnoLet(Novo Nordisk)
胰岛素,正常人和人NPH的混合物
Novolin N InnoLet(Novo Nordisk)
胰岛素,人NPH
Novolin R InnoLet(Novo Nordisk)
胰岛素,人NPH
PDR的其它药物:
适应症=2型糖尿病
Fortamet延释片(Andrx Labs)
盐酸二甲双胍
Lantus注射剂(Sanofi-Aventis)
甘精胰岛素
Prandin片(0.5,1,and 2mg)(Novo Nordisk)
瑞格列奈
抗肥胖症药物
胰脂肪酶抑制剂
·奥利斯特(Roche′s Xenical,Roche Nippon′s xenical)
5-羟色胺和去甲肾上腺素再摄取抑制剂
·西布曲明(Abbott/Knoll′s Meridia,AstraZeneca′s Reductil,Eisai′sReductil)
去甲肾上腺素能减食欲剂
·苯丁胺(GlaxoSmithKline′s Fastin,Medeva′s Ionamin)
·氯苯咪吲哚(Wyeth-Ayerst′s Mazanor,Novartis′s Sanorex)
外周作用药
·ATL-962(Alizyme)
·HMR-1426(Aventis)
·GI-181771(GlaxoSmithKline)
中枢作用药
·重组人睫状节神经细胞营养因子(Axokine)(Regeneron)
·利莫那班(SR-141716)(Sanofi-Synthélabo)
·BVT-933(GlaxoSmithKline/Biovitrum)
·安非他酮SR(GlaxoSmithKline)
·P-57(Phytopharm)
热量生成剂
·TAK-677(AJ-9677)(Dainippon/Takeda)
大麻素CB1拮抗剂
·Acomplia(Sanofi-Aventis)
·SLV319(Solvay)
睫状节神经细胞营养因子(CNTF)激动剂
·Axokine(Regeneron)
其它抗肥胖药物
·1426(Sanofi-Aventis)
·1954(Sanofi-Aventis)
·c-2624(Merck & Co)
·c-5093(Merck & Co)
·T71(Tularik)
缩胆囊素(CCK)激动剂
·GI 181771(GSK)
脂质代谢调节剂
·AOD9604(Monash University/Metabolic Pharmaceuticals)
脂肪酶抑制剂
·ATL962(Alizyme,Takeda)
高血糖素样肽1激动剂
·AC137(Amylin)
瘦素激动剂
·第二代瘦素(Amgen)
β-3肾上腺素激动剂
·SR 58611(Sanofi-Aventis)
·CP 331684(Pfizer)
·LY 377604(Eli Lilly)
·n5984(Nisshin Kyorin Pharmaceutical)
肽激素
·肽YY[3-36](Nastech)
CNS调节剂:
·S2367(Shionogi & Co Ltd)
神经细胞营养因子:
·Peg axokine(Regeneron)
5HT2C 5-羟色胺受体激动剂
·APD356(Arena Pharmaceutical)
肽YY[3-36]
·AC 162352(Amylin)
PDR的其它药物:
适应症=肥胖症
Adipex-P胶囊(Gate)
盐酸苯丁胺
Adipex-P片(Gate)
盐酸苯丁胺
Desoxyn片,USP(Ovation)
盐酸脱氧麻黄碱
Ionamin胶囊(Celltech)
苯丁胺树脂
Meridia胶囊(Abbott)
盐酸西布茶明单水合物
Xenical胶囊(Roche Laboratories)
奥利斯特
PDR的其它药物:
开处方=食欲抑制剂
Adipex-P胶囊(Gate)
盐酸苯丁胺
Adipex-P片(Gate)
盐酸苯丁胺
Desoxyn片,USP(Ovation)
盐酸脱氧麻黄碱
Ionamin胶囊(Celltech)
苯丁胺树脂
Meridia胶囊(Abbott)
盐酸西布茶明单水合物
抗动脉粥样硬化药物
HMG-CoA还原酶抑制剂(他汀类药物)
阿伐他汀(Warner-Lambert/Pfizer′s Lipitor)
普伐他丁(Bristol-Myers Squibb′s Pravachol/Sankyo′s Mevalotin)
辛伐他丁Simvastatin(Merck & Co.′s Zocor)
洛伐他丁(Merck & Co.′s Mevacor)
氟伐他丁(Novartis′s Lescol)
西立伐他汀(Bayer′s Lipobay/GlaxoSmithKline′s Baycol)
·罗苏伐他汀(AstraZeneca′s Crestor)
·Pitivastatin(伊伐他汀/risivastatin)(Nissan/Kowa/Sankyo/Novartis)
氯贝特类药物
苯扎贝特(Boehringer Mannheim/Roche′s Bezalip,Kissei′s Bezatol)
氯贝特(Wyeth-Ayerst′s Atromid-S,generics)
非诺贝特(Fournier′s Lipidil,Abbott′s Tricor,Takeda′s Lipantil,generics)
吉非罗齐(Pfizer′s Lopid,generics)
胆汁酸多价螯合剂
考来烯胺Bristol-Myers Squibb′s Questran and Questran Light,generics
考来替泊Pharmacia′s Colestid
烟酸
烟酸—即释型(Aventis′s Nicobid,Upsher-Smith′s Niacor,Aventis′sNicolar,Sanwakagaku′s Perycit,generics)
烟酸—缓释型(Kos Pharmaceuticals′Niaspan,Upsher-Smith′s SIo-Niacin)
抗血小板剂
·阿司匹林(Bayer′s Aspirin,generics)
·氯吡格雷(Sanofi-Synthélabo/Bristol-Myers Squibb′s Plavix)
·噻氯匹啶(Sanofi-Synthélabo′s Ticlid,Daiichi′s Panaldine,generics)
血管紧张素转换酶抑制剂
·雷米普利(Aventis′s Altace)
·伊拉普利(Merck & Co.′s Vasotec)
血管紧张素II受体拮抗剂
·氯沙坦钾(Merck & Co.′s Cozaar)
脂酰辅酶A胆固醇乙酰转移酶(ACAT)抑制剂
·阿伐麦布(Pfizer)
·Eflucimibe(BioMérieux Pierre Fabre/Eli Lilly)
·CS-505(Sankyo and Kyoto)
·SMP-797(Sumito)
胆固醇吸收抑制剂
·依泽替米贝(Schering-Plough/Merck & Co.)
·帕马苷(Pfizer)
胆固醇酯转移蛋白(CETP)抑制剂
·CP-529414(Pfizer)
·JTT-705(Japan Tobacco)
·CETi-I(Avant Immunotherapeutics)
微粒体甘油三酯转移蛋白(MTTP)抑制剂
·英普他派(Bayer)
·R-103757(Janssen)
其它胆固醇调节剂
·NO-1886(Otsuka/TAP Pharmaceutical)
·CI-1027(Pfizer)
·WAY-135433(Wyeth-Ayerst)
胆汁酸调节剂
·GTl 02-279(GelTex/Sankyo)
·HBS-107(Hisamitsu/Banyu)
过氧化物酶体增殖活化受体(PPAR)激动剂
·Tesaglitazar(AZ-242)(AstraZeneca)
·Netoglitazone(MCC-555)(Mitsubishi/Johnson & Johnson)
·GW-409544(Ligand Pharmaceuticals/GlaxoSmithKline)
·GW-501516(Ligand Pharmaceuticals/GlaxoSmithKline)
基于基因的疗法
·AdGVVEGF 121.10(GenVec)
·ApoAl(UCB Pharma/Groupe Fournier)
·EG-004(Trinam)(Ark Therapeutics)
·ATP-结合盒式(cassette)转运蛋白-Al(ABCAl)(CVTherapeutics/Incyte,Aventis,Xenon)
组合血管保护剂
·AGI-1067(Atherogenics)
其它抗动脉粥样硬化药物
·BO-653(Chugai Pharmaceuticals)
糖蛋白Ilb/IIIa抑制剂
·罗昔非班(Bristol-Myers Squibb)
·更托非班(Yamanouchi)
·Cromafiban(Millennium Pharmaceuticals)
阿司匹林和阿司匹林样化合物
·控释阿司匹林制剂(slow-release aspirin)(Pharmacia)
·帕米格雷(Kanebo/Angelini Ricerche/CEPA)
联合疗法
·Advicor(烟酸/洛伐他丁)(Kos Pharmaceuticals)
·氨氯地平/阿伐他汀(Pfizer)
·辛伐他丁/依泽替米贝(Merck & Co./Schering-Plough)
IBAT抑制剂
·S-8921(Shionogi)
角鲨烯合酶抑制剂
·BMS-188494 I(Bristol-Myers Squibb)
·CP-210172(Pfizer)
·CP-295697(Pfizer)
·CP-294838(Pfizer)
单核细胞趋化蛋白(MCP)-1抑制剂
·RS-504393(Roche Bioscience)
·其它MCP-1抑制剂(GlaxoSmithKline,Teijin,and Bristol-MyersSquibb)
PDR的其它药物:
适应症=高胆固醇血症
Advicor片(Kos)
洛伐他丁、烟酸
Altoprev缓释片(Andrx Labs)
洛伐他丁
Caduet片(Pfizer)
苯磺酸氨氯地平、阿托伐他汀钙
Crestor片(AstraZeneca)
罗苏伐他汀钙
Lescol胶囊(Novartis)
氟伐他汀钠
Lescol胶囊(Reliant)
氟伐他汀钠
Lescol XL片(Novartis)
氟伐他汀钠
Lescol XL片(Reliant)
氟伐他汀钠
Lipitor片(Parke-Davis)
阿托伐他汀钙
Lofibra胶囊(Gate)
非诺贝特
Mevacor片(Merck)
洛伐他汀
烟酸缓释片(Kos)
烟酸
Pravachol片(Bristol-Myers Squibb)
普伐他汀钠
Tricor片(Abbott)
非诺贝特
Vytorin 10/10片(Merck/Schering Plough)
依泽替米贝、辛伐他丁
Vytorin 10/10片(Schering)
依泽替米贝、辛伐他丁
Vytorin 10/20片(Merck/Schering Plough)
依泽替米贝、辛伐他丁
Vytorin 10/20片(Schering)
依泽替米贝、辛伐他丁
Vytorin 10/40片(Merck/Schering Plough)
依泽替米贝、辛伐他丁
Vytorin 10/40片(Schering)
依泽替米贝、辛伐他丁
Vytorin 10/80片(Merck/Schering Plough)
依泽替米贝、辛伐他丁
Vytorin 10/80片(Schering)
依泽替米贝、辛伐他丁
WelChol片(Sankyo)
盐酸考来维仑
Zetia片(Schering)
依泽替米贝
Zetia片(Merck/Schering Plough)
依泽替米贝
Zocor片(Merck)
辛伐他丁
抗血脂紊乱药
HMG-CoA还原酶抑制剂
·阿伐他汀(Pfizer′s Lipitor/Tahor/Sortis/Torvast/Cardyl)
·辛伐他汀Simvastatin(Merck′s Zocor/Sinvacor,BoehringerIngelheim′s Denan,Banyu′s Lipovas)
·普伐他丁(Bristol-Myers Squibb′s Pravachol,Sankyo′sMevalotin/Sanaprav)
·氟伐他丁(Novartis′s Lescol/Locol/Lochol,Fujisawa′s Cranoc,Solvay′s Digaril)
·洛伐他丁(Merck′s Mevacor/Mevinacor,Bexal′s Lovastatina,Cepa;Schwarz Pharma′s Liposcler)
·罗苏伐他汀(AstraZeneca′s Crestor)
·匹伐他汀(Nissan Chemical,Kowa Kogyo,Sankyo and Novartis)
HMG-CoA还原酶抑制剂联合疗法
·辛伐他丁/依泽替米贝(Merck and Schering-Plough)
氯贝特类
·非诺贝特(Abbott′s Tricor,Fournier′s Lipidil/Lipantil)
·苯扎贝特(Roche′s Béfizal/Cedur/Bezalip,Kissei′s Bezatol,generics)
·吉非罗齐(Pfizer′s Lopid/Lipur,generics)
·冠心平(Wyeth′s Atromid-S,generics)
·环丙贝特(Sanofi-Synthélabo′s Modalim)
胆汁酸多价螯合剂
·考来烯胺(Bristol-Myers Squibb′s Questran)
·考来替泊(Pfizer′s Colestid)
·考来维仑(Genzyme/Sankyo′s Welchol)
胆固醇吸收抑制剂
·依泽替米贝(Merck and Schering-Plough′s Zetia)
·帕马苷(Pfizer)
烟酸衍生物
·烟酸(Kos′s Niaspan,Yamanouchi′s Nyclin)
脂酰辅酶A胆固醇乙酰转移酶抑制剂
·阿伐麦布(Pfizer)
·Eflucimibe(Eli Lilly)
胆固醇酯转移蛋白抑制剂
·Torcetrapib(Pfizer)
·JTT-705(Japan Tobacco)
·CETi-1(Avant Immunotherapeutics)
微粒体甘油三酯转移蛋白抑制剂
·英普他派(Bayer)
·CP-346086(Pfizer)
过氧化物酶体增殖活化受体激动剂
·GW-501516(Ligand Pharmaceuticals and GlaxoSmithKline)
·Tesaglitazar(AstraZeneca)
·LY-929(Ligand Pharmaceuticals and Eli Lilly)
·LY-465608(Ligand Pharmaceuticals and Eli Lilly)
·LY-518674(Ligand Pharmaceuticals and Eli Lilly)
·MK-767(Merck and Kyorin)
角鲨烯合酶抑制剂
·TAK-475(Takeda)
其它新途径
·MBX-102(Metabolex)
·NO-1886(Otsuka)
·Gemcabene(Pfizer)
肝X受体激动剂
·GW-3965(GlaxoSmithKline)
·TU-0901317(Tularik)
胆汁酸调节剂
·BTG-511(British Technology Group)
·HBS-107(Hisamitsu and Banyu)
·BARI-1453(Aventis)
·S-8921(Shionogi)
·SD-5613(Pfizer)
·AZD-7806(AstraZeneca)
PDR的其它药物:
适应症=高胆固醇血症
Advicor片(Kos)
洛伐他丁、烟酸
Altoprev缓释片(Andrx Labs)
洛伐他丁
Caduet片(Pfizer)
苯磺酸氨氯地平、阿托伐他汀钙
Crestor片(AstraZeneca)
罗苏伐他汀钙
Lescol胶囊(Novartis)
氟伐他丁钠
Lescol胶囊(Reliant)
氟伐他丁钠
Lescol XL片(Novartis)
氟伐他丁钠
Lescol XL片(Reliant)
氟伐他丁钠
Lipitor片(Parke-Davis)
阿托伐他汀钙
Lofibra胶囊(Gate)
非诺贝特
Mevacor片(Merck)
洛伐他丁
烟酸缓释片(Kos)
烟酸
Pravachol片(Bristol-Myers Squibb)
普伐他汀钠
Tricor片(Abbott)
非诺贝特
Vytorin 10/10片(Merck/Schering Plough)
依泽替米贝、辛伐他汀
Vytorin 10/10片(Schering)
依泽替米贝、辛伐他汀
Vytorin 10/20片(Merck/Schering Plough)
依泽替米贝、辛伐他汀
Vytorin 10/20片(Schering)
依泽替米贝、辛伐他汀
Vytorin 10/40片(Merck/Schering Plough)
依泽替米贝、辛伐他汀
Vytorin 10/40片(Schering)
依泽替米贝、辛伐他汀
Vytorin 10/80片(Merck/Schering Plough)
依泽替米贝、辛伐他汀
Vytorin 10/80片(Schering)
依泽替米贝、辛伐他汀
WelChol片(Sankyo)
盐酸考来维仑
Zetia片(Schering)
依泽替米贝
Zetia片(Merck/Schering Plough)
依泽替米贝
Zocor片(Merck)
辛伐他汀
抗高血压药物
利尿剂
·氯噻酮(Alliance′s Hygotron,generics)
·甲苯喹唑酮(Generics)
·吲达帕胺(Servier′s Natrilix/Tertensif,Aventis′s Lozol,Merck′sIndapamide,generics)
·布美他尼(Leo′s Burinex,Sankyo′s Lunetoron,Roche′s Bumex,generics)
·依他尼酸(Merck & Co.′s Edecrin)
·呋塞米(Aventis′s Lasilix/Lasix/Eutensin/Seguril,generics)
·托塞米(Roche′s Demadex,generics)
·盐酸阿米洛利(Merck & Co.′s Midamor,generics)
·螺内酯(Pharmacia′s Spirolang/Aldactone,Mylan′s Spironolactone,generics)
·氨苯蝶啶(GlaxoSmithKline′s Dyrenium,Goldshield′s Dytac,Isei′sTriamterene/Triteren)
α阻滞剂
·甲磺酸喹唑嗪(Pfizer′s Zoxan/Cardura/Cardenalin,Hexal′s Doxacor,generics)
·盐酸哌唑嗪(Pfizer′s Minipress,generics)
·盐酸特拉唑嗪(Abbott′s Hytrin/Flotrin/Heitrin/Itrin/Deflox,Mitsubishi Welpharma′s Vasomet,generics)
β阻滞剂
·盐酸醋丁洛尔(Bayer′s Prent,Wyeth′s Sectral,Aventis′s Acetanol,generics)
·阿替洛尔(AstraZeneca/Sumitomo′s Tenormin,generics)
·倍他洛尔(Sanofi-Synthélabo′s Kerlone,generics)
·富马酸比索洛尔(Merck KGaA′s Cardicor,Lipha Sante′s Detensiel/Cardensiel,Lederle′s Monocor/Zebeta,generics)
·盐酸卡替洛尔(Lipha Sante/Otsuka′s Mike Ian,Abbott′s Cartrol)
·酒石酸美多洛尔(Novartis′s Lopressor/Prelis,AstraZeneca′sSeloken/Betaloc,generics)
·琥珀酸美托洛尔(AstraZeneca′s Toprol-XL Herz-mite,generics)
·纳多洛尔(Bristol-Myers Squibb/Sanofi-Synthélabo′s Corgard,generics)
·硫酸喷布洛尔(Schwarz Pharma′s Levatol,Wolff/A ventis′sBetaPressin)
·吲哚洛尔(Novartis′s Visken,generics)
·盐酸普萘洛尔(AstraZeneca′s Inderal/Dociton,Wyeth′s Inderal LA,generics)
·马来酸噻吗洛尔timolol(Merck & Co.′s Blocadren,generics)
·卡维地洛(Roche′s Coreg/Dilatrend/Coropres/Eucardic,GlaxoSmithKline′s Coreg)
钙通道阻滞剂
·苯磺酸氨氯地平(Pfizer′s Amlor/Istin/Norvasc)
·费乐地平(AstraZeneca′s Flodil/Modip/Plendil/Splendil)
·依拉地平(Novartis′s Lomir/Prescal)
·尼卡地平(Roche/Yamanouchi′s Cardene,generics)
·硝苯地平(Bayer′s Adalat,generics)
·尼索地平(AstraZeneca′s Sular,Bayer′s Syscor MR/Baymycard)
·盐酸地尔硫(Sanofi-Synthélabo′s Tildiem Angizem 60,Pfizer′sDinisor,Generics)
·盐酸维拉帕米(Knoll′s Isoptin Press/Manidon Retard/Securon,Pharmacia′s Calan/Covera,generics)
·阿折地平(Sankyo/UBE)
·普拉地平(Otsuka)
·分级(Graded)地尔硫制剂(Biovail)
·(S)-氨氯地平(Sepracor/Emcure)
·氯维地平(AstraZeneca/The Medicines Company)
血管紧张素转换酶抑制剂
·盐酸贝那普利(Novartis′s Cibacen/Lotensin)
·卡托普利(Bristol-Myers Squibb′s Lopril/Lopirin/Capoten/Acepress,Sanofi-Synthélabo′s Alopresin,generics)
·马来酸依那普利(Merck & Co.′s Vasotec,Banyu′s Renivoce,generics)
·福森普利钠(Bristol-Myers Squibb′s Fosinorm/Tensogard/Fosinil/Staril/Monopril)
·赖诺普利(Merck & Co.′s Prinivil,AstraZeneca′s Zestril)
·莫昔普利(Schwarz′s Moex/Fempress/Univasc)
·哌道普利(Servier′s Conversyl)
·盐酸喹那普利(Pfizer′s Accupril/Acuitel/Accuprin/Acuprel,Sanofi-Synthélabo′s Korec,generics)
·雷米普利(Aventis′s Altace)
·群多普利(Abbott′s Gopten/Mavik)
血管紧张素II受体拮抗剂
·氯沙坦(Merck & Co.′s Cozaar)
·缬沙坦(Novartis′s Tareg/Diovan,Aventis′s Nisis)
·依贝沙坦(Bristol-Myers Squibb/Sanofi-Synthélabo′s Aprovel/Karvea)
·坎地沙坦(AstraZeneca′s Atacand/Ratacand/Amias,Takeda′sBlopress)
·替米沙坦(Boehringer Ingelheim′s Micardis)
·依普沙坦(Solvay′s Teveten)
·奥美沙坦(Sankyo/Recordati/Menarini/Forest/Kowa)
·YM-358(Yamanouchi)
联合疗法
·盐酸贝那普利/氢氯噻嗪(Novartis′s Cibadrex/Lotensin HCT)
·卡托普利/氢氯噻嗪(Bristol-Myers Squibb′s Capozide/Ecazide)
·马来酸伊拉普利/氢氯噻嗪(Merck & Co.′s Vasorectic/Co Renitec/Innozide,AstraZeneca′s Lexxel,generics)
·赖诺普利/氢氯噻嗪(Merck & Co.′s Prinzide,AstraZeneca′sZestorectic)
·氯沙坦/氢氯噻嗪(Merck & Co.′s Hyzaar)
·阿替洛尔/氯噻酮(AstraZeneca′s Tenoretic,generics)
·富马酸比索洛尔/氢氯噻嗪(Lederle′s Ziac,generics)
·酒石酸美多洛尔/氢氯噻嗪(Novartis′s Lopressor HCT,Pharmacia′sSelopresin/Selozide)
·氨氯地平苯磺酸盐/盐酸贝那普利(Pfizer′s Norvasc,Novartis′sLotrel)
·费乐地平/马来酸依那普利(AstraZeneca′s Lexxel)
·盐酸维拉帕米/群多普利(Knoll/Abbott′s Tarka,Aventis′s Udramil)
·乐卡地平和伊拉普利(Recordati/Pierre Fabre)
·奥美沙坦/氢氯噻嗪(Sankyo)
·依普沙坦/氢氯噻嗪(Unimed)
·氨氯地平苯磺酸盐/阿伐他汀(Pfizer)
·尼群地平/伊拉普利(Vita Invest)
血管肽酶抑制剂
·奥马曲拉(Bristol-Myers Squibb)
·Gemopatrilat(Bristol-Myers Squibb)
·法西多曲(Eli Lilly)
·山帕曲拉(Pfizer/Shire)
·AVE 7688(Aventis)
·M100240(Aventis)
·Zl3752A(Zambon/GSK)
·796406(Zambon/GSK)
双重中性肽链内切酶和内皮素转化酶(NEP/ECE)抑制剂
·SLV306(Solvay)
NEP抑制剂
·依卡曲尔(Bioproject)
醛固酮拮抗剂
·依普利酮(Pharmacia)
肾素抑制剂
·阿利吉仑(Novartis)
·SPP500(Roche/Speedel)
·SPP600(Speedel)
·SPP800(Locus/Speedel)
血管紧张素疫苗
·PMD-3117(Protherics)
ACE/NEP抑制剂
·AVE-7688(Aventis)
·GW-660511(Zambon SpA)
Na+/K+ATP酶调节剂
·PST-2238(Prassis-Sigma-Tau)
内皮素拮抗剂
·PD-156707(Pfizer)
血管扩张剂
·NCX-4016(NicOx)
·LP-805(Pola/Wyeth)
天然肽
·BDNP(Mayo Foundation)
血管紧张素受体阻滞剂(ARBs)
·pratosartan(Pratosartan/Boryung)
AGE交联破碎剂
·alagebrium chloride(Alteon)
内皮素受体拮抗剂
·替唑生坦(Genentech)
·Ambrisentan(Myogen)
·BMS 193884(BMS)
·西他生坦(Encysive Pharmaceuticals)
·SPP301(Roche/Speedel)
·达卢生坦(Myogen/Abbott)
·J104132(Banyu/Merck & Co.)
·TBC3711(Encysive Pharmaceuticals)
·SB234551(GSK/Shionogi)
其它抗高血压药物
·MC4232(University of Manitoba/Medicure)
PDR的其它药物:
适应症=高血压
Accupril片(Parke-Davis)
盐酸喹那普利
Accuretic片(Parke-Davis)
氢氯噻嗪、盐酸喹那普利
Aceon片(2mg、4mg、8mg)(Solvay)
哌林多普利特丁胺
硝苯地平CC片(Bayer)
硝苯地平
Aldoclor片(Merck)
氯噻嗪、甲基多巴
Aldoril片(Merck)
氢氯噻嗪、甲基多巴
Altace胶囊(King)
雷米普利
Atacand片(AstraZeneca LP)
坎地沙坦西酯
Atacand HCT 16-12.5片(AstraZeneca LP)
坎地沙坦西酯、氢氯噻嗪
Atacand HCT 32-12.5片(AstraZeneca LP)
坎地沙坦西酯、氢氯噻嗪
Avalide片(Bristol-Myers Squibb)
氢氯噻嗪、依贝沙坦
Avapro片(Bristol-Myers Squibb)
依贝沙坦
Avapro片(Sanofi-Aventis)
依贝沙坦
Benicar片(Sankyo)
奥美沙坦Medoxomil酯
Benicar HCT片(Sankyo)
氢氯噻嗪、奥美沙坦酯
Blocadren片(Merck)
马来酸噻吗洛尔
Caduet片(Pfizer)
苯磺酸氨氯地平、阿托伐他汀钙
Captopril片(Mylan)
卡托普利
Cardene IV.(ESP Pharma)
盐酸尼卡地平
Cardizem LA缓释片(Biovail)
盐酸地尔硫
Catapres片(Boehringer Ingelheim)
盐酸可乐定
Catapres-TTS(Boehringer Ingelheim)
可乐定
Clorpres片(Mylan Bertek)
氯噻酮、盐酸可乐定
Coreg片(GlaxoSmithKline)
卡维地洛
Corzide 40/5片(King)
氟克尿噻、纳多洛尔
Corzide 80/5片(King)
氟克尿噻、纳多洛尔
Covera-HS片(Searle)
盐酸维拉帕米
Cozaar片(Merck)
氯沙坦钾
Demadex片和注射液(Roche Laboratories)
托塞米
Diovan HCT片(Novartis)
氢氯噻嗪、缬沙坦
Diovan片(Novartis)
缬沙坦、
Diuril口服混悬液(Merck)
氯噻嗪
Diuril片(Merck)
氯噻嗪
Dyazide胶囊(GlaxoSmithKline)
氢氯噻嗪、氨苯蝶啶
DynaCirc CR片(Reliant)
依拉地平
Furosemide片(Mylan)
呋塞米
HydroDIURIL片(Merck)
氢氯噻嗪
Hytrin胶囊(Abbott)
盐酸特拉唑嗪
Hyzaar 50-12.5片(Merck)
氢氯噻嗪、氯沙坦钾
Hyzaar 100-25片(Merck)
氢氯噻嗪、氯沙坦钾
Indapamide片(Mylan)
吲达帕胺
Inderal LA长效胶囊(Wyeth)
盐酸普萘洛尔
InnoPran XL胶囊(Reliant)
盐酸普萘洛尔
Inspra片(Pfizer)
依普利酮
Inversine片(Targacept)
盐酸美加明
Isoptin SR片(Abbott)
盐酸维拉帕米
Lotensin片(Novartis)
盐酸贝那普利
Lotensin HCT片(Novartis)
盐酸贝那普利、氢氯噻嗪
Lotrel胶囊(Novartis)
苯磺酸氨氯地平、盐酸贝那普利
Mavik片(Abbott)
群多普利
Maxzide片(Mylan Bertek)
氢氯噻嗪、氨苯蝶啶
Maxzide-25mg片(Mylan Bertek)
氢氯噻嗪、氨苯蝶啶
Micardis片(Boehringer Ingelheim)
替米沙坦
Micardis HCT片(Boehringer Ingelheim)
氢氯噻嗪、替米沙坦
Midamor片(Merck)
盐酸阿米洛利
Moduretic片(Merck)
盐酸阿米洛利、氢氯噻嗪
Nadolol片(Mylan)
纳多洛尔
Norvasc片(Pfizer)
苯磺酸氨氯地平
Prinivil片(Merck)
赖诺普利
Prinzide片(Merck)
氢氯噻嗪、赖诺普利
Sular片(First Horizon)
尼索地平
Tarka片(Abbott)
群多普利、盐酸维拉帕米
Teveten片(Biovail)
依普沙坦甲磺酸盐
Teveten HCT片(Biovail)
依普沙坦甲磺酸盐、氢氯噻嗪
Tiazac胶囊(Forest)
盐酸地尔硫
Timolide片(Merck)
氢氯噻嗪、马来酸噻吗洛尔
Toprol-XL片(AstraZeneca LP)
美托洛尔琥珀酸盐
Uniretic片(Schwarz)
氢氯噻嗪、盐酸莫西普利
Univasc片(Schwarz)
盐酸莫西普利
Vaseretic片(Merck)
马来酸依那普利、氢氯噻嗪
Vasotec IV.Injection(Merck)
马来酸依那普利
Verelan PM胶囊(Schwarz)
盐酸维拉帕米
Zaroxolyn片(Celltech)
甲苯喹唑酮
Claims (82)
1.一种治疗或预防选自肥胖症、胰岛素抗性、高血糖症和2型糖尿病的病症的方法,该方法包括给予动物已知降低ER应力的药物。
2.权利要求1的方法,它还包括给予选自抗糖尿病剂、减肥药、抗血脂紊乱剂、抗动脉粥样硬化剂和抗高血压剂的药物。
3.权利要求2的方法,其中所述抗糖尿病剂选自:双胍类、二甲双胍、磺酰脲类、胰岛素、胰岛素类似物、PPARg激动剂、氯茴苯酸类和DPP-IV抑制剂。
4.权利要求2的方法,其中所述减肥药选自:胰脂肪酶抑制剂、5-羟色胺再摄取抑制剂、去甲肾上腺素再摄取抑制剂、去甲肾上腺素能减食欲剂、外周作用剂、中枢作用剂以及热量生成剂。
5.权利要求2的方法,其中所述抗血脂紊乱剂或抗动脉粥样硬化剂选自:HMG-CoA还原酶抑制剂、烟酸、抗血小板剂、ACE抑制剂、阿司匹林、阿司匹林类似物和MCP-1抑制剂。
6.权利要求2的方法,其中抗高血压剂选自:利尿剂、β-阻滞剂、Ca+2通道阻滞剂、ACE抑制剂和AT-II抑制剂。
7.权利要求1的方法,其中所述病症为胰岛素抗性。
8.权利要求1的方法,其中所述病症为2型糖尿病。
9.权利要求1的方法,其中所述病症为肥胖症。
10.权利要求1的方法,其中所述动物为哺乳动物。
11.权利要求1的方法,其中所述动物为人。
12.权利要求1的方法,其中所述给药步骤包括口服给予药物。
13.权利要求1的方法,其中所述给药步骤包括经注射给予药物。
14.权利要求1的方法,其中所述给药步骤包括静脉内给予药物。
15.权利要求1的方法,其中所述药物为化学陪伴分子。
16.权利要求15的方法,其中所述化学陪伴分子选自:甘油、D2O、二甲亚砜(DMSO)、甘氨酸三甲铵乙内酯(甜菜碱)、甘油磷酸胆碱(GPC)、甲胺类和三甲胺N-氧化物(TMAO)。
17.权利要求1的方法,其中所述药物为甘油。
18.权利要求1的方法,其中所述药物为甘油的衍生物。
19.权利要求1的方法,其中所述药物为三甲胺N-氧化物(TMAO)。
20.权利要求1的方法,其中所述药物为三甲胺N-氧化物(TMAO)的盐的衍生物。
22.权利要求21的方法,其中R1、R2和R3独立为低级C1-C6烷基。
23.权利要求1的方法,其中所述药物为苯基丁酸(PBA)。
24.权利要求1的方法,其中所述药物是PBA的衍生物、盐或异构体。
25.权利要求1的方法,其中所述药物,或其药学上可接受的衍生物或盐具有下式:
其中n是1或2;
R0是芳基、杂芳基或苯氧基,所述芳基和苯氧基为未取代的或独立地被一或多个卤素、羟基或低级烷基取代;
R1和R2独立为H、低级烷氧基、羟基、低级烷基或卤素;和
R3和R4独立为H、低级烷基、低级烷氧基或卤素。
26.权利要求25的方法,其中R0是苯基、萘基或苯氧基,所述苯基、萘基和苯氧基为未取代的或独立地被一或多个卤素、羟基或低级烷基的部分取代。
27.权利要求25的方法,其中:
R0是苯基、萘基或苯氧基,所述苯基、萘基和苯氧基为未取代的或独立被1-4个卤素、羟基或1-4个碳原子的低级烷基的部分取代;
R1和R2独立为H、羟基、1-2个碳原子的低级烷氧基、1-4个碳原子的低级直链或支链烷基或卤素;以及
R3和R4独立为H、1-2个碳原子的低级烷氧基、1-4个碳原子的低级直链或支链烷基或卤素。
28.权利要求25的方法,其中n是1。
29.权利要求25的方法,其中n是2。
30.权利要求25的方法,其中R0是苯基。
31.权利要求25的方法,其中R0是取代的苯基。
32.权利要求25的方法,其中在R0的苯基上的取代基是1-4个卤素部分。
33.权利要求25的方法,其中R3和R4均为-H。
34.权利要求1的方法,其中所述药物为牛熊去氧胆酸(TUDCA)。
35.权利要求1的方法,其中所述药物为TUDCA的衍生物、盐或异构体。
36.权利要求1的方法,其中所述药物,或其药学上可接受的盐或衍生物具有下式:
其中R是-H或C1-C4烷基;
R1是-CH2-SO3R3以及R2是-H;或者R1是-COOH以及R2是-CH2-CH2-CONH2、-CH2-CONH2、-CH2-CH2-SCH3或-CH2-S-CH2-COOH;以及
R3是-H或碱性氨基酸残基。
37.权利要求36的方法,其中R1是-CH2-SO3H和R2是-H。
38.权利要求37的方法,其中R是-H。
39.权利要求1的方法,其中所述药物的给药剂量范围为100mg/kg/日-5g/kg/日。
40.权利要求1的方法,其中所述药物的给药剂量范围为500mg/kg/日-3g/kg/日。
41.权利要求1的方法,其中所述药物的给药剂量范围为500mg/kg/日-1g/kg/日。
42.一种治疗或预防肥胖症的方法,该方法包括给予人已知能减低ER应力的药物。
43.一种降低血糖水平的方法,该方法包括给予动物选自PBA、TUDCA及其衍生物的药物。
44.一种增加胰岛素敏感性的方法,该方法包括给予动物选自PBA、TUDCA及其衍生物的药物。
45.一种筛选用于治疗或预防肥胖症、胰岛素抗性或糖尿病的药物的方法,该方法包括以下步骤:
提供一种被筛选的药物;
使该药物与细胞接触;和
测定ER应力标记是否降低。
46.一种筛选用于调节胰岛素作用或胰岛素受体信号的药物的方法,该方法包括以下步骤:
提供一种被筛选的药物;
使该药物与细胞接触;和
测定ER应力标记是否降低。
47.权利要求46的方法,其中ER应力标记选自:剪接形式的XBP-1、磷酸化状态的PERK、磷酸化的eIF2α、mRNA水平的GRP78/BIP、蛋白水平的GRP78/BIP和JNK活性。
48.权利要求46的方法,其中所述细胞为哺乳动物细胞。
49.权利要求46的方法,其中所述细胞为人体细胞。
50.权利要求46的方法,其中所述细胞为脂肪细胞。
51.权利要求46的方法,其中所述细胞为肝细胞。
52.权利要求46的方法,其中所述细胞正经历ER应力。
53.权利要求46的方法,其中所述细胞已用衣霉素或毒胡萝卜素处理以诱导ER应力。
54.一种筛选用于降低ER应力的药物的方法,该方法包括以下步骤:
提供一种被筛选的药物;
使该药物与细胞接触;和
测定ER应力标记是否降低。
55.一种筛选用于阻止ER应力的药物的方法,该方法包括以下步骤:
提供一种被筛选的药物;
使该药物与细胞接触;
接着使细胞与带有ER应力诱导物的药物接触;和
测定ER应力标记是否降低。
56.权利要求55的方法,其中所述ER应力诱导物选自衣霉素或毒胡萝卜素。
57.一种通过权利要求45的方法鉴定的化合物。
58.一种包含权利要求57的化合物的药用组合物。
59.一种药用组合物,它包含(1)已知降低ER应力的药物,和(2)选自抗糖尿病剂、减肥药、抗血脂紊乱剂、抗动脉粥样硬化剂和抗高血压剂。
60.权利要求59的药用组合物,其中所述已知降低ER应力的药物是化学陪伴分子。
61.权利要求59的药用组合物,其中所述已知降低ER应力的药物选自:甘油、D2O、二甲亚砜(DMSO)、甘氨酸三甲铵乙内酯(甜菜碱)、甘油磷酸胆碱(GPC)、甲胺类和三甲胺N-氧化物(TMAO)。
62.权利要求59的药用组合物,其中所述已知降低ER应力的药物是TUDCA或其衍生物。
63.权利要求59的药用组合物,其中所述已知降低ER应力的药物是PBA或其衍生物。
64.权利要求59的药用组合物,它包含PBA和二甲双胍。
65.一种降低ER应力或治疗或预防与ER应力有关的疾病的方法,该方法包括以下步骤:
给予动物选自PBA、TUDCA及其衍生物的药物。
66.一种诊断胰岛素抗性、高血糖症或2型糖尿病的方法,该方法包括:
测定至少一种ER应力标记的表达水平,其中ER应力标记水平的增加表明受试者面临胰岛素抗性、高血糖症或2型糖尿病的风险。
67.权利要求66的方法,其中所述ER应力标记选自:剪接形式的XBP-1、磷酸化状态的PERK、磷酸化的eIF2α、mRNA水平的GRP78/BIP、蛋白水平的GRP78/BIP和JNK活性。
68.权利要求66的方法,其中所述测定步骤包括测定至少两种ER应力标记的水平。
69.一种调节PERK、IRE-1α、JNK、IRS-1、IRS-2、Akt或胰岛素受体活性的方法,该方法包括:
给予动物选自PBA、TUDCA及其衍生物的药物。
70.权利要求69的方法,其中PERK活性降低。
71.权利要求69的方法,其中IRE-1α活性降低。
72.权利要求69的方法,其中JNK激酶活性降低。
73.权利要求69的方法,其中IRS-1活性降低。
74.权利要求69的方法,其中IRS-2活性降低。
75.权利要求69的方法,其中Akt活性降低。
76.权利要求69的方法,其中胰岛素受体活性降低。
77.一种增加胰岛素作用或胰岛素受体信号的方法,该方法包括:
给予动物选自PBA、TUDCA及其衍生物的药物。
78.权利要求77的方法,它还包括给予选自下列的药物:胰岛素、降血糖药、降胆固醇药、食欲抑制剂、阿司匹林、维生素、矿物质和抗高血压药。
79.一种调节胰岛素受体信号的方法,该方法包括:
给予动物已知降低ER应力的药物。
80.权利要求79的方法,其中所述药物选自:甘油、D2O、二甲亚砜(DMSO)、甘氨酸三甲铵乙内酯(甜菜碱)、甘油磷酸胆碱(GPC)、甲胺类和三甲胺N-氧化物(TMAO)。
81.权利要求79的方法,其中所述药物选自PBA、TUDCA及其衍生物。
82.权利要求79的方法,它还包括给予选自下列的药物:胰岛素、降血糖药、降胆固醇药、食欲抑制剂、阿司匹林、维生素、矿物质和抗高血压药。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US61009304P | 2004-09-15 | 2004-09-15 | |
| US60/610,093 | 2004-09-15 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN101056656A true CN101056656A (zh) | 2007-10-17 |
Family
ID=36060695
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CNA2005800388745A Pending CN101056656A (zh) | 2004-09-15 | 2005-09-15 | 在治疗肥胖症和糖尿病中降低er应力 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US20100075894A1 (zh) |
| EP (1) | EP1799263A4 (zh) |
| JP (1) | JP2008513465A (zh) |
| CN (1) | CN101056656A (zh) |
| AU (1) | AU2005284798B2 (zh) |
| CA (1) | CA2580370A1 (zh) |
| WO (1) | WO2006031931A2 (zh) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN110317776A (zh) * | 2019-07-31 | 2019-10-11 | 遵义医学院附属医院 | 一种内质网应激细胞模型的建立方法 |
| WO2020029221A1 (zh) * | 2018-08-10 | 2020-02-13 | 黄福星 | 具有抑制脂肪形成及抗氧化活性的组合物及其用途 |
| CN113876937A (zh) * | 2021-07-23 | 2022-01-04 | 中国科学院动物研究所 | Pzp的用途以及包括pzp的用于抵抗肥胖的药物组合物 |
Families Citing this family (25)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2902009B1 (fr) * | 2006-06-13 | 2012-12-07 | Bioprojet Soc Civ | Utilisation d'un inhibiteur de vasopeptidase pour le traitement de l'hypertension arterielle pulmonaire |
| GB0710976D0 (en) * | 2007-06-07 | 2007-07-18 | Bioalvo | Am Screening method |
| JP2009078977A (ja) * | 2007-09-25 | 2009-04-16 | Japan Health Science Foundation | 心筋の小胞体ストレス抑制剤 |
| AU2009246539B2 (en) * | 2008-05-12 | 2014-12-04 | Children's Medical Center Corporation | Methods and compositions for the treatment of obesity |
| US8524656B2 (en) | 2008-07-08 | 2013-09-03 | Jacques Galipeau | GM-CSF and truncated CCL2 conjugates and methods and uses thereof |
| CN102316872B (zh) | 2008-11-26 | 2016-12-21 | 萨蒂奥根制药公司 | 治疗肥胖症和糖尿病的胆汁酸再循环抑制剂 |
| WO2010062863A2 (en) * | 2008-11-26 | 2010-06-03 | Satiogen Pharmaceuticals, Inc. | Compositions containing satiogens and methods of use |
| CA2768851A1 (en) * | 2009-07-23 | 2011-01-27 | The Trustees Of Princeton University | Inhibitors of mtor kinase as anti-viral agents |
| KR20120080579A (ko) * | 2009-08-25 | 2012-07-17 | 프레지던트 앤드 펠로우즈 오브 하바드 칼리지 | 암 치료와 예방에 있어 메트포르민의 사용 |
| US20110294767A1 (en) | 2010-05-26 | 2011-12-01 | Satiogen Pharmaceuticals, Inc. | Bile acid recycling inhibitors and satiogens for treatment of diabetes, obesity, and inflammatory gastrointestinal conditions |
| TW201305098A (zh) * | 2010-10-27 | 2013-02-01 | Prometic Biosciences Inc | 用於糖尿病的化合物和藥物組合物 |
| WO2012109238A2 (en) | 2011-02-07 | 2012-08-16 | President And Fellows Of Harvard College | Methods for increasing immune responses using agents that directly bind to and activate ire-1 |
| US20130274184A1 (en) * | 2011-10-11 | 2013-10-17 | The Trustees Of Columbia University In The City Of New York | Er stress relievers in beta cell protection |
| CN104023727B (zh) | 2011-10-28 | 2017-04-05 | 鲁美纳医药公司 | 用于治疗小儿胆汁淤积性肝病的胆汁酸再循环抑制剂 |
| WO2013134774A1 (en) | 2012-03-09 | 2013-09-12 | Cornell University | Modulation of breast cancer growth by modulation of xbp1 activity |
| TW201823460A (zh) * | 2012-05-29 | 2018-07-01 | 美商再生元醫藥公司 | 生產細胞株增強子 |
| JP6403217B2 (ja) | 2013-07-30 | 2018-10-10 | 京都府公立大学法人 | 角膜内皮ecm治療薬 |
| WO2015048331A1 (en) | 2013-09-25 | 2015-04-02 | Cornell University | Compounds for inducing anti-tumor immunity and methods thereof |
| PL3064222T3 (pl) * | 2013-10-31 | 2021-04-19 | Kyoto Prefectural Public University Corporation | Lek terapeutyczny zawierający inhibitor sygnału tgf-beta w chorobach związanych z retikulum endoplazmatycznym i śmiercią komórki w śródbłonku rogówki |
| DK3203998T3 (da) * | 2014-10-10 | 2021-05-31 | Liminal Biosciences Ltd | Substituerede aromatiske forbindelser og farmaceutiske sammensætninger til forebyggelse og behandling af diabetes |
| CN106519002A (zh) * | 2016-10-18 | 2017-03-22 | 南通大学 | Grp78截短体及其应用 |
| CN115645535B (zh) * | 2017-03-06 | 2024-07-09 | 坪田实验室股份有限公司 | 小鼠近视诱导模型及用于近视预防/抑制的内质网应激抑制剂 |
| WO2019117454A1 (ko) * | 2017-12-12 | 2019-06-20 | 순천향대학교 산학협력단 | 세포 소기관 스트레스 조절 인자를 이용하는 고효율 세포전환용 배지 첨가제 |
| US11234992B2 (en) | 2018-02-28 | 2022-02-01 | The Regents Of The University Of California | Methods and therapies for treating atherosclerosis and/or hyperlipidemia using oligosaccharides |
| US20220175851A1 (en) * | 2019-03-13 | 2022-06-09 | The Regents Of The University California | Compositions, methods for regulating uterine, placental growth |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5605930A (en) * | 1991-10-21 | 1997-02-25 | The United States Of America As Represented By The Department Of Health And Human Services | Compositions and methods for treating and preventing pathologies including cancer |
| CA2147180A1 (en) * | 1992-10-15 | 1994-04-28 | Gokhan S. Hotamisligil | Treatment of insulin resistance in obesity linked type ii diabetes using antagonists to tnf-.alpha. function |
| EP0773029A4 (en) * | 1993-07-19 | 1997-09-03 | Tokyo Tanabe Co | HEPATITIS C VIRUS PROLIFERATION INHIBITOR |
| IT1276130B1 (it) * | 1995-11-14 | 1997-10-27 | Gentili Ist Spa | Associazione glibenclamide-metformina, composizioni farmaceutiche che la contengono e loro uso nel trattamento del diabete mellito di tipo |
| WO2002085396A1 (en) * | 2001-04-24 | 2002-10-31 | President And Fellows Of Harvard College | Inhibition of jun kinase |
| SE0202157D0 (sv) * | 2002-07-09 | 2002-07-09 | Biovitrum Ab | Methods for identification of compounds modulating insulin resistance |
| EP1572944A4 (en) * | 2002-08-30 | 2007-12-26 | Harvard College | METHOD AND COMPOSITIONS FOR MODULATING THE ACTIVITY OF XBP-1 |
| US7767402B2 (en) * | 2003-06-19 | 2010-08-03 | University Of Massachusetts | Methods and compositions for controlling appetite and modulating insulin sensitivity |
-
2005
- 2005-09-15 CN CNA2005800388745A patent/CN101056656A/zh active Pending
- 2005-09-15 WO PCT/US2005/032841 patent/WO2006031931A2/en active Application Filing
- 2005-09-15 AU AU2005284798A patent/AU2005284798B2/en not_active Ceased
- 2005-09-15 EP EP05808876A patent/EP1799263A4/en not_active Withdrawn
- 2005-09-15 CA CA002580370A patent/CA2580370A1/en active Pending
- 2005-09-15 JP JP2007532444A patent/JP2008513465A/ja active Pending
-
2009
- 2009-08-13 US US12/541,020 patent/US20100075894A1/en not_active Abandoned
Cited By (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2020029221A1 (zh) * | 2018-08-10 | 2020-02-13 | 黄福星 | 具有抑制脂肪形成及抗氧化活性的组合物及其用途 |
| JP2021534232A (ja) * | 2018-08-10 | 2021-12-09 | 黄福星HUANG Fuhsing | 脂肪形成抑制と抗酸化活性を有する組成物およびその用途 |
| JP7197701B2 (ja) | 2018-08-10 | 2022-12-27 | 黄福星 | 脂肪形成抑制と抗酸化活性を有する組成物およびその用途 |
| CN110317776A (zh) * | 2019-07-31 | 2019-10-11 | 遵义医学院附属医院 | 一种内质网应激细胞模型的建立方法 |
| CN113876937A (zh) * | 2021-07-23 | 2022-01-04 | 中国科学院动物研究所 | Pzp的用途以及包括pzp的用于抵抗肥胖的药物组合物 |
| CN113876937B (zh) * | 2021-07-23 | 2022-08-23 | 中国科学院动物研究所 | Pzp的用途以及包括pzp的用于抵抗肥胖的药物组合物 |
Also Published As
| Publication number | Publication date |
|---|---|
| CA2580370A1 (en) | 2006-03-23 |
| JP2008513465A (ja) | 2008-05-01 |
| AU2005284798A1 (en) | 2006-03-23 |
| EP1799263A2 (en) | 2007-06-27 |
| EP1799263A4 (en) | 2009-07-29 |
| WO2006031931A2 (en) | 2006-03-23 |
| WO2006031931A3 (en) | 2007-03-22 |
| US20100075894A1 (en) | 2010-03-25 |
| AU2005284798B2 (en) | 2012-02-02 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN101056656A (zh) | 在治疗肥胖症和糖尿病中降低er应力 | |
| CN1655804A (zh) | 神经调节蛋白用于心血管疾病治疗的方法和组合物 | |
| US20060073213A1 (en) | Reducing ER stress in the treatment of obesity and diabetes | |
| CN1356872A (zh) | 调节蛋白激酶活性和用于癌症化疗的3-亚杂芳基-2-吲哚满酮化合物 | |
| CN1870983A (zh) | 用于改善脂质代谢的组合物和食品 | |
| CN101048402A (zh) | 咔唑衍生物、其溶剂合物或其药学上允许的盐 | |
| CN1871239A (zh) | β-联蛋白/TCF激活转录的调节 | |
| CN101080408A (zh) | 三环杂环、它们的制备和作为药剂的应用 | |
| CN1921872A (zh) | 用于激活PPR-γ受体而治疗自身免疫性疾病和阿尔茨海默病的提取自穿心莲的半日花烷型二萜类组合物 | |
| CN1697654A (zh) | Cox-2抑制剂与抗病毒剂的组合在治疗乳头瘤病毒感染中的用途 | |
| CN101048139A (zh) | 药物活性化合物的控释组合物 | |
| CN101076331A (zh) | 包含烟酸受体部分促效剂的用于治疗发红和脂质相关病症的组合物 | |
| CN1165310C (zh) | 含有(e)-7-[4-(4-氟苯基)-6-异丙基-2-[甲基(甲基磺酰基)氨基]嘧啶-5基](3r,(5s)-3,5-二羟基庚-6-烯酸以及p450同工酶3a4的抑制剂,诱导剂或底物的药物组合物) | |
| CN1934101A (zh) | 脱氢苯基阿夕斯丁及其类似物以及脱氢苯基阿夕斯丁及其类似物的合成 | |
| JP7040798B2 (ja) | 非アルコール性脂肪性肝疾患を処置するための5-[[4-[2-[5-(1-ヒドロキシエチル)ピリジン-2-イル]エトキシ]フェニル]メチル]-1,3-チアゾリジン-2,4-ジオン | |
| CN1867562A (zh) | 四唑衍生物和其代谢相关的疾病的治疗方法 | |
| CN101039921A (zh) | 3-[5-氯-4-[(2,4-二氟苄基)氧基]-6-氧代嘧啶-1(6h)-基]-n-(2-羟乙基)-4-甲基苯甲酰胺的晶形 | |
| CN1220490C (zh) | 哌嗪环氧乙烷衍生物在制备用于诱导肿瘤细胞死亡的药物中的应用 | |
| CN1929833A (zh) | Hm74的氧杂十氢萘调节剂 | |
| CN1816533A (zh) | 包含缬沙坦的药物组合物 | |
| CN1307989C (zh) | 植烷酸在制备治疗糖尿病的药物中的用途 | |
| CN1394142A (zh) | 应用环醚制备影响葡萄糖耐量的药物 | |
| CN100341492C (zh) | 一种参芪降糖软胶囊及其制备检测方法 | |
| CN1364167A (zh) | G蛋白偶联受体6的小分子调节剂 | |
| CN1568993A (zh) | 治疗高血脂症的组合物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C12 | Rejection of a patent application after its publication | ||
| RJ01 | Rejection of invention patent application after publication |
Application publication date: 20071017 |