CN100482262C - 治疗免疫疾病的草药药物组合物 - Google Patents
治疗免疫疾病的草药药物组合物 Download PDFInfo
- Publication number
- CN100482262C CN100482262C CNB018204228A CN01820422A CN100482262C CN 100482262 C CN100482262 C CN 100482262C CN B018204228 A CNB018204228 A CN B018204228A CN 01820422 A CN01820422 A CN 01820422A CN 100482262 C CN100482262 C CN 100482262C
- Authority
- CN
- China
- Prior art keywords
- radix
- concentrate
- panacis quinquefolii
- pharmaceutical composition
- rhizoma pinelliae
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K36/00—Medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicines
- A61K36/18—Magnoliophyta (angiosperms)
- A61K36/185—Magnoliopsida (dicotyledons)
- A61K36/28—Asteraceae or Compositae (Aster or Sunflower family), e.g. chamomile, feverfew, yarrow or echinacea
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K36/00—Medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicines
- A61K36/06—Fungi, e.g. yeasts
- A61K36/062—Ascomycota
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K36/00—Medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicines
- A61K36/18—Magnoliophyta (angiosperms)
- A61K36/185—Magnoliopsida (dicotyledons)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K36/00—Medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicines
- A61K36/18—Magnoliophyta (angiosperms)
- A61K36/185—Magnoliopsida (dicotyledons)
- A61K36/25—Araliaceae (Ginseng family), e.g. ivy, aralia, schefflera or tetrapanax
- A61K36/258—Panax (ginseng)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K36/00—Medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicines
- A61K36/18—Magnoliophyta (angiosperms)
- A61K36/185—Magnoliopsida (dicotyledons)
- A61K36/34—Campanulaceae (Bellflower family)
- A61K36/344—Codonopsis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K36/00—Medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicines
- A61K36/18—Magnoliophyta (angiosperms)
- A61K36/185—Magnoliopsida (dicotyledons)
- A61K36/48—Fabaceae or Leguminosae (Pea or Legume family); Caesalpiniaceae; Mimosaceae; Papilionaceae
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K36/00—Medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicines
- A61K36/18—Magnoliophyta (angiosperms)
- A61K36/185—Magnoliopsida (dicotyledons)
- A61K36/48—Fabaceae or Leguminosae (Pea or Legume family); Caesalpiniaceae; Mimosaceae; Papilionaceae
- A61K36/484—Glycyrrhiza (licorice)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K36/00—Medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicines
- A61K36/18—Magnoliophyta (angiosperms)
- A61K36/88—Liliopsida (monocotyledons)
- A61K36/888—Araceae (Arum family), e.g. caladium, calla lily or skunk cabbage
- A61K36/8888—Pinellia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/02—Nasal agents, e.g. decongestants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/04—Antipruritics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
- A61P27/14—Decongestants or antiallergics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/08—Antiallergic agents
Landscapes
- Health & Medical Sciences (AREA)
- Natural Medicines & Medicinal Plants (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Engineering & Computer Science (AREA)
- Mycology (AREA)
- Botany (AREA)
- Epidemiology (AREA)
- Medical Informatics (AREA)
- Microbiology (AREA)
- Biotechnology (AREA)
- Alternative & Traditional Medicine (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Pulmonology (AREA)
- Immunology (AREA)
- Rheumatology (AREA)
- Physical Education & Sports Medicine (AREA)
- Dermatology (AREA)
- Pain & Pain Management (AREA)
- Ophthalmology & Optometry (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Otolaryngology (AREA)
- Medicines Containing Plant Substances (AREA)
- Medicinal Preparation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
本发明提供了药物组合物,其包含沿阶草属植物(沿阶草),半夏属植物(半夏),生甘草属植物(甘草根)和一种选自下述物质的草药:长柄菊,台湾adenostema,或鱼腥草。备选地,可以加入第五种草药,其可以是党参或西洋参。这些药物组合物对于治疗患有免疫疾病,特别是IgE介导的疾病的患者是有效的,所述IgE介导的疾病例如哮喘,特异性反应性湿疹,特异性反应性皮炎,过敏性鼻炎和类风湿性关节炎。本发明还提供了制备药物组合物的方法。
Description
发明领域
本发明涉及药物组合物,它们治疗具有免疫疾病的患者的应用,和制备药物组合物的方法。具体地,药物组合物包含草药,它们是(1)沿阶草属植物(麦冬(Tuber Ophiopogonis)),(2)半夏属植物(半夏(TuberPinelliae)),(3)生甘草属植物(甘草根(Radix Glycyrrhizae)),和(4)下述草药的一种:长柄菊(lantern tridax)(Herba Tridacis procumbentis),台湾adenostema(Herba Adenostematis)和鱼腥草(heartleaf houttuynia)(Herbahouttuyniae)。任选地,可加入第五种草药,其是党参(tang-shen)(RadixCodonopsitis)或西洋参(Radix Pancis Quinquefolii)。草药药物组合物被用来有效治疗免疫球蛋白E(Ig E)介导的疾病,其包括,但不局限于过敏性鼻炎,过敏性结膜炎,过敏性哮喘,特异反应性湿疹,特异反应性皮炎,食物过敏,高IgE综合征,和类风湿性关节炎。
发明背景
抗原诱导的,特别是过敏原诱导的免疫疾病折磨着超过20%的世界人口,并且导致严重的健康问题。这类免疫疾病的一个实例是哮喘。在近几年,过敏反应相关的免疫疾病的发作已转向较年轻的人群,并且越来越多的儿童和青少年已表现过敏原诱导的免疫疾病的症状。
例如,在台湾,小儿哮喘的流行从1974年的1.3%增加到1985年的5.07%和1991年的5.8%。同样,过敏性鼻炎的发病率从1985年的7.84%增加到1991年的20.67%。另外,遗传性过敏性湿疹1974年为1.43%,增加到1985年的1.23%和1991年的3.84%。早期发作的过敏原相关的免疫疾病可能是由于环境污染引起的。
呼吸性过敏反应是Ig E介导的免疫反应。Brinker,自然疗法医学杂志(J.Naturopathic Medicine)4:64-68(1993)。存在两种主要的呼吸性过敏反应:过敏性鼻炎和过敏性支气管哮喘。过敏性鼻炎,也已知为枯草热,是由抗原/Ig E与致敏的肥大细胞和嗜碱性粒细胞结合引起的。所述结合导致cAMP降低,其反过来导致esosinophil趋化因子和组胺的释放。然后,组胺结合H1-受体,并导致血管舒张、毛细血管渗透性和平滑肌收缩的增加,如同被带有清涕的鼻充血、打喷嚏和眼睛发痒所证实。
过敏性哮喘是另一种Ig E介导的免疫反应,其中肥大细胞释放组胺,舒缓激肽和花生四烯酸代谢物包括过敏反应的白细胞三烯慢反应物和血栓烷/前列腺素支气管收缩药。血小板激活因子是许多白细胞释放的另一种有效的哮喘介质。在这种条件下,cAMP减少后释放的组胺作用于H1受体,引起支气管痉挛;由于胆碱能的反射作用和在过敏反应中产生部分前列腺素,组胺也导致支气管收缩。
由于受影响的人群的百分比和疾病的严重程度在增加,对过敏反应的治疗方法仍然主要依赖于经验和意外发现而不是依赖于科学方法。大多数过敏患者用针对于控制由效应细胞释放的介质产生的症状的药物来进行治疗。某些药物似乎短期内能有效缓解症状而没有副作用,然而,还没有发现对于防止疾病恶化和持久破坏长期有效而没有任何副作用的药物。例如,已知长期口服疗法如类固醇疗法治疗哮喘与多数衰弱作用如生长延缓,骨质疏松症和肾上腺抑制相关。
传统的中国草药和药物结合提供了一种治疗免疫疾病的备选方案。已知传统的中国草药和草药化合物能提高免疫系统功能和治疗各种慢性(chronicle)免疫疾病。例如,Hamasaki等.,民族药物学杂志(J.Ethnopharmacology),(1997)56:123-131公开了中国草药—Shinpi-To,其抑制在大鼠嗜碱性粒细胞性白血病-2H3细胞中Ig E介导的白细胞三烯合成。Shinpi-To是冻干颗粒状的中国草药,从7种药用草药包括草麻黄(Ephedra sinica Stapf),杏(Prunus armeniaca Linne),厚朴(Magnolia obovataThunberg),陈皮(Citrus unshiu Markovich),甘草(Glycyrrhiza uvalensisFischer),柴胡(Bupleurum falcatum L),和紫苏(Perillae herba)(Perillafrutescens Britton var.acuta Kudo)的提取物中制得。Shinpi-To用于治疗小儿哮喘。
Toda等.,民族药物学杂志(J.Ethnopharmacology)(1988)24:303-309公开了中国草药—Saiboku-To,其显示对小鼠腹膜肥大细胞释放组胺的抑制作用。Saiboku-To包含10种草药,包括柴胡(Bupleurum falcatum L.),半夏(Pinelliae ternata Breitenbach),茯苓(Poria cocos Wolf),黄苓(Scutellaria baicalensis Georgi),中国枣(Zizyhus vulgaris Lam),人参(Panaxginseng C.A.Meyer),厚朴(Magnolia obovata Thunberg),光果甘草(Glycyrrhiza glabra L.),紫苏(Perilla frutescens Britton var.acuta Kudo)和姜(Zingiber officinale Roscoe)。
Li等.,免疫药理学(Immunopharmacology),(1999),43:11-21公开了中国草药—Hochu-Ekki-To,其显示对修复压力诱导的免疫抑制的作用。Hochu-Ekki-To由10种成分组成,包括人参(Ginseng Rx),Atractylodis albaRz,Astragali Rx,当归(Angelicae sinensis Rx),大枣(Jujubae Fr),Citrireticulatae Pc,柴胡(Bupleuri Rx),甘草(Glycyrrhizae Rx),Preparata,Zingiberis recens Rz,和升麻(Cimicifugae Rz)。
Zou等.,中国传统和西方医学杂志(Chinese Traditional and Western Medical Magazine),529-532(1996)公开了中国草药—Wenyang Tongluo混合物,来治疗寒型哮喘。它显示了提供肺通气功能、调节外周血淋巴细胞的肾上腺素β-受体、降低5-羟色胺的血清水平的作用。Wenyang Tongluo混合物包含12种草药,包括红参(Red Ginseng),Zhi Fu Pian,Yin Yang Huo,干姜(Zingiberis recens Rz.),Zhi Huang Zhi,当归(Angelicae sinesis Rx),麻黄(Ephedra),Polygalae Rx,桑白皮(Sang Baipi),生石膏(Sheng Shi Gao),五味子(Schisandrae Fr)和甘草(Glycyrrhizae Rx.Preparata)。
治疗之气管炎和支气管哮喘的煎剂已公开于国际互联网(www.herb.com.tw)。所述煎剂由6种草药制得,包括麦冬(OphiopogonisRx),半夏(Pinelliae Rz),Preparata,Oryzae Sm,大枣(Jujubae Fr),人参(Ginseng Rx),和甘草(Glycyrrhizae Rx)。
在从草药中开发药物组合物过程中,中国草药的质量控制是关键。草药的含量和活性成分可能随着一些因素如生长条件和生长位置、收获季节和技术、和收获草药的制造和加工而波动。如果不满足这些关键因素的任何一种,则可能草药的功效受到影响。然而,尚没有报道或采纳可靠监测中国草药的质量的科学方法。
本发明提供了新的并且无毒的药物组合物,其得自主要发现于中国和台湾的草药。在任何文献或报道中尚未发现结合使用这些草药。这些药物组合物能有效治疗患有免疫疾病,特别是Ig E介导的疾病。已证实本发明的药物组合物特别作用于白细胞介素4(IL-4)合成的负调节和抑制Ig E。另外,为有效控制草药的质量,本发明利用薄层层析法(TLC)和高效液相色谱(HPLC)对每种草药进行指纹图谱,以保证用于组合物的每种草药包含一致的和重现的成分。
发明概述
本发明提供了药物组合物,其包含沿阶草属植物(麦冬),半夏属植物(半夏),生甘草属植物(甘草根)作为必需草药,和选自长柄菊,台湾Adenostema,和鱼腥草的草药。本发明的药物组合物还包含草药党参或西洋参。优选的草药重量比,沿阶草属植物:半夏属植物:生甘草属植物:西洋参/党参:长柄菊/台湾Adenostema/鱼腥草为3:2:1:1:1。
最优选的药物组合物包含沿阶草属植物,半夏属植物,生甘草属植物,西洋参和长柄菊。这些草药的有效成分可以用水或有机溶剂提取,也可以是直接研磨草药获得的粉末形式。
在一个实施方案中,药物组合物包含水性提取物形式的沿阶草属植物,其余的草药为粉末形式。沿阶草属植物的水性提取物优选通过在水中提取来制备。
在另一个实施方案中,药物组合物包含沿阶草属植物、半夏属植物、生甘草属植物和西洋参的水性提取物,优选通过在水中提取来制备;和长柄菊的水性提取物,优选在醇(最优选在50%醇)中提取来制备。
本发明还提供了制备药物组合物的方法,其中制备了草药的水性提取物和/或粉末。在一个实施方案中,除了沿阶草属植物,所有其它草药切成片状,脱水,研磨,并通过筛网来生产草药粉末。通过在水中煎煮和浓缩沿阶草属植物来提取沿阶草属植物的成分。然后通过使浓缩的沿阶草属植物—水混合物通过筛网获得沿阶草属植物提取物(被过滤的)。其次,将沿阶草属植物滤液与草药粉末混合以形成草药混合物。然后将草药混合物置于流动造粒机中以生产颗粒。任选过筛颗粒以生产具有均匀大小的颗粒。
在另一个实施方案中,如下制备药物组合物:
(a)优选单独过滤和浓缩每种沿阶草属植物,半夏属植物,生甘草属植物,西洋参和长柄菊的水性提取物。(b)除了不被制粒的沿阶草属植物,从浓缩物中分别制粒每种半夏属植物,生甘草属植物,西洋参和长柄菊的浓缩物,以形成单独的颗粒。(c)在制粒前,向浓缩物中加入赋形剂,优选玉米淀粉,以获得合适形式的颗粒。(d)然后将各单独的颗粒和沿阶草属植物浓缩物一起混合以形成混合的颗粒,然后将这些颗粒包入胶囊。
优选地,沿阶草属植物浓缩物的固体内容物为沿阶草属植物原材料的约20-30%重量,优选约25%重量。浓缩物的固体内容物是除水之外的浓缩物。就沿阶草属植物而言,浓缩物包含大量的水(即约58%的沿阶草属植物浓缩物是水)。其余草药的固体内容物约与浓缩物相同(即,忽略水含量)。半夏属植物的浓缩物为半夏属植物原材料的约15-25%重量,优选约20%重量。生甘草属植物的浓缩物为生甘草属植物原材料的约15-25%重量,优选约20%重量。西洋参的浓缩物为西洋参原材料的约19-29%重量,优选约24.3%重量。长柄菊的浓缩物为长柄菊原材料的约5-10%重量,优选约7.8%重量。
半夏属植物颗粒为半夏属植物原材料的约20-30%重量,优选约25%重量。生甘草属植物颗粒为生甘草属植物原材料的约16-26%重量,优选约21%重量。西洋参颗粒为西洋参原材料的约27-37%重量,优选约32%重量。长柄菊颗粒为长柄菊原材料的约37-47%重量,优选42%重量。
同样,该方法需要分别对沿阶草属植物、半夏属植物、生甘草属植物、西洋参和长柄菊进行提取。另外,通过煎熬,在水中提取沿阶草属植物、半夏属植物、生甘草属植物和西洋参。通过回流,在醇,优选50%醇中提取长柄菊。提取后,过滤每个单独的提取物,以去除残留的草药。然后,在约55℃的温度,约30托的真空下,通过减压浓缩对滤液进行浓缩,以形成浓缩物。除了沿阶草属植物,向每种浓缩物中加入适量的赋形剂,优选玉米淀粉,以形成提取膏,其在约105℃的入口温度和约76-77℃的出口温度下,通过喷雾干燥进行制粒。将来自半夏属植物、生甘草属植物、西洋参和长柄菊的各自颗粒与沿阶草属植物的浓缩物混合,以形成混合的颗粒,这些颗粒可包入胶囊。
另外,水性提取物的体积与草药的重量的比率约为20:1。对于水提取,优选的煎熬时间约为30分钟。优选的醇提取时间也约为30分钟。
本发明的两种药物组合物,一种包含沿阶草属植物的水提取物和其它草药的粉末,另一种包含所有草药的水提取物,这两种组合物均对治疗免疫疾病有效。然而,包含所有草药的水提取物的药物组合物是比较受欢迎的,因为证实了它比含沿阶草属植物的水提取物和其它草药粉末的药物组合物具有更好的药效和功效。这两种方法的治疗效果的不同可能是由于在提取过程中,活性成分释放的效力增加的缘故。
本发明的药物组合物在治疗患有免疫疾病,特别是Ig E介导的疾病的患者是有效的,所述疾病包括,但不局限于过敏性鼻炎,过敏性结膜炎,过敏性哮喘,特异反应性皮炎,食物过敏,高IgE综合征,特异反应性湿疹,和类风湿性关节炎。
附图简述
图1表示沿阶草属植物的HPLC色谱图。利用方法1的HPLC分析(参见下文),在214nm波长处检测它的完整色谱图。色谱图显示,存在两个离散峰,6115-1和6115-2,它们分别具有11.5分钟和13分钟的保留时间。这两个峰可用于鉴定沿阶草属植物。
图2表示半夏属植物的HPLC色谱图。利用方法2的HPLC分析,在260nm波长处检测到两个化学标记腺嘌呤和鸟苷。腺嘌呤具有14.8分钟的保留时间。鸟苷具有17分钟的保留时间。
图3表示生甘草属植物的HPLC色谱图。利用方法1的HPLC分析,在250nm波长处检测到化学标记甘草甜(Gly)。Gly具有46.4分钟的保留时间。
图4表示西洋参的HPLC色谱图。利用方法3的HPLC分析,在203nm波长处检测到化学标记人参皂甙Rb1(Rb1)。Rb1具有37.5分钟的保留时间。
图5表示长柄菊的HPLC色谱图。利用方法2的HPLC分析,在250.0nm波长处检测到4个独特的峰,FY-1—FY-4。FY-1具有28分钟的保留时间。FY-2具有31.6分钟的保留时间。FY-3具有33.5分钟的保留时间。FY-4具有18.3分钟的保留时间。
图6表示吸入Der p5激发,然后用5(A-F)煎剂组处理后,Der p5(屋尘螨(Dermatophagoides pteronyssimus)过敏原5)特异性Ig G和Ig E抗体的水平。用ELISA测量血清Ig G和Ig E水平。数值是平均值±SEM,条框指示SEM。A:White-Draining粉末组;B:Green-Blue Dragon煎剂组;C:沿阶草属植物煎剂组;D:Dryness-Clearing lung-Rescuing煎剂组;E:苏子Qi-Downbearing煎剂组(Perilla Fruit Qi-Downbearing Decoctiongroup);和F:安慰剂组。
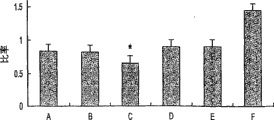
图7表示吸入Der p5激发,然后用5(A-F)煎剂组处理后,IL-4基因在脾细胞中的表达。用RT-PCR(逆转录-聚合酶链式反应)确定IL-4基因的表达。数值为平均值±SEM,条框指示SEM。A:White-Draining粉末组;B:Green-BlueDragon煎剂组;C:沿阶草属植物煎剂组;D:Dryness-Clearing lung-Rescuing煎剂组;E:苏子Qi-Downbearing煎剂组;和F:安慰剂组。*指示p<0.05。
图8表示用过敏原Der p5(屋尘螨过敏原5)激发和用单独的草药治疗后小鼠血清Ig G水平。泳道1表示沿阶草属植物治疗的作用。泳道2表示党参治疗的作用。泳道3表示半夏属植物治疗的作用。泳道4表示生甘草属植物治疗的作用。泳道5是安慰剂治疗。用ELISA测量血清Ig G水平。数值为平均值±SEM,条框指示SEM。
图9表示Der p5(屋尘螨过敏原5)激发和用单独的草药或药物组合物(即,STA-36,下文)治疗后小鼠血清Ig E水平。泳道1表示沿阶草属植物治疗的作用。泳道2表示党参治疗的作用。泳道3表示半夏属植物治疗的作用。泳道4表示生甘草属植物治疗的作用。泳道5表示STA-36治疗的作用。泳道6是安慰剂治疗。用ELISA测量血清Ig G水平。数值为平均值±SEM,条框指示SEM。
图10表示Der p5(屋尘螨过敏原5)激发和用单独的草药或药物组合物(即,STA-36,下文)治疗后,在小鼠脾细胞中IL-4基因的表达。用RT-PCR(逆转录-聚合酶链式反应)确定IL-4基因的表达。泳道1表示沿阶草属植物治疗的作用。泳道2表示党参治疗的作用。泳道3表示半夏属植物治疗的作用。泳道4表示生甘草属植物治疗的作用。泳道5表示STA-36治疗的作用。泳道6是安慰剂治疗。
图11比较了下述形式的西洋参对IgG2a和IgE水平的作用:(1)粉末,(2)在95%醇中的水性提取物,(3)在水中的水性提取物,和(4)在50%醇中的水性提取物。数值是平均值±SEM。图形表示根据降低IgE和增加IgG,用50%醇提取的西洋参产生了比用水提取的西洋参稍强的作用。
图12比较了下述形式的长柄菊对IgE、IgG2a、IL-4和IFN-γ水平的作用:(1)粉末,(2)在95%醇中的水性提取物,(3)在水中的水性提取物,和(4)在50%醇中的水性提取物。数值是平均值±SEM。*表示与对照明显的不同。结果指出长柄菊的50%乙醇提取物对抑制IgE和增加IgG最有效。
图13是雌性BALB/c小鼠血清中,STA-36,STA-34和对照(安慰剂组)对IgG和IgE作用的比较研究。*表示在STA-4和对照之间显著差异(p<0.05)。数值是平均值±SEM。STA-36的剂量(20mg/20g小鼠)为STA-4剂量((10mg/20g小鼠)的两倍(即STA-3:STA-4=2:1)。结果表示根据IgE,尽管STA-36和STA-4均表现对IgE的抑制,但相对于对照而言,仅STA-4是具有统计学意义。对于IgG,STA-36和STA-4均表现IgG的增加。然而,尽管在IgG水平方面,STA-36比STA-4显示较大的增加,但没有增加相对于对照而言是具有统计学意义的。
图14是STA-36和STA-4对肺功能的作用的比较研究。数值是平均值±SEM。与对照相比,在肺功能方面,STA-36和STA-4均表现明显的改善(如通过测量乙酰胆碱所确定的)。在STA-36和STA-4的治疗之间,尽管STA-4比STA-36的作用强,然而STA-36和STA-4之间的差异不具有统计学意义,这可能是由于每组使用的动物数量不足的缘故。STA-36的剂量(20mg/20g小鼠)是STA-4剂量(10mg/20g小鼠)的两倍。
图15比较了STA-4和那些传统药物(用来治疗哮喘)包括酮替芬,强的松龙,和Aminophline对IgE、IgG、IL-4和IFN-γ的作用。数值是平均值±SEM。*表示与对照明显不同。本研究结果指出STA-4显著降低了IgE水平,但显著增加了IgG2a,Il-4和IFN-γ水平。
发明详述
抗原或过敏原介导的哮喘是主要由于慢性炎症反应导致的呼吸道疾病。炎症反应通过细胞释放炎性因子例如血小板激活因子、组胺、前列腺素和白细胞三烯而被介导。炎症反应刺激T淋巴细胞(T细胞),特别是CD4+细胞中的抗原应答。存在两种类型的CD4+细胞,Th1和Th2CD4+细胞。Th1型CD4+细胞分泌细胞因子(IFN-γ)。Th2型CD4+细胞分泌白细胞介素-4(IL-4)。大多数过敏性哮喘患者是Th2型。过敏原刺激Th2细胞产生过量的IL-4,其反过来诱导B淋巴细胞产生和分泌IgE。
本发明提供了7种药物组合物:STA-31,STA-32,STA-33,STA-34,STA-35,STA-36,和STA-4。所有的组合物具有对免疫疾病,特别是对抑制IgE产生和负调节白细胞介素-4(IL-4)基因合成的药物作用。草药药物组合物的草药含量示于表1中。
表1.药物组合物中的草药组成
| 草药组成 | 草药#1(制剂形式) | 草药#2(制剂形式) | 草药#3(制剂形式) | 草药#4(制剂形式) | 草药#5(制剂形式) |
| STA-31 | 沿阶草属植物(aq.ext.) | 半夏属植物(粉末) | 生甘草属植物(粉末) | 党参(粉末) | Adenostema(粉末) |
| STA-32 | 沿阶草属植物(aq.ext.) | 半夏属植物(粉末) | 生甘草属植物(粉末) | 党参(粉末) | 鱼腥草(粉末) |
| STA-33 | 沿阶草属植物(aq.ext.) | 半夏属植物(粉末) | 生甘草属植物(粉末) | 党参(粉末) | Tridax(粉末) |
| STA-34 | 沿阶草属植物(aq.ext.) | 半夏属植物(粉末) | 生甘草属植物(粉末) | 人参(粉末) | Adenostema(粉末) |
| STA-35 | 沿阶草属植物(aq.ext.) | 半夏属植物(粉末) | 生甘草属植物(粉末) | 人参(粉末) | 鱼腥草(粉末) |
| STA-36 | 沿阶草属植物(aq.ext.) | 半夏属植物(粉末) | 生甘草属植物(粉末) | 人参(粉末) | Tridax(粉末) |
| STA-4 | 沿阶草属植物(aq.ext.) | 半夏属植物(aq.ext.) | 生甘草属植物(aq.ext.) | 人参(aq.ext.) | Tridax(50%醇提取物) |
aq.ext.=用水提取的水性提取物;沿阶草属植物=麦冬;半夏属植物=半夏;生甘草属植物=甘草根;党参=Radix Codonopsitis;人参=西洋参;Adenostema=下田菊(HerbaAdenostemmatis);鱼腥草=鱼腥草;Tridax=长柄菊。
在7种组合物中,优选STA-36组合物,最优选STA-4组合物。STA-36和STA-4治疗免疫疾病包括抑制IgE产生特别有效。
每种药物组合物包含5种草药,其中3种是必需的草药。必需的草药是沿阶草属植物(也已知为黑韭葱),半夏属植物和生甘草属植物。第四种草药可以是党参或西洋参。第五种草药选自台湾adenostema,长柄菊和鱼腥草。依照可利用的草药文献,仅在台湾发现了台湾adenostema和鱼腥草。在台湾和南美州发现了长柄菊。组合物的药名,植物名,科和主要成分示于表2中。
表2.STA药物组合物中草药的药名/植物名和主要成分
| 草药 | 药名 | 植物/动物名 | 科 | 主要成分 |
| 沿阶草属植物(黑韭葱) | TuberOphiopogonisJaponici | 麦冬KerGawl | 百合科 | 麦冬皂甙,鲁斯可皂甙元,β-谷甾醇,豆甾醇 |
| 党参 | RadixCodonopsitisPilosulae | Codonopsispilosula(Franch.)Nannf. | 桔梗科 | 皂甙,生物碱,蒲公英赛醇乙酸酯,木栓酮,蔗糖,葡萄糖,菊糖 |
| 西洋参 | Radix PanacisQuinquefolii | PanaxquinquefoliumL | 五加科 | 皂甙,人参甙 |
| 半夏属植物 | 半夏,Rhizoma | 半夏 | 天南星科 | 毒芹碱,原白头翁脑,高龙胆酸,尼古丁,天冬氨 |
| PinelliaTernatae | 酸,谷氨酸,精氨酸,β-谷甾醇,胆固醇 | |||
| 生甘草属植物 | 甘草节(梢) | Glycyrrhizaeuralensis Fisher或洋甘草Linné(Glycyrrhizaglabra Linné) | 豆科 | 吖啶-2-羧酸,天冬氨酸,高丝氨酸,二氨基丁酸,洋地黄糖苷 |
| 长柄菊 | Herba Tridacisprocumbentis | TridaxprocumbensLinn. | 菊科 | 多糖 |
| 台湾Adenostema | HerbaAdenostemmatis | Adenostemalavenia(L.)Ktze. | 菊科 | |
| 鱼腥草 | 鱼腥草 | 蕺菜 | 三白草科 | 癸酰基乙醛,月桂醛,甲基-正-壬酮,月桂烯,癸醛,癸酸,蕺菜碱,硫酸钙,氯化钙,异槲皮甙,瑞诺甙,金丝桃甙 |
沿阶草属植物(沿阶草属植物根)属于百合科。沿阶草属植物的块茎(根)具有药用的作用。沿阶草属植物的最佳收获季节是夏季。收获后,清洗干净沿阶草属植物的块茎,以去除不需要的污垢或支根,在阳光下干燥后保存以备后用。沿阶草属植物的块茎是根的增大部分。可在中国的一些省份如浙江,四川和江苏找到沿阶草属植物。Yu等.(1991),China Journal of Chinese Materia Medica,16:584-585报道了沿阶草属植物的水提取物可促进小鼠中静脉注射炭颗粒的清除,拮抗由clophosphamide引起的白细胞减少。为了在草药组合物中被有效地利用,可用由水或其它有机溶剂提取的水性提取物来制备麦冬。优选草药的剂型是用水提取的提取物。
党参属于桔梗科。党参的药用部分在根部。可收集野生或栽培的党参。党参的典型收获季节是秋季。收获后,在阳光下干燥党参的根,并切成段以备用。可在台湾的南投县和台中县找到党参。为了在草药组合物中被有效地利用,可通过用水或其它有机熔剂提取的水性提取物或研磨未加工的草药得到的粉末来制备草药。优选的草药制剂是通过用水提取的水性提取物或研磨的粉末。
西洋参属于五加科。西洋参的药用部分在根部。可在北美和加拿大找到西洋参。在法国和中国北方也广泛栽培有西洋参。西洋参的最佳收获季节是秋季。为了在草药组合物中被有效地利用,可通体用水或其它有机溶剂提取的水性提取物或研磨的粉末形式来制备。优选的草药剂型是通过用水提取的水性提取物或研磨的粉末。
半夏属植物(半夏,Rhizoma Pinellia Ternata)属于天南星科。半夏属植物的块茎(去除木栓层后)具有药用的作用。这类植物生长在中国的四川,河北,河南,贵州和安徽省。半夏属植物的正常收获季节是在7月和9月之间。半夏属植物可在台湾的台中县找到。为了在草药组合物中被有效地利用,可通过用水或其它有机溶剂提取的水性提取物或研磨的粉末来制备草药。优选的草药剂型是用水提取的水性提取物或研磨的粉末。
生甘草属植物(甘草节(梢))属于豆科。生甘草属植物的具有(未削皮)或不具有(削皮)周皮的根和生殖根具有药用的作用。以干燥的材料来计算,生甘草属植物包含不少于2.5%的甘草酸(C42H62O16),其可用作生甘草属植物的化学标记。可在中国内蒙古,甘肃,新疆和中国东北找到生甘草属植物。生甘草属植物的最佳收获季节是春季或秋季。在台湾,可在台中县找到生甘草属植物。甘草属植物的根具有抗炎症性能,并且可单独使用,以有助于缓解哮喘的症状。参见H.W.Morningstar,Sentient Times:Alternative for Personal and Community Transformation(1998),6:16-17。甘草属植物的根还可用于治疗支气管炎。参见T.David,Miracle Medicines of the Rainforest:A Doctor′s Revolutionary Work With Cancer And AIDS Patients(1997),66-79页。为了在草药组合物中被有效地利用,可通过用水或其它有机溶剂提取的水性提取物或以研磨的粉末形式来制备草药。优选的草药剂型是用水提取的水性提取物或研磨的粉末。
长柄菊属于菊科。长柄菊的药用作用来自于干燥的整株植株。可在台湾的南头县,台中县和云林县和台中市找到长柄菊。也能在南美找到长柄菊。Diwan等.,Indian Journal of Physiology & Pharmacology(1983),27:32-36公开了长柄菊叶的叶汁提取物具有类似于地塞米松对伤口收缩和肉芽形成的作用,但明显中和了地塞米松对抗张强度和上皮形成的作用。Gan等.,China Medical College Annual Bulletin(1977),8:526公开了长柄菊的叶可用于减轻炎症,缓解发热的症状,和治疗肺炎和咳嗽。
为了在草药组合物中被有效地利用,可通过用水或其它有机溶剂提取的水性提取物或以研磨粉末的形式来制备长柄菊。优选的草药剂型是研磨的粉末或用醇,优选用50%的醇提取的水性提取物。
台湾adenostema(Herba Adenostemmatis)属于菊科。台湾adenostema通常生长在近水或湿地。台湾adenostema的药用作用来自于整株植株,可以新鲜或干燥的形式使用。最佳收获季节是夏季或早秋。不仅可在台湾,而且可在中国的云南,广西,贵州,江西和浙江找到台湾adenostema。台湾adenostema包含11-羟基化的kauranic acid。为了在草药组合物中被有效地利用,可以研磨的粉末形式来制备草药。优选的草药剂型是研磨的粉末。
鱼腥草(Heartleaf houttuynia或Houttuynia Herb)(Houttuyniae cumRadice Houttuyniae Cordatae)是蕺菜的地上部分。它属于三白草科。鱼腥草遍布长江流域和中国的南方生长。最佳收获季节是晚夏和早秋之间的开花季节。可在台湾的台中县找到Hanhong鱼腥草。为了在草药组合物中被有效地利用,可以研磨粉末的形式来制备草药。优选的草药剂型是研磨的粉末。
通常,如下制备组合物:
A.STA-31,STA-32,STA-33,STA-34,STA-35和STA-36的制备:
(1)切下半夏属植物、生甘草属植物和西洋参的根和长柄菊的整株植株,脱水,研磨并通过筛网(优选40-120目),以产生草药粉末。
(2)将沿阶草属植物的根切成小片,并浸入到煎药容器的水中,其中水的体积至少高于沿阶草属植物顶部10cm。在97-103℃下加热被浸没的沿阶草属植物约60分钟,煎煮两次,以产生沿阶草属植物提取物溶液。然后,将沿阶草属植物提取物溶液通过筛网(约100目)。收集滤液。然后在50-60℃,压力为400-650mm-Hg的真空条件下浓缩沿阶草属植物滤液,以获得具有理想浓度的液体浓缩物。优选液体浓缩物为沿阶草属植物滤液的约1/14。
(3)将沿阶草属植物的液体浓缩物与其余草药的草药粉末混合。然后将混合物移至流化制粒机中,并置于由过滤用的织物制成的喷射管中。将制粒机的温度调至90-110℃。预热约5分钟后,以每次约40-55秒的时间喷射混合物,喷射适当的次数,并以每10秒钟的频率轻拍喷射管。制粒后,干燥颗粒,然后冷却。使颗粒通过筛网,并包装在PE袋中。颗粒的优选的水含量为少于6%。可将颗粒进一步包囊于任何传统的胶囊中,所述胶囊包括,但不局限于天然明胶,果胶,酪蛋白,胶原质,蛋白质,改性淀粉和聚乙烯吡咯烷酮。
B.STA-4草药组合物的制备:
用下述方法制备STA-4草药组合物:
I.对于长柄菊:
(1)将长柄菊的整株植株切成小片。
(2)加入约20倍(以体积计)的50%醇(体积/体积)(即,提取剂),并与约1倍(以重量计)的小片长柄菊混合。
(3)通过回流加热来加热草药和它的提取剂,加热约30分钟。该过程产生了长柄菊的醇提取物。
(4)提取物冷却后,通过筛网(约100目)过滤长柄菊醇提取物。收集滤液。然后用减压浓缩法,在50-60℃(优选55℃)的温度下,在真空条件下(30托)浓缩滤液,以获得浓缩物。优选地,浓缩物的固体含量为原材料重量的约7.8%。浓缩物的固体内容物是除50%醇外的浓缩物。对于长柄菊而言,浓缩物的固体内容物约与浓缩物相同(因为在浓缩物中仅存在非常少量的水)。
(5)向浓缩物中加入适量的玉米淀粉(作为赋形剂),以产生草药膏。
(6)用喷雾-干燥法干燥草药膏,以形成长柄菊颗粒(优选约为原材料重量的42%)。
II.对于半夏属植物,生甘草属植物和西洋参:
(1)分别将半夏属植物的块茎和甘草属植物的根和西洋参的根切成小片。
(2)对于每种草药,分别加入约20倍(以体积计)的水,并与约1倍(以重量计)的单个草药小片混合。
(3)通过煎煮加热浸没在水中的每种草药约30分钟,导致分别产生沿阶草属植物,半夏属植物,生甘草属植物和西洋参的水提取物。
(4)冷却各自的提取物后,将每种提取物分别通过筛网(约100目)过滤。收集每种滤液,然后用减压浓缩法在50-60℃(优选55℃)的温度下,在真空条件下(30托)浓缩滤液,以获得每种草药的液体浓缩物。优选地,半夏属植物浓缩物的固体内容物为半夏属植物原材料的约20%;生甘草属植物浓缩物的固体内容物为生甘草属植物原材料的约20%;西洋参浓缩物的固体内容物为西洋参原材料的约24.3%。半夏属植物、生甘草属植物或西洋参的浓缩物的固体内容物是除水以外的浓缩物。
(5)向每种浓缩物中加入适量的玉米淀粉(作为赋形剂),然后用喷雾-干燥法制粒以产生各自的颗粒。
(6)将各自的颗粒与长柄菊颗粒一起混合以形成混合的颗粒。
III.对于沿阶草属植物:
按照程序II(1)-(4)浓缩沿阶草属植物的块茎。在沿阶草属植物的浓缩物与半夏属植物、生甘草属植物和西洋参的浓缩物之间的差别在于沿阶草属植物浓缩物包含大量的水,而其余的浓缩物几乎不含水。对于9g的沿阶草属植物原材料,浓缩物约为5.4g,其中固体内容物约为2.25g和水为3.15g。
将沿阶草属植物的液体浓缩物与其余的草药颗粒相混合。
作为比较,在下表3a中举例说明了原材料,STA-36和STA-4的克重量:
表3a.STA-36和STA-4的内含物和重量
| 沿阶草属植物 | 半夏属植物 | 生甘草属植物 | 西洋参 | 长柄菊 | 总重量(口服剂型) | STA-36/STA-4的比率(剂量) | |
| 原材料 | 9g | 6g | 3g | 3g | 3g | 24g | |
| STA-36 | 5.4g(2.25SC<sup>*</sup>+3.15g水) | 6g(草药粉末) | 3g(草药粉末) | 3g(草药粉末) | 3g(草药粉末) | 20.4g(草药粉末) | 2 |
| STA-4 | 5.40g浓缩物(2.25gSC<sup>*</sup>+3.15g水) | 1.50g颗粒(1.20gSC<sup>*</sup>+0.30g玉米淀粉 | 0.63g颗粒(0.60gSC<sup>*</sup>+0.03g玉米淀粉 | 0.96g颗粒(0.73gSC<sup>*</sup>+0.23g玉米淀粉 | 1.25g颗粒(0.23gSC<sup>*</sup>+1.02g玉米淀粉 | 10.20g(9.74g颗粒和沿阶草属植物浓缩物+0.46g玉米淀粉) | 1 |
*SC=固体内容物(其为干燥的浓缩物[排除了水或溶剂的浓缩物])。
在表3a中,“原材料”行表示加工前每种草药的重量。“STA-36”和“STA-4”行表示(1)每种草药的最终剂型;和(2)每种草药的最终重量。例如,在STA-36中,除了为浓缩物形式的沿阶草属植物,半夏属植物,生甘草属植物,西洋参和长柄菊均为草药粉末形式。同样,在STA-36中,除了沿阶草属植物以外,其重量少于它的原材料,其余草药的草药粉末均保持与它们的原材料相同的重量。
在STA-4中,仅沿阶草属植物保持与STA-36中相同的最终剂型,即,浓缩物。如表3a中所示,经历了提取、浓缩和制粒后,其余草药的克重量已被大幅减少。另外,为有助于在制粒过程中稳定浓缩物,向每种草药浓缩物中加入赋形剂(如玉米淀粉)。向每种浓缩物中加入的玉米淀粉的量依据浓缩物的稳定性而改变。即使STA-4和STA-36衍生自相同量的原材料,但颗粒形式的STA-4的终产品约为STA-36的终产品重量的一半。STA-4在总的克重量的减少,但保持了与STA-36相同或更好的对免疫疾病的治疗作用,使得它获得了来自STA-36的另一种改进,因为这意味着患者不需为获得相同或更好的治疗效果而摄入两倍量的草药。
下述实施例是解释本发明,不应被理解为限制本发明。在未脱离本发明的范围的条件下,在此处可进行合理的改变,例如技术人员进行那些合理的改变。
实施例1
STA-31,STA-32,STA-33,STA-34,STA-35,和STA-36的制备
药物组合物的内含物示于表1中,在组合物中草药的重量示于表3中。
表3.STA-3中使用的每种草药的重量
| 试验编号 | 名称 | 沿阶草属植物(kg) | 党参,或三七或西洋参(kg) | 半夏属植物(kg) | 甘草属植物(kg) | 长柄菊,或台湾adenostema,或鱼腥草(kg) |
| 1 | STA-31 | 3.00 | 1.00(党参) | 2.00 | 1.00 | 1.00(台湾adenostema) |
| 2 | STA-32 | 3.00 | 1.00(党参) | 2.00 | 1.00 | 1.00(鱼腥草) |
| 3 | STA-33 | 3.00 | 1.00(党参) | 2.00 | 1.00 | 1.00(长柄菊) |
| 4 | STA-34 | 3.00 | 1.00(西洋参) | 2.00 | 1.00 | 1.00(台湾adenostema) |
| 5 | STA- | 3.00 | 1.00 | 2.00 | 1.00 | 1.00 |
| 35 | (西洋参) | (鱼腥草) | ||||
| 6 | STA-36 | 3.00 | 1.00(西洋参) | 2.00 | 1.00 | 1.00(长柄菊) |
制备药物组合物的方法在基本上与制备组合物的一般方法(见上文)相同。
(1)除了沿阶草属植物,将所有适用的草药,用量如表3所示,切片,脱水,研磨,并通过筛网(优选40-120目),以产生草药粉末。
(2)将用量如表3所示的沿阶草属植物浸没在煎-煮容器的水中,其中水的体积至少高于沿阶草属植物顶部10cm。在97-103℃下加热浸没的沿阶草属植物约60分钟,进行两次,以产生沿阶草属植物提取物溶液。然后,将沿阶草属植物提取物溶液通过筛网(约100目)。收集滤液。然后在50-60℃,在400-650mm-Hg压力的真空条件下浓缩沿阶草属植物滤液,以获得具有理想浓度的液体浓缩物。优选液体浓缩物约为沿阶草属植物滤液的1/14。
(4)将沿阶草属植物的液体浓缩物与其余草药的草药粉末混合。然后将混合物移至流化制粒机中,并置于由过滤织物制成的喷射管中。将成粒机的温度调至90-110℃。在预热约5分钟后,以每次约40-55秒的时间喷射混合物,喷射适当的次数,并以每10秒钟的频率轻拍喷射管。制粒后,干燥颗粒,然后冷却。使颗粒通过筛网,并包装在PE袋中。颗粒的优选的水含量为少于6%。可将颗粒进一步包囊于任何传统的胶囊中,所述胶囊包括,但不局限于天然明胶,果胶,酪蛋白,胶原质,蛋白质,改性淀粉和聚乙烯吡咯烷酮。
实施例2
使用高效液相色谱(HPLC)对药物组合物的质量控制
本发明使用HPLC技术以保证良好控制草药的质量。开发了三种HPLC方法以调控每种草药的理化特性。如下描述三种HPLC方法:
(A)HPLC分析的方法1
方法1在室温下,使用封端的预柱Lichrospher RP-18(5μm,4.0 ID X10mm,Merck)和Cosmosil 5C18-MS柱(5μm,Nacalai tesque 5C18-MS,4.6ID X 250mm)。柱的流动相为含(A)H2O:KH2PO4:10% H3PO4(1000ml:2.72g:1ml,体积/重量/体积),(B)CH3CN,(C)H2O和(D)CH3OH的梯度。洗脱梯度示于表4中。流速为1.0ml/min。检测波长为250nm。分析的总保留时间为60分钟。
表4.方法1的流动相梯度
运行后:15分钟。
(B)HPLC分析的方法2
HPLC分析的方法2在35℃温度下,使用封端的预柱LichrospherRP-18(5μm,4.0ID X 10mm,Merck)和Cosmosil 5C18-MS柱(5μm,Nacalai tesque 5C18-MS,4.6ID X 250mm)。柱的流动相为含(A)10mMKH2PO4+10mM K2HPO4+0.01%H3PO4(KH2PO4:K2HPO4:10%H3PO4:H2O=1.36g:1.74g:1ml:1000ml),(B)CH3CN,(C)H2O,和(D)CH3OH的梯度。洗脱梯度示于表5中。流速为1.0ml/min。检测波长为260nm。分析的总保留时间为60分钟。
表5.方法2的流动相梯度
| 时间(分钟) | (A) | (B) | (C) | (D) |
| 起初 | 100 | 0 | 0 | 0 |
| 25 | 60 | 0 | 20 | 20 |
| 30 | 20 | 0 | 20 | 60 |
| 35 | 100 | 0 | 0 | 0 |
运行后:15分钟。
(C)HPLC分析的方法3
HPLC分析的方法3在35℃温度下,使用封端的预柱LichrospherRP-18(5μm,4.0ID X 10mm,Merck)和Cosmosil 5C18-MS柱(5μm,Nacalai tesque 5C18-MS,4.6ID X 250mm)。柱的流动相为含(A)H2O:KH2PO4(1000ml:2.72g,体积/重量),(B)CH3CN,(C)H2O,和(D)CH3OH的梯度。洗脱梯度示于表6中。流速为1.0ml/min。检测波长为203nm。分析的总保留时间为60分钟。
表6.方法3的流动相梯度
| 时间(分钟) | (A) | (B) | (C) | (D) |
| 起初 | 80 | 20 | 0 | 0 |
| 40 | 65 | 35 | 0 | 0 |
| 55 | 0 | 80 | 20 | 0 |
| 60 | 0 | 20 | 80 | 0 |
运行后:15分钟。
在组合物中使用的草药的HPLC分析,其包括方法、主要标记,每种草药的检测波长,归纳于表7中。STA-36的HPLC色谱示于图1—5。
表7.在STA-36中使用的草药的HPLC分析
HPLC分析前,将0.5g草药样品与20ml含70%甲醇的溶液混合。室温下将样品溶液超声15分钟,并置于40℃的以160rpm转速转动的水浴20分钟。然后将样品溶液静止约30分钟,以使得碎屑沉淀。然后吸出10ml的上清液并通过0.45μm的滤器。滤液用于HPLC分析。取20μl的滤液用于HPLC分析。
结果:
沿阶草属植物的HPLC色谱图示于图1。如表7所示,使用HPLC分析的方法在214nm的波长处检测沿阶草属植物。在沿阶草属植物HPLC色谱上鉴定了两个独特的峰,6115-1和6115-2。6115-1具有11.5分钟的保留时间。6115-2具有13分钟的保留时间。尽管在这两个峰中化学成分尚未鉴定,但它们可用于保证沿阶草属植物的质量的目的。
半夏属植物的HPLC色谱图示于图2。如表7所示,使用HPLC分析的方法2在250nm的波长处检测半夏属植物,半夏属植物显示两种独特的化学标记,即腺嘌呤和鸟苷,两种均是核酸的组成成分。腺嘌呤还具有增加血清缩醛酶的作用。腺嘌呤具有14.8分钟的保留时间。鸟苷具有17分钟的保留时间。
甘草的HPLC色谱图示于图3。如表7所示,使用HPLC分析的方法1在250nm的波长处检测甘草,在甘草HPLC色谱中发现化学标记“甘草甜(glycyrrhizini)”。甘草甜(C42H62O16)是非常甜的物质。已知其具有解毒、抗炎症和溶血作用,并且已用于治疗阿狄森氏病。甘草甜的保留时间是46.4分钟。
西洋参的HPLC色谱图示于图4。如表7所示,使用方法3在250nm波长处检测西洋参,在西洋参HPLC色谱中发现化学标记“人参皂甙Rb1”。人参皂甙Rb1具有扩张血管,缓解疲劳和避免溶血的药物作用。
长柄菊的HPLC色谱图示于图5。如表7所示,使用HPLC分析的方法1在250nm波长处检测长柄菊,鉴定了四个独特的峰,FY-1—FY-4。FY-1具有28.0分钟的保留时间。FY-2具有31.6分钟的保留时间。FY-3具有33.5分钟的保留时间。FY-4具有18.3分钟的保留时间。由于这四个峰连续出现,即使与这四个峰相关的化学内容物尚未鉴定,它们也可用于鉴定和保证长柄菊质量的目的。
实施例3
生甘草属植物、沿阶草属植物、半夏属植物和长柄菊的薄层层析(TLC)
特性
除了HPLC,某些在STA-36组合物中使用的草药,包括生甘草,沿阶草属植物,半夏属植物和长柄菊,可用薄层层析(TLC)方法表征。
依据草药的特征,TLC方法使用硅胶60F254(其结合到TLC板上)和三种流动相(或分散)溶剂。第一种溶剂包含乙酸乙酯,4N氨水,和乙醇,它们的体积比为4:1:2(体积/体积/体积)。第一种溶剂特别用于表征生甘草。第二种溶剂包含丁醇,4N氨水和乙醇,它们的体积比为5:2:1(体积/体积/体积)。第二种溶剂特别用于表征沿阶草属植物和西洋参。第三种溶剂包含氯仿(CHCl3)和甲醇,它们的体积比为5:1(体积/体积)。第三种溶剂特别用于表征长柄菊。对于每个TLC测定,在TLC板的起始点,加入5μl样品。将板置于施用了流动相溶剂的TLC室中。允许移动最多9cm的溶剂。TLC测定结果描述如下:
(A)生甘草属植物
使用附着于TLC板的硅胶60F254固定相和含乙酸乙酯:4N氨水:乙醇=4:1:2(体积/体积/体积)的流动相溶剂,通过TLC分析生甘草。施用样品后,将TLC板置于包含流动相溶剂的TLC室中,所述TLC室具有不超过样品施用点的上部液体标记。从样品施用点计算,允许移动最多9cm的溶剂。然后,将TLC板从TLC室中取出,并空气干燥。用含香兰醛/H2SO4的喷射剂喷雾干燥的TLC板。然后,在105℃温度下加热活化2分钟。在TLC板的约Rf=0.5处显示表示生甘草属植物的黄色斑点。Rf=(斑点和样品施用点间的距离[cm])/总的迁移距离[即,9cm]。
(B)沿阶草属植物
使用附着于TLC板的硅胶60 F254固定相和含丁醇:4N氨水:乙醇=5:2:1(体积/体积/体积)的流动相溶剂,通过TLC分析沿阶草属植物。施用样品后,将TLC板置于包含流动相溶剂的TLC室中,所述TLC室具有不超过样品施用点的上部液体标记。从样品施用点计算,允许移动最多9cm的溶剂。然后,将TLC板从TLC室中取出,并空气干燥。用含香兰醛/H2SO4的喷射剂喷雾干燥的TLC板。然后,在105℃温度下加热活化2分钟。在TLC板的约Rf=0.4处显示表示沿阶草属植物的棕色斑点。
(C)西洋参
使用附着于TLC板的硅胶60F254固定相和含丁醇:4N氨水:乙醇=5:2:1(体积/体积/体积)的流动相溶剂,通过TLC分析西洋参。施用样品后,将TLC板置于包含流动相溶剂的TLC室中,所述TLC室具有不超过样品施用点的上部液体标记。从样品施用点计算,允许移动最多9cm的溶剂。然后,将TLC板从TLC室中取出,并空气干燥。用含香兰醛/H2SO4的喷射剂喷雾干燥的TLC板。然后,在105℃温度下加热活化2分钟。在TLC板的约Rf=0.3处显示表示西洋参的略带紫色的斑点。
(D)长柄菊
使用附着于TLC板的硅胶60 F254固定相和含氯仿:甲醇=5:1(体积/体积)的流动相溶剂,通过TLC分析长柄菊。施用样品后,将TLC板置于包含流动相溶剂的TLC室中,所述TLC室具有不超过样品施用点的上部液体标记。从样品施用点计算,允许移动最多9cm的溶剂。然后,将TLC板从TLC室中取出,并空气干燥。将干燥的TLC板置于UV检测仪下,并在366nm处检测波长。在TLC板的约Rf=0.3处显示表示长柄菊的浅黄色荧光斑点。
实施例4
五种传统中国草药煎剂对小鼠中过敏原诱导的IgG、IgE和IL-4的作用
利用D.P.(屋尘螨Dermatophagoides pteronyssimus)过敏原“Der p5”致敏的BALB/c小鼠研究五种传统中国草药煎剂对过敏原诱导的免疫球蛋白G(IgG)、免疫球蛋白E(IgE)合成的抑制的作用和对白细胞介素-(IL-4)表达的作用。屋尘螨是充当抗原,并且在哮喘人群中产生过敏性哮喘反应。
这些传统中国煎剂示于表8中。已知这些传统中国煎剂对治疗患有肺相关疾病例如哮喘的患者具有特殊的作用。
表8.五种传统中国草药煎剂
| 传统中国草药煎剂的名称 | 草药成分(带有重量比) |
| White-draing粉末 | 甘草属植物(2.25),桑根皮(4.5),枸杞子根皮(4.5),磨圆的粒状粳稻/japonica rice(6) |
| little green-blue dragon煎剂 | 半夏属植物(4),麻黄属植物(4),中国芍药(4),中国细辛(1.5),甘草属植物(4),干细辛(4),桂枝(4),五味子(1.5) |
| 沿阶草属植物煎剂 | 人参(2),磨圆的粒状粳稻/japonica rice(4),半夏属植物(2),枣(Chinese date/jujube)(2),甘草属植物(2),沿阶草属植物(8) |
| Dryness-Clearing Lung-Rescuing煎剂 | 白桑叶(7.5),阿胶(2),人参(2),石膏(6.5),甘草属植物(2.5),沿阶草属植物(3),杏种子/核(2),黑sesame seed(2.5),枇杷叶(2) |
| 苏子Qi-Downbearing煎剂 | 紫苏子(5),陈皮(3),半夏属植物(5),中国独活(2),前胡(2),生甘草属植物(2),桂皮(3),厚朴(2),鲜姜根茎(2),枣(Chinesedate/jujube)(1) |
试验设计:
(A)草药材料的制备:
将50mg每种上述指定的草药制剂(所有均来自Sun Ten Sci.Pharm.Corp.,台北,台湾)分别与180μl吐温80混合,并均化(均化器DC-3S,Xinguang Precision Instrument Industrial Limited,Inc.,台湾)。向匀浆中加入水,使得终体积至2ml,终浓缩为25mg/ml。每隔一天对每只小鼠施用0.4ml/每20g体重的一种草药组合物溶液或安慰剂,持续14天。
(B)动物
4-6周龄的雌性BALB/c小鼠获自中国国家动物饲养中心(NationalAnimal-breeding Center,Republic of China),并用于该研究。小鼠的年龄和性别与每个试验相匹配。
(C)免疫原Derp5(屋尘螨种群5免疫原)纯化
pGEX-2T质粒用于在大肠杆菌中表达Der p5-谷胱甘肽S转移酶(GST)。融合蛋白的分子量约为42kD。通过谷胱甘肽结合的琼脂糖凝胶柱层析纯化蛋白。通过在含氨苄青霉素(100μg/ml)的LB肉汤上培养被转染的大肠杆菌来筛选Der p5-GST阳性细菌菌株的单克隆。进一步培养Der p5-GST阳性大肠杆菌克隆,以生产足量的Der p5-GST。然后,收集细菌培养物并离心。弃去上清液,用TBS(pH7.5)洗涤沉淀,并收集于离心管中。然后立即用TBS洗涤,向沉淀中加入0.1M苯基甲基磺酰氟,然后加入DNase I,吐温20和溶菌酶。通过冻-融过程裂解沉淀,以释放Der p5+GST蛋白。随后,向细胞裂解物中加入EDTA,然后离心。弃去沉淀,将上清液倒到谷胱甘肽结合的琼脂糖凝胶吸附柱上,该琼脂糖凝胶吸附柱已吸附了Der p5-GST蛋白。首先在4℃用TBS缓冲液洗涤该柱,然后在Tris-碱(pH8.0)中还原谷胱甘肽以从琼脂糖凝胶柱中分离Der p5-GST。用SDS-PAGE确定Der p5-GST蛋白的纯度。用常规的蛋白分析方法测定蛋白量。
(D)动物致敏化
起初用10μg屋尘螨种群5(“Der p5”)免疫原和4mg氢氧化铝(WyethPharmaceuticals,Punchbowl,澳大利亚)在腹膜内致敏BALB/c小鼠。第一次致敏后7天,除了安慰剂对照组,用中国草药煎剂喂养小鼠。
第一次致敏后3周,用Der p5再次激发小鼠。第二次加强注射后3天,将小鼠置于圆形的塑料容器中,在该容器中小鼠被0.1%Der p5喷雾进一步激发。
每次加强注射后,在第二天,从每只小鼠的尾静脉采集50μl血样。将血样置于室温1小时,然后离心。收集血清并保存于-80℃,用于ELISA(参见如下)分析。
(E)Derp5-特异的IgG和IgE的测定
通过酶联免疫吸附测定(ELISA)测定Der p5-特异的IgG和IgE的量。用100μl纯化的Der p5包被蛋白质高度结合的培养板,所述Der p5在包被缓冲液(0.1M NaHCO3,pH8.2)中稀释至5μg/ml的浓度。在4℃过夜孵育后,洗涤培养板三次,并用3%(重量/体积)BSA-PBS缓冲液于25℃封闭2小时。在重复试验中,以1∶100的稀释度使用血清来测量IgG,以1∶10的稀释度使用血清测量IgE。在4℃过夜孵育后,加入在0.05%明胶缓冲液中稀释的生物素结合的单克隆大鼠抗小鼠IgE mAb或大鼠抗小鼠IgG mAb,持续加入1小时。然后加入抗生物素蛋白-碱性磷酸酶(1∶1000),并在25℃孵育1小时,然后洗涤六次。加入磷酸酶底物对-硝基苯基磷酸氢二钠进行显色。在微量培养板自动读数仪(Metertech,台湾)中于405nm处对培养板进行读数。读数参考市售的异型标准物小鼠抗TNP mAb,IgG1(107.3),IgG2a(G155-178)和IgE(IgE-3)。
(F)通过RT-PCR(逆转录酶-聚合酶链式反应)在脾细胞中表达IL-4
基因
在用Der p5免疫原致敏和激发动物,然后分别用列于表8的五种草药煎剂或安慰剂处理后,从BALB/c小鼠中分离脾细胞。用Der p5(15μg/ml)孵育脾细胞4小时。用Tridzol试剂(Gibco BRL,Life Technologies,)美国)提取RNA。利用已市售(ready to go)的T-引发的第一链试剂盒(Pharmacia Biotch,美国),使用提取的RNA生产cDNA。CDNA用作聚合酶链式反应(PCR)的模板。具有下述序列的IL-4特异引物对:
5’-GAATGTACCAGGAGCCATATC-3’(序列号:1);和
5’-CTCAGTACTACGAGTAATCCA-3’(序列号:2);
用于PCR扩增和检测IL-4基因。具有下述序列的HPRT(次黄嘌呤-鸟嘌呤转磷酸核糖基酶)特异引物对:
5’-GTTGGATACAGGCCAGACTTTGTTG-3’(序列号:3);和
5’-GATTCAACTTGCGCTCATCTTAGGC-3’(序列号:4);
用于PCR扩增和检测HPRT。在下述条件下用热循环仪(Thermo-cycler)进行PCR:95℃变性5分钟,然后95℃1分钟,72℃1分钟和55℃3分钟进行35个循环。然后在2%琼脂糖凝胶上电泳PCR产物。
(G)统计学分析
为评估Der p5激发后Der p5-特异的IgG,IgE和IL-4/HPRT比率的变化,重复测量ANOVA以比较各组之间的差异。分析变化后,用Duncan多程检验法来区分试验和对照组之间的差异。p<0.05用于表示统计学的显著差异。
结果:
如图6所示,在Der p5激发,然后用五种传统中国草药煎剂处理的小鼠中,IgG和IgE的水平与对照(安慰剂)组无明显的差异。在White-Draining粉末组(A),little green-bluedragon煎剂组(B),沿阶草属植物煎剂组(C),Dryness-Clearing Lung-Rescuing煎剂组(D),苏子Qi-Downbearing煎剂组(E)和安慰剂组(F)中IgE的ELISA单元分别为99.3±23,106.3±34,104.9±23,105.7±23,93.9±21和97.8±19。
图6的结果证实五种传统中国草药煎剂不抑制IgE的产生。
如图7所示,除了沿阶草属植物煎剂显示IL-4/HPRT明显减少,其余的传统中国草药煎剂对抑制IL-4基因产生无作用。
实施例5
在STA-31,STA-32,STA-33,STA-34,STA-35和STA-36中单独草药
对在小鼠中免疫原诱导的IgG,IgE和IL-4的作用
使用被D.P.免疫原“Der p5”致敏的BALN/c小鼠研究单独草药和STA-36对免疫原诱导的IgG,IgE和IL-4的作用,所述单独草药包括沿阶草属植物,半夏属植物,生甘草属植物和党参。本实施例的试验设计与实施例4(Example5)中所描述的相同(见上文)。
结果:
用免疫原Der p5激发,然后用沿阶草属植物,党参,半夏属植物和生甘草属植物处理后,小鼠血清中IgG水平示于图8中。结果指出,在沿阶草属植物,党参和半夏属植物处理组和安慰剂处理组之间IgG水平无显著差异。生甘草属植物处理后的IgG水平明显低于安慰剂处理组的水平。
然而,如图9所示,用Der p5激发,然后用沿阶草属植物,党参和STA-36组合物处理后,小鼠血清中的IgE水平明显低于安慰剂处理组的水平。事实上,用STA-36组合物处理后,IgE水平被减少了约超过2.5倍。半夏属植物和生甘草属植物处理后IgE水平与安慰剂处理的IgE水平无显著差异。
如图10所示,用Der p5激发,然后分别用沿阶草属植物、党参、半夏属植物和生甘草属植物处理后,小鼠脾细胞中IL-4基因的表达(通过RT-PCR测量并表示为IL-4/HPRT比率)与用安慰剂处理组无显著差异。然而,用STA-36处理后,IL-4基因的表达比率明显低于安慰剂处理组的表达比率,表明STA-36可负调节IL-4基因的表达。
实施例6
在动物中测定IgG,IgE,IL-4和IFN-γ的方法
使用被D.P.(屋尘螨)免疫原“Der p5”致敏的BALB/c小鼠,研究STA-36和STA-4草药组合物以及单独的草药对抑制免疫原诱导的免疫球蛋白G(IgG),免疫球蛋白E(IgE),白细胞介素-4(IL-4)和干扰素γ(IFN-γ)的作用。屋尘螨充当免疫原,并且在过敏人群中产生过敏性哮喘反应
试验设计:
(A)动物
4-6周龄的雌性BALB/c小鼠获自中国国家动物饲养中心,并用于该研究。小鼠的年龄和性别与每个试验相匹配。
(B)免疫原Der p5(屋尘螨种群5免疫原)的纯化
pGEX-2T质粒用于在大肠杆菌中表达Der p5-谷胱甘肽S转移酶(GST)。融合蛋白的分子量约为42kD。通过谷胱甘肽结合的琼脂糖凝胶柱层析纯化蛋白。通过在含氨苄青霉素(100μg/ml)的LB肉汤上培养被转染的大肠杆菌来筛选Der p5-GST阳性细菌菌株的单克隆。进一步培养Der p5-GST阳性大肠杆菌克隆,以生产足量的Der p5-GST。然后,收集细菌培养物并离心。弃去上清液,用TBS(pH7.5)洗涤沉淀,并收集于离心管中。然后立即用TBS洗涤,向沉淀中加入0.1M苯基甲基磺酰氟,然后加入DNase I,吐温20和溶菌酶。通过冻-融过程裂解沉淀,以释放Der p5+GST蛋白。随后,向细胞裂解物中加入EDTA,然后离心。弃去沉淀,将上清液倒到谷胱甘肽结合的琼脂糖凝胶吸附柱上,该琼脂糖凝胶吸附柱已吸附了Der p5-GST蛋白。首先在4℃用TBS缓冲液洗涤该柱,然后在Tris-碱(pH8.0)中还原谷胱甘肽以从琼脂糖凝胶柱中分离Der p5-GST。用SDS-PAGE确定Der p5-GST蛋白的纯度。用常规的蛋白分析方法测定蛋白量。
(C)动物致敏化
起初用10μg屋尘螨种群5(“Der p5”)免疫原和4mg氢氧化铝(WyethPharmaceuticals,Punchbowl,澳大利亚)在腹膜内致敏BALB/c小鼠。第一次致敏后7天,除了安慰剂对照组,用STA-36和STA-4草药组合物喂养小鼠,直至21天结束。
在21天结束时,给小鼠第二次加强注射Der p5。第二次加强注射48小时后,将小鼠置于圆形塑料容器中,在该容器中通过0.1%Der p5喷雾进一步激发小鼠。
激发后几小时,用100mg/ml苯巴比妥麻醉小鼠。从尾静脉或心脏采集血样。将血样置于室温下1小时,然后1000rpm离心约10分钟,以收集血清,保存于-80℃用于IgE和IgG2a的ELISA(参见下文)分析。1000rpm离心洗涤肺泡获得的流体10分钟。流体的上清液用于分析细胞因子,白细胞介素-4(IL-4)和干扰素γ(IFN-γ)。用PBS重新解离流体的沉淀(含细胞),并用细胞离心涂片器(cytospin)计数炎性细胞。
(D)Der D5特异的IgG和IgE的ELISA测定
同酶联免疫吸附测定(ELISA)确定Der p5特异的IgG和IgE的量。用100μl(10mg/ml)纯化的Der p5包被高蛋白高度结合的微孔培养板(Costar,No.3590),所述纯化的Der p5在包被缓冲液中稀释至5μg/ml的浓度。在4℃过夜孵育后,在含0.05%吐温20的PBS溶液中(pH7.4)洗涤培养板三次,并在25℃用3%(重量/体积)BSA-PBS缓冲液封闭2小时。
在重复试验中,IgG测量使用1:100稀释的血清,IgE测量使用1:10稀释的血清。4℃过夜孵育后,加入在0.05%明胶缓冲液中稀释的生物素结合的单克隆大鼠抗小鼠IgE mAb(PharMinge 02122D)或大鼠抗小鼠IgGmAb(PharMinge,02022D),持续加入2小时。然后加入抗生物素蛋白-碱性磷酸酶(1:1000)(Strptavidin-AP,PharMinge 13043E),并在25℃孵育1小时,然后洗涤六次。加入磷酸酶底物对-硝基苯基磷酸氢二钠(pNPP碱性磷酸酶底物,Sigma N-2770)进行显色。在微量培养板自动读数仪(ELISAreader,Dynex MRX)中于405nm处对培养板进行读数。读数参考市售的异型标准物小鼠抗TNP mAb,IgG1(107.3),IgG2a(G155-178)和IgE(IgE-3)。
(E)细胞因子(IL-4和IFN-γ)的ELISA测定
用纯化的抗细胞因子抗体(对于IL-4,使用2μg/ml PharMinge 18191D的IL-4抗体;对于IFN-γ,使用3μg/ml PharMinge 18181D的IFN-γ抗体)包被高蛋白高度结合的微孔培养板(Costar,No.3590)。用含3%BSA、pH7.4的PBS溶液包被培养板,然后用含0.05%吐温20、pH7.4的PBS溶液洗涤。
然后,向微孔中加入100μl来自肺泡的流体的上清液和细胞因子标准物溶液,4℃过夜反应。然后,向微孔中加入100μl生物素-抗-小鼠-IL-4(PharMinge 18042D,1μg/ml)或生物素-抗-IFN-γ(PharMinge 18112D,1μg/ml)。反应2小时后,向微孔中搅动加入100μl抗生物素蛋白-碱性磷酸酶(1:1000)(streptavidin-AP,PharMinge 13043E)1小时。向微孔中加入200μl磷酸酶底物对-硝基苯基磷酸氢二钠(pNPP碱性磷酸酶底物,SigmaN-2770)以显色。在微量培养板自动读数仪(ELISA读数仪,Dynex MRX)中于405nm对培养板进行读数。
(F)肺功能的测量
向小鼠静脉内注射100mg/ml苯巴比妥后,将PE50管插入到气管中。将该管与压力检测装置连接以测量在吸气和呼气过程中呼吸压力的变化。将另一个PE50管插入到食道中以测量代替跨肺压(TPP)的食道压力。当将压力信号传递至Bio-Recorder BR8000,信号被扩大,并转换成气体体积和跨肺压,以计算气管压力。在试验过程中,在尾静脉保留注射乙酰胆碱(Ach)的针以诱导气管压力的变化。
4.统计
所有试验中包含的数据以“平均值±SEM”来计算。转变到PC100后,由乙酰胆碱诱导的气管阻力变化以μg/kg测量。基于光吸收值显示IgE和IgG2a测量。不成对的学生t检验(student’s t test)用来确定各组之间的差异显著性。p<0.05用来表示统计学上的显著差异。
实施例7
草药的水性提取物对IgG和IgE的作用
在西洋参和长柄菊试验各种水提取方法,以确定在草药组合物中使用的水性提取物的最佳形式。
检验(1)粉末,(2)95%乙醇提取物,(3)水提取物和(4)50%乙醇提取物形式的西洋参对抑制IgE和IgG2a的药用作用。如图11所示,用50%乙醇提取的西洋参产生最佳的IgE抑制作用,尽管它对IgG2a减少的作用不如95%乙醇提取的西洋参。由于抗原诱导的免疫疾病主要是IgE介导的疾病,似乎在草药组合物中使用50%乙醇提取的西洋参可为组合物提供最佳的IgE减少结果。然而,当将产自西洋参的乙醇提取物的颗粒加入到其余的颗粒中时,产自西洋参水提取物的颗粒提供抑制IgE和增加IgG的较好的作用。因此,在STA-4组合物中,西洋参从水中提取。
同样检测(1)粉末,(2)95%乙醇提取物,(3)水提取物和(4)50%乙醇提取物形式的长柄菊对抑制IgE,IgG2a,IL-4和IFN-γ的药用作用。如图12所示,用50%乙醇提取的长柄菊产生最佳的IgE和IgG2a抑制作用,尽管已证实长柄菊的水提取物对IL-4和IFN-γ具有最佳的抑制作用。然而,由于在研究过程中,长柄菊的水提取物诱导动物血液凝固,故不考虑将其用于人类。
实施例8
比较STA-36和STA-4对IgE,IgG,IL-4,IFN-γ和肺功能的作用
如实施例3所述(见上文),在试验动物中进行STA-36和STA-4的草药组合物对IgE,IgG,IL-4和IFN-γ以及肺功能的药用作用之间的比较研究。该研究的结果示于图13-15中。
图13表示STA-36和STA-4的草药组合物在小鼠中对IgG和IgE的作用的比较研究。如图13所示,证实与对照相比,STA-36和STA-4的草药组合物均抑制IgE,STA-4的作用远比STA-36的作用强。STA-4对IgE的抑制作用在统计上显著高于对照。然而,证实STA-36和STA-4均对IgG无抑制作用。但事实上,相反,与对照相比,STA-36和STA-4处理组中IgG水平均增加。
图14表示STA-36和STA-4对小鼠肺功能的作用。STA-36和STA-4均比对照显示肺功能的明显改善(p<0.05)。在两者中,STA-4比STA-36显示对肺功能更好的改善,尽管可能由于每个试验组中不足的动物数(n),使得STA-4和STA-36之间的数值无显著差异。
图15比较了STA-4与传统哮喘药物即酮替酚、泼尼松龙和aminophline对IgE,IgG,IL-4和IFN-γ的作用。结果显示,仅STA-4表现IgE显著减少和IgG、IL-4和IFN-γ的显著增加,因此,推测STA-4比酮替酚、泼尼松龙和aminophline在治疗哮喘方面具有更好的治疗作用。
图15中的结果还表明STA-4的治疗作用可能与常规机制不同,所述常规机制即药物抑制IL-4合成,其随后间接降低IgE水平。在本发明中,摄入STA-4后,IL-4和IFN-γ均充分增加,因此IgE的减少不是由于IL-4的降低所致。正相反,STA-4处理后,IFN-γ(由TH1细胞产生和分泌)的量显著增加。IFN-γ刺激B细胞合成并分泌IgG2a,这解释了为什么在STA-4治疗过程中IgG2a的量增加。因此,推测STA-4作用至少部分衍生自IgG2a,其依据与免疫原的第二次接触,与免疫原相互作用,以减少过敏反应。
实施例9
STA-36和STA-4的草药组合物的毒性试验
基于28天亚急性口服毒性研究,检验草药组合物的毒性,在所述亚急性口服毒性研究中,测定死亡率,眼科检查,临床征兆和粗略尸检。结果示于表9-11:
表9.摄入STA-36和STA-4后小鼠的死亡率
| 2%吐温80含水溶液 | STA-36 | STA-4 | |
| 剂量(mg/kg/天) | 5000 | 5000 | |
| 性别 | 雄性 | 雄性 | 雄性 |
| 小鼠数 | 10 | 10 | 10 |
| 死亡率 | 0/10 | 0/10 | 0/10 |
表10.摄入STA-36和STA-4后小鼠的眼科检查和临床征兆
| 2%吐温80含水溶液 | STA-36 | STA-4 | |
| 剂量(mg/kg/天) | 5000 | 5000 | |
| 性别 | 雄性 | 雄性 | 雄性 |
| 小鼠数 | 10 | 10 | 10 |
| 开始前(0天) | 0/10 | 0/10 | 0/10 |
| 尸检前(28天) | 0/10 | 0/10 | 0/10 |
| 临床征兆 | 0/10 | 0/10 | 0/10 |
表11.摄入STA-36和STA-4后粗略的尸检
| 2%吐温80含水溶液 | STA-36 | STA-4 | |
| 剂量(mg/kg/天) | 5000 | 5000 | |
| 性别 | 雄性 | 雄性 | 雄性 |
| 小鼠数 | 10 | 10 | 10 |
| 器官异常 | 0/10 | 0/10 | 0/10 |
表9-11的结果证实在研究中STA-36和STA-4均未表现亚急性毒性征兆。
已详细描述了本发明和通过参考优选的实施方案,对于本领域的技术人员是明显的,即在未脱离本发明的范围的条件下,可以进行修改和改变,所述本发明的范围如后附的权利要求所限定。
<110>许清祥
许顺吉
<120>治疗免疫疾病的草药药物组合物
<130>33211-176057
<140>NO
<141>NO
<160>4
<170>MICROSOFT WORD
<210>1
<211>21
<212>DNA
<213>人工序列
<220>
<223>人工序列的描述:引物
<400>1
gaatgtacca ggagccatat c 21
<210>2
<211>21
<212>DNA
<213>人工序列
<220>
<223>人工序列的描述:引物
<400>2
ctcagtacta cgagtaatcc a 21
<210>3
<211>25
<212>DNA
<213>人工序列
<220>
<223>人工序列的描述:引物
<400>3
gttggataca ggccagactt tgttg 25
<210>4
<211>25
<212>DNA
<213>人工序列
<220>
<223>人工序列的描述:引物
<400>4
gattcaactt gcgctcatct taggc 25
Claims (40)
1.一种治疗因抗原或过敏原所引起的免疫疾病的药物组合物,其活性成分由以下各项药效原料制得:
i)麦冬;
ii)半夏;
iii)甘草;
iv)党参或西洋参;和
v)一种选自长柄菊,麻芝糊和鱼腥草的草药,其中所述麦冬,所述半夏,所述甘草,所述党参或西洋参和所述草药的重量比是3:2:1:1:1。
2.依照权利要求1的药物组合物,其中所述草药是长柄菊。
3.依照权利要求2的药物组合物,其中麦冬是水性提取物形式,所述半夏,所述甘草,所述长柄菊,所述党参或西洋参是粉末形式。
4.依照权利要求2的药物组合物,其中药效原料iv)是党参。
5.依照权利要求5的药物组合物,其中所述党参是粉末形式。
6.依照权利要求2的药物组合物,其中药物原料iv)是西洋参。
7.依照权利要求6的药物组合物,其中所述草药是所述西洋参,其为粉末形式。
8.依照权利要求6的药物组合物,其中所述麦冬,所述半夏,所述甘草,长柄菊和所述西洋参是水性提取物形式。
9.依照权利要求8的药物组合物,其中每一种所述麦冬、半夏、甘草、长柄菊和西洋参的水性提取物被单独过滤和浓缩,以形成每种麦冬,半夏,甘草,长柄菊和西洋参的浓缩物。
10.依照权利要求9的药物组合物,其中每一种所述半夏、甘草、长柄菊和西洋参的浓缩物被单独制粒,以形成各自的颗粒;其中所述来自半夏,甘草,长柄菊和西洋参的颗粒与所述麦冬的浓缩物相混合,以形成混合的颗粒。
11.依照权利要求10的药物组合物,其中在制粒前,向每一种所述半夏,甘草,长柄菊和西洋参的浓缩物中加入赋形剂。
12.依照权利要求11的药物组合物,其中所述赋形剂是玉米淀粉。
13.依照权利要求8的药物组合物,其中所述麦冬的水性提取物是麦冬的水提取物。
14.依照权利要求8的药物组合物,其中所述半夏的水性提取物是半夏的水提取物。
15.权利要求8的药物组合物,其中所述甘草的水性提取物是甘草的水提取物。
16.权利要求8的药物组合物,其中所述长柄菊的水性提取物是长柄菊的乙醇提取物。
17.权利要求16的药物组合物,其中所述长柄菊的醇提取物是50%乙醇提取物。
18.权利要求8的药物组合物,其中所述西洋参的水性提取物是西洋参的水提取物。
19.依照权利要求9的药物组合物,其中所述麦冬浓缩物的固体内容物为麦冬重量的20-30%;所述半夏浓缩物的固体内容物为半夏重量的15-25%;所述甘草浓缩物的固体内容物为甘草重量的15-25%,所述西洋参浓缩物的固体内容物为西洋参重量的19-29%,所述长柄菊浓缩物的固体内容物为长柄菊重量的5-10%。
20.依照权利要求10的药物组合物,其中所述半夏颗粒为半夏重量的20-30%,所述甘草颗粒为甘草重量的16-26%,所述西洋参颗粒为西洋参重量的27-37%,所述长柄菊颗粒为长柄菊重量的37-47%。
21.权利要求1的药物组合物在制备用于治疗受试者中抗原或过敏原诱导的疾病的药物中的应用,所述药物通过降低IgE的水平来治疗疾病。
22.依照权利要求21的应用,其中所述疾病包含至少一种选自过敏性鼻炎,过敏性结膜炎,过敏性哮喘,特异反应性湿疹,特异反应性皮炎,食物过敏,高IgE综合征,和类风湿性关节炎。
23.一种制备依照权利要求3的药物组合物的方法,其包含:
研磨半夏,甘草和长柄菊,以形成草药粉末;
在水中煎煮麦冬,以形成麦冬的水性提取物;
将所述草药粉末与所述麦冬的水性提取物混合,以形成一种草药混合物;研磨党参,以形成党参粉末;并将所述党参粉末与所述草药混合物相混合;研磨西洋参,以形成西洋参粉末,并将所述西洋参粉末与所述草药混合物相混合。
24.依照权利要求23的方法,其中所述草药混合物被制成颗粒。
25.依照权利要求24的方法,其中所述制粒的草药混合物被包入胶囊。
26.权利要求2的药物组合物在制备用于通过降低患者IgE水平来治疗患有抗原或过敏原所引起疾病的患者的药物中的应用。
27.依照权利要求26的应用,其中所述疾病选自过敏性鼻炎,过敏性结膜炎,过敏性哮喘,特异反应性皮炎,食物过敏,高IgE综合征,特异反应性湿疹,和类风湿性关节炎。
28.一种免疫疾病药物,其活性成分为依照权利要求2的药物组合物。
29.一种制备依照权利要求8的药物组合物的方法,其包含:
通过煎煮,在水中提取麦冬;过滤并浓缩所述麦冬的水提取物,以形成麦冬的浓缩物;
通过煎煮,在水中提取半夏;过滤并浓缩所述半夏的水提取物,以形成半夏的浓缩物;通过喷雾-干燥制粒所述半夏的浓缩物;
通过煎煮,在水中提取甘草;过滤并浓缩所述甘草的水提取物,以形成甘草的浓缩物;通过喷雾-干燥制粒所述甘草的浓缩物;
回流条件下,在乙醇中提取长柄菊;过滤并浓缩所述长柄菊,以形成长柄菊的浓缩物;通过喷雾-干燥制粒所述长柄菊的浓缩物;
将半夏、甘草、西洋参和长柄菊颗粒与麦冬浓缩物相混合,以形成混合的颗粒。
30.依照权利要求29的方法,其中所述长柄菊的乙醇提取物是50%乙醇提取物。
31.依照权利要求29的方法,其中在制粒前,向每一种所述半夏,甘草,和长柄菊浓缩物中加入赋形剂。
32.依照权利要求29的方法,其中所述赋形剂是玉米淀粉。
33.依照权利要求29的方法,其还包含:
通过煎煮在水中提取西洋参;过滤并浓缩所述西洋参的水提取物,以形成西洋参的浓缩物;通过喷雾-干燥制粒所述西洋参浓缩物;和将所述西洋参的所述颗粒与混合的颗粒相混合。
34.依照权利要求29的方法,其中所述麦冬的所述浓缩物的固体内容物为所述麦冬重量的20-30%;所述半夏的所述浓缩物的固体内容物为所述半夏重量的15-25%;所述甘草的所述浓缩物的固体内容物为所述甘草重量的15-25%;所述西洋参的所述浓缩物的固体内容物为所述西洋参重量的19-29%;所述长柄菊的所述浓缩物的固体内容物为所述长柄菊重量的5-10%。
35.依照权利要求29的方法,其中所述半夏的颗粒为所述半夏重量的20-30%,所述甘草的所述颗粒为所述甘草重量的16-26%,所述西洋参的所述颗粒为所述西洋参重量的27-37%,所述长柄菊的所述颗粒为所述长柄菊重量的37-47%。
36.依照权利要求29的方法,其中在55℃温度和30托真空条件下,通过减压浓缩来浓缩每一种所述浓缩物。
37.依照权利要求29的方法,其中在105℃的入口温度和76-77℃的出口温度下,喷雾-干燥每一种所述浓缩物。
38.权利要求8的药物组合物在制备用于通过降低患者IgE水平来治疗抗原或过敏原引起的疾病的患者的药物中的应用。
39.依照权利要求38的应用,其中所述疾病选自过敏性鼻炎,过敏性结膜炎,过敏性哮喘,特异反应性皮炎,食物过敏,高IgE综合征,特异反应性湿疹,和类风湿性关节炎。
40.一种通过降低免疫球蛋白E来治疗因抗原或过敏原所引起的免疫疾病药物,其活性成分为依照权利要求8的药物组合物。
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US09/735,536 US6383525B1 (en) | 2000-12-14 | 2000-12-14 | Herbal compositions for treating immunological disorders |
| US09/735,536 | 2000-12-14 | ||
| US09/949,610 | 2001-09-12 | ||
| US09/949,610 US6503542B2 (en) | 2000-12-14 | 2001-09-12 | Herbal compositions for treating immunological disorders |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN1479625A CN1479625A (zh) | 2004-03-03 |
| CN100482262C true CN100482262C (zh) | 2009-04-29 |
Family
ID=27112906
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CNB018204228A Expired - Fee Related CN100482262C (zh) | 2000-12-14 | 2001-12-03 | 治疗免疫疾病的草药药物组合物 |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US6503542B2 (zh) |
| EP (1) | EP1359927A4 (zh) |
| JP (1) | JP4399162B2 (zh) |
| CN (1) | CN100482262C (zh) |
| AU (2) | AU4154402A (zh) |
| CA (1) | CA2431852A1 (zh) |
| CH (1) | CH695663A5 (zh) |
| WO (1) | WO2002047704A1 (zh) |
Families Citing this family (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP4721626B2 (ja) * | 2002-06-24 | 2011-07-13 | 昭 粟屋 | アレルギー性鼻炎・結膜炎あるいは皮膚アレルギーやアトピー性皮膚炎の予防・治療法 |
| US8083707B2 (en) * | 2003-04-17 | 2011-12-27 | Tosaya Carol A | Non-contact damage-free ultrasonic cleaning of implanted or natural structures having moving parts and located in a living body |
| US7087250B2 (en) * | 2003-08-30 | 2006-08-08 | Artista Marchioni | Therapeutic composition providing respiratory relief |
| JP4571952B2 (ja) * | 2004-02-05 | 2010-10-27 | アクセス ビジネス グループ インターナショナル リミテッド ライアビリティ カンパニー | 抗アレルギー組成物及び関連方法 |
| CA2559465A1 (en) * | 2004-03-19 | 2005-10-06 | Xiu-Min Li | Herbal therapy for the treatment of asthma |
| DE602004025103D1 (de) * | 2004-08-12 | 2010-03-04 | Tian Shengxun | Heilkräuterzusammensetzung zur Behandlung von AIDS |
| CN103901154B (zh) * | 2014-03-28 | 2016-01-20 | 成都九芝堂金鼎药业有限公司 | 一种治疗糖尿病的中药制剂的薄层鉴别方法 |
| CN103933408A (zh) * | 2014-05-15 | 2014-07-23 | 肖贻泰 | 一种治疗急性痛风性关节炎的中药汤剂 |
| FR3046541B1 (fr) * | 2016-01-12 | 2018-02-09 | Societe Industrielle Limousine D'application Biologique | Principe actif obtenu a partir d'ophiopogon japonicus pour le traitement de la dermatite atopique |
| CN106822724A (zh) * | 2016-12-26 | 2017-06-13 | 西林县大银子铁皮石斛种销农民专业合作社 | 一种用于益气生津的保健药酒 |
| JP7262319B2 (ja) * | 2018-07-10 | 2023-04-21 | 洋 竹森 | メラニン生成抑制剤、及びメラニン生成抑制剤の製造方法 |
| CN108837090A (zh) * | 2018-09-03 | 2018-11-20 | 苏州瑞华骨科医院有限公司 | 一种用于重症监护呼吸系统感染的中药组合物及制备方法 |
| CN112697949B (zh) * | 2020-12-09 | 2022-05-27 | 浙江金城阜通制药有限公司 | 一种保元汤及其类似方提取物及制剂的薄层鉴别方法 |
| DE202022104060U1 (de) | 2022-07-19 | 2022-09-15 | Waleed Al-Abdulmonem | Eine neuartige polytherapeutische Formulierung mit Anti-Asthmatik-Potenzial |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2042254A5 (zh) * | 1970-03-31 | 1971-02-05 | Satas | |
| FR2607610B1 (fr) * | 1986-11-27 | 1990-09-07 | Flonic Sa | Systeme d'emission de tickets |
| US5281583A (en) | 1990-08-20 | 1994-01-25 | Den'ichi Mizuno | LPS-containing analgesics and veterinary analgesics |
| GB9104286D0 (en) * | 1991-02-28 | 1991-04-17 | Phytopharm Ltd | Pharmaceutical compositions for the treatment of skin disorders |
| GB2291347A (en) * | 1994-06-24 | 1996-01-24 | Phytopharm Ltd | Pharmaceutical compositions comprising extracts of Chinese herbs |
| JPH08268638A (ja) * | 1995-02-01 | 1996-10-15 | Star Micronics Co Ltd | 用紙排出装置 |
| JPH0986010A (ja) * | 1995-09-21 | 1997-03-31 | Matsushita Electric Ind Co Ltd | サーマルプリンタ |
| US6200570B1 (en) | 1997-12-08 | 2001-03-13 | Counsel Of Scientific And Industrial Research | Herbal formulation useful as a therapeutic and cosmetic applications for the treatment of general skin disorders |
| US5908628A (en) * | 1998-05-01 | 1999-06-01 | Hou; Liping | Compositions with analgesic, antipyretic and antiinflammatory properties |
| FR2800315B1 (fr) * | 1999-10-29 | 2002-01-04 | Poste | Module d'impression pour deux supports d'impression et distributeurs equipes avec de tels modules |
| US6383525B1 (en) * | 2000-12-14 | 2002-05-07 | Globoasia L.L.C. | Herbal compositions for treating immunological disorders |
-
2001
- 2001-09-12 US US09/949,610 patent/US6503542B2/en not_active Expired - Fee Related
- 2001-12-03 AU AU4154402A patent/AU4154402A/xx active Pending
- 2001-12-03 CN CNB018204228A patent/CN100482262C/zh not_active Expired - Fee Related
- 2001-12-03 CA CA002431852A patent/CA2431852A1/en not_active Abandoned
- 2001-12-03 WO PCT/US2001/045136 patent/WO2002047704A1/en active IP Right Grant
- 2001-12-03 JP JP2002549274A patent/JP4399162B2/ja not_active Expired - Fee Related
- 2001-12-03 EP EP01988215A patent/EP1359927A4/en not_active Withdrawn
- 2001-12-03 CH CH01030/03A patent/CH695663A5/it not_active IP Right Cessation
- 2001-12-03 AU AU2002241544A patent/AU2002241544B9/en not_active Ceased
Also Published As
| Publication number | Publication date |
|---|---|
| WO2002047704A9 (en) | 2003-04-17 |
| US6503542B2 (en) | 2003-01-07 |
| WO2002047704A1 (en) | 2002-06-20 |
| AU2002241544B2 (en) | 2007-03-08 |
| EP1359927A4 (en) | 2007-04-04 |
| CA2431852A1 (en) | 2002-06-20 |
| AU4154402A (en) | 2002-06-24 |
| CH695663A5 (it) | 2006-07-31 |
| AU2002241544B9 (en) | 2007-08-16 |
| JP4399162B2 (ja) | 2010-01-13 |
| JP2004518648A (ja) | 2004-06-24 |
| CN1479625A (zh) | 2004-03-03 |
| US20020122833A1 (en) | 2002-09-05 |
| EP1359927A1 (en) | 2003-11-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN100482262C (zh) | 治疗免疫疾病的草药药物组合物 | |
| CN113521232B (zh) | 一种含有白术的中药组合物 | |
| US6383525B1 (en) | Herbal compositions for treating immunological disorders | |
| AU2002241544A1 (en) | Herbal pharmaceutical compositions for treating immunological disorders | |
| CN111973651A (zh) | 甘草在治疗与肠道菌群紊乱相关疾病中的用途 | |
| CN115414435B (zh) | 中药复方葛厚石苓颗粒及其制备方法和应用 | |
| CN103316074B (zh) | 一种花锚提取物、黄芪提取物与甘草提取物的组合药物及其制剂、应用 | |
| CN105748979A (zh) | 一种抗rsv病毒的中药复方提取物及其制备方法和用途 | |
| CN106511925B (zh) | 一种加味小柴胡颗粒的制备方法及其加味小柴胡颗粒的应用 | |
| CN115184492A (zh) | 清金益气颗粒指纹图谱建立方法及其成分含量测定方法 | |
| CN1857608B (zh) | 老年咳喘胶囊的制备方法 | |
| CN112386646B (zh) | 一种药物组合物及其制备方法与应用 | |
| CN109223930B (zh) | 一种治疗小儿风热感冒的药物糖浆及其制备方法 | |
| CN112022904A (zh) | 连翘在治疗与肠道菌群紊乱相关疾病中的用途 | |
| CN101670088A (zh) | 一种治疗急、慢性支气管炎的中药组合物及其制备、质量控制方法 | |
| CN111743952A (zh) | 生地在调节肠道微生物中的用途 | |
| CN104524171A (zh) | 一种中药制剂在制备治疗肝炎药物中的用途 | |
| CN118078763B (zh) | 一种扶正祛湿抗毒颗粒剂及其制备方法 | |
| CN111904989A (zh) | 柴胡在调节肠道微生物中的用途 | |
| CN113499384B (zh) | 一种中药组合物和药物制剂及其制备方法和在抗冠状病毒中的应用 | |
| CN113181259B (zh) | 小儿芪参复感颗粒及其制备方法 | |
| CN110025704B (zh) | 用于治疗仔猪腹泻的复方中草药制剂及其制备方法 | |
| CN102397508B (zh) | 一种藏药组合物在制备治疗支气管哮喘药物中的应用 | |
| CN107037175B (zh) | 少阳感冒冲剂的检测方法 | |
| TWI233804B (en) | Herbal pharmaceutical compositions for treating immunological disorders |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C14 | Grant of patent or utility model | ||
| GR01 | Patent grant | ||
| C17 | Cessation of patent right | ||
| CF01 | Termination of patent right due to non-payment of annual fee |
Granted publication date: 20090429 Termination date: 20131203 |