BRPI0706709B1 - Composição e processo para preparar a composição - Google Patents
Composição e processo para preparar a composição Download PDFInfo
- Publication number
- BRPI0706709B1 BRPI0706709B1 BRPI0706709-7A BRPI0706709A BRPI0706709B1 BR PI0706709 B1 BRPI0706709 B1 BR PI0706709B1 BR PI0706709 A BRPI0706709 A BR PI0706709A BR PI0706709 B1 BRPI0706709 B1 BR PI0706709B1
- Authority
- BR
- Brazil
- Prior art keywords
- acid
- glycolipid
- pka
- formula
- fact
- Prior art date
Links
- 0 CC(**)C(**C(C1CCN(C)*)C1=C)C(C(C(CCCO)O)N=O)N Chemical compound CC(**)C(**C(C1CCN(C)*)C1=C)C(C(C(CCCO)O)N=O)N 0.000 description 2
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/39—Medicinal preparations containing antigens or antibodies characterised by the immunostimulating additives, e.g. chemical adjuvants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/12—Viral antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/12—Viral antigens
- A61K39/155—Paramyxoviridae, e.g. parainfluenza virus
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/12—Viral antigens
- A61K39/245—Herpetoviridae, e.g. herpes simplex virus
- A61K39/265—Infectious rhinotracheitis virus
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/04—Immunostimulants
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H13/00—Compounds containing saccharide radicals esterified by carbonic acid or derivatives thereof, or by organic acids, e.g. phosphonic acids
- C07H13/12—Compounds containing saccharide radicals esterified by carbonic acid or derivatives thereof, or by organic acids, e.g. phosphonic acids by acids having the group -X-C(=X)-X-, or halides thereof, in which each X means nitrogen, oxygen, sulfur, selenium or tellurium, e.g. carbonic acid, carbamic acid
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H15/00—Compounds containing hydrocarbon or substituted hydrocarbon radicals directly attached to hetero atoms of saccharide radicals
- C07H15/02—Acyclic radicals, not substituted by cyclic structures
- C07H15/12—Acyclic radicals, not substituted by cyclic structures attached to a nitrogen atom of the saccharide radical
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/55—Medicinal preparations containing antigens or antibodies characterised by the host/recipient, e.g. newborn with maternal antibodies
- A61K2039/552—Veterinary vaccine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/555—Medicinal preparations containing antigens or antibodies characterised by a specific combination antigen/adjuvant
- A61K2039/55511—Organic adjuvants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/555—Medicinal preparations containing antigens or antibodies characterised by a specific combination antigen/adjuvant
- A61K2039/55511—Organic adjuvants
- A61K2039/55572—Lipopolysaccharides; Lipid A; Monophosphoryl lipid A
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2710/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA dsDNA viruses
- C12N2710/00011—Details
- C12N2710/16011—Herpesviridae
- C12N2710/16051—Methods of production or purification of viral material
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2710/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA dsDNA viruses
- C12N2710/00011—Details
- C12N2710/16011—Herpesviridae
- C12N2710/16711—Varicellovirus, e.g. human herpesvirus 3, Varicella Zoster, pseudorabies
- C12N2710/16734—Use of virus or viral component as vaccine, e.g. live-attenuated or inactivated virus, VLP, viral protein
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2760/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssRNA viruses negative-sense
- C12N2760/00011—Details
- C12N2760/18011—Paramyxoviridae
- C12N2760/18311—Metapneumovirus, e.g. avian pneumovirus
- C12N2760/18351—Methods of production or purification of viral material
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2760/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssRNA viruses negative-sense
- C12N2760/00011—Details
- C12N2760/18011—Paramyxoviridae
- C12N2760/18511—Pneumovirus, e.g. human respiratory syncytial virus
- C12N2760/18534—Use of virus or viral component as vaccine, e.g. live-attenuated or inactivated virus, VLP, viral protein
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2760/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssRNA viruses negative-sense
- C12N2760/00011—Details
- C12N2760/18011—Paramyxoviridae
- C12N2760/18611—Respirovirus, e.g. Bovine, human parainfluenza 1,3
- C12N2760/18634—Use of virus or viral component as vaccine, e.g. live-attenuated or inactivated virus, VLP, viral protein
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2760/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssRNA viruses negative-sense
- C12N2760/00011—Details
- C12N2760/18011—Paramyxoviridae
- C12N2760/18611—Respirovirus, e.g. Bovine, human parainfluenza 1,3
- C12N2760/18651—Methods of production or purification of viral material
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Immunology (AREA)
- Virology (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Microbiology (AREA)
- Mycology (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- Biochemistry (AREA)
- Genetics & Genomics (AREA)
- Molecular Biology (AREA)
- Biotechnology (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Crystallography & Structural Chemistry (AREA)
- Pulmonology (AREA)
- Communicable Diseases (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Saccharide Compounds (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Medicinal Preparation (AREA)
- Emulsifying, Dispersing, Foam-Producing Or Wetting Agents (AREA)
- Agricultural Chemicals And Associated Chemicals (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Abstract
Description
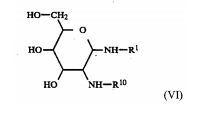
a) um glicolipídio de Fórmula I; em que a Fórmula I éem que
R1 é hidrogênio, ou radical alquila saturado possuindo até 20 átomos de carbono;
X é -CH2-, -O- ou -NH-;
R2 é hidrogênio, ou um radical alquila saturado possuindo até 20 átomos de carbono;
R3, R4, e R5 são independentemente hidrogênio, -SO42-, -PO42-, -CO-alquilC1- 10;
R6 é L-alanil, L-alfa-aminobutil, L-arginil, L-asparginil, L-aspartil, L-cisteinil, Lglutamil, L-glicil, L-histidil, L-hidroxipropil, L-isoleucil, L-leucil, L-lisil, L-metionil, Lornitinil, L-fenilalani, L-prolil, L-seril, L-treonil, L-tirosil, L-triptofanil, e L-valil ou seus D-isômeros;
em uma forma sal, onde a forma salina é derivada de um ácido fraco;
b) um álcool em que o álcool é HO-alquilC1-3;
c) um ácido fraco, em que 1) o ácido fraco está em excesso molar com referência ao teor de glicolipídio, e 2) é qualquer ácido que possui um valor de pKa entre cerca de 1,0 e cerca de 9,5 usando tabelas ou valores padrões; e
d) um tensoativo não-iônico, onde o tensoativo não-iônico é um agente que reduz a tensão superficial do material em que ele está dissolvido e possui um componente que é hidrofóbico e um outro componente que é hidrofílico.
- a) uma Solução Estoque de Glicosilamida; e
- b) um tampão adequado, onde o tampão é um apropriado para uso veterinário ou médico e pode manter um pH relativamente constante numa solução aquosa de entre cerca de 6,0 e cerca de 8,0.
Ele pode ser metanol, etanol, ou propanol em qualquer forma, tal como n-propanol ou iso-propanol. Etanol é preferido.
R1 é hidrogênio, ou radical alquila saturado possuindo até 20 átomos de carbono;
X é -CH2-, -O- ou -NH-;
R2 é hidrogênio, ou radical alquila saturado possuindo até 20 átomos de carbono;
R3, R4, e R5 são independentemente hidrogênio, -SO4 2-, -PO4 2-, ou -COalquilC1-10;
R6 é L-alanil, L-alfa-aminobutil, L-arginil, L-asparginil, L-aspartil, L-cisteinil, Lglutamil, L-glicil, L-histidil, L-hidroxipropil, L-isoleucil, L-leucil, L-lisil, L-metionil, Lornitinil, L-fenilalani, L-prolil, L-seril, L-treonil, L-tirosil, L-triptofanil, e L-valil ou seus D-isômeros;
ou um sal farmaceuticamente aceitável desses mencionados.
R1 é hidrogênio, ou saturated alquilC12-18;
R2 é hidrogênio, ou saturated alquilC7-11;
X é -CH2,;
R4, e R5 são independentemente hidrogênio;
R6 é selecionado de L-leucil;
H2N-R1 (V)
onde R1 tem o significado acima mencionado, para produzir glicosilaminas (Fórmula VI)
R11-CO-CH20R4 (VII)
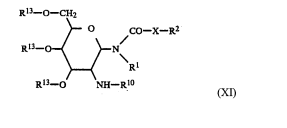
R2 possuindo o significado acima mencionado, e R11 representando halogênio tal como, por exemplo, cloro, ou representando -O-CO-R2 com o significado acima mencionado para R2, ou representando -O-CO-O-alquila inferior. Desse modo, glicosilamidas (Fórmula VIII)em que R1, e R2 possuem os significados acima mencionados, e R10 é igual como R6 e X representa -CH2-, são obtidos. As condições para as N-acilações desse tipo estão indicadas em DE-OS (German Published Specification ) No. 3.213.650.
R12-CO-O-R2 (IX)
R12 representando halogênio tal como, por exemplo, cloro ou bromo, e R2 possuindo o significado acima mencionado, então os glicosilcarbamatos (VIII) são obtidos, X na Fórmula VIII representando oxigênio.
R2-NCO (X)
com R2 possuindo o significado acima mencionado, glicosiluréias de Fórmula VIII são obtidas, e X é -NH-. Essa reação de acilação, como as reações acima mencionadas, é preferivelmente realizada em solventes orgânicos, com as temperaturas de reação estando entre -20° C e 60° C, preferivelmente entre 0° C e 25° C. Solventes adequados são os acima mencionados álcoois, éteres, hidrocarbonetos halogenados, ou dimetilformamida.
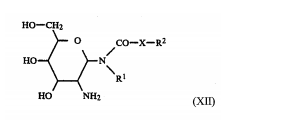
R13 representando acetil, benzoil ou p-nitrobenzoil.
uréias de acordo com Fórmula XII, ou de seus sais, com a adequados derivados aminoácidos. Adequados derivados aminoácidos são aminoácidos N-bloqueados Fórmula (XIII)com R7 possuindo o significado acima mencionado,
R8 representando hidrogênio ou metil, e
R14 representando um grupo protetor que é usualmente utilizado na síntese de peptídeos e pode ser seletivamente eliminado novamente embora mantendo a ligação peptídeo.
Ácido 2-(N-morfolino)etano-sulfônico (também conhecido como MES);
Ácido 3-(N-morfolino)propano-sulfônico (também conhecido como MOPS);
Ácido N-[tris (hidroximetil] -2-aminoetano-sulfônico (também conhecido como TES);
Ácido 4-(2-hidroxietil)piperazin-1-etano-sulfônico (também conhecido como HEPES);
[tris (hidroximetil)metil] glicina (também conhecido como TRIS).
Qualquer reação química que possa converter a forma acetato do glicolipídio de volta para a forma não acetato pode provocar a floculação do glicolipídio contido na Solução aquosa. Quando ocorre a floculação do glicolipídio, as moléculas do glicolipídio saem da solução como escamas finas, sedimentando no fundo do recipiente. A concentração inicial do ácido fraco na Solução Estoque de Glicosilamida de glicolipídio e álcool determina se irá ocorrer qualquer floculação do glicolipídio. O ácido fraco deverá estar em excesso molar com referência ao glicolipídio para evitar floculação.
Tabela 1.
Uma composição não adequada para uso comercial.
Tabela 2.
Composição de a Solução Estoque de Glicosilamida.
Uma solução estoque 2M de fosfato monobásico de sódio foi preparada mediante dissolver 138 gramas de sal de NaH2PO4.H2O em 250 mL de água DI em um béquer e levando o volume final para 500 mL. De modo similar, uma solução estoque 2M de fosfato dibásico de sódio foi preparada mediante dissolver 142 gramas de NaH2PO4 em 300 mL de Água DI em um béquer trazendo o volume final a 500 mL. Ambas as soluções estoques foram esterilizadas por filtração usando um filtro de 0,2 mícron.
Tabela 3.
Composições da solução estoque 1M da solução tampão de fosfato de sódio em diferentes pHs
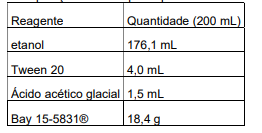
Tabela 4.
Preparação de composições de glicosilamida contendo quantidade equimolar de ácido acético e glicolipídios. (Ver Exemplo 1)Tabela 5.
Preparação de solução de Adjuvante Glicolipídio usando Solução estoque de Glicosilamida contendo duas vezes a quantidade molar de ácido acético como glicolipídio (ver Exemplo 2)
Uma concentração crescente de ácido acético foi acrescentado a essa mistura d adjuvante glicolipídio floculada. O ácido acético foi diluído 16,6 vezes com água para conseguir uma solução de trabalho de concentração 1 Molar. Em seguida, 15 L dessa solução 1M foi acrescentada a 15 mL da mistura de adjuvante glicolipídio para aumentar a concentração de ácido acético em 1 mM. Com concentração crescente de ácido acético, o pH dos adjuvantes glicolipídios reduziu e os floculados se dissolveram. Todavia, os adjuvantes glicolipídios permaneceram um tanto turvos. Essa observação confirma que o aumento da concentração de ácido acético converte a base livre de Bay 15-5381 numa forma acetato, a qual é mais solúvel em solução aquosa.
Tabela 7.
Titulação de adjuvante glicolipídio com ácido acético.
Tabela 8.
Composição de uma solução estoque de Glicosilamida
Tabela 9
Preparação de Soluções de Adjuvante Glicolipídio estáveis com e sem NaCl
Tabela 10.
Titulação de uma Solução estável de Adjuvante Glicolipídio com NaOH
Tabela 11
Sumário dos parâmetros usados no método HPLC para quantificar Bay 15- 5381®Tabela 12
Padrões de Bay 15-5831®.
Tabela 13
Características da batelada de 30 L de adjuvante glicolipídio com o aumento da concentração de NaOH
Tabela 15.
Quantificação de Bay 15-5831® após a realização dos testes de estresse
Tabela 16
Ensaio Viricida para a Solução de Adjuvante Glicolipídio.
Claims (15)
- Composição CARACTERIZADA pelo fato de que compreende:
a) um glicolipídio de Fórmula I;
em que a fórmula I éem que
R1 é hidrogênio, ou um radical alquila saturado tendo até 20 átomos de carbono;
X é -CH2-, -O- ou -NH-; R2 é hidrogênio, ou um radical alquila saturado ou insaturado tendo até 20 átomos de carbono;
R3, R4, e R5 são independentemente hidrogênio, -COC1-10-alquil;
R6 é L-alanil, L-alfa-aminobutil, L-arginil, L-asparginil, L-aspartil, L-cisteinil, Lglutamil, L-glicil, L-histidil, L-hidroxipropil, L-isoleucil, L-leucil, L-lisil, L-metionil, Lornitinil, L-fenilalani, L-prolil, L-seril, L-treonil, L-tirosil, L-triptofanil e L-valil, ou seus D-isômeros;
em uma forma salina, onde a forma salina é derivada de um ácido fraco;
b) um álcool em que o álcool é HO-C1-3-alquil;
c) um ácido fraco, em que o ácido fraco 1) está em excesso molar com referência ao teor de glicolipídio, e 2) é qualquer ácido tendo um valor de pKa (o -log da Ka) entre 1,0 e 9,5 usando tabelas ou valores padrões; e
d) um tensoativo não-iônico, em que o tensoativo não-iônico é um agente que reduz a tensão superficial do material em que ele está dissolvido e possui um componente que é hidrofóbico e um outro componente que é hidrofílico;
adicionalmente em que a composição tem um pH de 6 a 8. - Composição, de acordo com a reivindicação 1, CARACTERIZADA pelo fato de que o glicolipídio é um composto de Fórmula II(a): e o ácido fraco é selecionado a partir de um ou qualquer combinação dos seguintes ácidos fracos, ácido acético, H(C2H3O2) (pKa 4,76); ácido ascórbico (1), H2(C6H6O6) (pKa 4,10); ácido acetilsalicílico, H8(C9O4), (pKa 3,5,); ácido butanóico H(C4H7O2) (pKa 4,83); ácido carbônico, forma 1, H2CO3, (pKa 4,83); ácido cítrico, forma 1, H3(C6H5O7), (pKa 3,14); ácido cítrico forma 2, H2C6H5O7 - , (pKa 4,77); ácido cítrico, forma 3, (HC6H5O7) = , (pKa 6,39); ácido fórmico, H(CHO2), (pKa 3,75); ácido fumárico, H4(C4O4) (pKa 3,03); ácido heptanóico, H(C7H13O2), (pKa 4,89); ácido hexanóico, H(C6H11O2), (pKa 4,84); isocitrato, H8(C6O7) (pKa 3,29); ácido lático, H(C3H5O3), (pKa 3,08); ácido maleico, H4(C4O4) (pKa 1,83); ácido nicotínico, H5(C6NO2) (pK 3,39); ácido oxálico forma 1, H2(C2O4), (pKa 1,23); ácido oxálico, forma 2, (HC2O4) - , (pKa 4,19); ácido pentanóico, H(C5H9O2), (pKa 4,84); ácido fosfórico forma 1, H3PO4, (pKa 2,16); ácido propanóico, H(C3H5O2), (pKa 4,86); ácido pirúvico, H4(C3O3) (pKa 2,39) e ácido succínico H6(C4O4) (pKa 4,19).
- Composição, de acordo com a reivindicação 2, CARACTERIZADA pelo fato de que o glicolipídio é um composto de Fórmula II(b): e o ácido fraco é selecionado a partir de um ou qualquer combinação dos seguintes ácidos fracos: ácido acético, ácido acetilsalicílico, ácido cítrico, ácido fórmico, ácido fumárico, isocitrato, ácido maleico, ácido nicotínico, ácido fosfórico, ácido pirúvico e ácido succínico.
- Composição, de acordo com a reivindicação 2, CARACTERIZADA pelo fato de que o ácido fraco é selecionado a partir do grupo que consiste em: ácido acético, ácido acetilsalicílico, ácido cítrico forma 1, ácido cítrico forma 2, ácido cítrico forma 3, ácido fórmico, ácido fumárico, isocitrato, ácido maleico, ácido nicotínico, ácido fosfórico forma 1, ácido pirúvico e ácido succínico.
- Composição, de acordo com qualquer uma das reivindicações 1 a 5, CARACTERIZADA pelo fato de que o referido ácido fraco está em uma quantidade que é maior que o equivalente molar do glicolipídio, ou está em uma quantidade maior que o equivalente molar do glicolipídio na seguinte proporção;
- a) 1,25 vezes maior,
- b) 2,0 vezes maior,
- c) 2,5 vezes maior,
- d) 2,7 vezes maior,
- e) 3,0 vezes maior,
- f) 5,0 vezes maior,
- Composição, de acordo com qualquer uma das reivindicações 1 a 6, CARACTERIZADA pelo fato de que o alcool é o alcool etílico.
- Composição, de acordo com qualquer uma das reivindicações 1 a 7, CARACTERIZADA pelo fato de que o referido tensoativo não-iônico é selecionado a partir de qualquer um ou uma combinação do grupo que consiste em: monolaurato de Sorbitano, monopalmitato de Sorbitano, monostearato de Sorbitano, tristearato de Sorbitano, monooleato de Sorbitano, trioleato de Sorbitano, monolaurato de Polioxietilensorbitano, monopalmitato de Polioxietilensorbitano, monosterato de Polioxietilensorbitano, monooleato de Polioxietilensorbitano, trioleato de Polioxietilensorbitano, e outros sorbitanos e polioxietileno sorbitanos comumente usados em vacinas.
- Composição CARACTERIZADA pelo fato de que compreende:
a) um glicolipídio de Fórmula I;
em que a fórmula I é:em que
R1 é hidrogênio, ou um radical alquila saturado possuindo até 20 átomos de carbono;
X é -CH2-, -O- ou -NH;
R2 é independentemente hidrogênio ou um radical alquila saturado ou insaturado possuindo até 20 átomos de carbono;
R3, R4, e R5 são independentemente hidrogênio, -SO4 2-, -PO4 2-, -COC1-10- alquil;
R6 é L-alanil, L-alfa-aminobutil, L-arginil, L-asparginil, L-aspartil, L-cisteinil, Lglutamil, L-glicil, L-histidil, L-hidroxipropil, L-isoleucil, L-leucil, L-lisil, L-metionil, Lornitinil, L-fenilalani, L-prolil, L-seril, L-treonil, L-tirosil, L-triptofanil e L-valil, ou seus D-isômeros;
na forma de um sal, em que a forma de um sal é derivada de um ácido fraco;
b) um álcool em que o álcool é HO-C1-3-alquil;
c) um ácido fraco, em que o ácido fraco 1) está em excesso molar com referência ao teor de glicolipídio, e 2) é qualquer ácido que possui um valor de pKa (o -log de Ka) entre 1,0 e 9,5 usando tabelas ou valores padrões; e
d) um tensoativo não-iônico, em que o tensoativo não-iônico é um agente que reduz a tensão superficial do material em que ele está dissolvido e possui um componente que é hidrofóbico e um outro componente que é hidrofílico; e
e) um tampão aquoso, em que o tampão aquoso apropriado é adequado para uso em vacina e pode manter o pH dos outros ingredientes dentro de uma faixa de pH de 6 a 8, com a condição de que não mais que 50 mM de NaCl seja usado;
adicionalmente em que a composição tem um pH de 6 a 8. - Composição, de acordo com a reivindicação 9, CARACTERIZADA pelo fato de que o pH da solução é ajustado para um pH relativamente constante em uma solução aquosa de entre 6 e 7, e o tampão é selecionado a partir do grupo que consiste em tampões fosfato tendo um ou outro ou ambos sais monobásico e dibásico de fosfato de sódio e/ou fosfato de potássio em proporções iguais ou diferentes.
- Composição, de acordo com a reivindicação 9, CARACTERIZADA pelo fato de que o referido tampão é selecionado a partir do grupo:
- a) ácido 2-(N-morfolino)etano-sulfônico (também conhecido como MES);
- b) ácido 3-(N-morfolino)propano-sulfônico (também conhecido como MOPS);
- c) ácido N-[tris (hidroximetil] -2-aminoetano-sulfônico (também conhecido como TES);
- d) ácido 4-(2-hidroxietil)piperazin-1-etano-sulfônico (também conhecido como HEPES);
- e) [tris (hidroximetil)metil] glicina (também conhecido como TRIS); e
- f) fosfato de sódio ou potássio; ou qualquer combinação dos mesmos.
- Composição, de acordo com qualquer uma das reivindicações 1 a 11, CARACTERIZADA pelo fato de que adicionalmente compreende um antígeno selecionado a partir do grupo consistindo em vírus do herpes bovino vivo modificado, vírus sincicial respiratório bovino vivo modificado e vírus para-influenza vivo modificado Tipo 3, ou qualquer combinação dos mesmos.
- Composição CARACTERIZADA pelo fato de que compreende:
a) acetato de N-(2-desóxi-2-L-leucilamino-β-D-glicopiranosil)-N-octadecildodecanamida, possuindo uma estrutura de Fórmula III:Fórmula III
b) etanol;
c) ácido acético;
d) tensoativo não-iônico, selecionado de: monolaurato de Sorbitano, monopalmitato de Sorbitano, monostearato de Sorbitano, tristearato de Sorbitano, monooleato de Sorbitano, trioleato de Sorbitano, monolaurato de Polioxietilensorbitano, monopalmitato de Polioxietilensorbitano, monosterato de Polioxietilensorbitano, monooleato de Polioxietilensorbitano, trioleato de Polioxietilensorbitano;
e) um tampão aquoso, em que o pH da solução é ajustado para um pH relativamente constante em uma solução aquosa tamponada de entre 6 e 7, e o tampão é selecionado a partir dos seguintes:
1) ácido 2-(N-morfolino)etano-sulfônico (também conhecido como MES);
2) ácido 3-(N-morfolino)propano-sulfônico (também conhecido como MOPS);
3) ácido N-[tris (hidroximetil] -2-aminoetano-sulfônico (também conhecido como TES);
4) ácido 4-(2-hidroxietil)piperazin-1-etano-sulfônico (também conhecido como HEPES); e
5) [tris (hidroximetil)metil] glicina (também conhecido como TRIS);
ou qualquer combinação dos mesmos,
com a condição de que não mais que 15 mM de NaCl seja usado e;
6) um antígeno consistindo essencialmente de vírus do herpes bovino vivo modificado, vírus sincicial respiratório bovino vivo modificado e vírus para-influenza vivo modificado Tipo 3. - Processo para preparar uma composição CARACTERIZADO pelo fato de que compreende misturar juntos os seguintes:
- A) um glicolipídio de Fórmula I;
- B) um álcool, em que o álcool é HO-C1-3-alquil;
- C) um ácido fraco, em que a quantidade do ácido fraco está em excesso molar com referência ao teor do glicolipídio; e
- D) um tensoativo não-iônico.
- Processo para preparar uma composição CARACTERIZADO pelo fato de que compreende misturar juntos os seguintes:
- A) um glicolipídio de Fórmula I;
- B) um álcool, em que o álcool é HO-C1-3-alquil;
- C) um ácido fraco, em que a quantidade do ácido fraco está em excesso molar com referência ao teor do glicolipídio;
- D) um tensoativo não-iônico; e em seguida acrescentar,
- E) um tampão adequado.
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US76227906P | 2006-01-26 | 2006-01-26 | |
| US60/762,279 | 2006-01-26 | ||
| US81498406P | 2006-06-20 | 2006-06-20 | |
| US60/814,984 | 2006-06-20 | ||
| PCT/IB2007/000258 WO2007085962A2 (en) | 2006-01-26 | 2007-01-15 | Novel glycolipid adjuvant compositions |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| BRPI0706709A2 BRPI0706709A2 (pt) | 2011-04-05 |
| BRPI0706709B1 true BRPI0706709B1 (pt) | 2021-03-23 |
| BRPI0706709B8 BRPI0706709B8 (pt) | 2021-05-25 |
Family
ID=38309580
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI0706709A BRPI0706709B8 (pt) | 2006-01-26 | 2007-01-15 | composição e processo para preparar a composição |
Country Status (21)
| Country | Link |
|---|---|
| US (1) | US8460679B2 (pt) |
| EP (2) | EP1991266B1 (pt) |
| JP (1) | JP5538725B2 (pt) |
| KR (2) | KR20110140140A (pt) |
| AR (1) | AR059192A1 (pt) |
| AU (1) | AU2007209104B2 (pt) |
| BR (1) | BRPI0706709B8 (pt) |
| CA (1) | CA2634888C (pt) |
| CY (1) | CY1114310T1 (pt) |
| DK (1) | DK1991266T3 (pt) |
| ES (1) | ES2425576T3 (pt) |
| HK (1) | HK1128078A1 (pt) |
| ME (3) | ME00045B (pt) |
| NO (1) | NO341463B1 (pt) |
| NZ (1) | NZ569375A (pt) |
| PL (1) | PL1991266T3 (pt) |
| PT (1) | PT1991266E (pt) |
| RS (2) | RS52930B (pt) |
| RU (1) | RU2392965C2 (pt) |
| TW (1) | TWI372631B (pt) |
| WO (1) | WO2007085962A2 (pt) |
Families Citing this family (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2402024A1 (en) * | 2006-06-28 | 2012-01-04 | Statens Serum Institut | Expanding the t cell repertoire to include subdominant epitopes by vaccination with antigens delivered as protein fragments or peptide cocktails |
| HUE028921T2 (en) * | 2008-06-27 | 2017-01-30 | Zoetis Services Llc | New adjuvant preparations |
| WO2010039934A1 (en) | 2008-10-03 | 2010-04-08 | Novartis Ag | Bovine herpes virus -1 compositions, vaccines and methods |
| CN105188710A (zh) | 2013-03-15 | 2015-12-23 | 葛兰素史密丝克莱恩生物有限公司 | 包含缓冲的氨基烷基氨基葡糖苷磷酸酯衍生物的组合物及其用于增强免疫应答的用途 |
| EP3046580A2 (en) | 2013-09-19 | 2016-07-27 | Zoetis Services LLC | Oil-based adjuvants |
| CN105899199A (zh) | 2013-11-26 | 2016-08-24 | 硕腾服务有限责任公司 | 诱导免疫应答的组合物 |
| US10478487B2 (en) | 2015-01-16 | 2019-11-19 | Zoetis Services Llc | Foot-and-mouth disease vaccine |
| CA2992892C (en) * | 2015-07-20 | 2019-12-31 | Zoetis Services Llc | Liposomal adjuvant compositions |
| GB201703529D0 (en) | 2017-03-06 | 2017-04-19 | Cambridge Entpr Ltd | Vaccine composition |
| CN110713520B (zh) * | 2019-11-06 | 2021-01-01 | 中国石油天然气股份有限公司 | 油酰基氨基酸-γ-L-谷氨酰-L-半胱氨酰-甘氨酸多肽及其制备与应用 |
| TW202206098A (zh) | 2020-08-11 | 2022-02-16 | 美商碩騰服務公司 | 抗冠狀病毒疫苗 |
| WO2022072431A1 (en) | 2020-09-30 | 2022-04-07 | Zoetis Services Llc | Novel pasteurella multocida strains and vaccines having hyac and nanp deletions |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4291019A (en) * | 1979-07-09 | 1981-09-22 | Iowa State University Research Foundation, Inc. | Vaccine for infectious bovine rhinotracheitis |
| DE3213650A1 (de) | 1982-04-14 | 1983-10-27 | Bayer Ag, 5090 Leverkusen | N-glycosylierte carbonsaeureamid-derivate, verfahren zu ihrer herstellung sowie ihre verwendung zur beeinflussung der koerpereigenen abwehr |
| DE3403495A1 (de) | 1983-11-23 | 1985-05-30 | Bayer Ag, 5090 Leverkusen | Phosphorylierte glycosylamide, -harnstoffe, -carbamate und -thiocarbamate, verfahren zu ihrer herstellung sowie ihre verwendung |
| DE3346623A1 (de) | 1983-12-14 | 1985-07-04 | Bayer Ag, 5090 Leverkusen | N-glycosylierte harnstoffe, carbamate und thiocarbamate, verfahren zu ihrer herstellung sowie ihre verwendung |
| DE3521994A1 (de) | 1985-06-20 | 1987-01-02 | Bayer Ag | N-(2-aminoacylamido-2-desoxy-hexosyl)-amide-, -carbamate und -harnstoffe, verfahren zu ihrer herstellung sowie ihre verwendung in arzneimitteln |
| NZ232740A (en) * | 1989-04-20 | 1992-06-25 | Riker Laboratories Inc | Solution for parenteral administration comprising a 1h-imidazo(4,5-c) quinolin-4-amine derivative, an acid and a tonicity adjuster |
| US6764682B1 (en) | 1994-06-16 | 2004-07-20 | Aventis Pasteur Limited | Adjuvant compositions containing more than one adjuvant |
| US5718904A (en) | 1995-06-02 | 1998-02-17 | American Home Products Corporation | Adjuvants for viral vaccines |
| US6290971B1 (en) | 1995-06-15 | 2001-09-18 | Aventis Pasteur Limited | Adjuvant compositions comprising a mineral salt and another immunostimulating compound |
| FI109332B (fi) * | 1998-12-17 | 2002-07-15 | Orion Yhtymae Oyj | Toremifeenin liukoisia koostumuksia |
| JP2004510747A (ja) | 2000-10-02 | 2004-04-08 | グラクソスミスクライン バイオロジカルズ ソシエテ アノニム | 分割エンベロープウイルス調製物 |
-
2007
- 2007-01-15 ME MEP-2008-45A patent/ME00045B/me unknown
- 2007-01-15 CA CA2634888A patent/CA2634888C/en active Active
- 2007-01-15 PL PL07705530T patent/PL1991266T3/pl unknown
- 2007-01-15 AU AU2007209104A patent/AU2007209104B2/en active Active
- 2007-01-15 BR BRPI0706709A patent/BRPI0706709B8/pt active IP Right Grant
- 2007-01-15 DK DK07705530.9T patent/DK1991266T3/da active
- 2007-01-15 EP EP07705530.9A patent/EP1991266B1/en active Active
- 2007-01-15 EP EP12165409A patent/EP2481423A1/en not_active Withdrawn
- 2007-01-15 NZ NZ569375A patent/NZ569375A/en unknown
- 2007-01-15 KR KR1020117028574A patent/KR20110140140A/ko not_active Application Discontinuation
- 2007-01-15 ES ES07705530T patent/ES2425576T3/es active Active
- 2007-01-15 PT PT77055309T patent/PT1991266E/pt unknown
- 2007-01-15 WO PCT/IB2007/000258 patent/WO2007085962A2/en active Application Filing
- 2007-01-15 JP JP2008551904A patent/JP5538725B2/ja active Active
- 2007-01-15 RU RU2008129203/15A patent/RU2392965C2/ru active
- 2007-01-15 ME MEP-45/08A patent/MEP4508A/xx unknown
- 2007-01-15 RS RS20130372A patent/RS52930B/en unknown
- 2007-01-15 RS RSP-2008/0318A patent/RS20080318A/sr unknown
- 2007-01-15 ME MEP-2013-95A patent/ME01545B/me unknown
- 2007-01-15 KR KR1020087018207A patent/KR101202553B1/ko active IP Right Grant
- 2007-01-25 AR ARP070100334A patent/AR059192A1/es not_active Application Discontinuation
- 2007-01-25 TW TW096102865A patent/TWI372631B/zh active
- 2007-01-26 US US11/698,335 patent/US8460679B2/en active Active
-
2008
- 2008-08-04 NO NO20083405A patent/NO341463B1/no unknown
-
2009
- 2009-06-19 HK HK09105528.1A patent/HK1128078A1/xx unknown
-
2013
- 2013-09-03 CY CY20131100756T patent/CY1114310T1/el unknown
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5538725B2 (ja) | 新規糖脂質アジュバント組成物 | |
| ES2236799T3 (es) | Procedimiento de replicacion de virus de influenza en un cultivo celular y virus de influenza obtenibles por el procedimiento. | |
| CN1326564C (zh) | 单磷酰基脂质a的水性免疫佐剂组合物 | |
| TWI398272B (zh) | 化學定義的安定劑 | |
| DE69534670T2 (de) | Immunstimulierende zusammensetzungen,die ein minerales salz und ein weiteres adjuvant enthalten | |
| ES2333334T5 (es) | Lawsonia intracellularis de origen europeo y vacunas, agentes de diagnóstico y métodos de uso de la misma | |
| ES2300285T3 (es) | Derivados de mono- y disacarido. | |
| US4537769A (en) | Stabilization of influenza virus vaccine | |
| DE69918283T2 (de) | Stabilisierte herpesvirusformulierung | |
| KR101026053B1 (ko) | 바이로솜-같은-입자 | |
| RU2522219C2 (ru) | Композиции и способы иммунизации с применением лигандов cd1d | |
| PT99389A (pt) | Processo de preparacao de derivados de muramildipeptido e de vacina para a gripe contendo os derivados | |
| JP2002514186A (ja) | ウイルス性細胞接着阻害剤としての複合糖質 | |
| CN1124013A (zh) | 含3-邻位-脱酰基的单磷酰基脂质a的流感疫苗组合物 | |
| CN111961592B (zh) | 一种rna病毒保存液及其制备方法和应用 | |
| CN101554480A (zh) | 用于生产型动物的改良dna疫苗 | |
| US20160120982A1 (en) | Vaccine stabilizer | |
| RU2067002C1 (ru) | Живая культуральная вакцина эпм против чумы плотоядных | |
| AU2020256873A1 (en) | Thawing fluid, preparation method therefor and use thereof | |
| CN117088805A (zh) | 可离子化脂质化合物及其在递送领域的应用 | |
| RU1615919C (ru) | Вакцина против вирусного энтерита, ботулизма и чумы плотоядных, способ ее изготовления и способ профилактики этих заболеваний | |
| WO2006138248A2 (en) | Vaccines for protection from bartonella infection and related methods | |
| Weiss et al. | Immunological Investigations on Tropical Sprue in Porto Rico: 4. The Biology of Monilia psilosis in Relation to Sprue | |
| BRPI1003332A2 (pt) | formulaÇço de adjuvantes para imunizaÇço de animais com vÍrus rÁbico |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B06F | Objections, documents and/or translations needed after an examination request according [chapter 6.6 patent gazette] | ||
| B25A | Requested transfer of rights approved |
Owner name: PAH USA 15 LLC (US) |
|
| B25D | Requested change of name of applicant approved |
Owner name: ZOETIS P LLC (US) |
|
| B25C | Requirement related to requested transfer of rights |
Owner name: ZOETIS P LLC (US) Free format text: A FIM DE ATENDER A TRANSFERENCIA REQUERIDA ATRAVES DA PETICAO NO 860150304717 DE 23/12/2015, E NECESSARIO E NECESSARIO APRESENTAR A TRADUCAO JURAMENTADA DO DOCUMENTO DE CESSAO, CONFORME ART. 18 DO DEC. 13.609/43. |
|
| B07D | Technical examination (opinion) related to article 229 of industrial property law [chapter 7.4 patent gazette] | ||
| B25A | Requested transfer of rights approved |
Owner name: ZOETIS SERVICES LLC (US) |
|
| B25G | Requested change of headquarter approved |
Owner name: ZOETIS SERVICES LLC (US) |
|
| B07E | Notification of approval relating to section 229 industrial property law [chapter 7.5 patent gazette] | ||
| B06A | Patent application procedure suspended [chapter 6.1 patent gazette] | ||
| B06A | Patent application procedure suspended [chapter 6.1 patent gazette] | ||
| B09A | Decision: intention to grant [chapter 9.1 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] |
Free format text: PRAZO DE VALIDADE: 10 (DEZ) ANOS CONTADOS A PARTIR DE 23/03/2021, OBSERVADAS AS CONDICOES LEGAIS. |
|
| B16C | Correction of notification of the grant [chapter 16.3 patent gazette] |
Free format text: PRAZO DE VALIDADE: 20 (VINTE) ANOS CONTADOS A PARTIR DE 15/01/2007 OBSERVADAS AS CONDICOES LEGAIS. PATENTE CONCEDIDA CONFORME ADI 5.529/DF |