BRPI0414059B1 - síntese seletiva de pirimidinas substituídas em cf3 - Google Patents
síntese seletiva de pirimidinas substituídas em cf3 Download PDFInfo
- Publication number
- BRPI0414059B1 BRPI0414059B1 BRPI0414059A BRPI0414059A BRPI0414059B1 BR PI0414059 B1 BRPI0414059 B1 BR PI0414059B1 BR PI0414059 A BRPI0414059 A BR PI0414059A BR PI0414059 A BRPI0414059 A BR PI0414059A BR PI0414059 B1 BRPI0414059 B1 BR PI0414059B1
- Authority
- BR
- Brazil
- Prior art keywords
- amine
- lewis acid
- group
- formula
- groups
- Prior art date
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D239/00—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings
- C07D239/02—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings
- C07D239/24—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members
- C07D239/28—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, directly attached to ring carbon atoms
- C07D239/32—One oxygen, sulfur or nitrogen atom
- C07D239/42—One nitrogen atom
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Epidemiology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Catalysts (AREA)
Abstract
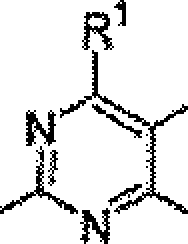
"síntese seletiva de pirimidinas substituídas em cf3". a presente invenção refere-se com um método de preparar um composto de fórmula (i) em que x^ 1^, x^ 2^ e r^ 3^ -r^ 4^ são como aqui definido. o método inclui reagir um composto de fórmula (ii) com uma amina de fórmula (iii) (hnr^ 3^r^ 4^) na presença de um ácido de lewis e uma base não-nucleófila. a porção 2,4-diaminopirimidina é um componente comum em várias moléculas semelhantes a fármaco biologicamente ativas e verificou-se que derivados de pirimidina são úteis no tratamento de crescimento celular anormal, tal como câncer, em mamíferos.
Description
(54) Título: SÍNTESE SELETIVA DE P1RIMIDINAS SUBSTITUÍDAS EM CF3 (51) IntCI.: C07D 239/42; A61P 35/00.
(30) Prioridade Unionista: 05/09/2003 US 60/500,733.
(73) Titular(es): PFIZER PRODUCTS INC..
(72) Inventorfes): JOHN CHARLES KATH; DANIEL TYLER RICHTER; MICHAEL JOSEPH LUZZIO.
(86) Pedido PCT: PCT IB2004002744 de 24/08/2004 (87) Publicação PCT: WO 2005/023780 de 17/03/2005 (85) Data do Início da Fase Nacional: 02/03/2006 (57) Resumo: SÍNTESE SELETIVA DE PIRIMIDINAS SUBSTITUÍDAS EM CF3. A presente invenção refere-se com um método de preparar um composto de fórmula (I) em que ΧΛ 1Λ, ΧΛ 2Λ e RA 3Λ -RA 4A são como aqui definido. O método inclui reagir um composto de fórmula (II) com uma amina de fórmula (III) (HNRA 3ARA 4A) na presença de um ácido de Lewis e uma base nãonucleófila. A porção 2,4-diaminopirimidina é um componente comum em várias moléculas semelhantes a fármaco biologicamente ativas e verificou-se que derivados de pirimidina são úteis no tratamento de crescimento celular anormal, tal como câncer, em mamíferos.
• i i · · · ······ ·· • · · ··· · ··· · · · ·· ··· ·· ····· · «·· · · ··· · · · ··
Relatório Descritivo da Patente de Invenção para SÍNTESE
SELETIVA DE PIRIMIDINAS SUBSTITUÍDAS EM CF3.
Antecedentes da Invenção
R2 nfW
A porção 2,4-diaminopirimidina (1) é um componente comum de várias moléculas similares a droga biologicamente ativas. Verificou-se que os derivados de pirimidina são úteis no tratamento do crescimento celular anormal, tal como câncer, em mamíferos. Estas porções são comumente sintetizadas começando com o intermediário pirimidina 2 (em que X é um grupo de saída; mais comumente um halogênio) e um equivalente de amina 10 3, HNR3R4 (ver Esquema 1 abaixo). Para a grande maioria das reações que envolvem pirimidinas de fórmula 2 e aminas de fórmula 3, é sabido que esta primeira adição de amina ocorre preferenciaimente (ou exclusivamente) na posição 4 mais reativa de pirimidina (Chemistry of Heterocyclic Compounds, The Pyrímidines, Volume 52, Wiley, Nova Iorque 1994, p. 371.) para propor15 cionar o intermediário 4. Os fatores primários que influenciam a seletividade desta adição inicial de amina são os efeitos estereoeletrônicos associados com substituintes presentes tanto na pirimidina 2 como na amina 3 e em
menor grau no solvente reacional. O aquecimento subseqüente de 4 com uma segunda amina (5) proporciona a 2,4-diaminopirimidina 1 desejada.
ESQUEMA 1 x
X
R1
HNR^R6 5 nr5r*
Um exemplo representativo da química anteriormente referida pode ser encontrado em WO 00391901 e está indicado no esquema 2. Outros exemplos que utilizam este esquema sintético geral incluem Montebugnoli et ai., Tetrahedron 2002, (58), p. 2147. Chemistry of Heterocyclic 25 Compounds, The Pyrimidines, Volume 52, Wiley, Nova Iorque 1994, pp. 371417. A adição seletiva de amina a 2,4-dicloro-5-carboxamidopirimidinas está descrita em WO 02/04429. Adições seletivas de amina a 2,4-dicloro-5halopirimidinas estão descritas em WO 01/65655.
• *«
ESQUEMA 2
anilina base de Hunig n-BuOH; Δ 4h
Apesar de existirem vários exemplos gerais em que pirimidinas específicas (2), aminas (3) ou condições reacionais proporcionam misturas não-seletivas de 2-cloro-4-amino-pirimidina (4) e a 2-amino-4-cloro-pirimidina isomérica (6) (Esquema 3), estas reações têm uma utilidade limitada não só devido à sua falta de seletividade (e o seu impacto no rendimento global) mas também porque a separação dos isômeros resultantes é geralmente 10 extremamente difícil. É geralmente requerida HPLC preparativa como um meio para isolar individualmente os isômeros puros (4 e 6), que podem então ser novamente transformados em compostos tais como 1 ou o seu isômero 7 respectivamente.
ESQUEMA 3
Um exemplo deste tipo de reação que proporciona misturas de isômeros é a adição de 4-metil-anilina a 2,4-dicloro-5-trifluorometilpÍrimÍdina (Esquema 4). Esta pirimidina deficiente em elétron tem uma ligeira preferência para adição de amina à posição 2 de pirimidina. A análise por HPLC da mistura reacional bruta mostra uma mistura de 1,4 a 1 e (4-cloro-5trifluorometil-pirimidin-2-il)“p-tolil-amina (8) e (2-cloro-5-trifluorometÍI-pirimidin-4-il)-p-tolil-amina (9). Outros exemplos de adição de amina não-seletiva a
2,4-dihalogenopirímidinas estão descritos em Chemistry of Heterocyclic
Compounds, The Pyrimidines, Volume 52, Wiley, Nova Iorque 1994, pp. 371417. Luo etal. Tetrahedron Lett., 2002, (43) p. 5739. Yoshida et al. J. Chem.
Soc, Perkin Trans. I: Organic and Bioorganic Chemistry, 1992 (7) p. 919. EP
ΊΊ • ··
647639 descreve adições de piperidinas a 2,4-dicloropirimidina.
ESQUEMA 4
Cl
OCEl-BuOH (1:1)
NEt3
Em contraste com as reações descritas acima, existem apenas poucos exemplos muito específicos em que uma amina (3) é adicionada a uma pirimidina de fórmula 2 de uma forma seletiva para proporcionar preferencialmente a 2-amino-4-cloro-pirimidina 6. O exemplo mais significativo 15 deste tipo de reação é a adição de N-metil piperidina a 2,4-dícloro-5-metil pirimidina para proporcionar 4-cloro-5-metil-2-piperidinopirimidina (Esquema 5) encontrado em Yoshida et. al. J. Chem. Soc, Perkin Trans. /: Organic and Bioorganic Chemistry, 1992 (7) p. 919. Neste caso, o efeito estérico do substituinte 5-metila na pirimidina acoplado com o fato do nucleófila amina ser 20 uma amina terciária (em vez de ser primária ou secundária) proporciona a
Sumário da Invenção
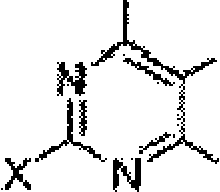
Verificou-se surpreendentemente que pela adição de um ácido de Lewis ao meio reacional, pode adicionar-se seletivamente uma funcionalidade amina à posição C-2 de um anel piridimina substituído em CF3. Assim, a presente invenção refere-se a um processo para preparar um composto de fórmula 11 • ♦ ♦ ♦ · · · * · · · · · <r tt · * * f · • *
·«·*·· •wn · * · « · * * ·· em que X2 é um grupo de saída tal como um halogeneto, sulfonato de arila, sulfonato de alquila, sulfonato de perfluoroalquila, sulfinato de arila ou sulfinato de alquila; e
R3 e R4 são substituintes selecionados independentemente do grupo que consiste em hidrogênio, um grupo aromático e um grupo alifático; ou toma10 dos conjuntamente -NR3R4 podem formar um anel aromático ou alifático com 4 a 11 membros;
em que o processo compreende fazer reagir um composto de fórmula 10 com uma amina de fórmula 3 (HNR3R4) na presença de um ácido de Lewis e uma base não-nucleófila para formar um composto de fórmula 11, em que X1 15 é um grupo de saída como um halogeneto, sulfonato de arila, sulfonato de alquila, sulfonato de perfluoroalquila, sulfinato de arila ou sulfinato de alquila.
Em uma modalidade preferida, amina 3 é uma amina aromática e utiliza-se 0,25-10 equivalentes de ácido de Lewis em relação à quantidade de pirímidina 10, e preferencialmente utiliza-se 0,5-3,0 equivalentes de ácido 20 de Lewis em relação à quantidade de pirimidina 10.
Em uma modalidade preferida alternativa, a amina 3 é uma ami· na alifática e utiliza-se 0,5-10 equivalentes de ácido de Lewis em relação à quantidade de pirimidina 10 e preferencialmente utiliza-se 1-4 equivalentes de ácido de Lewis em relação à quantidade de pirimidina 10.
Em outra modalidade preferida, X1 e X2 são iguais ou diferentes e cada um é independentemente halogeneto e o ácido de Lewis é um sal de zinco ou magnésio.
Em uma modalidade mais preferida, X1 e X2 são cloreto e o ácido de Lewis é cloreto de zinco.
Os compostos preparados pelo método da presente invenção incluem todos os estereoisômeros (por exemplo, isômeros cis e trans) e todos os isômeros óticos dos compostos de fórmula 11 (por exemplo, enanciômeros R e S) bem como misturas racêmicas, diastereoméricas e outras misturas destes isômeros.
Os compostos e os sais preparados pelo método da presente invenção podem existir em várias formas tautoméricas, incluindo a forma enol e imina, e a forma ceto e enamina e isômeros geométricos e as suas misturas. A preparação de todas estas formas tautoméricas está incluída no âmbito da presente invenção. Os tautômeros existem como misturas de um conjunto tautomérico em solução. Na forma sólida, geralmente predomina um tautômero. Apesar de a preparação de um tautômero poder ser descrita, a presente invenção abrange a preparação de todos os tautômeros dos presentes compostos.
A presente invenção inclui também a preparação de atropisômeros da presente invenção. Os atropisômeros referem-se a compostos de 20 fórmula 11 que podem ser separados em isômeros rotacionalmente restritos.
Os compostos preparados pelo método da presente invenção podem conter ligações duplas similares a uma ligação olefínica. Quando estas ligações estão presentes, os compostos podem existir em configurações cis e trans e como suas misturas e a presente invenção contempla a prepa25 ração destes compostos.
Tal como aqui utilizado, o termo aromático, e especificamente, um grupo aromático refere-se a um radical arila ou heteroarila como aqui definido.
Além disso, uma amina aromática ou radical amina aromática refere-se a qualquer amina ou radical amina ligado a pelo menos um átomo de carbono sp2 que é parte de um grupo arila ou heteroarila. Uma amina ou radical amina serão referidos como uma amina aromática ou radical mesmo
se o nitrogênio da amina estiver ligado a um hidrogênio ou a um átomo de carbono sp3, além do átomo de carbono sp2. Assim, por exemplo cada -HN(C6-Cio)arila e -N^CrCeJalquilXÍCe-C-ioíarila) refere-se a radicais amina aromática como aqui definido, apesar do fato de cada nitrogênio da amina 5 estar ligado a substituintes não-aromáticos.
O termo ''arila'' refere-se a radicais aromáticos tais como fenila, naftila, tetrahidronaftila, indanila e outros similares. Um grupo arila pode estar opcionalmente substituído com 1-3 substituintes adequados, como aqui definido. Arila refere-se também a um radical fenila fundido a um heteroci10 cio não-aromático. Exemplos destes grupos incluem mas não se limitam a 2oxo-indolinila, cromanila, indolinila e 2-oxo-3,4-dihidroquinolinila opcionalmente substituídas por 1 a 3 substituintes adequados.
Tal como aqui utilizado, o termo heteroarila refere-se a um grupo heterocíclico aromático geralmente com um heteroátomo selecionado .15 de O, S e N no anel, em que o grupo heterocíclico aromático pode estar substituído com até três substituintes adequados como aqui definido. Além do referido um heteroátomo, o grupo heterocíclico aromático pode ter opcionalmente até quatro átomos de N no anel. Exemplos de grupos heteroarila incluem mas não se limitam a piridila, pirazinila, pirimidinila, piridazinila, tieni20 Ia, furila, imidazolila, pirrolila, oxazolila (por exemplo, 1,3-oxazolila, 1,2oxazolila), tiazolila (por exemplo, 1,2-tiazolila, 1,3-tiazolila), pirazolila, tetrazolila, tríazolila (por exemplo, 1,2, 3-triazolila, 1,2,4-triazolila), oxadiazolila (por exemplo, 1,2,3-oxadiazolila), tiadiazolila (por exemplo, 1,3,4-tiadiazolila), quinolila, isoquinolila, benzotienila, benzofurila, indolila, e outros similares;
opcionalmente substituídos por 1 a 3 substituintes adequados. Alternativamente, qualquer carbono no anel, -CH-, do grupo heteroarila anteriormente referido, pode estar substituído por um grupo selecionado de -C=O ou -SO2. Heteroarila refere-se também a um dos grupos heteroarila anteriormente referidos fundido com um heterociclo não-aromático. Exemplos destes gru30 pos incluem mas não se limitam a 1,3-Dihidro-pirrolo[2,3-b]piridin-2-ona, 3,4Dihidro-1 H-[1,8]naftiridin-2-ona, 1,3-Dihidro-pirrolo[2,3-b]piridina e 3,4Dihidro-2H-pirano[2,3-b]piridina.
• · · · • ·· * · * * · · • » · · • · ·
Grupo alifático refere-se a um radical alquila, cicloalquila ou heterocicloalquila, como aqui definido. Os grupos alifáticos podem estar substituídos com até três substituintes adequados como aqui definido.
Tal como aqui utilizado, o termo amina alifática ou radical amina alifático refere-se a qualquer amina ou radical amina no qual a amina ou átomo de nitrogênio do radical está ligado a um carbono sp3 que faz parte de um grupo alquila, cicloalquila ou heterocicloalquila. Os grupos amina alifática podem estar substituídos com até três substituintes adequados tal como aqui definido.
O termo alquila refere-se a grupos alquila C1-C10 lineares ou ramificados (tais como metila, etila, n-propila, isopropila, n-butila, isobutila, sec-butila, terc-butila, etc.) opcionalmente substituídos por 1 a 3 substituintes adequados tal como aqui definido.
O termo cicloalquila ou ciclila refere-se a um anel carbocíclico C3-C12 mono, bicíclico ou tricíclico (por exemplo, ciclopropila, ciclobutila, ciclopentila, ciclohexila, cicloheptila, ciclooctila, ciclononila, ciclopentenila, ciclohexenila, biciclo[2.2.1 Jheptanila, biciclo[3.2.1 Joctanila e biciclo[5.2.0Jnonanila), etc.) que está opcionalmente substituído por 1 a 3 substituintes adequados como aqui definido. As espécies bicíclicas ou tricíclicas podem estar fundidas, em ponte ou espirocíclicas. Assim, exemplos de grupos cicloalquila ou ciclila, tal como aqui definido, incluem, mas não se limitam a ciclopropila, ciclobutila, ciclopentila, ciclohexila, cicloheptila, ciclohexenila, biciclo[2.2.1 Jheptanila, biciclo[3.2.1 Joctanila, biciclo[3.1 .OJhexila e espiro[2.4]heptila.
O termo heterocicloalquila ou heterociclila ou heterociclo refere-se a um grupo mono, bicíclico ou tricíclico que contém 3 a 9 átomos de carbono e 1 a 4 heteroátomos selecionados de -N, -NR, -O-, -S-, -SO ou -SO2, em que o radical cíclico está opcionalmente substituído por 1 a 3 substituintes adequados como aqui definido. As espécies bicíclicas ou tricíclicas podem estar fundidas, em ponte ou espirocíclicas. Exemplos destes grupos incluem mas não se imitam a azetidinila, pirrolidinila, píperidinila, morfolinila, piperazinila, tetrahidrofuranila, oxeetanila, tiomorfolinila, quinuclidinila, 5-aza30 espiro[2.4]heptila e 3-aza-biciclo[3.1.0]hexila.
Tal como aqui utilizado, o termo halogênio” inclui flúor, cloro, bromo ou iodo ou fluo reto, cloreto, brometo ou íodeto.
Tal como aqui utilizado, o termo carbonila” ou (C=O) (como utilizado em frases tais como alquilcarbonila, alquil-(C=O)- ou alcoxicarbonila) refere-se ao ligante da porção > C=O a uma segunda porção tal como um grupo alquila ou amina (isto é, um grupo amido).
Quando -NR3R4 ou -NR5R6 tomados conjuntamente formam uma amina cíclica, a referida amina pode ser um anel mono, bicíclico ou tricíclico 10 que compreende 3 a 9 átomos de carbono e 0 a 3 heteroátomos selecionados de -N, -O-, -S-, -SO ou -SO2 (excluindo o átomo de nitrogênio em -NR3R4 ou -NR5R6). A amina cíclica pode estar opcionalmente substituída com 1 a 3 substituintes adequados como aqui definido. As espécies bicíclicas ou tricíclicas podem estar fundidas, em ponte ou espirocíclicas. Exem15 pios destas aminas cíclicas incluem mas não se limitam a morfolina, azetidina, piperazina, piperidina, pirrolidina, indolina, tiomorfolina.
Um substituinte adequado1' pretende significar um grupo funcional química e farmaceuticamente aceitável. Estes substituintes adequados para os grupos arila, heteroarila, alquila, cicloalquila, heterocicloalquila ante20 riormente referidos podem ser descritos facilmente pelos versados na técnica. Exemplos ilustrativas dos referidos substituintes adequados incluem, mas não se limitam a, hidrogênio, grupos halo, grupos perfluoroalquila, grupos perfluoroalcóxi, grupos alquila, grupos alquenila, grupos alquinila, grupos hidróxi, grupos oxo, grupos alquiltio, grupos ariltio, grupos alquilsulfonila, gru25 pos arilsulfonila, grupos heteroarilsulfonila, grupos sulfonato de alquila, grupos sulfonato de arila, grupos sulfonato de perfluoroalquila, grupos alcóxi, grupos arila ou heteroarila, grupos cicloalquila ou heterocicloalquila, grupos arilóxi ou heteroarilóxi, grupos aralquila ou heteroaralquila, grupos aralcóxi ou heteroaralcóxi, grupos H0-(C=O)-, grupos amina, grupos alquila e dialqui30 lamino, grupos carbamoíla, grupos alquilcarbonila, grupos alcoxicarbonila, grupos alquilaminocarbonila, grupos dialquilaminocarbonila, grupos sulfonamido, grupos alquilsulfonamido, grupos dialquilsulfonamido, grupos amido,
grupos N-acila, grupos arilcarbonila, grupos ariloxicarbonila e outros similares. Os grupos metileno podem também estar substituídos por um grupo carbonila (C=O). Aqueles versados na técnica compreenderão que muitos substituintes podem estar substituídos por substituintes adicionais.
Modalidades”, tal como aqui utilizada, refere-se a grupamentos específicos de compostos ou utilizações em subgêneros individuais. Cada subgênero pode ser reconhecível de acordo com um substituinte específico tal como um grupo R3 ou R4 específico. Outros subgêneros são reconhecíveis de acordo com combinações de vários substituintes, tal como todos os 10 compostos em que R3 é hidrogênio e R4 é (Ci-C6)alquila, opcionalmente substituída por-(C3-Cio)ciclila.
Descrição pormenorizada da invenção
Nyrcp3 HNR3R4 (3) r3 jÇX 2 γ2 ácido de Lewis j Λ N X Base R4
11
X— grupo de saída
Os compostos de fórmula 11 podem ser preparados pela reação de pirimidina 10 e um nucleófila amina primária ou secundária (3) na presen15 ça de um ácido de Lewis e de uma base não-nucleófila em um solvente orgânico ou mistura de solventes. Os grupos de saída (X1, X2, que podem ser iguais ou diferentes) em pirimidina 10 adequada para deslocação, incluem mas não se limitam a halogenetos, sulfonatos e sulfinatos. Preferencialmente, cada grupo de saída é um halogeneto. Em outra modalidade preferida, o 20 halogênio é um cloreto. Nucleófilos amina primária e secundária incluem aminas aromáticas, alifáticas ou cíclicas como descrito acima. Ácidos de Lewis incluem mas não se limitam aos sais de Zn, Mg, Sn, Ti, Al, B, Li, Ag, Na, K, Ca, Va, Cr, Mn, Fe, Co, Ni, In, Zr, Sm e Cu. Em uma modalidade preferida, os sais de Zn, Mg, Sn, Ti, Al, B, Li, Ag, e Cu são preferidos. Mais prefe25 rencialmente, um sal de Zn ou Mg é utilizado como o ácido de Lewis. Equivalentes adequados de ácido de Lewis em relação à quantidade de pirimidina 10 necessários para efetuar adição seletiva de amina estão na faixa de 0,25-10 equivalentes, e preferencialmente 0,5-3 equivalentes quando o nu10 cleófila amina é aromático ou 0,5-10 equivalentes, e preferencialmente 1-4 equivalentes quando a amina é alifática (ou uma amina aromática capaz de formar um ligando multidentado com o ácido de Lewis). Os solventes orgânicos adequados incluem mas não se limitam a tetrahidrofurano, 1,25 dicloroetano, f-butanol, éter, cloreto de metileno, acetonitrila, metanol, etanol,
• ·
2-propanol, dioxano, 1,2-dimetoxietano, tolueno, clorofórmio, acetato de etila ou suas misturas, preferencialmente uma mistura de solventes halogenados e alcoólicos. Bases adequadas não-nucleófilas incluem mas não se limitam à trietilamina, Ν,Ν-diisopropil-etilamina, diaza-biciloundeceno (DBU) ou bases ligadas à resina tais como MP-Carbonato. As temperaturas para este processo variam de -30°C a 50°C; preferencial mente a reação é realizada a 0°C à temperatura ambiente.
A reação pode ser realizada em uma única etapa ou em várias etapas seqüenciais, sem qualquer efeito adverso no rendimento global ou na 15 seletividade da reação.
Os compostos de fórmula 11, quando combinados com uma amina primária ou secundária HNR5R6 (5) são úteis na preparação de compostos de fórmula 12, em que R5 e R6 independentemente representam hidrogênio, um grupo aromático ou um grupo alifático, ou NR5R6 tomado con20 juntamente pode formar um anel aromático ou alifático com 4-11 membros.
Alternativamente, os compostos de fórmula 11 são úteis na preparação de compostos de fórmula 13a ou 13b pela adição de um nucleófila oxigênio ou enxofre, respectivamente. Os compostos de fórmula 11 (em que X é um halogeneto ou sulfonato de perfluoroalquila) são úteis também na preparação de compostos de fórmula 14 ou 15a/b, em que R7 é um grupo aromático ou um grupo alifático, através da formação de ligação carbono-carbono cataii-
| sada por paládio. | |||
| r’'i^m'nrír, | YR5 R* | VX | r3x A Λ |
| K* 12 | 13a: Y«O 13b: Y=S | 14 | 15a: |
| 15b: |
Os compostos de fórmula 12-15 são úteis, por exemplo, no tra11 tamento de crescimento celular anormal, tal como câncer, em mamíferos. Por exemplo, os compostos 12-15 são inibidores de proteína quinase. Em particular, os compostos de fórmula 12 são inibidores seletivos de determinadas tirosino quinases receptoras e não receptoras, por exemplo, FAK 5 (quinase de adesão focal). Compostos como estes estão descritos nos pedidos de patente U.S. números de série 10/734 039 (número do documento de advogado PC25339) e 10/733215 (número de documento de advogado PC25937).
EXEMPLOS
Os exemplos que se seguem ilustram a preparação dos compostos da presente invenção. Os dados RMN estão descritos em partes por milhão e são referenciados ao sinal lock do deutério do solvente da amostra. Os reagentes comerciais foram utilizados sem mais purificação. THF referese a tetrahidrofurano e DMF refere-se à Ν,Ν-dimetilformamida. A cromato15 grafia refere-se à cromatografia em coluna utilizando sílica-gel .040 mm e executada em condições de cromatografia instantânea. Os espectros de massa de baixa resolução (LRMS) foram registados em uma plataforma de ionização química à pressão atmosférica Fisons, que utiliza uma mistura 50/50 de acetonitrila/água com ácido fórmico a 0,1% como o agente ionizan20 te. Todas as reações não-aquosas foram realizadas sob atmosfera de nitrogênio por conveniência e para maximizar os rendimentos. A concentração sob pressão reduzida significa que foi utilizado um evaporador rotativo. Os nucleófilos de amina aromática ou alifática foram adquiridos e utilizados sem mais purificação ou preparados de acordo com métodos correntes de sínte25 se de amina conhecidos pelos versados na técnica.
Quando se refere à cromatografia HPLC nas preparações e nos exemplos adiante, as condições gerais utilizadas, a menos que contrariamente indicado, são as seguintes. A coluna utilizada é uma coluna RXC18 ZORBAX (fabricada por Hewlett Packard) com 150 mm distância e 4,6 mm 30 de diâmetro interior. As amostras são testadas em um sistema Hewlett Packard-1100. Utiliza-se um método gradiente de solvente com 100% de acetato de amônio/tampão de ácido acético (0,2 M) a 100% de acetonitrila durante
.../A
• · · · · · • * · · ·· ······ ·· ····· «·· • · · ♦ ·· • · · ·· minutos. O sistema prossegue em um ciclo de lavagem com 100% de acetonitrila durante 1,5 minuto e em seguida 100% de solução de tampão durante 3 minutos. A vazão durante este período é uma constante de 3 mL/minuto.
Exemplo 1
Preparação de 2,4-dicloro-5-triflluorometilpirimidina: 5-TrifluorometiIuracila (250 g, 1,39 mol) e oxicloreto de fósforo (655 mL, 6,94 moles, 5 equiv.) foram carregados em um frasco de 4 gargalos de 3 L equipado com um agitador mecânico, um condensador a refluxo, uma ampola de adição e um ter10 moacoplador interno. Os conteúdos foram mantidos sob uma atmosfera de nitrogênio enquanto se adicionou ácido fosfórico concentrado (85% em peso,
9,5 mL, 0,1 equiv.) em uma porção à pasta fluida resultando em um exotermo moderado. Adicionou-se então gota a gota diisopropiletilamina (245 mL, 1,39 mol, 1 equiv.) durante 15 minutos a uma taxa tal que a temperatura in- terna da reação chegou a 85-90°C no final da adição. No final da adição de amina a mistura reacional era uma solução amarelo clara homogênea. O aquecimento foi iniciado e a solução amarela foi mantida a 100°C durante 20 horas, altura em que a análise por HPLC da mistura reacional indicou que o material de partida estava consumido. Retirou-se o aquecimento externo e os conteúdos do frasco foram arrefecidos para 40°C e em seguida adicionados gota a gota a uma mistura arrefecida de HCI 3 N (5 L, 10 equiv.) e éter dietílico ( 2 L) mantendo a temperatura do reator de desativação entre 10 e 15°C. As camadas foram separadas e a camada aquosa foi extraída uma vez com éter (1 L). As camadas orgânicas foram combinadas, lavadas com água até as lavagens estarem neutras (5 x 1,5 L lavagens), secas com MgSO4 e concentradas para proporcionar 288 g (95% de rendimento de um óleo amarelo-laranja claro com 96% de pureza (HPLC). Este material pode ser mais purificado por destilação (p.e. 109°C a 79 mmHg).
Exemplo 2
Procedimento geral para adição de amina não-seletiva:
Método A: Uma mistura de (2-cloro-5-trifluorometil-pirimidin-4-il)-p-tolil-amina (9) e (4-cloro-5-trifluorometil-pirimidin-2-il)-p-tolil-amina (8) A uma solução de
5-trifluorometil-2,4-dicloropirimidina (500 mg; 2,3 mmoles) em DCE/f-butanol (20 mL) adicionou-se 4-metilanilina (247 mg; 1 equiv.) seguido por adição gota a gota de trietilamina (1,1 equiv.). Após agitação de um dia para o outro a reação foi concentrada e retomada em acetato de etila, lavada com NaH5 CO3 saturado, seca sobre Na2SO4 e 0 solvente foi removido. A análise por
HPLC analítica revelou que a reação em bruto continha uma mistura 1,4:1 de 8:9. A mistura resultante de isômeros foi separada em um sistema de
HPLC preparativa Shimadzu utilizando um gradiente corrente (Waters X Terra Prep MSC18 coluna 5m, 50 x 50 mm; 0,1% de NH4OH em 40-90% 10 ACN/H2O 75 mL/min, 15 min eluição de gradiente) para proporcionar; (2cloro-5-trifluorometil-pirimidin-4-il)-p-tolil-amina (9) (122 mg): 1H RMN (CDCh, 400 MHz) δ 2,35 (s, 3H), 6,99 (br s, 1H), 7,19 (d, J = 8,3 Hz, 2H), 7,38 (d, J = 8,3 Hz, 2H), 8,38 (s, 1H); 13C RMN (CDCh, 100 MHz) δ 163,9, 157,6, 156,0 (q, J = 5 Hz), 136,1, 133,7, 130,0, 123,8 (q, J = 270 Hz), 122,8, 106,6 15 (q, J = 32 Hz), 21,2; tempo de retenção HPLC: 7,236 min. LRMS (M+): 288,1,
290,1 e ((4-cloro-5-triluorometil-pirimidin-2-il)-p-tolil-amina (8) (205 mg): 1H
RMN (CDCh, 400 MHz) 2,33 (s, 3H), 7,17 (d, J = 8,3 Hz, 2H), 7,42 (d, J = 8,3
Hz, 2H), 7,46 (br s, 1H), 8,52 (s, 1H); 13C RMN (CDCh, 100 MHz) 160,9,
157,6 (br), 134,8, 129,9, 122,8 (q, J = 269 Hz), 121,1, 113,7 (q, J = 34 Hz), 20 21,1; tempo de retenção HPLC: 8,137 mín. LRMS (M+): 288,1,290,1. A confirmação das estruturas dos dois isômeros foi obtida por análise por raios X de cristais únicos.
Procedimentos gerais para a adição seletiva de aminas utilizando um ácido de Lewís:
Método B: (4-Cloro-5-trifluorometil-pirimidin-2-il)-p-tolil-amima (8). A uma solução de 5-triluorometil-2,4-dicloropirimidina (2 g; 9,2 mmoles) em 1:1 de
DCE/t-BuOH (80 mL) adicionou-se cloreto de zinco (11 mL de uma solução
M em éter; 1,2 equiv.) a 0°C. Após uma hora, adicionou-se 4-metilanilina (988 mg; 1 equiv.) seguido pela adição gota a gota de uma solução de trieti30 lamina (1,03 g; 1,1 equiv.) em 10 ml de DCE/t-BuOH. Após agitação, durante
1,5 hora, a reação foi concentrada. A análise por HPLC analítica revelou que a reação em bruto continha < 5% do isômero 9. O produto desejado 8 foi
obtido como um sólido branco (2,25 g; 85%) após cristalização a partir de metanol. Tempo de retenção HPLC; 8,169 min. LRMS (M+); 288,2, 290,1.
A aplicação do Método B com uma variedade de outras aminas permite a preparação de várias outras 2-amino-4-cloro-5-triluorometilpirimi5 dinas incluindo, mas sem se limitar às abaixo descritas.
5-(4-Cloro-5-trifluorometil-pirimidin-2-ilamino)-1,3-dihidro-indol-2ona: 1H RMN (DMSO-d6, 400 MHz) δ 3,29 (s, 2H), 6,76 (d, J = 7,9 Hz, 2H), 7,39 (d, J = 8,3 Hz), 7,51 (br s, 1 H), 8,71 (s, 1H), 10,33 (s, 1H), 10,49 (s, 1H). 13C RMN (DMSO-de, 100 MHz) δ 177,0, 161,3, 158,7 (br), 140,7, 132,8, 10 126,9, 123,7 (q, J = 268 Hz), 121,0, 118,7, 111,2 (q, J = 32 Hz), 109,6, 36,7;
tempo de retenção HPLC: 5,759 min. LRMS (M+) 329,1, 331,1.
(4-Cloro-5-trifluorometil-pirimidin-2-il)-(4-metóxi-fenil)-amina: 1H
RMN (CDCI3, 400 MHz) δ 3,80 (s, 3H), 6,91 (d, J = 9,1 Hz, 2H), 7,38 (br s,
1H), 7,43 (d, J = 8,7 Hz, 2H), 8,50 (s, 1H); 13C RMN (CDCh, 100 MHz) δ ,15 161,1, 157,6 (br), 157,2, 130,3, 123,2, 122,9 (q, J = 269 Hz), 114,5,113,5 (q,
J = 34 Hz), 112,5, 55,7; tempo de retenção HPLC: 7,550 min. LRMS (M+)
304,2,306,1.
(4-Cloro-5-trifluorometil-pirimidin-2-il)-(4-nitro-fenil)-amina: 1H
RMN (CDCh, 400 MHz) δ 7,80 (br s, 1 H), 7,82 (d, J = 24 Hz, 2H), 8,26 (d, J 20 = 23 Hz, 2H), 8,67 (s, 1 H); 13C RMN (DMSO-d6, 100 MHz) δ 160,7,158,9 (q,
4,5 Hz), 158,6, 145,7, 142,7, 125,6, 123,3 (q, J = 269 Hz), 120,0, 113,8 (q, J = 34 Hz); tempo de retenção HPLC; 7,720 min. LRMS (M+) 318,3, 320,3.
(4-Cloro-5-trifluorometil-pirimidin-2-il)-(3,4-dicloro-fenil)-amina: 1H
RMN (CDCh, 400 MHz) δ 7,39 (m, 3H), 7,86 (s, 1H), 8,60 (s, 1H); 13C
RMN(CDCI3, 100 MHz) δ 160,2, 159,8, 157,6 (q, J = 5 Hz), 137,2, 133,2, 130,9, 127,9, 112,6 (q, J = 270 Hz), 121,9, 119,5, 115,0 (q, J = 34 Hz); tempo de retenção HPLC: 8,837 min. LRMS (M+) 342,1, 344,1.
(4-Cloro-5-trifluorometil-pirimidin-2-il)-o-tolil-amina: 1H RMN (CDCh, 400 MHz) δ 2,30 (s, 3H), 7,15 (m, 2H), 7,26 (m, 3H), 7,35 (d, J = 7,5 Hz,
1H), 8,51 (s, 1H); ’3C RMN(CDCI3, 100 MHz) δ 161,5, 159,7, 157,8 (q, J = 4,5
Hz), 135,4, 131,1, 127,0, 126,3, 124,0, 122,8 (q, J = 270 Hz), 113,8 (q, J = 34 Hz), 18,3; tempo de retenção HPLC: 7,663 min. LRMS (M+) 288,1,290,1.
(3-Cloro-fenil)-(4-cloro-5-trifluorometil-pirimidin-2-il)-amina: 1H
RMN (CDCI3, 400 MHz) δ 7,11 (d, J = 9,1 Hz, 1H), 7,28 (t, J = 8,1 Hz, 1H),
7,38 (brs, 1 H), 7,41 (d, J = 9,1 Hz, 1H), 7,75 (s, 1H), 8,59 (s, 1H); 13C RMN (CDCI3, 100 MHz) δ 60,4, 159,7, 157,6 (q, J = 4,5 Hz), 138,8, 135,1, 124,6,
122,6 (q, J = 269 Hz), 120,4,118,3, 114,7 (q, J = 34 Hz); tempo de retenção
HPLC: 8,301 min. LRMS (M+) 308,1, 310,1.
(4-Cloro-fenil)-(4-cloro-5-trifluorometil-pirimidin-2-il)-amina: 1H
RMN (CDCI3, 400 MHz) δ 7,33 (d, J = 9,1 Hz, 2H), 7,42 (s, 1H), 7,53 (d, J = 8,7 Hz, 2H), 8,56 (s, 1H); 13C RMN (CDCI3, 100 MHz) δ 160,5, 159,7, 157,6 10 (q, J = 5 Hz), 136,2, 129,8, 129,4 122,7 (q, J = 270 Hz), 118,6, 114,4 (q, J =
Hz); tempo de retenção HPLC: 8,316 min. LRMS (M+) 308,1, 310,0.
(4-Cloro-5-trifluorometil-pirimidin-2-il)-metil-p-tolil-amina: 1H RMN (CDCI3, 400 MHz) δ 2,36 (s, 3H), 3,52 (s, 3H), 7,13 (d, J = 8,3 Hz, 2H), 7,23 (d, J = 9,1 Hz, 2H), 8,39 (br s, 1H); 13C RMN (CDCI3, 100 MHz) δ 162,4, 15 159,1, 157,2, 141,3, 137,3, 130,4, 126,4, 123,2 (q, J =269 Hz), 111,7 (q, J =
Hz), 39,6, 21,4; tempo de retenção HPLC: 8,708 min. LRMS (M+) 302,2,
304,1.
(4-Cloro-5-trifluorometil-pirimidin-2-il)-(3-oxazol-5-il-fenil)-amina:
1H RMN (DMSO-de, 400 MHz) δ 7,44 (m, 2H), 7,63 (s, 1H), 7,65 (m, 1H), 20 8,07 (s, 1H), 8,44 (s, 1H), 8,82 (s, 1H), 10,78 (s, 1H); 13C RMN(DMSO-de,
100 MHz) δ 161,2, 158,9 (br), 158,4, 152,6,151,0,139,8, 130,2, 128,5, 123,6 (q, J = 269 Hz), 122,9, 121,2, 120,1, 116,4, 112,3 (q, J = 34 Hz); tempo de retenção HPLC: 7,374 min. LRMS (M+) 341,2, 343,1.
4-(4-Cloro-5-trifluorometil-pirimidin-2-ilamino)-benzamida: 1H
RMN (DMSO-de, 400 MHz) δ 7,26 (s, 1H), 7,74 (d, J = 8,7 Hz, 2H), 7,83 (d, J = 9,1 Hz, 2H), 8,44 (br s, 1H), 8,84 (s, 1H), 10,87 (s, 1H); 13C RMN (DMSOde, 100 MHz) δ 168,0, 161,0, 158,9 (br), 158,4, 141,8, 129,6, 129,0, 123,5 (q, J = 268 Hz), 119,9, 112,6 (q, J = 34 Hz); tempo de retenção HPLC: 5,605 min. LRMS (M+) 317,1,319,3.
(4-Cloro-5-trifluorometil-pirimidin-2-il)-(4-metanossulfonil-fenil)amina: 1H RMN (DMSO-de, 400 MHz) δ 3,15 (s, 3H), 7,87 (d, J = 8,7 Hz, 2H), 7,93 (d, J = 8,7 Hz, 2H), 8,89 (s, 1H), 11,10 (s, 1 H): 13C RMN (DMSO-de,
100 MHz) δ 60,9, 158,9 (br), 158,5, 143,9, 135,3, 128,8, 123,4 (q, J = 269 Hz), 120,4, 113,3 (q, J = 34 Hz), 44,5; tempo de retenção HPLC: 6,542 min. LRMS (M+) 352,1, 354,1.
4-(4-Cloro-5-trifluorometil-pirimidin-2-ilamino)benzenossulfona* 5 mida: 1H RMN (DMSO-d6, 400 MHz) δ 7,25 (s, 2H), 7,76 (d, J = 9,1 Hz, 2H),
7,83 (d, J = 9,1, 2H), 8,85 (s, 1H), 10,98 (s,1H); 133C RMN(DMSO-d6, 100 MHz) δ 161,0, 158,9 (br), 158,5, 142,2, 139,2, 127,3, 123,5 (q, J = 269 Hz), 120,3, 113,0 (q, J = 33 Hz); tempo de retenção HPLC: 5,983 min. LRMS (M+)
353,2, 355,2.
Para os casos em que o nucleófila amina é alifático ou é uma amina aromática com aptidão para servir como um ligando multidentado para o ácido de Lewis, são necessários equivalentes adicionais de ácido de
Lewis para a reação continuar de forma seletiva.
Método C: N-(4-Cloro-5-trifluorometil-pirimidin-2-il)-N',N'-dimetil-benzeno-1,415 diamina: A uma solução de 5-trifluorometil-2,4-dicloropirimidina (500 mg; 2,3 mmol) em 1:1 de DCE/f-BuOH (20 mL) adicionou-se cloreto de zinco (5,1 mL de uma solução 1 M em éter; 2,2 equiv.) a 0°C. Após uma hora, N,N-dimetil1,4-fenilenodiamina (313 mg; 1 equiv.) foi adicionada seguida pela adição gota a gota de uma solução de trietilamina (279 mg; 1,1 equiv.) em 5 mL de 20 DCE/f-BuOH. Após agitação, durante 24 horas, a reação foi concentrada.
O produto foi obtido como um sólido verde claro (531 mg; 73%) após cristalização a partir de 25% de H2O/metanol. 1H RMN(DMSO-de, 400 MHz) δ 2,83 (s, 6H), 6,69 (m, 2H), 7,39 (m, 2H), 8,65 (s, 1H), 10,32 (s, 1H); 13C RMN(CDCI3, 100 ΜΗζ)δ 161,3, 158,8 (br), 158,5 (br), 148,3, 128,2, 123,8 (q, 25 J = 268 Hz), 123,0, 113,1, 110,8 (br), 41,0; tempo de retenção de HPLC:
7,901 min. LRMS (M+) 317,3, 319,3.
A aplicação do Método C com várias outras aminas permite a preparação de uma variedade de outras 2-amino-4-cloro-5-trifluorometilpirimidinas incluindo, mas sem se limitar às adiante descritas.
(4-Cloro-5-trifluorometil-pirimidin-2-il)-(2-metoxi-fenil)-amina: 1H
RMN(CDCI31 400 MHz) δ 3,90 (s, 3H), 6,91 (d, J = 8,1 Hz, 1H), 7,01 (m, 1H), 7,07 (m, 1H), 8,09 (s, 1H), 8,38 (d, J = 7,9 Hz, 1H), 8,57 (s, 1H); 13C »*· · · · ♦ » ·*· * * · * · · * » * · * ♦ ··· · « ·*· · · · »r
RMN(CDCI3, 100 MHz) δ 160,4, 159,3, 157,5 (q, J = 4,5 Hz), 148,6, 127,4, 124,1, 122,9 (q, J = 269 Hz), 121,1, 119,8, 113,7 (q, J = 34 Hz), 110,4, 56,0; tempo de retenção de HPLC: 8,151 min. LRMS (M+) 304,2, 306,2.
(4-Cloro-5-trifluorometil-pirimidin-2-il)-(4-metil-benzil)-amina: 1H ” 5 RMN (DMSO-d6, 400 MHz) δ 2,23 (s, 3H), 4,46 (m, 2H), 7,09 (m, 2H), 7,15 (m, 2H), 8,57 (2s, 1H), 8,98 (m,1 H); tempo de retenção de HPLC: 8,238 min. LRMS (M+) 302,0, 304,0.
(4-Cloro-5-trifluorometil-pirimidin-2-ÍI)-ciclohexil-amina: 1H RMN (DMSO-d6, 400 MHz) δ 1,10 (m, 1H), 1,23 (m, 4H), 1,55 (m, 1H), 1,65 (m, 10 2H), 1,81 (m, 2H), 3,69 (m, 2H), 8,47 (m, 1H), 8,55 (2 br s, 1H); tempo de retenção de HPLC: 8,548 min. LRMS (M+) 280,1,282,1.
(4-Cloro-5-trifluorometil-pirimidin-2-il)-ciclohexilmetil-amina: 1H
RMN (DMSO-de, 400 MHz) δ 0,86 (m, 2H), 1,11 (m, 3H), 1,50 (m, 1H), 1,58 (m, 1H), 1,64 (m, 4H), 3,12 (m, 2H), 8,55 (m, 2H); tempo de retenção HPLC: „ 15 9,039 min. LRMS (M+) 294,1,296,1.
4-Cloro-2-piperidin-1-il-5-trifluorometil-pirimidina 1H RMN (CDCI3d6, 400 MHz) δ 1,60 (m, 4H), 1,68 (m, 2H), 3,82 (m, 4H), 8,36 (s, 1H); 13C RMN (DMSO-de, 100 MHz). δ 161,5, 159,1, 157,2 (q, J = 4,5 Hz), 123,4 (q, J = 268 Hz), 109,8 (q, J = 34 Hz), 45,4, 25,9, 24,7; tempo de retenção: 8,915 20 min. LRMS (M+) 266,1,268,2.
A presente invenção não deve ser limitada no seu âmbito pelas modalidades específicas aqui descritas. Na verdade, várias modificações da invenção além das aqui descritas serão evidentes para os versados na técnica a partir da descrição anterior e das ilustrações que as acompanham.
Pretende-se que estas modificações estejam no âmbito das reivindicações anexas.
Todas as patentes, pedidos de patente, publicações, métodos de ensaio, literatura e outros materiais aqui citados estão aqui incorporados por referência na íntegra.
Claims (13)
- REIVINDICAÇÕES1. Método para preparar um composto de fórmula n-^Vcf’ em que X2 é um grupo de saída, eR3 e R4 são substituintes selecionados independentemente do grupo que5 consiste em hidrogênio, um grupo aromático e um grupo alifático; ou tomados conjuntamente -NR3R4 podem formar um anel aromático ou alifático com 4-11 membros;sendo o referido método caracterizado pelo fato de que compreende reagir um composto de fórmula 10 com uma amina de fórmula 3 (HNR3R4) na presença de um ácido de Lewis e de uma base não-nucleófila para formar um composto de fórmula 11, em que X1 é um grupo de saída.
- 2. Método de acordo com a reivindicação 1, caracterizado pelo15 fato de que X1 e X2 são grupos de saída iguais ou diferentes selecionados independentemente do grupo que consiste em haleto, sulfonato de arila, sul· fonato de alquila, sulfonato de perfluoroalquila, sulfinato de arila e sulfinato de alquila.
- 3. Método de acordo com a reivindicação 2, caracterizado pelo20 fato de que X1 e X2 são iguais ou diferentes e cada um é indepentemente haleto.
- 4. Método de acordo com a reivindicação 3, caracterizado pelo fato de que X1 e X2 são cloreto.
- 5. Método de acordo com a reivindicação 1, caracterizado pelo25 fato de que a referida amina, HNR3R4, é uma amina aromática e utiliza-se 0,25-10 equivalentes de ácido de Lewis em relação à quantidade de pirimidl· na 10.
- 6. Método de acordo com a reivindicação 1, caracterizado pelo fato de que a referida amina, HNR3R4, é uma amina aromática e utiliza-se0,5-3 equivalentes de ácido de Lewis em relação à quantidade de pirimídina10.5
- 7. Método de acordo com a reivindicação 5, caracterizado pelo fato de que o ácido de Lewis é um sal de um íon metálico selecionado do grupo que consiste em Zn, Mg, Sn, Ti, Al, B, Li, Ag e Cu.
- 8. Método de acordo com a reivindicação 7, caracterizado pelo fato de que o referido ácido de Lewis é um sal ou Zn ou Mg.
- 10 9. Método de acordo com a reivindicação 7, caracterizado pelo fato de que o referido ácido de Lewis é ZnCI2.10. Método de acordo com a reivindicação 1, caracterizado pelo fato de que a referida amina, HNR3R4, é uma amina alifática ou é uma amina aromática com aptidão para servir como um ligando multidentado para o áci-15 do de Lewis e utiliza-se 0,5-10 equivalentes de ácido de Lewis em relação à quantidade de pirimidina 10.
- 11. Método de acordo com a reivindicação 1, caracterizado pelo fato de que a referida amina, HNR3R4, é uma amina alifática ou é uma amina aromática com aptidão para servir como um ligando multidentado para o áci-20 do de Lewis e utiliza-se 1-4 equivalentes de ácido de Lewis em relação à quantidade de pirimidina 10.
- 12. Método de acordo com a reivindicação 10, caracterizado pelo fato de que o ácido de Lewis é um sal de um íon metálico selecionado do grupo que consiste em Zn, Mg, Sn, Ti, Al, B, Li, Ag, e Cu.25
- 13. Método de acordo com a reivindicação 12, caracterizado pelo fato de que o referido ácido de Lewis é um sal de Zn ou Mg.
- 14. Método de acordo com a reivindicação 12, caracterizado pelo fato de que o referido ácido de Lewis é ZnCfe.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US50073303P | 2003-09-05 | 2003-09-05 | |
| PCT/IB2004/002744 WO2005023780A1 (en) | 2003-09-05 | 2004-08-24 | Selective synthesis of cf3-substituted pyrimidines |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| BRPI0414059A BRPI0414059A (pt) | 2006-10-24 |
| BRPI0414059B1 true BRPI0414059B1 (pt) | 2018-11-06 |
| BRPI0414059B8 BRPI0414059B8 (pt) | 2021-05-25 |
Family
ID=34272990
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI0414059A BRPI0414059B8 (pt) | 2003-09-05 | 2004-08-24 | síntese seletiva de pirimidinas substituídas em cf3 |
Country Status (24)
| Country | Link |
|---|---|
| US (1) | US7122670B2 (pt) |
| EP (1) | EP1663991B1 (pt) |
| JP (1) | JP4842816B2 (pt) |
| KR (1) | KR100694732B1 (pt) |
| CN (1) | CN100465164C (pt) |
| AR (1) | AR045557A1 (pt) |
| BR (1) | BRPI0414059B8 (pt) |
| CA (1) | CA2537373C (pt) |
| CO (1) | CO5650237A2 (pt) |
| CY (1) | CY1106370T1 (pt) |
| DE (1) | DE602004004287T2 (pt) |
| DK (1) | DK1663991T3 (pt) |
| ES (1) | ES2276344T3 (pt) |
| HK (1) | HK1091824A1 (pt) |
| IL (1) | IL173363A (pt) |
| MX (1) | MXPA06002552A (pt) |
| NO (1) | NO334383B1 (pt) |
| NZ (1) | NZ544969A (pt) |
| PL (1) | PL1663991T3 (pt) |
| PT (1) | PT1663991E (pt) |
| RU (1) | RU2315759C2 (pt) |
| TW (1) | TWI283667B (pt) |
| WO (1) | WO2005023780A1 (pt) |
| ZA (1) | ZA200600747B (pt) |
Families Citing this family (22)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GEP20084357B (en) * | 2002-12-20 | 2008-04-29 | Pfizer Prod Inc | Pyrimidine derivatives for the treatment of abnormal cell growth |
| US20060205945A1 (en) * | 2004-05-14 | 2006-09-14 | Pfizer Inc | Pyrimidine derivatives for the treatment of abnormal cell growth |
| JP4778717B2 (ja) * | 2005-03-25 | 2011-09-21 | 富士フイルム株式会社 | 複素環式化合物の製造方法 |
| DE102007010801A1 (de) | 2007-03-02 | 2008-09-04 | Bayer Cropscience Ag | Diaminopyrimidine als Fungizide |
| CN101678215B (zh) * | 2007-04-18 | 2014-10-01 | 辉瑞产品公司 | 用于治疗异常细胞生长的磺酰胺衍生物 |
| KR101294731B1 (ko) * | 2007-06-04 | 2013-08-16 | 삼성디스플레이 주식회사 | 어레이 기판, 이를 갖는 표시패널 및 이의 제조방법 |
| UY31714A (es) * | 2008-03-20 | 2009-11-10 | Boehringer Ingelheim Int | Preparación selectiva de pirimidinas sustituidas |
| WO2009115583A1 (en) * | 2008-03-20 | 2009-09-24 | Boehringer Ingelheim International Gmbh | Regioselective preparation of substituted pyrimidines |
| DE102009006643A1 (de) | 2009-01-29 | 2010-08-05 | Saltigo Gmbh | Herstellung von halogenierten N-heteroaromatischen Polyhalogenderivaten |
| TW201100441A (en) | 2009-06-01 | 2011-01-01 | Osi Pharm Inc | Amino pyrimidine anticancer compounds |
| US8933227B2 (en) | 2009-08-14 | 2015-01-13 | Boehringer Ingelheim International Gmbh | Selective synthesis of functionalized pyrimidines |
| WO2011018517A1 (en) | 2009-08-14 | 2011-02-17 | Boehringer Ingelheim International Gmbh | Regioselective preparation of 2-amino-5-trifluoromethylpyrimidine derivatives |
| JP6000273B2 (ja) | 2010-11-29 | 2016-09-28 | オーエスアイ・ファーマシューティカルズ,エルエルシー | 大環状キナーゼ阻害剤 |
| UY33817A (es) | 2010-12-21 | 2012-07-31 | Boehringer Ingelheim Int | ?nuevas oxindolpirimidinas bencílicas?. |
| EP2675793B1 (en) | 2011-02-17 | 2018-08-08 | Cancer Therapeutics Crc Pty Limited | Fak inhibitors |
| CN103534240B (zh) | 2011-02-17 | 2015-12-09 | 癌症疗法Crc私人有限公司 | 选择性fak抑制剂 |
| WO2014126954A1 (en) | 2013-02-13 | 2014-08-21 | OSI Pharmaceuticals, LLC | Regioselective synthesis of substituted pyrimidines |
| US9656970B2 (en) | 2014-05-08 | 2017-05-23 | Tosoh F-Tech, Inc. | 5-(trifluoromethyl)pyrimidine derivatives and method for producing same |
| JP6391985B2 (ja) * | 2014-05-16 | 2018-09-19 | 東ソー・ファインケム株式会社 | 2−置換−4−(2,2,2−トリフルオロエトキシ)−5−(トリフルオロメチル)ピリミジン誘導体及びその製造方法 |
| JP6391988B2 (ja) * | 2014-05-21 | 2018-09-19 | 東ソー・ファインケム株式会社 | 5−(トリフルオロメチル)ピリミジン誘導体の製造方法及び新規5−(トリフルオロメチル)ピリミジン誘導体 |
| CN108440499A (zh) * | 2018-03-22 | 2018-08-24 | 盐城师范学院 | 一种色瑞替尼及其关键中间体的制备方法 |
| CN114213339B (zh) * | 2021-12-20 | 2023-10-31 | 苏州康纯医药科技有限公司 | 一种表皮细胞生长因子受体突变抑制剂的制备方法 |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2003030909A1 (en) * | 2001-09-25 | 2003-04-17 | Bayer Pharmaceuticals Corporation | 2- and 4-aminopyrimidines n-substtituded by a bicyclic ring for use as kinase inhibitors in the treatment of cancer |
| ATE407678T1 (de) * | 2001-10-17 | 2008-09-15 | Boehringer Ingelheim Pharma | Pyrimidinderivate, arzneimittel enthaltend diese verbindungen, deren verwendung und verfahren zu ihrer herstellung |
-
2004
- 2004-08-24 PT PT04769170T patent/PT1663991E/pt unknown
- 2004-08-24 MX MXPA06002552A patent/MXPA06002552A/es active IP Right Grant
- 2004-08-24 ES ES04769170T patent/ES2276344T3/es active Active
- 2004-08-24 PL PL04769170T patent/PL1663991T3/pl unknown
- 2004-08-24 KR KR1020067004428A patent/KR100694732B1/ko active IP Right Grant
- 2004-08-24 BR BRPI0414059A patent/BRPI0414059B8/pt active IP Right Grant
- 2004-08-24 CN CNB2004800254318A patent/CN100465164C/zh active Active
- 2004-08-24 DK DK04769170T patent/DK1663991T3/da active
- 2004-08-24 CA CA002537373A patent/CA2537373C/en active Active
- 2004-08-24 DE DE602004004287T patent/DE602004004287T2/de active Active
- 2004-08-24 RU RU2006106727/04A patent/RU2315759C2/ru not_active IP Right Cessation
- 2004-08-24 NZ NZ544969A patent/NZ544969A/en unknown
- 2004-08-24 JP JP2006525198A patent/JP4842816B2/ja active Active
- 2004-08-24 WO PCT/IB2004/002744 patent/WO2005023780A1/en active IP Right Grant
- 2004-08-24 EP EP04769170A patent/EP1663991B1/en active Active
- 2004-08-27 US US10/928,954 patent/US7122670B2/en active Active
- 2004-09-02 AR ARP040103140A patent/AR045557A1/es not_active Application Discontinuation
- 2004-09-03 TW TW093126748A patent/TWI283667B/zh active
-
2006
- 2006-01-25 IL IL173363A patent/IL173363A/en active IP Right Grant
- 2006-01-26 ZA ZA200600747A patent/ZA200600747B/xx unknown
- 2006-02-23 CO CO06018320A patent/CO5650237A2/es not_active Application Discontinuation
- 2006-04-03 NO NO20061509A patent/NO334383B1/no unknown
- 2006-11-09 HK HK06112349.7A patent/HK1091824A1/xx unknown
-
2007
- 2007-03-12 CY CY20071100341T patent/CY1106370T1/el unknown
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| BRPI0414059B1 (pt) | síntese seletiva de pirimidinas substituídas em cf3 | |
| JP5624762B2 (ja) | 新規ピロリノン誘導体およびそれを含有する医薬組成物 | |
| JP5637562B2 (ja) | 新規ピロリノン誘導体およびそれを含有する医薬組成物 | |
| US9499483B2 (en) | Crystal of pyrrole derivative and method for producing the same | |
| EP2938612A1 (en) | Protein kinase inhibitors | |
| EP2938614A1 (en) | Azaindole derivatives as multi kinase inhibitors | |
| AU2017203986B2 (en) | Novel furanone derivative | |
| MX2014014622A (es) | Compuesto de pirrolo [2,1-f] [1,2,4]triazina, y metodo de preparacion y aplicacion el mismo. | |
| AU2014292132B2 (en) | Spiroquinoxaline derivatives as inhibitors of non-apoptotic regulated cell-death | |
| BR112020000564A2 (pt) | novos derivados de heteroarilamida como inibidores seletivos das histonas desacetilases 1 e/ou 2 (hdac1-2) | |
| CN101426768A (zh) | 可用作adg受体调节剂的磺酰胺化合物 | |
| CN105524045A (zh) | 四环类间变性淋巴瘤激酶抑制剂 | |
| IE56652B1 (en) | Antihypertensive n-piperazinylalkanoylanilides | |
| JP2015533778A (ja) | がんの治療のための新規フェニル−ピリジン/ピラジンアミド | |
| AU2004270480B2 (en) | Selective synthesis of CF3-substituted pyrimidines | |
| ES2245893B1 (es) | Mejoras en el objeto de la patente de invencion n.p200301747 que se refiere a "3-nitro-pirazolo(1,5-a)pirimidinas 7-sustituidas y composiciones y metodos relacionados". | |
| JP2017525733A (ja) | Ftl3およびjakの阻害剤としての大環状n−アリール−トリシクロピリミジン−2−アミンポリエーテルの誘導体 | |
| WO2020200154A1 (zh) | 一类噻吩并氮杂环类化合物、制备方法和用途 | |
| CN116963733A (zh) | 作为enpp1抑制剂的咪唑化合物 | |
| JP2009256274A (ja) | 5員複素環化合物を有効成分とする抗ガン剤および新規5員複素環化合物 | |
| JP2008120699A (ja) | 新規ピリジニウム誘導体および医薬 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B06F | Objections, documents and/or translations needed after an examination request according [chapter 6.6 patent gazette] | ||
| B15K | Others concerning applications: alteration of classification |
Free format text: PARA: INT. CL. C07D 239/42; A61P 35/00 Ipc: C07D 239/42 (2011.01), A61P 35/00 (2011.01) |
|
| B07D | Technical examination (opinion) related to article 229 of industrial property law [chapter 7.4 patent gazette] | ||
| B07E | Notification of approval relating to section 229 industrial property law [chapter 7.5 patent gazette] | ||
| B09A | Decision: intention to grant [chapter 9.1 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] |
Free format text: PRAZO DE VALIDADE: 10 (DEZ) ANOS CONTADOS A PARTIR DE 06/11/2018, OBSERVADAS AS CONDICOES LEGAIS. |
|
| B16C | Correction of notification of the grant [chapter 16.3 patent gazette] |
Free format text: PRAZO DE VALIDADE: 20 (VINTE) ANOS CONTADOS A PARTIR DE 24/08/2004 OBSERVADAS AS CONDICOES LEGAIS. PATENTE CONCEDIDA CONFORME ADI 5.529/DF |