BR112012033783B1 - aparelho de detecção - Google Patents
aparelho de detecção Download PDFInfo
- Publication number
- BR112012033783B1 BR112012033783B1 BR112012033783-1A BR112012033783A BR112012033783B1 BR 112012033783 B1 BR112012033783 B1 BR 112012033783B1 BR 112012033783 A BR112012033783 A BR 112012033783A BR 112012033783 B1 BR112012033783 B1 BR 112012033783B1
- Authority
- BR
- Brazil
- Prior art keywords
- biological
- detection
- channel
- probe
- microdevice
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N27/00—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means
- G01N27/26—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means by investigating electrochemical variables; by using electrolysis or electrophoresis
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N35/00—Automatic analysis not limited to methods or materials provided for in any single one of groups G01N1/00 - G01N33/00; Handling materials therefor
- G01N35/08—Automatic analysis not limited to methods or materials provided for in any single one of groups G01N1/00 - G01N33/00; Handling materials therefor using a stream of discrete samples flowing along a tube system, e.g. flow injection analysis
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/145—Measuring characteristics of blood in vivo, e.g. gas concentration, pH value; Measuring characteristics of body fluids or tissues, e.g. interstitial fluid, cerebral tissue
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L3/00—Containers or dishes for laboratory use, e.g. laboratory glassware; Droppers
- B01L3/50—Containers for the purpose of retaining a material to be analysed, e.g. test tubes
- B01L3/502—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures
- B01L3/5027—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L3/00—Containers or dishes for laboratory use, e.g. laboratory glassware; Droppers
- B01L3/50—Containers for the purpose of retaining a material to be analysed, e.g. test tubes
- B01L3/502—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures
- B01L3/5027—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip
- B01L3/502707—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip characterised by the manufacture of the container or its components
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/70—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving virus or bacteriophage
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01D—MEASURING NOT SPECIALLY ADAPTED FOR A SPECIFIC VARIABLE; ARRANGEMENTS FOR MEASURING TWO OR MORE VARIABLES NOT COVERED IN A SINGLE OTHER SUBCLASS; TARIFF METERING APPARATUS; MEASURING OR TESTING NOT OTHERWISE PROVIDED FOR
- G01D21/00—Measuring or testing not otherwise provided for
- G01D21/02—Measuring two or more variables by means not covered by a single other subclass
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N27/00—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means
- G01N27/02—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means by investigating impedance
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N27/00—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means
- G01N27/26—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means by investigating electrochemical variables; by using electrolysis or electrophoresis
- G01N27/416—Systems
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/483—Physical analysis of biological material
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/483—Physical analysis of biological material
- G01N33/487—Physical analysis of biological material of liquid biological material
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/5005—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/5302—Apparatus specially adapted for immunological test procedures
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B2560/00—Constructional details of operational features of apparatus; Accessories for medical measuring apparatus
- A61B2560/04—Constructional details of apparatus
- A61B2560/0406—Constructional details of apparatus specially shaped apparatus housings
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2200/00—Solutions for specific problems relating to chemical or physical laboratory apparatus
- B01L2200/06—Fluid handling related problems
- B01L2200/0647—Handling flowable solids, e.g. microscopic beads, cells, particles
- B01L2200/0652—Sorting or classification of particles or molecules
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2200/00—Solutions for specific problems relating to chemical or physical laboratory apparatus
- B01L2200/06—Fluid handling related problems
- B01L2200/0647—Handling flowable solids, e.g. microscopic beads, cells, particles
- B01L2200/0663—Stretching or orienting elongated molecules or particles
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/06—Auxiliary integrated devices, integrated components
- B01L2300/0627—Sensor or part of a sensor is integrated
- B01L2300/0645—Electrodes
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/06—Auxiliary integrated devices, integrated components
- B01L2300/0627—Sensor or part of a sensor is integrated
- B01L2300/0654—Lenses; Optical fibres
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/06—Auxiliary integrated devices, integrated components
- B01L2300/0681—Filter
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2400/00—Moving or stopping fluids
- B01L2400/04—Moving fluids with specific forces or mechanical means
- B01L2400/0403—Moving fluids with specific forces or mechanical means specific forces
- B01L2400/0415—Moving fluids with specific forces or mechanical means specific forces electrical forces, e.g. electrokinetic
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2400/00—Moving or stopping fluids
- B01L2400/04—Moving fluids with specific forces or mechanical means
- B01L2400/0403—Moving fluids with specific forces or mechanical means specific forces
- B01L2400/043—Moving fluids with specific forces or mechanical means specific forces magnetic forces
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N15/10—Investigating individual particles
- G01N15/14—Electro-optical investigation, e.g. flow cytometers
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N35/00—Automatic analysis not limited to methods or materials provided for in any single one of groups G01N1/00 - G01N33/00; Handling materials therefor
- G01N35/10—Devices for transferring samples or any liquids to, in, or from, the analysis apparatus, e.g. suction devices, injection devices
- G01N35/1095—Devices for transferring samples or any liquids to, in, or from, the analysis apparatus, e.g. suction devices, injection devices for supplying the samples to flow-through analysers
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10T—TECHNICAL SUBJECTS COVERED BY FORMER US CLASSIFICATION
- Y10T436/00—Chemistry: analytical and immunological testing
- Y10T436/14—Heterocyclic carbon compound [i.e., O, S, N, Se, Te, as only ring hetero atom]
- Y10T436/142222—Hetero-O [e.g., ascorbic acid, etc.]
- Y10T436/143333—Saccharide [e.g., DNA, etc.]
Abstract
APARELHO PARA DETECTAR UMA DOENÇA EM UM MATERIAL BIOLÓGICO Entre outros, a presente invenção fornece aparelho para detectar uma doença, compreendendo um sistema de administração de material biológico a ser detectado e é capaz de medir no nível microscópico uma propriedade elétrica, magnética, eletromagnética, térmica, óptica, acústica biológica, química, física ou mecânica do material biológico.
Description
[001] Este pedido reivindica a prioridade para o Pedido US N° 61/360,041, depositado em 30 de Junho de 2010; o Pedido US N° 61/389.960, depositado em 05 de Outubro de 2010; o Pedido US N° 61/430,641, depositado em 07 de Janeiro de 2011 o Pedido US N°. 61/467.097, depositado em 24 de Março de 2011 e o Pedido US N° 61/498.954, depositado em 20 de Junho de 2011, nas quais os seus conteúdos são aqui incorporados por referência na sua totalidade.
[002] Muitas doenças graves e com alta morbidade e mortalidade, incluindo câncer e doenças cardíacas, são muito difíceis de diagnosticar precocemente e com precisão. As tecnologias atuais de diagnóstico de doenças dependem tipicamente de dados macroscópicos e informações tais como a temperatura corporal, pressão sanguínea, e das imagens digitalizadas do corpo. Para detecção de doenças graves, como o câncer, muitos dos aparelhos de diagnóstico comumente usados hoje são baseados em tecnologias de imagem, incluindo raios-x, tomografia computadorizada e ressonância magnética nuclear (RMN). Enquanto eles oferecem vários graus de utilidade no diagnóstico de doenças, a maioria deles não pode fornecer um diagnóstico totalmente preciso seguro, e que seja custo-eficaz em doenças graves como o câncer em um estágio inicial. Além disso, muitas das técnicas de diagnóstico existentes e aparelhos relacionados são invasivas e, por vezesnão são facilmente acessíveis, especialmente em regiões remotas ou em áreas rurais.
[003] Mesmo os recentes testes de DNA não têm se mostrado eficazes, de uma forma rápida e confiável, precisa e econômica, no diagnóstico de uma ampla gama de doenças. Nos últimos anos, tem havido alguns esforços na utilização de nano tecnologias para diversas aplicações biológicas, sendo a maior parte do trabalho voltado para o mapeamento genético e evolução moderada no campo da detecção da doença. Por exemplo, Pantel et al. discutiram a utilização de Sistemas d Sensores MicroEletromecânicos (MEMS) para a detecção in vitro de células cancerígenas no sangue e na medula óssea (ver, por exemplo, Klaus Pantel et al, Nature Reviews, 2008, 8, 329); Kubena et al. divulgado na Patente EUA Número 6,922,1 18 a implantação de MEMS para detectar agentes biológicos e Weissman et al. descrito na patente US número 6.330,885 usando sensores MEMS para a detecção do acréscimo de material biológico.
[004] No entanto, até à data, a maioria das tecnologias descritas acima têm sido limitadas a casos isolados de detecção, utilizando sistemas de construção relativamente simples e dimensões grandes, mas muitas vezes com funções limitadas, e falta de sensibilidade e especificidade. Além disso, algumas das tecnologias existentes, utilizando nanopartículas e abordagens biológicas têm as desvantagens de necessitarem de procedimentos de preparação da amostra que são complicados (tais como a utilização de produtos químicos ou marcadores biológicos), dificuldade na interpretação dos dados, de demasiada confiança na alteração visual e cor como meio de diagnóstico (que é subjetivo e com resolução limitada), tornando-os impróprios para a detecção precoce do estágio da doença, por exemplo, para doenças graves como o câncer.
[005] Estas desvantagens exigem novas soluções novas as quais não apenas as supera, mas também trazem maior precisão, especificidade, eficiência, não são invasiva, e aumentam a detecção do estágio inicial doenças, a custos reduzidos.
[006] A presente invenção em geral refere-se a um aparelho inovador para detecção de doenças que utiliza novos microdispositivos (ou funcionalidades) integradas neles para a realização de diagnóstico ao nível microscópico em uma célula única, in vivo ou in vitro, uma única molécula biológica (por exemplo, DNA, RNA ou proteína), um único material biológico (por exemplo, um vírus), ou outra composição biológica fundamental suficientemente pequena. Estes aparelhos podem ser feitos usando o estado da técnica das tecnologias de fabricação de microdispositivos e fluxos de novos processos, tais como as tecnologias de fabricação de circuitos integrados. Tal como aqui usado, o termo “ aparelho de detecção de doença “pode ser intercambiado com termos tais como dispositivo de detecção de doenças ou aparelho integrado com microdispositivos, ou quaisquer outros termos similares com o mesmo significado. O aparelho da presente invenção contendo vários microdispositivos, pode detectar vários parâmetros de uma amostra biológica a ser analisada. Estes aparelhos de detecção de doença são capazes de detectar doenças nas suas fases iniciais com um elevado grau de sensibilidade, especificidade, velocidade, conveniência (por exemplo, o tamanho reduzido do aparelho), e a acessibilidade (por exemplo, custos reduzidos).
[007] Um componente fundamental do aparelho de detecção é ser uma nova classe de microdispositivos e os seus processos de fabricação inventivos que permitem a essas novos microdispositivos operar a um nível muito superior que o de um aparelho ou tecnologias convencionais de detecção de doença, devido à sensibilidade de detecção muito melhorada, especificidade e velocidade. Os exemplos de técnicas de fabricação que podem ser usados para fazer os microdispositivos aqui descritos incluem, mas não se limitam a, a técnicas de fabricação mecânica, química, físico-química, química mecânica, biofísica, biofísico-mecânica, eletromecânica, bioeletromecânica, microeletromecânica, eletroquímico-mecânica, eletrobioquímico-mecânica, técnicas de nanofabricação de circuitos integrados, e as técnicas de fabricação de semicondutores e processos. Para uma descrição geral de algumas das tecnologias de fabricação aplicáveis, ver, por exemplo, R. Zaouk et al, Introduction to Microfabrication Techniques, in Microfluidic Techniques (S. Minteer, ed.), 2006, Humana Press; Microsystem Engineering of Lab-on-a-chip Devices, 1st Ed. (Geschke, Klank & Tel Leman, eds.), John Wiley & Sons., 2004. As funcionalidades do microdispositivo que incluíram pelo menos o sentir, detectar, medir, diagnosticar, monitorar e analisar para o diagnóstico da doença. Várias microdispositivos podem ser integrados em um aparelho de detecção para tornar o aparelho mais avançado e mais sofisticado para melhor medição da sensibilidade, especificidade, velocidade e funcionalidades, com capacidade para medir o mesmo parâmetro ou mesmo um conjunto de parâmetros diferentes.
[008] Os componentes opcionais do aparelho incluem meios para executar pelo menos a função de direcionar, controlar, forçar, receber, amplificar, ou armazenar informações a partir de cada sonda. Esses meios podem ser, por exemplo, uma unidade central de controle, que inclui um circuito de controle, uma unidade de endereçamento, um circuito amplificador, um circuito de processamento da lógica, uma unidade de memória, um chip de aplicação específica, um transmissor de sinal, um receptor de sinal, ou um sensor.
[009] Especificamente, um aspecto da presente invenção fornece um aparelho para detectar uma doença, cada um compreendendo um primeiro microdispositivo e um primeiro substrato de suporte do microdispositivo, em que os primeiro microdispositivos contacta um material biológico a ser analisado e é capaz de medir o nível microscópico uma propriedade mecânica, elétrica, magnética, eletromagnética, térmica, óptica, acústica, biológica, química, eletromecânica, eletroquímica, eletroquímico-mecânico, bioquímica, biomecânica, bioeletromecânica, bioeletroquímicas, bioeletroquímico- mecânica, e física do material biológico. Opcionalmente, o aparelho pode ainda incluir um dispositivo para a leitura dos dados a partir da medição da propriedade.
[0010] Em algumas formas de realização, a diferença na propriedade medida do material biológico testado e a de uma amostra biológica a partir de um indivíduo livre da doença, é indicativa da possível ocorrência da doença em uma fase precoce.
[0011] Em algumas outras formas de realização, a propriedade elétrica é a carga superficial, potencial do superfície, oscilação no sinal elétrico (por exemplo, oscilação nos íons, campo elétrico pulsando, carga superficial pulsando, tensão pulsando), campo elétrico, distribuição do campo elétrico, distribuição da carga elétrica, ou impedância; a propriedade térmica é a temperatura, a propriedade química é o valor p1-I, força iônica, força de ligação; a propriedade física é a densidade; e a propriedade mecânica é a dureza, resistência ao cisalhamento, força de alongamento, tensão de fratura, adesão, elasticidade, e a densidade.
[0012] Em algumas outras formas de realização, cada aparelho compreende ainda, pelo menos, um ou mais dispositivos adicionais de microdispositivos. Nestas formas de realização, cada um dos microdispositivos contidos no aparelho compreende um material condutor, um material eletricamente isolante, ou um material semicondutor; e cada um dos microdispositivos pode compreender o mesmo ou diferente(s) material(is) e pode medir propriedades iguais ou diferentes, ao mesmo tempo, ou a tempos diferentes. Estes vários microdispositivos podem estar espaçados sobre o substrato, por exemplo, com uma distância de pelo menos 10 angstroms. Os vários microdispositivos integrados em um aparelho de detecção de doença pode sequencialmente e/ou simultaneamente medir vários parâmetros em um material biológico a ser detectados em níveis macroscópicos e/ou microscópicas. Por vezes, em um aparelho com vários microdispositivos, alguns microdispositivos podem agir como sondas para perturbar o material biológico e provocar uma resposta biológica a partir do material biológico, enquanto outros microdispositivos no aparelho podem funcionar como dispositivos de detecção para medir o resposta desencadeada pelo material biológico.
[0013] Em algumas outras formas de realização, cada um dos microdispositivos tem o tamanho variando entre cerca de I angstrom (A) a cerca de 5 milímetros (por exemplo, entre 5A a 1 milímetro).
[0014] Em algumas outras formas de realização, o aparelho compreende um ou mais substratos adicionais em que os microdispositivos são colocados. Cada um dos substratos podem compreender o mesmo ou um material diferente (por exemplo, um material condutor ou isolante), podendo apresentar na mesma ou em uma forma diferente (por exemplo, uma placa ou um tubo), e cada substrato pode ser um objeto bi- ou tridimensional. Eles podem tomar a forma de cilindros, placas, ou quaisquer outras formas e configurações desejadas, a fim de melhorar ainda mais a sensibilidade de medição, a especificidade, a velocidade, o tamanho da amostra, e reduzir o custo e o tamanho.
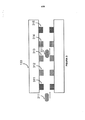
[0015] Em termos de aparelho de detecção para integrar os microdispositivos, em um novo design do aparelho de detecção para aumentar a sensibilidade de medição, os microdispositivos montados em duas placas separadas por uma distância pequena com a amostra a ser medida entre as duas placas podem ser utilizados para detectar a doença com maior velocidade, os microdispositivos medindo as células, DNAs, e materiais desejados na amostra em paralelo. A área da superfície das placas pode ser maximizada a fim de ter um número máximo de microdispositivos colocados sobre as placas e aumentar a eficiência de medição e velocidade. Opcionalmente, vários microdispositivos integrados na superfície das placas podem ser espaçados com o seu espaçamento correspondente ao das células, DNAs, e materiais a serem medidos.
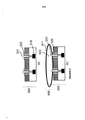
[0016] Numa outra nova configuração, um aparelho de detecção integrado com os microdispositivos é moldado na forma de um cilindro, com vários microdispositivos com sondas de detecção integrados/montados nas superfícies interiores do cilindro e com a amostra a ser medida (por exemplo, sangue) fluindo através do cilindro.
[0017] Em ainda uma outra configuração inovadora, um aparelho de detecção integrado com microdispositivos é moldado na forma de um tubo retangular, com vários microdispositivos com sondas de detecção integrados/montados nas superfícies interiores do tubo e com a amostra a ser medida (por exemplo, sangue) fluindo através do tubo retangular.
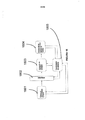
[0018] Em um outro aspecto, a invenção proporciona um outro conjunto de aparelhos para detectar uma doença em um material biológico, compreendendo um sistema para a administração do material biológico a ser detectado, e uma sonda e um dispositivo de sondagem para detecção e sondagem do material biológico.
[0019] A diferença entre a propriedade medida do material biológico e a de uma amostra biológica padrão é indicativa da possível ocorrência da doença.
[0020] Em algumas formas de realização, o dispositivo de sondagem e detecção compreende um primeiro microdispositivo e um primeiro substrato que suporta o primeiro microdispositivo, o primeiro microdispositivo contacta com o material biológico a ser detectado e é capaz de medir o nível microscópico, uma propriedade elétrica, química, magnética, eletromagnética, térmica, óptica, acústica, biológica, eletromecânica, eletroquímica, eletroquímico-mecânica, bioquímica, biofísico-química, biomecânica, bioeletromecânica, bioeletroquímica, bioeletroquímico-mecânica, física, ou propriedade mecânica do material biológico. Por exemplo, a propriedade elétrica pode ser a carga de superfície, o potencial de superfície, o potencial de repouso, a corrente elétrica, a distribuição do campo elétrico, dipolo elétrico, quádruplo elétrico, carga e distribuição de nuvem elétrica tridimensional, as propriedades elétricas no telômero de DNA e cromossomas, ou impedância; a propriedade térmica pode ser a temperatura, ou a frequência vibracional do material ou moléculas biológicas, a propriedade óptica pode ser a absorção óptica, transmissão óptica, reflexão óptica, propriedade óptica-elétrica, brilho, ou emissão fluorescente; a propriedade química pode ser o valor de pH, reação química, reação bioquímica, a reação bioeletroquímica, a velocidade da reação, a energia da reação, concentração de oxigênio, a taxa de consumo de oxigênio, a força iônica, o comportamento catalítico, ou força de ligação; a propriedade física pode ser a densidade ou o tamanho geométrico; a propriedade acústica é a frequência, a velocidade de ondas acústicas, distribuição do espectro de intensidade e distribuição acústica, intensidade acústica, a absorção acústica, ou ressonância acústica; e a propriedade mecânica é a pressão interna, a dureza, a resistência ao cisalhamento, a força de alongamento, tensão de ruptura, a aderência, a frequência de ressonância mecânica, elasticidade, plasticidade, e a compressibilidade.
[0021] Em algumas formas de realização do aparelho, o dispositivo de detecção e sonda aplica-se ao material biológico a uma tensão que varia entre 1 mV a cerca de 10 V, ou entre I mV a cerca de 1.0 V.
[0022] Em algumas formas de realização do aparelho, o primeiro microdispositivo compreende um material condutor, um material eletricamente isolante, um material biológico, e um material semicondutor
[0023] Em algumas formas de realização do aparelho, o primeiro microdispositivo tem um tamanho que varia desde cerca de 1 angstrom até cerca de 5 milímetros
[0024] Em algumas formas de realização do aparelho, o dispositivo de detecção e de sondagem compreende ainda um ou mais microdispositivos adicionais, cada um dos quais é também capaz de medir o nível microscópico, a propriedade elétrica, magnética, eletromagnética, térmica, óptica, acústica, química, biológica, eletromecânica, eletroquímica, eletroquímico-mecânica, bioquímica, biomecânica, bioeletromecânica, bioeletroquímica, bioeletroquímico-mecânica, física ou mecânica da entidade biológica. A propriedade elétrica pode ser a carga de superfície, o potencial de superfície, o potencial de repouso, a corrente elétrica, a distribuição da corrente elétrica, dipolo elétrico, quadripolo elétrico, distribuição e carda da nuvem tridimensional elétrica, propriedades elétricas em telômeros do DNA e cromossomo, ou impedância; a propriedade térmica pode ser a temperatura, ou a frequência vibracional do material biológico e moléculas; a propriedade óptica pode ser a absorção óptica, transmissão óptica, reflexão óptica, propriedade óptica elétrica, brilho ou emissão fluorescente; a propriedade química pode ser o valor de pH, reação química, biorreação química, reação bioeletroquímica, velocidade de reação, energia de reação, concentração de oxigênio, taxa de consumo de oxigênio, força iônica, comportamento catalítico, ou a força de ligação; a propriedade física pode ser a densidade ou o tamanho geométrico; a propriedade acústica pode ser a frequência, a velocidade de ondas acústicas, frequência acústica e distribuição da intensidade do espectro acústico, absorção acústica, ou ressonância acústica; e a propriedade mecânica pode ser a pressão interna, a dureza, a resistência ao cisalhamento, a força de alongamento, fratura por tensão, adesão, frequência de ressonância mecânica, elasticidade, plasticidade, e a compressibilidade.
[0025] Em algumas formas de realização do aparelho, cada um dos outros microdispositivos compreende um material condutor, um material eletricamente isolante, um material biológico, ou um material semicondutor. Além disso, cada uma dos outros microdispositivos compreende um material que é o mesmo ou diferente do material do primeiro microdispositivo, e é capaz de medir a mesma ou uma propriedade diferente do material biológico que o primeiro microdispositivo realiza.
[0026] Em algumas formas de realização do aparelho, o primeiro microdispositivo e cada um dos outros microdispositivos são capazes de medir a carga de superfície, o potencial de superfície, potencial de repouso, a corrente elétrica, a distribuição do campo elétrico, dipolo elétrico, quádruplo elétrico, distribuição tridimensional da nuvem elétrica ou carga, propriedades elétricas em telômeros de DNA e cromossomas, impedância, temperatura, frequência vibracional, absorção óptica, reflexão óptica, transmissão óptica, propriedade óptica-elétrica, brilho, emissão fluorescente, pH, reação química, biorreação química, reação bioeletroquímica, velocidade de reação, energia de reação, concentração de oxigênio, taxa de consumo de oxigênio, força iônica, comportamento catalítico, força de ligação, densidade, tamanho geométrico, frequência, velocidade das ondas acústicas, frequência e distribuição do espectro de intensidade acústica, intensidade acústica, a absorção acústica, ressonância acústica, a pressão interna, a dureza, a força de cisalhamento, a força de alongamento, tensão de ruptura, aderência, frequência de ressonância mecânica, elasticidade, plasticidade, e compressibilidade. Podem medir as mesmas e diferentes propriedades, nos mesmos tempos ou em tempos diferentes.
[0027] Em algumas formas de realização do aparelho, o dispositivo de sondagem e os microdispositivos são colocados com uma distância desejada entre si
[0028] Em algumas formas de realização do aparelho, cada um dos outros microdispositivos tem um tamanho que varia desde cerca de 1 angstrom até cerca de 5 milímetros.
[0029] Em algumas formas de realização do aparelho, os microdispositivos estão espaçados para fora sobre o substrato por uma distância de pelo menos 10 angstroms (por exemplo, a partir de cerca de 5 mícrons até cerca de 100 mícrons).
[0030] Em algumas formas de realização do aparelho, o substrato tem a forma de uma placa, um tubo, ou de um conjunto de tubos, ou o substrato é um objeto tridimensional.
[0031] Em algumas formas de realização do aparelho, o dispositivo de sondagem e detecção compreende ainda um segundo substrato do mesmo material ou diferente do primeiro substrato.
[0032] Em algumas formas de realização, o aparelho compreende ainda um dispositivo para a leitura dos dados a partir da medição da propriedade do dispositivo de sondagem e detecção.
[0033] Em algumas formas de realização, cada aparelho compreende ainda um sistema de administração de fluidos que compreende um gerador de pressão, um regulador de pressão, uma válvula de estrangulamento, um medidor de pressão, e kits de distribuição. O gerador de pressão pode incluir um sistema de pistão do motor e uma caixa contendo gás comprimido; o regulador de pressão pode regular a pressão para baixo e para cima a um valor desejado; o medidor de pressão realimenta o valor medido para a válvula de estrangulamento, que, em seguida, regula o pressão para se aproximar do valor-alvo.
[0034] O fluido a ser administrado no aparelho pode ser um líquido ou gás. Exemplos de líquidos incluem sangue, urina, saliva, lágrimas, solução salina, e suor, enquanto que exemplos do gás incluem nitrogênio, argônio, hélio, neon, criptônio, xenônio, e radônio.
[0035] Em algumas formas de realização do aparelho, o dispositivo de detecção e de sondagem compreende ainda um controlador de sistema que compreende um pré-amplificador, um amplificador lock-in, um medidor elétrico, um medidor térmico, uma matriz de comutação, um barramento de sistema, um dispositivo de armazenamento não volátil, uma memória de acesso aleatório, um processador, e uma interface de utilizador. A interface pode incluir um sensor que pode ser, por exemplo, um sensor térmico, um medidor de fluxo, e/ou um medidor de piezo.
[0036] Em algumas formas de realização, o aparelho pode incluir ainda uma interface biológica, um sistema controlador, ou pelo menos um sistema para a recuperação ou tratamento de resíduos hospitalares. A recuperação e tratamento de resíduos médicos é realizada pelo mesmo sistema ou através de dois sistemas diferentes.
[0037] Em algumas formas de realização, o aparelho inclui ainda um sistema de fornecimento de testes de amostra, um sistema de distribuição da amostra teste, um canal de distribuição, uma unidade de pré-processamento, um dispositivo de detecção, um sistema de posicionamento global, um dispositivo de movimento, um transmissor de sinal, um receptor de sinal, um sensor, uma unidade de armazenamento de memória, uma unidade de processamento lógico, um chip de aplicação específica, uma unidade de reciclagem e recuperação da amostra teste, um dispositivo microeletromecânico, um dispositivo multifuncional, ou um instrumento de microcirurgia para efetuar a limpeza, manutenção ou função médica. Tais componentes adicionais podem ser fabricados por meio de métodos conhecidos na arte, por exemplo, tal como descrito em PCT/US2011/024672, Pedido EUA No. 12/416,280, e PCT/US2010/041 00 1, todos os quais são aqui incorporados por referência nas suas totalidades.
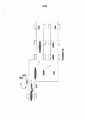
[0038] Em algumas formas de realização do aparelho, o sistema de administração do material biológico compreende pelo menos um canal no interior do qual o material biológico a ser detectado percorre em uma determinada direção; o dispositivo de sondagem e detecção compreende pelo menos um microdispositivo de sondagem e pelo menos um microdispositivo detecção, em que pelo menos um microdispositivo de sondagem está localizado antes do microdispositivo de detecção em relação à direção na qual o material biológico percorre, e o microdispositivo sondagem e o microdispositivo de detecção podem ser anexados ao interior ou exterior da parede do canal
[0039] Em algumas formas de realização do aparelho, as formas e tamanhos de diferentes secções do canal podem ser as mesmas ou diferentes, a largura do canal intervala entre cerca de 1 nm a cerca de 1 mm; o canal pode ser reto, curvo, ou em ângulo; a parede interior do canal define um espaço circular, oval, ou poligonal; a parede interior do canal define um espaço circular ou retangular, o canal é um nanotubo circular em carbono.
[0040] Em algumas formas de realização do aparelho, o nanotubo de carbono tem um diâmetro que varia entre 0,5 nm a cerca de 100 nm, e um comprimento que varia entre 5.0 nm a cerca de 10 mm.
[0041] Em algumas formas de realização do aparelho, a parede interior do canal tem pelo menos uma concavidade que pode ser na mesma secção que o microdispositivo de sondagem ou de detecção. A ranhura côncava pode ser um espaço cúbico ou um espaço angular; a ranhura côncava pode ter uma profundidade que varia entre 10 nm a cerca de 1 mm.
[0042] Em algumas formas de realização do aparelho, é injetado um fluido para dentro do canal, seja antes ou depois do material biológico passar através de um microdispositivo de sondagem, para auxiliar o trajeto, ou para a separação do material biológico no interior do canal. O fluido de distribuição pode ser injetado no interior do canal através de um canal de distribuição de fluido ligada a uma abertura na parede do canal.
[0043] O dispositivo pode detectar as doenças de mais do que um material biológico, e o canal compreende um dispositivo localizado no seu interior para separar ou dividir os materiais biológicos com base em níveis diferentes de uma mesma propriedade deste materiais biológicos. O dispositivo de separação ou de divisão pode ser, por exemplo, uma fenda e separa ou divide os materiais biológicos com base nas suas propriedades, tais como cargas de superfície.
[0044] O aparelho pode ainda incluir um dispositivo de filtragem para remover objetos irrelevantes do material biológico para detecção.
[0045] O material biológico pode ser o DNA, telômeros de DNA, RNA, cromossoma, célula, subestrutura celular, proteína, e vírus.
[0046] Em algumas formas de realização, o aparelho pode incluir ainda uma unidade para administrar material biológico, um canal, uma unidade de detecção, uma unidade de armazenamento de dados, uma unidade de análise de dados, uma unidade de controle central, uma unidade de recirculação biológica da amostra, uma unidade de eliminação de resíduos, uma unidade de pré-processamento, uma unidade de processamento de sinais, ou unidade de processamento de resíduos. Todos os componentes adicionais podem ser integrados em um único dispositivo ou placa juntamente com o sistema de distribuição e sondagem e sonda de detecção. A unidade de pré- processamento pode compreender uma unidade de filtração da amostra; uma unidade de distribuição para distribuir um íon desejado, um componente biológico, ou um componente bioquímica; uma unidade de recarga; uma unidade de fornecimento de pressão constante; e uma unidade perturbação de pré-sondagem da amostra. A unidade de filtração da amostra pode compreender um canal de entrada, um canal de distribuição do fluido, uma câmara de aceleração, e uma fenda. A unidade de processamento de sinais podem compreender um amplificador, um amplificador lock-in, um conversor de A/D (analógico para digital ou uma alternativa para direcionar a corrente elétrica), um microcomputador, um manipulador, um mostrador, e as ligações de rede. A unidade de processamento de sinal pode coletar mais do que um sinal, e os sinais podem ser integrados para cancelar o ruído ou para aumentar a relação entre o sinal e o ruído.
[0047] Em algumas formas de realização do aparelho, é injetado um líquido biocompatível no canal de distribuição do fluido para separar o material biológico, ou o fluido biocompatível é injetado na entrada do canal de fluido de distribuição e administrado a uma abertura na parede do canal de entrada. O fluido biocompatível compreende a água, solução salina, um líquido rico em oxigênio, e plasma.
[0048] Em algumas formas de realização do aparelho, o ângulo entre o canal de entrada e o canal de distribuição do fluido varia entre °0 a cerca de 180°, desde cerca de 30° até cerca de 150°, a desde cerca de 60° até cerca de 120°, ou desde cerca de 75 ° até cerca 105 °, ou cerca de 90°; a largura de cada um dos canais varia entre cerca de 1 nm a cerca de 1 mm; e pelo menos um dos canais compreende um dispositivo de sondagem ligado à parede lateral do canal, no qual o dispositivo de sondagem é capaz de medição o nível microscópico uma propriedade elétrica, magnética, eletromagnética, térmica, ótica, acústica,biológica, química, eletromecânica, eletroquímica, eletroquímico-mecânica, bioquímica, biomecânica, bioeletromecânica, bioeletroquímica, bioeletroquímico-mecânica, física e mecânica do material biológico. A unidade de filtração da amostra pode compreender um canal de entrada, um microfiltro biocompatível, e um canal de saída.
[0049] Em algumas formas de realização do aparelho, o microfiltro biocompatível é capaz de filtrar um material biológico baseado em pelo menos uma propriedade selecionada a partir do tamanho físico, dureza, elasticidade, resistência ao corte, peso, característica de superfície, óptica, acústica, térmica, química, mecânica, biológica, bioquímica, elétrica, eletroquímica, magnética, propriedade eletromagnética, eletromecânica, eletroquímico-mecânica e eletroquímico-biológica.
[0050] Em algumas formas de realização do aparelho, a unidade de recarga carrega nutrientes ou e gás respirador ao material biológico. O nutriente pode incluir um eletrólito biocompatível forte ou fraco aminoácido, mineral, íons, oxigênio, líquido rico em oxigênio, gotejamento intravenoso, glucose, ou uma proteína, e o gás respirador pode incluir oxigênio.
[0051] Em algumas formas de realização, o material biológico a ser testado compreende sangue, urina, saliva, lágrimas, solução salina, ou suor
[0052] Em ainda outro aspecto, a invenção fornece um aparelho alternativo para detectar uma doença em um material biológico. O aparelho compreende uma câmara de lançamento para lançar uma sonda a uma velocidade e direção desejadas, uma unidade de detecção, um objeto de sonda, um componente de detecção, um canal para o transporte do material biológico a ser testado, e o objeto de sonda.
[0053] Em algumas formas de realização deste dispositivo, a câmara de lançamento compreende um pistão para liberar o objeto de sonda e um canal para direcionar o objeto de sonda.
[0054] Ainda um outro conjunto de aparelhos para detectar uma doença em um material biológico, tal como previsto pela presente invenção, são aqueles fabricados por um método que compreende: fornecer um substrato; sequencialmente depositar um primeiro material e um segundo material como duas camadas sobre o substrato para formar uma pilha de material; formatando o segundo material para formar uma primeira característica desejada; deposição de um terceiro material na pilha de material para cobrir o segundo material; opcionalmente formatando o primeiro material e terceiro material para formar uma segunda característica desejada, e, opcionalmente, depositando um quarto material na pilha de material; sendo que o dispositivo de detecção é capaz de interagir com o material biológico para gerar um sinal de resposta.
[0055] Em algumas formas de realização, nestes métodos usados para a fabricação do aparelho, o segundo material pode ser padronizado por processos microeletrônicos.
[0056] Em algumas formas de realização, nestes métodos usados para a fabricação do aparelho, o primeiro material e o terceiro material podem ser os mesmos ou diferentes
[0057] Em algumas formas de realização, nestes métodos usados para a fabricação do aparelho, o primeiro material e o terceiro material são padronizado por litografia e processos ataque químico seletivos para o segundo material de modo a formar pelo menos um tipo de característica nas camadas do terceiro e primeiro materiais.
[0058] Em algumas formas de realização, nestes métodos usados para a fabricação do aparelho, o método de fabricação pode ainda compreender o capeamento do topo da pilha do material de modo a formar uma vala encerrada. A vala encerrada pode, por exemplo, ser usada para observar e registrar características e comportamentos do material biológico. O capeamento pode compreender, por exemplo, a colocação de um segundo dispositivo no topo da pilha de material, e o segundo dispositivo pode ser um dispositivo idêntico ao do dispositivo de detecção sendo encerrado, uma peça de vidro ou cristal, ou um dispositivo funcional selecionado a partir do grupo que consiste de um dispositivo de formação de imagem, um sensor óptico, um dispositivo de armazenamento de memória, uma transmissão de sinal, um componente de processamento lógico, um circuito para armazenagem, transmissão e processamento de sinais.
[0059] Em algumas formas de realização, nestes métodos utilizados para a fabricação do aparelho, a primeiro ou segunda característica é selecionada a partir do grupo que consiste em câmaras divididas, ligadas com canais, gerador da sonda (sonda), sondas de detecção, linhas de interconexão elétricas, linhas de transmissão ópticas e linhas piezoelétricas. Por exemplo, as câmaras divididos podem ser para o pré-tratamento do material biológico ou seja, a triagem inicial e reforço da concentração do material biológico com doença para testes adicionais, as câmaras ligadas com canais são para o pré- processamento e detecção, os canais podem ser para o fluxo do material biológico, o gerador de sonda (sonda) pode ser para gerar sondas e perturbar o sinal, tendo em vista o desencadeamento de um sinal de resposta do material biológico, a sonda de detecção pode ser para as propriedades de medição do material biológico e o sinal de resposta, as linhas elétricas de interligação conectiva podem ser para a transmissão de sinais, as linhas de transmissão ópticas podem ser para a transmissão de sinais, e as linhas piezoelétricas podem ser para o efeito piezoelétrico durante a sondagem dos materiais biológicos.
[0060] Em algumas formas de realização, nestes métodos usados para a fabricação do aparelho, o segundo material é padronizado utilizando litografia e processos ataque químico seletivos para o primeiro material de modo a formar um componente desejado tal como uma sonda de detecção
[0061] Em algumas formas de realização, nestes métodos usados para a fabricação do aparelho, os primeiro e terceiros materiais são padronizados utilizando litografia e processos ataque químico seletivos para o segundo material, a fim de formar pelo menos um tipo de rego nas camadas dos terceiro e primeiro materiais, em que o segundo material se encontra razoavelmente alinhado com a parede do rego.
[0062] Em algumas formas de realização, nestes métodos usados para a fabricação do aparelho, a espessura do quarto material é mais fina do que a do terceiro material.
[0063] Em algumas formas de realização, o segundo e o quarto materiais formam sondas de detecção.
[0064] Em algumas formas de realização, o segundo e o quarto materiais formam uma sonda e um detector, respectivamente.
[0065] Em algumas formas de realização, o aparelho pode ainda incluir um dispositivo para criação de imagens a fim de observar e registrar as propriedades e comportamentos do material biológico.
[0066] Em algumas formas de realização, o aparelho pode ainda incluir uma unidade de pré-tratamento com câmaras de pré-triagem e melhorando um material biológico com doença para testes adicionais, os canais para o transporte de amostras de fluidos, sondas para sondar e perturbar o material biológico a ser testado a fim de gerar sinais de resposta, as sondas de detecção para a medição de propriedades e sinais de resposta do material biológico, e um dispositivo de formação de imagem, uma câmara, uma estação de visualização, um detector acústico, um detector térmico, um detector de emissão de íons, ou um gravador térmico para a observação e registro das propriedades e comportamentos do material biológico.
[0067] Em algumas formas de realização, o aparelho pode ainda incluir uma memória de armazenamento, uma transmissão de sinal, um componente de processamento lógico, ou um circuito para o armazenamento de dados, transmissão do sinal, ou processamento do sinal. Estes dispositivos adicionais podem ser fabricados através de processos de microeletrônica sobre o substrato onde o primeiro material é depositado.
[0068] Em algumas formas de realização, o aparelho pode ter dimensões de canal que variam entre 2 mícrons x 2 mícrons até cerca de 100 mícrons x 100 mícrons em área de secção transversal para um canal em forma de quadrado, um raio que varia entre cerca de 1 mícron a cerca de 20 mícrons em área transversal para um canal circular, e uma dimensão de sonda típica que varia entre 0,5 mícrons x 0,5 mícrons até cerca de 20 mícrons x 20 mícrons em área de secção transversal para uma sonda em forma de quadrado.
[0069] Em algumas formas de realização, o aparelho pode ter dimensões de canal típicas que variam entre 6 mícrons x 6 mícrons até cerca de 14 mícrons x 14 mícrons de área na secção transversal em um canal em forma de quadrado, um raio que varia entre cerca de 3 mícrons e cerca de 8 mícrons de área de seção transversal em um canal circular, e uma dimensão de sonda típica variando entre cerca de 0,5 mícrons x 0,5 mícrons até cerca de 10 mícrons x 10 mícrons de área na secção transversal em uma sonda em forma de quadrado.
[0070] Em algumas formas de realização, o primeiro e o quarto materiais compreendem um óxido não dopado (Si02), nitreto de silício, óxido dopado, um material polimérico, vidro ou um material isolante.
[0071] Em algumas formas de realização, o segundo e o terceiro materiais compreendem um material eletricamente condutor, alumínio, uma liga de alumínio, cobre, liga de cobre, tungstênio, uma liga de tungstênio, ouro, liga de ouro, prata, uma liga de prata, ou um material piezoelétrico. Exemplos de materiais piezoelétricos incluem, mas não estão limitados a, quartzo, berlinita, gálio, ortofosfato, GaPO4, turmalina, cerâmica, bário, titanato, BaTiO3, zirconato de chumbo, titanato de PZT, óxido de zinco, nitreto de alumínio, e um fluoreto de polivinilideno.
[0072] Em ainda algumas outras concretizações, o segundo e o quarto materiais compreendem um material eletricamente condutor ou um material piezoelétrico. Exemplos de materiais eletricamente condutores incluem, mas não estão limitados a, alumínio, ligas de alumínio, cobre, liga de cobre, tungstênio, liga de tungstênio, ouro, liga de ouro, prata, liga de prata; enquanto que exemplos de material piezo elétrico incluem, mas não estão limitados a, quartzo, berlinita, gálio, ortofosfato GaPO4, turmalina, cerâmica, bário, titanato, BaTiO3, zirconato de chumbo, titanato de PZT, óxido de zinco, nitreto de alumínio, e um fluoreto de polivinilideno.
[0073] Em algumas formas de realização do aparelho, o dispositivo de detecção compreende pelo menos uma sonda, pelo menos um detector, ou pelo menos uma sonda e detetor, a sonda gerando um sinal de sondagem ou perturbador para o material biológico a fim deste dar um sinal de resposta, enquanto que o detector mede o sinal de resposta gerado deste modo.
[0074] Em algumas formas de realização do aparelho, o segundo material é padronizado pelos processos microeletrônicos de modo a formar uma primeira característica desejada; o primeiro e o terceiro materiais são opcionalmente padronizados através de processos microeletrônicos para formar uma segunda característica desejada; e o primeiro e o terceiro materiais podem ser os mesmos, ou serem diferentes.
[0075] Em algumas formas de realização, os métodos para fabricar o aparelho incluem ainda o capeamento do topo da pilha do material de modo a formar rasgo encerrado, em que tal rego é utilizado para o transporte da amostra teste ou local de detecção.
[0076] Um dos principais aspectos inovadores do presente pedido de patente é a concepção e fluxos do processo de fabricação de microdispositivos e métodos para a utilização dos microdispositivos para medição das propriedades ao nível microscópico e em um espaço tridimensional, de um material biológico (por exemplo, uma única célula ou uma única molécula biológica, tal como o DNA e RNA). Os microdispositivos têm microssondas dispostas de uma maneira tridimensional, com tamanhos característicos tão pequenos como uma célula, um DNA, um RNA e sendo capazes de captar, classificar sondar, medir, e modificar materiais biológicos.
[0077] Um outro aspecto da presente invenção diz respeito a métodos para a fabricação de um microdispositivo. Os métodos incluem a deposição de vários materiais sobre um substrato e, nos interinos do depósito de dois em dois materiais, configurar os materiais pela tecnologia microeletrônica e processos associados, em que o microdispositivo é capaz de medir o nível microscópico as propriedades elétrica, magnética, eletromagnética, térmica, óptica, acústica, química, biológica, física, físico-química, bioquímica, biofísica, mecânica, química biomecânica, eletrobiomecânica, bioeletromecânica-química, eletromecânica-química, microeletromecânica de um material biológico, com o qual o microdispositivo entra em contato.
[0078] Ainda outro aspecto da presente invenção diz respeito a métodos para a fabricação de um microdispositivo, que inclui a deposição de um primeiro material sobre o substrato, configurando o primeiro material por um processo de microeletrônica para dar origem a pelo menos uma parte residual padronizada e deixando a superfície do substrato descoberto pelo primeiro material, depositando um material não condutor sobre o primeiro material processado e o substrato, criando uma abertura no segundo material e expondo parte do primeiro material padronizado, encerrando a abertura no segundo material com um terceiro material. Em algumas formas de realização, o processo compreende um processo microeletrônico com a deposição de uma fina película, fotolitografia, gravação, limpeza e/ou polimento mecânico-químico.
[0079] No entanto, em ainda outro aspecto, a invenção proporciona métodos para a fabricação de um microdispositivo, que inclui uma primeira etapa de deposição de um primeiro material sobre um substrato; a segunda etapa, a deposição de um segundo material sobre o primeiro material e, em seguida, a padronização do segundo material através de uma microtecnologia ou processo; e repetir o segundo passo, pelo menos uma vez, utilizando um material que pode ser o mesmo ou diferente do material do primeira ou segunda etapas. Os materiais utilizados nas etapas repetidas podem ser os mesmos ou diferentes do material da primeira ou segunda etapas. Em algumas formas de realização, pelo menos um dos materiais utilizados na fabricação do microdispositivos é um material piezoelétrico ou um material condutor.
[0080] Em algumas formas de realização, podem ser acoplados vários microdispositivos fabricados, unificados, e ligados por métodos físicos ou elétricos a fim de constituir os dispositivos mais avançados
[0081] Em algumas formas de realização, os aparelhos da presente invenção podem ser integrados em um único dispositivo (por exemplo, utilizando uma tecnologia de processamento de semicondutores) ou montados sobre uma placa (por exemplo, usando uma tecnologia de acondicionamento de computadores).
[0082] Em algumas formas de realização, a padronização de um material é feito por um processo de microeletrônica (por exemplo, deposição de vapor químico, deposição física de vapor, ou deposição da camada atômica a fim de depositar vários materiais sobre um substrato como um isolante ou condutor; litografia ou ataque químico para transferir os padrões desde o design até à estrutura; planarização mecânico-química, limpeza química para a remoção de partículas, pico térmico de recozimento para reduzir os defeitos dos cristais, difusão ou implantação iônica para a dopagem elementos em camadas específicas). Em algumas formas de realização, a planarização e padronização é feita através de polimento químico, polimento mecânico, ou polimento mecânico-químico.
[0083] Em algumas outras formas de realização, os métodos incluem ainda a remoção de uma pilha de várias camadas de materiais através de ataque químico a úmido, a seco, ou por ataque químico a vapor.
[0084] Em algumas formas de realização, o microdispositivo pode mover-se em qualquer direção. Por exemplo, dois microdispositivos pode mover-se em direções opostas
[0085] Em algumas formas de realização, o microdispositivo fabricado é padronizado para ser capaz de captar, classificar, sondar, medir, ou modificar um material biológico; ou que ele possa reconstituir através da membrana de uma célula.
[0086] Ainda um outro aspecto da presente invenção diz respeito a métodos para a fabricação de um dispositivo ou aparelho para detectar doença em um material biológico, que inclui o fornecimento de um substrato, sequencialmente depositar um primeiro material e um segundo material como duas camadas diferentes sobre o substrato de modo a formar uma pilha de material, padronizar o segundo material através de processos da microeletrônica para formar uma primeira característica desejada, depositando um terceiro material sobre a pilha de material, opcionalmente padronizar o primeiro e o terceiro materiais através de processos microeletrônicos para formar uma segunda característica desejada, e, opcionalmente, depositar um quarto material sobre a pilha de material.
[0087] Em algumas formas de realização, os métodos incluem ainda as etapas de fabricação (utilizando processos que incluem mas não se limitando a, depositar, padronizar, polir, limpar) componentes adicionais sobre o substrato antes de depositar sequencialmente o primeiro material e o segundo material na forma de camadas sobre o substrato, em que os componentes adicionais compreendem um componente de armazenamento de dados, um componente de processamento de sinais, um componente de armazenamento de memória, um componente de transmissão de sinais, um componente de processamento lógico, e um componente de RF (radiofrequência).
[0088] Em algumas outras formas de realização, os métodos incluem ainda as etapas de fabricação de pelo menos um circuito sobre o substrato antes de depositar sequencialmente o primeiro material e o segundo material na de camadas sobre o substrato, em que o circuito compreende um circuito de armazenamento de dados, um circuito de processamento de sinais, um circuito de armazenamento de memória, um circuito de transmissão de sinais, e um circuito de processamento lógico.
[0089] Em ainda algumas outras concretizações, os métodos da presente invenção incluem ainda um passo de planarização, o terceiro material químico utilizando processo de polimento mecânico ou um processo de ataque químico reverso, após a etapa de depositar o terceiro material sobre a pilha de material e antes do passo de padronização do primeiro e o terceiro materiais.
[0090] Os exemplos dos processos microeletrônicos adequados incluem, mas não se limitam a, deposição de uma camada fino, litografia, ataque químico, polimento, limpeza, implantação iônica, difusão, e acondicionamento que é normalmente usada em microeletrônica.
[0091] Os primeiro e terceiro materiais podem ser os mesmos ou diferentes. Eles podem ser, por exemplo, materiais eletricamente isolantes, tal como o óxido, óxido dopado, nitreto de silício, ou um polímero.
[0092] O segundo material pode ser um material eletricamente condutor, um material piezoelétrico, um material semicondutor, um material térmico sensível, um material óptico, um material sensível à pressão, um material de emissão de íons sensíveis, ou qualquer combinação dos mesmos. Por exemplo, o segundo material pode ser feito de cobre, alumínio, tungstênio, ouro, prata, vidro, uma liga de alumínio, liga de cobre, uma liga de tungstênio, uma liga de ouro, uma liga de prata, quartzo, berlinita, ortofosfato, gálio, GaPO4, turmalina, cerâmica, titanato de bário, BaTiO3, titanato, zirconato de chumbo, PZT, óxido de zinco, nitreto de alumínio, ou um fluoreto de polivinilideno.
[0093] Em algumas formas de realização, a primeira característica desejada pode ser uma sonda, enquanto que a segunda funcionalidade desejada pode ser uma forma de recesso, ou rego nas camadas do primeiro e o terceiro materiais.
[0094] Ainda em outra forma de realização, os métodos da presente invenção compreendem ainda a deposição de um quarto material sobre a pilha de material e, em seguida, padronizar o quarto material para formar uma reentrância, tal como um furo em um local selecionado.
[0095] Em ainda outra concretização, os métodos da presente invenção compreendem ainda um passo para remoção do terceiro material da pilha de material através de ataque químico a úmido ou vapor para formar uma câmara de detecção entre o quarto material e o substrato. Além disso, eles podem também incluir um passo de remoção do primeiro material da pilha de materiais através de ataque químico a úmido ou vapor para formar um canal. O canal pode ligar a câmara de detecção formada com as câmaras adicionais.
[0096] Em ainda outra forma de realização, os métodos da presente invenção incluem ainda um passo para selagem ou capeamento do topo da pilha do material de modo a formar uma vala encerrada. Em um exemplo deste passo, a parte superior da pilha do material é selado ou coberto com um dispositivo adicional sobra a pilha de material. Exemplos de um tal dispositivo adicional incluem, mas não estão limitados a, um dispositivo de formação de imagem e uma sonda de detecção. O dispositivo acima referido na parte superior da pilha de material compreende um dispositivo óptico, um dispositivo de formação de imagem, câmera, estação de visualização, detector acústico, detector térmico, detector de emissão de íons, e registrador térmico.
[0097] Em ainda outro aspecto, a presente invenção fornece métodos para a fabricação de um dispositivo para detectar doenças em um material biológico, que incluem o fornecimento de um substrato, sequencialmente depositar um primeiro e um segundo materiais como camadas sobre o substrato para formar uma pilha de material, padronizar o segundo material através de litografia e ataque químico para formar uma área rebaixada na camada do segundo material, depositando um terceiro material sobre a pilha de material, remover uma porção do terceiro material acima do segundo material através de ataque químico reverso ou processo de polimento, padronizando o terceiro material por litografia e ataque químico para formar pelo menos uma porção de área rebaixada na camada do terceiro material, depositar um quarto material sobre a pilha de material, e remover a porção do quarto material acima do terceiro material através de ataque químico reverso ou processo de polimento, a fim de manter pelo menos uma porção do segundo e o quarto materiais na mesma camada.
[0098] Os primeiro e terceiro materiais usados nos métodos da presente invenção podem ser os mesmos ou diferentes. Em algumas formas de realização, são os mesmas. Eles podem ser, por exemplo, um material eletricamente isolante. Exemplos dos primeiro e terceiro materiais incluem, mas não estão limitados a, óxido, óxido dopado, nitreto de silício, ou um polímero.
[0099] Em algumas formas de realização, após a deposição e processamento do terceiro e do quarto material, pelo menos mais um material é depositado e processado a fim de formar uma camada de topo com a formação de uma câmara ou canais de detecção por debaixo delas.
[00100] Os exemplos do segundo material incluem, mas não estão limitados a, materiais eletricamente condutores, materiais piezoelétricos, materiais semicondutores, materiais sensíveis térmicos, um material sensível à pressão, um material sensível à emissão de íons, material óptico, ou quaisquer combinações destes.
[00101] Em algumas formas de realização, um novo aparelho de detecção que compreende uma câmara de detecção e/ou canais de transporte da amostra de teste é formado por métodos que incluem as etapas de: deposição de um primeiro material, padronização do primeiro material (“material A”), para formar, pelo menos, uma área rebaixada, depositando um segundo material (“material B”), a remoção do segundo material (“material B”) das áreas acima do primeiro material (“material A”) usando polimento e/ou processos ataque químico reverso, deixando o segundo material (“material B”) na área rebaixada da primeira camada de material, deposição de um terceiro material (“material C”) para cobrir o primeiro material (“material A”) e o segundo material (“material B”), padronização do terceiro material (“material C”) para formar pelo menos um furo menor que a(s) área(s) de reentrância (s) na 3a camada de material e acima dela, eliminando o segundo material (“material B”), opcionalmente usando ataque químico vaporizado ou molhado, formando uma cavidade encerrada na primeira camada de material.
[00102] Em ainda algumas outras concretizações, um novo aparelho de detecção pode ser integrado com pelo menos um microinjetor e pelo menos um detector, no qual o microinjetor pode injetar um objeto desejado no material biológico a ser testado para gerar uma resposta por parte do material biológico e o detector detectando a resposta assim gerada pelo material biológico.
[00103] A invenção proporciona ainda métodos para a detecção da resposta dinâmica de um material biológico a um sinal. Estes métodos incluem o fornecimento de um aparelho que compreende dois microdispositivos dos quais um é um microdispositivo de sondagem e o outro é um microdispositivo de detecção posicionado a uma distância do microdispositivo de sondagem; contactando o material biológico com o microdispositivo de sondagem mediante o qual o microdispositivos de sondagem mede uma propriedade biológica do objeto o nível microscópico, ou envia um sinal estimulante para o material biológico, e o microdispositivo de detecção mede a resposta do material biológico através das propriedades do material biológico o nível microscópico. Opcionalmente, o microdispositivo de detecção tem contato com o material biológico durante as medições.
[00104] Em algumas formas de realização, o sinal é elétrico, magnético, eletromagnético, térmico, ótico, acústico, químico, biológico, eletromecânico, eletroquímico, eletroquímico-mecânico, bioquímico, biomecânico, bioeletromecânico, bioeletroquímico, bioeletroquímico- mecânico, físico, ou mecânico.
[00105] Em algumas outras modalidades, a propriedade ao nível microscópico é elétrica, magnética, eletromagnética, térmica, óptica, acústica, biológica, química, eletromecânica, eletroquímica, eletroquímico-mecânica, bioquímica, bioquímico-física, biomecânica, bioeletromecânica, bioeletroquímica, bioeletroquímico-mecânica, física ou mecânica.
[00106] Exemplos das propriedades elétricas incluem, mas não estão limitadas a, carga superficial, potencial de superfície, potencial de repouso, corrente elétrica, distribuição do campo elétrico, dipolo elétrico, quádruplo elétrico, distribuição tridimensional da nuvem elétrica e/ou carga, propriedades elétricas em telômeros do DNA e cromossomas (também chamado de extremidade pegajosa do DNA) ou impedância. Exemplos das propriedades térmicas incluem a temperatura, e frequência de vibração do material biológico e moléculas. Exemplos das propriedades ópticas incluem a absorção óptica, transmissão óptica, reflexão óptica, propriedades óptico- elétricas, brilho, e emissão fluorescente. Exemplos das propriedades químicas incluem o valor de pH, reação química, biorreação química, reação bioeletroquímica, velocidade da reação, energia da reação, velocidade de reação, concentração de oxigênio, taxa de consumo de oxigênio, força iônica, comportamento catalítico e força de ligação. Exemplos das propriedades físicas incluem a densidade e o tamanho geométrico. Exemplos das propriedades acústicas incluem a velocidade, frequência de ondas acústicas, frequência acústica e a distribuição do espectro de intensidade, intensidade acústica, absorção acústica e ressonância acústica. Exemplos de propriedades mecânicas incluem a pressão interna, dureza, resistência ao cisalhamento, força de alongamento, tensão na ruptura, aderência, frequência de ressonância mecânica, elasticidade, plasticidade e compressibilidade. Os dados da medição de um ou mais das propriedades no nível microscópico podem ser utilizados na detecção de doenças, por exemplo, cancro na sua fase inicial, ou para a estimativa da expectativa de vida do transportador do material biológico.
[00107] Em algumas outras formas de realização, o aparelho inclui ainda um terceiro microdispositivo que é diferente do microdispositivo de sondagem e do microdispositivo de detecção; e o terceiro microdispositivo mede a mesma ou uma propriedade diferente do material biológico das que a sondagem microdispositivo de sondagem e o de detecção fazem.
[00108] Em ainda algumas outras concretizações, o aparelho inclui ainda um microdispositivo relógio que é diferente do microdispositivo de sondagem e do microdispositivo de detecção; e o tipo de relógio do microdispositivo é colocado a uma distância fixa antes dos microdispositivos de detecção e sondagem, e detectando microdispositivos com um sinal distintivo quando um material biológico passa e atua como um dispositivo relógio.
[00109] Ainda em algumas formas de realização, os dados registrados pelo microdispositivo de detecção são filtrados através de uma tecnologia de fase lock-in para eliminar o ruído não sincronizado com o sinal de relógio, e melhorar a relação sinal-ruído e, portanto, a sensibilidade da medição.
[00110] Um outro aspecto da presente invenção diz respeito a métodos para detectar doença de um material biológico, envolvendo o fornecimento de um aparelho que compreende um canal, uma sonda de detecção, um dispositivo de formação de imagem, um componente de armazenamento de memória, um componente de sinal de transmissão, ou um componente de processamento lógico, pré-processando o material biológico a fim de aumentar a sua concentração, medindo as propriedades do material biológico, opcionalmente, contactar o material biológico com o sonda de detecção através do canal para originar um sinal de resposta, utilizando a sonda de detecção para detectar o sinal de resposta do material biológico, opcionalmente separando o material biológico com doença dos materiais biológicos saudáveis, com base no sinal de resposta, opcionalmente enviando o material biológico, separado, suspeito de doença para novos testes, e analisando o sinal de resposta chegando a uma conclusão de diagnóstico. O material biológico pode ser DNA, uma subestrutura em uma célula, uma célula, ou uma proteína.
[00111] Em algumas formas de realização, os métodos da presente invenção também incluem a detecção do sinal de resposta e os comportamentos de interação ou eventos ocorridos entre pelo menos dois materiais biológicos, ou pelo menos entre um material biológico com pelo menos um material não biológico. Pelo menos dois materiais biológicos podem ser diferentes ou iguais, em tipo de composição. Exemplos de interações ou acontecimentos ocorridos entre pelo menos dois objetos biológicas incluem, mas não estão limitados a, um DNA colidindo com outro DNA, uma célula colidindo com outra célula, um DNA colidindo com uma célula, uma proteína colidindo com uma outra proteína, ou um DNA colidindo com uma proteína. Exemplos de interações ou acontecimentos ocorridos entre, pelo menos, um material biológico e pelo menos um material não biológico incluem, mas não se limitando a, uma partícula inorgânica colidindo com um material biológico, uma partícula biológica que colide com um material biológico, ou uma partícula de compósito colidindo com um material biológico.
[00112] Os exemplos dos sinais de resposta incluem, mas não estão limitados a, um sinal elétrico, magnético, eletromagnético, térmico, óptico, acústico, biológico, químico, eletromecânico, eletroquímico, eletroquímico- mecânico, bioquímico, bioquímico-físico, biomecânico, bioeletromecânico, bioeletroquímico, bioeletromecânico-químico, físico e mecânico
[00113] Outro aspeto da presente invenção diz respeito a métodos para detectar doenças de um material biológico. Os métodos incluem o fornecimento de um aparelho que compreende uma unidade de pré- tratamento, pelo menos um dispositivo de detecção, uma câmara dividida com canais de ligação entre si, e um dispositivo de injeção (por exemplo, para injeção de uma sonda no material biológico a ser testado), e medição de sinais de resposta do material biológico, em que o material da sonda compreende uma partícula orgânica, uma partícula inorgânica, um material biológico, ou um objeto baseado em compósitos.
[00114] Ainda um outro aspecto da presente invenção diz respeito a métodos para detectar uma doença em um material biológico através da interação com um objeto de teste, que envolve o fornecimento de um aparelho que compreende uma câmara de lançamento, uma unidade de detecção, e canais, lançando uma sonda na direção do material biológico, fazendo com que uma colisão entre a sonda e o material biológico dê origem a um sinal de resposta, gravando e detectando o sinal de resposta durante e após a colisão. O objeto de sonda pode compreender uma partícula orgânica, uma partícula inorgânica, um material biológico, ou um objeto com base em compósito.
[00115] Ainda um outro aspecto da presente invenção diz respeito a métodos para detectar uma doença de um material biológico na sua fase inicial. Estes métodos incluem os passos de coleta de uma primeira amostra (incluindo uma célula ou uma molécula biológica) de tecido do material biológico, ou de órgãos, potencialmente portadores da doença, a coleta de uma segunda amostra do mesmo tecido ou órgão de um segundo indivíduo livre da doença, separadamente contactar primeira e segunda amostras, usando um aparelho de detecção de doença da presente invenção, e comparando os dados das medições das primeira e segunda amostras. Conforme mencionado acima, um aparelho de detecção de doença da presente invenção inclui um microdispositivo e um substrato de suporte do microdispositivo, em que o microdispositivo é capaz de medir o nível microscópico a propriedade elétrica, magnética, eletromagnética, térmica, óptica, acústica, biológica, química, física ou mecânica de uma amostra biológica.
[00116] Ainda um outro aspecto da presente invenção refere-se a um método de comunicação celular. O microdispositivo pode gerar cálcio microscópico artificial (e outros elementos) cujas oscilações estimulam as comunicações biológicas intracelulares. Este sinal artificial podem ser codificado para interagir com proteínas celulares, núcleos, e eventualmente regula a determinação e o destino da célula.
[00117] Ainda um outro aspecto da presente invenção diz respeito a métodos para a determinação da resposta celular ou molecular a um sinal. Os métodos incluem o passo de fazer contactar uma célula ou molécula biológica com um aparelho de detecção de doença da presente invenção, que inclui um primeiro microdispositivo, um segundo microdispositivo, e um primeiro substrato de suporte do primeiro e segundo microdispositivos. O primeiro microdispositivo no aparelho é capaz de medir, o nível microscópico, um sinal elétrico, magnético, eletromagnético, térmico, óptico, acústico, biológico, químico, eletromecânico, eletroquímico, eletroquímico-mecânico, bioquímico, biomecânico, bioeletromecânico, bioeletroquímico, bioeletroquímico-mecânico, físico ou mecânico da célula, e o segundo microdispositivo contacta com a célula ou molécula biológica e estimula-a com um sinal.
[00118] Em algumas formas de realização destes métodos, o aparelho compreende ainda um terceiro microdispositivo que é capaz de medir o nível microscópico a mesma propriedade elétrica, magnética, eletromagnética, térmica, óptica, acústica, biológica, química, eletromecânica, eletromecânico- química, bioquímica, biomecânica, bioeletromecânica, bioeletroquímica, bioeletroquímico-mecânica, física ou mecânica da célula ou molécula biológica tal como o primeiro a microdispositivo é capaz de fazer.
[00119] Em algumas outras formas de realização, a célula contacta com os primeiro, segundo e terceiro microdispositivos nessa ordem.
[00120] Em algumas formas de realização, o sinal é elétrico, magnético, eletromagnético, térmico, óptico, acústico, biológico, químico, eletromecânico, eletroquímico, eletroquímico-mecânico, bioquímico, biomecânico, bioeletromecânico, bioeletroquímico, bioeletroquímico- mecânico, físico ou mecânico.
[00121] Em algumas formas de realização do aparelho da presente invenção, o sistema de administração do material biológico inclui, pelo menos, um canal no interior do qual o material biológico a ser detectado percorre em uma determinada direção; o dispositivo de detecção e sondagem inclui pelo menos uma microdispositivo de sondagem e, pelo menos, um microdispositivo de detecção, em que pelo menos, o microdispositivo sondagem está localizado antes do microdispositivo de detecção em relação à direção à qual o material biológico percorre, e o microdispositivos de sondagem e detecção podem ser anexados ao interior ou exterior da parede do canal. Em algumas outras formas de realização, são utilizados canais múltiplos com diferentes geometrias.
[00122] Em alguns exemplos destas formas de realização, o dispositivo de detecção e sondagem inclui pelo menos dois dispositivos de detecção capazes de medir as micropropriedades iguais ou diferentes do material biológico. Exemplos das propriedades elétricas incluem, mas não estão limitados a, carga de superfície, potencial de superfície, potencial de repouso, corrente elétrica, distribuição do campo elétrico, dipolo elétrico, quádruplo elétrico, distribuição tridimensional da nuvem elétrica e/ou carga, propriedades elétricas no telômero de DNA e cromossomas, e impedância; exemplos das propriedades térmicas incluem a temperatura, frequência de vibração do material biológico e moléculas; exemplos das propriedades ópticas incluem a absorção óptica, transmissão óptica, reflexão óptica, propriedades óptico-elétricas, brilho, emissão fluorescente; exemplos das propriedades químicas incluem o valor de pH, reação química, reação bioquímica, bioeletroquímica, velocidade da reação, energia da reação, concentração de oxigênio, taxa de consumo de oxigênio, força iônica, comportamento catalítico, força da ligação; exemplos das propriedades acústicas incluem a frequência, velocidade das ondas acústicas, frequência e intensidade acústicas; distribuição de intensidade do espetro, intensidade acústica, absorção acústica e ressonância acústica; exemplos das propriedades físicas incluem a densidade e o tamanho geométrico; e exemplos de propriedades mecânicas incluem a pressão interna, dureza, resistência ao cisalhamento, força de alongamento, o stress de fratura, adesão, frequência de ressonância mecânica, elasticidade, plasticidade, e compressibilidade. Por exemplo, os microdispositivos de detecção são capazes de medir o nível microscópico a carga de superfície, o potencial elétrico, o brilho, a emissão fluorescente, o tamanho geométrico, forma, frequência, pressão interna, e a temperatura do material biológico.
[00123] Em algumas outras formas de realização, as formas e tamanhos de diferentes secções do canal podem ser as mesmas ou diferentes, a largura do canal pode ser cerca de 1 nm a 1 mm (por exemplo, 1-750 nm, 1600 nm; 100-800 nm, 200-750 nm, ou 400-650 nm), o canal pode ser reto, curvo, ou em ângulo, a parede interior do canal define um espaço circular, oval, ou poligonal (por exemplo, retangular).
[00124] Um exemplo de um canal adequado é um nanotubo circular em carbono, o qual pode ter um diâmetro de, por exemplo, cerca de 0,5 W- 100 nm, e um comprimento de, por exemplo, cerca de 5.0 nm-10 mm.
[00125] Em algumas formas de realização, a parede interior do canal tem pelo menos uma concavidade que pode estar na mesma secção que o microdispositivo de sondagem ou detecção. A ranhura côncava pode ser, por exemplo, um espaço cúbico ou um espaço angular. Ele pode ter uma profundidade de, por exemplo, cerca de 10 nm até 1 mm.
[00126] Em algumas outras formas de realização, um fluido de distribuição pode ser injetado no interior do canal, seja antes ou depois do material biológico passar por um microdispositivo de sondagem, o qual vai auxiliar a percorrer ou a separar o material biológico no interior do canal. O fluido de distribuição adequado é um líquido biocompatível ou solução, por exemplo, água ou solução salina. O fluido de distribuição pode ser injetado no interior do canal através de um canal de distribuição de fluido ligado a uma abertura na parede do canal. Utilizando tal fluido de distribuição permite, entre outros, a preparação da superfície do canal (na qual material biológico viaja), a limpeza do canal, a desinfecção do aparelho, e aumentando a sensibilidade de medição do aparelho.
[00127] Em ainda algumas outras concretizações, o aparelho da presente invenção pode ser para detectar as doenças em mais do que um material biológico, e o canal compreende um dispositivo localizado no seu interior para separar ou dividir os materiais biológicos com base em níveis diferentes de uma mesma propriedade dos mesmos. Um exemplo de um tal dispositivo de separação ou de divisão é uma fenda que pode, por exemplo, separar ou dividir materiais biológicos com base nas suas cargas superficiais, sua densidade, sua dimensão, ou outras propriedades, tais como sinais elétricos, térmicos, ópticos, químicos, físicos, magnéticos, eletromagnéticos e propriedades mecânicas. Exemplos das propriedades elétricas incluem, mas não estão limitadas a, carga de superfície, potencial de superfície, potencial de repouso, corrente elétrica, distribuição do campo elétrico, dipolo elétrico, quádruplo elétrico, distribuição tridimensional da nuvem elétrica e/ou carga, propriedades elétricas no telômero de DNA e de cromossomas, e impedância; exemplos das propriedades térmicas incluem a temperatura, frequência de vibração do material biológico e moléculas; exemplos das propriedades ópticas incluem absorção óptica, transmissão óptica, reflexão óptica, propriedades óptico-elétricas, brilho, emissão fluorescente; exemplos das propriedades químicas incluem o valor do pH, força da reação química, reação bioquímica, reação bioeletroquímica, velocidade da reação, energia da reação, velocidade de reação, concentração de oxigênio, taxa de consumo de oxigênio, força iônica, comportamento catalítico e de ligação; exemplos das propriedades físicas incluem a densidade e o tamanho geométrico; exemplos das propriedades acústicas incluem frequência, velocidade das ondas acústicas, frequência acústica, distribuição do espectro de intensidade, intensidade acústica, absorção acústica, ressonância acústica; e exemplos de propriedades mecânicas incluem a pressão interna, dureza, resistência à fratura, força de alongamento, fratura por tensão, adesão, frequência de ressonância mecânica, elasticidade, plasticidade, e compressibilidade.
[00128] Em ainda algumas outras concretizações, o aparelho da presente invenção pode ainda incluir um dispositivo de filtragem para remover objetos irrelevantes ao material biológico para detecção
[00129] Em outro aspecto, a invenção proporciona métodos para a obtenção de informação dinâmica de um material biológico, compreendendo o contato de cada material biológico (por exemplo, incluindo, mas não se limitando a, uma célula, subestrutura de uma célula, tal como membrana celular, um DNA, um RNA, uma proteína ou um vírus), com um aparelho que compreende um primeiro microdispositivo, um segundo microdispositivo, e um primeiro substrato suportando o primeiro e segundo microdispositivos, em que o primeiro microdispositivo é capaz de medir o nível microscópico uma propriedade elétrica, magnética, eletromagnética, térmica, óptica, acústica, biológica, química, física ou mecânica do material biológico, e o segundo microdispositivo entra em contato com os materiais biológicos e estimula-os por meio de um sinal.
[00130] Ainda em outra concretização, o microdispositivo no aparelho de detecção pode comunicar com materiais biológicos tais como células, DNA, RNA, vírus, ou proteínas. Além disso, o microdispositivo pode captar, classificar, analisar, tratar e modificar materiais biológicos, tais como células, DNA, RNA, células do sangue, proteínas, e vírus. Especificamente, uma matriz de microdispositivos dispostos em uma forma desejada pode captar, classificar, detectar e modificar estruturas de DNA.
[00131] Em algumas formas de realização, o aparelho compreende ainda um terceiro microdispositivo que seja capaz de medir o nível microscópico a mesma propriedade elétrica, magnética, eletromagnética, térmica, óptica, acústica, biológica, química, bioquímica, física ou mecânica da célula, tal como o primeiro microdispositivo faz. Em algumas outras formas de realização, a célula contacta com o primeiro, segundo e terceiro microdispositivo nessa ordem. Em ainda algumas outras concretizações, o sinal é um sinal elétrico, um sinal magnético, eletromagnético, térmico, óptico, acústico, biológico, químico, físico, ou mecânico. elétrico.
[00132] Em outro aspecto, esta invenção proporciona métodos alternativos para detectar uma informação dinâmica do material biológico. Cada método inclui um aparelho que compreende um microdispositivo relógio, um microdispositivo de sondagem, e um primeiro microdispositivo de detecção, em que o microdispositivo de sondagem está colocado entre o microdispositivo relógio e o microdispositivo de detecção; contactando o material biológico com o relógio do dispositivo em que o relógio do microdispositivo registra a chegada do material biológico, e opcionalmente mede uma propriedade do material biológico no nível microscópico; contactando o material biológico com a sonda em que um sinal periódico da sonda é enviado ao material biológico; utilizando o microdispositivo de detecção para detectar o sinal de resposta do material biológico; e processando o sinal detectado pelo microdispositivo de detecção usando a tecnologia de fase lock-in para filtrar componentes do sinal que não estão sincronizados com a frequência do sinal da sonda, e amplificando o sinal sincronizado com o sinal da sonda.
[00133] Em algumas formas de realização destes métodos, há uma distância de pelo menos 10 angstroms entre o relógio do microdispositivo e o primeiro microdispositivo de detecção.
[00134] Em algumas outras realizações, o sinal de resposta é um sinal elétrico, magnético, eletromagnético, térmico, óptico acústico, biológico, químico, eletromecânico, eletroquímico, eletroquímico-mecânico, bioquímico, biomecânico, eletrobiomecânico, bioeletroquímico, bioeletroquímico-mecânico, físico ou mecânico.
[00135] Em algumas outras concretizações, o primeiro microdispositivo de sondagem, opcionalmente mede a mesma propriedade do material biológico o nível microscópico que o primeiro microdispositivo de detecção.
[00136] Em ainda algumas outras concretizações, o aparelho utilizado nos métodos compreende ainda um segundo microdispositivo de sondagem capaz de enviar um sinal estimulante para o material biológico, que é diferente do sinal enviado pelo primeiro microdispositivo de sondagem.
[00137] Em ainda algumas outras concretizações, o aparelho utilizado nos métodos compreende ainda um segundo microdispositivo de detecção capaz de medir a mesma propriedade do material biológico o nível microscópico que o primeiro microdispositivo de detecção.
[00138] Em ainda algumas outras modalidades, a propriedade elétrica é a carga de superfície, o potencial de superfície, potencial de repouso, corrente elétrica, distribuição de campo elétrico, dipolo elétrico, quádruplo elétrico, distribuição tridimensional da nuvem elétrica ou carga, propriedades elétricas em telômeros do DNA e cromossomas, ou impedância; a propriedade térmica é a temperatura, frequência vibracional do material biológico ou molécula; a propriedade óptica é a absorção óptica, transmissão óptica, reflexão óptica, propriedade óptica-elétrica, brilho ou emissão fluorescente; a propriedade química é o valor de pH, reação química, reação bioquímica, reação bioeletroquímica, velocidade da reação, energia da reação, concentração de oxigênio, taxa de consumo de oxigênio, força iônica, comportamento catalítico, força de ligação; a propriedade física é a densidade e o tamanho geométrico; a propriedade acústica é a velocidade de frequência de ondas acústicas, frequência acústica e a distribuição do espectro de intensidade, intensidade acústica, absorção acústica, ressonância acústica; e a propriedade mecânica é a pressão interna, dureza, resistência ao cisalhamento, força de alongamento, tensão de ruptura, aderência, frequência de ressonância mecânica, elasticidade, plasticidade, e compressibilidade.
[00139] Em algumas concretizações, os dados registrados pelo primeiro microdispositivo de detecção são filtrados usando uma tecnologia de fase lock-in para eliminar o ruído não sincronizado com os dados gravados pelo primeiro microdispositivo de sondagem ou com o microdispositivo relógio. Os dados filtrados podem ter uma maior relação sinal-ruído.
[00140] Outro aspeto inovador da presente invenção é a obtenção de dados em tempo real e informação ao nível da estrutura celular, tal como a utilização de um microcomparador de tensão, sonda de quatro pontos e outros esquemas de circuitos para medir a superfície da célula e propriedades elétricas brutas, incluindo o potencial de repouso e a carga superficial para diferenciar células normais de células cancerosas. A diferenciação da carga das células de superfície pode ser um fator importante para decidir o status saudável ou não de uma célula e, consequentemente, o tratamento adequado da mesma.
[00141] Por exemplo, para uma rápida abordagem a fim de obter informação dinâmica sobre um material biológico (por exemplo, uma célula, uma subestrutura de uma célula, uma molécula de DNA ou RNA, ou um vírus), é utilizado um primeiro microdispositivo para enviar um sinal que perturba o material biológico a ser diagnosticado e, em seguida, um segundo microdispositivo é utilizado para medir com precisão a resposta do material biológico. em uma disposição, o primeiro microdispositivo e o segundo dispositivo estão posicionados a uma distância desejada L, enquanto que material biológico a ser medido flui desde o primeiro microdispositivo para o segundo microdispositivo. Quando a amostra biológica passa, o primeiro microdispositivo, o microdispositivo envia um sinal para a amostra biológica em trânsito, em seguida, o segundo microdispositivo detecta a resposta ou a retenção do sinal de perturbação na entidade. A partir da distância entre os dois microdispositivos, intervalo de tempo, a natureza da perturbação pelo primeiro microdispositivo, e alterações medidas sobre o material biológico durante o tempo trânsito, podem ser medidas as propriedades microscópicas e dinâmicas do material biológico e podem ser obtidos os dados. em uma outra disposição, o primeiro microdispositivo é utilizado para sondar o material biológico, primeiro através da aplicação de um sinal (tal como uma carga) e, em seguida, detectar a resposta do material biológico usando um segundo microdispositivo como uma função do tempo.
[00142] Outra área inovadora desta aplicação é a invenção de microssondas de recuo e microssondas para medir uma variedade de propriedades físicas (como as propriedades mecânicas) dos materiais biológicos. Exemplos de tais propriedades físicas incluem, mas não se limitam a, dureza, resistência ao cisalhamento, força de alongamento, tensão de ruptura, e as propriedades relacionadas com as membranas celulares, pois que as membranas podem representar um componente crítico no diagnóstico de doenças.
[00143] Ainda um outro aspecto desta invenção é a concepção do fabrico e a integração dos diferentes componentes no aparelho de detecção de doenças. Esses componentes incluem, por exemplo, uma unidade de contenção e administração da amostra; uma variedade de canais de distribuição da amostra, uma unidade central de detecção da doença que compreende várias sondas de detecção, uma unidade central de controle que compreende uma unidade de processamento lógico, uma unidade de memória, um sensor, um transmissor de sinais, um receptor de sinais e um chip de aplicação específica; e uma unidade de tratamento de resíduos em que a amostra utilizada pode ser tratada, reciclada, transformada para reutilização ou eliminada.
[00144] Outro aspecto inovador do aplicativo atual é o design, integração e fluxo de processo de fabricação de microdispositivos capazes de fazerem medições altamente sensíveis e avançadas de sinais muito fracos em sistemas biológicos para detecção de doenças em ambiente complicado em que os sinais são muito fracos, e o ruído de fundo relativamente elevado. Essas capacidades inovadoras que utilizam a classe de microdispositivos revelados na presente invenção para detectar doenças, por exemplo, fazem medições dinâmicas, medições em tempo real (por exemplo, o tempo de voo das medições, e combinando os sinais de resposta da sonda de detecção), técnica da fase lock-in para reduzir o ruído de fundo, e as sondas de 4 pontos para medirem sinais muito fracos, bem como sondas únicas e inovadoras para medir vários sinais eletromagnético, eletrônico e as propriedades magnéticas das amostras biológicas de uma única célula, material biológico (por exemplo, vírus) ou molécula (por exemplo, DNA ou RNA).
[00145] Finalmente, um outro aspecto da presente invenção refere-se a um aparelho para detectar doenças em um material biológico. O aparelho inclui um dispositivo de detecção fabricado por um método que compreende: fornecer um substrato; sequencialmente depositar um primeiro material e um segundo material em duas camadas sobre o substrato para formar uma pilha de material; padronizar o segundo material por meio de processos microeletrônicos para formar uma primeira característica desejada ; deposição de um terceiro material sobre a pilha de material a fim de cobrir o segundo material; opcionalmente, padronização do primeiro e o terceiro materiais através de processos microeletrônicos a fim de formar uma segunda característica desejada; e, opcionalmente, a deposição de um quarto material sobre a pilha de material. O primeiro e terceiro materiais podem ser os mesmos ou diferentes. O dispositivo de detecção é capaz de sondar um material biológico a ser detectado, e dando origem a um sinal de resposta.
[00146] Em algumas formas de realização, o método de fabricação compreende ainda o capeamento da parte superior da pilha de material, de modo a formar rasgo encerrado.
[00147] Em algumas outras formas de realização, o capeamento compreende a selagem ou capeamento do topo da pilha de material com um dispositivo de formação de imagem sobre a pilha de material.
[00148] Em ainda algumas outras concretizações, o aparelho inclui ainda uma unidade de pré-processamento (câmaras) para a pré-triagem e melhorando um material biológico com doença para testes adicionais, os canais para o transporte de amostras fluidas, as sondas para sondar e perturbar o material biológico a ser testado, a fim de gerar sinais de resposta, as sondas de detecção para a medição das propriedades e sinais de resposta do material biológico, e um dispositivo de formação de imagem para observar e registrar as propriedades e comportamentos do material biológico.
[00149] Em ainda algumas outras concretizações, o dispositivo de detecção tem dimensões típicas de canais em forma de quadrado que variam entre 2 mícrons x 2 mícrons até cerca de 100 mícrons x 100 mícrons em área de secção transversal, e um raio que varia entre cerca de 1 mícron a cerca de 20 mícrons em área de secção transversal de um canal circular; uma dimensão típica da sonda em forma de quadrado varia de cerca de 0,5 mícrons x 0,5 mícrons a cerca de 20 mícrons x 20 mícrons em área seccional transversal. Em alternativa, o dispositivo de detecção em um canal em forma de quadrado tem dimensões típicas de cerca de 6 x 6 mícrons a cerca de 14 mícrons x 14 mícrons de área de secção transversal, um raio que varia de cerca de 3 mícrons e cerca de 8 mícrons de área de secção transversal (canal circular) e uma dimensão de sonda típica em forma de quadrado entre 0,5 mícrons x 0,5 mícrons a cerca de 10 mícrons x 10 mícrons de área de secção transversal.
[00150] Em ainda algumas formas de realização, o primeiro e o quarto materiais compreendem, óxido não dopado (Si02), óxido dopado, nitreto de silício, um material polimérico, vidro ou um material eletricamente isolante; e os segundo e terceiros materiais compreendem um material condutor elétrico, alumínio, uma liga de alumínio, cobre, liga de cobre, tungstênio, uma liga de tungstênio, ouro, liga de ouro, prata, uma liga de prata, um material óptico, um material sensível térmico, um material magnético, um material sensível à pressão, um material sensível ao stress mecânico, um material sensível à emissão de íons, e um material piezoelétrico.
[00151] Em ainda algumas outras concretizações, os segundo e quartos materiais podem ser fabricados no mesmo nível como detectores, ou como sondas e detectores, o primeiro e o terceiro materiais compreendem, óxido não dopado (SiO2), óxido dopado, nitreto de silício, um material polimérico, vidro ou um material eletricamente isolante, os segundo e quartos e materiais compreendem um material eletricamente condutor (por exemplo, alumínio, ligas de alumínio, cobre, liga de cobre, tungstênio, uma liga de tungstênio, ouro, liga de ouro, prata, ou uma liga de prata), um material óptico (por exemplo, material óptico anisotrópico, vidro, vidro-cerâmica, meios de laser, material óptico não linear, fósforo e cintilador, material transparente), um material térmico sensível, um material magnético, um material sensível à pressão, um material sensível ao stress mecânico, um material sensível à emissão de íons, e um material piezoelétrico (por exemplo, quartzo, berlinita, gálio, ortofosfato GaPO4, turmalina, cerâmica, bário, titanato, BaTiO3, zirconato de chumbo, titanato de PZT, óxido de zinco, nitreto de alumínio, e um fluoreto de polivinilideno).
[00152] Noutras formas de realização, o dispositivo de detecção compreende pelo menos uma sonda, um detector, uma sonda e sensor em que a sonda gera um sinal perturbador para o material biológico para este emitir um sinal de resposta, e em que o detector mede a sinal de resposta assim produzido.
[00153] Tal como aqui utilizado, o termo “ou” pretende-se incluir tanto “e” e “ou”. Pode ser intercambiado com “e/ou”
[00154] Tal como aqui utilizado, um substantivo singular é destinado a incluir o seu significado no plural. Por exemplo, um microdispositivo pode significar quer um único microdispositivo quer vários microdispositivos.
[00155] Como usado aqui, o “padronização” significa moldar um material em uma determinada forma física ou padrão, incluindo um plano (em cujo caso “padronização” também significa “planarização”)
[00156] Como aqui utilizado, o termo “um material biológico “ou” uma amostra biológica “para a análise ou teste ou diagnóstico refere-se ao objeto a ser analisado por um aparelho de detecção de doenças. Ele pode ser uma célula única, um única entidade biológica molecular (por exemplo, DNA, RNA e proteínas), um simples material biológico (por exemplo, uma única célula ou um vírus), e qualquer outra unidade suficientemente pequena com composição biológica fundamental, ou uma amostra de órgão de um tecido que possa apresentar uma doença ou distúrbio.
[00157] Como aqui utilizado, o termo “doença” é intermutável com “desordem” e refere-se geralmente a qualquer propriedade anormal microscópica ou condição (por exemplo, uma condição física) de um material biológico (por exemplo, um mamífero ou espécie biológica).
[00158] Como aqui utilizado, o termo “indivíduo” refere-se geralmente a um mamífero, ou seja, um ser humano
[00159] Como usado aqui, o “nível microscópico” refere-se ao objeto a ser analisado pelo aparelho de detecção de doenças da presente invenção, sendo de natureza microscópica e pode ser uma única célula, um única entidade molecular biológica (por exemplo, DNA, RNA e proteínas), um único material biológico (por exemplo, um única célula ou um vírus), e outra unidade suficientemente pequena, ou uma composição biológica fundamental.
[00160] Tal como aqui utilizado, um “microdispositivo” ou “ microdispositivo “ pode ser qualquer um de uma grande variedade de materiais, propriedades, formas e grau de complexidade e integração. O termo tem um significado geral para uma aplicação de um único material para um dispositivo muito complexo que compreende vários materiais com múltiplas sub unidades e funções. A complexidade contemplada na presente invenção varia entre uma única pequena partícula, até um conjunto de propriedades desejadas para uma unidade relativamente complicada, integrada com diversas unidades funcionais nele contidos. Por exemplo, um simples microdispositivo podia ser um único artigo esférico com um diâmetro tão pequeno quanto 100 angstroms, com uma dureza desejada, uma carga de superfície desejada, ou um químico orgânico desejado absorvido na sua superfície. Um dispositivo mais complexo pode ser um microdispositivo de 1milímetro com um sensor, uma calculadora simples, uma unidade de memória, uma unidade lógica, e um cortador, tudo integrado nele. No primeiro caso, as partículas podem ser formadas através de um processo de precipitação coloidal pirogenada, enquanto que o dispositivo com vários componentes integrados pode ser fabricado usando vários processos de fabricação integrada de circuitos.
[00161] Os microdispositivos utilizados na presente invenção podem variar em tamanho (por exemplo, diâmetro) desde cerca de 1 angstrom até cerca de 5 milímetros. Por exemplo, um microdispositivo variando em tamanho na ordem de cerca de 10 angstroms até 100 mícrons pode ser usado no presente invento para direcionar moléculas biológicas, entidades ou composições de pequenas dimensões, tais como as estruturas celulares, DNA, e bactérias. E, um microdispositivo variando em tamanho entre cerca de 1 até cerca de 5 milímetros pode ser utilizado na presente invenção para alvejar materiais biológicos relativamente grandes, tais como uma parte de um órgão humano. Como um exemplo, um simples microdispositivo definido no presente pedido de patente pode ser uma única partícula com um diâmetro inferior a 100 angstroms, com propriedades de superfície desejadas (por exemplo, com a carga de superfície ou um revestimento químico) para uma absorção ou adsorção preferencial em um tipo de célula alvo.
[00162] A presente invenção proporciona ainda um aparelho para detectar uma doença em um material biológico, que compreende uma unidade de pré-processamento, uma unidade de sondagem e detecção, uma unidade de processamento de sinais, e uma unidade de processamento de resíduos.
[00163] Em algumas formas de realização do aparelho, a unidade de pré-processamento inclui uma unidade de filtração da amostra, uma unidade de recarga, uma unidade de fornecimento de pressão constante, e uma unidade de pré-sondagem perturbadora. Isto aumenta a proporção de contração de certas substâncias com interesse (tais como as células cancerosas) e, portanto, torna o aparelho mais eficaz e eficiente para a detecção do objeto alvo biológico (tal como as células cancerosas).
[00164] Em algumas formas de realização, a unidade de filtragem pode filtrar uma substância indesejada através filtração física (ou seja, com base na carga eletrônica ou tamanho da substância), ou via separação por reação química (e assim remover completamente as substâncias indesejáveis), reação bioquímica, reação eletromecânica, reação eletroquímica, ou reação biológica.
[00165] Em algumas formas de realização, a unidade de filtração da amostra pode incluir um canal de entrada, um canal de fluido perturbador, uma câmara de aceleração, e uma fenda. A fenda e as paredes interiores do canal de entrada definem dois canais (ou seja, um canal superior e um canal inferior) em que o material biológico pode ser separado devido às diferenças nas sua propriedades (por exemplo, propriedade elétricas ou físicas).
[00166] Em algumas concretizações, um fluido biocompatível pode ser injetado no canal de fluido perturbador para separar o material biológico. Por exemplo, o fluido biocompatível pode ser injetado a partir da entrada do canal de fluido perturbador e passar por uma abertura na parede do canal de entrada. O fluido biocompatível pode ser líquido ou semilíquido, e pode incluir água, solução salina, plasma, um líquido rico em oxigênio, ou qualquer combinação dos mesmos.
[00167] Em algumas outras formas de realização, o ângulo entre o canal de entrada e as fronteiras do canal do fluido perturbador varia entre cerca de 0° a cerca de 180° (por exemplo, a partir de cerca de 30 ° até cerca de 150°, a partir de cerca de 60 ° até cerca de 120°, ou a partir de cerca de 75° a cerca de 105 °, ou cerca de 90)
[00168] Em algumas outras formas de realização, a largura de cada canal pode variar de cerca de 1 nm a cerca de 1 mm (por exemplo, desde cerca de 2 nm até cerca de 0,6 mm ou cerca de 10 nm a cerca de 0,2 mm.
[00169] Em algumas outras formas de realização, pelo menos um dos canais compreende um dispositivo de sondagem ligado à parede lateral do canal, e o dispositivo de sondagem é capaz de medir o nível microscópico, uma propriedade ou sinal elétrico, magnético, eletromagnético, térmico, óptico, acústico, biológico, químico, eletromecânico, eletroquímico, eletroquímico-mecânico, bioquímico, biomecânico, bioeletromecânico, bioeletroquímico, bioeletroquímico-mecânico, físico e/o mecânico do material biológico. Exemplos da propriedade elétrica incluem a taxa de superfície, potencial de superfície, potencial de repouso, corrente elétrica e distribuição, dipolo elétrico, elétrico quadripolo elétrico, distribuição da nuvem tridimensional elétrica ou carga, propriedades elétricas em telômeros do DNA e cromossomas, e impedância. Exemplos de propriedades térmicas incluem a temperatura e frequência de vibração. Exemplos de propriedade ópticas incluem a absorção óptica, transmissão óptica, reflexão óptica, propriedade optico-elétrica, brilho e emissão fluorescente. Exemplos da propriedade química incluir o valor do pH, reação química, biorreação química, reação bioeletroquímica, velocidade da reação, energia da reação, velocidade de reação, concentração de oxigênio, taxa de consumo de oxigênio, força iônica, comportamento catalítico, resistência e aderência. Exemplos de propriedades físicas incluem a densidade e o tamanho geométrico. Exemplos de propriedades acústicas incluem a frequência, velocidade de ondas acústicas, intensidade acústica, distribuição do espectro de intensidade, absorção acústica e ressonância acústica. Exemplos de propriedades mecânicas incluem a pressão interna, dureza, resistência ao cisalhamento, força de alongamento, tensão de ruptura, adesão, frequência de ressonância mecânica, elasticidade, plasticidade e compressibilidade.
[00170] Em algumas formas de realização, pelo menos um dos canais compreende dois dispositivos de sondagem ligados às paredes laterais do canal, e os dispositivos de sondagem sendo capazes de medir o nível microscópico propriedade ou sinal elétrico, magnético, eletromagnético, térmico, óptico, acústico, químico, biológico, eletromecânico, eletroquímico, eletroquímico-mecânico, bioquímico, biomecânico, bioeletromecânico, bioeletroquímico, bioeletroquímico-mecânico, e as propriedades físicas e mecânicas do material biológico. Os dispositivos de sondagem medem propriedades iguais ou diferentes, ao mesmo tempo ou em tempos diferentes.
[00171] Os dois ou mais dispositivos de sondagem podem ser colocados a uma distância desejada entre si (de pelo menos 10 angstroms). Exemplos da distância desejada são desde 10 nm a cerca de 100 mm, desde 100 nm a cerca de 10 mm, desde 1 mm a cerca de 10 mm.
[00172] Em algumas formas de realização, a unidade de filtração da amostra pode incluir um canal de entrada, um filtro biocompatível, um canal de saída, ou qualquer combinação dos mesmos. Quando um material biológico passa através do canal de entrada para o canal de saída, um material biológico que apresente tamanho superior ao do orifício do filtro será bloqueado contra o canal de saída, e esse material biológico será lavado ao canal de saída. Um fluido biocompatível é injetado a partir da saída para transportar o material biológico acumulado à volta do filtro e lavar o canal. O material biológico com um tamanho grande é então filtrado para posterior análise e detecção no componente ou unidade de detecção do aparelho.
[00173] Em algumas formas de realização, a unidade de pré-sondagem perturbadora pode incluir um microdispositivo com um canal, uma fenda localizada no interior do canal, e, opcionalmente, duas placas fora do canal. As duas placas podem aplicar um sinal, por exemplo, uma tensão eletrônica, para o material biológico que percorre através do canal, e separá-lo, com base na carga eletrônica que o material biológico transporta. A fenda e os canais interiores do canal definem dois canais, onde os materiais biológicos separadas entram e, opcionalmente, são detectadas as suas propriedades ao nível microscópico.
[00174] Em algumas formas de realização, a unidade de pré-sondagem perturbadora aplica ao objeto uma sinal biológico, elétrico, magnético, eletromagnético, térmico, óptico, acústico, químico, eletromecânico, eletroquímico, eletroquímico-mecânico, biomecânico, bioeletromecânico, bioeletroquímico, bioeletroquímico-mecânico, físico ou mecânico. O sinal pode ser aplicado, por exemplo, com as duas placas descritos acima ou por outros meios (dependendo da natureza do sinal). O sinal aplicado como pode ser pulsado ou constante
[00175] Em algumas formas de realização, a unidade de recarga recarrega nutrientes ou gás respirador (tal como oxigênio) para o material biológico. Alternativamente, também pode limpar metabolitos do material biológico. Com uma tal unidade de carregamento, a estabilidade de vida do material biológico na amostra é mantida e o seu uso é estendido, dando assim resultados de detecção mais precisos e confiáveis. Exemplos de nutrientes incluem eletrólitos biocompatíveis fortes ou fracos, aminoácidos, minerais, íons, oxigênio, líquidos ricos em oxigênio, gotejamento intravenoso, glicose e proteínas. Outro exemplo de nutrientes é uma solução contendo nanopartículas que podem ser seletivamente absorvidas por certos materiais biológicos (por exemplo, células e vírus).
[00176] O sistema de recarga pode ser separado a partir de fora dos outros componentes do aparelho. Alternativamente, também pode ser instalado no interior de um dos outros componentes, por exemplo, na unidade de sondagem de detecção ou na unidade de processamento de resíduos.
[00177] Em algumas outras formas de realização, a unidade de processamento do sinal compreende um amplificador (por exemplo, um amplificador lock-in), um AID (corrente elétrica alternada/direta ou analógico para digital), conversor, um microcomputador, um manipulador, um visor e conexões de rede.
[00178] Em alguns exemplos, a unidade de processamento de sinais coleta mais de um sinal (isto é, múltiplos sinais), e os múltiplos sinais podem ser integrados para cancelar o ruído ou para melhorar a relação sinal-ruído. Os vários sinais podem ser sinais de vários locais ou de vários tempos.
[00179] Os materiais biológicos que podem ser detectados pelo aparelho incluem, por exemplo, sangue, urina, saliva, lágrimas, e suor. Os resultados de detecção podem indicar a possível ocorrência, ou presença, de um doença (por exemplo, uma doença na sua fase inicial) no material biológico.
[00180] Como usado aqui, o termo “absorção” geralmente significa uma ligação física entre a superfície e o material ligado a ela (absorvida sobre ela, neste caso). Por outro lado, o termo “adsorção”, significa, geralmente, uma ligação mais forte, química entre os dois. Estas propriedades são de grande importância para a presente invenção uma vez que podem ser eficazmente utilizadas para a ligação seletiva aos alvos, através de microdispositivos que operam ao nível microscópico.
[00181] Como utilizado aqui, o termo “contato” (como em “o primeiro microdispositivo contacta com uma entidade biológica”) destina-se a incluir o contato “direto” (ou físico) e o “não direto” (ou indireto ou não físico). Quando dois indivíduos estão em contato “direto”, geralmente não há espaço mensurável ou uma distância entre os pontos de contato dos dois objetos; quando se encontram em contato “indireto”, existe um espaço mensurável ou uma distância entre os pontos de contato dos dois objetos
[00182] Como usado aqui, o termo “sonda” ou “sondagem”, para além do seu significado de dicionário, pode significar a aplicação de um sinal (por exemplo, sinais elétricos, acústicos, magnéticos ou térmicos) a um objeto, e assim estimulando o objeto e fazendo com que tenha algum tipo de resposta intrínseca.
[00183] Como aqui utilizado, o termo “propriedade elétrica” refere-se à carga de superfície, potencial de superfície, campo elétrico, a distribuição de carga, distribuição do campo elétrico, potencial de repouso, potencial de ação, ou impedância de um material biológico a ser analisado.
[00184] Como aqui utilizado, o termo “propriedade magnética” refere- se a diamagnético, paramagnético ou ferromagnético.
[00185] Como aqui utilizado, o termo “propriedade eletromagnética” refere-se à propriedade que tem tanto dimensões elétricas como magnéticas.
[00186] Tal como aqui utilizado, o termo “propriedade térmica” refere- se à temperatura, ponto de congelamento, ponto de fusão, temperatura de evaporação, temperatura de transição do vidro, e condutividade térmica.
[00187] Tal como aqui utilizado, o termo “propriedade óptica” refere- se à reflexão, absorção óptica, espalhamento óptico, propriedades dependentes do comprimento de onda, cor, brilho, brilho, cintilações, e dispersão
[00188] Tal como aqui utilizado, o termo “propriedade acústica” refere-se às características encontradas dentro de uma estrutura que determinam a qualidade de som na sua relevância para ser ouvido. Pode geralmente ser medido pelo coeficiente de absorção acústico. Ver, por exemplo., Patente dos Estados Unidos N° 3.915.016, meios e métodos para a determinação de uma propriedade de um material acústico; TJ Cox et al., Acoustic Absorbers and Diffusers, 2004, Span Press
[00189] Tal como usado aqui, o termo “propriedade biológica” pretende incluir as propriedades químicas e físicas de um material biológico.
[00190] Tal como aqui utilizado, o termo “propriedade química” refere-se ao valor de pH, força iônica, ou força de ligação dentro da amostra biológica
[00191] Tal como aqui utilizado, o termo “propriedade física” refere-se a qualquer propriedade mensurável, cujo valor descreve um sistema físico, em qualquer dado momento no tempo. As propriedades físicas de uma amostra biológica podem incluir, mas não estão limitadas a absorção, albedo, área, fragilidade, ponto de ebulição, capacitância, cor, concentração, densidade, carga dielétrica, carga elétrica, condutividade elétrica, impedância elétrica, campo elétrico, potencial elétrico, emissão, taxa de fluxo, fluidez, frequência, indutância, impedância intrínseca, intensidade, irradiação, luminância, brilho, impedância, maleabilidade, campo magnético, fluxo magnético, massa, ponto de fusão, momento, permeabilidade, permissividade, tensão, luminosidade, solubilidade, calor específico, força, temperatura, tensão, condutividade térmica, velocidade, viscosidade, volume, e impedância da onda.
[00192] Tal como aqui utilizado, o termo “propriedade mecânica” designa a força, dureza, elasticidade, plasticidade, fragilidade, ductilidade, força de cisalhamento, força de alongamento, stress, fratura e aderência da amostra biológica
[00193] Como usado aqui, o termo “material condutor” (ou o seu equivalente “condutor elétrico”) é um material que contém cargas elétricas móveis. Um material condutor pode ser um metal (por exemplo, cobre, prata, ou ouro) ou não metálico (por exemplo, grafite, soluções de sais, plasmas, ou polímeros condutores). Nos condutores metálicos, tais como o cobre ou alumínio, as partículas móveis carregadas são elétrons (ver condução elétrica). As cargas positivas poderão também ser móveis sob a forma de uma treliça de átomos em que estão ausentes elétrons (conhecidos como orifícios), ou sob a forma de íons, tais como nos eletrólitos de uma bateria.
[00194] Tal como aqui utilizado, o termo “material de isolamento elétrico” (também conhecido como “isolador” ou “dielétrico”) refere-se a um material que resiste ao fluxo de corrente elétrica. Um material isolante tem átomos com elétrons de valência fortemente ligados. Exemplos de materiais isolantes eletricamente incluem o vidro, polímeros orgânicos (por exemplo, borracha, plástico, e o Teflon).
[00195] Tal como aqui utilizado, o termo “semicondutor” (também conhecido como “material semicondutor”) refere-se a um material com uma condutividade elétrica devido ao fluxo de elétrons (por oposição à condutividade iônica) intermédia em magnitude entre um condutor e um isolante. Exemplos de semicondutores inorgânicos incluem o silício, materiais baseados em silício e germânio. Exemplos de semicondutores orgânicos incluem hidrocarbonetos aromáticos tais como o compostos aromáticos policíclicos, pentaceno, antraceno, e rubreno; e semicondutores orgânicos poliméricos, tais como o poli (3-hexiltiofeno), poli (p-fenileno-vinileno), poliacetileno e seus derivados. Materiais semicondutores podem ser sólidos cristalinos (por exemplo, silício), amorfos (por exemplo, silício amorfo hidrogenado e misturas de arsênio, selênio e telúrio, em uma variedade de proporções), ou mesmo líquidos.
[00196] Tal como usado aqui, o termo “material biológico” tem o mesmo significado de “biomaterial”, como entendido por um perito na arte. Sem limitar o seu significado, os materiais biológicos ou biomateriais geralmente podem ser produzidos quer na natureza ou sintetizados em laboratório, utilizando uma variedade de abordagens químicas, utilizando compostos orgânicos (por exemplo, pequenas moléculas orgânicas ou polímeros) ou compostos orgânicos (por exemplo, componentes metálicos ou cerâmicos). Em geral, podem ser utilizados e/ou adaptados para uma aplicação médica, e, portanto, compreendem todo ou parte de uma estrutura ou dispositivo biomédico que realiza, aumenta, ou substitui uma função natural. Essas funções podem ser benignas, como as utilizadas para uma válvula cardíaca, ou podem ser bioativas com uma funcionalidade mais interativa, tais como os implantes de quadril revestidos por hidroxil-apatite. Os biomateriais também podem ser usados todos os dias em aplicações dentárias, cirurgia, e na administração de drogas. Por exemplo, pode ser colocada dentro do corpo uma construção com impregnados de produtos farmacêuticos, o que permite a liberação prolongada de um fármaco durante um período prolongado de tempo. Um biomaterial pode também ser um auto- enxerto, aloenxerto ou xenoenxerto, que pode ser utilizado como um material de transplante. Todos estes materiais que têm encontrado aplicações em outros campos médicos ou biomédicos, também podem ser utilizado na presente invenção.
[00197] Tal como aqui utilizado, o termo “processo ou tecnologia microeletrônica” geralmente inclui as tecnologias ou processos utilizados para a fabricação de componentes microeletrônicos e óptico-eletrônicos. Exemplos incluem a litografia, gravura (por exemplo, ataque químico a úmido, a seco ou ataque químico a vapor), oxidação, difusão, implantação, recozimento, deposição de película, limpeza, implantação direta, polimento, planarização (por exemplo, polimento mecânico-químico), crescimento epitaxial, metalização, integração de processos, simulação, ou quaisquer combinações destes. Podem ser encontrados descrições adicionais sobre tecnologias e processos microeletrônicos, em por exemplo, Jaeger, Introduction to Microeletronic Fabrication, 2a Ed., Prentice Hall, 2002; Ralph E. Williams, Modem GaAs Processing Methods, 2a Ed., Artech House, 1990; Robert F. Pierret, Advanced Semiconductor Fundamentals, 2a Ed., Prentice Hall, 2002; S. Campbell, The Science and Engineering of Microeletronic Fabrication, 2a Ed., Oxford University Press, 2001, cujos conteúdos estão aqui incorporados por referência na sua totalidade.
[00198] Tal como aqui utilizado, o termo “seletivo” tal como consta, por exemplo, “o material B padronizado usando um processo a de microeletrônica seletivo para o material A”, significa que o processo é eficaz na microeletrônica do material B, mas não sobre o material A, ou é substancialmente mais eficaz no material de B do que no material A (ou seja, do que resulta uma taxa muito mais elevada na remoção de material de B do que o material de A e removendo assim muito mais material B do que material A.
[00199] Tal como usado aqui, o termo “nanotubo de carbono” geralmente refere-se a alótropos de carbono com uma nanoestrutura cilíndrica. Ver, por exemplo, Carbon Nanotube Science, by P.J.F. Harris, Cambridge University Press, 2009, para mais detalhes sobre nanotubos de carbono.
[00200] Através da utilização de um único microdispositivo ou uma combinação de microdispositivos integrados em um aparelho de detecção de doenças, as capacidades de detecção da doença podem ser melhoradas significativamente em termos de sensibilidade, especificidade, velocidade e custo, tamanho do aparelho, funcionalidade e facilidade de utilização, juntamente com invasividade reduzida e efeitos colaterais. Um grande número de tipos de microdispositivos capazes de medir uma vasta gama de propriedades microscópicas em amostras biológicas para detectar doenças podem ser integrados em um único aparelho de detecção que utiliza microtecnologias de fabricação e novos fluxos de processos aqui revelados. Por outro lado, para efeitos de demonstração e ilustração, alguns novos exemplos detalhados foram mostrados aqui, ilustrando como a microeletrônica e as nanotécnicas de fabricação e associados fluxos de processos podem ser utilizados para fabricar microdispositivos de detecção muito sensíveis, multifuncionais, miniaturizados, em que os princípios e as abordagens gerais de microeletrônica que usam a fabricação de nano tecnologias no design e fabricação de dispositivos de detecção de alto desempenho, foram contemplados e ensinados, os quais podem e devem ser expandidos para várias combinações de processos de fabricação, incluindo, mas não se limitando a, deposição de camada fina, padronização (litografia e ataque químico), planarização (incluindo polimento mecânico-químico), implantação iônica, difusão, limpeza, vários materiais, e diversas sequências de processos, fluxos e suas combinações.
[00201] A Figura 1 (a) é uma ilustração em perspectiva de um aparelho de detecção de doenças da presente invenção em que uma amostra biológica é colocada em movimento através dele. A Figura 1 (b) e a Figura 1 (c) ilustram o aparelho que compreende a detecção múltipla de microdispositivos individuais.
[00202] A Figura 2 (a) é uma ilustração em corte transversal de um aparelho de detecção de doenças da presente invenção com vários microdispositivos. A amostra biológica é colocada no aparelho, ou movendo- se através dele, enquanto uma ou mais propriedades microscópicas desta amostra biológica são medidas com os vários microdispositivos. As Figuras 2 (b)-2 (l) são ilustrações em perspectiva do novo fluxo de processos para a fabricação do microdispositivo. As Figuras 2 (m)-2 (n) são vistas em corte transversal de um aparelho que compreende múltiplos microdispositivos individuais
[00203] A Figura 3 é uma ilustração em corte transversal de um aparelho de detecção de doenças da presente invenção com vários microdispositivos de sondas de detecção diferentes. A amostra biológica é colocada no aparelho, ou movendo-se através dele, e uma ou mais propriedades microscópicas desta amostra são medidas com o múltiplo microdispositivo.
[00204] A Figura 4 é uma ilustração em perspectiva de um aparelho de detecção de doenças da presente invenção. Inclui duas placas separadas por um espaçamento estreito com uma amostra biológica a ser analisada colocada entre as placas, com vários microdispositivos colocados nas superfícies interiores das placas para medir um ou vários parâmetros desejados da amostra ao nível microscópico.
[00205] A Figura 5 ilustra um novo fluxo de processos para a fabricação de um aparelho de detecção de doenças da presente invenção, utilizando as tecnologias da microeletrônica.
[00206] A Figura 6 é uma ilustração em perspectiva de um aparelho de detecção de doenças fabricado por um método da presente invenção. O aparelho é capaz de sondar uma única célula e medir e as suas propriedades microscópicas.
[00207] A Figura 7 é uma ilustração em corte transversal de um aparelho de detecção de doenças da presente invenção com vários microdispositivos colocados a uma distância desejada durante o tempo de trânsito, e cujas medições apresentam maior sensibilidade, especificidade e velocidade, incluindo a informação dinâmica que varia com o tempo.
[00208] A Figura 8 é uma ilustração em perspectiva de um novo conjunto de sondas microscópicas, incluídas em um aparelho de detecção de doenças da presente invenção, para detectar vários estados eletrônicos ou magnéticos, configurações, ou outras propriedades de uma amostra biológica (por exemplo, uma célula, uma molécula de DNA ou RNA, um telômero de DNA ou cromossoma, um vírus, ou uma amostra de tecido)
[00209] A Figura 9 é uma ilustração em perspectiva de uma nova sonda de quatro pontos, incluída em um aparelho de detecção de doenças da presente invenção, que se destina à detecção de fracos sinais eletrônicos em uma amostra biológica (por exemplo, uma célula, uma molécula de DNA ou RNA, um telômero de DNA ou de cromossoma, um vírus, ou uma amostra de tecido).
[00210] A Figura 10 ilustra um novo fluxo de processos para a fabricação de uma classe de microdispositivos, capazes de captar, classificar, sondar, medir, e modificar um material biológico (por exemplo, uma célula, uma molécula de DNA ou RNA, um telômero de DNA ou cromossoma, um vírus, ou uma amostra de tecido) ao nível microscópico e em um espaço tridimensional.
[00211] A Figura 11 ilustra um novo fluxo de processos para a fabricação de uma classe de microdispositivos capazes de medir as propriedades físicas de um material biológico (por exemplo, uma célula, uma molécula de DNA ou RNA, um telômero de DNA ou cromossoma, um vírus, ou uma amostra de tecido), tais como as suas propriedades mecânicas (por exemplo, dureza, resistência ao corte, resistência à tensão na ruptura, elongação) e outras propriedades relacionadas com a membrana celular.
[00212] A Figura 12 ilustra como um microdispositivo com duas microssondas é capaz de se mover em direções opostas, quando uma força aplicada puder ser utilizada para sondar as propriedades de um material biológico (por exemplo, as propriedades mecânicas de uma membrana celular).
[00213] A Figura 13 ilustra um novo arranjo para aplicações de detecção de doenças, em que são utilizados tanto o gerador de sinal de relógio como sondas de detecção de sinal, juntamente com o sinal de relógio esquematicamente gravado, o sinal da sonda (sinal detectado pela sonda do microdispositivo), o sinal processado e melhorado após filtragem utilizando a técnica de processamento fase lock-in para aumentar o sinal detectado.
[00214] A Figura 14 ilustra ainda um novo arranjo para aplicações de detecção de doenças em que são usados os geradores de sinal de relógio, um gerador de sinal da sonda e as sondas de detecção de sinais, juntamente com o sinal de relógio esquematicamente gravado, o sinal detectado pela sonda do microdispositivo em resposta ao sinal da sonda, e processando e reforçando o sinal após filtragem através da tecnologia de processamento usando fase lockin para aumentar o sinal detectado, e mostrando o sinal detectado em função do tempo (atraso da resposta do sinal ao longo do tempo, neste caso)
[00215] A Figura 15 ilustra um novo arranjo para aplicações de detecção de doenças, em que um novo conjunto de microfiltros são utilizados para detectar materiais biológicos através da separação de materiais biológicos pelas suas diferentes propriedades específicas, tais como o tamanho, peso, forma, propriedades elétricas e propriedades de superfície.
[00216] A Figura 16 ilustra um sistema de distribuição de fluido, que é uma parte do pré-tratamento para o aparelho de detecção de doenças, e que libera uma amostra ou material auxiliar para um dispositivo, a uma pressão e velocidade desejadas.
[00217] As Figuras 17 (b)-17 (c) ilustram um novo dispositivo que pode envolver-se em comunicações celulares ao nível da célula individual, simulando sinais celulares, e recebe respostas da célula que pode ser um sinal elétrico, magnético, eletromagnético, térmico, óptico, acústico, biológico, químico, eletromecânico, eletroquímico, eletroquímico-mecânico, bioquímico, biomecânico, bioeletromecânico, bioeletroquímico, bioeletroquímico-mecânico, físico, ou mecânico. A Figura 17 (a) ilustra a forma como o sinal é processado e respondido em uma única célula.
[00218] A Figura 18 ilustra um diagrama de um aparelho de detecção de doenças, compreendendo vários módulos funcionais.
[00219] A Figura 19 ilustra um microdispositivo capaz de comunicar, captar, classificar, ar tratar, e modificar um DNA e medindo várias propriedades do DNA (por exemplo, propriedade elétrica, magnética, eletromagnética, térmica, óptica, acústica, biológica, química eletromecânica, eletroquímica, eletroquímico-mecânica, bioquímica, biomecânica, bioeletromecânica, eletrobioquímica, bioeletroquímico-mecânica, física e mecânica.
[00220] A Figura 20 ilustra um aparelho da presente invenção, que pode detectar a carga de superfície em materiais biológicos e separá-los por uma fenda com base na carga.
[00221] A Figura 21 ilustra um outro aparelho segundo a presente invenção, que pode detectar as propriedades ópticas do material biológico através de um conjunto de sensores ópticos
[00222] A Figura 22 ilustra um outro aparelho da presente invenção, que pode separar materiais biológicos de tamanho geométrico diferente, e detectar as suas propriedades respectivas.
[00223] A Figura 23 ilustra um aparelho da presente invenção que pode medir a propriedade acústica de um material biológico.
[00224] A Figura 24 ilustra um aparelho da presente invenção que pode medir a pressão interna de um material biológico.
[00225] A Figura 25 ilustra um aparelho da presente invenção que tem côncavos entre os pares de sondas, na parte inferior e no teto do canal.
[00226] A Figura 26 ilustra um outro aparelho segundo a presente invenção que tem côncavos de forma diferente dos ilustrados na Figura 25.
[00227] A Figura 27 ilustra um aparelho da presente invenção que tem um canal escalonado.
[00228] A Figura 28 ilustra um aparelho da presente invenção que tem um conjunto de medidores térmicos.
[00229] A Figura 29 ilustra um aparelho da presente invenção que inclui um nano tubo de carbono como o canal com o DNA nele contido.
[00230] A Figura 30 ilustra um aparelho integrado da presente invenção que inclui um dispositivo de detecção e um sensor óptico
[00231] A Figura 31 ilustra um aparelho integrado da presente invenção que inclui um dispositivo de detecção e um sistema de circuitos lógicos
[00232] A Figura 32 ilustra um aparelho da presente invenção que inclui um dispositivo de detecção e um filtro
[00233] A Figura 33 ilustra a forma como os microdispositivos do presente invento podem ser utilizados para medir os fatores geométricos do DNA.
[00234] A Figura 34 ilustra um processo para a fabricação de um microdispositivo da presente invenção com uma tampa no topo do rego, para formar um canal.
[00235] A Figura 35 é um diagrama de um aparelho da presente invenção para detectar uma doença em um material biológico
[00236] A Figura 36 mostra um exemplo de uma unidade de filtração da amostra
[00237] A Figura 37 mostra um outro exemplo de uma unidade de filtração da amostra
[00238] A Figura 38 é um diagrama de uma unidade de pré- processamento de um aparelho da presente invenção
[00239] A Figura 39 é um diagrama de uma unidade de processamento de informação de um aparelho da presente invenção
[00240] A Figura 40 mostra a integração de resultados de múltiplos sinais no cancelamento de ruído e na melhoria da relação sinal/ruído.
[00241] A Figura 41 mostra uma forma de realização do processo da presente invenção para a fabricação de um dispositivo de detecção de pelo menos uma câmara de detecção e pelo menos um detector.
[00242] A Figura 42 mostra uma outra concretização de um processo da presente invenção para a fabricação de um dispositivo de detecção com câmaras de detecção encerradas, detectores, e canais para o transporte de amostras biológicas, tais como amostras de fluidos.
[00243] A Figura 43 mostra um novo método de detecção de doenças em que, pelo menos, uma sonda é lançada para um material biológico a uma velocidade e direção desejadas, resultando em uma colisão.
[00244] A Figura 44 ilustra um novo processo de fabricação desta invenção para a formação de múltiplos componentes com diferentes materiais ao mesmo nível do dispositivo.
[00245] A Figura 45 mostra um processo da presente invenção para detectar um material biológico utilizando um dispositivo de detecção de doenças.
[00246] A Figura 46 mostra uma outra concretização do processo de detecção, em que os materiais saudáveis e materiais biológicos com doença são separados, em que os materiais biológicos com doença são administrados para teste adicional.
[00247] A Figura 47 é um dispositivo de detecção em matriz biológica, em que uma série de dispositivos de detecção são fabricados em um aparelho.
[00248] A Figura 48 mostra uma outra concretização de um dispositivo de detecção de doenças da presente invenção, incluindo a entrada e a saída do dispositivo, o canal em que o material biológico passa, e os dispositivos de detecção alinhados ao longo das paredes do canal.
[00249] Um aspecto da presente invenção refere-se a um aparelho para a detecção, in vivo ou in vitro, de doenças em um material biológico (por exemplo, o ser humano, de um órgão, tecido ou células de uma cultura). Cada aparelho inclui um sistema de fornecimento de fluido biológico e um dispositivo de sondagem e detecção. O aparelho é capaz de medir as propriedades microscópicas de uma amostra biológica. Através do sistema de administração constante da pressão do fluido, as materiais biológicos microscópicos podem ser administrados no interior ou sobre o microdispositivo diagnóstico do aparelho. Em comparação com os aparelhos tradicionais de detecção ou tecnologias, o aparelho da presente invenção é vantajoso em prover um aumento da sensibilidade de detecção, especificidade e velocidade, com custos e tamanho reduzidos. O aparelho pode incluir ainda uma interface biológica, uma sonda de controle e um circuito de análise de dados, ou um sistema de recuperação ou tratamento de resíduos hospitalares. Microdispositivos adicionais, por exemplo, um segundo dispositivo de detecção também podem ser incluído, ou integrado, no aparelho para reforçar a capacidade de detecção.
[00250] Como componente essencial do aparelho, o microdispositivo deve incluir meios para realizar, pelo menos, a função de direcionar, controlar, forçar, receber, ampliar e armazenar as informações de cada endereço de sondagem. Como exemplo, tais meios podem ser uma unidade central de controle, que inclui um circuito de controle, uma unidade de endereçamento, um circuito amplificador, um circuito de processamento lógico, uma unidade de memória, um chip de aplicação específica, um transmissor de sinais, um receptor de sinais e um sensor.
[00251] Em algumas formas de realização, o sistema de fornecimento do fluido compreende um gerador de pressão, uma regulador de pressão, uma válvula de estrangulamento, um medidor de pressão, e kits de distribuição. Como exemplos destas formas de realização, o gerador de pressão pode incluir um sistema de pistão motor e uma caixa contendo gás comprimido; o regulador de pressão (que pode ser composto de vários reguladores) pode regular a pressão para um valor desejado; o medidor de pressão relança o valor medido para a válvula de estrangulamento, que, em seguida, regula a pressão para se aproximar do valor alvo.
[00252] O fluido biológico a ser administrado pode ser uma amostra biológica de um indivíduo para ser detectada uma doença, ou algo não necessariamente para relacionado a doença. Em algumas forma de realização, o fluido a ser administrado é um líquido (por exemplo, uma amostra de sangue, uma amostra de urina, ou uma solução salina) ou um gás (por exemplo, nitrogênio, argônio, hélio, neônio, criptônio, xenônio, ou radônio). O regulador de pressão pode ser um regulador de pressão único ou vários reguladores de pressão, que são colocados em sucessão, quer para regular para um valor baixo ou alto até um nível desejado, especialmente quando a pressão inicial é demasiado elevada ou demasiado baixa para um único regulador ajustar até ao nível desejado, ou até um nível que seja aceitável para um dispositivo ou destino final.
[00253] Em algumas outras formas de realização, o controlador do sistema inclui um pré-amplificador, um amplificador lock-in, um dispositivo de medição elétrico, um medidor térmico, uma matriz de comutação, um barramento de sistema, um dispositivo de armazenamento não volátil, uma memória de acesso aleatório, um processador, e uma interface de utilizador. O interface pode incluir um sensor que pode ser um sensor de temperatura, um medidor de fluxo, um medidor piezo, ou outro sensor.
[00254] Em ainda algumas outras concretizações, o aparelho da presente invenção inclui ainda uma interface biológica, um controlador de sistema, um sistema para a recuperação ou tratamento de resíduos hospitalares. A recuperação e tratamento de resíduos médicos pode ser realizada através do mesmo sistema ou através de dois sistemas diferentes.
[00255] Um outro aspecto da presente invenção fornece um aparelho para interagir com uma célula, o qual inclui um dispositivo para o envio de um sinal para a célula e, opcionalmente, receber uma resposta para o sinal emitido da célula.
[00256] Em algumas formas de realização, a interação com a célula pode ser a sondagem, a detecção, comunicação, o tratamento, ou a modificação de um sinal codificado, que pode ser elétrico, magnético, eletromagnético, térmico, óptico, acústico, biológico, químico, eletromecânico, eletroquímico, eletroquímico-mecânico, bioquímico, biomecânico, bioeletromecânico, bioeletroquímico, bioeletroquímico- mecânico, físico, mecânico, ou uma combinação dos mesmos.
[00257] Em algumas outras formas de realização, o dispositivo contido no aparelho pode incluir várias superfícies revestidas por um ou mais elementos ou combinações de elementos, e um sistema de controle para a liberação dos elementos. Em alguns casos, o sistema de controle pode causar a liberação dos elementos da superfície do dispositivo através de energia térmica, energia óptica, energia acústica, energia elétrica, energia eletromagnética, energia magnética, energia de radiação, e/ou energia mecânica de uma maneira controlada. A energia pode ser sob a forma de impulsos com frequências desejadas.
[00258] Em algumas outras formas de realização, o dispositivo contido no aparelho inclui um primeiro componente para armazenar ou liberar um elemento ou uma combinação de elementos para a superfície da célula ou dentro da célula; e um segundo componente para controlar a liberação dos elementos (por exemplo, um circuito para controlar a liberação dos elementos). Os elementos podem ser um componente, um composto químico, Ca, C, Cl, Co, Cu, H, I, Fe, Mg, Mn, N, 0, P, F, K, Na, S, Zn, ou uma combinação dos mesmos. O sinal pulsado, ou constante, pode ser na forma de um elemento liberado ou uma combinação de elementos, e pode ser realizado em solução em um líquido, gás ou uma combinação dos mesmos. Em alguns casos, o sinal pode ter uma frequência que varia de cerca 1 x 10-4 Hz a cerca de 100 MHz ou que varia de cerca 1 x 10-4 Hz a cerca de 10 Hz, ou a uma concentração de oscilação que varia entre cerca de 1.0 nmol/L a cerca de 10,0 mmol/L. Igualmente, o sinal compreende a oscilação de um componente biológico, um composto químico, Ca, C, Cl, Co, Cu, H, I, Fe, Mg, Mn, N, 0, P, F, K, Na, S, Zn, ou uma combinação dos mesmos, por exemplo, a desejadas frequências de oscilação.
[00259] Em algumas formas de realização, o sinal a ser enviado para a célula pode ser sob a forma de elemento oscilante, composto, ou uma densidade de oscilação de um componente biológico, e uma resposta ao sinal a partir da célula reveste a forma de elemento oscilante, composto, ou uma densidade de oscilação de um componente biológico.
[00260] Em algumas formas de realização, o dispositivo pode ser revestido com um filme biológico, por exemplo, para melhorar a compatibilidade entre o dispositivo e a célula.
[00261] Em algumas outras formas de realização, o dispositivo pode incluir componentes para gerar um sinal a ser enviado para a célula, recebendo uma resposta ao sinal a partir da célula, analisar a resposta, processar a resposta, e fazendo a interface entre o dispositivo e a célula.
[00262] Ainda um outro aspecto da presente invenção fornece dispositivos cada um incluindo um microfiltro, um obturador, um contador de células, um seletor, um kit microcirúrgico, um temporizador, e um circuito de processamento de dados. O microfiltro pode discriminar células anormais através de uma propriedade física (por exemplo, dimensão, forma ou velocidade), uma propriedade mecânica, propriedade elétrica, propriedades magnéticas, propriedades eletromagnéticas, térmica (por exemplo, temperatura), propriedades ópticas, propriedades acústicas, propriedades biológicas, propriedades químicas, e bioquímicas. Os dispositivos podem também incluir um ou mais microfiltros. Cada um destes microfiltros pode ser integrado com dois marcadores celulares, um dos quais está instalado na entrada de cada filtro, enquanto o outro é instalado na saída do filtro de cada poço. A forma do microfiltro é um retângulo, uma elipse, um círculo ou polígono, e as dimensões do microfiltro são cerca de 0,1 μm até cerca de 500 pm, ou a partir de cerca de 5 um a cerca de 200 um. Como aqui utilizado, o termo “dimensão” designa o tamanho físico ou característica do filtro de abertura, ou seja, comprimento, diâmetro, largura ou altura. O filtro pode ser revestido por um filme biológico ou filme biocompatível, a fim de aumentar a compatibilidade entre o dispositivo e a célula.
[00263] Em algumas formas de realização destes dispositivos, o obturador ensanduichado por duas membranas de filtro pode ser controlado por um temporizador (assim obturador do tempo). O temporizador pode ser desencadeado pelo contador de células. Por exemplo, quando uma célula passa através do contador de células na entrada do filtro, o relógio é disparado para repor o obturador para a posição inicial, e move-se a uma velocidade predefinida para o trajeto da célula, e o temporizador registra o tempo da passagem de células através do contador de células, que se encontra na saída.
[00264] Ainda um outro aspecto da presente invenção fornece métodos para a fabricação de um microdispositivo com uma vala e sonda embutidas em paredes laterais da vala. Um vala é um túnel não encerrado (ver, por exemplo, a Figura 2 (i), (2030), o qual pode ser acoplado a uma outra vala simétrica (ver, por exemplo, a Figura 2 (k), 2031) de modo a formar um canal encerrado (ver, por exemplo, a Figura 2 (1), 2020). O método pode incluir a deposição de vapor químico, deposição física de vapor, ou deposição da camada atômica para depositar vários materiais sobre um substrato; litografia ou ataque químico para transferir padrões do design para a estrutura; planarização mecânico-química para planarizar a superfície, limpeza química para a remoção de partículas, difusão ou implantação iônica para dosear elementos em camadas específicas; ou térmicos de recozimento para reduzir os defeitos de cristal e ativar íons difusos. Um exemplo de tal método inclui: a deposição de um primeiro material sobre um substrato; depositando um segundo material sobre o primeiro material e padronizando o segundo material via um processo de microeletrônica (por exemplo, litografia, ataque químico) de modo a formar uma ponta de detecção; deposição de um terceiro material sobre o segundo material e, em seguida, o padronizar o segundo material por um processo de planarização; deposição de um quarto material sobre o terceiro material e padronização do quarto material por um processo de microeletrônica (por exemplo, litografia, ataque químico) e, em seguida, por um processo de microeletrônica (por exemplo, um outro ataque químico) em que o material serve como um quarto máscara dura. Uma máscara dura geralmente refere-se a um material (por exemplo, dielétrico, ou um composto metálico inorgânico) utilizado no processamento de semicondutores como uma máscara ataque químico em vez de polímeros e outros materiais orgânicos “macios”.
[00265] Em algumas formas de realização, o método inclui ainda dois dispositivos de acoplamento que são, portanto, fabricados e simétricos (isto é, um espelho invertido) para formar um dispositivo de detecção com canais. A entrada de cada canal pode ser, opcionalmente, de boca de sino, por exemplo, de tal modo que o tamanho da abertura do canal (entrada) seja maior do que o corpo do canal, tornando assim mais fácil uma célula entrar no canal. A forma da seção transversal de cada canal pode ser um retângulo, elipse, círculo ou polígono. As valas dos dois microdispositivos acoplados podem ser alinhadas pelas marcas de alinhamento projetadas no disposição do microdispositivo. A dimensão do vala pode variar desde cerca de 0,1 μm até cerca de 500 μm.
[00266] Alternativamente, o método pode também incluir a cobertura da vala do microdispositivo através de uma tela plana. Tal painel pode incluir, ou ser feito com silicone, SiGe, SiO2, Al2O3, ou outros materiais ópticos. Exemplos de outros materiais ópticos potencialmente adequados incluem polímero de acrilato, AgInSbTe, alexandrite sintética, triselenide de arsênio, trisulfide de arsênio, fluoreto de bário, CR-39, seleneto de cádmio, cloreto de cádmio, césio, carbonato de cálcio, fluoreto de cálcio, vidro calcogeneto, fosforeto de gálio, GeSbTe, germânio, dióxido de germânio, código de vidro, silsesquioxano de hidrogênio, Islândia longarina, cristal líquido, fluoreto de lítio, lumicera, METATOY, fluoreto de magnésio, óxido de magnésio, metamateriais, nêutrons super espelho, fósforo, picarina, poli (metacrilato de metilo), policarbonato, brometo de potássio, safira, scotophor, spectralon, metais espéculos, vibrador de anel dividido, fluoreto de estrôncio, granada de ítrio alumínio, fluoreto de lítio ítrio, ortovanadato de ítrio, ZBLAN, seleneto de zinco, sulfeto de zinco.
[00267] Em outras formas de realização, o método pode ainda incluir a integração de três ou mais microdispositivos fabricados para assim produzir um dispositivo avançado com uma matriz de canais.
[00268] No entanto, ainda um outro aspecto da presente invenção refere-se a microdispositivos, cada um incluindo um vala, uma sonda incorporada nas paredes ou base da vala, uma estrutura de suporte para mover a sonda, e um conjunto de circuitos de controle, em que o microdispositivo é capaz de captar, classificar e modificar um DNA e medir suas propriedades (por exemplo, propriedades elétricas, térmicas ou ópticas). A vala pode ser utilizada para envolver a dupla hélice de DNA.
[00269] Em algumas formas de realização, a largura das faixas de da vala tem cerca de 1 nm até cerca de 10 nm, a profundidade das vala é entre cerca de 1 nm e cerca de 10 um, e o comprimento é cerca de 1 nm até cerca de 10 mm. A sonda pode incluir, ou ser feita de, um material condutor e, opcionalmente, uma estrutura de suporte flexível para estender ou retrair a sonda. A sonda também pode ter uma ponta ao lado da vala e ponta corresponde espacialmente quer um sulco maior quer com um sulco menor do DNA. A ponta pode corresponder espacialmente aos sulcos entrelaçados do DNA, que podem ser variáveis. A ponta também pode coincidir com a extremidade de cada filamento da hélice de DNA. Em alguns exemplos, o diâmetro da ponta pode variar de cerca de 1 angstrom até cerca de 10 μm.
[00270] Em algumas outras formas de realização, o microdispositivo pode ainda incluir um conjunto de valas, por exemplo, para melhorar a eficiência.
[00271] Um outro aspecto da presente invenção diz respeito a um conjunto de fluxos de processos novos para a fabricação de microdispositivos (incluindo microssondas e indentação de microssondas) para as suas aplicações na detecção de doenças através da determinação das propriedades microscópicas de uma amostra biológica. Os microdispositivos podem ser integrados em um aparelho de detecção de doenças da presente invenção para medir uma ou mais propriedades ao nível microscópico.
[00272] Ainda outro aspecto da presente invenção é o de se envolver em comunicações celulares e regular a decisão ou resposta celular (tais como a divisão, diferenciação celular, diferenciação e morte celular) através de sinais fabricados. Isto poderia ainda ser utilizado para detectar e tratar doenças.
[00273] Para aumentar ainda mais a capacidade de medição, vários microdispositivos podem ser implementados em uma peça de equipamento de detecção empregando a técnica de tempo de voo, em que pelo menos um microdispositivo de sondagem e um microssensor são colocado a uma distância pré-conhecida. O microdispositivo de sondagem pode aplicar um sinal (por exemplo, uma tensão, uma carga, um campo elétrico, um raio laser, ou uma onda acústica) a uma amostra biológica a ser medida, e o microdispositivo de detecção pode medir a resposta vinda da amostra biológica, após a amostra ter percorrido uma distância conhecida e um período de tempo desejado. Por exemplo, um microdispositivo de sondagem pode aplicar uma carga elétrica de uma primeira célula, e, em seguida, um microdispositivo de detecção e mede subsequentemente a carga da superfície após um período de tempo desejado (T) tem passado e a célula tenha percorrido uma certa distância (L).
[00274] Os microdispositivos contidos no aparelho da presente invenção podem ter uma grande variedade de desenhos, estruturas, funcionalidades, e aplicações devido às suas propriedades diferentes, o grau elevado de flexibilidade e capacidade de integração e miniaturização. Eles incluem, por exemplo, uma um comparador de tensão, uma sonda de quatro pontos, uma calculadora, um circuito de lógica, uma unidade de memória, um microcortador, um micromartelo, um microescudo, um microcorante, um micropino, uma microfaca, uma microagulha, um microfio, micropinça, um microabsorvedor de óptica, um microespelho, um micro-onda, um microfiltro, um micro-helicóptero, um microtriturador, microbombas, um microabsorvedor, um microdetector de sinais, um microperfurador, um microssugador, um microtestador, um micro-recipiente, um transmissor de sinal, um gerador de sinal, um sensor de atrito, um sensor de carga elétrica, um sensor de temperatura, um detector de dureza, um gerador de ondas acústicas, um gerador de ondas ópticas, um gerador de calor, um refrigerador e um microgerador de carga.
[00275] Além disso, deve notar-se que os avanços na tecnologia de fabricação já fez fabricações de uma grande variedade de microdispositivos e integração de várias funções para o mesmo dispositivo que são altamente viáveis e rentáveis. O tamanho da célula humana típica é de cerca de 10 mícrons. Utilizando o estado da técnica das técnicas de fabricação de circuitos integrados, a dimensão mínima definida em um microdispositivo pode ser tão pequeno como 0,1 mícron ou menos. Assim, é ideal para utilizar os microdispositivos divulgados para aplicações biológicas.
[00276] Em termos de materiais para os microdispositivos, o princípio geral ou consideração é a compatibilidade do material com um material biológico. Porque o momento em que um microdispositivo está em contato com uma amostra biológica (por exemplo, uma célula, uma molécula biológica, tal como DNA, RNA, ou proteína, ou uma amostra de tecido ou órgão) pode variar, dependendo da sua aplicação a que se destina, podem ser usados um material diferente ou uma combinação diferente de materiais para fazer o microdispositivo. Em alguns casos especiais, os materiais podem se dissolver em um dado pH de uma forma controlada e, portanto, pode ser selecionado como um material apropriado. Outras considerações incluem o custo, simplicidade, facilidade de uso e praticidade. Com os avanços significativos em tecnologias de microfabricação, como a tecnologia de fabricação de circuitos integrados, dispositivos altamente integradas com dimensão mínima tão pequenas quanto 0,1 mícron podem ser construídos agora de forma comercialmente rentável. Um bom exemplo é o projeto e fabricação de microdispositivos eletromecânicos (MEMS), que agora estão sendo usados em uma ampla variedade de aplicações na indústria de circuitos integrados.
[00277] Descritos abaixo estão vários exemplos de aparelhos da presente invenção que contêm uma classe de microdispositivos inovadores que são integrados no aparelho de detecção de doenças da presente invenção, e do seu processo de fabricação.
[00278] A Figura 1 é uma ilustração em perspectiva de um aparelho de detecção de doença 111 deste invento em que uma amostra biológica 211, tal como uma amostra de sangue, colocada no mesmo, ou em movimento através dele, é testada. Nesta figura, um exemplo de um aparelho de detecção de doença 111 tem a forma de um cilindro, no qual uma amostra biológica 211 flui através dele (a partir do lado esquerdo para o lado direito na figura) e pode ser testada para uma ou mais propriedades a níveis microscópicos.
[00279] Para aumentar a velocidade de detecção e sensibilidade, um grande número de microdispositivos podem ser integrados em um único aparelho de detecção de doenças da presente invenção, tal como o aparelho ilustrado na Figura 1 (b) e na Figura 1 (c) com os microdispositivos espaçados para medir um grande número de entidades desejadas (tais como células, DNAs, RNAs, proteínas, etc) na amostra biológica. Para alcançar os requisitos acima referidos, o aparelho de detecção deve ser otimizado com a sua área de superfície de contato máxima em relação à amostra biológica, e com um grande número de microdispositivos integrados na superfície maximizada.
[00280] A Figura 2 (a) é uma vista em corte transversal de um aparelho de detecção de doenças da presente invenção 122 com múltiplos microdispositivos idênticos 311. Uma amostra biológica, tal como uma amostra de sangue 211 é posta em movimento através dele ou podendo ser testada em relação a uma ou mais propriedades ao nível microscópico, incluindo, por exemplo, propriedades elétricas (por exemplo, carga de superfície, potencial de superfície, corrente e impedância, outras propriedades elétricas), propriedades magnéticas, propriedades eletromagnéticas, propriedades mecânicas (tais como a densidade, a dureza, a resistência ao corte, resistência, alongamento tensão de fratura, adesão), características biológicas, propriedades químicas (por exemplo, pH, força iônica), propriedades bioquímicas, propriedades térmicas (por exemplo, temperatura), e propriedades ópticas.
[00281] Em vez de medir uma única propriedade de um material biológico diagnosticar doenças,vários microdispositivos podem ser integrados em um aparelho de detecção para detectar várias propriedades. A Figura 3 é uma ilustração em corte transversal de um aparelho de detecção de doenças da presente invenção 133 com vários microdispositivos 311, 312, 313, 314, e 315, com diferentes sondas de detecção, em que uma amostra 211, tal como uma amostra de sangue é colocada, ou em movimento através dele. podendo ser testada em relação a várias propriedades incluindo, mas não se limitando a, propriedades elétricas (por exemplo, carga de superfície, potencial de superfície, e impedância), propriedades magnéticas, propriedades eletromagnéticas, propriedades mecânicas (por exemplo, densidade, dureza e adesão), propriedades térmicas (ou seja, temperatura), propriedades biológicas, propriedades químicas (por exemplo, pH), propriedades físicas, propriedades acústicas, e propriedades ópticas.
[00282] As Figuras 2 (b)-2 (n) ilustram um fluxo do processo da presente invenção para a fabricação de microdispositivos para a captura, classificação, sondagem, medição e modificação de materiais biológicos (por exemplo, uma única célula, uma molécula de DNA e RNA). Em primeiro lugar, um material 2002 (por exemplo, um material não condutor) e um outro material 2003 (por exemplo, um material condutor) são sequencialmente depositadas sobre um substrato 2001 (ver Figura 2 (b) e Figura 2 (c)). O primeiro material 2003 é, então, subsequentemente padronizado pela litografia e processos ataque químico (ver Figura 2 (d)). Outro material 2004 é, então, depositado (como mostrado na Figura 2 (e)) e planarizado (como mostrado na Figura 2 (f)). Uma outra camada de material 2005 é depositado (como mostrado na Figura 2 (g)) e padronizado como uma máscara dura (como mostrado na Figura 2 (h)), seguida por ataque químico (como mostrado na Figura 20)), o qual é parado sobre o substrato 2001. A Figura 2 (i) é uma ilustração em perspectiva do dispositivo, enquanto que a Figura 2 (j) é uma ilustração vertical do dispositivo.
[00283] Como mostrado na Figura 2 (k), o dispositivo 2080 e um dispositivo de espelho simétrico 2081 podem ser acoplados em conjunto (como mostra a Figura 2 (l)). Como tal, o aparelho é fabricado tendo a via com a sonda embutida na parede lateral.
[00284] Como ilustrado na Figura 2 (m) e Figura 2 (n), um grande número de dispositivos de detecção de microrganismos podem ser integrados em conjunto para melhorar a eficiência da detecção.
[00285] Tal como aqui ilustrado, é desejável otimizar a concepção do aparelho de detecção para maximizar a área de superfície de medição, uma vez que quanto maior a área de superfície, maior o número de microdispositivos, que podem ser colocados sobre o aparelho de detecção para medir simultaneamente a amostra, aumentando assim a velocidade de detecção e também minimizar a quantidade de amostra necessária para o teste. A Figura 4 é uma ilustração em perspectiva de um aparelho de detecção de doenças da presente invenção 144. Inclui duas placas separadas por um espaçamento estreito com uma amostra, tal como uma amostra de sangue, a ser medida colocada entre as placas, com várias microdispositivos colocados no interior.
[00286] Ainda outro aspecto da presente invenção diz respeito a um conjunto de fluxos de processo de fabricação para fazer novos microdispositivos para efeitos de detecção de doenças. A Figura 5 ilustra um fluxo de um novo processo para a fabricação de um aparelho de detecção de doenças, utilizando tecnologias e processos de microeletrônica. Em primeiro lugar, a 412 de material é depositada sobre um substrato de 411 (Figura 5 (a)). Em seguida, é padronizado por fotolitografia e processos de ataque químico (Figura 5 (b)). Após a deposição, o material 413 é planarizado usando polimento mecânico-químico conforme mostrado na Figura 5 (d). Em seguida, são formadas no material de 413 áreas rebaixadas sob a forma de padrão de orifício, usando fotoprocessos de ataque químico e litografia, conforme mostrado na Figura 5 (e), seguindo-se a deposição de material 414 (Figura 5 (f)). O material 414 acima da superfície do material 413 é removido através de polimento mecânico-químico (Figura 5 (g), seguido de deposição do material 415. Em seguida, o material 415 é padronizado usando fotoprocessos de ataque químico e litografia (Figura 5 (i)). Em seguida, o material 414 é depositado e o seu excesso acima do substrato 415 é removido através de polimento mecânico-químico (Figuras 5 (j) e (k)). Finalmente, é levado a cabo um processo de ataque químico de curta duração ou polimento químico-mecânico ao excesso de material 415 e seletivo para material de 414 (Figura 5) (1), resultando em uma ligeira saliência do material 414. O material 412 pode ser um material piezoelétrico. Quando uma tensão é aplicada a ele na direção certa, ele vai expandir e empurrar para cima, resultando em movimento ascendente na ponta do meio do material 414. Assim, é fabricado um microdispositivo de duas microssondas capazes de medir uma gama de propriedades (incluindo as propriedades mecânicas e elétricas) de amostras biológicas, usando um novo fluxo de processos de fabricação.
[00287] O aparelho de detecção integrado com os microdispositivos divulgados no presente pedido são totalmente capazes de detecção de propriedades previamente escolhidas em uma única célula, um DNA de cadeia simples, um RNA individual, ou o teor de material biológico de pequeno porte de um individuo. A Figura 6 é uma ilustração em perspectiva de um microdispositivo 555 fabricado por um novo processo de fluxo divulgado neste pedido de patente (por exemplo, o novo fluxo de processo ilustrado na Figura 5 acima), e como tal, um dispositivo é capaz de sondar uma única célula 666 e medir a célula para coletar os parâmetros pretendidos. A Figura 6 (a) ilustra uma perspectiva em secção transversal de um microdispositivo 555 com um par de microssondas 531 e 520, onde a microssonda 531 tem a forma de uma ponta e a microssonda 520 tem a forma de um anel. Ambas as sondas micro531 e 520 podem ser condutoras e podem servir como um par de sondas para medir as propriedades elétricas de uma amostra biológica. A microssonda 531 está em contato com uma base 518 que pode ser um material piezoelétrico. Quando uma tensão é aplicada à base 518 feita de um material piezoelétrico, a base 518 pode expandir e empurrar a ponta da microssonda 531 para cima, o que pode ser útil para medir várias propriedades de uma amostra biológica, tal como uma única célula. Na Figura 6 (b), é mostrado o microdispositivo 555 para medir uma única célula 666, utilizando a ponta da sonda 531 que penetra através da membrana da célula 611 e para o espaço interior da célula 622, enquanto que a sonda de anel 520 entra em contato com a membrana de célula 611, no lado de fora da superfície da membrana. Desta forma, o microdispositivo 555 pode fazer várias medições da célula, incluindo as suas propriedades elétricas (por exemplo, potencial elétrico, corrente através da membrana celular, carga de superfície na membrana, e impedância), propriedades mecânicas (por exemplo, dureza, quando a ponta da sonda 531 for concebida como uma sonda de microindentação), propriedades térmicas (por exemplo, temperatura), propriedades físicas e químicas (por exemplo, o pH).
[00288] Em outro aspecto, a invenção proporciona a concepção, integração e fluxo do processo de fabricação de microdispositivos capazes de fazer medições altamente sensíveis e avançadas sobre sinais muito fracos em sistemas biológicos para detectar doenças em ambiente complicado com sinal muito fraco e um ruído de fundo relativamente alto. Essas capacidades inovadoras que utilizam a classe de microdispositivos descritos na presente invenção para detectar doenças incluem, mas não se limitando a, fazer medições dinâmicas, medições em tempo real (por exemplo, o tempo de medição de voo, e combinando do sinal da sonda utilizando a detecção do sinal de resposta) técnica de fase lock-in para reduzir o ruído de fundo, e as técnicas da sonda de 4 picos para medir sinais muito fracos, e sondas únicas e inovadoras para medir várias propriedades eletrônicas, eletromagnéticas e magnéticas de amostras biológicas em uma única célula (por exemplo, um dos telômeros de DNA e cromossoma), molécula única (por exemplo, DNA, RNA e proteína), material biológico único (por exemplo, virus).
[00289] Por exemplo, em uma abordagem de tempo de voo para obter uma informação dinâmica sobre a amostra biológica (por exemplo, uma célula, uma subestrutura de uma célula, um DNA, um RNA, ou um vírus), um primeiro microdispositivo é usado para enviar um sinal para perturbar o material biológico a ser diagnosticado e, em seguida, um segundo microdispositivo é utilizado para medir com precisão a resposta do material biológico. em uma forma de realização, o primeiro microdispositivo e o segundo microdispositivo estão posicionados a uma distância L desejada ou pré-determinada, e um material biológico que flui desde primeiro microdispositivo para o segundo microdispositivo a ser medido. Quando o material biológico passa o primeiro microdispositivo, o primeiro microdispositivo envia um sinal para o material biológico, e, em seguida, o segundo microdispositivo detecta a resposta ou a retenção do sinal de perturbação no material biológico. A partir da distância entre os dois microdispositivos, intervalo de tempo, natureza da perturbação pelo primeiro microdispositivo, e alterações medidas sobre o material biológico durante o tempo de voo, as propriedades microscópicas e dinâmicas do material biológico podem ser obtidas. Noutra forma de realização, um primeiro microdispositivo é utilizado para sondar o material biológico através da aplicação de um sinal (por exemplo, uma carga eletrônica) e a resposta do material biológico é detectada por um segundo microdispositivo, como uma função do tempo.
[00290] Para aumentar ainda mais a sensibilidade de detecção, é usado um novo processo de detecção de doenças, em que é utilizado a técnica do tempo de voo. A Figura 7 é uma perspectiva em corte transversal do aparelho de detecção 155 com vários microdispositivos 321 e 331 colocados a uma distância desejada 700 para medições do tempo para atingir uma informação dinâmica sobre uma amostra biológica 211 (por exemplo, uma célula), apresentado uma maior sensibilidade, especificidade e velocidade da medição. Neste tempo de medição de voo, uma ou mais propriedades da amostra biológica 211 são primeiramente medido quando a amostra 211 passa do primeiro microdispositivo 321. As mesmas propriedades são então medidas de novo quando a amostra 211 passa o segundo microdispositivo 331, após ter percorrido a distância 700, A modificação das propriedades da amostra 211 do microdispositivo 321 para a microdispositivo 331, indica como ela reage com o meio circundante (por exemplo, um ambiente biológico particular) durante esse período. Também pode revelar e fornecer informações sobre como suas propriedades evoluem com o tempo. Alternativamente, na configuração representada na Figura 7, o microdispositivo pode ser primeiro utilizado como uma sonda para fornecer um sinal de sonda (por exemplo, uma carga elétrica) à amostra 211 enquanto esta amostra passa pelo microdispositivo 321. Subsequentemente, a resposta da amostra ao sinal da sonda, pode ser detectada pelo microdispositivo 331 À medida que a amostra passa por ele (por exemplo, alteração da carga elétrica sobre a amostra durante a trajeto). Podem ser feitas medições na amostra biológica 211 através de medições de contato ou de não contato. Em uma forma de realização, uma série de microdispositivos podem ser implantados em um espaçamento desejado para medir as propriedades do material biológico ao longo do tempo.
[00291] A utilização de microdispositivos (por exemplo, através do fluxos do processo de fabricação da presente invenção) tal como discutido acima e ilustrado na Figura 7, pode ser útil para detectar um conjunto de novas propriedades microscópicas de uma amostra biológica (por exemplo, uma célula, uma subestrutura celular ou uma molécula biológica, tal como o DNA, RNA ou proteína) que não tenham sido considerados em tecnologias de detecção existentes. Tais propriedades microscópicas podem ser elétricas, magnéticas, eletromagnéticas, térmicas, ópticas, acústicas, biológicas, químicas, eletromecânicas, eletroquímicas, eletroquímico-mecânicas, químicas, biobiomecânicas, bioeletromecânicas, depósito-eletroquímicas, bioeletroquímico-mecânicas, propriedades físicas, e mecânicas de uma amostra biológica que é um único material biológico (tal como uma célula, uma subestrutura celular, uma molécula biológica-por exemplo, DNA, RNA, proteína ou uma amostra de um tecido ou órgão). Sabe-se que os materiais biológicos incluem ligações tais como OH, CO, CH, para complexar estruturas tridimensionais tais como o DNA e RNA. Alguns deles têm uma única assinatura em termos da sua configuração eletrônica.
[00292] Alguns deles podem ter únicas configurações e propriedades elétricas, magnético, eletromagnéticas, térmicas, óticas, acústicas, químicas, biológicas, eletromecânicas, eletroquímicas, eletroquímico-mecânicas, bioquímicas, biomecânicas, bioeletromecânicas, bioeletroquímicas, bioeletroquímico-mecânicas, físicas e mecânicas. O material biológico normal e material biológico com doença podem transportar assinaturas diferentes, em relação às propriedades acima referidas. No entanto, nenhum dos parâmetros acima indicados ou propriedades têm sido usados rotineiramente como uma propriedade de detecção de doenças. Utilizando um aparelho de detecção de doenças que inclua um ou mais microdispositivos do presente invento, as propriedades podem ser detectadas, medidas, e utilizadas como sinais úteis para detectar doenças, em especial durante a fase inicial de detecção de doenças graves como o câncer.
[00293] A Figura 8 é uma ilustração em perspectiva de um novo conjunto de sondas microscópicas 341, 342, 343, 344, 345, 346, e 347 concebidas e configuradas para detectar várias propriedades eletrônicas, magnéticas, ou estados eletromagnéticos, configurações ou outras propriedades o nível microscópico nas amostras biológica 212, 213, 214, e 215, que podem ser de uma única célula, DNA, RNA, e tecido ou amostra. Como um exemplo, em termos de determinação das propriedades eletrônicas, as formas das amostras biológicas 212, 213, 214, e 215 na Figura 8 podem representar monopolo eletrônico (amostra 212), dipolo (amostras 213 e 214), e quádruplos (amostra 215). Os microdispositivos 341, 342, 343, 344, 345, 346, e 347 estão otimizados para maximizar a sensibilidade de medição dos referidos parâmetros, incluindo, mas não se limitando a, estados eletrônicos, carga eletrônica, distribuição da nuvem eletrônica, campo elétrico, propriedades magnéticas e eletromagnéticas, e os microdispositivos podem ser concebidos e dispostos em três configurações tridimensionais. Para algumas doenças tais como o cancro, é provável que os estados eletrônicos e as correspondentes propriedades eletrônicas difiram entre células normais e cancerosas, DNA, RNA, e tecidos. Portanto, a detecção de doenças pode ser aumentada através da determinação das propriedades eletrônicas, magnéticas e eletromagnéticas em níveis microscópicos, incluindo na célula, o DNA, e os níveis de RNA, sensibilidade e especificidade.
[00294] Para além dos exemplos anteriores de medição das propriedades elétricas (por exemplo, carga, estados eletrônicos, carga eletrônica, distribuição da nuvem eletrônica, campo elétrico, corrente e potencial elétrico, e impedância), propriedades mecânicas (por exemplo, dureza, densidade, resistência ao cisalhamento e resistência à fratura) e propriedades químicas (por exemplo, pH) em uma único célula, e na Figura 8 para medir estados elétricos, magnéticos ou eletromagnéticos ou configurações de amostras biológicas em células e moléculas (por exemplo, DNA, RNA e proteínas), outros microdispositivos são divulgados neste pedido de patente para medições elétricas sensíveis.
[00295] A Figura 9 é uma ilustração em perspectiva de uma sonda de quatro picos para detectar um sinal eletrônico fraco em uma amostra biológica, tal como uma célula, em que uma sonda de quatro picos 348 é concebida para medir as propriedades elétricas (impedância e fraca corrente elétrica) de uma amostra biológica 216.
[00296] Um dos principais aspectos do presente invento é o fluxo de processo de concepção e fabrico de microdispositivos e métodos de utilização dos microdispositivos para a captura e/ou medição de materiais biológicos (por exemplo, células, estruturas celulares, DNA e RNA) a níveis microscópicos e no espaço tridimensional, em que os microdispositivos possuem microssondas dispostas em três dimensões com forma e tamanhos característicos tão pequenos como uma célula, DNA, ou RNA, e capazes de captar, classificar, sondar, medir e modificar materiais biológicos. Tais microdispositivos podem ser fabricados utilizando o estado da técnica das técnicas de processamento de microeletrônica, tais como os utilizados no fabrico de circuitos integrados. Utilizando tecnologias de deposição de película fina, tais como feixe molecular de epitaxia (MEB) e deposição de camadas atômicas (ALD), a espessura da película em poucas monocamadas pode ser conseguida (por exemplo, 4 A a 10 A). Além disso, utilizando feixes eletrônicos e/ou litografia de raios-x, pode ser obtido o tamanho do dispositivo em função da sequência dos nanômetros, tornando o microdispositivo capaz de captar, sondar, medir, e modificar um material biológico (por exemplo, uma única célula, um DNA de cadeia simples ou uma molécula de RNA).
[00297] A Figura 10 ilustra um fluxo de processo da presente invenção para a fabricação de microdispositivos para a captura, classificação, sondagem, medição e modificação de sujeitos biológicos (por exemplo, uma única célula, uma molécula de DNA ou RNA). Neste fluxo de processo, são utilizados processos de microeletrônica para fabricar microdispositivos projetados para atingir os as mencionadas funções únicas. Especificamente, um primeiro material 712 (tipicamente um material condutor) é primeiro depositado sobre um substrato 711 (Figura 10 (a) e Figura 10 (b)). O primeiro material 712 é subsequentemente padronizado usando técnicas de processos de ataque químico e litografia (Figura 10 (c)). Um segundo material 713 é então depositado e planarizado usando o processo químico-mecânico de polimento para remover o excesso do segundo material 713 por cima do primeiro material 712 (como mostrado na Figura 10 (e)). Uma outra camada de material 714 é depositada e padronizada, seguida por deposição e planarização por polimento mecânico-químico de uma outra camada 712 (Figura 10 (f)). Em seguida, um terceiro material 715 é depositado e padronizado, utilizando processos de litografia e ataque químico (Figura 10 (g) e Figura 10 (h)), seguindo-se a deposição e planarização de um quarto material 716, tipicamente um material de sacrifício (Figura 10 (i) e Figura 10(j)). O fluxo do processo de deposição e padronização do material 712 e 715 é repetido alternativamente, seguindo-se a deposição do material 716 e planarização por polimento mecânico-químico (Figura 10 (k)-(m)), e forma-se uma pilha de películas com várias camadas alternadas com o material 712 (por exemplo, um material condutor) e o material 715 (por exemplo, um isolante). Finalmente, o material 716 entre as camadas da película 771 e 772 é removido através de ataque químico a úmido, ataque químico a seco (o que pode exigir processos de litografia) ou ataque químico a vapor, seletivo para todos os outros materiais (Figura 10 (n)). Conforme ilustrado na Figura 10 (o), no caso de 712 ser um material condutor ligado a um circuito elétrico ou a uma fonte elétrica (por exemplo, uma fonte de carga), cada ponta da sonda formada por 712 na camada (por exemplo, 781 e 782) podem ter uma carga ou um campo elétrico na superfície (por exemplo, 781 e 782), as quais (cada extremidade da sonda) podem ser selecionadas para ter uma carga positiva ou uma carga negativa, ou um campo elétrico positivo ou negativo. Por outro lado, a ponta da sonda tal também pode ser sensível às propriedades de material biológico a ser medido (por exemplo, nuvem eletrônica, campo elétrico, e temperatura quando a ponta da sonda for um detector térmico, ou a emissão de luz quando a ponta da sonda for um sensor óptico). Usando a fonte do circuito elétrico ou fonte elétrica, podem ser colocadas várias combinações de distribuição de carga elétrica ou campo elétrico sobre o microdispositivo, como mostrado na Figura 10 (o) e na Figura 10 (p), que podem ser usadas para separar e classificar vários materiais biológicos tais como uma célula ou uma molécula de DNA. Por exemplo, um material biológico com uma distribuição de carga inversa daquela na Figura 10 (p) pode ficar retido pelo microdispositivo mostrado na Figura 10 (p). Uma matriz de microdispositivos com diferentes distribuições de carga ou de campo elétrico podem aprisionar as respectivos materiais biológicos em alta velocidade, o que pode servir como um dispositivo de triagem. A Figura 1 O (q) ilustra o uso de um microdispositivo capaz de captar um DNA e de medir diferentes propriedades (por exemplo, propriedades elétricas, térmicas ou ópticas) de um DNA, em que ponta da sonda corresponde espacialmente a um sulco grande ou pequeno de um DNA de dupla hélice. A Figura 10 (r) ilustra como as pontas da sonda estão ligadas ao circuito elétrico, em que apenas se mostram os cabos elétricos. Deve notar-se que o microdispositivo mostrado neste exemplo pode ser integrado em um único chip com um bilhão ou mais de tais microdispositivos para captar e/ou triar células, DNAs, RNAs, proteínas, e outros objetos biológico, em alta velocidade.
[00298] Um outro aspecto da presente invenção refere-se a microssondas de recuo e microssondas para medição de uma gama de propriedades físicas (tais como propriedades mecânicas) dos materiais biológicos. Exemplos das propriedades mecânicas incluem a dureza, a resistência ao cisalhamento, a força de alongamento o tensão de fraturas e outras propriedades relacionadas com a membrana celular, que se crê serem um componente crítico no diagnóstico de doenças.
[00299] A Figura 11 ilustra um novo fluxo de processos de fabricação de microdispositivos capazes de sondar uma variedade de propriedades biológicas de objetos, tais como propriedades mecânicas de membrana celular (por exemplo, força mecânica de uma membrana celular). Neste fluxo do processo, um material 812 é primeiro depositado sobre um substrato 811, seguindo-se a deposição de um outro material 813 (Figura 11 (a)). Segue-se a padronização do material 813 usando litografia e processos de ataque químico, e um material 814 é depositado (Figura 11 (b)) e planarizado (Figura 1 l (c)). Em seguida, uma outra camada de material 813 é depositada e padronizada usando técnicas de litografia e processos de ataque químico para remover porções do material 813, seguindo-se a deposição e planarização de um material 815 (que pode ser um material piezoelétrico e pode servir como um condutor) (Figura 1 l (d)). Uma camada de material 813 é em seguida depositada, seguindo-se a deposição e padronização de uma camada adicional 813, deposição e planarização do material 816 (Figura 11 (e)). Em seguida, o material 816 é colocado de volta a uma reduzida espessura, e padronizado, seguindo-se a padronização da camada tripla de material 813 (Figura 11 (f)). Outra camada 814 é depositada (Figura 11 (g)) e planarizada através de polimento mecânico-químico (Figura 1 l (h)), e padronizada (Fig. 11 (i)). Finalmente, as camadas múltiplas 813 são removidas através de ataque químico, úmido ou a seco, ou a vapor (Figura 11 (j)) A Figura 11 (k) é uma perspectiva em corte seccional do microdispositivo em um plano perpendicular ao da Figura 11 (j) (90-graus de rotação da Figura 110, A Figura 11 (1) ilustra um microdispositivo com duas micropontas 871 e 872, que podem se mover em direções opostas, quando uma voltagem é aplicada aos condutores piezoelétricos 881 e 882, que podem ser utilizados para sondar materiais biológicos tais como células.
[00300] A Figura 12 é uma ilustração de como os microdispositivos são fabricados usando o novo processo de fabricação mostrado na Figura l 1. Na Figura 12, um microdispositivo 850 com duas microssondas 866 e 855 pode mover-se em sentidos opostos sobre a força a ser aplicada (Figura 12 (a)). Quando as pontas das duas sondas perfurarem uma célula 870, como a distância entre as duas microssondas é aumentada com o aumento da força aplicada, a célula é esticada. Finalmente, à medida que a força aplicada atingir um valor crítico, a célula é dividida em duas partes (Figura 12 (b)). A resposta dinâmica da célula para a força aplicada fornece informação sobre a célula, particularmente sobre as propriedades mecânicas (por exemplo, elasticidade) da membrana celular. A força no ponto em que a célula é dilacerada reflete a resistência da célula e pode ser chamado de um ponto de ruptura: quanto maior for a resistência mecânica da membrana da célula, maior será a força no ponto de ruptura.
[00301] Outra nova abordagem proporcionada pela presente invenção é o uso do bloqueio de fase na medição para detectar doenças, o que reduz o ruído de fundo e aumenta eficazmente a relação sinal-ruído. Em geral, neste método de medição, um sinal periódico é utilizado para sondar a amostra biológica e a resposta coerente para a frequência deste sinal periódica da sonda é detectado e amplificado, enquanto que são filtrados os outros sinais não coerentes com a frequência do sinal de sonda, e assim efetivamente reduz o ruído de fundo. Em uma das formas de realização desta invenção, um microdispositivo de sondagem pode enviar um sinal periódico da sonda (por exemplo, um grupo de laser pulsado, uma onda térmica pulsada, ou um campo elétrico alternado) a um material biológico, e a resposta ao sinal da sonda pelo material biológico pode ser detectado através de um microdispositivo de detecção. A técnica de bloqueio em fase pode ser utilizada para filtrar o ruído indesejável e melhorar o sinal da resposta que é sincronizado com a frequência do sinal da sonda. Os dois exemplos seguintes ilustram as novas características do sistema de tempo de detecção de voo, em combinação com a técnica de fase lock-in de detecção de sinal para aumentar a sensibilidade detecção de sinais fraco e, por conseguinte, na medição de detecção de doenças.
[00302] A Figura 13 é uma ilustração de um novo tempo do sistema de detecção de voo para as aplicações de detecção de doenças. Especificamente, a Figura 13 (a) mostra uma configuração para a medição de um material biológico 911 utilizando a sonda de detecção 933 e o gerador de relógio 922, e a Figura 13 (b) contém o sinal gravado 921 devido à estrutura 922, o sinal 931 registrado pelo sinal da sonda 933, e sinal processado 941, utilizando a técnica de bloqueio de fase para filtrar o ruído no sinal gravado 931, em que apenas uma resposta sincronizada com o sinal de relógio 921 é mantida. Na configuração mostrada na Figura 13 (a), quando um material biológico, tal como uma célula 911 passa em uma estrutura 922, desencadeia um sinal claro (por exemplo, um sinal de dispersão de luz se 922 for uma fonte de luz, ou um aumento acentuado na tensão se 922 for uma estrutura de orifício em uma resistência). Portanto, 922 pode ser utilizado para registrar a chegada do material biológico, e como um relógio quando múltiplas estruturas 922 forem colocados a uma distância periódica, como mostrado no traço do sinal gravado 921 na Figura 13 (b). Além disso, quando 922 for colocado a uma distância conhecida em frente de uma sonda 933, assinala a chegada de um material biológico que vem na direção de 933, e a resposta do sinal gravado em 933 é retardado por um tempo t em relação ao sinal desencadeado por 922, onde t iguala a distância entre 922 e 933 dividido pela velocidade de percurso do material biológico. Como ilustrado na Figura 13 (b), o sinal 921, devido à estrutura 922, é claro e periódico com uma periodicidade que é proporcional à distância entre a estrutura de 922, enquanto que o sinal medido pelo sensor 933 tem um nível de ruído elevado e relativamente fraco sinal relacionado com o material biológico. Com a utilização da técnica de bloqueio de fase para filtrar o ruído no sinal gravado 931, pela sonda de detecção não sincronizado 933 e pelo sinal de relógio 921, a relação sinal- ruído pode ser grandemente melhorada, conforme mostrado no sinal 941 na Figura 13 (b).
[00303] A Figura 14 ilustra ainda um outro arranjo do tempo de voo para detecção de doença em que são usados um gerador de sinal de relógio 922, um gerador de sinal da sonda 944 e uma sonda de detecção de sinal 955, juntamente com o sinal de relógio esquematicamente gravado 921, sinal total de resposta gravado 951 (com exceção do sinal de relógio), e o sinal 950 processado utilizando a técnica de bloqueio de fase. Neste arranjo, um gerador de sinal da sonda 944 é utilizado para perturbar o material biológico 911 (por exemplo, aquecimento de 911 utilizando um feixe óptico, ou adicionando uma carga elétrica a 911), e é subsequentemente medida uma resposta ao sinal de sonda em função do tempo, utilizando para tal uma variedade de sondas de detecção 955. O sinal filtrado em 952 mostra a resposta dinâmica ao sinal da sonda por 944, à medida que diminui com o tempo. Uma vez que a célula normal e anormal podem responder de forma diferente ao sinal da sonda, este arranjo com microssondas adequadas pode ser utilizado para detectar doenças tais como o cancro. Em outra forma de realização que utiliza esta configuração (mostrada na Figura 14), o gerador de sinal da sonda 944 pode enviar um sinal periódico ao material biológico 911, e o sinal detectado a partir da resposta do material biológico pela sonda de detecção 955 pode ser processado com base na técnica do bloqueio de fase, em que o ruído não sincronizado com a frequência do sinal de sonda é filtrado e o sinal que está sincronizado com a frequência do sinal da sonda é amplificado.
[00304] A Figura 15 é uma ilustração em perspectiva do novo microfiltro de múltiplas funções. Um obturador temporizado 1502 é ensanduichado entre dois pedaços de membrana de filtro 1501 com regos. Quando um material biológico 1511 se move através do rego, é detectada pela primeira vez pelo contador 1512, que desencadeia o relógio do painel de barreira 1502. Em seguida, as células maiores serão filtradas ou bloqueadas pelos buracos do filtro 1001, enquanto que somente os objetos específicos com bastante velocidade serão capazes atravessar o caminho 1503 antes do obturador temporizado 1502 fechar o caminho do filtro (ver a Figura 15 (b)). Caso contrário, será retido à medida que o obturador temporizado 1502 se mover para bloquear o caminho como mostrado na Figura 15 (c).
[00305] A Figura 16 ilustra um sistema de distribuição de fluido, que inclui um gerador de pressão, um regulador de pressão, uma válvula de estrangulamento, um medidor de pressão, e kits de distribuição. O gerador de pressão de fluido1605 sustenta o fluido com a pressão desejada, e a pressão é ainda regulada pelo regulador 1601 e, em seguida, manipulada com precisão pela válvula de estrangulamento 1602. Ao mesmo tempo, a pressão é monitorizada em tempo real e alimentada de volta pelo manômetro 1603 para a válvula de estrangulamento 1602. O fluido regulado é então conduzido em paralelo para os vários dispositivos onde uma pressão constante é necessária para conduzir a amostra de fluido.
[00306] A Figura 17 ilustra como um microdispositivo em um aparelho de detecção de doenças da presente invenção pode comunicar, investigar, detectar e, opcionalmente, tratar e modificar materiais biológicos em um nível microscópico. A Figura 17 (a) ilustra a sequência de eventos celulares a partir do reconhecimento do sinal para determinação dos destinos das células. Em primeiro lugar, como os sinais 1701 são detectados pelos receptores 1702 sobre a superfície da célula, a célula irá integrar e codificar os sinais em uma mensagem biologicamente inteligível, tal como a oscilação de cálcio 1703. Por conseguinte, o que corresponde as proteínas correspondentes 1704 na célula irão interagir com a mensagem, e de seguida serem modificadas e transformarem-se em proteínas interagidas por íons 1705. Através da translocação, estas proteínas modificadas 1705 passarão a mensagem transmitida para as proteínas nucleares, e a modificação controlada nas proteínas nucleares irá modular a expressão do gene 1707 que inclui a transcrição, tradução, processos hipergenéticos, e modificações da cromatina. Através do RNA mensageiro 1709, a mensagem é, por sua vez, passada a proteínas específicas 1710, mudando assim a sua concentração que vai determinar ou regular a decisão da célula ou atividades, tais como a diferenciação, divisão, ou até mesmo a sua morte.
[00307] A Figura 17 (b) ilustra um aparelho da presente invenção que é capaz de detectar, comunicar, tratar, modificar e sondar uma única célula, por um meio de contato ou sem contato. O aparelho está equipado com microssondas e microinjetores que são direcionados e modulados pelo circuito de controle 1720, Cada microinjetor individual é fornecido com um microcartucho separado, que transporta os produtos químicos ou compostos concebidos.
[00308] Para ilustrar como um aparelho do presente invento pode ser usado para simular um sinal intracelular, é considerada a oscilação de cálcio como um mecanismo de exemplo. Em primeiro lugar, um canal Cat- liberação-ativação (CRAC) tem de ser aberto até à sua extensão máxima, o que pode ser alcançado por várias maneiras. Em um exemplo dos métodos aplicáveis, um material bioquímico (por exemplo, tapsigargina) armazenada no cartucho 1724 é liberada através de um injetor 1725 para a célula, e o CRAC vai abrir ao estímulo do material biológico. Em outro exemplo dos métodos aplicáveis, o injetor 1724 força uma tensão específica sobre a membrana celular, o que faz também com que o CRAC se abra.
[00309] A concentração de Ca+2 de uma solução no injetor 1728 pode ser regulada, uma vez que é uma combinação desejável de uma solução de contendo Ca+2 1726, e uma solução isenta de Ca+2 1727. Enquanto o injetor 1730 contiver uma solução isenta de Ca+2*, os injetores 1728 e 1730 são alternadamente ligados e desligados a uma frequência desejada. Como tal, é conseguida uma oscilação do Ca+2 e o conteúdo no interior da membrana da célula é então exposto a uma oscilação do Ca+2. Por conseguinte, as atividades ou destino da célula está a ser manipulado pelo sinal regulado gerado pelo aparelho.
[00310] Ao mesmo tempo, a resposta da célula (por exemplo, sob a forma de uma propriedade elétrica, magnética, eletromagnética, térmica, óptica, acústica ou mecânica) pode ser monitorizada e registrada pelas sondas integrados neste aparelho.
[00311] A Figura 17 (c) ilustra uma outra concepção de um aparelho que é capaz de configurar a comunicação com uma única célula. O aparelho está equipado com microssondas que são revestidas com compostos biologicamente compatíveis ou elementos, por exemplo, Ca, C, Cl, Co, Cu, H, I, Fe, Mg, Mn, N, 0, P, F, K, Na, S, ou Zn. Estas sondas podem gerar sinais químicos oscilantes com um tal elemento ou composto para interagir com a célula, resulta em uma resposta que afeta as atividades da célula ou destino final, como descrito acima. Da mesma forma, este aparelho pode também sondar e registrar a resposta da célula (por exemplo, sob a forma de uma propriedade elétrica, magnética, eletromagnética, térmica, óptica, acústica, química, biológica, eletromecânica, eletroquímica, eletroquímica-mecânica, bioquímica, biomecânica, bioeletromecânica, bioeletroquímica, bioeletroquímico-mecânica, física, ou mecânica).
[00312] A Figura 18 mostra o diagrama de blocos do sistema de um aparelho de detecção de doenças desta invenção. Este exemplo inclui sistema de fornecimento de um fluido 1801, uma interface biológica 1802, um e dispositivo de detecção e sondagem 1803, um controlador de sistema de 1805, um sistema de tratamento dos resíduos médicos 1804. A amostra biológica ou material é transportado para a interface 1802 através do o sistema de distribuição do fluido 1801, entretanto, os parâmetros do líquido (ou propriedades) são comunicadas ao controlador de sistema 1805 que compreende uma unidade de processamento lógica, uma unidade de memória, um chip de aplicação específica, um sensor, um transmissor de sinal, e um receptor de sinal; e, em seguida, o controlador do sistema 1805 pode dar comando adicional ao sistema. A interface 1802 é um conjunto que faz a ponte entre uma amostra de fluido e o dispositivo de detecção, e monitoriza os parâmetros ou propriedades da amostra biológica (por exemplo, pressão, temperatura, viscosidade, ou taxa de fluxo) e, em seguida, comunica os dados para o controlador de sistema 1805 enquanto distribui a amostra biológica para dispositivo de sondagem e detecção a sondagem, e a uma determinada velocidade ou pressão (que pode ser comandada pelo controlador de sistema 1805).
[00313] O controlador do sistema 1805 é o comandante central e monitor de todo o sistema (ou aparelho), onde todos os parâmetros e informações de vários módulos são processadas e trocadas e onde são dadas as instruções, e onde o comando é emitido. O controlador de sistema 1805 pode incluir, por exemplo, um pré-amplificador, um medidor elétrico, um medidor térmico, uma matriz de comutação, um barramento de sistema, um dispositivo de armazenamento não volátil, uma memória de acesso aleatório, um processador, e uma interface de utilizador através da qual o utilizador do aparelho pode manipular, configurar o aparelho, ler os parâmetros de funcionamento, e o resultado final. O pré-amplificador pode processar o sinal bruto a um sinal reconhecível para os medidores. Os medidores podem forçar e medir sinais correspondentes que podem ser, por exemplo, elétricos, magnéticos, eletromagnéticos, térmicos, ópticos, acústicos, biológicos, químicos, eletromecânicos, eletroquímicos, eletroquímico-mecânicos, bioquímicos, biomecânicos, bioeletromecânicos, bioeletroquímicos, bioeletroquímico-mecânicos, físicos, mecânicos, e as suas combinações. A matriz de comutação pode mudar os terminais de teste de diferentes matrizes da sonda. A interface de utilizador inclui montagens de entrada e saída, que veda o sistema de distribuição de fluido e o dispositivo de sondagem e detecção.
[00314] O dispositivo de detecção e sondagem 1803 é o módulo funcional nuclear do aparelho de detecção de doenças da presente invenção, uma vez que é a unidade que sonda a amostra biológica e coleta os sinais celulares (ou respostas) relacionados. O sistema de recuperação e tratamento dos resíduos 1804 recupera a amostra de resíduos biológica para proteger a privacidade do seu hospedeiro biológico, e evita poluir o meio ambiente.
[00315] As Figuras 19 (b)-(n) ilustram um fluxo de processo para a fabricação de um microdispositivo para aprisionar, triar, sondar, medir, tratar, e modificar um material biológico (por exemplo, uma única célula, uma molécula de DNA ou RNA). Um primeiro material 1902 (por exemplo, um material piezoelétrico condutor) e um segundo material 1903 (por exemplo, um material condutor) são sequencialmente depositados sobre um substrato 1901 (ver Figuras 19 (b) e 19 (c)). O segundo material 1903 é subsequentemente padronizado por litografia e processos de ataque químico (ver Figura 19 (d)). Em seguida, um terceiro material 1904 é depositado (como mostrado na Figura 19 (e)) e planarizado (ver Figura 19 (f)). Uma camada de um quarto material 1905 é subsequentemente depositada (ver Figura 19 (g)) e padronizada como uma máscara rígida (ver Figura 19 (h)), seguido por ataque químico para remover os materiais terceiro e primeiro de áreas desejadas, que se acumulam no substrato 1901. A Figura 19 (i) é uma ilustração em perspectiva do dispositivo, enquanto que a Figura 19 (j) é uma ilustração vertical do mesmo dispositivo.
[00316] A Figura 19 (k) ilustra o uso de um microdispositivo capaz de captar um DNA 1920 e medir propriedades diferentes (por exemplo, químicas, elétricas, magnéticas, físicas, térmicas, biológicas, bioquímicas, e propriedades ópticas) de um DNA. Cada ponta da sonda 1912 corresponde espacialmente com qualquer um sulco maior ou menor de um DNA de dupla hélice. Enquanto isso, duas sondas (1911 e 1910), configuradas na extremidade do sulco, podem forçar ou medir os sinais de cada uma das extremidades da cadeia do DNA de dupla hélice. As sondas podem ser feitas de um material condutor, opcionalmente com uma estrutura de apoio piezoelétrico, que pode esticar para a frente e para trás a uma distância desejada. Todas as sondas são enumeradas, direcionadas e controladas por um circuito de controle.
[00317] A Figura 19 (1) mostra uma forma simplificada do dispositivo representado na Figura 19 (k). Neste dispositivo, as pontas de sonda correspondem espacialmente aos sulcos entrelaçados de um DNA de dupla hélice. O número de intervalos de ranhura entre as sondas adjacentes é variável. Se for necessário, o DNA pode ser movido (por exemplo, puxando pelas sondas 1910 e 1911), e as sondas podem se mover ao longo da direção de vala, mapear as propriedades totais e/ou parciais de um DNA.
[00318] A Figura 20 ilustra um aparelho da presente invenção que é capaz de detectar ou medir a carga da superfície de um material biológico 2010, Ele inclui um canal, um par de placas 2022, e uma fenda 2030 que separa o canal em um canal superior 2041 e um canal inferior 2051. Quando um material biológico 2010 transportando uma carga de superfície (carga positiva mostrada na Figura 20 (a)) passa através do canal, sob a influência da tensão aplicada sobre as placas 2022 (com tensão positiva na placa superior e negativa na placa do fundo), ele irá se mover no sentido da placa de fundo, como mostrado na Figura 20 (b). Assim, o material biológico 2010 irá passar através do canal inferior 2051 quando atingir a fenda 2030, (Se o material biológico 2010 transportar uma carga negativa, ele passaria através do canal superior 2041.) Desta forma, um material biológico com o tipo de carga desconhecida (negativo ou positivo) pode ser medido usando este aparelho.
[00319] Este dispositivo compreende pelo menos duas partes de canal, uma das quais é o canal 2060, onde o material biológico é carregado ou modificado, e a outra compreende é uma placa ou fenda para separar os materiais biológicos (ou seja, onde os materiais biológicos são separados) .
[00320] Como a carga de superfície irá afetar a forma de um material biológico, usando as novas e múltiplas placas, poderá ser obtida a informação sobre a distribuição de forma e de carga dos materiais biológicos. O princípio geral e concepção do microdispositivo podem ser estendidos a um escopo mais alargado, tornando assim possível a obtenção de outra informação sobre o material biológico através da separação mediante a aplicação de outros parâmetros tais como o gradiente iônico, gradiente térmico, feixe óptico, ou outra forma de energia.
[00321] A Figura 21 ilustra um outro aparelho da presente invenção para a detecção ou medição de propriedades microscópicas de um material biológico 2110, utilizando um microdispositivo que inclui um canal, um conjunto de sondas 2120, e um conjunto de sensores ópticos 2132 (ver Figura 21 (a)). Os sinais detectados pelas sondas 2120 podem ser correlacionados com informações que incluam imagens recolhidas pelos sensores ópticos 2132 para aumentar a sensibilidade de detecção e especificidade. Os sensores ópticos podem ser, por exemplo, uma câmara CCD, um detector de luz de fluorescência, um sensor de imagem CMOS, ou qualquer combinação dos mesmos.
[00322] Em alternativa, pode ser concebida uma sonda 2120 para provocar a emissão óptica, tal como a emissão de luz de fluorescência 2143 do material biológico visado biológica, tal como as células com doença, os quais podem então ser detectadas por uma sonda óptica 2132, conforme ilustrado na Figura 21 (c). Especificamente, os materiais biológicos podem ser primeiramente tratados com uma solução de etiquetas, que podem reagir seletivamente nas células com doença. Subsequentemente, após a reação (contato ou sem contato) com a sonda 2120, ocorrem as emissões ópticas de células com doença e podem ser detectadas por meio dos sensores ópticos 2132. Este novo processo utilizando microdispositivos é mais sensível do que os métodos convencionais tais como a espectroscopia de fluorescência como sendo o ponto de disparo de emissão ao lado da sonda óptica, e o sinal desencadeado 2143 pode ser gravado em tempo real e no local, e com uma perda mínima de sinal.
[00323] A Figura 22 ilustra uma outra forma de realização do aparelho da presente invenção, que pode ser usada para separar materiais biológicos de tamanho geometricamente diferente e detectar as suas propriedades. Ele inclui, pelo menos, um canal de entrada 2210, um canal perturbador do fluido 2220, uma câmara de aceleração 2230, e dois canais para seleção 2240 e 2250, O ângulo entre 2220 e 2210 se situa entre 0° e 180°. O material biológico 2201 flui na direção x entre 2210 e 2230, O fluido de distribuição biocompatível 2202 flui dentre 2220 e 2230, Em seguida, o líquido 2202 vai acelerar 2201 na direção y. No entanto, a aceleração correlaciona-se com o raio dos materiais biológicos e os maiores são menos acelerados do que os mais pequenos. Assim, os objetos maiores e menores são separados em diferentes canais. Enquanto isso, as sondas podem ser opcionalmente montada de lado na parede lateral de 2210, 2220, 2230, 2240, e 2250, Eles poderiam detectar propriedades elétricas, magnéticas, eletromagnéticas, térmicas, ópticas, acústicas, biológicas, químicas, físicas e mecânicas, o nível microscópico.
[00324] O canal incluído no aparelho da presente invenção pode ter uma largura de, por exemplo, desde 1 nm a 1 mm. O aparelho deve ter pelo menos um canal de entrada e pelo menos dois canais de saída.
[00325] A Figura 23 mostra um outro aparelho da presente invenção com um detector acústico 2320 para medir a propriedade acústica de um material biológico 2301. Este aparelho inclui um canal 2310, e, pelo menos, um emissor de ultrassom e um receptor de ultrassom instalado ao longo da parede lateral do canal. Quando o material biológico 2301 passa através do canal 2310, o sinal de ultrassom emitido de 2320 será recebido após a informação em 2301 ser transportada pelo receptor 2330, A frequência do sinal de ultrassom pode ser, por exemplo, entre 2 MHz e 10 GHz, e a largura da vala do canal pode ser, por exemplo, a partir de 1 nm até 1 mm. O transdutor acústico (isto é, o emissor de ultrassom) pode ser fabricado usando um material piezoelétrico (por exemplo, quartzo, berlinita, ortofosfato, gálio, GaPO4, turmalinas, cerâmica, bário, titanato, BaTiO3, zirconato de chumbo, titanato PZT, óxido de zinco, nitreto de alumínio e fluoretos de polivinilideno).
[00326] A Figura 24 mostra um outro aparelho da presente invenção que inclui um detector de pressão do material biológico 2401. Ele inclui, pelo menos, um canal 2410 e pelo menos um detector piezoelétrico 2420, Quando o material biológico 2401 passa pelo canal, o detector piezoelétrico 2420 irá detectar a pressão de 2401, transformando as informações em um sinal elétrico, e enviá-lo para um leitor de sinais. Da mesma forma, a largura da vala no aparelho pode ser, por exemplo, a partir de 1 nm até 1 mm, e o material piezoelétrico pode ser, por exemplo, quartzo, berlinita, ortofosfato, gálio, GaPO4, turmalinas, cerâmica, bário, titanato, BaTiO3, zirconato de chumbo, titanato de PZT, óxido de zinco, nitreto de alumínio ou fluoretos de polivinilideno).
[00327] A Figura 25 mostra um outro aparelho da presente invenção que inclui uma ranhura côncava 2530 entre um par de sondas, na parte inferior ou no teto do canal. Quando um material biológico 2510 passa, o côncavo 2530 pode captar seletivamente o material biológico com especiais características geométricas e faz a sondagem de forma mais eficiente. A forma da projeção da concavidade pode ser retangular, poligonal, elipse ou redonda. A sonda pode detectar propriedades elétricas, magnéticas, eletromagnética, térmicas, ópticas, acústicas, químicas, biológicas, físicas e mecânicas. Do mesmo modo, a largura da microvala pode ser, por exemplo, a partir de 1 nm até 1 mm. A Figura 25 (a) é uma vista de cima a baixo deste aparelho, a Figura 25 (b) é uma vista lateral, enquanto que a Figura 25 (c) é uma vista em perspectiva.
[00328] A Figura 26 é um outro aparelho da presente invenção que também inclui ranhuras côncavas 2630 (de uma forma diferente das mostradas na Figura 25) na parte inferior e no teto do canal. Quando um material biológico 2610 passa através, as ranhuras côncavas 2630 vão gerar um fluxo fluídico turbulento, que pode captar seletivamente os objetos microbiológicos que apresentem determinadas características geométricas. A sonda pode detectar propriedades elétricas, magnéticas, eletromagnéticas, térmicas, ópticas, acústicas, biológicas, químicas, físicas e mecânicas. A profundidade da ranhura côncava pode ser, por exemplo, desde 10 nm até 1 mm, e a largura do canal pode ser, por exemplo, a partir de 1 nm até 1 mm.
[00329] A Figura 27 ilustra um aparelho da presente invenção, com um canal em cascada 2710, Quando um material biológico 2701 passa através do canal 2710, podem ser utilizadas pares de sondas de diferentes distâncias para medir diferentes propriedades microscópicas, ou mesmo ou mesmo a mesma propriedade microscópica em várias etapas (2720, 2730, 2740) com a sonda de lado a cada passo. Este mecanismo pode ser utilizado no bloqueio de fase, de modo que o sinal para a mesma propriedade microscópica pode ser acumulado. As sondas podem detectar ou medir as propriedades microscópicas elétricas, magnéticas, eletromagnéticas, térmicas, ópticas, acústicas, biológicas, químicas, físicas e mecânicas.
[00330] A Figura 28 ilustra um outro aparelho da presente invenção com medidores térmicos 2830, Ele inclui um canal, um conjunto de sondas 2820, e um conjunto de medidores térmicos 2830, Os medidores térmicos 2830 podem ser um sensor de infravermelhos, um testador transistor sublimiar de fugas, ou um termistor.
[00331] A Figura 29 ilustra um aparelho específico da presente invenção que inclui um nanotubo de carbono 2920 com um canal no seu interior 2910, sondas 2940 que permitem detectar o campo microscópico elétrico, e as propriedades magnéticas, eletromagnéticas, térmicas, ópticas, acústicas, química, biológicas, físicas e mecânicas. Como mostrado, o nanotubo de carbono 2920 contém uma molécula de DNA de dupla hélice 2930, O nanotubo de carbono pode forçar e sentir os sinais elétricos através da sondas laterais 2940, O diâmetro do nano tubo de carbono pode ser, por exemplo, a partir de 0,5 nm até 50 nm, e o seu comprimento pode variar entre, por exemplo, 5 nm a 10 mm.
[00332] A Figura 30 mostra um aparelho integrado da presente invenção, que inclui um dispositivo de detecção (mostrado na Figura 30 (a)) e um sensor óptico (mostrado na Figura 30 (b)), que pode ser, por exemplo, um sensor de imagem CMOS (CIS), um Dispositivo com Carga Acoplada (CCD), um detector de luz de fluorescência, ou outro sensor de imagem. O dispositivo de detecção compreende pelo menos uma sonda e um canal, e o dispositivo de formação de imagem compreende, pelo menos, 1 pixel. A Figura 30 (c-1) e Figura 30 (c-2) ilustram o dispositivo com o dispositivo de detecção e de sensor óptico integrados. Como ilustrado na Figura 30 (d), quando os materiais biológicos 3001, 3002, 3003 atravessam a passagem, a sonda 3010 no canal 3020 pode medir as suas propriedades elétricas, magnéticas, eletromagnéticas, térmicas, óptica, acústicas, biológicas, químicas, físicas e as propriedades mecânicas (ver Figura 30 (e)), enquanto que a imagem poderia ser gravada de forma síncrona por o sensor óptico (Figura 30 (f)). Tanto o sinal de imagem como a da sonda são combinados em conjunto para fornecer um diagnóstico e detecção melhorada bem como a sua sensibilidade e especificidade. Um tal dispositivo de detecção e um dispositivo de detecção óptica podem ser projetados em um sistema de chips ou serem empacotados em um chip.
[00333] A Figura 31 mostra um aparelho com um microdispositivo de detecção (Figura 31 (a)) e um circuito lógico (Fig. 31 (b)). O dispositivo de detecção compreende pelo menos uma sonda e um canal, e o circuito lógico compreende um endereço, um amplificador e uma RAM. Quando um material biológico 3101 passa através do canal, a sua propriedade pode ser detectado pela sonda 3130, e o sinal pode ser tratado, analisado, armazenado, processado e plotado em tempo real. A Figura 31 (c-1) e a Figura 3 I (c-2) ilustram o dispositivo com o dispositivo de detecção e os circuitos integrados. Do mesmo modo, o dispositivo de detecção e o circuito integrado podem ser concebidos em um Sistema de chips ou serem empacotados em um chip.
[00334] A Figura 32 mostra um aparelho da presente invenção que compreende um dispositivo de detecção (Figura 32 (a)) e um filtro (Figura 32 (b)). Quando um material biológico 3201 passa através do dispositivo, é realizada uma filtração no filtro, e os objetos irrelevantes podem ser removidos. A remanescente propriedade dos objetos pode então ser detectada pelo dispositivo sensor (Figura 31 (a)). A filtração antes da sondagem irá melhorar a precisão do dispositivo. A largura do canal pode também variar, por exemplo, a partir de 1 nm até 1 mm.
[00335] A Figura 33 mostra os fatores geométricos do DNA 3330 tais como o espaçamento no sulco menor do DNA (3310) tem um impacto sobre a distribuição espacial das propriedades eletrostáticas na região, que por sua vez pode afetar reações bioquímicas ou químicas no segmento do DNA. Através da sondagem, medição e modificação das propriedades espaciais do DNA (tal como o espaçamento do espaço menor), utilizando o detector descrito e a sonda 3320, pode-se detectar as propriedades, tais como defeitos de DNA, prever reações/processos para o segmento de DNA, e consertar ou manipular as propriedades geométricas e desde modo a distribuição espacial do campo/carga eletrostática, com impactos bioquímicos ou reações químicas no segmento do DNA. Por exemplo, a ponta 3320 pode ser usada para aumentar o espaçamento do sulco menor 3310,
[00336] A Figura 34 mostra o processo de fabricação de um microdispositivo deste invento que tem uma superfície plana na tampa para formar um canal. Isso vai eliminar a necessidade para o acoplamento de duas valas para formar um canal, que pode ser entediante para requerer um alinhamento perfeito.
[00337] A tampa pode ser transparente e permitir a observação com um microscópio. Ela pode incluir, ou ser feitas de silicone, SiGe, SiO2, vários tipos de vidro, e Al203.
[00338] Enquanto que, para efeitos de demonstração e ilustração, a novel acima citada, exemplos detalhados mostram como as técnicas de microeletrônica e/ou nanofabricação e associados fluxos de processos podem ser utilizados para fabricar dispositivos de detecção miniaturizados de alta sensibilidade, multifuncionais e poderosos, foram contemplados e ensinados os princípios e abordagens gerais de empregar a microeletrônica e nano tecnologias de fabricação no design e fabricação de dispositivos de detecção de alto desempenho, os quais podem, e devem, ser expandidos tendo em vista várias combinações de processos de fabricação, incluindo mas não se limitando a, deposição de filmes finos, padronização (litografia e ataque químico), planarização (incluindo polimentos mecânico-químicos), implantação iônica, difusão, limpeza, vários materiais, combinação de processos e passos e várias sequências de processos e fluxos. Por exemplo, no desenho alternativo do dispositivo de detecção e os fluxos de processo de fabrico, o número de materiais envolvidos pode ser inferior ou superior a quatro materiais (que tenham sido utilizados no exemplo acima), e o número de passos do processo pode ser inferior ou superior aquelas sequências de processos demonstradas, dependendo das necessidades e metas específicas de desempenho. Por exemplo, em algumas aplicações de detecção de doenças, um quinto material, tal como um filme baseado em biomaterial fino, pode ser usado para revestir uma ponta de detecção de metal a fim de aumentar o contato entre a ponta de detecção e um material biológico a ser medido, melhorando assim a sensibilidade de medição.
[00339] As aplicações para o aparelho de detecção e métodos da presente invenção incluem a detecção de doenças (por exemplo, na sua fase inicial), particularmente doenças graves como o cancro Uma vez que as células cancerosas e células normais diferem em um número de maneiras, incluindo diferenças em possíveis propriedades microscópicas, tais como o potencial elétrico, a carga superficial, densidade, adesão e pH, os novos microdispositivos aqui descritos são capazes de detectar essas diferenças e, por conseguinte, são aplicáveis, tendo uma maior capacidade em detectar doenças (por exemplo, câncer), particularmente na sua fase inicial. Além disso, os microdispositivos para a medição do potencial elétrico e parâmetros da carga elétrica microdispositivos capazes de realizar as medições de propriedades mecânicas (por exemplo, densidade) podem também ser fabricados e utilizados como aqui divulgado. Na medição de propriedades mecânicas para a detecção precoce da doença, o foco será sobre as propriedades mecânicas que provavelmente diferenciam as células cancerosas ou com doença das células normais. Como um exemplo, pode-se diferenciar as células cancerosas das células normais, usando um aparelho de detecção da presente invenção, que é integrado com os microdispositivos capazes de realizar medições de microindentação.
[00340] A Figura 35 é um diagrama de um aparelho da presente invenção para detectar uma doença em um material biológico. Este aparelho inclui uma unidade de pré-processamento, uma unidade de sondagem e detecção, um processamento de sinal, e uma unidade de processamento de resíduos.
[00341] A Figura 36 mostra um exemplo de uma sub unidade de filtragem da amostra na unidade de pré-processamento, que pode separar as células de diferentes dimensões ou tamanhos. Este dispositivo compreende pelo menos um canal de entrada 3610, um canal perturbador de fluido 3620, uma câmara de aceleração 3630, e dois canais de seleção (3640 e 3650). Os ângulos 3620 entre 3660 e 3610 varia de 0 ° a 180 °.
[00342] O material biológico 3601 flui na direção x do canal de entrada 3610 para a câmara de aceleração 3630, Um fluido biocompatível 3602 flui do canal de fluido perturbador 3620 para a câmara de aceleração 3630, que em seguida acelera o material biológico 3601 na direção y. A aceleração correlaciona-se com o raio do material biológico e os maiores são menos acelerados do que os mais pequenos. Em seguida, os objetos maiores e menores são separados em diferentes canais de seleção. Enquanto isso, as sondas podem ser, opcionalmente, montadas sobre o paredes laterais dos canais 3610, 3620, 3630, 3640 e 3650, As sondas podem detectar, no nível microscópico, as propriedades elétrica, magnética, eletromagnética, térmica, óptica, acústica, biológicos, químicos, bioquímicos, eletromecânica, eletroquímica, eletroquímico-mecânico, físico, e mecânicas.
[00343] A Figura 37 é um diagrama de um outro exemplo de uma unidade de filtração da amostra no aparelho da presente invenção. 3701 representa pequenas células, enquanto que 3702 representa células grandes. Quando uma válvula 3704 estiver aberta e outra válvula 3703 estiver encerrada, os materiais biológicos (3701 fluem 3702) para a saída A. As células grandes, com tamanho superior ao orifício de filtração são bloqueadas contra a saída A, enquanto que as pequenas células são liberadas através da saída A. A válvula de entrada 3704 e a válvula de saída 3707 são então, encerradas, e um fluido biocompatível é injetado através da válvula de entrada do fluido 3706. O fluido transporta grandes células que são escoadas para fora através da saída B. Em seguida, as células maiores são analisadas e detectadas na parte de detecção da invenção.
[00344] A Figura 38 é um diagrama de uma unidade de pré- processamento em um aparelho da presente invenção. Esta unidade inclui uma unidade de filtração da amostra, uma unidade de recarga ou sistema para a recarga do nutriente ou gás para o material biológico, uma unidade de fornecimento de pressão constante, e um exemplo de unidade perturbadora de pré-sondagem
[00345] A Figura 39 é um diagrama de uma unidade de processamento de informação, ou sinais, de um aparelho da presente invenção. Esta unidade inclui um amplificador (tal como um amplificador lock-in) para amplificar o sinal, um conversor AID, e um microcomputador (por exemplo, um dispositivo contendo um chip de computador ou um subdispositivo para processamento da informação), um manipulador, um mostrador, e as ligações de rede.
[00346] A Figura 40 mostra a integração de múltiplos sinais que resultam no cancelamento do ruído e aumento da relação sinal/ruído. Nesta figura, um material biológico 4001 é testado pela Sonda I entre T1 e T2, e pela sonda 2 entre T3 e T4. 4002 é 4001 testou sinal proveniente da sonda 1, e 4003 é a partir da sonda 2. 4002 é o sinal testado de 4001 da S e 4003 é da Sonda 2. Um ruído cancela o outro em certa medida, e resulta em uma intensidade de sinal ou na relação sinal/ruído melhorada. O mesmo princípio pode ser aplicado aos dados coletados a partir de mais do que 2 microdispositivos ou unidades de sondagem.
[00347] A Figura 41 mostra uma forma de realização do fluxo dos processos de fabricação da presente invenção para a produção de um dispositivo de detecção com pelo menos uma câmara de detecção e, pelo menos, um detector. Neste exemplo, seguindo um fluxo de processo de fabricação opcional de armazenamento de dados, processamento de dados e análise de componentes (incluindo transistores, dispositivos de memória, circuitos lógicos e dispositivos RF), um material 4122 é primeiro depositado sobre um substrato 4111, seguindo-se a deposição de um outro material 4133 (material para detectores futuros). O material 4133 pode ser selecionado a partir de materiais eletricamente condutores, piezoelétricos, materiais semicondutores, materiais sensíveis térmicos, materiais de emissão sensíveis a íons, materiais sensíveis à pressão, materiais sensíveis ao tensão mecânica ou materiais óticos. Opcionalmente, pode também consistir de materiais compósito ou uma pilha de material desejado. Se necessário, um detector integrado com um conjunto de subcomponentes pode ser colocado a este nível. Em seguida, o material 4133 é padronizado através de processos de litografia e ataque químico, formando um conjunto de características desejadas indicadas na Figura 41 (c). Outro material 4144 é subsequentemente depositado, o qual pode ser o mesmo ou diferente do material 4122. O material 4122 pode ser um material eletricamente isolante, tal como o óxido (SiO2), óxido dopado, nitreto de silício, ou um material polimérico. Em seguida, o material 4144 é opcionalmente planarizado, usando o polimento (por exemplo, usando polimento mecânico-químico) ou o processo reverso envolvendo ataque químico. A pilha de material é então padronizada utilizando litografia e processos de ataque químico, a alcançando o substrato 4111. Finalmente, como mostrado na Figura 41 (g), uma camada de nivelamento, ou a superfície de um outro componente 4155 é colocada no topo da pilha do material (e assim vedar ou fazer o capeamento), formando uma câmara de detecção encerrada 4166 com o detector 4177 para a detecção da amostra biológica
[00348] A Figura 42 ilustra outra forma de realização do método de fabricação da presente invenção para um dispositivo de detecção de detecção com câmaras encerradas, detectores, e canais para o transporte de amostras biológicas, tais como amostras de fluidos. Nesta concretização, seguindo um fluxo de processo opcional de fabricar um armazenamento de dados, processamento e análise de componentes (incluindo os transistores, dispositivos de memória, circuitos lógicos, e dispositivos de RF), um material 4222 é primeiro depositado sobre um substrato 4211, seguindo-se a deposição de um outro material 4233 (material de detectores futuros). O material 4233 pode ser selecionado a partir de materiais condutores de eletricidade, materiais piezoelétricos, materiais semicondutores, materiais sensíveis térmicos, materiais sensíveis à emissão de íons, materiais sensíveis à pressão, materiais sensíveis ao tensão mecânica e materiais ópticos. Opcionalmente, pode também incluir materiais compósitos ou uma pilha de material desejado. Se necessário, podem ser colocados a este nível um detector integrado com um conjunto de subcomponentes.
[00349] Em seguida, os materiais 4222 e 4233 são padronizados utilizando litografia e processos de ataque químico (Figura 42 (c)). Estas duas camadas (4222 e 4233) podem ser padronizados através de processos em separado, sequencialmente, ou podem ser padronizados no mesmo processo, dependendo da concepção do dispositivo, dos tipos de materiais e dos produtos químicos. O substrato 4211 é em seguida atacado quimicamente como mostrado na Figura 42 (d), formando uma zona rebaixada (cavidade), 4211, na qual as pilhas 4222 e 4233 podem ser usadas como uma máscara rígida durante o processo de ataque químico.
[00350] Um material 4244é depositado na área de recesso, e a porção de material 4244 acima do material 4233 é removido utilizando um polimento (química ou mecânico) ou um processo de ataque químico reverso. O material 4244 pode ser selecionado a partir de óxidos, óxidos dopados, nitreto de silício, e materiais poliméricos. A camada 4255 é então depositado sobre um material 4244, e padronizada de modo a formar pequenos orifícios em posições selecionadas. Em seguida, é utilizada a técnica de ataque químico a úmido ou a vapor para remover o material 4244, formando uma câmara de detecção encerrada 4266.
[00351] Opcionalmente, como mostrado na Figura 42 (i), o material 4233 também pode ser removido usando processos de ataque químico a úmido ou a vapor, formando canais 4288 que ligam as câmaras de detecção diferentes, formando assim câmaras de detecção com um detector 4277 alinhado com as paredes da câmara de detecção, e em que as amostras biológicas gasosos ou fluídicas através das câmaras. Finalmente, a superfície superior da câmara de detecção é selada com uma outra camada de material (por exemplo, 4255).
[00352] A Figura 43 mostra um novo método de detecção de doenças da presente invenção em que pelo menos uma sonda é lançada a uma velocidade e direção desejadas na direção de um material biológico, resultando em uma colisão. A resposta dada pelo material biológico, durante e/ou após a colisão é detectada e registrada, a qual pode proporcionar informação detalhada e microscópica no material biológico, tal como o peso, a densidade, a elasticidade, a rigidez, a estrutura de ligação (entre diferentes componentes do material biológico), propriedades elétricas, tais como a carga elétrica, propriedades magnéticas, informação estrutural e propriedades de superfície. Por exemplo, para um mesmo tipo de célula, espera-se que uma célula cancerosa irá experimentar uma menor distância itinerante após a colisão do que a de uma célula normal, devido à sua maior densidade, maior peso, e possivelmente maior volume. Como mostrado na Figura 43 (a), uma sonda 4311 é lançada para um material biológico 4322. Após a colisão com a sonda 4311, o material biológico 4322 pode ser empurrado (disperso) para uma distância de acordo com as suas propriedades, como mostrado na Figura 43 (b).
[00353] A Figura 43 (c) mostra um diagrama esquemático de um novo dispositivo de detecção de doenças com uma câmera de lançamento da sonda 4344, um conjunto de detectores 4333, um objeto de sonda 4322 e um material biológico a ser testado 4311. Em geral, o objeto de teste pode ser uma partícula inorgânica, uma partícula orgânica, uma partícula composta, ou um material biológico em si. A câmara de lançamento compreende um pistão para lançar o objeto, um sistema de controle com uma interface ligada a um circuito eletrônico ou um computador para instruções, e um canal para direcionar o objeto.
[00354] A Figura 44 ilustra um novo processo de fabricação que forma componentes múltiplos com diferentes materiais, ao nível mesmo dispositivo. Em primeiro lugar, um primeiro material 4422 é depositado sobre um substrato 4411 (ver Figura 44 (a)), seguindo-se a deposição de um segundo material 4433. Em seguida, o segundo material 4433 é padronizado para formar pelo menos uma porção de área rebaixada na camada 4433, utilizando técnicas de processos de ataque químico e litografia (ver Figura 44 (c)). Um terceiro material 4444 é subsequentemente depositado. O terceiro material pode ser o mesmo ou diferente do segundo material 4422.
[00355] O terceiro material diretamente acima do segundo material é retirado por meio de processos de ataque químico reverso e/ou processos de polimento (tal como o polimento mecânico-químico) (ver Figura 44 (e)). Opcionalmente, o terceiro material é em seguida padronizado para formar pelo menos uma porção de área rebaixada na camada 4444 (Figura 44 (f)). Um quarto material 4455 é então depositado. Opcionalmente, a porção do quarto material 4455 diretamente acima do terceiro material 4444 ou acima dos segundo e terceiros materiais são removidos por meio de ataque químico reverso e/ou polimento (tal como o polimento mecânico-químico). O processo acima pode continuar a repetir-se para formar várias características usando os mesmos materiais ou diferentes ao nível do mesmo dispositivo. Assim, este fluxo de processo forma pelo menos dois componentes 4466 e 4477 com materiais diferentes ou, com os mesmos materiais, ao nível mesmo dispositivo. Por exemplo, em um forma de realização, um componente pode ser utilizado como uma sonda e o outro pode ser usado como um detector.
[00356] A Figura 45 ilustra um método para detectar uma doença em um material biológico. Um material biológico 4501 passa através do canal 4531 a uma velocidade v, e a sonda 4511 é pode detectar grosseiramente as propriedades do material biológico a alta velocidade.
[00357] A sonda 4512 é um dispositivo de sondagem fino que é revestido por um material piezoelétrico. Existe uma distância A L entre a sonda 4511 e a sonda 4512.
[00358] Quando os materiais biológicos são testadas atravessarem 4511, se a entidade for identificada como sendo uma suspeita anormal, o sistema iria provocar a sonda piezoelétrica 4512 para se estender para dentro do canal e medir as propriedades específicas após um tempo de atraso de t. A sonda 4512 retrai-se após a entidade suspeita ter atravessado.
[00359] O dispositivo de sondagem é capaz de medir o nível microscópico uma propriedade elétrica, magnética, eletromagnética, térmica, óptica, acústica, biológica, química, eletromecânica, eletroquímica, eletroquímico-mecânica, bioquímica, biomecânica, bioeletromecânica, bioeletroquímica, bioeletroquímica-mecânica, física e mecânica do material biológico.
[00360] A largura do microcanal pode variar de cerca de 1 nm até cerca de 1 mm.
[00361] A Figura 46 mostra um processo de detecção de uma doença em um material biológico. Um material biológico 4601 passa através do canal 4631 a uma velocidade v . A sonda 4611 é uma sonda que pode grosseiramente detectar as propriedades do material biológico a alta velocidade. 4621 e 4622 são válvulas piezoelétricas para controlar os microcanais 4631 e 4632. 4612 é um dispositivo fino de sondagem que pode sondar as propriedades biológicas mais detalhadamente. 4631 é o canal de descarga para escoar objetos normais biológicas. 4632 é o canal de detecção onde as entidades suspeitas são detectados em detalhe.
[00362] Quando um material biológico é testado enquanto atravessa 4611, se for normal, a válvula 4621 do canal de descarga é aberta enquanto que a válvula de canal de detecção 4622 fica encerrada, o material biológico é então escoado sem uma detecção minuciosa. Quando o material biológico é testada enquanto atravessa 4611, se suspeita-se que seja anormal ou doente, a válvula 4621 do canal de descarga fica encerrada, enquanto que a válvula de canal de detecção 4622 fica aberta, o material biológico é então conduzido para o canal de detecção para uma sondagem mais detalhada.
[00363] A largura do microcanal pode variar de cerca de 1 nm a cerca de 1 mm .
[00364] O dispositivo de sondagem é capaz de medir o nível microscópico, uma propriedade elétrica, magnética, eletromagnética, térmica, óptica, acústica, biológica, química, eletromecânica, eletroquímica, eletroquímico-mecânica, bioquímica, biomecânica, bioeletromecânica, bioeletroquímica, bioeletroquímico-mecânica, física e mecânica do material biológico.
[00365] A Figura 47 ilustra um dispositivo de detecção em matriz biológica. 4701 são microcanais que podem atingir os fluidos e materiais biológicos. 4702 são sondas incorporadas de lado dos canais. Os sensores estão ligados por linhas de bits 4721 e linhas-texto 4722. Os sinais são aplicados e coletados pelo decodificador R\selecionar linha 4742 e o seletor do decodificador de coluna 4741. Como ilustrado na Figura 47-b, o dispositivo de detecção biológica-microcanal matriz 4700 pode ser incorporado em uma microcanal 4701. A dimensão do microcanal varia de cerca de 1 μm até cerca de 1 mm. A forma do microcanal pode ser retangular, elipse, circular ou poligonal.
[00366] O dispositivo de sondagem é capaz de medir em nível microscópico propriedades elétricas, magnéticas, eletromagnéticas, térmicas, ópticas, acústicas, biológicas, químicas, eletromecânicas, eletroquímicas, eletroquímica-mecânicas, bioquímicas, biomecânicas bioeletromecânicas, bioeletroquímicas, bioeletroquímico-mecânicas, físicas e mecânicas do material biológico.
[00367] A Figura 48 ilustra um dispositivo da presente invenção para detectar doença. 4801 é a entrada do dispositivo de detecção, e 4802 é a saída do dispositivo. 4820 é o canal no qual o material biológicos passa. 4811 é o componente óptico do dispositivo de detecção.
[00368] Como ilustrado na Figura 48 (b), o componente óptico 4811 consiste de um emissor óptico 4812 e um receptor óptico 4813. O emissor emite um pulso óptico (por exemplo, feixe de laser de impulsos) e, quando o material biológico 4801passa através do componente óptico, o sensor óptico detecta a difração do pulso óptico, em seguida, identifica a morfologia da entidade.
[00369] A largura do microcanal pode variar desde 1 nm até cerca de 1 milímetro.
[00370] Embora as concretizações específicas do presente invento tenham sido aqui ilustradas, será apreciado pelos peritos na arte que as modificações e variações podem ser feitas sem se afastar do espírito da invenção. Os exemplos e as ilustrações acima não se destinam a limitar o âmbito da presente invenção. Qualquer combinação dos aparelhos de detecção, microdispositivos, processos de fabrico, e aplicações da presente invenção, juntamente com qualquer extensão óbvia ou análogos, estão dentro do âmbito da presente invenção. Além disso, pretende-se que esta invenção englobe qualquer arranjo que seja calculado para conseguir o mesmo propósito, e todas essas variações e modificações caem dentro do âmbito das reivindicações anexas.
[00371] Todas as publicações referidas acima são aqui incorporadas por referência na sua totalidade. Todas as características descritas neste fascículo (incluindo quaisquer reivindicações anexas, resumos e figuras) podem ser substituídas por características alternativas que servem o mesmo, ou equivalente propósito, a menos que expressamente indicado de outra forma. Assim, a menos que expressamente declarado em contrário, cada característica revelada é um exemplo de uma série genérica de características equivalentes ou similares.
[00372] É para ser entendido que embora a invenção tenha sido descrita em conjunção com a descrição detalhada da mesma, a descrição anterior se destina a ilustrar, e não a limitar, o âmbito do invento, que é definido pelo âmbito das reivindicações anexas. Outros aspectos, vantagens e modificações estão dentro do âmbito das reivindicações que se seguem. Todas as publicações aqui referenciadas são incorporadas por referência na sua totalidade.
Claims (44)
1. Aparelho de detecção, caracterizado pelo fato de compreender um sistema para administrar um material biológico a ser detectado, e um dispositivo de sondagem e detecção para sondar e detectar o material biológico; em que o sistema para administrar um material biológico compreende um canal ou câmara; em que o dispositivo de sondagem e detecção compreende um primeiro microdispositivo de sondagem e um primeiro microdispositivo de detecção; pelo menos um do primeiro microdispositivo de sondagem e primeiro microdispositivo de detecção é apoiado por um primeiro substrato que forma uma parte do canal ou da câmara; e o primeiro microdispositivo de sondagem e o primeiro microdispositivo de detecção são anexados a uma parede interior ou exterior do canal ou da câmara; em que pelo menos um microdispositivo de sondagem é capaz de aplicar um sinal ao material biológico, assim estimulando o material biológico e fazendo com que este tenha uma resposta intrínseca; em que o material biológico compreende uma amostra líquida de sangue, urina, suor ou saliva, que adicionalmente compreende uma ou mais células, proteínas ou DNAs; em que pelo menos um microdispositivo de detecção compreende um sensor configurado para contatar a amostra biológica a ser detectada e diretamente mede, no nível microscópico, a resposta intrínseca da amostra biológica, em que quando a amostra biológica viaja em uma certa direção no sistema, a detecção ocorre após a amostra biológica viajar uma distância a partir da função de sonda.
2. Aparelho, de acordo com a reivindicação 1, caracterizado pelo fato de que cada microdispositivo de detecção é opcionalmente capaz de medir, no nível microscópico, uma propriedade da amostra biológica; a propriedade medida por cada microdispositivo de detecção ou o sinal de resposta medido por cada microdispositivo detector compreende as propriedades elétricas, magnéticas, eletromagnéticas, térmicas, ópticas, acústicas, biológicas, químicas, eletromecânicas, eletroquímicas, eletroquímico-mecânicas, biofísicas, físico-químicas, bioquímicas, biofísico- químicas, biomecânicas, bioeletromecânicas, bioeletroquímicas, bioeletroquímico-mecânicas, físicas e mecânicas do material biológico.
3. Aparelho de acordo com a reivindicação 2, caracterizado pelo fato de que a propriedade elétrica é a carga superficial, potencial da superfície, potencial de repouso, potencial de ação, tensão elétrica, corrente elétrica, distribuição do campo elétrico, distribuição da carga elétrica, dipolo elétrico, quádruplo elétrico, distribuição tridimensional de nuvem elétrica ou carga, propriedades elétricas em telômeros do DNA e de cromossomos, mudanças dinâmicas nas propriedades elétricas, mudanças dinâmicas em potencial, mudanças dinâmicas na carga de superfície, mudanças dinâmicas na corrente, mudanças dinâmicas no campo elétrico, mudanças dinâmicas na tensão elétrica, mudanças dinâmicas na distribuição de energia elétrica, mudanças dinâmicas na distribuição da nuvem eletrônica, e/ou impedância; a propriedade térmica é a temperatura, ou a frequência vibracional do material biológico ou moléculas; a propriedade óptica é a absorção óptica, reflexão óptica, transmissão óptica, propriedade óptica-elétrica, brilho ou emissão fluorescente; a propriedade química é o valor do pH, reação química, reação bioquímica, reação bioeletroquímica, velocidade da reação, energia da reação, concentração de oxigênio, taxa de consumo de oxigênio, força iônica, comportamento catalítico, e força de ligação; a propriedade física é a densidade ou o tamanho geométrico; a propriedade acústica é a frequência e velocidade das ondas acústicas, frequência e intensidade do espectro distribuição acústica, intensidade acústica, absorção acústica, e ressonância acústica, e a propriedade mecânica é a pressão interna, dureza, resistência ao corte, força de alongamento força de resistência à fratura, adesão, frequência de ressonância mecânica, elasticidade, plasticidade e compressibilidade.
4. Aparelho de acordo com a reivindicação 2, caracterizado pelo fato de que o dispositivo de detecção de sondagem e se aplica ao material biológico uma tensão compreendida entre cerca de 1 mV e cerca de 10 V ou entre cerca de 1 mV e cerca de 1,0 V.
5. Aparelho de acordo com a reivindicação 2, caracterizado pelo fato de que cada microdispositivo de detecção compreende um material eletricamente condutor, um material eletricamente isolante, um material biológico, ou um material semicondutor.
6. Aparelho de acordo com a reivindicação 2, caracterizado pelo fato de que cada microdispositivo de detecção tem um tamanho que varia de cerca de 11 angstrom até cerca de 5 milímetros.
7. Aparelho de acordo com a reivindicação 2, caracterizado pelo fato de que os microdispositivos de detecção são espaçados para fora sobre o substrato, por uma distância de pelo menos 10 angstroms ou em que a distância entre 2 microdispositivos adjacentes varia entre cerca de 5 mícrons e cerca de 100 mícrons.
8. Aparelho de acordo com a reivindicação 2, caracterizado pelo fato de que o substrato é um objeto tridimensional ou está na forma de uma laje, um tubo, uma matriz de tubos, um retângulo, ou uma matriz de retângulos.
9. Aparelho de acordo com a reivindicação 2, caracterizado pelo fato de que o dispositivo de sondagem e detecção compreende adicionalmente uma segundo substrato do mesmo material ou diferente do primeiro substrato.
10. Aparelho de acordo com a reivindicação 2, caracterizado pelo fato de que compreende adicionalmente um dispositivo para a leitura dos dados a partir da medição da propriedade do dispositivo de sondagem e detecção.
11. Aparelho de acordo com a reivindicação 1, caracterizado pelo fato de compreender adicionalmente um sistema de fornecimento de fluido, o qual compreende um gerador de pressão, um regulador de pressão, uma válvula de estrangulamento, um manômetro de pressão, e um kit de distribuição; um controlador de sistema que compreende um pré- amplificador, um amplificador lock-in, um medidor elétrico, um medidor térmico, uma matriz de comutação, um barramento de sistema, um dispositivo de armazenamento não volátil, uma memória de acesso aleatório, um circuito lógico, um receptor de sinais, um transmissor de sinais, um processador, ou uma interface de utilizador; uma interface biológica, um controlador de sistema, ou pelo menos um sistema para a recuperação ou tratamento de resíduos hospitalares; um sistema de administração de teste da amostras, sistema de distribuição de teste da amostra, um canal de distribuição, um dispositivo de detecção, um sistema de posicionamento global, um dispositivo de movimento, um transmissor de sinal, um receptor de sinal, um sensor, uma unidade de armazenamento de memória, uma unidade de processamento lógico, um chip de aplicação específica, uma unidade de recuperação e reciclagem do teste da amostra, um microdispositivo eletromecânico, um dispositivo multifuncional, ou um microinstrumento para efetuar cirurgia, limpeza, ou função médica; uma unidade para administrar material biológico, um canal, uma unidade de detecção, uma unidade de armazenamento de dados, uma unidade de análise de dados, uma unidade de controle central, um unidade de recirculação da amostra biológica, ou uma unidade de eliminação de resíduos; ou uma unidade de pré-processamento, uma unidade de processamento de sinais, ou unidade de processamento de eliminação.
12. Aparelho de acordo com a reivindicação 11, caracterizado pelo fato de que o gerador de pressão compreende um sistema de motor a pistão ou um depósito contendo gás comprimido; ou em que o medidor de pressão relança o valor medido para a válvula de estrangulamento, que, em seguida, regula a pressão para se aproximar do valor alvo; a interface compreende um sensor; a recuperação e tratamento de resíduos médicos são realizados pelo mesmo ou por dois sistemas diferentes; a unidade de pré-processamento compreende uma unidade de filtração da amostra, uma unidade de recarga, uma unidade de fornecimento de pressão constante, ou uma unidade de perturbação de pré-sondagem da amostra; a unidade de processamento do sinal compreende um amplificador, um amplificador lock-in, um conversor A/D, um microcomputador, um manipulador, um monitor, ou uma ligação de rede.
13. Aparelho de acordo com a reivindicação 11, caracterizado pelo fato de que o fluido a ser administrado é um líquido ou gás.
14. Aparelho de acordo com a reivindicação 13, caracterizado pelo fato de que o líquido é sangue, urina, saliva, lágrimas, solução salina, ou suor; e em que o gás é nitrogênio, argônio, hélio, neon, criptônio, xenônio, ou radônio.
15. Aparelho de acordo com a reivindicação 12, caracterizado pelo fato de que o sensor é um sensor térmico, um medidor de fluxo, um sensor óptico, ou um medidor de piezo.
16. Aparelho de acordo com a reivindicação 1, caracterizado pelo fato de que o sistema para administrar material biológico compreende pelo menos um canal no interior do qual o material biológico a ser detectado percorre em uma determinada direção; o dispositivo de sondagem e detecção compreende pelo menos um microdispositivo de sondagem e pelo menos um microdispositivo de detecção, pelo menos um microdispositivo sondagem está localizado antes do microdispositivo de detecção em relação à direção de passagem dos materiais biológicos, e o microdispositivo de sondagem e o microdispositivo de detecção podem estar ligados ao interior ou exterior da parede do canal.
17. Aparelho de acordo com a reivindicação 16, caracterizado pelo fato de que o dispositivo de sondagem e detecção compreende pelo menos dois dispositivos de detecção capazes de medir ao micronível, as propriedades iguais ou diferentes do material biológico.
18. Aparelho de acordo com a reivindicação 17, caracterizado pelo fato de que os microdispositivos de detecção são capazes de medir o nível microscópico, a carga de superfície, o potencial de superfície, o potencial de repouso, o potencial de ação, a tensão elétrica, a corrente elétrica, a distribuição do campo elétrico, a distribuição da carga elétrica, dipolo elétrico, quádruplo elétrico, distribuição tridimensional da nuvem ou carga elétrico, propriedades elétricas em telômeros do DNA e cromossomos, mudanças dinâmicas nas propriedades elétricas, mudanças dinâmicas em potencial, mudanças dinâmicas na carga de superfície, mudanças dinâmicas na corrente, mudanças dinâmicas no campo elétrico, mudanças dinâmicas na tensão elétrica, mudanças dinâmicas na distribuição elétrica, mudanças dinâmicas na distribuição da nuvem eletrônica, impedância, temperatura, frequência vibracional, absorção óptica, transmissão óptica, reflexão óptica, propriedade óptica-elétrica, brilho, emissão fluorescente, pH, reação química, reação bioquímica, reação bioeletro-química, velocidade da reação, energia da reação, velocidade de reação, concentração de oxigênio, taxa de consumo de oxigênio, força iônica, comportamento catalítico, força de ligação, densidade, tamanho geométrico, frequência e velocidade das ondas acústicas, distribuição do espectro de frequência e intensidade, intensidade acústica, absorção acústica, ressonância acústica, pressão interna, dureza, resistência ao cisalhamento, força de alongamento, tensão na ruptura, aderência, frequência de ressonância mecânica, elasticidade, plasticidade ou compressibilidade.
19. Aparelho de acordo com a reivindicação 16, caracterizado pelo fato de que o canal pode ser reto, curvo, ou angular ou em que a largura do canal varia entre cerca de 1 nm a cerca de 1 mm; ou a parede interior do canal define um espaço circular, oval, retangular, ou poligonal, ou tem pelo menos uma concavidade que pode ser na mesma seção do microdispositivo de sondagem ou detecção.
20. Aparelho de acordo com a reivindicação 19, caracterizado pelo fato de que o canal é um nanotubo circular de carbono.
21. Aparelho de acordo com a reivindicação 20, caracterizado pelo fato de que o nanotubo de carbono tem um diâmetro que varia entre cerca 0,5 nm a cerca de 100 nm, e um comprimento que varia de cerca de 5.0 nm até cerca de 10 mm.
22. Aparelho de acordo com a reivindicação 19, caracterizado pelo fato de que a ranhura côncava tem um espaço cúbico ou angular ou em que a ranhura côncava tem uma profundidade que varia entre cerca 10 nm até cerca de 1 mm.
23. Aparelho de acordo com a reivindicação 16, caracterizado pelo fato de que um fluido de distribuição é injetado para dentro do canal, opcionalmente através de um canal de distribuição de fluido ligado a uma abertura na parede do canal, seja antes ou depois do material biológico passar pelo microdispositivo de sondagem, para auxiliar a percorrer ou a se separar do material biológico dentro do canal.
24. Aparelho de acordo com a reivindicação 16, caracterizado pelo fato de que o aparelho serve para detectar doenças em mais que um material biológico, e o canal compreende um dispositivo localizado no seu interior para separar ou dividir os materiais biológicos com base em níveis diferentes de uma mesma propriedade.
25. Aparelho de acordo com a reivindicação 24, caracterizado pelo fato de que o dispositivo de separação ou divisão é uma fenda e separa ou divide materiais biológicos baseadas em suas cargas de superfície.
26. Aparelho de acordo com a reivindicação 16, caracterizado pelo fato de compreender adicionalmente um dispositivo de filtragem para remover objetos irrelevantes ao material biológico para detecção.
27. Aparelho de acordo com a reivindicação 1, caracterizado pelo fato de que o material biológico é um telômero de DNA ou cromossomo.
28. Aparelho de acordo com a reivindicação 11, caracterizado pelo fato de que o aparelho é integrado em um único dispositivo ou painel.
29. Aparelho de acordo com a reivindicação 12, caracterizado pelo fato de que a unidade de filtração da amostra compreende um canal de entrada, um canal de fluido de perturbação, uma câmara de aceleração, ou uma fenda, ou compreende um canal de entrada, um microfiltro biocompatível, ou um canal de saída; a unidade perturbadora de pré-sondagem da amostra compreende um microdispositivo com um canal, um par de placas, ou uma fenda situada no canal para separar o canal em um canal superior e um canal inferior; a unidade de recarga recarrega nutriente ou gás respirador para o material biológico; a unidade de processamento do sinal compreende um amplificador, um amplificador lock-in, um conversor A/D, um microcomputador, um manipulador, um monitor, ou uma ligação de rede.
30. Aparelho de acordo com a reivindicação 29, caracterizado pelo fato de que um fluido biocompatível é injetado no interior do canal perturbador do fluido, opcionalmente a partir da entrada do canal perturbador do fluido e administrado a uma abertura na parede do canal de entrada, para separar o material biológico.
31. Aparelho de acordo com a reivindicação 30, caracterizado pelo fato de que o fluido biocompatível compreende água, solução salina, um líquido rico em oxigênio, e plasma.
32. Aparelho de acordo com a reivindicação 29, caracterizado pelo fato de que o ângulo entre o canal de entrada e o canal perturbador do fluido varia entre cerca de 0°-180°, ou entre 30°-150°, ou entre 60°-120°, ou entre 75°-105°, ou cerca de 90°.
33. Aparelho de acordo com a reivindicação 29, caracterizado pelo fato de que a largura de cada um dos canais varia entre cerca de 1 nm até cerca de 1 mm.
34. Aparelho de acordo com a reivindicação 29, caracterizado pelo fato de pelo menos um dos canais compreender um ou mais dispositivos de sondagem ligados à parede lateral do canal, no qual cada dispositivo de sondagem é capaz de medir o nível microscópico uma propriedade bioelétrica, magnética, eletromagnética, térmica, óptica, acústica, biológica, química, físico-química, biofísica, biofísico-química, eletromecânica, eletroquímica, eletroquímico-mecânica, bioquímica, biomecânica, bioeletromecânica, bioeletroquímica, bioeletroquímico-mecânica, física e mecânica do material biológico.
35. Aparelho de acordo com a reivindicação 29, caracterizado pelo fato de que o microfiltro biocompatível é capaz de filtrar o material biológico com base em pelo menos uma propriedade elétrica, magnética, eletromagnética, tamanho físico, dureza, elasticidade, resistência ao corte, peso, característica de superfície, ótica, acústica, térmica, química, mecânica, biológica, bioquímica, físico-química, biofísica, biofísico-química, elétrica, eletroquímica, magnética, eletromagnética, eletromecânica, eletroquímico- mecânica e eletroquímico-biológica.
36. Aparelho de acordo com a reivindicação 34, caracterizado pelo fato de que a propriedade elétrica é a carga superficial, potencial da superfície, potencial de repouso, potencial de ação, tensão elétrica, corrente elétrica, distribuição do campo elétrico, distribuição da carga elétrica, dipolo elétrico, quádruplo elétrico, distribuição tridimensional da nuvem elétrica ou carga, propriedades elétricas em telômeros do DNA e de cromossomos, mudanças dinâmicas nas propriedades elétricas, mudanças dinâmicas em potencial, mudanças dinâmicas na carga de superfície, mudanças dinâmicas na corrente, mudanças dinâmicas no campo elétrico, dinâmico mudanças na tensão elétrica, mudanças dinâmicas na distribuição de energia elétrica, mudanças dinâmicas na distribuição da nuvem eletrônica e impedância; a propriedade térmica é a temperatura e frequência de vibração; a propriedade óptica é a absorção óptica, transmissão óptica, reflexão óptica, propriedade óptico-elétrica, brilho e emissão fluorescente; a propriedade química é o valor de pH, reação química, reação bioquímica, reação bioeletroquímica, velocidade de reação, energia da reação, concentração de oxigênio, taxa de consumo de oxigênio, força iônica, comportamento catalítico, força de ligação; a propriedade física é a densidade ou o tamanho geométrico; a propriedade acústica é frequência, velocidade das ondas acústicas, frequência acústica e distribuição do espectro de intensidade, intensidade acústica, absorção acústica, e ressonância acústica; e a propriedade mecânica é pressão interna, dureza, resistência ao cisalhamento, força de alongamento, tensão na ruptura, adesão, frequência de ressonância mecânica, elasticidade, plasticidade e compressibilidade.
37. Aparelho de acordo com a reivindicação 34, caracterizado pelo fato de que os dois ou mais dispositivos de sondagem são colocados com uma desejada distância entre si.
38. Aparelho de acordo com a reivindicação 29, caracterizado pelo fato de que a unidade perturbadora de pré-sondagem da amostra se aplica ao material biológico um sinal elétrico, magnético, eletromagnético, térmico, óptico, acústico, biológico, químico, físico, químico, eletromecânico, eletroquímico, eletroquímico-mecânico, bioquímico, biofísico, biofísico- mecânico, biomecânico, bioeletromecânico, bioeletroquímico, bioeletroquímico-mecânico, físico ou mecânico, e opcionalmente o sinal é pulsado ou constante.
39. Aparelho de acordo com a reivindicação 29, caracterizado pelo fato de que o nutriente compreende um eletrólito biocompatível forte ou fraco, aminoácido, mineral, íons, oxigênio, líquido rico em oxigênio, gotejamento intravenoso, glucose, ou uma proteína; e o gás respirador compreende o oxigênio.
40. Aparelho de acordo com a reivindicação 1, caracterizado pelo fato de que o material biológico compreende sangue, urina, saliva, lacrimal, soro fisiológico, e suor.
41. Aparelho de detecção, caracterizado pelo fato de compreender uma câmara de lançamento para lançar um objeto de sonda a uma velocidade e direção desejadas, uma unidade de detecção, um objeto de sonda, um componente de detecção, um canal para o transporte do material biológico a ser testado, e o objeto de sonda, em que o objeto de sonda é lançado para aplicar um sinal ao material biológico, assim estimulando o material biológico e fazendo com que este tenha uma resposta intrínseca; em que a amostra biológica compreende uma amostra líquida de sangue, urina, suor ou saliva, que adicionalmente compreende uma ou mais células, proteínas ou DNAs; em que a unidade de detecção compreende um sensor configurado para contatar o material biológico a ser detectado e medir diretamente, em nível microscópico, a resposta intrínseca do material biológico, em que quando o material biológico viaja em uma certa direção no sistema, a detecção ocorre após o material biológico viajar uma distância a partir da função de sonda.
42. Aparelho de acordo com a reivindicação 41, caracterizado pelo fato de que a câmara de lançamento compreende um pistão para liberar o objeto de sonda, e um canal para direcionar o objeto de sonda.
43. Aparelho de acordo com a reivindicação 41, caracterizado pelo fato de que a unidade de detecção ou o componente de detecção é capaz de medir em nível microscópico uma propriedade elétrica, magnética, eletromagnética, térmica, óptica, acústica, biológica, química, eletromecânica, eletroquímica, eletroquímica-mecânica, bioquímica, físico-química, biofísica, biofísico-mecânica, biomecânica, bioeletromecânica, bioeletroquímica, bioeletroquímico-mecânica, física e mecânica do material biológico.
44. Aparelho de acordo com a reivindicação 44, caracterizado pelo fato de que a propriedade eletrônica é a carga de superfície, potencial de superfície, potencial de repouso, potencial de ação, tensão elétrica, corrente elétrica, distribuição do campo elétrico, distribuição da carga elétrica, dipolo elétrico, quádruplo elétrico, distribuição tridimensional da nuvem elétrica ou carga, propriedades elétricas em telômeros do DNA e de cromossomos, mudanças dinâmicas nas propriedades elétricas, mudanças dinâmicas em potencial, mudanças dinâmicas na carga de superfície, mudanças dinâmicas na corrente, mudanças dinâmicas no campo elétrico, mudanças dinâmicas na tensão elétrica, mudanças dinâmicas na distribuição de energia elétrica, mudanças dinâmicas na distribuição da nuvem eletrônica, e impedância; a propriedade térmica é a temperatura ou frequência de vibração; a propriedade óptica é a absorção óptica, transmissão óptica, reflexão óptica, propriedade óptico-elétrica, brilho ou emissão fluorescente; a propriedade química é o valor de pH, reação química, reação bioquímica, de reação bioeletroquímica, velocidade da reação, energia da reação, concentração de oxigênio, taxa de consumo de oxigênio, força iônica, comportamento catalítico, força de ligação; a propriedade física é a densidade ou o tamanho geométrico; a propriedade acústica é frequência e velocidade das ondas acústicas, frequência acústica e distribuição do espectro de intensidade, intensidade acústica, absorção acústica, ressonância acústica; e a propriedade mecânica é a pressão interna, dureza, resistência ao cisalhamento, força de alongamento, tensão na ruptura, adesão, frequência de ressonância mecânica, elasticidade, plasticidade e compressibilidade.
Applications Claiming Priority (11)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US36004110P | 2010-06-30 | 2010-06-30 | |
| US61/360041 | 2010-06-30 | ||
| US38996010P | 2010-10-05 | 2010-10-05 | |
| US61/389960 | 2010-10-05 | ||
| US201161430641P | 2011-01-07 | 2011-01-07 | |
| US61/430641 | 2011-01-07 | ||
| US201161467097P | 2011-03-24 | 2011-03-24 | |
| US61/467097 | 2011-03-24 | ||
| US201161498954P | 2011-06-20 | 2011-06-20 | |
| US61/498954 | 2011-06-20 | ||
| PCT/US2011/042637 WO2012003348A2 (en) | 2010-06-30 | 2011-06-30 | Apparatus for disease detection |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| BR112012033783A2 BR112012033783A2 (pt) | 2016-11-01 |
| BR112012033783B1 true BR112012033783B1 (pt) | 2021-02-09 |
Family
ID=45402656
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BR112012033783-1A BR112012033783B1 (pt) | 2010-06-30 | 2011-06-30 | aparelho de detecção |
Country Status (12)
| Country | Link |
|---|---|
| US (2) | US10161927B2 (pt) |
| EP (1) | EP2588860A4 (pt) |
| JP (1) | JP6566508B2 (pt) |
| KR (3) | KR102018210B1 (pt) |
| CN (7) | CN105342553B (pt) |
| AU (2) | AU2011272837B2 (pt) |
| BR (1) | BR112012033783B1 (pt) |
| CA (1) | CA2803632A1 (pt) |
| IL (1) | IL224016B (pt) |
| NZ (1) | NZ606052A (pt) |
| WO (1) | WO2012003348A2 (pt) |
| ZA (1) | ZA201300435B (pt) |
Families Citing this family (52)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9487812B2 (en) * | 2012-02-17 | 2016-11-08 | Colorado School Of Mines | Optical alignment deformation spectroscopy |
| US9878326B2 (en) | 2007-09-26 | 2018-01-30 | Colorado School Of Mines | Fiber-focused diode-bar optical trapping for microfluidic manipulation |
| US9885644B2 (en) | 2006-01-10 | 2018-02-06 | Colorado School Of Mines | Dynamic viscoelasticity as a rapid single-cell biomarker |
| US10722250B2 (en) | 2007-09-04 | 2020-07-28 | Colorado School Of Mines | Magnetic-field driven colloidal microbots, methods for forming and using the same |
| CN103562728B (zh) | 2011-03-24 | 2016-08-17 | 安派科生物医学科技有限公司 | 用于疾病检测的微器件 |
| CN106995780B (zh) * | 2011-05-05 | 2019-11-22 | 安派科生物医学科技有限公司 | 肿瘤细胞检测仪 |
| ES2797448T3 (es) | 2011-08-01 | 2020-12-02 | Bio Rad Laboratories | Sistema de captura de células |
| WO2013126412A1 (en) * | 2012-02-20 | 2013-08-29 | Advanced Tactical Ordnance LLC | Chimeric dna identifier |
| EP2823305B1 (en) * | 2012-03-08 | 2021-02-24 | Anpac Bio-Medical Science (Lishui) Co., Ltd. | Micro-devices for improved disease detection |
| TWI630385B (zh) | 2012-07-16 | 2018-07-21 | 昌和生物醫學科技(揚州)有限公司 | 增強疾病檢測與鑒定的器件與方法 |
| US11371951B2 (en) | 2012-09-27 | 2022-06-28 | Sensirion Ag | Gas sensor comprising a set of one or more sensor cells |
| US8802568B2 (en) | 2012-09-27 | 2014-08-12 | Sensirion Ag | Method for manufacturing chemical sensor with multiple sensor cells |
| EP2941645B1 (en) * | 2013-01-07 | 2018-06-13 | Shanghai Xinshenpai Technology Co., Ltd. | Apparatus for improved detection of cancer or heart disease |
| US8896211B2 (en) | 2013-01-16 | 2014-11-25 | Orteron (T.O) Ltd | Physical means and methods for inducing regenerative effects on living tissues and fluids |
| US10266802B2 (en) | 2013-01-16 | 2019-04-23 | Orteron (T.O) Ltd. | Method for controlling biological processes in microorganisms |
| WO2014122873A1 (ja) * | 2013-02-08 | 2014-08-14 | ソニー株式会社 | 微小粒子分析装置及び微小粒子分析システム |
| CA2906962C (en) | 2013-03-15 | 2022-10-11 | Anpac Bio-Medical Science (Lishui) Co., Ltd. | Methods and apparatus for enhanced detection of diseases |
| BR112015027225B1 (pt) | 2013-04-30 | 2021-11-03 | Hewlett-Packard Development Company, L.P. | Dispositivo sensor microfluídico |
| CN104162457B (zh) * | 2013-05-16 | 2020-08-04 | 昌微系统科技(上海)有限公司 | 一种微流体器件及其制造方法 |
| EP3060124B1 (en) * | 2013-10-23 | 2020-04-15 | Verily Life Sciences LLC | Spatial modulation of magnetic particles in vasculature by external magnetic field |
| KR101731240B1 (ko) | 2014-04-24 | 2017-04-28 | 다이치 키겐소 카가쿠 코교 컴퍼니 리미티드 | 가넷형 화합물의 제조 방법, 가넷형 화합물 및 상기 가넷형 화합물을 포함한 전고체 리튬 2차 전지 |
| KR101528773B1 (ko) * | 2014-05-16 | 2015-06-15 | 연세대학교 산학협력단 | 대기중의 바이오 입자 및 넌바이오 입자 실시간 검출장치 및 이를 이용한 검출방법 |
| EP2952885B1 (en) * | 2014-06-02 | 2016-07-27 | Sensirion AG | Gas sensor |
| US11536707B2 (en) * | 2014-09-23 | 2022-12-27 | Tearlab Research, Inc. | Systems and methods for integration of microfluidic tear collection and lateral flow analysis of analytes of interest |
| US10704965B2 (en) * | 2014-12-09 | 2020-07-07 | Technion Research & Development Foundation Ltd. | High resolution pressure sensing |
| USD765215S1 (en) | 2015-01-22 | 2016-08-30 | United Tactical Systems, Llc | Non-lethal projectile |
| US10705012B2 (en) * | 2015-04-23 | 2020-07-07 | Singapore University Of Technology And Design | Device and method for analysing and controlling cell motility |
| US10379131B2 (en) | 2015-11-18 | 2019-08-13 | Elbit Systems Of America/Kmc Systems, Inc. | Systems and methods for detecting a liquid level |
| US10030961B2 (en) | 2015-11-27 | 2018-07-24 | General Electric Company | Gap measuring device |
| JP6540891B2 (ja) | 2016-05-13 | 2019-07-10 | 株式会社村田製作所 | 嚥下センサおよびそれを備える嚥下能力診断システム |
| CN106357741A (zh) * | 2016-08-28 | 2017-01-25 | 武汉山不厌高科技有限公司 | 一种尿液分析数据的云平台 |
| CN106353702B (zh) * | 2016-09-14 | 2018-11-13 | 广东顺德中山大学卡内基梅隆大学国际联合研究院 | 一种基于面内伸缩模态谐振器的mems磁场传感器及制备方法 |
| GB201704772D0 (en) | 2017-01-05 | 2017-05-10 | Illumina Inc | Automated volumetric reagent delivery testing |
| EP3448980A4 (en) * | 2017-03-10 | 2019-05-01 | Shanghai Xinshenpai Technology Co., Ltd. | NEW APPARATUS AND METHODS FOR DETECTING DISEASE |
| CN110869994B (zh) * | 2017-09-28 | 2022-09-13 | 株式会社耐奥飞特 | 钉板、康复训练系统及康复训练方法 |
| JP2021518744A (ja) * | 2018-04-23 | 2021-08-05 | アンパック バイオ−メディカル サイエンス カンパニー リミテッドAnpac Bio−Medical Science Co.,Ltd. | 疾患を検出する新規の装置および方法 |
| CN108846896A (zh) * | 2018-06-29 | 2018-11-20 | 南华大学 | 一种自动分子蛋白质分子体学诊断系统 |
| WO2020012263A1 (en) * | 2018-07-09 | 2020-01-16 | Presens Precision Sensing Gmbh | System for analysis of a fluid sample |
| CN109044411B (zh) * | 2018-09-06 | 2021-04-23 | 清华大学深圳研究生院 | 基于毛细力驱动的泪液检测接触镜 |
| CN109540969B (zh) * | 2018-11-13 | 2021-01-05 | 中国科学院微电子研究所 | SiC氧化中SiC-SiO2界面碳杂质类型与位置分布的测定方法 |
| WO2020102768A1 (en) * | 2018-11-16 | 2020-05-22 | NeuroSilica, Inc. | A novel multilayered composite material utilizing quantum dot based photovoltaic effect for bi-directional brain-computer interface |
| US10665581B1 (en) | 2019-01-23 | 2020-05-26 | Sandisk Technologies Llc | Three-dimensional semiconductor chip containing memory die bonded to both sides of a support die and methods of making the same |
| US10879260B2 (en) | 2019-02-28 | 2020-12-29 | Sandisk Technologies Llc | Bonded assembly of a support die and plural memory dies containing laterally shifted vertical interconnections and methods for making the same |
| CN109975411B (zh) * | 2019-04-17 | 2021-09-24 | 江苏至上检测科技有限公司 | 轴零件批量相控阵超声检测流水线 |
| CN110772247A (zh) * | 2019-09-19 | 2020-02-11 | 北京航空航天大学 | 一种用于同步同位检测生物电信号与压力信号的传感器件 |
| CN111060170B (zh) * | 2019-11-20 | 2021-03-02 | 郑州大学 | 柔性微流管道气体流量传感器及其制备方法、使用方法 |
| JP7290345B2 (ja) * | 2020-02-25 | 2023-06-13 | Blue Industries株式会社 | 遺伝子解析用前処理キット、核酸分析用チップ、解析システム、生体物質分析用チップ |
| KR102402112B1 (ko) * | 2020-04-27 | 2022-05-25 | 한국식품연구원 | 메타 구조체를 이용한 품질 분석용 나노 센서 |
| CN112394159A (zh) * | 2020-09-30 | 2021-02-23 | 中铁二十三局集团第六工程有限公司 | 一种用于隧道测量的tbm机械改进勘测装置及其使用方法 |
| KR102495522B1 (ko) * | 2021-03-26 | 2023-02-06 | 한국과학기술원 | 맥박 센싱 모듈 및 이를 이용하여 혈압을 산출하기 위한 시스템 |
| CN113457758B (zh) * | 2021-07-14 | 2023-05-23 | 浙江理工大学 | 一种导纳式测量出汗率的微流控通道 |
| CN117470719B (zh) * | 2023-12-27 | 2024-03-12 | 山西省生态环境监测和应急保障中心(山西省生态环境科学研究院) | 一种具有多功能的环境监测机器人 |
Family Cites Families (58)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4361026A (en) | 1980-06-24 | 1982-11-30 | Muller Richard S | Method and apparatus for sensing fluids using surface acoustic waves |
| US4737268A (en) * | 1986-03-18 | 1988-04-12 | University Of Utah | Thin channel split flow continuous equilibrium process and apparatus for particle fractionation |
| AU6354190A (en) * | 1989-08-21 | 1991-04-03 | Board Of Regents Of The University Of Washington, The | Multiple-probe diagnostic sensor |
| JP2832117B2 (ja) * | 1991-11-29 | 1998-12-02 | キヤノン株式会社 | サンプル測定デバイス及びサンプル測定システム |
| DE19520298A1 (de) * | 1995-06-02 | 1996-12-05 | Bayer Ag | Sortiervorrichtung für biologische Zellen oder Viren |
| NZ315428A (en) * | 1995-07-25 | 2000-02-28 | Horus Therapeutics Inc | Computer assisted methods for diagnosing diseases |
| FR2777293B1 (fr) * | 1998-04-10 | 2000-05-19 | Bio Merieux | Procede d'electro-separation d'un echantillon biologique et dispositif de mise en oeuvre |
| AU763433B2 (en) * | 1998-05-22 | 2003-07-24 | California Institute Of Technology | Microfabricated cell sorter |
| US20030235920A1 (en) * | 2000-02-28 | 2003-12-25 | James Wyatt | Diagnostic device and method |
| CN1122499C (zh) * | 1999-06-17 | 2003-10-01 | 曾金铃 | 疾病诊断预测系统 |
| JP2003510034A (ja) * | 1999-08-26 | 2003-03-18 | ザ トラスティーズ オブ プリンストン ユニバーシティ | 流体の静電容量の変化を検出するためのマイクロ流体およびナノ流体電子素子並びに使用方法 |
| JP2001347499A (ja) | 2000-06-05 | 2001-12-18 | Sony Corp | 微細装置の製造方法 |
| US7351376B1 (en) | 2000-06-05 | 2008-04-01 | California Institute Of Technology | Integrated active flux microfluidic devices and methods |
| US20050009004A1 (en) * | 2002-05-04 | 2005-01-13 | Jia Xu | Apparatus including ion transport detecting structures and methods of use |
| ATE419387T1 (de) * | 2001-04-23 | 2009-01-15 | Samsung Electronics Co Ltd | Verfahren zur herstellung eines chips zum molekularen nachweis |
| DK1460415T3 (da) * | 2001-11-19 | 2011-04-26 | Panasonic Corp | Måleindretning til måling af et elektrisk signal, der afgives af en biologisk prøve |
| US7252987B2 (en) * | 2001-12-06 | 2007-08-07 | Islet Technology, Inc. | System for analysis and selection of encapsulated cellular materials |
| ES2217208T3 (es) * | 2002-02-01 | 2004-11-01 | Leister Process Technologies | Componente microfluido y procedimiento para la clasificacion de particulas en un fluido. |
| AU2003243165A1 (en) | 2002-04-26 | 2003-11-10 | The Penn State Research Foundation | Integrated nanomechanical sensor array chips |
| JP2004069395A (ja) * | 2002-08-02 | 2004-03-04 | Nec Corp | マイクロチップ、マイクロチップの製造方法および成分検出方法 |
| AU2003278461A1 (en) * | 2002-10-16 | 2004-05-04 | Cellectricon Ab | Nanoelectrodes and nanotips for recording transmembrane currents in a plurality of cells |
| JP2004249674A (ja) * | 2003-02-21 | 2004-09-09 | Riso Kagaku Corp | 排版ボックス及び孔版印刷装置 |
| DK2309245T3 (en) | 2003-03-28 | 2016-01-04 | Inguran Llc | Methods for providing sex-sorted animal semen |
| CN1240994C (zh) * | 2003-04-10 | 2006-02-08 | 北京大学 | 一种微悬臂梁传感器及其制作方法 |
| JP3913189B2 (ja) * | 2003-04-17 | 2007-05-09 | キヤノン株式会社 | 微細粒子分離回収装置 |
| US7667010B2 (en) * | 2003-11-18 | 2010-02-23 | Phynexus, Inc. | Open channel solid phase extraction systems and methods |
| US7309467B2 (en) * | 2003-06-24 | 2007-12-18 | Hewlett-Packard Development Company, L.P. | Fluidic MEMS device |
| WO2005003715A2 (en) * | 2003-07-02 | 2005-01-13 | Canon Kabushiki Kaisha | Promoted ionization for secondary ion mass spectrometry |
| US9135402B2 (en) * | 2007-12-17 | 2015-09-15 | Dexcom, Inc. | Systems and methods for processing sensor data |
| CN1874720B (zh) * | 2003-09-03 | 2010-11-17 | 生命修复国际股份有限公司 | 个人诊断装置 |
| WO2005033263A1 (en) * | 2003-10-01 | 2005-04-14 | Athena Capital Partners, Llc | Circulating flow device for assays of cell cultures, cellular components and cell products |
| JP4735119B2 (ja) * | 2004-08-09 | 2011-07-27 | 日本精工株式会社 | 反応器及びその製造方法 |
| JP4466308B2 (ja) * | 2004-10-06 | 2010-05-26 | 富士電機ホールディングス株式会社 | 微粒子測定装置 |
| US20060275779A1 (en) * | 2005-06-03 | 2006-12-07 | Zhiyong Li | Method and apparatus for molecular analysis using nanowires |
| WO2007029720A1 (ja) * | 2005-09-06 | 2007-03-15 | Arkray, Inc. | 微細流路用流量計およびこれを用いた分析装置、分析装置用カートリッジ |
| JP5175213B2 (ja) * | 2005-12-22 | 2013-04-03 | ハネウェル・インターナショナル・インコーポレーテッド | 携帯用サンプル分析システム |
| US20070178507A1 (en) * | 2006-01-31 | 2007-08-02 | Wei Wu | Method and apparatus for detection of molecules using nanopores |
| WO2008066965A2 (en) * | 2006-06-23 | 2008-06-05 | The Regents Of The University Of California | Articles comprising large-surface-area bio-compatible materials and methods for making and using them |
| US7807454B2 (en) * | 2006-10-18 | 2010-10-05 | The Regents Of The University Of California | Microfluidic magnetophoretic device and methods for using the same |
| US7698926B2 (en) | 2007-04-26 | 2010-04-20 | Honeywell International Inc. | Electrical connection of energy harvesting devices |
| JP5027296B2 (ja) * | 2007-04-27 | 2012-09-19 | エヌエックスピー ビー ヴィ | バイオセンサチップ |
| EP2160220A4 (en) | 2007-06-14 | 2012-07-04 | Advanced Neuromodulation Sys | ELECTRODE ARRANGEMENTS BASED ON MICROPHONES AND RELEVANT NERVE STIMULATION SYSTEMS, DEVICES AND METHOD |
| CN101687191A (zh) * | 2007-07-03 | 2010-03-31 | Nxp股份有限公司 | 操纵流体微滴的微流控芯片以及方法 |
| WO2009018467A2 (en) | 2007-07-31 | 2009-02-05 | Massachusetts Institute Of Technology | Bio-sensing nanodevice |
| US7952705B2 (en) * | 2007-08-24 | 2011-05-31 | Dynamic Throughput Inc. | Integrated microfluidic optical device for sub-micro liter liquid sample microspectroscopy |
| US20090116207A1 (en) * | 2007-11-05 | 2009-05-07 | Samuel Long Yak Lim | Method for micro component self-assembly |
| US20090181361A1 (en) * | 2008-01-14 | 2009-07-16 | Weidong Xu | Rapid test for detecting infection |
| KR100975010B1 (ko) * | 2008-02-29 | 2010-08-09 | 성균관대학교산학협력단 | 다중 크기 압전 마이크로 칸티레버 공진자 어레이를 이용한 물리센서 및 그 제작방법 |
| CN102150037B (zh) * | 2008-07-11 | 2014-06-04 | 康奈尔大学 | 集成电荷传感器的纳米流体通道及基于该纳米流体通道的方法 |
| US8387803B2 (en) * | 2008-08-26 | 2013-03-05 | Ge Healthcare Bio-Sciences Ab | Particle sorting |
| TWI383144B (zh) * | 2008-09-23 | 2013-01-21 | Univ Nat Chiao Tung | 感測元件、製造方法及其生物檢測系統 |
| US8169006B2 (en) * | 2008-11-29 | 2012-05-01 | Electronics And Telecommunications Research Institute | Bio-sensor chip for detecting target material |
| KR101518858B1 (ko) * | 2008-12-03 | 2015-05-13 | 삼성전자주식회사 | 반도체 발광소자 및 그 제조방법 |
| CN101561446A (zh) * | 2009-06-04 | 2009-10-21 | 大连理工大学 | 一种玻璃微纳流控芯片、制作组装方法及其辅助装配装置 |
| US8685251B2 (en) * | 2009-12-05 | 2014-04-01 | Home Dialysis Plus, Ltd. | Ultra-pasteurization for dialysis machines |
| CN101630946A (zh) * | 2009-08-27 | 2010-01-20 | 浙江大学 | 一种薄膜体声波谐振器及其制备方法 |
| CN101696449B (zh) * | 2009-11-10 | 2017-05-17 | 苏州吉玛基因股份有限公司 | 核酸芯片、其制备方法及用途 |
| US10126291B2 (en) | 2013-02-18 | 2018-11-13 | Anpac Bio-Medical Science Co., Ltd. | Apparatus for disease detection |
-
2011
- 2011-06-30 CN CN201510541055.8A patent/CN105342553B/zh active Active
- 2011-06-30 US US13/807,859 patent/US10161927B2/en active Active
- 2011-06-30 NZ NZ606052A patent/NZ606052A/en not_active IP Right Cessation
- 2011-06-30 CN CN201180041957.5A patent/CN103109186B/zh active Active
- 2011-06-30 KR KR1020137002538A patent/KR102018210B1/ko active IP Right Grant
- 2011-06-30 CN CN201510541244.5A patent/CN105149023B/zh active Active
- 2011-06-30 CA CA2803632A patent/CA2803632A1/en not_active Abandoned
- 2011-06-30 CN CN201510540946.1A patent/CN105353143B/zh active Active
- 2011-06-30 BR BR112012033783-1A patent/BR112012033783B1/pt active IP Right Grant
- 2011-06-30 JP JP2013518724A patent/JP6566508B2/ja not_active Expired - Fee Related
- 2011-06-30 CN CN201510541079.3A patent/CN105342554B/zh active Active
- 2011-06-30 WO PCT/US2011/042637 patent/WO2012003348A2/en active Application Filing
- 2011-06-30 KR KR1020197025373A patent/KR102173440B1/ko active IP Right Grant
- 2011-06-30 EP EP11801429.9A patent/EP2588860A4/en not_active Withdrawn
- 2011-06-30 CN CN201510541279.9A patent/CN105572399B/zh active Active
- 2011-06-30 AU AU2011272837A patent/AU2011272837B2/en not_active Ceased
- 2011-06-30 CN CN201510540902.9A patent/CN105342552B/zh active Active
-
2012
- 2012-01-27 KR KR1020137025626A patent/KR20130131453A/ko active Search and Examination
- 2012-12-30 IL IL224016A patent/IL224016B/en active IP Right Grant
-
2013
- 2013-01-16 ZA ZA2013/00435A patent/ZA201300435B/en unknown
-
2016
- 2016-09-30 AU AU2016235024A patent/AU2016235024B2/en not_active Ceased
-
2018
- 2018-11-14 US US16/191,019 patent/US11366099B2/en active Active
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US11366099B2 (en) | Apparatus for disease detection | |
| US11275048B2 (en) | Micro-devices for disease detection | |
| US20210364511A1 (en) | Micro-devices for disease detection and treatment | |
| US9689863B2 (en) | Micro-devices for improved disease detection | |
| US10126291B2 (en) | Apparatus for disease detection | |
| US11340214B2 (en) | Apparatus for disease detection | |
| AU2018204829B2 (en) | Micro-devices for disease detection | |
| AU2017200348B2 (en) | Micro-devices for disease detection | |
| NZ614830B2 (en) | Micro-devices for disease detection | |
| NZ706837B2 (en) | Micro-Devices for Disease Detection |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B08F | Application dismissed because of non-payment of annual fees [chapter 8.6 patent gazette] | ||
| B08G | Application fees: restoration [chapter 8.7 patent gazette] | ||
| B06F | Objections, documents and/or translations needed after an examination request according [chapter 6.6 patent gazette] | ||
| B06U | Preliminary requirement: requests with searches performed by other patent offices: procedure suspended [chapter 6.21 patent gazette] | ||
| B09A | Decision: intention to grant [chapter 9.1 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] |
Free format text: PRAZO DE VALIDADE: 20 (VINTE) ANOS CONTADOS A PARTIR DE 30/06/2011, OBSERVADAS AS CONDICOES LEGAIS. |
|
| B25A | Requested transfer of rights approved |
Owner name: CHANGWEI SYSTEM TECHNOLOGY (SHANGHAI) CO., LTD. (CN) |