WO2019168058A1 - 新規光架橋性アルギン酸誘導体 - Google Patents
新規光架橋性アルギン酸誘導体 Download PDFInfo
- Publication number
- WO2019168058A1 WO2019168058A1 PCT/JP2019/007655 JP2019007655W WO2019168058A1 WO 2019168058 A1 WO2019168058 A1 WO 2019168058A1 JP 2019007655 W JP2019007655 W JP 2019007655W WO 2019168058 A1 WO2019168058 A1 WO 2019168058A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- group
- formula
- alkyl group
- alkyl
- alginic acid
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08B—POLYSACCHARIDES; DERIVATIVES THEREOF
- C08B37/00—Preparation of polysaccharides not provided for in groups C08B1/00 - C08B35/00; Derivatives thereof
- C08B37/006—Heteroglycans, i.e. polysaccharides having more than one sugar residue in the main chain in either alternating or less regular sequence; Gellans; Succinoglycans; Arabinogalactans; Tragacanth or gum tragacanth or traganth from Astragalus; Gum Karaya from Sterculia urens; Gum Ghatti from Anogeissus latifolia; Derivatives thereof
- C08B37/0084—Guluromannuronans, e.g. alginic acid, i.e. D-mannuronic acid and D-guluronic acid units linked with alternating alpha- and beta-1,4-glycosidic bonds; Derivatives thereof, e.g. alginates
Definitions
- the present invention relates to a novel alginic acid derivative, a novel photocrosslinked alginic acid, a production method thereof, and the like.
- Alginic acid is a high molecular acidic polysaccharide molecule extracted from the cell walls of natural brown algae such as lessonia, macrocystis, laminaria, ascophyllum, dabilia, kajika, arame, and kombu.
- G component a C-5 epimer
- ⁇ -L-guluronic acid (G component) which is a linear heteropolymer in which two types of uronic acid are linked by 1-4.
- the chemical structure is such that a homopolymer block (MM) of mannuronic acid, a homopolymer block (GG) of guluronic acid, and a block (MG) in which mannuronic acid and guluronic acid are randomly arranged are arbitrary permutations and ratios. It is a block copolymer combined in a complicated manner.
- Alginic acid is widely used in fields such as medicine, biotechnology, cosmetics, textiles, papermaking, and food.
- Alginate alkali metal salts of monovalent alginic acid eg, sodium alginate, etc.
- alkaline earth metal alginates eg, calcium alginate, etc.
- It has the property of gelation (insolubilization), and attempts have been made to modify or mold it into a material suitable for various applications using the property (Patent Documents 1 to 3).
- Patent Documents 4 to 6 As a method for obtaining a crosslinked polysaccharide, a polysaccharide derivative in which a cinnamic acid derivative having photocrosslinkability is introduced into a polysaccharide containing hyaluronic acid, alginic acid or the like is known (Patent Documents 4 to 6).
- JP 2010-209130 A JP 2007-99902 A International Publication No. 2004/099259 JP-A-9-87236 International Publication No. 2002/060971 International Publication No. 2005/026214
- the present inventors have obtained an alginic acid derivative in which a photoreactive group represented by the formula (I) is introduced into any one or more carboxyl groups of alginic acid. Using this, a bead (pigment-containing bead), which is one of the photocrosslinked alginate structures, is molded.
- the gel has high stability and has a transmittance according to the purpose as compared with a conventional gel.
- the present invention has been completed. That is, the present invention is as follows.
- a novel photocrosslinked alginic acid obtained by carrying out the reaction, a photocrosslinked alginic acid structure obtained by irradiating the gel obtained by dropping the alginic acid derivative into a solution containing a divalent metal ion, and the above Methods for producing alginic acid derivatives, photocrosslinked alginic acid, and photocrosslinked alginic acid structures are provided. That is, exemplary embodiments can be as follows [1] to [24].
- a medical material comprising the photocrosslinked alginic acid structure according to any one of [7] to [9].
- a photocrosslinking alginate structure is obtained by irradiating a gel obtained by dropping the solution of the alginic acid derivative according to [1] above into a solution containing a divalent metal ion to obtain a photocrosslinked alginic acid structure.
- the alginic acid derivative according to [1] is partially ion-crosslinked with a divalent metal ion to form a specific structure, and then the structure is chemically cross-linked by light irradiation to form a photocrosslinked alginic acid.
- a photocrosslinked alginic acid structure having content retention obtained by crosslinking the alginic acid derivative according to [1] by irradiation with divalent metal ions and light.
- the present invention provides, for example, a novel alginic acid derivative that can be used for chemical crosslinking formation, an intermediate (amino compound) for producing the derivative, and the like.
- the alginic acid derivative has a reactive group that is not present in the living body, and even if an unreacted group remains, the alginic acid derivative is safe for a living organism that is unlikely to undergo a crosslinking reaction with a biological component such as a cell. Expected.
- the crosslinking reaction is completed by a photoreaction, so that it can be used safely and easily.
- the photocrosslinked alginic acid is chemically cross-linked by photoreaction (photocyclization reaction).
- Chemical cross-linking and cross-linking using, for example, divalent metal ions using calcium ions can be used in combination, and by adjusting the reaction conditions, the stability is preferably non-cross-linked alginic acid or non-chemical cross-linked alginic acid (for example, , And calcium ion crosslinked alginic acid). Also preferably, the gel physical properties of the crosslinked product can be adjusted, and the substance permeability can also be adjusted. The present invention has at least one or more of these effects.
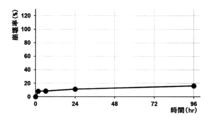
- FIG. 3 is a graph showing the evaluation of gel stability of a photocrosslinked alginate structure (produced using EX1-b, EX2-b, (control) A-2). It is a figure which shows the evaluation of the gel leak rate of a photocrosslinked alginate structure (made using EX1-a1, EX2-a1, (control) A-2). (A) Time at 50% leakage (hr), (B) Time at 80% leakage (hr). It is a figure which shows the evaluation of the gel stability of a photocrosslinking alginate structure (made using EX6-b).
- FIG. 3 is a graph showing evaluation of gel stability of a photocrosslinked alginate structure (prepared using EX9-a and EX12-a).
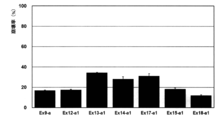
- FIG. 3 is a graph showing evaluation of gel stability of a photocrosslinked alginate structure (created using EX13-a1, EX14-a1, and EX17-a1).
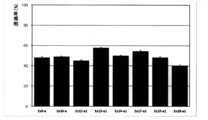
- FIG. 3 is a graph showing evaluation of gel stability of a photocrosslinked alginate structure (created using EX15-a1 and EX18-a1). Evaluation of gel stability after EDTA treatment of photocrosslinked alginate structure (prepared using EX9-a, EX12-a1, EX13-a1, EX14-a1, EX17-a1, EX15-a1, EX18-a1)
- FIG. 9-a, EX12-a1, EX13-a1, EX14-a1, EX17-a1, EX15-a1, EX18-a1 FIG.
- the first aspect is as follows. Any one or more carboxyl groups of alginic acid have the following formula (I) [wherein the right outside of the wavy line is not included]: [In the formula (I), Ar is C 6-10 aryl group, or a Hajime Tamaki (wherein C 6 ⁇ 10 aryl group, or a heterocyclic group, a hydroxyl group, a cyano group, a nitro group, a halogen atom, C 1 ⁇ 6 alkyl group, a halogenated A C 1-6 alkyl group, a C 1-6 alkoxy group, and an —NR A R B group (in the —NR A R B group, R A and R B are each independently a hydrogen atom, C 1-6 alkyl, group, C 2 ⁇ 7 alkanoyl group, or a C 1 ⁇ 6 is a radical selected from alkylsulf
- C 1-6 means that the number of constituent carbon atoms is 1 to 6, and unless otherwise specified, the total number of carbon atoms of a linear, branched, or cyclic group. Represent. For a group containing a chain group and a cyclic group, it means “total number of carbon atoms in the chain and ring”. Unless otherwise specified, each group in the subordinate aspect of the aspect [1] is the same as the definition of each group in the aspect [1].
- C 6 ⁇ 10 aryl group for example, phenyl, 1-naphthyl, 2-naphthyl, indanyl, indenyl, or 1,2,3,4-tetrahydronaphthyl, And the like.
- heterocyclic group examples include “heteroaryl group” and “non-aromatic heterocyclic group”.
- the “heteroaryl group” contains 1 to 5, preferably 1 to 3 heteroatoms selected from the group consisting of a nitrogen atom, a sulfur atom, and an oxygen atom.
- Monocyclic, polycyclic or condensed cyclic (however, in the case of polycyclic or condensed cyclic, it may be partially hydrogenated), preferably 5 to 8 members, More preferably, it means a 5- to 7-membered heteroaryl ring.
- heteroaryl group examples include “monocyclic heteroaryl group”, “condensed heteroaryl group”, and “partially hydrogenated fused ring”.
- heteroaryl group and the like.
- the “monocyclic heteroaryl group” is a monocyclic heteroaryl ring having 5 to 8, more preferably 5 to 6 ring members. Are preferred (“5- to 6-membered heteroaryl group”).
- the “5- to 6-membered heteroaryl group” means a 5- to 6-membered heteroaryl ring containing 1 to 4 heteroatoms selected from a nitrogen atom, a sulfur atom and an oxygen atom.
- the “5- to 6-membered heteroaryl group” means a monovalent group formed by removing any hydrogen atom from the heteroaryl ring, unless otherwise specified.
- examples of the “5- to 6-membered heteroaryl group” include pyrrolyl, furyl, thienyl, imidazolyl, pyrazolyl, oxazolyl, isoxazolyl, thiazolyl, isothiazolyl, 1,2,3- Triazolyl, 1,2,4-triazolyl, 1,2,3-oxadiazolyl, 1,2,4-oxadiazolyl, 1,3,4-oxadiazolyl, furazanyl, 1,2,3-thiadiazolyl, 1,2,4- Thiadiazolyl, 1,3,4-thiadiazolyl, tetrazolyl, pyridyl, pyridazinyl, pyrimidinyl, pyrazinyl, 1,2,3-triazinyl, 1,2,4-triazinyl, 1,3,5-triazinyl, 2H-1,2, 3-thiadiazinyl, 4H-1,2,4-
- the “5-membered heteroaryl group” is a 5-membered heteroaryl ring containing 1 to 4 heteroatoms selected from a nitrogen atom, a sulfur atom and an oxygen atom,
- the “5-membered heteroaryl group” means a monovalent group formed by removing any hydrogen atom from the heteroaryl ring, unless otherwise specified.
- the “6-membered heteroaryl group” is a 6-membered heteroaryl ring containing 1 to 4 heteroatoms selected from a nitrogen atom, a sulfur atom and an oxygen atom
- the “6-membered heteroaryl group” means a monovalent group formed by removing any hydrogen atom from the heteroaryl ring unless otherwise specified, and includes, for example, pyridyl (pyridinyl), pyridazinyl, pyrimidinyl, pyrazinyl, 1 , 2,3-triazinyl, 1,2,4-triazinyl, 1,3,5-triazinyl, 2H-1,2,3-thiadiazinyl, 4H-1,2,4-thiadiazinyl, 6H-1,3,4 A group such as thiadiazinyl, pyridazin-3 (2H) -one, pyrimidin-2 (1H) -one, pyrazin-2 (1H) -one, or
- the “5- to 6-membered heteroaryl group” is substituted with the “C 1-6 alkyl group”.
- a “partially hydrogenated condensed heteroaryl group” is a condensed product formed by condensing a “heterocyclic group” and an “aryl group” or a “heterocyclic group” and a “heteroaryl group”. In the ring, it means a monovalent group formed by removing any hydrogen atom from a partially hydrogenated condensed ring.
- the arbitrary hydrogen atom is a hydrogen atom in any of the "heterocyclic group", “aryl group” and “heteroaryl group” in the condensed ring, or a hydrogen atom in the hydrogenated ring part.
- quinoline is partially hydrogenated tetrahydroquinolyl
- 5,6,7,8-tetrahydroquinolyl, 1,2,3,4-tetrahydroquinolyl and the like can be mentioned.
- these groups can be, for example, 5,6,7,8-tetrahydroquinolyl-2-yl, -3-yl, -4-yl, -5-yl.
- -6-yl, -7-yl, -8-yl and the like 1,2,3,4-tetrahydroquinolyl, for example, -1-yl, -2-yl, -3- Il, -4-yl, -5-yl, -6-yl, -7-yl, -8-yl and the like are exemplified.
- the “partially hydrogenated condensed heteroaryl group” those having 8 to 12 ring members are preferable, that is, as the “partially hydrogenated 8- to 12-membered condensed heteroaryl group”.
- non-aromatic heterocyclic group means a “3- to 14-membered saturated or unsaturated non-aromatic heterocyclic group”.
- the “3- to 14-membered saturated or unsaturated non-aromatic heterocyclic group” means 1 to 4 heteroatoms selected from an oxygen atom, a sulfur atom and a nitrogen atom. It means a monovalent group formed by removing any hydrogen atom from a 3 to 14-membered saturated or unsaturated heterocyclic ring.
- examples of the ⁇ non-aromatic heterocyclic group '' include aziridinyl, azetidinyl, oxiranyl, thiylyl, oxetanyl, thietanyl, pyrrolidinyl, tetrahydrofuryl, dihydrofuryl, thiolanyl, pyrazolinyl, pyrazolidinyl, Imidazolidinyl, piperidinyl, dihydropyranyl, tetrahydropyranyl (2-tetrahydro-2H-pyranyl, 3-tetrahydro-2H-pyranyl, 4-tetrahydro-2H-pyranyl (4-tetrahydro-2H-pyran-4-yl group)) , Tetrahydrothiopyranyl, piperazinyl, dioxanyl, oxazolidinyl, isoxazolinyl, 1,3-oxazolidiny
- halogen atom examples include a fluorine atom, a chlorine atom, a bromine atom, or an iodine atom.
- halogenated in “halogenated C 1-6 alkyl group” and the like means that several, preferably 1 to 5 of the above “halogen atoms” are used as substituents. It means having.
- C 1-6 alkyl group examples include methyl, ethyl, propyl, isopropyl, butyl, isobutyl, sec-butyl, tert-butyl, pentyl, isopentyl, neopentyl, Or groups, such as hexyl, are mentioned.
- halogenated C 1-6 alkyl group means that the above “C 1-6 alkyl” is optionally substituted with several, preferably 1-5 halogen atoms.
- a group such as fluoromethyl, difluoromethyl, trifluoromethyl, 2,2,2-trifluoroethyl, 1,1,2,2-tetrafluoroethyl, or pentafluoroethyl. Is mentioned.
- the “C 1-6 alkoxy group” represents an alkoxy in which the “C 1-6 alkyl” is bonded to an oxygen atom, and includes, for example, methoxy, ethoxy, propoxy, isopropoxy , Butoxy, isobutoxy, sec-butoxy, tert-butoxy, pentyloxy, or hexyloxy, and the like.
- —NR A R B group means a group in which two hydrogen atoms on the nitrogen atom of the “amino group” are substituted with —R A , —R B. To do.
- selection R A and R B are each independently a hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or a C 1 ⁇ 6 alkylsulfonyl group
- examples of such groups include amino, N-methylamino, N, N-dimethylamino, N-acetylamino, N-methanesulfonylamino, and N-acetyl-N-methylamino.
- —NR a R b group means a group in which two hydrogen atoms on the nitrogen atom of the “amino group” are substituted with —R a , —R b. To do.
- R a and R b are each independently a hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or a C 1 ⁇ 6 alkylsulfonyl group
- a group such as amino, methylamino, ethylamino, N, N-dimethylamino, N-acetylamino, N-methanesulfonylamino, or N-acetyl-N-methylamino It is done.
- C 2 ⁇ 7 alkanoyl group the carbonyl group in the “C 1 ⁇ 6 alkyl group” bonded, means “C 1 ⁇ 6 alkyl group” A group such as acetyl, propionyl, butyryl, isobutyryl, valeryl, isovaleryl, pivaloyl, hexanoyl, heptanoyl, cyclopropylcarbonyl, cyclobutylcarbonyl, cyclopentylcarbonyl, cyclohexylcarbonyl, cyclopropylmethylcarbonyl, or 2-methylcyclopropylcarbonyl Is mentioned.
- C 1 ⁇ 6 alkylsulfonyl group means a group substituted in
- examples include groups such as methylsulfonyl, ethylsulfonyl, propylsulfonyl, or isopropylsulfonyl.
- cyclic ether means a cyclic hydrocarbon (for example, a cyclic hydrocarbon having 3 to 8 carbon atoms among monocyclic or polycyclic saturated hydrocarbon ring groups) a (C 3 ⁇ 8 cycloalkyl ring), means cyclopropane, cyclobutane, cyclopentane, cyclohexane, cyclopentane, ethers carbon has a structure substituted with an oxygen cyclooctane etc.), for example, epoxides, oxetanes , Tetrahydrofuran, tetrahydropyran, 1,3-dioxolane, 1,3-dioxane, 1,4-dioxane, 1,3-dioxepane, 1,4-dioxepane, 1,4-dioxocane, 1,5-dioxocane, etc.
- a cyclic ether is mentioned.
- the term "4-N- (C 2 ⁇ 7 alkanoyl) morpholine ring” is a hydrogen atom NH groups morpholine ring substituted on the "C 2 ⁇ 7 alkanoyl group” Examples thereof include 4-N-acetyl-morpholine ring, 4-N-ethylcarbonyl-morpholine ring, and the like.
- the “3-N- (C 1-6 alkylsulfonyl) oxazolidine ring” means that the hydrogen atom of the NH group of the oxazolidine ring is the above “C 1-6 alkylsulfonyl group”.
- a substituted ring means a substituted group, and examples thereof include 3-N-methanesulfonyl-oxazolidine ring, 3-N-ethylsulfonyl-oxazolidine ring, and the like.
- the “4-N— (C 1-6 alkylsulfonyl) morpholine ring” means that the hydrogen atom of the NH group of the morpholine ring is the above “C 1-6 alkylsulfonyl group”.
- a substituted ring means a ring such as a 4-N-methanesulfonyl-morpholine ring and a 4-N-ethylsulfonyl-morpholine ring.
- the term "4-N- (C 2 ⁇ 7 alkanoyl) -1,4-oxazepane ring", a hydrogen atom of the NH group of the 1,4-oxazepan ring said "C 1-6 alkylsulfonyl group ” means a ring substituted with, for example, a 4-N-methanesulfonyl-1,4-oxazepane ring, a 4-N-ethylsulfonyl-1,4-oxazepane ring, etc. Is mentioned.
- hydroxy C 1-6 alkyl group means that any hydrogen atom of the “C 1-6 alkyl” is optionally substituted with 1 to 5 hydroxyl groups.
- thiol C 1-6 alkyl group refers to several “C 1-6 alkyl”, preferably 1 to 5 thiol groups (—SH group). And a group such as thiolmethyl, 2-thiolethyl, or 3-thiolpropyl, and the like.
- C 1-6 alkylthio C 1-6 alkyl group means the hydrogen atom of the thiol group (—SH group) of the “thiol C 1-6 alkyl group”.
- C 1-6 alkyl group means a group substituted with, for example, a group such as methylthiomethyl, methylthioethyl, ethylthiomethyl, or ethylthioethyl.
- the “carboxy C 1-6 alkyl group” means any hydrogen atom of the “C 1-6 alkyl”, preferably 1 to 5 carboxy groups. This means a substituted group, and examples thereof include carboxymethyl, carboxyethyl, and the like.
- NR a R b -C 1 ⁇ 6 alkyl group refers to any hydrogen atoms "-NR a R b group” of the "C 1 ⁇ 6 alkyl” ( as used herein, R a and R b are each independently hydrogen atom, is C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or a C 1 ⁇ 6 group selected from an alkylsulfonyl group )), And groups such as aminomethyl, aminoethyl, aminopropyl, aminobutyl, N-methylaminomethyl, N-acetylaminomethyl, or N-methanesulfonylaminomethyl Is mentioned.
- R a and R b are each independently a hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group Or a group optionally selected from a C 1-6 alkylsulfonyl group.
- R a and R b are each independently a hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group Or a group optionally selected from a C 1-6 alkylsulfonyl group.
- aminocarbonylmethyl, aminocarbonylethyl, N-methylaminocarbonylmethyl, N-acetyl examples include aminocarbonylethyl, N-methanesulfonylaminocarbonylethyl, and the like.
- the “guanidino C 1-6 alkyl group” means an arbitrary hydrogen atom of the “C 1-6 alkyl group” represented by a “guanidino group (—NH—C ( ⁇ NH) —”.
- NH 2 "have been substituted meant, for example, guanidino methyl, groups such as guanidino ethyl, or guanidino propyl.
- C 7 ⁇ 16 aralkyl group the arbitrary hydrogen atom of the "C 1 ⁇ 6 alkyl group” substituted with the "C 6 ⁇ 10 aryl group” Group, for example, benzyl group, phenethyl group, diphenylmethyl group, trityl group, biphenylmethyl group, naphthylmethyl group, indanylmethyl group, or 1,2,3,4-tetrahydronaphthalen-1-ylmethyl group, And the like.
- hydroxy C 6 ⁇ 10 aryl C 1 ⁇ 6 alkyl group "C 6 ⁇ 10 aryl group” of the "C 7 ⁇ 16 aralkyl group” It means a group optionally substituted with several, preferably 1 to 5 hydroxyl groups, and examples thereof include groups such as 2-hydroxybenzyl group, 3-hydroxybenzyl group, or 4-hydroxybenzyl group. It is done.
- heteroaryl C 1-6 alkyl group means a group in which any hydrogen atom of the “heteroaryl group” is substituted with the “C 1-6 alkyl group”.
- a 2-pyridylmethyl group, a 4-imidazolylmethyl group, or a 3-indolylmethyl group for example, a 2-pyridylmethyl group, a 4-imidazolylmethyl group, or a 3-indolylmethyl group.
- non-aromatic heterocycle means “3 to 14-membered saturated or unsaturated non-aromatic heterocycle”.
- the “3- to 14-membered saturated or unsaturated non-aromatic heterocycle” contains 1 to 4 heteroatoms selected from oxygen, sulfur and nitrogen atoms. Means a 3 to 14 membered saturated or unsaturated heterocycle.
- non-aromatic heterocycle examples include aziridine, azetidine, pyrrolidine, pyrazolidine, oxazolidine, thiazolidineisoxazolidine, isothiazolidine, imidazolidine, piperidine, piperazine, morpholine, and thiol.
- the ring examples include morpholine, oxazepan, diazepan, thiazepan, oxazocan, diazocan, thiazocan, and oxazine.
- C 3-8 cycloalkyl ring means a cyclic saturated hydrocarbon ring having a carbon number 3-8 (including monocyclic or polycyclic) Examples thereof include cyclopropane, cyclobutane, cyclopentane, cyclohexane, cyclopentane, and cyclooctane.
- Ar is preferably, C 6 ⁇ 10 aryl group, or heteroaryl group (wherein C 6 ⁇ 10 aryl group or a heteroaryl group, a hydroxyl group, A cyano group, a nitro group, a halogen atom, a C 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1-6 alkoxy group, and an —NR A R B group (in the —NR A R B group, R A and R B are each independently a hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or a group selected from C 1 - 6 alkylsulfonyl group) 1 optionally selected from - three groups may be substituted with a hydrogen atom on the ring, the C 6 ⁇ 10 aryl group or a heteroaryl group, C 1 ⁇ 6 alkyl and C 1 ⁇ 6 alk
- 3-N- (C 2 ⁇ 7 alkanoyl) oxazolidine ring 3-N- (C 1 ⁇ 6 alkylsulfonyl) oxazolidine ring, 4-N- (C 2 ⁇ 7 alkanoyl) morpholine, 4-N- (C 1 1-6 alkylsulfonyl) morpholine, 4-N- (C 2 ⁇ 7 alkanoyl) -1,4-oxazepane ring, or 4-N- (C 1 ⁇ 6 alkylsulfonyl) -1,4-oxazepane forms a ring May be);
- Ar is C 6 ⁇ 10 aryl group, or a 5-6 membered heteroaryl group (wherein C 6 ⁇ 10 aryl group, or a 5-6 membered heteroaryl group, a hydroxyl group, a cyano group, a nitro group, A halogen atom, a C 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1-6 alkoxy group, and a —NR A R B group (in the —NR A R B group, R A and R B are each independently hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or a group selected from C 1 ⁇ 6 alkylsulfonyl group) 1-3 groups chosen arbitrarily from the ring may be substituted with a hydrogen atom of the above, the C 6 ⁇ 10 aryl group or a 5-6 membered heteroaryl group, C 1 ⁇ 6 alkyl and C 1 ⁇ 6 al
- Ar is a phenyl group or a pyridyl group (the phenyl group or pyridyl group is a hydroxyl group, a cyano group, a nitro group, a halogen atom, a C 1-6 alkyl group, a halogenated C 1-6 alkyl group).
- C 1 ⁇ 6 alkoxy group, and in -NR A R B group (-NR A R B group, R A and R B are each independently a hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 1 to 3 groups arbitrarily selected from an alkanoyl group or a C 1-6 alkylsulfonyl group) may be substituted with a hydrogen atom on the ring, and the phenyl group or pyridyl group may When a C 1-6 alkyl group and a C 1-6 alkoxy group or two C 1-6 alkoxy groups are adjacently substituted, each of the C 1-6 alkyl group and the C 1-6 alkoxy group From alkyl groups Bonding between carbon atoms from which one arbitrary hydrogen atom is removed, or bonding between carbon atoms from which one arbitrary hydrogen atom is removed from each alkyl group of the two C 1-6 alkoxy groups by, it may form a cyclic ether, or, in the phenyl or
- Ar is particularly preferably a phenyl group or a 2-pyridyl group (the phenyl group or 2-pyridyl group is one to three groups arbitrarily selected from a cyano group, a fluorine atom, a trifluoromethyl group, and a methoxy group) May be substituted with a hydrogen atom on the ring, and when two methoxy groups are adjacently substituted on a phenyl group or 2-pyridyl group, the methyl of each group of the two methoxy groups
- a 1,4-dioxane ring may be formed by bonding between carbon atoms in which one arbitrary hydrogen atom is removed from the group);
- Ar is, for example, a phenyl group, 4-fluorophenyl group, 4- (trifluoromethyl) phenyl group, 4-methoxyphenyl group, 4-cyanophenyl group, 2,3-dihydrobenzo [b] [1,4].
- Ar is particularly preferably a phenyl group, 2-pyridyl group, or 5-pyridyl group (the phenyl group, 2-pyridyl group, or In the 5-pyridyl group, 1 to 3 groups arbitrarily selected from a cyano group, a fluorine atom, a trifluoromethyl group, a methoxy group, and an N-acetylamino group may be substituted with a hydrogen atom on the ring, When two methoxy groups are adjacently substituted on a phenyl group, 2-pyridyl group, or 5-pyridyl group, one hydrogen atom is selected from the methyl group of each group of the two methoxy groups.
- a 1,4-dioxane ring may be formed by bonding between the removed carbon atoms);
- Ar is, for example, a phenyl group, a 4-fluorophenyl group, a 4- (trifluoromethyl) phenyl group, a 4-methoxyphenyl group, a 3,4-dimethoxyphenyl group, a 4- (N-acetylamino) phenyl group, 4 -Cyanophenyl group, 2,3-dihydrobenzo [b] [1,4] dioxinyl group, 2-pyridyl group, 2-methoxy-5-pyridyl group, and the like.
- Ar is particularly preferably a phenyl group, a 2-pyridyl group, or a 5-pyridyl group (the phenyl group, 2-pyridyl group, or In the 5-pyridyl group, 1 to 3 groups arbitrarily selected from a cyano group, a methoxy group, and an N-acetylamino group may be substituted with a hydrogen atom on the ring, and a phenyl group, a 2-pyridyl group, Or when two methoxy groups are adjacently substituted on the 5-pyridyl group, bonded between carbon atoms in which one hydrogen atom is removed from the methyl group of each group of the two methoxy groups To form a 1,4-dioxane ring) Ar is, for example, a phenyl group, 4-methoxyphenyl group, 3,4-dimethoxyphenyl group, 4-cyanophen
- Ar is preferably, C 6 ⁇ 10 aryl group, or heteroaryl group (wherein C 6 ⁇ 10 aryl group or a heteroaryl group, a hydroxyl group, A cyano group, a nitro group, a halogen atom, a C 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1-6 alkoxy group, and an —NR A R B group (in the —NR A R B group, R A And R B are each independently a hydrogen atom or a group selected from a C 1-6 alkyl group), and 1 to 3 groups arbitrarily selected from the above may be substituted with hydrogen atoms on the ring Good);
- Ar is C 6 ⁇ 10 aryl group, or a 5-6 membered heteroaryl group (wherein C 6 ⁇ 10 aryl group, or a 5-6 membered heteroaryl group, a hydroxyl group, a cyano group, a nitro group, A halogen atom, a C 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1-6 alkoxy group, and a —NR A R B group (in the —NR A R B group, R A and R B are each Independently a hydrogen atom or a group selected from C 1-6 alkyl groups) 1 to 3 groups optionally selected from may be substituted with hydrogen atoms on the ring;
- Ar is a phenyl group (the phenyl group is a hydroxyl group, a cyano group, a nitro group, a halogen atom, a C 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1-6 alkoxy group,
- —NR A R B group in the —NR A R B group, R A and R B are each independently a hydrogen atom or a group selected from a C 1-6 alkyl group). 1 to 3 groups may be replaced with hydrogen atoms on the ring);
- Ar is particularly preferably a phenyl group (wherein the phenyl group is optionally substituted by 1 to 3 groups selected from a fluorine atom and a trifluoromethyl group with a hydrogen atom on the ring); Ar is, for example, a phenyl group, a 4-fluorophenyl group, or a 4- (trifluoromethyl) phenyl group.
- Ar is preferably, C 6 ⁇ 10 aryl group, or heteroaryl group (wherein C 6 ⁇ 10 aryl group or a heteroaryl group, a hydroxyl group, A cyano group, a nitro group, a halogen atom, a C 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1-6 alkoxy group, and an —NR A R B group (in the —NR A R B group, R A and R B are each independently a hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or a group selected from C 1 - 6 alkylsulfonyl group) 1 optionally selected from - three groups may be substituted with a hydrogen atom on the ring, the C 6 ⁇ 10 aryl group or a heteroaryl group, C 1 ⁇ 6 alkyl and C 1 ⁇ 6 alk
- 3-N- (C 2 ⁇ 7 alkanoyl) oxazolidine ring 3-N- (C 1 ⁇ 6 alkylsulfonyl) oxazolidine ring, 4-N- (C 2 ⁇ 7 alkanoyl) morpholine, 4-N- (C 1-6 alkylsulfonyl) morpholine, 4-N- (C 2 ⁇ 7 alkanoyl) -1,4-oxazepane ring, or 4-N- (C 1 ⁇ 6 alkylsulfonyl) -1,4-oxazepane ring formation
- Ar is C 6 ⁇ 10 aryl group, or a 5-6 membered heteroaryl group (wherein C 6 ⁇ 10 aryl group, or a 5-6 membered heteroaryl group, a hydroxyl group, a cyano group, a nitro group, A halogen atom, a C 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1-6 alkoxy group, and a —NR A R B group (in the —NR A R B group, R A and R B are each independently hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or a group selected from C 1 ⁇ 6 alkylsulfonyl group) 1-3 groups chosen arbitrarily from the ring may be substituted with a hydrogen atom of the above, the C 6 ⁇ 10 aryl group or a 5-6 membered heteroaryl group, C 1 ⁇ 6 alkyl and C 1 ⁇ 6 al
- Ar is a phenyl group or a pyridyl group (the phenyl group or pyridyl group is a hydroxyl group, a cyano group, a nitro group, a halogen atom, a C 1-6 alkyl group, a halogenated C 1-6 alkyl group).
- C 1 ⁇ 6 alkoxy group, and in -NR A R B group (-NR A R B group, R A and R B are each independently a hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 1 to 3 groups arbitrarily selected from an alkanoyl group or a C 1-6 alkylsulfonyl group) may be substituted with a hydrogen atom on the ring, and the phenyl group or pyridyl group may When a C 1-6 alkyl group and a C 1-6 alkoxy group or two C 1-6 alkoxy groups are adjacently substituted, each of the C 1-6 alkyl group and the C 1-6 alkoxy group From alkyl groups Bonding between carbon atoms from which one arbitrary hydrogen atom is removed, or bonding between carbon atoms from which one arbitrary hydrogen atom is removed from each alkyl group of the two C 1-6 alkoxy groups by, it may form a cyclic ether, or, in the phenyl or
- Ar is particularly preferably a phenyl group or a 2-pyridyl group (the phenyl group or 2-pyridyl group is a hydrogen atom on the ring, which is optionally selected from 1 to 3 groups selected from a cyano group and a methoxy group)
- the phenyl group or 2-pyridyl group is a hydrogen atom on the ring, which is optionally selected from 1 to 3 groups selected from a cyano group and a methoxy group
- any hydrogen atom from the methyl group of each group of the two methoxy groups is 1
- a 1,4-dioxane ring may be formed by bonding between the removed carbon atoms);
- Ar is, for example, a phenyl group, a 4-methoxyphenyl group, a 4-cyanophenyl group, a 2,3-dihydrobenzo [b] [1,4] dioxinyl group, or a 2-pyridyl group.
- Ar is particularly preferably a phenyl group or a 5-pyridyl group (the phenyl group or 5-pyridyl group is a cyano group, a methoxy group, And 1 to 3 groups arbitrarily selected from N-acetylamino group may be substituted with a hydrogen atom on the ring, and two methoxy groups are substituted on the phenyl group or 5-pyridyl group.
- a 1,4-dioxane ring may be formed by bonding between carbon atoms obtained by removing one arbitrary hydrogen atom from the methyl group of each of two methoxy groups) Yes;
- Ar is, for example, 4-cyanophenyl group, 4-methoxyphenyl group, 3,4-dimethoxyphenyl group, 4- (N-acetylamino) phenyl group, 2,3-dihydrobenzo [b] [1,4].
- —X— is preferably —O— or —NH—.
- —X— is preferably —O—.
- -A- is more preferably the formula (AL-1) or (AL-2) [in each formula, the outside of the wavy line at both ends is not included]: (N in the formula (AL-1) is an integer of 1 to 8; m in the formula (AL-2) is an integer of 1 to 5; the formula (AL-1) or (AL-2 )
- methylene group (—CH 2 —) is a halogen atom, a hydroxyl group, a C 1-6 alkyl group, a hydroxy C 1-6 alkyl group, a —NR a R b group (—NR a R b group)
- R a and R b are each independently a hydrogen atom, a C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or a C 1 ⁇ 6 group selected from alkylsulfonyl group), C 7 ⁇
- -A- is more preferably the formula (AL-1) or (AL-2) [in each formula, the outside of the wavy line at both ends is not included]: (N in the formula (AL-1) is an integer of 2 to 6; m in the formula (AL-2) is an integer of 1 to 3);
- -A- is particularly preferably the formula (AL-1-1), (AL-2-1) or (AL-2-2) [in each formula, the outside of the wavy line at both ends is not included]: It is.
- -A- is particularly preferably a group represented by the formula (AL-1-1) or (AL-2-1) [in each formula, The outside of the wavy line is not included]: It is.
- -A- is particularly preferably a group represented by the formula (AL-2-1) or (AL-2-2) [in each formula, The outside of the wavy line is not included]: It is.
- n, m, and j in the formulas (AL-1) to (AL-4) which are —A— are preferably n
- m is preferably an integer of 1 to 7, More preferably, it is an integer of 1 to 5, more preferably an integer of 1 to 3, particularly preferably 1 or 2
- j is preferably an integer of 0 to 8, more preferably 1 to 6.
- An integer of 2 to 4 more preferably an integer of 2 to 4.
- a preferable embodiment of the formula (AL-3) or the formula (AL-4) contained in -A- includes the following formula (AL-3 -1) or formula (AL-4-1) [In each formula, the outside of the wavy line at both ends is not included]: (In formula (AL-3-1) or formula (AL-4-1), n represents an integer of 1 to 18; m represents an integer of 1 to 9; j represents an integer of 0 to 9) -R 1 and -R 2 are each independently a hydrogen atom, a halogen atom, a hydroxyl group, a methyl group, an isopropyl group, an isobutyl group, a sec-butyl group, a hydroxymethyl group, a 2-hydroxyethyl group, a thiol Methyl group, methylthioethyl group, carboxymethyl group, carboxyethyl group, aminocarbonylmethyl group, aminocarbonyleth
- n is Preferably, it is an integer of 1 to 10, more preferably an integer of 1 to 8, more preferably an integer of 2 to 6, particularly preferably 3, and m is preferably an integer of 1 to 7. More preferably an integer of 1 to 5, still more preferably an integer of 1 to 3, particularly preferably 1 or 2, and j is preferably an integer of 0 to 8, more preferably 1 An integer of ⁇ 6, more preferably an integer of 2 ⁇ 4.
- the combination of Ar, p, —X—, and —A— is preferably Ar is C 6 ⁇ 10 aryl group, or heteroaryl group (wherein C 6 ⁇ 10 aryl group, or a heteroaryl group, a hydroxyl group, a cyano group, a nitro group, a halogen atom, C 1 ⁇ 6 alkyl group, a halogenated A C 1-6 alkyl group, a C 1-6 alkoxy group, and an —NR A R B group (in the —NR A R B group, R A and R B are each independently a hydrogen atom, C 1-6 alkyl, group, C 2 ⁇ 7 alkanoyl group, or a C 1 ⁇ 6 is a radical selected from alkylsulfonyl group) 1 to 3 groups selected arbitrarily from well be replaced with a hydrogen atom on the ring, wherein C 6 ⁇ 10 aryl group or
- Ar, p, -X -, - A- combinations include, preferably, Ar is, C 6 ⁇ 10 aryl group, or heteroaryl group (wherein C 6 ⁇ 10 aryl group, or a heteroaryl group, a hydroxyl group, a cyano group, a nitro group, a halogen atom, C 1 ⁇ 6 alkyl group, a halogenated C 1 ⁇ 6 alkyl group, C 1 ⁇ 6 alkoxy group, And —NR A R B group (in the —NR A R B group, R A and R B are each independently a hydrogen atom or a group selected from a C 1-6 alkyl group).
- 1 to 3 groups may be replaced with hydrogen atoms on the ring); p is an integer of 1; —X— is —O— or —NH—; -A- is the formula (AL-1) or (AL-2) in the above embodiment [1-3] [in each formula, the outside of the wavy line at both ends is not included] (n in the formula (AL-1) is 1 is an integer of 1 to 10; m in formula (AL-2) is an integer of 1 to 7;
- the hydrogen atom of the methylene group (—CH 2 —) in the formula (AL-1) or (AL-2) is a halogen atom, a hydroxyl group, a C 1-6 alkyl group, a hydroxy C 1-6 alkyl group, a thiol C 1 1-6 alkyl group, C 1 - 6 alkylthio C 1 - 6 alkyl group, a carboxy C 1 - 6 alkyl group, -NR a R b group, (R a R b N
- Ar, p, -X -, - A- combinations include, preferably, Ar is, C 6 ⁇ 10 aryl group, or heteroaryl group (wherein C 6 ⁇ 10 aryl group, or a heteroaryl group, a hydroxyl group, a cyano group, a nitro group, a halogen atom, C 1 ⁇ 6 alkyl group, a halogenated C 1 ⁇ 6 alkyl group, C 1 ⁇ 6 alkoxy group, and in -NR A R B group (-NR A R B group, R A and R B are each independently a hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl or C 1 ⁇ 6, good one to three groups selected arbitrarily from a group selected from alkylsulfonyl group) be replaced with a hydrogen atom on the ring, the C 6 ⁇ 10 aryl group or a heteroaryl group
- Ar, p, -X -, - A- combinations include, preferably, Ar is, C 6 ⁇ 10 aryl group, or heteroaryl group (wherein C 6 ⁇ 10 aryl group, or a heteroaryl group, a hydroxyl group, a cyano group, a nitro group, a halogen atom, C 1 ⁇ 6 alkyl group, a halogenated C 1 ⁇ 6 alkyl group, C 1 ⁇ 6 alkoxy group, and in -NR A R B group (-NR A R B group, R A and R B are each independently a hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl or C 1 ⁇ 6, good one to three groups selected arbitrarily from a group selected from alkylsulfonyl group) be replaced with a hydrogen atom on the ring, the C 6 ⁇ 10 aryl group or a heteroaryl group
- the combination of Ar, p, —X—, and —A— is more preferably Ar is C 6 ⁇ 10 aryl group, or a 5-6 membered heteroaryl group (wherein C 6 ⁇ 10 aryl group, or a 5-6 membered heteroaryl group, a hydroxyl group, a cyano group, a nitro group, a halogen atom, C A 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1-6 alkoxy group, and a —NR A R B group (in the —NR A R B group, R A and R B are each independently hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or a C 1 ⁇ 6 alkylsulfonyl is a radical selected from the group) 1 to 3 groups selected arbitrarily from a hydrogen atom on the ring It may be substituted
- the combination of Ar, p, -X-, and -A- is more preferably Ar is C 6 ⁇ 10 aryl group, or a 5-6 membered heteroaryl group (wherein C 6 ⁇ 10 aryl group, or a 5-6 membered heteroaryl group, a hydroxyl group, a cyano group, a nitro group, a halogen atom, C A 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1-6 alkoxy group, and a —NR A R B group (in the —NR A R B group, R A and R B are each independently 1 to 3 groups arbitrarily selected from a hydrogen atom or a C 1-6 alkyl group) may be substituted with a hydrogen atom on the ring); p is an integer of 1; —X— is —O— or —NH—; -A- is the formula (AL-1)
- the combination of Ar, p, -X-, and -A- is more preferably Ar is C 6 ⁇ 10 aryl group, or a 5-6 membered heteroaryl group (wherein C 6 ⁇ 10 aryl group, or a 5-6 membered heteroaryl group, a hydroxyl group, a cyano group, a nitro group, a halogen atom, C A 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1-6 alkoxy group, and a —NR A R B group (in the —NR A R B group, R A and R B are each independently hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or a C 1 ⁇ 6 alkylsulfonyl is a radical selected from the group) 1 to 3 groups selected arbitrarily from a hydrogen atom on the ring It may be substitute
- the combination of Ar, p, -X-, and -A- is more preferably Ar is C 6 ⁇ 10 aryl group, or a 5-6 membered heteroaryl group (wherein C 6 ⁇ 10 aryl group, or a 5-6 membered heteroaryl group, a hydroxyl group, a cyano group, a nitro group, a halogen atom, C A 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1-6 alkoxy group, and a —NR A R B group (in the —NR A R B group, R A and R B are each independently hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or a C 1 ⁇ 6 alkylsulfonyl is a radical selected from the group) 1 to 3 groups selected arbitrarily from a hydrogen atom on the ring It may be substitute
- the combination of Ar, p, —X—, and —A— is more preferably Ar is a phenyl group or a pyridyl group (the phenyl group or pyridyl group is a hydroxyl group, a cyano group, a nitro group, a halogen atom, a C 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1- 6 alkoxy group, and in -NR A R B group (-NR A R B group, R A and R B are each independently a hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or 1 to 3 groups arbitrarily selected from C 1-6 alkylsulfonyl groups) may be substituted with hydrogen atoms on the ring, and the phenyl group or pyridyl group may be substituted with C 1 to When 6 alky
- Ar represents a phenyl group (the phenyl group is a hydroxyl group, a cyano group, a nitro group, a halogen atom, a C 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1-6 alkoxy group, and —NR A 1 to 3 arbitrarily selected from R B groups (R A and R B in —NR A R B groups are each independently a hydrogen atom or a C 1-6 alkyl group) Groups may be substituted with hydrogen atoms on the ring); p is an integer of 1; —X— is —O— or —NH—: -A- is the formula (AL-1) or (AL-2) in the above embodiment [1-3] [in each formula, the outside of the wavy line at both ends is not included] (n in the
- the combination of Ar, p, -X-, and -A- is more preferably Ar is a phenyl group or a pyridyl group (the phenyl group or pyridyl group is a hydroxyl group, a cyano group, a nitro group, a halogen atom, a C 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1- 6 alkoxy group, and in -NR A R B group (-NR A R B group, R A and R B are each independently a hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or 1 to 3 groups arbitrarily selected from C 1-6 alkylsulfonyl groups) may be substituted with hydrogen atoms on the ring, and the phenyl group or pyridyl group may be substituted with C 1 to When 6 al
- the combination of Ar, p, -X-, and -A- is more preferably Ar is a phenyl group or a pyridyl group (the phenyl group or pyridyl group is a hydroxyl group, a cyano group, a nitro group, a halogen atom, a C 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1- 6 alkoxy group, and in -NR A R B group (-NR A R B group, R A and R B are each independently a hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or 1 to 3 groups arbitrarily selected from C 1-6 alkylsulfonyl groups) may be substituted with hydrogen atoms on the ring, and the phenyl group or pyridyl group may be substituted with C 1 to When 6 al
- the combination of Ar, p, -X-, and -A- is particularly preferably Ar is a phenyl group or a 2-pyridyl group (the phenyl group or 2-pyridyl group is a ring formed by 1 to 3 groups arbitrarily selected from a cyano group, a fluorine atom, a trifluoromethyl group, and a methoxy group)
- the above hydrogen atom may be substituted, and when two methoxy groups are substituted on the phenyl group or the 2-pyridyl group, any methyl group from each group of the two methoxy groups
- a 1,4-dioxane ring may be formed by bonding between carbon atoms from which one hydrogen atom is removed);
- Examples of combinations of Ar, p, -X-, and -A- include, for example, Ar is a phenyl group, 4-fluorophenyl group, 4- (trifluoromethyl
- the combination of Ar, p, —X—, and —A— is particularly preferably Ar represents a phenyl group, a 2-pyridyl group, or a 5-pyridyl group (the phenyl group, 2-pyridyl group, or 5-pyridyl group includes a cyano group, a fluorine atom, a trifluoromethyl group, a methoxy group, and an N- One to three groups arbitrarily selected from an acetylamino group may be substituted with a hydrogen atom on the ring, and two methoxy groups are adjacent to each other on a phenyl group, a 2-pyridyl group, or a 5-pyridyl group.
- a 1,4-dioxane ring may be formed by bonding between carbon atoms obtained by removing one arbitrary hydrogen atom from the methyl group of each group of two methoxy groups.
- Ar is phenyl group, 4-fluorophenyl group, 4- (trifluoromethyl) phenyl group, 4-methoxyphenyl group, 3,4- Dimethoxyphenyl group, 4- (N-acetylamino) phenyl group, 4-cyanophenyl group, 2,3-dihydrobenzo [b] [1,4] dioxinyl group, 2-pyridyl group, or 2-methoxy-5- A pyridyl group; p is an integer of 1 or 2; —X— is —O— or —NH—: -A- is the formula (AL-1-1), (AL-2-1), or (AL-2-2) in the above embodiment
- the combination of Ar, p, —X—, and —A— is particularly preferably Ar is a phenyl group, a 2-pyridyl group, or a 5-pyridyl group (the phenyl group, 2-pyridyl group, or 5-pyridyl group is arbitrarily selected from a cyano group, a methoxy group, and an N-acetylamino group) 1 to 3 groups may be substituted with hydrogen atoms on the ring, and when two methoxy groups are substituted on the phenyl group, 2-pyridyl group, or 5-pyridyl group, A 1,4-dioxane ring may be formed by bonding between carbon atoms obtained by removing one hydrogen atom from the methyl group of each of two methoxy groups);
- Examples of combinations of Ar, p, -X-, and -A- include, for example, Ar is a phenyl group, or a 5-pyridyl group (the
- the combination of Ar, p, -X-, and -A- is particularly preferably Ar is a phenyl group (the phenyl group is a fluorine atom) And 1 to 3 groups arbitrarily selected from trifluoromethyl groups may be substituted with hydrogen atoms on the ring);
- Ar is, for example, a phenyl group, a 4-fluorophenyl group, or a 4- (trifluoromethyl) phenyl group;
- p is an integer of 1;
- —X— is —O— or —NH—:
- -A- is the formula (AL-1-1), (AL-2-1), or (AL-2-2) in the above embodiment [1-3] [in each formula, the outside of the wavy line at both ends is not included. ];
- the combination of Ar, p, -X-, and -A- is particularly preferably Ar is a phenyl group (the phenyl group is a fluorine atom) And 1
- the combination of Ar, p, -X-, and -A- is particularly preferably Ar is a phenyl group or a 2-pyridyl group (the phenyl group or 2-pyridyl group is a group in which 1 to 3 groups arbitrarily selected from a cyano group and a methoxy group are substituted with hydrogen atoms on the ring; In the case where two methoxy groups are adjacently substituted on the phenyl group or 2-pyridyl group, one hydrogen atom is removed from the methyl group of each group of the two methoxy groups.
- a 1,4-dioxane ring may be formed by bonding between carbon atoms);
- Ar is, for example, a phenyl group, a 4-methoxyphenyl group, a 4-cyanophenyl group, 2,3-dihydrobenzo [b] [1, 4] a dioxynyl group or a 2-pyridyl group;
- p is an integer of 1 or 2;
- —X— is —O—:
- -A- is the formula (AL-1-1) or (AL-2-1) in the above embodiment [1-3] (in each formula, the outside of the wavy line at both ends is not included);
- the combination of Ar, p, -X-, and -A- is the following partial structural formula [in each formula, the right side of the wavy line is not included] As shown in
- Ar is a phenyl group or a 5-pyridyl group (described above).
- phenyl group or 5-pyridyl group 1 to 3 groups arbitrarily selected from a cyano group, a methoxy group, and an N-acetylamino group may be substituted with a hydrogen atom on the ring.
- two methoxy groups are adjacently substituted on the 2-pyridyl group, they are bonded between carbon atoms obtained by removing one hydrogen atom from the methyl group of each group of the two methoxy groups.
- Ar is 4-cyanophenyl group, 4-methoxyphenyl group, 3,4-dimethoxyphenyl group, 4- (N-acetylamino) phenyl A group, 2,3-dihydrobenzo [b] [1,4] dioxinyl group, or 2-methoxy-5-pyridyl group
- p is an integer of 1 or 2
- —X— is —O— or —NH—:
- -A- is the formula (AL-2-1) or (AL-2-2) in the above embodiment [1-3] (in each formula, the outside of the wavy line at both ends is not included);
- the combination of Ar, p, -X-, and -A- is the following partial structural formula [in each formula, the right side of the wavy line is not included] As shown in
- any one or more carboxyl groups of alginic acid are represented by the following formula (I):
- Ar is C 6 ⁇ 10 aryl group, or a Hajime Tamaki (wherein C 6 ⁇ 10 aryl group, or a heterocyclic group, a hydroxyl group, a cyano group, a nitro group, a halogen atom, C 1 ⁇ 6 alkyl group, a halogenated A C 1-6 alkyl group, a C 1-6 alkoxy group, and an —NR A R B group (in the —NR A R B group, R A and R B are each independently a hydrogen atom, C 1-6 alkyl, group, C 2 ⁇ 7 alkanoyl group, or a group selected from C 1 ⁇ 6 alkylsulfonyl group (, -NH 2, -NH (C 1 ⁇ 6 alkyl group),
- Ar is C 6 ⁇ 10 aryl group, or heteroaryl group (wherein C 6 ⁇ 10 aryl group, or a heteroaryl group, a hydroxyl group, A cyano group, a nitro group, a halogen atom, a C 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1-6 alkoxy group, and an —NR A R B group (in the —NR A R B group, R A and R B are each independently a hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or a group selected from C 1 ⁇ 6 alkylsulfonyl group (, -NH 2, - 1 to 3 groups arbitrarily selected from NH (C 1-6 alkyl group) and —N (C 1-6 alkyl group 2 )) may be substituted with hydrogen atoms on the ring
- Ar is C 6 ⁇ 10 aryl group, or a 5-6 membered heteroaryl group (wherein C 6 ⁇ 10 aryl group, or a 5-6 membered heteroaryl group, a hydroxyl group, a cyano group, a nitro group, A halogen atom, a C 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1-6 alkoxy group, and a —NR A R B group (in the —NR A R B group, R A and R B are each independently, a hydrogen atom, a C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or a C 1 ⁇ 6 group selected from alkylsulfonyl group (, -NH 2, -NH (C 1 ⁇ 6 Alkyl group), and 1 to 3 groups arbitrarily selected from —N (C 1-6 alkyl group) 2 ) may be substituted with hydrogen atoms on the ring;
- Ar is a phenyl group or a pyridyl group (the phenyl group or pyridyl group is a hydroxyl group, a cyano group, a nitro group, a halogen atom, a C 1-6 alkyl group, a halogenated C 1-6 alkyl group).
- R A and R B are each independently a hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or a group selected from C 1 ⁇ 6 alkylsulfonyl group (, -NH 2, -NH (C 1 ⁇ 6 alkyl group), and -N (C 1 ⁇ 6 alkyl group) 2 is excluded ))
- a cyclic ether may be formed by bonding between carbon
- C 1 ⁇ 6 alkoxy group and -NHR G group (R G in -NHR G groups are C 2 ⁇ 7 alkanoyl or C 1 ⁇ 6 alkylsulfonyl group) when is substituted adjacently, the A carbon atom from which one arbitrary hydrogen atom has been removed from an alkyl group of a C 1-6 alkoxy group and a nitrogen atom from which one hydrogen atom has been removed from the —NHR G group are combined to form 3-N— ( C 2 ⁇ 7 Al Hexanoyl) oxazolidine ring, 3-N- (C 1 ⁇ 6 alkylsulfonyl) oxazolidine ring, 4-N- (C 2 ⁇ 7 alkanoyl) morpholine, 4-N- (C 1 ⁇ 6 alkylsulfonyl) morpholine, 4 -N- (C 2 ⁇ 7 alkanoyl) -1,4-oxazepane ring, or 4-N-
- Ar is particularly preferably a phenyl group, a 2-pyridyl group, or a 5-pyridyl group (the phenyl group, 2-pyridyl group, or In the 5-pyridyl group, 1 to 3 groups arbitrarily selected from a cyano group, a fluorine atom, a trifluoromethyl group, a methoxy group, and an N-acetylamino group may be substituted with a hydrogen atom on the ring, When two methoxy groups are adjacently substituted on a phenyl group, 2-pyridyl group, or 5-pyridyl group, one hydrogen atom is selected from the methyl group of each group of the two methoxy groups.
- the phenyl group of the Ar Is 1 to 3 substituents selected arbitrarily from a good substituent group may be substituted with hydrogen atoms is replaced with a hydrogen atom on the phenyl group);
- Ar is, for example, a phenyl group, 4-methoxyphenyl group, 3,4-dimethoxyphenyl group, 4-cyanophenyl group, 4- (N-acetylamino) phenyl group, 2,3-dihydrobenzo [b] [1 , 4] dioxynyl group, 2-pyridyl group, 2-methoxy-5-pyridyl group, and the like.
- Ar is a phenyl group (the phenyl group is a hydroxyl group, a cyano group, a nitro group, a halogen atom, a C 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1-6 alkoxy group,
- Ar is, for example, a 4-fluorophenyl group, or 4- (trifluoromethyl) A phenyl group, and the like.
- Ar is C 6 ⁇ 10 aryl group, or heteroaryl group (wherein C 6 ⁇ 10 aryl group, or a heteroaryl group, a hydroxyl group, A cyano group, a nitro group, a halogen atom, a C 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1-6 alkoxy group, and an —NR A R B group (in the —NR A R B group, R A and R B are each independently a hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or a group selected from C 1 ⁇ 6 alkylsulfonyl group (, -NH 2, - 1 to 3 groups arbitrarily selected from NH (C 1-6 alkyl group) and —N (C 1-6 alkyl group 2 )) may be substituted with hydrogen atoms on the
- Ar is C 6 ⁇ 10 aryl group, or a 5-6 membered heteroaryl group (wherein C 6 ⁇ 10 aryl group, or a 5-6 membered heteroaryl group, a hydroxyl group, a cyano group, a nitro group, A halogen atom, a C 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1-6 alkoxy group, and a —NR A R B group (in the —NR A R B group, R A and R B are each independently, a hydrogen atom, a C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or a C 1 ⁇ 6 group selected from alkylsulfonyl group (, -NH 2, -NH (C 1 ⁇ 6 alkyl group), and -N (C 1 ⁇ 6 alkyl group) 2 are excluded)) 1-3 groups selected arbitrarily from well be replaced with a hydrogen atom on the
- Ar is a phenyl group or a pyridyl group (the phenyl group or pyridyl group is a hydroxyl group, a cyano group, a nitro group, a halogen atom, a C 1-6 alkyl group, a halogenated C 1-6 alkyl group).
- R A and R B are each independently a hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or a group selected from C 1 ⁇ 6 alkylsulfonyl group (, -NH 2, -NH (C 1 ⁇ 6 alkyl group), and -N (C 1 ⁇ 6 alkyl group) 2 is excluded ))
- a cyclic ether may be formed by bonding between carbon
- C 1 ⁇ 6 alkoxy group and -NHR G group (R G in -NHR G groups are C 2 ⁇ 7 alkanoyl or C 1 ⁇ 6 alkylsulfonyl group) when is substituted adjacently, the A carbon atom from which one arbitrary hydrogen atom has been removed from an alkyl group of a C 1-6 alkoxy group and a nitrogen atom from which one hydrogen atom has been removed from the —NHR G group are combined to form 3-N— ( C 2 ⁇ 7 Al Hexanoyl) oxazolidine ring, 3-N- (C 1 ⁇ 6 alkylsulfonyl) oxazolidine ring, 4-N- (C 2 ⁇ 7 alkanoyl) morpholine, 4-N- (C 1 ⁇ 6 alkylsulfonyl) morpholine, 4 -N- (C 2 ⁇ 7 alkanoyl) -1,4-oxazepane ring, or 4-N-
- Ar is a phenyl group or a 2-pyridyl group (the phenyl group or 2-pyridyl group is a hydrogen atom on the ring, which is optionally selected from 1 to 3 groups selected from a cyano group and a methoxy group)
- Ar is particularly preferably a phenyl group or a 5-pyridyl group (the phenyl group or 5-pyridyl group is a cyano group, a methoxy group, And 1 to 3 groups arbitrarily selected from N-acetylamino group may be substituted with a hydrogen atom on the ring, and two methoxy groups are substituted on the phenyl group or 5-pyridyl group.
- a 1,4-dioxane ring may be formed by bonding between carbon atoms obtained by removing one hydrogen atom from the methyl group of each group of two methoxy groups)
- Ar phenyl group
- n 3
- the phenyl group of Ar is substituted with a hydrogen atom on the phenyl group.
- Ar is, for example, 4-cyanophenyl group, 4-methoxyphenyl group, 3,4-dimethoxyphenyl group, 4- (N-acetylamino) phenyl group, 2,3-dihydrobenzo [b] [1,4].
- —X— is preferably —O— or —NH—.
- —X— is preferably —O—.
- -A- is particularly preferably represented by the formula (AL-1-1) or (AL-2-1) [in each formula, The outside of the wavy line is not included].
- -A- is particularly preferably represented by the formula (AL-2-1) or (AL-2-2) [in each formula, The outside of the wavy line is not included].
- the combination of Ar, p, —X—, and —A— is preferably Ar is C 6 ⁇ 10 aryl group, or heteroaryl group (wherein C 6 ⁇ 10 aryl group, or a heteroaryl group, a hydroxyl group, a cyano group, a nitro group, a halogen atom, C 1 ⁇ 6 alkyl group, a halogenated A C 1-6 alkyl group, a C 1-6 alkoxy group, and an —NR A R B group (in the —NR A R B group, R A and R B are each independently a hydrogen atom, C 1-6 alkyl, group, C 2 ⁇ 7 alkanoyl group, or a group selected from C 1 ⁇ 6 alkylsulfonyl group (, -NH 2, -NH (C 1 ⁇ 6 alkyl group), and -N (C 1 ⁇ 6 alkyl) 2 are
- R G in the C 6 ⁇ 10 aryl group or a heteroaryl group, C 1 ⁇ 6 alkoxy group and -NHR G group (-NHR G group, C 2 ⁇ 7 alkanoyl or C 1 ⁇ 6 alkylsulfonyl A carbon atom obtained by removing one arbitrary hydrogen atom from the alkyl group of the C 1-6 alkoxy group and one hydrogen atom of the —NHR G group.
- Ar, p, -X -, - A- combinations include, preferably, Ar is, C 6 ⁇ 10 aryl group, or heteroaryl group (wherein C 6 ⁇ 10 aryl group, or a heteroaryl group, a hydroxyl group, a cyano group, a nitro group, a halogen atom, C 1 ⁇ 6 alkyl group, a halogenated C 1 ⁇ 6 alkyl group, C 1 ⁇ 6 alkoxy group, And —NR A R B group (in the —NR A R B group, R A and R B are each independently a hydrogen atom or a group selected from a C 1-6 alkyl group (provided that —NH 2) , —NH (C 1-6 alkyl group), and —N (C 1-6 alkyl group) 2 are excluded))) 1-3 ) are optionally substituted with hydrogen atoms on the ring Is good);
- Ar, p, -X -, - A- combinations include, preferably, Ar is, C 6 ⁇ 10 aryl group, or heteroaryl group (wherein C 6 ⁇ 10 aryl group, or a heteroaryl group, a hydroxyl group, a cyano group, a nitro group, a halogen atom, C 1 ⁇ 6 alkyl group, a halogenated C 1 ⁇ 6 alkyl group, C 1 ⁇ 6 alkoxy group, and in -NR A R B group (-NR A R B group, R A and R B are each independently a hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl or C 1 ⁇ 6, A group selected from alkylsulfonyl groups (excluding —NH 2 , —NH (C 1-6 alkyl group), and —N (C 1-6 alkyl group) 2 )) 1
- Ar, p, -X -, - A- combinations include, preferably, Ar is, C 6 ⁇ 10 aryl group, or heteroaryl group (wherein C 6 ⁇ 10 aryl group, or a heteroaryl group, a hydroxyl group, a cyano group, a nitro group, a halogen atom, C 1 ⁇ 6 alkyl group, a halogenated C 1 ⁇ 6 alkyl group, C 1 ⁇ 6 alkoxy group, and in -NR A R B group (-NR A R B group, R A and R B are each independently a hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl or C 1 ⁇ 6, A group selected from alkylsulfonyl groups (excluding —NH 2 , —NH (C 1-6 alkyl group), and —N (C 1-6 alkyl group) 2 )) 1
- the combination of Ar, p, —X—, and —A— is more preferably Ar is C 6 ⁇ 10 aryl group, or a 5-6 membered heteroaryl group (wherein C 6 ⁇ 10 aryl group, or a 5-6 membered heteroaryl group, a hydroxyl group, a cyano group, a nitro group, a halogen atom, C A 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1-6 alkoxy group, and a —NR A R B group (in the —NR A R B group, R A and R B are each independently hydrogen atom, a C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or a C 1 ⁇ 6 group selected from alkylsulfonyl group (, -NH 2, -NH (C 1 ⁇ 6 alkyl group), and -
- the combination of Ar, p, —X—, and —A— is more preferably Ar is C 6 ⁇ 10 aryl group, or a 5-6 membered heteroaryl group (wherein C 6 ⁇ 10 aryl group, or a 5-6 membered heteroaryl group, a hydroxyl group, a cyano group, a nitro group, a halogen atom, C A 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1-6 alkoxy group, and a —NR A R B group (in the —NR A R B group, R A and R B are each independently A hydrogen atom or a group selected from a C 1-6 alkyl group (excluding —NH 2 , —NH (C 1-6 alkyl group), and —N (C 1-6 alkyl group) 2 ) 1 to 3 groups arbitrarily selected from) may be substituted with hydrogen
- the combination of Ar, p, -X-, and -A- is more preferably Ar is C 6 ⁇ 10 aryl group, or a 5-6 membered heteroaryl group (wherein C 6 ⁇ 10 aryl group, or a 5-6 membered heteroaryl group, a hydroxyl group, a cyano group, a nitro group, a halogen atom, C A 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1-6 alkoxy group, and a —NR A R B group (in the —NR A R B group, R A and R B are each independently hydrogen atom, a C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or a C 1 ⁇ 6 group selected from alkylsulfonyl group (, -NH 2, -NH (C 1 ⁇ 6 alkyl group), and
- the combination of Ar, p, —X—, and —A— is more preferably Ar is C 6 ⁇ 10 aryl group, or a 5-6 membered heteroaryl group (wherein C 6 ⁇ 10 aryl group, or a 5-6 membered heteroaryl group, a hydroxyl group, a cyano group, a nitro group, a halogen atom, C A 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1-6 alkoxy group, and a —NR A R B group (in the —NR A R B group, R A and R B are each independently hydrogen atom, a C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or a C 1 ⁇ 6 group selected from alkylsulfonyl group (, -NH 2, -NH (C 1 ⁇ 6 alkyl group), and
- the combination of Ar, p, —X—, and —A— is more preferably Ar is a phenyl group or a pyridyl group (the phenyl group or pyridyl group is a hydroxyl group, a cyano group, a nitro group, a halogen atom, a C 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1- 6 alkoxy group, and in -NR A R B group (-NR A R B group, R A and R B are each independently a hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or A group selected from C 1-6 alkylsulfonyl groups (excluding —NH 2 , —NH (C 1-6 alkyl group), and —N (C 1-6 alkyl group) 2 )) 1 to 3 groups selected well be
- R G is in -NHR G group, a C 2 ⁇ 7 alkanoyl or C 1 ⁇ 6 alkylsulfonyl group) alkoxy group and -NHR G groups if is substituted adjacently, the C 1 ⁇ 6 alkoxy by nitrogen atoms in which arbitrary hydrogen atom from an alkyl group radicals is one excluded hydrogen atoms of the carbon atoms and the -NHR G group was removed one binds, 3-N- (C 2 ⁇ 7 alkanoyl Oxa Lysine ring, 3-N- (C 1 ⁇ 6 alkylsulfonyl) oxazolidine ring, 4-N- (C 2 ⁇ 7 alkanoyl) morpholine, 4-N- (C 1 ⁇ 6 alkylsulfonyl) morpholine, 4-N - it is (C 2 ⁇ 7 alkanoyl) -1,4-oxazepane ring, or 4-N- may be formed (C 1 ⁇
- Ar is more preferably a phenyl group (the phenyl group is a hydroxyl group) , A cyano group, a nitro group, a halogen atom, a C 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1-6 alkoxy group, and a —NR A R B group (in the —NR A R B group, A and R B are each independently a hydrogen atom or a group selected from a C 1-6 alkyl group (provided that —NH 2 , —NH (C 1-6 alkyl group), and —N ( 1 to 3 alkyl groups selected from (C 1-6 alkyl group) 2 )))) are optionally substituted with hydrogen atoms on the ring; p is an integer of 1; —X— is —O—
- the combination of Ar, p, —X—, and —A— is more preferably Ar is a phenyl group or a pyridyl group (the phenyl group or pyridyl group is a hydroxyl group, a cyano group, a nitro group, a halogen atom, a C 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1- 6 alkoxy group, and in -NR A R B group (-NR A R B group, R A and R B are each independently a hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or A group selected from C 1-6 alkylsulfonyl groups (excluding —NH 2 , —NH (C 1-6 alkyl group), and —N (C 1-6 alkyl group) 2 )) 1 to 3 groups selected well
- R G is in -NHR G group, a C 2 ⁇ 7 alkanoyl or C 1 ⁇ 6 alkylsulfonyl group) alkoxy group and -NHR G groups if is substituted adjacently, the C 1 ⁇ 6 alkoxy by nitrogen atoms in which arbitrary hydrogen atom from an alkyl group radicals is one excluded hydrogen atoms of the carbon atoms and the -NHR G group was removed one binds, 3-N- (C 2 ⁇ 7 alkanoyl Oxa Lysine ring, 3-N- (C 1 ⁇ 6 alkylsulfonyl) oxazolidine ring, 4-N- (C 2 ⁇ 7 alkanoyl) morpholine, 4-N- (C 1 ⁇ 6 alkylsulfonyl) morpholine, 4-N - it is (C 2 ⁇ 7 alkanoyl) -1,4-oxazepane ring, or 4-N- may be formed (C 1 ⁇
- the combination of Ar, p, —X—, and —A— is more preferably Ar is a phenyl group or a pyridyl group (the phenyl group or pyridyl group is a hydroxyl group, a cyano group, a nitro group, a halogen atom, a C 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1- 6 alkoxy group, and in -NR A R B group (-NR A R B group, R A and R B are each independently a hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or A group selected from C 1-6 alkylsulfonyl groups (excluding —NH 2 , —NH (C 1-6 alkyl group), and —N (C 1-6 alkyl group) 2 )) 1 to 3 groups selected well
- R G is in -NHR G group, a C 2 ⁇ 7 alkanoyl or C 1 ⁇ 6 alkylsulfonyl group) alkoxy group and -NHR G groups if is substituted adjacently, the C 1 ⁇ 6 alkoxy by nitrogen atoms in which arbitrary hydrogen atom from an alkyl group radicals is one excluded hydrogen atoms of the carbon atoms and the -NHR G group was removed one binds, 3-N- (C 2 ⁇ 7 alkanoyl Oxa Lysine ring, 3-N- (C 1 ⁇ 6 alkylsulfonyl) oxazolidine ring, 4-N- (C 2 ⁇ 7 alkanoyl) morpholine, 4-N- (C 1 ⁇ 6 alkylsulfonyl) morpholine, 4-N - it is (C 2 ⁇ 7 alkanoyl) -1,4-oxazepane ring, or 4-N- may be formed (C 1 ⁇
- the combination of Ar, p, -X-, and -A- is particularly preferably Ar is a phenyl group or a 2-pyridyl group (the phenyl group or 2-pyridyl group is a ring formed by 1 to 3 groups arbitrarily selected from a cyano group, a fluorine atom, a trifluoromethyl group, and a methoxy group)
- the above hydrogen atom may be substituted, and when two methoxy groups are substituted on the phenyl group or the 2-pyridyl group, any methyl group from each group of the two methoxy groups
- a 1,4-dioxane ring may be formed by bonding between carbon atoms from which one hydrogen atom is removed.
- Examples of combinations of Ar, p, -X-, and -A- include, for example, Ar represents a phenyl group, 4-fluorophenyl group, 4- (trifluoromethyl) phenyl group, 4-methoxyphenyl group, 4-cyanophenyl group, 2,3-dihydrobenzo [b] [1,4] dioxinyl group Or a 2-pyridyl group;
- p is an integer of 1 or 2;
- —X— is —O— or —NH—:
- -A- is the formula (AL-1-1), (AL-2-1) or (AL-2-2) in the above
- the combination of Ar, p, —X—, and —A— is particularly preferably Ar represents a phenyl group, a 2-pyridyl group, or a 5-pyridyl group (the phenyl group, 2-pyridyl group, or 5-pyridyl group includes a cyano group, a fluorine atom, a trifluoromethyl group, a methoxy group, and an N- One to three groups arbitrarily selected from an acetylamino group may be substituted with a hydrogen atom on the ring, and two methoxy groups are adjacent to each other on a phenyl group, a 2-pyridyl group, or a 5-pyridyl group.
- a 1,4-dioxane ring may be formed by bonding between carbon atoms obtained by removing one arbitrary hydrogen atom from the methyl group of each group of two methoxy groups.
- Ar phenyl group
- n 3
- a hydrogen atom on the phenyl group in the phenyl group of Ar Is optionally selected from the group of substituents that may be substituted.
- Ar is phenyl group, 4-fluorophenyl group, 4- (trifluoromethyl) phenyl group, 4-methoxyphenyl group, 3,4- Dimethoxyphenyl group, 4- (N-acetylamino) phenyl group, 4-cyanophenyl group, 2,3-dihydrobenzo [b] [1,4] dioxinyl group, 2-pyridyl group, or 2-methoxy-5- A pyridyl group;
- p is an integer of 1 or 2;
- —X— is —O— or —NH—:
- -A- is the formula (AL-1-1), (AL-2-1) or (AL-2-2) in the above embodiment [1a-3] [in each formula, the outside of the wavy line at both ends is not included. ];
- Ar is, for example, a phenyl group, a 4-fluorophenyl group, or a 4- (trifluor
- the combination of Ar, p, -X-, and -A- is particularly preferably Ar is a phenyl group or a 2-pyridyl group (the phenyl group or 2-pyridyl group is a group in which 1 to 3 groups arbitrarily selected from a cyano group and a methoxy group are substituted with hydrogen atoms on the ring; In the case where two methoxy groups are adjacently substituted on the phenyl group or 2-pyridyl group, one hydrogen atom is removed from the methyl group of each group of the two methoxy groups.
- Ar is, for example, a phenyl group, a 4-methoxyphenyl group, a 4-cyanophenyl group, 2,3-dihydrobenzo [b] [1, 4] a dioxynyl group or a 2-pyridyl group;
- p is an integer of 1 or 2;
- —X— is —O—:
- -A- is the formula (AL-1-1) or (AL-2-1) in the above embodiment [1-3] (in each formula, the outside of the wavy line at both ends is not included);
- the combination of Ar, p, -X-, and -A- is the following partial structural formula [in each formula, the right side of the wavy line is not included] As shown in
- Ar is particularly preferably Ar is a phenyl group or a 5-pyridyl group (described above).
- phenyl group or 5-pyridyl group 1 to 3 groups arbitrarily selected from a cyano group, a methoxy group, and an N-acetylamino group may be substituted with a hydrogen atom on the ring.
- any one or more carboxyl groups of alginic acid are represented by the following formula (I):
- Ar is preferably a phenyl group (the phenyl group is a hydroxyl group, a cyano group, a nitro group, a halogen atom, a C 1-6 alkyl group, a halogenated group) A C 1-6 alkyl group, a C 1-6 alkoxy group, and an —NR A R B group (in the —NR A R B group, R A and R B are each independently a hydrogen atom, C 1-6 alkyl, group, C 2 ⁇ 7 alkanoyl group, or a group selected from C 1 ⁇ 6 alkylsulfonyl group (, -NH 2, -NH (C 1 ⁇ 6 alkyl group), and -N (C 1 ⁇ 6 1 to 3 groups arbitrarily selected from the alkyl group) 2 ))))))) may be substituted with hydrogen atoms on the ring, and the phenyl group includes a
- a cyclic ether may be formed by bonding between carbon atoms in which any one hydrogen atom is removed from each alkyl group of the two C 1-6 alkoxy groups, or , C 1 ⁇ 6 alkoxy group and -NHR G group (R G in -NHR G groups are C 2 ⁇ 7 alkanoyl or C 1 ⁇ 6 alkylsulfonyl group) when is substituted adjacently, the A carbon atom from which one arbitrary hydrogen atom has been removed from an alkyl group of a C 1-6 alkoxy group and a nitrogen atom from which one hydrogen atom has been removed from the —NHR G group are combined to form 3-N— ( C 2 ⁇ 7 alkanoyl Oxazolidine ring,
- phenyl group of Ar 1 to 3 groups arbitrarily selected from a substituent group which may be substituted with a hydrogen atom on the phenyl group are substituted with a hydrogen atom on the phenyl group).
- Ar is, for example, a phenyl group, 4-fluoropheny Group, 4- (trifluoromethyl) phenyl group, a 4-methoxyphenyl group, 4-cyanophenyl group, or 2,3-dihydro-benzo [b] [1,4] dioxinyl group, and the like.
- Ar is, for example, a phenyl group, a 4-fluorophenyl group, a 4- (trifluoromethyl) phenyl group, a 4-methoxyphenyl group, a 3,4-dimethoxyphenyl group, a 4- (N-acetylamino) phenyl group, 4 A cyanophenyl group, or a 2,3-dihydrobenzo [b] [1,4] dioxinyl group, and the like.
- Ar is a phenyl group (the phenyl group is a hydroxyl group, a cyano group, a nitro group, a halogen atom, a C 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1-6 alkoxy group,
- Ar is C 6 ⁇ 10 aryl group (the C 6 ⁇ 10 aryl group, a hydroxyl group, a cyano group, a nitro group, a halogen atom, C A 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1-6 alkoxy group, and a —NR A R B group (in the —NR A R B group, R A and R B are each independently hydrogen atom, a C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or a C 1 ⁇ 6 group selected from alkylsulfonyl group (, -NH 2, -NH (C 1 ⁇ 6 alkyl group), and -N (C 1 ⁇ 6 alkyl group) 2 are excluded)) 1-3 groups selected arbitrarily from well be replaced with a hydrogen atom on the ring, the C 6 ⁇ 10 aryl group, a hydroxyl group, a cyano group, a nitro group
- the C 6 ⁇ 10 aryl group, R G in C 1 ⁇ 6 alkoxy group and -NHR G group (-NHR G group, C 2 ⁇ 7 alkanoyl or C 1 ⁇ 6 alkylsulfonyl group Are adjacently substituted, a carbon atom obtained by removing one arbitrary hydrogen atom from the alkyl group of the C 1-6 alkoxy group and a hydrogen atom of the —NHR G group are removed.
- Ar is a phenyl group (the phenyl group is a hydroxyl group, a cyano group, a nitro group, a halogen atom, a C 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1-6 alkoxy group, and in -NR A R B group (-NR A R B group, R A and R B are each independently a hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl or C 1 ⁇ 6, A group selected from alkylsulfonyl groups (excluding —NH 2 , —NH (C 1-6 alkyl group), and —N (C 1-6 alkyl group) 2 )) 1 Up to 3 groups may be substituted with hydrogen atoms on the ring, and the phenyl group is adjacent to a C 1-6 alkyl group and a C 1-6 alkoxy group or two C 1-6 alkoxy groups.
- the C 1 ⁇ 6 alkyl group By arbitrary hydrogen atom from an alkyl group of each group of fine C 1 ⁇ 6 alkoxy group is bonded between the one excluded carbon atoms, or, optionally from each group of the two C 1 ⁇ 6 alkoxy group May form a cyclic ether by bonding between carbon atoms from which one hydrogen atom is removed, or a C 1-6 alkoxy group and a —NHR G group (—NHR G group) may be bonded to the phenyl group.
- R G when it is C 2 ⁇ 7 alkanoyl or C 1 ⁇ 6 alkylsulfonyl group) is substituted adjacently, any hydrogen atom is one of the alkyl group in the C 1 ⁇ 6 alkoxy group in by removed nitrogen atom to which a hydrogen atom has been removed one of the carbon atoms and the -NHR G groups are bonded, 3-N- (C 2 ⁇ 7 alkanoyl) oxazolidine ring, 3-N- (C 1 ⁇ 6 alkyl sulfo Yl) oxazolidine ring, 4-N- (C 2 ⁇ 7 alkanoyl) morpholine, 4-N- (C 1 ⁇ 6 alkylsulfonyl) morpholine, 4-N- (C 2 ⁇ 7 alkanoyl) -1,4 An oxazepan ring or a 4-N- (C 1-6 alkylsulfonyl) -1,4-oxazepan ring
- Ar is a phenyl group (wherein the phenyl group may be optionally substituted by 1 to 3 groups selected from a cyano group and a methoxy group with a hydrogen atom on the ring, In the case where two methoxy groups are adjacently substituted, 1,4-dioxane is bonded by bonding between carbon atoms in which any hydrogen atom is removed from the methyl group of each of the two methoxy groups.
- Ar is more preferably a phenyl group (the phenyl group is arbitrarily selected from a cyano group, a methoxy group, and an N-acetylamino group 1 Up to 3 groups may be substituted with hydrogen atoms on the ring, and when two methoxy groups are adjacently substituted on the phenyl group, from the methyl group of each group of the two methoxy groups A 1,4-dioxane ring may be formed by bonding between carbon atoms from which one hydrogen atom is removed.
- Ar is, for example, a 4-cyanophenyl group, a 4-methoxyphenyl group, a 3,4-dimethoxyphenyl group, a 4- (N-acetylamino) phenyl group, or 2,3-dihydrobenzo [b] [1,4 A dioxynyl group, and the like.
- -A- is particularly preferably the formula (AL-1-1) or (AL-2-1) [in each formula, The outside of the wavy line is not included].
- n, m and j in formula (AL-3-1) or formula (AL-4-1) in the above embodiment [1b-2-2] are preferable, more Preferred, more preferred, and particularly preferred numerical ranges are the same as those defined in the above embodiment [1-3-2-1].
- the combination of Ar, p and —A— is preferably Ar is C 6 ⁇ 10 aryl group (the C 6 ⁇ 10 aryl group, a hydroxyl group, a cyano group, a nitro group, a halogen atom, C 1 ⁇ 6 alkyl group, a halogenated C 1 ⁇ 6 alkyl group, C 1 ⁇ 6 alkoxy group, and in -NR A R B group (-NR A R B group, R A and R B are each independently a hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or A group selected from C 1-6 alkylsulfonyl groups (excluding —NH 2 , —NH (C 1-6 alkyl group), and —N (C 1-6 alkyl group) 2 )) 1-3 groups may be substituted with a hydrogen atom on ring selected in the C 6 ⁇
- Ar, p as a combination of -A-,
- Ar, C 6 ⁇ 10 aryl group the C 6 ⁇ 10 aryl group , Hydroxyl group, cyano group, nitro group, halogen atom, C 1-6 alkyl group, halogenated C 1-6 alkyl group, C 1-6 alkoxy group, and —NR A R B group (—NR A R B group And R A and R B are each independently a hydrogen atom or a group selected from a C 1-6 alkyl group (provided that —NH 2 , —NH (C 1-6 alkyl group), and 1 to 3 groups arbitrarily selected from -N (C 1-6 alkyl group 2 )))) may be substituted with hydrogen atoms on the ring);
- p is an integer of 1;
- -X- is -O-;
- -A- is the formula (AL-1) or (AL-2) in the
- Ar, p as a combination of -A-,
- Ar, C 6 ⁇ 10 aryl group (the C 6 ⁇ 10 aryl group , Hydroxyl group, cyano group, nitro group, halogen atom, C 1-6 alkyl group, halogenated C 1-6 alkyl group, C 1-6 alkoxy group, and —NR A R B group
- R a and R B are each independently a hydrogen atom, a C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or a group selected from C 1 ⁇ 6 alkylsulfonyl group (which - 1 to 3 groups arbitrarily selected from NH 2 , —NH (C 1-6 alkyl group), and —N (C 1-6 alkyl group) 2 are substituted with hydrogen atoms on the ring
- the C 6 ⁇ 10 aryl group the C 6 ⁇ 10 aryl group , Hydroxyl group, cyano group, nitro group, hal
- Ar, p as a combination of -A-,
- Ar, C 6 ⁇ 10 aryl group (the C 6 ⁇ 10 aryl group , Hydroxyl group, cyano group, nitro group, halogen atom, C 1-6 alkyl group, halogenated C 1-6 alkyl group, C 1-6 alkoxy group, and —NR A R B group
- R a and R B are each independently a hydrogen atom, a C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or a group selected from C 1 ⁇ 6 alkylsulfonyl group (which - 1 to 3 groups arbitrarily selected from NH 2 , —NH (C 1-6 alkyl group), and —N (C 1-6 alkyl group) 2 are substituted with hydrogen atoms on the ring
- the C 6 ⁇ 10 aryl group the C 6 ⁇ 10 aryl group , Hydroxyl group, cyano group, nitro group, hal
- the combination of Ar, p, —X—, and —A— is more preferably Ar represents a phenyl group (the phenyl group is a hydroxyl group, a cyano group, a nitro group, a halogen atom, a C 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1-6 alkoxy group, and —NR A in R B group (-NR A R B group, R A and R B are each independently a hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or a C 1 ⁇ 6 alkylsulfonyl group 1 to 3 groups optionally selected from (excluding —NH 2 , —NH (C 1-6 alkyl group), and —N (C 1-6 alkyl group) 2 ))
- a group may be substituted with a hydrogen atom on the ring,
- Ar is more preferably a phenyl group (the phenyl group is a hydroxyl group) , A cyano group, a nitro group, a halogen atom, a C 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1-6 alkoxy group, and a —NR A R B group (in the —NR A R B group, A and R B are each independently a hydrogen atom or a group selected from a C 1-6 alkyl group (provided that —NH 2 , —NH (C 1-6 alkyl group), and —N ( 1 to 3 alkyl groups selected from (C 1-6 alkyl group) 2 )))) are optionally substituted with hydrogen atoms on the ring; p is an integer of 1; —X— is —O
- Ar represents a phenyl group (the phenyl group is a hydroxyl group, a cyano group, a nitro group, a halogen atom, a C 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1-6 alkoxy group, and —NR A in R B group (-NR A R B group, R A and R B are each independently a hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or a C 1 ⁇ 6 alkylsulfonyl group 1 to 3 groups optionally selected from (excluding —NH 2 , —NH (C 1-6 alkyl group), and —N (C 1-6 alkyl group) 2 ))
- a group may be substituted with a hydrogen atom on the ring
- Ar represents a phenyl group (the phenyl group is a hydroxyl group, a cyano group, a nitro group, a halogen atom, a C 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1-6 alkoxy group, and —NR A in R B group (-NR A R B group, R A and R B are each independently a hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or a C 1 ⁇ 6 alkylsulfonyl group 1 to 3 groups optionally selected from (excluding —NH 2 , —NH (C 1-6 alkyl group), and —N (C 1-6 alkyl group) 2 ))
- a group may be substituted with a hydrogen atom on the ring
- Ar represents a phenyl group (wherein the phenyl group may be substituted with 1 to 3 groups arbitrarily selected from a cyano group, a fluorine atom, a trifluoromethyl group, and a methoxy group with a hydrogen atom on the ring;
- 1 is obtained by bonding between carbon atoms obtained by removing one hydrogen atom from the methyl group of each group of the two methoxy groups.
- Examples of combinations of Ar, p, -X-, and -A- include, for example, Ar is a phenyl group, 4-fluorophenyl group, 4- (trifluoromethyl) phenyl group, 4-methoxyphenyl group, 4-cyanophenyl group, or 2,3-dihydrobenzo [b] [1,4] dioxinyl A group; p is an integer of 1 or 2; —X— is —O—: -A- is the formula (AL-1-1) or (AL-2-1) in the above embodiment [1b-2] [in each formula, the outside of the wavy line at both ends is not included]; For example, the combination of Ar, p, -X-, and -A- is the following partial structural formula [in each formula, the right side of the wavy line is not included] As shown in [1b-3-3-1] In the alginic acid derivative of the aspect [1b], the combination of Ar, p, —X—, and —A
- Ar is, for example, a phenyl group, a 4-fluorophenyl group, or a 4- (trifluoro
- Ar represents a phenyl group (wherein the phenyl group may be optionally substituted by 1 to 3 groups selected from a cyano group and a methoxy group with a hydrogen atom on the ring; Are adjacently substituted, a 1,4-dioxane ring is formed by bonding between the carbon atoms obtained by removing one hydrogen atom from the methyl group of each of the two methoxy groups.
- Ar is, for example, a phenyl group, a 4-methoxyphenyl group, a 4-cyanophenyl group, or 2,3-dihydrobenzo [b] [1] , 4] a dioxynyl group;
- p is an integer of 1 or 2;
- —X— is —O—:
- -A- is the formula (AL-1-1) or (AL-2-1) in the above embodiment [1b-2] [in each formula, the outside of the wavy line at both ends is not included];
- Ar is more preferably a phenyl group (the phenyl group is a cyano group) 1 to 3 groups arbitrarily selected from a methoxy group and an N-acetylamino group may be substituted with a hydrogen atom on the ring, and two methoxy groups are substituted on the phenyl group adjacent to each other.
- Ar is 4-cyanophenyl group, 4-methoxyphenyl group, 3,4-dimethoxyphenyl group, 4- (N-acetylamino) phenyl A group, or a 2,3-dihydrobenzo [b] [1,4] dioxinyl group
- p is an integer of 1 or 2
- —X— is —O—
- -A- is the formula (AL-2-1) in the above embodiment [1b-2] [in each formula, the outside of the wavy line at both ends is not included];
- the combination of Ar, p, -X-, and -A- is the following partial structural formula [in each formula, the right side of the wavy line is not included] As shown in
- the second aspect is as follows.
- the third aspect is as follows.
- the fourth aspect is as follows. Photocrosslinked alginic acid obtained by irradiating the alginic acid derivative according to the aspect [1], [1a] or [1b] with light.
- the embodiment 4-1 is a preferred embodiment of the embodiment [4], specifically, the embodiments [1-4-1], [1-4-1a], [1- 4-1b], [1-4-1c], [1a-4-1], [1a-4-1a], [1a-4-1b], or [1a-4-1c] A photocrosslinked alginic acid obtained by irradiating with light; More preferably, the above embodiments [1-4-2], [1-4-2a], [1-4-2b], [1-4-2c], [1a-4-2], [1a-4] -2a], [1a-4-2b], or a photocrosslinked alginic acid obtained by irradiating the alginic acid derivative according to [1a-4-2c] with light; More preferably, the embodiments [1-4-3], [1-4-3a], [1-4-3b], [1-4-3c], [1a-4-3], [1a-4-] 3a], [1a-4-3b], or a photocrosslinked alginic acid obtained by irradiating the alginic acid derivative according to [1
- the embodiment 4-2 is a preferred embodiment of the embodiment [4]. Specifically, the embodiments [1b-3-1], [1b-3-1a], [1b- 3-1b], or a photocrosslinked alginic acid obtained by irradiating the alginic acid derivative according to [1b-3-1c] with light; More preferably, it is obtained by irradiating the alginic acid derivative according to the above embodiment [1b-3-2], [1b-3-2a], [1b-3-2b], or [1b-3-2c] with light.
- a photocrosslinked alginate More preferably, it is a photocrosslinked alginic acid obtained by irradiating the alginic acid derivative according to the embodiment [1b-3-3a] with light,
- the following formula [in each formula, the right side of the wavy line is not included]:
- the 5-1st aspect is as follows.
- a mode 5-2 is as follows.
- the photocrosslinked alginic acid according to [4] which has the same structure as defined in [1a] or [1b].
- the sixth aspect is as follows.
- a seventh aspect is as follows. As a bridge obtained by irradiating the gel obtained by dripping the solution of the alginic acid derivative according to the above aspect [1], [1a] or [1b] into a solution containing a divalent metal ion, 2 A photocrosslinked alginate structure comprising ionic crosslinks partially formed by valent metal ions and chemical crosslinks formed by light irradiation.
- the embodiment 7-1 is a preferred embodiment of the embodiment [7], specifically, the embodiments [1-4-1], [1-4-1a], [1- 4-1b], [1-4-1c], [1a-4-1], [1a-4-1a], [1a-4-1b], or [1a-4-1c] Formed by irradiating light onto a gel obtained by dripping the solution of 2 into a solution containing divalent metal ions, and formed by ion crosslinking and light irradiation partially formed by divalent metal ions as a bridge.
- a photocrosslinked alginate structure comprising a chemical crosslink; More preferably, the above embodiments [1-4-2], [1-4-2a], [1-4-2b], [1-4-2c], [1a-4-2], [1a-4] -2a], [1a-4-2b], or [1a-4-2c], the gel obtained by dropping a solution of an alginic acid derivative into a solution containing a divalent metal ion is irradiated with light.
- a photocrosslinked alginate structure comprising an ionic crosslink formed partially by divalent metal ions as a crosslink and a chemical crosslink formed by light irradiation; More preferably, the embodiments [1-4-3], [1-4-3a], [1-4-3b], [1-4-3c], [1a-4-3], [1a-4] -3a], [1a-4-3b], or [1a-4-3c], the gel obtained by dropping a solution of the alginic acid derivative into a solution containing a divalent metal ion is irradiated with light.
- a photocrosslinked alginate structure comprising an ionic crosslink formed partially by divalent metal ions as a crosslink and a chemical crosslink formed by light irradiation;
- the gel obtained by dropping the solution of the alginic acid derivative described in the above embodiment [1-4-4a] or [1a-4-4a] into a solution containing a divalent metal ion is irradiated with light.
- a photocrosslinked alginate structure comprising an ionic crosslink formed partially by divalent metal ions as a crosslink and a chemical crosslink formed by light irradiation;
- the following formula [in each formula, the right side of the wavy line is not included]: A part of a divalent metal ion as a crosslink obtained by irradiating a gel obtained by dropping a solution of an alginic acid derivative introduced with a photoreactive group selected from the above into a solution containing a divalent metal ion.
- a photocrosslinked alginate structure comprising a chemically formed ionic crosslink and a chemical crosslink formed by light irradiation; Or, particularly preferably, a gel obtained by dropping a solution of an alginic acid derivative according to the above embodiment [1-4-4b] or [1a-4-4b] into a solution containing a divalent metal ion.
- a photocrosslinked alginic acid structure obtained by photoirradiation including ionic crosslinks partially formed by divalent metal ions as crosslinks and chemical crosslinks formed by light irradiation;
- the following formula [in each formula, the right side of the wavy line is not included]: A part of a divalent metal ion as a crosslink obtained by irradiating a gel obtained by dropping a solution of an alginic acid derivative introduced with a photoreactive group selected from the above into a solution containing a divalent metal ion.
- a photocrosslinked alginate structure comprising a chemically formed ionic crosslink and a chemical crosslink formed by light irradiation; Or, particularly preferably, a gel obtained by dropping a solution of an alginic acid derivative according to the above embodiment [1-4-4c] or [1a-4-4c] into a solution containing a divalent metal ion.
- a photocrosslinked alginic acid structure obtained by photoirradiation including ionic crosslinks partially formed by divalent metal ions as crosslinks and chemical crosslinks formed by light irradiation;
- the following formula [in each formula, the right side of the wavy line is not included]: A part of a divalent metal ion as a crosslink obtained by irradiating a gel obtained by dropping a solution of an alginic acid derivative introduced with a photoreactive group selected from the above into a solution containing a divalent metal ion.
- a photocrosslinked alginate structure comprising a chemically formed ionic crosslink and a chemical crosslink formed by light irradiation;
- the gel is obtained by dropping the solution of the alginic acid derivative according to the embodiment [1-4-4] or [1a-4-4] into a solution containing a divalent metal ion.
- a photocrosslinked alginic acid structure obtained by photoirradiation including ionic crosslinks partially formed by divalent metal ions as crosslinks and chemical crosslinks formed by light irradiation;
- the following formula [in each formula, the right side of the wavy line is not included]: A part of a divalent metal ion as a crosslink obtained by irradiating a gel obtained by dropping a solution of an alginic acid derivative introduced with a photoreactive group selected from the above into a solution containing a divalent metal ion.
- a photocrosslinked alginate structure comprising a chemically formed ionic crosslink and a chemical crosslink formed by light irradiation; Or, particularly preferably, by dropping the solution of the alginic acid derivative according to the embodiment [1-4-4-1] or [1a-4-4-1] into a solution containing a divalent metal ion.
- a photocrosslinked alginate structure obtained by irradiating the resulting gel with light including ionic crosslinks partially formed by divalent metal ions as crosslinks and chemical crosslinks formed by light irradiation;
- the following formula [in each formula, the right side of the wavy line is not included]: A part of a divalent metal ion as a crosslink obtained by irradiating a gel obtained by dropping a solution of an alginic acid derivative introduced with a photoreactive group selected from the above into a solution containing a divalent metal ion.
- a photocrosslinked alginate structure comprising a chemically formed ionic crosslink and a chemical crosslink formed by light irradiation; Or, particularly preferably, by dropping the solution of the alginic acid derivative according to the above embodiment [1-4-4-2] or [1a-4-4-2] into a solution containing a divalent metal ion.
- a photocrosslinked alginate structure obtained by irradiating the resulting gel with light including ionic crosslinks partially formed by divalent metal ions as crosslinks and chemical crosslinks formed by light irradiation;
- the following formula [in each formula, the right side of the wavy line is not included]: A part of a divalent metal ion as a crosslink obtained by irradiating a gel obtained by dropping a solution of an alginic acid derivative introduced with a photoreactive group selected from the above into a solution containing a divalent metal ion.
- a photocrosslinked alginate structure comprising a chemically formed ionic crosslink and a chemical crosslink formed by light irradiation; Most preferably, the following formula [in each formula, the right side of the wavy line is not included]: A part of a divalent metal ion as a crosslink obtained by irradiating a gel obtained by dropping a solution of an alginic acid derivative introduced with a photoreactive group selected from the above into a solution containing a divalent metal ion. It is a photocrosslinked alginic acid structure comprising an ionically formed ionic crosslink and a chemical crosslink formed by light irradiation.
- the embodiment 7-2 is a preferred embodiment of the embodiment [7], specifically, the embodiments [1b-3-1], [1b-3-1a], [1b- 3-1b], or [1b-3-1c], a solution obtained by irradiating the gel obtained by dropping a solution of the alginic acid derivative in a solution containing a divalent metal ion, as a crosslink.
- a photocrosslinked alginate structure comprising ionic crosslinks partially formed by valent metal ions and chemical crosslinks formed by light irradiation; More preferably, the solution of the alginic acid derivative according to the above aspect [1b-3-2], [1b-3-2a], [1b-3-2b], or [1b-3-2c] is a divalent metal.
- a photocrosslinked alginate structure comprising ionic crosslinks partially formed by valent metal ions and chemical crosslinks formed by light irradiation;
- the following formula [in each formula, the right side of the wavy line is not included]: A part of a divalent metal ion as a crosslink obtained by irradiating a gel obtained by dropping a solution of an alginic acid derivative introduced with a photoreactive group selected from the above into a solution containing a divalent metal ion.
- a photocrosslinked alginate structure comprising a chemically formed ionic crosslink and a chemical crosslink formed by light irradiation; Or, more preferably, a crosslink obtained by irradiating the gel obtained by dropping the solution of the alginic acid derivative according to the embodiment [1b-3-3b] into a solution containing a divalent metal ion.
- a photocrosslinked alginic acid structure including ionic crosslinks partially formed by divalent metal ions and chemical crosslinks formed by light irradiation;
- the following formula [in each formula, the right side of the wavy line is not included]: A part of a divalent metal ion as a crosslink obtained by irradiating a gel obtained by dropping a solution of an alginic acid derivative introduced with a photoreactive group selected from the above into a solution containing a divalent metal ion.
- a photocrosslinked alginate structure comprising a chemically formed ionic crosslink and a chemical crosslink formed by light irradiation; Or, more preferably, a crosslink obtained by irradiating the gel obtained by dripping the solution of the alginic acid derivative according to the embodiment [1b-3-3c] into a solution containing a divalent metal ion.
- a photocrosslinked alginic acid structure including ionic crosslinks partially formed by divalent metal ions and chemical crosslinks formed by light irradiation;
- the following formula [in each formula, the right side of the wavy line is not included]: A part of a divalent metal ion as a crosslink obtained by irradiating a gel obtained by dropping a solution of an alginic acid derivative introduced with a photoreactive group selected from the above into a solution containing a divalent metal ion.
- a photocrosslinked alginate structure comprising a chemically formed ionic crosslink and a chemical crosslink formed by light irradiation; Or, more preferably, a crosslink obtained by irradiating the gel obtained by dripping the solution of the alginic acid derivative according to the aspect [1b-3-3] into a solution containing a divalent metal ion.
- a photocrosslinked alginic acid structure including ionic crosslinks partially formed by divalent metal ions and chemical crosslinks formed by light irradiation;
- the following formula [in each formula, the right side of the wavy line is not included]: A part of a divalent metal ion as a crosslink obtained by irradiating a gel obtained by dropping a solution of an alginic acid derivative introduced with a photoreactive group selected from the above into a solution containing a divalent metal ion.
- a photocrosslinked alginate structure comprising a chemically formed ionic crosslink and a chemical crosslink formed by light irradiation; Or, more preferably, it is obtained by irradiating the gel obtained by dropping the solution of the alginic acid derivative described in the above embodiment [1b-3-3-1] into a solution containing a divalent metal ion.
- a photocrosslinked alginate structure comprising ionic crosslinks partially formed by divalent metal ions as crosslinks and chemical crosslinks formed by light irradiation;
- divalent metal ions as crosslinks and chemical crosslinks formed by light irradiation
- the following formula [in each formula, the right side of the wavy line is not included]: A part of a divalent metal ion as a crosslink obtained by irradiating a gel obtained by dropping a solution of an alginic acid derivative introduced with a photoreactive group selected from the above into a solution containing a divalent metal ion.
- a photocrosslinked alginate structure comprising a chemically formed ionic crosslink and a chemical crosslink formed by light irradiation; Or, more preferably, it is obtained by irradiating the gel obtained by dropping the solution of the alginic acid derivative described in the above embodiment [1b-3-3-2] into a solution containing a divalent metal ion.
- a photocrosslinked alginate structure comprising ionic crosslinks partially formed by divalent metal ions as crosslinks and chemical crosslinks formed by light irradiation;
- divalent metal ions as crosslinks and chemical crosslinks formed by light irradiation
- the following formula [in each formula, the right side of the wavy line is not included]: A part of a divalent metal ion as a crosslink obtained by irradiating a gel obtained by dropping a solution of an alginic acid derivative introduced with a photoreactive group selected from the above into a solution containing a divalent metal ion.
- a photocrosslinked alginate structure comprising a chemically formed ionic crosslink and a chemical crosslink formed by light irradiation; Particularly preferably, the following formula [in each formula, the right side of the wavy line is not included]: A part of a divalent metal ion as a crosslink obtained by irradiating a gel obtained by dropping a solution of an alginic acid derivative introduced with a photoreactive group selected from the above into a solution containing a divalent metal ion. It is a photocrosslinked alginic acid structure comprising an ionically formed ionic crosslink and a chemical crosslink formed by light irradiation.
- the 8-1st aspect is as follows.
- the eighth aspect is as follows.
- the photocrosslinked alginic acid structure according to [7] which has the same structure as defined in [1a] or [1b].
- a ninth aspect is as follows.
- the tenth aspect is as follows.
- the eleventh aspect is as follows.
- a medical material comprising the photocrosslinked alginic acid structure according to any one of the above embodiments [7] to [10].
- the twelfth aspect is as follows.
- the thirteenth aspect is as follows.
- the thirteenth aspect is a preferred aspect of the method for producing a photocrosslinked alginic acid according to the above aspect [13].
- the above [1-4-1], [1 -4-1a], [1-4-1b], [1-4-1c], [1a-4-1], [1a-4-1a], [1a-4-1b], or [1a- 4-1c] is a method for producing a photocrosslinked alginic acid, comprising irradiating the alginic acid derivative according to 4-1c with light; More preferably, the above embodiments [1-4-2], [1-4-2a], [1-4-2b], [1-4-2c], [1a-4-2], [1a-4] -2a], [1a-4-2b], or [1a-4-2c], a method for producing a photocrosslinked alginic acid, comprising irradiating the alginic acid derivative with light; More preferably, the embodiments [1-4-3], [1-4-3a], [1-4-3b], [1-4-3c], [1a-4-3], [1a
- a method for producing a photocrosslinked alginic acid comprising irradiating a light-induced alginic acid derivative introduced with a photoreactive group selected from: Or, particularly preferably, it is a method for producing photocrosslinked alginic acid, which comprises irradiating the alginic acid derivative according to the embodiment [1-4-4b] or [1a-4-4b] with light.
- a method for producing a photocrosslinked alginic acid comprising irradiating a light-induced alginic acid derivative introduced with a photoreactive group selected from:
- a method for producing a photocrosslinked alginic acid which comprises irradiating the alginic acid derivative according to the aspect [1-4-4c] or [1a-4-4c] with light.
- a method for producing a photocrosslinked alginic acid comprising irradiating a light-induced alginic acid derivative introduced with a photoreactive group selected from:
- a method for producing photocrosslinked alginic acid which comprises irradiating the alginic acid derivative according to the embodiment [1-4-4] or [1a-4-4] with light.
- a method for producing a photocrosslinked alginic acid comprising irradiating a light-induced alginic acid derivative introduced with a photoreactive group selected from: Or, particularly preferably, in the method for producing a photocrosslinked alginic acid, comprising irradiating the alginic acid derivative according to the above embodiment [1-4-4-1] or [1a-4-4-1] with light.
- a method for producing a photocrosslinked alginic acid comprising irradiating a light-induced alginic acid derivative introduced with a photoreactive group selected from: Or, particularly preferably, in a method for producing a photocrosslinked alginic acid, which comprises irradiating the alginic acid derivative according to the embodiment [1-4-4-2] or [1a-4-4-2] with light.
- a thirteenth aspect is a preferred aspect of the method for producing a photocrosslinked alginic acid according to the aforementioned aspect [13], and specifically includes the above [1b-3-1], [1b -3-1a], [1b-3-1b], or [1b-3-1c], a method for producing a photocrosslinked alginic acid, comprising irradiating the alginic acid derivative with light; More preferably, the alginic acid derivative according to the aspect [1b-3-2], [1b-3-2a], [1b-3-2b], or [1b-3-2c] is irradiated with light.
- a process for producing photocrosslinked alginic acid comprising: More preferably, it is a method for producing a photocrosslinked alginic acid, comprising irradiating the alginic acid derivative according to the embodiment [1b-3-3a] with light,
- the following formula [in each formula, the right side of the wavy line is not included]:
- a method for producing a photocrosslinked alginic acid comprising irradiating a light-induced alginic acid derivative introduced with a photoreactive group selected from:
- it is a method for producing a photocrosslinked alginic acid, which comprises irradiating the alginic acid derivative according to the embodiment [1b-3-3b] with light.
- a method for producing a photocrosslinked alginic acid comprising irradiating a light-induced alginic acid derivative introduced with a photoreactive group selected from: Or more preferably, it is a method for producing a photocrosslinked alginic acid, which comprises irradiating the alginic acid derivative according to the embodiment [1b-3-3c] with light.
- a method for producing a photocrosslinked alginic acid comprising irradiating a light-induced alginic acid derivative introduced with a photoreactive group selected from: Or more preferably, it is a method for producing a photocrosslinked alginic acid, which comprises irradiating the alginic acid derivative according to the embodiment [1b-3-3-3] with light.
- a method for producing a photocrosslinked alginic acid comprising irradiating a light-induced alginic acid derivative introduced with a photoreactive group selected from:
- a method for producing a photo-crosslinked alginic acid comprising irradiating a light-induced alginic acid derivative introduced with a photoreactive group selected from:
- the fourteenth aspect is as follows.
- the fourteenth aspect is as follows.
- the method for producing a photocrosslinked alginic acid according to [13] which has the same structure as defined in [1a] or [1b].
- the fifteenth aspect is as follows.
- the sixteenth aspect is as follows.
- the gel obtained by dropping the solution of the alginic acid derivative according to the aspect [1], [1a] or [1b] into a solution containing a divalent metal ion is irradiated with light to obtain a photocrosslinked alginate structure.
- the 16th aspect is a preferred aspect of the method for producing the photocrosslinked alginic acid structure according to the above aspect [16], specifically, the above aspect [1-4-1] [1-4-1a], [1-4-1b], [1-4-1c], [1a-4-1], [1a-4-1a], [1a-4-1b], or Including irradiating the gel obtained by dropping the solution of the alginic acid derivative described in [1a-4-1c] into a solution containing a divalent metal ion to obtain a photocrosslinked alginic acid structure.
- a method for producing a photocrosslinked alginate structure wherein the alginic acid structure comprises ionic crosslinks partially formed by divalent metal ions as crosslinks and chemical crosslinks formed by light irradiation; More preferably, the above embodiments [1-4-2], [1-4-2a], [1-4-2b], [1-4-2c], [1a-4-2], [1a-4] -2a], [1a-4-2b], or [1a-4-2c], the gel obtained by dropping a solution of the alginic acid derivative into a solution containing a divalent metal ion is irradiated with light.
- the photocrosslinked alginic acid structure comprises an ionic crosslink partially formed by divalent metal ions as a crosslink and a chemical crosslink formed by light irradiation.
- the embodiments [1-4-3], [1-4-3a], [1-4-3b], [1-4-3c], [1a-4-3], [1a-4] -3a], [1a-4-3b], or [1a-4-3c] the gel obtained by dropping a solution of the alginic acid derivative into a solution containing a divalent metal ion is irradiated with light.
- a photocrosslinked alginic acid structure wherein the photocrosslinked alginic acid structure comprises an ionic crosslink partially formed by divalent metal ions as a crosslink and a chemical crosslink formed by light irradiation.
- the gel obtained by dropping the solution of the alginic acid derivative described in the above embodiment [1-4-4a] or [1a-4-4a] into a solution containing a divalent metal ion is irradiated with light.
- the photocrosslinked alginic acid structure includes an ion bridge partially formed by divalent metal ions as a bridge and a chemical bridge formed by light irradiation.
- a method of manufacturing a body For example, the following formula [in each formula, the right side of the wavy line is not included]: A photo-crosslinked alginate structure is obtained by irradiating a gel obtained by dropping a solution of an alginic acid derivative introduced with a photoreactive group selected from the above into a solution containing a divalent metal ion, A method for producing a photocrosslinked alginate structure, wherein the crosslinked alginic acid structure comprises ionic crosslinking partially formed by divalent metal ions as crosslinks and chemical crosslinking formed by light irradiation; Or, particularly preferably, a gel obtained by dropping a solution of an alginic acid derivative according to the above embodiment [1-4-4b] or [1a-4-4b] into a solution containing a divalent metal ion.
- Photoirradiation to obtain a photocrosslinked alginate structure wherein the photocrosslinked alginate structure includes ion crosslinking partially formed by divalent metal ions as a bridge and chemical crosslinking formed by light irradiation.
- a method for producing a crosslinked alginate structure For example, the following formula [in each formula, the right side of the wavy line is not included]: A photo-crosslinked alginate structure is obtained by irradiating a gel obtained by dropping a solution of an alginic acid derivative introduced with a photoreactive group selected from the above into a solution containing a divalent metal ion, A method for producing a photocrosslinked alginate structure, wherein the crosslinked alginic acid structure comprises ionic crosslinking partially formed by divalent metal ions as crosslinks and chemical crosslinking formed by light irradiation; Or, particularly preferably, a gel obtained by dropping a solution of an alginic acid derivative according to the above embodiment [1-4-4c] or [1a
- Photoirradiation to obtain a photocrosslinked alginate structure wherein the photocrosslinked alginate structure includes ion crosslinking partially formed by divalent metal ions as a bridge and chemical crosslinking formed by light irradiation.
- a method for producing a crosslinked alginate structure For example, the following formula [in each formula, the right side of the wavy line is not included]: A photo-crosslinked alginate structure is obtained by irradiating a gel obtained by dropping a solution of an alginic acid derivative introduced with a photoreactive group selected from the above into a solution containing a divalent metal ion, A method for producing a photocrosslinked alginate structure, wherein the crosslinked alginic acid structure comprises ionic crosslinking partially formed by divalent metal ions as crosslinks and chemical crosslinking formed by light irradiation; Or, particularly preferably, the gel is obtained by dropping the solution of the alginic acid derivative according to the embodiment [1-4-4] or [1a-4-4]
- Photoirradiation to obtain a photocrosslinked alginate structure wherein the photocrosslinked alginate structure includes ion crosslinking partially formed by divalent metal ions as a bridge and chemical crosslinking formed by light irradiation.
- a method for producing a crosslinked alginate structure For example, the following formula [in each formula, the right side of the wavy line is not included]: A photo-crosslinked alginate structure is obtained by irradiating a gel obtained by dropping a solution of an alginic acid derivative introduced with a photoreactive group selected from the above into a solution containing a divalent metal ion, A method for producing a photocrosslinked alginate structure, wherein the crosslinked alginic acid structure comprises ionic crosslinking partially formed by divalent metal ions as crosslinks and chemical crosslinking formed by light irradiation; Or, particularly preferably, by dropping the solution of the alginic acid derivative according to the embodiment [1-4-4-1] or [1a-4-4-1] into
- a method for producing a photocrosslinked alginic acid structure For example, the following formula [in each formula, the right side of the wavy line is not included]: A photo-crosslinked alginate structure is obtained by irradiating a gel obtained by dropping a solution of an alginic acid derivative introduced with a photoreactive group selected from the above into a solution containing a divalent metal ion, A method for producing a photocrosslinked alginate structure, wherein the crosslinked alginic acid structure comprises ionic crosslinking partially formed by divalent metal ions as crosslinks and chemical crosslinking formed by light irradiation; Or, particularly preferably, by dropping the solution of the alginic acid derivative according to the above embodiment [1-4-4-2] or [1a-4-4-2]
- a photo-crosslinked alginate structure is obtained by irradiating a gel obtained by dropping a solution of an alginic acid derivative introduced with a photoreactive group selected from the above into a solution containing a divalent metal ion,
- a method for producing a photocrosslinked alginate structure, wherein the crosslinked alginic acid structure comprises ionic crosslinking partially formed by divalent metal ions as crosslinks and chemical crosslinking formed by light irradiation;
- the embodiment 16-2 is a preferred embodiment of the method for producing the photocrosslinked alginic acid structure according to the embodiment [16], specifically, the embodiment [1b-3-1]. , [1b-3-1a], [1b-3-1b], or a gel obtained by dropping a solution of the alginic acid derivative described in [1b-3-1c] into a solution containing a divalent metal ion Irradiating with light to obtain a photocrosslinked alginic acid structure, wherein the photocrosslinked alginic acid structure includes ion crosslinking partially formed by divalent metal ions as a crosslink and chemical crosslinking formed by light irradiation,
- the photocrosslinked alginate structure includes an ionic crosslink partially formed by divalent metal ions as a crosslink and a chemical crosslink formed by light irradiation, and a method for producing a photocrosslinked alginate structure
- a photo-crosslinked alginate structure is obtained by irradiating a gel obtained by dropping a solution of an alginic acid derivative introduced with a photoreactive group selected from the above into a solution containing a divalent metal ion
- a method for producing a photocrosslinked alginate structure, wherein the crosslinked alginic acid structure comprises ionic crosslinking partially formed by divalent metal ions as crosslinks and chemical crosslinking formed by light irradiation;
- the gel obtained by dropping the solution of the alginic acid derivative according to the above embodiment [1b-3-3b] into a solution containing a divalent metal ion is i
- a method for producing a photocrosslinked alginate structure wherein the photocrosslinked alginate structure comprises ionic crosslinking partially formed by divalent metal ions as a bridge and chemical crosslinking formed by light irradiation.
- the following formula [in each formula, the right side of the wavy line is not included]:
- a photo-crosslinked alginate structure is obtained by irradiating a gel obtained by dropping a solution of an alginic acid derivative introduced with a photoreactive group selected from the above into a solution containing a divalent metal ion,
- a method for producing a photocrosslinked alginate structure, wherein the crosslinked alginic acid structure comprises ionic crosslinking partially formed by divalent metal ions as crosslinks and chemical crosslinking formed by light irradiation;
- the gel obtained by dropping the solution of the alginic acid derivative according to the above embodiment [1b-3-3c] into a solution containing a divalent metal ion is irradi
- a method for producing a photocrosslinked alginate structure wherein the photocrosslinked alginate structure comprises ionic crosslinking partially formed by divalent metal ions as a bridge and chemical crosslinking formed by light irradiation.
- the following formula [in each formula, the right side of the wavy line is not included]:
- a photo-crosslinked alginate structure is obtained by irradiating a gel obtained by dropping a solution of an alginic acid derivative introduced with a photoreactive group selected from the above into a solution containing a divalent metal ion,
- a method for producing a photocrosslinked alginate structure, wherein the crosslinked alginic acid structure comprises ionic crosslinking partially formed by divalent metal ions as crosslinks and chemical crosslinking formed by light irradiation;
- the gel obtained by dropping the solution of the alginic acid derivative according to the above embodiment [1b-3-3] into a solution containing a divalent metal ion is irradiated
- a method for producing a photocrosslinked alginate structure wherein the photocrosslinked alginate structure comprises ionic crosslinking partially formed by divalent metal ions as a bridge and chemical crosslinking formed by light irradiation.
- the following formula [in each formula, the right side of the wavy line is not included]:
- a photo-crosslinked alginate structure is obtained by irradiating a gel obtained by dropping a solution of an alginic acid derivative introduced with a photoreactive group selected from the above into a solution containing a divalent metal ion,
- a method for producing a photocrosslinked alginate structure, wherein the crosslinked alginic acid structure comprises ionic crosslinking partially formed by divalent metal ions as crosslinks and chemical crosslinking formed by light irradiation;
- the gel obtained by dropping the solution of the alginic acid derivative described in the above embodiment [1b-3-3-1] into a solution containing a divalent metal ion is irradi
- a photo-crosslinked alginate structure is obtained by irradiating a gel obtained by dropping a solution of an alginic acid derivative introduced with a photoreactive group selected from the above into a solution containing a divalent metal ion,
- the gel obtained by dropping the solution of the alginic acid derivative described in the above embodiment [1b-3-3-3] into a solution containing a divalent metal ion is irradi
- a photo-crosslinked alginate structure is obtained by irradiating a gel obtained by dropping a solution of an alginic acid derivative introduced with a photoreactive group selected from the above into a solution containing a divalent metal ion,
- a photo-crosslinked alginate structure is obtained by irradiating a gel obtained by dropping a
- the seventeenth aspect is as follows.
- the seventeenth aspect is as follows.
- the method for producing a photocrosslinked alginic acid structure according to the above [16].
- the eighteenth aspect is as follows.
- the alginic acid derivative according to the aspect [1], [1a] or [1b] is partially ion-crosslinked with a divalent metal ion to form a specific structure
- a method for producing a photocrosslinked alginate structure comprising obtaining a photocrosslinked alginate structure by chemically crosslinking the structure by light irradiation.
- the twentieth aspect is as follows.
- the twenty-first aspect is as follows.
- a photocrosslinked alginate structure having retention of contents obtained by crosslinking the alginic acid derivative according to the aspect [1], [1a] or [1b] by irradiation with divalent metal ions and light.
- the twenty-second aspect is as follows.
- the alginic acid derivative according to any one of the aspects [1] to [3] the photocrosslinked alginic acid according to any one of the aspects [4] to [6]
- the aspect, which are biocompatible and the aspect, which are biocompatible.
- [7] The photocrosslinked alginate structure according to any one of [10] to [10].
- the twenty-third aspect is as follows.
- a cyclic ether is formed by bonding between carbon atoms formed by bonding, or by bonding between carbon atoms in which any one hydrogen atom is removed from each alkyl group of the two C 1-6 alkoxy groups.
- the C 1 - 6 hydrogen atoms of any one excluded carbon atoms is a hydrogen atom and the -NHR G group from an alkyl group of an alkoxy group But By one removed nitrogen atom is attached, 3-N- (C 2 ⁇ 7 alkanoyl) oxazolidine ring, 3-N- (C 1 ⁇ 6 alkylsulfonyl) oxazolidine ring, 4-N- (C 2 ⁇ 7 alkanoyl) morpholine, 4-N- (C 1 ⁇ 6 alkylsulfonyl) morpholine, 4-N- (C 2 ⁇ 7 alkanoyl) -1,4-oxazepane ring or 4-N- (C 1 ⁇ 6 , Alkylsulfonyl) -1,4-oxazepane ring may be formed); —X— is —O— or —NH—; -A- is
- n in formula (AL-1) is an integer of 1 to 10
- m in formula (AL-2) Is an integer from 1 to 7
- Ar is C 6 ⁇ 10 aryl group, or 5-6 membered heteroaryl group (wherein C 6 ⁇ 10 aryl group, or a 5-6 membered heteroaryl group, a hydroxyl group, a cyano group, a nitro group, a halogen atom, C 1 ⁇ 6 alkyl group, a halogenated C 1 ⁇ 6 alkyl group, C 1-6 alkoxy group, and —NR A R B group (in the —NR A R B group, R A and R B are each independently a hydrogen atom, C 1-6 alkyl group, C 2-7 alkanoyl group, or a C 1 ⁇ 6 alkylsulfonyl is a radical selected from the group) 1 to 3 groups selected arbitrarily from well be replaced with a hydrogen atom on the ring, the C 6 ⁇ 10 aryl group or 5- to 6-
- any hydrogen atom is one of the alkyl group in the C 1 ⁇ 6 alkoxy group removal Charcoal By hydrogen atom and the -NHR G groups are bonded one removed nitrogen atom, 3-N- (C 2 ⁇ 7 alkanoyl) oxazolidine ring, 3-N- (C 1 ⁇ 6 alkylsulfonyl) oxazolidine ring, 4-N- (C 2 ⁇ 7 alkanoyl) morpholine, 4-N- (C 1 ⁇ 6 alkylsulfonyl) morpholine, 4-N- (C 2 ⁇ 7 alkylsulfonyl) morpholine, 4-N- (C 2 ⁇ 7 alkylsulfonyl) morpholine, 4-N- (C 2 ⁇ 7 alkylsulfonyl) morpholine, 4-N- (C 2 ⁇ 7 alkylsulfonyl) morpholine, 4-N- (C 2 ⁇ 7 alkylsul
- n in formula (AL-1) is an integer of 1 to 8; m in formula (AL-2) Is an integer from 1 to 5;
- the hydrogen atom of the methylene group (—CH 2 —) in the formula (AL-1) or (AL-2) is a halogen atom, a hydroxyl group, a C 1-6 alkyl group, a hydroxy C 1-6 alkyl group, —NR a in R b group (-NR a R b group, R a and R b are each independently a hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or a C 1 ⁇ 6 alkylsulfonyl group selected as a group), C 7 ⁇ 16 aralkyl group, or a plurality by a group selected from heteroaryl C 1 ⁇ 6 alkyl group (e.g., 1 to
- the embodiment 23-3 is a further preferred embodiment of the compound of the formula (AM-1) of the embodiment [23].
- Ar is a phenyl group or a pyridyl group (described above).
- the phenyl group or pyridyl group is a hydroxyl group, a cyano group, a nitro group, a halogen atom, a C 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1-6 alkoxy group, and a —NR A R B group.
- R A and R B are each independently selected from hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or a C 1 ⁇ 6 alkylsulfonyl group
- R A and R B are each independently selected from hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or a C 1 ⁇ 6 alkylsulfonyl group
- Optionally selected from 1 to 3 groups may be substituted with hydrogen atoms on the ring, and the phenyl group or pyridyl group includes a C 1-6 alkyl group and a C 1-6 alkoxy group.
- a cyclic ether may be formed by bonding between carbon atoms in which one hydrogen atom is removed from each alkyl group of the two C 1-6 alkoxy groups, or the phenyl group or pyridyl group to, C 1 ⁇ 6 alkoxy group and -NHR G group (R G in -NHR G groups are C 2 ⁇ 7 alkanoyl or C 1 ⁇ 6 alkylsulfonyl group) when is substituted adjacently, A carbon atom in which one arbitrary hydrogen atom is removed from the alkyl group of the C 1-6 alkoxy group and a nitrogen atom in which one hydrogen atom of the —NHR G group is removed are combined to form 3-N— (C 2 ⁇ 7 A Alkanoy
- the embodiment 23-4 is a particularly preferred embodiment of the compound of the formula (AM-1) of the embodiment [23].
- Ar is a phenyl group or a 2-pyridyl group.
- 1 to 3 groups arbitrarily selected from a cyano group, a fluorine atom, a trifluoromethyl group, and a methoxy group may be substituted with a hydrogen atom on the ring,
- two methoxy groups are adjacently substituted on a phenyl group or 2-pyridyl group, between the carbon atoms obtained by removing one hydrogen atom from the methyl group of each group of the two methoxy groups To form a 1,4-dioxane ring
- Ar is a phenyl group, 4-fluorophenyl group, 4- (trifluoromethyl) phenyl group, 4-methoxyphenyl group, 4-cyanophenyl group, 2,3-d
- the twenty-fourth aspect is as follows.
- a cyclic ether is formed by bonding between carbon atoms formed by bonding, or by bonding between carbon atoms in which any one hydrogen atom is removed from each alkyl group of the two C 1-6 alkoxy groups.
- Ar is C 6 ⁇ 10 aryl group, or 5-6 membered heteroaryl group (wherein C 6 ⁇ 10 aryl group, or a 5-6 membered heteroaryl group, a hydroxyl group, a cyano group, a nitro group, a halogen atom, C 1 ⁇ 6 alkyl group, a halogenated C 1 ⁇ 6 alkyl group, C 1-6 alkoxy group, and —NR A R B group (in the —NR A R B group, R A and R B are each independently a hydrogen atom, C 1-6 alkyl group, C 2-7 alkanoyl group, or a C 1 ⁇ 6 alkylsulfonyl is a radical selected from the group) 1 to 3 groups selected arbitrarily from well be replaced with a hydrogen atom on the ring, the C 6 ⁇ 10 aryl group or 5- to 6-
- any hydrogen atom is one of the alkyl group in the C 1 ⁇ 6 alkoxy group removal Charcoal By hydrogen atom and the -NHR G groups are bonded one removed nitrogen atom, 3-N- (C 2 ⁇ 7 alkanoyl) oxazolidine ring, 3-N- (C 1 ⁇ 6 alkylsulfonyl) oxazolidine ring, 4-N- (C 2 ⁇ 7 alkanoyl) morpholine, 4-N- (C 1 ⁇ 6 alkylsulfonyl) morpholine, 4-N- (C 2 ⁇ 7 alkylsulfonyl) morpholine, 4-N- (C 2 ⁇ 7 alkylsulfonyl) morpholine, 4-N- (C 2 ⁇ 7 alkylsulfonyl) morpholine, 4-N- (C 2 ⁇ 7 alkylsulfonyl) morpholine, 4-N- (C 2 ⁇ 7 alkylsul
- the embodiment 24-3 is a more preferred embodiment of the compound of formula (AM-2) of embodiment [24], specifically, Ar is a phenyl group or a pyridyl group (described above).
- the phenyl group or pyridyl group is a hydroxyl group, a cyano group, a nitro group, a halogen atom, a C 1-6 alkyl group, a halogenated C 1-6 alkyl group, a C 1-6 alkoxy group, and a —NR A R B group.
- R A and R B are each independently selected from hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or a C 1 ⁇ 6 alkylsulfonyl group
- R A and R B are each independently selected from hydrogen atom, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or a C 1 ⁇ 6 alkylsulfonyl group
- Optionally selected from 1 to 3 groups may be substituted with hydrogen atoms on the ring, and the phenyl group or pyridyl group includes a C 1-6 alkyl group and a C 1-6 alkoxy group.
- a cyclic ether may be formed by bonding between carbon atoms in which one hydrogen atom is removed from each alkyl group of the two C 1-6 alkoxy groups, or the phenyl group or pyridyl group to, C 1 ⁇ 6 alkoxy group and -NHR G group (R G in -NHR G groups are C 2 ⁇ 7 alkanoyl or C 1 ⁇ 6 alkylsulfonyl group) when is substituted adjacently, A carbon atom in which one arbitrary hydrogen atom is removed from the alkyl group of the C 1-6 alkoxy group and a nitrogen atom in which one hydrogen atom of the —NHR G group is removed are combined to form 3-N— (C 2 ⁇ 7 A Alkanoy
- —X— is —O— or —NH—:
- -A- is the formula (AL-1) or (AL-2) in the embodiment [24] [in each formula, the outside of the wavy line at both ends is not included]
- n in the formula (AL-1) is 2 Or a pharmaceutically acceptable salt thereof, or a solvate thereof, which is an integer of ⁇ 6;
- m in the formula (AL-2) is an integer of 1 to 3.
- the embodiment 24-4 is a particularly preferred embodiment of the compound of the formula (AM-2) of the embodiment [24].
- Ar is a phenyl group (ring of the phenyl group).
- the upper hydrogen atom may be substituted with 1 to 3 methoxy groups);
- Ar is a phenyl group or a 4-methoxyphenyl group;
- —X— is —O—:
- -A- is a compound of the formula (AL-1-1) in the above embodiment [1-3] [in which the outside of the wavy line at both ends is not included], or a pharmaceutically acceptable salt thereof, or Their solvates;
- alginic acid when described as alginic acid, at least one alginic acid selected from the group consisting of alginic acid, alginic acid esters, and salts thereof (for example, sodium alginate) (sometimes referred to as “alginic acids”).
- alginic acid used may be naturally derived or synthetic, but is preferably naturally derived.
- Alginic acids preferably used are bioabsorbable polysaccharides extracted from brown algae such as Lessonia, Macrocystis, Laminaria, Ascophyllum, Davilia, Kajika, Alame, Kombu, etc., and D-mannuronic acid (M) And L-guluronic acid (G).
- D-mannuronic acid homopolymer fraction MM fraction
- L-guluronic acid homopolymer fraction GG fraction
- D-mannuronic acid and L-guluronic acid are randomly arranged.
- This is a block copolymer in which the fractions (M / G fraction) are arbitrarily bound.
- alginic acid may be expressed as (ALG) -COOH, where alginic acid is (ALG) and one of the arbitrary carboxyl groups of alginic acid is -COOH.
- the alginic acid is sodium alginate.
- the sodium alginate commercially available sodium alginate can be used.
- sodium alginate of A-1, A-2 and A-3 release source: Mochida Pharmaceutical Co., Ltd.
- Table 1 shows the viscosity, weight average molecular weight, and M / G ratio of a 1 w / w% aqueous solution of each sodium alginate.
- the physical properties of sodium alginate A-1, A-2, A-3, B-1, B-2, and B-3 were measured by the following various methods.
- the measurement method is not limited to this method, but each physical property value may differ from the above depending on the measurement method.
- Viscosity measurement of sodium alginate According to the Japanese Pharmacopoeia (16th edition) viscosity measurement method, it was measured using a rotational viscometer method (cone plate type rotational viscometer). Specific measurement conditions are as follows. The sample solution was prepared using MilliQ water. As a measuring instrument, a cone plate type rotational viscometer (visco-viscoelasticity measuring device Rheostress RS600 (Thermo Haake GmbH) sensor: 35/1) was used. The number of revolutions was 1 rpm when measuring a 1 w / w% sodium alginate solution. The reading time was measured for 2 minutes, and an average value from 1 minute to 2 minutes from the start. The average value of three measurements was taken as the measurement value. The measurement temperature was 20 ° C.
- Da (Dalton) may be added as a unit in the molecular weights of alginic acid, alginic acid derivatives, crosslinked alginic acid, and crosslinked alginic acid.
- the composition ratio (M / G ratio) of D-mannuronic acid and L-guluronic acid of alginic acids varies depending on the type of organisms that are mainly derived from seaweeds, etc., and is also affected by the location and season of the organism. , Ranging from a high G type with an M / G ratio of about 0.2 to a high M type with an M / G ratio of about 5. It is known that the gelation ability of alginic acids and the properties of the generated gel are affected by the M / G ratio, and generally the gel strength increases when the G ratio is high. In addition, the M / G ratio affects the hardness, brittleness, water absorption, flexibility, and the like of the gel.
- the M / G ratio of the alginic acids and / or salts thereof used is usually 0.2 to 4.0, more preferably 0.4 to 3.0, still more preferably 0.5 to 3.0. is there.
- a numerical range indicated by using “to” indicates a range including the numerical values described before and after “to” as the minimum value and the maximum value, respectively.
- alginate and “alginate” to be used are not particularly limited. However, in order to react with a crosslinking agent, it is necessary not to have a functional group that inhibits the crosslinking reaction. Preferred examples of the alginate include propylene glycol alginate.
- examples of the alginate include a monovalent salt of alginic acid and a divalent salt of alginic acid.
- the monovalent salt of alginic acid preferably includes sodium alginate, potassium alginate, ammonium alginate, etc., more preferably sodium alginate or potassium alginate, and particularly preferably sodium alginate.
- Preferred examples of the divalent salt of alginic acid include calcium alginate, magnesium alginate, barium alginate, strontium alginate, and the like.
- Alginic acid is a high molecular weight polysaccharide, and it is difficult to accurately determine the molecular weight, but generally a weight average molecular weight of 10 to 10 million, preferably 10,000 to 8 million, more preferably 20,000 to 3 million. Range. In measuring the molecular weight of a natural substance-derived polymer substance, it is known that the value may vary depending on the measurement method.
- the weight average molecular weight measured by gel permeation chromatography (GPC) or gel filtration chromatography (also referred to as size exclusion chromatography) is preferably 100,000 or more, more preferably 500,000 or more, Preferably, it is 5 million or less, more preferably 3 million or less.
- the preferable range is 100,000 to 5,000,000, more preferably 150,000 to 3,000,000.
- the absolute weight average molecular weight can be measured.
- the weight average molecular weight (absolute molecular weight) measured by GPC-MALS method is preferably 10,000 or more, more preferably 50,000 or more, still more preferably 60,000 or more, and preferably 1,000,000 or less, more preferably 80 10,000 or less, more preferably 700,000 or less, and particularly preferably 500,000 or less.
- the preferable range is 10,000 to 1,000,000, more preferably 50,000 to 800,000, still more preferably 60,000 to 700,000, and particularly preferably 60,000 to 500,000.
- a measurement error of 10% to 20% may occur.
- the value may vary within the range of about 320,000 to 480,000 for 400,000, 400,000 to 600,000 for 500,000, and about 800,000 to 1,200,000 for 1,000,000.
- the molecular weight of alginic acids can be measured according to a conventional method.
- Typical conditions when gel filtration chromatography is used for molecular weight measurement are as described in the examples of the present specification to be described later.
- the column for example, Superose 6 Increase 10/300 GL column (GE Healthcare Science) can be used, and as a developing solvent, for example, 10 mmol / L phosphate buffer (pH 7.4) containing 0.15 mol / L NaCl.
- Blue dextran, thyroglobulin, ferritin, aldolase, conalbumin, ovalbumin, ribonuclease A and aprotinin can be used as molecular weight standards.
- the viscosity of alginic acid used in the present specification is not particularly limited, but is preferably 10 mPa ⁇ s to 1000 mPa ⁇ s, more preferably 50 mPa ⁇ s when the viscosity is measured as an aqueous solution of 1 w / w% alginic acid. s to 800 mPa ⁇ s.
- the viscosity of the aqueous solution of alginic acid can be measured according to a conventional method.
- a rotational viscometer method such as a coaxial double cylindrical rotational viscometer, a single cylindrical rotational viscometer (Brookfield viscometer), a cone-plate rotational viscometer (cone plate viscometer), etc.
- a rotational viscometer method such as a coaxial double cylindrical rotational viscometer, a single cylindrical rotational viscometer (Brookfield viscometer), a cone-plate rotational viscometer (cone plate viscometer), etc.
- a cone plate viscometer is used.
- Alginic acids are initially high in molecular weight and high in viscosity when extracted from brown algae, but in the process of drying and purification by heat, the molecular weight decreases and the viscosity decreases.
- Alginic acids having different molecular weights can be produced by techniques such as temperature control in the production process, selection of brown algae as a raw material, and molecular weight fractionation in the production process. Furthermore, it is possible to obtain alginic acids having a target molecular weight by mixing with another lot of alginic acids having different molecular weights or viscosities.
- alginic acid is alginic acid that has not been treated with low endotoxin in some embodiments, or alginic acid that has been treated with low endotoxin in some embodiments.
- Low endotoxin refers to a low endotoxin level that does not substantially cause inflammation or fever. More preferably, it is desirable to use alginic acids treated with low endotoxin.
- the low endotoxin treatment can be performed by a known method or a method analogous thereto.
- the method of Takada et al. See, for example, JP-A-9-32001 for purifying sodium hyaluronate
- the method of Yoshida et al. Eg, JP-A-8-269102 for purifying ⁇ 1,3-glucan. Etc.
- a method of William et al. for example, see JP-T-2002-530440, etc.
- biopolymer salts such as alginate, gellan gum, etc.
- James et al. For example, international publication for purifying polysaccharides, etc.
- Low endotoxin treatment is not limited to these, and uses washing, filtration (endotoxin removal filter, charged filter, etc.), ultrafiltration, column (endotoxin adsorption affinity column, gel filtration column, ion exchange resin column, etc.) Purification, adsorption to hydrophobic substances, resin or activated carbon, organic solvent treatment (extraction with organic solvent, precipitation / precipitation by addition of organic solvent, etc.), surfactant treatment (for example, see JP-A-2005-036036) ) Or other known methods, or a combination thereof. These processing steps may be appropriately combined with known methods such as centrifugation. It is desirable to select appropriately according to the type of alginic acid.
- the endotoxin level can be confirmed by a known method, and can be measured by, for example, a method using Limulus reagent (LAL), a method using Endspecy (registered trademark) ES-24S set (Seikagaku Corporation), or the like. .
- LAL Limulus reagent
- Endspecy registered trademark
- ES-24S set Seikagaku Corporation
- the endotoxin treatment method to be used is not particularly limited.
- the endotoxin content of alginic acids is 500 endotoxin units (EU) / g or less when the endotoxin measurement is performed with Limulus reagent (LAL).
- LAL Limulus reagent
- EU endotoxin units
- Low endotoxin-treated sodium alginate can be obtained from commercially available products such as Sea Matrix (registered trademark) (Mochida Pharmaceutical Co., Ltd.), PRONOVA TM UP LVG (FMCBioPolymer), and the like.
- alginic acid derivatives are provided.
- a part of the carboxyl group of alginic acid has the following formula (I) [wherein the right side of the wavy line is not included]: [Ar, p, -X-, -A- are as defined above, for example, the same as the definition in the first embodiment]
- a photoreactive group in part of the carboxyl group of alginic acid includes a portion (photoreactive portion) where cyclization proceeds in the photoreaction.
- the photoreactive moiety may be a moiety that causes a dimerization reaction (cyclization reaction) or a polymerization reaction upon irradiation with light.
- cyclization reaction cyclization reaction
- polymerization reaction upon irradiation with light.
- Specific examples thereof include cinnamic acid moieties, substituted cinnamic acid moieties, phenylpenta-2,4-dienoic.
- Examples include an acid moiety, a substituted phenylpenta-2,4-dienoic acid moiety, or a heterocyclic substituted acrylic acid moiety.
- alkene part in Formula (I) is described as a trans form as one form, what is necessary is just the coupling
- photoreactive moieties those having a vinylene group capable of forming a cyclobutane ring by a dimerization reaction are preferred.
- cinnamic acid moiety, substituted cinnamic acid moiety, phenylpenta-2,4-dienoic acid moiety, substituted phenyl A penta-2,4-dienoic acid moiety and a heterocyclic substituted acrylic acid moiety are preferred.
- the photoreactive group may be bound to a spacer for binding to both the photoreactive moiety and alginic acid and keeping both at a certain distance.
- a spacer is bonded to a photoreactive moiety such as cinnamic acid moiety, substituted cinnamic acid moiety, phenylpenta-2,4-dienoic acid moiety, substituted phenylpenta-2,4-dienoic acid moiety, and heterocyclic substituted acrylic acid moiety
- alginic acid derivatives are provided:
- One or more carboxyl groups of alginic acid have the following formula (I) [wherein the right side of the wavy line is not included]: [Ar, p, -X-, -A- is as defined above, for example, the same definition as in the first embodiment] Alginate derivative introduced with a photoreactive group .
- photoreactive group is introduced means that any one or more carboxyl groups of alginic acid form an amide bond with the terminal amino group of the linker in the photoreactive group. It means that one or more carboxyl groups and a photoreactive group are bonded via a linker.
- Ar is C 6-10 aryl group, or a Hajime Tamaki (wherein C 6 ⁇ 10 aryl group, or a heterocyclic group, a hydroxyl group, a cyano group, a nitro group, a halogen atom, C 1 ⁇ 6 alkyl group, halogenated C 1-6 alkyl group, C 1-6 alkoxy group, and —NR A R B group (in the —NR A R B group, R A and R B are each independently a hydrogen atom substituted, C 1 ⁇ 6 alkyl group, C 2 ⁇ 7 alkanoyl group, or a C 1 ⁇ 6 alkylsulfonyl is a radical selected from the group) 1 to 3 groups selected arbitrarily from a hydrogen atom on the ring may be, the C 6-10 aryl group or a heterocyclic group, when C 1 ⁇ 6 alkyl and C 1 ⁇ 6 alkoxy group or two C 1 ⁇ 6 alkoxy groups are
- Ar is C 6 ⁇ 10 aryl group, or a Hajime Tamaki (wherein C 6 ⁇ 10 aryl group or a heterocyclic group, a hydroxyl group, a cyano group, a nitro group, a halogen atom, C 1 ⁇ 6 An alkyl group, a halogenated C 1-6 alkyl group, a C 1-6 alkoxy group, and a —NR A R B group (in the —NR A R B group, R A and R B are each independently a hydrogen atom, C 1 ⁇ 6 alkyl group, a group selected from C 2 ⁇ 7 alkanoyl group, or a C 1 ⁇ 6 alkylsulfonyl group (, -NH 2, -NH (C 1 ⁇ 6 alkyl group), and -N (C 1 ⁇ 6 alkyl group) 2 are excluded)) 1-3 groups selected arbitrarily from well be replaced with a hydrogen atom on the ring, the C 6 ⁇ 10 ⁇ 10
- Ar is C 6 ⁇ 10 aryl group (the C 6 ⁇ 10 aryl group, a hydroxyl group, a cyano group, a nitro group, a halogen atom, C 1 ⁇ 6 alkyl group, a halogenated C 1 ⁇ 6 alkyl Group, C 1-6 alkoxy group, and —NR A R B group (in the —NR A R B group, R A and R B are each independently a hydrogen atom, a C 1-6 alkyl group, C 2— 7 alkanoyl group, or a group selected from C 1 ⁇ 6 alkylsulfonyl group (, -NH 2, -NH (C 1 ⁇ 6 alkyl group), and -N (C 1 ⁇ 6 alkyl group) 2 1-3 groups selected from excluded)) optionally has may be substituted with a hydrogen atom on the ring, the C 6 ⁇ 10 aryl group, C 1 ⁇ 6 alkyl and C 1 ⁇ 6 alkoxy group
- any linear group can be used as long as it does not inhibit the photoreaction of the photoreactive moiety.
- formulas (AL-1) to (AL-4) [in each formula, the outside of the wavy line at both ends is not included]: (In the formulas (AL-1) to (AL-4), n represents an integer of 1 to 18; m represents an integer of 1 to 9; j represents an integer of 0 to 9;
- the hydrogen atom of the methylene group (—CH 2 —) in the formulas (AL-1) to (AL-4) is a halogen atom, a hydroxyl group, a C 1-6 alkyl group, a hydroxy C 1-6 alkyl group, or a thiol C 1.
- the photoreactive group absorbs light (eg, having a wavelength around 180-650 nm) and dimerizes (eg, dimerizes into a troxylic acid derivative).
- light eg, having a wavelength around 180-650 nm
- dimerizes eg, dimerizes into a troxylic acid derivative.
- the photocrosslinking reaction proceeds even when the introduction rate of the photoreactive group (photocrosslinking group) is low. Due to the photocrosslinking reaction, the alginic acid derivative forms a three-dimensional network structure via the photocrosslinking group. Preferred alginic acid derivatives have improved stability after photocrosslinking.
- novel alginic acid derivative introduced with the photoreactive group represented by the formula (I) in the present specification is introduced into alginic acids by substituting the photoreactive group with a part of the carboxyl group of alginic acid, For example, it can be produced by the method of the following formula (for details, refer to the general production method described later).
- the weight average molecular weight of the novel alginic acid derivative introduced with the photoreactive group represented by the formula (I) in this specification is 100,000 Da to 3 million Da, preferably 300,000 Da to 2.5 million Da. More preferably, it is 500,000 Da to 2 million Da.
- the molecular weight of the alginic acid derivative can be determined by the same method as that for the aforementioned alginic acids.
- the photoreactive group represented by the formula (I) does not have to be bonded to all the carboxyl groups of the alginic acid structural unit.
- the rate of introduction of the photoreactive group represented by the formula (I) in the alginic acid derivative is preferably 0.5% to 30%, more preferably 0.5% to 20%, Preferably, it is 1.0% to 15%.
- the rate of introduction of the photoreactive group represented by the formula (I) is the uronic acid monosaccharide in which the photoreactive group represented by the formula (I) is introduced among the uronic acid monosaccharide units which are repeating units of alginic acids. It is a value representing the number of units as a percentage. In the present specification, unless otherwise specified,% used for the introduction rate of the photoreactive group represented by the formula (I) in the alginic acid derivative means mol%.
- the introduction rate of the photoreactive group represented by the formula (I) can be determined by the method described in Examples described later.
- the alginic acid derivative can be obtained by subjecting the terminal amino group of the linker in the photoreactive group moiety to a condensation reaction with the carboxyl group of alginic acid.
- a compound represented by the formula (IM-A-1) [wherein RD represents a C 1-6 alkyl group] can be produced.
- ⁇ Process 2> [Production Method A] Using the compound of formula (IM-A-1) obtained in ⁇ Step 1>, water and a solvent miscible with water (for example, methanol, ethanol, tetrahydrofuran, N, N-dimethylformamide) In a mixed solvent of a solvent such as dimethyl sulfoxide), an inorganic base such as lithium hydroxide, sodium hydroxide, or potassium hydroxide is added and hydrolyzed at a temperature at which the solvent is refluxed from 0 ° C. A compound of formula (IM-A-2) can be prepared.
- a solvent miscible with water for example, methanol, ethanol, tetrahydrofuran, N, N-dimethylformamide
- a mixed solvent of a solvent such as dimethyl sulfoxide
- an inorganic base such as lithium hydroxide, sodium hydroxide, or potassium hydroxide is added and hydrolyzed at a temperature at which the solvent is refluxe
- an active methylene compound such as malonic acid or Meldrum's acid may be used instead of Wittig reagent or Horner-Emmons reagent, and the formula (SM-1).
- a compound of formula (IM-A-2) is produced by adding a base such as piperidine in a basic solvent such as pyridine to the aldehyde represented and reacting at a temperature at which the solvent is refluxed from room temperature. Can do.
- halogen solvents such as dichloromethane and chloroform
- ether solvents such as diethyl ether and tetrahydrofuran
- aromatic hydrocarbon solvents such as toluene and benzene
- polar solvents such as N, N-dimethylformamide
- methanol By reacting in a solvent selected from alcohol solvents such as ethanol and 2-propanol in the presence or absence of a base such as triethylamine and pyridine at a temperature at which the solvent is refluxed from 0 ° C., the formula (IM ⁇ The compound of A-3) can be produced.
- the carboxylic acid represented by the formula (IM-A-2) is converted into a method known in the literature, for example, “Experimental Chemistry Course 5th edition 16, carboxylic acids and derivatives, acid halides, acid anhydrides, 99-118”.
- a base such as triethylamine or pyridine using the formula (RG-A-1).
- a solvent selected from halogen solvents such as dichloromethane and chloroform, ether solvents such as diethyl ether and tetrahydrofuran, aromatic hydrocarbon solvents such as toluene and benzene, polar solvents such as N, N-dimethylformamide, etc.
- ⁇ Step 4> [Production Method A] Using the formula (IM-A-3) obtained in ⁇ Step 3>, a method known in the literature, such as “Protective Groups in Organic Synthesis (Protective Groups in Organic Synthesis), 4th edition, 2007, John Wiley & Sons ”, by selecting the appropriate deprotection method depending on the type of protecting group. By carrying out, it can be produced as a compound represented by the formula (AM-1) or a salt of the formula (AM-1).
- the salt of formula (AM-1) is not particularly limited as long as it is a pharmaceutically acceptable salt.
- a pharmaceutically acceptable salt for example, hydrochloride, hydrofluoride, hydrobromide, trifluoroacetate, etc.
- the salt is not particularly limited as long as it is a pharmaceutically acceptable salt.
- the salt is not particularly limited as long as it is a pharmaceutically acceptable salt.
- a compound represented by (IM-B-1) can be produced.
- the salt of formula (AM-2) is not particularly limited as long as it is a pharmaceutically acceptable salt.
- a pharmaceutically acceptable salt for example, hydrochloride, hydrofluoride, hydrobromide, trifluoroacetate, etc.
- the salt is not particularly limited as long as it is a pharmaceutically acceptable salt.
- the salt is not particularly limited as long as it is a pharmaceutically acceptable salt.
- SM-1 and trialkyl 4-phosphonocrotonate (the compound can be produced from a commercially available compound or a commercially-available production method known in the literature: for example, triethyl 4-phosphonocrotonate, etc.) Is used according to a method known in the literature, for example, the method described in “Journal of American Chemical Society, 127 (43), 15028-15029, 2005” and the like (IM-B -3) can be produced.
- an amine compound represented by the formula (AM-1) or the formula (AM-2) (including a subordinate formula of each formula) is a pharmaceutically acceptable salt (for example, an acid addition salt). ) May be formed.
- a salt is not particularly limited as long as it is a pharmaceutically acceptable salt, and examples thereof include a salt with an inorganic acid, a salt with an organic acid, and a salt with an acidic amino acid.
- the salt with inorganic acid include salts with hydrochloric acid, hydrobromic acid, hydroiodic acid, nitric acid, sulfuric acid, phosphoric acid and the like.
- the salt with an organic acid include, for example, formic acid, acetic acid, trifluoroacetic acid, propionic acid, butyric acid, valeric acid, enanthic acid, capric acid, myristic acid, palmitic acid, stearic acid, lactic acid, sorbic acid, Salts with aliphatic monocarboxylic acids such as mandelic acid, salts with aliphatic dicarboxylic acids such as oxalic acid, malonic acid, succinic acid, fumaric acid, maleic acid, malic acid, tartaric acid, and aliphatic tricarboxylic acids such as citric acid Salts with acids, salts with aromatic monocarboxylic acids such as benzoic acid and salicylic acid, salts of aromatic dicarboxylic acids such as phthalic acid, cinnamic acid, glycolic acid, pyruvic acid, oxylic acid, salicylic acid, N-acetylcysteine, etc.
- Salt with organic carboxylic acid salt with organic sulfonic acid such as methanesulfonic acid, benzenesulfonic acid, p-toluenesulfonic acid, aspartic acid, gluta Acid addition salts with acidic amino acids such as phosphate and the like.
- Preferable examples of the salt with acidic amino acid include salts with aspartic acid, glutamic acid and the like. Of these, pharmaceutically acceptable salts are preferred.
- the salt is formed by mixing the compound of the present invention with a solution containing an appropriate amount of acid or base to form the desired salt, and then separated by filtration, or the mixed solvent is distilled off.
- a solution containing an appropriate amount of acid or base to form the desired salt
- the mixed solvent is distilled off.
- Handbook of Pharmaceutical Salts: Properties, Selection, and Use, Stahl & Wermuth (Wiley-VCH, 2002) are published as detailed reviews on salt, and are described in detail in this document.
- an amine compound represented by formula (AM-1) or formula (AM-2) (including subordinate formulas of each formula) or a salt thereof is solvated with a solvent such as water, ethanol or glycerol.
- a solvent such as water, ethanol or glycerol.
- 1,3-dicyclohexylcarbodiimide (DCC), 1-ethyl-3- (3-dimethylaminopropyl) carbodiimide hydrochloride (WSC.HCl), benzotriazol-1-yloxytris (dimethylamino) phosphonium hexafluorophosphate (BOP reagent), bis (2-oxo-3-oxazolidinyl) phosphinic chloride (BOP-Cl ), 2-chloro-1,3-dimethylimidazolinium hexafluorophosphate (CIP), 4- (4,6-dimethoxy-1,3,5-triazin-2-yl) -4-methylmorpholinium
- a condensing agent such as chloride (DMT-MM)
- water an ether solvent such as 1,4-dioxane
- an alcohol solvent such as methanol and ethanol
- a polar solvent such as N, N-dimethylformamide, or the
- the introduction rate of the photocrosslinking group can be adjusted as follows. Condensation, such as increasing or decreasing the equivalent amount of condensing agent used in the reaction, increasing or decreasing the reaction temperature, changing the reaction time, changing the concentration of alginic acid, or adding an organic solvent mixed with water to increase the solubility of the photocrosslinking group introduction reagent Depending on the properties of the agent and the photocrosslinkable amine to be introduced, the conditions can be adjusted by appropriate selection and combination of the conditions.
- Cross-linked Alginic Acid is either (i) via a divalent metal ion bond, (ii) via a chemical bond, or (iii) via both a divalent metal ion bond and a chemical bond. There is something. Any cross-linked alginic acid has the property of forming a gel-like, semi-solid, and possibly sponge-like morphology.
- Cross-linked alginic acid via a divalent metal ion bond proceeds at an ultra-high speed and is reversible, whereas cross-linked alginic acid via a chemical bond proceeds slowly under relatively mild conditions. And irreversible.
- the physical properties of the crosslinked alginic acid are adjusted by, for example, changing the concentration of the aqueous solution containing the divalent metal ion to be used (for example, calcium chloride aqueous solution) or the introduction rate of the reactive group introduced into the alginic acid. Is possible.
- a specific structure can be instantly made from an alginate solution by an ionic cross-linking reaction, and a cross-linking reaction by a chemical bond is used for strengthening the structure of the structure (for example, obtaining long-term stability). It is possible to do. Also, for example, in a crosslinked alginic acid structure via both divalent metal ion bonds and chemical bonds, the divalent metal ions incorporated by ionic crosslinking are reversibly released, leaving only the crosslinks due to chemical bonds. It is also possible to create a structure.
- Photocrosslinked alginic acid can be obtained by performing photocyclization reaction by irradiating the alginic acid derivative having the photoreactive group represented by the formula (I) introduced thereto.
- an alginic acid derivative forms a three-dimensional network structure via a photocrosslinking group (crosslinking by a cyclobutane ring formed by photoreaction).
- Preferred alginic acid derivatives are those with improved stability of crosslinked alginic acid after crosslinking.
- the light to be irradiated is not particularly limited as long as it acts on a photoreactive group (photocrosslinking group) and causes a reaction such as polymerization or dimerization (preferably photodimerization reaction (photocyclization reaction)).
- a photoreactive group photocrosslinking group
- dimerization preferably photodimerization reaction (photocyclization reaction)
- the light wavelength of the light source to be used is preferably in the range of 180 to 650 nm, more preferably in the range of 300 to 410 nm.
- specific light amounts and wavelengths for causing the photocrosslinking reaction are as follows. That is, the illuminance of HLR100T-2 (manufactured by Sen Special Light Source Co., Ltd.) is 170 mW / cm 2 (distance of 50 mm from the light source), the main wavelength is 365 nm, and the irradiation time is 10 minutes. With irradiation at a distance of 100 mm from the light source, the exposure dose is 25 J / cm 2 .
- the photocrosslinked alginic acid is obtained by dimerizing the photoreactive moiety (alkene moiety) of the photoreactive group represented by formula (I) by a photocyclization reaction, for example, the following formula (II-L-1 ) To (II-L-3): [In the formulas (II-L-1) to (II-L-3), —CONH— and —NHCO— at both ends represent an amide bond via any carboxyl group of alginic acid; —A—, —X -And Ar have a chemical bridge formed with a cyclobutane ring (torxyl acid derivative) represented by the above-mentioned embodiment [1], [1a] or [1b].
- the introduction rate of the crosslinking represented by the above formula is, for example, 0.1 to 80%, 0.3 to 60%, 0.5 to 30%, or 1.0 to 10 % Range.
- the concentration of the alginic acid derivative for obtaining the photocrosslinked alginic acid is, for example, in the range of 1 to 500 mg / mL, or 5 to 100 mg / mL.
- the temperature at which the photocrosslinking reaction is performed is usually room temperature (about 0 ° C. to about 35 ° C.).
- the reaction time for forming the crosslinked alginic acid (hydrogel) is, for example, several seconds to 24 hours, several seconds to 12 hours, several seconds to 30 minutes, or several seconds to 10 minutes.
- the reaction solvent or reaction solution used for the photocrosslinking reaction is not particularly limited.
- tap water pure water (for example, distilled water, ion exchange water, RO water, RO-EDI water, etc.), ultrapure water
- Examples include a medium for cell culture, phosphate buffered saline (PBS), and physiological saline, and ultrapure water is preferable.
- PBS phosphate buffered saline
- the photocrosslinked alginic acid comprises a chemical cross-link by a cyclobutane ring (torxylic acid derivative) formed by a photoreaction as a cross-link and an ionic cross-link partially formed by a divalent metal ion (eg, calcium ion). It may be a crosslinked alginic acid.
- a photocrosslinked alginic acid structure is obtained by subjecting a photoreactive group represented by the formula (I) to a light-irradiated alginic acid derivative to perform a crosslinking reaction.
- a photoreactive group represented by the formula (I) to a light-irradiated alginic acid derivative to perform a crosslinking reaction.
- it can be prepared by the following method, but is not limited thereto.
- a solution of an alginic acid derivative into which a photoreactive group represented by the above formula (I) is introduced is dropped into a solution containing a divalent metal ion, whereby ion crosslinking (divalent metal)
- ion crosslinking divalent metal
- a specific structure in which a cross-link (partially formed by ions) is formed is obtained.
- the structure is irradiated with light and subjected to photocrosslinking (chemical crosslinking: cyclobutane ring (truxyl acid derivative)), whereby a photocrosslinked alginic acid structure, which is a specific structure, can be obtained.
- the photocrosslinked alginic acid structure can be obtained by a method including irradiating light to an alginic acid derivative having a photoreactive group (photocrosslinking group).
- the light to be irradiated is not particularly limited as long as it acts on the photocrosslinking group and causes a reaction such as polymerization or dimerization (preferably photodimerization reaction).
- the light to be irradiated is not particularly limited as long as it acts on a photoreactive group (photocrosslinking group) and causes a reaction such as polymerization or dimerization (preferably photodimerization reaction (photocyclization reaction)).
- LED Light Emitting Diode
- visible light, LED light, or ultraviolet light is preferable, and ultraviolet light is more preferable.
- the light wavelength of the light source to be used is preferably in the range of 180 to 650 nm, more preferably in the range of 300 to 410 nm.
- specific light amounts and wavelengths for causing the photocrosslinking reaction are as follows. That is, the illumination intensity of HLR100T-2 (manufactured by Sen Special Light Source Co., Ltd.) is 170 mW / cm 2 (distance of 50 mm from the light source), the main wavelength is 365 nm, and the irradiation time is 10 minutes. . With irradiation at a distance of 100 mm from the light source, the exposure dose is 25 J / cm 2 .
- the divalent metal ion used in the above method is not particularly limited, and examples thereof include calcium ion, magnesium ion, barium ion, strontium ion, zinc ion, and the like, preferably calcium ion.
- the solution containing calcium ions used in the above method is not particularly limited, and examples thereof include aqueous solutions such as a calcium chloride aqueous solution, a calcium carbonate aqueous solution, and a calcium gluconate aqueous solution, and a calcium chloride aqueous solution is preferable.
- the calcium ion concentration of the solution containing calcium ions used in the above method is not particularly limited, and examples thereof include 1 mM to 1 M, preferably 5 mM to 500 mM, and more preferably 10 mM to 300 mM.
- the solvent or solution used in the above method is not particularly limited.
- tap water for example, distilled water, ion exchange water, RO water, RO-EDI water, etc.
- ultrapure water cell culture medium
- PBS Phosphate buffered saline
- physiological saline Phosphate buffered saline
- photocrosslinked alginate structure examples include fibrous structures, fibers, beads, gels, and substantially spherical gels.
- Preferred cross-linked alginate structures are those with improved stability.
- the crosslinked alginic acid structure may have an ability to retain the content (content retention).
- the physical properties of the alginate gel can be adjusted by physical properties such as hardness, elasticity, repulsive force, tearing force, stress at break.
- biocompatibility means a biomaterial (here, an alginic acid derivative into which a photoreactive group represented by formula (I) has been introduced, and a photocrosslinked alginic acid structure produced using the alginic acid derivative).
- Biocompatibility refers to a property that does not cause a reaction such as an interaction between a body and a living body, a local reaction of a tissue adjacent to the biomaterial, or a systemic reaction.
- the biocompatibility of the alginic acid derivative or the photocrosslinked alginic acid structure is confirmed in the examples relating to biocompatibility described later.
- Stability of Photocrosslinked Alginic Acid Structure The stability of the photocrosslinked alginic acid structure can be confirmed, for example, by measuring gel stability and measuring permeability by measuring gel permeability.
- Phosphate buffered saline PBS
- concentration ⁇ g / mL
- the value obtained by dividing the measured alginic acid concentration by the total alginic acid concentration obtained by decomposing the crosslinked alginic acid structure gel is shown as a disintegration rate.
- the gel stability can be determined by the method described in Examples described later.
- the gel disintegration rate of the photocrosslinked alginate structure is preferably 0% to 90%, more preferably 0% to 70%, and further preferably 0% to 50%.
- the stability of the crosslinked alginic acid structure means that the lower the concentration of alginic acid leaked into the aqueous solution, that is, the lower the gel disintegration rate, the higher the stability.
- the gel permeability after 24 hours from the addition of physiological saline of photocrosslinked alginic acid is preferably 0% to 90%, more preferably 0% to 70%. More preferably, it is 0% to 50%.
- dextran having a molecular weight of 150,000 is encapsulated, for example, if the purpose of use of the photocrosslinked alginate structure gel is to release or produce proteins or antibodies, it is preferably 1% to 100%, more preferably It is 10% to 100%, more preferably 30% to 100%. Further, if the purpose of use is an immune septum, it is preferably 0% to 90%, more preferably 0% to 70%, still more preferably 0% to 50%.
- the permeability of the photocrosslinked alginate structure means that the lower the transmittance, the lower the permeability of the contents and the off-gel substance.
- the gel permeability can be adjusted by adjusting the molecular weight and concentration of alginic acid used, the type and introduction rate of cross-linking groups introduced into alginic acid, the type and concentration of divalent metal ions used for gelation, or a combination thereof. is there.
- a crosslinked alginic acid structure gel encapsulating fluorescein isothiocyanate-dextran as a content can be prepared by the following method.
- a solution of an alginate derivative into which a photoreactive group represented by the formula (I) is introduced is mixed with a fluorescein isothiocyanate-dextran solution.
- a photocrosslinked alginate structure gel containing isothiocyanate-dextran is obtained.
- Alginic Acid derivatives can be used in place of conventional alginic acid in a wide range of fields such as food, medicine, cosmetics, textiles and papermaking. Specific uses of alginic acid derivatives or photocrosslinked alginic acid structures include medical treatments such as wound dressing materials, postoperative adhesion prevention materials, base materials for sustained drug release, base materials for cell culture, base materials for cell transplantation, etc. Materials.
- Examples of the shape of the photocrosslinked alginate structure when used as a medical material include fibers, fibers, beads, gels, substantially spherical gels, and the like, preferably beads, gels, or substantially spherical gels. It is more preferable to use this gel.
- JEOL JNM-ECX400 FT-NMR was used for nuclear magnetic resonance spectrum (NMR) measurement.
- the “introduction rate” in the examples is described in “mol%” by measurement using the carbazole method. A part was measured by 1 H-NMR in D 2 O, and described as “mol% (NMR integration ratio)” from the ratio of the proton integration value of the photocrosslinking group and alginic acid.
- Root temperature in the examples usually indicates a temperature of about 0 ° C. to about 35 ° C.
- sodium alginate having the physical property values shown in Table 1 was used as sodium alginate before the introduction of a reactive group or a complementary reactive group.
- Tables 2-1 and 2-2 show the alginic acid derivatives (EX1-a1, EX1-b, EX1-c) into which photoreactive groups were introduced, obtained in (Example 1) to (Example 19).
- the physical property values (specifically, photoreactive group introduction rate (mol%), molecular weight, and weight average molecular weight (10,000 Da)) of a1) are shown.
- Example 1 The compound (3.1 g) obtained in ⁇ Step 1> was dissolved in ethanol (15.7 mL). Under cooling with ice water, 1N-aqueous sodium hydroxide solution (17.7 mL) was added, and the mixture was stirred at 50 ° C. for 1.5 hours. Under ice water cooling, the pH was adjusted to 2 with 2N hydrochloric acid. The deposited precipitate was collected by filtration, washed with water, and dried under reduced pressure to obtain the title compound (2.6 g) as a white solid.
- Example 1 Compound (500 mg) obtained in ⁇ Step 2> and tert-butyl (3-hydroxypropyl) carbamate (commercial product: CAS No. 58888-58-8: 527 mg) were mixed with N-methylpyrrolidone (5.0 mL). Diisopropylethylamine (1.26 mL) and 1- [bis (dimethylamino) methylene] -1H-1,2,3-triazolo [4,5-b] pyridinium 3-oxide hexafluorophosphate (1.37 g) And stirred at room temperature for 21 hours. Water (20 mL) and methyl tert-butyl ether (30 mL) were added to the reaction solution to separate the layers.
- the organic layer was washed successively with saturated aqueous sodium hydrogen carbonate (10 mL), water (10 mL, twice) and saturated brine (10 mL), dried over anhydrous sodium sulfate, and the solvent was evaporated under reduced pressure.
- the obtained oil was purified by silica gel column chromatography (heptane to 50% ethyl acetate / heptane) and then triturated with heptane.
- the obtained solid was collected by filtration, washed with heptane, and dried under reduced pressure to obtain the title compound (511 mg) as a white solid.
- Example 1 4N-hydrogen chloride / dioxane (2.1 mL) was added to the compound (300 mg) obtained in ⁇ Step 3> under ice-water cooling. The reaction solution was stirred at room temperature for 1 hour, diisopropyl ether (6.3 mL) was added, and the mixture was stirred for 1 hour. The precipitated solid was collected by filtration, washed with diisopropyl ether, and dried under reduced pressure to obtain the title compound (223 mg) as a white solid.
- Example 1 Using sodium alginate (A-1) aqueous solution (15 mL) adjusted to 1 wt% and the compound (39.3 mg) obtained in (Example 1) ⁇ Step 4> Example 1) The same operation as in ⁇ Step 5-1> was performed to give the title compound (135 mg) as a white solid.
- Example 1 Using sodium alginate (A-3) aqueous solution (30 mL) adjusted to 0.5 wt% and the compound (39.3 mg) obtained in (Example 1) ⁇ Step 4>, Example 1 The same operation as in ⁇ Step 5-1> was performed to obtain the title compound (154 mg) as a white solid.
- the organic layer was washed successively with 1N-citric acid (20 mL), half-saturated aqueous sodium bicarbonate (20 mL, 2 times), water (10 mL), saturated brine (10 mL), dried over anhydrous sodium sulfate, and solvent Was distilled off under reduced pressure.
- the obtained oil was purified by silica gel column chromatography (heptane-30% ethyl acetate / heptane) and then triturated with heptane.
- the obtained solid was collected by filtration, washed with heptane, and then dried under reduced pressure to obtain the title compound (1.3 g) as a white solid.
- Example 2 Using the compound (1.2 g) obtained in ⁇ Step 1>, the same operation as in (Example 1) ⁇ Step 4> was performed to give the title compound (0.9 g) as a white solid. Got as.
- Example 1 Using a sodium alginate adjusted to 0.5% by weight (Mochida Pharmaceutical Co., Ltd .: A-3) aqueous solution (20 mL) and the compound obtained in Example 2 ⁇ Step 2> (24.4 mg), Example 1 The same operation as in ⁇ Step 5-1> was performed to obtain the title compound (104 mg) as a white solid.
- Example 3 Using the compound (200 mg) obtained in ⁇ Step 1>, the same operation as in (Example 1) ⁇ Step 4> was performed to obtain the title compound (148 mg) as a white solid.
- Example 1 Using a sodium alginate (Mochida Pharmaceutical Co., Ltd .: A-2) aqueous solution (10.9 mL) adjusted to 1% by weight and the compound (31.2 mg) obtained in (Example 3) ⁇ Step 2>
- Example 1 The same operation as in ⁇ Step 5-1> was performed to obtain the title compound (109 mg) as a white solid.
- Example 4 Using the compound (0.42 g) obtained in ⁇ Step 2>, the same operation as in (Example 1) ⁇ Step 4> was performed to give the title compound (0.4 g) as a colorless liquid. Obtained.
- Example 5 Using the compound (0.77 g) obtained in ⁇ Step 1>, the same operation as in (Example 1) ⁇ Step 4> was performed to give the title compound (0.56 g) as a white powder. Got as.
- Example 6 Compound (0.20 g) obtained in ⁇ Step 1>, tert-butyl (3-bromopropyl) carbamate (0.27 g), potassium carbonate (0.16 g), potassium iodide (20 mg) was added with N-methylpyrrolidone (2.0 mL) and stirred at 40 ° C. for 1 hour, 70 ° C. for 4.5 hours, and 100 ° C. for 2.5 hours, and then tert-butyl (3-bromopropyl). ) Carbamate (0.16 g), potassium carbonate (96 mg) and potassium iodide (20 mg) were added, and the mixture was stirred at 100 ° C. for 2 hours.
- Example 6 Using the compound (0.31 g) obtained in ⁇ Step 2>, the same operation as in (Example 1) ⁇ Step 4> was performed, and the title compound (0.23 g) was converted to light beige. Obtained as a solid.
- Example 7 Compound (0.20 g) obtained in ⁇ Step 1>, tert-butyl (3-bromopropyl) carbamate (0.41 g), potassium carbonate (0.24 g), potassium iodide N-methylpyrrolidone (2.0 mL) was added to (40 mg) and stirred at 80 ° C. for 1 hour. Ethyl acetate (20 mL) and water (10 mL) were added to the reaction solution, and the phases were separated. The organic layer was washed successively with water (5 mL, 3 times) and saturated brine (5 mL), dried over anhydrous sodium sulfate, and the solvent was evaporated under reduced pressure. The obtained oil was purified by silica gel column chromatography (heptane-60% ethyl acetate / heptane) to give the title compound (0.36 g) as a white solid.
- Example 7 Using the compound (0.36 g) obtained in ⁇ Step 2>, the same operation as in (Example 1) ⁇ Step 4> was performed to give the title compound (0.27 g) as a white solid. Got as.
- Example 8 Using the compound (0.40 g) obtained in ⁇ Step 2>, the same operation as in (Example 1) ⁇ Step 4> was performed, and the title compound (0.34 g) was pale green. Obtained as a solid.
- Example 9 Using the compound (0.52 g) obtained in ⁇ Step 1>, the same operation as in (Example 1) ⁇ Step 4> was performed to give the title compound (0.38 g) as a white solid Got as.
- Example 6 To the compound (0.30 g) obtained in ⁇ Step 1>, thionyl chloride (250 ⁇ L) and N, N-dimethylformamide (1.3 ⁇ L) were added and stirred at 80 ° C. for 30 minutes. did. The resulting solution was concentrated under reduced pressure and azeotroped twice with methylene chloride (1 mL). The obtained solid was dissolved in methylene chloride (1.5 mL), and tert-butyl (2- (2-hydroxyethoxy) ethyl) carbamate (commercial product: CAS No. 139115-91-6) was cooled with ice water.
- Example 10 Using the compound (0.54 g) obtained in ⁇ Step 1>, the same operation as in (Example 1) ⁇ Step 4> was performed to give the title compound (0.42 g) as a white solid Got as.
- Example 11 Using the compound (0.34 g) obtained in ⁇ Step 1>, the same operation as in (Example 1) ⁇ Step 4> was performed to give the title compound (0.25 g) as a white solid Got as.
- Example 12 The compound obtained in ⁇ Step 1> (256 mg), tert-butyl (3-bromopropyl) carbamate (448 mg), potassium carbonate (260 mg), potassium iodide (42 mg) and N -Methylpyrrolidone (2.6 mL) was added, and the mixture was stirred at 80 ° C for 2.5 hours. Ethyl acetate (25 mL) and water (12 mL) were added to the reaction solution to separate the layers. The organic layer was washed successively with water (5 mL, 3 times) and saturated brine (5 mL), dried over anhydrous sodium sulfate, and the solvent was evaporated under reduced pressure. The obtained oil was purified by silica gel column chromatography (heptane-40% ethyl acetate / heptane) to give the title compound (402 mg) as a white solid.
- Example 12 Using the compound (0.40 g) obtained in ⁇ Step 2>, the same operation as in (Example 1) ⁇ Step 4> was performed to give the title compound (0.32 g) as a white solid Got as.
- Example 1 Sodium alginate (Mochida Pharmaceutical Co., Ltd .: A-2) aqueous solution (40 mL) adjusted to 1% by weight and the compound obtained in Example 12 ⁇ Step 3> (30.0 mg), 4- (4 , 6-dimethoxy-1,3,5-triazin-2-yl) -4-methylmorpholinium chloride (112 mg), 1 molar concentration—aqueous sodium bicarbonate (151 ⁇ L), and reacted at 30 ° C. for 4 hours. (Example 1) The same operation as in ⁇ Step 5-1> was performed to give the title compound (381 mg) as a white solid.
- Example 7 To the compound (0.40 g) obtained in ⁇ Step 1>, thionyl chloride (0.3 4 mL) and N, N-dimethylformamide (1.8 ⁇ L) were added, and the mixture was stirred at 80 ° C. for 40 minutes. The resulting solution was concentrated under reduced pressure and azeotroped twice with methylene chloride (1 mL).
- Example 13 The compound (0.78 g) obtained in ⁇ Step 1> was dissolved in 1,4-dioxane (2.35 mL), and 4N-hydrogen chloride / dioxane (5. 48 mL) was added slowly. The reaction was stirred at room temperature for 1 hour 30 minutes and diisopropyl ether (50 mL) was added. The precipitated solid was collected by filtration, washed with diisopropyl ether, and dried under reduced pressure to obtain the title compound (0.56 g) as a white solid.
- the organic layer was washed successively with half-saturated multistory water (10 mL), water (5 mL) and saturated brine (5 mL), dried over anhydrous sodium sulfate, and the solvent was evaporated under reduced pressure.
- the obtained oil was purified by silica gel column chromatography (8% ethyl acetate / heptane to 68% ethyl acetate / heptane) to give the title compound (0.51 g) as a colorless oil.
- Example 14 The compound (0.51 g) obtained in ⁇ Step 1> was dissolved in 1,4-dioxane (1.52 mL), and 4N-hydrogen chloride / dioxane (3. 56 mL) was added slowly. The reaction solution was stirred at room temperature for 1 hour and 30 minutes, and diisopropyl ether (50 mL) was added to give a gum-like compound. After the solution was concentrated under reduced pressure, diisopropyl ether (30 mL) was added to the resulting solid and triturated. The solid was collected by filtration, washed with diisopropyl ether, and then dried under reduced pressure to obtain the title compound (0.4 g) as a pale pink amorphous.
- Example 15 To the compound obtained in ⁇ Step 1> (0.30 g), thionyl chloride (210 ⁇ L) and N, N-dimethylformamide (1.1 ⁇ L) were added, and the mixture was stirred at 80 ° C. for 30 minutes. did. The resulting solution was concentrated under reduced pressure and azeotroped twice with methylene chloride (1 mL). The obtained acid chloride was dissolved in methylene chloride (1.5 mL), and tert-butyl (2- (2-hydroxyethoxy) ethyl) carbamate (0.35 g) and triethylamine (0. 6 mL) and N, N-dimethylaminopyridine (35 mg) in methylene chloride (1.5 mL).
- Example 15 Using the compound (0.53 g) obtained in ⁇ Step 2>, (Example 1) ⁇ The same operation as in Step 4> was performed to obtain the title compound (0.39 g) as a white solid.
- Example 15 Sodium alginate (Mochida Pharmaceutical Co., Ltd .: A-2) aqueous solution (40 mL) adjusted to 1% by weight and (Example 15) ethanol (4 mL) solution of the compound (34 mg) obtained in ⁇ Step 3> , 4- (4,6-dimethoxy-1,3,5-triazin-2-yl) -4-methylmorpholinium chloride (112 mg), 1 molar concentration—sodium bicarbonate water (151 ⁇ L), 30 ° C. And the same operation as in Example 1 ⁇ Step 5-1> was performed to obtain the title compound (392 mg) as a white solid.
- Example 16 A suspension of the compound (0.40 g) obtained in ⁇ Step 1> and methylene chloride (4 mL) was subjected to oxalyl chloride (0.59 mL), N, N under ice cooling. -Dimethylformamide (1.7 ⁇ L) was added, and the mixture was stirred at room temperature for 1 hour and 30 minutes. The obtained solution was concentrated under reduced pressure, suspended in methylene chloride (2 mL), and tert-butyl (2- (2-hydroxyethoxy) ethyl) carbamate (0.46 g), N— under ice-water cooling.
- Ethyldiisopropylamine (1.17 mL) was added to a methylene chloride (2 mL) solution. After stirring at room temperature for 30 minutes, ethyl acetate (20 mL) and water (10 mL) were added to separate the layers. The organic layer was washed successively with half-saturated multistory water (10 mL), water (5 mL) and saturated brine (5 mL), dried over anhydrous sodium sulfate, and the solvent was evaporated under reduced pressure.
- the resulting crude product was purified by silica gel column chromatography (8% ethyl acetate / heptane to 68% ethyl acetate / heptane: once, 16% ethyl acetate / heptane to 100% ethyl acetate: twice) to give the title A fraction containing the compound (0.15 g) was obtained.
- Example 17 To the compound (0.40 g) obtained in ⁇ Step 1>, thionyl chloride (0.28 mL) and N, N-dimethylformamide (1.5 ⁇ L) were added, and the mixture was heated at 80 ° C. for 40 minutes. Stir for minutes. The resulting solution was concentrated under reduced pressure and azeotroped twice with methylene chloride (1 mL). The obtained solid was dissolved in methylene chloride (2 mL), and tert-butyl (2- (2-hydroxyethoxy) ethyl) carbamate (0.48 g), triethylamine (0.82 mL) was cooled with ice water.
- N, N-dimethylaminopyridine (0.05 g) in methylene chloride (2 mL).
- ethyl acetate (20 mL) and water (10 mL) were added to separate the layers.
- the organic layer was washed successively with half-saturated multilayered water (10 mL), water (5 mL) and saturated brine (5 mL), dried over anhydrous sodium sulfate, and the solvent was evaporated under reduced pressure.
- the resulting crude product was purified twice by silica gel column chromatography (25% ethyl acetate / heptane to ethyl acetate) to obtain the title compound (0.63 g) as a brown gum-like compound.
- Example 17 Using the compound (0.63 g) obtained in ⁇ Step 2>, the same operation as in (Example 13) ⁇ Step 2> was performed, and the title compound (0.47 g) was pale yellow. Obtained as a solid.
- Example 12 To the compound (0.30 g) obtained in ⁇ Step 1>, thionyl chloride (0.21 mL) and N, N-dimethylformamide (1.1 ⁇ L) were added, and the mixture was 30 at 80 ° C. Stir for minutes. The resulting solution was concentrated under reduced pressure and azeotroped twice with methylene chloride (1 mL). The obtained solid was dissolved in methylene chloride (1.5 mL), and tert-butyl (2- (2-hydroxyethoxy) ethyl) carbamate (0.3 g), triethylamine (0.61) was cooled with ice water.
- Example 18 Using the compound (0.44 g) obtained in ⁇ Step 1>, the same operation as in (Example 13) ⁇ Step 2> was performed, and the title compound (0.343 g) was pale yellow. Obtained as a solid.
- Example 19 Using the compound (0.39 g) obtained in ⁇ Step 1>, the same operation as in (Example 1) ⁇ Step 4> was performed, and the title compound (0.25 g) was pale yellow. Obtained as a gum.
- the introduction rate of the photoreactive group means a value expressed as a percentage of the number of photocrosslinking groups introduced per uronic acid monosaccharide unit which is a repeating unit of alginic acid.
- the amount of alginic acid necessary for calculating the introduction rate is measured by the carbazole sulfate method using a calibration curve, and the amount of the photocrosslinking group is measured by an absorbance measurement method using the calibration curve.
- the introduction ratio of reactive groups or complementary reactive groups was calculated by the integration ratio of 1 H-NMR.
- the amount of alginic acid required for calculating the introduction rate is measured by the carbazole sulfate method using a calibration curve, and the amount of the reactive group or complementary reactive group is measured by the absorbance measurement method using the calibration curve.
- the alginate derivative-introduced solid with an introduced photoreactive group obtained in Examples was dissolved in 10 mmol / L phosphate buffer (pH 7.4) containing 0.15 mol / L NaCl.
- a 1% solution was prepared and passed through a polyethersulfone filtration filter (Minisart High Flow Filter, Sartorius) having a pore size of 0.22 ⁇ m to remove insoluble matters, and then a sample for gel filtration was obtained.
- the spectrum of each sample was measured with a spectrophotometer DU-800 (Beckman-Coulter), and the measurement wavelength in gel filtration of each compound was determined. For compounds having no specific absorption wavelength, a differential refractometer was used.
- the alginate derivative-introduced solid with an introduced photoreactive group obtained in Examples was dissolved in 10 mmol / L phosphate buffer (pH 7.4) containing 0.15 mol / L NaCl.
- a 1% solution was prepared, passed through a cellulose acetate filtration filter (DISMIC-25cs, ADVANTEC) having a pore size of 0.2 ⁇ m to remove insoluble matters, and then used as a gel filtration sample.
- the spectrum of each sample was measured with a spectrophotometer DU-800 (Beckman-Coulter), and the measurement wavelength in gel filtration of each compound was determined. For compounds having no specific absorption wavelength, a differential refractometer was used.
- the molecular weight of alginic acid into which a photoreactive group has been introduced is blue dextran (molecular weight: 2 million Da, SIGMA), thyroglobulin (molecular weight: 669,000 Da, GE Healthcare Science) ferritin (molecular weight: 440,000 Da, GE Health) Care Science Inc.) Aldolase (Molecular weight 1580 Da, GE Healthcare Science Inc.), Conalbumin (Molecular weight 75,000 Da, GE Healthcare Science Inc.), Ovalbumin (Molecular weight 44,000 Da, GE Healthcare) Science), Ribonuclease A (molecular weight: 1.37,000 Da, GE Healthcare Science) and aprotinin (molecular weight: 6500 Da, GE Healthcare Science) were used as standard products, and photoreactive groups (photocrosslinking groups) were introduced.
- blue dextran molecular weight: 2 million Da, SIGMA
- thyroglobulin molecular weight: 669,000 Da, GE Healthcare Science
- ferritin molecular
- the molecular weight (Mi) at the elution time i of the previously obtained chromatogram was calculated.
- the absorbance at elution time i was read and taken as Hi. From these data, the weight average molecular weight (Mw) was determined from the following equation.
- the solution is dropped into a calcium chloride solution having a concentration of 300 mmol / L for 30 seconds, and 5 minutes.
- a photoreactive group-introduced alginate gel was obtained.
- This gel was washed once with 10 mL of phosphate buffered saline (PBS), and then irradiated with light for 10 minutes in water using a UV curing device (Sen Special Light Source Co., Ltd., HLR100T-2) to produce photocrosslinked alginic acid.
- a structure gel was obtained. 19.5 mL of PBS was added to the gel contained in the container, shaken at 37 ° C., the aqueous solution was recovered over time, and the same amount of PBS as the recovered amount was replenished.
- alginate lyase (Nippon Gene, 319-08261) was added to the test solution and shaken at 37 ° C. for 1 hour to completely disintegrate the gel, and an aqueous solution was recovered.
- the concentration of alginic acid in the recovered aqueous solution was measured by the carbazole sulfate method, and the values corrected for the alginic acid concentration in the aqueous solution at each time point with the alginic acid concentration already recovered were calculated from the alginic acid concentration at all time points and the alginic acid concentration after the end of the test.
- a value obtained by dividing the value by the alginic acid concentration as a percentage was taken as the disintegration rate, and was used as an index of gel stability.
- Example 6 The alginic acid derivative (EX6-b) obtained in ⁇ Step 4-2> was dissolved in water to a concentration of 1% to obtain an alginate aqueous solution. This aqueous solution was put into a syringe equipped with an 18-gauge syringe needle, this syringe was placed in a syringe pump set at a flow rate of 1 mL / min, dropped into a calcium chloride solution having a concentration of 30 mmol / L for 30 seconds, The mixture was stirred for 5 minutes to obtain a photoreactive group-introduced alginate gel.
- This gel was washed once with 10 mL of phosphate buffered saline (PBS), and then irradiated with light in water for 3, 10 and 60 minutes using a UV curing device (Sen Special Light Source Co., Ltd., HLR100T-2). And a photocrosslinked alginate gel was obtained. Add 20 mL of PBS to this gel, shake at 37 ° C, collect the aqueous solution after 1, 2, 4, 8, 24, 48, 72, 144 hours, and replenish with the same amount of PBS as collected. did.
- PBS phosphate buffered saline
- alginate lyase CREATE enzymes, NATE 1563
- concentration of alginic acid in the recovered aqueous solution was measured by the carbazole sulfate method, and the values corrected for the alginic acid concentration in the aqueous solution at each time point with the alginic acid concentration already recovered were calculated from the alginic acid concentration at all time points and the alginic acid concentration after the end of the test.
- a value obtained by dividing the value by the alginic acid concentration as a percentage was taken as the disintegration rate, and was used as an index of gel stability.
- This aqueous solution was put into a syringe equipped with an 18-gauge syringe needle, this syringe was placed in a syringe pump set at a flow rate of 1 mL / min, dropped into a calcium chloride solution having a concentration of 30 mmol / L for 30 seconds, The mixture was stirred for 5 minutes to obtain a photocrosslinking group-introduced alginate gel.
- This gel was washed once with 10 mL of phosphate buffered saline (PBS), and then irradiated with light for 10 minutes in PBS using a UV curing device (Sen Special Light Source Co., Ltd., HLR100T-2). A crosslinked alginate gel was obtained.
- PBS phosphate buffered saline
- the concentration of alginic acid in the recovered aqueous solution was measured by the carbazole sulfate method, and the values corrected for the alginic acid concentration in the aqueous solution at each time point with the alginic acid concentration already recovered were calculated from the alginic acid concentration at all time points and the alginic acid concentration after the end of the test.
- a value obtained by dividing the value by the alginic acid concentration as a percentage was taken as the disintegration rate, and was used as an index of gel stability.
- This gel was washed once with 10 mL of phosphate buffered saline (PBS), and then irradiated with light for 10 minutes in water using a UV curing device (Sen Special Light Source Co., Ltd., HLR100T-2) to effect photocrosslinking.
- An alginate gel was obtained.
- 20 mL of PBS was added and shaken at 37 ° C., and the aqueous solution was recovered after 1.5, 6, 24, and 96 hours, and supplemented with the same amount of PBS as the recovered amount.
- 5 ⁇ L of alginate lyase (Nippon Gene, 319-08261) was added to the test solution and shaken overnight at 37 ° C.
- the concentration of alginic acid in the recovered aqueous solution was measured by the carbazole sulfate method, and the values corrected for the alginic acid concentration in the aqueous solution at each time point with the alginic acid concentration already recovered were calculated from the alginic acid concentration at all time points and the alginic acid concentration after the end of the test.
- a value obtained by dividing the value by the alginic acid concentration as a percentage was taken as the disintegration rate, and was used as an index of gel stability.
- Alginic acid derivative (EX13-a1) obtained in (Example 13), Alginic acid derivative (EX14-a1) obtained in (Example 14), and Alginic acid derivative (EX17-a1) obtained in (Example 17) ) was dissolved in water to a concentration of 1% to obtain an alginate aqueous solution.
- This aqueous solution was put into a syringe equipped with an 18-gauge syringe needle, this syringe was placed in a syringe pump set at a flow rate of 1 mL / min, dropped into a calcium chloride solution having a concentration of 30 mmol / L for 30 seconds, The mixture was stirred for 5 minutes to obtain a photoreactive group-introduced alginate gel.
- This gel was washed once with 10 mL of phosphate buffered saline (PBS), and then irradiated with light for 10 minutes in water using a UV curing device (Sen Special Light Source Co., Ltd., HLR100T-2) to effect photocrosslinking.
- PBS phosphate buffered saline
- the concentration of alginic acid in the recovered aqueous solution was measured by the carbazole sulfate method, and the values corrected for the alginic acid concentration in the aqueous solution at each time point with the alginic acid concentration already recovered were calculated from the alginic acid concentration at all time points and the alginic acid concentration after the end of the test.
- a value obtained by dividing the value by the alginic acid concentration as a percentage was taken as the disintegration rate, and was used as an index of gel stability.
- the results are shown in FIG.
- the photocrosslinked alginate gels of this example are all stable (in 96 hours, the photocrosslinked alginate gel derived from EX13-a1 is about 38%, the photocrosslinked alginate gel derived from EX14-a1 is about 37%, It was confirmed that the photocrosslinked alginate gel derived from EX17-a1 has a decay rate of about 43%.
- This aqueous solution was put into a syringe equipped with an 18-gauge syringe needle, this syringe was placed in a syringe pump set at a flow rate of 1 mL / min, dropped into a calcium chloride solution having a concentration of 30 mmol / L for 30 seconds, The mixture was stirred for 5 minutes to obtain a photoreactive group-introduced alginate gel.
- This gel was washed once with 10 mL of phosphate buffered saline (PBS), and then irradiated with light for 10 minutes in water using a UV curing device (Sen Special Light Source Co., Ltd., HLR100T-2) to effect photocrosslinking.
- PBS phosphate buffered saline
- the concentration of alginic acid in the recovered aqueous solution was measured by the carbazole sulfate method, and the values corrected for the alginic acid concentration in the aqueous solution at each time point with the alginic acid concentration already recovered were calculated from the alginic acid concentration at all time points and the alginic acid concentration after the end of the test.
- a value obtained by dividing the value by the alginic acid concentration as a percentage was taken as the disintegration rate, and was used as an index of gel stability.
- This aqueous solution was put into a syringe equipped with an 18-gauge syringe needle, this syringe was placed in a syringe pump set at a flow rate of 1 mL / min, dropped into a calcium chloride solution having a concentration of 30 mmol / L for 30 seconds, The mixture was stirred for 5 minutes to obtain a photoreactive group-introduced alginate gel. The gel was washed once with 10 mL of physiological saline, and then irradiated with light for 10 minutes in water using a UV curing apparatus (Sen Special Light Source Co., Ltd., HLR100T-2) to obtain a photocrosslinked alginate gel.
- a UV curing apparatus Tin Special Light Source Co., Ltd., HLR100T-2
- the concentration of alginic acid in the recovered aqueous solution was measured by the carbazole sulfate method, and the values corrected for the alginic acid concentration in the aqueous solution at each time point with the alginic acid concentration already recovered were calculated from the alginic acid concentration at all time points and the alginic acid concentration after the end of the test.
- a value obtained by dividing the value by the alginic acid concentration as a percentage was taken as the disintegration rate, and was used as an index of gel stability.
- the results are shown in FIG.
- the photocrosslinked argin gel obtained by performing EDTA treatment of this example and excluding calcium crosslinks is highly stable (the photocrosslinked alginate gel derived from Ex9-a is about 17% and the light derived from Ex12-a1 in 24 hours).
- the photocrosslinked alginate gel derived from Ex9-a is about 17% and the light derived from Ex12-a1 in 24 hours.
- the solution is dropped into a calcium chloride solution having a concentration of 100 mmol / L for 30 seconds, and 5 minutes.
- the mixture was stirred to obtain an alginic acid gel with a blue dextran-encapsulated photocrosslinking group.
- After this gel was washed once with 10 mL of PBS, it was irradiated with light for 10 minutes in water using a UV curing device (Sen Special Light Source Co., Ltd., HLR100T-2), and the photocrosslinked alginate structure gel encapsulated in blue dextran was obtained. Obtained.
- the alginic acid derivative (EX17-a1) obtained in (Example 17) and the alginic acid derivative (EX18-a1) obtained in (Example 18) were dissolved in water to a concentration of 2%, and an alginate aqueous solution was prepared.
- fluorescein isothiocyanate-dextran (Sigma Aldrich, FD150S) having a molecular weight of 150,000 prepared to 1/5 volume of 1 mg / mL, and 4/5 volumes of water, and 0.1 mg / mL fluorescein was added.
- a 1.0% aqueous alginate solution containing isothiocyanate-dextran was obtained.
- fluorescein isothiocyanate-dextran-containing 1.0% alginate aqueous solution is placed in a syringe equipped with an 18 gauge needle, and this syringe is placed in a syringe pump set at a flow rate of 1 mL / min.
- the solution was dropped into a calcium chloride solution having a concentration of 30 mmol / L for 30 seconds and stirred for about 5 minutes to obtain an alginate gel.
- This gel was washed once with 10 mL of physiological saline to obtain a fluorescein isothiocyanate-dextran-encapsulated photoreactive group-introduced alginic acid gel.
- This gel was washed once with 10 mL of physiological saline, and then irradiated with light for 10 minutes in water using a UV curing device (Sen Special Light Source Co., Ltd., HLR100T-2), and the light contained in fluorescein isothiocyanate-dextran. A crosslinked alginate gel was obtained.
- the photocrosslinked alginate gel of this example has a transmittance of about 40% after 3 hours from the start of measurement, has a transmittance of about 60% after 24 hours from the start of measurement, and has excellent permeability. It is a thing.
- biocompatibility evaluation The biocompatibility is evaluated by the following method.
- the biocompatibility evaluation method in this specification shows an example, and is not limited to this method.
- Example 1 Introduction rate (NMR integration ratio) produced by the same method as in ⁇ Step 5-1> 4.1 mol% of alginic acid derivative (EX1-a3), (Example 9) in ⁇ Step 3> Alginic acid derivative (EX9-a) obtained, (Example 10) Alginic acid derivative (EX10-a) obtained in ⁇ Step 3>, (Example 12) Alginic acid derivative obtained in ⁇ Step 4> (EX12- a) and alginic acid (A-2; control) were each dissolved in water to a concentration of 1.0 w / w%, and 1/10 volume of physiological saline having an 11-fold concentration was added to the aqueous alginic acid solution.
- CHO cells were mixed with each alginate physiological saline solution so as to be 5.0 ⁇ 10 6 cells / mL to obtain cell solutions, and each cell solution was then injected into a syringe barrel equipped with an 18 gauge needle.
- the syringe was placed in a syringe pump set at a flow rate of 1 mL / min, dropped into a calcium chloride solution having a concentration of 30 mmol / L, stirred for 5 minutes, and then 10 mL of phosphate buffered saline.
- PBS irradiated with light for 10 minutes in PBS using a UV curing device (Sen Special Light Source Co., Ltd., HLR100T-2), washed once with a medium having the composition shown in the table below, and CHO cells Encapsulated alginate gels (gel CHO-1a3), (gel CHO-9a), (gel CHO-10a), (gel CHO-12a), and (gel CHO-REF) were obtained.
- Each CHO cell-encapsulated alginate gel was seeded in a 6-well plate (FALCON, Cat # 351146), a medium having the composition shown in Table 3 below was added at 5 mL / well, the gel was impregnated, and 37 ° C, 5% CO the cells were cultured in the incubator, alginic acid derivatives photoreactive group is introduced, and to make sure that biocompatibility is in the photocrosslinking alginate structures (beads).
Abstract
Description
すなわち、本発明は以下の通りである。
すなわち、例示的な態様は、以下の〔1〕~〔24〕の通りであり得る。
好ましくは、アルギン酸誘導体は、生体に無い反応基を導入したもので、未反応の基が残っていても、細胞等の生体成分との架橋反応が進行する恐れがない生体生物にとって、安全性が期待されるものである。また、好ましくは、架橋反応は、光反応により完結するため、安全で容易に使用することができる。
いくつかの態様の光架橋アルギン酸は、光反応(光環化反応)にて化学架橋されたものである。化学架橋と例えばカルシウムイオンを利用した2価金属イオンを利用した架橋とを組み合わせて用いることができ、反応条件を調整することにより、好ましくはその安定性が非架橋アルギン酸又は非化学架橋アルギン酸(例えば、カルシウムイオン架橋された架橋アルギン酸)と比較して改善したものである。
また、好ましくは、架橋体のゲル物性を調整することができ、物質透過性を調整することもできる。
本発明は、少なくともこれらの効果の1つ以上を有するものである。
より具体的には、以下の態様[1]~[24]が含まれ得る。
[1]第1の態様は、次の通りである。アルギン酸の任意の1つ以上のカルボキシル基に、下記式(I)[式中、波線右外側は含まない]:
Arは、C6-10アリール基、又は複素環基(前記C6~10アリール基、又は複素環基は、ヒドロキシル基、シアノ基、ニトロ基、ハロゲン原子、C1~6アルキル基、ハロゲン化C1~6アルキル基、C1~6アルコキシ基、及び-NRARB基(-NRARB基における、RA及びRBは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、前記C6~10アリール基又は複素環基に、C1~6アルキル基及びC1~6アルコキシ基が又は2つのC1~6アルコキシ基が隣接して置換する場合、当該C1~6アルキル基及びC1~6アルコキシ基の各基のアルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、又は、当該2つのC1~6アルコキシ基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、環状エーテルを形成しても良く、又は、前記C6~10アリール基又は複素環基に、C1~6アルコキシ基及び-NHRG基(-NHRG基におけるRGは、C2~7アルカノイル基又はC1~6アルキルスルホニル基である)が隣接して置換している場合、当該C1~6アルコキシ基のアルキル基から任意の水素原子が1つ除かれた炭素原子と当該-NHRG基の水素原子が1つ除かれた窒素原子が結合することにより、3-N-(C2~7アルカノイル)オキサゾリジン環、3-N-(C1~6アルキルスルホニル)オキサゾリジン環、4-N-(C2~7アルカノイル)モルホリン環、4-N-(C1~6アルキルスルホニル)モルホリン環、4-N-(C2~7アルカノイル)-1,4-オキサゼパン環、又は4-N-(C1~6アルキルスルホニル)-1,4-オキサゼパン環を形成しても良い)を表わし;
pは、1、又は2の整数を表わし;
-X-は、-O-、-NH-、又は-N(C1-6アルキル)-を表わし;
-A-は、式(AL-1)~(AL-4)[各式中、両端の波線外側は含まない]:
式(AL-1)~(AL-4)中のメチレン基(-CH2-)の水素原子は、ハロゲン原子、水酸基、C1~6アルキル基、ヒドロキシC1~6アルキル基、チオールC1~6アルキル基、C1~6アルキルチオC1~6アルキル基、カルボキシC1~6アルキル基、-NRaRb基、(RaRbN)-C1~6アルキル基、(RaRbN)C(=O)-C1~6アルキル基(前記-NRaRb基、(RaRbN)-C1~6アルキル基、又は(RaRbN)C(=O)-C1~6アルキル基における、Ra及びRbは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)、グアニジノC1~6アルキル基、C7~16アラルキル基、ヒドロキシC6~10アリールC1~6アルキル基、又はヘテロアリールC1~6アルキル基から選択される基で複数個(例えば、1~10個、又は1~5個)置き換えられても良く;式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の2つの水素原子がC1~6アルキル基に置き換えられる場合、当該各C1~6アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することによりC3~8シクロアルキル環を形成しても良く;式(AL-3)又は式(AL-4)中の-NH-基は、隣接する炭素原子に置換する前記置換基と共に、非芳香族複素環を形成しても良い)]で表される光反応性基が導入された、アルギン酸誘導体。
尚、特に断りのない限り、態様[1]の下位の態様における各基についても、態様[1]中の各基の定義と同じものとする。
本明細書中、特に断りのない限り、前記「5~6員ヘテロアリール基」としては、例えば、ピロリル、フリル、チエニル、イミダゾリル、ピラゾリル、オキサゾリル、イソキサゾリル、チアゾリル、イソチアゾリル、1,2,3-トリアゾリル、1,2,4-トリアゾリル、1,2,3-オキサジアゾリル、1,2,4-オキサジアゾリル、1,3,4-オキサジアゾリル、フラザニル、1,2,3-チアジアゾリル、1,2,4-チアジアゾリル、1,3,4-チアジアゾリル、テトラゾリル、ピリジル、ピリダジニル、ピリミジニル、ピラジニル、1,2,3-トリアジニル、1,2,4-トリアジニル、1,3,5-トリアジニル、2H-1,2,3-チアジアジニル、4H-1,2,4-チアジアジニル、6H-1,3,4-チアジアジニル、ピリダジン-3(2H)-オン、ピリミジン-2(1H)-オン、ピラジン-2(1H)-オン、又はピリジン-2(1H)-オン等の基が挙げられる。
本明細書中、特に断りのない限り、「3~14員の飽和もしくは不飽和の非芳香族複素環基」とは、酸素原子、硫黄原子及び窒素原子から選ばれるヘテロ原子を1~4個含有する3~14員の飽和もしくは不飽和の複素環から、任意の水素原子を除いてできる1価の基を意味する。
本明細書中、特に断りのない限り、「非芳香族複素環基」としては、例えば、アジリジニル、アゼチジニル、オキシラニル、チイラニル、オキセタニル、チエタニル、ピロリジニル、テトラヒドロフリル、ジヒドロフリル、チオラニル、ピラゾリニル、ピラゾリジニル、イミダゾリジニル、ピペリジニル、ジヒドロピラニル、テトラヒドロピラニル(2-テトラヒドロ-2H-ピラニル、3-テトラヒドロ-2H-ピラニル、4-テトラヒドロ-2H-ピラニル(4-テトラヒドロ-2H-ピラン-4-イル基))、テトラヒドロチオピラニル、ピペラジニル、ジオキサニル、オキサゾリジニル、イソキサゾリニル、1,3-オキサゾリジニル、イソキサゾリジニル、チアゾリニル、イソチアゾリニル、1,3-チアゾリジニル、イソチアゾリジニル、オキサジアゾリニル、1,3,4-オキサジアゾリジニル、モルホリニル、チオモルホリニル、キヌクリジニル、アゼパニル、ジアゼピニル、又はオキセパニル等の基が挙げられる。
本明細書中、特に断りのない限り、「ハロゲン化C1~6アルキル基」等における「ハロゲン化」とは、置換基として数個の、好ましくは1~5個の前記「ハロゲン原子」を有することを意味する。
Arは、例えば、フェニル基、4-フルオロフェニル基、4-(トリフルオロメチル)フェニル基、4-メトキシフェニル基、4-シアノフェニル基、2,3-ジヒドロベンゾ[b][1,4]ジオキシニル基、又は2-ピリジル基、等である。
Arは、例えば、フェニル基、4-フルオロフェニル基、4-(トリフルオロメチル)フェニル基、4-メトキシフェニル基、3,4-ジメトキシフェニル基、4-(N-アセチルアミノ)フェニル基、4-シアノフェニル基、2,3-ジヒドロベンゾ[b][1,4]ジオキシニル基、2-ピリジル基、又は2-メトキシ-5-ピリジル基、等である。
Arは、例えば、フェニル基、4-メトキシフェニル基、3,4-ジメトキシフェニル基、4-シアノフェニル基、4-(N-アセチルアミノ)フェニル基、2,3-ジヒドロベンゾ[b][1,4]ジオキシニル基、2-ピリジル基、又は2-メトキシ-5-ピリジル基、等である。
Arは、例えば、フェニル基、4-フルオロフェニル基、又は4-(トリフルオロメチル)フェニル基、等である。
Arは、例えば、フェニル基、4-メトキシフェニル基、4-シアノフェニル基、2,3-ジヒドロベンゾ[b][1,4]ジオキシニル基、又は2-ピリジル基、等である。
Arは、例えば、4-シアノフェニル基、4-メトキシフェニル基、3,4-ジメトキシフェニル基、4-(N-アセチルアミノ)フェニル基、2,3-ジヒドロベンゾ[b][1,4]ジオキシニル基、又は2-メトキシ-5-ピリジル基、等である。
Arは、C6~10アリール基、又はヘテロアリール基(前記C6~10アリール基、又はヘテロアリール基は、ヒドロキシル基、シアノ基、ニトロ基、ハロゲン原子、C1~6アルキル基、ハロゲン化C1~6アルキル基、C1~6アルコキシ基、及び-NRARB基(-NRARB基における、RA及びRBは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、前記C6~10アリール基又はヘテロアリール基に、C1~6アルキル基及びC1~6アルコキシ基が又は2つのC1~6アルコキシ基が隣接して置換する場合、当該C1~6アルキル基及びC1~6アルコキシ基の各基のアルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、又は、当該2つのC1~6アルコキシ基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、環状エーテルを形成しても良く、又は、前記C6~10アリール基又はヘテロアリール基に、C1~6アルコキシ基及び-NHRG基(-NHRG基におけるRGは、C2~7アルカノイル基又はC1~6アルキルスルホニル基である)が隣接して置換している場合、当該C1~6アルコキシ基のアルキル基から任意の水素原子が1つ除かれた炭素原子と当該-NHRG基の水素原子が1つ除かれた窒素原子が結合することにより、3-N-(C2~7アルカノイル)オキサゾリジン環、3-N-(C1~6アルキルスルホニル)オキサゾリジン環、4-N-(C2~7アルカノイル)モルホリン環、4-N-(C1~6アルキルスルホニル)モルホリン環、4-N-(C2~7アルカノイル)-1,4-オキサゼパン環、又は4-N-(C1~6アルキルスルホニル)-1,4-オキサゼパン環を形成しても良い)であり;
pは、1、又は2の整数であり;
-X-は、-O-、又は-NH-であり;
-A-は、前記態様[1-3]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、1~10の整数であり;式(AL-2)中のmは、1~7の整数であり;
式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の水素原子は、ハロゲン原子、水酸基、C1~6アルキル基、ヒドロキシC1~6アルキル基、チオールC1~6アルキル基、C1~6アルキルチオC1~6アルキル基、カルボキシC1~6アルキル基、-NRaRb基、(RaRbN)-C1~6アルキル基、(RaRbN)C(=O)-C1~6アルキル基(前記-NRaRb基、(RaRbN)-C1~6アルキル基、又は(RaRbN)C(=O)-C1~6アルキル基における、Ra及びRbは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)、グアニジノC1~6アルキル基、C7~16アラルキル基、ヒドロキシC6~10アリールC1~6アルキル基、又はヘテロアリールC1~6アルキル基から選択される基で複数個(例えば、1~10個、又は1~5個)置き換えられても良く;式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の2つの水素原子がC1~6アルキル基に置き換えられた場合、当該各C1~6アルキル基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することによりC3~8シクロアルキル環を形成しても良い)である。
pは、1の整数であり;
-X-は、-O-、又は-NH-であり;
-A-は、前記態様[1-3]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、1~10の整数であり;式(AL-2)中のmは、1~7の整数であり;
式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の水素原子は、ハロゲン原子、水酸基、C1~6アルキル基、ヒドロキシC1~6アルキル基、チオールC1~6アルキル基、C1~6アルキルチオC1~6アルキル基、カルボキシC1~6アルキル基、-NRaRb基、(RaRbN)-C1~6アルキル基、(RaRbN)C(=O)-C1~6アルキル基(前記-NRaRb基、(RaRbN)-C1~6アルキル基、又は(RaRbN)C(=O)-C1~6アルキル基における、Ra及びRbは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)、グアニジノC1~6アルキル基、C7~16アラルキル基、ヒドロキシC6~10アリールC1~6アルキル基、又はヘテロアリールC1~6アルキル基から選択される基で複数個(例えば、1~10個、又は1~5個)置き換えられても良く;式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の2つの水素原子がC1~6アルキル基に置き換えられた場合、当該各C1~6アルキル基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することによりC3~8シクロアルキル環を形成しても良い)である。
pは、1、又は2の整数であり;
-X-は、-O-であり;
-A-は、前記態様[1-3]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、1~10の整数であり;式(AL-2)中のmは、1~7の整数であり;
式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の水素原子は、ハロゲン原子、水酸基、C1~6アルキル基、ヒドロキシC1~6アルキル基、チオールC1~6アルキル基、C1~6アルキルチオC1~6アルキル基、カルボキシC1~6アルキル基、-NRaRb基、(RaRbN)-C1~6アルキル基、(RaRbN)C(=O)-C1~6アルキル基(前記-NRaRb基、(RaRbN)-C1~6アルキル基、又は(RaRbN)C(=O)-C1~6アルキル基における、Ra及びRbは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)、グアニジノC1~6アルキル基、C7~16アラルキル基、ヒドロキシC6~10アリールC1~6アルキル基、又はヘテロアリールC1~6アルキル基から選択される基で複数個(例えば、1~10個、又は1~5個)置き換えられても良く;式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の2つの水素原子がC1~6アルキル基に置き換えられた場合、当該各C1~6アルキル基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することによりC3~8シクロアルキル環を形成しても良い)である。
pは、1、又は2の整数であり;
-X-は、-O-又は-NH-であり;
-A-は、前記態様[1-3]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、1~10の整数であり;式(AL-2)中のmは、1~7の整数であり;
式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の水素原子は、ハロゲン原子、水酸基、C1~6アルキル基、ヒドロキシC1~6アルキル基、チオールC1~6アルキル基、C1~6アルキルチオC1~6アルキル基、カルボキシC1~6アルキル基、-NRaRb基、(RaRbN)-C1~6アルキル基、(RaRbN)C(=O)-C1~6アルキル基(前記-NRaRb基、(RaRbN)-C1~6アルキル基、又は(RaRbN)C(=O)-C1~6アルキル基における、Ra及びRbは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)、グアニジノC1~6アルキル基、C7~16アラルキル基、ヒドロキシC6~10アリールC1~6アルキル基、又はヘテロアリールC1~6アルキル基から選択される基で複数個(例えば、1~10個、又は1~5個)置き換えられても良く;式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の2つの水素原子がC1~6アルキル基に置き換えられた場合、当該各C1~6アルキル基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することによりC3~8シクロアルキル環を形成しても良い)である。
Arは、C6~10アリール基、又は5~6員ヘテロアリール基(前記C6~10アリール基、又は5~6員ヘテロアリール基は、ヒドロキシル基、シアノ基、ニトロ基、ハロゲン原子、C1~6アルキル基、ハロゲン化C1~6アルキル基、C1~6アルコキシ基、及び-NRARB基(-NRARB基における、RA及びRBは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、前記C6~10アリール基又は5~6員ヘテロアリール基に、C1~6アルキル基及びC1~6アルコキシ基が又は2つのC1~6アルコキシ基が隣接して置換する場合、当該C1~6アルキル基及びC1~6アルコキシ基の各基のアルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、又は、当該2つのC1~6アルコキシ基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、環状エーテルを形成しても良く、又は、前記C6~10アリール基又は5~6員ヘテロアリール基に、C1~6アルコキシ基及び-NHRG基(-NHRG基におけるRGは、C2~7アルカノイル基又はC1~6アルキルスルホニル基である)が隣接して置換している場合、当該C1~6アルコキシ基のアルキル基から任意の水素原子が1つ除かれた炭素原子と当該-NHRG基の水素原子が1つ除かれた窒素原子が結合することにより、3-N-(C2~7アルカノイル)オキサゾリジン環、3-N-(C1~6アルキルスルホニル)オキサゾリジン環、4-N-(C2~7アルカノイル)モルホリン環、4-N-(C1~6アルキルスルホニル)モルホリン環、4-N-(C2~7アルカノイル)-1,4-オキサゼパン環、又は4-N-(C1~6アルキルスルホニル)-1,4-オキサゼパン環を形成しても良い)であり;
pは、1又は2の整数であり;
-X-は、-O-、又は-NH-であり;
-A-は、前記態様[1-3]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、1~8の整数であり;式(AL-2)中のmは、1~5の整数であり;
式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の水素原子は、ハロゲン原子、水酸基、C1~6アルキル基、ヒドロキシC1~6アルキル基、-NRaRb基(-NRaRb基における、Ra及びRbは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)、C7~16アラルキル基、又はヘテロアリールC1~6アルキル基から選択される基で複数個(例えば、1~10個、又は1~5個)置き換えられても良く;式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の2つの水素原子がC1~6アルキル基に置き換えられる場合、当該各C1~6アルキル基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することによりC3~8シクロアルキル環を形成しても良い)である。
Arは、C6~10アリール基、又は5~6員ヘテロアリール基(前記C6~10アリール基、又は5~6員ヘテロアリール基は、ヒドロキシル基、シアノ基、ニトロ基、ハロゲン原子、C1~6アルキル基、ハロゲン化C1~6アルキル基、C1~6アルコキシ基、及び-NRARB基(-NRARB基における、RA及びRBは、各々独立して、水素原子、又はC1~6アルキル基から選択される基であり)から任意に選ばれる1~3個の基が環上の水素原子と置換しても良い)であり;
pは、1の整数であり;
-X-は、-O-、又は-NH-であり;
-A-は、前記態様[1-3]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、1~8の整数であり;式(AL-2)中のmは、1~5の整数であり;
式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の水素原子は、ハロゲン原子、水酸基、C1~6アルキル基、ヒドロキシC1~6アルキル基、-NRaRb基(-NRaRb基における、Ra及びRbは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)、C7~16アラルキル基、又はヘテロアリールC1~6アルキル基から選択される基で複数個(例えば、1~10個、又は1~5個)置き換えられても良く;式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の2つの水素原子がC1~6アルキル基に置き換えられる場合、当該各C1~6アルキル基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することによりC3~8シクロアルキル環を形成しても良い)である。
Arは、C6~10アリール基、又は5~6員ヘテロアリール基(前記C6~10アリール基、又は5~6員ヘテロアリール基は、ヒドロキシル基、シアノ基、ニトロ基、ハロゲン原子、C1~6アルキル基、ハロゲン化C1~6アルキル基、C1~6アルコキシ基、及び-NRARB基(-NRARB基における、RA及びRBは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、前記C6~10アリール基又は5~6員ヘテロアリール基に、C1~6アルキル基及びC1~6アルコキシ基が又は2つのC1~6アルコキシ基が隣接して置換する場合、当該C1~6アルキル基及びC1~6アルコキシ基の各基のアルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、又は、当該2つのC1~6アルコキシ基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、環状エーテルを形成しても良く、又は、前記C6~10アリール基又は5~6員ヘテロアリール基に、C1~6アルコキシ基及び-NHRG基(-NHRG基におけるRGは、C2~7アルカノイル基又はC1~6アルキルスルホニル基である)が隣接して置換している場合、当該C1~6アルコキシ基のアルキル基から任意の水素原子が1つ除かれた炭素原子と当該-NHRG基の水素原子が1つ除かれた窒素原子が結合することにより、3-N-(C2~7アルカノイル)オキサゾリジン環、3-N-(C1~6アルキルスルホニル)オキサゾリジン環、4-N-(C2~7アルカノイル)モルホリン環、4-N-(C1~6アルキルスルホニル)モルホリン環、4-N-(C2~7アルカノイル)-1,4-オキサゼパン環、又は4-N-(C1~6アルキルスルホニル)-1,4-オキサゼパン環を形成しても良い)であり;
pは、1又は2の整数であり;
-X-は、-O-であり;
-A-は、前記態様[1-3]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、1~8の整数であり;式(AL-2)中のmは、1~5の整数であり;
式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の水素原子は、ハロゲン原子、水酸基、C1~6アルキル基、ヒドロキシC1~6アルキル基、-NRaRb基(-NRaRb基における、Ra及びRbは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)、C7~16アラルキル基、又はヘテロアリールC1~6アルキル基から選択される基で複数個(例えば、1~10個、又は1~5個)置き換えられても良く;式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の2つの水素原子がC1~6アルキル基に置き換えられる場合、当該各C1~6アルキル基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することによりC3~8シクロアルキル環を形成しても良い)である。
Arは、C6~10アリール基、又は5~6員ヘテロアリール基(前記C6~10アリール基、又は5~6員ヘテロアリール基は、ヒドロキシル基、シアノ基、ニトロ基、ハロゲン原子、C1~6アルキル基、ハロゲン化C1~6アルキル基、C1~6アルコキシ基、及び-NRARB基(-NRARB基における、RA及びRBは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、前記C6~10アリール基又は5~6員ヘテロアリール基に、C1~6アルキル基及びC1~6アルコキシ基が又は2つのC1~6アルコキシ基が隣接して置換する場合、当該C1~6アルキル基及びC1~6アルコキシ基の各基のアルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、又は、当該2つのC1~6アルコキシ基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、環状エーテルを形成しても良く、又は、前記C6~10アリール基又は5~6員ヘテロアリール基に、C1~6アルコキシ基及び-NHRG基(-NHRG基におけるRGは、C2~7アルカノイル基又はC1~6アルキルスルホニル基である)が隣接して置換している場合、当該C1~6アルコキシ基のアルキル基から任意の水素原子が1つ除かれた炭素原子と当該-NHRG基の水素原子が1つ除かれた窒素原子が結合することにより、3-N-(C2~7アルカノイル)オキサゾリジン環、3-N-(C1~6アルキルスルホニル)オキサゾリジン環、4-N-(C2~7アルカノイル)モルホリン環、4-N-(C1~6アルキルスルホニル)モルホリン環、4-N-(C2~7アルカノイル)-1,4-オキサゼパン環、又は4-N-(C1~6アルキルスルホニル)-1,4-オキサゼパン環を形成しても良い)であり;
pは、1又は2の整数であり;
-X-は、-O-又は-NH-であり;
-A-は、前記態様[1-3]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、1~8の整数であり;式(AL-2)中のmは、1~5の整数であり;
式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の水素原子は、ハロゲン原子、水酸基、C1~6アルキル基、ヒドロキシC1~6アルキル基、-NRaRb基(-NRaRb基における、Ra及びRbは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)、C7~16アラルキル基、又はヘテロアリールC1~6アルキル基から選択される基で複数個(例えば、1~10個、又は1~5個)置き換えられても良く;式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の2つの水素原子がC1~6アルキル基に置き換えられる場合、当該各C1~6アルキル基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することによりC3~8シクロアルキル環を形成しても良い)である。
Arは、フェニル基、又はピリジル基(前記フェニル基、又はピリジル基は、ヒドロキシル基、シアノ基、ニトロ基、ハロゲン原子、C1~6アルキル基、ハロゲン化C1~6アルキル基、C1~6アルコキシ基、及び-NRARB基(-NRARB基における、RA及びRBは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、前記フェニル基又はピリジル基に、C1~6アルキル基及びC1~6アルコキシ基が又は2つのC1~6アルコキシ基が隣接して置換する場合、当該C1~6アルキル基及びC1~6アルコキシ基の各基のアルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、又は、当該2つのC1~6アルコキシ基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、環状エーテルを形成しても良く、又は、前記フェニル基又はピリジル基に、C1~6アルコキシ基及び-NHRG基(-NNHRG基におけるRGは、C2~7アルカノイル基又はC1~6アルキルスルホニル基である)が隣接して置換している場合、当該C1~6アルコキシ基のアルキル基から任意の水素原子が1つ除かれた炭素原子と当該-NHRG基の水素原子が1つ除かれた窒素原子が結合することにより、3-N-(C2~7アルカノイル)オキサゾリジン環、3-N-(C1~6アルキルスルホニル)オキサゾリジン環、4-N-(C2~7アルカノイル)モルホリン環、4-N-(C1~6アルキルスルホニル)モルホリン環、4-N-(C2~7アルカノイル)-1,4-オキサゼパン環、又は4-N-(C1~6アルキルスルホニル)-1,4-オキサゼパン環を形成しても良い)であり;
pは、1又は2の整数であり;
-X-は、-O-、又は-NH-であり:
-A-は、前記態様[1-3]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、2~6の整数であり;式(AL-2)中のmは、1~3の整数である)である。
Arは、フェニル基(前記フェニル基は、ヒドロキシル基、シアノ基、ニトロ基、ハロゲン原子、C1~6アルキル基、ハロゲン化C1~6アルキル基、C1~6アルコキシ基、及び-NRARB基(-NRARB基における、RA及びRBは、各々独立して、水素原子、又はC1~6アルキル基から選択される基であり)から任意に選ばれる1~3個の基が環上の水素原子と置換しても良い)であり;
pは、1の整数であり;
-X-は、-O-、又は-NH-であり:
-A-は、前記態様[1-3]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、2~6の整数であり;式(AL-2)中のmは、1~3の整数である)である。
Arは、フェニル基、又はピリジル基(前記フェニル基、又はピリジル基は、ヒドロキシル基、シアノ基、ニトロ基、ハロゲン原子、C1~6アルキル基、ハロゲン化C1~6アルキル基、C1~6アルコキシ基、及び-NRARB基(-NRARB基における、RA及びRBは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、前記フェニル基又はピリジル基に、C1~6アルキル基及びC1~6アルコキシ基が又は2つのC1~6アルコキシ基が隣接して置換する場合、当該C1~6アルキル基及びC1~6アルコキシ基の各基のアルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、又は、当該2つのC1~6アルコキシ基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、環状エーテルを形成しても良く、又は、前記フェニル基又はピリジル基に、C1~6アルコキシ基及び-NHRG基(-NHRG基におけるRGは、C2~7アルカノイル基又はC1~6アルキルスルホニル基である)が隣接して置換している場合、当該C1~6アルコキシ基のアルキル基から任意の水素原子が1つ除かれた炭素原子と当該-NHRG基の水素原子が1つ除かれた窒素原子が結合することにより、3-N-(C2~7アルカノイル)オキサゾリジン環、3-N-(C1~6アルキルスルホニル)オキサゾリジン環、4-N-(C2~7アルカノイル)モルホリン環、4-N-(C1~6アルキルスルホニル)モルホリン環、4-N-(C2~7アルカノイル)-1,4-オキサゼパン環、又は4-N-(C1~6アルキルスルホニル)-1,4-オキサゼパン環を形成しても良い)であり;
pは、1又は2の整数であり;
-X-は、-O-であり:
-A-は、前記態様[1-3]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、2~6の整数であり;式(AL-2)中のmは、1~3の整数である)である。
Arは、フェニル基、又はピリジル基(前記フェニル基、又はピリジル基は、ヒドロキシル基、シアノ基、ニトロ基、ハロゲン原子、C1~6アルキル基、ハロゲン化C1~6アルキル基、C1~6アルコキシ基、及び-NRARB基(-NRARB基における、RA及びRBは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、前記フェニル基又はピリジル基に、C1~6アルキル基及びC1~6アルコキシ基が又は2つのC1~6アルコキシ基が隣接して置換する場合、当該C1~6アルキル基及びC1~6アルコキシ基の各基のアルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、又は、当該2つのC1~6アルコキシ基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、環状エーテルを形成しても良く、又は、前記フェニル基又はピリジル基に、C1~6アルコキシ基及び-NHRG基(-NHRG基におけるRGは、C2~7アルカノイル基又はC1~6アルキルスルホニル基である)が隣接して置換している場合、当該C1~6アルコキシ基のアルキル基から任意の水素原子が1つ除かれた炭素原子と当該-NHRG基の水素原子が1つ除かれた窒素原子が結合することにより、3-N-(C2~7アルカノイル)オキサゾリジン環、3-N-(C1~6アルキルスルホニル)オキサゾリジン環、4-N-(C2~7アルカノイル)モルホリン環、4-N-(C1~6アルキルスルホニル)モルホリン環、4-N-(C2~7アルカノイル)-1,4-オキサゼパン環、又は4-N-(C1~6アルキルスルホニル)-1,4-オキサゼパン環を形成しても良い)であり;
pは、1又は2の整数であり;
-X-は、-O-又は-NH-であり:
-A-は、前記態様[1-3]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、2~6の整数であり;式(AL-2)中のmは、1~3の整数である)である。
Arは、フェニル基、又は2-ピリジル基(前記フェニル基、又は2-ピリジル基は、シアノ基、フッ素原子、トリフルオロメチル基、及びメトキシ基から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、フェニル基又は2-ピリジル基上に、2つのメトキシ基が隣接して置換している場合には、2つのメトキシ基の各基のメチル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより1,4-ジオキサン環を形成しても良い)であり;
Ar、p、-X-、-A-の組み合わせとしては、例えば、Arは、フェニル基、4-フルオロフェニル基、4-(トリフルオロメチル)フェニル基、4-メトキシフェニル基、4-シアノフェニル基、2,3-ジヒドロベンゾ[b][1,4]ジオキシニル基、又は2-ピリジル基であり;
pは、1又は2の整数であり;
-X-は、-O-、又は-NH-であり:
-A-は、前記態様[1-3]中の式(AL-1-1)、(AL-2-1)又は(AL-2-2)[各式中、両端の波線外側は含まない]であり;
例えば、Ar、p、-X-、-A-の組み合わせは、下記部分構造式[各式中、波線右側は含まない]:
Arは、フェニル基、2-ピリジル基、又は5-ピリジル基(前記フェニル基、2-ピリジル基、又は5-ピリジル基は、シアノ基、フッ素原子、トリフルオロメチル基、メトキシ基、及びN-アセチルアミノ基から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、フェニル基、2-ピリジル基、又は5-ピリジル基上に、2つのメトキシ基が隣接して置換している場合には、2つのメトキシ基の各基のメチル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより1,4-ジオキサン環を形成しても良い)であり;
Ar、p、-X-、-A-の組み合わせとしては、例えば、Arは、フェニル基、4-フルオロフェニル基、4-(トリフルオロメチル)フェニル基、4-メトキシフェニル基、3,4-ジメトキシフェニル基、4-(N-アセチルアミノ)フェニル基、4-シアノフェニル基、2,3-ジヒドロベンゾ[b][1,4]ジオキシニル基、2-ピリジル基、又は2-メトキシ-5-ピリジル基であり;
pは、1又は2の整数であり;
-X-は、-O-、又は-NH-であり:
-A-は、前記態様[1-3]中の式(AL-1-1)、(AL-2-1)又は(AL-2-2)[各式中、両端の波線外側は含まない]であり;
例えば、Ar、p、-X-、-A-の組み合わせは、下記部分構造式[各式中、波線右側は含まない]:
Arは、フェニル基、2-ピリジル基、又は5-ピリジル基(前記フェニル基、2-ピリジル基、又は5-ピリジル基は、シアノ基、メトキシ基、及びN-アセチルアミノ基から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、フェニル基、2-ピリジル基、又は5-ピリジル基上に、2つのメトキシ基が隣接して置換している場合には、2つのメトキシ基の各基のメチル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより1,4-ジオキサン環を形成しても良い)であり;
Ar、p、-X-、-A-の組み合わせとしては、例えば、Arは、フェニル基、4-メトキシフェニル基、3,4-ジメトキシフェニル基、4-(N-アセチルアミノ)フェニル基、4-シアノフェニル基、2,3-ジヒドロベンゾ[b][1,4]ジオキシニル基、2-ピリジル基、又は2-メトキシ-5-ピリジル基であり;
pは、1又は2の整数であり;
-X-は、-O-、又は-NH-であり:
-A-は、前記態様[1-3]中の式(AL-1-1)、(AL-2-1)又は(AL-2-2)[各式中、両端の波線外側は含まない]であり;
例えば、Ar、p、-X-、-A-の組み合わせは、下記部分構造式[各式中、波線右側は含まない]:
Ar、p、-X-、-A-の組み合わせとしては、Arは、例えば、フェニル基、4-フルオロフェニル基、又は4-(トリフルオロメチル)フェニル基であり;
pは、1の整数であり;
-X-は、-O-、又は-NH-であり:
-A-は、前記態様[1-3]中の式(AL-1-1)、(AL-2-1)又は(AL-2-2)[各式中、両端の波線外側は含まない]であり;
例えば、Ar、p、-X-、-A-の組み合わせは、下記部分構造式[各式中、波線右側は含まない]:
Arは、フェニル基、又は2-ピリジル基(前記フェニル基、又は2-ピリジル基は、シアノ基、及びメトキシ基から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、フェニル基又は2-ピリジル基上に、2つのメトキシ基が隣接して置換している場合には、2つのメトキシ基の各基のメチル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより1,4-ジオキサン環を形成しても良い)であり;
Ar、p、-X-、-A-の組み合わせとしては、例えば、Arは、例えば、フェニル基、4-メトキシフェニル基、4-シアノフェニル基、2,3-ジヒドロベンゾ[b][1,4]ジオキシニル基、又は2-ピリジル基であり;
pは、1又は2の整数であり;
-X-は、-O-であり:
-A-は、前記態様[1-3]中の式(AL-1-1)、又は(AL-2-1)[各式中、両端の波線外側は含まない]であり;
例えば、Ar、p、-X-、-A-の組み合わせは、下記部分構造式[各式中、波線右側は含まない]:
Ar、p、-X-、-A-の組み合わせとしては、例えば、 Arは、4-シアノフェニル基、4-メトキシフェニル基、3,4-ジメトキシフェニル基、4-(N-アセチルアミノ)フェニル基、2,3-ジヒドロベンゾ[b][1,4]ジオキシニル基、又は2-メトキシ-5-ピリジル基であり;
pは、1又は2の整数であり;
-X-は、-O-又は-NH-であり:
-A-は、前記態様[1-3]中の式(AL-2-1)、又は(AL-2-2)[各式中、両端の波線外側は含まない]であり;
例えば、Ar、p、-X-、-A-の組み合わせは、下記部分構造式[各式中、波線右側は含まない]:
Arは、C6~10アリール基、又は複素環基(前記C6~10アリール基、又は複素環基は、ヒドロキシル基、シアノ基、ニトロ基、ハロゲン原子、C1~6アルキル基、ハロゲン化C1~6アルキル基、C1~6アルコキシ基、及び-NRARB基(-NRARB基における、RA及びRBは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり(但し、-NH2、-NH(C1~6アルキル基)、及び-N(C1~6アルキル基)2は除く))から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、前記C6~10アリール基又は複素環基に、C1~6アルキル基及びC1~6アルコキシ基が又は2つのC1~6アルコキシ基が隣接して置換する場合、当該C1~6アルキル基及びC1~6アルコキシ基の各基のアルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、又は、当該2つのC1~6アルコキシ基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、環状エーテルを形成しても良く、又は、前記C6~10アリール基又は複素環基に、C1~6アルコキシ基及び-NHRG基(-NHRG基におけるRGは、C2~7アルカノイル基又はC1~6アルキルスルホニル基である)が隣接して置換している場合、当該C1~6アルコキシ基のアルキル基から任意の水素原子が1つ除かれた炭素原子と当該-NHRG基の水素原子が1つ除かれた窒素原子が結合することにより、3-N-(C2~7アルカノイル)オキサゾリジン環、3-N-(C1~6アルキルスルホニル)オキサゾリジン環、4-N-(C2~7アルカノイル)モルホリン環、4-N-(C1~6アルキルスルホニル)モルホリン環、4-N-(C2~7アルカノイル)-1,4-オキサゼパン環、又は4-N-(C1~6アルキルスルホニル)-1,4-オキサゼパン環を形成しても良い)を表わし;
pは、1、又は2の整数を表わし;
-X-は、-O-、-NH-、又は-N(C1-6アルキル)-を表わし;
-A-は、式(AL-1)~(AL-4)[各式中、両端の波線外側は含まない]:
式(AL-1)~(AL-4)中のメチレン基(-CH2-)の水素原子は、ハロゲン原子、水酸基、C1~6アルキル基、ヒドロキシC1~6アルキル基、チオールC1~6アルキル基、C1~6アルキルチオC1~6アルキル基、カルボキシC1~6アルキル基、-NRaRb基、(RaRbN)-C1~6アルキル基、(RaRbN)C(=O)-C1~6アルキル基(前記-NRaRb基、(RaRbN)-C1~6アルキル基、又は(RaRbN)C(=O)-C1~6アルキル基における、Ra及びRbは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)、グアニジノC1~6アルキル基、C7~16アラルキル基、ヒドロキシC6~10アリールC1~6アルキル基、又はヘテロアリールC1~6アルキル基から選択される基で複数個(例えば、1~10個、又は1~5個)置き換えられても良く;式(AL-1)~(AL-4)中のメチレン基(-CH2-)の2つの水素原子がC1~6アルキル基に置き換えられた場合、当該各C1~6アルキル基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することによりC3~8シクロアルキル環を形成しても良く;式(AL-3)又は式(AL-4)中の-NH-基は、隣接する炭素原子に置換する前記置換基と共に、非芳香族複素環を形成しても良い)](但し、式(I)において、Ar=フェニル基、p=1、-A-=式(AL-1)、かつn=3の場合、当該Arのフェニル基では前記Ar環上の水素原子と置換しても良い置換基群から任意に選ばれる1~3個の基が前記フェニル基上の水素原子と置換する)で表される光反応性基が導入された、アルギン酸誘導体である。
前記C6~10アリール基又は5~6員ヘテロアリール基に、C1~6アルキル基及びC1~6アルコキシ基が又は2つのC1~6アルコキシ基が隣接して置換する場合、当該C1~6アルキル基及びC1~6アルコキシ基の各基のアルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、又は、当該2つのC1~6アルコキシ基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、環状エーテルを形成しても良く;
又は、前記C6~10アリール基又は5~6員ヘテロアリール基に、C1~6アルコキシ基及び-NHRG基(-NHRG基におけるRGは、C2~7アルカノイル基又はC1~6アルキルスルホニル基である)が隣接して置換している場合、当該C1~6アルコキシ基のアルキル基から任意の水素原子が1つ除かれた炭素原子と当該-NHRG基の水素原子が1つ除かれた窒素原子が結合することにより、3-N-(C2~7アルカノイル)オキサゾリジン環、3-N-(C1~6アルキルスルホニル)オキサゾリジン環、4-N-(C2~7アルカノイル)モルホリン環、4-N-(C1~6アルキルスルホニル)モルホリン環、4-N-(C2~7アルカノイル)-1,4-オキサゼパン環、又は4-N-(C1~6アルキルスルホニル)-1,4-オキサゼパン環を形成しても良い)(但し、式(I)において、Ar=フェニル基、p=1、-A-=式(AL-1)、かつn=3の場合、当該Arのフェニル基では前記Ar環上の水素原子と置換しても良い置換基群から任意に選ばれる1~3個の基が前記フェニル基上の水素原子と置換する)であり;
Arは、例えば、フェニル基、4-フルオロフェニル基、4-(トリフルオロメチル)フェニル基、4-メトキシフェニル基、3,4-ジメトキシフェニル基、4-(N-アセチルアミノ)フェニル基、4-シアノフェニル基、2,3-ジヒドロベンゾ[b][1,4]ジオキシニル基、2-ピリジル基、又は2-メトキシ-5-ピリジル基、等である。
Arは、例えば、フェニル基、4-メトキシフェニル基、3,4-ジメトキシフェニル基、4-シアノフェニル基、4-(N-アセチルアミノ)フェニル基、2,3-ジヒドロベンゾ[b][1,4]ジオキシニル基、2-ピリジル基、又は2-メトキシ-5-ピリジル基、等である。
Arは、例えば、4-シアノフェニル基、4-メトキシフェニル基、3,4-ジメトキシフェニル基、4-(N-アセチルアミノ)フェニル基、2,3-ジヒドロベンゾ[b][1,4]ジオキシニル基、又は2-メトキシ-5-ピリジル基、等である。
Arは、C6~10アリール基、又はヘテロアリール基(前記C6~10アリール基、又はヘテロアリール基は、ヒドロキシル基、シアノ基、ニトロ基、ハロゲン原子、C1~6アルキル基、ハロゲン化C1~6アルキル基、C1~6アルコキシ基、及び-NRARB基(-NRARB基における、RA及びRBは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり(但し、-NH2、-NH(C1~6アルキル基)、及び-N(C1~6アルキル基)2は除く))から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、前記C6~10アリール基又はヘテロアリール基に、C1~6アルキル基及びC1~6アルコキシ基が又は2つのC1~6アルコキシ基が隣接して置換する場合、当該C1~6アルキル基及びC1~6アルコキシ基の各基のアルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、又は、当該2つのC1~6アルコキシ基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、環状エーテルを形成しても良く、又は、前記C6~10アリール基又はヘテロアリール基に、C1~6アルコキシ基及び-NHRG基(-NHRG基におけるRGは、C2~7アルカノイル基又はC1~6アルキルスルホニル基である)が隣接して置換している場合、当該C1~6アルコキシ基のアルキル基から任意の水素原子が1つ除かれた炭素原子と当該-NHRG基の水素原子が1つ除かれた窒素原子が結合することにより、3-N-(C2~7アルカノイル)オキサゾリジン環、3-N-(C1~6アルキルスルホニル)オキサゾリジン環、4-N-(C2~7アルカノイル)モルホリン環、4-N-(C1~6アルキルスルホニル)モルホリン環、4-N-(C2~7アルカノイル)-1,4-オキサゼパン環、又は4-N-(C1~6アルキルスルホニル)-1,4-オキサゼパン環を形成しても良い)であり;
pは、1、又は2の整数であり;
-X-は、-O-、又は-NH-であり;
-A-は、前記態様[1a-3]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、1~10の整数であり;式(AL-2)中のmは、1~7の整数であり)であり;
式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の水素原子は、ハロゲン原子、水酸基、C1~6アルキル基、ヒドロキシC1~6アルキル基、チオールC1~6アルキル基、C1~6アルキルチオC1~6アルキル基、カルボキシC1~6アルキル基、-NRaRb基、(RaRbN)-C1~6アルキル基、(RaRbN)C(=O)-C1~6アルキル基(前記-NRaRb基、(RaRbN)-C1~6アルキル基、又は(RaRbN)C(=O)-C1~6アルキル基における、Ra及びRbは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)、グアニジノC1~6アルキル基、C7~16アラルキル基、ヒドロキシC6~10アリールC1~6アルキル基、又はヘテロアリールC1~6アルキル基から選択される基で複数個(例えば、1~10個、又は1~5個)置き換えられても良く;式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の2つの水素原子がC1~6アルキル基に置き換えられた場合、当該各C1~6アルキル基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することによりC3~8シクロアルキル環を形成しても良い)(但し、式(I)において、Ar=フェニル基、p=1、-A-=式(AL-1)、かつn=3の場合、当該Arのフェニル基では前記Ar環上の水素原子と置換しても良い置換基群から任意に選ばれる1~3個の基が前記フェニル基上の水素原子と置換する)である。
pは、1の整数であり;
-X-は、-O-、又は-NH-であり;
-A-は、前記態様[1a-3]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、1~10の整数であり;式(AL-2)中のmは、1~7の整数であり;
式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の水素原子は、ハロゲン原子、水酸基、C1~6アルキル基、ヒドロキシC1~6アルキル基、チオールC1~6アルキル基、C1~6アルキルチオC1~6アルキル基、カルボキシC1~6アルキル基、-NRaRb基、(RaRbN)-C1~6アルキル基、(RaRbN)C(=O)-C1~6アルキル基(前記-NRaRb基、(RaRbN)-C1~6アルキル基、又は(RaRbN)C(=O)-C1~6アルキル基における、Ra及びRbは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)、グアニジノC1~6アルキル基、C7~16アラルキル基、ヒドロキシC6~10アリールC1~6アルキル基、又はヘテロアリールC1~6アルキル基から選択される基で複数個(例えば、1~10個、又は1~5個)置き換えられても良く;式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の2つの水素原子がC1~6アルキル基に置き換えられた場合、当該各C1~6アルキル基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することによりC3~8シクロアルキル環を形成しても良い)(但し、式(I)において、Ar=フェニル基、p=1、-A-=式(AL-1)、かつn=3の場合、当該Arのフェニル基では前記Ar環上の水素原子と置換しても良い置換基群から任意に選ばれる1~3個の基が前記フェニル基上の水素原子と置換する)である。
pは、1、又は2の整数であり;
-X-は、-O-であり;
-A-は、前記態様[1a-3]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、1~10の整数であり;式(AL-2)中のmは、1~7の整数であり;
式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の水素原子は、ハロゲン原子、水酸基、C1~6アルキル基、ヒドロキシC1~6アルキル基、チオールC1~6アルキル基、C1~6アルキルチオC1~6アルキル基、カルボキシC1~6アルキル基、-NRaRb基、(RaRbN)-C1~6アルキル基、(RaRbN)C(=O)-C1~6アルキル基(前記-NRaRb基、(RaRbN)-C1~6アルキル基、又は(RaRbN)C(=O)-C1~6アルキル基における、Ra及びRbは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)、グアニジノC1~6アルキル基、C7~16アラルキル基、ヒドロキシC6~10アリールC1~6アルキル基、又はヘテロアリールC1~6アルキル基から選択される基で複数個(例えば、1~10個、又は1~5個)置き換えられても良く;式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の2つの水素原子がC1~6アルキル基に置き換えられた場合、当該各C1~6アルキル基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することによりC3~8シクロアルキル環を形成しても良い)(但し、式(I)において、Ar=フェニル基、p=1、-A-=式(AL-1)、かつn=3の場合、当該Arのフェニル基では前記Ar環上の水素原子と置換しても良い置換基群から任意に選ばれる1~3個の基が前記フェニル基上の水素原子と置換する)である。
pは、1、又は2の整数であり;
-X-は、-O-又は-NH-であり;
-A-は、前記態様[1a-3]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、1~10の整数であり;式(AL-2)中のmは、1~7の整数であり;
式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の水素原子は、ハロゲン原子、水酸基、C1~6アルキル基、ヒドロキシC1~6アルキル基、チオールC1~6アルキル基、C1~6アルキルチオC1~6アルキル基、カルボキシC1~6アルキル基、-NRaRb基、(RaRbN)-C1~6アルキル基、(RaRbN)C(=O)-C1~6アルキル基(前記-NRaRb基、(RaRbN)-C1~6アルキル基、又は(RaRbN)C(=O)-C1~6アルキル基における、Ra及びRbは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)、グアニジノC1~6アルキル基、C7~16アラルキル基、ヒドロキシC6~10アリールC1~6アルキル基、又はヘテロアリールC1~6アルキル基から選択される基で複数個(例えば、1~10個、又は1~5個)置き換えられても良く;式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の2つの水素原子がC1~6アルキル基に置き換えられた場合、当該各C1~6アルキル基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することによりC3~8シクロアルキル環を形成しても良い)(但し、式(I)において、Ar=フェニル基、p=1、-A-=式(AL-1)、かつn=3の場合、当該Arのフェニル基では前記Ar環上の水素原子と置換しても良い置換基群から任意に選ばれる1~3個の基が前記フェニル基上の水素原子と置換する)である。
Arは、C6~10アリール基、又は5~6員ヘテロアリール基(前記C6~10アリール基、又は5~6員ヘテロアリール基は、ヒドロキシル基、シアノ基、ニトロ基、ハロゲン原子、C1~6アルキル基、ハロゲン化C1~6アルキル基、C1~6アルコキシ基、及び-NRARB基(-NRARB基における、RA及びRBは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり(但し、-NH2、-NH(C1~6アルキル基)、及び-N(C1~6アルキル基)2は除く))から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、前記C6~10アリール基又は5~6員ヘテロアリール基に、C1~6アルキル基及びC1~6アルコキシ基が又は2つのC1~6アルコキシ基が隣接して置換する場合、当該C1~6アルキル基及びC1~6アルコキシ基の各基のアルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、又は、当該2つのC1~6アルコキシ基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、環状エーテルを形成しても良く、又は、前記C6~10アリール基又は5~6員ヘテロアリール基に、C1~6アルコキシ基及び-NHRG基(-NHRG基におけるRGは、C2~7アルカノイル基又はC1~6アルキルスルホニル基である)が隣接して置換している場合、当該C1~6アルコキシ基のアルキル基から任意の水素原子が1つ除かれた炭素原子と当該-NHRG基の水素原子が1つ除かれた窒素原子が結合することにより、3-N-(C2~7アルカノイル)オキサゾリジン環、3-N-(C1~6アルキルスルホニル)オキサゾリジン環、4-N-(C2~7アルカノイル)モルホリン環、4-N-(C1~6アルキルスルホニル)モルホリン環、4-N-(C2~7アルカノイル)-1,4-オキサゼパン環、又は4-N-(C1~6アルキルスルホニル)-1,4-オキサゼパン環を形成しても良い)であり;
pは、1又は2の整数であり;
-X-は、-O-、又は-NH-であり;
-A-は、前記態様[1a-3]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、1~8の整数であり;式(AL-2)中のmは、1~5の整数であり)であり;
式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の水素原子は、ハロゲン原子、水酸基、C1~6アルキル基、ヒドロキシC1~6アルキル基、-NRaRb基(-NRaRb基における、Ra及びRbは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)、C7~16アラルキル基、又はヘテロアリールC1~6アルキル基から選択される基で複数個(例えば、1~10個、又は1~5個)置き換えられても良く;式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の2つの水素原子がC1~6アルキル基に置き換えられる場合、当該各C1~6アルキル基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することによりC3~8シクロアルキル環を形成しても良い)(但し、式(I)において、Ar=フェニル基、p=1、-A-=式(AL-1)、かつn=3の場合、当該Arのフェニル基では前記Ar環上の水素原子と置換しても良い置換基群から任意に選ばれる1~3個の基が前記フェニル基上の水素原子と置換する)である。
Arは、C6~10アリール基、又は5~6員ヘテロアリール基(前記C6~10アリール基、又は5~6員ヘテロアリール基は、ヒドロキシル基、シアノ基、ニトロ基、ハロゲン原子、C1~6アルキル基、ハロゲン化C1~6アルキル基、C1~6アルコキシ基、及び-NRARB基(-NRARB基における、RA及びRBは、各々独立して、水素原子、又はC1~6アルキル基から選択される基であり(但し、-NH2、-NH(C1~6アルキル基)、及び-N(C1~6アルキル基)2は除く))から任意に選ばれる1~3個の基が環上の水素原子と置換しても良い)であり;
pは、1の整数であり;
-X-は、-O-、又は-NH-であり;
-A-は、前記態様[1a-3]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、1~8の整数であり;式(AL-2)中のmは、1~5の整数であり;
式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の水素原子は、ハロゲン原子、水酸基、C1~6アルキル基、ヒドロキシC1~6アルキル基、-NRaRb基(-NRaRb基における、Ra及びRbは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)、C7~16アラルキル基、又はヘテロアリールC1~6アルキル基から選択される基で複数個(例えば、1~10個、又は1~5個)置き換えられても良く;式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の2つの水素原子がC1~6アルキル基に置き換えられる場合、当該各C1~6アルキル基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することによりC3~8シクロアルキル環を形成しても良い)(但し、式(I)において、Ar=フェニル基、p=1、-A-=式(AL-1)、かつn=3の場合、当該Arのフェニル基では前記Ar環上の水素原子と置換しても良い置換基群から任意に選ばれる1~3個の基が前記フェニル基上の水素原子と置換する)である。
Arは、C6~10アリール基、又は5~6員ヘテロアリール基(前記C6~10アリール基、又は5~6員ヘテロアリール基は、ヒドロキシル基、シアノ基、ニトロ基、ハロゲン原子、C1~6アルキル基、ハロゲン化C1~6アルキル基、C1~6アルコキシ基、及び-NRARB基(-NRARB基における、RA及びRBは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり(但し、-NH2、-NH(C1~6アルキル基)、及び-N(C1~6アルキル基)2は除く))から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、前記C6~10アリール基又は5~6員ヘテロアリール基に、C1~6アルキル基及びC1~6アルコキシ基が又は2つのC1~6アルコキシ基が隣接して置換する場合、当該C1~6アルキル基及びC1~6アルコキシ基の各基のアルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、又は、当該2つのC1~6アルコキシ基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、環状エーテルを形成しても良く、又は、前記C6~10アリール基又は5~6員ヘテロアリール基に、C1~6アルコキシ基及び-NHRG基(-NHRG基におけるRGは、C2~7アルカノイル基又はC1~6アルキルスルホニル基である)が隣接して置換している場合、当該C1~6アルコキシ基のアルキル基から任意の水素原子が1つ除かれた炭素原子と当該-NHRG基の水素原子が1つ除かれた窒素原子が結合することにより、3-N-(C2~7アルカノイル)オキサゾリジン環、3-N-(C1~6アルキルスルホニル)オキサゾリジン環、4-N-(C2~7アルカノイル)モルホリン環、4-N-(C1~6アルキルスルホニル)モルホリン環、4-N-(C2~7アルカノイル)-1,4-オキサゼパン環、又は4-N-(C1~6アルキルスルホニル)-1,4-オキサゼパン環を形成しても良い)であり;
pは、1又は2の整数であり;
-X-は、-O-であり;
-A-は、前記態様[1a-3]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、1~8の整数であり;式(AL-2)中のmは、1~5の整数であり;
式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の水素原子は、ハロゲン原子、水酸基、C1~6アルキル基、ヒドロキシC1~6アルキル基、-NRaRb基(-NRaRb基における、Ra及びRbは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)、C7~16アラルキル基、又はヘテロアリールC1~6アルキル基から選択される基で複数個(例えば、1~10個、又は1~5個)置き換えられても良く;式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の2つの水素原子がC1~6アルキル基に置き換えられる場合、当該各C1~6アルキル基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することによりC3~8シクロアルキル環を形成しても良い)(但し、式(I)において、Ar=フェニル基、p=1、-A-=式(AL-1)、かつn=3の場合、当該Arのフェニル基では前記Ar環上の水素原子と置換しても良い置換基群から任意に選ばれる1~3個の基が前記フェニル基上の水素原子と置換する)である。
Arは、C6~10アリール基、又は5~6員ヘテロアリール基(前記C6~10アリール基、又は5~6員ヘテロアリール基は、ヒドロキシル基、シアノ基、ニトロ基、ハロゲン原子、C1~6アルキル基、ハロゲン化C1~6アルキル基、C1~6アルコキシ基、及び-NRARB基(-NRARB基における、RA及びRBは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり(但し、-NH2、-NH(C1~6アルキル基)、及び-N(C1~6アルキル基)2は除く))から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、前記C6~10アリール基又は5~6員ヘテロアリール基に、C1~6アルキル基及びC1~6アルコキシ基が又は2つのC1~6アルコキシ基が隣接して置換する場合、当該C1~6アルキル基及びC1~6アルコキシ基の各基のアルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、又は、当該2つのC1~6アルコキシ基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、環状エーテルを形成しても良く、又は、前記C6~10アリール基又は5~6員ヘテロアリール基に、C1~6アルコキシ基及び-NHRG基(-NHRG基におけるRGは、C2~7アルカノイル基又はC1~6アルキルスルホニル基である)が隣接して置換している場合、当該C1~6アルコキシ基のアルキル基から任意の水素原子が1つ除かれた炭素原子と当該-NHRG基の水素原子が1つ除かれた窒素原子が結合することにより、3-N-(C2~7アルカノイル)オキサゾリジン環、3-N-(C1~6アルキルスルホニル)オキサゾリジン環、4-N-(C2~7アルカノイル)モルホリン環、4-N-(C1~6アルキルスルホニル)モルホリン環、4-N-(C2~7アルカノイル)-1,4-オキサゼパン環、又は4-N-(C1~6アルキルスルホニル)-1,4-オキサゼパン環を形成しても良い)であり;
pは、1又は2の整数であり;
-X-は、-O-又は-NH-であり;
-A-は、前記態様[1a-3]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、1~8の整数であり;式(AL-2)中のmは、1~5の整数であり;
式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の水素原子は、ハロゲン原子、水酸基、C1~6アルキル基、ヒドロキシC1~6アルキル基、-NRaRb基(-NRaRb基における、Ra及びRbは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)、C7~16アラルキル基、又はヘテロアリールC1~6アルキル基から選択される基で複数個(例えば、1~10個、又は1~5個)置き換えられても良く;式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の2つの水素原子がC1~6アルキル基に置き換えられる場合、当該各C1~6アルキル基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することによりC3~8シクロアルキル環を形成しても良い)(但し、式(I)において、Ar=フェニル基、p=1、-A-=式(AL-1)、かつn=3の場合、当該Arのフェニル基では前記Ar環上の水素原子と置換しても良い置換基群から任意に選ばれる1~3個の基が前記フェニル基上の水素原子と置換する)である。
Arは、フェニル基、又はピリジル基(前記フェニル基、又はピリジル基は、ヒドロキシル基、シアノ基、ニトロ基、ハロゲン原子、C1~6アルキル基、ハロゲン化C1~6アルキル基、C1~6アルコキシ基、及び-NRARB基(-NRARB基における、RA及びRBは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり(但し、-NH2、-NH(C1~6アルキル基)、及び-N(C1~6アルキル基)2は除く))から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、前記フェニル基又はピリジル基に、C1~6アルキル基及びC1~6アルコキシ基が又は2つのC1~6アルコキシ基が隣接して置換する場合、当該C1~6アルキル基及びC1~6アルコキシ基の各基のアルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、又は、当該2つのC1~6アルコキシ基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、環状エーテルを形成しても良く、又は、前記フェニル基又はピリジル基に、C1~6アルコキシ基及び-NHRG基(-NHRG基におけるRGは、C2~7アルカノイル基又はC1~6アルキルスルホニル基である)が隣接して置換している場合、当該C1~6アルコキシ基のアルキル基から任意の水素原子が1つ除かれた炭素原子と当該-NHRG基の水素原子が1つ除かれた窒素原子が結合することにより、3-N-(C2~7アルカノイル)オキサゾリジン環、3-N-(C1~6アルキルスルホニル)オキサゾリジン環、4-N-(C2~7アルカノイル)モルホリン環、4-N-(C1~6アルキルスルホニル)モルホリン環、4-N-(C2~7アルカノイル)-1,4-オキサゼパン環、又は4-N-(C1~6アルキルスルホニル)-1,4-オキサゼパン環を形成しても良い)であり;
pは、1又は2の整数であり;
-X-は、-O-、又は-NH-であり:
-A-は、前記態様[1a-3]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、2~6の整数であり;式(AL-2)中のmは、1~3の整数である)(但し、式(I)において、Ar=フェニル基、p=1、-A-=式(AL-1)、かつn=3の場合、当該Arのフェニル基では前記フェニル基上の水素原子と置換しても良い置換基群から任意に選ばれる1~3個の基が前記フェニル基上の水素原子と置換する)である。
pは、1の整数であり;
-X-は、-O-、又は-NH-であり:
-A-は、前記態様[1a-3]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、2~6の整数であり;式(AL-2)中のmは、1~3の整数である)(但し、式(I)において、Ar=フェニル基、p=1、-A-=式(AL-1)、かつn=3の場合、当該Arのフェニル基では前記フェニル基上の水素原子と置換しても良い置換基群から任意に選ばれる1~3個の基が前記フェニル基上の水素原子と置換する)である。
Arは、フェニル基、又はピリジル基(前記フェニル基、又はピリジル基は、ヒドロキシル基、シアノ基、ニトロ基、ハロゲン原子、C1~6アルキル基、ハロゲン化C1~6アルキル基、C1~6アルコキシ基、及び-NRARB基(-NRARB基における、RA及びRBは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり(但し、-NH2、-NH(C1~6アルキル基)、及び-N(C1~6アルキル基)2は除く))から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、前記フェニル基又はピリジル基に、C1~6アルキル基及びC1~6アルコキシ基が又は2つのC1~6アルコキシ基が隣接して置換する場合、当該C1~6アルキル基及びC1~6アルコキシ基の各基のアルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、又は、当該2つのC1~6アルコキシ基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、環状エーテルを形成しても良く、又は、前記フェニル基又はピリジル基に、C1~6アルコキシ基及び-NHRG基(-NHRG基におけるRGは、C2~7アルカノイル基又はC1~6アルキルスルホニル基である)が隣接して置換している場合、当該C1~6アルコキシ基のアルキル基から任意の水素原子が1つ除かれた炭素原子と当該-NHRG基の水素原子が1つ除かれた窒素原子が結合することにより、3-N-(C2~7アルカノイル)オキサゾリジン環、3-N-(C1~6アルキルスルホニル)オキサゾリジン環、4-N-(C2~7アルカノイル)モルホリン環、4-N-(C1~6アルキルスルホニル)モルホリン環、4-N-(C2~7アルカノイル)-1,4-オキサゼパン環、又は4-N-(C1~6アルキルスルホニル)-1,4-オキサゼパン環を形成しても良い)であり;
pは、1又は2の整数であり;
-X-は、-O-であり:
-A-は、前記態様[1a-3]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、2~6の整数であり;式(AL-2)中のmは、1~3の整数である)(但し、式(I)において、Ar=フェニル基、p=1、-A-=式(AL-1)、かつn=3の場合、当該Arのフェニル基では前記フェニル基上の水素原子と置換しても良い置換基群から任意に選ばれる1~3個の基が前記フェニル基上の水素原子と置換する)である。
Arは、フェニル基、又はピリジル基(前記フェニル基、又はピリジル基は、ヒドロキシル基、シアノ基、ニトロ基、ハロゲン原子、C1~6アルキル基、ハロゲン化C1~6アルキル基、C1~6アルコキシ基、及び-NRARB基(-NRARB基における、RA及びRBは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり(但し、-NH2、-NH(C1~6アルキル基)、及び-N(C1~6アルキル基)2は除く))から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、前記フェニル基又はピリジル基に、C1~6アルキル基及びC1~6アルコキシ基が又は2つのC1~6アルコキシ基が隣接して置換する場合、当該C1~6アルキル基及びC1~6アルコキシ基の各基のアルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、又は、当該2つのC1~6アルコキシ基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、環状エーテルを形成しても良く、又は、前記フェニル基又はピリジル基に、C1~6アルコキシ基及び-NHRG基(-NHRG基におけるRGは、C2~7アルカノイル基又はC1~6アルキルスルホニル基である)が隣接して置換している場合、当該C1~6アルコキシ基のアルキル基から任意の水素原子が1つ除かれた炭素原子と当該-NHRG基の水素原子が1つ除かれた窒素原子が結合することにより、3-N-(C2~7アルカノイル)オキサゾリジン環、3-N-(C1~6アルキルスルホニル)オキサゾリジン環、4-N-(C2~7アルカノイル)モルホリン環、4-N-(C1~6アルキルスルホニル)モルホリン環、4-N-(C2~7アルカノイル)-1,4-オキサゼパン環、又は4-N-(C1~6アルキルスルホニル)-1,4-オキサゼパン環を形成しても良い)であり;
pは、1又は2の整数であり;
-X-は、-O-又は-NH-であり:
-A-は、前記態様[1a-3]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、2~6の整数であり;式(AL-2)中のmは、1~3の整数である)(但し、式(I)において、Ar=フェニル基、p=1、-A-=式(AL-1)、かつn=3の場合、当該Arのフェニル基では前記フェニル基上の水素原子と置換しても良い置換基群から任意に選ばれる1~3個の基が前記フェニル基上の水素原子と置換する)である。
Arは、フェニル基、又は2-ピリジル基(前記フェニル基、又は2-ピリジル基は、シアノ基、フッ素原子、トリフルオロメチル基、及びメトキシ基から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、フェニル基又は2-ピリジル基上に、2つのメトキシ基が隣接して置換している場合には、2つのメトキシ基の各基のメチル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより1,4-ジオキサン環を形成しても良い)(但し、式(I)において、Ar=フェニル基、p=1、-A-=式(AL-1)、かつn=3の場合、当該Arのフェニル基では前記フェニル基上の水素原子と置換しても良い置換基群から任意に選ばれる1~3個の基が前記フェニル基上の水素原子と置換する)であり;
Ar、p、-X-、-A-の組み合わせとしては、例えば、
Arは、フェニル基、4-フルオロフェニル基、4-(トリフルオロメチル)フェニル基、4-メトキシフェニル基、4-シアノフェニル基、2,3-ジヒドロベンゾ[b][1,4]ジオキシニル基、又は2-ピリジル基であり;
pは、1又は2の整数であり;
-X-は、-O-、又は-NH-であり:
-A-は、前記態様[1a-3]中の式(AL-1-1)、(AL-2-1)又は(AL-2-2)[各式中、両端の波線外側は含まない]であり;
例えば、Ar、p、-X-、-A-の組み合わせは、下記部分構造式[各式中、波線右側は含まない]:
Arは、フェニル基、2-ピリジル基、又は5-ピリジル基(前記フェニル基、2-ピリジル基、又は5-ピリジル基は、シアノ基、フッ素原子、トリフルオロメチル基、メトキシ基、及びN-アセチルアミノ基から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、フェニル基、2-ピリジル基、又は5-ピリジル基上に、2つのメトキシ基が隣接して置換している場合には、2つのメトキシ基の各基のメチル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより1,4-ジオキサン環を形成しても良い)(但し、式(I)において、Ar=フェニル基、p=1、-A-=式(AL-1)、かつn=3の場合、当該Arのフェニル基では前記フェニル基上の水素原子と置換しても良い置換基群から任意に選ばれる1~3個の基が前記フェニル基上の水素原子と置換する)であり;
Ar、p、-X-、-A-の組み合わせとしては、例えば、Arは、フェニル基、4-フルオロフェニル基、4-(トリフルオロメチル)フェニル基、4-メトキシフェニル基、3,4-ジメトキシフェニル基、4-(N-アセチルアミノ)フェニル基、4-シアノフェニル基、2,3-ジヒドロベンゾ[b][1,4]ジオキシニル基、2-ピリジル基、又は2-メトキシ-5-ピリジル基であり;
pは、1又は2の整数であり;
-X-は、-O-、又は-NH-であり:
-A-は、前記態様[1a-3]中の式(AL-1-1)、(AL-2-1)又は(AL-2-2)[各式中、両端の波線外側は含まない]であり;
例えば、Ar、p、-X-、-A-の組み合わせは、下記部分構造式[各式中、波線右側は含まない]:
Arは、フェニル基、2-ピリジル基、又は5-ピリジル基(前記フェニル基、2-ピリジル基、又は5-ピリジル基は、シアノ基、メトキシ基、及びN-アセチルアミノ基から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、フェニル基、2-ピリジル基、又は5-ピリジル基上に、2つのメトキシ基が隣接して置換している場合には、2つのメトキシ基の各基のメチル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより1,4-ジオキサン環を形成しても良い)(但し、式(I)において、Ar=フェニル基、p=1、-A-=式(AL-1)、かつn=3の場合、当該Arのフェニル基では前記フェニル基上の水素原子と置換しても良い置換基群から任意に選ばれる1~3個の基が前記フェニル基上の水素原子と置換する)であり;
Ar、p、-X-、-A-の組み合わせとしては、例えば、Arは、フェニル基、4-メトキシフェニル基、3,4-ジメトキシフェニル基、4-(N-アセチルアミノ)フェニル基、4-シアノフェニル基、2,3-ジヒドロベンゾ[b][1,4]ジオキシニル基、2-ピリジル基、又は2-メトキシ-5-ピリジル基であり;
pは、1又は2の整数であり;
-X-は、-O-、又は-NH-であり:
-A-は、前記態様[1a-3]中の式(AL-1-1)、(AL-2-1)又は(AL-2-2)[各式中、両端の波線外側は含まない]であり;
例えば、Ar、p、-X-、-A-の組み合わせは、下記部分構造式[各式中、波線右側は含まない]:
Ar、p、-X-、-A-の組み合わせとしては、Arは、例えば、フェニル基、4-フルオロフェニル基、又は4-(トリフルオロメチル)フェニル基であり;
pは、1の整数であり;
-X-は、-O-、又は-NH-であり:
-A-は、前記態様[1-3]中の式(AL-1-1)、(AL-2-1)又は(AL-2-2)[各式中、両端の波線外側は含まない]であり;
例えば、Ar、p、-X-、-A-の組み合わせは、下記部分構造式[各式中、波線右側は含まない]:
Arは、フェニル基、又は2-ピリジル基(前記フェニル基、又は2-ピリジル基は、シアノ基、及びメトキシ基から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、フェニル基又は2-ピリジル基上に、2つのメトキシ基が隣接して置換している場合には、2つのメトキシ基の各基のメチル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより1,4-ジオキサン環を形成しても良い)(但し、式(I)において、Ar=フェニル基、p=1、-A-=式(AL-1)、かつn=3の場合、当該Arのフェニル基では前記フェニル基上の水素原子と置換しても良い置換基群から任意に選ばれる1~3個の基が前記フェニル基上の水素原子と置換する)であり;
Ar、p、-X-、-A-の組み合わせとしては、例えば、Arは、例えば、フェニル基、4-メトキシフェニル基、4-シアノフェニル基、2,3-ジヒドロベンゾ[b][1,4]ジオキシニル基、又は2-ピリジル基であり;
pは、1又は2の整数であり;
-X-は、-O-であり:
-A-は、前記態様[1-3]中の式(AL-1-1)、又は(AL-2-1)[各式中、両端の波線外側は含まない]であり;
例えば、Ar、p、-X-、-A-の組み合わせは、下記部分構造式[各式中、波線右側は含まない]:
Ar、p、-X-、-A-の組み合わせとしては、例えば、 Arは、4-シアノフェニル基、4-メトキシフェニル基、3,4-ジメトキシフェニル基、4-(N-アセチルアミノ)フェニル基、2,3-ジヒドロベンゾ[b][1,4]ジオキシニル基、又は2-メトキシ-5-ピリジル基であり;
pは、1又は2の整数であり;
-X-は、-O-又は-NH-であり:
-A-は、前記態様[1a-3]中の式(AL-2-1)、又は(AL-2-2)[各式中、両端の波線外側は含まない]であり;
例えば、Ar、p、-X-、-A-の組み合わせは、下記部分構造式[各式中、波線右側は含まない]:
Arは、C6~10アリール基(前記C6~10アリール基は、ヒドロキシル基、シアノ基、ニトロ基、ハロゲン原子、C1~6アルキル基、ハロゲン化C1~6アルキル基、C1~6アルコキシ基、及び-NRARB基(-NRARB基における、RA及びRBは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり(但し、-NH2、-NH(C1~6アルキル基)、及び-N(C1~6アルキル基)2は除く))から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、前記C6~10アリール基に、C1~6アルキル基及びC1~6アルコキシ基が又は2つのC1~6アルコキシ基が隣接して置換する場合、当該C1~6アルキル基及びC1~6アルコキシ基の各基のアルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、又は、当該2つのC1~6アルコキシ基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、環状エーテルを形成しても良く、又は、前記C6~10アリール基に、C1~6アルコキシ基及び-NHRG基(-NHRG基におけるRGは、C2~7アルカノイル基又はC1~6アルキルスルホニル基である)が隣接して置換している場合、当該C1~6アルコキシ基のアルキル基から任意の水素原子が1つ除かれた炭素原子と当該-NHRG基の水素原子が1つ除かれた窒素原子が結合することにより、3-N-(C2~7アルカノイル)オキサゾリジン環、3-N-(C1~6アルキルスルホニル)オキサゾリジン環、4-N-(C2~7アルカノイル)モルホリン環、4-N-(C1~6アルキルスルホニル)モルホリン環、4-N-(C2~7アルカノイル)-1,4-オキサゼパン環、又は4-N-(C1~6アルキルスルホニル)-1,4-オキサゼパン環を形成しても良い)を表わし;
pは、1、又は2の整数を表わし;
-X-は、-O-を表わし;
-A-は、式(AL-1)~(AL-4)[各式中、両端の波線外側は含まない]:
式(AL-1)~(AL-4)中のメチレン基(-CH2-)の水素原子は、ハロゲン原子、水酸基、C1~6アルキル基、ヒドロキシC1~6アルキル基、チオールC1~6アルキル基、C1~6アルキルチオC1~6アルキル基、カルボキシC1~6アルキル基、-NRaRb基、(RaRbN)-C1~6アルキル基、(RaRbN)C(=O)-C1~6アルキル基(前記-NRaRb基、(RaRbN)-C1~6アルキル基、又は(RaRbN)C(=O)-C1~6アルキル基における、Ra及びRbは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)、グアニジノC1~6アルキル基、C7~16アラルキル基、ヒドロキシC6~10アリールC1~6アルキル基、又はヘテロアリールC1~6アルキル基から選択される基で複数個(例えば、1~10個、又は1~5個)置き換えられても良く;式(AL-1)~(AL-4)中のメチレン基(-CH2-)の2つの水素原子がC1~6アルキル基に置き換えられた場合、当該各C1~6アルキル基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することによりC3~8シクロアルキル環を形成しても良く;式(AL-3)又は式(AL-4)中の-NH-基は、隣接する炭素原子に置換する前記置換基と共に、非芳香族複素環を形成しても良い)](但し、式(I)において、Ar=フェニル基、p=1、-A-=式(AL-1)、かつn=3の場合、当該Arのフェニル基では前記Ar環上の水素原子と置換しても良い置換基群から任意に選ばれる1~3個の基が前記フェニル基上の水素原子と置換する)で表される光反応性基が導入された、アルギン酸誘導体である。
Arは、例えば、フェニル基、4-フルオロフェニル基、4-(トリフルオロメチル)フェニル基、4-メトキシフェニル基、3,4-ジメトキシフェニル基、4-(N-アセチルアミノ)フェニル基、4-シアノフェニル基、又は2,3-ジヒドロベンゾ[b][1,4]ジオキシニル基、等である。
Arは、例えば、フェニル基、4-メトキシフェニル基、3,4-ジメトキシフェニル基、4-シアノフェニル基、4-(N-アセチルアミノ)フェニル基、又は、2,3-ジヒドロベンゾ[b][1,4]ジオキシニル基、等である。
Arは、例えば、4-シアノフェニル基、4-メトキシフェニル基、3,4-ジメトキシフェニル基、4-(N-アセチルアミノ)フェニル基、又は2,3-ジヒドロベンゾ[b][1,4]ジオキシニル基、等である。
Arは、C6~10アリール基(前記C6~10アリール基は、ヒドロキシル基、シアノ基、ニトロ基、ハロゲン原子、C1~6アルキル基、ハロゲン化C1~6アルキル基、C1~6アルコキシ基、及び-NRARB基(-NRARB基における、RA及びRBは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり(但し、-NH2、-NH(C1~6アルキル基)、及び-N(C1~6アルキル基)2は除く))から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、前記C6~10アリール基に、C1~6アルキル基及びC1~6アルコキシ基が又は2つのC1~6アルコキシ基が隣接して置換する場合、当該C1~6アルキル基及びC1~6アルコキシ基の各基のアルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、又は、当該2つのC1~6アルコキシ基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、環状エーテルを形成しても良く、又は、前記C6~10アリール基に、C1~6アルコキシ基及び-NHRG基(-NHRG基におけるRGは、C2~7アルカノイル基又はC1~6アルキルスルホニル基である)が隣接して置換している場合、当該C1~6アルコキシ基のアルキル基から任意の水素原子が1つ除かれた炭素原子と当該-NHRG基の水素原子が1つ除かれた窒素原子が結合することにより、3-N-(C2~7アルカノイル)オキサゾリジン環、3-N-(C1~6アルキルスルホニル)オキサゾリジン環、4-N-(C2~7アルカノイル)モルホリン環、4-N-(C1~6アルキルスルホニル)モルホリン環、4-N-(C2~7アルカノイル)-1,4-オキサゼパン環、又は4-N-(C1~6アルキルスルホニル)-1,4-オキサゼパン環を形成しても良い)であり;
pは、1、又は2の整数であり;
-X-は、-O-であり;
-A-は、前記態様[1b-2]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、1~10の整数であり;式(AL-2)中のmは、1~7の整数であり)であり;
式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の水素原子は、ハロゲン原子、水酸基、C1~6アルキル基、ヒドロキシC1~6アルキル基、チオールC1~6アルキル基、C1~6アルキルチオC1~6アルキル基、カルボキシC1~6アルキル基、-NRaRb基、(RaRbN)-C1~6アルキル基、(RaRbN)C(=O)-C1~6アルキル基(前記-NRaRb基、(RaRbN)-C1~6アルキル基、又は(RaRbN)C(=O)-C1~6アルキル基における、Ra及びRbは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)、グアニジノC1~6アルキル基、C7~16アラルキル基、ヒドロキシC6~10アリールC1~6アルキル基、又はヘテロアリールC1~6アルキル基から選択される基で複数個(例えば、1~10個、又は1~5個)置き換えられても良く;式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の2つの水素原子がC1~6アルキル基に置き換えられた場合、当該各C1~6アルキル基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することによりC3~8シクロアルキル環を形成しても良い)(但し、式(I)において、Ar=フェニル基、p=1、-A-=式(AL-1)、かつn=3の場合、当該Arのフェニル基では前記Ar環上の水素原子と置換しても良い置換基群から任意に選ばれる1~3個の基が前記フェニル基上の水素原子と置換する)である。
pは、1の整数であり;
-X-は、-O-であり;
-A-は、前記態様[1b-2]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、1~10の整数であり;式(AL-2)中のmは、1~7の整数であり;
式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の水素原子は、ハロゲン原子、水酸基、C1~6アルキル基、ヒドロキシC1~6アルキル基、チオールC1~6アルキル基、C1~6アルキルチオC1~6アルキル基、カルボキシC1~6アルキル基、-NRaRb基、(RaRbN)-C1~6アルキル基、(RaRbN)C(=O)-C1~6アルキル基(前記-NRaRb基、(RaRbN)-C1~6アルキル基、又は(RaRbN)C(=O)-C1~6アルキル基における、Ra及びRbは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)、グアニジノC1~6アルキル基、C7~16アラルキル基、ヒドロキシC6~10アリールC1~6アルキル基、又はヘテロアリールC1~6アルキル基から選択される基で複数個(例えば、1~10個、又は1~5個)置き換えられても良く;式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の2つの水素原子がC1~6アルキル基に置き換えられた場合、当該各C1~6アルキル基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することによりC3~8シクロアルキル環を形成しても良い)(但し、式(I)において、Ar=フェニル基、p=1、-A-=式(AL-1)、かつn=3の場合、当該Arのフェニル基では前記Ar環上の水素原子と置換しても良い置換基群から任意に選ばれる1~3個の基が前記フェニル基上の水素原子と置換する)である。
pは、1、又は2の整数であり;
-X-は、-O-であり;
-A-は、前記態様[1b-2]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、1~10の整数であり;式(AL-2)中のmは、1~7の整数であり;
式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の水素原子は、ハロゲン原子、水酸基、C1~6アルキル基、ヒドロキシC1~6アルキル基、チオールC1~6アルキル基、C1~6アルキルチオC1~6アルキル基、カルボキシC1~6アルキル基、-NRaRb基、(RaRbN)-C1~6アルキル基、(RaRbN)C(=O)-C1~6アルキル基(前記-NRaRb基、(RaRbN)-C1~6アルキル基、又は(RaRbN)C(=O)-C1~6アルキル基における、Ra及びRbは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)、グアニジノC1~6アルキル基、C7~16アラルキル基、ヒドロキシC6~10アリールC1~6アルキル基、又はヘテロアリールC1~6アルキル基から選択される基で複数個(例えば、1~10個、又は1~5個)置き換えられても良く;式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の2つの水素原子がC1~6アルキル基に置き換えられた場合、当該各C1~6アルキル基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することによりC3~8シクロアルキル環を形成しても良い)(但し、式(I)において、Ar=フェニル基、p=1、-A-=式(AL-1)、かつn=3の場合、当該Arのフェニル基では前記Ar環上の水素原子と置換しても良い置換基群から任意に選ばれる1~3個の基が前記フェニル基上の水素原子と置換する)である。
pは、1、又は2の整数であり;
-X-は、-O-であり;
-A-は、前記態様[1b-2]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、1~10の整数であり;式(AL-2)中のmは、1~7の整数であり;
式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の水素原子は、ハロゲン原子、水酸基、C1~6アルキル基、ヒドロキシC1~6アルキル基、チオールC1~6アルキル基、C1~6アルキルチオC1~6アルキル基、カルボキシC1~6アルキル基、-NRaRb基、(RaRbN)-C1~6アルキル基、(RaRbN)C(=O)-C1~6アルキル基(前記-NRaRb基、(RaRbN)-C1~6アルキル基、又は(RaRbN)C(=O)-C1~6アルキル基における、Ra及びRbは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)、グアニジノC1~6アルキル基、C7~16アラルキル基、ヒドロキシC6~10アリールC1~6アルキル基、又はヘテロアリールC1~6アルキル基から選択される基で複数個(例えば、1~10個、又は1~5個)置き換えられても良く;式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の2つの水素原子がC1~6アルキル基に置き換えられた場合、当該各C1~6アルキル基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することによりC3~8シクロアルキル環を形成しても良い)(但し、式(I)において、Ar=フェニル基、p=1、-A-=式(AL-1)、かつn=3の場合、当該Arのフェニル基では前記Ar環上の水素原子と置換しても良い置換基群から任意に選ばれる1~3個の基が前記フェニル基上の水素原子と置換する)である。
Arは、フェニル基(前記フェニル基は、ヒドロキシル基、シアノ基、ニトロ基、ハロゲン原子、C1~6アルキル基、ハロゲン化C1~6アルキル基、C1~6アルコキシ基、及び-NRARB基(-NRARB基における、RA及びRBは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり(但し、-NH2、-NH(C1~6アルキル基)、及び-N(C1~6アルキル基)2は除く))から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、前記フェニル基に、C1~6アルキル基及びC1~6アルコキシ基が又は2つのC1~6アルコキシ基が隣接して置換する場合、当該C1~6アルキル基及びC1~6アルコキシ基の各基のアルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、又は、当該2つのC1~6アルコキシ基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、環状エーテルを形成しても良く、又は、前記フェニル基に、C1~6アルコキシ基及び-NHRG基(-NHRG基におけるRGは、C2~7アルカノイル基又はC1~6アルキルスルホニル基である)が隣接して置換している場合、当該C1~6アルコキシ基のアルキル基から任意の水素原子が1つ除かれた炭素原子と当該-NHRG基の水素原子が1つ除かれた窒素原子が結合することにより、3-N-(C2~7アルカノイル)オキサゾリジン環、3-N-(C1~6アルキルスルホニル)オキサゾリジン環、4-N-(C2~7アルカノイル)モルホリン環、4-N-(C1~6アルキルスルホニル)モルホリン環、4-N-(C2~7アルカノイル)-1,4-オキサゼパン環、又は4-N-(C1~6アルキルスルホニル)-1,4-オキサゼパン環を形成しても良い)であり;
pは、1又は2の整数であり;
-X-は、-O-であり:
-A-は、前記態様[1b-2]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、2~6の整数であり;式(AL-2)中のmは、1~3の整数である)(但し、式(I)において、Ar=フェニル基、p=1、-A-=式(AL-1)、かつn=3の場合、当該Arのフェニル基では前記フェニル基上の水素原子と置換しても良い置換基群から任意に選ばれる1~3個の基が前記フェニル基上の水素原子と置換する)である。
pは、1の整数であり;
-X-は、-O-であり:
-A-は、前記態様[1b-2]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、2~6の整数であり;式(AL-2)中のmは、1~3の整数である)(但し、式(I)において、Ar=フェニル基、p=1、-A-=式(AL-1)、かつn=3の場合、当該Arのフェニル基では前記フェニル基上の水素原子と置換しても良い置換基群から任意に選ばれる1~3個の基が前記フェニル基上の水素原子と置換する)である。
Arは、フェニル基(前記フェニル基は、ヒドロキシル基、シアノ基、ニトロ基、ハロゲン原子、C1~6アルキル基、ハロゲン化C1~6アルキル基、C1~6アルコキシ基、及び-NRARB基(-NRARB基における、RA及びRBは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり(但し、-NH2、-NH(C1~6アルキル基)、及び-N(C1~6アルキル基)2は除く))から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、前記フェニル基に、C1~6アルキル基及びC1~6アルコキシ基が又は2つのC1~6アルコキシ基が隣接して置換する場合、当該C1~6アルキル基及びC1~6アルコキシ基の各基のアルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、又は、当該2つのC1~6アルコキシ基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、環状エーテルを形成しても良く、又は、前記フェニル基に、C1~6アルコキシ基及び-NHRG基(-NHRG基におけるRGは、C2~7アルカノイル基又はC1~6アルキルスルホニル基である)が隣接して置換している場合、当該C1~6アルコキシ基のアルキル基から任意の水素原子が1つ除かれた炭素原子と当該-NHRG基の水素原子が1つ除かれた窒素原子が結合することにより、3-N-(C2~7アルカノイル)オキサゾリジン環、3-N-(C1~6アルキルスルホニル)オキサゾリジン環、4-N-(C2~7アルカノイル)モルホリン環、4-N-(C1~6アルキルスルホニル)モルホリン環、4-N-(C2~7アルカノイル)-1,4-オキサゼパン環、又は4-N-(C1~6アルキルスルホニル)-1,4-オキサゼパン環を形成しても良い)であり;
pは、1又は2の整数であり;
-X-は、-O-であり:
-A-は、前記態様[1b-2]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、2~6の整数であり;式(AL-2)中のmは、1~3の整数である)(但し、式(I)において、Ar=フェニル基、p=1、-A-=式(AL-1)、かつn=3の場合、当該Arのフェニル基では前記フェニル基上の水素原子と置換しても良い置換基群から任意に選ばれる1~3個の基が前記フェニル基上の水素原子と置換する)である。
Arは、フェニル基(前記フェニル基は、ヒドロキシル基、シアノ基、ニトロ基、ハロゲン原子、C1~6アルキル基、ハロゲン化C1~6アルキル基、C1~6アルコキシ基、及び-NRARB基(-NRARB基における、RA及びRBは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり(但し、-NH2、-NH(C1~6アルキル基)、及び-N(C1~6アルキル基)2は除く))から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、前記フェニル基に、C1~6アルキル基及びC1~6アルコキシ基が又は2つのC1~6アルコキシ基が隣接して置換する場合、当該C1~6アルキル基及びC1~6アルコキシ基の各基のアルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、又は、当該2つのC1~6アルコキシ基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、環状エーテルを形成しても良く、又は、前記フェニル基に、C1~6アルコキシ基及び-NHRG基(-NHRG基におけるRGは、C2~7アルカノイル基又はC1~6アルキルスルホニル基である)が隣接して置換している場合、当該C1~6アルコキシ基のアルキル基から任意の水素原子が1つ除かれた炭素原子と当該-NHRG基の水素原子が1つ除かれた窒素原子が結合することにより、3-N-(C2~7アルカノイル)オキサゾリジン環、3-N-(C1~6アルキルスルホニル)オキサゾリジン環、4-N-(C2~7アルカノイル)モルホリン環、4-N-(C1~6アルキルスルホニル)モルホリン環、4-N-(C2~7アルカノイル)-1,4-オキサゼパン環、又は4-N-(C1~6アルキルスルホニル)-1,4-オキサゼパン環を形成しても良い)であり;
pは、1又は2の整数であり;
-X-は、-O-であり:
-A-は、前記態様[1a-3]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、2~6の整数であり;式(AL-2)中のmは、1~3の整数である)(但し、式(I)において、Ar=フェニル基、p=1、-A-=式(AL-1)、かつn=3の場合、当該Arのフェニル基では前記フェニル基上の水素原子と置換しても良い置換基群から任意に選ばれる1~3個の基が前記フェニル基上の水素原子と置換する)である。
Arは、フェニル基(前記フェニル基は、シアノ基、フッ素原子、トリフルオロメチル基、及びメトキシ基から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、フェニル基上に、2つのメトキシ基が隣接して置換している場合には、2つのメトキシ基の各基のメチル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより1,4-ジオキサン環を形成しても良い)(但し、式(I)において、Ar=フェニル基、p=1、-A-=式(AL-1)、かつn=3の場合、当該Arのフェニル基では前記フェニル基上の水素原子と置換しても良い置換基群から任意に選ばれる1~3個の基が前記フェニル基上の水素原子と置換する)であり;
Ar、p、-X-、-A-の組み合わせとしては、例えば、
Arは、フェニル基、4-フルオロフェニル基、4-(トリフルオロメチル)フェニル基、4-メトキシフェニル基、4-シアノフェニル基、又は2,3-ジヒドロベンゾ[b][1,4]ジオキシニル基であり;
pは、1又は2の整数であり;
-X-は、-O-であり:
-A-は、前記態様[1b-2]中の式(AL-1-1)、又は(AL-2-1)[各式中、両端の波線外側は含まない]であり;
例えば、Ar、p、-X-、-A-の組み合わせは、下記部分構造式[各式中、波線右側は含まない]:
[1b-3-3-1]前記態様[1b]のアルギン酸誘導体において、Ar、p、-X-、-A-の組み合わせとしては、更に好ましくは、
Arは、フェニル基(前記フェニル基は、シアノ基、フッ素原子、トリフルオロメチル基、メトキシ基、及びN-アセチルアミノ基から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、フェニル基上に、2つのメトキシ基が隣接して置換している場合には、2つのメトキシ基の各基のメチル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより1,4-ジオキサン環を形成しても良い)(但し、式(I)において、Ar=フェニル基、p=1、-A-=式(AL-1)、かつn=3の場合、当該Arのフェニル基では前記フェニル基上の水素原子と置換しても良い置換基群から任意に選ばれる1~3個の基が前記フェニル基上の水素原子と置換する)であり;
Ar、p、-X-、-A-の組み合わせとしては、例えば、Arは、フェニル基、4-フルオロフェニル基、4-(トリフルオロメチル)フェニル基、4-メトキシフェニル基、3,4-ジメトキシフェニル基、5-(N-アセチルアミノ)フェニル基、4-シアノフェニル基、又は2,3-ジヒドロベンゾ[b][1,4]ジオキシニル基であり;
pは、1又は2の整数であり;
-X-は、-O-であり:
-A-は、前記態様[1b-2]中の式(AL-1-1)、又は(AL-2-1)[各式中、両端の波線外側は含まない]であり;
例えば、Ar、p、-X-、-A-の組み合わせは、下記部分構造式[各式中、波線右側は含まない]:
[1b-3-3-2]前記態様[1b]のアルギン酸誘導体において、Ar、p、-X-、-A-の組み合わせとしては、更に好ましくは、
Arは、フェニル基(前記フェニル基は、シアノ基、メトキシ基、及びN-アセチルアミノ基から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、フェニル基上に、2つのメトキシ基が隣接して置換している場合には、2つのメトキシ基の各基のメチル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより1,4-ジオキサン環を形成しても良い)(但し、式(I)において、Ar=フェニル基、p=1、-A-=式(AL-1)、かつn=3の場合、当該Arのフェニル基では前記フェニル基上の水素原子と置換しても良い置換基群から任意に選ばれる1~3個の基が前記フェニル基上の水素原子と置換する)であり;
Ar、p、-X-、-A-の組み合わせとしては、例えば、Arは、フェニル基、4-メトキシフェニル基、3,4-ジメトキシフェニル基、4-(N-アセチルアミノ)フェニル基、4-シアノフェニル基、又は2,3-ジヒドロベンゾ[b][1,4]ジオキシニル基、2-ピリジル基であり;
pは、1又は2の整数であり;
-X-は、-O-であり:
-A-は、前記態様[1b-2]中の式(AL-1-1)、又は(AL-2-1)[各式中、両端の波線外側は含まない]であり;
例えば、Ar、p、-X-、-A-の組み合わせは、下記部分構造式[各式中、波線右側は含まない]:
Ar、p、-X-、-A-の組み合わせとしては、Arは、例えば、フェニル基、4-フルオロフェニル基、又は4-(トリフルオロメチル)フェニル基であり;
pは、1の整数であり;
-X-は、-O-であり:
-A-は、前記態様[1b-2]中の式(AL-1-1)、又は(AL-2-1)[各式中、両端の波線外側は含まない]であり;
例えば、Ar、p、-X-、-A-の組み合わせは、下記部分構造式[各式中、波線右側は含まない]:
Arは、フェニル基(前記フェニル基は、シアノ基、及びメトキシ基から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、フェニル基上に、2つのメトキシ基が隣接して置換している場合には、2つのメトキシ基の各基のメチル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより1,4-ジオキサン環を形成しても良い)(但し、式(I)において、Ar=フェニル基、p=1、-A-=式(AL-1)、かつn=3の場合、当該Arのフェニル基では前記フェニル基上の水素原子と置換しても良い置換基群から任意に選ばれる1~3個の基が前記フェニル基上の水素原子と置換する)であり;
Ar、p、-X-、-A-の組み合わせとしては、例えば、Arは、例えば、フェニル基、4-メトキシフェニル基、4-シアノフェニル基、又は2,3-ジヒドロベンゾ[b][1,4]ジオキシニル基であり;
pは、1又は2の整数であり;
-X-は、-O-であり:
-A-は、前記態様[1b-2]中の式(AL-1-1)、又は(AL-2-1)[各式中、両端の波線外側は含まない]であり;
例えば、Ar、p、-X-、-A-の組み合わせは、下記部分構造式[各式中、波線右側は含まない]:
Ar、p、-X-、-A-の組み合わせとしては、例えば、 Arは、4-シアノフェニル基、4-メトキシフェニル基、3,4-ジメトキシフェニル基、4-(N-アセチルアミノ)フェニル基、又は2,3-ジヒドロベンゾ[b][1,4]ジオキシニル基であり;
pは、1又は2の整数であり;
-X-は、-O-であり:
-A-は、前記態様[1b-2]中の式(AL-2-1)[各式中、両端の波線外側は含まない]であり;
例えば、Ar、p、-X-、-A-の組み合わせは、下記部分構造式[各式中、波線右側は含まない]:
より好ましくは、前記態様[1-4-2]、[1-4-2a]、[1-4-2b]、[1-4-2c]、[1a-4-2]、[1a-4-2a]、[1a-4-2b]、又は[1a-4-2c]に記載のアルギン酸誘導体に光照射することにより得られる光架橋アルギン酸であり;
更に好ましくは前記態様[1-4-3]、[1-4-3a]、[1-4-3b]、[1-4-3c]、[1a-4-3]、[1a-4-3a]、[1a-4-3b]、又は[1a-4-3c]に記載のアルギン酸誘導体に光照射することにより得られる光架橋アルギン酸であり;
特に好ましくは、前記態様[1-4-4a]又は[1a-4-4a]に記載のアルギン酸誘導体に光照射することにより得られる光架橋アルギン酸であり;
例えば、下記式[各式中、波線右側は含まない]:
又は、特に好ましくは、前記態様[1-4-4b]、又は[1a-4-4b]に記載のアルギン酸誘導体に光照射することにより得られる光架橋アルギン酸であり;
例えば、下記式[各式中、波線右側は含まない]:
又は、特に好ましくは、前記態様[1-4-4c]、又は[1a-4-4c]に記載のアルギン酸誘導体に光照射することにより得られる光架橋アルギン酸であり;
例えば、下記式[各式中、波線右側は含まない]:
又は、特に好ましくは、前記態様[1-4-4]、又は[1a-4-4]に記載のアルギン酸誘導体に光照射することにより得られる光架橋アルギン酸であり;
例えば、下記式[各式中、波線右側は含まない]:
又は、特に好ましくは、前記態様[1-4-4-1]、又は[1a-4-4-1]に記載のアルギン酸誘導体に光照射することにより得られる光架橋アルギン酸であり;
例えば、下記式[各式中、波線右側は含まない]:
又は、特に好ましくは、前記態様[1-4-4-2]、又は[1a-4-4-2]に記載のアルギン酸誘導体に光照射することにより得られる光架橋アルギン酸であり;
例えば、下記式[各式中、波線右側は含まない]:
最も好ましくは、下記式[各式中、波線右側は含まない]:
より好ましくは、前記態様[1b-3-2]、[1b-3-2a]、[1b-3-2b]、又は[1b-3-2c]に記載のアルギン酸誘導体に光照射することにより得られる光架橋アルギン酸であり;
更に好ましくは、前記態様[1b-3-3a]に記載のアルギン酸誘導体に光照射することにより得られる光架橋アルギン酸であり、
例えば、下記式[各式中、波線右側は含まない]:
又は、更に好ましくは、前記態様[1b-3-3b]に記載のアルギン酸誘導体に光照射することにより得られる光架橋アルギン酸であり、
例えば、下記式[各式中、波線右側は含まない]:
又は、更に好ましくは、前記態様[1b-3-3c]に記載のアルギン酸誘導体に光照射することにより得られる光架橋アルギン酸であり、
例えば、下記式[各式中、波線右側は含まない]:
又は、更に好ましくは、前記態様[1b-3-3]に記載のアルギン酸誘導体に光照射することにより得られる光架橋アルギン酸であり、
例えば、下記式[各式中、波線右側は含まない]:
又は、更に好ましくは、前記態様[1b-3-3-1]に記載のアルギン酸誘導体に光照射することにより得られる光架橋アルギン酸であり、
例えば、下記式[各式中、波線右側は含まない]:
又は、更に好ましくは、前記態様[1b-3-3-2]に記載のアルギン酸誘導体に光照射することにより得られる光架橋アルギン酸であり、
例えば、下記式[各式中、波線右側は含まない]:
特に好ましくは、下記式[各式中、波線右側は含まない]:
より好ましくは、前記態様[1-4-2]、[1-4-2a]、[1-4-2b]、[1-4-2c]、[1a-4-2]、[1a-4-2a]、[1a-4-2b]、又は[1a-4-2c]に記載のアルギン酸誘導体の溶液を、2価金属イオンを含む溶液中に滴下することで得られるゲルに光照射することにより得られる、架橋として2価金属イオンにより部分的に形成されるイオン架橋及び光照射により形成される化学架橋を含む、光架橋アルギン酸構造体であり;
更に好ましくは、前記態様[1-4-3]、[1-4-3a]、[1-4-3b]、[1-4-3c]、[1a-4-3]、[1a-4-3a]、[1a-4-3b]、又は[1a-4-3c]に記載のアルギン酸誘導体の溶液を、2価金属イオンを含む溶液中に滴下することで得られるゲルに光照射することにより得られる、架橋として2価金属イオンにより部分的に形成されるイオン架橋及び光照射により形成される化学架橋を含む、光架橋アルギン酸構造体であり;
特に好ましくは、前記態様[1-4-4a]又は[1a-4-4a]に記載のアルギン酸誘導体の溶液を、2価金属イオンを含む溶液中に滴下することで得られるゲルに光照射することにより得られる、架橋として2価金属イオンにより部分的に形成されるイオン架橋及び光照射により形成される化学架橋を含む、光架橋アルギン酸構造体であり;
例えば、下記式[各式中、波線右側は含まない]:
又は、特に好ましくは、前記態様[1-4-4b]、又は[1a-4-4b]に記載のアルギン酸誘導体の溶液を、2価金属イオンを含む溶液中に滴下することで得られるゲルに光照射することにより得られる、架橋として2価金属イオンにより部分的に形成されるイオン架橋及び光照射により形成される化学架橋を含む、光架橋アルギン酸構造体であり;
例えば、下記式[各式中、波線右側は含まない]:
又は、特に好ましくは、前記態様[1-4-4c]、又は[1a-4-4c]に記載のアルギン酸誘導体の溶液を、2価金属イオンを含む溶液中に滴下することで得られるゲルに光照射することにより得られる、架橋として2価金属イオンにより部分的に形成されるイオン架橋及び光照射により形成される化学架橋を含む、光架橋アルギン酸構造体であり;
例えば、下記式[各式中、波線右側は含まない]:
又は、特に好ましくは、前記態様[1-4-4]、又は[1a-4-4]に記載のアルギン酸誘導体の溶液を、2価金属イオンを含む溶液中に滴下することで得られるゲルに光照射することにより得られる、架橋として2価金属イオンにより部分的に形成されるイオン架橋及び光照射により形成される化学架橋を含む、光架橋アルギン酸構造体であり;
例えば、下記式[各式中、波線右側は含まない]:
又は、特に好ましくは、前記態様[1-4-4-1]、又は[1a-4-4-1]に記載のアルギン酸誘導体の溶液を、2価金属イオンを含む溶液中に滴下することで得られるゲルに光照射することにより得られる、架橋として2価金属イオンにより部分的に形成されるイオン架橋及び光照射により形成される化学架橋を含む、光架橋アルギン酸構造体であり;
例えば、下記式[各式中、波線右側は含まない]:
又は、特に好ましくは、前記態様[1-4-4-2]、又は[1a-4-4-2]に記載のアルギン酸誘導体の溶液を、2価金属イオンを含む溶液中に滴下することで得られるゲルに光照射することにより得られる、架橋として2価金属イオンにより部分的に形成されるイオン架橋及び光照射により形成される化学架橋を含む、光架橋アルギン酸構造体であり;
例えば、下記式[各式中、波線右側は含まない]:
最も好ましくは、下記式[各式中、波線右側は含まない]:
より好ましくは、前記態様[1b-3-2]、[1b-3-2a]、[1b-3-2b]、又は[1b-3-2c]に記載のアルギン酸誘導体の溶液を、2価金属イオンを含む溶液中に滴下することで得られるゲルに光照射することにより得られる、架橋として2価金属イオンにより部分的に形成されるイオン架橋及び光照射により形成される化学架橋を含む、光架橋アルギン酸構造体であり;
更に好ましくは、前記態様[1b-3-3a]に記載のアルギン酸誘導体の溶液を、2価金属イオンを含む溶液中に滴下することで得られるゲルに光照射することにより得られる、架橋として2価金属イオンにより部分的に形成されるイオン架橋及び光照射により形成される化学架橋を含む、光架橋アルギン酸構造体であり;
例えば、下記式[各式中、波線右側は含まない]:
又は、更に好ましくは、前記態様[1b-3-3b]に記載のアルギン酸誘導体の溶液を、2価金属イオンを含む溶液中に滴下することで得られるゲルに光照射することにより得られる、架橋として2価金属イオンにより部分的に形成されるイオン架橋及び光照射により形成される化学架橋を含む、光架橋アルギン酸構造体であり;
例えば、下記式[各式中、波線右側は含まない]:
又は、更に好ましくは、前記態様[1b-3-3c]に記載のアルギン酸誘導体の溶液を、2価金属イオンを含む溶液中に滴下することで得られるゲルに光照射することにより得られる、架橋として2価金属イオンにより部分的に形成されるイオン架橋及び光照射により形成される化学架橋を含む、光架橋アルギン酸構造体であり;
例えば、下記式[各式中、波線右側は含まない]:
又は、更に好ましくは、前記態様[1b-3-3]に記載のアルギン酸誘導体の溶液を、2価金属イオンを含む溶液中に滴下することで得られるゲルに光照射することにより得られる、架橋として2価金属イオンにより部分的に形成されるイオン架橋及び光照射により形成される化学架橋を含む、光架橋アルギン酸構造体であり;
例えば、下記式[各式中、波線右側は含まない]:
又は、更に好ましくは、前記態様[1b-3-3-1]に記載のアルギン酸誘導体の溶液を、2価金属イオンを含む溶液中に滴下することで得られるゲルに光照射することにより得られる、架橋として2価金属イオンにより部分的に形成されるイオン架橋及び光照射により形成される化学架橋を含む、光架橋アルギン酸構造体であり;
例えば、下記式[各式中、波線右側は含まない]:
又は、更に好ましくは、前記態様[1b-3-3-2]に記載のアルギン酸誘導体の溶液を、2価金属イオンを含む溶液中に滴下することで得られるゲルに光照射することにより得られる、架橋として2価金属イオンにより部分的に形成されるイオン架橋及び光照射により形成される化学架橋を含む、光架橋アルギン酸構造体であり;
例えば、下記式[各式中、波線右側は含まない]:
特に好ましくは、下記式[各式中、波線右側は含まない]:
より好ましくは、前記態様[1-4-2]、[1-4-2a]、[1-4-2b]、[1-4-2c]、[1a-4-2]、[1a-4-2a]、[1a-4-2b]、又は[1a-4-2c]に記載のアルギン酸誘導体に光照射を行うことを含む、光架橋アルギン酸を製造する方法であり;
更に好ましくは、前記態様[1-4-3]、[1-4-3a]、[1-4-3b]、[1-4-3c]、[1a-4-3]、[1a-4-3a]、[1a-4-3b]、又は[1a-4-3c]に記載のアルギン酸誘導体に光照射を行うことを含む、光架橋アルギン酸を製造する方法であり;
特に好ましくは、前記態様[1-4-4a]又は[1a-4-4a]に記載のアルギン酸誘導体に光照射を行うことを含む、光架橋アルギン酸を製造する方法であり、
例えば、下記式[各式中、波線右側は含まない]:
又は、特に好ましくは、前記態様[1-4-4b]、又は[1a-4-4b]に記載のアルギン酸誘導体に光照射を行うことを含む、光架橋アルギン酸を製造する方法であり、
例えば、下記式[各式中、波線右側は含まない]:
又は、特に好ましくは、前記態様[1-4-4c]、又は[1a-4-4c]に記載のアルギン酸誘導体に光照射を行うことを含む、光架橋アルギン酸を製造する方法であり、
例えば、下記式[各式中、波線右側は含まない]:
又は、特に好ましくは、前記態様[1-4-4]、又は[1a-4-4]に記載のアルギン酸誘導体に光照射を行うことを含む、光架橋アルギン酸を製造する方法であり、
例えば、下記式[各式中、波線右側は含まない]:
又は、特に好ましくは、前記態様[1-4-4-1]、又は[1a-4-4-1]に記載のアルギン酸誘導体に光照射を行うことを含む、光架橋アルギン酸を製造する方法であり、
例えば、下記式[各式中、波線右側は含まない]:
又は、特に好ましくは、前記態様[1-4-4-2]、又は[1a-4-4-2]に記載のアルギン酸誘導体に光照射を行うことを含む、光架橋アルギン酸を製造する方法であり、
例えば、下記式[各式中、波線右側は含まない]:
最も好ましくは、下記式[各式中、波線右側は含まない]:
より好ましくは、前記態様[1b-3-2]、[1b-3-2a]、[1b-3-2b]、又は[1b-3-2c]に記載のアルギン酸誘導体に光照射を行うことを含む、光架橋アルギン酸を製造する方法であり;
更に好ましくは、前記態様[1b-3-3a]に記載のアルギン酸誘導体に光照射を行うことを含む、光架橋アルギン酸を製造する方法であり、
例えば、下記式[各式中、波線右側は含まない]:
又は、更に好ましくは、前記態様[1b-3-3b]に記載のアルギン酸誘導体に光照射を行うことを含む、光架橋アルギン酸を製造する方法であり、
例えば、下記式[各式中、波線右側は含まない]:
又は、更に好ましくは、前記態様[1b-3-3c]に記載のアルギン酸誘導体に光照射を行うことを含む、光架橋アルギン酸を製造する方法であり、
例えば、下記式[各式中、波線右側は含まない]:
又は、更に好ましくは、前記態様[1b-3-3]に記載のアルギン酸誘導体に光照射を行うことを含む、光架橋アルギン酸を製造する方法であり、
例えば、下記式[各式中、波線右側は含まない]:
又は、更に好ましくは、前記態様[1b-3-3-1]に記載のアルギン酸誘導体に光照射を行うことを含む、光架橋アルギン酸を製造する方法であり、
例えば、下記式[各式中、波線右側は含まない]:
又は、更に好ましくは、前記態様[1b-3-3-2]に記載のアルギン酸誘導体に光照射を行うことを含む、光架橋アルギン酸を製造する方法であり、
例えば、下記式[各式中、波線右側は含まない]:
特に好ましくは、下記式[各式中、波線右側は含まない]:
より好ましくは、前記態様[1-4-2]、[1-4-2a]、[1-4-2b]、[1-4-2c]、[1a-4-2]、[1a-4-2a]、[1a-4-2b]、又は[1a-4-2c]に記載のアルギン酸誘導体の溶液を、2価金属イオンを含む溶液中に滴下することで得られるゲルに光照射して光架橋アルギン酸構造体を得ることを含み、光架橋アルギン酸構造体が、架橋として2価金属イオンにより部分的に形成されるイオン架橋及び光照射により形成される化学架橋を含む、光架橋アルギン酸構造体を製造する方法であり;
更に好ましくは、前記態様[1-4-3]、[1-4-3a]、[1-4-3b]、[1-4-3c]、[1a-4-3]、[1a-4-3a]、[1a-4-3b]、又は[1a-4-3c]に記載のアルギン酸誘導体の溶液を、2価金属イオンを含む溶液中に滴下することで得られるゲルに光照射して光架橋アルギン酸構造体を得ることを含み、光架橋アルギン酸構造体が、架橋として2価金属イオンにより部分的に形成されるイオン架橋及び光照射により形成される化学架橋を含む、光架橋アルギン酸構造体を製造する方法であり;
特に好ましくは、前記態様[1-4-4a]又は[1a-4-4a]に記載のアルギン酸誘導体の溶液を、2価金属イオンを含む溶液中に滴下することで得られるゲルに光照射して光架橋アルギン酸構造体を得ることを含み、光架橋アルギン酸構造体が、架橋として2価金属イオンにより部分的に形成されるイオン架橋及び光照射により形成される化学架橋を含む、光架橋アルギン酸構造体を製造する方法であり、
例えば、下記式[各式中、波線右側は含まない]:
又は、特に好ましくは、前記態様[1-4-4b]、又は[1a-4-4b]に記載のアルギン酸誘導体の溶液を、2価金属イオンを含む溶液中に滴下することで得られるゲルに光照射して光架橋アルギン酸構造体を得ることを含み、光架橋アルギン酸構造体が、架橋として2価金属イオンにより部分的に形成されるイオン架橋及び光照射により形成される化学架橋を含む、光架橋アルギン酸構造体を製造する方法であり、
例えば、下記式[各式中、波線右側は含まない]:
又は、特に好ましくは、前記態様[1-4-4c]、又は[1a-4-4c]に記載のアルギン酸誘導体の溶液を、2価金属イオンを含む溶液中に滴下することで得られるゲルに光照射して光架橋アルギン酸構造体を得ることを含み、光架橋アルギン酸構造体が、架橋として2価金属イオンにより部分的に形成されるイオン架橋及び光照射により形成される化学架橋を含む、光架橋アルギン酸構造体を製造する方法であり、
例えば、下記式[各式中、波線右側は含まない]:
又は、特に好ましくは、前記態様[1-4-4]、又は[1a-4-4]に記載のアルギン酸誘導体の溶液を、2価金属イオンを含む溶液中に滴下することで得られるゲルに光照射して光架橋アルギン酸構造体を得ることを含み、光架橋アルギン酸構造体が、架橋として2価金属イオンにより部分的に形成されるイオン架橋及び光照射により形成される化学架橋を含む、光架橋アルギン酸構造体を製造する方法であり、
例えば、下記式[各式中、波線右側は含まない]:
又は、特に好ましくは、前記態様[1-4-4-1]、又は[1a-4-4-1]に記載のアルギン酸誘導体の溶液を、2価金属イオンを含む溶液中に滴下することで得られるゲルに光照射して光架橋アルギン酸構造体を得ることを含み、光架橋アルギン酸構造体が、架橋として2価金属イオンにより部分的に形成されるイオン架橋及び光照射により形成される化学架橋を含む、光架橋アルギン酸構造体を製造する方法であり、
例えば、下記式[各式中、波線右側は含まない]:
又は、特に好ましくは、前記態様[1-4-4-2]、又は[1a-4-4-2]に記載のアルギン酸誘導体の溶液を、2価金属イオンを含む溶液中に滴下することで得られるゲルに光照射して光架橋アルギン酸構造体を得ることを含み、光架橋アルギン酸構造体が、架橋として2価金属イオンにより部分的に形成されるイオン架橋及び光照射により形成される化学架橋を含む、光架橋アルギン酸構造体を製造する方法であり、
例えば、下記式[各式中、波線右側は含まない]:
最も好ましくは、下記式[各式中、波線右側は含まない]:
より好ましくは、前記態様[1b-3-2]、[1b-3-2a]、[1b-3-2b]、又は[1b-3-2c]に記載のアルギン酸誘導体の溶液を、2価金属イオンを含む溶液中に滴下することで得られるゲルに光照射して光架橋アルギン酸構造体を得ることを含み、光架橋アルギン酸構造体が、架橋として2価金属イオンにより部分的に形成されるイオン架橋及び光照射により形成される化学架橋を含む、光架橋アルギン酸構造体を製造する方法であり;
更に好ましくは、前記態様[1b-3-3a]に記載のアルギン酸誘導体の溶液を、2価金属イオンを含む溶液中に滴下することで得られるゲルに光照射して光架橋アルギン酸構造体を得ることを含み、光架橋アルギン酸構造体が、架橋として2価金属イオンにより部分的に形成されるイオン架橋及び光照射により形成される化学架橋を含む、光架橋アルギン酸構造体を製造する方法であり、
例えば、下記式[各式中、波線右側は含まない]:
又は、更に好ましくは、前記態様[1b-3-3b]に記載のアルギン酸誘導体の溶液を、2価金属イオンを含む溶液中に滴下することで得られるゲルに光照射して光架橋アルギン酸構造体を得ることを含み、光架橋アルギン酸構造体が、架橋として2価金属イオンにより部分的に形成されるイオン架橋及び光照射により形成される化学架橋を含む、光架橋アルギン酸構造体を製造する方法であり、
例えば、下記式[各式中、波線右側は含まない]:
又は、更に好ましくは、前記態様[1b-3-3c]に記載のアルギン酸誘導体の溶液を、2価金属イオンを含む溶液中に滴下することで得られるゲルに光照射して光架橋アルギン酸構造体を得ることを含み、光架橋アルギン酸構造体が、架橋として2価金属イオンにより部分的に形成されるイオン架橋及び光照射により形成される化学架橋を含む、光架橋アルギン酸構造体を製造する方法であり、
例えば、下記式[各式中、波線右側は含まない]:
又は、更に好ましくは、前記態様[1b-3-3]に記載のアルギン酸誘導体の溶液を、2価金属イオンを含む溶液中に滴下することで得られるゲルに光照射して光架橋アルギン酸構造体を得ることを含み、光架橋アルギン酸構造体が、架橋として2価金属イオンにより部分的に形成されるイオン架橋及び光照射により形成される化学架橋を含む、光架橋アルギン酸構造体を製造する方法であり、
例えば、下記式[各式中、波線右側は含まない]:
又は、更に好ましくは、前記態様[1b-3-3-1]に記載のアルギン酸誘導体の溶液を、2価金属イオンを含む溶液中に滴下することで得られるゲルに光照射して光架橋アルギン酸構造体を得ることを含み、光架橋アルギン酸構造体が、架橋として2価金属イオンにより部分的に形成されるイオン架橋及び光照射により形成される化学架橋を含む、光架橋アルギン酸構造体を製造する方法であり、
例えば、下記式[各式中、波線右側は含まない]:
又は、更に好ましくは、前記態様[1b-3-3-2]に記載のアルギン酸誘導体の溶液を、2価金属イオンを含む溶液中に滴下することで得られるゲルに光照射して光架橋アルギン酸構造体を得ることを含み、光架橋アルギン酸構造体が、架橋として2価金属イオンにより部分的に形成されるイオン架橋及び光照射により形成される化学架橋を含む、光架橋アルギン酸構造体を製造する方法であり、
例えば、下記式[各式中、波線右側は含まない]:
特に好ましくは、下記式[各式中、波線右側は含まない]:
Arは、C6~10アリール基、又は複素環基(前記C6~10アリール基、又は複素環基は、ヒドロキシル基、シアノ基、ニトロ基、ハロゲン原子、C1~6アルキル基、ハロゲン化C1~6アルキル基、C1~6アルコキシ基、及び-NRARB基(-NRARB基における、RA及びRBは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、前記C6~10アリール基又は複素環基に、C1~6アルキル基及びC1~6アルコキシ基が又は2つのC1~6アルコキシ基が隣接して置換する場合、当該C1~6アルキル基及びC1~6アルコキシ基の各基のアルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、又は、当該2つのC1~6アルコキシ基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、環状エーテルを形成しても良く、又は、前記C6~10アリール基又は複素環基に、C1~6アルコキシ基及び-NHRG基(-NHRG基におけるRGは、C2~7アルカノイル基又はC1~6アルキルスルホニル基である)が隣接して置換している場合、当該C1~6アルコキシ基のアルキル基から任意の水素原子が1つ除かれた炭素原子と当該-NHRG基の水素原子が1つ除かれた窒素原子が結合することにより、3-N-(C2~7アルカノイル)オキサゾリジン環、3-N-(C1~6アルキルスルホニル)オキサゾリジン環、4-N-(C2~7アルカノイル)モルホリン環、4-N-(C1~6アルキルスルホニル)モルホリン環、4-N-(C2~7アルカノイル)-1,4-オキサゼパン環、又は4-N-(C1~6アルキルスルホニル)-1,4-オキサゼパン環を形成しても良い)を表わし;
-X-は、-O-、-NH-、又は-N(C1-6アルキル)-を表わし;
-A-は、式(AL-1)~(AL-4)(但し、-X-が、-NH-、又は-N(C1-6アルキル)の場合、式(AL-1)は除く);
)[各式中、両端の波線外側は含まない
]:
式(AL-1)~(AL-4)中のメチレン基(-CH2-)の水素原子は、ハロゲン原子、水酸基、C1~6アルキル基、ヒドロキシC1~6アルキル基、チオールC1~6アルキル基、C1~6アルキルチオC1~6アルキル基、カルボキシC1~6アルキル基、-NRaRb基、(RaRbN)-C1~6アルキル基、(RaRbN)C(=O)-C1~6アルキル基(前記-NRaRb基、(RaRbN)-C1~6アルキル基、又は(RaRbN)C(=O)-C1~6アルキル基における、Ra及びRbは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)、グアニジノC1~6アルキル基、C7~16アラルキル基、ヒドロキシC6~10アリールC1~6アルキル基、又はヘテロアリールC1~6アルキル基から選択される基で複数個(例えば、1~10個、又は1~5個)置き換えられても良く;式(AL-1)~(AL-4)中のメチレン基(-CH2-)の2つの水素原子がC1~6アルキル基に置き換えられた場合、当該各C1~6アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することによりC3~8シクロアルキル環を形成しても良く;式(AL-3)又は式(AL-4)中の-NH-基は、隣接する炭素原子に置換する前記置換基と共に、非芳香族複素環を形成しても良い](但し、2-(2-アミノエトキシ)エチル(E)-3-(4-メトキシフェニル)アクリレート、2-(2-アミノエトキシ)エチルシンナメート、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(4-プロポキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(3-メトキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(3,4-ジメトキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(4-エトキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(4-ニトロフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(4-イソプロピルフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(4-フルオロフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(2,5-ジメトキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(2-プロポキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(4-クロロフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(3-イソプロポキシフェニル)アクリルアミド、N-(2-(2-アミノエトキシ)エチル)シンナミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(p-トリル)アクリルアミド、(E)-N-(2-(2-(2-アミノエトキシ)エトキシ)エチル)-3-(4-ヒドロキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(フラン-2-イル)アクリルアミド、1,3-ジアミノプロパン-2-イルシンナメート、5-アミノペンチル(E)-3-(4-メトキシフェニル)アクリレート、3-アミノプロピル(E)-3-(4-メトキシフェニル)アクリレート、ジアミノメチルシンナメート、6-アミノヘキシルシンナメート、4-アミノブチルシンナメート、5-アミノペンチルシンナメート、8-アミノオクチルシンナメート、12-アミノドデシルシンナメート、3-アミノプロピルシンナメート、2-アミノエチルシンナメート、1,2-ジアミノエチルシンナメート、2-アミノエチル(E)-3-(ピリジン-4-イル)アクリレート、2-アミノエチル(E)-3-(チオフェン-2-イル)アクリレート、及び2-アミノエチル(E)-3-(フラン-2-イル)アクリレートは除く)で表される化合物、又は製薬学的に許容されるその塩、又はそれらの溶媒和物。
-X-は、-O-、又は-NH-であり;
-A-は、前記態様[23]中の式(AL-1)又は(AL-2)(但し、-X-が、-NH-、又は-N(C1-6アルキル)の場合、式(AL-1)は除く)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、1~10の整数であり;式(AL-2)中のmは、1~7の整数であり;
式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の水素原子は、ハロゲン原子、水酸基、C1~6アルキル基、ヒドロキシC1~6アルキル基、チオールC1~6アルキル基、C1~6アルキルチオC1~6アルキル基、カルボキシC1~6アルキル基、-NRaRb基、(RaRbN)-C1~6アルキル基、(RaRbN)C(=O)-C1~6アルキル基(前記-NRaRb基、(RaRbN)-C1~6アルキル基、又は(RaRbN)C(=O)-C1~6アルキル基における、Ra及びRbは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)、グアニジノC1~6アルキル基、C7~16アラルキル基、ヒドロキシC6~10アリールC1~6アルキル基、又はヘテロアリールC1~6アルキル基から選択される基で複数個(例えば、1~10個、又は1~5個)置き換えられても良く)(但し、2-(2-アミノエトキシ)エチル(E)-3-(4-メトキシフェニル)アクリレート、2-(2-アミノエトキシ)エチルシンナメート、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(4-プロポキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(3-メトキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(3,4-ジメトキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(4-エトキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(4-ニトロフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(4-イソプロピルフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(4-フルオロフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(2,5-ジメトキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(2-プロポキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(4-クロロフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(3-イソプロポキシフェニル)アクリルアミド、N-(2-(2-アミノエトキシ)エチル)シンナミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(p-トリル)アクリルアミド、(E)-N-(2-(2-(2-アミノエトキシ)エトキシ)エチル)-3-(4-ヒドロキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(フラン-2-イル)アクリルアミド、1,3-ジアミノプロパン-2-イルシンナメート、5-アミノペンチル(E)-3-(4-メトキシフェニル)アクリレート、3-アミノプロピル(E)-3-(4-メトキシフェニル)アクリレート、ジアミノメチルシンナメート、6-アミノヘキシルシンナメート、4-アミノブチルシンナメート、5-アミノペンチルシンナメート、8-アミノオクチルシンナメート、3-アミノプロピルシンナメート、2-アミノエチルシンナメート、1,2-ジアミノエチルシンナメート、2-アミノエチル(E)-3-(ピリジン-4-イル)アクリレート、2-アミノエチル(E)-3-(チオフェン-2-イル)アクリレート、及び2-アミノエチル(E)-3-(フラン-2-イル)アクリレートは除く)である化合物、又は製薬学的に許容されるその塩、又はそれらの溶媒和物である。
-X-は、-O-、又は-NH-であり;
-A-は、前記態様[23]中の式(AL-1)又は(AL-2)(但し、-X-が、-NH-、又は-N(C1-6アルキル)の場合、式(AL-1)は除く)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、1~8の整数であり;式(AL-2)中のmは、1~5の整数であり;
式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の水素原子は、ハロゲン原子、水酸基、C1~6アルキル基、ヒドロキシC1~6アルキル基、-NRaRb基(-NRaRb基における、Ra及びRbは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)、C7~16アラルキル基、又はヘテロアリールC1~6アルキル基から選択される基で複数個(例えば、1~10個、又は1~5個)置き換えられても良く)(但し、2-(2-アミノエトキシ)エチル(E)-3-(4-メトキシフェニル)アクリレート、2-(2-アミノエトキシ)エチルシンナメート、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(4-プロポキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(3-メトキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(3,4-ジメトキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(4-エトキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(4-ニトロフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(4-イソプロピルフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(4-フルオロフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(2,5-ジメトキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(2-プロポキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(4-クロロフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(3-イソプロポキシフェニル)アクリルアミド、N-(2-(2-アミノエトキシ)エチル)シンナミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(p-トリル)アクリルアミド、(E)-N-(2-(2-(2-アミノエトキシ)エトキシ)エチル)-3-(4-ヒドロキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(フラン-2-イル)アクリルアミド、1,3-ジアミノプロパン-2-イルシンナメート、5-アミノペンチル(E)-3-(4-メトキシフェニル)アクリレート、3-アミノプロピル(E)-3-(4-メトキシフェニル)アクリレート、ジアミノメチルシンナメート、6-アミノヘキシルシンナメート、4-アミノブチルシンナメート、5-アミノペンチルシンナメート、8-アミノオクチルシンナメート、3-アミノプロピルシンナメート、2-アミノエチルシンナメート、1,2-ジアミノエチルシンナメート、2-アミノエチル(E)-3-(ピリジン-4-イル)アクリレート、2-アミノエチル(E)-3-(チオフェン-2-イル)アクリレート、及び2-アミノエチル(E)-3-(フラン-2-イル)アクリレートは除く)である化合物、又は製薬学的に許容されるその塩、又はそれらの溶媒和物である。
-X-は、-O-、又は-NH-であり:
-A-は、前記態様[23]中の式(AL-1)又は(AL-2)(但し、-X-が、-NH-、又は-N(C1-6アルキル)の場合、式(AL-1)は除く)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、2~6の整数であり;式(AL-2)中のmは、1~3の整数である)(但し、2-(2-アミノエトキシ)エチル(E)-3-(4-メトキシフェニル)アクリレート、2-(2-アミノエトキシ)エチルシンナメート、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(4-プロポキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(3-メトキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(3,4-ジメトキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(4-エトキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(4-ニトロフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(4-イソプロピルフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(4-フルオロフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(2,5-ジメトキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(2-プロポキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(4-クロロフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(3-イソプロポキシフェニル)アクリルアミド、N-(2-(2-アミノエトキシ)エチル)シンナミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(p-トリル)アクリルアミド、(E)-N-(2-(2-(2-アミノエトキシ)エトキシ)エチル)-3-(4-ヒドロキシフェニル)アクリルアミド、1,3-ジアミノプロパン-2-イルシンナメート、5-アミノペンチル(E)-3-(4-メトキシフェニル)アクリレート、3-アミノプロピル(E)-3-(4-メトキシフェニル)アクリレート、6-アミノヘキシルシンナメート、4-アミノブチルシンナメート、5-アミノペンチルシンナメート、3-アミノプロピルシンナメート、2-アミノエチルシンナメート、1,2-ジアミノエチルシンナメート、及び2-アミノエチル(E)-3-(ピリジン-4-イル)アクリレートは除く)ある化合物、又は製薬学的に許容されるその塩、又はそれらの溶媒和物である。
例えば、Arは、フェニル基、4-フルオロフェニル基、4-(トリフルオロメチル)フェニル基、4-メトキシフェニル基、4-シアノフェニル基、2,3-ジヒドロベンゾ[b][1,4]ジオキシニル基、又は2-ピリジル基であり;
-X-は、-O-、又は-NH-であり:
-A-は、前記態様[1-3]中の式(AL-1-1)、(AL-2-1)又は(AL-2-2)[各式中、両端の波線外側は含まない](但し、2-(2-アミノエトキシ)エチル(E)-3-(4-メトキシフェニル)アクリレート、2-(2-アミノエトキシ)エチルシンナメート、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(3-メトキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(3,4-ジメトキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(4-フルオロフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(2,5-ジメトキシフェニル)アクリルアミド、N-(2-(2-アミノエトキシ)エチル)シンナミド、3-アミノプロピル(E)-3-(4-メトキシフェニル)アクリレート、及び3-アミノプロピルシンナメートは除く)である化合物、又は製薬学的に許容されるその塩、又はそれらの溶媒和物であり;
例えば、下記式:
-X-は、-O-、-NH-、又は-N(C1-6アルキル)-を表わし;
-A-は、式(AL-1)~(AL-4)[各式中、両端の波線外側は含まない]:
式(AL-1)~(AL-4)中のメチレン基(-CH2-)の水素原子は、ハロゲン原子、水酸基、C1~6アルキル基、ヒドロキシC1~6アルキル基、チオールC1~6アルキル基、C1~6アルキルチオC1~6アルキル基、カルボキシC1~6アルキル基、-NRaRb基、(RaRbN)-C1~6アルキル基、(RaRbN)C(=O)-C1~6アルキル基(前記-NRaRb基、(RaRbN)-C1~6アルキル基、又は(RaRbN)C(=O)-C1~6アルキル基における、Ra及びRbは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)、グアニジノC1~6アルキル基、C7~16アラルキル基、ヒドロキシC6~10アリールC1~6アルキル基、又はヘテロアリールC1~6アルキル基から選択される基で複数個(例えば、1~10個、又は1~5個)置き換えられても良く;式(AL-1)~(AL-4)中のメチレン基(-CH2-)の2つの水素原子がC1~6アルキル基に置き換えられた場合、当該各C1~6アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することによりC3~8シクロアルキル環を形成しても良く);式(AL-3)又は式(AL-4)中の-NH-基は、隣接する炭素原子に置換する前記置換基と共に、非芳香族複素環を形成しても良い)]で表される化合物、又は製薬学的に許容されるその塩、又はそれらの溶媒和物。
-X-は、-O-、又は-NH-であり;
-A-は、前記態様[23]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、1~10の整数であり;式(AL-2)中のmは、1~7の整数であり;
式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の水素原子は、ハロゲン原子、水酸基、C1~6アルキル基、ヒドロキシC1~6アルキル基、チオールC1~6アルキル基、C1~6アルキルチオC1~6アルキル基、カルボキシC1~6アルキル基、-NRaRb基、(RaRbN)-C1~6アルキル基、(RaRbN)C(=O)-C1~6アルキル基(前記-NRaRb基、(RaRbN)-C1~6アルキル基、又は(RaRbN)C(=O)-C1~6アルキル基における、Ra及びRbは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)、グアニジノC1~6アルキル基、C7~16アラルキル基、ヒドロキシC6~10アリールC1~6アルキル基、又はヘテロアリールC1~6アルキル基から選択される基で複数個(例えば、1~10個、又は1~5個)置き換えられても良く;式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の2つの水素原子がC1~6アルキル基に置き換えられる場合、当該各C1~6アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することによりC3~8シクロアルキル環を形成しても良い)である化合物、又は製薬学的に許容されるその塩、又はそれらの溶媒和物である。
-X-は、-O-、又は-NH-であり;
-A-は、前記態様[24]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、1~8の整数であり;式(AL-2)中のmは、1~5の整数である)であり;
式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の水素原子は、ハロゲン原子、水酸基、C1~6アルキル基、ヒドロキシC1~6アルキル基、-NRaRb基(-NRaRb基における、Ra及びRbは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)、C7~16アラルキル基、又はヘテロアリールC1~6アルキル基から選択される基で複数個(例えば、1~10個、又は1~5個)置き換えられても良く;式(AL-1)又は(AL-2)中のメチレン基(-CH2-)の2つの水素原子がC1~6アルキル基に置き換えられる場合、当該各C1~6アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することによりC3~8シクロアルキル環を形成しても良い)である化合物、又は製薬学的に許容されるその塩、又はそれらの溶媒和物である。
-X-は、-O-、又は-NH-であり:
-A-は、前記態様[24]中の式(AL-1)又は(AL-2)[各式中、両端の波線外側は含まない](式(AL-1)中のnは、2~6の整数であり;式(AL-2)中のmは、1~3の整数であり)である化合物、又は製薬学的に許容されるその塩、又はそれらの溶媒和物である。
例えば、Arは、フェニル基、又は4-メトキシフェニル基であり;
-X-は、-O-であり:
-A-は、前記態様[1-3]中の式(AL-1-1)[式中、両端の波線外側は含まない]である化合物、又は製薬学的に許容されるその塩、又はそれらの溶媒和物であり;
例えば、下記式:
本明細書中、アルギン酸と記載する場合、アルギン酸、アルギン酸エステル、及びそれらの塩(例えば、アルギン酸ナトリウム)からなる群から選択される少なくとも1種のアルギン酸(「アルギン酸類」という場合がある)を意味する。用いられるアルギン酸は、天然由来でも合成物であってもよいが、天然由来であるのが好ましい。好ましく用いられるアルギン酸類は、レッソニア、マクロシスティス、ラミナリア、アスコフィラム、ダービリア、カジカ、アラメ、コンブなどの褐藻類から抽出される生体内吸収性の多糖類であって、D-マンヌロン酸(M)とL-グルロン酸(G)という2種類のウロン酸が直鎖状に重合したポリマーである。より具体的には、D-マンヌロン酸のホモポリマー画分(MM画分)、L-グルロン酸のホモポリマー画分(GG画分)、およびD-マンヌロン酸とL-グルロン酸がランダムに配列した画分(M/G画分)が任意に結合したブロック共重合体である。
日本薬局方(第16版)の粘度測定法に従い、回転粘度計法(コーンプレート型回転粘度計)を用いて測定した。具体的な測定条件は以下のとおりである。試料溶液の調製は、MilliQ水を用いて行った。測定機器は、コーンプレート型回転粘度計(粘度粘弾性測定装置レオストレスRS600(Thermo Haake GmbH)センサー:35/1)を用いた。回転数は、1w/w%アルギン酸ナトリウム溶液測定時は1rpmとした。読み取り時間は、2分間測定し、開始1分から2分までの平均値とした。3回の測定の平均値を測定値とした。測定温度は20℃とした。
(1)ゲル浸透クロマトグラフィー(GPC)と、(2)GPC-MALSの2種類の測定法で測定した。測定条件は以下のとおりである。
試料に溶離液を加え溶解後、0.45μmメンブランフィルターろ過したものを測定溶液とした。
(1)ゲル浸透クロマトグラフィー(GPC)測定
[測定条件(相対分子量分布測定)]
カラム:TSKgel GMPW-XL×2+G2500PW-XL(7.8mm I.D.×300mm×3本)
溶離液:200mM硝酸ナトリウム水溶液
流量:1.0mL/min
濃度:0.05%
検出器:RI検出器
カラム温度:40℃
注入量:200μL
分子量標準:標準プルラン、グルコース
[屈折率増分(dn/dc)測定(測定条件)]
示差屈折率計:Optilab T-rEX
測定波長:658nm
測定温度:40℃
溶媒:200mM硝酸ナトリウム水溶液
試料濃度:0.5~2.5mg/mL(5濃度)
カラム:TSKgel GMPW-XL×2+G2500PW-XL(7.8mm I.D.×300mm×3本)
溶離液:200mM硝酸ナトリウム水溶液
流量:1.0mL/min
濃度:0.05%
検出器:RI検出器、光散乱検出器(MALS)
カラム温度:40℃
注入量:200μL
ここでは、アルギン酸誘導体が提供される。アルギン酸誘導体は、アルギン酸のカルボキシル基の一部が下記式(I)[式中、波線右側は含まない]:
ここで、光反応性基である前記式(I)中、部分構造式(I-S)[式中、波線右側は含まない]:
式(AL-1)~(AL-4)中のメチレン基(-CH2-)の水素原子は、ハロゲン原子、水酸基、C1~6アルキル基、ヒドロキシC1~6アルキル基、チオールC1~6アルキル基、C1~6アルキルチオC1~6アルキル基、カルボキシC1~6アルキル基、-NRaRb基、(RaRbN)-C1~6アルキル基、(RaRbN)C(=O)-C1~6アルキル基(前記-NRaRb基、(RaRbN)-C1~6アルキル基、又は(RaRbN)C(=O)-C1~6アルキル基における、Ra及びRbは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)、グアニジノC1~6アルキル基、C7~16アラルキル基、ヒドロキシC6~10アリールC1~6アルキル基、又はヘテロアリールC1~6アルキル基等の基から選択される基で複数個(例えば、1~10個、又は1~5個)置き換えられても良く;式(AL-1)~(AL-4)中のメチレン基(-CH2-)の2つの水素原子がC1~6アルキル基に置き換えられた場合、当該各C1~6アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することによりC3~8シクロアルキル環を形成しても良く;式(AL-3)又は式(AL-4)中の-NH-基は、隣接する炭素原子に置換する前記置換基と共に、非芳香族複素環を形成しても良い)である。
アルギン酸誘導体は、光反応基部分におけるリンカーの末端アミノ基とアルギン酸類のカルボキシル基を縮合反応させることにより得られる。
式(SM-1)で表されるアルデヒド(式(SM-1)のアルデヒドは、市販化合物、又は市販化合物から文献公知の製造方法により製造できる化合物である)を用い、文献公知の方法、例えば、『実験化学講座 第5版 13、有機化合物の合成I、炭化水素、アルケンの合成、118-139頁、2004年、丸善』、等に記載された方法に準じて、ウィッティヒ試薬(例えば、エトキシカルボニルメチルトリフェニルホスホニウムクロリド、エトキシカルボニルメチルトリフェニルホスホニウムブロミド、トリフェニルホスホラニリデンエチルアセテート、ビス-2,2,2-トリフルオロエトキシホスフィニルアセテート、ジオルトトリルホスホノエチルアセテート、ジメチルホスホノエチルアセテート、ジエチルホスホノエチルアセテート、又は1-トリメチルシリルエチルアセテート、等)又はホーナー・エモンズ試薬を、水素化ナトリウム、ブチルリチウム、ピペラジン、モルホリン、トリエチルアミン、リチウムジイソプロピルアミド、リチウムビス(トリメチルシリル)アミド、ソジウムビス(トリメチルシリル)アミド、ポタシウムビス(トリメチルシリル)アミド、又はホスファゼンベース-P4-tert-ブチル等の塩基存在下、メタノール、エタノールなどのアルコール系溶媒、N,N-ジメチルホルムアミドなどの極性溶媒、1,4-ジオキサン、テトラヒドロフラン等のエーテル系溶媒、ベンゼン、トルエン、キシレン等の芳香族炭化水素系溶媒、又はこれらの混合溶媒等から選択される溶媒中、-78℃から溶媒が還流する温度で反応を行うことで、式(IM-A-1)[式中RDは、C1~6アルキル基を表わす]で表わされる化合物を製造することができる。
[製造方法A]<工程1>で得られる、式(IM-A-1)の化合物を用いて、水及び、水と混和する溶媒(例えば、メタノール、エタノール、テトラヒドロフラン、N,N- ジメチルホルムアミド、ジメチルスルホキシド等の溶媒)の混合溶媒中、無機塩基、例えば、水酸化リチウム、水酸化ナトリウム、又は水酸化カリウム、等を加えて、0℃から溶媒が還流する温度で加水分解することで、式(IM-A-2)の化合物を製造することができる。
[製造方法A]<工程2>または上記別法で得られる、式(IM-A-1)の化合物及び式(RG-A-1)(式(RG-A-1)の化合物は、市販化合物、又は市販化合物から文献公知の製造方法により製造できる化合物である。Pは、アミノ基の保護基であり、例えば、グリーン(Greene)らの『プロテクティブ・グループス・イン・オルガニック・シンセシス(Protective Groups in Organic Synthesis) 第4版、2007年、ジョン ウィリー アンド サンズ(John Wiley & Sons)』の成書に記載された、保護基を適宜選択することが可能である)を用いて、文献公知の方法、例えば、『実験化学講座 第5版 16、有機化合物の合成IV、カルボン酸および誘導体、エステル類、35-70頁、酸アミドおよび酸イミド、118-154頁、アミノ酸・ペプチド、258-283頁、2007年、丸善』、等に記載された方法に準じて1,3-ジシクロヘキシルカルボジイミド(DCC)、1-エチル-3-(3-ジメチルアミノプロピル)カルボジイミド塩酸塩(WSC・HCl)、ベンゾトリアゾール-1-イルオキシトリス(ジメチルアミノ)ホスホニウムヘキサフルオロホスフェイト(BOP試薬)、ビス(2-オキソ-3-オキサゾリジニル)ホスフィニッククロリド(BOP-Cl)、2-クロロ-1,3-ジメチルイミダゾリニウムヘキサフルオロホスフェイト(CIP)、4-(4,6-ジメトキシ-1,3,5-トリアジン-2-イル)-4-メチルモルホリニウムクロリド(DMT-MM)等の縮合剤の存在下、ジクロロメタン、クロロホルム等のハロゲン系溶媒、ジエチルエーテル、テトラヒドロフラン等のエーテル系溶媒、トルエン、ベンゼン等の芳香族炭化水素系溶媒、N,N-ジメチルホルムアミド等の極性溶媒、メタノール、エタノール、2-プロパノール等のアルコール系溶媒等から選択される溶媒中、トリエチルアミン、ピリジン等の塩基の存在下または非存在下、0℃から溶媒が還流する温度で反応させることにより、式(IM-A-3)の化合物を製造することができる。
[製造方法A]<工程3>で得られる、式(IM-A-3)を用いて、文献公知の方法、例えば、『グリーン(Greene)らの『プロテクティブ・グループス・イン・オルガニック・シンセシス(Protective Groups in Organic Synthesis) 第4版、2007年、ジョン ウィリー アンド サンズ(John Wiley & Sons)』の成書に記載の方法により、保護基の種類により適宜脱保護法を選択して反応を行うことで、式(AM-1)で表わされる化合物、又は式(AM-1)の塩として製造することができる。
式(SM-2)及び式(RG-B-1)[式(SM-2))及び式(RG-B-1)の化合物は、市販化合物、又は市販化合物から文献公知の製造方法により製造できる化合物である]を用いて、文献公知の方法、例えば 『Organic Reactions,27,1982年、(Hoboken, NJ, United States)』に記載された方法に準じて、酢酸パラジウム(II)(Pd(OAc)2)等のパラジウム触媒、トリス(o-トリル)ホスフィン等のホスフィン系試薬、及びトリエチルアミン等の有機塩基存在下、トルエン、キシレン、N,N-ジメチルホルムアミド、N,N-ジメチルアセトアミド、N-メチルピロリドン、1,2-ジメトキシエタン、アセトニトリル(アセトニトリル/水)、1,4-ジオキサン(1,4-ジオキサン/水)、テトラヒドロフラン(テトラヒドロフラン/水)等の溶媒もしくはこれらの混合溶媒から選択される溶媒を用いて、0℃から溶媒が還流する温度で反応を行うことで、式(IM-B-1)で表される化合物を製造することができる。
[製造方法B]<工程1>で得られる式(IM-B-1)を用いて、前記[製造方法A]<工程3>に準じる反応を行うことで、式(IM-B-2)の化合物を製造することができる。
[製造方法B]<工程2>で得られる式(IM-B-2)を用いて、前記[製造方法A]<工程4>に準じる反応を行うことで、式(AM-2)で表わされる化合物、又は式(AM-2)の塩として製造することができる。
式(SM-1)及び4-ホスホノクロトン酸トリアルキル(当該化合物は、市販化合物、又は市販化合物から文献公知の製造方法により製造できる:例えば、4-ホスホノクロトン酸トリエチル、等がある)を用いて、文献公知の方法、例えば 『Journal of American Chemical Society、127(43)、15028-15029頁、2005年』等に記載された方法に準じて反応を行うことで、式(IM-B-3)で表わされる化合物を製造することができる。
[製造方法B]<工程4>で得られる式(IM-B-3)を用いて、[製造方法A]<工程2>に準じる反応を行うことで、式(IM-B-1)で表わされる化合物を製造することができる。
0.5重量%~1重量%のアルギン酸水溶液と式(AM-1)、式(AM-2)又はそれらの塩を、文献公知の方法、例えば、『実験化学講座 第5版 16、有機化合物の合成IV、カルボン酸および誘導体、酸アミドおよび酸イミド、118-154頁、アミノ酸・ペプチド、258-283頁、2007年、丸善』、等に記載された方法に準じて1,3-ジシクロヘキシルカルボジイミド(DCC)、1-エチル-3-(3-ジメチルアミノプロピル)カルボジイミド塩酸塩(WSC・HCl)、ベンゾトリアゾール-1-イルオキシトリス(ジメチルアミノ)ホスホニウムヘキサフルオロホスフェイト(BOP試薬)、ビス(2-オキソ-3-オキサゾリジニル)ホスフィニッククロリド(BOP-Cl)、2-クロロ-1,3-ジメチルイミダゾリニウムヘキサフルオロホスフェイト(CIP)、4-(4,6-ジメトキシ-1,3,5-トリアジン-2-イル)-4-メチルモルホリニウムクロリド(DMT-MM)等の縮合剤の存在下、水、1、4-ジオキサン等のエーテル系溶媒、メタノール、エタノール等のアルコール系溶媒、N,N-ジメチルホルムアミド等の極性溶媒、又はそれらの混合溶媒中(但し、混合溶媒は、アルギン酸が析出しない程度の混合溶媒である)、炭酸水素ナトリウム、炭酸ナトリウム等の無機塩基又はトリエチルアミン、ピリジン等の有機塩基の存在下又は非存在下、0℃から50℃の温度で反応させることにより、式(I)で表わされる光反応性基が導入されたアルギン酸誘導体を製造することができる。
架橋アルギン酸は、(i)2価の金属イオン結合を介したものと、(ii)化学結合を介したものと、又は(iii)2価の金属イオン結合及び化学結合の両方を介したものがある。何れの架橋アルギン酸は、ゲル状から半固体、場合によってはスポンジ様の形態を形成する特性を有している。
光架橋アルギン酸は、前記式(I)で表わされる光反応性基が導入されたアルギン酸誘導体に光照射をして光環化反応を行うことにより得ることができるものである。光架橋アルギン酸構造体は、アルギン酸誘導体が光架橋基(光反応により形成されるシクロブタン環による架橋)を介して三次元の網目構造を形成する。好ましいアルギン酸誘導体は、架橋後の架橋アルギン酸の安定性が改善したものである。
光架橋アルギン酸構造体は、前記式(I)で表わされる光反応性基が導入されたアルギン酸誘導体に光照射をして架橋反応を施すことを含む方法により得ることができる。例えば、以下の方法によって調製することが可能だが、これらに限定されるものでない。
本明細書において、アルギン酸誘導体、又は光架橋アルギン酸構造体は、生体適合性を有する。本明細書において、生体適合性とは、生体用材料(ここでは、式(I)で表わされる光反応性基が導入されたアルギン酸誘導体、及び当該アルギン酸誘導体を用いて製造された光架橋アルギン酸構造体のことを言う)と生体間の相互作用、前記生体用材料に隣接する組織の局所的反応、又は全身的反応等の反応を引き起こさない性質を、生体適合性(biocompatibility)を有するという。
光架橋アルギン酸構造体の安定性は、例えば、ゲル安定性を測定すること、透過性はゲル透過率を測定することなどで確認することができる。
容器に入れた光架橋アルギン酸構造体ゲルにリン酸緩衝生理食塩水(PBS)を添加し、PBS中に漏出したアルギン酸の濃度(μg/mL)を測定する。測定したアルギン酸濃度を、架橋アルギン酸構造体ゲルを分解することで得た全アルギン酸濃度で除した値を百分率で示した値を、崩壊率とする。ゲル安定性は、具体的には、後述の実施例に記載の方法により求めることができる。
フルオレセインイソチオシアナート-デキストランを内包した光架橋アルギン酸構造体ゲルを作製し、容器に入れた前記ゲルに生理食塩水を添加し、生理食塩水中に漏出したデキストラン濃度を測定する。測定したデキストランの濃度を、フルオレセインイソチオシアネート-デキストラン内包の光架橋アルギン酸構造体ゲルを分解することで得た全デキストラン濃度で除した値を百分率で示した値がゲル透過率である。ゲル透過率は、具体的には、後述の実施例に記載の方法により求めることができる。
例えば、内容物としてフルオレセインイソチオシアナート-デキストランを内包した架橋アルギン酸構造体ゲルは以下の方法にて調製できる。
(1)式(I)で表わされる光反応性基が導入されたアルギン酸誘導体の溶液とフルオレセインイソチオシアナート-デキストラン溶液を混和する。
(2)(1)で得られた混合溶液を、カルシウムイオンを含む溶液中に滴下し得られたゲルに、光照射を行うことで、イオン架橋及び光架橋(化学架橋)が形成されたフルオレセインイソチオシアナート-デキストラン内包の光架橋アルギン酸構造体ゲルが得られる。
アルギン酸誘導体は、食品、医療、化粧品、繊維、製紙などの幅広い分野で、従来のアルギン酸の代わりに用いることができる。アルギン酸誘導体または光架橋アルギン酸構造体の好ましい用途としては、具体的には、創傷被覆材、術後癒着防止材、薬剤徐放用基材、細胞培養用基材、細胞移植用基材等の医療用材料が挙げられる。
4>と同様の操作を行い、標記化合物(0.9 g)を白色固体として得た。
500 mg)とtert-ブチル(3-ヒドロキシプロピル)カルバメート(405 mg)の塩化メチレン(5.0 mL)溶液に、1-ヒドロキシベンゾトリアゾール一水和物(372 mg)、N、N-ジメチル-4-アミノピリジン(28 mg)、1-エチル-3-(3-ジメチルアミノプロピル)カルボジイミド 塩酸塩(488 mg)加え、室温で16時間攪拌した。反応液にN-メチルピロリドン(3 mL)を加え、50℃で6時間攪拌した。酢酸エチル(20 mL)、水(10mL)を加え、分液した。有機層を水(5 mL、3回)、飽和食塩水(5 mL)で順次洗浄し、無水硫酸ナトリウムで乾燥後、溶媒を減圧留去した。得られた油状物をシリカゲルカラムクロマトグラフィー(ヘプタン~30%酢酸エチル/ヘプタン)で精製後、ヘプタンでトリチュレートした。得られた固体をろ取し、ヘプタンで洗浄後、減圧乾燥して、標記化合物(263 mg)を白色固体として得た。
程4>と同様の操作を行い標記化合物(148 mg)を白色固体として得た。
程4>と同様の操作を行い標記化合物(0.4 g)を無色液体として得た。
程4>と同様の操作を行い、標記化合物(0.56 g)を白色粉末として得た。
4 mL)、N,N-ジメチルホルムアミド(1.8 μL)を加え、80℃で40分間
撹拌した。得られた溶液を減圧濃縮し、塩化メチレン(1 mL)で2回共沸した。得られた固体に、塩化メチレン(2 mL)を加え、氷水冷下で、tert-ブチル(2-(2-ヒドロキシエトキシ)エチル)カルバメート(0.57 g)、トリエチルアミン(0.97 mL)、N,N-ジメチルアミノピリジン(0.06 g)の塩化メチレン(2 mL)溶液に加えた。室温で30分間撹拌した後、酢酸エチル(20 mL)、水(10 mL)を加え、分液した。有機層を半飽和重層水(10 mL)、水(5 mL)、飽和食塩水(5 mL)で、順次洗浄し、無水硫酸ナトリウムで乾燥後、溶媒を減圧留去した。得られた油状物をシリカゲルカラムクロマトグラフィー(16%酢酸エチル/ヘプタン~酢酸エチル)で精製して、標記化合物(0.78 g)を白色アモルファスとして得た。
ン(2.35 mL)に溶解させ、水冷下、4規定-塩化水素/ジオキサン(5.48
mL)をゆっくり加えた。反応液を室温で1時間30分攪拌し、ジイソプロピルエーテル
(50 mL)を加えた。析出した固体をろ取し、ジイソプロピルエーテルで洗浄した
後、減圧乾燥することにより標記化合物(0.56 g)を白色固体として得た。
工程4>と同様の操作を行い、標記化合物(0.39 g)を白色固体として得た。
操作を行い、標記化合物(0.14 g)を白色固体として得た。
化合物として得た。
光反応性基(光架橋基)の導入率は、アルギン酸の繰り返し単位であるウロン酸単糖単位あたりに導入された光架橋基の数を百分率で表した値を意味する。導入率の算出に必要なアルギン酸の量は、検量線を利用したカルバゾール硫酸法により測定し、光架橋基の量は、検量線を利用した吸光度測定法により測定する。
実施例で得られた光反応性基が導入されたアルギン酸誘導体の固体を0.15 mol/LのNaClを含む10mmol/Lリン酸緩衝液(pH7.4)に溶解し0.2%溶液を調製し、孔径0.2μmのセルロースアセテート製ろ過フィルター(DISMIC-25cs、ADVANTEC社)を通し不溶物を除いた後、この200μLをSuperose6 Increase10/300 GLカラム(GEヘルスケアサイエンス社)に供した。ゲルろ過は、クロマトグラフ装置としてAKTA Explorer 10Sを、展開溶媒として0.15 mol/ALaClを含む10mmol/Lリン酸緩衝液(pH7.4)を使用し、室温で流速0.6mL/mimの条件で実施した。サンプルの溶出プロファイルは、280 nmの吸収をモニターし作製した。得られたクロマトグラムは、Unicorn5.31ソフトウエア(GEヘルスケアサイエンス社)にて解析し、ピーク範囲を決定した。
(ゲル安定性の測定(1))
(実施例1)<工程5-2>で得られたアルギン酸誘導体(EX1-b)、(実施例2)<工程3-2>で得られたアルギン酸誘導体(EX2-b)、及びアルギン酸(A-2;対照)を、濃度が1%となるよう水に溶かしてアルギン酸水溶液を得た。この水溶液を18ゲージの注射針を装着した注射筒に入れ、この注射筒を流速1mL/分に設定したシリンジポンプに設置し、濃度が300mmol/Lの塩化カルシウム溶液に30秒間滴下し、5分間撹拌して光反応性基導入アルギン酸ゲルを得た。このゲルを10mLのリン酸緩衝生理食塩水(PBS)で1度洗浄した後、UV硬化装置(セン特殊光源株式会社、HLR100T-2)を用いて水中で10分間光照射を行い、光架橋アルギン酸構造体ゲルを得た。容器に入れた前記ゲルに19.5mLのPBSを添加し、37℃で振盪して、経時的に水溶液を回収し、回収した量と同量のPBSを補充した。試験終了後、試験溶液にアルギン酸リアーゼ(ニッポンジーン、319-08261)を2μL添加し、37℃で1時間振盪させてゲルを全て崩壊させ、水溶液を回収した。回収した水溶液中のアルギン酸濃度をカルバゾール硫酸法により測定し、各時点の水溶液中アルギン酸濃度を既に回収したアルギン酸濃度で補正した値を、全時点のアルギン酸濃度および試験終了後のアルギン酸濃度から算出した全アルギン酸濃度で除した値を百分率で表した値を崩壊率とし、ゲル安定性の指標とした。
対照として用いたアルギン酸(A-2)から作成した光架橋アルギン酸構造体ゲルが4時間でほぼ溶解したのに対し、本実施例の光架橋アルギン酸誘導体はいずれも安定性が向上した。また、アルギン酸誘導体(EX2-b)から作成した光架橋アルギン酸構造体ゲルに比し、アルギン酸誘導体(EX1-b)から作成した光架橋アルギン酸構造体ゲルで、安定性がより向上した。
(実施例6)<工程4-2>で得られたアルギン酸誘導体(EX6-b)を、濃度が1%となるよう水に溶かしてアルギン酸水溶液を得た。この水溶液を18ゲージの注射針を装着した注射筒に入れ、この注射筒を流速1 mL/分に設定したシリンジポンプに設置し、濃度が30 mmol/Lの塩化カルシウム溶液に30秒間滴下し、5分間撹拌して光反応性基導入アルギン酸ゲルを得た。このゲルを10 mLのリン酸緩衝生理食塩水(PBS)で1度洗浄した後、UV硬化装置(セン特殊光源株式会社、HLR100T-2)を用いて水中で3、10、60分間光照射を行い、光架橋アルギン酸ゲルを得た。このゲルに20 mLのPBSを添加し、37℃で振盪して、1、2、4、8、24、48、72、144時間後に水溶液を回収し、回収した量と同量のPBSを補充した。試験終了後、試験溶液にアルギン酸リアーゼ(Creative enzymes、NATE-1563)を10 μL添加し、37℃で終夜振盪させてゲルを全て崩壊させ、水溶液を回収した。回収した水溶液中のアルギン酸濃度をカルバゾール硫酸法により測定し、各時点の水溶液中アルギン酸濃度を既に回収したアルギン酸濃度で補正した値を、全時点のアルギン酸濃度および試験終了後のアルギン酸濃度から算出した全アルギン酸濃度で除した値を百分率で表した値を崩壊率とし、ゲル安定性の指標とした。
対照として用いたアルギン酸誘導体(EX6-b)から作成したカルシウム架橋アルギン酸構造体ゲル(光照射時間0分)が1時間で98.7%溶解したのに対し、アルギン酸誘導体(EX6-b)から作成した各光架橋アルギン酸ゲル(光照射時間:3分、10分、及び30分)は安定性が向上した。
(実施例9)で得られたアルギン酸誘導体(EX9-a)、及び(実施例12)で得られたアルギン酸誘導体(EX12-a)を、濃度が1%となるよう水に溶かしてアルギン酸水溶液を得た。この水溶液を18ゲージの注射針を装着した注射筒に入れ、この注射筒を流速1 mL/分に設定したシリンジポンプに設置し、濃度が30 mmol/Lの塩化カルシウム溶液に30秒間滴下し、5分間撹拌して光架橋基導入アルギン酸ゲルを得た。このゲルを10 mLのリン酸緩衝生理食塩水(PBS)で1度洗浄した後、UV硬化装置(セン特殊光源株式会社、HLR100T-2)を用いてPBS中で10分間光照射を行い、光架橋アルギン酸ゲルを得た。このゲルに20 mLのPBSを添加し、37℃で振盪して、1.5、6、24、96時間後に水溶液を回収し、回収した量と同量のPBSを補充した。試験終了後、試験溶液にアルギン酸リアーゼ(ニッポンジーン、319-08261)を5 μL添加し、37℃で3時間振盪させてゲルを全て崩壊させ、水溶液を回収した。回収した水溶液中のアルギン酸濃度をカルバゾール硫酸法により測定し、各時点の水溶液中アルギン酸濃度を既に回収したアルギン酸濃度で補正した値を、全時点のアルギン酸濃度および試験終了後のアルギン酸濃度から算出した全アルギン酸濃度で除した値を百分率で表した値を崩壊率とし、ゲル安定性の指標とした。
本実施例の光架橋アルギン酸ゲルはいずれも安定性が高い(96時間で、EX9-a由来の光架橋アルギン酸ゲルが約12%、EX12-a由来の光架橋アルギン酸ゲルが約11%の崩壊率)ことが確認できた。
(実施例10)で得られたアルギン酸誘導体(EX10-a)を、濃度が1%となるよう水に溶かしてアルギン酸水溶液を得た。この水溶液を18ゲージの注射針を装着した注射筒に入れ、この注射筒を流速1 mL/分に設定したシリンジポンプに設置し、濃度が30 mmol/Lの塩化カルシウム溶液に30秒間滴下し、5分間撹拌して光反応性基導入アルギン酸ゲルを得た。このゲルを10 mLのリン酸緩衝生理食塩水(PBS)で1度洗浄した後、UV硬化装置(セン特殊光源株式会社、HLR100T-2)を用いて水中で10分間光照射を行い、光架橋アルギン酸ゲルを得た。このゲルに20 mLのPBSを添加し、37℃で振盪して、1.5、6、24、96時間後に水溶液を回収し、回収した量と同量のPBSを補充した。試験終了後、試験溶液にアルギン酸リアーゼ(ニッポンジーン、319-08261)を5 μL添加し、37℃で終夜振盪させてゲルを全て崩壊させ、水溶液を回収した。回収した水溶液中のアルギン酸濃度をカルバゾール硫酸法により測定し、各時点の水溶液中アルギン酸濃度を既に回収したアルギン酸濃度で補正した値を、全時点のアルギン酸濃度および試験終了後のアルギン酸濃度から算出した全アルギン酸濃度で除した値を百分率で表した値を崩壊率とし、ゲル安定性の指標とした。
本実施例の光架橋アルギンゲルは、安定性が高い(96時間で約16%の崩壊率)ことが確認できた。
(実施例13)で得られたアルギン酸誘導体(EX13-a1)、(実施例14)で得られたアルギン酸誘導体(EX14-a1)、及び(実施例17)で得られたアルギン酸誘導体(EX17-a1)を、濃度が1%となるよう水に溶かしてアルギン酸水溶液を得た。この水溶液を18ゲージの注射針を装着した注射筒に入れ、この注射筒を流速1 mL/分に設定したシリンジポンプに設置し、濃度が30 mmol/Lの塩化カルシウム溶液に30秒間滴下し、5分間撹拌して光反応性基導入アルギン酸ゲルを得た。このゲルを10 mLのリン酸緩衝生理食塩水(PBS)で1度洗浄した後、UV硬化装置(セン特殊光源株式会社、HLR100T-2)を用いて水中で10分間光照射を行い、光架橋アルギン酸ゲルを得た。このゲルに19.5 mLのPBSを添加し、37℃で振盪して、1.5、6、24、96時間後に水溶液を回収し、回収した量と同量のPBSを補充した。試験終了後、試験溶液にアルギン酸リアーゼ(ニッポンジーン、319-08261)を10 μL添加し、37℃で終夜振盪させてゲルを全て崩壊させ、水溶液を回収した。回収した水溶液中のアルギン酸濃度をカルバゾール硫酸法により測定し、各時点の水溶液中アルギン酸濃度を既に回収したアルギン酸濃度で補正した値を、全時点のアルギン酸濃度および試験終了後のアルギン酸濃度から算出した全アルギン酸濃度で除した値を百分率で表した値を崩壊率とし、ゲル安定性の指標とした。
本実施例の光架橋アルギン酸ゲルは、いずれも安定性(96時間で、EX13-a1由来の光架橋アルギン酸ゲルが約38%、EX14-a1由来の光架橋アルギン酸ゲルが約37%の崩壊率、EX17-a1由来の光架橋アルギン酸ゲルが約43%の崩壊率)があることが確認できた。
(実施例1)で得られたアルギン酸誘導体(EX15-a1)、及び(実施例18)で得られたアルギン酸誘導体(EX18-a1)を、濃度が1%となるよう水に溶かしてアルギン酸水溶液を得た。この水溶液を18ゲージの注射針を装着した注射筒に入れ、この注射筒を流速1 mL/分に設定したシリンジポンプに設置し、濃度が30 mmol/Lの塩化カルシウム溶液に30秒間滴下し、5分間撹拌して光反応性基導入アルギン酸ゲルを得た。このゲルを10 mLのリン酸緩衝生理食塩水(PBS)で1度洗浄した後、UV硬化装置(セン特殊光源株式会社、HLR100T-2)を用いて水中で10分間光照射を行い、光架橋アルギン酸ゲルを得た。このゲルに19.5 mLのPBSを添加し、37℃で振盪して、1.5、6、24、96時間後に水溶液を回収し、回収した量と同量のPBSを補充した。試験終了後、試験溶液にアルギン酸リアーゼ(ニッポンジーン、319-08261)を10 μL添加し、37℃で終夜振盪させてゲルを全て崩壊させ、水溶液を回収した。回収した水溶液中のアルギン酸濃度をカルバゾール硫酸法により測定し、各時点の水溶液中アルギン酸濃度を既に回収したアルギン酸濃度で補正した値を、全時点のアルギン酸濃度および試験終了後のアルギン酸濃度から算出した全アルギン酸濃度で除した値を百分率で表した値を崩壊率とし、ゲル安定性の指標とした。
本実施例の光架橋アルギン酸ゲルは、いずれも安定性が高い(96時間で、EX15-a1由来の光架橋アルギン酸ゲルが約24%、EX18-a1由来の光架橋アルギン酸ゲルが約5%の崩壊率)ことが確認できた。
(実施例9)で得られたアルギン酸誘導体(EX9-a)、(実施例12)で得られたアルギン酸誘導体(EX12-a1)、(実施例13)で得られたアルギン酸誘導体(EX13-a1)、(実施例14)で得られたアルギン酸誘導体(EX14-a1)、(実施例15)で得られたアルギン酸誘導体(EX15-a1)、(実施例17)で得られたアルギン酸誘導体(EX17-a1)、及び(実施例18)で得られたアルギン酸誘導体(EX18-a1)を、濃度が1%となるよう水に溶かしてアルギン酸水溶液を得た。この水溶液を18ゲージの注射針を装着した注射筒に入れ、この注射筒を流速1 mL/分に設定したシリンジポンプに設置し、濃度が30 mmol/Lの塩化カルシウム溶液に30秒間滴下し、5分間撹拌して光反応性基導入アルギン酸ゲルを得た。このゲルを10 mLの生理食塩水で1度洗浄した後、UV硬化装置(セン特殊光源株式会社、HLR100T-2)を用いて水中で10分間光照射を行い、光架橋アルギン酸ゲルを得た。このゲルに19.5 mLの5 mMエチレンジアミン四酢酸二カリウム塩二水和物(EDTA・2K)/生理食塩水溶液を添加し、37℃で振盪して24時間後に水溶液を回収し、回収した量と同量の5 mMエチレンジアミン四酢酸二カリウム塩二水和物(EDTA・2K)/生理食塩水溶液を補充した。試験終了後、試験溶液にアルギン酸リアーゼ(ニッポンジーン、319-08261)を10あるいは20 μL添加し、37℃で3時間以上振盪させてゲルを全て崩壊させ、水溶液を回収した。回収した水溶液中のアルギン酸濃度をカルバゾール硫酸法により測定し、各時点の水溶液中アルギン酸濃度を既に回収したアルギン酸濃度で補正した値を、全時点のアルギン酸濃度および試験終了後のアルギン酸濃度から算出した全アルギン酸濃度で除した値を百分率で表した値を崩壊率とし、ゲル安定性の指標とした。
本実施例のEDTA処理を行ってカルシウム架橋を除いた光架橋アルギンゲルは、いずれも安定性が高い(24時間で、Ex9-a由来の光架橋アルギン酸ゲルが約17%、Ex12-a1由来の光架橋アルギン酸ゲルが約18%、Ex13-a1由来の光架橋アルギン酸ゲルが約34%、Ex14-a1由来の光架橋アルギン酸ゲルが約28%、Ex17-a1由来の光架橋アルギン酸ゲルが約31%、Ex15-a1由来の光架橋アルギン酸ゲルが約18%、Ex18-a1由来の光架橋アルギン酸ゲルが約12%)があることが確認できた。
(ゲル漏出率の測定(1))
(実施例1)<工程5-1>で得られたアルギン酸誘導体(EX1-a1)、(実施例2)<工程3-1>で得られたアルギン酸誘導体(EX2-a1)、及びアルギン酸(A-2;対照)を、濃度が1%となるよう水に溶かしてアルギン酸水溶液を得た。この光架橋基導入アルギン酸水溶液に、10mg/mLの濃度に調製したブルーデキストラン(Amersham bioscience、分子量200万)水溶液を等量混和し、5mg/mLブルーデキストラン含有0.5%光架橋基導入アルギン酸水溶液を調製した。この水溶液を18ゲージの注射針を装着した注射筒に入れ、この注射筒を流速1mL/分に設定したシリンジポンプに設置し、濃度が100mmol/Lの塩化カルシウム溶液に30秒間滴下し、5分間撹拌してブルーデキストラン内包光架橋基導入アルギン酸ゲルを得た。このゲルを10mLのPBSで1度洗浄した後、UV硬化装置(セン特殊光源株式会社、HLR100T-2)を用いて水中で10分間光照射を行い、ブルーデキストラン内包の光架橋アルギン酸構造体ゲルを得た。容器に入れたこのゲルに2mLのPBSを添加し、37℃で振盪して、経時的に上清の水溶液を回収し、吸光度測定後に試験溶液中に戻した。回収した水溶液中のブルーデキストラン濃度を、検量線を用いた吸光度測定法(610 nm)により測定した。漏出率は、ブルーデキストラン含有光架橋基導入アルギン酸水溶液0.5mLをPBS2mLに添加した際のブルーデキストラン濃度を100%として、各時点の水溶液中ブルーデキストラン濃度を除した値を百分率で表した。
結果を図2(A)(B)に示した。
(実施例9)で得られたアルギン酸誘導体(EX9-a)、(実施例10)で得られたアルギン酸誘導体(EX10-a)(実施例12)で得られたアルギン酸誘導体(EX12-a1)、(実施例13)で得られたアルギン酸誘導体(EX13-a1)、(実施例14)で得られたアルギン酸誘導体(EX14-a1)、(実施例15)で得られたアルギン酸誘導体(EX15-a1)、(実施例17)で得られたアルギン酸誘導体(EX17-a1)、及び(実施例18)で得られたアルギン酸誘導体(EX18-a1)を、濃度が2%となるよう水に溶かしてアルギン酸水溶液を得た。このアルギン酸水溶液に1/5容量の1 mg/mLに調製した分子量15万のフルオレセインイソチオシアナート-デキストラン(シグマアルドリッチ、FD150S)、及び4/5容量の水を加え、0.1 mg/mLフルオレセインイソチオシアナート-デキストラン含有1.0%アルギン酸水溶液を得た。
本実施例の光架橋アルギン酸ゲルは、測定開始3時間後で約40%の透過率を有しており、測定開始24時間後で約60%の透過性を有しており、透過性に優れたものである。
下記の方法にて、生体適合性の評価を実施する。尚、本明細書における生体適合性の評価方法は、一例を示すものであり、本方法になんら限定されるものではない。
(実施例1)<工程5-1>と同様の方法で製造した導入率(NMR積分比)=4.1 mol%のアルギン酸誘導体(EX1-a3)、(実施例9)<工程3>で得られたアルギン酸誘導体(EX9-a)、(実施例10)<工程3>で得られたアルギン酸誘導体(EX10-a)、(実施例12)<工程4>で得られたアルギン酸誘導体(EX12-a)及びアルギン酸(A-2;対照)を、それぞれ濃度が1.0 w/w%となるよう水に溶かして得られたアルギン酸水溶液に、11倍濃度の生理食塩水を1/10容量添加し、濃度が0.9 w/w%のアルギン酸生理食塩水溶液(1a3)、(9a)、(10a)、(12a)及び(REF)を得た。
Claims (28)
- アルギン酸の任意の1つ以上のカルボキシル基に、下記式(I)[式中、波線右外側は含まない]:
Arは、C6-10アリール基、又は複素環基(前記C6~10アリール基、又は複素環基は、ヒドロキシル基、シアノ基、ニトロ基、ハロゲン原子、C1~6アルキル基、ハロゲン化C1~6アルキル基、C1~6アルコキシ基、及び-NRARB基(-NRARB基における、RA及びRBは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)から任意に選ばれる1~3個の基が環上の水素原子と置換しても良く、前記C6~10アリール基又は複素環基に、C1~6アルキル基及びC1~6アルコキシ基が又は2つのC1~6アルコキシ基が隣接して置換する場合、当該C1~6アルキル基及びC1~6アルコキシ基の各基のアルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、又は、当該2つのC1~6アルコキシ基の各アルキル基から任意の水素原子が1つ除かれた炭素原子間で結合することにより、環状エーテルを形成しても良く、又は、前記C6~10アリール基又は複素環基に、C1~6アルコキシ基及び-NHRG基(-NHRG基におけるRGは、C2~7アルカノイル基又はC1~6アルキルスルホニル基である)が隣接して置換している場合、当該C1~6アルコキシ基のアルキル基から任意の水素原子が1つ除かれた炭素原子と当該-NHRG基の水素原子が1つ除かれた窒素原子が結合することにより、3-N-(C2~7アルカノイル)オキサゾリジン環、3-N-(C1~6アルキルスルホニル)オキサゾリジン環、4-N-(C2~7アルカノイル)モルホリン環、4-N-(C1~6アルキルスルホニル)モルホリン環、4-N-(C2~7アルカノイル)-1,4-オキサゼパン環、又は4-N-(C1~6アルキルスルホニル)-1,4-オキサゼパン環を形成しても良い)を表わし;
pは、1、又は2の整数を表わし;
-X-は、-O-、-NH-、又は-N(C1-6アルキル)-を表わし;
-A-は、式(AL-1)~(AL-4)[各式中、両端の波線外側は含まない]:
式(AL-1)~(AL-4)中のメチレン基(-CH2-)の水素原子は、ハロゲン原子、水酸基、C1~6アルキル基、ヒドロキシC1~6アルキル基、チオールC1~6アルキル基、C1~6アルキルチオC1~6アルキル基、カルボキシC1~6アルキル基、-NRaRb基、(RaRbN)-C1~6アルキル基、(RaRbN)C(=O)-C1~6アルキル基(前記-NRaRb基、(RaRbN)-C1~6アルキル基、又は(RaRbN)C(=O)-C1~6アルキル基における、Ra及びRbは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)、グアニジノC1~6アルキル基、C7~16アラルキル基、ヒドロキシC6~10アリールC1~6アルキル基、又はヘテロアリールC1~6アルキル基から選択される基で複数個(例えば、1~10個、又は1~5個)置き換えられても良く;式(AL-1)~(AL-4)中のメチレン基(-CH2-)の2つの水素原子がC1~6アルキル基に置き換えられた場合、当該アルキル基が互いに結合してC3~8シクロアルキル環を形成しても良く;式(AL-3)又は式(AL-4)中の-NH-基は、隣接する炭素原子に結合する前記置換基と共に、非芳香族複素環を形成しても良い)]で表される光反応性基が導入された、アルギン酸誘導体。 - 式(I)で表わされる光反応性基の導入率が、0.5%~30%である、請求項1に記載のアルギン酸誘導体。
- アルギン酸誘導体のゲルろ過クロマトグラフィー法により測定した重量平均分子量が、10万Da~300万Daである、請求項1に記載のアルギン酸誘導体。
- 請求項1に記載のアルギン酸誘導体に光照射することにより得られる、光架橋アルギン酸。
- 照射する光が、紫外線又はLED光から選ばれる光である、請求項4~請求項6のいずれか1項に記載の光架橋アルギン酸。
- 請求項1に記載のアルギン酸誘導体の溶液を、2価金属イオンを含む溶液中に滴下することで得られるゲルに光照射することにより得られる、架橋として2価金属イオンにより部分的に形成されるイオン架橋及び光照射により形成される化学架橋を含む、光架橋アルギン酸構造体。
- 照射する光が、紫外線又はLED光から選ばれる光である、請求項8~請求項10のいずれか1項に記載の光架橋アルギン酸構造体。
- ビーズ又は略球形のゲルである、請求項8~請求項11のいずれか1項に記載の光架橋アルギン酸構造体。
- 請求項8~請求項11のいずれか1項に記載の光架橋アルギン酸構造体を含む医療用材料。
- ビーズ又は略球形のゲルである、請求項13に記載の医療用材料。
- 請求項1に記載のアルギン酸誘導体に光照射を行うことを含む、請求項4に記載の光架橋アルギン酸を製造する方法。
- 照射する光が、紫外線又はLED光から選ばれる光である、請求項15~請求項17のいずれか1項に記載の光架橋アルギン酸を製造する方法。
- 請求項1に記載のアルギン酸誘導体の溶液を、2価金属イオンを含む溶液中に滴下することで得られるゲルに光照射して光架橋アルギン酸構造体を得ることを含み、光架橋アルギン酸構造体が、架橋として2価金属イオンにより部分的に形成されるイオン架橋及び光照射により形成される化学架橋を含む、光架橋アルギン酸構造体を製造する方法。
- 照射する光が、紫外線又はLED光から選ばれる光である、請求項19~請求項21のいずれか1項に記載の光架橋アルギン酸構造体を製造する方法。
- 請求項1に記載のアルギン酸誘導体を、2価金属イオンにより部分的にイオン架橋して特定の構造体を形成した後に、当該構造体に光照射により化学架橋することにより光架橋アルギン酸構造体を得ることを含む、光架橋アルギン酸構造体を製造する方法。
- 照射する光が、紫外線又はLED光から選ばれる光である、請求項23に記載の光架橋アルギン酸構造体を製造する方法。
- 請求項1に記載のアルギン酸誘導体を、2価金属イオン及び光照射により架橋して得られる、内容物の保持性を有する光架橋アルギン酸構造体。
- 生体適合性がある、請求項1~3のいずれか1項に記載のアルギン酸誘導体、請求項4~7のいずれか1項に記載の光架橋アルギン酸、及び請求項8~12のいずれか1項に記載の光架橋アルギン酸構造体。
- 下記式(AM-1):
-X-は、-O-、-NH-、又は-N(C1-6アルキル)-を表わし;
-A-は、式(AL-1)~(AL-4)(但し、-X-が、-NH-、又は-N(C1-6アルキル)の場合、式(AL-1)は除く)[各式中、両端の波線外側は含まない]:
式(AL-1)~(AL-4)中のメチレン基(-CH2-)の水素原子は、ハロゲン原子、水酸基、C1~6アルキル基、ヒドロキシC1~6アルキル基、チオールC1~6アルキル基、C1~6アルキルチオC1~6アルキル基、カルボキシC1~6アルキル基、-NRaRb基、(RaRbN)-C1~6アルキル基、(RaRbN)C(=O)-C1~6アルキル基(前記-NRaRb基、(RaRbN)-C1~6アルキル基、又は(RaRbN)C(=O)-C1~6アルキル基における、Ra及びRbは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)、グアニジノC1~6アルキル基、C7~16アラルキル基、ヒドロキシC6~10アリールC1~6アルキル基、又はヘテロアリールC1~6アルキル基から選択される基で複数個(例えば、1~10個、又は1~5個)置き換えられても良く;式(AL-1)~(AL-4)中のメチレン基(-CH2-)の2つの水素原子がC1~6アルキル基に置き換えられた場合、当該アルキル基が互いに結合して、C3~8シクロアルキル環を形成してもよく;式(AL-3)又は式(AL-4)中の-NH-基は、隣接する炭素原子に結合する前記置換基と共に、非芳香族複素環を形成してもよい)](但し、2-(2-アミノエトキシ)エチル(E)-3-(4-メトキシフェニル)アクリレート、2-(2-アミノエトキシ)エチルシンナメート、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(4-プロポキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(3-メトキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(3,4-ジメトキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(4-エトキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(4-ニトロフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(4-イソプロピルフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(4-フルオロフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(2,5-ジメトキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(2-プロポキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(4-クロロフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(3-イソプロポキシフェニル)アクリルアミド、N-(2-(2-アミノエトキシ)エチル)シンナミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(p-トリル)アクリルアミド、(E)-N-(2-(2-(2-アミノエトキシ)エトキシ)エチル)-3-(4-ヒドロキシフェニル)アクリルアミド、(E)-N-(2-(2-アミノエトキシ)エチル)-3-(フラン-2-イル)アクリルアミド、1,3-ジアミノプロパン-2-イルシンナメート、5-アミノペンチル(E)-3-(4-メトキシフェニル)アクリレート、3-アミノプロピル(E)-3-(4-メトキシフェニル)アクリレート、ジアミノメチルシンナメート、6-アミノヘキシルシンナメート、4-アミノブチルシンナメート、5-アミノペンチルシンナメート、8-アミノオクチルシンナメート、12-アミノドデシルシンナメート、3-アミノプロピルシンナメート、2-アミノエチルシンナメート、1,2-ジアミノエチルシンナメート、2-アミノエチル(E)-3-(ピリジン-4-イル)アクリレート、2-アミノエチル(E)-3-(チオフェン-2-イル)アクリレート、及び2-アミノエチル(E)-3-(フラン-2-イル)アクリレートは除く)で表される化合物、又は製薬学的に許容されるその塩、又はそれらの溶媒和物。 - 下記式(AM-2):
-X-は、-O-、-NH-、又は-N(C1-6アルキル)-を表わし;
-A-は、式(AL-1)~(AL-4)[各式中、両端の波線外側は含まない]:
式(AL-1)~(AL-4)中のメチレン基(-CH2-)の水素原子は、ハロゲン原子、水酸基、C1~6アルキル基、ヒドロキシC1~6アルキル基、チオールC1~6アルキル基、C1~6アルキルチオC1~6アルキル基、カルボキシC1~6アルキル基、-NRaRb基、(RaRbN)-C1~6アルキル基、(RaRbN)C(=O)-C1~6アルキル基(前記-NRaRb基、(RaRbN)-C1~6アルキル基、又は(RaRbN)C(=O)-C1~6アルキル基における、Ra及びRbは、各々独立して、水素原子、C1~6アルキル基、C2~7アルカノイル基、又はC1~6アルキルスルホニル基から選択される基であり)、グアニジノC1~6アルキル基、C7~16アラルキル基、ヒドロキシC6~10アリールC1~6アルキル基、又はヘテロアリールC1~6アルキル基から選択される基で複数個(例えば、1~10個、又は1~5個)置き換えられても良く;式(AL-1)~(AL-4)中のメチレン基(-CH2-)の2つの水素原子がC1~6アルキル基に置き換えられた場合、当該アルキル基が互いに結合して、C3~8シクロアルキル環を形成してもよく;式(AL-3)又は式(AL-4)中の-NH-基は、隣接する炭素原子に結合する前記置換基と共に、非芳香族複素環を形成してもよい)]で表される化合物、又は製薬学的に許容されるその塩、又はそれらの溶媒和物。
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP19760579.3A EP3760647A4 (en) | 2018-02-28 | 2019-02-27 | NEW DERIVATIVE OF PHOTORETICULABLE ALGINIC ACID |
| CA3092253A CA3092253A1 (en) | 2018-02-28 | 2019-02-27 | Novel photocrosslinkable alginic acid derivative |
| US16/976,027 US11472891B2 (en) | 2018-02-28 | 2019-02-27 | Photocrosslinkable alginic acid derivative |
| CN201980015855.2A CN111918881B (zh) | 2018-02-28 | 2019-02-27 | 新型光交联性海藻酸衍生物 |
| JP2020503590A JP7346380B2 (ja) | 2018-02-28 | 2019-02-27 | 新規光架橋性アルギン酸誘導体 |
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2018-035943 | 2018-02-28 | ||
| JP2018035943 | 2018-02-28 | ||
| JP2018205325 | 2018-10-31 | ||
| JP2018-205325 | 2018-10-31 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2019168058A1 true WO2019168058A1 (ja) | 2019-09-06 |
Family
ID=67806253
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2019/007655 WO2019168058A1 (ja) | 2018-02-28 | 2019-02-27 | 新規光架橋性アルギン酸誘導体 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US11472891B2 (ja) |
| EP (1) | EP3760647A4 (ja) |
| JP (1) | JP7346380B2 (ja) |
| CN (1) | CN111918881B (ja) |
| CA (1) | CA3092253A1 (ja) |
| WO (1) | WO2019168058A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2022145419A1 (ja) | 2020-12-28 | 2022-07-07 | 持田製薬株式会社 | 化学架橋アルギン酸を用いた多層構造体 |
Citations (21)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1993013136A1 (en) | 1991-12-20 | 1993-07-08 | Howmedica Inc. | Ultra-pure polysaccharide materials for medical use |
| JPH08143604A (ja) * | 1994-11-17 | 1996-06-04 | Seikagaku Kogyo Co Ltd | 光架橋性ヒアルロン酸誘導体とその架橋体およびそれらの製造方法 |
| JPH08269102A (ja) | 1995-03-30 | 1996-10-15 | Shiseido Co Ltd | エンドトキシンフリーのβ1,3−グルカン及びその製造法並びに医療用ゲル素材 |
| US5589591A (en) | 1986-07-03 | 1996-12-31 | Advanced Magnetics, Inc. | Endotoxin-free polysaccharides |
| JPH0987236A (ja) | 1995-09-20 | 1997-03-31 | Seikagaku Kogyo Co Ltd | 桂皮酸誘導体 |
| JPH09324001A (ja) | 1996-04-02 | 1997-12-16 | Kyowa Hakko Kogyo Co Ltd | ヒアルロン酸ナトリウムの精製法 |
| JPH11512778A (ja) * | 1995-11-15 | 1999-11-02 | 生化学工業株式会社 | 光架橋ヒアルロン酸ゲルおよびその製造法 |
| WO2002060971A1 (en) | 2001-01-31 | 2002-08-08 | Seikagaku Corporation | Crosslinked polysaccharide sponge |
| JP2002530440A (ja) | 1998-11-13 | 2002-09-17 | シーピー ケルコ ユー.エス.インク. | エンドトキシンレベルが低い生体高分子塩、その生体高分子組成物およびこれを製造する方法 |
| WO2004081054A1 (ja) * | 2003-03-11 | 2004-09-23 | Seikagaku Corporation | 光架橋多糖組成物およびその製造方法 |
| WO2004099259A1 (ja) | 2003-05-09 | 2004-11-18 | Toho Chemical Industry Co., Ltd. | カチオン変性アルギン酸誘導体及び該物質を含む化粧料組成物 |
| JP2005036036A (ja) | 2003-07-16 | 2005-02-10 | Tanabe Seiyaku Co Ltd | エンドトキシン除去方法 |
| WO2005026214A1 (ja) | 2003-09-12 | 2005-03-24 | Seikagaku Corporation | 多糖擬スポンジ |
| WO2005107827A1 (ja) * | 2004-05-07 | 2005-11-17 | Seikagaku Corporation | 髄核充填剤 |
| JP2006042758A (ja) * | 2004-07-02 | 2006-02-16 | Seikagaku Kogyo Co Ltd | 胚性幹細胞の培養用基材及びその用途 |
| JP2006111867A (ja) * | 2004-09-15 | 2006-04-27 | Seikagaku Kogyo Co Ltd | 光反応性多糖、その光架橋多糖生成物及び医用材料 |
| WO2007004675A1 (ja) * | 2005-07-06 | 2007-01-11 | Seikagaku Corporation | 薬剤導入光架橋ヒアルロン酸誘導体ゲル |
| JP2007099902A (ja) | 2005-10-04 | 2007-04-19 | Kaneka Corp | アルギン酸誘導体、ポリアクリル酸誘導体およびそれらの製造方法 |
| JP2010209130A (ja) | 2009-03-06 | 2010-09-24 | Teijin Ltd | アルギン酸誘導体およびその製造方法 |
| CN103936710A (zh) * | 2013-01-18 | 2014-07-23 | 内蒙古大学 | N-取代的胡椒基戊二烯酰胺衍生物及其制备方法和应用 |
| CN105348250A (zh) * | 2015-10-20 | 2016-02-24 | 吐尔孙拜克·叶尔达 | 一种药用化合物胡椒酸己二胺及其制备工艺 |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2162957C (en) | 1994-11-17 | 2011-08-02 | Michinori Waki | Cinnamic acid derivative |
| US6025444A (en) | 1994-11-17 | 2000-02-15 | Seikagaku Kogyo Kabushiki Kaisha (Seikagaku Corporation) | Cinnamic acid derivative |
| AU2005283282B2 (en) | 2004-09-15 | 2011-05-19 | Seikagaku Corporation | Photoreactive polysaccharide, photocrosslinked polysaccharide products, the method of making them and medical materials therefrom |
| JP4545073B2 (ja) * | 2004-09-17 | 2010-09-15 | 三菱重工業株式会社 | ガスバリア膜及び容器 |
| CN103923224B (zh) | 2014-04-15 | 2016-03-02 | 武汉大学 | 一种光照-镁离子双交联海藻酸盐水凝胶及其制备方法 |
-
2019
- 2019-02-27 US US16/976,027 patent/US11472891B2/en active Active
- 2019-02-27 CN CN201980015855.2A patent/CN111918881B/zh active Active
- 2019-02-27 EP EP19760579.3A patent/EP3760647A4/en active Pending
- 2019-02-27 JP JP2020503590A patent/JP7346380B2/ja active Active
- 2019-02-27 WO PCT/JP2019/007655 patent/WO2019168058A1/ja unknown
- 2019-02-27 CA CA3092253A patent/CA3092253A1/en active Pending
Patent Citations (22)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5589591A (en) | 1986-07-03 | 1996-12-31 | Advanced Magnetics, Inc. | Endotoxin-free polysaccharides |
| WO1993013136A1 (en) | 1991-12-20 | 1993-07-08 | Howmedica Inc. | Ultra-pure polysaccharide materials for medical use |
| JPH08143604A (ja) * | 1994-11-17 | 1996-06-04 | Seikagaku Kogyo Co Ltd | 光架橋性ヒアルロン酸誘導体とその架橋体およびそれらの製造方法 |
| JPH08269102A (ja) | 1995-03-30 | 1996-10-15 | Shiseido Co Ltd | エンドトキシンフリーのβ1,3−グルカン及びその製造法並びに医療用ゲル素材 |
| JPH0987236A (ja) | 1995-09-20 | 1997-03-31 | Seikagaku Kogyo Co Ltd | 桂皮酸誘導体 |
| JPH11512778A (ja) * | 1995-11-15 | 1999-11-02 | 生化学工業株式会社 | 光架橋ヒアルロン酸ゲルおよびその製造法 |
| JPH09324001A (ja) | 1996-04-02 | 1997-12-16 | Kyowa Hakko Kogyo Co Ltd | ヒアルロン酸ナトリウムの精製法 |
| JP2002530440A (ja) | 1998-11-13 | 2002-09-17 | シーピー ケルコ ユー.エス.インク. | エンドトキシンレベルが低い生体高分子塩、その生体高分子組成物およびこれを製造する方法 |
| WO2002060971A1 (en) | 2001-01-31 | 2002-08-08 | Seikagaku Corporation | Crosslinked polysaccharide sponge |
| WO2004081054A1 (ja) * | 2003-03-11 | 2004-09-23 | Seikagaku Corporation | 光架橋多糖組成物およびその製造方法 |
| WO2004099259A1 (ja) | 2003-05-09 | 2004-11-18 | Toho Chemical Industry Co., Ltd. | カチオン変性アルギン酸誘導体及び該物質を含む化粧料組成物 |
| JP2005036036A (ja) | 2003-07-16 | 2005-02-10 | Tanabe Seiyaku Co Ltd | エンドトキシン除去方法 |
| WO2005026214A1 (ja) | 2003-09-12 | 2005-03-24 | Seikagaku Corporation | 多糖擬スポンジ |
| JP2011102405A (ja) * | 2003-09-12 | 2011-05-26 | Seikagaku Kogyo Co Ltd | 多糖擬スポンジ |
| WO2005107827A1 (ja) * | 2004-05-07 | 2005-11-17 | Seikagaku Corporation | 髄核充填剤 |
| JP2006042758A (ja) * | 2004-07-02 | 2006-02-16 | Seikagaku Kogyo Co Ltd | 胚性幹細胞の培養用基材及びその用途 |
| JP2006111867A (ja) * | 2004-09-15 | 2006-04-27 | Seikagaku Kogyo Co Ltd | 光反応性多糖、その光架橋多糖生成物及び医用材料 |
| WO2007004675A1 (ja) * | 2005-07-06 | 2007-01-11 | Seikagaku Corporation | 薬剤導入光架橋ヒアルロン酸誘導体ゲル |
| JP2007099902A (ja) | 2005-10-04 | 2007-04-19 | Kaneka Corp | アルギン酸誘導体、ポリアクリル酸誘導体およびそれらの製造方法 |
| JP2010209130A (ja) | 2009-03-06 | 2010-09-24 | Teijin Ltd | アルギン酸誘導体およびその製造方法 |
| CN103936710A (zh) * | 2013-01-18 | 2014-07-23 | 内蒙古大学 | N-取代的胡椒基戊二烯酰胺衍生物及其制备方法和应用 |
| CN105348250A (zh) * | 2015-10-20 | 2016-02-24 | 吐尔孙拜克·叶尔达 | 一种药用化合物胡椒酸己二胺及其制备工艺 |
Non-Patent Citations (12)
| Title |
|---|
| "Experimental Chemistry Course 5th Edition", vol. 13, 2004, article "Synthesis of Organic Compounds I: Synthesis of hydrocarbons and alkenes", pages: 118 - 139 |
| "Experimental Chemistry Course", vol. 16, 2007, article "Synthesis of Organic Compounds IV: Carboxylic acids, derivatives, acid amides and acid imides", pages: 118 - 154 |
| ACID AMIDES AND ACID IMIDES, pages 118 - 154 |
| AMINO ACIDS AND PEPTIDES, 2007, pages 258 - 283 |
| APPL. MICROBIOL. BIOTECHNOL., vol. 40, 1994, pages 638 - 643 |
| CHEMICAL ABSTRACTS, Columbus, Ohio, US; abstract no. 151539-59-2 |
| JOURNAL OF AMERICAN CHEMICAL SOCIETY, vol. 127, no. 43, 2005, pages 15028 - 15029 |
| JOURNAL OF THE AMERICAN CHEMICAL SOCIETY, vol. 127, no. 43, 2005, pages 15028 - 15029 |
| ORGANIC REACTIONS, vol. 27, 1982 |
| SHIMADA CHIYAKO ET AL.: "Quantitative structure-cytotoxicity relationship of piperic acid amides", ANTICANCER RESEARCH, vol. 34, no. 9, 2014, pages 4877 - 4884, XP055634081 * |
| STAHLWERMUTH: "Handbook of Pharmaceutical Salts: Properties, Selection and Use", 2002, WILEY-VCH |
| TAKAO KOICHI ET AL.: "Synthesis and biological evaluation of piperic acid amides as free radical scavengers and alpha-glucosidase inhibitors", CHEMICAL & PHARMACEUTICAL BULLETIN, vol. 63, no. 5, 2015, pages 326 - 333, XP055634078 * |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2022145419A1 (ja) | 2020-12-28 | 2022-07-07 | 持田製薬株式会社 | 化学架橋アルギン酸を用いた多層構造体 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN111918881A (zh) | 2020-11-10 |
| CN111918881B (zh) | 2022-08-12 |
| US11472891B2 (en) | 2022-10-18 |
| CA3092253A1 (en) | 2019-09-06 |
| JPWO2019168058A1 (ja) | 2021-02-12 |
| US20210380727A1 (en) | 2021-12-09 |
| EP3760647A1 (en) | 2021-01-06 |
| EP3760647A4 (en) | 2021-12-01 |
| JP7346380B2 (ja) | 2023-09-19 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN109776451B (zh) | 光交联水凝胶材料的制备、原料、产品及应用 | |
| CN109776450A (zh) | 光偶合协同交联水凝胶材料的制备、原料、产品及应用 | |
| JP6815561B2 (ja) | 新規な架橋アルギン酸 | |
| WO2007004675A1 (ja) | 薬剤導入光架橋ヒアルロン酸誘導体ゲル | |
| CN104136419A (zh) | 能够形成药物封装微球的在n末端上官能化的氨基酸衍生物 | |
| WO2021125255A1 (ja) | 新規な架橋アルギン酸 | |
| CN109161037A (zh) | 一种水凝胶复合物、制备方法及应用 | |
| TW200831113A (en) | Pharmaceutical agent having long-lasting effect of treating arthritic disorders | |
| CN106794362A (zh) | 用于治疗应用的一氧化碳‑释放分子及其制备和使用方法 | |
| CN106519072A (zh) | 可注射型玻尿酸/聚乙二醇水凝胶及其制备方法和应用 | |
| WO2019168058A1 (ja) | 新規光架橋性アルギン酸誘導体 | |
| WO2021125279A1 (ja) | 化学架橋アルギン酸ゲルファイバ | |
| JP7404228B2 (ja) | 非ステロイド性抗炎症性化合物結合アルギン酸誘導体 | |
| WO2022145419A1 (ja) | 化学架橋アルギン酸を用いた多層構造体 | |
| CN115244087B (zh) | 用于3d打印的生物墨水、有关缀合物和由光反应性连接基组成的中间体的制备方法 | |
| HUE031774T2 (en) | Crosslinked hyaluronic acid derivatives, process and their use | |
| WO2021060336A1 (ja) | 新規な架橋アルギン酸構造体 | |
| JP6281901B2 (ja) | 水溶性ポルフィリン誘導体とそれらの製造方法 | |
| WO2021060351A1 (ja) | NSAIDs結合アルギン酸誘導体 | |
| WO2024062713A1 (ja) | ゲル形成用材料及びゲル組成物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 19760579 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 3092253 Country of ref document: CA |
|
| ENP | Entry into the national phase |
Ref document number: 2020503590 Country of ref document: JP Kind code of ref document: A |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| ENP | Entry into the national phase |
Ref document number: 2019760579 Country of ref document: EP Effective date: 20200928 |