WO2018065360A1 - Benzimidazolhaltige cyclische dinukleotide, verfahren zu deren herstellung und ihre verwendung zur aktivierung von stimulator von interferongenen (sting)-abhängigen signalwegen - Google Patents
Benzimidazolhaltige cyclische dinukleotide, verfahren zu deren herstellung und ihre verwendung zur aktivierung von stimulator von interferongenen (sting)-abhängigen signalwegen Download PDFInfo
- Publication number
- WO2018065360A1 WO2018065360A1 PCT/EP2017/074966 EP2017074966W WO2018065360A1 WO 2018065360 A1 WO2018065360 A1 WO 2018065360A1 EP 2017074966 W EP2017074966 W EP 2017074966W WO 2018065360 A1 WO2018065360 A1 WO 2018065360A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- monophosphate
- riboside
- cyclic
- monophosphorothioate
- benzimidazole
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
- 0 Cc(ncnc1N(C=C)C(N)=*)c1N Chemical compound Cc(ncnc1N(C=C)C(N)=*)c1N 0.000 description 6
- REIOMGZOJGOXBJ-UHFFFAOYSA-N CC(C)N(C=CC(C)=N1)C1=O Chemical compound CC(C)N(C=CC(C)=N1)C1=O REIOMGZOJGOXBJ-UHFFFAOYSA-N 0.000 description 1
- LPVDSAMLQSSLPJ-UHFFFAOYSA-N CC(N=C(N)NC1=O)=C1N Chemical compound CC(N=C(N)NC1=O)=C1N LPVDSAMLQSSLPJ-UHFFFAOYSA-N 0.000 description 1
- XGAORKRFBMZKFU-UHFFFAOYSA-N CN(C=C)C(N=CNC1=O)=C1N Chemical compound CN(C=C)C(N=CNC1=O)=C1N XGAORKRFBMZKFU-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H21/00—Compounds containing two or more mononucleotide units having separate phosphate or polyphosphate groups linked by saccharide radicals of nucleoside groups, e.g. nucleic acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7084—Compounds having two nucleosides or nucleotides, e.g. nicotinamide-adenine dinucleotide, flavine-adenine dinucleotide
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P19/00—Preparation of compounds containing saccharide radicals
- C12P19/26—Preparation of nitrogen-containing carbohydrates
- C12P19/28—N-glycosides
- C12P19/38—Nucleosides
- C12P19/40—Nucleosides having a condensed ring system containing a six-membered ring having two nitrogen atoms in the same ring, e.g. purine nucleosides
Definitions
- the present invention is in the field of immunotherapy.
- the present invention is cyclic dinucleotides (CDNs) of the formula (I) as defined in the claims.
- CDNs cyclic dinucleotides
- they are benzimidazole-containing CDNs, their pharmacologically suitable salts, and their corresponding prodrugs, which are capable of inducing the production of type 1 interferons in human and animal cells.
- the CDNs according to the invention can furthermore be used as reagents in signal transduction and as modulators for CDN-binding proteins and their isoforms.
- the CDNs according to the invention are suitable as ligands for affinity chromatography, for antibody production and for diagnostic applications.
- Immunotherapy is a rapidly growing area of research in medicine that activates, deactivates, or otherwise modulates the patient's immune system for therapeutic success.
- Immunotherapeutic approaches involve cells, antigens, antibodies, nucleic acids, peptides, proteins, naturally occurring ligands or synthetic molecules.
- Cytokines are small glycoproteins that mediate the immune response through complex signaling cascades. The direct therapeutic application of cytokines is severely limited for a variety of reasons, including the very low cytokine half-lives in the bloodstream, which would imply extremely short treatment intervals and very high dosages.
- a more promising approach in immunotherapy is therapeutic cytokine induction in which the patient is treated with an immunomodulatory agent, thereby stimulating the production of one or more therapeutically useful cytokines in the patient's body.
- the STING protein is a transmembrane receptor protein and plays a central role in the physiological production of cytokines in the innate immune system.
- IRF3 interferon regulatory factor 3
- IL-1a proinflammatory cytokines
- IL-1 ⁇ proinflammatory cytokines
- NF- ⁇ nuclear factor kappa light-chain enhancer of activated B cells
- CDNs as STING activators are described in US / 2014/0329889, WO / 2014/189805, WO / 2014/093936, WO / 2015/077354, WO / 2015/185565, WO / 2016/096174, WO / 2016/096577 and WO / 2016/145102.
- CDNs with the nucleobases adenine, guanine, hypoxanthine and isoguanine have been described and investigated.
- nucleobases are extraordinarily polar heterocycles which, while having good water solubility, cause poor membrane permeability of the synthetic CDNs.
- poor membrane permeability of the CDNs described so far is to be regarded as a limiting factor of decisive importance for the therapeutic use.
- the primary object of the present invention was to provide the membrane permeability and / or the biological activity of improved CDNs.
- the problem is solved in the present invention by the provision of lipophilic benzimidazole-containing CDNs of the formula (I) as defined in the claims.
- the replacement of at least one of the nucleobases adenine, guanine, hypoxanthine or isoguanine with a purine structure against a benzimidazole unit or against a substituted benzimidazole without a purine structure leads to synthetic CDNs which are considerably improved and hitherto unknown Characterize lipophilic properties.
- the CDNs according to the invention with at least one benzimidazole-based structural unit are characterized by good STING-mediated interferon production.
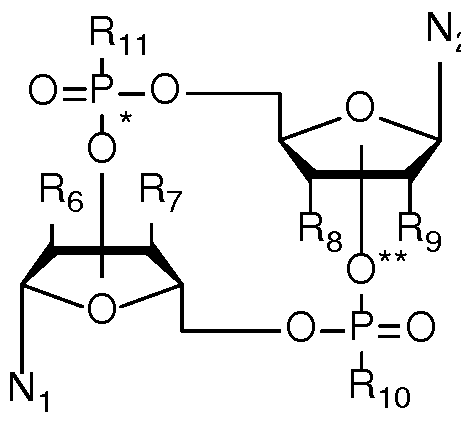
- Variable Linkable Structural Unit and “Variable Linkable Structural Units”: whenever in a ring system side chains or substituents are named or represented as “variable linking structural units” or “variable linking structural units”, as in the following formula:
- variable linking structural unit may or may replace these variable linking structural units of any of the hydrogen atoms attached to the ring system.
- all hydrogen atoms are included, regardless of whether the hydrogen atoms are explicitly represented or implied by the structure or description shown. All substitution variants resulting from this definition are included by the term variable-linking structural unit or variable-linking structural units as long as they lead to chemically stable structures or no restrictions are mentioned in this text.
- the definitions described give rise to three specific structures which are represented in formula:
- variable-linker moieties associated with an annular ribose system can only replace R moieties at positions commonly referred to as the 2'-position and the 3'-position.
- the radicals R in the 2'-position and 3'-position of the ribose system are not limited to hydrogen atoms but can be specified as under R 6 -R 9 .
- N 2 R 12 and N 2 may be the same or different.
- R 10 and Rn are both oxygen and the double bond of the phosphate is delocalized between the two exocyclic oxygen atoms.
- natural CDNs In aqueous solution at physiological pH, natural CDNs have a total of two negative charges due to their two single negatively charged phosphate units. The negative charge is delocalized in each case via the two exocyclic oxygen atoms and corresponding cations, such as Na + or K + act as counterions.
- all structures are shown in the free acid form with localized double bond for the sake of clarity. The location of the abovementioned double bond depends on the nature of the radicals R 10 and R.
- the nature of the structural representation in the present invention is for the sake of clarity and does not claim to correspond to the exactly accurate charge distribution and electron density distribution at the phosphate units.
- both R 10 and R may be sulfur or borane on the two phosphates, resulting in phosphorothioates or boranophosphates.
- the compounds according to the invention contain either one or two phosphorothioate units or one or two boranophosphate units or one phosphorothioate unit and one boranophosphate unit.
- a single phosphorothioate-containing CDN of the exemplary description c [N 1 (2 ', 5') pS-N 2 (3 ', 5') p] comprises two different stereoisomers: c [N 1 (2 ', 5') pS [Rp] -N 2 (3 ', 5') p], c [N 1 (2 ', 5') p S [Sp] -N 2 (3 ', 5') p], where N 2 and the nucleobase units meet and correspond to the proviso that not equal to N may be 2 or may be equal to N 2.
- Halogen is F, Cl, Br, and I.
- Alkyl is an alkyl group represented by a hydrocarbon of 1 to 28 carbon atoms, preferably 1 to 20 carbon atoms, with or without (integrated) heteroatoms, preferably, but not limited to, O, S, Si, N, Se, B wherein the linkage to the basic structure in formula (I), unless otherwise defined, is via carbon.
- the polystyrene resin may be linearly saturated - and is preferably, but not limited to, methyl, ethyl, propyl, butyl or pentyl.
- linearly unsaturated - preferably comprises 2 to 20 carbon atoms and is more preferably ethylene, propylene, butylene and pentylene, but is not limited thereto or may be branched saturated - and then comprises at least three carbon atoms and is preferably isopropyl sec-butyl or tert-butyl, without, however, being limited thereto. or may be branched unsaturated - and then comprises at least three carbon atoms and is preferably isopropenyl, isobutenyl, isopentenyl or 4-methyl-3-pentenyl, but not limited thereto
- saturated means a hydrocarbon containing neither C-C double bonds nor C-C triple bonds.
- Substituted saturated alkyl groups may have one or more multiple bonds between carbon and oxygen, carbon and sulfur, or carbon and nitrogen, which may also occur as part of a keto-enol or imine-enamine tautomerism.
- alkyl group within the meaning of this text can be unsubstituted or substituted.
- Possible substituents include one or more (unsubstituted) alkyl groups, halogen-substituted alkyl groups, halogen atoms, substituted and unsubstituted aryl groups, substituted and unsubstituted heteroaryl groups, amino, oxo, nitro, cyano, azido, hydroxy, mercapto, keto, Carboxy, carbamoyl, epoxy, methoxy, methylthio, ethynyl groups, but are not limited thereto.
- alkyl contains a polyethylene glycol chain (PEG)
- PEG polyethylene glycol chain
- - (EO) n - can be used as an abbreviation for - (CH 2 CH 2 0) n -, wherein the number of PEG units either as indicated in the respective example, or 1-500 can be.
- Aralkyl refers to an alkyl group as described above attached to an unsubstituted or substituted, aromatic or heteroaromatic hydrocarbon and which consists of one or more aromatic rings each having 3-8 ring atoms.
- Substituents for both the alkyl and aryl moieties include one or more halogen atoms, alkyl or haloalkyl groups, substituted or unsubstituted aryl groups, substituted or unsubstituted heteroaryl groups, amino, nitro, cyano, azido, hydroxy, mercapto , Carboxy, methoxy, methylthio groups, but are not limited thereto.
- Aryl describes an unsubstituted or substituted, aromatic or heteroaromatic hydrocarbon which consists of one or more aromatic rings each having 3-8 ring atoms.
- Substituents for both the alkyl and aryl moieties include one or more halogen atoms, alkyl or haloalkyl groups, substituted or unsubstituted aryl groups, substituted or unsubstituted heteroaryl groups, amino, nitro, cyano, azido, hydroxy, mercapto , Carboxy, methoxy, methylthio groups, but are not limited thereto.
- Acyl describes a -C (O) alkyl group, wherein the specification of the alkyl group has been defined above.
- Aracyl describes a -C (O) -aryl group, the specification of the aryl group being defined above.
- Carbamoyl describes a -C (0) -NH 2 group, wherein the two hydrogen atoms may be independently substituted by alkyl, aryl or aralkyl groups, and the specification of the alkyl, aryl and aralkyl groups defined above.
- O-Acyl describes a -O-C (O) -alkyl group, the specification of the alkyl group being defined above.
- O-Aracyl describes a -O-C (O) -aryl group, wherein the specification of the alkyl group has been defined above.
- O-Aralkyl describes an aralkyl group attached via oxygen, the specification of the aralkyl group being defined above.
- O-aryl describes an aryl group attached via oxygen, the specification of the aryl group being defined above.
- O-carbamoyl describes a carbamoyl group attached via oxygen, the specification of the carbamoyl group being defined above.
- S-alkyl describes an alkyl group attached via sulfur, the specification of the alkyl group being defined above.
- S-aryl describes an aryl group attached via sulfur, the specification of the aryl group being defined above.
- S-Aralkyl describes an aralkyl group attached via sulfur, the specification of the aralkyl group being defined above.
- NH-alkyl and N-bisalkyl describe one or two alkyl groups which are attached via nitrogen, wherein the specification of the alkyl group has been defined above.
- NH-aryl and N-bisaryl describe one or two aryl groups attached via nitrogen, the specification of the alkyl group being defined above.
- NH carbamoyl describes a carbamoyl group attached via nitrogen, the specification of the carbamoyl group being defined above.
- Amido-alkyl describes an alkyl group attached via an NH-C (O) bond, the specification of the alkyl group being defined above.
- Amido-aryl describes an aryl group attached via an NH-C (0) bond, the specification of the aryl group being defined above.
- Amido-aralkyl describes an aralkyl group attached via an NH-C (O) bond, the specification of the aralkyl group being defined above.
- Figure 1 Synthesis of cyclic (adenosine (3 '-> 5') monophosphate - benzimidazole riboside (3 '-> 5') monophosphate) (c [A (3 ', 5') pBI (3 ', 5 ') p]).
- Figure 3 Synthesis of cyclic (guanosine (2 '-> 5') monophosphorothioate - 5,6-dichlorobenzimidazole riboside (3 '-> 5') monophosphorothioate) (c [G (2 ', 5') pS- DCIBI (3 ', 5') pS]).
- FIG. 1 Biological activity of novel CDNs according to the invention by means of THP1-Blue TM cells and SEAP reporters.
- THP1 -Blue TM cells ((THP1-ISG); InvivoGen, catalog number: thp-isg; Concentration: 5 x 10 5 / ml_, 180 ⁇ _ / ⁇ (96-well plate) were mixed with CDNs of the invention Concentrations (0 ⁇ g / mL, 10 ⁇ g / mL, 20 ⁇ g / mL, 40 ⁇ g / mL) in medium (RPMI-1640, 2 mM L-glutamine, 1 .5 g / L sodium bicarbonate, 4.5 g / L glucose, 10 mM Hepes, 1 mM sodium pyruvate, 10% FCS, 100 ⁇ g / mL Zeocin TM, 1 10 ⁇ g / mL Normocin TM, Pen-Strep 50 U / mL) for 24 hours at 37 ° C in 5% C0 2.
- medium RPMI-1640, 2 mM L-glu
- Quantification was performed with the SEAP Detection Reagent QUANTI-Blue TM (InvivoGen; catalog number: rep-qb1; incubation time: 30 min at 37 ° C in 5% C0 2 ) over the optical density (OD) at 625 nm.
- FIG. 2 Biological activity of novel CDNs according to the invention by means of THP1 -Blue TM cells and by means of THP1 Dual TM KO STING cells as control cells and SEAP reporter.
- THP1 -Blue TM cells ((THP1-ISG); InvivoGen, catalog number: thp-isg; Concentration: 5 x 10 5 / mL, 180 [iL / we ⁇ (96-well plate) and THP1 Dual TM KO STING cells ((STING KO) InvivoGen, catalog number: thpd-kostg; concentration: 5 ⁇ 10 5 / mL, 180 ⁇ / v ⁇ (96-well plate) were incubated with CDNs according to the invention at a concentration of 40 ⁇ g / mL each in medium (RPMI-1640, 2 mM L-glutamine, 1 .5 g / L sodium bicarbonate, 4.5 g / L glucose, 10 mM Hepes, 1 mM sodium pyruvate, 10% FCS, 100 ⁇ g / mL Zeocin TM, 1 ⁇ g / mL Normocin TM, Pen-
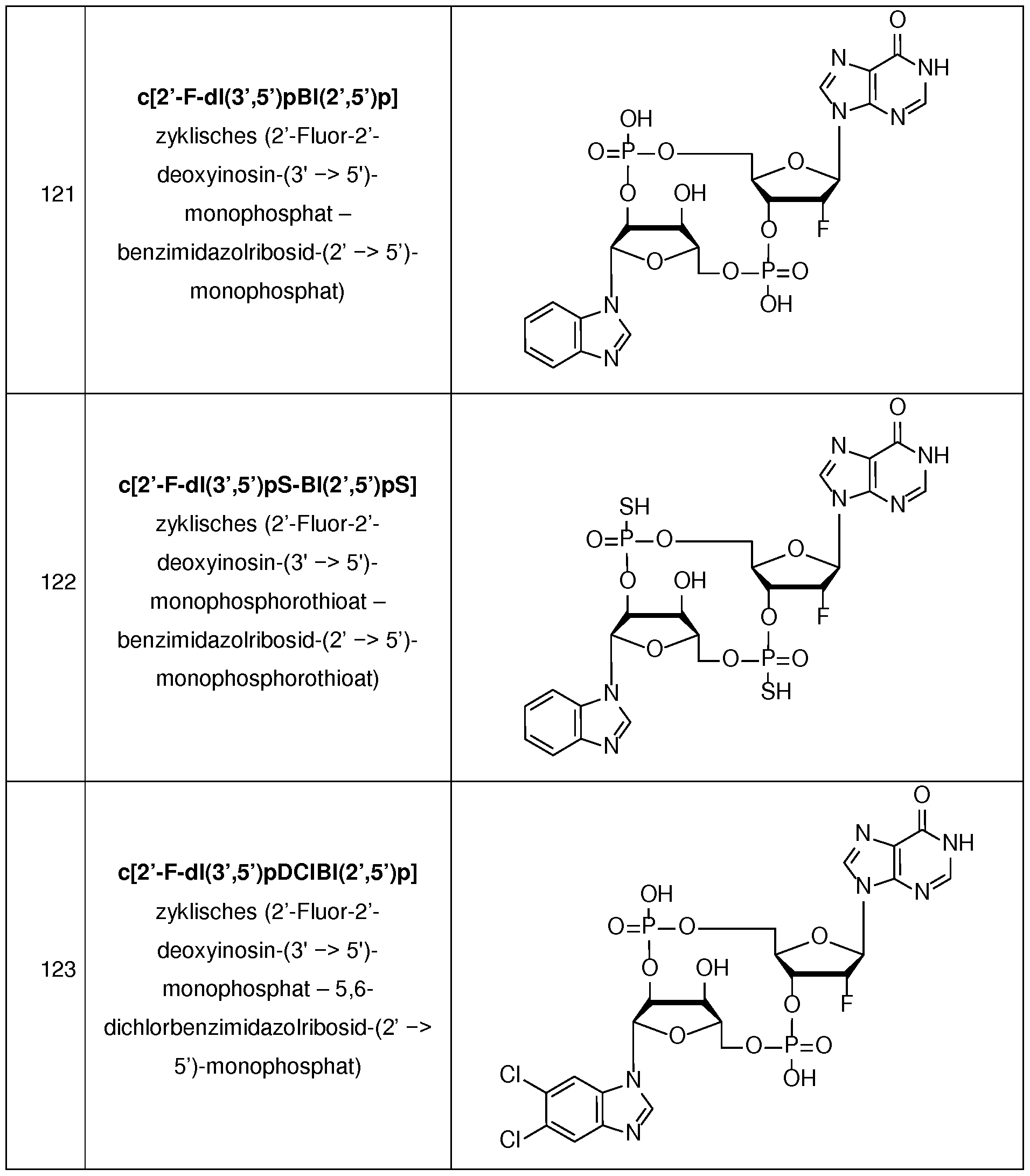
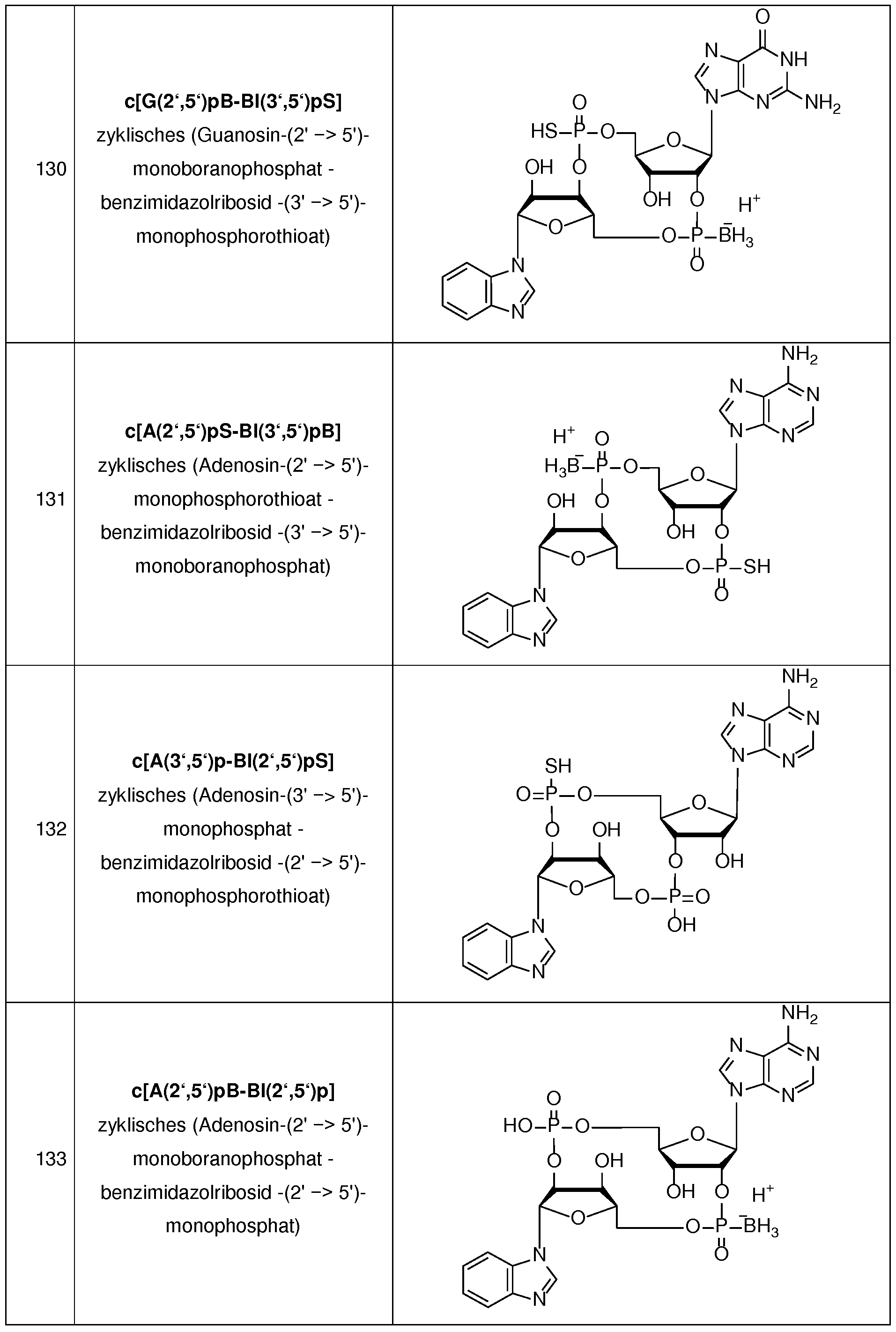
- Table 1 Abbreviations, names and structures of novel, inventive compounds.
- Table 2 HPLC retention times and lipophile values (log k ' g ) of novel, CDNs according to the invention.
- the benzimidazole-containing cyclic dinucleotides according to the invention are compounds of the formula (I)
- Methylanthranoyl aminobutylamino, dimethylamino, diethylamino, 4-morpholino, 1-piperidino or 1-piperazino
- radical R 1 is as defined in the following groups 1 or 2: Group 1:
- Q is S, S (O), S (O) 2 , O, NH, CH 2 or C (O);
- XX 2 and X 3 are each independently H, OH, NH 2 , N 3 , SH, CN, NO 2 , F, Cl, Br,
- n 1 - 6;
- Q is S, S (O), S (O) 2 , O or NH;
- Ft 2 is H, F, Cl, Br, NH 2 , NO 2 , CN, CH 3, OH, CF 3 , SH, O-CH 3 , OCF 3 , N (CH 3 ) 2 , S-CH 3 or C (0) OH;
- R 3 is H, F, Cl, Br, NH 2 , NO 2 , CN, CH 3, OH, CF 3 , SH, O-CH 3 , OCF 3 , N (CH 3 ) 2 , S-CH 3 or C (0) OH;
- Ft 4 is H, F, Cl, Br, NH 2, N0 2, CN, CH 3, OH, CF 3, SH, 0-CH 3, OCF 3, N (CH 3) 2, S-CH 3, or C (0) OH
- Ft 5 is H, F, Cl, Br, NH 2 , NO 2 , CN, CH 3, OH, CF 3 , SH, O-CH 3 , OCF 3 , N (CH 3 ) 2 , S-CH 3 or C (0) OH;
- PAS is a photoactivatable protecting group, preferably o-nitrobenzyl, 1- (o-nitrophenyl) ethylidenes, 4,5-dimethoxy-2-nitrobenzyl, 7-dimethylamino-coumarin-4-yl (DMACM) caged), 7-diethylamino-coumarin-4-yl (DEACM-caged) and 6,7-bis (carboxymethoxy) coumarin-4-yl) methyl (BCMCM-caged), and wherein BAS is a bio-activatable protecting group, preferably methyl, acetoxymethyl, pivaloyloxymethyl, methoxymethyl, propionyloxymethyl, butyryloxymethyl, cyanoethyl, phenyl, benzyl, 4-acetoxybenzyl, 4-pivaloyloxybenzyl, 4-isobutyryloxybenzyl, 4-octanoyloxybenzyl, 4-benzoyloxybenzyl,
- PAS is a photoactivatable protecting group, preferably o-nitrobenzyl, 1- (o-nitrophenyl) ethylidenes, 4,5-dimethoxy-2-nitrobenzyl, 7-dimethylamino-coumarin-4-yl (DMACM) caged), 7-diethylamino-coumarin-4-yl (DEACM-caged) and 6,7-bis (carboxymethoxy) coumarin-4-yl) methyl (BCMCM-caged), and where BAS is a bio-activatable protecting group, preferably Methyl,
- RT to R 5 are defined as described above.
- R 12 is a structure and one, two, three, four or all of RR 2 , R 3 , R 4 and R 5 are the same or different from the other same-residue group.
- CDNs All synthetic CDNs described hitherto in the literature have exclusively the nucleobases adenine, guanine, hypoxanthine or isoguanine with purine structure or substituted purine bases.
- a common feature of such CDNs is the pronounced polarity of the underlying purine nucleobases, resulting in very poor membrane permeability of the resulting CDNs CDNs leads.
- the solution of the present invention is the replacement of at least one of the polar nucleobases adenine, guanine, hypoxanthine or isoguanine with purine structure against a lipophilic structural unit, which surprisingly results in the CDNs continuing to bind to the receptor protein STING bind and / or activate STING-mediated signaling pathways.
- the use according to the invention of the benzimidazole unit which is alternative to the purine skeleton leads, surprisingly, despite a slight structural deviation from the purine skeleton, to a significantly higher lipophilicity.
- the novel CDNs according to the invention replace at least one of the known nucleobases having a purine structure by a benzimidazole unit (or by a substituted benzimidazole). have significantly higher lipophilic values. It is generally accepted that increased lipophilicity values correlate with improved membrane permeability.
- the properties of the new compounds according to the invention in the activation of STING-mediated signaling pathways in generally recognized and literature-described cell biological examination systems, as shown in Examples 19 to 22, are also surprising and unexpected.
- STING-induced dimerization of IRF3, the STING-induced phosphorylation of IRF3, and the STING-induced phosphorylation of TBK1 are also surprising and unexpected.
- STING-mediated increase in interferon- ⁇ production in the STING-mediated increase in interferon- ⁇ production (Example 20), the increase in mRNA formed for interferon ⁇ and ⁇ (Example 21) as well as the amount of secreted interferon ⁇ (Example 22), several of the compounds of the present invention exhibit biological activities.
- the new benzimidazole-containing CDNs are able to activate STING-dependent signaling pathways.
- the replacement of one or both of the native purine bases with one or two benzimidazole artificial units or one or two substituted benzimidazole units does not result in the biological inactivity of the resulting CDNs.
- the result was that many of the CDNs of the present invention are capable of binding to the STING protein with good affinities, as shown in Example 23 by isothermal titration calorimetry (ITC).
- ITC isothermal titration calorimetry
- the above-defined compound of the formula (I) is a compound in which R 10 or R is SH and corresponds to the general description c [N 1 (2 ', 5') pS-N 2 (3 ', 5') p], c [N 1 (2 ', 5') p S -N 2 (2 ', 5') p], c [N 1 (3 ', 5') p S -N 2 (2 ', 5') p] or (as defined above).
- the above defined compound of formula (I) is a compound in which Rio or R BH 3 andmender general description c [Ni (2 ', 5') pB-N 2 (3 ', 5') p ], c [Ni (2 ', 5') pB-N 2 (2 ', 5') p], c [N 1 (3 ', 5') pB-N 2 (2 ', 5') p] or c [Ni (3 ', 5') pB-N 2 (3 ', 5') p] (as defined above).
- the above-defined compound of the formula (I) is a compound in which R 1 or R 3 is BH and corresponds to the general description c [Ni (2 ', 5') pN 2 (3 ', 5') p B] , c [Ni (2 ', 5') pN 2 (2 ', 5') B], c [N 1 (3 ', 5') pN 2 (2 ', 5') pB] or c [Ni ( 3 ', 5') pN 2 (3 ', 5') pB] (as defined above).
- the above-defined compound of the formula (I) is a compound in which R 2 and R 3 are BH and corresponds to the general description c [Ni (2 ', 5') pB-N 2 (3 ', 5') pB], c [Ni (2 ', 5') pB-N 2 (2 ', 5') pB], c [Ni (3 ', 5') pB-N 2 (2 ', 5') pB] or c [Ni (3 ', 5') pB-N 2 (3 ', 5') pB] (as defined above).
- the above-defined compound of the formula (I) is a compound in which R 10 is R or R and correspondingly R or R 10 is BH 3 and corresponds to the general description c [N 1 (2 ', 5') pS-N 2 (3 ', 5') pB], c [N 1 (2 ', 5') p S -N 2 (2 ', 5') p B], c [Ni (3 ', 5') p S -N 2 (2 ', 5') p] c or [Ni (3 ', 5') pS-N 2 (3 ', 5') p] (as defined above).
- the above defined compound of formula (I) is a compound in which Rio, Rn BH 3 and corresponds corresponding Rn or R 10 is SH and the general description of c [N 1 (2 ', 5') pB-N 2 (3 ', 5') pS], c [N 1 (2 ', 5') pB-N 2 (2 ', 5') pS], c [Ni (3 ', 5') pB-N 2 (2 ', 5') pS] or c [Ni (3 ', 5') pB-N 2 (3 ', 5') pS] (as defined above).
- the above defined compound of formula (I) is a compound in which Rio and Rn SH and corresponds to the general description of c [Ni (2 ', 5') pS-N 2 (3 ', 5') pS ], c [Ni (2 ', 5') p S -N 2 (2 ', 5') p S], c [Ni (3 ', 5') p S -N 2 (2 ', 5') p S] or c [Ni (3 ', 5') p S -N 2 (3 ', 5') p S] (as defined above).
- the above-defined compound of the formula (I) may be a compound in which R 2 is CH 3 .
- the above-defined compound of the formula (I) may be a compound in which R 2 is N0 2 . In another particular embodiment, the above-defined compound of the formula (I) may be a compound in which R 2 is NH 2 .
- the above-defined compound of the formula (I) may be a compound in which R 2 is Cl.
- the compound as defined above may be a compound having the formula (I), in which R 3 and R 4 are CH 3.
- the above-defined compound of the formula (I) may be a compound in which R 3 and R 4 are O-CH 3 .
- the compound as defined above may be a compound having the formula (I), in which R 3 and R 4 N0. 2
- the above-defined compound of the formula (I) may be a compound in which R 3 and R 4 are each Cl.
- the above-defined compound of the formula (I) may be a compound in which RR 3 and R 4 are each Cl.
- the above-defined compound of the formula (I) may be a compound in which R is CF 3 and R 3 and R 4 are each Cl.
- the above-defined compound of the formula (I) may be a compound in which R 6 or R 7 and R 8 or R 9 are each OH.
- the compound as defined above may be a compound having the formula (I), in which R 6 or R 7 and R F 8 or R 9 is OH.
- the compound as defined above may be a compound having the formula (I) in which R 6 or R 7 and R 8 or R 9 in each case F.
- the compounds which are depicted in Table 1 and are defined in Claim 8 are particularly preferred. It should be noted that throughout the present description of the invention, and in particular for the compounds in Table 1, in case of doubt of uniqueness, the depicted structure is valid. It is further noted that the compounds of Table 1 are shown as free acid. However, the present invention also encompasses physiologically acceptable salt forms of these compounds, for example with cations such as Na + , K + , Li + , NH 4 + , Et 3 NH + and (- Pr) 2 EtNH + or mixed forms of the cations listed above, without but to be limited to these.
- physiologically acceptable salt forms of these compounds for example with cations such as Na + , K + , Li + , NH 4 + , Et 3 NH + and (- Pr) 2 EtNH + or mixed forms of the cations listed above, without but to be limited to these.
- Table 1 Abbreviations, names and structures of novel, inventive compounds.
- the compounds according to the present invention can additionally be labeled according to known and established methods.
- a fluorescent dye that can be coupled to the compound for example but not limited to confocal fluorescence microscopy, is the intracellular distribution of (binding to) the binding proteins in living cells or to allow fluorescence correlation spectroscopy, fluorescence resonance energy transfer (FRET) studies or determinations of the concentration of the compound in living cells.
- FRET fluorescence resonance energy transfer
- the compounds according to the invention may also be labeled with (radioactive) nuclides instead of or in addition to fluorescent dyes.
- Suitable isotopes and synthesis techniques are well established and known in the art.
- the invention additionally encompasses PEGylated forms of the compounds described, with PEGylation being generally known to improve solubility in water as well as pharmacokinetic and biodistribution properties.
- the invention comprises the described compounds in their prodrug form, wherein the negative charge of the (modified or unmodified) phosphate group is masked by a biologically activatable protective group. It is generally accepted that such structures increase lipophilicity and thus improve both membrane permeability and bioavailability, which generally results in a 10-1000 fold increased potential compared to the parent compound.
- bio-activatable protecting groups can be introduced by known and established prior art methods. Non-limiting preferred examples include acetoxymethyl, propionyloxymethyl, butyryloxymethyl, pivaloyloxymethyl, acetoxyethyl, acetoxybutyl and acetoxyisobutyl.
- Non-limiting preferred examples of the corresponding radicals R 10 and / or according to the invention are acetoxymethyloxy, propionyloxymethyloxy and butyryloxymethyloxy.
- Preferred examples of more labile protecting groups include, but are not limited to, alkyl or aryl groups, as well as substituted alkyl or aryl groups.
- further preferred examples of chemically labile protecting groups of the radicals R 10 and / or R according to the invention are methyl, ethyl, 2-cyanoethyl, propyl, benzyl, phenyl and polyethylene glycol.
- the compounds in their prodrug form are inherently inactive, but extremely membrane permeable, resulting in greatly increased intracellular concentrations. Finally, enzymatic hydrolysis of the ester linkage leads to deprotection and releases the biologically active parent compound.
- the present invention also includes photo-activatable protecting groups (also referred to as "caged” or photolyzable groups) as an alternative or supplement to bio-activatable protecting groups.
- These protecting groups can be introduced by known and established prior art methods.
- photoactivatable protecting groups also constitute a masking of the negative charge of the (modified or unmodified) phosphate group and thus bring about an increase in lipophilicity and, as a result, an increase in membrane permeability and bioavailability.
- Non-limiting preferred examples of photoactivatable protecting groups are o-nitrobenzyl, 1- (o-nitrophenyl) ethylidenes, 4,5-dimethoxy-2-nitrobenzyl, 7-dimethylamino-coumarin-4-yl (DMACM). caged), 7-diethylamino-coumarin-4-yl (DEACM-caged) and 6,7-bis (carboxymethoxy) coumarin-4-yl) methyl (BCMCM-caged).
- the compounds according to the present invention may preferably also be immobilized on (insoluble) support materials.
- support materials include agarose, dextran, cellulose, starch and other carbohydrate-based polymers, synthetic polymers such as polyacrylamide, polyethyleneimines, polystyrene and like materials, apatite, glass, silica gel, gold, graphenes, fullerenes, carboranes , Titanium dioxide, zirconia, alumina, and a surface of a chip suitable for binding various ligands.
- Also part of the invention is a process for the chemoenzymatic preparation of a compound according to the invention having the general structural unit c [N 1 (2 ', 5') pN 2 (3 ', 5') p] or c [N 1 (3 ', 5' ) pN 2 (3 ', 5') p] by transglycosylation of c-diAMP, c-diGMP, 2 ', 3'-cGAMP or 3', 3'-cGAMP by means of a purine nucleoside phosphorylase (PNPase).
- PNPase purine nucleoside phosphorylase
- Also part of the invention is a process for the chemoenzymatic preparation of a compound according to the invention having the general structural unit c [N 1 (2 ', 5') pN 2 (3 ', 5') p], c [N 1 (2 ', 5' ) pS-N 2 (3 ', 5') p], c [N 1 (2 ', 5') pS-N 2 (3 ', 5') pS], c [N 1 (2 ', 5' ) p-N 2 (3 ', 5') p], c [N 1 (2 ', 5') pB-N 2 (3 ', 5') p], c [N 1 (2 ', 5' ) pB-N 2 (3 ', 5') pS] or c [N 1 (2 ', 5') pS-N 2 (3 ', 5') pB] by dimerization and cyclization of 5'-O-triphosphates , 5'-
- part of the invention is a process for the chemoenzymatischen preparation of a compound of the invention with the general structural unit c [N 1 (3 ', 5') pN 2 (3 ', 5') p], ⁇ ⁇ ', ⁇ ⁇ ⁇ - ⁇ ⁇ ', ⁇ ⁇ ⁇ ', ⁇ ⁇ ⁇ - ⁇ ⁇ ', ⁇ ⁇ ⁇ ], or cIN ⁇ S'.j'JpB-N ⁇ S'.o'JpB], wherein alternatively the benzimidazole radical is substituted by an optionally substituted Purinbase may be replaced by dimerization and cyclization of 5'-O-triphosphates or 5'-O- (1 -Boranotriphosphaten) with an enzyme DNA integrity scanning protein (DisA) from Bacillus subtilis. In the latter method, it is also possible that the radical R 12 according to formula (I) may also represent an optionally substituted purine base.
- the inventive method makes the compounds of the invention in a relatively simple manner accessible.
- Part of the invention is also the use of a compound of the invention as a medicament.
- a compound of formula (I) may be used in pharmacologically acceptable form for the treatment or prevention of a disease wherein the disease is selected from the group consisting of cancer, infectious disease of bacterial or viral origin, acute organ transplant rejection , Type 1 diabetes mellitus, rheumatoid arthritis, psoriasis, Crohn's disease, restenosis, allergic asthma and other diseases whose condition can be improved or cured by activation of the STING pathway.
- the present invention relates to a method of treating or preventing one of said diseases by administering a therapeutically or prophylactically effective amount of a compound of formula (I) to a subject or a patient in need of prophylaxis or therapy ,
- a compound of formula (I) according to the present invention may be used as a research reagent, preferably as a research reagent for the study of a disease or dysfunction.
- diseases or disorders are cancer, infectious diseases of a bacterial or viral nature, acute organ transplant rejection, type I diabetes mellitus, rheumatoid arthritis, psoriasis, Crohn's disease, restenosis, allergic asthma, or any other condition whose activation by STING pathway can be improved or cured
- DMSO dimethyl sulfoxide
- Reaction progress and purity control of the isolated products are carried out with reversed phase HPLC (RP-18, ODS-A-YMC, 120-S-1 1, 250 ⁇ 4 mm, 1.5 mL / min (YMC, Dinslaken, Germany)), with UV detection at the A max of the respective nucleobases. All chromatographic investigations were carried out at room temperature.
- the syntheses described are typically carried out in a 20-200 ⁇ scale in 2 mL polypropylene reaction vessels with screw cap and seal. Also suitable are syntheses in the scale of 0.5 ⁇ - 1 mmol in 2 ml_ polypropylene reaction vessels with screw cap and seal or in 10 mL to 500 ml_ round bottom flask. Reactions under a protective gas atmosphere or degassing usually take place in 10 or 25 mL round bottom flasks.
- the purification of the crude products is carried out, for example, by preparative MPLC (Merck, LiChroprep RP-18, 15-25 ⁇ ), preparative anion chromatography (GE Healthcare, Sepharose Q Fast Flow, 45-165 ⁇ ) or preparative HPLC (RP-18, ODS- A-YMC, 120-S-1 1, 250 x 16 mm, UV 254 nm), whereby the composition of the eluent depends on the respective substance and is generally identical to the analytical HPLC.
- YMC * gel SIL (6 nm, S-75 ⁇ ) silica gel was used.
- Desalting is achieved by repeated lyophilization or preparative HPLC (RP-18, ODS-A-YMC, 120-S-1, 250 x 16 mm, UV 254 nm), as is common in nucleotide chemistry.
- the product-containing solutions are frozen at -70 ° C for 15 minutes and evaporated in vacuo either by freeze-drying or in a centrifuge.
- concentration is carried out by means of rotary evaporator under reduced pressure in a diaphragm pump vacuum or in a high-oil pump at water bath temperatures not exceeding 28 ° C to 33 ° C.
- Triethylammonium salts are converted, for example, by means of cation exchange chromatography (GE Healthcare, SP Sepharose TM Fast Flow, 45-165 ⁇ ) into the corresponding sodium salts.
- Yields are determined according to Lambert-Beer by means of UV spectroscopy with a JASCO V-650 spectrophotometer (JASCO Germany GmbH, Gross-Umstadt) at A max . Unknown extinction coefficients are derived from literature-known values of structurally similar compounds. Mass spectra are measured with an Esquire LC 6000 spectrometer (Bruker Daltonic, Bremen, Germany) in ESI-MS mode with 50% water / 49.5% methanol / 0.5% NH 3 (pH 9) as matrix.
- the HPLC system was composed as follows: Pump: Elite LaChrom L 2130; Detector: Elite La Chrome L 2455 DAD; Column oven: Elite La Chrome L 2350; Autosampier: Elite La Chrome L 2200; Software package: Computer EZ Chrome Elite (all VWR / Hitachi, Darmstadt, Germany).
- the enzyme that normally removes the nucleobases of ribo and deoxyribo purine nucleosides is used here to target the natural nucleobases of the natural CDNs (c-diGMP, c-diAMP, 2 ', 3'-cGAMP, 3', 3'- cGAMP) against other unnatural bases (transglycosylation).
- the higher stability of the glycosidic bond to benzimidazole is used in comparison to the natural purine bases.
- c-diGMP Biolog Life Science Institute Research Laboratory and Biochemica Sales GmbH, Bremen, Germany (hereinafter also abbreviated to "Biolog GmbH, Bremen") and one of the free benzimidazole nucleobases as defined in claim 1, are incorporated herein by reference
- Variants of the enzyme are commercially available eg from Sigma-Aldrich and can according to the invention in homogeneous solution or even preferably on natural carrier material, such as dextran, agarose, cellulose or of synthetic Such as acrylamide, polystyrene, etc.
- PNPases that can be derived from lower species are preferred.
- benzimidazole analogs are poorly soluble in water; Here, the benzimidazole analog is previously enriched by heating and sonication in the solution and an existing suspension used. Preference is given to the addition of solubilizers, such as DMSO or DMF or surfactants in a concentration which does not interfere significantly with the enzymatic conversion. However, because of the high thermostability of the PNPases, the reaction is in any case preferably carried out in the temperature range from 30 ° C. to 60 ° C.
- the enzymatic reaction is carried out in 0.01M-1M TRIS-HCl buffer in the pH range 6-10 in the presence of 1-15% glycerol and 0.0001M-0.1M dithiothreitol (DTT) at 20 ° C - 50 ° C performed.
- DTT dithiothreitol
- the enzymatic synthesis is carried out in 20 mM TRIS-HCl buffer in a pH range of 6.5-8.5, 0.001 M DTT, at 37 ° C.
- Example 1 Synthesis of cyclic (guanosine (3 '-> 5') - monophosphates benzimidazole riboside- (3 '-> 5') - monophosphate (crG (3 ', 5') pBI (3 ', 5') Pl) , and cyclic (benzimidazole riboside- (3 '-> 5') - monophosphate - benzimidazole riboside- (3 '-> 5') - monophosphate) (crBI (3'.5 ') pBI (3'.5') Pl)
- the typical yield is between 15 and 45% for the symmetrical product with two benzimidazole units and between 7 and 16% for the asymmetric mixed product.
- Example 2 Synthesis of cyclic (adenosine (3 '-> 5') - monophosphates - 5,6-dimethylbenzimidazole riboside (2 '-> 5') monophosphate ( ⁇ (3 ', 5') ⁇ (2 ', 5 ') ⁇ 1)
- the typical yield is between 15 and 45%, depending on the state of the enzyme.
- Activated nucleoside 5'-monophosphates can dimerize, polymerize and also cyclize under the influence of clays.
- the distribution of the different species depends on the selected reaction conditions. In the reaction, both 2 ', 5' and 3 ', 5'-linked adducts form in the reaction mixture next to each other.
- Example 3 Synthesis of cyclic (5,6-dichlorobenzimidazole riboside (2 '-> 5') - monophosphate - 5,6-dichlorobenzimidazole riboside (3 '-> 5') monophosphate) (crDCIBI (2 ', 5') pDCIBI (3 ', 5') Pl) and cyclic (5,6-dichlorobenzimidazole riboside (3 ' ⁇ 5') monophosphate 5,6-dichlorobenzimidazole riboside (3 ' ⁇ 5') monophosphate) (crDCIBI ( 3 ', 5') pDCIBI (3 ', 5') Pl)
- the progress of the reaction or the decrease in the educt signal is monitored by reversed phase HPLC.
- reaction solution is filtered, gently concentrated on a rotary evaporator and purified by preparative HPLC.
- the cyclic reaction products are isolated in the triethylammonium form and lyophilized.
- the typical yield is about 5% for the 2 '-> 5' / 3 '-> 5'-linked product and about 35% for the 3' -> 5 '/ 3' -> 5'-linked product.
- chemoenzymatic reactions can be carried out either in homogeneous solution or preferably with an enzyme immobilized on natural support material, such as dextran, agarose, cellulose or of a synthetic nature, such as acrylamide, polystyrene, etc.
- natural support material such as dextran, agarose, cellulose or of a synthetic nature, such as acrylamide, polystyrene, etc.
- the chemoenzymatic reaction is carried out with DisA immobilized on 10 Sepharose 4 Fast Flow (GE Healthcare).
- the enzyme is enzymatically active at temperatures of 15 ° C - 50 ° C over a wide pH range of pH 5 - pH 1 1 in unbuffered or buffered solution in the presence of divalent metal salts and reducing agents.
- Buffers are buffer systems which are generally known to the person skilled in the art for biological applications and proteins.
- the enzymatic reaction is carried out in 0.01 M-1 M alkylammonium-containing buffers in a pH range of 7-10 with 0.01 M-1 M magnesium chloride and 0.0001 M-0.1 M dithiothreitol (DTT) at 20 ° C. 40 ° C performed.
- DTT dithiothreitol
- the enzymatic synthesis is carried out in a buffer solution of 0.1 M ethanolamine buffer, 0.025 M magnesium chloride, 0.001 M DTT, pH 9.5 at 20 37 ° C.
- the resulting immobilized enzyme was then washed with 30 ml of 30 mM NaH 2 PO 4 , pH 7 and then stored as a slurry (total volume ⁇ 3 ml) in 30 mM NaH 2 PO 4 , pH 7 with 1% NaN 3 at 4 ° C.
- a buffer was exchanged for 0.1 M ethanolamine buffer, 0.025 M magnesium chloride, 0.001 M DTT, pH 9.5 (reaction buffer) 35.
- reaction buffer pH 9.5
- DisA-Sepharose slurry 100 ⁇ l of DisA-Sepharose slurry, as prepared in Example 4, were mixed with 0.5 ⁇ l of 2'-fluoro-2'-deoxyadenosine-5'-O-triphosphate (BIOLOG GmbH, Bremen) in 0.1 M ethanolamine buffer, 0.025 M magnesium chloride, 0.001 M DTT, pH 9.5 quantitatively reacted at 37 ° C within 26 h (> 94% product formation).
- BIOLOG GmbH 2'-fluoro-2'-deoxyadenosine-5'-O-triphosphate
- Example 7 Chemoenzymatic synthesis of cyclic (adenosine (3 '->5') - monophosphate adenosine - (3 '->5') - monophosphate) (c-diAMP), cyclic (adenosine (3 '-> 5 ') Monophosphate - 8-chloroadenosine - (3'-> 5 ') - monophosphate) (8-CI-c-diAMP) and cyclic (8-chloroadenosine (3'-> 5 ') - monophosphate -8-chloroadenosine - (3 '->5') - monophosphate) (8,8'-di-CI-c-diAMP) 100 ⁇ M of disA-Sepharose slurry, as prepared in Example 4, were mixed with 0.5 ⁇ adenosine-5'-O-triphosphate and 0.5 ⁇ 8-chloroadenosine-5'-O-triphosphate (BIOLOG
- DisA-Sepharose slurry prepared as in Example 4, were mixed with 0.5 ⁇ l of 2-chloroadenosine 5'-O-triphosphate (BIOLOG GmbH, Bremen) in 0.1 M ethanolamine buffer, 0.025 M magnesium chloride, 0.001 M DTT, pH 9.5 quantitatively reacted at 37 ° C within 20 h (> 93% product formation).
- Example 10 Chemoenzymatic synthesis of cyclic (adenosine (3 '-> 5') - monophosphate adenosine - (3 '-> 5') - monophosphate) (c-diAMP), cyclic (adenosine (3 '-> 5 ') -monophosphate-benzimidazole riboside- (3' -> 5 ') -monophosphate) (crA (3', 5 ') pBI (3', 5 ') Pl) and cyclic (benzimidazole riboside- (3' -> 5 ') - monophosphate - benzimidazole riboside - (3 '-> 5') - monophosphate) (crBI (3'.5 ') pBI (3'.5') Pl)
- DisA-Sepharoselurry 25 ml of DisA-Sepharoselurry, as prepared in Example 4, with 50 ⁇ adenosine 5'-O-triphosphate and 100 ⁇ benzimidazole riboside 5'-O-triphosphate (BIOLOG GmbH, Bremen) in 0.1 M ethanolamine buffer, 0.025 M magnesium chloride, 0.001 M DTT, pH 9.5 reacted at 30-37 ° C within 3 days (> 75% product formation).
- DisA-Sepharoselurry 25 ml of DisA-Sepharoselurry, as prepared in Example 4, with 50 ⁇ 2'-fluoro-2'-deoxyadenosine 5'-O-triphosphate and 50 .mu.mol benzimidazole riboside 5'-O-triphosphate (BIOLOG GmbH, Bremen) in 12 mL 0.1 M ethanolamine buffer, 0.025 M magnesium chloride, 0.001 M DTT, pH 9 at 30 ° C - 37 ° C reacted within 43 h (> 75% product formation).
- Example 12 Chemoenzymatic synthesis of cyclic (adenosine (3 ' ⁇ 5') monoboranophosphate adenosine (3 ' ⁇ 5') monoboranophosphate) (c-diAMPBB), cyclic (adenosine (3 '-> 5 ') - monoboranophosphate - benzimidazole riboside - (3' -> 5 ') - monophosphate) (crA (3', 5 ') pB-BI (3', 5 ') Pl) and cyclic (Benzimidazolribosid- (3' -> 5 ') -monophosphate - benzimidazole riboside - (3' -> 5 ') - monophosphate) (crBI (3', 5 ') pBI (3', 5 ') Pl)
- DisA-Sepharose slurry 100 ⁇ l of DisA-Sepharose slurry, as prepared in Example 4, are mixed with 0.5 ⁇ g of adenosine-5'-O- (1-boranotriphosphate) and 0.5 ⁇ g of benzimidazole-riboside-5'-0-triphosphate (BIOLOG GmbH, Bremen). reacted in 0.1 M ethanolamine buffer, 0.025 M magnesium chloride, 0.001 M DTT, pH 9.5 at 37 ° C within 3 days (> 75% product formation).
- Example 12A Chemoenzymatic synthesis of cyclic (benzimidazole riboside (3 ' ⁇ 5') monophosphate benzimidazole riboside (3 ' ⁇ 5') monophosphate) (crBI (3 ', 5') pBI (3 ', 5') ) Pl)
- Example 12B Chemoenzymatic synthesis of cyclic (5,6-dichlorobenzimidazole riboside (3 '-> 5') - monophosphate - 5,6-dichlorobenzimidazole riboside (3 '-> 5') monophosphate) (0 ⁇ (3'.5 ' ) ⁇ (3'.5 ') ⁇ )
- Example 12C Chemoenzymatic Synthesis of Cyclic (2-fluoro-2-deoxyadenosine (3 ' ⁇ 5') Monophosphate -2-Fluoro-2-Deoxyadenosine- (3 '-> 5') Monophosphate) (2'- 2 "-di-Fc-didAMP) cyclic (2'-fluoro-2'-deoxyadenosine (3 ' ⁇ 5') monophosphate 5,6-dichlorobenzimidazole riboside - (3 '-> 5') - monophosphate) ( cr2'-F-dA (3 ', 5') pDCIBI (3 ', 5') Pl) and cyclic (5,6-dichlorobenzimidazole riboside (3 ' ⁇ 5') monophosphate 5,6-dichlorobenzimidazole riboside ( 3 '-> 5') - monophosphate) (crDCIBI (3 ', 5') pDCIBI (3
- DisA-Sepharoselurry 25 ml of DisA-Sepharoselurry, as prepared in Example 4, with 100 ⁇ 2'-fluoro-2'-deoxyadenosin-5'-O-triphosphate and 100 .mu.mol 5,6-dichlorbenzimidazolribosid-5'-O-triphosphate (BIOLOG GmbH , Bremen) in 50 mL 0.1 M ethanolamine buffer, 0.025 M magnesium chloride, 0.001 M DTT, pH 9.5 at 30 - 37 ° C within 3 days ( ⁇ 70% product formation).
- Example 12D Chemoenzymatic synthesis of cyclic (adenosine (3 ' ⁇ 5') monophosphate adenosine (3 ' ⁇ 5') monophosphate) (c-diAMP), cyclic (adenosine (3 ' ⁇ 5) ') - monophosphate - 5,6-dichlorobenzimidazole riboside - (3'-> 5 ') - monophosphate) (crA (3', 5 ') pDCIBI (3', 5 ') P1) and cyclic (5,6-dichlorobenzimidazole riboside) (3 '->5') - monophosphate : 5,6-dichlorobenzimidazole riboside (3 ' ⁇ 5') monophosphate)
- Example 12E Chemo-enzymatic synthesis of cyclic (2-fluoro-2-deoxyinosine (3 ' ⁇ 5') monophosphate benzimidazole riboside (3 ' ⁇ 5') monophosphate) (cr 2'-F-dl (3 ') , 5 ') pBI (3', 5 ') Pl) 5.5 ⁇ (c [2'-F-dA (3', 5 ') pBI (3', 5 ') p]) from Example 1 1 were in analogy to known literature synthesis 8 with adenosine monophosphate deaminase (Deamyzyme 5000, Amano Enzyme Europe Ltd, Great Britain) within 2 days quantitatively converted to c [2'-F-dl (3 ', 5') pBI (3 ', 5') p].
- the enzyme cGAMP synthase (cGAS) is able to biocatalytically produce the non-canonical 2 ', 3'-cGAMP from GTP and ATP in the presence of double-stranded DNA.
- the enzyme is not highly specific and it has already been shown that the chemoenzymatic synthesis of mono- and diphosphorothioate-containing CDNs is possible with this enzyme 3 .
- the same enzyme (recombinantly expressed from the mouse) is used to prepare the benzimidazole-containing CDNs of the present invention.
- the chemoenzymatic reactions can be carried out either in homogeneous solution or preferably with an enzyme immobilized on natural support material, such as dextran, agarose, cellulose or of a synthetic nature, such as acrylamide, polystyrene, etc.
- the enzyme is enzymatically active at temperatures of 15 ° C - 50 ° C over a wide pH range of pH 5 - pH 1 1 in unbuffered or buffered solution in the presence of divalent metal salts, double-stranded DNA and reducing agents.
- Buffers are buffer systems which are generally known to the person skilled in the art for biological applications and proteins.
- the enzymatic reaction is carried out in 0.01M-1M buffers in a pH range of 7-10 with 0.005M-1M magnesium chloride, 0.01 mg / mL-1 mg / mL herring sperm DNA, and 0.0001 M - 0.1 M dithiothreitol (DTT) at 20 ° C - 40 ° C performed.
- 0.01M-1M buffers in a pH range of 7-10 with 0.005M-1M magnesium chloride, 0.01 mg / mL-1 mg / mL herring sperm DNA, and 0.0001 M - 0.1 M dithiothreitol (DTT) at 20 ° C - 40 ° C performed.
- the enzymatic synthesis is carried out in a buffer solution of 0.02 M TRIS-HCl, 0.02 M magnesium chloride, 0.1 mg / mL herring sperm DNA, 0.001 M DTT, pH 8 at 37 ° C.
- 10 ⁇ cGAS (mouse, amino acids 147-507) are mixed with 1 ⁇ guanosine-5'-O- (1-boranotriphosphate) and 1 ⁇ benzimidazole riboside 5'-O- (1-thiotriphosphate) (BIOLOG GmbH, Bremen) in 0.002 M TRIS-HCl, 0.02 M magnesium chloride, 0.1 mg / mL herring sperm DNA, 0.001 M DTT, pH 8 in 1 mL total solution at 37 ° C within 3 days (> 75% product formation).
- Example 15 Chemical synthesis of cyclic (adenosine (3 '-> 5') - monophosphate - benzimidazole riboside (3 ' ⁇ 5') monophosphate) (crA (3 ', 5') pBI (3 ', 5') ) pl)
- Figure 1 Synthesis of cyclic (adenosine (3 '->5') monophosphate - benzimidazole riboside (3 '->5') monophosphate) (c [A (3 ', 5') pBI (3 ', 5 ') p]).
- the phosphoramidite 5'-DMTr-2'-TBDMS-3'-CEP-adenosine (Chemgenes Inc., USA) is dissolved in dry acetonitrile and treated with 2 equivalents of water and 1.2 equivalents of pyridinium trifluoroacetate and stirred for 15 minutes at room temperature. Thereafter, the volatiles are evaporated under reduced pressure. Subsequently, 100 equivalents of ferric butylamine are added, the resulting solution is stirred for 30 minutes at room temperature and then evaporated again under reduced pressure. The residue is dissolved in acetonitrile and evaporated again under reduced pressure. The resulting residue is dissolved in dichloromethane and 10 equivalents of water are added.
- Example 15.b Synthesis of linear dinucleotide 5'-OH-2'-TBDMS-benzimidazole riboside- (3'-5 ') -vano-ethanol-phosphate-2'-TBDMS-3'-H-phosphonate-N 6 -Bz-adenosine
- LC-MS analysis of the crude product confirms the presence of the cyclic dinucleotide 2'-TBDMS-N 6 -Bz-adenosine (3'-> 5 ') -monophosphate-2'-TBDMS-benzimidazole riboside (3'->5' ) cyanoethyl phosphate. If necessary, the cyclic dinucleotide is stored at -70 ° C. The crude product is dissolved in a minimum amount of dichloromethane and purified by preparative flash chromatography on silica gel with a methanol / dichloromethane gradient. Product-containing fractions are evaporated under reduced pressure and purified in Example 15.e. implemented further. If necessary, the cyclic dinucleotide is stored at -70 ° C.
- Example 15.f. The resulting crude product of cyclic 2'-TBDMS-adenosine (3'-> 5 ') -monophosphate-2'-TBDMS-benzimidazole riboside (3'->5') monophosphate is used in Example 15.f. implemented further. If necessary, the cyclic dinucleotide is stored at -70 ° C.
- Example 15.f.f. Synthesis of cyclic (adenosine (3'-> 5 ') - monophosphate - benzimidazole riboside (3' ⁇ 5 ') monophosphate) ( ⁇ (3'.5') ⁇ - ⁇ (3'.5 ') ⁇ 1)
- the crude product is diluted and purified on a Q Sepharose TM Fast Flow anion exchanger with a triethylammonium bicarbonate gradient.
- the product-containing fractions are combined, the solvent is evaporated under reduced pressure and the target compound is then highly purified by preparative reversed phase chromatography (RP-18) with a suitable acetonitrile / 20 mM triethylammonium formate eluent.
- the desalting of the target compound is also carried out with preparative reversed phase chromatography (RP-18) and the desalted target compound is then present as the triethylammonium salt.
- RP-18 preparative reversed phase chromatography
- the sodium salt of the target compound is obtained by passage of a dilute product solution through a SP Sepharose TM Fast Flow cation exchanger (Na + form). 0 ⁇ (3'.5 ') ⁇ (3'.5') ⁇ 1: 3 ', 5' / 3 ', 5'
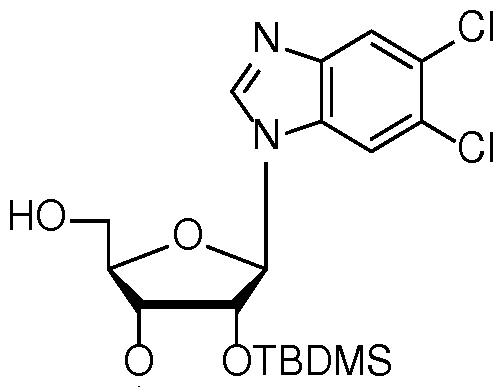
- the phosphoramidite 5'-DMTr-2'-TBDMS-3'-CEP-5,6-dichlorobenzimidazole riboside (BIOLOG GmbH, Bremen) is prepared analogously to Example 15.a. converted into the above target compound.
- Example 16.b Synthesis of linear dinucleotide 5'-OH-2'-TBDMS-5,6-dichlorobenzimidazole riboside- (3'-5 ') -canoethyl-phosphorothioate-2'-TBDMS-3'-H-phosphonate-5,6-dichlorobenzimidazole riboside
- the above target compound is analogous to Example 15.b. produced.
- the above target compound is analogous to Example 15.c. produced.
- Example 16d Synthesis of cyclic (2-TBDMS-5,6-dichlorobenzimidazole riboside- (3 ' ⁇ 5') - monophosphorothioate-2'-TBDMS-5,6-dichlorobenzimidazole riboside- (3'-5 ') -cyanoethyl phosphorothioate)
- Example 15.d The abovementioned target compound is prepared analogously to Example 15.d. produced. Instead of iodine from Example 15.d. Here, 1.5 equivalents of 3H-1,2-benzodithiol-3-one are added to establish the phosphorothioate unit.
- the abovementioned target compound is prepared analogously to Example 15.e. produced.
- Example 16.f Synthesis of cyclic (5,6-dichlorobenzimidazole riboside- (3'-> 5 ') -monophosphorothioate-5,6-dichlorobenzimidazole riboside (3' ⁇ 5 ') monophosphorothioate) (crDCIBI (3'.5') pS-DCIBI ( 3'.5 ') PSL)
- Example 15.f. The above target compound is analogous to Example 15.f. produced.
- Figure 3 Synthesis of cyclic (guanosine (2 '->5') monophosphorothioate - 5,6-dichlorobenzimidazole riboside (3 '->5') monophosphorothioate) (c [G (2 ', 5') pS- DCIBI (3 ', 5') pS]).
- the phosphoramidite 5'-DMTr-2'-TBDMS-3'-CEP-5,6-dichlorobenzimidazole riboside (0.7 mmol) (BIOLOG GmbH, Bremen) was dissolved in 12 mL dry acetonitrile and treated with 2 equivalents of water and 1, 2 Added equivalents of pyridinium trifluoroacetate and stirred for 15 min at room temperature. Thereafter, the volatiles were evaporated under reduced pressure. Then, 100 equivalents of ferric butylamine were added, and the resulting solution was stirred for 30 minutes at room temperature and then re-evaporated under reduced pressure. The residue was dissolved in 30 mL acetonitrile and evaporated again under reduced pressure.
- Example 17.b Synthesis of the linear dinucleotide 5'-OH-3'-TBDMS-N 2 -isobutyrylquanosin- (2 ⁇ 5 ') - cvanoethyl phosphorothioate-2'-TBDMS-3'-H-phosphonate-5,6-dichlorbenzimidazolribosid
- the resulting crude product of cyclic (guanosine (2 '->5') - monophosphorothioate - 5,6-dichlorobenzimidazolriboside (3 '->5') - monophosphorothioat) was suspended with water, treated in an ultrasonic bath and the aqueous phase with three times Shaken out chloroform. After subsequent filtration, the crude product was diluted and purified on a Q Sepharose TM Fast Flow anion exchanger with a triethylammonium bicarbonate gradient.
- the product-containing fractions were evaporated under reduced pressure and the two major isomers of the target compound were then purified by preparative reversed phase chromatography (RP-18) with a suitable acetonitrile / 20 mM triethylammonium formate eluent.
- Major isomer 1 elutes faster in reversed-phase chromatography than major isomer 2 (HI2).
- HI1 and HI2 are those isomer fractions of the respective compound to which the percentage most dominant HPLC signals of this compound are assigned. This definition for major isomer 1 and major isomer 2 applies analogously to other compounds in this text as well.
- the desalting of the two main isomers of the target compound was also carried out with preparative reversed phase chromatography (RP-18) and the desalted main isomers of the target compound were then present as the triethylammonium salt.
- the sodium salts of the major isomers of the target compound were obtained by passage of a dilute product solution through a SP Sepharose TM Fast Flow cation exchanger (Na + form).
- Example 17G cyclic (guanosine (2 '-> 5') - monophosphorothioate - benzimidazole riboside (3 ')
- Example 17H cyclic (adenosine (3 ' ⁇ 5') monophosphorothioate benzimidazole riboside (2 ' ⁇ 5') monophosphorothioate), (crA (3 ', 5') pS-BI (2 ', 5') pSl), major isomer 1 and major isomer 2.
- Example 171 cyclic (2'-fluoro-2'-deoxyadenosine (3 ' ⁇ 5') monophosphorothioate benzimidazole riboside (2 ' ⁇ 5') monophosphorothioate).
- Example 17J cyclic (5,6-dichlorobenzimidazole riboside (2 '->5') monophosphorothioate - 5,6-dichlorobenzimidazole riboside (3 ' ⁇ 5') monophosphorothioate).
- CrDCIBire'.S'toS-DCIBiP'.S ⁇ PSL Major isomer 1 and major isomer 2.
- Example 17K cyclic (adenosine (2 '->5') monophosphorothioate - 5,6-dichlorobenzimidazole riboside (3 '->5') monophosphorothioate), (crA (2 ', 5') pS-PCIBI (3 ', 5') PSL), major isomer 1 and 2.
- Example 17L cyclic (2'-fluoro-2'-deoxyadenosine (3 '->5') - monophosphorothioate - 5,6-dichlorobenzimidazole riboside (2 '->5') monophosphorothioate), (cr2'-F-) dA (3 ', 5') pS-DCIBI (2 ', 5') pSl), major isomer 1 and major isomer 2.
- Example 17M cyclic (adenosine (3 ' ⁇ 5') monophosphorothioate 5,6-dichlorobenzimidazole riboside (2 ' ⁇ 5') monophosphorothioate), (crA (3 ', 5') pS-DCIBI (2 ', 5') PSL), major isomer 1 and 2.
- Main isomer 1 (faster eluting isomer), (CRA (3'.5 ') pS-DCIBI (2'.5') pSl.HI1)
- Example 17N cyclic (adenosine (2 '-> 5') - monophosphorothioate - benzimidazole riboside (3 '
- CDNs such as c-diAMP (log k ' g 0.991), c-diGMP (log k' g 0.840) or 2 ', 3'-cGAMP (log k' g 0.766 (Table 2) showed very polar behavior here and there seems very unlikely that they can penetrate cellular membranes by passive diffusion.
- the CDNs according to the invention having at least one benzimidazole nucleobase have considerably higher lipophilicity and therefore show correspondingly higher retention times and thus also very high log k ' g values in this measuring system, as is shown by way of example for 1 1 novel CDNs according to the invention in Table 2.
- substitution of sulfur or borane for an oxygen in the phosphate moiety of the CDNs of the present invention further increases lipophilicity so that the phosphorothioate and especially the boranophosphate analogs of the benzimidazole CDNs are orders of magnitude more lipophilic than their parent compounds.
- Substitutions at positions 4, 5, 6, and 7 on the 6-membered ring and in position 2 of the imidazole moiety of the benzimidazole skeleton generally also increase lipophilicity.
- Table 2 HPLC retention times and lipophile values (log k ' g ) of novel, CDNs according to the invention.
- Example 19 Determination of the STING-Induced Dimerization of IRF3 After the Invention of the Inventive CDNs, the STING-Induced Phosphorylation of IRF3, and the STING-Induced Phosphorylation of TBK1
- THP-1 cells (Sigma catalog number 88081201 -1 VL) were isolated from the peripheral blood of a one-year male patient with acute leukemia.
- a cell lysate is prepared which is partly applied to a native polyacrylamide gel and partly to two denaturing polyacrylamide gels (SDS-PAGE).
- the developed gels are analyzed using the Western Blot technique.
- an IRF3 antibody is used in the case of the native gel.
- a single band is detected which shows a running behavior corresponding to the molecular weight of IRF3.
- the administration of the CDN according to the invention leads to the formation of a second band whose running behavior corresponds to twice the molecular weight of IRF3. This band is the dimer induced by the CDN of the invention.
- Example 20 Determination of the activity induced by STING after administration of the CDNs according to the invention with the aid of an interferon- ⁇ -promoter-reporter construct
- THP1 -Blue TM cells are derived from THP-1 cells.
- THP1 -Blue TM cells were stimulated by administration of a CDN according to the invention or a buffer control in the culture dish.
- the gene for secreted embryonic alkaline phosphatase (SEAP) is under the control of an interferon- ⁇ promoter.
- SEAP embryonic alkaline phosphatase
- the culture supernatant was removed and the enzymatic activity of the SEAP was determined photometrically in a colorimetric assay by measuring the absorbance at 625 nm (optical density, OD 625 nm).
- the administration of the CDN according to the invention induced an increase in the measured activity of the SEAP, which represents a measure of the activity of the STING signaling pathway.
- THP-1 cells (Sigma catalog number 88081201 -1 VL) were isolated from the peripheral blood of a one-year male patient with acute leukemia.
- THP1 cells are stimulated by administration of a CDN according to the invention or a buffer control in the culture switch. After stimulation, the mRNA is isolated from the cells and converted into cDNA with the aid of the enzyme reverse transcriptase.
- the relative concentration of the cDNA obtained after the administration of a CDN according to the invention by the RNA coding in each case for interferon ⁇ and ⁇ in comparison to the buffer control is determined by means of quantitative PCR.
- the administration of a CDN according to the invention leads to an increase in the formation of mRNA coding for interferon ⁇ and ⁇ . This effect is no longer observed in cells from which STING was genetically removed (knock out).
- THP-1 cells (Sigma, catalog number 88081201 -1 VL) were isolated from the peripheral blood of a one-year male patient with acute leukemia.
- HEK293 is a cell line made from human embryonic kidney.
- THP1 cells and HEK293 cells in which STING has been artificially expressed are stimulated by the administration of a CDN according to the invention or a buffer control.
- the culture medium is removed and the amount of interferon ⁇ secreted by the cells into the medium is determined by means of an enzymatically linked immunoassay (ELISA).
- ELISA enzymatically linked immunoassay
- the system "Human IFN-beta ELISA Kit" R & D Systems, catalog number 41410) is used according to the instructions of the manufacturer
- the administration of a CDN according to the invention leads to a significant increase in the detectable amount of interferon .beta.
- Example 23 Determination of the Affinity of the Interaction of the CDNs According to the Invention and STING by Isothermal Titration Calorimetry (ITC).
- Constructs of human STING are expressed as GST-fusion proteins in bacteria.
- the purification with proteolytic cleavage of the GST tag is carried out by means of affinity chromatography and size exclusion chromatography.
- STING solutions with a concentration of up to 200 ⁇ are presented in the measuring cell and titrated with a CDN according to the invention in identical buffer solution.
- the heat tones obtained during the titration clearly show an interaction of the CDNs according to the invention with STING.
- the particular affinities are of the same order of magnitude as or exceed the natural cyclic nucleotides.
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Molecular Biology (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Genetics & Genomics (AREA)
- Biotechnology (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- Microbiology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Engineering & Computer Science (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Epidemiology (AREA)
- Saccharide Compounds (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Abstract
Beschrieben werden neue zyklische Dinukleotide, die im Gegensatz zu ihren natürlichen Vertretern, lipophile Nukleobasen tragen und dadurch höhere Membrangängigkeit und gesteigerte Aktivität besitzen.
Description
d , u DEREN HERSTELLUNG UND IHRE VERWENDUNG ZUR AKTIVIERUNG VON STIMULATOR VON INTERFERONGENEN (STING)-ABHÄNGIGEN
SIGNALWEGEN
Beschrieben werden neue zyklische Dinukleotide, die im Gegensatz zu ihren natürlichen Vertretern, lipophile Nukleobasen tragen und dadurch höhere Membrangängigkeit und gesteigerte Aktivität besitzen.
Die vorliegende Erfindung ist im Bereich der Immuntherapie angesiedelt. Es handelt sich bei der vorliegenden Erfindung um zyklische Dinukleotide (CDNs) der Formel (I) wie in den Ansprüchen definiert. Im Besonderen handelt es sich um benzimidazolhaltige CDNs, deren pharmakologisch geeigneten Salze, sowie ihre korrespondierenden Prodrugs, die in der Lage sind die Produktion von Typ 1 Interferonen in menschlichen und tierischen Zellen zu induzieren.
Die erfindungsgemässen CDNs können des Weiteren als Reagenzien in der Signaltransduktion und als Modulatoren für CDN-Bindungsproteine und deren Isoformen eingesetzt werden. Darüber hinaus eignen sich die erfindungsgemässen CDNs als Liganden für die Affinitätschromatographie, für die Antikörperproduktion sowie für diagnostische Applikationen.
Die Immuntherapie ist ein rasant wachsendes Forschungsgebiet in der Medizin, bei dem das Immunsystem des Patienten aktiviert, deaktiviert oder anderweitig moduliert wird um einen therapeutischen Behandlungserfolg zu erzielen. Immuntherapeutische Konzepte betreffen Zellen, Antigene, Antikörper, Nukleinsäuren, Peptide, Proteine, natürlich vorkommenden Liganden oder synthetischen Molekülen. Zytokine sind kleine Glykoproteine, die die Immunantwort durch komplexe Signalkaskaden vermittelt. Die direkte therapeutische Anwendung von Zytokinen ist aus unterschiedlichen Gründen stark limitiert, unter anderem durch die sehr geringen Halbwertszeiten der Zytokine im Blutstrom, was außerordentlich kurze Behandlungsintervalle und sehr hohen Dosierungen implizieren würde. Ein vielversprechenderer Ansatz in der Immuntherapie ist hingegen die therapeutische Zytokininduktion, bei der der Patient mit einem immunmodulatorischen Wirkstoff behandelt wird, wodurch die Produktion von einem oder mehreren therapeutisch nützlichen Zytokin(en) im Körper des Patienten angeregt wird. Das STING-Protein ist ein transmembranes Rezeptorprotein und nimmt eine zentrale Rolle bei der physiologischen Produktion von Zytokinen im angeborenen Immunsystem ein. Die Aktivierung von STING führt über den IRF3 (interferon regulatory factor 3) Signalweg zur Produktion von Typ 1 Interferonen (z.B. IFN-α und IFN-ß) und zur Produktion von proinflammatorischen Zytokinen (IL-1a, IL- 1 ß, TNF-α, etc.) über den NF-κΒ (nuclear factor kappa-light-chain-enhancer of activated B cells) Signalweg.
Zurzeit ist bekannt, dass das humane STING-Protein durch Bindung von 3 Kategorien von CDNs aktiviert wird.
1. Exogene 3'3'-CDNs (c-diGMP, c-diAMP, 3'3'-cGAMP) aus Bakterien und Archaea.
2. Endogen gebildetes 2'3'-cGAMP.
3. Synthetische CDNs, die als synthetische Analoga der oben aufgeführten natürlichen CDNs zu verstehen sind.
Das STING-Protein wird gegenwärtig als vielversprechendes Drugtarget für unzählige medizinische Indikationen (u. a. Krebs, Vakzinadjuvantien, infektiöse Krankheiten) exploriert und CDNs als STING- Modulatoren sind Leitstrukturen für die Entwicklung von Therapeutika.
Einige Beispiele für CDNs als STING Aktivatoren sind in US/2014/0329889, WO/2014/189805, WO/2014/093936, WO/2015/077354, WO/2015/185565, WO/2016/096174, WO/2016/096577 und WO/2016/145102 beschrieben. Allerdings wurden bisher nur sehr wenige Strukturen synthetisiert und biologisch getestet. In den publizierten Arbeiten werden keine eingehenden Struktur- Aktivitätsbeziehungen offengelegt. Darüber hinaus wurden bislang nur CDNs mit den Nukleobasen Adenin, Guanin, Hypoxanthin und Isoguanin beschrieben und untersucht. Diese Nukleobasen sind ausserordentlich polare Heterocyclen, die zwar eine gute Wasserlöslichkeit aufweisen, jedoch eine schlechte Membranpermeabilität der synthetischen CDNs bedingen. Die schlechte Membrangängigkeit der bisher beschriebenen CDNs ist jedoch als limitierender Faktor von entscheidender Bedeutung für den therapeutischen Einsatz anzusehen.
Die vorrangige Aufgabenstellung für die vorliegende Erfindung war die Bereitstellung hinsichtlich der Membranpermeabilität und/oder der biologischen Aktivität verbesserter CDNs.
Die Aufgabenstellung wird in der vorliegenden Erfindung durch die Bereitstellung von lipophilen, benzimidazolhaltigen CDNs der Formel (I), wie in den Ansprüchen definiert, gelöst. In diesem Zusammenhang kann im Besonderen gezeigt werden, dass der Austausch von mindestens einer der Nukleobasen Adenin, Guanin, Hypoxanthin oder Isoguanin mit Purinstruktur gegen eine Benzimidazoleinheit oder gegen ein substituiertes Benzimidazol ohne Purinstruktur zu synthetischen CDNs führt, die sich durch erheblich verbesserte und bisher nicht bekannte Lipophilieeigenschaften auszeichnen. Überraschenderweise zeichnen sich die erfindungsgemässen CDNs mit mindestens einer benzimidazolbasierten Struktureinheit trotz des Austausches von mindestens einer der Purinnukleobasen durch gute STING-vermittelte Interferonproduktion aus.
Formel (I)
Chemische Definitionen und verwendete Termini
Im Folgenden werden die zur Beschreibung der vorliegenden Erfindung benutzten chemischen Definitionen und chemischen Begriffe aufgelistet und beschrieben, die in der vorliegenden Erfindung benutzt werden um die erfindungsgemäßen Verbindungen zu spezifizieren. Diese Definitionen und Begriffe gelten für diese Beschreibung.
„Variabel verknüpfbare Struktureinheit" und„variabel verknüpfbare Struktureinheiten": Immer wenn in einem Ringsystem Seitenketten oder Substituenten als„variabel verknüpfbare Struktureinheit" oder „variabel verknüpfbare Struktureinheiten" benannt oder dargestellt sind, wie z.B. in der nachfolgenden Formel:
kann diese variabel verknüpfbare Struktureinheit oder können diese variabel verknüpfbaren Struktureinheiten jedes der Wasserstoffatome ersetzen, die an dem Ringsystem gebunden sind. In der Gesamtheit der ersetzbaren Wasserstoffatome sind alle Wasserstoffatome eingeschlossen, unabhängig davon ob die Wasserstoffatome explizit dargestellt sind oder durch die dargestellte Struktur oder Beschreibung impliziert sind. Alle sich aus dieser Definition ergebenden Substitutionsvarianten werden durch den Begriff variabel verknüpfbare Struktureinheit oder variabel verknüpfbare Struktureinheiten eingeschlossen, solange sie zu chemisch stabilen Strukturen führen oder keine Einschränkungen in diesem Text erwähnt sind. Für die oben angegebene Formel ergeben sich aus den beschriebenen Definitionen drei spezifische Strukturen, die in Formel dargestellt sind:
Abweichend von vorstehender Definition können variabel verknüpfbare Struktureinheit(en) im Zusammenhang mit einem ringförmigen Ribose-System nur Reste R an Positionen ersetzen, die üblicherweise als 2'-Position und 3'-Position bezeichnet werden. Ebenfalls abweichend von vorstehender Definition sind die Reste R in 2'-Position und 3'-Position des Ribose-Systems nicht nur auf Wasserstoffatome beschränkt, sondern können wie unter R6 - R9 spezifiziert sein.
In der nachfolgenden Formel:
führt dies bei den variabel verknüpfbaren Struktureinheiten * und ** beim Ersatz von R6 oder R7, beziehungsweise R8 oder R9 zu folgenden spezifischen Strukturen:
Die oben dargestellten spezifischen Strukturen entsprechen den erfindungsgemäßen CDNs mit den spezifischen Verknüpfungen c[N1 (3',5')pN2(3',5')p], c[N1 (2',5')pN2(3',5')p], c[N1 (3',5')pN2(2',5')p], c[N1 (2',5')pN2(2',5')p], wobei und N2 den Nukleobaseeinheiten und den Maßgaben entsprechen,
dass eine Benzimidazoleinheit der Struktur
ist, N2 = R12 entspricht und N2 gleich oder ungleich sein kann.
Die Reste R R2, R3, R4, R5, R6, R7, R8, R9, R10 und R sind im Zweifelsfall im Anspruch 1 definiert.
In natürlich vorkommenden CDNs sind R10 und Rn beide Sauerstoff und die Doppelbindung des Phosphates ist zwischen den beiden exozyklischen Sauerstoffatomen delokalisiert. In wässriger Lösung bei physiologischem pH-Wert haben natürliche CDNs aufgrund ihrer zwei einfach negativ geladenen Phosphateinheiten insgesamt zwei negative Ladungen. Die negative Ladung ist dabei jeweils über die beiden exozyklischen Sauerstoffatome delokalisiert und korrespondierende Kationen, wie beispielsweise Na+ oder K+ fungieren als Gegenionen. In der vorliegenden Erfindung sind alle Strukturen der Übersicht halber in der freien Säureform mit lokalisierter Doppelbindung dargestellt. Dabei hängt die Lokalisierung der oben genannten Doppelbindung von der Natur der Reste R10 und R ab. Die Art der strukturellen Darstellung in der vorliegenden Erfindung erfolgt der Übersicht halber und beansprucht nicht der exakt akuraten Ladungsverteilung und Elektronendichteverteilung an den Phosphateinheiten zu entsprechen.
Wenn R10 und R nicht Sauerstoff sind, besitzt das Phosphoratom vier unterschiedliche Liganden und ist damit chiral. Zur Unterscheidung der dabei auftretenden zwei stereoisomeren Formen wird hier die Rp/Sp-Nomenklatur nach Cahn-Ingold-Prelog benutzt; das "p" indiziert dabei das Phosphoratom als Chiralitätszentrum. Bei den erfindungsgemäßen Verbindungen können an den beiden Phosphaten sowohl R10 als auch R Schwefel oder Boran sein, wodurch Phosphorothioate bzw. Boranophosphate resultieren. Daraus resultierend enthalten die erfindungsgemäßen Verbindungen entweder eine oder zwei Phosphorothioateinheiten oder eine oder zwei Boranophosphateinheiten oder eine Phosphorothioateinheit und eine Boranophosphateinheit. Aufgrund der phosphorbedingten stereoisomeren Formen liegen z.B. im Falle eines doppelt phosphorothioathaltigen erfindungsgemäßen CDNs der Beschreibung c[N1 (2',5')pS-N2(3',5')pS] vier verschiedene Stereoisomere vor, die wie nachfolgend spezifiziert werden können : c[N1 (2',5')pS[Rp]- N2(3',5')pS[Sp]], c[N1 (2',5')pS[Rp]-N2(3',5')pS[Rp]], c[N1 (2',5')pS[Sp]-N2(3',5')pS[Rp]], c[N1 (2',5')pS[Sp]-N2(3',5')pS[Sp]], wobei und N2 den Nukleobaseeinheiten entsprechen und der Maßgabe entsprechen, dass ungleich N2 sein kann oder gleich N2 sein kann. Die vorliegende Beschreibung betrifft bei Angabe der allgemeinen Abkürzung c[N1 (2',5')pS-N2(3',5')pS] alle 4 stereoisomeren Formen der angegebenen Abkürzung.
Im Falle von erfindungsgemäßen Verbindungen mit zwei Boranophosphateinheiten der beispielhaften Beschreibung c[N1 (3',5')pB-N2(3',5')pB] werden analog die folgenden vier spezifischen Stereoisomere umfasst: ^Ν^',δ^ρΒΙΡρΙ-Ν^',δ^ρΒ^ρ]], ctN^^pBtRpJ-N^^pBtRp]], οΙΝ^',δ^ρΒ^ρ]- N2(3',5')pB[Rp]], c[N1 (3',5')pB[Sp]-N2(3',5')pB[Sp]], wobei ^ und N2 den Nukleobaseeinheiten entsprechen und der Maßgabe entsprechen, dass N ungleich N2 sein kann oder N gleich N2 sein kann.
Im Falle von erfindungsgemäßen Verbindungen mit einer Phosphorothioateinheit und einer Boranophosphateinheit der beispielhaften Beschreibung c[N1 (3',5')pB-N2(2',5')pS] werden analog die folgenden vier spezifischen Stereoisomere umfasst: c[N1 (3',5')pB[Rp]-N2(2',5')pS[Sp]], ctN S'^pBtRpl-N^'^pStRp]], c[N1 (3',5')pB[Sp]-N2(2',5')pS[Rp]], ctN^^pBtSpJ-N^^pStSp]],
wobei ΝΪ und N2 den Nukleobaseeinheiten entsprechen und der Maßgabe entsprechen, dass 1^ ungleich N2 sein kann oder gleich N2 sein kann.
Bei einem einfach phosphorothioathaltigen CDNs der beispielhaften Beschreibung c[N1 (2',5')pS- N2(3',5')p] werden zwei verschiedene Stereoisomere umfasst: c[N1 (2',5')pS[Rp]-N2(3',5')p], c[N1 (2',5')pS[Sp]-N2(3',5')p], wobei und N2 den Nukleobaseeinheiten entsprechen und der Maßgabe entsprechen, dass ungleich N2 sein kann oder gleich N2 sein kann.
Im Falle eines einfach boranophosphathaltigen CDNs der beispielhaften Beschreibung c[N1 (2',5')p- N2(2',5')pB] werden zwei verschiedene Stereoisomere spezifiziert, impliziert und beansprucht: c[N1 (2',5')p-N2(2',5')pB[Rp]], c[N1 (2',5')p-N2(2',5')pB[Sp]], wobei ^ und N2 den Nukleobaseeinheiten entsprechen und der Maßgabe entsprechen, dass ungleich N2 sein kann oder gleich N2 sein kann.
Fachleuten ist bekannt, dass für medizinische Anwendungen, besonders aber wenn es sich um ein Medikament handelt, nur physiologisch unbedenkliche Salzformen der erfindungsgemäßen Verbindungen zum Einsatz kommen können. Die Dokumente WO 2017/027645 A1 und WO 2017/027646 A1 befassen sich mit zyklischen Dinukleotidverbindungen. Sie sind jedoch erst nach dem Prioritätsdatum der vorliegenden Anmeldung veröffentlicht und offenbaren weder die generischen Formeln des vorliegenden Textes noch darunter fallende Einzelverbindungen.
Im Folgenden werden die zur Beschreibung der vorliegenden Erfindung benutzten Termini definiert. Diese Definitionen gelten für die gesamte Beschreibung der Erfindung.
Halogen steht für F, Cl, Br, und I.
Alkyl steht für eine Alkylgruppe, repräsentiert durch einen Kohlenwasserstoff mit 1 bis 28 Kohlenstoffatomen, bevorzugt 1 - 20 Kohlenstoffatome, mit oder ohne (integrierten) Heteroatomen, bevorzugt, aber nicht begrenzt auf, O, S, Si, N, Se, B, wobei die Verknüpfung mit der Grundstruktur in Formel (I) sofern nicht abweichend definiert, über Kohlenstoff erfolgt.
Die Alkylgruppe im Sinne dieses Textes
kann linear gesättigt sein - und ist bevorzugt Methyl, Ethyl, Propyl, Butyl oder Pentyl, ohne allerdings darauf beschränkt zu sein,
oder kann linear ungesättigt sein - und umfasst bevorzugt 2 bis 20 Kohlenstoffatomen und ist weiter bevorzugt Ethylen, Propylen, Butylen und Pentylen, ohne allerdings darauf beschränkt zu sein, oder kann verzweigt gesättigt sein - und umfasst dann aus mindestens drei Kohlenstoffatome und und ist bevorzugt Isopropyl, sek.-Butyl oder tert.-Butyl, ohne allerdings darauf beschränkt zu sein,
oder kann verzweigt ungesättigt sein - und umfasst dannmindestens drei Kohlenstoffatome und ist bevorzugt Isopropenyl, Isobutenyl, Isopentenyl oder 4-Methyl-3-pentenyl, ohne allerdings darauf beschränkt zu sein,
oder kann zyklisch gesättigt sein - und umfasst dann bevorzugt 3 - 8 Ringatome und ist bevorzugt Cyclopentyl, Cyclohexyl, Cycloheptyl, Piperidino oder Piperazino, ohne allerdings darauf beschränkt zu sein,
oder kann zyklisch ungesättigt sein - und umfasst dann bevorzugt 3 - 8 Ringatome.
Hierbei steht der Begriff "gesättigt" für einen Kohlenwasserstoff, der weder C-C Doppelbindungen noch C-C Dreifachbindungen enthält.
Bei substituierten gesättigten Alkylgruppen können allerdings eine oder mehrere Mehrfachbindungen zwischen Kohlenstoff und Sauerstoff, Kohlenstoff und Schwefel oder Kohlenstoff und Stickstoff vorhanden sein, die auch als Bestandteil einer Keto-Enol- oder Imin-Enamin-Tautomerie auftreten können.
Eine Alkylgruppe im Sinne dieses Textes kann unsubstituiert oder substituiert sein kann. Mögliche Substituenten umfassen eine oder mehrere (unsubstituierte) Alkylgruppen, halogensubstituierte Alkylgruppen, Halogenatome, substituierte und unsubstituierte Arylgruppen, substituierte und unsubstituierte Heteroarylgruppen, Amino-, Oxo-, Nitro-, Cyano-, Azido-, Hydroxy-, Mercapto-, Keto-, Carboxy-, Carbamoyl-, Epoxy-, Methoxy-, Methylthio, Ethynyl-Gruppen, ohne allerdings darauf beschränkt zu sein.
Wenn Alkyl, wie hier definiert, eine Polyethylenglycol-Kette (PEG) enthält, kann die bevorzugte Anzahl der Kohlenstoffatome um die Anzahl der PEG Kohlenstoffatome ansteigen, wobei die PEG-Kette bevorzugt 1 bis 500 Ethylenglycol-Gruppen ( -(CH2CH20)n- mit n = 1 bis 500) enthält. Dabei kann - (EO)n- als Abkürzung für -(CH2CH20)n- verwendet werden, wobei die Anzahl der PEG-Einheiten entweder wie im jeweiligen Beispiel angegeben, oder aber 1 - 500 sein kann.
Aralkyl beschreibt eine Alkylgruppe, wie vorstehend beschrieben, die an einen unsubstituierten oder substituierten, aromatischen oder heteroaromatischen Kohlenwasserstoff gebunden ist, und der aus einem oder mehreren aromatischen Ringen mit jeweils 3 - 8 Ringatomen besteht. Substituenten sowohl für den Alkyl- als auch den Aryl-Teil umfassen ein oder mehrere Halogenatome, Alkyl oder Halogenalkyl-Gruppen, substituierte oder unsubstituierte Arylgruppen, substituierte oder unsubstituierte Heteroarylgruppen, Amino-, Nitro-, Cyano-, Azido-, Hydroxy-, Mercapto-, Carboxy-, Methoxy-, Methylthio-Gruppen, ohne allerdings darauf beschränkt zu sein.
Aryl beschreibt einen unsubstituierten oder substituierten, aromatischen oder heteroaromatischen Kohlenwasserstoff, der aus einem oder mehreren aromatischen Ringen mit jeweils 3 - 8 Ringatomen besteht. Substituenten sowohl für den Alkyl- als auch den Aryl-Teil umfassen ein oder mehrere Halogenatome, Alkyl oder Halogenalkyl-Gruppen, substituierte oder unsubstituierte Arylgruppen, substituierte oder unsubstituierte Heteroarylgruppen, Amino-, Nitro-, Cyano-, Azido-, Hydroxy-, Mercapto-, Carboxy-, Methoxy-, Methylthio-Gruppen, ohne allerdings darauf beschränkt zu sein.
Acyl beschreibt eine -C(0)-Alkyl-Gruppe, wobei die Spezifikationn der Alkyl-Gruppe vorstehend definiert wurde.
Aracyl beschreibt eine -C(0)-Aryl-Gruppe, wobei die Spezifikation der Aryl-Gruppe vorstehend definiert wurde.
Carbamoyl beschreibt eine -C(0)-NH2-Gruppe, wobei die beiden Wasserstoff-Atome unabhängig voneinander durch Alkyl-, Aryl- oder Aralkylgruppen substituiert sein können und die Spezifikation der Alkyl, Aryl- und Aralkyl-Gruppen vorstehend definiert wurde.
O-Acyl beschreibt eine -0-C(0)-Alkyl-Gruppe, wobei die Spezifikation der Alkyl-Gruppe vorstehend definiert wurde.
O-Alkyl beschreibt eine Alkyl-Gruppe, die über Sauerstoff angebunden ist, wobei die Spezifikation der Alkyl-Gruppe vorstehend definiert wurde.
O- Aracyl beschreibt eine -0-C(0)-Aryl Gruppe, wobei_die Spezifikation der Alkyl-Gruppe vorstehend definiert wurde.
O-Aralkyl beschreibt eine Aralkyl-Gruppe, die über Sauerstoff angebunden ist, wobei die Spezifikation der Aralkyl-Gruppe vorstehend definiert wurde.
O-Aryl beschreibt eine Aryl-Gruppe, die über Sauerstoff angebunden ist, wobei die Spezifikation der Aryl-Gruppe vorstehend definiert wurde.
O-Carbamoyl beschreibt eine Carbamoyl-Gruppe, die über Sauerstoff angebunden ist, wobei die Spezifikation der Carbamoyl-Gruppe vorstehend definiert wurde.
S-Alkyl beschreibt eine Alkyl-Gruppe, die über Schwefel angebunden ist, wobei die Spezifikation der Alkyl-Gruppe vorstehend definiert wurde.
S-Aryl beschreibt eine Aryl-Gruppe, die über Schwefel angebunden ist, wobei die Spezifikation der Aryl-Gruppe vorstehend definiert wurde.
S-Aralkyl beschreibt eine Aralkyl-Gruppe, die über Schwefel angebunden ist, wobei die Spezifikation der Aralkyl-Gruppe vorstehend definiert wurde.
NH-Alkyl und N-Bisalkyl beschreiben eine, bzw. zwei Alkyl-Gruppen, die über Stickstoff angebunden sind, wobei die Spezifikation der Alkyl-Gruppe vorstehend definiert wurde.
NH-Aryl und N-Bisaryl beschreiben eine, bzw. zwei Aryl-Gruppe, die über Stickstoff angebunden sind, wobei die Spezifikation der Alkyl-Gruppe vorstehend definiert wurde.
NH-Carbamoyl beschreibt eine Carbamoyl-Gruppe, die über Stickstoff angebunden ist, wobei die Spezifikation der Carbamoyl-Gruppe vorstehend definiert wurde.
Amido-alkyl beschreibt eine Alkylgruppe, die über eine NH-C(0)-Bindung angebunden ist, wobei die Spezifikation der Alkyl-Gruppe vorstehend definiert wurde.
Amido-aryl beschreibt eine Arylgruppe, die über eine NH-C(0)-Bindung angebunden ist, wobei die Spezifikation der Aryl-Gruppe vorstehend definiert wurde.
Amido-aralkyl beschreibt eine Aralkylgruppe, die über eine NH-C(0)-Bindung angebunden ist, wobei die Spezifikation der Aralkyl-Gruppe vorstehend definiert wurde.
Beschreibung der Formeln, Abbildungen, Figuren und Tabellen
Formel (I): Generelle Darstellung der Konstitution der neuen, erfindungsgemäßen Verbindungen (siehe Anspruch 1 ).
Abbildung 1 : Synthese von zyklischem (Adenosin-(3' -> 5')-monophosphat - benzimidazolribosid-(3' -> 5')-monophosphat) (c[A(3',5')pBI(3',5')p]).
Legende Abbildung 1 : Syntheseschritte: a) Pyridiniumtrifluoracetat / H20; b) ferf.-Butylamin; c) Dichloressigsäure / H20; d) A, Pyridin ; e) ferf.-Butylhydroperoxid; f) Dichloressigsäure / H20; g) 2- Chlor-5,5-dimethyl-1 ,3,2-dioxaphosphorinan-2-oxid; h) lod, H20; i) Methylamin / Ethanol; j) Triethylamintrihydrofluorid.
Abbildung 2: Synthese von zyklischem (5,6-Dichlorbenzimidazolribosid-(3'— >5')- monophosphorothioat - 5,6-dichlorbenzimidazolribosid-(3'^5')-monophosphorothioat)
(c[DCIBI(3',5')pS-DCIBI(3',5')pS]).
Legende Abbildung 2: Syntheseschritte: a) Pyridiniumtrifluoracetat / H20; b) ferf.-Butylamin; c) Dichloressigsäure / H20; d) A, Pyridin; e) 3-((N,N-dimethylaminomethylidene)amino)-3H-1 ,2,4- dithiazole-5-thione (DDTT); f) Dichloressigsäure / H20; g) 2-Chlor-5,5-dimethyl-1 ,3,2- dioxaphosphorinan-2-oxid; h) 3-H-1 ,2-Benzodithiol-3-on; i) Methylamin / Ethanol; j) Triethylamintrihydrofluorid.
Abbildung 3: Synthese von zyklischem (Guanosin-(2' -> 5')-monophosphorothioat - 5,6- dichlorbenzimidazolribosid-(3' -> 5')-monophosphorothioat) (c[G(2',5')pS-DCIBI(3',5')pS]).
Legende Abbildung 3: Syntheseschritte: a) Pyridiniumtrifluoracetat / H20; b) ferf.-Butylamin; c) Dichloressigsäure / H20; d) A, Pyridin; e) 3-((N,N-dimethylaminomethylidene)amino)-3H-1 ,2,4- dithiazole-5-thione (DDTT); f) Dichloressigsäure / H20; g) 2-Chlor-5,5-dimethyl-1 ,3,2-
dioxaphosphorinan-2-oxid; h) 3-H-1 ,2-Benzodithiol-3-on; i) Methylamin / Ethanol; j) Triethylamintrihydrofluorid.
Figur 1 : Biologische Aktivität neuer, erfindungsgemäßer CDNs mittels THP1 -Blue™ Zellen und SEAP- Reporter.
Legende Figur 1 : THP1 -Blue™ Zellen ((THP1-ISG); InvivoGen, Katalognummer: thp-isg; Konzentration: 5 x 105/ml_, 180 μΙ_/ννβΙΙ (96-well-Platte) wurden mit erfindungsgemäßen CDNs in unterschiedlichen Konzentrationen (0 μg/mL; 10 μg/mL; 20 μg/mL; 40 μg/mL) in Medium (RPMI-1640, 2 mM L-Glutamin, 1 .5 g/L Natriumbicarbonat, 4.5 g/L Glukose, 10 mM Hepes, 1 mM Natriumpyruvat, 10 % FCS, 100 μg/mL Zeocin™, 1 10 μg/mL Normocin™, Pen-Strep 50 U/mL) 24 Stunden bei 37 °C in 5% C02 inkubiert. Die Quantifizierung wurde mit dem SEAP Detektionsreagenz QUANTI-Blue™ (InvivoGen; Katalognummer: rep-qb1 ; Inkubationszeit: 30 min bei 37 °C in 5% C02) über die Optische Dichte (OD) bei 625 nm durchgeführt.
Figur 2: Biologische Aktivität neuer, erfindungsgemäßer CDNs mittels THP1 -Blue™ Zellen und mittels THP1 Dual™ KO STING Zellen als Kontrollzellen und SEAP-Reporter.
Legende Figur 2: THP1 -Blue™ Zellen ((THP1-ISG); InvivoGen, Katalognummer: thp-isg; Konzentration: 5 x 105/mL, 180 [iL/we\\ (96-well-Platte) und THP1 Dual™ KO STING Zellen ((STING KO) InvivoGen, Katalognummer: thpd-kostg; Konzentration: 5 x 105/mL, 180 μίΛ/νβΙΙ (96-well-Platte) wurden mit erfindungsgemäßen CDNs in einer Konzentrationen von jeweils 40 μg/mL in Medium (RPMI-1640, 2 mM L-Glutamin, 1 .5 g/L Natriumbicarbonat, 4.5 g/L Glukose, 10 mM Hepes, 1 mM Natriumpyruvat, 10 % FCS, 100 μg/mL Zeocin™, 1 10 μg/mL Normocin™, Pen-Strep 50 U/mL) 24 Stunden bei 37 °C in 5% C02 inkubiert. Für Inkubationen mit THP1 Dual™ KO STING Zellen, wurden dem Medium des weiteren 10 μg/mL Blasticidin zugegeben. Die Quantifizierung wurde mit dem SEAP Detektionsreagent QUANTI-Blue™ (InvivoGen; Katalognummer: rep-qb1 ; Inkubationszeit: 15 min bei 37 °C in 5% C02) über die Optische Dichte (OD) bei 625 nm durchgeführt.
Tabelle 1 : Abkürzungen, Namen und Strukturen neuer, erfindungsgemäßer Verbindungen. Tabelle 2: HPLC-Retentionszeiten und Lipophiliewerte (log k'g) neuer, erfindungsgemäßer CDNs.
Die benzimidazolhaltigen cyclischen Dinukleotide gemäß der Erfindung sind Verbindungen der Formel (I)
(i)
in der der mit * markierte O als R6 oder R7 und der mit ** markierte O als R8 oder R9 verknüpft ist; und in der R^
H, Cl, Br, I, F, N3, N02, OH, SH, NH2, CF3, Alkyl, Aryl, Aralkyl, Acyl, Aracyl, S-alkyl, S-aryl, S-aralkyl, S-acyl, S-aracyl, S(0)-alkyl, S(0)-aryl, S(0)-aralkyl, S(0)-acyl, S(0)-aracyl, S(0)2-alkyl, S(0)2-aryl, S(0)2-aralkyl, S(0)2-acyl, S(0)2-aracyl, NR13R14 (wobei R13 und R14 unabhängig voneinander H, Alkyl, Aryl oder Aralkyl sein können), 2-Furyl, 3-Furyl, 2-Brom-5-Furyl, (2-Furyl)thio, (3-(2-Methyl)furyl)thio, (3-Furyl)thio, 2-Thienyl, 3-Thienyl, (5-(1 -Methyl)tetrazolyl)thio, 2-(N-(7-Nitrobenz-2-oxa-1 ,3-diazol-4- yl)amino)ethylthio, (4-Brom-2,3-dioxobutyl)thio, [2-[(Fluoresceinylthioureido)amino]ethyl]thio, (7-(4- Methyl)coumarinyl)thio, (4-(7-Methoxy)coumarinyl)thio, (2-Naphtyl)thio, 4-Pyridyl, (4-Pyridyl)thio, 2- Pyridylthio, 5-Amino-3-oxopentylamino, 8-Amino-3,6-dioxaoctylamino, 19-Amino-4J, 10, 13,16- pentaoxanonadecylamino, 17-Amino-9-aza-heptadecylamino, 4-(N-
Methylanthranoyl)aminobutylamino, Dimethylamino, Diethylamino, 4-Morpholino, 1 -Piperidino oder 1 -Piperazino ist
wobei
m = 0 - 6;
Q = S, S(O), S(0)2, O, NH, CH2 oder C(O) ist;
X X2 und X3 sind jeweils unabhängig voneinander H, OH, NH2, N3, SH, CN, N02, F, Cl, Br,
I, (CH2)nCH3 (mit n = 0-5), /'-Pr, f-Bu, (C H2)nC=CH (mi{ n = Q_5^ (CH2)nCH=CH2 (mit n = 0- 5), CH2OH, (CH2)nOCH3 (mit n = 1 -2), CH2N(CH3)2, 0(CH2)nCH3 (mit n = 0-5), 0/-Pr, OCy,
OCyp, OBn, OC(0)CH3, OC(0)Ph, OCF3, N(CH3)2, NH(CH2)nCH3 (mit n = 0-5),
NHC(0)f-Bu, NHC(0)Ph, NHC(0)Of-Bu, NHC(0)CH3, NHC(0)CH2N3, B(OH)2, CF3,
C(0)OH, C(0)OCH3, C(0)0/-Pr, C(0)Of-Bu, C(0)OPh, C(0)OBn, C(0)NH2, C(0)N(CH3)2,
C(0)NHPh, C(0)NHBn, C(0)CF3, CH2C(0)OH, CH2C(0)OCH3, CH2C(0)0/'-Pr,
CH2C(0)Of-Bu, CH2C(0)OBn, S(CH2)nCH3 (mit n = 0-5), S(CH2)nOEt (mit n = 1 -4), SBn,
S02CH3, S02CF3, (mit Y, = H, SH, CN, Ph, F, CH3, OCH3, SCH3, 4-Thiophenyl,
wobei
m = 0 - 6;
n = 1 - 6;
Q = S, S(O), S(0)2, O oder NH ist;
Ft2 ist H, F, Cl, Br, NH2, N02, CN, CH3, OH, CF3, SH, 0-CH3, OCF3, N(CH3)2, S-CH3 oder C(0)OH;
R3 ist H, F, Cl, Br, NH2, N02, CN, CH3, OH, CF3, SH, 0-CH3, OCF3, N(CH3)2, S-CH3 oder C(0)OH;
Ft4 ist H, F, Cl, Br, NH2, N02, CN, CH3, OH, CF3, SH, 0-CH3, OCF3, N(CH3)2, S-CH3 oder C(0)OH; Ft5 ist H, F, Cl, Br, NH2, N02, CN, CH3, OH, CF3, SH, 0-CH3, OCF3, N(CH3)2, S-CH3 oder C(0)OH;
R6 oder R7 ist H, OH, NH2, F, 0-CH3, S-CH3, OCH2CEC, OCH2CH=CH2, O-Acyl, O-Aracyl, 0-C(0)NH- (CH2)6NH2 oder O- (Ν'- Methylanthraniloyl)wobei der andere Rest R6 oder R7 die Verknüpfung in dem mit * markierten O darstellt;
R8 oder R9 ist H, OH, NH2, F, 0-CH3, S-CH3, OCH2CEC, OCH2CH=CH2,0-Acyl, O-Aracyl, 0-C(0)NH- (CH2)6NH2 oder, O- (Ν'- IVIethylanthraniloyl), wobei der andere Rest R8 oder R9 die Verknüpfung in dem mit ** markierten O darstellt.
ist OH, SH, borano (BH3), S-PAS, O-PAS, S-BAS oder O-BAS,
wobei PAS eine photo-aktivierbare Schutzgruppe ist, vorzugsweise o-Nitro-benzyl, 1 - (o-Nitrophenyl)-ethylidene, 4,5-Dimethoxy-2-nitro-benzyl, 7-Dimethylamino-coumarin- 4-yl (DMACM-caged), 7-Diethylamino-coumarin-4-yl (DEACM-caged) and 6,7- Bis(carboxymethoxy)coumarin-4-yl)methyl (BCMCM-caged),
und wobei BAS eine bio-aktivierbare Schutzgruppe ist, vorzugsweise Methyl, Acetoxymethyl, Pivaloyloxymethyl, Methoxymethyl, Propionyloxymethyl, Butyryloxymethyl, Cyanoethyl, Phenyl, Benzyl, 4-Acetoxybenzyl, 4-Pivaloyloxybenzyl, 4-lsobutyryloxybenzyl, 4-Octanoyloxybenzyl, 4-Benzoyloxybenzyl; R ist OH, SH, borano (BH3), S-PAS, O-PAS, S-BAS oder O-BAS,
wobei PAS eine photo-aktivierbare Schutzgruppe ist, vorzugsweise o-Nitro-benzyl, 1 - (o-Nitrophenyl)-ethylidene, 4,5-Dimethoxy-2-nitro-benzyl, 7-Dimethylamino-coumarin- 4-yl (DMACM-caged), 7-Diethylamino-coumarin-4-yl (DEACM-caged) and 6,7- Bis(carboxymethoxy)coumarin-4-yl)methyl (BCMCM-caged), und wobei BAS eine bio-aktivierbare Schutzgruppe ist, vorzugsweise Methyl,
Acetoxymethyl, Pivaloyloxymethyl, Methoxymethyl, Propionyloxymethyl, Butyryloxymethyl, Cyanoethyl, Phenyl, Benzyl, 4-Acetoxybenzyl, 4-Pivaloyloxybenzyl, 4-lsobutyryloxybenzyl, 4-Octanoyloxybenzyl, 4-Benzoyloxybenzyl;
Bevorzugt ist eine definierte Verbindung der Formel (I) wie oben beschrieben,
wobei R12 eine Struktur
ist und einer, zwei, drei, vier oder alle der Reste R R2, R3, R4 und R5 gleich oder verschieden zu dem anderen Rest mit gleichem Index sind.
Alle bisher in der Literatur beschriebenen synthetischen CDNs weisen ausschließlich die Nukleobasen Adenin, Guanin, Hypoxanthin oder Isoguanin mit Purinstruktur oder substituierte Purinbasen auf. Ein gemeinsames Charakteristikum derartiger CDNs ist die ausgesprochen hohe Polarität der zugrunde liegenden Purinnukleobasen, die zu einer sehr schlechten Membranpermeabilität der resultierenden
CDNs führt. Um dieses generelle Manko der bisher beschriebenen CDNs zu korrigieren, ist Lösung der vorliegenden Erfindung der Austausch von mindestens einer der polaren Nukleobasen Adenin, Guanin, Hypoxanthin oder Isoguanin mit Purinstruktur gegen eine lipophile Struktureinheit, die überraschenderweise dazu führt, dass die CDNs weiterhin an das Rezeptorprotein STING binden und/oder STING-vermittelte Signalwege aktivieren können.
Der erfindungsgemäße Einsatz der zum Puringerüst alternativen Benzimidazoleinheit führt, überraschenderweise trotz nur geringer struktureller Abweichung vom Puringrundgerüst zu einer wesentlich höheren Lipophilie. Im Besonderen kann in der vorliegenden Erfindung mittels Lipophiliebestimmung in einem allgemein anerkannten und publizierten HPLC-Gradientensystem (Beispiel 18) gezeigt werden, dass die neuen erfindungsgemäßen CDNs nach Austausch von mindestens einer der bekannten Nukleobasen mit Purinstruktur gegen eine Benzimidazoleinheit (oder gegen ein substituiertes Benzimidazol) deutlich höhere Lipophiliewerte aufweisen. Es ist allgemein akzeptiert, dass erhöhte Lipophiliewerte mit verbesserter Membranpermeabilität korrelieren.
Des Weiteren überraschend und unerwartet sind die Eigenschaften der neuen erfindungsgemäßen Verbindungen bei der Aktivierung STING-vermittelter Signalwege in allgemein anerkannten und literaturbeschriebenen zellbiologischen Untersuchungssystemen, wie in den Beispielen 19 bis 22 dargestellt. Sowohl bei der STING-induzierten Dimerisierung von IRF3, der durch STING induzierten Phosphorylierung von IRF3 und der durch STING induzierten Phosphorylierung von TBK1 (Beispiel 19), bei der STING-vermittelten Erhöhung der Interferon ß Produktion (Beispiel 20), der Erhöhung der gebildeten mRNA für Interferon α und ß (Beispiel 21 ), als auch bei der Menge an sekretiertem Interferon ß (Beispiel 22) zeigen etliche der erfindungsgemäßen Verbindungen biologische Aktivitäten. Trotz der Tatsache, dass mindestens eine der nativen Nukleobasen oder Nukleobasederivate ausgetauscht wurde, sind die neuen benzimidazolhaltigen CDNs in der Lage STING-abhängige Signalwege zu aktivieren. Überraschenderweise führt der Ersatz einer oder beider nativer Purinbasen gegen ein oder zwei artifizielle Benzimidazoleinheiten oder ein oder zwei substituierte Benzimidazoleinheiten nicht zur biologischen Inaktivität der resultierenden CDNs. Aus oben angegebenen Gründen ebenfalls unerwartet war das Ergebnis, dass etliche der erfindungsgemäßen CDNs in der Lage sind mit guten Affinäten an das STING-Protein zu binden, wie in Beispiel 23 mittels Isothermal Titration Calorimetry (ITC) dargestellt. Die bestimmten Affinitäten etlicher der erfindungsgemäßen Verbindungen liegen in derselben Größenordnung wie die Affinitäten der natürlichen zyklischen Nukleotide oder übertreffen diese.
Bevorzugte erfindungsgemäße Verbindungen der allgemeinen Formel (I)
Bevorzugt ist die vorstehend definierte Verbindung mit der Formel (I) eine Verbindung, in der R10 oder R SH ist und entspricht der allgemeinen Beschreibung c[N1 (2',5')pS-N2(3',5')p], c[N1 (2',5')pS- N2(2',5')p], c[N1 (3',5')pS-N2(2',5')p] oder
(wie vorstehend definiert).
Ebenfalls bevorzugt ist die vorstehend definierte Verbindung mit der Formel (I) eine Verbindung, in der Rio oder R SH ist und entspricht der allgemeinen Beschreibung c[Ni (2',5')p-N2(3',5')pS], c[Ni (2',5')p- N2(2',5')S], c[Ni (3',5')p-N2(2',5')pS] oder c[Ni (3',5')p-N2(3',5')pS] (wie vorstehend definiert).
Ebenfalls bevorzugt ist die vorstehend definierte Verbindung mit der Formel (I) eine Verbindung, in der Rio oder R BH3 ist und entsprichtder allgemeinen Beschreibung c[Ni (2',5')pB-N2(3',5')p], c[Ni (2',5')pB-N2(2',5')p], c[N1 (3',5')pB-N2(2',5')p] oder c[Ni (3',5')pB-N2(3',5')p] (wie vorstehend definiert).
Ebenfalls bevorzugt ist die vorstehend definierte Verbindung mit der Formel (I) eine Verbindung, in der Rio oder R BH3 ist und entspricht der allgemeinen Beschreibung c[Ni (2',5')p-N2(3',5')pB], c[Ni (2',5')p-N2(2',5')B], c[N1 (3',5')p-N2(2',5')pB] oder c[Ni (3',5')p-N2(3',5')pB] (wie vorstehend definiert).
Ebenfalls bevorzugt ist die vorstehend definierte Verbindung mit der Formel (I) eine Verbindung, in der Rio und R BH3 sind und entspricht der allgemeinen Beschreibung c[Ni (2',5')pB-N2(3',5')pB], c[Ni (2',5')pB-N2(2',5')pB], c[Ni (3',5')pB-N2(2',5')pB] oder c[Ni (3',5')pB-N2(3',5')pB] (wie vorstehend definiert).
Ebenfalls bevorzugt ist die vorstehend definierte Verbindung mit der Formel (I) eine Verbindung, in der Rio oder R SH und korrespondierend R oder R10 BH3 ist und entspricht der allgemeinen Beschreibung c[N1 (2',5')pS-N2(3',5')pB], c[N1 (2',5')pS-N2(2',5')pB], c[Ni (3',5')pS-N2(2',5')pB] oder c[Ni (3',5')pS-N2(3',5')pB] (wie vorstehend definiert).
Ebenfalls bevorzugt ist die vorstehend definierte Verbindung mit der Formel (I) eine Verbindung, in der Rio oder Rn BH3 und entspricht korrespondierend Rn oder R10 SH ist und der allgemeinen Beschreibung c[N1 (2',5')pB-N2(3',5')pS], c[N1 (2',5')pB-N2(2',5')pS], c[Ni (3',5')pB-N2(2',5')pS] oder c[Ni (3',5')pB-N2(3',5')pS] (wie vorstehend definiert).
Weiter bevorzugt ist die vorstehend definierte Verbindung mit der Formel (I) eine Verbindung, in der Rio und Rn SH sind und entspricht der allgemeinen Beschreibung c[Ni (2',5')pS-N2(3',5')pS], c[Ni (2',5')pS-N2(2',5')pS], c[Ni (3',5')pS-N2(2',5')pS] oder c[Ni (3',5')pS-N2(3',5')pS] (wie vorstehend definiert).
Weiter bevorzugt ist bei der vorstehend definierten Verbindung mit der Formel (I) eine Verbindung, in der die Phosphatbrücken der„variabel verknüpfbaren Struktureinheiten" über R8 and R7 ausgebildet sind und zu Verbindungen führen, die üblicherweise als 3', 5'-3', 5'-verknüpft bezeichnet werden. Weiter bevorzugt ist bei der vorstehend definierten Verbindung mit der Formel (I) eine Verbindung, in der die Phosphatbrücken der„variabel verknüpfbaren Struktureinheiten" über R8 and R6 ausgebildet sind und zu Verbindungen führen, die üblicherweise als 2', 5'-3', 5'-verknüpft bezeichnet werden.
In einer weiteren besonderen Ausführungsform kann die vorstehend definierte Verbindung mit der Formel (I) eine Verbindung sein, in der R2 CH3 ist.
In einer weiteren besonderen Ausführungsform kann die vorstehend definierte Verbindung mit der Formel (I) eine Verbindung sein, in der R2 N02 ist.
In einer weiteren besonderen Ausführungsform kann die vorstehend definierte Verbindung mit der Formel (I) eine Verbindung sein, in der R2 NH2 ist.
In einer weiteren besonderen Ausführungsform kann die vorstehend definierte Verbindung mit der Formel (I) eine Verbindung sein, in der R2 Cl ist.
In einer weiteren besonderen Ausführungsform kann die vorstehend definierte Verbindung mit der Formel (I) eine Verbindung sein, in der R3 und R4 CH3 sind.
In einer weiteren besonderen Ausführungsform kann die vorstehend definierte Verbindung mit der Formel (I) eine Verbindung sein, in der R3 und R4 0-CH3 sind.
In einer weiteren besonderen Ausführungsform kann die vorstehend definierte Verbindung mit der Formel (I) eine Verbindung sein, in der R3 und R4 N02 sind.
In einer weiteren besonderen Ausführungsform kann die vorstehend definierte Verbindung mit der Formel (I) eine Verbindung sein, in der R3 und R4 jeweils Cl sind.
In einer weiteren besonderen Ausführungsform kann die vorstehend definierte Verbindung mit der Formel (I) eine Verbindung sein, in der R3 und R4 jeweils Cl sind und nicht H ist.
In einer weiteren besonderen Ausführungsform kann die vorstehend definierte Verbindung mit der Formel (I) eine Verbindung sein, in der R R3 und R4 jeweils Cl sind.
In einer weiteren besonderen Ausführungsform kann die vorstehend definierte Verbindung mit der Formel (I) eine Verbindung sein, in der R CF3 ist und R3 und R4 jeweils Cl sind.
In einer weiteren besonderen Ausführungsform kann die vorstehend definierte Verbindung mit der Formel (I) eine Verbindung sein, in der R6 oder R7 und R8 oder R9 jeweils OH sind.
In einer weiteren besonderen Ausführungsform kann die vorstehend definierte Verbindung mit der Formel (I) eine Verbindung sein, in der R6 oder R7 F ist und R8 oder R9 OH ist.
In einer weiteren besonderen Ausführungsform kann die vorstehend definierte Verbindung mit der Formel (I) eine Verbindung sein, in der R6 oder R7 OH ist und R8 oder R9 F ist.
In einer weiteren besonderen Ausführungsform kann die vorstehend definierte Verbindung mit der Formel (I) eine Verbindung sein, in der R6 oder R7 und R8 oder R9 jeweils F sind.
Jede sinnvolle Kombination aus den vorstehend beschriebenen Ausführungsformen ist ebenfalls erfindungsgemäß.
Insbesondere bevorzugte Ausführungsformen der Erfindung basierend auf obigen Erläuterungen, sind wie in einem der Ansprüche 2, 3, 4, 5, 6 oder 7 definiert.
Erfindungsgemäß werden ganz besonders die Verbindungen bevorzugt, die in Tabelle 1 abgebildet und im Anspruch 8 definiert sind.
Es sei darauf hingewiesen, dass in der gesamten vorliegenden Beschreibung der Erfindung und insbesondere für die Verbindungen in Tabelle 1 , im Zweifel der Eindeutigkeit die abgebildete Struktur gültig ist. Es wird ferner darauf hingewiesen, dass die Verbindungen aus Tabelle 1 als freie Säure dargestellt sind. Die vorliegende Erfindung umfasst allerdings auch physiologisch akzeptable Salzformen dieser Verbindungen, beispielsweise mit Kationen wie Na+, K+, Li+, NH4 +, Et3NH+ und ( - Pr)2EtNH+ oder Mischformen aus den vorstehend aufgeführten Kationen, ohne aber auf diese beschränkt zu sein.
Tabelle 1 : Abkürzungen, Namen und Strukturen neuer, erfindungsgemäßer Verbindungen.
c[2'-F-dA(3',5')pS- DCIBI(2',5')pS] zyklisches (2'-Fluor-2'- deoxyadenosin-(3' -> 5')- monophosphorothioat - 5,6- dichlorbenzimidazolribosid-(2' -> 5')-monophosphorothioat)
c[2'-F-dA(3',5')pTCIBI(2',5')p] zyklisches (2'-Fluor-2'- deoxyadenosin-(3' -> 5')- monophosphat - 2,5,6- trichlorbenzimidazolribosid-(2' -> 5')-monophosphat)
c[2'-F-dA(3',5')pS- TCIBI(2',5')pS] zyklisches (2'-Fluor-2'- deoxyadenosin-(3' -> 5')- monophosphorothioat - 2,5,6 trichlorbenzimidazolribosid-(2' - 5')-monophosphorothioat)
Wie oben beschrieben, können die Verbindungen gemäß der vorliegenden Erfindung zusätzlich nach bekannten und etablierten Methoden markiert werden. Als nicht einschränkendes Beispiel für eine Markierung sei an dieser Stelle, ein fluoreszenter Farbstoff genannt, der an die Verbindung gekuppelt werden kann, um beispielsweise, aber nicht darauf beschränkt, durch konfokale Fluoreszenzmikroskopie die intrazelluläre Verteilung von (an die Verbindung) bindenden Proteinen in lebenden Zellen zu bestimmen oder um Fluoreszenzkorrelationsspektroskopie, Fluoreszenz- Resonanz-Energie-Transfer (FRET) Untersuchungen oder Bestimmungen der Konzentration der Verbindung in lebenden Zellen zu ermöglichen. Es sei darauf hingewiesen, dass auch Hydrate der beschriebenen Verbindungen zum Umfang der Erfindung gehören.
Die Verbindungen gemäß der Erfindung können anstelle von oder zusätzlich zu fluoreszierenden Farbstoffen auch mit (radioaktiven) Nukliden markiert sein. Geeignete Isotope und Synthesetechniken sind im Stand der Technik etabliert und bekannt.
Die Erfindung umfasst zusätzlich PEGylierte Formen der beschriebenen Verbindungen, wobei PEGylierung allgemein bekannt dafür ist, die Löslichkeit in Wasser sowie pharmakokinetische und Bioverteilungseigenschaften zu verbessern.
Des Weiteren umfasst die Erfindung die beschriebenen Verbindungen in ihrer Prodrug Form, wobei die negative Ladung der (modifizierten oder unmodifizierten) Phosphat-Gruppe durch eine bio- aktivierbare Schutzgruppe maskiert ist. Es ist allgemein anerkannt, dass solche Strukturen die Lipophilie erhöhen und damit sowohl die Membranpermeabilität als auch die Bioverfügbarkeit verbessern, was in der Regel zu einem 10-1000 fach erhöhten Potential im Vergleich zur Mutterverbindung führt. Solche bio-aktivierbaren Schutzgruppen können nach bekannten und etablierten Methoden aus dem Stand der Technik eingeführt werden. Als nicht einschränkende bevorzugte Beispiele seien Acetoxymethyl, Propionyloxymethyl, Butyryloxymethyl, Pivaloyloxymethyl, Acetoxyethyl, Acetoxybutyl und Acetoxyisobutyl genannt. Nicht einschränkende bevorzugte Beispiele für die korrespondierenden Reste R10 und/oder gemäß der Erfindung sind Acetoxymethyloxy, Propionyloxymethyloxy and Butyryloxymethyloxy. Bevorzugte Beispiele für labilere Schutzgruppen beinhalten, aber sind nicht beschränkt auf, Alkyl- oder Aryl-Gruppen sowie substituierte Alkyl- oder Aryl-Gruppen. Konkrete, aber nicht einschränkende, weiter bevorzugte Beispiele für chemisch labile Schutzgruppen der Reste R10 und/oder R gemäß der Erfindung sind Methyl, Ethyl, 2-Cyanoethyl, Propyl, Benzyl, Phenyl und Polyethylenglycol. Die Verbindungen in ihrer Prodrug Form sind an sich inaktiv, aber extrem Membranpermeabel, was zu stark erhöhten intrazellulären Konzentrationen führt. Enzymatische Hydrolyse der Ester-Bindung führt schließlich zur Abspaltung der Schutzgruppe und setzt die biologisch aktive Mutterverbindung frei.
Die vorliegende Erfindung umfasst als Alternative oder Ergänzung zu bio-aktivierbaren Schutzgruppen auch photo-aktivierbare Schutzgruppen (auch als„caged" oder photolysierbare Gruppen bezeichnet).
Diese Schutzgruppen können nach bekannten und etablierten Methoden aus dem Stand der Technik eingeführt werden. Analog zu bio-aktivierbaren Schutzgruppen stellen auch photo-aktivierbare Schutzgruppen eine Maskierung der negativen Ladung der (modifizierten oder unmodifizierten) Phosphat-Gruppe dar und bewirken dadurch eine Steigerung der Lipophilie und daraus resultierend eine Erhöhung der Membranpermeabilität und Bioverfügbarkeit. Nicht einschränkende bevorzugte Beispiele für photo-aktivierbare Schutzgruppen sind o-Nitro-benzyl, 1 -(o-Nitrophenyl)-ethylidene, 4,5- Dimethoxy-2-nitro-benzyl, 7-Dimethylamino-coumarin-4-yl (DMACM-caged), 7-Diethylamino-coumarin- 4-yl (DEACM-caged) and 6,7-Bis(carboxymethoxy)coumarin-4-yl)methyl (BCMCM-caged).
Die Verbindungen gemäß der vorliegenden Erfindung können bevorzugt auch an (unlöslichen) Trägermaterialien immobilisiert sein. Nicht beschränkende bevorzugte Beispiele für solche Trägermaterialien beinhalten Agarose, Dextran, Cellulose, Stärke und andere Kohlenhydrat- basierende Polymere, synthetische Polymere wie Polyacrylamid, Polyethylenimine, Polystyrol und ähnliche Materialien, Apatit, Glas, Kieselsäure(gel), Gold, Graphene, Fullerene, Carborane, Titandioxid, Zirkoniumdioxid, Aluminiumoxid und eine für die Bindung diverser Liganden geeignete Oberfläche eines Chips.
Teil der Erfindung ist auch ein Verfahren zur chemoenzymatischen Herstellung einer erfindungsgemäßen Verbindung mit der allgemeinen Struktureinheit c[N1 (2',5')pN2(3',5')p] oder c[N1 (3',5')pN2(3',5')p] durch Transglycosylierung von c-diAMP, c-diGMP, 2',3'-cGAMP oder 3',3'- cGAMP mittels einer Purin-Nukleosid-Phosphorylase (PNPase).
Ebenfalls Teil der Erfindung ist ein Verfahren zur chemoenzymatischen Herstellung einer erfindungsgemäßen Verbindung mit der allgemeinen Struktureinheit c[N1 (2',5')pN2(3',5')p], c[N1 (2',5')pS-N2(3',5')p], c[N1 (2',5')pS-N2(3',5')pS], c[N1 (2',5')pB-N2(3',5')p], c[N1 (2',5')pB-N2(3',5')pB], c[N1 (2',5')pB-N2(3',5')pS] oder c[N1 (2',5')pS-N2(3',5')pB] durch Dimerisierung und Zyklisierung von 5'- O-Triphosphaten, 5'-0-(1 -Thiotriphosphaten) oder 5'-0-(1 -Boranotriphosphaten) mit einer cGAMP Synthase (cGAS).
Zudem ist Teil der Erfindung ein Verfahren zur chemoenzymatischen Herstellung einer erfindungsgemäßen Verbindung mit der allgemeinen Struktureinheit c[N1 (3',5')pN2(3',5')p], οΙΝ^',δ^ρΒ-Ν^',δ οΙΝ^',δ^ρ-Ν^',δ^ρΒ], oder cIN^S'.ö'JpB-N^S'.ö'JpB], wobei alternativ der Benzimidazolrest in durch eine ggf. substituierte Purinbase ersetzt sein kann, durch Dimerisierung und Zyklisierung von 5'-0-Triphosphaten oder 5'-0-(1 -Boranotriphosphaten) mit einem Enzym DNA integrity scanning protein (DisA) aus Bacillus subtilis. In dem letztgenannten Verfahren ist es auch möglich, das der Rest R12 gemäß Formel (I) ebenfalls eine ggf. substituierte Purinbase darstellen kann.
Das erfindungsgemäße Verfahren macht die erfindungsgemäßen Verbindungen auf verhältnismäßig einfache Weise zugängig.
Teil der Erfindung ist auch die Verwendung einer erfindungsgemäßen Verbindung als Medikament.
Als Teil der der Erfindung kann eine Verbindungen der Formel (I) in pharmakologisch akzeptabler Form für die Behandlung oder Vorbeugung einer Krankheit verwendet werden, wobei die Krankheit ausgewählt ist aus der Gruppe bestehend aus Krebs, infektiöse Erkrankung bakterieller oder viraler Ursache, akuter Abstoßung eines Organtransplantes, Diabetes mellitus Typ I, rheumatischer Arthritis, Psoriasis, Crohn's Krankheit, Restenosis, allergisches Asthma und anderen Krankheiten, deren Zustand durch eine Aktivierung des STING-Signalweges verbessert oder geheilt werden kann.
In einem weiteren Aspekt, bezieht sich die vorliegende Erfindung auf eine Methode zur Behandlung oder Vorbeugung einer der genannten Krankheiten durch Administration einer therapeutisch oder prophylaktisch effektiven Menge einer Verbindung der Formel (I) für eine Person oder einen Patienten, der eine Prophylaxe oder eine Therapie benötigt.
In einem zusätzlichen Aspekt kann eine Verbindung der Formel (I) gemäß der vorliegenden Erfindung als Forschungsreagenz, verzugsweise als Forschungsreagenz für das Studium einer Krankheit oder Disfunktion, verwendet werden. Dabei sind bevorzugte Krankheiten oder Disfunktionen als Anwendungsgebiet Krebs, infektiöse Erkrankungen bakterieller oder viraler Natur, akute Abstoßung eines Organtransplantes, Diabetes mellitus Typ I, rheumatische Arthritis, Psoriasis, Crohn's Krankheit, Restenosis, allergisches Asthma oder eine andere Krankheit, deren Zustand durch eine Aktivierung des STING-Signalweges verbessert oder geheilt werden kann
Die Erfindung wird weitergehend illustriert durch die folgenden Abbildungen und Beispiele, welche bevorzugte Ausführungsformen der Erfindung beschreiben, die Erfindung jedoch in keinster Weise eingrenzen.
Beispiele
1. Synthese
Allgemeine experimentelle Methoden
Alle eingesetzten Lösungsmittel und Reagenzien sind kommerziell erhältlich, wobei Lösungsmittel die höchsten Reinheitskriterien erfüllen (p.A. oder HPLC oder gradient HPLC). Dimethylsulfoxid (DMSO) wird vor Gebrauch mindestens 2 Wochen über aktiviertem Molekularsieb gelagert.
Reaktionsfortschritt und Reinheitskontrolle der isolierten Produkte werden mit Reversed Phase HPLC durchgeführt (RP-18, ODS-A-YMC, 120-S-1 1 , 250 x 4 mm, 1 ,5 mL/min (YMC, Dinslaken, Deutschland)), mit UV-Detektion beim Amax der jeweiligen Nucleobasen. Alle chromatografischen Untersuchungen wurden bei Raumtemperatur durchgeführt.
Die beschriebenen Synthesen werden typischerweise im 20 - 200 μιτιοΙ Maßstab in 2 mL Polypropylen-Reaktionsgefäßen mit Schraubkappe und Dichtung durchgeführt. Gut geeignet sind auch Synthesen im Maßstab von 0,5 μιτιοΙ - 1 mmol in 2 ml_ Polypropylen-Reaktionsgefäßen mit Schraubkappe und Dichtung oder in 10 mL bis 500 ml_ Rundkolben. Reaktionen unter Schutzgas- Athmosphäre oder auch Entgasungen laufen in der Regel in 10 oder 25 mL Rundkolben ab.
Schlecht lösliche Reagenzien werden durch Behandlung der Suspension im Ultraschall-Bad oder durch Erwärmen (70 °C) in Lösung gebracht; in Einzelfällen müssen auch Suspensionen eingesetzt werden.
Die Aufreinigung der Rohprodukte erfolgt zum Beispiel mittels präparativer MPLC (Merck, LiChroprep RP-18, 15 - 25 μιτι), präparativer Anionenchromatografie (GE Healthcare, Sepharose Q Fast Flow, 45 - 165 μηι) oder präparativer HPLC (RP-18, ODS-A-YMC, 120-S-1 1 , 250 x 16 mm, UV 254 nm), wobei sich die Komposition des Eluenten nach der jeweiligen Substanz richtet und in der Regel identisch zu der analytischen HPLC ist. Für die präparative Flash Chromatographie wurde YMC*Gel SIL (6 nm, S- 75 μιτι) Kieselgel eingesetzt.
Die Entsalzung wird, wie in der Nukleotid-Chemie üblich, entweder durch wiederholte Gefriertrocknungsschritte oder durch präparative HPLC (RP-18, ODS-A-YMC, 120-S-1 1 , 250 x 16 mm, UV 254 nm) erreicht. Dazu werden die produkthaltigen Lösungen bei -70 °C für 15 Minuten eingefroren und im Vakuum entweder durch Gefriertrocknung oder in einer Zentrifuge evaporiert.
Falls produkthaltige Lösungen größeren Volumens aufkonzentriert werden müssen, erfolgt das Aufkonzentrieren mittels Rotationsverdampfer unter reduziertem Druck im Membranpumpenvakuum oder im Ölpumpenhochvakuum bei Wasserbadtemperaturen, die nicht 28 °C bis 33 °C überschreiten.
Die isolierten Produkte liegen je nach verwendetem Puffer, danach entweder als Triethylammonium- Salz oder als Natrium-Salz vor. Triethylammoniumsalze werden zum Beispiel mittels Kationenaustauschchromatografie (GE Healthcare, SP Sepharose™ Fast Flow, 45 - 165 μιτι) in die korrespondierenden Natriumsalze überführt.
Ausbeuten werden nach Lambert-Beer mittels UV-Spektroskopie mit einem JASCO V-650 Spectrophotometer (JASCO Germany GmbH, Gross-Umstadt) bei Amax bestimmt. Unbekannte Extinktionskoeffizienten werden dabei von literatur-bekannten Werten strukturell ähnlicher Verbindungen abgeleitet. Massenpektren werden mit einem Esquire LC 6000 spektrometer (Bruker Daltonic, Bremen, Germany) im ESI-MS Modus mit 50 % Wasser / 49,5 % Methanol / 0,5 % NH3 (pH 9) als Matrix gemessen.
NMR-Spektren wurden mit einem 400 MHz Bruker Avance III HD bei 300 K gemessen. Die chemischen Verschiebungen wurden in parts per million (ppm) angegeben und für 1 H NMR Spektren auf das Signal des Restprotonengehalts des Lösungsmittel kalibriert (D20: δ = 4.80 ppm ). 31 P NMR- Spektren wurden auf das Signal der externen Referenz 85 % Phosphorsäure (δ = 0 ppm) kalibriert. 31 P NMR-Spektren wurden protonenentkoppelt aufgenommen.
Lipophiliebestimmungen wurden in Analogie zu Krass et al7 mit HPLC durchgeführt. Die HPLC-Anlage setzte sich wie folgt zusammen: Pumpe: Elite LaChrom L 2130; Detektor: Elite La Chrom L 2455 DAD; Säulenofen: Elite La Chrom L 2350; Autosampier: Elite La Chrom L 2200; Softwarepaket: Computer EZ Chrom Elite (alles VWR / Hitachi, Darmstadt, Deutschland).
Gradient 1 : Stationäre Phase: Polygosil 60-10, RP-18; 250 x 4 mm (Macherey & Nagel, Düren, Deutschland). Laufmittel A: 10 mL 1 M Triethylammoniumphosphatpuffer (TEAP), pH 6,5 + 990 mL Methanol. Laufmittel B: 10 mL 1 M TEAP, pH 6,5 + 990 mL H20. Zeitprogramm : 0 min: 100 % B; 60 min: 100 % A; 65 min: 100 % A; 70 min: 100 % B; 90 min: 100 % B. Flußrate: 1 ,0 mL / min.
Gradient 2: Stationäre Phase: RP-18, ODS-A-YMC, 120-S-1 1 , 250 x 4 mm. Laufmittel A: 10 mL 1 M Triethylammoniumformiatpuffer (TEAF), pH 6,8 + 990 mL Acetonitril. Laufmittel B: 10 mL 1 M TEAF, pH 6,8 + 990 mL H20. Zeitprogramm: 0 min: 100 % B; 60 min: 60 % A; 65 min: 60 % A; 70 min: 100 % B; 90 min: 100 % B. Flußrate: 1 ,0 mL / min.
Generelles Syntheseverfahren A:
Transglycosylierung mit Purin-Nukleosid-Phosphorylasen (PNPase)
Das Enzym, das normalerweise die Nukleobase von Ribo- und Desoxyribo-Purinnukleosiden entfernt, wird hier eingesetzt, um die natürlichen Nukleobasen der natürlichen CDNs (c-diGMP, c-diAMP, 2', 3'- cGAMP, 3',3'-cGAMP) gegen andere, unnatürliche Basen auszutauschen (Transglycosylierung). Dabei wird die höhere Stabilität der glykosidischen Bindung zu Benzimidazol im Vergleich zu den natürlichen Purinbasen genutzt.
Typischerweise wird c-diGMP (Biolog Life Science Institute Forschungslabor und Biochemica-Vertrieb GmbH, Bremen, Deutschland (nachfolgend auch als„Biolog GmbH, Bremen" verkürzend verwendet) und eine der freien Benzimidazol-Nukleobasen, wie sie in Anspruch 1 definiert sind, in gepufferter wässriger Lösung mit Purin-Nukleosid-Phosphorylasen (PNPase) inkubiert. Varianten des Enzyms sind z. B. bei Sigma-Aldrich kommerziell erhältlich und können erfindungsgemäß in homogener Lösung oder auch bevorzugt an natürlichem Trägermaterial, wie Dextran, Agarose, Zellulose oder von synthetischer Natur wie Acrylamid, Polystyrol etc. immobilisiert, eingesetzt werden. Alternativ und besonders wenn die Spezifität der kommerziellen PNPasen die Umsetzung spezieller Benzimidazol- Analoga nicht zulässt, werden PNPasen bevorzugt, die aus niederen Spezies gewonnen werden können.
Viele Benzimidazol-Analoga sind schlecht in Wasser löslich; hier wird das Benzimidazol-Analog vorher durch Erwärmen und Ultraschall-Behandlung in der Lösung angereichert und eine bestehende Suspension eingesetzt. Bevorzugt ist die Zugabe von Löslichkeitsvermittlern, wie DMSO oder DMF oder Tensiden in einer Konzentration, die die enzymatische Umsetzung nicht wesentlich stört. Die Reaktion wird wegen der hohen Thermostabilität der PNPasen allerdings ohnehin bevorzugt im Temperaturbereich von 30 °C - 60 °C durchgeführt.
In einer bevorzugten Anwendungsform der Erfindung wird die enzymatische Reaktion in 0.01 M - 1 M TRIS-HCI Puffer in einem pH-Bereich von 6 - 10 in Anwesenheit von 1 -15 % Glyzerin und 0.0001 M - 0.1 M Dithiothreitol (DTT) bei 20 °C - 50 °C durchgeführt.
In einer besonders bevorzugten Anwendungsform der Erfindung wird die enzymatische Synthese in 20 mM TRIS-HCI Puffer in einem pH-Bereich von 6,5 - 8,5, 0.001 M DTT, bei 37 °C durchgeführt.
Beispiel 1 : Synthese von zyklischem (Guanosin-(3' -> 5')-monophosphate benzimidazolribosid-(3' -> 5')-monophosphat (crG(3',5')pBI(3',5')Pl), und zyklischem (Benzimidazolribosid-(3' -> 5')-monophosphat - benzimidazolribosid-(3' -> 5')-monophosphat) (crBI(3'.5')pBI(3'.5')Pl)
11 ,8 mg / 100 μιτιοΙ Benzimidazol werden in 1 ml Tris-HCI Puffer (20 mM, pH 8.0, 10 % Glyzerin) suspendiert. Nach Zugabe von 50 μΙ DMSO wird das verschlossene Reaktionsröhrchen im Wasserbad auf 70 °C erwärmt und anschließend für einige Minuten im Ultraschall-Bad beschallt.
Nach Zugabe von 2 mg DTT werden 10 μιτιοΙ von c-diGMP (Natriumsalz) und 50 Einheiten PNPase addiert und die Mischung bei bei 37 °C im Thermomixer geschüttelt.
In regelmäßigen Zeitabständen werden Proben entnommen und in der HPLC analysiert. Nach Stillstand der Umsetzung wird die Rohproduktlösung filtriert und mittels semipreparativer HPLC auf einer Reversed Phase Kieselgel-Säule (RP-18) unter Verwendung von Triethylammoniumformiat- puffer aufgetrennt.
Dabei eluieren zunächst Reste von c-diGMP und Guanin, später können c[G(3',5')pBI(3',5')p] und anschließend c[BI(3',5')pBI(3',5')p] gewonnen werden. Überschüssiges Benzimidazol wird beim Säulenspülen entfernt. Beide Produkte liegen in der Triethylammonium-Form vor.
Die typische Ausbeute liegt je nach Zustand des Enzyms zwischen 15 und 45 % für das symmetrische Produkt mit zwei Benzimidazoleinheiten und bei 7 - 16 % für das asymmetrische Mischprodukt.
crGi3'.5')DBIi3'.5')Dl : 3 ,5'/3',5' 0ΓΒΙ(3\5')ΡΒΙ(3\5')Ρ1: 3 , 5 /3 , 5'
C22H25N7012P2; MW 641 ,43 (freie Säure) C24H26N4012P2; MW 624,44 (freie Säure)
UV: Xmax: -250 nm UV: Xmax: 245 nm, ε 9810
ESI-MS (+) : m/z 743 [M + TEA + H] + ESI-MS (+) : m/z 726 [M + TEA + H] +
ESI-MS (-) : m/z 640 [M - H] " ESI-MS (-) : m/z 623 [M - H] "
Beispiel 2: Synthese von zyklischem (Adenosin-(3' -> 5')-monophosphate - 5,6- dimethylbenzimidazolribosid-(2' -> 5')-monophosphat (οΓΑ(3',5')ρΡΜΒΙ(2',5')ρ1)
15 mg / 100 μιτιοΙ 5,6-Dimethylbenzimidazol werden in 1 ml Tris-HCI Puffer (20 mM, pH 8.0, 10 % Glyzerin) suspendiert. Nach Zugabe von 50 μΙ DMSO wird das verschlossene Reaktionsröhrchen im Wasserbad auf 70 °C erwärmt und anschließend für einige Minuten im Ultraschall-Bad beschallt.
Nach Zugabe von 2 mg DTT werden 1 0 μιτιοΙ von 2',3'-c-GAMP (Natriumsalz) und 50 Einheiten PNPase addiert und die Mischung bei bei 37 °C im Thermomixer geschüttelt.
In regelmäßigen Zeitabständen werden Proben entnommen und in der HPLC analysiert. Nach Stillstand der Umsetzung wird die Rohproduktlösung filtriert und mittels semipreparativer HPLC auf einer Reversed Phase Kieselgel-Säule (RP-18) unter Verwendung von Triethylammoniumformiat- puffer aufgetrennt. Dabei eluieren zunächst Reste von 2',3'-cGAMP und Guanin und mit wesentlich späterer Retentionszeit wird anschließend das c[A(3',5')pDMBI(2',5')p] isoliert. Überschüssiges 5,6- Dimethylbenzimidazol wird beim Säulenspülen entfernt. Beide Produkte liegen in der Triethylammonium-Form vor.
Die typische Ausbeute liegt je nach Zustand des Enzyms zwischen 15 und 45%.
0ΓΑ(3'.5')ΡΡΜ ΒΙ(2'.5')Ρ1: 3 ,572 ,5'
C24H29N7012P2; MW 669,48 (freie Säure)
UV: Xmax: -270 nm
ESI-MS (+) : m/z 771 [M + TEA + H] +
ESI-MS (-) : m/z 668 [M - H] "
Generelles Syntheseverfahren B:
Katalytische Dimerisierung und Zyklisierung von Nucleosid-5'-monophosphaten
Aktivierte Nucleosid-5'-monophosphate können unter dem Einfluß von Tonerden dimerisieren, polymerisieren und auch zyklisieren. Die Verteilung der unterschiedlichen Spezies ist abhängig von den gewählten Reaktionsbedingungen. Bei der Umsetzung bilden sich im Reaktionsgemisch nebeneinander sowohl 2', 5' als auch 3',5'-verknüpfte Addukte.
Beispiel 3: Synthese von zyklischem (5,6-Dichlorbenzimidazolribosid-(2' -> 5')-monophosphat - 5,6-dichlorbenzimidazolribosid-(3' -> 5')-monophosphat) (crDCIBI(2',5')pDCIBI(3',5')Pl) und zyklischem (5,6-Dichlorbenzimidazolribosid-(3' -> 5')-monophosphat - 5,6- dichlorbenzimidazolribosid-(3' -> 5')-monophosphat) (crDCIBI(3',5')pDCIBI(3',5')Pl)
Die Synthese folgt einer Vorschrift von Urata et al.1 , in der die Umsetzung von Imidazol-aktiviertem Adenosin-5'-0-monophosphat beschrieben wird.
100 mg 5,6-Dichlorbenzimidazol-5'-0-monophosphat Imidazolid (Biolog GmbH, Bremen) werden in 10 ml Puffer gelöst, der 0,2 M NaCI, 75 mM MgCI2, 0,1 M HEPES enthält. Nach Zugabe von 50 mg Montmorillonite (Na+-Form) wird der pH-Wert mit NaOH oder HCl auf 8,0 eingestellt und die Mischung bei RT stehen gelassen.
Der Reaktionsfortschritt, bzw. die Abnahme des Eduktsignals wird mit Reversed Phase HPLC überwacht.
Nach Abschluß der Umsetzung wird die Reaktionslösung filtriert, am Rotationsverdampfer schonend eingeengt und mit präparativer HPLC aufgereinigt. Die zyklischen Reaktionsprodukte werden in der Triethylammonium-Form isoliert und lyophilisiert.
Die typische Ausbeute liegt beim 2' -> 5' / 3' -> 5'-verknüpften Produkt bei etwa 5 % und beim 3' -> 5' / 3' -> 5'-verknüpften Produkt bei ca. 35 %.
Chemoenzymatische Dimerisierung und Zyklisierung von Nucleosid-5'-0-triphosphaten mit DisA zur Herstellung von benzimidazolhaltigen CDNs
Das DNA integrity scanning protein DisA from Bacillus subtilis2, welches in Bacillus subtilis c-diAMP aus ATP biokatalysiert, wurde eingesetzt um aus purinbasierten Nukleosidtriphosphaten mit Modifikationen in der Purinbase und in der Ribose die korrespondierenden CDNs herzustellen. Das gleiche Enzym wird eingesetzt um die benzimidazolhaltigen CDNs der vorliegenden Erfindung 5 herzustellen.
Die chemoenzymatische Reaktionen können entweder in homogener Lösung oder auch bevorzugt mit an natürlichem Trägermaterial, wie Dextran, Agarose, Zellulose oder von synthetischer Natur wie Acrylamid, Polystyrol etc. immobilisiertem Enzym durchgeführt werden.
In einer besonders bevorzugten Anwendungsform wird die chemoenzymatische Reaktion mit an 10 Sepharose 4 Fast Flow (GE Healthcare) immobilisierter DisA durchgeführt.
Das Enzym ist bei Temperarturen von 15°C - 50°C über einen weiten pH-Bereich von pH 5 - pH 1 1 in ungepufferter oder gepufferter Lösung in Gegenwart von zweiwertigen Metallsalzen und Reduktionsmitteln enzymatisch aktiv. Als Puffer dienen Puffersysteme, die für biologische Anwendungen und Proteine dem Fachmann allgemein bekannt sind.
15 In einer bevorzugten Anwendungsform der Erfindung wird die enzymatische Reaktion in 0.01 M - 1 M alkylammoniumhaltigen Puffern in einem pH-Bereich von 7 - 10 mit 0.01 M - 1 M Magnesiumchlorid und 0.0001 M - 0.1 M Dithiothreitol (DTT) bei 20°C - 40°C durchgeführt.
In einer besonders bevorzugten Anwendungsform der Erfindung wird die enzymatische Synthese in einer Pufferlösung von 0.1 M Ethanolaminpuffer, 0.025 M Magnesiumchlorid, 0.001 M DTT, pH 9,5 bei 20 37°C durchgeführt.
Beispiel 4: Immobilisierung von DisA an NHS-aktivierte Sepharose 4 fast flow
~5 mL aufgeschlämmter NHS-aktivierte Sepharose 4 Fast Flow-Slurry (GE Healthcare; #17-0906-01 ) 25 wurden gemäß der Angaben im Herstellerprotokoll gewaschen und im letzten Schritt in einer Fritte kurz von Waschwasser befreit und sofort in eine vorbereitete Lösung bestehend aus 0,5 mL DisA- Lösung (15,5 mg/mL DisA (per UV A280 nm) in 50 mM HEPES, pH 7,5, 200 mM NaCI, 10 % Glyzerin), 0,4 mL 50 mM HEPES, pH 7,5, 200 mM NaCI, 10 % Glyzerin und 0,1 mL 1 M NaH2P04, pH 7,5 in ein 3,5 mL Polypropylenreagiergefäß (PP) mit Schraubdeckel und Dichtung gegeben (Sartstedt) gegeben 30 und 5 min bei Raumtemperatur geschüttelt. Anschließend wird für weitere 16 h bei 4 °C geschüttelt.
Das resultierende immobilisierte Enzym wurde danach mit 30 mL 30 mM NaH2P04, pH 7 gewaschen und anschließend als Slurry (Gesamtvolumen ~ 3 mL) in 30 mM NaH2P04, pH 7 mit 1 % NaN3 bei 4°C gelagert. Vor den chemoenzymatischen Reaktionen wurde ein Puffertausch auf 0.1 M Ethanolaminpuffer, 0.025 M Magnesiumchlorid, 0.001 M DTT, pH 9,5 (Reaktionspuffer) 35 vorgenommen. Dafür wurde die jeweils benötigte Menge Slurry nach dem Aufschütteln in ein 2 mL PP-Reagiergefäß transferiert und bei 300 rpm in einer Laborzentrifuge (Biofuge primo, Heraeus) zentrifugiert. Danach wurde der Überstand abgenommen und die verbliebene Sepharose mit 1 mL
Reaktionspuffer versetzt, suspendiert und erneut mit 300 rpm zentrifugiert. Der Überstand wurde zwei weitere Male abgenommen und die Sepharose jeweils wieder mit 1 mL Reaktionspuffer versetzt. Nach diesem Puffertausch wurden -2,5 mL DisA-Sepharoseslurry in 0.1 M Ethanolaminpuffer, 0.025 M Magnesiumchlorid, 0.001 M DTT, pH 9,5, erhalten.
Beispiel 5: Chemoenzymatische Synthese von zyklischem (2 -Fluor-2 -deoxyadenosin-(3' -> 5')- monophosphat -2'-fluor-2'-deoxyadenosin-(3' -> 5')-monophosphat) (2',2"-Di-F-c-didAMP)
100 \iL DisA-Sepharoseslurry, wie in Beispiel 4 hergestellt, wurden mit 0,5 μιτιοΙ 2'-Fluor-2'- deoxyadenosin-5'-0-triphosphat (BIOLOG GmbH, Bremen) in 0.1 M Ethanolaminpuffer, 0.025 M Magnesiumchlorid, 0.001 M DTT, pH 9,5 bei 37°C innerhalb von 26 h quantitativ umgesetzt (> 94 % Produktbildung).
2'-2"-Di-F-c-didAMP: 3 ,5'/3',5'
C2oH22F2N1001oP2; MW 662,4 (freie Säure)
UV: Amax: 259 nm, ε 27000
ESI-MS (+): m/z 663 [M + H] +
ESI-MS (-): m/z 661 [M - H] "
Beispiel 6: Chemoenzymatische Synthese von zyklischem (N -Benzyladenosin-(3' -> 5')- monophosphat - N6-benzyladenosin -(3' -> 5')-monophosphat) (6,6 -Di-Bn-c-diAMP)
100 \iL DisA-Sepharoseslurry, wie in Beispiel 4 hergestellt, wurden mit 0,5 μιτιοΙ N6-Benzyladenosin- 5'-0-triphosphat (BIOLOG GmbH, Bremen) in 0.1 M Ethanolaminpuffer, 0.025 M Magnesiumchlorid, 0.001 M DTT, pH 9,5 bei 37°C innerhalb von 30 min quantitativ umgesetzt (> 95 % Produktbildung).
6,6 -Di-Bn-c-diAMP: 3 ,5'/3',5'
C34H36N10O12P2; MW 838,7 (freie Säure)
UV: Amax: 268 nm, ε 36900
ESI-MS (+): m/z 839 [M + H] +
ESI-MS (-): m/z 837 [M - H] "
Beispiel 7: Chemoenzymatische Synthese von zyklischem (Adenosin-(3' -> 5')-monophosphat - adenosin -(3' -> 5')-monophosphat) (c-diAMP), zyklischem (Adenosin-(3' -> 5')-monophosphat - 8-chloradenosin -(3' -> 5')-monophosphat) (8-CI-c-diAMP) und zyklischem (8-Chloradenosin-(3' -> 5')-monophosphat -8-chloradenosin -(3' -> 5')-monophosphat) (8,8'-Di-CI-c-diAMP)
100 μΙ_ DisA-Sepharoseslurry, wie in Beispiel 4 hergestellt, wurden mit 0,5 μιτιοΙ Adenosin-5'-0- triphosphat und 0,5 μιτιοΙ 8-Chloradenosin-5'-0-triphosphat (BIOLOG GmbH, Bremen) in 0.1 M Ethanolaminpuffer, 0.025 M Magnesiumchlorid, 0.001 M DTT, pH 9,5 bei 37°C innerhalb von 3 Tagen quantitativ umgesetzt (> 93 % Produktbildung; -21 % c-diAMP, -51 ,5 % 8-CI-cdiAMP, -21 ,5 % 8,8'-
5 Di-CI-c-diAMP).
monophosphat - 2-chloradenosin -(3' -> 5')-monophosphat) (2,2 -Di-CI-c-diAMP)
10 100 \iL DisA-Sepharoseslurry, wie in Beispiel 4 hergestellt, wurden mit 0,5 μιτιοΙ 2-Chloradenosin-5'- O-triphosphat (BIOLOG GmbH, Bremen) in 0.1 M Ethanolaminpuffer, 0.025 M Magnesiumchlorid, 0.001 M DTT, pH 9,5 bei 37°C innerhalb von 20 h quantitativ umgesetzt (> 93 % Produktbildung).
2.2 -Di-CI-c-diAMP: 3 , 5 /3 , 5'
C20H22CI2N10O12P2; MW 727,3 (freie Säure)
UV: Amax: 262 nm , ε 25750
ESI-MS (+) : m/z 727 [M + H] +
ESI-MS (-) : m/z 725 [M - H] "
Beispiel 9: Chemoenzvmatische Synthese von zyklischem (7-Deazaadenosin-(3' -> 5')-
15 monophosphat - 7-deazaadenosin -(3' -> 5')-monophosphat) (7,7'-Di-CH-c-diAMP)
100 μΙ_ DisA-Sepharoseslurry, wie in Beispiel 4 hergestellt, wurden mit 0,5 μιτιοΙ 7-Deazaadenosin-5'- O-triphosphat (BIOLOG GmbH, Bremen) in 0.1 M Ethanolaminpuffer, 0.025 M Magnesiumchlorid, 0.001 M DTT, pH 9,5 bei 37°C innerhalb von 20 h quantitativ umgesetzt (> 99 % Produktbildung).
7.7'-Di-CH-c-diAMP: 3 , 5 /3 , 5'
C22H26N8012P2; MW 656,4 (freie Säure)
UV: Amax: 269 nm, ε 21600
ESI-MS (+): m/z 657 [M + H] +
ESI-MS (-): m/z 655 [M - H] "
Beispiel 10: Chemoenzymatische Synthese von zyklischem (Adenosin-(3' -> 5')-monophosphat -adenosin -(3' -> 5')-monophosphat) (c-diAMP), zyklischem (Adenosin-(3' -> 5')-monophosphat - benzimidazolribosid -(3' -> 5')-monophosphat) (crA(3',5')pBI(3',5')Pl) und zyklischem (Benzimidazolribosid-(3' -> 5')-monophosphat - benzimidazolribosid -(3' -> 5')-monophosphat) (crBI(3'.5')pBI(3'.5')Pl)
25 mL DisA-Sepharoseslurry, wie in Beispiel 4 hergestellt, wurden mit 50 μιτιοΙ Adenosin-5'-0- triphosphat und 100 μιτιοΙ Benzimidazolribosid-5'-0-triphosphat (BIOLOG GmbH, Bremen) in 0.1 M Ethanolaminpuffer, 0.025 M Magnesiumchlorid, 0.001 M DTT, pH 9,5 bei 30 - 37°C innerhalb von 3 Tagen umgesetzt (> 75 % Produktbildung).
C22H25N7012P2; MW 641 ,4 (freie Säure) C24H26N4012P2; MW 624,4 (freie Säure)
UV: Amax: 254 nm, ε 16150 UV: Amax: 245 nm, ε 9810
ESI-MS (+): m/z 642 [M + H] + ESI-MS (+): m/z 625 [M + H] +
ESI-MS (-): m/z 640 [M - H] " ESI-MS (-): m/z 623 [M - H] "
c-diAMP: 3 , 5 /3 , 5'
C20H24N10O12P2; MW 658,4 (freie Säure)
UV: Amax: 259 nm, ε 27000
ESI-MS (+): m/z 659 [M + H] +
ESI-MS (-): m/z 657 [M - H] "
Beispiel 11 : Chemoenzymatische Synthese von zyklischem (2 -Fluor-2 -deoxyadenosin-(3' -> 5')-monophosphat -2'-fluor-2'-deoxyadenosin -(3' -> 5')-monophosphat) (2'-2"-Di-F-c-didAMP), zyklischem (2 -Fluor-2 -deoxyadenosin-(3' -> 5')-monophosphat - benzimidazolribosid -(3' -> 5')-monophosphat) (cr2'-F-dA(3',5')pBI(3',5')Pl) und zyklischem (Benzimidazolribosid-(3' -> 5')- monophosphat - benzimidazolribosid -(3' -> 5')-monophosphat) (crBI(3',5')pBI(3',5')Pl)
25 mL DisA-Sepharoseslurry, wie in Beispiel 4 hergestellt, wurden mit 50 μιτιοΙ 2'-Fluor-2'- deoxyadenosin-5'-0-triphosphat und 50 μmol Benzimidazolribosid-5'-0-triphosphat (BIOLOG GmbH, Bremen) in 12 mL 0.1 M Ethanolaminpuffer, 0.025 M Magnesiumchlorid, 0.001 M DTT, pH 9 bei 30°C - 37°C innerhalb von 43 h umgesetzt (> 75 % Produktbildung).
Beispiel 12: Chemoenzymatische Synthese von zyklischem (Adenosin-(3' -> 5')- monoboranophosphat - adenosin -(3' -> 5')-monoboranophosphat) (c-diAMPBB), zyklischem (Adenosin-(3' -> 5')-monoboranophosphat - benzimidazolribosid -(3' -> 5')-monophosphat) (crA(3',5')pB-BI(3',5')Pl) und zyklischem (Benzimidazolribosid-(3' -> 5')-monophosphat - benzimidazolribosid -(3' -> 5')-monophosphat) (crBI(3',5')pBI(3',5')Pl)
100 \iL DisA-Sepharoseslurry, wie in Beispiel 4 hergestellt, werden mit 0,5 μιτιοΙ Adenosin-5'-0-(1 - Boranotriphosphat) und 0,5 μιτιοΙ Benzimidazolribosid-5'-0-triphosphat (BIOLOG GmbH, Bremen) in 0.1 M Ethanolaminpuffer, 0.025 M Magnesiumchlorid, 0.001 M DTT, pH 9,5 bei 37°C innerhalb von 3 Tagen umgesetzt (> 75 % Produktbildung).
c-diAMPBB: 3 , '5 /3 , 5' crAi3'.5')DB-Bli3'.5')Dl: 3 , 5 /3 , 5'
C2oH3oB2N1o01oP2; MW 654,1 (freie Säure)
Ps; MW 639,3 (freie Säure) UV: Amax: 259 nm, ε 27000 UV: Amax: -254 nm
ESI-MS (+): m/z 655 [M + H] + ESI-MS (+): m/z 640 [M + H] +
ESI-MS (-): m/z 653 [M - H] " ESI-MS (-): m/z 638 [M - H] "
0ΓΒΙ(3'.5')ρΒΙ(3'.5')ρ1: 3',5'/3',5'
C24H26N4012P2; MW 624,4 (freie Säure)
UV: Amax: 245 nm, ε 9810
ESI-MS (+): m/z 625 [M + H] +
ESI-MS (-): m/z 623 [M - H] ""
Beispiel 12A: Chemoenzymatische Synthese von zyklischem (Benzimidazolribosid-(3' -> 5')- monophosphat - benzimidazolribosid -(3' -> 5')-monophosphat) (crBI(3',5')pBI(3',5')Pl)
21 mL DisA-Sepharoseslurry, wie in Beispiel 4 hergestellt, wurden mit 400 μιτιοΙ Benzimidazolribosid- 5'-0-triphosphat (BIOLOG GmbH, Bremen) in 35 mL 0.1 M Ethanolaminpuffer, 0.025 M Magnesiumchlorid, 0.001 M DTT, pH 9,5 bei 30 - 37°C innerhalb von 14 Tagen umgesetzt (> 55 % Produktbildung).
crBI(3'.5')pBI(3'.5')Pl : 3 ,5 /3', 5'
C24H26N4012P2; MW 624,4 (freie Säure)
UV: Amax: 245 nm, ε 9810
ESI-MS (+): m/z 625 [M + H] +
ESI-MS (-): m/z 623 [M - H] ""
Beispiel 12B: Chemoenzymatische Synthese von zyklischem (5,6-Dichlorbenzimidazolribosid- (3' -> 5')-monophosphat - 5,6-dichlorbenzimidazolribosid-(3' -> 5')-monophosphat) (0ΓΡαΒΙ(3'.5')ρΡαΒΙ(3'.5')Ρΐ)
4,5 mL DisA-Sepharoseslurry, wie in Beispiel 4 hergestellt, wurden mit 160 μιτιοΙ 5,6- dichlorbenzimidazolribosid-5'-0-triphosphat (BIOLOG GmbH, Bremen) in 50 mL 0.1 M Ethanolaminpuffer, 0.025 M Magnesiumchlorid, 0.001 M DTT, pH 9,5 bei 30 - 37°C innerhalb von 6 Tagen umgesetzt (~ 50 % Produktbildung).
0ΓΡ0ΙΒΙ(3'.5')ΡΡ0ΙΒΙ(3'.5')Ρ1: 3',5'/3',5'
C24H22Cl4N4012P2; MW 762,22 (freie Säure)
UV: max: 254 nm, ε 1 1500
ESI-MS (+): m/z 761/763/765 [M + H] +
ESI-MS (-): m/z 759/761/763 [M - H] "
Beispiel 12C: Chemoenzymatische Synthese von zyklischem (2 -Fluor-2 -deoxyadenosin-(3' -> 5')-monophosphat -2 -fluor-2 -deoxyadenosin -(3' -> 5')-monophosphat) (2'-2"-Di-F-c-didAMP), zyklischem (2'-Fluor-2'-deoxyadenosin-(3' ^> 5')-monophosphat 5,6- dichlorbenzimidazolribosid -(3' -> 5')-monophosphat) (cr2'-F-dA(3',5')pDCIBI(3',5')Pl) und zyklischem (5,6-Dichlorbenzimidazolribosid-(3' -> 5')-monophosphat - 5,6- dichlorbenzimidazolribosid-(3' -> 5')-monophosphat) (crDCIBI(3',5')pDCIBI(3',5')Pl)
25 mL DisA-Sepharoseslurry, wie in Beispiel 4 hergestellt, wurden mit 100 μιτιοΙ 2'-Fluor-2'- deoxyadenosin-5'-0-triphosphat und 100 μmol 5,6-dichlorbenzimidazolribosid-5'-0-triphosphat (BIOLOG GmbH, Bremen) in 50 mL 0.1 M Ethanolaminpuffer, 0.025 M Magnesiumchlorid, 0.001 M DTT, pH 9,5 bei 30 - 37°C innerhalb von 3 Tagen umgesetzt (~ 70 % Produktbildung).
Beispiel 12D: Chemoenzymatische Synthese von zyklischem (Adenosin-(3' -> 5')- monophosphat -adenosin -(3' -> 5')-monophosphat) (c-diAMP), zyklischem (Adenosin-(3' -> 5')- monophosphat - 5,6-dichlorbenzimidazolribosid -(3' -> 5')-monophosphat) (crA(3',5')pDCIBI(3',5')Pl) und zyklischem (5,6-Dichlorbenzimidazolribosid-(3' -> 5')-
monophosphat : 5,6-dichlorbenzimidazolribosid-(3' ^> 5')-monophosphat)
(0ΓΡ0ΙΒΙ(3'.5')ΡΡ0ΙΒΙ(3'.5')Ρ1)
20 mL DisA-Sepharoseslurry, wie in Beispiel 4 hergestellt, wurden mit 200 μιτιοΙ Adenosin-5'-0- triphosphat und 100 μιτιοΙ 5,6-dichlorbenzimidazolribosid-5'-0-triphosphat (BIOLOG GmbH, Bremen) in 50 mL 0.1 M Ethanolaminpuffer, 0.025 M Magnesiumchlorid, 0.001 M DTT, pH 9,5 bei 30 - 37°C innerhalb von 2 Tagen umgesetzt (> 75 % Produktbildung).
Beispiel 12E: Chemoenzymatische Synthese von zyklischem (2 -Fluor-2 -deoxyinosin-(3' -> 5')- monophosphat - benzimidazolribosid -(3' -> 5')-monophosphat) (cr2'-F-dl(3',5')pBI(3',5')Pl) 5,5 μιτιοΙ (c[2'-F-dA(3',5')pBI(3',5')p]) aus Beispiel 1 1 wurden analog bekannter Literatursynthese8 mit Adenosinmonophosphatdeaminase (Deamyzyme 5000, Amano Enzyme Europe Ltd, Großbritannien) innerhalb von 2 Tagen quantitativ zu c[2'-F-dl(3',5')pBI(3',5')p] umgesetzt.
cr2'-F-dl(3'.5')pBI(3'.5')Pl : 3 ,5'/3',5'
C22H23FN7012P2; MW 644,4 (freie Säure)
UV: Amax: 247 nm, ε 17000
ESI-MS (+): m/z 645 [M + H] +
ESI-MS (-): m/z 643 [M - H] "
Generelles Syntheseverfahren D:
Chemoenzymatische Dimerisierung und Zyklisierung von Nucleosid-5'-0-triphosphaten mit cGAS zur Herstellung von benzimidazolhaltigen CDNs
Das Enzym cGAMP synthase (cGAS) ist in der Lage in Gegenwart von doppelsträngiger DNA das nicht-kanonische 2',3'-cGAMP aus GTP und ATP biokatalytisch herzustellen. Das Enzym ist nicht hochspezifisch und es konnte bereits gezeigt werden, dass die chemoenzymatische Synthese von mono- und diphosphorothioathaltige CDNs mit diesem Enzym möglich ist3. Das gleiche Enzym (rekombinant exprimiert aus der Maus) wird eingesetzt um die benzimidazolhaltigen CDNs der vorliegenden Erfindung herzustellen.
Die chemoenzymatische Reaktionen können entweder in homogener Lösung oder auch bevorzugt mit an natürlichem Trägermaterial, wie Dextran, Agarose, Zellulose oder von synthetischer Natur wie Acrylamid, Polystyrol etc. immobilisiertem Enzym durchgeführt werden. Das Enzym ist bei Temperaturen von 15°C - 50°C über einen weiten pH-Bereich von pH 5 - pH 1 1 in ungepufferter oder gepufferter Lösung in Gegenwart von zweiwertigen Metallsalzen, doppelsträngiger DNA und Reduktionsmitteln enzymatisch aktiv. Als Puffer dienen Puffersysteme, die für biologische Anwendungen und Proteine dem Fachmann allgemein bekannt sind.
In einer bevorzugten Anwendungsform der Erfindung wird die enzymatische Reaktion in 0.01 M - 1 M Puffern in einem pH-Bereich von 7 - 10 mit 0.005 M - 1 M Magnesiumchlorid, 0,01 mg/mL - 1 mg/mL Heringssperma-DNA und 0.0001 M - 0.1 M Dithiothreitol (DTT) bei 20°C - 40°C durchgeführt.
In einer besonders bevorzugten Anwendungsform der Erfindung wird die enzymatische Synthese in einer Pufferlösung von 0.02 M TRIS-HCI, 0.02 M Magnesiumchlorid, 0,1 mg/mL Heringssperma-DNA, 0.001 M DTT, pH 8 bei 37°C durchgeführt.
Beispiel 13: Chemoenzymatische Synthese von zyklischem (Guanosin-(2' -> 5')- monoboranophosphat - benzimidazolribosid -(3' -> 5')-monophosphat) (crG(2',5')pB-BI(3',5')Pl)
10 μΜ cGAS (Maus, Aminosäuren 147 - 507) werden mit 1 μιτιοΙ Guanosin-5'-0-(1 - boranotriphosphat) und 1 μιτιοΙ Benzimidazolribosid-5'-0-triphosphat (BIOLOG GmbH, Bremen) in 0.002 M TRIS-HCI, 0.02 M Magnesiumchlorid, 0,1 mg/mL Heringssperma-DNA, 0.001 M DTT, pH 8 in 1 mL Gesamtlösung bei 37°C innerhalb von 3 Tagen umgesetzt (> 75 % Produktbildung).
crG(2'.5')pB-BI(3'.5')Pl : 2 , 5 /3 , 5'
C22H28BN7012P2; MW 655,3 (freie Säure)
UV: Xmax: -250 nm,
ESI-MS (+): m/z 656 [M + H] +
ESI-MS (-): m/z 654 [M - H] "
Beispiel 14: Chemoenzymatische Synthese von zyklischem (Guanosin-(2' -> 5')- monoboranophosphat - benzimidazolribosid -(3' -> 5')-monophosphorothioat) (ciG(2 ,5 )pB- BK3'.5')PS1)
10 μΜ cGAS (Maus, Aminosäuren 147 - 507) werden mit 1 μιτιοΙ Guanosin-5'-0-(1 - boranotriphosphat) und 1 μιτιοΙ Benzimidazolribosid-5'-0-(1 -thiotriphosphat) (BIOLOG GmbH, Bremen) in 0.002 M TRIS-HCI, 0.02 M Magnesiumchlorid, 0,1 mg/mL Heringssperma-DNA, 0.001 M DTT, pH 8 in 1 mL Gesamtlösung bei 37°C innerhalb von 3 Tagen umgesetzt (> 75 % Produktbildung).
crG(2'.5')pB-BI(3'.5')pSl: 2 ,5'/3',5'
PsS; MW 671 ,3 (freie Säure)
UV: Xmax: -250 nm,
ESI-MS (+): m/z 672 [M + H] +
ESI-MS (-): m/z 670 [M - H] "
Generelles Syntheseverfahren E:
Chemische Synthesemethode zur Herstellung benzimidazolhaltigen CDNs
Die chemische Synthese der benzimidazolhaltigen CDNs der vorliegenden Erfindung basiert auf publizierten Arbeiten von Gaffney et al. 20104 und Gao et al 20135.
Beispiel 15: Chemische Synthese von zyklischem (Adenosin-(3' -> 5')-monophosphat - benzimidazolribosid-(3' -> 5')-monophosphat) (crA(3',5')pBI(3',5')pl)
DMOCP = y V
R = TBDMS R = TBDMS
(c[A(3'-5')p-BI(3'-5')p])
Abbildung 1 : Synthese von zyklischem (Adenosin-(3' -> 5')-monophosphat - benzimidazolribosid-(3' -> 5')-monophosphat) (c[A(3',5')pBI(3',5')p]). Syntheseschritte: a) Pyridiniumtrifluoracetat / H20; b) ferf.-Butylamin; c) Dichloressigsäure / H20; d) A, Pyridin; e) ferf.-Butylhydroperoxid; f) Dichloressigsäure / H20; g) 2-Chlor-5,5-dimethyl-1 ,3,2-dioxaphosphorinan-2-oxid; h) lod, H20; i) Methylamin / Ethanol; j) Triethylamintrihydrofluorid.
Beispiel 15.a. Synthese des H-Phosphonatzwischenproduktes 5'-OH-2'-TBDMS-3'-H- phosphonat-N6-Bz-adenosin
z
P-OH
H
Das Phosphoramidit 5'-DMTr-2'-TBDMS-3'-CEP-adenosin (Chemgenes Inc., USA) wird in trockenem Acetonitril gelöst und mit 2 Äquivalenten Wasser sowie 1 ,2 Äquivalenten Pyridiniumtrifluoracetat versetzt und 15 min bei Raumtemperatur gerührt. Danach werden die flüchtigen Bestandteile unter reduziertem Druck evaporiert. Anschließend werden 100 Äquivalente ferf.-Butylamin zugegeben, die resultierende Lösung wird für 30 min bei Raumtemperatur gerührt und danach erneut unter reduziertem Druck evaporiert. Der Rückstand wird in Acetonitril gelöst und erneut unter reduziertem Druck evaporiert. Der resultierende Rückstand wird in Dichlormethan gelöst und 10 Äquivalente Wasser werden zugegeben. Anschließend werden 9 Äquivalente Dichloressigsaure aus einer 3 % igen Lösung von Dichloressigsaure in Dichlormethan zugegeben und die Lösung wird 10 min bei Raumtemperatur gerührt. Nach dieser Periode werden 18 Äquivalente Pyridin addiert und die Lösung wird für 10 min bei Raumtemperatur gerührt. LC-MS-Analytik des Rohproduktes bestätigt die Anwesenheit des H-Phosphonatzwischenproduktes. Anschließend werden die flüchtigen Bestandteile unter reduziertem Druck evaporiert and danach dreimal jeweils mit trockenem Acetonitril gelöst jeweils erneut unter reduziertem Druck evaporiert. Bei der letzten Evaporierung wird nicht zur Trockene eingeengt, sondern das Rohprodukt in einer geringen Menge Acetonitril belassen um bei der nächsten Reaktion eingesetzt zu werden. Bei Bedarf wird die resultierende Lösung des H- Phosphonatzwischenproduktes bei -70 °C gelagert.
Beispiel 15.b. Synthese des linearen Dinukleotides 5'-OH-2'-TBDMS-benzimidazolribosid- (3'^5')-cvanoethyl-phosphat-2'-TBDMS-3'-H-phosphonat-N6-Bz-adenosin
0=P-OH
H R = TBDMS Das Phosphoramidit 5'-DMTr-2'-TBDMS-3'-CEP-benzimidazolribosid (BIOLOG GmbH; die Synthese dieser Verbindung und Analoga gehört zum Stand der Technik und wurde beschrieben von Parsch6; 1 ,35 Äquivalente bezogen auf das nominelle H-Phosphonatzwischenprodukt aus Beispiel 15.a.) wird viermal jeweils in trockenem Acetonitril gelöst und unter reduziertem Druck evaporiert. Bei der letzten Evaporierung wird nicht zur Trockene eingeengt, sondern das Phosphoramidit in einer geringen Menge Acetonitril belassen. Die absolutierte Lösung wird unter Argonschutzgas zum 5'-OH-2'- TBDMS-3'-H-phosphonat-N6-Bz-adenosin aus Beispiel 15.a. gegeben und die resultierende Lösung wird 30 min bei Raumtemperatur unter Argonschutzgas gerührt. Anschließend wird tert.- Butylhydroperoxid in Decan (5,5 M; 2 Äquivalente) zugegeben und weitere 30 min bei Raumtemperatur unter Argonschutzgas gerührt. Nach dieser Zeit werden die flüchtigen Bestandteile der Mischung unter reduziertem Druck evaporiert und der Rückstand wird in Dichlormethan gelöst und 10 Äquivalente Wasser werden zugegeben. Danach wird Dichloressigsäure in Dichlormethan (3 %; 18 Äquivalente) zugegeben und 20 min bei Raumtemperatur gerührt. Anschließend wird Pyridin in deutlichem Überschuß zugegeben und weitere 5 min bei Raumtemperatur gerührt. LC-MS-Analytik des Rohproduktes bestätigt die Anwesenheit des linearen Dinukleotides 5'-OH-2'-TBDMS- benzimidazolribosid-(3'^5')-cyanoethyl-phosphat-2'-TBDMS-3'-H-phosphonat-N6-Bz-adenosin. Die flüchtigen Bestandteile der Mischung werden unter reduziertem Druck evaporiert und anschließend zweimal jeweils in trockenem Pyridin gelöst und jeweils unter reduziertem Druck evaporiert. Der Rückstand wird erneut in trockenem Pyridin gelöst um in der nächsten Reaktion umgesetzt zu werden. Bei Bedarf wird die resultierende Lösung des linearen Dinukleotides bei -70 °C gelagert.
Beispiel 15.c. Synthese des zyklischen (2'-TBDMS-N6-Bz-adenosin-(3'^5')-H-phosphonat-2'- TBDMS-benzimidazolribosid-(3'^5')-cvanoethyl-phosphat) z
2-Chlor-5,5-dimethyl-1 ,3,2-dioxaphosphorinan-2-oxicl (DMOCP; 3,5 Äquivalente bezogen auf das nominelle lineare Dinukleotid 5'-OH-2'-TBDMS-benzimidazolribosid-(3'^5')-cyanoethyl-phosphat-2'- TBDMS-3'-H-phosphonat-N6-Bz-adenosin aus Beispiel 15.b.) werden unter Argonschutzgasatmosphäre zum Rohprodukt in Pyridin aus Beispiel 15.b. gegeben und 20 min bei Raumtemperatur unter Argonschutzgas gerührt. LC-MS-Analytik des Rohproduktes bestätigt die Anwesenheit des zyklischen Dinukleotides 2'-TBDMS-N6-Bz-adenosin-(3'— >5')-H-phosphonat-2'- TBDMS-benzimidazolribosid-(3'— >5')-cyanoethyl-phosphat, welches sofort in Beispiel 15.d. weiter umgesetzt wird.
Beispiel 15.d. Synthese des zyklischen (2'-TBDMS-N6-Bz-adenosin-(3'^5')-monophosphat-2 - TBDMS-benzimidazolribosid-(3'^5')-cvanoethyl-phosphat)
NHBz
Zum Rohprodukt aus Beispiel 15.c. werden lod (1 ,3 Äquivalente) und Wasser (30 Äquivalente) gegeben und die Mischung wird 20 min bei Raumtemperatur gerührt. Anschließend wird wässriges NaHS03 (0,15 %) zugesetzt bis sich die Rohlösung vollständig entfärbt. Danach wird ein dem Volumen der Rohlösung entsprechendes Volumen an wässriger NaHC03-Lösung zugegeben und weitere 5 min gerührt. Nun wird die wässrige Phase dreimal mit Ethylacetat / Methyl-ferf.-Butylether (1 :1 (v:v)) ausgeschüttelt. Die kombinierten organischen Phasen werden über MgS04 getrocknet und danach unter reduziertem Druck evaporiert. LC-MS-Analytik des Rohproduktes bestätigt die Anwesenheit des zyklischen Dinukleotides 2'-TBDMS-N6-Bz-adenosin-(3'— >5')-monophosphat-2'- TBDMS-benzimidazolribosid-(3'— >5')-cyanoethyl-phosphat. Bei Bedarf wird das zyklische Dinukleotid bei -70 °C gelagert. Das Rohprodukt wird in einer minimalen Menge Dichlormethan gelöst und mittels präparativer Flashchromatographie an Kieselgel mit einem Methanol / Dichlormethan-Gradienten aufgereinigt. Produkthaltige Fraktionen werden unter reduziertem Druck evaporiert und in Beispiel 15.e. weiter umgesetzt. Bei Bedarf wird das zyklische Dinukleotid bei -70 °C gelagert.
Beispiel 15.e. Synthese des zyklischen (2'-TBDMS-adenosin-(3'^5')-monophosphat-2'-TBDMS- benzimidazolribosid-(3'^5')-monophosphat)
Das zyklische Dinukleotid 2'-TBDMS-N6-Bz-adenosin-(3'^5')-monophosphat-2'-TBDMS- benzimidazolribosid-(3'— >5')-cyanoethyl-phosphat aus Beispiel 15.d. wird unter Argonschutgasatmosphäre mit einem Überschuß von 33 % Methylamin in absolutem Ethanol versetzt und unter Argonschutzgas für 4 h bei Raumtemperatur gerührt. Anschließend werden die flüchtigen Bestandteile der Mischung unter reduziertem Druck evaporiert und 4 - 16 h im Hochvakuum getrocknet. LC-MS-Analytik des Rohproduktes bestätigt die Anwesenheit der Zielverbindung. Das resultierende Rohprodukt vom zyklischen 2'-TBDMS-adenosin-(3'— >5')-monophosphat-2'-TBDMS- benzimidazolribosid-(3'— >5')-monophosphat wird im Beispiel 15.f. weiter umgesetzt. Bei Bedarf wird das zyklische Dinukleotid bei -70 °C gelagert.
Beispiel 15.f. Synthese des zyklischen (Adenosin-(3'— >5')-monophosphat - benzimidazolribosid- (3'^5')-monophosphat) (ΟΓΑ(3'.5')Ρ-ΒΙ(3'.5')Ρ1)
Das zyklische Dinukleotid 2'-TBDMS-adenosin-(3'^5')-monophosphat-2'-TBDMS- benzimidazolribosid-(3'— >5')-monophosphat aus Beispiel 15.e. wird unter Argonschutzgasatmoshäre in einer Mischung aus trockenem Pyridin und trockenem Triethylamin (2:1 ; (v:v)) gelöst und unter reduziertem Druck aufkonzentriert. Anschließend werden 25 Äquivalente Triethylamintrihydrofluorid und trockenes Triethylamin unter Argonschutzgasatmosphäre simultan zugegeben und die resultierende Lösung wird unter Argonschutz 3,5 h bei 50 °C gerührt. Danach wird die Mischung auf Raumtemperatur abgekühlt und überschüssiges Triethylamintrihydrofluorid wird durch Zugabe von Methoxytrimethylsilan gefolgt von weiterem Rühren für 30 min bei Raumtemperatur abgefangen. LC- MS-Analytik des Rohproduktes bestätigt die Anwesenheit der Zielverbindung. Nach dieser Zeit werden alle flüchtigen Bestandteile der Mischung unter reduziertem Druck evaporiert. Der Rückstand wird weitere 4 - 16 h im Hochvakuum getrocknet. Das resultierende Rohprodukt vom zyklischen Adenosin-(3'— >5')-monophosphat - benzimidazolribosid-(3'— >5')-monophosphat wird mit Wasser suspendiert, im Ultraschallbad behandelt und die wässrige Phase dreimal mit Chloroform ausgeschüttelt. Nach anschließendem Filtrieren wird das Rohprodukt verdünnt und an einem Q Sepharose™ Fast Flow Anionentauscher mit einem Triethylammoniumbicarbonat-Gradienten aufgereinigt. Die produkthaltigen Fraktionen werden vereint, das Lösungsmittel unter reduziertem Druck evaporiert und die Zielverbindung wird danach mit präparativer Reversed Phase Chromatographie (RP-18) mit einem geeignetem Acetonitril / 20 mM Triethylammoniumformiat- Laufmittel hochgereinigt.
Die Entsalzung der Zielverbindung erfolgt ebenfalls mit präparativer Reversed Phase Chromatographie (RP-18) und die entsalzte Zielverbindung liegt anschliessend als Triethylammoniumsalz vor.
Das Natriumsalz der Zielverbindung wird mittels Passage einer verdünnten Produktlösung durch einen SP Sepharose™ Fast Flow Kationentauscher (Na+-Form) erhalten.
0ΓΑ(3'.5')ΡΒΙ(3'.5')Ρ1: 3',5'/3',5'
C22H25N7012P2; MW 641 ,4 (freie Säure)
UV: Amax: 254 nm, ε 16150
ESI-MS (+): m/z 642 [M + H] +
ESI-MS (-): m/z 640 [M - H] "
Beispiel 16: Chemische Synthese von zyklischem (5,6-Dichlorbenzimidazolribosid-(3' -> 5')- monophosphorothioat - 5,6-dichlorbenzimidazolribosid-(3' -> 5')-monophosphorothioat)
DMOCP - y Y
R = TBDMS R = TBDMS c[DCIBI(3',5')pS-DCIBI(3',5')pS]
Abbildung 2: Synthese von zyklischem (5,6-Dichlorbenzimidazolribosid-(3'^5')-monophosphorothioat - 5,6-dichlorbenzimidazolribosid-(3'^5')-monophosphorothioat) (c[DCIBI(3',5')pS-DCIBI(3',5')pS]). Syntheseschritte: a) Pyridiniumtrifluoracetat / H20; b) ferf.-Butylamin; c) Dichloressigsäure / H20; d) A, Pyridin; e) 3-((N,N-dimethylaminomethylidene)amino)-3H-1 ,2,4-dithiazole-5-thione (DDTT); f) Dichloressigsäure / H20; g) 2-Chlor-5,5-dimethyl-1 ,3,2-dioxaphosphorinan-2-oxid; h) 3-1-1-1 ,2- Benzodithiol-3-οη; i) Methylamin / Ethanol; j) Triethylamintrihydrofluorid.
Beispiel 16.a. Synthese des H-Phosphonatzwischenproduktes 5'-OH-2'-TBDMS-3'-H- phosphonat-5,6-dichlorbenzimidazolribosid
P-OH
H
Das Phosphoramidit 5'-DMTr-2'-TBDMS-3'-CEP-5,6-dichlorbenzimidazolribosid (BIOLOG GmbH, Bremen) wird analog zu Beispiel 15.a. in die oben genannte Zielverbindung überführt.
Beispiel 16.b. Synthese des linearen Dinukleotides 5'-OH-2'-TBDMS-5,6- dichlorbenzimidazolribosid-(3'^5')-cvanoethyl-phosphorothioat-2'-TBDMS-3'-H-phosphonat- 5,6-dichlorbenzimidazolribosid
0=P-OH
H R = TBDMS
Die oben genannte Zielverbindung wird analog zu Beispiel 15.b. hergestellt.
Abweichend von Beispiel 15.b. wird anstelle von 5'-DMTr-2'-TBDMS-3'-CEP-benzimidazolribosid hier 5'-DMTr-2'-TBDMS-3'-CEP-5,6-dichlorbenzimidazolribosid (BIOLOG GmbH, Bremen) als zweiter Nukleotidbaustein eingesetzt.
Des Weiteren werden anstelle von tert.-Butylhydroperoxid in Decan aus Beispiel 15.b. hier 1 ,1 Äquivalente 3-((N,N-dimethylaminomethylidene)amino)-3H-1 ,2,4-dithiazole-5-thione (DDTT) zur Etablierung der Cyanoethyl-phosphorothioat-Einheit zugegeben.
Beispiel 16.c. Synthese des zyklischen (2'-TBDMS-5,6-dichlorbenzimidazolribosid-(3'^5')-H- phosphonat-2'-TBDMS-5,6-dichlorbenzimidazolribosid-(3'^5')-cvanoethyl-phosphorothioat)
Die oben genannte Zielverbindung wird analog zu Beispiel 15.c. hergestellt.
Beispiel 16.d. Synthese des zyklischen (2 -TBDMS-5,6-dichlorbenzimidazolribosid-(3'^5')- monophosphorothioat-2'-TBDMS-5,6-dichlorbenzimidazolribosid-(3'^5')-cvanoethyl- phosphorothioat)
Die oben genannte Zielverbindung wird analog zu Beispiel 15.d. hergestellt.
Anstelle von lod aus Beispiel 15.d. werden hier 1 ,5 Äquivalente 3H-1 ,2-Benzodithiol-3-on zur Etablierung der Phosphorothioat-Einheit zugegeben.
Beispiel 16.e. Synthese des zyklischen (2'-TBDMS-5,6-dichlorbenzimidazolribosid-(3'^5')- monophosphorothioat-2'-TBDMS-5,6-dichlorbenzimidazolribosid-(3'^5')- monophosphorothioat)
Die oben genannte Zielverbindung wird analog zu Beispiel 15.e. hergestellt.
Beispiel 16.f. Synthese des zyklischen (5,6-Dichlorbenzimidazolribosid-(3'— >5')- monophosphorothioat - 5,6-dichlorbenzimidazolribosid-(3'^5')-monophosphorothioat) (crDCIBI(3'.5')pS-DCIBI(3'.5')pSl)
Die oben genannte Zielverbindung wird analog zu Beispiel 15.f. hergestellt.
crDCIBI(3'.5')pS-DCIBI(3'.5')pSl : 3',5'/3',5'
C24H22Cl4N4O10P2S2; MW 794,3 (freie Säure)
UV: max: 254 nm, ε 12950
ESI-MS (+): m/z 795 [M + H] +
ESI-MS (-): m/z 793 [M - H] -
Beispiel 17: Chemische Synthese von zyklischem (Guanosin-(2' -> 5')-monophosphorothioat 5,6-dichlorbenzimidazolribosid-(3' -> 5')-monophosphorothioat) (crG(2',5')pS-DCIBI(3',5')pSl)
c[G(2'-5')pS-DCIBI(3'-5')pS]
Abbildung 3: Synthese von zyklischem (Guanosin-(2' -> 5')-monophosphorothioat - 5,6- dichlorbenzimidazolribosid-(3' -> 5')-monophosphorothioat) (c[G(2',5')pS-DCIBI(3',5')pS]). Syntheseschritte: a) Pyridiniumtrifluoracetat / H20; b) ferf.-Butylamin; c) Dichloressigsäure / H20; d) A, Pyridin; e) 3-((N,N-dimethylaminomethylidene)amino)-3H-1 ,2,4-dithiazole-5-thione (DDTT); f) Dichloressigsäure / H20; g) 2-Chlor-5,5-dimethyl-1 ,3,2-dioxaphosphorinan-2-oxid; h) 3-1-1-1 ,2- Benzodithiol-3-οη; i) Methylamin / Ethanol; j) Triethylamintrihydrofluorid.
Beispiel 17.a. Synthese des H-Phosphonatzwischenproduktes 5'-OH-2'-TBDMS-3'-H- phosphonat-5,6-dichlorbenzimidazolribosid
P-OH
H
Das Phosphoramidit 5'-DMTr-2'-TBDMS-3'-CEP-5,6-dichlorbenzimidazolribosid (0,7 mmol) (BIOLOG GmbH, Bremen) wurde in 12 mL trockenem Acetonitril gelöst und mit 2 Äquivalenten Wasser sowie 1 ,2 Äquivalenten Pyridiniumtrifluoracetat versetzt und 15 min bei Raumtemperatur gerührt. Danach wurden die flüchtigen Bestandteile unter reduziertem Druck evaporiert. Anschließend wurden 100 Äquivalente ferf.-Butylamin zugegeben, die resultierende Lösung wurde für 30 min bei Raumtemperatur gerührt und wurde danach erneut unter reduziertem Druck evaporiert. Der Rückstand wurde in 30 mL Acetonitril gelöst und erneut unter reduziertem Druck evaporiert. Der resultierende Rückstand wurde in 20 mL Dichlormethan gelöst und 10 Äquivalente Wasser wurden zugegeben. Anschließend wurden 9 Äquivalente Dichloressigsäure aus einer 3 % igen Lösung von Dichloressigsäure in Dichlormethan zugegeben und die Lösung wurde 10 min bei Raumtemperatur gerührt. Nach dieser Periode wurden 18 Äquivalente Pyridin addiert und die Lösung wurde für 5 min bei Raumtemperatur gerührt. LC-MS-Analytik des Rohproduktes bestätigte die Anwesenheit des H- Phosphonatzwischenproduktes. Anschließend wurden die flüchtigen Bestandteile unter reduziertem Druck evaporiert und danach dreimal jeweils mit 10 mL trockenem Acetonitril gelöst und jeweils erneut unter reduziertem Druck evaporiert. Bei der letzten Evaporierung wurde nicht zur Trockene eingeengt, sondern das Rohprodukt in ca. 4 mL Acetonitril belassen um bei der nächsten Reaktion eingesetzt zu werden.
Beispiel 17.b. Synthese des linearen Dinukleotides 5'-OH-3'-TBDMS-N2-isobutyrylquanosin- (2'^5')-cvanoethyl-phosphorothioat-2'-TBDMS-3'-H-phosphonat-5,6- dichlorbenzimidazolribosid
Das Phosphoramidit 5'-DMTr-3'-TBDMS-2'-CEP-N2-isobutyrylguanosin (Chemgenes Inc., USA), 1 ,35 Äquivalente bezogen auf das nominelle H-Phosphonatzwischenprodukt (OJ mmol) aus Beispiel 17.a.) 5 wurde viermal jeweils in 12 mL trockenem Acetonitril gelöst und unter reduziertem Druck evaporiert. Bei der letzten Evaporierung wurde nicht zur Trockene eingeengt, sondern das Phosphoramidit in ca. 3 mL Acetonitril belassen. Die absolutierte Lösung wurde unter Argonschutzgas zum 5'-OH-2'- TBDMS-3'-H-phosphonat-5,6-dichlorbenzimidazolribosid aus Beispiel 17.a. gegeben und die resultierende Lösung wurde 15 min bei Raumtemperatur unter Argonschutzgas gerührt. Anschließend
10 wurden 1 ,1 Äquivalente 3-((N,N-dimethylaminomethylidene)amino)-3H-1 ,2,4-dithiazole-5-thione (DDTT) zugegeben und weitere 30 min bei Raumtemperatur unter Argonschutzgas gerührt. Nach Zwischenlagerung für 16 h bei -70 °C, wurden die flüchtigen Bestandteile der Mischung unter reduziertem Druck evaporiert und der Rückstand wurde in 20 mL Dichlormethan gelöst und 10Äquivalente Wasser wurden zugegeben. Danach wurde Dichloressigsäure in Dichlormethan (3 %;
15 18 Äquivalente) zugegeben und 20 min bei Raumtemperatur gerührt. Anschließend wurden 10 mL Pyridin zugegeben und weitere 10 min bei Raumtemperatur gerührt. LC-MS-Analytik des Rohproduktes bestätigte die Anwesenheit des linearen Dinukleotides 5'-OH-3'-TBDMS-N2- isobutyrylguanosin-(2'^5')-cyanoethyl-phosphorothioat-2'-TBDMS-3'-H-phosphonat-5,6- dichlorbenzimidazolribosid. Die flüchtigen Bestandteile der Mischung wurden unter reduziertem Druck
20 evaporiert und anschließend zweimal jeweils in 20 mL trockenem Pyridin gelöst und jeweils unter reduziertem Druck evaporiert. Der Rückstand wurde erneut in 30 mL trockenem Pyridin gelöst und auf ein Volumen von ca. 20 mL coevaporiert um in der nächsten Reaktion umgesetzt zu werden.
Beispiel 17.c. Synthese des zyklischen (3'-TBDMS-N2-isobutyrylquanosin-(2'— >5')-cvanoethyl- 25 phosphorothioat-2'-TBDMS-5,6-dichlorbenzimidazolribosid-(3'^5')-H-phosphonat)
2-Chlor-5,5-dimethyl-1 ,3,2-dioxaphosphorinan-2-oxicl (DMOCP; 3,5 Äquivalente bezogen auf das nominelle linearen Dinukleotides 5'-OH-3'-TBDMS-N2-isobutyrylguanosin-(2'— >5')-cyanoethyl- phosphorothioat-2'-TBDMS-3'-H-phosphonat-5,6-dichlorbenzimidazolribosid (0,7 mmol) aus Beispiel 17.b.) wurden unter Argonschutzgasatmosphäre zum Rohprodukt in Pyridin aus Beispiel 17.b. gegeben und 20 min bei Raumtemperatur unter Argonschutzgas gerührt. LC-MS-Analytik des Rohproduktes bestätigte die Anwesenheit des zyklischen Dinukleotides 3'-TBDMS-N2- isobutyrylguanosin-(2'^5')-cyanoethyl-phosphorothioat-2'-TBDMS-5,6-dichlorbenzimidazolribosid- (3'— >5')-H-phosphonat, welches sofort in Beispiel 17.d. weiter umgesetzt wurde.
Beispiel 17.d. Synthese des zyklischen (3'-TBDMS-N2-isobutyrylquanosin-(2'^5')-cvanoethyl- phosphorothioat-2'-TBDMS-5,6-dichlorbenzimidazolribosid-(3'^5')-monophosphorothioat)
Zum Rohprodukt aus Beispiel 17.c. wurden 3H-1 ,2-Benzodithiol-3-on (1 ,5 Äquivalente) und Wasser (35 Äquivalente) gegeben und die Mischung wurde 30 min bei Raumtemperatur gerührt. Danach
wurden der Rohlösung 3.3 g NaHC03 in 120 mL Wasser zugegeben und weitere 5 min gerührt. Nun wurde die wässrige Phase dreimal mit Ethylacetat / Methyl-ferf.-Butylether (1 :1 (v:v);1 x 120 mL, 2 x 60 mL) ausgeschüttelt. Die kombinierten organischen Phasen wurden über MgS04 getrocknet und danach unter reduziertem Druck evaporiert. LC-MS-Analytik des Rohproduktes bestätigte die Anwesenheit des zyklischen Dinukleotides 3'-TBDMS-N2-isobutyrylguanosin-(2'^5')-cyanoethyl- phosphorothioat-2'-TBDMS-5,6-dichlorbenzimidazolribosid-(3'^5')-monophosphorothioat. Der Rückstand wurde zweimal mit 50 mL Toluol coevaporiert und über Nacht im Hochvakuum getrocknet. Das Rohprodukt wurde in einer minimalen Menge Dichlormethan gelöst und mittels präparativer Flashchromatographie an Kieselgel mit einem Methanol / Dichlormethan-Gradienten aufgereinigt. Produkthaltige Fraktionen wurden unter reduziertem Druck evaporiert und in Beispiel 17.e. weiter umgesetzt
Beispiel 17.e. Synthese des zyklischen (3'-TBDMS-quanosin-(2' -> 5')-monophosphorothioat-2 - TBDMS-5,6-dichlorbenzimidazolribosid-(3' -> 5')-monophosphorothioat)
Das zyklische Dinukleotid 3'-TBDMS-N2-isobutyrylguanosin-(2'^5')-cyanoethyl-phosphorothioat-2'- TBDMS-5,6-dichlorbenzimidazolribosid-(3'^5')-monophosphorothioat aus Beispiel 17.d. wurde unter Argonschutzgasatmosphäre mit einem Überschuß von 33 % Methylamin in absolutem Ethanol (150 mL) versetzt und unter Argonschutzgas für 4 h bei Raumtemperatur gerührt. Anschließend wurden die flüchtigen Bestandteile der Mischung unter reduziertem Druck evaporiert und 16 h im Hochvakuum getrocknet. LC-MS-Analytik des Rohproduktes bestätigte die Anwesenheit der Zielverbindung. Das resultierende Rohprodukt vom zyklischen 3'-TBDMS-guanosin-(2' -> 5')-monophosphorothioat-2'- TBDMS-5,6-dichlorbenzimidazolribosid-(3' -> 5')-monophosphorothioat wurde im Beispiel 17.f. weiter umgesetzt.
Beispiel 17.f. Synthese des zyklischen (Guanosin-(2' -> 5')-monophosphorothioat - 5,6- dichlorbenzimidazolribosid-(3' -> 5')-monophosphorothioat) (crG(2',5')pS-DCIBI(3',5')pSl)
Das zyklische Dinukleotid 3'-TBDMS-guanosin-(2' -> 5')-monophosphorothioat-2'-TBDMS-5,6- dichlorbenzimidazolribosid-(3' -> 5')-monophosphorothioat aus Beispiel 17.e. wurde unter Argonschutzgasatmoshäre in einer Mischung aus trockenem Pyridin und trockenem Triethylamin (2:1 ; (v:v), 60 ml_) gelöst und unter reduziertem Druck aufkonzentriert auf ca. 10 ml_. Anschließend wurden 50 Äquivalente Triethylamintrihydrofluorid und 17 ml_ trockenes Triethylamin unter Argonschutzgasatmosphäre simultan zugegeben und die resultierende Lösung wurde unter Argonschutz 4 h bei 55 °C gerührt. Danach wurde die Mischung auf Raumtemperatur abgekühlt und überschüssiges Triethylamintrihydrofluorid wurde durch Zugabe von 15 ml_ Methoxytrimethylsilan gefolgt von weiterem Rühren für 30 min bei Raumtemperatur abgefangen. LC-MS-Analytik des Rohproduktes bestätigte die Anwesenheit der Zielverbindung. Nach dieser Zeit wurden alle flüchtigen Bestandteile der Mischung unter reduziertem Druck evaporiert. Der Rückstand wurde weitere 16 h im Hochvakuum getrocknet. Das resultierende Rohprodukt vom zyklischen (Guanosin-(2' -> 5')- monophosphorothioat - 5,6-dichlorbenzimidazolribosid-(3' -> 5')-monophosphorothioat) wurde mit Wasser suspendiert, im Ultraschallbad behandelt und die wässrige Phase dreimal mit Chloroform ausgeschüttelt. Nach anschließendem Filtrieren wurde das Rohprodukt verdünnt und an einem Q Sepharose™ Fast Flow Anionentauscher mit einem Triethylammoniumbicarbonat-Gradienten aufgereinigt. Die produkthaltigen Fraktionen wurden unter reduziertem Druck evaporiert und die beiden Hauptisomeren der Zielverbindung wurden danach mit präparativer Reversed Phase Chromatographie (RP-18) mit einem geeignetem Acetonitril / 20 mM Triethylammoniumformiat- Laufmittel hochgereinigt. Dabei eluiert Hauptisomer 1 (HI1 ) schneller von in der Reversed Phase Chromatographie als Hauptisomer 2 (HI2). Dabei sind HI1 und HI2 diejenigen Isomerfraktionen der jeweiligen Verbindung, denen die prozentual dominantesten HPLC-Signale dieser Verbindung zuzuordnen sind. Diese Definition für Hauptisomer 1 und Hauptisomer 2 gilt analog auch für andere Verbindungen in diesem Text.
Die Entsalzung der beiden Hauptisomeren der Zielverbindung erfolgte ebenfalls mit praparativer Reversed Phase Chromatographie (RP-18) und die entsalzten Hauptisomeren der Zielverbindung lagen anschliessend als Triethylammoniumsalz vor.
Die Natriumsalze der Hauptisomeren der Zielverbindung wurde mittels Passage einer verdünnten Produktlösung durch einen SP Sepharose™ Fast Flow Kationentauscher (Na+-Form) erhalten.
crG(2'.5')pS-DCIBI(3'.5')pSl: 2'.5'/3,.5' C22H23CI2N7O11 P2S2; MW 758,4 (freie Säure)
Hauptisomer 1 (schneller eluierendes Isomer),
(crG(2'.5')pS-DCIBI(3'.5')pSl.HI1)
UV: max: 256 nm, ε 17850
ESI-MS (+): m/z 758 [M + H] +
ESI-MS (-): m/z 756 [M - H] "
31 P{1 H} NMR (162 MHz, D20) δ 56,29 (s, 1 P),
56,05 (s, 1 P).
Hauptisomer 2 (langsamer eluierendes Isomer),
(crG(2'.5')pS-DCIBI(3'.5')pSl.HI2)
UV: max: 256 nm, ε 17850
ESI-MS (+): m/z 758 [M + H] +
ESI-MS (-): m/z 756 [M - H] "
31 P{1 H} NMR (162 MHz, D20) δ 55.90 (s, 1 P),
52,02 (s, 1 P).
In Anlehnung an Beispiel 17.a.-17.f. wurden die nachfolgenden Beispiele 17G bis 17N hergestellt: Beispiel 17G: zyklisches (Guanosin-(2' -> 5')-monophosphorothioat - benzimidazolribosid-(3'
-> 5')-monophosphorothioat), (crG(2',5')pS-BI(3',5')pSl), Hauptisomer 1 und Hauptisomer 2. crG(2'.5')pS-BI(3'.5')pSl: 2'.5'/3,.5'
C22H25N7O11 P2S2; MW 689,6 (freie Säure)
Hauptisomer 1 (schneller eluierendes Isomer),
(crG(2'.5')pS-BI(3'.5')pSl.HI1)
UV: Xmax: 252 nm, ε 17850
ESI-MS (+): m/z 690 [M + H] +
ESI-MS (-): m/z 688 [M - H] "
Hauptisomer 2 (langsamer eluierendes Isomer),
(crG(2'.5')pS-BI(3'.5')pSl.HI2)
UV: Xmax: 252 nm, ε 17850
ESI-MS (+): m/z 690 [M + H] +
ESI-MS (-): m/z 688 [M - H] "
Beispiel 17H : zyklisches (Adenosin-(3' -> 5')-monophosphorothioat - benzimidazolribosid-(2' -> 5')-monophosphorothioat), (crA(3',5')pS-BI(2',5')pSl), Hauptisomer 1 und Hauptisomer 2. crA(3'.5')pS-BI(2'.5')pSl: 3 ,5'/2',5'
C22H25N7O10P2S2; MW 673,6 (freie Säure)
Hauptisomer 1 (schneller eluierendes Isomer),
(crA(3'.5')pS-BI(2'.5')pSl.HI1)
UV: Xmax: 253 nm, ε 17600 ESI-MS (+): m/z 674 [M + H] +
ESI-MS (-): m/z 672 [M - H] "
Hauptisomer 2 (langsamer eluierendes Isomer),
(crA(3'.5')pS-BI(2'.5')pSl.HI2)
UV: max: 253 nm, ε 17600 ESI-MS (+): m/z 674 [M + H] + ESI-MS (-): m/z 672 [M - H] "
Beispiel 171: zyklisches (2'-Fluor-2'-deoxyadenosin-(3' -> 5')-monophosphorothioat - benzimidazolribosid-(2' -> 5')-monophosphorothioat). (cr2'-F-dA(3',5')pS-BI(2',5')pSl). Hauptisomer 1 und Hauptisomer 2. cr2'-F-dA(3'.5')pS-BI(2'.5')pSl : 3',572',5'
C22H24FN709P2S2; MW 675,5 (freie Säure)
Hauptisomer 1 (schneller eluierendes Isomer),
(cr2'-F-dA(3'.5')pS-BI(2'.5')pSl.HI1)
UV: λΠ3Χ: 253 nm, ε 17600
ESI-MS (+): m/z 676 [M + H] +
ESI-MS (-): m/z 674 [M - H] "
Hauptisomer 2 (langsamer eluierendes Isomer),
(cr2'-F-dA(3'.5')pS-BI(2'.5')pSl.HI2)
UV: λΠ3Χ: 253 nm, ε 17600
ESI-MS (+): m/z 676 [M + H] +
ESI-MS (-): m/z 674 [M - H] "
Beispiel 17J: zyklisches (5.6-Dichlorbenzimidazolribosid-(2' -> 5')-monophosphorothioat - 5.6- dichlorbenzimidazolribosid-(3' -> 5')-monophosphorothioat). (crDCIBire'.S'toS-DCIBiP'.S^pSl). Hauptisomer 1 und Hauptisomer 2.
οΓΡΟΙΒΙ^'.δΊρβ-ΡΟΙΒΙΟ'.ΰΊρβΙ^'.δ'/Β'.δ'
C24H22Cl4N4O10P2S2; MW 794,3 (freie Säure)
Hauptisomer 1 (schneller eluierendes Isomer),
(crPCIBIte'.S'toS-PCIBIß'.S'toSl.HII)
UV: Xmax: 254 nm, ε 12950
ESI-MS (+): m/z 795 [M + H] +
ESI-MS (-): m/z 793 [M - H] "
Hauptisomer 2 (langsamer eluierendes Isomer),
(0ΓΡ0ΙΒΙ(2'.5')Ρ5-Ρ0ΙΒΙ(3'.5')Ρ51.ΗΙ2)
UV: Xmax: 254 nm, ε 12950
ESI-MS (+): m/z 795 [M + H] +
ESI-MS (-): m/z 793 [M - H] "
Beispiel 17K: zyklisches (Adenosin-(2' -> 5')-monophosphorothioat - 5,6- dichlorbenzimidazolribosid-(3' -> 5')-monophosphorothioat), (crA(2',5')pS-PCIBI(3',5')pSl), Hauptisomer 1 und Hauptisomer 2. crA(2'.5')pS-PCIBI(3'.5')pSl: 2',5,/3,,5'
C22H23CI2N7O10P2S2; MW 742,4 (freie Säure)
Hauptisomer 1 (schneller eluierendes Isomer),
(crA(2'.5')pS-PCIBI(3'.5')pSl.HI1)
UV: Xmax: 260 nm, ε 19400
ESI-MS (+): m/z 742 [M + H] +
ESI-MS (-): m/z 740 [M - H] "
Hauptisomer 2 (langsamer eluierendes Isomer),
(crA(2'.5')pS-PCIBI(3'.5')pSl.HI2)
UV: Xmax: 260 nm, ε 19400
ESI-MS (+): m/z 742 [M + H] +
ESI-MS (-): m/z 740 [M - H] "
Beispiel 17L: zyklisches (2'-Fluor-2'-deoxyadenosin-(3' -> 5')-monophosphorothioat - 5,6- dichlorbenzimidazolribosid-(2' -> 5')-monophosphorothioat), (cr2'-F-dA(3',5')pS- DCIBI(2',5')pSl), Hauptisomer 1 und Hauptisomer 2. cr2'-F-dA(3'.5')pS-DCIBI(2'.5')pSl: 3'.5,/2,.5'
C22H22CI2FN709P2S2; MW 744,4 (freie Säure)
Hauptisomer 1 (schneller eluierendes Isomer),
(cr2'-F-dA(3'.5')pS-DCIBI(2'.5')pSl.HI1)
UV: max: 260 nm, ε 19400
ESI-MS (+): m/z 745 [M + H] +
ESI-MS (-): m/z 743 [M - H] "
Hauptisomer 2 (langsamer eluierendes Isomer),
(cr2'-F-dA(3'.5')pS-DCIBI(2'.5')pSl.HI2)
UV: max: 260 nm, ε 19400
ESI-MS (+): m/z 745 [M + H] +
ESI-MS (-): m/z 743 [M - H] "
Beispiel 17M: zyklisches (Adenosin-(3' -> 5')-monophosphorothioat - 5,6- dichlorbenzimidazolribosid-(2' -> 5')-monophosphorothioat), (crA(3',5')pS-DCIBI(2',5')pSl), Hauptisomer 1 und Hauptisomer 2. crA(3'.5')pS-DCIBI(2'.5')pSl: 3',5,/2,,5'
C22H23CI2N7O10P2S2; MW 741 (freie Säure)
Hauptisomer 1 (schneller eluierendes Isomer),
(crA(3'.5')pS-DCIBI(2'.5')pSl.HI1)
UV: max: 260 nm, ε 19400
ESI-MS (+):m/z742 [M + H] +
ESI-MS (-):m/z741 [M - H] "
Hauptisomer 2 (langsamer eluierendes Isomer),
(crA(3'.5')pS-DCIBI(2'.5')pSl.HI2)
UV: max: 260 nm, ε 19400
ESI-MS (+):m/z742 [M + H] +
ESI-MS (-):m/z741 [M - H] "
Beispiel 17N: zyklisches (Adenosin-(2' -> 5')-monophosphorothioat - benzimidazolribosid-(3'
-> 5')-monophosphorothioat), (crA(2',5')pS-BI(3',5')pSl), Hauptisomer 1 und Hauptisomer 2. crA(2'.5')pS-BI(3'.5')pSl:2',5,/3,,5'
C22H25N7O10P2S2; MW 673,1 (freie Säure)
Hauptisomer 1 (schneller eluierendes Isomer),
(crA(2'.5')pS-BI(3'.5')pSl.HI1)
UV: max: 253 nm, ε 17600
ESI-MS (+):m/z674 [M + H] +
ESI-MS (-):m/z672 [M - H] "
Hauptisomer 2 (langsamer eluierendes Isomer),
(crA(2'.5')pS-BI(3'.5')pSl.HI2)
UV: max: 253 nm, ε 17600
ESI-MS (+):m/z674 [M + H] +
ESI-MS (-):m/z672 [M - H] "
Beispiel 18: Lipophilie-Messunqen der erfindunqsqemäßen CDNs mittels Gradienten-HPLC
Obwohl der allgemein akzeptierte Indikator für die zu erwartende Fähigkeit einer chemischen Verbindung, zelluläre Membranen durch passive Diffusion zu überwinden, der Oktanol/Wasser Koeffizient Log P ist, ist seine praktische Bestimmung für sehr polare Substanzen wie mehrfach geladene Nukleotide schwierig. Oft muss daher ein Hinweis über die Membrangängigkeit durch Fragmentanalysen oder Berechnungen erhalten werden. Aus diesem Grund wurde hier eine etablierte HPLC-Methode eingesetzt, die auf der Messung der Retention auf einer Reversed Phase-Säule beruht7. Im Gegensatz zu Log P liefert die Methode den Indikator log k'g, der eine Einordnung verschiedener Nucleotide mit gleicher Ladung nach ihrer Lipophilie ermöglicht. Da CDNs zweifach negativ geladene Moleküle sind, die auf einer Reversed Phase-HPLC-Säule nur sehr unzureichend retardiert werden, wurden die Messungen mit dem lipophilen Triethylammoniumkation durchgeführt (lonenpaar-Chromatografie). Zur Lipophiliebestimmung wurde entsprechend etablierter Methode HPLC-Gradient 1 benutzt7.
Unmodifizierte CDNs, wie c-diAMP (log k'g 0,991 ), c-diGMP (log k'g 0,840) oder 2',3'-cGAMP (log k'g 0,766 (Tabelle 2) zeigten hier sehr polares Verhalten und es erscheint sehr unwahrscheinlich, dass sie zelluläre Membranen durch passive Diffusion durchdringen können.
Die erfindungsgemäßen CDNs mit mindestens einer Benzimidazol-Nukleobase besitzen dagegen erheblich höhere Lipophilie und zeigten daher in diesem Meßsystem entsprechend erheblich höhere Retentionszeiten und damit auch sehr hohe log k'g-Werte wie beispielhaft für 1 1 neue, erfindungsgemäße CDNs in Tabelle 2 gezeigt ist.
Die Substitution eines Sauerstoffs im Phosphat-Teil der erfindungsgemäßen CDNs durch Schwefel oder Boran erhöht die Lipophilie noch weiter, sodass die Phosphorothioat- und vor allem die Boranophosphat-Analoga der Benzimidazol-CDNs um Größenordnungen lipophiler als ihre Stammverbindungen sind. Substitutionen in Position 4, 5, 6 und 7 am 6-Ring und in Position 2 des Imidazolteils vom Benzimidazol-Grundgerüsts erhöhen in aller Regel ebenfalls die Lipophilie.
Tabelle 2: HPLC-Retentionszeiten und Lipophiliewerte (log k'g) neuer, erfindungsgemäßer CDNs.
# Verbindung HPLC- HPLC- log k'g
Retentionszeit Retentionszeitt
Gradient 1 Gradient 2
Thioharnstoff 2,567 2,813
c-diGMP 12,520 11 ,700 0,840 c-diAMP 14,280 13,187 0,991
2',3'-cGAMP 1 1 ,647 11 ,440 0,766
7 c[DCIBI(3',5')pDCIBI(3',5')p] 37,400 34,227 2,970
1 c[BI(3',5')pBI(3',5')p] 22,933 20,687 1 ,732
98.HI1 c[A(3',5')pS-BI(2',5')pS],HI1 20,507 19,880 1 ,524
98.HI2 c[A(3',5')pS-BI(2',5')pS],HI2 21 ,207 20,793 1 ,584
79 c[2'-F-dA(3',5')pBI(3',5')p] 18,153 16,760 1 ,322
81 c[2'-F-dA(3',5')pDCIBI(3',5')p] 26,520 24,873 2,039
23,1-111 c[G(2',5')pS-BI(3',5')pS],HI 1 20,327 20,673 1 ,509
23.HI2 c[G(2',5')pS-BI(3',5')pS],HI2 22,393 22,687 1 ,658
85 c[2'-F-dl(3',5')pBI(3',5')p] 16,847 16,280 1 ,21 1
29.HI1 c[G(2',5')pS-DCIBI(3',5')pS],HI1 29,780 29,740 2,318
29.HI2 c[G(2',5')pS-DCIBI(3',5')pS],HI2 30,773 31 ,027 2,403
Biologische Beispiele
Beispiel 19: Bestimmung der nach Gabe der erfindunqsqemäßen CDNs durch STING induzierten Dimerisierung von IRF3, der durch STING induzierten Phosphorylierung von IRF3 und der durch STING induzierten Phosphorylierung von TBK1
Zelllinie: THP-1 Zellen (Sigma Katalognummer 88081201 -1 VL) wurden aus dem peripheren Blut eines einjährigen männlichen Patienten mit akuter Leukämie isoliert.
Nach Gabe eines erfindungsgemäßen CDNs oder einer Pufferkontrolle zu THP1 -Zellen in der Kulturschale wird ein Zelllysat dargestellt, das zu einem Teil auf ein natives Polyacrylamidgel und zu einem Teil auf zwei denaturierende Polyacrylamidgele (SDS-PAGE) aufgetragen wird. Die entwickelten Gele werden mit der Western Blot Technik analysiert. Im Falle des nativen Geles wird ein IRF3 Antikörper verwendet. In der Pufferkontrolle wird eine einzelne Bande detektiert, die ein Laufverhalten entsprechend des Molekulargewichtes von IRF3 zeigt. Die Gabe des erfindungsgemäßen CDNs führt zur Ausbildung einer zweiten Bande deren Laufverhalten dem doppelten Molekulargewicht von IRF3 entspricht. Bei dieser Bande handelt es sich um das durch das erfindungsgemäße CDN induzierte Dimer. Für die beiden denaturierenden Gele wird entweder ein Antikörper gegen phosphoryliertes IRF3 eingesetzt oder gegen phosphoryliertes TBK1 . In der Pufferkontrolle wird jeweils eine sehr schwache Bande detektiert. Diesen Banden nehmen in ihrer Intensität nach Gabe des erfindungsgemäßenen CDNs stark zu. Die Zunahme der Intensitäten gibt die durch das erfindungsgemäße CDN induzierte Phosphorylierung von IRF3 beziehungsweise TBK1 wieder. Die Dimerisierung von IRF3, sowie die untersuchten Phosphorylierungen sind eine direkte Folge der Aktivierung von STING.
Die beispielhaft getesteten Verbindungen 4, 1 1 , 29 und 30 (siehe Tabelle 1 , oben) aus der Gruppe der erfindungsgemäßen CDNs liefern positive Ergebnisse in diesem Assay.
Beispiel 20: Bestimmung der nach Gabe der erfindungsgemäßen CDNs durch STING induzierten Aktivität mit Hilfe eines Interferon-ß-Promotor-Reporter-Konstruktes
Zelllinie: THP1 -Blue™ Zellen (InvivoGen, Katalognummer: thp-isg), sind von THP-1 Zellen abgeleitet. THP1 -Blue™ Zellen wurden durch Gabe eines erfindungsgemäßen CDNs oder einer Pufferkontrolle in der Kulturschale stimuliert. In diesen genetisch modifizierten Zellen findet sich das Gen für secreted embryonal alkaline Phosphatase (SEAP) unter der Kontrolle eines Interferon-ß-Promotors. Nach der Stimulation der Zellen mit einem erfindungsgemäßen CDN wurde der Überstand der Kultur abgenommen und die enzymatische Aktivität der SEAP in einem kolorimetrischen Assay photometrisch durch Messung der Extinktion bei 625 nm (Optische Dichte; OD 625 nm) bestimmt. Die Gabe des erfindungsgemäßen CDNs induzierte eine Zunahme der gemessenen Aktivität der SEAP, die ein Maß der Aktivität des STING Signalweges darstellt.
Die beispielhaft getesteten Verbindungen 23,HI2; 29,HI2; 79; 81 ; 98,1-111 lieferten konzentrationsabhängig (0 μg/mL; 10 μg/mL; 20 μg/mL; 40 μg/mL) positive Ergebnisse in diesem
Assay in Form erhöhter OD bei 625 nm und zeigten um bis zu Faktor >10 erhöhte SEAP-Aktivitäten im Vergleich zu den Kontrollsubstanzen 3'3'-cGAMP und c-diAMP (siehe Figur 1 ).
Dieser Effekt der erhöhten OD bei 625 nm wurde in Zellen, aus denen STING genetisch entfernt wurde (knock out; STING KO), nicht mehr beobachtet, wie beispielhaft mit den Verbindungen 29,HI2; 79; 98,HI1 (jeweils in einer Konzentration von 40 μg/mL eingesetzt) in einem Vergleichsexperiment mit THP1 -Blue™ Zellen und mit THP1 Dual™ KO STING Zellen (InvivoGen, Katalognummer: thpd- kostg) gezeigt (siehe Figur 2).
Beispiel 21 : Bestimmungen der Mengen der nach Gabe der erfindunqsqemäßen CDNs gebildeten mRNA für Interferon α und ß
Zelllinie: THP-1 Zellen (Sigma Katalognummer 88081201 -1 VL) wurden aus dem peripheren Blut eines einjährigen männlichen Patienten mit akuter Leukämie isoliert.
THP1 Zellen werden durch Gabe eines erfindungsgemäßen CDNs oder einer Pufferkontrolle in der Kulturschalte stimuliert. Nach der Stimulation wird die mRNA aus den Zellen isoliert und mit Hilfe des Enzyms Reverse Transkriptase in cDNA umgesetzt. Die relative Konzentration der nach der Gabe eines erfindungsgemäßen CDNs von der jeweils für Interferon α und ß codierenden RNA erhaltenen cDNA im Vergleich zur Pufferkontrolle wird mit Hilfe von quantitativer PCR bestimmt. Die Gabe eines erfindungsgemäßen CDNs führt zu einer Zunahme der Bildung von für Interferon α und ß codierende mRNA. Dieser Effekt wird in Zellen, aus denen STING genetisch entfernt wurde (knock out), nicht mehr beobachtet.
Die beispielhaft getesteten Verbindungen aus Beispiel 19 liefern positive Ergebnisse in diesem Assay.
Beispiel 22: Bestimmungen der Mengen des nach Gabe der erfindungsgemäßen CDNs sekretierten Interferons ß
Zelllinie: THP-1 Zellen (Sigma, Katalognummer 88081201 -1 VL) wurden aus dem peripheren Blut eines einjährigen männlichen Patienten mit akuter Leukämie isoliert. Bei HEK293 handelt es sich um eine Zelllinie, die aus menschlicher embryonaler Niere dargestellt wurde.
THP1 Zellen und HEK293 Zellen, in denen STING künstlich zur Expression gebracht wurde, werden durch die Gabe eines erfindungsgemäßen CDNs oder einer Pufferkontrolle stimuliert. Nach der Stimulation wird das Kulturmedium abgenommen und die Menge des durch die Zellen in das Medium sekretierten Interferons ß mit Hilfe eines enzymatisch gekoppelten Immunotestes (enzymatic linked immunoassay, ELISA) bestimmt. Hierzu wird das System„Human IFN-beta ELISA Kit" (R&D Systems, Katalognummer 41410) gemäß der Angaben des Herstellers eingesetzt. Die Gabe eines erfindungsgemäßen CDNs führt zu einem deutlichen Anstieg der nachweisbaren Menge an Interferon ß.
Die beispielhaft getesteten Verbindungen aus Beispiel 19 liefern positive Ergebnisse in diesem Assay.
Beispiel 23: Bestimmung der Affinität der Interaktion der erfindungsgemäßen CDNs und STING durch Isothermal Titration Calorimetry (ITC).
Konstrukte von humanem STING werden als GST-Fusions-Proteine in Bakterien zur Expression gebracht. Die Aufreinigung unter proteolytischer Abspaltung des GST-tags erfolgt mit Hilfe von Affinitätschromatographie und Größenausschlusschromatographie. STING-Lösungen mit einer Konzentration von bis zu 200 μΜ werden in der Messzelle vorgelegt und mit einem erfindungsgemäßen CDN in identischer Pufferlösung titriert. Die während der Titration erhaltenen Wärmetönungen zeigen eindeutig eine Interaktion des erfindungsgemäßen CDNs mit STING. Die bestimmten Affinitäten liegen in derselben Größenordnung wie die der natürlichen zyklischen Nukleotide oder übertreffen diese.
Die beispielhaft getesteten Verbindungen aus Beispiel 19 liefern positive Ergebnisse in diesem Assay.
Abkürzunasverzeichnis
TRIS-HCI Tris(hydroxymethyl)aminomethan,hydrochlorid
DMSO Dimethylsulfoxid
UV Ultraviolett
ε Extinktionskoeffizient
^max Wellenlänge des Absorptionsmaximums
FtP-18 reversed phase octadecyl-modifiziertes Kieselgel
DMTr Dimethoxytrityl
TBDMS Tertiärbutyl-dimethylsilyl
CEP 0-Cyanoethyl-/V,/V-diisopropylphosphoramidit
HEPES 4-(2-Hydroxyethyl)-1 -piperazinoethansulfonsäure
HPLC high Performance liquid chromatography
MW Molekulargewicht
m/z Masse zu Ladungs-Quotient
NHS /V-Hydroxysuccinimid
Bz Benzoyl
/Bu Isobutyryl
tert tertiär
Literatur
1. Urata, H. ; Fujimori, M. ; Aono, C; Yamakawa, T.; Harada, E.; Akagi, M., Regio- and diastereo- selectivity of montmorillonite-catalyzed oligomerization of racemic adenosine 5'-phosphorimidazolide.
Nucleosides Nucleotides Nucleic Acids 2008, 27 (4), 421 -30.
2. Mehne, F. M. ; Schroder-Tittmann, K. ; Eijlander, R. T. ; Herzberg, C ; Hewitt, L.; Kaever, V. ; Lewis, R. J.; Kuipers, O. P. ; Tittmann, K. ; Stulke, J., Control of the diadenylate cyclase CdaS in Bacillus subtilis: an autoinhibitory domain limits cyclic di-AMP production. J Biol Chem 2014, 289 (30), 21098-107.
3. Li, L ; Yin, Q.; Kuss, P. ; Maliga, Z. ; Millan, J. L ; Wu, H. ; Mitchison, T. J., Hydrolysis of 2'3'- cGAMP by ENPP1 and design of nonhydrolyzable analogs. Nat Chem Biol 2014, 70 (12), 1043-8.
4. Gaffney, B. L.; Veliath, E.; Zhao, J. ; Jones, R. A., One-flask syntheses of c-di-GMP and the [Rp,Rp] and [Rp,Sp] thiophosphate analogues. Org Lett 2010, 72 (14), 3269-71 .
5. Gao, P. ; Ascano, M.; Wu, Y. ; Barchet, W.; Gaffney, B. L.; Zillinger, T. ; Serganov, A. A.; Liu, Y.; Jones, R. A. ; Hartmann, G.; Tuschl, T. ; Patel, D. J., Cyclic [G(2',5')pA(3',5')p] is the metazoan second messenger produced by DNA-activated cyclic GMP-AMP synthase. Ce// 2013, 753 (5), 1094-107. 6. Parsch, J. ; Engels, J. W., C-F...H-C hydrogen bonds in ribonucleic acids. J Am Chem Soc 2002, 724 (20), 5664-72.
7. Krass, J. D. ; Jastorff, B.; Genieser, H. G., Determination of lipophilicity by gradient elution high-performance liquid chromatography. Anal Chem 1997, 69 (13), 2575-81 .
8. Margolin A. L.; Borcherding D. R. ; Wolf-Kugel D. ; Margolin N., AMP deaminase as a novel practical catalyst in the synthesis of 6-oxopurine ribosides and their analogs. J. Org. Chem. 1994, 59(24), 7214-7218.
Claims
Ansprüche
Verbindung der Formel (I)
(I)
in der der mit * markierte O als R6 oder R7 und der mit ** markierte O als R8 oder R9 verknüpft ist; und in der R^
H, Cl, Br, I, F, N3, N02, OH, SH, NH2, CF3, Alkyl, Aryl, Aralkyl, Acyl, Aracyl, S-alkyl, S-aryl, S-aralkyl, S-acyl, S-aracyl, S(0)-alkyl, S(0)-aryl, S(0)-aralkyl, S(0)-acyl, S(0)-aracyl, S(0)2-alkyl, S(0)2-aryl, S(0)2-aralkyl, S(0)2-acyl, S(0)2-aracyl, NR13R14 (wobei R13 und R14 unabhängig voneinander H, Alkyl, Aryl oder Aralkyl sein können), 2-Furyl, 3-Furyl, 2-Brom-5-Furyl, (2-Furyl)thio, (3-(2-Methyl)furyl)thio, (3-Furyl)thio, 2-Thienyl, 3-Thienyl, (5-(1 -Methyl)tetrazolyl)thio, 2-(N-(7-Nitrobenz-2-oxa-1 ,3-diazol-4- yl)amino)ethylthio, (4-Bromo-2,3-dioxobutyl)thio, [2-[(Fluoresceinylthioureido)amino]ethyl]thio, (7-(4- Methyl)coumarinyl)thio, (4-(7-Methoxy)coumarinyl)thio, (2-Naphtyl)thio, 4-Pyridyl, (4-Pyridyl)thio, 2- Pyridylthio, 5-Amino-3-oxopentylamino, 8-Amino-3,6-dioxaoctylamino, 19-Amino-4J, 10, 13,16- pentaoxanonadecylamino, 17-Amino-9-aza-heptadecylamino, 4-(N-
Methylanthranoyl)aminobutylamino, Dimethylamino, Diethylamino, 4-Morpholino, 1 -Piperidino oder 1 -Piperazino ist
oder der Rest R^ ist wie in den folgenden Gruppen 1 oder 2 definiert:
wobei
m = 0 - 6;
Q = S, S(O), S(0)2, O, NH, CH2 oder C(O) ist;
X X2 und X3 sind jeweils unabhängig voneinander H, OH, NH2, N3, SH, CN, N02, F, Cl, Br,
I, (CH2)nCH3 (mit n = 0-5), /'-Pr, f-Bu, (C H2)nC=CH (mi{ n = (CH2)nCH=CH2 (mit n = 0- 5), CH2OH, (CH2)nOCH3 (mit n = 1 -2), CH2N(CH3)2, 0(CH2)nCH3 (mit n = 0-5), 0/-Pr, OCy,
OCyp, OBn, OC(0)CH3, OC(0)Ph, OCF3, N(CH3)2, NH(CH2)nCH3 (mit n = 0-5),
NHC(0)f-Bu, NHC(0)Ph, NHC(0)Of-Bu, NHC(0)CH3, NHC(0)CH2N3, B(OH)2, CF3,
C(0)OH, C(0)OCH3, C(0)0/-Pr, C(0)Of-Bu, C(0)OPh, C(0)OBn, C(0)NH2, C(0)N(CH3)2,
C(0)NHPh, C(0)NHBn, C(0)CF3, CH2C(0)OH, CH2C(0)OCH3, CH2C(0)0/'-Pr,
CH2C(0)Of-Bu, CH2C(0)OBn, S(CH2)nCH3 (mit n = 0-5), S(CH2)nOEt (mit n = 1 -4), SBn,
S02CH3, S02CF3, ' = (mit = H, SH, CN, Ph, F, CH3, OCH3, SCH3, 4-Thiophenyl,
N02, Pentyl), ' \= (mit Y2 = H, SH, F), 1 \=/ (mit Y3 = H, SH), ' , oder
H
wobei
m = 0 - 6;
n = 1 - 6;
Q = S, S(O), S(0)2, O oder NH ist;
Ft2 ist H, F, Cl, Br, NH2, N02, CN, CH3, OH, CF3, SH, 0-CH3, OCF3, N(CH3)2, S-CH3 oder C(0)OH;
R3 ist H, F, Cl, Br, NH2, N02, CN, CH3, OH, CF3, SH, 0-CH3, OCF3, N(CH3)2, S-CH3 oder C(0)OH;
R4 ist H, F, Cl, Br, NH2, N02, CN, CH3, OH, CF3, SH, 0-CH3, OCF3, N(CH3)2, S-CH3 oder C(0)OH; R5 ist H, F, Cl, Br, NH2, N02, CN, CH3, OH, CF3, SH, 0-CH3, OCF3, N(CH3)2, S-CH3 oder C(0)OH;
R6 oder R7 ist H, OH, NH2, F, 0-CH3, S-CH3, OCH2CEC, OCH2CH=CH2, O-Acyl, O-Aracyl, 0-C(0)NH- (CH2)6NH2 oder O- (Ν'- methylanthraniloyl)wobei der andere Rest R6 oder R7 die Verknüpfung in dem mit * markierten O darstellt.
R8 oder R9 ist H, OH, NH2, F, 0-CH3, S-CH3, OCH2CEC, OCH2CH=CH2,0-Acyl, O-Aracyl, 0-C(0)NH- (CH2)6NH2 oder, O- (Ν'- methylanthraniloyl), wobei der andere Rest R8 oder R9 die Verknüpfung in dem mit ** markierten O darstellt.
R10 ist OH, SH, borano (BH3), S-PAS, O-PAS, S-BAS oder O-BAS,
wobei PAS eine photo-aktivierbare Schutzgruppe ist, vorzugsweise o-Nitro-benzyl, 1 - (o-Nitrophenyl)-ethylidene, 4,5-Dimethoxy-2-nitro-benzyl, 7-Dimethylamino-coumarin-
4-yl (DMACM-caged), 7-Diethylamino-coumarin-4-yl (DEACM-caged) and 6,7- Bis(carboxymethoxy)coumarin-4-yl)methyl (BCMCM-caged), und wobei BAS eine bio-aktivierbare Schutzgruppe ist, vorzugsweise Methyl, Acetoxymethyl, Pivaloyloxymethyl, Methoxymethyl, Propionyloxymethyl, Butyryloxymethyl, Cyanoethyl, Phenyl, Benzyl, 4-Acetoxybenzyl, 4-Pivaloyloxybenzyl, 4-lsobutyryloxybenzyl, 4-Octanoyloxybenzyl, 4-Benzoyloxybenzyl;
R ist OH, SH, borano (BH3), S-PAS, O-PAS, S-BAS oder O-BAS,
wobei PAS eine photo-aktivierbare Schutzgruppe ist, vorzugsweise o-Nitro-benzyl, 1 - (o-Nitrophenyl)-ethylidene, 4,5-Dimethoxy-2-nitro-benzyl, 7-Dimethylamino-coumarin- 4-yl (DMACM-caged), 7-Diethylamino-coumarin-4-yl (DEACM-caged) and 6,7- Bis(carboxymethoxy)coumarin-4-yl)methyl (BCMCM-caged),
und wobei BAS eine bio-aktivierbare Schutzgruppe ist, vorzugsweise Methyl, Acetoxymethyl, Pivaloyloxymethyl, Methoxymethyl, Propionyloxymethyl, Butyryloxymethyl, Cyanoethyl, Phenyl, Benzyl, 4-Acetoxybenzyl, 4-Pivaloyloxybenzyl, 4-lsobutyryloxybenzyl, 4-Octanoyloxybenzyl, 4-Benzoyloxybenzyl;
R12 ist
wobei RT bis R5 wie vorstehend beschrieben definiert sind.
2. Verbindung der Formel (I) nach Anspruch 1
R2, R3, R4 und R5 gleich oder verschieden zu dem anderen Rest mit gleichem Index sind.
3. Verbindung der Formel (I) nach einem der vorangegangenen Ansprüche, wobei
oder
R10 und/oder R BH3 ist
oder
Rio SH und RH BH3 oder Rio BH3 und R SH ist.
4. Verbindung der Formel (I) nach einem der vorangegangenen Ansprüche, wobei die Verknüpfungen über O* und O** als R7 und R8 ausgebildet sind und zu Verbindungen führen, die üblicherweise als 3',
5'-3', 5'-verknüpft bezeichnet werden.
5. Verbindung der Formel (I) nach einem der Ansprüche 1 bis 4, wobei die die Verknüpfungen über O* und O** als R6 and R8 ausgebildet sind und zu Verbindungen führen, die üblicherweise als 2', 5'-3', 5'- verknüpft bezeichnet werden.
6. Verbindung der Formel (I) nach einem der vorangegangenen Ansprüche, wobei R3 und R4 jeweils Cl sind
oder
Ri , R3 und R4 jeweils Cl sind
oder Ri CF3 ist und R3 und R4 jeweils Cl sind.
7. Verbindung der Formel (I) nach einem der vorangegangenen Ansprüche, wobei R6 oder R7 und R8 oder R9 jeweils OH sind
oder
R6 oder R7 F ist und R8 oder R9 OH ist
oder
R6 oder R7 OH ist und R8 oder R9 F ist
oder
R6 oder R7 und R8 oder R9 jeweils F sind.
8. Verbindung der Formel (I) nach einem der vorangegangenen Ansprüche, ausgewählt aus der Gruppe bestehend aus
(1 ) zyklisches (Benzimidazolribosid-(3' -> 5')-monophosphat - benzimidazolribosid-(3' -> 5')- monophosphat)
(2) zyklisches (Benzimidazolribosid-(2' -> 5')-monophosphat - benzimidazolribosid-(3' -> 5')- monophosphat)
(3) zyklisches (Benzimidazolribosid-(2' -> 5')-monophosphat - benzimidazolribosid-(2' -> 5') monophosphat)
(4) zyklisches (Benzimidazolribosid-(3' -> 5')-monophosphorothioat - benzimidazolribosid-(3' -:
5')-monophosphorothioat)
(5) zyklisches (Benzimidazolribosid-(2' -> 5')-monophosphorothioat - benzimidazolribosid-(3' -:
5')-monophosphorothioat)
(6) zyklisches (Benzimidazolribosid-(2' -> 5')-monophosphorothioat - benzimidazolribosid-(2' -:
5')-monophosphorothioat)
(7) zyklisches (5,6-Dichlorbenzimidazolribosid-(3' -> 5')-monophosphat - 5,6 dichlorbenzimidazolribosid-(3' -> 5')-monophosphat)
(8) zyklisches (5,6-Dichlorbenzimidazolribosid-(2' -> 5')-monophosphat - 5,6 dichlorbenzimidazolribosid-(3' -> 5')-monophosphat)
(9) zyklisches (5,6-Dichlorbenzimidazolribosid-(2' -> 5')-monophosphat - 5,6 dichlorbenzimidazolribosid-(2' -> 5')-monophosphat)
(10) zyklisches (5,6-Dichlorbenzimidazolribosid-(3' -> 5')-monophosphorothioat - 5,6 dichlorbenzimidazolribosid-(3' -> 5')-monophosphorothioat)
(1 1 ) zyklisches (5,6-Dichlorbenzimidazolribosid-(2' -> 5')-monophosphorothioat - 5,6 dichlorbenzimidazolribosid-(3' -> 5')-monophosphorothioat)
(12) zyklisches (5,6-Dichlorbenzimidazolribosid-(2' -> 5')-monophosphorothioat - 5,6 dichlorbenzimidazolribosid-(2' -> 5')-monophosphorothioat)
(13) zyklisches (2,5,6-Trichlorbenzimidazolribosid-(3' -> 5')-monophosphat - 2,5,6 trichlorbenzimidazolribosid-(3' -> 5')-monophosphat)
(14) zyklisches (2,5,6-Trichlorbenzimidazolribosid-(2' -> 5')-monophosphat - 2,5,6 trichlorbenzimidazolribosid-(3' -> 5')-monophosphat)
(15) zyklisches (2,5,6-Trichlorbenzimidazolribosid-(2' -> 5')-monophosphat - 2,5,6 trichlorbenzimidazolribosid-(2' -> 5')-monophosphat)
(16) zyklisches (2,5,6-Trichlorbenzimidazolribosid-(3' -> 5')-monophosphorothioat - 2,5,6 trichlorbenzimidazolribosid-(3' -> 5')-monophosphorothioat)
(17) zyklisches (2,5,6-Trichlorbenzimidazolribosid-(2' -> 5')-monophosphorothioat - 2,5,6 trichlorbenzimidazolribosid-(3' -> 5')-monophosphorothioat)
(18) zyklisches (2,5,6-Trichlorbenzimidazolribosid-(2' -> 5')-monophosphorothioat - 2,5,6 trichlorbenzimidazolribosid-(2' -> 5')-monophosphorothioat)
(19) zyklisches (Guanosin-(3' -> 5')-monophosphat - benzimidazolribosid-(3' -> 5') monophosphat)
(20) zyklisches (Guanosin-(2' -> 5')-monophosphat - benzimidazolribosid-(3' -> 5') monophosphat)
(21 ) zyklisches (Guanosin-(2' -> 5')-monophosphat - benzimidazolribosid-(2' -> 5') monophosphat)
(22) zyklisches (Guanosin-(3' -> 5')-monophosphorothioat - benzimidazolribosid-(3' -> 5') monophosphorothioat)
(23) zyklisches (Guanosin-(2' -> 5')-monophosphorothioat - benzimidazolribosid-(3' -> 5')- monophosphorothioat)
(24) zyklisches (Guanosin-(2' -> 5')-monophosphorothioat - benzimidazolribosid-(2' -> 5')- monophosphorothioat)
(25) zyklisches (Guanosin-(3' -> 5')-monophosphat - 5,6-dichlorbenzimidazolribosid-(3' -> 5')- monophosphat)
(26) zyklisches (Guanosin-(2' -> 5')-monophosphat - 5,6-dichlorbenzimidazolribosid-(3' -> 5')- monophosphat)
(27) zyklisches (Guanosin-(2' -> 5')-monophosphat - 5,6-dichlorbenzimidazolribosid-(2' -> 5')- monophosphat)
(28) zyklisches (Guanosin-(3' -> 5')-monophosphorothioat - 5,6-dichlorbenzimidazolribosid-(3' -> 5')-monophosphorothioat)
(29) zyklisches (Guanosin-(2' -> 5')-monophosphorothioat - 5,6-dichlorbenzimidazolribosid-(3' -> 5')-monophosphorothioat)
(30) zyklisches (Guanosin-(2' -> 5')-monophosphorothioat - 5,6-dichlorbenzimidazolribosid-(2' -> 5')-monophosphorothioat)
(31 ) zyklisches (Guanosin-(3' -> 5')-monophosphat - 2,5,6-trichlorbenzimidazolribosid-(3' -> 5')- monophosphat)
(32) zyklisches (Guanosin-(2' -> 5')-monophosphat - 2,5,6-trichlorbenzimidazolribosid-(3' -> 5')- monophosphat)
(33) zyklisches (Guanosin-(2' -> 5')-monophosphat - 2,5,6-trichlorbenzimidazolribosid-(2' -> 5')- monophosphat)
(34) zyklisches (Guanosin-(3' -> 5')-monophosphorothioat - 2,5,6-trichlorbenzimidazolribosid-(3' -> 5')-monophosphorothioat)
(35) zyklisches (Guanosin-(2' -> 5')-monophosphorothioat - 2,5,6-trichlorbenzimidazolribosid-(3' -> 5')-monophosphorothioat)
(36) zyklisches (Guanosin-(2' -> 5')-monophosphorothioat - 2,5,6-trichlorbenzimidazolribosid-(2' -> 5')-monophosphorothioat)
(37) zyklisches (Adenosin-(3' -> 5')-monophosphat - benzimidazolribosid-(3' -> 5')- monophosphat)
(38) zyklisches (Adenosin-(2' -> 5')-monophosphat - benzimidazolribosid-(3' -> 5')- monophosphat)
(39) zyklisches (Adenosin-(2' -> 5')-monophosphat - benzimidazolribosid-(2' -> 5')- monophosphat)
(40) zyklisches (Adenosin-(3' -> 5')-monophosphorothioat - benzimidazolribosid-(3' -> 5')- monophosphorothioat)
(41 ) zyklisches (Adenosin-(2' -> 5')-monophosphorothioat - benzimidazolribosid-(3' -> 5')- monophosphorothioat)
(42) zyklisches (Adenosin-(2' -> 5')-monophosphorothioat - benzimidazolribosid-(2' -> 5')- monophosphorothioat)
(43) zyklisches (Adenosin-(3' -> 5')-monophosphat - 5,6-dichlorbenzimidazolribosid-(3' -> 5')- monophosphat)
(44) zyklisches (Adenosin-(2' -> 5')-monophosphat - 5,6-dichlorbenzimidazolribosid-(3' -> 5')- monophosphat)
(45) zyklisches (Adenosin-(2' -> 5')-monophosphat - 5,6-dichlorbenzimidazolribosid-(2' -> 5')- monophosphat)
(46) zyklisches (Adenosin-(3' -> 5')-monophosphorothioat - 5,6-dichlorbenzimidazolribosid-(3' -> 5')-monophosphorothioat)
(47) zyklisches (Adenosin-(2' -> 5')-monophosphorothioat - 5,6-dichlorbenzimidazolribosid-(3' -> 5')-monophosphorothioat)
(48) zyklisches (Adenosin-(2' -> 5')-monophosphorothioat - 5,6-dichlorbenzimidazolribosid-(2' -> 5')-monophosphorothioat)
(49) zyklisches (Adenosin-(3' -> 5')-monophosphat - 2,5,6-trichlorbenzimidazolribosid-(3' -> 5')- monophosphat)
(50) zyklisches (Adenosin-(2' -> 5')-monophosphat - 2,5,6-trichlorbenzimidazolribosid-(3' -> 5')- monophosphat)
(51 ) zyklisches (Adenosin-(2' -> 5')-monophosphat - 2,5,6-trichlorbenzimidazolribosid-(2' -> 5')- monophosphat)
(52) zyklisches (Adenosin-(3' -> 5')-monophosphorothioat - 2,5,6-trichlorbenzimidazolribosid-(3' -> 5')-monophosphorothioat)
(53) zyklisches (Adenosin-(2' -> 5')-monophosphorothioat - 2,5,6-trichlorbenzimidazolribosid-(3' -> 5')-monophosphorothioat)
(54) zyklisches (Adenosin-(2' -> 5')-monophosphorothioat - 2,5,6-trichlorbenzimidazolribosid-(2' -> 5')-monophosphorothioat)
(55) zyklisches (lnosin-(3' -> 5')-monophosphat - benzimidazolribosid-(3' -> 5')-monophosphat)
(56) zyklisches (lnosin-(2' -> 5')-monophosphat - benzimidazolribosid-(3' -> 5')-monophosphat)
(57) zyklisches (lnosin-(2' -> 5')-monophosphat - benzimidazolribosid-(2' -> 5')-monophosphat)
(58) zyklisches (lnosin-(3' -> 5')-monophosphorothioat - benzimidazolribosid-(3' -> 5')- monophosphorothioat)
(59) zyklisches (lnosin-(2' -> 5')-monophosphorothioat - benzimidazolribosid-(3' -> 5')- monophosphorothioat)
(60) zyklisches (lnosin-(2' -> 5')-monophosphorothioat - benzimidazolribosid-(2' -> 5')- monophosphorothioat)
(61 ) zyklisches (lnosin-(3' -> 5')-monophosphat - 5,6-dichlorbenzimidazolribosid-(3' -> 5')- monophosphat)
(62) zyklisches (lnosin-(2' -> 5')-monophosphat - 5,6-dichlorbenzimidazolribosid-(3' -> 5')- monophosphat)
(63) zyklisches (lnosin-(2' -> 5')-monophosphat - 5,6-dichlorbenzimidazolribosid-(2' -> 5')- monophosphat)
(64) zyklisches (lnosin-(3' -> 5')-monophosphorothioat - 5,6-dichlorbenzimidazolribosid-(3' -> 5') monophosphorothioat)
(65) zyklisches (lnosin-(2' -> 5')-monophosphorothioat - 5,6-dichlorbenzimidazolribosid-(3' -> 5') monophosphorothioat)
(66) zyklisches (lnosin-(2' -> 5')-monophosphorothioat - 5,6-dichlorbenzimidazolribosid-(2' -> 5') monophosphorothioat)
(67) zyklisches (lnosin-(3' -> 5')-monophosphat - 2,5,6-trichlorbenzimidazolribosid-(3' -> 5') monophosphat)
(68) zyklisches (lnosin-(2' -> 5')-monophosphat - 2,5,6-trichlorbenzimidazolribosid-(3' -> 5') monophosphat)
(69) zyklisches (lnosin-(2' -> 5')-monophosphat - 2,5,6-trichlorbenzimidazolribosid-(2' -> 5') monophosphat)
(70) zyklisches (lnosin-(3' -> 5')-monophosphorothioat - 2,5,6-trichlorbenzimidazolribosid-(3' -:
5')-monophosphorothioat)
(71 ) zyklisches (lnosin-(2' -> 5')-monophosphorothioat - 2,5,6-trichlorbenzimidazolribosid-(3' -:
5')-monophosphorothioat)
(72) zyklisches (lnosin-(2' -> 5')-monophosphorothioat - 2,5,6-trichlorbenzimidazolribosid-(2' -:
5')-monophosphorothioat)
(73) zyklisches (2'-Fluor-2'-deoxyguanosin-(3' -> 5')-monophosphat - benzimidazolribosid-(3' -:
5')-monophosphat)
(74) zyklisches (2'-Fluor-2'-deoxyguanosin-(3' -> 5')-monophosphorothioat - benzimidazolribosid (3' -> 5')-monophosphorothioat)
(75) zyklisches (2'-Fluor-2'-deoxyguanosin-(3' -> 5')-monophosphat - 5,6 dichlorbenzimidazolribosid-(3' -> 5')-monophosphat)
(76) zyklisches (2'-Fluor-2'-deoxyguanosin-(3' -> 5')-monophosphat - 5,6 dichlorbenzimidazolribosid-(3' -> 5')-monophosphat)
(77) zyklisches (2'-Fluor-2'-deoxyguanosin-(3' -> 5')-monophosphat - 2,5,6 trichlorbenzimidazolribosid-(3' -> 5')-monophosphat)
(78) zyklisches (2'-Fluor-2'-deoxyguanosin-(3' -> 5')-monophosphorothioat - 5,6 dichlorbenzimidazolribosid-(3' -> 5')-monophosphorothioat)
(79) zyklisches (2'-Fluor-2'-deoxyadenosin-(3' -> 5')-monophosphat - benzimidazolribosid-(3' -:
5')-monophosphat)
(80) zyklisches (2'-Fluor-2'-deoxyadenosin-(3' -> 5')-monophosphorothioat - benzimidazolribosid (3' -> 5')-monophosphorothioat)
(81 ) zyklisches (2'-Fluor-2'-deoxyadenosin-(3' -> 5')-monophosphat - 5,6 dichlorbenzimidazolribosid-(3' -> 5')-monophosphat)
(82) zyklisches (2'-Fluor-2'-deoxyadenosin-(3' -> 5')-monophosphorothioat - 5,6 dichlorbenzimidazolribosid-(3' -> 5')-monophosphorothioat)
(83) zyklisches (2'-Fluor-2'-deoxyadenosin-(3' -> 5')-monophosphat - 2,5,6 trichlorbenzimidazolribosid-(3' -> 5')-monophosphat)
(84) zyklisches (2'-Fluor-2'-deoxyadenosin-(3' -> 5')-monophosphorothioat - 2,5,6- trichlorbenzimidazolribosid-(3' -> 5')-monophosphorothioat)
(85) zyklisches (2'-Fluor-2'-deoxyinosin-(3' -> 5')-monophosphat - benzimidazolribosid-(3' -> 5')- monophosphat)
(86) zyklisches (2'-Fluor-2'-deoxyinosin-(3' -> 5')-monophosphorothioat - benzimidazolribosid-(3' -> 5')-monophosphorothioat)
(87) zyklisches (2'-Fluor-2'-deoxyinosin-(3' -> 5')-monophosphat - 5,6-dichlorbenzimidazolribosid- (3' -> 5')-monophosphat)
(88) zyklisches (2'-Fluor-2'-deoxyinosin-(3' -> 5')-monophosphorothioat - 5,6- dichlorbenzimidazolribosid-(3' -> 5')-monophosphorothioat)
(89) zyklisches (2'-Fluor-2'-deoxyinosin-(3' -> 5')-monophosphat - 2,5,6- trichlorbenzimidazolribosid-(3' -> 5')-monophosphat)
(90) zyklisches (2'-Fluor-2'-deoxyinosin-(3' -> 5')-monophosphorothioat - 2,5,6- trichlorbenzimidazolribosid-(3' -> 5')-monophosphorothioat)
(91 ) zyklisches (Guanosin-(3' -> 5')-monophosphat - benzimidazolribosid-(2' -> 5')- monophosphat)
(92) zyklisches (Guanosin-(3' -> 5')-monophosphorothioat - benzimidazolribosid-(2' -> 5')- monophosphorothioat)
(93) zyklisches (Guanosin-(3' -> 5')-monophosphat - 5,6-dichlorbenzimidazolribosid-(2' -> 5')- monophosphat)
(94) zyklisches (Guanosin-(3' -> 5')-monophosphorothioat - 5,6-dichlorbenzimidazolribosid-(2' -> 5')-monophosphorothioat)
(95) zyklisches (Guanosin-(3' -> 5')-monophosphat - 2,5,6-trichlorbenzimidazolribosid-(2' -> 5')- monophosphat)
(96) zyklisches (Guanosin-(3' -> 5')-monophosphorothioat - 2,5,6-trichlorbenzimidazolribosid-(2' -> 5')-monophosphorothioat)
(97) zyklisches (Adenosin-(3' -> 5')-monophosphat - benzimidazolribosid-(2' -> 5')- monophosphat)
(98) zyklisches (Adenosin-(3' -> 5')-monophosphorothioat - benzimidazolribosid-(2' -> 5')- monophosphorothioat)
(99) zyklisches (Adenosin-(3' -> 5')-monophosphat - 5,6-dichlorbenzimidazolribosid-(2' -> 5')- monophosphat)
(100) zyklisches (Adenosin-(3' -> 5')-monophosphorothioat - 5,6- dichlorbenzimidazolribosid-(2' -> 5')-monophosphorothioat)
(101 ) zyklisches (Adenosin-(3' -> 5')-monophosphat - 2,5,6-trichlorbenzimidazolribosid-(2' -> 5')-monophosphat)
(102) zyklisches (Adenosin-(3' -> 5')-monophosphorothioat - 2,5,6- trichlorbenzimidazolribosid-(2' -> 5')-monophosphorothioat)
(103) zyklisches (lnosin-(3' -> 5')-monophosphat - benzimidazolribosid-(2' -> 5')- monophosphat)
(104) zyklisches (lnosin-(3' -> 5')-monophosphorothioat - benzimidazolribosid-(2' -> 5')- monophosphorothioat)
(105) zyklisches (lnosin-(3' -> 5')-monophosphat - 5,6-dichlorbenzimidazolribosid-(2' -> 5')- monophosphat)
(106) zyklisches (lnosin-(3' -> 5')-monophosphorothioat - 5,6-dichlorbenzimidazolribosid-(2' -> 5')-monophosphorothioat)
(107) zyklisches (lnosin-(3' -> 5')-monophosphat - 2,5,6-trichlorbenzimidazolribosid-(2' -> 5')-monophosphat)
(108) zyklisches (lnosin-(3' -> 5')-monophosphorothioat - 2,5,6-trichlorbenzimidazolribosid- (2' -> 5')-monophosphorothioat)
(109) zyklisches (2'-Fluor-2'-deoxyguanosin-(3' -> 5')-monophosphat - benzimidazolribosid- (2' -> 5')-monophosphat)
(1 10) zyklisches (2'-Fluor-2'-deoxyguanosin-(3' -> 5')-monophosphorothioat benzimidazolribosid-(2' -> 5')-monophosphorothioat)
(1 1 1 ) zyklisches (2'-Fluor-2'-deoxyguanosin-(3' -> 5')-monophosphat - 5,6- dichlorbenzimidazolribosid-(2' -> 5')-monophosphat)
(1 12) zyklisches (2'-Fluor-2'-deoxyguanosin-(3' -> 5')-monophosphat - 5,6- dichlorbenzimidazolribosid-(2' -> 5')-monophosphat)
(1 13) zyklisches (2'-Fluor-2'-deoxyguanosin-(3' -> 5')-monophosphat - 2,5,6- trichlorbenzimidazolribosid-(2' -> 5')-monophosphat)
(1 14) zyklisches (2'-Fluor-2'-deoxyguanosin-(3' -> 5')-monophosphorothioat - 5,6- dichlorbenzimidazolribosid-(2' -> 5')-monophosphorothioat)
(1 15) zyklisches (2'-Fluor-2'-deoxyadenosin-(3' -> 5')-monophosphat - benzimidazolribosid- (2' -> 5')-monophosphat)
(1 16) zyklisches (2'-Fluor-2'-deoxyadenosin-(3' -> 5')-monophosphorothioat benzimidazolribosid-(2' -> 5')-monophosphorothioat)
(117) zyklisches (2'-Fluor-2'-deoxyadenosin-(3' -> 5')-monophosphat - 5,6- dichlorbenzimidazolribosid-(2' -> 5')-monophosphat)
(1 18) zyklisches (2'-Fluor-2'-deoxyadenosin-(3' -> 5')-monophosphorothioat - 5,6- dichlorbenzimidazolribosid-(2' -> 5')-monophosphorothioat)
(1 19) zyklisches (2'-Fluor-2'-deoxyadenosin-(3' -> 5')-monophosphat - 2,5,6- trichlorbenzimidazolribosid-(2' -> 5')-monophosphat)
(120) zyklisches (2'-Fluor-2'-deoxyadenosin-(3' -> 5')-monophosphorothioat - 2,5,6- trichlorbenzimidazolribosid-(2' -> 5')-monophosphorothioat)
(121 ) zyklisches (2'-Fluor-2'-deoxyinosin-(3' -> 5')-monophosphat - benzimidazolribosid-(2' -> 5')-monophosphat)
(122) zyklisches (2'-Fluor-2'-deoxyinosin-(3' -> 5')-monophosphorothioat
benzimidazolribosid-(2' -> 5')-monophosphorothioat)
(123) zyklisches (2'-Fluor-2'-deoxyinosin-(3' -> 5')-monophosphat - 5,6- dichlorbenzimidazolribosid-(2' -> 5')-monophosphat)
(124) zyklisches (2'-Fluor-2'-deoxyinosin-(3' -> 5')-monophosphorothioat - 5,6- dichlorbenzimidazolribosid-(2' -> 5')-monophosphorothioat)
(125) zyklisches (2'-Fluor-2'-deoxyinosin-(3' -> 5')-monophosphat - 2,5,6- trichlorbenzimidazolribosid-(2' -> 5')-monophosphat)
(126) zyklisches (2'-Fluor-2'-deoxyinosin-(3' -> 5')-monophosphorothioat - 2,5,6- trichlorbenzimidazolribosid-(2' -> 5')-monophosphorothioat)
(127) zyklisches (Adenosin-(3' -> 5')-monophosphate - 5,6-dimethylbenzimidazolribosid-(2' -> 5')-monophosphat
(128) zyklisches (Adenosin-(3' -> 5')-monoboranophosphat - benzimidazolribosid -(3' -> 5')-monophosphat)
(129) zyklisches (Guanosin-(2' -> 5')-monoboranophosphat - benzimidazolribosid -(3' -> 5')- monophosphat)
(130) zyklisches (Guanosin-(2' -> 5')-monoboranophosphat - benzimidazolribosid -(3' -> 5')- monophosphorothioat)
(131 ) zyklisches (Adenosin-(2' -> 5')- monophosphorothioat - benzimidazolribosid -(3' -> 5')- monoboranophosphat)
(132) zyklisches (Adenosin-(3' -> 5')- monophosphat - benzimidazolribosid -(2' -> 5')- monophosphorothioat)
(133) zyklisches (Adenosin-(2' -> 5')- monoboranophosphat - benzimidazolribosid -(2' -> 5')- monophosphat)
9. Verfahren zur chemoenzymatischen Herstellung einer Verbindung der allgemeinen Formel (I) nach einem der Ansprüche 1 bis 8 mit der allgemeinen Struktureinheit c[N1 (2',5')pN2(3',5')p] oder c[N1 (3',5')pN2(3',5')p] durch Transglycosylierung von c-diAMP, c-diGMP, 2',3'-cGAMP oder 3',3'- cGAMP mittels einer Purin-Nukleosid-Phosphorylasen (PNPase).
10. Verfahren zur chemoenzymatischen Herstellung einer Verbindung der allgemeinen Formel (I) nach einem der Ansprüche 1 bis 8 mit der allgemeinen Struktureinheit c[N1 (2',5')pN2(3',5')p], c[N1 (2',5')pS-N2(3',5')p], c[N1 (2',5')pS-N2(3',5')pS], c[N1 (2',5')pB-N2(3',5')p], c[N1 (2',5')pB-N2(3',5')pB], c[N1 (2',5')pB-N2(3',5')pS] oder c[N1 (2',5')pS-N2(3',5')pB] durch Dimerisierung und Zyklisierung von 5'- O-Triphosphaten, 5'-0-(1 -Thiotriphosphaten) oder 5'-0-(1 -Boranotriphosphaten) mit einer cGAMP Synthase (cGAS).
11 . Verfahren zur chemoenzymatischen Herstellung einer Verbindung der allgemeinen Formel (I) nach einem der Ansprüche 1 bis 8 mit der allgemeinen Struktureinheit c[N1 (3',5')pN2(3',5')p], οΙΝ^',δ^ρΒ-Ν^',δ οΙΝ^',δ^ρ-Ν^',δ^ρΒ], oder Ι^',δ^ρΒ-Ν^',δ^ρΒ], wobei alternativ der Benzimidazolrest in durch eine gegebenenfalls substituierte Purinbase ersetzt sein kann, durch Dimerisierung und Zyklisierung von 5'-0-Triphosphaten oder 5'-0-(1 -Boranotriphosphaten) mit einem Enzym DNA integrity scanning protein (DisA) aus Bacillus subtilis.
12. Verbindung der Formel (I) nach einem der Ansprüche 1 bis 8 für die Verwendung als Medikament.
13. Verbindung der Formel (I) nach einem der Ansprüche 1 bis 8 in pharmakologisch akzeptabler Form für die Behandlung oder Vorbeugung einer Krankheit, ausgewählt aus der Gruppe bestehend aus Krebs, infektiöse Erkrankung bakterieller oder viraler Ursache, akuter Abstoßung eines Organtransplantes, Diabetes mellitus Typ I, rheumatischer Arthritis, Psoriasis, Crohn's Krankheit, Restenosis, allergisches Asthma und anderen Krankheiten, deren Zustand durch eine Aktivierung des STING-Signalweges verbessert oder geheilt werden kann.
14. Verbindung der Formel (I) nach einem der Ansprüche 1 -8 für die Verwendung als Forchungsreagenz, verzugsweise als Forschungsreagenz für das Studium einer Krankheit oder Disfunktion, vorzugsweise einer Krankheit oder Disfunktion ausgewählt aus der Gruppe bestehend aus Krebs, infektiöser Erkrankungen bakterieller oder viraler Ursache, akuter Abstoßung eines Organtransplantes, Diabetes mellitus Typ I, rheumatische Arthritis, Psoriasis, Crohn's Krankheit, Restenosis, allergisches Asthma und anderen Krankheiten, deren Zustand durch eine Aktivierung des STING-Signalweges verbessert oder geheilt werden kann.
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US16/339,938 US11001605B2 (en) | 2016-10-07 | 2017-10-02 | Cyclic dinucleotides containing benzimidazole, method for the production of same, and use of same to activate stimulator of interferon genes (sting)-dependent signaling pathways |
| EP17786843.7A EP3523314A1 (de) | 2016-10-07 | 2017-10-02 | Benzimidazolhaltige cyclische dinukleotide, verfahren zu deren herstellung und ihre verwendung zur aktivierung von stimulator von interferongenen (sting)-abhängigen signalwegen |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE102016219566.2 | 2016-10-07 | ||
| DE102016219566 | 2016-10-07 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2018065360A1 true WO2018065360A1 (de) | 2018-04-12 |
Family
ID=60138340
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/EP2017/074966 Ceased WO2018065360A1 (de) | 2016-10-07 | 2017-10-02 | Benzimidazolhaltige cyclische dinukleotide, verfahren zu deren herstellung und ihre verwendung zur aktivierung von stimulator von interferongenen (sting)-abhängigen signalwegen |
Country Status (3)
| Country | Link |
|---|---|
| US (1) | US11001605B2 (de) |
| EP (1) | EP3523314A1 (de) |
| WO (1) | WO2018065360A1 (de) |
Cited By (58)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2019043634A2 (en) | 2017-08-30 | 2019-03-07 | Beijing Xuanyi Pharmasciences Co., Ltd. | CYCLIC DI-NUCLEOTIDES AS STIMULATORS OF INTERFERON GENE MODULATORS |
| WO2019084060A1 (en) | 2017-10-24 | 2019-05-02 | Silverback Therapeutics, Inc. | CONJUGATES AND METHODS OF USE FOR THE SELECTIVE DELIVERY OF IMMUNOMODULATORY AGENTS |
| WO2019165374A1 (en) | 2018-02-26 | 2019-08-29 | Gilead Sciences, Inc. | Substituted pyrrolizine compounds as hbv replication inhibitors |
| WO2019193543A1 (en) | 2018-04-06 | 2019-10-10 | Institute Of Organic Chemistry And Biochemistry Ascr, V.V.I. | 3'3'-cyclic dinucleotides |
| WO2019193542A1 (en) | 2018-04-06 | 2019-10-10 | Institute Of Organic Chemistry And Biochemistry Ascr, V.V.I. | 2'3'-cyclic dinucleotides |
| WO2019193533A1 (en) | 2018-04-06 | 2019-10-10 | Institute Of Organic Chemistry And Biochemistry Ascr, V.V.I. | 2'2'-cyclic dinucleotides |
| WO2019195181A1 (en) | 2018-04-05 | 2019-10-10 | Gilead Sciences, Inc. | Antibodies and fragments thereof that bind hepatitis b virus protein x |
| WO2019200247A1 (en) | 2018-04-12 | 2019-10-17 | Precision Biosciences, Inc. | Optimized engineered meganucleases having specificity for a recognition sequence in the hepatitis b virus genome |
| WO2019211799A1 (en) | 2018-05-03 | 2019-11-07 | Institute Of Organic Chemistry And Biochemistry Ascr, V.V.I. | 2'3'-cyclic dinucleotide analogue comprising a cyclopentanyl modified nucleotide |
| US10519188B2 (en) | 2016-03-18 | 2019-12-31 | Immunesensor Therapeutics, Inc. | Cyclic di-nucleotide compounds and methods of use |
| WO2020028097A1 (en) | 2018-08-01 | 2020-02-06 | Gilead Sciences, Inc. | Solid forms of (r)-11-(methoxymethyl)-12-(3-methoxypropoxy)-3,3-dimethyl-8-0x0-2,3,8,13b-tetrahydro-1h-pyrido[2,1-a]pyrrolo[1,2-c] phthalazine-7-c arboxylic acid |
| WO2020050406A1 (ja) | 2018-09-06 | 2020-03-12 | 第一三共株式会社 | 新規環状ジヌクレオチド誘導体及びその抗体薬物コンジュゲート |
| WO2020056008A1 (en) | 2018-09-12 | 2020-03-19 | Silverback Therapeutics, Inc. | Compositions for the treatment of disease with immune stimulatory conjugates |
| WO2020057546A1 (zh) | 2018-09-21 | 2020-03-26 | 上海迪诺医药科技有限公司 | 环状二核苷酸类似物、其药物组合物及应用 |
| WO2020074004A1 (zh) * | 2018-10-12 | 2020-04-16 | 上海济煜医药科技有限公司 | 环二核苷酸类化合物及其应用 |
| WO2020092528A1 (en) | 2018-10-31 | 2020-05-07 | Gilead Sciences, Inc. | Substituted 6-azabenzimidazole compounds having hpk1 inhibitory activity |
| WO2020092621A1 (en) | 2018-10-31 | 2020-05-07 | Gilead Sciences, Inc. | Substituted 6-azabenzimidazole compounds as hpk1 inhibitors |
| US10662416B2 (en) | 2016-10-14 | 2020-05-26 | Precision Biosciences, Inc. | Engineered meganucleases specific for recognition sequences in the hepatitis B virus genome |
| WO2020132566A1 (en) * | 2018-12-21 | 2020-06-25 | Nimbus Titan, Inc. | Sting pyrazole agonists and uses thereof |
| CN111349132A (zh) * | 2018-12-21 | 2020-06-30 | 上海济煜医药科技有限公司 | 肿瘤免疫类化合物及其应用 |
| WO2020178770A1 (en) | 2019-03-07 | 2020-09-10 | Institute Of Organic Chemistry And Biochemistry Ascr, V.V.I. | 3'3'-cyclic dinucleotides and prodrugs thereof |
| WO2020178768A1 (en) | 2019-03-07 | 2020-09-10 | Institute Of Organic Chemistry And Biochemistry Ascr, V.V.I. | 3'3'-cyclic dinucleotide analogue comprising a cyclopentanyl modified nucleotide as sting modulator |
| WO2020178769A1 (en) | 2019-03-07 | 2020-09-10 | Institute Of Organic Chemistry And Biochemistry Ascr, V.V.I. | 2'3'-cyclic dinucleotides and prodrugs thereof |
| WO2020214652A1 (en) | 2019-04-17 | 2020-10-22 | Gilead Sciences, Inc. | Solid forms of a toll-like receptor modulator |
| WO2020214663A1 (en) | 2019-04-17 | 2020-10-22 | Gilead Sciences, Inc. | Solid forms of a toll-like receptor modulator |
| WO2020237025A1 (en) | 2019-05-23 | 2020-11-26 | Gilead Sciences, Inc. | Substituted exo-methylene-oxindoles which are hpk1/map4k1 inhibitors |
| WO2020263830A1 (en) | 2019-06-25 | 2020-12-30 | Gilead Sciences, Inc. | Flt3l-fc fusion proteins and methods of use |
| WO2021034804A1 (en) | 2019-08-19 | 2021-02-25 | Gilead Sciences, Inc. | Pharmaceutical formulations of tenofovir alafenamide |
| US10966999B2 (en) | 2017-12-20 | 2021-04-06 | Institute Of Organic Chemistry And Biochemistry Ascr, V.V.I. | 3′3′ cyclic dinucleotides with phosphonate bond activating the sting adaptor protein |
| WO2021067181A1 (en) | 2019-09-30 | 2021-04-08 | Gilead Sciences, Inc. | Hbv vaccines and methods treating hbv |
| WO2021067644A1 (en) | 2019-10-01 | 2021-04-08 | Silverback Therapeutics, Inc. | Combination therapy with immune stimulatory conjugates |
| US10980825B2 (en) | 2016-12-01 | 2021-04-20 | Takeda Pharmaceutical Company Limited | Cyclic dinucleotide |
| WO2021113765A1 (en) | 2019-12-06 | 2021-06-10 | Precision Biosciences, Inc. | Optimized engineered meganucleases having specificity for a recognition sequence in the hepatitis b virus genome |
| WO2021168274A1 (en) | 2020-02-21 | 2021-08-26 | Silverback Therapeutics, Inc. | Nectin-4 antibody conjugates and uses thereof |
| US11110106B2 (en) | 2018-10-29 | 2021-09-07 | Venenum Biodesign, LLC | Sting agonists for treating bladder cancer and solid tumors |
| WO2021177438A1 (ja) | 2020-03-06 | 2021-09-10 | 第一三共株式会社 | 新規環状ジヌクレオチド誘導体を含む抗体薬物コンジュゲート |
| WO2021188959A1 (en) | 2020-03-20 | 2021-09-23 | Gilead Sciences, Inc. | Prodrugs of 4'-c-substituted-2-halo-2'-deoxyadenosine nucleosides and methods of making and using the same |
| WO2021206158A1 (ja) | 2020-04-10 | 2021-10-14 | 小野薬品工業株式会社 | がん治療方法 |
| US11161864B2 (en) | 2018-10-29 | 2021-11-02 | Venenum Biodesign, LLC | Sting agonists |
| US11203610B2 (en) | 2017-12-20 | 2021-12-21 | Institute Of Organic Chemistry And Biochemistry Ascr, V.V.I. | 2′3′ cyclic dinucleotides with phosphonate bond activating the sting adaptor protein |
| WO2022006327A1 (en) | 2020-07-01 | 2022-01-06 | Silverback Therapeutics, Inc. | Anti-asgr1 antibody conjugates and uses thereof |
| WO2022031894A1 (en) | 2020-08-07 | 2022-02-10 | Gilead Sciences, Inc. | Prodrugs of phosphonamide nucleotide analogues and their pharmaceutical use |
| WO2022050300A1 (ja) | 2020-09-02 | 2022-03-10 | 第一三共株式会社 | 新規エンド-β-N-アセチルグルコサミニダーゼ |
| WO2022241134A1 (en) | 2021-05-13 | 2022-11-17 | Gilead Sciences, Inc. | COMBINATION OF A TLR8 MODULATING COMPOUND AND ANTI-HBV siRNA THERAPEUTICS |
| WO2022245671A1 (en) | 2021-05-18 | 2022-11-24 | Gilead Sciences, Inc. | Methods of using flt3l-fc fusion proteins |
| WO2022271677A1 (en) | 2021-06-23 | 2022-12-29 | Gilead Sciences, Inc. | Diacylglyercol kinase modulating compounds |
| WO2022271684A1 (en) | 2021-06-23 | 2022-12-29 | Gilead Sciences, Inc. | Diacylglyercol kinase modulating compounds |
| WO2022271650A1 (en) | 2021-06-23 | 2022-12-29 | Gilead Sciences, Inc. | Diacylglyercol kinase modulating compounds |
| WO2022271659A1 (en) | 2021-06-23 | 2022-12-29 | Gilead Sciences, Inc. | Diacylglyercol kinase modulating compounds |
| US11542293B2 (en) | 2017-11-10 | 2023-01-03 | Takeda Pharmaceutical Company Limited | Sting modulator compounds, and methods of making and using |
| US11725024B2 (en) | 2020-11-09 | 2023-08-15 | Takeda Pharmaceutical Company Limited | Antibody drug conjugates |
| WO2023167238A1 (ja) | 2022-03-02 | 2023-09-07 | 第一三共株式会社 | Fc含有分子の製造方法 |
| US11787833B2 (en) | 2019-05-09 | 2023-10-17 | Aligos Therapeutics, Inc. | Modified cyclic dinucleoside compounds as sting modulators |
| WO2024048490A1 (ja) | 2022-08-29 | 2024-03-07 | 第一三共株式会社 | 変異Fc領域を含む抗体薬物コンジュゲート |
| WO2025240246A1 (en) | 2024-05-13 | 2025-11-20 | Gilead Sciences, Inc. | Combination therapies with ribavirin |
| WO2025240243A1 (en) | 2024-05-13 | 2025-11-20 | Gilead Sciences, Inc. | Combination therapies with bulevirtide and an inhibitory nucleic acid targeting hepatitis b virus |
| WO2025240242A1 (en) | 2024-05-13 | 2025-11-20 | Gilead Sciences, Inc. | Combination therapies with ribavirin |
| WO2025240244A1 (en) | 2024-05-13 | 2025-11-20 | Gilead Sciences, Inc. | Combination therapies comprising bulevirtide and lonafarnib for use in the treatment of hepatitis d virus infection |
Citations (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2014093936A1 (en) | 2012-12-13 | 2014-06-19 | Aduro Biotech, Inc. | Compositions comprising cyclic purine dinucleotides having defined stereochemistries and methods for their preparation and use |
| WO2014179335A1 (en) * | 2013-04-29 | 2014-11-06 | Memorial Sloan Kettering Cancer Center | Compositions and methods for altering second messenger signaling |
| US20140329889A1 (en) | 2013-05-03 | 2014-11-06 | The Regents Of The University Of California | Cyclic di-nucleotide induction of type i interferon |
| WO2014189805A1 (en) | 2013-05-18 | 2014-11-27 | Auro Biotech, Inc. | Compositions and methods for activating "stimulator of interferon gene"-dependent signalling |
| WO2015077354A1 (en) | 2013-11-19 | 2015-05-28 | The University Of Chicago | Use of sting agonist as cancer treatment |
| WO2015185565A1 (en) | 2014-06-04 | 2015-12-10 | Glaxosmithkline Intellectual Property Development Limited | Cyclic di-nucleotides as modulators of sting |
| WO2016096577A1 (en) | 2014-12-16 | 2016-06-23 | Invivogen | Combined use of a chemotherapeutic agent and a cyclic dinucleotide for cancer treatment |
| WO2016096174A1 (en) | 2014-12-16 | 2016-06-23 | Invivogen | Fluorinated cyclic dinucleotides for cytokine induction |
| WO2016145102A1 (en) | 2015-03-10 | 2016-09-15 | Aduro Biotech, Inc. | Compositions and methods for activating "stimulator of interferon gene" -dependent signalling |
| WO2017027646A1 (en) | 2015-08-13 | 2017-02-16 | Merck Sharp & Dohme Corp. | Cyclic di-nucleotide compounds as sting agonists |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4482708A (en) * | 1982-08-09 | 1984-11-13 | Nguyen Nicolas C | 3', 5'-Dinucleoside phosphates of 5,6-dichloro-1-β-D-ribofuranosyl-1-benzimidazole and methods of making and using the same |
-
2017
- 2017-10-02 WO PCT/EP2017/074966 patent/WO2018065360A1/de not_active Ceased
- 2017-10-02 EP EP17786843.7A patent/EP3523314A1/de not_active Withdrawn
- 2017-10-02 US US16/339,938 patent/US11001605B2/en active Active
Patent Citations (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2014093936A1 (en) | 2012-12-13 | 2014-06-19 | Aduro Biotech, Inc. | Compositions comprising cyclic purine dinucleotides having defined stereochemistries and methods for their preparation and use |
| WO2014179335A1 (en) * | 2013-04-29 | 2014-11-06 | Memorial Sloan Kettering Cancer Center | Compositions and methods for altering second messenger signaling |
| US20140329889A1 (en) | 2013-05-03 | 2014-11-06 | The Regents Of The University Of California | Cyclic di-nucleotide induction of type i interferon |
| WO2014189805A1 (en) | 2013-05-18 | 2014-11-27 | Auro Biotech, Inc. | Compositions and methods for activating "stimulator of interferon gene"-dependent signalling |
| WO2015077354A1 (en) | 2013-11-19 | 2015-05-28 | The University Of Chicago | Use of sting agonist as cancer treatment |
| WO2015185565A1 (en) | 2014-06-04 | 2015-12-10 | Glaxosmithkline Intellectual Property Development Limited | Cyclic di-nucleotides as modulators of sting |
| WO2016096577A1 (en) | 2014-12-16 | 2016-06-23 | Invivogen | Combined use of a chemotherapeutic agent and a cyclic dinucleotide for cancer treatment |
| WO2016096174A1 (en) | 2014-12-16 | 2016-06-23 | Invivogen | Fluorinated cyclic dinucleotides for cytokine induction |
| WO2016145102A1 (en) | 2015-03-10 | 2016-09-15 | Aduro Biotech, Inc. | Compositions and methods for activating "stimulator of interferon gene" -dependent signalling |
| WO2017027646A1 (en) | 2015-08-13 | 2017-02-16 | Merck Sharp & Dohme Corp. | Cyclic di-nucleotide compounds as sting agonists |
| WO2017027645A1 (en) | 2015-08-13 | 2017-02-16 | Merck Sharp & Dohme Corp. | Cyclic di-nucleotide compounds as sting agonists |
Non-Patent Citations (8)
| Title |
|---|
| GAFFNEY, B. L.; VELIATH, E.; ZHAO, J.; JONES, R. A.: "One-flask syntheses of c-di-GMP and the [Rp,Rp] and [Rp,Sp] thiophosphate analogues", ORG LETT, vol. 12, no. 14, 2010, pages 3269 - 71 |
| GAO, P.; ASCANO, M.; WU, Y.; BARCHET, W.; GAFFNEY, B. L.; ZILLINGER, T.; SERGANOV, A. A.; LIU, Y.; JONES, R. A.; HARTMANN, G.: "Cyclic [G(2',5')pA(3',5')p] is the metazoan second messenger produced by DNA-activated cyclic GMP-AMP synthase", CE, vol. 153, no. 5, 2013, pages 1094 - 107, XP055172271, DOI: doi:10.1016/j.cell.2013.04.046 |
| KRASS, J. D.; JASTORFF, B.; GENIESER, H. G.: "Determination of lipophilicity by gradient elution high-performance liquid chromatography", ANAL CHEM, vol. 69, no. 13, 1997, pages 2575 - 81 |
| LI, L.; YIN, Q.; KUSS, P.; MALIGA, Z.; MILLAN, J. L.; WU, H.; MITCHISON, T. J.: "Hydrolysis of 2'3'-cGAMP by ENPP1 and design of nonhydrolyzable analogs", NAT CHEM BIO/, vol. 10, no. 12, 2014, pages 1043 - 8, XP055209816, DOI: doi:10.1038/nchembio.1661 |
| MARGOLIN A. L.; BORCHERDING D. R.; WOLF-KUGEL D.; MARGOLIN N.: "AMP deaminase as a novel practical catalyst in the synthesis of 6-oxopurine ribosides and their analogs", J. ORG. CHEM., vol. 59, no. 24, 1994, pages 7214 - 7218, XP002988972, DOI: doi:10.1021/jo00103a010 |
| MEHNE, F. M.; SCHRODER-TITTMANN, K.; EIJLANDER, R. T.; HERZBERG, C.; HEWITT, L.; KAEVER, V.; LEWIS, R. J.; KUIPERS, O. P.; TITTMAN: "Control of the diadenylate cyclase CdaS in Bacillus subtilis: an autoinhibitory domain limits cyclic di-AMP production", J BIOL CHEM, vol. 289, no. 30, 2014, pages 21098 - 107 |
| PARSCH, J.; ENGELS, J. W.: "C-F...H-C hydrogen bonds in ribonucleic acids", J AM CHEM SOC, vol. 124, no. 20, 2002, pages 5664 - 72 |
| URATA, H.; FUJIMORI, M.; AONO, C.; YAMAKAWA, T.; HARADA, E.; AKAGI, M.: "Regio- and diastereoselectivity of montmorillonite-catalyzed oligomerization of racemic adenosine 5'-phosphorimidazolide", NUCLEOSIDES NUCLEOTIDES NUCLEIC ACIDS, vol. 27, no. 4, 2008, pages 421 - 30 |
Cited By (103)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10519188B2 (en) | 2016-03-18 | 2019-12-31 | Immunesensor Therapeutics, Inc. | Cyclic di-nucleotide compounds and methods of use |
| US11299512B2 (en) | 2016-03-18 | 2022-04-12 | Immunesensor Therapeutics, Inc. | Cyclic di-nucleotide compounds and methods of use |
| US11274285B2 (en) | 2016-10-14 | 2022-03-15 | Precision Biosciences, Inc. | Engineered meganucleases specific for recognition sequences in the Hepatitis B virus genome |
| US10662416B2 (en) | 2016-10-14 | 2020-05-26 | Precision Biosciences, Inc. | Engineered meganucleases specific for recognition sequences in the hepatitis B virus genome |
| US10980825B2 (en) | 2016-12-01 | 2021-04-20 | Takeda Pharmaceutical Company Limited | Cyclic dinucleotide |
| US12171777B2 (en) | 2016-12-01 | 2024-12-24 | Takeda Pharmaceutical Company Limited | Methods of making a cyclic dinucleotide |
| US11666594B2 (en) | 2016-12-01 | 2023-06-06 | Takeda Pharmaceutical Company Limited | Antibody-drug conjugates comprising a cyclic dinucleotide |
| CN111263767A (zh) * | 2017-08-30 | 2020-06-09 | 北京轩义医药科技有限公司 | 作为干扰素基因调节剂的刺激剂的环状二核苷酸 |
| EP3692048A4 (de) * | 2017-08-30 | 2021-10-20 | Beijing Xuanyi Pharmasciences Co., Ltd. | Cyclische di-nukleotide als stimulator von modulatoren von interferon-genen |
| US11773132B2 (en) | 2017-08-30 | 2023-10-03 | Beijing Xuanyi Pharmasciences Co., Ltd. | Cyclic di-nucleotides as stimulator of interferon genes modulators |
| WO2019043634A2 (en) | 2017-08-30 | 2019-03-07 | Beijing Xuanyi Pharmasciences Co., Ltd. | CYCLIC DI-NUCLEOTIDES AS STIMULATORS OF INTERFERON GENE MODULATORS |
| CN111263767B (zh) * | 2017-08-30 | 2023-07-18 | 北京轩义医药科技有限公司 | 作为干扰素基因调节剂的刺激剂的环状二核苷酸 |
| WO2019084060A1 (en) | 2017-10-24 | 2019-05-02 | Silverback Therapeutics, Inc. | CONJUGATES AND METHODS OF USE FOR THE SELECTIVE DELIVERY OF IMMUNOMODULATORY AGENTS |
| US12054512B2 (en) | 2017-11-10 | 2024-08-06 | Takeda Pharmaceutical Company Limited | Sting modulator compounds, and methods of making and using |
| US11542293B2 (en) | 2017-11-10 | 2023-01-03 | Takeda Pharmaceutical Company Limited | Sting modulator compounds, and methods of making and using |
| US10966999B2 (en) | 2017-12-20 | 2021-04-06 | Institute Of Organic Chemistry And Biochemistry Ascr, V.V.I. | 3′3′ cyclic dinucleotides with phosphonate bond activating the sting adaptor protein |
| US11203610B2 (en) | 2017-12-20 | 2021-12-21 | Institute Of Organic Chemistry And Biochemistry Ascr, V.V.I. | 2′3′ cyclic dinucleotides with phosphonate bond activating the sting adaptor protein |
| WO2019165374A1 (en) | 2018-02-26 | 2019-08-29 | Gilead Sciences, Inc. | Substituted pyrrolizine compounds as hbv replication inhibitors |
| WO2019195181A1 (en) | 2018-04-05 | 2019-10-10 | Gilead Sciences, Inc. | Antibodies and fragments thereof that bind hepatitis b virus protein x |
| US11149052B2 (en) | 2018-04-06 | 2021-10-19 | Institute Of Organic Chemistry And Biochemistry Ascr, V.V.I. | 2′3′-cyclic dinucleotides |
| WO2019193533A1 (en) | 2018-04-06 | 2019-10-10 | Institute Of Organic Chemistry And Biochemistry Ascr, V.V.I. | 2'2'-cyclic dinucleotides |
| WO2019193542A1 (en) | 2018-04-06 | 2019-10-10 | Institute Of Organic Chemistry And Biochemistry Ascr, V.V.I. | 2'3'-cyclic dinucleotides |
| US11292812B2 (en) | 2018-04-06 | 2022-04-05 | Institute Of Organic Chemistry And Biochemistry Ascr, V.V.I. | 3′3′-cyclic dinucleotides |
| WO2019193543A1 (en) | 2018-04-06 | 2019-10-10 | Institute Of Organic Chemistry And Biochemistry Ascr, V.V.I. | 3'3'-cyclic dinucleotides |
| WO2019200247A1 (en) | 2018-04-12 | 2019-10-17 | Precision Biosciences, Inc. | Optimized engineered meganucleases having specificity for a recognition sequence in the hepatitis b virus genome |
| US11142750B2 (en) | 2018-04-12 | 2021-10-12 | Precision Biosciences, Inc. | Optimized engineered meganucleases having specificity for a recognition sequence in the Hepatitis B virus genome |
| US11788077B2 (en) | 2018-04-12 | 2023-10-17 | Precision Biosciences, Inc. | Polynucleotides encoding optimized engineered meganucleases having specificity for a recognition sequence in the Hepatitis B virus genome |
| WO2019211799A1 (en) | 2018-05-03 | 2019-11-07 | Institute Of Organic Chemistry And Biochemistry Ascr, V.V.I. | 2'3'-cyclic dinucleotide analogue comprising a cyclopentanyl modified nucleotide |
| WO2020028097A1 (en) | 2018-08-01 | 2020-02-06 | Gilead Sciences, Inc. | Solid forms of (r)-11-(methoxymethyl)-12-(3-methoxypropoxy)-3,3-dimethyl-8-0x0-2,3,8,13b-tetrahydro-1h-pyrido[2,1-a]pyrrolo[1,2-c] phthalazine-7-c arboxylic acid |
| KR20230122685A (ko) | 2018-09-06 | 2023-08-22 | 다이이찌 산쿄 가부시키가이샤 | 신규 고리형 디뉴클레오티드 유도체 및 그 항체 약물콘쥬게이트 |
| EP4524154A2 (de) | 2018-09-06 | 2025-03-19 | Daiichi Sankyo Company, Limited | Antikörper-wirkstoff-konjugate von cyclischen dinukleotidderivaten |
| KR20250078590A (ko) | 2018-09-06 | 2025-06-02 | 다이이찌 산쿄 가부시키가이샤 | 신규 고리형 디뉴클레오티드 유도체 및 그 항체 약물 콘쥬게이트 |
| US12370263B2 (en) | 2018-09-06 | 2025-07-29 | Daiichi Sankyo Company, Limited | Cyclic dinucleotide derivative based antibody-drug conjugates |
| KR20210057066A (ko) | 2018-09-06 | 2021-05-20 | 다이이찌 산쿄 가부시키가이샤 | 신규 고리형 디뉴클레오티드 유도체 및 그 항체 약물 콘쥬게이트 |
| WO2020050406A1 (ja) | 2018-09-06 | 2020-03-12 | 第一三共株式会社 | 新規環状ジヌクレオチド誘導体及びその抗体薬物コンジュゲート |
| KR20230028589A (ko) | 2018-09-06 | 2023-02-28 | 다이이찌 산쿄 가부시키가이샤 | 신규 고리형 디뉴클레오티드 유도체 및 그 항체 약물 콘쥬게이트 |
| WO2020056008A1 (en) | 2018-09-12 | 2020-03-19 | Silverback Therapeutics, Inc. | Compositions for the treatment of disease with immune stimulatory conjugates |
| US12152051B2 (en) | 2018-09-21 | 2024-11-26 | Shanghai De Novo Pharmatech Co., Ltd. | Cyclic dinucleotide analogue, pharmaceutical composition thereof, and application |
| JP7218431B2 (ja) | 2018-09-21 | 2023-02-06 | シャンハイ ドーァ ノボ ファーマテック カンパニー,リミティド | 環状ジヌクレオチド類似体、その医薬組成物及び使用 |
| WO2020057546A1 (zh) | 2018-09-21 | 2020-03-26 | 上海迪诺医药科技有限公司 | 环状二核苷酸类似物、其药物组合物及应用 |
| JP2022500476A (ja) * | 2018-09-21 | 2022-01-04 | シャンハイ ドーァ ノボ ファーマテック カンパニー,リミティド | 環状ジヌクレオチド類似体、その医薬組成物及び使用 |
| CN112867727A (zh) * | 2018-10-12 | 2021-05-28 | 上海济煜医药科技有限公司 | 环二核苷酸类化合物及其应用 |
| JP7492523B2 (ja) | 2018-10-12 | 2024-05-29 | シャンハイ ジェミンケア ファーマシューティカル カンパニー,リミティド | 環状ジヌクレオチド化合物及びその使用 |
| JP2022508786A (ja) * | 2018-10-12 | 2022-01-19 | シャンハイ ジェミンケア ファーマシューティカルズ カンパニー、リミテッド | 環状ジヌクレオチド化合物及びその使用 |
| EP3868773A4 (de) * | 2018-10-12 | 2022-07-13 | Shanghai Jemincare Pharmaceuticals Co., Ltd. | Zyklische dinukleotidverbindung und verwendungen davon |
| CN112867727B (zh) * | 2018-10-12 | 2024-05-17 | 上海济煜医药科技有限公司 | 环二核苷酸类化合物及其应用 |
| US11401295B2 (en) | 2018-10-12 | 2022-08-02 | Shanghai Jemincare Pharmaceuticals Co., Ltd. | Cyclic dinucleotide compound and uses thereof |
| WO2020074004A1 (zh) * | 2018-10-12 | 2020-04-16 | 上海济煜医药科技有限公司 | 环二核苷酸类化合物及其应用 |
| US11161864B2 (en) | 2018-10-29 | 2021-11-02 | Venenum Biodesign, LLC | Sting agonists |
| US11110106B2 (en) | 2018-10-29 | 2021-09-07 | Venenum Biodesign, LLC | Sting agonists for treating bladder cancer and solid tumors |
| US11883420B2 (en) | 2018-10-29 | 2024-01-30 | Venenum Biodesign, LLC | Sting agonists for treating bladder cancer and solid tumors |
| EP4371987A1 (de) | 2018-10-31 | 2024-05-22 | Gilead Sciences, Inc. | Substituierte 6-azabenzimidazolverbindungen als hpk1-inhibitoren |
| WO2020092528A1 (en) | 2018-10-31 | 2020-05-07 | Gilead Sciences, Inc. | Substituted 6-azabenzimidazole compounds having hpk1 inhibitory activity |
| EP4671244A1 (de) | 2018-10-31 | 2025-12-31 | Gilead Sciences, Inc. | Substituierte 6-azabenzimidazolverbindungen als hpk1-inhibitoren |
| WO2020092621A1 (en) | 2018-10-31 | 2020-05-07 | Gilead Sciences, Inc. | Substituted 6-azabenzimidazole compounds as hpk1 inhibitors |
| CN111349132A (zh) * | 2018-12-21 | 2020-06-30 | 上海济煜医药科技有限公司 | 肿瘤免疫类化合物及其应用 |
| CN111349132B (zh) * | 2018-12-21 | 2021-06-04 | 上海济煜医药科技有限公司 | 肿瘤免疫类化合物及其应用 |
| WO2020132566A1 (en) * | 2018-12-21 | 2020-06-25 | Nimbus Titan, Inc. | Sting pyrazole agonists and uses thereof |
| US11766447B2 (en) | 2019-03-07 | 2023-09-26 | Institute Of Organic Chemistry And Biochemistry Ascr, V.V.I. | 3′3′-cyclic dinucleotide analogue comprising a cyclopentanyl modified nucleotide as sting modulator |
| WO2020178770A1 (en) | 2019-03-07 | 2020-09-10 | Institute Of Organic Chemistry And Biochemistry Ascr, V.V.I. | 3'3'-cyclic dinucleotides and prodrugs thereof |
| WO2020178768A1 (en) | 2019-03-07 | 2020-09-10 | Institute Of Organic Chemistry And Biochemistry Ascr, V.V.I. | 3'3'-cyclic dinucleotide analogue comprising a cyclopentanyl modified nucleotide as sting modulator |
| WO2020178769A1 (en) | 2019-03-07 | 2020-09-10 | Institute Of Organic Chemistry And Biochemistry Ascr, V.V.I. | 2'3'-cyclic dinucleotides and prodrugs thereof |
| US12318403B2 (en) | 2019-03-07 | 2025-06-03 | Institute Of Organic Chemistry And Biochemistry Ascr, V.V.I. | 2′3′-cyclic dinucleotides and prodrugs thereof |
| WO2020214663A1 (en) | 2019-04-17 | 2020-10-22 | Gilead Sciences, Inc. | Solid forms of a toll-like receptor modulator |
| EP4458416A2 (de) | 2019-04-17 | 2024-11-06 | Gilead Sciences, Inc. | Feste formen eines toll-like-rezeptormodulators |
| WO2020214652A1 (en) | 2019-04-17 | 2020-10-22 | Gilead Sciences, Inc. | Solid forms of a toll-like receptor modulator |
| US11787833B2 (en) | 2019-05-09 | 2023-10-17 | Aligos Therapeutics, Inc. | Modified cyclic dinucleoside compounds as sting modulators |
| WO2020237025A1 (en) | 2019-05-23 | 2020-11-26 | Gilead Sciences, Inc. | Substituted exo-methylene-oxindoles which are hpk1/map4k1 inhibitors |
| WO2020263830A1 (en) | 2019-06-25 | 2020-12-30 | Gilead Sciences, Inc. | Flt3l-fc fusion proteins and methods of use |
| WO2021034804A1 (en) | 2019-08-19 | 2021-02-25 | Gilead Sciences, Inc. | Pharmaceutical formulations of tenofovir alafenamide |
| WO2021067181A1 (en) | 2019-09-30 | 2021-04-08 | Gilead Sciences, Inc. | Hbv vaccines and methods treating hbv |
| EP4458975A2 (de) | 2019-09-30 | 2024-11-06 | Gilead Sciences, Inc. | Hbv-impfstoffe und verfahren zur behandlung von hbv |
| WO2021067644A1 (en) | 2019-10-01 | 2021-04-08 | Silverback Therapeutics, Inc. | Combination therapy with immune stimulatory conjugates |
| EP4567109A2 (de) | 2019-12-06 | 2025-06-11 | Precision Biosciences, Inc. | Optimierte, manipulierte meganukleasen mit spezifität für eine erkennungssequenz im hepatitis-b-virus-genom |
| WO2021113765A1 (en) | 2019-12-06 | 2021-06-10 | Precision Biosciences, Inc. | Optimized engineered meganucleases having specificity for a recognition sequence in the hepatitis b virus genome |
| US12410418B2 (en) | 2019-12-06 | 2025-09-09 | Precision Biosciences, Inc. | Optimized engineered meganucleases having specificity for a recognition sequence in the Hepatitis B virus genome |
| WO2021168274A1 (en) | 2020-02-21 | 2021-08-26 | Silverback Therapeutics, Inc. | Nectin-4 antibody conjugates and uses thereof |
| US12364768B2 (en) | 2020-02-21 | 2025-07-22 | Araris Biotech Ag | Nectin-4 antibody conjugates and uses thereof |
| US11179473B2 (en) | 2020-02-21 | 2021-11-23 | Silverback Therapeutics, Inc. | Nectin-4 antibody conjugates and uses thereof |
| WO2021177438A1 (ja) | 2020-03-06 | 2021-09-10 | 第一三共株式会社 | 新規環状ジヌクレオチド誘導体を含む抗体薬物コンジュゲート |
| KR20220151630A (ko) | 2020-03-06 | 2022-11-15 | 다이이찌 산쿄 가부시키가이샤 | 신규 고리형 디뉴클레오티드 유도체를 포함하는 항체 약물 컨쥬게이트 |
| WO2021188959A1 (en) | 2020-03-20 | 2021-09-23 | Gilead Sciences, Inc. | Prodrugs of 4'-c-substituted-2-halo-2'-deoxyadenosine nucleosides and methods of making and using the same |
| WO2021206158A1 (ja) | 2020-04-10 | 2021-10-14 | 小野薬品工業株式会社 | がん治療方法 |
| US11541126B1 (en) | 2020-07-01 | 2023-01-03 | Silverback Therapeutics, Inc. | Anti-ASGR1 antibody TLR8 agonist comprising conjugates and uses thereof |
| WO2022006327A1 (en) | 2020-07-01 | 2022-01-06 | Silverback Therapeutics, Inc. | Anti-asgr1 antibody conjugates and uses thereof |
| EP4667477A2 (de) | 2020-08-07 | 2025-12-24 | Gilead Sciences, Inc. | Prodrugs von phosphonamidnukleotidanaloga und deren pharmazeutische verwendung |
| WO2022031894A1 (en) | 2020-08-07 | 2022-02-10 | Gilead Sciences, Inc. | Prodrugs of phosphonamide nucleotide analogues and their pharmaceutical use |
| WO2022050300A1 (ja) | 2020-09-02 | 2022-03-10 | 第一三共株式会社 | 新規エンド-β-N-アセチルグルコサミニダーゼ |
| US12221460B2 (en) | 2020-11-09 | 2025-02-11 | Takeda Pharmaceutical Company Limited | Antibody drug conjugates |
| US11725024B2 (en) | 2020-11-09 | 2023-08-15 | Takeda Pharmaceutical Company Limited | Antibody drug conjugates |
| WO2022241134A1 (en) | 2021-05-13 | 2022-11-17 | Gilead Sciences, Inc. | COMBINATION OF A TLR8 MODULATING COMPOUND AND ANTI-HBV siRNA THERAPEUTICS |
| WO2022245671A1 (en) | 2021-05-18 | 2022-11-24 | Gilead Sciences, Inc. | Methods of using flt3l-fc fusion proteins |
| WO2022271684A1 (en) | 2021-06-23 | 2022-12-29 | Gilead Sciences, Inc. | Diacylglyercol kinase modulating compounds |
| WO2022271677A1 (en) | 2021-06-23 | 2022-12-29 | Gilead Sciences, Inc. | Diacylglyercol kinase modulating compounds |
| WO2022271650A1 (en) | 2021-06-23 | 2022-12-29 | Gilead Sciences, Inc. | Diacylglyercol kinase modulating compounds |
| WO2022271659A1 (en) | 2021-06-23 | 2022-12-29 | Gilead Sciences, Inc. | Diacylglyercol kinase modulating compounds |
| WO2023167238A1 (ja) | 2022-03-02 | 2023-09-07 | 第一三共株式会社 | Fc含有分子の製造方法 |
| KR20250054799A (ko) | 2022-08-29 | 2025-04-23 | 다이이찌 산쿄 가부시키가이샤 | 변이 Fc 영역을 포함하는 항체 약물 콘쥬게이트 |
| WO2024048490A1 (ja) | 2022-08-29 | 2024-03-07 | 第一三共株式会社 | 変異Fc領域を含む抗体薬物コンジュゲート |
| WO2025240246A1 (en) | 2024-05-13 | 2025-11-20 | Gilead Sciences, Inc. | Combination therapies with ribavirin |
| WO2025240243A1 (en) | 2024-05-13 | 2025-11-20 | Gilead Sciences, Inc. | Combination therapies with bulevirtide and an inhibitory nucleic acid targeting hepatitis b virus |
| WO2025240242A1 (en) | 2024-05-13 | 2025-11-20 | Gilead Sciences, Inc. | Combination therapies with ribavirin |
| WO2025240244A1 (en) | 2024-05-13 | 2025-11-20 | Gilead Sciences, Inc. | Combination therapies comprising bulevirtide and lonafarnib for use in the treatment of hepatitis d virus infection |
Also Published As
| Publication number | Publication date |
|---|---|
| US20200040028A1 (en) | 2020-02-06 |
| EP3523314A1 (de) | 2019-08-14 |
| US11001605B2 (en) | 2021-05-11 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP3523314A1 (de) | Benzimidazolhaltige cyclische dinukleotide, verfahren zu deren herstellung und ihre verwendung zur aktivierung von stimulator von interferongenen (sting)-abhängigen signalwegen | |
| EP3546473B1 (de) | Fluorierte cyclische [(2',5')p(3',5')p]-dinukleotide zur cytokininduktion | |
| Kim et al. | Potential anti-AIDS drugs. 2', 3'-Dideoxycytidine analogs | |
| DE60126762T2 (de) | Kombinatorische Herstellung von Nukleotid- und Nukleosid- (XITP) Analogen | |
| DE3854297T2 (de) | Nucleoside und nucleotide mit antiviraler, antitumoraler, antimetastatischer sowie immunstimulierender wirkung. | |
| Martin et al. | Synthesis and antiviral activity of monofluoro and difluoro analogs of pyrimidine deoxyribonucleosides against human immunodeficiency virus (HIV-1) | |
| DE69829760T3 (de) | Bi- und tri-zyklische - nukleosid, nukleotid und oligonukleotid-analoga | |
| Ravi et al. | Adenine nucleotide analogues locked in a Northern methanocarba conformation: enhanced stability and potency as P2Y1 receptor agonists | |
| KR20110115601A (ko) | 암 및 바이러스 감염 치료용 퓨린 뉴클레오시드 모노포스페이트 프로드럭 | |
| DD296687A5 (de) | Nucleosid-derivate und deren verwendung als arzneimittel | |
| Nahum et al. | Adenosine 5 ‘-O-(1-boranotriphosphate) derivatives as novel P2Y1 receptor agonists | |
| Ginsburg-Shmuel et al. | UDP made a highly promising stable, potent, and selective P2Y6-receptor agonist upon introduction of a boranophosphate moiety | |
| Eletskaya et al. | Enzymatic synthesis of novel purine nucleosides bearing a chiral benzoxazine fragment | |
| Ottria et al. | Synthesis and evaluation of in vitro anticancer activity of some novel isopentenyladenosine derivatives | |
| Białek-Pietras et al. | Synthesis, susceptibility to enzymatic phosphorylation, cytotoxicity and in vitro antiviral activity of lipophilic pyrimidine nucleoside/carborane conjugates | |
| Kharitonova et al. | Chemoenzymatic synthesis and antiherpes activity of 5-substituted 4, 6-difluorobenzimidazoles ribo-and 2′-deoxyribonucleosides | |
| Ginsburg-Shmuel et al. | 5-OMe-UDP is a potent and selective P2Y6-receptor agonist | |
| Rios Morales et al. | Diastereoselective Synthesis of cycloSaligenyl‐Nucleosyl‐Phosphotriesters | |
| Weising et al. | Triphosphate prodrugs of the anti-HIV-active compound 3′-deoxy-3′-fluorothymidine (FLT) | |
| Díaz-Rodríguez et al. | Synthesis and anti-HIV activity of conformationally restricted bicyclic hexahydroisobenzofuran nucleoside analogs | |
| Kulikowski et al. | Synthesis and antiviral activities of arabinofuranosyl-5-ethylpyrimidine nucleosides. Selective antiherpes activity of 1-(. beta.-D-arabinofuranosyl)-5-ethyluracil | |
| Li et al. | Novel nucleobase-simplified cyclic ADP-ribose analogue: A concise synthesis and Ca 2+-mobilizing activity in T-lymphocytes | |
| WO2015197655A1 (en) | Methods and products from the reaction of tetrazines with nucleic acid polymers bearing ethenyl aromatic groups | |
| KR102515251B1 (ko) | 새로운 트라이아진 기반의 양친매성 화합물 및 이의 활용 | |
| Velanguparackel et al. | Synthesis, anti-HIV and cytostatic evaluation of 3′-deoxy-3′-fluorothymidine (FLT) pro-nucleotides |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 17786843 Country of ref document: EP Kind code of ref document: A1 |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| ENP | Entry into the national phase |
Ref document number: 2017786843 Country of ref document: EP Effective date: 20190507 |