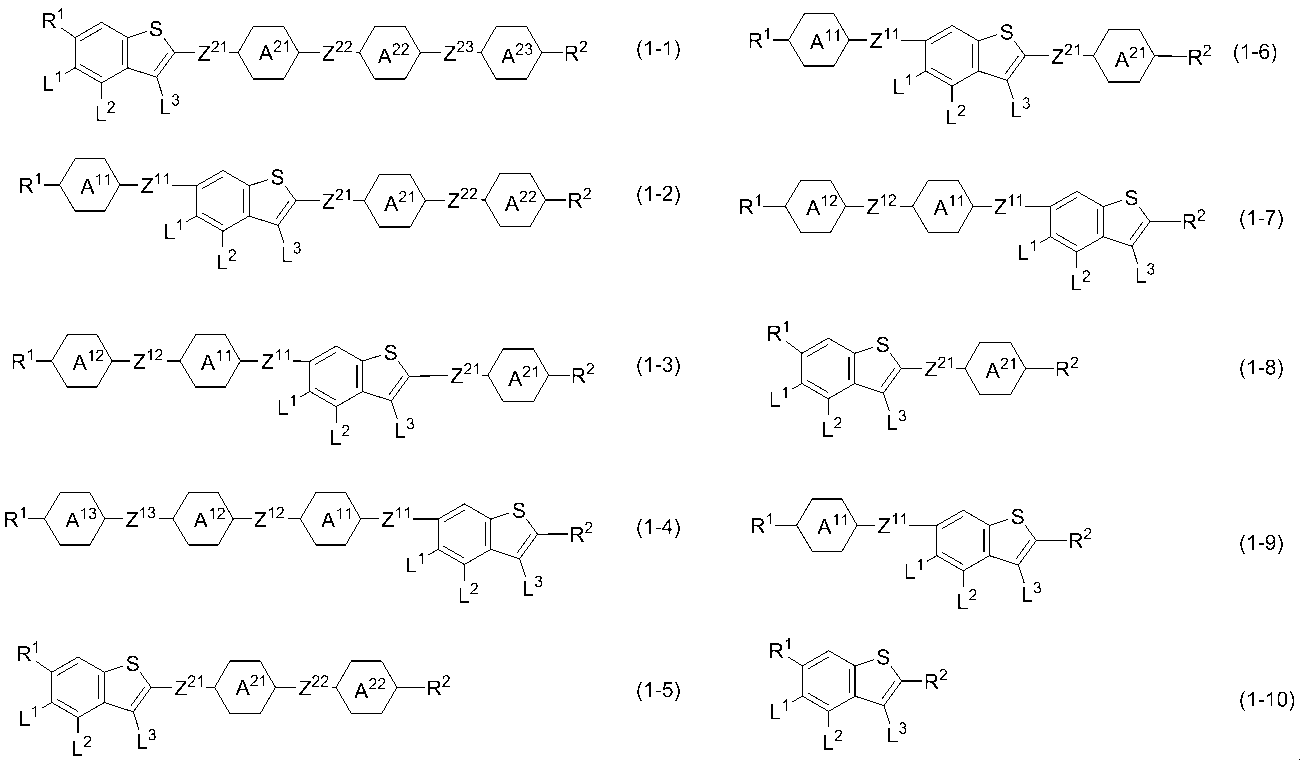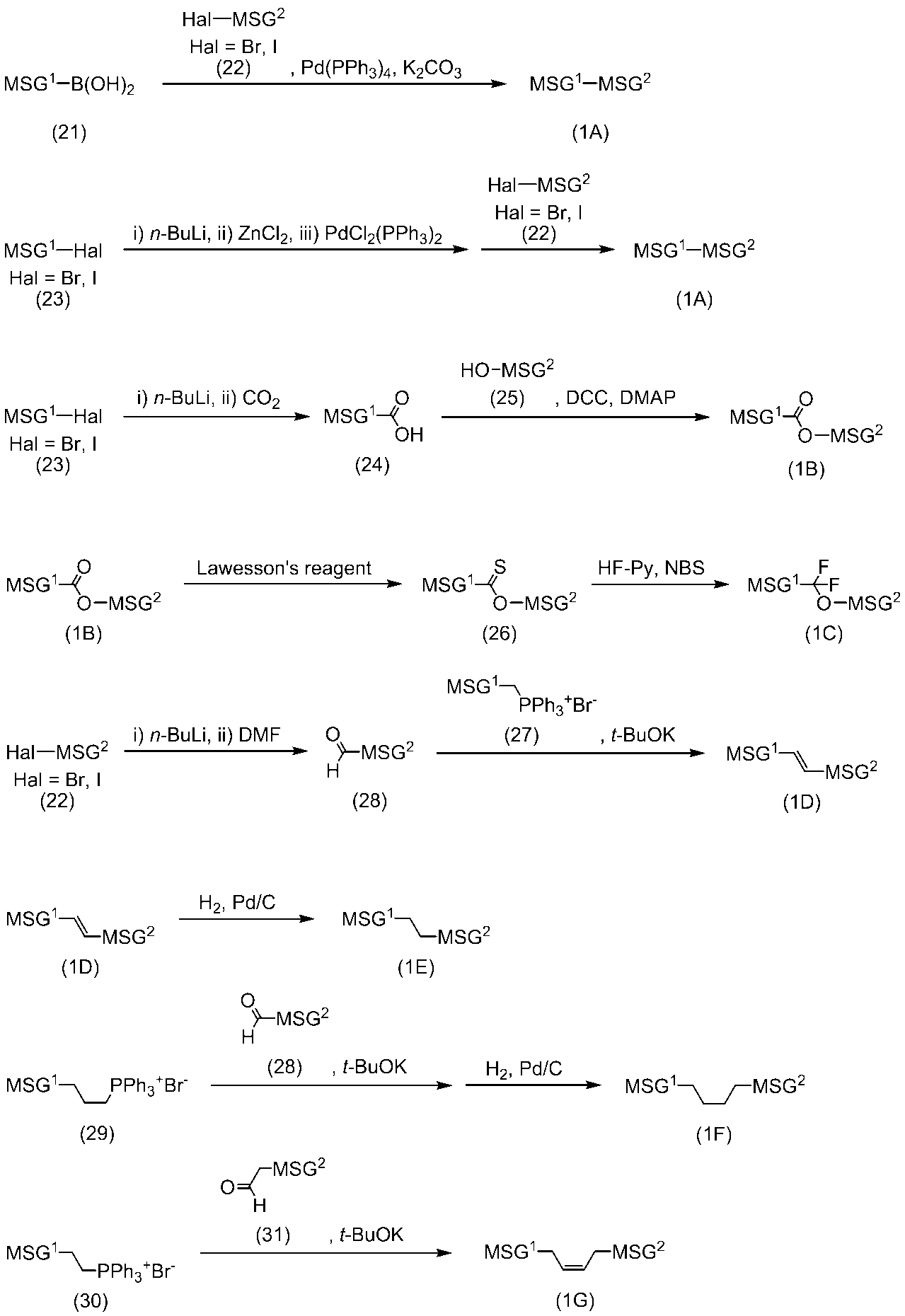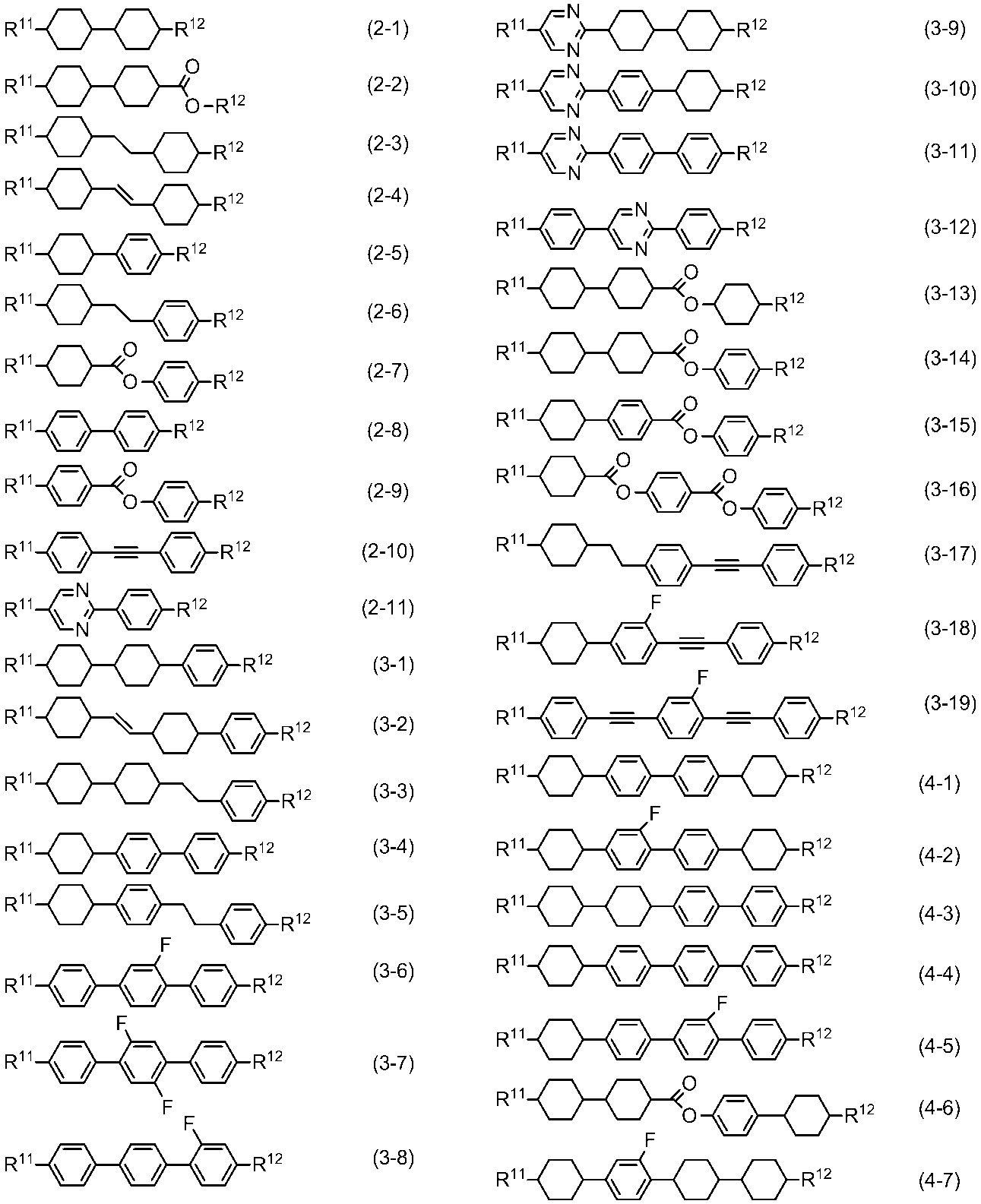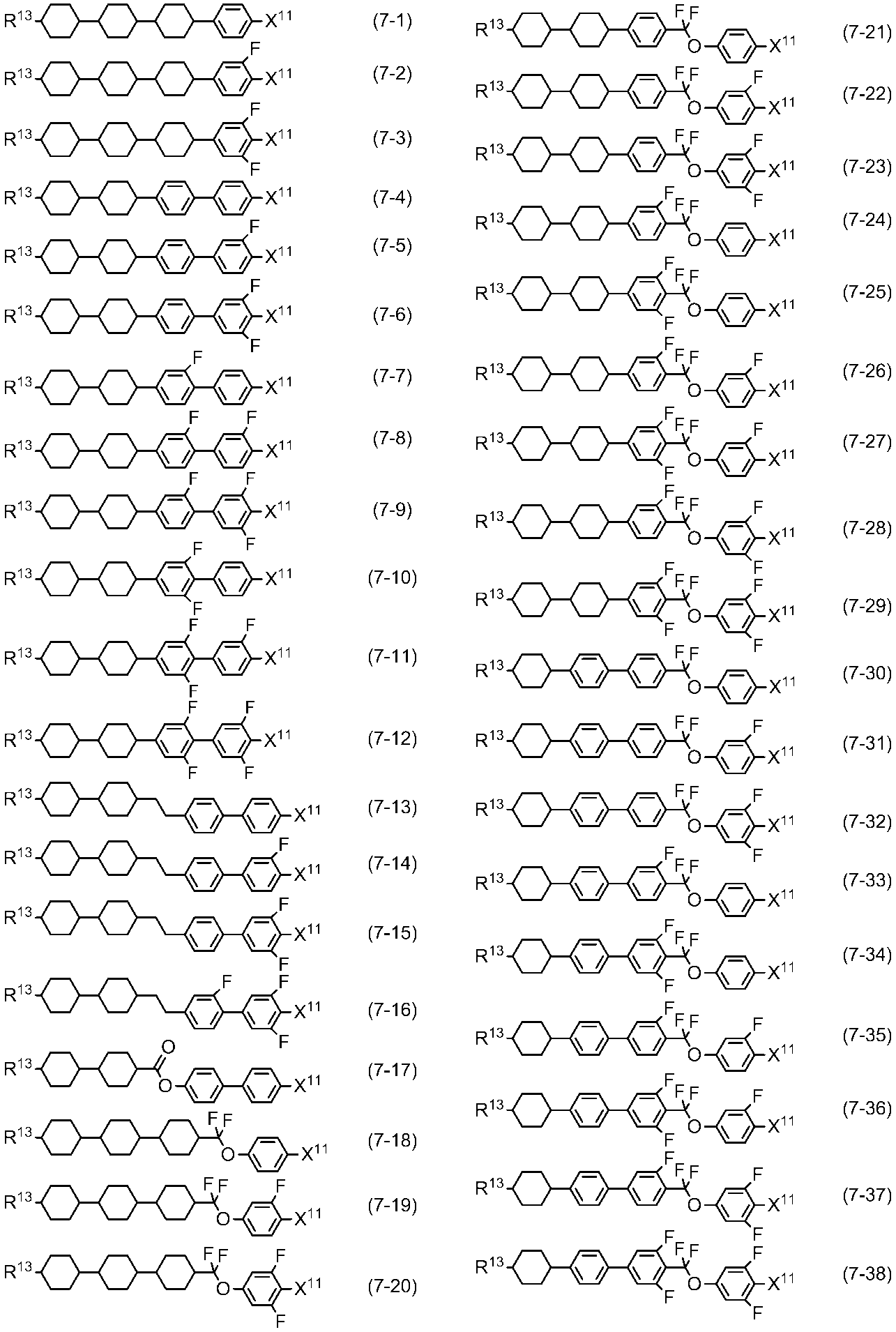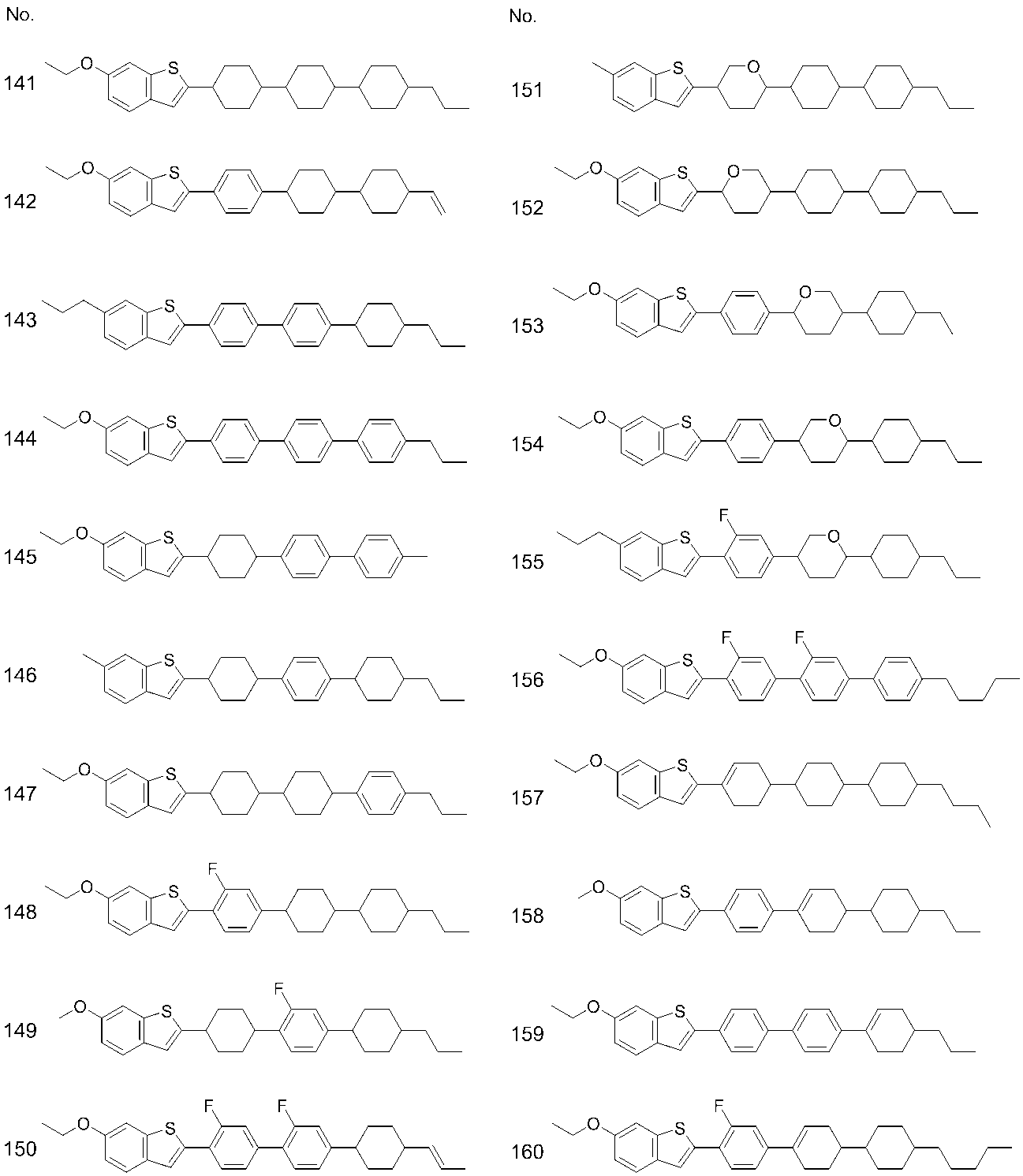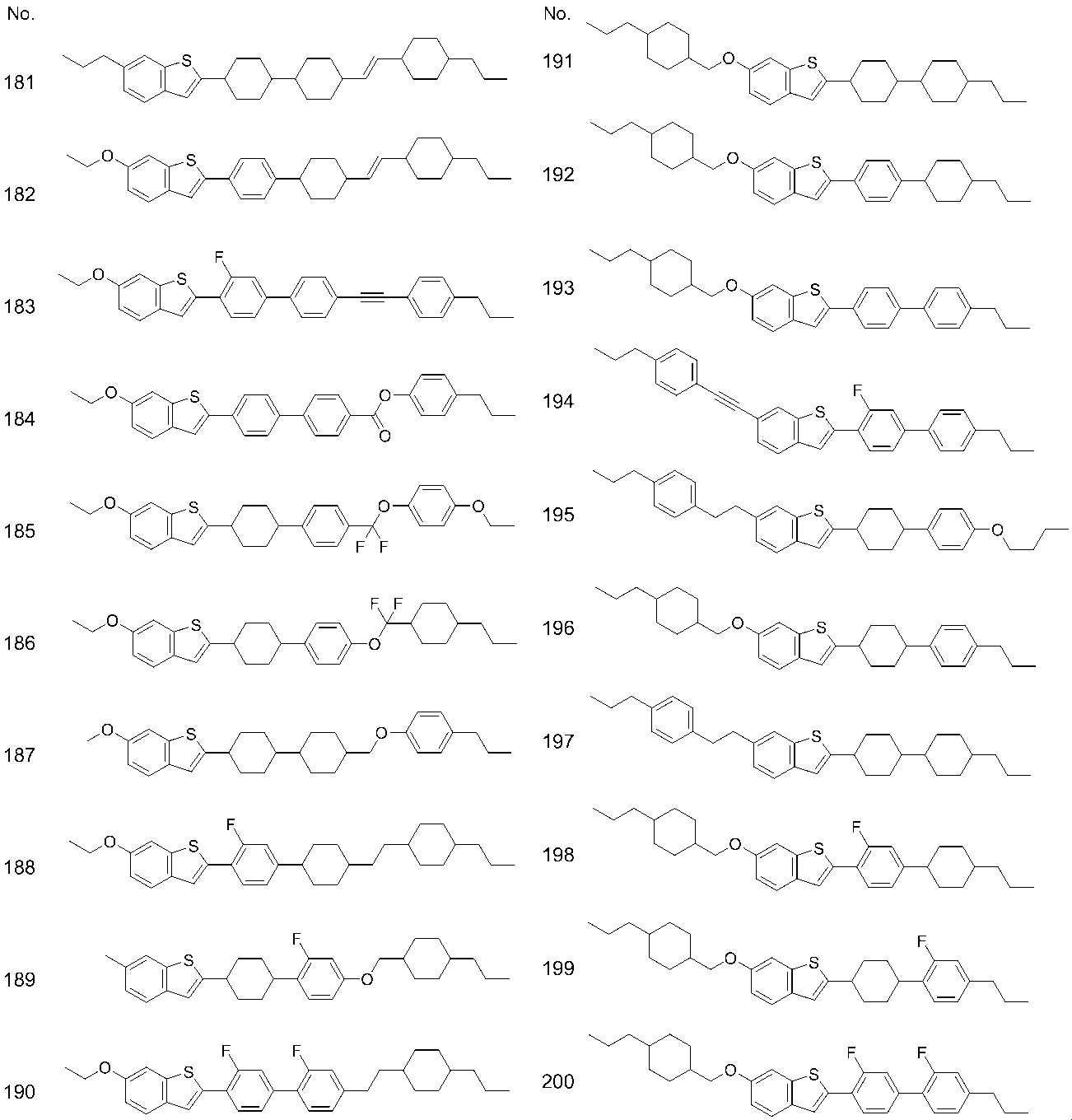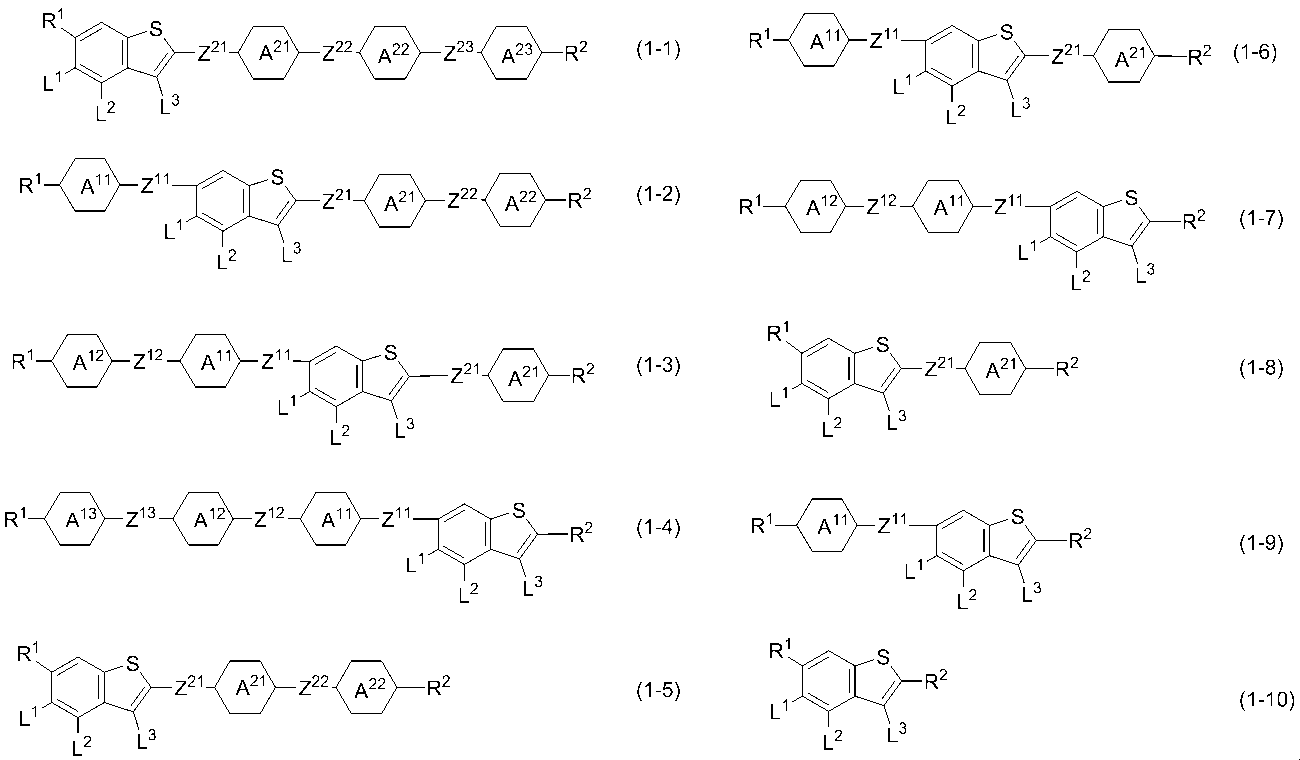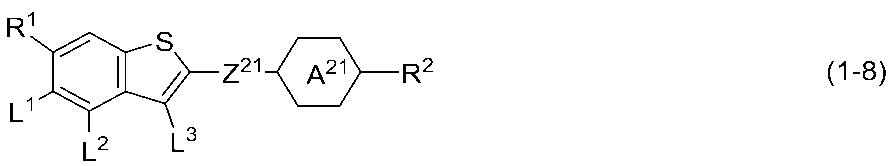WO2017064892A1 - ベンゾチオフェンを有する液晶性化合物、液晶組成物および液晶表示素子 - Google Patents
ベンゾチオフェンを有する液晶性化合物、液晶組成物および液晶表示素子 Download PDFInfo
- Publication number
- WO2017064892A1 WO2017064892A1 PCT/JP2016/070418 JP2016070418W WO2017064892A1 WO 2017064892 A1 WO2017064892 A1 WO 2017064892A1 JP 2016070418 W JP2016070418 W JP 2016070418W WO 2017064892 A1 WO2017064892 A1 WO 2017064892A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- ring
- carbons
- independently
- hydrogen
- replaced
- Prior art date
Links
- 0 C=NC1CC*CC1 Chemical compound C=NC1CC*CC1 0.000 description 12
- PEQRFJRKTICJRN-VAWYXSNFSA-N C=CC(CC1)CCC1N/C=C/C(CC1)CCC1N Chemical compound C=CC(CC1)CCC1N/C=C/C(CC1)CCC1N PEQRFJRKTICJRN-VAWYXSNFSA-N 0.000 description 1
- VZNHJVJAZKQUNL-UHFFFAOYSA-N C=NC(CC1)CCC1N Chemical compound C=NC(CC1)CCC1N VZNHJVJAZKQUNL-UHFFFAOYSA-N 0.000 description 1
- KSMVBYPXNKCPAJ-UHFFFAOYSA-N CC(CC1)CCC1N Chemical compound CC(CC1)CCC1N KSMVBYPXNKCPAJ-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D333/00—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom
- C07D333/50—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom condensed with carbocyclic rings or ring systems
- C07D333/52—Benzo[b]thiophenes; Hydrogenated benzo[b]thiophenes
- C07D333/54—Benzo[b]thiophenes; Hydrogenated benzo[b]thiophenes with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to carbon atoms of the hetero ring
- C07D333/56—Radicals substituted by oxygen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D333/00—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom
- C07D333/50—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom condensed with carbocyclic rings or ring systems
- C07D333/52—Benzo[b]thiophenes; Hydrogenated benzo[b]thiophenes
- C07D333/54—Benzo[b]thiophenes; Hydrogenated benzo[b]thiophenes with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to carbon atoms of the hetero ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D333/00—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom
- C07D333/50—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom condensed with carbocyclic rings or ring systems
- C07D333/52—Benzo[b]thiophenes; Hydrogenated benzo[b]thiophenes
- C07D333/62—Benzo[b]thiophenes; Hydrogenated benzo[b]thiophenes with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to carbon atoms of the hetero ring
- C07D333/64—Oxygen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D333/00—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom
- C07D333/50—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom condensed with carbocyclic rings or ring systems
- C07D333/52—Benzo[b]thiophenes; Hydrogenated benzo[b]thiophenes
- C07D333/62—Benzo[b]thiophenes; Hydrogenated benzo[b]thiophenes with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to carbon atoms of the hetero ring
- C07D333/68—Carbon atoms having three bonds to hetero atoms with at the most one bond to halogen
- C07D333/70—Carbon atoms having three bonds to hetero atoms with at the most one bond to halogen attached in position 2
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings
- C07D409/04—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings
- C07D409/10—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings
- C07D409/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/10—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing at least two benzene rings
- C09K19/12—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing at least two benzene rings at least two benzene rings directly linked, e.g. biphenyls
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/10—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing at least two benzene rings
- C09K19/14—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing at least two benzene rings linked by a carbon chain
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/10—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing at least two benzene rings
- C09K19/14—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing at least two benzene rings linked by a carbon chain
- C09K19/18—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing at least two benzene rings linked by a carbon chain the chain containing carbon-to-carbon triple bonds, e.g. tolans
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/10—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing at least two benzene rings
- C09K19/20—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing at least two benzene rings linked by a chain containing carbon and oxygen atoms as chain links, e.g. esters or ethers
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/30—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing saturated or unsaturated non-aromatic rings, e.g. cyclohexane rings
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/32—Non-steroidal liquid crystal compounds containing condensed ring systems, i.e. fused, bridged or spiro ring systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/34—Non-steroidal liquid crystal compounds containing at least one heterocyclic ring
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/34—Non-steroidal liquid crystal compounds containing at least one heterocyclic ring
- C09K19/3491—Non-steroidal liquid crystal compounds containing at least one heterocyclic ring having sulfur as hetero atom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/52—Liquid crystal materials characterised by components which are not liquid crystals, e.g. additives with special physical aspect: solvents, solid particles
- C09K19/54—Additives having no specific mesophase characterised by their chemical composition
-
- G—PHYSICS
- G02—OPTICS
- G02F—OPTICAL DEVICES OR ARRANGEMENTS FOR THE CONTROL OF LIGHT BY MODIFICATION OF THE OPTICAL PROPERTIES OF THE MEDIA OF THE ELEMENTS INVOLVED THEREIN; NON-LINEAR OPTICS; FREQUENCY-CHANGING OF LIGHT; OPTICAL LOGIC ELEMENTS; OPTICAL ANALOGUE/DIGITAL CONVERTERS
- G02F1/00—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics
- G02F1/01—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour
- G02F1/13—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour based on liquid crystals, e.g. single liquid crystal display cells
Definitions
- the present invention relates to a liquid crystal compound and a liquid crystal composition. More specifically, the present invention relates to a compound having benzothiophene, a liquid crystal composition containing this compound and having a nematic phase, and a liquid crystal display device containing this composition.
- Liquid crystal display elements are widely used for displays such as personal computers and televisions. This element utilizes the optical anisotropy and dielectric anisotropy of a liquid crystalline compound.
- PC phase change
- TN twisted nematic
- STN super twisted nematic
- BTN bistable twisted nematic
- ECB electrically controlled birefringence
- OCB optical compensated bend
- IPS There are modes such as (in-plane switching), VA (vertical alignment), FFS (Fringe Field Switching), and PSA (polymer sustained alignment).
- liquid crystal composition having appropriate physical properties is used.
- the liquid crystal compound contained in the composition has the physical properties shown in the following (1) to (8).
- (1) High stability to heat, light, etc. (2) High clearing point, (3) Low minimum temperature of liquid crystal phase, (4) Small viscosity ( ⁇ ), (5) Appropriate optical anisotropy ( ⁇ n) (6) Large dielectric anisotropy ( ⁇ ), (7) Appropriate elastic constant (K), (8) Excellent compatibility with other liquid crystal compounds.
- the effect of the physical properties of the liquid crystal compound on the characteristics of the device is as follows.
- a compound having high stability against heat, light, etc. increases the voltage holding ratio of the device. This increases the lifetime of the device.
- a compound having a high clearing point as in (2) widens the usable temperature range of the device.
- a compound having a lower minimum temperature of the liquid crystal phase such as a nematic phase or a smectic phase, particularly a lower minimum temperature of the nematic phase also extends the usable temperature range of the device.
- a compound having a small viscosity shortens the response time of the device.
- a compound having a large optical anisotropy improves the contrast of the device.
- a compound having a large optical anisotropy or a small optical anisotropy that is, an appropriate optical anisotropy is required.
- a compound having a large dielectric anisotropy as in (6) lowers the threshold voltage of the device. This reduces the power consumption of the element.
- a compound having a small dielectric anisotropy shortens the response time of the device by reducing the viscosity of the composition.
- a compound having a large elastic constant shortens the response time of the device.
- a compound having a small elastic constant lowers the threshold voltage of the device. Therefore, an appropriate elastic constant is required according to the characteristics to be improved.
- a compound having excellent compatibility with other liquid crystal compounds as in (8) is preferred. This is because liquid crystal compounds having different physical properties are mixed to adjust the physical properties of the composition.
- Patent Documents 1 and 2 disclose compounds (A) to (D) and the like. However, the properties of these compounds are not described, and it is unclear whether they are suitable as liquid crystal compounds.
- the first problem is high stability against heat and light, high clearing point (or high maximum temperature of nematic phase), low minimum temperature of liquid crystal phase, small viscosity, appropriate optical anisotropy, large positive dielectric constant difference. It is to provide a liquid crystal compound satisfying at least one of physical properties such as isotropic property, appropriate elastic constant, and excellent compatibility with other liquid crystal compounds.
- the second problem is that it contains this compound and has high stability to heat and light, high maximum temperature of nematic phase, low minimum temperature of nematic phase, small viscosity, appropriate optical anisotropy, large dielectric anisotropy
- Another object of the present invention is to provide a liquid crystal composition satisfying at least one of physical properties such as a large specific resistance and an appropriate elastic constant.
- An object of the present invention is to provide a liquid crystal composition having an appropriate balance regarding at least two physical properties.
- a third problem is to provide a liquid crystal display device comprising this composition and having a wide temperature range in which the device can be used, a short response time, a large voltage holding ratio, a low threshold voltage, a large contrast ratio, and a long lifetime. That is.
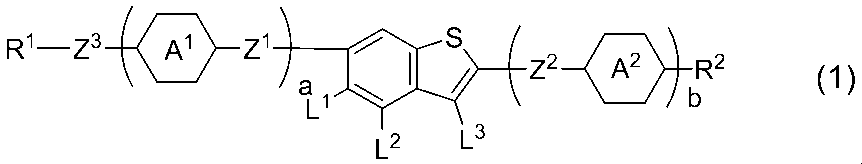
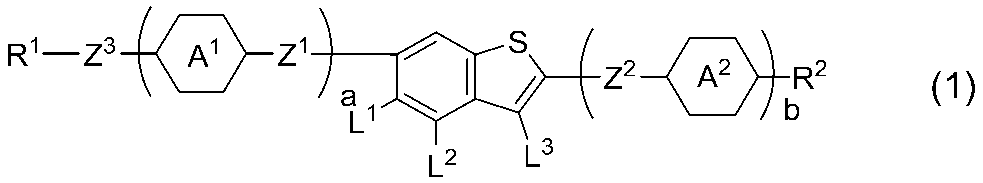
- the present invention relates to a compound represented by the formula (1), a liquid crystal composition containing the compound, and a liquid crystal display device including the composition.
- R 1 and R 2 are independently hydrogen or alkyl having 1 to 20 carbons, in which at least one —CH 2 — may be replaced by —O— or —S—, and at least 1 Two — (CH 2 ) 2 — may be replaced by —CH ⁇ CH—, in which at least one hydrogen may be replaced by a halogen;
- Ring A 1 and Ring A 2 are independently 1,4-cyclohexylene, 1,4-cyclohexenylene, 1,4-phenylene, tetrahydropyran-2,5-diyl, 1,3-dioxane-2, 5-diyl, pyrimidine-2,5-diyl, 2,6,7-trioxabicyclo [2.2.2] octane-1,4-diyl, naphthalene-2,6-diyl,
- the first advantage is high stability to heat and light, high clearing point (or high maximum temperature of nematic phase), low minimum temperature of liquid crystal phase, small viscosity, appropriate optical anisotropy, large dielectric anisotropy
- Another object of the present invention is to provide a liquid crystalline compound satisfying at least one of physical properties such as an appropriate elastic constant and excellent compatibility with other liquid crystalline compounds.
- the second advantage is that it contains this compound, high stability to heat and light, high maximum temperature of nematic phase, low minimum temperature of nematic phase, small viscosity, appropriate optical anisotropy, large dielectric anisotropy
- Another object of the present invention is to provide a liquid crystal composition satisfying at least one of physical properties such as a large specific resistance and an appropriate elastic constant.
- the advantage is to provide a liquid crystal composition having an appropriate balance regarding at least two physical properties.
- the third advantage is to provide a liquid crystal display device comprising this composition and having a wide temperature range in which the device can be used, a short response time, a large voltage holding ratio, a low threshold voltage, a large contrast ratio, and a long lifetime. That is.
- liquid crystal compound liquid crystal composition
- liquid crystal display element liquid crystal display element
- compound liquid crystal phase
- element physical properties of the composition
- This compound has a six-membered ring such as 1,4-cyclohexylene and 1,4-phenylene, and its molecular structure is rod-like.
- Liquid crystal display element is a general term for liquid crystal display panels and liquid crystal display modules.
- the “polymerizable compound” is a compound added for the purpose of forming a polymer in the composition.
- the liquid crystal composition is prepared by mixing a plurality of liquid crystal compounds.
- the ratio (content) of the liquid crystal compound is expressed as a percentage by weight (% by weight) based on the weight of the liquid crystal composition.
- This composition requires additives such as polymerizable compounds, polymerization initiators, polymerization inhibitors, optically active compounds, antioxidants, UV absorbers, light stabilizers, heat stabilizers, dyes, and antifoaming agents. Added accordingly.
- the ratio (addition amount) of the additive is represented by a weight percentage (% by weight) based on the weight of the liquid crystal composition, similarly to the ratio of the liquid crystal compound. Weight parts per million (ppm) may be used.
- the ratio of the polymerization initiator and the polymerization inhibitor is exceptionally expressed based on the weight of the polymerizable compound.
- “Clearing point” is a transition temperature between a liquid crystal phase and an isotropic phase in a liquid crystal compound.
- “Lower limit temperature of liquid crystal phase” is a transition temperature of a solid-liquid crystal phase (smectic phase, nematic phase, etc.) in a liquid crystal compound.
- the “maximum temperature of the nematic phase” is a transition temperature of a nematic phase to an isotropic phase in a mixture or liquid crystal composition of a liquid crystal compound and a mother liquid crystal, and may be abbreviated as “maximum temperature”.
- “Lower limit temperature of nematic phase” may be abbreviated as “lower limit temperature”.
- increasing dielectric anisotropy means that when the composition has a positive dielectric anisotropy, the value increases positively, and the composition having a negative dielectric anisotropy When it is a thing, it means that the value increases negatively.
- the compound represented by Formula (1) may be abbreviated as Compound (1).
- At least one compound selected from the group of compounds represented by formula (1) may be abbreviated as compound (1).
- “Compound (1)” means one compound represented by formula (1), a mixture of two compounds, or a mixture of three or more compounds. These rules also apply to compounds represented by other formulas.
- symbols such as A 1 surrounded by hexagons respectively correspond to rings such as ring A 1 .
- the hexagon represents a six-membered ring such as cyclohexane or benzene.
- the hexagon may represent a condensed ring such as naphthalene or a bridged ring such as adamantane.
- the symbol of the terminal group R 1 is used for a plurality of compounds.
- two groups represented by two arbitrary R 1 may be the same or different.
- R 1 of the compound (1-1) is ethyl and R 1 of the compound (1-2) is ethyl.
- R 1 of compound (1-1) is ethyl and R 1 of compound (1-2) is propyl.
- This rule also applies to symbols such as R 11 and Z 11 .
- compound (8) when i is 2, two rings D 1 exist. In this compound, the two groups represented by the two rings D 1 may be the same or different. When i is greater than 2, it also applies to any two rings D 1 . This rule also applies to other symbols.
- the expression “at least one 'A'” means that the number of 'A' is arbitrary.
- the expression “at least one 'A' may be replaced by 'B'” means that when the number of 'A' is one, the position of 'A' is arbitrary and the number of 'A' is 2 Even when there are more than two, it means that their positions can be selected without limitation. This rule also applies to the expression “at least one 'A' is replaced by 'B'”.
- the expression “at least one A may be replaced by B, C, or D” means that any A is replaced by B, any A is replaced by C, and any A is D Is replaced with a case where a plurality of A is replaced with at least two of B, C, and D.
- alkyl in which at least one —CH 2 — may be replaced by —O— or —CH ⁇ CH— includes alkyl, alkenyl, alkoxy, alkoxyalkyl, alkoxyalkenyl, alkenyloxyalkyl. Note that it is not preferable that two consecutive —CH 2 — are replaced by —O— to form —O—O—.
- Halogen is fluorine, chlorine, bromine and iodine. Preferred halogens are fluorine and chlorine. A more preferred halogen is fluorine.
- Alkyl is linear or branched and does not include cyclic alkyl. Linear alkyl is generally preferred over branched alkyl. The same applies to terminal groups such as alkoxy and alkenyl. As the configuration of 1,4-cyclohexylene, trans is preferable to cis for increasing the maximum temperature.
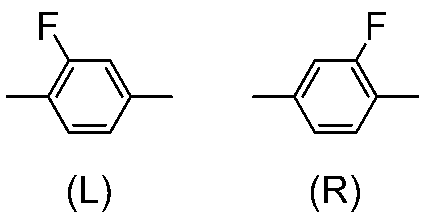
- 2-Fluoro-1,4-phenylene means the following two divalent groups. In the chemical formula, fluorine may be leftward (L) or rightward (R). This rule also applies to asymmetric divalent groups generated by removing two hydrogens from the ring, such as tetrahydropyran-2,5-diyl.
- the present invention includes the following items.
- R 1 and R 2 are independently hydrogen or alkyl having 1 to 20 carbons, in which at least one —CH 2 — may be replaced by —O— or —S—, and at least 1 Two — (CH 2 ) 2 — may be replaced by —CH ⁇ CH—, in which at least one hydrogen may be replaced by a halogen; Ring A 1 and Ring A 2 are independently 1,4-cyclohexylene, 1,4-cyclohexenylene, 1,4-phenylene, tetrahydropyran-2,5-diyl, 1,3-dioxane-2, 5-diyl, pyrimidine-2,5-diyl, 2,6,7-trioxabicyclo [2.2.2] octane-1,4-diyl, naphthalene-2,6-diyl, or pyridine-2,5 -Diyl, wherein at least one hydrogen on these rings may be replaced by
- R 1 and R 2 are independently hydrogen, alkyl having 1 to 10 carbons, alkoxy having 1 to 9 carbons, alkenyl having 2 to 10 carbons, or 1 carbon in which at least one hydrogen is replaced by fluorine.
- Ring A 1 and Ring A 2 are independently 1,4-cyclohexylene, 1,4-cyclohexenylene, 1,4-phenylene in which at least one hydrogen may be replaced by halogen, or tetrahydropyran-2 , 5-diyl
- Z 1 and Z 2 are independently a single bond, — (CH 2 ) 2 —, —CH ⁇ CH—, —CF ⁇ CF—, —C ⁇ C—, —COO—, —OCO—, —CF 2 O—, —OCF 2 —, —CH 2 O—, —OCH 2 —, — (CH 2 ) 4 —, — (CH 2 ) 2 CF 2 O—, — (CH 2 )
- a and b is 0, 1, 2, or 3;
- R 1 and R 2 are independently hydrogen, alkyl having 1 to 10 carbons, alkoxy having 1 to 9 carbons, alkenyl having 2 to 10 carbons, or fluorinated alkyl having 1 to 10 carbons;
- Ring A 1 and Ring A 2 are independently 1,4-cyclohexylene, 1,4-cyclohexenylene, 1,4-phenylene in which at least one hydrogen may be replaced by halogen, or tetrahydropyran-2 , 5-Diyl present;
- Z 1 and Z 2 are independently a single bond, — (CH 2 ) 2 —, —CH ⁇ CH—, —CF ⁇ CF—, —C ⁇ C—, —COO—, —OCO—, —CF 2 O—, —OCF 2 —, —CH 2 O—, —OCH 2 —, — (CH 2 ) 4 —, — (CH 2 ) 2 CF 2 O
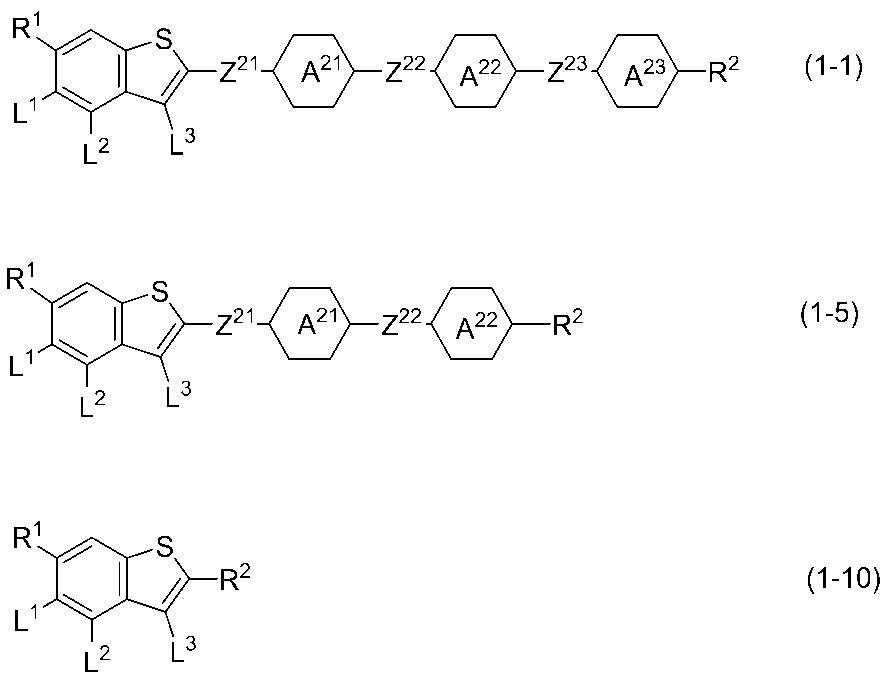
- Item 4. The compound according to any one of Items 1 to 3, which is represented by any one of formulas (1-1) to (1-10).
- R 1 and R 2 are independently hydrogen, alkyl having 1 to 10 carbons, alkoxy having 1 to 9 carbons, alkenyl having 2 to 10 carbons, or 1 carbon in which at least one hydrogen is replaced by fluorine.
- Ring A 11 , Ring A 12 , Ring A 13 , Ring A 21 , Ring A 22 , and Ring A 23 are each independently 1,4-cyclohexylene, 1,4-cyclohexenylene, 1,4-phenylene, 1,4-phenylene in which at least one hydrogen is replaced by halogen, or tetrahydropyran-2,5-diyl;
- Z 11 , Z 12 , Z 13 , Z 21 , Z 22 and Z 23 are each independently a single bond, — (CH 2 ) 2 —, —CH ⁇ CH—, —CF ⁇ CF—, —C ⁇ C—.
- R 1 and R 2 are independently hydrogen, alkyl having 1 to 10 carbons, alkoxy having 1 to 9 carbons, alkenyl having 2 to 10 carbons, or 1 carbon in which at least one hydrogen is replaced by fluorine.
- Ring A 21 is 1,4-cyclohexylene, 1,4-cyclohexenylene, 1,4-phenylene, 1,4-phenylene in which at least one hydrogen is replaced by halogen, or tetrahydropyran-2,5- Is diyl;
- Z 21 is independently — (CH 2 ) 2 —, —CH ⁇ CH—, —CF ⁇ CF—, —C ⁇ C—, —COO—, —OCO—, —CF 2 O—, —OCF 2 —, —CH 2 O—, —OCH 2 —, — (CH 2 ) 4 —, — (CH 2 ) 2 CF 2 O—, — (CH 2 ) 2 OCF 2 —, —CF 2 O (CH 2 ) 2 —, —OCF 2 (CH 2 ) 2 —, —CH ⁇ CH— (CH 2 ) 2 —, or — (CH 2 ) 2 —CH ⁇ CH—;
- L 1 is independently
- R 1 and R 2 are independently hydrogen, fluorine, alkyl having 1 to 10 carbons, alkoxy having 1 to 9 carbons, alkenyl having 2 to 10 carbons, or fluorinated alkyl having 1 to 10 carbons Is;
- Ring A 11 , Ring A 12 , Ring A 13 , Ring A 21 , Ring A 22 , and Ring A 23 are each independently 1,4-cyclohexylene, 1,4-cyclohexenylene, wherein at least one hydrogen is halogen 1,4-phenylene, tetrahydropyran-2,5-diyl, which may be replaced by Z 11 , Z 12 , Z 13 , Z 21 , Z 22 , and Z 23 are each independently a single bond, — (CH 2 ) 2 —, —CH ⁇ CH—, —C ⁇ C—, —CF 2 O —, —OCF 2 —, —CH 2 O—, or
- Item 6. The compound according to item 6, represented by any one of formulas (1-1), (1-5), and (1-10).
- R 1 and R 2 are independently hydrogen, fluorine, alkyl having 1 to 10 carbons, alkoxy having 1 to 9 carbons, alkenyl having 2 to 10 carbons, or carbon in which at least one hydrogen is replaced by fluorine.
- Ring A 21 , Ring A 22 , and Ring A 23 are independently 1,4-cyclohexylene, 1,4-phenylene in which at least one hydrogen may be replaced by halogen;
- Z 21 , Z 22 , and Z 23 are each independently a single bond, — (CH 2 ) 2 —, —CH ⁇ CH—, —C ⁇ C—, —CH 2 O—, or —OCH 2 —.
- L 1 , L 2 , and L 3 are independently hydrogen or fluorine.
- R 1 and R 2 are independently hydrogen, fluorine, alkyl having 1 to 10 carbons, alkoxy having 1 to 9 carbons, alkenyl having 2 to 10 carbons, or carbon in which at least one hydrogen is replaced by fluorine.
- Ring A 21 is 1,4-cyclohexylene, or 1,4-phenylene in which at least one hydrogen may be replaced by halogen;
- Z 21 is a single bond, — (CH 2 ) 2 —, —CH ⁇ CH—, —C ⁇ C—, —CH 2 O—, or —OCH 2 —;
- L 1 , L 2 , and L 3 are independently hydrogen or fluorine.
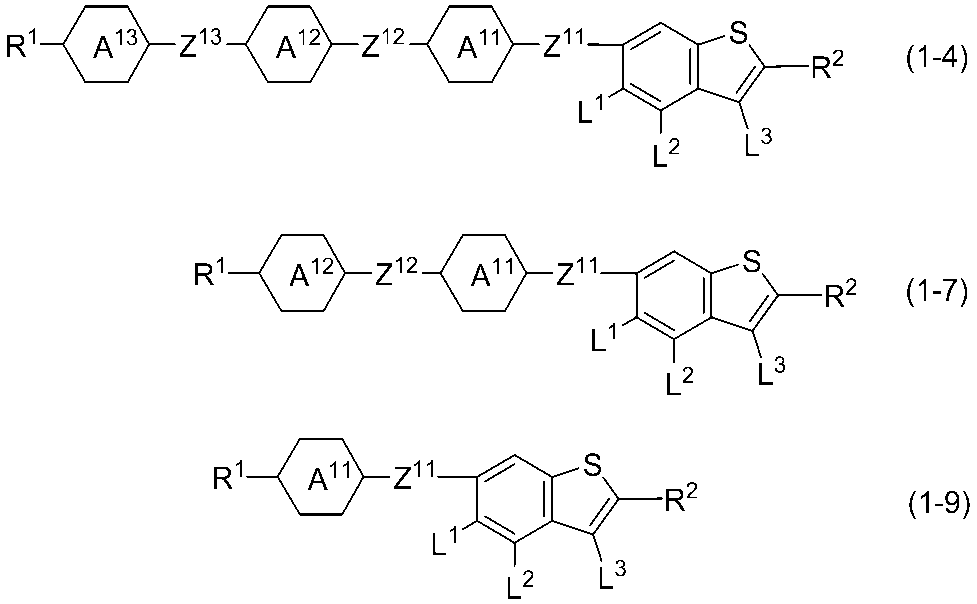
- Item 8. The compound according to item 5, represented by any one of formulas (1-4), (1-7), and (1-9): In formulas (1-4), (1-7), and (1-9), R 1 and R 2 are independently hydrogen, fluorine, alkyl having 1 to 10 carbons, alkoxy having 1 to 9 carbons, alkenyl having 2 to 10 carbons, or carbon in which at least one hydrogen is replaced by fluorine.
- Ring A 11 , Ring A 12 , and Ring A 13 are independently 1,4-cyclohexylene, 1,4-phenylene in which at least one hydrogen may be replaced by halogen;
- Z 11 , Z 12 , and Z 13 are each independently a single bond, — (CH 2 ) 2 —, —CH ⁇ CH—, —C ⁇ C—, —CH 2 O—, or —OCH 2 —.
- L 1 , L 2 , and L 3 are independently hydrogen or fluorine.
- Item 9 A liquid crystal composition containing at least one compound according to any one of items 1 to 8.
- Item 10 The liquid crystal composition according to item 9, further comprising at least one compound selected from the group of compounds represented by formulas (2) to (4).
- R 11 and R 12 are independently alkyl having 1 to 10 carbons or alkenyl having 2 to 10 carbons, and in the alkyl or alkenyl, at least one —CH 2 — may be replaced by —O—.
- Ring B 1 , Ring B 2 , Ring B 3 , and Ring B 4 are independently 1,4-cyclohexylene, 1,4-phenylene, 2-fluoro-1,4-phenylene, 2,5-difluoro- 1,4-phenylene or pyrimidine-2,5-diyl;
- Z 11 , Z 12 , and Z 13 are each independently a single bond, —CH 2 CH 2 —, —CH ⁇ CH—, —C ⁇ C—, or —COO—.
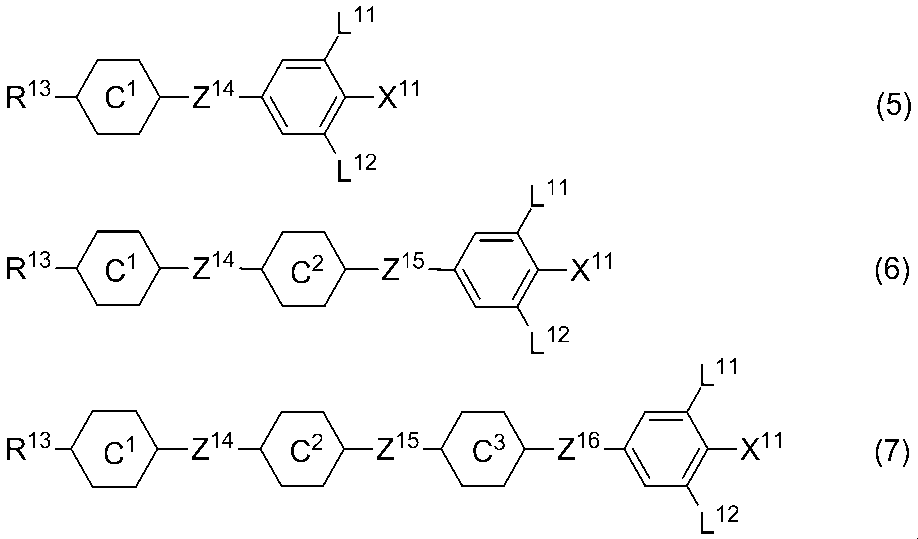
- Item 11 The liquid crystal composition according to item 9 or 10, further comprising at least one compound selected from the group of compounds represented by formulas (5) to (7).
- R 13 is alkyl having 1 to 10 carbons or alkenyl having 2 to 10 carbons, in which at least one —CH 2 — may be replaced by —O—, and at least one hydrogen is May be replaced by fluorine;
- X 11 is fluorine, chlorine, —OCF 3 , —OCHF 2 , —CF 3 , —CHF 2 , —CH 2 F, —OCF 2 CHF 2 , or —OCF 2 CHFCF 3 ;
- Ring C 1 , Ring C 2 , and Ring C 3 are independently 1,4-cyclohexylene, 1,4-phenylene in which at least one hydrogen may be replaced by fluorine, tetrahydropyran-2,5-diyl 1,3-dioxane-2,5-diyl, or pyrim
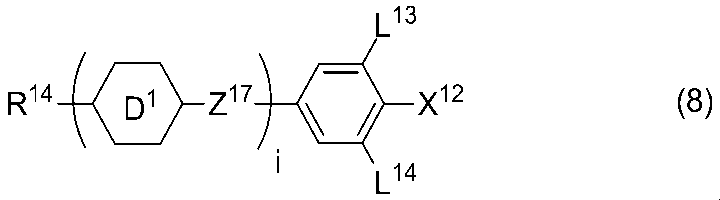
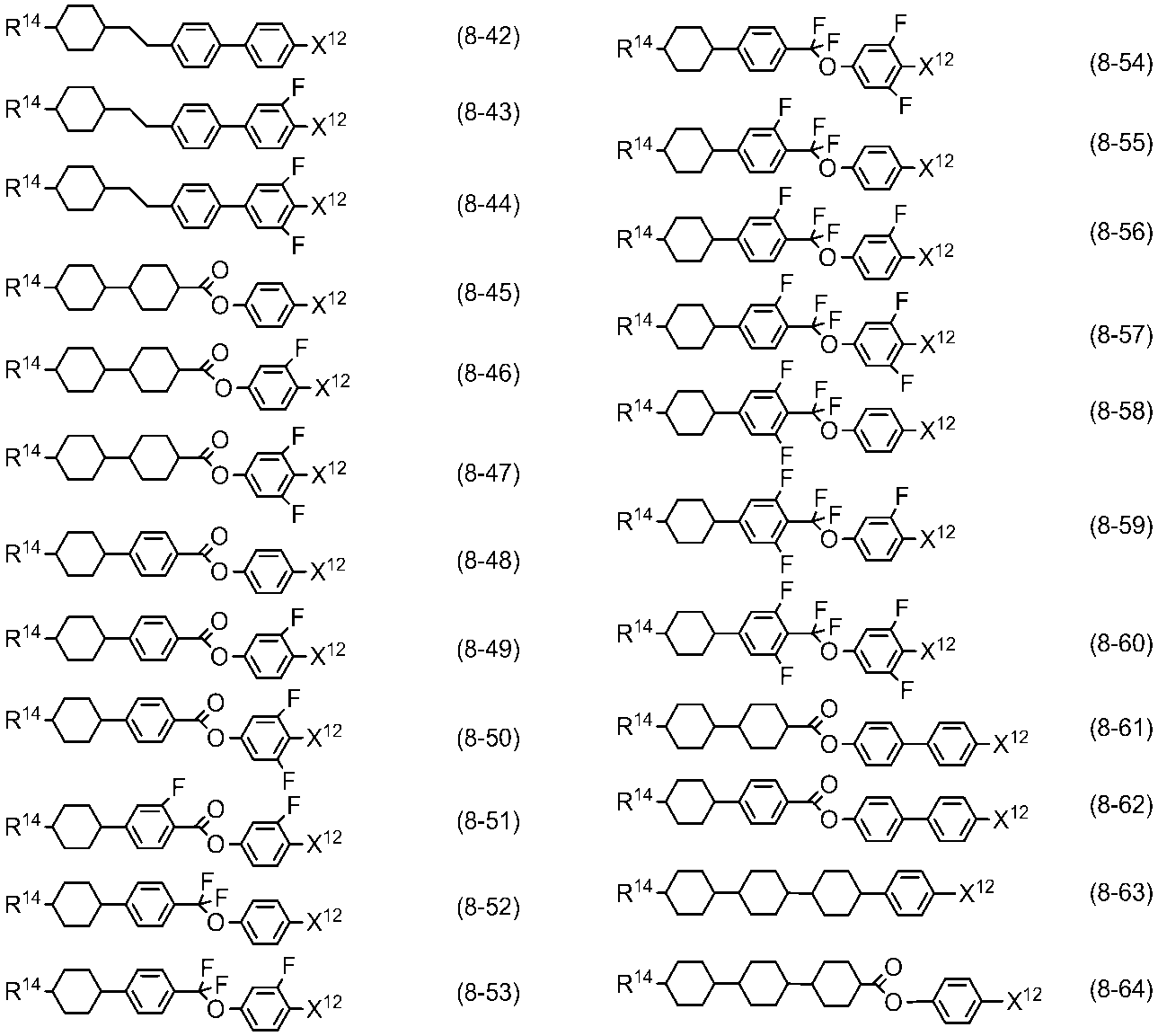
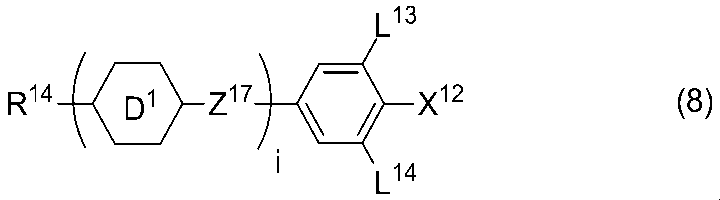
- Item 12. The liquid crystal composition according to any one of items 9 to 11, further comprising at least one compound selected from the group of compounds represented by formula (8).
- R 14 is alkyl having 1 to 10 carbons or alkenyl having 2 to 10 carbons, in which at least one —CH 2 — may be replaced by —O—, and at least one hydrogen is May be replaced by fluorine;
- X 12 is —C ⁇ N or —C ⁇ C—C ⁇ N;
- Ring D 1 is 1,4-cyclohexylene, 1,4-phenylene in which at least one hydrogen may be replaced with fluorine, tetrahydropyran-2,5-diyl, 1,3-dioxane-2,5-diyl Or pyrimidine-2,5-diyl;
- Z 17 represents a single bond, -CH 2 CH 2 -, - C ⁇ C -, - COO -, - CF 2 O -, - OCF 2 -, or
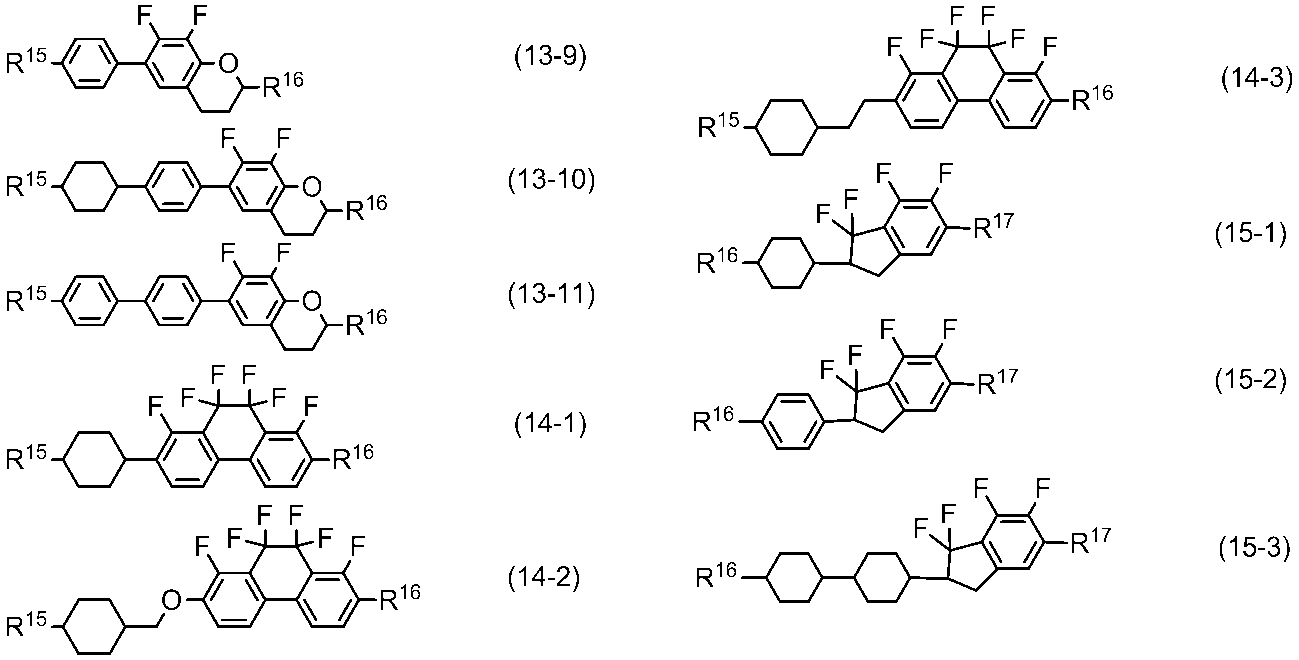
- Item 13 The liquid crystal composition according to any one of items 9 to 12, further containing at least one compound selected from the group of compounds represented by formulas (9) to (15).
- R 15 and R 16 are independently alkyl having 1 to 10 carbons or alkenyl having 2 to 10 carbons, in which at least one —CH 2 — may be replaced by —O—.
- at least one hydrogen may be replaced by fluorine
- R 17 is hydrogen, fluorine, alkyl having 1 to 10 carbons, or alkenyl having 2 to 10 carbons, and in the alkyl and alkenyl, at least one —CH 2 — may be replaced by —O—.
- Ring E 1 , Ring E 2 , Ring E 3 , and Ring E 4 are independently 1,4-cyclohexylene, 1,4-cyclohexenylene, wherein at least one hydrogen may be replaced with fluorine, 4-phenylene, tetrahydropyran-2,5-diyl, or decahydronaphthalene-2,6-diyl;
- ring E 5 and ring E 6 are independently 1,4-cyclohexylene, 1,4-cyclohex Senylene, 1,4-phenylene, tetrahydropyran-2,5-diyl, or decahydronaphthalene-2,6-diyl;
- Z 18, Z 19, Z 20 , and Z 21 are independently a single bond, -CH 2 CH 2 -, - COO -, - CH 2 O -, - OCF 2 -, or -OCF 2 CH 2 CH 2 -Is;
- L 15 and L 16 are independently 1,4-cyclohe
- Item 9 further contains at least one of a polymerizable compound, a polymerization initiator, a polymerization inhibitor, an optically active compound, an antioxidant, an ultraviolet absorber, a light stabilizer, a heat stabilizer, a dye, and an antifoaming agent. 14. The liquid crystal composition according to any one of items 13.
- Item 15 A liquid crystal display device comprising the liquid crystal composition according to any one of items 9 to 14.
- Item 16 The liquid crystal display element according to item 15, wherein the liquid crystal composition according to any one of items 9 to 14 is encapsulated.
- Item 17 The liquid crystal display element according to item 15, wherein the liquid crystal composition according to any one of items 9 to 14 is used for switching between 2D and 3D.
- Embodiment of Compound (1) The compound (1) of the present invention has a 1-benzothiophene ring structure. A preferred example of compound (1) will be described. Preferred examples of the terminal group, ring structure, bonding group, and substituent in the compound (1) also apply to the sub-formula of the compound (1) such as the compound (1-1) and the compound (1-2). In the compound (1), physical properties can be arbitrarily adjusted by appropriately combining these kinds of groups. Since there is no great difference in the physical properties of the compound, the compound (1) may contain an isotope such as 2 H (deuterium) and 13 C in an amount larger than the natural abundance. In addition, the definition of the symbol of the compound (1) is as described in item 1.
- R 1 is hydrogen, fluorine, or alkyl having 1 to 20 carbons, in which at least one —CH 2 — may be replaced by —O— or —S—, and at least one —CH 2 CH 2 — may be replaced by —CH ⁇ CH—, and in these groups at least one hydrogen may be replaced by fluorine.
- R 1 are hydrogen, alkyl, alkoxy, alkoxyalkyl, alkoxyalkoxy, alkenyl, alkenyloxy, alkenyloxyalkyl, alkoxyalkenyl, alkylthio, alkylthioalkyl, alkenylthio, alkenylthioalkyl, and alkylthioalkenyl.
- Preferred R 1 is alkyl, alkoxy, alkoxyalkyl, alkoxyalkoxy, alkenyl, alkenyloxy, alkenyloxyalkyl, or alkoxyalkenyl. More preferred R 1 is alkyl, alkoxy, alkoxyalkyl, alkenyl, or alkenyloxy. Particularly preferred R 1 is alkyl or alkenyl. Most preferred R 1 is alkyl.
- Preferred alkyl is —CH 3 , —C 2 H 5 , —C 3 H 7 , —C 4 H 9 , —C 5 H 11 , —C 6 H 13 , or —C 7 H 15 .
- Preferred alkoxy is —OCH 3 , —OC 2 H 5 , —OC 3 H 7 , —OC 4 H 9 , —OC 5 H 11 , —OC 6 H 13 , or —OC 7 H 15 .
- Preferred alkoxyalkyl is —CH 2 OCH 3 , —CH 2 OC 2 H 5 , —CH 2 OC 3 H 7 , — (CH 2 ) 2 —OCH 3 , — (CH 2 ) 2 —OC 2 H 5 , — (CH 2 ) 2 —OC 3 H 7 , — (CH 2 ) 3 —OCH 3 , — (CH 2 ) 4 —OCH 3 , or — (CH 2 ) 5 —OCH 3 .
- Preferred alkenyl is —CH ⁇ CH 2 , —CH ⁇ CHCH 3 , —CH 2 CH ⁇ CH 2 , —CH ⁇ CHC 2 H 5 , —CH 2 CH ⁇ CHCH 3 , — (CH 2 ) 2 —CH ⁇ CH 2 , —CH ⁇ CHC 3 H 7 , —CH 2 CH ⁇ CHC 2 H 5 , — (CH 2 ) 2 —CH ⁇ CHCH 3 , or — (CH 2 ) 3 —CH ⁇ CH 2 .
- Preferred R 1 is hydrogen, —CH 3 , —C 2 H 5 , —C 3 H 7 , —C 4 H 9 , —C 5 H 11 , —C 6 H 13 , —OCH 3 , —OC 2 H 5 , —OC 3 H 7 , —OC 4 H 9 , —OC 5 H 11 , —CH 2 OCH 3 , —CH ⁇ CH 2 , —CH ⁇ CHCH 3 , — (CH 2 ) 2 —CH ⁇ CH 2 , — CH 2 CH ⁇ CHC 2 H 5 , — (CH 2 ) 2 —CH ⁇ CHCH 3 , —OCH 2 CH ⁇ CH 2 , —OCH 2 CH ⁇ CHCH 3 , or —OCH 2 CH ⁇ CHC 2 H 5 .
- R 1 is —C 3 H 7 , —C 4 H 9 , —C 5 H 11 , —C 6 H 13 , — (CH 2 ) 2 —CH ⁇ CH 2 , or — (CH 2 ) 2 —.
- CH CHCH 3.
- R 1 When R 1 is linear, the temperature range of the liquid crystal phase is wide and the viscosity is small. When R 1 is a branched chain, the compatibility with other liquid crystal compounds. A compound in which R 1 is optically active is useful as a chiral dopant. By adding this compound to the composition, a reverse twisted domain generated in the liquid crystal display device can be prevented. A compound in which R 1 is not optically active is useful as a component of the composition.
- R 1 When R 1 is alkenyl, the preferred configuration depends on the position of the double bond. An alkenyl compound having a preferred configuration has a low viscosity, a high maximum temperature, or a wide temperature range of the liquid crystal phase.
- —CH ⁇ CH— in alkenyl depends on the position of the double bond. —CH ⁇ CHCH 3 , —CH ⁇ CHC 2 H 5 , —CH ⁇ CHC 3 H 7 , —CH ⁇ CHC 4 H 9 , —C 2 H 4 CH ⁇ CHCH 3 , and —C 2 H 4 CH ⁇ CHC 2
- the trans configuration is preferable.
- -CH 2 CH CHCH 3
- An alkenyl compound having a preferred configuration has a high clearing point or a wide temperature range of a liquid crystal phase.
- Mol. Cryst. Liq. Cryst., 1985, 131, 109 and Mol. Cryst. Liq. Cryst., 1985, 131, 327 have detailed descriptions.
- ring A 1 and ring A 2 are independently 1,4-cyclohexylene, 1,4-cyclohexenylene, 1,4-phenylene, tetrahydropyran-2,5-diyl, 1, 3-dioxane-2,5-diyl, pyrimidine-2,5-diyl, 2,6,7-trioxabicyclo [2.2.2] octane-1,4-diyl, naphthalene-2,6-diyl, Pyridine-2,5-diyl, wherein at least one hydrogen on these rings may be replaced with a halogen.
- Preferred ring A 1 or ring A 2 is 1,4-cyclohexylene, 1,4-phenylene, 2-fluoro-1,4-phenylene, 2,3-difluoro-1,4-phenylene, 2,6-difluoro. -1,4-phenylene, 2,3,5-trifluoro-1,4-phenylene, tetrahydropyran-2,5-diyl, 1,3-dioxane-2,5-diyl, or pyrimidine-2,5- It is a diyl.
- ring A 1 or ring A 2 are 1,4-cyclohexylene, 1,4-phenylene, 2-fluoro-1,4-phenylene, 2,6-difluoro-1,4-phenylene or tetrahydropyran, - 2,5-diyl.
- Particularly preferred ring A 1 or ring A 2 is 1,4-cyclohexylene, 1,4-phenylene, 2-fluoro-1,4-phenylene, or 2,6-difluoro-1,4-phenylene.
- Z 1 and Z 2 are each independently a single bond or alkylene having 1 to 4 carbon atoms, in which at least one —CH 2 — may be replaced by —O— or —COO—, and at least One — (CH 2 ) 2 — may be replaced with —CH ⁇ CH— or —C ⁇ C—, in which at least one hydrogen may be replaced with a halogen.
- Preferred Z 1 or Z 2 is a single bond, — (CH 2 ) 2 —, —CH ⁇ CH—, —CF ⁇ CF—, —C ⁇ C—, —COO—, —OCO—, —CF 2 O—.
- More preferred Z 1 and Z 2 are a single bond, — (CH 2 ) 2 —, —CH ⁇ CH—, —CF 2 O—, —OCF 2 —, —CH 2 O—, —C ⁇ C—, — (CH 2 ) 2 OCF 2 — or —OCH 2 —.
- Z 3 is -O- or a single bond.
- a compound in which Z 3 is —O— is preferable because it has a high clearing point and high optical anisotropy.
- a compound in which Z 3 is a single bond is preferred because of its low viscosity.
- L 1 , L 2 and L 3 are independently hydrogen, fluorine or chlorine.
- Preferred L 1 , L 2 and L 3 are a combination of hydrogen and fluorine.
- Preferred L 1 , L 2 and L 3 fluorine and a combination of fluorine.
- a and b are independently 0, 1, 2, 3, or 4, and the sum of a and b is 4 or less. Preferred sum of a and b is 0, 1, or 2.
- Examples of preferred compound (1) are compounds (1-1) to (1-10) described in item 5.
- ring A 11 , ring A 12 , ring A 13 , ring A 21 , ring A 22 and ring A 23 in compounds (1-1) to (1-10) and the effect of these groups on physical properties Is the same as that of ring A 1 and ring A 2 in formula (1), and preferred examples of Z 11 , Z 12 , Z 13 , Z 21 , Z 22, and Z 23 , and their groups affect physical properties. effect, Z 1, and is similar to that of Z 2 in formula (1).
- preferable compounds include compounds (No. 1) to (No. 200) shown in Example 5.
- linking group Z A scheme is first shown for the method of generating linking groups Z 1 to Z 2 . Next, the reactions described in the schemes in terms (1) to (11) will be described.
- MSG 1 (or MSG 2 ) is a monovalent organic group having at least one ring.
- the monovalent organic groups represented by a plurality of MSG 1 (or MSG 2 ) used in the scheme may be the same or different.
- Compounds (1A) to (1J) correspond to compound (1).
- ring A 1 and ring A 2 1,4-cyclohexylene, 1,4-phenylene, 2-fluoro-1,4-phenylene, 2,6-difluoro-1,4-phenylene, tetrahydropyran-2,5 -For rings such as diyl, 1,3-dioxane-2,5-diyl, pyrimidine-2,5-diyl, or pyridine-2,5-diyl, starting materials are commercially available or synthetic methods are well known It has been.
- Method for synthesizing compound (1) An example of a method for synthesizing compound (1) is as follows. In these compounds, the definitions of R 1 , R 2 , ring A 1 , ring A 2 , Z 1 , Z 2 , Z 3 , L 1 , L 2 , L 3 , a, and b are as defined in item 1 above. Are the same.
- the compound (b-1) synthesized by a known method is reacted with Mg to prepare a Grignard reagent, and S and bromoacetaldehyde diethyl acetal are reacted to obtain (b-2). This is reacted with polyphosphoric acid in toluene or chlorobenzene to obtain (b-3).
- B-3) is lithiated with LDA to give (b-4), and various reagents are reacted therewith to obtain various intermediates.
- the compound (1) is derived by a known method.
- Liquid crystal composition 3-1 Component Compound
- the liquid crystal composition of the present invention will be described.
- This composition comprises at least one compound (1) as component A.
- Compound (1) is useful for increasing the maximum temperature of the composition.
- the composition may comprise two or more compounds (1).
- the component of the composition may be only compound (1).
- the composition preferably contains at least one compound (1) in the range of 1% by weight to 99% by weight in order to develop excellent physical properties.
- the preferred content of the compound (1) is in the range of 5% to 60% by weight.
- the preferred content of compound (1) is 30% by weight or less.
- the composition may contain the compound (1) and a liquid crystal compound not described in the present specification.
- This composition preferably includes the compound (1) as the component A and further includes a liquid crystal compound selected from the components B, C, D, and E shown below.
- Component B is compounds (2) to (4).
- Component C is compounds (5) to (7).
- Component D is compound (8).
- Component E is compounds (9) to (15).
- the composition may contain other liquid crystal compounds different from the compounds (2) to (15).
- a composition with appropriately selected ingredients has high stability to heat and light, high maximum temperature, low minimum temperature, low viscosity, appropriate optical anisotropy (ie, large optical anisotropy or small optical anisotropy) , Large dielectric anisotropy, large specific resistance, and appropriate elastic constant (ie, large elastic constant or small elastic constant).
- Component B is a compound in which two terminal groups are alkyl or the like.
- Preferred examples of component B include compounds (2-1) to (2-11), compounds (3-1) to (3-19), and compounds (4-1) to (4-7). it can.
- R 11 and R 12 are independently alkyl having 1 to 10 carbons or alkenyl having 2 to 10 carbons, in which at least one —CH 2 — is —O - May be replaced with at least one hydrogen may be replaced with fluorine.
- Component B is a compound close to neutrality because the absolute value of dielectric anisotropy is small.
- Compound (2) is mainly effective in reducing viscosity or adjusting optical anisotropy.
- Compounds (3) and (4) are effective in expanding the temperature range of the nematic phase by increasing the maximum temperature, or adjusting the optical anisotropy.
- the content of component B is preferably 30% by weight or more, more preferably 40% by weight or more based on the weight of the liquid crystal composition.
- Component C is a compound having a halogen or fluorine-containing group at the right end.
- Preferable examples of component C include compounds (5-1) to (5-16), compounds (6-1) to (6-113), and compounds (7-1) to (7-57).
- R 13 is alkyl having 1 to 10 carbons or alkenyl having 2 to 10 carbons, and in the alkyl and alkenyl, at least one —CH 2 — may be replaced by —O—.
- At least one hydrogen may be replaced by fluorine;
- X 11 is fluorine, chlorine, —OCF 3 , —OCHF 2 , —CF 3 , —CHF 2 , —CH 2 F, —OCF 2 CHF 2 , or -OCF is a 2 CHFCF 3.
- Component C has a positive dielectric anisotropy and is very excellent in stability to heat, light, etc., and is used when preparing a composition for a mode such as IPS, FFS, OCB.
- the content of Component C is suitably in the range of 1% to 99% by weight based on the weight of the liquid crystal composition, preferably in the range of 10% to 97% by weight, more preferably in the range of 40% to 95%. % Range.
- the content of component C is preferably 30% by weight or less.
- Component D is a compound (8) in which the right terminal group is —C ⁇ N or —C ⁇ C—C ⁇ N.
- Preferable examples of component D include compounds (8-1) to (8-64).
- R 14 is alkyl having 1 to 10 carbons or alkenyl having 2 to 10 carbons, and in the alkyl and alkenyl, at least one —CH 2 — may be replaced by —O—.
- At least one hydrogen may be replaced by fluorine;
- X 12 is —C ⁇ N or —C ⁇ C—C ⁇ N.
- component D Since component D has a positive dielectric anisotropy and a large value, it is mainly used when a composition for a mode such as TN is prepared. By adding this component D, the dielectric anisotropy of the composition can be increased.
- Component D has the effect of expanding the temperature range of the liquid crystal phase, adjusting the viscosity, or adjusting the optical anisotropy. Component D is also useful for adjusting the voltage-transmittance curve of the device.
- the content of Component D is suitably in the range of 1% to 99% by weight, preferably 10% by weight, based on the weight of the liquid crystal composition. It is in the range of 97% by weight, more preferably in the range of 40% to 95% by weight.
- the content of component D is preferably 30% by weight or less.
- Component E is compounds (9) to (15). These compounds have phenylene in which the lateral position is substituted with two halogens, such as 2,3-difluoro-1,4-phenylene.
- Preferred examples of component E include compounds (9-1) to (9-8), compounds (10-1) to (10-17), compounds (11-1), compounds (12-1) to (12- 3), compounds (13-1) to (13-11), compounds (14-1) to (14-3), and compounds (15-1) to (15-3).
- R 15 and R 16 are independently alkyl having 1 to 10 carbons or alkenyl having 2 to 10 carbons, in which at least one —CH 2 — is —O And at least one hydrogen may be replaced by fluorine;
- R 17 is hydrogen, fluorine, alkyl having 1 to 10 carbons, or alkenyl having 2 to 10 carbons, and the alkyl And in alkenyl, at least one —CH 2 — may be replaced with —O— and at least one hydrogen may be replaced with fluorine.
- Component E has a large negative dielectric anisotropy.
- Component E is used in preparing a composition for a mode such as IPS, VA, PSA.
- the dielectric anisotropy of the composition increases negatively, but the viscosity increases. Therefore, as long as the threshold voltage requirement of the element is satisfied, the content is preferably small.
- the dielectric anisotropy is about ⁇ 5
- the content is preferably 40% by weight or more for sufficient voltage driving.
- the compound (9) is a bicyclic compound, it is mainly effective in reducing the viscosity, adjusting the optical anisotropy, or increasing the dielectric anisotropy.
- the compounds (10) and (11) are tricyclic compounds, there are effects of increasing the maximum temperature, increasing the optical anisotropy, or increasing the dielectric anisotropy.
- Compounds (12) to (15) have the effect of increasing the dielectric anisotropy.
- the content of component E is preferably 40% by weight or more, more preferably 50% by weight, based on the weight of the liquid crystal composition. To 95% by weight.
- component E is added to a composition having a positive dielectric anisotropy, the content of these compounds is preferably 30% by weight or less.
- a liquid crystal composition satisfying at least one of physical properties such as property, large specific resistance, large specific resistance, and an appropriate elastic constant can be prepared. If necessary, a liquid crystal compound different from the components B, C, D, and E may be added.
- the liquid crystal composition is prepared by a known method. For example, the component compounds are mixed and dissolved in each other by heating.
- additives may be added to the composition.
- the additive include a polymerizable compound, a polymerization initiator, a polymerization inhibitor, an optically active compound, an antioxidant, an ultraviolet absorber, a light stabilizer, a heat stabilizer, a dye, and an antifoaming agent.
- Such additives are well known to those skilled in the art and are described in the literature.
- the composition contains a polymer.
- the polymerizable compound is added for the purpose of forming a polymer in the composition.
- a polymer is produced in the composition by polymerizing the polymerizable compound by irradiating ultraviolet rays with a voltage applied between the electrodes.
- Preferred examples of the polymerizable compound are acrylate, methacrylate, vinyl compound, vinyloxy compound, propenyl ether, epoxy compound (oxirane, oxetane), and vinyl ketone. Further preferred examples are compounds having at least one acryloyloxy and compounds having at least one methacryloyloxy. Further preferred examples include compounds having both acryloyloxy and methacryloyloxy.
- More preferred examples are compounds (M-1) to (M-17).
- R 25 to R 31 are independently hydrogen or methyl; s, v, and x are independently 0 or 1; t and u are independently 1 to 10 It is an integer.
- L 21 to L 26 are independently hydrogen or fluorine; L 27 and L 28 are independently hydrogen, fluorine, or methyl.
- the polymerizable compound can be rapidly polymerized by adding a polymerization initiator. By optimizing the reaction temperature, the amount of the remaining polymerizable compound can be reduced.
- photo radical polymerization initiators are BASF's Darocur series to TPO, 1173, and 4265, and Irgacure series to 184, 369, 500, 651, 784, 819, 907, 1300, 1700, 1800, 1850. , And 2959.
- photo radical polymerization initiators include 4-methoxyphenyl-2,4-bis (1,3,5-trichloromethyl) triazine, 2- (4-butoxystyryl) -5-trichloromethyl-1,3, 4-oxadiazole, 9-phenylacridine, 9,10-benzphenazine, benzophenone / Michler's ketone mixture, hexaarylbiimidazole / mercaptobenzimidazole mixture, 1- (4-isopropylphenyl) -2-hydroxy-2-methylpropane -1-one, benzyldimethyl ketal, 2-methyl-1- [4- (methylthio) phenyl] -2-morpholinopropan-1-one, 2,4-diethylxanthone / methyl p-dimethylaminobenzoate, benzophenone / Methyltriethanolamine mixture.
- Polymerization can be performed by adding a photoradical polymerization initiator to the liquid crystal composition and then irradiating it with ultraviolet rays in an applied electric field.
- the unreacted polymerization initiator or the decomposition product of the polymerization initiator may cause display defects such as image burn-in on the device.
- photopolymerization may be performed without adding a polymerization initiator.
- a preferable wavelength of light to be irradiated is in a range of 150 nm to 500 nm.
- a more preferred wavelength is in the range of 250 nm to 450 nm, and a most preferred wavelength is in the range of 300 nm to 400 nm.
- a polymerization inhibitor When storing the polymerizable compound, a polymerization inhibitor may be added to prevent polymerization.
- the polymerizable compound is usually added to the composition without removing the polymerization inhibitor.
- the polymerization inhibitor include hydroquinone, hydroquinone derivatives such as methylhydroquinone, 4-tert-butylcatechol, 4-methoxyphenol, phenothiazine and the like.
- the optically active compound has an effect of preventing reverse twisting by inducing a helical structure in liquid crystal molecules to give a necessary twist angle.
- the helical pitch can be adjusted by adding an optically active compound.
- Two or more optically active compounds may be added for the purpose of adjusting the temperature dependence of the helical pitch.
- Preferred examples of the optically active compound include the following compounds (Op-1) to (Op-18).
- ring J is 1,4-cyclohexylene or 1,4-phenylene
- R 28 is alkyl having 1 to 10 carbons.
- An antioxidant is effective for maintaining a large voltage holding ratio.
- Preferred examples of the antioxidant include the following compounds (AO-1) and (AO-2); IRGANOX 415, IRGANOX 565, IRGANOX 1010, IRGANOX 1035, IRGANOX 3114, and IRGANOX 1098 (trade name; BASF) be able to.
- the ultraviolet absorber is effective for preventing a decrease in the maximum temperature.
- Preferable examples of the ultraviolet absorber are benzophenone derivatives, benzoate derivatives, triazole derivatives and the like.
- AO-3 and (AO-4) Specific examples include the following compounds (AO-3) and (AO-4); TINUVIN 329, TINUVIN P, TINUVIN 326, TINUVIN 234, TINUVIN 213, TINUVIN 400, TINUVIN 328, and TINUVIN 99-2 (trade name: BASF); and 1,4-diazabicyclo [2.2.2] octane (DABCO).
- a light stabilizer such as an amine having steric hindrance is preferable in order to maintain a large voltage holding ratio.
- Preferred examples of the light stabilizer include the following compounds (AO-5) and (AO-6); TINUVIN 144, TINUVIN 765, and TINUVIN 770DF (trade name; BASF).
- a thermal stabilizer is also effective for maintaining a large voltage holding ratio, and a preferred example is IRGAFOS 168 (trade name: BASF).
- a dichroic dye such as an azo dye or an anthraquinone dye, is added to the composition in order to adapt to a GH (guest host) mode device.
- Antifoaming agents are effective for preventing foaming.
- Preferred examples of the antifoaming agent include dimethyl silicone oil and methylphenyl silicone oil.
- R 40 is alkyl having 1 to 20 carbons, alkoxy having 1 to 20 carbons, —COOR 41 , or —CH 2 CH 2 COOR 41 , where R 41 is 1 carbon atom To 20 alkyls.
- R 42 is alkyl having 1 to 20 carbons.
- R 43 is hydrogen, methyl or O ⁇ (oxygen radical);
- ring G is 1,4-cyclohexylene or 1,4-phenylene;
- z is 1, 2 or, 3.
- Liquid crystal display element A liquid crystal composition has operation modes, such as PC, TN, STN, OCB, and PSA, and can be used for the liquid crystal display element driven by an active matrix.
- This composition has operation modes such as PC, TN, STN, OCB, VA, and IPS, and can also be used for a liquid crystal display element driven by a passive matrix method.
- These elements can be applied to any of a reflective type, a transmissive type, and a transflective type.
- This composition is also suitable for an NCAP (nematic-curvilinear-aligned-phase) element, in which the composition is microencapsulated.
- This composition can also be used for polymer dispersed liquid crystal display elements (PDLCD) and polymer network liquid crystal display elements (PNLCD).
- PDLCD polymer dispersed liquid crystal display elements
- PLCD polymer network liquid crystal display elements
- a PSA mode liquid crystal display element is produced.
- a preferred ratio is in the range of approximately 0.1% by weight to approximately 2% by weight.
- a more desirable ratio is in the range of approximately 0.2% by weight to approximately 1.0% by weight.
- a PSA mode element can be driven by a driving method such as an active matrix or a passive matrix. Such an element can be applied to any of a reflection type, a transmission type, and a transflective type.
- the present invention will be described in more detail with reference to examples (including synthesis examples and usage examples). The invention is not limited by these examples.
- the present invention includes a mixture of the composition of Use Example 1 and the composition of Use Example 2.
- the present invention also includes compositions prepared by mixing at least two of the compositions of use examples.
- Example of Compound (1) Compound (1) was synthesized by the following procedure. The synthesized compound was identified by a method such as NMR analysis. The physical properties of the compound and composition and the characteristics of the device were measured by the following methods.
- NMR analysis DRX-500 manufactured by Bruker BioSpin Corporation was used for measurement.
- the sample was dissolved in a deuterated solvent such as CDCl 3 and measured at room temperature, 500 MHz, and 16 integrations. Tetramethylsilane was used as an internal standard.
- CFCl 3 was used as an internal standard and the number of integrations was 24.
- s is a singlet
- d is a doublet
- t is a triplet
- q is a quartet
- quint is a quintet
- sex is a sextet
- m is a multiplet
- br is broad.
- a GC-2010 gas chromatograph manufactured by Shimadzu Corporation was used for measurement.
- capillary column DB-1 length 60 m, inner diameter 0.25 mm, film thickness 0.25 ⁇ m
- Helium (1 ml / min) was used as the carrier gas.
- the temperature of the sample vaporizing chamber was set to 300 ° C.
- the temperature of the detector (FID) portion was set to 300 ° C.
- the sample was dissolved in acetone to prepare a 1% by weight solution, and 1 ⁇ l of the obtained solution was injected into the sample vaporization chamber.
- a GC Solution system manufactured by Shimadzu Corporation was used.
- HPLC analysis Prominence (LC-20AD; SPD-20A) manufactured by Shimadzu Corporation was used for measurement.
- YMC-Pack ODS-A length 150 mm, inner diameter 4.6 mm, particle diameter 5 ⁇ m
- acetonitrile and water were appropriately mixed and used.
- a detector a UV detector, an RI detector, a CORONA detector, or the like was appropriately used. When a UV detector was used, the detection wavelength was 254 nm.
- a sample was dissolved in acetonitrile to prepare a 0.1 wt% solution, and 1 ⁇ L of this solution was introduced into the sample chamber.
- a recorder a C-R7Aplus manufactured by Shimadzu Corporation was used.
- Ultraviolet-visible spectroscopic analysis For the measurement, PharmaSpec UV-1700 manufactured by Shimadzu Corporation was used. The detection wavelength was 190 nm to 700 nm. The sample was dissolved in acetonitrile to prepare a 0.01 mmol / L solution, and the sample was placed in a quartz cell (optical path length 1 cm) and measured.
- Measurement sample When measuring the phase structure and transition temperature (clearing point, melting point, polymerization start temperature, etc.), the compound itself was used as a sample. When measuring physical properties such as the upper limit temperature, viscosity, optical anisotropy, dielectric anisotropy of the nematic phase, a mixture of a compound and a mother liquid crystal was used as a sample.
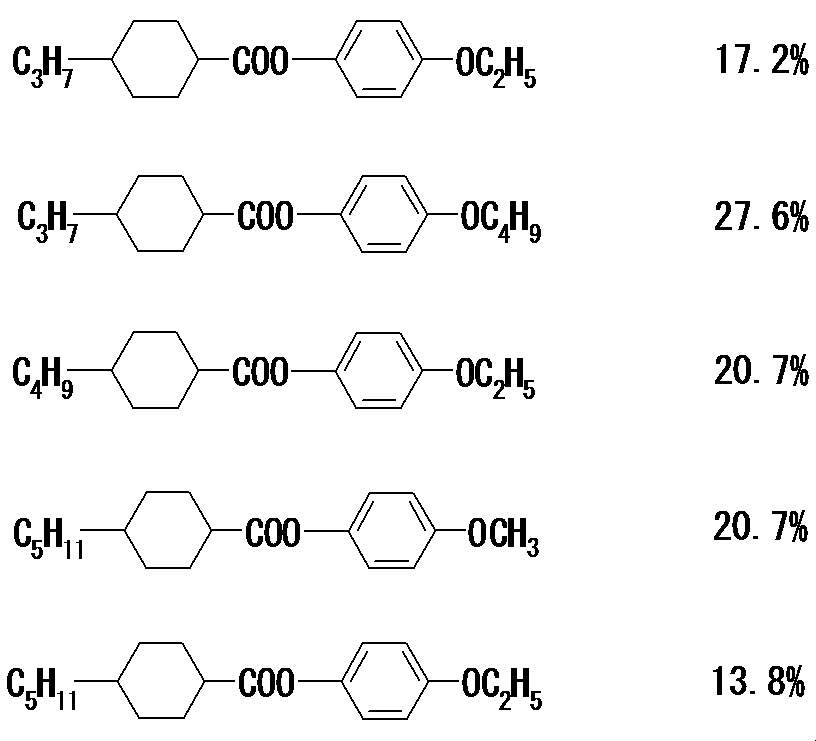
- Mother liquid crystal (A) The following mother liquid crystal (A) was used as the mother liquid crystal. The ratio of each component was expressed in wt%.
- the ratio of the compound and the mother liquid crystal (A) was 15% by weight: 85% by weight.
- the ratio of the compound to the mother liquid crystal (A) is 10% by weight: 90% by weight, 5% by weight: 95% by weight, 1% by weight: 99%.
- the characteristics of the sample were measured at a rate at which crystals (or smectic phases) did not precipitate at 25 ° C. in the order of weight%. Unless otherwise specified, the ratio of the compound to the mother liquid crystal (A) was 15% by weight: 85% by weight.
- Measurement method Physical properties were measured by the following method. Many of these are the methods described in the JEITA standard (JEITA ED-2521B) established by the Japan Electronics and Information Technology Industries Association (JEITA; Japan Electronics and Information Technology Industries Association) or a modified method thereof. there were. No thin film transistor (TFT) was attached to the TN device used for the measurement.
- JEITA Japan Electronics and Information Technology Industries Association
- TFT thin film transistor
- Phase structure A sample was placed on a hot plate (Mettler's FP-52 type hot stage or Linkam's 10083L cooling and heating hot stage) equipped with a polarizing microscope. While heating this sample at a rate of 3 ° C./min, the phase state and its change were observed with a polarizing microscope to identify the type of phase.
- a hot plate Metaltler's FP-52 type hot stage or Linkam's 10083L cooling and heating hot stage
- the temperature at which a compound transitions from a solid to a liquid crystal phase such as a smectic phase or a nematic phase may be abbreviated as “lower limit temperature of liquid crystal phase”.
- the temperature at which the compound transitions from the liquid crystal phase to the liquid may be abbreviated as “clearing point”.
- the crystal was represented as C. When the types of crystals can be distinguished, they are expressed as C 1 or C 2 , respectively.
- the smectic phase is represented as S and the nematic phase is represented as N.
- the smectic phase when a smectic A phase, a smectic B phase, a smectic C phase, or a smectic F phase can be distinguished, they are represented as S A , S B , S C , or S F , respectively.
- the liquid (isotropic) was designated as I.
- the transition temperature is expressed as “C 50.0 N 100.0 I”, for example. This indicates that the transition temperature from the crystal to the nematic phase is 50.0 ° C., and the transition temperature from the nematic phase to the liquid is 100.0 ° C.
- T NI or NI Maximum temperature of nematic phase
- a sample was placed on a hot plate of a melting point measurement apparatus equipped with a polarizing microscope and heated at a rate of 1 ° C./min. The temperature was measured when a part of the sample changed from a nematic phase to an isotropic liquid.
- TNI When the sample was a mixture of compound (1) and mother liquid crystals, it was indicated by the symbol TNI .
- TNI When the sample was a mixture of compound (1) and compounds such as components B, C and D, it was indicated by the symbol NI.
- the upper limit temperature of the nematic phase may be abbreviated as “upper limit temperature”.
- T C Minimum Temperature of a Nematic Phase
- a sample having a nematic phase was placed in a glass bottle and stored in a freezer at 0 ° C., ⁇ 10 ° C., ⁇ 20 ° C., ⁇ 30 ° C., and ⁇ 40 ° C. for 10 days, and then the liquid crystal phase was observed.
- the TC was described as ⁇ 20 ° C.
- the lower limit temperature of the nematic phase may be abbreviated as “lower limit temperature”.
- Viscosity Bulk viscosity; ⁇ ; measured at 20 ° C .; mPa ⁇ s
- An E-type viscometer manufactured by Tokyo Keiki Co., Ltd. was used for the measurement.
- Viscosity (Rotational viscosity; ⁇ 1; measured at 25 ° C .; mPa ⁇ s) The measurement followed the method described in M. Imai et al., Molecular Crystals and Liquid Crystals, Vol. 259, 37 (1995). A sample was put in a TN device having a twist angle of 0 ° and a distance (cell gap) between two glass substrates of 5 ⁇ m. A voltage was applied to this device in steps of 0.5 V in the range of 16 V to 19.5 V. After no application for 0.2 seconds, the application was repeated under the condition of only one rectangular wave (rectangular pulse; 0.2 seconds) and no application (2 seconds). The peak current and peak time of the transient current generated by this application were measured.
- Threshold voltage (Vth; measured at 25 ° C .; V) An LCD5100 luminance meter manufactured by Otsuka Electronics Co., Ltd. was used for the measurement.
- the light source was a halogen lamp.
- a sample was put in a normally white mode TN device in which the distance between two glass substrates (cell gap) was about 0.45 / ⁇ n ( ⁇ m) and the twist angle was 80 degrees.
- the voltage (32 Hz, rectangular wave) applied to this element was increased stepwise from 0V to 10V by 0.02V.
- the device was irradiated with light from the vertical direction, and the amount of light transmitted through the device was measured.
- a voltage-transmittance curve was created in which the transmittance was 100% when the light amount reached the maximum and the transmittance was 0% when the light amount was the minimum.
- the threshold voltage was expressed as a voltage when the transmittance reached 90%.
- VHR-1 Voltage holding ratio
- the TN device used for the measurement had a polyimide alignment film, and the distance (cell gap) between the two glass substrates was 5 ⁇ m. This element was sealed with an adhesive that was cured with ultraviolet rays after the sample was placed.
- the device was charged by applying a pulse voltage (5 V, 60 microseconds) at 25 ° C.
- the decaying voltage was measured for 16.7 milliseconds with a high-speed voltmeter, and the area A between the voltage curve and the horizontal axis in a unit cycle was determined.
- Area B was the area when it was not attenuated.
- the voltage holding ratio was expressed as a percentage of area A with respect to area B.
- the transmittance was 100% when the light amount was the maximum, and the transmittance was 0% when the light amount was the minimum.
- the rise time ( ⁇ r: rise time; millisecond) was the time required for the transmittance to change from 90% to 10%.
- the fall time ( ⁇ f: fall time; millisecond) was the time required to change the transmittance from 10% to 90%.
- the response time was expressed as the sum of the rise time and the fall time thus obtained.
- Raw material Solmix (registered trademark) A-11 was a mixture of ethanol (85.5%), methanol (13.4%) and isopropanol (1.1%), and was obtained from Nippon Alcohol Sales Co., Ltd.
- Tetrahydrofuran may be abbreviated as THF.
- Tetrabutylammonium bromide may be abbreviated as TBAB.
- N, N-dimethylformamide may be abbreviated as DMF.
- 2-propanol is sometimes abbreviated as IPA. 1,2-dimethoxyethane may be abbreviated as DME.
- Hexamethyldisilazane potassium may be abbreviated as KHMDS.
- Step 1 Under a nitrogen atmosphere, compound (T-1) (3 g) and THF (100 ml) were placed in a reactor and cooled to 0 ° C. Magnesium (0.36 g) was added thereto and stirred for 2 hours. Propanal (0.98g) was added there, and it returned to room temperature, and stirred for 1 hour. The reaction solution was poured into water and extracted with toluene. The combined organic layers were washed with water, saturated aqueous sodium hydrogen carbonate, and water, and dried over anhydrous magnesium sulfate. Paratoluenesulfonic acid monohydrate (1 g) was added thereto, and the mixture was refluxed for 1 hour while removing water.
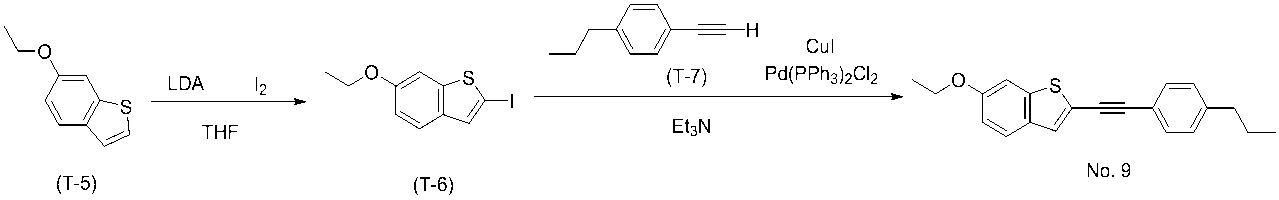
- Step 1 Under a nitrogen atmosphere, the compound (T-5) (1.5 g) and THF (70 ml) were placed in a reactor and cooled to -74 ° C. Thereto, lithium diisopropylamide (1M; n-hexane solution; 9.26 ml) was added dropwise in the temperature range of ⁇ 74 ° C. to ⁇ 70 ° C., and the mixture was further stirred for 2 hours. Subsequently, iodine (2.56 g) was added in a temperature range of ⁇ 75 ° C. to ⁇ 70 ° C., and the mixture was stirred for 8 hours while returning to 25 ° C.
- lithium diisopropylamide (1M; n-hexane solution; 9.26 ml
- reaction mixture was poured into an aqueous sodium hydrogen sulfite solution and extracted with toluene.
- the combined organic layers were washed with water, saturated aqueous sodium hydrogen carbonate, and water, and dried over anhydrous magnesium sulfate. This solution was concentrated under reduced pressure to obtain compound (T-6) (2.6 g).
- T-1) (1.5 g) and (T-7) (1.5 g) synthesized by a known method are dissolved in toluene, and water, ethanol, Pd (PPh 3 ) 4 (0.8 g ), TBAB (0.22 g) and potassium carbonate (2.9 g) were added and heated to reflux for 6 hours. After completion of the reaction, the mixture was extracted with toluene, washed with water, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure to obtain a light brown solid. The solid was converted into a solution and subjected to silica gel column chromatography (heptane) to give (T-8) as colorless crystals (1.7 g).
- Comparative Example Compound (1) was compared with a similar compound from the viewpoint of physical properties.
- No. 200 can be synthesized from the following compound (No. 1) according to the synthesis method of compound (1) and the synthesis procedures described in Examples 1 to 4.
- composition examples Examples illustrate the compositions of the present invention in detail.
- the present invention includes a mixture of the composition of Use Example 1 and the composition of Use Example 2.
- the present invention also includes a mixture in which at least two of the compositions of the use examples are mixed.
- the compounds in the use examples were represented by symbols based on the definitions in Table 1 below.
- Table 1 the configuration regarding 1,4-cyclohexylene is trans.
- the number in parentheses after the symbol corresponds to the number of the compound.
- the symbol ( ⁇ ) means other liquid crystal compounds.
- the ratio (percentage) of the liquid crystal compound is a weight percentage (% by weight) based on the weight of the liquid crystal composition.
- the liquid crystalline compound of the present invention has high stability to heat and light, high clearing point (or high maximum temperature), low minimum temperature of liquid crystal phase, small viscosity, appropriate optical anisotropy, large dielectric anisotropy, It satisfies at least one of physical properties such as an appropriate elastic constant and excellent compatibility with other liquid crystal compounds.
- This compound has particularly excellent compatibility with other liquid crystal compounds.
- the liquid crystal composition of the present invention contains this compound and has physical properties such as a high maximum temperature, a low minimum temperature, a small viscosity, an appropriate optical anisotropy, a large dielectric anisotropy, a large specific resistance, and an appropriate elastic constant. Satisfy at least one of the following.
- the liquid crystal display element of the present invention contains this composition and has a wide temperature range in which the element can be used, a short response time, a large voltage holding ratio, a low threshold voltage, a large contrast ratio, and a long lifetime. Therefore, it can be widely used for liquid crystal display elements used in personal computers and televisions.
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Crystallography & Structural Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Physics & Mathematics (AREA)
- Nonlinear Science (AREA)
- General Physics & Mathematics (AREA)
- Optics & Photonics (AREA)
- Liquid Crystal Substances (AREA)
- Plural Heterocyclic Compounds (AREA)
Abstract
Description
式(1)において、
R1およびR2は独立して、水素または炭素数1から20のアルキルであり、このアルキルにおいて、少なくとも1つの-CH2-は-O-または-S-で置き換えられてもよく、少なくとも1つの-(CH2)2-は-CH=CH-で置き換えられてもよく、これらの基において、少なくとも1つの水素はハロゲンで置き換えられてもよく;
環A1および環A2は独立して、1,4-シクロヘキシレン、1,4-シクロヘキセニレン、1,4-フェニレン、テトラヒドロピラン-2,5-ジイル、1,3-ジオキサン-2,5-ジイル、ピリミジン-2,5-ジイル、2,6,7-トリオキサビシクロ[2.2.2]オクタン-1,4-ジイル、ナフタレン-2,6-ジイル、またはピリジン-2,5-ジイルであり、これらの環上の少なくとも1つの水素はハロゲンで置き換えられていてもよく;
aおよびbは独立して、0、1、2、3、または4であり、aおよびbの和は4以下であり、aまたはbが2以上のとき、2つの環A1、2つの環A2、2つのZ1、または2つのZ2は、同一であっても、異なっていてもよく;
Z1およびZ2は独立して、単結合または炭素数1から4のアルキレンであり、このアルキレンにおいて、少なくとも1つの-CH2-は-O-または-COO-で置き換えられてもよく、少なくとも1つの-(CH2)2-は-CH=CH-または-C≡C-で置き換えられてもよく、これらの基において、少なくとも1つの水素はハロゲンで置き換えられてもよく、Z1およびZ2が同時に-CH=CH-または-C≡C-のいずれかであることはなく、aが0でbが1であるとき、Z2は炭素数1から4のアルキレンであり、このアルキレンにおいて、少なくとも1つの-CH2-は-O-または-COO-で置き換えられてもよく、少なくとも1つの-(CH2)2-は-CH=CH-または-C≡C-で置き換えられてもよく、少なくとも1つの水素はハロゲンで置き換えられてもよく;Z3は、-O-、または単結合であり;
L1、L2、およびL3は独立して、水素、フッ素、または塩素である。
式(1)において、
R1およびR2は独立して、水素または炭素数1から20のアルキルであり、このアルキルにおいて、少なくとも1つの-CH2-は-O-または-S-で置き換えられてもよく、少なくとも1つの-(CH2)2-は-CH=CH-で置き換えられてもよく、これらの基において、少なくとも1つの水素はハロゲンで置き換えられてもよく;
環A1および環A2は独立して、1,4-シクロヘキシレン、1,4-シクロヘキセニレン、1,4-フェニレン、テトラヒドロピラン-2,5-ジイル、1,3-ジオキサン-2,5-ジイル、ピリミジン-2,5-ジイル、2,6,7-トリオキサビシクロ[2.2.2]オクタン-1,4-ジイル、ナフタレン-2,6-ジイル、またはピリジン-2,5-ジイルであり、これらの環上の少なくとも1つの水素はハロゲンで置き換えられていてもよく;
aおよびbは独立して、0、1、2、3、または4であり、aおよびbの和は4以下であり、aまたはbが2以上のとき、2つの環A1、2つの環A2、2つのZ1、または2つのZ2は、同一であっても、異なっていてもよく;
Z1およびZ2は独立して、単結合または炭素数1から4のアルキレンであり、このアルキレンにおいて、少なくとも1つの-CH2-は-O-または-COO-で置き換えられてもよく、少なくとも1つの-(CH2)2-は-CH=CH-または-C≡C-で置き換えられてもよく、これらの基において、少なくとも1つの水素はハロゲンで置き換えられてもよく、Z1およびZ2が同時に-CH=CH-または-C≡C-のいずれかであることはなく、aが0でbが1であるとき、Z2は炭素数1から4のアルキレンであり、このアルキレンにおいて、少なくとも1つの-CH2-は-O-または-COO-で置き換えられてもよく、少なくとも1つの-(CH2)2-は-CH=CH-または-C≡C-で置き換えられてもよく、少なくとも1つの水素はハロゲンで置き換えられてもよく;Z3は、-O-または単結合であり;
L1、L2、およびL3は独立して、水素、フッ素、または塩素である。
R1およびR2は独立して、水素、炭素数1から10のアルキル、炭素数1から9のアルコキシ、炭素数2から10のアルケニル、または少なくとも1つの水素がフッ素に置き換えられた炭素数1から10のアルキルであり;
環A1および環A2は独立して、1,4-シクロヘキシレン、1,4-シクロヘキセニレン、少なくとも1つの水素がハロゲンで置き換えられてもよい1,4-フェニレン、またはテトラヒドロピラン-2,5-ジイルであり;
Z1およびZ2は独立して、単結合、-(CH2)2-、-CH=CH-、-CF=CF-、-C≡C-、-COO-、-OCO-、-CF2O-、-OCF2-、-CH2O-、-OCH2-、-(CH2)4-、-(CH2)2CF2O-、-(CH2)2OCF2-、-CF2O(CH2)2-、-OCF2(CH2)2-、-CH=CH-(CH2)2-、または-(CH2)2-CH=CH-であり、aが0でbが1であるとき、Z2は、-(CH2)2-、-CH=CH-、-CF=CF-、-C≡C-、-COO-、-OCO-、-CF2O-、-OCF2-、-CH2O-、-OCH2-、-(CH2)4-、-(CH2)2CF2O-、-(CH2)2OCF2-、-CF2O(CH2)2-、-OCF2(CH2)2-、-CH=CH-(CH2)2-、または-(CH2)2-CH=CH-であり;
aおよびbは独立して、0、1、2、3、または4であり、aおよびbの和は4以下であり;
L1、L2、およびL3は独立して、水素、フッ素、または塩素である、項1に記載の化合物。
aおよびbの和が、0、1、2、または3であり;
R1およびR2は独立して、水素、炭素数1から10のアルキル、炭素数1から9のアルコキシ、炭素数2から10のアルケニル、炭素数1から10のフッ素化アルキル;
環A1および環A2は独立して、1,4-シクロヘキシレン、1,4-シクロヘキセニレン、少なくとも1つの水素がハロゲンで置き換えられてもよい1,4-フェニレン、またはテトラヒドロピラン-2,5-ジイルあり;
Z1およびZ2は独立して、単結合、-(CH2)2-、-CH=CH-、-CF=CF-、-C≡C-、-COO-、-OCO-、-CF2O-、-OCF2-、-CH2O-、-OCH2-、-(CH2)4-、-(CH2)2CF2O-、-(CH2)2OCF2-、-CF2O(CH2)2-、-OCF2(CH2)2-、-CH=CH-(CH2)2-、または-(CH2)2-CH=CH-であり、aが0でbが1であるとき、Z2は、-(CH2)2-、-CH=CH-、-CF=CF-、-C≡C-、-COO-、-OCO-、-CF2O-、-OCF2-、-CH2O-、-OCH2-、-(CH2)4-、-(CH2)2CF2O-、-(CH2)2OCF2-、-CF2O(CH2)2-、-OCF2(CH2)2-、-CH=CH-(CH2)2-、または-(CH2)2-CH=CH-であり;
L1、L2、およびL3は独立して、水素、フッ素、または塩素である、項1または2に記載の化合物。
式(1-1)から(1-7)、および(1-9)から(1-10)において、
R1およびR2は独立して、水素、炭素数1から10のアルキル、炭素数1から9のアルコキシ、炭素数2から10のアルケニル、または少なくとも1つの水素がフッ素に置き換えられた炭素数1から10のアルキルであり;
環A11、環A12、環A13、環A21、環A22、および環A23は独立して、1,4-シクロヘキシレン、1,4-シクロヘキセニレン、1,4-フェニレン、少なくとも1つの水素がハロゲンで置き換えられた1,4-フェニレン、またはテトラヒドロピラン-2,5-ジイルあり;
Z11、Z12、Z13、Z21、Z22およびZ23は独立して、単結合、-(CH2)2-、-CH=CH-、-CF=CF-、-C≡C-、-COO-、-OCO-、-CF2O-、-OCF2-、-CH2O-、-OCH2-、-(CH2)4-、-(CH2)2CF2O-、-(CH2)2OCF2-、-CF2O(CH2)2-、-OCF2(CH2)2-、-CH=CH-(CH2)2-、または-(CH2)2-CH=CH-であり;
L1、L2およびL3は独立して、水素、フッ素、または塩素であり;
式(1-8)において、
R1およびR2は独立して、水素、炭素数1から10のアルキル、炭素数1から9のアルコキシ、炭素数2から10のアルケニル、または少なくとも1つの水素がフッ素に置き換えられた炭素数1から10のアルキルであり;
環A21は、1,4-シクロヘキシレン、1,4-シクロヘキセニレン、1,4-フェニレン、少なくとも1つの水素がハロゲンで置き換えられた1,4-フェニレン、またはテトラヒドロピラン-2,5-ジイルであり;
Z21が独立して、-(CH2)2-、-CH=CH-、-CF=CF-、-C≡C-、-COO-、-OCO-、-CF2O-、-OCF2-、-CH2O-、-OCH2-、-(CH2)4-、-(CH2)2CF2O-、-(CH2)2OCF2-、-CF2O(CH2)2-、-OCF2(CH2)2-、-CH=CH-(CH2)2-、または-(CH2)2-CH=CH-であり;
L1、L2、およびL3は独立して、水素、フッ素、または塩素である。
R1およびR2は独立して、水素、フッ素、炭素数1から10のアルキル、炭素数1から9のアルコキシ、炭素数2から10のアルケニル、または炭素数1から10のフッ素化アルキルでありであり;
環A11、環A12、環A13、環A21、環A22、および環A23は独立して、1,4-シクロヘキシレン、1,4-シクロヘキセニレン、少なくとも1つの水素がハロゲンで置き換えられてもよい1,4-フェニレン、テトラヒドロピラン-2,5-ジイルであり;
Z11、Z12、Z13、Z21、Z22、およびZ23は独立して、単結合、-(CH2)2-、-CH=CH-、-C≡C-、-CF2O-、-OCF2-、-CH2O-、または-OCH2-であり;
L1、L2、およびL3は独立して、水素、フッ素、または塩素であり;
式(1-8)において、
R1およびR2は独立して、水素、フッ素、炭素数1から10のアルキル、炭素数1から9のアルコキシ、炭素数2から10のアルケニル、または炭素数1から10のフッ素化アルキルであり;
環A11、環A12、環A13、環A21、環A22、および環A23は独立して、1,4-シクロヘキシレン、1,4-シクロヘキセニレン、少なくとも1つの水素がハロゲンで置き換えられてもよい1,4-フェニレン、テトラヒドロピラン-2,5-ジイルであり;
Z11、Z12、Z13、Z21、Z22、およびZ23は独立して、-(CH2)2-、-CH=CH-、-C≡C-、-CF2O-、-OCF2-、-CH2O-、または-OCH2-であり;
L1、L2、およびL3は独立して、水素、フッ素、または塩素であり、
式(1-1)から(1-10)の少なくとも1つで表される項4に記載の化合物。
式(1-1)、(1-5)および(1-10)において、
R1およびR2は独立して、水素、フッ素、炭素数1から10のアルキル、炭素数1から9のアルコキシ、炭素数2から10のアルケニル、または少なくとも1つの水素がフッ素に置き換えられた炭素数1から10のアルキルであり;
環A21、環A22、および環A23は独立して、1,4-シクロヘキシレン、少なくとも1つの水素がハロゲンで置き換えられてもよい1,4-フェニレンであり;
Z21、Z22、およびZ23は独立して、単結合、-(CH2)2-、-CH=CH-、-C≡C-、-CH2O-、または-OCH2-であり;
L1、L2、およびL3は独立して、水素、またはフッ素である。
式(1-8)において、
R1およびR2は独立して、水素、フッ素、炭素数1から10のアルキル、炭素数1から9のアルコキシ、炭素数2から10のアルケニル、または少なくとも1つの水素がフッ素に置き換えられた炭素数1から10のアルキルであり;
環A21は、1,4-シクロヘキシレン、または少なくとも1つの水素がハロゲンで置き換えられてもよい1,4-フェニレンであり;
Z21は、単結合、-(CH2)2-、-CH=CH-、-C≡C-、-CH2O-、または-OCH2-であり;
L1、L2、およびL3は独立して、水素またはフッ素である。
式(1-4)、(1-7)、および(1-9)において、
R1およびR2は独立して、水素、フッ素、炭素数1から10のアルキル、炭素数1から9のアルコキシ、炭素数2から10のアルケニル、または少なくとも1つの水素がフッ素に置き換えられた炭素数1から10のアルキルであり;
環A11、環A12、および環A13は独立して、1,4-シクロヘキシレン、少なくとも1つの水素がハロゲンで置き換えられてもよい1,4-フェニレンであり;
Z11、Z12、およびZ13は独立して、単結合、-(CH2)2-、-CH=CH-、-C≡C-、-CH2O-、または-OCH2-であり;
L1、L2、およびL3は独立して、水素またはフッ素である。
式(2)から(4)において、
R11およびR12は独立して、炭素数1から10のアルキルまたは炭素数2から10のアルケニルであり、このアルキルまたはアルケニルにおいて、少なくとも1つの-CH2-は-O-で置き換えられてもよく、少なくとも1つの水素はフッ素で置き換えられてもよく;
環B1、環B2、環B3、および環B4は独立して、1,4-シクロヘキシレン、1,4-フェニレン、2-フルオロ-1,4-フェニレン、2,5-ジフルオロ-1,4-フェニレン、またはピリミジン-2,5-ジイルであり;
Z11、Z12、およびZ13は独立して、単結合、-CH2CH2-、-CH=CH-、-C≡C-、または-COO-である。
式(5)から(7)において、
R13は炭素数1から10のアルキルまたは炭素数2から10のアルケニルであり、このアルキルおよびアルケニルにおいて、少なくとも1つの-CH2-は-O-で置き換えられてもよく、少なくとも1つの水素はフッ素で置き換えられてもよく;
X11は、フッ素、塩素、-OCF3、-OCHF2、-CF3、-CHF2、-CH2F、-OCF2CHF2、または-OCF2CHFCF3であり;
環C1、環C2、および環C3は独立して、1,4-シクロヘキシレン、少なくとも1つの水素がフッ素で置き換えられてもよい1,4-フェニレン、テトラヒドロピラン-2,5-ジイル、1,3-ジオキサン-2,5-ジイル、またはピリミジン-2,5-ジイルであり;
Z14、Z15、およびZ16は独立して、単結合、-CH2CH2-、-CH=CH-、-C≡C-、-COO-、-CF2O-、-OCF2-、-CH2O-、または-(CH2)4-であり;
L11およびL12は独立して、水素またはフッ素である。
式(8)において、
R14は炭素数1から10のアルキルまたは炭素数2から10のアルケニルであり、このアルキルおよびアルケニルにおいて、少なくとも1つの-CH2-は-O-で置き換えられてもよく、少なくとも1つの水素はフッ素で置き換えられてもよく;
X12は、-C≡Nまたは-C≡C-C≡Nであり;
環D1は、1,4-シクロヘキシレン、少なくとも1つの水素がフッ素で置き換えられてもよい1,4-フェニレン、テトラヒドロピラン-2,5-ジイル、1,3-ジオキサン-2,5-ジイル、またはピリミジン-2,5-ジイルであり;
Z17は、単結合、-CH2CH2-、-C≡C-、-COO-、-CF2O-、-OCF2-、または-CH2O-であり;
L13およびL14は独立して、水素またはフッ素であり;
iは、1、2、3、または4である。
式(9)から(15)において、
R15およびR16は独立して、炭素数1から10のアルキルまたは炭素数2から10のアルケニルであり、このアルキルおよびアルケニルにおいて、少なくとも1つの-CH2-は-O-で置き換えられてもよく、少なくとも1つの水素はフッ素で置き換えられてもよく;
R17は、水素、フッ素、炭素数1から10のアルキル、または炭素数2から10のアルケニルであり、このアルキルおよびアルケニルにおいて、少なくとも1つの-CH2-は-O-で置き換えられてもよく、少なくとも1つの水素はフッ素で置き換えられてもよく;
環E1、環E2、環E3、および環E4は独立して、1,4-シクロヘキシレン、1,4-シクロヘキセニレン、少なくとも1つの水素がフッ素で置き換えられてもよい1,4-フェニレン,テトラヒドロピラン-2,5-ジイル、またはデカヒドロナフタレン-2,6-ジイルであり;環E5および環E6は独立して、1,4-シクロヘキシレン、1,4-シクロヘキセニレン、1,4-フェニレン,テトラヒドロピラン-2,5-ジイル、またはデカヒドロナフタレン-2,6-ジイルであり;
Z18、Z19、Z20、およびZ21は独立して、単結合、-CH2CH2-、-COO-、-CH2O-、-OCF2-、または-OCF2CH2CH2-であり;
L15およびL16は独立して、フッ素または塩素であり;
S11は、水素またはメチルであり;
Xは、-CHF-または-CF2-であり;
j、k、m、n、p、q、r、およびsは独立して、0または1であり、k、m、n、およびpの和は、1または2であり、q、r、およびsの和は、0、1、2、または3であり、tは、1、2、または3である。
本発明の化合物(1)は、1-ベンゾチオフェン環の構造を有す。化合物(1)の好ましい例について説明をする。化合物(1)における末端基、環構造、結合基、および置換基の好ましい例は、化合物(1-1)、化合物(1-2)等の化合物(1)の下位式にも適用される。化合物(1)において、これらの基の種類を適切に組み合わせることによって、物性を任意に調整することが可能である。化合物の物性に大きな差異がないので、化合物(1)は、2H(重水素)、13Cなどの同位体を天然存在比の量より多く含んでもよい。なお、化合物(1)の記号の定義は、項1に記載したとおりである。
化合物(1)の合成法を説明する。化合物(1)は、有機合成化学の方法を適切に組み合わせることによって合成できる。出発物に目的の末端基、環および結合基を導入する方法は、「オーガニック・シンセシス」(Organic Syntheses, John Wiley & Sons, Inc.)、「オーガニック・リアクションズ」(Organic Reactions, John Wiley & Sons, Inc.)、「コンプリヘンシブ・オーガニック・シンセシス」(Comprehensive Organic Synthesis, Pergamon Press)、「新実験化学講座」(丸善)などの成書に記載されている。
結合基Z1からZ2を生成する方法に関して、最初にスキームを示す。次に項(1)から項(11)でスキームに記載した反応を説明する。このスキームにおいて、MSG1(またはMSG2)は少なくとも1つの環を有する1価の有機基である。スキームで用いた複数のMSG1(またはMSG2)が表わす一価の有機基は、同一であってもよいし、または異なってもよい。化合物(1A)から(1J)は化合物(1)に相当する。
公知の方法で合成されるアリールホウ酸(21)とハロゲン化物(22)とを、炭酸塩およびテトラキス(トリフェニルホスフィン)パラジウムのような触媒の存在下で反応させて化合物(1A)を合成する。この化合物(1A)は、公知の方法で合成されるハロゲン化物(23)にn-ブチルリチウムを、次いで塩化亜鉛を反応させ、ジクロロビス(トリフェニルホスフィン)パラジウムのような触媒の存在下でハロゲン化物(22)を反応させることによっても合成される。
ハロゲン化物(23)にn-ブチルリチウムを、続いて二酸化炭素を反応させてカルボン酸(24)を得る。公知の方法で合成される化合物(25)とカルボン酸(24)とをDCC(1,3-ジシクロヘキシルカルボジイミド)とDMAP(4-ジメチルアミノピリジン)の存在下で脱水させて化合物(1B)を合成する。
化合物(1B)をローソン試薬のような硫黄化剤で処理してチオノエステル(26)を得る。チオノエステル(26)をフッ化水素ピリジン錯体とNBS(N-ブロモスクシンイミド)でフッ素化し、化合物(1C)を合成する。M. Kuroboshi et al., Chem. Lett., 1992,827.を参照。化合物(1C)はチオノエステル(26)をDAST((ジエチルアミノ)サルファートリフルオリド)でフッ素化しても合成される。W. H. Bunnelle et al., J. Org. Chem. 1990, 55, 768.を参照。Peer. Kirsch et al., Angew. Chem. Int. Ed. 2001, 40, 1480.に記載の方法によってこれらの結合基を生成させることも可能である。
ハロゲン化物(22)をn-ブチルリチウムで処理した後、DMF(N,N-ジメチルホルムアミド)などのホルムアミドと反応させてアルデヒド(28)を得る。公知の方法で合成されるホスホニウム塩(27)をカリウムt-ブトキシドのような塩基で処理して発生させたリンイリドを、アルデヒド(28)に反応させて化合物(1D)を合成する。反応条件によってはシス体が生成するので、必要に応じて公知の方法によりシス体をトランス体に異性化する。
化合物(1D)をパラジウム炭素のような触媒の存在下で水素化することにより、化合物(1E)を合成する。
ホスホニウム塩(27)の代わりにホスホニウム塩(29)を用い、項(4)の方法に従って-(CH2)2-CH=CH-を有する化合物を得る。これを接触水素化して化合物(1F)を合成する。
ホスホニウム塩(27)の代わりにホスホニウム塩(30)を、アルデヒド(28)の代わりにアルデヒド(31)を用い、項(4)の方法に従って化合物(1G)を合成する。反応条件によってはトランス体が生成するので、必要に応じて公知の方法によりトランス体をシス体に異性化する。
ジクロロパラジウムとハロゲン化銅との触媒存在下で、ハロゲン化物(23)に2-メチル-3-ブチン-2-オールを反応させたのち、塩基性条件下で脱保護して化合物(32)を得る。ジクロロパラジウムとハロゲン化銅との触媒存在下、化合物(32)をハロゲン化物(22)と反応させて、化合物(1H)を合成する。
ハロゲン化物(23)をn-ブチルリチウムで処理したあと、テトラフルオロエチレンを反応させて化合物(33)を得る。ハロゲン化物(22)をn-ブチルリチウムで処理したあと化合物(33)と反応させて化合物(1I)を合成する。
アルデヒド(28)を水素化ホウ素ナトリウムなどの還元剤で還元して化合物(34)を得る。化合物(34)を臭化水素酸などで臭素化して臭化物(35)を得る。炭酸カリウムなどの塩基存在下で、臭化物(35)を化合物(36)と反応させて化合物(1J)を合成する。
J. Am. Chem. Soc., 2001, 123, 5414. に記載された方法に従い、ジケトン(-COCO-)をフッ化水素触媒の存在下、四フッ化硫黄でフッ素化して-(CF2)2-を有する化合物を得る。
1,4-シクロヘキシレン、1,4-フェニレン、2-フルオロ-1,4-フェニレン、2,6-ジフルオロ-1,4-フェニレン、テトラヒドロピラン-2,5-ジイル、1,3-ジオキサン-2,5-ジイル、ピリミジン-2,5-ジイル、またはピリジン-2,5-ジイルなどの環に関しては出発物が市販されているか、または合成法がよく知られている。
化合物(1)を合成する方法の例は、次のとおりである。これらの化合物において、R1、R2、環A1、環A2、Z1、Z2、Z3、L1、L2、L3、a、およびbの定義は、前記の項1と同一である。公知の方法によって合成された化合物(b-1)をMgと反応させグリニアール試薬調整し、S及びブロモアセトアルデヒドジエチルアセタールを反応させ(b-2)を得る。これをトルエンまたはクロロベンゼン中でポリリン酸と反応させることにより(b-3)を得る。(b-3)をLDAによりリチオ化し(b-4)とし、ここに種々の試薬を反応させ種々の中間体を得る。これを用い公知の方法で化合物(1)へ誘導する。
3-1.成分化合物
本発明の液晶組成物について説明をする。この組成物は、少なくとも1つの化合物(1)を成分Aとして含む。化合物(1)は、組成物の上限温度を上げるために有用である。組成物は、2つまたは3つ以上の化合物(1)を含んでもよい。組成物の成分が化合物(1)のみであってもよい。組成物は、化合物(1)の少なくとも1つを1重量%から99重量%の範囲で含有することが、優良な物性を発現させるために好ましい。誘電率異方性が正である組成物において、化合物(1)の好ましい含有量は5重量%から60重量%の範囲である。誘電率異方性が負である組成物において、化合物(1)の好ましい含有量は30重量%以下である。組成物は、化合物(1)と、本明細書中に記載しなかった液晶性化合物とを含んでもよい。
液晶組成物は公知の方法によって調製される。例えば、成分化合物を混合し、そして加熱によって互いに溶解させる。用途に応じて、この組成物に添加物を添加してよい。添加物の例は、重合性化合物、重合開始剤、重合禁止剤、光学活性化合物、酸化防止剤、紫外線吸収剤、光安定剤、熱安定剤、色素、消泡剤などである。このような添加物は当業者によく知られており、文献に記載されている。
液晶組成物は、PC、TN、STN、OCB、PSAなどの動作モードを有し、アクティブマトリックスで駆動する液晶表示素子に使用できる。この組成物は、PC、TN、STN、OCB、VA、IPSなどの動作モードを有し、パッシブマトリクス方式で駆動する液晶表示素子にも使用することができる。これらの素子は、反射型、透過型、半透過型のいずれのタイプにも適用ができる。
化合物(1)は、下記の手順により合成した。合成した化合物は、NMR分析などの方法により同定した。化合物や組成物の物性、および素子の特性は、下記の方法により測定した。
偏光顕微鏡を備えた融点測定装置のホットプレート(メトラー社FP-52型ホットステージまたは、リンカム社製10083L冷却加熱ホットステージ)に試料を置いた。この試料を、3℃/分の速度で加熱しながら相状態とその変化を偏光顕微鏡で観察し、相の種類を特定した。
測定には、パーキンエルマー社製の走査熱量計、Diamond DSCシステムまたはエスアイアイ・ナノテクノロジー社製の高感度示差走査熱量計、X-DSC7000を用いた。試料は、3℃/分の速度で昇降温し、試料の相変化に伴う吸熱ピークまたは発熱ピークの開始点を外挿により求め、転移温度を決定した。化合物の融点、重合開始温度もこの装置を使って測定した。化合物が固体からスメクチック相、ネマチック相などの液晶相に転移する温度を「液晶相の下限温度」と略すことがある。化合物が液晶相から液体に転移する温度を「透明点」と略すことがある。
化合物の割合が、20重量%、15重量%、10重量%、5重量%、3重量%、および1重量%となるように母液晶と化合物とを混合した試料を調製し、試料をガラス瓶に入れた。このガラス瓶を、-10℃または-20℃のフリーザー中に一定期間保管したあと、結晶またはスメクチック相が析出しているかどうか観察をした。
偏光顕微鏡を備えた融点測定装置のホットプレートに試料を置き、1℃/分の速度で加熱した。試料の一部がネマチック相から等方性液体に変化したときの温度を測定した。試料が化合物(1)と母液晶との混合物であるときは、TNIの記号で示した。試料が化合物(1)と成分B、C、Dのような化合物との混合物であるときは、NIの記号で示した。ネマチック相の上限温度を「上限温度」と略すことがある。
ネマチック相を有する試料をガラス瓶に入れ、0℃、-10℃、-20℃、-30℃、および-40℃のフリーザー中に10日間保管したあと、液晶相を観察した。例えば、試料が-20℃ではネマチック相のままであり、-30℃では結晶またはスメクチック相に変化したとき、TCを<-20℃と記載した。ネマチック相の下限温度を「下限温度」と略すことがある。
測定には東京計器株式会社製のE型回転粘度計を用いた。
測定は、M. Imai et al., Molecular Crystals and Liquid Crystals, Vol. 259, 37 (1995) に記載された方法に従った。ツイスト角が0°であり、そして2枚のガラス基板の間隔(セルギャップ)が5μmであるTN素子に試料を入れた。この素子に16Vから19.5Vの範囲で0.5V毎に段階的に印加した。0.2秒の無印加のあと、ただ1つの矩形波(矩形パルス;0.2秒)と無印加(2秒)の条件で印加を繰り返した。この印加によって発生した過渡電流(transient current)のピーク電流(peak current)とピーク時間(peak time)を測定した。これらの測定値とM. Imaiらの論文、40頁の計算式(8)とから回転粘度の値を得た。この計算に必要な誘電率異方性の値は、この回転粘度を測定した素子を用い、下に記載した方法で求めた。
測定は、波長589nmの光を用い、接眼鏡に偏光板を取り付けたアッベ屈折計により行なった。主プリズムの表面を一方向にラビングしたあと、試料を主プリズムに滴下した。屈折率(n∥)は偏光の方向がラビングの方向と平行であるときに測定した。屈折率(n⊥)は偏光の方向がラビングの方向と垂直であるときに測定した。光学異方性(Δn)の値は、Δn=n∥-n⊥、の式から計算した。
2枚のガラス基板の間隔(セルギャップ)が9μmであり、そしてツイスト角が80度であるTN素子に試料を入れた。この素子にサイン波(10V、1kHz)を印加し、2秒後に液晶分子の長軸方向における誘電率(ε∥)を測定した。この素子にサイン波(0.5V、1kHz)を印加し、2秒後に液晶分子の短軸方向における誘電率(ε⊥)を測定した。誘電率異方性の値は、Δε=ε∥-ε⊥、の式から計算した。
測定には横河・ヒューレットパッカード株式会社製のHP4284A型LCRメータを用いた。2枚のガラス基板の間隔(セルギャップ)が20μmである水平配向素子に試料を入れた。この素子に0ボルトから20ボルト電荷を印加し、静電容量および印加電圧を測定した。測定した静電容量(C)と印加電圧(V)の値を「液晶デバイスハンドブックク」(日刊工業新聞社)、75頁にある式(2.98)、式(2.101)を用いてフィッティングし、式(2.99)からK11およびK33の値を得た。次に171頁にある式(3.18)に、先ほど求めたK11およびK33の値を用いてK22を算出した。弾性定数Kは、このようにして求めたK11、K22、およびK33の平均値で表した。
測定には大塚電子株式会社製のLCD5100型輝度計を用いた。光源はハロゲンランプであった。2枚のガラス基板の間隔(セルギャップ)が約0.45/Δn(μm)であり、ツイスト角が80度であるノーマリーホワイトモード(normally white mode)のTN素子に試料を入れた。この素子に印加する電圧(32Hz、矩形波)は0Vから10Vまで0.02Vずつ段階的に増加させた。この際に、素子に垂直方向から光を照射し、素子を透過した光量を測定した。この光量が最大になったときが透過率100%であり、この光量が最小であったときが透過率0%である電圧-透過率曲線を作成した。しきい値電圧は透過率が90%になったときの電圧で表した。
測定に用いたTN素子はポリイミド配向膜を有し、そして2枚のガラス基板の間隔(セルギャップ)は5μmであった。この素子は試料を入れたあと紫外線で硬化する接着剤で密閉した。この素子に25℃でパルス電圧(5Vで60マイクロ秒)を印加して充電した。減衰する電圧を高速電圧計で16.7ミリ秒のあいだ測定し、単位周期における電圧曲線と横軸との間の面積Aを求めた。面積Bは減衰しなかったときの面積であった。電圧保持率は面積Bに対する面積Aの百分率で表した。
25℃の代わりに、80℃で測定した以外は、上記の方法で電圧保持率を測定した。得られた結果をVHR-2の記号で示した。
(14)比抵抗(ρ;25℃で測定;Ωcm)
電極を備えた容器に試料1.0mLを注入した。この容器に直流電圧(10V)を印加し、10秒後の直流電流を測定した。比抵抗は次の式から算出した。(比抵抗)={(電圧)×(容器の電気容量)}/{(直流電流)×(真空の誘電率)}。
測定には大塚電子株式会社製のLCD5100型輝度計を用いた。光源はハロゲンランプであった。ローパス・フィルター(Low-pass filter)は5kHzに設定した。2枚のガラス基板の間隔(セルギャップ)が5.0μmであり、ツイスト角が80度であるノーマリーホワイトモード(normally white mode)のTN素子に試料を入れた。この素子に矩形波(60Hz、5V、0.5秒)を印加した。この際に、素子に垂直方向から光を照射し、素子を透過した光量を測定した。この光量が最大になったときが透過率100%であり、この光量が最小であったときが透過率0%であるとみなした。立ち上がり時間(τr:rise time;ミリ秒)は、透過率が90%から10%に変化するのに要した時間であった。立ち下がり時間(τf:fall time;ミリ秒)は透過率10%から90%に変化するのに要した時間であった。応答時間は、このようにして求めた立ち上がり時間と立ち下がり時間との和で表した。
ソルミックス(登録商標)A-11は、エタノール(85.5%)、メタノール(13.4%)とイソプロパノール(1.1%)の混合物であり、日本アルコール販売(株)から入手した。テトラヒドロフランをTHFと略すことがある。テトラブチルアンモニウムブロミドをTBABと略すことがある。N,N-ジメチルホルムアミドをDMFと略すことがある。2-プロパノールをIPAと略すことがある。1,2-ジメトキシエタンをDMEと略すことがある。ヘキサメチルジシラザンカリウムをKHMDSと略すことがある。
窒素雰囲気下、反応器へ化合物(T-1)(3g)とTHF(100ml)とを入れて、0℃に冷却した。そこへ、マグネシウム(0.36g)を添加し、2時間撹拌した。そこへプロパナール(0.98g)を添加し、室温に戻し1時間撹拌した。反応溶液を水に注ぎ、トルエンで抽出した。一緒にした有機層を水、飽和重曹水、および水で洗浄し、無水硫酸マグネシウムで乾燥した。そこにパラトルエンスルホン酸1水和物(1g)を添加し、水を抜きながら1時間還流した。室温に戻し、溶液をシルカゲルカラムクロマトグラフィー(トルエン)により精製し、濃縮し100ml溶液とした。そこにパラジウムカーボン(1g)、ソルミックス(100ml)を加え、水素雰囲気下、一晩撹拌した。反応溶液をろ過し、濃縮することにより化合物(T-2)(2.8g)を得た。
窒素雰囲気下、反応器へ化合物(T-2)(2.8g)とTHF(100ml)とを入れて、-60℃に冷却した。そこへ、リチウムジイソプロピルアミド(1M;n-ヘキサン溶液;19.06ml)を滴下し、さらに2時間攪拌した。続いてホウ酸トリイソブチル(4.18g)のTHF(10ml)溶液を滴下し、室温に戻しつつ2時間攪拌した。反応混合物を塩酸水溶液に注ぎ込み、酢酸エチルで抽出した。一緒にした有機層を水、飽和重曹水、および水で洗浄し、無水硫酸マグネシウムで乾燥した。この溶液を減圧下で濃縮し、化合物(T-3)(3.3g)を得た。
(T-3)(3.3g)と公知の方法で合成した(T-4)(7g)をトルエンに溶解させ、水、エタノール、Pd(PPh3)4(1.7g)、TBAB(0.48g)および炭酸カリウム(6.2g)を加えて6時間加熱還流した。反応終了後トルエンにて抽出し、水にて洗浄した後、無水硫酸マグネシウムで乾燥し、減圧濃縮して淡茶色固体を得た。この固体を溶液にして、シリカゲルカラムクロマトグラフィー(ヘプタン)、および再結晶(エタノール)することにより、(No.43)を無色結晶として(1.6g)得た。
窒素雰囲気下、反応器へ化合物(T-5)(1.5g)とTHF(70ml)とを入れて、-74℃に冷却した。そこへ、リチウムジイソプロピルアミド(1M;n-ヘキサン溶液;9.26ml)を-74℃から-70℃の温度範囲で滴下し、さらに2時間攪拌した。続いてヨウ素(2.56g)のを-75℃から-70℃の温度範囲で添加し、25℃に戻しつつ8時間攪拌した。反応混合物を亜硫酸水素ナトリウム水溶液に注ぎ込み、トルエンで抽出した。一緒にした有機層を水、飽和重曹水、および水で洗浄し、無水硫酸マグネシウムで乾燥した。この溶液を減圧下で濃縮し、化合物(T-6)(2.6g)を得た。
(T-6)(2.6g)、公知の方法で合成した(T-7)(1.6g)、よう化銅(0.16g)、Pd(PPh3)2Cl2(0.6g)及びトリエチルアミン(100ml)を容器に採り、一晩攪拌した。反応混合物を水に注ぎトルエンにて抽出し、水にて洗浄した後、無水硫酸マグネシウムで乾燥し、減圧濃縮して淡茶色固体を得た。この固体を溶液にして、シリカゲルカラムクロマトグラフィー(容量比で、ヘプタン:トルエン=3:2)、および再結晶(エタノール)することにより、(No.9)を無色結晶として(1.4g)得た。
(T-1)(1.5g)と公知の方法で合成した(T-7)(1.5g)をトルエンに溶解させ、水、エタノール、Pd(PPh3)4(0.8g)、TBAB(0.22g)および炭酸カリウム(2.9g)を加えて6時間加熱還流した。反応終了後トルエンにて抽出し、水にて洗浄した後、無水硫酸マグネシウムで乾燥し、減圧濃縮して淡茶色固体を得た。この固体を溶液にして、シリカゲルカラムクロマトグラフィー(ヘプタン)することにより、(T-8)を無色結晶として(1.7g)得た。
窒素雰囲気下、反応器へ化合物(T-8)(1.7g)とTHF(100ml)とを入れて、-74℃に冷却した。そこへ、リチウムジイソプロピルアミド(1M;n-ヘキサン溶液;7.4ml)を-74℃から-70℃の温度範囲で滴下し、さらに2時間攪拌した。続いてヨードプロパン(1.6g)のTHF(10ml)溶液を-75℃から-70℃の温度範囲で滴下し、25℃に戻しつつ8時間攪拌した。反応混合物を水に注ぎ込み、トルエンで抽出し、水にて洗浄した後、無水硫酸マグネシウムで乾燥し、減圧濃縮して淡茶色固体を得た。このものをシリカゲルカラムクロマトグラフィー(容量比で、ヘプタン:トルエン=3:1)、及び再結晶(エタノール)することにより、(No.33)を無色結晶として(0.7g)得た。
化合物(1)と類似の化合物とを物性の観点から比較した。
実施例1において、(T-4)の代わりに以下の(T-7)を用いることで(S-1)を合成した。
実施例2において、(T-4)の代わりに以下の(T-7)を用いることで(S-2)を合成した。
実施例により本発明の組成物を詳細に説明する。本発明は、使用例1の組成物と使用例2の組成物との混合物を含む。本発明は、使用例の組成物の少なくとも2つを混合した混合物をも含む。使用例における化合物は、下記の表1の定義に基づいて記号により表した。表1において、1,4-シクロヘキシレンに関する立体配置はトランスである。使用例において記号の後にあるかっこ内の番号は化合物の番号に対応する。(-)の記号はその他の液晶性化合物を意味する。液晶性化合物の割合(百分率)は、液晶組成物の重量に基づいた重量百分率(重量%)である。最後に、組成物の物性値をまとめた。物性は、先に記載した方法にしたがって測定し、測定値を(外挿することなく)そのまま記載した。
3-btB(2F)B-3 (No.43) 3%
2O-btB(2F)B-3 (No.56) 3%
2-HB-C (8-1) 5%
3-HB-C (8-1) 12%
3-HB-O2 (2-5) 15%
2-BTB-1 (2-10) 4%
3-HHB-F (6-1) 4%
3-HHB-1 (3-1) 5%
3-HHB-O1 (3-1) 5%
3-HHB-3 (3-1) 12%
3-HHEB-F (6-10) 3%
5-HHEB-F (6-10) 3%
2-HHB(F)-F (6-2) 7%
3-HHB(F)-F (6-2) 7%
5-HHB(F)-F (6-2) 7%
3-HHB(F,F)-F (6-3) 5%
NI=99.7℃;η=23.1mPa・s;Δn=0.116;Δε=4.9.
2O-btTB-3 (No.9) 5%
3-HB-CL (5-2) 12%
3-HH-4 (2-1) 12%
3-HB-O2 (2-5) 7%
3-HHB(F,F)-F (6-3) 3%
3-HBB(F,F)-F (6-24) 30%
5-HBB(F,F)-F (6-24) 23%
5-HBB(F)B-2 (4-5) 4%
5-HBB(F)B-3 (4-5) 4%
NI=70.0℃;η=20.2mPa・s;Δn=0.125;Δε=5.5.
3-Bbt-3 (No.33) 5%
7-HB(F,F)-F (5-4) 3%
3-HB-O2 (2-5) 7%
2-HHB(F)-F (6-2) 10%
3-HHB(F)-F (6-2) 10%
5-HHB(F)-F (6-2) 10%
2-HBB(F)-F (6-23) 8%
3-HBB(F)-F (6-23) 6%
5-HBB(F)-F (6-23) 16%
2-HBB-F (6-22) 4%
3-HBB-F (6-22) 4%
5-HBB-F (6-22) 3%
3-HBB(F,F)-F (6-24) 4%
5-HBB(F,F)-F (6-24) 10%
NI=84.0℃;η=25.0mPa・s;Δn=0.118;Δε=5.6.
3-btB(2F)TB-O4 (No.78) 3%
5-HB-CL (5-2) 16%
3-HH-4 (2-1) 12%
3-HH-5 (2-1) 4%
3-HHB-F (6-1) 4%
3-HHB-CL (6-1) 3%
4-HHB-CL (6-1) 4%
3-HHB(F)-F (6-2) 9%
4-HHB(F)-F (6-2) 8%
5-HHB(F)-F (6-2) 9%
7-HHB(F)-F (6-2) 7%
5-HBB(F)-F (6-23) 4%
1O1-HBBH-5 (4-1) 3%
3-HHBB(F,F)-F (7-6) 2%
4-HHBB(F,F)-F (7-6) 3%
5-HHBB(F,F)-F (7-6) 3%
3-HH2BB(F,F)-F (7-15) 3%
4-HH2BB(F,F)-F (7-15) 3%
2O-btB(2F)B-O4 (No.55) 3%
3-HHB(F,F)-F (6-3) 9%
3-H2HB(F,F)-F (6-15) 8%
4-H2HB(F,F)-F (6-15) 8%
5-H2HB(F,F)-F (6-15) 8%
3-HBB(F,F)-F (6-24) 21%
5-HBB(F,F)-F (6-24) 17%
3-H2BB(F,F)-F (6-27) 10%
5-HHBB(F,F)-F (7-6) 3%
5-HHEBB-F (7-17) 2%
3-HH2BB(F,F)-F (7-15) 3%
1O1-HBBH-4 (4-1) 4%
1O1-HBBH-5 (4-1) 4%
4O-BTB(F)bt-3 (No.96) 3%
3-BB(F)bt-3 (No.84) 3%
5-HB-F (5-2) 10%
6-HB-F (5-2) 9%
7-HB-F (5-2) 6%
2-HHB-OCF3 (6-1) 7%
3-HHB-OCF3 (6-1) 5%
4-HHB-OCF3 (6-1) 7%
5-HHB-OCF3 (6-1) 5%
3-HH2B-OCF3 (6-4) 4%
5-HH2B-OCF3 (6-4) 3%
3-HHB(F,F)-OCF2H (6-3) 4%
3-HHB(F,F)-OCF3 (6-3) 5%
3-HH2B(F)-F (6-5) 3%
3-HBB(F)-F (6-23) 10%
5-HBB(F)-F (6-23) 10%
5-HBBH-3 (4-1) 3%
3-HB(F)BH-3 (4-2) 3%
3-Bbt(3F)-O2 (No.38) 5%
2O-btB(2F)B(2F)B-5 (No.156) 1%
5-HB-CL (5-2) 11%
3-HH-4 (2-1) 7%
3-HHB-1 (3-1) 4%
3-HHB(F,F)-F (6-3) 7%
3-HBB(F,F)-F (6-24) 20%
5-HBB(F,F)-F (6-24) 14%
3-HHEB(F,F)-F (6-12) 10%
4-HHEB(F,F)-F (6-12) 3%
5-HHEB(F,F)-F (6-12) 4%
2-HBEB(F,F)-F (6-39) 3%
3-HBEB(F,F)-F (6-39) 4%
5-HBEB(F,F)-F (6-39) 3%
3-HHBB(F,F)-F (7-6) 4%
3-btB(2F)B-3 (No.43) 3%
2O-btTB-3 (No.9) 4%
3-HB-CL (5-2) 5%
5-HB-CL (5-2) 4%
3-HHB-OCF3 (6-1) 4%
3-H2HB-OCF3 (6-13) 5%
5-H4HB-OCF3 (6-19) 15%
V-HHB(F)-F (6-2) 4%
3-HHB(F)-F (6-2) 4%
5-HHB(F)-F (6-2) 4%
3-H4HB(F,F)-CF3 (6-21) 8%
5-H4HB(F,F)-CF3 (6-21) 10%
5-H2HB(F,F)-F (6-15) 5%
5-H4HB(F,F)-F (6-21) 6%
2-H2BB(F)-F (6-26) 5%
3-H2BB(F)-F (6-26) 9%
3-HBEB(F,F)-F (6-39) 5%
NI=76.3℃;η=30.9mPa・s;Δn=0.117;Δε=8.5.
2O-btB(2F)B-3 (No.56) 3%
5-HB-CL (5-2) 17%
7-HB(F,F)-F (5-4) 3%
3-HH-4 (2-1) 10%
3-HH-5 (2-1) 5%
3-HB-O2 (2-5) 15%
3-HHB-1 (3-1) 8%
3-HHB-O1 (3-1) 4%
2-HHB(F)-F (6-2) 7%
3-HHB(F)-F (6-2) 7%
5-HHB(F)-F (6-2) 7%
3-HHB(F,F)-F (6-3) 6%
3-H2HB(F,F)-F (6-15) 4%
4-H2HB(F,F)-F (6-15) 4%
NI=74.0℃;η=16.2mPa・s;Δn=0.083;Δε=2.9.
3-Bbt-3 (No.33) 5%
3-btB(2F)TB-O4 (No.78) 3%
5-HB-CL (5-2) 3%
7-HB(F)-F (5-3) 7%
3-HH-4 (2-1) 9%
3-HH-5 (2-1) 10%
3-HB-O2 (2-5) 13%
3-HHEB-F (6-10) 8%
5-HHEB-F (6-10) 5%
3-HHEB(F,F)-F (6-12) 8%
4-HHEB(F,F)-F (6-12) 3%
3-GHB(F,F)-F (6-109) 4%
4-GHB(F,F)-F (6-109) 6%
5-GHB(F,F)-F (6-109) 7%
2-HHB(F,F)-F (6-3) 4%
3-HHB(F,F)-F (6-3) 5%
2O-btB(2F)B-O4 (No.55) 3%
3-HB-O1 (2-5) 15%
3-HH-4 (2-1) 5%
3-HB(2F,3F)-O2 (9-1) 12%
5-HB(2F,3F)-O2 (9-1) 12%
2-HHB(2F,3F)-1 (10-1) 11%
3-HHB(2F,3F)-1 (10-1) 10%
3-HHB(2F,3F)-O2 (10-1) 13%
5-HHB(2F,3F)-O2 (10-1) 13%
3-HHB-1 (3-1) 6%
3-Bbt(3F)-O2 (No.38) 5%
2-HH-5 (2-1) 3%
3-HH-4 (2-1) 15%
3-HH-5 (2-1) 4%
3-HB-O2 (2-5) 12%
3-H2B(2F,3F)-O2 (9-4) 13%
5-H2B(2F,3F)-O2 (9-4) 13%
3-HHB(2F,3CL)-O2 (10-12) 5%
2-HBB(2F,3F)-O2 (10-7) 3%
3-HBB(2F,3F)-O2 (10-7) 9%
5-HBB(2F,3F)-O2 (10-7) 9%
3-HHB-1 (3-1) 3%
3-HHB-3 (3-1) 3%
3-HHB-O1 (3-1) 3%
3-BB(F)bt-3 (No.84) 3%
2-HH-3 (2-1) 21%
3-HH-4 (2-1) 9%
1-BB-3 (2-8) 9%
3-HB-O2 (2-5) 2%
3-BB(2F,3F)-O2 (9-3) 9%
5-BB(2F,3F)-O2 (9-3) 5%
2-HH1OB(2F,3F)-O2 (10-5) 12%
3-HH1OB(2F,3F)-O2 (10-5) 21%
3-HHB-1 (3-1) 4%
3-HHB-O1 (3-1) 3%
2-BBB(2F)-5 (3-8) 2%
4O-BTB(F)bt-3 (No.96) 3%
2O-btB(2F)B(2F)B-5 (No.156) 1%
2-HH-3 (2-1) 16%
7-HB-1 (2-5) 10%
5-HB-O2 (2-5) 8%
3-HB(2F,3F)-O2 (9-1) 17%
5-HB(2F,3F)-O2 (9-1) 16%
3-HHB(2F,3CL)-O2 (10-12) 3%
4-HHB(2F,3CL)-O2 (10-12) 3%
3-HH1OCro(7F,8F)-5 (13-6) 4%
5-HBB(F)B-2 (4-5) 9%
5-HBB(F)B-3 (4-5) 10%
3-btB(2F)B-3 (No.43) 3%
1-BB-3 (2-8) 10%
3-HH-V (2-1) 29%
3-BB(2F,3F)-O2 (9-3) 13%
2-HH1OB(2F,3F)-O2 (10-5) 20%
3-HH1OB(2F,3F)-O2 (10-5) 14%
3-HHB-1 (3-1) 5%
2-BBB(2F)-5 (3-8) 6%
NI=75.5℃;η=16.0mPa・s;Δn=0.114;Δε=-3.0.
2O-btB(2F)B-3 (No.56) 3%
2-HH-3 (2-1) 6%
3-HH-V1 (2-1) 10%
1V2-HH-1 (2-1) 8%
1V2-HH-3 (2-1) 7%
3-BB(2F,3F)-O2 (9-3) 8%
5-BB(2F,3F)-O2 (9-3) 4%
3-H1OB(2F,3F)-O2 (9-5) 7%
2-HH1OB(2F,3F)-O2 (10-5) 8%
3-HH1OB(2F,3F)-O2 (10-5) 18%
3-HDhB(2F,3F)-O2 (10-3) 5%
3-HHB-1 (3-1) 3%
3-HHB-3 (3-1) 2%
2-BB(2F,3F)B-3 (11-1) 11%
NI=87.9℃;η=21.8mPa・s;Δn=0.118;Δε=-4.2.
2O-btTB-3 (No.9) 5%
1V2-BEB(F,F)-C (8-15) 5%
3-HB-C (8-1) 18%
2-BTB-1 (2-10) 10%
5-HH-VFF (2-1) 30%
3-HHB-1 (3-1) 4%
VFF-HHB-1 (3-1) 8%
VFF2-HHB-1 (3-1) 10%
3-H2BTB-2 (3-17) 4%
3-H2BTB-3 (3-17) 3%
3-H2BTB-4 (3-17) 3%
NI=79.8℃;η=13.0mPa・s;Δn=0.136;Δε=6.0.
3-Bbt-3 (No.33) 5%
5-HB(F)B(F,F)XB(F,F)-F
(7-41) 5%
3-BB(F)B(F,F)XB(F,F)-F
(7-47) 3%
4-BB(F)B(F,F)XB(F,F)-F
(7-47) 7%
5-BB(F)B(F,F)XB(F,F)-F
(7-47) 3%
3-HH-V (2-1) 41%
3-HH-V1 (2-1) 7%
3-HHEH-5 (3-13) 3%
3-HHB-1 (3-1) 3%
V-HHB-1 (3-1) 3%
V2-BB(F)B-1 (3-6) 5%
1V2-BB―F (5-1) 3%
3-BB(F,F)XB(F,F)-F (6-97) 10%
3-HHBB(F,F)-F (7-6) 2%
NI=77.7℃;η=12.2mPa・s;Δn=0.108;Δε=6.1.
3-btB(2F)TB-O4 (No.78) 3%
3-GB(F)B(F,F)XB(F,F)-F
(7-57) 5%
3-BB(F)B(F,F)XB(F,F)-F
(7-47) 3%
4-BB(F)B(F,F)XB(F,F)-F
(7-47) 7%
5-BB(F)B(F,F)XB(F,F)-F
(7-47) 3%
3-HH-V (2-1) 41%
3-HH-V1 (2-1) 6%
3-HHEH-5 (3-13) 3%
3-HHB-1 (3-1) 4%
V-HHB-1 (3-1) 5%
V2-BB(F)B-1 (3-6) 5%
1V2-BB―F (5-1) 3%
3-BB(F,F)XB(F,F)-F (6-97) 5%
3-GB(F,F)XB(F,F)-F (6-113) 4%
3-HHBB(F,F)-F (7-6) 3%
Claims (17)
- 式(1)で表される化合物。
式(1)において、
R1およびR2は独立して、水素または炭素数1から20のアルキルであり、このアルキルにおいて、少なくとも1つの-CH2-は-O-または-S-で置き換えられてもよく、少なくとも1つの-(CH2)2-は-CH=CH-で置き換えられてもよく、これらの基において、少なくとも1つの水素はハロゲンで置き換えられてもよく;
環A1および環A2は独立して、1,4-シクロヘキシレン、1,4-シクロヘキセニレン、1,4-フェニレン、テトラヒドロピラン-2,5-ジイル、1,3-ジオキサン-2,5-ジイル、ピリミジン-2,5-ジイル、2,6,7-トリオキサビシクロ[2.2.2]オクタン-1,4-ジイル、ナフタレン-2,6-ジイル、またはピリジン-2,5-ジイルであり、これらの環上の少なくとも1つの水素はハロゲンで置き換えられてもよく;
aおよびbは独立して、0、1、2、3、または4であり、aおよびbの和は4以下であり、aまたはbが2以上のとき、2つの環A1、2つの環A2、2つのZ1、または2つのZ2は、同一であっても、異なっていてもよく;
Z1およびZ2は独立して、単結合または炭素数1から4のアルキレンであり、このアルキレンにおいて、少なくとも1つの-CH2-は-O-または-COO-で置き換えられてもよく、少なくとも1つの-(CH2)2-は-CH=CH-または-C≡C-で置き換えられてもよく、これらの基において、少なくとも1つの水素はハロゲンで置き換えられてもよく、Z1およびZ2が同時に-CH=CH-または-C≡C-のいずれかであることはなく、aが0でbが1であるとき、Z2は炭素数1から4のアルキレンであり、このアルキレンにおいて、少なくとも1つの-CH2-は-O-または-COO-で置き換えられてもよく、少なくとも1つの-(CH2)2-は-CH=CH-または-C≡C-で置き換えられてもよく、少なくとも1つの水素はハロゲンで置き換えられてもよく;Z3は、-O-または単結合であり;
L1、L2、およびL3は独立して、水素、フッ素、または塩素である。 - 式(1)において、
R1およびR2は独立して、水素、炭素数1から10のアルキル、炭素数1から9のアルコキシ、炭素数2から10のアルケニル、炭素数1から10のフッ素化アルキルであり;
環A1および環A2は独立して、1,4-シクロヘキシレン、1,4-シクロヘキセニレン、少なくとも1つの水素がハロゲンで置き換えられてもよい1,4-フェニレン、またはテトラヒドロピラン-2,5-ジイルであり;
Z1およびZ2は独立して、単結合、-(CH2)2-、-CH=CH-、-CF=CF-、-C≡C-、-COO-、-OCO-、-CF2O-、-OCF2-、-CH2O-、-OCH2-、-(CH2)4-、-(CH2)2CF2O-、-(CH2)2OCF2-、-CF2O(CH2)2-、-OCF2(CH2)2-、-CH=CH-(CH2)2-、または-(CH2)2-CH=CH-であり、aが0でbが1であるとき、Z2は、-(CH2)2-、-CH=CH-、-CF=CF-、-C≡C-、-COO-、-OCO-、-CF2O-、-OCF2-、-CH2O-、-OCH2-、-(CH2)4-、-(CH2)2CF2O-、-(CH2)2OCF2-、-CF2O(CH2)2-、-OCF2(CH2)2-、-CH=CH-(CH2)2-、または-(CH2)2-CH=CH-であり;
aおよびbは独立して、0、1、2、3、または4であり、aおよびbの和は4以下であり;
L1、L2、およびL3は独立して、水素、フッ素、または塩素である、請求項1に記載の化合物。 - 式(1)において、
aおよびbの和が、0、1、2、または3であり;
R1およびR2は独立して、水素、炭素数1から10のアルキル、炭素数1から9のアルコキシ、炭素数2から10のアルケニル、または少なくとも1つの水素がフッ素で置き換えられた炭素数1から10のアルキルであり;
環A1および環A2は独立して、1,4-シクロヘキシレン、1,4-シクロヘキセニレン、少なくとも1つの水素がハロゲンで置き換えられていてもよい1,4-フェニレン、またはテトラヒドロピラン-2,5-ジイルあり;
Z1およびZ2は独立して、単結合、-(CH2)2-、-CH=CH-、-CF=CF-、-C≡C-、-COO-、-OCO-、-CF2O-、-OCF2-、-CH2O-、-OCH2-、-(CH2)4-、-(CH2)2CF2O-、-(CH2)2OCF2-、-CF2O(CH2)2-、-OCF2(CH2)2-、-CH=CH-(CH2)2-、または-(CH2)2-CH=CH-であり、aが0でbが1であるとき、Z2は、-(CH2)2-、-CH=CH-、-CF=CF-、-C≡C-、-COO-、-OCO-、-CF2O-、-OCF2-、-CH2O-、-OCH2-、-(CH2)4-、-(CH2)2CF2O-、-(CH2)2OCF2-、-CF2O(CH2)2-、-OCF2(CH2)2-、-CH=CH-(CH2)2-、または-(CH2)2-CH=CH-であり;
L1、L2、およびL3は独立して、水素、フッ素、または塩素である、請求項1に記載の化合物。 - 式(1-1)から(1-10)のいずれか一つで表される請求項1から3のいずれか1項に記載の化合物。
式(1-1)から(1-7)、および(1-9)から(1-10)において、
R1およびR2は独立して、水素、炭素数1から10のアルキル、炭素数1から9のアルコキシ、炭素数2から10のアルケニル、または炭素数1から10のフッ素化アルキルであり;
環A11、環A12、環A13、環A21、環A22、および環A23は独立して、1,4-シクロヘキシレン、1,4-シクロヘキセニレン、1,4-フェニレン、少なくとも1つの水素がハロゲンで置き換えられた1,4-フェニレン、またはテトラヒドロピラン-2,5-ジイルであり;
Z11、Z12、Z13、Z21、Z22、およびZ23は独立して、単結合、-(CH2)2-、-CH=CH-、-CF=CF-、-C≡C-、-COO-、-OCO-、-CF2O-、-OCF2-、-CH2O-、-OCH2-、-(CH2)4-、-(CH2)2CF2O-、-(CH2)2OCF2-、-CF2O(CH2)2-、-OCF2(CH2)2-、-CH=CH-(CH2)2-、または-(CH2)2-CH=CH-であり;
L1、L2およびL3は独立して、水素、フッ素、または塩素であり;
式(1-8)において、
R1およびR2は独立して、水素、炭素数1から10のアルキル、炭素数1から9のアルコキシ、炭素数2から10のアルケニル、または少なくとも1つの水素がフッ素で置き換えられた炭素数1から10のアルキルであり;
環A21は、1,4-シクロヘキシレン、1,4-シクロヘキセニレン、1,4-フェニレン、少なくとも1つの水素がハロゲンで置き換えられた1,4-フェニレン、またはテトラヒドロピラン-2,5-ジイルあり;
Z21が独立して、-(CH2)2-、-CH=CH-、-CF=CF-、-C≡C-、-COO-、-OCO-、-CF2O-、-OCF2-、-CH2O-、-OCH2-、-(CH2)4-、-(CH2)2CF2O-、-(CH2)2OCF2-、-CF2O(CH2)2-、-OCF2(CH2)2-、-CH=CH-(CH2)2-、または-(CH2)2-CH=CH-であり;
L1、L2、およびL3は独立して、水素、フッ素、または塩素である。 - 式(1-1)から(1-7)、および(1-9)から(1-10)において、
R1およびR2は独立して、水素、フッ素、炭素数1から10のアルキル、炭素数1から9のアルコキシ、炭素数2から10のアルケニル、または少なくとも1つの水素がフッ素で置き換えられた炭素数1から10のアルキルであり;
環A11、環A12、環A13、環A21、環A22、および環A23は独立して、1,4-シクロヘキシレン、1,4-シクロヘキセニレン、少なくとも1つの水素がハロゲンで置き換えられてもよい1,4-フェニレン、テトラヒドロピラン-2,5-ジイルであり;
Z11、Z12、Z13、Z21、Z22、およびZ23は独立して、単結合、-(CH2)2-、-CH=CH-、-C≡C-、-CF2O-、-OCF2-、-CH2O-、または-OCH2-であり;
L1、L2、およびL3は独立して、水素、フッ素、または塩素であり;
式(1-8)において、
R1およびR2は独立して、水素、フッ素、炭素数1から10のアルキル、炭素数1から9のアルコキシ、炭素数2から10のアルケニル、または炭素数1から10のフッ素化アルキルであり;
環A11、環A12、環A13、環A21、環A22、および環A23は独立して、1,4-シクロヘキシレン、1,4-シクロヘキセニレン、または少なくとも1つの水素がハロゲンで置き換えられてもよい1,4-フェニレン、テトラヒドロピラン-2,5-ジイルであり;
Z11、Z12、Z13、Z21、Z22、およびZ23は独立して、-(CH2)2-、-CH=CH-、-C≡C-、-CF2O-、-OCF2-、-CH2O-、または-OCH2-であり;
L1、L2、およびL3は独立して、水素、フッ素、または塩素であるり、
式(1-1)から(1-10)のいずれか1つで表される請求項4に記載の化合物。 - 式(1-1)、(1-5)、および(1-10)のいずれか一つで表される請求項5に記載の化合物。
式(1-1)、(1-5)、および(1-10)において、
R1およびR2は独立して、水素、フッ素、炭素数1から10のアルキル、炭素数1から9のアルコキシ、炭素数2から10のアルケニル、または少なくとも1つの水素がフッ素に炭素数1から10のフッ素化アルキルであり;
環A21、環A22、および環A23は独立して、1,4-シクロヘキシレン、または少なくとも1つの水素がハロゲンで置き換えられてもよい1,4-フェニレンであり;
Z21、Z22、およびZ23は独立して、単結合、-(CH2)2-、-CH=CH-、-C≡C-、-CH2O-、または-OCH2-であり;
L1、L2、およびL3は独立して、水素またはフッ素である。 - 式(1-4)、(1-7)、および(1-9)のいずれか一つで表せられる請求項5に記載の化合物。
式(1-4)、(1-7)、および(1-9)において、
R1およびR2は独立して、水素、フッ素、炭素数1から10のアルキル、炭素数1から9のアルコキシ、炭素数2から10のアルケニル、または炭素数1から10のフッ素化アルキルでありであり;
環A11、環A12、および環A13は独立して、1,4-シクロヘキシレン、または少なくとも1つの水素がハロゲンで置き換えられてもよい1,4-フェニレンであり;
Z11、Z12、およびZ13は独立して、単結合、-(CH2)2-、-CH=CH-、-C≡C-、-CH2O-、または-OCH2-であり;
L1、L2、およびL3は独立して、水素またはフッ素である。 - 請求項1から8のいずれか1項に記載の化合物を少なくとも1つ含有する液晶組成物。
- 式(2)から(4)で表される化合物の群から選択される少なくとも1つの化合物をさらに含有する、請求項9に記載の液晶組成物。
式(2)から(4)において、
R11およびR12は独立して、炭素数1から10のアルキルまたは炭素数2から10のアルケニルであり、このアルキルまたはアルケニルにおいて、少なくとも1つの-CH2-は-O-で置き換えられてもよく、少なくとも1つの水素はフッ素で置き換えられてもよく;
環B1、環B2、環B3、および環B4は独立して、1,4-シクロヘキシレン、1,4-フェニレン、2-フルオロ-1,4-フェニレン、2,5-ジフルオロ-1,4-フェニレン、またはピリミジン-2,5-ジイルであり;
Z11、Z12、およびZ13は独立して、単結合、-CH2CH2-、-CH=CH-、-C≡C-、または-COO-である。 - 式(5)から(7)で表される化合物の群から選択される少なくとも1つの化合物をさらに含有する、請求項9または10に記載の液晶組成物。
式(5)から(7)において、
R13は炭素数1から10のアルキルまたは炭素数2から10のアルケニルであり、このアルキルおよびアルケニルにおいて、少なくとも1つの-CH2-は-O-で置き換えられてもよく、少なくとも1つの水素はフッ素で置き換えられてもよく;
X11は、フッ素、塩素、-OCF3、-OCHF2、-CF3、-CHF2、-CH2F、-OCF2CHF2、または-OCF2CHFCF3であり;
環C1、環C2、および環C3は独立して、1,4-シクロヘキシレン、少なくとも1つの水素がフッ素で置き換えられてもよい1,4-フェニレン、テトラヒドロピラン-2,5-ジイル、1,3-ジオキサン-2,5-ジイル、またはピリミジン-2,5-ジイルであり;
Z14、Z15、およびZ16は独立して、単結合、-CH2CH2-、-CH=CH-、-C≡C-、-COO-、-CF2O-、-OCF2-、-CH2O-、または-(CH2)4-であり;
L11およびL12は独立して、水素またはフッ素である。 - 式(8)で表される化合物の群から選択される少なくとも1つの化合物をさらに含有する、請求項9から11のいずれか1項に記載の液晶組成物。
式(8)において、
R14は炭素数1から10のアルキルまたは炭素数2から10のアルケニルであり、このアルキルおよびアルケニルにおいて、少なくとも1つの-CH2-は-O-で置き換えられてもよく、少なくとも1つの水素はフッ素で置き換えられてもよく;
X12は、-C≡Nまたは-C≡C-C≡Nであり;
環D1は、1,4-シクロヘキシレン、少なくとも1つの水素がフッ素で置き換えられてもよい1,4-フェニレン、テトラヒドロピラン-2,5-ジイル、1,3-ジオキサン-2,5-ジイル、またはピリミジン-2,5-ジイルであり;
Z17は、単結合、-CH2CH2-、-C≡C-、-COO-、-CF2O-、-OCF2-、または-CH2O-であり;
L13およびL14は独立して、水素またはフッ素であり;
iは、1、2、3、または4である。 - 式(9)から(15)で表される化合物の群から選択される少なくとも1つの化合物をさらに含有する、請求項9から12のいずれか1項に記載の液晶組成物。
式(9)から(15)において、
R15およびR16は独立して、炭素数1から10のアルキルまたは炭素数2から10のアルケニルであり、このアルキルおよびアルケニルにおいて、少なくとも1つの-CH2-は-O-で置き換えられてもよく、少なくとも1つの水素はフッ素で置き換えられてもよく;
R17は、水素、フッ素、炭素数1から10のアルキル、または炭素数2から10のアルケニルであり、このアルキルおよびアルケニルにおいて、少なくとも1つの-CH2-は-O-で置き換えられてもよく、少なくとも1つの水素はフッ素で置き換えられてもよく;
環E1、環E2、環E3、および環E4は独立して、1,4-シクロヘキシレン、1,4-シクロヘキセニレン、少なくとも1つの水素がフッ素で置き換えられてもよい1,4-フェニレン,テトラヒドロピラン-2,5-ジイル、またはデカヒドロナフタレン-2,6-ジイルであり、環E5および環E6は独立して、1,4-シクロヘキシレン、1,4-シクロヘキセニレン、1,4-フェニレン,テトラヒドロピラン-2,5-ジイル、またはデカヒドロナフタレン-2,6-ジイルであり;
Z18、Z19、Z20、およびZ21は独立して、単結合、-CH2CH2-、-COO-、-CH2O-、-OCF2-、または-OCF2CH2CH2-であり;
L15およびL16は独立して、フッ素または塩素であり;
S11は、水素またはメチルであり;
Xは、-CHF-または-CF2-であり;
j、k、m、n、p、q、r、およびsは独立して、0または1であり、k、m、n、およびpの和は、1または2であり、q、r、およびsの和は、0、1、2、または3であり、tは、1、2、または3である。 - 重合性化合物、重合開始剤、重合禁止剤、光学活性化合物、酸化防止剤、紫外線吸収剤、光安定剤、熱安定剤、色素、および消泡剤の少なくとも1つをさらに含有する、請求項9から13のいずれか1項に記載の液晶組成物。
- 請求項9から14のいずれか1項に記載の液晶組成物を含有する液晶表示素子。
- 請求項9から14のいずれか1項に記載の液晶組成物をカプセルに内包させることを特徴とする請求項15に記載の液晶表示素子。
- 請求項9から14のいずれか1項に記載の液晶組成物を2D-3D間スイッチングに使用することを特徴とする請求項15に記載の液晶表示素子。
Priority Applications (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US15/766,298 US20180290997A1 (en) | 2015-10-13 | 2016-07-11 | Liquid crystal compound having benzothiophene, liquid crystal composition and liquid crystal display device |
| EP16855146.3A EP3363795A4 (en) | 2015-10-13 | 2016-07-11 | LIQUID CRYSTAL COMPOUND HAVING BENZOTHIOPHENE, LIQUID CRYSTAL COMPOSITION, AND LIQUID CRYSTAL DISPLAY ELEMENT |
| JP2017545103A JP6850410B2 (ja) | 2015-10-13 | 2016-07-11 | ベンゾチオフェンを有する液晶性化合物、液晶組成物および液晶表示素子 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2015201951 | 2015-10-13 | ||
| JP2015-201951 | 2015-10-13 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2017064892A1 true WO2017064892A1 (ja) | 2017-04-20 |
Family
ID=58517498
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2016/070418 WO2017064892A1 (ja) | 2015-10-13 | 2016-07-11 | ベンゾチオフェンを有する液晶性化合物、液晶組成物および液晶表示素子 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20180290997A1 (ja) |
| EP (1) | EP3363795A4 (ja) |
| JP (1) | JP6850410B2 (ja) |
| TW (1) | TWI694068B (ja) |
| WO (1) | WO2017064892A1 (ja) |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20170233655A1 (en) * | 2016-02-17 | 2017-08-17 | Jnc Corporation | Liquid crystal composition and liquid crystal display device |
| JP2017222778A (ja) * | 2016-06-15 | 2017-12-21 | Jnc株式会社 | 液晶組成物および液晶表示素子 |
| CN112851562A (zh) * | 2021-01-22 | 2021-05-28 | 烟台显华化工科技有限公司 | 一种芳香环液晶化合物及其液晶组合物和应用 |
| CN113717195A (zh) * | 2021-10-18 | 2021-11-30 | 苏州汉朗光电有限公司 | 3,4-二氟-二噻吩并[2,3-b;3`,2`-d]噻吩衍生物及其应用 |
| CN117466849A (zh) * | 2023-12-27 | 2024-01-30 | 中节能万润股份有限公司 | 一种含异硫氰基的液晶单体化合物及其制备方法 |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN111253366B (zh) * | 2018-11-30 | 2022-06-17 | 四川师范大学 | 苯基苯并噻吩类棒状液晶化合物及其制备方法 |
| CN112266794B (zh) * | 2020-09-30 | 2022-09-09 | 北京八亿时空液晶科技股份有限公司 | 一种含噻吩的液晶化合物及其制备方法和应用 |
| CN116970405B (zh) * | 2023-06-28 | 2024-09-10 | 北京燕化集联光电技术有限公司 | 一种液晶化合物、组合物及其应用 |
| CN116987509B (zh) * | 2023-06-30 | 2024-09-10 | 北京燕化集联光电技术有限公司 | 液晶化合物、组合物及其应用 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2000328062A (ja) * | 1999-03-24 | 2000-11-28 | Clariant Internatl Ltd | ベンゾチオフェン化合物およびそれらの液晶混合物における使用 |
| CN1370533A (zh) * | 2001-02-27 | 2002-09-25 | 中国人民解放军军事医学科学院放射医学研究所 | 一类新的苯并噻吩类化合物在防治妇女绝经后综合症和其它与雌激素相关疾病中的用途 |
| WO2014075382A1 (zh) * | 2012-09-29 | 2014-05-22 | 昆山维信诺显示技术有限公司 | 苯并噻吩类衍生物及其在有机电致发光领域中的应用 |
Family Cites Families (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CH559758A5 (en) * | 1968-03-20 | 1975-03-14 | Ciba Geigy Ag | Heterocyclic, ethylenic double bond-contg. optical brighteners - e.g. stilbenyl-benzothiophene and benzofuran derivs, for use outside textile industry |
| CH540247A (de) * | 1967-04-21 | 1973-09-28 | Ciba Geigy Ag | Verfahren zur Herstellung von heterocyclischen, Asthylendoppelbindungen enthaltenden Verbindungen |
| US4358593A (en) * | 1981-04-03 | 1982-11-09 | Eli Lilly And Company | Process for preparing 3-(4-aminoethoxybenzoyl)benzo[b]thiophenes |
| US5073564A (en) * | 1990-07-06 | 1991-12-17 | Fmc Corporation | Ethynylbenzothiophene pesticides |
| JPH07179856A (ja) * | 1993-12-21 | 1995-07-18 | Canon Inc | 液晶性化合物、これを含有する液晶組成物、該液晶組成物を用いた液晶素子並びにこれらを用いた表示方法、表示装置 |
| US6168728B1 (en) * | 1997-03-13 | 2001-01-02 | Chisso Corporation | Acetylene derivatives, and liquid crystal composition and liquid crystal display device each comprising the same |
| JP2003509507A (ja) | 1999-09-21 | 2003-03-11 | キネティック リミテッド | 液晶化合物 |
| JP2009203203A (ja) * | 2008-02-29 | 2009-09-10 | Toyo Ink Mfg Co Ltd | アントラセン誘導体及びその用途 |
| KR101310377B1 (ko) * | 2008-10-17 | 2013-09-23 | 엘지디스플레이 주식회사 | 영상표시장치 |
| CN102712558B (zh) * | 2009-11-05 | 2014-11-19 | 出光兴产株式会社 | 含杂环的非对称性芳香族化合物、有机薄膜晶体管用化合物、以及使用它的有机薄膜晶体管 |
| DE102012004393A1 (de) * | 2011-03-22 | 2012-09-27 | Merck Patent Gmbh | Verbindungen für ein flüssigkristallines Medium und deren Verwendung für Hochfrequenzbauteile |
| KR101808530B1 (ko) * | 2011-05-25 | 2017-12-14 | 엘지디스플레이 주식회사 | 영상 표시 장치 |
| CN103184053B (zh) * | 2011-12-29 | 2015-03-11 | 苏州汉朗光电有限公司 | 高散射态近晶相液晶材料及其显示器件 |
| KR20140081735A (ko) * | 2012-12-21 | 2014-07-01 | 주식회사 동진쎄미켐 | 중수소로 치환된 신규한 유기발광 화합물 및 이를 포함하는 유기발광소자 |
| EP2918658B1 (de) * | 2014-03-10 | 2020-05-13 | Merck Patent GmbH | Flüssigkristalline Medien mit homöotroper Ausrichtung |
| TWI708770B (zh) * | 2015-06-08 | 2020-11-01 | 日商捷恩智股份有限公司 | 具有苯并噻吩的液晶性化合物、液晶組成物及液晶顯示元件 |
| JP6696312B2 (ja) * | 2016-06-15 | 2020-05-20 | Jnc株式会社 | 液晶組成物および液晶表示素子 |
-
2016
- 2016-06-23 TW TW105119657A patent/TWI694068B/zh active
- 2016-07-11 US US15/766,298 patent/US20180290997A1/en not_active Abandoned
- 2016-07-11 EP EP16855146.3A patent/EP3363795A4/en not_active Withdrawn
- 2016-07-11 JP JP2017545103A patent/JP6850410B2/ja active Active
- 2016-07-11 WO PCT/JP2016/070418 patent/WO2017064892A1/ja active Application Filing
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2000328062A (ja) * | 1999-03-24 | 2000-11-28 | Clariant Internatl Ltd | ベンゾチオフェン化合物およびそれらの液晶混合物における使用 |
| CN1370533A (zh) * | 2001-02-27 | 2002-09-25 | 中国人民解放军军事医学科学院放射医学研究所 | 一类新的苯并噻吩类化合物在防治妇女绝经后综合症和其它与雌激素相关疾病中的用途 |
| WO2014075382A1 (zh) * | 2012-09-29 | 2014-05-22 | 昆山维信诺显示技术有限公司 | 苯并噻吩类衍生物及其在有机电致发光领域中的应用 |
Non-Patent Citations (2)
| Title |
|---|
| "Thionaphthene", IWANAMI RIKAGAKU JITEN 5TH EDITION, 24 April 1998 (1998-04-24), pages 830, XP009510555 * |
| See also references of EP3363795A4 * |
Cited By (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20170233655A1 (en) * | 2016-02-17 | 2017-08-17 | Jnc Corporation | Liquid crystal composition and liquid crystal display device |
| US10059878B2 (en) * | 2016-02-17 | 2018-08-28 | Jnc Corporation | Liquid crystal composition and liquid crystal display device |
| JP2017222778A (ja) * | 2016-06-15 | 2017-12-21 | Jnc株式会社 | 液晶組成物および液晶表示素子 |
| CN112851562A (zh) * | 2021-01-22 | 2021-05-28 | 烟台显华化工科技有限公司 | 一种芳香环液晶化合物及其液晶组合物和应用 |
| CN113717195A (zh) * | 2021-10-18 | 2021-11-30 | 苏州汉朗光电有限公司 | 3,4-二氟-二噻吩并[2,3-b;3`,2`-d]噻吩衍生物及其应用 |
| CN117466849A (zh) * | 2023-12-27 | 2024-01-30 | 中节能万润股份有限公司 | 一种含异硫氰基的液晶单体化合物及其制备方法 |
| CN117466849B (zh) * | 2023-12-27 | 2024-04-02 | 中节能万润股份有限公司 | 一种含异硫氰基的液晶单体化合物及其制备方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| TW201713637A (zh) | 2017-04-16 |
| JPWO2017064892A1 (ja) | 2018-09-13 |
| JP6850410B2 (ja) | 2021-03-31 |
| TWI694068B (zh) | 2020-05-21 |
| EP3363795A4 (en) | 2019-10-09 |
| US20180290997A1 (en) | 2018-10-11 |
| EP3363795A1 (en) | 2018-08-22 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6566031B2 (ja) | ベンゾチオフェンを有する液晶性化合物、液晶組成物および液晶表示素子 | |
| JP6850410B2 (ja) | ベンゾチオフェンを有する液晶性化合物、液晶組成物および液晶表示素子 | |
| JP7160050B2 (ja) | メトキシメチルアクリル基を有する重合性化合物、液晶組成物、および液晶表示素子 | |
| JP2016185913A (ja) | アルケニルジオキサン化合物、液晶組成物および液晶表示素子 | |
| JP6524699B2 (ja) | ビニレン基を有する液晶性化合物、液晶組成物および液晶表示素子 | |
| JP6578690B2 (ja) | ハロゲン化されたアルキルを有する液晶化合物、液晶組成物および液晶表示素子 | |
| JP6493677B2 (ja) | 極性化合物、液晶組成物および液晶表示素子 | |
| JP2016014014A (ja) | ジヒドロピラン化合物、液晶組成物および液晶表示素子 | |
| JP2017165710A (ja) | ターシクロヘキシルを有する液晶性化合物、液晶組成物および液晶表示素子 | |
| JP6511975B2 (ja) | ジヒドロピラン化合物を含有する液晶組成物および液晶表示素子 | |
| JP6435923B2 (ja) | ジヒドロピラン化合物、液晶組成物および液晶表示素子 | |
| JP6617596B2 (ja) | シクロヘキセン環を有する液晶性化合物、液晶組成物および液晶表示素子 | |
| JP6555144B2 (ja) | 液晶性化合物、液晶組成物および液晶表示素子 | |
| JP6402919B2 (ja) | ペルフルオロアルキル末端基とcf2o結合基とを有する化合物、液晶組成物および液晶表示素子 | |
| JP6638814B2 (ja) | 重合性極性化合物、液晶組成物および液晶表示素子 | |
| JP6708042B2 (ja) | ジフルオロメチレンオキシ基を有する液晶性化合物、液晶組成物および液晶表示素子 | |
| WO2020080120A1 (ja) | 化合物、液晶組成物、および液晶表示素子 | |
| JP6919394B2 (ja) | フルオレンとcf2oを有する液晶性化合物、液晶組成物及び液晶表示素子 | |
| JP6766556B2 (ja) | 液晶性化合物、液晶組成物および液晶表示素子 | |
| TWI787521B (zh) | O鍵結基的液晶性化合物、液晶組成物和液晶顯示元件 | |
| JP6863406B2 (ja) | ハロゲン化されたアルキルを有する液晶化合物、液晶組成物および液晶表示素子 | |
| JP6642260B2 (ja) | 四環を有する液晶性化合物、液晶組成物および液晶表示素子 | |
| JP2017007986A (ja) | アントラセン骨格を有する化合物、液晶組成物および液晶表示素子 | |
| JP2017007987A (ja) | ジヒドロアントラセン骨格を有する化合物、液晶組成物および液晶表示素子 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 16855146 Country of ref document: EP Kind code of ref document: A1 |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 15766298 Country of ref document: US |
|
| ENP | Entry into the national phase |
Ref document number: 2017545103 Country of ref document: JP Kind code of ref document: A |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2016855146 Country of ref document: EP |