WO2015170733A1 - 血管内治療補助具 - Google Patents
血管内治療補助具 Download PDFInfo
- Publication number
- WO2015170733A1 WO2015170733A1 PCT/JP2015/063266 JP2015063266W WO2015170733A1 WO 2015170733 A1 WO2015170733 A1 WO 2015170733A1 JP 2015063266 W JP2015063266 W JP 2015063266W WO 2015170733 A1 WO2015170733 A1 WO 2015170733A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- filter
- ring
- endovascular treatment
- treatment aid
- end side
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2/00—Filters implantable into blood vessels; Prostheses, i.e. artificial substitutes or replacements for parts of the body; Appliances for connecting them with the body; Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
- A61F2/01—Filters implantable into blood vessels
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2/00—Filters implantable into blood vessels; Prostheses, i.e. artificial substitutes or replacements for parts of the body; Appliances for connecting them with the body; Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
- A61F2/01—Filters implantable into blood vessels
- A61F2/013—Distal protection devices, i.e. devices placed distally in combination with another endovascular procedure, e.g. angioplasty or stenting
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B17/00—Surgical instruments, devices or methods, e.g. tourniquets
- A61B17/22—Implements for squeezing-off ulcers or the like on the inside of inner organs of the body; Implements for scraping-out cavities of body organs, e.g. bones; Calculus removers; Calculus smashing apparatus; Apparatus for removing obstructions in blood vessels, not otherwise provided for
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2/00—Filters implantable into blood vessels; Prostheses, i.e. artificial substitutes or replacements for parts of the body; Appliances for connecting them with the body; Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
- A61F2/01—Filters implantable into blood vessels
- A61F2/011—Instruments for their placement or removal
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2/00—Filters implantable into blood vessels; Prostheses, i.e. artificial substitutes or replacements for parts of the body; Appliances for connecting them with the body; Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
- A61F2/01—Filters implantable into blood vessels
- A61F2002/016—Filters implantable into blood vessels made from wire-like elements
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2230/00—Geometry of prostheses classified in groups A61F2/00 - A61F2/26 or A61F2/82 or A61F9/00 or A61F11/00 or subgroups thereof
- A61F2230/0063—Three-dimensional shapes
- A61F2230/0067—Three-dimensional shapes conical
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2250/00—Special features of prostheses classified in groups A61F2/00 - A61F2/26 or A61F2/82 or A61F9/00 or A61F11/00 or subgroups thereof
- A61F2250/0058—Additional features; Implant or prostheses properties not otherwise provided for
- A61F2250/0096—Markers and sensors for detecting a position or changes of a position of an implant, e.g. RF sensors, ultrasound markers
- A61F2250/0098—Markers and sensors for detecting a position or changes of a position of an implant, e.g. RF sensors, ultrasound markers radio-opaque, e.g. radio-opaque markers
Definitions
- the present invention belongs to the medical device field, and particularly relates to an endovascular treatment aid for supplementing free thrombus or the like when a transcutaneous treatment is performed on a blood vessel.
- Balloon angioplasty is a treatment that maintains a blood vessel lumen and maintains blood flow by expanding an inflatable balloon at the distal end of a balloon catheter at a blockage or stenosis site in the blood vessel.
- Balloon angioplasty is a treatment that maintains a blood vessel lumen and maintains blood flow by expanding an inflatable balloon at the distal end of a balloon catheter at a blockage or stenosis site in the blood vessel.
- Balloon angioplasty is a treatment that maintains a blood vessel lumen and maintains blood flow by expanding an inflatable balloon at the distal end of a balloon catheter at a blockage or stenosis site in the blood vessel.
- thrombus, plaque, etc. that have accumulated on the blood vessel wall, and then these substances are carried over the bloodstream, causing the peripheral thin blood vessels There is a risk of causing an infarction.
- stent placement is performed by introducing a stent in the form of a substantially cylindrical tube or mesh sleeve made of a material such as nitinol or a cobalt alloy, permanently or temporarily into a stenosis site in a blood vessel, thereby vascular lumen. It is a treatment to ensure and maintain blood flow.
- a stent is placed in a blood vessel, as with balloon angioplasty, thrombus and plaque accumulated on the blood vessel wall are unintentionally released, which may cause infarction. .
- a device to be used in combination with a therapeutic device such as a balloon catheter or a stent
- a therapeutic device such as a balloon catheter or a stent
- it is disposed percutaneously on the peripheral side of the lesion to be placed in the blood vessel, and the blood vessel Endovascular treatment aids have been developed to capture thrombus, plaque, etc. released from the wall.
- a device having a structure in which a shaft having an outer diameter that can pass through a guide wire lumen of a treatment device such as a balloon catheter and a filter fixed to the tip thereof has been reported.
- the filter has a plurality of apertures in a mesh or sheet membrane made of a polymer material, and has a shape in which the distal side, that is, the distal end side of the blood vessel is closed, and the central side, that is, the proximal end side of the blood vessel is opened.
- the endovascular treatment aid When such an endovascular treatment aid is used, the endovascular treatment aid is housed in a delivery sheath with the filter closed, and delivered to an appropriate location on the peripheral side of the lesion. After delivery, the delivery sheath is pulled out of the body, the filter is released, and the opening of the filter self-expands to adhere to the blood vessel wall. When the endovascular treatment aid is collected, the collection sheath is delivered along the endovascular treatment aid, and a filter containing a thrombus, plaque or the like is housed in the collection sheath and removed from the body.
- a ring-shaped member made of superelastic metal is used at the opening of the filter as an endovascular treatment aid that can improve the adhesion to the blood vessel wall and reduce leakage of thrombus, plaque, etc.
- an intravascular treatment assisting tool that folds the filter into a bag shape by deforming the superelastic metal when the support member supporting the filter is focused and the opening of the filter is closed (Patent Document 2). ).
- a radiopaque material can be used on the ring-shaped filter opening to facilitate observation of whether the filter is securely attached to the vessel wall during surgery or whether the filter opening is securely closed during recovery.
- An endovascular treatment aid that enables observation under radiation has been reported by arranging a coil (Patent Document 3).
- JP 2008-35923 A Japanese Patent No. 4073869 Japanese Patent No. 4680201 WO2003 / 084437 WO2008 / 005898 Publication WO2013 / 059069
- the superelastic characteristic metal used for the ring-shaped filter opening is lacking in radiopacity, so that observation by radiation transmission used during normal surgery is not possible. It may not be possible to know whether the filter is securely attached to the blood vessel wall or whether the filter opening is reliably closed at the time of recovery.
- Patent Documents 4 to 6 it is described that an antithrombotic compound is imparted to an endovascular treatment aid, but there is no description about the optimal type and combination of antithrombotic compounds.
- endovascular treatment that can confirm that the endovascular treatment aid is firmly attached to the blood vessel and solve the two points of preventing leakage of substances such as captured thrombus and plaque at a time.
- No assistive device has been known so far.
- an object of the present invention is to provide an endovascular treatment aid that can confirm that the endovascular treatment aid is in close contact with the blood vessel and that prevents leakage of substances such as captured plaque. .
- a flexible shaft The shaft is fixed to the shaft so as to be a closed end portion at the distal end side in the longitudinal direction and to be an opening portion at the proximal end side in the longitudinal direction, and a ring having an elastic restoring force is fixed to the opening portion,
- a filter that can be opened and closed like an umbrella, with the ring as the bottom when open, From a linear member that is fixed to each other so as to connect the ring and a part of the shaft, and that allows the filter to be closed by a tension generated by applying an external force to the base end side in the longitudinal direction.
- a supporting member With The ring is wound with a coil formed of a radiopaque material, When the filter is closed, the ring is alternately formed with a plurality of peaks facing the distal end side in the longitudinal direction and a plurality of valleys facing the proximal end side in the longitudinal direction, and the peaks and the valleys
- the coil has a shape close to each other, and the coil includes a position fixed by a support member on the ring, and is arranged on the ring so as not to include the position of the peak of the mountain and the peak of the valley. Endovascular treatment aids.
- a cationic polymer containing at least one compound selected from the group consisting of alkyleneimine, vinylamine, allylamine, lysine, protamine and diallyldimethylammonium chloride as a constituent monomer is covalently bonded to the above-mentioned filter, and anticoagulant
- the surface amount of the anionic sulfur compound having anticoagulant activity due to antifactor Xa activity in the filter after being immersed in physiological saline at 37 ° C. for 30 minutes is 30 mIU / cm 2 or more, (1)
- the thickness of the antithrombotic compound layer formed from the cationic polymer and the anionic sulfur compound having anticoagulant activity on the surface of the filter is 1 to 600 nm.
- the present invention by identifying the position of the coil formed of the radiopaque material wound on the ring, it is possible to confirm that the endovascular treatment aid is firmly attached to the blood vessel, and It is possible to provide an endovascular treatment aid that prevents leakage of substances such as trapped plaque.
- the endovascular treatment assisting device of the present invention is provided on the shaft so as to be a flexible shaft and a closed end portion at a distal end side in the longitudinal direction of the shaft and an opening portion at a proximal end side in the longitudinal direction.
- a ring that is fixed and has an elastic restoring force is fixed to the opening, and when open, has a conical shape with the ring as a bottom surface, a filter that can be opened and closed like an umbrella, and a part of the ring and the shaft
- a support member made of a linear member that allows the filter to be closed by a tension generated by applying an external force to the base end side in the longitudinal direction.
- the ring is wound with a coil made of a radiopaque material, and when the filter is closed, the ring is a plurality of rings facing the tip side in the longitudinal direction. Mountains and a plurality of valleys facing the base end side in the longitudinal direction are alternately generated, and the mountains and the valleys are close to each other, and the coil is fixed by a support member on the ring. Selected from the group consisting of alkyleneimine, vinylamine, allylamine, lysine, protamine, and diallyldimethylammonium chloride, which are arranged on the ring so as not to include the positions of the peak of the mountain and the peak of the valley. A cationic polymer containing the compound as a constituent monomer is covalently bonded to the filter, and an anionic sulfur compound having anticoagulant activity is bonded to the filter and / or the cationic polymer. Yes.
- FIG. 1 is a schematic diagram of a side surface in the longitudinal direction of an endovascular treatment aid 1 according to an embodiment of the present invention.
- the intravascular treatment aid 1 shown in FIG. 1 can pass through a guide wire lumen of a treatment device such as a balloon catheter, and captures a flexible linear shaft 2 and a thrombus, plaque, and the like. It has a possible filter part 3, an outer tube 4, and an annular member 5 arranged on the distal end side in the longitudinal direction from the outer tube 4.
- the shaft 2 has flexibility in order to surely deliver it to the distal side of the lesioned portion to be placed in the blood vessel.
- having flexibility means returning to the original shape after being bent 180 degrees so as to have a radius of curvature of 100D, where D is the diameter of the shaft.
- the filter unit 3 is disposed on the distal end side in the longitudinal direction of the shaft 2 and has a plurality of apertures, and can be opened and closed like an umbrella, the proximal end side in the longitudinal direction of the filter 6, that is, the opening of the filter 6.
- An annular ring 7 made of a flexible wire provided on the side and having elastic restoring force, a coil 8 and a shaft 2 made of a radiopaque material wound on the ring 7, a filter 6 and a ring 7 and a support member 9 made of a linear member that enables the filter 6 to be closed by a tension generated by applying an external force to the base end side in the longitudinal direction.
- the distance between the distal end side of the filter 6 in the longitudinal direction and the distal end side of the shaft 2 is preferably 5 to 20 mm, and more preferably 10 to 15 mm.
- the distance between the distal end side in the longitudinal direction of the balloon portion of the balloon catheter and the proximal end side in the longitudinal direction of the filter 6 is preferably 10 mm or less.
- the distal end side in the longitudinal direction is the distal side of the blood vessel
- the proximal end side in the longitudinal direction is the central side of the blood vessel.
- the outer tube 4 Since the outer tube 4 has a through hole and is disposed on the shaft 2 so as to be movable, the outer tube 4 can swing on the shaft 2. Moreover, in order to improve the kink resistance of the shaft 2 and to secure rigidity for closing the filter portion 3, a braided layer using a metal wire such as stainless steel or a resin such as polyamide may be incorporated.
- the fixing position of the outer tube 4 on the shaft 2 is not particularly limited, but is preferably on the proximal end side in the longitudinal direction with respect to the opening of the filter portion 3.
- the annular member 5 Since the annular member 5 has a through hole and is arranged on the shaft 2 so as to be movable, the annular member 5 can swing on the shaft 2.
- the fixing position of the annular member 5 on the shaft 2 is not particularly limited, but is preferably on the proximal end side in the longitudinal direction with respect to the opening of the filter portion 3. Moreover, it is preferable that it is the front end side in the longitudinal direction rather than the outer tube 4. Further, the proximal end portion in the longitudinal direction of the annular member 5 may or may not be fixed to the distal end portion in the longitudinal direction of the outer tube 4, but the intravascular treatment aid 1 is placed in the blood vessel during the operation.
- the outer tube 4 on the proximal side operated by the operator may be oscillated from the distal end side to the proximal end side in the longitudinal direction. Therefore, if the annular member 5 is not fixed, the annular member 5 may not follow the peristalsis of the outer tube 4 and the relative position between the annular member 5 and the filter portion 3 may not be adjusted. 5 is preferably fixed to the distal end portion of the outer tube 4 in the longitudinal direction.
- the filter 6 is fixed to the shaft 2 so that the front end side in the longitudinal direction is closed, and this fixed portion is a closed end portion. Moreover, the base end side in the longitudinal direction is open, and this portion is defined as an opening.
- the opening of the filter 6 is fixed to the entire circumference of the annular ring 7 by an elastomer material, and the filter 6 has a conical shape with the ring 7 as a bottom surface in an open state. It becomes a shape. Further, it can be opened and closed in an umbrella shape following the movement of the ring 7.
- the coil 8 is fixed to the ring 7 by an elastomer material, it is possible to prevent the displacement due to the deformation of the filter 6 and the ring 7 while maintaining the flexibility of the ring 7.
- the support member 9 is composed of a plurality of linear members, and each linear member is fixed to the filter 6, the ring 7, and the coil 8 at the end of the filter 6 on the opening side.
- the filter 6, the ring 7 and the coil 8 are connected to a part of the shaft 2 by being focused and fixed at the same place.
- the support member 9 is composed of a plurality of linear members.
- the support member 9 has a number that can close the filter 6 and the ring 7.
- the fixing position of the support member 9 on the shaft 2 is not particularly limited, but it is preferable that the support member 9 is on the proximal end side in the longitudinal direction with respect to the opening of the filter unit 3.
- FIG. 2 is a schematic side view in the longitudinal direction when the filter unit 3 of the endovascular treatment aid 1 according to the embodiment of the present invention is closed.
- the through hole of the outer tube 4 and the annular member 5 has an inner diameter through which the linear support member 9 can pass, so that an external force is applied to the base end side in the longitudinal direction of the support member 9 to apply tension.
- the support member 9 is drawn while being focused between the through hole and the shaft 2, and swings on the shaft 2.
- the tip of the annular member 5 in the longitudinal direction reaches a position where the support member 9 is pulled to the end of the filter portion 3 on the opening side, that is, when the annular member 5 has finished focusing the support member 9, the filter The opening of the part 3 is in a closed state. Further, by making the lengths of the support members 9 equal, the shaft 2 is placed on the central axis of the ring 7.
- FIG. 3 is a schematic front view in the longitudinal direction showing the positional relationship among the ring 7, the coil 8, the support member 9, and the shaft 2 of the filter portion 3 of the endovascular treatment aid 1 according to the embodiment of the present invention.
- the ring 7 when the opening of the filter unit 3 is closed is formed in a small folded shape, so that it is supported at the dividing points equally divided by four or more evenly provided on the circumference of the ring 7.
- the member 9 is fixed either on each intermediate position between adjacent dividing points or on every other intermediate position.
- Every other dividing point becomes the apex of the mountain facing the tip side in the longitudinal direction of the shaft 2, and every other dividing point adjacent to the dividing point that became the apex of the peak is the longitudinal direction of the shaft 2.
- the ring 7 can be bent into a corrugated shape along the shaft 2 so as to be the apex of the valley facing the base end side. That is, when the opening of the filter unit 3 is closed, the ring 7 alternately has a plurality of peaks facing the distal end side in the longitudinal direction of the shaft 2 and a plurality of valleys facing the proximal end side in the longitudinal direction, and mountains and valleys are close to each other.
- the ring 7 is set with four division points 10 so as to equally divide the circumference into four, and the support member 9 is at an intermediate position between the adjacent division points 10. It is preferably fixed.
- the intermediate position does not have to be exactly the intermediate position between the dividing points, and may be slightly deviated to any one of the dividing points (the center angle formed by the two adjacent support members and the shaft is ⁇ Deviation of about 5 degrees or less).
- the coil 8 includes a position fixed by the support member 9 on the ring 7 and is disposed at a position on the ring that does not include the peak of the mountain and the peak of the valley. Thereby, since the deformation of the ring 7 is not disturbed by the coil 8, the distortion of the ring 7 when bent can be prevented.
- FIG. 3 when the opening of the filter unit 3 is closed, when viewed from the front in the longitudinal direction, the target structure and the small folded shape are taken.
- the ring 7 and the coil 8 are preferably fixed by a support member 9 at each intermediate position of the coil 8. It is preferable that the coil 8 has a more stable structure by penetrating the wire constituting the ring 7.
- the material of the shaft 2 is a member that becomes the core of the endovascular treatment aid 1, and is preferably a metal such as stainless steel, tungsten, or cobalt alloy that is used for a general guide wire.
- the material of the outer tube 4 is a material in which the supporting member 9 is focused by the annular member 5 and the rigidity necessary for closing the filter portion 3 by the tension and the flexibility of ensuring the followability of the blood vessel can be achieved.
- Any material may be used, and examples thereof include metals such as nickel alloys and stainless steels, and more preferred are resins such as polyimide and polyamide.
- the material of the outer tube 4 is a resin such as polyimide or polyamide
- a polyimide in which polytetrafluoroethylene, a tetrafluoroethylene copolymer and a lubricant are blended in order to improve the sliding performance on the shaft 2
- a highly slippery resin such as polyamide or polyethylene
- a braided layer using a metal wire such as stainless steel or a resin such as polyamide. It is also possible to incorporate.
- the outer tube 4 is considered to have a sheath function.
- the outer diameter of the outer tube 4 is set to a diameter that can be accommodated in a treatment device such as a balloon catheter, and the inner diameter of the through hole is closed.
- the endovascular treatment aid 1 can be configured not to require a sheath.
- the material of the annular member 5 examples include metals such as stainless steel, platinum alloy, palladium alloy, etc.
- metals such as stainless steel, platinum alloy, palladium alloy, etc.
- polyimide or Resins such as polyamide and polyurethane are more preferable.
- resins such as polycarbonate, polypropylene, and polyethylene that can be molded with a mold or the like are more preferable.
- the material of the filter 6 is a polymer such as polyester, polyurethane, polyether urethane, polyamide, vinyl chloride, polycarbonate, polystyrene, polyethylene, polypropylene, polymethylpentene, polymethyl methacrylate and polytetrafluoroethylene, or a super alloy such as a nickel alloy. Although it is comprised with the metal which is rich in an elastic characteristic, it is preferable to comprise especially using polyester.
- the shape of the filter 6 becomes a filter by forming a polymer into a sheet shape and opening a plurality of apertures. However, in order to further increase the aperture ratio of the filter and secure the amount of blood passing through, the polymer or metal is made into a fiber shape.
- PET polyethylene terephthalate
- PET polytrimethylene terephthalate
- polybutylene terephthalate polyethylene naphthalate
- polybutylene naphthalate polybutylene naphthalate
- PET is an antithrombogenic material.
- the versatility is high and more preferable.
- the opening size may be anything as long as it can capture blood clots, plaques, etc. while ensuring blood flow.
- the hole diameter should be 30 to 100 ⁇ m.
- it is formed so that one side is 30 to 100 ⁇ m. Since the opening size is small, not only thrombus and plaque released from the blood vessel wall but also thrombus due to the filter 6 which is a foreign substance to the human body is considered to be formed. It is preferable to bind the compound.
- the material of the ring 7 may be any material as long as it is a flexible wire having an elastic restoring force that can be bent, but it has superelastic characteristics that can be restored to the original ring shape while changing to various shapes. Rich materials are appropriate. Therefore, it can be composed of a shape memory polymer, but more preferably a metal such as a nickel alloy.
- the elastomer material for fixing between the ring 7 and the filter 6 may be urethane acrylate adhesive, polyurethane, polyamide elastomer or the like.
- Shore hardness (Shore D) based on ISO868: 2003 is preferably about 25D to 55D, more preferably the Shore hardness (Shore A) is 80 A or less.
- any material may be used for the coil 8 as long as it is made of a radiopaque material, such as gold, platinum alloy, palladium alloy and the like.
- the shape of the metal wire used for the coil 8 may be a flat wire or a round wire.
- the wire diameter of the metal wire used as the radiopaque material is preferably 30 to 70 ⁇ m, but more preferably 30 to 40 ⁇ m in order to reduce the bulk when the opening of the filter unit 3 is closed.
- the fixing amount of the coil 8 on the ring 7 is too small, it is difficult to obtain the desired good contrast.
- the fixing amount is too large, the deformation of the ring 7 is disturbed. Therefore, the total length of the coil 8 with respect to the circumference of the ring 7 is preferably 1/6 to 4/6, and more preferably 2/6.
- the elastomer material for fixing the coil 8 and the ring 7 may be a urethane acrylate adhesive, polyurethane, polyamide elastomer or the like.
- the Shore hardness (Shore D) based on ISO868: 2003 is preferably about 20D to 40D, more preferably the Shore hardness (Shore A) is 90A or less, and even more preferably. Has a Shore hardness (Shore A) of 80 A or less.
- the material of the support member 9 may be any material as long as it does not hinder the restoring force of the ring 7 and does not break when converged on the annular member 5, and may be a thin metal wire.
- Aramid fiber, polyarylate fiber High-strength resinous fibers such as polyester fibers are more preferable.
- the filter 6 and the support member 9 are fixed via the ring 7, but the support member 9 may be directly fixed to the filter 6 without the ring 7. .
- the support member 9 is preferably formed of a metal such as a nickel alloy having superelastic characteristics.
- the endovascular treatment aid is one that suppresses thrombus formation caused by this and exhibits high antithrombotic properties for a long period of time.
- antithrombogenicity is a property that blood does not coagulate on the surface in contact with blood, and inhibits blood coagulation that progresses by, for example, platelet aggregation or activation of blood coagulation factors typified by thrombin.
- the antithrombotic compound is a compound having antithrombogenicity, and in particular, the antithrombotic compound can be bonded to the surface of the filter 6 having a large contact area with blood and easily forming a thrombus. is needed.
- a cationic polymer containing as constituent monomer A at least one compound selected from the group consisting of alkyleneimine, vinylamine, allylamine, lysine, protamine and diallyldimethylammonium chloride, and An anionic sulfur compound having anticoagulant activity is used.
- the cationic polymer is covalently bonded to the surface of the filter 6, and an anionic sulfur compound having anticoagulant activity is bonded to the filter 6 and / or the cationic polymer. It is in the state which gave antithrombogenicity.
- the constituent monomer A which is a monomer constituting the cationic polymer has a cationic nitrogen atom
- the polymer becomes cationic
- the compound containing a sulfur atom having anticoagulant activity is an anion. Both can be ionically bonded.
- the anionic sulfur compound having anticoagulant activity include heparin or heparin derivatives, dextran sulfate, polyvinyl sulfonic acid and polystyrene sulfonic acid, and heparin or heparin derivatives are more preferable.
- Heparin or a heparin derivative may be purified or not, and is not particularly limited as long as it can inhibit the blood coagulation reaction.
- Heparin generally used in clinical practice In addition to unfractionated heparin and low molecular weight heparin, antithrombin III has high affinity heparin.
- Specific examples of heparin include “heparin sodium” (Organon API).
- examples of heparin derivatives include fragmin, clexane, organalan, and elixir.
- the cationic polymer Since the cationic polymer has a cationic property and may develop hemolytic toxicity, it is not preferable to elute it in the blood. Therefore, the cationic polymer is preferably covalently bonded to the surface of the filter 6. Covalent bonding between the cationic polymer and the surface of the filter 7 can be performed by covalently bonding the functional group of the cationic polymer and the functional group of the surface of the filter 6 by a well-known method. For example, the amino group of the cationic polymer and the carboxyl group of the polyester constituting the filter 7 are converted into 4 (-4,6-dimethoxy-1,3,5-triazin-2-yl) -4-methylmorpholinium chloride.
- a condensing agent such as n-hydrate (“DMT-MM”).
- DMT-MM condensing agent
- a method in which a cationic polymer is brought into contact with the filter 7 under heating conditions to be covalently bonded by an aminolysis reaction can also be used.
- produce on the surface of the filter 7 and a cationic polymer by irradiating a radiation, and make the surface of the filter 7 and a polymer covalently bond by the recombination reaction are mentioned.
- the covalent bond refers to a chemical bond generated by sharing electrons between atoms.
- it is a covalent bond of atoms, such as carbon, nitrogen, oxygen, sulfur, etc. which the surface of the cationic polymer and the filter 6 has, and may be a single bond or a multiple bond.
- the kind of covalent bond is not limited, For example, an amine bond, an azide bond, an amide bond, an imine bond etc. are mentioned. Among these, an amide bond is more preferable from the viewpoint of easy formation of a covalent bond and stability after bonding.
- an amide bond is formed between the cationic polymer and the surface of the filter 6 so that the configuration of the cationic polymer on the surface of the filter 6 is an anion having anticoagulant activity. It was found that the ionic bond state with the sulfur compound is optimized. The confirmation of the covalent bond can be determined from the fact that it does not elute even if it is washed with a solvent that dissolves the polymer.
- the cationic polymer may be a homopolymer or a copolymer.
- the cationic polymer may be a random copolymer, a block copolymer, a graft copolymer or an alternating copolymer, but the repeating unit containing a nitrogen atom is continuous.
- a block copolymer is more preferable because the block portion and an anionic sulfur compound having anticoagulant activity interact to form strong ionic bonds.
- the homopolymer means a polymer compound obtained by polymerizing one kind of constituent monomer
- the copolymer means a polymer compound obtained by copolymerization of two or more kinds of monomers.
- the block copolymer is a copolymer having a molecular structure in which at least two kinds of polymers having different repeating units are connected by covalent bonds to form a long chain.
- a block constitutes a block copolymer. Each of at least two kinds of polymers having different repeating units.
- the structure of the cationic polymer may be linear or branched.
- branched anionic sulfur compounds having anticoagulant activity and a more stable ionic bond at multiple points can be formed, and therefore a branched one is more preferable.
- the cationic polymer has at least one functional group among primary to tertiary amino groups and quaternary ammonium groups.
- the quaternary ammonium groups are Since the ionic interaction with the anionic sulfur compound having anticoagulant activity than the primary to tertiary amino groups is strong and the elution rate of the anionic sulfur compound having anticoagulant activity is easy to control, preferable.
- the number of carbon atoms of the three alkyl groups constituting the quaternary ammonium group is not particularly limited. However, if the number is too large, the hydrophobicity is high and the steric hindrance increases. An anionic sulfur compound having anticoagulant activity effectively cannot be ionically bonded. Further, since too much hemolytic toxicity is likely to occur, the number of carbon atoms per alkyl group bonded to the nitrogen atom constituting the quaternary ammonium group is preferably 1 to 12, and more preferably 2 to 6 Is preferred.
- the three alkyl groups bonded to the nitrogen atom constituting the quaternary ammonium group may all have the same carbon number or may be different.
- polyalkyleneimine as the cationic polymer because of the large amount of adsorption based on anionic interaction with an anionic sulfur compound having anticoagulant activity.
- the polyalkyleneimine include polyethyleneimine (hereinafter “PEI”), polypropyleneimine and polybutyleneimine, and further alkoxylated polyalkyleneimine. Among them, PEI is more preferable.
- PEI examples include “LUPASOL” (registered trademark) (manufactured by BASF) and “EPOMIN” (registered trademark) (manufactured by Nippon Shokubai Co., Ltd.). It may be a copolymer with another monomer or a modified product.
- the modified body refers to a monomer in which the repeating unit of the monomer constituting the cationic polymer is the same, but a part of which has undergone radical decomposition, recombination, or the like by irradiation with radiation, for example.
- the cationic polymer of the present invention may be composed of at least one selected from the group consisting of alkyleneimine, vinylamine, allylamine, lysine, protamine and diallyldimethylammonium chloride as a monomer constituting the cationic polymer.
- a copolymer may be formed with one or more other monomers that do not adversely affect the properties.
- Such other constituent monomers for forming the copolymer are not particularly limited, and examples thereof include ethylene glycol, propylene glycol, vinyl pyrrolidone, vinyl alcohol, vinyl caprolactam, vinyl acetate, styrene, methyl methacrylate,
- Examples of the constituent monomer B include hydroxyethyl methacrylate and siloxane.
- the weight of the constituent monomer B is too large, the ionic bond between the cationic polymer and the anionic sulfur compound having anticoagulant activity is weakened. Therefore, the weight of the constituent monomer B with respect to the total weight of the cationic polymer is 10 weights. % Or less is preferable.
- the weight average molecular weight of the cationic polymer is smaller than that of an anionic sulfur compound having anticoagulant activity, so that a stable ionic bond is not formed, and the desired antithrombogenicity is obtained. It becomes difficult to be.
- the weight average molecular weight of the cationic polymer is too large, the anionic sulfur compound having anticoagulant activity is encapsulated by the cationic polymer and buried.
- the weight average molecular weight of the cationic polymer is preferably from 600 to 2,000,000, more preferably from 1,000 to 1500,000, and even more preferably from 10,000 to 1,000,000.
- the weight average molecular weight of the cationic polymer can be measured by, for example, a gel permeation chromatography method or a light scattering method.
- the present inventors in order to suppress thrombus formation caused by an intravascular treatment aid and to exhibit high antithrombogenicity for a long period of time, the present inventors have conducted intensive studies. As a result, X-ray photoelectron spectroscopy ( Hereinafter, it has been found that there is a preferable value for the abundance ratio of sulfur atoms to the abundance of all atoms on the surface of the filter 6 measured by “XPS”).
- the abundance ratio of atoms is represented by “number of atoms%”.
- the number of atoms% indicates the abundance ratio of specific atoms in terms of the number of atoms when the abundance of all atoms is 100.
- the abundance ratio of sulfur atoms to the abundance of all atoms on the surface of the filter 6 measured by XPS is preferably 3.0 to 6.0 atomic%, and 3.2 to 5.5 atomic numbers. % Is more preferable, and 3.5 to 5.0 atomic% is even more preferable. If the ratio of sulfur atoms to the total amount of atoms is less than 3.0%, the amount of anionic sulfur compounds that have anticoagulant activity will be reduced. The desired antithrombogenicity required to suppress formation is difficult to obtain.
- the abundance ratio of sulfur atoms with respect to the abundance of all atoms exceeds 6.0 atomic%, a sufficient amount of an anionic sulfur compound having anticoagulant activity is present, and the desired antithrombogenicity is Although obtained, a large amount of the cationic polymer covalently bonded to the filter 6 is required for ionic bonding. Further, the cationic polymer exposed as the anionic sulfur compound having anticoagulant activity is eluted is not preferable because it may develop hemolytic toxicity.
- the abundance ratio of sulfur atoms with respect to the abundance of all atoms on the surface of the filter 6 measured by XPS can be determined by XPS.
- the surface of the filter 6 measured by XPS means that the X electron escape angle under the XPS measurement conditions, that is, when the inclination of the detector with respect to the surface formed by the antithrombotic compound and the filter 6 is 90 °. It means that the detected depth from the measurement surface is 10 nm.
- the filter 6 may or may not contain sulfur atoms.
- the atomic information of the surface of the filter 6 measured by XPS is obtained from the binding energy value of the bound electrons in the substance obtained by irradiating the surface of the filter 6 with X-rays and measuring the energy of the photoelectrons generated.
- Information on the valence and the binding state can be obtained from the energy shift of the peak of the binding energy value. Furthermore, quantitative determination using the area ratio of each peak, that is, the existence ratio of each atom, valence, and bonding state can be calculated.
- the S2p peak indicating the presence of a sulfur atom is observed at a binding energy value near 161 eV to 170 eV, and in the present invention, the area ratio of the S2p peak to the total peak is 3.0 to 6.0 atomic%. It was found that it is preferable.
- the abundance ratio of sulfur atoms to the abundance of all atoms is calculated by rounding off the second decimal place.
- the abundance ratio of nitrogen atoms to the abundance of all atoms on the surface of the filter 6 measured by XPS is preferably 7.0 to 12.0 atomic percent, more preferably 7.5 to 11.0 atomic percent. 8.0 to 10.0 atomic% is even more preferable.
- the ratio of nitrogen atoms to the total amount of atoms is less than 7.0%, the amount of cationic polymer that binds to the filter 6 is reduced, so that thrombus formation caused by an endovascular treatment aid is suppressed.
- the abundance ratio of nitrogen atoms with respect to the abundance of all atoms exceeds 12.0 atomic%, the amount of the cationic polymer that binds to the filter 6 increases, so that the anticoagulant activity that ionically bonds to the cationic polymer. It has been found that a sufficient amount of the anionic sulfur compound having an anion is present, but as the anionic sulfur compound having an anticoagulant activity is eluted, a large amount of the cationic polymer is exposed, so that hemolytic toxicity is exhibited.
- the N1s peak indicating the presence of a nitrogen atom is observed in the vicinity of a binding energy value of 396 eV to 403 eV.
- the area ratio of the N1s peak to the entire peak is 7.0 to 12.0 atomic%. It was found that it is preferable.
- the N1s peak is mainly composed of an n1 component (near 399 eV) attributed to a carbon-nitrogen (hereinafter “CN”) bond, an ammonium salt, CN (a structure different from n1), or a nitrogen oxide.
- the peak can be divided into n2 components (near 401 to 402 eV) belonging to (hereinafter “NO”).
- the existence ratio of each divided peak component is calculated by the following formula 1.
- the abundance ratio of nitrogen atoms to the abundance of all atoms and the abundance ratio of each divided peak component are calculated by rounding off the first decimal place.
- Division ratio N1s ratio ⁇ (division percent / 100) Equation 1
- Split ratio Abundance ratio of each split peak component (%)
- N1s ratio abundance ratio of nitrogen atom to abundance of all atoms (%)
- Divided percent Abundance ratio of each divided peak component in N1s peak (%)
- the n2 component attributed to NO obtained by the division of the N1s peak indicates the presence of a quaternary ammonium group, and the abundance ratio of the n2 component to the total components of the N1s peak, that is, the divided percent (n2 ) Is preferably 20 to 70 atomic%, more preferably 25 to 65 atomic%, and further preferably 30 to 60 atomic%.
- the divided percent (n2) is less than 20 atomic%, the quaternary ammonium group is present in a small amount, so that the ionic interaction with the anionic sulfur compound having anticoagulant activity is weak, and the dissolution rate is increased and blood vessels are increased.
- the divided percent (n2) exceeds 70 atomic%, the ionic interaction with the anionic sulfur compound having anticoagulant activity is too strong. Not only cannot the coagulation activity be expressed for a long time, but also the elution rate tends to be slow.
- the abundance ratio of the n2 component, that is, the division ratio (n2) is calculated by the equation 1, it is preferably 1.4 to 8.4 atomic% for the above reasons, and 1.8 to 7.2 atoms. Several percent is more preferred, and 2.4 to 6.0 atomic percent is even more preferred.
- the C1s peak indicating the presence of carbon atoms is seen in the vicinity of a binding energy value of 282 to 292 eV, and the C1s peak is mainly a carbon-hydrogen (hereinafter “CHx”) bond that suggests the presence of saturated hydrocarbons or the like.
- CHx carbon-hydrogen
- the c3 component attributed to the C ⁇ O bond obtained by splitting the C1s peak indicates the presence of an amide group in the present invention.
- the abundance ratio of the c3 component with respect to all components of the C1s peak ie, In the present invention, it has been found that the abundance ratio of the amide group is preferably 2.0 atomic% or more, more preferably 3.0 atomic% or more.
- the abundance ratio of the amide group is less than 2.0 atomic%, since the covalent bond due to the amide bond is reduced between the cationic polymer and the filter 6, the amount of the cationic polymer is reduced and the cationic property is reduced. Since the ion binding state between the polymer and the anionic sulfur compound having anticoagulant activity is deteriorated, it is difficult to obtain the desired antithrombogenicity.
- an antithrombotic compound in addition, an anionic polymer containing at least one compound selected from the group consisting of acrylic acid, methacrylic acid, ⁇ -glutamic acid, ⁇ -glutamic acid and aspartic acid as a constituent monomer, or Selected from the group consisting of dicarboxylic acids such as oxalic acid, malonic acid, succinic acid, fumaric acid, glutaric acid, adipic acid, pimelic acid, suberic acid, azelaic acid, sebacic acid, malic acid, tartaric acid, dodecanedioic acid, and citric acid It is preferable that at least one anionic compound to be bound to the filter 6 and / or the cationic polymer. These anionic polymers and / or anionic compounds can be bound to the cationic polymer by ionic bonds.
- the anionic polymer is not particularly limited, but the higher the weight ratio of the anionic functional group, the greater the amount of binding with the filter 6, so that polyacrylic acid (hereinafter “PAA”), polymethacrylic acid, Acid, poly ⁇ -glutamic acid, poly ⁇ -glutamic acid, and polyaspartic acid are preferably used, and PAA is more preferable.
- PAA polyacrylic acid
- PAA polymethacrylic acid
- Acid poly ⁇ -glutamic acid
- poly ⁇ -glutamic acid poly ⁇ -glutamic acid
- polyaspartic acid polyaspartic acid
- PAA examples include “polyacrylic acid” (manufactured by Wako Pure Chemical Industries, Ltd.) and the like, but may be a copolymer with other monomers as long as the effects of the present invention are not hindered. It may be a body.
- the anionic polymer is eluted in the blood from the viewpoint of safety and the like. Therefore, the anionic polymer is preferably bonded to the surface of the filter 6 and more preferably covalently bonded.
- the anionic polymer may be a homopolymer or a copolymer.
- the anionic polymer may be a random copolymer, a block copolymer, a graft copolymer, or an alternating copolymer.
- the anionic polymer may be composed of only the above-mentioned constituent monomers, but may form a copolymer with constituent monomers other than those described above as long as the antithrombotic properties are not adversely affected.
- Constituent monomers for forming the copolymer used in addition to acrylic acid, methacrylic acid, ⁇ -glutamic acid, ⁇ -glutamic acid and aspartic acid are not particularly limited, but examples thereof include ethylene glycol, propylene glycol, and vinylpyrrolidone.
- constituent monomers B such as vinyl alcohol, vinyl caprolactam, vinyl acetate, styrene, methyl methacrylate, hydroxyethyl methacrylate, and siloxane.
- the weight of the constituent monomer B is too large, the number of reaction points for binding to the filter 7 or other antithrombotic compound is reduced. Therefore, the weight of the constituent monomer B with respect to the total weight of the anionic polymer is 10% by weight. The following is preferable.
- the anionic compound is not particularly limited. However, the higher the weight ratio of the anionic functional group, the greater the amount of binding with the filter 6 or other antithrombotic compound. Therefore, oxalic acid, malonic acid, succinic acid Acid, fumaric acid, glutaric acid, adipic acid, pimelic acid, suberic acid, azelaic acid, sebacic acid, malic acid, tartaric acid and citric acid are preferably used, and succinic acid is more preferred.
- the weight average molecular weight of the anionic polymer is preferably from 600 to 2,000,000, more preferably from 10,000 to 1,000,000.
- the surface amount of an anionic sulfur compound having anticoagulant activity due to antifactor Xa activity in the filter 6 after being immersed in physiological saline at 37 ° C. for 30 minutes was measured.
- the anti-factor Xa activity is an index representing the degree of inhibiting the activity of factor Xa that promotes the conversion of prothrombin to thrombin, and the surface amount in activity units can be known.
- “Test Team (registered trademark) Heparin S” manufactured by Sekisui Medical Co., Ltd.
- Teest Team Heparin was used.
- the anti-factor Xa activity is preferably 30mIU / cm 2, and more preferably 50 mIU / cm 2.
- the filter 6 to which an anionic sulfur compound having anticoagulant activity is bound is cut into a test piece having an effective surface area of about 0.26 cm 2 and 0.5 mL of physiological saline. For 30 minutes at 37 ° C.
- the endovascular treatment aid of the present invention was immersed in physiological saline at 37 ° C. for 30 minutes, although the total binding amount of the anionic sulfur compound having anticoagulant activity due to the antifactor Xa activity in the filter 6 was small. It is characterized by a high surface mass afterwards.
- the total binding amount is an anion having anticoagulant activity based on antifactor Xa activity, calculated from human plasma after being immersed in human plasma (product number 12271210; manufactured by Cosmo Bio Inc.) at 37 ° C. for 24 hours. This is an amount obtained by adding the elution amount of the active sulfur compound and the surface amount of the anionic sulfur compound having anticoagulant activity due to the antifactor Xa activity in the filter 6 after being immersed for 24 hours.
- the elution amount of the anionic sulfur compound having anticoagulant activity due to the antifactor Xa activity is such that the effective surface area of the filter 6 to which the anionic sulfur compound having anticoagulant activity is bound is about 4.24 cm 2 .
- the sample was reacted according to the test team heparin operation procedure (endpoint method), the absorbance at 405 nm was measured with a microplate reader, and calculated separately based on a calibration curve prepared using heparin sodium injection. did.
- the specimen heating time in the endpoint method was 5 minutes. Further, the surface amount of the anionic sulfur compound having anticoagulant activity due to the anti-factor Xa activity in the filter 6 after being immersed for 24 hours is the above-mentioned 37 ° C. using the filter 6 after being immersed for 24 hours. The calculation was performed in the same manner as the surface amount of the anionic sulfur compound having anticoagulant activity due to the antifactor Xa activity in the filter 6 after being immersed in physiological saline for 30 minutes.
- the filter 6 has a total binding amount of an anionic sulfur compound having anticoagulant activity due to the antifactor Xa activity of 10,000 mIU / cm 2 or less and is immersed in physiological saline at 37 ° C. for 30 minutes.
- the surface amount of the anionic sulfur compound having anticoagulant activity due to the anti-factor Xa activity is preferably 30 mIU / cm 2 or more, the total binding amount is 5000 mIU / cm 2 or less, and the surface amount is 50 mIU / cm 2. More preferably, it is cm 2 or more.
- the endovascular treatment aid of the present invention is characterized by the elution behavior of the anionic sulfur compound having anticoagulant activity in the filter 6. That is, the anionic sulfur compound having anticoagulant activity does not substantially elute even when immersed in physiological saline at 37 ° C., but quickly dissolves when immersed in human plasma at 37 ° C. (Product No. 12271210; manufactured by Cosmo Bio Inc.). To do. Specifically, in human plasma at 37 ° C., 50% or more, more preferably 70% or more, and even more preferably 80% or more of the total binding amount is eluted after 1 hour immersion, and total binding is possible even after 15 minutes immersion. More than 50%, more preferably more than 70%, even more preferably more than 80% of the amount is eluted.
- the thickness of the anti-thrombotic compound layer is too thick, it will not only destroy the fine structure of the surface of the filter 6, but also change the aperture size, or the side of the opening when the filter unit 3 is closed. There is a possibility that the formation of a thrombus may be caused by a change in the outer diameter of the. That is, it is preferably 1 to 600 nm.
- the thickness of the antithrombotic compound layer can be confirmed by a combination of, for example, a scanning transmission electron microscope (hereinafter, “STEM”) or XPS. Specifically, the distance from the start point to the end point of the point where the atoms derived from the antithrombotic material layer were observed when the atomic distribution was observed in the vertical direction toward the inside starting from the interface of the filter 6. That is, it is measured from an average value obtained from at least three thickness values.
- STEM scanning transmission electron microscope
- the interface of the filter 6 measured with the STEM refers to the boundary between, for example, an acrylic resin to be embedded when preparing the sample before the measurement with the STEM, and the surface composed of the filter 6 and the antithrombotic compound layer. Point to.
- the STEM has detectors such as an energy dispersive X-ray spectrometer (hereinafter referred to as “EDX”) and an electron energy loss spectrometer (hereinafter referred to as “EELS”). Show.
- EDX energy dispersive X-ray spectrometer
- EELS electron energy loss spectrometer
- the presence of atoms is determined by whether or not the peak intensity derived from each atom is recognized by subtracting the background in the spectrum obtained from the STEM measurement.
- Example 1 An endovascular treatment aid 1 according to the embodiment of the present invention shown in FIG. 1 was produced.
- the filter 6 is composed of a monofilament polyester (PET) fiber having a wire diameter of ⁇ 28 ⁇ m so that the opening size is 100 ⁇ m on one side, and this mesh has a length of about 10 mm in the longitudinal direction and a filter opening.
- the circular diameter of the part was made to be 6 mm.
- the coil 8 was made of a Pd—Re alloy wire having a wire diameter of ⁇ 40 ⁇ m and had an outer diameter of ⁇ 0.16 mm, an inner diameter of ⁇ 0.08 mm, and a total length of 1 mm. Four of these coils were produced, and a NiTi alloy wire having a wire diameter of 42 ⁇ m was penetrated. In addition, when the NiTi alloy wire is made into a ring with an inner diameter of ⁇ 6 mm in advance so that the four coils 8 are arranged at positions not including the peak of the peak and the peak of the valley when the opening of the filter unit 3 is closed, the ring was placed so as to be divided into four equal parts on the circumference and fixed with polyurethane.
- a NiTi alloy wire with four coils 8 fixed thereto is wound in a ring shape 5 times so that the inner diameter becomes ⁇ 6 mm, and this is made into a ring 7, and this is used as a ring 7.
- the outer diameter part of was fixed with polyurethane.
- the support member 9 is made of four aramid fibers having a wire diameter of about 60 ⁇ m and is fixed to the filter 6, the ring 7, and the coil 8 so that each of the four is arranged at an intermediate position of the coil 8.
- the filter part 3 was produced.
- the shaft 2 uses a stainless steel wire having an outer diameter of 0.2 mm and a longitudinal length of 1800 mm, and is tapered so that the outer diameter is about 0.06 mm to ⁇ 0.15 mm from the tip to about 20 mm in the longitudinal direction. From there, the outer diameter of the shaft 2 is about 0.15 mm with a length of about 30 mm, and further, a taper shape is given so that the outer diameter is about 20 mm from that with an outer diameter of 0.15 mm to 0.2 mm. Produced.
- the shaft 2 is passed through the polyimide tube that bundles the closed end and the opening of the filter unit 3 and the support member 9 so that the support members 9 all have the same length, that is, the shaft is connected to the central axis of the ring 7.
- the shaft 2 and the support member are arranged using a polyimide tube having an inner diameter of 0.25 mm, an outer diameter of ⁇ 0.29 mm, and a length of 1.5 mm at an outer diameter portion of ⁇ 0.15 mm on the shaft 2. 9 was fixed with an adhesive.
- the outer tube 4 has a three-layer structure in which the inner layer is polytetrafluoroethylene, the intermediate layer is a braided layer made of stainless steel flat wire, and the outer layer is polyimide.
- the inner diameter is 0.23 mm
- the outer diameter is 0.36 mm
- the length is 1500 mm.
- a polyimide tube having an inner diameter of 0.4 mm, an outer diameter of 0.52 mm, and a length of 5 mm was fixed to the tip of the outer tube 4 with an adhesive so that a length of 4 mm protruded, and this was used as an annular member 5.
- the assembly of the outer tube 4 and the annular member 5 was arranged on the shaft 2 so that the annular member 5 came to the distal end side, and the endovascular treatment aid 1 was produced.
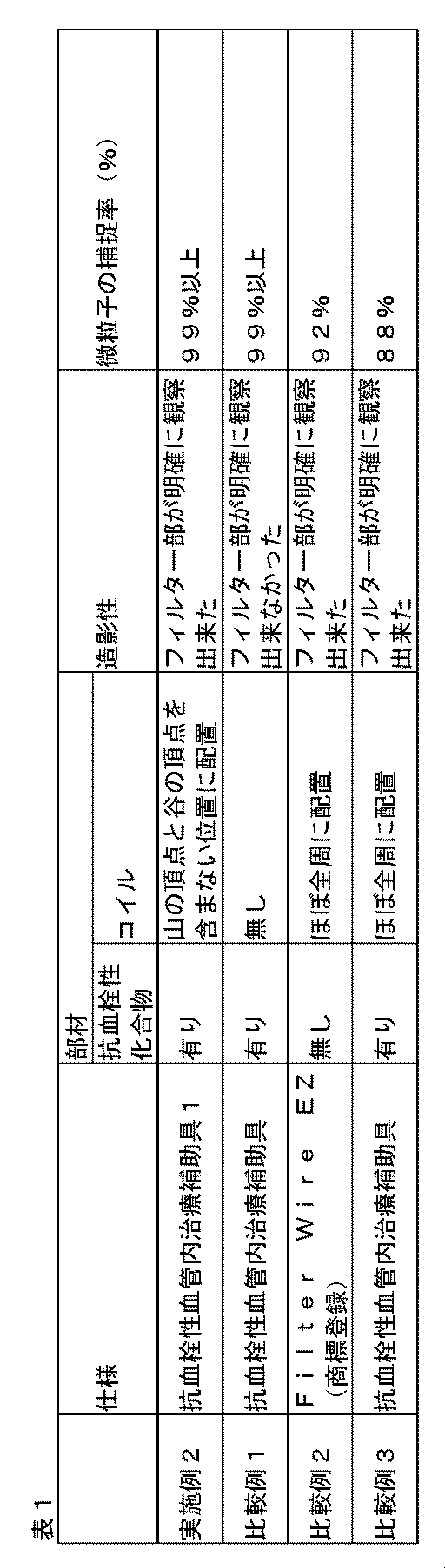
- Comparative Example 1 As Comparative Example 1, an endovascular treatment aid produced in exactly the same manner except that the coil 8 was not used and the coil 8 was not fixed on the ring 7 was produced.
- Comparative Example 2 A support member is fixed on the shaft, and the support member forms a ring of a filter part, and a metal coil formed of a radiopaque material is attached to the ring over the entire circumference, and the ring is attached to the ring.
- Filter Wire EZ which is a thrombus capture catheter of Boston Scientific, in which a filter with a plurality of holes made of urethane sheet is fixed, and the tip of the filter is sealed and attached on the tip side of the shaft ( (Registered Trademark) was designated as Comparative Example 2.
- Comparative Example 2 was an endovascular treatment aid having a ring diameter of about 6 mm, a shaft length of 1900 mm, and a shaft diameter of 0.36 mm.
- Comparative Example 3 As Comparative Example 3, an endovascular treatment aid produced in the same manner as in the Example, except that the coil 8 was fixed over almost the entire circumference on the ring 7.
- Contrast-enhanced comparative experiment Contrast-enhanced comparative experiment of Example, Comparative Example 1, Comparative Example 2, and Comparative Example 3 using a radiation apparatus OEC9800Plus (GE Medical Systems) in an animal experiment using a pig weighing 35 kg Went.
- OEC9800Plus GE Medical Systems
- a tube 11 having an inner diameter of ⁇ 5 mm is prepared, and water is passed through it.
- a gauze 12 is prepared at the tip of the tube 11, the tube 11 is bent to about 45 degrees, and each of the example, comparative example 1, comparative example 2, and comparative example 3 is housed in a delivery sheath at the bent vertex. Then, after delivery to the target indwelling part, the delivery sheath is removed, the filter part is deployed and indwelled in the tube 11, and about 4000 fine particles 13 having a diameter of 150 ⁇ m are flowed into the tube 11.
- Example and Comparative Example 1 the capture rate of fine particles was 99% or more, whereas in Comparative Example 2, it was about 92%, and in Comparative Example 3, it was about 88%.
- Example 2 An endovascular treatment aid 1 according to the embodiment of the present invention shown in FIG. 1 was produced. Specifically, a mesh was prepared with monofilament polyester (PET) fibers having a wire diameter of ⁇ 28 ⁇ m so that the aperture size was 100 ⁇ m per side.
- PET monofilament polyester
- the mesh is immersed in an aqueous solution of 5.0% by weight potassium permanganate (manufactured by Wako Pure Chemical Industries, Ltd.) and 0.6 mol / L sulfuric acid (manufactured by Wako Pure Chemical Industries, Ltd.), and at 60 ° C. for 3 hours.
- the mesh was hydrolyzed and oxidized by the reaction (step of hydrolyzing and oxidizing).
- the aqueous solution after the reaction was removed and washed with hydrochloric acid (Wako Pure Chemical Industries, Ltd.) and distilled water.
- the mesh was then added to 0.5 wt% 4 (-4,6-dimethoxy-1,3,5-triazin-2-yl) -4-methylmorpholinium chloride n hydrate (hereinafter “DMT-MM”). ) (Condensation agent manufactured by Wako Pure Chemical Industries, Ltd.), 5.0% by weight PEI (LUPASOL (registered trademark) P; manufactured by BASF) in water and reacted at 30 ° C. for 2 hours to condense PEI on the mesh Covalently bonded by reaction (first coating step). The aqueous solution after the reaction was removed and washed with distilled water.
- DMT-MM 0.5 wt% 4 (-4,6-dimethoxy-1,3,5-triazin-2-yl) -4-methylmorpholinium chloride n hydrate
- PEI LPASOL (registered trademark) P; manufactured by BASF
- the mesh was immersed in a 1% by weight methanol aqueous solution of ethyl bromide (Wako Pure Chemical Industries, Ltd.) or pentyl bromide (Wako Pure Chemical Industries, Ltd.) and reacted at 35 ° C. for 1 hour.
- the mixture was heated to 50 ° C. and reacted for 4 hours to quaternize the PEI covalently bonded to the surface of the mesh (quaternary ammonium conversion step).
- the aqueous solution after the reaction was removed and washed with methanol or distilled water.
- a mesh using PEI (average molecular weight of about 600; manufactured by Wako Pure Chemical Industries, Ltd.) and ethyl bromide was used as mesh A and PEI (LUPASOL (registered trademark) P; manufactured by BASF).
- the mesh that was not subjected to the quaternary ammoniumation step was Mesh B, PEI (LUPASOL (registered trademark) P; manufactured by BASF) and the mesh using ethyl bromide was Mesh C, PEI (LUPASOL (registered trademark) P; BASF)
- Mesh D a mesh using pentyl bromide was designated as Mesh D.
- the filter 6 was prepared so that the length in the longitudinal direction was about 8 mm and the circular diameter on the opening side was 4 mm, and they were designated as Sample A, Sample B, Sample C, and Sample D, respectively. In Example 2, Samples A to D were used as the filter 6.
- the coil 8 was made of a palladium-rhenium alloy wire having a wire diameter of 40 ⁇ m, and had an outer diameter of 0.16 mm, an inner diameter of 0.08 mm, and a total length of 1 mm.
- Four coils 8 were produced and a nickel titanium alloy wire having a wire diameter of ⁇ 42 ⁇ m was penetrated.
- the nickel titanium alloy wire is made into a ring 7 having an inner diameter of ⁇ 6 mm in advance so that the four coils 8 are arranged at positions not including the peak of the peak and the peak of the valley when the opening of the filter unit 3 is closed.
- the ring 7 was wound around the circumference so as to be divided into four equal parts and fixed with polyurethane.
- a nickel-titanium alloy wire with four coils 8 fixed thereto is wound in a ring shape five times so that the inner diameter becomes ⁇ 6 mm, and this is used as a ring 7.
- the inner diameter portion of the ring 7 and the opening of the filter 6 are formed.
- the outer diameter part of the partial circle was fixed with polyurethane.
- the support member 9 uses four polyarylate fibers having a wire diameter of about 60 ⁇ m, and each of the four is arranged at each intermediate position of the coil 8 so as to have the positional relationship shown in FIG. Then, the filter part 3 was manufactured by being tied to the ring 7 and the coil 8.
- the shaft 2 uses a stainless steel wire having an outer diameter of 0.2 mm and a longitudinal length of 1800 mm, and is tapered so that the outer diameter is about 0.06 mm to ⁇ 0.15 mm from the tip to about 20 mm in the longitudinal direction. From there, the outer diameter of the shaft 2 is about 0.15 mm with a length of about 30 mm, and further, a taper shape is given so that the outer diameter is about 20 mm from that with an outer diameter of 0.15 mm to 0.2 mm. Produced.
- the shaft 2 passes through the polyimide tube that bundles the closed end portion of the filter portion 3, the opening portion, and the support member 9 so as to be coaxial, so that all the support members 9 have the same length, that is, on the central axis of the ring 7.
- the member 9 was fixed with an adhesive.
- the outer tube 4 has a three-layer structure in which the inner layer is polytetrafluoroethylene, the intermediate layer is a braided layer made of stainless steel flat wire, and the outer layer is polyimide.
- the inner diameter is 0.23 mm
- the outer diameter is 0.36 mm
- the length is 1500 mm.
- a polyimide tube having an inner diameter of 0.4 mm, an outer diameter of 0.52 mm, and a length of 5 mm was fixed to the tip of the outer tube 4 with an adhesive so that a length of 4 mm protruded, and this was used as an annular member 5.
- a polyimide tube having an inner diameter of 0.4 mm, an outer diameter of 0.52 mm, and a length of 0.5 mm was fixed to the tip of the outer tube 4 with an adhesive so that the ends of the outer tube 4 and the polyimide tube were combined.
- the annular member 5 has a total length of 2.5 mm, an inner diameter of ⁇ 0.4 mm, and an outer diameter of the portion that is not a huge portion of ⁇ 0.5 mm.
- the assembly of the outer tube 4 and the annular member 5 was arranged on the shaft 2 so that the annular member 5 was on the distal end side in the longitudinal direction, and the endovascular treatment aid 1 was produced.
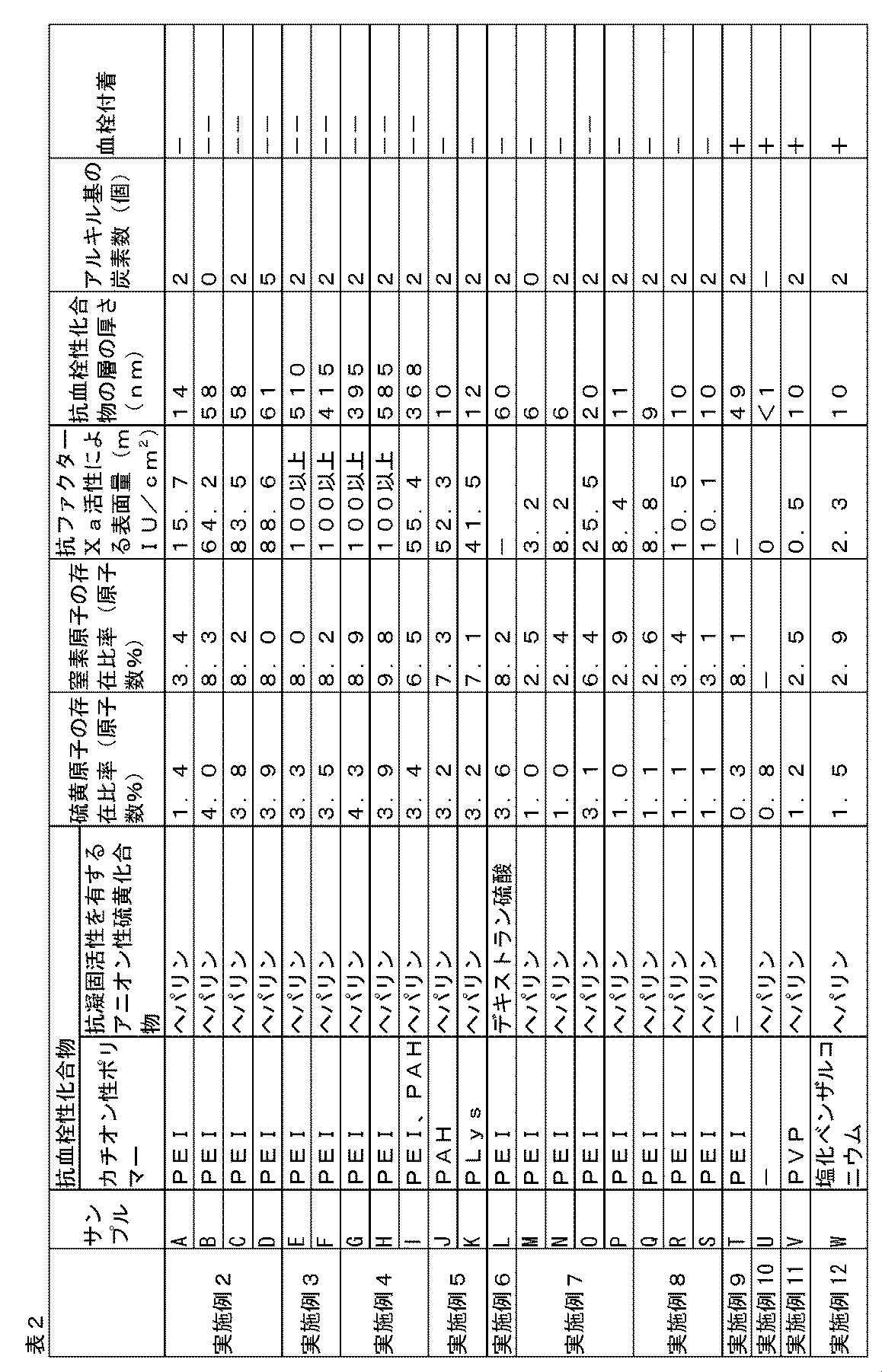
- samples A to D used for the endovascular treatment aid 1 were evaluated by a human whole blood test. The results are shown in Table 2. As shown in Table 2, in the evaluation by the human whole blood test, the sample A had no thrombus adhesion ( ⁇ ), and the samples B to D had no thrombus adhesion ( ⁇ ).
- Example 3 After performing the same operation as mesh B of Example 2 and performing the first coating step, the mesh was made of 0.5 wt% DMT-MM, 40 wt% succinic anhydride (manufactured by Wako Pure Chemical Industries, Ltd.). It was immersed in dimethylacetamide and reacted at 50 ° C. for 17 hours (first additional step). The solution after the reaction was removed and washed with methanol or distilled water.
- the mesh was immersed in an aqueous solution of 0.5 wt% DMT-MM and 5.0 wt% PEI and reacted at 30 ° C for 2 hours (second additional step).
- the aqueous solution after the reaction was removed and washed with distilled water.
- the same operation as mesh C of Example 2 was performed, and after performing a quaternary ammonium conversion step using ethyl bromide, a second coating step was performed.
- the same thing as Example 2 was used except the antithrombotic compound.
- the filter 6 produced by the mesh subjected to the second additional step with PEI (LUPASOL (registered trademark) P; manufactured by BASF) is sample E, PEI (LUPASOL (registered trademark) SK; manufactured by BASF).
- PEI (LUPASOL (registered trademark) SK; manufactured by BASF).
- the filter 6 produced with the mesh which performed 2 additional processes was made into the sample F.
- the samples E and F used for the endovascular treatment aid 1 were evaluated by a human whole blood test. The results are shown in Table 2. As shown in Table 2, there was no thrombus adhesion ( ⁇ ) in the evaluation by the human whole blood test.
- Example 4 After performing the same operation as mesh B of Example 2 and performing the first coating step, the mesh was made of 0.5 wt% DMT-MM, 0.5 wt% PAA (manufactured by Wako Pure Chemical Industries, Ltd.). It was immersed in an aqueous solution and reacted at 30 ° C. for 2 hours (first additional step). The aqueous solution after the reaction was removed and washed with an aqueous sodium carbonate solution or distilled water.
- the mesh was immersed in an aqueous solution of 0.5 wt% DMT-MM and 5.0 wt% PEI and reacted at 30 ° C for 2 hours (second additional step).
- the aqueous solution after the reaction was removed and washed with distilled water.
- the same operation as mesh C of Example 2 was performed, and after performing a quaternary ammonium conversion step using ethyl bromide, a second coating step was performed.
- the same thing as Example 2 was used except the antithrombotic compound.
- the filter 6 produced with the mesh which performed the 2nd additional process with PEI is sample G, PEI (LUPASOL (registered trademark) P; made by BASF).
- PEI LPASOL (registered trademark) P; made by BASF.
- the filter 6 produced by the mesh subjected to the second additional step in Sample H was subjected to the second additional step using Sample H, polyallylamine hydrochloride (hereinafter referred to as “PAH”) (weight average molecular weight 900,000; manufactured by Sigma-Aldrich).
- PAH polyallylamine hydrochloride
- the samples GI used for the endovascular treatment aid 1 were evaluated by a human whole blood test. The results are shown in Table 2. As shown in Table 2, there was no thrombus adhesion ( ⁇ ) in the evaluation by the human whole blood test.
- Example 5 The same operation as in Example 2 was performed, and PEI was changed to PAH (weight average molecular weight 900,000; manufactured by Sigma-Aldrich) or poly-L-lysine hydrobromide (hereinafter referred to as PLys) (weight average molecular weight 3 to 7).
- the first coating step was carried out by changing to Sigma-Aldrich.
- the same operation as mesh C of Example 2 was performed, and after performing a quaternary ammonium conversion step using ethyl bromide, a second coating step was performed. The same thing as Example 2 was used except the antithrombotic compound.
- the filter 6 produced with the mesh which changed PEI to PAH and performed the 1st coating process and produced the mesh 6 which changed the sample J and changed the PEI into PLys and carried out the 1st coating process.
- Sample K was designated. The same thing as Example 2 was used except the antithrombotic compound.
- the samples J and K used for the endovascular treatment aid 1 were evaluated by a human whole blood test. The results are shown in Table 2. As shown in Table 2, there was no thrombus adhesion ( ⁇ ) in the evaluation by the human whole blood test.
- Example 6 The same operation as mesh C of Example 2 was performed, and heparin sodium (manufactured by Organon API) was changed to dextran sodium sulfate (manufactured by Wako Pure Chemical Industries, Ltd.) to prepare a mesh that was subjected to the second coating step. Filter 6 was designated as sample L. The same thing as Example 2 was used except the antithrombotic compound.
- the sample L used for the endovascular treatment aid 1 was evaluated by a human whole blood test. The results are shown in Table 2. As shown in Table 2, there was no thrombus adhesion ( ⁇ ) in the evaluation by the human whole blood test.
- Example 7 The mesh was immersed in an aqueous solution of 5% PEI, and was covalently bonded by irradiating with 5 kGy of ⁇ rays using a JS-8500 type cobalt 60 ⁇ ray irradiation device (manufactured by Nordion International) (first coating step). . After the reaction, the aqueous solution was removed and washed with Triton-X100 (manufactured by Sigma-Aldrich), physiological saline or distilled water. The same operation as mesh C of Example 2 was performed, and after performing a quaternary ammonium conversion step using ethyl bromide, a second coating step was performed. The same thing as Example 2 was used except the antithrombotic compound.
- Triton-X100 manufactured by Sigma-Aldrich
- PEI average molecular weight of about 600; manufactured by Wako Pure Chemical Industries, Ltd.
- the filter 6 produced with a mesh that was not subjected to the quaternary ammonium conversion step was sample M, PEI (average molecular weight of about 600).
- a filter 6 produced by a mesh using LUPASOL (registered trademark) SK (made by BASF) and ethyl bromide was used as sample P.
- the samples M to P used for the endovascular treatment aid 1 were evaluated by a human whole blood test. The results are shown in Table 2. As shown in Table 2, in the evaluation by the human whole blood test, the samples M, N and P had no thrombus adhesion ( ⁇ ), and the sample O had no thrombus adhesion ( ⁇ ).
- Example 8 The mesh was immersed in an aqueous solution of 5% PEI, heated at 80 ° C. for 2 hours, and PEI was covalently bonded to the mesh by an aminolysis reaction (first coating step). The aqueous solution after the reaction was removed and washed with distilled water. The same operation as mesh C of Example 2 was performed, and after performing a quaternary ammonium conversion step using ethyl bromide, a second coating step was performed. The same thing as Example 2 was used except the antithrombotic compound.
- the filter 6 produced with the mesh which performed the 1st coating process with PEI is sample Q, PEI (LUPASOL (registered trademark) P; manufactured by BASF).
- PEI LPASOL (registered trademark) P; manufactured by BASF.
- the samples Q to S used for the endovascular treatment aid 1 were evaluated by a human whole blood test. The results are shown in Table 2. As shown in Table 2, there was no thrombus adhesion ( ⁇ ) in the evaluation by the human whole blood test.
- Example 9 The same operation as that of mesh C of Example 2 was performed, and the first coating step was performed using PEI (LUPASOL (registered trademark) P; manufactured by BASF), and the quaternary ammonium formation step was performed using ethyl bromide. Then, the filter 6 produced with the mesh which did not implement the 2nd coating process was used as the sample T. The same thing as Example 2 was used except the antithrombotic compound.
- PEI LPASOL (registered trademark) P; manufactured by BASF
- the sample T used in the endovascular treatment aid 1 was evaluated by a human whole blood test. The results are shown in Table 2. As shown in Table 2, there was (+) thrombus adhesion in the evaluation by the human whole blood test.
- Example 10 The same operation as that of the mesh C of Example 2 was performed, and the filter 6 produced using the mesh subjected to the second coating step without performing the first coating step and the quaternary ammonium conversion step using PEI was sampled. U. The same thing as Example 2 was used except the antithrombotic compound.
- the sample U used for the endovascular treatment aid 1 was evaluated by a human whole blood test. The results are shown in Table 2. As shown in Table 2, there was (+) thrombus adhesion in the evaluation by the human whole blood test.
- Example 11 The same operation as in Example 2 was performed, and PEI was changed to polyvinyl pyrrolidone (hereinafter, “PVP”) (K-90; manufactured by ISP Co.) to carry out the first coating step.
- PVP polyvinyl pyrrolidone
- the same operation as that of mesh C of Example 2 was performed, and after performing a quaternary ammonium conversion step using ethyl bromide, a filter 6 made of the mesh subjected to the second coating step was used as sample V.
- the same thing as Example 2 was used except the antithrombotic compound.
- the sample V used for the endovascular treatment aid 1 was evaluated by a human whole blood test. The results are shown in Table 2. As shown in Table 2, there was (+) thrombus adhesion in the evaluation by the human whole blood test.
- Example 12 The same operation as in Example 2 was performed, and PEI was changed to benzalkonium chloride (manufactured by Wako Pure Chemical Industries, Ltd.) to perform the first coating step.
- the same operation as that of mesh C in Example 2 was performed, and after performing a quaternary ammonium conversion step using ethyl bromide, a filter 6 made of the mesh subjected to the second coating step was used as sample W.
- the same thing as Example 2 was used except the antithrombotic compound.
- the sample W used for the endovascular treatment aid 1 was evaluated by a human whole blood test. The results are shown in Table 2. As shown in Table 2, there was (+) thrombus adhesion in the evaluation by the human whole blood test.
- evaluation 1 Human whole blood test
- the same kind of material as the filter 6 (samples A to W) to which the antithrombotic compound was bound and the untreated filter 6 (positive control) were cut into test pieces each having an effective surface area of 1.0 cm 2 and physiological saline at 37 ° C. And then immersed in a 2 mL microtube.
- Heparin sodium injection solution manufactured by Ajinomoto Pharmaceutical Co., Inc. was added to fresh human blood at 0.5 U / mL, and 2 mL of this human blood was added and incubated at 37 ° C. for 2 hours.
- the test piece was taken out and rinsed with PBS (-) (manufactured by Nissui Pharmaceutical Co., Ltd.), and the attached thrombus weight was quantified.
- the thrombus weight was obtained by measuring the dry weights of the test piece before the test and the test piece after the rinsing, respectively.
- Each sample A to W and the positive control was tested three times, and if the average value of three relative thrombus weight values calculated by the following formula 3 was 20% or more, there was a thrombus adhesion (+) If less than 20% and less than 10%, there was no thrombus adhesion, and it was determined as ( ⁇ ) and ( ⁇ ), respectively.
- the present invention can be used as an intravascular treatment assisting tool for intravascular treatment such as balloon angioplasty or stent placement using a balloon catheter or stent.
- SYMBOLS 1 Endovascular treatment auxiliary tool, 2 ... Shaft, 3 ... Filter part, 4 ... Outer tube, 5 ... Ring member, 6 ... Filter, 7 ... Ring, 8 ... Coil, 9 ... Support member, 10 ... Dividing point, 11 ... Tube, 12 ... Gauze, 13 ... Fine particles
Abstract
Description
上記シャフトの長手方向における先端側で閉止端部となり、かつ、上記長手方向における基端側で開口部となるように上記シャフトに固定され、弾性復元力を有するリングが上記開口部に固定され、開いている時には上記リングを底面として円錐状の形状となる、傘状に開閉可能なフィルターと、
上記リングと上記シャフトの一部とを繋ぐようにそれぞれに固定され、かつ、上記長手方向における基端側に外力を加えることで生じる張力によって上記フィルターを閉じることを可能にする線状の部材からなる支持部材と、
を備え、
上記リングには、放射線不透過材料で形成されたコイルが巻かれ、
上記フィルターが閉じられた時、上記リングは、上記長手方向における先端側を向く複数の山と上記長手方向における基端側を向く複数の谷とが交互に生じ、かつ、上記山同士及び上記谷同士が近接した形状となるとともに、上記コイルは、上記リング上の支持部材により固定される位置を含み、かつ、上記山の頂点と上記谷の頂点の位置を含まないように上記リング上に配置された血管内治療補助具。
装置 :ESCALAB220iXL(VG Scientific社製)
励起X線 :monochromaticAlKα1,2線(1486.6eV)
X線径 :1mm
X電子脱出角度 :90°(フィルター6の表面に対する検出器の傾き)
分割ratio : 各分割ピーク成分の存在比率(%)
N1sratio : 全原子の存在量に対する窒素原子の存在比率(%)
分割percent : N1sピークにおける各分割ピーク成分の存在比率(%)
分割ratio : 各分割ピーク成分の存在比率(%)
C1sratio : 全原子の存在量に対する炭素原子の存在比率(%)
分割percent : C1sピークにおける各分割ピーク成分の存在比率(%)
装置 :電界放出型透過電子顕微鏡JEM-2100F(JEOL社製)
EELS検出器 :GIF Tridiem(GATAN社製)
EDX検出器 :JED-2300T(JEOL社製)
画像取得 :Digital Micrograph(GATAN社製)
試料調整 :超薄切片法(銅製マイクログリッドに懸架し、包埋樹脂はアクリル系樹脂を使用。)
加速電圧 :200kV
ビーム径 :直径0.7nm
エネルギー分解能 :約1.0eVFWHM
図1に示す、本発明の実施形態に係る血管内治療補助具1を作製した。具体的には、フィルター6を、線径φ28μmのモノフィラメントのポリエステル(PET)繊維で開孔サイズが1辺100μmとなるようにメッシュで構成し、このメッシュを長手方向の長さ10mm程度、フィルター開口部の円径がφ6mmとなるように作製した。
比較例1として、コイル8を用いず、リング7上にコイル8が固定されない点以外は全く同様にして作製された血管内治療補助具を作製した。
シャフト上に支持部材が固定されており、支持部材がフィルター部のリングを形成し、そのリング上には放射線不透過材料で形成された金属コイルがほぼ全周に渡って取り付けられ、リングにはウレタン製のシート状の複数の開孔のあるフィルターが固定されており、フィルターの先端はシャフトの先端側で封止されて取り付けて構成されているBoston Scientific社の血栓捕捉カテーテルであるFilterWire EZ(登録商標)を比較例2とした。比較例2は、リング径が約φ6mm、シャフト長1900mm、シャフト径φ0.36mmの、血管内治療補助具であった。
比較例3として、コイル8をリング7上のほぼ全周に渡り固定した以外は、実施例と同様に作製された血管内治療補助具を作製した。
体重35kgの豚を用いた動物実験にて、放射線装置OEC9800Plus(GE Medical Systems)を使用して、実施例及び比較例1、比較例2及び比較例3の造影性の比較実験を行った。結果として、実施例、比較例2及び比較例3は、フィルター部が明確に観察出来たことに対し、比較例1はフィルター部の確認が出来なかった。
図4の微粒子の捕捉率を比較する実験モデルの模式図に示すように、内径φ5mmのチューブ11を用意し、その中に水を通過させる。チューブ11の先にはガーゼ12を用意しておき、チューブ11を45度程度に湾曲させ、湾曲させた頂点に実施例及び比較例1、比較例2、比較例3のそれぞれを送達シースに収納してから目的の留置部まで送達し、目的の留置部に送達後、送達シースを抜去してフィルター部をチューブ11内に展開留置し、チューブ11内にφ150μmの微粒子13を4000個程度流す。そして、血管内治療補助具の回収操作を行い、流した微粒子の総数と、漏洩した微粒子の数から、微粒子の捕捉率を比較する実験を行った。結果として、実施例及び比較例1では、微粒子の捕捉率が99%以上であったのに対し、比較例2では92%程度であり、比較例3では88%程度となった。
図1に示す、本発明の実施形態に係る血管内治療補助具1を作製した。具体的には、線径φ28μmのモノフィラメントのポリエステル(PET)繊維で開孔サイズが1辺100μmとなるようにメッシュを作製した。
実施例2のメッシュBと同様の操作を行い、第1の被覆工程を実施した後、メッシュを0.5重量%DMT-MM、40重量%無水コハク酸(和光純薬工業株式会社製)のジメチルアセトアミドに浸漬し、50℃で17時間反応させた(第1の追加工程)。反応後の溶液を除去し、メタノールや蒸留水で洗浄した。
実施例2のメッシュBと同様の操作を行い、第1の被覆工程を実施した後、メッシュを0.5重量%DMT-MM、0.5重量%PAA(和光純薬工業株式会社製)の水溶液に浸漬し、30℃で2時間反応させた(第1の追加工程)。反応後の水溶液を除去し、炭酸ナトリウム水溶液や蒸留水で洗浄した。
実施例2と同様の操作を行い、PEIをPAH(重量平均分子量90万;シグマ-アルドリッチ社製)、もしくはポリ-L-リシン臭化水素酸塩(以下、PLys)(重量平均分子量3~7万;シグマ-アルドリッチ社製)に変更して第1の被覆工程を実施した。実施例2のメッシュCと同様の操作を行い、臭化エチルを用いて第4級アンモニウム化工程を実施した後、第2の被覆工程を実施した。抗血栓性化合物以外は、実施例2と同様のものを用いた。
実施例2のメッシュCと同様の操作を行い、ヘパリンナトリウム(Organon API社製)をデキストラン硫酸ナトリウム(和光純薬工業株式会社製)に変更して第2の被覆工程を実施したメッシュにより作製したフィルター6をサンプルLとした。抗血栓性化合物以外は、実施例2と同様のものを用いた。
メッシュを5%PEIの水溶液に浸漬し、JS-8500型コバルト60γ線照射装置(ノーディオン・インターナショナル社製)を使用して5kGyのγ線を照射し共有結合させた(第1の被覆工程)。反応後の水溶液を除去し、Triton-X100(シグマ-アルドリッチ社製)、生理食塩水や蒸留水で洗浄した。実施例2のメッシュCと同様の操作を行い、臭化エチルを用いて第4級アンモニウム化工程を実施した後、第2の被覆工程を実施した。抗血栓性化合物以外は、実施例2と同様のものを用いた。
メッシュを5%PEIの水溶液に浸漬し、80℃で2時間加熱し、メッシュにPEIをアミノリシス反応により共有結合させた(第1の被覆工程)。反応後の水溶液を除去し、蒸留水で洗浄した。実施例2のメッシュCと同様の操作を行い、臭化エチルを用いて第4級アンモニウム化工程を実施した後、第2の被覆工程を実施した。抗血栓性化合物以外は、実施例2と同様のものを用いた。
実施例2のメッシュCと同様の操作を行い、PEI(LUPASOL(登録商標) P;BASF社製)を用いて第1の被覆工程、臭化エチルを用いて第4級アンモニウム化工程を実施した後、第2の被覆工程を実施しなかったメッシュにより作製したフィルター6をサンプルTとした。抗血栓性化合物以外は、実施例2と同様のものを用いた。
実施例2のメッシュCと同様の操作を行い、PEIを用いた第1の被覆工程と第4級アンモニウム化工程を実施せず、第2の被覆工程を実施したメッシュにより作製したフィルター6をサンプルUとした。抗血栓性化合物以外は、実施例2と同様のものを用いた。
実施例2と同様の操作を行い、PEIをポリビニルピロリドン(以下、「PVP」)(K-90;ISP社製)に変更して第1の被覆工程を実施した。実施例2のメッシュCと同様の操作を行い、臭化エチルを用いて第4級アンモニウム化工程を実施した後、第2の被覆工程を実施したメッシュにより作製したフィルター6をサンプルVとした。抗血栓性化合物以外は、実施例2と同様のものを用いた。
実施例2と同様の操作を行い、PEIを塩化ベンザルコニウム(和光純薬工業株式会社製)に変更して第1の被覆工程を実施した。実施例2のメッシュCと同様の操作を行い、臭化エチルを用いて第4級アンモニウム化工程を実施した後、第2の被覆工程を実施したメッシュにより作製したフィルター6をサンプルWとした。抗血栓性化合物以外は、実施例2と同様のものを用いた。
抗血栓性化合物を結合したフィルター6(サンプルA~W)及び未処理のフィルター6と同種の材料(陽性対照)をそれぞれ有効表面積1.0cm2の試験片にカットし、37℃の生理食塩水で30分間浸漬してから2mLのマイクロチューブに入れた。ヒト新鮮血に0.5U/mLとなるようにヘパリンナトリウム注射液(味の素製薬株式会社製)を添加した後、このヒト血液を2mL添加し、37℃で2時間インキュベートした。インキュベート後に試験片を取り出し、PBS(-)(日水製薬株式会社製)でリンスした後、付着した血栓重量を定量した。血栓重量は、試験前の試験片とリンス後の試験片の乾燥重量をそれぞれ測定し、その差によって求めた。各サンプルA~Wおよび陽性対照についてそれぞれ試験を3回実施し、以下の式3により算出した血栓重量の相対値の3回の平均値が20%以上であれば血栓付着は有りとして(+)、20%未満、10%未満であれば血栓付着は無しとしてそれぞれ(-)、(--)と判定した。
Bt : 抗血栓性化合物を結合したフィルター6の血栓重量
Bp : 陽性対照の血栓重量
体重35kgの豚を用いた動物実験にて、放射線装置OEC9800Plus(GE Medical Systems)を使用して、実施例2の造影性の実験を行った。
図4の微粒子の捕捉率を比較する実験モデルの模式図に示すように、内径φ5mmのチューブ11を用意し、その中に水を通過させる。チューブ11の先にはガーゼ12を用意しておき、チューブ11を45度程度に湾曲させ、湾曲させた頂点に実施例2を送達シースに収納してから目的の留置部まで送達し、目的の留置部に送達後、送達シースを抜去してフィルター部をチューブ11内に展開留置し、チューブ11内にφ150μmの微粒子13を4000個程度流す。そして、血管内治療補助具の回収操作を行い、流した微粒子の総数と、漏洩した微粒子の数から、微粒子の捕捉率を測定する実験を行った。結果を表1に示す。なお、表1には、上記比較例1~3についての結果も併せて示す。
Claims (10)
- 可撓性のシャフトと、
前記シャフトの長手方向における先端側で閉止端部となり、かつ、前記長手方向における基端側で開口部となるように前記シャフトに固定され、弾性復元力を有するリングが前記開口部に固定され、開いている時には前記リングを底面として円錐状の形状となる、傘状に開閉可能なフィルターと、
前記リングと前記シャフトの一部とを繋ぐようにそれぞれに固定され、かつ、前記長手方向における基端側に外力を加えることで生じる張力によって前記フィルターを閉じることを可能にする線状の部材からなる支持部材と、
を備え、
前記リングには、放射線不透過材料で形成されたコイルが巻かれ、
前記フィルターが閉じられた時、前記リングは、前記長手方向における先端側を向く複数の山と前記長手方向における基端側を向く複数の谷とが交互に生じ、かつ、前記山同士及び前記谷同士が近接した形状となるとともに、前記コイルは、前記リング上の支持部材により固定される位置を含み、かつ、前記山の頂点と前記谷の頂点の位置を含まないように前記リング上に配置された血管内治療補助具。 - 前記フィルターの開口部と前記リングとの間がエラストマー材料により固定されている、請求項1記載の血管内治療補助具。
- 前記コイルと前記リングとの間がエラストマー材料により固定されている、請求項1又は2記載の血管内治療補助具。
- アルキレンイミン、ビニルアミン、アリルアミン、リジン、プロタミン及びジアリルジメチルアンモニウムクロライドからなる群から選択される少なくとも1種の化合物を構成モノマーとして含むカチオン性ポリマーが前記フィルターに共有結合しており、抗凝固活性を有するアニオン性硫黄化合物が、前記フィルター及び/又は前記カチオン性ポリマーに結合している、請求項1~3のいずれか一項記載の血管内治療補助具。
- X線光電子分光法(XPS)で測定した前記フィルターの表面の全原子の存在量に対する窒素原子の存在比率が、7.0~12.0原子数%である請求項1~4のいずれか一項記載の血管内治療補助具。
- X線光電子分光法(XPS)で測定した前記フィルターの表面の全原子の存在量に対する硫黄原子の存在比率が、3.0~6.0原子数%である、請求項1~5のいずれか一項記載の血管内治療補助具。
- 前記抗凝固活性を有するアニオン性硫黄化合物は、ヘパリン及びヘパリン誘導体から成る群より選ばれる少なくとも1種である、請求項1~6のいずれか一項記載の血管内治療補助具。
- 37℃の生理食塩水に30分間浸漬した後の前記フィルターにおける、抗ファクターXa活性による前記抗凝固活性を有するアニオン性硫黄化合物の表面量が30mIU/cm2以上である、請求項1~7のいずれか一項記載の血管内治療補助具。
- 前記フィルターの表面に前記カチオン性ポリマーと前記抗凝固活性を有するアニオン性硫黄化合物により形成される抗血栓性化合物の層の厚さが、1~600nmである、請求項1~8のいずれか一項記載の血管内治療補助具。
- 前記フィルターは、ポリエステルで形成される、請求項1~9のいずれか一項記載の血管内治療補助具。
Priority Applications (6)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CA2947823A CA2947823C (en) | 2014-05-09 | 2015-05-08 | Endovascular treatment aid |
| EP15789105.2A EP3141213B1 (en) | 2014-05-09 | 2015-05-08 | Endovascular treatment aid |
| JP2016517936A JP6602292B2 (ja) | 2014-05-09 | 2015-05-08 | 血管内治療補助具 |
| US15/308,387 US10098725B2 (en) | 2014-05-09 | 2015-05-08 | Endovascular treatment aid |
| CN201580024290.6A CN106456307B (zh) | 2014-05-09 | 2015-05-08 | 血管内治疗辅助工具 |
| KR1020167028454A KR102370117B1 (ko) | 2014-05-09 | 2015-05-08 | 혈관내 치료 보조구 |
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2014097540 | 2014-05-09 | ||
| JP2014-097540 | 2014-05-09 | ||
| JP2014-154889 | 2014-07-30 | ||
| JP2014154889 | 2014-07-30 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2015170733A1 true WO2015170733A1 (ja) | 2015-11-12 |
Family
ID=54392581
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2015/063266 WO2015170733A1 (ja) | 2014-05-09 | 2015-05-08 | 血管内治療補助具 |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US10098725B2 (ja) |
| EP (1) | EP3141213B1 (ja) |
| JP (1) | JP6602292B2 (ja) |
| KR (1) | KR102370117B1 (ja) |
| CN (1) | CN106456307B (ja) |
| CA (1) | CA2947823C (ja) |
| TW (1) | TWI660721B (ja) |
| WO (1) | WO2015170733A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2022044755A (ja) * | 2016-03-23 | 2022-03-17 | アビオメド オイローパ ゲーエムベーハー | フィルタを備えた血液ポンプ |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2018168832A1 (ja) * | 2017-03-13 | 2018-09-20 | 東レ株式会社 | フィルターデバイス |
| KR102081902B1 (ko) * | 2017-08-14 | 2020-02-26 | 사회복지법인 삼성생명공익재단 | 결석 분쇄에 이용될 수 있는 결석 고정 장치 |
| CN109009592B (zh) * | 2018-06-19 | 2021-06-25 | 西安交通大学医学院第二附属医院 | 颈内动脉一体式释放伞状保护支架 |
| CN110680459A (zh) * | 2019-11-08 | 2020-01-14 | 刘昌伟 | 应用于动、静脉血栓的取栓装置 |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2003505216A (ja) * | 1999-07-30 | 2003-02-12 | インセプト エルエルシー | 塞栓、血栓及び異物の除去用脈管装置並びに使用方法 |
| JP4073869B2 (ja) * | 2001-09-28 | 2008-04-09 | 寛治 井上 | 遊離血栓捕獲器具 |
| JP4680201B2 (ja) * | 2003-11-06 | 2011-05-11 | ボストン サイエンティフィック リミテッド | 平板化されたチップフィルタワイヤ設計 |
| WO2012176841A1 (ja) * | 2011-06-24 | 2012-12-27 | 東レ株式会社 | 遊離血栓捕獲器具 |
| WO2013047623A1 (ja) * | 2011-09-27 | 2013-04-04 | Inoue Kanji | 血管内遊離物捕獲器具 |
| WO2015080177A1 (ja) * | 2013-11-28 | 2015-06-04 | 東レ株式会社 | 抗血栓性材料 |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS6041947B2 (ja) * | 1977-12-09 | 1985-09-19 | ユニチカ株式会社 | ポリエステル成形体表面に抗血栓性を付与する方法 |
| US5182317A (en) * | 1988-06-08 | 1993-01-26 | Cardiopulmonics, Inc. | Multifunctional thrombo-resistant coatings and methods of manufacture |
| US5769816A (en) * | 1995-11-07 | 1998-06-23 | Embol-X, Inc. | Cannula with associated filter |
| JP2854284B2 (ja) * | 1996-02-15 | 1999-02-03 | 株式会社人工血管技術研究センター | 抗血栓性人工血管 |
| US6530939B1 (en) | 1999-07-30 | 2003-03-11 | Incept, Llc | Vascular device having articulation region and methods of use |
| US20030187495A1 (en) | 2002-04-01 | 2003-10-02 | Cully Edward H. | Endoluminal devices, embolic filters, methods of manufacture and use |
| US7195648B2 (en) * | 2002-05-16 | 2007-03-27 | Cordis Neurovascular, Inc. | Intravascular stent device |
| US7252675B2 (en) | 2002-09-30 | 2007-08-07 | Advanced Cardiovascular, Inc. | Embolic filtering devices |
| WO2006111943A1 (en) * | 2005-04-18 | 2006-10-26 | Salviac Limited | An embolic protection device |
| US7718106B2 (en) * | 2006-05-30 | 2010-05-18 | Boston Scientific Scimed, Inc. | Medical devices and related systems and methods |
| WO2008005898A2 (en) | 2006-06-30 | 2008-01-10 | Ev3 Endovascular, Inc. | Medical devices with amorphous metals and methods therefor |
| JP4483835B2 (ja) | 2006-08-01 | 2010-06-16 | ニプロ株式会社 | 血栓捕捉部材回収用シースおよび血栓捕捉カテーテル |
| US20130096606A1 (en) | 2011-10-17 | 2013-04-18 | William C. Bruchman | Embolic protection devices and related systems and methods |
-
2015
- 2015-05-08 KR KR1020167028454A patent/KR102370117B1/ko active IP Right Grant
- 2015-05-08 CN CN201580024290.6A patent/CN106456307B/zh not_active Expired - Fee Related
- 2015-05-08 JP JP2016517936A patent/JP6602292B2/ja active Active
- 2015-05-08 WO PCT/JP2015/063266 patent/WO2015170733A1/ja active Application Filing
- 2015-05-08 CA CA2947823A patent/CA2947823C/en active Active
- 2015-05-08 EP EP15789105.2A patent/EP3141213B1/en active Active
- 2015-05-08 TW TW104114651A patent/TWI660721B/zh not_active IP Right Cessation
- 2015-05-08 US US15/308,387 patent/US10098725B2/en active Active
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2003505216A (ja) * | 1999-07-30 | 2003-02-12 | インセプト エルエルシー | 塞栓、血栓及び異物の除去用脈管装置並びに使用方法 |
| JP4073869B2 (ja) * | 2001-09-28 | 2008-04-09 | 寛治 井上 | 遊離血栓捕獲器具 |
| JP4680201B2 (ja) * | 2003-11-06 | 2011-05-11 | ボストン サイエンティフィック リミテッド | 平板化されたチップフィルタワイヤ設計 |
| WO2012176841A1 (ja) * | 2011-06-24 | 2012-12-27 | 東レ株式会社 | 遊離血栓捕獲器具 |
| WO2013047623A1 (ja) * | 2011-09-27 | 2013-04-04 | Inoue Kanji | 血管内遊離物捕獲器具 |
| WO2015080177A1 (ja) * | 2013-11-28 | 2015-06-04 | 東レ株式会社 | 抗血栓性材料 |
Non-Patent Citations (1)
| Title |
|---|
| See also references of EP3141213A4 * |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2022044755A (ja) * | 2016-03-23 | 2022-03-17 | アビオメド オイローパ ゲーエムベーハー | フィルタを備えた血液ポンプ |
| US11833278B2 (en) | 2016-03-23 | 2023-12-05 | Abiomed Europe Gmbh | Blood pump with filter |
Also Published As
| Publication number | Publication date |
|---|---|
| EP3141213A4 (en) | 2018-01-10 |
| JPWO2015170733A1 (ja) | 2017-04-20 |
| CN106456307B (zh) | 2019-03-22 |
| US20170065397A1 (en) | 2017-03-09 |
| CN106456307A (zh) | 2017-02-22 |
| CA2947823A1 (en) | 2015-11-12 |
| KR20170007252A (ko) | 2017-01-18 |
| EP3141213B1 (en) | 2018-10-10 |
| EP3141213A1 (en) | 2017-03-15 |
| JP6602292B2 (ja) | 2019-11-06 |
| TWI660721B (zh) | 2019-06-01 |
| US10098725B2 (en) | 2018-10-16 |
| CA2947823C (en) | 2021-11-23 |
| TW201544083A (zh) | 2015-12-01 |
| KR102370117B1 (ko) | 2022-03-04 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| WO2015170732A1 (ja) | 血管内治療補助具 | |
| JP6602292B2 (ja) | 血管内治療補助具 | |
| EP1965842B1 (en) | Medical devices having multiple charged layers | |
| JP6435863B2 (ja) | 抗血栓性材料 | |
| US8784473B2 (en) | Endoprosthesis with filament repositioning or retrieval member and guard structure | |
| CA2638218A1 (en) | Medical articles having enhanced therapeutic agent binding | |
| US8585752B2 (en) | Stent and stent delivery system | |
| US20110282437A1 (en) | Endoprosthesis | |
| CA3066882C (en) | Filter device | |
| JP2001058010A (ja) | カテーテル |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 15789105 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2016517936 Country of ref document: JP Kind code of ref document: A |
|
| ENP | Entry into the national phase |
Ref document number: 20167028454 Country of ref document: KR Kind code of ref document: A |
|
| ENP | Entry into the national phase |
Ref document number: 2947823 Country of ref document: CA |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 15308387 Country of ref document: US |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| REEP | Request for entry into the european phase |
Ref document number: 2015789105 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2015789105 Country of ref document: EP |