Fluortenside
Gegenstand der vorliegenden Erfindung sind neue Verbindungen mit fluorierten Endgruppen, deren Verwendung als oberflächenaktive
Substanzen und Mittel enthaltend diese Verbindungen.
Fluorhaltige Tenside besitzen aufgrund ihrer speziellen Oberflächenaktivität einzigartige Anwendungseigenschaften. Fluortenside, deren statische Oberflächenspannung sehr niedrig ist (16-20 mN/m), sind in
verschiedensten Anwendungen einsetzbar und tragen z.B. zur
verbesserten Benetzung von Oberflächen bei. So werden sie z.B. als Grenzflächenvermittler bzw. Emulgator oder Viskositätsminderer in Farben, Lacken oder Klebstoffen verwendet. Klassische Fluortenside sind aus langkettigen, perfluorierten Alkylketten (C6-C8) aufgebaut und gelten potentiell als bioakkumulativ und toxisch. In der Regel enthalten Fluortenside jedoch Perfluoralkylsubstituenten, die in der Umwelt durch biologische und andere Oxidationsprozesse zu
Perfluoralkancarbonsäuren und -sulfonsäuren abgebaut werden. Diese gelten als persistent und stehen z. T. im Verdacht gesundheitliche Schäden zu verursachen (G. L. Kennedy, Jr., J. L. Butenhoff, G. W. Olsen, J. C. O'Connor, A. M. Seacat, R. G. Perkins, L. B. Biegel, S. R. Murphy, D. G. Farrar, Critical Reviews in Toxicology 2004, 34, 351-384). Längerkettige Perfluoralkancarbonsäuren und -sulfonsäuren reichern sich zudem in der Nahrungskette an. Kürzerkettige Fluorbausteine sind von ihrem
ökotoxikologischem Profile günstiger, zeigen jedoch in ihren
Anwendungsbereichen oft schlechtere Eigenschaften.
In WO 03/010128 werden Perfluoralkyl-substituierte Amine, Säuren, Aminosäuren und Thioethersäuren beschrieben, die eine C3-20- Perfluoralkyl-Gruppe aufweisen. Aus JP-A-2001/133984 sind
oberflächenaktive Verbindungen mit Perfluoralkoxy-Ketten bekannt, die
BESTÄTIGUNGSKOPIE
sich zum Einsatz in Antireflex-Beschichtungen eignen. Aus JP-A-09/111286 ist die Verwendung von Perfluorpolyethertensiden in Emulsionen bekannt. In WO 2006/072401 und WO 2010/003567 werden oberflächenaktive Verbindungen mit Trifluormethoxygruppen beschrieben. Verbindungen mit speziellen Fluoralkylgruppen sind in US 7,635,789, US 2008/0093582, JP 2004-18394 und WO 2010/002623 beschrieben. Teilfluorierte
Verbindungen sind in US 7,737,307, EP 1 522 536 und WO 2010/002622 beschrieben. Spezielle Anwendungen von Sulfosuccinaten und/oder Sulfotricarballylaten mit verschiedenen fluorierten Seitenketten sind in US 4,968,599 und US 4,988,610 sowie US 6, 890, 608 beschrieben und in A.R. Pitt et al., Colloids and Surfaces A: Physicochemical and Engineering Aspects, 1996, 114, 321-335; A.R. Pitt, Progr. Colloid Polym. Sei, 1997, 103, 307-317 und Z.-T. Liu et al., Ind. Eng. Chem. Res. 2007, 46, 22-28. Weitere Fluortenside, insbesondere Succinate und Tricarballylate mit fluorierten Alkylgruppen, sind in WO 2009/149807, WO 2010/003567, WO 2010/149262, WO
2011/082770 und WO 2012/084118 beschrieben. Weiterhin besteht Bedarf nach alternativen oberflächenaktiven Substanzen, die vorzugsweise beim Abbau nicht zu langkettigen persistenten
Verbindungen abbauen.
Es wurden nun neue Verbindungen gefunden, die als oberflächenaktive Substanzen geeignet sind und bevorzugt einen oder mehrere der o.g.
Nachteile nicht aufweisen.
Ein erster Gegenstand der vorliegenden Erfindung sind Verbindungen der Formel (I)
ZnSpacerXx (I)
wobei
Z = Rf-Oo1-A1 a1-Oo2-A2a2-Oo3-Bb- n = 1 , 2, 3,4, 5 oder 6, bevorzugt 2-4, insbesondere 2-3, Rf = fluoriertes Alkyl, linear oder verzweigt, bevorzugt fluoriertes C1-C6- Alkyl, besonders bevorzugt perfluoriertes C1-C4-Alkyl, insbesondere perfluoriertes C1-C3-Alkyl,
A1 und A2 = unabhängig voneinander -(CF2)- oder -(CF(CF3)-CF2)- oder -(CF2-O)- oder -(CF2-CF2)-O-,
ai und a2 = unabhängig voneinander 0-4,
B = -CHF-CF2-Y-(CH2)m- Y = O oder S, bevorzugt O,
b = 1 ,
m = 0 oder 1 ,
Spacer = eine gesättigte oder ungesättigte, verzweigte oder unverzweigte, ggf. Heteroatome enthaltende, Kohlenwasserstoffeinheit,
X eine hydrophile Gruppe ist,
x = 1 , 2, 3 oder 4, bevorzugt 1 , o1 , o2 und o3 = unabhängig voneinander 0 oder 1 , wobei alle Indizes so gewählt sind, dass keine -O-O-Bindungen vorliegen.
Wenn X = -OH, -OAlkyl, -COOH oder -COOAlkyl ist, dann ist n bevorzugt 2- 4, insbesondere 2-3.
Wenn X = -SO3H oder -SO3" ist, dann ist Z bevorzugt nicht über eine -OCO- Bindung an den Spacer gebunden.
Bei den Kohlenwasserstoff-Einheiten des Spacers der Verbindungen der Formel (I) kann es sich um aliphatische oder aromatische, gegebenenfalls mit Heteroatomen versehene Einheiten handeln. Vorzugsweise ist die Gruppe Z in den oberflächenaktiven Verbindungen dabei an eine
gesättigte, verzweigte oder unverzweigte Kohlenwasserstoff-Einheit, bevorzugt an eine gesättigte, verzweigte oder unverzweigte Alkylengruppe, wobei ein oder mehrere nicht benachbarte C-Atome durch O oder N, bevorzugt O, ersetzt sein können, gebunden. Bevorzugt sind z. B. C1-C6- Alkylengruppen, insbesondere C1-C4-Alkylengruppen. In einer
Erfindungsvariante wird als bevorzugte Heteroatome enthaltende
Kohlenwasserstoffeinheit eine Polyethylen- oder Polypropylenglykoleinheit verwendet.
In einer Erfindungsvariante kommt die Gruppe Z in der oberflächenaktiven Verbindung mehrfach vor, bevorzugt zweimal oder dreimal. In einer anderen Erfindungsvariante kommt die Gruppe Z in der oberflächenaktiven Verbindung nur einmal vor. In einer Erfindungsvariante können
Verbindungen der Formel (I) verschiedene Gruppe Z enthalten.
Bevorzugt sind Verbindungen der Formel (I) in denen n = 2-3 und x = 1 ist.
Bevorzugt sind Verbindungen der Formel (I) in denen Z gleich:
Rf-CHF-CF2-Y-(CH2)m- oder
Rf-O-CHF-CF2-Y-(CH2)m- oder
Rf-0-(CF2)i-4-CHF-CF2-Y-(CH2)m- oder
Rf-0-(CF2)i-4-O-CHF-CF2-Y-(CH2)m- oder
Rf-0-(CF(CF3)-CF2)i-4-CHF-CF2-Y-(CH2)m- oder
Rf-0-(CF(CF3)-CF2)i-4-O-CHF-CF2-Y-(CH2)m- oder
Rf-0-(CF2-O)i-4-CHF-CF2-Y-(CH2)m- oder
Rf-0-(CF2-CF2-O)i-4-CHF-CF2-Y-(CH2)m- oder
Rf-0-(CF2-O)i-4-(CF2-CF2-O)i-4-CHF-CF2-Y-(CH2)m- ist mit m = 0 oder 1.
Insbesondere bevorzugt sind Verbindungen der Formel (I) in denen Z gleich:
Rf-CHF-CF2-Y-(CH2)m- oder
Rf-0-CHF-CF2-Y-(CH2)m- oder
Rf-O-(CF2)i-4-CHF-CF2-Y-(CH2)m- oder
Rf-O-(CF2)i-4-0-CHF-CF2-Y-(CH2)m- ist.
Vor allem Verbindungen der Formel (I) mit Z = Rf-O-CHF-CF2-Y-(CH2)m- oder Rf-O-(CF2)i-4-O-CHF-CF2-Y-(CH2)m- sind bevorzugt. Bevorzugt sind Verbindungen der Formel (I) in denen Rf gleich:
CF3- oder CF3-CF2- oder CF3-CF2-CF2- ist.
Im Besonderen sind Verbindungen der Formel (I) bevorzugt, in denen n =
2-3, x = 1 , der Spacer eine gesättigte, verzweigte oder unverzweigte Kohlenwasserstoff-Einheit ist, Rf gleich CF3-, CF3-CF2- oder CF3-CF2-CF2- ist und Z gleich:
Rf-CHF-CF2-Y-(CH2)m- oder
Rf-0-CHF-CF2-Y-(CH2)m- oder
Rf-0-(CF2)i-4-CHF-CF2-Y-(CH2)m- oder
R^-(CF2)i-4-O-CHF-CF2-Y-(CH2)m- oder
Rf-0-(CF(CF3)-CF2)i-4-CHF-CF2-Y-(CH2)m- oder
Rt-0--(CF(C F3)-C F2)i -4-O-C H F-CF2-Y-(C H2)m- oder
Rf-0-(CF2-O)i-4-CHF-CF2-Y-(CH2)m- oder
Rf-O-(CF2-CF2-0)i-4-CHF-CF2-Y-(CH2)m- oder
Rf-0-(CF2-O)i-4-(CF2-CF2-O)i-4-CHF-CF2-Y-(CH2)m- ist mit m = 0 oder 1.
Insbesondere bevorzugt sind hierbei Verbindungen, in denen Z gleich:
Rf-CHF-CF2-Y-(CH2)m- oder
Rf-0-CHF-CF2-Y-(CH2)m- oder
Rf-0-(CF2)i-4-CHF-CF2-Y-(CH2)m- oder
Rf-O-(CF2)i-4-O-CHF-CF2-Y-(CH2)m- ist, vor allem Verbindungen mit Z = Rf-
0-CHF-CF2-Y-(CH2)m- oder Rf-0-(CF2)i-4-O-CHF-CF2-Y-(CH2)m-.
Besonders bevorzugt sind Verbindungen in denen die genannten
Variablen, insbesondere alle Variablen, die bevorzugten Bedeutungen, insbesondere die besonders bevorzugten Bedeutungen, haben.
In den erfindungsgemäßen Verbindungen ist X eine hydrophile Gruppe, bevorzugt eine anionische, kationische, nicht-ionische oder amphotere Gruppe. Eine bevorzugte anionische Gruppe X kann ausgewählt sein aus
-COO-, -SO3-, -OSOs", -PO32-, -OPOs2-, -(OCH2CH2)s-0-(CH2)t-COO-
, -(OCH2CH2)s-O-(CH2)t -SOs-, -(OCH2CH2)s-O-(CH2)t-OS03-
, -(OCH2CH2)s-O-(CH2)t-PO3 2-, -(OCH2CH2)s-O-(CH2)t-OP03 2- oder aus den
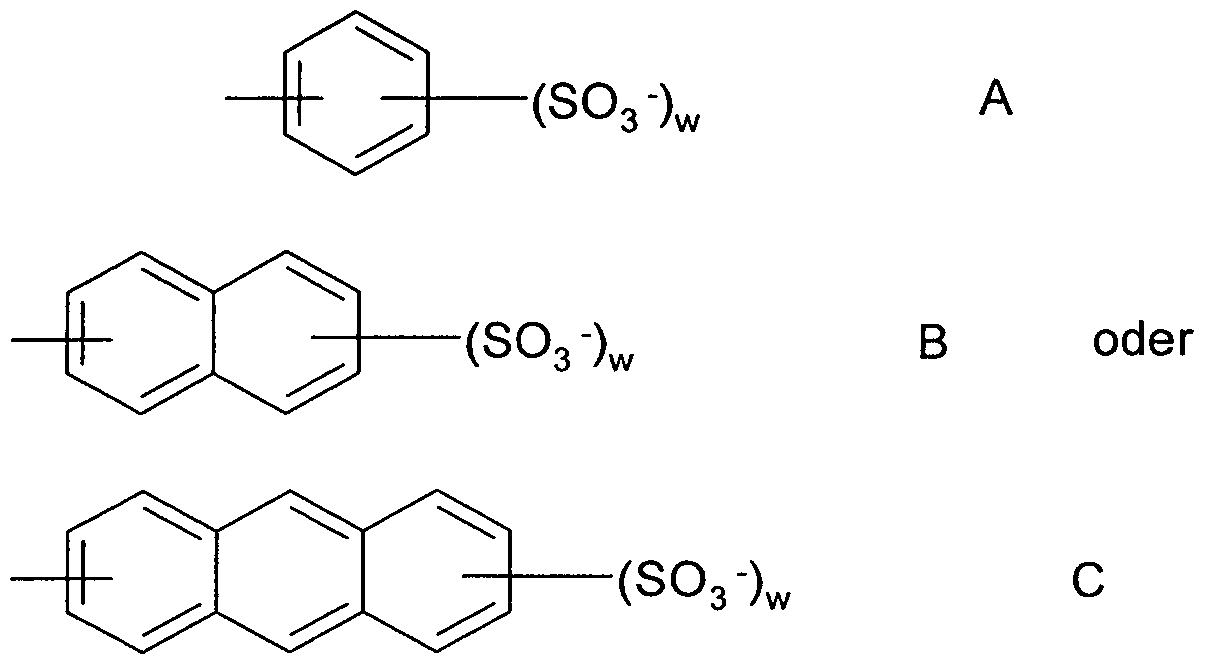
Formeln A bis C,
wobei s steht für eine ganze Zahl aus dem Bereich von 1 bis 1000, t steht für eine ganze Zahl ausgewählt aus 1 , 2, 3 oder 4 und w steht für eine ganze Zahl ausgewählt aus 1 , 2 oder 3.
Zu den bevorzugten anionischen Gruppen gehören dabei
insbesondere -COO", -S03 ", -OS03-, -PO3 2", -OPO3 2", die Teilformel A, sowie -(OCH2CH2)s-O-(CH2)t-COO-, -(OCH2CH2)s-O-(CH2)t-SO3- und -(OCH2CH2)s-0-(CH2)t-OS03 ", wobei jede einzelne dieser Gruppen für sich genommen bevorzugt sein kann.
Zu den ganz besonders bevorzugten anionischen Gruppen gehören dabei -SOs", -OSO3", -COO", -PO32-, oder OPO3 2". Insbesondere eine
Sulfonatgruppe -SO3" ist bevorzugt.
Bevorzugtes Gegenion für anionische Gruppen X ist ein einwertiges Kation, insbesondere H+, ein Alkalimetall-Kation oder NR4 +, wobei R = H oder C1 - C6-Alkyl ist und alle R gleich oder verschieden sein können. Insbesondere bevorzugt sind H+, Na+, K+, Li+ und NH4 +, besonders bevorzugt Na+.
Eine bevorzugte kationische Gruppe X kann ausgewählt sein aus
-NR R2R3 + Z- -PR1R2R3 + Z-,
wobei R steht für H oder Ci
-4-Alkyl in beliebiger Position,
Z- steht für CI", Br, , CH3SO3-, CF3SO3-, CHsPhSOs", PhSOs"
R1, R2 und R3 jeweils unabhängig voneinander stehen für H, Ci-3o-Alkyl,
Ar oder -Ch Ar und
Ar steht für einen unsubstituierten oder ein- oder mehrfach
substituierten aromatischen Ring oder kondensierte Ringsysteme mit 6 bis 18 C-Atomen, worin auch ein oder zwei CH-Gruppen durch N ersetzt sein können.
Zu den bevorzugten kationischen Gruppen gehören dabei
insbesondere -NR R
2R
3 + Z
" und
wobei jede einzelne dieser Gruppen für sich genommen bevorzugt sein kann.
Eine bevorzugte nicht-ionische Gruppe kann ausgewählt sein aus: lineares oder verzweigtes Alkyl, wobei ein oder mehrere nicht benachbarte C-Atome durch O, S, und/oder N ersetzt
sind, -OH, -SH, -O-(Glycosid)0-, -S-(Glycosid)0\ -OCH2-CHOH-CH2-OH, -O CH2Ar(-NCO)p-, -OAr(-NCO)P-, Aminoxid,
u steht für eine ganze Zahl aus dem Bereich von 1 bis 6, bevorzugt 1 bis 4 o' steht für eine ganze Zahl aus dem Bereich von 1 bis 10,
p' steht für 1 oder 2,
Ar steht für einen unsubstituierten, ein- oder mehrfach substituierten aromatischen Ring oder kondensierte Ringsysteme mit 6 bis 18 C-Atomen, worin auch ein oder zwei CH-Gruppen durch C=O ersetzt sein können und, Glycosid steht für ein verethertes Kohlenhydrat, vorzugsweise für ein mono- di-, tri- oder oligo-Glucosid.
Zu den bevorzugten nicht-ionischen Gruppen gehören dabei insbesondere lineares oder verzweigtes Alkyl, wobei ein oder mehrere nicht benachbarte C-Atome durch O, S und/oder N ersetzt sind, -OH und -O-(Glycosid)0'.
Wenn X = Alkyl, wobei ein oder mehrere nicht benachbarte C-Atome durch O, S, und/oder N ersetzt sind, dann ist es bevorzugt gleich R4-(B-A)m-- mit
R4 = H oder C1 -4-Alkyl, insbesondere H oder CH3, A = lineares oder verzweigtes Alkylen, bevorzugt mit 1 bis 10 Kohlenstoffatomen,
insbesondere mit 1 bis 4 Kohlenstoffatomen, B = O oder S, bevorzugt O, und m" = eine ganze Zahl bevorzugt aus dem Bereich von 1 bis 100, besonders bevorzugt 1 bis 30.
Insbesondere bevorzugt als nicht-ionische Gruppe X ist die Gruppe R -(O-CH2CHR5)m"- mit m" = eine ganze Zahl aus dem Bereich von 1 bis 100, bevorzugt 1 bis 30, insbesondere auch 1 -25, und R4 und R5 = H oder CI-4-Alkyl, insbesondere H oder CH3. Insbesondere bevorzugt ist R4-(B- A)m "- eine Polyethylen- oder Polypropylenglykoleinheit.
Insbesondere bevorzugt als nicht-ionische Gruppe X ist die
Gruppe -CH(OH)-CH2-NH-Sach mit Sach = verschiedene Zucker und die Gruppe -Y-(CH2-CH2-O)v-R4 mit Y = S, O oder NH, bevorzugt O, R4 = H oder Alkyl, bevorzugt H oder C z, und v = 1 -100, bevorzugt 1-30, insbesondere auch 1 -25.
Eine bevorzugte amphotere Gruppe kann ausgewählt sein aus den funktionellen Gruppen der Acetyldiamine, der N-Alkylaminosäuren, der N- Alkylaminosulfonsäuren, der Betaine, der Sulfobetaine, bzw.
entsprechender Derivate, insbesondere ausgewählt aus, wobei M steht für H oder ein Alkalimetall-Ion, vorzugsweise Li+, Na+ oder K+:
-NH-CH2-COOM; -NH-CH2-CH2-COOM
oder i)-N
+R R
2-CH2-COO-, wobei R
1 und R
2 jeweils unabhängig voneinander stehen für einen C1-8-Alkylrest, vorzugsweise Methyl oder Ethyl
-C(=O)-NH-(CH2)i-3-N+R1R2-CH2-CH(OH)-CH2-(O)(o oden)-(S oder P)O3-, wobei R1 und R2 jeweils unabhängig voneinander stehen für einen C1-8- Alkylrest, vorzugsweise Methyl oder Ethyl
Besonders bevorzugte erfindungsgemäße Verbindungen sind solche, die als hydrophile Gruppe X eine der bevorzugten anionische Gruppen, der bevorzugten nicht-ionischen Gruppen oder der bevorzugten
zwitterionischen Gruppen enthalten.
Insbesondere bevorzugt sind Verbindungen, die die Gruppen -SO3", -OSOs", -COO-, -PO32- oder OPOa2", Polyethylen- oder
Polypropylenglykole, -CH(OH)-CH2-NH-Sach, -Y-(CH2-CH2-O)v-R4,
Betaine, oder Sulfobetaine enthalten. Bevorzugte Gegenionen sind hierbei H+, Na+, K+ und NH4 +, insbesondere Na+. Insbesondere bevorzugt sind: -SO3", -COO-, Polyethylen- oder Polypropylenglykole, Sulfobetaine, die Gruppe -CH(OH)-CH2-NH-Sach und die Gruppe -Y-(CH2-CH2-O)v-R4. Hierbei ist Sach = verschiedene Zucker und Y = S, O oder NH, bevorzugt O, R4 = H oder Alkyl, bevorzugt H oder CH3, und v = 1-100, bevorzugt 1-30, insbesondere auch 1-25. Besonders vorteilhaft können auch Verbindungen mit X = -SO3" sein. Besonders vorteilhaft sind Verbindungen der Formel (I), in denen eine oder mehrere der Variablen die bevorzugten Bedeutungen haben. Besonders vorteilhaft sind Verbindungen der Formel (I), in denen alle genannten Variablen die bevorzugten Bedeutungen, insbesondere die besonders bevorzugten Bedeutungen, haben.
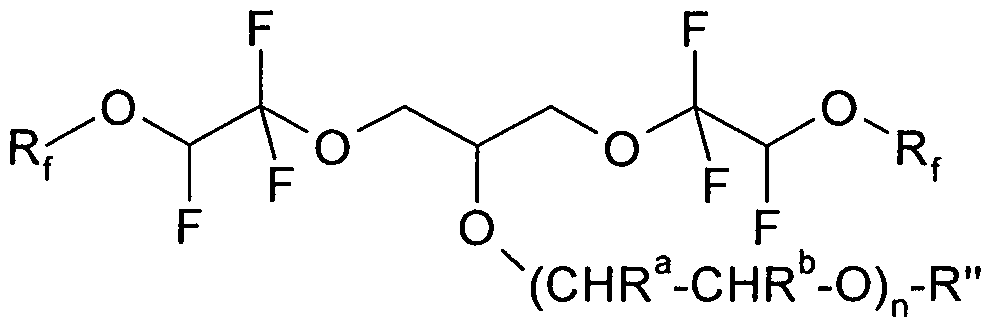
In einer Erfindungsvariante sind Verbindungen der Formel (I) bevorzugt, in denen die Gruppierung (Spacer-X) eine der folgenden Bedeutungen hat: CR5(CH2)n OH, CR5(CH2)n-SH, CR5(CH2)n COOH, CR5(CH2)n"SO3H, CR5(CH2)n-NH2, CR5(CH2)n"NR'2, CR5(CH2)n"N+(CH3)3 CI",
CR5(CH2)n' NR'2-CH2-COO-, CR5(CH2)n O(CHRa-CHRbO)nR",
CR5(CH2)n"S(CHRa-CHRbO)nR" oder CR5(CH2)n-NH(CHRa-CHRbO)nR"ist, mit n = 1-30, bevorzugt = 1-25, insbesondere 4-25, R5, R', R", Ra und Rb unabhängig voneinander = H oder Alkyl, bevorzugt H oder C1-C4 Alkyl. R5 ist bevorzugt H oder CH3, insbesondere H.
Insbesondere bevorzugt sind auch Verbindungen der Formel (I), in denen diese Gruppierungen (Spacer-X) vorliegen, vor allem die bevorzugten Gruppierung, in denen n = 2-3, bevorzugt = 2, x = 1 , und Rf gleich CF3-, CF3-CF2- oder CF3-CF2-CF2- ist und Z gleich:
Rf-CHF-CF2-Y-(CH2)m- oder
Rf-O-CHF-CF2-Y-(CH2)m- oder
Rf-O-(CF2)i-4-CHF-CF2-Y-(CH2)m- oder
Rf-O-(CF2)i-4-O-CHF-CF2-Y-(CH2)m- oder
Rf-O-(CF(CF3)-CF2)i-4-CHF-CF2-Y-(CH2)m- oder
Rf-O-(CF(CF3)-CF2)i-4-O-CHF-CF2-Y-(CH2)m- oder
Rf-O-(CF2-O)i-4-CHF-CF2-Y-(CH2)m- oder
R^-(CF2-CF2-O)i-4-CHF-CF2-Y-(CH2)m- oder
Rf-O-(CF2-0)i-4-(CF2-CF2-0)i-4-CHF-CF2-Y-(CH2)m- ist mit m = 0 oder 1.
Insbesondere bevorzugt sind hierbei Verbindungen, in denen Z gleich:
Rf-CHF-CF2-Y-(CH2)m- oder
Rf-O-CHF-CF2-Y-(CH2)m- oder
Rf-O-(CF2)i-4-CHF-CF2-Y-(CH2)m- oder
Rf-O-(CF2)i-4-O-CHF-CF2-Y-(CH2)m- ist, vor allem Verbindungen mit Z = Rf-
0-CHF-CF2-Y-(CH2)m- oder R^O-(CF2)i-4-O-CHF-CF2-Y-(CH2)m-.
Besonders bevorzugte Verbindungen der Erfindung sind Verbindungen der Formeln (IIa) und (IIb):
[F(CF2)n (O)oCHF-CF2-Y-(CH2)m]2Spacer-X Formel (IIa)
[F(CF2)n (O)o-(CF2)i-4-O-CHF-CF2-Y-(CH2)m]2Spacer-X Formel (IIb) mit n' = 1-6, bevorzugt 1-3, m = 0 oder 1 , o= 0 oder 1 , bevorzugt 1 , Y = O oder S, bevorzugt O, und die Gruppierung (Spacer-X) = CR5(CH2)n OH, CR5(CH2)n' SH, CR5(CH2)n COOH, CR5(CH2)n"SO3H, CR5(CH2)n "NH2, CR5(CH2)n"NR'2> CR5(CH2)n"N+(CH3)3 CI",
CR5(CH2)n"NR'2-CH2-COO-, CR5(CH2)n O(CHRa-CHRbO)nR",
CR5(CH2)n"S(CHRa-CHRbO)nR" oder CR5(CH2)n'NH(CHRa-CHRbO)nR"ist, mit n" = 0 oder 1 , n = 1-30, bevorzugt = 1-25, insbesondere 4-25, R5, R', R", Ra und Rb unabhängig voneinander = H oder Alkyl, bevorzugt H oder C1-C4 Alkyl. R5 ist bevorzugt H oder CH3> insbesondere H.
Insbesondere bevorzugt sind Verbindungen der Formeln (IIa) und (IIb) in denen eine oder mehrere der Variablen die bevorzugten Bedeutungen
haben. Besonders vorteilhaft sind Verbindungen der Formeln (IIa) und (IIb), in denen alle genannten Variablen die bevorzugten Bedeutungen haben.
Bevorzugt sind vor allem Verbindungen der Formeln (III), (ΙΙ ), (IV) und (IV) in denen die Variablen die für die Formel (I) angegebenen Bedeutungen haben, insbesondere die bevorzugten Bedeutungen:
In einer Erfindungsvariante sind Verbindungen der Formeln (III) und (IV) bevorzugt, in denen X eine hydrophile Gruppe ist, wie sie in der
Gruppierung (Spacer-X) in den Formeln (IIa) und (IIb) genannt ist,
insbesondere solche Verbindungen, in denen Rf gleich CF3-, CF3-CF2- oder
In einer weiteren Erfindungsvariante sind Verbindungen der Formeln (III') und (IV) bevorzugt, in denen X eine hydrophile Gruppe ist, wie sie in der Gruppierung (Spacer-X) in den Formeln (IIa) und (IIb) genannt ist,
insbesondere solche Verbindungen, in denen Rf gleich CF3-, CF3-CF2- oder CF3-CF2-CF2- ist.
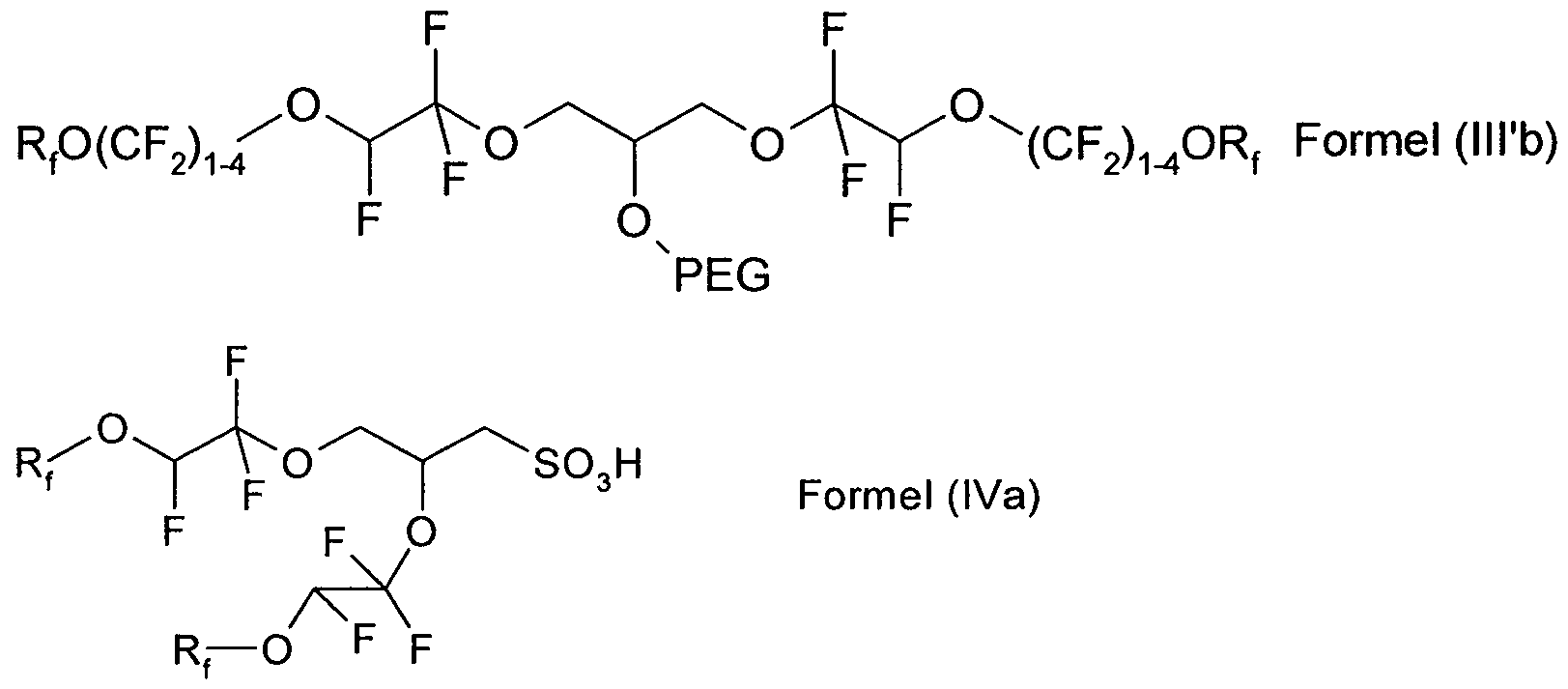
Bevorzugt sind auch Verbindungen der Formeln (lila), (lll'a), (lllb), (lll'b), (IVa), (IV'a), (IVb), (IV'b), (IVc) und (IV'c), in denen die Variablen die für die Formeln (I) und (IIa) und (IIb) angegebenen Bedeutungen haben,
insbesondere die bevorzugten Bedeutungen, und PEG für
Polyethylenglycol, Polypropylenglycol, Polyethylenglycolalkylether oder Polypropylenglycolalkylether steht. Alkylether sind bevorzugt C1-C4- Alkylether, insbesondere C1-C2-Alkylether, vor allem Methylether.
Formel (lll'a)
Formel (lllb)
Formel (IVb)
Formel (IVb)
Formel (IVc)
Formel (IVc)
Insbesondere die folgenden Verbindungen der Formeln (V) bis (XII) sind besonders bevorzugt:
n~6 und R=H oder Methyl Formel (V)
n~12 und R=H oder Methyl Formel (VI)
n~12 und R=H oder Methyl Formel (VII)
R=Methyl oder Ethyl Formel (IX)
30
R=Methyl oder Ethyl Formel (X)
R=H, Methyl oder Ethyl Formel (XI)
Kation+ = H+, Na+, K+ oder NH4+ Formel (XII)
Die erfindungsgemäßen Verbindungen sind nach dem Fachmann bekannten Verfahren herstellbar. Die folgenden Schemata zeigen
Beispielsynthesen für erfindungsgemäße Verbindungen. Diese Verfahren sind dem Fachmann generell bekannt und können unter üblichen
Bedingungen durchgeführt werden.
Die erfindungsgemäßen Verbindungen, insbesondere Verbindungen der Formeln (IIa) und (IIb), bevorzugt Verbindungen der Formeln (III), (III'), (IV) und (IV), können bevorzugt nach den folgenden Syntheserouten
(beispielhaft dargestellt für Verbindungen mit Rf = C4F9) hergestellt werden. Besonders bevorzugt sind hierbei Verbindungen der Formeln (lila), (lllb), (IVa), (IVb), (IVc), (lll'a), (lll'b), (IV'a), (IV'b) und (IV'c), insbesondere der Formeln (V) bis (XII).
Trifunktionelle Verbindungen müssen dabei so geschützt/aktiviert werden, dass nur zwei Perfluorolefinmoleküle mit dem Molekül reagieren können. Dies lässt sich durch bekannte Schutzgruppen und entsprechende
Syntheseabfolge realisieren. Verbindungen wie lassen sich bevorzugt durch Umsetzung eines PEG-ylierten Glycerins (ein mit PEG umgesetztes Glycerin)herstellen.
Der entsprechende Thioether 5 ist über das geschützte Thioglycerin 2 zugänglich. Eine Zwischenstufe ist dabei Verbindung 3, die auch durch Oxidation zum entsprechenden Sulfonat 4 umgesetzt werden kann.
Bei Verwendung von Serinol geht man an bestem von dessen Oxalatsalz aus oder der tert-Butyloxycarbonyl (BOC) geschützten Verbindung aus.
Verbindungen wie 7 lassen sich bevorzugt aus einem monogeschütztem Glycerin 6 herstellen.
Bevorzugt können die folgenden beispielhaft genannten
Perfluorolefinverbindungen eingesetzt werden:
CF3-CF=CF2 CF3-CF2-CF2-OCF=CF2
CF3-CF2-CF=CF2 CF3-CF2-OCF=CF2
CF3-CF2-CF2-CF=CF2 CF3-OCF=CF2
Bevorzugt können die folgenden beispielhaft genannten Alkohole eingesetzt werden:
Sinnvoll kann es dabei sein die Selektivität der einzelnen funktionellen Gruppen zu schützen:
Vorteil bei diesen Verbindungen ist, dass nach der Umsetzung mit dem Perfluorolefin die Schutzgruppe durch Verkochen in wässriger Natronlauge bzw ansäuern leicht entfernt werden kann.
Die Herstellung weiterer erfindungsgemäßer Verbindungen, insbesondere weiterer Verbindungen der Formeln (IIa) und (IIb), bevorzugt weiterer Verbindungen der Formeln (III), (III'), (IV) und (IV), insbesondere weiterer Verbindungen der Formeln (lila), (lllb), (IVa), (IVb), (IVc), (lll'a), (lll'b), (IV'a), (IV'b) und (IVc), kann analog zu den oben gezeigten beispielhaften Reaktionen oder nach anderen dem Fachmann an sich aus der Literatur bekannten Methoden erfolgen. Besonders bevorzugt sind hierbei
Verbindungen der Formeln (V) bis (XII). Die Herstellung weiterer erfindungsgemäßer Verbindungen kann auch nach anderen dem
Fachmann an sich aus der Literatur bekannten Methoden erfolgen.
Diese Verfahren sind dem Fachmann generell bekannt und können unter üblichen Bedingungen durchgeführt werden. Die verwendeten Alkohole sind kommerziell erhältlich und/oder ihre Herstellung ist dem Fachmann geläufig.
Vorteile der erfindungsgemäßen Verbindungen können insbesondere sein:
- eine Oberflächenaktivität, die der konventioneller Kohlenwasserstoff- Tenside hinsichtlich Effizienz und/oder Effektivität gleich oder überlegen ist,
- biologische und/oder abiotische Abbaubarkeit der Substanzen ohne Bildung persistenter perfluorierter Abbauprodukte wie PFOA
(Perfluoroctansäure) oder PFOS (Perfluoroctansulfonat),
- nach einfachen Verfahren herstellbar,
- schwache Schaumwirkung und/oder geringe Schaumstabilisierung,
- gute Verarbeitbarkeit in Formulierungen und/oder
- Lagerstabilität.
Bevorzugt können die erfindungsgemäßen Verbindungen eine besondere Oberflächenaktivität aufweisen. Die erfindungsgemäßen Verbindungen der Formel (I), insbesondere die Verbindungen der Formeln (IIa) und (IIb) und bevorzugt der Formeln (III), (III'), (IV) und (IV), insbesondere der Formeln (lila), (lllb), (IVa), (IVb), (IVc), (lll'a), (lll'b), (IV'a), (IV'b) und (IVc), besonders bevorzugt der Formeln (V) -(XII), können außerdem gegenüber den Fluortensiden des Standes der Technik deutlich verbesserte
Umwelteigenschaften aufweisen, da sie weder chemisch noch biologisch zu langkettigen PFCAs oder PFASs abbauen.
Bevorzugt können die erfindungsgemäßen Verbindungen durch
entsprechende Umwelteinflüsse vollständig in
mineralisierbare/regenerierbare Verbindungen überführt werden. Der Abbau der erfindungsgemäßen Verbindungen kann bevorzugt nach zwei Mechanismen erfolgen. Im ersten Schritt kann durch biologische Aktivität das Kohlenstoffgerüst soweit abgebaut werden, dass (teil)fluorierte Verbindungen entstehen, die nicht toxisch sind und einen hohen
Dampfdruck besitzen. Aufgrund der hohen Flüchtigkeit, können diese Verbindungen in die Atmosphäre gelangen und in der Stratosphäre durch die dort vorherrschende intensive UV-Strahlung zu niedermolekularen Verbindungen (HF, COF2 etc.) zersetzt werden. Diese
Zersetzungsprodukte können dann mit dem Regen aus der Atmosphäre ausgewaschen, in den Boden überführt und dort mineralisiert werden.
Um diesen Zyklus durchlaufen zu können ist es bevorzugt, dass die
Endprodukte bei der biologischen Zersetzung nicht perfluoriert sind und keine (stabilen) Salze entstehen können. Ein weiterer Gegenstand der Erfindung ist ein Verfahren zum Abbau von fluorhaltigen Verbindungen umfassend die folgenden Schritte:
a) biologische und/oder abiotischer Abbau des Kohlenstoffgerüsts der fluorhaltigen Verbindungen unter Bildung von, vorzugsweise nicht toxischen, fluorhaltigen Verbindungen mit einem ausreichend hohen Dampfdruck,
b) Überführen der in Schritt a) gebildeten fluorhaltigen Verbindungen mit hohem Dampfdruck in eine Gasphase,
c) Abbau der in Schritt a) gebildeten fluorhaltigen Verbindungen mit hohem Dampfdruck zu niedermolekularen Verbindungen durch UV-Bestrahlung in der Gasphase,
d) Überführen der in Schritt c) gebildeten niedermolekularen Verbindungen aus der Gasphase in eine flüssige und/oder feste Phase,
e) Mineralisierung der Schritt c) gebildeten niedermolekularen
Verbindungen der flüssigen und/oder festen Phase.
Bevorzugt werden in Schritt a) keine fluorhaltigen, Salze gebildet.
Insbesondere werden in Schritt a) keine perfluorierten Verbindungen gebildet.
Bevorzugt werden fluorhaltige Tenside dem beschriebenen Abbauverfahren unterzogen, insbesondere solche Tenside, die auf teilfluorierten beruhen.
In dem genannten Abbauverfahren werden bevorzugt Verbindungen der Formel (I), bevorzugt der Formeln (IIa) und (IIb), insbesondere der Formeln (III), (III1), (IV) und (IV) eingesetzt. Besonders bevorzugt sind hierbei Verbindungen der Formeln (lila), (lllb), (IVa), (IVb), (IVc), (lll'a), (lll'b), (IV'a), (IVb) und (IVc), insbesondere solche der Formeln (V) bis (XII).
Ein weiterer Gegenstand der vorliegenden Erfindung ist die Verwendung der erfindungsgemäßen Verbindungen und den vorstehend beschriebenen bevorzugten Ausführungsformen als oberflächenaktive Mittel,
beispielsweise zur Verbesserung des Verlaufsverhaltens und des
Benetzungsvermögens von Coatingformulierungen. Fluortenside der
Formeln (IIa) und (IIb), insbesondere der Formeln (III), (III'), (IV) und (IV), werden bevorzugt verwendet, insbesondere die genannten besonders bevorzugten Verbindungen. Bevorzugt sind vor allem Verbindungen der Formeln (lila), (lllb), (IVa), (IVb), (IVc), (lll'a), (lll'b), (IVa), (IV'b) und (IV'c), insbesondere Verbindungen der Formeln (V) bis (XII).
Neben den Verbindungen der Formel (I), insbesondere der bevorzugten Verbindungen der Formeln (IIa), (IIb), (III), (III'), (IV), (IV'),(llla), (lllb), (IVa), (IVb), (IVc), (lll'a), (lll'b), (IVa), (IV'b) und (IV'c), vor allem der Formeln (V)- (XII), können die erfindungsgemäßen Mischungen auch Lösemittel, Additive, Hilfs- und Füllstoffe sowie nicht fluorierte Tenside enthalten.
Beispielhaft seien genannt Silikonpartikel, Weichmacher und
oberflächenmodifizierte Pigmente.
Bevorzugte Einsatzgebiete sind beispielsweise die Verwendung der erfindungsgemäßen Fluortenside der Formel (I) und der bevorzugten Verbindungen der Formeln (IIa), (IIb), (III), (III'), (IV), (IV'),(llla), (lllb), (IVa), (IVb), (IVc), (lll'a), (lll'b), (IVa), (IV'b) und (IV'c), vor allem der Formeln (V)- (XII), als Additive in Zubereitungen zur Oberflächenbeschichtung, wie Farben, Lacken, Schutzanstrichen, Spezialcoatings in elektronischen oder Halbleiter-Anwendungen (z.B. Photolacken, Top Antireflective Coatings, Bottom Antireflective Coatings) oder in optischen Anwendungen (z.B.
photographischen Beschichtungen, Beschichtungen optischer Elemente), in Agrochemikalien, in Poliermitteln und Wachsen, z.B. für Mobiliar, Fußböden und Automobile, insbesondere in Bodenpolituren, in Feuerlöschmitteln, Schmierstoffen, in photolithographischen Verfahren, insbesondere in Immersionsphotolithographie-Verfahren, z.B. in Entwicklerlösungen, Spüllösungen, Immersionsölen und/oder in den Photoresists selbst, vor allem zur Herstellung von gedruckten Schaltungen oder in
Additivzubereitungen zur Additivierung entsprechender Zubereitungen.
Darüber hinaus eignen sich die erfindungsgemäß als Tensid verwendbaren Verbindungen für Wasch- und Reinigungsanwendungen, sowie für eine Verwendung als Additive/Tenside in kosmetischen Produkten wie z. B. Haar- und Körperpflegeprodukten (z.B. Shampoos, Haarspülungen und Haarkonditionierern), Schaumbädern, Cremes oder Lotionen mit einer oder mehreren der folgenden Funktionen: Emulgatoren, Netzmittel,
Schaummittel, Gleitmittel, Antistatikum, Erhöher der Resistenz gegen Hautfette.
Dabei werden die erfindungsgemäßen Fluortenside für die Anwendung üblicherweise in entsprechend ausgelegten Zubereitungen eingebracht. Übliche Einsatzkonzentrationen sind 0.01 - 1.0 Gew.-% der
erfindungsgemäßen Tenside bezogen auf die Gesamtzubereitung.
Entsprechende Mittel, enthaltend die erfindungsgemäßen Fluortensiden, sind ebenfalls Gegenstand der vorliegenden Erfindung. Bevorzugt enthalten solche Mittel einen für den jeweiligen Verwendungszweck geeigneten Träger, sowie gegebenenfalls weitere Aktivstoffe und/oder gegebenenfalls Hilfsstoffe. Bevorzugte Mittel sind Färb- und
Lackzubereitungen, Feuerlöschmittel, Schmierstoffe, Wasch- und
Reinigungsmittel und Enteiser oder Entwicklerlösungen, Spüllösungen, Immersionsöle und Photoresists für photolithograqphische Verfahren, insbesondere für Immersionsphotolithographie-Verfahren und insbesondere zur Herstellung gedruckter Schaltungen, Agrochemikalien, Bodenpolituren, kosmetische Produkte, kosmetische Produkte oder Hydrophobiermittel zur Textilausrüstung oder Glasbehandlung. Bei bevorzugten Mitteln handelt es sich dabei um Färb- und Lackzubereitungen und Druckfarben.
Außerdem sind auch wasserbasierte Lackformulierungen, die die
erfindungsgemäßen Fluortenside allein oder im Gemische mit Additiven enthalten, Gegenstand der vorliegenden Erfindung. Bevorzugt werden Lackformulierungen auf Basis der folgenden synthetischen Filmbildner verwendet: Polykondensationsharze wie Aikydharze, gesättigt/ungesättigte
Polyester, Polyamide/imide, Silikonharze; Phenolharze; Harnstoffharze und Melaminharze, Polyadditionsharze wie Polyurethane und Epoxidharze, Polymerisationsharze wie Polyolefine, Polyvinylverbindungen und
Polyacrylate.
Außerdem sind die erfindungsgemäßen Fluortenside auch zum Einsatz in Lacken auf Basis von Naturstoffen und modifizierten Naturstoffen geeignet. Bevorzugt sind Lacke auf Basis von Ölen, Polysacchariden wie Stärke und Cellulose als auch auf Basis von Naturharzen wie cyclischen
Oligoterpenen, Polyterpenen und/oder Schellack.
Die erfindungsgemäßen Fluortenside können sowohl in physikalisch härtenden (Thermoplaste) als auch in vernetzenden (Elastomere und Duromere) wässrigen Lacksystemen verwendet werden. Bevorzugt verbessern die erfindungsgemäßen Fluortenside die Verlaufs- und
Benetzungseigenschaften der Lacksysteme.
Alle hier genannten Verwendungen erfindungsgemäß einzusetzender Fluortenside, insbesondere der bevorzugten Verbindungen, sind
Gegenstand der vorliegenden Erfindung. Die jeweilige Anwendung von Fluortenside zu den genannten Zwecken ist dem Fachmann bekannt, so dass der Einsatz der erfindungsgemäß einzusetzenden Fluortenside keine Probleme bereitet.
Die vollständigen Offenbarungen aller aufgeführten Anmeldungen und Veröffentlichungen sind durch Bezugnahme in diese Anmeldung eingeführt. Für die vorliegende Erfindung bedeutet sowohl die Pluralform eines Begriffs als auch die Singularform eines Begriffs auch die jeweils andere Form, soweit nicht ausdrücklich anderes angegeben ist. Alle Merkmale der vorliegenden Erfindung können in jeder Art miteinander kombiniert werden, es sei denn dass sich bestimmte Merkmale ausschließen. Dies gilt vor allem für bevorzugte und besonders bevorzugte Merkmale. Weitere
Merkmale, Vorteile und Varianten der Erfindung ergeben sich auch aus den Ansprüchen und Beispielen. Die folgenden Beispiele erläutern die
vorliegende Erfindung näher, ohne den Schutzbereich zu beschränken.
5 Beispiele
Die NMR-Spektren werden mit einem Bruker 400 MHz Spektrometer mit internem Standard gemessen.
Die IR-Spektren werden mit einem Brucker Alpha Platinum-ATR
Spektrometer gemessen.
10
Bestimmung der statischen Oberflächenspannung
Es werden die statischen Oberflächenspannungen γ von wässrigen
Tensidlösungen mit verschiedenen Konzentrationen c (Gramm pro Liter) bestimmt.
15 Gerät: Tensiometer der Firma Dataphysics (Modell DCAT 11)
Temperatur der Messlösungen: 20°±0,2°C
Eingesetzte Messmethode: Messung der Oberflächenspannung mit der Wilhelmy Plattenmethode nach DIN EN 14370.
Platte: Platin, Länge= 19,9mm
20 Bei der Plattenmethode wird die Oberflächen- bzw. Grenzflächenspannung der Tensidlösung aus der auf die benetzte Länge einer Platte wirkenden Kraft nach folgender Formel berechnet.
F _ F
25 Y " L · COS Θ ~ L γ= Grenz- oder Oberflächenspannung; F= auf die Waage wirkende Kraft; L= benetzte Länge (19,9 mm); θ= Kontaktwinkel)Die Platte besteht aus angerautem Platin und wird also optimal benetzt, so dass der Kontaktwinkel -,Q Θ nahe bei 0° liegt. Der Term cos Θ erreicht daher annähernd den Wert 1 , so dass nur noch die gemessene Kraft und die Länge der Platte
berücksichtigt werden müssen.
Abkürzunqen
EO Ethylenoxideinheiten
THF Tetra hydrofu ran
MTBE tert-Butylmethylether
Sdp. Siedepunkt
w% Gewichtsprozent
Beispiel 1 : Generelle Arbeitsweise Ethoxylierung
Für die Ethoxylierung wird der entsprechende Alkohol nach Stand der Technik mit einem Katalysator (z.B. Kaliumhydroxid) unter Inertgas in einem Druckreaktor geben und eine entsprechende Menge Ethylenoxid einkondensiert (Sdp: 10,5°C). Der Reaktor wird verschlossen und bei ca. 5 bar auf 80-150°C aufgeheizt. Nach Beendigung der Reaktion wird das Gemisch entspannt und eventuelle Nebenprodukte unter vermindertem Druck aus dem Produkt entfernt.
Beispiel 2:
An das Isopropylidenglycerol (Sigma-Aldrich) werden wie unter Beispiel 1
1H-NMR (DMSO): 4.13 CH (m), 3.93 CH (dd), 3.7-3.3 -14 CH2 (m), 1.26 CH3 (s), 1.21 CH3 (s)
13C-NMR (DMSO): 108. 8 quart. C; 74.7, 72.8, 72.0, 70.6, 70.2, 66.5, 60.7 sec. C; 27.0, 25.8 prim. C
25 g dieser Verbindung werden in 125 ml THF gelöst und in einem
Dreihalskolben mit Rückflusskühler, Thermometer, Rührvorrichtung und
Septum vorgelegt. Unter Schutzgasatmosphäre werden 9 g Kalium-tert.- butylat (Sigma-Aldrich) zugegeben, wobei ein leichter Temperaturanstieg (auf 32°C) beobachtet wird. Nach 20 min wird langsam 10 g Dimethylsulfat (Sigma-Aldrich) zugegeben. Es ist drauf zu achten, dass bei der Zugabe die Temperatur 37 °C nicht übersteigt. Nach einer Stunde Rühren bei Raumtemperatur wird das Reaktionsgemisch für 2 Stunden bis zur
Siedetemperatur erhitzt.
Nach Abkühlung auf Raumtemperatur wir der Ansatz mit 50 ml 10%iger Nhta-Lösung versetzt und 1 Stunde nachgerührt um restliches
Dimethylsulfat zu zersetzen.
Der Ansatz wird mit 20 ml_ 2N HCl versetzt (pH=1) und 6 Stunden unter Rückfluss erwärmt um die Isopropylidenschutzgruppe zu entfernen.
Das Lösemittel wird vollständig entfernt und der Rückstand in 50 ml Aceton dispergiert.
Salzrückstände werden über eine Fritte abgetrennt und das Lösemittel unter reduziertem Druck abdestilliert.
NMR-Analytik:
1H-NMR (DMSO): 3.8-3.3 -14 CH2 (m), 3.2 OCH3 (s)
5 g dieser Verbindung werden in einem Autoklaven mit 11 g 1 , 1 , 1 ,2,2,3,3 Heptafluoro-3-trifluorovinyloxypropan (ABCR) versetzt, 10 ml Acetonitril und 2,4 g Kaliumcarbonat vermischt und für 66 Stunden auf 80°C erwärmt (Innendruck 3,7 bar). Das Rektionsgemisch wird mit 100 ml Wasser und 100 ml MTBE versetzt die Phasen getrennt und die wässrige Phase mit 2 x 50 ml MTBE ausgeschüttelt. Die vereinigten organischen Phasen werden erst mit 50 ml Wasser und dann mit 50 ml gesättigter NaCI Lösung gewaschen, über Na2SO4 getrocknet und das Lösungsmittel unter vermindertem Druck abgetrennt.
Die Ausbeute beträgt 6 g einer viskosen, bernsteinfarbenen Substanz. Folgende Struktur ergibt sich aus den ermittelten spektroskopischen Daten
NMR-Analytik
1H-NMR (DMSO): 5.9 CHF (d), 3.8-3.4 -14 CH2 (m), 3.3 OCH3 (s)
Statische Oberflächenspannung:
γ 18,9 mN/m (0,1 w%); CMC [g/l] 0,01
Beispiel 3:
An das Isopropylidenglycerol werden wie unter Beispiel 1 beschrieben 12 EO angelagert.
NMR-Analytik
H-NMR (DMSO): 4.13 CH (1 m), 3.93 CH (1 dd), 3.7-3.3 CH2 (26, m), 1.26 CHs (3, s), 1.21 CH3 (3, s)
Die weitere Umsetzung erfolgt analog Beispiel 2
NMR-Analytik:
1H-NMR (DMSO): 3.8-3.3 CH2 (26, m), 3.2 OCH3 (3, s)
Die Ausbeute beträgt 7,6 g einer viskosen, bernsteinfarbenen Substanz. Folgende Struktur ergibt sich aus den ermittelten spektroskopischen Daten (NMR):
NMR-Analytik:
1H-NMR (DMSO): 5.9 CHF (2, d), 3.8-3.4 CH (-26, m), 3.3 OCH3 (3, s)
Statische Oberflächenspannung:
γ 18,0 mN/m (0,1 w%)
Beispiel 4:
3700 g 1 ,1 ,2,2,3,3 Hexafluoro-1-trifluoromethoxy-3-trifluorovinyloxypropan werden in einem Autoklaven mit 500 g Glycerin-1-acetat, 670 g
Kaliumcarbonat und 2300 g Acetonitril und für 68 Stunden auf 80°C erwärmt (Innendruck 2,3 bar).
Der Ansatz wird mit Wasser gewaschen und die organische Phase abgetrennt. Der Ansatz wird mit 500mL 32%-ige Natronlauge und 500mL Wasser versetzt und 72 Stunden bei Siedetemperatur gerührt.
Das Produkt wird mit MTBE extrahiert, erneut mit Wasser gewaschen, über Na2S0 getrocknet und im Vakuum fraktioniert destilliert Hauptfraktion (Sdp 82 °C bei 0,37 mbar).
NMR-Analytik
1H-NMR (DMSO): 6.6 CHF (2, m), 5.2 - 3.7 CH (5, m)
Der teilfluorierte Alkohol wird analog Beispiel 1 ethoxyliert wobei 12 EO angelagert werden. Folgende Struktur ergibt sich aus den ermittelten spektroskopischen Daten (NMR:
NMR-Analytik
1H-NMR (DMSO): 6.8 CHF (2, d), 4.9-4.0 CH (5, m), 3.8-3.2 CH2CH2O (48, m)
Statische Oberflächenspannung:
γ 18,62 mN/m (0,1 w%)
Beispiel 5:
Analog Beispiel 5 wird ein Tenside mit 24 EO Einheiten synthetisiert.
Folgende Struktur ergibt sich aus den ermittelten spektroskopischen Daten (NMR):
n~24 NMR-Analytik
1 H-NMR (DMSO): 6.8 CHF (2, d), 4.9-4.0 CH (5, m), 3.8-3.2 CH2CH2O
(-96, m)
Statische Oberflächenspannung:
γ 17,58 mN/m (0,1 w%)
Beispiel 6:
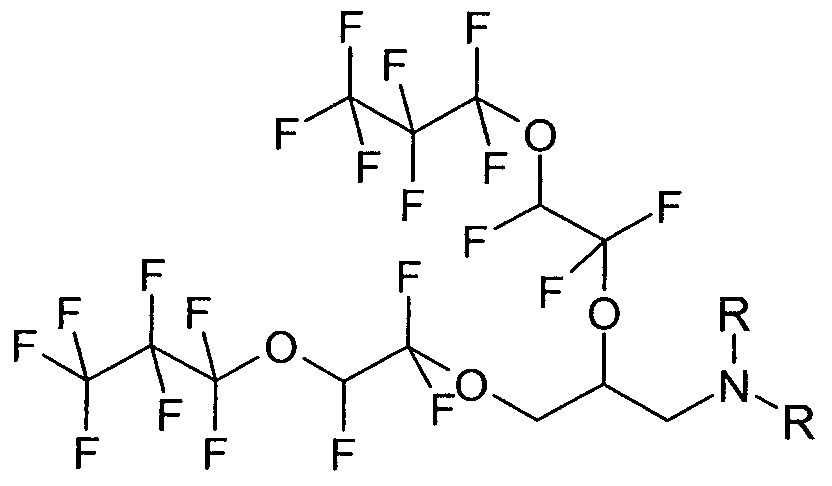
3,12g (0,056mol) Kaliumhydroxid werden mit 15ml Acetonitril und 2,83g (0,024mol) 3-Dimethylamino-propan-1 ,2-diol (ABCR) im Druckreaktor zusammen gegeben. Anschließend werden 13,90g (0,052mol)
1 ,1,1 ,2,2,3,3-Heptafluor-3-trifluorvinyloxypropan dazu gegeben. Der
Druckreaktor wird verschlossen und das Gemisch auf 80°C erhitzt. Es wird 18 Stunden bei dieser Reaktion nachgerührt.
Das Reaktionsgemisch wird nach Beendigung der Reaktion abkühlen gelassen, filtriert und das Lösemittel im Vakuum entfernt.
Zur weiteren Aufarbeitung wird das Produkt unter Vakuum fraktioniert destilliert.
Man erhält 9,66g (63%) hellgelbes Öl.
NMR-Analytik:
H-NMR (DMSO): 6.89-6.65 CHF (2, dt) , 5.20 CH (1 , tt) , 4.34-4.16 CH2 (2m) , 3.56-3.37 CH2 (2m) , 2.88 CH3 (6, s)
7,4g (0,011mol) [2,3-Bis-(1 ,1 ,2-trifluor-2-heptafluorpropyloxyethoxy)- propyl]-dimethylamin, 1 ,41g (0,012mol) Chloressigsäure Natriumsalz (VWR) und 10mL Ethanol 90% werden in einen Rundkolben gegeben und 96 h am Rückfluss gerührt.
Das Reaktionsgemisch wird filtriert und das Lösemittel im Vakuum entfernt. Das Rohprodukt wird auf Kieselgel gegeben und mit Toluol/Essigester 2/1 vom Edukt getrennt.
Das Produkt wird mit Aceton vom Kieselgel gewaschen. Ausbeute 4,4 g.
NMR-Analytik:
1H-NMR (DMSO): 6.89-6.65 CHF (2, dd) , 5.5 CH (1 , s) , 4.54-4.16 CH2 (4m) , 4.0 CH2 (2,s), 3.40 CH3 (6, ds)
Statische Oberflächenspannung:
15,89 mN/m (1.0 w%)
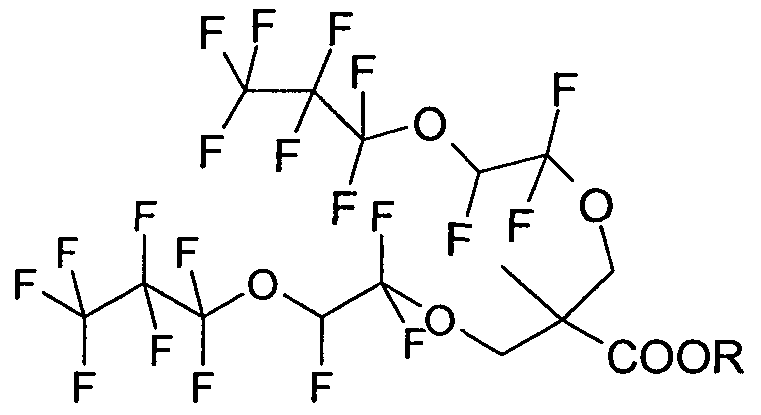
Beispiel 7:
5,0g (0,034mol) 3-Hydroxy-2-hydroxymethyl-2-methyl-propionsäuremethyl ester (VWR), 15ml_ (0,084mol) 1 ,1 ,1 ,2,2, 3,3-Heptafluor-3-trifluorvinyloxy- propan, 6,1g (0,044mol) Kaliumcarbonat und 25mL Acetonitril werden im Druckreaktor zusammen gegeben und auf 80°C erhitzt. Es wird für 48
Stunden bei dieser Temperatur nachgerührt.
Anschließend wird abkühlen gelassen, das Gemisch filtriert und das
Lösemittel wird im Vakuum entfernt.
Das Rohprodukt wird über KG gefrittet und man erhält 17,1g (0,025mol) 2- Methyl-3-(1 , 1 ,2-trifluor-2-heptafluorpropyloxy-ethoxy)-2-(1 , 1 ,2-trifluor-2- heptafluorpropyloxy-ethoxymethyl)-propionsäuremethylester.
10,00g (0,015mol) 2-Methyl-3-(1 ,1 ,2-trifluor-2-heptafluorpropyloxy-ethoxy)- 2-(1 ,1 ,2-trifluor-2-heptafluorpropyloxy-ethoxymethyl)-propionsäure methyl ester werden mit 1 ,47 g (0,037mol) NaOH in 15ml (0,257mol) Ethanol zusammen geben und für 18 Stunden am Rückfluss gerührt.
Anschließend wird das Lösemittel im Vakuum entfernt, der Rückstand in Aceton suspendiert und filtriert das Natriumhydroxid zu entfernen.
Das Aceton wird im Vakuum abdestilliert und man erhält 9,4g (0,014mol) des entsprechenden Fluortensid als Natriumsalz.
Charakterisierung per IR: COO st as 1607cm 1
Statische Oberflächenspannung:
16,45 mN/m (1.0 w%)