WO2014208742A1 - オリゴ糖ペプチドの精製方法 - Google Patents
オリゴ糖ペプチドの精製方法 Download PDFInfo
- Publication number
- WO2014208742A1 WO2014208742A1 PCT/JP2014/067224 JP2014067224W WO2014208742A1 WO 2014208742 A1 WO2014208742 A1 WO 2014208742A1 JP 2014067224 W JP2014067224 W JP 2014067224W WO 2014208742 A1 WO2014208742 A1 WO 2014208742A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- sgp
- resin
- synthetic
- egg yolk
- solution
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K1/00—General methods for the preparation of peptides, i.e. processes for the organic chemical preparation of peptides or proteins of any length
- C07K1/14—Extraction; Separation; Purification
- C07K1/145—Extraction; Separation; Purification by extraction or solubilisation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K9/00—Peptides having up to 20 amino acids, containing saccharide radicals and having a fully defined sequence; Derivatives thereof
- C07K9/001—Peptides having up to 20 amino acids, containing saccharide radicals and having a fully defined sequence; Derivatives thereof the peptide sequence having less than 12 amino acids and not being part of a ring structure
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D15/00—Separating processes involving the treatment of liquids with solid sorbents; Apparatus therefor
- B01D15/08—Selective adsorption, e.g. chromatography
- B01D15/10—Selective adsorption, e.g. chromatography characterised by constructional or operational features
- B01D15/12—Selective adsorption, e.g. chromatography characterised by constructional or operational features relating to the preparation of the feed
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D15/00—Separating processes involving the treatment of liquids with solid sorbents; Apparatus therefor
- B01D15/08—Selective adsorption, e.g. chromatography
- B01D15/26—Selective adsorption, e.g. chromatography characterised by the separation mechanism
- B01D15/265—Adsorption chromatography
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D15/00—Separating processes involving the treatment of liquids with solid sorbents; Apparatus therefor
- B01D15/08—Selective adsorption, e.g. chromatography
- B01D15/26—Selective adsorption, e.g. chromatography characterised by the separation mechanism
- B01D15/36—Selective adsorption, e.g. chromatography characterised by the separation mechanism involving ionic interaction
- B01D15/361—Ion-exchange
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K1/00—General methods for the preparation of peptides, i.e. processes for the organic chemical preparation of peptides or proteins of any length
- C07K1/14—Extraction; Separation; Purification
- C07K1/36—Extraction; Separation; Purification by a combination of two or more processes of different types
Definitions
- the present invention relates to a method for simply purifying oligosaccharide peptides contained in egg yolk components.
- Sialylglycopeptide (Sialyl GlycoPeptide: hereinafter referred to as “SGP”), which is an oligosaccharide peptide contained in chicken egg yolk, is useful as a raw material for pharmaceuticals because the contained oligosaccharide chain is human.
- Patent Document 1 As a method for purifying SGP, in Patent Document 1 and the like, an extraction operation for precipitating with a water-soluble organic solvent such as ethanol is performed on the extract from a chicken defatted egg yolk-containing material to a plurality of aqueous solutions.
- a water-soluble organic solvent such as ethanol
- ODS-based reverse phase resin a kind of resin for reverse phase partition chromatography
- Patent Document 2 the technique known before Patent Document 1 requires a plurality of concentrated desalting operations, is insufficient in terms of purity and yield (Patent Document 2), and is not suitable for mass purification. This was due to purification by column chromatography (Non-patent Document 1).
- the present inventor has intensively studied on the purification method of SGP, and by adding a deproteinizing agent that is not normally used for protein / peptide purification to the aqueous solution of egg yolk component, SGP is dissolved by removing insoluble components. Other unnecessary proteins that remain in the liquid part are removed by a deproteinizing agent, and the obtained dissolved liquid part is adsorbed on a synthetic adsorption resin and eluted to obtain high-purity SGP in a high yield.
- the present invention was completed by finding that it can be purified and by further study.
- the present invention provides the following inventions.
- the protein removal agent is a synthetic silica-based protein removal agent, an additive having a protein coagulation action, or an additive having a protein degradation action.
- the synthetic silica-based deproteinizing agent is synthetic silica gel or synthetic silica colloid.
- the synthetic silica-based deproteinizing agent has a particle size of about 1 to 50 ⁇ m, a specific surface area of about 100 to 1500 m 2 / g, a pore volume of about 0.5 to 3 ml / g, and an average pore size of about 1 to
- the method of (3) which is a synthetic silica gel satisfying 50 nm.
- the aqueous solution containing an avian egg yolk component is an aqueous solution of chicken egg yolk or defatted egg yolk.
- the aqueous solution containing an avian egg yolk component is a solution from which insoluble components have been removed in advance.
- the method of (1) further including the process of collect
- the resin capable of separating SGP is a reverse phase resin, a normal phase resin, an ion exchange resin, a gel filtration resin, or a synthetic adsorption resin.
- the removal operation of protein components other than SGP from the egg yolk component is completed by performing the addition / removal operation of the deproteinizing agent with respect to the aqueous solution once. It is possible to purify. Further, since no organic solvent is used in this process, it is safe and does not require special equipment. Furthermore, by using a synthetic adsorption resin such as SEPABEADS SP207SS (Mitsubishi Chemical Corporation) as a column packing resin used for column chromatography operation for recovering SGP from the solution after deproteinization operation, an alkaline solution is obtained. The resin regeneration operation by the used washing
- FIG. 1 is a chart of the HPLC measurement results of the SGP standard.
- FIG. 2 is a chart of LC / MS measurement results of the SGP standard.
- FIG. 3 is a chart of 1 H-NMR measurement results of the SGP sample.
- FIG. 4 is a chart of the HPLC measurement results of the glycopeptide purified in Example 1.
- FIG. 5 is a chart of LC / MS measurement results of the glycopeptide purified in Example 1.
- 6 is a chart of 1 H-NMR measurement results of the glycopeptide purified in Example 1.
- FIG. FIG. 7 is a chart of HPLC measurement results of the glycopeptide purified in Example 2.
- FIG. 1 is a chart of the HPLC measurement results of the SGP standard.
- FIG. 2 is a chart of LC / MS measurement results of the SGP standard.
- FIG. 3 is a chart of 1 H-NMR measurement results of the SGP sample.
- FIG. 4 is a chart of the HPLC measurement results of the glycopeptid
- FIG. 8 is a graph showing the relative protein concentration (bar graph) and SGP recovery rate (line graph) of the supernatant after treatment when various SYLORUTEs, which are synthetic silica gels, are used as additives in each pH condition.
- Y-axis shows relative protein concentration (%) and SGP recovery (%), both%.
- the horizontal axis indicates the pH of the solution during treatment for each additive.
- the bar graph shows the relative protein concentration when the white bar is treated for 15 minutes and the black bar is treated for 60 minutes.
- ⁇ indicates the SGP recovery rate when 15 minutes are processed and ⁇ indicates 60 minutes.
- FIG. 9 is a graph showing the relative protein concentration (bar graph) and the SGP recovery rate (line graph) of the supernatant after treatment when various Mizucassorb, which is a synthetic silica gel, is used as an additive under various pH conditions.
- Y-axis shows relative protein concentration (%) and SGP recovery (%), both%.
- the horizontal axis indicates the pH of the solution during treatment for each additive.
- the bar graph shows the relative protein concentration when the white bar is treated for 15 minutes and the black bar is treated for 60 minutes.
- ⁇ indicates the SGP recovery rate when 15 minutes are processed and ⁇ indicates 60 minutes.
- FIG. 10 shows the relative protein concentration (bar graph) and SGP recovery rate (line graph) of the supernatant after treatment with various carplexes and microdo KM-386P, which are synthetic silica gels, as additives. It is a graph showing. Y-axis shows relative protein concentration (%) and SGP recovery (%), both%. The horizontal axis indicates the pH of the solution during treatment for each additive.
- the bar graph shows the relative protein concentration when the white bar is treated for 15 minutes and the black bar is treated for 60 minutes.
- ⁇ indicates the SGP recovery rate when 15 minutes are processed and ⁇ indicates 60 minutes.
- FIG. 11 is a graph showing the relative protein concentration (bar graph) and SGP recovery rate (line graph) of the supernatant after treatment when various copoloks, which are synthetic silica colloids, are treated under various pH conditions.
- Y-axis shows relative protein concentration (%) and SGP recovery (%), both%.
- the horizontal axis indicates the pH of the solution during treatment for each additive.
- the bar graph shows the relative protein concentration when the white bar is treated for 15 minutes and the black bar is treated for 60 minutes.
- ⁇ indicates the SGP recovery rate when 15 minutes are processed and ⁇ indicates 60 minutes.
- FIG. 12 shows the relative protein concentration (bar graph) of the supernatant after treatment when treated under various pH conditions using Celite 545, which is a general filter aid, Fibracel BH-40, and various topcoperlites as additives. It is a graph showing SGP collection
- FIG. 13 is a graph showing the relative protein concentration (bar graph) and SGP recovery rate (line graph) of the supernatant after treatment when tannic acid and papain are used as additives in each pH condition.
- Y-axis shows relative protein concentration (%) and SGP recovery (%), both%.
- the horizontal axis indicates the pH of the solution during treatment for each additive.
- the bar graph shows the relative protein concentration when the white bar is processed for 15 minutes and the black bar is processed for 60 minutes (for papain, the hatched bar is processed for 20 hours).
- ⁇ represents the SGP recovery rate after 15-minute processing
- ⁇ represents 60-minute processing (for papain, ⁇ represents 20-hour processing).
- FIG. 14 is a chart of HPLC measurement results of the glycopeptide purified in Example 4.
- FIG. 15 is a chart of HPLC measurement results of the glycopeptide purified in Example 5.
- FIG. 16 is a chart of HPLC measurement results of the glycopeptide purified in Example 6.
- FIG. 17 is a chart of HPLC measurement results of the glycopeptide purified in Example 7.
- FIG. 18 is a chart of HPLC measurement results of the glycopeptide purified in Reference Example 1.
- the present invention provides a method for purifying a sialylglycopeptide, comprising the following step A; Step A: A step of mixing an aqueous solution containing an avian egg yolk component and a protein removal agent to obtain a solution portion.
- Step A A step of mixing an aqueous solution containing an avian egg yolk component and a protein removal agent to obtain a solution portion.
- “mixing” two or more materials means an operation in which all the materials are brought into contact with each other and the components of each material are uniformly distributed or dissolved.
- the mixing operation is not particularly limited as long as the above-described mixed state can be achieved, and examples thereof include shaking stirring, stirring with a stirring bar, stirring with a stirring blade, and the like.
- the time required for these operations is not particularly limited, and is, for example, 10 seconds or longer, preferably 5 minutes or longer, more preferably 15 minutes or longer.
- the temperature at which this operation is performed is not particularly limited as long as the components contained in each material are not altered or denatured, but is preferably 4 ° C to 40 ° C.
- “to obtain a solution part” means to remove insoluble matters contained in a solution or a mixed solution and collect only the solution part dissolved in a solvent.
- Typical separation operations include filtration, centrifugation and the like.
- filter paper, glass filter, membrane filter, filter cloth, and the like can be used.
- filtration mode natural filtration, suction filtration, pressure filtration, etc. are employable as a filtration mode.
- the type of filter, filtration mode, centrifugation conditions [number of rotations, time, temperature] and the like can be appropriately selected depending on the state of the solution and the like subjected to separation.
- the separation operation may be performed after a filter aid such as celite is appropriately mixed with the solution or the like before the separation operation.
- filter aids As the filter aid used individually, various commonly known filter aids can be employed as long as they do not have a deproteinization effect.
- the “dissolved liquid part” refers to a liquid sample that contains a liquid as a main component and that is obtained by removing insoluble matters and does not substantially contain insoluble matters. Each component contained in the dissolved liquid part is present in a dissolved state in the liquid at least when the dissolved liquid part is obtained.
- the solution part may produce insoluble matter during storage due to changes in liquid conditions (pH, temperature, etc.), but such insoluble matter is substantially removed by a normal method such as filtration. The state which does not contain an insoluble matter can be recovered.
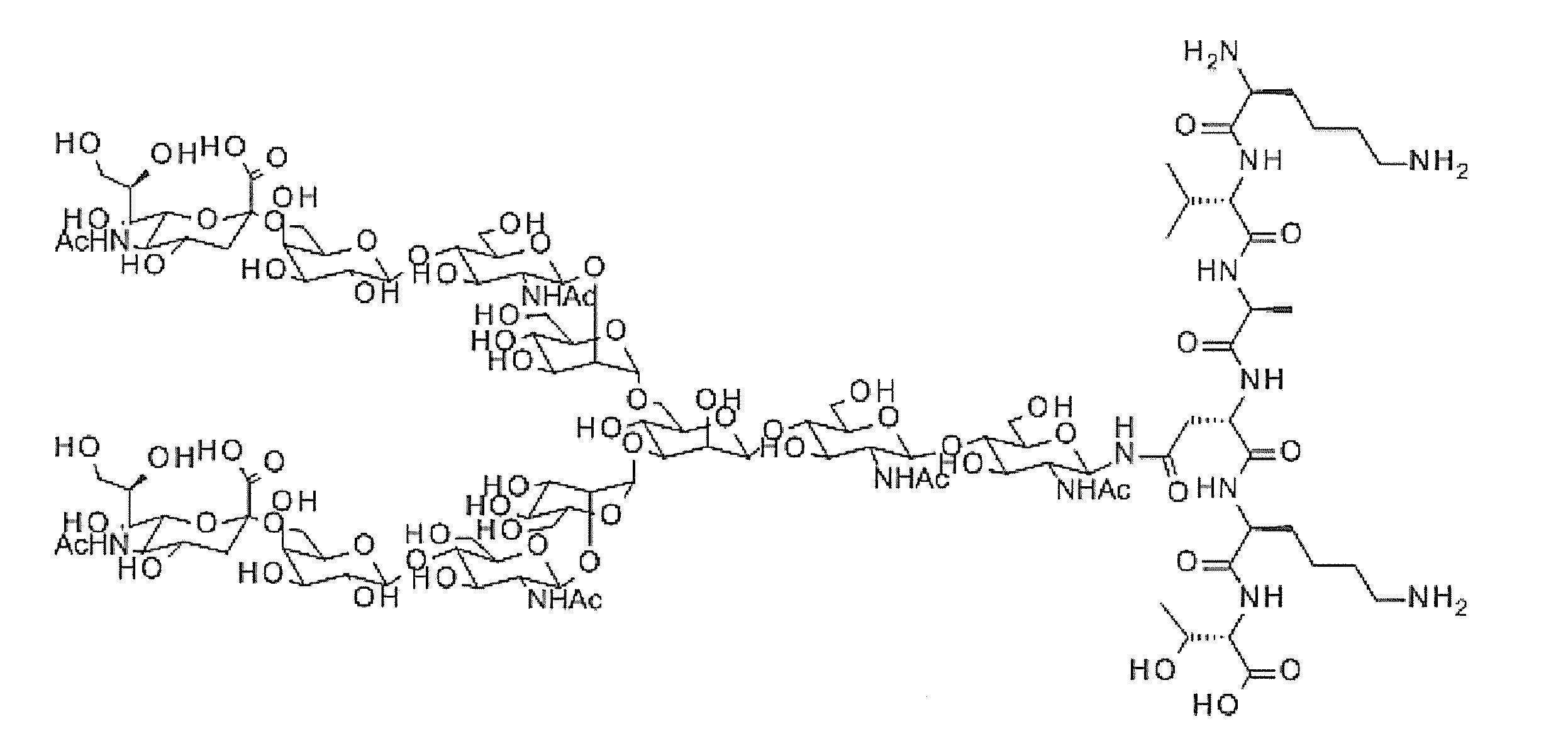
- sialyl glycopeptide (Sialyl GlycoPeptide: hereinafter referred to as“ SGP ”): means reduction of sialylglycan consisting of 11 sugars represented by the following structural formula (I) and sequence formula (II): An oligosaccharide in which the 1-position carbon of GlcNAc at the terminal and the nitrogen atom derived from the side chain amide group at the 4-position Asn of Lys-Val-Ala-Asn-Lys-Thr- (SEQ ID NO: 1) are ⁇ -N glycosidic bonded It is a glycopeptide.
- SGP is a glycopeptide contained in avian egg yolk, but purified SGP is commercially available and can be purchased.
- the HPLC chart, LC / MS spectrum, and 1 H-NMR spectrum (measured under the conditions described in Example 1) of SGP manufactured by Tokyo Chemical Industry Co., Ltd. are as shown in FIG. 1, FIG. 2, and FIG. 3, respectively. Therefore, it is possible to identify that the obtained glycopeptide is SGP.
- the “SGP product” is a product containing SGP as one of main components, such as research reagents, industrial raw materials, pharmaceutical additives, food additives, and the like.
- the SGP purified by the method of the present invention is processed into a state (freeze-dried powder, solution, etc.) according to the product form, enclosed in an appropriate container, packaged, and used as a product. Manufactured. Since SGP obtained by the purification method of the present invention has high purity, it is also useful as a raw material for such SGP products.
- SGP can be detected or quantified by HPLC or the like using a resin capable of separating SGP.
- HPLC conditions include the following conditions.
- HPLC 1260 Infinity LC (Agilent Technologies, Inc.) Column: L-Column 2 ODS 3 ⁇ m ⁇ 3.0 ⁇ 50 mm (Scientific Substance Evaluation Research Organization) Column temperature: 40 ° C Mobile phase A: H 2 O solution containing 0.1% HCOOH (v / v) Mobile phase B: MeCN solution containing 0.1% HCOOH (v / v) Gradient (mobile phase B%): 0% (0 minutes), 10% (5 minutes), 30% (7 minutes), 30% (8 minutes) Flow rate: 0.6 ml / min Detection wavelength: 210 nm
- HPLC 1260 Infinity LC (Agilent Technologies, Inc.) Column: Inertsil Amide 3 ⁇ m ⁇ 3.0 ⁇ 75 mm (GL Sciences Inc.) Column temperature: 40 ° C Mobile phase A: H 2 O solution containing 0.1% HCOOH (v / v) Mobile phase B: MeCN solution containing 0.1% HCOOH (v / v) Gradient (mobile phase B%): 70% (0 minutes), 30% (6 minutes), 10% (6.01 minutes), 10% (7.5 minutes) Flow rate: 0.6 ml / min Detection wavelength: 210 nm.
- SGP contained in the solution can be calculated as a peak area value belonging to SGP in the obtained HPLC chart by subjecting the target solution to the above HPLC.
- the recovery rate of the SGP of the target solution with respect to the SGP content of the starting material solution it can be calculated by the following equation.
- the purity of the test SGP can be calculated as a relative purity with the purity of the standard SGP as 100%.
- the standard product SGP for example, a commercially available SGP manufactured by Tokyo Chemical Industry Co., Ltd. can be used.
- As a measuring method a predetermined amount of an aqueous solvent such as water is added to a precisely weighed test SGP, and a completely dissolved test SGP solution is subjected to HPLC measurement under the above conditions, and in the obtained HPLC chart The peak area value of the test SGP is measured.
- the same operation is performed for the standard SGP, and after preparing a standard SGP solution having the same concentration as the SGP, HPLC measurement under the same conditions is performed, and the purity of the test SGP is calculated by the following formula: Can do.
- Test SGP purity (%) (Test SGP peak area value / standard product SGP peak area value) ⁇ 100.
- SGP is known to be contained in the egg yolk of avian eggs, and since the sugar chain structure contained is a human type, even if it is ingested or taken by humans, it does not easily cause an allergic reaction.
- the “aqueous solution containing an avian egg yolk component” means a solution obtained by mixing an egg yolk component of an avian egg with an aqueous solvent.
- the origin of the egg is not particularly limited as long as it is a bird, and examples thereof include chickens, quails, pigeons, ostriches, and crows, but chicken-derived eggs are preferred.
- the egg yolk is separated from the whole egg white from the whole egg as it is, dried as dried egg yolk, degreased defatted egg yolk, or powdered egg yolk powder, or defatted egg yolk powder of the present invention Can be used in the method.
- Egg yolk powder, defatted egg yolk powder, etc. are sold and can be purchased (York Protein H (Kewpie Corporation), Sunny Pro DF (Taiyo Chemical Corporation), etc.).
- aqueous solvents can be used as long as they are water-based aqueous solvents that do not substantially contain components that denature proteins.
- it is water.
- the egg yolk component-containing solution used in the deproteinization step may be used as it is by mixing egg yolk components such as egg yolk, defatted egg yolk, and their powders with an aqueous solvent, but if necessary, separate insolubles. Only the dissolved solution part may be used.
- the “protein removal agent” means a material having an effect of reducing the amount of protein in the solution by adding it to a protein-containing solution (referred to as “protein removal effect” in this specification).
- the mode of the deproteinization effect of the deproteinizing agent used in the present invention is not particularly limited as long as the SGP content in the solution does not decrease.
- a protein adsorbing like synthetic silica, tannic acid Various deproteinizing agents such as those having a protein coagulation action such as those having a proteolytic action such as papain can be employed, but are preferably deproteinizing agents that adsorb proteins, more preferably Is a synthetic silica-based deproteinizing agent.
- synthetic silica-based protein removing agent used in the present invention, various forms such as powdered synthetic silica gel and colloidal synthetic silica colloid can be employed.
- the synthetic silica gel is not particularly limited as long as it has a deproteinization effect.
- average particle diameter about 1 to 50 (preferably about 2 to 30) ⁇ m
- ratio Surface area about 100-1500 (preferably about 200-800) m 2 / g
- pore volume about 0.5-3 (preferably about 1-2) ml / g
- average pore size about 1-
- Synthetic silica gel satisfying 50 preferably about 5 to 30 nm
- Such synthetic silica gels are commercially available as filter aids.
- SYLOPUTE 202, SYLOPUTE 303, SYLOPUTE 403 (Fuji Silysia Chemical Co., Ltd.), Carplex BS-303, Carplex BS- 306 (DSL Japan Co., Ltd.), Microdo KM-386P (KD corporation), Mizukasorb A751C, Mizukasorb C-1, Mizukasorb C-6 (Mizusawa Chemical Co., Ltd.) and the like
- SYLOPUTE 202, SYLOPUTE 303, SYLOPUTE 403 (Fuji Silysia Chemical Co., Ltd.)
- Carplex BS-303, Carplex BS- 306 DSL Japan Co., Ltd.
- Microdo KM-386P KD corporation
- Mizukasorb A751C Mizukasorb C-1, Mizukasorb C-6 (Mizusawa Chemical Co., Ltd.) and the like
- Synthetic silica colloids include those charged negatively and those charged positively, and various types can be applied to the present invention.
- a synthetic silica colloid that is negatively charged is employed, a good deproteinization effect can be obtained by adjusting the solution during the treatment to be acidic (pH 3 to 4).
- a synthetic silica colloid having a weak negative charge is preferred.
- Copolok 200, Copolok 300, Copolok 306 (Otsuka Foods Co., Ltd.) and the like can be employed as the synthetic silica colloid.
- the mixing ratio at the time of mixing the egg yolk component-containing solution and the deproteinizing agent varies depending on the type of deproteinizing agent used.
- the deproteinizing agent is 0.1 to 50% (v / V or w / v).
- the egg yolk component-containing aqueous solution is preferably adjusted to be weakly acidic.
- the time for mixing the egg yolk component-containing solution and the deproteinizing agent is not particularly limited. However, when an additive having a proteolytic action is used as the deproteinizing agent, the SGP is decomposed by being treated for a long time. The SGP content of the solution after treatment may decrease. Therefore, the mixing time when using a deproteinizing agent having a proteolytic action is usually 5 hours or less, preferably 3 hours or less, more preferably 2 hours or less, and optimally 1 hour or less. is there. After mixing the egg yolk component solution and the protein-removing agent, the insoluble matter is separated to obtain a solution portion.
- the SGP content in the solution part obtained by the above separation operation can be confirmed by a method such as HPLC.
- the protein content in the solution part can be identified and quantified by various known methods.
- SDS-PAGE can be used as a protein identification method.
- an ultraviolet absorption method (absorbance 280 nm), a Bradford method, or the like can be employed as a protein quantification method.
- SGP can be purified from the deproteinized solution obtained through the above deproteinization step using various column fillers.
- column fillers used for such purification include synthetic adsorption resins, reverse phase resins, normal phase resins, ion exchange resins, gel filtration resins, and the like.
- the reverse phase resin is a resin in which a hydrophobic functional group such as a butyl group (C4), an octyl group (C8), an octadecyl group (C18), a triacontyl group (C30), or a phenyl group is added to a base material of silica gel.
- Synthetic adsorption resin is a filler made of porous cross-linked polymer.
- Synthetic adsorption resin is a filler made of porous cross-linked polymer.
- styrene-divinylbenzene synthetic adsorbent styrene-divinylbenzene modified synthetic adsorption resin, methacrylic synthetic adsorption resin, phenol System synthetic adsorption resin and the like. Since fillers such as ODS-based reverse phase resins known to be usable for SGP purification are based on silica gel, they cannot be washed with an alkaline solution.
- a synthetic adsorption resin As the column filler, the resin can be regenerated by washing with an alkaline solution in addition to washing with an organic solvent, so that impurities can be sufficiently removed. It is possible to reuse the synthetic adsorption resin.
- various synthetic adsorption resins can be adopted as long as they can adsorb SGP, but styrene-divinylbenzene synthetic adsorption resin is preferable, and styrene-divinyl is more preferable.
- Benzene-based modified synthetic adsorption resin Specific products include SEPABEADS SP207SS (Mitsubishi Chemical Corporation).
- the solution after deproteinization obtained in the above step is passed through a column packed with a column packing, and if necessary, washed with an appropriate solvent according to the chromatography separation mode. Then, elution is performed using a mobile phase corresponding to the separation mode of chromatography, and SGP can be purified by collecting a fraction containing SGP in the eluate.
- the conditions of the deproteinized solution may be appropriately adjusted in accordance with the column filler to be used and the chromatography mode. When an insoluble matter is generated due to the change in the solution conditions, a filter aid such as celite is appropriately mixed with the solution, and only the solution portion is recovered.
- the SGP contained in the elution fraction can be monitored under the above-mentioned HPLC conditions. If the elution is performed under the same conditions as before, the elution fraction of SGP can be specified from the elution time. Such purification conditions can be set as appropriate according to the type and properties of the column packing employed.
- the solution after deproteinization is adjusted to neutral or alkaline (preferably around pH 9) of pH 7 or higher, and only the solution part from which insoluble matter has been removed is the SEPABEADS SP207SS.
- elution can be performed with a concentration gradient of water-2% acetone water.
- the obtained purified SGP solution may be stored frozen as it is, but may also be stored after concentration or freeze-drying as necessary.
- Example 1 Purification of SGP using synthetic silica gel-1> After adding 5 L of water to 500 g of defatted egg yolk powder (Kewpie Corp.) and stirring well for 15 minutes, it was filtered with a filter press (Iwata Machinery Co., Ltd.).
- SEPABEADS SP207SS (Mitsubishi Chemical Corporation) 207 mL (35 ⁇ ⁇ 215 mm) as a synthetic adsorption resin was packed in a column, and the resin was washed with acetone and then with water, and then equilibrated with 20 mM Na 2 HPO 4 .
- the filtrate obtained above was equilibrated with the resin at a flow rate of 50 mL / min.
- the resin with the filtrate was washed with 2 L of water at a flow rate of 50 mL / min and then developed at a flow rate of 2% acetone water (v / v) at 25 mL / min, and the eluate was fractionated every 25 mL. (Elution fractions 1 to 40)
- the eluted fractions 18 to 26 were combined and freeze-dried to obtain 764.4 mg of glycopeptide.
- the obtained glycopeptide and a standard were subjected to 1 H-NMR measurement, LC / MS measurement and HPLC analysis under the following conditions.
- the measurement results of the sample by HPLC, LC / MS and 1 H-NMR are shown in FIG. 1, FIG. 2 and FIG. 3, respectively.
- the measurement results of the obtained glycopeptide by HPLC, LC / MS and 1 H-NMR are shown in FIGS. 4, 5 and 6, respectively.
- the obtained glycopeptide was compared with the sample by 1 H-NMR measurement and LC / MS measurement, and the same mass spectrum and 1 H-NMR spectrum as the sample were obtained. It was confirmed that it was SGP represented by Formula (II). Moreover, in the result of HPLC, the purity of the obtained SGP was 104% due to the relative area value ratio of the peak attributed to SGP between the obtained SGP and the sample.
- HPLC 1260 Infinity LC (Agilent Technologies, Inc.) Column: L-Column 2 ODS 3 ⁇ m ⁇ 3.0 ⁇ 50 mm (Scientific Substance Evaluation Research Organization) Column temperature: 40 ° C Mobile phase A: H 2 O solution containing 0.1% HCOOH (v / v) Mobile phase B: MeCN solution containing 0.1% HCOOH (v / v) Gradient (mobile phase B%): 0% (0 minutes), 10% (5 minutes), 30% (7 minutes), 30% (8 minutes) Flow rate: 0.6 ml / min Detection wavelength: 210 nm.
- NMR NMR: AVANCE500 (500 MHz, Bruker BioSpin Corporation) Solvent: DEUTERIUM OXIDE + 0.1% TMSP (euriso-top).
- Example 2 Purification of SGP using synthetic silica gel-2>
- the glycopeptide was purified from the defatted egg yolk powder, and the column elution fractions 20 to 30 were combined and freeze-dried to obtain 694.1 mg of the glycopeptide.
- the obtained glycopeptide was confirmed to be SGP by comparison with a preparation by 1 H-NMR measurement and LC / MS measurement.
- Example 1 the HPLC analysis was performed on the same conditions as Example 1 (FIG. 7). From the HPLC results, the purity was calculated in the same manner as in Example 1. As a result, the purity of the obtained SGP was 102%.
- Example 3 Examination of application of various protein removal agents to SGP purification> Next, the applicability of various protein removal agents, various general filter aids, and various additives to SGP purification was examined. In the purification method of the present invention, it is important that impurities, particularly unnecessary proteins, are removed from the solution to be subjected to column chromatography and that SGP remains. The examination was performed using the protein content in the solution and the SGP recovery rate as indices.
- Verification of protein removal performance and SGP recovery rate in defatted egg yolk powder About synthetic silica gel, synthetic silica colloid, general filter aid, additive with protein coagulation action, and additive with proteolytic action, defatted egg yolk powder The protein removal performance with respect to the protein in the inside was evaluated, and the recovery rate against SGP in the defatted egg yolk was evaluated.
- Copolok 200 (Otsuka Foods Co., Ltd.), Copolok 300 (Otsuka Foods Co., Ltd.), and Copolok 306 (Otsuka Foods Co., Ltd.) were used.
- Celite 545 (Imers Minerals California, Inc.), Fibracel BH-40 (Imers Minerals California, Inc.), Topcoperlite No. 31 (Toko Perlite Industry Co., Ltd.), Topco Perlite No. 31 (Toko Perlite Industry Co., Ltd.) was used.
- Tannic acid (Tokyo Chemical Industry Co., Ltd.) was used as an additive having a protein coagulation action.
- Papain (Wako Pure Chemical Industries, Ltd.) was used as an additive having a proteolytic action.
- tannic acid 1% (w / v) was added to the dispensing solution, and the mixture was stirred at room temperature for 15 minutes and 60 minutes.
- papain 1% (w / v) was added to the dispensing solution, and the mixture was contacted with stirring at room temperature for 15 minutes and 60 minutes and at 50 degrees for 20 hours. All the stirring in the experiment was performed with a reciprocating (reciprocating) shaker. Each treated sample was centrifuged at 10,000 rpm for 5 minutes, and the resulting supernatant was collected, and the protein content and the SGP recovery rate were measured by the following methods. The results are shown in FIGS.
- Copolok 200 shows a certain deproteinization effect and SGP recovery rate, and it is considered that highly pure SGP can be purified at any pH.
- Copolok 300 and 306 a sufficient deproteinization effect and SGP recovery are shown near pH 3 or 4, but at pH 6 or higher, the protein concentration of the solution after treatment was high.
- Colloidal synthetic silica was also shown to have a high deproteinization effect.
- tannic acid and papain which are known to have a deproteinization effect other than synthetic silica, showed a certain deproteinization effect and SGP recovery rate for tannic acid regardless of pH. .
- papain treatment was performed, both the deproteinization effect and the SGP recovery rate fluctuated greatly depending on the pH, indicating that the conditions from acidity were appropriate.
- the recovery rate of SGP decreases, so the treatment time should be several hours or less, and it is considered that about 15 to 60 minutes is appropriate.
- Example 4 Purification of SGP using synthetic silica gel-3> After adding 5 L of water to 500 g of defatted egg yolk powder (Kewpie Corp.) and stirring well for 15 minutes, it was filtered with a filter press (Iwata Machinery Co., Ltd.). After adding 250 g of Mizuka Sorb A751C (Mizusawa Chemical Co., Ltd.) to the obtained water extract and stirring well for 15 minutes, it was filtered with a filter press (Iwata Machinery Co., Ltd.). The obtained filtrate was adjusted to pH 9 with 1M NaOH and stirred well. After standing for 30 minutes, 100 g of Celite 545 (Imers Minerals California, Inc.) was added, and filtration was performed with a filter press (Iwata Kikai Co., Ltd.).
- the obtained glycopeptide was confirmed to be SGP by comparison with a preparation by 1 H-NMR measurement and LC / MS measurement. About obtained SGP, the HPLC analysis was performed on the same conditions as Example 1, and purity was computed (FIG. 14, purity: 98%).
- Example 5 Purification of SGP using synthetic silica gel-4> The glycopeptide was purified from the defatted egg yolk by the same operation as in Example 4, and the column elution fractions 17 to 22 were combined and freeze-dried to obtain 784.1 mg of the glycopeptide. The obtained glycopeptide was confirmed to be SGP by comparison with a preparation by 1 H-NMR measurement and LC / MS measurement. About obtained SGP, the HPLC analysis was performed on the same conditions as Example 1, and purity was computed (FIG. 15, purity: 99%).
- Example 6 Purification of SGP using ODS reverse phase resin> After adding 5 L of water to 500 g of defatted egg yolk powder (Kewpie Corp.) and stirring well for 15 minutes, it was filtered with a filter press (Iwata Machinery Co., Ltd.). After adding 250 g of Mizuka Sorb A751C (Mizusawa Chemical Co., Ltd.) to the obtained water extract and stirring well for 15 minutes, it was filtered with a filter press (Iwata Machinery Co., Ltd.). The obtained filtrate was adjusted to pH 6.5 with 1M NaOH and stirred well.
- Celite 545 (Imers Minerals California, Inc.) was added, and filtration was performed with a filter press (Iwata Kikai Co., Ltd.). Wakogel 100C18 (Wako Pure Chemical Industries, Ltd.) 192 mL (35 ⁇ ⁇ 200 mm) was packed in the column as an ODS-based reverse phase resin, and the resin was washed with acetonitrile and subsequently with water, and then equilibrated with 20 mM HCOONH 4 .
- the filtrate obtained above was equilibrated with the resin at a flow rate of 50 mL / min.
- the resin with the filtrate was washed with 2 L of water at a flow rate of 50 mL / min and developed at a flow rate of 1% acetonitrile water (v / v) at 25 mL / min, and the eluate was fractionated every 25 mL.
- Elution fractions 1 to 14 Further, 2% acetonitrile water (v / v) was developed at a flow rate of 25 mL / min, and the eluate was fractionated every 25 mL.
- Elution fraction 15 to 40 The eluted fractions 8 to 24 were combined and freeze-dried to obtain 565.6 mg of glycopeptide.
- the obtained glycopeptide was confirmed to be SGP by comparison with a preparation by 1 H-NMR measurement and LC / MS measurement. About obtained SGP, the HPLC analysis was performed on the same conditions as Example 1, and purity was computed (FIG. 16, purity: 98%).
- Example 7 Purification of SGP using dried egg yolk powder> Dried egg yolk powder no. 1 (Kewpie Co., Ltd.) 500 g was added with 5 L of water and stirred well for 15 minutes, then 1 kg of Celite 545 (Imers Minerals California, Inc.) was added, and the mixture was filtered with a suction filter can (Sugia Magen). It was. After adding 250 g of Mizukasorb A751C (Mizusawa Chemical Co., Ltd.) to the obtained aqueous extract and stirring well for 15 minutes, the mixture was filtered with a suction filter can (Sugiamagen). The obtained filtrate was adjusted to pH 9 with 1M NaOH and stirred well. After standing for 30 minutes, 100 g of Celite 545 (Imers Minerals California, Inc.) was added, and filtration was performed with a suction filter can (Sugiamagen, Inc.).
- the obtained glycopeptide was confirmed to be SGP by comparison with a preparation by 1 H-NMR measurement and LC / MS measurement. About the obtained SGP, the HPLC analysis was performed on the same conditions as Example 1, and purity was computed (FIG. 17, purity: 93%).
- Example 1 Purification of SGP using general filter aid>
- 250 g of Celite 545 Imers Minerals California, Inc.
- a general filter aid instead of synthetic silica gel (Mizukasorb A751C), 250 g of Celite 545 (Imers Minerals California, Inc.), a general filter aid, was used, and column elution fractions 14 to 24 were obtained.
- 955.0 mg of glycopeptide was obtained by lyophilization.
- the obtained glycopeptide was confirmed to be SGP by comparison with a preparation by 1 H-NMR measurement and LC / MS measurement.
- the HPLC analysis was performed on the same conditions as Example 1, and purity was computed (FIG. 18, purity: 83%).
- Celite 545 does not have a deproteinizing effect. Therefore, in this reference example, unnecessary proteins in the solution are not sufficiently removed. As a result, after the separation operation with the synthetic adsorbent, Even so, the purity of the obtained SGP was not sufficient as compared with other examples using a deproteinizing agent. Also from this, in order to obtain high purity SGP, it is necessary to sufficiently remove unnecessary protein in the solution part by mixing and separating the yolk component-containing solution with a filter aid having a deproteinizing effect. was shown to be important.
Landscapes
- Chemical & Material Sciences (AREA)
- Analytical Chemistry (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Biophysics (AREA)
- Biochemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Genetics & Genomics (AREA)
- Medicinal Chemistry (AREA)
- Molecular Biology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Health & Medical Sciences (AREA)
- Peptides Or Proteins (AREA)
Abstract
Description
(1) 以下の工程Aを含むことを特徴とする、シアリルグリコペプチド(SGP)の精製方法、
工程A:鳥類の卵黄成分を含む水性溶液と除タンパク剤を混合させ、溶解液部を得る工程。
(2) 除タンパク剤が、合成シリカ系除タンパク剤、タンパク質凝固作用を有する添加剤、又はタンパク質分解作用を有する添加剤である(1)の方法。
(3) 合成シリカ系除タンパク剤が、合成シリカゲル又は合成シリカコロイドである(2)の方法。
(4) 合成シリカ系除タンパク剤が、粒子径:約1~50μm、比表面積:約100~1500m2/g、細孔容積:約0.5~3ml/g、平均細孔径:約1~50nmを満たす合成シリカゲルである(3)の方法。
(5) 鳥類の卵黄成分を含む水性溶液が、ニワトリの卵黄又は脱脂卵黄の水溶液である、(1)の方法。
(6) 鳥類の卵黄成分を含む水性溶液が、事前に不溶成分が除去された溶液である、(1)の方法。
(7) 工程Aで得られた溶解液部を、SGPを分離可能な樹脂を用いたカラムクロマトグラフィー操作により、SGPを含有する画分を回収する工程を、さらに含む(1)の方法。
(8) SGPを分離可能な樹脂が、逆相樹脂、順相樹脂、イオン交換樹脂、ゲルろ過樹脂又は合成吸着樹脂である(7)の方法。
(9) 合成吸着樹脂が、スチレン-ジビニルベンゼン系合成吸着樹脂、スチレン-ジビニルベンゼン系修飾型合成吸着樹脂、メタクリル系合成吸着樹脂、フェノール系合成吸着樹脂である(8)の方法。
(10) 合成吸着樹脂が、スチレン-ジビニルベンゼン系修飾型合成吸着樹脂である(9)の方法。
(11)(1)乃至(10)のいずれかの方法で精製されたSGPを適切な形態で包装する工程を含む、SGP製品の製造方法。
工程A:鳥類の卵黄成分を含む水性溶液と除タンパク剤を混合させ、溶解液部を得る工程。
<混合・分離>
本発明において、2つ以上の材料を「混合させる」とは全ての材料を接触させ、各材料の成分が均一に分布又は溶解した状態にせしめる操作を意味する。混合させる操作は、上記の混合状態を達成できる操作であれば、特に限定されず、例えば、振とう攪拌、攪拌子による攪拌、攪拌羽による攪拌等を挙げることができる。これらの操作に要する時間は特に限定されず、例えば、10秒以上、好ましくは5分間以上、より好ましくは15分間以上である。この操作を行う際の温度は、各材料に含まれる成分が変質、変性しない温度であれば、特に限定されるものではないが、4℃乃至40℃が好ましい。
本発明において、「溶解液部を得る」とは、溶液又は混合液中に含まれる不溶物を除去し、溶媒中に溶解した溶解液部のみを回収することを意味する。溶解液部と不溶物を分離する操作としては、公知の様々な方法を採用することができる。代表的な分離操作としては、ろ過、遠心分離等が挙げられる。ろ過に用いるフィルターは、ろ紙、ガラスフィルター、メンブレンフィルター、ろ布等を用いることができる。また、ろ過の様式としては、自然ろ過、吸引ろ過、加圧ろ過等を採用することができる。フィルターの種類、ろ過様式、遠心分離の条件[回転数、時間、温度]等は、分離に供される溶液等の状態に応じて、適宜選択することができる。また、溶液からの不溶物の除去効率を向上させるために、分離操作の前に、適宜セライト等のろ過助剤を溶液等に予め混合させた後で、分離操作を行っても良い。
本発明において、「シアリルグリコペプチド(Sialyl GlycoPeptide:以下、「SGP」という):とは、以下の構造式(I)及び配列式(II)で示される、11個の糖からなるシアリルグリカンの還元末端のGlcNAcの1位炭素と、Lys-Val-Ala-Asn-Lys-Thr-(配列番号1)の4位Asnの側鎖アミド基に由来する窒素原子が、β-Nグリコシド結合した、オリゴ糖ペプチドである。
SGPは、鳥類の卵黄に含まれる糖ペプチドであるが、精製されたSGPが市販されており、購入することもできる。例えば、東京化成工業(株)製のSGPのHPLCチャート、LC/MSスペクトル及び1H-NMRスペクトル(実施例1に記載の条件で測定)は、それぞれ図1、図2及び図3に示すようなピークを示すため、これを標準品として、得られた糖ペプチドがSGPであることを同定することができる。
本発明において、「SGP製品」とは、SGPを主要な構成の一つとして含む製品であり、例えば、研究試薬、工業用原料、医薬品添加剤、食品添加剤等である。SGP製品として製造される場合、本発明の方法で精製されたSGPは、製品形態に応じた状態(凍結乾燥粉末、溶液等)に処理され、適切な容器に封入さ手、包装され、製品として製造される。本発明の精製方法で得られるSGPは高純度であるため、このようなSGP製品の原料としても有用である。
HPLC:1260 Infinity LC(Agilent Technologies,Inc.)
カラム:L-Column2 ODS 3μm φ3.0×50mm(科学物質評価研究機構)
カラム温度:40℃
移動相A:0.1%HCOOHを含むH2O溶液(v/v)
移動相B:0.1%HCOOHを含むMeCN溶液(v/v)
グラジエント(移動相B%):0%(0分)、10%(5分)、30%(7分)、30%(8分)
流速:0.6ml/分
検出波長:210nm
HPLC:1260 Infinity LC(Agilent Technologies,Inc.)
カラム:Inertsil Amide 3μm φ3.0×75mm(ジーエルサイエンス(株))
カラム温度:40℃
移動相A:0.1%HCOOHを含むH2O溶液(v/v)
移動相B:0.1%HCOOHを含むMeCN溶液(v/v)
グラジエント(移動相B%):70%(0分)、30%(6分)、10%(6.01分)、10%(7.5分)
流速:0.6ml/分
検出波長:210nm。
SGPは、鳥類の卵の卵黄に含まれていることが知られており、含まれる糖鎖構造がヒト型であるため、ヒトが摂取又は服用しても、アレルギー反応を起こしにくい。
本発明において、「除タンパク剤」とは、タンパク質を含む溶液に添加することで、当該溶液中のタンパク質量を低減させる効果(本明細書において「除タンパク効果」という)を有する材料を意味する。本発明に用いられる除タンパク剤の除タンパク効果の様式としては、当該溶液中のSGP含有量が低減しないものであれば特に限定されず、例えば合成シリカのようにタンパク質を吸着するもの、タンニン酸のようにタンパク質凝固作用を有するもの、パパインのようにタンパク質分解作用を有するもの等、様々な除タンパク剤を採用することができるが、好ましくは、タンパク質を吸着させる除タンパク剤であり、より好ましくは、合成シリカ系除タンパク剤である。
本発明において、卵黄成分含有溶液と除タンパク剤を混合させる際の混合比率は、用いる除タンパク剤の種類により異なるが、例えば、溶液量に対して除タンパク剤を0.1~50%(v/v又はw/v)で混合させても良い。
また、必要に応じて、除タンパク剤と混合させる前の、卵黄成分含有溶液のpHを適宜調製しても良い。除タンパク剤の種類によっては、pH依存的に除タンパク効果や上清へのSGPの回収率が変動するものがあるため、用いる除タンパク剤に合わせて適切なpHを選択することで、SGPの精製効率を向上させることができる。例えば、各種SYLOPUTE、各種ミズカソーブ、各種カープレックス、マイクロドKM-386P等は、pH3~6程度の弱酸性において、除タンパク効果が高く、上清へのSGPの回収率も高い傾向があるため、SGPの精製効率を向上させるためには、卵黄成分含有水性溶液を弱酸性に調整することが好ましい。
卵黄成分溶液と除タンパク剤を混合させた後は、不溶物を分離させ、溶解液部を得る。
上記の除タンパク工程を経て得られた除タンパク溶液から、様々なカラム充填剤を用いて、SGPを精製することができる。このような精製に用いられるカラム充填剤としては、合成吸着樹脂、逆相樹脂、順相樹脂、イオン交換樹脂、ゲルろ過樹脂等を挙げることができる。逆相樹脂としては、ブチル基(C4)、オクチル基(C8),オクタデシル基(C18)、トリアコンチル基(C30)、フェニル基等の疎水性官能基を、シリカゲルの基材へ付加させた樹脂であり、特にオクタデシル基を付加したODS系逆相樹脂(Wakogel 100C18(和光純薬工業(株))を用いたSGPの精製については、特許文献1に記載されている。また、イオン交換樹脂であるToyopearl DEAE-650M(東ソー(株))、CM-Sephadex C-25(GE Healthcare UK Ltd.)、Dowex 50Wx2(The Dow Chemical Company)を用いたSGPの精製、ゲルろ過樹脂であるSephadex G-50(GE Healthcare UK Ltd.)、Sephadex G-25(GE Healthcare UK Ltd.)を用いたSGPの精製については、非特許文献1に、それぞれ記載されており、これらの文献に記載の条件を参考に、適宜精製することができる。
本発明は、精製工程におけるカラム充填剤として、合成吸着樹脂を採用するSGPの精製方法を提供する。合成吸着樹脂とは、多孔質架橋構造ポリマーからなる充填剤であり、ポリマーの種類により、スチレン-ジビニルベンゼン系合成吸着剤、スチレン-ジビニルベンゼン系修飾型合成吸着樹脂、メタクリル系合成吸着樹脂、フェノール系合成吸着樹脂等が挙げられる。SGPの精製に利用できることが知られていたODS系逆相樹脂等の充填剤は、シリカゲルを基材とするため、アルカリ性溶液を用いた洗浄ができない。そのため有機溶媒を用いた洗浄だけでは不純物の除去が不十分であるため、再利用することができなかった。しかし、カラム充填剤として、合成吸着樹脂を採用することによって、有機溶媒を用いた洗浄に加え、アルカリ性溶液を用いた洗浄により樹脂回生が可能であることから、不純物の除去が十分に行なうことができ、合成吸着樹脂を再利用することが可能である。このような合成吸着樹脂としては、SGPを吸着できるものであれば様々な合成吸着樹脂を採用することができるが、好ましくは、スチレン-ジビニルベンゼン系合成吸着樹脂であり、より好ましくはスチレン-ジビニルベンゼン系修飾型合成吸着樹脂である。具体的な製品としてはSEPABEADS SP207SS(三菱化学(株))等を挙げることができる。
<実施例1.合成シリカゲルを用いたSGPの精製―1>
脱脂卵黄粉(キユーピー(株))500gに水5Lを添加し、15分間よく撹拌した後、フィルタープレス(薮田機械(株))でろ過を行なった。
得られたろ液は1M-NaOHでpH9に調整し、よく攪拌した。30分間放置した後、セライト545(Imerys Minerals California,Inc.) 100gを添加し、フィルタープレス(薮田機械(株))でろ過を行なった。
溶出画分18乃至26を合わせて、凍結乾燥することで、764.4mgの糖ペプチドを得た。
HPLC:1260 Infinity LC(Agilent Technologies,Inc.)
カラム:L-Column2 ODS 3μm φ3.0×50mm(科学物質評価研究機構)
カラム温度:40℃
移動相A:0.1%HCOOHを含むH2O溶液(v/v)
移動相B:0.1%HCOOHを含むMeCN溶液(v/v)
グラジエント(移動相B%):0%(0分)、10%(5分)、30%(7分)、30%(8分)
流速:0.6ml/分
検出波長:210nm。
MS:6130 Quadrupole LC/MS(Agilent Technologies,Inc.)
イオン化:ESI
モード:Positive
HPLC:1260 Infinity LC(Agilent Technologies,Inc.)
カラム:L-Column2 ODS 3μm φ3.0×50mm(科学物質評価研究機構)
カラム温度:40℃
移動相A:0.1%HCOOHを含むH2O溶液(v/v)
移動相B:0.1%HCOOHを含むMeCN溶液(v/v)
グラジエント(移動相B%):0%(0分)、10%(5分)、30%(7分)、30%(8分)
流速:0.6ml/分
検出波長:210nm。
NMR:AVANCE500(500MHz、ブルカー・バイオスピン(株))
溶媒:DEUTERIUM OXIDE+0.1%TMSP(euriso-top)。
実施例1と同様の操作により、脱脂卵黄粉から糖ペプチドの精製を行ない、カラム溶出画分20乃至30を合わせて凍結乾燥することで、694.1mgの糖ペプチドを得た。
得られた糖ペプチドは1H-NMR測定及びLC/MS測定による標品との比較により、SGPであることが確認された。
次に、様々な除タンパク剤、様々な一般的なろ過助剤、様々な添加剤のSGP精製への適用可能性について検討した。
本発明の精製方法においては、カラムクロマトグラフィーに供する溶液において、不純物、特に不要なタンパク質が除去され、且つ、SGPが残存していることが重要であるため、除タンパク剤等で処理した後の溶液中のタンパク質含量及びSGP回収率を指標とした検討を行った。
合成シリカゲル、合成シリカコロイド、一般的なろ過助剤、タンパク質凝固作用を持つ添加剤、及び、タンパク分解作用を持つ添加剤について、脱脂卵黄粉中のタンパク質に対するタンパク質除去性能を評価し、また、脱脂卵黄粉中のSGPに対する回収率を評価した。
合成シリカゲルとして、SYLOPUTE202(富士シリシア化学(株))、SYLOPUTE303(富士シリシア化学(株))、SYLOPUTE403(富士シリシア化学(株))、ミズカソーブA751C(水澤化学工業(株))、ミズカソーブC1(水澤化学工業(株))、ミズカソーブC6(水澤化学工業(株))、カープレックスBS-303(DSL.ジャパン(株))、カープレックスBS-306(DSL.ジャパン(株))、マイクロドKM-386P(KD Corporation)を使用した。
合成シリカコロイドとして、コポロック200(大塚食品(株))、コポロック300(大塚食品(株))、コポロック306(大塚食品(株))を使用した。
タンパク質凝固作用を持つ添加剤として、タンニン酸(東京化成工業(株))を使用した。タンパク分解作用を持つ添加剤としてパパイン(和光純薬工業(株))を使用した。
脱脂卵黄粉(キユーピー(株))に対して10倍量の水を添加し(濃度100mg/mL)、15分間よく撹拌した後、FILTER PAPER No.2(東洋濾紙(株))でろ過を行なった。得られた脱脂卵黄水溶液はpH3、pH4、pH5、pH6、pH7、pH8に調整した後、それぞれ10mLを分注した。
合成シリカゲル及び一般的なろ過助剤については、分注液に5%(w/v)添加し、室温で15分及び60分攪拌接触させた。
シリカコロイドについては、分注液に5%(v/v)添加し、室温で15分及び60分攪拌接触させた。
パパインについては、分注液に1%(w/v)添加し、室温で15分及び60分攪拌接触、50度で20時間攪拌接触させた。
実験における攪拌は、全てレシプロ(往復)式シェーカーで行なった。
各処理試料は10,000rpm回転で5分遠心分離し、得られた上澄み液を回収し、以下の方法でタンパク質含有量の測定及びSGP回収率の測定を行った。結果を図8~図13に示す。
スタンダードと上澄み液をそれぞれ15μL分注し、発色液1.5mLをそれぞれに添加して、攪拌後、室温で10分以上保持して、測定した。なお、発色液にはCoomassie Protein Assay Reagent(Thermo Fisher Scientific,Inc.)を使用し、スタンダードには、BSA(牛血清アルブミン、Thermo Fisher Scientific,Inc.)を使用して、測定波長は吸光度595nmとした。結果は、脱脂卵黄水溶液のタンパク質濃度を100%としたときの相対タンパク質濃度(%)を図内に表示した。
実施例1のHPLC条件により分析を行い、SGPのピーク面積値を測定した。同様に、脱脂卵黄水溶液及び各上澄み液各5μLをHPLCへ注入し、実施例1のHPLC条件により分析を行い、SGPのピーク面積値を測定した。SGPの回収率は、同様に、脱脂卵黄水溶液のSGPのピーク面積値を100%としたときの相対ピーク面積値(%)を図内に表示した。
図8~10に示されるように、各種合成シリカゲルで処理した溶液においては、タンパク質濃度が低く、合成シリカが高い除タンパク効果を有することが示された。一方で、当該処理後溶液中のSGPの回収率は高く、SGPは合成シリカには吸着せず、溶液中に溶解していることが示された。また、これらの効果は、処理時の溶液のpHにより若干の影響を受け、酸性よりの条件において、除タンパク効果及びSGP回収率共に高い傾向がある。しかし、いずれの条件においても、処理後の溶液から高純度のSGPが精製できるものと考えられる。
脱脂卵黄粉(キユーピー(株))500gに水5Lを添加し、15分間よく撹拌した後、フィルタープレス(薮田機械(株))でろ過を行なった。
得られた水抽出液にミズカソーブA751C(水澤化学工業(株))250gを添加し、15分間よく攪拌した後、フィルタープレス(薮田機械(株))でろ過を行なった。
得られたろ液は1M-NaOHでpH9に調整し、よく攪拌した。30分間放置した後、セライト545(Imerys Minerals California,Inc.) 100gを添加し、フィルタープレス(薮田機械(株))でろ過を行なった。
上記で得られたろ液を平衡化した該樹脂に、流速50mL/分で付した。ろ液を付した該樹脂を、水2L流速50mL/分で洗浄後、2%アセトン水(v/v)流速25mL/分で展開し、溶出液を25mL毎に分画した。(溶出画分1乃至40)
溶出画分17乃至22を合わせて、凍結乾燥することで、733.8mgの糖ペプチドを得た。
実施例4と同様の操作により、脱脂卵黄粉から糖ペプチドの精製を行ない、カラム溶出画分17乃至22を合せて凍結乾燥することで、784.1mgの糖ペプチドを得た。
得られた糖ペプチドは1H-NMR測定及びLC/MS測定による標品との比較により、SGPであることが確認された。得られたSGPについて、実施例1と同じ条件でHPLC分析を行い、純度を算出した(図15、純度:99%)。
脱脂卵黄粉(キユーピー(株))500gに水5Lを添加し、15分間よく撹拌した後、フィルタープレス(薮田機械(株))でろ過を行なった。
得られた水抽出液にミズカソーブA751C(水澤化学工業(株))250gを添加し、15分間よく攪拌した後、フィルタープレス(薮田機械(株))でろ過を行なった。
得られたろ液は1M-NaOHでpH6.5に調整し、よく攪拌した。30分間放置した後、セライト545(Imerys Minerals California,Inc.) 100gを添加し、フィルタープレス(薮田機械(株))でろ過を行なった。
ODS系逆相樹脂としてWakogel 100C18(和光純薬工業(株))192mL(35Φx200mm)をカラムに充填し、該樹脂をアセトニトリル、続いて水で洗浄後、20mM-HCOONH4で平衡化した。
溶出画分8乃至24を合わせて、凍結乾燥することで、565.6mgの糖ペプチドを得た。
乾燥卵黄粉No.1(キユーピー(株))500gに水5Lを添加し、15分間よく撹拌した後、セライト545(Imerys Minerals California,Inc.) 1kgを添加し、吸引ろ過缶((株)スギヤマゲン)でろ過を行なった。
得られた水抽出液にミズカソーブA751C(水澤化学工業(株))250gを添加し、15分間よく攪拌した後、吸引ろ過缶((株)スギヤマゲン)でろ過を行なった。
得られたろ液は1M-NaOHでpH9に調整し、よく攪拌した。30分間放置した後、セライト545(Imerys Minerals California,Inc.) 100gを添加し、吸引ろ過缶((株)スギヤマゲン)でろ過を行なった。
上記で得られたろ液を平衡化した該樹脂に、流速50mL/分で付した。ろ液を付した該樹脂を、水2L流速50mL/分で洗浄後、2%アセトン水(v/v)流速25mL/分で展開し、溶出液を25mL毎に分画した。(溶出画分1乃至40)
溶出画分18乃至21を合わせて、凍結乾燥することで、212.2mgの糖ペプチドを得た。
実施例4と同様の方法において、合成シリカゲル(ミズカソーブA751C)の代わりに、一般的なろ過助剤であるセライト545(Imerys Minerals California,Inc.)250gを用いて、カラム溶出画分14乃至24を合わせて、凍結乾燥することで、955.0mgの糖ペプチドを得た。
得られた糖ペプチドは1H-NMR測定及びLC/MS測定による標品との比較により、SGPであることが確認された。得られたSGPについて、実施例1と同じ条件でHPLC分析を行い、純度を算出した(図18、純度:83%)。
Claims (11)
- 以下の工程Aを含むことを特徴とする、シアリルグリコペプチドの精製方法、
工程A:鳥類の卵黄成分を含む水性溶液と除タンパク剤を混合させ、溶解液部を得る工程。
- 除タンパク剤が、合成シリカ系除タンパク剤、タンパク質凝固作用を有する添加剤、又は、タンパク質分解作用を有する添加剤、である請求項1の方法。
- 合成シリカ系除タンパク剤が、合成シリカゲル又は合成シリカコロイドである請求項2の方法。
- 合成シリカ系除タンパク剤が、粒子径:約1~50 μm、比表面積:約100~1500 m2/g、細孔容積:約0.5~3 ml/g、平均細孔径:約1~50 nmを満たす合成シリカゲルである、、請求項3の方法。
- 鳥類の卵黄成分を含む水性溶液が、ニワトリの卵黄または脱脂卵黄の水溶液である、請求項1の方法。
- 鳥類の卵黄成分を含む水性溶液が、事前に不溶成分が除去された溶液である、請求項1の方法。
- 工程Aで得られた溶解液部を、シアリルグリコペプチドを分離可能な樹脂を用いたカラムクロマトグラフィーにより、シアリルグリコペプチドを含有する画分を回収する工程を、さらに含む請求項1の方法。
- シアリルグリコペプチドを分離可能な樹脂が、逆相樹脂、順相樹脂、イオン交換樹脂、ゲルろ過樹脂または合成吸着樹脂である請求項7の方法。
- 合成吸着樹脂が、スチレン-ジビニルベンゼン系合成吸着樹脂、スチレン-ジビニルベンゼン系修飾型合成吸着樹脂、メタクリル系合成吸着樹脂またはフェノール系合成吸着樹脂である請求項8の方法。
- 合成吸着樹脂が、スチレン-ジビニルベンゼン系修飾型合成吸着樹脂である請求項9の方法。
- 請求項1乃至10のいずれかの方法で精製されたSGPを適切な形態で包装する工程を含む、SGP製品の製造方法。
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP14817084.8A EP3015473B1 (en) | 2013-06-28 | 2014-06-27 | Method for purifying oligosaccharide peptide |
| JP2015524139A JP6368305B2 (ja) | 2013-06-28 | 2014-06-27 | オリゴ糖ペプチドの精製方法 |
| US14/392,207 US20160168204A1 (en) | 2013-06-28 | 2014-06-27 | Method for purifying oligosaccharide peptide |
| ES14817084T ES2906120T3 (es) | 2013-06-28 | 2014-06-27 | Procedimiento de purificación del péptido oligosacárido |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2013-136619 | 2013-06-28 | ||
| JP2013136619 | 2013-06-28 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2014208742A1 true WO2014208742A1 (ja) | 2014-12-31 |
Family
ID=52142065
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2014/067224 WO2014208742A1 (ja) | 2013-06-28 | 2014-06-27 | オリゴ糖ペプチドの精製方法 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US20160168204A1 (ja) |
| EP (1) | EP3015473B1 (ja) |
| JP (1) | JP6368305B2 (ja) |
| ES (1) | ES2906120T3 (ja) |
| TW (1) | TW201534613A (ja) |
| WO (1) | WO2014208742A1 (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPWO2017110984A1 (ja) * | 2015-12-25 | 2018-10-18 | 第一三共株式会社 | 限外ろ過膜を用いたオリゴ糖ペプチドの精製法 |
| WO2022191313A1 (ja) | 2021-03-12 | 2022-09-15 | 第一三共株式会社 | 糖鎖及び糖鎖を含む医薬品の製造方法 |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP4366853A1 (en) * | 2021-07-06 | 2024-05-15 | Waters Technologies Corporation | Use of neutral ph mobile phases in reversed phase chromatography of acidic peptides |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH06245784A (ja) * | 1993-02-19 | 1994-09-06 | Taiyo Kagaku Co Ltd | シアル酸及びシアル酸誘導体含有組成物の製造方法 |
| WO1996002255A1 (fr) | 1994-07-15 | 1996-02-01 | Taiyo Kagaku Co., Ltd. | Composition medicamenteuse contenant un derive d'acide sialique |
| JP2002121138A (ja) * | 2000-10-12 | 2002-04-23 | Taiyo Kagaku Co Ltd | 腸管感染症予防組成物 |
| WO2005097155A1 (ja) * | 2004-04-08 | 2005-10-20 | Takara Bio Inc. | 神経突起伸長誘導剤 |
| WO2011027868A1 (ja) | 2009-09-03 | 2011-03-10 | 公益財団法人野口研究所 | 11糖シアリルオリゴ糖ペプチドの製造方法 |
| JP2012191932A (ja) * | 2011-03-03 | 2012-10-11 | Asahi Kasei Corp | 11糖シアリルオリゴ糖アスパラギンの製造方法 |
| JP2012224577A (ja) * | 2011-04-19 | 2012-11-15 | Asahi Kasei Corp | 糖ペプチド誘導体及びその製造方法 |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5877894A (ja) * | 1981-11-05 | 1983-05-11 | Mitsui Toatsu Chem Inc | 蛋白質の除去方法 |
| JPH0899988A (ja) * | 1994-09-29 | 1996-04-16 | Takehiko Yamamoto | シアル酸類含有オリゴ糖の製造法 |
| US6680376B2 (en) * | 2000-12-08 | 2004-01-20 | Good Biotech Corporation | Process for selectively isolating avian immunoglobulins |
| PL2684589T3 (pl) * | 2006-07-14 | 2022-11-21 | Imerys Filtration Minerals, Inc. | Sposób wytwarzania kompozycji do odfiltrowywania i usuwania cząstek i/lub składników z płynu |
| JP4682377B2 (ja) * | 2009-10-06 | 2011-05-11 | 独立行政法人農業・食品産業技術総合研究機構 | 植物からのシアル酸含有化合物の抽出法 |
| KR20100032675A (ko) * | 2008-09-18 | 2010-03-26 | 김모정 | 난황유를 포함하는 치질 치료용 좌약 및 이의 제조방법 |
| WO2010067593A1 (ja) * | 2008-12-09 | 2010-06-17 | 国立大学法人 北海道大学 | グルコースを主成分とする糖含有液の製造方法 |
-
2014
- 2014-06-26 TW TW103122019A patent/TW201534613A/zh unknown
- 2014-06-27 JP JP2015524139A patent/JP6368305B2/ja active Active
- 2014-06-27 WO PCT/JP2014/067224 patent/WO2014208742A1/ja active Application Filing
- 2014-06-27 EP EP14817084.8A patent/EP3015473B1/en active Active
- 2014-06-27 ES ES14817084T patent/ES2906120T3/es active Active
- 2014-06-27 US US14/392,207 patent/US20160168204A1/en not_active Abandoned
Patent Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH06245784A (ja) * | 1993-02-19 | 1994-09-06 | Taiyo Kagaku Co Ltd | シアル酸及びシアル酸誘導体含有組成物の製造方法 |
| WO1996002255A1 (fr) | 1994-07-15 | 1996-02-01 | Taiyo Kagaku Co., Ltd. | Composition medicamenteuse contenant un derive d'acide sialique |
| JP2002121138A (ja) * | 2000-10-12 | 2002-04-23 | Taiyo Kagaku Co Ltd | 腸管感染症予防組成物 |
| WO2005097155A1 (ja) * | 2004-04-08 | 2005-10-20 | Takara Bio Inc. | 神経突起伸長誘導剤 |
| WO2011027868A1 (ja) | 2009-09-03 | 2011-03-10 | 公益財団法人野口研究所 | 11糖シアリルオリゴ糖ペプチドの製造方法 |
| JP2011162762A (ja) * | 2009-09-03 | 2011-08-25 | Asahi Kasei Corp | 11糖シアリルオリゴ糖ペプチドの製造方法 |
| JP2012191932A (ja) * | 2011-03-03 | 2012-10-11 | Asahi Kasei Corp | 11糖シアリルオリゴ糖アスパラギンの製造方法 |
| JP2012224577A (ja) * | 2011-04-19 | 2012-11-15 | Asahi Kasei Corp | 糖ペプチド誘導体及びその製造方法 |
Non-Patent Citations (5)
| Title |
|---|
| AKIRA SEKO ET AL., BIOCHIMICA ET BIOPHYSICA ACTA, vol. 1335, 1997, pages 23 - 32 |
| BRADFORD, M. M., ANAL. BIOCHEM., vol. 72, 1976, pages 248 - 254 |
| KOKETSU, M. ET AL.: "An efficient preparation and structural characterization of sialylglycopeptides from protease treated egg yolk.", J. CARBOHYDR. CHEM., vol. 14, no. 6, August 1995 (1995-08-01), pages 833 - 841, XP008182588 * |
| See also references of EP3015473A4 |
| SHUICHI SUGAWARA ET AL.: "Sialyloligosaccharide Peptide (SGP) no Kenkyu Kaihatsu", ANNUAL REPORT OF THE NOGUCHI INSTITUTE, vol. 54, 30 September 2011 (2011-09-30), pages 44 - 48, XP008182573 * |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPWO2017110984A1 (ja) * | 2015-12-25 | 2018-10-18 | 第一三共株式会社 | 限外ろ過膜を用いたオリゴ糖ペプチドの精製法 |
| WO2022191313A1 (ja) | 2021-03-12 | 2022-09-15 | 第一三共株式会社 | 糖鎖及び糖鎖を含む医薬品の製造方法 |
| KR20230157983A (ko) | 2021-03-12 | 2023-11-17 | 다이이찌 산쿄 가부시키가이샤 | 당사슬 및 당사슬을 포함하는 의약품의 제조 방법 |
Also Published As
| Publication number | Publication date |
|---|---|
| JPWO2014208742A1 (ja) | 2017-02-23 |
| ES2906120T3 (es) | 2022-04-13 |
| EP3015473B1 (en) | 2021-12-29 |
| JP6368305B2 (ja) | 2018-08-01 |
| EP3015473A4 (en) | 2017-02-22 |
| EP3015473A1 (en) | 2016-05-04 |
| US20160168204A1 (en) | 2016-06-16 |
| TW201534613A (zh) | 2015-09-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Martínez-Maqueda et al. | Extraction/fractionation techniques for proteins and peptides and protein digestion | |
| ES2743156T3 (es) | Método simple para eliminación simultánea de múltiples impurezas a partir de sobrenadantes de cultivo a niveles ultrabajos | |
| JP5566226B2 (ja) | 11糖シアリルオリゴ糖ペプチドの製造方法 | |
| EP2871968B1 (en) | Potato protein isolates | |
| JP6368305B2 (ja) | オリゴ糖ペプチドの精製方法 | |
| RU2010105312A (ru) | Хроматографические способы | |
| Baieli et al. | Isolation of lactoferrin from whey by dye-affinity chromatography with Yellow HE-4R attached to chitosan mini-spheres | |
| JP2007526225A (ja) | 不燃性溶媒によるタンパク質−リポ多糖類複合体からのリポ多糖類の除去 | |
| Sheng et al. | Retention mechanism and enrichment of glycopeptides on titanium dioxide | |
| JP6887957B2 (ja) | 限外ろ過膜を用いたオリゴ糖ペプチドの精製法 | |
| Baieli et al. | Efficient wheat germ agglutinin purification with a chitosan‐based affinity chromatographic matrix | |
| CN103936850B (zh) | 用于鸡卵黄免疫球蛋白提取的复合型去脂液及应用 | |
| US2442452A (en) | Method of isolating lysozyme from its naturally occurring mixtures with other biologic components | |
| Boxi et al. | Current trends in protein purification: A review | |
| EP1941051A1 (en) | Method for concentrating, purifying and removing prion protein | |
| JP2019182757A (ja) | 9糖シアリルオリゴ糖ペプチド及びその製造方法 | |
| CN101750242A (zh) | 用于检测肉制品和水产品中有害物质的样品预处理方法 | |
| JP2010148442A (ja) | 硫酸化糖鎖を有する糖ペプチドを濃縮する方法及びそのためのキット | |
| JP5282207B2 (ja) | 新規レクチン及びその製造方法並びに糖鎖検出方法 | |
| RU2803848C1 (ru) | Способ хроматографической очистки экзосом и их разделения от вирионов вируса гриппа А на основе гидрофобного взаимодействия с сорбентом | |
| CN103561758A (zh) | 通过沉降灭活/去除凝血因子的方法 | |
| US20090258419A1 (en) | Method for removing prion protein | |
| US9605052B2 (en) | Method for extracting IgY (γ-livetin) from egg yolk | |
| JP2010172880A (ja) | 固定化金属イオンアフィニティー吸着によって回収された金属結合性物質による重金属汚染土壌の浄化方法 | |
| Hagen-Braun et al. | Characterization of the Murine Myelin Basic Protein: Structural Analysis of an Intrinsically Unstructured Protein |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 14817084 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2015524139 Country of ref document: JP Kind code of ref document: A |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2014817084 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 14392207 Country of ref document: US |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |