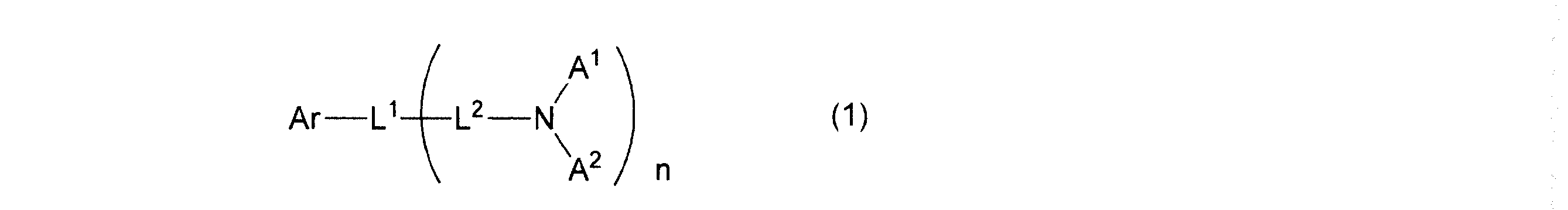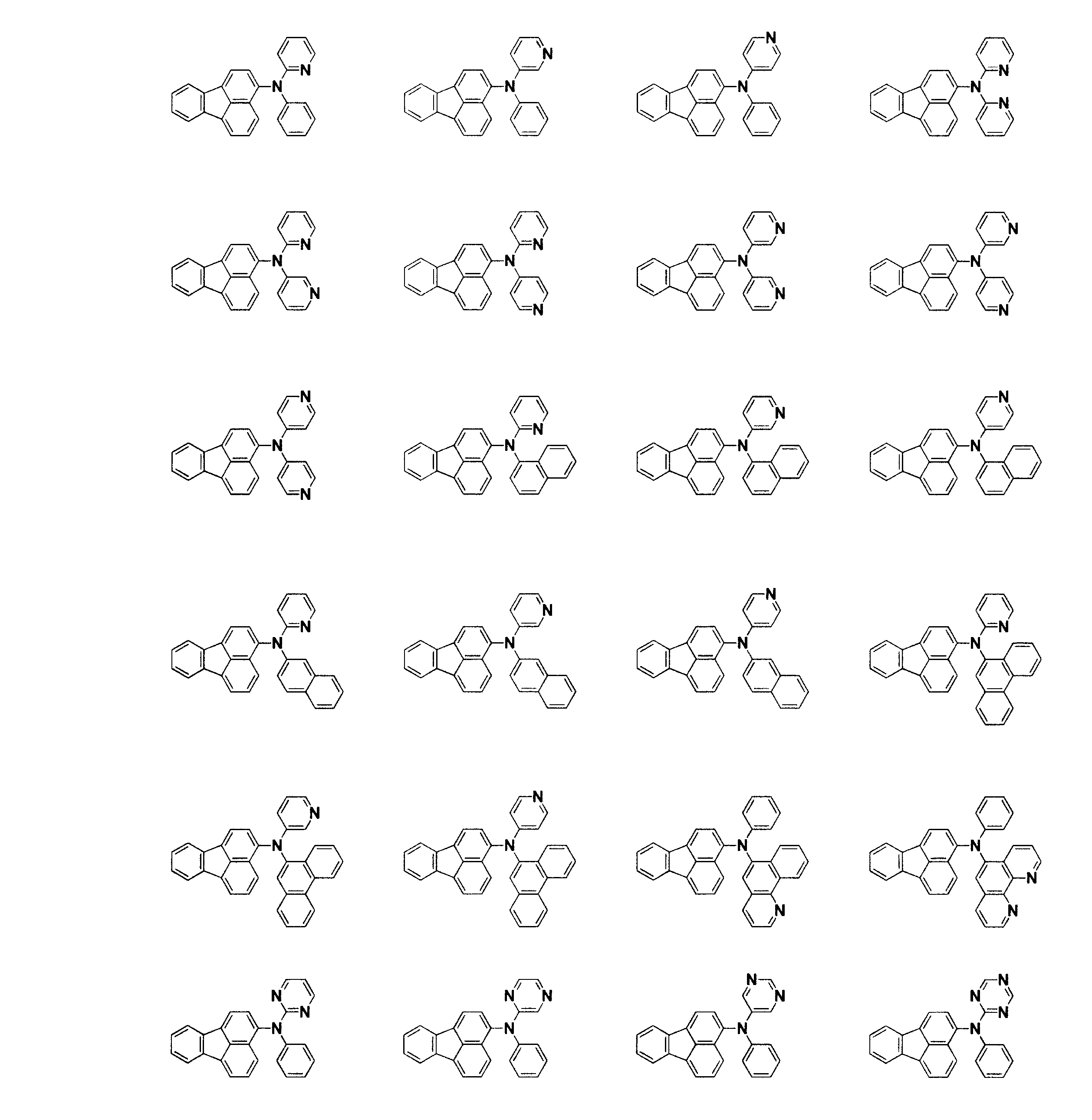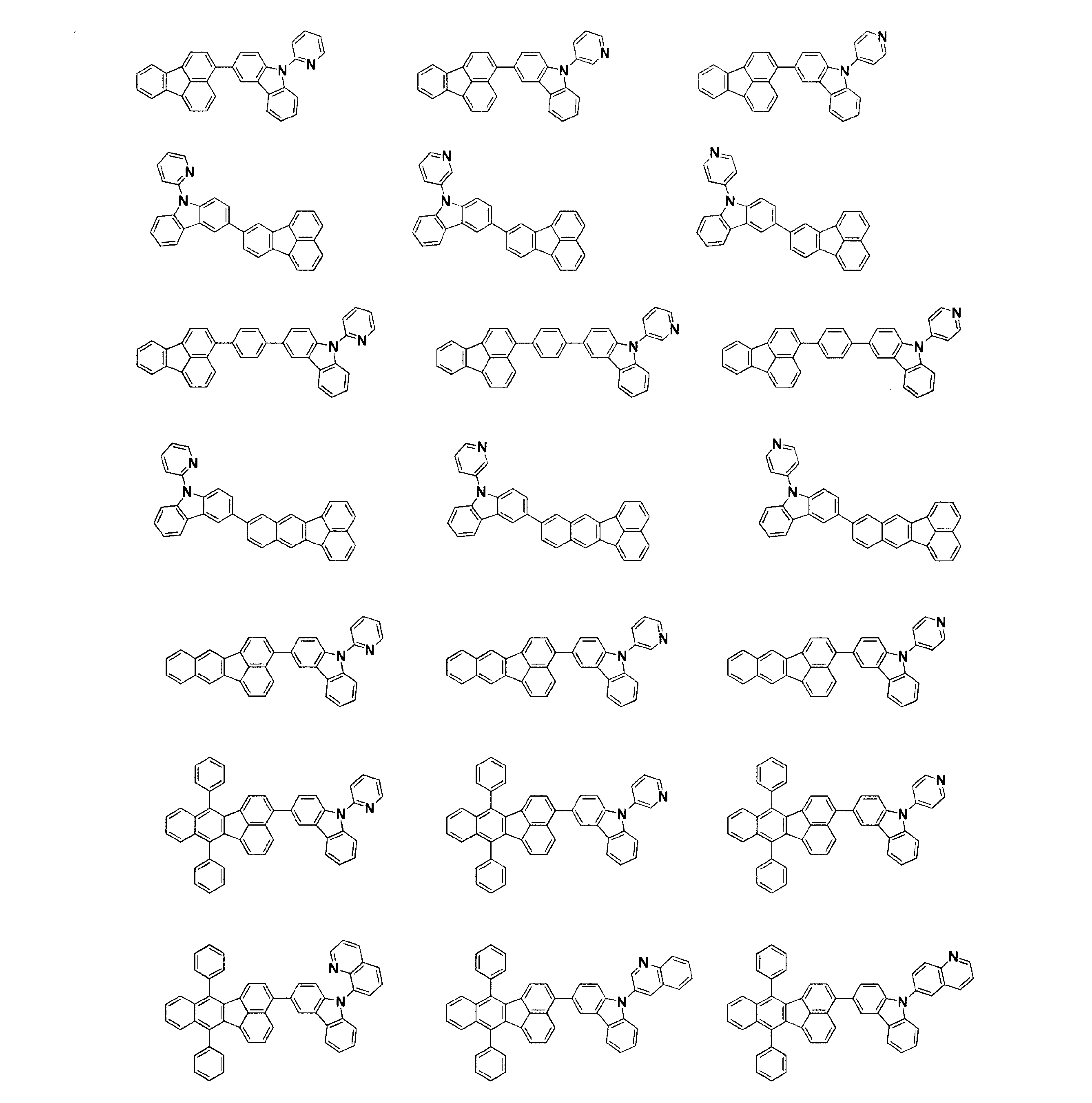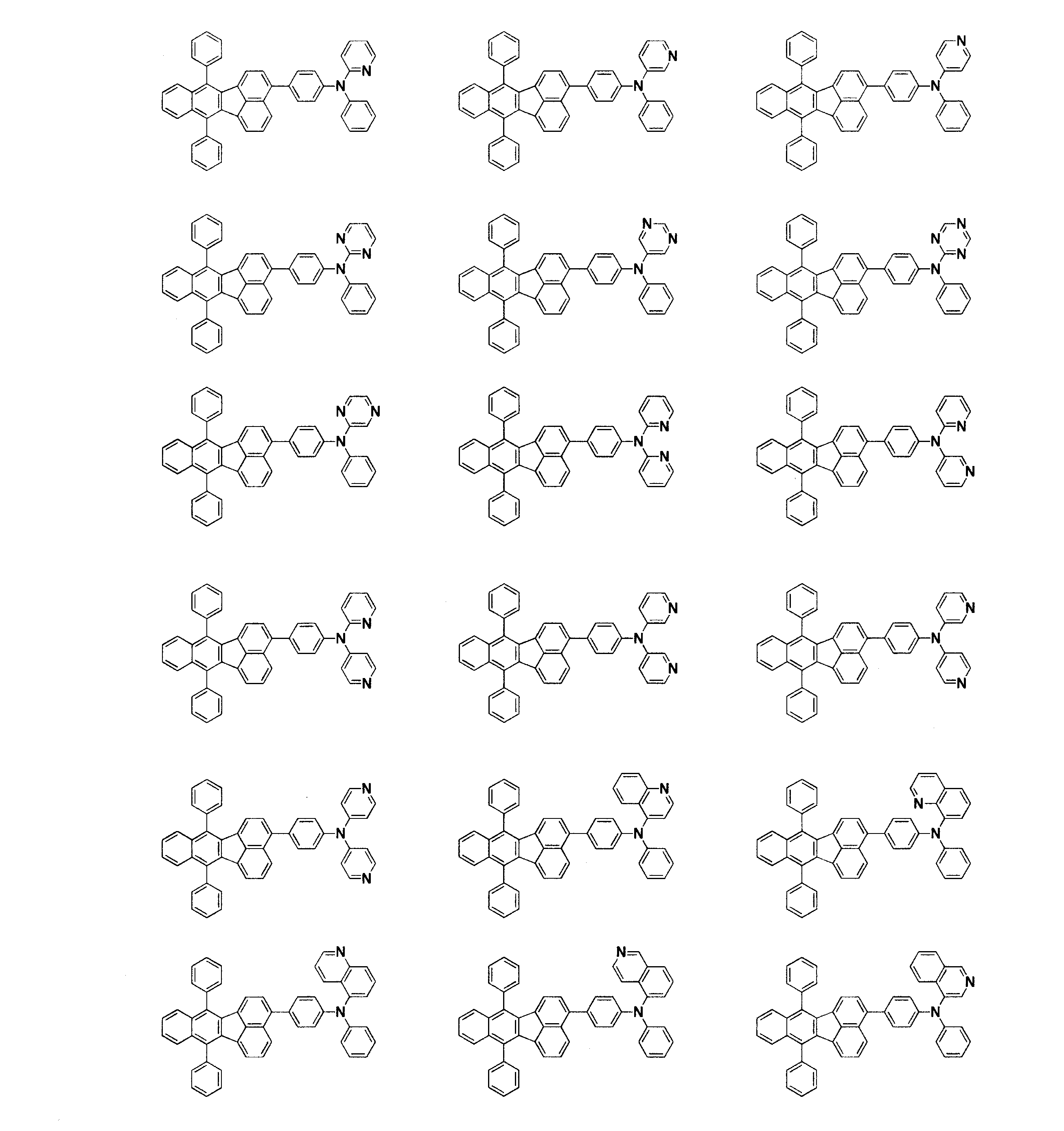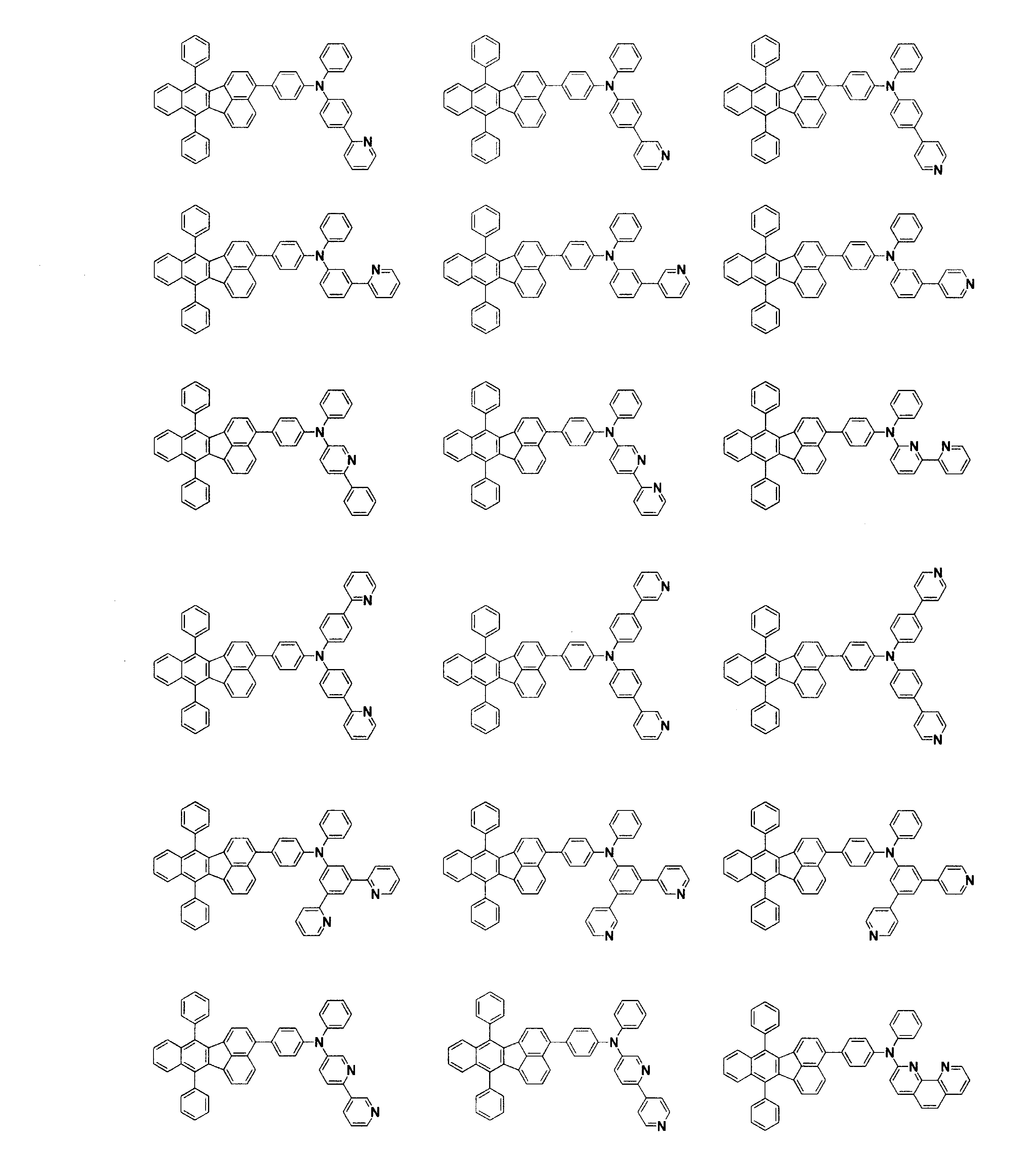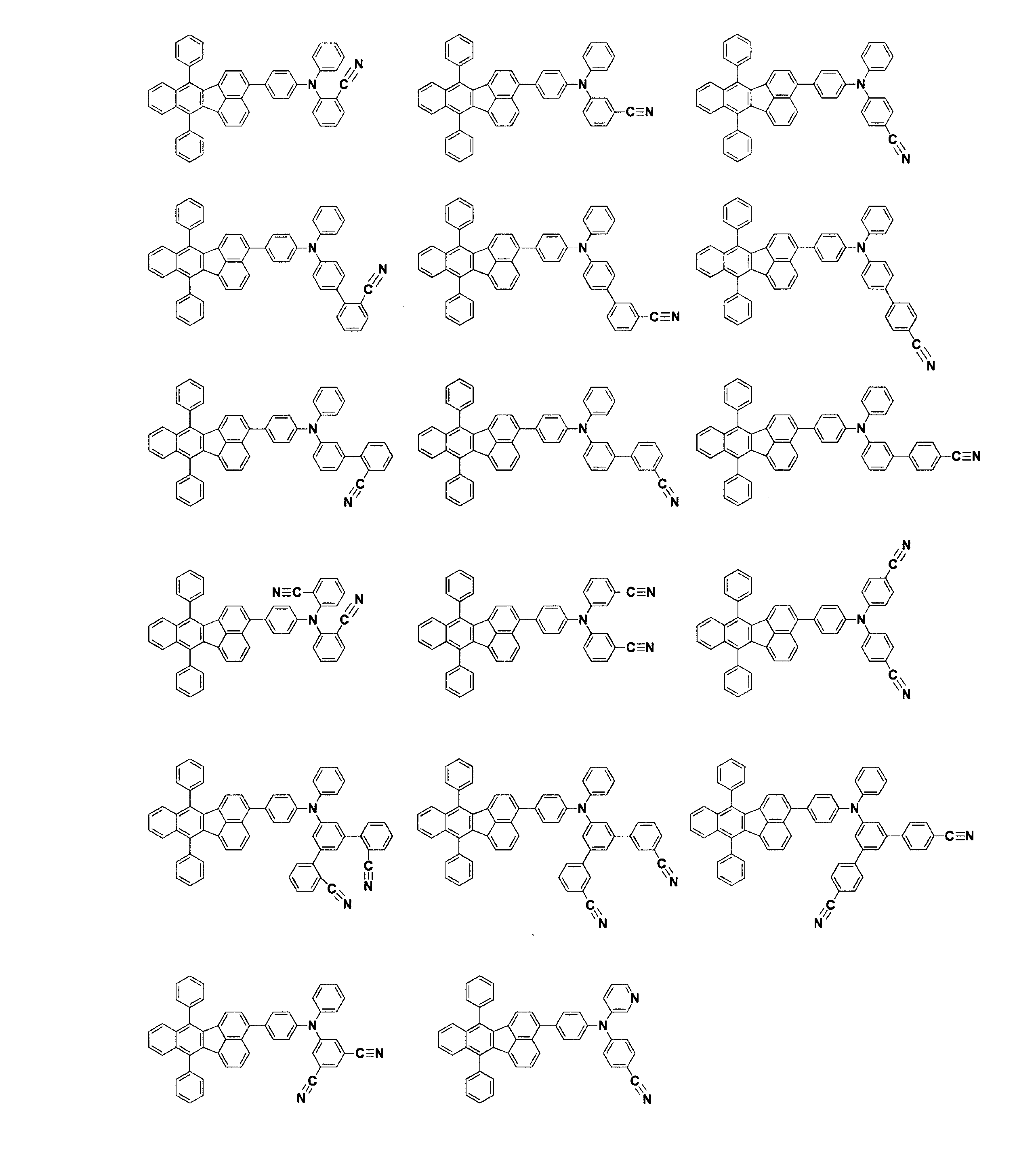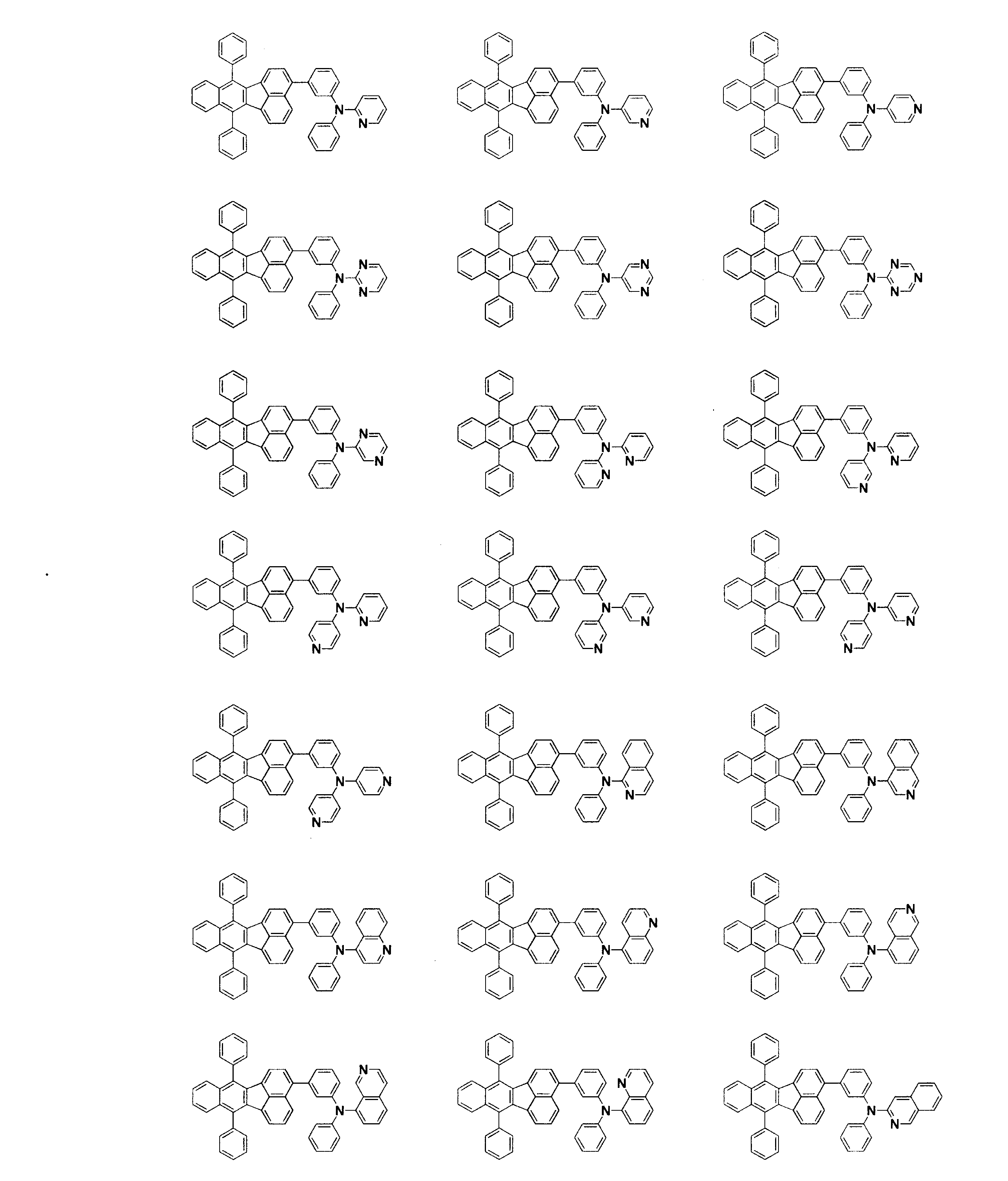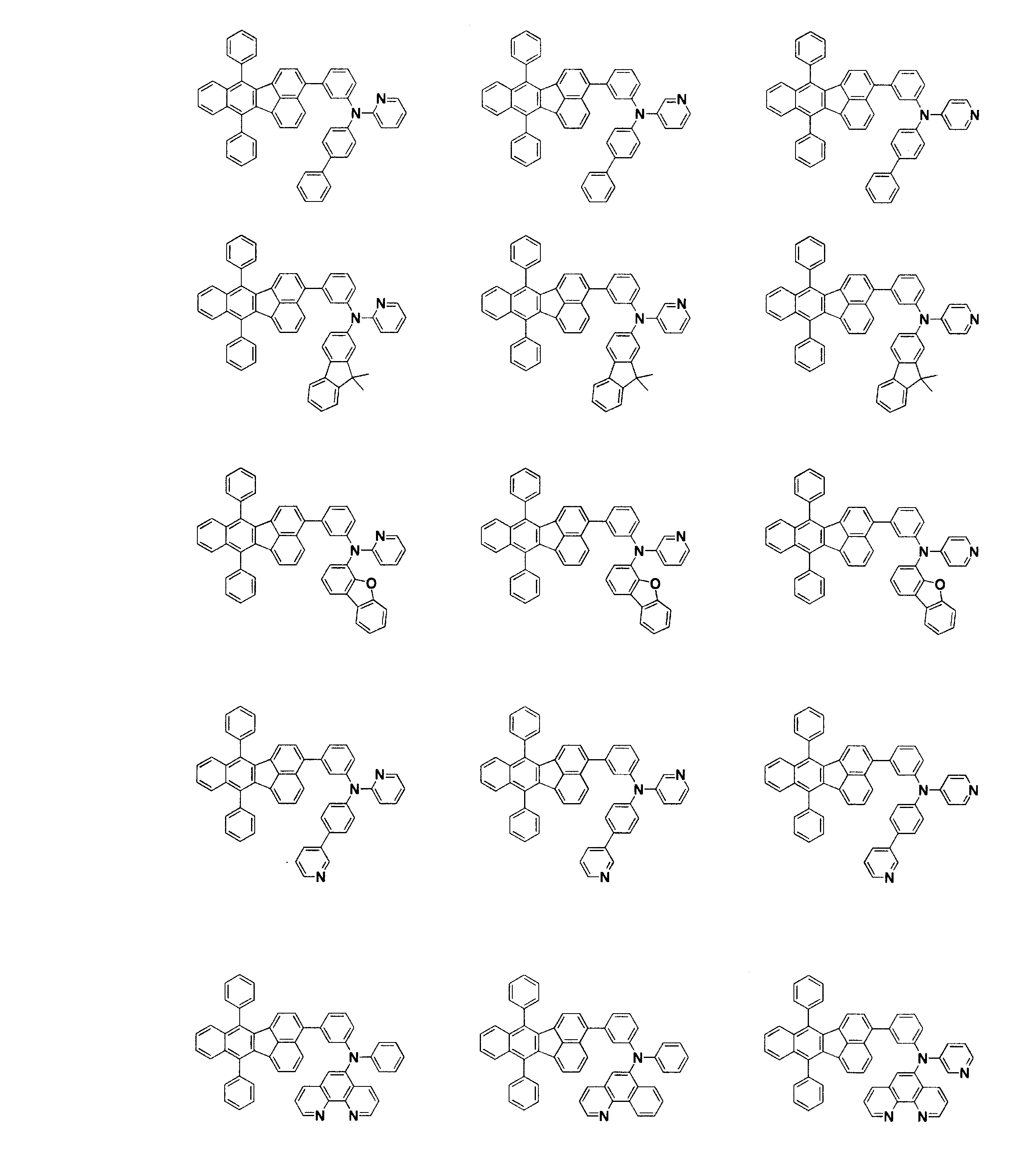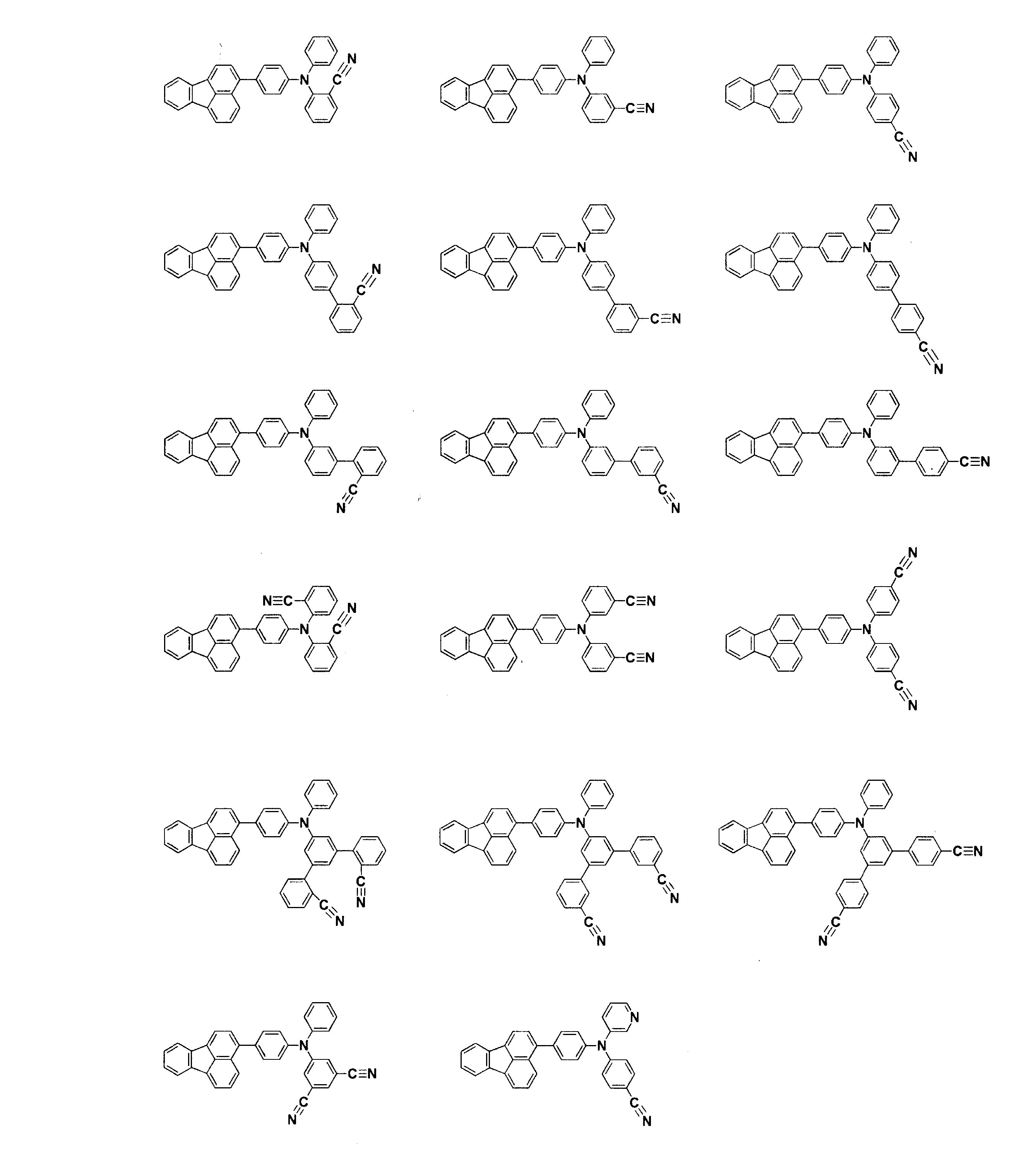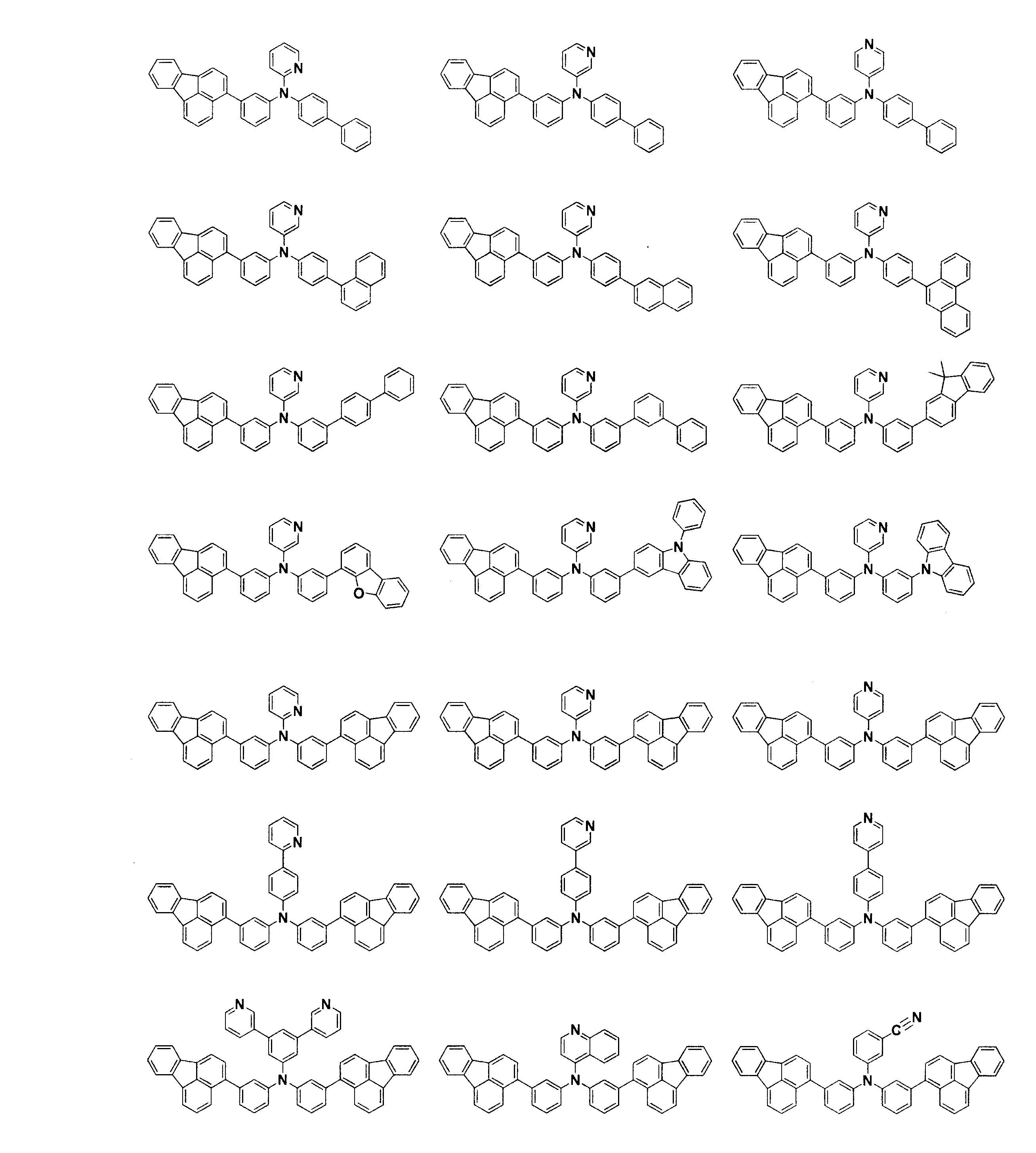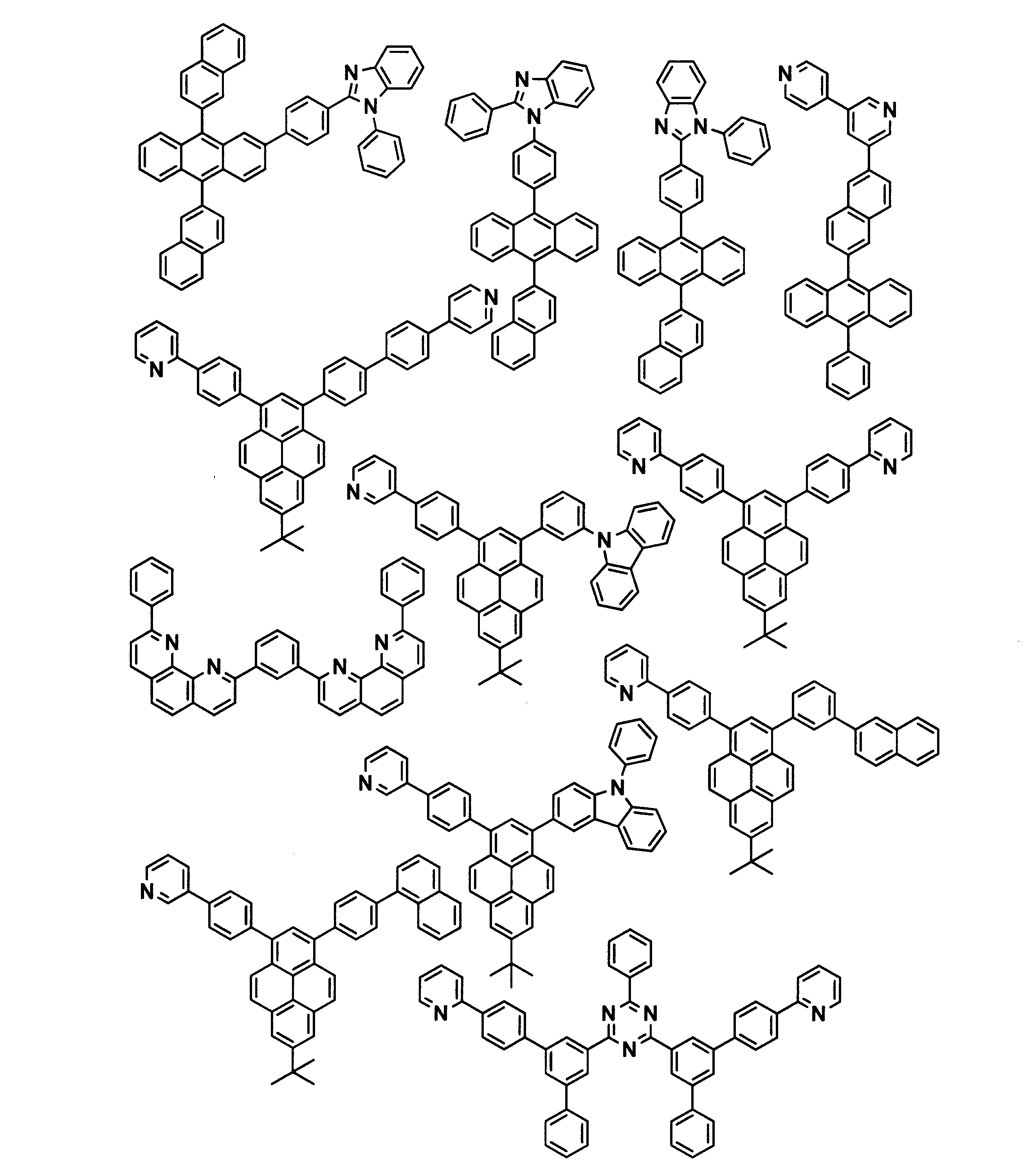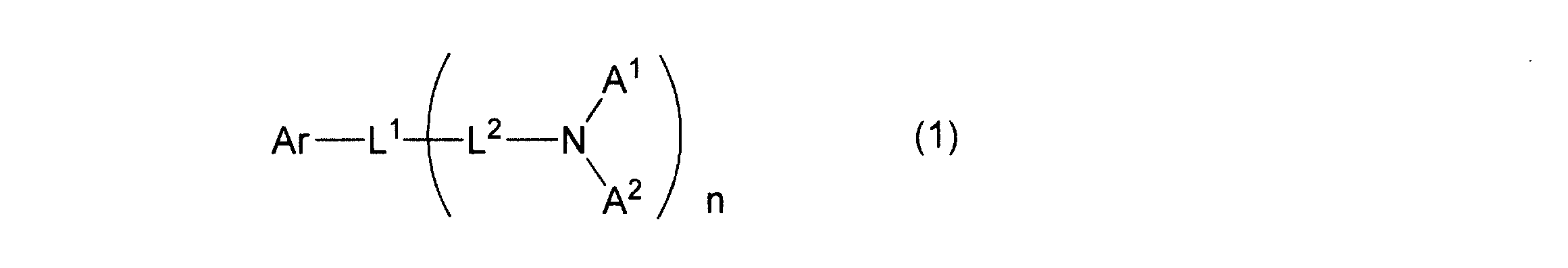WO2014057874A1 - フルオランテン誘導体、それを含有する発光素子材料および発光素子 - Google Patents
フルオランテン誘導体、それを含有する発光素子材料および発光素子 Download PDFInfo
- Publication number
- WO2014057874A1 WO2014057874A1 PCT/JP2013/077047 JP2013077047W WO2014057874A1 WO 2014057874 A1 WO2014057874 A1 WO 2014057874A1 JP 2013077047 W JP2013077047 W JP 2013077047W WO 2014057874 A1 WO2014057874 A1 WO 2014057874A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- group
- ring
- substituted
- electron
- aryl
- Prior art date
Links
- 0 Cc1c(-c(c-2c3*)c(*)c4c3c(*)c(*)c(*)c4*)c3c-2c(N)c(*)c(*)c3c(C)c1* Chemical compound Cc1c(-c(c-2c3*)c(*)c4c3c(*)c(*)c(*)c4*)c3c-2c(N)c(*)c(*)c3c(C)c1* 0.000 description 1
- NOZJMICHIDECFV-UHFFFAOYSA-N c(cc1)cc(-c2ccc3)c1-c(cc1)c2c3c1N(c1cccc2c1cccc2)c1ccccn1 Chemical compound c(cc1)cc(-c2ccc3)c1-c(cc1)c2c3c1N(c1cccc2c1cccc2)c1ccccn1 NOZJMICHIDECFV-UHFFFAOYSA-N 0.000 description 1
- FLMPVSFNSNHCML-UHFFFAOYSA-N c(cc1)cc(-c2ccc3)c1-c(cc1)c2c3c1N(c1cccnc1)c1cccc2c1cccc2 Chemical compound c(cc1)cc(-c2ccc3)c1-c(cc1)c2c3c1N(c1cccnc1)c1cccc2c1cccc2 FLMPVSFNSNHCML-UHFFFAOYSA-N 0.000 description 1
- NFCLAYODCWEEQM-UHFFFAOYSA-N c(cc1)cc(-c2ccc3)c1-c(cc1)c2c3c1N(c1cccnc1)c1ccccn1 Chemical compound c(cc1)cc(-c2ccc3)c1-c(cc1)c2c3c1N(c1cccnc1)c1ccccn1 NFCLAYODCWEEQM-UHFFFAOYSA-N 0.000 description 1
- PVHIIGQQVHSDDB-UHFFFAOYSA-N c(cc1)cc(-c2ccc3)c1-c(cc1)c2c3c1N(c1ccncc1)c1cccc2c1cccc2 Chemical compound c(cc1)cc(-c2ccc3)c1-c(cc1)c2c3c1N(c1ccncc1)c1cccc2c1cccc2 PVHIIGQQVHSDDB-UHFFFAOYSA-N 0.000 description 1
- NEBAVNBLYNUVHC-UHFFFAOYSA-N c(cc1)cc(-c2ccc3)c1-c(cc1)c2c3c1N(c1ccncc1)c1ccccn1 Chemical compound c(cc1)cc(-c2ccc3)c1-c(cc1)c2c3c1N(c1ccncc1)c1ccccn1 NEBAVNBLYNUVHC-UHFFFAOYSA-N 0.000 description 1
- LQZIXRABGMBKSV-UHFFFAOYSA-N c(cc1)cc(-c2ccc3)c1-c(cc1)c2c3c1N(c1ccncc1)c1cccnc1 Chemical compound c(cc1)cc(-c2ccc3)c1-c(cc1)c2c3c1N(c1ccncc1)c1cccnc1 LQZIXRABGMBKSV-UHFFFAOYSA-N 0.000 description 1
- YSRZAHYKCPXWDP-UHFFFAOYSA-N c(cc1)cc(-c2cccc3c22)c1-c2ccc3N(c1cc2ccccc2c2c1cccc2)c1ccccn1 Chemical compound c(cc1)cc(-c2cccc3c22)c1-c2ccc3N(c1cc2ccccc2c2c1cccc2)c1ccccn1 YSRZAHYKCPXWDP-UHFFFAOYSA-N 0.000 description 1
- GIQMZXJOYRTMKW-UHFFFAOYSA-N c(cc1)cc(-c2cccc3c22)c1-c2ccc3N(c1ccc(cccc2)c2c1)c1ccccn1 Chemical compound c(cc1)cc(-c2cccc3c22)c1-c2ccc3N(c1ccc(cccc2)c2c1)c1ccccn1 GIQMZXJOYRTMKW-UHFFFAOYSA-N 0.000 description 1
- RRAYHOIQTWBETL-UHFFFAOYSA-N c(cc1)cc(-c2cccc3c22)c1-c2ccc3N(c1ccncc1)c1cc(cccc2)c2c2ccccc12 Chemical compound c(cc1)cc(-c2cccc3c22)c1-c2ccc3N(c1ccncc1)c1cc(cccc2)c2c2ccccc12 RRAYHOIQTWBETL-UHFFFAOYSA-N 0.000 description 1
- QEMIWHYDVMJLKU-UHFFFAOYSA-N c(cc1)cc(-c2cccc3c22)c1-c2ccc3N(c1ccncc1)c1cc(cccc2)c2cc1 Chemical compound c(cc1)cc(-c2cccc3c22)c1-c2ccc3N(c1ccncc1)c1cc(cccc2)c2cc1 QEMIWHYDVMJLKU-UHFFFAOYSA-N 0.000 description 1
- NZOOHROOIAWHFE-UHFFFAOYSA-N c(cc1)ccc1N(c(cc1)c2c3c1-c1ccccc1-c3ccc2)c1ccccn1 Chemical compound c(cc1)ccc1N(c(cc1)c2c3c1-c1ccccc1-c3ccc2)c1ccccn1 NZOOHROOIAWHFE-UHFFFAOYSA-N 0.000 description 1
- RUPRKXPDOPWJIQ-UHFFFAOYSA-N c(cc1)ccc1N(c(cc1)c2c3c1-c1ccccc1-c3ccc2)c1ncccn1 Chemical compound c(cc1)ccc1N(c(cc1)c2c3c1-c1ccccc1-c3ccc2)c1ncccn1 RUPRKXPDOPWJIQ-UHFFFAOYSA-N 0.000 description 1
- LGJFLIIHVDMYOG-UHFFFAOYSA-N c(cc1)ccc1N(c1ccc-2c3c1cccc3-c1c-2cccc1)C1=N[I]=NC=N1 Chemical compound c(cc1)ccc1N(c1ccc-2c3c1cccc3-c1c-2cccc1)C1=N[I]=NC=N1 LGJFLIIHVDMYOG-UHFFFAOYSA-N 0.000 description 1
- PHKKMNDHMDARCF-UHFFFAOYSA-N c(cc1)ccc1N(c1ccc-2c3c1cccc3-c1c-2cccc1)c(c1ccccc11)cc2c1nccc2 Chemical compound c(cc1)ccc1N(c1ccc-2c3c1cccc3-c1c-2cccc1)c(c1ccccc11)cc2c1nccc2 PHKKMNDHMDARCF-UHFFFAOYSA-N 0.000 description 1
- JKRPHYAOVKSCTQ-UHFFFAOYSA-N c(cc1)ccc1N(c1ccc-2c3c1cccc3-c1c-2cccc1)c1cc2cccnc2c2c1cccn2 Chemical compound c(cc1)ccc1N(c1ccc-2c3c1cccc3-c1c-2cccc1)c1cc2cccnc2c2c1cccn2 JKRPHYAOVKSCTQ-UHFFFAOYSA-N 0.000 description 1
- OBUCXYFTNZUIRU-UHFFFAOYSA-N c(cc1)ccc1N(c1ccc-2c3c1cccc3-c1ccccc-21)c1nccnc1 Chemical compound c(cc1)ccc1N(c1ccc-2c3c1cccc3-c1ccccc-21)c1nccnc1 OBUCXYFTNZUIRU-UHFFFAOYSA-N 0.000 description 1
- NTAHSAGWWDMXSR-UHFFFAOYSA-N c(cc1)ccc1N(c1cccnc1)c1ccc-2c3c1cccc3-c1ccccc-21 Chemical compound c(cc1)ccc1N(c1cccnc1)c1ccc-2c3c1cccc3-c1ccccc-21 NTAHSAGWWDMXSR-UHFFFAOYSA-N 0.000 description 1
- YNBLRHLDERNECI-UHFFFAOYSA-N c(cc1)ccc1N(c1ccncc1)c1ccc-2c3c1cccc3-c1ccccc-21 Chemical compound c(cc1)ccc1N(c1ccncc1)c1ccc-2c3c1cccc3-c1ccccc-21 YNBLRHLDERNECI-UHFFFAOYSA-N 0.000 description 1
- GBXZIUBHLVKSCX-UHFFFAOYSA-N c(cc1)ccc1N(c1cncnc1)c1ccc-2c3c1cccc3-c1c-2cccc1 Chemical compound c(cc1)ccc1N(c1cncnc1)c1ccc-2c3c1cccc3-c1c-2cccc1 GBXZIUBHLVKSCX-UHFFFAOYSA-N 0.000 description 1
- KTRALMZGNKPUOP-UHFFFAOYSA-N c(cc1-c2c3c4ccc2)ccc1-c3ccc4N(c1ccccn1)c1ccccn1 Chemical compound c(cc1-c2c3c4ccc2)ccc1-c3ccc4N(c1ccccn1)c1ccccn1 KTRALMZGNKPUOP-UHFFFAOYSA-N 0.000 description 1
- PWJNXGSWQUTNHM-UHFFFAOYSA-N c(cc1-c2ccc3)ccc1-c(cc1)c2c3c1N(c1cc2ccccc2cc1)c1cccnc1 Chemical compound c(cc1-c2ccc3)ccc1-c(cc1)c2c3c1N(c1cc2ccccc2cc1)c1cccnc1 PWJNXGSWQUTNHM-UHFFFAOYSA-N 0.000 description 1
- REEFWAPFNSRPJK-UHFFFAOYSA-N c(cc1-c2ccc3)ccc1-c(cc1)c2c3c1N(c1cccnc1)c1cc(cccc2)c2c2ccccc12 Chemical compound c(cc1-c2ccc3)ccc1-c(cc1)c2c3c1N(c1cccnc1)c1cc(cccc2)c2c2ccccc12 REEFWAPFNSRPJK-UHFFFAOYSA-N 0.000 description 1
- LMOUQAAACHZNTA-UHFFFAOYSA-N c(cc1-c2ccc3)ccc1-c(cc1)c2c3c1N(c1ccncc1)c1ccncc1 Chemical compound c(cc1-c2ccc3)ccc1-c(cc1)c2c3c1N(c1ccncc1)c1ccncc1 LMOUQAAACHZNTA-UHFFFAOYSA-N 0.000 description 1
- UKNSRAPCVVVYSA-UHFFFAOYSA-N c(cc1-c2cccc3c22)ccc1-c2ccc3N(c1cccnc1)c1cccnc1 Chemical compound c(cc1-c2cccc3c22)ccc1-c2ccc3N(c1cccnc1)c1cccnc1 UKNSRAPCVVVYSA-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6572—Polycyclic condensed heteroaromatic hydrocarbons comprising only nitrogen in the heteroaromatic polycondensed ring system, e.g. phenanthroline or carbazole
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C255/00—Carboxylic acid nitriles
- C07C255/49—Carboxylic acid nitriles having cyano groups bound to carbon atoms of six-membered aromatic rings of a carbon skeleton
- C07C255/58—Carboxylic acid nitriles having cyano groups bound to carbon atoms of six-membered aromatic rings of a carbon skeleton containing cyano groups and singly-bound nitrogen atoms, not being further bound to other hetero atoms, bound to the carbon skeleton
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/24—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with substituted hydrocarbon radicals attached to ring carbon atoms
- C07D213/36—Radicals substituted by singly-bound nitrogen atoms
- C07D213/38—Radicals substituted by singly-bound nitrogen atoms having only hydrogen or hydrocarbon radicals attached to the substituent nitrogen atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/60—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D213/72—Nitrogen atoms
- C07D213/74—Amino or imino radicals substituted by hydrocarbon or substituted hydrocarbon radicals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D215/00—Heterocyclic compounds containing quinoline or hydrogenated quinoline ring systems
- C07D215/02—Heterocyclic compounds containing quinoline or hydrogenated quinoline ring systems having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen atoms or carbon atoms directly attached to the ring nitrogen atom
- C07D215/16—Heterocyclic compounds containing quinoline or hydrogenated quinoline ring systems having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen atoms or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D215/38—Nitrogen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B57/00—Other synthetic dyes of known constitution
- C09B57/001—Pyrene dyes
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B57/00—Other synthetic dyes of known constitution
- C09B57/008—Triarylamine dyes containing no other chromophores
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B57/00—Other synthetic dyes of known constitution
- C09B57/10—Metal complexes of organic compounds not being dyes in uncomplexed form
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
-
- H—ELECTRICITY
- H05—ELECTRIC TECHNIQUES NOT OTHERWISE PROVIDED FOR
- H05B—ELECTRIC HEATING; ELECTRIC LIGHT SOURCES NOT OTHERWISE PROVIDED FOR; CIRCUIT ARRANGEMENTS FOR ELECTRIC LIGHT SOURCES, IN GENERAL
- H05B33/00—Electroluminescent light sources
- H05B33/10—Apparatus or processes specially adapted to the manufacture of electroluminescent light sources
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/30—Coordination compounds
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/30—Coordination compounds
- H10K85/341—Transition metal complexes, e.g. Ru(II)polypyridine complexes
- H10K85/342—Transition metal complexes, e.g. Ru(II)polypyridine complexes comprising iridium
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/622—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing four rings, e.g. pyrene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/623—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing five rings, e.g. pentacene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/626—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing more than one polycyclic condensed aromatic rings, e.g. bis-anthracene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/631—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/631—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine
- H10K85/633—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine comprising polycyclic condensed aromatic hydrocarbons as substituents on the nitrogen atom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/631—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine
- H10K85/636—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine comprising heteroaromatic hydrocarbons as substituents on the nitrogen atom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/654—Aromatic compounds comprising a hetero atom comprising only nitrogen as heteroatom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2603/00—Systems containing at least three condensed rings
- C07C2603/02—Ortho- or ortho- and peri-condensed systems
- C07C2603/52—Ortho- or ortho- and peri-condensed systems containing five condensed rings
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1007—Non-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1011—Condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1014—Carbocyclic compounds bridged by heteroatoms, e.g. N, P, Si or B
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1029—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1044—Heterocyclic compounds characterised by ligands containing two nitrogen atoms as heteroatoms
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1059—Heterocyclic compounds characterised by ligands containing three nitrogen atoms as heteroatoms
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1088—Heterocyclic compounds characterised by ligands containing oxygen as the only heteroatom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/14—Carrier transporting layers
- H10K50/15—Hole transporting layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/14—Carrier transporting layers
- H10K50/16—Electron transporting layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/17—Carrier injection layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/80—Constructional details
- H10K50/805—Electrodes
- H10K50/81—Anodes
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/80—Constructional details
- H10K50/805—Electrodes
- H10K50/82—Cathodes
Abstract
Description
化合物[1]の合成
ブロモフルオランテン26.0g、ビス(ピナコラート)ジボロン35.2g、酢酸カリウム27.2g、ジメチルホルムアミド462mLを混合し、窒素置換した。この混合溶液に[1,1’-ビス(ジフェニルホスフィノ)フェロセン]パラジウム(II)ジクロリド・ジクロロメタン錯体0.75gを加え、100℃に加熱した。1時間後、室温に冷却した後、酢酸エチル250mL、トルエン250mL、水250mLを加え分液した。水層を酢酸エチル200mL、トルエン200mLで抽出した後、先の有機層と合わせ、水500mLで3回洗浄した。有機層を硫酸マグネシウムで乾燥し、溶媒を留去した。シリカゲルカラムクロマトグラフィーにより精製し、溶出液をエバポレートし、真空乾燥することにより、中間体Aを16.4g得た。
化合物[1]: 1H-NMR (CDCl3(d=ppm)) δ 7.10-7.25(m,6H),7.32-7.43(m,4H),7.47-7.55(m,3H),7.61-7.67(m,2H),7.90-8.01(m,5H),8.27(d,1H),8.49(d,1H)。
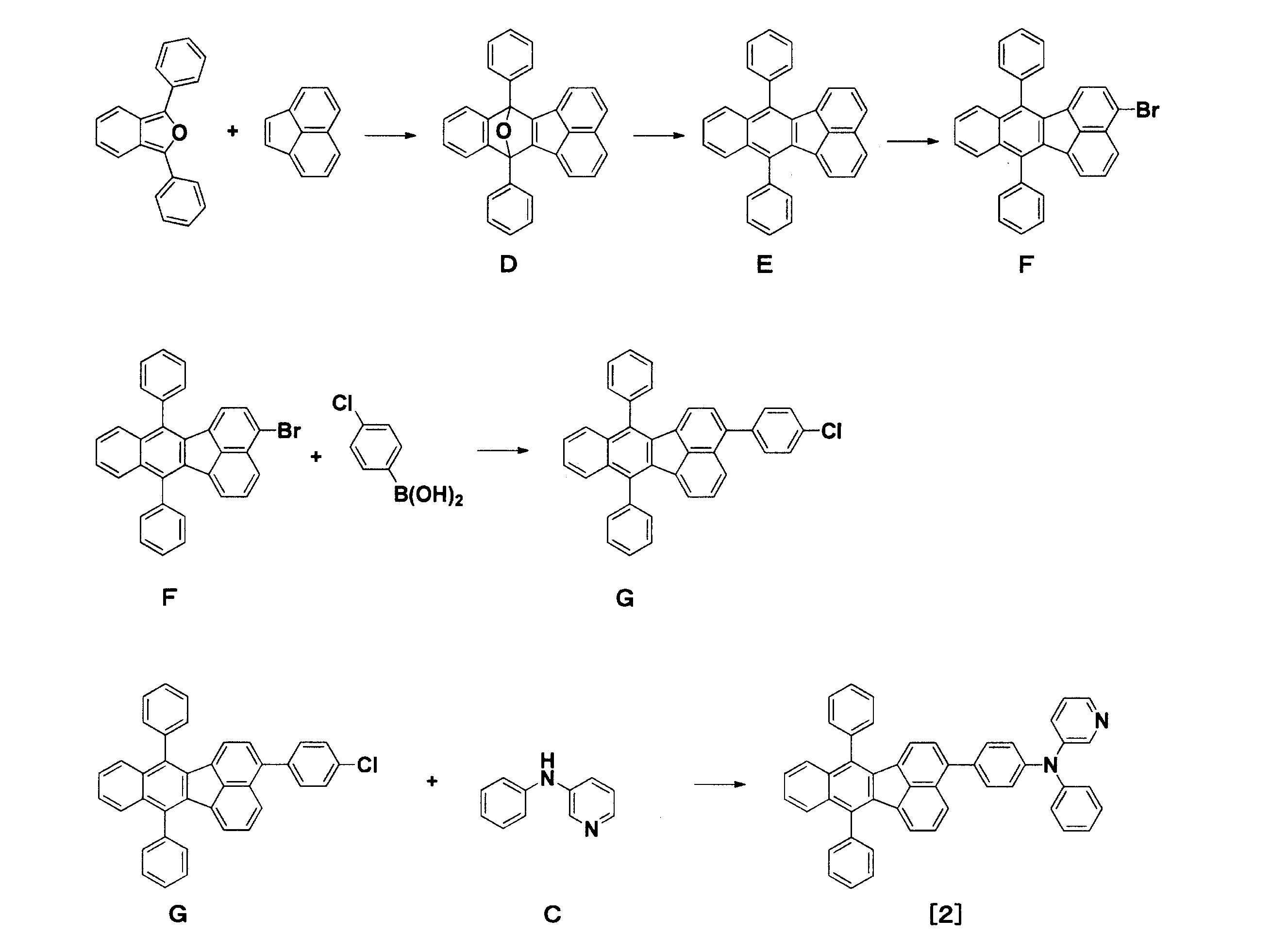
化合物[2]の合成
アセナフチレン14.0g、ジフェニルイソベンゾフラン25.0gおよびo-キシレン200mlを混合し、窒素気流下で加熱還流した。2時間後、室温に冷ました後、溶媒を留去し、エーテル300mLを加えた。得られた析出物をろ過し、真空乾燥することにより、中間体D27.7g(収率71%)を得た。
化合物[2]: 1H-NMR (CDCl3(d=ppm)) δ 6.63-6.67(m,2H),7.08-7.21(m,6H),7.29-7.48(m,9H),7.56-7.71(m,12H),7.86(d,1H),8.24(dd,1H),8.45(d,1H)。
化合物[3]の合成
中間体F10.0g、ビス(ピナコラート)ジボロン7.9g、酢酸カリウム6.1g、ジメチルホルムアミド52mLを混合し、窒素置換した。この混合溶液に[1,1’-ビス(ジフェニルホスフィノ)フェロセン]パラジウム(II)ジクロリド・ジクロロメタン錯体0.51gを加え、100℃に加熱した。1時間後、室温に冷却した後、水200mLを加え、析出した固体をろ過した。得られた固体をトルエンに溶解し、活性炭とQuadraSil(登録商標)を加え、シリカパッドでろ過した。ろ液の溶媒を留去した後、メタノールを加え、析出した固体をろ過し、真空乾燥することにより、中間体Hを10.8g得た。
化合物[3]: 1H-NMR (DMSO-d6(d=ppm)) δ 6.57-6.66(m,2H),7.33(t,1H),7.40-7.63(m,14H),7.69-7.80(m,7H),7.88(d,1H),8.19(dt,1H),8.32(d,1H),8.43(s,1H),8.77(dd,1H),8.94(d,1H)。
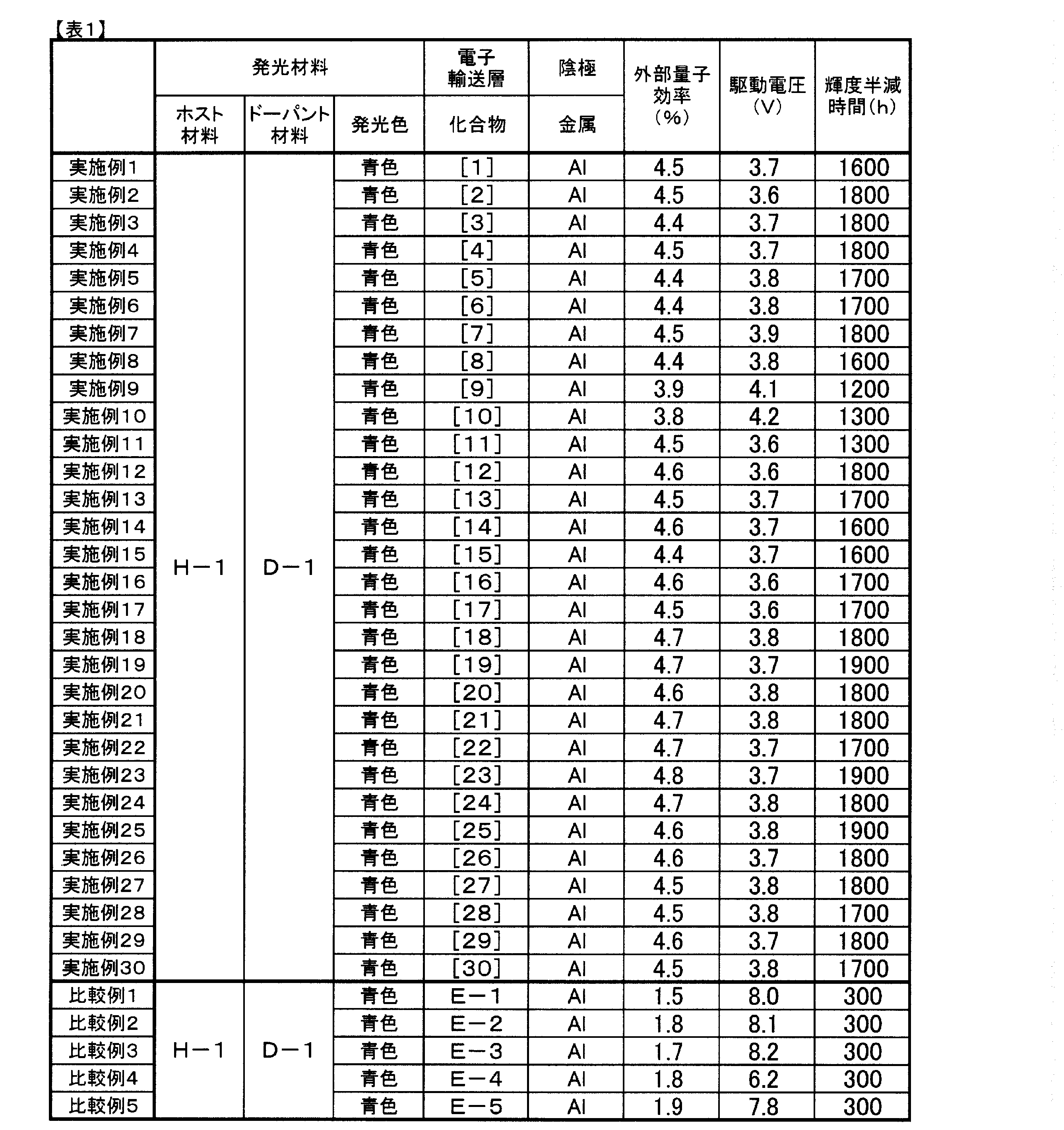
ITO透明導電膜を165nm堆積させたガラス基板(ジオマテック(株)製、11Ω/□、スパッタ品)を38×46mmに切断し、エッチングを行った。得られた基板を“セミコクリーン56”(商品名、フルウチ化学(株)製)で15分間超音波洗浄してから、超純水で洗浄した。この基板を素子を作製する直前に1時間UV-オゾン処理し、真空蒸着装置内に設置して、装置内の真空度が5×10-4Pa以下になるまで排気した。抵抗加熱法によって、まず正孔注入層として、HAT-CN6を5nm、正孔輸送層として、HT-1を50nm蒸着した。次に、発光層として、ホスト材料H-1、ドーパント材料D-1をドープ濃度が5重量%になるようにして20nmの厚さに蒸着した。次に、電子輸送層として化合物[1]を30nmの厚さに蒸着して積層した。次に、フッ化リチウムを0.5nm蒸着した後、アルミニウムを1000nm蒸着して陰極とし、5×5mm角の素子を作製した。ここで言う膜厚は、水晶発振式膜厚モニター表示値である。この発光素子の1000cd/m2時の特性は、駆動電圧3.7V、外部量子効率4.5%であった。また初期輝度を1000cd/m2に設定し、定電流駆動させたところ輝度50%低下する輝度半減時間は1600時間であった。なおHAT-CN6、HT-1、H-1、D-1は以下に示す化合物である。
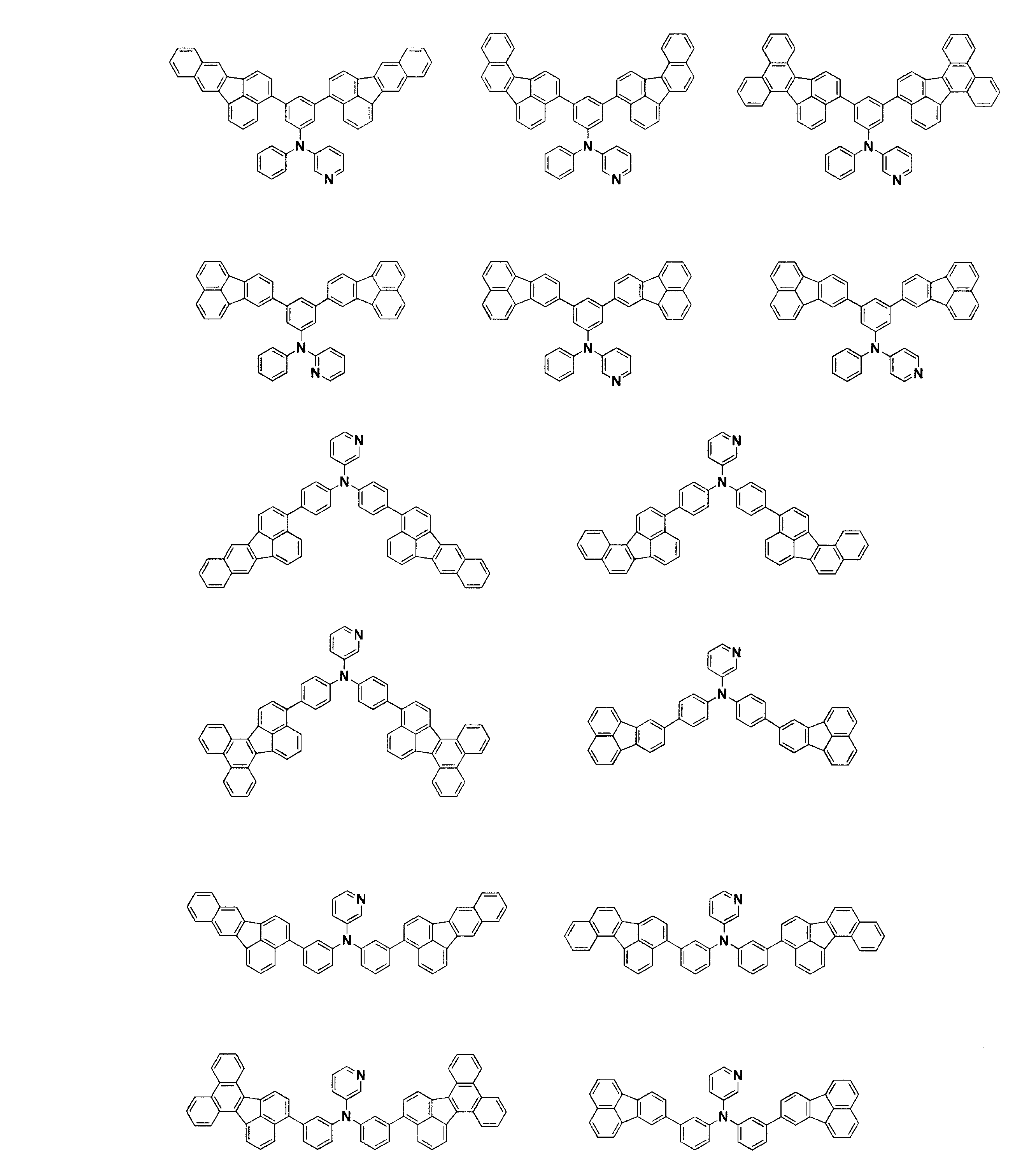
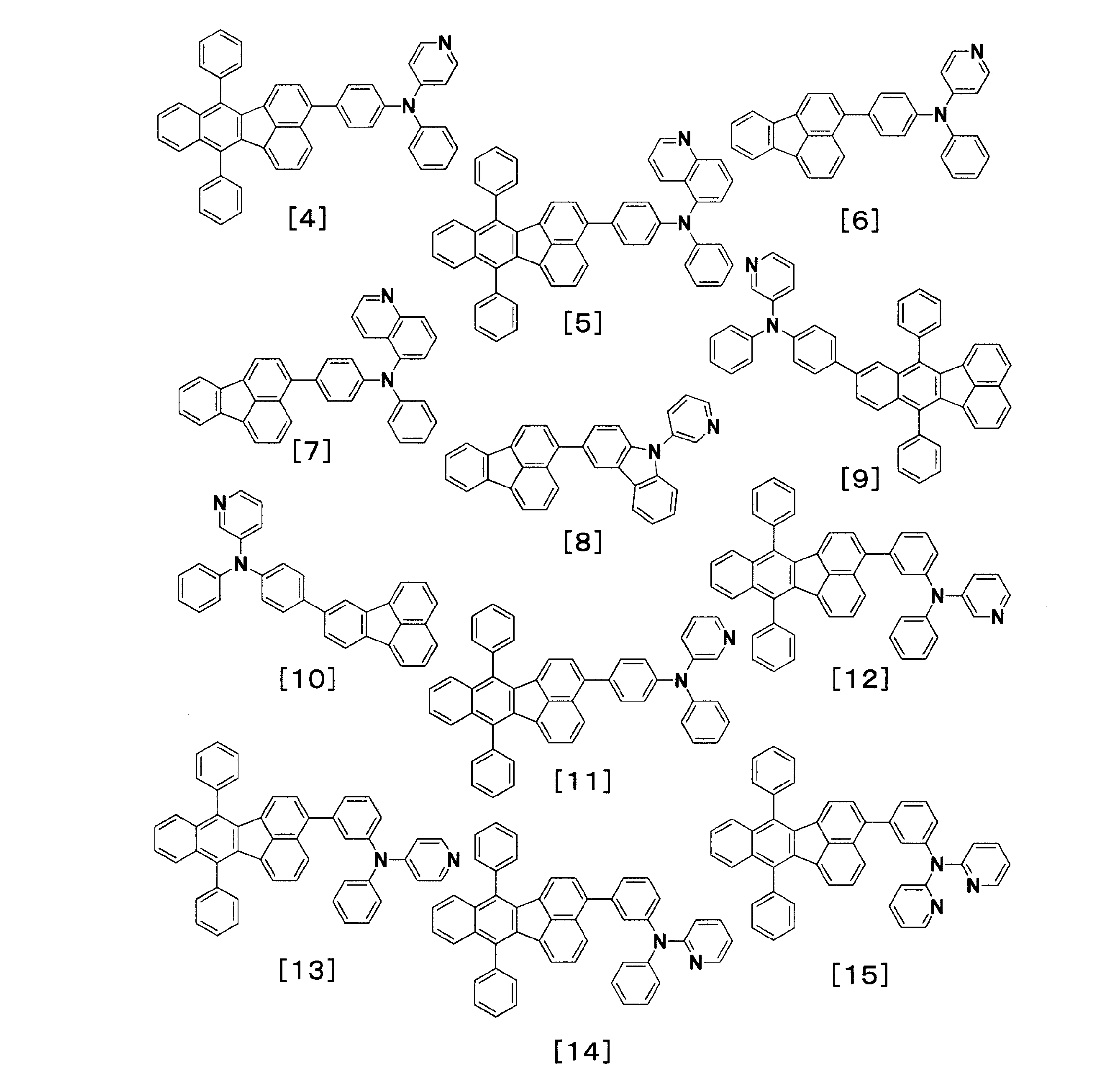
電子輸送層に表1に記載した化合物を用いた以外は実施例1と同様にして発光素子を作成し、評価した。結果を表1に示す。なお、化合物[4]~[30]は下記に示す化合物である。
電子輸送層に表1に記載した化合物を用いた以外は実施例1と同様にして発光素子を作成し、評価した。結果を表1に示す。なお、E-1~E-5は以下に示す化合物である。
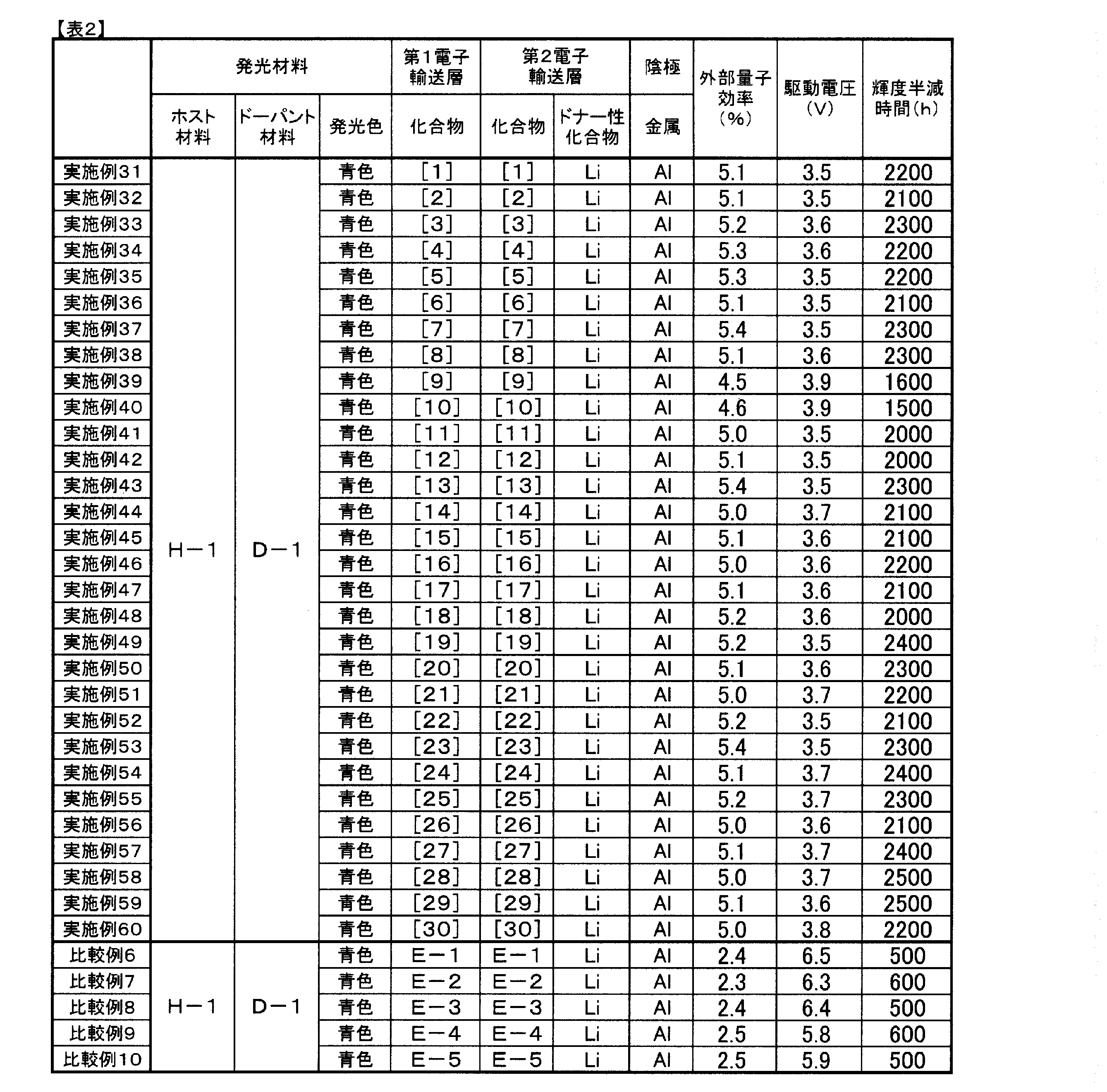
ITO透明導電膜を165nm堆積させたガラス基板(ジオマテック(株)製、11Ω/□、スパッタ品)を38×46mmに切断し、エッチングを行った。得られた基板を“セミコクリーン56”(商品名、フルウチ化学(株)製)で15分間超音波洗浄してから、超純水で洗浄した。この基板を素子を作製する直前に1時間UV-オゾン処理し、真空蒸着装置内に設置して、装置内の真空度が5×10-4Pa以下になるまで排気した。抵抗加熱法によって、まず正孔注入層として、HAT-CN6を5nm、正孔輸送層として、HT-1を50nm蒸着した。次に、発光層として、ホスト材料H-1、ドーパント材料D-1をドープ濃度が5重量%になるようにして20nmの厚さに蒸着した。次に、第1電子輸送層として化合物[1]を20nmの厚さに蒸着して積層した。さらに第2電子輸送層として電子輸送材料に化合物[1]を、ドナー性材料としてリチウムを用い、化合物[1]とリチウムの蒸着速度比が20:1になるようにして10nmの厚さに積層した。次に、フッ化リチウムを0.5nm蒸着した後、アルミニウムを1000nm蒸着して陰極とし、5×5mm角の素子を作製した。この発光素子の1000cd/m2時の特性は、駆動電圧3.5V、外部量子効率5.1%であった。また初期輝度を1000cd/m2に設定し、定電流駆動させたところ輝度50%低下する輝度半減時間は2200時間であった。
電子輸送層に表2に記載した化合物を用いた以外は実施例31と同様にして発光素子を作成し、評価した。結果を表2に示す。
電子輸送層に表2に記載した化合物を用いた以外は実施例31と同様にして発光素子を作成し、評価した。結果を表2に示す。
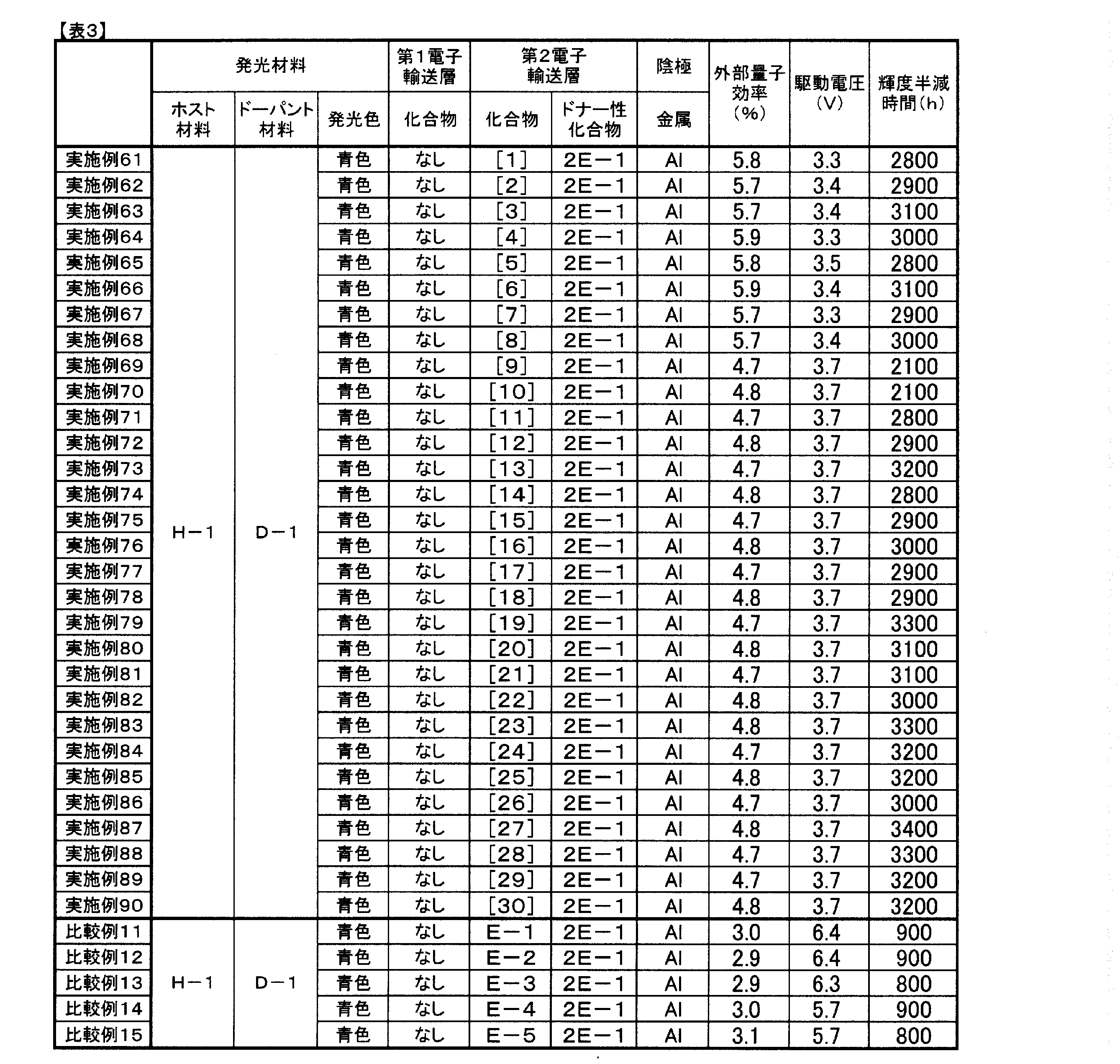
ITO透明導電膜を165nm堆積させたガラス基板(ジオマテック(株)製、11Ω/□、スパッタ品)を38×46mmに切断し、エッチングを行った。得られた基板を“セミコクリーン56”(商品名、フルウチ化学(株)製)で15分間超音波洗浄してから、超純水で洗浄した。この基板を素子を作製する直前に1時間UV-オゾン処理し、真空蒸着装置内に設置して、装置内の真空度が5×10-4Pa以下になるまで排気した。抵抗加熱法によって、まず正孔注入層として、HAT-CN6を5nm、正孔輸送層として、HT-1を50nm蒸着した。次に、発光層として、ホスト材料H-1、ドーパント材料D-1をドープ濃度が5重量%になるようにして20nmの厚さに蒸着した。さらに電子輸送層として電子輸送材料に化合物[1]を、ドナー性材料として2E-1を用い、化合物[1]と2E-1の蒸着速度比が1:1になるようにして30nmの厚さに積層した。この電子輸送層は表2では第2電子輸送層として示す。次に、フッ化リチウムを0.5nm蒸着した後、アルミニウムを1000nm蒸着して陰極とし、5×5mm角の素子を作製した。この発光素子の1000cd/m2時の特性は、駆動電圧3.3V、外部量子効率5.8%であった。また初期輝度を1000cd/m2に設定し、定電流駆動させたところ輝度50%低下する輝度半減時間は2800時間であった。
電子輸送層、ドナー性材料として表3に記載した化合物を用いた以外は実施例61と同様にして発光素子を作成し、評価した。結果を表3に示す。2E-1は下記に示す化合物である。
電子輸送層、ドナー性材料として表3に記載した化合物を用いた以外は実施例61と同様にして発光素子を作成し、評価した。結果を表3に示す。
ITO透明導電膜を165nm堆積させたガラス基板(ジオマテック(株)製、11Ω/□、スパッタ品)を38×46mmに切断し、エッチングを行った。得られた基板を“セミコクリーン56”(商品名、フルウチ化学(株)製)で15分間超音波洗浄してから、超純水で洗浄した。この基板を素子を作製する直前に1時間UV-オゾン処理し、真空蒸着装置内に設置して、装置内の真空度が5×10-4Pa以下になるまで排気した。抵抗加熱法によって、まず正孔注入層として、HAT-CN6を5nm、正孔輸送層として、HT-1を50nm蒸着した。この正孔輸送層は表3では第1正孔輸送層として示す。次に、発光層として、ホスト材料H-2、ドーパント材料D-2をドープ濃度が10重量%になるようにして20nmの厚さに蒸着した。次に、電子輸送層として化合物[1]を30nmの厚さに蒸着して積層した。次に、フッ化リチウムを0.5nm蒸着した後、アルミニウムを1000nm蒸着して陰極とし、5×5mm角の素子を作製した。ここで言う膜厚は、水晶発振式膜厚モニター表示値である。この発光素子の4000cd/m2時の特性は、駆動電圧4.0V、外部量子効率10.8%であった。また初期輝度を4000cd/m2に設定し、定電流駆動させたところ輝度半減時間は1200時間であった。なおH-2、D-2は以下に示す化合物である。
ITO透明導電膜を165nm堆積させたガラス基板(ジオマテック(株)製、11Ω/□、スパッタ品)を38×46mmに切断し、エッチングを行った。得られた基板を“セミコクリーン56”(商品名、フルウチ化学(株)製)で15分間超音波洗浄してから、超純水で洗浄した。この基板を素子を作製する直前に1時間UV-オゾン処理し、真空蒸着装置内に設置して、装置内の真空度が5×10-4Pa以下になるまで排気した。抵抗加熱法によって、まず正孔注入層として、HAT-CN6を5nm、第1正孔輸送層として、HT-1を40nm蒸着した。さらに第2正孔輸送層としてHT-2を10nm蒸着した。次に、発光層として、ホスト材料H-2、ドーパント材料D-2をドープ濃度が10重量%になるようにして20nmの厚さに蒸着した。次に、電子輸送層として化合物[4]を30nmの厚さに蒸着して積層した。次に、フッ化リチウムを0.5nm蒸着した後、アルミニウムを1000nm蒸着して陰極とし、5×5mm角の素子を作製した。ここで言う膜厚は、水晶発振式膜厚モニター表示値である。この発光素子の4000cd/m2時の特性は、駆動電圧3.9V、外部量子効率13.8%であった。また初期輝度を4000cd/m2に設定し、定電流駆動させたところ輝度半減時間は1900時間であった。なお、HT-2は以下に示す化合物である。
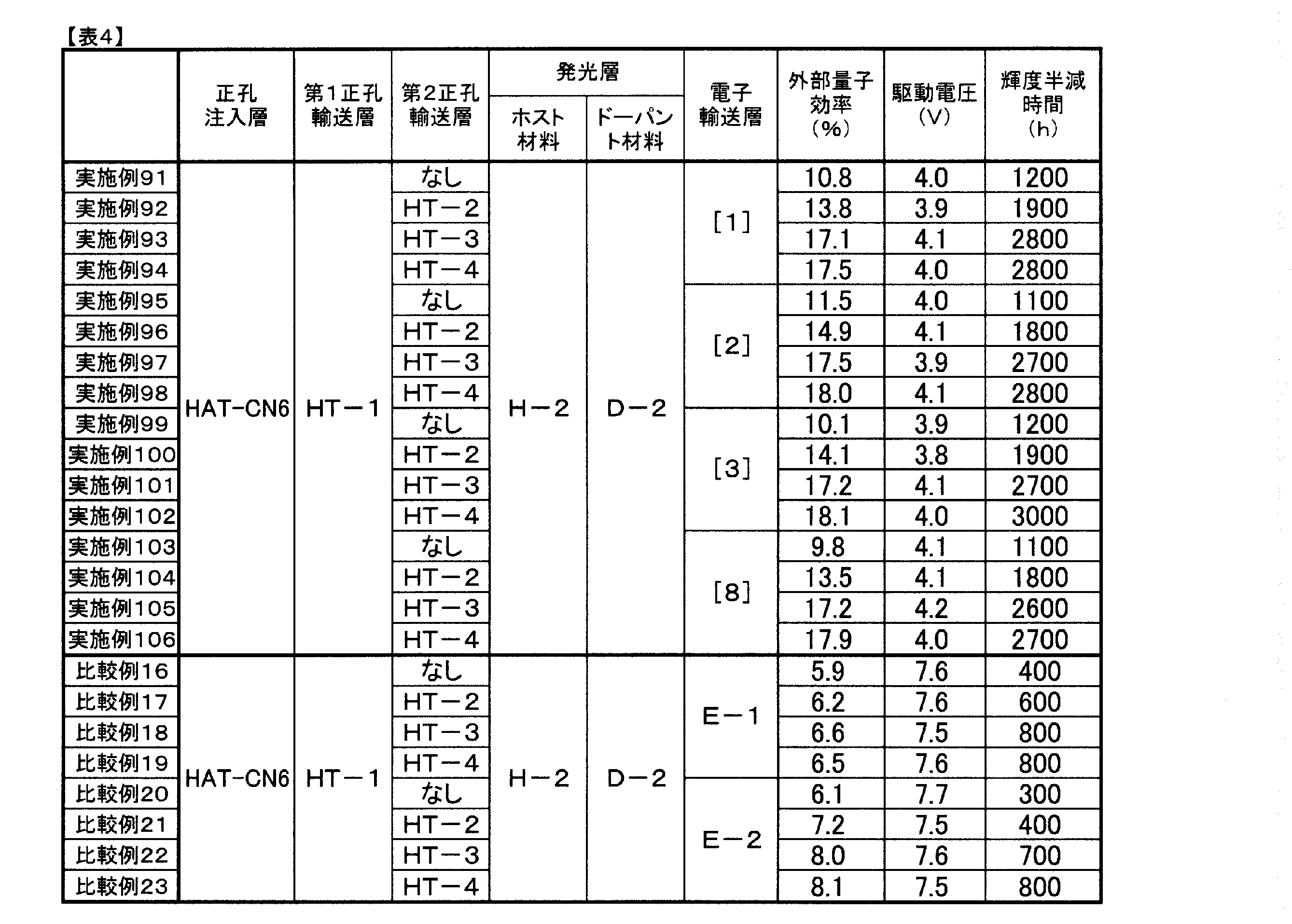
電子輸送層として表4記載の化合物を用いた以外は、実施例91と同様にして素子を作成し、評価した。結果を表4に示す。
電子輸送層として表4記載の化合物を用いた以外は実施例91と同様に発光素子を作成し、評価した。結果を表4に示す。
第2正孔輸送層および電子輸送層として表4記載の化合物を用いた以外は、実施例92と同様にして素子を作成し、評価した。結果を表4に示す。なおHT-3、HT-4は以下に示す化合物である。
第2正孔輸送層および電子輸送層として表4記載の化合物を用いた以外は、実施例32と同様にして素子を作成し、評価した。結果を表4に示す。
Claims (15)
- 下記一般式(1)で表されるフルオランテン誘導体。
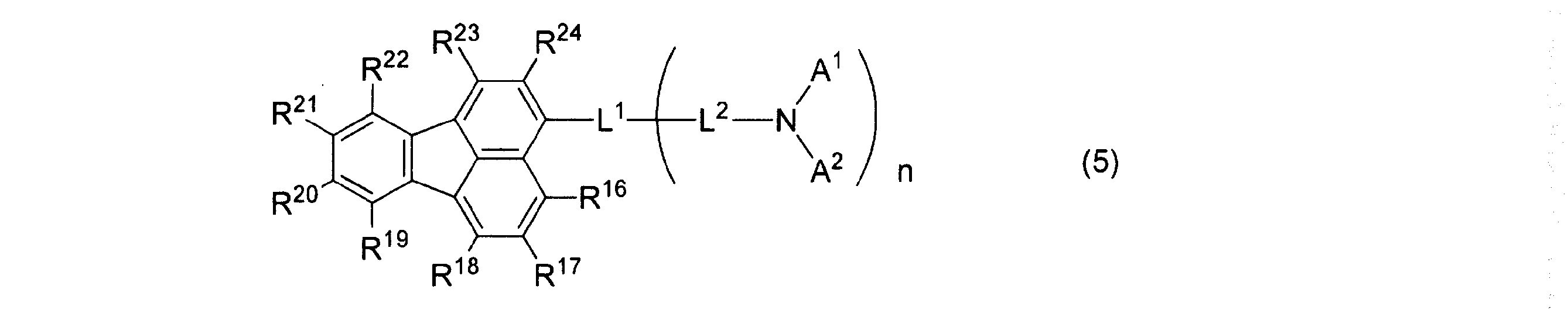
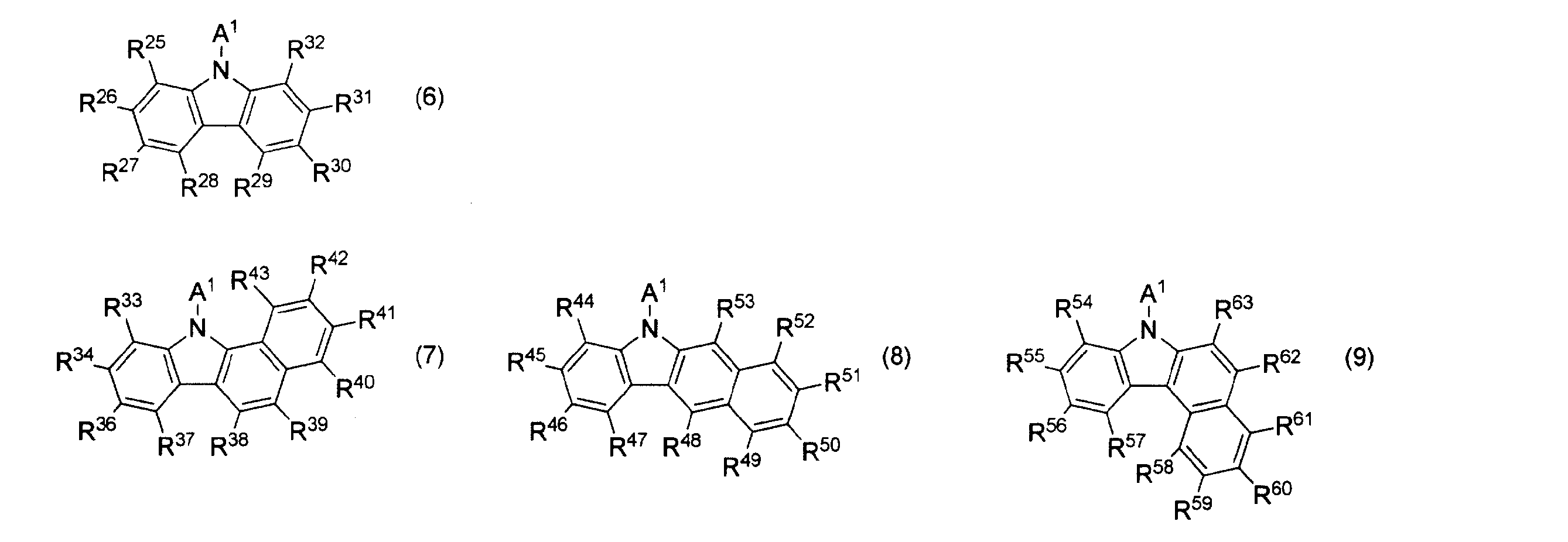
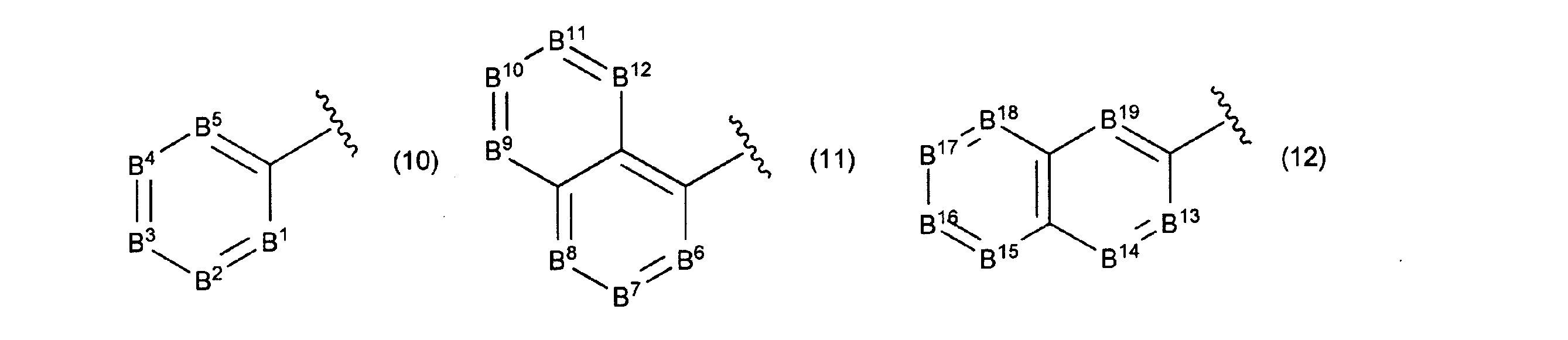
- L2-N(A1)(A2)が下記一般式(6)~(9)で表されるいずれかの構造である請求項1~5のいずれかに記載のフルオランテン誘導体。
- nが1である請求項1~6のいずれかに記載のフルオランテン誘導体。
- R7およびR12が置換もしくは無置換のアリール基である請求項2、3、6のいずれかに記載のフルオランテン誘導体。
- R7およびR12がフェニル基である請求項2、3、6のいずれかに記載のフルオランテン誘導体。
- 請求項1~11のいずれかに記載のフルオランテン誘導体を含有する発光素子材料。
- 陽極と陰極の間に有機層が存在し、電気エネルギーにより発光する発光素子であって、前記有機層に請求項1~11のいずれか記載のフルオランテン誘導体を含有することを特徴とする発光素子。
- 前記有機層が電子輸送層を有し、請求項1~11のいずれか記載のフルオランテン誘導体が前記電子輸送層に含有される請求項13記載の発光素子。
- 前記有機層が正孔輸送層を有し、前記正孔輸送層がカルバゾール骨格を有する材料を含有する請求項13または14に記載の発光素子。
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US14/434,846 US9935273B2 (en) | 2012-10-12 | 2013-10-04 | Fluoranthene derivative, light-emitting device material containing same, and light-emitting device |
| JP2013547035A JP6183214B2 (ja) | 2012-10-12 | 2013-10-04 | フルオランテン誘導体、それを含有する発光素子材料および発光素子 |
| EP13844716.4A EP2907803B1 (en) | 2012-10-12 | 2013-10-04 | Fluoranthene derivative, luminescent element material containing same, and luminescent element |
| CN201380052576.6A CN104768926B (zh) | 2012-10-12 | 2013-10-04 | 1,2‑苯并苊衍生物、含有其的发光元件材料及发光元件 |
| KR1020157008652A KR101973973B1 (ko) | 2012-10-12 | 2013-10-04 | 플루오란텐 유도체, 그것을 함유하는 발광 소자 재료 및 발광 소자 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2012226612 | 2012-10-12 | ||
| JP2012-226612 | 2012-10-12 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2014057874A1 true WO2014057874A1 (ja) | 2014-04-17 |
Family
ID=50477341
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2013/077047 WO2014057874A1 (ja) | 2012-10-12 | 2013-10-04 | フルオランテン誘導体、それを含有する発光素子材料および発光素子 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US9935273B2 (ja) |
| EP (1) | EP2907803B1 (ja) |
| JP (1) | JP6183214B2 (ja) |
| KR (1) | KR101973973B1 (ja) |
| CN (1) | CN104768926B (ja) |
| TW (1) | TWI582074B (ja) |
| WO (1) | WO2014057874A1 (ja) |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2015050173A1 (ja) * | 2013-10-03 | 2015-04-09 | 出光興産株式会社 | 化合物、有機エレクトロルミネッセンス素子及び電子機器 |
| WO2016116523A1 (de) * | 2015-01-20 | 2016-07-28 | Cynora Gmbh | Organische moleküle, insbesondere zur verwendung in optoelektronischen bauelementen |
| KR20160110656A (ko) * | 2015-03-10 | 2016-09-22 | 삼성디스플레이 주식회사 | 화합물 및 이를 포함하는 유기 발광 소자 |
| WO2020039708A1 (ja) | 2018-08-23 | 2020-02-27 | 国立大学法人九州大学 | 有機エレクトロルミネッセンス素子 |
| WO2021054337A1 (ja) * | 2019-09-17 | 2021-03-25 | Jsr株式会社 | 組成物、レジスト下層膜、レジスト下層膜の形成方法、パターニングされた基板の製造方法及び化合物 |
Families Citing this family (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5827772B2 (ja) | 2013-06-04 | 2015-12-02 | 出光興産株式会社 | 含窒素複素環誘導体、これを用いた有機エレクトロルミネッセンス素子用材料、並びにこれを用いた有機エレクトロルミネッセンス素子及び電子機器 |
| KR102562893B1 (ko) * | 2015-11-03 | 2023-08-04 | 삼성디스플레이 주식회사 | 축합환 화합물 및 이를 포함한 유기 발광 소자 |
| US11302870B2 (en) | 2016-11-02 | 2022-04-12 | Merck Patent Gmbh | Materials for electronic devices |
| CN107586273A (zh) * | 2017-09-01 | 2018-01-16 | 上海道亦化工科技有限公司 | 一种苊类有机电致发光化合物及其有机电致发光器件 |
| CN113248426A (zh) * | 2021-04-07 | 2021-08-13 | 浙江华显光电科技有限公司 | 一种杂环三芳胺化合物及含有其的有机光电器件 |
| KR20230001569A (ko) * | 2021-06-28 | 2023-01-05 | 엘티소재주식회사 | 헤테로고리 화합물, 및 이를 포함하는 유기 발광 소자 |
| CN113683580A (zh) * | 2021-09-10 | 2021-11-23 | 上海钥熠电子科技有限公司 | 含荧蒽衍生物的胺化合物和包含其的有机电致发光器件 |
| CN114685287A (zh) * | 2022-04-19 | 2022-07-01 | 上海钥熠电子科技有限公司 | 三芳胺化合物、包含该化合物的有机电致发光器件 |
| CN115073306A (zh) * | 2022-07-14 | 2022-09-20 | 北京八亿时空液晶科技股份有限公司 | 一种苊衍生物及包含它的有机电致发光元件 |
| CN115108921A (zh) * | 2022-07-14 | 2022-09-27 | 北京八亿时空液晶科技股份有限公司 | 一种苊衍生物及其应用 |
Citations (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2003060956A2 (en) | 2002-01-18 | 2003-07-24 | Lg Chem, Ltd. | New material for transporting electrons and organic electroluminescent display using the same |
| WO2004063159A1 (ja) | 2003-01-10 | 2004-07-29 | Idemitsu Kosan Co., Ltd. | 含窒素複素環誘導体及びそれを用いた有機エレクトロルミネッセンス素子 |
| WO2007100010A1 (ja) | 2006-02-28 | 2007-09-07 | Idemitsu Kosan Co., Ltd. | 有機エレクトロルミネッセンス素子 |
| WO2008059713A1 (en) | 2006-11-15 | 2008-05-22 | Idemitsu Kosan Co., Ltd. | Fluoranthene compound, organic electroluminescent device using the fluoranthene compound, and organic electroluminescent material-containing solution |
| CN101186593A (zh) * | 2007-12-18 | 2008-05-28 | 江南大学 | C60三芳胺衍生物在太阳能电池中的应用 |
| CN101525334A (zh) * | 2009-04-13 | 2009-09-09 | 江南大学 | 一种有机太阳能电池材料及其制备 |
| JP2009215559A (ja) | 2008-02-29 | 2009-09-24 | Gracel Display Inc | 新規な有機電界発光化合物及びこれを使用する有機電界発光素子 |
| JP2009215281A (ja) | 2007-12-31 | 2009-09-24 | Gracel Display Inc | 新規な有機エレクトロルミネセント化合物及びこれを使用する有機エレクトロルミネセント素子 |
| WO2010001817A1 (ja) | 2008-07-01 | 2010-01-07 | 東レ株式会社 | 発光素子 |
| WO2010113743A1 (ja) | 2009-03-30 | 2010-10-07 | 東レ株式会社 | 発光素子材料および発光素子 |
| WO2011046166A1 (ja) * | 2009-10-14 | 2011-04-21 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子およびこれを用いた照明装置 |
| WO2012108388A1 (ja) | 2011-02-07 | 2012-08-16 | 出光興産株式会社 | ビスカルバゾール誘導体及びそれを用いた有機エレクトロルミネッセンス素子 |
| CN102924296A (zh) * | 2011-08-08 | 2013-02-13 | 海洋王照明科技股份有限公司 | 含荧蒽有机化合物、其制备方法及应用 |
| KR20130029131A (ko) * | 2011-05-19 | 2013-03-22 | (주)씨에스엘쏠라 | 유기발광화합물 및 이를 이용한 유기 광소자 |
| CN103012206A (zh) * | 2011-09-28 | 2013-04-03 | 海洋王照明科技股份有限公司 | 双荧蒽有机半导体材料及其制备方法和应用 |
| US20130234118A1 (en) * | 2012-03-06 | 2013-09-12 | Samsung Display Co. Ltd. | Amine-based compound, organic light-emitting diode including the same, and organic light-emitting apparatus including the amine-based compound |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2005272805A (ja) | 2004-02-24 | 2005-10-06 | Sony Corp | 有機材料および有機電界発光素子 |
| KR20080047210A (ko) * | 2006-11-24 | 2008-05-28 | 삼성전자주식회사 | 유기 발광 화합물 및 이를 구비한 유기 발광 소자 |
| KR20090105495A (ko) * | 2008-04-02 | 2009-10-07 | (주)그라쎌 | 신규한 유기 발광 화합물 및 이를 발광재료로서 채용하고있는 유기 전기 발광 소자 |
| CN104592206B (zh) * | 2010-04-20 | 2019-12-31 | 出光兴产株式会社 | 双咔唑衍生物、有机电致发光元件用材料及使用其的有机电致发光元件 |
-
2013
- 2013-10-04 EP EP13844716.4A patent/EP2907803B1/en active Active
- 2013-10-04 US US14/434,846 patent/US9935273B2/en active Active
- 2013-10-04 KR KR1020157008652A patent/KR101973973B1/ko active IP Right Grant
- 2013-10-04 CN CN201380052576.6A patent/CN104768926B/zh active Active
- 2013-10-04 JP JP2013547035A patent/JP6183214B2/ja active Active
- 2013-10-04 WO PCT/JP2013/077047 patent/WO2014057874A1/ja active Application Filing
- 2013-10-09 TW TW102136440A patent/TWI582074B/zh active
Patent Citations (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2003060956A2 (en) | 2002-01-18 | 2003-07-24 | Lg Chem, Ltd. | New material for transporting electrons and organic electroluminescent display using the same |
| WO2004063159A1 (ja) | 2003-01-10 | 2004-07-29 | Idemitsu Kosan Co., Ltd. | 含窒素複素環誘導体及びそれを用いた有機エレクトロルミネッセンス素子 |
| WO2007100010A1 (ja) | 2006-02-28 | 2007-09-07 | Idemitsu Kosan Co., Ltd. | 有機エレクトロルミネッセンス素子 |
| WO2008059713A1 (en) | 2006-11-15 | 2008-05-22 | Idemitsu Kosan Co., Ltd. | Fluoranthene compound, organic electroluminescent device using the fluoranthene compound, and organic electroluminescent material-containing solution |
| CN101186593A (zh) * | 2007-12-18 | 2008-05-28 | 江南大学 | C60三芳胺衍生物在太阳能电池中的应用 |
| JP2009215281A (ja) | 2007-12-31 | 2009-09-24 | Gracel Display Inc | 新規な有機エレクトロルミネセント化合物及びこれを使用する有機エレクトロルミネセント素子 |
| JP2009215559A (ja) | 2008-02-29 | 2009-09-24 | Gracel Display Inc | 新規な有機電界発光化合物及びこれを使用する有機電界発光素子 |
| WO2010001817A1 (ja) | 2008-07-01 | 2010-01-07 | 東レ株式会社 | 発光素子 |
| WO2010113743A1 (ja) | 2009-03-30 | 2010-10-07 | 東レ株式会社 | 発光素子材料および発光素子 |
| CN101525334A (zh) * | 2009-04-13 | 2009-09-09 | 江南大学 | 一种有机太阳能电池材料及其制备 |
| WO2011046166A1 (ja) * | 2009-10-14 | 2011-04-21 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子およびこれを用いた照明装置 |
| WO2012108388A1 (ja) | 2011-02-07 | 2012-08-16 | 出光興産株式会社 | ビスカルバゾール誘導体及びそれを用いた有機エレクトロルミネッセンス素子 |
| KR20130029131A (ko) * | 2011-05-19 | 2013-03-22 | (주)씨에스엘쏠라 | 유기발광화합물 및 이를 이용한 유기 광소자 |
| CN102924296A (zh) * | 2011-08-08 | 2013-02-13 | 海洋王照明科技股份有限公司 | 含荧蒽有机化合物、其制备方法及应用 |
| CN103012206A (zh) * | 2011-09-28 | 2013-04-03 | 海洋王照明科技股份有限公司 | 双荧蒽有机半导体材料及其制备方法和应用 |
| US20130234118A1 (en) * | 2012-03-06 | 2013-09-12 | Samsung Display Co. Ltd. | Amine-based compound, organic light-emitting diode including the same, and organic light-emitting apparatus including the amine-based compound |
Non-Patent Citations (6)
| Title |
|---|
| APPL. PHYS. LETT., vol. 74, 1999, pages 865 |
| M.E.EL-KHOULY ET AL.: "Stabilization of the Charge-Separated States of Covalently Linked Zinc Porphyrin-Triphenylamine-[60]Fullerene", CHEMPHYSCHEM, vol. 11, no. 8, 2010, pages 1726 - 1734, XP027229496 * |
| M.ZHANG ET AL.: "Synthesis and properties of a new [60] fullerene-donor system containing dicyanovinyl groups", MATERIALS LETTERS, vol. 64, no. 20, 2010, pages 2244 - 2246, XP027229496 * |
| N.NIAMNONT ET AL.: "Tunable star-shaped triphenylamine fluorophores for fluorescence quenching detection and identification of nitro -aromatic explosives", CHEMICAL COMMUNICATIONS, vol. 49, no. 8, 28 January 2013 (2013-01-28), pages 780 - 782, XP055253361 * |
| ORG. ELECTRON., vol. 4, 2003, pages 113 |
| See also references of EP2907803A4 |
Cited By (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2015050173A1 (ja) * | 2013-10-03 | 2015-04-09 | 出光興産株式会社 | 化合物、有機エレクトロルミネッセンス素子及び電子機器 |
| JP2015071567A (ja) * | 2013-10-03 | 2015-04-16 | 出光興産株式会社 | フルオランテン誘導体、有機エレクトロルミネッセンス素子及び電子機器 |
| US10622569B2 (en) | 2013-10-03 | 2020-04-14 | Idemitsu Kosan Co., Ltd. | Compound, organic electroluminescent element, and electronic device |
| WO2016116523A1 (de) * | 2015-01-20 | 2016-07-28 | Cynora Gmbh | Organische moleküle, insbesondere zur verwendung in optoelektronischen bauelementen |
| KR20160110656A (ko) * | 2015-03-10 | 2016-09-22 | 삼성디스플레이 주식회사 | 화합물 및 이를 포함하는 유기 발광 소자 |
| KR102420083B1 (ko) * | 2015-03-10 | 2022-07-13 | 삼성디스플레이 주식회사 | 화합물 및 이를 포함하는 유기 발광 소자 |
| WO2020039708A1 (ja) | 2018-08-23 | 2020-02-27 | 国立大学法人九州大学 | 有機エレクトロルミネッセンス素子 |
| WO2021054337A1 (ja) * | 2019-09-17 | 2021-03-25 | Jsr株式会社 | 組成物、レジスト下層膜、レジスト下層膜の形成方法、パターニングされた基板の製造方法及び化合物 |
Also Published As
| Publication number | Publication date |
|---|---|
| US9935273B2 (en) | 2018-04-03 |
| EP2907803A1 (en) | 2015-08-19 |
| KR20150065175A (ko) | 2015-06-12 |
| EP2907803A4 (en) | 2016-09-21 |
| CN104768926B (zh) | 2017-09-22 |
| JP6183214B2 (ja) | 2017-08-23 |
| JPWO2014057874A1 (ja) | 2016-09-05 |
| KR101973973B1 (ko) | 2019-08-23 |
| EP2907803B1 (en) | 2021-08-18 |
| CN104768926A (zh) | 2015-07-08 |
| TWI582074B (zh) | 2017-05-11 |
| TW201420566A (zh) | 2014-06-01 |
| US20150280139A1 (en) | 2015-10-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6769303B2 (ja) | フェナントロリン誘導体、それを含有する電子デバイス、発光素子および光電変換素子 | |
| JP6183214B2 (ja) | フルオランテン誘導体、それを含有する発光素子材料および発光素子 | |
| JP6627507B2 (ja) | フルオランテン誘導体、それを含有する電子デバイス、発光素子および光電変換素子 | |
| JP6051864B2 (ja) | 発光素子材料および発光素子 | |
| JP6020173B2 (ja) | 発光素子材料および発光素子 | |
| WO2016009823A1 (ja) | モノアミン誘導体、それを用いた発光素子材料および発光素子 | |
| JP6269060B2 (ja) | 発光素子材料および発光素子 | |
| WO2014057873A1 (ja) | ホスフィンオキサイド誘導体およびそれを有する発光素子 | |
| EP3275880B1 (en) | 2-(quinazolin-6-yl)-9h-carbazole and 3-(quinazolin-6-yl)-9h-carbazole compounds, and electronic devices, luminescent elements, photoelectric conversion elements, and image sensors containing same | |
| JP6318617B2 (ja) | 発光素子材料および発光素子 | |
| JP2014138006A (ja) | 発光素子材料および発光素子 | |
| JP2016160208A (ja) | 化合物、それを含有する発光素子、光電変換素子およびイメージセンサ | |
| WO2014024750A1 (ja) | 発光素子材料および発光素子 | |
| JP2014175590A (ja) | 有機電界発光素子 | |
| JP2014093501A (ja) | 発光素子材料および発光素子 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| ENP | Entry into the national phase |
Ref document number: 2013547035 Country of ref document: JP Kind code of ref document: A |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 13844716 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 20157008652 Country of ref document: KR Kind code of ref document: A |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 14434846 Country of ref document: US |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2013844716 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: IDP00201502851 Country of ref document: ID |