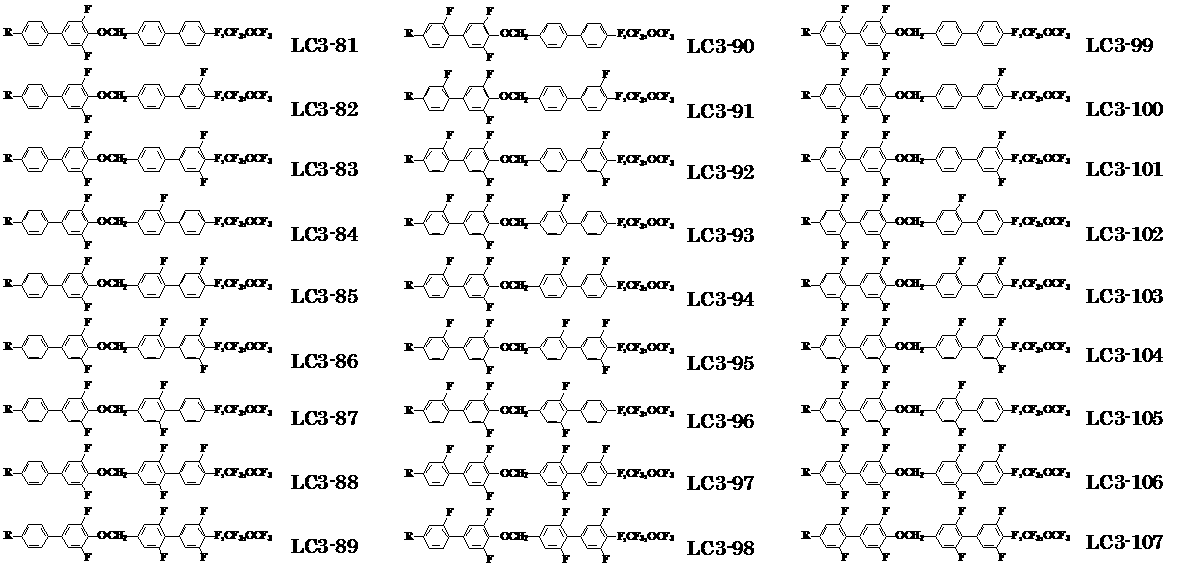WO2013141116A1 - ネマチック液晶組成物 - Google Patents
ネマチック液晶組成物 Download PDFInfo
- Publication number
- WO2013141116A1 WO2013141116A1 PCT/JP2013/057053 JP2013057053W WO2013141116A1 WO 2013141116 A1 WO2013141116 A1 WO 2013141116A1 JP 2013057053 W JP2013057053 W JP 2013057053W WO 2013141116 A1 WO2013141116 A1 WO 2013141116A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- liquid crystal
- general formula
- crystal composition
- ocf
- group
- Prior art date
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/30—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing saturated or unsaturated non-aromatic rings, e.g. cyclohexane rings
- C09K19/3001—Cyclohexane rings
- C09K19/3059—Cyclohexane rings in which at least two rings are linked by a carbon chain containing carbon to carbon triple bonds
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/10—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing at least two benzene rings
- C09K19/20—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing at least two benzene rings linked by a chain containing carbon and oxygen atoms as chain links, e.g. esters or ethers
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/30—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing saturated or unsaturated non-aromatic rings, e.g. cyclohexane rings
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/32—Non-steroidal liquid crystal compounds containing condensed ring systems, i.e. fused, bridged or spiro ring systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/32—Non-steroidal liquid crystal compounds containing condensed ring systems, i.e. fused, bridged or spiro ring systems
- C09K19/322—Compounds containing a naphthalene ring or a completely or partially hydrogenated naphthalene ring
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/42—Mixtures of liquid crystal compounds covered by two or more of the preceding groups C09K19/06 - C09K19/40
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/52—Liquid crystal materials characterised by components which are not liquid crystals, e.g. additives with special physical aspect: solvents, solid particles
- C09K19/54—Additives having no specific mesophase characterised by their chemical composition
- C09K19/542—Macromolecular compounds
-
- G—PHYSICS
- G02—OPTICS
- G02F—OPTICAL DEVICES OR ARRANGEMENTS FOR THE CONTROL OF LIGHT BY MODIFICATION OF THE OPTICAL PROPERTIES OF THE MEDIA OF THE ELEMENTS INVOLVED THEREIN; NON-LINEAR OPTICS; FREQUENCY-CHANGING OF LIGHT; OPTICAL LOGIC ELEMENTS; OPTICAL ANALOGUE/DIGITAL CONVERTERS
- G02F1/00—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics
- G02F1/01—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour
- G02F1/13—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour based on liquid crystals, e.g. single liquid crystal display cells
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K2019/0444—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit characterized by a linking chain between rings or ring systems, a bridging chain between extensive mesogenic moieties or an end chain group
- C09K2019/0448—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit characterized by a linking chain between rings or ring systems, a bridging chain between extensive mesogenic moieties or an end chain group the end chain group being a polymerizable end group, e.g. -Sp-P or acrylate
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K2019/0444—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit characterized by a linking chain between rings or ring systems, a bridging chain between extensive mesogenic moieties or an end chain group
- C09K2019/0466—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit characterized by a linking chain between rings or ring systems, a bridging chain between extensive mesogenic moieties or an end chain group the linking chain being a -CF2O- chain
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/10—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing at least two benzene rings
- C09K19/12—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing at least two benzene rings at least two benzene rings directly linked, e.g. biphenyls
- C09K2019/121—Compounds containing phenylene-1,4-diyl (-Ph-)
- C09K2019/123—Ph-Ph-Ph
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/10—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing at least two benzene rings
- C09K19/12—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing at least two benzene rings at least two benzene rings directly linked, e.g. biphenyls
- C09K2019/121—Compounds containing phenylene-1,4-diyl (-Ph-)
- C09K2019/124—Ph-Ph-Ph-Ph
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/30—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing saturated or unsaturated non-aromatic rings, e.g. cyclohexane rings
- C09K19/3001—Cyclohexane rings
- C09K19/3003—Compounds containing at least two rings in which the different rings are directly linked (covalent bond)
- C09K2019/3012—Cy-Cy-Cy-Ph, or more Cy rings
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/30—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing saturated or unsaturated non-aromatic rings, e.g. cyclohexane rings
- C09K19/3001—Cyclohexane rings
- C09K19/3003—Compounds containing at least two rings in which the different rings are directly linked (covalent bond)
- C09K2019/3016—Cy-Ph-Ph
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/30—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing saturated or unsaturated non-aromatic rings, e.g. cyclohexane rings
- C09K19/3001—Cyclohexane rings
- C09K19/3003—Compounds containing at least two rings in which the different rings are directly linked (covalent bond)
- C09K2019/3019—Cy-Cy-Ph-Ph
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/30—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing saturated or unsaturated non-aromatic rings, e.g. cyclohexane rings
- C09K19/3001—Cyclohexane rings
- C09K19/3003—Compounds containing at least two rings in which the different rings are directly linked (covalent bond)
- C09K2019/3025—Cy-Ph-Ph-Ph
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/30—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing saturated or unsaturated non-aromatic rings, e.g. cyclohexane rings
- C09K19/3001—Cyclohexane rings
- C09K19/3059—Cyclohexane rings in which at least two rings are linked by a carbon chain containing carbon to carbon triple bonds
- C09K2019/3062—Cy-C≡C-Ph
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/30—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing saturated or unsaturated non-aromatic rings, e.g. cyclohexane rings
- C09K19/3001—Cyclohexane rings
- C09K19/3066—Cyclohexane rings in which the rings are linked by a chain containing carbon and oxygen atoms, e.g. esters or ethers
- C09K19/3068—Cyclohexane rings in which the rings are linked by a chain containing carbon and oxygen atoms, e.g. esters or ethers chain containing -COO- or -OCO- groups
- C09K2019/3077—Cy-Cy-COO-Ph
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/52—Liquid crystal materials characterised by components which are not liquid crystals, e.g. additives with special physical aspect: solvents, solid particles
- C09K19/54—Additives having no specific mesophase characterised by their chemical composition
- C09K19/542—Macromolecular compounds
- C09K2019/548—Macromolecular compounds stabilizing the alignment; Polymer stabilized alignment
Definitions
- the present invention relates to a nematic liquid crystal composition having a positive dielectric anisotropy ( ⁇ ) useful as an electro-optical liquid crystal display material.
- Liquid crystal display elements are used in various measuring instruments, automobile panels, word processors, electronic notebooks, printers, computers, televisions, watches, advertisement display boards, etc., including clocks and calculators.
- Typical liquid crystal display methods include TN (twisted nematic) type, STN (super twisted nematic) type, vertical alignment type using TFT (thin film transistor), and IPS (in-plane switching) type.
- the liquid crystal composition used in these liquid crystal display elements is stable against external factors such as moisture, air, heat, light, etc., and exhibits a liquid crystal phase in the widest possible temperature range centering on room temperature, and has low viscosity. And a low driving voltage is required.
- the liquid crystal composition has several to several tens of kinds of compounds in order to optimize the dielectric anisotropy ( ⁇ ) and the refractive index anisotropy ( ⁇ n) for each display element. It is composed of
- a liquid crystal composition having a negative ⁇ is used for a vertical alignment type display
- a liquid crystal composition having a positive ⁇ is used for a horizontal alignment type display such as a TN type, STN type, or IPS type.
- a driving method has been reported in which a liquid crystal composition having a positive ⁇ is vertically aligned when no voltage is applied and a horizontal electric field is applied to display the liquid crystal composition, and the necessity of a liquid crystal composition having a positive ⁇ is further increased. Yes.
- low voltage driving, high-speed response, and a wide operating temperature range are required in all driving systems.
- ⁇ is positive, the absolute value is large, the viscosity ( ⁇ ) is small, and a high nematic phase-isotropic liquid phase transition temperature (T ni ) is required.
- T ni nematic phase-isotropic liquid phase transition temperature
- the problem to be solved by the present invention is that the viscosity ( ⁇ ) is sufficiently low without reducing or increasing the refractive index anisotropy ( ⁇ n) and the nematic phase-isotropic liquid phase transition temperature (T ni ),
- another object is to provide a liquid crystal composition having a positive dielectric anisotropy ( ⁇ ).
- the present inventor has studied various fluorobenzene derivatives and found that the above problem can be solved by combining specific compounds, and has completed the present invention.
- the present invention is a liquid crystal composition having a positive dielectric anisotropy, wherein the liquid crystal composition is selected from compounds represented by general formula (LC0-1) and / or general formula (LC0-2) A liquid crystal containing one or more compounds, and further containing one or more compounds selected from the group of compounds represented by formulas (LC1) to (LC5) A composition is provided, and a liquid crystal display element using the liquid crystal composition is further provided.
- R 01 to R 41 each independently represents an alkyl group having 1 to 15 carbon atoms, and one or two or more —CH 2 — in the alkyl group is not directly adjacent to an oxygen atom. May be substituted with —O—, —CH ⁇ CH—, —CO—, —OCO—, —COO—, —C ⁇ C—, —CF 2 O— or —OCF 2 —.
- R 51 and R 52 each independently represents an alkyl group having 1 to 15 carbon atoms, and one of the alkyl groups Or two or more —CH 2 — are substituted with —O—, —CH ⁇ CH—, —CO—, —OCO—, —COO— or —C ⁇ C— so that the oxygen atom is not directly adjacent.
- a 01 to A 42 may be independently any one of the following structures:
- one or more —CH 2 — of the cyclohexane ring may be substituted with —O— so that the oxygen atom is not directly adjacent to the cyclohexane ring.
- Two or more —CH ⁇ may be substituted with —N ⁇ so that the nitrogen atom is not directly adjacent
- X 61 and X 62 are each independently —H, —Cl, —F, —CF 3 or -Represents OCF 3
- a 51 to A 53 each independently represents one of the following structures:
- X 01 to X 03 each represents a hydrogen atom or a fluorine atom; 11 to X 43 each independently represent —H, —Cl, —F, —CF 3 or —OCF 3 , and Y 01 to Y 41 represent —Cl, —F, —CF 3 or —OCF 3 , Z 01 and Z 02 are each independently a single bond, —CH ⁇ CH—, —C ⁇ C—, —CH 2 CH 2 —, — (CH 2 ) 4 —, —OCH 2 —, —CH 2 O— , -OCF 2 - or -CF 2 O-a represents, Z 31 ⁇
- the liquid crystal composition of the present invention is characterized in that ⁇ is positive and its absolute value is large. Also, ⁇ is low, rotational viscosity ( ⁇ 1 ) is small, liquid crystallinity is excellent, and a stable liquid crystal phase is exhibited over a wide temperature range. In addition, it is chemically stable to heat, light, water, etc., has good solubility, has good phase stability at low temperature, and can be driven at low voltage. It is a thing.
- the liquid crystal composition according to the present invention contains one or more compounds selected from the compounds represented by the general formula (LC0-1) and / or the general formula (LC0-2). Since a liquid crystal composition containing one or more compounds selected from the compound group represented by formula (LC5) from LC1) exhibits a stable liquid crystal phase even at low temperatures, it is a practical liquid crystal composition. It can be said that there is.
- R 01 to R 41 each independently represents an alkyl group having 1 to 15 carbon atoms, and one or more of the alkyl groups in the alkyl group —CH 2 — means —O—, —CH ⁇ CH—, —CO—, —OCO—, —COO—, —C ⁇ C—, —CF 2 O— or —, so that oxygen atoms are not directly adjacent to each other.
- OCF 2 — may be substituted, and one or more hydrogen atoms in the alkyl group may be optionally substituted with halogen, but an alkyl group having 1 to 8 carbon atoms, 2 to 8 carbon atoms Or an alkoxy group having 1 to 8 carbon atoms, preferably a straight chain, and R 51 and R 52 each independently represents an alkyl group having 1 to 15 carbon atoms.
- One or two or more —CH 2 — in which the oxygen atom is directly It may be substituted with —O—, —CH ⁇ CH—, —CO—, —OCO—, —COO— or —C ⁇ C— so that they are not adjacent to each other, but an alkyl group having 1 to 8 carbon atoms, An alkenyl group having 2 to 8 carbon atoms or an alkoxy group having 1 to 8 carbon atoms is preferable, and a straight chain is preferable.
- a 01 to A 42 are each independently a trans-1,4-cyclohexylene group, 1,4-phenylene group, 3-fluoro-1,4-phenylene group or 3,5-difluoro-1,4-phenylene group. Is preferred.
- a 51 to A 53 are each independently preferably a trans-1,4-cyclohexylene group, a 1,4-phenylene group, a 2-fluoro-1,4-phenylene group or a 3-fluoro-1,4-phenylene group.
- X 01 to X 03 are preferably a hydrogen atom or a fluorine atom
- X 11 to X 43 are each independently preferably a hydrogen atom or a fluorine atom.
- Y 01 to Y 41 are preferably —F, —CF 3 or —OCF 3 .
- Z 01 and Z 02 are each independently a single bond, —CH ⁇ CH—, —C ⁇ C—, —CH 2 CH 2 —, — (CH 2 ) 4 —, —OCH 2 —, —CH 2 O— , —OCF 2 — or —CF 2 O— is preferred, and one of Z 01 and Z 02 present is —CH ⁇ CH—, —C ⁇ C—, —CH 2 CH 2 —, — (CH 2 ) 4.
- the others preferably represent single bonds, and more preferably all represent single bonds.
- Z 31 to Z 42 are each independently a single bond, —CH ⁇ CH—, —C ⁇ C—, —CH 2 CH 2 —, — (CH 2 ) 4 —, —OCH 2 —, —CH 2 O—. , —OCF 2 — or —CF 2 O— is preferred, and at least one of Z 31 and Z 32 present is not a single bond.
- Z 41 each independently represents a single bond, —CH ⁇ CH—, —C ⁇ C—, —CH 2 CH 2 — or — (CH 2 ) 4 —.
- Z 51 and Z 52 are each independently a single bond, —CH ⁇ CH—, —C ⁇ C—, —CH 2 CH 2 —, — (CH 2 ) 4 —, —OCH 2 —, —CH 2 O—.
- m 01 and m 02 each independently preferably represents an integer of 0 to 2
- m 21 preferably represents an integer of 0 or 1.
- m 31 to m 42 each independently preferably represents an integer of 0 to 2
- m 31 + m 32 and m 41 + m 42 each independently preferably represents 1, 2 or 3.
- m 51 preferably represents an integer of 1 or 2.
- liquid crystal compounds represented by the general formulas (LC0-1) and (LC0-2) are represented by the following general formulas (LC0-1-1) to (LC0-2-4).
- X 23 , X 24 , X 25 and X 26 each independently represent a hydrogen atom, Cl, F, CF 3 or OCF 3
- X 22 , R 21 and Y 21 have the same meaning as in claim 1. It is more preferable that it is a compound represented by.
- X 33 , X 34 , X 35 , X 36 , X 37 and X 38 each independently represent H, Cl, F, CF 3 or OCF 3
- X 32 , R 31 , A 31 , Y 31 and Z 31 represent the same meaning as in claim 1, R represents R 31 , F, CF 3 , OCF 3 represents any of F, CF 3, or OCF 3
- (F) represents H or It is preferably a compound represented by any one of F.
- X 44 , X 46 , X 47 , X 71 and X 72 each independently represent H, Cl, F, CF 3 or OCF 3
- X 42 , X 43 , R 41 and Y 41 are claimed. It is preferably a compound represented by the same meaning as in item 1.
- the content of the compound represented by the general formula (LC0-1) and / or the general formula (LC0-2) is preferably 5 to 50% by mass, and 10 to 40% by mass. % Is more preferable.
- the contents of the compounds represented by the general formulas (LC-1) to (LC-4) are each independently preferably 10 to 60% by mass and more preferably 10 to 40% by mass.
- the content of the compound represented by the general formula (LC-5) is preferably 10 to 90% by mass, and more preferably 15 to 70% by mass.
- the liquid crystal composition of the present invention may contain a polymerizable compound in order to produce a liquid crystal display element such as a polymer stabilization (PS) mode.
- PS polymer stabilization
- Examples of the polymerizable compound that can be used include a photopolymerizable monomer that undergoes polymerization by energy rays such as light.
- the structure has, for example, a liquid crystal skeleton in which a plurality of six-membered rings such as biphenyl derivatives and terphenyl derivatives are connected. Examples thereof include a polymerizable compound.
- the polymerizable compound is represented by the general formula (PC1).
- P 1 represents a polymerizable functional group
- Sp 1 represents a spacer group having 0 to 20 carbon atoms
- Q 1 represents a single bond, —O—, —NH—, —NHCOO—, —OCONH— , —CH ⁇ CH—, —CO—, —COO—, —OCO—, —OCOO—, —OOCO—, —CH ⁇ CH—, —CH ⁇ CH—COO—, —OCO—CH ⁇ CH— or — C ⁇ C—
- n 1 and n 2 each independently represent 1, 2 or 3
- MG represents a mesogenic group or mesogenic support group
- R 3 represents a halogen atom, a cyano group or the number of carbon atoms Represents an alkyl group of 1 to 25, and one or more CH 2 groups in the alkyl group are —O—, —S—, —NH—, —N ( CH 3) -, - CO - , -
- MG in the polymerizable compound general formula (PC1) has the following structure:
- C 1 to C 3 are each independently 1,4-phenylene group, 1,4-cyclohexylene group, 1,4-cyclohexenyl group, tetrahydropyran-2,5-diyl group, 1,3 -Dioxane-2,5-diyl group, tetrahydrothiopyran-2,5-diyl group, 1,4-bicyclo (2,2,2) octylene group, decahydronaphthalene-2,6-diyl group, pyridine-2 , 5-diyl group, pyrimidine-2,5-diyl group, pyrazine-2,5-diyl group, 1,2,3,4-tetrahydronaphthalene-2,6-diyl group, 2,6-naphthylene group, phenanthrene -2,7-diyl group, 9,10-dihydrophenanthrene-2,7-diyl group, 1,2,3,4,
- the groups are —O—, —S—, —NH—, —N (CH 3 ) —, —CO—, —COO—, —OCO—, —OCOO—, —SCO—, so that the O atom is not directly adjacent. May be replaced by -COS- or -C ⁇ C- P 1 and P 2 are each independently represented by the following general formulas (PC1-a) to (PC1-d)
- R 61 to R 63 , R 71 to R 73 , and R 81 to R 83 each independently represents a hydrogen atom, a halogen atom, or an alkyl group having 1 to 5 carbon atoms).
- polymerizable compound general formula (PC1) is represented by the general formula (PC1) -1 or the general formula (PC1) -2.
- P 1 , Sp 1 , Q 1 , P 2 , Sp 2 , Q 2 and MG represent the same meaning as in the general formula (PC1), and n 3 and n 4 are independently 1, 2 or 3 respectively. It is preferable that it is a polymeric compound represented by this.
- the general formula (PC1) is from the general formula (PC1) -3 to the general formula (PC1) -8.
- W 1 is independently F, CF 3 , OCF 3 , CH 3 , OCH 3 , an alkyl group having 2 to 5 carbon atoms, an alkoxy group, an alkenyl group, COOW 2 , OCOW 2 or OCOW 2 (Wherein W 2 represents a linear or branched alkyl group having 1 to 10 carbon atoms or an alkenyl group having 2 to 5 carbon atoms, and n 3 , n 4 and n 6 are each independently 0, It is more preferably a polymerizable compound represented by 1, 2, 3, or 4.
- Sp 1 , Sp 2 , Q 1 and Q 2 in the general formula (PC1) -3 to general formula (PC1) -8 are all single bonds, and n 3 + n 4 is 3 in n 3 and n 4 .
- P 1 and P 2 are general formula (PC1-c)
- W 1 is F, CF 3 , OCF 3 , CH 3 or OCH 3
- n 6 is 1 or more. .
- MG in the general formula (PC1) is a discotic liquid crystal compound represented by the general formula (PC1) -9.
- R 7 is independently P 1 -Sp 1 -Q 1 or the general formula (PC1-e)
- R 91 and R 92 each independently represent a hydrogen atom, a halogen atom or a methyl group, and R 93 represents a carbon atom.
- the amount of the polymerizable compound used is preferably 0.1 to 2.0% by mass.
- the liquid crystal composition of the present invention can contain one or more antioxidants in order to improve the stability, and can also contain one or more UV absorbers.
- the liquid crystal display device using the liquid crystal composition of the present invention is useful for achieving both high-speed response and suppression of display failure, and is particularly useful for a liquid crystal display device for active matrix driving, including TN mode, OCB mode, It can be applied to a liquid crystal display element for IPS mode, FFS mode or VA-IPS mode.
- a polymer stabilized (PS) mode liquid crystal display element can be produced.
- a liquid crystal composition containing a polymerizable compound is sandwiched between two substrates, and the polymerizable compound in the liquid crystal composition is polymerized by energy such as ultraviolet rays with or without voltage applied. Can be produced.
- the orientation state of the liquid crystal molecules can be memorized by polymerizing the polymerizable compound, whereby the stability of the orientation state can be improved. In addition, an improvement in response speed can be expected.
- T NI Nematic phase-isotropic liquid phase transition temperature (° C)
- Tn lower limit temperature of nematic phase (° C)
- ⁇ dielectric constant in the direction perpendicular to the molecular long axis direction at 25 ° C.
- ⁇ dielectric anisotropy at 25 ° C. no: refractive index for ordinary light at 25 ° C.
- ⁇ n refractive index anisotropic at 25 ° C.
- sex Vth Applied voltage (V) in a cell having a cell thickness of 6 ⁇ m in which the transmittance changes by 10% when a rectangular wave with a frequency of 1 KHz is applied at 25 ° C.
- ⁇ 20 Bulk viscosity at 20 ° C. (mPa ⁇ s)
- ⁇ 1 rotational viscosity (mPa ⁇ s)
- the following abbreviations are used in compound descriptions.
- Example 1 The prepared liquid crystal composition and its physical property values are shown below.
- the liquid crystal composition is a liquid crystal composition that does not contain the compounds represented by the general formulas (LC0-1) and (LC0-2) of the present application. It can be seen that Example 1 has a much lower viscosity, ⁇ 1 is smaller, and the combination of the present invention is very excellent (Example 2).
- the prepared liquid crystal composition and its physical property values are shown below.
- Example 3 The prepared liquid crystal composition and its physical property values are shown below.
- Example 4 The prepared liquid crystal composition and its physical property values are shown below.
- Example 5 The prepared liquid crystal composition and its physical property values are shown below.
- Example 6 The prepared liquid crystal composition and its physical property values are shown below.
- Example 7 The prepared liquid crystal composition and its physical property values are shown below.
- Example 8 The prepared liquid crystal composition and its physical property values are shown below.
- Example 9 The prepared liquid crystal composition and its physical property values are shown below.
- Example 10 The prepared liquid crystal composition and its physical property values are shown below.
- Example 11 The prepared liquid crystal composition and its physical property values are shown below.
- Example 12 The prepared liquid crystal composition and its physical property values are shown below.
- the liquid crystal compositions of Examples 2 to 12 have a low viscosity, a small ⁇ 1 , and the combination of the present invention is very excellent.
- Example 13 Using a first substrate having a pair of transparent electrodes having a comb-shaped electrode structure on the same substrate and a second substrate not having an electrode structure, a vertical alignment film is formed on each substrate, and the first substrate and An IPS empty cell having a gap interval of 4.0 microns was fabricated on the second substrate.
- a liquid crystal display device was produced by injecting the liquid crystal composition shown in Example 9 into this empty cell. When the electro-optical characteristics of this display element were measured, the applied voltage at which the transmittance changed by 10% was 1.53 v. The response speed when 5v was applied was 5.2 milliseconds, and the response speed when the voltage was turned off was 13.4 seconds.
- a polymerizable liquid crystal composition CLC-A was prepared by adding 1% and uniformly dissolving.
- the physical properties of CLC-A were almost the same as those of the liquid crystal composition shown in Example 3.
- UV light is irradiated to the liquid crystal cell by a high-pressure mercury lamp through a filter that cuts UV light of 300 nm or less while applying a rectangular wave of 1.8 V at a frequency of 1 KHz. did.
- the cell surface was adjusted to have an irradiation intensity of 20 mW / cm 2 and irradiated for 600 seconds to obtain a vertically aligned liquid crystal display element in which the polymerizable compound in the polymerizable liquid crystal composition was polymerized.
- the applied voltage at which the transmittance changed by 10% was 1.61 v.
- the response speed when 5v was applied was 5.2 milliseconds.
- the response speed when the voltage was turned off was 5.2 milliseconds, which was very fast compared to the liquid crystal display device manufactured using only the liquid crystal composition shown in Example 9.
Landscapes
- Chemical & Material Sciences (AREA)
- Crystallography & Structural Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Organic Chemistry (AREA)
- Physics & Mathematics (AREA)
- Nonlinear Science (AREA)
- General Physics & Mathematics (AREA)
- Optics & Photonics (AREA)
- Liquid Crystal Substances (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
Description
本発明は、正の誘電率異方性を有する液晶組成物であって、前記液晶組成物が一般式(LC0-1)及び/又は一般式(LC0-2)で表される化合物から選ばれる1種又は2種以上の化合物を含有し、さらに一般式(LC1)から一般式(LC5)で表される化合物群から選ばれる1種又は2種以上の化合物を含有することを特徴とする液晶組成物を提供し、更に、当該液晶組成物を用いた液晶表示素子を提供する。
これらの一般式(LC0-1)から一般式(LC5)中、R01~R41はそれぞれ独立して炭素数1~15のアルキル基を表し、該アルキル基中の1つ又は2つ以上の-CH2-は、酸素原子が直接隣接しないように、-O-、-CH=CH-、-CO-、-OCO-、-COO-、-C≡C-、-CF2O-又は-OCF2-で置換されてよく、該アルキル基中の1つ又は2つ以上の水素原子は任意にハロゲンで置換されていてもよいが、炭素数1~8のアルキル基、炭素数2~8のアルケニル基又は炭素数1~8のアルコキシ基であることが好ましく、直鎖であることが好ましく、R51及びR52はそれぞれ独立して炭素数1~15のアルキル基を表し、該アルキル基中の1つ又は2つ以上の-CH2-は、酸素原子が直接隣接しないように、-O-、-CH=CH-、-CO-、-OCO-、-COO-又は-C≡C-で置換されてよいが、炭素数1~8のアルキル基、炭素数2~8のアルケニル基又は炭素数1~8のアルコキシ基であることが好ましく、直鎖であることが好ましい。A01~A42はそれぞれ独立してトランス-1,4-シクロヘキシレン基、1,4-フェニレン基、3-フルオロ-1,4-フェニレン基又は3,5-ジフルオロ-1,4-フェニレン基が好ましい。A51~A53はそれぞれ独立してトランス-1,4-シクロヘキシレン基、1,4-フェニレン基、2-フルオロ-1,4-フェニレン基又は3-フルオロ-1,4-フェニレン基が好ましい。X01~X03は水素原子又はフッ素原子が好ましく、X11~X43はそれぞれ独立して水素原子又はフッ素原子が好ましい。Y01~Y41は-F、-CF3又は-OCF3が好ましい。
Z01及びZ02はそれぞれ独立して単結合、-CH=CH-、-C≡C-、-CH2CH2-、-(CH2)4-、-OCH2-、-CH2O-、-OCF2-又は-CF2O-が好ましく、存在するZ01及びZ02のうち一つが-CH=CH-、-C≡C-、-CH2CH2-、-(CH2)4-、-OCH2-、-CH2O-、-OCF2-又は-CF2O-を表す場合、他は単結合を表すことが好ましく、全てが単結合を表すことが更に好ましい。Z31~Z42はそれぞれ独立して単結合、-CH=CH-、-C≡C-、-CH2CH2-、-(CH2)4-、-OCH2-、-CH2O-、-OCF2-又は-CF2O-が好ましく、存在するZ31及びZ32の内少なくとも1つは単結合でない。m42が0の場合、Z41はそれぞれ独立して単結合、-CH=CH-、-C≡C-、-CH2CH2-又は-(CH2)4-を表す。Z51及びZ52はそれぞれ独立して単結合、-CH=CH-、-C≡C-、-CH2CH2-、-(CH2)4-、-OCH2-、-CH2O-、-OCF2-又は-CF2O-が好ましく、単結合、-CH2CH2-、-OCF2-又は-CF2O-が更に好ましく、単結合が特に好ましい。m01、m02はそれぞれ独立して0~2の整数を表すことが好ましく、m21は0又は1の整数を表すことが好ましい。m31~m42はそれぞれ独立して0~2の整数を表すことが好ましく、m31+m32及びm41+m42はそれぞれ独立して1、2又は3が好ましい。m51は1又は2の整数を表すことが好ましい。A01、A02、A23、A31、A32、A41、A42、A52、Z01、Z02、Z31、Z32、Z41、Z42及び/又はZ52が複数存在する場合、それらは同一であっても、異なっていてもよい。
また、本発明の液晶組成物には、高分子安定化(PS)モードなどの液晶表示素子を作製するために、重合性化合物を含有することができる。使用できる重合性化合物として、光などのエネルギー線により重合が進行する光重合性モノマーなどが挙げられ、構造として、例えば、ビフェニル誘導体、ターフェニル誘導体などの六員環が複数連結した液晶骨格を有する重合性化合物などが挙げられる。具体的には重合性化合物が一般式(PC1)
Sp1及びSp2がそれぞれ独立してアルキレン基を表し、該アルキレン基は1つ以上のハロゲン原子又はCNにより置換されていても良く、この基中に存在する1つ又は2つ以上のCH2基はO原子が直接隣接しないように-O-、-S-、-NH-、-N(CH3)-、-CO-、-COO-、-OCO-、-OCOO-、-SCO-、-COS-又は-C≡C-により置き換えられていてもよく、
P1及びP2がそれぞれ独立して以下の一般式(PC1-a)~一般式(PC1-d)
重合性化合物の使用量は好ましくは0.1~2.0質量%である。
本発明の液晶組成物を用いた液晶表示素子は高速応答と表示不良の抑制を両立させた有用なものであり、特に、アクティブマトリックス駆動用液晶表示素子に有用であり、TNモード、OCBモード、IPSモード、FFSモード又はVA-IPSモード用液晶表示素子に適用できる。
上述の重合性化合物を含有する本発明の液晶組成物を用いることで、高分子安定化(PS)モード液晶表示素子を作製することができる。具体的には、二枚の基板間に重合性化合物を含有する液晶組成物を狭持し、電圧印加下あるいは電圧無印加下で紫外線等のエネルギーによって液晶組成物中の重合性化合物を重合させることで作製することができる。この液晶表示素子においては、重合性化合物の高分子化によって液晶分子の配向状態を記憶化させることができ、それによって配向状態の安定性を向上させることができる。また、応答速度の改善も期待できる。
TN-I :ネマチック相-等方性液体相転移温度(℃)
T-n :ネマチック相の下限温度(℃)
ε⊥ :25℃での分子長軸方向に対し垂直な方向の誘電率
Δε :25℃での誘電率異方性
no :25℃での常光に対する屈折率
Δn :25℃での屈折率異方性
Vth :25℃での周波数1KHzの矩形波を印加した時の透過率が10%変化するセル厚6μmのセルでの印加電圧(V)
η20 :20℃でのバルク粘性(mPa・s)
γ1 :回転粘性(mPa・s)
化合物記載に下記の略号を使用する。
以下に、調製した液晶組成物とその物性値を示す。
以下に、調製した液晶組成物とその物性値を示す。
(実施例2)
以下に、調製した液晶組成物とその物性値を示す。
以下に、調製した液晶組成物とその物性値を示す。
以下に、調製した液晶組成物とその物性値を示す。
以下に、調製した液晶組成物とその物性値を示す。
以下に、調製した液晶組成物とその物性値を示す。
以下に、調製した液晶組成物とその物性値を示す。
以下に、調製した液晶組成物とその物性値を示す。
以下に、調製した液晶組成物とその物性値を示す。
以下に、調製した液晶組成物とその物性値を示す。
以下に、調製した液晶組成物とその物性値を示す。
以下に、調製した液晶組成物とその物性値を示す。
(実施例13)
櫛形電極構造の透明電極を同一基板に一対設けた第一の基板と電極構造を設けない第二の基板を使用し各々の基板上に垂直配向性の配向膜を形成し、第一の基板と第二の基板をギャップ間隔4.0ミクロンのIPS用空セルを作製した。この空セルに実施例9で示された液晶組成物を注入し液晶表示素子を作製した。この表示素子の電気光学特性を測定したところ、透過率が10%変化する印加電圧は、1.53vであった。また、5vを印加した時の応答速度は5.2ミリ秒であり、電圧をオフにした時の応答速度は13.4秒であった。
この実施例3で示された液晶組成物99%に対して、式(PC-1)-3-1で表される重合性化合物
上述のIPS用空セルにCLC-Aを挟持した後、周波数1KHzで1.8Vの矩形波を印加しながら、300nm以下の紫外線をカットするフィルターを介して、高圧水銀灯により液晶セルに紫外線を照射した。セル表面の照射強度が20mW/cm2となるように調整して600秒間照射して、重合性液晶組成物中の重合性化合物を重合させた垂直配向性液晶表示素子を得た。この表示素子の電気光学特性を測定したところ、透過率が10%変化する印加電圧は、1.61vであった。また、5vを印加した時の応答速度は5.2ミリ秒であった。また、電圧をオフにした時の応答速度は5.2ミリ秒と、実施例9で示された液晶組成物のみで作製した液晶表示素子と比較して、非常に速いものであった。
Claims (14)
- 正の誘電率異方性を有する液晶組成物であって、前記液晶組成物が一般式(LC0-1)及び/又は一般式(LC0-2)で表される化合物から選ばれる1種又は2種以上の化合物を含有し、さらに一般式(LC1)から一般式(LC5)で表される化合物群から選ばれる1種又は2種以上の化合物を含有することを特徴とする液晶組成物。
- 一般式(LC0-1)及び/又は一般式(LC0-2)で表される化合物から選ばれる1種又は2種以上の化合物を含有し、さらに一般式(LC1)から一般式(LC4)で表される化合物群から選ばれる1種又は2種以上の化合物を含有し、さらに一般式(LC5)で表される化合物群より選ばれる1種又は2種以上の化合物を含有する請求項1記載の液晶組成物。
- 一般式(LC0-1)及び/又は一般式(LC0-2)で表される化合物より選ばれる1種又は2種以上の化合物、及び一般式(LC3-1)から一般式(LC3-22)で表される化合物からなる群より選ばれる化合物及び/又は一般式(LC3-23)から一般式(LC3-121)で表される化合物からなる群より選ばれる1種又は2種以上の化合物を含有する請求項1から4のいずれか一項に記載の液晶組成物。
- 重合性化合物を1種又は2種以上含有する請求項1から7のいずれか一項に記載の液晶組成物。
- 酸化防止剤を1種又は2種以上含有する請求項1から8のいずれか一項に記載の液晶組成物。
- UV吸収剤を1種又は2種以上含有する請求項1から9のいずれか一項に記載の液晶組成物。
- 請求項1から10のいずれか一項に記載の液晶組成物を用いた液晶表示素子。
- 請求項1から10のいずれか一項に記載の液晶組成物を用いたアクティブマトリックス駆動用液晶表示素子。
- 請求項1から10のいずれか一項に記載の液晶組成物を用いたTNモード、OCBモード、IPSモード又はVA-IPSモード用液晶表示素子
- 請求項8に記載の液晶組成物を用い、電圧印加下あるいは電圧無印加下で該液晶組成物中に含有する重合性化合物を重合させて作製した高分子安定化のTNモード、OCBモード、IPSモード又はVA-IPSモード用液晶表示素子。
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201380015404.1A CN104220556B (zh) | 2012-03-19 | 2013-03-13 | 向列液晶组合物 |
| EP13764021.5A EP2835410B1 (en) | 2012-03-19 | 2013-03-13 | Nematic liquid crystal composition |
| JP2013550064A JP5582264B2 (ja) | 2012-03-19 | 2013-03-13 | ネマチック液晶組成物 |
| US14/386,154 US20150159086A1 (en) | 2012-03-19 | 2013-03-13 | Nematic liquid crystal composition |
| KR1020147026050A KR101539703B1 (ko) | 2012-03-19 | 2013-03-13 | 네마틱 액정 조성물 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2012-061932 | 2012-03-19 | ||
| JP2012061932 | 2012-03-19 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2013141116A1 true WO2013141116A1 (ja) | 2013-09-26 |
Family
ID=49222576
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2013/057053 WO2013141116A1 (ja) | 2012-03-19 | 2013-03-13 | ネマチック液晶組成物 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US20150159086A1 (ja) |
| EP (1) | EP2835410B1 (ja) |
| JP (1) | JP5582264B2 (ja) |
| KR (1) | KR101539703B1 (ja) |
| CN (2) | CN105647541B (ja) |
| TW (1) | TWI570221B (ja) |
| WO (1) | WO2013141116A1 (ja) |
Cited By (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2014057780A1 (ja) * | 2012-10-09 | 2014-04-17 | Dic株式会社 | フッ素化ナフタレン構造を持つ化合物及びその液晶組成物 |
| WO2015076093A1 (ja) * | 2013-11-19 | 2015-05-28 | Dic株式会社 | ネマチック液晶組成物及びこれを用いた液晶表示素子 |
| WO2015098661A1 (ja) * | 2013-12-25 | 2015-07-02 | Dic株式会社 | 液晶組成物用酸化防止剤、液晶組成物及びこれを用いた液晶表示素子 |
| WO2015098740A1 (ja) * | 2013-12-25 | 2015-07-02 | Dic株式会社 | ネマチック液晶組成物及びこれを用いた液晶表示素子 |
| US9573923B2 (en) | 2013-10-03 | 2017-02-21 | Dic Corporation | Liquid crystal compound having 2, 6-difluorophenylether structure, and liquid crystal composition containing the same |
| US9637466B2 (en) | 2013-07-25 | 2017-05-02 | Dic Corporation | Liquid crystal compound having 2, 6-difluorophenyl ether structure and liquid crystal composition thereof |
| US10000700B2 (en) | 2014-07-31 | 2018-06-19 | Dic Corporation | Nematic liquid crystal composition |
| US10253258B2 (en) | 2014-07-31 | 2019-04-09 | Dic Corporation | Nematic liquid crystal composition |
| US10544365B2 (en) | 2013-08-30 | 2020-01-28 | Dic Corporation | Nematic liquid crystal composition |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013241519A (ja) * | 2012-05-21 | 2013-12-05 | Dic Corp | ネマチック液晶組成物 |
| JP6085912B2 (ja) * | 2012-08-01 | 2017-03-01 | Dic株式会社 | 化合物、液晶組成物および液晶表示素子 |
| US9605208B2 (en) | 2012-08-22 | 2017-03-28 | Dic Corporation | Nematic liquid crystal composition |
| JP5648881B2 (ja) * | 2012-09-03 | 2015-01-07 | Dic株式会社 | ネマチック液晶組成物 |
| JP6070110B2 (ja) * | 2012-11-27 | 2017-02-01 | Dic株式会社 | フッ素化ナフタレン構造を持つ化合物 |
| WO2014156947A1 (ja) * | 2013-03-28 | 2014-10-02 | Dic株式会社 | ネマチック液晶組成物及びこれを用いた液晶表示素子 |
| WO2016035667A1 (ja) * | 2014-09-05 | 2016-03-10 | Dic株式会社 | 液晶組成物及びそれを使用した液晶表示素子 |
| CN106590686B (zh) * | 2015-10-16 | 2019-04-23 | 江苏和成显示科技有限公司 | 液晶组合物及其应用 |
| CN106590687B (zh) * | 2015-10-16 | 2019-02-15 | 江苏和成显示科技有限公司 | 液晶组合物及其应用 |
Citations (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1996032365A1 (fr) | 1995-04-12 | 1996-10-17 | Chisso Corporation | Compose de cristaux liquides substitues par fluor, composition de cristaux liquides et afficheur a cristaux liquides |
| JPH09157202A (ja) | 1995-12-05 | 1997-06-17 | Chisso Corp | 酸素原子含有結合基を持つアルケニル化合物、液晶組成物および液晶表示素子 |
| WO1998023564A1 (fr) | 1996-11-28 | 1998-06-04 | Chisso Corporation | Derives de benzene a substitution de fluor, composition a cristaux liquides et element d'affichage a cristaux liquides |
| JP2000169413A (ja) * | 1998-12-08 | 2000-06-20 | Dainippon Ink & Chem Inc | 6−トリフルオロメトキシナフタレン誘導体である新規液晶性化合物とそれを含有する液晶組成物及びその製造方法 |
| JP2001019649A (ja) * | 1999-07-06 | 2001-01-23 | Dainippon Ink & Chem Inc | 6−フルオロナフタレン誘導体である新規液晶性化合物とそれを含有する液晶組成物 |
| JP2003183656A (ja) | 2001-10-12 | 2003-07-03 | Merck Patent Gmbh | 液晶媒体 |
| JP2003286217A (ja) * | 2002-03-29 | 2003-10-10 | Chisso Corp | ナフタレン環を有する液晶性化合物、液晶組成物および液晶表示素子 |
| JP2005232215A (ja) * | 2004-02-17 | 2005-09-02 | Dainippon Ink & Chem Inc | 高分子分散型液晶表示素子用組成物及び高分子分散型液晶表示素子 |
| JP2005232214A (ja) * | 2004-02-17 | 2005-09-02 | Dainippon Ink & Chem Inc | 高分子分散型液晶表示素子用組成物及び高分子分散型液晶表示素子 |
| JP2006257274A (ja) * | 2005-03-17 | 2006-09-28 | Dainippon Ink & Chem Inc | 高分子分散型液晶表示素子用組成物及び高分子分散型液晶表示素子 |
| JP2007503405A (ja) * | 2003-08-25 | 2007-02-22 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフトング | 液晶媒体で使用するための化合物 |
| JP2007503487A (ja) * | 2003-08-25 | 2007-02-22 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフトング | メソゲン性化合物、電気光学ディスプレイ用媒体および電気光学ディスプレイ |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2269561C (en) * | 1998-04-22 | 2007-06-05 | Dainippon Ink And Chemicals, Inc. | Naphthalene derivative and liquid crystal composition comprising the same |
| JP2009292729A (ja) * | 2007-02-28 | 2009-12-17 | Chisso Corp | Cf2o結合基を有する5環液晶化合物、液晶組成物および液晶表示素子 |
| JP2009067780A (ja) * | 2007-08-22 | 2009-04-02 | Chisso Corp | クロロナフタレン部位を有する液晶化合物、液晶組成物および光素子 |
| US9039929B2 (en) * | 2011-08-02 | 2015-05-26 | Dic Corporation | Nematic liquid crystal composition |
| JP5648881B2 (ja) * | 2012-09-03 | 2015-01-07 | Dic株式会社 | ネマチック液晶組成物 |
-
2013
- 2013-03-07 TW TW102108007A patent/TWI570221B/zh active
- 2013-03-13 KR KR1020147026050A patent/KR101539703B1/ko active IP Right Grant
- 2013-03-13 CN CN201610048859.9A patent/CN105647541B/zh active Active
- 2013-03-13 WO PCT/JP2013/057053 patent/WO2013141116A1/ja active Application Filing
- 2013-03-13 CN CN201380015404.1A patent/CN104220556B/zh active Active
- 2013-03-13 JP JP2013550064A patent/JP5582264B2/ja active Active
- 2013-03-13 EP EP13764021.5A patent/EP2835410B1/en active Active
- 2013-03-13 US US14/386,154 patent/US20150159086A1/en not_active Abandoned
Patent Citations (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1996032365A1 (fr) | 1995-04-12 | 1996-10-17 | Chisso Corporation | Compose de cristaux liquides substitues par fluor, composition de cristaux liquides et afficheur a cristaux liquides |
| JPH09157202A (ja) | 1995-12-05 | 1997-06-17 | Chisso Corp | 酸素原子含有結合基を持つアルケニル化合物、液晶組成物および液晶表示素子 |
| WO1998023564A1 (fr) | 1996-11-28 | 1998-06-04 | Chisso Corporation | Derives de benzene a substitution de fluor, composition a cristaux liquides et element d'affichage a cristaux liquides |
| JP2000169413A (ja) * | 1998-12-08 | 2000-06-20 | Dainippon Ink & Chem Inc | 6−トリフルオロメトキシナフタレン誘導体である新規液晶性化合物とそれを含有する液晶組成物及びその製造方法 |
| JP2001019649A (ja) * | 1999-07-06 | 2001-01-23 | Dainippon Ink & Chem Inc | 6−フルオロナフタレン誘導体である新規液晶性化合物とそれを含有する液晶組成物 |
| JP2003183656A (ja) | 2001-10-12 | 2003-07-03 | Merck Patent Gmbh | 液晶媒体 |
| JP2003286217A (ja) * | 2002-03-29 | 2003-10-10 | Chisso Corp | ナフタレン環を有する液晶性化合物、液晶組成物および液晶表示素子 |
| JP2007503405A (ja) * | 2003-08-25 | 2007-02-22 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフトング | 液晶媒体で使用するための化合物 |
| JP2007503487A (ja) * | 2003-08-25 | 2007-02-22 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフトング | メソゲン性化合物、電気光学ディスプレイ用媒体および電気光学ディスプレイ |
| JP2005232215A (ja) * | 2004-02-17 | 2005-09-02 | Dainippon Ink & Chem Inc | 高分子分散型液晶表示素子用組成物及び高分子分散型液晶表示素子 |
| JP2005232214A (ja) * | 2004-02-17 | 2005-09-02 | Dainippon Ink & Chem Inc | 高分子分散型液晶表示素子用組成物及び高分子分散型液晶表示素子 |
| JP2006257274A (ja) * | 2005-03-17 | 2006-09-28 | Dainippon Ink & Chem Inc | 高分子分散型液晶表示素子用組成物及び高分子分散型液晶表示素子 |
Cited By (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2014057780A1 (ja) * | 2012-10-09 | 2014-04-17 | Dic株式会社 | フッ素化ナフタレン構造を持つ化合物及びその液晶組成物 |
| US9315727B2 (en) | 2012-10-09 | 2016-04-19 | DIC Corporation (Tokyo) | Compound having fluorinated naphthalene structure and liquid crystal composition of the same |
| US9637466B2 (en) | 2013-07-25 | 2017-05-02 | Dic Corporation | Liquid crystal compound having 2, 6-difluorophenyl ether structure and liquid crystal composition thereof |
| US10544365B2 (en) | 2013-08-30 | 2020-01-28 | Dic Corporation | Nematic liquid crystal composition |
| US9573923B2 (en) | 2013-10-03 | 2017-02-21 | Dic Corporation | Liquid crystal compound having 2, 6-difluorophenylether structure, and liquid crystal composition containing the same |
| WO2015076093A1 (ja) * | 2013-11-19 | 2015-05-28 | Dic株式会社 | ネマチック液晶組成物及びこれを用いた液晶表示素子 |
| JP5950057B2 (ja) * | 2013-12-25 | 2016-07-13 | Dic株式会社 | ネマチック液晶組成物及びこれを用いた液晶表示素子 |
| US20170029698A1 (en) * | 2013-12-25 | 2017-02-02 | Dic Corporation | Antioxidant for liquid crystal composition, liquid crystal composition, and liquid crystal display device using liquid crystal composition |
| JP5950058B2 (ja) * | 2013-12-25 | 2016-07-13 | Dic株式会社 | 液晶組成物用酸化防止剤、液晶組成物及びこれを用いた液晶表示素子 |
| JPWO2015098661A1 (ja) * | 2013-12-25 | 2017-03-23 | Dic株式会社 | 液晶組成物用酸化防止剤、液晶組成物及びこれを用いた液晶表示素子 |
| WO2015098740A1 (ja) * | 2013-12-25 | 2015-07-02 | Dic株式会社 | ネマチック液晶組成物及びこれを用いた液晶表示素子 |
| US10174254B2 (en) | 2013-12-25 | 2019-01-08 | Dic Corporation | Nematic liquid crystal composition and liquid crystal display element using the same |
| WO2015098661A1 (ja) * | 2013-12-25 | 2015-07-02 | Dic株式会社 | 液晶組成物用酸化防止剤、液晶組成物及びこれを用いた液晶表示素子 |
| US10000700B2 (en) | 2014-07-31 | 2018-06-19 | Dic Corporation | Nematic liquid crystal composition |
| US10253258B2 (en) | 2014-07-31 | 2019-04-09 | Dic Corporation | Nematic liquid crystal composition |
Also Published As
| Publication number | Publication date |
|---|---|
| TWI570221B (zh) | 2017-02-11 |
| EP2835410A4 (en) | 2015-12-23 |
| US20150159086A1 (en) | 2015-06-11 |
| CN105647541B (zh) | 2018-04-13 |
| KR101539703B1 (ko) | 2015-07-27 |
| CN105647541A (zh) | 2016-06-08 |
| CN104220556B (zh) | 2017-08-08 |
| EP2835410A1 (en) | 2015-02-11 |
| JP5582264B2 (ja) | 2014-09-03 |
| EP2835410B1 (en) | 2017-10-04 |
| JPWO2013141116A1 (ja) | 2015-08-03 |
| KR20140121484A (ko) | 2014-10-15 |
| CN104220556A (zh) | 2014-12-17 |
| TW201341510A (zh) | 2013-10-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5582264B2 (ja) | ネマチック液晶組成物 | |
| JP5376269B2 (ja) | ネマチック液晶組成物 | |
| JP5780431B2 (ja) | ネマチック液晶組成物 | |
| JP5534115B1 (ja) | ネマチック液晶組成物 | |
| JP5534114B1 (ja) | ネマチック液晶組成物 | |
| JP5534382B1 (ja) | ネマチック液晶組成物 | |
| JP5776864B1 (ja) | ネマチック液晶組成物 | |
| JP5534381B1 (ja) | ネマチック液晶組成物 | |
| JP5648881B2 (ja) | ネマチック液晶組成物 | |
| JP5783083B2 (ja) | ネマチック液晶組成物 | |
| JP5783084B2 (ja) | ネマチック液晶組成物 | |
| JP5910800B1 (ja) | ネマチック液晶組成物 | |
| JP2013241519A (ja) | ネマチック液晶組成物 | |
| WO2016017615A1 (ja) | ネマチック液晶組成物 | |
| JP6061040B2 (ja) | ネマチック液晶組成物及びこれを用いた液晶表示素子 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| ENP | Entry into the national phase |
Ref document number: 2013550064 Country of ref document: JP Kind code of ref document: A |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 13764021 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 20147026050 Country of ref document: KR Kind code of ref document: A |
|
| REEP | Request for entry into the european phase |
Ref document number: 2013764021 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2013764021 Country of ref document: EP |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 14386154 Country of ref document: US |