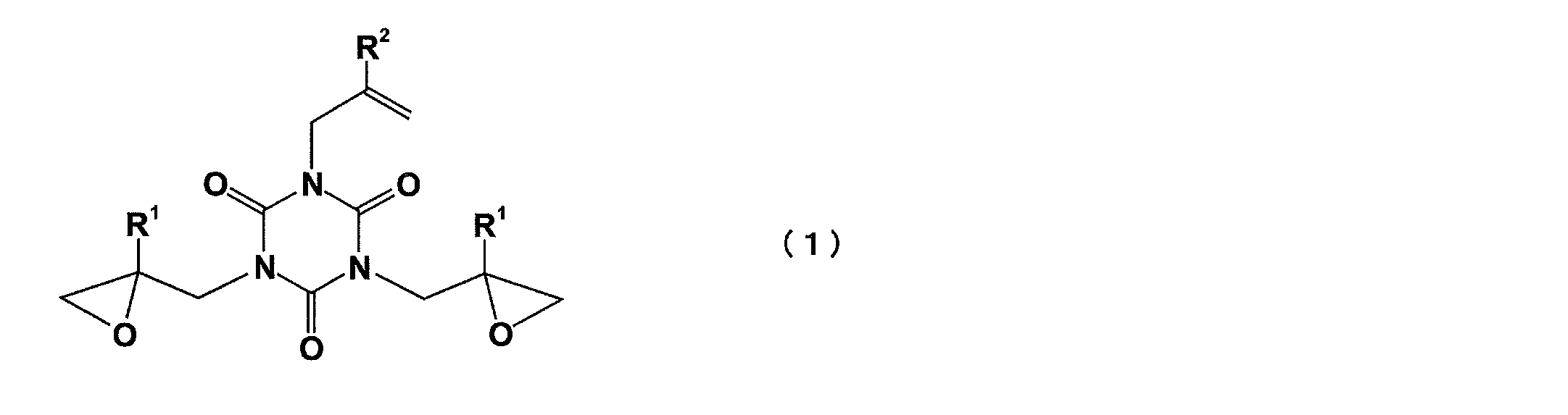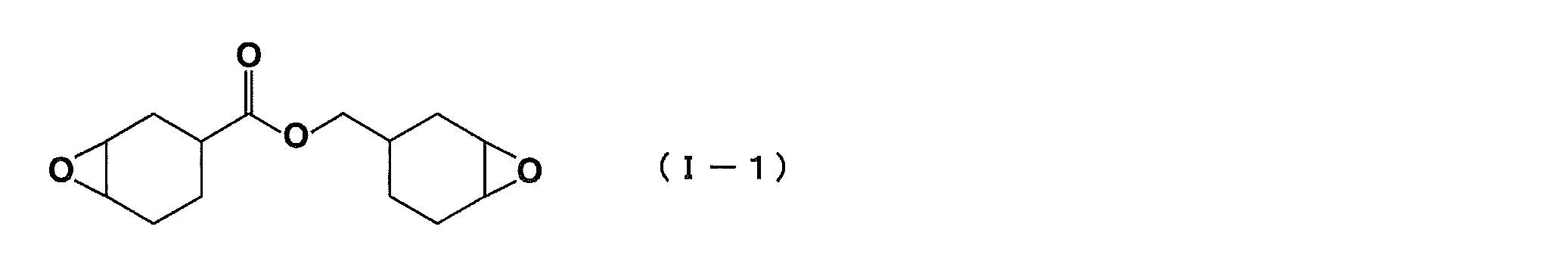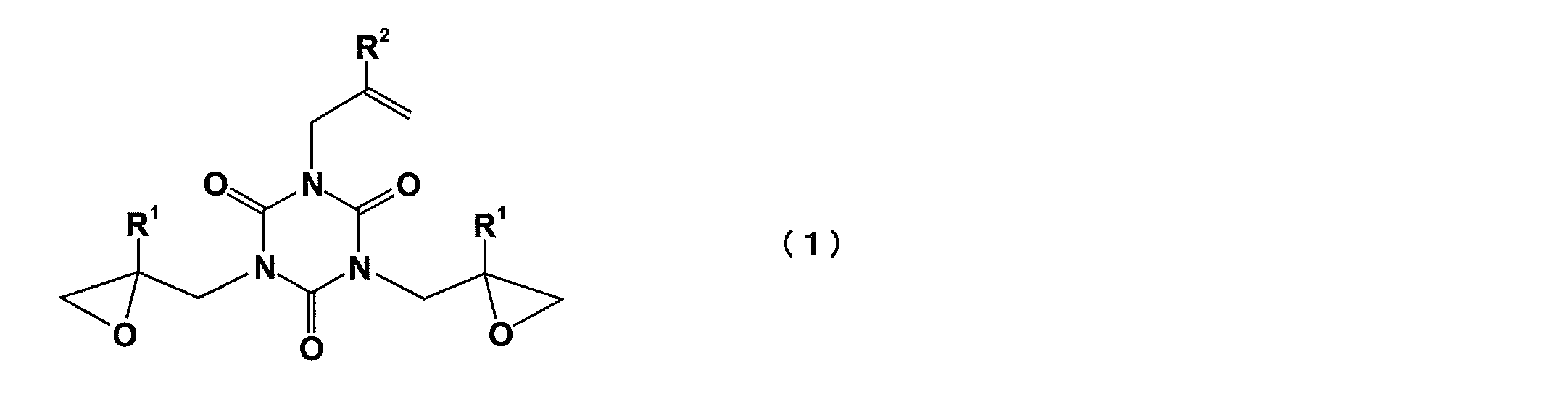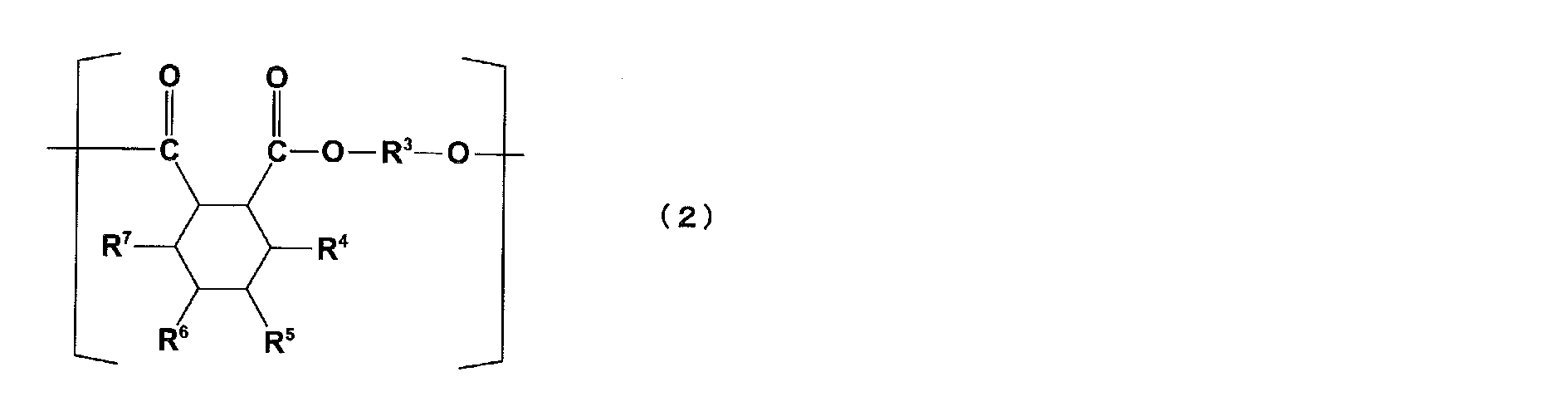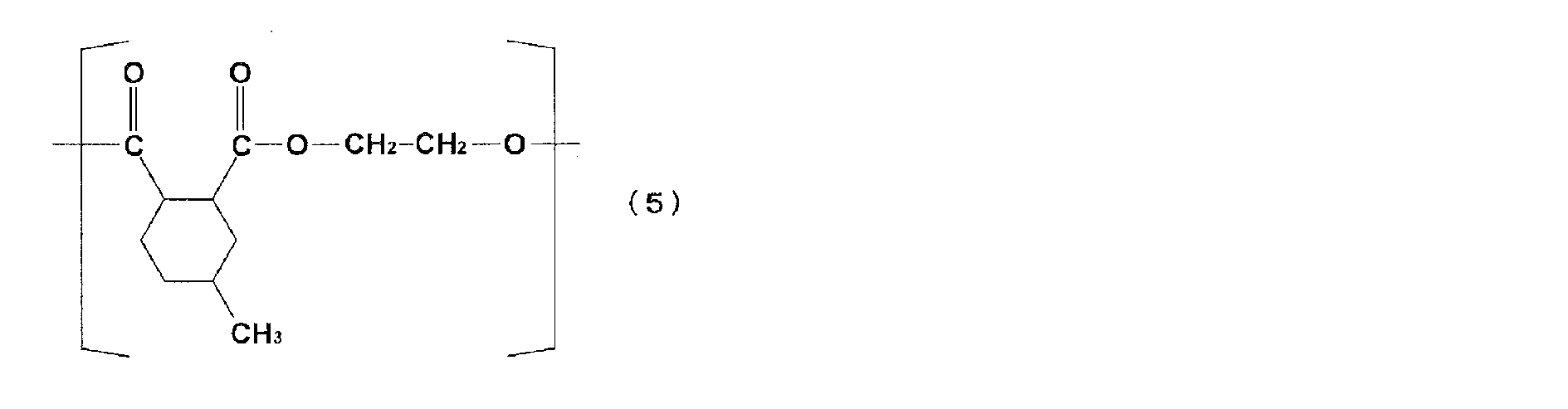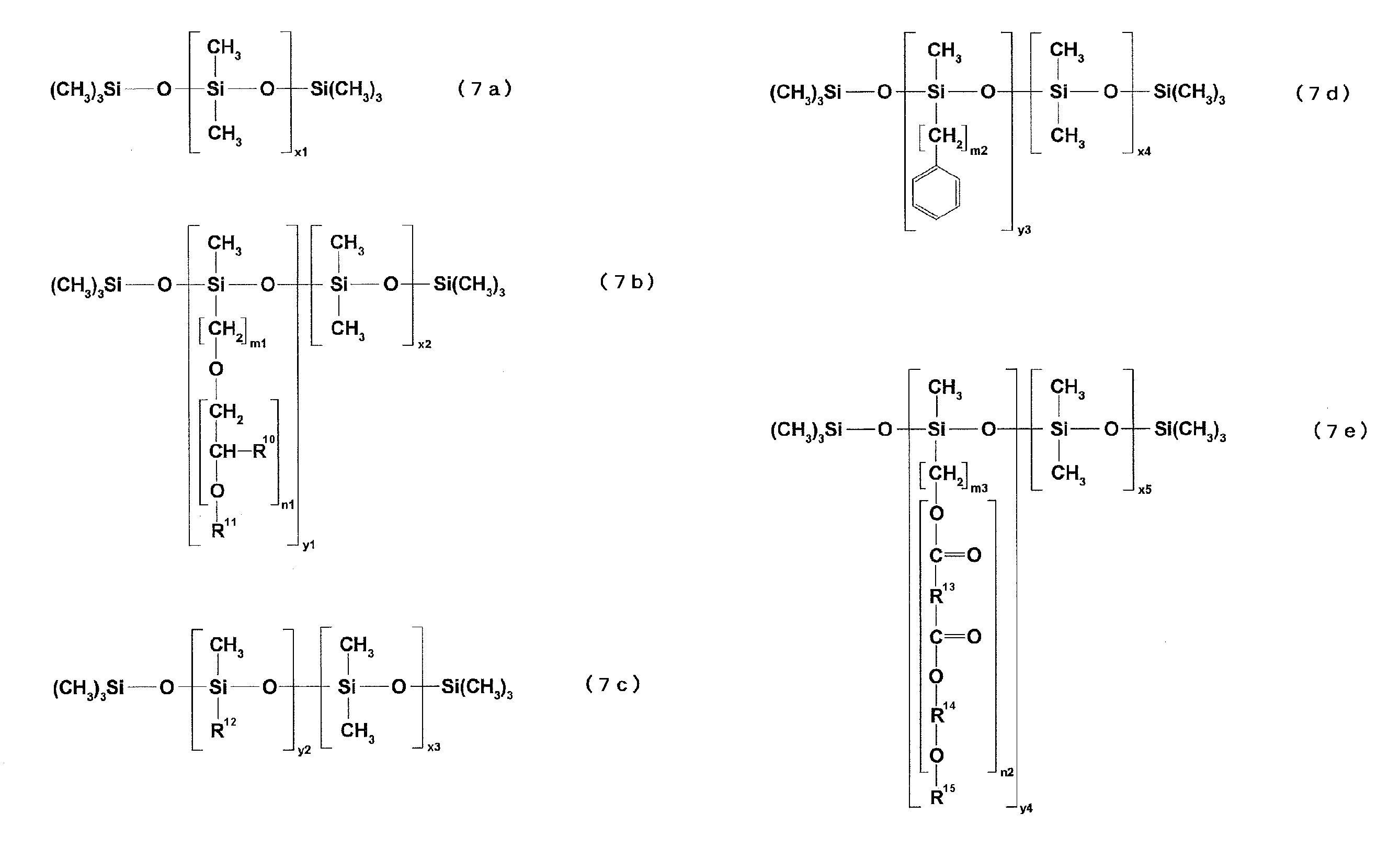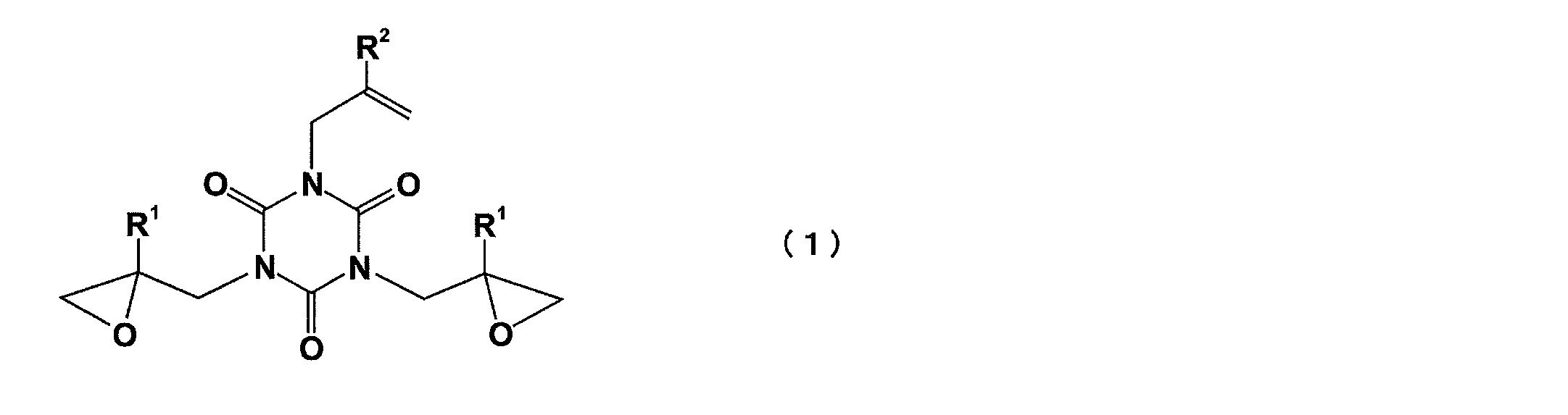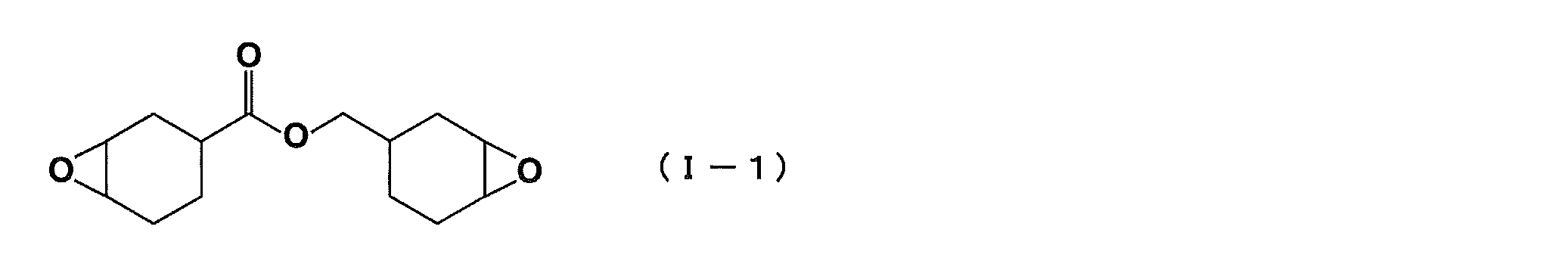WO2013011832A1 - 硬化性エポキシ樹脂組成物 - Google Patents
硬化性エポキシ樹脂組成物 Download PDFInfo
- Publication number
- WO2013011832A1 WO2013011832A1 PCT/JP2012/066968 JP2012066968W WO2013011832A1 WO 2013011832 A1 WO2013011832 A1 WO 2013011832A1 JP 2012066968 W JP2012066968 W JP 2012066968W WO 2013011832 A1 WO2013011832 A1 WO 2013011832A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- group
- resin composition
- alicyclic
- epoxy resin
- compound
- Prior art date
Links
- 239000000203 mixture Substances 0.000 title claims abstract description 136
- 229920000647 polyepoxide Polymers 0.000 title claims abstract description 130
- 239000003822 epoxy resin Substances 0.000 title claims abstract description 128
- -1 isocyanurate compound Chemical class 0.000 claims abstract description 171
- 125000002723 alicyclic group Chemical group 0.000 claims abstract description 153
- 239000003795 chemical substances by application Substances 0.000 claims abstract description 109
- 150000001875 compounds Chemical class 0.000 claims abstract description 95
- 125000003700 epoxy group Chemical group 0.000 claims abstract description 83
- 229920001225 polyester resin Polymers 0.000 claims abstract description 63
- 239000004645 polyester resin Substances 0.000 claims abstract description 63
- 239000004593 Epoxy Substances 0.000 claims abstract description 60
- KPUWHANPEXNPJT-UHFFFAOYSA-N disiloxane Chemical class [SiH3]O[SiH3] KPUWHANPEXNPJT-UHFFFAOYSA-N 0.000 claims abstract description 45
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims abstract description 28
- 230000003287 optical effect Effects 0.000 claims description 114
- 239000004065 semiconductor Substances 0.000 claims description 107
- 229920005862 polyol Polymers 0.000 claims description 64
- 239000002245 particle Substances 0.000 claims description 59
- 229920001971 elastomer Polymers 0.000 claims description 51
- 239000005060 rubber Substances 0.000 claims description 51
- 125000000217 alkyl group Chemical group 0.000 claims description 46
- NIXOWILDQLNWCW-UHFFFAOYSA-N acrylic acid group Chemical group C(C=C)(=O)O NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 claims description 45
- 229910052731 fluorine Inorganic materials 0.000 claims description 36
- 125000004432 carbon atom Chemical group C* 0.000 claims description 35
- YCKRFDGAMUMZLT-UHFFFAOYSA-N Fluorine atom Chemical compound [F] YCKRFDGAMUMZLT-UHFFFAOYSA-N 0.000 claims description 33
- 229920001400 block copolymer Polymers 0.000 claims description 33
- 239000011737 fluorine Substances 0.000 claims description 33
- 238000007789 sealing Methods 0.000 claims description 25
- 229920001296 polysiloxane Polymers 0.000 claims description 23
- 239000003054 catalyst Substances 0.000 claims description 19
- 239000011342 resin composition Substances 0.000 claims description 19
- 238000005538 encapsulation Methods 0.000 claims description 5
- ZWAJLVLEBYIOTI-UHFFFAOYSA-N cyclohexene oxide Chemical group C1CCCC2OC21 ZWAJLVLEBYIOTI-UHFFFAOYSA-N 0.000 claims description 4
- 125000004209 (C1-C8) alkyl group Chemical group 0.000 abstract 1
- 238000001723 curing Methods 0.000 description 101
- 239000000047 product Substances 0.000 description 87
- 229920000642 polymer Polymers 0.000 description 69
- 239000000178 monomer Substances 0.000 description 67
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 54
- 229920000570 polyether Polymers 0.000 description 44
- 238000004519 manufacturing process Methods 0.000 description 42
- 150000003077 polyols Chemical class 0.000 description 42
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 36
- 229920000728 polyester Polymers 0.000 description 35
- 239000004721 Polyphenylene oxide Substances 0.000 description 33
- 239000002253 acid Substances 0.000 description 30
- 229920005989 resin Polymers 0.000 description 28
- 239000011347 resin Substances 0.000 description 28
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 25
- 238000002156 mixing Methods 0.000 description 25
- 125000000962 organic group Chemical group 0.000 description 25
- CERQOIWHTDAKMF-UHFFFAOYSA-N Methacrylic acid Chemical compound CC(=C)C(O)=O CERQOIWHTDAKMF-UHFFFAOYSA-N 0.000 description 21
- 238000000034 method Methods 0.000 description 20
- 125000001424 substituent group Chemical group 0.000 description 19
- 150000008065 acid anhydrides Chemical class 0.000 description 18
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 18
- 230000007423 decrease Effects 0.000 description 18
- MTHSVFCYNBDYFN-UHFFFAOYSA-N diethylene glycol Chemical compound OCCOCCO MTHSVFCYNBDYFN-UHFFFAOYSA-N 0.000 description 18
- 150000002009 diols Chemical class 0.000 description 18
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 18
- 229920005573 silicon-containing polymer Polymers 0.000 description 18
- 239000000126 substance Substances 0.000 description 18
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 17
- 238000006116 polymerization reaction Methods 0.000 description 17
- WERYXYBDKMZEQL-UHFFFAOYSA-N butane-1,4-diol Chemical compound OCCCCO WERYXYBDKMZEQL-UHFFFAOYSA-N 0.000 description 16
- 239000004417 polycarbonate Substances 0.000 description 16
- 229920000515 polycarbonate Polymers 0.000 description 16
- NIXOWILDQLNWCW-UHFFFAOYSA-M Acrylate Chemical compound [O-]C(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-M 0.000 description 15
- 238000012360 testing method Methods 0.000 description 15
- PPBRXRYQALVLMV-UHFFFAOYSA-N Styrene Chemical compound C=CC1=CC=CC=C1 PPBRXRYQALVLMV-UHFFFAOYSA-N 0.000 description 14
- 125000002947 alkylene group Chemical group 0.000 description 14
- 238000010438 heat treatment Methods 0.000 description 14
- 229920000058 polyacrylate Polymers 0.000 description 14
- 239000004205 dimethyl polysiloxane Substances 0.000 description 13
- 229920000435 poly(dimethylsiloxane) Polymers 0.000 description 13
- OFOBLEOULBTSOW-UHFFFAOYSA-N Malonic acid Chemical compound OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 12
- 150000002430 hydrocarbons Chemical group 0.000 description 12
- 239000000463 material Substances 0.000 description 12
- 230000000052 comparative effect Effects 0.000 description 11
- ZFSLODLOARCGLH-UHFFFAOYSA-N isocyanuric acid Chemical compound OC1=NC(O)=NC(O)=N1 ZFSLODLOARCGLH-UHFFFAOYSA-N 0.000 description 11
- 229920005906 polyester polyol Polymers 0.000 description 11
- 235000013772 propylene glycol Nutrition 0.000 description 11
- 229920002554 vinyl polymer Polymers 0.000 description 11
- CQEYYJKEWSMYFG-UHFFFAOYSA-N butyl acrylate Chemical compound CCCCOC(=O)C=C CQEYYJKEWSMYFG-UHFFFAOYSA-N 0.000 description 10
- BVKZGUZCCUSVTD-UHFFFAOYSA-N carbonic acid Chemical group OC(O)=O BVKZGUZCCUSVTD-UHFFFAOYSA-N 0.000 description 10
- 238000006243 chemical reaction Methods 0.000 description 10
- PEDCQBHIVMGVHV-UHFFFAOYSA-N glycerol group Chemical group OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 10
- 239000000654 additive Substances 0.000 description 9
- IISBACLAFKSPIT-UHFFFAOYSA-N bisphenol A Chemical compound C=1C=C(O)C=CC=1C(C)(C)C1=CC=C(O)C=C1 IISBACLAFKSPIT-UHFFFAOYSA-N 0.000 description 9
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 9
- 230000035939 shock Effects 0.000 description 9
- PUPZLCDOIYMWBV-UHFFFAOYSA-N (+/-)-1,3-Butanediol Chemical compound CC(O)CCO PUPZLCDOIYMWBV-UHFFFAOYSA-N 0.000 description 8
- MYRTYDVEIRVNKP-UHFFFAOYSA-N 1,2-Divinylbenzene Chemical compound C=CC1=CC=CC=C1C=C MYRTYDVEIRVNKP-UHFFFAOYSA-N 0.000 description 8
- 235000010443 alginic acid Nutrition 0.000 description 8
- 229920000615 alginic acid Polymers 0.000 description 8
- 125000001153 fluoro group Chemical group F* 0.000 description 8
- 230000004907 flux Effects 0.000 description 8
- 238000009472 formulation Methods 0.000 description 8
- 125000000524 functional group Chemical group 0.000 description 8
- 125000003187 heptyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 8
- 150000002596 lactones Chemical class 0.000 description 8
- SLCVBVWXLSEKPL-UHFFFAOYSA-N neopentyl glycol Chemical compound OCC(C)(C)CO SLCVBVWXLSEKPL-UHFFFAOYSA-N 0.000 description 8
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 8
- 238000003756 stirring Methods 0.000 description 8
- 229910000831 Steel Inorganic materials 0.000 description 7
- 125000005587 carbonate group Chemical group 0.000 description 7
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 description 7
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 7
- 125000005647 linker group Chemical group 0.000 description 7
- 239000007788 liquid Substances 0.000 description 7
- 229920003229 poly(methyl methacrylate) Polymers 0.000 description 7
- 239000004926 polymethyl methacrylate Substances 0.000 description 7
- 239000010959 steel Substances 0.000 description 7
- DNIAPMSPPWPWGF-VKHMYHEASA-N (+)-propylene glycol Chemical compound C[C@H](O)CO DNIAPMSPPWPWGF-VKHMYHEASA-N 0.000 description 6
- YPFDHNVEDLHUCE-UHFFFAOYSA-N 1,3-propanediol Substances OCCCO YPFDHNVEDLHUCE-UHFFFAOYSA-N 0.000 description 6
- 229940035437 1,3-propanediol Drugs 0.000 description 6
- 229940043375 1,5-pentanediol Drugs 0.000 description 6
- KAKZBPTYRLMSJV-UHFFFAOYSA-N Butadiene Chemical compound C=CC=C KAKZBPTYRLMSJV-UHFFFAOYSA-N 0.000 description 6
- SOGAXMICEFXMKE-UHFFFAOYSA-N Butylmethacrylate Chemical compound CCCCOC(=O)C(C)=C SOGAXMICEFXMKE-UHFFFAOYSA-N 0.000 description 6
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 6
- ALQSHHUCVQOPAS-UHFFFAOYSA-N Pentane-1,5-diol Chemical compound OCCCCCO ALQSHHUCVQOPAS-UHFFFAOYSA-N 0.000 description 6
- KKEYFWRCBNTPAC-UHFFFAOYSA-N Terephthalic acid Chemical compound OC(=O)C1=CC=C(C(O)=O)C=C1 KKEYFWRCBNTPAC-UHFFFAOYSA-N 0.000 description 6
- 239000011951 cationic catalyst Substances 0.000 description 6
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 6
- DIOQZVSQGTUSAI-UHFFFAOYSA-N decane Chemical compound CCCCCCCCCC DIOQZVSQGTUSAI-UHFFFAOYSA-N 0.000 description 6
- GHLKSLMMWAKNBM-UHFFFAOYSA-N dodecane-1,12-diol Chemical compound OCCCCCCCCCCCCO GHLKSLMMWAKNBM-UHFFFAOYSA-N 0.000 description 6
- 150000002148 esters Chemical class 0.000 description 6
- QQVIHTHCMHWDBS-UHFFFAOYSA-N isophthalic acid Chemical compound OC(=O)C1=CC=CC(C(O)=O)=C1 QQVIHTHCMHWDBS-UHFFFAOYSA-N 0.000 description 6
- 229910052751 metal Inorganic materials 0.000 description 6
- 239000002184 metal Substances 0.000 description 6
- 125000001570 methylene group Chemical group [H]C([H])([*:1])[*:2] 0.000 description 6
- BDJRBEYXGGNYIS-UHFFFAOYSA-N nonanedioic acid Chemical compound OC(=O)CCCCCCCC(O)=O BDJRBEYXGGNYIS-UHFFFAOYSA-N 0.000 description 6
- 125000004430 oxygen atom Chemical group O* 0.000 description 6
- XNGIFLGASWRNHJ-UHFFFAOYSA-N phthalic acid Chemical compound OC(=O)C1=CC=CC=C1C(O)=O XNGIFLGASWRNHJ-UHFFFAOYSA-N 0.000 description 6
- 229920000166 polytrimethylene carbonate Polymers 0.000 description 6
- 238000007151 ring opening polymerisation reaction Methods 0.000 description 6
- 150000003839 salts Chemical class 0.000 description 6
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 6
- 229910000679 solder Inorganic materials 0.000 description 6
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 6
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 6
- BJZYYSAMLOBSDY-QMMMGPOBSA-N (2s)-2-butoxybutan-1-ol Chemical compound CCCCO[C@@H](CC)CO BJZYYSAMLOBSDY-QMMMGPOBSA-N 0.000 description 5
- PXGZQGDTEZPERC-UHFFFAOYSA-N 1,4-cyclohexanedicarboxylic acid Chemical compound OC(=O)C1CCC(C(O)=O)CC1 PXGZQGDTEZPERC-UHFFFAOYSA-N 0.000 description 5
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 5
- SXFJDZNJHVPHPH-UHFFFAOYSA-N 3-methylpentane-1,5-diol Chemical compound OCCC(C)CCO SXFJDZNJHVPHPH-UHFFFAOYSA-N 0.000 description 5
- ZJCCRDAZUWHFQH-UHFFFAOYSA-N Trimethylolpropane Chemical compound CCC(CO)(CO)CO ZJCCRDAZUWHFQH-UHFFFAOYSA-N 0.000 description 5
- YIMQCDZDWXUDCA-UHFFFAOYSA-N [4-(hydroxymethyl)cyclohexyl]methanol Chemical compound OCC1CCC(CO)CC1 YIMQCDZDWXUDCA-UHFFFAOYSA-N 0.000 description 5
- 125000003710 aryl alkyl group Chemical group 0.000 description 5
- 150000001993 dienes Chemical class 0.000 description 5
- 235000011187 glycerol Nutrition 0.000 description 5
- XXMIOPMDWAUFGU-UHFFFAOYSA-N hexane-1,6-diol Chemical compound OCCCCCCO XXMIOPMDWAUFGU-UHFFFAOYSA-N 0.000 description 5
- WNLRTRBMVRJNCN-UHFFFAOYSA-N hexanedioic acid Natural products OC(=O)CCCCC(O)=O WNLRTRBMVRJNCN-UHFFFAOYSA-N 0.000 description 5
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 5
- 125000005010 perfluoroalkyl group Chemical group 0.000 description 5
- 239000013034 phenoxy resin Substances 0.000 description 5
- 229920006287 phenoxy resin Polymers 0.000 description 5
- 229920002857 polybutadiene Polymers 0.000 description 5
- 229920001223 polyethylene glycol Polymers 0.000 description 5
- 125000004805 propylene group Chemical group [H]C([H])([H])C([H])([*:1])C([H])([H])[*:2] 0.000 description 5
- CXMXRPHRNRROMY-UHFFFAOYSA-N sebacic acid Chemical compound OC(=O)CCCCCCCCC(O)=O CXMXRPHRNRROMY-UHFFFAOYSA-N 0.000 description 5
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 5
- DNIAPMSPPWPWGF-GSVOUGTGSA-N (R)-(-)-Propylene glycol Chemical compound C[C@@H](O)CO DNIAPMSPPWPWGF-GSVOUGTGSA-N 0.000 description 4
- SMZOUWXMTYCWNB-UHFFFAOYSA-N 2-(2-methoxy-5-methylphenyl)ethanamine Chemical compound COC1=CC=C(C)C=C1CCN SMZOUWXMTYCWNB-UHFFFAOYSA-N 0.000 description 4
- SVTBMSDMJJWYQN-UHFFFAOYSA-N 2-methylpentane-2,4-diol Chemical compound CC(O)CC(C)(C)O SVTBMSDMJJWYQN-UHFFFAOYSA-N 0.000 description 4
- QWGRWMMWNDWRQN-UHFFFAOYSA-N 2-methylpropane-1,3-diol Chemical compound OCC(C)CO QWGRWMMWNDWRQN-UHFFFAOYSA-N 0.000 description 4
- YEJRWHAVMIAJKC-UHFFFAOYSA-N 4-Butyrolactone Chemical compound O=C1CCCO1 YEJRWHAVMIAJKC-UHFFFAOYSA-N 0.000 description 4
- OZJPLYNZGCXSJM-UHFFFAOYSA-N 5-valerolactone Chemical compound O=C1CCCCO1 OZJPLYNZGCXSJM-UHFFFAOYSA-N 0.000 description 4
- YXALYBMHAYZKAP-UHFFFAOYSA-N 7-oxabicyclo[4.1.0]heptan-4-ylmethyl 7-oxabicyclo[4.1.0]heptane-4-carboxylate Chemical compound C1CC2OC2CC1C(=O)OCC1CC2OC2CC1 YXALYBMHAYZKAP-UHFFFAOYSA-N 0.000 description 4
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 4
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 4
- AEMRFAOFKBGASW-UHFFFAOYSA-N Glycolic acid Chemical compound OCC(O)=O AEMRFAOFKBGASW-UHFFFAOYSA-N 0.000 description 4
- RRHGJUQNOFWUDK-UHFFFAOYSA-N Isoprene Chemical compound CC(=C)C=C RRHGJUQNOFWUDK-UHFFFAOYSA-N 0.000 description 4
- BAPJBEWLBFYGME-UHFFFAOYSA-N Methyl acrylate Chemical compound COC(=O)C=C BAPJBEWLBFYGME-UHFFFAOYSA-N 0.000 description 4
- VVQNEPGJFQJSBK-UHFFFAOYSA-N Methyl methacrylate Chemical compound COC(=O)C(C)=C VVQNEPGJFQJSBK-UHFFFAOYSA-N 0.000 description 4
- 229920000459 Nitrile rubber Polymers 0.000 description 4
- 239000004793 Polystyrene Substances 0.000 description 4
- GOOHAUXETOMSMM-UHFFFAOYSA-N Propylene oxide Chemical compound CC1CO1 GOOHAUXETOMSMM-UHFFFAOYSA-N 0.000 description 4
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical group [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 4
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 4
- 230000000996 additive effect Effects 0.000 description 4
- 125000003368 amide group Chemical group 0.000 description 4
- OWBTYPJTUOEWEK-UHFFFAOYSA-N butane-2,3-diol Chemical compound CC(O)C(C)O OWBTYPJTUOEWEK-UHFFFAOYSA-N 0.000 description 4
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 4
- 150000001768 cations Chemical class 0.000 description 4
- 239000011248 coating agent Substances 0.000 description 4
- 238000000576 coating method Methods 0.000 description 4
- 238000007796 conventional method Methods 0.000 description 4
- SZXQTJUDPRGNJN-UHFFFAOYSA-N dipropylene glycol Chemical compound OCCCOCCCO SZXQTJUDPRGNJN-UHFFFAOYSA-N 0.000 description 4
- 238000009826 distribution Methods 0.000 description 4
- 230000000694 effects Effects 0.000 description 4
- 125000004185 ester group Chemical group 0.000 description 4
- RTZKZFJDLAIYFH-UHFFFAOYSA-N ether Substances CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 4
- 238000005227 gel permeation chromatography Methods 0.000 description 4
- LNEPOXFFQSENCJ-UHFFFAOYSA-N haloperidol Chemical compound C1CC(O)(C=2C=CC(Cl)=CC=2)CCN1CCCC(=O)C1=CC=C(F)C=C1 LNEPOXFFQSENCJ-UHFFFAOYSA-N 0.000 description 4
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 4
- 230000014759 maintenance of location Effects 0.000 description 4
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 4
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 4
- 238000006068 polycondensation reaction Methods 0.000 description 4
- 230000000379 polymerizing effect Effects 0.000 description 4
- 229920002223 polystyrene Polymers 0.000 description 4
- 125000004368 propenyl group Chemical group C(=CC)* 0.000 description 4
- 239000000758 substrate Substances 0.000 description 4
- MUTGBJKUEZFXGO-OLQVQODUSA-N (3as,7ar)-3a,4,5,6,7,7a-hexahydro-2-benzofuran-1,3-dione Chemical compound C1CCC[C@@H]2C(=O)OC(=O)[C@@H]21 MUTGBJKUEZFXGO-OLQVQODUSA-N 0.000 description 3
- KMOUUZVZFBCRAM-OLQVQODUSA-N (3as,7ar)-3a,4,7,7a-tetrahydro-2-benzofuran-1,3-dione Chemical compound C1C=CC[C@@H]2C(=O)OC(=O)[C@@H]21 KMOUUZVZFBCRAM-OLQVQODUSA-N 0.000 description 3
- ZWVMLYRJXORSEP-UHFFFAOYSA-N 1,2,6-Hexanetriol Chemical compound OCCCCC(O)CO ZWVMLYRJXORSEP-UHFFFAOYSA-N 0.000 description 3
- GZZLQUBMUXEOBE-UHFFFAOYSA-N 2,2,4-trimethylhexane-1,6-diol Chemical compound OCCC(C)CC(C)(C)CO GZZLQUBMUXEOBE-UHFFFAOYSA-N 0.000 description 3
- WMYINDVYGQKYMI-UHFFFAOYSA-N 2-[2,2-bis(hydroxymethyl)butoxymethyl]-2-ethylpropane-1,3-diol Chemical compound CCC(CO)(CO)COCC(CC)(CO)CO WMYINDVYGQKYMI-UHFFFAOYSA-N 0.000 description 3
- AJKXDPSHWRTFOZ-UHFFFAOYSA-N 2-ethylhexane-1,6-diol Chemical compound CCC(CO)CCCCO AJKXDPSHWRTFOZ-UHFFFAOYSA-N 0.000 description 3
- AAAWJUMVTPNRDT-UHFFFAOYSA-N 2-methylpentane-1,5-diol Chemical compound OCC(C)CCCO AAAWJUMVTPNRDT-UHFFFAOYSA-N 0.000 description 3
- LBKFGYZQBSGRHY-UHFFFAOYSA-N 3-hydroxy-4-methoxybenzoic acid Chemical compound COC1=CC=C(C(O)=O)C=C1O LBKFGYZQBSGRHY-UHFFFAOYSA-N 0.000 description 3
- YWVFNWVZBAWOOY-UHFFFAOYSA-N 4-methylcyclohexane-1,2-dicarboxylic acid Chemical compound CC1CCC(C(O)=O)C(C(O)=O)C1 YWVFNWVZBAWOOY-UHFFFAOYSA-N 0.000 description 3
- FKBMTBAXDISZGN-UHFFFAOYSA-N 5-methyl-3a,4,5,6,7,7a-hexahydro-2-benzofuran-1,3-dione Chemical compound C1C(C)CCC2C(=O)OC(=O)C12 FKBMTBAXDISZGN-UHFFFAOYSA-N 0.000 description 3
- NLHHRLWOUZZQLW-UHFFFAOYSA-N Acrylonitrile Chemical compound C=CC#N NLHHRLWOUZZQLW-UHFFFAOYSA-N 0.000 description 3
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 3
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 3
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 3
- VQTUBCCKSQIDNK-UHFFFAOYSA-N Isobutene Chemical group CC(C)=C VQTUBCCKSQIDNK-UHFFFAOYSA-N 0.000 description 3
- 229930195725 Mannitol Natural products 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 3
- RVGRUAULSDPKGF-UHFFFAOYSA-N Poloxamer Chemical compound C1CO1.CC1CO1 RVGRUAULSDPKGF-UHFFFAOYSA-N 0.000 description 3
- 239000005062 Polybutadiene Substances 0.000 description 3
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 3
- LUSFFPXRDZKBMF-UHFFFAOYSA-N [3-(hydroxymethyl)cyclohexyl]methanol Chemical compound OCC1CCCC(CO)C1 LUSFFPXRDZKBMF-UHFFFAOYSA-N 0.000 description 3
- 150000007513 acids Chemical class 0.000 description 3
- 125000003647 acryloyl group Chemical group O=C([*])C([H])=C([H])[H] 0.000 description 3
- 239000001361 adipic acid Substances 0.000 description 3
- 235000011037 adipic acid Nutrition 0.000 description 3
- 125000001931 aliphatic group Chemical group 0.000 description 3
- 125000005907 alkyl ester group Chemical group 0.000 description 3
- XYLMUPLGERFSHI-UHFFFAOYSA-N alpha-Methylstyrene Chemical compound CC(=C)C1=CC=CC=C1 XYLMUPLGERFSHI-UHFFFAOYSA-N 0.000 description 3
- 125000003118 aryl group Chemical group 0.000 description 3
- 125000004429 atom Chemical group 0.000 description 3
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 3
- 239000013522 chelant Substances 0.000 description 3
- 229920001577 copolymer Polymers 0.000 description 3
- 239000011258 core-shell material Substances 0.000 description 3
- 125000004122 cyclic group Chemical group 0.000 description 3
- RXKJFZQQPQGTFL-UHFFFAOYSA-N dihydroxyacetone Chemical compound OCC(=O)CO RXKJFZQQPQGTFL-UHFFFAOYSA-N 0.000 description 3
- 235000019329 dioctyl sodium sulphosuccinate Nutrition 0.000 description 3
- YHAIUSTWZPMYGG-UHFFFAOYSA-L disodium;2,2-dioctyl-3-sulfobutanedioate Chemical compound [Na+].[Na+].CCCCCCCCC(C([O-])=O)(C(C([O-])=O)S(O)(=O)=O)CCCCCCCC YHAIUSTWZPMYGG-UHFFFAOYSA-L 0.000 description 3
- 125000001033 ether group Chemical group 0.000 description 3
- 125000000816 ethylene group Chemical group [H]C([H])([*:1])C([H])([H])[*:2] 0.000 description 3
- 239000001530 fumaric acid Substances 0.000 description 3
- 125000003827 glycol group Chemical group 0.000 description 3
- 229930195733 hydrocarbon Natural products 0.000 description 3
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 3
- 239000011976 maleic acid Substances 0.000 description 3
- 239000000594 mannitol Substances 0.000 description 3
- 235000010355 mannitol Nutrition 0.000 description 3
- 238000005259 measurement Methods 0.000 description 3
- VYKXQOYUCMREIS-UHFFFAOYSA-N methylhexahydrophthalic anhydride Chemical compound C1CCCC2C(=O)OC(=O)C21C VYKXQOYUCMREIS-UHFFFAOYSA-N 0.000 description 3
- 150000002825 nitriles Chemical class 0.000 description 3
- 229910052757 nitrogen Inorganic materials 0.000 description 3
- WXZMFSXDPGVJKK-UHFFFAOYSA-N pentaerythritol Chemical compound OCC(CO)(CO)CO WXZMFSXDPGVJKK-UHFFFAOYSA-N 0.000 description 3
- 229920001610 polycaprolactone Polymers 0.000 description 3
- 239000004632 polycaprolactone Substances 0.000 description 3
- 238000012643 polycondensation polymerization Methods 0.000 description 3
- 229920000909 polytetrahydrofuran Polymers 0.000 description 3
- USHAGKDGDHPEEY-UHFFFAOYSA-L potassium persulfate Chemical compound [K+].[K+].[O-]S(=O)(=O)OOS([O-])(=O)=O USHAGKDGDHPEEY-UHFFFAOYSA-L 0.000 description 3
- 239000000600 sorbitol Substances 0.000 description 3
- 241000894007 species Species 0.000 description 3
- 125000000101 thioether group Chemical group 0.000 description 3
- 229920000428 triblock copolymer Polymers 0.000 description 3
- 238000004383 yellowing Methods 0.000 description 3
- PAPBSGBWRJIAAV-UHFFFAOYSA-N ε-Caprolactone Chemical class O=C1CCCCCO1 PAPBSGBWRJIAAV-UHFFFAOYSA-N 0.000 description 3
- 0 *C1(CN(C(N(CC2(*)OC2)C(N2CC(*)=C)=O)=O)C2=O)OC1 Chemical compound *C1(CN(C(N(CC2(*)OC2)C(N2CC(*)=C)=O)=O)C2=O)OC1 0.000 description 2
- HIVSALLSJIAQQF-UHFFFAOYSA-N 1,5-Dimethoxy-3-hydroxybenzoic acid Natural products COC1=CC(O)=CC(OC)=C1C(O)=O HIVSALLSJIAQQF-UHFFFAOYSA-N 0.000 description 2
- UNVGBIALRHLALK-UHFFFAOYSA-N 1,5-Hexanediol Chemical compound CC(O)CCCCO UNVGBIALRHLALK-UHFFFAOYSA-N 0.000 description 2
- DLKQHBOKULLWDQ-UHFFFAOYSA-N 1-bromonaphthalene Chemical compound C1=CC=C2C(Br)=CC=CC2=C1 DLKQHBOKULLWDQ-UHFFFAOYSA-N 0.000 description 2
- GQHTUMJGOHRCHB-UHFFFAOYSA-N 2,3,4,6,7,8,9,10-octahydropyrimido[1,2-a]azepine Chemical compound C1CCCCN2CCCN=C21 GQHTUMJGOHRCHB-UHFFFAOYSA-N 0.000 description 2
- DGASMILFPABBSL-UHFFFAOYSA-N 2,3-dimethylhexane-1,5-diol Chemical compound CC(O)CC(C)C(C)CO DGASMILFPABBSL-UHFFFAOYSA-N 0.000 description 2
- GOXQRTZXKQZDDN-UHFFFAOYSA-N 2-Ethylhexyl acrylate Chemical compound CCCCC(CC)COC(=O)C=C GOXQRTZXKQZDDN-UHFFFAOYSA-N 0.000 description 2
- JVSWJIKNEAIKJW-UHFFFAOYSA-N 2-Methylheptane Chemical compound CCCCCC(C)C JVSWJIKNEAIKJW-UHFFFAOYSA-N 0.000 description 2
- AFABGHUZZDYHJO-UHFFFAOYSA-N 2-Methylpentane Chemical compound CCCC(C)C AFABGHUZZDYHJO-UHFFFAOYSA-N 0.000 description 2
- DSKYSDCYIODJPC-UHFFFAOYSA-N 2-butyl-2-ethylpropane-1,3-diol Chemical compound CCCCC(CC)(CO)CO DSKYSDCYIODJPC-UHFFFAOYSA-N 0.000 description 2
- LAIUFBWHERIJIH-UHFFFAOYSA-N 3-Methylheptane Chemical compound CCCCC(C)CC LAIUFBWHERIJIH-UHFFFAOYSA-N 0.000 description 2
- PFEOZHBOMNWTJB-UHFFFAOYSA-N 3-methylpentane Chemical compound CCC(C)CC PFEOZHBOMNWTJB-UHFFFAOYSA-N 0.000 description 2
- YHFGMFYKZBWPRW-UHFFFAOYSA-N 3-methylpentane-1,1-diol Chemical compound CCC(C)CC(O)O YHFGMFYKZBWPRW-UHFFFAOYSA-N 0.000 description 2
- CDBAMNGURPMUTG-UHFFFAOYSA-N 4-[2-(4-hydroxycyclohexyl)propan-2-yl]cyclohexan-1-ol Chemical compound C1CC(O)CCC1C(C)(C)C1CCC(O)CC1 CDBAMNGURPMUTG-UHFFFAOYSA-N 0.000 description 2
- FJKROLUGYXJWQN-UHFFFAOYSA-N 4-hydroxybenzoic acid Chemical compound OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 2
- JHWGFJBTMHEZME-UHFFFAOYSA-N 4-prop-2-enoyloxybutyl prop-2-enoate Chemical compound C=CC(=O)OCCCCOC(=O)C=C JHWGFJBTMHEZME-UHFFFAOYSA-N 0.000 description 2
- MWSKJDNQKGCKPA-UHFFFAOYSA-N 6-methyl-3a,4,5,7a-tetrahydro-2-benzofuran-1,3-dione Chemical compound C1CC(C)=CC2C(=O)OC(=O)C12 MWSKJDNQKGCKPA-UHFFFAOYSA-N 0.000 description 2
- WDJHALXBUFZDSR-UHFFFAOYSA-N Acetoacetic acid Natural products CC(=O)CC(O)=O WDJHALXBUFZDSR-UHFFFAOYSA-N 0.000 description 2
- HRPVXLWXLXDGHG-UHFFFAOYSA-N Acrylamide Chemical compound NC(=O)C=C HRPVXLWXLXDGHG-UHFFFAOYSA-N 0.000 description 2
- 239000004215 Carbon black (E152) Substances 0.000 description 2
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 description 2
- 239000004641 Diallyl-phthalate Substances 0.000 description 2
- JIGUQPWFLRLWPJ-UHFFFAOYSA-N Ethyl acrylate Chemical compound CCOC(=O)C=C JIGUQPWFLRLWPJ-UHFFFAOYSA-N 0.000 description 2
- IAYPIBMASNFSPL-UHFFFAOYSA-N Ethylene oxide Chemical compound C1CO1 IAYPIBMASNFSPL-UHFFFAOYSA-N 0.000 description 2
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 2
- GYCMBHHDWRMZGG-UHFFFAOYSA-N Methylacrylonitrile Chemical compound CC(=C)C#N GYCMBHHDWRMZGG-UHFFFAOYSA-N 0.000 description 2
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 2
- OFBQJSOFQDEBGM-UHFFFAOYSA-N Pentane Chemical compound CCCCC OFBQJSOFQDEBGM-UHFFFAOYSA-N 0.000 description 2
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 2
- ATUOYWHBWRKTHZ-UHFFFAOYSA-N Propane Chemical compound CCC ATUOYWHBWRKTHZ-UHFFFAOYSA-N 0.000 description 2
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 2
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 description 2
- XMUZQOKACOLCSS-UHFFFAOYSA-N [2-(hydroxymethyl)phenyl]methanol Chemical compound OCC1=CC=CC=C1CO XMUZQOKACOLCSS-UHFFFAOYSA-N 0.000 description 2
- AYVGBNGTBQLJBG-UHFFFAOYSA-N [3-(hydroxymethyl)cyclopentyl]methanol Chemical compound OCC1CCC(CO)C1 AYVGBNGTBQLJBG-UHFFFAOYSA-N 0.000 description 2
- 238000007259 addition reaction Methods 0.000 description 2
- 239000000853 adhesive Substances 0.000 description 2
- 230000001070 adhesive effect Effects 0.000 description 2
- 150000001335 aliphatic alkanes Chemical class 0.000 description 2
- 125000003545 alkoxy group Chemical group 0.000 description 2
- 229910052782 aluminium Inorganic materials 0.000 description 2
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 2
- 150000008064 anhydrides Chemical class 0.000 description 2
- 125000005410 aryl sulfonium group Chemical group 0.000 description 2
- 239000012298 atmosphere Substances 0.000 description 2
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 2
- ZPOLOEWJWXZUSP-WAYWQWQTSA-N bis(prop-2-enyl) (z)-but-2-enedioate Chemical compound C=CCOC(=O)\C=C/C(=O)OCC=C ZPOLOEWJWXZUSP-WAYWQWQTSA-N 0.000 description 2
- QUDWYFHPNIMBFC-UHFFFAOYSA-N bis(prop-2-enyl) benzene-1,2-dicarboxylate Chemical compound C=CCOC(=O)C1=CC=CC=C1C(=O)OCC=C QUDWYFHPNIMBFC-UHFFFAOYSA-N 0.000 description 2
- 239000011203 carbon fibre reinforced carbon Substances 0.000 description 2
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 2
- 238000010538 cationic polymerization reaction Methods 0.000 description 2
- PMMYEEVYMWASQN-IMJSIDKUSA-N cis-4-Hydroxy-L-proline Chemical compound O[C@@H]1CN[C@H](C(O)=O)C1 PMMYEEVYMWASQN-IMJSIDKUSA-N 0.000 description 2
- 235000015165 citric acid Nutrition 0.000 description 2
- 239000002131 composite material Substances 0.000 description 2
- 238000013329 compounding Methods 0.000 description 2
- 238000005336 cracking Methods 0.000 description 2
- 238000004132 cross linking Methods 0.000 description 2
- QSAWQNUELGIYBC-UHFFFAOYSA-N cyclohexane-1,2-dicarboxylic acid Chemical compound OC(=O)C1CCCCC1C(O)=O QSAWQNUELGIYBC-UHFFFAOYSA-N 0.000 description 2
- PFURGBBHAOXLIO-UHFFFAOYSA-N cyclohexane-1,2-diol Chemical compound OC1CCCCC1O PFURGBBHAOXLIO-UHFFFAOYSA-N 0.000 description 2
- XBZSBBLNHFMTEB-UHFFFAOYSA-N cyclohexane-1,3-dicarboxylic acid Chemical compound OC(=O)C1CCCC(C(O)=O)C1 XBZSBBLNHFMTEB-UHFFFAOYSA-N 0.000 description 2
- VCVOSERVUCJNPR-UHFFFAOYSA-N cyclopentane-1,2-diol Chemical compound OC1CCCC1O VCVOSERVUCJNPR-UHFFFAOYSA-N 0.000 description 2
- NUUPJBRGQCEZSI-UHFFFAOYSA-N cyclopentane-1,3-diol Chemical compound OC1CCC(O)C1 NUUPJBRGQCEZSI-UHFFFAOYSA-N 0.000 description 2
- PYRZPBDTPRQYKG-UHFFFAOYSA-N cyclopentene-1-carboxylic acid Chemical compound OC(=O)C1=CCCC1 PYRZPBDTPRQYKG-UHFFFAOYSA-N 0.000 description 2
- WOWBFOBYOAGEEA-UHFFFAOYSA-N diafenthiuron Chemical compound CC(C)C1=C(NC(=S)NC(C)(C)C)C(C(C)C)=CC(OC=2C=CC=CC=2)=C1 WOWBFOBYOAGEEA-UHFFFAOYSA-N 0.000 description 2
- 125000005594 diketone group Chemical group 0.000 description 2
- ROORDVPLFPIABK-UHFFFAOYSA-N diphenyl carbonate Chemical compound C=1C=CC=CC=1OC(=O)OC1=CC=CC=C1 ROORDVPLFPIABK-UHFFFAOYSA-N 0.000 description 2
- TVIDDXQYHWJXFK-UHFFFAOYSA-N dodecanedioic acid Chemical compound OC(=O)CCCCCCCCCCC(O)=O TVIDDXQYHWJXFK-UHFFFAOYSA-N 0.000 description 2
- 238000010556 emulsion polymerization method Methods 0.000 description 2
- SUPCQIBBMFXVTL-UHFFFAOYSA-N ethyl 2-methylprop-2-enoate Chemical compound CCOC(=O)C(C)=C SUPCQIBBMFXVTL-UHFFFAOYSA-N 0.000 description 2
- 238000011156 evaluation Methods 0.000 description 2
- 230000006870 function Effects 0.000 description 2
- 230000009477 glass transition Effects 0.000 description 2
- 150000004820 halides Chemical class 0.000 description 2
- 238000013007 heat curing Methods 0.000 description 2
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 2
- 229940051250 hexylene glycol Drugs 0.000 description 2
- 229920001519 homopolymer Polymers 0.000 description 2
- 125000002768 hydroxyalkyl group Chemical group 0.000 description 2
- 125000004029 hydroxymethyl group Chemical group [H]OC([H])([H])* 0.000 description 2
- 239000011810 insulating material Substances 0.000 description 2
- NNPPMTNAJDCUHE-UHFFFAOYSA-N isobutane Chemical compound CC(C)C NNPPMTNAJDCUHE-UHFFFAOYSA-N 0.000 description 2
- 238000004898 kneading Methods 0.000 description 2
- 239000004310 lactic acid Substances 0.000 description 2
- 235000014655 lactic acid Nutrition 0.000 description 2
- 239000004816 latex Substances 0.000 description 2
- 229920000126 latex Polymers 0.000 description 2
- 238000010550 living polymerization reaction Methods 0.000 description 2
- FPYJFEHAWHCUMM-UHFFFAOYSA-N maleic anhydride Chemical compound O=C1OC(=O)C=C1 FPYJFEHAWHCUMM-UHFFFAOYSA-N 0.000 description 2
- 230000015654 memory Effects 0.000 description 2
- FQPSGWSUVKBHSU-UHFFFAOYSA-N methacrylamide Chemical compound CC(=C)C(N)=O FQPSGWSUVKBHSU-UHFFFAOYSA-N 0.000 description 2
- VNWKTOKETHGBQD-UHFFFAOYSA-N methane Chemical compound C VNWKTOKETHGBQD-UHFFFAOYSA-N 0.000 description 2
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 2
- KYTZHLUVELPASH-UHFFFAOYSA-N naphthalene-1,2-dicarboxylic acid Chemical compound C1=CC=CC2=C(C(O)=O)C(C(=O)O)=CC=C21 KYTZHLUVELPASH-UHFFFAOYSA-N 0.000 description 2
- OEIJHBUUFURJLI-UHFFFAOYSA-N octane-1,8-diol Chemical compound OCCCCCCCCO OEIJHBUUFURJLI-UHFFFAOYSA-N 0.000 description 2
- WWZKQHOCKIZLMA-UHFFFAOYSA-N octanoic acid Chemical compound CCCCCCCC(O)=O WWZKQHOCKIZLMA-UHFFFAOYSA-N 0.000 description 2
- 125000006353 oxyethylene group Chemical group 0.000 description 2
- 239000003973 paint Substances 0.000 description 2
- PNJWIWWMYCMZRO-UHFFFAOYSA-N pent‐4‐en‐2‐one Natural products CC(=O)CC=C PNJWIWWMYCMZRO-UHFFFAOYSA-N 0.000 description 2
- 150000002989 phenols Chemical class 0.000 description 2
- 230000000704 physical effect Effects 0.000 description 2
- 229920003023 plastic Polymers 0.000 description 2
- 239000004033 plastic Substances 0.000 description 2
- 229920001451 polypropylene glycol Polymers 0.000 description 2
- 230000008569 process Effects 0.000 description 2
- FBCQUCJYYPMKRO-UHFFFAOYSA-N prop-2-enyl 2-methylprop-2-enoate Chemical compound CC(=C)C(=O)OCC=C FBCQUCJYYPMKRO-UHFFFAOYSA-N 0.000 description 2
- 125000006239 protecting group Chemical group 0.000 description 2
- 238000010992 reflux Methods 0.000 description 2
- 239000000565 sealant Substances 0.000 description 2
- 229910052710 silicon Inorganic materials 0.000 description 2
- 125000003808 silyl group Chemical group [H][Si]([H])([H])[*] 0.000 description 2
- 229910052708 sodium Inorganic materials 0.000 description 2
- 239000011734 sodium Substances 0.000 description 2
- 239000000243 solution Substances 0.000 description 2
- 229920003048 styrene butadiene rubber Polymers 0.000 description 2
- 229920001897 terpolymer Polymers 0.000 description 2
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 2
- 239000010936 titanium Substances 0.000 description 2
- 229910052719 titanium Inorganic materials 0.000 description 2
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical class CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 2
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 description 2
- WKOLLVMJNQIZCI-UHFFFAOYSA-N vanillic acid Chemical compound COC1=CC(C(O)=O)=CC=C1O WKOLLVMJNQIZCI-UHFFFAOYSA-N 0.000 description 2
- TUUBOHWZSQXCSW-UHFFFAOYSA-N vanillic acid Natural products COC1=CC(O)=CC(C(O)=O)=C1 TUUBOHWZSQXCSW-UHFFFAOYSA-N 0.000 description 2
- KSEBMYQBYZTDHS-HWKANZROSA-M (E)-Ferulic acid Natural products COC1=CC(\C=C\C([O-])=O)=CC=C1O KSEBMYQBYZTDHS-HWKANZROSA-M 0.000 description 1
- BJEPYKJPYRNKOW-REOHCLBHSA-N (S)-malic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O BJEPYKJPYRNKOW-REOHCLBHSA-N 0.000 description 1
- RBACIKXCRWGCBB-UHFFFAOYSA-N 1,2-Epoxybutane Chemical compound CCC1CO1 RBACIKXCRWGCBB-UHFFFAOYSA-N 0.000 description 1
- 125000005654 1,2-cyclohexylene group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([*:2])C([H])([*:1])C1([H])[H] 0.000 description 1
- 125000005837 1,2-cyclopentylene group Chemical group [H]C1([H])C([H])([H])C([H])([*:1])C([H])([*:2])C1([H])[H] 0.000 description 1
- 125000005838 1,3-cyclopentylene group Chemical group [H]C1([H])C([H])([H])C([H])([*:2])C([H])([H])C1([H])[*:1] 0.000 description 1
- 125000004955 1,4-cyclohexylene group Chemical group [H]C1([H])C([H])([H])C([H])([*:1])C([H])([H])C([H])([H])C1([H])[*:2] 0.000 description 1
- ALVZNPYWJMLXKV-UHFFFAOYSA-N 1,9-Nonanediol Chemical compound OCCCCCCCCCO ALVZNPYWJMLXKV-UHFFFAOYSA-N 0.000 description 1
- RTBFRGCFXZNCOE-UHFFFAOYSA-N 1-methylsulfonylpiperidin-4-one Chemical compound CS(=O)(=O)N1CCC(=O)CC1 RTBFRGCFXZNCOE-UHFFFAOYSA-N 0.000 description 1
- KWKAKUADMBZCLK-UHFFFAOYSA-N 1-octene Chemical group CCCCCCC=C KWKAKUADMBZCLK-UHFFFAOYSA-N 0.000 description 1
- 125000004206 2,2,2-trifluoroethyl group Chemical group [H]C([H])(*)C(F)(F)F 0.000 description 1
- PTBDIHRZYDMNKB-UHFFFAOYSA-N 2,2-Bis(hydroxymethyl)propionic acid Chemical compound OCC(C)(CO)C(O)=O PTBDIHRZYDMNKB-UHFFFAOYSA-N 0.000 description 1
- JVYDLYGCSIHCMR-UHFFFAOYSA-N 2,2-bis(hydroxymethyl)butanoic acid Chemical compound CCC(CO)(CO)C(O)=O JVYDLYGCSIHCMR-UHFFFAOYSA-N 0.000 description 1
- 125000004778 2,2-difluoroethyl group Chemical group [H]C([H])(*)C([H])(F)F 0.000 description 1
- PQXKWPLDPFFDJP-UHFFFAOYSA-N 2,3-dimethyloxirane Chemical compound CC1OC1C PQXKWPLDPFFDJP-UHFFFAOYSA-N 0.000 description 1
- BJELTSYBAHKXRW-UHFFFAOYSA-N 2,4,6-triallyloxy-1,3,5-triazine Chemical compound C=CCOC1=NC(OCC=C)=NC(OCC=C)=N1 BJELTSYBAHKXRW-UHFFFAOYSA-N 0.000 description 1
- AHDSRXYHVZECER-UHFFFAOYSA-N 2,4,6-tris[(dimethylamino)methyl]phenol Chemical compound CN(C)CC1=CC(CN(C)C)=C(O)C(CN(C)C)=C1 AHDSRXYHVZECER-UHFFFAOYSA-N 0.000 description 1
- VCYCUECVHJJFIQ-UHFFFAOYSA-N 2-[3-(benzotriazol-2-yl)-4-hydroxyphenyl]ethyl 2-methylprop-2-enoate Chemical compound CC(=C)C(=O)OCCC1=CC=C(O)C(N2N=C3C=CC=CC3=N2)=C1 VCYCUECVHJJFIQ-UHFFFAOYSA-N 0.000 description 1
- DNUYOWCKBJFOGS-UHFFFAOYSA-N 2-[[10-(2,2-dicarboxyethyl)anthracen-9-yl]methyl]propanedioic acid Chemical compound C1=CC=C2C(CC(C(=O)O)C(O)=O)=C(C=CC=C3)C3=C(CC(C(O)=O)C(O)=O)C2=C1 DNUYOWCKBJFOGS-UHFFFAOYSA-N 0.000 description 1
- WDQMWEYDKDCEHT-UHFFFAOYSA-N 2-ethylhexyl 2-methylprop-2-enoate Chemical compound CCCCC(CC)COC(=O)C(C)=C WDQMWEYDKDCEHT-UHFFFAOYSA-N 0.000 description 1
- VHBSECWYEFJRNV-UHFFFAOYSA-N 2-hydroxybenzoic acid Chemical compound OC(=O)C1=CC=CC=C1O.OC(=O)C1=CC=CC=C1O VHBSECWYEFJRNV-UHFFFAOYSA-N 0.000 description 1
- 125000000954 2-hydroxyethyl group Chemical group [H]C([*])([H])C([H])([H])O[H] 0.000 description 1
- OMIGHNLMNHATMP-UHFFFAOYSA-N 2-hydroxyethyl prop-2-enoate Chemical compound OCCOC(=O)C=C OMIGHNLMNHATMP-UHFFFAOYSA-N 0.000 description 1
- VHSHLMUCYSAUQU-UHFFFAOYSA-N 2-hydroxypropyl methacrylate Chemical compound CC(O)COC(=O)C(C)=C VHSHLMUCYSAUQU-UHFFFAOYSA-N 0.000 description 1
- GWZMWHWAWHPNHN-UHFFFAOYSA-N 2-hydroxypropyl prop-2-enoate Chemical compound CC(O)COC(=O)C=C GWZMWHWAWHPNHN-UHFFFAOYSA-N 0.000 description 1
- FZIIBDOXPQOKBP-UHFFFAOYSA-N 2-methyloxetane Chemical compound CC1CCO1 FZIIBDOXPQOKBP-UHFFFAOYSA-N 0.000 description 1
- 125000000094 2-phenylethyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])C([H])([H])* 0.000 description 1
- UIDDPPKZYZTEGS-UHFFFAOYSA-N 3-(2-ethyl-4-methylimidazol-1-yl)propanenitrile Chemical compound CCC1=NC(C)=CN1CCC#N UIDDPPKZYZTEGS-UHFFFAOYSA-N 0.000 description 1
- WVRNUXJQQFPNMN-VAWYXSNFSA-N 3-[(e)-dodec-1-enyl]oxolane-2,5-dione Chemical compound CCCCCCCCCC\C=C\C1CC(=O)OC1=O WVRNUXJQQFPNMN-VAWYXSNFSA-N 0.000 description 1
- DSADESJTZDXCPN-UHFFFAOYSA-N 3-hydroxy-4-phenylbenzoic acid Chemical compound OC1=CC(C(=O)O)=CC=C1C1=CC=CC=C1 DSADESJTZDXCPN-UHFFFAOYSA-N 0.000 description 1
- XDLMVUHYZWKMMD-UHFFFAOYSA-N 3-trimethoxysilylpropyl 2-methylprop-2-enoate Chemical compound CO[Si](OC)(OC)CCCOC(=O)C(C)=C XDLMVUHYZWKMMD-UHFFFAOYSA-N 0.000 description 1
- VPWNQTHUCYMVMZ-UHFFFAOYSA-N 4,4'-sulfonyldiphenol Chemical compound C1=CC(O)=CC=C1S(=O)(=O)C1=CC=C(O)C=C1 VPWNQTHUCYMVMZ-UHFFFAOYSA-N 0.000 description 1
- VNGLVZLEUDIDQH-UHFFFAOYSA-N 4-[2-(4-hydroxyphenyl)propan-2-yl]phenol;2-methyloxirane Chemical compound CC1CO1.C=1C=C(O)C=CC=1C(C)(C)C1=CC=C(O)C=C1 VNGLVZLEUDIDQH-UHFFFAOYSA-N 0.000 description 1
- WPSWDCBWMRJJED-UHFFFAOYSA-N 4-[2-(4-hydroxyphenyl)propan-2-yl]phenol;oxirane Chemical compound C1CO1.C=1C=C(O)C=CC=1C(C)(C)C1=CC=C(O)C=C1 WPSWDCBWMRJJED-UHFFFAOYSA-N 0.000 description 1
- IPXDGHZTUBSPSG-UHFFFAOYSA-N 4-hydroxy-2-phenylbenzoic acid Chemical compound OC(=O)C1=CC=C(O)C=C1C1=CC=CC=C1 IPXDGHZTUBSPSG-UHFFFAOYSA-N 0.000 description 1
- LPADJMFUBXMZNL-UHFFFAOYSA-N 4-hydroxy-3-phenylbenzoic acid Chemical compound OC(=O)C1=CC=C(O)C(C=2C=CC=CC=2)=C1 LPADJMFUBXMZNL-UHFFFAOYSA-N 0.000 description 1
- SXIFAEWFOJETOA-UHFFFAOYSA-N 4-hydroxy-butyl Chemical group [CH2]CCCO SXIFAEWFOJETOA-UHFFFAOYSA-N 0.000 description 1
- 229940090248 4-hydroxybenzoic acid Drugs 0.000 description 1
- NDWUBGAGUCISDV-UHFFFAOYSA-N 4-hydroxybutyl prop-2-enoate Chemical compound OCCCCOC(=O)C=C NDWUBGAGUCISDV-UHFFFAOYSA-N 0.000 description 1
- 125000004203 4-hydroxyphenyl group Chemical group [H]OC1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 1
- QXBYUPMEYVDXIQ-UHFFFAOYSA-N 4-methyl-3a,4,5,6,7,7a-hexahydro-2-benzofuran-1,3-dione Chemical compound CC1CCCC2C(=O)OC(=O)C12 QXBYUPMEYVDXIQ-UHFFFAOYSA-N 0.000 description 1
- OECTYKWYRCHAKR-UHFFFAOYSA-N 4-vinylcyclohexene dioxide Chemical compound C1OC1C1CC2OC2CC1 OECTYKWYRCHAKR-UHFFFAOYSA-N 0.000 description 1
- XBWHBPMCIGBGTA-UHFFFAOYSA-N 5-methyl-2-oxaspiro[3.5]non-5-ene-1,3-dione Chemical compound CC1=CCCCC11C(=O)OC1=O XBWHBPMCIGBGTA-UHFFFAOYSA-N 0.000 description 1
- ULKLGIFJWFIQFF-UHFFFAOYSA-N 5K8XI641G3 Chemical compound CCC1=NC=C(C)N1 ULKLGIFJWFIQFF-UHFFFAOYSA-N 0.000 description 1
- KAUQJMHLAFIZDU-UHFFFAOYSA-N 6-Hydroxy-2-naphthoic acid Chemical compound C1=C(O)C=CC2=CC(C(=O)O)=CC=C21 KAUQJMHLAFIZDU-UHFFFAOYSA-N 0.000 description 1
- RBHIUNHSNSQJNG-UHFFFAOYSA-N 6-methyl-3-(2-methyloxiran-2-yl)-7-oxabicyclo[4.1.0]heptane Chemical compound C1CC2(C)OC2CC1C1(C)CO1 RBHIUNHSNSQJNG-UHFFFAOYSA-N 0.000 description 1
- 229930185605 Bisphenol Natural products 0.000 description 1
- BTBUEUYNUDRHOZ-UHFFFAOYSA-N Borate Chemical compound [O-]B([O-])[O-] BTBUEUYNUDRHOZ-UHFFFAOYSA-N 0.000 description 1
- XZHWAGZSWOAEPI-UHFFFAOYSA-N C(C=CC1=CC(O)=C(O)C=C1)(=O)O.OC=1C=C(C=CC(=O)O)C=CC1O Chemical compound C(C=CC1=CC(O)=C(O)C=C1)(=O)O.OC=1C=C(C=CC(=O)O)C=CC1O XZHWAGZSWOAEPI-UHFFFAOYSA-N 0.000 description 1
- SGWYUOYBPZDXMV-UHFFFAOYSA-N CC1=C(C=C(C(=O)O)C=C1)O.CC=1C=C(C(=O)O)C=CC1O Chemical compound CC1=C(C=C(C(=O)O)C=C1)O.CC=1C=C(C(=O)O)C=CC1O SGWYUOYBPZDXMV-UHFFFAOYSA-N 0.000 description 1
- JCHFMJJRHVOGAA-UHFFFAOYSA-N COC1=CC(C(O)=O)=CC(OC)=C1O.COC1=CC(C(O)=O)=CC(OC)=C1O Chemical compound COC1=CC(C(O)=O)=CC(OC)=C1O.COC1=CC(C(O)=O)=CC(OC)=C1O JCHFMJJRHVOGAA-UHFFFAOYSA-N 0.000 description 1
- GAWIXWVDTYZWAW-UHFFFAOYSA-N C[CH]O Chemical group C[CH]O GAWIXWVDTYZWAW-UHFFFAOYSA-N 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- OIFBSDVPJOWBCH-UHFFFAOYSA-N Diethyl carbonate Chemical compound CCOC(=O)OCC OIFBSDVPJOWBCH-UHFFFAOYSA-N 0.000 description 1
- BRLQWZUYTZBJKN-UHFFFAOYSA-N Epichlorohydrin Chemical compound ClCC1CO1 BRLQWZUYTZBJKN-UHFFFAOYSA-N 0.000 description 1
- OTMSDBZUPAUEDD-UHFFFAOYSA-N Ethane Chemical compound CC OTMSDBZUPAUEDD-UHFFFAOYSA-N 0.000 description 1
- BDAGIHXWWSANSR-UHFFFAOYSA-M Formate Chemical compound [O-]C=O BDAGIHXWWSANSR-UHFFFAOYSA-M 0.000 description 1
- WOBHKFSMXKNTIM-UHFFFAOYSA-N Hydroxyethyl methacrylate Chemical compound CC(=C)C(=O)OCCO WOBHKFSMXKNTIM-UHFFFAOYSA-N 0.000 description 1
- 241000512299 Nerita Species 0.000 description 1
- NGLTUCWUYFASQM-UHFFFAOYSA-N O1C(C1)C1CC=CCC1.OCC(CO)(CC)CO Chemical compound O1C(C1)C1CC=CCC1.OCC(CO)(CC)CO NGLTUCWUYFASQM-UHFFFAOYSA-N 0.000 description 1
- CWKWGPZWOJWPTK-UHFFFAOYSA-N OCC1CCCC(CO)C1.OCC1CCCC(CO)C1 Chemical compound OCC1CCCC(CO)C1.OCC1CCCC(CO)C1 CWKWGPZWOJWPTK-UHFFFAOYSA-N 0.000 description 1
- PMKKXYIGCYGBDK-UHFFFAOYSA-N OCC1CCCCC1CO.OCC1CCCCC1CO Chemical compound OCC1CCCCC1CO.OCC1CCCCC1CO PMKKXYIGCYGBDK-UHFFFAOYSA-N 0.000 description 1
- 239000008118 PEG 6000 Substances 0.000 description 1
- YGYAWVDWMABLBF-UHFFFAOYSA-N Phosgene Chemical compound ClC(Cl)=O YGYAWVDWMABLBF-UHFFFAOYSA-N 0.000 description 1
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 1
- LGRFSURHDFAFJT-UHFFFAOYSA-N Phthalic anhydride Natural products C1=CC=C2C(=O)OC(=O)C2=C1 LGRFSURHDFAFJT-UHFFFAOYSA-N 0.000 description 1
- 229920002004 Pluronic® R Polymers 0.000 description 1
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 1
- 229920000604 Polyethylene Glycol 200 Polymers 0.000 description 1
- 229920002538 Polyethylene Glycol 20000 Polymers 0.000 description 1
- 229920002582 Polyethylene Glycol 600 Polymers 0.000 description 1
- 229920002584 Polyethylene Glycol 6000 Polymers 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 229920000297 Rayon Polymers 0.000 description 1
- 229910018557 Si O Inorganic materials 0.000 description 1
- BLRPTPMANUNPDV-UHFFFAOYSA-N Silane Chemical group [SiH4] BLRPTPMANUNPDV-UHFFFAOYSA-N 0.000 description 1
- 239000006087 Silane Coupling Agent Substances 0.000 description 1
- 239000002174 Styrene-butadiene Substances 0.000 description 1
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 1
- ATJFFYVFTNAWJD-UHFFFAOYSA-N Tin Chemical compound [Sn] ATJFFYVFTNAWJD-UHFFFAOYSA-N 0.000 description 1
- QYKIQEUNHZKYBP-UHFFFAOYSA-N Vinyl ether Chemical class C=COC=C QYKIQEUNHZKYBP-UHFFFAOYSA-N 0.000 description 1
- XDODWINGEHBYRT-UHFFFAOYSA-N [2-(hydroxymethyl)cyclohexyl]methanol Chemical compound OCC1CCCCC1CO XDODWINGEHBYRT-UHFFFAOYSA-N 0.000 description 1
- NXKFMUFJMLNJOB-UHFFFAOYSA-N [2-(hydroxymethyl)cyclopentyl]methanol Chemical compound OCC1CCCC1CO NXKFMUFJMLNJOB-UHFFFAOYSA-N 0.000 description 1
- YFESLUXJCTZZFA-UHFFFAOYSA-N [4-(hydroxymethyl)cyclohexyl]methanol Chemical compound OCC1CCC(CO)CC1.OCC1CCC(CO)CC1 YFESLUXJCTZZFA-UHFFFAOYSA-N 0.000 description 1
- 150000003926 acrylamides Chemical class 0.000 description 1
- 150000001252 acrylic acid derivatives Chemical class 0.000 description 1
- 125000005396 acrylic acid ester group Chemical group 0.000 description 1
- 125000002252 acyl group Chemical group 0.000 description 1
- 238000012644 addition polymerization Methods 0.000 description 1
- 239000003463 adsorbent Substances 0.000 description 1
- 230000001476 alcoholic effect Effects 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 229920003232 aliphatic polyester Polymers 0.000 description 1
- 150000001336 alkenes Chemical class 0.000 description 1
- 125000004183 alkoxy alkyl group Chemical group 0.000 description 1
- 125000004453 alkoxycarbonyl group Chemical group 0.000 description 1
- BJEPYKJPYRNKOW-UHFFFAOYSA-N alpha-hydroxysuccinic acid Natural products OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 1
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 1
- 150000001408 amides Chemical class 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- JFCQEDHGNNZCLN-UHFFFAOYSA-N anhydrous glutaric acid Natural products OC(=O)CCCC(O)=O JFCQEDHGNNZCLN-UHFFFAOYSA-N 0.000 description 1
- 238000010539 anionic addition polymerization reaction Methods 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 230000003078 antioxidant effect Effects 0.000 description 1
- 238000005452 bending Methods 0.000 description 1
- QRUDEWIWKLJBPS-UHFFFAOYSA-N benzotriazole Chemical compound C1=CC=C2N[N][N]C2=C1 QRUDEWIWKLJBPS-UHFFFAOYSA-N 0.000 description 1
- 239000012964 benzotriazole Substances 0.000 description 1
- DMRQNVSXQIVTKL-UHFFFAOYSA-N buta-1,3-diene-1,1-diol Chemical compound OC(O)=CC=C DMRQNVSXQIVTKL-UHFFFAOYSA-N 0.000 description 1
- YHWCPXVTRSHPNY-UHFFFAOYSA-N butan-1-olate;titanium(4+) Chemical compound [Ti+4].CCCC[O-].CCCC[O-].CCCC[O-].CCCC[O-] YHWCPXVTRSHPNY-UHFFFAOYSA-N 0.000 description 1
- 239000001273 butane Substances 0.000 description 1
- JHIWVOJDXOSYLW-UHFFFAOYSA-N butyl 2,2-difluorocyclopropane-1-carboxylate Chemical compound CCCCOC(=O)C1CC1(F)F JHIWVOJDXOSYLW-UHFFFAOYSA-N 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- CREMABGTGYGIQB-UHFFFAOYSA-N carbon carbon Chemical compound C.C CREMABGTGYGIQB-UHFFFAOYSA-N 0.000 description 1
- 238000005266 casting Methods 0.000 description 1
- 125000002091 cationic group Chemical group 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- HNEGQIOMVPPMNR-IHWYPQMZSA-N citraconic acid Chemical compound OC(=O)C(/C)=C\C(O)=O HNEGQIOMVPPMNR-IHWYPQMZSA-N 0.000 description 1
- 229940018557 citraconic acid Drugs 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 238000004040 coloring Methods 0.000 description 1
- 239000013065 commercial product Substances 0.000 description 1
- 238000000748 compression moulding Methods 0.000 description 1
- 238000009833 condensation Methods 0.000 description 1
- 230000005494 condensation Effects 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 238000007334 copolymerization reaction Methods 0.000 description 1
- 230000001186 cumulative effect Effects 0.000 description 1
- 150000004292 cyclic ethers Chemical class 0.000 description 1
- 125000002993 cycloalkylene group Chemical group 0.000 description 1
- ZWVAVPQCOZURMT-UHFFFAOYSA-N cyclohexane-1,2-diol cyclohexane-1,3-diol Chemical compound C1(O)CC(O)CCC1.C1(O)C(O)CCCC1 ZWVAVPQCOZURMT-UHFFFAOYSA-N 0.000 description 1
- RLMGYIOTPQVQJR-UHFFFAOYSA-N cyclohexane-1,3-diol Chemical compound OC1CCCC(O)C1 RLMGYIOTPQVQJR-UHFFFAOYSA-N 0.000 description 1
- NZNMSOFKMUBTKW-UHFFFAOYSA-M cyclohexanecarboxylate Chemical compound [O-]C(=O)C1CCCCC1 NZNMSOFKMUBTKW-UHFFFAOYSA-M 0.000 description 1
- OIWOHHBRDFKZNC-UHFFFAOYSA-N cyclohexyl 2-methylprop-2-enoate Chemical compound CC(=C)C(=O)OC1CCCCC1 OIWOHHBRDFKZNC-UHFFFAOYSA-N 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- KBLWLMPSVYBVDK-UHFFFAOYSA-N cyclohexyl prop-2-enoate Chemical compound C=CC(=O)OC1CCCCC1 KBLWLMPSVYBVDK-UHFFFAOYSA-N 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 229920000359 diblock copolymer Polymers 0.000 description 1
- 150000001990 dicarboxylic acid derivatives Chemical class 0.000 description 1
- 150000001991 dicarboxylic acids Chemical class 0.000 description 1
- 125000001028 difluoromethyl group Chemical group [H]C(F)(F)* 0.000 description 1
- IEJIGPNLZYLLBP-UHFFFAOYSA-N dimethyl carbonate Chemical compound COC(=O)OC IEJIGPNLZYLLBP-UHFFFAOYSA-N 0.000 description 1
- XXBDWLFCJWSEKW-UHFFFAOYSA-N dimethylbenzylamine Chemical compound CN(C)CC1=CC=CC=C1 XXBDWLFCJWSEKW-UHFFFAOYSA-N 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- GMSCBRSQMRDRCD-UHFFFAOYSA-N dodecyl 2-methylprop-2-enoate Chemical compound CCCCCCCCCCCCOC(=O)C(C)=C GMSCBRSQMRDRCD-UHFFFAOYSA-N 0.000 description 1
- 238000002296 dynamic light scattering Methods 0.000 description 1
- 238000004945 emulsification Methods 0.000 description 1
- 125000001301 ethoxy group Chemical group [H]C([H])([H])C([H])([H])O* 0.000 description 1
- 230000001747 exhibiting effect Effects 0.000 description 1
- KSEBMYQBYZTDHS-HWKANZROSA-N ferulic acid Chemical compound COC1=CC(\C=C\C(O)=O)=CC=C1O KSEBMYQBYZTDHS-HWKANZROSA-N 0.000 description 1
- 235000001785 ferulic acid Nutrition 0.000 description 1
- 229940114124 ferulic acid Drugs 0.000 description 1
- KSEBMYQBYZTDHS-UHFFFAOYSA-N ferulic acid Natural products COC1=CC(C=CC(O)=O)=CC=C1O KSEBMYQBYZTDHS-UHFFFAOYSA-N 0.000 description 1
- 239000003063 flame retardant Substances 0.000 description 1
- 150000004675 formic acid derivatives Chemical class 0.000 description 1
- 150000002240 furans Chemical class 0.000 description 1
- 125000003055 glycidyl group Chemical group C(C1CO1)* 0.000 description 1
- VOZRXNHHFUQHIL-UHFFFAOYSA-N glycidyl methacrylate Chemical compound CC(=C)C(=O)OCC1CO1 VOZRXNHHFUQHIL-UHFFFAOYSA-N 0.000 description 1
- 238000010559 graft polymerization reaction Methods 0.000 description 1
- 125000005843 halogen group Chemical group 0.000 description 1
- 125000006341 heptafluoro n-propyl group Chemical group FC(F)(F)C(F)(F)C(F)(F)* 0.000 description 1
- 125000004836 hexamethylene group Chemical group [H]C([H])([*:2])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[*:1] 0.000 description 1
- FDVKPDVESAUTEE-UHFFFAOYSA-N hexane-1,6-diol;2-methylpentane-2,4-diol Chemical compound CC(O)CC(C)(C)O.OCCCCCCO FDVKPDVESAUTEE-UHFFFAOYSA-N 0.000 description 1
- 238000005984 hydrogenation reaction Methods 0.000 description 1
- 150000002460 imidazoles Chemical class 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- 239000011256 inorganic filler Substances 0.000 description 1
- 229910003475 inorganic filler Inorganic materials 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 239000001282 iso-butane Substances 0.000 description 1
- 239000012948 isocyanate Substances 0.000 description 1
- 150000002513 isocyanates Chemical class 0.000 description 1
- CNQCVBJFEGMYDW-UHFFFAOYSA-N lawrencium atom Chemical group [Lr] CNQCVBJFEGMYDW-UHFFFAOYSA-N 0.000 description 1
- 239000001630 malic acid Substances 0.000 description 1
- 235000011090 malic acid Nutrition 0.000 description 1
- IJFXRHURBJZNAO-UHFFFAOYSA-N meta--hydroxybenzoic acid Natural products OC(=O)C1=CC=CC(O)=C1 IJFXRHURBJZNAO-UHFFFAOYSA-N 0.000 description 1
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 1
- 125000006178 methyl benzyl group Chemical group 0.000 description 1
- 125000002950 monocyclic group Chemical group 0.000 description 1
- IJDNQMDRQITEOD-UHFFFAOYSA-N n-butane Chemical compound CCCC IJDNQMDRQITEOD-UHFFFAOYSA-N 0.000 description 1
- YPHQUSNPXDGUHL-UHFFFAOYSA-N n-methylprop-2-enamide Chemical compound CNC(=O)C=C YPHQUSNPXDGUHL-UHFFFAOYSA-N 0.000 description 1
- 125000004923 naphthylmethyl group Chemical group C1(=CC=CC2=CC=CC=C12)C* 0.000 description 1
- 239000012299 nitrogen atmosphere Substances 0.000 description 1
- 125000006344 nonafluoro n-butyl group Chemical group FC(F)(F)C(F)(F)C(F)(F)C(F)(F)* 0.000 description 1
- ZCYXXKJEDCHMGH-UHFFFAOYSA-N nonane Chemical compound CCCC[CH]CCCC ZCYXXKJEDCHMGH-UHFFFAOYSA-N 0.000 description 1
- BKIMMITUMNQMOS-UHFFFAOYSA-N normal nonane Natural products CCCCCCCCC BKIMMITUMNQMOS-UHFFFAOYSA-N 0.000 description 1
- HMZGPNHSPWNGEP-UHFFFAOYSA-N octadecyl 2-methylprop-2-enoate Chemical compound CCCCCCCCCCCCCCCCCCOC(=O)C(C)=C HMZGPNHSPWNGEP-UHFFFAOYSA-N 0.000 description 1
- TVMXDCGIABBOFY-UHFFFAOYSA-N octane Chemical compound CCCCCCCC TVMXDCGIABBOFY-UHFFFAOYSA-N 0.000 description 1
- 125000002347 octyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 235000006408 oxalic acid Nutrition 0.000 description 1
- 125000001820 oxy group Chemical group [*:1]O[*:2] 0.000 description 1
- 125000005702 oxyalkylene group Chemical group 0.000 description 1
- 125000006340 pentafluoro ethyl group Chemical group FC(F)(F)C(F)(F)* 0.000 description 1
- 125000004817 pentamethylene group Chemical group [H]C([H])([*:2])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[*:1] 0.000 description 1
- ULDDEWDFUNBUCM-UHFFFAOYSA-N pentyl prop-2-enoate Chemical compound CCCCCOC(=O)C=C ULDDEWDFUNBUCM-UHFFFAOYSA-N 0.000 description 1
- 125000005804 perfluoroheptyl group Chemical group FC(F)(F)C(F)(F)C(F)(F)C(F)(F)C(F)(F)C(F)(F)C(F)(F)* 0.000 description 1
- 125000005005 perfluorohexyl group Chemical group FC(F)(F)C(F)(F)C(F)(F)C(F)(F)C(F)(F)C(F)(F)* 0.000 description 1
- 125000005007 perfluorooctyl group Chemical group FC(C(C(C(C(C(C(C(F)(F)F)(F)F)(F)F)(F)F)(F)F)(F)F)(F)F)(F)* 0.000 description 1
- 125000005008 perfluoropentyl group Chemical group FC(C(C(C(C(F)(F)F)(F)F)(F)F)(F)F)(F)* 0.000 description 1
- 125000004344 phenylpropyl group Chemical group 0.000 description 1
- 150000003003 phosphines Chemical class 0.000 description 1
- 150000003014 phosphoric acid esters Chemical class 0.000 description 1
- 239000000049 pigment Substances 0.000 description 1
- 229920001983 poloxamer Polymers 0.000 description 1
- 229920001521 polyalkylene glycol ether Polymers 0.000 description 1
- 229920001748 polybutylene Polymers 0.000 description 1
- 239000003505 polymerization initiator Substances 0.000 description 1
- 150000007519 polyprotic acids Polymers 0.000 description 1
- 229920000734 polysilsesquioxane polymer Polymers 0.000 description 1
- 229920002635 polyurethane Polymers 0.000 description 1
- 239000004814 polyurethane Substances 0.000 description 1
- XRVCFZPJAHWYTB-UHFFFAOYSA-N prenderol Chemical compound CCC(CC)(CO)CO XRVCFZPJAHWYTB-UHFFFAOYSA-N 0.000 description 1
- 229950006800 prenderol Drugs 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- QTECDUFMBMSHKR-UHFFFAOYSA-N prop-2-enyl prop-2-enoate Chemical compound C=CCOC(=O)C=C QTECDUFMBMSHKR-UHFFFAOYSA-N 0.000 description 1
- 239000001294 propane Substances 0.000 description 1
- 125000002572 propoxy group Chemical group [*]OC([H])([H])C(C([H])([H])[H])([H])[H] 0.000 description 1
- NHARPDSAXCBDDR-UHFFFAOYSA-N propyl 2-methylprop-2-enoate Chemical compound CCCOC(=O)C(C)=C NHARPDSAXCBDDR-UHFFFAOYSA-N 0.000 description 1
- PNXMTCDJUBJHQJ-UHFFFAOYSA-N propyl prop-2-enoate Chemical compound CCCOC(=O)C=C PNXMTCDJUBJHQJ-UHFFFAOYSA-N 0.000 description 1
- YQUVCSBJEUQKSH-UHFFFAOYSA-N protochatechuic acid Natural products OC(=O)C1=CC=C(O)C(O)=C1 YQUVCSBJEUQKSH-UHFFFAOYSA-N 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 238000010526 radical polymerization reaction Methods 0.000 description 1
- 229920005604 random copolymer Polymers 0.000 description 1
- 230000009257 reactivity Effects 0.000 description 1
- 238000007142 ring opening reaction Methods 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- 238000004904 shortening Methods 0.000 description 1
- SCPYDCQAZCOKTP-UHFFFAOYSA-N silanol Chemical compound [SiH3]O SCPYDCQAZCOKTP-UHFFFAOYSA-N 0.000 description 1
- 239000000377 silicon dioxide Substances 0.000 description 1
- LIVNPJMFVYWSIS-UHFFFAOYSA-N silicon monoxide Inorganic materials [Si-]#[O+] LIVNPJMFVYWSIS-UHFFFAOYSA-N 0.000 description 1
- 229920002050 silicone resin Polymers 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 239000011973 solid acid Substances 0.000 description 1
- 150000005846 sugar alcohols Polymers 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 239000011975 tartaric acid Substances 0.000 description 1
- 235000002906 tartaric acid Nutrition 0.000 description 1
- 238000011191 terminal modification Methods 0.000 description 1
- 229920006027 ternary co-polymer Polymers 0.000 description 1
- ISXSCDLOGDJUNJ-UHFFFAOYSA-N tert-butyl prop-2-enoate Chemical compound CC(C)(C)OC(=O)C=C ISXSCDLOGDJUNJ-UHFFFAOYSA-N 0.000 description 1
- 150000003512 tertiary amines Chemical class 0.000 description 1
- TZLPVFCPHOVVII-UHFFFAOYSA-N tetrakis(4-methylphenyl)phosphanium tetraphenylphosphanium Chemical class C1(=CC=C(C=C1)[P+](C1=CC=C(C=C1)C)(C1=CC=C(C=C1)C)C1=CC=C(C=C1)C)C.C1(=CC=CC=C1)[P+](C1=CC=CC=C1)(C1=CC=CC=C1)C1=CC=CC=C1 TZLPVFCPHOVVII-UHFFFAOYSA-N 0.000 description 1
- 125000000383 tetramethylene group Chemical group [H]C([H])([*:1])C([H])([H])C([H])([H])C([H])([H])[*:2] 0.000 description 1
- QURCVMIEKCOAJU-UHFFFAOYSA-N trans-isoferulic acid Natural products COC1=CC=C(C=CC(O)=O)C=C1O QURCVMIEKCOAJU-UHFFFAOYSA-N 0.000 description 1
- 238000005809 transesterification reaction Methods 0.000 description 1
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 description 1
- SRPWOOOHEPICQU-UHFFFAOYSA-N trimellitic anhydride Chemical compound OC(=O)C1=CC=C2C(=O)OC(=O)C2=C1 SRPWOOOHEPICQU-UHFFFAOYSA-N 0.000 description 1
- BPSIOYPQMFLKFR-UHFFFAOYSA-N trimethoxy-[3-(oxiran-2-ylmethoxy)propyl]silane Chemical compound CO[Si](OC)(OC)CCCOCC1CO1 BPSIOYPQMFLKFR-UHFFFAOYSA-N 0.000 description 1
- 125000003258 trimethylene group Chemical group [H]C([H])([*:2])C([H])([H])C([H])([H])[*:1] 0.000 description 1
- NLSXASIDNWDYMI-UHFFFAOYSA-N triphenylsilanol Chemical compound C=1C=CC=CC=1[Si](C=1C=CC=CC=1)(O)C1=CC=CC=C1 NLSXASIDNWDYMI-UHFFFAOYSA-N 0.000 description 1
- 239000006097 ultraviolet radiation absorber Substances 0.000 description 1
- 229920001567 vinyl ester resin Polymers 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
- JBCJMTUHAXHILC-UHFFFAOYSA-N zinc;octanoic acid Chemical compound [Zn+2].CCCCCCCC(O)=O JBCJMTUHAXHILC-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L63/00—Compositions of epoxy resins; Compositions of derivatives of epoxy resins
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G59/00—Polycondensates containing more than one epoxy group per molecule; Macromolecules obtained by polymerising compounds containing more than one epoxy group per molecule using curing agents or catalysts which react with the epoxy groups
- C08G59/18—Macromolecules obtained by polymerising compounds containing more than one epoxy group per molecule using curing agents or catalysts which react with the epoxy groups ; e.g. general methods of curing
- C08G59/20—Macromolecules obtained by polymerising compounds containing more than one epoxy group per molecule using curing agents or catalysts which react with the epoxy groups ; e.g. general methods of curing characterised by the epoxy compounds used
- C08G59/22—Di-epoxy compounds
- C08G59/226—Mixtures of di-epoxy compounds
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G59/00—Polycondensates containing more than one epoxy group per molecule; Macromolecules obtained by polymerising compounds containing more than one epoxy group per molecule using curing agents or catalysts which react with the epoxy groups
- C08G59/18—Macromolecules obtained by polymerising compounds containing more than one epoxy group per molecule using curing agents or catalysts which react with the epoxy groups ; e.g. general methods of curing
- C08G59/20—Macromolecules obtained by polymerising compounds containing more than one epoxy group per molecule using curing agents or catalysts which react with the epoxy groups ; e.g. general methods of curing characterised by the epoxy compounds used
- C08G59/22—Di-epoxy compounds
- C08G59/26—Di-epoxy compounds heterocyclic
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G59/00—Polycondensates containing more than one epoxy group per molecule; Macromolecules obtained by polymerising compounds containing more than one epoxy group per molecule using curing agents or catalysts which react with the epoxy groups
- C08G59/18—Macromolecules obtained by polymerising compounds containing more than one epoxy group per molecule using curing agents or catalysts which react with the epoxy groups ; e.g. general methods of curing
- C08G59/20—Macromolecules obtained by polymerising compounds containing more than one epoxy group per molecule using curing agents or catalysts which react with the epoxy groups ; e.g. general methods of curing characterised by the epoxy compounds used
- C08G59/22—Di-epoxy compounds
- C08G59/30—Di-epoxy compounds containing atoms other than carbon, hydrogen, oxygen and nitrogen
- C08G59/306—Di-epoxy compounds containing atoms other than carbon, hydrogen, oxygen and nitrogen containing silicon
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L27/00—Compositions of homopolymers or copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by a halogen; Compositions of derivatives of such polymers
- C08L27/02—Compositions of homopolymers or copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by a halogen; Compositions of derivatives of such polymers not modified by chemical after-treatment
- C08L27/12—Compositions of homopolymers or copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by a halogen; Compositions of derivatives of such polymers not modified by chemical after-treatment containing fluorine atoms
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L67/00—Compositions of polyesters obtained by reactions forming a carboxylic ester link in the main chain; Compositions of derivatives of such polymers
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L83/00—Compositions of macromolecular compounds obtained by reactions forming in the main chain of the macromolecule a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon only; Compositions of derivatives of such polymers
- C08L83/04—Polysiloxanes
- C08L83/06—Polysiloxanes containing silicon bound to oxygen-containing groups
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01L—SEMICONDUCTOR DEVICES NOT COVERED BY CLASS H10
- H01L23/00—Details of semiconductor or other solid state devices
- H01L23/28—Encapsulations, e.g. encapsulating layers, coatings, e.g. for protection
- H01L23/29—Encapsulations, e.g. encapsulating layers, coatings, e.g. for protection characterised by the material, e.g. carbon
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01L—SEMICONDUCTOR DEVICES NOT COVERED BY CLASS H10
- H01L23/00—Details of semiconductor or other solid state devices
- H01L23/28—Encapsulations, e.g. encapsulating layers, coatings, e.g. for protection
- H01L23/31—Encapsulations, e.g. encapsulating layers, coatings, e.g. for protection characterised by the arrangement or shape
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01L—SEMICONDUCTOR DEVICES NOT COVERED BY CLASS H10
- H01L33/00—Semiconductor devices having potential barriers specially adapted for light emission; Processes or apparatus specially adapted for the manufacture or treatment thereof or of parts thereof; Details thereof
- H01L33/48—Semiconductor devices having potential barriers specially adapted for light emission; Processes or apparatus specially adapted for the manufacture or treatment thereof or of parts thereof; Details thereof characterised by the semiconductor body packages
- H01L33/52—Encapsulations
- H01L33/56—Materials, e.g. epoxy or silicone resin
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G77/00—Macromolecular compounds obtained by reactions forming a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon in the main chain of the macromolecule
- C08G77/04—Polysiloxanes
- C08G77/14—Polysiloxanes containing silicon bound to oxygen-containing groups
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01L—SEMICONDUCTOR DEVICES NOT COVERED BY CLASS H10
- H01L2224/00—Indexing scheme for arrangements for connecting or disconnecting semiconductor or solid-state bodies and methods related thereto as covered by H01L24/00
- H01L2224/01—Means for bonding being attached to, or being formed on, the surface to be connected, e.g. chip-to-package, die-attach, "first-level" interconnects; Manufacturing methods related thereto
- H01L2224/42—Wire connectors; Manufacturing methods related thereto
- H01L2224/47—Structure, shape, material or disposition of the wire connectors after the connecting process
- H01L2224/48—Structure, shape, material or disposition of the wire connectors after the connecting process of an individual wire connector
- H01L2224/4805—Shape
- H01L2224/4809—Loop shape
- H01L2224/48091—Arched
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01L—SEMICONDUCTOR DEVICES NOT COVERED BY CLASS H10
- H01L2224/00—Indexing scheme for arrangements for connecting or disconnecting semiconductor or solid-state bodies and methods related thereto as covered by H01L24/00
- H01L2224/01—Means for bonding being attached to, or being formed on, the surface to be connected, e.g. chip-to-package, die-attach, "first-level" interconnects; Manufacturing methods related thereto
- H01L2224/42—Wire connectors; Manufacturing methods related thereto
- H01L2224/47—Structure, shape, material or disposition of the wire connectors after the connecting process
- H01L2224/48—Structure, shape, material or disposition of the wire connectors after the connecting process of an individual wire connector
- H01L2224/481—Disposition
- H01L2224/48151—Connecting between a semiconductor or solid-state body and an item not being a semiconductor or solid-state body, e.g. chip-to-substrate, chip-to-passive
- H01L2224/48221—Connecting between a semiconductor or solid-state body and an item not being a semiconductor or solid-state body, e.g. chip-to-substrate, chip-to-passive the body and the item being stacked
- H01L2224/48245—Connecting between a semiconductor or solid-state body and an item not being a semiconductor or solid-state body, e.g. chip-to-substrate, chip-to-passive the body and the item being stacked the item being metallic
- H01L2224/48247—Connecting between a semiconductor or solid-state body and an item not being a semiconductor or solid-state body, e.g. chip-to-substrate, chip-to-passive the body and the item being stacked the item being metallic connecting the wire to a bond pad of the item
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01L—SEMICONDUCTOR DEVICES NOT COVERED BY CLASS H10
- H01L2224/00—Indexing scheme for arrangements for connecting or disconnecting semiconductor or solid-state bodies and methods related thereto as covered by H01L24/00
- H01L2224/01—Means for bonding being attached to, or being formed on, the surface to be connected, e.g. chip-to-package, die-attach, "first-level" interconnects; Manufacturing methods related thereto
- H01L2224/42—Wire connectors; Manufacturing methods related thereto
- H01L2224/47—Structure, shape, material or disposition of the wire connectors after the connecting process
- H01L2224/48—Structure, shape, material or disposition of the wire connectors after the connecting process of an individual wire connector
- H01L2224/481—Disposition
- H01L2224/48151—Connecting between a semiconductor or solid-state body and an item not being a semiconductor or solid-state body, e.g. chip-to-substrate, chip-to-passive
- H01L2224/48221—Connecting between a semiconductor or solid-state body and an item not being a semiconductor or solid-state body, e.g. chip-to-substrate, chip-to-passive the body and the item being stacked
- H01L2224/48245—Connecting between a semiconductor or solid-state body and an item not being a semiconductor or solid-state body, e.g. chip-to-substrate, chip-to-passive the body and the item being stacked the item being metallic
- H01L2224/48257—Connecting between a semiconductor or solid-state body and an item not being a semiconductor or solid-state body, e.g. chip-to-substrate, chip-to-passive the body and the item being stacked the item being metallic connecting the wire to a die pad of the item
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01L—SEMICONDUCTOR DEVICES NOT COVERED BY CLASS H10
- H01L2924/00—Indexing scheme for arrangements or methods for connecting or disconnecting semiconductor or solid-state bodies as covered by H01L24/00
- H01L2924/15—Details of package parts other than the semiconductor or other solid state devices to be connected
- H01L2924/181—Encapsulation
Definitions
- the present invention relates to a curable epoxy resin composition, a cured product obtained by curing the curable epoxy resin composition, a resin composition for optical semiconductor encapsulation comprising the curable epoxy resin composition, and the optical semiconductor encapsulation.
- the present invention relates to an optical semiconductor device in which an optical semiconductor element is sealed with a resin composition for use.
- Optical semiconductor devices using light semiconductor elements such as LEDs as light sources are currently used in various applications such as various indoor or outdoor display boards, light sources for image reading, traffic signals, large display units, and the like.
- Such an optical semiconductor device generally has a structure in which an optical semiconductor element is sealed with a resin (sealing resin).
- the sealing resin plays a role for protecting the optical semiconductor element from moisture, impact and the like.
- a cured product of a resin composition containing monoallyl diglycidyl isocyanurate and bisphenol A type epoxy resin is known as an encapsulating resin for optical semiconductors having excellent heat resistance (see Patent Document 1).
- the cured product is used as a sealing resin for a high-power blue / white light semiconductor device, coloring proceeds due to light and heat emitted from the optical semiconductor element, and light that should originally be output As a result, there has been a problem that the luminous intensity of light output from the optical semiconductor device decreases with time.
- 3,4-epoxycyclohexylmethyl (3,4-epoxy) cyclohexanecarboxylate, 3,4-epoxycyclohexylmethyl (3) are encapsulating resins that have higher heat resistance and light resistance and are less likely to be colored (yellowing).
- 4-epoxy) cyclohexanecarboxylate and ⁇ -caprolactone adducts liquid alicyclic epoxy resins having an alicyclic skeleton such as 1,2,8,9-diepoxylimonene are known.
- the cured products of these alicyclic epoxy resins are vulnerable to various stresses, and when a thermal shock such as a cold cycle (repeating heating and cooling) is applied, cracks (cracks) occur. Had.
- an object of the present invention is to provide a curable epoxy resin composition that provides a cured product having excellent transparency, heat resistance, light resistance, and crack resistance. Another object of the present invention is to provide a cured product having excellent transparency, heat resistance, light resistance, and crack resistance obtained by curing the curable epoxy resin composition. Another object of the present invention is to provide a resin composition for encapsulating an optical semiconductor comprising the above curable epoxy resin composition, which can provide an optical semiconductor device in which a decrease in luminous intensity with time is suppressed. is there. Another object of the present invention is to provide an optical semiconductor device that is obtained by encapsulating an optical semiconductor element using the above resin composition for encapsulating an optical semiconductor, in which a decrease in light intensity over time is suppressed. It is in.
- an alicyclic epoxy compound a monoallyl diglycidyl isocyanurate compound, a siloxane derivative having two or more epoxy groups in the molecule, and an alicyclic polyester resin.
- a curable epoxy resin composition containing an essential component and further containing a curing agent and a curing accelerator or a curing catalyst gives a cured product having excellent transparency, heat resistance, light resistance, and crack resistance,
- the optical semiconductor device obtained by encapsulating the optical semiconductor element with the cured product has found that the light intensity of light hardly decreases with time, and has completed the present invention.
- the present invention relates to an alicyclic epoxy compound (A) and the following formula (1).
- R 1 and R 2 represent a hydrogen atom or an alkyl group having 1 to 8 carbon atoms
- a curable epoxy resin composition comprising a curing accelerator (G) is provided.
- the present invention provides an alicyclic epoxy compound (A) and the following formula (1): [Wherein R 1 and R 2 represent a hydrogen atom or an alkyl group having 1 to 8 carbon atoms]
- a curable epoxy resin composition is provided.
- the curable epoxy resin composition is provided in which the alicyclic epoxy compound (A) is an alicyclic epoxy compound having a cyclohexene oxide group.
- the said alicyclic polyester resin (D) provides the said curable epoxy resin composition which is an alicyclic polyester resin which has an alicyclic ring in a principal chain.
- the curable epoxy resin composition containing rubber particles is provided.
- the curable epoxy resin composition comprising at least one leveling agent selected from the group consisting of a silicone leveling agent and a fluorine leveling agent is provided.
- the curable epoxy resin composition containing a polyol compound is provided.
- the curable epoxy resin composition containing an acrylic block copolymer is provided.
- the present invention also provides a cured product obtained by curing the curable epoxy resin composition.
- the present invention also provides a resin composition for sealing an optical semiconductor comprising the curable epoxy resin composition.
- the present invention also provides an optical semiconductor device in which an optical semiconductor element is sealed with the above-described resin composition for sealing an optical semiconductor.
- the curable epoxy resin composition of the present invention has the above-mentioned configuration, it is possible to obtain a cured product having excellent transparency, heat resistance, light resistance, and crack resistance by curing the resin composition. it can.
- an optical semiconductor device obtained by encapsulating an optical semiconductor element using the curable epoxy resin composition of the present invention hardly deteriorates in light intensity over time, and exhibits excellent quality and durability.
- the curable epoxy resin composition of the present invention is a case where it is used as a sealing resin (resin for forming a sealing resin) of an optical semiconductor device provided with an optical semiconductor element with high output and high brightness.
- the light intensity of the light emitted from the optical semiconductor device is hardly reduced.
- FIG. 1 is a schematic view showing an embodiment of an optical semiconductor device in which an element (optical semiconductor element) is sealed with a curable epoxy resin composition of the present invention.
- the left figure (a) is a perspective view, and the right figure (b) is a sectional view.
- FIG. 2 is an example of the surface temperature profile of the optical semiconductor device in the solder heat resistance test of the example (temperature profile in one of the two heating operations in the reflow furnace).
- the curable epoxy resin composition of the present invention comprises an alicyclic epoxy compound (A) and the following formula (1).
- the alicyclic epoxy compound (A) constituting the curable epoxy resin composition of the present invention is a compound having at least an alicyclic (aliphatic ring) structure and an epoxy group in the molecule (in one molecule). More specifically, the alicyclic epoxy compound (A) includes, for example, (i) an epoxy group composed of two adjacent carbon atoms and oxygen atoms constituting the alicyclic ring (“alicyclic epoxy group”). And (ii) a compound in which an epoxy group is directly bonded to the alicyclic ring by a single bond. However, the alicyclic epoxy compound (A) does not include a siloxane derivative (C) having two or more epoxy groups in the molecule described later.
- a compound having an epoxy group (alicyclic epoxy group) composed of two adjacent carbon atoms and oxygen atoms constituting an alicyclic ring is arbitrarily selected from known or commonly used compounds. be able to. Especially, it is preferable that the said compound has an epoxy group comprised by two adjacent carbon atoms and oxygen atoms which comprise a cyclohexane ring, ie, an alicyclic epoxy compound which has a cyclohexene oxide group.
- X represents a single bond or a linking group (a divalent group having one or more atoms).
- the linking group include divalent hydrocarbon groups, carbonyl groups, ether groups (ether bonds), thioether groups (thioether bonds), ester groups (ester bonds), carbonate groups (carbonate bonds), amide groups (amides). Bond), and a group in which a plurality of these are linked.
- Examples of the alicyclic epoxy compound in which X in the formula (I) is a single bond include compounds represented by the following formula.
- an alicyclic epoxy compound for example, a commercial product such as a trade name “Celoxide 8000” (manufactured by Daicel Corporation) can be used.
- Examples of the divalent hydrocarbon group include a linear or branched alkylene group having 1 to 18 carbon atoms and a divalent alicyclic hydrocarbon group.
- Examples of the linear or branched alkylene group having 1 to 18 carbon atoms include a methylene group, a methylmethylene group, a dimethylmethylene group, an ethylene group, a propylene group, and a trimethylene group.
- Examples of the divalent alicyclic hydrocarbon group include 1,2-cyclopentylene group, 1,3-cyclopentylene group, cyclopentylidene group, 1,2-cyclohexylene group, 1,3-cyclohexene group.
- divalent cycloalkylene groups including cycloalkylidene groups
- the linking group X is preferably a linking group containing an oxygen atom, specifically, —CO— (carbonyl group), —O—CO—O— (carbonate group), —COO— (ester group). ), —O— (ether group), —CONH— (amide group), a group in which a plurality of these groups are linked, one or more of these groups, and one or more of divalent hydrocarbon groups Examples include linked groups. Examples of the divalent hydrocarbon group include those exemplified above.
- alicyclic epoxy compound represented by the above formula (I) include compounds represented by the following formulas (I-1) to (I-10).
- commercially available products such as trade names “Celoxide 2021P” and “Celoxide 2081” (manufactured by Daicel Corporation) may be used.
- l and m each represents an integer of 1 to 30.
- R in the following formula (I-5) is an alkylene group having 1 to 8 carbon atoms, and is a methylene group, ethylene group, propylene group, isopropylene group, butylene group, isobutylene group, s-butylene group, pentylene group, hexylene.
- linear or branched alkylene groups such as a group, heptylene group, and octylene group.
- a linear or branched alkylene group having 1 to 3 carbon atoms such as a methylene group, an ethylene group, a propylene group, and an isopropylene group is preferable.
- n1 to n6 each represents an integer of 1 to 30.
- Examples of the compound in which the epoxy group is directly bonded to the alicyclic ring with a single bond include compounds represented by the following formula (II).
- R ′ is a group obtained by removing p —OH from a p-valent alcohol, and p and n each represent a natural number.
- Examples of the p-valent alcohol [R ′-(OH) p ] include polyhydric alcohols such as 2,2-bis (hydroxymethyl) -1-butanol (alcohols having 1 to 15 carbon atoms, etc.).
- p is preferably 1 to 6, and n is preferably 1 to 30.
- n in each () (in parentheses) may be the same or different.
- the compound examples include 1,2-epoxy-4- (2-oxiranyl) cyclohexane adduct of 2,2-bis (hydroxymethyl) -1-butanol, trade name “EHPE 3150” ((stock) ) Manufactured by Daicel).
- the alicyclic epoxy compound (A) can be used alone or in combination of two or more.
- the alicyclic epoxy compound (A) 3,4-epoxycyclohexylmethyl (3,4-epoxy) cyclohexanecarboxylate represented by the above formula (I-1), trade name “Celoxide 2021P” Is particularly preferred.
- the amount of use (content) of the alicyclic epoxy compound (A) is not particularly limited, but when the curable epoxy resin composition of the present invention contains a curing agent (E) as an essential component, a curable epoxy resin.
- the content is preferably 10 to 90% by weight, more preferably 15 to 80% by weight, and still more preferably 17 to 70% by weight, based on the composition (100% by weight).
- the curable epoxy resin composition of the present invention contains the curing catalyst (F) as an essential component
- the amount (content) of the alicyclic epoxy compound (A) is set to be the curable epoxy resin composition ( 100% by weight) is preferably 25 to 90% by weight, more preferably 30 to 85% by weight, and still more preferably 35 to 80% by weight.
- the usage-amount (content) of an alicyclic epoxy compound (A) with respect to the total amount (100 weight%) of an alicyclic epoxy compound (A) and a monoallyl diglycidyl isocyanurate compound (B) is especially limited. However, it is preferably 50 to 95% by weight, more preferably 60 to 95% by weight, and still more preferably 70 to 95% by weight.
- the amount of the alicyclic epoxy compound (A) used is less than 50% by weight, the solubility of the monoallyl diglycidyl isocyanurate compound (B) is not sufficient, and it may be easily precipitated when placed at room temperature.
- the usage-amount of an alicyclic epoxy compound (A) exceeds 95 weight%, the crack resistance of hardened
- the monoallyl diglycidyl isocyanurate compound (B) constituting the curable epoxy resin composition of the present invention is represented by the following general formula (1).
- R 1 and R 2 are the same or different and each represents a hydrogen atom or an alkyl group having 1 to 8 carbon atoms.
- alkyl group having 1 to 8 carbon atoms examples include methyl, ethyl, propyl, isopropyl, butyl, isobutyl, s-butyl, pentyl, hexyl, heptyl, octyl and the like. Examples thereof include a chain or branched alkyl group. Of these, a linear or branched alkyl group having 1 to 3 carbon atoms such as a methyl group, an ethyl group, a propyl group, and an isopropyl group is preferable.
- R 1 and R 2 in the above formula (1) are particularly preferably hydrogen atoms.
- monoallyl diglycidyl isocyanurate compound (B) examples include monoallyl diglycidyl isocyanurate, 1-allyl-3,5-bis (2-methylepoxypropyl) isocyanurate, 1- (2-methyl And propenyl) -3,5-diglycidyl isocyanurate, 1- (2-methylpropenyl) -3,5-bis (2-methylepoxypropyl) isocyanurate, and the like.
- a monoallyl diglycidyl isocyanurate compound (B) can be used individually or in combination of 2 or more types.
- the monoallyl diglycidyl isocyanurate compound (B) can be arbitrarily mixed as long as it dissolves in the alicyclic epoxy compound (A), and the alicyclic epoxy compound (A) and the monoallyl diglycidyl isocyanurate compound (B).
- the ratio of alicyclic epoxy compound (A): monoallyl diglycidyl isocyanurate compound (B) is preferably 50:50 to 95: 5 (weight ratio), more preferably 50: 50 to 90:10 (weight ratio). Outside this range, the solubility of the monoallyl diglycidyl isocyanurate compound (B) may be difficult to obtain, or crack resistance may be reduced.
- the monoallyl diglycidyl isocyanurate compound (B) may be modified in advance by adding a compound that reacts with an epoxy group such as alcohol or acid anhydride.
- siloxane derivative (C) having two or more epoxy groups in the molecule has a siloxane skeleton, and has two or more epoxy groups in the molecule. It is a compound that has.
- the siloxane derivative (C) having two or more epoxy groups in the molecule plays a role of improving the heat resistance, light resistance, and crack resistance of the cured product and suppressing the decrease in luminous intensity of the optical semiconductor device.
- the siloxane skeleton in the siloxane derivative (C) having two or more epoxy groups in the molecule is not particularly limited.
- a cyclic siloxane skeleton; linear silicone, cage-type or ladder-type polysilsesquioxane And a polysiloxane skeleton are preferable from the viewpoint of improving the heat resistance and light resistance of the cured product and suppressing the decrease in luminous intensity.
- the siloxane derivative (C) having two or more epoxy groups in the molecule is preferably a cyclic siloxane having two or more epoxy groups in the molecule or a linear silicone having two or more epoxy groups in the molecule.
- numerator can be used individually or in combination of 2 or more types.
- the siloxane derivative (C) having two or more epoxy groups in the molecule is a cyclic siloxane having two or more epoxy groups
- the number of Si—O units forming the siloxane ring (the number of silicon atoms forming the siloxane ring)
- it is not particularly limited, it is preferably 2 to 12 and more preferably 4 to 8 from the viewpoint of improving the heat resistance and light resistance of the cured product.
- the weight average molecular weight of the siloxane derivative (C) having two or more epoxy groups in the molecule is not particularly limited, but is preferably 100 to 3000, more preferably 180 from the viewpoint of improving the heat resistance and light resistance of the cured product. ⁇ 2000.
- the number of epoxy groups (number of epoxy groups in one molecule) of the siloxane derivative (C) having two or more epoxy groups in the molecule is not particularly limited as long as it is two or more, but the heat resistance of the cured product, From the viewpoint of improving light resistance, 2 to 4 are preferable.
- the epoxy equivalent (based on JIS K7236) of the siloxane derivative (C) having two or more epoxy groups in the molecule is not particularly limited, but is preferably 180 to 400 from the viewpoint of improving the heat resistance and light resistance of the cured product. More preferably, it is 240 to 400, and more preferably 240 to 350.
- the epoxy group in the siloxane derivative (C) having two or more epoxy groups in the molecule is not particularly limited, but from the viewpoint of improving the heat resistance and light resistance of the cured product, adjacent two carbons constituting the aliphatic ring.
- An epoxy group composed of an atom and an oxygen atom (alicyclic epoxy group) is preferable, and among them, a cyclohexene oxide group is particularly preferable.
- siloxane derivative (C) having two or more epoxy groups in the molecule examples include 2,4-di [2- (3- ⁇ oxabicyclo [4.1.0] heptyl ⁇ ) ethyl. ] -2,4,6,6,8,8-hexamethyl-cyclotetrasiloxane, 4,8-di [2- (3- ⁇ oxabicyclo [4.1.0] heptyl ⁇ ) ethyl] -2,2 , 4,6,6,8-hexamethyl-cyclotetrasiloxane, 2,4-di [2- (3- ⁇ oxabicyclo [4.1.0] heptyl ⁇ ) ethyl] -6,8-dipropyl-2, 4,6,8-tetramethyl-cyclotetrasiloxane, 4,8-di [2- (3- ⁇ oxabicyclo [4.1.0] heptyl ⁇ ) ethyl] -2,6-dipropyl-2,4 6,8-tty
- siloxane derivative (C) having two or more epoxy groups in the molecule examples include alicyclic epoxy group-containing silicone resins described in JP-A-2008-248169 and JP-A-2008-19422.
- An organopolysilsesquioxane resin having at least two epoxy functional groups in one molecule can also be used.
- siloxane derivative (C) having two or more epoxy groups in the molecule examples include a trade name “X-40-2678” (Shin-Etsu Chemical Co., Ltd.), which is a cyclic siloxane having two or more epoxy groups in the molecule. )), Trade name “X-40-2670” (manufactured by Shin-Etsu Chemical Co., Ltd.), and trade name “X-40-2720” (manufactured by Shin-Etsu Chemical Co., Ltd.) can also be used. .
- the amount (content) of the siloxane derivative (C) having two or more epoxy groups in the molecule is not particularly limited, the total amount (100 weight) of the component (A), the component (B), and the component (C). %) To 5 to 60% by weight, more preferably 8 to 55% by weight, still more preferably 10 to 50% by weight, and particularly preferably 15 to 40% by weight.
- the amount of the siloxane derivative (C) having two or more epoxy groups in the molecule is less than 5% by weight, the heat resistance and light resistance of the cured product may be lowered.
- numerator exceeds 60 weight%, the crack resistance of hardened
- the total amount of the derivative (C) is not particularly limited, but is preferably 30% by weight or more (for example, 30 to 100% by weight), and particularly preferably 40% by weight or more from the viewpoint of improving heat resistance, light resistance, and crack resistance. preferable.
- the alicyclic polyester resin (D) constituting the curable epoxy resin composition of the present invention is a polyester resin having at least an alicyclic structure (aliphatic ring structure).
- the alicyclic polyester resin (D) plays a role of improving the heat resistance, light resistance, and crack resistance of the cured product and suppressing the light intensity of the optical semiconductor device.
- the alicyclic polyester resin (D) is an alicyclic polyester resin having an alicyclic ring (alicyclic structure) in the main chain. preferable.
- the alicyclic polyester resin (D) is preferably a polyester resin in which a polymer main chain is constituted by part or all of the carbon atoms constituting the alicyclic ring.
- an alicyclic polyester resin (D) can be used individually or in combination of 2 or more types.
- the alicyclic structure in the alicyclic polyester resin (D) is not particularly limited, and examples thereof include monocyclic hydrocarbon structures and bridged ring hydrocarbon structures (for example, bicyclic hydrocarbons). Saturated monocyclic hydrocarbon structures and saturated bridged ring hydrocarbon structures in which all of the alicyclic rings (carbon-carbon bonds constituting the alicyclic rings) are carbon-carbon single bonds are preferred. Moreover, the alicyclic structure in the alicyclic polyester resin (D) may be introduced into only one of the structural unit derived from dicarboxylic acid or the structural unit derived from diol, or both may be introduced. Well, not particularly limited.
- the alicyclic polyester resin (D) has a structural unit derived from a monomer component having an alicyclic structure.
- the monomer having an alicyclic structure include diols and dicarboxylic acids having a known or commonly used alicyclic structure, and are not particularly limited.
- the alicyclic polyester resin (D) may have a structural unit derived from a monomer component having no alicyclic structure.
- the monomer component having no alicyclic structure is not particularly limited.
- aromatic dicarboxylic acids such as terephthalic acid, isophthalic acid, phthalic acid, and naphthalenedicarboxylic acid (including derivatives such as acid anhydrides); adipic acid Aliphatic dicarboxylic acids such as sebacic acid, azelaic acid, succinic acid, fumaric acid, maleic acid (including derivatives such as acid anhydrides); ethylene glycol, propylene glycol, 1,2-propanediol, 1,3-propane Diol, 1,3-butanediol, 1,4-butanediol, neopentyl glycol, 1,5-pentanediol, 1,6-hexanediol, 3-methylpentanediol, diethylene glyco
- a monomer component having no alicyclic structure also includes those obtained by bonding an appropriate substituent (for example, an alkyl group, an alkoxy group, a halogen atom, etc.) to the dicarboxylic acid or diol having no alicyclic structure.
- an appropriate substituent for example, an alkyl group, an alkoxy group, a halogen atom, etc.
- the ratio of the monomer unit having an alicyclic ring to the total monomer units (total monomer components) (100 mol%) constituting the alicyclic polyester resin (D) is not particularly limited, but is 10 mol% or more (for example, 10 to 80). Mol%) is preferable, more preferably 25 to 70 mol%, still more preferably 40 to 60 mol%. When the ratio of the monomer unit having an alicyclic ring is less than 10 mol%, the heat resistance, light resistance, and crack resistance of the cured product may be lowered.
- the alicyclic polyester resin (D) is particularly preferably an alicyclic polyester containing at least one structural unit represented by the following formulas (2) to (4).
- R 3 represents a linear, branched, or cyclic alkylene group having 2 to 15 carbon atoms.
- R 4 to R 7 are each independently a hydrogen atom or a linear or branched chain. Represents an alkyl group having 1 to 4 carbon atoms, and two selected from R 4 to R 7 may combine to form a ring.
- R 3 represents a linear, branched, or cyclic alkylene group having 2 to 15 carbon atoms.
- R 4 to R 7 are each independently a hydrogen atom or a linear or branched chain. (It represents an alkyl group having 1 to 4 carbon atoms and may form a ring in which two members selected from R 4 to R 7 are bonded.)
- R 3 represents a linear, branched, or cyclic alkylene group having 2 to 15 carbon atoms.
- R 4 to R 7 are each independently a hydrogen atom or a linear or branched chain. (It represents an alkyl group having 1 to 4 carbon atoms and may form a ring in which two members selected from R 4 to R 7 are bonded.)
- Preferred specific examples of the structural units represented by the above formulas (2) to (4) include, for example, a structure derived from 4-methyl-1,2-cyclohexanedicarboxylic acid and ethylene glycol represented by the following formula (5) Units are listed.
- the alicyclic polyester resin (D) having the structural unit can be obtained, for example, by polycondensation of methylhexahydrophthalic anhydride and ethylene glycol.
- the structural units represented by the above formulas (2) to (4) include, for example, those derived from 1,4-cyclohexanedicarboxylic acid and neopentyl glycol represented by the following formula (6):
- a structural unit is mentioned.
- the alicyclic polyester resin (D) having the structural unit can be obtained, for example, by polycondensation of 1,4-cyclohexanedicarboxylic acid and neopentyl glycol.
- the terminal structure of the alicyclic polyester resin (D) is not particularly limited, and may be a hydroxyl group or a carboxyl group, or a structure in which these hydroxyl group or carboxyl group is appropriately modified (for example, the terminal hydroxyl group is a mono group). It may be a structure esterified with a carboxylic acid or an acid anhydride, or a structure in which a terminal carboxyl group is esterified with an alcohol.
- the total content of the structural units (total content; all monomers constituting the structural unit)
- the unit is not particularly limited, but 20 mol% or more (for example, with respect to the total structural unit (100 mol%; all monomer units constituting the alicyclic polyester resin (D)) of the alicyclic polyester resin (D) (for example, 20 to 100 mol%), more preferably 50 to 100 mol%, still more preferably 80 to 100 mol%. If the content of the structural units represented by the above formulas (2) to (4) is less than 20 mol%, the heat resistance, light resistance and crack resistance of the cured product may be lowered.
- the number average molecular weight of the alicyclic polyester resin (D) is not particularly limited, but is preferably 300 to 100,000, more preferably 300 to 30,000. If the number average molecular weight of the alicyclic polyester resin (D) is less than 300, the toughness of the cured product may not be sufficient, and crack resistance may decrease. On the other hand, when the number average molecular weight of the alicyclic polyester resin (D) exceeds 100,000, the compatibility with other components (for example, the curing agent (E)) may be reduced, and the transparency of the cured product may be reduced. is there. In addition, the number average molecular weight of alicyclic polyester resin (D) can be measured as a value of standard polystyrene conversion, for example by GPC (gel permeation chromatography) method.
- GPC gel permeation chromatography
- the alicyclic polyester resin (D) is not particularly limited and can be produced by a known or conventional method. More specifically, for example, the alicyclic polyester resin (D) may be obtained by polycondensation of the above-described dicarboxylic acid and diol by a conventional method, or the above-mentioned dicarboxylic acid derivative (an acid anhydride, ester). , Acid halides, and the like) and diols may be obtained by polycondensation by a conventional method.
- the blending amount (content) of the alicyclic polyester resin (D) is not particularly limited, but when the curing agent (E) is an essential component, the alicyclic polyester resin.
- the amount is preferably 1 to 60% by weight, more preferably 5 to 30% by weight, based on the total amount (100% by weight) of (D) and the curing agent (E).
- the blending amount of the alicyclic polyester resin (D) is less than 1% by weight, the crack resistance of the cured product may be lowered.
- the blending amount of the alicyclic polyester resin (D) exceeds 60% by weight, the transparency and heat resistance of the cured product may be lowered.
- the amount (content) of the alicyclic polyester resin (D) is not particularly limited, but the alicyclic polyester The content is preferably 50 to 99% by weight, more preferably 65 to 99% by weight, based on the total amount (100% by weight) of the resin (D) and the curing catalyst (F).
- cured material may fall that the compounding quantity of an alicyclic polyester resin (D) is less than 50 weight%.
- the blending amount of the alicyclic polyester resin (D) exceeds 99% by weight, the transparency and heat resistance of the cured product may be lowered.
- the curing agent (E) constituting the curable epoxy resin composition of the present invention plays a role of curing a compound having an epoxy group.
- curing agent (E) a well-known thru
- curing agent can be used as a hardening
- an acid anhydride which is liquid at 25 ° C. is preferable, and more specifically, for example, methyltetrahydrophthalic anhydride, methylhexahydrophthalic anhydride, dodecenyl succinic anhydride, methylendomethylene. Examples include tetrahydrophthalic anhydride.
- solid acid anhydrides at room temperature such as phthalic anhydride, tetrahydrophthalic anhydride, hexahydrophthalic anhydride, and methylcyclohexene dicarboxylic acid anhydride are also liquid at room temperature (about 25 ° C.). It can use preferably as a hardening
- curing agent (E) can be used individually or in combination of 2 or more types.
- anhydride of a saturated monocyclic hydrocarbon dicarboxylic acid (including a ring having a substituent such as an alkyl group bonded thereto). ) Is preferred.
- the curing agent (E) as the curing agent (E), a product name “Ricacid MH-700” (manufactured by Shin Nippon Rika Co., Ltd.), a product name “HN-5500” (manufactured by Hitachi Chemical Co., Ltd.), etc. Commercial products can also be used.
- the use amount (content) of the curing agent (E) is not particularly limited, but is 50 to 200 parts by weight with respect to the total amount (100 parts by weight) of the compound having an epoxy group contained in the curable epoxy resin composition. And more preferably 100 to 145 parts by weight. More specifically, it is preferably used at a ratio of 0.5 to 1.5 equivalents per 1 equivalent of epoxy groups in the compound having all epoxy groups contained in the curable epoxy resin composition of the present invention. .
- curing agent (E) is less than 50 weight part, hardening will become inadequate and there exists a tendency for the toughness of hardened
- the curing accelerator (G) is a compound having a function of accelerating the curing rate when the compound having an epoxy group is cured by the curing agent (E).
- the curing accelerator (G) known or conventional curing accelerators can be used, and are not particularly limited.
- 1,8-diazabicyclo [5.4.0] undecene-7 DBU
- Salts thereof eg, phenol salts, octylates, p-toluenesulfonates, formates, tetraphenylborate salts
- 1,5-diazabicyclo [4.3.0] nonene-5 DBN
- salts thereof Eg, phenol salt, octylate, p-toluenesulfonate, formate, tetraphenylborate salt
- Imidazole compounds phosphoric acid esters, phosphines such as triphenylphosphine; tetraphenylphosphonium tetra (p- tolyl) phosphonium compounds such as borate, tin octylate, organic metal salts such as zinc octylate; metal chelate and the like.
- a hardening accelerator (G) can be used individually or in combination of 2 or more types.
- the amount of use (content) of the curing accelerator (G) is not particularly limited, but is from 0.05 to 0.05 based on the total amount (100 parts by weight) of the compound having an epoxy group contained in the curable epoxy resin composition.
- the amount is preferably 5 parts by weight, more preferably 0.1 to 3 parts by weight, still more preferably 0.2 to 3 parts by weight, and particularly preferably 0.25 to 2.5 parts by weight.
- the usage-amount of a hardening accelerator (G) is less than 0.05 weight part, the hardening promotion effect may become inadequate.
- the curable epoxy resin composition of the present invention may contain a curing catalyst (F) instead of the above-mentioned curing agent (E).
- a curing catalyst (F) instead of the above-mentioned curing agent (E).
- the curing catalyst (F) by using the curing catalyst (F), the curing reaction of the compound having an epoxy group can be advanced to obtain a cured product.
- the cationic catalyst cationic polymerization initiator
- Examples of the cation catalyst that generates cation species by ultraviolet irradiation include hexafluoroantimonate salt, pentafluorohydroxyantimonate salt, hexafluorophosphate salt, and hexafluoroarsenate salt. These cationic catalysts can be used alone or in combination of two or more.
- cationic catalyst examples include trade names “UVACURE1590” (manufactured by Daicel Cytec Co., Ltd.), trade names “CD-1010”, “CD-1011”, “CD-1012” (above, manufactured by Sartomer, USA), Commercial products such as trade name “Irgacure 264” (manufactured by Ciba Japan Co., Ltd.) and trade name “CIT-1682” (manufactured by Nippon Soda Co., Ltd.) can also be preferably used.
- Examples of the cation catalyst that generates cation species by heat treatment include aryldiazonium salts, aryliodonium salts, arylsulfonium salts, and allene-ion complexes. These cationic catalysts can be used alone or in combination of two or more.
- Examples of the cationic catalyst include trade names “PP-33”, “CP-66”, “CP-77” (manufactured by ADEKA), trade names “FC-509” (manufactured by 3M), Name “UVE1014” (manufactured by GE), trade name “Sun-Aid SI-60L”, “Sun-Aid SI-80L”, “Sun-Aid SI-100L”, “Sun-Aid SI-110L”, “Sun-Aid SI-150L” (and above)
- Commercially available products such as Sanshin Chemical Co., Ltd.) and trade name “CG-24-61” (manufactured by Ciba Japan Co., Ltd.) can be preferably used.
- a compound of a chelate compound of a metal such as aluminum or titanium and acetoacetic acid or diketones and a silanol such as triphenylsilanol, or a metal such as aluminum or titanium and acetoacetic acid or diketones A compound of the above chelate compound and a phenol such as bisphenol S can also be used.
- the use amount (content) of the curing catalyst (F) is not particularly limited, but is 0.01 to 15 with respect to the total amount (100 parts by weight) of the compound having an epoxy group contained in the curable epoxy resin composition. Part by weight is preferable, more preferably 0.01 to 12 parts by weight, still more preferably 0.05 to 10 parts by weight, and particularly preferably 0.1 to 10 parts by weight.
- the curable epoxy resin composition of the present invention preferably further includes at least one leveling agent selected from the group consisting of a silicone leveling agent (polysiloxane leveling agent) and a fluorine leveling agent.
- a silicone leveling agent polysiloxane leveling agent
- a fluorine leveling agent By including the leveling agent, the curable epoxy resin composition of the present invention can form a cured product exhibiting higher heat resistance and crack resistance, and an optical semiconductor device produced using the cured product is It is difficult to cause a decrease in luminous intensity.
- the silicone leveling agent is a leveling agent containing a compound having a polysiloxane skeleton.
- known or conventional silicone leveling agents can be used and are not particularly limited. For example, trade names “BYK-300”, “BYK-301 / 302”, “BYK-306”, “ BYK-307, BYK-310, BYK-315, BYK-313, BYK-320, BYK-322, BYK-323, BYK-325, BYK- 330 ”,“ BYK-331 ”,“ BYK-333 ”,“ BYK-337 ”,“ BYK-341 ”,“ BYK-344 ”,“ BYK-345 / 346 ”,“ BYK-347 ”,“ BYK- ” 348 ”,“ BYK-349 ”,“ BYK-370 ”,“ BYK-375 ”,“ BYK-377 ”,“ BYK
- the compound having a polysiloxane skeleton is particularly preferably a silicone polymer (except for the component (C)) having at least a structural unit (repeating structural unit) represented by the following formula (7).
- the silicone leveling agent is preferably a leveling agent containing at least the silicone polymer.
- R 8 in the above formula (7) represents a linear or branched alkyl group which may have a substituent.
- the linear or branched alkyl group include a methyl group, an ethyl group, a propyl group, an isopropyl group, a butyl group (n-butyl group), an isobutyl group, a s-butyl group, a t-butyl group, and pentyl.
- the substituent that the linear or branched alkyl group may have is not particularly limited, but for example, a hydroxyl group that may be protected with a protecting group [for example, a hydroxyl group, A substituted oxy group (for example, an alkoxy group having 1 to 4 carbon atoms such as a methoxy group, an ethoxy group, or a propoxy group)], a carboxyl group optionally protected by a protecting group [for example, a —COOR a group, etc .:
- R a represents a hydrogen atom or an alkyl group, and examples of the alkyl group include a methyl group, an ethyl group, a propyl group, an isopropyl group, a butyl group, an isobutyl group, a s-butyl group, a t-butyl group, and a hexyl group.
- acryloyl group methacryloyl group, acryloyloxy group, methacryloyloxy group, vinyl , Propenyl group, an epoxy group, such as glycidyl groups.
- R 9 in the above formula (7) is a linear or branched alkyl group which may have a substituent, an aralkyl group which may have a substituent, an organic group containing a polyether chain, Or the organic group containing a polyester chain
- strand is shown.
- the linear or branched alkyl group for R 9 is not particularly limited, and examples thereof include a methyl group, an ethyl group, a propyl group, an isopropyl group, a butyl group (n-butyl group), an isobutyl group, and an s-butyl group.
- straight-chain or branched alkyl groups having 1 to 30 carbon atoms such as a group, t-butyl group and pentyl group.
- the aralkyl group is not particularly limited, and examples thereof include a benzyl group, a methylbenzyl group, a phenethyl group, a methylphenethyl group, a phenylpropyl group, and a naphthylmethyl group.
- the substituent that the linear or branched alkyl group may have and the substituent that the aralkyl group may have are not particularly limited.
- the substituent that the linear or branched alkyl group may have and the substituent that the aralkyl group may have are not particularly limited.
- examples thereof include the exemplified substituents.
- the organic group containing a polyether chain in R 9 is a monovalent organic group containing at least a polyether structure.
- the polyether structure in the organic group containing a polyether chain is not particularly limited as long as it has a structure having a plurality of ether bonds.
- polyethylene glycol structure polyethylene oxide structure
- polypropylene glycol structure polypropylene oxide structure
- polyoxyalkylene structures such as polybutylene glycol (polytetramethylene glycol) structures and polyether structures derived from multiple types of alkylene glycol (or alkylene oxide) (for example, poly (propylene glycol / ethylene glycol) structures). It is done.
- each alkylene glycol in the polyether structure derived from a plurality of types of alkylene glycols may be a block type (block copolymer type) or a random type (random copolymer type). Also good.
- the organic group containing the polyether chain may be an organic group consisting only of the polyether structure, or one or two or more of the polyether structure and one or two or more linking groups (one or more atoms may be bonded). It may be an organic group having a structure in which a divalent group) is linked.
- Examples of the linking group in the organic group containing a polyether chain include, for example, a divalent hydrocarbon group (particularly, a linear or branched alkylene group), a thioether group (—S—), an ester group (—COO—). ), An amide group (—CONH—), a carbonyl group (—CO—), a carbonate group (—OCOO—), a group in which two or more of these are bonded, and the like.
- the organic group containing the polyether chain is the substituent exemplified in the above R 8 (for example, hydroxyl group, carboxyl group, acryloyl group, methacryloyl group, acryloyloxy group, methacryloyloxy group, vinyl group, propenyl group, etc.
- examples of the organic group containing such a polyether structure include an organic group having the above substituent at the terminal (end on the opposite side to the silicon atom in Formula (7)). It is done.
- the organic group containing a polyester chain in R 9 is a monovalent organic group containing at least a polyester structure.
- the polyester structure in the organic group containing a polyester chain is not particularly limited as long as it has a structure having a plurality of ester bonds, and examples thereof include an aliphatic polyester structure, an alicyclic polyester structure, and an aromatic polyester structure. .
- examples of the polyester structure include a polyester structure formed by polymerization of polycarboxylic acid (particularly dicarboxylic acid) and polyol (particularly diol).
- the polycarboxylic acid is not particularly limited, and examples thereof include aromatic dicarboxylic acids such as terephthalic acid, isophthalic acid, phthalic acid and naphthalenedicarboxylic acid (including derivatives such as acid anhydrides and esters); adipic acid and sebacic acid Aliphatic dicarboxylic acids such as azelaic acid, succinic acid, fumaric acid and maleic acid (including derivatives such as acid anhydrides and esters); 1,2-cyclohexanedicarboxylic acid, 1,3-cyclohexanedicarboxylic acid, 1,4 -Cyclohexanedicarboxylic acid, 4-methyl-1,2-cyclohexanedicarboxylic acid, highmic acid, 1,4-decahydronaphthalenedicarboxylic acid,
- the polyol is not particularly limited.
- polyester structure examples include a polyester structure formed by polymerization of hydroxycarboxylic acid and a polyester structure formed by polymerization of lactone which is a cyclic ester of the hydroxycarboxylic acid (ring-opening polymerization).
- the hydroxycarboxylic acid is not particularly limited.
- p-hydroxybenzoic acid p-hydroxybenzoic acid, m-hydroxybenzoic acid, o-hydroxybenzoic acid (salicylic acid), 3-methoxy-4-hydroxybenzoic acid (vanillic acid), 4 -Methoxy-3-hydroxybenzoic acid (isovanillic acid), 3,5-dimethoxy-4-hydroxybenzoic acid (syringic acid), 2,6-dimethoxy-4-hydroxybenzoic acid, 3-methyl-4-hydroxybenzoic acid 4-methyl-3-hydroxybenzoic acid, 3-phenyl-4-hydroxybenzoic acid, 4-phenyl-3-hydroxybenzoic acid, 2-phenyl-4-hydroxybenzoic acid, 6-hydroxy-2-naphthoic acid, 3,4-dihydroxycinnamic acid (caffeic acid), (E) -3- (4-hydroxy-3-methoxy-phenyl) Nyl) propane-2-enolic acid (ferulic acid), 3- (4-hydroxyphenyl) -2-propenonic acid (coumaric
- the lactone is not particularly limited, and examples thereof include ⁇ -butyrolactone, ⁇ -valerolactone, ⁇ -caprolactone, ⁇ -enanthlactone, and ⁇ -caprolactone.
- the polyester structure may be formed from a single hydroxycarboxylic acid or lactone, or may be formed from two or more hydroxycarboxylic acids or lactones.
- the polyester structure is not limited to the structure exemplified above.
- the polyester structure formed by polymerization of the above polycarboxylic acid and polyol the polyester structure formed by polymerization of hydroxycarboxylic acid, and the polymerization of lactone.
- a structure in which two or more of the formed polyester structures are combined may be used.
- the organic group containing the polyester chain may be an organic group consisting only of the polyester structure, or an organic group having a structure in which one or two or more of the polyester structures and one or two or more connecting groups are connected. It may be.
- Examples of the linking group in the organic group containing a polyester chain include a divalent hydrocarbon group (particularly, a linear or branched alkylene group), a thioether group (—S—), an ester group (—COO—). Amide group (—CONH—), carbonyl group (—CO—), carbonate group (—OCOO—), a group in which two or more of these are bonded, and the like.
- the organic group containing the polyester chain is the substituent exemplified in the above R 8 (for example, hydroxyl group, carboxyl group, acryloyl group, methacryloyl group, acryloyloxy group, methacryloyloxy group, vinyl group, propenyl group, etc.)
- examples of the organic group containing such a polyester structure include an organic group having the above substituent at the terminal (end on the opposite side to the silicon atom in Formula (7)).
- the silicone polymer may be a polymer having only a structural unit represented by the formula (7) as a repeating structural unit, or may have a structural unit other than the structural unit represented by the formula (7). It may be a polymer.
- the structural unit other than the structural unit represented by the formula (7) in the silicone polymer is not particularly limited, and examples thereof include a structural unit having a hydrosilyl group (Si—H).
- the silicone polymer may be a polymer having only one type of structural unit represented by formula (7), or a polymer having two or more types of structural units represented by formula (7). It may be. Moreover, the polymer which has 2 or more types of structural units other than the structural unit represented by Formula (7) may be sufficient.
- silicone polymer examples include polymers (polydimethylsiloxane or modified polydimethylsiloxane) represented by the following formulas (7a) to (7e).
- the silicone polymer represented by the above formula (7a) is polydimethylsiloxane.
- the x1 (the number of repeating dimethylsilyloxy structural units [—Si (CH 3 ) 2 —O—]) in the formula (7a) is not particularly limited, but is preferably 2 to 3000, more preferably 3 to 1500.
- the silicone-based polymer represented by the above formula (7b) is a polyether-modified product of polydimethylsiloxane in which a polyether structure is introduced into the side chain of polydimethylsiloxane.
- R 10 in formula (7b) represents a hydrogen atom or a methyl group.
- R 11 represents a hydrogen atom or a linear or branched alkyl group which may have a substituent.
- M1 (the number of repeating methylene structural units) in the formula (7b) is not particularly limited, but can be appropriately selected from a range of 1 to 30, for example.
- n1 (the number of repeating oxyethylene structural units or oxypropylene structural units) is not particularly limited, but can be appropriately selected from a range of 2 to 3000, for example.
- y1 (the number of repeating structural units including a polyether structure (polyether side chain)) in the formula (7b) is not particularly limited, but is preferably 1 to 3000, and more preferably 3 to 1500.
- x2 (the number of repeating dimethylsilyloxy structural units) is not particularly limited, but is preferably 2 to 3000, and more preferably 3 to 1500.
- the addition form of the structural unit having a polyether structure and the dimethylsilyloxy structural unit in the silicone polymer represented by the formula (7b) may be a block type or a random type. Moreover, when y1 is an integer greater than or equal to 2, the structural unit which has the polyether structure enclosed by the parenthesis to which y1 was attached
- the silicone polymer represented by the above formula (7c) is a polydimethylsiloxane long-chain alkyl-modified product (polymethylalkylsiloxane) in which a side chain of polydimethylsiloxane has an alkyl group that is longer than a methyl group. It is.
- R 12 in the formula (7c) represents a linear or branched alkyl group having 2 or more carbon atoms.
- y2 (the number of repeating methylalkylsilyloxy structural units) is not particularly limited, but is preferably 2 to 3000, more preferably 3 to 1500.
- x3 (the number of repeating dimethylsilyloxy structural units) is not particularly limited, but is preferably 0 to 3000, and more preferably 2 to 1500.
- the addition form of the methylalkylsilyloxy structural unit and the dimethylsilyloxy structural unit in the silicone polymer represented by the formula (7c) may be a block type or a random type.
- the methylalkylsilyloxy structural units surrounded by parentheses with y2 may be the same or different.
- the silicone polymer represented by the above formula (7d) is an aralkyl modified product of polydimethylsiloxane in which an aralkyl group is introduced into the side chain of polydimethylsiloxane.
- M2 the number of repeating methylene structural units in the formula (7d) is not particularly limited, but can be appropriately selected from a range of 1 to 30, for example.
- y3 the number of repeating methylaralkylsilyloxy structural units
- x4 (the number of repeating dimethylsilyloxy structural units) is not particularly limited, but is preferably 0 to 3000, and more preferably 2 to 1500.
- the addition form of the methylaralkylsilyloxy structural unit and the dimethylsilyloxy structural unit in the silicone polymer represented by the formula (7d) may be a block type or a random type.
- the methylaralkylsilyloxy structural units enclosed in parentheses with y3 may be the same or different.
- the silicone-based polymer represented by the above formula (7e) is a polyester-modified polydimethylsiloxane in which a polyester structure is introduced into the side chain of polydimethylsiloxane.
- R 13 and R 14 in formula (7e) are the same or different and each represents a divalent organic group (for example, a divalent hydrocarbon group).
- R 15 represents a hydrogen atom or a linear or branched alkyl group which may have a substituent.
- R 15 include the substituents exemplified in R 8 above.
- M3 (the number of repeating methylene structural units) in the formula (7e) is not particularly limited, but can be appropriately selected from a range of 1 to 30, for example.
- n2 (the number of repetitions of the condensation structure of polyol and polycarboxylic acid) is not particularly limited, but can be appropriately selected from the range of 2 to 3000, for example.
- y4 (the number of repeating structural units including a polyester structure (polyester side chain)) in the formula (7e) is not particularly limited, but is preferably 1 to 3000, and more preferably 3 to 1500.
- x5 (the number of repeating dimethylsilyloxy structural units) is not particularly limited, but is preferably 2 to 3000, and more preferably 3 to 1500.
- the addition form of the structural unit having a polyester structure and the dimethylsilyloxy structural unit in the silicone-based polymer represented by the formula (7e) may be a block type or a random type.
- y4 is an integer greater than or equal to 2
- subjected may be the same respectively, and may differ.
- the silicone polymer can be obtained by a known or conventional production method, and the production method is not particularly limited.
- a monomer having a structure corresponding to the structural unit represented by the formula (7) is polymerized.
- a compound having a predetermined structure for example, a compound having a polyether structure or a polyester structure
- the reactive group of the silicone polymer polydimethylsiloxane, etc.
- It can be produced by a method of reacting and bonding.
- a commercial item can also be used as said silicone type polymer.
- the fluorine-based leveling agent is a leveling agent containing a compound having a fluorinated alkyl group in which some or all of the hydrogen atoms of the alkyl group are substituted with fluorine atoms.
- the fluorine leveling agent may be a known or conventional fluorine leveling agent, and is not particularly limited.
- the fluorine leveling agent is preferably a leveling agent containing at least the fluorine-containing acrylic polymer or a leveling agent containing at least the fluorine-containing polyether polymer.
- R 16 in the above formula (8) is a hydrogen atom, a fluorine atom, or a linear or branched alkyl group having 1 to 4 carbon atoms in which part or all of the hydrogen atoms may be substituted with fluorine atoms.
- R 17 in the above formula (8) represents a fluorinated alkyl group (an alkyl group in which some or all of the hydrogen atoms are substituted with fluorine atoms).
- the fluorinated alkyl group is not particularly limited, and examples thereof include a difluoromethyl group, a 2,2-difluoroethyl group, a 2,2,2-trifluoroethyl group, and a 2,2,3,3-tetrafluoropropyl group.
- the fluorine-containing acrylic polymer may be a polymer having only the structural unit represented by the formula (8) as the repeating structural unit, or other than the structural unit represented by the formula (8). It may be a polymer having a structural unit.
- the fluorine-containing acrylic polymer may be a polymer having only one type of structural unit represented by formula (8), or may have two or more types of structural units represented by formula (8). It may be a polymer.
- the polymer which has 2 or more types of structural units other than the structural unit represented by Formula (8) may be sufficient.
- the structural unit other than the structural unit represented by the formula (8), which the fluorine-containing acrylic polymer may have, is not particularly limited and is a monomer component (monomer component) of the acrylic polymer. And structural units derived from known or commonly used monomers.
- fluorine-containing acrylic polymer examples include a fluorine-containing acrylic polymer represented by the following formula (8a).
- R 18 in formula (8a) represents a hydrogen atom or a methyl group.
- R 19 represents a linear or branched alkyl group.
- the linear or branched alkyl group is not particularly limited. For example, methyl group, ethyl group, propyl group, isopropyl group, butyl group (n-butyl group), isobutyl group, s-butyl group, t -Linear or branched alkyl groups having 1 to 30 carbon atoms such as butyl group and pentyl group.
- r, s, and t each represent an integer of 1 to 3000.
- R 24 in the above formula (9) represents a trivalent linear or branched hydrocarbon group.
- the trivalent linear or branched hydrocarbon group include methane, ethane, propane, n-butane, isobutane, n-pentane, n-hexane, 2-methylpentane, 3-methylpentane, and heptane.
- groups obtained by removing three hydrogen atoms from a linear or branched alkane such as 2-methylheptane, 3-methylheptane, octane, nonane and decane.
- a group (alkane-triyl group) obtained by removing three hydrogen atoms from a linear or branched alkane having 1 to 10 carbon atoms is preferable.
- R 25 in the above formula (9) represents a fluorinated alkyl group.
- the fluorinated alkyl group may be any alkyl group in which some or all of the hydrogen atoms are substituted with fluorine atoms, and is not particularly limited. Examples thereof include those exemplified as R 17 in the above formula (8). Can be mentioned.
- R 25 an alkyl group in which a part of hydrogen atoms is substituted with a fluorine atom is preferable.
- Z in the above formula (9) represents an integer of 1 to 30. Among these, an integer of 1 to 10 is preferable.
- the fluorine-containing polyether polymer may be a polymer having only the structural unit represented by the formula (9) as a repeating structural unit, or other than the structural unit represented by the formula (9).
- the polymer which has the following structural unit may be sufficient.
- the fluorine-containing polyether polymer may be a polymer having only one type of structural unit represented by the formula (9), or two or more types of structural units represented by the formula (9). It may be a polymer.
- the polymer which has 2 or more types of structural units other than the structural unit represented by Formula (9) may be sufficient.
- the structural unit other than the structural unit represented by the formula (9) that the fluorine-containing polyether polymer may have is not particularly limited, and for example, an oxyethylene unit [—OCH 2 CH 2 — And oxyalkylene structural units such as oxypropylene units [—CH (CH 3 ) CH 2 O—].
- R 26 in the following formula represents a hydrogen atom or a linear or branched alkyl group having 1 to 4 carbon atoms (for example, methyl group, ethyl group, propyl group, n-butyl group, etc.).
- R 25 and z in the following formula are the same as described above.
- fluorine-containing polyether polymer examples include a fluorine-containing polyether polymer represented by the following formula (9a).
- U, v, and w in the formula (9a) each represent an integer of 1 to 50.
- the total of u and w is preferably an integer of 2 to 80, more preferably an integer of 4 to 30, and still more preferably an integer of 6 to 14.
- v is preferably an integer of 2 to 50, more preferably an integer of 5 to 20.
- the fluorine-containing polyether polymer can be obtained by a known or conventional production method, and the production method is not particularly limited.
- a monomer that gives a structural unit represented by the formula (9) by polymerization For example, it can be produced by a method of polymerizing (for example, ring-opening polymerization) of a cyclic ether compound such as an epoxy compound or an oxetane compound.
- a commercial item can also be used as the said fluorine-containing polyether type polymer.
- the non-volatile content (blending amount) of the leveling agent in the curable epoxy resin composition of the present invention is not particularly limited, but the total amount of the compound having an epoxy group contained in the curable epoxy resin composition (100 parts by weight) ) Is preferably 0.1 to 10 parts by weight, more preferably 0.1 to 5 parts by weight, still more preferably 0.1 to 4 parts by weight. If the content of the leveling agent is less than 0.1 parts by weight, the crack resistance of the cured product may be lowered. On the other hand, when the compounding amount of the leveling agent exceeds 10 parts by weight, the transparency and heat resistance of the cured product may be deteriorated.
- the content (blending amount) of the silicone polymer, the fluorinated acrylic polymer, and the fluorinated polyether polymer is not particularly limited.
- the amount is preferably 0.1 to 10 parts by weight, more preferably 0.1 to 5 parts by weight, still more preferably based on the total amount (100 parts by weight) of the epoxy group-containing compound contained in the curable epoxy resin composition. 0.1 to 4 parts by weight. If the content of the silicone polymer, the fluorinated acrylic polymer, and the fluorinated polyether polymer is less than 0.1 parts by weight, the crack resistance of the cured product may be lowered.
- the “content (blending amount) of the silicone polymer, fluorine-containing acrylic polymer, and fluorine-containing polyether polymer” refers to the silicone polymer, fluorine-containing acrylic polymer, and fluorine-containing polymer. When two or more kinds of ether polymers are included, it means the total of these contents (total content).
- the optical semiconductor device obtained by sealing the optical semiconductor element with the cured product of the resin composition has excellent heat resistance.
- it exhibits crack resistance and suppresses a decrease in light intensity over time (particularly, a decrease in light intensity of an optical semiconductor device that emits high-luminance light).
- Such an effect is due to the improved adhesion of the curable epoxy resin composition (or cured product thereof) of the present invention to an optical semiconductor element or a package material (for example, a reflector material) by the incorporation of a leveling agent. It is guessed.
- the curable epoxy resin composition of the present invention preferably further contains a polyol compound.
- the curable epoxy resin composition of the present invention can form a cured product having higher heat resistance and crack resistance by containing the polyol compound, and an optical semiconductor device produced using the cured product is It is even less likely to cause a decrease in light intensity.
- the polyol compound is a polymer (oligomer or polymer) having a number average molecular weight of 200 or more having two or more hydroxyl groups in the molecule (in one molecule), such as polyether polyol, polyester polyol, polycarbonate polyol, etc. Is included.
- the said polyol compound can be used individually or in combination of 2 or more types.
- the hydroxyl group (two or more hydroxyl groups) of the polyol compound may be an alcoholic hydroxyl group or a phenolic hydroxyl group. Further, the number of hydroxyl groups (number of hydroxyl groups in one molecule) of the polyol compound is not particularly limited as long as it is 2 or more.
- the position of the hydroxyl group (two or more hydroxyl groups) of the polyol compound is not particularly limited, but it is preferably present at least at the end of the polyol (end of the polymer main chain) from the viewpoint of reactivity with the curing agent. It is particularly preferable that it is present at least at both ends of the polyol.
- the polyol compound may be a solid or liquid as long as it can form a liquid curable epoxy resin composition after blending with other components.
- the number average molecular weight of the polyol compound may be 200 or more and is not particularly limited, but is preferably 200 to 100,000, more preferably 300 to 50,000, and still more preferably 400 to 40,000. If the number average molecular weight is less than 200, peeling or cracking may occur when the solder reflow process is performed. On the other hand, when the number average molecular weight exceeds 100,000, the liquid curable epoxy resin composition may not be precipitated or dissolved.
- the number average molecular weight of the said polyol compound means the number average molecular weight of standard polystyrene conversion measured by gel permeation chromatography (GPC).
- polystyrene resin examples include a polyester polyol (including a polyester polyol oligomer) having an ester skeleton (polyester skeleton) in the molecule, and a polyether polyol (polyether polyol oligomer) having an ether skeleton (polyether skeleton) in the molecule. And a polycarbonate polyol (including a polycarbonate polyol oligomer) having a carbonate skeleton (polycarbonate skeleton) in the molecule.
- polyol compound include a phenoxy resin and an epoxy equivalent of 1000 g / eq. Also included are bisphenol-type polymer epoxy resins exceeding the above, polybutadienes having a hydroxyl group, acrylic polyols, and the like.
- polyester polyol examples include polyester polyols obtained by condensation polymerization (for example, transesterification) of polyols, polycarboxylic acids (polybasic acids), and hydroxycarboxylic acids, and polyester polyols obtained by ring-opening polymerization of lactones. Etc.
- polyol examples include ethylene glycol, diethylene glycol, 1,2-propanediol, 2-methyl-1,3-propanediol, 1,3-propanediol, 1,4- Butanediol, 1,3-butanediol, 2,3-butanediol, 1,5-pentanediol, 2-methyl-1,5-pentanediol, 3-methyl-1,5-pentanediol, 2,3, 5-trimethyl-1,5-pentanediol, 1,6-hexanediol, 2-ethyl-1,6-hexanediol, 2,2,4-trimethyl-1,6-hexanediol, 2,6-hexanediol 1,8-octanediol, 1,4-cyclohexanedimethanol, 1,2-dimethylol Rhohexane
- Examples of the polycarboxylic acid as a monomer component constituting the polyester polyol include oxalic acid, adipic acid, sebacic acid, fumaric acid, malonic acid, succinic acid, glutaric acid, azelaic acid, citric acid, and 2,6-naphthalene.
- Examples include merit acid and trimellitic anhydride.
- Examples of the hydroxycarboxylic acid include lactic acid, malic acid, glycolic acid, dimethylolpropionic acid, and dimethylolbutanoic acid.
- Examples of the lactones include ⁇ -caprolactone, ⁇ -valerolactone, ⁇ -butyrolactone, and the like.
- the polyester polyol can be produced by a known or conventional production method, and is not particularly limited. For example, condensation polymerization of the polyol and polycarboxylic acid, condensation polymerization of the hydroxycarboxylic acid, and ring-opening polymerization of the lactones. Etc. can be manufactured.
- the conditions for the polymerization are not particularly limited, and can be appropriately selected from known or common reaction conditions.
- the polyol, polycarboxylic acid, and hydroxycarboxylic acid are known or commonly used derivatives (for example, a hydroxyl group is protected with an acyl group, an alkoxycarbonyl group, an organic silyl group, an alkoxyalkyl group, an oxacycloalkyl group, etc. Derivatives and derivatives in which the carboxyl group is derived from an alkyl ester, an acid anhydride, an oxide halide, or the like can also be used.
- polyester polyol examples include, for example, trade names "Placcel 205", “Placcel 205H”, “Placcel 205U”, “Placcel 205BA”, “Placcel 208", "Placcel 210", “Placcel 210CP”, “Placcel 210BA”, “Placcel 212”, “Plaxel 212CP”, “Plaxel 220”, “Plaxel 220CPB”, “Plaxel 220NP1”, “Plaxel 220BA”, “Plaxel 220ED”, “Plaxel 220EB”, “Plaxel 220EC”, “Plaxel 230”, “Plaxel 230CP”, “Plaxel 240”, “Plaxel 240CP”, “Plaxel 210N”, “Plaxel 220N”, “Plaxel L205AL”, “Plaxel L208” L, Plaxel L212AL, Plaxel L220AL, Plaxel L230AL, Plaxel 305, Plaxe
- polyether polyol examples include polyether polyols obtained by addition reaction of cyclic ether compounds to polyols, polyether polyols obtained by ring-opening polymerization of alkylene oxide, and the like.
- examples of the polyether polyol include ethylene glycol, diethylene glycol, 1,2-propanediol (propylene glycol), 2-methyl-1,3-propanediol, 1,3-propanediol, , 4-butanediol (tetramethylene glycol), 1,3-butanediol, 2,3-butanediol, 1,5-pentanediol, 2-methyl-1,5-pentanediol, 3-methyl-1,5 -Pentanediol, 2,3,5-trimethyl-1,5-pentanediol, 1,6-hexanediol, 2-ethyl-1,6-hexanediol, 2,2,4-trimethyl-1,6-hexane Diol, 2,6-hexanediol, 1,8-octanediol, 1,4-cyclohexanedimethano 1,2-diol
- the polyether polyol can be produced by a known or conventional production method, and is not particularly limited. For example, addition reaction of a cyclic ether compound to a polyol (ring-opening addition polymerization), ring-opening polymerization of an alkylene oxide ( (Homopolymerization or copolymerization).
- the conditions for the polymerization are not particularly limited, and can be appropriately selected from known or common reaction conditions.
- polyether polyol examples include trade name “PEP-101” (manufactured by Freund Sangyo Co., Ltd.), trade names “Adeka Pluronic L”, “Adeka Pluronic P”, “Adeka Pluronic F”, “Adeka Pluronic R”.
- the above polycarbonate polyol is a polycarbonate having two or more hydroxyl groups in the molecule.
- the polycarbonate polyol is preferably a polycarbonate diol having two terminal hydroxyl groups in the molecule.
- the polycarbonate polyol is prepared by a phosgene method or a carbonate exchange reaction using a dialkyl carbonate such as dimethyl carbonate or diethyl carbonate or diphenyl carbonate (Japanese Patent Laid-Open No. 62-187725, Japanese Patent Laid-Open No. No. 2-175721, JP-A-2-49025, JP-A-3-220233, JP-A-3-252420 and the like. Since the carbonate bond in the polycarbonate polyol is difficult to be thermally decomposed, the cured resin containing the polycarbonate polyol exhibits excellent stability even under high temperature and high humidity.
- Examples of the polyol used in the carbonate exchange reaction together with the dialkyl carbonate or diphenyl carbonate include 1,6-hexanediol, ethylene glycol, diethylene glycol, 1,3-propanediol, 1,4-butanediol, and 1,3-butane.
- polycarbonate polyol examples include, for example, trade names “Placcel CD205PL”, “Plaxel CD205HL”, “Plaxel CD210PL”, “Plaxel CD210HL”, “Plaxel CD220PL”, “Plaxel CD220HL” (manufactured by Daicel Corporation) Names “UH-CARB50”, “UH-CARB100”, “UH-CARB300”, “UH-CARB90 (1/3)”, “UH-CARB90 (1/1)”, “UC-CARB100” (and above, Ube) Products manufactured by Kosan Co., Ltd.), trade names such as “PCDL T4671”, “PCDL T4672”, “PCDL T5650J”, “PCDL T5651”, “PCDL T5652” (above, manufactured by Asahi Kasei Chemicals) be able to
- polyols other than the above-described polyether polyol, polyester polyol, and polycarbonate polyol include, for example, trade names “YP-50”, “YP-50S”, “YP-55U”, “YP-70”, “ZX-1356-2.
- phenoxy resins such as Nippon Steel Chemical Co., Ltd., trade names “jER1256”, “jER4250”, “jER4275” (manufactured by Mitsubishi Chemical Corporation); trade names “Epototo YD-014”, “ Epototo YD-017, Epototo YD-019, Epototo YD-020G, Epototo YD-904, “Epototo YD-907”, “Epototo YD-6020” (manufactured by Nippon Steel Chemical Co., Ltd.), trade names “jER1007”, “jER1009”, “jER1010”, “jER1005F”, “jER1009F”, “j
- the use amount (content) of the polyol compound is not particularly limited, but is 1 to 50 parts by weight with respect to the total amount (100 parts by weight) of the component (A), the component (B), and the component (C). More preferred is 1.5 to 40 parts by weight, still more preferred is 5 to 30 parts by weight.
- the content of the polyol compound exceeds 50 parts by weight, the Tg of the cured product is excessively lowered, the volume change due to heating is increased, and problems such as non-lighting of the optical semiconductor device may occur. Moreover, although bending strength improves, transparency may fall.
- the content of the polyol compound is less than 1 part by weight, the reflow resistance is lowered, and the heat treatment in the reflow process may cause peeling or cracking of the sealing resin from the lead frame in the optical semiconductor device. .
- the curable epoxy resin composition of the present invention preferably further contains an acrylic block copolymer. More specifically, when the curable epoxy resin composition of the present invention includes an acrylic block copolymer, an optical semiconductor device manufactured using the curable epoxy resin composition is particularly high in luminance and high output. Even if it exists, it exists in the tendency for a light intensity to fall easily. That is, by using the acrylic block copolymer, a cured product obtained by curing the curable epoxy resin composition of the present invention can exhibit higher levels of heat resistance, light resistance, and crack resistance.
- the acrylic block copolymer is a block copolymer containing an acrylic monomer as an essential monomer component.
- acrylic monomer examples include methyl acrylate, ethyl acrylate, n-butyl acrylate, t-butyl acrylate, 2-ethylhexyl acrylate, methyl methacrylate, ethyl methacrylate, n-butyl methacrylate, methacrylic acid.
- (Meth) acrylic acid alkyl esters such as t-butyl acid, 2-ethylhexyl methacrylate, lauryl methacrylate and stearyl methacrylate; (meth) acrylic acid esters having an alicyclic structure such as cyclohexyl acrylate and cyclohexyl methacrylate; methacryl (Meth) acrylic acid ester having an aromatic ring such as benzyl acid; (fluoro) alkyl ester of (meth) acrylic acid such as 2-trifluoroethyl methacrylate; acrylic acid, methacrylic acid, maleic acid, maleic anhydride, etc.
- a monomer other than the acrylic monomer may be used as a monomer component.
- the monomer other than the acrylic monomer include aromatic vinyl compounds such as styrene and ⁇ -methylstyrene, conjugated dienes such as butadiene and isoprene, and olefins such as ethylene, propylene and isobutene.
- acrylic block copolymer for example, the diblock copolymer which consists of two polymer blocks, the triblock copolymer which consists of three polymer blocks, four or more polymer blocks And a multi-block copolymer composed of these.
- the acrylic block copolymer from the viewpoint of improving heat resistance, light resistance, and crack resistance, a polymer block (S) (soft block) having a low glass transition temperature (Tg) and a polymer block ( A block copolymer in which polymer blocks (H) (hard blocks) having a higher Tg than S) are alternately arranged is preferred, more preferably a polymer block (S) in the middle and a polymer at both ends thereof. A triblock copolymer having an HSH structure having a block (H) is preferred.
- Tg of the polymer which comprises the polymer block (S) of the said acrylic block copolymer is not specifically limited, Less than 30 degreeC is preferable.
- Tg of the polymer which comprises a polymer block (H) is although it does not specifically limit, 30 degreeC or more is preferable.
- each polymer block (H) may have the same composition and may differ.
- each polymer block (S) may have the same composition and may differ.
- the monomer component constituting the polymer block (H) in the acrylic block copolymer is not particularly limited.
- the Tg of the homopolymer is examples thereof include monomers having a temperature of 30 ° C. or higher, and more specifically, methyl methacrylate, styrene, acrylamide, acrylonitrile and the like.
- the monomer component constituting the polymer block (S) in the acrylic block copolymer is not particularly limited, and examples thereof include monomers having a Tg of a homopolymer of less than 30 ° C., and more specifically, Acrylic acid C 2-10 alkyl ester such as butyl acrylate and 2-ethylhexyl acrylate, butadiene (1,4-butadiene) and the like.
- the polymer block (S) is a polymer composed of butyl acrylate (BA) as a main monomer, A polymethyl methacrylate-block-polybutyl acrylate-block-polymethyl methacrylate terpolymer (PMMA-b-PBA-b-), in which the polymer block (H) is a polymer composed mainly of methyl methacrylate (MMA). PMMA) and the like.
- BA butyl acrylate
- PMMA-b-PBA-b-PMMA A polymethyl methacrylate-block-polybutyl acrylate-block-polymethyl methacrylate terpolymer
- H polymer composed mainly of methyl methacrylate
- PMMA methyl methacrylate
- the PMMA-b-PBA-b-PMMA is a hydrophilic group (for example, a hydroxyl group, a carboxyl group, an amino group, etc.) for the purpose of improving compatibility with the component (A) and the component (B), if necessary.
- a monomer having a group for example, hydroxyethyl (meth) acrylate, hydroxypropyl (meth) acrylate, (meth) acrylic acid, or the like, copolymerized with a PMMA block and / or a PBA block. Good.
- the number average molecular weight of the acrylic block copolymer is not particularly limited, but is preferably 3000 to 500000, more preferably 30000 to 400000. If the number average molecular weight is less than 3000, the toughness of the cured product is not sufficient, and crack resistance may be reduced. On the other hand, when the number average molecular weight exceeds 500,000, the compatibility with the alicyclic epoxy compound (A) is lowered, and the transparency of the cured product may be lowered.
- the acrylic block copolymer can be produced by a known or commonly used block copolymer production method.
- the method for producing the acrylic block copolymer in particular, living polymerization (living radical polymerization, living anion polymerization, living room polymerization, etc., from the viewpoint of easy control of the molecular weight, molecular weight distribution, terminal structure, etc. of the acrylic block copolymer. Cationic polymerization etc.) are preferred.
- the living polymerization can be carried out by a known or conventional method.
- acrylic block copolymer examples include, for example, trade names “Nano Strength M52N”, “Nano Strength M22N”, “Nano Strength M51”, “Nano Strength M52”, “Nano Strength M53” (manufactured by Arkema, PMMA- Commercial products such as “b-PBA-b-PMMA”, trade names “Nanostrength E21”, “Nanostrength E41” (manufactured by Arkema, PSt (polystyrene) -b-PBA-b-PMMA) can also be used.
- usage-amount (content) of the said acrylic block copolymer It is 1 with respect to the total amount (100 weight part) of the said component (A), a component (B), and a component (C). Is preferably 30 to 30 parts by weight, more preferably 3 to 15 parts by weight, and still more preferably 5 to 10 parts by weight.
- usage-amount of an acrylic block copolymer is less than 1 weight part, the toughness of hardened
- the usage-amount of an acrylic block copolymer exceeds 30 weight part compatibility with an alicyclic epoxy compound (A) may fall, and transparency of hardened
- the curable epoxy resin composition of the present invention may further contain rubber particles.
- the rubber particles include rubber particles such as particulate NBR (acrylonitrile-butadiene rubber), reactive terminal carboxyl group NBR (CTBN), metal-free NBR, and particulate SBR (styrene-butadiene rubber).
- the rubber particles are preferably rubber particles having a multilayer structure (core-shell structure) composed of a core portion having rubber elasticity and at least one shell layer covering the core portion.
- the rubber particles are particularly composed of a polymer (polymer) having (meth) acrylic acid ester as an essential monomer component, and react with a compound having an epoxy group such as an alicyclic epoxy compound (A) on the surface.
- Rubber particles having a hydroxyl group and / or a carboxyl group (either one or both of a hydroxyl group and a carboxyl group) as the functional group to be obtained are preferred.
- the cured product becomes clouded by a thermal shock such as a cold cycle and the transparency is lowered, which is not preferable.
- the polymer constituting the core portion having rubber elasticity in the rubber particles is not particularly limited, but (meth) acrylic acid esters such as methyl (meth) acrylate, ethyl (meth) acrylate, and butyl (meth) acrylate are used.
- the essential monomer component is preferred.
- examples of the polymer constituting the core portion having rubber elasticity include other aromatic vinyls such as styrene and ⁇ -methylstyrene, nitriles such as acrylonitrile and methacrylonitrile, conjugated dienes such as butadiene and isoprene, ethylene, propylene, Isobutene or the like may be contained as a monomer component.
- the polymer which comprises the said core part which has the rubber elasticity contains 1 type, or 2 or more types selected from the group which consists of aromatic vinyl, a nitrile, and a conjugated diene with a (meth) acrylic acid ester as a monomer component. It is preferable to include it in combination. That is, as the polymer constituting the core part, for example, (meth) acrylic acid ester / aromatic vinyl, (meth) acrylic acid ester / conjugated diene and other binary copolymers; (meth) acrylic acid ester / aromatic And terpolymers such as group vinyl / conjugated dienes.
- the polymer constituting the core part may contain silicone such as polydimethylsiloxane and polyphenylmethylsiloxane, polyurethane, and the like.
- the polymer constituting the core part includes, as other monomer components, divinylbenzene, allyl (meth) acrylate, ethylene glycol di (meth) acrylate, diallyl maleate, triallyl cyanurate, diallyl phthalate, butylene glycol diacrylate, etc.
- One monomer (one molecule) may contain a reactive crosslinking monomer having two or more reactive functional groups.
- the core part of the rubber particles is a core part composed of a (meth) acrylic ester / aromatic vinyl binary copolymer (particularly butyl acrylate / styrene). It is preferable in that the rate can be easily adjusted.
- the core portion of the rubber particles can be manufactured by a commonly used method, for example, by a method of polymerizing the monomer by an emulsion polymerization method.
- the whole amount of the monomer may be charged at once and may be polymerized, or after polymerizing a part of the monomer, the remainder may be added continuously or intermittently to polymerize,
- a polymerization method using seed particles may be used.
- the polymer constituting the shell layer of the rubber particles is preferably a polymer different from the polymer constituting the core portion.
- the shell layer preferably has a hydroxyl group and / or a carboxyl group as a functional group capable of reacting with a compound having an epoxy group such as the alicyclic epoxy compound (A).
- the polymer constituting the shell layer preferably contains a (meth) acrylate ester such as methyl (meth) acrylate, ethyl (meth) acrylate, butyl (meth) acrylate as an essential monomer component.
- a (meth) acrylate ester such as methyl (meth) acrylate, ethyl (meth) acrylate, butyl (meth) acrylate as an essential monomer component.
- a (meth) acrylate ester such as methyl (meth) acrylate, ethyl (meth) acrylate, butyl (meth) acrylate as an essential monomer component.
- a (meth) acrylate ester such as methyl (meth) acrylate, ethyl (meth) acrylate, butyl (meth) acrylate
- an essential monomer component for example, when butyl acrylate is used as the (meth) acrylic acid ester in the core
- Examples of monomer components that may be contained in addition to (meth) acrylic acid esters include aromatic vinyls (aromatic vinyl compounds) such as styrene and ⁇ -methylstyrene, and nitriles such as acrylonitrile and methacrylonitrile. .
- aromatic vinyls aromatic vinyl compounds
- styrene and ⁇ -methylstyrene aromatic vinyl compounds
- nitriles such as acrylonitrile and methacrylonitrile.
- the rubber particles as a monomer component constituting the shell layer, it is preferable to contain the monomer alone or in combination of two or more together with (meth) acrylic acid ester, and in particular, to contain at least aromatic vinyl. Is preferable in that the refractive index of the rubber particles can be easily adjusted.
- the polymer constituting the shell layer forms a hydroxyl group and / or a carboxyl group as a functional group capable of reacting with a compound having an epoxy group such as an alicyclic epoxy compound (A) as a monomer component.
- a compound having an epoxy group such as an alicyclic epoxy compound (A) as a monomer component.
- Hydroxyalkyl (meth) acrylates such as 2-hydroxyethyl (meth) acrylate, ⁇ , ⁇ -unsaturated acids such as (meth) acrylic acid, ⁇ , ⁇ -unsaturated acid anhydrides such as maleic anhydride, etc. It is preferable to contain the monomer.
- the polymer constituting the shell layer in the rubber particles preferably contains one or more selected from the above monomers in combination with (meth) acrylic acid ester as a monomer component. That is, the shell layer is composed of, for example, a ternary copolymer such as (meth) acrylic acid ester / aromatic vinyl / hydroxyalkyl (meth) acrylate, (meth) acrylic acid ester / aromatic vinyl / ⁇ , ⁇ -unsaturated acid.
- a shell layer composed of a polymer or the like is preferable.
- the polymer constituting the shell layer includes, as the other monomer components, divinylbenzene, allyl (meth) acrylate, ethylene glycol di (meth) acrylate, diallyl maleate, trimethyl, as well as the above-described monomer.
- a reactive crosslinking monomer having two or more reactive functional groups may be contained in one monomer (one molecule) such as allyl cyanurate, diallyl phthalate, or butylene glycol diacrylate.
- the rubber particles can be obtained by covering the core portion with a shell layer.
- the method of coating the core part with a shell layer include a method of coating the surface of the core part having rubber elasticity obtained by the above method by applying a copolymer constituting the shell layer, and the above method Examples thereof include a graft polymerization method in which the core portion having rubber elasticity obtained by the above is used as a trunk component, and each component constituting the shell layer is used as a branch component.
- the average particle diameter of the rubber particles is not particularly limited, but is preferably 10 to 500 nm, more preferably 20 to 400 nm.
- the maximum particle size of the rubber particles is not particularly limited, but is preferably 50 to 1000 nm, more preferably 100 to 800 nm. If the average particle diameter exceeds 500 nm or the maximum particle diameter exceeds 1000 nm, the dispersibility of the rubber particles in the cured product may be reduced, and crack resistance may be reduced. On the other hand, if the average particle size is less than 10 nm or the maximum particle size is less than 50 nm, the effect of improving the crack resistance of the cured product may be difficult to obtain.
- the refractive index of the rubber particles is not particularly limited, but is preferably 1.40 to 1.60, more preferably 1.42 to 1.58.
- the difference between the refractive index of the rubber particles and the refractive index of the cured product obtained by curing the curable epoxy resin composition (the curable epoxy resin composition of the present invention) containing the rubber particles is ⁇ 0.03. Is preferably within. When the difference in refractive index exceeds ⁇ 0.03, the transparency of the cured product decreases, sometimes it becomes cloudy and the light intensity of the optical semiconductor device tends to decrease, and the function of the optical semiconductor device is lost. There is.
- the refractive index of the rubber particles is, for example, by casting 1 g of rubber particles into a mold and compression-molding at 210 ° C. and 4 MPa to obtain a flat plate having a thickness of 1 mm. And using a multi-wavelength Abbe refractometer (trade name “DR-M2”, manufactured by Atago Co., Ltd.) in a state where the prism and the test piece are in close contact using monobromonaphthalene as an intermediate solution, It can be determined by measuring the refractive index at 20 ° C. and sodium D line.
- DR-M2 multi-wavelength Abbe refractometer
- the refractive index of the cured product of the curable epoxy resin composition of the present invention is, for example, a test of 20 mm in length, 6 mm in width, and 1 mm in thickness from a cured product obtained by the heat curing method described in the section of the optical semiconductor device below.
- a multi-wavelength Abbe refractometer (trade name “DR-M2”, manufactured by Atago Co., Ltd.) is used with the prism and the test piece in close contact using monobromonaphthalene as an intermediate solution. It can be obtained by measuring the refractive index at 20 ° C. and sodium D line.
- the content (blending amount) of the rubber particles in the curable epoxy resin composition of the present invention is not particularly limited, but the total amount (100 parts by weight) of the compound having an epoxy group contained in the curable epoxy resin composition.
- the amount is preferably 0.5 to 30 parts by weight, more preferably 1 to 20 parts by weight.
- the content of the rubber particles is less than 0.5 parts by weight, the crack resistance of the cured product tends to decrease.
- the content of the rubber particles exceeds 30 parts by weight, the heat resistance of the cured product tends to decrease.
- the curable epoxy resin composition of the present invention can use various additives within a range that does not impair the effects of the present invention.
- a compound having a hydroxyl group such as ethylene glycol, diethylene glycol, propylene glycol, or glycerin
- the reaction can be allowed to proceed slowly.
- silane coupling agents such as ⁇ -glycidoxypropyltrimethoxysilane, surfactants, inorganic fillers such as silica and alumina, flame retardants, colorants, etc., within a range that does not impair the viscosity and transparency.
- Conventional additives such as an antioxidant, an ultraviolet absorber, an ion adsorbent, a pigment, a phosphor, and a release agent can be used.
- the curable epoxy resin composition of the present invention comprises the above-described alicyclic epoxy compound (A), monoallyl diglycidyl isocyanurate compound (B), and siloxane derivative (C) having two or more epoxy groups in the molecule. And an alicyclic polyester resin (D), a curing agent (E) and a curing accelerator (G), or a curing catalyst (F) may be included, and the preparation method thereof is not particularly limited.
- an ⁇ -containing compound having an epoxy group as an essential component such as an alicyclic epoxy compound (A), a monoallyl diglycidyl isocyanurate compound (B), or a siloxane derivative (C) having two or more epoxy groups in the molecule
- the agent and the ⁇ agent containing the curing agent (E) and the curing accelerator (G) or the curing catalyst (F) as essential components are separately prepared, and the ⁇ agent and the ⁇ agent are stirred at a predetermined ratio.
- -It can prepare by the method of mixing and defoaming under vacuum as needed.
- the alicyclic polyester resin (D) may be preliminarily mixed (blended) as a component of the ⁇ agent and / or the ⁇ agent, or when the ⁇ agent and the ⁇ agent are mixed, You may mix
- the alicyclic polyester resin (D) and the curing agent (E) are mixed in advance to obtain these mixtures (a mixture of the alicyclic polyester resin (D) and the curing agent (E)), and then the curing accelerator (G) and other additives are blended into the mixture. It is preferable to prepare by preparing an agent and subsequently mixing the ⁇ agent and the ⁇ agent.
- the temperature at which the alicyclic polyester resin (D) and the curing agent (E) are mixed is not particularly limited, but is preferably 60 to 130 ° C, more preferably 90 to 120 ° C.
- the mixing time is not particularly limited, but is preferably 30 to 100 minutes, and more preferably 45 to 80 minutes. Although mixing is not specifically limited, It is preferable to carry out in nitrogen atmosphere. Moreover, the above-mentioned well-known apparatus can be used for mixing.
- the heating temperature (curing temperature) at the time of curing is not particularly limited, but is preferably 45 to 200 ° C, more preferably 100 to 190 ° C, still more preferably 100 to 180 ° C. Further, the heating time (curing time) for curing is not particularly limited, but is preferably 30 to 600 minutes, more preferably 45 to 540 minutes, and further preferably 60 to 480 minutes. If the curing temperature is too low and / or if the curing time is too short, curing may be insufficient.
- the curing conditions depend on various conditions, but can be appropriately adjusted by shortening the curing time when the curing temperature is increased, and increasing the curing time when the curing temperature is lowered.
- the resin composition for optical semiconductor encapsulation of the present invention comprises the curable epoxy resin composition of the present invention.
- the resin composition for sealing an optical semiconductor of the present invention the optical semiconductor element is sealed with a cured product having excellent physical properties such as transparency, heat resistance, light resistance, and crack resistance.
- An optical semiconductor device that does not easily deteriorate with time can be obtained.
- the optical semiconductor device is less likely to decrease in light intensity over time even when it includes an optical semiconductor element with high output and high brightness.
- the optical semiconductor device of the present invention is obtained by sealing an optical semiconductor element with the curable epoxy resin composition (resin composition for optical semiconductor sealing) of the present invention.
- the optical semiconductor element is sealed by injecting a curable epoxy resin composition into a predetermined mold and heat-curing under predetermined conditions. Thereby, an optical semiconductor device in which the optical semiconductor element is sealed with the curable epoxy resin composition is obtained.
- the curing temperature and the curing time at the time of sealing for example, the same conditions as in forming the cured product can be employed.
- the curable epoxy resin composition of the present invention is not limited to the above-mentioned optical semiconductor element sealing application (for optical semiconductor sealing).
- an adhesive for optical semiconductor sealing
- an electrical insulating material for electrical insulating material
- a laminate for optical semiconductor sealing
- a coating for ink
- a paint for example, an adhesive, an electrical insulating material, a laminate, a coating, an ink, a paint
- Applications such as sealants, resists, composite materials, transparent substrates, transparent sheets, transparent films, optical elements, optical lenses, optical members, stereolithography, electronic paper, touch panels, solar cell substrates, optical waveguides, light guide plates, holographic memories, etc.
- sealants for sealants, resists, composite materials, transparent substrates, transparent sheets, transparent films, optical elements, optical lenses, optical members, stereolithography, electronic paper, touch panels, solar cell substrates, optical waveguides, light guide plates, holographic memories, etc.
- sealants for sealants, resists, composite materials, transparent substrates, transparent sheets, transparent
- silicone leveling agent (“BYK-300”, “AC FS 180”) and fluorine leveling agent (“BYK-340”, “AC 110a”) in Tables 2 and 3 Indicates the quantity (the quantity of the product itself).
- Production Example 1 (Production of epoxy resin: Examples 1 to 12, Comparative Examples 1 to 6) Monoallyl diglycidyl isocyanurate (trade name “MA-DGIC”, Shikoku Kasei Kogyo Co., Ltd.), alicyclic epoxy compound (trade name “Celoxide 2021P”, manufactured by Daicel Corporation; trade name “EHPE3150”, Co., Ltd.
- Production Example 2 (Production of a curing agent composition containing at least a curing agent (hereinafter referred to as “K agent”): Examples 1 to 12 and Comparative Examples 1 to 6) Curing agent (acid anhydride) (trade name “Licacid MH-700”, manufactured by Hitachi Chemical Co., Ltd.), a mixture of curing agent (acid anhydride) and alicyclic polyester resin (trade name “HN-7200”, Hitachi Chemical Co., Ltd.), a mixture of curing agent (anhydride) and alicyclic polyester resin (trade name “HN-5700”, manufactured by Hitachi Chemical Co., Ltd.), curing accelerator (trade name “U” -CAT 18X ", manufactured by San Apro Co., Ltd.), additives (trade name” Ethylene Glycol ", manufactured by Wako Pure Chemical Industries, Ltd.) according to the formulation (mixing ratio) shown in Table 1 (Trade name “Awatori Nertaro AR-250”, manufactured by Shinky Co., Ltd.) was mixed uniform
- Examples 1-12, Comparative Examples 1-6 Manufacture of curable epoxy resin composition
- the epoxy resin obtained in Production Example 1 and the K agent obtained in Production Example 2 were mixed with a self-revolving stirrer (trade name “Awatori Kneading” so that the formulation (unit: parts by weight) shown in Table 1 was obtained.
- Taro AR-250 "(manufactured by Shinky Co., Ltd.) was mixed uniformly and defoamed to obtain a curable epoxy resin composition.
- the curable epoxy resin composition obtained above is cast into a lead frame (InGaN element, 3.5 mm ⁇ 2.8 mm) of an optical semiconductor shown in FIG. 1, and then 5 in a 120 ° C. oven (resin curing oven).
- An optical semiconductor device in which the optical semiconductor element was sealed with a cured resin (cured product) heated for a time was obtained.
- 100 is a reflector (light reflecting resin composition)
- 101 is a metal wiring
- 102 is an optical semiconductor element
- 103 is a bonding wire
- 104 is a transparent sealing resin (cured product).
- Production Example 3 Manufacture of rubber particles
- 500 g of ion-exchanged water and 0.68 g of sodium dioctylsulfosuccinate were charged, and the temperature was raised to 80 ° C. while stirring under a nitrogen stream.
- a monomer mixture consisting of 9.5 g of butyl acrylate, 2.57 g of styrene, and 0.39 g of divinylbenzene corresponding to about 5% by weight of the amount required to form the core portion is added here.
- the obtained latex was frozen at minus 30 ° C., dehydrated and washed with a suction filter, and then blown and dried at 60 ° C. overnight to obtain rubber particles.
- the resulting rubber particles had an average particle size of 254 nm and a maximum particle size of 486 nm.
- the average particle size and the maximum particle size of the rubber particles are determined based on a nanotrac TM particle size distribution measuring device (trade name “UPA-EX150”, manufactured by Nikkiso Co., Ltd.) using the dynamic light scattering method as a measurement principle. ) Is used to measure the following sample, and in the obtained particle size distribution curve, the average particle size, which is the particle size when the cumulative curve becomes 50%, is the average particle size, and the frequency (%) of the particle size distribution measurement result is The maximum particle size at the time when it exceeded 0.00% was defined as the maximum particle size.
- a sample obtained by dispersing 1 part by weight of the rubber particle-dispersed epoxy compound obtained in Production Example 4 in 20 parts by weight of tetrahydrofuran was used as a sample.
- Production Example 4 Manufacture of rubber particle-dispersed epoxy compounds 10 parts by weight of the rubber particles obtained in Production Example 3 were heated to 60 ° C. under a nitrogen stream, and a dissolver (1000 rpm, 60 minutes) was used to prepare Celoxide 2021P (3,4-epoxycyclohexylmethyl (3 , 4-epoxy) cyclohexanecarboxylate (manufactured by Daicel Co., Ltd.) was dispersed in 56 parts by weight and vacuum degassed to obtain a rubber particle-dispersed epoxy compound (viscosity at 25 ° C .: 834 mPa ⁇ s).
- the viscosity (viscosity at 25 ° C.) of the rubber particle-dispersed epoxy compound (10 parts by weight of rubber particles dispersed in 56 parts by weight of Celoxide 2021P (manufactured by Daicel Corporation)) is a digital viscometer (trade name “ DVU-EII type "(manufactured by Tokimec Co., Ltd.).
- Production Example 6 (Production of K agent: Examples 13 to 28) Mixture of curing agent (acid anhydride) and alicyclic polyester resin (trade name “HN-7200”, manufactured by Hitachi Chemical Co., Ltd.), curing accelerator (trade name “U-CAT 18X”, San Apro Co., Ltd.) ) And additives (trade name “ethylene glycol”, manufactured by Wako Pure Chemical Industries, Ltd.) according to the formulation (mixing ratio) shown in Table 2, a self-revolving stirrer (trade name “Awatori Netaro AR” -250 ", manufactured by Shinkey Co., Ltd.), and mixed uniformly and degassed to obtain K agent.
- curing agent acid anhydride
- alicyclic polyester resin trade name “HN-7200”, manufactured by Hitachi Chemical Co., Ltd.
- curing accelerator trade name “U-CAT 18X”, San Apro Co., Ltd.
- additives trade name “ethylene glycol”, manufactured by Wako Pure Chemical Industries, Ltd.
- Examples 13 to 28 Manufacture of curable epoxy resin composition
- the epoxy resin obtained in Production Example 5 and the K agent obtained in Production Example 6 were mixed with a self-revolving stirrer (trade name “Awatori Kneading” so that the formulation shown in Table 2 (unit: parts by weight) was obtained.
- Taro AR-250 (manufactured by Shinky Co., Ltd.) was mixed uniformly and defoamed to obtain a curable epoxy resin composition.
- the curable epoxy resin composition obtained above is cast into a lead frame (InGaN element, 3.5 mm ⁇ 2.8 mm) of an optical semiconductor shown in FIG. 1, and then 5 in a 120 ° C. oven (resin curing oven). An optical semiconductor device in which the optical semiconductor element was sealed with a cured resin (cured product) heated for a time was obtained.
- Production Example 7 (Production of epoxy resin: Examples 29 to 43, Comparative Examples 7 to 11) Monoallyl diglycidyl isocyanurate (trade name “MA-DGIC”, Shikoku Kasei Kogyo Co., Ltd.), alicyclic epoxy compound (trade name “Celoxide 2021P”, manufactured by Daicel Corporation; trade name “EHPE3150”, Co., Ltd.
- Production Example 8 (Production of alicyclic polyester resin: Examples 29 to 43, Comparative Examples 9 to 11)
- a reaction vessel equipped with a stirrer, a thermometer and a reflux condenser 172 parts by weight of 1,4-cyclohexanedicarboxylic acid (manufactured by Tokyo Chemical Industry Co., Ltd.), 208 parts by weight of neopentyl glycol (manufactured by Tokyo Chemical Industry Co., Ltd.)
- 0.1 part by weight of tetrabutyl titanate (manufactured by Wako Pure Chemical Industries, Ltd.) was charged, heated to 160 ° C., and further heated from 160 ° C. to 250 ° C. over 4 hours.
- the pressure was reduced to 5 mmHg over 1 hour, further reduced to 0.3 mmHg or less, and then reacted at 250 ° C. for 1 hour to obtain an alicyclic polyester resin.
- Examples 29 to 43, Comparative Examples 7 to 11 Manufacture of curable epoxy resin composition
- a curable epoxy resin composition was obtained.
- the curable epoxy resin composition obtained above is cast into a lead frame (InGaN element, 3.5 mm ⁇ 2.8 mm) of an optical semiconductor shown in FIG. 1, and then 5 in a 120 ° C. oven (resin curing oven). An optical semiconductor device in which the optical semiconductor element was sealed with a cured resin (cured product) heated for a time was obtained.
- FIG. 2 shows an example of the surface temperature profile of the optical semiconductor device during heating in the reflow furnace (temperature profile in one of the two heating operations). Thereafter, the length of cracks generated in the sealing resin of the optical semiconductor device (cured product of the curable epoxy resin composition) was observed using a digital microscope (VHX-900, manufactured by Keyence Corporation), Of the two optical semiconductor devices, the number of optical semiconductor devices having cracks having a length of 90 ⁇ m or more was measured. The results are shown in the column of “Solder heat resistance test” in Tables 1 to 3.
- Thermal shock test The optical semiconductor devices obtained in Examples and Comparative Examples (two used for each curable epoxy resin composition) were exposed in an atmosphere of ⁇ 40 ° C. for 30 minutes, and then in an atmosphere of 100 ° C. A thermal shock with one cycle of exposure for 30 minutes was applied for 200 cycles using a thermal shock tester. Thereafter, the length of cracks generated in the sealing resin of the optical semiconductor device (cured product of the curable epoxy resin composition) was observed using a digital microscope (VHX-900, manufactured by Keyence Corporation), Of the two optical semiconductor devices, the number of optical semiconductor devices having cracks having a length of 90 ⁇ m or more was measured. The results are shown in the column of “thermal shock test” in Tables 1 to 3.
- Example and the comparative example is as follows.
- [Epoxy resin] CEL2021P (Celoxide 2021P): 3,4-epoxycyclohexylmethyl (3,4-epoxy) cyclohexanecarboxylate, manufactured by Daicel Corporation
- EHPE3150 1,2-epoxy of 2,2-bis (hydroxymethyl) -1-butanol -4- (2-oxiranyl) cyclohexene adduct, manufactured by Daicel Corporation
- MA-DGIC monoallyl diglycidyl isocyanurate, manufactured by Shikoku Kasei Kogyo Co., Ltd.
- X-40-2678 two epoxy groups in the molecule
- X-40-2720 Shin-Etsu Chemical Co., Ltd.
- X-40-2720 Siloxane derivative having 3 epoxy groups in the molecule
- X-E-40-2670 Shin-Etsu Chemical Co., Ltd .: 4 epoxies in the molecule Group-containing siloxane derivatives, manufactured by Shin-Etsu Chemical Co., Ltd.
- AC FS 180 Silicone type leveling agent, manufactured by Algin Chemie BYK-340: Fluorine type leveling agent, manufactured by Big Chemie Japan Co., Ltd.
- AC 110a Fluorine type leveling Agent, manufactured by Algin Chemie [Polyol compound] CD220PL (Placcel CD220PL): Polycarbonate diol, manufactured by Daicel Corporation PTMG2000: Polytetramethylene ether glycol, Mitsubishi Chemical Corporation Plaquel 308: Polycaprolactone polyol, Daicel Corporation YP-70: Phenoxy resin, Nippon Steel Epototo YD-6020 manufactured by Kagaku Co., Ltd .: Hydroxyl-containing long-chain epoxy resin, manufactured by Nippon Steel Chemical Co., Ltd.
- HN-7200 4-methylhexahydrophthalic anhydride and alicyclic ring Mixture of polyester resin, manufactured by Hitachi Chemical Co., Ltd.
- Test equipment Resin curing oven ESPEC Co., Ltd. “GPHH-201” ⁇ Constant temperature bath Espec Co., Ltd., “Small high temperature chamber ST-120B1” ⁇ Total luminous flux measuring machine "Optical Laboratories USA”, “Multi-spectral Radiation Measurement System OL771” ⁇ Thermal shock tester Espec Co., Ltd., “Small Thermal Shock Apparatus TSE-11-A” ⁇ Reflow furnace “UNI-5016F” manufactured by Nippon Antom Co., Ltd.
- Reflector resin composition for light reflection
- Metal wiring Metal wiring
- Optical semiconductor element Optical semiconductor element
- Bonding wire Transparent sealing resin
- the curable epoxy resin composition of the present invention can be preferably used for the above-mentioned optical semiconductor element sealing application (for optical semiconductor sealing).
- the curable epoxy resin composition of the present invention is, for example, an adhesive, an electrical insulating material, a laminate, a coating, an ink, a paint, a sealant, a resist, a composite material, a transparent substrate, a transparent sheet, a transparent film, and an optical element.
Landscapes
- Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Microelectronics & Electronic Packaging (AREA)
- Power Engineering (AREA)
- Computer Hardware Design (AREA)
- Condensed Matter Physics & Semiconductors (AREA)
- Physics & Mathematics (AREA)
- General Physics & Mathematics (AREA)
- Manufacturing & Machinery (AREA)
- Epoxy Resins (AREA)
- Led Device Packages (AREA)
- Structures Or Materials For Encapsulating Or Coating Semiconductor Devices Or Solid State Devices (AREA)
- Compositions Of Macromolecular Compounds (AREA)
Abstract
Description
また、本発明の他の目的は、上記硬化性エポキシ樹脂組成物を硬化してなる、優れた透明性、耐熱性、耐光性、及び耐クラック性を兼ね備えた硬化物を提供することにある。
また、本発明の他の目的は、経時での光度低下が抑制された光半導体装置を得ることができる、上記硬化性エポキシ樹脂組成物からなる光半導体封止用樹脂組成物を提供することにある。
また、本発明の他の目的は、上記光半導体封止用樹脂組成物を用いて光半導体素子を封止することにより得られる、経時での光度低下が抑制された光半導体装置を提供することにある。
で表されるモノアリルジグリシジルイソシアヌレート化合物(B)と、分子内に2以上のエポキシ基を有するシロキサン誘導体(C)と、脂環式ポリエステル樹脂(D)と、硬化剤(E)と、硬化促進剤(G)とを含むことを特徴とする硬化性エポキシ樹脂組成物を提供する。
で表されるモノアリルジグリシジルイソシアヌレート化合物(B)と、分子内に2以上のエポキシ基を有するシロキサン誘導体(C)と、脂環式ポリエステル樹脂(D)と、硬化触媒(F)とを含むことを特徴とする硬化性エポキシ樹脂組成物を提供する。
本発明の硬化性エポキシ樹脂組成物は、脂環式エポキシ化合物(A)と、下記式(1)
で表されるモノアリルジグリシジルイソシアヌレート化合物(B)と、分子内に2以上のエポキシ基を有するシロキサン誘導体(C)と、脂環式ポリエステル樹脂(D)と、硬化剤(E)と、硬化促進剤(G)とを少なくとも含む樹脂組成物、又は、脂環式エポキシ化合物(A)と、上記式(1)で表されるモノアリルジグリシジルイソシアヌレート化合物(B)と、分子内に2以上のエポキシ基を有するシロキサン誘導体(C)と、脂環式ポリエステル樹脂(D)と、硬化触媒(F)とを少なくとも含む樹脂組成物である。
本発明の硬化性エポキシ樹脂組成物を構成する脂環式エポキシ化合物(A)は、分子内(1分子内)に脂環(脂肪族環)構造とエポキシ基とを少なくとも有する化合物である。より具体的には、脂環式エポキシ化合物(A)には、例えば、(i)脂環を構成する隣接する2つの炭素原子と酸素原子とで構成されるエポキシ基(「脂環エポキシ基」と称する場合がある)を有する化合物、及び(ii)脂環にエポキシ基が直接単結合で結合している化合物等が含まれる。但し、脂環式エポキシ化合物(A)には、後述の分子内に2以上のエポキシ基を有するシロキサン誘導体(C)は含まれないものとする。
本発明の硬化性エポキシ樹脂組成物を構成するモノアリルジグリシジルイソシアヌレート化合物(B)は、下記の一般式(1)で表される。
本発明の硬化性エポキシ樹脂組成物を構成する分子内(一分子中)に2以上のエポキシ基を有するシロキサン誘導体(C)は、シロキサン骨格を有し、なおかつ分子内に2以上のエポキシ基を有する化合物である。分子内に2以上のエポキシ基を有するシロキサン誘導体(C)は、硬化物の耐熱性、耐光性、耐クラック性を向上させ、光半導体装置の光度低下を抑制する役割を担う。
本発明の硬化性エポキシ樹脂組成物を構成する脂環式ポリエステル樹脂(D)は、脂環構造(脂肪族環構造)を少なくとも有するポリエステル樹脂である。脂環式ポリエステル樹脂(D)は、硬化物の耐熱性、耐光性、耐クラック性を向上させ、光半導体装置の光度低下を抑制する役割を担う。特に、硬化物の耐熱性、耐光性、耐クラック性向上の観点で、脂環式ポリエステル樹脂(D)は、主鎖に脂環(脂環構造)を有する脂環式ポリエステル樹脂であることが好ましい。即ち、脂環式ポリエステル樹脂(D)は、脂環を構成する炭素原子の一部又は全部によりポリマー主鎖が構成されたポリエステル樹脂であることが好ましい。なお、脂環式ポリエステル樹脂(D)は単独で、又は2種以上を組み合わせて使用できる。
本発明の硬化性エポキシ樹脂組成物を構成する硬化剤(E)は、エポキシ基を有する化合物を硬化させる役割を担う。硬化剤(E)としては、エポキシ樹脂用硬化剤として公知乃至慣用の硬化剤を使用することができる。中でも、硬化剤(E)としては、25℃で液状の酸無水物が好ましく、より具体的には、例えば、メチルテトラヒドロ無水フタル酸、メチルヘキサヒドロ無水フタル酸、ドデセニル無水コハク酸、メチルエンドメチレンテトラヒドロ無水フタル酸などが挙げられる。また、例えば、無水フタル酸、テトラヒドロ無水フタル酸、ヘキサヒドロ無水フタル酸、メチルシクロヘキセンジカルボン酸無水物などの常温(約25℃)で固体状の酸無水物についても、常温(約25℃)で液状の酸無水物に溶解させて液状の混合物とすることで、硬化剤(E)として好ましく使用することができる。硬化剤(E)は単独で、又は2種以上を組み合わせて使用することができる。中でも、硬化剤(E)としては、耐熱性、耐光性、耐クラック性の観点で、特に、飽和単環炭化水素ジカルボン酸の無水物(環にアルキル基等の置換基が結合したものも含む)が好ましい。
本発明の硬化性エポキシ樹脂組成物において硬化促進剤(G)は、エポキシ基を有する化合物が硬化剤(E)により硬化する際に、硬化速度を促進する機能を有する化合物である。硬化促進剤(G)としては、公知乃至慣用の硬化促進剤を使用することができ、特に限定されないが、例えば、1,8-ジアザビシクロ[5.4.0]ウンデセン-7(DBU)、及びその塩(例えば、フェノール塩、オクチル酸塩、p-トルエンスルホン酸塩、ギ酸塩、テトラフェニルボレート塩);1,5-ジアザビシクロ[4.3.0]ノネン-5(DBN)、及びその塩(例えば、フェノール塩、オクチル酸塩、p-トルエンスルホン酸塩、ギ酸塩、テトラフェニルボレート塩);ベンジルジメチルアミン、2,4,6-トリス(ジメチルアミノメチル)フェノール、N,N-ジメチルシクロヘキシルアミンなどの3級アミン;2-エチル-4-メチルイミダゾール、1-シアノエチル-2-エチル-4-メチルイミダゾールなどのイミダゾール類;リン酸エステル、トリフェニルホスフィンなどのホスフィン類;テトラフェニルホスホニウムテトラ(p-トリル)ボレートなどのホスホニウム化合物;オクチル酸スズ、オクチル酸亜鉛などの有機金属塩;金属キレートなどが挙げられる。硬化促進剤(G)は単独で、又は2種以上を組み合わせて使用できる。
本発明の硬化性エポキシ樹脂組成物は、上述の硬化剤(E)の代わりに、硬化触媒(F)を含んでいてもよい。硬化剤(E)を用いた場合と同様に、硬化触媒(F)を用いることにより、エポキシ基を有する化合物の硬化反応を進行させ、硬化物を得ることができる。上記硬化触媒(F)としては、特に限定されないが、例えば、紫外線照射又は加熱処理を施すことによりカチオン種を発生して、重合を開始させるカチオン触媒(カチオン重合開始剤)を用いることができる。
本発明の硬化性エポキシ樹脂組成物は、さらに、シリコーン系レベリング剤(ポリシロキサン系レベリング剤)及びフッ素系レベリング剤からなる群から選ばれた少なくとも1種のレベリング剤を含むことが好ましい。本発明の硬化性エポキシ樹脂組成物は、上記レベリング剤を含むことにより、より高度な耐熱性及び耐クラック性を示す硬化物を形成でき、該硬化物を用いて作製した光半導体装置は、経時での光度低下が生じにくい。
上記シリコーン系レベリング剤とは、ポリシロキサン骨格を有する化合物を含むレベリング剤である。上記シリコーン系レベリング剤としては、公知乃至慣用のシリコーン系レベリング剤を使用でき、特に限定されないが、例えば、商品名「BYK-300」、「BYK-301/302」、「BYK-306」、「BYK-307」、「BYK-310」、「BYK-315」、「BYK-313」、「BYK-320」、「BYK-322」、「BYK-323」、「BYK-325」、「BYK-330」、「BYK-331」、「BYK-333」、「BYK-337」、「BYK-341」、「BYK-344」、「BYK-345/346」、「BYK-347」、「BYK-348」、「BYK-349」、「BYK-370」、「BYK-375」、「BYK-377」、「BYK-378」、「BYK-UV3500」、「BYK-UV3510」、「BYK-UV3570」、「BYK-3550」、「BYK-SILCLEAN3700」、「BYK-SILCLEAN3720」(以上、ビックケミー・ジャパン(株)製)、商品名「AC FS 180」、「AC FS 360」、「AC S 20」(以上、Algin Chemie製)、商品名「ポリフローKL-400X」、「ポリフローKL-400HF」、「ポリフローKL-401」、「ポリフローKL-402」、「ポリフローKL-403」、「ポリフローKL-404」(以上、共栄社化学(株)製)、商品名「KP-323」、「KP-326」、「KP-341」、「KP-104」、「KP-110」、「KP-112」(以上、信越化学工業(株)製)、商品名「LP-7001」、「LP-7002」、「8032 ADDITIVE」、「57 ADDITIVE」、「L-7604」、「FZ-2110」、「FZ-2105」、「67 ADDITIVE」、「8618 ADDITIVE」、「3 ADDITIVE」、「56 ADDITIVE」(以上、東レ・ダウコーニング(株)製)などの市販品を使用することができる。シリコーン系レベリング剤は単独で、又は2種以上を組み合わせて使用することができる。
上記フッ素系レベリング剤とは、アルキル基の水素原子の一部又は全部がフッ素原子で置換されたフッ素化アルキル基を有する化合物を含むレベリング剤である。上記フッ素系レベリング剤としては、公知乃至慣用のフッ素系レベリング剤を使用でき、特に限定されないが、例えば、商品名「BYK-340」(ビックケミー・ジャパン(株)製)、商品名「AC 110a」、「AC 100a」(以上、Algin Chemie製)、商品名「メガファックF-114」、「メガファックF-410」、「メガファックF-444」、「メガファックEXP TP-2066」、「メガファックF-430」、「メガファックF-472SF」、「メガファックF-477」、「メガファックF-552」、「メガファックF-553」、「メガファックF-554」、「メガファックF-555」、「メガファックR-94」、「メガファックRS-72-K」、「メガファックRS-75」、「メガファックF-556」、「メガファックEXP TF-1367」、「メガファックEXP TF-1437」、「メガファックF-558」、「メガファックEXP TF-1537」(以上、DIC(株)製)、商品名「FC-4430」、「FC-4432」(以上、住友スリーエム(株)製)、商品名「フタージェント 100」、「フタージェント 100C」、「フタージェント 110」、「フタージェント 150」、「フタージェント 150CH」、「フタージェント A-K」、「フタージェント 501」、「フタージェント 250」、「フタージェント 251」、「フタージェント 222F」、「フタージェント 208G」、「フタージェント 300」、「フタージェント 310」、「フタージェント 400SW」(以上、(株)ネオス製)、商品名「PF-136A」、「PF-156A」、「PF-151N」、「PF-636」、「PF-6320」、「PF-656」、「PF-6520」、「PF-651」、「PF-652」(以上、北村化学産業(株)製)などの市販品を使用することもできる。フッ素系レベリング剤は単独で、又は2種以上を組み合わせて使用することができる。
本発明の硬化性エポキシ樹脂組成物は、さらに、ポリオール化合物を含むことが好ましい。本発明の硬化性エポキシ樹脂組成物は、上記ポリオール化合物を含むことにより、より高度な耐熱性及び耐クラック性を示す硬化物を形成でき、該硬化物を用いて作製した光半導体装置は、経時での光度低下がいっそう生じにくい。上記ポリオール化合物とは、分子内(一分子中)に2個以上の水酸基を有する数平均分子量が200以上の重合体(オリゴマー又はポリマー)であり、例えば、ポリエーテルポリオール、ポリエステルポリオール、ポリカーボネートポリオール等が含まれる。なお、上記ポリオール化合物は単独で、又は2種以上を組み合わせて使用することができる。
本発明の硬化性エポキシ樹脂組成物は、さらに、アクリルブロック共重合体を含むことが好ましい。より詳しくは、本発明の硬化性エポキシ樹脂組成物がアクリルブロック共重合体を含む場合、当該硬化性エポキシ樹脂組成物を用いて製造された光半導体装置は、特に高輝度・高出力の場合であっても光度が低下しにくい傾向にある。即ち、アクリルブロック共重合体を用いることにより、本発明の硬化性エポキシ樹脂組成物を硬化して得られる硬化物は、より高いレベルの耐熱性、耐光性、及び耐クラック性を発揮できる。
本発明の硬化性エポキシ樹脂組成物は、さらに、ゴム粒子を含んでいてもよい。上記ゴム粒子としては、例えば、粒子状NBR(アクリロニトリル-ブタジエンゴム)、反応性末端カルボキシル基NBR(CTBN)、メタルフリーNBR、粒子状SBR(スチレン-ブタジエンゴム)などのゴム粒子が挙げられる。上記ゴム粒子としては、ゴム弾性を有するコア部分と、該コア部分を被覆する少なくとも1層のシェル層とからなる多層構造(コアシェル構造)を有するゴム粒子が好ましい。上記ゴム粒子は、特に、(メタ)アクリル酸エステルを必須モノマー成分とするポリマー(重合体)で構成されており、表面に脂環式エポキシ化合物(A)などのエポキシ基を有する化合物と反応し得る官能基としてヒドロキシル基及び/又はカルボキシル基(ヒドロキシル基及びカルボキシル基のいずれか一方又は両方)を有するゴム粒子が好ましい。上記ゴム粒子の表面にヒドロキシル基及び/又はカルボキシル基が存在しない場合、冷熱サイクル等の熱衝撃により硬化物が白濁して透明性が低下するため好ましくない。
本発明の硬化性エポキシ樹脂組成物は、上記以外にも、本発明の効果を損なわない範囲内で各種添加剤を使用することができる。添加剤として、例えば、エチレングリコール、ジエチレングリコール、プロピレングリコール、グリセリンなどの水酸基を有する化合物(上述のポリオール化合物を除く)を使用すると、反応(硬化反応)を緩やかに進行させることができる。その他にも、粘度や透明性を損なわない範囲内で、γ-グリシドキシプロピルトリメトキシシランなどのシランカップリング剤、界面活性剤、シリカ、アルミナなどの無機充填剤、難燃剤、着色剤、酸化防止剤、紫外線吸収剤、イオン吸着体、顔料、蛍光体、離型剤などの慣用の添加剤を使用することができる。
本発明の硬化性エポキシ樹脂組成物は、上述の脂環式エポキシ化合物(A)と、モノアリルジグリシジルイソシアヌレート化合物(B)と、分子内に2以上のエポキシ基を有するシロキサン誘導体(C)と、脂環式ポリエステル樹脂(D)と、硬化剤(E)及び硬化促進剤(G)、又は、硬化触媒(F)とを含んでいればよく、その調製方法は特に限定されない。例えば、脂環式エポキシ化合物(A)、モノアリルジグリシジルイソシアヌレート化合物(B)、分子内に2以上のエポキシ基を有するシロキサン誘導体(C)等のエポキシ基を有する化合物を必須成分として含むα剤と、硬化剤(E)及び硬化促進剤(G)、又は、硬化触媒(F)を必須成分として含むβ剤とを別々に調製し、当該α剤とβ剤とを所定の割合で攪拌・混合し、必要に応じて真空下で脱泡する方法により調製することができる。なお、脂環式ポリエステル樹脂(D)は、あらかじめα剤及び/又はβ剤の構成成分として混合(配合)しておいてもよいし、α剤とβ剤とを混合する際にα剤、β剤以外の第三成分として配合してもよい。
本発明の硬化性エポキシ樹脂組成物を硬化させることにより、透明性、耐熱性、耐光性、及び耐クラック性などの諸物性に優れた硬化物を得ることができる。硬化の際の加熱温度(硬化温度)としては、特に限定されないが、45~200℃が好ましく、より好ましくは100~190℃、さらに好ましくは100~180℃である。また、硬化の際に加熱する時間(硬化時間)としては、特に限定されないが、30~600分が好ましく、より好ましくは45~540分、さらに好ましくは60~480分である。硬化温度が低すぎる場合、及び/又は、硬化時間が短すぎる場合は、硬化が不十分となる場合がある。一方、硬化温度が高すぎる場合、及び/又は、硬化時間が長すぎる場合は、樹脂成分の分解が起こる場合がある。硬化条件は種々の条件に依存するが、硬化温度を高くした場合は硬化時間を短く、硬化温度を低くした場合は硬化時間を長くする等により、適宜調整することができる。
本発明の光半導体封止用樹脂組成物は、本発明の硬化性エポキシ樹脂組成物からなる。本発明の光半導体封止用樹脂組成物を用いることにより、透明性、耐熱性、耐光性、及び耐クラック性などの諸物性に優れた硬化物により光半導体素子が封止された、光度が経時で低下しにくい光半導体装置を得ることができる。上記光半導体装置は、特に、高出力、高輝度の光半導体素子を備える場合であっても、光度が経時で低下しにくい。
本発明の光半導体装置は、本発明の硬化性エポキシ樹脂組成物(光半導体封止用樹脂組成物)で光半導体素子を封止することにより得られる。光半導体素子の封止は、硬化性エポキシ樹脂組成物を所定の成形型内に注入し、所定の条件で加熱硬化して行う。これにより、硬化性エポキシ樹脂組成物によって光半導体素子が封止されてなる光半導体装置が得られる。封止の際の硬化温度と硬化時間としては、例えば、上記硬化物を形成する際と同様の条件を採用することができる。
(エポキシ樹脂の製造:実施例1~12、比較例1~6)
モノアリルジグリシジルイソシアヌレート(商品名「MA-DGIC」、四国化成工業(株))、脂環式エポキシ化合物(商品名「セロキサイド2021P」、(株)ダイセル製;商品名「EHPE3150」、(株)ダイセル製)、分子内に2個のエポキシ基を有するシロキサン誘導体(商品名「X-40-2678」、信越化学工業(株)製)、分子内に3個のエポキシ基を有するシロキサン誘導体(商品名「X-40-2720」、信越化学工業(株)製)、分子内に4個のエポキシ基を有するシロキサン誘導体(商品名「X-40-2670」、信越化学工業(株)製)を、表1に示す配合処方(配合割合)(単位:重量部)に従って混合し(実施例1~12の場合は、80℃で1時間攪拌することでモノアリルジグリシジルイソシアヌレートを溶解させた)、エポキシ樹脂(エポキシ樹脂組成物)を得た。なお、表1における「-」は、当該成分の配合を行わなかったことを示し、表2、表3においても同様である。
(硬化剤を少なくとも含む硬化剤組成物(以下、「K剤」と称する)の製造:実施例1~12、比較例1~6)
硬化剤(酸無水物)(商品名「リカシッド MH-700」、日立化成工業(株)製)、硬化剤(酸無水物)と脂環式ポリエステル樹脂の混合物(商品名「HN-7200」、日立化成工業(株)製)、硬化剤(酸無水物)と脂環式ポリエステル樹脂の混合物(商品名「HN-5700」、日立化成工業(株)製)、硬化促進剤(商品名「U-CAT 18X」、サンアプロ(株)製)、添加剤(商品名「エチレングリコール」、和光純薬工業(株)製)を、表1に示す配合処方(配合割合)に従って、自公転式攪拌装置(商品名「あわとり練太郎AR-250」、(株)シンキー製)を使用して均一に混合し、脱泡してK剤を得た。
(硬化性エポキシ樹脂組成物の製造)
表1に示す配合処方(単位:重量部)となるように、製造例1で得られたエポキシ樹脂、製造例2で得られたK剤を、自公転式攪拌装置(商品名「あわとり練太郎AR-250」、(株)シンキー製)を使用して均一に混合し、脱泡して硬化性エポキシ樹脂組成物を得た。
上記で得た硬化性エポキシ樹脂組成物を、図1に示す光半導体のリードフレーム(InGaN素子、3.5mm×2.8mm)に注型した後、120℃のオーブン(樹脂硬化オーブン)で5時間加熱し、硬化した樹脂(硬化物)で光半導体素子を封止した光半導体装置を得た。なお、図1において、100はリフレクター(光反射用樹脂組成物)、101は金属配線、102は光半導体素子、103はボンディングワイヤ、104は透明封止樹脂(硬化物)を示す。
(ゴム粒子の製造)
還流冷却器付きの1L重合容器に、イオン交換水500g、及びジオクチルスルホコハク酸ナトリウム0.68gを仕込み、窒素気流下に撹拌しながら、80℃に昇温した。ここに、コア部分を形成するために必要とする量の約5重量%分に該当するアクリル酸ブチル9.5g、スチレン2.57g、及びジビニルベンゼン0.39gからなる単量体混合物を一括添加し、20分間撹拌して乳化させた後、ペルオキソ二硫酸カリウム9.5mgを添加し、1時間撹拌して最初のシード重合を行い、続いて、ペルオキソ二硫酸カリウム180.5mgを添加し、5分間撹拌した。ここに、コア部分を形成するために必要とする量の残り(約95重量%分)のアクリル酸ブチル180.5g、スチレン48.89g、ジビニルベンゼン7.33gにジオクチルスルホコハク酸ナトリウム0.95gを溶解させてなる単量体混合物を2時間かけて連続的に添加し、2度目のシード重合を行い、その後、1時間熟成してコア部分を得た。
次いで、ペルオキソ二硫酸カリウム60mgを添加して5分間撹拌し、ここに、メタクリル酸メチル60g、アクリル酸1.5g、及びアリルメタクリレート0.3gにジオクチルスルホコハク酸ナトリウム0.3gを溶解させてなる単量体混合物を30分かけて連続的に添加し、シード重合を行った。その後、1時間熟成し、コア部分を被覆するシェル層を形成した。
次いで、室温(25℃)まで冷却し、目開き120μmのプラスチック製網で濾過することにより、コアシェル構造を有するゴム粒子を含むラテックスを得た。得られたラテックスをマイナス30℃で凍結し、吸引濾過器で脱水洗浄した後、60℃で一昼夜送風乾燥してゴム粒子を得た。得られたゴム粒子の平均粒子径は254nm、最大粒子径は486nmであった。
(ゴム粒子分散エポキシ化合物の製造)
製造例3で得られたゴム粒子10重量部を、窒素気流下、60℃に加温した状態でディゾルバー(1000rpm、60分間)を使用して、セロキサイド2021P(3,4-エポキシシクロヘキシルメチル(3,4-エポキシ)シクロヘキサンカルボキシレート、(株)ダイセル製)56重量部に分散させ、真空脱泡して、ゴム粒子分散エポキシ化合物(25℃での粘度:834mPa・s)を得た。
なお、上記ゴム粒子分散エポキシ化合物(ゴム粒子10重量部をセロキサイド2021P((株)ダイセル製)56重量部に分散させたもの)の粘度(25℃における粘度)は、デジタル粘度計(商品名「DVU-EII型」、(株)トキメック製)を使用して測定した。
(エポキシ樹脂の製造:実施例13~28)
モノアリルジグリシジルイソシアヌレート(商品名「MA-DGIC」、四国化成工業(株))、脂環式エポキシ化合物(商品名「セロキサイド2021P」、(株)ダイセル製)、分子内に2個のエポキシ基を有するシロキサン誘導体(商品名「X-40-2678」、信越化学工業(株)製)、分子内に3個のエポキシ基を有するシロキサン誘導体(商品名「X-40-2720」、信越化学工業(株)製)、分子内に4個のエポキシ基を有するシロキサン誘導体(商品名「X-40-2670」、信越化学工業(株)製)、シリコーン系レベリング剤(商品名「BYK-300」、ビックケミー・ジャパン(株)製;商品名「AC FS 180」、Algin Chemie製)、フッ素系レベリング剤(商品名「BYK-340」、ビックケミー・ジャパン(株)製;商品名「AC 110a」、Algin Chemie製)、ポリカーボネートジオール(商品名「プラクセル CD220PL」、(株)ダイセル製)、ポリテトラメチレンエーテルグリコール(商品名「PTMG2000」、三菱化学(株)製)、ポリカプロラクトンポリオール(商品名「プラクセル 308」、(株)ダイセル製)、フェノキシ樹脂(商品名「YP-70」、新日鐵化学(株)製)、水酸基含有長鎖エポキシ樹脂(商品名「エポトートYD-6020」、新日鐵化学(株)製)、アクリルブロック共重合体(商品名「ナノストレングス M52N」、アルケマ製)、製造例4で得られたゴム粒子分散エポキシ化合物を、表2に示す配合処方(配合割合)(単位:重量部)に従って混合し、80℃で1時間攪拌することでモノアリルジグリシジルイソシアヌレートを溶解させ、エポキシ樹脂(エポキシ樹脂組成物)を得た。
(K剤の製造:実施例13~28)
硬化剤(酸無水物)と脂環式ポリエステル樹脂の混合物(商品名「HN-7200」、日立化成工業(株)製)、硬化促進剤(商品名「U-CAT 18X」、サンアプロ(株)製)、添加剤(商品名「エチレングリコール」、和光純薬工業(株)製)を、表2に示す配合処方(配合割合)に従って、自公転式攪拌装置(商品名「あわとり練太郎AR-250」、(株)シンキー製)を使用して均一に混合し、脱泡してK剤を得た。
(硬化性エポキシ樹脂組成物の製造)
表2に示す配合処方(単位:重量部)となるように、製造例5で得られたエポキシ樹脂、製造例6で得られたK剤を、自公転式攪拌装置(商品名「あわとり練太郎AR-250」、(株)シンキー製)を使用して均一に混合し、脱泡して硬化性エポキシ樹脂組成物を得た。
上記で得た硬化性エポキシ樹脂組成物を、図1に示す光半導体のリードフレーム(InGaN素子、3.5mm×2.8mm)に注型した後、120℃のオーブン(樹脂硬化オーブン)で5時間加熱し、硬化した樹脂(硬化物)で光半導体素子を封止した光半導体装置を得た。
(エポキシ樹脂の製造:実施例29~43、比較例7~11)
モノアリルジグリシジルイソシアヌレート(商品名「MA-DGIC」、四国化成工業(株))、脂環式エポキシ化合物(商品名「セロキサイド2021P」、(株)ダイセル製;商品名「EHPE3150」、(株)ダイセル製)、分子内に2個のエポキシ基を有するシロキサン誘導体(商品名「X-40-2678」、信越化学工業(株)製)、分子内に3個のエポキシ基を有するシロキサン誘導体(商品名「X-40-2720」、信越化学工業(株)製)、分子内に4個のエポキシ基を有するシロキサン誘導体(商品名「X-40-2670」、信越化学工業(株)製)、シリコーン系レベリング剤(商品名「BYK-300」、ビックケミー・ジャパン(株)製;商品名「AC FS 180」、Algin Chemie製)、フッ素系レベリング剤(商品名「BYK-340」、ビックケミー・ジャパン(株)製;商品名「AC 110a」、Algin Chemie製)、ポリカーボネートジオール(商品名「プラクセル CD220PL」、(株)ダイセル製)、ポリテトラメチレンエーテルグリコール(商品名「PTMG2000」、三菱化学(株)製)、ポリカプロラクトンポリオール(商品名「プラクセル308」、(株)ダイセル製)、フェノキシ樹脂(商品名「YP-70」、新日鐵化学(株)製)、水酸基含有長鎖エポキシ樹脂(商品名「エポトートYD-6020」、新日鐵化学(株)製)、アクリルブロック共重合体(商品名「ナノストレングス M52N」、アルケマ製)、製造例4で得られたゴム粒子分散エポキシ化合物を、表3に示す配合処方(配合割合)(単位:重量部)に従って混合し(実施例29~43の場合は、80℃で1時間攪拌することでモノアリルジグリシジルイソシアヌレートを溶解させた)、エポキシ樹脂(エポキシ樹脂組成物)を得た。
(脂環式ポリエステル樹脂の製造:実施例29~43、比較例9~11)
攪拌機、温度計及び還流冷却器を備えた反応容器に、1,4-シクロヘキサンジカルボン酸(東京化成工業(株)製)172重量部、ネオペンチルグリコール(東京化成工業(株)製)208重量部、テトラブチルチタネート(和光純薬工業(株)製)0.1重量部を仕込んで、160℃になるまで加熱し、さらに160℃から250℃まで4時間かけて昇温した。次いで、1時間かけて5mmHgまで減圧し、さらに0.3mmHg以下まで減圧してから250℃で1時間反応させ、脂環式ポリエステル樹脂を得た。
(硬化性エポキシ樹脂組成物の製造)
表3に示す配合処方(単位:重量部)となるように、製造例7で得られたエポキシ樹脂、製造例8で得られた脂環式ポリエステル樹脂、硬化触媒(商品名「サンエイド SI-100L」、三新化学工業(株)製)を、自公転式攪拌装置(商品名「あわとり練太郎AR-250」、(株)シンキー製)を使用して均一に混合し、脱泡して硬化性エポキシ樹脂組成物を得た。
上記で得た硬化性エポキシ樹脂組成物を、図1に示す光半導体のリードフレーム(InGaN素子、3.5mm×2.8mm)に注型した後、120℃のオーブン(樹脂硬化オーブン)で5時間加熱し、硬化した樹脂(硬化物)で光半導体素子を封止した光半導体装置を得た。
実施例及び比較例で得られた光半導体装置について、以下の方法で評価試験を行った。
実施例及び比較例で得られた光半導体装置の全光束を全光束測定機を用いて測定し、これを「初期(0時間)の全光束(lm)」とした。さらに、85℃の恒温槽内で100時間、上記光半導体装置に60mAの電流を継続的に流した後の全光束を測定し、これを「100時間後の全光束(lm)」とした。そして、次式より光度保持率を算出した。結果を表1~3の「光度保持率」の欄に示す。
{光度保持率(%)}
={100時間後の全光束(lm)}/{初期(0時間)の全光束(lm)}×100
実施例及び比較例で得られた光半導体装置(各硬化性エポキシ樹脂組成物につき2個用いた)を、30℃、70%RHの条件下で168時間静置して吸湿させた。次いで、上記光半導体装置をリフロー炉に入れ、下記加熱条件にて加熱した。その後、上記光半導体装置を室温環境下に取り出して放冷した後、再度リフロー炉に入れて同条件で加熱した。即ち、当該はんだ耐熱性試験においては、光半導体装置に対して下記加熱条件による熱履歴を二度与えた。
〔加熱条件(光半導体装置の表面温度基準)〕
(1)予備加熱:150~190℃で60~120秒
(2)予備加熱後の本加熱:217℃以上で60~150秒、最高温度260℃
但し、予備加熱から本加熱に移行する際の昇温速度は最大で3℃/秒に制御した。
図2には、リフロー炉による加熱の際の光半導体装置の表面温度プロファイル(二度の加熱のうち一方の加熱における温度プロファイル)の一例を示す。
その後、光半導体装置の封止樹脂(硬化性エポキシ樹脂組成物の硬化物)に生じたクラックの長さを、デジタルマイクロスコープ(VHX-900、(株)キーエンス製)を使用して観察し、光半導体装置2個のうち長さが90μm以上のクラックを有する光半導体装置の個数を計測した。結果を表1~3の「はんだ耐熱性試験」の欄に示す。
実施例及び比較例で得られた光半導体装置(各硬化性エポキシ樹脂組成物につき2個用いた)に対し、-40℃の雰囲気下に30分曝露し、続いて、100℃の雰囲気下に30分曝露することを1サイクルとした熱衝撃を、熱衝撃試験機を用いて200サイクル分与えた。その後、光半導体装置の封止樹脂(硬化性エポキシ樹脂組成物の硬化物)に生じたクラックの長さを、デジタルマイクロスコープ(VHX-900、(株)キーエンス製)を使用して観察し、光半導体装置2個のうち長さが90μm以上のクラックを有する光半導体装置の個数を計測した。結果を表1~3の「熱衝撃試験」の欄に示す。
通電試験において光度保持率が90%以上であり、なおかつ、はんだ耐熱性試験と熱衝撃試験において共に、長さ90μm以上のクラックが生じた光半導体装置の個数が0個となったものを、総合判定○(良好)とした。これ以外のものを総合判定×(不良)とした。結果を表1~3の「総合判定」の欄に示す。
[エポキシ樹脂]
CEL2021P(セロキサイド 2021P):3,4-エポキシシクロヘキシルメチル(3,4-エポキシ)シクロヘキサンカルボキシレート、(株)ダイセル製
EHPE3150:2,2-ビス(ヒドロキシメチル)-1-ブタノールの1,2-エポキシ-4-(2-オキシラニル)シクロヘキセン付加物、(株)ダイセル製
MA-DGIC:モノアリルジグリシジルイソシアヌレート、四国化成工業(株)製
X-40-2678:分子内に2個のエポキシ基を有するシロキサン誘導体、信越化学工業(株)製
X-40-2720:分子内に3個のエポキシ基を有するシロキサン誘導体、信越化学工業(株)製
X-40-2670:分子内に4個のエポキシ基を有するシロキサン誘導体、信越化学工業(株)製
[レベリング剤]
BYK-300:シリコーン系レベリング剤、ビックケミー・ジャパン(株)製
AC FS 180:シリコーン系レベリング剤、Algin Chemie製
BYK-340:フッ素系レベリング剤、ビックケミー・ジャパン(株)製
AC 110a:フッ素系レベリング剤、Algin Chemie製
[ポリオール化合物]
CD220PL(プラクセル CD220PL):ポリカーボネートジオール、(株)ダイセル製
PTMG2000:ポリテトラメチレンエーテルグリコール、三菱化学(株)製
プラクセル308:ポリカプロラクトンポリオール、(株)ダイセル製
YP-70:フェノキシ樹脂、新日鐵化学(株)製
エポトートYD-6020:水酸基含有長鎖エポキシ樹脂、新日鐵化学(株)製
[アクリルブロック共重合体]
M52N(ナノストレングス M52N):アクリルブロック共重合体、アルケマ製
[K剤]
MH-700(リカシッド MH-700):4-メチルヘキサヒドロ無水フタル酸/ヘキサヒドロ無水フタル酸=70/30、新日本理化(株)製
HN-7200:4-メチルヘキサヒドロ無水フタル酸と脂環式ポリエステル樹脂の混合物、日立化成工業(株)製
HN-5700:4-メチルヘキサヒドロ無水フタル酸/3-メチルヘキサヒドロ無水フタル酸=70/30と脂環式ポリエステル樹脂の混合物、日立化成工業(株)製
U-CAT 18X:硬化促進剤、サンアプロ(株)製
エチレングリコール:和光純薬工業(株)製
[硬化触媒]
サンエイド SI-100L:アリールスルホニウム塩、三新化学工業(株)製
・樹脂硬化オーブン
エスペック(株)製、「GPHH-201」
・恒温槽
エスペック(株)製、「小型高温チャンバー ST-120B1」
・全光束測定機
米国オプトロニックラボラトリーズ製、「マルチ分光放射測定システム OL771」
・熱衝撃試験機
エスペック(株)製、「小型冷熱衝撃装置 TSE-11-A」
・リフロー炉
日本アントム(株)製、「UNI-5016F」
101:金属配線
102:光半導体素子
103:ボンディングワイヤ
104:透明封止樹脂
Claims (12)
- 前記脂環式エポキシ化合物(A)が、シクロヘキセンオキシド基を有する脂環式エポキシ化合物である請求項1又は2に記載の硬化性エポキシ樹脂組成物。
- 前記脂環式ポリエステル樹脂(D)が、主鎖に脂環を有する脂環式ポリエステル樹脂である請求項1~4のいずれか1項に記載の硬化性エポキシ樹脂組成物。
- さらに、ゴム粒子を含む請求項1~5のいずれか1項に記載の硬化性エポキシ樹脂組成物。
- さらに、シリコーン系レベリング剤及びフッ素系レベリング剤からなる群より選ばれた少なくとも1種のレベリング剤を含む請求項1~6のいずれか1項に記載の硬化性エポキシ樹脂組成物。
- さらに、ポリオール化合物を含む請求項1~7のいずれか1項に記載の硬化性エポキシ樹脂組成物。
- さらに、アクリルブロック共重合体を含む請求項1~8のいずれか1項に記載の硬化性エポキシ樹脂組成物。
- 請求項1~9のいずれか1項に記載の硬化性エポキシ樹脂組成物を硬化してなる硬化物。
- 請求項1~9のいずれか1項に記載の硬化性エポキシ樹脂組成物からなる光半導体封止用樹脂組成物。
- 請求項11に記載の光半導体封止用樹脂組成物で光半導体素子を封止した光半導体装置。
Priority Applications (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020137028932A KR101914320B1 (ko) | 2011-07-20 | 2012-07-03 | 경화성 에폭시 수지 조성물 |
| CN201280034246.XA CN103649217B (zh) | 2011-07-20 | 2012-07-03 | 固化性环氧树脂组合物 |
| JP2013524650A JP5938041B2 (ja) | 2011-07-20 | 2012-07-03 | 硬化性エポキシ樹脂組成物 |
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2011-159338 | 2011-07-20 | ||
| JP2011159338 | 2011-07-20 | ||
| JP2012012311 | 2012-01-24 | ||
| JP2012-012311 | 2012-01-24 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2013011832A1 true WO2013011832A1 (ja) | 2013-01-24 |
Family
ID=47558011
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2012/066968 WO2013011832A1 (ja) | 2011-07-20 | 2012-07-03 | 硬化性エポキシ樹脂組成物 |
Country Status (5)
| Country | Link |
|---|---|
| JP (1) | JP5938041B2 (ja) |
| KR (1) | KR101914320B1 (ja) |
| CN (1) | CN103649217B (ja) |
| TW (1) | TWI558761B (ja) |
| WO (1) | WO2013011832A1 (ja) |
Cited By (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN104448820A (zh) * | 2013-09-17 | 2015-03-25 | 深圳光启创新技术有限公司 | 氰酸酯改性组合物、氰酸酯预浸料、超材料基板、其制备方法及包括其的超材料 |
| WO2016039232A1 (ja) * | 2014-09-11 | 2016-03-17 | 株式会社カネカ | 注型用エポキシ樹脂組成物 |
| WO2016047357A1 (ja) * | 2014-09-25 | 2016-03-31 | Dic株式会社 | エポキシ樹脂組成物、硬化物、繊維強化複合材料、繊維強化樹脂成形品、及び繊維強化樹脂成形品の製造方法 |
| EP2891673A4 (en) * | 2012-08-31 | 2016-05-18 | Daicel Corp | HARDENING COMPOSITION, HARDENED PRODUCT, OPTICAL ITEM AND OPTICAL DEVICE |
| CN105829444A (zh) * | 2013-12-26 | 2016-08-03 | 株式会社大赛璐 | 透镜用固化性组合物、以及透镜及光学装置 |
| JP2016160316A (ja) * | 2015-02-27 | 2016-09-05 | 株式会社ダイセル | 硬化性エポキシ樹脂組成物 |
| WO2016200739A1 (en) * | 2015-06-09 | 2016-12-15 | Koninklijke Philips N.V. | Led fabrication using high-refractive-index adhesives |
| JP2017071708A (ja) * | 2015-10-08 | 2017-04-13 | 信越化学工業株式会社 | 熱硬化性エポキシ樹脂組成物及び光半導体装置 |
| US11104824B2 (en) | 2014-03-31 | 2021-08-31 | Daicel Corporation | Curable composition and shaped product |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP6619954B2 (ja) * | 2015-06-17 | 2019-12-11 | 株式会社ダイセル | 成形体 |
| JP2020050797A (ja) * | 2018-09-27 | 2020-04-02 | パナソニックIpマネジメント株式会社 | 樹脂組成物、プリプレグ、樹脂付きフィルム、樹脂付き金属箔、金属張積層板、及びプリント配線板 |
| JP7390237B2 (ja) * | 2020-03-31 | 2023-12-01 | 京セラ株式会社 | 異方導電性樹脂組成物、異方導電性接着フィルム、及びマイクロledディスプレイ装置 |
Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2000344867A (ja) * | 1999-06-01 | 2000-12-12 | Shikoku Chem Corp | 熱硬化性エポキシ樹脂組成物 |
| JP2004131553A (ja) * | 2002-10-09 | 2004-04-30 | Yokohama Tlo Co Ltd | エポキシ樹脂組成物 |
| JP2008007782A (ja) * | 2006-06-27 | 2008-01-17 | Lumination Llc | オプトエレクトロニックデバイス |
| JP2008143954A (ja) * | 2006-12-06 | 2008-06-26 | Jsr Corp | イソシアヌル環含有重合体、その製造法およびそれを含有する組成物 |
| JP2008260853A (ja) * | 2007-04-12 | 2008-10-30 | Hitachi Chem Co Ltd | 新規硬化性樹脂とその製造方法、及びエポキシ樹脂組成物、電子部品装置 |
| WO2009096374A1 (ja) * | 2008-01-28 | 2009-08-06 | Kaneka Corporation | 脂環式エポキシ樹脂組成物、その硬化物、及びその製造方法、並びにゴム状重合体含有樹脂組成物 |
| JP2009227849A (ja) * | 2008-03-24 | 2009-10-08 | Sanyo Chem Ind Ltd | 光半導体素子封止用エポキシ樹脂組成物 |
| JP2009256604A (ja) * | 2008-03-28 | 2009-11-05 | Shin Etsu Chem Co Ltd | 光半導体素子封止用エポキシ・シリコーン混成樹脂組成物及びそれからなるトランスファー成型用タブレット |
| WO2010092947A1 (ja) * | 2009-02-10 | 2010-08-19 | 日産化学工業株式会社 | 長鎖アルキレン基含有エポキシ化合物 |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP4560982B2 (ja) * | 2000-04-17 | 2010-10-13 | 三菱電機株式会社 | 高圧回転機用絶縁コイルの製造方法 |
| JP2003277591A (ja) * | 2002-03-26 | 2003-10-02 | Sumitomo Bakelite Co Ltd | エポキシ樹脂組成物、プリプレグ及び積層板 |
| EP1657268B1 (en) * | 2003-08-21 | 2015-05-27 | Asahi Kasei Chemicals Corporation | Photosensitive composition and cured product thereof |
| FR2926244B1 (fr) * | 2008-01-16 | 2010-02-19 | Bic Soc | Instrument d'ecriture muni d'une gomme protegee par un manchon |
| JP5037385B2 (ja) * | 2008-02-26 | 2012-09-26 | 新日鐵化学株式会社 | エポキシシリコーン樹脂を含む硬化性樹脂組成物 |
-
2012
- 2012-07-03 CN CN201280034246.XA patent/CN103649217B/zh active Active
- 2012-07-03 WO PCT/JP2012/066968 patent/WO2013011832A1/ja active Application Filing
- 2012-07-03 KR KR1020137028932A patent/KR101914320B1/ko active IP Right Grant
- 2012-07-03 JP JP2013524650A patent/JP5938041B2/ja active Active
- 2012-07-19 TW TW101125955A patent/TWI558761B/zh active
Patent Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2000344867A (ja) * | 1999-06-01 | 2000-12-12 | Shikoku Chem Corp | 熱硬化性エポキシ樹脂組成物 |
| JP2004131553A (ja) * | 2002-10-09 | 2004-04-30 | Yokohama Tlo Co Ltd | エポキシ樹脂組成物 |
| JP2008007782A (ja) * | 2006-06-27 | 2008-01-17 | Lumination Llc | オプトエレクトロニックデバイス |
| JP2008143954A (ja) * | 2006-12-06 | 2008-06-26 | Jsr Corp | イソシアヌル環含有重合体、その製造法およびそれを含有する組成物 |
| JP2008260853A (ja) * | 2007-04-12 | 2008-10-30 | Hitachi Chem Co Ltd | 新規硬化性樹脂とその製造方法、及びエポキシ樹脂組成物、電子部品装置 |
| WO2009096374A1 (ja) * | 2008-01-28 | 2009-08-06 | Kaneka Corporation | 脂環式エポキシ樹脂組成物、その硬化物、及びその製造方法、並びにゴム状重合体含有樹脂組成物 |
| JP2009227849A (ja) * | 2008-03-24 | 2009-10-08 | Sanyo Chem Ind Ltd | 光半導体素子封止用エポキシ樹脂組成物 |
| JP2009256604A (ja) * | 2008-03-28 | 2009-11-05 | Shin Etsu Chem Co Ltd | 光半導体素子封止用エポキシ・シリコーン混成樹脂組成物及びそれからなるトランスファー成型用タブレット |
| WO2010092947A1 (ja) * | 2009-02-10 | 2010-08-19 | 日産化学工業株式会社 | 長鎖アルキレン基含有エポキシ化合物 |
Cited By (34)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10018810B2 (en) | 2012-08-31 | 2018-07-10 | Daicel Corporation | Curable composition, cured product thereof, optical member and optical device |
| US11029497B2 (en) | 2012-08-31 | 2021-06-08 | Daicel Corporation | Curable composition, cured product thereof, optical member and optical device |
| EP2891673A4 (en) * | 2012-08-31 | 2016-05-18 | Daicel Corp | HARDENING COMPOSITION, HARDENED PRODUCT, OPTICAL ITEM AND OPTICAL DEVICE |
| CN104448820A (zh) * | 2013-09-17 | 2015-03-25 | 深圳光启创新技术有限公司 | 氰酸酯改性组合物、氰酸酯预浸料、超材料基板、其制备方法及包括其的超材料 |
| EP3486286A1 (en) * | 2013-12-26 | 2019-05-22 | Daicel Corporation | Curable composition for lens, lens and optical device |
| KR20180069922A (ko) * | 2013-12-26 | 2018-06-25 | 주식회사 다이셀 | 렌즈용 경화성 조성물, 및 렌즈 및 광학 장치 |
| KR20160103006A (ko) * | 2013-12-26 | 2016-08-31 | 주식회사 다이셀 | 렌즈용 경화성 조성물, 및 렌즈 및 광학 장치 |
| CN109400847B (zh) * | 2013-12-26 | 2021-05-18 | 株式会社大赛璐 | 透镜用固化性组合物、以及透镜及光学装置 |
| US10604617B2 (en) | 2013-12-26 | 2020-03-31 | Daicel Corporation | Curable composition for lens, lens and optical device |
| JPWO2015098736A1 (ja) * | 2013-12-26 | 2017-03-23 | 株式会社ダイセル | レンズ用硬化性組成物、並びにレンズ及び光学装置 |
| KR102055796B1 (ko) * | 2013-12-26 | 2019-12-13 | 주식회사 다이셀 | 렌즈용 경화성 조성물, 및 렌즈 및 광학 장치 |
| US10465038B2 (en) | 2013-12-26 | 2019-11-05 | Daicel Corporation | Curable composition for lens, lens and optical device |
| EP3088465A4 (en) * | 2013-12-26 | 2017-06-21 | Daicel Corporation | Curable composition for lens, and lens and optical device |
| JP2019189874A (ja) * | 2013-12-26 | 2019-10-31 | 株式会社ダイセル | レンズ用硬化性組成物、並びにレンズ及び光学装置 |
| JP6232160B1 (ja) * | 2013-12-26 | 2017-11-15 | 株式会社ダイセル | レンズの製造方法、レンズおよび光学装置 |
| JP2018008518A (ja) * | 2013-12-26 | 2018-01-18 | 株式会社ダイセル | レンズの製造方法、レンズおよび光学装置 |
| JP2018049280A (ja) * | 2013-12-26 | 2018-03-29 | 株式会社ダイセル | レンズの製造方法 |
| CN109400847A (zh) * | 2013-12-26 | 2019-03-01 | 株式会社大赛璐 | 透镜用固化性组合物、以及透镜及光学装置 |
| KR101869178B1 (ko) * | 2013-12-26 | 2018-06-19 | 주식회사 다이셀 | 렌즈용 경화성 조성물, 및 렌즈 및 광학 장치 |
| CN105829444A (zh) * | 2013-12-26 | 2016-08-03 | 株式会社大赛璐 | 透镜用固化性组合物、以及透镜及光学装置 |
| US11104824B2 (en) | 2014-03-31 | 2021-08-31 | Daicel Corporation | Curable composition and shaped product |
| JPWO2016039232A1 (ja) * | 2014-09-11 | 2017-06-22 | 株式会社カネカ | 注型用エポキシ樹脂組成物 |
| EP3192835A4 (en) * | 2014-09-11 | 2018-05-02 | Kaneka Corporation | Epoxy resin composition for casting |
| US10287387B2 (en) | 2014-09-11 | 2019-05-14 | Kaneka Corporation | Epoxy resin composition for casting |
| WO2016039232A1 (ja) * | 2014-09-11 | 2016-03-17 | 株式会社カネカ | 注型用エポキシ樹脂組成物 |
| KR20170065498A (ko) * | 2014-09-25 | 2017-06-13 | 디아이씨 가부시끼가이샤 | 에폭시 수지 조성물, 경화물, 섬유 강화 복합 재료, 섬유 강화 수지 성형품, 및 섬유 강화 수지 성형품의 제조 방법 |
| JP5954516B1 (ja) * | 2014-09-25 | 2016-07-20 | Dic株式会社 | エポキシ樹脂組成物、硬化物、繊維強化複合材料、繊維強化樹脂成形品、及び繊維強化樹脂成形品の製造方法 |
| WO2016047357A1 (ja) * | 2014-09-25 | 2016-03-31 | Dic株式会社 | エポキシ樹脂組成物、硬化物、繊維強化複合材料、繊維強化樹脂成形品、及び繊維強化樹脂成形品の製造方法 |
| KR102309169B1 (ko) * | 2014-09-25 | 2021-10-08 | 디아이씨 가부시끼가이샤 | 에폭시 수지 조성물, 경화물, 섬유 강화 복합 재료, 섬유 강화 수지 성형품, 및 섬유 강화 수지 성형품의 제조 방법 |
| JP2016160316A (ja) * | 2015-02-27 | 2016-09-05 | 株式会社ダイセル | 硬化性エポキシ樹脂組成物 |
| WO2016200739A1 (en) * | 2015-06-09 | 2016-12-15 | Koninklijke Philips N.V. | Led fabrication using high-refractive-index adhesives |
| US10892385B2 (en) | 2015-06-09 | 2021-01-12 | Lumileds Llc | LED fabrication using high-refractive-index adhesives |
| CN108369984A (zh) * | 2015-06-09 | 2018-08-03 | 亮锐有限责任公司 | 使用高折射率粘合剂的发光二极管制作 |
| JP2017071708A (ja) * | 2015-10-08 | 2017-04-13 | 信越化学工業株式会社 | 熱硬化性エポキシ樹脂組成物及び光半導体装置 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN103649217A (zh) | 2014-03-19 |
| JPWO2013011832A1 (ja) | 2015-02-23 |
| TW201311807A (zh) | 2013-03-16 |
| KR101914320B1 (ko) | 2018-11-01 |
| KR20140041474A (ko) | 2014-04-04 |
| JP5938041B2 (ja) | 2016-06-22 |
| TWI558761B (zh) | 2016-11-21 |
| CN103649217B (zh) | 2017-02-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5938041B2 (ja) | 硬化性エポキシ樹脂組成物 | |
| JP5938040B2 (ja) | 硬化性エポキシ樹脂組成物 | |
| JP5764419B2 (ja) | 硬化性エポキシ樹脂組成物 | |
| JP5695269B2 (ja) | 硬化性エポキシ樹脂組成物 | |
| JP6046497B2 (ja) | 硬化性エポキシ樹脂組成物 | |
| JP5875269B2 (ja) | 硬化性エポキシ樹脂組成物 | |
| JP5852014B2 (ja) | 硬化性エポキシ樹脂組成物 | |
| JPWO2018135557A1 (ja) | 硬化性エポキシ樹脂組成物 | |
| WO2014109317A1 (ja) | 硬化性エポキシ樹脂組成物 | |
| JP2013213147A (ja) | 硬化性エポキシ樹脂組成物 | |
| JP6376907B2 (ja) | 硬化性エポキシ樹脂組成物 | |
| JP5808599B2 (ja) | プライマー組成物および該プライマー組成物を用いた光半導体装置 | |
| WO2019124476A1 (ja) | 硬化性エポキシ樹脂組成物及びその硬化物、並びに光半導体装置 | |
| JP5899025B2 (ja) | 硬化性エポキシ樹脂組成物 | |
| JP6082746B2 (ja) | 硬化性エポキシ樹脂組成物及びその硬化物、並びに光半導体装置 | |
| JP5919200B2 (ja) | 硬化性エポキシ樹脂組成物 | |
| JP6118313B2 (ja) | 硬化性エポキシ樹脂組成物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 12815159 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2013524650 Country of ref document: JP Kind code of ref document: A |
|
| ENP | Entry into the national phase |
Ref document number: 20137028932 Country of ref document: KR Kind code of ref document: A |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| 122 | Ep: pct application non-entry in european phase |
Ref document number: 12815159 Country of ref document: EP Kind code of ref document: A1 |