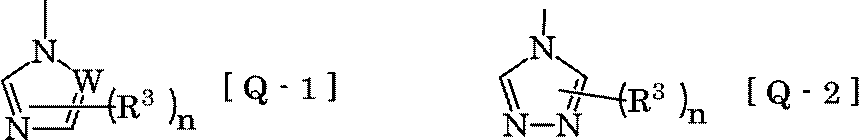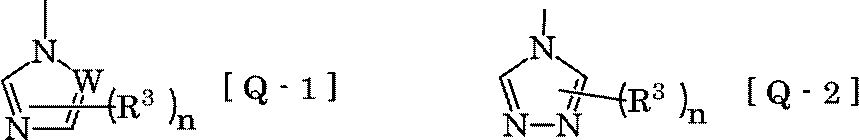WO2011161945A1 - アルコキシイミノ誘導体及び有害生物防除剤 - Google Patents
アルコキシイミノ誘導体及び有害生物防除剤 Download PDFInfo
- Publication number
- WO2011161945A1 WO2011161945A1 PCT/JP2011/003522 JP2011003522W WO2011161945A1 WO 2011161945 A1 WO2011161945 A1 WO 2011161945A1 JP 2011003522 W JP2011003522 W JP 2011003522W WO 2011161945 A1 WO2011161945 A1 WO 2011161945A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- group
- alkyl group
- compound
- reaction
- alkyl
- Prior art date
Links
Classifications
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N55/00—Biocides, pest repellants or attractants, or plant growth regulators, containing organic compounds containing elements other than carbon, hydrogen, halogen, oxygen, nitrogen and sulfur
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D249/00—Heterocyclic compounds containing five-membered rings having three nitrogen atoms as the only ring hetero atoms
- C07D249/02—Heterocyclic compounds containing five-membered rings having three nitrogen atoms as the only ring hetero atoms not condensed with other rings
- C07D249/08—1,2,4-Triazoles; Hydrogenated 1,2,4-triazoles
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N37/00—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom having three bonds to hetero atoms with at the most two bonds to halogen, e.g. carboxylic acids
- A01N37/44—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom having three bonds to hetero atoms with at the most two bonds to halogen, e.g. carboxylic acids containing at least one carboxylic group or a thio analogue, or a derivative thereof, and a nitrogen atom attached to the same carbon skeleton by a single or double bond, this nitrogen atom not being a member of a derivative or of a thio analogue of a carboxylic group, e.g. amino-carboxylic acids
- A01N37/50—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom having three bonds to hetero atoms with at the most two bonds to halogen, e.g. carboxylic acids containing at least one carboxylic group or a thio analogue, or a derivative thereof, and a nitrogen atom attached to the same carbon skeleton by a single or double bond, this nitrogen atom not being a member of a derivative or of a thio analogue of a carboxylic group, e.g. amino-carboxylic acids the nitrogen atom being doubly bound to the carbon skeleton
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/02—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with one or more oxygen or sulfur atoms as the only ring hetero atoms
- A01N43/04—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with one or more oxygen or sulfur atoms as the only ring hetero atoms with one hetero atom
- A01N43/06—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with one or more oxygen or sulfur atoms as the only ring hetero atoms with one hetero atom five-membered rings
- A01N43/08—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with one or more oxygen or sulfur atoms as the only ring hetero atoms with one hetero atom five-membered rings with oxygen as the ring hetero atom
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/02—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with one or more oxygen or sulfur atoms as the only ring hetero atoms
- A01N43/04—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with one or more oxygen or sulfur atoms as the only ring hetero atoms with one hetero atom
- A01N43/06—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with one or more oxygen or sulfur atoms as the only ring hetero atoms with one hetero atom five-membered rings
- A01N43/10—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with one or more oxygen or sulfur atoms as the only ring hetero atoms with one hetero atom five-membered rings with sulfur as the ring hetero atom
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/02—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with one or more oxygen or sulfur atoms as the only ring hetero atoms
- A01N43/04—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with one or more oxygen or sulfur atoms as the only ring hetero atoms with one hetero atom
- A01N43/20—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with one or more oxygen or sulfur atoms as the only ring hetero atoms with one hetero atom three- or four-membered rings
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/34—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with one nitrogen atom as the only ring hetero atom
- A01N43/40—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with one nitrogen atom as the only ring hetero atom six-membered rings
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/48—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with two nitrogen atoms as the only ring hetero atoms
- A01N43/50—1,3-Diazoles; Hydrogenated 1,3-diazoles
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/48—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with two nitrogen atoms as the only ring hetero atoms
- A01N43/56—1,2-Diazoles; Hydrogenated 1,2-diazoles
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/64—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with three nitrogen atoms as the only ring hetero atoms
- A01N43/647—Triazoles; Hydrogenated triazoles
- A01N43/653—1,2,4-Triazoles; Hydrogenated 1,2,4-triazoles
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/713—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with four or more nitrogen atoms as the only ring hetero atoms
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/72—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with nitrogen atoms and oxygen or sulfur atoms as ring hetero atoms
- A01N43/74—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with nitrogen atoms and oxygen or sulfur atoms as ring hetero atoms five-membered rings with one nitrogen atom and either one oxygen atom or one sulfur atom in positions 1,3
- A01N43/78—1,3-Thiazoles; Hydrogenated 1,3-thiazoles
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/72—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with nitrogen atoms and oxygen or sulfur atoms as ring hetero atoms
- A01N43/82—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with nitrogen atoms and oxygen or sulfur atoms as ring hetero atoms five-membered rings with three ring hetero atoms
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/72—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with nitrogen atoms and oxygen or sulfur atoms as ring hetero atoms
- A01N43/84—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with nitrogen atoms and oxygen or sulfur atoms as ring hetero atoms six-membered rings with one nitrogen atom and either one oxygen atom or one sulfur atom in positions 1,4
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N47/00—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom not being member of a ring and having no bond to a carbon or hydrogen atom, e.g. derivatives of carbonic acid
- A01N47/08—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom not being member of a ring and having no bond to a carbon or hydrogen atom, e.g. derivatives of carbonic acid the carbon atom having one or more single bonds to nitrogen atoms
- A01N47/10—Carbamic acid derivatives, i.e. containing the group —O—CO—N<; Thio analogues thereof
- A01N47/18—Carbamic acid derivatives, i.e. containing the group —O—CO—N<; Thio analogues thereof containing a —O—CO—N< group, or a thio analogue thereof, directly attached to a heterocyclic or cycloaliphatic ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C259/00—Compounds containing carboxyl groups, an oxygen atom of a carboxyl group being replaced by a nitrogen atom, this nitrogen atom being further bound to an oxygen atom and not being part of nitro or nitroso groups
- C07C259/02—Compounds containing carboxyl groups, an oxygen atom of a carboxyl group being replaced by a nitrogen atom, this nitrogen atom being further bound to an oxygen atom and not being part of nitro or nitroso groups with replacement of the other oxygen atom of the carboxyl group by halogen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D249/00—Heterocyclic compounds containing five-membered rings having three nitrogen atoms as the only ring hetero atoms
- C07D249/02—Heterocyclic compounds containing five-membered rings having three nitrogen atoms as the only ring hetero atoms not condensed with other rings
- C07D249/08—1,2,4-Triazoles; Hydrogenated 1,2,4-triazoles
- C07D249/10—1,2,4-Triazoles; Hydrogenated 1,2,4-triazoles with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/06—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/12—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/06—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/06—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic System
- C07F7/02—Silicon compounds
- C07F7/08—Compounds having one or more C—Si linkages
- C07F7/0803—Compounds with Si-C or Si-Si linkages
- C07F7/081—Compounds with Si-C or Si-Si linkages comprising at least one atom selected from the elements N, O, halogen, S, Se or Te
- C07F7/0812—Compounds with Si-C or Si-Si linkages comprising at least one atom selected from the elements N, O, halogen, S, Se or Te comprising a heterocyclic ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic System
- C07F7/02—Silicon compounds
- C07F7/08—Compounds having one or more C—Si linkages
- C07F7/10—Compounds having one or more C—Si linkages containing nitrogen having a Si-N linkage
Definitions
- the present invention relates to a novel alkoxyimino derivative or a salt thereof, and a pest control agent containing the derivative or a salt thereof as an active ingredient.
- Patent Document 1 discloses a hydroxymoylazole derivative, but is limited to a compound having a carbamic acid ester structure, and does not disclose an alkoxyimino derivative according to the present invention.
- Patent Document 2 discloses a hydroxymoyl derivative, but is limited to an O-acyl derivative and does not disclose an alkoxyimino derivative according to the present invention.
- Pesticides such as insecticides and acaricides used for useful crops are safe for human livestock, have little impact on the environment, and have a sufficient effect on pests at low doses It is desired to be a drug.
- pests that have acquired resistance have emerged through the use of insecticides and acaricides for many years, it is difficult to completely control pests with conventional drugs.
- An object of the present invention is to provide an excellent pest control agent that solves the above-mentioned problems of conventional pest control agents.
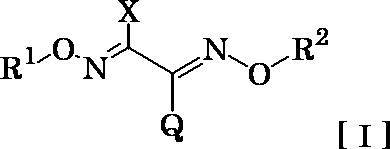
- the present inventors synthesized various alkoxyimino derivatives and studied their physiological activities. As a result, the inventors have found that the alkoxyimino derivative represented by the following general formula [I] has a high effect on pests and pests that have acquired resistance, and thus completed the present invention.
- the present invention has a gist characterized by the following.
- R 2 represents a C 1 -C 6 alkyl group, a C 2 -C 6 alkenyl group, a C 2 -C 6 alkynyl group, a C 3 -C 6 cycloalkyl group, a C 1 -C 6 haloalkyl group, a C 2 -C 6 Haloalkenyl group, C 2 -C 6 haloalkynyl group, C 1 -C 6 alkylthio C 1 -C 6 alkyl group, C 1 -C 6 alkylsulfinyl C 1 -C 6 alkyl group, C 1 -C 6 alkylsulfonyl C 1 to C 6 alkyl group, C 1 to C 6 alkoxy C 1 to C 6 alkyl group, C 1 to C 6 haloalkoxy C 1 to C 6 alkyl group, cyano C 1 to C
- R 1 is a C 1 -C 10 alkyl group, a C 2 -C 6 alkenyl group, a C 2 -C 6 alkynyl group, a C 3 -C 6 cycloalkyl group, a C 3 -C 6 cycloalkyl C 1 -C 6 alkyl Group, C 1 -C 6 haloalkyl group, C 2 -C 6 haloalkenyl group, C 1 -C 6 alkylthio C 1 -C 6 alkyl group, C 1 -C 6 alkoxy C 1 -C 6 alkyl group, C 1- C 6 haloalkoxy C 1 -C 6 alkyl group, tri (C 1 -C 6 alkyl) silyl C 1 -C 6 alkyl group, cyano C 1 -C 6 alkyl group, gem-di (C 1 -C 6 alkoxy) A C 1 -C 6 alkyl group, a hydroxy C 1 -C
- a phenyl group which may a substituent substituted by phenyl C 1 may be ⁇ C 6 alkyl group selected from substituent group alpha
- phenyl C 2 may be substituted with a substituent selected from substituent group alpha ⁇
- an oxygen atom which may be the same or different
- a sulfur atom and a nitrogen atom which are selected from 1
- a heterocyclic group having 1 to 9 carbon atoms having 5 heteroatoms (the group is a 1 to 5 halogen atom, a C 1 to C 6 alkyl group, a C 1 to C 6 haloalkyl group, a C 1 to C 6 alkoxy group);
- a heterocyclic group having 1 to 9 carbon atoms and having 1 to 5 heteroatoms selected from oxygen, sulfur and nitrogen atoms which may be the same or different
- a 3- to 8-membered ring may be formed, and the alkylene chain may contain one oxygen atom, sulfur atom or nitrogen atom;
- R 8 and R 9 are each a hydrogen atom, a C 1 -C 6 alkyl group or a C 1 -C 6 alkoxycarbonyl group,
- R 10 is an R 6 R 7 N group or Q;
- R 11 is a C 1 -C 6 alkyl group, The alkoxyimino derivative according to (1) or an agriculturally acceptable salt thereof.
- a pest control agent comprising the alkoxyimino derivative or the agriculturally acceptable salt thereof described in any one of (1) to (4) as an active ingredient.
- the agrochemical in the present invention means an insecticide / acaricide, nematicide, etc. in the field of agriculture and horticulture.
- the C 1 -C 6 alkyl group means a linear or branched alkyl group having 1 to 6 carbon atoms unless otherwise specified, and includes, for example, methyl, ethyl, n-propyl, isopropyl, n-butyl, sec -Butyl, isobutyl, tert-butyl, n-pentyl, 1-methylbutyl, 2-methylbutyl, isopentyl, 1-ethylpropyl, 1,1-dimethylpropyl, 1,2-dimethylpropyl, neopentyl, n-hexyl, 1 -Methylpentyl, 2-methylpentyl, 3-methylpentyl, isohexyl, 1-ethylbutyl, 2-ethylbutyl, 1,1-dimethylbutyl, 1,2-dimethylbutyl, 1,3-dimethylbutyl, 2,2-dimethyl Butyl, 2,3-
- the C 1 ⁇ C 10 alkyl group unless otherwise specified, a linear or branched alkyl group having 1 to 10 carbon atoms, for example, in addition to the example of the C 1 ⁇ C 8 alkyl group, n- Nonyl, isononyl, n-decanyl, isodecanyl, 7,7-dimethyloctyl or n-undecanyl can be exemplified.
- the C 1 -C 6 haloalkyl group is the same or different, and is a straight chain having 1 to 6 carbon atoms substituted with 1 to 13 halogen atoms, more preferably 1 to 5 halogen atoms.
- a chain or branched alkyl group such as 2-fluoroethyl, 2,2,2-trifluoroethyl, 3,3,3-trifluoropropyl or 2,2,2-trichloroethyl be able to.
- a C 1 -C 6 haloalkoxy group is, unless otherwise limited, a carbon number in which the haloalkyl moiety is substituted with 1 to 11, preferably 1 to 5, the same or different halogen atoms as defined above.
- the C 1 -C 6 alkylsulfinyl group means a linear or branched alkyl-S (O) — group having 1 to 6 carbon atoms, wherein the alkyl part of the alkylsulfinyl has the above-mentioned meaning, unless otherwise limited. Examples include groups such as methylsulfinyl or ethylsulfinyl.
- C 1 -C 6 alkylthio C 1 -C 6 alkyl group means, unless otherwise specified, the number of carbon atoms substituted by an alkylthio group having 1 to 6 carbon atoms, wherein the alkyl portion and the alkyl portion of alkylthio have the above-mentioned meanings.
- a C 1 -C 6 alkoxy C 1 -C 6 alkyl group unless otherwise limited, has 1 to 6 carbon atoms substituted with alkoxy having 1 to 6 carbon atoms, the alkyl and alkoxy moieties having the above-mentioned meanings. 6 alkyl groups such as methoxymethyl, ethoxymethyl, isopropoxymethyl, pentyloxymethyl, methoxyethyl or butoxyethyl.
- a phenoxy C 1 -C 6 alkyl group means an alkyl group having 1 to 6 carbon atoms in which the alkyl moiety is substituted with the phenyl-O— group having the above-mentioned meaning, for example, phenoxyethyl, 4 And groups such as -trifluoromethylphenoxypropyl or 2- (2-chlorophenoxy) propyl.
- the phenyl C 1 -C 6 alkyl group means an alkyl group having 1 to 6 carbon atoms substituted by a phenyl group, wherein the alkyl part has the above-mentioned meaning, unless specifically limited, for example, benzyl, 1-phenylethyl Or 2-phenylethyl can be mentioned.
- the phenyl C 2 -C 6 alkenyl group means an alkenyl group having 2 to 6 carbon atoms in which the alkyl portion is substituted with the phenyl group having the above-mentioned meaning, unless otherwise limited, and includes, for example, styryl or 3-phenyl-2 -Propenyl and the like can be mentioned.
- gem-di (C 1 -C 6 alkoxy) C 1 -C 6 alkyl group has the same carbon number substituted with two alkoxy groups having the above meanings, and has 1 to 6 carbon atoms Represents an alkyl group, and examples thereof include a diethoxymethyl group and a 2-dimethoxypropyl group.
- a hydroxy C 1 -C 6 alkyl group represents an alkyl group having 1 to 6 carbon atoms in which an alkyl moiety is substituted with a hydroxyl group, such as 2-hydroxyethyl, 3-hydroxy-n-butyl or Examples thereof include a 3-hydroxy-n-propyl group.
- the C 1 -C 6 alkoxycarbonyl group means alkoxy-C ( ⁇ O) — in which the alkoxy moiety has the above-mentioned meaning unless specifically limited, and examples thereof include a methoxycarbonyl or isopropoxycarbonyl group.
- the compounds encompassed by the present invention may have E-isomers and Z-isomers depending on the type of substituents, but the present invention is not limited to these E-isomers, Z-isomers or E-isomers. -A mixture containing isomers and Z-isomers in any proportion.
- the compounds included in the present invention may have optical isomers resulting from the presence of one or more asymmetric carbon atoms and asymmetric sulfur atoms. Body, racemate or diastereomer.
- Compound [Ia-I] can be produced by reacting compound [Ib-I] and compound [II] in a solvent in the presence of a base.
- W is a nitrogen atom
- compound [Ic-I] can be produced in the same manner.
- halogenating agent examples include carbon tetrachloride or carbon tetrabromide in the presence of phosphorus pentachloride, thionyl chloride or triphenylphosphine.
- the amount of the halogenating agent to be used may be appropriately selected from the range of 1.0 to 20.0 mol, preferably 1.0 to 6.0 mol, relative to 1.0 mol of compound [III].
- the compound [Ia-VI] can be isolated by concentrating the reaction mixture or pouring it into water, extracting it with an organic solvent, and then concentrating it.
- the isolated compound [Ia-VI] can be further purified by column chromatography or the like, if necessary.
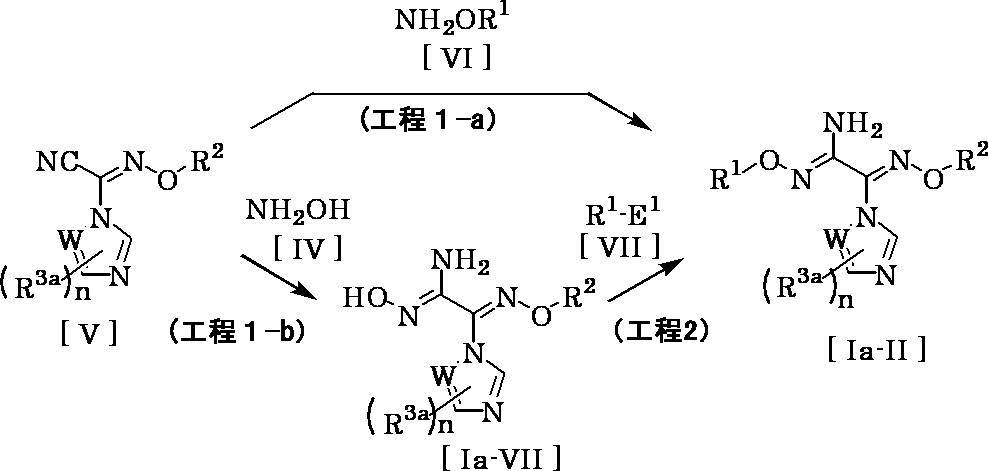
- Step 1-b Compound [Ia-VII] can be produced by reacting compound [V] with compound [IV] in a solvent.
- the compound [IV] to be used may be a salt such as hydrochloride or sulfate, and in this case, the reaction may be carried out in the presence of a base.
- the amount of compound [IV] used in this reaction may be appropriately selected from the range of usually 1 to 5 equivalents, preferably 1 to 2 equivalents, relative to 1 equivalent of compound [V].
- Compound [Ia-II] can be produced by reacting compound [Ia-VII] with compound [VII] in a solvent in the presence of a base.
- the amount of the solvent is usually 0.1 to 50 liters, preferably 0.2 to 3.0 liters, per 1 mol of compound [Ia-VII].
- reaction time of this reaction varies depending on the reaction temperature, reaction substrate, reaction amount, etc., but is usually in the range of 1 to 48 hours.
- Compound [V] can be produced by reacting compound [IX] with a dehydrating agent in a solvent.
- reaction time of this reaction varies depending on the reaction temperature, reaction substrate, reaction amount, etc., but is usually in the range of 1 to 48 hours.
- Examples of the solvent and the base that can be used in this reaction include those described in the above [Production Method 1].
- the amount of the solvent is usually 0.1 to 50 liters, preferably 0.2 to 3.0 liters, per 1 mol of compound [X].
- reaction time of this reaction varies depending on the reaction temperature, reaction substrate, reaction amount, etc., but is usually in the range of 1 to 48 hours.
- Examples of the base that can be used in this reaction include inorganic bases such as potassium carbonate, sodium hydride and sodium hydroxide; and organic bases such as 1,8-diazabicyclo [5.4.0] undec-7-ene (DBU). Can be mentioned.
- the amount of the base used may be appropriately selected from the range of 0.01 to 100 mol, preferably 0.1 to 10 mol, relative to 1 mol of compound [VIII].
- acids that can be used in this reaction include inorganic acids such as hydrochloric acid, hydrobromic acid, and sulfuric acid; and organic acids such as acetic acid and trifluoroacetic acid.
- the amount of the acid to be used can be 1 mol to large excess, preferably 1 to 100 mol, per 1 mol of compound [VIII].
- Examples of the solvent that can be used in this reaction include alcohols such as methanol or ethanol; ethers such as tetrahydrofuran; ketones such as acetone or methyl isobutyl ketone; amides such as N, N-dimethylformamide and N, N-dimethylacetamide.
- a sulfur compound such as dimethyl sulfoxide or sulfolane; acetonitrile; water; or a mixture thereof.
- the amount of the solvent to be used is 0.01 to 100 liters, preferably 0.1 to 10 liters, per 1 mol of the formula [VIII].
- the reaction temperature for this reaction is usually selected from the range of the boiling point of the inert solvent used from ⁇ 20 ° C., preferably in the range of 0 ° C. to 100 ° C.
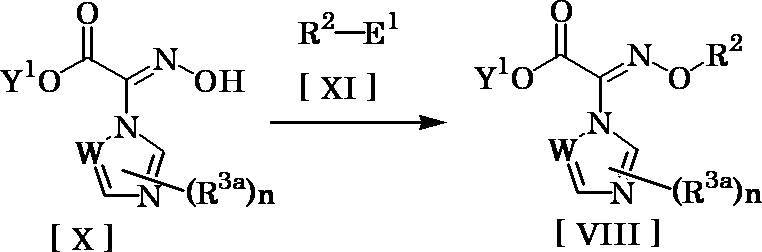
- Step 6 Compound [III] can be produced by reacting compound [XII] with compound [VI] in a solvent using a condensing agent.
- the compound [VI] to be used may be a salt such as hydrochloride or sulfate, and in this case, the reaction may be carried out in the presence of a base.
- condensing agent examples include dicyclohexylcarbodiimide (DCC), N- (3-dimethylaminopropyl) -N′-ethylcarbodiimide hydrochloride (EDC or WSC), N, N-carbonyldiimidazole, 2-chloro-1,3- Dimethylimidazolium chloride, 2-chloro-1-pyridinium iodide, and the like can be used.
- the amount of the condensing agent to be used is usually appropriately selected from the range of 1 to 20 equivalents relative to 1 equivalent of compound [XII], and preferably 1.0 to 10 equivalents.
- the amount of compound [XIII] or compound [XIV] used in this reaction may be appropriately selected from the range of 1.0 to 5.0 equivalents relative to 1.0 equivalent of compound [III]. Is 1.1 to 2.0 equivalents.
- the compound [Ia-VIII] can be isolated by pouring the reaction mixture into water, extracting with an organic solvent, and then concentrating.
- the isolated compound [Ia-VIII] can be further purified by column chromatography or the like, if necessary.
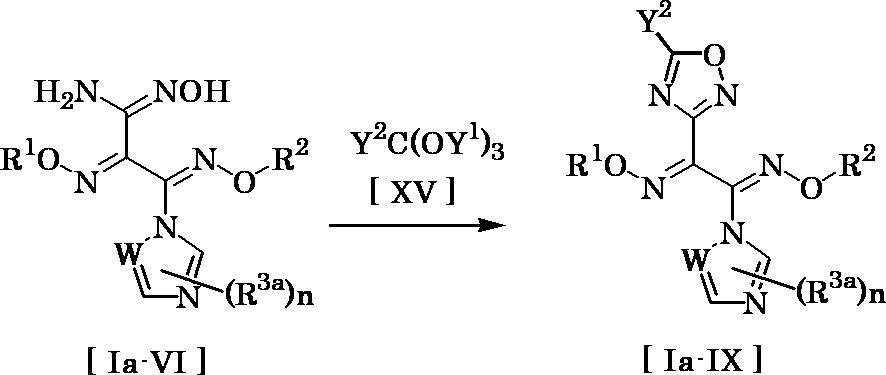
- Compound [Ia-IX] can be produced by reacting compound [Ia-VI] with compound [XV] in the presence of a catalytic amount of an acid.
- the amount of compound [XV] used in this reaction may be appropriately selected from the range of usually 1 to 5 equivalents, preferably 1 to 2 equivalents, relative to 1 equivalent of compound [Ia-VI]. It may be used as a solvent.
- a solvent may be used, and examples of the solvent that can be used include alcohols such as methanol, ethanol and propanol, and sulfur compounds such as dimethyl sulfoxide and sulfolane.
- the amount of the solvent is usually 0.1 to 50 liters, preferably 0.2 to 3.0 liters, per 1 mol of compound [Ia-VI].
- acids that can be used in this reaction include inorganic acids such as sulfuric acid; sulfonic acids such as p-toluenesulfonic acid; Lewis acids such as boron trifluoride; or acetic acids such as trifluoroacetic acid.
- the reaction temperature of this reaction is usually any temperature from room temperature to the reflux temperature in the reaction system, preferably in the range of 50 ° C to 140 ° C.
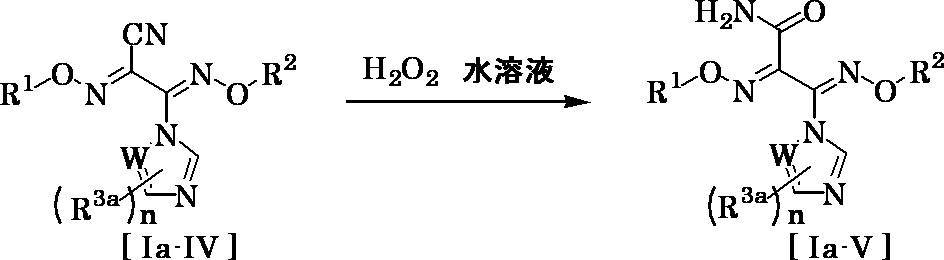
- the amount of compound [XVI] used in this reaction may be appropriately selected from the range of usually 1 to 10 equivalents, preferably 2 to 5 equivalents, relative to 1 equivalent of compound [Ia-IV].
- reaction time of this reaction varies depending on the reaction temperature, reaction substrate, reaction amount, etc., but is usually in the range of 1 to 48 hours.
- the compound [Ia-X] can be isolated by performing an operation such as concentration of the reaction mixture or pouring into water, extraction with an organic solvent, and concentration.
- the isolated compound [Ia-X] can be further purified by column chromatography or the like, if necessary.
- Compound [Ia-XI] can be produced by reacting compound [Ia-X] with an oxidizing agent in a solvent.
- the compound [Ia-XI] can be isolated by pouring the reaction mixture into water, extracting with an organic solvent, and then concentrating.
- the isolated compound [Ia-XI] can be further purified by column chromatography, recrystallization or the like, if necessary.
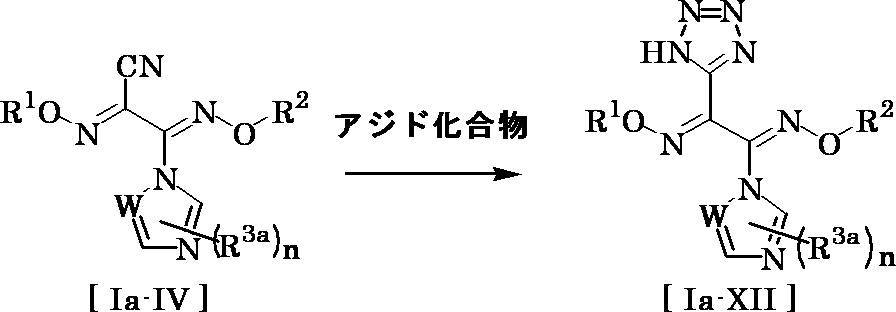
- Compound [Ia-XII] can be produced by reacting compound [Ia-IV] with an azide compound.
- Examples of the azide compound that can be used in this reaction include trialkylmetals such as trimethyltin azide or trimethylsilicon azide, or sodium azide.
- the reaction may be carried out in the presence of a Lewis acid such as zinc bromide or aluminum chloride, or in the presence of a tin compound such as dibutyltin oxide.
- the reaction temperature of this reaction is usually any temperature from room temperature to the reflux temperature in the reaction system, preferably in the range of 50 ° C to 140 ° C.
- reaction time of this reaction varies depending on the reaction temperature, reaction substrate, reaction amount, etc., but is usually in the range of 1 to 24 hours.
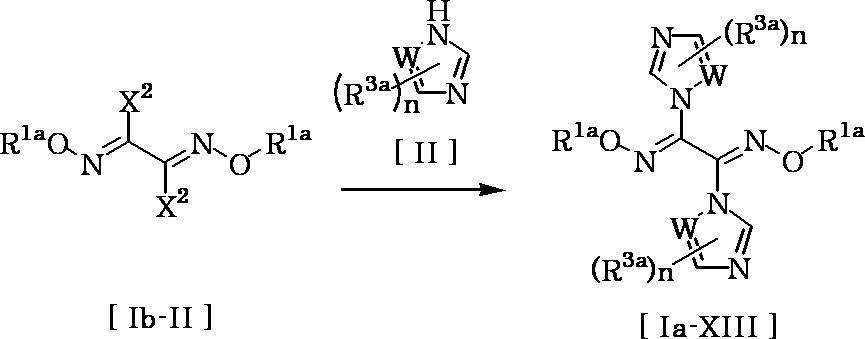
- Compound [Ia-XIII] can be produced by reacting compound [Ib-II] with compound [II] in a solvent in the presence of a base.
- the amount of compound [II] used in this reaction may be appropriately selected from the range of usually 1 to 5 equivalents, preferably 1 to 2 equivalents, relative to 1 equivalent of compound [Ib-II].
- Examples of the base that can be used in this reaction include those described in the above [Production Method 1].
- the amount of the base used may be appropriately selected from the range of 1.0 to 20.0 mol, preferably 1.0 to 6.0 mol, per 1 mol of compound [Ib-II].
- Examples of the solvent that can be used in this reaction include the same solvents as those described in the above [Production Method 1].
- the amount of the solvent is usually 0.1 to 50 liters, preferably 0.2 to 3.0 liters, per 1 mol of compound [Ib-II].
- the compound [Ia-XIII] can be isolated by pouring the reaction mixture into water, extracting with an organic solvent, and then concentrating.
- the isolated compound [Ia-XIII] can be further purified by column chromatography, recrystallization or the like, if necessary.
- Examples of the solvent that can be used in this reaction include the same solvents as those described in the above [Production Method 1].
- the amount of the solvent is usually 0.1 to 50 liters, preferably 0.2 to 3.0 liters, relative to 1 mole of compound [Ia-XIII].
- reaction time of this reaction varies depending on the reaction temperature, reaction substrate, reaction amount, etc., but is usually in the range of 1 to 48 hours.
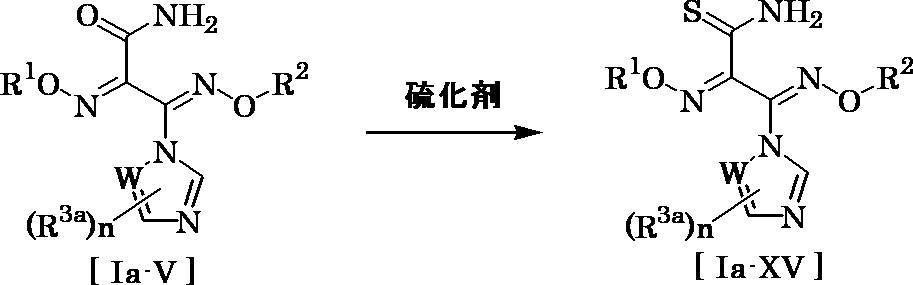
- the amount of the sulfurizing agent used in this reaction may be appropriately selected from the range of usually 1 to 5 equivalents, preferably 1 to 2 equivalents, relative to 1 equivalent of compound [Ia-V].
- Examples of the solvent that can be used in this reaction include ethers such as diethyl ether, 1,2-dimethoxyethane, and tetrahydrofuran; nitriles such as acetonitrile and propionitrile; and aromatic hydrocarbons such as benzene, toluene, xylene, and pyridine. Or halogenated hydrocarbons such as 1,2-dichloroethane or chlorobenzene.
- the amount of the solvent is usually 0.1 to 50 liters, preferably 0.2 to 3.0 liters, per 1 mol of compound [Ia-V].
- reaction time of this reaction varies depending on the reaction temperature, reaction substrate, reaction amount, etc., but is usually in the range of 1 to 24 hours.
- Step 9-a Compound [Ia-XVI] can be produced by reacting compound [Ia-IV], hydrogen chloride, and C1-C6 alcohols (Y 1 OH) such as methanol or ethanol.
- the reaction temperature of this reaction is usually any temperature from ⁇ 50 ° C. to the reflux temperature in the reaction system, preferably in the range of ⁇ 10 ° C. to 100 ° C.
- Step 9-b Compound [Ia-XVI] comprises compound [Ia-IV] and a metal salt (Y 1 OM) of a C1-C6 alcohol such as sodium methoxide or sodium ethoxide, and a C1-C6 alcohol (Y It can also be produced by reacting in 1 OH).
- a metal salt Y 1 OM
- a C1-C6 alcohol such as sodium methoxide or sodium ethoxide
- Y It can also be produced by reacting in 1 OH).
- the amount of the metal salt of alcohol used in this reaction may be appropriately selected from the range of catalytic amount to 10 equivalents, preferably 0.1 to 5 equivalents, relative to 1 equivalent of compound [Ia-IV]. is there.
- the amount of alcohol used in this reaction is usually 0.1 to 50 liters, preferably 0.2 to 3.0 liters, per 1 mol of compound [Ia-IV].
- the reaction temperature of this reaction is usually any temperature from ⁇ 50 ° C. to the reflux temperature in the reaction system, preferably in the range of ⁇ 10 ° C. to 100 ° C.
- reaction time of this reaction varies depending on the reaction temperature, reaction substrate, reaction amount, etc., but is usually in the range of 1 to 48 hours.
- reaction mixture may be concentrated and used in the next reaction as it is, but it is poured into water, extracted with an organic solvent, and then concentrated, dried, etc. to give compound [Ia -XVI] can also be isolated.
- the isolated compound [Ia-XVI] can be further purified by column chromatography, recrystallization or the like, if necessary.
- reaction time of this reaction varies depending on the reaction temperature, reaction substrate, reaction amount, etc., but is usually in the range of 1 to 48 hours.
- the compound [Ia-XVII] can be isolated by pouring the reaction mixture into water, extracting with an organic solvent, and then concentrating and drying.
- the isolated compound [Ia-XVII] can be further purified by column chromatography, recrystallization or the like, if necessary.
- the amount of compound [XVIII] used in this reaction may be appropriately selected from the range of usually 1 to 10 equivalents, preferably 2 to 5 equivalents, relative to 1 equivalent of compound [Ia-XVII].
- Examples of the solvent that can be used in this reaction include ethers such as 1,4-dioxane, 1,2-dimethoxyethane, and tetrahydrofuran; aromatic hydrocarbons such as benzene, toluene, and xylene; or halogenation such as chloroform or dichloromethane. There may be mentioned hydrocarbons.
- the amount of the solvent is usually 0.1 to 50 liters, preferably 0.2 to 3.0 liters, per 1 mol of compound [Ia-XVII].
- Lewis acids examples include aluminums such as trimethylaluminum or aluminum chloride.
- the amount of the Lewis acid to be used is usually appropriately selected from the range of 1 to 3 equivalents, preferably 1 to 2 equivalents, relative to 1 equivalent of the compound [Ia-XVII].
- Examples of the solvent that can be used in this reaction include alcohols such as methanol, ethanol, and propanol; ethers such as 1,4-dioxane, 1,2-dimethoxyethane, and tetrahydrofuran; aromatic hydrocarbons such as benzene, toluene, and xylene. Or halogenated hydrocarbons such as chloroform or dichloromethane.
- the amount of the solvent is usually 0.1 to 50 liters, preferably 0.2 to 3.0 liters, per 1 mol of compound [Ia-XVII].
- the reaction temperature of this reaction is usually any temperature from ⁇ 50 ° C. to the reflux temperature in the reaction system, preferably in the range of ⁇ 10 ° C. to 100 ° C.
- reaction time of this reaction varies depending on the reaction temperature, reaction substrate, reaction amount, etc., but is usually in the range of 1 to 48 hours.
- the compound [Ia-XVIII] can be isolated by concentrating the reaction mixture or pouring it into water, extracting with an organic solvent, and then concentrating.
- the isolated compound [Ia-XVIII] can be further purified by column chromatography or the like, if necessary.
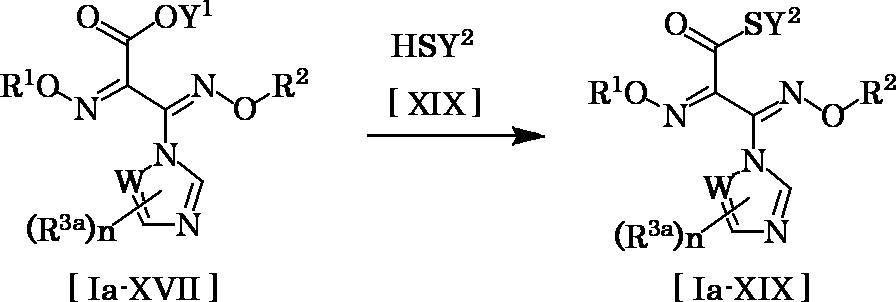
- the amount of compound [XIX] used in this reaction may be appropriately selected from the range of usually 1 to 10 equivalents, preferably 2 to 5 equivalents, relative to 1 equivalent of compound [Ia-XVII].
- Lewis acid examples include aluminum compounds such as trimethylaluminum or aluminum chloride.
- the amount of the Lewis acid to be used is usually appropriately selected from the range of 1 to 3 equivalents, preferably 1 to 2 equivalents, relative to 1 equivalent of compound [Ia-XVII].
- the reaction temperature of this reaction is usually any temperature from ⁇ 50 ° C. to the reflux temperature in the reaction system, preferably in the range of ⁇ 10 ° C. to 100 ° C.
- reaction time of this reaction varies depending on the reaction temperature, reaction substrate, reaction amount, etc., but is usually in the range of 1 to 48 hours.
- the compound [Ia-XIX] can be isolated by concentrating the reaction mixture or pouring it into water, extracting it with an organic solvent, and concentrating it.
- the isolated compound [Ia-XIX] can be further purified by column chromatography or the like, if necessary.
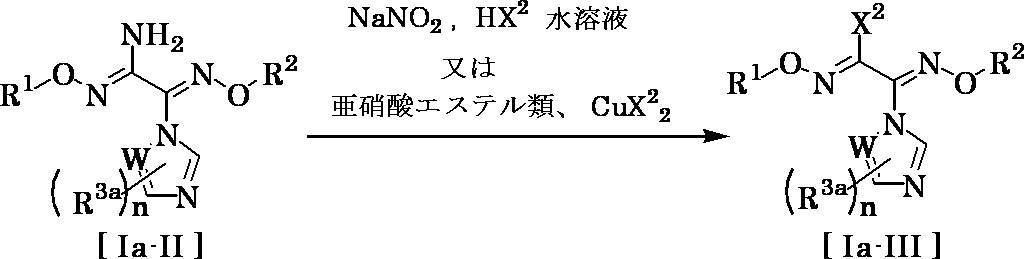
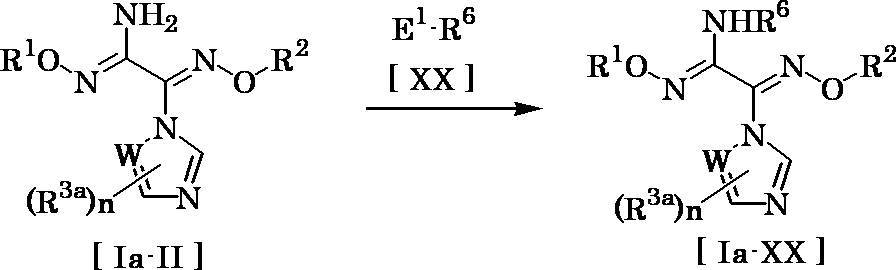
- Compound [Ia-XX] can be produced by reacting compound [Ia-II] with compound [XX] in a solvent in the presence of a base.
- the amount of the base used may be appropriately selected from the range of usually 1 to 20 equivalents, preferably 1 to 10 equivalents, relative to 1 equivalent of compound [Ia-II].
- reaction time of this reaction varies depending on the reaction temperature, reaction substrate, reaction amount, etc., but is usually in the range of 1 to 24 hours.
- the compound [Ia-XX] can be isolated by pouring the reaction mixture into water, extracting with an organic solvent, and then concentrating.
- the isolated compound [Ia-XX] can be further purified by column chromatography or the like, if necessary.
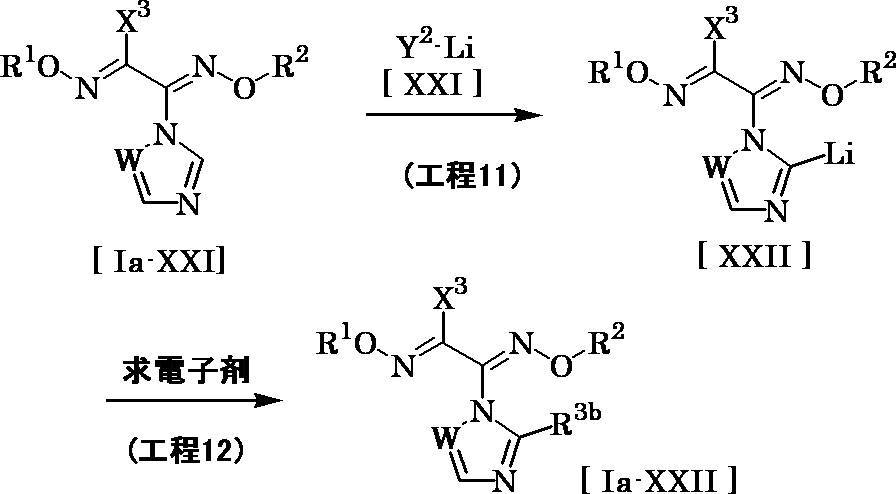
- the amount of compound [XXI] used in this reaction may be appropriately selected from the range of 1.0 to 5.0 equivalents relative to 1.0 equivalent of compound [Ia-XXI]. 1 to 2.0 equivalents.
- Examples of the solvent that can be used in this reaction include ethers such as diethyl ether, 1,2-dimethoxyethane, and tetrahydrofuran.
- the amount of the solvent is usually 0.1 to 50 liters, preferably 0.2 to 3.0 liters, per 1 mol of compound [Ia-XXI].
- the reaction temperature of this reaction is usually any temperature from ⁇ 100 ° C. to the reflux temperature in the reaction system, preferably in the range of ⁇ 70 ° C. to 0 ° C.
- reaction mixture containing the compound [XXII] is used in the next reaction without purification.
- Step 12 Compound [Ia-XXII] can be produced by reacting a reaction mixture containing compound [XXII] with an electrophile in a solvent.
- Examples of the electrophile that can be used in this reaction include halogens such as chlorine and bromine; halogenated C 1 -C 6 alkyls such as methyl iodide and ethyl bromide; 1-chloro-2-bromoethane, hexachloroethane and the like. And halogenated C 1 -C 6 haloalkyl; di C 1 -C 6 alkyl disulfide such as dimethyl disulfide and diethyl disulfide; or sulfur; or N, N-dimethylformamide and the like.
- the amount of the electrophile to be used may be appropriately selected from the range of 1.0 to 5.0 mol, preferably 1.1 to 2.0 mol, relative to 1.0 mol of compound [XXII].
- the reaction temperature of this reaction is usually any temperature from ⁇ 100 ° C. to the reflux temperature in the reaction system, preferably in the range of ⁇ 70 ° C. to 0 ° C.
- the compound [Ia-XXII] can be isolated by pouring the reaction mixture into water, extracting with an organic solvent, and then concentrating.
- the isolated compound [Ia-XXII] can be further purified by column chromatography or the like, if necessary.
- Step 13 Compound [XXV] can be produced by reacting compound [XXIII] with compound [XXIV] in the presence of a Lewis acid in a solvent.
- Examples of the solvent and Lewis acid that can be used in this reaction include those described in the above [Production Method 18].
- the amount of the solvent is usually 0.1 to 50 liters, preferably 0.2 to 3.0 liters, per 1 mol of compound [XXIII].
- the amount of Lewis acid to be used is usually appropriately selected from the range of 1 to 3 equivalents, preferably 1 to 2 equivalents, relative to 1 equivalent of compound [XXIII].
- a base may be used in place of the Lewis acid, and examples of the base include the same ones as described in the above [Production Method 18].
- the amount of the base used may be appropriately selected from the range of usually 1 to 3 equivalents, preferably 1 to 2 equivalents, relative to 1 equivalent of compound [XXIII].
- the reaction temperature of this reaction is usually any temperature from ⁇ 50 ° C. to the reflux temperature in the reaction system, preferably in the range of ⁇ 10 ° C. to 100 ° C.
- reaction time of this reaction varies depending on the reaction temperature, reaction substrate, reaction amount, etc., but is usually in the range of 1 to 48 hours.
- the compound [XXV] can be isolated by performing an operation such as concentration of the reaction mixture or pouring into water, extraction with an organic solvent, and concentration.
- the isolated compound [XXV] can be further purified by column chromatography or the like, if necessary.
- Compound [XXV] is obtained by reacting compound [XXVIII] produced by hydrolyzing compound [XXIII] in the presence of an acid or base with compound [XXIV] in a solvent in the presence of a condensing agent. Can also be manufactured. *
- the amount of compound [XXIV] used in this reaction may be appropriately selected from the range of usually 1.0 to 5 equivalents, preferably 1.1 to 2 equivalents, relative to 1 equivalent of compound [XXVIII]. .
- Examples of the condensing agent and solvent that can be used in this reaction include those described in the above [Production Method 9].
- the amount of the condensing agent to be used is usually appropriately selected from the range of 1 to 20 equivalents, preferably 1.2 to 10 equivalents, relative to 1 equivalent of compound [XXVIII].
- the amount of the solvent is usually 0.1 to 50 liters, preferably 0.2 to 3.0 liters, relative to 1 mol of compound [XXVIII].
- the reaction temperature of this reaction is usually any temperature from ⁇ 50 ° C. to the reflux temperature in the reaction system, preferably in the range of ⁇ 10 ° C. to 100 ° C.
- the compound [XXV] can be isolated by performing operations such as pouring the reaction mixture into water, extracting with an organic solvent, and concentrating.
- the isolated compound [XXV] can be further purified by column chromatography or the like, if necessary.
- Step 14 Compound [Ib-III] can be produced by reacting compound [XXV] with a halogenating agent in a solvent.
- halogenating agent examples include those described in the above [Production Method 3].
- the amount of the halogenating agent to be used may be appropriately selected from the range of 1.0 to 20.0 mol, preferably 1.0 to 6.0 mol, relative to 1.0 mol of compound [XXV].
- Examples of the solvent that can be used in this reaction include the same solvents as described in the above [Production Method 3].
- the amount of the solvent is usually 0.1 to 50 liters, preferably 0.2 to 3.0 liters, relative to 1.0 mol of the compound [XXV].
- the reaction temperature of this reaction is usually any temperature from ⁇ 50 ° C. to the reflux temperature in the reaction system, preferably in the range of 0 ° C. to 100 ° C.
- the compound [Ib-III] can be isolated by performing an operation such as concentration of the reaction mixture or pouring into water, extraction with an organic solvent, and concentration.
- the isolated compound [Ib-III] can be further purified by column chromatography, recrystallization or the like, if necessary.
- the compound [XXIII] is, for example, Journal of Medicinal Chemistry, pages 4608 to 4612 (1992) or Journal of Organic Chemistry, 496. It can be produced according to the method described on pages 500 to 2001 (2001).
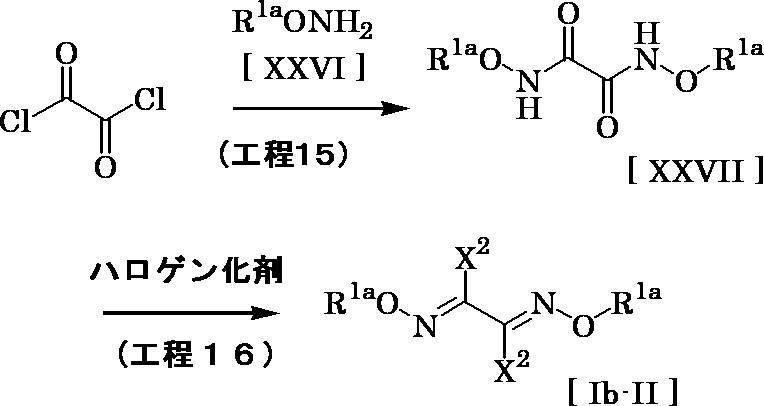
- Step 15 Compound [XXVII] can be produced by reacting oxalyl dichloride with compound [XXVI] in the presence of a base in a solvent.
- the amount of compound [XXVI] used in this reaction may be appropriately selected from the range of usually 2 to 5 equivalents relative to 1 equivalent of oxalyl dichloride, preferably 2.0 to 3.0 equivalents.
- the solvent that can be used for the reaction examples include ethers such as diethyl ether, 1,2-dimethoxyethane, and tetrahydrofuran; nitriles such as acetonitrile and propionitrile; aliphatic hydrocarbons such as hexane and heptane; benzene, toluene, or Mention may be made of aromatic hydrocarbons such as xylene; halogenated hydrocarbons such as 1,2-dichloroethane or chlorobenzene; or mixtures thereof.
- the amount of the solvent is usually 0.1 to 50 liters, preferably 0.2 to 3.0 liters per mole of oxalyl dichloride.
- Bases that can be used in this reaction are, for example, alkali metal carbonates such as sodium carbonate or potassium carbonate; inorganic bases such as alkali metal bicarbonates such as sodium hydrogen carbonate or potassium hydrogen carbonate; sodium hydride or potassium hydride.
- Metal bases such as triethylamine or 1,8-diazabicyclo [5.4.0] -7-undecene, and the like.
- the amount of the base used may be appropriately selected from the range of usually 2 to 10 equivalents, preferably 2 to 5 equivalents, relative to 1 equivalent of the compound oxalyl dichloride.
- the reaction temperature of this reaction is usually any temperature from ⁇ 20 ° C. to the reflux temperature in the reaction system, preferably in the range of ⁇ 10 ° C. to 100 ° C.
- reaction time of this reaction varies depending on the reaction temperature, reaction substrate, reaction amount, etc., but is usually in the range of 1 to 48 hours.
- the compound [XXVII] can be isolated by pouring the reaction mixture into water, extracting with an organic solvent, and then concentrating.
- the isolated compound [XXVII] can be further purified by column chromatography, recrystallization or the like, if necessary.
- halogenating agent examples include those described in the above [Production Method 3].
- the amount of the halogenating agent used may be appropriately selected from the range of 1.0 to 20.0 mol, preferably 1.0 to 6.0 mol, relative to 1.0 mol of the general formula [XXVII].
- Examples of the solvent that can be used in this reaction include the same solvents as described in the above [Production Method 3].
- the amount of the solvent is usually 0.1 to 50 liters, preferably 0.2 to 3.0 liters, per 1 mol of compound [XXVII].
- reaction time of this reaction varies depending on the reaction temperature, reaction substrate, reaction amount, etc., but is usually in the range of 1 to 48 hours.
- the compound [Ib-II] can be isolated by performing an operation such as concentration of the reaction mixture or pouring into water, extraction with an organic solvent, and concentration.
- the isolated compound [Ib-II] can be further purified by column chromatography, recrystallization or the like, if necessary.
- Step 17 Compound [XXIX] can be produced by reacting compound [Ia-XXIII] with hydrogen in the presence of a catalyst in a solvent.
- Examples of the catalyst used in this reaction include palladium, palladium hydroxide, or palladium or palladium hydroxide supported on activated carbon.
- the solvent that can be used for the reaction examples include ethers such as diethyl ether, 1,4-dioxane or tetrahydrofuran; alcohols such as methanol or ethanol; acetates such as ethyl acetate or butyl acetate; or acetic acid. it can.
- the amount of the solvent is usually 0.1 to 50 liters, preferably 0.2 to 3.0 liters per 1 mol of [Ia-XXIII].
- the reaction temperature of this reaction is usually any temperature from ⁇ 50 ° C. to the reflux temperature in the reaction system, preferably in the range of 0 ° C. to 100 ° C.
- reaction time of this reaction varies depending on the reaction temperature, reaction substrate, reaction amount, etc., but is usually in the range of 1 to 48 hours.
- the compound [XXIX] can be isolated by concentrating the reaction mixture or pouring it into water and extracting it with an organic solvent, followed by concentration.
- the isolated compound [XXIX] can be further purified by column chromatography, recrystallization or the like, if necessary.
- Step 18 Compound [Ia-I] can be produced by reacting compound [XXIX] and [VII] in the presence of a base in a solvent.
- the amount of compound [VII] used in this reaction may be appropriately selected from the range of usually 1.0 to 5.0 equivalents relative to 1 equivalent of compound [XXIX], preferably 1.0 to 2. 0 equivalents.
- the amount of the solvent is usually 0.1 to 50 liters, preferably 0.2 to 3.0 liters, relative to 1 mol of the compound [XXIX].
- the amount of the base used may be appropriately selected from the range of 0.5 to 20 equivalents, preferably 1 to 10 equivalents, per 1 equivalent of the compound [XXIX].
- the reaction temperature of this reaction is usually any temperature from ⁇ 50 ° C. to the reflux temperature in the reaction system, preferably in the range of ⁇ 10 ° C. to 100 ° C.
- reaction time of this reaction varies depending on the reaction temperature, reaction substrate, reaction amount, etc., but is usually in the range of 1 to 24 hours.
- the pest control agent of the present invention is characterized by containing an alkoxyimino derivative represented by the general formula [I] of the present invention or an agriculturally acceptable salt thereof as an active ingredient.
- the pest control agent of the present invention is typically an insecticide.
- the pest control agent of the present invention can contain an additive component (carrier) usually used in agricultural chemical preparations, if necessary.
- a carrier such as a solid carrier or a liquid carrier, a surfactant, a binder or a tackifier, a thickener, a colorant, a spreading agent, a spreading agent, an antifreezing agent, an anti-caking agent, A disintegrating agent, a decomposition inhibitor, etc. are mentioned, In addition, you may use a preservative, a plant piece, etc. as an additional component as needed.
- additive components may be used alone or in combination of two or more.
- the solid carrier examples include pyrophyllite clay, kaolin clay, meteorite clay, talc, diatomaceous earth, zeolite, bentonite, acid clay, activated clay, attapulgus clay, vermiculite, perlite, pumice, white carbon (synthetic silicic acid, Synthetic silicates, etc.), mineral carriers such as titanium dioxide; plant carriers such as wood flour, corn stalks, walnut shells, fruit nuclei, rice straw, sawdust, bran, soybean flour, powdered cellulose, starch, dextrin, saccharides; Inorganic salt carriers such as calcium carbonate, ammonium sulfate, sodium sulfate, potassium chloride; polymer carriers such as polyethylene, polypropylene, polyvinyl chloride, polyvinyl acetate, ethylene-vinyl acetate copolymer, urea-aldehyde resin, etc. it can.
- liquid carrier examples include monohydric alcohols such as methanol, ethanol, propanol, isopropanol, butanol, and cyclohexanol; polyhydric alcohols such as ethylene glycol, diethylene glycol, propylene glycol, hexylene glycol, polyethylene glycol, polypropylene glycol, and glycerin.
- monohydric alcohols such as methanol, ethanol, propanol, isopropanol, butanol, and cyclohexanol
- polyhydric alcohols such as ethylene glycol, diethylene glycol, propylene glycol, hexylene glycol, polyethylene glycol, polypropylene glycol, and glycerin.
- Polyhydric alcohol derivatives such as propylene glycol ethers; ketones such as acetone, methyl ethyl ketone, methyl isobutyl ketone, diisobutyl ketone, cyclohexanone, isophorone; ethers such as ethyl ether, dioxane, cellosolve, dipropyl ether, tetrahydrofuran; Aliphatic hydrocarbons such as normal paraffin, naphthene, isoparaffin, kerosene, mineral oil; toluene, C 9 -C 10 alkylbenzene, xylene, solvent naphtha, alkylnaphthalene, aromatic hydrocarbons such as high-boiling aromatic hydrocarbons;, dichloroethane, chloroform, halogenated hydrocarbons such as carbon tetrachloride, ethyl acetate, diisopropyl phthalate, dibutyl Esters such
- the surfactant is not particularly limited, but is preferably one that gels in water or exhibits swelling properties.
- sorbitan fatty acid ester polyoxyethylene sorbitan fatty acid ester, sucrose fatty acid ester, polyoxyethylene fatty acid Esters, polyoxyethylene resin acid esters, polyoxyethylene fatty acid diesters, polyoxyethylene alkyl ethers, polyoxyethylene alkyl phenyl ethers, polyoxyethylene dialkyl phenyl ethers, polyoxyethylene alkyl phenyl ether formalin condensates, polyoxyethylene polyoxy Propylene block polymer, alkyl polyoxyethylene polypropylene block polymer ether, polyoxyethylene alkylamine, polyoxyethylene fat Amide, polyoxyethylene fatty acid bisphenyl ether, polyalkylene benzyl phenyl ether, polyoxyalkylene styryl phenyl ether, acetylene diol, polyoxyalkylene-added acetylenic di
- binders and tackifiers include carboxymethyl cellulose and salts thereof, dextrin, water-soluble starch, xanthan gum, guar gum, sucrose, polyvinyl pyrrolidone, gum arabic, polyvinyl alcohol, polyvinyl acetate, sodium polyacrylate, and an average molecular weight of 6000 to 20000.
- thickeners examples include xanthan gum, guar gum, carboxymethylcellulose, polyvinylpyrrolidone, carboxyvinyl polymer, acrylic polymer, starch derivatives, water-soluble polymers such as polysaccharides; inorganic fine powders such as high-purity bentonite and white carbon Can be mentioned.
- the colorant examples include inorganic pigments such as iron oxide, titanium oxide, and Prussian blue; organic dyes such as alizarin dyes, azo dyes, and metal phthalocyanine dyes.
- the spreading agent examples include silicone surfactant, cellulose powder, dextrin, modified starch, polyaminocarboxylic acid chelate compound, cross-linked polyvinyl pyrrolidone, maleic acid and styrenes, methacrylic acid copolymer, polyhydric alcohol polymer, A half ester with a dicarboxylic acid anhydride, a water-soluble salt of polystyrene sulfonic acid, and the like can be given.
- various surfactants such as sodium dialkylsulfosuccinate, polyoxyethylene alkyl ether, polyoxyethylene alkylphenyl ether, polyoxyethylene fatty acid ester; paraffin, terpene, polyamide resin, polyacrylate,
- surfactants such as sodium dialkylsulfosuccinate, polyoxyethylene alkyl ether, polyoxyethylene alkylphenyl ether, polyoxyethylene fatty acid ester; paraffin, terpene, polyamide resin, polyacrylate
- examples include polyoxyethylene, wax, polyvinyl alkyl ether, alkylphenol formalin condensate, and synthetic resin emulsion.
- antifreezing agent examples include polyhydric alcohols such as ethylene glycol, diethylene glycol, propylene glycol, and glycerin.
- Disintegrants include, for example, sodium tripolyphosphate, sodium hexametaphosphate, metal stearate, cellulose powder, dextrin, methacrylic acid ester copolymer, polyvinylpyrrolidone, polyaminocarboxylic acid chelate compound, sulfonated styrene / isobutylene / maleic anhydride Examples thereof include a copolymer and a starch / polyacrylonitrile graft copolymer.
- decomposition inhibitor examples include desiccants such as zeolite, quicklime, and magnesium oxide; phenol-based, amine-based, sulfur-based, phosphoric acid-based antioxidants; salicylic acid-based, benzophenone-based ultraviolet absorbers, and the like. be able to.
- the pest control agent of the present invention is powder, granule, granule, wettable powder, water solvent, granule wettable powder, tablet, jumbo agent, emulsion, oil agent, liquid agent, flowable agent, emulsion agent, microemulsion agent. , Suspoemulsion agent, microdispersion agent, microcapsule agent, smoking agent, aerosol agent, bait agent, paste agent and the like.
- preparations containing the compound of the present invention or dilutions thereof are generally performed by a commonly used application method, that is, spraying (for example, spraying, misting, atomizing, dusting, dusting, water surface application, box application, etc. ), Soil application (for example, mixing, irrigation, etc.), surface application (for example, application, powder coating, coating, etc.), immersion, poison bait, smoke application, and the like. It is also possible to feed the livestock with the above-mentioned active ingredient mixed with feed to control the occurrence and growth of harmful insects, particularly harmful insects, in the excreta.
- the mixture ratio of the active ingredient in the pest control agent of this invention selects suitably as needed.
- powders, granules, etc. 0.01 to 20% (mass), preferably 0.05 to 10% (mass)
- mass 0.1-30% (mass), preferably 0.5-20% (mass)
- wettable powder, granulated wettable powder, etc. 1 to 70% (mass), preferably 5 to 50% (mass)
- it is 1 to 95% (mass), preferably 10 to 80% (mass).
- an emulsion In the case of an emulsion, etc., 5 to 90% (mass), preferably 10 to 80% (mass) When used as an oil, etc., 1 to 50% (mass), preferably 5 to 30% (mass) In the case of a flowable agent, etc., 5 to 60% (mass), preferably 10 to 50% (mass) In the case of an emulsion agent, a microemulsion agent, a suspoemulsion agent, etc., 5 to 70% (mass), preferably 10 to 60% (mass) In the case of tablets, baits, pastes, etc., 1 to 80% (mass), preferably 5 to 50% (mass) When used as a smoke agent, etc., 0.1 to 50% (mass), preferably 1 to 30% (mass) In the case of an aerosol or the like, 0.05 to 20% (mass), preferably 0.1 to 10% (mass) It is better to select from the range.
- the application of the pest control agent of the present invention is generally carried out at an active ingredient concentration of 0.1 to 5000 ppm when it is diluted with a diluent.
- the application amount per unit area is 0.1 to 5000 g per ha as an active ingredient compound, but is not limited thereto.
- GABA receptor (chloride channel) inhibitor (2A) cyclodiene organochlorine compounds: chlordane, endosulfan, gamma-BHC (gamma-BCH); (2B) Phenylpyrazole compounds: acetoprol, etiprole, fipronil, pyrafluprole, pyriprole, RZI-02-003 (code number) 3.
- pyrethroid compounds acrinathrin, allethrin (including d-cis-trans, d-trans), bifenthrin, bioallethrin, bioarethrin S -Cyclomethenyl (bioallethrin S-cyclopentenyl) bioresmethrin, cycloprothrin, cyfluthrin (including beta-), cyhalothrin (including gamma-, lambda-), cypermethrin (cypermethrin) ) [Including alpha-, beta-, theta-, zeta-], cyphenothrin [including (1R) -trans-isomers], deltamethrin, empentrin, esfenvalerate Etofenprox, fenpropathrin, fenvalerate, flucythrinate, flume Phosphorus (flumethrin
- Nicotinic Acetylcholine Receptor Agonist / Antagonist (4A) Neonicotinoid compounds: acetamiprid, clothianidin, dinotefuran, imidacloprid, nitenpyram, thiamethroprid, thiamethopridam ); (4B) Nicotine compounds: nicotine-sulfate 5. Nicotinic acetylcholine receptor allosteric activator spinosyn compounds: spinetoram, spinosad; 6).
- Agents that activate chloride channels Abamectin, milbemycin compounds: Abamectin, emamectin benzoate, lepimectin, milbemectin, ivermectin, polynactins 7). Juvenile hormone-like drugs diofenolan, hydroprene, kinoprene, methothrin, phenoxycarb, pyriproxyfen 8). Agents with non-specific action (multi-point of action) 1,3-dichloropropene (1,3-dichloropropene), DCIP, ethylene dibromide, methyl bromide, chloropicrin, sulfuryl fluoride (sulfuryl fluoride) 9.
- BT agent Bacillus sphaericus, Bacillus thuringiensis subsp. Aizawai, Bacillus thuringiensis subsp. Israelensis, Bacillus thuringiensis subsp. Kurstaki, Bacillus thuringiensis subsp.
- Bt crop proteins (Cry1Ab, C2, mCry3A, Cry3Ab, Cry3Bb, Cry34 / 35Ab1), Bacillus popilliae, Bacillus subtillis 12 ATP biosynthetic enzyme inhibitor diafenthiuron; Organotin compounds: azocyclotin, cyhexatin, fenbutatin oxide; Propargite, tetradifon 13. Uncouplers Chlorfenapyr, DNOC (DNOC) 14 Nicotinic acetylcholine channel blocker Nereistoxin compounds: bensultap, cartap, thiocyclam, thiosultap 15.
- Chitin biosynthesis inhibitor type 0
- Benzoylurea compounds bistrifluron, chlorfluazuron, diflubenzuron, flucycloxuron, flufenoxuron, hexaflumuron, lufenuron ), Novaluron, noviflumuron, teflubenzuron, triflumuron, fluazuron 16.
- Chitin biosynthesis inhibitor type 1 Buprofezin 17.
- Molting inhibitor for Diptera
- Cyromazine Cyromazine 18.
- Ecdysone agonist promoting molting
- Diacylhydrazine compounds chromafenozide, halofenozide, methoxyfenozide, tebufenozide; 19.
- Octopamine agonist Amitraz 20 Mitochondrial electron transport system (complex III) inhibitors Cyflumetofen, hydramethylnon, acequinocyl, fluacrypyrim, cyenopyrafen 21.
- Lipid biosynthesis inhibitor Tetranic insecticide / acaricide: spirodiclofen, spiromesifen, spirotetramat 24.
- Mitochondrial electron transport (complex IV) inhibitors Aluminum phosphide, hydrogen phosphine, zinc phosphide, calcium cyanide 25.
- Nerve inhibitor (Behavior unknown) bifenazate 26.
- Aconitase inhibitor sodium fluoroacetate 27.
- Aryloxyphenoxypropionic acid compounds Clodinafop-propargyl, cyhalofop-butyl, dicloofop-methyl, diclohop P-methyl, phenoxaprop-P-ethyl, fluazifop-butyl, fluazifop-P-butyl, haloxyfop, haloxyhop -Etoxyl (haloxyfop-etotyl) Haloxyfop-P, Metamifop, Propaquizafop, Quizalofop-ethyl, Quizalofop-P-ethyl, Quizalofop P.
- Photosynthesis II herbicide 1 in Photosystem II Phenylcarbamate-based compound: desmedipham, phenmedipham; (C1-2) pyridazinone compounds: chloridazon, brompyrazon; (C1-3) Triazine-based compounds: ametrin, atrazine, cyanazine, desmethrin, dimethametryn, eglinazine-ethyl, prometon, promethrin , Propazine, simazine, simetryn, terbumeton, terbuthylazine, terbutryn, trietazine; (C1-4) triazinone compounds: metamitron, metribuzin; (C1-5) triazolinone compounds: amicarbazone; (C1-6) Uracil compounds: Bromacil, Lenacil, terbacil; C2.
- White lice (Aleurocanthus spiniferus), Tobacco white lice (Bemisia tabaci), Silver leaf white lice (Bemisia ifargentifolii), Onsuji white lice (Trialeurodes vaporariorum), etc.
- Species of the scales such as pineapples, scales (Dysmicoccus brevipes), citrus scales (Planococcus citri), stag beetles (Pseudococcus comstocki), etc.
- Scorpionidae Caloptilia theivora
- Butterfly moth Physically ringoniella
- Etc. Argyresthia conjugella
- Nokona regalis etc.
- Carpina sasakii, etc. Illiberis pruni, etc.
- Monema flavescens etc.
- Ancylolomia japonica Chilo suppressalis
- Cob Moth Cnaphalocrocis medinalis
- green eel borer Ostrinia furnacalis
- European corn borer Ostrinia bilnubilalis
- insects of the order of the dipteran are Bourletiellahortensis belonging to the family Maltovicidae.
- spotted pests examples include Lepisma saccharina and Ctenolepisma villosa.
- Examples of the termite pests include the American termite (Incisitermes minor) of the Lepidoptera family, the termites of the termite family (Coptotermes formosanus) and the like, the termites of the termite family (Odontotermes formosanus) and the like.
- insects of the order of the stag beetle examples include Trogium pulsatorium, such as Cocha sectaceae, and Liposcelis corrodens, etc.
- Examples of the lice pests include the lice of the mosquito family Haematopinus suis and the like, the human lice of the human lice family (Pediculus humanus), the dog lice of the mosquito lice family (Linognathus setosus) and the like, and the lice of the lice family
- plant parasitic mites examples include Penthaleus major, Mite mite (Phytonemus pallidus), Phytonemus pallidus, Polyphagotarsonemus latus, and the like. Grape spider mite (Brevipalpus lewisi) etc., Spider spider spider mite (Tuckerella von pavoniformis) etc. kanzawai, etc., Trisetacus pini, etc., Acarops pelekassi, Epitrimerus pyri, Phyllocoptruta oleivora, Harina, etc. Examples include Diptacus crenatae of the family Scarabidae, Aleuroglyphus ovatus, Tyrophagus putrescentiae, Rhizoglyphus robini, and the like.
- Helicotylenchus dihystera etc., Paratylencus ⁇ curvitatus, etc., Meloidogyne incognita, Meloidogyne hapla, etc.
- Nematode Globodera rostochiensis
- Soybean cyst nematode Heterodera glycines
- Tylenchorhynchus claytoni etc.
- Psyrenxaceae species Psilenchus sp.
- Liver dystoma (Distomum sp.), Pulmonary dystoma (Paragonimus westermanii), Yokokawa (Metagonimusokoyokokawai), Schistosoma japonicum, Taenia solium, and Saenori (Senja) Taeniarhynchus saginatus), Echinococcus sp., Broad-headed crested worm (Diphyllobothriumthr) latum).
- the pest control agent of the present invention exhibits an excellent control effect against the above pests.
- the pest control agent of the present invention also exhibits a control effect on the pests exemplified above, which have acquired resistance to existing pest control agents.
- the pest control agent of the present invention can also be used for plants that have acquired characteristics such as pest resistance, disease resistance, and herbicide resistance by genetic recombination, artificial mating, and the like.
- Example 1 Production of 1- (2-cyano-1,2-diisopropoxyiminoethyl) -1H-1,2,4-triazole (present compound number I-50) (1) 2-cyano-2-isopropoxyimino To a dichloromethane solution (5 ml) of ethyl acetate 1.0 g (5.43 mmol) was added 0.73 g (6.54 mmol) of O-isopropylhydroxyamine hydrochloride, cooled to ⁇ 20 ° C., and trimethylaluminum hexane solution ( 1.4 mol / L) (4.34 ml, 6.08 mmol) was added, and the mixture was warmed to room temperature and stirred for 20 hours.
- reaction mixture was cooled to ⁇ 20 ° C., and 3.88 ml (5.43 mmol) of trimethylaluminum hexane solution was added, followed by stirring at room temperature for 6 hours.
- Water was added to the reaction mixture under ice cooling, followed by extraction with ethyl acetate.
- the organic layer was washed with a saturated aqueous sodium chloride solution and dried over anhydrous magnesium sulfate.
- Example 4 1- [2- (4,5-dihydro-1,3-thiazolin-2-yl) -1,2-diisopropoxyiminoethyl] -1H-1,2,4-triazole (present compound number I- 214) and 1- [1,2-diisopropoxyimino-2- (thiazol-2-yl) ethyl] -1H-1,2,4-triazole (present compound number I-215)
- (1) 1- (2-Cyano-1,2-diisopropoxyiminoethyl) -1H-1,2,4-triazole 0.70 g (2.65 mmol) and ammonium acetate 0.22 g (2.91 mmol) in methanol To the solution (5 ml), 0.22 g (2.91 mmol) of 2-aminoethanethiol was added and stirred at room temperature for 16 hours.
- reaction mixture was poured into water, extracted with ethyl acetate, washed with saturated brine, and dried over anhydrous magnesium sulfate.
- Example 5 1- [2-Isobutoxyimino-1-isopropoxyimino-2- (1,2,4-oxadiazol-2-yl) ethyl] -1H-1,2,4-triazole (Compound No. I of the present invention) -209) (1) 1- [2-cyano-2-isobutoxyimino-1-isopropoxyiminoethyl] -1H-1,2,4-triazole prepared according to Example 1 above. To an ethanol solution (10 ml) of 68 g (6.04 mmol), 0.46 g (6.62 mmol) of hydroxylamine hydrochloride and 0.54 g (6.58 mmol) of sodium acetate were added and stirred at 50 ° C.
- Example 7 Preparation of 1- (2-methylthio-1,2-diisopropoxyiminoethyl) -1H-1,2,4-triazole (present compound number I-228) 1,2-prepared in Example 6 above
- a tetrahydrofuran solution (5 ml) of 0.35 g (1.14 mmol) of diisopropoxyimino-1,2-bis (1H-1,2,4-triazol-1-yl) ethane heated under reflux was added sodium thiomethoxide. was added while confirming the reaction by thin layer chromatography and stirred for 5 hours.
- reaction mixture was cooled to room temperature, poured into water, extracted with ethyl acetate, washed with saturated brine, and dried over anhydrous magnesium sulfate.
- Example 8 Production of 1- (2-chloro-1,2-diisopropoxyiminoethyl) -1H-1,2,4-triazole (the present compound number I-4) (1) 2-hydroxyimino-2-1H- To a solution of ethyl 1,2,4-triazol-1-ylacetate (76 mmol) in N, N-dimethylformamide (100 ml) was added 14 g (82 mmol) of isopropyl iodide and 13 g (94 mmol) of potassium carbonate. Stir at room temperature for 5 hours. The reaction mixture was poured into water, extracted with ethyl acetate, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- 2-hydroxyimino-2-1H-1,2,4-triazol-1-yl ethyl acetate is a journal of the chemical society Perkin Transactions 1 (Journal of Chemical Society of Perkin Transactions. 2) to 2239 (1987).
- Example 9 Production of 1- (1,2-diisopropoxyimino-2-methoxyethyl) -1H-1,2,4-triazole (Compound No. I-165 of the present invention) N-isopropoxy-produced in Example 8 2-isopropoxyimino-2- (1H-1,2,4-triazol-1-yl) acetamide 0.4 g (1.57 mmol) and potassium carbonate 0.22 g (1.59 mmol) N, N— To the dimethylformamide solution (5 ml) was added 0.22 g (1.55 mmol) of iodomethane under ice cooling, and the mixture was further stirred at room temperature for 20 hours.
- reaction mixture was poured into water, extracted with ethyl acetate, washed with a saturated aqueous sodium chloride solution, and dried over anhydrous magnesium sulfate.
- VI-262 (CDCl 3): 1.40 (3H, t), 1.55-1.66 (2H, m), 2.04-2.14 (1H, m), 4.43 (2H , Q), 4.39-4.59 (2H, m)
- Compound No. VI-265 (CDCl 3): 1.92-1.97 (2H, m), 2.23 (6H, s), 2.37-2.40 (2H, t), 3.88 and 4 .17 (3H, s), 4.42, 4.50 (2H, s)
- Compound No. VI-267 (CDCl 3 ): 1.40 (9H, s), 1.41 (3H, t), 4.49 (2H, q) Compound No.
- Goldfish insecticide test A wettable powder prepared according to Formulation Example 2 was diluted with water to a concentration of 500 ppm as an active ingredient. Cabbage leaves were immersed in this diluted chemical solution, and after air drying, they were put in a plastic cup having a capacity of 60 mL. Ten second instar larvae were released from this plastic cup, and the lid was capped and placed in a thermostatic chamber at 25 ° C. Six days later, the number of surviving insects was counted, and the dead insect rate was determined by the formula of Formula 1.
Abstract
Description
一般式[I]
[式中、
Xは、水素原子、ハロゲン原子、シアノ基、C1~C8アルキル基、C2~C6アルケニル基、C2~C6アルキニル基、C3~C6シクロアルキル基、C3~C6シクロアルキルC1~C6アルキル基、C1~C6ハロアルキル基、C1~C6アルキルチオ基、C1~C6アルキルスルフィニル基、C1~C6アルキルスルホニル基、C1~C6アルキルチオC1~C6アルキル基、C1~C6アルキルスルフィニルC1~C6アルキル基、C1~C6アルキルスルホニルC1~C6アルキル基、C1~C6アルコキシ基、C1~C6アルコキシC1~C6アルキル基、チオカルバモイル基、R4R5NC(=O)基、R6R7N基、C1~C6アルコキシカルボニル基、カルボキシル基、R8O(HN=)C基、R9ON=(R10)C基、R11S(O=)C基、R12R13NSO2NH基、ヒドロキシC1~C6アルキル基、シアノC1~C6アルキル基、C1~C6アルキルカルボニル基、置換基群αから選ばれる置換基で置換されてもよいフェニル基又は同一若しくは相異なってもよい酸素原子、硫黄原子及び窒素原子から選択される1から5個のヘテロ原子を有する炭素数1から9の複素環基(該基は1~5個のハロゲン原子、C1~C6アルキル基、C1~C6ハロアルキル基、C1~C6アルコキシ基、オキソ基又はシアノ基で置換されていてもよい。)を表し、
R1は、C1~C10アルキル基、C2~C6アルケニル基、C2~C6アルキニル基、C3~C6シクロアルキル基、C3~C6シクロアルキルC1~C6アルキル基、C1~C6ハロアルキル基、C2~C6ハロアルケニル基、C2~C6ハロアルキニル基、C1~C6アルキルチオC1~C6アルキル基、C1~C6アルキルスルフィニルC1~C6アルキル基、C1~C6アルキルスルホニルC1~C6アルキル基、C1~C6アルコキシC1~C6アルキル基、C1~C6ハロアルコキシC1~C6アルキル基、C1~C6アルコキシイミノC1~C6アルキル基、トリ(C1~C6アルキル)シリルC1~C6アルキル基、シアノC1~C6アルキル基、gem-ジ(C1~C6アルコキシ)C1~C6アルキル基、ヒドロキシC1~C6アルキル基、アミノC1~C6アルキル基(該基はR14、R15で置換されていてもよい。)、置換基群αから選ばれる置換基で置換されてもよいフェニル基、置換基群αから選ばれる置換基で置換されてもよいフェニルC1~C6アルキル基、置換基群αから選ばれる置換基で置換されてもよいフェニルC2~C6アルケニル基、置換基群αから選ばれる置換基で置換されてもよいフェノキシC1~C6アルキル基、同一若しくは相異なってもよい酸素原子、硫黄原子及び窒素原子から選択される1から5個のヘテロ原子を有する炭素数1から9の複素環基(該基は1~5個のハロゲン原子、C1~C6アルキル基、C1~C6ハロアルキル基、C1~C6アルコキシ基又はシアノ基で置換されていてもよい。)、同一若しくは相異なってもよい酸素原子、硫黄原子及び窒素原子から選択される1から5個のヘテロ原子を有する炭素数1から9の複素環で置換されたC1~C6アルキル基(該基は1~5個のハロゲン原子、C1~C6アルキル基、C1~C6ハロアルキル基、C1~C6アルコキシ基、オキソ基又はシアノ基で置換されていてもよい。)又は同一若しくは相異なってもよい酸素原子、硫黄原子及び窒素原子から選択される1から5個のヘテロ原子を有する炭素数1から9の複素環で置換されたC2~C6アルケニル基(該基は1~5個のハロゲン原子、C1~C6アルキル基、C1~C6ハロアルキル基、C1~C6アルコキシ基又はシアノ基で置換されていてもよい。)を表し、
前記複素環基に窒素原子が含まれる場合は酸化されてN-オキシドになってもよく、
R2は、C1~C6アルキル基、C2~C6アルケニル基、C2~C6アルキニル基、C3~C6シクロアルキル基、C1~C6ハロアルキル基、C2~C6ハロアルケニル基、C2~C6ハロアルキニル基、C1~C6アルキルチオC1~C6アルキル基、C1~C6アルキルスルフィニルC1~C6アルキル基、C1~C6アルキルスルホニルC1~C6アルキル基、C1~C6アルコキシC1~C6アルキル基、C1~C6ハロアルコキシC1~C6アルキル基、シアノC1~C6アルキル基又は置換基群αで置換されてもよいフェニルC1~C6アルキル基を表し、
Qは、式[Q-1]若しくは式[Q-2]
で示される複素環基又はハロゲン原子を表し、
式[Q-1]におけるWは、窒素原子又はメチン基を表し、
式[Q-1]及び式[Q-2]で示される複素環基の窒素原子は酸化されてN-オキシドになってもよく、
式[Q-1]及び式[Q-2]におけるR3は、ハロゲン原子、シアノ基、ニトロ基、ヒドロキシル基、メルカプト基、C1~C6アルキル基、C1~C6ハロアルキル基、C1~C6アルコキシ基、C1~C6アルキルチオ基、C1~C6アルキルスルフィニル基、C1~C6アルキルスルホニル基、ホルミル基又はヒドロキシイミノC1~C4アルキル基を表し、
式[Q-1]及び式[Q-2]におけるnは、Wが窒素原子の場合は0、1又は2を、Wがメチン基の場合は0、1、2又は3を表し、
R4、R5、R6、R7、R12、R13、R14及びR15は、それぞれ、水素原子、C1~C6アルキル基、C1~C6アルコキシ基、C1~C6アルコキシC1~C6アルキル基、C1~C6アルキルカルボニル基、C1~C6アルコキシカルボニル基、C1~C6ハロアルキル基、C3~C6シクロアルキル基、C3~C6シクロアルキルC1~C6アルキル基、C1~C6アルキルスルホニル基又はシアノC1~C6アルキル基又は置換基群αから選ばれる置換基で置換されてもよいフェニル基を表し、
又、R4とR5、R6とR7、R12とR13及びR14とR15は、それぞれ一緒になってC2~C7アルキレン鎖を形成することにより、結合する窒素原子と共に3~8員環を形成してもよく、該アルキレン鎖は酸素原子、硫黄原子又は窒素原子を1個含んでもよく、更に該アルキレン鎖はハロゲン原子、C1~C6アルキル基、オキソ基で置換されてもよく、
R8及びR9は、それぞれ、水素原子、C1~C6アルキル基、C1~C6ハロアルキル基又はC1~C6アルコキシカルボニル基を表し、
R10は、R6R7N基又はQを表し、
R11は、C1~C6アルキル基を表す。]
で表されることを特徴とするアルコキシイミノ誘導体又はその農業上許容される塩。
「置換基群α」
ハロゲン原子、C1~C6アルキル基、C1~C6ハロアルキル基、C1~C6アルコキシ基、C1~C6ハロアルコキシ基、C1~C6アルコキシカルボニル基、ニトロ基及びシアノ基
(2)Xが、水素原子、ハロゲン原子、シアノ基、C1~C8アルキル基、C3~C6シクロアルキル基、C1~C6ハロアルキル基、C1~C6アルキルチオ基、C1~C6アルキルスルフィニル基、C1~C6アルキルスルホニル基、C1~C6アルコキシ基、チオカルバモイル基、R4R5NC(=O)基、R6R7N基、C1~C6アルコキシカルボニル基、カルボキシル基、R8O(HN=)C基、R9ON=(R10)C基、R11S(O=)C基、R12R13NSO2NH基、ヒドロキシC1~C6アルキル基、シアノC1~C6アルキル基、C1~C6アルキルカルボニル基、置換基群αから選ばれる置換基で置換されてもよいフェニル基又は同一若しくは相異なってよい酸素原子、硫黄原子及び窒素原子から選択される1から5個のヘテロ原子を有する炭素数1から9の複素環基(該基は1~5個のハロゲン原子、C1~C6アルキル基、C1~C6ハロアルキル基、C1~C6アルコキシ基、オキソ基又はシアノ基で置換されていてもよい。)であり、
R1が、C1~C10アルキル基、C2~C6アルケニル基、C2~C6アルキニル基、C3~C6シクロアルキル基、C3~C6シクロアルキルC1~C6アルキル基、C1~C6ハロアルキル基、C2~C6ハロアルケニル基、C1~C6アルキルチオC1~C6アルキル基、C1~C6アルコキシC1~C6アルキル基、C1~C6ハロアルコキシC1~C6アルキル基、トリ(C1~C6アルキル)シリルC1~C6アルキル基、シアノC1~C6アルキル基、gem-ジ(C1~C6アルコキシ)C1~C6アルキル基、ヒドロキシC1~C6アルキル基、アミノC1~C6アルキル基(該基はR14又はR15で置換されていてもよい。)、置換基群αから選ばれる置換基で置換されてもよいフェニル基、置換基群αから選ばれる置換基で置換されてもよいフェニルC1~C6アルキル基、置換基群αから選ばれる置換基で置換されてもよいフェニルC2~C6アルケニル基、置換基群αから選ばれる置換基で置換されてもよいフェノキシC1~C6アルキル基、同一若しくは相異なってもよい酸素原子、硫黄原子及び窒素原子から選択される1から5個のヘテロ原子を有する炭素数1から9の複素環基(該基は1~5個のハロゲン原子、C1~C6アルキル基、C1~C6ハロアルキル基、C1~C6アルコキシ基又はシアノ基で置換されていてもよい。)又は同一若しくは相異なってもよい酸素原子、硫黄原子及び窒素原子から選択される1から5個のヘテロ原子を有する炭素数1から9の複素環で置換されたC1~C6アルキル基(該基は1~5個のハロゲン原子、C1~C6アルキル基、C1~C6ハロアルキル基、C1~C6アルコキシ基、オキソ基又はシアノ基で置換されていてもよい。)であり、
前記複素環基に窒素原子が含まれる場合は酸化されてN-オキシドになってもよく、
R2が、C1~C6アルキル基、C2~C6アルケニル基、C2~C6アルキニル基、C3~C6シクロアルキル基、C1~C6ハロアルキル基、C1~C6アルコキシC1~C6アルキル基、シアノC1~C6アルキル基又は置換基群αで置換されてもよいフェニルC1~C6アルキル基であり、
Qが、式[Q-1]若しくは式[Q-2]
で示される複素環基又はハロゲン原子であり、
式[Q-1]におけるWが、窒素原子又はメチン基であり、
式[Q-1]及び式[Q-2]におけるR3が、メルカプト基又はC1~C6ハロアルキル基であり、
式[Q-1]及び式[Q-2]におけるnが、0又は1であり、
R4、R5、R6、R7、R12、R13、R14及びR15が、それぞれ、水素原子、C1~C6アルキル基、C1~C6アルコキシ基、C1~C6アルキルカルボニル基、C1~C6アルコキシカルボニル基、C1~C6ハロアルキル基、C3~C6シクロアルキルC1~C6アルキル基、シアノC1~C6アルキル基又は置換基群αから選ばれる置換基で置換されてもよいフェニル基であり、
又、R4とR5、R6とR7、R12とR13及びR14とR15は、それぞれ一緒になってC2~C7アルキレン鎖を形成することにより、結合する窒素原子と共に3~8員環を形成してもよく、該アルキレン鎖は酸素原子、硫黄原子又は窒素原子を1個含んでもよく、
R8及びR9が、それぞれ、水素原子、C1~C6アルキル基又はC1~C6アルコキシカルボニル基であり、
R10が、R6R7N基又はQであり、
R11が、C1~C6アルキル基である、
(1)に記載のアルコキシイミノ誘導体又はその農業上許容される塩。
Me :メチル基
Et :エチル基
Pr-n :n-プロピル基
Pr-i :イソプロピル基
Pr-c :シクロプロピル基
Bu-n :n-ブチル基
Bu-s :sec-ブチル基
Bu-i :イソブチル基
Bu-t :tert-ブチル基
Pen-n :n-ペンチル基
Pen-c :シクロペンチル基
Pen-i :イソペンチル基
Pen-neo :ネオペンチル基
Pen-2 :2-ペンチル基
Pen-3 :3-ペンチル基
Hex-n :n-ヘキシル基
Hex-c :シクロヘキシル基
5-CF3 :5位にトリフルオロメチル基が置換
3-Cl-5-CF3 :3位に塩素原子、5位にトリフルオロメチル基が置換
2,6-(Cl)2 :2位及び6位に塩素原子が置換
一般式[I]で表される本発明化合物のうち、[Ia-I]及び[Ic-I] で表される化合物は、例えば以下の方法に従って製造することができる。
(式中、R1、R2、W及びnは前記と同じ意味を表し、
X1は、水素原子、シアノ基、C1~C8アルキル基、C2~C6アルケニル基、C2~C6アルキニル基、C3~C6シクロアルキル基、C3~C6シクロアルキルC1~C6アルキル基、C1~C6ハロアルキル基、C1~C6アルキルチオ基、C1~C6アルキルチオC1~C6アルキル基、C1~C6アルキルスルフィニルC1~C6アルキル基、C1~C6アルキルスルホニルC1~C6アルキル基、C1~C6アルコキシ基、C1~C6アルコキシC1~C6アルキル基、チオカルバモイル基、R4R5NCO基、R6R7N基、C1~C6アルコキシカルボニル基、カルボキシル基、R8O(HN=)C基、R9ON=(R10 )C基、R11S(O=)C基、置換基群αで置換されてもよいフェニル基、同一若しくは相異なってもよい酸素原子、硫黄原子及び窒素原子から選択される1から5個のヘテロ原子を有する炭素数1から9の複素環基(該基は1~5個のハロゲン原子、C1~C6アルキル基、C1~C6ハロアルキル基、C1~C6アルコキシ基又はシアノ基で置換されていてもよい。)を表し、
R4、R5、R6、R7、R8、R9、R10、R11及び置換基群αは前記と同じ意味を表し、
R3aは、水素原子、ハロゲン原子、シアノ基、ニトロ基、C1~C6アルキル基、C1~C6ハロアルキル基、C1~C6アルコキシ基、C1~C6アルキルチオ基、C1~C6アルキルスルフィニル基、C1~C6アルキルスルホニル基、ホルミル基を表し、
E1は塩素原子、臭素原子、ヨウ素原子、メタンスルホニル基、メタンスルホニルオキシ基又はトリフルオロメタンスルホニルオキシ基等の脱離基を表す。)
一般式[I]で表される本発明化合物のうち、式[Ia-III]で表される化合物は、例えば以下の方法に従って製造することができる。
(式中、R1、R2、R3a、W及びnは前記と同じ意味を表し、X2はハロゲン原子を表し、好ましくは、塩素原子又は臭素原子を表す。)
一般式[I]で表される本発明化合物のうち、式[Ia-III]で表される化合物は、例えば以下の方法に従って製造することもできる。
(式中、R1、R2、R3a、X2、W及びnは前記と同じ意味を表す。)
一般式[I]で表される本発明化合物のうち、式[Ia-V]で表される化合物は、例えば以下の方法に従って製造することができる。
(式中、R1、R2、R3a、W及びnは前記と同じ意味を表す。)
一般式[I]で表される本発明化合物のうち、式[Ia-VI]で表される化合物は、例えば以下の反応式からなる方法で製造することができる。
(式中、R1、R2、R3a、W及びnは前記と同じ意味を表す。)
一般式[I]で表される本発明化合物のうち、式[Ia-II]で表される化合物は、例えば以下の反応式からなる方法で製造することができる。
(式中、R1、R2、R3a、W、n及びE1は前記と同じ意味を表す。)
化合物[V]と化合物[VI]とを塩基存在下、溶媒中で反応させることにより、化合物[Ia-II]を製造することができる。又、使用する[VI]は塩酸塩又は硫酸塩等の塩でもよい。
化合物[Ia-VII]は、化合物[V]と化合物[IV]とを、溶媒中で反応させることによって製造することができる。又、使用する化合物[IV]は塩酸塩又は硫酸塩等の塩でもよく、その場合、塩基の存在下で反応させてもよい。
化合物[Ia-VII]と化合物[VII]とを、溶媒中、塩基の存在下で反応させることにより、化合物[Ia-II]を製造することができる。
化合物[VIII]とアンモニアとを、溶媒中で反応させることにより、化合物[IX]を製造することができる。
化合物[IX]と脱水剤とを、溶媒中で反応させることにより、化合物[V]を製造することができる。
化合物[VIII]を酸存在下又は塩基存在下 、溶媒中、 加水分解することにより、化合物[XII]を製造することができる。
化合物[XII]と化合物[VI]とを溶媒中、縮合剤を用いて反応させることによって化合物[III]を製造することができる。又、使用する化合物[VI]は塩酸塩又は硫酸塩等の塩でもよく、その場合、塩基の存在下で反応させてもよい。
一般式[I]で表される本発明化合物のうち、式[Ia-VIII]で表される化合物は、例えば以下の方法に従って製造することができる。
(式中、R1、R2、R3a、Y1、W、n及びE1 は前記と同じ意味を表す。)
一般式[I]で表される本発明化合物のうち、式[Ia-IX]で表される化合物は、例えば以下の反応式からなる方法で製造することができる。
(式中、R1、R2、R3a、W、n及びY1は前記と同じ意味を表し、Y2はC1~C6アルキル基を表す。)
一般式[I]で表される本発明化合物のうち、式[Ia-XI]で表される化合物は、例えば以下の反応式からなる方法で製造することができる。
(式中、R1、R2、R3a、W及びnは前記と同じ意味を表す。)
化合物[Ia-IV]と化合物[XVI]とを、溶媒中で反応させることにより、化合物[Ia-X]を製造することができる。尚、使用する化合物[XVI]は塩酸塩又は硫酸塩等の塩でもよい。
化合物[Ia-X]と酸化剤とを、溶媒中で反応させることにより、化合物[Ia-XI]を製造することができる。
一般式[I]で表される本発明化合物のうち、式[Ia-XII]で表される化合物は、例えば以下の反応式からなる方法で製造することができる。
(式中、R1、R2、R3a、W及びnは前記と同じ意味を表す。)
一般式[I]で表される本発明化合物のうち、式[Ia-XIII]で表わされる化合物は、例えば以下の反応式からなる方法で製造することができる。
(式中、R3a、W、X2及びnは前記と同じ意味を表し、R1aはC1~C6アルキル基を表す。)
一般式[I]で表される本発明化合物のうち、式[Ia-XIV]で表わされる化合物は、例えば以下の反応式からなる方法で製造することができる。
(式中、R1a、R3a、W、Y1及びnは前記と同じ意味を表す。)
一般式[I]で表される本発明化合物のうち、式[Ia-XV]で表される化合物は、例えば以下の反応式からなる方法で製造することができる。
(式中、R1、R2、R3a、W及びnは前記と同じ意味を表す。)
一般式[I]で表される本発明化合物のうち、式[Ia-XVII]で表される化合物は、例えば以下の反応式からなる方法で製造することができる。
(式中、R1、R2、R3a、W、Y1及びnは前記と同じ意味を表し、Mはナトリウム、カリウム等のアルカリ金属を表す。 )
化合物[Ia-IV]、塩化水素及び メタノール又はエタノール等のC1~C6アルコール類(Y1OH) とを反応させることにより、化合物[Ia-XVI]を製造することができる。
化合物[Ia-XVI]は、化合物[Ia-IV]とナトリウムメトキシド又はナトリウムエトキシド等のC1~C6アルコールの金属塩類(Y1OM) とを、メタノール又はエタノール等のC1~C6アルコール(Y1OH) 中で反応させることにより製造することもできる。
化合物[Ia-XVII]は、化合物[Ia-XVI]を塩酸或いは硫酸等の酸の存在下、溶媒中で反応させることにより製造することができる。
一般式[I]で表される本発明化合物のうち、式[Ia-XVIII]で表される化合物は、例えば以下の反応式からなる方法で製造することができる。
(式中、R1、R2、R3a、R4、R5、W、Y1及びnは前記と同じ意味を表す。)
一般式[I]で表される本発明化合物のうち、式[Ia-XIX]で表される化合物は、例えば以下の反応式からなる方法で製造することができる。
(式中、R1、R2、R3a、W、Y1、Y2 及びnは前記と同じ意味を表す。)
一般式[I]で表される本発明化合物のうち、式[Ia-XX]で表される化合物は、例えば以下の反応式からなる方法で製造することができる。
(式中、R1、R2、R3a、R6、W、n及びE1は前記と同じ意味を表す。)
一般式[I]で表される本発明化合物のうち、式[Ia-XXII]で表される化合物は、例えば以下の反応式からなる方法で製造することができる。
(式中、R1、R2、W及びY2は前記と同じ意味を表し、
X3は、水素原子、シアノ基、C1~C8アルキル基、C2~C6アルケニル基、C2~C6アルキニル基、C3~C6シクロアルキル基、C3~C6シクロアルキルC1~C6アルキル基、C1~C6ハロアルキル基、C1~C6アルキルチオ基、C1~C6アルキルチオC1~C6アルキル基、C1~C6アルコキシ基、C1~C6アルコキシC1~C6アルキル基、R6R7N基、C1~C6アルコキシカルボニル基、置換基群αで置換されてもよいフェニル基、同一若しくは相異なってもよい酸素原子、硫黄原子及び窒素原子から選択される1から5個のヘテロ原子を有する炭素数1から9の複素環基(該基は1~5個のハロゲン原子、C1~C6アルキル基、C1~C6ハロアルキル基、C1~C6アルコキシ基又はシアノ基で置換されていてもよい。)を表し、R3bはハロゲン原子、メルカプト基、C1~C6アルキル基、C1~C6ハロアルキル基、C1~C6アルキルチオ基、ホルミル基を表し、
R6、R7及び置換基群αは前記と同じ意味を表す。)
化合物[Ia-XXI]とアルキルリチウム 化合物[XXI]とを、溶媒中で反応させることにより、化合物[XXII]を製造することができる。
化合物[XXII]を含む反応混合物と求電子剤とを、溶媒中で反応させることにより、化合物[Ia-XXII]を製造することができる。
一般式[I]で表される本発明化合物のうち、式[Ib-III]で表される化合物は、例えば以下の反応式からなる方法で製造することができる。
(式中、R1、R2、X1、X2及びY1は前記と同じ意味を表す。)
化合物[XXIII]と化合物[XXIV]とをルイス酸存在下、溶媒中で反応させることにより、化合物[XXV]を製造することができる。
化合物[XXV]とハロゲン化剤とを、溶媒中で反応させることにより、化合物[Ib-III]を製造することができる。
一般式[I]で表される本発明化合物のうち、式[Ib-II]で表わされる化合物は、例えば以下の反応式からなる方法で製造することができる。
(式中、R1a及びX2は前記と同じ意味を表す。)
二塩化オキサリルと化合物[XXVI]とを塩基存在下、溶媒中で反応させることにより、化合物[XXVII]を製造することができる。
化合物[XXVII]とハロゲン化剤とを、溶媒中で反応させることにより、化合物[Ib-II]を製造することができる。
一般式[Ia]で表される本発明化合物のうち、式[Ia-I]で表される化合物は、例えば以下の反応式からなる方法でも製造することができる。
化合物[Ia-XXIII ]と水素とを触媒存在下、溶媒中で反応させることにより、化合物[XXIX]を製造することができる。
化合物[XXIX]と[VII]とを塩基の存在下、溶媒中で反応させることにより、化合物[Ia-I]を製造することができる。
ラウリルアミン塩酸塩、ステアリルアミン塩酸塩、オレイルアミン塩酸塩、ステアリルアミン酢酸塩、ステアリルアミノプロピルアミン酢酸塩、アルキルトリメチルアンモニウムクロライド、アルキルジメチルベンザルコニウムクロライド等のアルキルアミン塩等のカチオン界面活性剤;
ジアルキルジアミノエチルベタイン、アルキルジメチルベンジルベタイン等のベタイン型、ジアルキルアミノエチルグリシン、アルキルジメチルベンジルグリシン等アミノ酸型等の両性界面活性剤
等を挙げることができる。
粉剤、粉粒剤等とする場合は0.01~20%(質量)、好ましくは0.05~10%(質量)
粒剤等とする場合は0.1~30%(質量)、好ましくは0.5~20%(質量)
水和剤、顆粒水和剤等とする場合は1~70%(質量)、好ましくは5~50%(質量)
水溶剤、液剤等とする場合は1~95%(質量)、好ましくは10~80%(質量)
乳剤等とする場合は5~90%(質量)、好ましくは10~80%(質量)
油剤等とする場合は1~50%(質量)、好ましくは5~30%(質量)
フロアブル剤等とする場合は5~60%(質量)、好ましくは10~50%(質量)
エマルション剤、マイクロエマルション剤、サスポエマルション剤等とする場合は5~70%(質量)、好ましくは10~60%(質量)
錠剤、ベイト剤、ペースト剤等とする場合は、1~80%(質量)、好ましくは5~50%(質量)
くん煙剤等とする場合は、0.1~50%(質量)、好ましくは1~30%(質量)
エアゾル剤等とする場合は、0.05~20%(質量)、好ましくは0.1~10%(質量)
の範囲から適宜選ぶのがよい。
1.アセチルコリンエステラーゼ阻害剤:
(1A)カルバマート化合物:アラニカルブ(alanycarb)、アルジカルブ(aldicarb)、アルドキシカルブ(aldoxycarb)、ベンダイオカルブ(bendiocarb)、ベンフラカルブ(benfuracarb)、ブトカルボキシム(butocarboxim)、ブトキシカルボキシム(butoxycarboxim)、カルバリル(carbaryl)、カルボフラン(carbofuran)、カルボスルファン(carbosulfan)、エチオフェンカルブ(ethiofencarb)、フェノブカルブ(fenobucarb)、ホルメタネート(formetanate)、フラチオカルブ(furathiocarb)、イソプロカルブ(isoprocarb)、メチオカルブ(methiocarb)、メソミル(methomyl)、メトルカルブ(metolcarb)、オキサミル(oxamyl)、ピリミカルブ(pirimicarb)、プロポキスル(propoxur)、チオジカルブ(thiodicarb)、チオファノックス(thiofanox)、トリアザメート(triazamate)、トリメタカルブ(trimethacarb)、XMC(XMC)、キシリルカルブ(xylylcarb);
(1B)有機リン化合物:アセフェート(acephate)、アザメチホス(azamethiphos)、アジンホス・エチル(azinphos-ethyl)、アジンホス・メチル(azinphos-methyl)、カズサホス(cadusafos)、クロルエトキシホス(chlorethoxyfos)、クロルフェンビンホス(chlorfenvinphos)、クロルメホス(chlormephos)、クロルピリホス(chlorpyrifos)、クロルピリホス・メチル(chlorpyrifos-methyl)、クマホス(coumaphos)、シアノホス(cyanophos)、デメトン・S・メチル(demeton-S-methyl)、ジアミダホス(diamidafos)、ダイアジノン(diazinon)、ジクロルボス(dichlorvos)、ジクロトホス(dicrotophos)、ジメトエート(dimethoate)、ジメチルビンホス(dimethylvinphos)、ジオキサベンゾホス(dioxabenzofos)、ジスルホトン(disulfoton)、DSP(DSP)、EPN、エチオン(ethion)、エトプロホス(ethoprophos)、エトリムホス(etrimfos)、ファムフル(famphur)、フェナミホス(fenamiphos)、フェニトロチオン(fenitrothion)、フェンチオン(fenthion)、フォノホス(fonofos)、ホスチアゼート(fosthiazate)、ホスチエタン(fosthietan)、ヘプテノホス(heptenophos)、イサミドホス(isamidofos)、イサゾホス(isazophos)、イソフェンホス(isofenphos-methyl)、イソプロピル O-(メトキシアミノチオホソホリル)サリチレート(isopropyl O-(methoxyaminothio-phosphoryl)salicylate)、イソキサチオン(isoxathion)、マラチオン(malathion)、メカルバム(mecarbam)、メタミドホス(methamidophos)、メチダチオン(methidathion)、メビンホス(mevinphos)、モノクロトホス(monocrotophos)、ナレッド(naled)、オメトエート(omethoate)、オキシジメトン・メチル(oxydemeton-methyl)、オキシデプロホス(oxydeprofos)、パラチオン(parathion)、パラチオン・メチル(parathion-methyl)、フェントエート(phenthoate)、ホレート(phorate)、ホサロン(phosalone)、ホスメット(phosmet)、ホスファミドン(phosphamidon)、ホキシム(phoxim)、ピリミホス・メチル(pirimiphos-methyl)、プロフェノホス(profenofos)、プロパホス(propaphos)、プロペタムホス(propetamphos)、プロチオホス(prothiofos)、ピラクロホス(pyraclofos)、ピリダフェンチオン(pyridaphenthion)、キナルホス(quinalphos)、スルホテップ(sulfotep)、テブピリムホス(tebupirimfos)、テメホス(temephos)、テルブホス(terbufos)、テトラクロルビンホス(tetrachlorvinphos)、チオメトン(thiometon)、チオナジン(thionazin)、トリアゾホス(triazophos)、トリクロルホン(trichlorfon)、バミドチオン(vamidothion)、ジクロフェンチオン(dichlofenthion)、イミシアホス(imicyafos)、イソカルボホス(isocarbophos)、メスルフェンホス(mesulfenfos)、フルピラゾホス(flupyrazofos)
2.GABA受容体(クロライドチャネル)阻害剤
(2A)シクロジエン有機塩素系化合物:クロルデン(chlordane)、エンドスルファン(endosulfan)、ガンマ-BHC(gamma-BCH);
(2B)フェニルピラゾール系化合物:アセトプロール(acetoprol)、エチプロール(ethiprole)、フィプロニル(fipronil)、ピラフルプロール(pyrafluprole)、ピリプロール(pyriprole)、RZI-02-003(コード番号)
3.ナトリウムチャネルに作用する剤
(3A)ピレスロイド系化合物:アクリナトリン(acrinathrin)、アレスリン(allethrin)[d-cis-trans、d-transを含む]、ビフェントリン(bifenthrin)、ビオアレスリン(bioallethrin)、ビオアレスリンS‐シクロペンテニル(bioallethrin S-cyclopentenyl)ビオレスメトリン(bioresmethrin)、シクロプロトリン(cycloprothrin)、シフルトリン(cyfluthrin)[beta-を含む]、シハロトリン(cyhalothrin)[gamma-,lambda-を含む]、シペルメトリン(cypermethrin)[alpha-,beta-,theta-,zeta-を含む]、シフェノトリン(cyphenothrin)[(1R)-trans-isomersを含む]、デルタメトリン(deltamethrin)、エンペントリン(empenthrin)、エスフェンバレレート(esfenvalerate)、エトフェンプロックス(etofenprox)、フェンプロパトリン(fenpropathrin)、フェンバレレート(fenvalerate)、フルシトリネート(flucythrinate)、フルメトリン(flumethrin)、タウフルバリネート[tau -を含む]、ハルフェンプロックス(halfenprox)、イミプロトリン(imiprothrin)、メトフルトリン(metofluthrin)、ペルメトリン(permethrin)、フェノトリン(phenothrin)[(1R)-trans-isomerを含む]、プラレトリン(prallethrin)、プロフルトリン(profluthrin)、ピレトリン(pyrethrine)、レスメトリン(resmethrin)、RU15525(コード番号)、シラフルオフェン(silafluofen)、テフルトリン(tefluthrin)、テトラメトリン(tetramethrin)、トラロメトリン(tralomethrin)、トランスフルトリン(transfluthrin)、ZXI8901(コード番号)、フルバリネート(fluvalinate)、テトラメチルフルスリン(tetramethylfluthrin)、メペルフルスリン(meperfluthrin);
(3B)DDT系化合物:DDT、メトキシクロル(methoxychlor)
4.ニコチン性アセチルコリン受容体アゴニスト/アンタゴニスト
(4A)ネオニコチノイド系化合物:アセタミプリド(acetamiprid)、クロチアニジン(clothianidin)、ジノテフラン(dinotefuran)、イミダクロプリド(imidacloprid)、ニテンピラム(nitenpyram)、チアクロプリド(thiacloprid)、チアメトキサム(thiamethoxam);
(4B)ニコチン系化合物:硫酸ニコチン(nicotine-sulfate)
5.ニコチン性アセチルコリン受容体アロステリックアクチベーター
スピノシン系化合物:スピネトラム(spinetoram)、スピノサド(spinosad);
6.クロライドチャネルを活性化する剤
アバメクチン、ミルベマイシン系化合物:アバメクチン(abamectin)、エマメクチンベンゾエート(emamectin benzoate)、レピメクチン(lepimectin)、ミルベメクチン(milbemectin)、イベルメクチン(ivermectin)、ポリナクチン複合体(polynactins)
7.幼若ホルモン様の剤
ジオフェノラン(diofenolan)、ハイドロプレン(hydroprene)、キノプレン(kinoprene)、メトトリン(methothrin)、フェノキシカルブ(fenoxycarb)、ピリプロキシフェン(pyriproxyfen)
8.非特異的作用(多作用点)の剤
1,3‐ジクロロプロペン(1,3-dichloropropene)、DCIP、エチレンジブロミド(ethylene dibromide)、メチルブロマイド(methyl bromide)、クロルピクリン(chloropicrin)、フッ化スルフリル(sulfuryl fluoride)
9.摂食阻害剤
ピメトロジン(pymetrozine)、フロニカミド(flonicamid)、ピリフルキナゾン(pyrifluquinazon)
10.ダニの成長制御剤
クロフェンテジン(clofentezine)、ジフロビダジン(diflovidazin)、ヘキサチアゾクス(hexythiazox)、エトキサゾール(etoxazole)
11.昆虫腸内膜を破壊する剤
BT剤:Bacillus sphaericus、Bacillus thuringiensis subsp. aizawai、Bacillus thuringiensis subsp. israelensis、Bacillus thuringiensis subsp. kurstaki、Bacillus thuringiensis subsp. tenebrionis、Bt crop proteins(Cry1Ab, Cry1Ac, Cry1Fa, Cry2Ab, mCry3A, Cry3Ab, Cry3Bb, Cry34/35Ab1)、Bacillus popilliae、Bacillus subtillis
12.ATP 生合成酵素阻害剤
ジアフェンチウロン(diafenthiuron);
有機スズ化合物:アゾシクロチン(azocyclotin)、シヘキサチン(cyhexatin)、フェンブタンチン・オキシド(fenbutatin oxide);
プロパルギット(propargite)、テトラジホン(tetradifon)
13.脱共役剤
クロルフェナピル(chlorfenapyr)、DNOC(DNOC)
14.ニコチン性アセチルコリンチャネルブロッカー剤
ネライストキシン系化合物:ベンスルタップ(bensultap)、カルタップ(cartap)、チオシクラム(thiocyclam)、チオスルタップ(thiosultap)
15.キチン生合成阻害剤(タイプ0)
ベンゾイルウレア系化合物:ビストリフルロン(bistrifluron)、クロルフルアズロン(chlorfluazuron)、ジフルベンズロン(diflubenzuron)、フルシクロクスロン(flucycloxuron)、フルフェノクスロン(flufenoxuron)、ヘキサフルムロン(hexaflumuron)、ルフェヌロン(lufenuron)、ノバルロン(novaluron)、ノビフルムロン(noviflumuron)、テフルベンズロン(teflubenzuron)、トリフルムロン(triflumuron)、フルアズロン(fluazuron)
16.キチン生合成阻害剤(タイプ1)
ブプロフェジン(buprofezin)
17.脱皮阻害剤(双翅目対象)
シロマジン(cyromazine)
18.エクダイソンアゴニスト(脱皮促進)
ジアシルヒドラジン系化合物:クロマフェノジド(chromafenozide)、ハロフェノジド(halofenozide)、メトキシフェノジド(methoxyfenozide)、テブフェノジド(tebufenozide);
19.オクトパミンアゴニスト
アミトラズ(amitraz)
20.ミトコンドリア電子伝達系(複合体III)阻害剤
シフルメトフェン(cyflumetofen)、ヒドラメチルノン(hydramethylnon)、アセキノシル(acequinocyl)、フルアクリピリム(fluacrypyrim)、シエノピラフェン(cyenopyrafen)
21.ミトコンドリア電子伝達系(複合体I)阻害剤
METI殺ダニ剤:フェナザキン(fenazaquin)、フェンピロキシメート(fenpyroximate)、ピリダベン(pyridaben)、ピリミジフェン(pyrimidifen)、テブフェンピラド(tebufenpyrad)、トルフェンピラド(tolfenpyrad);
その他:ロテノン(rotenone)
22.ナトリウムチャネル阻害剤
インドキサカルブ(indoxacarb)、メタフルミゾン(metaflumizon)
23.脂質生合成阻害剤
テトラニック系殺虫/殺ダニ剤:スピロジクロフェン(spirodiclofen)、スピロメシフェン(spiromesifen)、スピロテトラマト(spirotetramat)
24.ミトコンドリア電子伝達系(複合体IV)阻害剤
りん化アルミニウム(aluminium phosphide)、りん化水素(phosphine)、りん化亜鉛(zinc phosphide)、石灰窒素(calcium cyanide)
25.神経阻害(作用機作不明)剤
ビフェナゼート(bifenazate)
26.アコニターゼ阻害剤
フルオロ酢酸ナトリウム塩(sodium fluoroacetate)
27.共力剤
ピペロニルブトキシド(piperonyl butoxide)、DEF(DEF)
28.リアノジン受容体に作用する剤
クロラントラニリプロール(chlorantraniliprole)、フルベンジアミド(flubendiamide)、シアントラニリプロール(cyantraniliprole)
29.その他(作用性が不明)の剤
アザジラクチン(azadirachtin)、アミドフルメット(amidoflumet)、ベンクロチアズ(benclothiaz)、ベンゾキシメート(benzoximate)、ブロモプロピレート(bromopropylate)、キノメチオネート(chinomethionat)、CL900167(コード番号)、クリオライト(cryolite)、ジコホル(dicofol)、ジシクラニル(dicyclanil)、ジエノクロル(dienochlor)、ジノブトン(dinobuton)、酸化フェンブタスズ(fenbutatin oxide)、フェノチオカルブ(fenothiocarb)、フルエンスルホン(fluensulfone)、フルフェネリム(flufenerim)、フルスルファミド(flusulfamide)、カランジン(karanjin)、メタム(metham)、メトプレン(methoprene)、メトキシフェノジド(methoxyfenozide)、メチルイソチオシアネート(methyl isothiocyanate)、ピリダリル(pyridalyl)、ピリフルキナゾン(pyrifluquinazon)、スルコフロン(sulcofuron-sodium)、スルフルラミド(sulfluramid)、スルホキサフロル(sulfoxaflor)
30.昆虫病原性糸状菌、殺線虫微生物
ボーベリア・バッシアーナ(Beauveria bassiana)、ボーベリア・テネーラ(Beauveria tenella)、バーティシリウム レカニ(Verticillium lecanii)、ペキロマイセス・テヌイペス(Pacilimyces tenuipes)、ペキロマイセス・フモソロセウス(Paecilomyces fumosoroceus)、ボーベリア・ブロンニアティ(Beauveria brongniartii)、モナクロスポリウム・フィマトパガム(Monacrosporium phymatophagum)、パスツーリアペネトランス胞子(Pasteuriapenetrans)
31.性フェロモン
(Z)-11-ヘキサデセナール、(Z)-11-ヘキサデセニル=アセタート、リトルアA(litlure-A)、リトルアB(litlure-B)、Z-13-イコセン-10-オン、(Z,E)-9,12-テトラデカジエニル=アセタート、(Z)-9-テトラデセン-1-オール、(Z)-11-テトラデセニル=アセタート、(Z)-9,12-テトラデカジエニル=アセタート、(Z,E)-9,11-テトラデカジエニル=アセタート
混合又は併用してもよい公知の殺菌剤又は病害防除剤化合物を例示する。
1. 核酸生合成阻害剤
アシルアラニン化合物:ベナラキシル(benalaxyl)、ベナラキシル・M(benalaxyl-M)、フララキシル(furalaxyl)、メタラキシル(metalaxyl)、メタラキシル・M(metalaxyl-M);
オキサゾリジノン系化合物:オキサジキシル(oxadixyl);
ブチロラクトン系化合物:クロジラコン(clozylacon)、オフラセ(ofurace);
ヒドロキシ‐(2‐アミノ)ピリミジン系化合物:ブピリメート(bupirimate)、ジメチリモル(dimethirimol)、エチリモル(ethirimol);
イソキサゾール系化合物:ヒメキサゾール(hymexazol);
イソチアゾロン系化合物:オクチリノン(octhilinone);
カルボン酸系化合物:オキソリニック酸(oxolinic acid)
2. 有糸分裂及び細胞分裂阻害剤
ベンゾイミダゾール系化合物:ベノミル(benomyl)、カルベンダジム(carbendazim)、フベリダゾール(fuberidazole)、チアベンダゾール(thiabendazole);
チオファネート系化合物:チオファネート(thiophanate)、チオファネート・メチル(thiophanate-methyl);
N‐フェニルカルバマート系化合物:ジエトフェンカルブ(diethofencarb );
トルアミド系化合物:ゾキサミド(zoxamide);
フェニルウレア系化合物:ペンシクロン(pencycuron);
ピリニジルメチルベンズアミド系化合物:フルオピコリド(fluopicolide)
3. 呼吸阻害剤
ピリミジンアミン系化合物:ジフルメトリム(diflumetorim);
カルボキサミド系化合物:ベノダニル(benodanil)、フルトラニル(flutolanil)、メプロニル(mepronil)、フルオピラム(fluopyram)、フェンフラム(fenfuram)、カルボキシン(carboxin)、オキシカルボキシン(oxycarboxin)、チフルザミド(thifluzamide)、ビキサフェン(bixafen)、フラメトピル(furametpyr)、イソピラザム(isopyrazam)、ペンフルフェン(penflufen)、ペンチオピラド(penthiopyrad)、セダキサン(sedaxane)、ボスカリド(boscalid);
メトキシアクリレート系化合物:アゾキシストロビン(azoxystrobin)、エネストロブリン(enestroburin)、ピコキシストロビン(picoxystrobin)、ピラオキシストロビン(pyraoxystrobin);
メトキシカルバマート系化合物:ピラクロストロビン(pyraclostrobin)、ピラメトストロビン(pyrametostrobin);
オキシイミノアセテート化合物:クレソキシム・メチル(kresoxim-methyl)、トリフロキシストロビン(trifloxystrobin);
オキシイミノセトアミド系化合物:ジモキシストロビン(dimoxystrobin)、メトミノストロビン(metominostrobin)、オリサストロビン(orysastrobin);
オキサゾリジンジオン系化合物:ファモキサドン(famoxadone);
ジヒドロジオキサジン系化合物:フルオキサストロビン(fluoxastrobin);
イミダゾリノン系化合物:フェナミドン(fenamidone);
ベンジルカルバマート系化合物:ピリベンカルブ(pyribencarb);
シアノイミダゾール系化合物:シアゾファミド(cyazofamid);
スルファモイルトリアゾール系化合物:アミスルブロム(amisulbrom);
ジニトロフェニルクロトン酸系化合物:ビナパクリル(binapacryl)、メプチルジノカップ(meptyldinocap)、ジノカップ(dinocap);
2,6‐ジニトロアニリン系化合物:フルアジナム(fluazinam);
ピリミジノンヒドラゾン系化合物:フェリムゾン(ferimzone);
トリフェニルスズ系化合物:TPTA(TPTA)、TPTC(TPTC)、TPTH(TPTH);
チオフェンカルボキサミド系化合物:シルチオファム(silthiofam);
トリアゾロピリミジルアミン系化合物:アメトクトラジン(ametoctradin)
4. アミノ酸及びタンパク質合成阻害剤
アニリノピリミジン系化合物:シプロジニル(cyprodinil)、メパニピリム(mepanipyrim)、ピリメタニル(pyrimethanil);
エノピランウロン酸系抗生物質:ブラストサイジン-S(blasticidin-S)、ミルディオマイシン(mildiomycin);
へキソピラノシル系抗生物質:カスガマイシン(kasugamycin);
グルコピラノシル系抗生物質:ストレプトマイシン(streptomycin);
テトラサイクリン系抗生物質:オキシテトラサイクリン(oxytetracycline)
5. シグナル伝達系に作用する剤
キノリン系化合物:キノキシフェン(quinoxyfen);
キナゾリン系化合物:プロキナジド(proquinazid);
フェニルピロール系化合物:フェンピクロニル(fenpiclonil)、フルジオキソニル(fludioxonil);
ジカルボキシミド系化合物:クロゾリネート(chlozolinate)、イプロジオン(iprodione)、プロシミドン(procymidone)、ビンクロゾリン(vinclozolin);
6. 脂質及び細胞膜合成阻害剤
ホスホロチオレート系化合物:エジフェンホス(edifenphos)、イプロベンホス(iprobenfos)、ピラゾホス(pyrazophos);
ジチオラン系化合物:イソプロチオラン(isoprothiolane);
芳香族炭化水素系化合物:ビフェニル(biphenyl)、クロロネブ(chloroneb)、ジクロラン(dicloran)、キントゼン(quintozene )、テクナゼン(tecnazene)、トルクロホス・メチル(tolclofos-methyl);
1,2,4‐チアジアゾール系化合物:エトリジアゾール(etridiazole);
カルバマート系化合物:ヨードカルブ(iodocarb)、プロパモカルブ塩酸塩(propamocarb-hydrochloride)、プロチオカルブ(prothiocarb);
桂皮酸アミド系化合物:ジメトモルフ(dimethomorph)、フルモルフ(flumorph);
バリンアミドカルバマート系化合物:ベンチアバリカルブ・イソプロピル(benthiavalicarb-isopropyl)、イプロバリカルブ(iprovalicarb)、バリフェナレート(valifenalate);
マンデル酸アミド系化合物:マンジプロパミド(mandipropamid);
バチルスズブチリス及び殺菌性リポペプチド生産物:バチルスズブチリス(Bacillus subtilis)(strain:QST 713)
7. ステロール生合成阻害剤
ピペラジン系化合物:トリホリン(triforine);
ピリジン系化合物:ピリフェノックス(pyrifenox);
ピリミジン系化合物:フェナリモル(fenarimol)、ヌアリモル(nuarimol);
イミダゾール系化合物:イマザリル(imazalil)、オキスポコナゾールフマル酸塩(oxpoconazole-fumarate)、ペフラゾエート(pefurazoate)、プロクロラズ(prochloraz)、トリフルミゾール(triflumizole);
トリアゾール系化合物:アザコナゾール(azaconazole)、ビテルタノール(bitertanol)、ブロムコナゾール(bromuconazole)、シプロコナゾール(cyproconazole)、ジフェノコナゾール(difenoconazole)、ジニコナゾール(diniconazole)、ジニコナゾール・M(diniconazole-M)、エポキシコナゾール(epoxiconazole)、エタコナゾ-ル(etaconazole)、フェンブコナゾール(fenbuconazole)、フルキンコナゾール(fluquinconazole)、フルシラゾール(flusilazole)、フルトリアホール(flutriafol)、ヘキサコナゾール(hexaconazole)、イミベンコナゾール(imibenconazole)、イプコナゾール(ipconazole)、メトコナゾール(metconazole)、ミクロブタニル(myclobutanil)、ペンコナゾール(penconazole)、プロピコナゾール(propiconazole)、プロチオコナゾール(prothioconazole)、シメコナゾール(simeconazole)、テブコナゾール(tebuconazole)、テトラコナゾール(tetraconazole)、トリアジメホン(triadimefon)、トリアジメノール(triadimenol)、トリチコナゾール(triticonazole)、フルコナゾール(furconazole)、フルコナゾール・シス(furconazole -cis)、キンコナゾール(quinconazole);
モルホリン系化合物:アルジモルフ(aldimorph)、ドデモルフ(dodemorph)、フェンプロピモルフ(fenpropimorph)、トリデモルフ(tridemorph);
ピペリジン系化合物:フェンプロピジン(fenpropidin)、ピペラリン(piperalin);
スピロケタールアミン系化合物:スピロキサミン(spiroxamine);
ヒドロキシアニリド系化合物:フェンヘキサミド(fenhexamid);
チオカルバマート系化合物:ピリブチカルブ(pyributicarb);
アリルアミン系化合物:ナフティフィン(naftifine)、テルビナフィン(terbinafine)
8. グルカン合成阻害剤
グルコピラノシル系抗生物質:バリダマイシン(validamycin);
ペプチジルピリジンヌクレオチド化合物:ポリオキシン(polyoxin)
9. メラニン合成阻害剤
イソベンゾフラノン系化合物:フサライド(phthalide);
ピロロキノリン系化合物:ピロキロン(pyroquilon);
トリアゾロベンゾチアゾール系化合物:トリシクラゾール(tricyclazole);
カルボキサミド系化合物:カルプロパミド(carpropamid)、ジクロシメット(diclocymet);
プロピオンアミド系化合物:フェノキサニル(fenoxanil)
10. 植物病害抵抗性を誘導する剤
ベンゾチアジアゾール系化合物:アシベンゾラル・S・メチル(acibenzolar-S-methyl);
ベンゾイソチアゾール系化合物:プロベナゾール(probenazole);
チアジアゾールカルボキサミド系化合物:チアジニル(tiadinil)、イソチアニル(isotianil);
天然物:ラミナリン
11.作用性不明及び多作用点の剤
銅化合物:水酸化第二銅(copper hydroxide)、オクタン酸銅(copper dioctanoate)、塩基性塩化銅(copper oxychloride)、硫酸銅(copper sulfate)、酸化第一銅(cuprous oxide)、オキシキノリン銅(oxine-copper)、ボルドー液(Bordeaux mixture)、ノニルフェノールスルホン酸銅(copper nonyl phenol sulphonate);
硫黄化合物:硫黄(sulfur);
ジチオカルバマート系化合物:ファーバム(ferbam)、マンコゼブ(mancozeb)、マンネブ(maneb)、メチラム(metiram)、プロピネブ(propineb)、チウラム(thiram)、ジネブ(zineb)、ジラム(ziram)、クフラネブ(cufraneb);
フタルイミド系化合物:キャプタン(captan)、フォルペット(folpet)、カプタホール(captafol);
クロロニトリル系化合物:クロロタロニル(chlorothalonil);
スルファミド系化合物:ジクロフルアニド(dichlofluanid)、トリルフルアニド(tolylfluanid);
グアニジン系化合物:グアザチン(guazatine)、イミノクタジン・アルベシル酸塩(iminoctadine-albesilate)、イミノクタジン酢酸塩(iminoctadine-triacetate)、ドジン(dodine);
その他の化合物:アニラジン(anilazine)、ジチアノン(dithianon)、シモキサニル(cymoxanil)、ホセチル(fosetyl)(alminium, calcium, sodium)、亜リン酸及び塩(phosphorous acid and salts)、テクロフタラム(tecloftalam)、トリアゾキシド(triazoxide)、フルスルファミド(flusulfamide)、ジクロメジン(diclomezine)、メタスルホカルブ(methasulfocarb)、エタボキサム(ethaboxam)、シフルフェナミド(cyflufenamid)、メトラフェノン(metrafenone)、炭酸水素カリウム(potassium bicarbonate)、炭酸水素ナトリウム(sodium bicarbonate)、BAF-045(コード番号)、BAG-010(コード番号)、ベンチアゾール(benthiazole)、ブロノポール(bronopol)、カルボネ(carvone)、キノメチオネート(chinomethionat)、ダゾメット(dazomet)、DBEDC(DBEDC)、デバカルブ(debacarb)、ジクロロフェン(dichlorophen)、ジフェンゾコート(difenzoquat-methyl sulfate)、ジメチルジスルフィド(dimethyl disulfide)、ジフェニルアミン(diphenylamine)、エトキシキン(ethoxyquin)、フルメトベル(flumetover)、フルオルイミド(fluoroimide)、フルチアニル(flutianil)、フルキサピロキサド(fluxapyroxad)、フランカルボン酸(furancarboxylic acid)、メタム(metam)、ナーバム(nabam)、ナタマイシン(natamycin)、ニトラピリン(nitrapyrin)、ニトロタル・イソプロピル(nitrothal-isopropyl)、オルソフェニルフェノール(o-phenylphenol)、オキサジニラゾール(oxazinylazole)、硫酸オキシキノリン(oxyquinoline sulfate)、フェナジンオキシド(phenazine oxide)、ポリカーバメート(polycarbamate)、ピリオフェノン(pyriofenone)、S-2188(コード番号)、銀(silver)、SYP-Z-048(コード番号)、テブフロキン(tebufloquin)、トルニファニド(tolnifanide)、トリクラミド(trichlamide)、ミネラルオイル(mineral oils)、オーガニックオイル(organic oils);
A1.アセチルCoAカルボキシラーゼ(ACCase)阻害型除草剤
(A1-1) アリールオキシフェノキシプロピオン酸系化合物:クロジナホップ(clodinafop-propargyl)、シハロホップ・ブチル(cyhalofop-butyl)、ジクロホップ・メチル(diclofop-methyl)、ジクロホップ・P・メチル(diclofop-P-methyl)、フェノキサプロップ・P・エチル(fenoxaprop-P-ethyl)、フルアジホップ(fluazifop-butyl)、フルアジホップ・P(fluazifop-P-butyl)、ハロキシホップ(haloxyfop)、ハロキシホップ-エトティル(haloxyfop-etotyl)ハロキシホップ・P(haloxyfop-P)、メタミホップ(metamifop)、プロパキザホップ(propaquizafop)、キザロホップ(quizalofop-ethyl)、キザロホップ・P・エチル(quizalofop-P-ethyl)、キザロホップ・P・テフリル(quizalofop-P-tefuryl)、フェンチアプロップ・エチル(fenthiaprop-ethyl);
(A1-2) シクロヘキサンジオン系化合物:アロキシジム(alloxydim)、ブトロキシジム(butroxydim)、クレトジム(clethodim)、シクロキシジム(cycloxydim)、プロホキシジム(profoxydim)、セトキシジム(sethoxydim)、テプラロキシジム(tepraloxydim)、トラルコキシジム(tralkoxydim);
(A1-3) フェニルピラゾリン系化合物:アミノピラリド(aminopyralid)、ピノキサデン(pinoxaden);
B.アセト乳酸合成酵素(ALS)阻害型除草剤
(B-1) イミダゾリノン系化合物:イマザメタベンズ(imazamethabenz-methyl)、イマザモックス(imazamox)、イマザピク(imazapic)(アミン等との塩を含む)、イマザピル(imazapyr)(イソプロピルアミン等の塩を含む)、イマザキン(imazaquin)、イマゼタピル(imazethapyr);
(B-2) ピリミジニルオキシ安息香酸系化合物:ビスピリバック・ナトリウム塩(bispyribac-sodium)、ピリベンゾキシム(pyribenzoxim)、ピリフタリド(pyriftalid)、ピリミノバック・メチル(pyriminobac-methyl)、ピリチオバック・ナトリウム塩(pyrithiobac-sodium)、ピリミスルファン(pyrimisulfan);
(B-3) スルホニルアミノカルボニルトリアゾリノン系化合物:フルカルバゾン・ナトリウム塩(flucarbazone-sodium)、チエンカルバゾン(thiencarbazone)(ナトリウム塩、メチルエステル等を含む)、プロポキシカルバゾン・ナトリウム塩(propoxycarbazone-sodium)、プロカルバゾン・ナトリウム塩(procarbazone-sodium);
(B-4) スルホニルウレア系化合物:アミドスルフロン(amidosulfuron)、アジムスルフロン(azimsulfuron)、ベンスルフロン・メチル(bensulfuron-methyl)、クロリムロン・エチル(chlorimuron-ethyl)、クロルスルフロン(chlorsulfuron)、シノスルフロン(cinosulfuron)、シクロスルファムロン(cyclosulfamuron)、エタメトスルフロン・メチル(ethametsulfuron-methyl)、エトキシスルフロン(ethoxysulfuron)、フラザスルフロン(flazasulfuron)、フルピルスルフロン(flupyrsulfuron-methyl-sodium)、フォラムスルフロン(foramsulfuron)、ハロスルフロン・メチル(halosulfuron-methyl)、イマゾスルフロン(imazosulfuron)、ヨードスルフロンメチルナトリウム塩(iodosulfulon-methyl-sodium)、メソスフロン・メチル(mesosulfuron-methyl)、チフェンスルフロン・メチル(thifensulfuron-methyl)、トリアスルフロン(triasulfuron)、トリベニュロン・メチル(tribenuron-methyl)、トリフロキシスルフロンナトリウム塩(trifloxysulfuron-sodium)、トリフルスルフロン・メチル(triflusulfuron-methyl)、トリトスルフロン(tritosulfuron)、オルトスルファムロン(orthosulfamuron)、プロピリスルフロン(propyrisulfuron)、メタゾスルフロン(metazosulfuron)フルセトスルフロン(flucetosulfuron);
(B-5) トリアゾロピリミジン系化合物:クロランスラム・メチル(cloransulam-methyi)、ジクロスラム(diclosulam)、フロラスラム(florasulam)、フルメツラム(flumetsulam)、メトスラム(metosulam)、ペノキススラム(penoxsulam)、ピロクススラム(pyroxsulam);
C1.光化学系II(Photosystem II)での光合成阻害除草剤1
(C1-1)フェニルカルバマート系除化合物:デスメディファム(desmedipham)、フェンメディファム(phenmedipham);
(C1-2)ピリダジノン系化合物:クロリダゾン(chloridazon)、ブロムピラゾン(brompyrazon);
(C1-3)トリアジン系化合物:アメトリン(ametryn)、アトラジン(atrazine)、シアナジン(cyanazine)、デスメトリン(desmetryne)、ジメタメトリン(dimethametryn)、エグリナジン(eglinazine-ethyl)、プロメトン(prometon)、プロメトリン(prometryn)、プロパジン(propazine)、シマジン(simazine)、シメトリン(simetryn)、テルブメトン(terbumeton)、テルブチラジン(terbuthylazine)、テルブトリン(terbutryn)、トリエタジン(trietazine);
(C1-4)トリアジノン系化合物:メタミトロン(metamitron)、メトリブジン(metribuzin);
(C1-5)トリアゾリノン系化合物:アミカルバゾン(amicarbazone);
(C1-6)ウラシル系化合物:ブロマシル(bromacil)、レナシル(lenacil)、ターバシル(terbacil);
C2.光化学系II(Photosystem II)での光合成阻害除草剤2
(C2-1)アミド系化合物:ペンタノクロール(pentanochlor)、プロパニル(propanil);
(C2-2)尿素系化合物:クロルブロムロン(chlorbromuron)、クロロトルロン(chlorotoluron)、クロロクスロン(chloroxuron)、ジメフロン(dimefuron)、ジウロン(diuron)、エチジムロン(ethidimuron)、フェニュロン(fenuron)、フルオメツロン(fluometuron)、イソプロツロン(isoproturon)、イソウロン(isouron)、リニュロン(linuron)、メタベンズチアズロン(methabenzthiazuron)、メトブロムロン(metobromuron)、メトキスロン(metoxuron)、モノリニュロン(monolinuron)、ネブロン(neburon)、シデュロン(siduron)、テブチウロン(tebuthiuron)、メトベンズロン(metobenzuron);
C3.光化学系II(Photosystem II)での光合成阻害除草剤3
(C3-1)ベンゾチアジアゾン系化合物:ベンタゾン(bentazone);
(C3-2)ニトリル系化合物:ブロモフェノキシム(bromofenoxim)、ブロモキシニル(bromoxynil)(酪酸、オクタン酸又はヘプタン酸等のエステル体を含む)、アイオキシニル(ioxynil);
(C3-3)フェニルピラジン系除草性化合物:ピリダフォル(pyridafol)、ピリデート(pyridate);
D.光化学系Iからのラジカル生成型除草性剤
(D-1)ビピリジウム系化合物:ジクワット(diquat)、パラコート(paraquat dichloride);
E.プロトポルフィノリーゲンオキシダーゼ(PPO)阻害型除草剤
(E-1)ジフェニルエーテル系化合物:アシフルオルフェン(acifluorfen-sodium)、ビフェノックス(bifenox)、クロメトキシフェン(chlomethoxyfen)、エトキシフェン(ethoxyfen-ethyl)、フルオログリコフェン(fluoroglycofen-ethyl)、ホメサフェン(fomesafen)、ラクトフェン(lactofen)、オキシフルオルフェン(oxyfluorfen);
(E-2)N-フェニルフタルイミド系化合物:シニドン・エチル(cinidon-ethyl)、フルミクロラック・ペンチル(flumiclorac-pentyl)、フルミオキサジン(flumioxazin)、クロルフタリム(chlorphthalim);
(E-3)オキシジアゾール系化合物:オキサジアルギル(oxadiargyl)、オキサジアゾン(oxadiazon);
(E-4)オキサゾリジンジオン系化合物:ペントキサゾン(pentoxazone);
(E-5)フェニルピラゾール系化合物:フルアゾレート(fluazolate)、ピラフルフェン・エチル(pyraflufen-ethyl);
(E-6)ピリミジンジオン系化合物:ベンズフェンジゾン(benzfendizone)、ブタフェナシル(butafenacil)、サフルフェナシル(saflufenacil);
(E-7)チアジアゾール系化合物:フルチアセット・メチル(fluthiacet-methyl)、チジアジミン(thidiazimin);
(E-8)トリアゾリノン系化合物:アザフェニジン(azafenidin)、カルフェントラゾン・エチル(carfentrazone-ethyl)、スルフェントラゾン(sulfentrazone)、ベンカルバゾン(bencarbazone);
(E-9)その他の化合物:フルフェンピル・エチル(flufenpyr-ethyl)、プロフルアゾール(profluazol)、ピラクロニル(pyraclonil)、SYP-298(コード番号)、SYP-300(コード番号);
F1.フィトエンデサチュラーゼ(PDS)阻害剤除草剤
(F1-1)ピリダジノン系化合物:ノルフルラゾン(norflurazon);
(F1-2)ピリミジンカルボキサミド系化合物:ジフルフェニカン(diflufenican)、ピコリナフェン(picolinafen);
(F1-3)その他の化合物:
ベフルブタミド(beflubutamid)、フルリドン(fluridone)、フルロクロリドン(flurochloridone)、フルルタモン(flurtamone);
F2.4-ヒドロキシフェニルピルビン酸ジオキシゲナーゼ(HPPD)阻害型除草剤
(F2-1)カリステモン系化合物:メソトリオン(mesotrione);
(F2-2)イソキサゾール系化合物:ピラスルホトール(pyrasulfotole)、イソキサフルトール(isoxaflutole)、イソキサクロルトール(isoxachlortole);
(F2-3)ピラゾール系化合物:ベンゾフェナップ(benzofenap)、ピラゾリネート(pyrazolynate)、ピラゾキシフェン(pyrazoxyfen);
(F2-4)トリケトン系化合物:スルコトリオン(sulcotrione)、テフリルトリオン(tefuryltrion)、テムボトリオン(tembotrione)、ピラスルホトール(pyrasulfotole)、トプラメゾン(topramezone)、ビシクロピロン(bicyclopyrone);
F3.カロチノイド生合成阻害剤(ターゲット未知)除草剤
(F3-1)ジフェニルエーテル系化合物:アクロニフェン(aclonifen);
(F3-2)イソキサゾリジノン系化合物:クロマゾン(clomazone);
(F3-3)トリアゾール系化合物:アミトロール(amitrole);
G.EPSPシンターゼ合成阻害(芳香族アミノ酸生合成阻害)型除草剤
(G-1)グリシン系化合物:グリホサート(glyphosate)(ナトリウム、アミン、プロピルアミン、イソプロピルアミン、ジメチルアミン又はトリメシウム等の塩を含む);
H.グルタミン合成阻害剤除草剤
(H-1)ホスフィン酸系化合物:ビラナホス(bilanafos)、グルホシネート(glufosinate)(アミン又はナトリウム等の塩を含む);
I.ジヒドロプテロエート(DHP)阻害剤除草剤
(I-1)カルバマート系化合物:アシュラム(asulam);
K1.微小管の集合阻害型除草性剤
(K1-1)ベンズアミド系化合物:プロピザミド(propyzamide)、テブタム(tebutam);
(K1-2)安息香酸系化合物:クロルタル・ジメチル(chlorthal-dimethyl)
(K1-3)ジニトロアニリン系化合物:ベンフルラリン(benfluralin)、ブトラリン(butralin)、ジニトラミン(dinitramine)、エタルフルラリン(ethalfluralin)、フルクロラリン(fluchloralin)、オリザリン(oryzalin)、ペンジメタリン(pendimethalin)、プロジアミン(prodiamine)、トリフルラリン(trifluralin);
(K1-4)ホスホロアミデート系化合物:アミプロホス・メチル(amiprofos-methyl)、ブタミホス(butamifos);
(K1-5)ピリジン系化合物:ジチオピル(dithiopyr)、チアゾピル(thiazopyr);
K2.有糸分裂/微小管組織形成阻害型除草剤
(K2-1)カルバマート系化合物:カルベタミド(carbetamide)、クロルプロファム(chlorpropham)、プロファム(propham)、スエップ(swep)、カルブチレート(karbutilate);
K3.超長鎖脂肪酸伸長酵素(VLCFA)阻害型除草剤
(K3-1)アセトアミド系化合物:ジフェナミド(diphenamid)、ナプロパミド(napropamide)、ナプロアニリド(naproanilide);
(K3-2)クロロアセトアミド系化合物:アセトクロ-ル(acetochlor)、アラクロール(alachlor)、ブタクロール(butachlor)、ブテナクロール(butenachlor)、ジエタチル(diethatyl-ethyl)、 ジメタクロール(dimethachlor)、ジメテナミド(dimethenamid)、ジメテナミド・P(dimethenamid-P)、メタザクロール(metazachlor)、メトラクロール(metolachlor)、ペトキサミド(pethoxamid)、プレチラクロール(pretilachlor)、プロパクロール(propachlor)、プロピソクロール(propisochlor)、S-メトラクロール(S-metolachlor)、テニルクロール(thenylchlor);
(K3-3)オキシアセトアミド系化合物:フルフェナセット(flufenacet )、メフェナセット(mefenacet);
(K3-4)テトラドリノン系化合物:フェントラザミド(fentrazamide);
(K3-5)その他の化合物:アニロホス(anilofos)、ブロモブチド(bromobutide)、カフェンストロール(cafenstrole)、インダノファン(indanofan)、ピペロホス(piperophos)、フェノキサスルホン(fenoxasulfone)、ピロキサスルホン(pyroxasulfone)、イプフェンカルバゾン(ipfencarbazone);
L.セルロース合成阻害剤除草剤
(L-1)ベンズアミド系化合物:イソキサベン(isoxaben);
(L-2)ニトリル系化合物:ジクロベニル(dichlobenil)、クロルチアミド(chlorthiamid);
(L-3)トリアゾロカルボキサミド系化合物:フルポキサム(flupoxame);
M. アンカップラー(細胞膜破裂)型除草剤
(M-1)ジニトロフェノール系化合物:ジノテルブ(dinoterb)、DNOC(アミン又はナトリウム等の塩を含む);
N.脂質生合成(ACCase阻害以外)阻害型除草剤
(N-1)ベンゾフラン系化合物:ベンフレセート(benfuresate)、エトフメセート(ethofumesate);
(N-2)ハロゲン化カルボン酸系化合物:ダラポン(dalapon)、フルプロパネート(flupropanate)、TCA(ナトリウム、カルシウム又はアンモニア等の塩を含む);
(N-3)ホスホロジチオエート系化合物:ベンスリド(bensulide);
(N-4)チオカルバマート系化合物:ブチレート(butylate)、シクロエート(cycloate)、ジメピペレート(dimepiperate)、EPTC、エスプロカルブ(esprocarb)、モリネート(molinate)、オルベンカルブ(orbencarb)、ペブレート(pebulate)、プロスルホカルブ(prosulfocarb)、チオベンカルブ(thiobencarb)、チオカルバジル(tiocarbazil)、トリアレート(tri-allate)、バーナレート(vernolate);
O.合成オーキシン型除草剤
(O-1)安息香酸系化合物:クロランベン(chloramben)、2,3,6-TBA、ジカンバ(dicamba)(アミン、ジエチルアミン、イソプロピルアミン、ジグリコールアミン、ナトリウム又はリチウム等の塩を含む);
(O-2)フェノキシカルボン酸系化合物:2,4,5‐T、2,4-D(アミン、ジエチルアミン、トリエタノールアミン、イソプロピルアミン、ナトリウム又はリチウム等の塩を含む)、2,4-DB、クロメプロップ(clomeprop)、ジクロルプロップ(dichlorprop)、ジクロルプロップ-P(dichlorprop-P)、MCPA、MCPA・チオエチル(MCPA-thioethyl)、MCPB(ナトリウム塩、エチルエステル等を含む)、メコプロップ(mecoprop)(ナトリウム、カリウム、イソプロピルアミン、トリエタノールアミン、ジメチルアミン等の塩を含む)、メコプロップ-P・カリウム塩(mecoprop-P);
(O-3)ピリジンカルボン酸系化合物:クロピラリド(clopyralid)、フルロキシピル(fluroxypyr)、ピクロラム(picloram)、トリクロピル(triclopyr)、トリクロピル-ブトティル(triclopyr-butotyl);
(O-4)キノリンカルボン酸系化合物:キンクロラック(quinclorac)、キンメラック(quinmerac);
(O-5)その他の化合物:ベナゾリン(benazolin);
P.オーキシン輸送阻害型除草剤
(P-1)フタラマート(Phthalamates)系化合物:ナプタラム(naptalam)(ナトリウム等との塩を含む);
(P-2)セミカルバゾン系化合物:ジフルフェンゾピル(diflufenzopyr);
Z.作用性未知の除草剤
フラムプロップ・M(flamprop-M)(メチル、エチル、イソプロピルエステルを含む)、フラムプロップ(flamprop)(メチル、エチル、イソプロピルエステルを含む)、クロルフルレノール(chlorflurenol-methyl)、シンメチリン(cinmethylin)、クミルロン(cumyluron)、ダイムロン(daimuron)、メチルダイムロン(methyldymuron)、ジフェンゾコート(difenzoquat)、エトベンザニド(etobenzanid)、ホサミン(fosamine)、ピリブチカルブ(pyributicarb)、オキサジクロメホン(oxaziclomefone)、アクロレイン(acrolein)、AE-F‐150944(コード番号)、アミノシクロピラクロル(aminocyclopyrachlor)、シアナミド(cyanamide)、heptamaloxyloglucan、インダジフラム(indaziflam)、トリアジフラム(triaziflam)、キノクラミン(quinoclamine)、エンドタール二ナトリウム塩(endothal-disodium)、フェニソファム(phenisopham)
植物生長調節剤:1-メチルシクロプロペン(1-methylcyclopropene)、1-ナフチルアセトアミド(1-naphthylacetamide)、2,6-ジイソプロピルナフタレン(2,6-diisopropylnaphthalene)、4-CPA、ベンジルアミノプリン(benzylaminopurine)、アンシミドール(ancymidol)、アビグリシン(aviglycine)、カルボネ(carvone)、クロルメコート(chlormequat)、クロプロップ(cloprop)、クロキシホナック(cloxyfonac)、クロキシホナック・カリウム塩(cloxyfonac-potassium)、シクラニリド(cyclanilide)、サイトカイニン(cytokinins)ダミノジット(daminozide)、ジケグラック(dikegulac)、ジメチピン(dimethipin)、エテホン(ethephon)、エチクロゼート(ethychlozate)、フルメトラリン(flumetralin)、フルレノール(flurenol)、フルルプリミドール(flurprimidol)、ホルクロルフェニュロン(forchlorfenuron)、ジベレリン(gibberellin acid)、イナベンフィド(inabenfide)、インドール酢酸(indole acetic acid)、インドール酪酸(indole butyric acid)、マレイン酸ヒドラジド(maleic hydrazide)、メフルイジド(mefluidide)、メピコート・クロリド(mepiquat chloride)、デシルアルコール(n-decanol)、パクロブトラゾール(paclobutrazol)、プロヘキサジオン・カルシウム塩(prohexadione-calcium)、プロヒドロジャスモン(prohydrojasmon),シントフェン(sintofen)、チジアズロン(thidiazuron)、トリアコンタノール(triacontanol)、トリネキサパック・エチル(trinexapac-ethyl)、ウニコナゾール(uniconazole)、ウニコナゾール-P(uniconazole-P)
ベノキサコル(benoxacor)、フリラゾール(furilazole)、ジクロルミド(dichlormid)、ジシクロノン(dicyclonone)、DKA-24(N1,N2-ジアリル-N2-ジクロロアセチルグリシンアミド)、AD-67(4-ジクロロアセチル-1-オキサ-4-アザスピロ[4.5]デカン)、PPG-1292(2,2-ジクロロ-N-(1,3-ジオキサン-2-イルメチル)-N-(2-プロペニル)アセトアミド)、R-29148(3-ジクロロアセチル-2,2,5-トリメチル-1,3-オキサゾリジン)、クロキントセット-メキシル(cloquintcet-mexyl)、ナフタル酸無水物(1,8-Naphthalic Anhydride)、メフェンピル-ジエチル(mefenpyr-diethyl)、メフェンピル(mefenpyr)、メフェンピルエチル(mefenpyr-ethyl)、フェンクロラゾール-エチル(fenchlorazole O ethyl)、フェンクロリム(fenclorim)、MG-191(2-ジクロロメチル-2-メチル-1,3-ジオキサン)、シオメトリニル(cyometrinil)、フルラゾール(flurazole)、フルキソフェニム(fluxofenim)、イソキサジフェン(isoxadifen)、イソキサジフェン-エチル(isoxadifen-ethyl)、メコプロップ(mecoprop)、MCPA、ダイムロン(daimuron)、2,4-D、MON4660(コード番号)、オキサベトリニル(oxabetrinil)、シプロスルファミド(cyprosulfamide)、及び、TI-35(コード番号)。
1-(2-シアノ-1,2-ジイソプロポキシイミノエチル)-1H-1,2,4-トリアゾール(本発明化合物番号I-50)の製造
(1)2-シアノ-2-イソプロポキシイミノ酢酸エチル1.0g(5.43ミリモル)のジクロロメタン溶液(5ml)に、O-イソプロピルヒドロキシアミン塩酸塩0.73g(6.54ミリモル)を加え、-20℃に冷却し、トリメチルアルミニウムヘキサン溶液(1.4mol/L)4.34ml(6.08ミリモル)を加えた後、室温へ昇温し、20時間攪拌した。反応混合物を-20℃に冷却し、トリメチルアルミニウムヘキサン溶液を3.88ml(5.43ミリモル)追加し、室温で6時間攪拌した。反応混合物に氷冷下、水を加えた後、酢酸エチルで抽出し、有機層を飽和塩化ナトリウム水溶液で洗浄し、無水硫酸マグネシウムで乾燥した。溶媒を減圧下で留去し、残渣をシリカゲルカラムクロマトグラフィー(溶出溶媒 酢酸エチル:ヘキサン=1:1)で精製し、2-シアノ-2-イソプロポキシイミノ-N-イソプロポキシアセトアミド1.12g(収率97%)を得た。
1-[1,2-ジイソプロポキシイミノ-2-(1H-テトラゾール-5-イル)エチル]-1H-1,2,4-トリアゾール(本発明化合物番号I-213)の製造
1-(2-シアノ-1,2-ジイソプロポキシイミノエチル)-1H-1,2,4-トリアゾール0.40g(1.51ミリモル)のトルエン溶液(5ml)に、トリメチルシリルアジド0.35g(3.03ミリモル)及びジノルマルブチルスズオキシド0.38g(1.51ミリモル)を加え、加熱還流下3時間攪拌した。反応混合物を室温に冷却後、酢酸エチルで抽出し、飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した。溶媒を減圧下で留去し、残渣をシリカゲルカラムクロマトグラフィー(溶出溶媒 酢酸エチル:ヘキサン=1:0)で精製し、得られた結晶をイソプロピルエーテルで洗浄し標題化合物0.23g(収率47%)を得た。
1-(2-カルバモイル-1,2-ジイソプロポキシイミノエチル)-1H-1,2,4-トリアゾール(本発明化合物番号I-73)の製造
1-(2-シアノ-1,2-ジイソプロポキシイミノエチル)-1H-1,2,4-トリアゾール4.0g(15.1ミリモル)のジメチルスルホキシド溶液(2ml)に氷冷下、過酸化水素水3.5ml及び炭酸カリウム2.30g(16.6ミリモル)を加え、室温で10時間攪拌した。析出した結晶を水、イソプロピルエーテルの順に洗浄し、標題化合物3.28g(収率77%)を得た。
1-[2-(4,5-ジヒドロ-1,3-チアゾリン-2-イル)-1,2-ジイソプロポキシイミノエチル]-1H-1,2,4-トリアゾール(本発明化合物番号I-214)及び1-[1,2-ジイソプロポキシイミノ-2-(チアゾール-2-イル)エチル]-1H-1,2,4-トリアゾール(本発明化合物番号I-215)の製造
(1)1-(2-シアノ-1,2-ジイソプロポキシイミノエチル)-1H-1,2,4-トリアゾール0.70g(2.65ミリモル)と酢酸アンモニウム0.22g(2.91ミリモル)のメタノール溶液(5ml)に、2-アミノエタンチオール0.22g(2.91ミリモル)を加え、室温で16時間攪拌した。反応混合物を水にあけ、酢酸エチルで抽出し、飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した。溶媒を減圧下で留去し、残渣をシリカゲルカラムクロマトグラフィー(溶出溶媒 酢酸エチル:ヘキサン=2:1)で精製し、1-[2-(4,5-ジヒドロ-1,3-チアゾリン-2-イル)-1,2-ジイソプロポキシイミノエチル]-1H-1,2,4-トリアゾール0.47g(収率55%)を得た。
1-[2-イソブトキシイミノ-1-イソプロポキシイミノ-2-(1,2,4-オキサジアゾール-2-イル)エチル]-1H-1,2,4-トリアゾール(本発明化合物番号I-209)の製造
(1)前記実施例1に準じて製造された1-[2-シアノ-2-イソブトキシイミノ-1-イソプロポキシイミノエチル]-1H-1,2,4-トリアゾール1.68g(6.04ミリモル)のエタノール溶液(10ml)に、ヒドロキシルアミン塩酸塩0.46g(6.62ミリモル)及び酢酸ナトリウム0.54g(6.58ミリモル)を加え、50℃で3時間攪拌した。反応混合物の溶媒を減圧下で留去し、析出した結晶を水とイソプロピルエーテルで洗浄して1-[2-(N-ヒドロキシアミジノ)-2-イソブチルオキシイミノ-1-イソプロポキシイミノエチル]-1H-1,2,4-トリアゾール0.91g(収率48%)を得た。
1,2-ジイソプロポキシイミノ-1,2-ビス(1H-1,2,4-トリアゾール-1-イル)エタン(本発明化合物番号I-212)の製造
(1)O-イソプロピルヒドロキシルアミン塩酸塩8.79g(78.78ミリモル)のテトラヒドロフラン溶液(40ml)に、氷冷下で炭酸カリウム21.78g(157.59ミリモル)及び塩化オキサリル5.00g(39.39ミリモル)を加え、室温で15時間攪拌した。反応混合物を水にあけ、酢酸エチルで抽出し、飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した。溶媒を減圧下で留去し、N,N‘-ジイソプロポキシオキサミド3.39g(収率42%)を得た。
1-(2-メチルチオ-1,2-ジイソプロポキシイミノエチル)-1H-1,2,4-トリアゾール(本発明化合物番号I-228)の製造
前記実施例6で製造された1,2-ジイソプロポキシイミノ-1,2-ビス(1H-1,2,4-トリアゾール-1-イル)エタン0.35g(1.14ミリモル)の加熱還流したテトラヒドロフラン溶液(5ml)に、ナトリウムチオメトキシドを薄層クロマトグラフィーで反応を確認しながら加え、5時間攪拌した。反応混合物を室温に冷却し、水にあけて酢酸エチルで抽出し、飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した。溶媒を減圧下で留去し、残渣をシリカゲルカラムクロマトグラフィー(溶出溶媒 酢酸エチル:ヘキサン=1:2)で精製し、標題化合物0.17g(収率52%)を得た。
1-(2-クロロ-1,2-ジイソプロポキシイミノエチル)-1H-1,2,4-トリアゾール(本発明化合物番号I-4)の製造
(1)2-ヒドロキシイミノ-2-1H-1,2,4-トリアゾール-1-イル酢酸エチル14g(76ミリモル)のN,N-ジメチルホルムアミド溶液(100ml)に、ヨウ化イソプロピル14g(82ミリモル)と炭酸カリウム13g(94ミリモル)を加え、室温で5時間攪拌した。反応混合物を水にあけ、酢酸エチルで抽出し、無水硫酸マグネシウムで乾燥し、減圧下濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィー(溶出溶媒 酢酸エチル:ヘキサン=1:8)で精製して2-イソプロポキシイミノ-2-1H-1,2,4-トリアゾール-1-イル酢酸エチル9.0g(収率52%)を得た。
1-(1,2-ジイソプロポキシイミノ-2-メトキシエチル)-1H-1,2,4-トリアゾール(本発明化合物番号I-165)の製造
前記実施例8で製造したN-イソプロポキシ-2-イソプロポキシイミノ-2-(1H-1,2,4-トリアゾール-1-イル)アセトアミド0.4g(1.57ミリモル)と炭酸カリウム0.22g(1.59ミリモル)のN,N-ジメチルホルムアミド溶液(5ml)に、ヨードメタン0.22g(1.55ミリモル)を氷冷下で加え、更に室温で20時間攪拌した。反応混合物を水にあけ、酢酸エチルで抽出し、飽和塩化ナトリウム水溶液で洗浄し、無水硫酸マグネシウムで乾燥した。溶媒を減圧下で留去し、残渣をシリカゲルカラムクロマトグラフィー(溶出溶媒 酢酸エチル:ヘキサン=1:2)で精製し、標題化合物0.12g(収率29%)を得た。
1-(2-イソプロポキシイミノ-2-チオカルバモイル-1-メトキシイミノエチル)-1H-1,2,4-トリアゾール(本発明化合物番号II-224)の製造
1-(2-カルバモイル-2-イソプロポキシイミノ-1-メトキシイミノエチル)-1H-1,2,4-トリアゾール0.40g(1.6ミリモル)のテトラヒドロフラン(8ml)溶液に、ローソン試薬0.77g(1.9ミリモル)を室温で加え、40℃で2時間攪拌し、更に60℃で3時間撹拌した。反応混合物を室温に冷却後、ジイソプロピルエーテルを加え、水及び飽和食塩水で洗浄し、無水硫酸ナトリウムで乾燥し、溶媒を留去した。得られた残渣をシリカゲルカラムクロマトグラフィー(溶出溶媒 酢酸エチル:ヘキサン=1:2)により精製し、標題化合物0.25g(収率58%)を黄色粉末として得た。
2-イソプロポキシイミノ-3-メトキシイミノ-3-1H-1,2,4-トリアゾール-1-イルプロパンカルボキシミド酸メチル(本発明化合物番号II-223)の製造
1-(2-シアノ-2-イソプロポキシイミノ-1-メトキシイミノエチル)-1H-1,2,4-トリアゾール5.0g(21ミリモル)のメタノール(50ml)溶液に、ナトリウムメトキシド28%メタノール溶液1.6g(8.4ミリモル)を氷冷下で滴下し、更に氷冷下で2時間撹拌した。反応混合液に少量のクエン酸水溶液を加え、酢酸エチルで抽出し、飽和重曹水及び食塩水で洗浄し、無水硫酸ナトリウムで乾燥した。溶媒を留去し、得られた残渣をシリカゲルカラムクロマトグラフィー(溶出溶媒 酢酸エチル:ヘキサン=1:2)により精製し、標題化合物2.5g(収率44%)を黄色油状物質として得た。
1-(2-イソプロポキシイミノ-2-メトキシカルボニル-1-メトキシイミノエチル)-1H-1,2,4-トリアゾール(本発明化合物番号II-221)の製造
前記実施例11で製造した2-イソプロポキシイミノ-3-メトキシイミノ-3-1H-1,2,4-トリアゾール-1-イルプロパンカルボキシミド酸メチル2.5g(9.3ミリモル)のメタノール(20ml)溶液に、3mol/l塩酸(12ml)を氷冷下で加え、40分撹拌した。反応混合物に水を加え、酢酸エチルで抽出し、飽和重曹水及び食塩水で洗浄し、無水硫酸ナトリウムで乾燥した。溶媒を留去し、標題化合物2.4g(収率95%)を無色油状物質として得た。
1-(2-イソプロポキシイミノ-2-N,N-ジメチルカルバモイル-1-メトキシイミノエチル)-1H-1,2,4-トリアゾール(本発明化合物番号II-226)の製造
ジメチルアミン塩酸塩0.36g(4.4ミリモル)の1,2-ジクロロエタン(7ml)懸濁液に、トリメチルアルミニウム1mol/lヘキサン溶液4.4ml(4.4ミリモル)を室温で滴下し、更に80℃で30分撹拌した。この反応混合物に前記実施例12で製造した1-(2-イソプロポキシイミノ-2-メトキシカルボニル-1-メトキシイミノエチル)-1H-1,2,4-トリアゾール0.30g(1.1ミリモル)の1,2-ジクロロエタン(3ml)溶液を60℃で加え,更に1.5時間撹拌した。反応混合物を室温に冷却後、イソプロピルエーテルで希釈し少量の水を加えて撹拌し、生じた沈殿物をろ過した。溶媒を留去し、得られた残渣をシリカゲルカラムクロマトグラフィー(溶出溶媒 酢酸エチル:ヘキサン=2:1)により精製し、標題化合物0.30g(収率97%)を黄色油状物質として得た。
2-イソプロポキシイミノ-3-メトキシイミノ-3-1H-1,2,4-トリアゾール-1-イルプロパンチオ酸メチルS-エチル(本発明化合物番号II-222)の製造
1,2-ジクロロエタン(8ml)にトリメチルアルミニウム1mol/l ヘキサン溶液7.5ml(7.5ミリモル)を加え、この混合溶液にエタンチオール0.47g(7.5ミリモル)を室温で滴下し、30分撹拌した。この混合溶液に、前記実施例12で製造した1-(2-イソプロポキシイミノ-2-メトキシカルボニル-1-メトキシイミノエチル)-1H-1,2,4-トリアゾール0.50g(1.9ミリモル)の1,2-ジクロロエタン溶液を室温で加え、1.5時間撹拌した。反応混合物にイソプロピルエーテルで希釈し、少量の水を加えて撹拌し、生じた沈殿物をろ過した。溶媒を留去して得られた残渣をシリカゲルカラムクロマトグラフィー(溶出溶媒 酢酸エチル:ヘキサン=1:2)により精製し、標題化合物0.56g(収率98%)を黄色油状物質として得た。
1-(2-アミノ-1,2-ジイソプロポキシイミノエチル)-1H-1,2,4-トリアゾール(本発明化合物番号I-119)の製造
(1)前記実施例8の(1)で製造した2-イソプロポキシイミノ-2-1H-1,2,4-トリアゾール-1-イル酢酸エチル24.17g(106.84ミリモル)のメタノール溶液(40ml)に氷冷下、30%アンモニア水溶液12.13g(213.68ミリモル)を加え、3時間攪拌した。反応混合物の溶媒を減圧留去し、得られた残渣をジクロロメタン溶液(40ml)に溶解し、この溶液に氷冷下、ピリジン16.90g(213.65ミリモル)、トリフルオロ酢酸無水物24.68g(117.51ミリモル)を加え、4時間攪拌した。反応混合物を酢酸エチルで抽出し、飽和塩化ナトリウム水溶液で洗浄し、無水硫酸マグネシウムで乾燥した。溶媒を減圧下で留去し、残渣をシリカゲルカラムクロマトグラフィー(溶出溶媒 酢酸エチル:ヘキサン=2:1)で精製し、1-(1-シアノ-1-イソプロポキシイミノメチル)-1H-1,2,4-トリアゾール19.14g(収率100%)を得た。
1-(2-ブロモ-1,2-ジイソプロポキシイミノエチル)-1H-1,2,4-トリアゾール(本発明化合物番号I-142)の製造
前記実施例15で製造した1-(2-アミノ-1,2-ジイソプロポキシイミノエチル)-1H-1,2,4-トリアゾール0.13g(0.51ミリモル)に、水5ml、47%臭化水素酸0.5mlを加えた溶液へ氷冷下、亜硝酸ナトリウム0.04g(0.58ミリモル)と水3mlからなる水溶液を加え、攪拌した。4時間後、反応混合物を酢酸エチルで抽出し、有機層を飽和塩化ナトリウム水溶液で洗浄し、無水硫酸マグネシウムで乾燥した。溶媒を減圧下で留去し、残渣をシリカゲルカラムクロマトグラフィー(溶出溶媒 酢酸エチル:ヘキサン=1:2)で精製し、標題化合物0.11g(収率68%)を得た。
1-(2-アミノ-2-イソブトキシイミノ-1-イソプロポキシイミノエチル)-1H-1,2,4-トリアゾール(本発明化合物番号I-121)の製造
(1)前記実施例15の(1)で製造した1-(1-シアノ-1-イソプロポキシイミノメチル)-1H-1,2,4-トリアゾール15.06g(84.05ミリモル)のメタノール溶液(120ml)に、炭酸カリウム13.94g(100.86ミリモル)及びヒドロキシルアミン塩酸塩6.50g(93.54ミリモル)を加え、加熱還流下2時間攪拌した。反応混合物を室温に冷却後、反応溶液を2N-HClでpH4とし、酢酸エチルで抽出した。有機層を飽和塩化ナトリウム水溶液で洗浄し、無水硫酸マグネシウムで乾燥した。溶媒を減圧下で留去し、1-(2-アミノ-2-ヒドロキシイミノ-1-イソプロポキシイミノエチル)-1H-1,2,4-トリアゾール14.81g(収率83%)を得た。
1-[2-N-アセチルアミノ-2-イソブチルオキシイミノ-1-イソプロポキシイミノエチル]-1H-1,2,4-トリアゾール(本発明化合物番号I-217)の製造
前記実施例17で製造した1-(2-アミノ-2-イソブトキシイミノ-1-イソプロポキシイミノエチル)-1H-1,2,4-トリアゾール0.4g(1.49ミリモル)のトルエン溶液(5ml)に、塩化アセチル0.58g(7.39ミリモル)を加え、100℃で10時間攪拌した。反応混合物を室温に冷却後、酢酸エチルで抽出し、飽和塩化ナトリウム水溶液で洗浄し、無水硫酸マグネシウムで乾燥した。溶媒を減圧下で留去し、残渣をシリカゲルカラムクロマトグラフィー(溶出溶媒 酢酸エチル:ヘキサン=2:1)で精製し、標題化合物0.34g(収率74%)を得た。
1-[2-N-メトキシカルボニルアミノ-2-イソブチルオキシイミノ-1-イソプロポキシイミノエチル]-1H-1,2,4-トリアゾール(本発明化合物番号I-219)の製造
前記実施例17で製造した1-(2-アミノ-2-イソブトキシイミノ-1-イソプロポキシイミノエチル)-1H-1,2,4-トリアゾール0.34g(1.27ミリモル)のN,N-ジメチルアセトアミド溶液(5ml)に氷冷下、55% 水素化ナトリウム0.06g(1.40ミリモル)を加え、室温で5分間攪拌した。この混合物に、氷冷下でクロロ蟻酸メチルエステル0.13g(1.40ミリモル)を加え、室温で18時間攪拌した。反応混合物は、酢酸エチルで抽出し、塩化ナトリウム水溶液で洗浄し、無水硫酸マグネシウムで乾燥した。溶媒を減圧下で留去し、残渣をシリカゲルカラムクロマトグラフィー(溶出溶媒 酢酸エチル:ヘキサン=1:2)で精製し、ジ置換体(1-[2-N,N-ジメトキシカルボニルアミノ-2-イソブチルオキシイミノ-1-イソプロポキシイミノエチル]-1H-1,2,4-トリアゾール)を得た。ジ置換体のメタノール溶液(5ml)に炭酸カリウムをpH9程度になるまで加え、70℃で10時間攪拌した。反応混合物を室温に冷却後、酢酸エチルで抽出し、飽和塩化ナトリウム水溶液で洗浄し、無水硫酸マグネシウムで乾燥した。溶媒を減圧下で留去し、残渣をシリカゲルカラムクロマトグラフィー(溶出溶媒 酢酸エチル:ヘキサン=2:1)で精製し、標題化合物0.18g(収率43%)を得た。
1-(1,2-ジイソプロポキシイミノプロピル)-2-メルカプトイミダゾール(本発明化合物番号V-10)の製造
(1)ピルビン酸3.00g(34.07ミリモル)のジクロロメタン溶液(100ml)に、イソプロピルヒドロキシルアミン塩酸塩7.98g(71.52ミリモル)及びN-(3-ジメチルアミノプロピル)-N’-エチルカルボジイミド塩酸塩 (WSC)13.71g(71.52ミリモル、)を加えた。その後、氷冷下でN-メチルモルホリン14.47g(143.05ミリモル、)を加え、室温で20時間攪拌した。反応混合物を水にあけ酢酸エチルで抽出し、飽和塩化ナトリウム水溶液で洗浄し、無水硫酸マグネシウムで乾燥した。溶媒を減圧下で留去し、残渣をシリカゲルカラムクロマトグラフィー(溶出溶媒 酢酸エチル:ヘキサン=1:3)で精製し、2-イソプロポキシイミノ-N-イソプロポキシプロピオン酸アミド5.00g(収率73%)を得た。
1-(2-n-ブトキシイミノ-2-シアノ-1-エトキシイミノエチル)-1H-1,2,4-トリアゾール(本発明化合物番号III-51)の製造
(1)シンセシス(Synthesis)第46頁~第48頁(1999年)に記載されている方法で製造された2-シアノ-2-ヒドロキシイミノ酢酸メチル2.00g(15.6ミリモル)、n-ブチルブロマイド2.35g(17.2ミリモル)、炭酸カリウム2.59g(18.7ミリモル)及びDMF 10mlからなる混合物を室温で8時間攪拌した。反応混合物を水にあけ、酢酸エチルで抽出し、有機層を飽和塩化ナトリウム水溶液で洗浄し、無水硫酸マグネシウムで乾燥した。溶媒を減圧下留去し、2-n-ブトキシイミノ-2-シアノ酢酸メチルを2.05g(収率71%)を得た。
1-(2-n-ブトキシイミノ-2-カルバモイル-1-エトキシイミノエチル)-1H-1,2,4-トリアゾール(本発明化合物番号III-74)の製造
前記実施例17で製造した1-(2-n-ブトキシイミノ-2-シアノ-1-エトキシイミノエチル)-1H-1,2,4-トリアゾール0.98g(3.7ミリモル)のメタノール溶液(5ml)に、室温下、テトラブチルアンモニウムブロマイド60mg(0.19ミリモル)、炭酸カリウム55mg(0.40ミリモル)及び30wt%過酸化水素水1.7g(15ミリモル)を加え、10時間攪拌した。反応混合物にジチオ硫酸ナトリウムを加え10分間攪拌した後、反応混合物を減圧下濃縮した。得られた結晶をクエン酸水溶液、冷水、イソプロピルエーテルの順に洗浄し、標題化合物0.64g(収率61%)を得た。
1-[2-シアノ-1,2-ビス(n-プロポキシイミノ)エチル]-1H-1,2,4-トリアゾール(本発明化合物番号IV-90)の製造
(1)2-シアノ-2-ヒドロキシイミノ酢酸メチル2.50g(19.5ミリモル)、n-プロピルブロマイド2.60g(21.1ミリモル)、炭酸カリウム3.20g(23.2ミリモル)及びDMF10mlからなる混合物を、室温で8時間攪拌した。反応混合物を水にあけ、酢酸エチルで抽出し、有機層を飽和塩化ナトリウム水溶液で洗浄し、無水硫酸マグネシウムで乾燥した。溶媒を減圧下留去し、2-シアノ-2-n-プロポキシイミノ酢酸メチルを2.35g(収率71%)を得た。
1H-NMRデータ(CDCl3/TMS δ(ppm)):0.94‐1.02(6H,m),1.70‐1.84(4H,m),4.29‐4.37(4H,m),8.09(1H,s),8.66(1H,s)
1-[2-カルバモイル-1,2-ビス(n-プロポキシイミノ)エチル]-1H-1,2,4-トリアゾール(本発明化合物番号IV-101)の製造
前記実施例23で製造した1-[2-シアノ-1,2-ビス(n-プロポキシイミノ)エチル]-1H-1,2,4-トリアゾール1.06g(4.0ミリモル)のメタノール溶液(5ml)に、室温で、テトラブチルアンモニウムブロマイド65mg(0.20ミリモル)、炭酸カリウム55mg(0.40ミリモル)及び30wt%過酸化水素水1.8g(16ミリモル)を加え、10時間攪拌した。反応混合物にジチオ硫酸ナトリウムを加え10分間攪拌し、反応混合物を減圧下濃縮した。得られた結晶をクエン酸水溶液、、冷水、イソプロピルエーテルの順に洗浄し、標題化合物0.73g(収率64%)を得た。
1-[2-シアノ-2-(2,2,3,3,3-ペンタフルオロ-n-プロポキシイミノ)-1-(2,2,2-トリフルオロエトキシイミノ)エチル]-1H-1,2,4-トリアゾール(本発明化合物番号IV-185)の製造
(1)前記実施例1に準じて製造した1-[2-ベンジルオキシイミノ-2-シアノ-1-(2,2,2-トリフルオロエトキシイミノ)エチル]-1H-1,2,4-トリアゾール(本発明化合物番号IV-181)1.70g(4.83ミリモル)に5wt%パラジウム炭素0.34g(0.16ミリモル)を加え、窒素気流下エタノール10mlを加えた。この混合液に室温下、常圧で、1.5時間水素添加した。不溶物を濾別し、減圧下濃縮して得られた残渣をカラムクロマトグラフィー(酢酸エチル:ヘキサン=1:1)で精製し、1-[2-シアノ-2-ヒドロキシイミノ-1-(2,2,2-トリフルオロエトキシイミノ)エチル]-1H-1,2,4-トリアゾール1.26g(収率100%)を得た。
化合物番号I-229(CDCl3):1.30-1.41(12H,m),4.56-4.70(2H,m),8.01(1H,s),9.20(1H,s)
化合物番号I-265(CDCl3):0.92(9H,s),1.28-1.33(9H,m),1.60(2H,t),4.25-4.32(4H,m),4.59(1H,sept),8.04(1H,s),8.74(1H,s)
化合物番号I-281(CDCl3):1.36(6H,d),1.71(3H,d),4.60(1H,sept),5.49(1H,q),5.94(1H,s),7.36-7.39(6H,m),7.94(1H,s),9.14(1H,s)
化合物番号I-312(CDCl3):1.20-1.49(12H,m),3.69(2H,s),4.50-4.80(2H,m),7.87及び7.94(1H,s),9.29及び9.49(1H,s)
化合物番号II-232(CDCl3):1.01(6H,d),1.27(9H,s),4.08(3H,s),4.23(1H,sept),7.93(1H,s),9.11(1H,s)
化合物番号II-336(CDCl3):4.27(3H,s),5.01-5.22(1H,m),8.13(1H,s),8.78(1H,s)
化合物番号II-373(CDCl3):4.18(3H,s),4.79(2H,t),7.16(2H,m),7.79(1H,s)
化合物番号III-284(CDCl3):1.43(3H,t),1.75-1.81(2H,m),2.05-2.18(1H,m),4.38-4.63(4H,m),6.02(1H,s),7.26(1H,s),7.98(1H,s),9.17(1H,s)
化合物番号IV-1(CDCl3):0.96(3H,t),1.31(6H,d),1.73-1.81(2H,m),4.29(2H,t),4.54(1H,sept),8.07(1H,s),8.73(1H,s)
化合物番号IV-11(CDCl3):1.33(6H,d),3.40(3H,s),3.70(2H,t),4.40-4.58(3H,m),8.07(1H,s),8.85(1H,s)
化合物番号IV-121(CDCl3):4.19(3H,s),5.35(2H,s),7.39(5H,s),8.07(1H,s),8.65(1H,s)
化合物番号IV-152(CDCl3):0.92(6H,d),1.56-1.72(3H,m),4.03(3H,s),4.27(2H,t),6.09(1H,s),6.46(1H,s),7.07(1H,s),7.30(1H,s),7.89(1H,s)
化合物番号VI-25(CDCl3):1.37(6H,d),1.41(3H,t),4.50(2H,q),4.63(1H,sept)
化合物番号VI-29(CDCl3):0.99(6H,d),1.38(6H,d),2.04-2.18(1H,m),4.21(2H,d),4.63(1H,sept)
化合物番号VI-33(CDCl3):0.97(6H,d),1.38(6H,d),1.57-1.82(3H,m),4.47(2H,t),4.63(1H,sept)
化合物番号VI-38(CDCl3):0.97(9H,d),1.37(6H,d),1.72(2H,t),4.52(2H,t),4.62(1H,sept)
化合物番号VI-47(CDCl3):1.38(6H,d),4.65-4.80(3H,m)
化合物番号VI-53(CDCl3):0.94(6H,d),1.33(6H,d),1.99-2.12(1H,m),2.13(3H,s),4.00(2H,d),4.51(1H,sept)
化合物番号VI-93(CDCl3):0・96(3H,t),1.36(3H,t),1.40-1.49(2H,m),1.70-1.81(2H,m),4.35-4.46(4H,m)
化合物番号VI-96(CDCl3):1.39(3H,t),1.41(9H,s),4.40(2H,q)
化合物番号VI-97(CDCl3):0・92(3H,t),1.36-1.41(7H,m),1.74-1.81(2H,m),4.37-4.46(4H,m)
化合物番号VI-103(CDCl3):0.97(9H,s),1.39(3H,t),1.72(2H,t),4.41(2H,q),4.51(2H,t)
化合物番号VI-196(CDCl3):0.98(3H,t),1.39(6H,d),1.73-1.85(2H,m),4.31(2H,t),4.71(1H,sept)
化合物番号VI-197(CDCl3):0.95-1.00(6H,m),1.40-1.49(2H,m),1.74-1.84(4H,m),4.31(2H,t),4.45(2H,t)
化合物番号VI-198(CDCl3):0.36-0.67(4H,m),0.98(3H,t),1.22-1.31(1H,m),1.74-1.85(2H,m),4.26(2H,d),4.31(1H,t)
化合物番号VI-199(CDCl3):0.95-1.00(6H,m),1.36(3H,d),1.61-1.87(4H,m),4.31(2H,t),4.47-4.55(1H,m)
化合物番号VI-201(CDCl3):0.98(3H,t),1.73-1.85(2H,m),4.32(2H,t),4.91(2H,d),5.34-5.49(2H,m),5.96-6.09(1H,m)
化合物番号VI-204(CDCl3):0.97(6H,d),2.10(1H,sept),4.14(2H,d),4.25(3H,s)
化合物番号VI-205(CDCl3):0.95(6H,d),1.63-1.78(3H,m),4.25(3H,s),4.40(2H,t)
化合物番号VI-210(CDCl3):1.39(6H,d),4.71(1H,sep),4.83(2H,d),5.32-5.42(2H,m) ,5.98-6.08(1H,m)
化合物番号VI-212(CDCl3):1.41(6H,d),4.65-4.84(3H,m)
化合物番号VI-214(CDCl3):0.35-0.67(4H,m),1.19-1.31(2H,m),4.17(2H,d),4.26(2H,d)
化合物番号VI-217(CDCl3):1.40(9H,s),4.70(1H,sept)
化合物番号VI-259(CDCl3):1.40(3H,t),3.54(3H,s),4.43(2H,q),5.4(2H,s)
化合物番号VI-260(CDCl3):1.39(3H,t),2.04-2.08(2H,m),3.35(3H,s),3.50(2H,t),4.41(2H,q),4.54(2H,t)
化合物番号VI-262(CDCl3):1.40(3H,t),1.55-1.66(2H,m),2.04-2.14(1H,m),4.43(2H,q),4.39-4.59(2H,m)
化合物番号VI-265(CDCl3):1.92-1.97(2H,m),2.23(6H,s),2.37-2.40(2H,t),3.88及び4.17(3H,s),4.42,4.50(2H,s)
化合物番号VI-267(CDCl3):1.40(9H,s),1.41(3H,t),4.49(2H,q)
化合物番号VI-268(CDCl3):1.00(3H,t),1.40(9H,s),1.82(2H,m),4.39(2H,t)
化合物番号VI-272(CDCl3):0.89(3H,t),1.20-1.43(16H,m),1.74-1.81(2H,m),4.42(2H,t),4.63(1H,sept)
化合物番号VI-274(CDCl3):0.85(3H,t),0.96(6H,s),1.26-1.43(5H,m),4.20(2H,s),4.41(2H,q)
化合物番号VI-276(CDCl3):1.40(3H,t),4.45(2H,q),4.90(2H,t)
化合物番号VI-281(CDCl3):0.97(3H,t),1.01(9H,s),1.73-1.85(1H,m),4.11(2H,s),4.31(2H,t)
化合物番号VI-282(CDCl3):0.92-1.01(9H,m),1.65-1.85(5H,m),4.31(2H,t),4.48(2H,t)
化合物番号VI-283(CDCl3):1.43(3H,t),4.53(2H,q),5.07-5.27(1H,m)
化合物番号VI-284(CDCl3):1.36(6H,d),1.78(6H,d),4.61(2H,sept),4.65-4.92(2H,m)
5.45-5.49(1H,m)
化合物番号VI-285(CDCl3):1.47(6H,s),4.19(3H,s),4.43(2H,s)
化合物番号VI-287(CDCl3):1.10(6H,s),1.39(3H,t),3.48(2H,s),4.33(3H,s),4.43(2H,q)
化合物番号VI-289(CDCl3):4.20(3H,s),4.90(2H,t)
化合物番号VI-293(CDCl3):4.26(3H,s),5.08-5.26(1H,m)
化合物番号VI-298(CDCl3):0.97(3H,t),1.76-1.85(2H,m),4.35(2H,t),4.86(2H,t)
化合物番号VI-299(CDCl3):1.38(6H,d),4.67(1H,sept),4.85(2H,t)
化合物番号VI-300(CDCl3):1.23(3H,t),1.37(6H,d),3.56(2H,q),3.78(2H,t),4.57(2H,t),4.67(1H,sept)
化合物番号VI-304(CDCl3):4.79(2H,q),5.46(2H,s),7.40(5H,s)
化合物番号VI-307(CDCl3):1.60(3H,d),4.19(3H,s),4.90(1H,sept)
化合物番号VI-314(CDCl3):1.18(6H,d),1.35(6H,d),3.63(1H,sept),3.75-3.77(2H,m),4.54-4.56(2H,m),4.63(1H,sept)
表1~表51に記載の化合物 10部
シクロヘキサノン 30部
ポリオキシエチレンアルキルアリールエーテル 11部
アルキルベンゼンスルホン酸カルシウム 4部
メチルナフタリン 45部
以上を均一に溶解して乳剤とした。
表1~表51に記載の化合物 10部
ナフタレンスルホン酸ホルマリン縮合物ナトリウム塩 0.5部
ポリオキシエチレンアルキルアリールエーテル 0.5部
珪藻土 24部
クレー 65部
以上を均一に混合粉砕して水和剤とした。
表1~表51に記載の化合物 2部
珪藻土 5部
クレー 93部
以上を均一に混合粉砕して粉剤とした。
表1~表51に記載の化合物 5部
ラウリルアルコール硫酸エステルのナトリウム塩 2部
リグニンスルホン酸ナトリウム 5部
カルボキシメチルセルロース 2部
クレー 86部
以上を均一に混合粉砕した。この混合物に水20部相当量を加えて練り合せ、押出式造粒機を用いて14~32メッシュの粒状に加工した後、乾燥して粒剤とした。
製剤例2に準じて調製した水和剤を、有効成分として500ppmの濃度に水で希釈した。この希釈薬液に、ワタアブラムシの孵化幼虫が寄生しているキュウリ苗を浸漬し、風乾した。処理後のキュウリ苗は25℃の恒温室に置き、3日後に生存虫数を数え、数1の計算式により死虫率を求めた。
I-1,I-4,I-5,I-6,I-7,I-8,I-9,I-11,I-13,I-14,I-15,I-18,I-19,I-21,I-22,I-29,I-48,I-49,I-50,I-52,I-54,I-55,I-56,I-57,I-58,I-59,I-60,I-61,I-62,I-64,I-67,I-68,I-69,I-71,I-72,I-75,I-76,I-78,I-80,I-81,I-87,I-98,I-110,I-120,I-121,I-124,I-128,I-129,I-130,I-131,I-134,I-136,I-142,I-165,I-167,I-179,I-190,I-208,I-209,I-212,I-214,I-215,I-217,I-223,I-224,I-228,I-229,I-230,I-235,I-236,I-239,I-240,I-243,I-246,I-247,I-249,I-250,I-257,I-258,I-259,I-260,I-267,I-269,I-270,I-271,I-273,I-274,I-281,I-286,I-288,I-289,I-296,I-298,I-300,I-301,I-302,I-305,I-307,I-309,I-311,I-318,I-319,I-323,I-324,I-331,I-333,I-335,I-339,I-343,I-345,I-347,I-348,I-351,I-355,I-357,I-358,I-359,I-360,I-361,I-363,I-365,I-367,I-369,I-370,I-371,I-372,I-374,I-375,I-376,I-379,I-381,I-383,I-385,I-387,I-393,I-395,I-396,I-397,II-4,II-6,II-10,II-15,II-48,II-49,II-51,II-52,II-53,II-54,II-55,II-56,II-57,II-58,II-59,II-60,II-61,II-62,II-63,II-64,II-65,II-66,II-67,II-68,II-71,II-72,II-73,II-76,II-77,II-78,II-79,II-80,II-81,II-82,II-83,II-86,II-87,II-88,II-89,II-91,II-130,II-133,II-188,II-190,II-194,II-199,II-208,II-214,II-215,II-221,II-222,II-223,II-224,II-225,II-226,II-235,II-236,II-240,II-241,II-244,II-246,II-266,II-267,II-271,II-278,II-280,II-281,II-284,II-285,II-288,II-289,II-301,II-302,II-303,II-304,II-306,II-309,II-311,II-312,II-313,II-314,II-316,II-317,II-318,II-319,II-320,II-321,II-322,II-324,II-325,II-326,II-327,II-328,II-329,II-330,II-331,II-332,II-333,II-334,II-335,II-338,II-340,II-342,II-343,II-344,II-345,II-346,II-349,II-351,II-352,II-353,II-355,II-356,II-357,II-359,II-360,II-361,II-365,II-367,II-369,II-371,II-373,II-374,II-375,II-376,II-377,II-378,II-379,III-4,III-48,III-49,III-50,III-51,III-53,III-54,III-55,III-56,III-57,III-58,III-59,III-60,III-61,III-62,III-64,III-65,III-66,III-67,III-68,III-70,III-71,III-72,III-73,III-76,III-77,III-78,III-79,III-80,III-81,III-82,III-83,III-84,III-85,III-87,III-88,III-90,III-233,III-238,III-239,III-242,III-262,III-269,III-272,III-273,III-277,III-279,III-280,III-281,III-282,III-283,III-284,III-287,III-288,III-289,III-290,III-295,III-296,III-297,III-298,III-300,III-301,III-302,III-303,III-304,III-305,III-306,III-307,III-308,III-309,IV-1,IV-6,IV-22,IV-30,IV-33,IV-36,IV-37,IV-38,IV-39,IV-79,IV-89,IV-90,IV-91,IV-92,IV-95,IV-97,IV-98,IV-99,IV-102,IV-104,IV-107,IV-115,IV-117,IV-119,IV-152,IV-164,IV-170,IV-172,IV-176,IV-177,IV-178,IV-179,IV-180,IV-181,V-10,VI-96,VI-199,VI-217,VI-221,VI-222,VI-223,VI-269,VI-276,VI-291,VI-297
製剤例2に準じて調製した水和剤を、有効成分として500ppmの濃度になるように水で希釈した。この希釈薬剤液を、ワタアブラムシの孵化幼虫が寄生しているキュウリ苗の地際部に5ml灌注処理した。処理後のキュウリ苗は25℃の恒温室に置き、3日後に生存虫数を数え、数1の計算式により死虫率を求めた。
I-4,I-5,I-55,I-233,II-57,II-63,II-64,II-80,II-301,II-316,II-326,II-332,II-334,II-346,II-367,II-371,III-49,III-60,III-61,III-64,III-68,III-87,III-281,III-283,III-287,III-300,III-304,IV-95
製剤例2に準じて調製した水和剤を、有効成分として500ppmの濃度になるように水で希釈した。この希釈薬液に、イネの芽出し籾を浸漬し、容量60mLのプラスティックカップに入れた。このプラスティックカップにトビイロウンカ3齢幼虫を10頭放ち、蓋をして25℃の恒温室に置いた。6日後に生存虫数を数え、数1の計算式により死虫率を求めた。
I-1,I-4,I-5,I-6,I-7,I-8,I-9,I-11,I-13,I-14,I-15,I-16,I-18,I-19,I-21,I-22,I-29,I-47,I-48,I-49,I-50,I-51,I-52,I-53,I-54,I-55,I-56,I-57,I-58,I-59,I-60,I-61,I-62,I-64,I-67,I-68,I-69,I-70,I-71,I-72,I-73,I-74,I-75,I-76,I-77,I-78,I-79,I-80,I-81,I-82,I-83,I-84,I-85,I-87,I-90,I-91,I-92,I-96,I-98,I-110,I-119,I-120,I-121,I-124,I-128,I-129,I-130,I-131,I-133,I-134,I-136,I-142,I-165,I-167,I-179,I-186,I-188,I-190,I-199,I-208,I-209,I-210,I-211,I-212,I-213,I-214,I-215,I-217,I-218,I-219,I-220,I-221,I-223,I-224,I-225,I-226,I-228,I-229,I-230,I-231,I-233,I-234,I-235,I-236,I-237,I-239,I-240,I-241,I-242,I-243,I-244,I-245,I-246,I-247,I-249,I-250,I-251,I-254,I-255,I-256,I-257,I-258,I-259,I-260,I-261,I-262,I-263,I-264,I-265,I-266,I-267,I-268,I-269,I-270,I-271,I-272,I-273,I-274,I-275,I-278,I-279,I-281,I-282,I-285,I-286,I-287,I-288,I-289,I-290,I-296,I-297,I-298,I-299,I-300,I-301,I-302,I-304,I-305,I-306,I-307,I-308,I-309,I-310,I-311,I-312,I-313,I-315,I-318,I-319,I-321,I-322,I-323,I-324,I-327,I-331,I-332,I-333,I-335,I-336,I-339,I-343,I-345,I-346,I-347,I-348,I-351,I-353,I-354,I-355,I-357,I-358,I-359,I-360,I-361,I-365,I-367,I-369,I-370,I-371,I-372,I-373,I-374,I-375,I-376,I-377,I-378,I-379,I-380,I-381,I-382,I-383,I-384,I-385,I-386,I-387,I-389,I-390,I-391,I-392,I-393,I-394,I-395,I-396,I-397,I-398,II-4,II-6,II-10,II-15,II-47,II-48,II-49,II-50,II-51,II-52,II-53,II-54,II-55,II-56,II-57,II-58,II-59,II-60,II-61,II-62,II-63,II-64,II-65,II-66,II-67,II-68,II-70,II-71,II-72,II-73,II-74,II-75,II-76,II-77,II-78,II-79,II-80,II-81,II-82,II-83,II-84,II-85,II-86,II-87,II-88,II-89,II-90,II-91,II-121,II-125,II-130,II-133,II-185,II-188,II-190,II-194,II-199,II-208,II-214,II-215,II-221,II-222,II-223,II-224,II-225,II-226,II-227,II-232,II-235,II-236,II-238,II-240,II-241,II-244,II-245,II-246,II-247,II-266,II-267,II-268,II-269,II-271,II-278,II-279,II-280,II-281,II-282,II-283,II-284,II-285,II-286,II-288,II-289,II-301,II-302,II-303,II-304,II-306,II-311,II-312,II-313,II-314,II-316,II-317,II-318,II-319,II-320,II-321,II-322,II-323,II-324,II-325,II-326,II-327,II-328,II-329,II-330,II-331,II-332,II-333,II-334,II-335,II-336,II-338,II-339,II-340,II-341,II-342,II-343,II-344,II-345,II-346,II-347,II-348,II-349,II-350,II-351,II-352,II-353,II-354,II-355,II-356,II-357,II-358,II-359,II-360,II-361,II-362,II-365,II-366,II-367,II-368,II-369,II-370,II-371,II-372,II-373,II-374,II-375,II-376,II-377,II-378,II-379,II-380,II-381,III-4,III-47,III-48,III-49,III-50,III-51,III-52,III-53,III-54,III-55,III-56,III-57,III-58,III-59,III-60,III-61,III-62,III-64,III-65,III-66,III-67,III-68,III-70,III-71,III-72,III-73,III-74,III-75,III-76,III-77,III-78,III-79,III-80,III-81,III-82,III-83,III-84,III-85,III-87,III-88,III-89,III-90,III-91,III-233,III-234,III-238,III-239,III-242,III-243,III-262,III-263,III-264,III-266,III-267,III-269,III-270,III-272,III-273,III-279,III-280,III-281,III-282,III-283,III-284,III-287,III-288,III-289,III-290,III-295,III-296,III-297,III-298,III-299,III-300,III-301,III-302,III-303,III-304,III-305,III-306,III-307,III-308,III-309,IV-1,IV-4,IV-6,IV-11,IV-14,IV-15,IV-17,IV-18,IV-19,IV-20,IV-21,IV-22,IV-23,IV-25,IV-27,IV-30,IV-32,IV-33,IV-34,IV-35,IV-36,IV-37,IV-38,IV-39,IV-40,IV-42,IV-59,IV-61,IV-62,IV-64,IV-65,IV-74,IV-76,IV-77,IV-78,IV-79,IV-80,IV-86,IV-89,IV-90,IV-91,IV-92,IV-93,IV-95,IV-96,IV-97,IV-98,IV-99,IV-100,IV-101,IV-102,IV-103,IV-104,IV-106,IV-107,IV-108,IV-109,IV-110,IV-111,IV-112,IV-113,IV-114,IV-115,IV-116,IV-117,IV-118,IV-119,IV-120,IV-127,IV-129,IV-130,IV-131,IV-133,IV-134,IV-135,IV-146,IV-147,IV-149,IV-164,IV-165,IV-166,IV-167,IV-168,IV-169,IV-170,IV-171,IV-172,IV-173,IV-176,IV-177,IV-178,IV-179,IV-180,IV-181,IV-182,IV-183,IV-184,IV-185,IV-186,IV-187,V-10,V-181,VI-25,VI-26,VI-27,VI-28,VI-29,VI-30,VI-31,VI-32,VI-33,VI-34,VI-37,VI-38,VI-39,VI-41,VI-44,VI-45,VI-46,VI-53,VI-63,VI-89,VI-93,VI-96,VI-97,VI-99,VI-103,VI-110,VI-153,VI-155,VI-156,VI-157,VI-161,VI-163,VI-166,VI-172,VI-173,VI-194,VI-195,VI-196,VI-197,VI-198,VI-199,VI-200,VI-201,VI-202,VI-203,VI-204,VI-205,VI-206,VI-207,VI-209,VI-210,VI-211,VI-213,VI-214,VI-215,VI-217,VI-218,VI-221,VI-222,VI-223,VI-230,VI-232,VI-233,VI-234,VI-235,VI-239,VI-244,VI-246,VI-247,VI-248,VI-250,VI-255,VI-256,VI-257,VI-258,VI-259,VI-260,VI-261,VI-262,VI-263,VI-264,VI-267,VI-268,VI-274,VI-275,VI-277,VI-278,VI-281,VI-282,VI-283,VI-284,VI-286,VI-287,VI-290,VI-292,VI-294,VI-297,VI-300,VI-302,VI-303,VI-304,VI-305,VI-306,VI-307,VI-308,VI-309,VI-310,VI-314,VII-164
製剤例2に準じて調製した水和剤を、有効成分として1800ppmの濃度になるように水で希釈した。この希釈薬液を、2.5葉期まで育苗したペーパーポット植えのイネの地際部(ペーパーポットのサイズ:縦1.5cm×横1.5cm×高さ3cm)に250μLを潅注処理し、容量700mLのプラスティックカップに入れた。このプラスティックカップにトビイロウンカ3齢幼虫を5頭放ち、蓋をして25℃の恒温室に置いた。6日後に生存虫数を数え、数1の計算式により死虫率を求めた。
I-4,I-5,I-6,I-7,I-8,I-9,I-11,I-13,I-16,I-18,I-19,I-21,I-22,I-48,I-50,I-52,I-53,I-56,I-64,I-71,I-72,I-74,I-75,I-76,I-87,I-90,I-91,I-96,I-98,I-110,I-133,I-142,I-165,I-167,I-179,I-186,I-190,I-199,I-208,I-218,I-223,I-228,I-229,I-230,I-231,I-233,I-236,I-237,I-246,I-273,II-4,II-6,II-52,II-56,II-61,II-75,II-79,II-81,II-84,II-85,II-199,II-224,II-271,III-4,III-49,III-73,III-75,IV-4,IV-6,IV-25,IV-36,IV-40,IV-101
製剤例2に準じて調製した水和剤を、有効成分として500ppmの濃度になるように水で希釈した。この希釈薬液にキャベツ葉を浸漬させ、風乾後に容量60mLのプラスティックカップに入れた。このプラスティックカップにコナガの2齢幼虫を10頭放ち、蓋をして25℃の恒温室に置いた。6日後に生存虫数を数え、数1の計算式により死虫率を求めた。
I-378,II-353,II-355,III-78,IV-121,IV-155,VI-25,VI-28,VI-33,VI-46,VI-63,VI-110,VI-153,VI-172,VI-196,VI-201,VI-210,VI-215,VI-223,VI-232,VI-233,VI-255,VI-256,VI-260,VI-265
製剤例2に準じて調製した水和剤を有効成分として500ppmの濃度になるように水で希釈した。この希釈薬液にキャベツ葉を浸漬させ、風乾後に容量60mLのプラスティックカップに入れた。このプラスティックカップにオオタバコガの孵化幼虫を5頭放ち、蓋をして25℃の恒温室に置いた。6日後に生存虫数を数え、数1の計算式により死虫率を求めた。
I-374,II-353,III-78,VI-28,VI-46,VI-63,VI-212,VI-215,VI-222,VI-223,VI-231
Claims (8)
- 一般式[I]
[式中、
Xは、水素原子、ハロゲン原子、シアノ基、C1~C8アルキル基、C2~C6アルケニル基、C2~C6アルキニル基、C3~C6シクロアルキル基、C3~C6シクロアルキルC1~C6アルキル基、C1~C6ハロアルキル基、C1~C6アルキルチオ基、C1~C6アルキルスルフィニル基、C1~C6アルキルスルホニル基、C1~C6アルキルチオC1~C6アルキル基、C1~C6アルキルスルフィニルC1~C6アルキル基、C1~C6アルキルスルホニルC1~C6アルキル基、C1~C6アルコキシ基、C1~C6アルコキシC1~C6アルキル基、チオカルバモイル基、R4R5NC(=O)基、R6R7N基、C1~C6アルコキシカルボニル基、カルボキシル基、R8O(HN=)C基、R9ON=(R10)C基、R11S(O=)C基、R12R13NSO2NH基、ヒドロキシC1~C6アルキル基、シアノC1~C6アルキル基、C1~C6アルキルカルボニル基、置換基群αから選ばれる置換基で置換されてもよいフェニル基又は同一若しくは相異なってもよい酸素原子、硫黄原子及び窒素原子から選択される1から5個のヘテロ原子を有する炭素数1から9の複素環基(該基は1~5個のハロゲン原子、C1~C6アルキル基、C1~C6ハロアルキル基、C1~C6アルコキシ基、オキソ基又はシアノ基で置換されていてもよい。)を表し、
R1は、C1~C10アルキル基、C2~C6アルケニル基、C2~C6アルキニル基、C3~C6シクロアルキル基、C3~C6シクロアルキルC1~C6アルキル基、C1~C6ハロアルキル基、C2~C6ハロアルケニル基、C2~C6ハロアルキニル基、C1~C6アルキルチオC1~C6アルキル基、C1~C6アルキルスルフィニルC1~C6アルキル基、C1~C6アルキルスルホニルC1~C6アルキル基、C1~C6アルコキシC1~C6アルキル基、C1~C6ハロアルコキシC1~C6アルキル基、C1~C6アルコキシイミノC1~C6アルキル基、トリ(C1~C6アルキル)シリルC1~C6アルキル基、シアノC1~C6アルキル基、gem-ジ(C1~C6アルコキシ)C1~C6アルキル基、ヒドロキシC1~C6アルキル基、アミノC1~C6アルキル基(該基はR14、R15で置換されていてもよい。)、置換基群αから選ばれる置換基で置換されてもよいフェニル基、置換基群αから選ばれる置換基で置換されてもよいフェニルC1~C6アルキル基、置換基群αから選ばれる置換基で置換されてもよいフェニルC2~C6アルケニル基、置換基群αから選ばれる置換基で置換されてもよいフェノキシC1~C6アルキル基、同一若しくは相異なってもよい酸素原子、硫黄原子及び窒素原子から選択される1から5個のヘテロ原子を有する炭素数1から9の複素環基(該基は1~5個のハロゲン原子、C1~C6アルキル基、C1~C6ハロアルキル基、C1~C6アルコキシ基又はシアノ基で置換されていてもよい。)、同一若しくは相異なってもよい酸素原子、硫黄原子及び窒素原子から選択される1から5個のヘテロ原子を有する炭素数1から9の複素環で置換されたC1~C6アルキル基(該基は1~5個のハロゲン原子、C1~C6アルキル基、C1~C6ハロアルキル基、C1~C6アルコキシ基、オキソ基又はシアノ基で置換されていてもよい。)又は同一若しくは相異なってもよい酸素原子、硫黄原子及び窒素原子から選択される1から5個のヘテロ原子を有する炭素数1から9の複素環で置換されたC2~C6アルケニル基(該基は1~5個のハロゲン原子、C1~C6アルキル基、C1~C6ハロアルキル基、C1~C6アルコキシ基又はシアノ基で置換されていてもよい。)を表し、
前記複素環基に窒素原子が含まれる場合は酸化されてN-オキシドになってもよく、
R2は、C1~C6アルキル基、C2~C6アルケニル基、C2~C6アルキニル基、C3~C6シクロアルキル基、C1~C6ハロアルキル基、C2~C6ハロアルケニル基、C2~C6ハロアルキニル基、C1~C6アルキルチオC1~C6アルキル基、C1~C6アルキルスルフィニルC1~C6アルキル基、C1~C6アルキルスルホニルC1~C6アルキル基、C1~C6アルコキシC1~C6アルキル基、C1~C6ハロアルコキシC1~C6アルキル基、シアノC1~C6アルキル基又は置換基群αで置換されてもよいフェニルC1~C6アルキル基を表し、
Qは、式[Q-1]若しくは式[Q-2]
で示される複素環基又はハロゲン原子を表し、
式[Q-1]におけるWは、窒素原子又はメチン基を表し、
式[Q-1]及び式[Q-2]で示される複素環基の窒素原子は酸化されてN-オキシドになってもよく、
式[Q-1]及び式[Q-2]におけるR3は、ハロゲン原子、シアノ基、ニトロ基、ヒドロキシル基、メルカプト基、C1~C6アルキル基、C1~C6ハロアルキル基、C1~C6アルコキシ基、C1~C6アルキルチオ基、C1~C6アルキルスルフィニル基、C1~C6アルキルスルホニル基、ホルミル基又はヒドロキシイミノC1~C4アルキル基を表し、
式[Q-1]及び式[Q-2]におけるnは、Wが窒素原子の場合は0、1又は2を、Wがメチン基の場合は0、1、2又は3を表し、
R4、R5、R6、R7、R12、R13、R14及びR15は、それぞれ、水素原子、C1~C6アルキル基、C1~C6アルコキシ基、C1~C6アルコキシC1~C6アルキル基、C1~C6アルキルカルボニル基、C1~C6アルコキシカルボニル基、C1~C6ハロアルキル基、C3~C6シクロアルキル基、C3~C6シクロアルキルC1~C6アルキル基、C1~C6アルキルスルホニル基又はシアノC1~C6アルキル基又は置換基群αから選ばれる置換基で置換されてもよいフェニル基を表し、
又、R4とR5、R6とR7、R12とR13及びR14とR15は、それぞれ一緒になってC2~C7アルキレン鎖を形成することにより、結合する窒素原子と共に3~8員環を形成してもよく、該アルキレン鎖は酸素原子、硫黄原子又は窒素原子を1個含んでもよく、更に該アルキレン鎖はハロゲン原子、C1~C6アルキル基、オキソ基で置換されてもよく、
R8及びR9は、それぞれ、水素原子、C1~C6アルキル基、C1~C6ハロアルキル基又はC1~C6アルコキシカルボニル基を表し、
R10は、R6R7N基又はQを表し、
R11は、C1~C6アルキル基を表す。]
で表されることを特徴とするアルコキシイミノ誘導体又はその農業上許容される塩。
「置換基群α」
ハロゲン原子、C1~C6アルキル基、C1~C6ハロアルキル基、C1~C6アルコキシ基、C1~C6ハロアルコキシ基、C1~C6アルコキシカルボニル基、ニトロ基及びシアノ基 - Xが、水素原子、ハロゲン原子、シアノ基、C1~C8アルキル基、C3~C6シクロアルキル基、C1~C6ハロアルキル基、C1~C6アルキルチオ基、C1~C6アルキルスルフィニル基、C1~C6アルキルスルホニル基、C1~C6アルコキシ基、チオカルバモイル基、R4R5NC(=O)基、R6R7N基、C1~C6アルコキシカルボニル基、カルボキシル基、R8O(HN=)C基、R9ON=(R10)C基、R11S(O=)C基、R12R13NSO2NH基、ヒドロキシC1~C6アルキル基、シアノC1~C6アルキル基、C1~C6アルキルカルボニル基、置換基群αから選ばれる置換基で置換されてもよいフェニル基又は同一若しくは相異なってよい酸素原子、硫黄原子及び窒素原子から選択される1から5個のヘテロ原子を有する炭素数1から9の複素環基(該基は1~5個のハロゲン原子、C1~C6アルキル基、C1~C6ハロアルキル基、C1~C6アルコキシ基、オキソ基又はシアノ基で置換されていてもよい。)であり、
R1が、C1~C10アルキル基、C2~C6アルケニル基、C2~C6アルキニル基、C3~C6シクロアルキル基、C3~C6シクロアルキルC1~C6アルキル基、C1~C6ハロアルキル基、C2~C6ハロアルケニル基、C1~C6アルキルチオC1~C6アルキル基、C1~C6アルコキシC1~C6アルキル基、C1~C6ハロアルコキシC1~C6アルキル基、トリ(C1~C6アルキル)シリルC1~C6アルキル基、シアノC1~C6アルキル基、gem-ジ(C1~C6アルコキシ)C1~C6アルキル基、ヒドロキシC1~C6アルキル基、アミノC1~C6アルキル基(該基はR14又はR15で置換されていてもよい。)、置換基群αから選ばれる置換基で置換されてもよいフェニル基、置換基群αから選ばれる置換基で置換されてもよいフェニルC1~C6アルキル基、置換基群αから選ばれる置換基で置換されてもよいフェニルC2~C6アルケニル基、置換基群αから選ばれる置換基で置換されてもよいフェノキシC1~C6アルキル基、同一若しくは相異なってもよい酸素原子、硫黄原子及び窒素原子から選択される1から5個のヘテロ原子を有する炭素数1から9の複素環基(該基は1~5個のハロゲン原子、C1~C6アルキル基、C1~C6ハロアルキル基、C1~C6アルコキシ基又はシアノ基で置換されていてもよい。)又は同一若しくは相異なってもよい酸素原子、硫黄原子及び窒素原子から選択される1から5個のヘテロ原子を有する炭素数1から9の複素環で置換されたC1~C6アルキル基(該基は1~5個のハロゲン原子、C1~C6アルキル基、C1~C6ハロアルキル基、C1~C6アルコキシ基、オキソ基又はシアノ基で置換されていてもよい。)であり、
前記複素環基に窒素原子が含まれる場合は酸化されてN-オキシドになってもよく、
R2が、C1~C6アルキル基、C2~C6アルケニル基、C2~C6アルキニル基、C3~C6シクロアルキル基、C1~C6ハロアルキル基、C1~C6アルコキシC1~C6アルキル基、シアノC1~C6アルキル基又は置換基群αで置換されてもよいフェニルC1~C6アルキル基であり、
Qが、式[Q-1]若しくは式[Q-2]
で示される複素環基又はハロゲン原子であり、
式[Q-1]におけるWが、窒素原子又はメチン基であり、
式[Q-1]及び式[Q-2]におけるR3が、メルカプト基又はC1~C6ハロアルキル基であり、
式[Q-1]及び式[Q-2]におけるnが、0又は1であり、
R4、R5、R6、R7、R12、R13、R14及びR15が、それぞれ、水素原子、C1~C6アルキル基、C1~C6アルコキシ基、C1~C6アルキルカルボニル基、C1~C6アルコキシカルボニル基、C1~C6ハロアルキル基、C3~C6シクロアルキルC1~C6アルキル基、シアノC1~C6アルキル基又は置換基群αから選ばれる置換基で置換されてもよいフェニル基であり、
又、R4とR5、R6とR7、R12とR13及びR14とR15は、それぞれ一緒になってC2~C7アルキレン鎖を形成することにより、結合する窒素原子と共に3~8員環を形成してもよく、該アルキレン鎖は酸素原子、硫黄原子又は窒素原子を1個含んでもよく、
R8及びR9が、それぞれ、水素原子、C1~C6アルキル基又はC1~C6アルコキシカルボニル基であり、
R10が、R6R7N基又はQであり、
R11が、C1~C6アルキル基である、
請求項1に記載のアルコキシイミノ誘導体又はその農業上許容される塩。 - Qがハロゲン原子である請求項1又は2に記載のアルコキシイミノ誘導体又はその農業上許容される塩。
- 請求項1~4のいずれか1項に記載されたアルコキシイミノ誘導体又はその農業上許容される塩を有効成分として含有することを特徴とする有害生物防除剤。
- 殺虫剤である請求項5に記載の有害生物防除剤。
- 請求項1~4のいずれか1項に記載されたアルコキシイミノ誘導体又はその農業上許容される塩の有効成分量を使用することを特徴とする有害生物の防除方法。
- アルコキシイミノ誘導体又はその農業上許容される塩を殺虫剤として使用する請求項7に記載の有害生物の防除方法。
Priority Applications (6)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US13/806,317 US8895035B2 (en) | 2010-06-24 | 2011-06-21 | Alkoxyimino derivative and pest control agent |
| KR1020137001585A KR101806187B1 (ko) | 2010-06-24 | 2011-06-21 | 알콕시이미노 유도체 및 유해생물 방제제 |
| EP11797834.6A EP2594553B1 (en) | 2010-06-24 | 2011-06-21 | Alkoxyimino derivative and pest control agent |
| BR112012033095A BR112012033095B1 (pt) | 2010-06-24 | 2011-06-21 | derivado de alcoxiimino, agente e método de controle de peste |
| JP2012521323A JP5923038B2 (ja) | 2010-06-24 | 2011-06-21 | アルコキシイミノ誘導体及び節足動物防除剤 |
| CN201180036751.3A CN103180291B (zh) | 2010-06-24 | 2011-06-21 | 烷氧基亚氨基衍生物和有害生物防除剂 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2010-143577 | 2010-06-24 | ||
| JP2010143577 | 2010-06-24 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2011161945A1 true WO2011161945A1 (ja) | 2011-12-29 |
Family
ID=45371152
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2011/003522 WO2011161945A1 (ja) | 2010-06-24 | 2011-06-21 | アルコキシイミノ誘導体及び有害生物防除剤 |
Country Status (9)
| Country | Link |
|---|---|
| US (1) | US8895035B2 (ja) |
| EP (1) | EP2594553B1 (ja) |
| JP (1) | JP5923038B2 (ja) |
| KR (1) | KR101806187B1 (ja) |
| CN (1) | CN103180291B (ja) |
| BR (1) | BR112012033095B1 (ja) |
| MY (1) | MY167892A (ja) |
| TW (1) | TWI498082B (ja) |
| WO (1) | WO2011161945A1 (ja) |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2013080479A1 (ja) * | 2011-11-30 | 2013-06-06 | クミアイ化学工業株式会社 | グリオキシム誘導体及び有害生物防除剤 |
| WO2014084223A1 (ja) * | 2012-11-29 | 2014-06-05 | 住友化学株式会社 | テトラゾリノン化合物及びその用途 |
| WO2014203855A2 (ja) | 2013-06-21 | 2014-12-24 | イハラケミカル工業株式会社 | 2-アミノ-2-ヒドロキシイミノ-n-アルコキシアセトイミドイルシアニドの製造方法およびその製造中間体 |
| JPWO2015083719A1 (ja) * | 2013-12-02 | 2017-03-16 | 住友化学株式会社 | 植物病害防除用組成物及び植物病害の防除方法 |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2017502022A (ja) | 2013-12-18 | 2017-01-19 | ビーエーエスエフ ソシエタス・ヨーロピアBasf Se | N−置換イミノ複素環式化合物 |
| CN107439613A (zh) * | 2017-08-23 | 2017-12-08 | 太仓市新滨农场专业合作社 | 一种无残留的环保型农药 |
| CN109651191B (zh) * | 2019-01-07 | 2021-11-19 | 华南理工大学 | 一种二氟甲基肟醚衍生物及其合成方法 |
Citations (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS4955833A (ja) * | 1972-07-27 | 1974-05-30 | ||
| JPS52136120A (en) * | 1976-05-10 | 1977-11-14 | Schering Ag | New propanee1*22dioxydioxime and its method of manufacturing and insecticide containing said compound |
| DE3150984A1 (de) | 1981-12-23 | 1983-06-30 | Bayer Ag, 5090 Leverkusen | Oximcarbamate, verfahren zu ihrer herstellung und ihre verwendung als schaedlingsbekaempfungsmittel |
| JPH0640811A (ja) * | 1992-05-22 | 1994-02-15 | Katayama Chem Works Co Ltd | 工業用殺菌剤及び工業用殺菌方法 |
| JPH0741704A (ja) | 1993-07-29 | 1995-02-10 | Katayama Chem Works Co Ltd | 海生付着生物の付着防止剤 |
| JPH11512446A (ja) * | 1995-09-18 | 1999-10-26 | ビーエーエスエフ アクチェンゲゼルシャフト | フェニル酢酸、その製造及びそれを含む組成物 |
| JP2000506902A (ja) * | 1996-05-10 | 2000-06-06 | ビーエーエスエフ アクチェンゲゼルシャフト | フェニルカルバメート、その製造、及びそれを含む薬剤 |
| WO2001036399A1 (de) * | 1999-11-12 | 2001-05-25 | Basf Aktiengesellschaft | Azadioxacycloalkene |
| JP2001513782A (ja) * | 1997-03-05 | 2001-09-04 | ビーエーエスエフ アクチェンゲゼルシャフト | ハロゲン化ヒドロキシム酸、その製造方法及びその使用 |
| JP2003516384A (ja) * | 1999-12-06 | 2003-05-13 | バイエル アクチェンゲゼルシャフト | 殺微生物剤、殺虫剤及び殺ダニ剤効果を有するn−フェニルカルバメート |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5411990A (en) | 1992-05-18 | 1995-05-02 | Yoshitomi Pharmaceutical Industries Ltd. | Industrial microbicide and a method for killing microbes for industrial use |
| DE4415871A1 (de) * | 1994-05-05 | 1995-11-09 | Basf Ag | O-(Oxyimino)ethyl-Cyclohexenonoximether und deren Verwendung als Herbizide |
| CH689228A5 (de) * | 1994-10-07 | 1998-12-31 | Novartis Ag | Oximether, sowie diese enthaltende Pflanzenschutzmittel. |
| DE4441674A1 (de) * | 1994-11-23 | 1996-05-30 | Basf Ag | Iminooxymethylenanilide, Verfahren und Zwischenprodukte zu ihrer Herstellung und sie enthaltende Mittel |
| JPH0955833A (ja) | 1995-08-10 | 1997-02-25 | Ricoh Co Ltd | 画像読取装置 |
| DE19545094A1 (de) * | 1995-12-04 | 1997-06-05 | Basf Ag | Phenylessigsäurederivate, Verfahren und Zwischenprodukte zu ihrer Herstellung und sie enthaltende Mittel |
| DE19548783A1 (de) * | 1995-12-27 | 1997-07-03 | Basf Ag | Cyaniminooximether, Verfahren und Zwischenprodukte zu ihrer Herstellung und ihre Verwendung zur Bekämpfung von Schadpilzen und tierischen Schädlingen |
| ATE214364T1 (de) * | 1995-12-27 | 2002-03-15 | Basf Ag | Iminooxyphenylessigsäurederivate, verfahren und zwischenprodukte zu ihrer herstellung und ihre verwendung |
| JP2000509060A (ja) * | 1996-04-26 | 2000-07-18 | ビーエーエスエフ アクチェンゲゼルシャフト | 殺菌剤混合物 |
| DE19732846A1 (de) * | 1997-07-30 | 1999-02-04 | Basf Ag | Bisiminosubstituierte Phenylverbindungen |
-
2011
- 2011-06-21 BR BR112012033095A patent/BR112012033095B1/pt not_active IP Right Cessation
- 2011-06-21 WO PCT/JP2011/003522 patent/WO2011161945A1/ja active Application Filing
- 2011-06-21 KR KR1020137001585A patent/KR101806187B1/ko active IP Right Grant
- 2011-06-21 JP JP2012521323A patent/JP5923038B2/ja not_active Expired - Fee Related
- 2011-06-21 CN CN201180036751.3A patent/CN103180291B/zh not_active Expired - Fee Related
- 2011-06-21 MY MYPI2012005362A patent/MY167892A/en unknown
- 2011-06-21 US US13/806,317 patent/US8895035B2/en not_active Expired - Fee Related
- 2011-06-21 EP EP11797834.6A patent/EP2594553B1/en not_active Not-in-force
- 2011-06-23 TW TW100121941A patent/TWI498082B/zh not_active IP Right Cessation
Patent Citations (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS4955833A (ja) * | 1972-07-27 | 1974-05-30 | ||
| JPS52136120A (en) * | 1976-05-10 | 1977-11-14 | Schering Ag | New propanee1*22dioxydioxime and its method of manufacturing and insecticide containing said compound |
| DE3150984A1 (de) | 1981-12-23 | 1983-06-30 | Bayer Ag, 5090 Leverkusen | Oximcarbamate, verfahren zu ihrer herstellung und ihre verwendung als schaedlingsbekaempfungsmittel |
| JPS58110569A (ja) * | 1981-12-23 | 1983-07-01 | バイエル・アクチエンゲゼルシヤフト | オキシム−カルバメ−ト類、それらの製造方法及び害虫防除剤としてのそれらの使用 |
| JPH0640811A (ja) * | 1992-05-22 | 1994-02-15 | Katayama Chem Works Co Ltd | 工業用殺菌剤及び工業用殺菌方法 |
| JPH0741704A (ja) | 1993-07-29 | 1995-02-10 | Katayama Chem Works Co Ltd | 海生付着生物の付着防止剤 |
| JPH11512446A (ja) * | 1995-09-18 | 1999-10-26 | ビーエーエスエフ アクチェンゲゼルシャフト | フェニル酢酸、その製造及びそれを含む組成物 |
| JP2000506902A (ja) * | 1996-05-10 | 2000-06-06 | ビーエーエスエフ アクチェンゲゼルシャフト | フェニルカルバメート、その製造、及びそれを含む薬剤 |
| JP2001513782A (ja) * | 1997-03-05 | 2001-09-04 | ビーエーエスエフ アクチェンゲゼルシャフト | ハロゲン化ヒドロキシム酸、その製造方法及びその使用 |
| WO2001036399A1 (de) * | 1999-11-12 | 2001-05-25 | Basf Aktiengesellschaft | Azadioxacycloalkene |
| JP2003516384A (ja) * | 1999-12-06 | 2003-05-13 | バイエル アクチェンゲゼルシャフト | 殺微生物剤、殺虫剤及び殺ダニ剤効果を有するn−フェニルカルバメート |
Non-Patent Citations (5)
| Title |
|---|
| CHEMICAL SOCIETY PERKIN TRANSACTIONS, vol. 1, 1987, pages 2235 - 2239 |
| JOURNAL OF MEDICINAL CHEMISTRY, 1992, pages 4608 - 4612 |
| JOURNAL OF ORGANIC CHEMISTRY, 2001, pages 496 - 500 |
| JOURNAL OF THE CHEMICAL SOCIETY PERKIN TRANSACTIONS, vol. 1, 1987, pages 2235 - 2239 |
| SYNTHESIS, 1999, pages 46 - 48 |
Cited By (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2013080479A1 (ja) * | 2011-11-30 | 2013-06-06 | クミアイ化学工業株式会社 | グリオキシム誘導体及び有害生物防除剤 |
| US9044013B2 (en) | 2011-11-30 | 2015-06-02 | Kumiai Chemical Industry Co., Ltd. | Glyoxime derivative and pest control agent |
| WO2014084223A1 (ja) * | 2012-11-29 | 2014-06-05 | 住友化学株式会社 | テトラゾリノン化合物及びその用途 |
| US9725423B2 (en) | 2012-11-29 | 2017-08-08 | Sumitomo Chemical Company, Limited | Tetrazolinone compound and applications thereof |
| WO2014203855A2 (ja) | 2013-06-21 | 2014-12-24 | イハラケミカル工業株式会社 | 2-アミノ-2-ヒドロキシイミノ-n-アルコキシアセトイミドイルシアニドの製造方法およびその製造中間体 |
| JPWO2015083719A1 (ja) * | 2013-12-02 | 2017-03-16 | 住友化学株式会社 | 植物病害防除用組成物及び植物病害の防除方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP2594553A1 (en) | 2013-05-22 |
| KR101806187B1 (ko) | 2017-12-07 |
| JPWO2011161945A1 (ja) | 2013-08-19 |
| BR112012033095A2 (pt) | 2016-09-27 |
| CN103180291B (zh) | 2015-08-19 |
| EP2594553A4 (en) | 2016-01-20 |
| TW201204247A (en) | 2012-02-01 |
| JP5923038B2 (ja) | 2016-05-24 |
| MY167892A (en) | 2018-09-26 |
| US8895035B2 (en) | 2014-11-25 |
| TWI498082B (zh) | 2015-09-01 |
| EP2594553B1 (en) | 2019-03-13 |
| BR112012033095B1 (pt) | 2018-10-30 |
| US20130102568A1 (en) | 2013-04-25 |
| CN103180291A (zh) | 2013-06-26 |
| KR20130094292A (ko) | 2013-08-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5923038B2 (ja) | アルコキシイミノ誘導体及び節足動物防除剤 | |
| US10021880B2 (en) | Diarylimidazole compound and harmful organism control agent | |
| CN104350039A (zh) | 烷基苯基硫醚衍生物及有害生物防除剂 | |
| JP2015160813A (ja) | 有害生物防除剤組成物及び有害生物防除方法 | |
| TWI558319B (zh) | Glyoxime (GLYOXIME) derivatives and pest control agent | |
| CN111683930B (zh) | 新型异噁唑化合物或其盐 | |
| US20220267272A1 (en) | Pyridinium salt and pest control agent | |
| TWI771418B (zh) | 吡唑-3-羧酸醯胺衍生物及有害生物防治藥劑 | |
| AU2019278527B2 (en) | Pyrazole derivative and harmful organism-controlling agent | |
| US20220338475A1 (en) | Pest control method, and pest control agent composition and pest control agent set | |
| TW202019888A (zh) | 5-(1,2,4-三唑-5-基)苯甲醯胺衍生物及有害生物防除劑 | |
| JP7383850B2 (ja) | 複素環化合物及びその用途 | |
| WO2022003510A1 (en) | Triazolopyridine compounds useful as pesticides | |
| WO2022070023A1 (en) | Novel piperazine compound or the salt thereof for use as pesticides |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 11797834 Country of ref document: EP Kind code of ref document: A1 |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 12012502415 Country of ref document: PH |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2012521323 Country of ref document: JP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 13806317 Country of ref document: US Ref document number: 2011797834 Country of ref document: EP |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 1201006689 Country of ref document: TH |
|
| ENP | Entry into the national phase |
Ref document number: 20137001585 Country of ref document: KR Kind code of ref document: A |
|
| REG | Reference to national code |
Ref country code: BR Ref legal event code: B01A Ref document number: 112012033095 Country of ref document: BR |
|
| ENP | Entry into the national phase |
Ref document number: 112012033095 Country of ref document: BR Kind code of ref document: A2 Effective date: 20121221 |