WO2011024592A1 - 肝細胞の培養方法 - Google Patents
肝細胞の培養方法 Download PDFInfo
- Publication number
- WO2011024592A1 WO2011024592A1 PCT/JP2010/062707 JP2010062707W WO2011024592A1 WO 2011024592 A1 WO2011024592 A1 WO 2011024592A1 JP 2010062707 W JP2010062707 W JP 2010062707W WO 2011024592 A1 WO2011024592 A1 WO 2011024592A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- hepatocytes
- collagen
- permeable membrane
- gas permeable
- extracellular matrix
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M23/00—Constructional details, e.g. recesses, hinges
- C12M23/20—Material Coatings
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M23/00—Constructional details, e.g. recesses, hinges
- C12M23/24—Gas permeable parts
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M25/00—Means for supporting, enclosing or fixing the microorganisms, e.g. immunocoatings
- C12M25/14—Scaffolds; Matrices
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M41/00—Means for regulation, monitoring, measurement or control, e.g. flow regulation
- C12M41/46—Means for regulation, monitoring, measurement or control, e.g. flow regulation of cellular or enzymatic activity or functionality, e.g. cell viability
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/067—Hepatocytes
- C12N5/0671—Three-dimensional culture, tissue culture or organ culture; Encapsulated cells
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/5005—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells
- G01N33/5008—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics
- G01N33/5044—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics involving specific cell types
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2503/00—Use of cells in diagnostics
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2533/00—Supports or coatings for cell culture, characterised by material
- C12N2533/30—Synthetic polymers
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2533/00—Supports or coatings for cell culture, characterised by material
- C12N2533/50—Proteins
- C12N2533/54—Collagen; Gelatin
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Chemical & Material Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biomedical Technology (AREA)
- Wood Science & Technology (AREA)
- Organic Chemistry (AREA)
- Zoology (AREA)
- Biotechnology (AREA)
- Genetics & Genomics (AREA)
- Microbiology (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- General Engineering & Computer Science (AREA)
- Immunology (AREA)
- Cell Biology (AREA)
- Sustainable Development (AREA)
- Hematology (AREA)
- Analytical Chemistry (AREA)
- Urology & Nephrology (AREA)
- Clinical Laboratory Science (AREA)
- Molecular Biology (AREA)
- Toxicology (AREA)
- Tropical Medicine & Parasitology (AREA)
- Gastroenterology & Hepatology (AREA)
- Food Science & Technology (AREA)
- Medicinal Chemistry (AREA)
- Physics & Mathematics (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
Abstract
Description
上記の3次元培養方法では極性を持った肝細胞を初代細胞から作製するためには数週間から数カ月の時間を要する。
それに対して、コラーゲンゲルサンドイッチ法(非特許文献1:LeCluyse et al., Am J Physiol Cell Physiol, 1994, vol.266, pp.1764-1774)を用いるとコラーゲンゲル重層後3~4日程度で毛細胆管の形成と胆汁成分排出活性が検出され始める。しかし、コラーゲンゲルサンドイッチ法を用いても、胆汁成分排出活性が得られるまでには日数を要する。また、生体と同じように出口のある胆管によって連続的に代謝物を解析することはできない。薬物スクリーニングに使用するためには、形成される毛細胆管の数が少なく、活性が低いことも問題となる。
(1)ガス透過膜上に細胞外マトリクスで包埋された肝細胞を配置し、ガス透過性膜側から酸素を供給しつつ肝細胞を培養することを特徴とする、肝細胞培養方法。
(2)ガス透過性膜の表面がコラーゲンコーティングされており、該ガス透過性膜のコラーゲンコート面に細胞外マトリクスで包埋された肝細胞が配置される、(1)に記載の方法。
(3)ガス透過性膜がコラーゲンコート面を内側にして筒状に配置されており、該筒状の内部で細胞外マトリクスで包埋された肝細胞が配置される、(2)に記載の方法。
(4)前記細胞外マトリクスが溝を構成し、該溝に肝細胞が配置された、(1)~(3)のいずれかに記載の方法。
(5)前記ガス透過性膜がポリジメチルシロキサン膜である、(1)~(4)のいずれかの方法。
(6)前記ガス透過性膜がフルオロカーボン膜である、(1)~(4)のいずれかの方法。
(7)コラーゲンコーティングが共有結合によるものである、(1)~(6)のいずれかの方法。
(8)細胞外マトリクスがコラーゲンゲルまたはマトリゲル(商標)である、(1)~(7)のいずれかの方法。
(9)細胞外マトリクスが非生体成分からなる、(1)~(7)のいずれかの方法。
(10)ガス透過膜上に細胞外マトリクスで包埋された肝細胞を配置し、ガス透過性膜側から酸素を供給しつつ肝細胞を培養することを特徴とする、毛細胆管を形成した培養肝細胞の製造方法。
(11)ガス透過性膜の表面がコラーゲンコーティングされており、該ガス透過性膜のコラーゲンコート面に細胞外マトリクスで包埋された肝細胞が配置される、(10)に記載の方法。
(12)ガス透過性膜上に溝を有する細胞外マトリクス層が配置され、該細胞外マトリクス層の溝に肝細胞が配列された、(10)または(11)に記載の方法。
(13)(10)~(12)のいずれかの方法により毛細胆管を形成した培養肝細胞を製造し、得られた培養肝細胞を用いて化合物の代謝を評価する、化合物の代謝検定方法。
(14)(10)~(12)のいずれかの方法により毛細胆管を形成した培養肝細胞を製造し、得られた培養肝細胞を用いて化合物の輸送を評価する、化合物の輸送検定方法。
(15)培養肝細胞を含む本体部と、本体部に化合物を供給する化合物供給部と、本体部から化合物またはその代謝物を回収する回収部とを有する培養肝細胞を用いた化合物検定装置であって、前記本体部は、
ガス透過性膜と、
該ガス透過膜上に配置された細胞外マトリクスと、
該細胞外マトリクスに包埋された肝細胞と、
を有することを特徴とする、装置。
(16)ガス透過性膜の表面がコラーゲンコーティングされており、該ガス透過性膜のコラーゲンコート面に細胞外マトリクスで包埋された肝細胞が配置された、(15)に記載の装置。
(17)前記ガス透過性膜は、コラーゲンコート面を内側にして筒状にした筒状体を形成しており、該筒状体の内部にコラーゲンコート面に接着された肝細胞とそれを包埋する細胞外マトリクスを含む、(16)の装置。
(18)前記本体部は、前記化合物供給部からの供給物が流れるように半透膜で画定された空間を前記筒状体の軸方向に形成する流路であって、該半透膜を介して該供給物を前記細胞外マトリクスに包埋された肝細胞に供給可能な供給物用流路を、更に有する(17)の装置。
(19)前記回収部が、表面がコラーゲンコーティングされたガス透過性膜をコラーゲンコート面を内側にして筒状にした筒状体と、該筒状体の内側のコラーゲンコート面に接着された肝細胞と、該肝細胞を包埋する細胞外マトリクスと、該肝細胞の毛細胆管によって形成される流路を有する、(18)の装置。
(20)前記細胞外マトリクスが溝を構成し、該溝に肝細胞が配置された、(15)~(19)のいずれかに記載の方法。
(21)前記ガス透過性膜がポリジメチルシロキサン膜である、(15)~(20)のいずれかの装置。
(22)前記ガス透過性膜がフルオロカーボン膜である、(15)~(20)のいずれかの装置。
(23)コラーゲンコーティングが共有結合によるものである、(15)~(22)のいずれかの装置。
(24)細胞外マトリクスがコラーゲンゲルまたはマトリゲル(商標)である、(15)~(23)のいずれかの装置。
(25)細胞外マトリクスが非生体成分からなる、(15)~(23)のいずれかの装置。
(26)化合物代謝検定装置である、(15)~(25)のいずれかの装置。
(27)化合物輸送検定装置である、(15)~(25)のいずれかの装置。
また、「包埋」されている状態とは、該肝細胞の周辺が少なくとも1層の細胞外マトリクスで囲まれていることを言う。毛細胆管が効率的に形成される限り、該細胞外マトリクスは連続的でも非連続的でも構わない。
また、フルオロカーボン膜が培養面に配置された培養プレートLumox (In vitro systems and services社製)等、を適宜購入して使用することもできる。
一方、短期的な毛細胆管の形成効率は共有結合でも吸着結合でも同様であることから、短期的な測定に使用する場合には、いずれも使用することができる。試験に必要な毛細胆管を形成できるかぎり、肝細胞の培養条件に合わせて、適宜、最適な結合を選択することができる。
播種する細胞密度は、該細胞が正常に増殖可能であれば良い。通常、細胞密度は約0.1~12.0 x 105cells/cm2の間で播種することが好ましく、細胞が2~3層になるように播種してもよい。培養条件や使用する培養器具などに合わせて、適宜、好ましい細胞密度を設定することができる。
また、具体的な非生体成分からなる半透膜の例として、再生セルロース(セロファン)、アセチルセルロース、ポリアクリロニトリル、テフロン(登録商標)、ポリエステル系ポリマーアロイあるいはポリスルホンの多孔質膜が挙げられる。
また、上記の非生体成分の細胞外マトリクス様の物質に、該細胞外マトリクスを組み合わせて使用することもできる。
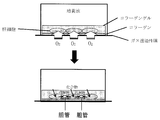
この場合、ガス透過性膜越しの気相は細胞への酸素供給のために酸素濃度1~20%の空気とすることができる。生体内の肝臓に倣って酸素濃度5~13%の間が最適である。この酸素濃度調節は市販のマルチガスインキュベーター(例えば、サンヨー電機社製MCO-5M)の設定によって容易に行うことができる。
また、上記の酸素供給の別の態様としては、ガス透過性膜越しに配置された人工素材や血管細胞からなる人工血管により供給されてもよい。
そして、一般的な細胞培養と同じく、通常37℃、5%CO2の条件で培養を行う。ただし、特殊な細胞や条件で培養を行う場合は、温度やCO2濃度は適宜変更すればよい。培養条件を調節することによって、肝細胞を2次元あるいは3次元に培養することや、毛細胆管の数を調節することができる。
すなわち、本発明の培養方法によれば、肝細胞の膜が分極し、肝細胞同士の間隙に沿って毛細胆管膜が、それ以外の部分には基底膜が形成される。この毛細胆管膜によって形成される毛細胆管は通常幅1~2マイクロメートル、長さは100マイクロメートル以上連結している。この毛細胆管ネットワークの途中には幅が5マイクロメートル程度に広くなったたまり場が形成されることがある。
すなわち、本発明の化合物検定装置は、本体部と、本体部に化合物を供給する化合物供給部と、本体部から化合物またはその代謝物を回収する化合物またはその代謝物の回収部とを有する培養肝細胞を用いた化合物検定装置であって、前記本体部は、表面がコラーゲンコーティングされたガス透過性膜と、該透過性膜のコラーゲンコート面に接着された肝細胞と、該肝細胞を包埋する細胞外マトリクスを有する。
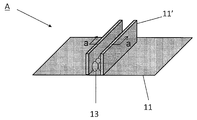
例えば、ガス透過性膜に微細加工を施し、ガス透過性膜の表面に溝や窪みや隔壁を形成してもよい。例えば、微細加工で施される隔壁により細胞の接着範囲と方向を限定して、細胞の配列方向および接着範囲、そしてそれにより形成される毛細胆管の配列方向および範囲を制御することができる。
また、ガス透過性膜上にコラーゲンゲルなどの細胞外マトリクスで溝や窪み(凹部)を形成し、その溝や窪みに細胞を配置することで、細胞の配列方向および接着範囲と方向を限定することができ、それにより形成される毛細胆管の配列方向および範囲を制御することで、毛細胆管内に排出された代謝物を連続的に回収することができる。このように、溝を有する細胞外マトリクスの溝に肝細胞を配置することも、「包埋」に含まれる。更に、前記の溝に配置された肝細胞を、細胞外マトリクスで覆うことで毛細胆管の形成を促進することができる。
溝や窪みの形状は、毛細胆管が形成された肝細胞が作製できれば、何でも良いが、生体内の肝細胞の配置を再現するため、肝細胞が約2列で配列できる幅が好ましい。すなわち、幅20μm 以上70μm以下、好ましくは 30μm 以上50μm以下、さらに好ましくは30μm程度が望ましい。また、溝や窪みの底面からガス透過性膜までの距離は狭い方が好ましいが、ガス透過性膜から十分に酸素を供給できる距離であれば良く、側面の高さは10μm以上1mm以下、好ましくは50μm以上500μm以下、更に好ましくは100μm程度が望ましい。
この隔壁は隣接する肝細胞同士が接着を妨げられる大きさであればよく、具体的には1マイクロメートル以上であることが好ましい。
また、図18で、溝や窪みで毛細胆管が形成された肝細胞を培養する方法の一例を説明する。図2のコラーゲンコート層12を有するガス透過性膜11の上に、図18(A)で示した溝が形成されたコラーゲンゲルなどの細胞外マトリクスを配置する。まず、前記ガス透過性膜11の上に、ゲル化前のコラーゲン溶液(濃度は0.1-30mg/mL、好ましくは0.3-3mg/mL、更に好ましくは約2.0mg/mL)を撒く。次に、該コラーゲン溶液が完全にゲル化する前に、凸部を持ったPDMS製の型を配置して、放置することでゲル化させることで凹部をもったコラーゲンゲルを作製する。前記凸部をもった型の形状としては、形成された溝の幅が、20μm 以上70μm以下、好ましくは 30μm 以上50μm以下、さらに好ましくは30μm程度であり、高さが10μm以上1mm以下、好ましくは50μm以上500μm以下、更に好ましくは100μm程度であり、また、長さは適宜変更して使用できる。また前記凸部をもった型の素材としては、ゲル化したコラーゲンの形を壊さないようなものであれば良く、例えば、重さや加工や取り扱いのし易さからPDMS製のものが良い。
続いて、図18(B)で示すように、上記で作製した凹部を持ったゲルに、培養培地に溶かした肝細胞を播き、何度か培地で洗浄することで、凹部のみに肝細胞を配列させて培養を行う。
続いて、約24時間後培養後、ゲル化前のコラーゲン溶液(濃度は0.1-30mg/mL、好ましくは0.3-3mg/mL、更に好ましくは約2.0mg/mL)もしくはマトリゲル溶液(濃度は、5-5000μg/mL、好ましくは50-500μg/mL、更に好ましくは約150μg/mL)を細胞上に重層し、さらに2-9日培養する。2日から毛細胆管の形成が認められるが、長期間培養する方がより長い毛細胆管を作らせることができる。薬物の評価試験等に最適な状態を適宜選択することができる。
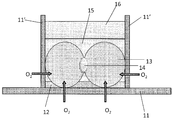
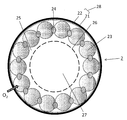
すなわち、ガス透過性膜がコラーゲンコート面を内側にして筒状に配置され、該筒状空間の内部で肝細胞を細胞外マトリクスに包埋して培養する態様も本発明の培養方法に含まれる。
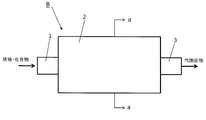
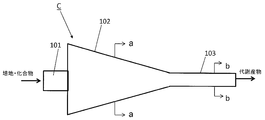
本発明の化合物検定装置Bは、本体部2と、本体部に化合物を供給する化合物供給部1と、本体部から化合物またはその代謝物を回収する回収部3とを有する装置であって、前記本体部2は、表面がコラーゲンコーティングされたガス透過性膜21をコラーゲンコート面22を内側にして筒状にした筒状体28と、筒状体28の内側のコラーゲンコート面22に接着された肝細胞23と、肝細胞23を包埋する細胞外マトリクス25とを有する。
そして、本体部2は、さらに、半透膜26で画定された空間を筒状体28の軸方向に形成してなる流路27を有する。この流路から半透膜26を介して該供給物を細胞外マトリクスに包埋された肝細胞に供給することができる。
ここで、半透膜の素材は化合物や培地成分を透過できるものであれば特に制限されないが、例えば、再生セルロース(セロファン)、アセチルセルロース、コラーゲンコーティングセルロース、ポリアクリロニトリル、テフロン(登録商標)、多孔質の窒化ケイ素、ポリエチレンテレフタレート、ポリエステル系ポリマーアロイあるいはポリスルホンの多孔質膜などが例示される。
なお、これらの素材は非生体成分の細胞マトリクス様物質として使用できるものであるため、これらの素材からなる半透膜を肝細胞を覆うように配置することにより、別途細胞外マトリクスを加えなくても極性を誘導させ、毛細胆管を形成させることができる。
化合物検定装置Bにおいては、肝細胞を培養・維持するための培地も化合物供給部1から供給され、流路27を通過する際に、培地成分が半透膜26を介して肝細胞に供給される。ただし、本発明の化合物検定装置においては、培地を供給する培地供給部は化合物供給部とは別に設けられていてもよい。
なお、流路27の形状は円筒形状に限定されず、その他の形状であってもよく、枝分かれしていてもよい。また、その径も特に制限されない。また、流路は複数設けられていてもよく、培地が通過する流路と化合物が通過する流路が別々になっていてもよい。
さらに、流路27および半透膜26は必須ではなく、ガス透過性膜によって形成される筒状体の内部全てが肝細胞とそれを包埋する細胞外マトリクスであってもよい。この場合は、培地や化合物が筒状体の内部に封入された細胞外マトリクスの中を通過するようにすればよい。
すなわち、本発明の方法で培養された肝細胞集団によって形成された胆管が集合して流路(腔)を形成し、代謝物が流れるようにしたものであってもよい。
このような態様の本発明の肝細胞培養装置について図4Aと図4Aのb-b断面図である4Bを参照して説明する。なお、a-a断面図は図3Bと同様である。
図4Aに示すように、本体部102はその径が徐々に小さくなるように形成され、回収部103に接続されている。そして、回収部103では、ガス透過性膜の内部に、毛細胆管腔を中心に形成するように肝細胞が導入されている。
形成させた毛細胆管からは極細の管や胆管上皮細胞からなる流路が設けられており、毛細胆管に排出された代謝物が滞りなく排泄され、分析のためのリザーバーに回収される。
このような化合物検定装置は後述するような薬物(化合物)輸送検定に好適に用いることができる。
薬物輸送検定としては、薬物がどのくらいの量と速度で肝細胞に取り込まれ、胆汁に排出されるかどうかの検定が例示される。または、ある化合物Aが化合物Bの輸送を阻害・促進するかどうかの検定が例示される。
薬物輸送検定の方法としては、例えば、非特許文献(Liu X et al., Am J Physiol, 1999, vol.277, pp.G12-21)の方法が挙げられる。
ハイスループットなスクリーニングの具体的な方法としては、例えば、微細な流路と高感度な検出器でごく微量の化合物を解析でき、さらにこれを自動あるいは半自動で行うような以下の方法などが挙げられる。
ハイスループットなスクリーニングのためには、ガス透過性膜上の区切られたごく微小な区画、または図2のようなガス透過性流路の極細流路の中で細胞外マトリクスに包埋され毛細胆管を形成した肝細胞が培養されている培養部分それぞれに、試験化合物暴露させる注入口と、それぞれの区画の肝細胞で代謝され毛細胆管に排出される代謝物を回収するための口が設けられたマイクロ流路デバイスを構築することで可能となる。
肝細胞の単離
5週齢のラット(購入先:三共ラボサービス)の肝臓から非特許文献(Seglen PO, 1976, in Methods in cell biology (Prescott DM ed) 13th ed, pp29-83, Academic press, New York)に従って肝臓由来の細胞を分離した。
方法は非特許文献(M. Nishikawa et al. Biotechnology and Bioengineering, 2008, vol.99, pp.1472-1481)に述べられている方法に従った。Silpot 184(東レ・ダウコーニング社製)の主剤と硬化剤を10:2で混合した混合液30gを258mm×174mm×45mmのプラスチック製容器に薄く伸ばし、80℃で2時間加熱し硬化させ、厚さ約1mmのPDMS膜を作製した。主剤と硬化剤の割合は10:2に限らず、10:1~10:2の間で作製されるのが通常である。このPDMS膜を24個の穴が開いたポリカーボネート製の枠と、枠と同じ位置に穴の開いた厚さ1.5mmのSUS製板の間に挟み、ねじで固定することでPDMS膜製24穴培養器を作製した。これに酸素プラズマ処理(5秒)を行った後、ウェルに1%酢酸,2%アミノシラン(信越シリコン社製)を加えて、室温で45分反応させた後、80℃で90分間加熱した。次いで、このように処理されたウェルに0.5mM Sulfosuccinimidyl 2-(m-azido-o-nitrobenzamido)-ethyl-1, 3'-dithiopropionate溶液(Thermo Fisher Scientific社製)を加えて紫外線照射(1分を2回)したのち、0.3mg/mLコラーゲン溶液(新田ゼラチン社製)を添加して18時間室温で放置し、PBSで洗浄して当日のうちに以下の実験に使用した。
コラーゲンゲルサンドイッチ法は非特許文献1(LeCluyse et al., Am J Physiol, 1994, vol.266, pp.1764-1774)に準じた。上記で調製した培養器に1穴あたり肝実質細胞を2x105個播種し、その4時間後、培地を交換した後、播種24時間後に1.7mg/mlコラーゲン溶液(ベクトンディッキンソン社製)を20μL重層して、37℃で1時間ゲル化を行わせたあと、血清不含培地を500μL加え、37℃/5%CO2で培養を行った。また、培養液は2日に1度の割合で交換した。
毛細胆管の面積を経時的に比較したところ、2日目から10日目までPDMS膜上のほうが従来のポリスチレン上での培養より、毛細胆管形成面積が広かった。一方、従来のポリスチレン上での培養では毛細胆管の経時的な漸減が見られたが、PDMS膜上の培養では顕著な毛細胆管の減少は見られなかった(図7)。
以上より、PDMS膜上で培養することにより、効率よく、安定かつ長期的に、毛細胆管を形成した肝細胞を調製できることがわかった。
実施例1で作製したコラーゲンを共有結合させたPDMS膜培養器と、コラーゲンを吸着結合させたPDMS膜培養器との、毛細胆管形成の効率を比較した。
コラーゲンを共有結合させたPDMS膜24穴培養器は実施例1と同様に作製した。コラーゲンを吸着結合させたPDMS膜24穴培養器は、実施例1のアミノシラン処理工程の後、酸素プラズマ処理したPDMS膜製24穴培養器に対して、1.7mg/mLのコラーゲン溶液(ベクトンディッキンソン社製)をウェルに少量添加して覆い、18時間室温で置いた後、PBSで洗浄して作製した。いずれも、当日のうちに以下の実験に用いた。
実施例1と同様の方法でコラーゲンゲルサンドイッチ肝細胞カルチャーを作製した。フルオレセインジアセテートを用いて毛細胆管の形成を観察したところ(図8)、培養4日目(コラーゲンゲル重層3日後)にはコラーゲンを吸着結合させた培養器(a)、共有結合させた培養器(b)どちらとも毛細胆管の形成が見られた。しかしながら、培養7日目では、コラーゲンを吸着結合させた培養器(c)のほうが共有結合させた培養器(d)より細胞の剥離が顕著となり、毛細胆管も消失してしまった。
このことから、コラーゲンを共有結合させた方が、安定かつ長期的に毛細胆管を形成した肝細胞を調製できる。
実施例1で作製したコラーゲンを共有結合させたPDMS膜培養器において、重層する細胞外マトリクス成分による毛細胆管形成の効率を比較した。
(細胞外マトリクス成分添加3日後)にはコラーゲンゲルサンドイッチ(a)、マトリゲルサンドイッチ群(b)とも毛細胆管の形成が観察され、培養7日目まで維持された。無処理群では毛細胆管が全く形成されず、培養3日目から細胞の剥離が顕著になり、5日目にはほとんどの細胞が剥がれてしまった(c)。
以上より、PDMS膜上ではコラーゲンの重層でもマトリゲルの重層でも毛細胆管の形成が可能なことがわかった。
実施例1で作製したPDMS膜培養器で培養された毛細胆管を形成したコラーゲンゲルサンドイッチ肝細胞を使用して、5-(and-6)-carboxy-2',7'-dichlorofluorescein (CDCF)の取り込みによる薬物トランスポーター(MRP2)の活性を非特許文献(Liu X et al., Am J Physiol, 1999, vol.277, pp.12-21)に従って以下のように測定した。また、従来のポリスチレン培養器で培養された肝細胞を比較として使用した。
Ca/Mg(+) HBSSは、HBSS (Invitrogen, 14175-079) を50mL、14g/L CaCl2を500μL、10g/L MgCl2/6H2Oを500μL加え用時調製した。CDCF溶液は、用時に1mM CDCF (in dimethyl sulfoxide: Molecular Probes, C-369)を用いて、Ca/Mg(+) HBSSで5μM CDCF溶液を作成し、37℃ウォーターバスで保温した。Ca/Mg(-) HBSSは、HBSS (Invitrogen, 14175-079) 50mLに100mM EGTAを500μL加えて調製した。0.5% Triton X-100/PBSは、PBSバッファーに0.5%になるようにTriton X-100を加えて調製した。
培養開始4日後(ゲル重層3日後)の肝細胞培養を二つ用意した。続いて、それぞれの培養を別々に温Ca/Mg(+) HBSS または 温Ca/Mg(-) HBSSバッファ0.5mLで2回洗浄した。続いて、それぞれの培養を別々に温Ca/Mg(+) HBSS または 温Ca/Mg(-) HBSSバッファ0.5mL中で37℃に10分間放置したのち、液を除いた。続いて、両培養に5μM CDCFを含んだ温Ca/Mg(+) HBSSバッファ0.5mLを加え、5分間インキュベートののち、CDCF溶液を除去した。続いて、両培養を0.5mLの冷Ca/Mg(+) HBSSバッファで3回洗浄し、液を除いた。続いて、0.5% Triton X-100を含むPBS を500μL加えて、室温で20分間浸透したのち、回収した液を13000 x g, 15分、4℃で遠心して、上澄みを回収し、100μLを取って、励起492nm、蛍光530nmを蛍光マイクロプレートリーダーで計測して、CDCF量を定量した。また、原液25μLをBCAプロテインアッセイキット(Thermo社製)によりタンパク量を計測した。胆汁排出インデックス(Bile Excretion Index: BEI)はタンパク量当たりの蛍光輝度値(Accumulation)からの以下の計算式より求めた。
以上より、ガス透過性膜のほうがポリスチレン製基板を用いるより、肝細胞にMRP排出活性が高い毛細胆管構造を構築させることができることがわかり、高感度(少量の化合物で精度良く)に化合物の評価を行えることがわかった。
実施例1で作製したPDMS膜培養器で培養された毛細胆管を形成した肝細胞を使用して、MRP2タンパク質の局在を、常法に従い細胞抗体染色により調べた。また、従来のポリスチレン培養器で培養された肝細胞を比較として使用した。
PDMS培養器と従来のポリスチレン培養器ともにMRP2タンパクが細胞間に検出されるが、PDMS培養器のほうがより広範囲にMRP2タンパクが発現している(図11)。MRP2は胆汁排出に関わる主要なトランスポーターであることから、PDMS培養器で作製した毛細胆管のほうがより高い胆汁排出活性を持っていると推測できる。
実施例2で作製したコラーゲン吸着結合したPDMS膜製24穴培養器およびコラーゲンコートポリスチレン製24穴プレート(Beckton Dickinson)に、ラットから調製した肝細胞を播種した。播種2時間後に培地を除いてマトリゲルを含んだWilliam's Medium E(含5μg/mLインスリン、5μg/mLトランスフェリン、5μg/mL亜セレン酸,1μMデキサメタゾン)に交換した。
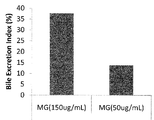
マトリゲル(MG)濃度の検討のため、コラーゲン吸着結合したPDMS膜製24穴培養器1穴辺り2x105個の細胞を播種し、播種2時間後に交換する培地中のマトリゲル濃度を50および150μg/mLにして48時間培養した後に実施例4に記載の方法の通りBEI測定した。その結果、図12に示すように、150μg/mLマトリゲルの方が50μg/mLより高いBEIを示した。
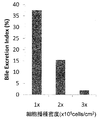
また、細胞播種密度の検討のため、肝細胞播種密度をコラーゲン吸着結合したPDMS膜製24穴培養器1穴辺り2x105個、4x105個、6x105個にして、150μg/mLマトリゲルで48時間培養した後に実施例4に記載の方法の通りBEI測定した。その結果、図13に示すように、2x105個がもっともBEIが高く、4x105個、6x105個の順にBEIは低下した。
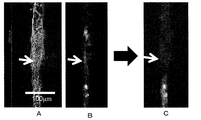
図14Aに示すように、PDMS膜上では播種後24時間および48時間後に、ポリスチレン上で96時間培養した肝細胞と同等のBEIを示した。図14BはPDMS膜製24穴培養器およびコラーゲンコートポリスチレン製24穴プレート上に肝細胞を播種後48時間および96時間後にCDCFが蓄積している部位を蛍光顕微鏡で撮影したものである。この像からもPDMS膜上の肝細胞のほうが従来の培養方法のそれより早期に活性をもった毛細胆管が形成されていることが確認できる。以上の結果から、PDMS膜製24穴培養器を用いてマトリゲルを重層して極性を誘導すると、播種後24時間後には極性が形成され、機能的な毛細胆管が現れる。これは、従来法によるものが同等のBEI値に到達するより72時間も早いことがわかった。
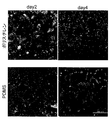
実施例6で作製した毛細胆管を形成した肝細胞を使用して、MRP2および基底膜マーカーCD147の局在を、常法に従い細胞抗体染色により調べた。また、コラーゲンコートポリスチレン製24穴プレートで培養した肝細胞と比較した。
図15に示すように、PDMS膜上で培養すると、培養48時間後にはMRP2タンパク質とCD147タンパク質が細胞間に検出される。一方、従来のポリスチレン上ではCD147の発現は見られるがMRP2タンパク質の局在はほとんど見られない。ポリスチレン上でも極性が形成されている培養120時間後と比較してもPDMS膜上の肝細胞のほうが広範囲にMRP2タンパクが発現している。CD147の局在様式は両者でほとんど同様である。これらの結果から、PDMS膜上で培養された肝細胞はポリスチレン上によるものに比べてより早くMRP2分子の局在が生じるとともに、MRP2の発現はポリスチレン上より増強されることが示された。
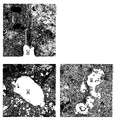
実施例6で作製した培養48時間後の肝細胞の微細構造を透過型電子顕微鏡(JEM1400 JEOL社製)で観察した。
図16Aで示すように、PDMS膜上で極性を誘導した肝細胞において、極性をもった肝細胞に典型的に見られる、毛細胆管腔(BC)、タイト結合(TJ)が見られる。図16Bはタイト結合部分の拡大写真、図16Cは腔壁に微小絨毛(MV)をもつ毛細胆管を示した。
この結果から、本法によって培養される肝細胞には構造的に生体と同等の極性が形成されることが示された。
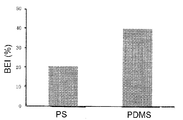
ガス透過性を持つフルオロカーボン膜が培養面に配置された24穴培養プレートLumox (In vitro systems and services社製)にラットから調製した肝細胞を1穴辺り1.0x105個または2.0x105個播種した。播種2時間後に培地を除いて150μg/mLマトリゲルを含んだWilliam's Medium E(含5μg/mLインスリン、5μg/mLトランスフェリン、5μg/mL亜セレン酸,1μM デキサメタゾン)に交換した。肝細胞播種後48時間に実施例4に記載の方法の通りBEI測定し、極性形成の程度を解析した。コラーゲンコートポリスチレン製24穴プレートで培養した細胞を比較対照とした。
図17に示すように、Lumox上ではポリスチレン(PS)製24穴プレートより高いBEIを示した。細胞播種密度1穴辺り1.0x105個と2.0x105個では1.0x105個のほうが高いBEIを与えた。
実施例1に記載の要領で作製したフルオロカーボン製の膜に100μg/mL コラーゲンI-P(新田ゼラチン社製)を含む0.001N HCl溶液を塗布したのち乾燥させ、コラーゲンコート処理を行った。
次に、前記で作製した基板の上に肝細胞を規則正しく並べた。図18Aに示すように、ゲル化前のコラーゲン溶液(濃度2.1mg/mL)に、幅が30μmで高さが100μmで長さが10mmの凸部を持ったPDMS製の型を配置して、37℃で60分間放置することでゲル化させることで凹部をもったコラーゲンゲルを作製した。
次に、図18Bに示したように、作製した凹部を持ったゲルに、培養培地に懸濁したラットの肝細胞を播き、2回培地で洗浄することで、凹部のみに肝細胞を配列させて培養を行った。
24時間後に、コラーゲン溶液(濃度2.1mg/mL)を細胞上に重層し、さらに9日間培養した。このようにして配列させた9日目の肝細胞の写真を図19に示す。連続的に毛細胆管が形成しているように観察された。
また、上記において、フルオロカーボン製酸素透過膜のコラーゲンコート処理の有無は結果に影響しなかった。
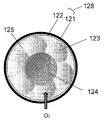
1、101:化合物供給部;2、102:本体部;3、103:回収部;11:ガス透過性膜;11’:隔壁;12:コラーゲンコート層;13:肝細胞;14:毛細胆管;15:コラーゲンマトリクス;16:培地;21:ガス透過性膜;22:コラーゲン;23:肝細胞;24:毛細胆管;25:細胞外マトリクス;26:半透膜;27:流路;28:筒状体。
Claims (27)
- ガス透過膜上に細胞外マトリクスで包埋された肝細胞を配置し、ガス透過性膜側から酸素を供給しつつ肝細胞を培養することを特徴とする、肝細胞培養方法。
- ガス透過性膜の表面がコラーゲンコーティングされており、該ガス透過性膜のコラーゲンコート面に細胞外マトリクスで包埋された肝細胞が配置される、請求項1に記載の肝細胞培養方法。
- ガス透過性膜がコラーゲンコート面を内側にして筒状に配置されており、該筒状の内部で細胞外マトリクスで包埋された肝細胞が配置される、請求項2に記載の方法。
- 前記細胞外マトリクスが溝を構成し、該溝に肝細胞が配置された、請求項1~3のいずれか一項に記載の方法。
- 前記ガス透過性膜がポリジメチルシロキサン膜である、請求項1~4のいずれか一項に記載の方法。
- 前記ガス透過性膜がフルオロカーボン膜である、請求項1~4のいずれか一項に記載の方法。
- コラーゲンコーティングが共有結合によるものである、請求項1~6のいずれか一項に記載の方法。
- 細胞外マトリクスがコラーゲンゲルまたはマトリゲル(商標)である、請求項1~7のいずれか一項に記載の方法。
- 細胞外マトリクスが非生体成分からなる、請求項1~7のいずれか一項に記載の方法。
- ガス透過膜上に細胞外マトリクスで包埋された肝細胞を配置し、ガス透過性膜側から酸素を供給しつつ肝細胞を培養することを特徴とする、毛細胆管を形成した培養肝細胞の製造方法。
- ガス透過性膜の表面がコラーゲンコーティングされており、該ガス透過性膜のコラーゲンコート面に細胞外マトリクスで包埋された肝細胞が配置される、請求項10に記載の方法。
- ガス透過性膜上に溝を有する細胞外マトリクス層が配置され、該細胞外マトリクス層の溝に肝細胞が配列された、請求項10または11に記載の方法。
- 請求項10~12のいずれか一項記載の方法により毛細胆管を形成した培養肝細胞を製造し、得られた培養肝細胞を用いて化合物の代謝を評価する、化合物の代謝検定方法。
- 請求項10~12のいずれか一項に記載の方法により毛細胆管を形成した培養肝細胞を製造し、得られた培養肝細胞を用いて化合物の輸送を評価する、化合物の輸送検定方法。
- 培養肝細胞を含む本体部と、本体部に化合物を供給する化合物供給部と、本体部から化合物またはその代謝物を回収する回収部とを有する培養肝細胞を用いた化合物検定装置であって、前記本体部は、
ガス透過性膜と、
該ガス透過膜上に配置された細胞外マトリクスと、
該細胞外マトリクスに包埋された肝細胞と、
を有することを特徴とする、装置。 - ガス透過性膜の表面がコラーゲンコーティングされており、該ガス透過性膜のコラーゲンコート面に細胞外マトリクスで包埋された肝細胞が配置された、請求項15に記載の装置。
- 前記ガス透過性膜は、コラーゲンコート面を内側にして筒状にした筒状体を形成しており、該筒状体の内部にコラーゲンコート面に接着された肝細胞とそれを包埋する細胞外マトリクスを含む、請求項16に記載の装置。
- 前記本体部は、前記化合物供給部からの供給物が流れるように半透膜で画定された空間を前記筒状体の軸方向に形成する流路であって、該半透膜を介して該供給物を前記細胞外マトリクスに包埋された肝細胞に供給可能な供給物用流路を、更に有する請求項17に記載の装置。
- 前記回収部が、表面がコラーゲンコーティングされたガス透過性膜をコラーゲンコート面を内側にして筒状にした筒状体と、該筒状体の内側のコラーゲンコート面に接着された肝細胞と、該肝細胞を包埋する細胞外マトリクスと、該肝細胞の毛細胆管によって形成される流路を有する、請求項18に記載の装置。
- 前記細胞外マトリクスが溝を構成し、該溝に肝細胞が配置された、請求項15~19のいずれか一項に記載の方法。
- 前記ガス透過性膜がポリジメチルシロキサン膜である、請求項15~20のいずれか一項に記載の装置。
- 前記ガス透過性膜がフルオロカーボン膜である、請求項15~20のいずれか一項に記載の装置。
- コラーゲンコーティングが共有結合によるものである、請求項15~22のいずれか一項に記載の装置。
- 細胞外マトリクスがコラーゲンゲルまたはマトリゲル(商標)である、請求項15~23のいずれか一項に記載の装置。
- 細胞外マトリクスが非生体成分からなる、請求項15~23のいずれか一項に記載の装置。
- 化合物代謝検定装置である、請求項15~25のいずれか一項に記載の装置。
- 化合物輸送検定装置である、請求項15~25のいずれか一項に記載の装置。
Priority Applications (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2011528714A JP5818001B2 (ja) | 2009-08-26 | 2010-07-28 | 肝細胞の培養方法 |
| EP10811643.5A EP2471908B1 (en) | 2009-08-26 | 2010-07-28 | Method for culture of hepatocytes |
| US13/392,226 US8906644B2 (en) | 2009-08-26 | 2010-07-28 | Method for culture of hepatocytes |
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2009195869 | 2009-08-26 | ||
| JP2009-195869 | 2009-08-26 | ||
| JP2010073486 | 2010-03-26 | ||
| JP2010-073486 | 2010-03-26 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2011024592A1 true WO2011024592A1 (ja) | 2011-03-03 |
Family
ID=43627702
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2010/062707 WO2011024592A1 (ja) | 2009-08-26 | 2010-07-28 | 肝細胞の培養方法 |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US8906644B2 (ja) |
| EP (1) | EP2471908B1 (ja) |
| JP (1) | JP5818001B2 (ja) |
| WO (1) | WO2011024592A1 (ja) |
Cited By (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013215152A (ja) * | 2012-04-11 | 2013-10-24 | Vessel Inc | 3次元細胞培養プレートとその製造方法 |
| JP2014187971A (ja) * | 2013-03-28 | 2014-10-06 | Lsi Medience Corp | 肝細胞培養用基板及び肝細胞培養方法 |
| KR101448377B1 (ko) | 2013-03-19 | 2014-10-07 | 경희대학교 산학협력단 | 세포 기능 평가용 양방향 동시측정 시스템 |
| JP2014223061A (ja) * | 2013-04-24 | 2014-12-04 | 株式会社Lsiメディエンス | 肝細胞培養方法 |
| WO2015080106A1 (ja) * | 2013-11-29 | 2015-06-04 | 株式会社日立ハイテクノロジーズ | 成分分析装置、薬効分析装置、及び分析方法 |
| WO2016147975A1 (ja) * | 2015-03-13 | 2016-09-22 | 国立研究開発法人医薬基盤・健康・栄養研究所 | 小腸上皮様細胞 |
| WO2016158417A1 (ja) * | 2015-03-27 | 2016-10-06 | 国立研究開発法人農業生物資源研究所 | 肝代謝物の毛細胆管様構造への蓄積と排泄を促進する肝細胞培養装置、並びに該肝細胞培養装置を用いた胆汁中又は血液中排泄感受性の候補化合物及び該候補化合物の肝代謝物の評価方法 |
| JP2017104117A (ja) * | 2017-01-31 | 2017-06-15 | 株式会社日立ハイテクノロジーズ | 成分分析装置、薬効分析装置、及び分析方法 |
| JP2018099123A (ja) * | 2018-01-22 | 2018-06-28 | 株式会社日立ハイテクノロジーズ | 分析方法 |
| WO2019021528A1 (ja) * | 2017-07-28 | 2019-01-31 | 株式会社日立製作所 | 酸素供給機構 |
| WO2021132586A1 (ja) * | 2019-12-27 | 2021-07-01 | 学校法人高崎健康福祉大学 | 肝細胞培養膜、それを備えた薬物輸送能評価キット、及び薬物輸送能評価方法 |
| WO2022158609A1 (ja) * | 2021-01-25 | 2022-07-28 | ニッタ株式会社 | 細胞培養容器 |
| JP7348997B1 (ja) | 2022-07-27 | 2023-09-21 | 浜松ホトニクス株式会社 | 毛細胆管領域の特定又は評価の方法、装置及びプログラム |
| WO2024080363A1 (ja) * | 2022-10-13 | 2024-04-18 | 国立大学法人東京大学 | デバイス、システム、方法、および薬剤評価方法 |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9512406B2 (en) | 2013-12-20 | 2016-12-06 | The J. David Gladstone Institute, a testamentary trust established under the Will of J. David Gladstone | Generating hepatocytes |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6394812B1 (en) * | 1999-07-22 | 2002-05-28 | Organogenesis Inc. | Vivo induction for enhanced function of isolated hepatocytes |
| WO2005047496A1 (ja) * | 2003-11-14 | 2005-05-26 | Keio University | 細胞培養法、細胞の三次元培養法、三次元組織、人工臓器、及び組織移植方法 |
| US7393687B2 (en) * | 2004-07-16 | 2008-07-01 | William Marsh Rice University | Biomimetic 3-dimensional scaffold with metabolic stream separation for bioartificial liver device |
| JP2006254722A (ja) * | 2005-03-15 | 2006-09-28 | Toray Ind Inc | 細胞足場材料 |
| EP1891201A4 (en) | 2005-05-18 | 2011-11-09 | Cornell Res Foundation Inc | PHARMACOKINETICS-BASED CULTURAL SYSTEM WITH BIOLOGICAL BARRIERS |
| JP4863655B2 (ja) * | 2005-06-17 | 2012-01-25 | 国立大学法人 東京医科歯科大学 | 細胞含有シート |
-
2010
- 2010-07-28 WO PCT/JP2010/062707 patent/WO2011024592A1/ja active Application Filing
- 2010-07-28 EP EP10811643.5A patent/EP2471908B1/en not_active Not-in-force
- 2010-07-28 JP JP2011528714A patent/JP5818001B2/ja not_active Expired - Fee Related
- 2010-07-28 US US13/392,226 patent/US8906644B2/en not_active Expired - Fee Related
Non-Patent Citations (3)
| Title |
|---|
| LECLUYSE, E L. ET AL.: "Formation of extensive canalicular networks by rat hepatocytes cultured in collagen-sandwich configuration", AMERICAN JOURNAL OF PHYSIOLOGY - CELL PHYSIOLOGY, vol. 266, 1994, pages C1764 - C1774, XP008151208 * |
| MASAKI NISHIKAWA ET AL.: "Development of highly functional hepatic tissue through mimicking spatio-temporal environment in the liver (<Featured Theme 2>Engineering and Biotechnology)", MONTHLY JOURNAL OF INSTITUTE OF INDUSTRIAL SCIENCE, vol. 60, no. 2, March 2008 (2008-03-01), pages 52 - 59, XP008151215 * |
| MATSUI, H. ET AL.: "ENHANCED DEVELOPMENT OF A BILE CANALICULI NETWORK IN HEPATOCYTE SANDWICH CULTURE WITH DIRECT OXYGEN SUPPLY THROUGH POLYDIMETHYLSILOXANE MEMBRANES", 7TH WORLD CONGRESS ON ALTERNATIVES AND ANIMAL USE IN THE LIFE SCIENCE(2009) FINAL PROGRAMME,, pages 47, XP008158420 * |
Cited By (23)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013215152A (ja) * | 2012-04-11 | 2013-10-24 | Vessel Inc | 3次元細胞培養プレートとその製造方法 |
| KR101448377B1 (ko) | 2013-03-19 | 2014-10-07 | 경희대학교 산학협력단 | 세포 기능 평가용 양방향 동시측정 시스템 |
| JP2014187971A (ja) * | 2013-03-28 | 2014-10-06 | Lsi Medience Corp | 肝細胞培養用基板及び肝細胞培養方法 |
| JP2014223061A (ja) * | 2013-04-24 | 2014-12-04 | 株式会社Lsiメディエンス | 肝細胞培養方法 |
| US10684276B2 (en) | 2013-11-29 | 2020-06-16 | Hitachi High-Tech Corporation | Componential analyzer, drug efficacy analyzer, and analysis method |
| US9880153B2 (en) | 2013-11-29 | 2018-01-30 | Hitachi High-Technologies Corporation | Componential analyzer, drug efficacy analyzer, and analysis method |
| CN107677779A (zh) * | 2013-11-29 | 2018-02-09 | 株式会社日立高新技术 | 成分分析装置、药效分析装置和分析方法 |
| US11789013B2 (en) | 2013-11-29 | 2023-10-17 | Hitachi High-Tech Corporation | Componential analyzer, drug efficacy analyzer, and analysis method |
| CN107677779B (zh) * | 2013-11-29 | 2020-06-12 | 株式会社日立高新技术 | 成分分析装置、药效分析装置和分析方法 |
| WO2015080106A1 (ja) * | 2013-11-29 | 2015-06-04 | 株式会社日立ハイテクノロジーズ | 成分分析装置、薬効分析装置、及び分析方法 |
| US10889805B2 (en) | 2015-03-13 | 2021-01-12 | National Institutes Of Biomedical Innovation, Health And Nutrition | Intestinal epithelioid cells |
| JPWO2016147975A1 (ja) * | 2015-03-13 | 2018-03-08 | 国立研究開発法人医薬基盤・健康・栄養研究所 | 小腸上皮様細胞 |
| WO2016147975A1 (ja) * | 2015-03-13 | 2016-09-22 | 国立研究開発法人医薬基盤・健康・栄養研究所 | 小腸上皮様細胞 |
| WO2016158417A1 (ja) * | 2015-03-27 | 2016-10-06 | 国立研究開発法人農業生物資源研究所 | 肝代謝物の毛細胆管様構造への蓄積と排泄を促進する肝細胞培養装置、並びに該肝細胞培養装置を用いた胆汁中又は血液中排泄感受性の候補化合物及び該候補化合物の肝代謝物の評価方法 |
| JPWO2016158417A1 (ja) * | 2015-03-27 | 2018-01-18 | 国立研究開発法人農業・食品産業技術総合研究機構 | 肝代謝物の毛細胆管様構造への蓄積と排泄を促進する肝細胞培養装置、並びに該肝細胞培養装置を用いた胆汁中又は血液中排泄感受性の候補化合物及び該候補化合物の肝代謝物の評価方法 |
| JP2017104117A (ja) * | 2017-01-31 | 2017-06-15 | 株式会社日立ハイテクノロジーズ | 成分分析装置、薬効分析装置、及び分析方法 |
| WO2019021528A1 (ja) * | 2017-07-28 | 2019-01-31 | 株式会社日立製作所 | 酸素供給機構 |
| JP2018099123A (ja) * | 2018-01-22 | 2018-06-28 | 株式会社日立ハイテクノロジーズ | 分析方法 |
| WO2021132586A1 (ja) * | 2019-12-27 | 2021-07-01 | 学校法人高崎健康福祉大学 | 肝細胞培養膜、それを備えた薬物輸送能評価キット、及び薬物輸送能評価方法 |
| WO2022158609A1 (ja) * | 2021-01-25 | 2022-07-28 | ニッタ株式会社 | 細胞培養容器 |
| JP7348997B1 (ja) | 2022-07-27 | 2023-09-21 | 浜松ホトニクス株式会社 | 毛細胆管領域の特定又は評価の方法、装置及びプログラム |
| WO2024024147A1 (ja) * | 2022-07-27 | 2024-02-01 | 浜松ホトニクス株式会社 | 毛細胆管領域の特定又は評価の方法、装置及びプログラム |
| WO2024080363A1 (ja) * | 2022-10-13 | 2024-04-18 | 国立大学法人東京大学 | デバイス、システム、方法、および薬剤評価方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP2471908A1 (en) | 2012-07-04 |
| EP2471908B1 (en) | 2016-10-05 |
| US8906644B2 (en) | 2014-12-09 |
| JP5818001B2 (ja) | 2015-11-18 |
| JPWO2011024592A1 (ja) | 2013-01-24 |
| EP2471908A4 (en) | 2013-11-06 |
| US20120183989A1 (en) | 2012-07-19 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5818001B2 (ja) | 肝細胞の培養方法 | |
| US20230159899A1 (en) | Devices and methods for simulating a function of liver tissue | |
| Guo et al. | A biomimetic human gut‐on‐a‐chip for modeling drug metabolism in intestine | |
| JP2019037237A (ja) | 操作した肝臓組織、そのアレイ、およびそれを製造する方法 | |
| JP6704604B2 (ja) | 肝代謝物の毛細胆管様構造への蓄積と排泄を促進する肝細胞培養装置、並びに該肝細胞培養装置を用いた胆汁中又は血液中排泄感受性の候補化合物及び該候補化合物の肝代謝物の評価方法 | |
| De Gregorio et al. | Intestine‐on‐chip device increases ECM remodeling inducing faster epithelial cell differentiation | |
| KR102621919B1 (ko) | iPSC-유래 세포의 장기 등가물로의 분화를 확립하는 신규한 다중 장기 칩 | |
| Lammel et al. | Development of three-dimensional (3D) spheroid cultures of the continuous rainbow trout liver cell line RTL-W1 | |
| Wang et al. | Paper supported long-term 3D liver co-culture model for the assessment of hepatotoxic drugs | |
| Sridhar et al. | Microstamped petri dishes for scanning electrochemical microscopy analysis of arrays of microtissues | |
| Grant et al. | Establishment of physiologically relevant oxygen gradients in microfluidic organ chips | |
| US20200224136A1 (en) | Intestine-chip: differential gene expression model | |
| Lee et al. | In Vitro three-dimensional (3D) cell culture tools for spheroid and organoid models | |
| Jiang et al. | Development of a high-throughput micropatterned agarose scaffold for consistent and reproducible hPSC-derived liver organoids | |
| Mughal et al. | Organs‐on‐Chips: Trends and Challenges in Advanced Systems Integration | |
| Kim et al. | Effect of shear stress on the proximal tubule-on-a-chip for multi-organ microphysiological system | |
| JP2021525075A (ja) | 幹細胞/増殖細胞区画及び分化細胞ゾーンを有する平面腸陰窩のアレイの形成 | |
| JP2013226112A (ja) | 肝細胞の培養方法 | |
| JP2014223061A (ja) | 肝細胞培養方法 | |
| Perin et al. | Generation of a glomerular filtration barrier on a glomerulus-on-a-Chip platform | |
| Chiabotto et al. | Narrative review of in vitro experimental models of hepatic fibrogenesis | |
| US20160168525A1 (en) | Cell Culturing Method, Particulate Culture Carrier, and Particle-Encompassing Cell Aggregate | |
| Kaisar et al. | In vitro BBB models: Working with static platforms and microfluidic systems | |
| Liang et al. | A microfluidic tool for real-time impedance monitoring of in vitro renal tubular epithelial cell barrier | |
| Son et al. | Assembly and disassembly of the micropatterned collagen sheets containing cells for location-based cellular function analysis |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 10811643 Country of ref document: EP Kind code of ref document: A1 |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2011528714 Country of ref document: JP |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 13392226 Country of ref document: US |
|
| REEP | Request for entry into the european phase |
Ref document number: 2010811643 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2010811643 Country of ref document: EP |