WO2007104576A1 - Arzneimittel enthaltend n-acetyl-mannosamin oder derivate hiervon und seine verwendung - Google Patents
Arzneimittel enthaltend n-acetyl-mannosamin oder derivate hiervon und seine verwendung Download PDFInfo
- Publication number
- WO2007104576A1 WO2007104576A1 PCT/EP2007/002348 EP2007002348W WO2007104576A1 WO 2007104576 A1 WO2007104576 A1 WO 2007104576A1 EP 2007002348 W EP2007002348 W EP 2007002348W WO 2007104576 A1 WO2007104576 A1 WO 2007104576A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- derivative
- unsubstituted
- atoms
- radical
- branched
- Prior art date
Links
- 0 CC1O[C@](COC)CC(*)[C@@]1NC(*)=O Chemical compound CC1O[C@](COC)CC(*)[C@@]1NC(*)=O 0.000 description 11
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7008—Compounds having an amino group directly attached to a carbon atom of the saccharide radical, e.g. D-galactosamine, ranimustine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
- A61K31/565—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids not substituted in position 17 beta by a carbon atom, e.g. estrane, estradiol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
Abstract
Die vorliegende Erfindung betrifft ein Arzneimittel enthaltend N-Acetyl-mannosamin oder ein Derivat hiervon zur Erhöhung des Spiegels eines Steroidhormons, insbesondere eines Sexualhormons, besonders von Testosteron, in einem Subjekt; eine pharmazeutische Zusammensetzung enthaltend N-Acetyl-mannosamin oder ein Derivat und eine Östrogen, gestagen öder androgen wirksame Verbindung sowie ein Arzneimittel enthaltend N-Acetyl-mannosamin, ein Derivat oder die pharmazeutische Zusammensetzung zur Vorbeugung vor oder Behandlung eines Sexualhormonmangels. Auch umfasst von der vorliegenden Erfindung sind die Verwendung der genannten Substanzen zur Herstellung eines Arzneimittels für die o.g. Zwecke sowie die diesbezügliche therapeutische Verfahren, die die genannten Substanzen einbeziehen.
Description
Arzneimittel enthaltend N-Acetyl-mannosamin oder Derivate hiervon und seine Verwendung
Die vorliegende Erfindung betrifft ein Arzneimittel enthaltend N-Acetyl-mannosamin oder ein Derivat hiervon zur Erhöhung des Spiegels eines Steroidhormons, insbesondere eines Sexualhormons, besonders von Testosteron, in einem Subjekt; eine pharmazeutische Zusammensetzung enthaltend N-Acetyl-mannosamin oder ein Derivat und eine Östrogen, ge- stagen oder androgen wirksame Verbindung sowie ein Arzneimittel enthaltend N-Acetyl- mannosamin, ein Derivat oder die pharmazeutische Zusammensetzung zur Vorbeugung vor oder Behandlung eines Sexualhormonmangels. Auch umfasst von der vorliegenden Erfindung sind die Verwendung der genannten Substanzen zur Herstellung eines Arzneimittels für die o.g. Zwecke sowie die diesbezügliche therapeutische Verfahren, die die ge- nannten Substanzen einbeziehen.
Die Steroidhormone bilden eine Klasse von Hormonen, die sich chemisch von Cholesterin ableiten. Sie sind alle Derivate des Kohlenwasserstoffs Gonan (Cyclopentanoperhydrophe- nanthren). Es ist eine Reihe von Krankheitsbildern bekannt, die von einem erniedrigten Spiegels eines Steroidhormons herrühren. Beispielsweise leiden Frauen nach der Menopause häufig an Symptomen, die mit einem erniedrigten Östrogenspiegel verbunden sind. Bei Männern in fortgeschrittenem Alter treten z.B. Störungen der Sexualfunktion wie z.B. erektile Dysfunktion als Folge reduzierter Testosteronspiegel auf. Diese Beschwerden werden konventionell durch Hormonersatztherapien behandelt. Diese haben jedoch - wie unten ausführlicher erläutert - zum Teil erhebliche Nebenwirkungen. Somit besteht ein Bedarf für alternative Ansätze zur Behandlung von und Vorbeugung vor Steroidhormon- mangel und den damit verbundenen Symptomen.
Überraschenderweise wurde nun gefunden, dass durch Verwendung von N-Acetyl- mannosamin oder eines Derivates hiervon der Spiegel eines Steroidhormons, insbesondere eines Sexualhormons wie Testosteron, in einem Subjekt erhöht werden kann.
Daher ist ein erster Gegenstand der vorliegenden Erfindung ein Arzneimittel enthaltend N- Acetyl-mannosamin oder eines Derivates hiervon zur Erhöhung des Spiegels eines Steroidhormons, insbesondere eines Sexualhormons wie Testosteron, in einem Subjekt bzw. die Verwendung von N-Acetyl-mannosamin oder eines Derivates hiervon zur Herstellung eines Arzneimittels zur Erhöhung des Spiegels eines Steroidhormons, insbesondere eines Sexualhormons wie Testosteron, in einem Subjekt.
N-Acetyl-mannosamin ist ein natürlich vorkommender Vorläufer von Neuraminsäuren, die essentielle Monosaccharide komplexer N- und O-Glykane von Glykoproteinen sowie Gangliosiden sind. Die Neuraminsäuren (= Sialinsäuren) befinden sich in terminaler Position und vermitteln aus dieser zelluläre Erkennungsvorgänge, sei es zu Nachbarzellen oder löslichen Mediatoren. Nach seiner Aufnahme durch die Zellen wird N-Acetyl-mannosamin oder ein Derivat hiervon zu der entsprechenden Neuraminsäure metabolisiert und in GIy- kokonjugate der Zellen eingebaut (Kayser et al., 1992, J. Biol. Chem. 267:16934-16938). Die Enzyme der Neuraminsäure-Biosynthese sind offenbar nicht streng spezifisch gegenüber der N-Acyl-Seitenkette, so dass auch Derivate von N-Acetyl-mannosamin enzyma- tisch umgesetzt werden. Als biologisch sehr wirkungsvoll erwies sich in den meisten Untersuchungen N-Propionyl-mannosamin (ManNProp).
Es konnte gezeigt werden, dass der natürliche Vorläufer N-Acetyl-mannosamin und noch stärker synthetische Vorläufer (z.B. N-Propionyl-mannosamin; ManNProp) in in vivo-Y ersuchen die Steroidhormonspiegel in Mäusen verändern. Auf dem gleichen Stoffwechselweg wie N-Acetyl-mannosamin (ManNAc) wird auch ManNProp zur N-Propionyl-Neura- minsäure metabolisiert und in Membranglykoproteine verschiedener Organe eingebaut.
Der pathochemische Mechanismus, der hinter dieser überraschenden Erhöhung der Ste- roidhormonkonzentration im Serum der Mäuse nach Behandlung mit ManNProp liegt, ist bisher nicht bekannt. Es wird jedoch angenommen, dass die Erhöhung mit einer Veränderung der Glykoproteinhormone, die die Bildung der Steroidhormone steuern, einhergeht. Dies sind insbesondere LH (zur Stimulierung der Androgen- und Progesteronsynthese; LH = lutheinisierendes Hormon) sowie CG (zur Regulation der Östrogenbiosynthese; CG = Chorion-Gonadotropin). Nach den bisherigen Erkenntnissen ist es wahrscheinlich, dass die Gabe von N-Acetyl-mannosamin oder einem Derivat hiervon zu einer veränderten GIy-
kanstruktur dieser Glykoproteine führt. Die Änderung der Glykanstrukrur könnte die genannten Hormone aktiver oder langlebiger machen. Es ist bekannt, dass terminale Galaktose in Glykoproteinen ihre Aufnahme durch die Leber fördert. Da z.B. N-Propionyl- Neuraminsäure eine geringere Affinität zu Sialidase besitzt, werden weniger Galaktose- reste freigesetzt, die vom Galaktose-spezifischen Ashwell-Rezeptor von Hepatozyten erkannt werden können (die Neuraminsäure verdeckt die Galaktose; ihre Entfernung macht solche desialylierten Glykoproteine dem Ashwell-Rezeptor zugänglich). Durch die längere Verweilzeit der „neuen" (modifizierten) Neuraminsäure, z.B. N-Propionyl-Neuraminsäure, würde die Galaktose länger maskiert und dem Ashwell-Rezepotr weniger zugänglich sein. Dadurch würden die modifizierten Glykoproteinhormone langlebiger.
Anhand ihrer physiologischen Wirkungen und ihrer Bildungsorte werden die Steroidhormone in vier Gruppen eingeteilt, nämlich die Corticosteroide, die Östrogene, die Gestagene und die Androgene.
Die Corticosteroide sind eine Gruppe von circa 50 in der Nebennierenrinde gebildeten Steroidhormonen sowie chemisch vergleichbare synthetische Stoffe. Zu den natürlichen Cor- ticoiden gehören das Cortison, das Cortisol, das Aldosteron, das Corticosteron und das Desoxycorticosteron. Künstliche Corticoide sind beispielsweise Fludrocortison, Prednison und Prednisolon, Methylprednisolon, Triamcinolon, Dexamethason, Betamethason und Paramethason.
Die Östrogene sind die wichtigsten weiblichen Geschlechtshormone aus der Klasse der Steroide, auch Follikelhormone genannt. Sie werden hauptsächlich in den Eierstöcken in Follikel und Gelbkörper, zu einem geringern Teil auch in den Nebennierenrinden produziert. Während der Schwangerschaft werden die Östrogene auch in der Plazenta gebildet. Bei Männern produzieren die Hoden kleinere Mengen an Östrogenen. Die Konzentration der Östrogene ändert sich erheblich im Verlauf des weiblichen Zyklus. Gesteuert wird die Produktion von der Hypophyse über die Gonadotropine (FSH und LH). Nach der Meno- pause fällt die Östrogensynthese im weiblichen Körper stark ab. Natürliche Östrogene sind das Östrogen, Östradiol-17-Beta und Östriol. Synthetische Östrogene sind z.B. Ethinyl, Östradiol und Stilben.
Neben den Östrogenen sind die Gestagene oder Gelbkörperhormone die zweite wichtige Klasse der weiblichen Sexualhormone. Zu den wichtigsten natürlich vorkommenden Vertretern zählen das Progesteron, das Pregnandiol und das Pregnelon.
Mit dem Sammelbegriff der Androgene werden Steroidhormone bezeichnet, die eine virili- sierende Wirkung besitzen. Sie werden beim Mann in den Leydig-Zellen des Hodens und der Nebennierenrinde gebildet. Bei der Frau findet die Bildung in den Ovarien und Nebennierenrinden statt. Zu den natürlich vorkommenden Vertretern der Androgene zählen u.a. das Testosteron, das Androsteron, das Androstendion und das Dehydroepiandrosteron (DHEA). Testosteron beeinflusst anabole Stoffwechselvorgänge wie Knochenbildung, Proteinbiosynthese (Muskelaufbau) und die Blutbildung. Im Zuge des Alterungsprozesses kommt es zu einer verminderten Sekretion hypophysärer, adrenaler und gonadaler Hormone. Zusätzlich kann die alterungsabhängige Zunahme des Sexualhormon-bindenden Globulins (SHBG) die Entwicklung des Testosteronmangels beschleunigen, da SHBG zum Ab- fall des ungebundenen, d.h. des biologisch aktiven, Testosteron führt. Die Regulation der Sekretion des Follikel-stimulierenden Hormons (FSH) und des Gonadotropins LH (luteinisierendes Hormon) oder Gonadoliberin aus der Hypophyse wird durch das LH-Releasing Hormon des Hypothalamus stimuliert. Die LH-Sekretion steht unter der negativen Rückkopplung durch Androgene. In den Sertoli-Zellen wird Inhibin gebildet, das die FSH- Sekretion der Hypophyse hemmt. LH stimulierte die Androgenbiosynthese in den Leydig- Zellen. Der Abbau der Androgene erfolgt in der Leber und in peripheren Geweben.
Die Sexualhormone haben neben ihrem Anteil an der Gonadenentwicklung, der Ausprägung der Geschlechtsmerkmale und der Steuerung der Sexualfunktion auch sexual- unspezifische Wirkungen. Hierzu zählen beispielsweise anabole Stoffwechselwirkungen, Wirkungen auf Knochenreifung und -längenwachstum, auf die Beschaffenheit von Muskulatur und Haut sowie die Funktion der Talgdrüsen. Auch die Corticosteroide beeinflussen den Kohlenhydrat-, Fett- und Eiweißstoffwechsel sowie den Mineral Stoffstoffwechsel. Darüber hinaus führen sie zu einer Unterdrückung immunologischer und entzündlicher Vorgänge.
Für Corticosteroide und insbesondere für die Sexualhormone sind eine Reihe von Störungen bekannt, die mit einer veränderten, insbesondere erniedrigten, Konzentration der Steroidhormone im Körper verbunden sind. Einige der häufigsten Krankheiten oder Störungen, bei denen ein Anstieg der Steroidhormonkonzentration angestrebt wird, sind im FoI- genden kurz beispielhaft erläutert:
Bei Morbus Addison liegt ein Mangel an körpereigenem Cortisol vor. Darüber hinaus wird eine Erhöhung des Spiegels an Cortisol bei bestimmten Krankheiten oder Störungen durch Cortisolverabreichung angestrebt. Hierzu zählen z.B. Allergien (Überreaktion des Immun- Systems), z. B der Atemwege (Asthma bronchiale, Heuschnupfen) der Haut (z. B. Nesselsucht, Neurodermitis); Autoimmunkrankheiten (Fehlreaktion des Immunsystems), z. B. der Gelenke / Muskeln (z. B. chronische Polyarthritis, Polymyalgie), des Darms (z. B. Morbus Crohn, Colitis ulcerosa), der Blutgefäße bzw. von Blutbestandteilen (Vaskulitis, Thrombo- penie); Organverpflanzungen gegen Abstoßungsreaktionen sowie Tumor- und Krebsthera- pie. Allerdings ist insbesondere eine Dauertherapie mit Cortison mit erheblichen Nebenwirkungen wie z.B. Schlafstörungen, Nervosität, Schwindel, Kopfschmerzen, Stimmungsschwankungen, verstärkte Körperbehaarung, verstärktes Hungergefühl und Gewichtszunahme (Cushing-Syndrom, Vollmondgesicht), Kalziummangel, Osteoporose, steigender Blutzuckerspiegel, latenter Diabetes mellitus, Ausbleiben des Eisprungs bei Frauen, des- halb vorübergehende Unfruchtbarkeit, Muskelschwäche, Magenschleimhautentzündung, Magengeschwür, Wachstumsstörungen bei Kindern, Blutdruckanstieg, Ödeme (Wasseransammlungen im Gewebe) und/oder erhöhte Infektionsgefahr durch Schwächung des Immunsystems verbunden.
Wie bereits oben erläutert, ist die Konzentration an Östrogen bei Frauen nach der Menopause stark erniedrigt. Wie Stichproben gezeigt haben, liegt der Anteil der post- menopausalen Frauen, die zumindest vorübergehend eine Hormonsubstitution erhalten, in Deutschland bei etwa 40%. Über einen längeren Zeitraum nimmt dieser Prozentsatz der Frauen ab. Der Anteil der Noch- An wenderinnen sinkt bis zum 60. Lebensjahr auf 10-20%. Die Hormonersatztherapie wird in erster Linie zur Behandlung post-menopausaler Beschwerden und zur Osteoporose-Prophylaxe eingesetzt. Darüber hinaus ist bekannt, dass durch den Östrogenmangel nach der Menopause kardiovaskuläre Risikofaktoren wie das
LDL-Cholesterin oder der Blutdruck ansteigen. Daher ist auch im Hinblick auf diese Risikofaktoren eine Hormonersatztherapie oder eine anderweitige Steigerung der Östrogenspiegel erwägenswert. Zu den klimakterischen Beschwerden zählen u.a. Hitze Wallungen, Schweißausbrüche, Schlaflosigkeit, Nervosität und Konzentrationsschwierigkeiten. Bei jüngeren Frauen, d.h. Frauen vor der Menopause, kann ein Östrogenmangel darüber hinaus eine reduzierte Fertilität oder Sterilität verursachen. Von den auf dem Markt befindlichen Hormonersatztherapien zur Behandlung erniedrigter Östrogenwerte zeigen unterschiedliche Untersuchungen ein erhöhtes Risiko für Brustkrebs und Herz-Kreislauf-Erkrankungen. Darüber hinaus zeigen jüngste Ergebnisse der „Woman's Health Initiative" (WHI) Studie und der „Million- Women"- Studie auch ein erhöhtes Risiko eine Thrombose zu erleiden. Man geht zurzeit davon aus, dass jede 100. Frau, die länger als 5 Jahre Hormone einnimmt, eine dieser schwerwiegenden Nebenwirkungen erleiden kann.
Beim Mann ist die wichtigste Sexualhormonstörung eine Testosteronstörung. Testosteron spielt für viele körperliche und physische Vorgänge eine große Rolle. Mit zunehmendem Alter nimmt der Anteil an Testosteron im Blut kontinuierlich ab. Dieser verringerte Testos- teronspiegel im Blut kann zu einer Reihe von Beschwerden führen, wie z.B. der Verschlechterung des allgemeinen Wohlbefindens, Gelenk- und Muskelbeschwerden, starkes Schwitzen, Schlafstörungen, Müdigkeit, Reizbarkeit, Nervosität, Ängstlichkeit, körperliche Erschöpfung und nachlassende Tatkraft, Abnahme der Muskelkraft, depressive Stimmung, verminderter Bartwuchs, Nachlassen der Potenz sowie Abnahme der Libido. Zusätzlich zu einem altersbedingten Sinken können die Testosteronwerte auch auf Grund genetischer Unterschiede sowie der Lebensweise des betroffenen Mannes außerhalb der Normwerte liegen. So beeinflussen Übergewicht, Stress, Alkohol, Drogen, bestimmte Erkrankungen oder Medikamente den Hormonspiegel. Beispiele dieser Erkrankungen sind chronische Erkrankungen, Infektionserkrankungen, Leber- und Nierenerkrankungen, Arteriosklerose und vor allen Dingen Diabetes mellitus. Man schätzt, dass derzeit bei circa 5% aller über 60-jährigen Männern eine Behandlung mit Testosteron tatsächlich zum Tragen kommt. Allerdings führt die Hormonersatztherapie nur in rund 3% zu einer messbaren Verbesse- rung der Potenz. Darüber hinaus können Testosteronersatztherapien die folgenden Nebenwirkungen besitzen: Aktivierung eines Prostatakrebses, Leberschäden, Thrombosegefahr und Herzinfarktrisiko. Dabei ist die gefährlichste Nebenwirkung die Möglichkeit, einen
klinisch stummen, so genannten „schlafenden" Prostatakrebs zum Leben zu erwecken. In der Regel hat ein aggressiver Prostatakrebs eine sehr schlechte Prognose.
Gemäß der vorliegenden Erfindung kann N-Acetyl-mannosamin oder ein Derivat hiervon alternativ zu oder in Kombination mit den bekannten Therapien zur Erhöhung des Spiegels eines Steroidhormons in einem Subjekt verwendet werden. Das Derivat von N-Acetyl- mannosamin kann ein jedes Molekül sein, das chemisch von N-Acetyl-mannosamin abgeleitet ist und geeignet ist, die den Spiegel eines Steroidhormons in einem Subjekt, insbesondere einem Säuger wie der Maus oder dem Menschen, zu erhöhen. Um die Steroidhor- mon erhöhende Eigenschaft eines Derivats zu untersuchen, kann beispielsweise ein Test durchgeführt werden, wie der, der in den Beispielen für Testosteron beschrieben ist. Dieser Test kann leicht an andere Steroidhormone angepasst werden.
Ein Derivat gemäß der vorliegenden Erfindung liegt vor, wenn der Spiegel eines Steroid- hormons in dem Testsubjekt nach Verabreichung des untersuchten Derivats im Vergleich zu dem Spiegel von Verabreichung oder im Vergleich zu einem Kontrollsubjekt, dem kein Derivat verabreicht wurde, statistisch signifikant erhöht ist. Statistische Tests, um dies zu beurteilen, sind dem Fachmann bekannt und schließen z.B. den Student' s t-Test oder den Chi2-Test ein.
In einer bevorzugten Ausführungsform wird der Spiegel des Steroidhormons in Anwesenheit des Derivats im Vergleich zur Kontrolle um mindestens etwa 10 %, weiter bevorzugt um mindestens etwa 50 %, noch weiter bevorzugt um mindestens etwa 100 %, sogar noch weiter bevorzugt um mindestens etwa 500 % und am meisten bevorzugt um mindestens etwa 1000 % erhöht.
In einer bevorzugten Ausführungsform der Erfindung ist das Derivat von N-Acetyl- mannosamin ein N-Acylhexopyranosamin, d.h. eine Hexose in Pyranoseform mit einer N- Acyl-Gruppe am C2-AtOm der Pyranose, oder ein Analog hiervon. In einer noch weiter bevorzugten Ausführungsform ist das N-Acetyl-mannosamin oder Derivat hiervon ein N- Acylmannosamin, ein N-Acylmannosamin-Analog, ein N-Acylglucosamin, ein N- Acylglucosamim-Analog, N-Acylgalactosamin oder ein N-Acylgalactosamin-Analog ist,
wobei diese Moleküle analog zum N-Acylhexopyranosamin aufgebaut sind. Sogar noch weiter bevorzugt sind die Substanzen, wenn die zugrunde liegende Hexose in D- Konformation, wie z. B. D-Mannose, vorliegt.
Die Acylgruppe des N-Acetyl-mannosamins oder des Derivats kann jede beliebige A- cylgruppe sein. Bevorzugt handelt es sich um einen geradkettigen oder verzweigten, gesättigten oder ungesättigten, unsubstituierten oder substituierten Acylrest mit 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 oder 12 C- Atomen, weiter bevorzugt mit 3, 4, 5, 6 oder 7 C- Atomen und noch weiter bevorzugt mit 3, 4 oder 5 C- Atomen.
In einer noch weiter bevorzugten Ausfuhrungsform ist die Acylgruppe, die wie oben definiert sein kann, substituiert. Beispiele von Substituenten sind: -OH, -F, -Cl, -Br, -I, -NH2, N3, CO-CH3, COOH oder =0. Substituten können aber auch die Substituenten sein, die weiter unten im Zusammenhang mit einem N-Acetyl-mannosamin oder Derivat hiervon der Formel (I) genannt sind. Alternativ oder zusätzlich können auch Mercaptan-, Phenyl-, Phenol- oder Benzylgruppen vorhanden sein.
Besonders bevorzugt ist die Substitution mit mindestens einer Oxo-Gruppe (=0), wobei der Sauerstoff der Oxo-Gruppe eine Doppelbindung zu einem C-Atom der Acylkette auf- weist. Beispiele von Acylketten mit einer Oxo-Gruppe sind: -CH2-CH2-C=O-CH3, -CH2-CH2-CH2-C=O-CH35 -CH2-CH2-CH2-CH2-C=O-CH35 -CH2-CH2-CH2-CH2-CH2-C=O-CH3.
In einer noch weiter bevorzugten Ausführungsform der Erfindung ist das wie oben definierte Analog dadurch gekennzeichnet, dass in dem Analog mindestens 1 , 2, 3 oder 4 OH- Gruppen, beispielsweise eine oder mehrere OH-Gruppen der Hexose, acyliert sind. Bevorzugt handelt es sich bei der Acylierung um eine Acetylierung, eine Propionylierung, eine Butanoylierung oder eine Pentanoylierung. Alternativ kann es sich auch um eine PEGylie- rung (PEG: Polyethylenglycol) handeln. Noch weiter bevorzugt ist ein Analog, in dem alle OH-Gruppen acyliert, insbesondere acetyliert, propionyliert oder butanoyliert, sind. Sogar noch weiter bevorzugt ist ein peracetyliertes N-Acylmannosamin, N-Acylglucosamin oder N-Acylgalactosamin, insbesondere ein peracetyliertes N-Acyl-D-mannosamin, N-Acyl-D- glucosamin oder N-Acyl-D-galactosamin.
In einer noch weiteren Ausfuhrungsform der Erfindung handelt es sich bei dem wie oben definierten Analog um ein Desoxy- oder ein Didesoxy-Derivat der zugrunde liegenden Hexose. Beispiele solcher Derivate sind: 2-Desoxyglucose, 4,6-Didesoxyglucose, Fucose,
2-Desoxygalactose, Rhamnose und 3-Desoxymannose.
In einer besonders bevorzugten Ausführungsform ist das N-Acetyl-mannosamin oder Derivat hiervon ein N-Propanoylmannosamin, N-Isopropanoylmannosamin, N-Cyclopro- panylcarbonylmannosamin? N-Cyclopropanoylmannosamin, N-Isobutyrylmannosamin, N- Butanoylmannosamin, N-Pentanoylmannosamin, N-Hexanoylmannosamin, N-Crotonoyl- mannosamin, N-Lävulinoylmannosamin, N-Glycolylmannosamin oder N-Azidoacetylman- nosamin. Sogar noch weiter bevorzugt sind die peracetylierten Formen dieser N-Acylman- nosamine, insbesondere der die peracetylierten Formen dieser N-Acyl-D-mannosamine.
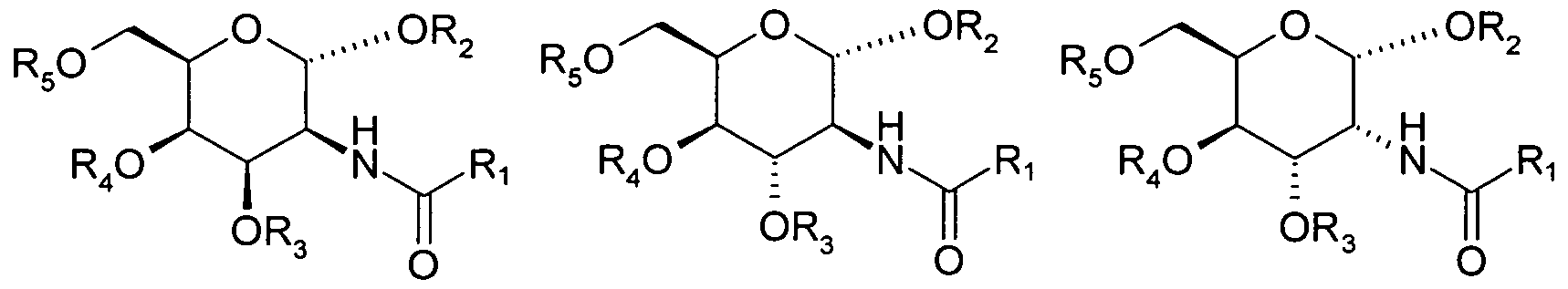
In einer anderen bevorzugten Ausführungsform der Erfindung ist das Derivat eine Sub- stanz der Formel (I)
(I) oder ein Salz oder ein Prodrug hiervon, wobei
- R] ein geradkettiger oder verzweigter, unsubstituierter oder substituierter Alkylrest mit 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 oder 12 C-Atomen, ein geradkettiger oder verzweigter, ein- oder mehrfach ungesättigter, unsubstituierter oder substituierter Alkenylrest mit 3, 4, 5, 6, 7, 8, 9, 10, 11 oder 12 C-Atomen, ein geradkettiger oder verzweigter, ein- oder mehrfach ungesättigter, unsubstituierter oder substituierter Alkinylrest mit 3, 4, 5, 6, 7, 8, 9, 10, 1 1 oder 12 C-Atomen oder ein unsubstituierter oder substituierter Cycloalkyl-, Cycloalkenyl- oder Cycloalkinylrest mit 3, 4, 5, 6, 7, 8, 9, 10, 1 1 oder 12 C-Atomen ist; und
- R2, R3, R4 und R5 unabhängig voneinander H oder ein geradkettiger oder verzweigter, unsubstituierter oder substituierter Alkylrest mit 1 , 2, 3, 4, 5, 6, 7, 8, 9, 10, 1 1 , 12, 13, 14, 15, 16, 17, 18, 19, oder 20 C-Atomen, ein geradkettiger oder verzweigter, ein- oder
mehrfach ungesättigter, unsubstituierter oder substituierter Alkenylrest mit 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 oder 20 C-Atomen, ein geradkettiger oder verzweigter, ein- oder mehrfach ungesättigter, unsubstituierter oder substituierter Alki- nylrest mit 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 oder 20 C-Atomen, ein Arylrest mit 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 oder 20 C-Atomen, ein unsubstituierter oder substituierter Cycloalkyl-, Cycloalkenyl- oder Cycloalkinylrest mit 3, 4, 5, 6, 7, 8, 9, 10, 11 oder 12 C-Atomen oder ein geradkettiger oder verzweigter, unsubstituierter- oder substituierter Acylrest mit 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 oder 12
C-Atomen sind.
Der Begriff "Prodrug" meint eine Verbindung, die in vivo in ein N-Acetyl-mannosamin oder ein Derivat hiervon, das gemäß der vorliegenden Erfindung verwendet werden kann, umgewandelt wird. Beispielsweise kann die Umwandlung mittels Hydrolyse im Blut erfolgen. Beispiele von Prodrugs schließen einen Ether oder ein Amin eines hierin beschriebe- nen N-Acetyl-mannosamin oder eines Derivates hiervon ein. Beispielsweise kann der Wasserstoff einer der Alkoholgruppen durch eine der folgenden Gruppen ersetzt werden: (Ci-C6)-Alkanoyloxymethylgruppe, 1-((C1- C6)-Alkanoyloxy)ethylgruppe, 1 -Methyl- 1- ((Ci- C6)-Alkanoyloxy)ethylgruppe, (Cj- C6)-Alkoxycarbonyloxymethylgruppe, N-(Ci- C6)-Alkoxycarbonylaminomethylgruppe, Succinoylgruppe oder (Cp C6)-Alkanolgruppe. Alternativ kann beispielsweise der Wasserstoff einer Aminogruppe, soweit vorhanden, durch eine der folgenden Gruppen ersetzt werden: (Ci-Cio)-Alkyl-carbonylgruppe oder (Ci-Ci0)- Alkyl-O-Carbonylgruppe.
Das Salz des oben genannten N-Acetyl-mannosamin oder eines Derivates hiervon kann jedes geeignete Salz sein. Insbesondere kann ein Salz so gewählt werden, dass es die Löslichkeit des N-Acetyl-mannosamin oder eines Derivates hiervon erhöht. Bevorzugt für die Verwendung an lebenden Zellen, insbesondere in einen Organismus, z.B. im Zuge einer Vorbeugung oder Behandlung einer Krankheit, sind pharmazeutisch geeignete oder nichttoxische Salze des oben genannten N-Acetyl-mannosamins oder eines Derivates hiervon. Beispiele von geeigneten Salzen sind weiter unter genannt.
Das N-Acetyl-mannosamin oder Derivat hiervon der Formel I kann beispielsweise eine der Konformationen (II) bis (XXXIII) aufweisen:
V VI VII
X Xl XII
XIII XIV XV
XVIII XIX XX
XXVI XXVII XXVIII
XXIX XXX XXXI
XXXII XXXIII
Besonders bevorzugt ist ein N-Acetyl-mannosamin oder eines Derivats hiervon der Formel (I), der eine der Konformationen (II), (III), (IV), (XVII), (XIX) oder (XX), insbesondere (II), (III) oder (IV), aufweist.
Bei den Substituten, mit dem die oben genannten Rest Ri, R2, R3, R4 und/oder R5 von N- Acetyl-mannosamin oder eines Derivates hiervon der Formeln (I) bis (XXXIII) substituiert sein können, kann es sich beispielsweise um eine Halogen-, Hydroxy-, Epoxy-, Amino-, Carbonyl-, Carbonylamid-, Aryl-, Azid-, Thio-, Thioacyl-, Thiocarbamid-, Mercaptan-, Phenyl-, Phenol- oder Benzolgruppe handeln. Es ist möglich, dass keiner, 1, 2, 3, 4 oder alle 5 Reste Ri, R2, R3, R4 und/oder R5, die wie oben definiert sind, einen oder mehrere Substituenten tragen. Bevorzugt ist ein N-Acetyl-mannosamin oder ein Derivat hiervon, das dadurch gekennzeichnet ist, dass der oder die Substituenten an den Resten Ri, R2, R3, R4 und/oder R5 unabhängig voneinander -CO-CH3, =0, -OH, -N3, -F, -Cl, -COOH oder - NH2 sind.
Vorzugsweise ist Rj ein geradkettiger oder verzweigter, ein- oder mehrfach ungesättigter, unsubstituierter oder substituierter Alkenyl oder Alkinylrest mit 1, 2, 3, 4, 5, 6, 7, 8, weiter bevorzugt 3, 4, 5, 6 oder 7, noch weiter bevorzugt 3, 4, oder 5 C- Atomen oder vorzugsweise ein unsubstituierter oder substituierter Cycloalkylrest mit 3, 4, 5 oder 6 C-Atomen ist.
In einer stärker bevorzugten Ausführungsform der Erfindung ist das N-Acetyl- mannosamin oder ein Derivat hiervon dadurch gekennzeichnet, dass Ri ein geradkettiger oder verzweigter, unsubstituierter oder substituierter Alkylrest mit 1, 2, 3, 4, 5, 6, 7 oder 8 C-Atomen, weiter bevorzugt 3, 4, 5, 6 oder 7, noch weiter bevorzugt 3, 4, oder 5 C- Atomen, ist. Ebenso bevorzugt ist die Verwendung von N-Acetyl-mannosamin oder eines Derivates hiervon, das dadurch gekennzeichnet ist, dass Ri gleich -(CH2)Ii-Ro mit n = 1, 2, 3, 4, 5, 6 oder 7, vorzugsweise 2, 3, 4 oder 5, ist, wobei R6 gleich H, -CO-CH3, -OH oder -N3 ist und wobei die -(CH2)n-Gruppe unsubstituiert oder substituiert sein kann.
Sehr stark bevorzugtes N-Acetyl-mannosamin oder eines Derivates hiervon sind dadurch gekennzeichnet, dass R, -CH3, -CH2-CH3, -CH2-CH2-CH3, -CH2-CH2-CH2-CH3, -CH2-CH2-CH2-CH2-CH3, -CH2-CH2-C=O-CH3, -CH2-CH2-CH2-C=O-CH3,
-CH2-CH2-CH2-CH2-C=O-CH35 -CH2-CH2-CH2-CH2-CH2-C=O-CH3, -CO-CH2-CH2-CH2-CH2-CH3, -CO-CH=CH-CH3, -CO-CH2-CH2-CO-CH3, -C(CH3)H-CH2-C=O-CH3 oder -CH2 — Q ist.
O π
Vorzugsweise sind R2, R3, R4 und R5 unabhängig voneinander H oder ein geradkettiger oder verzweigter, ein- oder mehrfach ungesättigter, unsubstituierter oder substituierter Al- kenyl oder Alkinylrest mit 3, 4, 5, 6, 7, 8, 9 oder 10 C-Atomen, ein Arylrest mit 6, 7, 8, 9 oder 10 C-Atomen oder unsubstituierter oder substituierter Cycloalkyl-, Cycloalkenyl- oder Cycloalkinylrest mit 3, 4, 5 oder 6 C-Atomen sind.
Noch weiter bevorzugt ist ein N-Acetyl-mannosamin oder ein Derivat hiervon, das dadurch gekennzeichnet ist, dass mindestens 1, 2, 3 oder 4 der Reste R2, R3, R4 und R5 unabhängig voneinander H oder ein geradkettiger oder verzweigter, unsubstituierter oder substituierter Alkylrest mit 1, 2, 3, 4, 5, 6, 7 oder 8 C-Atomen, vorzugsweise 3, 4, 5, 6 oder 7, insbesondere 3, 4, oder 5 C-Atomen ist.
In einer besonders bevorzugten Ausfuhrungsform sind die Reste R2, R3, R4 und R5 unabhängig voneinander H oder ein geradkettiger oder verzweigter, unsubstituierter oder substituierter Alkylrest mit 1, 2, 3, 4, 5, 6, 7 oder 8 C-Atomen, vorzugsweise H oder ein geradkettiger oder verzweigter, unsubstituierter oder substituierter Alkylrest mit 1, 2 oder 3 C- Atomen ist.
In einer noch stärker bevorzugten Ausfuhrungsform der Erfindung ist das N-Acetyl- mannosamin oder ein Derivat hiervon dadurch gekennzeichnet, dass die Reste R2, R3, R4 und R5 unabhängig voneinander ein geradkettiger oder verzweigter, unsubstituierter oder substituierter Acylrest mit 1, 2, 3, 4, 5, 6, 7 oder 8 C-Atomen, weiter bevorzugt 2, 3, 4, 5, 6 oder 7, noch weiter bevorzugt 2, 3 oder 4 C-Atomen, sind. Beispiele hierfür sind die folgenden Reste: -COCH3, -CO-CH2-CH3 oder -CO-CH2-CH2-CH3.
In einer anderen bevorzugten Ausführungsform sind die Reste wie oben definiert mit der Ausnahme, dass keiner, 1, 2, 3 oder 4 der Reste R2, R3, R4 und R5 Wasserstoff ist.
Besonders stark bevorzugte N-Acetyl-mannosamine oder Derivate hiervon sind dadurch gekennzeichnet,
- dass R1 -CH3, -CH2-CH3, -CH2-CH2-CH3, -CH2-CH2-CH2-CH3, -CH2-CH2-CH2-CH2-CH3, -CH2-CH2-C=O-CH3, -CH2-CH2-CH2-C=O-CH3, -CH2-CH2-CH2-CH2-C=O-CH3, -CH2-CH2-CH2-CH2-CH2-C=O-CH3,
-CO-CH2-CH2-CH2-CH2-CH3, -CO-CH=CH-CH3, -CO-CH2-CH2-CO-CH3, -C(CH3)H-CH2-C=O-CH3 oder -CH2 — Q ist; und
O
- dass mindestens 1, 2, 3 oder 4 der Reste R2, R3, R4 und R5 unabhängig voneinander H oder ein geradkettiger oder verzweigter, unsubstituierter Alkylrest mit 3, 4 oder 5 C-
Atomen sind, vorzugsweise dass alle Reste R2, R3, R4 und R5 unabhängig voneinander H, -CH2-CH3 oder CH2-CH2-CH3, stärker bevorzugt -COCH3, -CO-CH2-CH3 oder -CO-CH2-CH2-CH3 sind.
Wie bereits oben erläutert, kann das N-Acetyl-mannosamin oder Derivat hiervon in Form eines Salzes verwendet werden. Beispielsweise kann es sich bei diesem Salz um ein Alkalimetallsalz oder ein Erdalkalimetall salz, vorzugsweise um ein Lithium-, Natrium-, Kalium-, Calcium-, Magnesium-, Zink-, Mangan- oder Ammoniumsalz, handeln.
Alternativ kann das Salz auch beispielsweise ein Chlorid, Bromid, Iodid, Tartrat, Acetat, Methansulfonat, Maleat, Succinat oder Glutarat sein.
Die Substanzen auf Basis von N-Acylhexopyranosaminen, die gemäß der vorliegenden Erfindung verwendet werden können, können beispielsweise mittels bekannter Verfahren hergestellt werden (siehe z.B. Keppler et al., 1995, J Biol Chem 270: 1308-1314; Jacobs et al., 2001, Biochemistry 11 : 338-345).
Das N-Acetyl-mannosamin oder ein Derivat hiervon kann für die erfindungsgemäße Verwendung in jeder geeigneten Form formuliert sein. Beispiele solcher Formulierungen sind: in Form einer Lösung, einer Emulsion, einer Creme, eines Schaums, einer Gelmatrix, von Tropfen, als Suspensionen, als Konzentrate oder lyophilisiertes Pulver, Tabletten, Kapseln oder Suppositorien, Spray, in Form einer Salbe, eines Aerosol, als Brausetabletten, Pellets,
Dragees oder Pastillen. Besonders bevorzugt sind Retardformulierungen, bei denen es zu einer verzögerten oder langsamen Freisetzung des N-Acetyl-mannosamins oder eines Derivats hiervon kommt und Hormonpeaks vermieden werden. Solche Formulierungen sind dem Fachmann allgemein bekannt. Beispiele solcher Formulierungen sind: Invers mizella- re Lösungen (IML) aus Lecithin in Isopropylmyristat als Arzneistoffträger für Retardformulierungen, biologisch abbaubare Poly(milchsäure)-Polymere oder Retardmatrixtabletten.
Zur Verwendung in der Verbeugung und Behandlung kann das N-Acetyl-mannosamin oder Derivat hiervon zusammen mit geeigneten Hilfs- und Zusatzstoffen formuliert sein oder werden. Geeignete Hilfs- und Zusatzstoffe schließen z.B. Stabilisatoren oder Konservierungsmittel, Emulgatoren, Antioxidantien, Komplexbildner, Puffer, Geschmacksstoffe, Vitamine, Süßmittel, wie z. B. Glucose oder Aspartam, Farbstoffe oder osmotisch wirksame Substanzen wie z.B. Salze u.a. ein. Beispiele solcher Substanzen sind physiologische Kochsalzlösung, Antibiotika, Wasser, Kollagen-enthaltende Substanzen, für Gelformulierungen beispielsweise Aluminiumhydroxid oder Polyacrylsäure-Derivate, Alkaliseifen, Metallseifen, Aminseifen oder partielle Fettsäureester von Sorbitanen, Lipide wie z. B. Vaseline, neutrale und synthetische Wachse, Fettsäuren, Mono-, Di-, Triglyceride, Paraffine, natürliche Öle, Stärke, Lactose, Talcum, Stearinsäure, Zellulose, PVP oder Aerosil®. Die Hilfs- und Zusatzstoffe werden in Abhängigkeit von der beabsichtigen Formulierung und Verabreichung gewählt. Es liegt im Können des Fachmanns, geeignete Hilfs- und Zusatzstoffe für die beabsichtigte Formulierung und Verabreichung zu wählen.
Das N-Acetyl-mannosamin oder Derivat hiervon kann auf jede geeignete Weise verab- reicht werden. Beispiele solcher Verabreichungsformen sind: topisch, lokal, intravenös, intraarteriell, intraperitoneal, intramuskulär, oral, rektal, subkutan, intradermal, intraepithelial, intrafusal, intrakutan oder intrathekal.
Dem Fachmann ist bekannt, dass die spezifische therapeutisch und prophylaktisch wirksa- me Dosis von einer Reihe von Faktoren abhängig ist, die sowohl vom Patienten abhängige
Faktoren, wie z.B. Gewicht, Geschlecht, Alter, Gesundheitszustand, Art der Erkrankung, als auch formulierungsabhängige Faktoren, wie z.B. physikalische und chemische Eigen-
schaften der zu verabreichenden Substanz, Verabreichungsart, Dauer der Behandlung, einschließen. Er wird in der Lage sein, eine geeignete in Abhängigkeit von diesen Faktoren zu wählen. Beispielsweise könnte das N-Acetyl-mannosamin oder ein Derivat hiervon jedoch oral, dreimal täglich in Dosen vom 1 bis 15 g, besonders 2,5 bis 5 g und ganz besonders 3 bis 4 g verabreicht werden.
In einer bevorzugten Ausführungsform der Erfindung wird ein beliebiges, wie oben definiertes N-Acetylmannosamin oder Derivat hiervon zur Vorbeugung vor oder Behandlung eines Sexualhormonmangels verwendet. Insbesondere kann es sich bei dem Sexualhormon um ein Androgen, Östrogen oder Gestagen handeln, wobei
- das Androgen vorzugsweise Testosteron, Androsteron, Androstendion oder Dehydroe- piandrosteron ist;
- das Östrogen vorzugsweise Östradiol, Östron oder Östriol ist; oder
- das Gestagen vorzugsweise Progesteron, Pregnandiol oder Pregnelon ist.
Am meisten bevorzugt betreffen die hierin beschriebenen Gegenstände und Ausführungsformen eine Erhöhung des Testosteronspiegels und/oder einen Testosteronmangel.
Unter einem Sexualhormonmangel versteht man eine zu niedrige Konzentration eines wie oben definierten Sexualhormons in einem Subjekt, beispielsweise im Blutplasma. Der
Spiegel der Sexualhormone in einem Subjekt schwankt in Abhängigkeit von Geschlecht,
Alter, körperlicher Verfassung, dem weiblichen Zyklus, usw.. Beim Menschen sind für die
Sexualhormone Normwerte bekannt, die als normal angesehen werden. Diese hängen von der Untersuchungsmethode, der Reaktionstemperatur (25 vs. 37°C), usw. ab. Normwerte können beispielsweise durch Bezug auf die Referenz-Plasmapräparation CRM470 ermittelt werden. Beispielhafte Normwerte sind in der folgenden Tabelle angegeben:
Tabelle 1: Beispielhafte Normwerte für Sexualhormonspiegel in unterschiedlichen Proben
Bei Frauen sind unabhängig oder in Kombination miteinander Progesteron-, Östrogen- und Androgenmangelerscheinungen bekannt.
Die Symptome eines Progesteronmangels sind z.B. Unregelmäßigkeit der Menses, Wasserstau, Ödemneigung, Mastalgie, Gewichtszunahme, Depression und/oder Migräne. Die Diagnose des Progesteronmangels erfolgt meist klinisch auf Grund von z.B. Anovulation, einer Erhöhung des FSH durch Inhibin-Ausfall, und Progesteronwerte von 0 - 1,5 ng/ml in der Follikelphase bzw. 3,0 -20 ng/ml in der Lutealphase.
Ein Östrogenmangel ist in der Regel durch Hitzewallungen, Schweißausbrüche, Schlaflosigkeit, Haut- und Schleimhauttrockenheit, Gelenkbeschwerden (Arthropathia, Klimakteri- ka) und/oder Effluvium gekennzeichnet. Diagnostiziert wird ein Östrogenmangel klinisch in der Regel durch FSH- Werte über 20 mU/ml und/oder Östrogen-E2-Werte unter 50 pg/ml. Die klassischen Symptome eines Androgenmangels sind nicht partnerabhängiger Libidoverlust, chronisches Erschöpfungssyndrom, abdominelle Gewichtszunahme und/oder Mammahypertrophie. Die Diagnose erfolgt in der Regel über die Messung der Blutandrogenspiegel (z.B. Testosteron < 0,2 ng/ml und/oder DHEA < 1,0 μg/ml).
Androgenmangelsymptome bei Frauen wurden bisher wenig Aufmerksamkeit gewidmet, da im Zentrum des Interesses der Östrogenmangel und die damit verbundene Symptome standen. Unter dem Begriff "female androgene insufficiency" wird ein Symptomenkomplex zusammengefasst (u.a. reduzierter Allgemeinzustand, Müdigkeit, unklare Ursa- che, verringerte Libido) mit niedrigen Testosteron-Blutwerten und normalen Östrogen- Blutwerten.
Wie bereits oben erläutert ist der häufigste Sexualhormonmangel beim Mann ein Androgen- insbesondere ein Testosteronmangel. Von einer Androgenmangelsymptomatik kann bei Blutwerten unter der Normgrenze von 12 nmol/1 gesprochen werden. Diagnostiziert wird ein Androgenmangel an Hand des Gesamttestosteron- und des Sexualhormonbindenden Globulins (SHBG), woraus sich das freie Testosteron berechnen lässt. Klinisch manifestiert sich ein Testosteronmangel häufig durch Knochenschmerzen, Frakturen, Leistungsschwäche, Adipositas, Verlust an sexueller Aktivität, Potenzschwäche und/oder chro- nischer Müdigkeit.
Darüber hinaus ist auch ein Östrogenmangel beim Mann beschrieben. Dieser bewirkt, dass die Produktion des Leberproteins SHBG und so der Anteil an freiem Testosteron enorm ansteigt, was dazu führt, dass unkontrollierte Mengen an Testosteron in die Prostata ein- strömen können. Dort wird das Hormon in Dihydrotestosteron umgewandelt, was zu einer gutartigen Vergrößerung der Prostata oder Prostatakrebs führen kann. Der Normbereich für Östrogen bei Männern liegt zwischen 50 pg/ml bis 100 pg/ml.
In einer weiteren Ausführungsform ist die erfindungsgemäße Verwendung des wie oben definierten N-Acetylmannosamins oder Derivats hiervon dadurch gekennzeichnet, dass zusätzlich eine androgen, Östrogen oder gestagen wirksame Verbindung verwendet wird.
Wie bereits oben ausführlich erläutert ist gegenwärtig eine Reihe von Substanzen bekannt, die als Hormonersatztherapien z.B. bei Testosteron- oder Östrogenmangel verabreicht werden. Diese Verbindungen können zusammen mit den wie hierin definierten N-Acetyl- mannosamin oder den Derivaten hiervon eingesetzt werden, da so die zu verwendenden Konzentrationen dieser Substanzen durch die gleichzeitige Wirkung des N-Acetylmannosamins oder seines Derivats erniedrigt werden kann.
Eine androgen wirksame Verbindung ist eine Verbindung, die im Körper mindestens eine Wirkung eines natürlichen Androgens hervorruft. Beispiele solcher Verbindungen sind solche, die die Wirkung von Testosteron, Androsteron, Androstendion oder Dehydroepi- androsteron therapeutisch ersetzen. Beispiele solcher therapeutisch verwendeten Androgene sind Testosteronpropionat, Testosteronoenanthat, Testosteronundecanoat, Mesterolon, Testosteronwucciclat, α-Methyl-19-Nor-Testosteron (MENT), Androstanolol sowie verschiedene Formen von Testosteron und DHEA. Weitere Beispiele von androgen wirkenden Substanzen schließen selektive Progesteron-Rezptormodulatoren (SPRM) ein. Beispiele solcher Verbindungen sind in der Schrift US 2004 097591 offenbart. Weiterhin offenbart die WO 2004/022065 modifizierte Testosteronanaloga, die modifizierte Hydroxygruppen aufweisen. Andere Analoga sind in DB-B774,064 oder FR-A2035786 beschrieben.
Eine Östrogen wirksame Verbindung ist eine Verbindung, die im Körper mindestens eine Wirkung eines natürlichen Östrogens hervorruft. Analoges gilt für eine gestagen wirksame Verbindung. Beispiele von Östrogen-wirksamen Verbindungen sind neben Östradiol, Östron und Östriol, Mestranol, Etinylöstradiol, Östradiolundecylat, Östradiolvalerianat, Östradiolsuccinat, konjugierte Östrogene, Premarin, Tibolon oder Kombinationen hiervon. Weitere Beispiele von nicht-steroidalen Östrogen-wirksamen Verbindungen sind z.B. Clomiphin, Cyclofenil, Diethylstilboestrol (DES). Beispiele von Gestagen-wirksamen Verbindungen sind Norethisteronacetat, Hydroxyprogesteroncapronat, Norgestrel, Ly-
nestrenol und Chlormadinonacetat. Darüber hinaus kann es sich auch um ein Gestagen- Östrogen-Kombinationspräparat handeln, wie solche die z.B. unter den Handelsnamen Primosiston Oral ®, Primosiston Amp. ®, Duoluton ®, Progylut ®, Nuriphasic ®, Orgaluton ®, Cyclo-Progynova ® und Menova ® bekannt sind.
Bei der Östrogen, gestagen oder androgen wirksame Verbindung kann es sich um eine steroidale oder auch um eine nicht-steroidale Verbindung handeln. Beispiele sind ein natürlich vorkommendes Androgen, Östrogen oder Gestagen oderDerivat hiervon, Androisoxa- zol, Bolasteron, Clostebol, Ethylöstrenol, Formyldienolon, 4-Hydroxy-19-nortestosteron, Methenolon, Methyltrienolon, Nandrolon, Oxymesteron, Quinbolon, Stenbolon, Trenbo- lon, ein androgen wirkendes Steroid wie zum Beispiel Boldenon, Fluoxymesteron, Mesta- nolon, Mesterolon, Methandrostenolon, Methyltestosteron, 17-alpha-Methyltestosteron 3- C Yclopentyl Enol Ether, Norethandrolon, Normethandron, Oxandrolon, Oxymetholon, Prasteron, Stanlolon, Stanozolol, Dihydrotestosteron, Testosteron, eine Östrogen wirkendes Verbindung wie zum Beispiel Östradiolesters wie Östradiol-3,17-diacetat; Östradiol-3- acetat; Östradiol-17-acetat; Östradiol-3,17-divalerat; Östradiol-3-valerat; Östradiol-17- valerat; 3-Mono-, 17-Mono- oder 3,17-Dipropionatester, das entsprechende Cypionat, Heptanoat, Benzoate und ähnliche Ester; Ethynilöstradiol; Estron, ein Progestagen wie zum Beispiel Anageston, Chlormadinonacetat, Delmadinonacetat, Demegeston, Di- methisteron, Dihydrogesteron, Ethinylöstrenol, Ethisteron, Ethynodiol, Ethynodioldiacetat, Flurogestonacetate, Gestoden, Gestonoroncaproat, Haloprogesteron, 17-Hydroxy-16- methylenprogesteron, 17-alpha-Hydroxyprogesteron, 17-alpha-Hydroxyprogesteron- caproat, Medrogeston, Medroxyprogesteron, Megestrolacetat, Melengestrol, Norethindron, Norethindronacetat, Norethynodrel, Norgesteron, Norgestimat, Norgestrel, Norgestrienon, 19-Norprogesteron, Norvinisteron, Pentagestron, Progesteron, Promegeston, Quingestron oder Trengeston oder ein Salz, Ester, Amid, Enantiomer, Isomer Tautomer, Prodrug oder Derivat dieser Verbindungen. Es können auch Kombinationen der genannten Verbindungen verwendet werden.
Ein weiterer Gegenstand der vorliegenden Erfindung ist eine pharmazeutische Zusammensetzung enthaltend a) N-Acetyl-mannosamin und/oder ein Derivat hiervon;
b) eine Östrogen, gestagen oder androgen wirksame Verbindung; und c) ggf. Hilfs- und Zusatzstoffe, wobei die Bestandteile a), b) und c) wie oben definiert sein können.
Die Zusammensetzung kann anstatt der alleinigen Verwendung von N-Acetyl-mannosamin oder einem Derivat hiervon zu den oben beschriebenen Zwecken eingesetzt werden, wobei die oben gemachten Ausführungen ebenfalls gelten. Dies gilt insbesondere auch für die Formulierung und Anwendung der Zusammensetzung, wobei die die Komponente a) und die Komponente b) in einer Zusammensetzung oder auch als separate Präparate und z.B. über unterschiedliche Verabreichungswege eingesetzt werden können.
BEISPIELE
Beispiel 1: Analyse von Testosteronspiegeln in Mäusen nach Gabe von peracetylierter Mannosamine
Experimentelle Vorgehensweise:
Die synthetischen Derivate ManNProp (N-Propanoylmannosamin) und ManNAc (N- Acetylmannosamin) wurde wie von Keppler und Kollegen (Keppler et al., 1995, J. Biol. Chem. 270:1308-1314) beschrieben hergestellt und anschließend analog zu dem von CoI- lins und Mitarbeitern (Collins et al., 2000, Glycobiology 10:11-20) für N-Glycolylmanno- saminmonoacetat beschriebenen Verfahren peracetyliert.
Den männlichen Mäusen wurde über vier Tage intraperitoneal täglich peracetyliertes ManNProp (10 mg/kg Körpergewicht), peracetyliertes ManNAc (10 mg/kg Körpergewicht) oder PBS (Kontrolle) verabreicht. Der peracetylierte Zucker wurde wegen seiner Lipophilie und damit seiner besseren Membrangängigkeit verwendet, wodurch eine geringere Dosis im Vergleich zu nicht-peracetyliertem ManNProp oder ManNAc eingesetzt werden konnte.
Die Messungen der Testosteronkonzentration wurden mit einem kompetitiven Immunasssy im direkten Chemilumineszenzverfahren am mechanisierten Analysesystem ACS: 180
(Bayer Vital GmbH, Leverkusen, Deutschland) gemessen. In diesem Verfahren werden ein polyklonaler Kaninchen-anti-Testosteron-Antikörper und ein monoklonaler Maus-antiKaninchen-Antikörper eingesetzt. Das in der Serumprobe enthaltene Testosteron konkurriert mit Acridinium-markiertem Testosteron um eine begrenzte Mange an polyklonalen Kaninchen-anti-Testosteron-Antikörper. Diese werden dann an die monoklonalen Maus- anti-Kaninchen-Antikörper gebunden, die an paramagnetische Partikel einer Festphase gekoppelt sind. Um das Testosteron von endogenen Bindungsproteinen der Probe abzulösen und somit nachweisen zu können, wird Steroid-Releasing-Agens eingesetzt. Die Tes- tosteronkonzentration der Serumprobe verhält sich umgekehrt proportional zu dem vom System gemessenen Lichteinheiten. Nach Herstellerangaben liegt der Messbereich zwischen 0m35 und 52 μmol/1 mit Variationskoeffizienten von 0,9 bis 13,8 % im Intraassay- Vergleich.
Ergebnis: Die Tiere reagierten unterschiedlich. Die Einzel werte für die unterschiedlich behandelten Mäuse sowie Mittelwerte und Standardabweichungen sind in Tabelle 2 dargestellt. Am Tag 4 der Behandlung mit ManNProp zeigten fünf Mäuse eine 15- bis 30-fach über der Norm erhöhte Testosteronkonzentration; acht Mäuse reagierten nur mit einer Verdoppelung bis Verdreifachung. Bei Berücksichtigung aller Mäuse konnte nach 4-tägiger Behand- lung eine Versiebenfachung der Testosteronkonzentration erhalten werden.
Tabelle 2: Testosteronspiegel in unterschiedlich behandelten Mäusen
Signifikanztest (T-Test):
PBS vs. ManNACc (4 Tage): 0,048
PBS vs. ManNProp (4 Tage): 0,011
ManNAc (4 Tage) vs. ManNACc (4 Tage): 0,69
Beispiel 2: Histologische Untersuchung von Mäusen nach Gabe von peracetyliertem ManNProp
Experimentelle Vorgehensweise:
Die Mäuse aus Beispiel 1 wurden zusätzlich histologisch wie folgt untersucht: Die histo- pathologische Untersuchung jeder Probe wurde durchgeführt, in dem Schnitte der untersuchten Gewebe nach an sich bekannten Verfahren mittels Fixierung unter Verwendung von Formalin sowie Einbettung in Paraffin hergestellt wurden und die Schnitte mit Standard-Färbemethoden (Hämatoxylin-Eosin (H & E) sowie Elastica-van-Gieson (EvG)) zur mikroskopischen Analyse angefärbt wurden. Die so erhaltenen Schnitte wurden von zwei unabhängigen Pathologen untersucht und beurteilt.
Ergebnis:
Die auffälligsten histologischen Befunde an den untersuchten Mäusen waren eine deutlich gesteigerte Spermatogenese in Form einer Vermehrung der Zahl der Spermien und eine Verbreiterung des Keimepithels sowie eine Vergrößerung der Präputialdrüse.
Claims
1. Arzneimittel enthaltend N-Acetyl-mannosamin oder ein Derivat hiervon zur Erhöhung des Spiegels eines Steroidhormons, vorzugsweise eines Sexualhormons, insbesondere von Testosteron, in einem Subjekt.
2. Arzneimittel nach Anspruch 1, dadurch gekennzeichnet, dass das Derivat ein N- Acylmannosamin, N-Acylmannosamin- Analog, N-Acylglucosamin, N-Acylgluco- samim- Analog, N-Acylgalactosamin oder ein N- Acylgalactosamin- Analog ist, insbesondere dadurch gekennzeichnet, dass die Acylgruppe, vorzugsweise mit mindestens einer Oxo-Gruppe, substituiert ist.
3. Arzneimittel nach Anspruch 2, dadurch gekennzeichnet, dass in dem Analog mindestens 1, 2, 3 oder 4 OH-Gruppen acyliert sind, vorzugsweise dadurch gekennzeichnet, dass in dem Analog mindestens 1 , 2 oder 3 OH-Gruppen acetyliert, propionyliert, bu- tanoyliert, pentanoyliert oder PEGyliert, insbesondere acetyliert, propionyliert oder butanoyliert sind.
4. Arzneimittel nach Anspruch 2 oder 3, dadurch gekennzeichnet, dass das Analog ein
Desoxy- oder ein Didesoxy-Derivat ist.
5. Arzneimittel nach Anspruch 1, dadurch gekennzeichnet, dass das Derivat ein N- Propanoylmannosamin, N-Isopropanoylmannosamin, N-Cyclopropanoyl- carbonylmannosamin, N-Cyclopropanylmannosamin, N-Isobutyrylmannosamin, N- Butanoylmannosamin, N-Pentanoylmannosamin, N-Hexanoylmannosamin, N- Crotonoylmannosamin, N-Lävulinoylmannosamin, N-Glycolylmannosamin oder N-
Azidoacetylmannosamin ist.
6. Arzneimittel nach Anspruch 1, dadurch gekennzeichnet, dass das Derivat eine Substanz der Formel (I)
- Ri ein geradkettiger oder verzweigter, unsubstituierter oder substituierter Alkyl- rest mit 1 , 2, 3, 4, 5, 6, 7, 8, 9, 10, 1 1 oder 12 C-Atomen, ein geradkettiger oder verzweigter, ein- oder mehrfach ungesättigter, unsubstituierter oder substituierter Alkenylrest mit 3, 4, 5, 6, 7, 8, 9, 10, 1 1 oder 12 C-Atomen, ein geradkettiger o- der verzweigter, ein- oder mehrfach ungesättigter, unsubstituierter oder substituierter Alkinylrest mit 3, 4, 5, 6, 7, 8, 9, 10, 1 1 oder 12 C-Atomen oder ein unsubstituierter oder substituierter Cycloalkyl-, Cycloalkenyl- oder Cycloalkinylrest mit 3, 4, 5, 6, 7, 8, 9, 10, 1 1 oder 12 C-Atomen ist; und - R2, R3, R4 und R5 unabhängig voneinander H oder ein geradkettiger oder verzweigter, unsubstituierter oder substituierter Alkylrest mit 1 , 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, oder 20 C-Atomen, ein geradkettiger oder verzweigter, ein- oder mehrfach ungesättigter, unsubstituierter oder substituierter Alkenylrest mit 3, 4, 5, 6, 7, 8, 9, 10, 1 1 , 12, 13, 14, 15, 16, 17, 18, 19 oder 20 C- Atomen, ein geradkettiger oder verzweigter, ein- oder mehrfach ungesättigter, unsubstituierter oder substituierter Alkinylrest mit 3, 4, 5, 6, 7, 8, 9, 10, 1 1, 12, 13, 14, 15, 16, 17, 18, 19 oder 20 C-Atomen, ein Arylrest mit 6, 7, 8, 9, 10, 1 1 , 12, 13, 14, 15, 16, 17, 18, 19 oder 20 C-Atomen, ein unsubstituierter oder substituierter Cycloalkyl-, Cycloalkenyl- oder Cycloalkinylrest mit 3, 4, 5, 6, 7, 8, 9, 10, 1 1 oder 12 C-Atomen oder ein geradkettiger oder verzweigter, unsubstituierter oder substituierter Acylrest mit 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 oder 12 C-Atomen sind.
7. Arzneimittel nach Anspruch 6, dadurch gekennzeichnet, dass das Derivat der Formel (I) eine der Konformationen (II) bis (XXXIII) aufweist:
- -
V VI VII
XIII XIV XV
XVI XVII - -
XVi Il XIX XX
XXI * XXIl XXIII
XXIV XXV
XXVI XXVII XXVIII
XXXII XXXIII
8. Arzneimittel nach Anspruch 7, dadurch gekennzeichnet, dass das Derivat der Formel (I) eine der Konformationen (II), (III) oder (IV) aufweist.
9. Arzneimittel nach einem der Ansprüche 6 bis 8, dadurch gekennzeichnet, a) dass der oder die Substituenten an dem Rest R|, R2, R3, R4 und/oder R5 unabhängig voneinander -CO-CH3, =0, -OH, -N3, -F, -Cl, -COOH oder -NH2 ist/sind; b) dass Ri ein geradkettiger oder verzweigter, unsubstituierter oder substituierter Alkyl-, mit 1, 2, 3, 4, 5, 6, 7 oder 8 C- Atomen ist. c) dass Ri gleich -(CH2)P-R6 mit n = 1 , 2, 3, 4, 5, 6 oder 7 ist, wobei R6 gleich -H, -CO-CH3, -OH oder -N3 ist und wobei die -(CH2)n-Gruppe unsubstituiert oder substituiert sein kann; d) dass Ri -CH3, -CH2-CH3, -CH2-CH2-CH3, -CH2-CH2-CH2-CH3, -CH2-CH2-CH2-CH2-CH3, -CH2-CH2-C=O-CH3, -CH2-CH2-CH2-C=O-CH3, -CH2-CH2-CH2-CH2-C=O-CH35 -CH2-CH2-CH2-CH2-CH2-C=O-CH3, -CO-CH2-CH2-CH2-CH2-CH3, -CO-CH=CH-CH3 oder -CO-CH2-CH2-CO-CH3,
-C(CH3)H-CH2-C=O-CH3 oder -CH2 — C) ist;
e) dass mindestens 1, 2, 3 oder 4 der Reste R2, R3, R4 und R5 unabhängig voneinander H oder ein geradkettiger oder verzweigter, unsubstituierter oder substituierter Alkylrest mit 1 , 2, 3, 4, 5, 6, 7 oder 8 C-Atomen ist/sind; f) dass die Reste R2, R3, R4 und R5 unabhängig voneinander H oder ein geradkettiger oder verzweigter, unsubstituierter oder substituierter Alkylrest oder Acylrest mit 1, 2, 3, 4, 5, 6, 7 oder 8 C-Atomen sind; g) dass die Reste R2, R3, R4 und R5 unabhängig voneinander H oder ein geradketti- ger oder verzweigter, unsubstituierter oder substituierter Alkylrest oder Acylrest mit 1 , 2 oder 3 C-Atomen sind; h) dass keiner, 1 , 2, 3 oder 4 der Reste R2, R3, R4 und R5 Wasserstoff ist; i) dass das Salz ein Alkalimetallsalz oder ein Erdalkalimetallsalz ist; j) dass das Salz ein Lithium-, Natrium-, Kalium-, Calcium-, Magnesium-, Zink-, Mangan- oder Ammoniumsalz ist; k) dass das Salz ein Chlorid, Bromid, Iodid, Tartrat, Acetat, Methansulfonat, Ma- leat, Succinat oder Glutarat ist; und/oder 1) dass das Prodrug ein Ether oder Amin ist.
10. Arzneimittel nach einem der Anspruch 2 bis 9 zur Vorbeugung vor oder Behandlung eines Sexualhormonmangels, vorzugsweise dadurch gekennzeichnet, dass das Sexualhormon ein Androgen, Östrogen oder Gestagen, insbesondere Testosteron, ist.
11. Arzneimittel nach Anspruch 10, dadurch gekennzeichnet, dass
- das Androgen Testosteron, Androsteron, Androstendion oder Dehydroepi- androsteron ist;
- das Östrogen Östradiol, Östron oder Östriol ist; oder
- das Gestagen Progesteron, Pregnandiol oder Pregnelon ist.
12. Arzneimittel nach einem der Ansprüche 1 bis 11, dadurch gekennzeichnet, dass zusätzlich eine androgen, Östrogen oder gestagen wirksame Verbindung verwendet wird.
13. Pharmazeutische Zusammensetzung enthaltend a) N-Acetyl-mannosamin und/oder ein wie in den Ansprüchen 2 bis 10 definiertes Derivat hiervon; b) eine Östrogen oder androgen wirksame Verbindung; und c) ggf. Hilfs- und Zusatzstoffe.
14. Arzneimittel nach Anspruch 12 oder pharmazeutische Zusammensetzung nach Anspruch 13, dadurch gekennzeichnet, dass die androgen, Östrogen oder gestagen wirksame Verbindung ein Sexualhormon oder ein Derivat hiervon oder eine nichtsteroidale Östrogen oder androgen wirksame Verbindung ist, insbesondere dadurch gekennzeichnet, dass das Sexualhormon wie in einem der Ansprüche 10 oder 1 1 definiert ist.
15. Arzneimittel nach einem der Ansprüche 1 bis 1 1, dadurch gekennzeichnet, dass eine pharmazeutische Zusammensetzung nach einem der Ansprüche 13 oder 14 eingesetzt wird.
16. Verwendung von N-Acetyl-mannosamin oder ein Derivat hiervon zur Herstellung eins Arzneimittels zur Erhöhung des Spiegels eines Steroidhormons, vorzugsweise eines Sexualhormons, insbesondere von Testosteron, in einem Subjekt, wobei das Arzneimittel wie in einem der Ansprüche 2 bis 12, 14 oder 15 definiert ist.
17. Verfahren zur Erhöhung des Spiegels eines Steroidhormons, vorzugsweise eines Sexualhormons, insbesondere von Testosteron, in einem Subjekt, wobei eine wirksame Menge an einem Arzneimittel enthaltend N-Acetyl-mannosamin oder ein Derivat hiervon an ein Subjekt, wobei das Arzneimittel wie in einem der Anspräche 2 bis 12, 14 oder 15 definiert ist.
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE102006012161.9 | 2006-03-16 | ||
| DE102006012161A DE102006012161A1 (de) | 2006-03-16 | 2006-03-16 | Neue Verwendung von N-Acetyl-mannosamin oder Derivaten hiervon |
| DE102006047647.6 | 2006-10-09 | ||
| DE102006047647 | 2006-10-09 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2007104576A1 true WO2007104576A1 (de) | 2007-09-20 |
Family
ID=37950485
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/EP2007/002348 WO2007104576A1 (de) | 2006-03-16 | 2007-03-16 | Arzneimittel enthaltend n-acetyl-mannosamin oder derivate hiervon und seine verwendung |
Country Status (1)
| Country | Link |
|---|---|
| WO (1) | WO2007104576A1 (de) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2009083444A1 (en) | 2007-12-28 | 2009-07-09 | Bioiberica, S.A. | Composition for the treatment of osteoarthritis |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE19738484A1 (de) * | 1997-09-03 | 1999-03-04 | Reutter Werner Prof Dr Med | Verwendung von N-Propanoyl-Mannosamin als Medikament |
| JP2001078794A (ja) * | 1999-09-10 | 2001-03-27 | Marukin Chuyu Co Ltd | N−アセチルマンノサミンの製造法 |
| WO2004052269A1 (en) * | 2002-12-10 | 2004-06-24 | Gambro Lundia Ab | A method for preparing a medical solution for the manufacture of a medicament for peritoneal dialysis |
| US20050171194A1 (en) * | 2003-12-08 | 2005-08-04 | Yu Ruey J. | Enlargement of mucocutaneous or cutaneous organs and sites with topical compositions |
-
2007
- 2007-03-16 WO PCT/EP2007/002348 patent/WO2007104576A1/de active Application Filing
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE19738484A1 (de) * | 1997-09-03 | 1999-03-04 | Reutter Werner Prof Dr Med | Verwendung von N-Propanoyl-Mannosamin als Medikament |
| JP2001078794A (ja) * | 1999-09-10 | 2001-03-27 | Marukin Chuyu Co Ltd | N−アセチルマンノサミンの製造法 |
| WO2004052269A1 (en) * | 2002-12-10 | 2004-06-24 | Gambro Lundia Ab | A method for preparing a medical solution for the manufacture of a medicament for peritoneal dialysis |
| US20050171194A1 (en) * | 2003-12-08 | 2005-08-04 | Yu Ruey J. | Enlargement of mucocutaneous or cutaneous organs and sites with topical compositions |
Non-Patent Citations (3)
| Title |
|---|
| DATABASE WPI Week 200133, Derwent World Patents Index; AN 2001-313377, XP002431276 * |
| KIM E J ET AL: "Characterization of the metabolic flux and apoptotic effects of O-hydroxyl- and N-acyl-modified N-acetylmannosamine analogs in Jurkat cells", THE JOURNAL OF BIOLOGICAL CHEMISTRY, vol. 279, no. 18, 30 April 2004 (2004-04-30), pages 18342 - 18352, XP002431274 * |
| LAYNE D S ET AL: "The isolation from rabbit urine of a conjugate of 17 alpha estradiol with N-acetylglucosamine", THE JOURNAL OF BIOLOGICAL CHEMISTRY, vol. 239, no. 10, October 1964 (1964-10-01), pages 3221 - 3225, XP002431273 * |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2009083444A1 (en) | 2007-12-28 | 2009-07-09 | Bioiberica, S.A. | Composition for the treatment of osteoarthritis |
| EP2301554A1 (de) | 2007-12-28 | 2011-03-30 | Bioiberica, S.A. | Zusammensetzung zur Behandlung von Osteoartritis |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE60216630T2 (de) | Verwendung von östrogen in kombination mit progestogen für die hormonsubstitutiionstherapie | |
| DE60318092T2 (de) | Pharmazeutische zusammensetzung enthaltend estetrolderivate und anwendung in der krebsbehandlung | |
| DE69721377T2 (de) | Arzneimittel zur transdermalen Verabreichung von einem Östrogen oder Progestin oder einer Mischung davon | |
| DE60209907T2 (de) | Verwendung von oestrogenverbindungen zur steigerung der libido bei frauen | |
| DE69628163T2 (de) | Nor-pregnane zur induzierung hypothalamischer effekte | |
| DE69434697T2 (de) | Therapeutische Verwendungen von Dehydroepiandrosteron zur Behandlung von verminderter Libido und Osteoporose | |
| DE69333023T2 (de) | 3-beta-hydroxylierte natürliche Steroidderivate enthaltende Arzneimittelzusammensetzungen und ihre Verwendung | |
| DE60130147T2 (de) | Verwendung oraler formulierungen zur behandlung der weiblichen sexuellen störung | |
| DE602004011374T2 (de) | Transdermale pharmazeutische zusammensetzung | |
| DE69909016T2 (de) | Pharmazeutische Zusammensetzung von Estrogen und Progesteron | |
| DE602005005165T2 (de) | Verfahren zur verbesserung der bioverfügbarkeit von ospemifen | |
| DE60315939T2 (de) | Pharmazeutische zusammensetzung enthaltend ein androgen | |
| DD269557A5 (de) | Verfahren zur herstellung einer zusammensetzung zur wirksamen prephylaxe von brustkrebs bei frauen und zur empfaengnisverhuetung | |
| DE60223795T2 (de) | Tetrahydroxyliertes Östrogen enthaltendes Arzneistoffverabreichungssystem zur Verwendung in der hormonalen Kontrazeption | |
| DE3118218A1 (de) | Wasserloesliche einschluss-komplexe von in wasser nicht oder nur begrenzt loeslichen biologisch aktiven organischen verbindungen und deren waessrige loesungen sowie deren herstellung und diese verbindungen enthaltende arzneimittelpraeparate | |
| DE3733478A1 (de) | Antigestagen- und antioestrogenwirksame verbindungen zur geburtseinleitung und zum schwangerschaftsabbruch sowie zur behandlung gynaekologischer stoerungen und hormonabhaengiger tumore | |
| EP1100509B1 (de) | Verwendung von biogenen estrogensulfamaten zur hormonsubstitutionstherapie | |
| EP0775156A1 (de) | Pharmazeutische zusammensetzungen mit estra-1,3,5(10)-trien-derivaten | |
| DE60318447T2 (de) | Pharmazeutische zusammensetzung enthaltend estetrolderivate und anwendung in der krebsbehandlung | |
| EP1347764B1 (de) | Gelzusammensetzung auf alkoholischer basis zur behandlung von hypogonadismus durch transskrotale applikation | |
| DE69736833T2 (de) | Steroide als neurochemische stimulatoren des nasenraumes zur linderung der prämenstrualen symptome | |
| JP2000504025A (ja) | ヒトのlhまたはfsh血中濃度を変化させる神経化学的イニシエータであるステロイド | |
| WO2007104576A1 (de) | Arzneimittel enthaltend n-acetyl-mannosamin oder derivate hiervon und seine verwendung | |
| JPS60161998A (ja) | 1α,2α―メチレン―6―メチレン―又は―6α―メチル―プレグネン及びその製法 | |
| DE102006012161A1 (de) | Neue Verwendung von N-Acetyl-mannosamin oder Derivaten hiervon |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 07723326 Country of ref document: EP Kind code of ref document: A1 |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| 122 | Ep: pct application non-entry in european phase |
Ref document number: 07723326 Country of ref document: EP Kind code of ref document: A1 |