RU2328503C2 - N''-ЗАМЕЩЕННЫЕ 9a-N-(N'-КАРБАМОИЛ-ГАММА-АМИНОПРОПИЛЬНЫЕ) И 9a-N-(N'-ТИОКАРБАМОИЛ-ГАММА-АМИНОПРОПИЛЬНЫЕ), ПРОИЗВОДНЫЕ 9-ДЕЗОКСО-9-ДИГИДРО-9a-АЗА-9a-ГОМОЭРИТРОМИЦИНА A И 5-O-ДЕЗОЗАМИНИЛ-9-ДЕЗОКСО-9-ДИГИДРО-9a-АЗА-9a-ГОМОЭРИТРОНОЛИДА A - Google Patents
N''-ЗАМЕЩЕННЫЕ 9a-N-(N'-КАРБАМОИЛ-ГАММА-АМИНОПРОПИЛЬНЫЕ) И 9a-N-(N'-ТИОКАРБАМОИЛ-ГАММА-АМИНОПРОПИЛЬНЫЕ), ПРОИЗВОДНЫЕ 9-ДЕЗОКСО-9-ДИГИДРО-9a-АЗА-9a-ГОМОЭРИТРОМИЦИНА A И 5-O-ДЕЗОЗАМИНИЛ-9-ДЕЗОКСО-9-ДИГИДРО-9a-АЗА-9a-ГОМОЭРИТРОНОЛИДА A Download PDFInfo
- Publication number
- RU2328503C2 RU2328503C2 RU2005121892/04A RU2005121892A RU2328503C2 RU 2328503 C2 RU2328503 C2 RU 2328503C2 RU 2005121892/04 A RU2005121892/04 A RU 2005121892/04A RU 2005121892 A RU2005121892 A RU 2005121892A RU 2328503 C2 RU2328503 C2 RU 2328503C2
- Authority
- RU
- Russia
- Prior art keywords
- dihydro
- aminopropyl
- aza
- deoxo
- group
- Prior art date
Links
- -1 2,4-dichlorphenyl Chemical group 0.000 claims abstract description 52
- 239000000126 substance Substances 0.000 claims abstract description 18
- 150000003839 salts Chemical class 0.000 claims abstract description 13
- 150000007522 mineralic acids Chemical class 0.000 claims abstract description 10
- 150000007524 organic acids Chemical class 0.000 claims abstract description 10
- 125000006201 3-phenylpropyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])C([H])([H])C([H])([H])* 0.000 claims abstract description 9
- 230000000844 anti-bacterial effect Effects 0.000 claims abstract description 8
- 235000005985 organic acids Nutrition 0.000 claims abstract description 8
- 238000000034 method Methods 0.000 claims abstract description 7
- 239000008194 pharmaceutical composition Substances 0.000 claims abstract description 6
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 claims abstract description 5
- ZUSWDTWYONAOPH-UHFFFAOYSA-N [2-(trifluoromethyl)phenyl]hydrazine;hydrochloride Chemical group [Cl-].[NH3+]NC1=CC=CC=C1C(F)(F)F ZUSWDTWYONAOPH-UHFFFAOYSA-N 0.000 claims abstract description 4
- 239000012634 fragment Substances 0.000 claims abstract description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 claims description 84
- 125000001637 1-naphthyl group Chemical group [H]C1=C([H])C([H])=C2C(*)=C([H])C([H])=C([H])C2=C1[H] 0.000 claims description 17
- 125000005809 3,4,5-trimethoxyphenyl group Chemical group [H]C1=C(OC([H])([H])[H])C(OC([H])([H])[H])=C(OC([H])([H])[H])C([H])=C1* 0.000 claims description 9
- 125000001622 2-naphthyl group Chemical group [H]C1=C([H])C([H])=C2C([H])=C(*)C([H])=C([H])C2=C1[H] 0.000 claims description 8
- 125000004201 2,4-dichlorophenyl group Chemical group [H]C1=C([H])C(*)=C(Cl)C([H])=C1Cl 0.000 claims description 7
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 claims description 5
- 239000012948 isocyanate Substances 0.000 claims description 4
- 150000002513 isocyanates Chemical class 0.000 claims description 4
- 238000002360 preparation method Methods 0.000 claims description 3
- NONOKGVFTBWRLD-UHFFFAOYSA-N thioisocyanate group Chemical group S(N=C=O)N=C=O NONOKGVFTBWRLD-UHFFFAOYSA-N 0.000 claims description 2
- 239000003937 drug carrier Substances 0.000 claims 1
- 239000000203 mixture Substances 0.000 abstract description 27
- 150000001875 compounds Chemical class 0.000 abstract description 6
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 abstract description 5
- 239000003120 macrolide antibiotic agent Substances 0.000 abstract description 5
- 239000000654 additive Substances 0.000 abstract description 3
- 230000000996 additive effect Effects 0.000 abstract description 3
- 230000000694 effects Effects 0.000 abstract description 3
- 238000004519 manufacturing process Methods 0.000 abstract description 2
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 abstract 3
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 78
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 78
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 52
- 238000006243 chemical reaction Methods 0.000 description 29
- 239000002904 solvent Substances 0.000 description 28
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 26
- 229910021529 ammonia Inorganic materials 0.000 description 26
- 238000004587 chromatography analysis Methods 0.000 description 26
- 239000012043 crude product Substances 0.000 description 26
- 239000013078 crystal Substances 0.000 description 26
- 239000000741 silica gel Substances 0.000 description 26
- 229910002027 silica gel Inorganic materials 0.000 description 26
- 229960003276 erythromycin Drugs 0.000 description 6
- ULGZDMOVFRHVEP-RWJQBGPGSA-N Erythromycin Chemical compound O([C@@H]1[C@@H](C)C(=O)O[C@@H]([C@@]([C@H](O)[C@@H](C)C(=O)[C@H](C)C[C@@](C)(O)[C@H](O[C@H]2[C@@H]([C@H](C[C@@H](C)O2)N(C)C)O)[C@H]1C)(C)O)CC)[C@H]1C[C@@](C)(OC)[C@@H](O)[C@H](C)O1 ULGZDMOVFRHVEP-RWJQBGPGSA-N 0.000 description 5
- 229930006677 Erythromycin A Natural products 0.000 description 5
- MDKCFLQDBWCQCV-UHFFFAOYSA-N benzyl isothiocyanate Chemical compound S=C=NCC1=CC=CC=C1 MDKCFLQDBWCQCV-UHFFFAOYSA-N 0.000 description 4
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 3
- 241000193996 Streptococcus pyogenes Species 0.000 description 3
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 3
- 150000002576 ketones Chemical group 0.000 description 3
- GRUOGLPIAPZLHJ-UHFFFAOYSA-N 1-Isothiocyanato-3-phenylpropane Chemical compound S=C=NCCCC1=CC=CC=C1 GRUOGLPIAPZLHJ-UHFFFAOYSA-N 0.000 description 2
- GONOHGQPZFXJOJ-SNVBAGLBSA-N 1-[(1r)-1-isocyanatoethyl]naphthalene Chemical compound C1=CC=C2C([C@H](N=C=O)C)=CC=CC2=C1 GONOHGQPZFXJOJ-SNVBAGLBSA-N 0.000 description 2
- GZWGTVZRRFPVAS-UHFFFAOYSA-N 1-isocyanato-2-(trifluoromethyl)benzene Chemical compound FC(F)(F)C1=CC=CC=C1N=C=O GZWGTVZRRFPVAS-UHFFFAOYSA-N 0.000 description 2
- BDQNKCYCTYYMAA-UHFFFAOYSA-N 1-isocyanatonaphthalene Chemical compound C1=CC=C2C(N=C=O)=CC=CC2=C1 BDQNKCYCTYYMAA-UHFFFAOYSA-N 0.000 description 2
- JBDOSUUXMYMWQH-UHFFFAOYSA-N 1-naphthyl isothiocyanate Chemical compound C1=CC=C2C(N=C=S)=CC=CC2=C1 JBDOSUUXMYMWQH-UHFFFAOYSA-N 0.000 description 2
- XIXJQNFTNSQTBT-UHFFFAOYSA-N 2-isocyanatonaphthalene Chemical compound C1=CC=CC2=CC(N=C=O)=CC=C21 XIXJQNFTNSQTBT-UHFFFAOYSA-N 0.000 description 2
- GSLTVFIVJMCNBH-UHFFFAOYSA-N 2-isocyanatopropane Chemical compound CC(C)N=C=O GSLTVFIVJMCNBH-UHFFFAOYSA-N 0.000 description 2
- 241000894006 Bacteria Species 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 2
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 2
- 241000588655 Moraxella catarrhalis Species 0.000 description 2
- QAADZYUXQLUXFX-UHFFFAOYSA-N N-phenylmethylthioformamide Natural products S=CNCC1=CC=CC=C1 QAADZYUXQLUXFX-UHFFFAOYSA-N 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 2
- 239000002253 acid Substances 0.000 description 2
- 230000002378 acidificating effect Effects 0.000 description 2
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 2
- DUVOZUPPHBRJJO-UHFFFAOYSA-N ethyl 2-isocyanatoacetate Chemical compound CCOC(=O)CN=C=O DUVOZUPPHBRJJO-UHFFFAOYSA-N 0.000 description 2
- IPCSVZSSVZVIGE-UHFFFAOYSA-N hexadecanoic acid Chemical compound CCCCCCCCCCCCCCCC(O)=O IPCSVZSSVZVIGE-UHFFFAOYSA-N 0.000 description 2
- 238000000338 in vitro Methods 0.000 description 2
- 230000003993 interaction Effects 0.000 description 2
- YDNLNVZZTACNJX-UHFFFAOYSA-N isocyanatomethylbenzene Chemical compound O=C=NCC1=CC=CC=C1 YDNLNVZZTACNJX-UHFFFAOYSA-N 0.000 description 2
- 150000002540 isothiocyanates Chemical class 0.000 description 2
- 244000005700 microbiome Species 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 238000001556 precipitation Methods 0.000 description 2
- YGSDEFSMJLZEOE-UHFFFAOYSA-N salicylic acid Chemical compound OC(=O)C1=CC=CC=C1O YGSDEFSMJLZEOE-UHFFFAOYSA-N 0.000 description 2
- 238000001228 spectrum Methods 0.000 description 2
- 238000003786 synthesis reaction Methods 0.000 description 2
- HRKNNHYKWGYTEN-HOQMJRDDSA-N (2r,3s,4r,5r,8r,10r,11r,12s,13s,14r)-11-[(2s,3r,4s,6r)-4-(dimethylamino)-3-hydroxy-6-methyloxan-2-yl]oxy-2-ethyl-3,4,10-trihydroxy-13-[(2r,4r,5s,6s)-5-hydroxy-4-methoxy-4,6-dimethyloxan-2-yl]oxy-3,5,8,10,12,14-hexamethyl-1-oxa-6-azacyclopentadecan-15-one Chemical compound O([C@@H]1[C@@H](C)C(=O)O[C@@H]([C@@]([C@H](O)[C@@H](C)NC[C@H](C)C[C@@](C)(O)[C@H](O[C@H]2[C@@H]([C@H](C[C@@H](C)O2)N(C)C)O)[C@H]1C)(C)O)CC)[C@H]1C[C@@](C)(OC)[C@@H](O)[C@H](C)O1 HRKNNHYKWGYTEN-HOQMJRDDSA-N 0.000 description 1
- XCLJRCAJSCMIND-JCTYMORFSA-N (9S)-erythromycyclamine Chemical compound O([C@@H]1[C@@H](C)C(=O)O[C@@H]([C@@]([C@H](O)[C@@H](C)[C@@H](N)[C@H](C)C[C@@](C)(O)[C@H](O[C@H]2[C@@H]([C@H](C[C@@H](C)O2)N(C)C)O)[C@H]1C)(C)O)CC)[C@H]1C[C@@](C)(OC)[C@@H](O)[C@H](C)O1 XCLJRCAJSCMIND-JCTYMORFSA-N 0.000 description 1
- RXZBMPWDPOLZGW-XMRMVWPWSA-N (E)-roxithromycin Chemical compound O([C@@H]1[C@@H](C)C(=O)O[C@@H]([C@@]([C@H](O)[C@@H](C)C(=N/OCOCCOC)/[C@H](C)C[C@@](C)(O)[C@H](O[C@H]2[C@@H]([C@H](C[C@@H](C)O2)N(C)C)O)[C@H]1C)(C)O)CC)[C@H]1C[C@@](C)(OC)[C@@H](O)[C@H](C)O1 RXZBMPWDPOLZGW-XMRMVWPWSA-N 0.000 description 1
- LDMOEFOXLIZJOW-UHFFFAOYSA-N 1-dodecanesulfonic acid Chemical compound CCCCCCCCCCCCS(O)(=O)=O LDMOEFOXLIZJOW-UHFFFAOYSA-N 0.000 description 1
- OLBJNSPBWLCTOT-UHFFFAOYSA-N 2,4-dichloro-1-isocyanatobenzene Chemical compound ClC1=CC=C(N=C=O)C(Cl)=C1 OLBJNSPBWLCTOT-UHFFFAOYSA-N 0.000 description 1
- RVHOBHMAPRVOLO-UHFFFAOYSA-N 2-ethylbutanedioic acid Chemical compound CCC(C(O)=O)CC(O)=O RVHOBHMAPRVOLO-UHFFFAOYSA-N 0.000 description 1
- HACRKYQRZABURO-UHFFFAOYSA-N 2-phenylethyl isocyanate Chemical compound O=C=NCCC1=CC=CC=C1 HACRKYQRZABURO-UHFFFAOYSA-N 0.000 description 1
- YKAVHPRGGAUFDN-JTQLBUQXSA-N 24464-30-0 Chemical compound O([C@@H]1[C@@H](C)C(=O)O[C@@H]([C@@]2(C)O[C@]3([C@@H]([C@H]2O)C)[C@H](C)C[C@](O3)(C)[C@H](O[C@H]2[C@@H]([C@H](C[C@@H](C)O2)N(C)C)O)[C@H]1C)CC)[C@H]1C[C@@](C)(OC)[C@@H](O)[C@H](C)O1 YKAVHPRGGAUFDN-JTQLBUQXSA-N 0.000 description 1
- UOQHWNPVNXSDDO-UHFFFAOYSA-N 3-bromoimidazo[1,2-a]pyridine-6-carbonitrile Chemical compound C1=CC(C#N)=CN2C(Br)=CN=C21 UOQHWNPVNXSDDO-UHFFFAOYSA-N 0.000 description 1
- MJJXWPHZDBIHIM-UHFFFAOYSA-N 5-isocyanato-1,2,3-trimethoxybenzene Chemical compound COC1=CC(N=C=O)=CC(OC)=C1OC MJJXWPHZDBIHIM-UHFFFAOYSA-N 0.000 description 1
- 208000035143 Bacterial infection Diseases 0.000 description 1
- 239000005711 Benzoic acid Substances 0.000 description 1
- 208000035473 Communicable disease Diseases 0.000 description 1
- 241000194032 Enterococcus faecalis Species 0.000 description 1
- 241000943303 Enterococcus faecalis ATCC 29212 Species 0.000 description 1
- 241000588724 Escherichia coli Species 0.000 description 1
- 241001360526 Escherichia coli ATCC 25922 Species 0.000 description 1
- 241000606768 Haemophilus influenzae Species 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- 241000204031 Mycoplasma Species 0.000 description 1
- 150000001204 N-oxides Chemical class 0.000 description 1
- 235000021314 Palmitic acid Nutrition 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 230000029936 alkylation Effects 0.000 description 1
- 238000005804 alkylation reaction Methods 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 230000000845 anti-microbial effect Effects 0.000 description 1
- 229940088710 antibiotic agent Drugs 0.000 description 1
- 239000004599 antimicrobial Substances 0.000 description 1
- 229960004099 azithromycin Drugs 0.000 description 1
- MQTOSJVFKKJCRP-BICOPXKESA-N azithromycin Chemical compound O([C@@H]1[C@@H](C)C(=O)O[C@@H]([C@@]([C@H](O)[C@@H](C)N(C)C[C@H](C)C[C@@](C)(O)[C@H](O[C@H]2[C@@H]([C@H](C[C@@H](C)O2)N(C)C)O)[C@H]1C)(C)O)CC)[C@H]1C[C@@](C)(OC)[C@@H](O)[C@H](C)O1 MQTOSJVFKKJCRP-BICOPXKESA-N 0.000 description 1
- 230000001580 bacterial effect Effects 0.000 description 1
- 208000022362 bacterial infectious disease Diseases 0.000 description 1
- SRSXLGNVWSONIS-UHFFFAOYSA-N benzenesulfonic acid Chemical compound OS(=O)(=O)C1=CC=CC=C1 SRSXLGNVWSONIS-UHFFFAOYSA-N 0.000 description 1
- 229940092714 benzenesulfonic acid Drugs 0.000 description 1
- 235000010233 benzoic acid Nutrition 0.000 description 1
- 229960004365 benzoic acid Drugs 0.000 description 1
- 230000003115 biocidal effect Effects 0.000 description 1
- 230000037396 body weight Effects 0.000 description 1
- 238000002815 broth microdilution Methods 0.000 description 1
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 1
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 1
- 150000004292 cyclic ethers Chemical class 0.000 description 1
- 229960004100 dirithromycin Drugs 0.000 description 1
- WLOHNSSYAXHWNR-NXPDYKKBSA-N dirithromycin Chemical compound O([C@@H]1[C@@H](C)C(=O)O[C@@H]([C@@]([C@H]2O[C@H](COCCOC)N[C@H]([C@@H]2C)[C@H](C)C[C@@](C)(O)[C@H](O[C@H]2[C@@H]([C@H](C[C@@H](C)O2)N(C)C)O)[C@H]1C)(C)O)CC)[C@H]1C[C@@](C)(OC)[C@@H](O)[C@H](C)O1 WLOHNSSYAXHWNR-NXPDYKKBSA-N 0.000 description 1
- 201000010099 disease Diseases 0.000 description 1
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 1
- 239000003814 drug Substances 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 230000008020 evaporation Effects 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- XMBWDFGMSWQBCA-UHFFFAOYSA-N hydrogen iodide Chemical compound I XMBWDFGMSWQBCA-UHFFFAOYSA-N 0.000 description 1
- 229940071870 hydroiodic acid Drugs 0.000 description 1
- 125000001841 imino group Chemical group [H]N=* 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 230000003834 intracellular effect Effects 0.000 description 1
- 239000007927 intramuscular injection Substances 0.000 description 1
- 238000010255 intramuscular injection Methods 0.000 description 1
- 229940099563 lactobionic acid Drugs 0.000 description 1
- 150000007931 macrolactones Chemical class 0.000 description 1
- 229940041033 macrolides Drugs 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 239000002207 metabolite Substances 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- 238000007069 methylation reaction Methods 0.000 description 1
- GRVDJDISBSALJP-UHFFFAOYSA-N methyloxidanyl Chemical group [O]C GRVDJDISBSALJP-UHFFFAOYSA-N 0.000 description 1
- WQEPLUUGTLDZJY-UHFFFAOYSA-N n-Pentadecanoic acid Natural products CCCCCCCCCCCCCCC(O)=O WQEPLUUGTLDZJY-UHFFFAOYSA-N 0.000 description 1
- 230000017066 negative regulation of growth Effects 0.000 description 1
- ODUCDPQEXGNKDN-UHFFFAOYSA-N nitroxyl Chemical compound O=N ODUCDPQEXGNKDN-UHFFFAOYSA-N 0.000 description 1
- 239000012454 non-polar solvent Substances 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 1
- 235000006408 oxalic acid Nutrition 0.000 description 1
- 150000004893 oxazines Chemical class 0.000 description 1
- 238000006146 oximation reaction Methods 0.000 description 1
- FJKROLUGYXJWQN-UHFFFAOYSA-N papa-hydroxy-benzoic acid Natural products OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 1
- 244000052769 pathogen Species 0.000 description 1
- IZJDOKYDEWTZSO-UHFFFAOYSA-N phenethyl isothiocyanate Chemical compound S=C=NCCC1=CC=CC=C1 IZJDOKYDEWTZSO-UHFFFAOYSA-N 0.000 description 1
- 235000019260 propionic acid Nutrition 0.000 description 1
- 229940095574 propionic acid Drugs 0.000 description 1
- IUVKMZGDUIUOCP-BTNSXGMBSA-N quinbolone Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)CC[C@@]21C)C1=CCCC1 IUVKMZGDUIUOCP-BTNSXGMBSA-N 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 230000002829 reductive effect Effects 0.000 description 1
- 229960005224 roxithromycin Drugs 0.000 description 1
- 229960004889 salicylic acid Drugs 0.000 description 1
- 239000000243 solution Substances 0.000 description 1
- 238000006265 spirocyclization reaction Methods 0.000 description 1
- 230000002269 spontaneous effect Effects 0.000 description 1
- 239000008117 stearic acid Substances 0.000 description 1
- 239000007929 subcutaneous injection Substances 0.000 description 1
- 238000010254 subcutaneous injection Methods 0.000 description 1
- DKVBOUDTNWVDEP-NJCHZNEYSA-N teicoplanin aglycone Chemical compound N([C@H](C(N[C@@H](C1=CC(O)=CC(O)=C1C=1C(O)=CC=C2C=1)C(O)=O)=O)[C@H](O)C1=CC=C(C(=C1)Cl)OC=1C=C3C=C(C=1O)OC1=CC=C(C=C1Cl)C[C@H](C(=O)N1)NC([C@H](N)C=4C=C(O5)C(O)=CC=4)=O)C(=O)[C@@H]2NC(=O)[C@@H]3NC(=O)[C@@H]1C1=CC5=CC(O)=C1 DKVBOUDTNWVDEP-NJCHZNEYSA-N 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H17/00—Compounds containing heterocyclic radicals directly attached to hetero atoms of saccharide radicals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H17/00—Compounds containing heterocyclic radicals directly attached to hetero atoms of saccharide radicals
- C07H17/04—Heterocyclic radicals containing only oxygen as ring hetero atoms
- C07H17/08—Hetero rings containing eight or more ring members, e.g. erythromycins
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Molecular Biology (AREA)
- Engineering & Computer Science (AREA)
- Biochemistry (AREA)
- Biotechnology (AREA)
- Genetics & Genomics (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Medicinal Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Oncology (AREA)
- Communicable Diseases (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Epidemiology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Saccharide Compounds (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Plural Heterocyclic Compounds (AREA)
Abstract
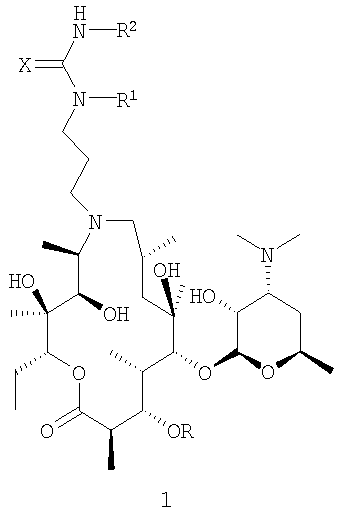
Настоящее изобретение относится к N''-замещенным 9a-N-(N'-карбамоил-γ-аминопропильным) и 9а-N-(N'-тиокарбамоил-γ-аминопропильным) производным 9-дезоксо-9-дигидро-9а-аза-9а-гомоэритромицина А или 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-аза-9а-гомоэритронолида А, новым полусинтетическим макролидным антибиотикам группы азалидов общей формулы 1, приведенной в описании, где R обозначает Н или кладинозильный фрагмент, R1 обозначает Н, R2 обозначает группу изопропил, 1-нафтил, 2-нафтил, бензил, 2-(трифторметил)фенил, 3-фенилпропил, β-фенилэтил, этоксикарбонилметил, 1-(1-нафтил)этил, 3,4,5-триметоксифенил и 2,4-дихлорфенил, и Х обозначает О или S, или к их фармацевтически приемлемым аддитивным солям с неорганическими или органическими кислотами, к способу их получения. Изобретение относится также к фармацевтической композиции, обладающей антибактериальной активностью, а также к применению соединений общей формулы 1 или их фармацевтически приемлемых солей для получения указанной композиции. 4 н. и 12 з.п. ф-лы, 1 табл.
Description
Область техники
Int. Cl. С07Н 17/08, А61К 31/71
Техническая задача
Настоящее изобретение относится к N''-замещенным 9а-N-(N'-карбамоил-γ-аминопропильным) и 9a-N-(N'-тиокарбамоил-γ-аминопропильным) производным 9-дезоксо-9-дигидро-9а-аза-9а-гомоэритромицина А или 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-аза-9а-гомоэритронолида А, новым полусинтетическим макролидным антибиотикам группы азалидов, обладающим противобактериальной активностью, которые имеют общую формулу 1,
где R представляет собой Н или кладинозильный фрагмент, R1 представляет собой Н, R2 представляет собой группу изопропил, 1-нафтил, 2-нафтил, бензил, 2-(трифторметил)фенил, 3-фенилпропил, β-фенилэтил, этоксикарбонилметил, 1-(1-нафтил)этил, 3,4,5-триметоксифенил и 2,4-дихлорфенил, а Х представляет собой О или S, к их фармацевтически приемлемым аддитивным солям с неорганическими или органическими кислотами, к способу получения фармацевтических композиций, а также к применению полученных фармацевтических композиций для лечения бактериальных инфекций.
ПРЕДЫДУЩИЙ УРОВЕНЬ ТЕХНИКИ
Эритромицин А является макролидным антибиотиком, структура которого характеризуется наличием 14-членного макролактонового цикла, содержащего карбонильную группу в положении С-9. Он был обнаружен McGuire в 1952 г. [Antibiot. Chemother., 2 (1952) 281] и в течение 40 лет считался надежным и эффективным противомикробным средством для лечения заболеваний, вызываемых грамположительными и некоторыми грамотрицательными микроорганизмами. Однако в кислой среде он легко превращается в ангидроэритромицин А, неактивный С-6/С-12 метаболит спирокетальной структуры [Р.Kurath et al., Experientia 27 (1971) 362]. Хорошо известно, что спироциклизация агликонового цикла эритромицина А успешно ингибируется химической трансформацией С-9 кетонов или гидроксильных групп в положении С-6 и/или С-12. Путем оксимирования С-9 кетонов [ et al., Tetrahedron Lett. 1967:1945] и последующей модификации полученного 9(Е)-оксима с получением 9-[О-(2-метоксиэтокси)метилоксим]эритромицина A (ROXITHROMYCIN) [G.S. Ambrieres, патент Франции 2473525, 1981], или 9(S)-эритромициламина [R.S. Egan et al., J. Org. Chem. 39 (1974) 2492], или его более сложного оксазинового производного, 9-дезоксо-11-дезокси-9,11-{имино[2-(2-метоксиэтоксиэтилиден]окси}-9(S)-эритромицина A (DIRITHROMYCIN) [P. Lugar et al., J. Crist. Mol. Struct. 9 (1979) 329], были синтезированы новые полусинтетические макролиды, основной характеристикой которых, кроме повышенной стабильности в кислой среде, является улучшенная фармакокинетика и продолжительный период полужизни по сравнению с исходным антибиотиком эритромицином А. В третьем способе модификации С-9 кетонов проводили перегруппировку Бекмана 9(Е)-оксима и восстановление полученного иминоэфира (G. Kobrehel et al., патент США 4328334, 1982) до 11-аза-10-дезоксо-10-дигидроэритромицина А (9-дезоксо-9а-аза-9а-гомоэритромицина А) с расширением кетолактонного цикла до 15-членного азалактонного цикла. Путем восстановительного N-метилирования 9а-аминогруппы по способу Эшвейлера-Кларка (Eschweiler-Clark) (G. Kobrehel et al., патент Бельгии 892397, 1982) или путем предварительной защиты аминогруппы превращением в соответствующие N-оксиды и затем путем алкилирования и восстановления [G.M. Bright, патент США 4474768, 1984] синтезируют N-метил-11-аза-10-дезоксо-10-дигидроэритромицин А (9-дезоксо-9а-метил-9а-аза-9а-гомоэритромицин A, AZITHROMYCIN) был синтезирован прототип азалидных антибиотиков, которые, в добавление к широкому противомикробному спектру действия, включающему в себя грамотрицательные бактерии и внутриклеточные микроорганизмы, характеризуются особым механизмом транспорта к месту применения, продолжительным периодом биологической полужизни и коротким периодом лечения. В ЕР 0316128 A (Bright G.M. et al.) раскрываются новые 9а-аллильные и 9а-пропаргильные производные 9-дезоксо-9а-аза-9а-гомоэритромицина А, а в патенте США №4492688 от 1985 (Bright G.M.) раскрываются синтез и противобактериальная активность соответствующих циклических простых эфиров. В J. Antibiot. 46(1993) 1239-1245 (G. Kobrehel et. al.) раскрываются синтез и спектр активности новых 9а,11-циклических карбаматов 9-дезоксо-9а-аза-11-дезокси-9а-гомоэритромицина А и его O-метильных производных.
В результате взаимодействия 9-дезоксо-9-дигидро-9а-аза-9а-гомоэритромицина А с изоцианатами или изотиоцианатами соответственно [ et al. Croat. Pat. 931480, 1993], получают 9a-N-(N'-карбамоильные) и 9a-N-(N'-тиокарбамоильные) производные 9-дезоксо-9-дигидро-9а-аза-9а-гомоэритромицина А с определенной противобактериальной активностью.
В соответствии с известным и признанным предыдущим уровнем техники, N''-замещенные-9а-N-(N'-карбамоил-γ-аминопропильные) и 9a-N-(N'-тиокарбамоил-γ-аминопропильные) производные 9-дезоксо-9-дигидро-9а-аза-9а-гомоэритромицина А или 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-аза-9а-гомоэритронолида А, их фармацевтически приемлемые аддитивные соли с неорганическими или органическими кислотами, способ их получения, а также способы получения и применение фармацевтических композиций еще не были раскрыты.
Было обнаружено, и это является целью настоящего изобретения, что N''-замещенные 9a-N-(N'-карбамоил-γ-аминопропильные) и 9a-N-(N'-тиокарбамоил-γ-аминопропильные) производные 9-дезоксо-9-дигидро-9а-аза-9а-гомоэритромицина А или 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-аза-9а-гомоэритронолида А, новые полусинтетические макролидные антибиотики группы азалидов, и их фармацевтически приемлемые аддитивные соли с неорганическими или органическими кислотами можно получить в результате взаимодействия 9a-N-(γ-аминопропильных) производных 9-дезоксо-9-дигидро-9а-аза-9а-гомоэритромицина А или 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-аза-9а-гомоэритронолида А с изоцианатами или изотиоцианатами и, необязательно, в результате взаимодействия полученных N''-замещенных 9a-N-(N'-карбамоил-γ-аминопропильных) или 9a-N-(N'-тиокарбамоил-γ-аминопропильных) производных 9-дезоксо-9-дигидро-9а-аза-9а-гомоэритромицина А или 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-аза-9а-гомоэритронолида А с неорганическими или органическими кислотами.
ТЕХНИЧЕСКОЕ РЕШЕНИЕ
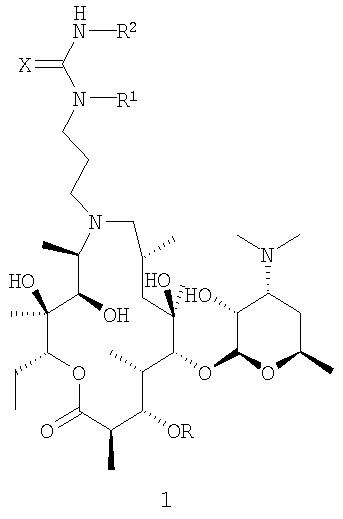
Было обнаружено, что новые N''-замещенные 9a-N-(N'-карбамоил-γ-аминопропильные) и 9a-N-(N'-тиокарбамоил-γ-аминопропильные) производные 9-дезоксо-9-дигидро-9а-аза-9а-гомоэритромицина А или 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-аза-9а-гомоэритронолида А общей формулы 1,
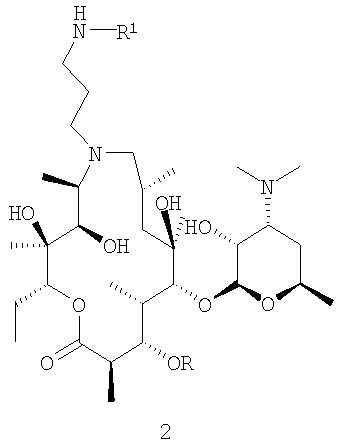
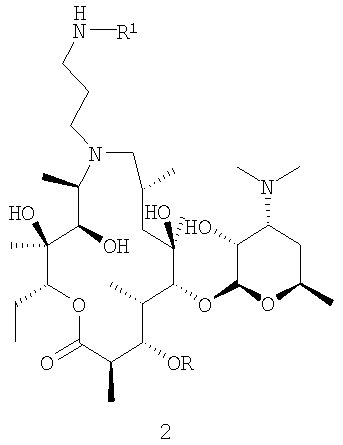
где R представляет собой Н или кладинозильную группу, R1 представляет собой Н, R2 представляет собой группу изопропил, 1-нафтил, 2-нафтил, бензил, 2-(трифторметил)фенил, 3-фенилпропил, β-фенилэтил, этоксикарбонилметил, 1-(1-нафтил)этил, 3,4,5-триметоксифенил и 2,4-дихлорфенил, а Х представляет собой О или S, и их фармацевтически приемлемые аддитивные соли с неорганическими или органическими кислотами, можно получить в результате взаимодействия 9a-N-(γ-аминопропильного) производного 9-дезоксо-9-дигидро-9а-аза-9а-гомоэритромицина A (US 4492668, пример 5; Bright et al. J. Antibiot. (1998) vol XLI, №8 p.1029-1047, пример 15а; и WO 02/055531 пример 1, интермедиат М11, где R4 представляет собой кладинозильную группу) или 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-аза-9а-гомоэритронолида А (WO 02/055531 пример 1, интермедиат М11, где R4 представляет собой гидроксильную группу) общей формулы 2,
где R представляет собой Н или кладинозильную группу и R1 представляет собой Н, с изоцианатами или тиоизоцианатами общей формулы 3,
где R2 и X имеют указанные выше значения, в толуоле, при комнатной температуре.
Фармацевтически приемлемые кислотно-аддитивные соли, которые также являются целью настоящего изобретения, получают в результате взаимодействия N''-замещенных 9a-N-(N'-карбамоил-γ-аминопропильных) или 9a-N-(N'-тиокарбамоил-γ-аминопропильных) производных 9-дезоксо-9-дигидро-9а-аза-9а-гомоэритромицина А или 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-аза-9а-гомоэритронолида А с, по меньшей мере, эквимолярным количеством соответствующей неорганической или органической кислоты, такой как хлористо-водородная кислота, иодисто-водородная кислота, серная кислота, фосфорная кислота, уксусная кислота, трифторуксусная кислота, пропионовая кислота, бензойная кислота, бензолсульфоновая кислота, метансульфоновая кислота, лаурилсульфоновая кислота, стеариновая кислота, пальмитиновая кислота, янтарная кислота, этилянтарная кислота, лактобионовая кислота, щавелевая кислота, салициловая кислота и т.п., в растворителе, инертном по отношению к данной реакции. Аддитивные соли выделяют упариванием растворителя или, альтернативно, фильтрацией после спонтанного осаждения, или осаждением в результате добавления неполярного растворителя.
N''-Замещенные 9a-N-(N'-карбамоил-γ-аминопропильные) и 9a-N-(N'-тиокарбамоил-γ-аминопропильные) производные 9-дезоксо-9-дигидро-9а-аза-9а-гомоэритромицина А и 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-аза-9а-гомоэритронолида А общей формулы 1 или их фармацевтически приемлемые аддитивные соли с неорганическими или органическими кислотами обладают противобактериальной активностью in vitro.
Минимальной ингибирующей концентрацией (MIC) называют концентрацию, которая вызывает 90% ингибирование роста, ее определяют методами бульонного разведения Национального комитета клинических лабораторных стандартов (National Committee for Clinical Laboratory Standards, NCCLS, протоколы М7-А2). Конечная концентрация тестируемых веществ находится в интервале от 64 до 0,125 мг/л. Уровни MIC для всех соединений определяют на ряде чувствительных и устойчивых грамположительных (S. aureus, S. pneumoniae и S. pyogenes) и грамотрицательных бактериальных штаммов (Е. coli, H. influenzae, E. faecalis, M. catarrhalis).
Из таблицы 1 видно, что стандартные штаммы чувствительны к новым соединениям общей формулы 1. Следовательно, их можно использовать в качестве терапевтических средств для лечения инфекционных заболеваний у животных, особенно у млекопитающих и людей, вызываемых широким спектром грамположительных и грамотрицательных бактерий, микоплазмы и большинством патогенных организмов, чувствительных к соединениям формулы 1. С данной целью вышеуказанные соединения и их фармацевтически приемлемые кислотно-аддитивные соли можно вводить перорально, как правило, в дозах от 0,2 мг/кг массы тела в день до приблизительно 250 мг/кг/день, наиболее предпочтительно 0,5-50 мг/кг/день, или парентерально в виде подкожных и внутримышечных инъекций.
Способ получения N''-замещенных 9a-N-(N'-карбамоил-γ-аминопропильных) производных 9-дезоксо-9-дигидро-9а-аза-9а-гомоэритромицина А или 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-аза-9а-гомоэритронолида А данного изобретения иллюстрируется нижеследующими примерами, которые ни в коей мере не должны толковаться как ограничение его объема.
| Таблица 1 | |||||||||||||
| Противобактериальная активность in vitro новых N''-замещенных 9a-N-(N'-карбамоил-γ-аминопропильных) и 9a-N-(N'-тиокарбамоил-γ-аминопропильных) производных 9-дезоксо-9-дигидро-9а-аза-9а-гомоэритромицина А, представленная в виде значений MIC в сравнении с активностью эритромицина А (Er) | |||||||||||||
| Тестируемые организмы | MIK, мкг/мл | ||||||||||||
| Соединение из примера | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12* | Er |
| S. aureus АТСС 13709 | 2 | 0,5 | 0,5 | 2 | 2 | 2 | 1 | 1 | 8 | 16 | 4 | 8 | ≤0,125 |
| S. pneumoniae | ≤0,125 | ≤0,125 | ≤0,125 | ≤0,125 | ≤0,125 | ≤0,125 | ≤0,125 | ≤0,125 | ≤0,125 | 8 | ≤0,125 | 16 | ≤0,125 |
| S. pyogenes | ≤0,125 | ≤0,125 | ≤0,125 | ≤0,125 | ≤0,125 | ≤0,125 | ≤0,125 | ≤0,125 | ≤0,125 | ≤0,125 | ≤0,125 | ≤0,125 | 0,25 |
| S. pyogenes iMLS | 8 | 2 | 4 | 2 | 4 | 8 | 4 | 4 | 16 | 8 | 32 | 2 | >64 |
| S. pyogenes M | 32 | 4 | 8 | 4 | 4 | 32 | 8 | 8 | 64 | 16 | 64 | 8 | 8 |
| M. catarrhalis ATCC 23246 | 0,5 | 0,25 | 1 | 1 | 2 | 8 | 1 | 1 | 4 | 4 | 16 | 0,5 | - |
| H. lnfluenzae ATCC 49247 | 32 | 1 | 2 | 2 | 2 | 16 | 2 | 2 | 32 | 2 | 16 | 2 | 2 |
| E. faecalis ATCC 29212 | 32 | 4 | 16 | 8 | 4 | 64 | 16 | 16 | >64 | 16 | >64 | 8 | 1 |
| E. coli ATCC 25922 | 16 | 8 | 16 | 16 | 8 | 32 | 16 | 32 | >64 | 64 | >64 | 32 | 32 |
Пример 1
9-Дезоксо-9-дигидро-9а-N-(N'-изопропилкарбамоил-γ-аминопропил)-9а-аза-9а-гомоэритромицин А
Смесь 1,0 г (1,26 ммоль) 9-дезоксо-9-дигидро-9а-аза-9а-(γ-аминопропил)-9а-гомоэритромицина A (US 4492668, пример 5; Bright et al. J. Antibiot. (1998) vol XLI, №8 p.1029-1047, пример 15а; и WO 02/055531 пример 1, интермедиат M11, где R4 представляет собой кладинозильную группу) и 0,1 г (1,3 ммоль) изопропилизоцианата в 10 мл сухого толуола перемешивают 30 минут при комнатной температуре до завершения реакции. Кристаллы неочищенного продукта фильтруют, и после хроматографии на колонке с силикагелем с использованием системы растворителей метиленхлорид:метанол:аммиак = 90:9:1,5 получают чистый 9-дезоксо-9-дигидро-9а-N-(N'-изопропилкарбамоил-γ-аминопропил)-9а-аза-9а-гомоэритромицин А.
МС (ES+) m/z: 877.
Пример 2
9-Дезоксо-9-дигидро-9а-N-[N'-(1-нафтил)карбамоил-γ-аминопропил]-9а-аза-9а-гомоэритромицин А
Смесь 1,0 г (1,26 ммоль) 9-дезоксо-9-дигидро-9а-аза-9а-(γ-аминопропил)-9а-гомоэритромицина А и 0,22 г (1,26 ммоль) 1-нафтилизоцианата в 10 мл сухого толуола перемешивают 30 минут при комнатной температуре до завершения реакции. Кристаллы неочищенного продукта фильтруют, и после хроматографии на колонке с силикагелем с использованием системы растворителей метиленхлорид:метанол:аммиак = 90:9:1,5 получают чистый 9-дезоксо-9-дигидро-9а-N-[N'-(1-нафтил)карбамоил-γ-аминопропил]-9а-аза-9а-гомоэритромицин А.
МС (ES+) m/z: 961.
Пример 3
9-Дезоксо-9-дигидро-9а-N-(N'-бензилкарбамоил-γ-аминопропил)-9а-аза-9а-гомоэритромицин А
Смесь 1,0 г (1,26 ммоль) 9-дезоксо-9-дигидро-9а-аза-9а-(γ-аминопропил)-9а-гомоэритромицина А и 0,17 г (1,3 ммоль) бензилизоцианата в 10 мл сухого толуола перемешивают 30 минут при комнатной температуре до завершения реакции. Кристаллы неочищенного продукта фильтруют, и после хроматографии на колонке с силикагелем с использованием системы растворителей метиленхлорид:метанол:аммиак = 90:9:1,5 получают чистый 9-дезоксо-9-дигидро-9а-N-(N'-бензилкарбамоил-γ-аминопропил)-9а-аза-9а-гомоэритромицин А.
МС (ES+) m/z: 925.
Пример 4
9-Дезоксо-9-дигидро-9а-N-(N'-бензилтиокарбамоил-γ-аминопропил)-9а-аза-9а-гомоэритромицин А
Смесь 1,0 г (1,26 ммоль) 9-дезоксо-9-дигидро-9а-аза-9а-(γ-аминопропил)-9а-гомоэритромицина А и 0,17 г (1,3 ммоль) бензилизотиоцианата в 10 мл сухого толуола перемешивают 30 минут при комнатной температуре до завершения реакции. Кристаллы неочищенного продукта фильтруют, и после хроматографии на колонке с силикагелем с использованием системы растворителей метиленхлорид:метанол:аммиак = 90:9:1,5 получают чистый 9-дезоксо-9-дигидро-9а-N-(N'-бензилтиокарбамоил-γ-аминопропил)-9а-аза-9а-гомоэритромицин А.
МС (ES+) m/z: 941.
Пример 5
9-Дезоксо-9-дигидро-9а-N-[N'-(1-нафтил)тиокарбамоил-γ-аминопропил]-9а-аза-9а-гомоэритромицин А
Смесь 1,0 г (1,26 ммоль) 9-дезоксо-9-дигидро-9а-аза-9а-(γ-аминопропил)-9а-гомоэритромицина А и 0,17 г (1,3 ммоль) 1-нафтилизотиоцианата в 10 мл сухого толуола перемешивают 30 минут при комнатной температуре до завершения реакции. Кристаллы неочищенного продукта фильтруют, и после хроматографии на колонке с силикагелем с использованием системы растворителей метиленхлорид:метанол:аммиак = 90:9:1,5 получают чистый 9-дезоксо-9-дигидро-9а-N-[N'-(1-нафтил)тиокарбамоил-γ-аминопропил]-9а-аза-9а-гомоэритромицин А.
МС (ES+) m/z: 977.
Пример 6
9-Дезоксо-9-дигидро-9а-N-[N'-(2-трифторметил)фенилкарбамоил-γ-аминопропил]-9а-аза-9а-гомоэритромицин А
Смесь 1,0 г (1,26 ммоль) 9-дезоксо-9-дигидро-9а-аза-9а-(γ-аминопропил)-9а-гомоэритромицина А и 0,24 г (1,3 ммоль) 2-(трифторметил)фенилизоцианата в 10 мл сухого толуола перемешивают 30 минут при комнатной температуре до завершения реакции. Кристаллы неочищенного продукта фильтруют, и после хроматографии на колонке с силикагелем с использованием системы растворителей метиленхлорид:метанол:аммиак = 90:9:1,5 получают чистый 9-дезоксо-9-дигидро-9а-N-[N'-(2-трифторметилфенил)карбамоил-γ-аминопропил]-9а-аза-9а-гомоэритромицин А.
МС (ES+) m/z: 979.
Пример 7
9-Дезоксо-9-дигидро-9а-N-[N'-(3-фенилпропил)тиокарбамоил-γ-аминопропил]-9а-аза-9а-гомоэритромицин А
Смесь 1,0 г (1,26 ммоль) 9-дезоксо-9-дигидро-9а-аза-9а-(γ-аминопропил)-9а-гомоэритромицина А и 0,22 г (1,3 ммоль) 3-фенилпропилизотиоцианата в 10 мл сухого толуола перемешивают 30 минут при комнатной температуре до завершения реакции. Кристаллы неочищенного продукта фильтруют, и после хроматографии на колонке с силикагелем с использованием системы растворителей метиленхлорид:метанол:аммиак = 90:9:1,5 получают чистый 9-дезоксо-9-дигидро-9а-N-[N'-(3-фенилпропил)тиокарбамоил-γ-аминопропил]-9а-аза-9а-гомоэритромицин А.
МС (ES+) m/z: 969.
Пример 8
9-Дезоксо-9-дигидро-9а-N-[N'-(β-фенилэтил)карбамоил-γ-аминопропил]-9а-аза-9а-гомоэритромицин А
Смесь 1,0 г (1,26 ммоль) 9-дезоксо-9-дигидро-9а-аза-9а-(γ-аминопропил)-9а-гомоэритромицина А и 0,21 г (1,3 ммоль) β-фенилэтилизоцианата в 10 мл сухого толуола перемешивают 30 минут при комнатной температуре до завершения реакции. Кристаллы неочищенного продукта фильтруют, и после хроматографии на колонке с силикагелем с использованием системы растворителей метиленхлорид:метанол:аммиак = 90:9:1,5 получают чистый 9-дезоксо-9-дигидро-9а-N-[N'-(β-фенилэтил)карбамоил-γ-аминопропил]-9а-аза-9а-гомоэритромицин А.
МС (ES+) m/z: 979.
Пример 9
9-Дезоксо-9-дигидро-9а-N-(N'-этоксикарбонилметилкарбамоил-γ-аминопропил)-9а-аза-9а-гомоэритромицин А
Смесь 1,0 г (1,26 ммоль) 9-дезоксо-9-дигидро-9а-аза-9а-(γ-аминопропил)-9а-гомоэритромицина А и 0,16 г (1,3 ммоль) этоксикарбонилметилизоцианата в 10 мл сухого толуола перемешивают 30 минут при комнатной температуре до завершения реакции. Кристаллы неочищенного продукта фильтруют, и после хроматографии на колонке с силикагелем с использованием системы растворителей метиленхлорид:метанол:аммиак = 90:9:1,5 получают чистый 9-дезоксо-9-дигидро-9а-N-(N'-этоксикарбонилметилкарбамоил-γ-аминопропил)-9а-аза-9а-гомоэритромицин А.
МС (ES+) m/z: 921.
Пример 10
9-Дезоксо-9-дигидро-9а-N-{N'-[1-(1-нафтил)этил]карбамоил-γ-аминопропил}-9а-аза-9а-гомоэритромицин А
Смесь 1,0 г (1,26 ммоль) 9-дезоксо-9-дигидро-9а-аза-9а-(γ-аминопропил)-9а-гомоэритромицина А и 0,25 г (1,3 ммоль) 1-(1-нафтил)этилизоцианата в 10 мл сухого толуола перемешивают 30 минут при комнатной температуре до завершения реакции. Кристаллы неочищенного продукта фильтруют, и после хроматографии на колонке с силикагелем с использованием системы растворителей метиленхлорид:метанол:аммиак = 90:9:1,5 получают чистый 9-дезоксо-9-дигидро-9а-N-{N'-[1-(1-нафтил)этил]карбамоил-γ-аминопропил}-9а-аза-9а-гомоэритромицин А.
МС (ES+) m/z: 989.
Пример 11
9-Дезоксо-9-дигидро-9а-N-[N'-(3,4,5-триметоксифенил)карбамоил-γ-аминопропил]-9а-аза-9а-гомоэритромицин А
Смесь 1,0 г (1,26 ммоль) 9-дезоксо-9-дигидро-9а-аза-9а-(γ-аминопропил)-9а-гомоэритромицина А и 0,26 г (1,3 ммоль) 3,4,5-триметоксифенилизоцианат в 10 мл сухого толуола перемешивают 30 минут при комнатной температуре до завершения реакции. Кристаллы неочищенного продукта фильтруют, и после хроматографии на колонке с силикагелем с использованием системы растворителей метиленхлорид:метанол:аммиак = 90:9:1,5 получают чистый 9-дезоксо-9-дигидро-9а-N-[N'-(3,4,5-триметоксифенил)карбамоил-γ-аминопропил]-9а-аза-9а-гомоэритромицин А.
МС (ES+) m/z: 1001.
Пример 12
9-Дезоксо-9-дигидро-9а-N-[N'-(2-нафтил)карбамоил-γ-аминопропил]-9а-аза-9а-гомоэритромицин А
Смесь 1,0 г (1,26 ммоль) 9-дезоксо-9-дигидро-9а-аза-9а-(γ-аминопропил)-9а-гомоэритромицина А и 0,23 г (1,3 ммоль) 2-нафтилизоцианата в 10 мл сухого толуола перемешивают 30 минут при комнатной температуре до завершения реакции. Кристаллы неочищенного продукта фильтруют, и после хроматографии на колонке с силикагелем с использованием системы растворителей метиленхлорид:метанол:аммиак = 90:9:1,5 получают чистый 9-дезоксо-9-дигидро-9а-N-[N'-(2-нафтил)карбамоил-γ-аминопропил]-9а-аза-9а-гомоэритромицин А.
МС (ES+) m/z: 961.
Пример 13
9-Дезоксо-9-дигидро-9а-N-[N'-(2,4-дихлорфенил)карбамоил-γ-аминопропил]-9а-аза-9а-гомоэритромицин А
Смесь 1,0 г (1,26 ммоль) 9-дезоксо-9-дигидро-9а-аза-9а-(γ-аминопропил)-9а-гомоэритромицина А и 0,23 г (1,3 ммоль) 2,4-дихлорфенилизоцианата в 10 мл сухого толуола перемешивают 30 минут при комнатной температуре до завершения реакции. Кристаллы неочищенного продукта фильтруют, и после хроматографии на колонке с силикагелем с использованием системы растворителей метиленхлорид:метанол:аммиак = 90:9:1,5 получают чистый 9-дезоксо-9-дигидро-9а-N-[N'-(2,4-дихлорфенил)карбамоил-γ-аминопропил]-9а-аза-9а-гомоэритромицин А.
МС (ES+) m/z: 979.
Пример 14
5-O-Дезозаминил-9-дезоксо-9-дигидро-9а-N-(N'-изопропилкарбамоил-γ-аминопропил)-9а-аза-9а-гомоэритронолид А
Смесь 1,0 г (1,57 ммоль) 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-N-(γ-аминопропил)-9а-аза-гомоэритронолида A (WO 02/055531 пример 1, интермедиат М11, где R4 представляет собой гидроксильную группу) и 0,13 г (1,57 ммоль) изопропилизоцианата в 10 мл сухого толуола перемешивают 30 минут при комнатной температуре до завершения реакции. Кристаллы неочищенного продукта фильтруют, и после хроматографии на колонке с силикагелем с использованием системы растворителей метиленхлорид:метанол:аммиак = 90:20:1,5 получают чистый 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-N-(N'-изопропилкарбамоил-γ-аминопропил)-9а-аза-9а-гомоэритронолид А.
МС (ES+) m/z: 719.
Пример 15
5-O-Дезозаминил-9-дезоксо-9-дигидро-9а-N-[N'-(1-нафтил)карбамоил-γ-аминопропил]-9а-аза-9а-гомоэритронолид А
Смесь 1,0 г (1,57 ммоль) 5-О-дезозаминил-9-дезоксо-9-дигидро-9а-N-(γ-аминопропил)-9а-аза-гомоэритронолида А и 0,13 г (1,57 ммоль) 1-нафтилизоцианата в 10 мл сухого толуола перемешивают 30 минут при комнатной температуре до завершения реакции. Кристаллы неочищенного продукта фильтруют, и после хроматографии на колонке с силикагелем с использованием системы растворителей метиленхлорид:метанол:аммиак = 90:20:1,5 получают чистый 5-О-дезозаминил-9-дезоксо-9-дигидро-9а-N-[N'-(1-нафтил)карбамоил-γ-аминопропил]-9а-аза-9а-гомоэритронолид А.
МС (ES+) m/z: 803.
Пример 16
5-O-Дезозаминил-9-дезоксо-9-дигидро-9а-N-(N'-бензилкарбамоил-γ-аминопропил)-9а-аза-9а-гомоэритронолид А
Смесь 1,0 г (1,57 ммоль) 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-N-(γ-аминопропил)-9а-аза-гомоэритронолида А и 0,21 г (1,57 ммоль) бензилизоцианата в 10 мл сухого толуола перемешивают 30 минут при комнатной температуре до завершения реакции. Кристаллы неочищенного продукта фильтруют, и после хроматографии на колонке с силикагелем с использованием системы растворителей метиленхлорид:метанол:аммиак = 90:20:1,5 получают чистый 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-N-(N'-бензилкарбамоил-γ-аминопропил)-9а-аза-9а-гомоэритронолид А.
МС (ES+) m/z: 767.
Пример 17
5-O-Дезозаминил-9-дезоксо-9-дигидро-9а-N-(N'-бензилтиокарбамоил-γ-аминопропил)-9а-аза-9а-гомоэритронолид А
Смесь 1,0 г (1,57 ммоль) 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-N-(γ-аминопропил)-9а-аза-гомоэритронолида А и 0,24 г (1,57 ммоль) бензилизотиоцианата в 10 мл сухого толуола перемешивают 30 минут при комнатной температуре до завершения реакции. Кристаллы неочищенного продукта фильтруют, и после хроматографии на колонке с силикагелем с использованием системы растворителей метиленхлорид:метанол:аммиак = 90:20:1,5 получают чистый 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-N-(N'-бензилтиокарбамоил-γ-аминопропил)-9а-аза-9а-гомоэритронолид А.
МС (ES+) m/z: 783.
Пример 18
5-O-Дезозаминил-9-дезоксо-9-дигидро-9а-N-[N'-(1-нафтил)тиокарбамоил-γ-аминопропил]-9а-аза-9а-гомоэритронолид А
Смесь 1,0 г (1,57 ммоль) 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-N-(γ-аминопропил)-9а-аза-гомоэритронолида А и 0,29 г (1,57 ммоль) 1-нафтилизотиоцианата в 10 мл сухого толуола перемешивают 30 минут при комнатной температуре до завершения реакции. Кристаллы неочищенного продукта фильтруют, и после хроматографии на колонке с силикагелем с использованием системы растворителей метиленхлорид:метанол:аммиак = 90:20:1,5 получают чистый 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-N-[N'-(1-нафтил)тиокарбамоил-γ-аминопропил]-9а-аза-9а-гомоэритронолид А.
МС (ES+) m/z: 819.
Пример 19
5-O-Дезозаминил-9-дезоксо-9-дигидро-9а-N-[N'-(2-(трифторметил)фенилкарбамоил)-γ-аминопропил]-9а-аза-9а-гомоэритронолид А
Смесь 1,0 г (1,57 ммоль) 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-N-(γ-аминопропил)-9а-аза-гомоэритронолида А и 0,30 г (1,57 ммоль) 2-(трифторметил)фенилизоцианата в 10 мл сухого толуола перемешивают 30 минут при комнатной температуре до завершения реакции. Кристаллы неочищенного продукта фильтруют, и после хроматографии на колонке с силикагелем с использованием системы растворителей метиленхлорид:метанол:аммиак = 90:20:1,5 получают чистый 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-N-[N'-(2-(трифторметил)фенилкарбамоил)-γ-аминопропил]-9а-аза-9а-гомоэритронолид А.
МС (ES+) m/z: 821.
Пример 20
5-O-Дезозаминил-9-дезоксо-9-дигидро-9а-N-[N'-(3-фенилпропил)тиокарбамоил-γ-аминопропил]-9а-аза-9а-гомоэритронолид А
Смесь 1,0 г (1,57 ммоль) 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-N-(γ-аминопропил)-9а-аза-гомоэритронолида А и 0,28 г (1,57 ммоль) 3-фенилпропилизотиоцианата в 10 мл сухого толуола перемешивают 30 минут при комнатной температуре до завершения реакции. Кристаллы неочищенного продукта фильтруют, и после хроматографии на колонке с силикагелем с использованием системы растворителей метиленхлорид:метанол:аммиак = 90:20:1,5 получают чистый 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-N-[N'-(3-фенилпропил)тиокарбамоил-γ-аминопропил]-9а-аза-9а-гомоэритронолид А.
МС (ES+) m/z: 811.
Пример 21
5-O-Дезозаминил-9-дезоксо-9-дигидро-9а-N-[N'-(β-фенилэтил)тиокарбамоил-γ-аминопропил]-9а-аза-9а-гомоэритронолид А
Смесь 1,0 г (1,57 ммоль) 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-N-(γ-аминопропил)-9а-аза-гомоэритронолида А и 0,26 г (1,57 ммоль) β-фенилэтилизотиоцианата в 10 мл сухого толуола перемешивают 30 минут при комнатной температуре до завершения реакции. Кристаллы неочищенного продукта фильтруют, и после хроматографии на колонке с силикагелем с использованием системы растворителей метиленхлорид:метанол:аммиак = 90:20:1,5 получают чистый 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-N-[N'-(β-фенилэтил)тиокарбамоил-γ-аминопропил]-9а-аза-9а-гомоэритронолид А.
MC (ES+) m/z: 797.
Пример 22
5-O-Дезозаминил-9-дезоксо-9-дигидро-9а-N-(N'-этоксикарбонилметилкарбамоил-γ-аминопропил)-9а-аза-9а-гомоэритронолид А
Смесь 1,0 г (1/57 ммоль) 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-N-(γ-аминопропил)-9а-аза-гомоэритронолида А и 0,20 г (1,57 ммоль) этоксикарбонилметилизоцианата в 10 мл сухого толуола перемешивают 30 минут при комнатной температуре до завершения реакции. Кристаллы неочищенного продукта фильтруют, и после хроматографии на колонке с силикагелем с использованием системы растворителей метиленхлорид:метанол:аммиак = 90:20:1,5 получают чистый 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-N-(N'-этоксикарбонилметилкарбамоил-γ-аминопропил)-9а-аза-9а-гомоэритронолид А.
MC (ES+) m/z: 763.
Пример 23
5-O-Дезозаминил-9-дезоксо-9-дигидро-9а-N-[N'-(2-нафтил)карбамоил-γ-аминопропил]-9а-аза-9а-гомоэритронолид А
Смесь 1,0 г (1,57 ммоль) 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-N-(γ-аминопропил)-9а-аза-гомоэритронолида и 0,27 г (1,57 ммоль) 2-нафтилизоцианата в 10 мл сухого толуола перемешивают 30 минут при комнатной температуре до завершения реакции. Кристаллы неочищенного продукта фильтруют, и после хроматографии на колонке с силикагелем с использованием системы растворителей метиленхлорид:метанол:аммиак = 90:20:1,5 получают чистый 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-N-[N'-(2-нафтил)карбамоил-γ-аминопропил]-9а-аза-9а-гомоэритронолид А.
МС (ES+) m/z: 803.
Пример 24
5-O-Дезозаминил-9-дезоксо-9-дигидро-9а-N-{N'-[1-(1-нафтил)этил]карбамоил-γ-аминопропил}-9а-аза-9а-гомоэритронолид А
Смесь 1,0 г (1,57 ммоль) 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-N-(γ-аминопропил)-9а-аза-гомоэритронолида А и 0,31 г (1,57 ммоль) 1-(1-нафтил)этилизоцианата в 10 мл сухого толуола перемешивают 30 минут при комнатной температуре до завершения реакции. Кристаллы неочищенного продукта фильтруют, и после хроматографии на колонке с силикагелем с использованием системы растворителей метиленхлорид:метанол:аммиак = 90:20:1,5 получают чистый 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-N-{N'-[1-(1-нафтил)этил]карбамоил-γ-аминопропил}-9а-аза-9а-гомоэритронолид А.
МС (ES+) m/z: 831.
Пример 25
5-O-Дезозаминил-9-дезоксо-9-дигидро-9а-N-[N'-(3,4,5-триметоксифенил)карбамоил-γ-аминопропил]-9а-аза-9а-гомоэритронолид А
Смесь 1,0 г (1,57 ммоль) 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-N-(γ-аминопропил)-9а-аза-гомоэритронолида А и 0,31 г (1,57 ммоль) 3,4,5-триметоксифенилизоцианата в 10 мл сухого толуола перемешивают 30 минут при комнатной температуре до завершения реакции. Кристаллы неочищенного продукта фильтруют, и после хроматографии на колонке с силикагелем с использованием системы растворителей метиленхлорид:метанол:аммиак = 90:20:1,5 получают чистый 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-N-[N'-(3,4,5-триметоксифенил)карбамоил-γ-аминопропил]-9а-аза-9а-гомоэритронолид А.
МС (ES+) m/z: 843.
Пример 26
5-O-Дезозаминил-9-дезоксо-9-дигидро-9а-N-[N'-(2,4-дихлорфенил)карбамоил-γ-аминопропил]-9а-аза-9а-гомоэритронолид А
Смесь 1,0 г (1,57 ммоль) 5-O-дезозаминил-9-дезоксо-9-дигидро-9a-N-(γ-аминопропил)-9а-аза-гомоэритронолида А и 0,31 г (1,57 ммоль) 2,4-дихлорфенилизоцианата в 10 мл сухого толуола перемешивают 30 минут при комнатной температуре до завершения реакции. Кристаллы неочищенного продукта фильтруют, и после хроматографии на колонке с силикагелем с использованием системы растворителей метиленхлорид:метанол:аммиак = 90:20:1,5 получают чистый 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-N-[N'-(3,4,5-триметоксифенил)карбамоил-γ-аминопропил]-9а-аза-9а-гомоэритронолид А.
МС (ES+) m/z: 821.
Claims (16)
1. Вещество общей формулы 1
где R представляет собой Н или кладинозильный фрагмент,
R1 представляет собой Н,
R2 представляет собой изопропильную, 1-нафтильную, 2-нафтильную, бензильную, 2-(трифторметил)фенильную, 3-фенилпропильную, β-фенилэтильную, этоксикарбонилметильную, 1-(1-нафтил)этильную, 3,4,5-триметоксифенильную или 2,4-дихлорфенильную группу,
Х представляет собой О или S,
или их фармацевтически приемлемые аддитивные соли с неорганическими или органическими кислотами.
2. Вещество по п.1, отличающееся тем, что R1 представляет собой Н, R2 представляет собой изопропильную группу, и Х представляет собой О.
3. Вещество по п.1, отличающееся тем, что R1 представляет собой Н, R2 представляет собой 1-нафтильную группу, и Х представляет собой О.
4. Вещество по п.1, отличающееся тем, что R1 представляет собой Н, R2 представляет собой 2-нафтильную группу, и Х представляет собой О.
5. Вещество по п.1, отличающееся тем, что R1 представляет собой Н, R2 представляет собой бензильную группу, и Х представляет собой О.
6. Вещество по п.1, отличающееся тем, что R1 представляет собой Н, R2 представляет собой 2-(трифторметил)фенильную группу, и Х представляет собой О.
7. Вещество по п.1, отличающееся тем, что R1 представляет собой Н, R2 представляет собой 3-фенилпропильную группу, и Х представляет собой S.
8. Вещество по п.1, отличающееся тем, что R1 представляет собой Н, R2 представляет собой β-фенилэтильную группу, и Х представляет собой S.
9. Вещество по п.1, отличающееся тем, что R1 представляет собой Н, R2 представляет собой этоксикарбонилметильную группу, и Х представляет собой О.
10. Вещество по п.1, отличающееся тем, что R1 представляет собой Н, R2 представляет собой 1-(1-нафтил)этильную группу, и Х представляет собой О.
11. Вещество по п.1, отличающееся тем, что R1 представляет собой Н, R2 представляет собой 3,4,5-триметоксифенильную группу, и Х представляет собой О.
12. Вещество по п.1, отличающееся тем, что R1 представляет собой Н, R2 представляет собой 2,4-дихлорфенильную группу, и Х представляет собой О.
13. Вещество по п.1, отличающееся тем, что R1 представляет собой Н, R2 представляет собой бензильную группу или 1-нафтильную группу, и Х представляет собой S.
14. Способ получения вещества общей формулы 1 по п.1, отличающийся тем, что производное 9-дезоксо-9-дигидро-9а-аза-9а-гомоэритромицина А или 5-O-дезозаминил-9-дезоксо-9-дигидро-9а-аза-9а-гомоэритронолида А общей формулы 2
где R представляет собой Н или кладинозильную группу, и
R1 представляет собой Н,
подвергают взаимодействию с изоцианатами или тиоизоцианатами общей формулы 3
где R2 и Х имеют значения как определено в п.1,
в толуоле при комнатной температуре, и затем, при необходимости, полученный продукт подвергают взаимодействию с неорганической или органической кислотой с образованием соответствующей фармацевтически приемлемой соли.
15. Фармацевтическая композиция, обладающая антибактериальной активностью, содержащая фармацевтически приемлемый носитель и эффективное количество вещества по п.1.
16. Применение вещества общей формулы 1 или его фармацевтически приемлемых солей по п.1 при получении фармацевтической композиции по п.15.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| HRP20020991A | 2002-12-12 | ||
| HR20020991A HRP20020991A2 (en) | 2002-12-12 | 2002-12-12 | N"-Substituted 9a-N-(N'-carbamoyl-Gamma-aminopropyl), 9a-N-(N'? -thiocarbamoyl-Gamma-aminopropyl), 9a-N-(N'-((Beta-cyanoethyl)-N'-carbamoyl-Gamma? -aminopropyl) and 9a-N-(N'-(Beta-cyanoethyl)-N'-thiocarbamoyl-Gamma? -aminopropyl) derivatives of 9-de |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2005121892A RU2005121892A (ru) | 2006-01-20 |
| RU2328503C2 true RU2328503C2 (ru) | 2008-07-10 |
Family
ID=32500425
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2005121892/04A RU2328503C2 (ru) | 2002-12-12 | 2003-12-10 | N''-ЗАМЕЩЕННЫЕ 9a-N-(N'-КАРБАМОИЛ-ГАММА-АМИНОПРОПИЛЬНЫЕ) И 9a-N-(N'-ТИОКАРБАМОИЛ-ГАММА-АМИНОПРОПИЛЬНЫЕ), ПРОИЗВОДНЫЕ 9-ДЕЗОКСО-9-ДИГИДРО-9a-АЗА-9a-ГОМОЭРИТРОМИЦИНА A И 5-O-ДЕЗОЗАМИНИЛ-9-ДЕЗОКСО-9-ДИГИДРО-9a-АЗА-9a-ГОМОЭРИТРОНОЛИДА A |
Country Status (24)
| Country | Link |
|---|---|
| US (1) | US7342000B2 (ru) |
| EP (1) | EP1585753B1 (ru) |
| JP (1) | JP2006510660A (ru) |
| KR (1) | KR20050085555A (ru) |
| CN (1) | CN100335489C (ru) |
| AR (1) | AR042351A1 (ru) |
| AT (1) | ATE327999T1 (ru) |
| AU (1) | AU2003285599A1 (ru) |
| BR (1) | BR0316569A (ru) |
| CA (1) | CA2509599A1 (ru) |
| CL (1) | CL2003002585A1 (ru) |
| CO (1) | CO5640139A2 (ru) |
| CY (1) | CY1106321T1 (ru) |
| DE (1) | DE60305741T2 (ru) |
| DK (1) | DK1585753T3 (ru) |
| ES (1) | ES2266883T3 (ru) |
| HR (1) | HRP20020991A2 (ru) |
| IS (1) | IS2309B (ru) |
| MX (1) | MXPA05006220A (ru) |
| PL (1) | PL377322A1 (ru) |
| PT (1) | PT1585753E (ru) |
| RS (1) | RS80204A (ru) |
| RU (1) | RU2328503C2 (ru) |
| WO (1) | WO2004052904A2 (ru) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| HRP20020885B1 (en) | 2002-11-11 | 2007-05-31 | GlaxoSmithKline istra�iva�ki centar Zagreb d.o.o. | SUBSTITUTED 9a-N-{N'-[4-(SULFONYL)PHENYLCARBAMOYL]}DERIVATIVES 9-DEOXO-9-DIHYDRO-9a-AZA-9a-HOMOERITHROMYCIN A AND 5-O-DESOZAMINYL-9-DEOXO-9-DIHYDRO-9a-AZA-9a-HOMOERITHRONOLIDE A |
| US20080200404A1 (en) * | 2005-01-14 | 2008-08-21 | Mirjana Bukvic Krajacic | Novel Antimalarial 9A-Carbamoyl-Aminoalkyl and 9A-Thiocarbamoyl-Aminoalkyl Azalides |
| JP2008526947A (ja) * | 2005-01-14 | 2008-07-24 | グラクソスミスクライン・イストラジヴァッキ・センタル・ザグレブ・ドルズバ・ゼー・オメイェノ・オドゴヴォルノスティオ | 抗マラリア活性を有する9a−カルバモイル−γ−アミノプロピル−および9a−チオカルバモイル−γ−アミノプロピル−アザリド |
| WO2007125414A2 (en) * | 2006-05-03 | 2007-11-08 | Glaxosmithkline Istrazivacki Centar Zagreb D.O.O. | 9a-substituted azalides for the tratment of malaria |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4492688A (en) * | 1983-11-25 | 1985-01-08 | Pfizer Inc. | Antibacterial cyclic ethers of 9-deoxo-9a-aza-9a-homoerythromycin A and intermediates therefor |
| EP0132944A1 (en) * | 1983-06-30 | 1985-02-13 | Pfizer Inc. | Antibacterial homoerythromycin A derivatives and intermediates therefor |
| SU1272996A3 (ru) * | 1982-11-15 | 1986-11-23 | Пфайзер Инк.(Фирма) | Способ получени 4 @ -эпи-9-дезоксо-9 а-метил-9а-аза-9а-гомоэритромицина А |
| RU2131878C1 (ru) * | 1993-12-08 | 1999-06-20 | Плива Фармацойтска, Кемийска, Прехрамбена и Козметичка Индустрия, Дионичко Друштво | 9а-n-(n'-карбамоил)- или 9а-n-(n'-тиокарбамоил) производные 9-деоксо-9а-аза-9а-гомоэритромицина а, способ их получения и фармацевтическая композиция на их основе |
| RU98123827A (ru) * | 1997-12-31 | 2000-10-10 | Плива Фармацойтска, Кемийска, Прехрамбена и Козметичка Индустрия, Дионичко Друштво | β,β-ДИЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ 9-ДЕЗОКСО-9А-N-ЭТЕНИЛ-9А-АЗА-9А-ГОМОЭРИТРОМИЦИНА А |
| WO2002068438A3 (en) * | 2001-02-28 | 2004-02-26 | Pliva D D | 9a-n-[n'-(phenylsulfonyl)carbamoyl] derivatives of 9-deoxo-9-dihydro-9a-aza-9a-homoerythromycin a and of 5-0-desosaminyl-9-deoxo-9-dihydro-9a-aza-9a-homoerythronolide a |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| YU43116B (en) * | 1979-04-02 | 1989-04-30 | Pliva Pharm & Chem Works | Process for preparing 11-aza-4-o-cladinosyl-6-o-desosaminyl-15-ethyl-7,13,14-trihydroxy-3,5,7,9,12,14-hexamethyl-oxacyclopentadecane-2-one(11-aza-10-deox |
| FR2473525A1 (fr) | 1980-01-11 | 1981-07-17 | Roussel Uclaf | Nouvelles oximes derivees de l'erythromycine, leur procede de preparation et leur application comme medicaments |
| BE892397A (nl) | 1982-03-08 | 1982-07-01 | Marchand Paul | Wereldwijde draadloze telefonie voor 10 miljard abonnees |
| US4474768A (en) * | 1982-07-19 | 1984-10-02 | Pfizer Inc. | N-Methyl 11-aza-10-deoxo-10-dihydro-erytromycin A, intermediates therefor |
| MX13723A (es) | 1987-11-10 | 1993-05-01 | Pfizer | Procedimiento para preparar derivados de 9-desoxo-9a-alil- y propargil-9a-aza-9a-homoeritromicina a |
| WO1997035590A1 (en) * | 1996-03-25 | 1997-10-02 | Platt Chris E | 10-aza-9-deoxo-11-deoxy-erythromycin a and derivatives combined with sulfisoxazole |
| HRP970714B1 (en) * | 1997-12-31 | 2003-08-31 | Pliva Pharm & Chem Works | Beta,beta-disubstituted derivatives of 9-deoxo-9a-n-ethenyl-9a-aza-9a-homoerythromycin a |
| HRP990130B1 (en) * | 1999-05-03 | 2004-06-30 | Pliva D D | HALOGEN DERIVATIVES 9a-N-(N'-ARYLCARBAMOYL)- AND 9a-N-(N'-ARYLTHIOCARBAMOYL)-9-DEOXO-9a-AZA-9a OF HOMOERYTHROMYCIN A |
| US20040077557A1 (en) * | 2000-12-21 | 2004-04-22 | Sulejman Ali | Macrolide antibiotics |
| HRP20020886A2 (en) | 2002-11-11 | 2005-06-30 | PLIVA-ISTRAŽIVAČKI INSTITUT d.o.o. | SUBSTITUTED 9a-N-[N'-(BENZENSULFONYL)CARBAMOYL-γ-AMINOPROPYL) AND 9a-N(N' -(?-CYANOETHIL)-N' -(b |
| HRP20020885B1 (en) | 2002-11-11 | 2007-05-31 | GlaxoSmithKline istra�iva�ki centar Zagreb d.o.o. | SUBSTITUTED 9a-N-{N'-[4-(SULFONYL)PHENYLCARBAMOYL]}DERIVATIVES 9-DEOXO-9-DIHYDRO-9a-AZA-9a-HOMOERITHROMYCIN A AND 5-O-DESOZAMINYL-9-DEOXO-9-DIHYDRO-9a-AZA-9a-HOMOERITHRONOLIDE A |
-
2002
- 2002-12-12 HR HR20020991A patent/HRP20020991A2/hr not_active Application Discontinuation
-
2003
- 2003-12-10 JP JP2004558858A patent/JP2006510660A/ja active Pending
- 2003-12-10 PL PL377322A patent/PL377322A1/pl unknown
- 2003-12-10 AT AT03778598T patent/ATE327999T1/de not_active IP Right Cessation
- 2003-12-10 MX MXPA05006220A patent/MXPA05006220A/es active IP Right Grant
- 2003-12-10 EP EP03778598A patent/EP1585753B1/en not_active Expired - Lifetime
- 2003-12-10 US US10/538,376 patent/US7342000B2/en not_active Expired - Fee Related
- 2003-12-10 KR KR1020057010623A patent/KR20050085555A/ko not_active Withdrawn
- 2003-12-10 DK DK03778598T patent/DK1585753T3/da active
- 2003-12-10 RS YU80204A patent/RS80204A/sr unknown
- 2003-12-10 WO PCT/HR2003/000062 patent/WO2004052904A2/en not_active Ceased
- 2003-12-10 AU AU2003285599A patent/AU2003285599A1/en not_active Abandoned
- 2003-12-10 CA CA002509599A patent/CA2509599A1/en not_active Abandoned
- 2003-12-10 AR ARP030104537A patent/AR042351A1/es not_active Application Discontinuation
- 2003-12-10 PT PT03778598T patent/PT1585753E/pt unknown
- 2003-12-10 DE DE60305741T patent/DE60305741T2/de not_active Expired - Fee Related
- 2003-12-10 RU RU2005121892/04A patent/RU2328503C2/ru not_active IP Right Cessation
- 2003-12-10 ES ES03778598T patent/ES2266883T3/es not_active Expired - Lifetime
- 2003-12-10 BR BR0316569-8A patent/BR0316569A/pt not_active IP Right Cessation
- 2003-12-10 CN CNB2003801057628A patent/CN100335489C/zh not_active Expired - Fee Related
- 2003-12-11 CL CL200302585A patent/CL2003002585A1/es unknown
-
2005
- 2005-05-31 IS IS7875A patent/IS2309B/is unknown
- 2005-07-08 CO CO05067476A patent/CO5640139A2/es not_active Application Discontinuation
-
2006
- 2006-08-25 CY CY20061101203T patent/CY1106321T1/el unknown
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SU1272996A3 (ru) * | 1982-11-15 | 1986-11-23 | Пфайзер Инк.(Фирма) | Способ получени 4 @ -эпи-9-дезоксо-9 а-метил-9а-аза-9а-гомоэритромицина А |
| EP0132944A1 (en) * | 1983-06-30 | 1985-02-13 | Pfizer Inc. | Antibacterial homoerythromycin A derivatives and intermediates therefor |
| US4492688A (en) * | 1983-11-25 | 1985-01-08 | Pfizer Inc. | Antibacterial cyclic ethers of 9-deoxo-9a-aza-9a-homoerythromycin A and intermediates therefor |
| RU2131878C1 (ru) * | 1993-12-08 | 1999-06-20 | Плива Фармацойтска, Кемийска, Прехрамбена и Козметичка Индустрия, Дионичко Друштво | 9а-n-(n'-карбамоил)- или 9а-n-(n'-тиокарбамоил) производные 9-деоксо-9а-аза-9а-гомоэритромицина а, способ их получения и фармацевтическая композиция на их основе |
| RU98123827A (ru) * | 1997-12-31 | 2000-10-10 | Плива Фармацойтска, Кемийска, Прехрамбена и Козметичка Индустрия, Дионичко Друштво | β,β-ДИЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ 9-ДЕЗОКСО-9А-N-ЭТЕНИЛ-9А-АЗА-9А-ГОМОЭРИТРОМИЦИНА А |
| WO2002068438A3 (en) * | 2001-02-28 | 2004-02-26 | Pliva D D | 9a-n-[n'-(phenylsulfonyl)carbamoyl] derivatives of 9-deoxo-9-dihydro-9a-aza-9a-homoerythromycin a and of 5-0-desosaminyl-9-deoxo-9-dihydro-9a-aza-9a-homoerythronolide a |
Also Published As
| Publication number | Publication date |
|---|---|
| HK1086273A1 (en) | 2006-09-15 |
| US7342000B2 (en) | 2008-03-11 |
| KR20050085555A (ko) | 2005-08-29 |
| PT1585753E (pt) | 2006-08-31 |
| IS7875A (is) | 2005-05-31 |
| ATE327999T1 (de) | 2006-06-15 |
| DE60305741D1 (de) | 2006-07-06 |
| CO5640139A2 (es) | 2006-05-31 |
| RU2005121892A (ru) | 2006-01-20 |
| AU2003285599A8 (en) | 2004-06-30 |
| WO2004052904A2 (en) | 2004-06-24 |
| ES2266883T3 (es) | 2007-03-01 |
| CN100335489C (zh) | 2007-09-05 |
| CY1106321T1 (el) | 2011-10-12 |
| US20060252709A1 (en) | 2006-11-09 |
| EP1585753B1 (en) | 2006-05-31 |
| CN1726222A (zh) | 2006-01-25 |
| AR042351A1 (es) | 2005-06-15 |
| MXPA05006220A (es) | 2005-11-17 |
| EP1585753A2 (en) | 2005-10-19 |
| DE60305741T2 (de) | 2007-06-14 |
| BR0316569A (pt) | 2005-10-04 |
| CL2003002585A1 (es) | 2005-01-28 |
| IS2309B (is) | 2007-10-15 |
| HRP20020991A2 (en) | 2005-02-28 |
| JP2006510660A (ja) | 2006-03-30 |
| CA2509599A1 (en) | 2004-06-24 |
| PL377322A1 (pl) | 2006-01-23 |
| DK1585753T3 (da) | 2006-10-02 |
| WO2004052904A3 (en) | 2004-09-02 |
| RS80204A (sr) | 2006-12-15 |
| AU2003285599A1 (en) | 2004-06-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| SK279075B6 (sk) | O-metylderiváty azitromycínu a a ich medziprodukt, | |
| EP0657464B1 (en) | 9a-N-(N'-Carbamoyl) and 9a-N-(N'-Thiocarbamoyl) derivatives of 9-deoxo-9a-aza-9a-homoerythromycin A | |
| SK5522000A3 (en) | 3,6-hemiketals from the class of 9a-azalides | |
| EP1414835B1 (en) | 9a-n-[n'-(phenylsulfonyl)carbamoyl] derivatives of 9-deoxo-9-dihydro-9a-aza-9a-homoerythromycin a and of 5-o-desosaminyl-9-deoxo-9-dihydro-9a-aza-9a-homoerythronolide a | |
| RU2328503C2 (ru) | N''-ЗАМЕЩЕННЫЕ 9a-N-(N'-КАРБАМОИЛ-ГАММА-АМИНОПРОПИЛЬНЫЕ) И 9a-N-(N'-ТИОКАРБАМОИЛ-ГАММА-АМИНОПРОПИЛЬНЫЕ), ПРОИЗВОДНЫЕ 9-ДЕЗОКСО-9-ДИГИДРО-9a-АЗА-9a-ГОМОЭРИТРОМИЦИНА A И 5-O-ДЕЗОЗАМИНИЛ-9-ДЕЗОКСО-9-ДИГИДРО-9a-АЗА-9a-ГОМОЭРИТРОНОЛИДА A | |
| RU2170739C2 (ru) | 9-n-этенильные производные 9(s)-эритромициламина и способ их получения | |
| EP1575969B1 (en) | SUBSTITUTED 9a-N-(N'- 4-(SULFONYL)PHENYL CARBAMOYL) DERIVATIVES OF 9-DEOXO-9-DIHYDRO-9a-AZA-9a-HOMOERITHROMYCIN A AND 5-0-DESOSAMINYL-9-DEOXO-9-DI-HYDRO-9A-AZA-9A-HOMOERITHRONOLIDE A | |
| US20070270356A1 (en) | Substituted 9A-N-[N'-(Benzenesulfonyl)Carbamoyl-Y-Aminopropyl] and 9A-N-[N'(B-Cyanoethyl)-N'-(Benzenesulfonyl)Carbamoyl-Y-Aminopropyl]Derivatives of 9-Deoxo-9-Dihydro-9A-Aza-9A-Homoerithomycin A |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20081211 |