RU2316554C2 - Производные индолина, используемые как ингибиторы протеинкиназы - Google Patents
Производные индолина, используемые как ингибиторы протеинкиназы Download PDFInfo
- Publication number
- RU2316554C2 RU2316554C2 RU2004122918/04A RU2004122918A RU2316554C2 RU 2316554 C2 RU2316554 C2 RU 2316554C2 RU 2004122918/04 A RU2004122918/04 A RU 2004122918/04A RU 2004122918 A RU2004122918 A RU 2004122918A RU 2316554 C2 RU2316554 C2 RU 2316554C2
- Authority
- RU
- Russia
- Prior art keywords
- formula
- group
- compound according
- compound
- pharmaceutically acceptable
- Prior art date
Links
- 125000003387 indolinyl group Chemical class N1(CCC2=CC=CC=C12)* 0.000 title abstract 2
- 229940045988 antineoplastic drug protein kinase inhibitors Drugs 0.000 title 1
- 239000003909 protein kinase inhibitor Substances 0.000 title 1
- 150000001875 compounds Chemical class 0.000 claims abstract description 142
- 150000003839 salts Chemical class 0.000 claims abstract description 32
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims abstract description 30
- 238000000034 method Methods 0.000 claims abstract description 27
- 239000008194 pharmaceutical composition Substances 0.000 claims abstract description 21
- 102000004278 Receptor Protein-Tyrosine Kinases Human genes 0.000 claims abstract description 19
- 108090000873 Receptor Protein-Tyrosine Kinases Proteins 0.000 claims abstract description 19
- 125000003386 piperidinyl group Chemical group 0.000 claims abstract description 18
- 229910052757 nitrogen Inorganic materials 0.000 claims abstract description 13
- 239000003814 drug Substances 0.000 claims abstract description 11
- 125000004433 nitrogen atom Chemical group N* 0.000 claims abstract description 11
- 125000004482 piperidin-4-yl group Chemical group N1CCC(CC1)* 0.000 claims abstract description 6
- 125000002529 biphenylenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3C12)* 0.000 claims abstract description 4
- 125000004956 cyclohexylene group Chemical group 0.000 claims abstract description 4
- 125000000843 phenylene group Chemical group C1(=C(C=CC=C1)*)* 0.000 claims abstract description 4
- 125000000217 alkyl group Chemical group 0.000 claims description 23
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 21
- -1 piperidinyl— 4-yl Chemical group 0.000 claims description 18
- 125000001424 substituent group Chemical group 0.000 claims description 16
- 125000006239 protecting group Chemical group 0.000 claims description 10
- 229910052739 hydrogen Inorganic materials 0.000 claims description 9
- 239000001257 hydrogen Substances 0.000 claims description 8
- 229940121358 tyrosine kinase inhibitor Drugs 0.000 claims description 8
- 239000005483 tyrosine kinase inhibitor Substances 0.000 claims description 8
- 229940079593 drug Drugs 0.000 claims description 7
- KVIAIJLTPHXNEB-UHFFFAOYSA-N 3-[[3,5-dimethyl-4-(3-oxo-3-piperazin-1-ylpropyl)-1h-pyrrol-2-yl]methylidene]-1h-indol-2-one Chemical compound CC=1NC(C=C2C3=CC=CC=C3NC2=O)=C(C)C=1CCC(=O)N1CCNCC1 KVIAIJLTPHXNEB-UHFFFAOYSA-N 0.000 claims description 6
- 125000002947 alkylene group Chemical group 0.000 claims description 6
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 claims description 6
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 claims description 6
- 150000004917 tyrosine kinase inhibitor derivatives Chemical class 0.000 claims description 6
- 230000002401 inhibitory effect Effects 0.000 claims description 5
- 238000004519 manufacturing process Methods 0.000 claims description 5
- GVNVAWHJIKLAGL-UHFFFAOYSA-N 2-(cyclohexen-1-yl)cyclohexan-1-one Chemical compound O=C1CCCCC1C1=CCCCC1 GVNVAWHJIKLAGL-UHFFFAOYSA-N 0.000 claims description 4
- 101150065749 Churc1 gene Proteins 0.000 claims description 4
- 102100038239 Protein Churchill Human genes 0.000 claims description 4
- 230000005764 inhibitory process Effects 0.000 claims description 4
- QQONPFPTGQHPMA-UHFFFAOYSA-N propylene Natural products CC=C QQONPFPTGQHPMA-UHFFFAOYSA-N 0.000 claims description 4
- 125000004805 propylene group Chemical group [H]C([H])([H])C([H])([*:1])C([H])([H])[*:2] 0.000 claims description 4
- 239000003085 diluting agent Substances 0.000 claims description 3
- 125000004193 piperazinyl group Chemical group 0.000 claims description 3
- 125000001140 1,4-phenylene group Chemical group [H]C1=C([H])C([*:2])=C([H])C([H])=C1[*:1] 0.000 claims description 2
- UCIAJIBDPDKOAD-UHFFFAOYSA-N 3-[[4-[3-(1,4-diazepan-1-yl)-3-oxopropyl]-3,5-dimethyl-1h-pyrrol-2-yl]methylidene]-1h-indol-2-one Chemical compound CC=1NC(C=C2C3=CC=CC=C3NC2=O)=C(C)C=1CCC(=O)N1CCCNCC1 UCIAJIBDPDKOAD-UHFFFAOYSA-N 0.000 claims description 2
- 238000010511 deprotection reaction Methods 0.000 claims description 2
- 150000002475 indoles Chemical class 0.000 claims 1
- 230000000694 effects Effects 0.000 abstract description 11
- 238000003786 synthesis reaction Methods 0.000 abstract description 3
- 230000015572 biosynthetic process Effects 0.000 abstract description 2
- 239000000126 substance Substances 0.000 abstract description 2
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 abstract 3
- 239000000543 intermediate Substances 0.000 description 30
- 239000000203 mixture Substances 0.000 description 28
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 27
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 25
- 210000004027 cell Anatomy 0.000 description 19
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 18
- 239000007787 solid Substances 0.000 description 18
- 239000000243 solution Substances 0.000 description 16
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 15
- 101100335081 Mus musculus Flt3 gene Proteins 0.000 description 15
- 102000005789 Vascular Endothelial Growth Factors Human genes 0.000 description 13
- 108010019530 Vascular Endothelial Growth Factors Proteins 0.000 description 13
- 238000000655 nuclear magnetic resonance spectrum Methods 0.000 description 13
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 13
- 101000692455 Homo sapiens Platelet-derived growth factor receptor beta Proteins 0.000 description 12
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 12
- 108010073929 Vascular Endothelial Growth Factor A Proteins 0.000 description 12
- 239000003112 inhibitor Substances 0.000 description 12
- 239000011541 reaction mixture Substances 0.000 description 12
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 11
- 102100026547 Platelet-derived growth factor receptor beta Human genes 0.000 description 10
- DTQVDTLACAAQTR-UHFFFAOYSA-M Trifluoroacetate Chemical compound [O-]C(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-M 0.000 description 10
- 239000002253 acid Substances 0.000 description 10
- 238000003828 vacuum filtration Methods 0.000 description 10
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 9
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 9
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 9
- 239000002775 capsule Substances 0.000 description 9
- 239000000706 filtrate Substances 0.000 description 9
- 238000012360 testing method Methods 0.000 description 9
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 8
- 201000010099 disease Diseases 0.000 description 8
- 102000005962 receptors Human genes 0.000 description 8
- 108020003175 receptors Proteins 0.000 description 8
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 7
- 230000035578 autophosphorylation Effects 0.000 description 7
- 239000007903 gelatin capsule Substances 0.000 description 7
- 239000003102 growth factor Substances 0.000 description 7
- 239000005457 ice water Substances 0.000 description 7
- FPIRBHDGWMWJEP-UHFFFAOYSA-N 1-hydroxy-7-azabenzotriazole Chemical compound C1=CN=C2N(O)N=NC2=C1 FPIRBHDGWMWJEP-UHFFFAOYSA-N 0.000 description 6
- KAESVJOAVNADME-UHFFFAOYSA-N 1H-pyrrole Natural products C=1C=CNC=1 KAESVJOAVNADME-UHFFFAOYSA-N 0.000 description 6
- 208000031261 Acute myeloid leukaemia Diseases 0.000 description 6
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 6
- 238000004458 analytical method Methods 0.000 description 6
- 239000004615 ingredient Substances 0.000 description 6
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 6
- 125000000168 pyrrolyl group Chemical group 0.000 description 6
- 238000003756 stirring Methods 0.000 description 6
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 5
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 5
- 238000003556 assay Methods 0.000 description 5
- 239000000872 buffer Substances 0.000 description 5
- 238000006243 chemical reaction Methods 0.000 description 5
- JYGFTBXVXVMTGB-UHFFFAOYSA-N indolin-2-one Chemical class C1=CC=C2NC(=O)CC2=C1 JYGFTBXVXVMTGB-UHFFFAOYSA-N 0.000 description 5
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 5
- 239000003826 tablet Substances 0.000 description 5
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 4
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 4
- 208000033776 Myeloid Acute Leukemia Diseases 0.000 description 4
- 102000016971 Proto-Oncogene Proteins c-kit Human genes 0.000 description 4
- 108010014608 Proto-Oncogene Proteins c-kit Proteins 0.000 description 4
- 125000003545 alkoxy group Chemical group 0.000 description 4
- 125000005843 halogen group Chemical group 0.000 description 4
- 238000001114 immunoprecipitation Methods 0.000 description 4
- XHXFXVLFKHQFAL-UHFFFAOYSA-N phosphoryl trichloride Chemical compound ClP(Cl)(Cl)=O XHXFXVLFKHQFAL-UHFFFAOYSA-N 0.000 description 4
- 238000002360 preparation method Methods 0.000 description 4
- 230000002829 reductive effect Effects 0.000 description 4
- WUWDLXZGHZSWQZ-WQLSENKSSA-N semaxanib Chemical compound N1C(C)=CC(C)=C1\C=C/1C2=CC=CC=C2NC\1=O WUWDLXZGHZSWQZ-WQLSENKSSA-N 0.000 description 4
- WSLDOOZREJYCGB-UHFFFAOYSA-N 1,2-Dichloroethane Chemical compound ClCCCl WSLDOOZREJYCGB-UHFFFAOYSA-N 0.000 description 3
- NHFDRBXTEDBWCZ-ZROIWOOFSA-N 3-[2,4-dimethyl-5-[(z)-(2-oxo-1h-indol-3-ylidene)methyl]-1h-pyrrol-3-yl]propanoic acid Chemical compound OC(=O)CCC1=C(C)NC(\C=C/2C3=CC=CC=C3NC\2=O)=C1C NHFDRBXTEDBWCZ-ZROIWOOFSA-N 0.000 description 3
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 3
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 3
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 3
- FFQBUJQSKAMRMH-UHFFFAOYSA-N FC(C(=O)O)(F)F.CC1=C(NC(=C1CCC(N1CCNCC1)=O)C)C=C1C(NC2=CC=CC=C12)=O Chemical compound FC(C(=O)O)(F)F.CC1=C(NC(=C1CCC(N1CCNCC1)=O)C)C=C1C(NC2=CC=CC=C12)=O FFQBUJQSKAMRMH-UHFFFAOYSA-N 0.000 description 3
- OZLGRUXZXMRXGP-UHFFFAOYSA-N Fluo-3 Chemical compound CC1=CC=C(N(CC(O)=O)CC(O)=O)C(OCCOC=2C(=CC=C(C=2)C2=C3C=C(Cl)C(=O)C=C3OC3=CC(O)=C(Cl)C=C32)N(CC(O)=O)CC(O)=O)=C1 OZLGRUXZXMRXGP-UHFFFAOYSA-N 0.000 description 3
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 3
- 229910004373 HOAc Inorganic materials 0.000 description 3
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 3
- 241000124008 Mammalia Species 0.000 description 3
- 229920000168 Microcrystalline cellulose Polymers 0.000 description 3
- 206010028980 Neoplasm Diseases 0.000 description 3
- 239000008156 Ringer's lactate solution Substances 0.000 description 3
- 229920002472 Starch Polymers 0.000 description 3
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 3
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 3
- 239000003153 chemical reaction reagent Substances 0.000 description 3
- 239000008121 dextrose Substances 0.000 description 3
- 150000002431 hydrogen Chemical group 0.000 description 3
- 230000003834 intracellular effect Effects 0.000 description 3
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 3
- 229940043355 kinase inhibitor Drugs 0.000 description 3
- 235000019359 magnesium stearate Nutrition 0.000 description 3
- 229940016286 microcrystalline cellulose Drugs 0.000 description 3
- 235000019813 microcrystalline cellulose Nutrition 0.000 description 3
- 239000008108 microcrystalline cellulose Substances 0.000 description 3
- 239000003921 oil Substances 0.000 description 3
- 239000003757 phosphotransferase inhibitor Substances 0.000 description 3
- 229920001223 polyethylene glycol Polymers 0.000 description 3
- 239000000843 powder Substances 0.000 description 3
- 230000002062 proliferating effect Effects 0.000 description 3
- 230000035755 proliferation Effects 0.000 description 3
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 3
- 239000011780 sodium chloride Substances 0.000 description 3
- 239000002904 solvent Substances 0.000 description 3
- 235000019698 starch Nutrition 0.000 description 3
- 239000008107 starch Substances 0.000 description 3
- 239000000725 suspension Substances 0.000 description 3
- 230000035899 viability Effects 0.000 description 3
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 description 2
- PAYRUJLWNCNPSJ-UHFFFAOYSA-N Aniline Chemical compound NC1=CC=CC=C1 PAYRUJLWNCNPSJ-UHFFFAOYSA-N 0.000 description 2
- COVZYZSDYWQREU-UHFFFAOYSA-N Busulfan Chemical compound CS(=O)(=O)OCCCCOS(C)(=O)=O COVZYZSDYWQREU-UHFFFAOYSA-N 0.000 description 2
- YXHKONLOYHBTNS-UHFFFAOYSA-N Diazomethane Chemical compound C=[N+]=[N-] YXHKONLOYHBTNS-UHFFFAOYSA-N 0.000 description 2
- 239000001828 Gelatine Substances 0.000 description 2
- 239000007821 HATU Substances 0.000 description 2
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 2
- OFOBLEOULBTSOW-UHFFFAOYSA-N Malonic acid Chemical compound OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 2
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 2
- GLUUGHFHXGJENI-UHFFFAOYSA-N Piperazine Chemical compound C1CNCCN1 GLUUGHFHXGJENI-UHFFFAOYSA-N 0.000 description 2
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 2
- 239000002202 Polyethylene glycol Substances 0.000 description 2
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 2
- 241000700159 Rattus Species 0.000 description 2
- 229940124639 Selective inhibitor Drugs 0.000 description 2
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical compound [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 description 2
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 2
- 238000010521 absorption reaction Methods 0.000 description 2
- 150000007513 acids Chemical class 0.000 description 2
- 239000004480 active ingredient Substances 0.000 description 2
- 125000002252 acyl group Chemical group 0.000 description 2
- 150000001412 amines Chemical class 0.000 description 2
- 239000007864 aqueous solution Substances 0.000 description 2
- 239000008280 blood Substances 0.000 description 2
- 210000004369 blood Anatomy 0.000 description 2
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 2
- 229910052794 bromium Inorganic materials 0.000 description 2
- 201000011510 cancer Diseases 0.000 description 2
- 238000001816 cooling Methods 0.000 description 2
- 239000012043 crude product Substances 0.000 description 2
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 2
- 239000002552 dosage form Substances 0.000 description 2
- 239000003937 drug carrier Substances 0.000 description 2
- 230000003511 endothelial effect Effects 0.000 description 2
- 238000001914 filtration Methods 0.000 description 2
- 229920000159 gelatin Polymers 0.000 description 2
- 235000019322 gelatine Nutrition 0.000 description 2
- 239000008187 granular material Substances 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 230000003993 interaction Effects 0.000 description 2
- 238000001990 intravenous administration Methods 0.000 description 2
- 238000010253 intravenous injection Methods 0.000 description 2
- 239000008101 lactose Substances 0.000 description 2
- 230000000670 limiting effect Effects 0.000 description 2
- 239000011159 matrix material Substances 0.000 description 2
- 125000001570 methylene group Chemical group [H]C([H])([*:1])[*:2] 0.000 description 2
- VMGAPWLDMVPYIA-HIDZBRGKSA-N n'-amino-n-iminomethanimidamide Chemical compound N\N=C\N=N VMGAPWLDMVPYIA-HIDZBRGKSA-N 0.000 description 2
- 230000003287 optical effect Effects 0.000 description 2
- 239000003960 organic solvent Substances 0.000 description 2
- 239000000546 pharmaceutical excipient Substances 0.000 description 2
- RLOWWWKZYUNIDI-UHFFFAOYSA-N phosphinic chloride Chemical compound ClP=O RLOWWWKZYUNIDI-UHFFFAOYSA-N 0.000 description 2
- 230000036470 plasma concentration Effects 0.000 description 2
- 238000012545 processing Methods 0.000 description 2
- 239000000047 product Substances 0.000 description 2
- QLNJFJADRCOGBJ-UHFFFAOYSA-N propionamide Chemical compound CCC(N)=O QLNJFJADRCOGBJ-UHFFFAOYSA-N 0.000 description 2
- 229940080818 propionamide Drugs 0.000 description 2
- 238000004007 reversed phase HPLC Methods 0.000 description 2
- 125000000383 tetramethylene group Chemical group [H]C([H])([*:1])C([H])([H])C([H])([H])C([H])([H])[*:2] 0.000 description 2
- QWQSYWFMIZZQPF-UHFFFAOYSA-N 1-(2-carboxyethyl)-2,4-dimethylpyrrole-3-carboxylic acid Chemical compound CC1=CN(CCC(O)=O)C(C)=C1C(O)=O QWQSYWFMIZZQPF-UHFFFAOYSA-N 0.000 description 1
- AZUYLZMQTIKGSC-UHFFFAOYSA-N 1-[6-[4-(5-chloro-6-methyl-1H-indazol-4-yl)-5-methyl-3-(1-methylindazol-5-yl)pyrazol-1-yl]-2-azaspiro[3.3]heptan-2-yl]prop-2-en-1-one Chemical compound ClC=1C(=C2C=NNC2=CC=1C)C=1C(=NN(C=1C)C1CC2(CN(C2)C(C=C)=O)C1)C=1C=C2C=NN(C2=CC=1)C AZUYLZMQTIKGSC-UHFFFAOYSA-N 0.000 description 1
- JHFAEUICJHBVHB-UHFFFAOYSA-N 1h-indol-2-ol Chemical compound C1=CC=C2NC(O)=CC2=C1 JHFAEUICJHBVHB-UHFFFAOYSA-N 0.000 description 1
- NGNBDVOYPDDBFK-UHFFFAOYSA-N 2-[2,4-di(pentan-2-yl)phenoxy]acetyl chloride Chemical compound CCCC(C)C1=CC=C(OCC(Cl)=O)C(C(C)CCC)=C1 NGNBDVOYPDDBFK-UHFFFAOYSA-N 0.000 description 1
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 1
- UHTQHHLSGVOGQR-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-4-ium-1-yl]ethanesulfonate Chemical compound OCCN1CCN(CCS(O)(=O)=O)CC1.OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 UHTQHHLSGVOGQR-UHFFFAOYSA-N 0.000 description 1
- SAGABBLUUSFKNW-UHFFFAOYSA-N 3-(2,4-dimethyl-1h-pyrrol-3-yl)propanoic acid Chemical compound CC1=CNC(C)=C1CCC(O)=O SAGABBLUUSFKNW-UHFFFAOYSA-N 0.000 description 1
- NLLSXQZFJKZXKL-UHFFFAOYSA-N 3-(2,4-dimethylpyrrol-1-yl)propanoic acid Chemical compound CC=1C=C(C)N(CCC(O)=O)C=1 NLLSXQZFJKZXKL-UHFFFAOYSA-N 0.000 description 1
- DUSIQYJZIANKDG-UHFFFAOYSA-N 3-(3-formyl-2,4-dimethylpyrrol-1-yl)propanoic acid Chemical compound CC1=CN(CCC(O)=O)C(C)=C1C=O DUSIQYJZIANKDG-UHFFFAOYSA-N 0.000 description 1
- RUILENPFHDHTRC-UHFFFAOYSA-N 3-(5-formyl-2,4-dimethyl-1h-pyrrol-3-yl)propanoic acid Chemical compound CC=1NC(C=O)=C(C)C=1CCC(O)=O RUILENPFHDHTRC-UHFFFAOYSA-N 0.000 description 1
- HFFCKKXPNMELRI-UHFFFAOYSA-N 3-[1-(2-carboxyethyl)-2,4-dimethylpyrrol-3-yl]propanoic acid Chemical compound CC1=CN(CCC(O)=O)C(C)=C1CCC(O)=O HFFCKKXPNMELRI-UHFFFAOYSA-N 0.000 description 1
- ZWODWHYQPZMBPT-UHFFFAOYSA-N 3-[2,4-dimethyl-5-[(2-oxo-1,3-dihydroindol-3-yl)methyl]-1h-pyrrol-3-yl]propanoic acid Chemical compound OC(=O)CCC1=C(C)NC(CC2C3=CC=CC=C3NC2=O)=C1C ZWODWHYQPZMBPT-UHFFFAOYSA-N 0.000 description 1
- WYLMTLWFCFZPRI-UHFFFAOYSA-N 3-[4-(2-carboxyethenyl)-3,5-dimethyl-1h-pyrrol-2-yl]propanoic acid Chemical compound CC=1NC(CCC(O)=O)=C(C)C=1C=CC(O)=O WYLMTLWFCFZPRI-UHFFFAOYSA-N 0.000 description 1
- MCSXGCZMEPXKIW-UHFFFAOYSA-N 3-hydroxy-4-[(4-methyl-2-nitrophenyl)diazenyl]-N-(3-nitrophenyl)naphthalene-2-carboxamide Chemical compound Cc1ccc(N=Nc2c(O)c(cc3ccccc23)C(=O)Nc2cccc(c2)[N+]([O-])=O)c(c1)[N+]([O-])=O MCSXGCZMEPXKIW-UHFFFAOYSA-N 0.000 description 1
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 1
- 235000011437 Amygdalus communis Nutrition 0.000 description 1
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 1
- 208000003174 Brain Neoplasms Diseases 0.000 description 1
- 206010006187 Breast cancer Diseases 0.000 description 1
- 208000026310 Breast neoplasm Diseases 0.000 description 1
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 1
- 229920000858 Cyclodextrin Polymers 0.000 description 1
- VGGSQFUCUMXWEO-UHFFFAOYSA-N Ethene Chemical group C=C VGGSQFUCUMXWEO-UHFFFAOYSA-N 0.000 description 1
- 239000005977 Ethylene Chemical group 0.000 description 1
- PIICEJLVQHRZGT-UHFFFAOYSA-N Ethylenediamine Chemical compound NCCN PIICEJLVQHRZGT-UHFFFAOYSA-N 0.000 description 1
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 1
- 206010017993 Gastrointestinal neoplasms Diseases 0.000 description 1
- 239000007995 HEPES buffer Substances 0.000 description 1
- 239000004705 High-molecular-weight polyethylene Substances 0.000 description 1
- 101100519721 Homo sapiens PDGFRB gene Proteins 0.000 description 1
- 101001052849 Homo sapiens Tyrosine-protein kinase Fer Proteins 0.000 description 1
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 description 1
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- 108091008606 PDGF receptors Proteins 0.000 description 1
- 108010038512 Platelet-Derived Growth Factor Proteins 0.000 description 1
- 102000010780 Platelet-Derived Growth Factor Human genes 0.000 description 1
- 102000011653 Platelet-Derived Growth Factor Receptors Human genes 0.000 description 1
- 239000004698 Polyethylene Substances 0.000 description 1
- 206010060862 Prostate cancer Diseases 0.000 description 1
- 208000000236 Prostatic Neoplasms Diseases 0.000 description 1
- 102000001253 Protein Kinase Human genes 0.000 description 1
- 102000004022 Protein-Tyrosine Kinases Human genes 0.000 description 1
- 108090000412 Protein-Tyrosine Kinases Proteins 0.000 description 1
- 241000220304 Prunus dulcis Species 0.000 description 1
- 206010041067 Small cell lung cancer Diseases 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- 101710120037 Toxin CcdB Proteins 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- 102100024537 Tyrosine-protein kinase Fer Human genes 0.000 description 1
- 229960000583 acetic acid Drugs 0.000 description 1
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 239000008186 active pharmaceutical agent Substances 0.000 description 1
- 125000004442 acylamino group Chemical group 0.000 description 1
- 238000005904 alkaline hydrolysis reaction Methods 0.000 description 1
- 125000004453 alkoxycarbonyl group Chemical group 0.000 description 1
- 235000020224 almond Nutrition 0.000 description 1
- 238000010640 amide synthesis reaction Methods 0.000 description 1
- 150000001408 amides Chemical group 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 230000003078 antioxidant effect Effects 0.000 description 1
- 125000003118 aryl group Chemical group 0.000 description 1
- 125000005101 aryl methoxy carbonyl group Chemical group 0.000 description 1
- 125000005002 aryl methyl group Chemical group 0.000 description 1
- 239000012298 atmosphere Substances 0.000 description 1
- 238000000889 atomisation Methods 0.000 description 1
- 235000010233 benzoic acid Nutrition 0.000 description 1
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid group Chemical group C(C1=CC=CC=C1)(=O)O WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 1
- 150000001559 benzoic acids Chemical class 0.000 description 1
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 1
- 125000001584 benzyloxycarbonyl group Chemical group C(=O)(OCC1=CC=CC=C1)* 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 230000037396 body weight Effects 0.000 description 1
- 229940098773 bovine serum albumin Drugs 0.000 description 1
- 125000001246 bromo group Chemical group Br* 0.000 description 1
- 239000007963 capsule composition Substances 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 210000000170 cell membrane Anatomy 0.000 description 1
- 230000003833 cell viability Effects 0.000 description 1
- 239000002738 chelating agent Substances 0.000 description 1
- BJDCWCLMFKKGEE-CMDXXVQNSA-N chembl252518 Chemical compound C([C@@](OO1)(C)O2)C[C@H]3[C@H](C)CC[C@@H]4[C@@]31[C@@H]2O[C@H](O)[C@@H]4C BJDCWCLMFKKGEE-CMDXXVQNSA-N 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 239000000460 chlorine Substances 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- 125000001309 chloro group Chemical group Cl* 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid group Chemical group C(CC(O)(C(=O)O)CC(=O)O)(=O)O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 229940125898 compound 5 Drugs 0.000 description 1
- 238000013270 controlled release Methods 0.000 description 1
- 239000006184 cosolvent Substances 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- 238000002784 cytotoxicity assay Methods 0.000 description 1
- 231100000263 cytotoxicity test Toxicity 0.000 description 1
- 238000006114 decarboxylation reaction Methods 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 239000008355 dextrose injection Substances 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 238000004821 distillation Methods 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 239000008298 dragée Substances 0.000 description 1
- 238000012377 drug delivery Methods 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 239000008157 edible vegetable oil Substances 0.000 description 1
- 239000003480 eluent Substances 0.000 description 1
- 210000002308 embryonic cell Anatomy 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 238000005538 encapsulation Methods 0.000 description 1
- 210000002919 epithelial cell Anatomy 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 239000000284 extract Substances 0.000 description 1
- 239000007850 fluorescent dye Substances 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 125000001153 fluoro group Chemical group F* 0.000 description 1
- PTCGDEVVHUXTMP-UHFFFAOYSA-N flutolanil Chemical compound CC(C)OC1=CC=CC(NC(=O)C=2C(=CC=CC=2)C(F)(F)F)=C1 PTCGDEVVHUXTMP-UHFFFAOYSA-N 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 239000000499 gel Substances 0.000 description 1
- 239000012362 glacial acetic acid Substances 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 239000001963 growth medium Substances 0.000 description 1
- 229940093915 gynecological organic acid Drugs 0.000 description 1
- 150000004820 halides Chemical class 0.000 description 1
- 229910052736 halogen Inorganic materials 0.000 description 1
- 150000002367 halogens Chemical class 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- 230000007062 hydrolysis Effects 0.000 description 1
- 238000006460 hydrolysis reaction Methods 0.000 description 1
- 230000002209 hydrophobic effect Effects 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 230000004941 influx Effects 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 239000000644 isotonic solution Substances 0.000 description 1
- 210000003734 kidney Anatomy 0.000 description 1
- 238000002372 labelling Methods 0.000 description 1
- 239000003446 ligand Substances 0.000 description 1
- 125000005647 linker group Chemical group 0.000 description 1
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 1
- 239000006194 liquid suspension Substances 0.000 description 1
- 238000011068 loading method Methods 0.000 description 1
- 239000006166 lysate Substances 0.000 description 1
- 239000012139 lysis buffer Substances 0.000 description 1
- 150000002689 maleic acids Chemical class 0.000 description 1
- 150000002691 malonic acids Chemical class 0.000 description 1
- 238000001819 mass spectrum Methods 0.000 description 1
- 238000013160 medical therapy Methods 0.000 description 1
- 239000002609 medium Substances 0.000 description 1
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 1
- 150000007522 mineralic acids Chemical class 0.000 description 1
- 125000004573 morpholin-4-yl group Chemical group N1(CCOCC1)* 0.000 description 1
- 230000035772 mutation Effects 0.000 description 1
- 229940080553 normosol-m Drugs 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 229910052763 palladium Inorganic materials 0.000 description 1
- UYWQUFXKFGHYNT-UHFFFAOYSA-N phenylmethyl ester of formic acid Natural products O=COCC1=CC=CC=C1 UYWQUFXKFGHYNT-UHFFFAOYSA-N 0.000 description 1
- DCWXELXMIBXGTH-QMMMGPOBSA-N phosphonotyrosine Chemical group OC(=O)[C@@H](N)CC1=CC=C(OP(O)(O)=O)C=C1 DCWXELXMIBXGTH-QMMMGPOBSA-N 0.000 description 1
- 230000026731 phosphorylation Effects 0.000 description 1
- 238000006366 phosphorylation reaction Methods 0.000 description 1
- DCWXELXMIBXGTH-UHFFFAOYSA-N phosphotyrosine Chemical compound OC(=O)C(N)CC1=CC=C(OP(O)(O)=O)C=C1 DCWXELXMIBXGTH-UHFFFAOYSA-N 0.000 description 1
- 239000006187 pill Substances 0.000 description 1
- 239000000244 polyoxyethylene sorbitan monooleate Substances 0.000 description 1
- 235000010482 polyoxyethylene sorbitan monooleate Nutrition 0.000 description 1
- 229920000053 polysorbate 80 Polymers 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 230000003389 potentiating effect Effects 0.000 description 1
- 230000003449 preventive effect Effects 0.000 description 1
- DBABZHXKTCFAPX-UHFFFAOYSA-N probenecid Chemical compound CCCN(CCC)S(=O)(=O)C1=CC=C(C(O)=O)C=C1 DBABZHXKTCFAPX-UHFFFAOYSA-N 0.000 description 1
- 229960003081 probenecid Drugs 0.000 description 1
- 235000019260 propionic acid Nutrition 0.000 description 1
- 108060006633 protein kinase Proteins 0.000 description 1
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 1
- 125000000719 pyrrolidinyl group Chemical group 0.000 description 1
- IUVKMZGDUIUOCP-BTNSXGMBSA-N quinbolone Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)CC[C@@]21C)C1=CCCC1 IUVKMZGDUIUOCP-BTNSXGMBSA-N 0.000 description 1
- 150000003254 radicals Chemical class 0.000 description 1
- 102000027426 receptor tyrosine kinases Human genes 0.000 description 1
- 108091008598 receptor tyrosine kinases Proteins 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 238000010992 reflux Methods 0.000 description 1
- BOLDJAUMGUJJKM-LSDHHAIUSA-N renifolin D Natural products CC(=C)[C@@H]1Cc2c(O)c(O)ccc2[C@H]1CC(=O)c3ccc(O)cc3O BOLDJAUMGUJJKM-LSDHHAIUSA-N 0.000 description 1
- 208000037803 restenosis Diseases 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- 239000012047 saturated solution Substances 0.000 description 1
- HFHDHCJBZVLPGP-UHFFFAOYSA-N schardinger α-dextrin Chemical compound O1C(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(O)C2O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC2C(O)C(O)C1OC2CO HFHDHCJBZVLPGP-UHFFFAOYSA-N 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 230000019491 signal transduction Effects 0.000 description 1
- 239000000741 silica gel Substances 0.000 description 1
- 229910002027 silica gel Inorganic materials 0.000 description 1
- 239000000377 silicon dioxide Substances 0.000 description 1
- 235000012239 silicon dioxide Nutrition 0.000 description 1
- 208000000587 small cell lung carcinoma Diseases 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 239000001632 sodium acetate Substances 0.000 description 1
- 235000017281 sodium acetate Nutrition 0.000 description 1
- 239000007974 sodium acetate buffer Substances 0.000 description 1
- 235000017557 sodium bicarbonate Nutrition 0.000 description 1
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 1
- HRZFUMHJMZEROT-UHFFFAOYSA-L sodium disulfite Chemical compound [Na+].[Na+].[O-]S(=O)S([O-])(=O)=O HRZFUMHJMZEROT-UHFFFAOYSA-L 0.000 description 1
- 229940001584 sodium metabisulfite Drugs 0.000 description 1
- 235000010262 sodium metabisulphite Nutrition 0.000 description 1
- 239000008247 solid mixture Substances 0.000 description 1
- 230000007928 solubilization Effects 0.000 description 1
- 238000005063 solubilization Methods 0.000 description 1
- 238000013222 sprague-dawley male rat Methods 0.000 description 1
- 239000007921 spray Substances 0.000 description 1
- 238000001694 spray drying Methods 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 239000008117 stearic acid Substances 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 235000011044 succinic acid Nutrition 0.000 description 1
- 150000003444 succinic acids Chemical class 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-N sulfuric acid Substances OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 208000024891 symptom Diseases 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 239000006188 syrup Substances 0.000 description 1
- 235000020357 syrup Nutrition 0.000 description 1
- QHQATUUBFDYJOC-UHFFFAOYSA-N tert-butyl 4-[3-[2,4-dimethyl-5-[(2-oxo-1h-indol-3-ylidene)methyl]-1h-pyrrol-3-yl]propanoyl]piperazine-1-carboxylate Chemical compound CC=1NC(C=C2C3=CC=CC=C3NC2=O)=C(C)C=1CCC(=O)N1CCN(C(=O)OC(C)(C)C)CC1 QHQATUUBFDYJOC-UHFFFAOYSA-N 0.000 description 1
- CWXPZXBSDSIRCS-UHFFFAOYSA-N tert-butyl piperazine-1-carboxylate Chemical compound CC(C)(C)OC(=O)N1CCNCC1 CWXPZXBSDSIRCS-UHFFFAOYSA-N 0.000 description 1
- 125000005931 tert-butyloxycarbonyl group Chemical group [H]C([H])([H])C(OC(*)=O)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- CZDYPVPMEAXLPK-UHFFFAOYSA-N tetramethylsilane Chemical compound C[Si](C)(C)C CZDYPVPMEAXLPK-UHFFFAOYSA-N 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 1
- HRXKRNGNAMMEHJ-UHFFFAOYSA-K trisodium citrate Chemical compound [Na+].[Na+].[Na+].[O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O HRXKRNGNAMMEHJ-UHFFFAOYSA-K 0.000 description 1
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 description 1
- 238000001262 western blot Methods 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/06—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
- A61K31/403—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil condensed with carbocyclic rings, e.g. carbazole
- A61K31/404—Indoles, e.g. pindolol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/08—Vasodilators for multiple indications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing three or more hetero rings
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Heart & Thoracic Surgery (AREA)
- Oncology (AREA)
- Cardiology (AREA)
- Hematology (AREA)
- Epidemiology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
- Indole Compounds (AREA)
- Peptides Or Proteins (AREA)
- Investigating Or Analysing Biological Materials (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
Abstract
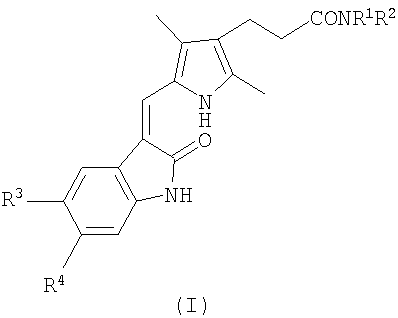
Изобретение относится к новым производным индолина формулы (I)
где (i) R1 означает Н, (1-4С)алкил; R2 означает -A1-NR5R6, в которой каждый из заместителей R5 и R6 независимо означает Н, (1-4С)алкил, А1 означает (СН2)m, (СН2)n-А2(СН2)p или (CH2CH2O)qCH2CH2, где m равно целому числу от 2 до 10, и каждое из n и p равно целому числу от 1 до 6, А2 означает СН=СН, фенилен, бифенилен, циклогексилен или пиперазинилен, и q равно 1, 2 или 3;
(ii) R1 и R2 вместе представляют -A3-NR7-A4, где каждый из А3 и А4 независимо означают (СН2)r или (CH2CH2O)sCH2CH2, где r равно целому числу от 2 до 6, s равно 1, 2 или 3, и R7 означает Н, (1-4С)алкил;
(iii) R1 и R2 вместе с атомом азота, к которому они присоединены, образуют пиперидинил, которая содержит заместитель формулы -A5-R8 в положении 4, в которой А5 представляет (1-4С)алкилен, и R8 представляет пиперидин-4-ил; или
(iv) R1 и R2 вместе с атомом азота, к которому они присоединены, образуют пиперидинил и
каждый из R3 и R4 независимо означает Н или его фармацевтически приемлемая соль. Соединения ингибируют рецепторы тирозинкиназы, что позволяет использовать их в формацевтических композициях для лечения. Описаны способы получения соединения I.
7 н. и 8 з.п. ф-лы. 1 табл.
Description
Область изобретения
Настоящее изобретение относится к новым производным индолинона, которые могут быть полезны в качестве лекарственных средств, к способам получения указанных соединений, промежуточным соединениям, полезным при получении указанных соединений, к фармацевтическим композициям, включающим данные соединения, и к применению данных соединений в качестве лекарственных средств.
Предпосылки изобретения
WO 96/40116 раскрывает, что определенные пирролзамещенные производные 2-индолинона, являющиеся ингибиторами рецептора тирозинкиназы, полезные при лечении состояний, чувствительных к ингибиторам рецептора тирозинкиназы, например пролиферативных нарушений, таких как рак. Предпочтительным соединением, описанным на странице 17, является 3-(2,3-диметилпиррол-5-ил)метилен]-2-индолинон, так же известный как SU5416. К сожалению, обнаружено, что это соединение проявляет слабую растворимость в воде и низкую биодоступность при пероральном и внутривенном введении.
WO 99/61422 описывает последующие пирролзамещенные производные 2-индолинона как ингибиторы рецептора тирозинкиназы. Предпочтительным соединением, описанным как соединение 5 на странице 214, является 3-[2,4-диметил-5-(2-оксо-1,2-дигидроиндол-3-илметил)-1Н-пиррол-3-ил]пропионовая кислота, так же известная как SU6668. Обнаружено, что это соединение обладает очень высокой пероральной активностью относительно SU5416, но сообщается о недостаточной способности этого соединения ингибировать рецептор тирозинкиназы Flt-3 (Abstract 497, Anne-Marie O'Farrell et al., America Society of Hematology Meeting, Orlando, Florida, USA, December 7-11, 2001). Flt-3 является важной мишенью для ингибитора тирозинкиназы, особенно при лечении острой миелоидной лейкемии (ОМЛ), поскольку у около 30% пациентов с ОМЛ обнаруживается наличие мутантных форм Flt-3, которые приводят к конститутивному тирозин-фосфорилированию Flt-3 (Levis et al., Blood, 1 August, 2001, Vol. 98. No. 3, рр. 885-887).
WO 01/60814 описывает пирролзамещенные производные 2-индолинона, содержащие определенные амидные заместители, непосредственно присоединенные к пиррольному кольцу как ингибиторы рецептора тирозинкиназы.
WO 02/055517 описывает индолиноны, содержащие арильные заместители в положении 4, которые проявляют способность модулировать протеинкиназу.
WO 01/42243 описывает определенные соединения, содержащие две или более пирролзамещенные 2-индолиноновые группы, ковалентно связанные вместе через положение 3 каждого пиррола одной или более связующими группами, так же полезные как ингибиторы рецептора тирозинкиназы.
Тем не менее, с учетом тяжести состояний, отвечающих на ингибиторы рецептора тирозинкиназы и недавней идентификации специфических мишеней ингибитора киназы, требуется наличие новых ингибиторов рецептора тирозинкиназы с различными свойствами.
Краткое описание изобретения
В настоящее время обнаружено, что пирролзамещенные производные 2-индолинона, содержащие определенные карбоксиамидоэтильные группы в положении 4 пиррола, являются ингибиторами рецептора тирозинкиназы в соответствии с требуемыми свойствами.
Соответственно настоящее изобретение предоставляет соединение формулы (I):
где (i) R1 представляет атом водорода или (1-4C)алкильную группу; и R2 представляет группу формулы -А1-NR5R6, в которой каждый из заместителей R5 и R6 независимо представляет атом водорода или (1-4C)алкильную группу, и А1 представляет (СН2)m, (СН2)n-А2-(СН2)p или (CH2CH2O)qCH2CH2, где m равно целому числу от 2 до 10, и каждое из n и p равно целому числу от 1 до 6, А2 представляет СН=CH, фенилен, бифенилен, циклогексилен или пиперазинилен, и q равно 1, 2 или 3;
(ii) R1 и R2 вместе представляют -A3-NR7-А4, где каждый из А3 и А4 независимо представляет (СН2)r или (CH2CH2O)sСН2СН2, где r равно целому числу от 2 до 6, s равно 1, 2 или 3, и R7 представляет атом водорода или (1-4C)алкильную группу;
(iii) R1 и R2 вместе с атомом азота, к которому они присоединены, представляют пиперидинильную группу, где пиперидинильная группа содержит заместитель формулы -А5-R8 в положении 4, в которой А представляет (1-4C)алкилен, и R8 представляет пиперидин-4-ил; или
(iv) R1 и R2 вместе с атомом азота, к которому они присоединены, представляют пирролидинильную, пиперидинильную или морфолиногруппу; и
R3 и R4, каждый независимо представляет атом водорода, атом галогена, (1-4C)алкильную группу, (1-4C)алкоксигруппу, фенильную группу, которая незамещена или замещена одним или двумя заместителями, выбранными независимо из атома галогена, (1-4C)алкильной группы и (1-4C)алкоксигруппы, группы формулы R9S(О)2NR10-, группы формулы R11N(R12)S(О)2-, группы формулы R13С(О)N(R14)- или группы формулы R15N(R16)С(О)-, в которых каждый из R9, R11, R13 и R15 независимо представляет (1-4C)алкильную группу или фенильную группу, незамещенную или замещенную одним или двумя заместителями, выбранными независимо из атома галогена, (1-4C)алкильной группы и (1-4C)алкоксигруппы, и каждый из R10, R12, R14 и R16 независимо представляет атом водорода или (1-4C)алкильную группу;
или фармацевтически приемлемую соль данного соединения.
Обнаружено, что соединения формулы (I) являются сильными и селективными ингибиторами одного или более рецепторов тирозинкиназы PDGFR (фактор роста, выбранный из тромбоцитов), с-Kit, VEGFR (фактор роста сосудистого эндотелия) и Flt-3 в исследованиях в цельных клетках.
Изобретение также предоставляет соединения формулы (Ia):
где R представляет водород, метил или этил; или их фармацевтически приемлемые соли.
Изобретение также предоставляет фармацевтические композиции, включающие соединения изобретения или их фармацевтически приемлемые соли и фармацевтически приемлемый носитель.
Кроме того, изобретение обеспечивает способ лечения состояния, восприимчивого к ингибитору тирозинкиназы; причем способ включает введение пациенту соединения изобретения в эффективном количестве.
Далее изобретение относится к соединению изобретения, как указано выше, для применения в медицинской терапии, а также к применению соединения изобретения в производстве лекарственного средства или композиций для лечения заболевания или состояния восприимчивого к ингибитору тирозинкиназы.
Подробное описание изобретения
Настоящее изобретение предоставляет замещенные производные 2-индолина, которые содержат в положении 4 пиррольного кольца карбоксиамидометильные заместители.
Как использовано в данном описании, термины "алкил" и "алкилен" означают разветвленную или неразветвленную группу. Тем не менее, названия специфических групп, таких как этил, этилен, пропил, пропилен, бутил или бутилен означают неразветвленные группы или радикалы, если не указано иначе, такие как, например, проп-2-ил. Примерами алкильных групп являются метил, этил, пропил, проп-2-ил и бутил.
Примерами алкиленовых групп являются метилен, этилен, пропилен и бутилен.
Термин "атом галогена" включает фтор, хлор и бром.
Термин "терапевтически эффективное количество" означает количество, достаточное для проведения лечения при введении пациенту, нуждающемуся в указанном лечении.
Термин "лечение", используемый в данном описании, относится к лечению заболевания или клинических состояний пациента, такого как млекопитающее (в частности, человека) и включает:
(а) предотвращение заболевания или клинического состояния, т.е. профилактическое лечение пациента;
(b) улучшение состояния при заболевании или клиническом состоянии, т.е. излечение или регрессию причины заболевания или клинического состояния пациента;
(с) подавление болезни или клинического состояния, т.е. замедление или прекращение развития заболевания или клинического состояния пациента; или
(d) облегчение симптомов заболевания или клинического состояния пациента.
Термин "фармацевтически приемлемая соль" относится к соли, полученной из основания или кислоты, которая является приемлемой для введения пациенту, такому как млекопитающее. Такие соли могут быть производными фармацевтически приемлемых неорганических или органических кислот.
Соли, производные фармацевтически приемлемых кислот, включают соли уксусной, бензолсульфоновой, бензойной, камфорсульфоновой, лимонной, этансульфоновой, фумаровой, глюконовой, глутаминовой, бромистоводородной, хлористоводородной, молочной, малеиновой, малоновой, миндальной, метансульфоновой, муконовой, азотной, пантотеиновой, фосфорной, янтарной, серной, винной, п-толуолсульфоновой, ксинафоновой (1-гидрокси-2-нафтойной) и подобных кислот. Особенно предпочтительными являются соли, производные фумаровой, бромистоводородой, хлористоводородной, уксусной, серной, фосфорной, метансульфоновой, п-толуолсульфоновой, ксинафоновой, винной, лимонной, малеиновой, малоновой, янтарной и бензойной кислот.
Предпочтительной подгруппой соединений формулы (I) является та, в которой:
(i) R1 представляет атом водорода или (1-4C)алкильную группу; и R2 представляет группу формулы -А1-NR5R6, в которой каждый из заместителей R5 и R6 независимо представляет атом водорода или (1-4C)алкильную группу, и А1 представляет (СН2)m, (СН2)n-А2-(СН2)p или (CH2CH2O)qCH2CH2, где m равно целому числу от 2 до 10, и каждое из n и p равно целому числу от 1 до 6, А2 представляет СН=CH, фенилен, бифенилен, циклогексилен или пиперазинилен, и q равно 1, 2 или 3;
(ii) R1 и R2 вместе представляют -A3NR7-A4-, где каждый из A3 и А4 независимо представляет (СН2)r или (СН2СН2O)sСН2СН2, где r равно целому числу от 2 до 6, s равно 1, 2 или 3, и R7 представляет атом водорода или (1-4C)алкильную группу; или
(iii) R1 и R2 вместе с атомом азота, к которому они присоединены, представляют пиперидинильную группу, где пиперидинильная группа содержит заместитель формулы -А5-R8 в положении 4, в которой А представляет (1-4C)алкилен, и R8 представляет пиперидин-4-ил.
Обнаружено, что соединения, принадлежащие к указанной выше предпочтительной подгруппе, показывают хорошую растворимость в воде и хорошую абсорбцию при пероральном введении.
В данной подгруппе соединений предпочтительно
(i) R1 представляет атом водорода или (1-4C)алкильную группу; и R2 представляет группу формулы -А1-NR5R6, в которой каждый из заместителей R5 и R6 независимо представляет атом водорода или (1-4C)алкильную группу, и А1 представляет (СН2)m, (СН2)n-А2-(СН2)p или (CH2CH2O)qCH2CH2, где m равно целому числу от 2 до 10, и каждое из n и p равно целому числу от 1 до 6, А2 представляет СН=CH, фенил-1,3-ен, фенил-1,4-ен, бифенил-2,2'-ен, циклогексил-1,3-ен или пиперазинил-1,4-ен, и q равно 1, 2 или 3;
(ii) R1 и R2 вместе представляют -A3-NR7-A4-, где каждое из A3 и А4 независимо представляет (СН2)r или (СН2СН2O)sСН2СН2, где r равно целому числу от 2 до 6, s равно 1, 2 или 3, и R7 представляет атом водорода или (1-4C)алкильную группу; или
(iii) R1 и R2 вместе с атомом азота, к которому они присоединены, представляют пиперидинильную группу, где пиперидинильная группа содержит заместитель формулы -А5-R8 в положении 4, в которой А представляет (1-4C)алкилен, и R8 представляет пиперидин-4-ил.
Предпочтительно
(i) R1 представляет метильную группу; и R2 представляет группу формулы -А1-NR5R6, в которой заместитель R5 представляет атом водорода, R6 представляет метильную группу, и А1 представляет (СН2)m, (СН2)n-А2-(СН2)p или (CH2CH2O)qCH2CH2, где m равно целому числу от 2 до 10, и каждое из n и p равно 1 или 2, А2 представляет СН=CH, фенил-1,3-ен, фенил-1,4-ен, бифенил-2,2'-ен, циклогексил-1,3-ен или пиперазинил-1,4-ен, и q равно 1, 2 или 3;
(ii) R1 и R2 вместе представляют -A3-NR7-A4-, где каждое из A3 и А4 независимо представляет (СН2)r или (СН2СН2O)sСН2СН2, где r равно целому числу от 2 до 6, s равно 1 или 2, и R7 представляет атом водорода или (1-4C)алкильную группу; или
(iii) R1 и R2 вместе с атомом азота, к которому они присоединены, представляют пиперидинильную группу, где пиперидинильная группа содержит заместитель формулы -А5-R8 в положении 4, в которой А представляет пропилен, и R8 представляет 4-пиперидинил.
Более предпочтительно
(i) R1 представляет метильную группу; и R2 представляет группу формулы -А1-NR5R6, в которой заместитель R5 представляет атом водорода, R6 представляет метильную группу, и А1 представляет (СН2)m, где m равно 2, 3, 4, 5, 6, 7, 8, 9 или 10; (СН2)n-А2-(СН2)p, где каждое из n и p равно 1, и А2 представляет СН=CH, фенил-1,3-ен, фенил-1,4-ен, бифенил-2,2'-ен или циклогексил-1,3-ен; (СН2)n-А2-(СН2)p, где каждое из n и p равно 2, и А2 представляет пиперазинил-1,4-ен; или (CH2CH2O)qCH2CH2, где q равно 2 или 3;
(ii) R1 и R2 вместе представляют -(СН2)2-NH-(СН2)2-, -(СН2)2-N(СН3)-(СН2)2-, -(СН2)2-N(СН2СН3)-(СН2)2-, -(СН2)2-NH-(СН2)3- или -(СН2СН2О)2СН2СН2-NH-(СН2СН2О)СН2СН2-; или
(iii) R1 и R2 вместе с атомом азота, к которому они присоединены, представляют пиперидинильную группу, где пиперидинильная группа содержит заместитель формулы -А5-R8 в положении 4, в которой А представляет пропилен, и R8 представляет пиперидин-4-ил.
Особенно предпочтительна подгруппа соединений, где R1 представляет метильную группу и R2 представляет группу формулы -А1-NR5R6, в которой заместитель R5 представляет атом водорода, R6 представляет метильную группу и А1 представляет (СН2)m или СН2-СН=СН2-СН2, где m равно целому числу от 2 до 6.
Обнаружено, что соединения, принадлежащие к данной подгруппе, демонстрируют особенно хорошую активность как ингибиторы одного или более указанных выше рецепторов тирозинкиназы.
В пределах данной подгруппы предпочтительно А1 представляет (СН2)m или СН2-СН=СН2-СН2, где m равно 2, 3 или 4.
Более предпочтительно, если А1 представляет (СН2)2, (СН2)3 или СН2-СН=СН2-СН2.
Особенно предпочтительными являются соединения, где А1 представляет (СН2)2.
Другой предпочтительной подгруппой соединений являются соединения, где R1 и R2 вместе представляют -A3-NR7-A4-, где каждый из A3 и А4 независимо представляет (СН2)r или (СН2СН2O)sСН2СН2, где r равно целому числу от 2 до 6, s равно 1, 2 или 3, и R7 представляет атом водорода или (1-4C)алкильную группу.
Обнаружено, что соединения, принадлежащие к данной подгруппе, также проявляют особенно хорошую активность.
В данной подгруппе предпочтительно R1 и R2 вместе представляют -(СН2)2-NR7-(СН2)2- или -(СН2)2-NR7(СН2)3-, в особенности -(СН2)2-NR7-(СН2)2-.
Примерами конкретных значений R7 являются водород, метил, этил, пропил, проп-2-ил и бутил.
Соединения, где R7 означает водород, являются особенно предпочтительными.
При рассмотрении R3 и R4 примерами конкретных значений являются:
водород;
для атома галогена: фтор, хлор или бром, особенно бром;
для (1-4С)алкильной группы: метил;
для (1-4С)алкоксигруппы: метокси;
для незамещенной или замещенной фенильной группы: фенил;
для R8, R10, R12 и R14: метил или фенил;
для R9, R11, R13 и R15: водород; и
для группы, формулы R12С(О)N(R13)-: CH3С(О)NH- и C6H5С(О)NH-.
Предпочтительно каждый из R3 и R4 независимо представляет атом водорода, атом брома, СН3С(О)NH- или С6Н5С(О)NH-. Более предпочтительно, если каждый из R3 и R4 независимо представляет атом водорода.
Другой предпочтительной группой соединений формулы (I) являются соединения, где:
(i) R1 представляет метильную группу, и R2 представляет группу формулы -А1-NHCH3, в которой А1 представляет (СН2)m, CH2CH=CHCH2, CH2-фенилен-CH2 или CH2-циклогексилен-CH2, где m равно целому числу от 2 до 8; или
(ii) R1 и R2 вместе представляют -(СН2)2-NH-(СН2)2-, -(СН2)2-N(СН3)-(СН2)2-, -(СН2)2-N(СН2СН3)-(СН2)2- или -(СН2)2-NH-(СН2)3-; и
R3 и R4 каждый независимо представляет атом водорода.
Обнаружено, что соединения, принадлежащие к данной подгруппе, показывают особенно хорошую активность как ингибиторы одного или более указанных выше рецепторов тирозинкиназы. В частности, такие соединения имеют значение IC50 для ингибирования VEGFR тирозинкиназы менее чем 1 мкмоль в внутриклеточном Ca2+ FLIPR или в методе иммунопреципитации, описанном ниже.
Более предпочтительной подгруппой соединений в пределах указанной выше подгруппы являются соединения, где:
(i) R1 представляет метильную группу, и R2 представляет группу формулы -А1-NHCH3, в которой А1 представляет (СН2)m, CH2CH=CHCH2 или CH2-(1,4-фенилен)-CH2, где m равно 2 или 3; или
(ii) R1 и R2 вместе представляют -(СН2)2-NH-(СН2)2-, -(СН2)2-N(СН3)-(СН2)2-, -(СН2)2-N(СН2СН3)-(СН2)2- или -(СН2)2-NH-(СН2)3-.
Соединения, принадлежащие к данной более предпочтительной подгруппе, имеют значение IC50 для ингибирования как VEGFR, так и PDGFR тирозинкиназы менее чем 1 мкмоль в внутриклеточном Ca2+ FLIPR или в методе иммунопреципитации, описанном ниже.
Особенно предпочтительной подгруппой соединений формулы (I) являются соединения формулы (Ia):
в которой R представляет водород, метил или этил, и их фармацевтически приемлемые соли.
Заслуживающими особого внимания соединениями формулы (Ia) являются:
3-[3,5-диметил-4-(3-оксо-3-пиперазин-1-илпропил)-1Н-пиррол-2-илметилен]-1,3-дигидроиндол-2-он и
3-[3,5-диметил-4-[3-оксо-3-(4-этил)пиперазин-1-илпропил]-1Н-пиррол-2-илметилен]-1,3-дигидроиндол-2-он.
Особенно предпочтительным является соединение, 3-[3,5-диметил-4-(3-оксо-3-пиперазин-1-илпропил)-1Н-пиррол-2-илметилен]-1,3-дигидроиндол-2-он и его фармацевтически приемлемые соли.
Обнаружено, что данное соединение является очень сильным и селективным ингибитором PDGFR, с-Kit, VEGFR и Flt-3. Обнаружено также, что оно обладает высокой растворимостью в воде и замечательной абсорбцией при пероральном введении крысам.
Другим соединением формулы (I), заслуживающим особого внимания, является 3-[3,5-диметил-4-(3-оксо-3-гомопиперазин-1-илпропил)-1Н-пиррол-2-илметилен]-1,3-дигидроиндол-2-он.
Соединения формулы (I) являются полезными в качестве ингибиторов рецептора тирозинкиназы при лечении пролиферативных нарушений, таких как формы рака, включая, но, не ограничиваясь ими, острую миелоидную лейкемию, мелкоклеточный рак легких, рак простаты, гастроинтестинальный рак, рак груди и рак мозга, и прочие пролиферативные нарушения, такие как рестеноз. Данные соединения также могут быть полезны для ограничения роста солидных опухолей.
В соответствии с другим аспектом настоящее изобретение относится к способу получения соединения формулы (I), включающий
(а) взаимодействие соединения формулы (II)
или его реакционноспособного производного с соединением формулы (III)
или его солью, где значения R1, R2, R3, и R4 определены выше, или
(b) для соединения формулы (I), в которой R5 или R7 представляют атом водорода, снятие защиты в соединении формулы (IV)
в которой R1a и R2a имеют значения, определенные выше для R1 и R2, кроме тех, в которых R5 или R7 заменены группами R5a или R7a соответственно, где R5a или R7a, каждый представляет аминозащитную группу, и значения R3 и R4 определены выше;
с последующим, если необходима фармацевтически приемлемая соль, получением фармацевтически приемлемой соли.
В способе (а) взаимодействие соединения формулы (II) с соединением формулы (III) можно удобно проводить, используя стандартный метод образования амида. Например, кислоту формулы (II) можно обработать таким конденсирующим агентом, как гексафторфосфат бензотриазол-1-илокситриспирролидинфосфония (РуВОР) или гексафторфосфат О-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилурония (HATU), в присутствии основания, такого как N,N-диизопропилэтиламин и 1-гидрокси-7-азабензотриазол (HOAt), с последующим добавлением соединения формулы (III). Подходящие растворители включают апротонные органические растворители, такие как диметилформамид. Температура проведения реакции находится в пределах от 0 до 50°С. Альтернативно соединение формулы (II) может быть преобразовано в галогенангидрид кислоты, например хлорангидрид, и затем подвергнуто взаимодействию с соединением формулы (III).
В способе (b) аминозащитная группа, представленная R5a или R7a, может быть общепринятой аминозащитной группой. Примеры аминозащитных групп приведены в Greene and Wuts, Protecting Groups in Organic Syntesis, 2nd Edition, John Wiley & Sons, NY, 1991 и McOmie, Protecting Groups in Organic Chemistry, Plenum Press, NY, 1973. Примеры аминозащитных групп включают ацильные группы, например (1-6С)алканоильные группы, такие как ацетил; (1-6С)алкоксикарбонильные группы, такие как трет-бутоксикарбонил; арилметоксикарбонильные группы, такие как бензилоксикарбонил; и арилметильные группы, такие как бензил.
Ацильная аминозащитная группа может быть легко удалена действием кислоты, такой как трифторуксусная кислота.
Соединения формулы (IV) могут быть получены взаимодействием соединения формулы (II) с амином формулы (V)
в которой R1a и R2a определены выше в способе получения(а).
Соединения формулы (II) известны, например, из WO 99/61422. Их также получают взаимодействием соединения формулы (VI)
с соединением формулы (VII)
Взаимодействие удобно проводить в присутствии основания, такого как пиридин, в органическом растворителе, таком как этанол, и при кипячении с обратным холодильником.
Соединения формулы (VII) известны, например, из WO 99/61422.
Соединения формулы (VI) могут быть получены взаимодействием соединения формулы (VIII)
в которой R8a представлен карбоксизащитной группой, например (1-6С)алкильной группой, такой как метил, с оксихлоридом фосфора и диметилформамидом, с последующим удалением защитной группы R8a, например щелочным гидролизом.
Соединения формулы (VIII) могут быть получены через соответствующую кислоту (R8a представляет водород), следуя методикам, описанным в прилагаемых примерах.
Некоторые из промежуточных соединений, описанных выше, являются, как полагают, новыми, например соединение формулы (VI). Все такие новые промежуточные соединения предоставлены как дополнительные аспекты изобретения.
Фармацевтические композиции
При применении в качестве лекарственных средств соединения изобретения обычно следует вводить в виде фармацевтических композиций. Композиции включают соединение изобретения в качестве активного ингредиента вместе с фармацевтически приемлемым разбавителем или носителем. Композиции могут производиться для какого-либо способа введения в организм, в частности для перорального, ректального, трансдермального, подкожного, внутривенного, внутримышечного или интраназального введения. Композиции могут производиться в какой-либо из удобных форм, например в форме таблеток, капсул, растворов, суспензий, дисперсий, сиропов, спреев, гелей, суппозиториев, пластинок и эмульсий.
Получение фармацевтических композиций, пригодных для частных способов введения, хорошо известно специалисту в области фармации. Дополнительно ингредиенты для таких композиций являются коммерчески доступными, например, от Sigma (St. Louis, MO). Стандартная методика получения фармацевтических композиций, которая приводится ниже в качестве иллюстрации, описана в Remington: The Science and Practice of Pharmacy, 20th Edition, Lippincott Williams & White, Baltimore, MD (2000); и H.C. Ansel et al., Pharmaceutical Dosage Forms and Drug Delivery Systems, 7th Edition, Lippincott Williams & White, Baltimore, MD (1999).
В соответствии с другим аспектом настоящее изобретение предоставляет фармацевтические композиции, которые включают терапевтически эффективное количество соединения формулы (I) или его фармацевтически приемлемой соли вместе с фармацевтически приемлемым разбавителем или носителем.
В предпочтительном варианте фармацевтические композиции изобретения пригодны для перорального введения. Пригодные для перорального введения фармацевтические композиции могут быть в форме капсул, таблеток, пилюль, пластинок, саше, драже, порошков, гранул или в форме растворов или жидкой суспензии и тому подобное; каждое содержит предписанное количество соединения настоящего изобретения в качестве активного компонента.
Композиция в форме таблеток может быть изготовлена, используя любой пригодный фармацевтический носитель(ли), обычно используемый(ые) для приготовления твердых композиций. Примеры таких носителей включают стеарат магния, крахмал, лактозу, сахарозу, микрокристаллическую целлюлозу и связующее вещество, например, поливинилпирролидон. Кроме того, активное соединение может быть введено в единичную дозированную форму с контролируемым высвобождением, такую как таблетка, заключенная в гидрофильную или гидрофобную матрицу.
Композиция в форме капсулы может быть приготовлена, используя обычные методики инкапсулирования, например введение активного соединения и наполнителя в жесткую желатиновую капсулу. Альтернативно может быть приготовлена и помещена в жесткую желатиновую капсулу полутвердая матрица активного соединения и полиэтиленгликоля с высокой молекулярной массой; или раствор активного соединения в полиэтиленгликоле или суспензия в съедобном масле может быть приготовлена и помещена в мягкую желатиновую капсулу.
В другом предпочтительном воплощении соединение изобретения может быть приготовлено для инъекции, например для внутривенной инъекции. Типичная композиция для внутривенной инъекции состоит из стерильного водного изотонического раствора, содержащего, например, активное соединение и декстрозу или хлорид натрия, или смесь декстрозы и хлорида натрия. Другие примеры пригодных эксципиентов включают лактатную инъекцию Рингера, лактатную инъекцию Рингера плюс декстрозную инъекцию, Normosol-М и декстроза, Isolyte Е, ацилированную инъекцию Рингера и тому подобное. Дополнительно могут быть включены в фармацевтическую композицию сорастворитель, например полиэтиленгликоль; хелатный агент, например этилендиаминтетрауксусная кислота; стабилизирущий агент, например циклодекстрин; и антиоксидант, например метабисульфит натрия.
В соответствии с другим аспектом настоящее изобретение предусматривает соединение формулы (I) или его фармацевтически приемлемую соль для применения в терапии.
Соединения формулы (I) полезны как ингибиторы рецептора тирозинкиназы. Согласно другому аспекту настоящее изобретение рассматривает применение соединения формулы (I) или его фармацевтически приемлемой соли для изготовления лекарственного средства для лечения состояния, чувствительного к ингибиторам тирозинкиназы.
Согласно еще одному аспекту настоящее изобретение предоставляет фармацевтическую композицию для лечения состояния, чувствительного к ингибиторам тирозинкиназы, которая включает соединение формулы (I) или его фармацевтически приемлемую соль.
Настоящее изобретение дополнительно предоставляет способ лечения состояния, чувствительного к ингибитору тирозинкиназы, который включает введение пациенту, нуждающемуся в указанном лечении, эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли.
Пациент может быть, например, млекопитающим, таким как домашнее животное или предпочтительно человек.
Доза (или эффективное количество) соединения, вводимая пациенту, может зависеть от многих факторов, включая конкретное используемое соединение, природу и тяжесть состояния, которое лечат, вид, к которому относится пациент, массу пациента и способ введения препарата. В общем, вводят дозу в пределах от 0,01 до 100 мкмоль на 1 кг массы тела.
Следующие неограничивающие примеры иллюстрируют типичные фармацевтические композиции изобретения.
Пример фармацевтической композиции А
Твердые желатиновые капсулы для перорального введения получают следующим образом:
| Ингредиенты | Количество |
| Соединение изобретения | 200 мг |
| Лактоза(распылительной сушки) | 250 мг |
| Стеарат магния | 10 мг |
Типичная методика: компоненты тщательно смешивают и затем заполняют жесткую желатиновую капсулу (460 мг композиции на капсулу)
Пример фармацевтической композиции В
Твердые желатиновые капсулы для перорального введения получают следующим образом:
| Ингредиенты | Количество |
| Соединение изобретения | 20 мг |
| Крахмал | 89 мг |
| Микрокристаллическая целлюлоза | 89 мг |
| Стеарат магния | 10 мг |
Типичная методика: компоненты тщательно смешивают, затем просеивают через сито No.45 U.S. и заполняют жесткую желатиновую капсулу (200 мг композиции на капсулу).
Пример фармацевтической композиции С
Капсулы для перорального введения получают следующим образом:
| Ингредиенты | Количество |
| Соединение изобретения | 100 мг |
| Полиоксиэтилен сорбитан моноолеат | 50 мг |
| Крахмал порошок | 250 мг |
Типичная методика: компоненты тщательно смешивают и затем заполняют жесткую желатиновую капсулу (300 мг композиции на капсулу).
Пример фармацевтической композиции D
Таблетки для перорального введения получают следующим образом:
| Ингредиенты | Количество |
| Соединение изобретения | 250 мг |
| Микрокристаллическая целлюлоза | 400 мг |
| Диоксид кремния субмикронный | 10 мг |
| Стеариновая кислота | 5 мг |
Типичная методика: компоненты тщательно смешивают и затем заполняют жесткую желатиновую капсулу (460 мг композиции на капсулу).
Пример фармацевтической композиции Е
Инъекционное лекарственное средство получают следующим образом:
| Ингредиенты | Количество |
| Соединение изобретения | 0,2 мг |
| Буферный раствор ацетата натрия(0,4М) | 400 мг |
| HCl (0,5N) или NaOH (0,5N) | сколько требуется до рН 4 |
| Вода (дистиллированная, стерильная) | сколько требуется до 20 мл |
Типичная методика: компоненты тщательно смешивают и рН доводят до 4±0,5, используя HCl (0,5N) или NaOH (0,5N).
Примеры синтеза
Следующие примеры синтезов приведены для иллюстрации изобретения и никоим образом не должны рассматриваться как ограничивающие объем изобретения.
Общая часть
Используемые реагенты и растворители получены от коммерческих поставщиков, если не указано иное. Все реакции проводят при комнатной температуре и без изоляции от окружающей атмосферы, если не указано иное. Масс-спектры ионного распыления (IS-МС) получены с помощью масс-спектрометра PE Sciex API150EX. Спектры ядерного магнитного резонанса (ЯМР) записаны при 300 МГц. Химический сдвиг в слабом поле (δ) выражается в миллионных долях относительно тетраметилсилана. Аналитическую ВЭЖХ с обращенной фазой (ОФ-ВЭЖХ) выполняли на приборе HP1100 с применением колонки 2,1 мм × 50 мм, 3,5 мкм С18 Zorbax Plus Bonus-RP. Для аналитического разделения, за 0,5 минут изократического периода следует 4,5 минут градиента смеси 0,1% трифторуксусная кислота/ацетонитрил 0,1% в воде при объемном расходе 0,5 мл/минута. Препаративную ОФ-ВЭЖХ выполняли, используя буфер трифторуксусной кислоты (ТФУК) в градиенте смеси ацетонитрил/вода на системе Varian ProStar с использованием колонки 2,5 или 10 см × 25 см, 8 мкм С18 Raining Dynamax при объемном расходе 10 или 50 мл/минута, соответственно.
Получение промежуточных соединений
Промежуточное соединение 1
2-Карбоксиэтил-3,5-диметил-1Н-пиррол-4-карбоновая кислота.
Диэтиловый эфир 3,5-диметил-2,4-пирролдикарбоновой кислоты (200 г, 836 ммоль) помещают в химический стакан объемом 1 л и обрабатывают 400 мл концентрированной серной кислоты (H2SO4). Смесь перемешивают, нагревают до 45°С с помощью тепловой пушки и затем выдерживают 25 минут при 36-42°С. Реакционную смесь выливают в 3 л колотого льда и перемешивают в течение 30 минут. Желтое твердое вещество выделяют фильтрованием и промывают 200 мл воды. Твердое вещество переносят в 4 л колбу Эрленмейера и обрабатывают 2 л 1N раствора гидроксида натрия (NaOH), затем 100 мл 10N NaOH. Основную смесь фильтруют и желтый твердый остаток отбрасывают. Фильтрат подкисляют H2SO4. Получившиеся в результате твердое вещество выделяют вакуумным фильтрованием и промывают 2×500 мл воды. После аспирационной сушки соединение помещают в 6 л колбу Эрленмейера и кипятят непродолжительное время в 4 л ацетона. После ночи стояния при комнатной температуре (КТ) твердое вещество отделяют фильтрованием и сушат в вакуумном эксикаторе с получением 139 г, 659 ммоль, 79% указанного в заголовке соединения. 1Н ЯМР (ДМСО-d6)δ: 4,22 (кв, 2Н), 2,44 (с, 3Н), 2,38 (с, 3Н), 1,27 (т, 3Н).
Промежуточное соединение 2
2-Карбоксиэтил-3,5-диметил-1Н-пиррол
Промежуточное соединение 1 (137 г, 650 ммоль) помещают в 500 мл колбу Эрленмейера и обрабатывают этаноламином (80 г, 1,3 моль). Затем смесь нагревают до 220°С греющей рубашкой, спустя приблизительно 30 минут образуется коричневый раствор, к этому времени выделение газа почти заканчивается. Реакционную смесь нагревают еще 30 минут, затем выливают в 2 л ледяной воды. Неочищенный продукт выделяют вакуумным фильтрованием и затем кипятят в 700 мл 95% этанола (EtOH). Смесь фильтруют в горячем виде, фильтрат медленно охлаждают до КТ и затем до -20°С. Образовавшиеся кристаллы выделяют вакуумным фильтрованием и сушат в вакуумном эксикаторе с получением 75,6 г, 453 ммоль, 70% указанного в заголовке соединения. 1Н ЯМР (ДМСО-d6)δ: 5,72 (с, 1Н), 4,17 (кв, 2Н), 2,18 (с, 3Н), 2,13 (с, 3Н), 1,25 (т, 3Н).
Промежуточное соединение 3
2-Карбоксиэтил-3,5-диметил-1Н-пиррол-4-карбоксальдегид
Промежуточное соединение 2 (75,6г, 453 ммоль) помещают в сухую трехгорлую круглодонную колбу емкостью 1 л. Твердое вещество обрабатывают безводным N,N-диметилформамидом (ДМФА, 43,8 мл, 566 ммоль). Колбу встряхивают, пока ДМФА не распределится во всей массе твердого вещества. Колбу охлаждают на ледяной бане и к смеси в течение 30 минут через капельную воронку добавляют оксихлорид фосфора (POCl3, 52,7 мл, 566 ммоль). Колбу встряхивают до полного распределения реагентов. Затем колбу погружают на масляную баню с температурой 100°С и нагревают при перемешивании магнитной мешалкой в течение 6 часов. Образовавшуюся глубоко-красную смесь охлаждают на бане с ледяной водой и обрабатывают 200 мл ледяной воды, что приводит к бурной экзотермической реакции. После добавления ледяной воды (200 мл) смесь доводят до рН 5 насыщенным раствором ацетата натрия (NaOAc). Неочищенный продукт выделяют вакуумным фильтрованием и перекристаллизовывают из 700 мл горячей смеси EtOH:вода 1:1, получая 65,8г, 337 ммоль, 74% указанного в заголовке соединения в виде темных игл. 1Н ЯМР (ДМСО-d6)δ: 9,88 (с, 1Н), 4,23 (кв, 2Н), 2,46 (с, 3Н), 2,43 (с, 3Н), 1,28 (т, 3Н).
Промежуточное соединение 4
3-(5-Карбоксиэтил-2,4-диметил-1Н-пиррол-3-ил)пропеновая кислота
Промежуточное соединение 3 (65,8 г, 337 ммоль) и малоновую кислоту (39,0г, 375 ммоль) смешивают в одногорлой круглодонной колбе объемом 500 мл, обрабатывают 350 мл абсолютного EtOH и кипятят с обратным холодильником в течение 30 минут. К полученному темному раствору добавляют анилин (34,0 мл, 375 ммоль) и смесь кипятят с обратным холодильником еще 5 часов. Растворитель отгоняют при пониженном давлении и твердое вещество обрабатывают 450 мл 2,5М хлористоводородной кислоты (HCl), нагревают и затем дают остыть до КТ. Пурпурное твердое вещество выделяют вакуумным фильтрованием, переносят в 1 л стакан и обрабатывают 250 мл 2N NaOH при перемешивании. Образовавшуюся суспензию фильтруют и полученное твердое вещество промывают 100 мл разбавленного основания. Пурпурный остаток отбрасывают. Красный фильтрат охлаждают на ледяной бане, перемешивают и подкисляют приблизительно 70 мл 6М HCl. Образовавшуюся плотную белую пасту отфильтровывают в вакууме, промывают водой и сушат на воздухе, получая таким образом указанное в заголовке соединение. 1Н ЯМР (ДМСО-d6)δ: 7,52 (д, 1Н), 5,93 (д, 1Н), 4,22 (кв, 2Н), 2,35 (с, 3Н), 2,31 (с, 3Н), 1,28 (т, 3Н).
Промежуточное соединение 5
3-(2-Карбоксиэтил-2,4-диметил-1Н-пиррол-3-ил)пропионовая кислота
Промежуточное соединение 4 растворяют в 220 мл 2N NaOH и смешивают c 3,5 г 10% палладия на активированном угле. Смесь гидрогенизуют при 50 psi (344,7 кПа) 28 часов, затем фильтруют в вакууме через Целит. Целит промывают 50 мл воды. Аликвоту фильтрата упаривают досуха и полноту восстановления до указанного в заголовке соединения подтверждают 1Н ЯМР (D2O)δ: 4,07 (кв, 2Н), 2,46 (т, 2Н), 2,06 (с, 3Н), 2,05 (т, 2Н), 2,00 (с, 3Н), 1,13 (т, 3Н). Остальной фильтрат используют на следующей стадии без дополнительной обработки.
Промежуточное соединение 6
3-(2,4-Диметил-1Н-пиррол-3-ил)пропионовая кислота
Фильтрат, полученный на предыдущей стадии, содержащий промежуточное соединение 5, обрабатывают 30 мл 10N NaOH и кипятят с обратным холодильником в течение 20 часов. Аликвоту реакционной смеси подкисляют и упаривают досуха. Полноту гидролиза/декарбоксилирования до указанного в заголовке соединения подтверждают 1Н ЯМР (ДМСО-d6)δ: 9,86 (с, 1Н), 6,18 (д, 2Н), 2,42 (м, 2Н), 2,03 (с, 3Н), 1,93 (м, 2Н), 1,87 (с, 3Н). Реакционную смесь используют на следующей стадии без дополнительной обработки.
Промежуточное соединение 7
Метил 3-(2,4-диметил-1Н-пиррол-3-ил)пропионат
Раствор промежуточного соединения 6, полученного на предыдущей стадии, концентрируют при 60°С и пониженном давлении приблизительно до объема 200 мл, охлаждают на бане с ледяной водой и подкисляют до рН 2 приблизительно 50 мл 50% H2SO4. Образовавшуюся смесь фильтруют через стеклянный фильтр. Фильтрат экстрагируют 2×100 мл диэтилового эфира (Et2O) и остаток экстрагируют 3×100 мл Et2O. Объединенные красные органические экстракты промывают 2×100 мл воды, переносят в 2 л колбу Эрленмейера и обрабатывают при перемешивании 680 мл эфирного раствора диазометана. После перемешивания 30 минут при КТ избыток диазометана гасят ледяной уксусной кислотой (HOAc). Реакционную смесь экстрагируют 2×200 мл насыщенного водного раствора бикарбоната натрия (NaHCO3), сушат над безводным сульфатом магния (MgSO4), фильтруют и упаривают, получая 52,6 г неочищенного красного масла. Масло очищают перегонкой при 145°С и 0,2 мм ртутного столба, получая указанное в заголовке соединение (38,4 г, 211 ммоль, 63% из расчета на промежуточное соединение 3). 1Н ЯМР (ДМСО-d6)δ: 9,92 (с, 1Н), 6,22 (с, 1Н), 3,54 (с, 3Н), 2,52 (т, 2Н), 2,32 (т, 3Н), 2,02 (с, 3Н), 1,87 (с, 3Н).
Промежуточное соединение 8
3-(5-Формил-2,4-диметимл-1Н-пиррол-3-ил)пропионовая кислота
В сухую 250 мл трехгорлую круглодонную колбу добавляют безводный ДМФА (13,8 г, 189 ммоль). Охлаждают на ледяной водяной бане и по каплям в течение 10 минут обрабатывают POCl3 (15,0 мл, 160 ммоль). Смесь разбавляют 120 мл безводного 1,2-дихлорэтана (ДХЭ) и нагревают до КТ, получая бледно-оранжевый раствор. Смесь охлаждают до -10°С на ледяной бане с солью, при этой температуре образуется твердое вещество. В течение 10 минут по каплям добавляют промежуточное соединение 7 (14,5 г, 80,0 ммоль), растворенный в 30 мл ДХЭ. Реакционную смесь удаляют с охлаждающей бани, перемешивают при КТ в течение 10 минут и затем упаривают при пониженном давлении при 30°С. Остаток переносят в 2 л стакан, используя приблизительно 100 мл метанола (МеОН), обрабатывают 800 мл 2N NaOH, нагревают до 90°C и затем дают остыть до КТ. Оранжевый раствор экстрагируют 2×200 мл Et2O, нагревают до 50°C, обрабатывают активированным углем, охлаждают до КТ и фильтруют через слой Целита. Фильтрат охлаждают на бане с ледяной водой и подкисляют до рН 3, используя приблизительно 120 мл 6N HCl. Образовавшееся твердое вещество выделяют вакуумным фильтрованием, промывают 3×40 мл воды и сушат на воздухе, получая 11,2 г, 57,0 ммоль указанного в заголовке соединения в виде коричневого порошка. 1Н ЯМР (ДМСО-d6)δ: 9,40 (с, 1Н), 2,52 (т, 2Н), 2,29 (т, 3Н), 2,19 (с, 3Н), 2,14 (с, 3Н).
Промежуточное соединение 9
3-[2,4-Диметил-5-(2-оксо-1,2-дигидроиндол-3-илиденметил)-1Н-пиррол-3-ил]пропионовая кислота
Промежуточное соединение 8 (11 г, 57 ммоль) и оксииндол (7,6 г, 57 ммоль) смешивают в 200 мл круглодонной колбе, суспендируют в 150 мл EtOH, обрабатывают пиперидином (8,5 мл, 86 ммоль) и кипятят с обратным холодильником в течение 4 часов. Реакционную смесь охлаждают до КТ, обрабатывают HOAc (14,4 мл, 250 ммоль), снова кипятят с обратным холодильником некоторое время, охлаждают и фильтруют. Оранжевое твердое вещество выделяют вакуумным фильтрованием, промывают 100 мл горячей смеси HOAc:EtOH 1:1, затем 100 мл горячего EtOH и сушат на воздухе, получая 15 г, 50 ммоль, 87% указанного в заголовке соединения. 1Н ЯМР (ДМСО-d6)δ: 10,8 (с, 1Н), 7,71 (д, 1Н), 7,55 (с, 1Н), 7,07 (т, 1Н), 6,95 (т, 1Н), 6,96 (д, 1Н), 2,63 (т, 2Н), 2,33 (т, 2Н), 2,28 (с, 3Н), 2,25 (с, 3Н).
Промежуточное соединение 10
Трет-бутиловый эфир 4-{3-[2,4-диметил-5-(2-оксо-1,2-дигидроиндол-3-илиденметил)-1Н-пиррол-3-ил]пропионил}пиперазин-1-карбоновой кислоты
Промежуточное соединение 9 (6,2 г, 20 ммоль), моно-Вос-пиперазин (4,1 г, 22 ммоль) и 1-гидрокси-7-азабензотриазол (НОАТ, 3,0 г, 22 ммоль) растворяют в 50 мл безводного ДМФА и обрабатывают N,N-диизопропилэтиламином (DIEA, 3,5 мл, 20 ммоль) и затем гексафторфосфатом бензотриазол-1-илокситриспирролидинофосфония (PyBOP, 11.4 г, 22 ммоль). Образовавшуюся смесь перемешивают ночь при КТ, получая желтое твердое вещество. Твердое вещество выделяют вакуумным фильтрованием, промывают ДМФА и ацетонитрилом и сушат, получая таким образом 1,3 г промежуточного соединения 10. Фильтрат упаривают и фракционируют хроматографией на 700 см3 силикагеля, используя в качестве элюента 5% МеОН в дихлорметане (ДХМ). Фракции, содержащие продукт, объединяют и выпаривают, затем поглощают 100 мл ацетонитрила. После охлаждения до КТ отделяют мелкое желтое твердое вещество вакуумным фильтрованием, промывают 2×20 мл ацетонитрила и сушат, получая дополнительно 5,7 г указанного в заголовке соединения. В общем, получают 7,0 г, 15 ммоль, 75% продукта. 1Н ЯМР (ДМСО-d6)δ: 10,7 (с, 1Н), 7,70 (д, 1Н), 7,55 (с, 1Н), 7,07 (т, 1Н), 6,95 (т, 1Н), 6,84 (д, 1Н), 3,41-3,19 (м, 8Н), 2,62 (т, 2Н), 2,43 (т, 2Н), 2,28 (с, 3Н), 2,24 (с, 3Н), 1,35 (с, 9Н). IS-МС, вычислено m/z для C27H34N4O4[M]+: 478; найдено 478,2.
Пример 1
Трифторацетат 3-[3,5-диметил-4-(3-оксо-3-пиперазин-1-илпропил)-1Н-пиррол-2-илметилен]-1,3-дигидроиндол-2-она
Промежуточное соединение 10 (4,78 г, 10,0 ммоль) суспендируют в 20 мл ДХМ и обрабатывают при комнатной температуре ТФУК. Через 30 минут реакционную смесь выпаривают при пониженном давлении, затем растворяют в 20 мл хлороформа и повторно выпаривают. Остаток снова растворяют в 20 мл хлороформа и по каплям прибавляют к 200 мл Et2O. Образовавшееся желтое твердое вещество выделяют вакуумным фильтрованием, промывают 3×20 мл Et2O и сушат, получая 4,8 г, 9,7 ммоль 97% указанного в заголовке соединения. 1Н ЯМР (ДМСО-d6)δ: 10,8 (с, 1Н), 8,74 (уш.с, 2Н), 7,71 (д, 1Н), 7,56 (с, 1Н), 7,07 (т, 1Н), 6,96 (т, 1Н), 6,85 (д, 1Н), 3,62 (уш.с, 4Н), 3,02 (уш.с, 4Н), 2,62 (т, 2Н), 2,5 (т, 2Н), 2,28 (с, 3Н), 2,25 (с, 3Н). IS-МС, вычислено m/z для C22H26N4O2[M+Н+]+: 379,2; найдено 379,0.
Пример 1а (альтернативный способ)
Трифторацетат 3-[3,5-диметил-4-(3-оксо-3-пиперазин-1-илпропил)-1Н-пиррол-2-илметилен]-1,3-дигидроиндол-2-она
Промежуточное соединение 9 (0,31 г, 1,0 ммоль) растворяют в 3 мл безводного ДМФА и обрабатывают НОАТ (0,14 г, 1,0 ммоль) и гексафторфосфатом О-(7-азабензтриазол-1-ил)-N,N,N',N'-тетраметилурония (HATU, 0,38 мг, 1,0 ммоль). После 10 минут перемешивания при КТ реакционную смесь прибавляют к раствору пиперазина (0,17 г, 2,0 ммоль) и перемешивают двое суток. Затем реакционную смесь фракционируют препаративной ВЭЖХ с обращенной фазой. Соответствующие фракции объединяют и лиофилизуют, получая 0,16 г, 0,34 ммоль, 34% указанного в заголовке соединения.
Пример 2
Трифторацетат 3-[2,4-диметил-5-(2-оксо-1,2-дигидроиндол-3-илиденметил)-1Н-пиррол-3-ил]-N-метил-N-(2-метиламиноэтил)пропионамида
Промежуточное соединение 10 (0,062 г, 0,20 ммоль) растворяют в 0,67 мл безводного ДМФА и обрабатывают НОАТ (0,030 г, 0,22 ммоль) и HATU (0,084 г, 0,22 ммоль). После 15 минут перемешивания при КТ активированную кислоту прибавляют к раствору N,N'-диметилендиамина (0,043 мл, 0,40 ммоль) в 0,50 мл безводного ДМФА. Реакционную смесь перемешивают ночь на вращающемся шейкере, затем разбавляют 0,50 мл 30% водного раствора ТФУК, фильтруют и фракционируют препаративной ВЭЖХ с обращенной фазой. Соответствующие фракции объединяют и лиофилизуют, получая 0,005 г, 0,010 ммоль, 5% указанного в заголовке соединения. IS-МС, вычислено m/z для C22H28N4O2[M+Н+]+: 381,2; найдено 381,0.
Примеры 3-24
По методикам, аналогично описанным выше в примерах 1а и 2, взаимодействием промежуточного соединения 10 с другими аминами получают соединения примеров 3-24.
Пример 3
Трифторацетат 3-[2,4-диметил-5-(2-оксо-1,2-дигидроиндол-3-илиденметил)-1Н-пиррол-3-ил]-N-метил-N-(3-метиламинопропил)пропионамида
IS-MC, вычислено m/z для C23H30N4O2[M+Н+]+: 395,2; найдено 395,0.
Пример 4
Трифторацетат 3-[2,4-диметил-5-(2-оксо-1,2-дигидроиндол-3-илиденметил)-1Н-пиррол-3-ил]-N-метил-N-(4-метиламинобутил)пропионамида
IS-MC, вычислено m/z для C24H32N4O2[M+Н+]+: 409,3; найдено 409,0.
Пример 5
Трифторацетат 3-[2,4-диметил-5-(2-оксо-1,2-дигидроиндол-3-илиденметил)-1Н-пиррол-3-ил]-N-метил-N-(5-метиламинопентил)пропионамида
IS-MC, вычислено m/z для C25H34N4O2[M+Н+]+: 423,3; найдено 423,2.
Пример 6
Трифторацетат 3-[2,4-диметил-5-(2-оксо-1,2-дигидроиндол-3-илиденметил)-1Н-пиррол-3-ил]-N-метил-N-(6-метиламиногексил)пропионамида
IS-MC, вычислено m/z для C26H36N4O2[M+Н+]+: 437,3; найдено 437,2.
Пример 7
Трифторацетат 3-[2,4-диметил-5-(2-оксо-1,2-дигидроиндол-3-илиденметил)-1Н-пиррол-3-ил]-N-метил-N-(7-метиламиногептил)пропионамида
IS-MC, вычислено m/z для C27H38N4O2[M+Н+]+: 451,3; найдено 451,2.
Пример 8
Трифторацетат 3-[2,4-диметил-5-(2-оксо-1,2-дигидроиндол-3-илиденметил)-1Н-пиррол-3-ил]-N-метил-N-(8-метиламинооктил)пропионамида
IS-MC, вычислено m/z для C28H40N4O2[M+Н+]+: 465,3; найдено 465,2.
Пример 9
Трифторацетат 3-[2,4-диметил-5-(2-оксо-1,2-дигидроиндол-3-илиденметил)-1Н-пиррол-3-ил]-N-метил-N-(9-метиламинононил)пропионамида
IS-MC, вычислено m/z для C29H42N4O2[M+Н+]+: 479,3; найдено 479,2.
Пример 10
Трифторацетат 3-[2,4-диметил-5-(2-оксо-1,2-дигидроиндол-3-илиденметил)-1Н-пиррол-3-ил]-N-метил-N-(10-метиламинодецил)пропионамида
IS-MC, вычислено m/z для C30H44N4O2[M+Н+]+: 493,4; найдено 492,8.
Пример 11
Трифторацетат 3-[2,4-диметил-5-(2-оксо-1,2-дигидроиндол-3-илиденметил)-1Н-пиррол-3-ил]-N-метил-N-(12-метиламинододецил)пропионамида
IS-MC, вычислено m/z для C32H48N4O2[M+Н+]+: 521,4; найдено 520,8.
Пример 12
Трифторацетат 3-[2,4-диметил-5-(2-оксо-1,2-дигидроиндол-3-илиденметил)-1Н-пиррол-3-ил]-N-метил-N-(4-метиламинобут-2-енил)пропионамида
IS-MC, вычислено m/z для C24H30N4O2[M+Н+]+: 407,2; найдено 407,0.
Пример 13
Трифторацетат 3-[2,4-диметил-5-(2-оксо-1,2-дигидроиндол-3-илиденметил)-1Н-пиррол-3-ил]-N-метил-N-(8-метиламино-3,6-диоксиоктил)пропионамида
IS-MC, вычислено m/z для C26H36N4O4[M+Н+]+: 469,3; найдено 469,0.
Пример 14
Трифторацетат 3-[2,4-диметил-5-(2-оксо-1,2-дигидроиндол-3-илиденметил)-1Н-пиррол-3-ил]-N-метил-N-(11-метиламино-3,6,9-триоксиундецил)пропионамида
IS-MC, вычислено m/z для C28H40N4O5[M+Н+]+: 513,3; найдено 512,8.
Пример 15
Трифторацетат 3-[2,4-диметил-5-(2-оксо-1,2-дигидроиндол-3-илиденметил)-1Н-пиррол-3-ил]-N-метил-N-(3-метиламинометилфенилметил)пропионамида
IS-MC, вычислено m/z для C28H32N4O2[M+Н+]+: 457,3; найдено 457,0.
Пример 16
Трифторацетат 3-[2,4-диметил-5-(2-оксо-1,2-дигидроиндол-3-илиденметил)-1Н-пиррол-3-ил]-N-метил-N-(4-метиламинометилфенилметил)пропионамида
IS-MC, вычислено m/z для C28H32N4O2[M+Н+]+: 457,3; найдено 457,2.
Пример 17
Трифторацетат 3-[2,4-диметил-5-(2-оксо-1,2-дигидроиндол-3-илиденметил)-1Н-пиррол-3-ил]-N-метил-N-(3-метиламинометилциклогексилметил)пропионамида
IS-MC, вычислено m/z для C28H38N4O2[M+Н+]+: 463,3; найдено 463,0.
Пример 18
Трифторацетат 3-[2,4-диметил-5-(2-оксо-1,2-дигидроиндол-3-илиденметил)-1Н-пиррол-3-ил]-N-метил-N-(2'-метиламинометилбифен-2-илметил)пропионамида
IS-MC, вычислено m/z для C34H36N4O2[M+Н+]+: 533,3; найдено 533,2.
Пример 19
Трифторацетат 3-[2,4-диметил-5-(2-оксо-1,2-дигидроиндол-3-илиденметил)-1Н-пиррол-3-ил]-N-метил-N-(3-[4-(3-метиламинопропил)пиперазин-1-ил]пропил)пропионамида
IS-MC, вычислено m/z для C30H44N6O2[M+Н+]+: 521,4; найдено 521,2.
Пример 20
Трифторацетат 3-[3,5-диметил-4-(3-оксо-3-пиперидин-1-илпропил)-1Н-пиррол-2-илметилен]-1,3-дигидроиндол-2-она
IS-MC, вычислено m/z для C23H27N3O2[M+Н+]+: 378,2; найдено 378,0.
Пример 21
Трифторацетат 3-[3,5-диметил-4-(3-оксо-3-(пиперидин-4-илпропил)пиперидин-1-илпропил)-1Н-пиррол-2-илметилен]-1,3-дигидроиндол-2-она
IS-MC, вычислено m/z для C31H42N4O2[M+Н+]+: 503,3; найдено 503,2.
Пример 22
Трифторацетат 3-[3,5-диметил-4-(3-оксо-3-(4-этил)пиперазин-1-илпропил)-1Н-пиррол-2-илметилен]-1,3-дигидроиндол-2-она
IS-MC, вычислено m/z для C24H30N4O2[M+Н+]+: 407,2; найдено 407,0.
Пример 23
Трифторацетат 3-[3,5-диметил-4-(3-оксо-3-гомопиперазин-1-илпропил)-1Н-пиррол-2-илметилен]-1,3-дигидроиндол-2-она
IS-MC, вычислено m/z для C23H28N4O2[M+Н+]+: 393,2; найдено 393,0.
Пример 24
Трифторацетат 3-[3,5-диметил-4-(3-оксо-3-(1,4,10-триокса-7,13-диазациклопентадекан-1-ил)-1Н-пиррол-2-илметилен]-1,3-дигидроиндол-2-она
IS-MC, вычислено m/z для C28H38N4O5[M+Н+]+: 511,3; найдено 511,0.
Следуя методикам Примеров 1а и 2, также получают следующие соединения:
5-бром-3-[3,5-диметил-4-(3-оксо-3-(4-проп-2-ил)пиперазин-1-илпропил)-1Н-пиррол-2-илметилен]-1,3-дигидроиндол-2-он и
трифторацетат 5-бром-3-[3,5-диметил-4-(3-оксо-3-(4-проп-2-ил)гомопиперазин-1-илпропил)-1Н-пиррол-2-илметилен]-1,3-дигидроиндол-2-она.
Биологические анализы
Способность тестируемых соединений к ингибированию рецептора тирозинкиназы показаны в следующих анализах.
Сокращения
HEPES - 4-(2-гидроксиэтил)-1-пиперазинэтансульфоновая кислота
EDTA - этилендиаминтетрауксусная кислота
PDGF - фактор роста, полученный из тромбоцитов
PDGFR - рецепторы фактора роста, полученного из тромбоцитов
VEGF - фактор роста, полученный из сосудов эндотелия
VEGFR - рецепторы фактора роста, полученного из сосудов эндотелия
HEK клетки - эмбриональные клетки почки человека
Flt-3 - fms-связанная тирозинкиназа 3
BSA - бычий сывороточный альбумин
AML - острая миелоидная лейкемия
ITD - внутренняя тандемная дупликация
MTT - 3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолбромид
HUVEC - умбиллические венозные эпителиальные клетки человека
Анализ выделения Ca
2+
(FLIPR Анализ)
Связывание факторов роста с соответствующими им рецепторами приводит к аутофосфорилированию рецептора. Это первый шаг в сигнальном каскаде, который приводит к выделению Ca2+ из внутренних источников и притока внеклеточного Ca2+.
Повышение уровня внутриклеточного Ca2+ определяют при нагружении клеток флуоресцентным красителем перед стимуляцией фактора роста с последующей оценкой флуоресцентного сигнала на Flourometric Image Plate Reader (FLIPR). Ингибитор киназы, который может проникнуть через клеточную мембрану, ингибирует аутофосфорилирование рецептора, следовательно, выделение Ca2+ замедляется или прекращается.
Для определения IC50 тестируемых соединений против VEGFR в анализе FLIPR применяют HUVEC (Walkersville, MD). Для определения IC50 против PDGFR использовали линию клеток HEK, которая экспрессирует PDGFR человека. 40-50000 клеток на лунку наносят на 96 луночный планшет. Клетки инкубируют 3-4 часа до прилипания к пластинке. Затем клетки дважды промывают FLIPR буфером (1XHBS, 2мМ CaCl2, 10мМ HEPES, рН 7,4, 2,5мМ пробенецид, 0,1% BSA). После второй промывки 50 мкл Са2+ чувствительного красителя FLUO-3 (FLUO-3 (AM) TEF Labs, 50 мкг в 10 мл FLIPR буфера) добавляют до остатка 50 мкл буфера в каждую лунку. После нанесения клеток в течение одного часа клетки дважды промывают и добавляют тестируемые соединения в 50 мкл как 2Х раствор в 50 мкл буфера в каждую лунку. Клетки инкубируют с соединениями 30 мин и затем добавляют VEGFR (40 нг/мл, BioSourse International) для VEGFR или PDGF (40 нг/мл, BioSourse International) для PDGFR. Изменения интенсивности флуоресценции измеряют на Flourometric Image Plate Reader (FLIPR) (Molecular Devices).
Анализ Пролиферации и Жизнеспособности (МТТ)
Считают, что ингибирование мутанта Flt-3 ITD воздействует на эффект пролиферации и жизнеспособности AML клеток с данной мутацией. Для того чтобы измерить активность тестируемых соединений анализ пролиферации и жизнеспособности (Roche Molecular Biochemicals, Indianapolis, IN) МТТ проводят с клеточной линией AML, называемой MV4-11. Клетки MV4-11 экспрессируют Flt-3 ITD. 50000 клеток на лунку в 100 мкл среды наносят на 96 луночный планшет и инкубируют с возрастающими концентрациями соединения в течение 48 часов. После инкубационного периода добавляют 10 мкл реакционной смеси для мечения МТТ. Реагент мечения МТТ метаболизируется жизнеспособными клетками до формазана, нерастворимой синей соли. Чтобы растворить формазановую соль добавляют 100 мкл солюбилизационного раствора. Планшет инкубируют при 37 градусах по Цельсию и затем определяют оптическую плотность лунок спектрофотометрически при 550 нм. Оптическая плотность растворов в клетках отражает эффект воздействия соединения на жизнеспособность клеток.
Иммунопреципитация/Western (IP/Western)
Связь факторов роста с рецепторными тирозинкиназами, подобным Flt-3 или PDGFR, ведет к аутофосфорилированию рецепторов. Ингибирование аутофосфорилирования является целью, преследуемой ингибиторами киназы. При проведении эксперимента IP/Western уровень аутофосфорилирования рецептора может быть зарегистрирован непосредственно.
5×106 клеток (HEK PDGFR клеточная линия для PDGFR, HEK c-Kit для c-Kit и THP-1, LH-60 или MV4-11 для Flt-3) инкубируют 30 минут в 2,5 мл культурной среды с определенной концентрацией тестируемого соединения. Для того чтобы стимулировать аутофосфорилирование рецептора, в течение 5 мин добавляют фактор роста (PDGF, SCF или Flt-3 лиганды, соответственно 50 нг/мл, Biosource International, Camarillo, СА). Затем клетки центрифугируют и лизируют в 500 мл лизисного буфера (50mM Tris рН 7,4, 1% NP-40, 150мM NaCl, 1mM EDTA, 1мМ NaЗV04). Лизат центрифугируют и добавляют 10 мкл антитела против соответствующего рецептора к супернатанту (анти-PDGFR(P20), анти-c-Kit (C19) и анти-Flt-3(S-18), Santa Cruz Biotechnology, Inc.). Иммунокомплексы выделяют с помощью гранул Protein G (Sigma, St.Louis, MO) и выполняют PAGE. Вестерн-блоттинг выполняют, используя антитела против остатков фосфотирозина (4G10, Upstate Biotechnology, Lake Placid, NY). Интенсивность сигнала фосфотирозина, соответствующую различным концентрациям лекарственного средства, предоставляет путь к определению IC50 тестируемого соединения для ингибирования аутофосфорилирования.
В общем, обнаружено, что соединения, описанные выше, имеют IC50 менее чем 10 мкМ в одном или более указанных выше анализов.
Фармакокинетика
Для определения фармакокинетики самцам крыс Sprague Dawley (линия CD, Charles River Laboratories, Wilmington, МА) вводят дозами тестируемые соединения внутривенно при концентрации 1 мг/кг и перорально (PO) при концентрации 10 мг/кг. Образцы крови берут у животных до введения доз и через 2, 5, 15 и 30 минут, а также через 1, 2, 4, 6 и 24 часа после введения доз. Концентрацию в плазме определяют жидкостной хроматографией-масс-спектрометрией (LC-MS)(MDS SCIEX API 4000, Applied Biosystems, Foster City, СА). Стандартные параметры фармакокинетики оценивают некомпартментными методами, использующими пакет WinNonlin версии 3.2 (Pharsight, Mountain View, СА). Пероральную биоактивность определяют как отношение площади под кривой (ОПК) на графике плазменной концентрации против времени для PO введения к соответствующему количеству для внутривенного введения. Пероральная биоактивность на крысах, например, 3-[3,5-диметил-4-(3-оксо-3-пиперазин-1-илпропил)-1Н-пиррол-2-илметилен]-1,3-дигидроиндол-2-она, определенная данным методом, составила 50,6%.
Результаты сравнительных анализов
В Таблице 1 приведены результаты анализов для двух соединений изобретения, соединения Примера 1, трифторацетата 3-[3,5-диметил-4-(3-оксо-3-пиперазин-1-илпропил)-1Н-пиррол-2-илметилен]-1,3-дигидроиндол-2-она, и соединения Примера 22, трифторацетата 3-[3,5-диметил-4-(3-оксо-3-(4-этил)пиперазин-1-илпропил)-1Н-пиррол-2-илметилен]-1,3-дигидроиндол-2-она. Для сравнения в Таблице 1 также приведены результаты анализов для двух предшествующих соединений, 3-[2,4-диметил-5-(2-оксо-1,2-дигидроиндол-3-илиденметил)-1H-пиррол-3-ил]пропионовой кислоты, идентифицированной как SU6668, и 3-(2,3-диметилпиррол-5-ил)метилен]-2-индолинона, идентифицированного, как SU5416. Получение первого соединения известно из уровня техники и описано выше как промежуточное соединение 9. Последнее соединение получают, как описано у Sun et al., J. Med. Chem. 1998, Vol. 41, No. 14, рр 2588-2603. Способность тестируемых соединений к ингибированию мутанта Flt-3 ITD определяют анализом на цитотоксичность. Ингибирование VEGFR и PDGFR киназ тестируют Ca2+FLIPR анализом, кроме специально указанных случаев. Как показано ниже, соединения Примеров 1 и 22 показывают субмикромолярную активность в Flt-3, VEGFR и PDGFR анализах.
| Таблица 1 | |||
| Flt-3 IC5о (мкМ) | VEGFR IC50 (мкМ) | PDGFR IC50 (мкМ) | |
| Соединение изобретения | |||
| Пример 1 | 0,24 | 0,02 | 0,03# |
| Пример 12 | - | 0,05 | 0,2 |
| Пример 18 | - | 1 | 2,6 |
| Пример 21 | - | >1** | 4 |
| Пример 22 | 0,22 | 0,03 | 0,09 |
| Пример 24 | - | 0,2 | 1,6 |
| Сравнительные соединения | |||
| SU 6668 | Нет активности* | Нет активности** | Нет активности**# |
| SU 5416 | ~1-10 | 0,05 | 0,06 |
| *Самая высокая исследованная концентрация 10 мкм | |||
| **Самая высокая исследованная концентрация 1 мкм | |||
| #Анализ иммунопреципитации/Western (IP) | |||
Claims (15)
- (57) 1. Производные индола формулы (I)где (i) R1 представляет атом водорода или (1-4С)алкильную группу; и R2 представляет группу формулы -A1-NR5R6, в которой каждый из заместителей R5 и R6 независимо представляет атом водорода или (1-4С)алкильную группу, и А1 представляет (СН2)m, (СН2)n-А2-(СН2)p или (CH2CH2O)qCH2CH2, где m равно целому числу от 2 до 10, и каждое из n и p равно целому числу от 1 до 6, А2 представляет СН=СН, фенилен, бифенилен, циклогексилен или пиперазинилен, и q равно 1, 2 или 3;(ii) R1 и R2 вместе представляют -A3-NR7-А4, где каждый из А3 и А4 независимо представляют (СН2)r или (CH2CH2O)sCH2CH2, где r равно целому числу от 2 до 6, s равно 1, 2 или 3, и R7 представляет атом водорода или (1-4С)алкильную группу;(iii) R1 и R2 вместе с атомом азота, к которому они присоединены, представляют пиперидинильную группу, где пиперидинильная группа содержит заместитель формулы -A5-R8 в положении 4, в которой А5 представляет (1-4С)алкилен, и R8 представляет пиперидин-4-ил; или(iv) R1 и R2 вместе с атомом азота, к которому они присоединены, представляют пиперидинильную группу; икаждый из R3 и R4 независимо представляет атом водорода;или его фармацевтически приемлемая соль.
- 2. Соединение по п.1,где (i) R1 представляет метильную группу; и R2 представляет группу формулы -A1-NR5R6, в которой заместитель R5 представляет атом водорода, R6 представляет метильную группу, и А1 представляет (СН2)m, где m равно 2, 3, 4, 5, 6, 7, 8, 9 или 10; (СН2)n-А2-(СН2)p, где каждый из n и p равно 1, А2 представляет СН=СН, фенил-1,3-ен, фенил-1,4-ен, бифенил-2,2′-ен или циклогексил-1,3-ен; (СН2)n-А2-(СН2)p, где каждый из n и p равно 2, А2 представляет пиперазин-1,4-илен; или (CH2CH2O)qCH2CH2, где q равно 2 или 3;(ii) R1 и R2 вместе представляют -(CH2)2-NH-(CH2)2-, -(CH2)2-N(CH3)-(СН2)2-, -(CH2)2-N(CH2CH3)-(CH2)2-, -(CH2)2-NH-(CH2)3- или -(CH2CH2O)2CH2CH2-NH-(CH2CH2O)CH2CH2-; или(iii) R1 и R2 вместе с атомом азота, к которому они присоединены, представляют пиперидинильную группу, где пиперидинильная группа содержит заместитель формулы -A5-R8 в положении 4, в которой А представляет пропилен, и R8 представляет пиперидин-4-ил.
- 3. Соединение по п.1, в котором(i) R1 представляет метильную группу; и R2 представляет группу формулы -A1-NHCH3, в которой А1 представляет (СН2)m, СН2СН=СНСН2, СН2-фенилен-СН2 или СН2-циклогексилен-СН2, где m равно целому числу от 2 до 8; или(ii) R1 и R2 вместе представляют -(CH2)2-NH-(CH2)2-, -(CH2)2-N(CH3)-(СН2)2-, -(CH2)2-N(CH2CH3)-(CH2)2- или -(CH2)2-NH-(CH2)3-; иR3 и R4, каждый независимо представляет атом водорода.
- 4. Соединение по п.3, в котором(i) R1 представляет метильную группу; и R2 представляет группу формулы -А1-NHCH3, в которой А1 представляет (СН2)m, СН2СН=СНСН2 или СН2-(1,4-фенилен)-СН2, где m равно 2 или 3; или(ii) R1 и R2 вместе представляют -(CH2)2-NH-(CH2)2-, -(CH2)2-N(CH3)-(СН2)2-, -(CH2)2-N(CH2CH3)-(CH2)2- или -(CH2)2-NH-(CH2)3-.
- 5. Соединение по п.1, выбранное из3-[3,5-диметил-4-(3-оксо-3-пиперазин-1-илпропил)-1Н-пиррол-2-илметилен]-1,3-дигидроиндол-2-она;3-[3,5-диметил-4-[3-оксо-3-(4-этил)пиперазин-1-илпропил]-1Н-пиррол-2-илметилен]-1,3-дигидроиндол-2-она;3-[3,5-диметил-4-(3-оксо-3-гомопиперазин-1-илпропил)-1Н-пиррол-2-илметилен]-1,3-дигидроиндол-2-она;и их фармацевтически приемлемых солей.
- 7. Соединение по п.6, выбранное из:3-[3,5-диметил-4-(3-оксо-3-пиперазин-1-илпропил)-1Н-пиррол-2-илметилен]-1,3-дигидроиндол-2-она;3-[3,5-диметил-4-[3-оксо-3-(4-этил)пиперазин-1-илпропил]-1Н-пиррол-2-илметилен]-1,3-дигидроиндол-2-она и их фармацевтически приемлемых солей.
- 8. Соединение по п.7, которое является 3-[3,5-диметил-4-(3-оксо-3-пиперазин-1-илпропил)-1Н-пиррол-2-илметилен]-1,3-дигидроиндол-2-оном или его фармацевтически приемлемой солью.
- 9. Способ получения соединения по любому из пп.1-8, включающий взаимодействие соединения формулы (II)или его реакционноспособного производного с соединением формулы (III)или его соли, где R1, R2, R3 и R4 такие, как определено в п.1,с последующим, если необходима фармацевтически приемлемая соль, получением фармацевтически приемлемой соли.
- 10. Способ получения соединения по любому из пп.1-8, включающий, для соединения формулы (I), в которой R5 и R7 представляют атомом водорода, снятие защиты в соединении формулы (IV)в которой R1a и R2a имеют значения, определенные в п.1 для R1 и R2, кроме тех, в которых R5 или R7 заменены группами R5a или R7aсоответственно, где каждый из R5a или R7a представляет аминозащитную группу, и значения R3 и R4 определены в п.1,с последующим, если необходима фармацевтически приемлемая соль, получением фармацевтически приемлемой соли.
- 11. Фармацевтическая композиция, ингибирующая рецепторы тирозинкиназы, включающая терапевтически эффективное количество соединения по любому из пп.1-8, вместе с фармацевтически приемлемым разбавителем или носителем.
- 12. Соединение по каждому из пп.1-8, ингибирующее рецепторы тирозинкиназы.
- 13. Применение соединения по любому из пп.1-8 для производства лекарственных средств для лечения состояния, чувствительного к ингибитору тирозинкиназы.
- 14. Фармацевтическая композиция, ингибирующая рецепторы тирозинкиназы, для производства лекарственного средства для лечения состояния, чувствительного к ингибитору тирозинкиназы, включающая соединение по любому из пп.1-8.
- 15. Способ ингибирования рецепторов тирозинкиназы, который включает введение пациенту, нуждающемуся в таком ингибировании, терапевтически эффективного количества соединения по любому из пп.1-8.
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US34381301P | 2001-12-27 | 2001-12-27 | |
| US34374601P | 2001-12-27 | 2001-12-27 | |
| US60/343,813 | 2001-12-27 | ||
| US60/343,746 | 2001-12-27 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2004122918A RU2004122918A (ru) | 2005-03-27 |
| RU2316554C2 true RU2316554C2 (ru) | 2008-02-10 |
Family
ID=26993599
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2004122918/04A RU2316554C2 (ru) | 2001-12-27 | 2002-12-20 | Производные индолина, используемые как ингибиторы протеинкиназы |
Country Status (21)
| Country | Link |
|---|---|
| US (3) | US6686362B2 (ru) |
| EP (1) | EP1458713B1 (ru) |
| JP (1) | JP4363985B2 (ru) |
| KR (1) | KR100965519B1 (ru) |
| CN (1) | CN1290844C (ru) |
| AT (1) | ATE302771T1 (ru) |
| AU (1) | AU2002360753B2 (ru) |
| BR (1) | BR0215360A (ru) |
| CA (1) | CA2470480C (ru) |
| CO (1) | CO5611126A2 (ru) |
| DE (1) | DE60205776T2 (ru) |
| DK (1) | DK1458713T3 (ru) |
| ES (1) | ES2247411T3 (ru) |
| HU (1) | HUP0500111A3 (ru) |
| IL (1) | IL162203A0 (ru) |
| MX (1) | MXPA04006271A (ru) |
| NO (1) | NO327550B1 (ru) |
| NZ (1) | NZ533219A (ru) |
| PL (1) | PL208283B1 (ru) |
| RU (1) | RU2316554C2 (ru) |
| WO (1) | WO2003057690A1 (ru) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EA019481B1 (ru) * | 2009-08-04 | 2014-04-30 | Ле Лаборатуар Сервье | Новые дигидроиндолоновые соединения, способ их получения и фармацевтические композиции, содержащие их |
| RU2680826C2 (ru) * | 2013-07-12 | 2019-02-28 | Ле Лаборатуар Сервье | Новая соль 3-[(3-{ [4-(4-морфолинилметил)-1н-пиррол-2-ил]метилен} -2-оксо-2,3-дигидро-1н-индол-5-ил)метил]-1,3-тиазолидин-2,4-диона, ее получение и содержащие ее композиции |
Families Citing this family (29)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP4588447B2 (ja) * | 2002-08-09 | 2010-12-01 | セラヴァンス, インコーポレーテッド | 過剰増殖および関連疾患に関連するオンコキナーゼ融合ポリペプチド、これをコードする核酸、ならびにこれを検出する方法および同定する方法 |
| RU2006117635A (ru) * | 2003-10-24 | 2007-12-10 | Шеринг Акциенгезельшафт (De) | Производные индолинона и их применение для лечения патологических состояний, таких как злокачественное новообразование |
| JP2007513967A (ja) * | 2003-12-11 | 2007-05-31 | セラヴァンス, インコーポレーテッド | 変異レセプターチロシンキナーゼが駆動する細胞増殖性疾患の処置において使用するための組成物 |
| SE0401790D0 (sv) * | 2004-07-07 | 2004-07-07 | Forskarpatent I Syd Ab | Tamoxifen response in pre- and postmenopausal breast cancer patients |
| US20060281788A1 (en) | 2005-06-10 | 2006-12-14 | Baumann Christian A | Synergistic modulation of flt3 kinase using a flt3 inhibitor and a farnesyl transferase inhibitor |
| US7825244B2 (en) | 2005-06-10 | 2010-11-02 | Janssen Pharmaceutica Nv | Intermediates useful in the synthesis of alkylquinoline and alkylquinazoline kinase modulators, and related methods of synthesis |
| US8071768B2 (en) | 2005-06-10 | 2011-12-06 | Janssen Pharmaceutica, N.V. | Alkylquinoline and alkylquinazoline kinase modulators |
| EP1951234A2 (en) | 2005-10-18 | 2008-08-06 | Janssen Pharmaceutica N.V. | Method of inhibiting flt3 kinase |
| PL2021335T3 (pl) | 2006-04-20 | 2011-10-31 | Janssen Pharmaceutica Nv | Związki heterocykliczne jako inhibitory kinazy C-FMS |
| US8697716B2 (en) | 2006-04-20 | 2014-04-15 | Janssen Pharmaceutica Nv | Method of inhibiting C-KIT kinase |
| KR101367646B1 (ko) | 2006-04-20 | 2014-02-27 | 얀센 파마슈티카 엔.브이. | C-fms 키나제의 저해제 |
| CA2663147A1 (en) | 2006-09-11 | 2008-03-20 | Curis, Inc. | Substituted 2-indolinone as ptk inhibitors containing a zinc binding moiety |
| JO3240B1 (ar) | 2007-10-17 | 2018-03-08 | Janssen Pharmaceutica Nv | c-fms مثبطات كيناز |
| HUE045270T2 (hu) | 2010-01-05 | 2019-12-30 | Inst Nat Sante Rech Med | FLT3 receptor anatgonisták fájdalom rendellenességek kezelésére |
| JP5734313B2 (ja) | 2010-01-12 | 2015-06-17 | アーべー・シオンス | チアゾールおよびオキサゾールキナーゼ阻害剤 |
| AU2013299922B2 (en) | 2012-08-07 | 2018-06-21 | Janssen Pharmaceutica Nv | Process for the preparation of heterocyclic ester derivatives |
| JOP20180012A1 (ar) | 2012-08-07 | 2019-01-30 | Janssen Pharmaceutica Nv | عملية السلفنة باستخدام نونافلوروبوتانيسولفونيل فلوريد |
| TWI569799B (zh) | 2012-09-21 | 2017-02-11 | 安羅格製藥股份有限公司 | 抑制組成型活性磷酸化flt3激酶的方法 |
| BR112015016282A2 (en) | 2013-01-07 | 2017-07-11 | Arog Pharmaceuticals, Inc. | crenolanib for treatment of mutated flt3 proliferative disorders |
| US10463658B2 (en) | 2013-10-25 | 2019-11-05 | Videra Pharmaceuticals, Llc | Method of inhibiting FLT3 kinase |
| EP3174859B1 (en) | 2014-07-31 | 2020-04-29 | INSERM - Institut National de la Santé et de la Recherche Médicale | Flt3 receptor antagonists |
| EP3254698A1 (en) | 2016-06-08 | 2017-12-13 | Universite De Montpellier | Flt3 receptor inhibitor at low dosage for the treatment of neuropathic pain |
| CA3024012A1 (en) | 2016-11-02 | 2018-05-11 | Arog Pharmaceuticals, Inc. | Crenolanib for treating flt3 mutated proliferative disorders associated mutations |
| US12534764B2 (en) | 2016-11-02 | 2026-01-27 | Arog Pharmaceuticals, Inc. | Crenolanib for treating FLT3 mutated proliferative disorders associated mutations |
| CA3062981A1 (en) | 2017-05-17 | 2018-11-22 | Inserm (Institut National De La Sante Et De La Recherche Medicale) | Flt3 inhibitors for improving pain treatments by opioids |
| WO2019057649A1 (en) | 2017-09-19 | 2019-03-28 | INSERM (Institut National de la Santé et de la Recherche Médicale) | METHODS AND PHARMACEUTICAL COMPOSITIONS FOR THE TREATMENT OF ACUTE MYELOID LEUKEMIA |
| US11713310B2 (en) | 2020-07-20 | 2023-08-01 | Arog Pharmaceuticals, Inc. | Crystal forms of crenolanib and methods of use thereof |
| US11969420B2 (en) | 2020-10-30 | 2024-04-30 | Arog Pharmaceuticals, Inc. | Combination therapy of crenolanib and apoptosis pathway agents for the treatment of proliferative disorders |
| WO2022090547A1 (en) | 2020-10-30 | 2022-05-05 | Dsm Ip Assets B.V. | Production of carotenoids by fermentation |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1999061422A1 (en) * | 1998-05-29 | 1999-12-02 | Sugen, Inc. | Pyrrole substituted 2-indolinone protein kinase inhibitors |
| RU2142460C1 (ru) * | 1989-02-23 | 1999-12-10 | Ф. Хоффманн-Ля Рош Аг | Замещенные пирролы и их фармацевтически приемлемые соли |
| WO2001060814A2 (en) * | 2000-02-15 | 2001-08-23 | Sugen, Inc. | Pyrrole substituted 2-indolinone protein kinase inhibitors |
Family Cites Families (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5880141A (en) | 1995-06-07 | 1999-03-09 | Sugen, Inc. | Benzylidene-Z-indoline compounds for the treatment of disease |
| CO4950519A1 (es) | 1997-02-13 | 2000-09-01 | Novartis Ag | Ftalazinas, preparaciones farmaceuticas que las comprenden y proceso para su preparacion |
| BR9916327A (pt) * | 1998-12-17 | 2001-09-18 | Hoffmann La Roche | Oxindóis de 4-alquenila (e alquinila) como inibidores de cinases dependentes de ciclina, em particular, cdk2 |
| JP2002533360A (ja) | 1998-12-31 | 2002-10-08 | スージェン・インコーポレーテッド | 蛋白質キナーゼ活性を調節するためおよび癌の化学療法において用いるための3−ヘテロアリーリデニル−2−インドリノン化合物 |
| DE19924401A1 (de) | 1999-05-27 | 2000-11-30 | Boehringer Ingelheim Pharma | Neue substituierte Indolinone, ihre Herstellung und ihre Verwendung als Arzneimittel |
| AU6998000A (en) | 1999-08-27 | 2001-03-26 | Boehringer Ingelheim Pharma Kg | Substituted indolinones as tyrosine kinase inhibitors |
| WO2001025238A2 (en) | 1999-10-06 | 2001-04-12 | Boehringer Ingelheim Pharmaceuticals, Inc. | Heterocyclic compounds useful as inhibitors of tyrosine kinases |
| UA75054C2 (ru) | 1999-10-13 | 2006-03-15 | Бьорінгер Інгельхайм Фарма Гмбх & Ко. Кг | Замещенные в положении 6 индолиноны, их получение и их применение как лекарственного средства |
| DE19949209A1 (de) | 1999-10-13 | 2001-04-19 | Boehringer Ingelheim Pharma | In 5-Stellung substituierte Indolinone, ihre Herstellung und ihre Verwendung als Arzneimittel |
| AU2576501A (en) | 1999-12-08 | 2001-06-18 | Advanced Medicine, Inc. | Protein kinase inhibitors |
| WO2002002551A1 (en) | 2000-06-30 | 2002-01-10 | Sugen, Inc. | 4-heteroaryl-3-heteroarylidenyl-2-indolinones and their use as protein kinase inhibitors |
| EA005809B1 (ru) | 2000-08-18 | 2005-06-30 | Милленниум Фармасьютикалз, Инк. | Производные хиназолина в качестве ингибиторов киназы |
| EP1349852A2 (en) | 2000-12-20 | 2003-10-08 | Sugen, Inc. | 4-(hetero)aryl substituted indolinones |
| JP4588447B2 (ja) | 2002-08-09 | 2010-12-01 | セラヴァンス, インコーポレーテッド | 過剰増殖および関連疾患に関連するオンコキナーゼ融合ポリペプチド、これをコードする核酸、ならびにこれを検出する方法および同定する方法 |
| JP2007513967A (ja) * | 2003-12-11 | 2007-05-31 | セラヴァンス, インコーポレーテッド | 変異レセプターチロシンキナーゼが駆動する細胞増殖性疾患の処置において使用するための組成物 |
-
2002
- 2002-12-20 BR BR0215360-2A patent/BR0215360A/pt not_active IP Right Cessation
- 2002-12-20 EP EP02796035A patent/EP1458713B1/en not_active Expired - Lifetime
- 2002-12-20 NZ NZ533219A patent/NZ533219A/en not_active IP Right Cessation
- 2002-12-20 MX MXPA04006271A patent/MXPA04006271A/es active IP Right Grant
- 2002-12-20 WO PCT/US2002/041252 patent/WO2003057690A1/en not_active Ceased
- 2002-12-20 CN CNB028261399A patent/CN1290844C/zh not_active Expired - Fee Related
- 2002-12-20 DE DE60205776T patent/DE60205776T2/de not_active Expired - Lifetime
- 2002-12-20 RU RU2004122918/04A patent/RU2316554C2/ru not_active IP Right Cessation
- 2002-12-20 AU AU2002360753A patent/AU2002360753B2/en not_active Ceased
- 2002-12-20 IL IL16220302A patent/IL162203A0/xx unknown
- 2002-12-20 CA CA2470480A patent/CA2470480C/en not_active Expired - Fee Related
- 2002-12-20 AT AT02796035T patent/ATE302771T1/de active
- 2002-12-20 JP JP2003558005A patent/JP4363985B2/ja not_active Expired - Fee Related
- 2002-12-20 KR KR1020047010148A patent/KR100965519B1/ko not_active Expired - Fee Related
- 2002-12-20 US US10/327,385 patent/US6686362B2/en not_active Expired - Lifetime
- 2002-12-20 DK DK02796035T patent/DK1458713T3/da active
- 2002-12-20 HU HU0500111A patent/HUP0500111A3/hu unknown
- 2002-12-20 ES ES02796035T patent/ES2247411T3/es not_active Expired - Lifetime
- 2002-12-20 PL PL369602A patent/PL208283B1/pl not_active IP Right Cessation
-
2003
- 2003-10-22 US US10/691,094 patent/US7060703B2/en not_active Expired - Lifetime
-
2004
- 2004-07-08 NO NO20042926A patent/NO327550B1/no not_active IP Right Cessation
- 2004-07-22 CO CO04070253A patent/CO5611126A2/es not_active Application Discontinuation
-
2006
- 2006-02-21 US US11/358,305 patent/US7223783B2/en not_active Expired - Lifetime
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2142460C1 (ru) * | 1989-02-23 | 1999-12-10 | Ф. Хоффманн-Ля Рош Аг | Замещенные пирролы и их фармацевтически приемлемые соли |
| WO1999061422A1 (en) * | 1998-05-29 | 1999-12-02 | Sugen, Inc. | Pyrrole substituted 2-indolinone protein kinase inhibitors |
| WO2001060814A2 (en) * | 2000-02-15 | 2001-08-23 | Sugen, Inc. | Pyrrole substituted 2-indolinone protein kinase inhibitors |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EA019481B1 (ru) * | 2009-08-04 | 2014-04-30 | Ле Лаборатуар Сервье | Новые дигидроиндолоновые соединения, способ их получения и фармацевтические композиции, содержащие их |
| RU2680826C2 (ru) * | 2013-07-12 | 2019-02-28 | Ле Лаборатуар Сервье | Новая соль 3-[(3-{ [4-(4-морфолинилметил)-1н-пиррол-2-ил]метилен} -2-оксо-2,3-дигидро-1н-индол-5-ил)метил]-1,3-тиазолидин-2,4-диона, ее получение и содержащие ее композиции |
| RU2680826C9 (ru) * | 2013-07-12 | 2019-03-01 | Ле Лаборатуар Сервье | Новая соль 3-[(3-{ [4-(4-морфолинилметил)-1н-пиррол-2-ил]метилен} -2-оксо-2,3-дигидро-1н-индол-5-ил)метил]-1,3-тиазолидин-2,4-диона, ее получение и содержащие ее композиции |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2316554C2 (ru) | Производные индолина, используемые как ингибиторы протеинкиназы | |
| CN115960088B (zh) | 一种新型冠状病毒主蛋白酶的抑制剂及其制备方法和用途 | |
| JP4917041B2 (ja) | タンパク質キナーゼ阻害剤としての化合物および組成物 | |
| RU2195461C2 (ru) | Пирамидо[5,4-d]пиримидины и лекарственные средства со свойствами ингибитора тирозинкиназы семейства рецепторов эпидермального фактора роста на их основе | |
| KR20190021345A (ko) | Egfr 저해제로 제공되는 아닐린 피리미딘 화합물의 결정 | |
| EP2698367A1 (en) | Benzimidazoles for the treatment of cancer | |
| WO2017016463A1 (zh) | Egfr抑制剂及其药学上可接受的盐和多晶型物及其应用 | |
| CN106543145B (zh) | c-Met激酶抑剂3-(4-氟苯基)嘧啶酮-5-甲酸酰胺衍生物、制备方法与应用 | |
| BR112020025013A2 (pt) | novos compostos de piridina e pirazina como inibidores do receptor 2 de canabinoide | |
| WO2021259049A1 (zh) | 吲哚类衍生物及其制备方法和应用 | |
| CN107089968A (zh) | 1‑(2‑氨基吡啶‑4‑基)‑3‑哌啶甲酰胺衍生物及其合成方法和应用 | |
| CN111471048B (zh) | 一种具有含氮桥环、螺环或并环结构的化合物及其用途 | |
| CN105693729A (zh) | 吲哚并[3,2-a]咔唑衍生物及其应用 | |
| JP2005524671A (ja) | 新規アゼパン誘導体類 | |
| CN110016052B (zh) | N-去乙基舒尼替尼的磷酰胺衍生物及其制备方法 | |
| HK1068886B (en) | Indolinone derivatives useful as protein kinase inhibitors | |
| ZA200404088B (en) | Indolinone derivatives useful as protein kinase inhibitors. | |
| CN120136896A (zh) | 二取代苯并咪唑类化合物及其用途 | |
| CN116120322A (zh) | 氮杂稠环酰胺类化合物的盐、其结晶形式及其用途 | |
| CN120865158A (zh) | 含吡唑结构的吲哚啉类化合物及其制备方法和应用 | |
| CN117946165A (zh) | 一种新型结构化合物axl抑制剂及其应用 | |
| CN116063298A (zh) | Wnt通路抑制剂的代谢物 | |
| WO2011102436A1 (ja) | TGF-βシグナル伝達阻害剤 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20111221 |