RU2313536C2 - Конкатемер пептида, индуцирующего выработку антител против аполипопротеина в-100, вакцина для лечения ожирения, способ получения конкатемера, полинуклеотид, экспрессирующий вектор - Google Patents
Конкатемер пептида, индуцирующего выработку антител против аполипопротеина в-100, вакцина для лечения ожирения, способ получения конкатемера, полинуклеотид, экспрессирующий вектор Download PDFInfo
- Publication number
- RU2313536C2 RU2313536C2 RU2003109439/13A RU2003109439A RU2313536C2 RU 2313536 C2 RU2313536 C2 RU 2313536C2 RU 2003109439/13 A RU2003109439/13 A RU 2003109439/13A RU 2003109439 A RU2003109439 A RU 2003109439A RU 2313536 C2 RU2313536 C2 RU 2313536C2
- Authority
- RU
- Russia
- Prior art keywords
- concatemer
- peptide
- vaccine
- pbl
- vector
- Prior art date
Links
- 108090000765 processed proteins & peptides Proteins 0.000 title claims abstract description 99
- 108091028732 Concatemer Proteins 0.000 title claims abstract description 35
- 229960005486 vaccine Drugs 0.000 title claims abstract description 33
- 208000008589 Obesity Diseases 0.000 title claims abstract description 28
- 235000020824 obesity Nutrition 0.000 title claims abstract description 28
- 239000013598 vector Substances 0.000 title claims abstract description 28
- 102000006991 Apolipoprotein B-100 Human genes 0.000 title claims abstract description 17
- 108010008150 Apolipoprotein B-100 Proteins 0.000 title claims abstract description 17
- 238000000034 method Methods 0.000 title claims abstract description 11
- 238000011282 treatment Methods 0.000 title claims abstract description 10
- 238000004519 manufacturing process Methods 0.000 title claims abstract description 5
- 108091033319 polynucleotide Proteins 0.000 title claims abstract 6
- 102000040430 polynucleotide Human genes 0.000 title claims abstract 6
- 239000002157 polynucleotide Substances 0.000 title claims abstract 6
- 230000001939 inductive effect Effects 0.000 title claims abstract 3
- 108010007622 LDL Lipoproteins Proteins 0.000 claims abstract description 15
- 102000007330 LDL Lipoproteins Human genes 0.000 claims abstract description 15
- 241000588724 Escherichia coli Species 0.000 claims abstract description 12
- 102000000853 LDL receptors Human genes 0.000 claims abstract description 4
- 108010001831 LDL receptors Proteins 0.000 claims abstract description 4
- 102000004882 Lipase Human genes 0.000 claims abstract description 4
- 239000004367 Lipase Substances 0.000 claims abstract description 4
- 108090001060 Lipase Proteins 0.000 claims abstract description 4
- 230000027455 binding Effects 0.000 claims abstract description 4
- 235000019421 lipase Nutrition 0.000 claims abstract description 4
- 125000003275 alpha amino acid group Chemical group 0.000 claims abstract 3
- 239000000243 solution Substances 0.000 claims description 40
- 102000004196 processed proteins & peptides Human genes 0.000 claims description 21
- 239000013604 expression vector Substances 0.000 claims description 4
- 238000002347 injection Methods 0.000 claims description 4
- 239000007924 injection Substances 0.000 claims description 4
- 239000000843 powder Substances 0.000 claims description 4
- 230000002265 prevention Effects 0.000 claims description 4
- 239000000839 emulsion Substances 0.000 claims description 3
- 239000000725 suspension Substances 0.000 claims description 3
- 230000009471 action Effects 0.000 claims description 2
- 239000000443 aerosol Substances 0.000 claims description 2
- 239000008187 granular material Substances 0.000 claims description 2
- 239000006187 pill Substances 0.000 claims description 2
- 239000006188 syrup Substances 0.000 claims description 2
- 235000020357 syrup Nutrition 0.000 claims description 2
- 239000003826 tablet Substances 0.000 claims description 2
- 230000001131 transforming effect Effects 0.000 claims description 2
- 239000007903 gelatin capsule Substances 0.000 claims 1
- 230000002068 genetic effect Effects 0.000 claims 1
- 230000000694 effects Effects 0.000 abstract description 7
- 239000000126 substance Substances 0.000 abstract description 7
- 239000003814 drug Substances 0.000 abstract description 3
- 230000005764 inhibitory process Effects 0.000 abstract 1
- 230000007721 medicinal effect Effects 0.000 abstract 1
- 238000011321 prophylaxis Methods 0.000 abstract 1
- 101150113162 pbl gene Proteins 0.000 description 60
- 241000699670 Mus sp. Species 0.000 description 34
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 34
- HVYWMOMLDIMFJA-DPAQBDIFSA-N cholesterol Chemical compound C1C=C2C[C@@H](O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCCC(C)C)[C@@]1(C)CC2 HVYWMOMLDIMFJA-DPAQBDIFSA-N 0.000 description 33
- 239000013612 plasmid Substances 0.000 description 27
- 108090000623 proteins and genes Proteins 0.000 description 22
- 102000004169 proteins and genes Human genes 0.000 description 22
- 239000000499 gel Substances 0.000 description 20
- 239000004202 carbamide Substances 0.000 description 17
- 108020004414 DNA Proteins 0.000 description 16
- 239000000872 buffer Substances 0.000 description 16
- XHVAWZZCDCWGBK-WYRLRVFGSA-M Aurothioglucose Chemical compound OC[C@H]1O[C@H](S[Au])[C@H](O)[C@@H](O)[C@@H]1O XHVAWZZCDCWGBK-WYRLRVFGSA-M 0.000 description 15
- 108091034117 Oligonucleotide Proteins 0.000 description 15
- 210000004027 cell Anatomy 0.000 description 15
- 108091005601 modified peptides Proteins 0.000 description 15
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 13
- JLCPHMBAVCMARE-UHFFFAOYSA-N [3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-hydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methyl [5-(6-aminopurin-9-yl)-2-(hydroxymethyl)oxolan-3-yl] hydrogen phosphate Polymers Cc1cn(C2CC(OP(O)(=O)OCC3OC(CC3OP(O)(=O)OCC3OC(CC3O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c3nc(N)[nH]c4=O)C(COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3CO)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cc(C)c(=O)[nH]c3=O)n3cc(C)c(=O)[nH]c3=O)n3ccc(N)nc3=O)n3cc(C)c(=O)[nH]c3=O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)O2)c(=O)[nH]c1=O JLCPHMBAVCMARE-UHFFFAOYSA-N 0.000 description 13
- 235000012000 cholesterol Nutrition 0.000 description 13
- 239000000203 mixture Substances 0.000 description 13
- 210000002966 serum Anatomy 0.000 description 12
- 241000699666 Mus <mouse, genus> Species 0.000 description 11
- 101100189471 Mus musculus Pbx1 gene Proteins 0.000 description 10
- 210000004369 blood Anatomy 0.000 description 10
- 239000008280 blood Substances 0.000 description 10
- 230000037396 body weight Effects 0.000 description 10
- 238000006243 chemical reaction Methods 0.000 description 10
- 239000012528 membrane Substances 0.000 description 10
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 9
- QKNYBSVHEMOAJP-UHFFFAOYSA-N 2-amino-2-(hydroxymethyl)propane-1,3-diol;hydron;chloride Chemical compound Cl.OCC(N)(CO)CO QKNYBSVHEMOAJP-UHFFFAOYSA-N 0.000 description 8
- 102000007592 Apolipoproteins Human genes 0.000 description 8
- 108010071619 Apolipoproteins Proteins 0.000 description 8
- 241001596967 Escherichia coli M15 Species 0.000 description 8
- 239000011347 resin Substances 0.000 description 8
- 229920005989 resin Polymers 0.000 description 8
- 238000002415 sodium dodecyl sulfate polyacrylamide gel electrophoresis Methods 0.000 description 8
- 238000001262 western blot Methods 0.000 description 8
- 238000008214 LDL Cholesterol Methods 0.000 description 7
- 108010058846 Ovalbumin Proteins 0.000 description 7
- 239000002671 adjuvant Substances 0.000 description 7
- 238000002474 experimental method Methods 0.000 description 7
- 150000002632 lipids Chemical class 0.000 description 7
- 239000002609 medium Substances 0.000 description 7
- 229940092253 ovalbumin Drugs 0.000 description 7
- 238000002264 polyacrylamide gel electrophoresis Methods 0.000 description 7
- 239000011780 sodium chloride Substances 0.000 description 7
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 7
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 6
- 241000283973 Oryctolagus cuniculus Species 0.000 description 6
- 230000000890 antigenic effect Effects 0.000 description 6
- 230000015572 biosynthetic process Effects 0.000 description 6
- 238000000502 dialysis Methods 0.000 description 6
- 239000001963 growth medium Substances 0.000 description 6
- 206010003210 Arteriosclerosis Diseases 0.000 description 5
- DBMJMQXJHONAFJ-UHFFFAOYSA-M Sodium laurylsulphate Chemical compound [Na+].CCCCCCCCCCCCOS([O-])(=O)=O DBMJMQXJHONAFJ-UHFFFAOYSA-M 0.000 description 5
- 239000000427 antigen Substances 0.000 description 5
- 102000036639 antigens Human genes 0.000 description 5
- 108091007433 antigens Proteins 0.000 description 5
- 208000011775 arteriosclerosis disease Diseases 0.000 description 5
- 201000010099 disease Diseases 0.000 description 5
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 5
- 238000001962 electrophoresis Methods 0.000 description 5
- 239000012634 fragment Substances 0.000 description 5
- 230000003287 optical effect Effects 0.000 description 5
- 239000006228 supernatant Substances 0.000 description 5
- 150000003626 triacylglycerols Chemical class 0.000 description 5
- 238000002965 ELISA Methods 0.000 description 4
- 102100029727 Enteropeptidase Human genes 0.000 description 4
- 108010013369 Enteropeptidase Proteins 0.000 description 4
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 4
- 230000000903 blocking effect Effects 0.000 description 4
- 239000003795 chemical substances by application Substances 0.000 description 4
- 210000002540 macrophage Anatomy 0.000 description 4
- 239000008188 pellet Substances 0.000 description 4
- 239000002244 precipitate Substances 0.000 description 4
- 239000011541 reaction mixture Substances 0.000 description 4
- 108091008146 restriction endonucleases Proteins 0.000 description 4
- 238000003786 synthesis reaction Methods 0.000 description 4
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- 229920001817 Agar Polymers 0.000 description 3
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 3
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 3
- 241001529936 Murinae Species 0.000 description 3
- 239000002033 PVDF binder Substances 0.000 description 3
- 108010067902 Peptide Library Proteins 0.000 description 3
- 229920001213 Polysorbate 20 Polymers 0.000 description 3
- 108010062497 VLDL Lipoproteins Proteins 0.000 description 3
- 239000008272 agar Substances 0.000 description 3
- AZDRQVAHHNSJOQ-UHFFFAOYSA-N alumane Chemical class [AlH3] AZDRQVAHHNSJOQ-UHFFFAOYSA-N 0.000 description 3
- 150000001413 amino acids Chemical group 0.000 description 3
- 238000000137 annealing Methods 0.000 description 3
- 229940098773 bovine serum albumin Drugs 0.000 description 3
- 238000005119 centrifugation Methods 0.000 description 3
- 230000000295 complement effect Effects 0.000 description 3
- 239000003480 eluent Substances 0.000 description 3
- ZMMJGEGLRURXTF-UHFFFAOYSA-N ethidium bromide Chemical compound [Br-].C12=CC(N)=CC=C2C2=CC=C(N)C=C2[N+](CC)=C1C1=CC=CC=C1 ZMMJGEGLRURXTF-UHFFFAOYSA-N 0.000 description 3
- 229960005542 ethidium bromide Drugs 0.000 description 3
- 238000000605 extraction Methods 0.000 description 3
- 239000000945 filler Substances 0.000 description 3
- 235000013305 food Nutrition 0.000 description 3
- 235000021588 free fatty acids Nutrition 0.000 description 3
- 230000003053 immunization Effects 0.000 description 3
- 238000002649 immunization Methods 0.000 description 3
- 230000006698 induction Effects 0.000 description 3
- 230000007246 mechanism Effects 0.000 description 3
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 3
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 3
- 229920002981 polyvinylidene fluoride Polymers 0.000 description 3
- 238000002360 preparation method Methods 0.000 description 3
- 238000000746 purification Methods 0.000 description 3
- 238000010186 staining Methods 0.000 description 3
- 239000003656 tris buffered saline Substances 0.000 description 3
- QRXMUCSWCMTJGU-UHFFFAOYSA-N 5-bromo-4-chloro-3-indolyl phosphate Chemical compound C1=C(Br)C(Cl)=C2C(OP(O)(=O)O)=CNC2=C1 QRXMUCSWCMTJGU-UHFFFAOYSA-N 0.000 description 2
- HRPVXLWXLXDGHG-UHFFFAOYSA-N Acrylamide Chemical compound NC(=O)C=C HRPVXLWXLXDGHG-UHFFFAOYSA-N 0.000 description 2
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 2
- 102000014914 Carrier Proteins Human genes 0.000 description 2
- 108010078791 Carrier Proteins Proteins 0.000 description 2
- 102000012410 DNA Ligases Human genes 0.000 description 2
- 108010061982 DNA Ligases Proteins 0.000 description 2
- 108010000912 Egg Proteins Proteins 0.000 description 2
- 102000002322 Egg Proteins Human genes 0.000 description 2
- 102000004190 Enzymes Human genes 0.000 description 2
- 108090000790 Enzymes Proteins 0.000 description 2
- 239000004471 Glycine Substances 0.000 description 2
- 108010023302 HDL Cholesterol Proteins 0.000 description 2
- 108010010234 HDL Lipoproteins Proteins 0.000 description 2
- 102000015779 HDL Lipoproteins Human genes 0.000 description 2
- 208000035150 Hypercholesterolemia Diseases 0.000 description 2
- 208000031226 Hyperlipidaemia Diseases 0.000 description 2
- 108010046315 IDL Lipoproteins Proteins 0.000 description 2
- 108010028554 LDL Cholesterol Proteins 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- UZQJVUCHXGYFLQ-AYDHOLPZSA-N [(2s,3r,4s,5r,6r)-4-[(2s,3r,4s,5r,6r)-4-[(2r,3r,4s,5r,6r)-4-[(2s,3r,4s,5r,6r)-3,5-dihydroxy-6-(hydroxymethyl)-4-[(2s,3r,4s,5s,6r)-3,4,5-trihydroxy-6-(hydroxymethyl)oxan-2-yl]oxyoxan-2-yl]oxy-3,5-dihydroxy-6-(hydroxymethyl)oxan-2-yl]oxy-3,5-dihydroxy-6-(hy Chemical compound O([C@H]1[C@H](O)[C@@H](CO)O[C@H]([C@@H]1O)O[C@H]1[C@H](O)[C@@H](CO)O[C@H]([C@@H]1O)O[C@H]1CC[C@]2(C)[C@H]3CC=C4[C@@]([C@@]3(CC[C@H]2[C@@]1(C=O)C)C)(C)CC(O)[C@]1(CCC(CC14)(C)C)C(=O)O[C@H]1[C@@H]([C@@H](O[C@H]2[C@@H]([C@@H](O[C@H]3[C@@H]([C@@H](O[C@H]4[C@@H]([C@@H](O[C@H]5[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O5)O)[C@H](O)[C@@H](CO)O4)O)[C@H](O)[C@@H](CO)O3)O)[C@H](O)[C@@H](CO)O2)O)[C@H](O)[C@@H](CO)O1)O)[C@@H]1O[C@H](CO)[C@@H](O)[C@H](O)[C@H]1O UZQJVUCHXGYFLQ-AYDHOLPZSA-N 0.000 description 2
- 239000012190 activator Substances 0.000 description 2
- 238000007792 addition Methods 0.000 description 2
- 238000001042 affinity chromatography Methods 0.000 description 2
- BFNBIHQBYMNNAN-UHFFFAOYSA-N ammonium sulfate Chemical compound N.N.OS(O)(=O)=O BFNBIHQBYMNNAN-UHFFFAOYSA-N 0.000 description 2
- 229910052921 ammonium sulfate Inorganic materials 0.000 description 2
- 235000011130 ammonium sulphate Nutrition 0.000 description 2
- 229960000723 ampicillin Drugs 0.000 description 2
- AVKUERGKIZMTKX-NJBDSQKTSA-N ampicillin Chemical compound C1([C@@H](N)C(=O)N[C@H]2[C@H]3SC([C@@H](N3C2=O)C(O)=O)(C)C)=CC=CC=C1 AVKUERGKIZMTKX-NJBDSQKTSA-N 0.000 description 2
- 210000003719 b-lymphocyte Anatomy 0.000 description 2
- 239000007853 buffer solution Substances 0.000 description 2
- -1 cachet Substances 0.000 description 2
- 238000011088 calibration curve Methods 0.000 description 2
- 230000006037 cell lysis Effects 0.000 description 2
- 239000001913 cellulose Substances 0.000 description 2
- 229920002678 cellulose Polymers 0.000 description 2
- 235000010980 cellulose Nutrition 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 238000004587 chromatography analysis Methods 0.000 description 2
- 150000001875 compounds Chemical class 0.000 description 2
- 238000012790 confirmation Methods 0.000 description 2
- 238000007796 conventional method Methods 0.000 description 2
- 239000003085 diluting agent Substances 0.000 description 2
- 238000004090 dissolution Methods 0.000 description 2
- 239000012153 distilled water Substances 0.000 description 2
- 229940079593 drug Drugs 0.000 description 2
- 230000002708 enhancing effect Effects 0.000 description 2
- 125000000487 histidyl group Chemical group [H]N([H])C(C(=O)O*)C([H])([H])C1=C([H])N([H])C([H])=N1 0.000 description 2
- 230000002209 hydrophobic effect Effects 0.000 description 2
- 210000003016 hypothalamus Anatomy 0.000 description 2
- 238000011534 incubation Methods 0.000 description 2
- 230000002401 inhibitory effect Effects 0.000 description 2
- 238000003780 insertion Methods 0.000 description 2
- 230000037431 insertion Effects 0.000 description 2
- 238000004255 ion exchange chromatography Methods 0.000 description 2
- 229930027917 kanamycin Natural products 0.000 description 2
- 229960000318 kanamycin Drugs 0.000 description 2
- SBUJHOSQTJFQJX-NOAMYHISSA-N kanamycin Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CN)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](N)[C@H](O)[C@@H](CO)O2)O)[C@H](N)C[C@@H]1N SBUJHOSQTJFQJX-NOAMYHISSA-N 0.000 description 2
- 229930182823 kanamycin A Natural products 0.000 description 2
- 239000002502 liposome Substances 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 229920002521 macromolecule Polymers 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- 239000002245 particle Substances 0.000 description 2
- 229920002401 polyacrylamide Polymers 0.000 description 2
- 238000011160 research Methods 0.000 description 2
- 239000012064 sodium phosphate buffer Substances 0.000 description 2
- 238000006467 substitution reaction Methods 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- DGVVWUTYPXICAM-UHFFFAOYSA-N β‐Mercaptoethanol Chemical compound OCCS DGVVWUTYPXICAM-UHFFFAOYSA-N 0.000 description 2
- IHUKVJKKTBLTEE-QMMMGPOBSA-N (2s)-2-acetamido-5-[[amino-(methylcarbamoylamino)methylidene]amino]-n-methylpentanamide Chemical compound CNC(=O)NC(N)=NCCC[C@H](NC(C)=O)C(=O)NC IHUKVJKKTBLTEE-QMMMGPOBSA-N 0.000 description 1
- HSINOMROUCMIEA-FGVHQWLLSA-N (2s,4r)-4-[(3r,5s,6r,7r,8s,9s,10s,13r,14s,17r)-6-ethyl-3,7-dihydroxy-10,13-dimethyl-2,3,4,5,6,7,8,9,11,12,14,15,16,17-tetradecahydro-1h-cyclopenta[a]phenanthren-17-yl]-2-methylpentanoic acid Chemical compound C([C@@]12C)C[C@@H](O)C[C@H]1[C@@H](CC)[C@@H](O)[C@@H]1[C@@H]2CC[C@]2(C)[C@@H]([C@H](C)C[C@H](C)C(O)=O)CC[C@H]21 HSINOMROUCMIEA-FGVHQWLLSA-N 0.000 description 1
- ASWBNKHCZGQVJV-UHFFFAOYSA-N (3-hexadecanoyloxy-2-hydroxypropyl) 2-(trimethylazaniumyl)ethyl phosphate Chemical compound CCCCCCCCCCCCCCCC(=O)OCC(O)COP([O-])(=O)OCC[N+](C)(C)C ASWBNKHCZGQVJV-UHFFFAOYSA-N 0.000 description 1
- QRXMUCSWCMTJGU-UHFFFAOYSA-L (5-bromo-4-chloro-1h-indol-3-yl) phosphate Chemical compound C1=C(Br)C(Cl)=C2C(OP([O-])(=O)[O-])=CNC2=C1 QRXMUCSWCMTJGU-UHFFFAOYSA-L 0.000 description 1
- WURBVZBTWMNKQT-UHFFFAOYSA-N 1-(4-chlorophenoxy)-3,3-dimethyl-1-(1,2,4-triazol-1-yl)butan-2-one Chemical compound C1=NC=NN1C(C(=O)C(C)(C)C)OC1=CC=C(Cl)C=C1 WURBVZBTWMNKQT-UHFFFAOYSA-N 0.000 description 1
- PRBJTPCAKUBWAO-UHFFFAOYSA-N 2-aminoacetic acid;pentanedial Chemical compound NCC(O)=O.O=CCCCC=O PRBJTPCAKUBWAO-UHFFFAOYSA-N 0.000 description 1
- WBTFUMUXXHWTLD-UHFFFAOYSA-N 4-phenoxybutan-2-ol Chemical compound CC(O)CCOC1=CC=CC=C1 WBTFUMUXXHWTLD-UHFFFAOYSA-N 0.000 description 1
- 102000002260 Alkaline Phosphatase Human genes 0.000 description 1
- 108020004774 Alkaline Phosphatase Proteins 0.000 description 1
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 1
- 102000005666 Apolipoprotein A-I Human genes 0.000 description 1
- 108010059886 Apolipoprotein A-I Proteins 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- 108010004103 Chylomicrons Proteins 0.000 description 1
- 241000037164 Collema parvum Species 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- 229920002271 DEAE-Sepharose Polymers 0.000 description 1
- 238000001712 DNA sequencing Methods 0.000 description 1
- 239000001828 Gelatine Substances 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- SXRSQZLOMIGNAQ-UHFFFAOYSA-N Glutaraldehyde Chemical compound O=CCCCC=O SXRSQZLOMIGNAQ-UHFFFAOYSA-N 0.000 description 1
- 241000700721 Hepatitis B virus Species 0.000 description 1
- 108091006054 His-tagged proteins Proteins 0.000 description 1
- 101000889953 Homo sapiens Apolipoprotein B-100 Proteins 0.000 description 1
- 206010020772 Hypertension Diseases 0.000 description 1
- 108060003951 Immunoglobulin Proteins 0.000 description 1
- 229920001202 Inulin Polymers 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- 108010013563 Lipoprotein Lipase Proteins 0.000 description 1
- 102100022119 Lipoprotein lipase Human genes 0.000 description 1
- 102000004895 Lipoproteins Human genes 0.000 description 1
- 108090001030 Lipoproteins Proteins 0.000 description 1
- 239000006137 Luria-Bertani broth Substances 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- 102000018697 Membrane Proteins Human genes 0.000 description 1
- 108010052285 Membrane Proteins Proteins 0.000 description 1
- 239000000020 Nitrocellulose Substances 0.000 description 1
- 108091028043 Nucleic acid sequence Proteins 0.000 description 1
- 206010057249 Phagocytosis Diseases 0.000 description 1
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 1
- 108091000080 Phosphotransferase Proteins 0.000 description 1
- 108010021757 Polynucleotide 5'-Hydroxyl-Kinase Proteins 0.000 description 1
- 102000008422 Polynucleotide 5'-hydroxyl-kinase Human genes 0.000 description 1
- 108010008281 Recombinant Fusion Proteins Proteins 0.000 description 1
- 102000007056 Recombinant Fusion Proteins Human genes 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- 229940126530 T cell activator Drugs 0.000 description 1
- 210000001744 T-lymphocyte Anatomy 0.000 description 1
- 101710120037 Toxin CcdB Proteins 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- 229920000392 Zymosan Polymers 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 238000009825 accumulation Methods 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- NIXOWILDQLNWCW-UHFFFAOYSA-N acrylic acid group Chemical group C(C=C)(=O)O NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 239000011543 agarose gel Substances 0.000 description 1
- 229910021529 ammonia Inorganic materials 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 230000003579 anti-obesity Effects 0.000 description 1
- 230000002788 anti-peptide Effects 0.000 description 1
- 230000002421 anti-septic effect Effects 0.000 description 1
- 230000001363 autoimmune Effects 0.000 description 1
- 230000001580 bacterial effect Effects 0.000 description 1
- 239000000440 bentonite Substances 0.000 description 1
- 229910000278 bentonite Inorganic materials 0.000 description 1
- SVPXDRXYRYOSEX-UHFFFAOYSA-N bentoquatam Chemical compound O.O=[Si]=O.O=[Al]O[Al]=O SVPXDRXYRYOSEX-UHFFFAOYSA-N 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- 239000003613 bile acid Substances 0.000 description 1
- UDSAIICHUKSCKT-UHFFFAOYSA-N bromophenol blue Chemical compound C1=C(Br)C(O)=C(Br)C=C1C1(C=2C=C(Br)C(O)=C(Br)C=2)C2=CC=CC=C2S(=O)(=O)O1 UDSAIICHUKSCKT-UHFFFAOYSA-N 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 239000000378 calcium silicate Substances 0.000 description 1
- 229910052918 calcium silicate Inorganic materials 0.000 description 1
- 235000012241 calcium silicate Nutrition 0.000 description 1
- OYACROKNLOSFPA-UHFFFAOYSA-N calcium;dioxido(oxo)silane Chemical compound [Ca+2].[O-][Si]([O-])=O OYACROKNLOSFPA-UHFFFAOYSA-N 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 235000020974 cholesterol intake Nutrition 0.000 description 1
- 150000001841 cholesterols Chemical class 0.000 description 1
- 238000003776 cleavage reaction Methods 0.000 description 1
- 238000010367 cloning Methods 0.000 description 1
- 238000004737 colorimetric analysis Methods 0.000 description 1
- 230000024203 complement activation Effects 0.000 description 1
- 239000012141 concentrate Substances 0.000 description 1
- 235000008504 concentrate Nutrition 0.000 description 1
- 230000021615 conjugation Effects 0.000 description 1
- 238000010276 construction Methods 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- NKLPQNGYXWVELD-UHFFFAOYSA-M coomassie brilliant blue Chemical compound [Na+].C1=CC(OCC)=CC=C1NC1=CC=C(C(=C2C=CC(C=C2)=[N+](CC)CC=2C=C(C=CC=2)S([O-])(=O)=O)C=2C=CC(=CC=2)N(CC)CC=2C=C(C=CC=2)S([O-])(=O)=O)C=C1 NKLPQNGYXWVELD-UHFFFAOYSA-M 0.000 description 1
- 208000029078 coronary artery disease Diseases 0.000 description 1
- 239000000287 crude extract Substances 0.000 description 1
- 238000012217 deletion Methods 0.000 description 1
- 230000037430 deletion Effects 0.000 description 1
- 239000012150 desalination buffer Substances 0.000 description 1
- 238000000586 desensitisation Methods 0.000 description 1
- 239000008121 dextrose Substances 0.000 description 1
- 235000005911 diet Nutrition 0.000 description 1
- 230000037213 diet Effects 0.000 description 1
- 235000014113 dietary fatty acids Nutrition 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 235000013345 egg yolk Nutrition 0.000 description 1
- 210000002969 egg yolk Anatomy 0.000 description 1
- 238000010828 elution Methods 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 238000006911 enzymatic reaction Methods 0.000 description 1
- 239000006167 equilibration buffer Substances 0.000 description 1
- 230000003203 everyday effect Effects 0.000 description 1
- 239000000284 extract Substances 0.000 description 1
- 239000000194 fatty acid Substances 0.000 description 1
- 229930195729 fatty acid Natural products 0.000 description 1
- 150000004665 fatty acids Chemical class 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 238000011049 filling Methods 0.000 description 1
- 239000000796 flavoring agent Substances 0.000 description 1
- 235000013355 food flavoring agent Nutrition 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 150000004676 glycans Chemical class 0.000 description 1
- 102000052249 human APOB Human genes 0.000 description 1
- 239000003906 humectant Substances 0.000 description 1
- 230000028993 immune response Effects 0.000 description 1
- 230000036039 immunity Effects 0.000 description 1
- 230000005847 immunogenicity Effects 0.000 description 1
- 102000018358 immunoglobulin Human genes 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- JYJIGFIDKWBXDU-MNNPPOADSA-N inulin Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)OC[C@]1(OC[C@]2(OC[C@]3(OC[C@]4(OC[C@]5(OC[C@]6(OC[C@]7(OC[C@]8(OC[C@]9(OC[C@]%10(OC[C@]%11(OC[C@]%12(OC[C@]%13(OC[C@]%14(OC[C@]%15(OC[C@]%16(OC[C@]%17(OC[C@]%18(OC[C@]%19(OC[C@]%20(OC[C@]%21(OC[C@]%22(OC[C@]%23(OC[C@]%24(OC[C@]%25(OC[C@]%26(OC[C@]%27(OC[C@]%28(OC[C@]%29(OC[C@]%30(OC[C@]%31(OC[C@]%32(OC[C@]%33(OC[C@]%34(OC[C@]%35(OC[C@]%36(O[C@@H]%37[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O%37)O)[C@H]([C@H](O)[C@@H](CO)O%36)O)[C@H]([C@H](O)[C@@H](CO)O%35)O)[C@H]([C@H](O)[C@@H](CO)O%34)O)[C@H]([C@H](O)[C@@H](CO)O%33)O)[C@H]([C@H](O)[C@@H](CO)O%32)O)[C@H]([C@H](O)[C@@H](CO)O%31)O)[C@H]([C@H](O)[C@@H](CO)O%30)O)[C@H]([C@H](O)[C@@H](CO)O%29)O)[C@H]([C@H](O)[C@@H](CO)O%28)O)[C@H]([C@H](O)[C@@H](CO)O%27)O)[C@H]([C@H](O)[C@@H](CO)O%26)O)[C@H]([C@H](O)[C@@H](CO)O%25)O)[C@H]([C@H](O)[C@@H](CO)O%24)O)[C@H]([C@H](O)[C@@H](CO)O%23)O)[C@H]([C@H](O)[C@@H](CO)O%22)O)[C@H]([C@H](O)[C@@H](CO)O%21)O)[C@H]([C@H](O)[C@@H](CO)O%20)O)[C@H]([C@H](O)[C@@H](CO)O%19)O)[C@H]([C@H](O)[C@@H](CO)O%18)O)[C@H]([C@H](O)[C@@H](CO)O%17)O)[C@H]([C@H](O)[C@@H](CO)O%16)O)[C@H]([C@H](O)[C@@H](CO)O%15)O)[C@H]([C@H](O)[C@@H](CO)O%14)O)[C@H]([C@H](O)[C@@H](CO)O%13)O)[C@H]([C@H](O)[C@@H](CO)O%12)O)[C@H]([C@H](O)[C@@H](CO)O%11)O)[C@H]([C@H](O)[C@@H](CO)O%10)O)[C@H]([C@H](O)[C@@H](CO)O9)O)[C@H]([C@H](O)[C@@H](CO)O8)O)[C@H]([C@H](O)[C@@H](CO)O7)O)[C@H]([C@H](O)[C@@H](CO)O6)O)[C@H]([C@H](O)[C@@H](CO)O5)O)[C@H]([C@H](O)[C@@H](CO)O4)O)[C@H]([C@H](O)[C@@H](CO)O3)O)[C@H]([C@H](O)[C@@H](CO)O2)O)[C@@H](O)[C@H](O)[C@@H](CO)O1 JYJIGFIDKWBXDU-MNNPPOADSA-N 0.000 description 1
- 229940029339 inulin Drugs 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 239000004816 latex Substances 0.000 description 1
- 229920000126 latex Polymers 0.000 description 1
- 230000037356 lipid metabolism Effects 0.000 description 1
- 210000004185 liver Anatomy 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- 239000000594 mannitol Substances 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 230000004060 metabolic process Effects 0.000 description 1
- 239000002207 metabolite Substances 0.000 description 1
- 229920000609 methyl cellulose Polymers 0.000 description 1
- 239000001923 methylcellulose Substances 0.000 description 1
- 235000010981 methylcellulose Nutrition 0.000 description 1
- LXCFILQKKLGQFO-UHFFFAOYSA-N methylparaben Chemical compound COC(=O)C1=CC=C(O)C=C1 LXCFILQKKLGQFO-UHFFFAOYSA-N 0.000 description 1
- 238000004452 microanalysis Methods 0.000 description 1
- 239000002480 mineral oil Substances 0.000 description 1
- 235000010446 mineral oil Nutrition 0.000 description 1
- 239000003226 mitogen Substances 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 238000010172 mouse model Methods 0.000 description 1
- 208000010125 myocardial infarction Diseases 0.000 description 1
- JPXMTWWFLBLUCD-UHFFFAOYSA-N nitro blue tetrazolium(2+) Chemical compound COC1=CC(C=2C=C(OC)C(=CC=2)[N+]=2N(N=C(N=2)C=2C=CC=CC=2)C=2C=CC(=CC=2)[N+]([O-])=O)=CC=C1[N+]1=NC(C=2C=CC=CC=2)=NN1C1=CC=C([N+]([O-])=O)C=C1 JPXMTWWFLBLUCD-UHFFFAOYSA-N 0.000 description 1
- 229920001220 nitrocellulos Polymers 0.000 description 1
- 239000003921 oil Substances 0.000 description 1
- 230000014207 opsonization Effects 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 239000006174 pH buffer Substances 0.000 description 1
- 230000008782 phagocytosis Effects 0.000 description 1
- 230000004526 pharmaceutical effect Effects 0.000 description 1
- 150000003904 phospholipids Chemical class 0.000 description 1
- 239000011574 phosphorus Substances 0.000 description 1
- 229910052698 phosphorus Inorganic materials 0.000 description 1
- 102000020233 phosphotransferase Human genes 0.000 description 1
- 239000013600 plasmid vector Substances 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 229920001282 polysaccharide Polymers 0.000 description 1
- 239000005017 polysaccharide Substances 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 239000000047 product Substances 0.000 description 1
- 108020001775 protein parts Proteins 0.000 description 1
- 238000001742 protein purification Methods 0.000 description 1
- 238000004445 quantitative analysis Methods 0.000 description 1
- 239000001397 quillaja saponaria molina bark Substances 0.000 description 1
- 230000009257 reactivity Effects 0.000 description 1
- 230000002207 retinal effect Effects 0.000 description 1
- NCYCYZXNIZJOKI-OVSJKPMPSA-N retinal group Chemical group C\C(=C/C=O)\C=C\C=C(\C=C\C1=C(CCCC1(C)C)C)/C NCYCYZXNIZJOKI-OVSJKPMPSA-N 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 229930182490 saponin Natural products 0.000 description 1
- 150000007949 saponins Chemical class 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- 230000007017 scission Effects 0.000 description 1
- 239000013049 sediment Substances 0.000 description 1
- 238000004062 sedimentation Methods 0.000 description 1
- 235000020183 skimmed milk Nutrition 0.000 description 1
- ZFMRLFXUPVQYAU-UHFFFAOYSA-N sodium 5-[[4-[4-[(7-amino-1-hydroxy-3-sulfonaphthalen-2-yl)diazenyl]phenyl]phenyl]diazenyl]-2-hydroxybenzoic acid Chemical compound C1=CC(=CC=C1C2=CC=C(C=C2)N=NC3=C(C=C4C=CC(=CC4=C3O)N)S(=O)(=O)O)N=NC5=CC(=C(C=C5)O)C(=O)O.[Na+] ZFMRLFXUPVQYAU-UHFFFAOYSA-N 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 238000000527 sonication Methods 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 235000010356 sorbitol Nutrition 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 230000009870 specific binding Effects 0.000 description 1
- 238000001228 spectrum Methods 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 239000000454 talc Substances 0.000 description 1
- 229910052623 talc Inorganic materials 0.000 description 1
- 235000012222 talc Nutrition 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 230000032258 transport Effects 0.000 description 1
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/775—Apolipopeptides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/04—Anorexiants; Antiobesity agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/06—Antihyperlipidemics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- General Chemical & Material Sciences (AREA)
- Public Health (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Pharmacology & Pharmacy (AREA)
- Engineering & Computer Science (AREA)
- Toxicology (AREA)
- Genetics & Genomics (AREA)
- Diabetes (AREA)
- Hematology (AREA)
- Obesity (AREA)
- Zoology (AREA)
- Gastroenterology & Hepatology (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Molecular Biology (AREA)
- Child & Adolescent Psychology (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Medicinal Preparation (AREA)
Abstract
Изобретение относится к иммунологии и биотехнологии. Предложен конкатемер пептида, индуцирующий выработку антител против аполипопротеина В-100, которые ингибируют действие липазы и препятствуют связыванию LDL с рецептором LDL. Указанный конкатемер состоит из аминокислотной последовательности пептида, повторяющейся четыре раза. Аминокислотная последовательность приведена в описании. Описана вакцина для лечения и профилактики ожирения на основе конкатемера и способ получения конкатемера в Е.coli с использованием вектора. Раскрыт полинуклеотид, кодирующий конкатемер и экспрессирующий вектор, содержащий указанный полинуклеотид. Использование изобретения позволяет подавлять ожирение. 5 н. и 2 з.п. ф-лы, 1 табл., 12 ил.
Description
Область техники
Настоящее изобретение относится к вакцине для лечения ожирения. Конкретнее, настоящее изобретение относится к вакцине, которая включает миметический пептидный эпитоп аполипопротеина В-100, его конкатемеры или модифицированные пептиды.
Предпосылки изобретения
Липиды сыворотки крови включают холестерин, триглицериды (TG), свободные жирные кислоты, фосфолипиды и тому подобное, и находятся в кровяном русле в форме липопротеина, который представляет комплекс липида и аполипопротеина.
Из этих липопротеинов липопротеин низкой плотности (LDL) является основным носителем TG и холестерина. Значительно возросло число пациентов, страдающих артериосклерозом, заболеванием коронарных артерий или инфарктом миокарда, вызванных повышенным содержанием LDL-холестерина в крови, за счет изменения рациона или других факторов.
Следовательно, предпринимались различные исследования для снижения уровня LDL-холестерина и установления причины вышеуказанных заболеваний для лечения пациентов, страдающих вышеуказанными заболеваниями.
LDL-холестерин, основной этиологический фактор при заболеваниях у взрослых, связанных с метаболизмом липидов, может превращаться под действием макрофагов в липопротеин высокой плотности (HDL). Кроме того, LDL-холестерин может также превратиться в другое вещество или превратиться в желчную кислоту в печени (Brown M.S. and Goldstein J.L., 1983, Annu. Rev. Biochem., 52:223-261).
Аполипопротеин В-100 представляет основную белковую часть LDL и находится также в липопротеине очень низкой плотности (VLDL) и хиломикроне. LDL-холестерин в крови можно удалить посредством фагоцитоза с участием макрофагов в случае, когда стимулируется образование антител, распознающих аполипопротеин В-100, поскольку аполипопротеин В-100 приводит к тому, что частицы LDL связываются с LDL-рецепторами, расположенными на поверхности клеток (Dalum I. et al., 1997, Mol. Immunol., 34(16-17): 1113-20).
В случае, когда макромолекула такая, как антитело, связывается с аполипопротеином В-100, который находится на поверхности LDL, липаза такая, как липопротеинлипаза, не может гидролизовать TG и тому подобное, за счет стерического несоответствия, вызванного тем, что макромолекула связана с аполипопротеином В-100. Следовательно, образование свободных жирных кислот, основного фактора для возникновения ожирения, можно ингибировать с помощью антител, которые могут связываться с аполипопротеином В-100.
Недавно было предпринято несколько исследований с целью снижения уровня LDL-холестерина и подавления возникновения артериосклероза с использованием вакцины на различных моделях на животных, таких как мышь или кролик. Например, C.R.Alving сообщил, что холестерин можно модифицировать метаболитами или его окислением и что модифицированный холестерин в некоторых случаях может быть сильным антигенным детерминантом (Alving C.R. et al., 1989, Biochem. Soc. Trans., 17(4): 637-9; Alving C.R. et al., 1996, J. Lab. Clin. Med., 127: 40-49; Alving C.R. et al., 1996, Curr. Top. Microbiol. Immunol., 210: 181-6).
Кроме того, сообщалось, что в сыворотке крови имеются эндогенные антитела к холестерину (Wu J.T., L.L., 1997, Clin. Lab. Med., 17(3): 595-604, Review). Также сообщалось, что в опыте, в котором у кроликов индуцировался артериосклероз и гиперхолестеринемия при скармливании содержащего холестерин корма, проявление гиперхолестеринемии и артериосклероза у кроликов, иммунизированных введением содержащих холестерин липосом, подавлялось или заметно снижалось по сравнению с контрольной группой.
Таким антителом, индуцированным вакциной к холестерину, является иммуноглобулин М (IgM), который связывается с VLDL, липопротеином промежуточной плотности (IDL) и LDL. Основываясь на вышесказанном, полагается, что возможно создание вакцины для лечения или профилактики гиперлипидемии или артериосклероза, вызванных высоким уровнем холестерина (Bailey J.M., 1994, Science, 264: 1067-1068; Palinski W. et al., 1995, Proc. Natl. Acad. Sci. U.S.A., 92(3): 821-5: Wu R. et al., 1999, Hypertension, 33(1): 53-9).
Заявители установили, что ожирение можно эффективно предотвратить миметическим пептидным эпитопом аполипопротеина В-100, и, основываясь на вышесказанном, разработали вакцину для лечения ожирения.
Раскрытие изобретения
Следовательно, целью настоящего изобретения является обеспечение миметического пептида для эпитопа аполипопротеина В-100, его конкатемера и модифицированных пептидов.
Другой целью настоящего изобретения является обеспечение способа получения вышеуказанного миметического пептида для эпитопа аполипопротеина В-100, его конкатемера и модифицированных пептидов.
Еще одной целью настоящего изобретения является обеспечение вакцины для лечения или профилактики ожирения, которая включает вышеуказанный миметический пептид для эпитопа аполипопротеина В-100, его конкатемер и модифицированные пептиды.
Цель настоящего изобретения достигается обеспечением миметического пептида для эпитопа аполипопротеина В-100, его конкатемера и модифицированных пептидов.
В настоящем изобретении использовалась библиотека пептидов фага для скрининга эпитопа человеческого аполипопротеина В-100, связанного с моноклональными антителами (MabB23). Подвергнутые скринингу вышеуказанные пептиды представляли миметические пептиды, в структурном отношении близкие к антигенной детерминанте, которая может распознаваться антителами, и данные миметические пептиды были синтезированы согласно аминокислотной последовательности подвергнутых скринингу пептидов.
Библиотека пептидов представляет способ поиска трехмерной формы антигенной детерминанты. То есть, фрагменты ДНК, которые кодируют произвольно секвенированные пептиды, вставляют в ДНК, которая кодирует минорный белок оболочки фага, и затем вставляют в RF (рамку считывания) ДНК и трансформируют в E.coli для их экспрессии. Экспрессированные на поверхности E.coli пептиды подвергают взаимодействию с антигеном для того, чтобы отобрать пептиды, структурно близкие к антигенной детерминанте.
Для того, чтобы получить антисыворотку, мышей иммунизируют введением вышеуказанных миметических пептидов. Было доказано, что полученная таким образом антисыворотка распознает первоначальный аполипопротеин В-100 и одновременно миметические пептиды и LDL (Identification of Antigenic Determinants for the Murine Monoclonal Antibodies Against Apolipoprotein A-1 and Apolipoprotein B-100 by using Phage-displayed Random Peptide library, Chi-Hoon Kim, Hanyang Univ., 1997).
Миметический пептид для эпитопа аполипопротеина В-100 по настоящему изобретению можно выбрать из пептидов с последовательностями SEQ.ID. № 1, SEQ.ID. № 2, SEQ.ID. № 3 или их комбинаций.
Миметические пептиды по настоящему изобретению можно использовать в форме конкатемера для того, чтобы улучшить их антигенную детерминанту. В качестве осуществления настоящего изобретения можно связать два или более миметических пептида друг с другом. Желателен конкатемер, состоящий из трех (3) - пятнадцати (15) пептидов. Более предпочтительно конкатемер по настоящему изобретению включает четыре (4) пептида с последовательностью SEQ.ID. № 1.
«Конкатемер» вышеуказанного миметического пептида по настоящему изобретению относится к полимеру, в котором концы вышеуказанных миметических пептидов связаны друг с другом.
«Модифицированный пептид» вышеуказанного миметического пептида по настоящему изобретению относится к вариантам миметических пептидов, которые могут распознаваться моноклональными или поликлональными антителами к аполипопротеину В-100. Такие варианты включают замены, делеции, добавления и химические замены одной или более аминокислот в миметическом пептиде по настоящему изобретению.
Еще одной целью настоящего изобретения является обеспечение способа получения миметического пептида, его конкатемера и модифицированных пептидов, который включает: i) стадию вставки ДНК, которая кодирует вышеуказанный миметический пептид, его конкатемер или модифицированный пептид, в вектор; ii) стадию трансформации вышеуказанного вектора в клетки-хозяева и затем их инкубацию и iii) стадию выделения вышеуказанного миметического пептида, его конкатемера или модифицированных пептидов из клеток-хозяев.
Приготовление вакцины можно проводить любым общепринятым способом с миметическим пептидом, его конкатемером или модифицированными пептидами по настоящему изобретению. Предпочтительно, чтобы в способе получения вышеуказанного препарата композиция, в которой активное соединение смешано или разбавлено иммунным адъювантом, препаратом для усиления иммунитета, носителем, наполнителем или разбавителем, была выбрана из группы, состоящей из таблетки, пилюли, гранулы, порошка, облатки, суспензии, эмульсии, жидкости, сиропа, аэрозоля, мягкой или твердой желатиновой капсулы, стерильного раствора для инъекций, стерильного порошка и тому подобное.
Иммунный адъювант, который можно использовать в композиции по настоящему изобретению, представляет вид белков, содержащих эпитоп Т-клеток (например, поверхностный белок вируса гепатита В), инертный носитель, такой как соль алюминия, бентонит, латекс, акриловую частицу и тому подобное; гидрофобный антиген (например, липид), эмульсии вода-масло и масло-вода, образователь депо (например, полисахарид), активатор Т-клеток, такой как PPD, полиаденин, полиурацил и тому подобное; активатор В-клеток (например, В-клеточный митоген), поверхностно-активное вещество, такое как сапонин, лизолецитин, ретинал, квил А (quil A), липосому и тому подобное; вещество для усиления активности макрофагов и активаторы альтернативного пути комплемента, такие как инулин, зимозан, эндотозин, лебамизол, С. parvum и тому подобное.
«Белок-носитель» по настоящему изобретению означает фармацевтически приемлемое вещество, такое как белок или соль алюминия, которые могут транспортировать миметический пептид, его конкатемер и модифицированные пептиды по настоящему изобретению, по кровяному руслу.
В качестве подходящих носителей, наполнителей или разбавителей в композиции по настоящему изобретению можно использовать соль алюминия, феноксиэтилэтанол, воду, физиологический раствор, лактозу, декстрозу, сахарозу, сорбит, маннит, силикат кальция, целлюлозу, метилцеллюлозу, аморфную целлюлозу, поливинилпирролидон, метилгидроксибензоат, пропилгидроксибензоат, тальк, стеарат магния и минеральное масло.
Кроме того, композиция по настоящему изобретению дополнительно может включать наполнитель, антикогезивный агент, лубрикант, увлажнитель, ароматизатор, эмульгатор и антисептик.
Композиция по настоящему изобретению может быть составлена обычным способом, хорошо известным в данной области, для индукции иммунного ответа у млекопитающего при одном (1) или более введениях.
Вакцину для лечения ожирения по настоящему изобретению можно вводить различными путями, такими как оральное, накожное, внутрикожное, внутривенное или внутримышечное введение, предпочтительно внутрикожное введение.
Эффективная доза вакцины по настоящему изобретению составляет 0,1-10 мкг (активного пептида) на кг массы тела, предпочтительно 0,5-1,0 мкг на кг. Однако реальную дозу активного вещества вакцины можно определить в зависимости от нескольких факторов, таких как иммунный статус, пути введения, состояние пациента, возраст, пол, масса тела и тому подобное. Следовательно, пределы указанных доз никоим образом не ограничивают объем настоящего изобретения.
Основным фармацевтическим действием вакцины по настоящему изобретению является профилактика или лечение ожирения посредством механизма, при котором антитела, индуцированные миметическим пептидом, его конкатемером или модифицированными пептидами, связываются с эпитопом аполипопротеина В-100 на поверхности LDL и тем самым стерически препятствуют и ингибируют липазу, которая участвует в образовании жирных кислот, являющихся основным этиологическим фактором ожирения.
Кроме того, вакцина по настоящему изобретению обладает действием подавлять гиперлипидемию посредством механизма, при котором LDL обнаруживается и легко удаляется макрофагом с помощью опсонизации, вызванной человеческими антителами, индуцированными миметическим пептидом, его конкатемером или модифицированными пептидами и конъюгированными с эпитопом аполипопротеина В-100 на поверхности LDL.
Другим фармацевтическим действием композиции по настоящему изобретению является профилактика или лечение ожирения путем подавления накопления липидов, таких как холестерин свободных жирных кислот в клетке, посредством механизма, при котором человеческие антитела, индуцированные миметическим пептидом, его конкатемером или модифицированными пептидами, связываются с эпитопом аполипопротеина В-100 на поверхности LDL, и тем самым препятствуют специфическому связыванию LDL с LDL-рецептором, расположенным на поверхности клеток.
Краткое описание фигур
Вышеуказанные цели и другие преимущества настоящего изобретения станут более понятными при подробном описании его предпочтительного осуществления при обращении к прилагаемым фигурам, на которых:
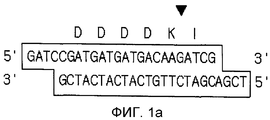
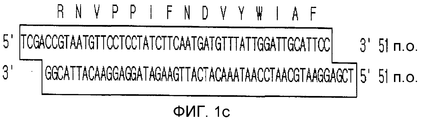
На фигурах 1а-1d представлены структуры и состав вектора для экспрессии миметического пептида по настоящему изобретению. На фиг. 1а представлена структура лидерной кассеты, на фиг. 1d представлена структура кассеты LB, на фигуре 1с представлена структура кассеты BL и на фигуре 1d представлена структура вектора экспрессии рВХ4.
На фигуре 2 представлены способы получения вектора рВХ1 и рВХ4 для экспрессии миметического пептида по настоящему изобретению.
На фигуре 3 представлены результаты электрофореза в полиакриламидном геле (PAGE), проведенного для идентификации кассеты LB.
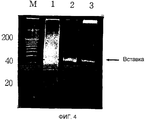
На фигуре 4 представлены результаты PAGE, проведенного для идентификации кассеты BL, включенной в плазмиду pBlue-BL.
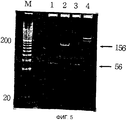
На фигуре 5 представлены результаты PAGE, проведенного для подтверждения направления и числа копий ДНК, вставленной в плазмиду pBX1 и pBX3.
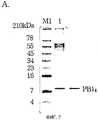
На фигуре 6 представлены результаты вестерн-блоттинга, проведенного для идентификации экспрессированного пептида PBl4.
На фигуре 7 представлены результаты PAGE с добавлением додецилсульфата натрия (SDS), проведенного для подтверждения очищенного пептида PBl4.
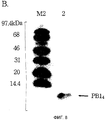
На фигуре 8 представлены результаты вестерн-блоттинга, проведенного для подтверждения реакционной способности очищенного пептида PBl4 против анти-PBl4-сыворотки.
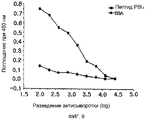
На фигуре 9 представлены результаты ELISA, проведенного для определения авидности мышиных антител, индуцированных пептидом PBl4.
На фигуре 10 представлен график, который показывает подавляющее действие PBl4 на увеличение массы тела мыши.
На фигурах 11а и 11b представлены графики, показывающие изменение массы тела мышей в зависимости от введения вакцины PBl4 по настоящему изобретению через 20 недель после введения препарата, который может нарушить функцию гипоталамуса.
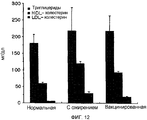
На фигуре 12 представлен график, который представляет влияние на концентрацию липидов в сыворотке крови при введении вакцины PBl4.
Наилучший способ осуществления настоящего изобретения
В последующем настоящее изобретение будет описано подробнее. Однако настоящее изобретение, поясняемое ниже, представлено только для пояснения осуществления настоящего изобретения и не предназначено для ограничения объема настоящего изобретения.
Пример 1: синтез и отжиг олигонуклеотида
Олигонуклеотиды получали химическим синтезом в Genemed Synthesis (San Francisco, CA, США) по последовательности, предоставленной настоящими заявителями. Для фосфорилирования 5'-конца олигонуклеотидов, 50 мкл 100 пмоль/мкл олигонуклеотида инкубировали с 10 мкл 10 мМ АТФ, 3 мкл 10 Е/мкл полинуклеотидкиназы Т4 (Takara, Otsu, Япония) и 7 мкл 10Х буфера для киназы в течение двух (2) ч при 37°С.
Каждую аликвотную пробу объемом 10 мкл вышеуказанных фосфорилированных олигонуклеотидов смешивали вместе, нагревали при 80°С в течение 5 мин и затем медленно охлаждали до комнатной температуры, проводя таким образом отжиг с получением специфической конъюгации комплементарных цепей.
Пример 2: лигирование
Смесь для проведения лигирования готовили смешением 1 мкл ДНК-вектора, 5 мкл ДНК-вставки, 1 мкл ДНК-лигазы Т4 (NEB, Beverly, MA, США), 1 мкл 10Х буферного раствора для ферментной реакции (NEB, Beverly, MA) и 2 мкл дистиллированной воды, затем инкубировали при 16°С в течение ночи.
Пример 3: конструирование экспрессирующего вектора рВХ для экспрессии миметического пептида аполипопротеина В-100
Стадия 1: планирование вектора
Плазмида-вектор для экспрессии миметического пептида обычно включает лидерную кассету и один или более генов пептида PBl. Как показано на фигуре 1, плазмиду рВХ1, которая включает один (1) ген PBl, получали клонированием лидерной кассеты (фиг. 1а) в сайт для поликлонирования плазмиды pQE30 (Qiagen, Hilden, Германия). Полученную плазмиду расщепляли HindIII и SalI и небольшой фрагмент замещали кассетой LB (фиг. 1b) с получением плазмиды рВХ1, которая подходит для удобной вставки множественных количеств кассеты BL (фиг. 1с).
Между тем, плазмиду pBluescript II SK+ расщепляли SalI и XhoI и лигировали с кассетами BL, где имели место производные единичные-множественные вставки кассеты BL. Отбирали предполагаемые повторы генов пептида PBl в плазмиде pBlue-BL, вырезали и субклонировали в pBX1 (фиг. 1d).
Стадия 2: получение вектора для экспрессии монопептида PBl
Лидерную кассету готовили отжигом олигонуклеотидов с последовательностями SEQ.ID. № 10 и SEQ.ID. № 11, синтезированных таким же способом, как в примерах 1 и 2. Затем вектор рQE30 (Qiagen, Hilden, Германия), который был расщеплен SalI и BamHI, лигировали с вышеуказанной лидерной кассетой для получения плазмиды pQE-лидер. В результате экспрессии вышеуказанного вектора pQE30 дополнительно включали шесть остатков гистидина в N-конец экспрессированного белка для удобной очистки белка. Вышеуказанную лидерную кассету конструировали с включением сайта узнавания (DDDDKI; SEQ.ID. № 12) для энтерокиназы для уменьшения до минимума дополнительных аминокислот.
По способу примера 1 синтезировали четыре олигонуклеотида, последовательности которых представлены SEQ.ID. № 4-7, фосфорилировали и затем отжигали соответственно с комплементарными олигонуклеотидами для синтеза кассеты LB, представленной на фигуре 1b (SEQ.ID. № 13 и 14). 40 мкл отожженных олигонуклеотидов смешивали с 3 мкл 1 Е/мкл ДНК-лигазы Т4, 5 мкл 10Х буфера для фермента и 2 мкл дистиллированной воды с получением смеси для лигирования. Затем смесь для лигирования инкубировали в течение ночи для связывания олигонуклеотидов друг с другом.
После завершения реакции реакционную смесь наносили на 20% полиакриламидный гель и проводили электрофорез. Кассету LB (олигонуклеотиды размером 52 п.о.) (фиг. 3) идентифицировали при окрашивании геля этидиумом бромидом (EtBr).
На фигуре 3 полоса М является ступенчатым фрагментом ДНК размером 20 п.о., и полоса 1 представляет реакционный раствор. Кассету LB извлекали из геля с помощью набора для экстракции из геля QIAEX II (Qiagen, Hilden, Германия).
Вышеуказанную плазмиду pQE30-лидер расщепляли HindIII и SalI и затем лигировали с вышеуказанной кассетой LB, следуя способу в примере 2, с получением вектора для экспрессии миметического пептида PBl. Полученный экспрессирующий вектор называли рВХ1 и пептид, экспрессированный вектором, называли пептидом PBl1 (смотри фиг. 2).
Стадия 3: получение вектора для экспрессии конкатемера пепетида PBl
1
По способу примера 1 синтезировали четыре олигонуклеотида, последовательности которых представлены SEQ.ID. № 4, 5, 8 и 9, фосфорилировали и затем отжигали соответственно с комплементарными олигонуклеотидами для синтеза кассеты BL на фигуре 1с (SEQ.ID. № 15 и 16). Затем данные олигонуклеотиды лигировали друг с другом по способу стадии 2 и затем наносили на 20% полиакриламидный гель для электрофореза. Идентифицировали олигонуклеотиды размером 55 п.о. (лидерная кассета) при окрашивании геля EtBr. Кассету BL извлекали из геля с помощью набора для экстракции из геля QIAEX II и расщепляли SalI и XhoI.
Между тем, плазмиду pBluescript II SK (Stratagene, La Jolla, CA, США) расщепляли SalI и XhoI. Вектор подвергали электрофорезу в 0,8% агарозном геле и извлекали с помощью набора для экстракции из геля QIAEX II (Qiagen, Hilden, Германия).
Проводили такую же реакцию лигирования, как в примере 2, для получения плазмиды pBlue-BL с использованием 5 мкл ДНК-кассеты BL и 1 мкл вышеуказанного вырезанного ДНК-вектора.
pBlue-BL расщепляли SalI и XhoI и экстрагировали кассету BL. Плазмиду рВХ2 получали вставкой данной кассеты BL в сайт SalI вектора рВХ1, полученного на стадии 2. Кроме того, получали векторы рВХ3 и рВХ4, приготовленные изменением числа кассет BL, которые вставляли в сайт SalI вектора рВХ1, с двух (2) до трех (3) (смотри фиг. 2).
Пептиды, экспрессированные векторами рВХ2, рВХ3 и рВХ4, представляли конкатемер, который включал два (2) - четыре (4) пептида PBl. Они были названы соответственно PBl2, PBl3 и PBl4.
Стадия 4: идентификация вставки
Клетки-хозяева (E.coli M15 [pREP4]; Qiagen, Hilden, Германия) трансформировали плазмидой pBlue-BL и высевали на чашку с 1% агаром и затем инкубировали в течение 16 ч при 37°С для того, чтобы могли образоваться колонии E.coli. Одну из колоний, образовавшихся на чашке с агаром, вносили в 10 мл среды LB и инкубировали при встряхивании при 37°С в течение шестнадцати (16) ч и затем выделяли плазмиду с помощью системы для очистки ДНК (Wizard PLUS SV DNA miniprep DNA purification system; Promega, Madison, Wl, США). Плазмиду, выделенную из трансформированной E.coli, инкубировали с рестриктазами SalI и XhoI для расщепления при 37°С в течение одного (1) ч и анализировали 20% PAGE (фиг. 4). На фигуре 4 полоса М является ступенчатым фрагментом ДНК размером 20 п.о., полоса 1 представляет олигонуклеотидный продукт, полученный на стадии 3, полоса 2 представляет ДНК кассеты BL, выделенной 20% PAGE на стадии 3, и полоса 3 представляет рекомбинантную плазмиду pBlue-BL, обработанную рестриктазами. Как представлено на фигуре 4, было подтверждено, что плазмида pBlue-BL содержала кассету BL.
E.coli (М15[pREP4]) трансформировали плазмидой рВХ1 или рВХ3 и ДНК плазмиды выделяли, как пояснено выше, для подтверждения числа и ориентации вставок в ДНК кассеты. Выделенную плазмиду расщепляли рестриктазами SalI и HindIII и анализировали 20% PAGE (фиг. 5). На фигуре 5 полоса М является ступенчатым фрагментом ДНК размером 20 п.о., полосы 1 и 3 представляют плазмиду рВХ1, содержащую кассету LB, но не BL, полоса 2 представляет плазмиду, несущую одну кассету LB и две BL с нужным направлением. С другой стороны, полоса 4 представляет плазмиду, имеющую одну кассету LB и две BL, однако, в обратном направлении. Как показано на фигуре 5, по тому, как много кассет В (кассет BL или LB) было вставлено и в каком направлении они были вставлены в вектор рВХ, можно получить карту воздействия рестриктаз.
Кроме того, было подтверждено, что последовательность ДНК кассет В, включенных в плазмиду, которая была получена из трансформированной E.coli, идентична желаемым последовательностям. Плазмиды получали с помощью набора Wizard PLUS DNA miniprep и секвенировали с использованием набора для секвенирования ДНК Sequennase (Ver. 2.1) (Amersham, Cleveland, Великобритания).
Пример 4: экспрессия пептида PBl
4
в E.coli и его выделение
Стадия 1: подтверждение экспрессии пептида PBl
4
Для подтверждения экспрессии пептида PBl4 три вида трансформированных E.coli М15[pREP4] культивировали в бульонном агаре LB, содержащем ампициллин и канамицин. Один вид E.coli М15[pREP4] трансформировали плазмидой рВХ4, другой - ложно трансформировали pQE30, и еще один представлял нетрансформированную E.coli М15[pREP4]. Каждую из образовавшихся колоний переносили с твердой среды соответственно в жидкую среду LB, которая содержала 100 мкл/мл ампициллина и 25 мкл/мл канамицина, и инкубировали в течение ночи. Культуру инкубировали при 37°С в течение одного (1) часа при встряхивании, пока оптическая плотность при 600 нм не достигала пределов 0,5-0,7. Затем в культуральную среду вносили 1 мМ изопропилтио-β-галактопиранозида (IPTG) для усиления экспрессии рекомбинантного белка и дополнительно культивировали при 37°С в течение пяти (5) ч. Отбирали 1 мл культуральной среды и центрифугировали при 14000 об/мин в течение двух (2) мин для осаждения бактериальных клеток. Клеточный осадок, полученный при центрифугировании, суспендировали в 50 мкл 2Х раствора SDS [100 мМ Трис-Cl, рН 6,8, 20% глицерина (мас./об.), 4% SDS (мас./об), 2% 2-меркаптоэтанола, 0,001% бромфенола синего] для проведения SDS-PAGE. Суспендированный раствор нагревали при 95°С в течение пяти (5) мин, и затем 10 мкл раствора вносили в лунку залитого геля и проводили электрофорез при 20 мА в течение пяти (5) ч (Mighty Small II, Hoefer, США). Концентрация акриламида в концентрирующем геле и разделяющем геле, которые использовали, соответственно равнялась 5% и 15%, и использовали в качестве стандарта белка-маркера размера предварительно окрашенный стандарт SeeBlue (250 kDa - 4 kDa; NOVEX, San Diego, CA, США) и стандарт с широким пределом Mark12 (200 kDa - 2,5 kDa). После проведения электрофореза гель окрашивали кумасси бриллиантовым синим R-250 в течение одного (1) ч и краситель удаляли обесцвечивающим раствором (5% метанола и 7% уксусной кислоты) в течение десяти (10) ч.
Для подтверждения того, что экспрессированный белок представлял собой пептид PBl4, белки в геле для электрофореза подвергали вестерн-блоттингу с использованием кроличьих анти-РВ1-антител (фиг. 6). Антисыворотку получали иммунизацией яичным белком, конъюнгированным с пептидом PBl, полученным химическим синтезом в Bio-Synthesis, Inc. (Lewisville, TX, США). На фигуре 6 полоса М является меткой предварительно окрашенного стандарта SeeBlue, полоса 1 представляет среду, использованную для инкубации E.coli М15[pREP4], которую не трансформировали, полоса 2 представляет среду, использованную для инкубации E.coli М15[pREP4], которую трансформировали вектором рQE30, полоса 3 представляет среду, использованную для инкубации E.coli М15[pREP4], которую трансформировали вектором рВХ4.
Как представлено на фигуре 6, только трансформированная pВХ4 E.coli экспрессировала рекомбинантный пептид RBl4, обладающий специфическим иммунитетом в отношении мышиной анти-PBl-сыворотки.
Стадия 2: определение растворимости экспрессированного пептида
E.coli М15[pREP4], которая была трансформирована вектором рВХ4, инкубировали таким же способом, как на стадии 1. Отбирали 10 мл культуральной среды и центрифугировали для сбора клеток. Клеточный осадок, полученный при центрифугировании, суспендировали в 5 мл раствора для лизиса клеток (300 мМ NaCl, 50 мМ NaH2PO4, 10 мМ имидазола, рН 8,0) с получением естественного белка из клеток. После охлаждения раствор с суспендированным осадком обрабатывали ультразвуком при 20 циклах для лизиса клеток. Супернатант получали центрифугированием при 4°С, 10000 об/мин в течение 30 мин. С раствором смешивали такой же объем 2Х раствора SDS и проводили SDS-PAGE таким же способом, как описано на стадии 1. Затем каждый раствор прогревали при 95°С в течение 5 мин. В результате проведения SDS-PAGE было подтверждено, что пептид PBl4 можно выделить и очистить из растворимого экстракта А, входящего в состав нерастворимого неочищенного экстракта В.
Стадия 3: очистка пептида PBl
4
Стадия 3-1: аффинная хроматография
Для очистки рекомбинантного пептида, полученного на стадии 1, использовали смолу Ni-NTA для очистки His-меченых белков. Аффинная хроматография с использованием силы притяжения между насыщенным в смоле Ni+ и остатков гистидина на конце экспрессированного белка является хорошо известным методом удобной очистки интересующего белка.
Прежде всего, E.coli М15[pREP4], которую трансформировали рВХ4, вносили в 1 л культуральной среды LB и инкубировали при 37°С до того, как оптическая плотность при 600 нм была выше 0,6. Соотношение культуральной среды LB и вектора рВХ4 составляло пятьдесят (50) к одному (1). IPTG добавляли до конечной концентрации 1 мМ и вновь инкубировали в течение пяти (5) ч. После инкубации клеточный осадок получали центрифугированием культуральной среды при 6000g в течение 30 мин, и осадок хранили при -70°С в течение ночи. Осадок, оттаявший на льду, суспендировали в растворе для растворения (300 мМ NaCl, 50 мМ NaH2PO4, 10 мМ имидазола, рН 8,0), при этом использовали 5 мл раствора для растворения на 1 г осадка. Клетки лизировали обработкой ультразвуком таким же способом, как на стадии 2, и затем центрифугировали при комнатной температуре при 10000g в течение 30 мин. Такой же объем буфера (8М мочевины, 0,1 М NaH2PO4, 0,01 М Трис-HCl, рН 8,0), как и осадок, добавляли к клеточному дебрису для ресуспендирования и для денатурации белков в них, и раствор суспендированного осадка обрабатывали ультразвуком для того, чтобы больше белков могло раствориться в буфере. Суспензию центрифугировали при 8000 об/мин в течение 30 мин для удаления клеточного дебриса, который не солюбилизировался в 8М мочевине. К 4 мл вышеуказанного супернатанта добавляли 1 мл смолы Ni-NTA при 4°С и встряхивали при 200 об/мин в течение 2 ч для захвата белков, включающих His-метку.
Данный супернатант, содержащий комплекс белок/Ni-NTA осторожно наносили на хроматографическую колонку (размеры: 2 см (внутренний диаметр) × 2,7 см (высота)). После оседания смолы при открытии крышки пропускали избыток буфера. Колонку промывали 20 мл буфера для создания рН среды (8М мочевины, 0,1 М NaH2PO4, 0,01 М Трис-HCl, рН 8,0) и затем 20 мл другого буфера (8М мочевины, 0,1М NaH2PO4, 0,01 М Трис-HCl, рН 6,3) для вымывания белков, которые не были специфически связаны со смолой Ni-NTA. Целевые белки, содержащие His-метку, элюировали два (2) раза 5 мл буфера с низким рН (8М мочевины, 0,1 М NaH2PO4, 0,01 М Трис-HCl, рН 5,9), затем четыре (4) раза 5 мл сильно кислого буфера (8М мочевины, 0,1 М NaH2PO4, 0,01 М Трис-HCl, рН 4,5) и затем использовали SDS-PAGE для подтверждения элюированных целевых белков с использованием 15% акриламидного геля (фиг. 7). На фигуре 7 полоса М является предварительно окрашенным маркером размера SeeBlue, и полоса 7 представляет очищенный пептид PBl4.
Вышеуказанные очищенные белки диализовали против PBS (8 г/л NaCl, 0,2 г/л KCl, 1,44 г/л NaH2PO4, 0,24 г/л KH2PO4) для восстановления их первоначальной конформации. Использованные пробирки для диализа были с ограничением молекулярной массы 3500 Da. Во время диализа вначале в течение 5 ч использовали 3 л PBS, содержащего 2М мочевины, и затем использовали два (2) раза в течение ночи 5 л PBS без мочевины.
Стадия 3-2: гиброфобная хроматография
Гидрофобную хроматографию проводили для повышения чистоты пептида PBl4, который получали на стадии 3-1.
Сульфат аммония постепенно добавляли до конечной концентрации, равной 20%, к раствору, содержащему пептид PBl4, который элюировали со смолы Ni-NTA на стадии 3-1, и затем рН доводили до 7,0. Раствор выдерживали в течение трех или более часов, после того как полностью расплавилось 10% сульфата аммония, и затем раствор наносили на колонку с фенилсефарозой [наполнение: фенилсефарозная смола для быстрого элюирования (Pharmacia, Швеция); размеры колонки: 1 см (внутренний диаметр) × 3 см (высота)].
Каждую фракцию, которую элюировали из колонки пропусканием элюента (8М мочевины, 0,1 М NaH2PO4, 0,01 М Трис-HCl, рН 6,3) через колонку со скоростью элюента 0,5 мл/мин при обращенном градиенте сульфата аммония от 10% до 0%, наносили на гель для SDS-PAGE. Собирали фракцию, содержащую пептид PBl4, и диализовали в буферном растворе для обессоливания, и в то же самое время удаляли мочевину, которую использовали в качестве денатурирующего агента.
Стадия 3-3: удаление His-метки
2М мочевину добавляли к буферному раствору (50 мМ NaCl, 20 мМ Трис-HCl, 2 мМ CaCl2, рН 7,4), который был пригоден для удаления денатурирующего агента и имидазола и т.д. из очищенного His-меченого белка и также активации энтерокиназы. Диализованный пептид PBl4, полученный на стадии 3-2, вновь диализовали с использованием указанного содержащего мочевину буфера для обессоливания пептида PBl4, и во время чего концентрацию мочевины постепенно снижали повторным диализом против буфера с пониженным содержанием мочевины. К раствору, содержащему пептид PBl4, в котором буфер заменяли на указанный второй буфер, добавляли 3 Е/мл энтерокиназы и инкубировали при 23°С. Раствор отбирали каждый час, затем анализировали при помощи SDS-PAGE для проверки удаления His-метки из His-меченого пептида PBl (PBl4 +his).
Стадия 3-4: ионообменная хроматография
Нежелательные белки и пептиды, которые образовались в результате обработки энтерокиназой, удаляли ионообменной хроматографией.
Раствор, содержащий пептид PBl4 -his, который получали на стадии 3-3, диализовали в буфере для диализа (2М мочевины, 0,1 М NaH2PO4, 0,01 М Трис-HCl, рН 7,0) и буфер в значительной степени обменивался. Раствор, который диализовали, наносили на смолу с DEAE-сефарозой (Phamacia, Uppsala, Швеция). Затем колонку уравновешивали буфером для уравновешивания (50 мМ натриевого фосфатного буфера, 2М мочевины, рН 7,0) и пептид элюировали в градиенте концентрации NaCl от 0 до 1М с использованием другого буфера (50 мМ натриевого фосфатного буфера, 2М мочевины, 1М NaCl)(скорость элюента: 0,5 мл/мин). Получали каждую фракцию и накапливали содержащую целевой белок фракцию. Присутствие пептида PBl4 -his подтверждали с помощью SDS-PAGE после концентрирования отсеков.
Стадия 4: количественный анализ PBl
4
Очищенный пептид PBl4, который получали таким же способом, как на стадии 3, анализировали количественно колориметрическим методом с использованием реагента ВСА для микроанализа (Pierce, Rockford, США).
Стадия 5: подтверждение свойств рекомбинантного пептида PBl4
Чистоту пептидов PBl4, которые выделяли на стадии 3, и их иммуногенность против антисыворотки, которую получали с использованием синтетического пептида PBl4 в качестве антигена, определяли вестерн-блоттингом с помощью ECL (Amersham, Cleveland, Великобритания). После SDS-PAGE (пример 2, стадия 1) гель инкубировали вместе с мембраной PVDF в буфере (0,3% Трис, 1,5% глицина, 20% метанола) при постоянном напряжении 60 В в течение трех (3) ч для переноса белка с геля на мембрану PVDF. Затем блоттированную мембрану инкубировали с 5 мл блокирующего раствора (TBS, рН 7,5, 5% сухого обезжиренного молока (мас./об.), 0,02% Твин-20) в течение 1,5 ч и затем три раза промывали TTBS (забуференный Трисом физиологический раствор, содержащий 0,1% Твина-20) соответственно в течение 15 мин, 5 мин и 5 мин. Антисыворотку против пептида PBl (смотри стадию 1 в примере 2) разбавляли раствором TTBS в соотношении один (1) к пяти тысячам (5000) и затем инкубировали с мембраной в течение 1,5 ч. Для подтверждения чистоты пептида PBl4 использовали антисыворотку против пептида PBl4 (пример 3). После промывания геля TTBS три раза соответственно в течение 15 мин, 5 мин и 5 мин, мембрану инкубировали в течение 1,5 ч при комнатной температуре с раствором, в котором конъюгированный с щелочной фосфатазой F(ab)'2-козий антимышиный IgG (Н+L) (Zymed, San Fransisco, CA) разбавляли раствором TTBS в соотношении один (1) к одной тысяче (1000). Мембрану вновь промывали три раза TTBS и затем окрашивали при добавлении BCIP/NBT (5-бром-4-хлор-3-индолил фосфата/нитросинего тетразолия (Sigma)). Раствор BCIP/NBT удаляли с использованием раствора TTBS после окрашивания. В результате вестерн-блоттинга экспрессированный пептид PBl4 можно было распознать с помощью анти-PBl4-сыворотки.
В случае ECL, мембрану PVDF (Gelman Science, BioTraceR) использовали вместо нитроцеллюлозной мембраны. Кроме того, первые антитела использовали в соотношении один (1) к десяти тысячам (10000) и HRP-конъюгированный кроличий антимышиный IgG (Pierce, Rockford, IL, США) использовали в качестве вторых антител в соотношении один (1) к десяти тысячам (10000). 1 мл раствора А реагента для вестерн-блоттинга ECL+Plus (Amersham) на 25 мл раствора В использовали в цветной реакции. Когда окраска в достаточной мере развивалась, мембрану вставляли в пленочную кассету соответственно на 5, 10, 20 и 30 сек для воздействия пленки, чтобы полосы на геле можно было детектировать (фиг 8). На фигуре 8 полоса М является ECL детектирующей меткой (Gibco BRL), и полоса 1 представляет пептид PBl4. Как следует из фиг. 8, экспрессированный пептид PBl4 можно было распознавать с помощью анти-PBl4-сыворотки.
Кроме того, вестерн-блоттинг, при котором пептид PBl4 с использованием поликлональных антител, выделенных из кроличьей сыворотки, при применении колонки с белком G (Bio-Rad, США) давал те же результаты.
Пример 5: получение мышиных анти-пептид PBl
4
-антител
Использованный в данном случае пептид PBl4 представлял пептид PBl4 -his, из которого была удалена his-метка на стадии 3-3 примера 2.
Стадия 1: лигирование пептида PBl
4
и OVA
В качестве белка-носителя овальбумин (OVA) добавляли к очищенному на стадии 3 в примере 2 пептиду PBl4, в молярном соотношении один (1) к десяти (10), и инкубировали в течение одного (1) ч при 4°С. К раствору пептид PBl4-овальбумин добавляли 2% (об./об.) глутарового альдегида в том же объеме и инкубировали в течение одного (1) ч при постоянном встряхивании. Затем к реакционной смеси добавляли глицин, пока конечная концентрация не становилась равной 0,2 М, для остановки реакции.
После реакции оставшийся в реакционной смеси глутаровый альдегид-глицин удаляли диализом с использованием мембраны для диализа MWCO 12000-14000 (SpectrumR , Dominguez, CA, США).
Стадия 2: иммунизация мышей
Пептид, с которым связывали OVA на стадии 1, концентрировали и использовали для иммунизации мышей. Количество антигена, которое вводили мышам, составляло 5 мкг, что равнялось количеству пептида PBl4 до связывания с OVA. Антиген, эмульгированный таким же количеством адъюванта, вводили мышам внутрибрюшинно в объеме 0,2 мл.
Полный адъювант Фрейнда (CFA) использовали в качестве адъюванта для первой инъекции и неполный адъювант Фрейнда (IFA) использовали в качестве адъюванта при бустер-иммунизации два (2) раза с двух-(2)-недельным интервалом. Контрольным мышам вводили BSA (бычий сывороточный альбумин).
Через пять (5) дней после последней инъекции у мышей отбирали 1 мл крови при пункции сердца, и кровь сворачивалась в течение 30 мин при 37°С. Затем кровь центрифугировали в течение 30 мин при 4°С, 2500g и сгусток удаляли из крови. Супернатант (т.е. сыворотку крови) инкубировали в течение ночи при 4°С для полного концентрирования оставшихся коагулированных веществ крови и центрифугировали в течение 20 мин при 10000g. Полученный супернатант разливали в несколько пробирок. Сыворотку крови, которую использовали в опыте, хранили при 4°С, остальное хранили при -20°С.
Стадия 3: определение авидности анти-PBl
4
-антител непрямого ELISA
Авидность антител определяли с использованием сыворотки крови, полученной на стадии 2. По 100 мкл пептида PBl4 вносили в каждую лунку 96-луночного планшета для микротитрования (Flacon: про-связывание) и его оставляли одного при 4°С в течение 6 ч или более и затем три (3) раза промывали TTBS (забуференный Трисом физиологический раствор, содержащий 0,05% Твин-20). В каждую лунку добавляли 200 мкл блокирующего раствора (1% BSA в TTBS) и инкубировали при 37°С в течение одного (1) ч и затем промывали три (3) раза TTBS. 100 мкл выделенной сыворотки, разбавленной блокирующим раствором в соотношении один (1) к 102-105, добавляли к реакционному раствору и инкубировали при 37°С в течение 1 ч и затем промывали три (3) раза по 200 мкл TTBS. 100 мкл HRP-конъюгированных анти-кроличьих IgG антител (Pierce, Rockford, IL), разбавляли блокирующим раствором в соотношении один (1) к 103, добавляли к реакционному раствору и инкубировали при 37°С в течение 1 ч и промывали три (3) раза по 200 мкл TTBS. Раствор А набора субстратов HRP (Bio-Rad) смешивали с раствором В в соотношении девять (9) к одному (1). 100 мкл полученной смеси добавляли к реакционному раствору и окрашивали в течение тридцати (30) мин и затем определяли оптическое поглощение реакционной смеси при 405 нм, как в случае анализа ELISA (EL312e, Bio-Tek Ins.)(фиг. 9). На фигуре 9 показано, что мышиные антитела, специфические к пептиду PBl4, можно использовать для вестерн-блоттинга и ELISA при тысячном (1) разведении (3,0 на оси Х на фигуре).
Пример 6: действие вакцины PBl
4
против ожирения с использованием модели на мышах
Стадия 1: индукция ожирения у мышей
В данном случае использовали мышей ICK в возрасте 5 недель (Корейский центр по проведению опытов на животных, Сеул, Корея). Мышей выращивали в питомнике, в котором температуру поддерживали при 17-25°С и кормили смешанным кормом (Sam Yang Feed Ltd., Seoul, Корея [ингредиенты: вода 11,8% или более, белок 20,0% или более, сырые липиды 3,0% или более, сырая клетчатка 10,0% или ниже, сырая зола 10,0% или ниже, кальций 0,6% или ниже и фосфор 0,4% или более]. Для индукции ожирения мышам вводили голдтиоглюкозу (GTG). GTG обладает способностью индуцировать десенсибилизацию вентро-медиальных ядер гипоталамуса (VMH). Следовательно, мыши, которым вводили GTG, не чувствовали сытости, и у них всегда имелось желание есть. Использованная в данном случае GTG является очень нестабильным соединением, которое легко разлагается в воде или при наличии влаги. Следовательно, 100 мг GTG (Sigma, Inc.) разбавляли 1 мл кунжутного масла (Sigma, Inc.) и использовали по методу Brecher et al. (Brechere G. and Waxler S.H. Proc. Soc. Exp. Biol. Med., 70: 498-501 (1949)) для введения нужного количества GTG.
Мышей распределяли для формирования опытной (двадцать (20) мышей) и контрольной группы (четыре (4) мыши) и животным опытной группы вводили 25 мкл GTG, в то время, как контрольной группе ничего не вводили.
До опыта определяли массу тела мышей в опытной группе, и были отобраны и использованы в опыте мыши, у которых отклонение в массе тела было незначительным. Значения массы тела, определенные у мышей через одну (1) неделю после введения GTG, находились в пределах 26,5-29,5 г.
У семи мышей в группе с введением GTG было индуцировано ожирение, в то время как у остальной части нет. Мышам, у которых не было индуцировано ожирение, вновь вводили GTG, и в этом случае у всех мышей было индуцировано ожирение.
Всех мышей с индуцированным ожирением распределяли на три (3) группы. Через неделю после второго введения GTG мышам опытной группы 1, состоящей из семи (7) мышей, вводили пептид PBl4, полученный на стадии 2 примера 3. Кроме того, мышам (опытная группа 2, состоящая из семи (7) мышей) другой группы из трех вводили овальбумин вместо пептида PBl4 в качестве ложного опыта и вакцину не вводили другой группе (опытная группа 3, состоящая из шести (6) мышей) с индуцированным ожирением. С другой стороны, 0,2 мл PBC вводили контрольной группе для сравнения с опытными группами в целях подтверждения действия вакцины по настоящему изобретению.
Кроме того, корм, использованный в данном случае, смешивали с яичным желтком и высушивали при 50°С для повышения потребления холестерина таким образом, чтобы уровень холестерина в сыворотке крови мышей мог повышаться. Корм обеспечивали в достаточном количестве, чтобы вызвать заболевание, связанное с уровнем холестерина. Каждый день определяли массу тела у мышей.
Как показано на фигуре 10, масса тела мышей, которым вводили вакцину в опытной группе 1 возрастала с 27,7±0,4 г до 52,2±1,7 г через 12 недель после введения GTG. Данные дают основание сделать заключение о том, что достоверное различие в повышении массы тела у мышей опытной группы 1 и контрольной группы отсутствовало. Однако масса тела у мышей опытной группы 2 которым вводили овальбумин после возникновения ожирения и опытной группы 3 которым после индукции ожирения вакцину не вводили, постоянно возрастала от 28,3±0,5 г до 68,9±2,8 г. Следовательно, было показано, что ожирение можно подавлять введением вакцины на основе пептида PBl4.
На фигуре 10 G1 и G2 представляют время введения GTG и V1, V2 и V3 представляют время введения вакцины на основе пептида PBl4.
На фигуре 11 представлен внешний вид мыши с индуцированным ожирением. Мышь в возрасте 20 недель из опытной группы 1 (фиг. 11а: нормальная мышь) сравнивали с мышью в возрасте 20 недель из опытной группы 3 (фиг. 11b: мышь с ожирением). Как показано на фиг. 11, было подтверждено, что вакцина по настоящему изобретению эффективна для подавления ожирения.
Стадия 2: определение уровня холестерина в крови
После первого введения GTG сравнивали уровень холестерина в крови у мыши в возрасте 12 недель из контрольной группы с таковым у мыши в возрасте 12 недель, которой вводили GTG, из опытной группы 1 и 2. Концентрацию общего холестерина, триглицеридов, HDL-холестерина и LDL-холестерина определяли ферментативным методом с использованием наборов Cholestezyme-V, Triglyzyme-V, HDL-C555 (Shin Yang Chemicals, Seoul, Корея) и LDL-EX (Denka Bio-Research, Ltd., Tokyo, Япония). В каждом опыте по данным оптической плотности строили калибровочную кривую с использованием стандартного калибратора-D (Denka Bio-Research, Ltd., Tokyo, Япония) для уменьшения ошибки опыта. Интересующее значение оптической плотности определяли по калибровочной кривой для установления концентрации и состава липидов, полученные данные представлены в таблице 1 и на фигуре 12.
Как представлено в таблице 1 и на фигуре 12, в результате индукции ожирения было показано, что достоверное различие в составе холестерина у мышей в опытных группах и контроле отсутствовало, в то время как в целом концентрация в крови общего холестерина, HDL-С и LDL-С незначительно повышалась.
Промышленная применимость
Вакцина по настоящему изобретению, которая содержит миметический пептид для эпитопа аполипопротеина В-100, его конкатемеры и модифицированные пептиды, может подавлять возникновение ожирения, не вызывая аутоиммунных реакций в организме.
Следовательно, циркуляторное заболевание, связанное с LDL, можно лечить вакциной по настоящему изобретению более эффективно, чем временными и дорогостоящими обычными способами, при которых ингибируется фермент, связанный с обменом холестерина.
Несмотря на то, что настоящее изобретение было подробно показано и описано при обращении к его конкретным примерам, специалистам в данной области, очевидно, понятно, что можно осуществить различные изменения в форме и деталях, не отступая от сущности и объема настоящего изобретения, определенных прилагаемой формулой изобретения.
Claims (7)
1. Конкатемер пептида, индуцирующий выработку антител против аполипопротеина В-100, которые ингибируют действие липазы и препятствуют связыванию LDL с рецептором LDL, где указанный конкатемер включает четыре (4) пептида, аминокислотная последовательность каждого из которых представлена в SEQ.ID. №1.
2. Вакцина для лечения или профилактики ожирения, которая включает конкатемер по п.1.
3. Вакцина по п.2, где указанную вакцину вводят путем внутрикожной инъекции.
4. Вакцина по п.2, где тип указанной вакцины выбран из группы, состоящей из таблеток, пилюль, гранул, облаток, эликсиров, суспензий, эмульсии, раствора, сиропов, аэрозолей, мягких или твердых желатиновых капсул, стерильного раствора для инъекций и стерильного порошка.
5. Способ получения конкатемера по п.1, который включает
i) стадию вставки полинуклеотида, кодируещего генетическую информацию о конкатемере по п.1, в вектор;
ii) стадию трансформации E.coli вектором, полученным на стадии i), и инкубации трансформированных E.coli;
iii) стадию выделения конкатемера по п.1 из E.coli, инкубированных на стадии ii).
6. Полинуклеотид, кодирующий конкатемер по п.1.
7.Экспрессирующий вектор, который включает полинуклеотид, кодирующий конкатемер по п.1.
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR2000/0052055 | 2000-09-04 | ||
| KR20000052055 | 2000-09-04 | ||
| KR2001/0054005 | 2001-09-04 | ||
| KR10-2001-0054005A KR100472841B1 (ko) | 2000-09-04 | 2001-09-04 | 아포지단백질 비-100의 에피토프에 대한 모조 펩타이드,그들의 연쇄물 또는 변형체와 이들을 함유하는 백신 조성물 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2003109439A RU2003109439A (ru) | 2004-07-20 |
| RU2313536C2 true RU2313536C2 (ru) | 2007-12-27 |
Family
ID=26638363
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2003109439/13A RU2313536C2 (ru) | 2000-09-04 | 2001-09-04 | Конкатемер пептида, индуцирующего выработку антител против аполипопротеина в-100, вакцина для лечения ожирения, способ получения конкатемера, полинуклеотид, экспрессирующий вектор |
Country Status (18)
| Country | Link |
|---|---|
| US (1) | US6825318B2 (ru) |
| EP (1) | EP1315517B1 (ru) |
| JP (1) | JP2004508029A (ru) |
| CN (1) | CN1231262C (ru) |
| AU (1) | AU8628601A (ru) |
| BG (1) | BG106655A (ru) |
| BR (1) | BR0107175A (ru) |
| CA (1) | CA2389739A1 (ru) |
| CZ (1) | CZ20021571A3 (ru) |
| EE (1) | EE200200238A (ru) |
| HU (1) | HUP0203251A2 (ru) |
| IL (1) | IL149379A0 (ru) |
| LT (1) | LT4989B (ru) |
| MX (1) | MXPA02004505A (ru) |
| NO (1) | NO20022147D0 (ru) |
| RU (1) | RU2313536C2 (ru) |
| SK (1) | SK6312002A3 (ru) |
| WO (1) | WO2002020040A1 (ru) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1636356A1 (en) * | 2003-06-11 | 2006-03-22 | Schering Aktiengesellschaft | Novel modified corin molecules having substitute activation sequences and uses thereof |
| KR100639397B1 (ko) * | 2004-03-18 | 2006-10-26 | (주)에스제이바이오메드 | 항비만용 면역원성 하이브리드 폴리펩타이드 및 이를포함하는 항비만 백신 조성물 |
| US20070054298A1 (en) * | 2005-08-12 | 2007-03-08 | Kent Kirshenbaum | Methods for enzyme-mediated coupling of oligomers |
| US8961982B2 (en) * | 2005-12-16 | 2015-02-24 | The Regents Of The University Of California | Modulation of developmental immune programming and protection against cardiovascular disease, diabetes, infectious diseases, and cancer |
| WO2007075335A2 (en) * | 2005-12-16 | 2007-07-05 | The Regents Of The University Of California | Modulation of in utero immune programming |
| KR100956893B1 (ko) * | 2006-09-25 | 2010-05-11 | (주)에스제이바이오메드 | 항비만용 면역원성 하이브리드 폴리펩타이드 및 이를포함하는 항비만 백신 조성물 |
| CN103520713B (zh) * | 2013-10-16 | 2015-10-28 | 西北农林科技大学 | 一种ApoB100酵母重组疫苗及其制备方法和应用 |
| WO2017210360A1 (en) | 2016-05-31 | 2017-12-07 | Cardiovax, Llc | Methods for diagnosing and treating systemic lupus erythematosus |
| US10858422B2 (en) | 2016-05-31 | 2020-12-08 | Abcentra, Llc | Methods for treating systemic lupus erythematosus with an anti-apolipoprotein B antibody |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2283474A1 (en) * | 1997-03-04 | 1998-09-11 | Bio-Technology General Corp. | Isolation of tissue specific peptide ligands and their use for targeting pharmaceuticals to organs |
| WO1999045020A1 (en) * | 1998-03-04 | 1999-09-10 | Bio-Technology General Corp. | Isolation of tissue specific peptide ligands and their use for targeting pharmaceuticals to organs |
| EP1267908B1 (en) * | 2000-03-03 | 2004-05-06 | GlaxoSmithKline Biologicals S.A. | Vaccine for the treatment of atherosclerosis |
-
2001
- 2001-09-04 HU HU0203251A patent/HUP0203251A2/hu unknown
- 2001-09-04 JP JP2002524523A patent/JP2004508029A/ja active Pending
- 2001-09-04 BR BR0107175-0A patent/BR0107175A/pt not_active Application Discontinuation
- 2001-09-04 IL IL14937901A patent/IL149379A0/xx unknown
- 2001-09-04 CN CNB018030572A patent/CN1231262C/zh not_active Expired - Fee Related
- 2001-09-04 EP EP01965715A patent/EP1315517B1/en not_active Expired - Lifetime
- 2001-09-04 AU AU86286/01A patent/AU8628601A/en not_active Abandoned
- 2001-09-04 CZ CZ20021571A patent/CZ20021571A3/cs unknown
- 2001-09-04 EE EEP200200238A patent/EE200200238A/xx unknown
- 2001-09-04 CA CA002389739A patent/CA2389739A1/en not_active Abandoned
- 2001-09-04 RU RU2003109439/13A patent/RU2313536C2/ru not_active IP Right Cessation
- 2001-09-04 SK SK631-2002A patent/SK6312002A3/sk unknown
- 2001-09-04 MX MXPA02004505A patent/MXPA02004505A/es unknown
- 2001-09-04 WO PCT/KR2001/001492 patent/WO2002020040A1/en not_active Application Discontinuation
-
2002
- 2002-04-25 BG BG106655A patent/BG106655A/bg unknown
- 2002-04-29 LT LT2002051A patent/LT4989B/lt not_active IP Right Cessation
- 2002-05-03 NO NO20022147A patent/NO20022147D0/no not_active Application Discontinuation
-
2003
- 2003-03-04 US US10/378,707 patent/US6825318B2/en not_active Expired - Lifetime
Non-Patent Citations (1)
| Title |
|---|
| KWAK, J.W., «Cloning and characterization of cDNAs coding for heavy and light chains of a monoclonal antibody (MabB23) specific for human plasma apolipoprotein B-100», Gene, 1996 Mar 9; 169(2), реф. * |
Also Published As
| Publication number | Publication date |
|---|---|
| RU2003109439A (ru) | 2004-07-20 |
| IL149379A0 (en) | 2002-11-10 |
| EP1315517A1 (en) | 2003-06-04 |
| US20030211997A1 (en) | 2003-11-13 |
| CZ20021571A3 (cs) | 2002-09-11 |
| BG106655A (bg) | 2004-08-31 |
| EP1315517B1 (en) | 2010-10-20 |
| NO20022147L (no) | 2002-05-03 |
| LT4989B (lt) | 2003-01-27 |
| SK6312002A3 (en) | 2002-09-10 |
| MXPA02004505A (es) | 2004-09-10 |
| NO20022147D0 (no) | 2002-05-03 |
| HUP0203251A2 (hu) | 2003-01-28 |
| BR0107175A (pt) | 2002-07-02 |
| AU8628601A (en) | 2002-03-22 |
| CN1231262C (zh) | 2005-12-14 |
| CN1392798A (zh) | 2003-01-22 |
| EE200200238A (et) | 2003-06-16 |
| LT2002051A (en) | 2002-09-25 |
| WO2002020040A1 (en) | 2002-03-14 |
| US6825318B2 (en) | 2004-11-30 |
| CA2389739A1 (en) | 2002-03-14 |
| EP1315517A4 (en) | 2005-02-09 |
| JP2004508029A (ja) | 2004-03-18 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US6410022B1 (en) | Modulation of cholesteryl ester transfer protein (CETP) activity | |
| JP4386209B2 (ja) | 癌治療における擬似ペプチド | |
| KR20000016414A (ko) | Apl 면역반응성 펩티드, 그것의 콘주게이트 및 apl항체-매개병변의 치료방법 | |
| RU2313536C2 (ru) | Конкатемер пептида, индуцирующего выработку антител против аполипопротеина в-100, вакцина для лечения ожирения, способ получения конкатемера, полинуклеотид, экспрессирующий вектор | |
| US7829667B2 (en) | Anti-obese immunogenic hybrid polypeptides and anti-obese vaccine composition comprising the same | |
| JP2010504094A (ja) | 抗肥満用免疫原性ハイブリッドポリペプチド及びこれを含む抗肥満ワクチン組成物(Anti−ObeseImmunogenicHybridPolypeptidesAndAnti−ObeseVaccineCompositionComprisingTheSame) | |
| JP2010504094A5 (ru) | ||
| JP2006502409A (ja) | バイオコンフォーマティック(bioconformatic)分析のためのモノクローナル抗体 | |
| KR100472841B1 (ko) | 아포지단백질 비-100의 에피토프에 대한 모조 펩타이드,그들의 연쇄물 또는 변형체와 이들을 함유하는 백신 조성물 | |
| JPH11507910A (ja) | Hdlコレステロールレベルを増大する方法 | |
| CA2098733A1 (en) | Lipid receptors for microorganisms and corresponding adhesins, dna sequences encoding adhesins, and use thereof | |
| AU2007200834B2 (en) | Mimetic peptides for epitope of apolipoprotein B-100, concatemer and modified peptides thereof, and the vaccine composition comprising the same | |
| AU7865900A (en) | AB5 toxin B subunit mutants with altered chemical conjugation characteristics | |
| TRZYNA et al. | Schistosoma mansoni: genetic non‐response to p40, the major protein antigen of the egg, reveals a novel mechanism enhancing IgM production during infection | |
| Witztum et al. | Autoimmunity to oxidized lipoproteins | |
| US5871739A (en) | Pharmaceutical composition | |
| EP1082346A1 (en) | Specific binding proteins for treating canine allergy | |
| WO2001002001A9 (en) | PEPTIDE LIGANDS THAT BIND IgM ANTIBODIES AND BLOCK INTERACTION WITH ANTIGEN | |
| KR100471115B1 (ko) | 장병원성 대장균 감염의 예방 및 치료를 위한 수용성단백질 및 이를 포함한 알 및 이들의 제조방법 | |
| JP2000505645A (ja) | カルシウム結合プロテオリピド組成物および方法 | |
| JPH0859501A (ja) | 医薬組成物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| FA92 | Acknowledgement of application withdrawn (lack of supplementary materials submitted) |
Effective date: 20051110 |
|
| FZ9A | Application not withdrawn (correction of the notice of withdrawal) |
Effective date: 20061017 |
|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20120905 |