RU2101278C1 - Способ превращения кетоксима или альдоксима в соответствующий амид - Google Patents
Способ превращения кетоксима или альдоксима в соответствующий амид Download PDFInfo
- Publication number
- RU2101278C1 RU2101278C1 RU93034459A RU93034459A RU2101278C1 RU 2101278 C1 RU2101278 C1 RU 2101278C1 RU 93034459 A RU93034459 A RU 93034459A RU 93034459 A RU93034459 A RU 93034459A RU 2101278 C1 RU2101278 C1 RU 2101278C1
- Authority
- RU
- Russia
- Prior art keywords
- oxime
- groups
- benzene rings
- organic
- group
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C231/00—Preparation of carboxylic acid amides
- C07C231/10—Preparation of carboxylic acid amides from compounds not provided for in groups C07C231/02 - C07C231/08
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L33/00—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof
- A23L33/10—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof using additives
- A23L33/13—Nucleic acids or derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/60—Sugars; Derivatives thereof
- A61K8/606—Nucleosides; Nucleotides; Nucleic acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q19/00—Preparations for care of the skin
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D201/00—Preparation, separation, purification or stabilisation of unsubstituted lactams
- C07D201/02—Preparation of lactams
- C07D201/04—Preparation of lactams from or via oximes by Beckmann rearrangement
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H19/00—Compounds containing a hetero ring sharing one ring hetero atom with a saccharide radical; Nucleosides; Mononucleotides; Anhydro-derivatives thereof
- C07H19/02—Compounds containing a hetero ring sharing one ring hetero atom with a saccharide radical; Nucleosides; Mononucleotides; Anhydro-derivatives thereof sharing nitrogen
- C07H19/04—Heterocyclic radicals containing only nitrogen atoms as ring hetero atom
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q19/00—Preparations for care of the skin
- A61Q19/02—Preparations for care of the skin for chemically bleaching or whitening the skin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q19/00—Preparations for care of the skin
- A61Q19/08—Anti-ageing preparations
Abstract
Использование: получение амидов из кетоксимов или альдоксимов перегруппировкой Бекмана. Сущность изобретения: амид получают перегруппировкой Бекмана в растворе сульфоксида, предпочтительно диметилсульфоксида, с использованием гетерогенного сильнокислого катализатора, включающего носитель с сульфированными бензольными кольцами, которые также содержат одну или более электроноакцепторных групп. Остальные заместители представляют собой С1-С5-алкил или арилалкил. Электроноакцепторной группой служит нитрогруппа, галоген или сульфокислотная группа. В качестве оксима используют циклический кетоксим С6-С12. Носителем в катализаторе является сульфированная полистиролдивинилбензольная смола. 11 з.п. ф-лы, 1 табл.
Description
Изобретение относится к получению амидов из кетоксимов или альдоксимов перегруппировкой Бекмана.
Осуществляют способ превращения кетоксима или альдоксима в соответствующий амид, при котором раствор оксима в органическом растворителе вводят в контакт с сильно кислым катализатором. Изобретение относится в особенности к способу превращения циклического кетоксима в соответствующий лактам (циклический амид).
Известен способ (патент Великобритании В-1342550), в котором оксим циклогексанона в диметилсульфоксиде (ДМСО) в качестве растворителя вводят в контакт с сильно кислым катализатором. Этот катализатор представляет собой сульфированную полистиролдивинилбензольную смолу и действует как ионообменник.
В промышленном масштабе превращение циклических кетоксимов в соответствующие лактамы, согласно перегруппировке Бекмана для получения ε-капролактама и оксима циклогексанона обычно осуществляют в гомогенной, очень кислой жидкой фазе, используя, например, олеум, необязательно растворенный в жидком диоксиде серы.
Содержащую лактам реакционную смесь затем нейтрализуют с помощью аммиачной воды, и лактам отделяют от образовавшегося раствора сульфата аммония. Следующей стадией является регенерация сульфата аммония из не содержащего лактама раствора путем кристаллизации.
Это означает, что при получении e-капролактама образуется большое количество сульфата аммония, например 1,7 1,9 т (NH4)2SO4 на тонну лактама, если превращение осуществляют в олеуме. Такое количество побочного продукта рассматривается как нежелательное ввиду увеличивающихся трудностей, с которыми встречаются при продаже сульфата аммония, и сопутствующих проблем загрязнения окружающей среды, и по этой причине уже некоторое время стремятся к способам осуществления превращения оксимов в лактамы без образования побочного продукта сульфата аммония.
Известен также способ осуществления превращения при высоких температурах в газовой фазе в присутствии твердого кислого катализатора, такого как оксид бора на диоксиде кремния (патент ФРГ В-2053065), но этот способ технически и экономически менее привлекателен, так как осуществление способа в газовой фазе вместе жидкой фазы связано с наличием большого объема, следствием которого является то, что расходы на оборудование и повышенные издержки высокие по сравнению с жидкофазным способом. Кроме того, высокая температура в случае способа в газовой фазе неблагоприятна для качества получаемого лактама.
В вышеуказанном патенте Великобритании B-1342550 предложено осуществлять превращение оксима в соответствующий лактам под действием сильнокислого ионообменника в H+-форме, причем ионообменник контактирует с растворенным в растворителе оксимом. В противоположность этому, при превращении оксимов в лактамы в гомогенной среде олеума, необязательно растворенного в жидком диоксиде серы, образующийся лактам выделяют путем нейтрализации кислоты аммиаком. В случае применения очень кислого ионообменника в такой нейтрализации нет необходимости, так как не используют никакого олеума. Однако селективность по лактаму и превращение оксима, относящиеся к известному способу (патент Великобритании В-1342550), довольно невысокие для этого способа по сравнению с вышеуказанным способом перегруппировки с использованием олеума.
Целью настоящего изобретения является разработка усовершенствованного способа с высокой селективностью по лактаму и высокой производительностью по лактаму путем перегруппировки циклических кетоксимов в соответствующие лактамы с использованием ионообменников.
Эта цель достигается путем контактирования раствора оксима в растворителе с гетерогенным, очень кислым катализатором, причем гетерогенный катализатор представляет собой носитель с сульфированными бензольными кольцами, и также сальдированные бензольные кольца содержат электроноакцепторную группу.
Найдено, что наличие злектроноакцепторных групп в сульфированном бензольном кольце оказывает положительное влияние на селективность по лактаму и производительность по лактаму.
Примеры кетоксимов или альдоксимов, которые могут быть использованы согласно настоящему изобретению, включают ненасыщенные и насыщенные, замещенные или незамещенные алифатические кетоксимы или альдоксимы или циклические кетоксимы с 2 30 C-атомами, такие как оксим ацетона, ацетальдоксим, бензальдоксим, пропанальдоксим, бутанальдоксим, оксим бутанона, оксим бутен-1-она, оксим циклопропанона, оксим циклогексанона, оксим циклооктанона, оксим циклододеканона, оксим циклопентенона, оксим циклододеканона, оксим 2-фенил-циклогексанона, оксим циклогексенона.
В качестве сырья для способа согласно изобретению предпочтительно используют циклический кетоксим. Предпочтительно циклический кетоксим содержит 5 12, в особенности 6 12 C-атомов. Примерами пригодных циклических кетоксимов являются оксимы циклогексанона, циклооктанона и циклододеканона.
Эта спецификация и примеры базируются в особенности на оксиме циклогексанона ввиду того, что в этом варианте образуется интересный с коммерческой точки зрения e-капролактам.
Возможными растворителями могут быть любые неорганические или органические растворители или смеси обоих.
Кетоксим предпочтительно растворяют в органическом растворителе. Возможными органическими растворителями (патент Великобритании В-1342550) являются толуол, диметилформамид и смеси уксусного ангидрида, толуола и циклогексана. Наиболее пригодным растворителем являются органический сульфоксид общей формулы R1SOR2, где R1 и R2 обозначают С1-С2-алкильные или С6-С12-арильные группы. Из этой группы органических сульфоксидов предпочтительно используют диметилсульфоксид (ДМСО), так как это вещество получают в промышленном масштабе, и оно может быть приобретено по недорогой цене.
Не придавая значения стоимости, здесь также могут быть использованы другие органические сульфоксиды, такие как диэтилсульфоксид, дибутилсульфоксид, дивинилсульфоксид и дифенилсульфоксид.
Концентрация оксима в органическою растворителе как правило составляет 0,1 40 мас. и предпочтительно 0,5 30 мас. и наиболее предпочтительно 1 20 мас.
Катализатор состоит из носителя, комбинированного с сульфированными бензольными кольцами, причем сульфированные бензольные кольца модифицированы электроноакцепторной группой. Катализатор обладает способностью к обмену ионов. Ионообменная емкость выражается в мг-экв. H+ на грамм сухого катализатора.
Катализатор согласно изобретению обычно имеет емкость 0,1 6 мг-экв. H+ на грамм сухого катализатора.
Модифицированные бензольные кольца могут быть описаны следующей общей формулой (I):
где R3 R7 независимо друг от друга обозначают одну или более электроноакцепторных групп, выбираемых из нитрогруппы (-NO2), галогена (-Cl, -Br, -F, -I), сульфокислотной группы (-SO3H), гидроксила, алкоксильной или циано (-C= N)-группы, причем остальные группы обозначают водород, алкил или арилалкил, где по меньшей мере одна группа обозначает: -R-P (формула (II)) или -P (формула (III)), где R может быть замещенным или незамещенным C1-C5-алкилом или замещенным или незамещенным C6-C12-арилом или арилалкилом и где P представляет собой часть органического или неорганического носителя.
где R3 R7 независимо друг от друга обозначают одну или более электроноакцепторных групп, выбираемых из нитрогруппы (-NO2), галогена (-Cl, -Br, -F, -I), сульфокислотной группы (-SO3H), гидроксила, алкоксильной или циано (-C= N)-группы, причем остальные группы обозначают водород, алкил или арилалкил, где по меньшей мере одна группа обозначает: -R-P (формула (II)) или -P (формула (III)), где R может быть замещенным или незамещенным C1-C5-алкилом или замещенным или незамещенным C6-C12-арилом или арилалкилом и где P представляет собой часть органического или неорганического носителя.
Предпочтительно электроноакцепторной группой является -Cl-, -F, -SO3H-группа или -NO2-группа. R в формуле (II) также может иметь электроноакцепторную способность за счет введения электроноакцепторных групп в R.
Предпочтительно бензольное кольцо содержит 1 3 электроноакцепторные группы, и в особенности 1 2 электроноакцепторные группы.
Носитель представляет собой материал, который является твердым в условиях способа и который нерастворим или едва растворим в используемом растворителе. Носитель может быть органического или неорганического происхождения.
Примерами органического носителя P являются (линейные) карбоцепные полимеры, такие как полиэтилен, полипропилен и полибутадиен. Обычно в бензольном кольце присутствуют одна или две -P- или -R-P-группы. Примерами пригодных смол являются полистирол (одна -P-группа, где P есть полиэтилен), полидивинилбензол (две -P-группы, где P есть полиэтилен) и смеси этих смол, в которых присутствуют бензольные кольца с одной и с двумя -P-группами, такие как полистиролдивинилбензольная смола. Эти смолы имеются в продаже и могут быть легко сульфированы, например, с помощью олеума.
R в формуле (II) может обозначать метильную, этильную, пропильную или фениленовую группу. R может быть также другим бензольным сульфированным кольцом, соединенным с бензольным кольцом формулы (I) через формильную группу (патент ФРГ А-3544210).
Предпочтительным вариантом согласно изобретению является сульфированная полистиролдивинилбензольная смола, в которой сульфированное бензольное кольцо также содержит электроноакцепторную группу. Такой ионообменник с хлором или бромом в качестве электроноакцепторных групп описан в патенте США А-4 269 943. Если эта сульфированная полистиролдивинилбензольная смола, модифицированная электроноакцепторными группами, используется в качестве катализатора, то ионообменник неожиданно проявляет более длительную стабильность в течение перегруппировки оксимов в лактамы, чем ионообменник из уровня техники. Дополнительное преимущество повышенной стабильности ионообменника согласно изобретению заключается в том, что с ним можно работать при более высоких температурах, так что дополнительно увенчивается производительность. Производительность здесь выражается количеством лактама, получаемого на активном каталитическом центре и в единицу времени. Количество активных каталитических центров на грамм катализатора выражается в экв. H+ на грамм катализатора и имеет такую же, как и указанную ранее, емкость.
Примерами неорганических носителей являются уголь и оксиды металлов со свободными OH-группами, такие как SiO2, Al2O3, ZnO, TiO2 и MgO. Связь между сульфированным бензольным кольцом и носителем может быть однократною химической связью (прямой или, например, через алкильную группу), примером неорганического носителя, комбинированного с сульфированными бензольными кольцами, является SiO2, связанный с сульфированным бензольным кольцом через алкильную группу
Для приемлемой скорости реакции желательна температура 75 200oС и предпочтительно 110 150oС.
Для приемлемой скорости реакции желательна температура 75 200oС и предпочтительно 110 150oС.
Как вариант способа согласно изобретению более предпочтителен непрерывный способ, чем периодическое производство, ибо при непрерывном способе достигают более высокого превращения оксима и более высокого выхода лактама. Предпочтительно используют реактор с неподвижным слоем, но также можно использовать реактор с непрерывным перемешиванием.
Изобретение поясняется на основе следующих примеров, не ограничивающих его объема охраны.
В примерах используется ряд терминов, которые ради ясности объясняются ниже:
Выход лактама (%) селективность по лактаму x превращение оксима / 100%
Ионообменная емкость выражена в мг-экв. H+ на грамм сухого ионообменника.
Выход лактама (%) селективность по лактаму x превращение оксима / 100%
Ионообменная емкость выражена в мг-экв. H+ на грамм сухого ионообменника.
В примерах используется продажная полистиролдивинилбензольная смола фирмы Rohm и Haas.
Используемыми ионообменниками являются:
Amberlyst 15 (Amberlyst торговое название фирмы Rohm и Haas): сульфированная полистиролдивинилбензольная смола в качестве стандартного материала;
Amberlyst 17: сульфированная полистиролдивинилбензольная смола, модифицированная хлором;
Amberlyst 35: сульфированная полистиролдивинилбензольная смола, модифицированная второй сульфокислотной группой на бензольном кольце.
Amberlyst 15 (Amberlyst торговое название фирмы Rohm и Haas): сульфированная полистиролдивинилбензольная смола в качестве стандартного материала;
Amberlyst 17: сульфированная полистиролдивинилбензольная смола, модифицированная хлором;
Amberlyst 35: сульфированная полистиролдивинилбензольная смола, модифицированная второй сульфокислотной группой на бензольном кольце.
Пример I. Ионообменник Amberlyst 17, емкость которого составляет 3,26 мг-экв. H+ на грамм сухого катализатора, предварительно обрабатывают путем последовательных промывок с помощью 5н. HCl, воды и ДМСО.
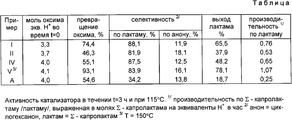
Концентрация исходного оксида циклогексанона составляет 5 мас. в ДМСО. Содержимое реактора образовано 0,25 л этой смеси и количеством ионообменника, как указано в таблице. Температура составляет 115o0, скорость мешалки составляет 2000 об. /мин, и время реакции 3 ч. Производительность по ε-капролактаму составляет 0,76 моль e-капролактама на эквивалент H+ в час. Некоторые другие результаты суммированы в таблице.
Пример II. Повторяют пример I, но с Amberlyst 35, емкость которого составляет 5,05 мг-экв. H+ на грамм сухого катализатора. Результаты представлены в таблице.
Пример III. При комнатной температуре 5 г сухого Amberlyst 15 в качестве ионообменника, который предварительно был высушен в вакууме при 60oC, добавляют 5-ю порциями (с интервалами в 15 мин) к смеси 41,5 г 65%-ной HNO3 и 73,6 г H2SO4 (в дальнейшем обозначается как нитрующая кислота) в круглодонной колбе емкостью 250 мл. Реакционную смесь затем нагревают до 95oC, после чего смесь выдерживают при этой температуре в течение 10 мин. Потом смесь медленно охлаждают до комнатной температуры в течение 2 ч, после чего ионообменник отфильтровывают от нитрующей кислоты и промывают 5 раз деминерализованной водой. Реакция промывной воды, затем перегоняемой, слабокислая (pH 6).
Полученный ионообменник имеет емкость 2,36 мг-экв. H+ на грамм сухого катализатора.
Пример IV. Повторяют пример I, но теперь используют ионообменник, полученный в примере III. Результаты представлены в таблице.
Пример V. Повторяют пример I, но при температуре 150oC. Соотношение между оксимом циклогексанона и эквивалентами H+ составляет 4,1 во время t 0. Производительность по e-капролактаму составляет 1,07 моль лактама на эквивалент H+ в час. Результаты представлены в таблице.
Пример VI. В реакторе с перемешиванием 1,5 кг смеси, как полученная в примере I, в течение 2 мин вводят в контакт с 10 г воды, которая содержит фосфорную кислоту и имеет pH 1,8, при температуре 100oC. Оксим циклогексанона гидролизуется на 100% в циклогексанон и гидроксиламин. Посредством периодической отгонки воду отгоняют под давлением 50 мм рт.ст. Перегонку продолжают при пониженном давлении (15 мм рт. ст. ). Циклогексанон и 16,1 г e-капролактама получают из раствора ДМСО.
Сравнительный пример А. Повторяют пример I, но используют Amberlyst-15, который имеет емкость 4.11 мг-экв. H+ на грамм сухого катализатора. Производительность по e-капролактаму составляет 0,25 моль лактама на эквивалент H+ в час. Некоторые другие результаты представлены в таблице.
Claims (12)
1. Способ превращения кетоксима или альдоксима в соответствующий амид, при котором раствор оксима в растворителе вводят в контакт с гетерогенным сильнокислым катализатором, отличающийся тем, что гетерогенный катализатор представляет собой носитель с сульфированными бензольными кольцами, причем сульфированные бензольные кольца также содержат электроноакцепторную группу.
2. Способ по п.1, отличающийся тем, что бензольные кольца имеют общую формулу
где R3 R7, независимо друг от друга, одна или более электроноакцепторных групп, причем остальные группы обозначают водород, алкил или арилалкил и по меньшей мере одна из групп R3 R7 обозначает -R-P или -Р, где R замещенный или незамещенный С1 С5-алкил или замещенный, или незамещенный С6 С1 2-арил, или арилалкил, Р часть органического или неорганического носителя.
где R3 R7, независимо друг от друга, одна или более электроноакцепторных групп, причем остальные группы обозначают водород, алкил или арилалкил и по меньшей мере одна из групп R3 R7 обозначает -R-P или -Р, где R замещенный или незамещенный С1 С5-алкил или замещенный, или незамещенный С6 С1 2-арил, или арилалкил, Р часть органического или неорганического носителя.
3. Способ по п. 1, отличающийся тем, что носитель имеет органическое происхождение.
4. Способ по п.3, отличающийся тем, что часть бензольных колец содержит одну, а часть бензольных колец содержит две -Р-группы, где Р линейная углеродная цепь, образованная сульфированной полистиролдивинилбензольной смолой.
5. Способ по любому из пп.1 4, отличающийся тем, что электронакцепторной группой может быть нитрогруппа (NO2), галоген (-Cl, -Br, -F, -J) или сульфокислотная группа (SO3H).
6. Способ по любому из пп.1 5, отличающийся тем, что растворителем является органический растворитель.
7. Способ по п.6, отличающийся тем, что органическим растворителем является органический сульфоксид общей формулы R1SOR2, где R1 и R2 С1 С5-алкильные или С6 - С1 2-арильные группы.
8. Способ по п.7, отличающийся тем, что органическим сульфоксидом является диметилсульфоксид.
9. Способ по любому из пп.1 8, отличающийся тем, что превращение происходит при температуре выше 75oС.
10. Способ по любому из пп.1 9, отличающийся тем, что оксимом является циклический кетоксим.
11. Способ по п.10, отличающийся тем, что циклический кетоксим содержит 6 12 атомов углерода.
12. Способ по п.10, отличающийся тем, что циклическим кетоксимом является оксим циклогексанона.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| NL9201160 | 1992-06-30 | ||
| NL9201160A NL9201160A (nl) | 1992-06-30 | 1992-06-30 | Werkwijze voor de omzetting van oximen in de overeenkomstige amides. |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU93034459A RU93034459A (ru) | 1996-02-27 |
| RU2101278C1 true RU2101278C1 (ru) | 1998-01-10 |
Family
ID=19860992
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU93034459A RU2101278C1 (ru) | 1992-06-30 | 1993-06-29 | Способ превращения кетоксима или альдоксима в соответствующий амид |
Country Status (20)
| Country | Link |
|---|---|
| EP (1) | EP0577203B1 (ru) |
| JP (1) | JPH07300454A (ru) |
| KR (1) | KR100291352B1 (ru) |
| CN (1) | CN1036583C (ru) |
| AT (1) | ATE148097T1 (ru) |
| BR (1) | BR9302701A (ru) |
| CZ (1) | CZ287271B6 (ru) |
| DE (1) | DE69307608T2 (ru) |
| DK (1) | DK0577203T3 (ru) |
| ES (1) | ES2097968T3 (ru) |
| GE (1) | GEP19971109B (ru) |
| GR (1) | GR3023169T3 (ru) |
| HU (1) | HU213633B (ru) |
| MX (1) | MX9303897A (ru) |
| NL (1) | NL9201160A (ru) |
| PL (1) | PL173841B1 (ru) |
| RU (1) | RU2101278C1 (ru) |
| SG (1) | SG48178A1 (ru) |
| TW (1) | TW223055B (ru) |
| UA (1) | UA43307C2 (ru) |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1095461C (zh) * | 1999-04-30 | 2002-12-04 | 中国科学院上海有机化学研究所 | 三氟乙酰基苯乙酮肟及其衍生物的合成方法 |
| FR2803197B1 (fr) * | 1999-12-30 | 2002-03-15 | Oreal | Composition pour la teinture d'oxydation des fibres keratiniques comprenant un polymere epaississant comportant au moins une chaine grasse et un alcool gras ayant plus de vingt atomes de carbone |
| CN100389107C (zh) * | 2003-06-30 | 2008-05-21 | 中国石油化工股份有限公司 | 一种制备己内酰胺的方法 |
| CN1312133C (zh) * | 2004-03-15 | 2007-04-25 | 中国石油化工股份有限公司 | 一种从离子液体中分离贝克曼重排反应产物的方法 |
| CN101250148B (zh) * | 2008-03-14 | 2010-08-25 | 湘潭大学 | 一种环己酮肟液相重排制取己内酰胺的方法 |
| CN102863385B (zh) * | 2012-10-09 | 2014-01-01 | 清华大学 | 一种由环己酮直接合成己内酰胺的方法 |
| CN108080027B (zh) * | 2017-12-23 | 2021-05-28 | 中国天辰工程有限公司 | 一种液相贝克曼重排制己内酰胺的树脂催化剂处理工艺 |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CH394212A (de) * | 1962-01-13 | 1965-06-30 | Inventa Ag | Verfahren zur Umlagerung cyclischer Oxime |
| US3944542A (en) * | 1971-05-15 | 1976-03-16 | Stamicarbon, B.V. | Conversion of ketoximes into lactams in organic sulfoxide solvents |
| NL9001545A (nl) * | 1990-07-06 | 1992-02-03 | Stamicarbon | Werkwijze voor het behandelen van amides. |
-
1992
- 1992-06-30 NL NL9201160A patent/NL9201160A/nl not_active Application Discontinuation
-
1993
- 1993-06-08 TW TW082104548A patent/TW223055B/zh active
- 1993-06-11 UA UA93002178A patent/UA43307C2/ru unknown
- 1993-06-21 GE GEAP1993912A patent/GEP19971109B/en unknown
- 1993-06-23 KR KR1019930011444A patent/KR100291352B1/ko not_active IP Right Cessation
- 1993-06-25 DE DE69307608T patent/DE69307608T2/de not_active Expired - Fee Related
- 1993-06-25 AT AT93201841T patent/ATE148097T1/de not_active IP Right Cessation
- 1993-06-25 ES ES93201841T patent/ES2097968T3/es not_active Expired - Lifetime
- 1993-06-25 SG SG1996007654A patent/SG48178A1/en unknown
- 1993-06-25 EP EP93201841A patent/EP0577203B1/en not_active Expired - Lifetime
- 1993-06-25 DK DK93201841.9T patent/DK0577203T3/da active
- 1993-06-28 JP JP5156825A patent/JPH07300454A/ja active Pending
- 1993-06-28 CZ CZ19931290A patent/CZ287271B6/cs not_active IP Right Cessation
- 1993-06-29 HU HU9301895A patent/HU213633B/hu not_active IP Right Cessation
- 1993-06-29 CN CN93107880A patent/CN1036583C/zh not_active Expired - Fee Related
- 1993-06-29 PL PL93299511A patent/PL173841B1/pl unknown
- 1993-06-29 MX MX9303897A patent/MX9303897A/es not_active IP Right Cessation
- 1993-06-29 BR BR9302701A patent/BR9302701A/pt not_active IP Right Cessation
- 1993-06-29 RU RU93034459A patent/RU2101278C1/ru active
-
1997
- 1997-04-18 GR GR970400826T patent/GR3023169T3/el unknown
Also Published As
| Publication number | Publication date |
|---|---|
| EP0577203B1 (en) | 1997-01-22 |
| NL9201160A (nl) | 1994-01-17 |
| MX9303897A (es) | 1993-12-01 |
| JPH07300454A (ja) | 1995-11-14 |
| ATE148097T1 (de) | 1997-02-15 |
| KR100291352B1 (ko) | 2001-09-17 |
| HUT65116A (en) | 1994-04-28 |
| CZ129093A3 (en) | 1994-01-19 |
| HU213633B (en) | 1997-08-28 |
| DK0577203T3 (da) | 1997-07-14 |
| CN1083807A (zh) | 1994-03-16 |
| PL299511A1 (en) | 1994-01-10 |
| CN1036583C (zh) | 1997-12-03 |
| TW223055B (ru) | 1994-05-01 |
| PL173841B1 (pl) | 1998-05-29 |
| DE69307608T2 (de) | 1997-09-04 |
| KR940000411A (ko) | 1994-01-03 |
| UA43307C2 (ru) | 2001-12-17 |
| ES2097968T3 (es) | 1997-04-16 |
| GEP19971109B (en) | 1997-10-10 |
| HU9301895D0 (en) | 1993-09-28 |
| BR9302701A (pt) | 1994-02-08 |
| DE69307608D1 (de) | 1997-03-06 |
| GR3023169T3 (en) | 1997-07-30 |
| CZ287271B6 (en) | 2000-10-11 |
| SG48178A1 (en) | 1998-04-17 |
| EP0577203A1 (en) | 1994-01-05 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2101278C1 (ru) | Способ превращения кетоксима или альдоксима в соответствующий амид | |
| KR0183044B1 (ko) | 옥심의 액상 전위에 의한 아미드의 제조방법 | |
| JP5447502B2 (ja) | アミド化合物の製造方法 | |
| JPH01203344A (ja) | エポキシドの異性化による環状ケトンの製法 | |
| JP4013334B2 (ja) | エポキシシクロドデカジエンの製造方法 | |
| RU1834885C (ru) | Способ очистки амидов, получаемых из оксимов при перегруппировке Бекмана | |
| US4689412A (en) | Method for preparing lactams having 8 to 15 carbon atoms from the corresponding oximes | |
| KR0157062B1 (ko) | 옥심에서 아미드로의 재배열을 위한 반응촉진제 및 옥심의 재배열에 의한 아미드 제조방법 | |
| EP0639565A1 (en) | Process for preparing a lactam | |
| JP2001302603A (ja) | アミド化合物の製造方法 | |
| JP2001302602A (ja) | アミド化合物の製造方法 | |
| CN107438594B (zh) | 一种用于合成环酰胺的有效的工艺 | |
| US6489474B1 (en) | Process for producing amide compound | |
| JP2608823B2 (ja) | オキシムの接触的液相ベックマン転位によるアミドの製造方法 | |
| US3404148A (en) | Preparation of omega-laurinolactam | |
| JP3139066B2 (ja) | オキシムの液相転位によるアミドの製造方法 | |
| JP4218277B2 (ja) | アミド化合物の製造方法 | |
| JP2640583B2 (ja) | オキシムの転位によるアミドの製造方法及びその反応促進剤 | |
| JPS6249262B2 (ru) | ||
| JP2549027B2 (ja) | オキシムの接触的液相転位によるアミドの製造方法 | |
| JPH0447655B2 (ru) | ||
| JP2000095757A (ja) | シクロアルカノンオキシムからラクタムを製造する方法 | |
| JP2002234870A (ja) | アミド化合物の製造方法 | |
| JP2003104973A (ja) | アミド化合物の製造方法 |